причины, симптомы, диагностика, лечение и профилактика
Миалгия – мышечные боли различного характера, выраженности, локализации. Развиваются в силу многочисленных причин, в том числе могут быть одним из симптомов какого-либо невралгического, ревматического, инфекционного, эндокринного заболевания.Согласно международной классификации болезней (МКБ-10), миалгии присвоен код М79.1.
Причины миалгии
Миалгия — следствие многих причин. Чаще всего ее связывают с неправильными физическими нагрузками. Так, при чрезмерных нагрузках, перенапряжении, неправильной техники выполнения физических упражнений повреждаются и воспаляются мышечные волокна, что влечет болезненные ощущения.
Недостаточная физическая активность, перенесенные травмы также провоцируют негативное состояние.
Миалгия часто сопровождает высокую температуру при инфекционных заболеваниях в острой стадии: гриппе, тонзиллите и других.
Мышечные боли, в качестве одного из симптомов, присущи:
-
сколиозу, кифозу;
-
артриту;
-
радикулиту;
-
артритам;
-
артралгии;
-
эндокринным патологиям.
Частые стрессовые ситуации, тревожные состояния и эмоциональные нагрузки приводят к активизации симпатической нервной системы, мышечным спазмам и болям.
Симптомы миалгии
Основной симптом миалгии – мышечные боли, которые в зависимости от причины имеют различную локализацию и бывают ноющими, тупыми, интенсивными, острыми, постоянными.
К основному симптому возможно присоединение следующих проявлений:
-
болевых ощущений в суставах;
-
тяжести в конечностях;
-
гипертонии;
-
головных болей;
-
головокружения, слабости;
-
тошноты, рвоты.
 Ревматическая полимиалгия характеризуется хроническим течением, постоянно и мучительно болят шея, плечевой, тазовый пояс, движения ограничены.
Ревматическая полимиалгия характеризуется хроническим течением, постоянно и мучительно болят шея, плечевой, тазовый пояс, движения ограничены.
Виды миалгии
Заболевание может протекать в трех формах:
-
Фибромиалгия. Относится к комплексным расстройствам. При мышечно-скелетных болях развивается депрессия, утренняя скованность, усталость, нарушается сон. На теле появляются болезненные участки – «болевые точки».
-
Миозит – воспаление скелетной мускулатуры. Проявляется острыми локальными болями на участках поражения, которые усиливаются в процессе движений и при надавливании. Постепенно движения в суставах становятся ограниченными, что приводит к мышечной слабости и атрофии пораженной мышцы.
-
Полимиозит. Относится к системным заболеваниям скелетной, гладкой мускулатуры, кожных покровов. Выраженные мышечные боли сопровождаются отеками и поражением кожи: эритематозными, папулезными, буллезными высыпаниями, пурпурой, гиперкератозом, гипер- и депигментацией.
 В дальнейшем возможно воспаление внутренних органов, развитие пневмонии, сердечной недостаточности, кишечной непроходимости.
В дальнейшем возможно воспаление внутренних органов, развитие пневмонии, сердечной недостаточности, кишечной непроходимости.
Миалгия может иметь острый и подострый характер. Болевые ощущения, длящиеся более трех месяцев, относят к хронической форме болезни.
Стадии развития миалгии
В своем развитии миалгия проходит несколько стадий:
-
Острые болевые ощущения возникают внезапно во время выполнения определенного физического действия или тактильного контакта. Часто появляются отеки и локальные воспаления.
-
Боли преследуют человека в течение всего дня. Они усиливаются после физических нагрузок, стрессовых ситуаций, при изменении погодных условий и в вечерние часы. Мышечные волокна становятся плотными, выпуклыми. Возможно учащение дыхания и сердцебиения.
-
Болевые ощущения не покидают человека даже в покое.
 Появляется постоянное ощущение усталости и слабости.
Появляется постоянное ощущение усталости и слабости.
Со временем мышечные волокна истончаются и уменьшаются в объеме, снижаются рефлексы.
Осложнения
Несвоевременное лечение миалгии вызывает опасность развития:
-
остеохондроза;
-
артритов, артрозов;
-
радикулита;
-
суставной контрактуры;
-
патологической подвижности позвонков в какой-либо области позвоночного столба.
На последней стадии заболевания развивается мышечная дистрофия, серьезные нервные расстройства. Человек может стать инвалидом.
Диагностика
Проведение диагностики предполагает применением современных лабораторных и инструментальных методов, которые направлены не только на выявление миалгии, но и на установления первопричин.
Первоначально врач анализирует жалобы пациента, собирает анамнез, осматривает и пальпирует пораженный участок. В дальнейшем человек направляется на:
сдачу общих и биохимических анализов;
-
УЗИ;
-
Компьютерную и магнитно-резонансную томографию;
-
игольчатую электронейромиографию.
Записаться на диагностику
В некоторых случаях берутся пробы на наличие вирусного или бактериального поражения.
Лечение миалгии
Лечебные мероприятия направлены на устранение первопричины миалгии и мышечных болей.
С этой целью целесообразно применение следующих консервативных методов:
-
физиотерапии: иглоукалывания, озонотерапии, электрофореза, стоун-терапии, гирудотерапии, грязелечения;
-
массажа: общего, медового, точечного.

Хорошим эффектом обладают противовоспалительные мази, препараты, методы народной медицины. Рекомендуется носить ортезы и другие поддерживающие изделия.
Питание при миалгии не требует серьезных ограничений. Не следует злоупотреблять солью, острой пищей, алкоголем и шоколадом.
Общеукрепляющая гимнастика – эффективный метод терапии. Упражнения подбирает лечащий врач для каждого пациента индивидуально, в зависимости от характера, стадии болезни, особенностей организма, наличия сопутствующих патологий. Рекомендуется:
Самолечение строго запрещено, так как не гарантирует желаемых результатов и может привести к опасным для здоровья последствиям.
Запишитесь на прием к неврологу
Профилактика миалгии
Для предупреждения болевого синдрома в мышцах, необходимо:
-
правильно распределять физические нагрузки;
-
вести здоровый и активный образ жизни;
-
обеспечить здоровый рацион;
-
следить за массой тела;
-
быть оптимистом.

Появление симптомов миалгии – безотлагательный повод обратиться к врачу для проведения диагностики и своевременного лечения. Ведь мышечные боли могут быть вызваны серьезными аутоиммунными заболеваниями и онкологией.
Наши специалисты
Детский невролог
Стаж: 21 год
Записаться на приём
Врач неврологСтаж: 11 лет
Записаться на приём
Врач-невролог
Стаж: 11 лет
Записаться на приём
Невролог, главный внештатный детский невролог МЗ СК, профессор, доктор медицинских наук, Заслуженный врач РФ
Стаж: 39 лет
Записаться на приём
Лечение заболевания «Миалгия» в нашем центре
| group | Номенклатура | Номенклатура | Цена | Цена |
|---|
Запишитесь на прием
Боль в мышцах: причины и симптомы.
 Диагностика, профилактика и лечение
Диагностика, профилактика и лечениеКоличество просмотров: 259 317
Дата последнего обновления: 16.11.2021 г.
Среднее время прочтения: 9 минут
Содержание:
Причины мышечной боли
Мышечное переутомление
Физическая нагрузка
Травмы
Воспаление мышц
Заболевания позвоночника и суставов
Стресс
ОРВИ и грипп
Другие причины
Особенности миалгии
Диагностика мышечной боли
Методы лечения миалгии
Вся наша жизнь в движении, а движение подразумевает работу примерно 400 скелетных мышц1, которые, к тому же, составляют 40-45% массы тела3. Поэтому неудивительно, что каждый человек в течение жизни неоднократно испытывает мышечную боль в разных частях тела — шее, спине, пояснице и конечностях1.
Боль в мышцах, или, по-научному, миалгия5, периодически возникает у 54% женщин и 45% мужчин трудоспособного возраста — от 27 до 50 лет, но подобная жалоба — не редкость даже у детей1.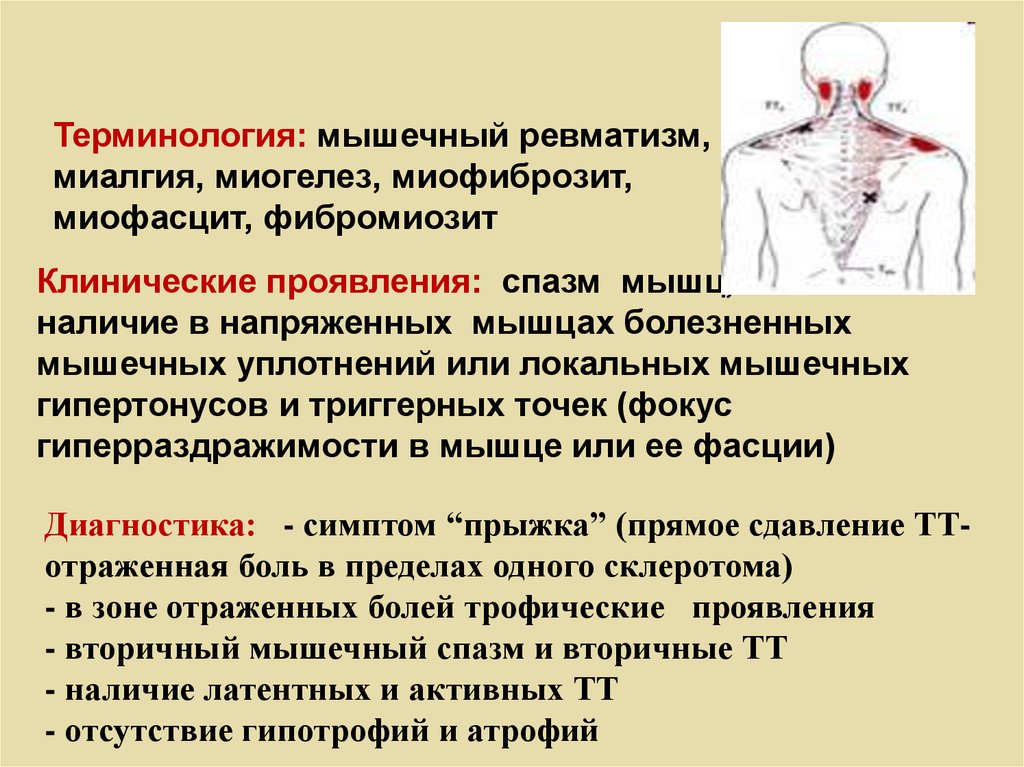 Миалгия может быть незначительной или очень сильной, нестерпимой1, в зависимости от ее причины.
Миалгия может быть незначительной или очень сильной, нестерпимой1, в зависимости от ее причины.
Причины мышечной боли
Благодаря большому количеству нервных окончаний мышечная ткань чутко реагирует на любое повреждение или раздражение. В ответ она выделяет вещества, стимулирующие боль4,5. Факторов, провоцирующих раздражение мышц, очень много. О самых распространенных мы расскажем далее.
Мышечное переутомление
В наш технологичный век у многих постепенно формируется новая «вредная привычка». Проводя большую часть дня перед экраном компьютера или держа в руке мобильные гаджеты, мы можем даже не заметить, что сидим в совершенно неудобной и неестественной позе. Особенно «достается» мышцам плечевого пояса, шеи, спины и правой руки, которая постоянно находится на компьютерной мышке у офисных работников1. Длительное пребывание в одной позе или стереотипность движений могут привести к перенапряжению задействованных в работе мышц, которое мы ощущаем как болезненность1.
Физическая нагрузка
«Ломота» в теле после физической нагрузки может возникать как у нетренированных людей, так и у профессиональных спортсменов8. А причина дискомфорта — накопление недоокисленных продуктов обмена веществ в мышечных клетках, в особенности, болезненные ощущения вызывает чрезмерное количество молочной кислоты (лактата)2. Реже причиной становится микротравма, но такое может наблюдаться, только если нарушены правила тренировки8.
Болезненность в мышцах из-за переутомления возникает не сразу, а через несколько часов или в течение 1-2 дней после тренировки или непривычной физической активности и проходит в течение недели8.
Травмы
Сильная боль может возникать при разрывах мышечных волокон и сухожилий. Обычно такое случается, если нагрузка чрезмерная, а мышцы не подготовлены к ней1. Но повредить их можно также при резких движениях3. В отличие от «ломоты» при переутомлении мышц, боль вследствие травмы возникает сразу, на пике нагрузки3.
Следует помнить, что даже небольшая, но недолеченная травма может стать причиной еще более выраженного растяжения3. Поэтому при болезненных ощущениях, возникающих во время физической нагрузки, обязательно обратитесь к врачу, чтобы исключить серьезную травму.
Вернуться к началу
Воспаление мышц
Воспалительный процесс в мышечной ткани (миозит) может возникать из-за переохлаждения, инфекции или накопления токсичных веществ16,17. Иногда воспаление ограничивается одной группой мышц. Когда же болят мышцы по всему телу, это может быть признаком аутоиммунных заболеваний и других серьезных болезней7.
Заболевания позвоночника и суставов
Мышцы реагируют на нарушение работы связанных с ними суставов4 и позвонков5. Поэтому миалгия является одним из симптомов болезней позвоночника5,11 и суставов конечностей 4. Например, при остеохондрозе или сколиозе (искривлении позвоночника) болезненность в шее, грудной клетке или пояснице связана с перенапряжением околопозвоночных мышц5,11. А в запущенных случаях, когда позвонок сдавливает нервный корешок, выходящий из спинного мозга, боль может «отдавать» в руку или ногу11.
А в запущенных случаях, когда позвонок сдавливает нервный корешок, выходящий из спинного мозга, боль может «отдавать» в руку или ногу11.
Нередко миалгия при остеохондрозе сочетается с чувством онемения или «ползания мурашек». В момент острой боли человек застывает, принимая вынужденное положение11.
Стресс
Длительное эмоциональное напряжение влияет на активность отделов мозга, участвующих в контроле болевых ощущений. Никаких повреждений в мышцах при этом не удается обнаружить, но тем не менее, человек жалуется на дискомфорт или болезненность, которая чаще всего носит хронический характер11.
ОРВИ и грипп
Ломота в мышцах и суставах при простуде и гриппе9 – результат воздействия на мышечные рецепторы бактерий, вирусов и веществ, которые образуются в тканях при инфекции10. Одновременно с болью в мышцах обычно повышается температура тела и возникают симптомы поражения различных отделов дыхательных путей: насморк, кашель и першение в горле9.
Другие причины
Практически любое заболевание внутренних органов может привести к миалгии11. Когда какой-либо орган поражается, он создает болевые импульсы, которые частично передаются мышцам, расположенным поблизости11.
Также причиной миалгии могут быть:
- эндокринные заболевания, например, дефицит гормонов щитовидной железы16,7;
- сосудистые патологии, нарушающие питание мышц конечностей15,16;
- синдром хронической усталости7;
- нарушение баланса микроэлементов в организме16;
- прием лекарственных препаратов, снижающих уровень холестерина в крови12.
Вернуться к началу
Особенности миалгии
Боль, исходящая из мышц, обычно глубокая6. Острая миалгия носит защитный характер, потому что вызывает реакции, направленные на устранение повреждающего фактора11. К таким реакциям относится, например, мышечный спазм4. Но, несмотря на защитный характер, почти всегда есть риск, что боль станет хронической11. Выделяют 2 основные причины хронизации:
Но, несмотря на защитный характер, почти всегда есть риск, что боль станет хронической11. Выделяют 2 основные причины хронизации:
- Повышенная чувствительность. В ответ на раздражение в мышце выделяются вещества, поддерживающие воспаление. Они еще больше раздражают болевые рецепторы в мышцах. В ответ на частые сигналы центральная нервная система снижает болевой порог, поэтому мы можем ощущать болезненность в мышце даже при не сильном ее раздражении11.
- Спазм. При сохранении боли и спазма формируется «порочный круг»: боль вызывает спазм, а спазм поддерживает боль1,5, 11.
Диагностика мышечной боли
Определить, почему возникла миалгия, не всегда просто. Только врач может разобраться в причинах и подобрать лечение, которое помогает избавиться от беспокоящих симптомов или облегчить их. Чтобы выяснить причину миалгии, врач проводит комплексное обследование, в том числе и неврологическое, назначает лабораторные анализы, УЗИ, компьютерную томографию и другие методы исследования3.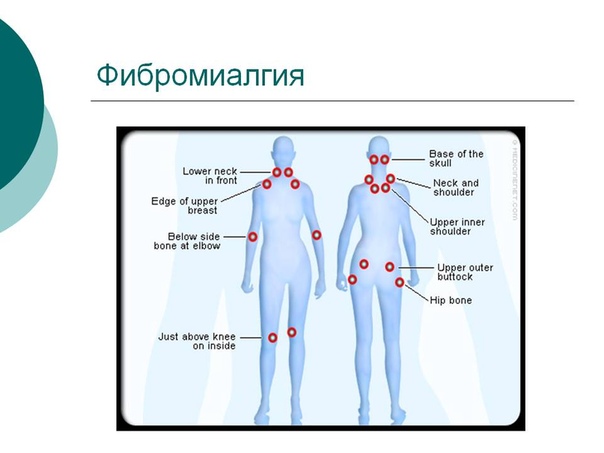
Лечением миалгии занимаются разные специалисты. В зависимости от ее причины, вам могут помочь травматолог, ревматолог, невролог или эндокринолог.
Методы лечения миалгии
Лечение боли в мышцах включает немедикаментозные и медикаментозные методы5,13. В каждом конкретном случае врач подбирает индивидуальные способы терапии.
Одной из главных задач является обезболивание5,13. В борьбе с болью врачи руководствуются «лестницей обезболивания», разработанной Всемирной организацией здравоохранения (ВОЗ). В соответствии с ней на первой ступени или этапе лечения слабой и умеренной боли рекомендуется использовать нестероидные противовоспалительные средства (НПВС)6, такие как МОТРИН®14. Препарат разрешен к применению взрослым и подросткам старше 15 лет14.
Действующее вещество МОТРИН® – напроксен – обладает обезболивающим, противовоспалительным и жаропонижающим действием. Препарат может применяться в составе комплексного лечения мышечного болевого синдрома слабой и умеренной выраженности, связанного с травмой, воспалением и заболеваниями опорно-двигательного аппарата14.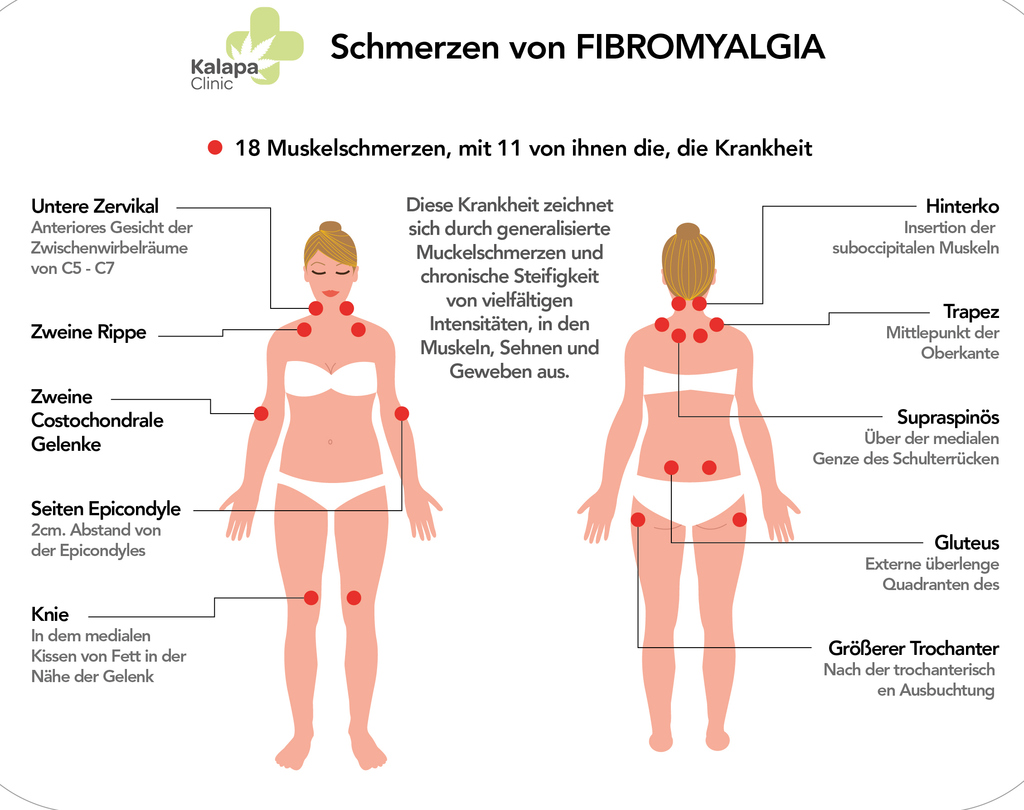 Одного приема МОТРИН® достаточно до 12 часов14. Препарат можно применять до 5 дней14.
Одного приема МОТРИН® достаточно до 12 часов14. Препарат можно применять до 5 дней14.
Нужно обязательно проконсультироваться с врачом, поскольку симптоматическое лечение и прием обезболивающих таблеток не заменяет основную терапию заболевания5. Если острые болевые ощущения не проходят, врач может использовать другие способы обезболивания13.
К немедикаментозным методам лечения миалгии относятся13:
- мануальная терапия;
- массаж;
- иглоукалывание;
- чрескожная электростимуляция;
- постизометрическая релаксация;
- лечебная физкультура.
Эти методы лечения направлены на расслабление зажатых мышц и позволяют снять спазм, вызывающий боль, прервав «порочный круг»13.
Миалгия может нарушать привычный ритм жизни, мешать работе и отдыху. Чтобы сохранить способность свободно двигаться, будьте физически активны и следите, чтобы ваши мышцы не перенапрягались. Старайтесь правильно организовать свое рабочее пространство, при сидячей работе регулярно делайте перерыв и двигайтесь или выполняйте упражнения, чтобы размять мышцы. Дозированная физическая нагрузка позволяет вашим мышцам оставаться в тонусе, укрепляет их18 и помогает предупредить боль в мышцах.
Старайтесь правильно организовать свое рабочее пространство, при сидячей работе регулярно делайте перерыв и двигайтесь или выполняйте упражнения, чтобы размять мышцы. Дозированная физическая нагрузка позволяет вашим мышцам оставаться в тонусе, укрепляет их18 и помогает предупредить боль в мышцах.
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Вернуться к началу
Литература:
- Воробьева О. В. Болезненный мышечный спазм // Медицинский совет / №5. – 2017. – С.24-27.
- The Influence of Green Apples on the Lactic Acid Level After Physical Activity Mutmainnah, Rachmat Kasmad, Maulana/ Proceedings of the 3rd International Conference on Education, Science, and Technology (ICEST 2019) Atlantis Press 2020P 146-149 https://doi.org/10.2991/assehr.k.201027.031
- Imaging of Orthopedic Sports Injuries F.
 M. Vanhoenacker · M. Maas · J. L. Gielen (Eds.) 2007 Springer-Verlag Berlin Heidelberg https://b-ok.asia/book/2199119/2c16d5
M. Vanhoenacker · M. Maas · J. L. Gielen (Eds.) 2007 Springer-Verlag Berlin Heidelberg https://b-ok.asia/book/2199119/2c16d5 - Mense, Siegfried. (2008). Muscle Pain: Mechanisms and Clinical Significance. Deutsches Ärzteblatt international. 105. 214-9. 10.3238/artzebl.2008.0214.
- Каратеев А. Е. Контроль скелетно-мышечной боли: можно ли создать общий алгоритм терапии? Клин. фармакол. тер., 2016, 25 (2), 43-53.
- Лесная О. А. Боль в практике врача: сложный феномен и непростые пути решения // Трудный пациент №3, ТОМ 17, 2019. – С. 21-26.
- Уроки дифференциального диагноза / Эрик Р. Бек [и др.]; пер. с англ. под ред. Л.В. Козловской. — М.: ГЭОТАР-Медиа, 2008. — 304 с.: ил. ISBN 978-5-9704-0898-8
- Cheung K, Hume P, Maxwell L. Delayed onset muscle soreness: treatment strategies and performance factors. Sports Med. 2003; 33(2):145-64. doi: 10.2165/00007256-200333020-00005. PMID: 12617692.
- Грипп и другие острые респираторные вирусные инфекции: принципы выбора препаратов для лечения, схемы назначения и Алгоритмы оказания медицинской помощи больным /f/ Методические рекомендации / Москва – 2019 год.

- Меньшикова С. В. Интоксикация. Грани патогенеза: старое и новое. Вариант решения. // С. В. Меньшикова, Г. Г. Кетова, М. А. Попилов, Главный врач Юга России, №2 (54), 2017 год, стр. 44-47.
- Марусиченко В. В. Скелетно-мышечные болевые синдромы: от патогенетических особенностей к рациональным терапевтическим подходам // «Международный неврологический журнал» / №4(106). – 2019. – С. 68-72.
- Joseph V. Pergolizzi Jr., Flaminia Coluzzi, Robert D. Colucci, Hanna Olsson, Jo Ann LeQuang, Jonathan Al-Saadi & Peter Magnusson (2020) Statins and muscle pain, Expert Review of Clinical Pharmacology, 13:3, 299-310, DOI: 10.1080/17512433.2020.1734451
- Латышева Н. В., Пилипович А. А., Данилов А. Б. Скелетно-мышечные боли // Регулярные выпуски «РМЖ» №0. — 10.12.2014. – С. 24.
- Инструкция по медицинскому применению препарата Мотрин® / Рег. номер PN002874/01 / https://www.motrin.ru/instrukciya
- Матвейков Г. П., Вечерский Г. А. Справочник по дифференциальной диагностике внутренних болезней // Минск: изд.
 «Беларусь»,1990 год. – 607 стр.
«Беларусь»,1990 год. – 607 стр. - Шостак НА. Миалгии: подходы к дифференциальной диагностике, лечение. Современная ревматология. 2013;(3):21–4
- Калягин А.Н. Методика исследования ревматологических больных: Учебное пособие для интернов, клинических ординаторов, врачей-курсантов. / Под ред. Ю.А. Горяева. – Иркутск: Изд-во ГОУ ВПО ИГМУ Росздрава, 2010. – 56 с.
- Centers for Disease Control and Prevention. Benefits of Physical Activity https://www.cdc.gov/physicalactivity/basics/pa-health/index.htm
Лечение мышечной боли без лекарств, мануальная терапия при миалгии, массаж мышц — показания, противопоказания — 8(495)120-02-05
Миалгия (от латинского my – мышца и algus – боль) – симптом, которому характерна боль в любых мышцах. Она возникает в напряженном или спокойном состоянии. Чаще всего локализируется в спине, особенно в поясничной области, которая испытывает максимальную физическую нагрузку. Спина состоит из больших массивов мышц. И естественно, что любая патология в мышцах, их напряжение, растяжение или воспаление будет проявляться болевым синдромом в спине.
Как возникает миалгия
Природа возникновения боли разная. Это может быть механическая травма или опухоль, когда раздражаются местные рецепторы. Или же может иметь место мышечно-фасциальная боль, которая возникает при нарушении кровообращения. Если к мышечной ткани не поступает достаточное количество кислорода, нарушается процесс утилизации глюкозы. В результате молочная кислота накапливается в мышцах, а ее избыток приводит к характерной боли. При воспалениях боль сопровождается отеками и повышенной температурой.
Воспаление мышечных волокон называется миозитом и возникает на фоне инфекционных заболеваний и серьёзных травм. Такая мышечная боль носит тупой характер, усиливается при физических нагрузках.
Виды миалгии
Миалгия чаще встречается у женщин. Стресс и переутомление, недосыпание и эмоциональное напряжение усиливают такую боль. У мужчин миалгия возникает в результате физической нагрузки, занятий спортом.
Первичная миалгия – это боль, поразившая обширные участки мышц. При надавливании на конкретный участок болевые ощущения концентрируются в месте воздействия.
При надавливании на конкретный участок болевые ощущения концентрируются в месте воздействия.
Фибромиалгия – это разновидность мышечной боли, которая возникает в волокнистых мышцах, сухожилиях и связках. Она может поражать плечи, затылок и шею. Сопровождается скованностью по утрам, способна вызывать бессонницу и головные боли.
Последствия миалгии
Мышечная боль зачастую не является опасной для жизнедеятельности. Она не приводит к потере трудоспособности, хотя и снижает ее. Но подобный симптом нельзя игнорировать, ведь в некоторых случаях боль в мышцах является симптомом полимиозита и ревматической полимиалгии. Это серьёзные заболевания, которые требуют неотлагательной медицинской помощи.
Ишиалгия: симптомы, диагностика, лечение ишиалгии
Ишиалгия (Sciatica) — боль в пояснице, распространяющаяся по заднее-наружной поверхности бедра на голень и стопу.
6 главных причин образования ишиалгии
Различные заболевания поясничного отдела позвоночника могут вызывать ишиалгию. Ишиалгия часто описывается как боль в ногах от средней до интенсивной. Она вызывается компрессией одного или нескольких из пяти пар нервных корешков в поясничном отделе позвоночника. Иногда доктора называют ишиалгию радикулопатией. Радикулопатия – это медицинский термин, используемый для описания боли, онемения, покалывания и слабости в руках или ногах, вызванной проблемами нервного корешка. Если проблема нерва имеется в шейном отделе, то это состояние называют шейной радикулопатией. Так как ишиалгия поражает поясничный отдел, то её также называют поясничной радикулопатией.
Ишиалгия часто описывается как боль в ногах от средней до интенсивной. Она вызывается компрессией одного или нескольких из пяти пар нервных корешков в поясничном отделе позвоночника. Иногда доктора называют ишиалгию радикулопатией. Радикулопатия – это медицинский термин, используемый для описания боли, онемения, покалывания и слабости в руках или ногах, вызванной проблемами нервного корешка. Если проблема нерва имеется в шейном отделе, то это состояние называют шейной радикулопатией. Так как ишиалгия поражает поясничный отдел, то её также называют поясничной радикулопатией.
Причины болей
5 пар нервных корешков в пояснично-крестцовом отделе объединяются с созданием седалищного нерва. Начинаясь с задней поверхности таза (крестца), седалищный нерв идет сзади под ягодицами и вниз через тазобедренный сустав в нижние конечности. Нервные корешки это не отдельные структуры, а часть общей нервной системы тела, способные передавать боль и ощущения в другие части тела. Радикулопатия вызывается компрессией нервного корешка, разрывом диска или разрастанием кости на промежутке до его соединения с седалищным нервом.
Радикулопатия вызывается компрессией нервного корешка, разрывом диска или разрастанием кости на промежутке до его соединения с седалищным нервом.
Компрессия седалищного нерва
Некоторые виды заболеваний позвоночника могут вызвать компрессию спинального нерва и ишиалгию или поясничную радикулопатию. Ниже перечислены 6 наиболее распространенных из них:
- грыжа диска;
- стеноз поясничного отдела позвоночника;
- спондилолистез;
- травма;
- синдром грушевидной мышцы;
- опухоли позвоночника.
Протрузия или грыжа диска
Протрузией диска называют такое состояние, когда центральная гелеобразнаая часть диска (студенистое ядро) выпирает в сторону позвоночного канала, при этом не нарушена целостность наружной стенки диска (фиброзного кольца). Грыжа диска образуется в том случае, когда студенистое ядро выходит за пределы фиброзного кольца. При протрузии либо при грыже диска, выпирающая часть диска может сдавливать прилегающий нервный корешок и вызывать ишиалгию. Последствия при грыже диска хуже. При этом выпавшее ядро диска не только вызывает прямую компрессию нервного корешка, но в тоже время вещество диска содержит кислоту, химический раздражитель (гиалуроновую кислоту), которая вызывает воспаление нерва. Компрессия нерва и раздражение вызывают воспаление и боль, часто приводя к онемению конечностей, покалыванию и слабости мышц.
При протрузии либо при грыже диска, выпирающая часть диска может сдавливать прилегающий нервный корешок и вызывать ишиалгию. Последствия при грыже диска хуже. При этом выпавшее ядро диска не только вызывает прямую компрессию нервного корешка, но в тоже время вещество диска содержит кислоту, химический раздражитель (гиалуроновую кислоту), которая вызывает воспаление нерва. Компрессия нерва и раздражение вызывают воспаление и боль, часто приводя к онемению конечностей, покалыванию и слабости мышц.
Стеноз поясничного отдела позвоночника
Стеноз позвоночного канала проявляется компрессией нерва и наиболее часто поражает людей зрелого возраста. Боль в нижних конечностях, похожая на ишиалгию, может быть результатом стеноза позвоночного канала поясничного отдела позвоночника. Боль обычно позиционная, проявляющаяся при изменении положения тела, вставании или хождении и облегчающаяся при сидении. Нервные корешки ответвляются от спинного мозга и выходят через фораминальное отверстие, ограниченное костями и связками. Нервные корешки выходят из этих отверстий и иннервируют другие части тела. Когда эти отверстия становятся узкими и вызывают компрессию нерва, в этом случае используется термин фораминальный стеноз.
Нервные корешки выходят из этих отверстий и иннервируют другие части тела. Когда эти отверстия становятся узкими и вызывают компрессию нерва, в этом случае используется термин фораминальный стеноз.
Спондилолистез
Спондилолистез наиболее часто поражает поясничный отдел позвоночника. При этом вышележащий позвонок смещается по отношению к нижележащему. Когда позвонок соскальзывает и смещается, происходит ущемление нервного корешка, что вызывает ишиалгические боли в ногах. Спондилолистез разделяют на врожденный и приобретенный (вследствие дегенеративных изменений, травмы, физической нагрузки или поднятии тяжестей.
Травма
Ишиалгия может быть результатом прямой компрессии нервного корешка, вызванной внешними силами на пояснично-крестцовый отдел позвоночника. Например, при дорожно-транспортной травме, падении и т.д. Это воздействие может повреждать нервы, когда фрагменты сломанной кости вызывают компрессию нервов.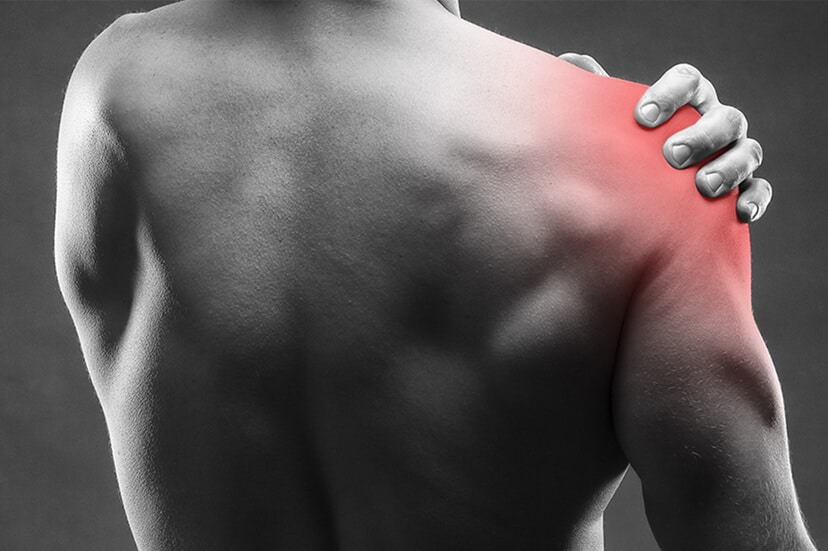
Синдром грушевидной мышцы
Этот синдром назван по имени грушевидной мышцы и боль вызывается при раздражении этой мышцей седалищного нерва. Грушевидная мышца локализуется в тазовой области, соединяет бедренную кость и участвует во вращении бедра. Седалищный нерв проходит под грушевидной мышцей. Синдром грушевидной мышцы развивается при спазме этой мышцы, таким образом сдавливая седалищный нерв. Из-за недостаточной информативности рентгеновских снимков и магнитно-резонансной томографии диагностика этой патологии затрудняется.
Опухоли позвоночника
Опухоли позвоночника характеризуются патологическим ростом тканей и делятся на доброкачественные и злокачественные. Встречаемость опухолей позвоночника довольно редкая. Однако при развитии опухоли поясничного отдела позвоночника имеется риск развития ишиалгии из-за компрессии нервного корешка.
Лечение ишиалгии
Для создания лечебного плана необходима диагностика, включающая неврологический осмотр, рентгеновский снимок и магнитно-резонансную томографию.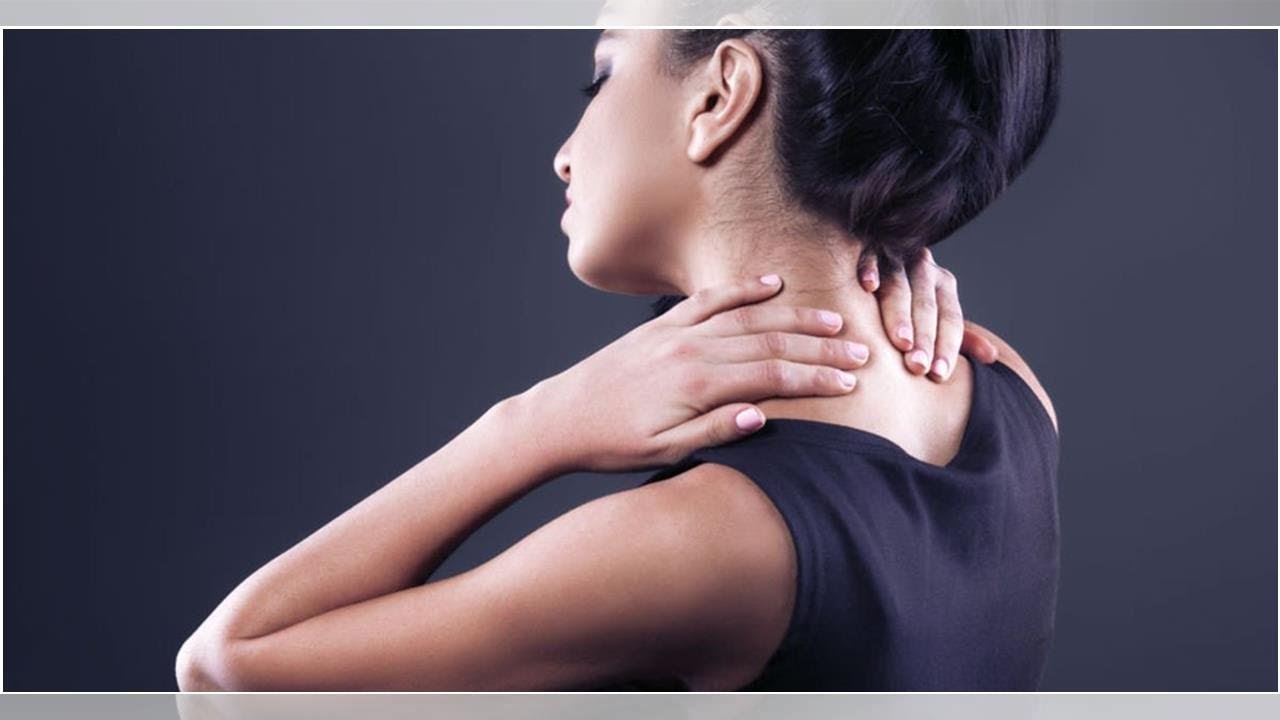 В зависимости от причины ишиалгии имеется несколько вариантов лечения. Консервативная терапия включает изменение активности, физиотерапевтические процедуры, противовоспалительную терапию и различного вида блокады для снятия воспаления нервного корешка. Хирургическое лечение включает в себя удаление грыжи диска через маленький разрез (микродискэктомия), а при стенозе — проведение декомпрессивной операции с частичным либо полным удалением дуги позвонка (ламинэктомия).
В зависимости от причины ишиалгии имеется несколько вариантов лечения. Консервативная терапия включает изменение активности, физиотерапевтические процедуры, противовоспалительную терапию и различного вида блокады для снятия воспаления нервного корешка. Хирургическое лечение включает в себя удаление грыжи диска через маленький разрез (микродискэктомия), а при стенозе — проведение декомпрессивной операции с частичным либо полным удалением дуги позвонка (ламинэктомия).
Получите квалифицированную консультацию специалиста, обратившись в ЦКБ РАН. Не стоит откладывать запись на прием к неврологу, при появлении любых тревожных симптомов. Напоминаем, что ранняя диагностика позволяет купировать проблему на зачаточном уровне. Записаться на прием в центральную клиническую больницу столицы можно по телефону или с помощью формы на сайте.
Фибромиалгия — лечение, симптомы, причины, диагностика
Фибромиалгия — хроническое заболевание, проявляющееся болью, тугоподвижностью и болезненностью мышц, сухожилий, и суставов. Фибромиалгия также характеризуется нарушением сна, чувством хронической усталости, депрессией, тревогой, нарушением функции кишечника. Фибромиалгию иногда называют фибромиалгическим синдромом или фиброзитом.
Фибромиалгия также характеризуется нарушением сна, чувством хронической усталости, депрессией, тревогой, нарушением функции кишечника. Фибромиалгию иногда называют фибромиалгическим синдромом или фиброзитом.
И хотя фибромиалгия – одно из наиболее распространенных заболеваний, поражающих мышцы, причина возникновения до сих пор неизвестна. Ткани, являющиеся источником болевых ощущений, не сопровождаются воспалением этой ткани. И поэтому, боли, доставляющие массу неудобств для пациента, не приводят к необратимым изменениям и разрушению тканей. Кроме того, не происходит повреждение внутренних органов. В этом плане фибромиалгия отличается от ревматологических заболеваний таких, как ревматоидный артрит, СКВ или полимиозит. При этих заболеваниях происходит воспаление тканей – это является основной причиной болей скованности, болезненности в суставах, сухожилиях и мышцах и, кроме того, происходит повреждение как тканей, так и внутренних органов.
Причины
Причина возникновения фибромиалгии не известна.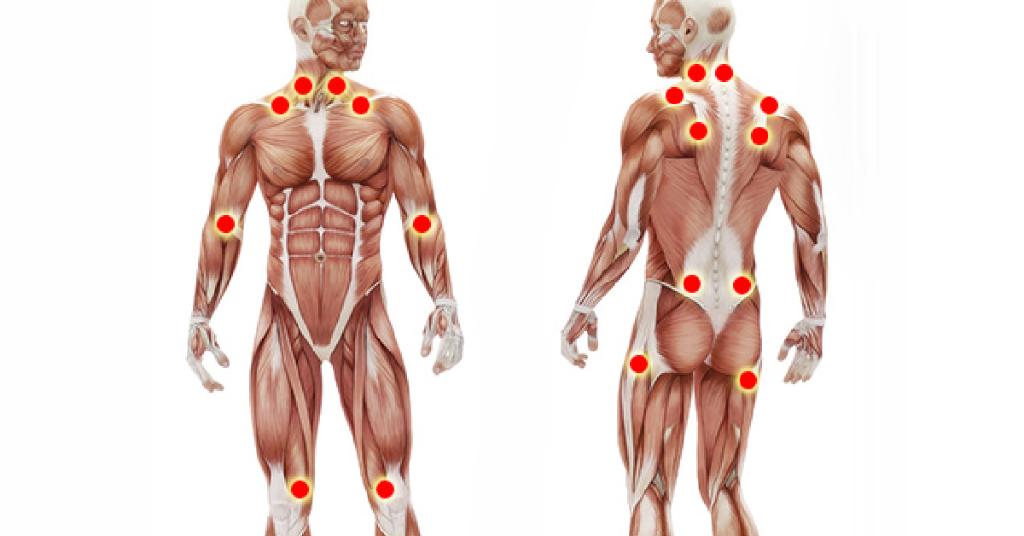 Пациенты с фибромиалгией испытывают болевые ощущения на раздражители, которые обычно не воспринимаются, как болезненные. Исследования показали, что у пациентов с фибромиалгией повышенный уровень нейротрансмиттера (который называют субстанция Р) и фактора роста нервов в спинномозговой жидкости. Кроме того, у пациентов с фибромиалгией снижен уровень серотонина в головном мозге. Исследование боли при фибромиалгии дали возможность предположить гиперчувствительность центральной нервной системы. Ученые также отметили нарушения восприятия боли у пациентов с фибромиалгией.
Пациенты с фибромиалгией испытывают болевые ощущения на раздражители, которые обычно не воспринимаются, как болезненные. Исследования показали, что у пациентов с фибромиалгией повышенный уровень нейротрансмиттера (который называют субстанция Р) и фактора роста нервов в спинномозговой жидкости. Кроме того, у пациентов с фибромиалгией снижен уровень серотонина в головном мозге. Исследование боли при фибромиалгии дали возможность предположить гиперчувствительность центральной нервной системы. Ученые также отметили нарушения восприятия боли у пациентов с фибромиалгией.
Кроме того, у пациентов с фибромиалгией отмечено уменьшение медленных движений глаз во время сна (что отчасти объясняет наличие чувства разбитости после сна или частые пробуждения). Дебют фибромиалгии нередко связан психологической фактором, травмой или инфекцией.
Кто подвержен фибромиалгии
Фибромиалгии подвержены в основном женщины (до 80% болеют женщины) в возрасте от 35 до 55 лет. Гораздо реже, фибромиалгия возникает у мужчин, детей и пожилых людей. Заболевание может проявиться самостоятельно или быть ассоциировано с другими заболеваниями такими, как СКВ или ревматоидный артрит. Распространенность этого заболевания различна в разных странах. Например, в Швеции и Великобритании 1% и в США – 4%.
Заболевание может проявиться самостоятельно или быть ассоциировано с другими заболеваниями такими, как СКВ или ревматоидный артрит. Распространенность этого заболевания различна в разных странах. Например, в Швеции и Великобритании 1% и в США – 4%.
Симптомы
Универсальный симптом фибромиалгии — это конечно боль. Как упоминалось выше, боль при фибромиалгии не вызвана воспалением ткани. Вместо этого у пациентов, судя по всему, повышенная чувствительность к различным сенсорным стимуляторам и необычно низкий порог чувствительности боли. Незначительные сенсорные стимуляции, которые обычно не причиняют другим людям сильного беспокойства, могут быть значительными и нарушать трудоспособность у пациентов с фибромиалгией.
Боль при фибромиалгии может быть в различных частях тела, причем с обеих сторон. Чаще всего боли бывают в области шеи, ягодиц, плеч, в грудной клетке, в верхней части туловища. Чувствительные зоны – это ограниченные участки, где повышенная чувствительность.
Усталость встречается у 90 % пациентов. Усталость может быть связана с патологическими нарушениями фаз сна, что часто наблюдается у этих пациентов. В норме существует несколько уровней глубины сна. Человеку необходимо дольше быть в глубокой стадии сна, чтобы восстановить силы организма. У пациентов с фибромиалгией недостаток в глубоком, укрепляющем уровне сна (так называемый стадией медленного движения глаз). Вследствие этого пациенты просыпаются утром с ощущением усталости и с тяжестью в мышцах и чувством нехватки сна (хотя количество часов сна было достаточным).
Ментальные или эмоциональные расстройства встречаются больше чем у половины пациентов с фибромиалгией. Эти расстройства включают плохую концентрацию внимания, нарушение фиксационной памяти, раздражительность, подавленное настроение. И в связи с тем, что диагноз фибромиалгии трудно верифицируется, таким пациентам нередко выставляется диагноз депрессия.
Другими симптомами фибромиалгии могут быть головные боли по типу мигрени или головных болей напряжения, различные ощущения онемения или покалывание в различных участках тела. Кроме того, возможно дискомфорт в животе (спастический кишечник ) раздраженный мочевой пузырь(частое иногда болезненное мочеиспускание). Но обследование не показывает признаки воспаления в кишечнике или мочевом пузыре. Каждый пациент с фибромиалгией, по своему уникален, и симптомы могут встречаться в различных комбинациях.
Кроме того, возможно дискомфорт в животе (спастический кишечник ) раздраженный мочевой пузырь(частое иногда болезненное мочеиспускание). Но обследование не показывает признаки воспаления в кишечнике или мочевом пузыре. Каждый пациент с фибромиалгией, по своему уникален, и симптомы могут встречаться в различных комбинациях.
Диагностика
Не существует каких-либо анализов или рентгенологических исследований, подтверждающих диагноз фибромиалгии. Анализы и обследования назначаются, чтобы исключить другие заболевания. Диагноз фибромиалгия выставляется на основании истории заболевания и данных физикального обследования. У пациентов с наличием хронических болей диагноз фибромиалгии может быть выставлен на основании обнаружения болезненных точек (до 80 % случаев) наличия воспаления тканей и при исключении других заболеваний. Многие заболевания симптомами напоминают фибромиалгию. Например, это такие заболевания как:
- Низкий уровень гормонов щитовидной железы (гипотиреоз),
- Дефицит витамина D
- Повышенная функция паращитовидных желез (вызывает повышение уровня кальция крови),
- Заболевания мышц, сопровождающиеся болью в мышцах (полимиозит),
- Костные заболевания, с болью в костях (болезнь Пэджета),
- Повышенный уровень кальция в крови (гиперкальцемия),
- Инфекционные болезни (гепатит, вирус Эпштейна – Бара, СПИД),
- Онкологические заболевания.

И, хотя анализы крови не верифицируют фибромиалгию, они необходимы для дифференциальной диагностики. Поэтому необходимо сделать анализы крови на гормоны щитовидной железы уровень кальция в крови (для исключения гиперкальциемии гиперпаратиреоза гипотиреоза). Уровень щелочной фосфатазы часто повышен у больных с болезнью Пэджета. Креатинфосфокиназа нередко повышена у пациентов с полимиозитом. Развернутый анализ крови и биохимия крови позволяет диагностировать гепатиты.
Фибромиалгия может дебютировать самостоятельно или в ассоциации с системными ревматологическими заболеваниями. При системных ревматологических заболеваниях (СКВ, ревматоидный полиартрит, полимиозит) происходит воспаление и повреждение различных тканей и органов. Для диагностики этих заболеваний имеют значение такие анализы как РОЭ уровень белков плазмы, антинуклеарный фактор, С реактивный белок, сиаловая кислота. При фибромиалгии эти анализы в пределах нормы.
Лечение
Так, как симптомы фибромиалгии весьма вариабельны у разных пациентов, программы лечения должны быть персонифицированы для каждого пациента. Программы лечения фибромиалгии дают наибольший эффект если сочетаются медикаментозные и немедикаментозные методы лечения.
Программы лечения фибромиалгии дают наибольший эффект если сочетаются медикаментозные и немедикаментозные методы лечения.
Снижение стресса
Практически невозможно измерить уровни стресса у различных пациентов. Для некоторых людей, пролитое на стол молоко является, чуть ли не трагедией. А для других, даже если танк въедет в комнату, не будет никакого беспокойства. Неплохой эффект для снижения стресса дают методики биологически-обратной связи, релаксации. Иногда достаточно, изменений в факторах окружающей среды (таких как шум, температура, изменения погоды) для усиления симптомов фибромиалгии. И воздействие на эти факторы может оказать положительное влияние. Очень полезно оптимальное количество сна.
ЛФК
Занятия низкоинтенсивными физическими нагрузками такими, как плавание, велосипед, ходьба Особенно полезны нагрузки в утренние часы. Механизм воздействия нагрузок на фибромиалгию не известен. Одним из факторов может быть улучшение сна (удлинение фазы быстрого сна).
Диета
Определенной диеты для лечения фибромиалгии не существует. Рекомендуется избегать употребления алкоголя и кофе в вечернее время для того, чтобы улучшить сон. При наличии синдрома раздраженного кишечника необходимо избегать продуктов, провоцирующих нарушения со стороны работы желудочно-кишечного тракта.
Медикаментозное лечение
Традиционно наиболее эффективными считались трициклические антидепрессанты, обычно применяемые для лечения депрессий. При лечении фибромиалгии трициклические антидепрессанты применяют в дозировках в несколько раз меньших, чем при лечении депрессии. Трициклические антидепрессанты снимают в какой-то степени усталость, снижают боль в мышцах, улучшают сон. Наука считает, что это связано с изменением уровня нейротрансмиттера под названием серотонин. Трициклическим антидепрессантом является, например амитриптилин или доксепин. Практика показала, что сочетание таких препаратов как флуоксетин (Прозак) с уменьшенной дозой амитриптилина увеличивает снижение симптоматики, улучшает сон и самочувствие. Но эти препараты, к сожалению, обладают побочными эффектами В 2007 году был синтезирован препарат под названием Лирика (прегабалин) и, это был первый препарат, разработанный специально для фибромиалгии. Лирика значительно уменьшает болевые ощущения у пациентов с фибромиалгией. Тем более, препарат имеет широкий терапевтический диапазон (позволяет подобрать дозировку в зависимости от симптомов). Аналогичным действием обладает другой препарат под названием Нейронтин (габапентин). И совсем недавно были синтезированы препараты, моментально увеличивающие уровень двух нейромедиаторов в головном мозге (серотонина и норадреналина). Это препараты – дулоксетин (Симбалта) и милнаципран (Савелла).
Но эти препараты, к сожалению, обладают побочными эффектами В 2007 году был синтезирован препарат под названием Лирика (прегабалин) и, это был первый препарат, разработанный специально для фибромиалгии. Лирика значительно уменьшает болевые ощущения у пациентов с фибромиалгией. Тем более, препарат имеет широкий терапевтический диапазон (позволяет подобрать дозировку в зависимости от симптомов). Аналогичным действием обладает другой препарат под названием Нейронтин (габапентин). И совсем недавно были синтезированы препараты, моментально увеличивающие уровень двух нейромедиаторов в головном мозге (серотонина и норадреналина). Это препараты – дулоксетин (Симбалта) и милнаципран (Савелла).
Кроме антидепрессантов нередко при фибромиалгии назначаются НПВС. Но их эффективность не так очевидна как при ревматологических состояниях.
Массаж и иглорефлексотерапия нередко оказывают определенный эффект при лечении фибромиалгии.
Миалгия, причины, симптомы и лечение
В медицине заболевание имеет классификацию с 5 типами болезни, которые отличают признаки, происхождение, течение патологии и локация симптомов.
Фибромиалгия
Самый распространённый тип болезни, возникает при усиленном переохлаждении, пребывании в сырости, перенагрузке суставов. Боль локализуется в шейном и поясничном отделах позвоночника, а также в области связочного аппарата. Бывает двух видов:
- Первичная. Развивается на фоне нарушений сна, патологического кровообращения, стрессовых ситуаций, а также ускоренного обмена веществ.
- Вторичная. Возникает на фоне заболеваний опорно-двигательного аппарата, кровеносных сосудов и внутренних органов.
Миозит
Сопровождается общим недомоганием и онемением пальцев конечностей. Локализуется в спине, шее, зоне груди и икроножных мышц. Обычно появляется как осложнение после острой инфекции или простуды, например, гриппа или тяжёлой формы ОРВИ. К другим признакам миозита относятся:
- высокая температура тела;
- удушающий кашель;
- чувство озноба;
- покраснение поражённой области;
- острые мышечные спазмы.

Полимиозит
Характерные признаки полимиозита — головные боли, шум в ушах, тошнота, ощущение натяжения суставов шеи и плечевого пояса. Часто диагностируют у пациентов с аутоимунными инфекциями или онкологией. Развивается из-за попадания вирусов в организм. Может возникнуть как аллергическая реакция на медикаменты.
Межрёберная миалгия
Сложная форма болезни, которая может развиваться без весомых причин. Выражается в сильном болевом синдроме в области груди и рёбер, который усиливается при кашле, быстрой ходьбе, глотании и других естественных действиях. Появляется вследствие сдавливания межрёберного нерва соседними напряжёнными мышцами.
Эпидемическая миалгия
Больше известна как болезнь Борнхольма. Симптомы могут длиться более недели даже при успешном лечении. Эпидемическую форму провоцируют вирусы, а также чрезмерные нагрузки и нервные потрясения. Среди симптомов значатся болезненность шеи, плеч, рук, груди и поясницы, а также озноб, высокая температура и повышенное потоотделение.
Ревматическая полимиалгия: симптомы, диагностика, лечение
Рассказывает Евгений Жиляев,
профессор, д.м.н., врач высшей категории.
Ревматическая полимиалгия (РПМ) – это воспалительное заболевание, которое проявляется болью и скованностью в группах мышц в области шеи, плеч и бедер.
Причины, приводящие к развитию заболевания, пока не установлены. Однако характерно частое сочетание ревматической полимиалгии с другим ревматологическим заболеванием из группы васкулитов – гигантоклеточным артериитом. Рядом авторов эти два заболевания рассматриваются вместе как две формы одного процесса.
Симптомы ревматической полимиалгии
Принято считать, что это заболевание развивается у людей старше 50 лет, преимущественно у женщин. Наиболее распространенными симптомами являются стойкая боль в проксимальных (расположенных ближе к туловищу) мышцах плеч, бедер и шеи. Боль особенно сильно проявляется по утрам после длительного отсутствия активности во время ночного сна. Могут припухать и болеть непосредственно суставы. Возникают проблемы при самообслуживании, движении (тяжело одеваться, расчесывать волосы, вставать из положения сидя, делать элементарные домашние дела), что причиняет значительный дискомфорт пациенту. Может подниматься температура тела, появляться общая слабость, пропадать аппетит и, как следствие, снижаться масса тела. Нередко при данном заболевании могут развиваться депрессия и анорексия.
Могут припухать и болеть непосредственно суставы. Возникают проблемы при самообслуживании, движении (тяжело одеваться, расчесывать волосы, вставать из положения сидя, делать элементарные домашние дела), что причиняет значительный дискомфорт пациенту. Может подниматься температура тела, появляться общая слабость, пропадать аппетит и, как следствие, снижаться масса тела. Нередко при данном заболевании могут развиваться депрессия и анорексия.
Диагностика ревматической полимиалгии
Не существует какого-либо одного высокочувствительного теста, позволяющего точно диагностировать ревматическую полимиалгию. Диагноз устанавливается на основании жалоб пациента, значительного повышения скорости оседания эритроцитов и содержания с-реактивного белка в крови. Так как эти симптомы не специфичны и могут наблюдаться при многих других заболеваниях, врач может рекомендовать дополнительное обследование.
Лечение ревматической полимиалгии
Заболевание характеризуется быстрым ответом на применение глюкокортикоидов (ГК) в относительно небольших дозах (12,5-20 мг преднизолона). По мере купирования симптомов доза ГК постепенно снижается. Продолжительность лечения в среднем занимает от одного года до двух лет. В некоторых случаях заболевание рецидивирует, что требует повторного назначения или увеличения дозы люкокортикоидов. Поэтому большое значение имеет приверженность лечению и строгое соблюдение рекомендаций лечащего врача.
По мере купирования симптомов доза ГК постепенно снижается. Продолжительность лечения в среднем занимает от одного года до двух лет. В некоторых случаях заболевание рецидивирует, что требует повторного назначения или увеличения дозы люкокортикоидов. Поэтому большое значение имеет приверженность лечению и строгое соблюдение рекомендаций лечащего врача.
В настоящий момент известны случаи назначения ряда других лекарственных средств, таких как метотрексат, азатиоприн, тоцилизумаб, однако, их преимущества над стандартным применением ГК в моно- или комбинированной терапии не доказаны.
Преимущества Европейского медицинского центра (ЕМС)
- Амбулаторное наблюдение ревматологом терапевтической клиники, купирование симптомов и подбор оптимальной терапии. В команде ревматологов ЕМС профессор, д.м.н. Евгений Валерьевич Жиляев.
- Ревматологи ЕМС имеют собственные научные наработки и значительный практический опыт в области лечения ревматической полимиалгии.

- Широкие диагностические возможности: полный спектр инструментальных и лабораторных методов обследования. Консультации врачей любых специальностей при необходимости.
- Для выработки наилучшей тактики лечения в сложных случаях организуется консилиум из экспертов смежных направлений.
- Возможность госпитализации для проведения обследования и лечения в комфортабельном стационаре ЕМС с возможностью круглосуточного посещения родными и близкими.
- Неотложная и экстренная помощь в клинике, вызов врача на дом в любую точку Москвы и Подмосковья (до 50 км от МКАД).
Автор: Евгений Жиляев, профессор, д.м.н., врач высшей категории.
Миалгия и усталость — трансляционные исследования боли
11.1. ВВЕДЕНИЕ
Мышечная усталость и боль — одни из самых распространенных жалоб в отделениях неотложной помощи и клиниках по всей стране. Усталость и боль часто бывают острыми, проходят спонтанно или, кажется, уменьшаются с помощью различных лекарств и методов лечения. Несмотря на эти ремиссии, популярные журналы (например, Time) подсчитали, что каждый год американцы тратят более 30 миллиардов долларов на лечебные травы и 50 миллиардов долларов на альтернативные методы лечения симптомов, включая мышечную боль и усталость.Эти статистические данные показывают, что даже острая мышечная боль и усталость являются серьезными проблемами для здоровья, которые не решаются адекватно современной медицинской практикой.
Несмотря на эти ремиссии, популярные журналы (например, Time) подсчитали, что каждый год американцы тратят более 30 миллиардов долларов на лечебные травы и 50 миллиардов долларов на альтернативные методы лечения симптомов, включая мышечную боль и усталость.Эти статистические данные показывают, что даже острая мышечная боль и усталость являются серьезными проблемами для здоровья, которые не решаются адекватно современной медицинской практикой.
Иногда мышечная боль и утомляемость принимают хронический характер, приводя к синдромам, включая синдром хронической усталости (CFS) и синдром фибромиалгии (FMS) — разрушительные состояния, характеризующиеся постоянной изнурительной усталостью, которая усугубляется даже легкими упражнениями в в случае CFS и хронической широко распространенной боли (CWP) с особым акцентом на мышцы, что может предотвратить большую часть или все действия в случае FMS.Оба эти состояния часто связаны друг с другом и с множеством других заболеваний, таких как височно-нижнечелюстное расстройство (ВНЧС), синдром раздраженного кишечника (СРК) и множественная химическая чувствительность. Эти синдромы разрушают жизни, плохо реагируют на текущие стратегии лечения и могут привести к истощению финансовых ресурсов больных. В совокупности эти расстройства ежегодно затрагивают от 7 до 20 миллионов человек в Соединенных Штатах, как сообщают различные авторитетные источники (Reeves et al.2007). Ясно, что пациенты с этими синдромами заслуживают согласованных исследовательских усилий для понимания, лечения и, в конечном итоге, излечения этих заболеваний.
Эти синдромы разрушают жизни, плохо реагируют на текущие стратегии лечения и могут привести к истощению финансовых ресурсов больных. В совокупности эти расстройства ежегодно затрагивают от 7 до 20 миллионов человек в Соединенных Штатах, как сообщают различные авторитетные источники (Reeves et al.2007). Ясно, что пациенты с этими синдромами заслуживают согласованных исследовательских усилий для понимания, лечения и, в конечном итоге, излечения этих заболеваний.
В отличие от кожной боли, которая была тщательно изучена и сравнительно хорошо изучена, молекулярные механизмы мышечной боли все еще неизвестны. Еще более загадочным является симптом изнуряющей усталости. Моссо в своей обширной книге по этому вопросу столетие назад заметил, что во всех культурах, кажется, есть только одно слово для обозначения усталости (Mosso 1904).Тем не менее, усталость описывает многие состояния, включая неспособность мышечных волокон нормально сокращаться, недостаточные двигательные командные сигналы, чувство усталости, тяжести, давления и слабости в мышцах, а также чувство умственной усталости, которое препятствует концентрации внимания и выполнению концептуальных задач.
Предметом большинства физиологических исследований усталости было произвольных мышечных сокращений. Снижение функции, вызывающее отказ произвольного сокращения мышц, может происходить на всех уровнях нервно-мышечной системы, включая моторную кору, передачу сигналов мотонейронам, сигналы мотонейронов в мышцу, связь возбуждения-сокращения в мышце и взаимодействия актин-миозиновых нитей.Однако наиболее частой неудачей является снижение моторного командного сигнала от моторной коры (см. Недавние отчеты и обзоры Беллинджер и др., 2008; Гибсон и др., 2003; Ноукс и др., 2005; Сент-Клер и Ноукс, 2004). Недавний обзор предполагает, что сбои в произвольном сокращении мышц чаще всего вызваны центральным компаратором, который объединяет гомеостатические данные от многих физиологических систем и отключает моторные команды, когда энергетические ресурсы находятся под угрозой (Noakes 2007). Предполагается, что один из гомеостатических входов «происходит из разницы между подсознательными представлениями об исходном физиологическом гомеостатическом состоянии и состоянием физиологической активности, вызванной физической активностью, которая создает представление второго порядка, которое воспринимается структурами, производящими сознание, как ощущение усталости». (Гибсон и др.2003, стр.174). Мы предполагаем, что существует более простое ощущение усталости, которое вызывается входными сигналами от определенных рецепторов, чувствительных к метаболитам, образующимся при сокращении мышц. Мы также предполагаем, что это элементарное ощущение передается, проводится и воспринимается в рамках уникальной сенсорной системы со свойствами, аналогичными другим сенсорным модальностям, таким как боль. Мы называем это «ощущением мышечной усталости».
(Гибсон и др.2003, стр.174). Мы предполагаем, что существует более простое ощущение усталости, которое вызывается входными сигналами от определенных рецепторов, чувствительных к метаболитам, образующимся при сокращении мышц. Мы также предполагаем, что это элементарное ощущение передается, проводится и воспринимается в рамках уникальной сенсорной системы со свойствами, аналогичными другим сенсорным модальностям, таким как боль. Мы называем это «ощущением мышечной усталости».
11.1.1. Усталость и боль как отдельные сенсорные системы
Что определяет конкретную сенсорную систему? В то время как Мюллеру (1840) и Беллу приписывают «доктрину специфических нервных энергий», концепция особой сенсорной системы с тех пор была изменена, чтобы требовать, как минимум, следующих трех основных элементов:
- 1.
Качественно уникальное восприятие, постоянно связанное с определенной формой энергии
- 2.
Специфические рецепторы энергии или стимула
- 3.

Конкретные системы передачи и области мозга, специализирующиеся на передаче и интеграции информация от рецепторов
11.1.2. Удовлетворяет ли боль этим требованиям?
Pain удовлетворяет этим трем и многим другим требованиям (Perl 1971, 1998, 2007).(1) Боль — это уникальное качественное переживание, которое обычно не путают с другими сенсорными переживаниями. Хотя не существует конкретной формы энергии, связанной с болью, все периферические стимулы, которые вызывают боль, повреждают ткани или угрожают повреждением тканей, если стимул сохраняется, составляют постоянную эффективных форм энергии. Следовательно, форма энергии — это «разрушительная форма энергии». (2) Специфическими рецепторами энергии являются «ноцицепторы», которые настроены на энергию, которая может повредить ткани.(3) Специфическая система передачи боли включает поверхностный дорсальный рог спинного мозга, спиноталамический тракт и части таламуса, островковую кору и поясную извилину головного мозга (Brooks et al. 2005; Craig 2003). Понимание концепции боли как особой сенсорной системы позволило открыть молекулярные рецепторы, которые позволяют сенсорным окончаниям быть чувствительными к стимулам, вызывающим повреждение и боль. Эта концепция также привела к открытию регулирующих веществ, таких как опиоиды, которые могут избирательно уменьшать боль, воздействуя на определенные области головного и спинного мозга.
2005; Craig 2003). Понимание концепции боли как особой сенсорной системы позволило открыть молекулярные рецепторы, которые позволяют сенсорным окончаниям быть чувствительными к стимулам, вызывающим повреждение и боль. Эта концепция также привела к открытию регулирующих веществ, таких как опиоиды, которые могут избирательно уменьшать боль, воздействуя на определенные области головного и спинного мозга.
11.1.3. Удовлетворяет ли ощущение мышечной усталости принципам определенной сенсорной системы?
(1) Хотя ранние эксперименты задокументировали ощущение «мышечной усталости или давления», возникающее при безболезненном скоплении метаболитов, вызванных сокращением мышц, уникальность этого ощущения до конца не выяснена. (2) Специфические рецепторы ощущения мышечной усталости не идентифицированы. (3) Хотя специфические проводящие пути спинного мозга для ощущения мышечной усталости имеют определенное основание (Wilson et al.2002), необходимы дополнительные исследования. Аналогичным образом, некоторые области мозга были идентифицированы как связанные с ощущением усталости (Caseras et al. 2008; Cook et al. 2004, 2007; Williamson et al. 1997), наиболее распространенными из которых являются префронтальная кора, кора островка и передняя часть мозга. и / или задняя поясная извилина. Однако и здесь требуется гораздо больше работы. Таким образом, для ощущения мышечной усталости удовлетворение трех требований для работы в качестве конкретной сенсорной системы является неполным.
2008; Cook et al. 2004, 2007; Williamson et al. 1997), наиболее распространенными из которых являются префронтальная кора, кора островка и передняя часть мозга. и / или задняя поясная извилина. Однако и здесь требуется гораздо больше работы. Таким образом, для ощущения мышечной усталости удовлетворение трех требований для работы в качестве конкретной сенсорной системы является неполным.
Сенсорная усталость имеет много общего с болью и одышкой (воздушным голодом).Все это защитные сенсорные явления. Боль вызывает поведение, которое защищает от повреждения тканей, вызванного механическими, химическими или термическими повреждениями. Одышка защищает от увеличения CO 2 и уменьшения O 2 , что может привести к гибели клеток от аноксии. Усталость — это первая линия защиты, которая защищает от чрезмерного использования запасов энергии, которое может привести к окоченению и смерти. Все три этих сенсорных феномена активируют защитные рефлексы. Ноцицептивный ввод активирует рефлексы отмены, а боль мотивирует сознательные действия, которые удаляют поврежденную часть тела от стимула, и активирует симпатические рефлексы, которые усиливают бегство. Одышка усиливает дыхательные процессы и активирует симпатические рефлексы для сохранения жизненно важных функций. Сенсорная усталость снижает двигательные команды и активирует симпатические рефлексы для увеличения запасов энергии за счет увеличения кровотока в работающих мышцах и уменьшения кровотока в неработающих мышцах. Каждое из этих ощущений вызывает уникальное когнитивное восприятие с мощными отвращающими коннотациями, позволяя людям распознать, какая система затронута, и задействовать поведение для изменения условий, вызывающих сенсорный опыт.Так почему же большинство ученых считает, что одышка и боль обладают характеристиками уникальных сенсорных систем, в то время как усталость сенсорных мышц редко считается таковой?
Одышка усиливает дыхательные процессы и активирует симпатические рефлексы для сохранения жизненно важных функций. Сенсорная усталость снижает двигательные команды и активирует симпатические рефлексы для увеличения запасов энергии за счет увеличения кровотока в работающих мышцах и уменьшения кровотока в неработающих мышцах. Каждое из этих ощущений вызывает уникальное когнитивное восприятие с мощными отвращающими коннотациями, позволяя людям распознать, какая система затронута, и задействовать поведение для изменения условий, вызывающих сенсорный опыт.Так почему же большинство ученых считает, что одышка и боль обладают характеристиками уникальных сенсорных систем, в то время как усталость сенсорных мышц редко считается таковой?
Отчасти проблема была семантической. Моссо (1904) продвигал и популяризировал путаницу между сенсорным феноменом утомления и определением утомления как потери способности сокращать мышцы. Сенсорное переживание усталости и потеря мышечного сокращения были настолько тесно взаимосвязаны в его трудах, что их нельзя было разделить, даже несмотря на то, что он ясно распознал и отмечал особый сенсорный компонент утомления. Этот исторический акцент на отказе мышечного сокращения как определении утомления сохраняется в большинстве влиятельных публикаций и по сей день (Davis and Bailey 1997), хотя некоторые начали рассматривать утомляемость отдельно от двигательной недостаточности, хотя и скорее как эмоциональную реакцию, чем сенсорная система (Гибсон и др., 2003). Семантика боли прошла аналогичную эволюцию с постоянным смешением сенсорных явлений с соответствующими последствиями в познании, памяти, эмоциях, вегетативной активации и моторном поведении.
Этот исторический акцент на отказе мышечного сокращения как определении утомления сохраняется в большинстве влиятельных публикаций и по сей день (Davis and Bailey 1997), хотя некоторые начали рассматривать утомляемость отдельно от двигательной недостаточности, хотя и скорее как эмоциональную реакцию, чем сенсорная система (Гибсон и др., 2003). Семантика боли прошла аналогичную эволюцию с постоянным смешением сенсорных явлений с соответствующими последствиями в познании, памяти, эмоциях, вегетативной активации и моторном поведении.
Другая проблема боли и утомления сенсорных мышц состоит в том, что у специальных рецепторов, кодирующих сенсорные сигналы, отсутствует особый макроскопический внешний аппарат, такой как глаз, ухо, нос или язык, который мы могли бы легко наблюдать. Что касается боли, особая природа ноцицепторов была тщательно продемонстрирована посредством тщательных физиологических экспериментов с записью, анатомических демонстраций и уникальных психофизических экспериментов (обобщено Perl 2007). Молекулярные характеристики, определяющие свойства ноцицепторов, были обнаружены с помощью удобных специальных агентов, таких как капсаицин, которые можно было использовать для их избирательной активации.Спинной мозг, ствол головного мозга, церебральные пути и центры интеграции боли были нанесены на карту с использованием процедур, однозначно активирующих кожные ноцицепторы.
Молекулярные характеристики, определяющие свойства ноцицепторов, были обнаружены с помощью удобных специальных агентов, таких как капсаицин, которые можно было использовать для их избирательной активации.Спинной мозг, ствол головного мозга, церебральные пути и центры интеграции боли были нанесены на карту с использованием процедур, однозначно активирующих кожные ноцицепторы.
Третья проблема заключается в том, что природа мышц очень затрудняет выявление сенсорных рецепторов, которые однозначно связаны с мышечной болью или сенсорной усталостью мышц. Открытие мышечных рецепторов для прямой активации путем рассечения вышележащих структур почти неизбежно нарушает кровообращение и активирует ноцицепторы, затрудняя любые попытки избирательно активировать рецепторы боли или сенсорной мышечной усталости.Несмотря на эти проблемы, было предпринято множество попыток определить природу органов чувств, участвующих в мышечной боли, и сенсорных сигналов, участвующих в регуляции симпатических рефлексов, которые, как известно, активируются изменениями метаболитов в мышцах, которые связаны с мышцами. сокращение. Большинство самых ранних экспериментов были непрямыми, с использованием симпатических рефлексов в качестве считывания сигналов от сенсорных рецепторов в мышцах.
сокращение. Большинство самых ранних экспериментов были непрямыми, с использованием симпатических рефлексов в качестве считывания сигналов от сенсорных рецепторов в мышцах.
11.2. ИМЕЮТ ЛИ СКЕЛЕТНЫЕ МЫШЦЫ ДВА УНИКАЛЬНЫХ ТИПА СЕНСОРНЫХ РЕЦЕПТОРОВ, ОБНАРУЖИВАЮЩИХ МЕТАБОЛИТЫ: ОДИН ТИП НОЦИЦЕПТИВНЫЙ (СПОСОБНЫЙ СИГНАЛИЗИРОВАТЬ БОЛЬ), ДРУГОЙ ЭРГОРЕЦЕПТИВНЫЙ (СПОСОБНЫЙ ОПРЕДЕЛЯТЬ МЫШЕЧНУЮ РАБОТУ)?
Более 70 лет назад Алам и Смирк (1937) четко указали, что как предболезненная «усталость», так и мышечная боль могут быть вызваны метаболитами, производимыми мышечным сокращением, причем первые активируются более низкими концентрациями метаболитов, чем метаболиты. последний.Метаболиты, продуцируемые сокращением мышц, вызывают повышение артериального давления и ощущение мышечной усталости и мышечной боли.
Первоначальное повышение артериального давления (см.) Сопровождалось не болью, а предболезненным феноменом, описанным как (1) «усталость или тяжесть, но не вызывающие заметного дискомфорта». Поскольку количество метаболитов продолжало увеличиваться, субъекты испытали (2) «период, когда ощущение в предплечье приобретает определенно ноющий характер и описывается как боль, которая, однако, легко переносится», а затем (3) «период сильной боли. »Следует.Они продемонстрировали, что ощущения и повышение артериального давления опосредованы афферентными нервными волокнами, иннервирующими тренирующуюся мышцу. Таким образом, концепция по крайней мере двух популяций сенсорных афферентов, передающих безболезненную и болезненную информацию, существует уже более 70 лет. Последующие эксперименты подтвердили и уточнили эти наблюдения, ясно продемонстрировав, что производимые сокращением метаболиты, обнаруживаемые сенсорными афферентами в мышцах, активируют симпатический прессорный рефлекс при нагрузке (обзор Kaufman and Hayes 2002 и McCord и Kaufman в главе 12 этого тома).Предполагается, что основным нервным путем для этого рефлекса являются афферентные нейроны скелетных мышц, которые проецируются в симпатические центры спинного мозга.
Поскольку количество метаболитов продолжало увеличиваться, субъекты испытали (2) «период, когда ощущение в предплечье приобретает определенно ноющий характер и описывается как боль, которая, однако, легко переносится», а затем (3) «период сильной боли. »Следует.Они продемонстрировали, что ощущения и повышение артериального давления опосредованы афферентными нервными волокнами, иннервирующими тренирующуюся мышцу. Таким образом, концепция по крайней мере двух популяций сенсорных афферентов, передающих безболезненную и болезненную информацию, существует уже более 70 лет. Последующие эксперименты подтвердили и уточнили эти наблюдения, ясно продемонстрировав, что производимые сокращением метаболиты, обнаруживаемые сенсорными афферентами в мышцах, активируют симпатический прессорный рефлекс при нагрузке (обзор Kaufman and Hayes 2002 и McCord и Kaufman в главе 12 этого тома).Предполагается, что основным нервным путем для этого рефлекса являются афферентные нейроны скелетных мышц, которые проецируются в симпатические центры спинного мозга. Эти центры проецируются на ствол головного мозга и гипоталамус, а эфферентные пути проецируются на симпатические ядра спинного мозга, которые направляются к кровеносным сосудам в скелетных мышцах.
Эти центры проецируются на ствол головного мозга и гипоталамус, а эфферентные пути проецируются на симпатические ядра спинного мозга, которые направляются к кровеносным сосудам в скелетных мышцах.
РИСУНОК 11.1
Вверху: упражнения без остановки кровообращения. Внизу: упражнение с остановкой кровообращения. Физические упражнения увеличивают количество метаболитов в работающих мышцах, но также активируют симпатические рефлексы, которые усиливают кровоток и снижают метаболиты.Если циркуляция (подробнее …)
Интересным достижением в этой области стало открытие, что сенсорные афференты, иннервирующие кровеносные сосуды, часто содержат пептид, связанный с геном кальцитонина (CGRP) (Kruger et al. 1989; Silverman and Kruger 1989) . Еще более интересной является гипотеза о том, что CGRP может высвобождаться сенсорными окончаниями по механизму «нейроэффектора», что означает, что сенсорные окончания сами по себе могут непосредственно оказывать воздействие на периферические ткани. Учитывая, что CGRP является мощным вазодилататором, активация мышечных сенсорных афферентов может высвобождать CGRP, который напрямую вызывает вазодилатационную часть прессорного рефлекса при физической нагрузке, который возникает в работающей мышце (Micevych and Kruger 1992).Второе открытие также указывает на очень прямое влияние сенсорных афферентов на симпатический выход (Папка и Макнил, 1993). Эти механизмы могут значительно усиливать или независимо контролировать прессорную реакцию при физической нагрузке, если сенсорные нейроны, содержащие CGRP, реагируют на метаболиты.
Учитывая, что CGRP является мощным вазодилататором, активация мышечных сенсорных афферентов может высвобождать CGRP, который напрямую вызывает вазодилатационную часть прессорного рефлекса при физической нагрузке, который возникает в работающей мышце (Micevych and Kruger 1992).Второе открытие также указывает на очень прямое влияние сенсорных афферентов на симпатический выход (Папка и Макнил, 1993). Эти механизмы могут значительно усиливать или независимо контролировать прессорную реакцию при физической нагрузке, если сенсорные нейроны, содержащие CGRP, реагируют на метаболиты.
Mense и его коллеги продемонстрировали по крайней мере две различные популяции мышечных рецепторов в экспериментах, основанных на механической стимуляции (см.) (Kniffki et al. 1978, 1981; Mense and Meyer 1985). Большинство сенсорных афферентов, не относящихся к веретену, относились к группе III (соответствующие афферентным волокнам Aδ в кожных нервах) или группе IV (немиелинизированные волокна, соответствующие афферентным волокнам C в кожных нервах). Некоторые из каждой группы волокон можно классифицировать как «ноцицепторы» (отвечающие на раздражители, повреждающие ткани) или не-ноцицепторы, способные обнаруживать движения мышц, и, следовательно, возможные «эргорецепторы» (рецепторы, способные обнаруживать работу мышц). Недавние оценки лаборатории Mense предполагают, что по крайней мере 40% афферентов механорецептивной группы IV могут быть не ноцицептивными (Mense 2009) (см.).
Некоторые из каждой группы волокон можно классифицировать как «ноцицепторы» (отвечающие на раздражители, повреждающие ткани) или не-ноцицепторы, способные обнаруживать движения мышц, и, следовательно, возможные «эргорецепторы» (рецепторы, способные обнаруживать работу мышц). Недавние оценки лаборатории Mense предполагают, что по крайней мере 40% афферентов механорецептивной группы IV могут быть не ноцицептивными (Mense 2009) (см.).
РИСУНОК 11.2
Экспериментальная установка и результаты для афферентных записей IV группы мышц.Настроить. B: Определение механического порога для блока IV группы. C: Пороговые значения давления 26 единиц LTM (серый) и 26 единиц HTM (черный). D: Распределение пороговых значений давления для LTM (подробнее …)
Идентификация ответов на метаболиты, продуцируемые мышцами, была более проблематичной, чем определение ответов на механическую стимуляцию. Adreani et al. (Adreani et al. 1997; Adreani and Kaufman 1998) сообщили, что около половины небольшой выборки мышечных афферентов групп III и IV реагировали на метаболиты, продуцируемые мышечным сокращением, которые, вероятно, были не ноцицептивными, в то время как другая половина отвечала на метаболиты. это, вероятно, вызовет болезненную реакцию.Попытки идентифицировать метаболиты, ответственные за активацию больших популяций мышечных сенсорных афферентов, были неоднозначными. Хотя было обнаружено, что многие вещества активируют афферентные мышцы, когда эти вещества наносятся индивидуально на сенсорные окончания в концентрациях, вызываемых безболезненным или даже болезненным сокращением мышц, активируются очень немногие из афферентных окончаний.
это, вероятно, вызовет болезненную реакцию.Попытки идентифицировать метаболиты, ответственные за активацию больших популяций мышечных сенсорных афферентов, были неоднозначными. Хотя было обнаружено, что многие вещества активируют афферентные мышцы, когда эти вещества наносятся индивидуально на сенсорные окончания в концентрациях, вызываемых безболезненным или даже болезненным сокращением мышц, активируются очень немногие из афферентных окончаний.
Моссо определил, что вещества, вырабатываемые при столбнячном сокращении мышц, могут вызывать усталость.Он цитирует свою работу 1890 года, показывающую, что кровь утомленного животного может вызывать у неутомимого животного поведение, подобное утомлению (Mosso 1904). На основании имеющихся данных Моссо пришел к выводу, что усталость была вызвана не недостатком кислорода или повышенным содержанием CO 2 в крови, а могла быть вызвана накоплением молочной кислоты, понижением pH и повышением температуры. Хотя некоторые выводы Моссо оказались неверными, в основном из-за отсутствия знаний в области базовой нейрофизиологии (потенциалы действия, мембранные потенциалы и т. Д.), были неизвестны в то время), его предположения о веществах, которые могут вызывать утомление сенсорных мышц, были явно дальновидными.
11.3. МОЛЕКУЛЯРНЫЕ РЕЦЕПТОРЫ, АКТИВИРУЕМЫЕ МЕТАБОЛИТАМИ, ПРОИЗВОДИМЫМИ ПРИ СОКРАЩЕНИИ МЫШЦ
За последние 10 лет были достигнуты большие успехи в идентификации метаболитов, продуцируемых сокращением мышц. Наиболее вероятные ионные каналы для обнаружения изменений pH, кислотно-чувствительные ионные каналы (ASIC), также называемые амилорид-чувствительными ионными каналами или амилорид-чувствительными ионными токами, были клонированы и секвенированы в 1997 году (Waldmann et al.1997а, б). Однако первоначально казалось, что эти каналы не могут играть роль в обнаружении нормальных значений pH, обнаруживаемых у людей. Они не могли пропускать ток, достаточный для активации сенсорных окончаний, с небольшими изменениями pH, наблюдаемыми в условиях, которые, как известно, вызывают мышечную боль у людей, например, изменение pH с 7,4 до 7,0, которое может вызвать стенокардию в сердце. Иммке и МакКлески (2001a) показали, что лактат играет роль в усилении реакции ASIC на значения pH от 7,4 до 7,0.Таким образом, молочная кислота в концентрациях, образующихся во время ишемии и экстремально активных мышечных сокращений, была более эффективной в активации мышечных сенсорных афферентов, чем одно только снижение pH, вызванное неишемическими явлениями (например, метаболическим ацидозом).
Позже был обнаружен еще один критический кофактор. АТФ в низких концентрациях, обнаруживаемых в мышечном интерстиции во время нормальных мышечных сокращений, значительно увеличивает чувствительность ASIC к pH и лактату (Naves and McCleskey 2005; Yagi et al. 2006).В целом, эти комбинации позволяют рецептору ASIC3 управлять устойчивым током в диапазоне pH 7,6–6,6, который способен активировать сенсорные окончания.
Другие исследователи в лаборатории МакКлески показали, что рецепторов ASIC было больше в сенсорных нервных волокнах, которые иннервируют скелетные и сердечные мышцы, чем в коже. Сенсорные нервные волокна, содержащие ASIC, были обнаружены снаружи небольших артериол и венул в фасции, окружающей мышцы и разделяющей пучки пучков (Connor et al.2005; Молливер и др. 2005). Это место оптимально для определения уровней метаболитов, продуцируемых мышцами, когда они удаляются сосудистой системой. Интересно, что фасция, по-видимому, является структурой, наиболее сильно иннервируемой ноцицепторами и наиболее вероятно участвующей в возникновении мышечной боли в мышцах человека (Gibson et al. 2009; Takahashi et al. 2005).
11.4. НЕОБХОДИМОСТЬ ТРАНСЛЯЦИОННЫХ МОСТОВ К ФИБРОМИАЛГИИ И СИНДРОМУ ХРОНИЧЕСКОЙ УСТАЛОСТИ
Наша группа признала, что данные МакКлески могут помочь ответить на ряд давних вопросов о том, как сенсорные афференты мышц определяют работу мышц, а также сигнализируют о мышечной боли, вызванной метаболитами.Во-первых, результаты, показывающие, что комбинации метаболитов более эффективны в активации нейронов DRG, чем отдельные метаболиты (Immke and McCleskey 2001b, 2003; Naves and McCleskey, 2005; Yagi et al. 2006), предложили нам способ понять активацию мышечных метаборецепторов. сенсорные нейроны. Представляя мышечные сенсорные нейроны с различными комбинациями (парами, тройками и т. Д.) Метаболитов, которые образуются при сокращении мышц, можно определить метаболиты, необходимые и достаточные для активации сенсорных нейронов таким же образом, как они активируются при сокращении мышц.Во-вторых, после определения эффективной комбинации метаболитов фактические молекулярные рецепторы, используемые мышечными сенсорными нейронами для обнаружения этой комбинации, могут быть подтверждены с помощью селективных антагонистов вероятных молекулярных рецепторов (в основном предложенных Иммке и МакКлески 2001b, 2003; Naves and McCleskey , 2005; Яги и др. 2006). Кроме того, идентичность молекулярных рецепторов может быть проверена с помощью ПЦР и количественной ПЦР в реальном времени для определения наличия достаточных количеств мРНК для этих специфических рецепторов в мышечных сенсорных нейронах.Используя это, можно определить существенное молекулярное различие между мышечными сенсорными нейронами, сигнализирующими о сенсорной усталости, и теми, которые сигнализируют о мышечной боли.
Это знание стало очевидным в то же самое время, когда мы (А.Л. и К.Л.) стали сотрудничать с Центром исследования боли в Университете штата Юта, возглавляемым доктором К. Ричардом Чепменом (см. Главу 1). Основным направлением исследований этого центра было патофизиология и лечение синдрома фибромиалгии (FMS), хронической широко распространенной боли (CWP) и синдрома хронической усталости (CFS) — трех синдромов, которые имеют общие симптомы хронической боли и усталости.Мы признали, что лучшее понимание сенсорной мышечной усталости и мышечной боли, а также симпатических рефлексов, активируемых мышечными афферентами, может улучшить понимание FMS и CFS. Кроме того, лучшее понимание FMS может дать представление об основной природе усталости сенсорных мышц и мышечной боли. Поскольку было очевидно, что многопрофильные исследования принесут большую пользу, мы сформировали большую рабочую группу, чтобы попытаться определить причины, механизмы и методы лечения сенсорной усталости и мышечной боли.Взаимодействия этой группы спровоцировали эксперименты на лабораторных животных и трансляционные клинические эксперименты, описанные ниже.
Чтобы определить, могут ли комбинации метаболитов решить проблему того, как обычно запускается прессорный ответ при физической нагрузке, и, возможно, как метаболиты вызывают чувство мышечной усталости, мы использовали кальциевую визуализацию нейронов ганглиев дорзального корешка, что позволило наблюдать большое количество случайно выбранные сенсорные нейроны. Чтобы сравнить нейроны, иннервирующие все структуры с этими иннервирующими мышцами, мы ретроградно метили нейроны ганглия задних конечностей (DRG) из мышц задних конечностей, вводя им индикатор DiI за 7-10 дней до сбора клеток.Мы решили провести эти эксперименты на мышах C57 Bl / 6 из-за наличия мутантных мышей с удаленными генами, которые предположительно способствуют обнаружению метаболитов. (Эти эксперименты подробно описаны в Light et al. 2008.)
Мы применили метаболиты индивидуально к диссоциированным нейронам DRG, культивированным в течение 24 часов, как показано на рис. Как показано на этом рисунке, даже pH 6 (очень низкий физиологически) активировал очень мало нейронов DRG, хотя pH 4, который определенно выходит за пределы физиологического диапазона, действительно активировал ~ 26% нейронов DRG, как отмечали другие (Leffler et al. .2006 г.). Мы также обнаружили, как и предыдущие исследования, что отдельные метаболиты были относительно неэффективными, за исключением АТФ, который может возбуждать до 60% нейронов DRG при нанесении в дозе 10 мкМ (Коннор и др., 2005; Рейнохл и др., 2003). Интересно, что в наших экспериментах, если нормальный уровень покоя АТФ вне мышечных клеток использовался для предварительной адаптации нейронов DRG, было обнаружено очень мало ответов только на АТФ, когда АТФ увеличивался ступенчатым образом (см.). Это означает, что рецепторы АТФ (такие как P2X5), чувствительные к низким концентрациям АТФ на нейронах DRG, обычно находятся в адаптированном состоянии и неспособны генерировать активирующие токи.Однако рецепторы, которые активируются только более высокими концентрациями АТФ (например, P2X4), могут быть непосредственно активированы уровнями метаболитов, продуцируемых болезненными уровнями метаболитов (2 мкМ или выше).
РИСУНОК 11.3
Процент всех нейронов DRG, отвечающих на прямое воздействие pH 6,0 или pH 4,0 (от 159 нейронов DRG). Кислый pH активирует несколько нейронов DRG при очень низком pH (6,0). Нефизиологический pH (4,0) равен r.
РИСУНОК 11.4
Процент нейронов DRG, отвечающих на различные комбинации метаболитов.Кальциевые ответы нейронов DRG мыши на различные комбинации метаболитов в указанных концентрациях. Обратите внимание, что нейроны наиболее чувствительны к комбинации трех метаболитов (подробнее …)
Когда два метаболита, предположительно участвующие в метаборецепции, применялись на физиологических уровнях, только комбинация АТФ и протонов вызывала реакции, которые вызывали симпатические рефлексы, наблюдаемые в люди с повышенным содержанием метаболитов (сравните с). Однако, когда АТФ, протоны и лактат применялись ступенчатым образом, аналогично тому, как они увеличивались с упражнениями в мышцах с закупоркой кровообращения, ответы нейронов DRG и особенно нейронов DRG, иннервирующих мышцы (определялись ретроградная маркировка), очень точно имитировала симпатические ответы, используемые другими в качестве считывания метаборецептивных ответов ().
Некоторые нейроны DRG реагировали на низкие уровни метаболитов, тогда как другие лучше всего отвечали на высокие уровни метаболитов (см.). Когда мы построили график средней амплитуды кальциевых ответов, результаты выявили профили ответов нейронов с низким уровнем метаболитов, которые соответствовали сигналам, вызывающим прессорный ответ при физической нагрузке. Эти профили также лучше всего подходят для восприятия мышечной усталости, которая сопровождает увеличение мышечных метаболитов.
РИСУНОК 11.5
Ответы нейронов DRG на применение указанных уровней метаболитов.
С другой стороны, ответы респондентов с высоким уровнем метаболитов лучше всего соответствуют восприятию боли, вызванной большим увеличением количества метаболитов в мышцах (см.).
РИСУНОК 11.6
Кальциевый ответ меченых мышцами нейронов DRG, отвечающих на изменения метаболитов, указанных в нижней части графика. (Перепечатано с разрешения Light AR, Hughen RW, Zhang J, Rainier J, Liu Z, Lee J. 2008. Нейроны ганглиев спинного корешка, иннервирующие скелет (подробнее …)
Чтобы определить, были ли молекулярные рецепторы, опосредующие кальциевые ответы, такими предложенный группой МакКлески, мы определили индуцированные метаболитами ответы нейронов DRG, иннервирующих мышцы, при применении селективных антагонистов.Эти эксперименты продемонстрировали, что наиболее вероятными молекулярными рецепторами, опосредующими ответы на метаболиты, являются рецептор ASIC (вероятно, ASIC3), рецептор P2X (вероятно, как P2X5, так и P2X4) и, что удивительно, TRPV1 (см.).
РИСУНОК 11.7
Процент нейронов DRG, отвечающих на метаболиты при значениях, указанных в нижней части графиков, при совместном применении антагонистов ASIC и TRPV1. (Перепечатано с разрешения Light AR, Hughen RW, Zhang J, Rainier J, Liu Z, Lee J. 2008. Ганглий дорзального корня (подробнее…)
Включение TRPV1 (половина чувствительности к метаболитам была отменена антагонистами TRPV1) было неожиданным, потому что реакции pH при 6,6 вряд ли будут опосредованы активацией этого рецептора. Было показано, что TRPV1 неактивен до тех пор, пока не будут достигнуты более низкие уровни pH (> pH 6,0), но мы ранее отметили, что большинство pH-чувствительных нейронов, меченных из мышц, реагировали на капсаицин, что указывает на то, что они, вероятно, экспрессируют функциональные рецепторы TRPV1. Но какова функциональная роль рецепторов TRPV1 на нейронах DRG, если не обнаружение активации протонами? Одна из возможностей — обнаружение эндогенных ваниллоидов, таких как анандамид (Cristino et al.2008; Toth et al. 2005). Они также могут определять температуру мышц, которая, как и метаболиты, является побочным продуктом сокращения мышц. При активации под действием температуры рецепторы TRPV1 могут действовать как рецепторы P2X5 в экспериментах Мак-Клески и могут не вносить непосредственный вклад в возбуждение, а, скорее, усиливать ответы нейронов DRG, когда температура мышц поднимается выше нормальной температуры тела. Sugiura et al. (2003) продемонстрировали аналогичный феномен в нейронах DRG — устойчивые токи, вызванные pH 6,0, усиливались повышением температуры.Интересно, что мы обнаружили, что нейроны DRG, определяющие низкий уровень метаболитов, реагировали на капсаицин так же часто, как и нейроны, обнаруживающие высокий уровень метаболитов. Кроме того, ответы на низкие метаболиты частично блокировались антагонистом TRPV1 LJO 328, вовлекая рецепторы TRPV1 в эти ответы. Таким образом, температура может быть фактором активации мышечных «рецепторов усталости», а также ноцицепторов. Это может объяснить повышенную сенсорную усталость, вызванную повышением температуры мышц и ядра (Drust et al.2005). Усиление кровотока, вызванное симпатическими рефлексами, активируемыми стимуляцией рецептора утомления, могло бы способствовать умеренному повышению температуры мышц и уменьшать другие метаболиты, вырабатываемые мышечным сокращением.
Участвуют ли другие метаболиты и рецепторы в передаче сигналов усталости сенсорных мышц и боли? МакКлески (личное сообщение) обнаружил, что молекула-предшественник пирувата может заменять лактат, но только на ~ 50% эффективнее в повышении реакции на метаболиты.Лактат не действует сам по себе и усиливает реакцию в наиболее распространенном диапазоне метаболитов, но тот факт, что пируват может действовать как заменитель, может объяснить недавние эксперименты, показывающие, что симпатические рефлексы, вызванные сокращением мышцы, были заблокированы у пациентов с болезнью Маккардла (генетическая потеря способности экспрессировать лактат в мышцах при сохранении пирувата) в некоторых условиях, но присутствует в других условиях (см. обзор Kaufman 2003).
Было высказано предположение, что несколько других метаболитов, связанных с сокращением мышц, играют важную роль в передаче сигналов, вызывающих прессорный рефлекс при физической нагрузке и / или мышечную боль.К ним относятся аммиак, моно- или дипротонированный фосфат, CO 2 , АДФ, аденозин, простагландины и калий. Мы протестировали аммиак и аммоний (виды, наиболее распространенные при низких значениях pH), CO 2 и ADP и обнаружили, что они неэффективны или ингибируют прямую активацию нейронов DRG, иннервирующих мышцы, или усиление ответов на метаболиты, показанные на рисунках. выше. Мы предполагаем, что эффекты калия будут неспецифическими, поскольку увеличение внеклеточного калия увеличивает возбудимость всех нейронов, как отмечено (Rybicki et al.1985). Мы еще не тестировали эффекты повышенного содержания фосфатов, аденозина или простагландинов, оставляя открытой возможность того, что они могут способствовать нормальным ощущениям мышечной усталости и боли, а также ответной реакции мышц при нагрузке.
Ретроспективно, метаболиты, которые, как мы обнаружили, синергетически активируют комбинацию молекулярных рецепторов, предполагает уникальную систему обнаружения для быстрого использования запасов энергии, которые могут сигнализировать организму о защите от метаболических и травматических повреждений.Комбинация протонов, лактата, АТФ и повышения температуры кажется особенно важной для сокращения мышц, а также применима к функции мозга. При метаболическом ацидозе или респираторном ацидозе не будет ложного сигнала сенсорной мышечной усталости или мышечной боли, поскольку в этих условиях будет увеличиваться только количество протонов, что будет неэффективно для активации мышечных афферентных нейронов, за исключением крайних случаев. С другой стороны, травматическое повреждение мышцы, которое вызовет выброс высоких концентраций АТФ, активирует ноцицепторы мышц и рецепторы усталости, что приводит к защитным поведенческим эффектам (уменьшению сокращения мышц и удалению поврежденной мышцы от источника травмы).
11,5. ОТВЕТСТВЕННЫ ЛИ ЭТИ МОЛЕКУЛЯРНЫЕ РЕЦЕПТОРЫ ЗА УСТАЛОСТЬ СЕНСОРНЫХ МЫШЦ И МЫШЕЧНУЮ БОЛЬ?
Как часть более крупной группы исследователей, заинтересованных в мышечной боли и ощущениях, связанных с мышечной усталостью, мы обнаружили, что они значительно увеличиваются у людей после изнурительных упражнений. Боль в мышцах и утомляемость сенсорных мышц быстро уменьшаются после завершения упражнения, но снова усиливаются в нетренированных мышцах через 12–24 часа и могут длиться 48 часов или дольше, прежде чем уменьшатся.Боль была тщательно изучена и часто называется мышечной болезненностью с отсроченным началом (DOMS), и большинство из нас (испытав это на собственном опыте) знают, что чувство мышечной усталости также усиливается во время DOMS. Объяснение DOMS состояло в том, что упражнения на нетренированные мышцы вызывают микроразрывы, которые приводят к воспалению; однако это объяснение спорно (Cheung et al. 2003). Независимо от того, присутствует ли микротравма или нет, сенсорные рецепторы, кодирующие мышечную боль и усталость, должны быть сенсибилизированы, чтобы эти усиленные ощущения были очевидны, потому что уровни метаболитов не увеличиваются в состоянии покоя в DOMS.Поскольку увеличение ASIC3 было показано на некоторых моделях долговременной мышечной боли (Voilley et al. 2001), мы предположили, что один или несколько молекулярных рецепторов, участвующих в передаче сигналов метаболитов о мышечной боли, выявляют повышенную мРНК (что может приводить к увеличению количество рецепторов и, следовательно, усиление передачи сигналов) после упражнений, которые вызвали DOMS.
Мы тренировали мышей, прогоняя их в шариках хомяка до тех пор, пока они не перестанут бегать (~ 2 часа), затем умерщвляли мышей через 16 часов и собирали DRG из шейных, грудных и поясничных областей спинного мозга.Мы предположили, что увеличение мРНК для ASIC3, P2X5, P2X4 и / или TRPV1 будет наблюдаться в шейных и поясничных нейронах DRG, иннервирующих группы мышц передних и задних конечностей, интенсивно тренируемых во время бега.
Как показано, мРНК для ASIC3, P2X4 и P2X5 была увеличена в тех нейронах DRG поясницы и шейки матки, иннервирующих тренируемые конечности. Увеличение было намного меньше в грудном отделе, который содержит мало нейронов, иннервирующих конечности. Мы интерпретируем это как означающее, что ASIC3, P2X4 и P2X5 способствуют усилению боли и сенсорной усталости, испытываемой во время DOMS, и, возможно, во время других событий, которые вызывают долгосрочное усиление мышечной боли и сенсорной мышечной усталости.
РИСУНОК 11.8
Увеличение мРНК DRG мыши, вызванное изнурительными упражнениями, измерено через 16 часов после тренировки (n = 6).
Несколько других медиаторов также могут участвовать в усилении боли и усталости, вызванных воспалительными состояниями. К ним относятся продукты путей арахидоновой кислоты (Hayes et al. 2006), цитокины (Hoheisel et al. 2005) и нейропептиды, такие как CGRP (Ambalavanar et al. 2006, 2007; Kruger et al. 1989; Micevych and Kruger 1992). .Необходима дальнейшая работа, чтобы определить всех участников этого процесса.
11.6. ПЕРЕВОД ОТ МЫШИ К ЧЕЛОВЕКУ
Следующий вопрос заключался в том, играют ли молекулярные рецепторы, которые мы идентифицировали у мышей, роль в сенсорных феноменах мышечной боли и усталости человека? Это представляло проблему, потому что сенсорная мышечная усталость и мышечная боль вызывают у мышей одно и то же поведение: они перестают бегать. Таким образом, отличить усталость сенсорных мышц от мышечной боли на модели грызунов сложно.У людей с СХУ усталость является определяющим симптомом, а мышечная боль — частым вторичным симптомом. У пациентов с FMS или CWP определяющим симптомом является широко распространенная мышечная боль, а наиболее частым вторичным симптомом является утомляемость. Они казались подходящими человеческими моделями для проверки идеи о том, что рецепторы ASIC, P2X и TRPV1 участвуют в мышечной боли и мышечной усталости. Однако вопрос заключался в том, как получить доступ к сенсорным афферентам.
Мы знали, что лейкоциты у людей обнаруживают изменения и накапливаются в тренированных мышцах в некоторых случаях после изнурительных упражнений (Kruger et al.2008 г.). Для этого эти клетки должны улавливать сигнал от мышцы, и мы предположили, что этим сигналом могут быть те же метаболиты, которые обнаруживаются афферентными нейронами, иннервирующими мышцы. Эти лейкоциты могут использовать одни и те же молекулярные рецепторы для обнаружения метаболитов.
Анализ мРНК из крови мышей показал, что все молекулярные рецепторы, которые, как мы обнаружили, были важны для обнаружения увеличения метаболитов в мышечных сенсорных нейронах, присутствовали в лейкоцитах, и аналогичный анализ мРНК крови человека также показал, что лейкоциты человека имеют значительные количества мРНК этих рецепторов.Изменилась ли мРНК лейкоцитов при физической нагрузке? Это оказалось трудным для определения у мышей, потому что количество крови, которое мы могли получить, было недостаточным для точного измерения мРНК этих генов. С другой стороны, у людей можно было легко получить достаточное количество крови несколько раз. Мы оценили увеличение мРНК в крови людей после упражнений и измерили гомологичную мРНК ионных каналов, которые были изменены в нейронах DRG, иннервирующих мышцу мыши, а также мРНК для адренергических рецепторов α2A, β1 и ($ β2, катехол-о-метилтрансферазы (COMT) и несколько провоспалительных и противовоспалительных цитокинов и рецепторов цитокинов, которые могут быть изменены при физической нагрузке.
Увеличение мРНК, полученной из лейкоцитов здорового субъекта, который выполнял максимальную, утомляющую силу и аэробные упражнения для всего тела в течение 45 минут (), было обнаружено для тех же молекулярных рецепторов, важных для обнаружения метаболитов в нейронах DRG мыши, которые были увеличены при истощении. упражнения в мышиных DRG. Ясно, что увеличение мРНК было тесно связано со временем DOMS и усталостью сенсорных мышц, которая появилась у этого субъекта после упражнений.
РИСУНОК 11.9
(см. Цветную вставку на следующей странице 166) мРНК увеличивается в лейкоцитах человека во время, указанное после 45 минут изнурительных упражнений. Все данные взяты от одной женщины. Упражнение состояло из аэробных и силовых упражнений, включая скалолазание в помещении, (подробнее …)
11.7. МОЛЕКУЛЯРНЫЕ РЕЦЕПТОРЫ, УЧАСТВУЮЩИЕ В СИНДРОМЕ ХРОНИЧЕСКОЙ УСТАЛОСТИ
Предыдущие наблюдения побудили нас определить, увеличилась ли мРНК сенсорной мышечной усталости и болевых рецепторов у пациентов с СХУ после упражнений, усугубляющих их симптомы.Основной отличительной чертой СХУ является то, что даже легкие упражнения значительно увеличивают утомляемость сенсорных мышц, а также мышечную боль (Holmes et al. 1988). Под руководством Андреа Уайт, нашего специалиста по физическим упражнениям, мы разработали 25-минутный протокол умеренных упражнений для всего тела, в котором каждый испытуемый непрерывно выполнял 70% максимальной частоты сердечных сокращений, прогнозируемой его возрастом. Мы подтвердили, что у нормальных, здоровых женщин и мужчин это умеренное упражнение вызывало минимальную мышечную боль или сенсорную мышечную усталость во время или сразу после завершения, и DOMS не развивался.Мы сравнили здоровую контрольную группу с пациентами с CFS и FMS, собирая лейкоциты и извлекая их мРНК с пятью интервалами: на исходном уровне перед тренировкой и через 30 минут, 8, 24 и 48 часов после окончания тренировки, чтобы исследовать ASIC3, P2X4, P2X5, TRPV1, адренергический α2A, адренергический β1 β1 и β β2, COMT, IL6, IL10, TNF-ctα, TLR4 и CD14.
Результаты (; Light et al., 2009a) показывают, что после умеренных упражнений у контрольных субъектов не было обнаружено значительного увеличения мРНК ни для одного из протестированных генов.Пациенты с CFS (70% с хронической широко распространенной болью, отвечающей диагностическим критериям FMS) продемонстрировали значительное увеличение экспрессии мРНК почти всех изученных генов, за исключением IL6 и IL10. Удивительным было то, что у пациентов с CFS увеличение экспрессии рецепторов, определяющих метаболит, и адренергических рецепторов было очевидным через 30 минут после начала упражнений. Вторым сюрпризом стала величина эффектов, которые значительно превзошли любое увеличение, которое мы наблюдали даже при максимальных физических нагрузках у контрольных субъектов.Помимо средних различий, мы обнаружили сильную корреляцию между увеличением мРНК ASIC3, P2X4, P2X5, TRPV1, адренергического α2Aα2A, адренергического β1, β2, COMT, IL10, TLR4 и CD14 у пациентов с CFS и их сообщениями об увеличении умственного развития. утомляемость в течение 2-дневного периода после тренировки. Мы обнаружили столь же сильную корреляцию между ASIC3, TRPV1, адренергическим α2Aα2A и ($ β2 и IL10) и сообщениями пациентов о боли в течение 2 дней после нагрузки.
РИСУНОК 11.10
(см. Цветную вставку на следующей странице 166) мРНК увеличивается у пациентов с СХУ после 25 минут умеренных упражнений (70% максимальной частоты сердечных сокращений с поправкой на возраст) (в центре), но не у контрольных субъектов (вверху). Гораздо более интенсивные упражнения (85% от максимального сердечного ритма с поправкой на возраст (подробнее …)
Эти данные указывают на то, что общий фактор транскрипции, вероятно, изменен при CFS, вызывая сильную регуляцию продукции мРНК в генах лейкоцитов, которые обнаруживают увеличение метаболитов, и предположительно влияет на продукцию цитокинов лейкоцитами.Происходит ли подобное действие на мышечные сенсорные нейроны у пациентов с CFS, неизвестно, но кажется вероятным, учитывая информацию, предполагающую, что периферические сигналы боли могут быть усилены, по крайней мере, у некоторых из этих пациентов (Staud et al. 2003).
11,8. ДИРЕГУЛИРУЕМЫЕ MRNAS ТАКЖЕ МОГУТ ОБЪЯСНИТЬ РАСПРОСТРАНЕННЫЕ СО-ЗАБОЛЕВАНИЯ CFS
. Многие из генов, которые, как мы обнаружили, не регулируются у пациентов с CFS после упражнений, также могут быть связаны с родственными расстройствами. У наших пациентов с CFS 70% соответствовали критериям FMS, который характеризуется широко распространенной болью с преобладанием мышечной боли.Ноцицепторы мышц, обнаруженные в наших исследованиях на мышах, использовали большинство молекулярных рецепторов, активируемых у пациентов с CFS, включая ASIC, P2X4 и TRPV1. Было показано, что чувствительность толстой кишки к воспалению опосредуется рецепторами ASIC и рецепторами TRPV1 (Christianson et al. 2006; Jones III et al. 2005; Page et al. 2005; Sugiura et al. 2007), что позволяет предположить, что нарушение регуляции этих рецепторов может увеличивают вероятность синдрома раздраженного кишечника (СРК), другого состояния, часто сопутствующего СХУ.Множественная химическая чувствительность может быть опосредована TRP-каналом, возможно, TRPV1 или TRPA1 (Pall and Anderson 2004).
Некоторые сенсорные модальности (но не все) становятся более чувствительными в некоторых случаях CFS. Гиперакузия при CFS может быть связана с увеличением количества рецепторов ASIC (Geisser et al. 2008; Hildebrand et al. 2004; Peng et al. 2004), поскольку рецепторы ASIC, по-видимому, усиливают слух. Клиническая депрессия может иметь общие некоторые из генов, которые были активированы у пациентов с CFS; например, TRPV1 недавно был вовлечен в депрессию (Di et al.2008), а ASIC могут играть роль в депрессии и тревоге (Coryell et al. 2007; Wemmie et al. 2003, 2004). Кроме того, полиморфизм COMT может быть фактором риска депрессии, хотя этот вопрос не лишен противоречий (Baekken et al. 2008; Funke et al. 2005; Ohara et al. 1998; Tsai et al. 2009). Возможно, гены, вносящие непосредственный вклад в сенсорное восприятие усталости, имеют общую вышестоящую регуляцию с генами, которые модифицированы в этих сопутствующих заболеваниях, которые разделяют усталость сенсорных мышц, гипералгезию и хроническую боль в качестве центральных симптомов, а также некоторые из тех же регулируемых генов.
Ряд других состояний, которые проявляют необъяснимую усталость сенсорных мышц, также могут иметь общую дисрегуляцию некоторых из тех же сенсорных, адренергических и цитокиновых генов. У нас есть предварительные доказательства того, что необъяснимая усталость при рассеянном склерозе, например, связана с исходными изменениями в TRPV1 и адренергических рецепторах β2, а также с изменениями некоторых генов ионных каналов и адренергических рецепторов после умеренных упражнений. Подобное нарушение регуляции может также объяснить значительно повышенную утомляемость сенсорных мышц, часто наблюдаемую при сердечной недостаточности, даже когда сосудистая динамика кажется адекватной для перфузии (Falk et al.2006; Хан и Синовей 2000). Если, например, сердечные сенсорные рецепторы нарушили регуляцию из-за первичного повреждения сердца, могло бы возникнуть сильное ощущение усталости, не связанное с какой-либо конкретной мышцей.
11.9. МОЖЕТ ЛИ ОСТРАЯ УСТАЛОСТЬ ПРИВЕСТИ К ХРОНИЧЕСКОЙ УСТАЛОСТИ?
Ключевой вопрос о CFS заключается в том, похож ли он на хроническую боль в том смысле, что острая боль может быть причиной хронической боли (Vierck, Jr., 2006). Ключ к разгадке в этом отношении может заключаться в том, находятся ли рецепторы, обнаруживающие метаболиты, связанные с утомлением сенсорных мышц, под контролем положительной обратной связи.Активация ASIC, P2X и TRPV1 увеличивает мРНК этих рецепторов в ганглиях задних корешков мышей после утомительных упражнений, и, действительно, они активируются после острой активации этих рецепторов метаболитами, что может привести к более устойчивой активации в будущих эпизодах продукции метаболитов. . Если увеличение мРНК, которое мы наблюдали у нормальных субъектов, и особенно у пациентов с CFS, транслируется в функциональные рецепторы, дальнейшее производство метаболитов будет производить больше рецепторов, вызывая усиление сигнала мышечной сенсорной усталости, если компенсирующие механизмы отсутствуют (например, отдых , усиление симпатического воздействия на гладкие мышцы сосудов для устранения метаболитов и увеличение емкости капилляров — все это снижает метаболиты).Также возможно, что усталость сенсорных мышц похожа на боль в том смысле, что постоянное сенсорное воздействие может вызывать центральное «возбуждение» и другие пластические изменения (такие как активация глии; Chacur et al. 2008), которые могут усиливать афферентные сигналы на многих уровнях в организме человека. центральная нервная система. Таким образом, сенсорные ощущения усталости и мышечной боли могут со временем усиливаться, а симпатические сигналы, вызванные усталостью сенсорных мышц и мышечной болью, могут усиливаться центрально в спинном и головном мозге. Имеются убедительные доказательства того, что сигналы усталости и мышечной боли усиливаются у пациентов с CFS и FMS (Caseras et al.2008; Cook et al. 2007; Geisser et al. 2008; Gracely et al. 2002; Schmaling et al. 2003), хотя относительный вклад центральных компонентов по сравнению с периферическими компонентами остается неопределенным.
11.10. ОБЩИЕ ПРИЧИНЫ ОСТРОЙ УСТАЛОСТИ МОГУТ ВЫЗВАТЬ ПОВЫШЕНИЕ РЕГУЛЯЦИИ мРНК МОЛЕКУЛЯРНЫХ РЕЦЕПТОРОВ, ПРЕДЛАГАЕМЫЕ ДЛЯ ОПРЕДЕЛЕНИЯ УСТАЛОСТИ СЕНСОРНЫХ МЫШЦ И БОЛИ
В настоящее время мы не знаем всех факторов, которые вызывают активацию молекулярных рецепторов, ответственных за обнаружение сокращения. продуцирует метаболиты в мышечных сенсорных нейронах.Mamet et al. (2003) предоставили доказательства того, что фактор роста нервов (NGF) может поддерживать и активировать рецепторы ASIC и может опосредовать воспалительные эффекты в отношении активации рецепторов ASIC. Таким образом, любое событие, которое увеличивает NGF, может увеличить утомляемость сенсорных мышц и боль.
Цитокиновые рецепторы также были продемонстрированы на сенсорных нейронах (например, Li et al. 2004). Поскольку цитокины участвуют в симптомах ряда вирусных инфекций, включая Эпштейн-Барр (Wright-Browne et al. 1998), вполне вероятно, что вирусные инфекции вызывают мышечную усталость и мышечную боль, повышая чувствительность афферентов сенсорных мышц, которые сигнализируют мышечная усталость и боль.Неизвестно, включают ли эти эффекты повышенную регуляцию молекулярных рецепторов, кодирующих метаболиты, но также кажется вероятным. Таким образом, острая вирусная инфекция может вызывать миалгию и усталость через цитокиновые пути.
Снижение митохондриальной эффективности (вирусные или невирусные причины) может привести к снижению аэробной способности. Это снижение может вызвать усиление гликолиза, что приведет к увеличению метаболитов, активирующих афференты сенсорных мышц. Любое такое увеличение может также привести к усилению ощущения мышечной усталости и боли в состоянии покоя и физических упражнений.Такое увеличение может также привести к увеличению количества молекулярных рецепторов, кодирующих метаболиты, вызывая дальнейшее усиление мышечной боли и усталости и, в конечном итоге, приводя к симпатической дисрегуляции и, возможно, CFS и FMS. Очевидно, что необходимы дальнейшие исследования механизмов, которые могут вызывать увеличение количества рецепторов, определяющих метаболиты, и могут прояснить множество состояний, при которых мышечная усталость и боль являются основными симптомами.
11.11. ПСИХИЧЕСКАЯ УСТАЛОСТЬ
Подобные процессы, хотя и выходят за рамки данного отчета, могут привести к нарушению регуляции рецепторов, кодирующих умственную усталость.Конечно, учитывая, что метаболические потребности мозга отличаются от потребностей мышц, конкретные молекулярные рецепторы, кодирующие метаболиты мозга, и то, как эти рецепторы регулируют церебральный кровоток, могут отличаться. Однако недавние сообщения предполагают нарушение регуляции глобального церебрального кровотока у пациентов с CFS (Mathew et al. 2008; Yoshiuchi et al. 2006), что может приводить к увеличению метаболитов, аналогичному тому, которое было обнаружено в скелетных мышцах пациентов с CFS.
11.12. СИМПАТЕТИЧЕСКАЯ ДИРЕГУЛЯЦИЯ СПОСОБСТВУЕТ УСИЛЕНИЮ СЕНСОРНОЙ УСТАЛОСТИ
Мышечные сенсорные афференты, которые могут кодировать сенсорную мышечную усталость, были связаны с симпатическими реакциями, вызванными сокращением мышц, в течение как минимум 70 лет (Alam and Smirk 1937; см. Также обсуждение в Light et al.2008 г.). Таким образом, афференты сенсорной усталости (и, возможно, афференты мышечной боли) могут быть сенсорным плечом (ами) симпатических рефлексов, связанных с сокращением мышц. Эти рефлексы обычно служат для увеличения притока крови к работающим мышцам, частично за счет отвода кровотока от неработающих мышц. Этот увеличенный кровоток способствует снижению метаболитов, прекращая сигналы, лежащие в основе усталости сенсорных мышц. Симпатический выходной сигнал опосредуется адренергическими рецепторами β2 на гладких мышцах сосудов в работающей мышце и адренергическими рецепторами α в неработающих мышцах, а также адренергическими рецепторами β1 в сердечной мышце.
Если симпатический сигнал не регулируется должным образом, повышенное количество метаболитов будет сохраняться, вызывая постоянный сигнал от сенсорных афферентов «усталости». Потенциально постоянный сигнал усталости от сенсорных афферентов может привести к симпатической дисрегуляции, посылая постоянный симпатический сигнал адренергическим рецепторам β на гладкие мышцы сосудов в скелетных мышцах, что приводит к подавлению этих адренергических рецепторов P. Такое подавление может привести к увеличению метаболитов в работающих мышцах, вызывая усиленный сигнал сенсорной мышечной усталости практически от всех мышц тела.Этот усиленный сигнал может привести к дальнейшему нарушению регуляции симпатических рефлексов. Точно так же, если симпатический сигнал не прерывается правильно, например, если СОМТ не регулируется либо по экологическим, либо по генетическим причинам (Goertzel et al. 2006), что приводит к усилению действия норадреналина и адреналина на сосудистые адренергические рецепторы β , может произойти понижающая регуляция. и метаболиты не могут регулироваться надлежащим образом. Аналогичным образом, изменения в эффективности адренергических рецепторов (как в случае некоторых полиморфизмов) могут привести к несоответствию между сенсорным сигналом, посылаемым в симпатическую нервную систему, и степенью расширения и / или сужения сосудов, что приводит к нарушению регуляции мышц. метаболиты (Дьяченко и др.2006 г.). Это нарушение регуляции метаболитов в мышцах может привести к повышенной утомляемости сенсорных мышц как в состоянии покоя, так и после упражнений.
11.13. АДРЕНЕРГИЧЕСКИЕ РЕЦЕПТОРЫ НА СЕНСОРНЫХ НЕЙРОНАХ?
Дилемма, касающаяся предполагаемого нарушения регуляции симпатических рефлексов у пациентов с CFS и FMS, проистекает из точки зрения, что нарушение регуляции является результатом сверхактивной симпатической нервной системы, которая «выгорает» из-за десенсибилизации или подавления периферических рецепторов в гладких мышцах сосудов в результате постоянной бомбардировки. с норадреналином.В двойном слепом плацебо-контролируемом перекрестном эксперименте, предназначенном для наблюдения за этой дисрегуляцией, мы (Light et al. 2009b) внутривенно вводили низкую дозу неселективного β адренергического антагониста пропранолола или плацебо пациентам с FMS или височно-нижнечелюстным расстройством. (TMD). Удивительно, но симпатические рефлексы (оцениваемые по катехоламинам плазмы и сердечно-сосудистым ответам на различные проблемы), которые были нарушены у пациентов с FMS, стали относительно нормализованными при введении пропранолола.Объяснением этого может быть сложная реорганизация центральной нервной системы и / или возможное воздействие на иммунную систему через адренергические рецепторы на лейкоциты или простое воздействие на сенсорные нейроны, которые контролируют симпатические рефлексы и мышечную боль. Сложные объяснения со стороны ЦНС и иммунитета кажутся невероятными, потому что большинство пациентов с ВНЧС и ФМС сообщали об уменьшении клинической боли пропранололом (а не плацебо; см.), Которое было почти мгновенным (в течение нескольких минут), без времени для реорганизации центральной симпатической системы или изменений в ней. иммунная функция.
РИСУНОК 11.11
Пропранолол снижает общую боль в теле. (Перепечатано с разрешения Light KC, Bragdon EE, Grewen KM, Brownley KA. 2009. Адренергическая дисрегуляция и боль с острой бета-блокадой и без нее у женщин с фибромиалгией и височно-нижнечелюстным расстройством. (Подробнее …)
Простым объяснением было что есть β-адренорецепторы не только на гладких мышцах сосудов в скелетных мышцах, но также на мышечных сенсорных нейронах, активация которых сигнализирует о боли в мышцах и запускает симпатические рефлексы.Чтобы полностью объяснить эти явления, предполагаемые адренергические рецепторы на мышечных сенсорных нейронах должны быть значительно активированы при TMD и FMS. Недавний отчет о клиническом случае, показывающий, что симптомы СХУ можно значительно уменьшить с помощью пропранолола, подтверждает эту возможность (Wyller et al. 2007). Однако ранее не было продемонстрировано наличие β-адренорецепторов на мышечных сенсорных нейронах.
11.14. НАЗАД К МЫШИ, ЧТОБЫ УЗНАТЬ, КАК АДРЕНЕРГИЧЕСКИЕ РЕЦЕПТОРЫ МОГУТ УВЕЛИЧИТЬ МЫШЕЧНУЮ БОЛЬ И УСТАЛОСТЬ
Как это ни парадоксально, но альфа-адренорецепторы были локализованы на сенсорных афферентных нейронах.Было показано, что альфа-адренорецепторы (как α1, так и α2) активизируют ноцицептивные сенсорные нейроны на животных моделях нейропатической боли и воспаления, что приводит к усилению ноцицептивных эффектов кожной стимуляции (Birder and Perl 1999; Lee et al. 1999; O ‘ Халлоран и Перл 1997; Сато и Перл 1991). Однако альфа-адренорецепторы на афферентных нервах спинного мозга, по-видимому, подавляют боль. Фактически, интратекальное лечение клонидином, агонистом альфа-адренорецепторов, часто используется для уменьшения различных типов боли у пациентов (Boyd 2001; Brown et al.2004; Сайты и др. 2003).
Только несколько сообщений предполагают, что бета-адренорецепторы играют роль в усилении боли после травмы (Khasar et al. 1999), и эти рецепторы не были обнаружены на мышечных сенсорных нейронах. Учитывая убедительные результаты экспериментов на людях, мы исследовали DRG мышей с помощью ПЦР, чтобы определить, присутствуют ли бета-адренорецепторы. Мы также индуцировали воспаление икроножных мышц и использовали количественную ПЦР в реальном времени, чтобы определить, активирована ли регуляция бета-адренорецепторов.Обнаружив мРНК адренергических рецепторов β1 и β2, присутствующих на нейронах DRG поясничного отдела мыши, мы также наблюдали, что мРНК рецептора β2 активируется через 24 часа после инъекции каррагинана в икроножную мышцу (см.), И это усиление продолжалось не менее 8 дней.
РИСУНОК 11.12
24-часовое процентное увеличение мРНК, вызванное каррагинан-индуцированным воспалением мышц. Обратите внимание на значительное увеличение адренорецепторов (n = 8 мышей).
Чтобы определить, активирована ли мРНК рецептора β 2 в большей степени в нейронах, иннервирующих мышцу, инъецированную каррагинаном, мы собрали нейроны DRG, меченные DiI, из мышцы, инъецированной каррагинаном, и сравнили их с нейронами, меченными DiI, с контралатеральной стороны. также вводили DiI, но не при воспалении каррагинана ().Эта процедура показала, что β2-адренергическая мРНК была намного выше в DiI-меченных нейронах из воспаленной каррагенаном мышцы, чем в нейронах DRG, иннервирующих мышцы, с контралатеральной стороны. 11.13. (подробнее …)
Джон Левин (Калифорнийский университет, Сан-Франциско) был достаточно заинтригован нашими наблюдениями на животных и людях, чтобы оценить возможные поведенческие эффекты (повышение уровня β-адренорецепторов у крыс с икроножными мышцами, воспаленными при инъекции каррагинана, как мы поступили с мышами.Он проверил чувствительность воспаленной мышцы через 1 час, 24 часа и 7 дней после воспаления. Он также проверил чувствительность мышц после инъекции пропранолола в дозах, сравнимых с теми, которые использовались в исследованиях на людях, описанных выше, и показал (), что пропранолол не действует через 1 час после индукции воспаления. Однако порог реакции отмены был значительно увеличен (что указывает на уменьшение боли) пропранололом через 24 часа после индукции воспаления, когда мРНК для бета-адренорецепторов увеличивалась в нейронах DRG.
РИСУНОК 11.14
Влияние пропранолола на вызванную воспалением мышечную боль у самцов крыс. Карра (1% в / м) по сравнению с пропранололом DRC (n = 6 крыс). (Любезно предоставлено доктором Олаинкой Диной и Джоном Левином, UCSF.)
Пропранолол увеличивал порог отмены даже на больший процент через 7 дней после воспаления — время, когда единственными обнаруживаемыми рецепторами в DRG мыши были β адренергических рецепторов. Доктор Левин также показал, что стресс через ось гипоталамус-гипофиз-надпочечники (HPA) в сочетании с активацией симпатической нервной системы может вызвать переключение адренергического сигнального пути, вызывающее гипералгезию у крыс.Таким образом, оказывается, что β адренергических рецепторов на сенсорных нейронах DRG способствуют повышенной чувствительности воспаленной мышцы. Неизвестно, играют ли бета-адренорецепторы роль в сигнале об усилении ощущения мышечной усталости, но это кажется вероятным. Та же ситуация может относиться к усилению мышечной боли и утомляемости сенсорных мышц у пациентов с различными состояниями, включая FMS и CFS. Понимание регуляции бета-адренорецепторов в мышечных сенсорных нейронах, а также того, как эта регуляция взаимодействует с активностью рецепторов ASIC, P2X и TRPV1 при передаче сигналов мышечной усталости и боли, может значительно улучшить нашу способность управлять рядом мышечных болей. и состояния сенсорной усталости мышц.
11.15. НАПРАВЛЕНИЯ БУДУЩИХ ИССЛЕДОВАНИЙ
И CFS, и FMS трудно диагностировать и лечить из-за нехватки объективных биомаркеров для диагностики или количественной оценки воздействия лечения на основные симптомы этих синдромов: мышечную боль и ощущение мышечной усталости. Основа для приемлемого с медицинской и юридической точки зрения объективного теста может быть основана на изменениях экспрессии лейкоцитарного гена после физических упражнений, которые мы наблюдали в наших группах пациентов. С помощью этих анализов анализы крови после упражнений могут обеспечить объективное подтверждение длительной и тяжелой усталости сенсорных мышц и состояния мышечной боли.В сочетании с анализами других генов, модифицированных другими заболеваниями, вызывающими утомление и мышечную боль, механизмы CFS и FMS можно отличить от других источников усталости и боли. Наблюдения за тем, как модуляция генов, вызванная физическими упражнениями, изменяется под действием лечения, также могут дать более глубокое понимание CFS и FMS и помочь в выборе более эффективных методов лечения этих синдромов.
Использование этих тестов мРНК в проспективном исследовании на популяции субъектов, у некоторых из которых развивается CFS и / или FMS, может предоставить тест для тех, кто подвержен развитию этих состояний, и может предоставить информацию, необходимую для предотвращения CFS и FMS.
Описанные здесь эксперименты также предлагают альтернативные направления исследований, которые могут улучшить понимание некоторых функциональных расстройств. Некоторые из генов, дисрегулируемых при CFS и FMS, вовлечены в синдром раздраженного кишечника (IBS), в частности, ASIC, TRPV1, адренергические (β2, IL10 и TLR4 рецепторы). Представление о том, что некоторые из них могут образовывать рецепторные комплексы, которые взаимодействуют Создание функциональных единиц может быть полезным для понимания этого синдрома.Точно так же множественная химическая чувствительность может выиграть от понимания рецепторных комплексов, которые могут обнаруживать множество различных химических сигналов.
Концепция рецепторных комплексов может также применяться к неуловимой молекулярной природе механических ноцицепторов, активируемых вредными механическими стимулами . Идентификация этих критических молекул может значительно улучшить лечение различных болевых состояний и синдромов. Одно особое соображение заключается в том, что понимание взаимодействия между механорецепторами и метаборецепторами мышечных сенсорных нейронов групп III и IV может помочь в описании и лечении синдрома беспокойных ног (RLS).Этот загадочный синдром характеризуется «неприятными ощущениями в ногах и неконтролируемым желанием двигаться в состоянии покоя, чтобы облегчить эти чувства» (NINDS 2001). Хотя в настоящее время они считаются центральной неврологической проблемой (во многом как CFS и FMS), симптомы (ощущение механической стимуляции внутри ног) и их облегчение при движении (усиление кровотока для удаления метаболитов) можно объяснить активацией мышц III группы. , не ноцицептивные механорецепторы, на которые также влияют мышечные метаболиты, вызываемые сокращением.Дальнейшее изучение афферентного вовлечения мышц III и IV групп в RLS заслуживает серьезного исследования.
Наконец, является ли усталость определенной сенсорной системой? Хотя наши первоначальные усилия показывают, что могут существовать специфические рецепторы, необходимо проделать большую работу по характеристике рецепторов утомления в скелетных мышцах, еще больше — по очень важным рецепторам утомления в сердечной мышце, и еще больше — по рецепторам утомления в головном мозге. и спинной мозг, а также определяет спинной мозг, ствол головного мозга, таламический и корковый отделы, которые обрабатывают сенсорный аспект утомления.С помощью специфического стимула («правильный» метаболитный «суп» для специфической активации этих рецепторов) можно идентифицировать области мозга, интегрирующие это явление. Возможно даже, что двигательные области, которые получают этот сигнал и отвечают за некогнитивное отключение двигательной команды, вызывающее отказ произвольного сокращения мышц, могут быть идентифицированы с использованием знаний, полученных при изучении афферентной системы. Вполне вероятно, что эти двигательные области содержат ключ к разгадке причин соматоформных расстройств, которые могут вызывать паралич определенных когнитивно контролируемых движений у некоторых пациентов.
Как и в любой плодотворной области исследований, остается много вопросов, но у нас есть инструменты и некоторые концепции, необходимые для начала исследования наиболее распространенных симптомов, которые приводят пациентов в клиники по всему миру: усталости и боли.
БЛАГОДАРНОСТИ
Исследования авторов, о которых здесь сообщается, были поддержаны грантом NIH R21 NS057821 от NINDS и NIAMS, с дополнительной вспомогательной поддержкой от NIH R21 AT0002209 от NCAM, грантом-катализатором от Центра медицинских наук Университета Юты, синергическим грантом от Университет штата Юта и грант кафедры анестезиологии Университета штата Юта.
Авторы также хотели бы выразить признательность за поддержку Центру геномики и визуализации Центра медицинских наук Университета штата Юта. Особая благодарность доктору Люсинде Бейтман за помощь в направлении пациентов. Спасибо доктору. Раджану Радхакришнану и Джесси Чжану за их помощь в проектах, описанных в этой главе. Кроме того, мы благодарим студентов бакалавриата, поддерживаемых программами UROP и BIOURP, включая Бенджамина Дженсена, Коди Ларсон, Таню Майкл, Клэй Петерсон, Ника Даскаласа, Шона Гоуэна, Шейна Хоторн, Соню Сарфраз, Туйет Нгуен и аспирантов из отдела физических упражнений и спорта. Отделение в составе К.Л. Фитшен, Люк Вендт и Тим Ванхайцма.
Симптомы фибромиалгии — боль и 9 других симптомов
Поскольку классические симптомы фибромиалгии — широко распространенная боль в мышцах и суставах и усталость — не очень характерны, это состояние часто неправильно диагностируется и неправильно понимается. У вас могут быть не все симптомы, а также другие проблемы со здоровьем.
Поскольку для этого нет лабораторных или визуальных тестов, когда вы пойдете на диагностику, ваш врач спросит о ваших симптомах, чтобы решить, есть ли у вас фибромиалгия
Общие симптомы и связанные с ними состояния
Многие люди с фибромиалгией — также так называемый синдром фибромиалгии или FMS — может иметь:
Боль и болезненные точки
Почти все люди с фибромиалгией болят во всем.Это может быть похоже на остеоартрит, бурсит и тендинит, но поражает все ваше тело. Обычно это заставляет вас пойти к врачу.
Боль может быть глубокой, острой, тупой, пульсирующей или ноющей. Вы чувствуете это своими мышцами, сухожилиями и связками вокруг суставов. У некоторых людей боль приходит и уходит. Он может путешествовать по вашему телу.
У вас также могут быть болезненные точки — специфические точки вокруг суставов, которые болят, когда вы нажимаете на них пальцем. Если вы надавите на чувствительную точку человека без фибромиалгии, он просто почувствует давление.Но такое же давление будет очень болезненным для человека с фиброзом.
Эти болезненные точки находятся в предсказуемых местах на теле. Часто они находятся под поверхностью кожи, а не в областях, вызывающих глубокую боль. Болит ткань вокруг мышц и суставов, а не сами суставы.
Усталость
Продолжительная усталость и чувство истощения — еще одна серьезная жалоба. Люди часто чувствуют усталость, даже если они должны чувствовать себя отдохнувшими, например, после хорошего ночного сна.Некоторые говорят, что это похоже на грипп. Некоторые сравнивают это с долгой работой и недостатком сна.
Вы можете чувствовать себя слишком уставшим, чтобы тренироваться, или более усталым после тренировки. Простые вещи, такие как покупка продуктов или приготовление ужина, могут уничтожить вас. Запуск такого проекта, как складывание одежды или глажка, может показаться слишком большим усилием. Возможно, вы даже слишком устали для секса.
Проблемы со сном
Большинство людей с фибромиалгией имеют проблемы со сном. Вы можете заснуть, но ваш сон легкий и легко нарушается.Когда вы встаете утром, вы устали и не отдохнули. Это не снимает усталости.
Тесты, проведенные в лабораториях сна, показывают, что людей с фиброзом постоянно прерывают всплески мозговой активности, аналогичные тем, которые происходят в мозгу, когда они бодрствуют. Эти перерывы ограничивают количество времени, которое вы проводите в глубоком сне, когда ваше тело восстанавливается, и в результате вы чувствуете усталость.
Расстройства настроения
До половины всех людей, страдающих фибромиалгией, страдают депрессией или тревожным расстройством, когда у них диагностировано фиброзное заболевание.
Постоянная усталость и боль может быть стрессовой. Вы, вероятно, беспокоитесь о том, чтобы идти в ногу с жизнью и о том, что вы можете сделать, чтобы почувствовать себя лучше. Вы можете стать менее активным и более замкнутым, что может привести к депрессии.
Также возможно, что тревога и депрессия могут быть частью фибромиалгии, как и боль.
Людям с диагнозом фибромиалгия и депрессия трудно сосредоточиться и кратковременную память, из-за которых трудно вспомнить повседневные вещи, например, куда они положили свои ключи или какие планы они составили на обед на завтра .
Утренняя скованность
Большинство людей с фибромиалгией чувствуют, что им нужно «расслабиться» после того, как они встали с постели, прежде чем они смогут начать свой день. Ощущение скованности в мышцах и суставах спины, рук и ног. Это не типичный скрип. Это больше похоже на скованность, которую испытывает человек с ревматоидным артритом.
Хотя некоторые люди говорят, что это длится всего несколько минут, жесткость обычно сохраняется более 15–20 минут каждый день. Иногда это длится часами, а может длиться весь день.
Отек и покалывание в руках и ногах
Хотя причина онемения, покалывания и жжения неясна, многие люди с фиброзом их ощущают. Эти ощущения, называемые парестезией, обычно возникают случайно. Они могут длиться несколько минут, а могут быть постоянными.
Ощущения могут быть особенно неприятными по утрам вместе с утренней скованностью. Но обычно они ничего не мешают.
Головные боли
До 2 из 5 человек с фиброзом также регулярно страдают мигренью или головными болями напряжения.Они могут быть результатом боли в шее и верхней части спины. Часто они вызваны напряжением мышц шеи. Они также могут быть вызваны болезненными точками на затылке и шее.
Головные боли могут значительно усложнить жизнь с фиброзом и вылечить болезнь.
Синдром раздраженного кишечника
Около двух третей людей с фибромиалгией часто испытывают боли в животе, газы и вздутие живота, а также чувствуют, что их рвет. У них также может быть запор и диарея.
Многие страдают кислотным рефлюксом или гастроэзофагеальной рефлюксной болезнью (ГЭРБ).
Проблемы с мочеиспусканием
Чувство позывов к мочеиспусканию, боли при этом или негерметичный мочевой пузырь могут возникнуть при фибромиалгии.
Эти симптомы также могут быть вызваны заболеваниями мочевого пузыря и почек, например инфекциями.
Менструальные спазмы
У женщин с фибромиалгией могут быть необычно болезненные менструальные спазмы, часто в течение многих лет, наряду с другими их симптомами.
Синдром беспокойных ног
Обычно это поражает ступни и ноги ниже колен.Это может быть больно, но чаще возникает ощущение, что вам нужно пошевелить ногами, чтобы им было удобно. Это особенно неприятно по ночам, потому что это может помешать вам уснуть.
Что такое миалгия? — Определение, симптомы и лечение — Видео и стенограмма урока
Причины и симптомы
Как упоминалось ранее, спортивные нагрузки или травмы, а также грипп могут вызывать мышечные боли и боли. Конечно, есть много других состояний, которые могут вызвать мышечную боль в дополнение к чрезмерному стрессу и чрезмерной нагрузке на мышцы.Эти состояния могут включать:
- Полимиозит — воспалительное заболевание мышц
- Фибромиалгия — заболевание, связанное с генетикой, эмоциями и инфекциями
- Гипотиреоз — или низкий уровень выработки гормонов щитовидной железы организмом
- Волчанка — аутоиммунное заболевание, при котором организм атакует само себя
- Ревматоидный артрит — воспалительное заболевание, поражающее суставы рук или ног
- Различные инфекции, вызываемые бактериями стафилококка
- Болезнь Лайма — болезнь, передающаяся клещом, заражающим людей бактерией
Миалгию могут вызывать и многие другие заболевания.Симптомы миалгии очевидны исходя из определения этого слова. Это мышечные боли и боли. Насколько сильны эти боли, как долго они продолжаются и находятся ли они только в одном месте или по всему телу, зависит от точной причины миалгии.
Например, мышечная боль, вызванная чрезмерной нагрузкой на мышцу во время тренировки в тренажерном зале, может быть локализована в определенной группе мышц. Если бы вы делали сгибания рук на бицепс, миалгия проявлялась бы в мышцах бицепса.Такая боль может пройти в считанные дни. Однако, если у вас грипп, мышечные боли, скорее всего, распространятся по всему телу. Вы можете испытывать боли в шее и плечах, по всей спине или даже во всем теле. Этот тип мышечной боли обычно проходит после того, как вы переболели гриппом. Другие типы мышечной боли, например, вызванные хроническими (длительными) воспалительными или аутоиммунными заболеваниями, могут быть обнаружены в определенных местах или по всему телу.Этот тип миалгии может быть довольно тяжелым.
Лечение
Лечение миалгии в первую очередь направлено на устранение ее причины. Без лечения источника проблемы, такого как инфекция или аутоиммунное заболевание, шанс успешного разрешения мышечной боли в долгосрочной перспективе ниже. Тем не менее, мы, безусловно, можем помочь лечить миалгию как таковую, одновременно занимаясь лечением основной проблемы. Таким образом, двусторонний подход к проблеме наиболее эффективен при лечении миалгии.
Способы лечения мышечных болей и болей включают:
- Отдых (сон)
- Использование безрецептурных болеутоляющих, таких как ибупрофен, при незначительных болях, например, вызванных гриппом
- Мягкие растяжки и упражнения, такие как йога, для снятия мышечного напряжения
- Использование метокарбамола, широко используемого миорелаксанта, который помогает уменьшить миалгию в случаях легкой или умеренной боли
- Опиоиды — сильные болеутоляющие средства, используемые для лечения более сильных мышечных болей
- Правильная физиотерапия может принести пользу многим пациентам с миалгией
Краткое содержание урока
Миалгия — это термин, буквально означающий мышечную боль.Этот тип боли может быть вызван стрессовой физической нагрузкой; вирусная инфекция, например грипп; или серьезные аутоиммунные заболевания, такие как волчанка, и это лишь некоторые из них. В зависимости от причины миалгии боль может быть локализованной или ощущаться по всему телу. Эта боль может варьироваться от легкой до сильной. Как лечится миалгия, также зависит от причины. Важно лечить основную причину, а также использовать лекарства и физиотерапию для симптоматического контроля самой мышечной боли.
Практика:
Что такое миалгия? — Тест по определению, симптомам и лечению
Инструкции: Выберите ответ и нажмите «Далее». В конце вы получите свой счет и ответы.
Каковы основные симптомы миалгии (выберите лучший ответ)?
Создайте учетную запись, чтобы пройти этот тест
Как участник, вы также получите неограниченный доступ к более чем 84 000 уроков математики, Английский язык, наука, история и многое другое.Кроме того, получайте практические тесты, викторины и индивидуальные тренировки, которые помогут вам добиться успеха.
Попробуй это сейчасНастройка займет всего несколько минут, и вы можете отменить ее в любой момент.
Уже зарегистрированы? Авторизуйтесь здесь для доступа
Фибромиалгия | Сидарс-Синай
Не то, что вы ищете?Что такое фибромиалгия?
Фибромиалгия — это состояние, вызывающее боль во всех мышцах и мягких тканях. в тело.Это постоянное (хроническое) состояние. Это может повлиять на вашу шею, плечи, спину, грудь, бедра, ягодицы, руки и ноги. Боль может усиливаться утром и вечером. Иногда боль может длиться целый день. Боль может усиливаться при активности, простуде или сырая погода, беспокойство и стресс. Это состояние чаще диагностируется у людей. в возрасте от 20 до 50 лет. Чаще всего встречается у женщин среднего возраста.
Что вызывает фибромиалгию?
причина неизвестна.Исследователи считают, что это может быть связано с проблемами со сном и стрессом. Это также может быть связано с иммунными, эндокринными или биохимическими проблемами.
Каковы симптомы фибромиалгия?
каждый симптомы у человека могут отличаться. Но хроническая боль — самый частый симптом. Боль самый часто поражает мышцы и точки прикрепления мышц к костям.Эти в связки и сухожилия.
Боль может начаться в одной части вашего тела, например, в шее и плечах. Но любая часть в тело может быть затронуто. Боль варьируется от легкой до сильной, с «обострениями» и временами из улучшение. Дискомфорт от фибромиалгии может ощущаться как жжение, болезненность, скованность, ноющая или грызущая боль, часто с болезненными пятнами в определенных частях ваш мышцы.Боль может ощущаться как артрит. Но это не повреждает мышцы или кости.
Другие общие симптомы фибромиалгии включают:
- Средний до сильной усталости (переутомления)
- Меньше упражнения на выносливость
- Сон проблемы ночью
- Подавленное настроение
- Беспокойство
- Головные боли
- Симптомы раздраженного кишечника, такие как боль в животе (брюшной полости) и вздутие живота, диарея и т. Д. запор
- Беспокойный ноги
- Болезненный менструальный цикл
- Проблема ясное мышление (так называемый «фиброзный туман»)
Эти симптомы могут походить на другие состояния здоровья.Обязательно обратитесь к своему врачу провайдер для диагностики.
Как протекает фибромиалгия поставлен диагноз?
Не существует тестов, которые могут подтвердить диагноз фибромиалгии. Вместо этого диагноз является на основе ваших симптомов, физического осмотра и, возможно, исключения других состояний.
Как протекает фибромиалгия обрабатывали?
Лечение будет зависеть от ваших симптомов, возраста и общего состояния здоровья.Это также будет зависеть от степени тяжести состояния.
Не существует известного лекарства от фибромиалгии, но симптомы можно контролировать. Легкие случаи могут выздоравливайте с помощью снижения стресса или изменения образа жизни. В более тяжелых случаях могут потребоваться быть лечиться с использованием подхода медицинской бригады. Это может включать ваше первичное медицинское обслуживание. провайдер, специалист вызвал ревматолога, физиотерапевта и боли клиника управления.Лечение может включать:
- Противовоспалительные препараты, облегчающие боль и помогающие уснуть
- Другое обезболивающие
- Лекарства, одобренные для лечения фибромиалгии (дулоксетин, прегабалин и милнаципран)
- Лекарства от депрессии (антидепрессанты)
- Упражнения (с малой нагрузкой) и физиотерапия для растяжения мышц и улучшения состояния сердечно-сосудистая система
- Методы релаксации или когнитивно-поведенческая терапия
- Нагрев или холодные процедуры
- Альтернативные методы лечения, такие как иглоукалывание, хиропрактика или массаж
Обсуждение с вашими поставщиками медицинских услуг о рисках, преимуществах и возможных побочных эффектах из все лекарства.
Жизнь с фибромиалгией
Фибромиалгия — хроническое заболевание, но с ней можно справиться, работая с вашим врачом. поставщики медицинских услуг. Помимо лекарств, облегчить симптомы могут изменение образа жизни. К ним относятся достаточный сон и упражнения.
Когда мне следует позвонить в медицинское учреждение провайдер?
Если ваши симптомы ухудшаются или у вас появляются новые симптомы, сообщите об этом своему лечащему врачу.
Ключевые моменты о фибромиалгия
- Фибромиалгия — хроническое заболевание, вызывающее боль в мышцах и мягких тканях. по телу.
- Исследователи считают, что это может быть связано с проблемами со сном, стрессом или иммунной, эндокринной недостаточностью. или биохимические проблемы.
- Симптомы может также включать недостаток энергии (усталость), проблемы со сном, депрессию, головные боли, а также другие проблемы.
- Есть нет известного лекарства, но симптомы можно контролировать.
- Лечение может включать в себя лекарства, упражнения, релаксацию, тепло или холод, а также массаж.
Следующие шаги
подсказок чтобы помочь вам получить максимальную пользу от визита к врачу:
- Знать причина вашего визита и то, что вы хотите.
- Раньше во время вашего визита запишите вопросы, на которые хотите получить ответы.
- Принесите кто-то с вами, чтобы помочь вам задать вопросы и запомнить, что говорит ваш поставщик ты.
- На посетите, запишите название нового диагноза и любые новые лекарства, методы лечения или тесты. Также запишите все новые инструкции, которые дает вам ваш провайдер.
- Знать почему прописано новое лекарство или лечение и как они вам помогут. Также знать каковы побочные эффекты ..
- Спросить, если ваше состояние можно лечить другими способами.
- Знать почему рекомендуется тест или процедура и что могут означать результаты.
- Знать чего ожидать, если вы не примете лекарство, не пройдете тест или процедуру.
- Если вы назначьте повторную встречу, запишите дату, время и цель для этого визит.
- Ноу как если у вас есть вопросы, вы можете обратиться к своему провайдеру.
Медицинский обозреватель: Дайан Хоровиц, доктор медицины
Медицинский обозреватель: Рита Сатер RN
Медицинский обозреватель: Раймонд Кент Терли BSN MSN RN
© 2000-2021 Компания StayWell, LLC.Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Фибромиалгия | Артрит | CDC
Что такое фибромиалгия?
Фибромиалгия (фибромиалгия) — это состояние, которое вызывает боль во всем теле (также называемую широко распространенной болью), проблемы со сном, усталость и часто эмоциональные и психические расстройства.Люди с фибромиалгией могут быть более чувствительны к боли, чем люди без фибромиалгии. Это называется обработкой аномального восприятия боли. Фибромиалгия поражает около 4 миллионов взрослых в США, около 2% взрослого населения. Причина фибромиалгии неизвестна, но ее можно эффективно лечить и контролировать.
Каковы признаки и симптомы фибромиалгии?
Наиболее частыми симптомами фибромиалгии являются
- Боль и скованность во всем теле
- Усталость и усталость
- Депрессия и тревога
- Проблемы со сном
- Проблемы с мышлением, памятью и концентрацией
- Головные боли, включая мигрень
Другие симптомы могут включать:
- Покалывание или онемение кистей и стоп
- Боль в лице или челюсти, включая заболевания челюсти, известные как синдром височно-нижнечелюстного сустава (также известный как ВНЧС)
- Проблемы с пищеварением, такие как боль в животе, вздутие живота, запор и даже синдром раздраженного кишечника (также известный как СРК)
Каковы факторы риска фибромиалгии?
Известные факторы риска включают:
- Возраст.Фибромиалгия может поражать людей любого возраста, включая детей. Однако большинству людей диагноз ставится в среднем возрасте, и с возрастом у вас больше шансов заболеть фибромиалгией.
- Волчанка или ревматоидный артрит. Если у вас волчанка или ревматоидный артрит (РА), у вас более вероятно развитие фибромиалгии.
Некоторые другие факторы слабо связаны с началом фибромиалгии, но необходимы дополнительные исследования, чтобы увидеть, реальны ли они. Эти возможные факторы риска включают:
- Пол.У женщин вероятность развития фибромиалгии в два раза выше, чем у мужчин.
- Стрессовые или травматические события, например автомобильные аварии, посттравматическое стрессовое расстройство (ПТСР)
- Повторяющиеся травмы. Травма в результате повторяющихся нагрузок на сустав, например частого сгибания колена.
- Болезнь (например, вирусные инфекции)
- Семейная история
- Ожирение
Как диагностируется фибромиалгия?
Врачи обычно диагностируют фибромиалгию, используя анамнез пациента, физический осмотр, рентген и анализ крови.
Как лечится фибромиалгия?
Фибромиалгию можно эффективно лечить с помощью лекарств и стратегий самоконтроля. Вы можете узнать о стратегиях самоуправления в разделе ниже, озаглавленном «Как я могу улучшить качество своей жизни»?
Фибромиалгию должен лечить врач или группа медицинских специалистов, специализирующихся на лечении фибромиалгии и других типов артрита, называемых ревматологами. Врачи обычно лечат фибромиалгию с помощью комбинации методов лечения, которые могут включать:
- Лекарства, включая рецептурные и безрецептурные обезболивающие
- Аэробные упражнения и упражнения для укрепления мышц
- Учебные классы для пациентов, обычно в отделениях первичной медико-санитарной помощи или в общинах
- Методы управления стрессом, такие как медитация, йога и массаж
- Хороший сон для улучшения качества сна
- Когнитивно-поведенческая терапия (КПТ) для лечения депрессии.КПТ — это тип разговорной терапии, предназначенный для изменения образа действий или мыслей людей
В дополнение к лечению люди могут управлять своей фибромиалгией с помощью описанных ниже стратегий самоконтроля, которые, как доказано, уменьшают боль и инвалидность, чтобы они могли заниматься важной для них деятельностью.
Каковы осложнения фибромиалгии?
Фибромиалгия может вызвать боль, инвалидность и ухудшить качество жизни. Взрослые США с фибромиалгией могут иметь такие осложнения, как:
- Больше госпитализаций.Если у вас фибромиалгия, вероятность госпитализации в два раза выше, чем у человека без фибромиалгии.
- Низкое качество жизни. Женщины с фибромиалгией могут испытывать более низкое качество жизни.
- Более высокие показатели большой депрессии. Взрослые с фибромиалгией более чем в 3 раза чаще страдают большой депрессией, чем взрослые без фибромиалгии. Скрининг и лечение депрессии чрезвычайно важны.
- Более высокий уровень смертности от самоубийств и травм. Смертность от самоубийств и травм выше среди пациентов с фибромиалгией, но общая смертность среди взрослых с фибромиалгией аналогична общей смертности населения.
- Более высокие показатели других ревматических состояний. Фибромиалгия часто сочетается с другими типами артрита, такими как остеоартрит, ревматоидный артрит, системная красная волчанка и анкилозирующий спондилит.
Как я могу улучшить качество своей жизни?
- Будьте физически активными . Специалисты рекомендуют взрослым быть умеренно физически активными в течение 150 минут в неделю. Ходите, плавайте или катайтесь на велосипеде по 30 минут в день пять дней в неделю. Эти 30 минут можно разбить на три отдельных десятиминутных занятия в течение дня.Регулярная физическая активность также может снизить риск развития других хронических заболеваний, таких как болезни сердца и диабет. Узнайте больше о физической активности при артрите. Вы можете заниматься самостоятельно или участвовать в программе физической активности, рекомендованной CDC.
- Перейти к рекомендованным программам физической активности . Те, кто заботится о том, как безопасно выполнять упражнения, могут участвовать в программах физической активности, которые доказали свою эффективность для уменьшения боли и инвалидности, связанных с артритом, и улучшения настроения и способности двигаться.Занятия проходят в местных школах, парках и общественных центрах. Эти занятия помогут вам почувствовать себя лучше. Узнайте больше о программах физической активности, рекомендованных CDC.
- Запишитесь на курс обучения самоуправлению , который помогает людям с артритом или другими заболеваниями, включая фибромиалгию, быть более уверенными в том, как контролировать свои симптомы, как жить хорошо и понимать, как это состояние влияет на их жизнь. Узнайте больше об образовательных программах по самоуправлению, рекомендованных CDC.
Узнать больше о фибромиалгии
Фибромиалгия: причины, симптомы и лечение
ФибромиалгияФибромиалгия — хроническое заболевание, вызывающее боль и болезненность во всем теле. По данным Национального института здоровья (NIH), от него страдают около 5 миллионов американцев. Расстройство обычно начинается в среднем возрасте и чаще всего встречается у женщин, но оно также может поражать мужчин и людей всех возрастов, включая детей.Люди с аутоиммунными заболеваниями, такими как волчанка или ревматоидный артрит, более подвержены заболеванию, чем население в целом.
Каковы симптомы фибромиалгии?Основные симптомы фибромиалгии:
- Распространенная боль по всему телу
- Обостренная болезненная реакция на давление во многих болезненных точках тела
Люди с фибромиалгией также могут испытывать следующие симптомы:
- Утомляемость от умеренной до сильной
- Затруднения со сном
- Жесткость сустава
- Головные боли
- Покалывание, онемение или жжение или покалывание в руках и ногах
- Менструальные периоды болезненные
- Раздраженный кишечник
- Проблемы с мышлением и памятью
Не существует анализа крови, других лабораторных или диагностических тестов или визуализационных исследований, которые могут идентифицировать фибромиалгию.Вот почему врачи должны исключить другие возможные причины таких симптомов, как боль и усталость, прежде чем ставить диагноз фибромиалгии. Боль и усталость являются симптомами многих состояний, включая синдром хронической усталости, ревматоидный артрит и волчанку.
Национальный институт артрита, скелетно-мышечных и кожных заболеваний, входящий в состав NIH, отмечает определенные рекомендации, которые врачи используют для диагностики фибромиалгии. К ним относятся:
- Распространенная боль продолжительностью более трех месяцев в анамнезе
- Чувство усталости и бодрствования при пробуждении
- Когнитивные проблемы (память или мысли)
- Боль в большом количестве областей по всему телу на предыдущей неделе
Национальная ассоциация фибромиалгии советует пациентам искать врача, имеющего большой опыт лечения фибромиалгии: «Поскольку люди с фибромиалгией, как правило, выглядят здоровыми, а обычные тесты обычно нормальны, для постановки диагноза необходим врач, знающий о заболевании. .”
Один метод, который широко использовался для диагностики фибромиалгии — исследование болезненных точек — больше не считается предпочтительным диагностическим тестом. В этом исследовании чувствительных точек, разработанном в 1990 году, врач оказывает давление на 18 конкретных точек тела; Считается, что пациент, который чувствует боль как минимум в 11 из этих точек, страдает фибромиалгией. Поскольку исследования позволили лучше понять причины фибромиалгии, в 2010 году Американский колледж ревматологии опубликовал новые диагностические критерии.Эти критерии рекомендуют врачам заменить обследование болезненных точек опросом с самоотчетом, в котором пациентов спрашивают, испытывали ли они боль в какой-либо из 19 различных частей тела за последнюю неделю. Пациентов также просят оценить степень выраженности определенных симптомов, например усталости.
В чем разница между фибромиалгией и миофасциальным болевым синдромом?Миофасциальный болевой синдром похож на фибромиалгию, но есть важные различия в симптомах и лечении.Одно большое отличие состоит в том, что миофасциальная боль ограничена определенной областью и связана с триггерными точками. Для получения дополнительной информации см. Страницу «Сделано для этого момента» с миофасциальным болевым синдромом.
У человека может быть как фибромиалгия, так и миофасциальный болевой синдром. Это делает особенно важным проконсультироваться с медицинским специалистом, который сможет диагностировать разницу и применить правильные методы лечения для каждого состояния.
Что вызывает фибромиалгию?По общему мнению, фибромиалгия является результатом гиперчувствительной и гиперактивной центральной нервной системы, когда головной и спинной мозг развивает повышенную болевую активность.Были предложены различные факторы риска, такие как генетическая предрасположенность, травма, множественные операции или хронический стресс, но они не являются окончательными.
Каковы лучшие методы лечения?В настоящее время нет лекарства от фибромиалгии. Однако есть способы справиться с болью и другими симптомами. Специалисты по обезболиванию понимают весь спектр вариантов обезболивания, в том числе то, как использовать их в сочетании для достижения успешного результата.
Врачи-анестезиологи специализируются на обезболивании, а некоторые из них специализируются на лечении пациентов с хронической болью.Спросите своего врача о направлении к врачу-анестезиологу, который специализируется на лечении хронической боли.
Варианты лечения обычно делятся на три категории: лекарства, изменение образа жизни и дополнительные методы лечения. Большинство пациентов чувствуют себя лучше, когда они используют компоненты из всех трех вариантов. Пациентам также может потребоваться попробовать разные лекарства, чтобы найти наиболее эффективное для них.
Лекарства
- Нестероидные противовоспалительные препараты, такие как аспирин, ибупрофен и напроксен
- Миорелаксанты
- Стероиды
- Прегабалин
- Дулоксетин или милнаципран
- Внутривенное введение лидокаина
- Налтрексон в низких дозах
- Трициклические антидепрессанты, такие как амитриптилин и нортриптилин
Изменение образа жизни
- Получение большого количества физических упражнений, которое, по утверждению Национального института здоровья, согласно исследованиям, является одним из самых эффективных методов лечения
- Развитие привычек сна и ритуалов перед сном
- Употребление в пищу продуктов, уменьшающих воспаление в организме
- Выявление и отказ от продуктов и ингредиентов, которые вызывают боль
- Бросить курить
- Снижение стресса с помощью медитации, осознанности, йоги или других техник
- Требования к наладочным работам
Дополнительные методы лечения
- Иглоукалывание
- Хиропрактика
- Массаж
- Ци гун
- Тай-чи
- Травяные добавки
- Когнитивно-поведенческая терапия
Врачи-анестезиологи привержены обеспечению безопасности пациентов и высококачественной помощи и обладают необходимыми знаниями, чтобы понимать и лечить все человеческое тело.
39-летняя женщина с лихорадкой и миалгией
39-летняя женщина с лихорадкой и миалгией
Рассмотрена ассамблеей интенсивной терапии
Представлено
Hugh Davis, MD
Резидент
Отделение внутренней медицины
Cedars Sinai Medical Center
Los Angeles, CA
Isabel Pedraza, MD
Директор отделения интенсивной терапии дыхательных путей
Отделение легочной / реанимационной помощи
Гильдия женщин Институт легких, отделение легочной медицины и реанимации, Cedars Sinai Медицинский центр
Los Angeles, CA
Оставьте свои комментарии авторам.
История болезни
39-летняя женщина европеоидной расы поступила в отделение неотложной помощи с недельной историей лихорадки и диффузных мышечных болей. Она также сообщает об однодневном анамнезе боли и отека в левой паховой области в дополнение к диффузной боли по всему правому бедру с вышележащими эритематозными изменениями кожи.
За неделю до обращения ее осмотрел лечащий врач с жалобами на лихорадку, озноб и диффузные мышечные боли. При обычном анализе мочи у нее была отмечена выраженная пиурия, и ей назначили левофлоксацин при подозрении на инфекцию мочевыводящих путей.Впоследствии у нее развился болезненный отек левого предплечья, который, как предполагалось, был тендинитом, вызванным фторхинолоном, и антибиотикотерапия была переведена с левофлоксацина на ципрофлоксацин с временным исчезновением симптомов.
Пациентка также была осмотрена гинекологом за три дня до обращения с жалобой на повторение симптомов. Осмотр органов малого таза в то время был ничем не примечательным. Культуры, взятые из влагалищного канала, и повторный анализ мочи без особенностей. Она была продолжена на ципрофлоксацине и доксициклине для дополнительного противомикробного покрытия.Несмотря на дополнительный прием антибиотика, ее симптомы ухудшились, появились постоянная лихорадка и миалгии в дополнение к общей слабости и тошноте.
Медицинский осмотр
При медицинском осмотре у пациента была обнаружена лихорадка с температурой 102 градуса по Фаренгейту. Ее пульс был 80 при артериальном давлении 100/60. Частота дыхания у нее была 18 при 100% насыщении кислородом комнатного воздуха.
Она выглядела больной и неудобной. Хотя шейная лимфаденопатия не была оценена, мускулатура ее шеи была диффузно чувствительной при пальпации.Ее сердечно-сосудистое обследование не выявило шумов, а ее легочное обследование было ничем не примечательным. Живот при пальпации диффузно болезненный, без перитонеальных признаков или органегалии. В левой паховой области был отмечен увеличенный болезненный лимфатический узел без окружающей эритемы или колебаний. Было обнаружено, что мускулатура ее конечностей диффузно чувствительна при пальпации, а на туловище и конечностях отмечалась пятнистая, бледная, бледная сыпь.
Лаборатория
Количество лейкоцитов 13 400 / мм3, гемоглобин 11.4 г / дл, тромбоцитов 292,000 / мм3
Различие значимо для 97% полиморфноядерных лимфоцитов
Тесты функции печени значимы для общего билирубина 1,9 мг / дл, прямого билирубина 1,2 мг / дл, AST 60 U / L, ALT 129 U / L, щелочной фосфатазы 344 U / L
Амилаза и липаза в пределах нормы
Химический состав сыворотки в пределах нормы
Общий анализ мочи был значимым для 5-10 лейкоцитов на HPF и следы лейкоцитарной эстеразы
Рентген грудной клетки не выявил сердечно-легочного заболевания.
На УЗИ брюшной полости острого процесса нет.
Было собранокультур крови, и пациенту была начата эмпирическая антибактериальная терапия ванкомицином и цефотаксимом. В течение 24 часов все культуры крови были положительными с окрашиванием по Граму, показывающим грамположительные кокки в парах и цепочках. Позднее этот организм был определен как бета-гемолитические стрептококки группы А по Лэнсфилду ( Streptococcus pyogenes) .
Эхокардиография показала подвижную подклапанную вегетацию размером 15 x 10 мм, вовлекающую сосочковые мышцы задней створки митрального клапана.(см. видео, показывающее вегетацию митрального клапана) Несмотря на лечение антибиотиками, у нее появилось спутанность сознания и помутнение зрения, связанные с головной болью и светобоязнью. Офтальмологическое обследование выявило двусторонний увеит, а МРТ головного мозга продемонстрировала многочисленные биополушарные поражения, соответствующие септическим эмболам (рис. 1).
Видео 1
Рис. 1. МРТ головного мозга, показывающая биополушарные инфаркты, соответствующие септической эмболии
Пациенту была проведена срединная стернотомия для резекции вегетации, которая прилегала к сосочковой мышце, сухожилиям и задней стенке левого желудочка, и положительно окрашена на грамположительные кокки.(Рисунок 2) После операции пациентка выздоровела без осложнений и была выписана домой на седьмой послеоперационный день для завершения шести недель внутривенного введения цефотаксима. Во время последующего наблюдения было обнаружено, что у пациентки все хорошо с полным исчезновением предшествующих симптомов. Повторные лабораторные данные, включая тесты функции печени, были полностью в пределах нормы.
Рис. 2: Микроскопические изображения эндокардиальной вегетации, показывающие грамположительные кокки.
Стрептококки группы А характеризуются присутствием белков М, которые являются преобладающим фактором вирулентности, связанным с инвазивной инфекцией. Было продемонстрировано, что Streptococcus pyogenes не является патогенным при отсутствии белка М. (1) Эти пальцевидные белки проходят через защитную капсулу гиалуроновой кислоты организма, таким образом проявляя свои патогенные эффекты, оставляя бактерии защищенными от окружающей среды хозяина. Существует более 150 подтипов M-белков, и были разработаны схемы классификации для дальнейшей классификации подтипов стрептококков группы A на основе характеристик отдельных M-белков.Имеются данные, позволяющие предположить, что приобретенный иммунитет хозяина специфичен для отдельных подтипов белков М, что обеспечивает ограниченную защиту от повторной инфекции. (2) Попадая в систему кровообращения хозяина, белки М образуют комплексы с фиброногеном и прикрепляются к эндотелию сосудов. (3) После прикрепления к эндоваскулярной поверхности комплексы приводят к активации циркулирующих полиморфноядерных лимфоцитов, высвобождению протеолитических ферментов и деградации эндотелия сосудов. Таким образом, деградированная эндотелиальная поверхность становится уязвимой для транслокации организма в плоскости окружающих тканей.После заражения белок М также действует, чтобы защитить вторгшийся организм от защиты хозяина. Например, было показано, что белок М облегчает адгезию к поверхности клеток (4), ингибирует фагоцитоз, препятствуя опсонизации через путь комплемента (5), и даже позволяет организму интернализоваться в эпителиальных клетках человека (6), что позволяет организм, чтобы избежать защиты хозяина.
В то время как стрептококки группы А хорошо приспособлены к инвазивной инфекции мягких тканей, этот организм, пожалуй, наиболее известен производством суперантигенов.Эти мощные факторы вирулентности оказывают мощный воспалительный эффект, связываясь с рецепторами MHC класса II на циркулирующих Т-клетках, вызывая, таким образом, обильное высвобождение интерлейкинов и цитокинов, способствуя экспоненциальному каскаду иммунологической активности, который характеризует синдром токсического шока стрептококка. (7) Эта жизнь — угрожающее состояние характеризуется лихорадкой, бактериемией, полиорганной недостаточностью и широко распространенными десквамативными кожными поражениями. Однако развитие синдрома токсического стрептококкового шока у пациентов со стрептококковой бактериемией группы А относительно нечасто.В одном исследовании было обнаружено, что хотя синдром стрептококкового токсического шока встречался только у 9% пациентов со стрептококковой бактериемией группы А, при его наличии он был связан со значительной смертностью. (8)
Помимо оперативного хирургического вмешательства, раннего и соответствующего Антибактериальная терапия имеет решающее значение для эффективного лечения инвазивного стрептококкового заболевания и синдрома токсического шока. При подозрении на синдром токсического шока начальная эмпирическая терапия должна быть направлена против Staphylococcus Aureus и Streptococcus Pyogenes и должна учитывать потенциальную устойчивость этих организмов к метициллину и эритромицину соответственно.Однако, как только подтверждена инфекция стрептококками группы А, в качестве схемы лечения выбирают пенициллин и клиндамицин. Этот режим рекомендован Американским обществом инфекционных болезней (уровень А2). (9)
В то время как стрептококки группы A остаются чувствительными к b-лактамным антибиотикам, бактерицидные эффекты пенициллина оказались менее эффективными в условиях высокой нагрузки на организм. Исследования, демонстрирующие неэффективность одних β-лактамов при лечении инвазивной стрептококковой инфекции группы А, относятся к началу 1950-х годов, когда Игл и его коллеги использовали мышиную модель, чтобы продемонстрировать, что один пенициллин неэффективен при лечении стрептококковых инфекций группы А с большим размером инокулята.(10) Этот феномен, который получил название «эффект инокулята», как полагают, объясняется подавлением экспрессии связывающих пенициллин белков, когда организм находится в стационарной фазе роста, что достигается быстрее при увеличении Бактериальная нагрузка. (11) Последующее исследование Стивенса и его коллег расширило раннюю работу Игла, чтобы продемонстрировать, что пенициллин, клиндамицин и эритромицин, по-видимому, одинаково эффективны на ранних этапах инфекционного процесса со 100% выживаемостью во всех группах.(12) Однако показатели выживаемости в этой модели инвазивной стрептококковой инфекции резко расходятся на более позднем этапе инфекционного процесса, при этом выживаемость только 60% в группе пенициллина по сравнению со 100% в группах клиндамицина и эритромицина через 12 дней после первоначальной инокуляции. Кроме того, было показано, что отсрочка начала антибактериальной терапии всего на 2 часа снижала выживаемость в группах лечения пенициллином и эритромицином до 30% и 70% соответственно, в то время как клиндамицин оставался столь же эффективным со 100% выживаемостью, несмотря на отсрочку лечения.Даже когда начало терапии клиндамицином откладывалось на 16,5 часов после инокуляции, выживаемость оставалась на уровне 70%. Снижение смертности, связанной с использованием клиндамицина, вероятно, связано с прямым ингибирующим действием этого препарата на определенные факторы патогенности и вирулентности стрептококков. Было показано, что продукция М-белка подавляется в присутствии клиндамицина, что приводит к усиленной опсонизации и фагоцитозу полиморфно-ядерными лейкоцитами.(13) Было показано, что использование клиндамицина приводит к большему снижению выработки экзотоксина по сравнению с использованием b-лактамов. (14, 15) Однако, хотя клиндамицин играет хорошо установленную роль в лечении инвазивных стрептококков группы А. При заболевании добавление пенициллина по-прежнему рекомендуется из-за постоянной чувствительности организма к b-лактамным антибиотикам и увеличения потенциала устойчивости к макролидам среди стрептококков группы А. (16, 17)
Соответствующее подозрение и раннее распознавание инвазивного стрептококкового заболевания имеет решающее значение для эффективного лечения инвазивной стрептококковой инфекции группы А.Центры по контролю и профилактике заболеваний хранят исчерпывающие эпидемиологические данные о стрептококковой инфекции группы А в рамках отчета об активном бактериальном надзоре (ABCS). По последним данным CDC, ежегодно происходит 12000 случаев инвазивной групповой стрептококковой инфекции с 1600 сопутствующими смертельными случаями (смертность 13,3%). (18) Имеющиеся данные свидетельствуют о двухмодальном возрастном распределении, с самыми высокими показателями среди младенцев. и пожилые. (18) Однако среди лиц, употребляющих наркотики внутривенно, во втором и третьем десятилетии жизни зарегистрировано резкое увеличение заболеваемости стрептококковой бактериемией группы А.(8) Доступные серии случаев показали, что стрептококк группы A является относительно редким изолятом из крови, составляющим примерно 1% всех бактериемий. (8) Модели на животных показали, что стрептококковая бактериемия группы A может сохраняться в течение нескольких недель после инокуляции и может могут быть ускорены незначительными травмами мышц и мягких тканей. (19)
Хотя важно понимать, что большая часть инвазивных стрептококковых инфекций группы А не имеет известного портала входа (20), национальные данные CDC продемонстрировали, что, когда место проникновения известно, наиболее распространенным является целлюлит (31 .5%) локализованная инфекция, связанная с инвазивной стрептококковой инфекцией группы А, за которой следуют пневмония (17%) и некротический фасциит (6,6%). (18) Подобное распределение локализованных инфекций было описано среди пациентов интенсивной терапии с инвазивной стрептококковой инфекцией группы А. (21) Среди потребителей инъекционных наркотиков в большинстве случаев присутствует идентифицируемый кожный входной портал, такой как гнойный флебит или кожный абсцесс, а тяжелые кожные инфекции связаны с более высокими показателями смертности.(8)
Среди различных проявлений инвазивной группы стрептококковой инфекции эндокардит является чрезвычайно редким осложнением. Общенациональное ретроспективное исследование во Франции выявило только 7 случаев, связанных со стрептококком группы А, за 10-летний период. Интересно, что среди пациентов со стрептококковой бактериемией группы A септическая эмболизация является обычным явлением и часто происходит без эхокардиографических доказательств эндокардита. (8) Когда присутствует поражение эндокарда, стрептококки группы A часто поражают в целом нормальные нативные сердечные клапаны, и было показано, что они имеют поражение эндокарда. Смертность 21%.(22) Таким образом, хотя эндокардит и встречается редко, его часто трудно отличить от бактериемии, что создает терапевтическую дилемму относительно типа и продолжительности терапии.
Среди пациентов с инвазивной стрептококковой инфекцией группы А потребность в лечении является обычным явлением. Проспективное обсервационное исследование пациентов в отделении интенсивной терапии с инвазивной стрептококковой инфекцией группы А показало, что прогрессирующая полиорганная недостаточность, такая как ОРДС, почечная недостаточность, требующая заместительной терапии, дисфункция печени, неврологическая дисфункция и коагулопатия, часто наблюдалась при запущенных состояниях болезни.(21) Среди пациентов ОИТ с инвазивным стрептококком группы А общая смертность высока (40%) и часто наступает менее чем через 7 дней после поступления в ОИТ. Неудивительно, что риск смерти среди пациентов в отделении интенсивной терапии, как было показано, связан с более высокими показателями оценки острой физиологии и хронического здоровья (APACHE II), количеством дисфункциональных органов и наличием синдрома токсического шока, вызванного стрептококками.
Внутривенный иммуноглобулин (IVIg) — это терапия, которая широко исследовалась в контексте инвазивного стрептококкового заболевания группы А, особенно синдрома стрептококкового токсического шока.Обоснование использования ИГВВ основано на наблюдении, что антитела, направленные против определенных факторов вирулентности стрептококков группы А, присутствуют на более низких уровнях у пациентов с инвазивным заболеванием по сравнению с контрольной группой. (23) Также было показано, что циркулирующие уровни анти- Антитела к белку М значительно увеличиваются у пациентов с синдромом токсического шока, вызванным стрептококком, после терапии ИГВВ, что приводит к опсонизации и очищению организма. (24) В многочисленных отчетах о случаях, опубликованных за последние несколько десятилетий, предполагается, что пациенты с инвазивным стрептококковым заболеванием улучшили исходы. при лечении IVIg.(25, 26) Однако более крупное обсервационное исследование, проведенное Каулом и его коллегами в 1999 г., продемонстрировало заметное снижение смертности среди пациентов с синдромом токсического шока, вызванного стрептококком, которые лечились с помощью ИГВВ, по сравнению с контрольной группой через 30 дней (34% против 67%). . (27) Кроме того, анализ сыворотки как у леченных пациентов, так и у контрольных пациентов продемонстрировал значительное снижение опосредованной Т-клетками продукции IL-6 и TNF-a. Последующее рандомизированное двойное слепое плацебо-контролируемое исследование продемонстрировало трехкратное снижение 28-дневной смертности (36% vs.10%) среди пациентов, получавших ИГВВ, но не достигших статистической значимости, возможно, из-за небольшого размера выборки с 10 и 11 пациентами в группах лечения и плацебо соответственно. (28) Однако интересно проспективное обсервационное исследование пациентов ОИТ с инвазивным стрептококком. инфекция не обнаружила связи между использованием ИГВВ и выживаемостью. (21) Ссылаясь на несоответствия в коммерчески доступных ИГВ и на необходимость более убедительного исследования роли ИГВВ в лечении инвазивной стрептококковой инфекции группы А, Американское общество инфекционных заболеваний предлагает оценку Рекомендация 2B по применению ИГВВ (умеренные доказательства в поддержку рекомендации по применению; обычно следует предлагать).(9)
Были проведены обширные исследования по изучению возможности использования вакцин для предотвращения стрептококковой инфекции группы А. Среди других стрептококковых антигенов М-белок исследовался как потенциальная мишень для вакцины. Вариабельность подтипов белка М и специфичность приобретенного иммунитета хозяина создают проблему для разработки вакцины. Однако было показано, что 26-валентная вакцина, нацеленная на преобладающие эпитопы М-белка, обнаруженные в Соединенных Штатах и Европе, индуцирует антитела хозяина, которые способны опсонизировать подтипы-мишени М-белка, а также несколько вариантов подтипов, которые не представлены.(29) Эта вакцина была оценена в фазах I и II клинических испытаний на людях, и было обнаружено, что она безопасна и эффективна для индукции выработки антител и последующей опсонизации. (30) Хотя эти результаты, безусловно, обнадеживают, стратегии вакцинации для предотвращения группы A стрептококковая инфекция остается исследуемой.
Ссылки
- Брукс Дж., Бутель Дж., Морс С. Явец, Мелник и медицинская микробиология Адельберга. Нью-Йорк: Макгроу Хилл; 2004.
- de Malmanche SA, Martin DR.Защитный иммунитет к группе стрептококков может быть только штаммоспецифичным. Med Microbiol Immunol 1994; 183 (6): 299-306
- Herwald H, Cramer H, Morgelin M, Russell W, Sollenberg U, Norrby-Teglund A, Flodgaard H, Lindbom L, Bjorck L. Белок M, классический бактериальный детерминанта вирулентности, образует комплексы с фибриногеном, которые вызывают утечку из сосудов. Cell 2004; 116 (3): 367-379.
- Фрик И.М., Шмидтхен А., Сджобринг У. Взаимодействие между m-белками Streptococcus pyogenes и гликозаминогликанами способствует адгезии бактерий к клеткам-хозяевам.Eur J Biochem 2003; 270 (10): 2303-2311
- Peterson PK, Schmeling D, Cleary PP, Wilkinson BJ, Kim Y, Quie PG. Ингибирование опсонизации альтернативного пути комплемента стрептококковым m-белком группы. J. Infect Dis 1979; 139 (5): 575-585.
- Греко Р., Де Мартино Л., Доннарумма Г., Конте М. П., Сеганти Л., Валенти П. Инвазия культивируемых клеток человека с помощью Streptococcus pyogenes. Рес Microbiol 1995; 146 (7): 551-560.
- Norrby-Teglund A, Thulin P, Gan BS, Kotb M, McGeer A, Andersson J, Low DE.Доказательства участия суперантигена в тяжелой группе стрептококковых инфекций тканей. J. Infect Dis 2001; 184 (7): 853-860.
- Бернальдо де Кирос Дж. К., Морено С., Серценадо Э, Диас Д., Беренгер Дж., Мираллес П., Каталонский П., Буза Е. Группа стрептококковой бактериемии. 10-летнее проспективное исследование. Медицина (Балтимор) 1997; 76 (4): 238-248.
- Стивенс Д.Л., Бисно А.Л., Чемберс Х.Ф., Эверетт Э.Д., Деллинджер П., Гольдштейн Э.Дж., Горбач С.Л., Хиршманн СП, Каплан Э.Л., Монтойя Дж.Г. и др. Практические рекомендации по диагностике и лечению инфекций кожи и мягких тканей.Clin Infect Dis 2005; 41 (10): 1373-1406
- Игл Х. Экспериментальный подход к проблеме неудачного лечения пенициллином. I. Группа стрептококковой инфекции у мышей. Am J Med 1952; 13 (4): 389-399.
- Стивенс Д.Л., Ян С., Брайант А.Е. Экспрессия пенициллин-связывающего белка на разных стадиях роста определяет эффективность пенициллина in vitro и in vivo: объяснение эффекта инокулята. J. Infect Dis 1993; 167 (6): 1401-1405.
- Стивенс Д.Л., Гиббонс А.Э., Бергстром Р., Винн В.Еще раз об эффекте орла: эффективность клиндамицина, эритромицина и пенициллина при лечении стрептококкового миозита. J. Infect Dis 1988; 158 (1): 23-28.
- Джеммелл К.Г., Петерсон П.К., Шмелинг Д., Ким И., Мэтьюз Дж., Ваннамейкер Л., Куи П.Г. Усиление опсонизации и фагоцитоза Streptococcus pyogenes после роста в присутствии клиндамицина. Дж. Клин Инвест 1981; 67 (5): 1249-1256.
- Sriskandan S, McKee A, Hall L, Cohen J. Сравнительные эффекты клиндамицина и ампициллина на суперантигенную активность Streptococcus pyogenes.J. Antimicrob Chemother 1997; 40 (2): 275-277.
- Койл Е.А., Ча Р., Рыбак М.Дж. Влияние линезолида, пенициллина и клиндамицина по отдельности и в комбинации на высвобождение стрептококкового пирогенного экзотоксина. Антимикробные агенты Chemother 2003; 47 (5): 1752-1755.
- Richter SS, Heilmann KP, Dohrn CL, Beekmann SE, Riahi F, Garcia-de-Lomas J, Ferech M, Goossens H, Doern GV. Повышение устойчивости Streptococcus pyogenes к телитромицину в европе. Журнал Antimicrob Chemother 2008; 61 (3): 603-611.
- Mazzariol A, Koncan R, Bahar G, Cornaglia G.Чувствительность Streptococcus pyogenes и Streptococcus pneumoniae к макролидам и телитромицину: данные итальянского многоцентрового исследования. J. Chemother 2007; 19 (5): 500-507.
- Центры по контролю и профилактике заболеваний. 2009. Отчет об активном базовом эпиднадзоре за бактериальными инфекциями, сеть программ новых инфекций, группа стрептококков, 2008 г. Доступно по адресу: http://www.cdc.gov/abcs/reports-findings/survreports/gas08.pdf.
- Секи М., Сайто М., Иида К., Таниай Х., Соедзима Т., Накаяма Х., Йошида С.Начало синдрома токсического шока, вызванного стрептококками, ускоряется у мышей из-за синяков. Microb Pathog 2008; 44 (4): 339-343.
- Стивенс DL. Инвазивная группа стрептококковых инфекций. Clin Infect Dis 1992; 14 (1): 2-11.
- Mehta S, McGeer A, Low DE, Hallett D, Bowman DJ, Grossman SL, Stewart TE. Заболеваемость и смертность пациентов с инвазивной стрептококковой инфекцией группы А, поступивших в ВИК. Сундук 2006; 130 (6): 1679-1686.
- Burkert T, Watanakunakorn C. Группа стрептококкового эндокардита: отчет о пяти случаях и обзор литературы.J. Infect 1991; 23 (3): 307-316.
- Basma H, Norrby-Teglund A, Guedez Y, McGeer A, Low DE, El-Ahmedy O, Schwartz B, Kotb M. Факторы риска в патогенезе инвазивных стрептококковых инфекций группы a: роль защитного гуморального иммунитета. Инфекция иммунной 1999; 67 (4): 1871-1877.
- Basma H, Norrby-Teglund A, McGeer A, Low DE, El-Ahmedy O, Dale JB, Schwartz B, Kotb M. Опсонические антитела к поверхностному белку m стрептококков группы А в объединенных нормальных иммуноглобулинах (ivig): потенциальные влияние на клиническую эффективность терапии ivig для тяжелой инвазивной группы стрептококковых инфекций.Инфекция Иммун 1998; 66 (5): 2279-2283.
- Барри В., Хаджинс Л., Донта СТ, Пезанти ЭЛ. Внутривенная иммуноглобулинотерапия при синдроме токсического шока. Джама 1992; 267 (24): 3315-3316.
- Ламот Ф., Д’Амико П., Гон П., Тремблей С., Брейди Дж., Патенауд СП. Клиническая полезность внутривенных иммуноглобулинов человека при инвазивной группе стрептококковых инфекций: отчет о клиническом случае и обзор. Clin Infect Dis 1995; 21 (6): 1469-1470.
- Каул Р., МакГир А., Норрби-Теглунд А., Котб М., Шварц Б., О’Рурк К., Талбот Дж., Низкий DE.Внутривенная иммуноглобулинотерапия при синдроме токсического шока стрептококка — сравнительное обсервационное исследование.


 В дальнейшем возможно воспаление внутренних органов, развитие пневмонии, сердечной недостаточности, кишечной непроходимости.
В дальнейшем возможно воспаление внутренних органов, развитие пневмонии, сердечной недостаточности, кишечной непроходимости.
 Появляется постоянное ощущение усталости и слабости.
Появляется постоянное ощущение усталости и слабости.


 M. Vanhoenacker · M. Maas · J. L. Gielen (Eds.) 2007 Springer-Verlag Berlin Heidelberg https://b-ok.asia/book/2199119/2c16d5
M. Vanhoenacker · M. Maas · J. L. Gielen (Eds.) 2007 Springer-Verlag Berlin Heidelberg https://b-ok.asia/book/2199119/2c16d5
 «Беларусь»,1990 год. – 607 стр.
«Беларусь»,1990 год. – 607 стр.