Дефект межпредсердной перегородки — причины, симптомы, диагностика и лечение
Дефект межпредсердной перегородки – врожденная аномалия сердца, характеризующаяся наличием открытого сообщения между правым и левым предсердиями. Дефект межпредсердной перегородки проявляется одышкой, повышенной утомляемостью, отставанием в физическом развитии, сердцебиением, бледностью кожи, шумами в сердце, наличием «сердечного горба», частыми респираторными заболеваниями. Дефект межпредсердной перегородки диагностируется с учетом данных ЭКГ, ФКГ, ЭхоКС, катетеризации полостей сердца, атриографии, ангиопульмонографии. При дефекте межпредсердной перегородки производится его ушивание, пластика или рентгенэндоваскулярная окклюзия.
Общие сведения
Дефект межпредсердной перегородки
Причины дефекта межпредсердной перегородки
Формирование дефекта связано с недоразвитием первичной или вторичной межпредсердной перегородки и эндокардиальных валиков в эмбриональном периоде. К нарушению органогенеза могут приводить генетические, физические, экологические и инфекционные факторы.
К нарушению органогенеза могут приводить генетические, физические, экологические и инфекционные факторы.
Риск развития дефекта межпредсердной перегородки у будущего ребенка существенно выше в тех семьях, где есть родственники с врожденными пороками сердца. Описаны случаи семейных дефектов межпредсердной перегородки в сочетании с атриовентрикулярной блокадой или с недоразвитием костей кисти (синдромом Холта-Орама).
Кроме наследственной обусловленности, к возникновению дефекта межпредсердной перегородки, могут приводить вирусные заболевания беременной (краснуха, ветряная оспа, герпес, сифилис и др.), сахарный диабет и другие эндокринопатии, прием некоторых медикаментов и алкоголя во время беременности, производственные вредности, ионизирующая радиация, гестационные осложнения (токсикозы, угроза выкидыша и др.).
Особенности гемодинамики при дефекте межпредсердной перегородки
В силу разницы давления в левом и правом предсердиях, при дефекте межпредсердной перегородки происходит артериовенозное шунтирование крови слева направо. Величина сброса крови зависит от размеров межпредсердного сообщения, соотношения сопротивления атриовентрикулярных отверстий, пластического сопротивления и объема заполнения желудочков сердца.
Величина сброса крови зависит от размеров межпредсердного сообщения, соотношения сопротивления атриовентрикулярных отверстий, пластического сопротивления и объема заполнения желудочков сердца.
Лево-правое шунтирование крови сопровождается увеличением наполняемости малого круга кровообращения, возрастанием объемной нагрузки правого предсердия и усилением работы правого желудочка. Ввиду несоответствия между площадью клапанного отверстия легочной артерии и объемом выброса из правого желудочка, происходит развитие относительного стеноза легочной артерии.
Длительная гиперволемия малого круга кровообращения постепенно приводит к развитию легочной гипертензии. Это наблюдается только тогда, когда легочный кровоток превышает норму в 3 и более раза. Легочная гипертензия при дефекте межпредсердной перегородки обычно развивается у детей старше 15 лет, при поздних склеротических изменениях легочных сосудов. Тяжелая легочная гипертензия вызывает правожелудочковую недостаточность и смену шунта, что проявляется вначале транзиторным веноартериальным сбросом (при физической нагрузке, натуживании, кашле и др. ), а затем и стойким, сопровождающимся постоянным цианозом в покое (синдром Эйзенменгера).
), а затем и стойким, сопровождающимся постоянным цианозом в покое (синдром Эйзенменгера).
Классификация дефектов межпредсердной перегородки
Дефекты межпредсердной перегородки различаются по количеству, размерам и расположению отверстий.
С учетом степени и характера недоразвития первичной и вторичной межпредсердных перегородок соответственно выделяют первичные, вторичные дефекты, а также полное отсутствие межпредсердной перегородки, обусловливающее общее, единственное предсердие (трехкамерное сердце).
К первичным ДМПП относят случаи недоразвития первичной межпредсердной перегородки с сохранением первичного межпредсердного сообщения. В большинстве случаев они сочетаются с расщеплением створок двух- и трехстворчатого клапанов, открытым атриовентрикулярным каналом. Первичный дефект межпредсердной перегородки, как правило, характеризуется большим размером (3-5 см) и локализуется в нижней части перегородки над предсердно-желудочковыми клапанами и не имеет нижнего края.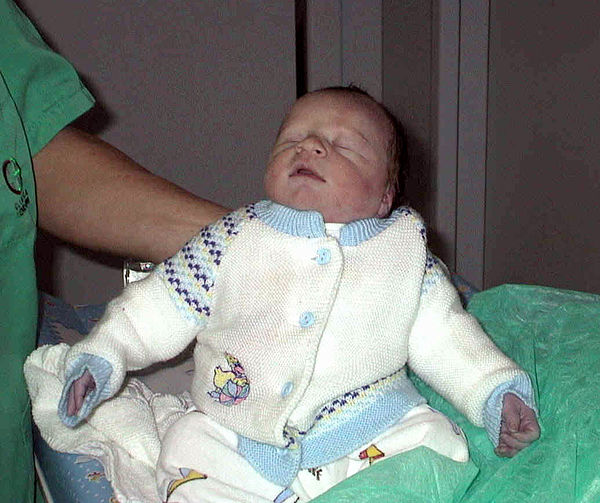
Вторичные ДМПП образованы недоразвитием вторичной перегородки. Обычно они имеют небольшие размеры (1-2 см) и располагаются в центре межпредсердной перегородки или в области устьев полых вен. Вторичные дефекты межпредсердной перегородки часто сочетаются с аномальным впадением легочных вен в правое предсердие. При этом типе порока межпредсердная перегородка сохранена в своей нижней части.
Встречаются комбинированные дефекты межпредсердной перегородки (первичный и вторичный, ДМПП в сочетании с дефектом венозного синуса). Также дефект межпредсердной перегородки может входить в структуру сложных ВПС (триады и пентады Фалло) или сочетаться с тяжелыми сердечными пороками — аномалией Эбштейна, гипоплазией камер сердца, транспозицией магистральных сосудов.
Формирование общего (единственного) предсердия связано с недоразвитием или полным отсутствием первичной и вторичной перегородок и наличием большого дефекта, занимающего площадь всей межпредсердной перегородки.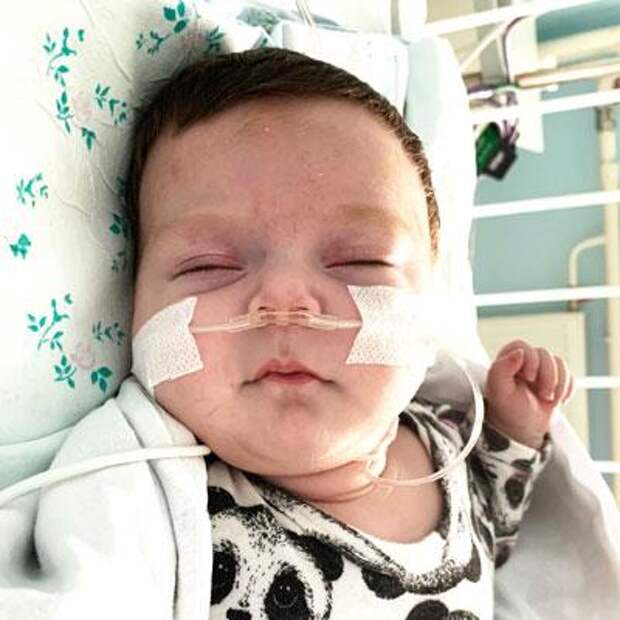 Структура стенок и оба предсердных ушка при этом сохранены. Трехкамерное сердце может сочетаться с аномалиями атриовентрикулярных клапанов, а также с аспленией.
Структура стенок и оба предсердных ушка при этом сохранены. Трехкамерное сердце может сочетаться с аномалиями атриовентрикулярных клапанов, а также с аспленией.
Одним из вариантов межпредсердной коммуникации является открытое овальное окно, обусловленное недоразвитием собственного клапана овального отверстия или его дефектом. Однако ввиду того, что открытое овальное отверстие не является истинным дефектом перегородки, связанным с недостаточностью ее ткани, данная аномалия не может быть причислена к дефектам межпредсердной перегородки.
Симптомы дефекта межпредсердной перегородки
Дефекты межпредсердной перегородки могут протекать с длительной гемодинамической компенсацией, а их клиника отличается значительным разнообразием. Выраженность симптоматики определяется величиной и локализацией дефекта, длительностью существования ВПС и развитием вторичных осложнений. На первом месяце жизни единственным проявлением дефекта межпредсердной перегородки обычно служит транзиторный цианоз при плаче и беспокойстве, что обычно связывается с перинатальной энцефалопатией.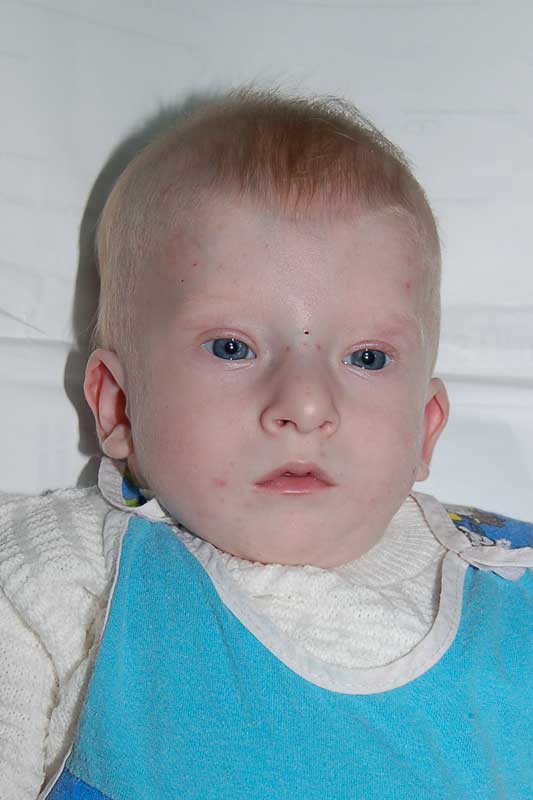
При дефектах межпредсердной перегородки средних и больших размеров симптоматика проявляется уже в первые 3-4 мес. или к концу первого года жизни и характеризуется стойкой бледностью кожных покровов, тахикардией, умеренным отставанием в физическом развитии, недостаточным приростом массы тела. Для детей с дефектами межпредсердной перегородки типично частое возникновение респираторных заболеваний — рецидивирующих бронхитов, пневмоний, протекающих с длительным влажным кашлем, стойкой одышкой, обильными влажными хрипами и др., обусловленными гиперволемией малого круга кровообращения. У детей первого десятилетия жизни отмечаются частые головокружения, склонность к обморокам, быстрая утомляемость и одышка при физической нагрузке.
Небольшие дефекты межпредсердной перегородки (до 10-15 мм) не вызывают нарушения физического развития детей и характерных жалоб, поэтому первые клинические признаки порока могут развиться лишь на втором-третьем десятилетии жизни. Легочная гипертензия и сердечная недостаточность при дефекте межпредсердной перегородки формируются примерно к 20 годам, когда возникает цианоз, аритмии, редко – кровохарканье.
Легочная гипертензия и сердечная недостаточность при дефекте межпредсердной перегородки формируются примерно к 20 годам, когда возникает цианоз, аритмии, редко – кровохарканье.
Диагностика дефекта межпредсердной перегородки
При объективном обследовании пациента с дефектом межпредсердной перегородки выявляется бледность кожных покровов, «сердечный горб», умеренное отставание в росте и весе. Перкуторно определяется увеличение границ сердца влево и вправо; при аускультации слева от грудины во II-III межреберьях выслушивается умеренно интенсивный систолический шум, который в отличие от дефекта межжелудочковой перегородки или стеноза легочной артерии, никогда не бывает грубым. Над легочной артерией выявляется расщепление II тона и акцентирование его легочного компонента. Аускультативные данные подтверждаются при проведении фонокардиографии.
При вторичных дефектах межпредсердной перегородки ЭКГ-изменения отражают перегрузку правых отделов сердца.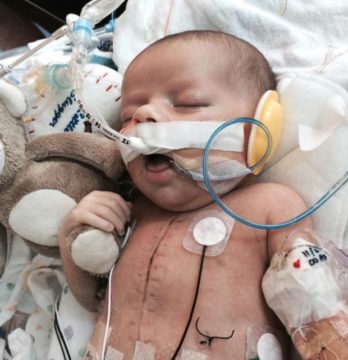 Могут регистрироваться неполная блокада правой ножки пучка Гиса, АВ-блокады, синдром слабости синусового узла. Рентгенография органов грудной клетки позволяет увидеть усиление легочного рисунка, выбухание ствола легочной артерии, увеличение тени сердца вследствие гипертрофии правого предсердия и желудочка. При рентгеноскопии обнаруживается специфичный признак дефекта межпредсердной перегородки — усиленная пульсация корней легких.
Могут регистрироваться неполная блокада правой ножки пучка Гиса, АВ-блокады, синдром слабости синусового узла. Рентгенография органов грудной клетки позволяет увидеть усиление легочного рисунка, выбухание ствола легочной артерии, увеличение тени сердца вследствие гипертрофии правого предсердия и желудочка. При рентгеноскопии обнаруживается специфичный признак дефекта межпредсердной перегородки — усиленная пульсация корней легких.
ЭхоКГ-исследование с цветным допплеровским картированием выявляет лево-правый сброс крови, наличие дефекта межпредсердной перегородки, позволяет определить его величину и локализацию. При зондировании полостей сердца обнаруживается повышение давления и насыщения крови кислородом в правых отделах сердца и легочной артерии. В случае диагностических трудностей обследование дополняется атриографией, вентрикулографией, флебографией яремных вен, ангиопульмонографией, МРТ сердца.
Дефект межпредсердной перегородки следует дифференцировать от дефекта межжелудочковой перегородки, открытого артериального протока, митральной недостаточности, изолированного стеноза легочной артерии, триады Фалло, аномального впадения легочных вен в правое предсердие.
Лечение дефекта межпредсердной перегородки
Лечение дефектов межпредсердной перегородки только хирургическое. Показаниями к кардиохирургической операции служит выявление гемодинамически значимого артериовенозного сброса крови. Оптимальный возраст для коррекции порока у детей — от 1 до 12 лет. Хирургическое лечение противопоказано при высокой легочной гипертензии с веноартериальным сбросом крови, обусловленной склеротическими изменениями легочных сосудов.
При дефектах межпредсердной перегородки прибегают к различным способам их закрытия: ушиванию, пластике с помощью перикардиального лоскута или синтетической заплаты в условиях гипотермии и ИК. Рентгенэндоваскулярная окклюзия дефекта межпредсердной перегородки позволяет закрывать отверстия не более 20 мм.
Хирургическая коррекция дефектов межпредсердной перегородки сопровождается хорошими отдаленными результатами: у 80-90% больных отмечается нормализации гемодинамики и отсутствие жалоб.
Прогноз дефекта межпредсердной перегородки
Малые дефекты межпредсердной перегородки совместимы с жизнью и могут обнаруживаться даже в пожилом возрасте. У некоторых больных с небольшим дефектом межпредсердной перегородки возможно спонтанное закрытие отверстия в течение первых 5-ти лет жизни. Продолжительность жизни лиц с большими дефектами межпредсердной перегородки при естественном течении порока составляет в среднем 35-40 лет. Гибель пациентов может наступить от правожелудочковой сердечной недостаточности, нарушений ритма и проводимости сердца (пароксизмальной тахикардии, мерцательной аритмии и др.), реже — от легочной гипертензии высокой степени.
Пациенты с дефектами межпредсердной перегородки (оперированные и неоперированные) должны находиться под наблюдением кардиолога и кардиохирурга.
Порок сердца у новорожденных: причины, диагностика, лечение
Врожденные пороки сердца (ВПС) — это анатомические дефекты в сердце и его сосудах, возникшие еще до рождения ребенка. Порок сердца у новорожденных — довольно распространенная патология, которая без лечения может привести к смерти, поэтому родителям необходимо знать признаки болезни сердца и вовремя обращаться за помощью, если они заметили их у своего ребенка.
Порок сердца у новорожденных — довольно распространенная патология, которая без лечения может привести к смерти, поэтому родителям необходимо знать признаки болезни сердца и вовремя обращаться за помощью, если они заметили их у своего ребенка.
Причины ВПС
К сожалению, никогда нельзя установить точную причину в каждом конкретном случае, однако существует множество предрасполагающих факторов:
- Генетические факторы — сюда входят различные хромосомные аномалии и мутации генов;
- Экологические факторы — на развитие плода и его органов отрицательно сказывается загрязнение окружающей среды;
- Наследственность;
- Прием некоторых лекарств во время беременности;
- Возраст родителей;
- Внутриутробная инфекция;
- Такие заболевания матери, как краснуха, сахарных диабет, тяжелый токсикоз и др.;
- Вредные привычки — особенно опасны в первом триместре беременности, когда закладываются и формируются основные органы.

Классифицируют ВПС у новорожденных по-разному. Одна из самых популярных классификаций делит пороки на «белые» и «синие».
Белые пороки
- Дефект межжелудочковой перегородки (ДМЖП)
В норме желудочки сердца разделены сплошной перегородкой. Если она не формируется до конца, в ней возникает один или несколько дефектов (отверстий), через которые смешивается артериальная и венозная кровь. Ткани и органы получают меньше кислорода и питательных веществ, что, в итоге, влияет на общее состояние младенца. Самочувствие еще зависит от того, сколько отверстий в перегородке, какой они величины и где расположены. Если крови смешивается мало, то развитие ребёнка не страдает, и порок можно выявить лишь во время обследования. Если отверстий в перегородке много и они большие, то появляется одышка, кожа приобретает бледный оттенок, ребенок сильно потеет. Эти проявления усиливаются, когда он плачет, сосет грудь, а иногда даже просто меняет положение тела.
- Дефект межпредсердной перегородки (ДМПП)
Кровообращение плода отличается от взрослого: кислород и питательные вещества он получает из крови матери через плаценту.
- Коарктация аорты
В данном случае происходит сужение просвета аорты, через который крови труднее покидать сердце, поэтому, чтобы ее выбрасывалось достаточно, желудочек вынужден работать с повышенной нагрузкой, что отрицательно сказывается на нем. Давление в верхней половине тела отличается от нижней: сверху оно повышено, снизу — понижено. У новорожденных и грудничков сердечная недостаточность и постоянная гипертония верхней части тела бывают настолько сильными, что угрожают необратимой травмой сосудов мозга, поэтому требуется хирургическое лечение.
- Стеноз устья аорты
Этот порок сердца у ребенка возникает, когда сужается клапан аорты. Через небольшое отверстие крови труднее покидать левый желудочек. Если стеноз небольшой, сначала симптомы могут не проявляться, и родители даже не подозревают о болезни ребенка. Если сужение большое, малыш тяжело дышит, его сердце бьется чаще. Иногда дети постарше могут жаловаться на приступы удушья и даже терять сознание.
- Открытый артериальный проток
До рождения ребенка кровь из его легочной артерии поступает в аорту по специальному сосуду, который называется артериальным протоком. Затем он закрывается. Если же остается открытым, то часть крови возвращается по нему обратно. Главные признаки порока, которые могут заметить родители — это бледная кожа, ребенку тяжело сосать грудь, он плохо растет и набирает вес.
- Стеноз легочной артерии
Это сужение легочной артерии в любом ее месте. Крови сложно проходить препятствие по такому сосуду, поэтому возникают симптомы сердечной недостаточности. Кроме них, при осмотре новорожденного можно заметить пульсацию вен на шее.
Кроме них, при осмотре новорожденного можно заметить пульсацию вен на шее.
Синие пороки
- Тетрада Фалло
Она включает в себя четыре дефекта:
- Стеноз легочной артерии;
- Дефект межжелудочковой перегородки;
- Смещение аорты вправо;
- Утолщение стенок правого желудочка.
Поскольку изменений много, болезнь проявляется рано. Губы ребенка начинают синеть уже в 3-4 месяца. Цианоз становится постоянным ближе к году. После активных игр малыш стремится сесть на корточки, поскольку так сердцу легче справиться с повышенной нагрузкой.
- Атрезия трехстворчатого клапана
Иногда вместо трехстворчатого клапана образуется плотная перегородка, через которую кровь течь не может. Она вынуждена через дефекты в сердце искать себе другой путь и в итоге попадает в аорту или легочную артерию.
- Аномальное впадение легочных вен
Этот порок сердца у детей возникает тогда, когда легочные вены соединяются с сосудами, идущими в правое предсердие, или же впадают непосредственно в него. Поскольку болезнь тяжелая, ее признаки проявляются очень рано, хотя цианоз кожи сначала можно и не увидеть. Однако постепенно он нарастает и становится заметным.
Поскольку болезнь тяжелая, ее признаки проявляются очень рано, хотя цианоз кожи сначала можно и не увидеть. Однако постепенно он нарастает и становится заметным.
- Транспозиция крупных сосудов
Врождённый порок, при котором круги кровообращения не соединяются друг с другом. Аорта и легочная артерия меняются местами, поэтому артериальная кровь снова попадает в легкие, а венозная течет к тканям и органам. Ребенок может жить, пока открыто овальное окно, но если оно закрывается, круги кровообращения больше не пересекаются и жизнь становится невозможной. Без лечения смерть наступает рано.
- Общий артериальный ствол
Артериальный ствол — это единый сосуд, по которому кровь поступает в оба круга кровообращения. Поскольку он один, кровь не может правильно разделяться и смешивается в нем. К обычным симптомам сердечной недостаточности добавляется увеличение печени и селезенки.
К МАРС-синдрому («малые аномалии развития сердца») относят пролапс митрального клапана, ложные хорды в левом желудочке и другие аномалии развития внешнего и внутреннего строения сердца. МАРС часто ставят детям, однако не стоит пугаться: он обычно протекает медленно, и симптомы исчезают уже к пяти годам. Подобные нарушения чаще всего не влияют на рост ребенка и работу его сердца.
МАРС часто ставят детям, однако не стоит пугаться: он обычно протекает медленно, и симптомы исчезают уже к пяти годам. Подобные нарушения чаще всего не влияют на рост ребенка и работу его сердца.
Общие симптомы ВПС
У всех пороков, как и у любых заболеваний, которые нарушают работу какого-то одного органа, есть общие симптомы. Их проявление зависит от тяжести заболевания и характера дефекта:
- Одышка, которая особенно заметна при кормлении ребенка, плаче и других физических нагрузках;
- Бледность или цианоз кожи — зависит от типа ВПС. Сперва ее можно заметить на губах и возле носа, а затем она распространяется дальше;
- Вялость, быстрая утомляемость;
- Ребенок плохо растет;
- Увеличение или уменьшение числа сердечных сокращений;
- Потливость;
- Медленная прибавка в весе.
Диагностика
Диагностика ВПС включает в себя следующие пункты:
- Сбор полного анамнеза — материнского, наследственного, семейного;
- Объективное обследование — осмотр, выявление типичных внешних признаков, подсчет пульса, дыхания, прослушивание шумов в сердце, определение размеров печени, селезенки;
- Лабораторное обследование — клинический и биохимический анализ крови;
- Инструментальное обследование — пульсоксиметрия, измерение артериального давления, ЭКГ, ЭХО-КГ, рентген грудной клетки;
- При необходимости проводят ангиографию и зондирование сердца.

Лечение
Когда выявляется врожденный порок сердца у младенцев, такие дети в обязательном порядке наблюдаются не только педиатром, но и кардиологом. Лечение может быть терапевтическим или хирургическим с максимальным устранением дефекта. Лекарства назначают до операции, чтобы правильно подготовить ребенка к ней, и после, чтобы организм быстрее восстановился. Иногда их приходится принимать постоянно.
Кроме медикаментозного лечения родители должны создавать детям с ВПС правильные условия для развития. Нужно увеличить число кормлений, уменьшая количество пищи на каждый прием, чтобы ребенок не так уставал. Он будет получать необходимую пищу, успевая отдыхать при этом. Рекомендуется почаще гулять на улице, но ограничивать физическую нагрузку в зависимости от тяжести заболевания. Сердце должно успевать справляться со своей работой. Поскольку дети с такими заболеваниями больше подвержены простудам и тяжелее их переносят, необходима правильная их профилактика.
При своевременно оказанном лечении и обеспечении необходимых условий жизни прогноз для большинства детей благоприятный, они могут нормально развиваться, расти и вести практически полноценную жизнь.
Профилактика ВПС
Поскольку известно много факторов, предрасполагающих к рождению детей с пороками сердца, важно проводить правильную их профилактику. Женщина, планирующая беременность, должна отказаться от вредных привычек, ведь никотин и алкоголь пагубно сказываются на развитии плода.
Вовремя сделанная прививка от краснухи убережет беременную от заболевания, а значит, и плод от аномалий. Принимать любые лекарства следует с осторожностью, ведь не только сильнодействующие препараты могут влиять на развитие будущего ребенка. Даже некоторые витамины и лекарства, отпускающиеся без рецепта, запрещены во время беременности. Стоит тщательно изучить инструкцию, а еще лучше – посоветоваться с врачом.
Особенное внимание нужно уделить правильному ведению беременности: вовремя посещать врача, принимать назначенные препараты и проходить все необходимые процедуры. Иногда пороки сердца выявляются еще до рождения ребенка.
youtube.com/embed/Qv6Kre097y8″ frameborder=»0″ allowfullscreen=»allowfullscreen»/>
Порок сердца: врожденный порок сердца у новорожденного, приобретенный порок сердца у взрослых
Закрыть- Болезни
- Инфекционные и паразитарные болезни
- Новообразования
- Болезни крови и кроветворных органов
- Болезни эндокринной системы
- Психические расстройства
- Болезни нервной системы
- Болезни глаза
- Болезни уха
- Болезни системы кровообращения
- Болезни органов дыхания
- Болезни органов пищеварения
- Болезни кожи
- Болезни костно-мышечной системы
- Болезни мочеполовой системы
- Беременность и роды
- Болезни плода и новорожденного
- Врожденные аномалии (пороки развития)
- Травмы и отравления
- Симптомы
- Системы кровообращения и дыхания
- Система пищеварения и брюшная полость
- Кожа и подкожная клетчатка
- Нервная и костно-мышечная системы
- Мочевая система
- Восприятие и поведение
- Речь и голос
- Общие симптомы и признаки
- Отклонения от нормы
- Диеты
- Снижение веса
- Лечебные
- Быстрые
- Для красоты и здоровья
- Разгрузочные дни
- От профессионалов
- Монодиеты
- Звездные
- На кашах
- Овощные
- Детокс-диеты
- Фруктовые
- Модные
- Для мужчин
- Набор веса
- Вегетарианство
- Национальные
- Лекарства
- Пищеварительный тракт и обмен веществ
- Кровь и система кроветворения
- Сердечно-сосудистая система
- Дерматологические препараты
- Mочеполовая система и половые гормоны
- Гормональные препараты
- Противомикробные препараты
- Противоопухолевые препараты и иммуномодуляторы
- Костно-мышечная система
- Нервная система
- Противопаразитарные препараты, инсектициды и репелленты
- Дыхательная система
- Органы чувств
- Прочие препараты
- Врачи
- Клиники
- Справочник
- Аллергология
- Анализы и диагностика
- Беременность
- Витамины
- Вредные привычки
- Геронтология (Старение)
- Дерматология
- Дети
- Женское здоровье
- Инфекция
- Контрацепция
- Косметология
- Народная медицина
- Обзоры заболеваний
- Обзоры лекарств
- О
Врожденный порок сердца — лечение, симптомы
Краткая характеристика заболевания
Врожденный порок сердца – это анатомический дефект сердца, его сосудов, или клапанов, возникающий еще внутриутробно.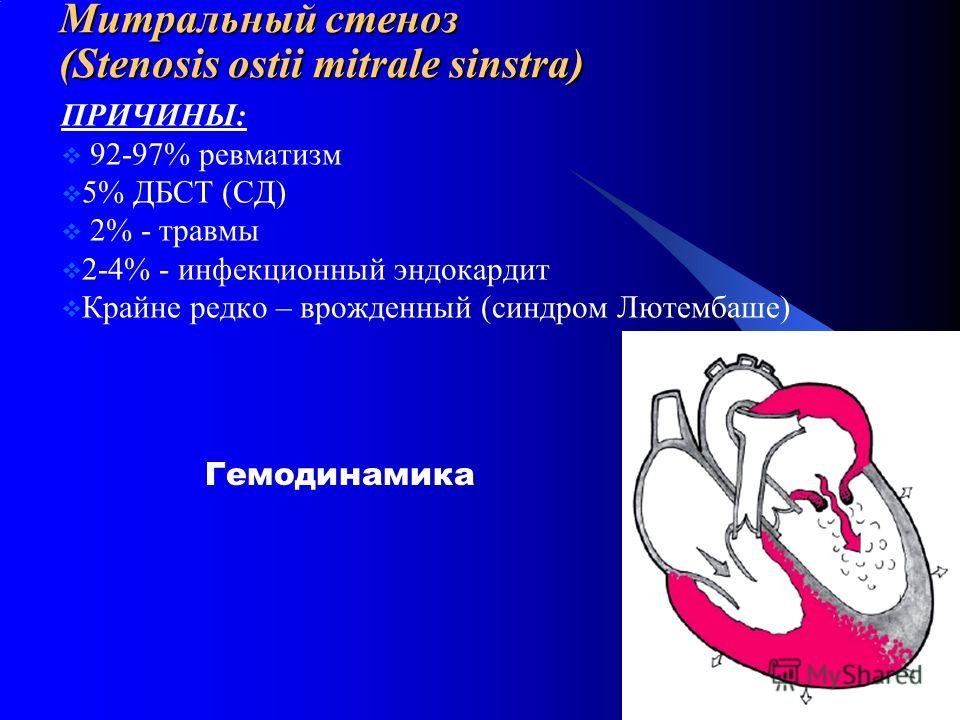
Врожденный порок сердца у детей может быть незаметен, но может проявиться сразу после рождения. В среднем это заболевание встречается в 30% случаев и занимает 1-е место среди заболеваний, вызывающих смерть новорожденных и детей до года. После года процент смертности падает, и в возрасте 1-15л. умирает порядка 5% детей.
Выделяют семь основных видов врожденного порока сердца у новорожденных: патология межжелудочковой перегородки, патология межпредсердной перегородки, аортальная коарктация, аортальный стеноз, открытый артериальный проток, транспозиция больших магистральных сосудов, стеноз легочной артерии.
Причины появления
Основные причины появления врожденного порока – это внешние воздействия на плод в 1м триместре беременности. Вызвать дефект развития сердца может вирусное заболевание матери (например, краснуха), радиационное облучение, медикаментозное воздействие, наркомания, алкоголизм матери.
Большую роль играет и здоровье отца ребенка, но при этом генетические факторы на развитие врожденного порока сердца у детей играют наименьшую роль.
Выделяют и такие факторы риска: токсикоз и угроза выкидыша в 1м триместре, наличие в прошлом беременностей, заканчивающихся рождением мертвого ребенка, наличие в семейном анамнезе детей с врожденными пороками (у ближайших родственников), эндокринные патологии обоих супругов, возраст матери.
Симптомы врожденного порока сердца
У новорожденных с врожденным пороком сердца отмечается синеватый или голубой цвет губ, ушных раковин, кожи. Также синюшность у ребенка может проявляться, когда он кричит или сосет грудь. Голубоватый цвет кожи характерен так называемым «синим порокам сердца», но есть еще и «белые врожденные пороки», при которых у ребенка наблюдаются побледнение кожи, холодные руки и ноги.
В сердце ребенка слышны шумы. Этот симптом не основной, но при его наличии следует позаботиться о дополнительном обследовании.
Известны случаи, когда порок сопровождается сердечной недостаточностью. Прогноз при этом в большинстве случаев неблагоприятный.
Анатомические патологии сердца можно увидеть на ЭКГ, эхокардиограмме, на рентгеновских снимках.
Если врожденный порок сердца сразу после рождения незаметен, ребенок может выглядеть здоровым на протяжении десяти первых лет жизни. Но после этого становится заметным отклонение в физическом развитии, проявляется синюшность или бледность кожи, при физических нагрузках появляется одышка.
Диагностика заболевания
Первичный диагноз врач ставит при осмотре ребенка и прослушивании сердца. Если есть причины подозревать врожденный порок сердца, ребенка отправляют на дообследование. Применяют различные методы диагностики, существует также возможность обследовать плод, находящийся в утробе матери.
Для обследования беременной женщины применяют фетальную эхокардиографию. Это ультразвуковая диагностика, безопасная для матери и плода, позволяющая выявить патологию и спланировать лечение врожденного порока сердца.
Эхокардиография – это еще один вид ультразвукового обследования, но уже родившегося ребенка, помогает увидеть структуру сердца, дефекты, суженные сосуды, оценить работу сердца.
Электрокардиография применяется для оценки сердечной проводимости, работы сердечной мышцы.
Для определения сердечной недостаточности применяют рентгенографию грудной клетки. Так можно увидеть избыточную жидкость в легких, расширение сердца.
Еще одним рентгенологическим методом выявления врожденного порока сердца является сосудистая катетеризация. Через бедренную артерию вводят в кровоток контраст и делают серию рентгеновских снимков. Так можно оценить структуру сердца, определить уровень давления в его камерах.
Для оценки насыщенности крови кислородом применяют пульсоксиметрию – с помощью датчика, надетого на палец ребенка, регистрируют уровень кислорода.
Лечение врожденного порока сердца
Метод лечения порока выбирают в зависимости от его типа. Так, применяют малоинвазивные процедуры с катетеризацией, открытое хирургическое вмешательство, трансплантацию, лекарственную терапию.
Катетерная техника позволяет проводить лечение врожденных пороков сердца без радикального хирургического вмешательства. Через вену на бедре вводят катетер, под рентген контролем его доводят до сердца, и подводят к месту дефекта специальные тонкие инструменты.
Через вену на бедре вводят катетер, под рентген контролем его доводят до сердца, и подводят к месту дефекта специальные тонкие инструменты.
Операцию назначают, если нет возможности использовать катетеризацию. Отличается этот метод более длительным и тяжелым периодом восстановления.
Иногда оперативное лечение врожденных пороков сердца, преимущественно в тяжелых случаях, проводят в несколько этапов.
При пороках, не подлежащих лечению, ребенку показана пересадка сердца.
Лекарственная терапия применяется зачастую для лечения взрослых, детей старшего возраста. С помощью медикаментов можно улучшить сердечную функцию, обеспечить нормальное кровоснабжение.
Профилактика заболевания
Условно профилактику врожденных пороков сердца делят на профилактику их развития, профилактику их неблагоприятного развития и профилактику осложнений.
Профилактика возникновения порока заключается больше в медико-генетическом консультировании на стадии подготовки к беременности, чем к каким-либо конкретным действиям. К примеру, следует предупреждать о нежелательности беременности у женщины, в семье которой (или в семье партнера) есть три и более человек с врожденными пороками. Не рекомендуется рожать детей семейной паре, где оба партнера страдают этим заболеванием. Тщательно обследоваться должна женщина, которая перенесла краснуху.
К примеру, следует предупреждать о нежелательности беременности у женщины, в семье которой (или в семье партнера) есть три и более человек с врожденными пороками. Не рекомендуется рожать детей семейной паре, где оба партнера страдают этим заболеванием. Тщательно обследоваться должна женщина, которая перенесла краснуху.
Для предупреждения неблагоприятного развития заболевания необходимо вовремя провести необходимые диагностические процедуры, подобрать и провести оптимальное лечение для коррекции состояния. За ребенком с врожденным пороком и перенесшим его лечение нужен тщательный особый уход. Зачастую смертность детей с врожденным пороком в возрасте до года связана с недостаточным уходом за ребенком.
Для профилактики осложнений заболевания следует заняться предупреждением непосредственно этих осложнений.
Из-за врожденного порока сердца может возникнуть: бактериальный эндокардит, полицитемия («сгущение крови»), вызывающее тромбоз, головные боли, воспаление периферических сосудов, тромбоэмболии сосудов мозга, респираторные заболевания, осложнения со стороны легких и их сосудов.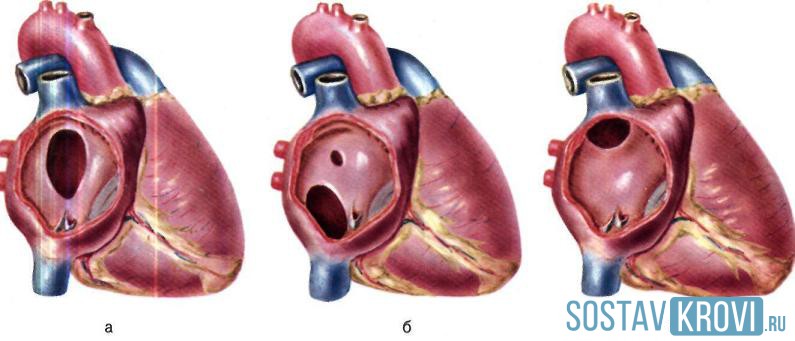
Видео с YouTube по теме статьи:
симптомы, сколько с ним живут?
Порок сердца: что это такое?
Порок сердца – это изменения анатомических структур сердца (камер, клапанов, перегородок) и отходящих от него сосудов, которые приводят к нарушению гемодинамики. Все пороки сердца делятся на две группы: врожденные и приобретенные. В детском возрасте выявляются, как правило, врожденные пороки сердца (ВПС). Они бывают двух типов:
- «Синие», при которых венозная кровь попадает в артерии, поэтому кожа приобретает синюшный оттенок. Эта группа ВПС является наиболее опасной, поскольку органы и ткани ребенка из-за смешивания артериальной и насыщенной углекислым газом венозной крови недополучают кислород. Наиболее часто встречающиеся «синие» ВПС – атрезия легочной артерии, тетрада Фало, транспозиция сосудов.

- «Белые», характеризующиеся сбросом крови в правые отделы сердца и бледностью кожи. Пороки этого типа легче переносятся больными, но со временем они приводят к развитию сердечной недостаточности и появлению проблем с легкими. Примеры – дефект межпредсердной перегородки, открытый артериальный проток и пр.
Причины
Врожденный порок сердца у детей развивается еще в утробе матери, причем происходит это тогда, когда формируется сердце – на протяжении первых 2 месяцев беременности. Если в этот период на женский организм влияют негативные факторы, риск возникновения ВПС у ребенка значительно возрастает. К факторам, приводящим к развитию порока сердца у плода, относят:
- Алкоголь, никотин, наркотики.
- Радиацию.
- Некоторые лекарственные средства (в том числе сульфаниламиды, аспирин, антибиотики).
- Вирус краснухи.
- Неблагоприятную экологию.
Помимо этого, большую роль в формировании пороков сердца играет генетика. Мутация определенных генов вызывает нарушение синтеза белков, из которых образуются перегородки сердца. Генетические мутации могут передаваться по наследству, а могут появляться из-за употребления женщиной наркотических веществ, алкоголя, влияния радиации и т.д.
Мутация определенных генов вызывает нарушение синтеза белков, из которых образуются перегородки сердца. Генетические мутации могут передаваться по наследству, а могут появляться из-за употребления женщиной наркотических веществ, алкоголя, влияния радиации и т.д.
Как определить порок сердца?
Диагностировать порок сердца опытный врач ультразвуковой диагностики может еще внутриутробно. Поэтому гинекологи настоятельно рекомендуют всем будущим мамам проходить плановые УЗИ. Внутриутробное выявление серьезных ВПС у плода дает женщине право выбора: рожать или не рожать тяжело больного ребенка. Если же женщина захочет вынашивать беременность до конца – организовать роды таким образом, чтобы новорожденному сразу же была оказана необходимая медицинская помощь (как правило, это реанимационные мероприятия) и в кратчайшие сроки была проведена операция.
Нередко случается так, что внутриутробно пороки сердца не выявляются, ребенок рождается, на первый взгляд, совершенно здоровым, а проблемы возникают уже позже. Поэтому для того чтобы не пропустить ВПС, не допустить прогрессирование патологии и развитие осложнений, каждого новорожденного тщательно обследуют в роддоме. Первое, что указывает на возможный порок – это шум, определяемый при выслушивании сердца. Если подобное обнаруживается, ребенка сразу же направляют в специализированную клинику для дальнейшего обследования (проведения ЭхоКГ, ЭКГ и других исследований).
Поэтому для того чтобы не пропустить ВПС, не допустить прогрессирование патологии и развитие осложнений, каждого новорожденного тщательно обследуют в роддоме. Первое, что указывает на возможный порок – это шум, определяемый при выслушивании сердца. Если подобное обнаруживается, ребенка сразу же направляют в специализированную клинику для дальнейшего обследования (проведения ЭхоКГ, ЭКГ и других исследований).
Однако обнаружить у новорожденного порок сердца в первые дни жизни удается не всегда (шумы могут попросту не выслушиваться), поэтому родителям важно знать, какие симптомы указывают на то, что с сердцем ребенка что-то не в порядке, чтобы своевременно обратиться к врачу. К таким признакам относят следующие:
- Бледность или синюшность кожи (особенно вокруг губ, на ручках, на пяточках).
- Плохую прибавку массы.
- Вялое сосание, частые передышки во время кормления.
- Учащенное сердцебиение (норма у новорожденных – 150 – 160 удпров в минуту).
При некоторых ВПС выраженные симптомы патологии появляются не на первом году жизни, а позже. В таких случаях заподозрить наличие патологии сердца можно по следующим признакам:
В таких случаях заподозрить наличие патологии сердца можно по следующим признакам:
- Отставанию от сверстников в физическом развитии.
- Одышке при физических нагрузках.
- Жалобам ребенка на головные боли, головокружение.
- Периодическим обморокам.
- Частым простудным заболеваниям, осложняющимся затяжными бронхитами и воспалениями легких.
Помимо этого, родители должны регулярно водить ребенка к педиатру или семейному доктору (в первый год жизни – каждый месяц, в последующем – ежегодно), поскольку только врач может услышать шумы в сердце и заметить то, на что не обращают внимания папы и мамы.
Если же в семье кто-то имеет ВПС или же беременность протекала на фоне отягощающих факторов (эндокринных и аутоиммунных болезней женщины, сильного токсикоза, угрозы прерывания беременности, инфекционных заболеваний, приема лекарственных средств, курения и злоупотребления спиртным и т.д.), ребенку желательно обследовать сердце с помощью ЭхоКГ даже при отсутствии каких-либо патологических симптомов.
Лечение и прогноз
Подход к лечению ВПС всегда индивидуальный. Одним пациентам операция проводится сразу же после рождения, другим – после полугода, а третьих врачи лечат консервативно, без каких-либо хирургических вмешательств. К врожденным порокам, которые хорошо переносятся больными и не всегда требуют хирургической коррекции (поскольку нередко самопроизвольно закрываются), относят следующие:
- Небольшие дефекты перегородок между желудочками и предсердиями.
- Открытый артериальный проток.
- Незначительные деформации сердечных клапанов.
Прогноз при этих ВПС обычно благоприятный, даже если требуется хирургическое лечение.
Намного хуже обстоит ситуация с большинством «синих» пороков. Эти пороки – более сложные и более опасные. К самым тяжелым ВПС относят:
- Транспозицию (смену мест) аорты и легочной артерии.
- Отхождение и аорты, и легочной артерии от правого желудочка.
- Тетраду Фало (включает сразу 4 аномалии развития сердца и магистральных сосудов).

- Грубые дефекты клапанов.
- Гипоплазию (недоразвитость) отделов сердца. Особенно опасным пороком является недоразвитость левых отделов. На вопрос о том, сколько с ним живут, можно ответить статистическими данными – при таком пороке отмечается практически 100% летальность.
- Атрезию (заращение) легочной артерии.
При грубых ВПС стремительно нарастает сердечная недостаточность, дети сразу же после рождения переходят в очень тяжелое состояние, требующее немедленного хирургического вмешательства. Успех такого лечения напрямую зависит от того, насколько оперативно новорожденный доставлен в специализированную кардиохирургическую клинику и как правильно выбрана лечебная тактика. Соблюдение этих двух условий возможно только в одном случае – если порок выявлен до рождения ребенка. Внутриутробная диагностика ВПС дает возможность врачам всех звеньев (и акушерам-гинекологам, и кардиохирургам) подготовиться к предстоящим родам и спланировать хирургическое вмешательство на сердце новорожденного.
Синдром Германского – Пудлака
Синдром Германского – Пудлака (HPS) — редкое аутосомно-рецессивное заболевание [1] , которое приводит к кожному альбинизму (снижению пигментации), проблемам с кровотечением из-за аномалии тромбоцитов (дефект пула накопления тромбоцитов) и накопление аномального жирно-белкового соединения (лизосомное накопление цероидного липофусцина).
Существует восемь классических форм заболевания, основанных на генетической мутации, из которой возникло заболевание. [2] Также был описан девятый тип. [3] Этот последний тип возникает из-за мутации в гене Паллидина (PLDN).
Прогноз
Течение HPS было легким в редких случаях заболевания, [4] , однако общий прогноз все еще считается плохим.
Заболевание может вызывать нарушение функции легких, кишечника, почек или сердца. Основным осложнением большинства форм заболевания является фиброз легких, который обычно проявляется у пациентов в возрасте от 40 до 50 лет. [5] Это фатальное осложнение, наблюдаемое при многих формах HPS, и является обычной причиной смерти от этого расстройства. [6]
Основным осложнением большинства форм заболевания является фиброз легких, который обычно проявляется у пациентов в возрасте от 40 до 50 лет. [5] Это фатальное осложнение, наблюдаемое при многих формах HPS, и является обычной причиной смерти от этого расстройства. [6]
Заболевание чаще встречается в Пуэрто-Рико, [7] , где были проведены многие клинические исследования этого заболевания.
Диагностика
Диагноз ГФС устанавливается на основании клинических данных о гипопигментации кожи и волос, характерных глазных симптомов и демонстрации отсутствия плотных тел при электронной микроскопии тромбоцитов на всем держателе.Молекулярно-генетическое тестирование гена HPS1 доступно на клинической основе людям из северо-западного Пуэрто-Рико. Молекулярное тестирование гена HPS3 доступно на клинической основе для лиц центрального пуэрториканского или еврейского происхождения ашкенази. Анализ последовательности доступен на клинической основе для мутаций в HPS1 и HPS4. Диагностика людей с другими типами HPS доступна только на исследовательской основе. [8]
Диагностика людей с другими типами HPS доступна только на исследовательской основе. [8]
Причины
HPS может быть вызвано мутациями в нескольких генах: HPS1, HPS3, HPS4, HPS5, HPS6 и HPS7.
HPS типа 2, фенотип которого включает иммунодефицит, вызван мутацией в гене AP3B1.
HPS типа 7 может быть результатом мутации в гене, кодирующем белок дисбиндин. [9]
Считается, что синдром Германского-Пудлака наследуется как аутосомно-рецессивный генетический признак. Дефектный ген, называемый HSP, ответственный за это заболевание, расположен на длинном плече хромосомы 10 (10q2). Некоторые исследования показывают, что нарушение функции лизосом может быть причиной развития болезни.HPS1, AP3B1, HPS3, HPS4, HPS5, HPS6, DTNBP1 и BLOC1S3 связаны с синдромом Германского Пудлака.
При аутосомно-рецессивных расстройствах состояние не возникает, если человек не унаследует две копии дефектного гена, ответственного за расстройство, по одной копии от каждого родителя. Если человек получает один нормальный ген и один ген заболевания, он будет носителем болезни, но обычно не проявляет симптомов. Риск передачи болезни детям пары, которые оба являются носителями рецессивного расстройства, составляет 25 процентов.Пятьдесят процентов их детей рискуют стать носителями болезни, но, как правило, у них не проявляются симптомы заболевания. Двадцать пять процентов их детей могут получить оба нормальных гена, по одному от каждого родителя, и будут генетически нормальными (для этого конкретного признака). Риск одинаков для каждой беременности. [10]
Если человек получает один нормальный ген и один ген заболевания, он будет носителем болезни, но обычно не проявляет симптомов. Риск передачи болезни детям пары, которые оба являются носителями рецессивного расстройства, составляет 25 процентов.Пятьдесят процентов их детей рискуют стать носителями болезни, но, как правило, у них не проявляются симптомы заболевания. Двадцать пять процентов их детей могут получить оба нормальных гена, по одному от каждого родителя, и будут генетически нормальными (для этого конкретного признака). Риск одинаков для каждой беременности. [10]
Симптомы
Существует три основных расстройства, вызванных синдромом Германского-Пудлака, которые приводят к этим симптомам:
- Альбинизм и проблемы с глазами: У людей разное количество пигмента кожи (меланина).Из-за альбинизма возникают проблемы с глазами, такие как светочувствительность (светобоязнь), косоглазие (косоглазие) и нистагм (непроизвольные движения глаз). Синдром Германского-Пудлака также ухудшает зрение.

- Нарушения свертываемости крови: у людей с синдромом дисфункция тромбоцитов. Поскольку тромбоциты необходимы для свертывания крови, у людей могут возникать синяки и кровотечение.
- Нарушения клеточного накопления: синдром заставляет воскоподобное вещество (цероид) накапливаться в тканях тела и вызывать повреждения, особенно в легких и почках. [11]
- Связан с гранулематозным колитом.
Лечение
Хотя лечения HPS не существует, лечение хронических кровотечений, связанных с этим заболеванием, включает терапию витамином E и антидиуретическим dDAVP. [12]
Рекомендации для пациентов с Hermansky-Pudlak
Требуется предоперационная консультация пневмолога. Бригада анестезиологов должна знать, что пациенты могут иметь послеоперационные легочные осложнения как часть синдрома.
Перед плановой офтальмологической операцией рекомендуется консультация гематолога перед операцией. Поскольку пациенты с синдромом склонны к кровотечениям, следует предотвращать и лечить интраоперационные, периоперационные и послеоперационные кровотечения. О, Дж; Ho, L; Ала-Мелло, S; Amato, D; Армстронг, L; Беллуччи, S; Каракушанский, Г; Ellis, Jp; Фонг, Кт; Зеленый, Js; Heon, E; Легиус, E; Левин, Av; Nieuwenhuis, Hk; Пинкерс, А; Тамура, Н; Уайтфорд, штат Мэриленд; Ямасаки, H; Сприц, Ра (март 1998 г.). Ли В., Чжан К., Ойсо Н., Новак Е.К., Гаутам Р., О’Брайен Е.П., Тинсли К.Л., Блейк Д.Д., Спритц Р.А., Коупленд Н.Г., Дженкинс Н.А., Амато Д., Роу Б.А., Старчевич М., Делл’Анджелика Е.К., Эллиотт Р.В., Мишра В., Кингсмор С.Ф., Пейлор Р.Э., Суонк Р.Т. (2003). «Синдром Германского-Пудлака типа 7 (HPS-7) возникает из-за мутантного дисбиндина, члена биогенеза связанного с лизосомами комплекса органелл 1 (BLOC-1)». Nat. Genet. 35 (1): 84–9. DOI: 10,1038 / нг1229. PMC 2860733. PMID 12923531. http: //www.pubmedcentral. Германский, Ф; Пудлак, П. (1 февраля 1959 г.). «Альбинизм, связанный с геморрагическим диатезом и необычными пигментированными ретикулярными клетками в костном мозге: отчет о двух случаях с гистохимическими исследованиями». (Бесплатный полный текст). Кровь 14 (2): 162–9. ISSN 0006-4971. PMID 13618373. http://www.bloodjournal.org/cgi/pmidlookup?view=long&pmid=13618373.
Внешние ссылки
| |||||||||||||||||||||||
| |||||||||||||||||
| |||||||||||||||||
вазоплегический синдром Wikipedia
Вазоплегический синдром ( VPS ) — это постперфузионный синдром, характеризующийся низким системным сосудистым сопротивлением и высоким сердечным выбросом.
Причины []
VPS чаще возникает после операции АКШ с помпой, чем после операции АКШ без помпы. [1] Гипотермия во время операции также может повысить риск развития ВПС после операции. [2]
Диагностика []
Определение []
Вазоплегический синдром определяется как низкое системное сосудистое сопротивление (индекс УВО <1,600 дин ∙ сек / см5 / м2) и высокий сердечный выброс (сердечный индекс> 2,5 л / мин / м2) в течение первых 4 часов после операции. Gomes WJ, Carvalho AC, Palma JH, Gonçalves Júnior I, Buffolo E (1994). «[Вазоплегический синдром: новая дилемма]». Rev Assoc Med Bras . 40 (4): 304. PMID 7633508. Синдром
— Викисловарь
Английский [править]
Этимология [править]
С древнегреческого συνδρομή (sundromḗ, «совпадение симптомов»), из σύνδρομος (súndromos, «бегать вместе»), из συν- (солнце-, «с») + μο ( дромос, «бег, курс»).
Произношение [править]
Существительное [править]
синдром ( множественное число синдромов )
- (патология) Распознаваемый образец признаков, симптомов и / или поведения, особенно болезни, медицинского или психологического состояния.
- Синдром Дауна ; приобретенный иммунодефицит синдром ; синдром беспокойной ноги ; избитая жена синдром
- 2013 Май-июнь, Кэти Л.Берк, «В новостях», в American Scientist , том 101, номер 3, стр. 193:
Летучие мыши являются носителями многих известных вирусов, которые могут инфицировать людей, включая тяжелый острый респираторный синдром и Эбола. В недавнем исследовании изучались экологические переменные, которые могут способствовать склонности летучих мышей переносить такие зоонозные заболевания, путем сравнения их с другим отрядом обычных резервуарных хозяев: грызунами.
- Любой набор характеристик, определяющих определенный тип, состояние и т. Д., обычно неблагоприятно.
- синдром «не у меня на заднем дворе» ; синдром кончика языка
- 1989 3 ноября, «Джимми Карсон возвращается домой; Он — Redwing », в The Argus-Press (Овессо, Мичиган) [news.google.com/newspapers?nid=1988&dat=19891103&id … sjid … pg …] :
Молодой суперзвезда Джимми Карсон не выдержал еще одного дня в Эдмонтоне, живя в пустоте, созданной уходом Уэйна Гретцки, чьи разбитые сердца фанаты так и не приняли его замену.Мне было очень трудно играть в Эдмонтоне во всем синдроме Гретцки , — сказал Карсон в четверг на следующий день после обмена с шестью игроками …
- 2012 , Стивен Д. Прайс, Отговорки на все случаи жизни: Алиби, извинения и решения, которые могут вывести вас из (или в) неприятностей [1] :
Говоря о медицине, кажется, получать удовольствие от оправданий для здоровья. Синдромы — плодородное поле. Допустим, вас обвиняют в неспособности принять на себя ответственность или иным образом вести себя как взрослый.Это не ваша вина, возражаете вы — вы страдаете синдромом Питера Пэна . Не можете навести порядок в своей комнате или офисе? Конечно, нет — вы страдаете от третичного синдрома Bag Lady .
Производные термины [править]
Переводы [править]
узнаваемый образец симптомов или поведения
|
Источники [править]
Произношение [править]
Существительное [править]
синдром м ( множественное число синдромов )
- синдром
Список литературы [править]
Интерлингва [править]
Существительное [править]
синдром ( множественное число синдромов )
- Синдром
Вазоплегический синдром — Инфогалактика: ядро планетарных знаний
Вазоплегический синдром (VPS) — это постперфузионный синдром, характеризующийся низким системным сосудистым сопротивлением и высоким сердечным выбросом.
Определение
Вазоплегический синдром определяется как низкое системное сосудистое сопротивление (индекс УВО <1,600 дин ∙ сек / см5 / м2) и высокий сердечный выброс (сердечный индекс> 2,5 л / мин / м2) в течение первых 4 часов после операции. [1]
Причины
VPS чаще возникает после операции АКШ с помпой, чем после операции АКШ без помпы. [2] Гипотермия во время операции также может повысить риск развития ВПС после операции. [3]
Лечение
Есть некоторые свидетельства в пользу использования метиленового синего для лечения этого состояния. [4] [5]
Эпидемиология
В одной серии случаев сообщается о 1 из 120 случаев. [6]
Ссылки
- ↑ «Реанимационная помощь | Полный текст | Вазоплегический синдром после операции искусственного кровообращения — факторы, связанные и клинические исходы: вложенное исследование случай-контроль».
- ↑ Sun X, Zhang L, Hill PC, et al.(Октябрь 2008 г.). «Отличается ли частота послеоперационного вазоплегического синдрома при операции по аортокоронарному шунтированию без помпы и без помпы?». евро J Cardiothorac Surg . 34 (4): 820–5. DOI: 10.1016 / j.ejcts.2008.07.012. PMID 18715792.
- ↑ Сю Дж, Лонг Ц, Ци Р, Се Л., Ши С., Чжан И (январь 2002). «[Изучение механизма вазоплегического синдрома при операциях на открытом сердце]». Чжунхуа И Сюэ За Чжи (на китайском языке). 82 (2): 127–30. PMID 11953144. CS1 maint: нераспознанный язык (ссылка)
- ↑ «BestBets: полезен ли метиленовый синий при лечении взрослых пациентов, у которых развивается вазоплегический синдром во время кардиохирургии».
- ↑ Ставицки С.П., Симс С., Сарани Б., Гроссман, доктор медицины, Грасиас В.Х. (май 2008 г.).«Метиленовый синий и вазоплегия: кто, когда и как?». Мини Рев Мед Хим . 8 (5): 472–90. DOI: 10,2174 / 138955708784223477. PMID 18473936.
- ↑ Gomes WJ, Carvalho AC, Palma JH, Gonçalves Júnior I, Buffolo E (1994). «[Вазоплегический синдром: новая дилемма]». Rev Assoc Med Bras . 40 (4): 304. PMID 7633508.







