Псевдотуберкулез: симптомы, лечение, профилактика. Справка
Основной путь распространения псевдотуберкулеза ‑ пищевой. Наибольшую опасность представляют продукты зимнего хранения (картофель, капуста, морковь и др.), которые могли быть заражены грызунами, молочные продукты, употребляемые в пищу без предварительной термической обработки, а также вода при употреблении ее из открытых водоемов. Псевдотубрекулез встречается во всех возрастных группах, но чаще у детей первых лет жизни.
Симптомы. Заболевание начинается остро: появляются озноб, лихорадка, повышение температуры тела до 38‑38,5 С, симптомы общей интоксикации; в первые дни болезни могут быть симптомы катара верхних дыхательных путей. Больных беспокоит головная боль, слабость, боли в мышцах и суставах. Одновременно с интоксикационным синдромом возникают тошнота, у части больных ‑ рвота, боли в животе, которые носят схваткообразный или постоянный характер. Локализация болей ‑ в подложечной области, вокруг пупка, справа внизу живота, иногда в правом подреберье.
К числу кардинальных признаков этого заболевания относится признак «капюшона» (покраснение лица и шеи), «перчаток» и «носков» (ограниченное покраснение кистей и стоп). Эти признаки появляются чаще всего на 2‑4‑й день болезни. Продолжительность сыпи ‑ 1‑7 дней. После ее исчезновения, со 2‑й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) ‑ кожи ладоней и стоп.
Часто язык больного, обложенный в первые дни болезни белым налетом, к 5‑7‑му дню очищается и становится «малиновым», что усиливает сходство псевдотуберкулеза со скарлатиной (скарлатиноподобные формы).
Помимо клинических симптомов для подтверждения диагноза используются специфические методы диагностики ‑ бактериологический и серологический.
Основными материалами для бактериологического исследования служат испражнения, кровь, цереброспинальная жидкость, лимфатические узлы и червеобразный отросток. Для определения присутствия псевдотуберкулезных антигенов в фекалиях и другом материале используют иммуноферментный анализ (ИФА).
Лечение. Для лечения псевдотуберкулеза применяют антибиотики (левомицетин, тетрациклин или стрептомицин), сульфаниламиды и химиопрепараты. Левомицетин назначают по 0,5 г 4 раза в сутки в течение 10‑14 дней. При симптомах выраженной интоксикации назначается внутривенное вливание 5 % раствора глюкозы или гемодеза.
Продолжительность лечения зависит от формы заболевания. Режим в разгар заболевания постельный. Иногда по показаниям требуется оперативное лечение. Больных выписывают из стационара после полного клинического выздоровления и двукратного отрицательного бактериологического исследования испражнений.
Профилактика. Вакцины, то есть прививки, от псевдотуберкулеза нет.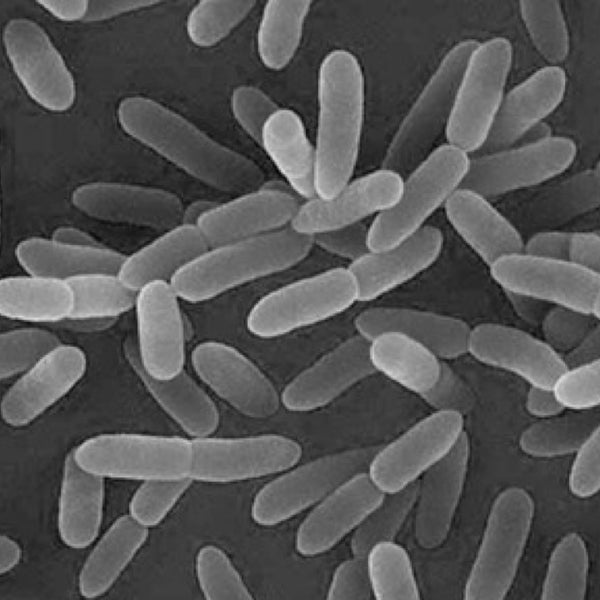 Основные меры профилактики — это контроль за состоянием овощехранилищ, борьба с грызунами, а также санитарно‑гигиенические мероприятия на пищевых предприятиях и пищеблоках ‑ соблюдение правил транспортировки, хранения, приготовления и реализации пищевых продуктов, запрещение употребления овощей (капуста, морковь) без термической обработки, постоянный санитарный надзор за водоснабжением.
Основные меры профилактики — это контроль за состоянием овощехранилищ, борьба с грызунами, а также санитарно‑гигиенические мероприятия на пищевых предприятиях и пищеблоках ‑ соблюдение правил транспортировки, хранения, приготовления и реализации пищевых продуктов, запрещение употребления овощей (капуста, морковь) без термической обработки, постоянный санитарный надзор за водоснабжением.
Материал подготовлен на основе информации открытых источников
Все справки>>
Иерсиниоз и псевдотуберкулез — Кабинет инфекционных заболеваний — Отделения
Иерсиниоз и псевдотуберкулез – это кишечные сапрозоонозы, вызываемые иерсиниями, характеризующиеся поражением желудочно-кишечного тракта, выраженной токсико-вазарной симптоматикой и наклонностью (наиболее выраженной при псевдотуберкулезе) к генерализованному течению. Оба заболевания имеют отчетливо выраженную тенденцию индуцировать развитие иммунопатологии.
Этиология
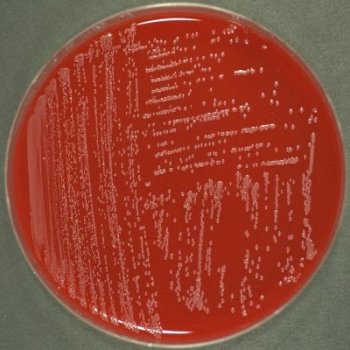
Возбудители иерсиниоза (Y. enterocolitica) и псевдотуберкулеза (Y. pseudotuberculosis) относятся к семейству кишечных бактерий. Иерсинии представляют собой грамотрицательные палочки, которые растут как на обычных, так и на обедненных питательными веществами средах. Последние используются при бактериологическом исследовании по методу Петерсона и Кука (1963).
Иерсинии содержат О- и Н-антигены. Различия в строении 0-антигенов позволили выделить более 50 сероваров Y. enterocolitica. Наибольшее значение в патологии человека имеют серовары 03; 05,27; 07,8 и 09. У возбудителя псевдотуберкулеза — установлено наличие 8 сероваров. Наиболее часто заболевания у людей вызываются 1-м сероваром.
Многие штаммы иерсиний продуцируют экзотоксин (термостабильный энтеротоксин). При разрушении бактерий выделяется эндотоксин. Иерсинии обладают также способностью кадгезии, инвазии и внутриклеточному размножению. Инвазивные свойства у Y. pseudotuberculosis выражены в большей степени, чем у Y. entero-colitica.
entero-colitica.
Иерсинии относятся к психрофилам. При температуре холодильника (4-8 °С) они способны длительно сохраняться и размножаться на овощах, корнеплодах и других пищевых продуктах. В то же время, некоторые из штаммов бактерий обладают повышенной термоустойчивостью к высокой температуре и способны выдержать режим пастеризации. При кипячении (100°С) все штаммы иерсиний погибают через несколько секунд. Чувствительны к действию обычных дезинфектантов.
Эпидемиология
Иерсинии (Y. enterocolitica и Y. pseudotuberculosis) широко распространены в природе. Их обнаруживали в почве, воде, выделяли из организма многих видов животных. Однако основным резервуаром возбудителя в природе, очевидно, являются мелкие грызуны, которые, обсеменяя различные объекты внешней среды, пищевые продукты, воду, способствуют распространению инфекции среди других животных. Другим резервуаром иерсиний является почва. Частое обнаружение в ней возбудителей болезней связано не только с загрязнением испражнениями животных, но и с наличием у иерсиний сапрофитических свойств.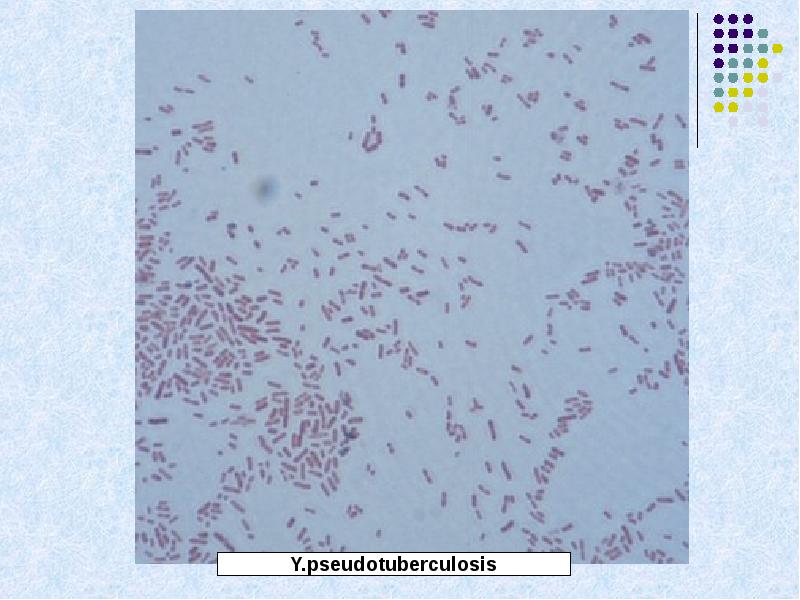 На основании этого заболевание может быть отнесено к сапрозоонозам.
На основании этого заболевание может быть отнесено к сапрозоонозам.
Основным источником инфекции для человека при иерсиниозе являются сельскохозяйственные животные, реже – синантропные грызуны. Больной человек как источник инфекции имеет несравненно меньшее значение. При псевдотуберкулезе основными источниками инфекции являются синантропные и дикие грызуны. Человек, как правило, источником псевдотуберкулеза не является.
Основной путь распространения обеих инфекций – пищевой. Факторами передачи Y. enterocolitica чаще всего являются инфицированные мясные продукты, молоко, овощи, корнеплоды, вода. К факторам передачи Y. pseudotuberculosis относятся овощные блюда (салаты из капусты, моркови и др.) и молочные продукты, употребляемые в пищу без предварительной термической обработки. Водный путь передачи имеет при обеих инфекциях несравненно меньшее значение. Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи не имеют существенного значения в эпидемиологии иерсиниозов.
Заболевание встречается во всех возрастных группах, но чаще у детей первых лет жизни. Сезонный подъем заболеваемости иерсиниозом отмечается в холодное время года с пиком в ноябре. В некоторых регионах наблюдается два сезонных подъема — осенью и весной. Пик заболеваемости псевдотуберкулезом приходится на весенние месяцы (март-май). Иерсиниоз и псевдотуберкулез протекают в виде спорадических и групповых заболеваний.
Патогенез
Входными воротами для возбудителей иерсиниоза и псевдотуберкулеза служит желудочно-кишечный тракт. Максимально выраженная местная реакция в ответ на инвазию иерсиний регистрируется со стороны слизистой оболочки подвздошной кишки и ее лимфоидных образований. В подвздошной кишке развивается различной выраженности воспалительный процесс – терминальный илеит. По лимфатическим сосудам иерсиний проникают в мезентериальные лимфатические узлы и вызывают мезаденит. В патологический процесс могут быть вовлечены червеобразный отросток и слепая кишка.
На фоне инфекционно-воспалительных изменений развиваются токсический и токсико-вазарный (парез вазамоторов) процессы, связанные с токсинемией. На этом этапе инфекционный процесс, приобретая черты локализованной формы, может завершиться.
На этом этапе инфекционный процесс, приобретая черты локализованной формы, может завершиться.
В случае прорыва лимфатического барьера кишечника, возникает бактериемия, обусловливающая развитие генерализованных форм заболевания. Наблюдается бактериально-токсическое поражение многих органов и систем, в первую очередь печени и селезенки, возможно развитие полилимфаденита, полиартрита, миозита, нефрита, уретрита, менингита и др.
При длительном нахождении иерсиний и их токсинов в крови и органах больного происходит сенсибилизация организма. У части больных, как правило, с фенотипом HLA-B27, иерсиниоз и псевдотуберкулез могут явиться толчком к возникновению иммунопатологических реакций и состояний.
Заключительное звено патогенеза – освобождение организма от возбудителя, ведущее к выздоровлению.
Развитие специфического иммунитета при иерсиниозе и псевдотуберкулезе происходит медленно и он не является достаточно прочным, с чем связано нередкое развитие обострений и рецидивов болезни.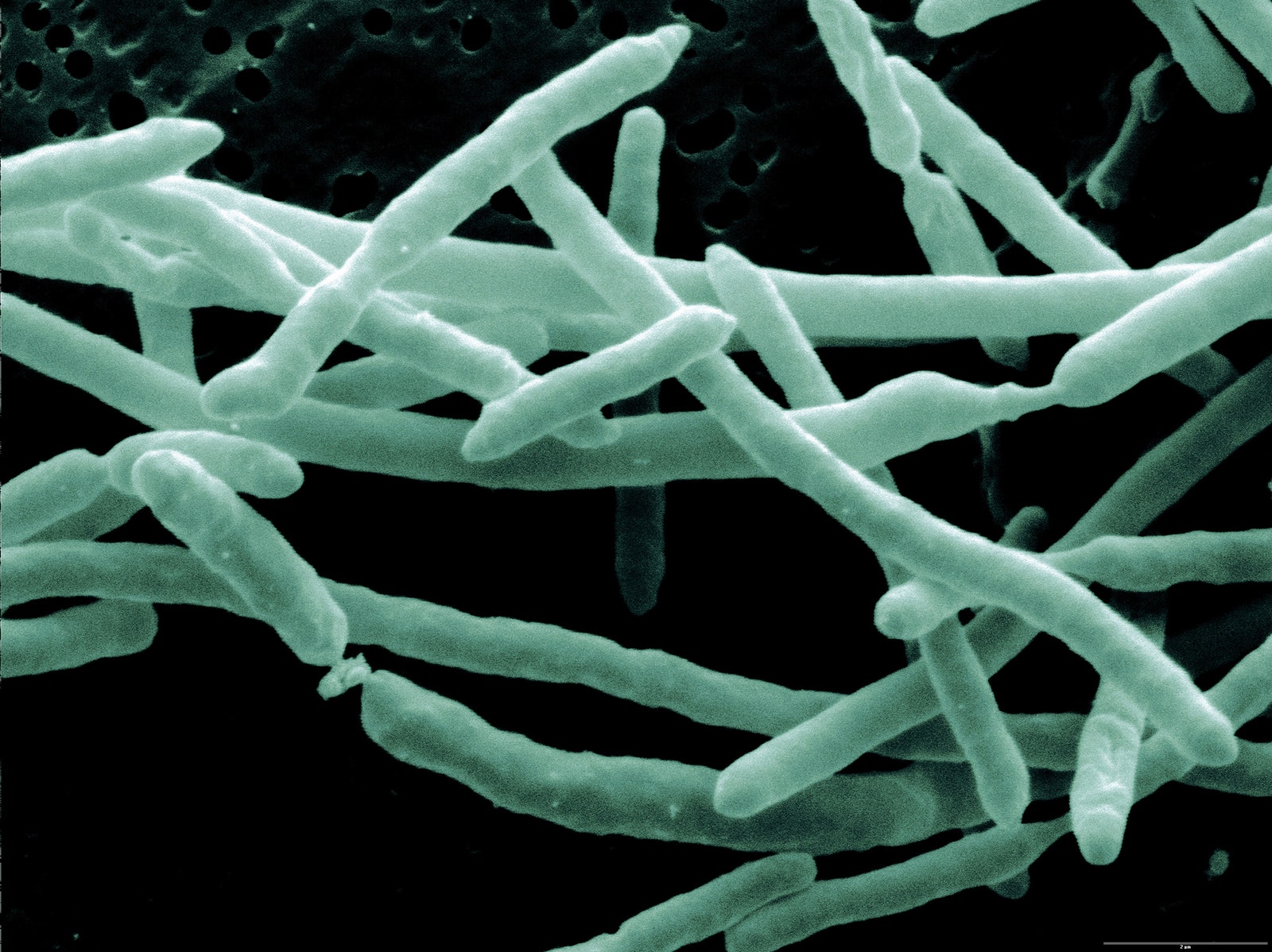
Клиника
Продолжительность инкубационного периода при иерсиниозе колеблется от 1 до 7 дней, а псевдотуберкулезе – от 3 до 21 дня.
На основе общих патогенетических закономерностей кишечных зоонозов и клинико-патогенетических особенностей иерсиниоза и псевдотуберкулеза могут быть выделены локализованная (гастро-интестиномезентериальная) и генерал и зеванная формы. Они могут иметьманифестноеили (реже) бессимптомное течение.
Локализованная (гастроинтестиномезентериальная) форма манифестного течения включает следующие варианты:
Генерализованная форма манифестного течения может иметь две разновидности: токсикобактериемическая и септическая.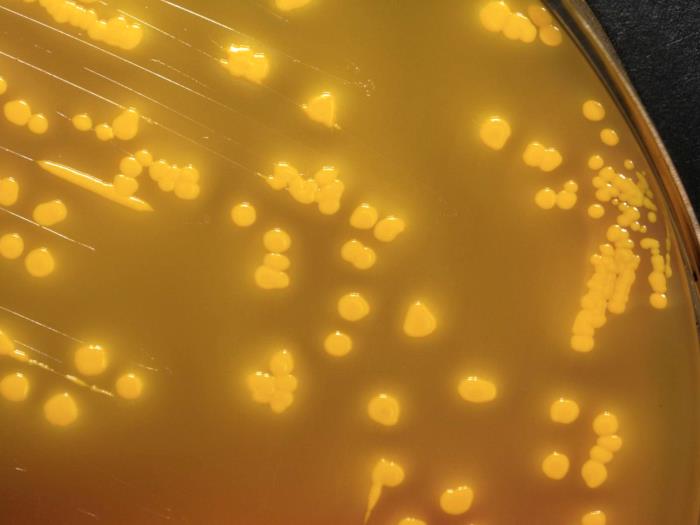 В зависимости от преобладания той или иной симптоматики токсикобактериемическая разновидность генерализованной формы может протекать в следующих вариантах: экзантематозном, артритическом, желтушном (иерсиниозный гепатит), менингеальном, катаральном, смешанном и в виде иерсиниоза (псевдотуберкулеза) редких локализаций. В редких случаях (например, у иммунокомпрометированных лиц с хронической патологией печени и признаками тезауризмоза железа) развивается иерсиниозный сепсис. Бессимптомное течение при генерализованной форме может быть представлено реконвалесцентным вариантом. Последний обычно не характерен для псевдотуберкулеза.
В зависимости от преобладания той или иной симптоматики токсикобактериемическая разновидность генерализованной формы может протекать в следующих вариантах: экзантематозном, артритическом, желтушном (иерсиниозный гепатит), менингеальном, катаральном, смешанном и в виде иерсиниоза (псевдотуберкулеза) редких локализаций. В редких случаях (например, у иммунокомпрометированных лиц с хронической патологией печени и признаками тезауризмоза железа) развивается иерсиниозный сепсис. Бессимптомное течение при генерализованной форме может быть представлено реконвалесцентным вариантом. Последний обычно не характерен для псевдотуберкулеза.
По тяжести манифестного течения заболевания выделяют легкое, среднетяжелое и тяжелое течение. По характеру течения — гладкое и осложненное, в том числе с обострениями и рецидивами. По продолжительности заболевания и его исходам – острое (до 3 мес.), хроническое (более 3 мес.) и клиника последствий (резидуальная фаза).
Локализованная (застроинтестиномезентериальная) форма встречается в 70% случаев иерсиниоза и почти 30% псевдотуберкулеза. Наиболее частыми проявлениями данной формы являются гастроэнтероколитический, гастроэнтеритический, энтероколитический и энтеритический варианты течения болезни. Они регистрируются во всех возрастных группах, но в основном у детей в возрасте до 10 лет.
Наиболее частыми проявлениями данной формы являются гастроэнтероколитический, гастроэнтеритический, энтероколитический и энтеритический варианты течения болезни. Они регистрируются во всех возрастных группах, но в основном у детей в возрасте до 10 лет.
Клиническая картина указанных вариантов характеризуется наличием интоксикационного синдрома и симптомов поражения желудочно-кишечного тракта на том или ином его уровне. Заболевание начинается остро: возникают озноб, повышение температуры тела до 38-38,5°С. Больных беспокоит головная боль, слабость, миалгии и артралгии. Одновременно с интоксикационным синдромом возникают тошнота, у части больных — рвота, боли в животе, которые носят схваткообразный или постоянный характер. Локализация болей – в эпигастрии, вокруг пупка, в правой подвздошной области, иногда в правом подреберье. Стул жидкий, вязкий, с резким запахом. У некоторых больных при вовлечении в патологический процесс толстой кишки в стуле обнаруживают примесь слизи, реже крови. Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Острый терминальный илеит сопровождается повышением температуры тела до 38-39°С, интенсивными болями в илеоцекальной области и диареей. Больные, как правило, описывают два вида болей: постоянного и на их фоне – схваткообразного типов. При рентгенологическом исследовании пораженная часть подвздошной кишки резко сужена и имеет сглаженный рельеф слизистой оболочки («симптом шнура»). Терминальный илеит имеет длительное и нередко осложненное течение. Среди возможных осложнений: инфарцирование и некроз слизистой оболочки с последующим ограниченным или (редко) разлитым перитонитом, спаечный процессе развитием кишечной непроходимости и др. Возможно развитие клиники последствий в виде хронического гранулематозно-язвенного поражения подвздошной кишки, морфологически не отличимого от болезни Крона.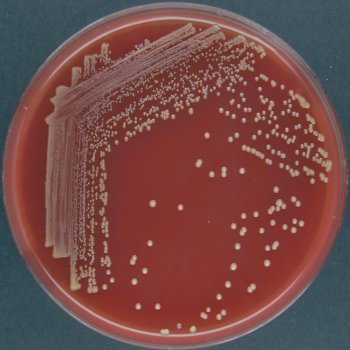
Острый мезаденит характеризуется умеренно выраженной интоксикацией, субфебрильной температурой, меньшей, чем при терминальном илеите силой схваткообразных и постоянного типа болей. В дебюте заболевания может иметь место тошнота, рвота, жидкий стул до 3-5 раз за сутки. В дальнейшем у значительной части больных наблюдается развитие (за 4-6 дней) «инфильтрата» в илеоцекальной области, представляющего собой группу увеличенных мезентериальных узлов, и перитонеальной симптоматики. Выявляют положительные симптомы Мак-Фаддена, Клейна, Падалки, «перекрестный» симптом Штернберга. Течение острого мезаденита нередко сопровождается обострениями и рецидивами. Возможен переход заболевания в затяжное и хроническое течение. Часть больных подвергаются оперативному вмешательству.
Острый иерсиниозный (псевдотуберкулезный) аппендицит в отличие от вульгарного имеет более медленный темп развития от катаральной до деструктивной форм. Как следствие этого – большая частота обнаружения катарально измененного червеобразного отростка в ходе оперативного вмешательства, чем при вульгарном аппендиците. Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Всем вариантам локализованной формы свойственна не только абдоминальная (желудочно-кишечная), но и внеабдоминальная симптоматика, обусловленная действием токсина и избыточной продукцией простагландинов на вазомоторы и эндотелий сосудов: инъекция сосудов склер и гиперемия конъюнктив, «малиновый» язык, гиперемия мягкого неба, артралгии, миалгии и др.
В периферической крови наблюдается лейкоцитоз, нейтрофилез, палочкоядерный сдвиг, увеличение СОЭ, иногда эозинофилия.
Генерализованная форма встречается примерно в 30% случаев манифестного течения иерсиниозаи 70% случаев псевдотуберкулеза. Она имеет две разновидности течения :токсикобактериемическая и септическая. Как при иерсиниозе, так и при псевдотуберкулезе обычно наблюдается токсикобактериемическое течение генерализованной формы. Септическое течение при обоих заболеваниях встречается крайне редко.
Септическое течение при обоих заболеваниях встречается крайне редко.
Токсикобактериемическое течение генерализованной формы наиболее хорошо изучено при экзантем атозном варианте псевдотуберкулеза, описанном ранее как дальневосточная скарлати неподобная лихорадка. Заболевание характеризуется острым началом. Больные жалуются на озноб, головную боль, миалгии и артралгии. Температура тела повышается до 38-40°С и держится на этом уровне в течение 5-7 сут, а при тяжелой форме и дольше. В первые дни болезни отмечаются тошнота, иногда рвота, жидкий стул, боли в животе. Нередко наблюдаются катаральные симптомы со стороны верхних дыхательных путей: першениеи умеренные боли при глотании, покашливание, насморк.
При объективном обследовании в 1-ю неделю заболевания кожа больных сухая, горячая, лицо одутловатое. Отмечается гиперемия конъюнктив, инъекция сосудов склер. Нередко, особенно у детей, определяется бледный носогубный треугольник. Слизистая оболочка ротоглотки диффузно гиперемирована. У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
Следует заметить, что подобный тип экзантемы практически не встречается при иерсиниозе. Для него более характерна мелкопятнистая сыпь на симметричных участках кожи туловища и/или конечностей, которая исчезает в срок от нескольких часов до 3-4 сут.
При пальпации находят умеренно увеличенные и болезненные периферические лимфоузлы. Определяются лабильность и учащение пульса, соответствующее температуре тела. л, палочкоядерный сдвиг, иногда эозинофилия, увеличение СОЭ до 25-50 мм/ч.
л, палочкоядерный сдвиг, иногда эозинофилия, увеличение СОЭ до 25-50 мм/ч.
Заболевание нередко сопровождается развитием признаков инфекционно-токсического интерстициального нефрита. В некоторых случаях тяжелого течения болезни наблюдаются признаки серозного менингита.
У части больных 2-я и 3-я недели болезни характеризуются появлением симптомов, свидетельствующих об иммунопатологической перестройке. В это тпериод нередко появляются уртикарные, макулезные и макулопапулезные высыпания с локализацией на туловище и конечностях, чаще в области крупных суставов. Возникает узловатая эритема. У некоторых больных развивается реактивный полиартрит, болезнь Рейтера.
Иногда в этот период заболевания выявляют миокардит, нефрит, уретрит, цистит, конъюнктивит, иридоциклит и другие поражения внутренних органов.
По преобладанию той или иной симптоматики в пределахтокси-кобактериемического течения генерализованной формы заболевания выделяют следующие варианты: экзантематозный, артритический, желтушный (иерсиниозный/псевдотуберкулезный гепатит), менингеальный, катаральный и иерсиниоз (псевдотуберкулез) редких локализаций.
Обострения и рецидивы часто осложняют течение иерсиниоза и псевдотуберкулеза. Они встречаются у 1/ больных и характеризуются повторной волной лихорадки и симптомами локальных поражений.
В период реконвалесценции температура тела снижается до нормальной, симптомы интоксикации исчезают, нормализуются функции внутренних органов.
Тяжесть течения иерсиниоза и псевдотуберкулеза определяется выраженностью интоксикационного синдрома и степенью вовлечения в патологический процесс внутренних органов. Чаще заболевание протекает в легкой и среднетяжелой формах.
Септическое течение генерализованной формы иерсиниоза и псевдотуберкулеза встречается очень редко. Оно, как правило, развивается при выраженном иммунодефиците, у лиц с хронической патологией печени и признаками тезауризмоза железа. Течение заболевания характеризуется тяжелой интоксикацией, микроабсцедированием внутренних органов, гепатоспленомегалией, нередко диареей, длительным рецидивирующим течением и, несмотря на лечение, высокой летальностью.
При всех формах манифестного течения иерсиниозной инфекции продолжительность заболевания обычно не превышает 1,5 мес. Однако иногда встречается затяжное течение болезни (от 1,5 до 3 мес) и в редких случаях хроническое (более 3 мес). Наличие заболевания, этиологически связанного с перенесенным иерсиниозом, но при доказанном бактериологически и серологически отсутствии возбудителя в организме больного должно расцениваться как клиника последствий иерсиниоза (резидуальная фаза).
Бессимптомное течение может быть острым (до 3 мес) и хроническим (более 3 мес). Последнее не характерно для псевдотуберкулеза. Кроме того, при иерсиниозев отличие от псевдотуберкулеза наблюдается не только субклиническое, но и реконвалесцентное бактериовыделение возбудителей болезни. Лица, имеющие бессимптомное течение заболевания, выявляются активно при обследовании работников пищевых предприятий и контактных – в очагах.
Прогноз в большинстве случаев, за исключением септического течения болезни, благоприятный.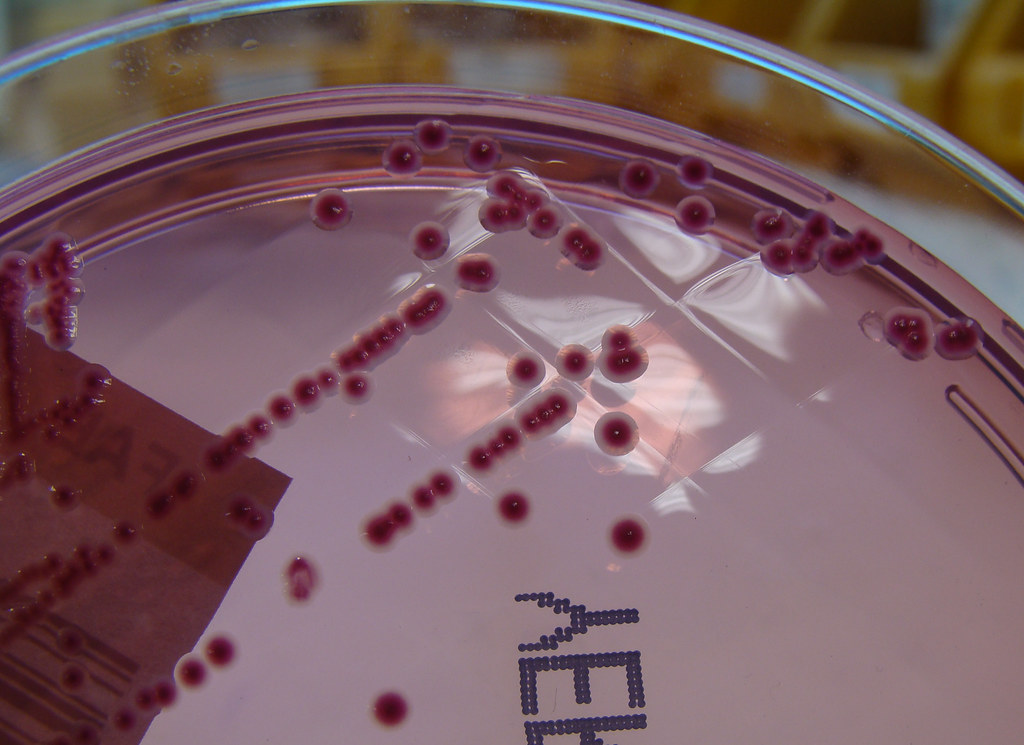
Диагностика
Из клинических признаков наибольшее диагностическое значение имеет сочетание синдрома поражения желудочно-кишечного тракта и «внекишечной» токсико-вазарной симптоматики. Данные эпидемиологического анамнеза, особенно при групповом характере заболеваемости, также имеют большое значение в распознавании иерсиниоза и псевдотуберкулеза. Однако решающим в установлении окончательного диагноза являются специфические методы диагностики – бактериологический и серологический.
Основными материалам и для бактериологического исследования служат испражнения, кровь, цереброспинальная жидкость, резецированные лимфатические узлы и червеобразный отросток. Для определения присутствия псевдотуберкулезных антигенов в фекалиях и другом материале используют иммуноферментный анализ (ИФА).
Серологическая диагностика имеет большое значение для подтверждения не только клинического диагноза, но и этиологической роли выделенных иерсиний. Она осуществляется с помощью РА и РНГА методом парных сывороток. Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
В экспресс-диагностике иерсиниоза используют РНГА с иммуноглобулиновыми диагностикумами и МФА.
Определенное значение в диагностике имеет также гистологическое исследование биоптатов лимфатических узлов и других органов.
Дифференциальная диагностика иерсиниоза и псевдотуберкулеза зависит от клинического варианта болезни. Наиболее часто возникает необходимость дифференцировать эти заболевания с острыми кишечными инфекциями, аппендицитом, различными заболеваниями суставов, вирусным гепатитом, сепсисом иной этиологии и др.
Лечение
В качестве этиотропных средств применяют антибиотики, сульфаниламиды и химиопрепараты. К препаратам выбора при генерализованной форме заболеваний относятся фторхинолоны. К препаратам резерва — цефалоспорины 3-го поколения, тетрациклины и левомицетин. Аминогликозиды обычно используют при лечении больных с иерсиниозным (псевдотуберкулезным) гепатитом. Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Патогенетическая терапия предусматривает назначение дезинтоксикационных, общеукрепляющих и стимулирующих, а также десенсибилизирующих средств. В некоторых случаях используют глюкозоэлектролитныеи полиионные растворы для регидратации.
Больных с септическим течением заболевания лечат в соответствие с принципами лечения сепсиса, используя 2-3 антибиотика (фторхинолоны, аминогликозиды, цефалоспорины) внутривенно в сочетании с интенсивной патогенетической терапией.
Больные с бессимптомным течением получают терапию в зависимости от варианта (субклинический или реконвалесцентный) и продолжительности бактериовыделения.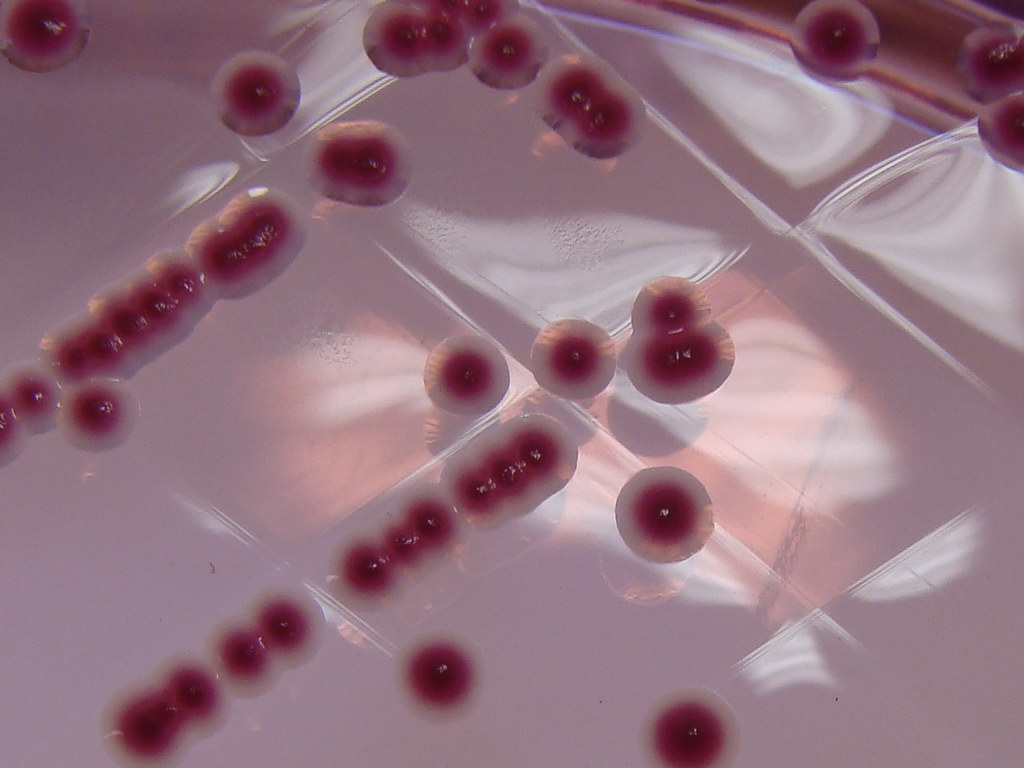 Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
По показаниям проводится оперативное лечение.
Профилактика
Контроль за состоянием овощехранилищ, борьба с грызунами.
Псевдотуберкулез: особенности развития, симптомы, лечение
Имеет ли это заболевание отношение к туберкулезу? Зачем о нем знать родителям?Последний месяц зимы и начало весны — это время, когда солнечных дней не так много, для прогулок не хватает времени — взрослые работают, дети посещают школу, детский сад, различные секции. Усталость накапливается и нужно как-то справляться с нагрузкой, а до теплых дней еще далеко. Именно в это время увеличивается заболеваемость псевдотуберкулезом.
Псевдотуберкулез (дальневосточная скарлатиноподобная лихорадка) — это острая кишечная бактериальная инфекция.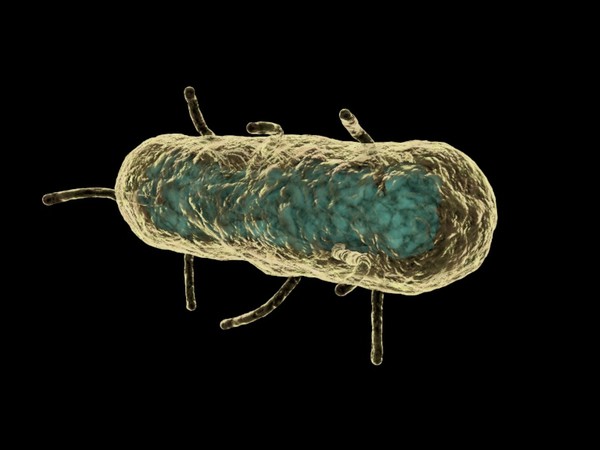 Заболевание характеризуется общей интоксикацией, поражением органов брюшной полости, суставов, часто сопровождается появлением сыпи. Клинические проявления маскируются под другие заболевания.
Заболевание характеризуется общей интоксикацией, поражением органов брюшной полости, суставов, часто сопровождается появлением сыпи. Клинические проявления маскируются под другие заболевания.
Отношения к туберкулезу не имеет.
Вызывается псевдотуберкулез бактерией Yersinia pseudotuberculosis. Особенность данной бактерии в том, что она может расти и размножаться при низкой температуре и повышенной влажности (выживает в холодильнике, в т.ч. и при повторном замораживании). В воде она сохраняет свои свойства от 2 до 8 месяцев, в масле и хлебе до 5 месяцев, в сахаре – не больше 3-х недель, в молоке – до 1 месяца. В почве может существовать примерно 1 год. Данный возбудитель также может присутствовать на кухонных предметах и таре, в которой хранятся продукты.
От человека к человеку инфекция передается крайне редко. Основным источником заражения являются грызуны, которые контактируют с пищевыми продуктами, водой, почвой и таким образом способствуют распространению инфекции.
Заболевание передается алиментарным путем, то есть при употреблении в пищу сырых овощей (листья салата, капуста, зеленый лук, морковь), если их неправильно хранили, недостаточно хорошо промыли или не обработали перед подачей на стол. Кроме этого заразиться можно, употребляя воду или молоко без термической обработки. Попадание возбудителя на уже готовые продукты возможно при несоблюдении правил хранения.
Риск заболеть у ребенка появляется, как только родители начинают давать ему свежие овощи и фрукты, или, например, пожевать кустик укропа чуть ополоснув его водой.
У взрослых заболевание протекает в более легкой форме, нет такой ярко выраженной клинической картины, выздоровление чаще наступает самостоятельно. Исключение составляют люди с патологией иммунной системы и хроническими заболеваниями печени.
Период от момента попадания возбудителя в организм до проявления клинических симптомов составляет от 3 до 18 дней, в среднем 10 дней.
Заболевание начинается остро.
Появляется озноб, головная боль, недомогание, боль в мышцах и суставах, першение в горле, кашель. Температура тела повышается до 38 — 40° С. На боли в животе дети начинают жаловаться в первые сутки активного проявления симптомов, иногда боли очень похожи на приступ аппендицита и сопровождаются тошнотой, рвотой, жидким стулом (до 4-5 раз в день, но чаще без примеси крови и слизи).
Сыпь, возникающая в первые несколько дней, похожа на скарлатинозную. После исчезновения сыпи появляется шелушение кожи.
В период разгара болезни появляются боли в суставах коленных, локтевых, голеностопных, реже мелких суставах кистей, стоп.
Нередко больные жалуются на тяжесть и боли в правом подреберье. Определяется желтушное окрашивание кожи и склер, фиксируется потемнение мочи.
К сожалению псевдотуберкулез может протекать с обострениями и рецидивами. Обострение характеризуется ухудшением общего состояния, повышением температуры тела, появлением болей в животе или суставах или усилением угасающих симптомов. Рецидив возникает после периода кажущегося выздоровления. Через 1 — 3 недели вновь появляются типичные признаки болезни.
Рецидив возникает после периода кажущегося выздоровления. Через 1 — 3 недели вновь появляются типичные признаки болезни.
Диагноз подтверждается результатами лабораторного обследования. В Детской клинике ЕМС лабораторные тесты проводятся круглосуточно, это позволяет экстренно производить забор крови и обеспечивать максимально быструю постановку диагноза.
В зависимости от тяжести и активности заболевания, наличия рецидивов доктор решает вопрос о необходимости назначения антибактериальной или симптоматической терапии. К сожалению Yersinia pseudotuberculosis не чувствительна к действию часто назначаемых антибактериальных препаратов.
Именно поэтому не нужно заниматься самолечением, необходимо поставить точный диагноз.
Педиатры Детской клиники ЕМС осуществляют лечение псевдотуберкулеза, при необходимости возможно наблюдение малыша в условиях комфортного стационара. В любой момент родители могут связаться с лечащим врачом и уточнить волнующие вопросы относительно лечения или изменения состояния ребенка.
Профилактика
Можно избежать заражения. Необходимо тщательно мыть овощи и фрукты специальными щеточками. Салат и зелень промывать в емкости с водой, тщательно мыть руки перед едой.
Псевдотуберкулез
Псевдотуберкулез
Син.: Дальневосточная скарлатиноподобная лихорадка
Псевдотуберкулез (pseudotuberculosis) – острое инфекционное заболевание, характеризующееся токсико‑аллергической и полиочаговой симптоматикой, протекающее с преимущественным поражением органов пищеварительной системы и в немалой части случаев – с экзантемой.
Исторические сведения
Возбудитель
инфекции описан в 1883 г. Л.Маляссе и
В.Виньялем, выделен в чистой культуре
и подробно изучен Р.Пфейффером в 1899 г.
В 1895 г. К.Эберт обнаружил во внутренних
органах погибших животных узелковые
образования, внешне напоминающие
туберкулезные бугорки, и назвал это
заболевание псевдотуберкулезом.
В 1959 г. стало складываться представление об эпидемическом характере заболевания. В это время на Дальнем Востоке возникла эпидемия ранее неизвестного заболевания, получившего название «дальневосточная скарлатиноподобная лихорадка» – ДСЛ. В 1965 г. В.А.Знаменский и А.К.Вишняков выделили из фекалий больных ДСЛ палочки псевдотуберкулеза. Опытом самозаражения (В.А.Знаменский) была доказана этиологическая роль этого микроорганизма в возникновении ДСЛ, которая стала рассматриваться как своеобразная клинико‑эпидемиологическая форма псевдотуберкулеза человека. В настоящее время это заболевание описано во многих странах мира.
Этиология
Возбудитель псевдотуберкулеза yersinia pseudotuberculosis относится к роду yersinia, семейству enterobacteriaceae.
Возбудитель псевдотуберкулеза растет на обычных и на обедненных питательными веществами средах.
При разрушении бактериальных клеток выделяется эндотоксин.
Одним
из наиболее важных для эпидемиологии
заболевания свойств возбудителя является
его психрофильность, т. е. способность
расти при низких температурах.
Псевдотуберкулезные бактерии могут
быстро размножаться при температуре
холодильника + 4‑8°С.
Они весьма устойчивы к повторному
замораживанию и оттаиванию, способны
длительно существовать в почве, воде,
на различных пищевых продукгах, а в
благоприятных условиях (при низких
температурах и повышенной влажности)
и размножаться. Вместе с тем возбудитель
псевдотуберкулеза чувствителен к
высыханию, воздействию солнечного
света. При кипячении погибает через
10–30 с. Растворы дезинфицирующих веществ
(хлорамин, гипохлорит кальция и др.)
убивают его в течение нескольких минут.
е. способность
расти при низких температурах.
Псевдотуберкулезные бактерии могут
быстро размножаться при температуре
холодильника + 4‑8°С.
Они весьма устойчивы к повторному
замораживанию и оттаиванию, способны
длительно существовать в почве, воде,
на различных пищевых продукгах, а в
благоприятных условиях (при низких
температурах и повышенной влажности)
и размножаться. Вместе с тем возбудитель
псевдотуберкулеза чувствителен к
высыханию, воздействию солнечного
света. При кипячении погибает через
10–30 с. Растворы дезинфицирующих веществ
(хлорамин, гипохлорит кальция и др.)
убивают его в течение нескольких минут.
Эпидемиология
Резервуар
бактерии. В естественных условиях
псевдотуберкулезом болеют многие виды
млекопитающих и птиц. Однако основным
резервуаром возбудителя и источником
заболевания для человека являются
синантропные и дикие грызуны. Они
инфицируют своими выделениями продукты
питания и воду, где возбудитель не только
сохраняется, но при низких температурах
и размножается. Другим резервуаром
псевдотуберкулезных бактерий является
почва. Частое обнаружение в ней возбудителя
связано не только с загрязнением
испражнениями животных, но и с наличием
у псевдотуберкулезной бактерии
сапрофитных свойств. На основании этого
заболевание может быть отнесено к
сапрозоонозам. Человек, как правило,
источником псевдотуберкулеза не
является.
Другим резервуаром
псевдотуберкулезных бактерий является
почва. Частое обнаружение в ней возбудителя
связано не только с загрязнением
испражнениями животных, но и с наличием
у псевдотуберкулезной бактерии
сапрофитных свойств. На основании этого
заболевание может быть отнесено к
сапрозоонозам. Человек, как правило,
источником псевдотуберкулеза не
является.
Ведущий путь передачи инфекции – пищевой. К основным факторам передачи относятся овощные блюда (салаты из капусты и моркови, винегреты и др.) и молочные продукты, употребляемые в пищу без предварительной термической обработки. Накоплению возбудителя в указанных продуктах способствует хранение их в условиях холодильника. Второе место занимает водный путь передачи. Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи существенного значения в эпидемиологии псевдотуберкулеза не имеют.
К
псевдотуберкулезу восприимчивы взрослые
и дети, но у последних он регистрируется
чаще. Это во многим связано с тем, что
большая часть детей находятся в
коллективах (ясли, детские сады, школы,
интернаты, училища и т. д.) с общим
пищеблоком.
д.) с общим
пищеблоком.
Псевдотуберкулез протекает в виде спорадических и групповых заболеваний, которые регистрируются в течение всего года. Сезонный подъем заболеваемости наблюдается в весенние месяцы (март – май).
Патогенез и патологоанатомическая картина
Как и при других кишечных инфекциях, возбудитель попадает в организм человека через рот с инфицированными продуктами и водой. Преодолев защитный барьер желудка, бактерии фиксируются в лимфатическом аппарате кишечника, вызывая развитие энтеральной фазы патогенеза псевдотуберкулеза. Патологоанатомические изменения в месте фиксации нередко бывают значительными (типа терминального илеита, аппендицита), но иногда выражены слабо или макроскопически не выявляются.
Симптоматика.
Инкубационный
период колеблется от 4 до 18 дней. Период
разгара болезни длится 1—3 дня. Заболевание
начинается остро с повышения температуры
до 38 °С. Больные жалуются на головную
боль, мышечные и суставные боли,
слабость. Многие больные одновременно
с ознобом отмечают появление болей
в животе, тошноту, иногда рвоту и жидкий
стул. В некоторых случаях появляются
боли в горле при глотании. На 3—4-й день
появляется ярко-красная сыпь на фоне
гиперемированной или обычной кожи. Сыпь
держится от нескольких часов до 5 дней.
Сыпь розеолезная, точечная, локализуется
на симметричных участках тела: боковых
поверхностях туловища, в подмышечных
впадинах, нижней части живота, паховых
областях, на руках — больше на сгибательной
поверхности. Сыпь может распространяться
и по всему туловищу. Язык первые 2—3 дня
покрыт белым налетом, затем очищается
и напоминает «малиновый» язык при
скарлатине.
Многие больные одновременно
с ознобом отмечают появление болей
в животе, тошноту, иногда рвоту и жидкий
стул. В некоторых случаях появляются
боли в горле при глотании. На 3—4-й день
появляется ярко-красная сыпь на фоне
гиперемированной или обычной кожи. Сыпь
держится от нескольких часов до 5 дней.
Сыпь розеолезная, точечная, локализуется
на симметричных участках тела: боковых
поверхностях туловища, в подмышечных
впадинах, нижней части живота, паховых
областях, на руках — больше на сгибательной
поверхности. Сыпь может распространяться
и по всему туловищу. Язык первые 2—3 дня
покрыт белым налетом, затем очищается
и напоминает «малиновый» язык при
скарлатине.
В разгар заболевания часто развиваются острые явления полиартрита с припухлостью мелких и крупных суставов конечностей, резкими болями, усиливающимися при движении.
К
3-му дню заболевания боли в животе могут
усилиться, печень умеренно увеличена.
К моменту появления сыпи температура
снижается до нормы или остается
субфебрильной. В этот момент выражена
картина терминального илеи-та или
мезентериита, симулирующих клинику
острого аппендицита.
В этот момент выражена
картина терминального илеи-та или
мезентериита, симулирующих клинику
острого аппендицита.
Полное клиническое выздоровление наступает к концу 3-й недели. Однако болезнь может принять волнообразное течение с подъемами температуры до 38 °С, и тогда выздоровление затягивается до 5 нед.
Характерны групповая заболеваемость лиц, питающихся в одном месте и потребляющих воду одного источника, острое начало болезни, скарлатиноподобная сыпь при отсутствии тонзиллита, полиартрит, боли в животе, диспепсические расстройства, терминальный илеит, паренхиматозный гепатит.
Возбудителя можно выделить из крови и слизи зева на высоте лихорадки и из фекалий на протяжении всего заболевания.
Лечение — в условиях инфекционного стационара
Профилактика
Борьба
с грызунами, постоянный санитарный
надзор за питанием и водоснабжением,
контроль за технологическим режимом
обработки и хранения пищевых продуктов,
особенно не подвергающихся термической
обработке.
Диагностика иерсиниоза и псевдотуберкулеза
Комплексное исследование для выявления возбудителя иерсиниоза (Yersinia enterocolitica) и псевдотуберкулеза (Yersinia pseudotuberculosis), включающее серологические тесты и полимеразную цепную реакцию (ПЦР).
Синонимы русские
Анализы на иерсиниоз и псевдотуберкулез.
Синонимы английские
Laboratory Diagnostics of Yersiniosis, Enteropathogenic Yersiniae Lab Panel.
Какой биоматериал можно использовать для исследования?
Венозную кровь, кал.
Как правильно подготовиться к исследованию?
- Исследование рекомендуется проводить до начала приема антибиотиков и других антибактериальных химиотерапевтических препаратов.
- Исключить прием слабительных препаратов, введение ректальных свечей, масел, ограничить (по согласованию с врачом) прием медикаментов, влияющих на перистальтику кишечника (белладонна, пилокарпин и др.
 ), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала.
), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала. - Не курить в течение 30 минут до исследования.
Общая информация об исследовании
Иерсинии — это грамотрицательные, факультативно-анаэробные палочки, относящиеся к семейству Enterobacteriaceae. Известно 11 видов иерсиний, три из которых являются возбудителями заболеваний человека: Yersinia pestis – это возбудитель чумы, Yersinia enterocolitica (Y. enterocolitica) и Yersinia pseudotuberculosis (Y. pseudotuberculosis) – кишечные патогены. Хотя Y. enterocolitica и Y. pseudotuberculosis относятся к разным видам, они имеют много общего, особенно в плане клинической картины и диагностики.
Основной «резервуар» иерсиний — дикие и домашние животные (свиньи, грызуны, овцы, козы, коровы, собаки, кошки и птицы). Считается, что человек не участвует в естественном жизненном цикле этих патогенов ни в качестве промежуточного, ни окончательного хозяина и его заражение, таким образом, носит случайный характер.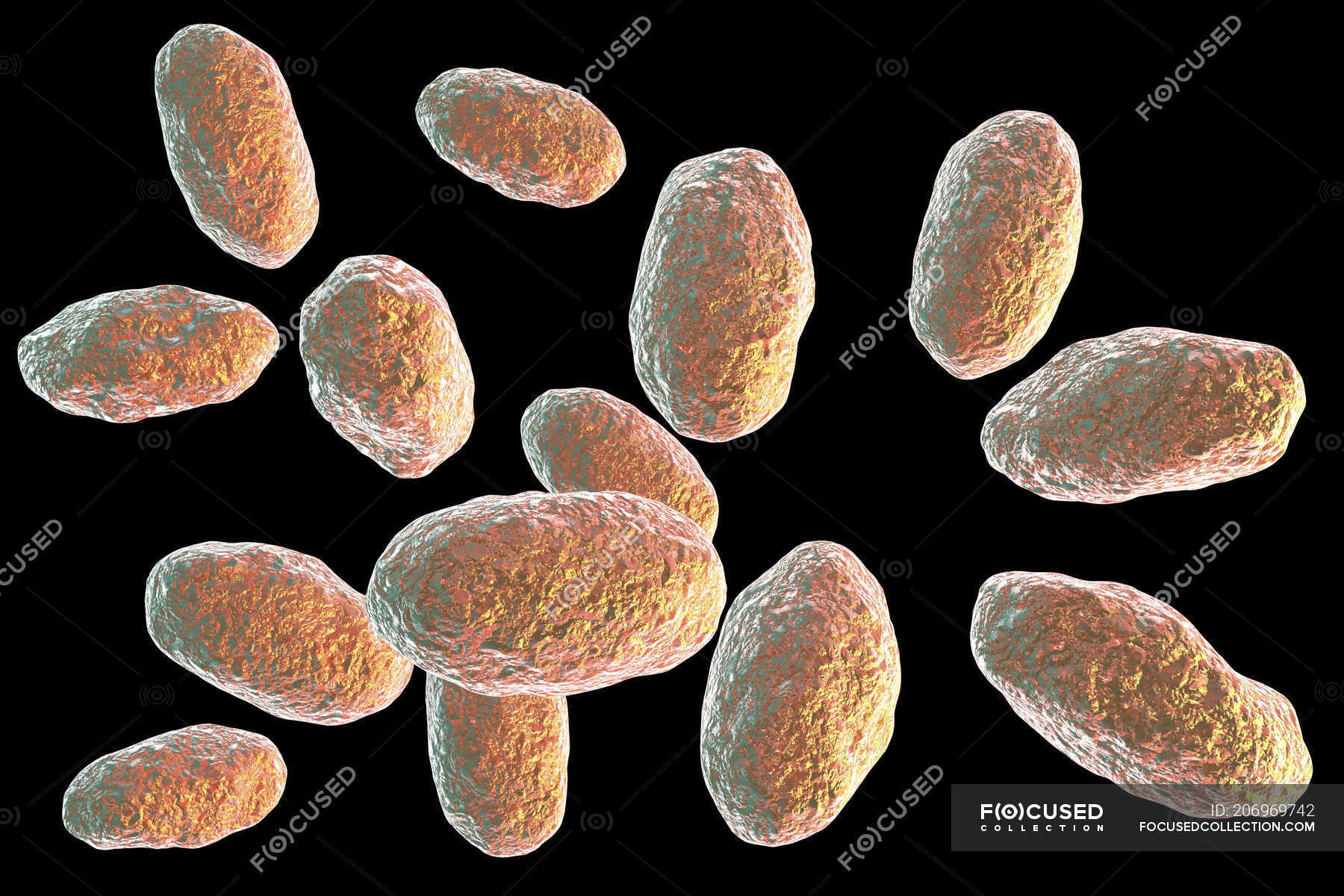 Как правило, заражение кишечными иерсиниями происходит фекально-оральным путем при употреблении контаминированных продуктов питания (молочные продукты, сырое или плохо приготовленное мясо, особенно свинина). Как Y. enterocolitica, так и Y. pseudotuberculosis сохраняют жизнеспособность в условиях пониженных температур. Случаи передачи инфекции от человека к человеку или при переливании инфицированной крови описаны, но очень редки.
Как правило, заражение кишечными иерсиниями происходит фекально-оральным путем при употреблении контаминированных продуктов питания (молочные продукты, сырое или плохо приготовленное мясо, особенно свинина). Как Y. enterocolitica, так и Y. pseudotuberculosis сохраняют жизнеспособность в условиях пониженных температур. Случаи передачи инфекции от человека к человеку или при переливании инфицированной крови описаны, но очень редки.
Следует отметить, что не все кишечные иерсинии являются патогенами. Так, к развитию заболевания у человека приводят серотипы Y. enterocolitica O:3, O:8, O:9 и O:5,27 и Y. pseudotuberculosis O:1 и O:2. Только указанные серотипы являются истинно энетропатогенными иерсиниями.
Особенностью энтеропатогенных иерсиний является их тропность к лимфатичекой ткани. Проникая через слизистую оболочку кишечника, эти микроорганизмы попадают в мезентериальные лимфатические узлы. Развивающийся воспалительный ответ сопровождается болью в области живота и диареей, а также мезентериальным лимфаденитом.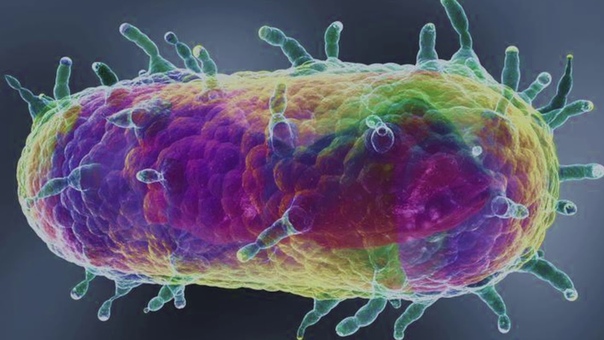 У иммунокомпетентных лиц заражение энтеропатогенными иерсиниями чаще ограничивается гастроэнтеритом и регионарным лимфаденитом. Если возбудителем заболевания является Y. enterocolitica, говорят об иерсиниозе, если Y. pseudotuberculosis – о псевдотуберкулезе. Иерсиниоз встречается чаще, чем псевдотуберкулез. Как при иерсиниозе, так и при псевдотуберкулезе могут наблюдаться иммунопатологические феномены в виде реактивного артрита и узловатой эритемы. У лиц с иммунодефицитом, а также маленьких детей могут наблюдаться тяжелые формы иерсиниоза и псевдотуберкулеза с диссеминацией бактерий и сепсисом.
У иммунокомпетентных лиц заражение энтеропатогенными иерсиниями чаще ограничивается гастроэнтеритом и регионарным лимфаденитом. Если возбудителем заболевания является Y. enterocolitica, говорят об иерсиниозе, если Y. pseudotuberculosis – о псевдотуберкулезе. Иерсиниоз встречается чаще, чем псевдотуберкулез. Как при иерсиниозе, так и при псевдотуберкулезе могут наблюдаться иммунопатологические феномены в виде реактивного артрита и узловатой эритемы. У лиц с иммунодефицитом, а также маленьких детей могут наблюдаться тяжелые формы иерсиниоза и псевдотуберкулеза с диссеминацией бактерий и сепсисом.
Диагностика иерсиниоза и псевдотуберкулеза достаточно сложна. Хотя бактериологический посев кала (крови или других биологических материалов) считается «золотым стандартом» диагностики, он трудноосуществим. Это связано с тем, что энтеропатогенные иерсинии сложно отличить от других кишечных микроорганизмов, которые в норме преобладают в кишечной флоре. После выявлении роста иерсиний проводят дополнительные биохимические тесты, устанавливающие их энтеропатогенность. Кроме того, метод бактериологического посева характеризуется достаточно низкой чувствительностью (для получения результата необходимо 103-106 КОЕ в грамме образца биоматериала). Учитывая эти особенности, диагностика иерсиниоза и псевдотуберкулеза носит комплексный характер и включает следующие дополнительные тесты:
Кроме того, метод бактериологического посева характеризуется достаточно низкой чувствительностью (для получения результата необходимо 103-106 КОЕ в грамме образца биоматериала). Учитывая эти особенности, диагностика иерсиниоза и псевдотуберкулеза носит комплексный характер и включает следующие дополнительные тесты:
- Полимеразная цепная реакция (ПЦР) – один из методов молекулярной диагностики, в ходе которого определяется генетический материал (ДНК) микроорганизма в образце биоматериала (в кале). Основными преимуществами ПЦР являются быстрота получения результата, высокая чувствительность и специфичность. В данное комплексное исследование входит анализ ПЦР на Y. pseudotuberculosis.
- Серологические тесты. Антитела к энтеропатогенным иерсиниям обычно могут быть определены в первые 2-4 недели болезни (IgM-антитела). Следует отметить, что из-за определенного антигенного сходства Yersinia с бактериями других родов (Salmonella, Morganella, Brucella) серологические тесты могут давать ложноположительные результаты.
 Еще одним недостатком серологических тестов является то, что антитела к иерсиниям (IgG-антитела) сохраняются в течение нескольких лет после инфицирования, что может препятствовать интерпретации результата. Следует помнить, что результат серологических тестов зависит от иммунного статуса организма.
Еще одним недостатком серологических тестов является то, что антитела к иерсиниям (IgG-антитела) сохраняются в течение нескольких лет после инфицирования, что может препятствовать интерпретации результата. Следует помнить, что результат серологических тестов зависит от иммунного статуса организма.
Точность ПЦР и серологических тестов в меньшей степени, чем бактериологического метода, подвержена влиянию антибактериальных препаратов. Однако максимально точный результат теста будет получен при анализе биоматериала, полученного до начала лечения.
Гастроэнтерит, возникающий при инфицировании энтеропатогенными иерсиниями, сложно отличить от сальмонеллеза, кампилобактериоза и других кишечных инфекций. По этой причине часто требуются дополнительные лабораторные анализы.
Для чего используется исследование?
- Для диагностики иерсиниоза и псевдотуберкулеза.
Когда назначается исследование?
- При подозрении на иерсиниоз или псевдотуберкулез: лихорадка, тошнота, боли в животе (боль может локализоваться в правой паховой области), диарея, а также узловатая эритема или реактивный артрит;
- в некоторых случаях при подозрении на острый аппендицит.

Что означают результаты?
Референсные значения
Для каждого показателя, входящего в состав комплекса:
Что может влиять на результат?
- Время, прошедшее с момента заражения;
- состояние иммунной системы организма;
- применение антибактериальных препаратов (аминогликозиды, ко-тримоксазол, цефалоспорины, тетрациклины, фторхинолоны).
Важные замечания
- Результат исследования оценивают с учетом анамнестических, клинических и дополнительных лабораторных данных.
Также рекомендуется
[09-150] Yersinia enterocolitica, ДНК [ПЦР]
[10-051] Посев на Yersinia spp.
[07-114] Yersinia pseudotuberculosis, Yersinia enterocolitica, IgА, полуколичественно
[09-134] Острые кишечные инфекции, скрининг (Shigella spp., E. coli (EIEC), Salmonella spp., Campylobacter spp., Adenovirus F, Rotavirus A, Norovirus 2 генотип, Astrovirus)
[02-012] Анализ кала на цисты простейших
[02-010] Анализ кала на яйца гельминтов
[02-001] Анализ кала на скрытую кровь
Кто назначает исследование?
Инфекционист, терапевт, врач общей практики.
Литература
- Galindo CL, Rosenzweig JA, Kirtley ML, Chopra AK. Pathogenesis of Y. enterocolitica and Y. pseudotuberculosis in Human Yersiniosis. J Pathog. 2011;2011:182051.
- McPhee S.J., Papadakis M. CURRENT Medical Diagnosis and Treatment / S. J. McPhee, M. Papadakis; 49 ed. — McGraw-Hill Medical, 2009.
Памятка для населения по профилактике заболеваний псевдотуберкулёзом
Ежегодно среди населения регистрируются заболевания псевдотуберкулёзом. Употребление в пищу в сыром виде (без термической обработки) не качественно обработанных овощей и фруктов, загрязнённых патогенными микроорганизмами – иерсиниями, может привести к заболеванию людей псевдотуберкулёзом.
Псевдотуберкулез — инфекционное заболевание человека бактериальной природы. Ведущее эпидемиологическое значение в качестве источника инфекции для человека имеют грызуны: полевые и домашние мыши и крысы, которые своими экскрементами обсеменяют овощи и фрукты, продукты питания, хранящиеся на складах.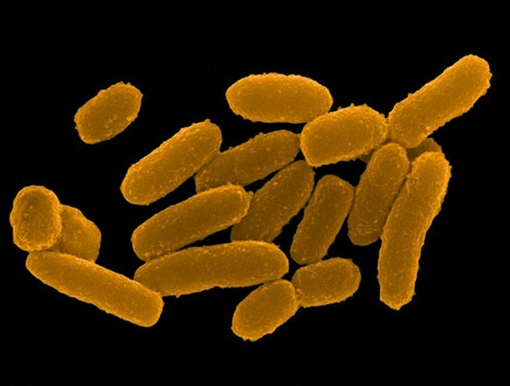 При этом внешний вид и вкусовые качества обсеменённых иерсиниями овощей и фруктов не изменяются.
При этом внешний вид и вкусовые качества обсеменённых иерсиниями овощей и фруктов не изменяются.
Заболевание характеризуется высокой температурой тела, интоксикацией, гиперемией зева или ангиной, мелкоточечной сыпью и/или сыпью в виде «перчаток» и «носок» на конечностях, кишечными проявлениями (боль в животе, жидкий стул, рвота), часто гепатоспленомегалией.
Название «псевдотуберкулез» заболевание получило из-за внешнего сходства паталогоанатомических изменений в органах с экспериментальным туберкулезом у животных.
Возбудитель заболевания – иерсиния псевдотуберкулезис, устойчива во внешней среде (почве, воде), а при низких температурах (+4 +8 градусов) и высокой влажности она способна размножаться. В тоже время возбудитель заболевания не стоек к высыханию, воздействию солнечного света, высокой температуре. Кипячение убивает микроба почти мгновенно, а при нагревании до 60-70 градусов — в течение 30 минут. Хорошо чувствителен он к дезсредствам, а также к 3% раствору уксусной кислоты.
Чаще всего заражение происходит при употреблении овощных салатов из свежей капусты, моркови, репчатого и зеленого лука, фруктов (яблоки, груши, виноград и т.д.), а также других пищевых продуктов длительного хранения, не имеющих индивидуальной упаковки (например: кондитерские изделия). Самым благоприятным пищевым субстратом для размножения псевдотуберкулезного микроба является свежая капуста, где размножение возбудителя начинается с 4-5 дня и максимума достигает на 10-й день. На свежей капусте, моркови, яблоках, луке репчатом он сохраняется в течение 2-х месяцев, в квашеной капусте 3 суток, на свежих огурцах, редисе — 14-22 дня.
При употреблении овощей и фруктов в свежем виде или салатов в зимне-весенний период года с целью профилактики псевдотуберкулёза необходимо соблюдать следующие правила:
-верхние 5-6 листов кочана капусты для приготовления салатов и употребления в сыром виде не используется, их можно использовать только для супов или тушения;
-освобождённый от верхних листьев кочан капусты, а также очищенные от кожуры овощи и фрукты перед шинковкой на салат или употреблением в сыром виде, необходимо тщательно промыть под проточной водой, а затем ошпарить кипятком или замочить на несколько минут в 3% растворе уксусной кислоты;
-приготовленные салаты хранят в холодильнике не более 6-ти часов в не заправленном виде, заправляют непосредственно перед употреблением в пищу.
-обрабатывать моющими средствами оборудование и инвентарь (овощерезки, разделочные доски, ножи), предназначенные для обработки овощей;
-обрабатывать столовую посуду, разделочные столы, кухонный инвентарь,
-тщательное мытье всех овощей, предназначенных для приготовления салатов или выдачи их в сыром виде, мытье в проточной водопроводной воде с последующим ошпариванием кипятком, не хранить очищенные овощи в холодной воде, особенно в холодильниках, мытье фруктов, в т.ч. бананов и цитрусовых;
-соблюдение регламентированных сроков хранения готовых блюд;
-тщательное мытье упаковок пищевых продуктов перед их использованием,
-своевременное проведение дератизационных мероприятий при появлении грызунов.
От больного к здоровому человеку заболевание не передается, поэтому не проводится дезинфекция помещения и предметов ухода за больными. Своевременное обращение к врачу и полноценное лечение предупреждает длительное течение заболевания.
(по письму Онищенко)
РПГА с Yersinia pseudotuberculosis (Y.
 pseudotuberculosis IHA)
pseudotuberculosis IHA)Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения и коэффициенты пересчёта: тест полуколичественный.
Результат предоставляется в форме «отрицательно» или «положительно» (в последнем случае с приведением титра – последнего разведения сыворотки дающего положительный результат). Диагностически достоверным считают прирост титров в 4 и более раз за 7-10 дней.
Условно-диагностический титр – 1:100. При групповых вспышках псевдотуберкулёза для детей до 5 лет условно-диагностический титр может быть снижен до 1:50.
Референсные значения: отрицательно.
Интерпретация результата
Положительно:
- текущая или перенесённая в прошлом инфекция. Рекомендовано обследовать больного не менее 2 раз – в начале заболевания и с интервалом в 7-10 дней, диагностически достоверным считают 4-кратный и более прирост титров антител. При необходимости оценивать одиночные результаты или отсутствии выраженной динамики титров допустимо использовать минимальный условно-диагностический титр 1:100. При групповых вспышках псевдотуберкулёза для детей до 5 лет условно диагностический титр может быть снижен до 1:50. Результат следует оценивать в комплексе с эпидобстановкой, формой и сроками болезни;
- редко — перекрёстные реакции (другие виды Yersinia,Vibrio, Salmonella, Brucella, Rickettsia).
Отрицательно:
- отсутствие инфекции данным сероваром Yersinia pseudotuberculosis;
- низкая концентрация или отсутствие антител в ранний период инфекции.
Псевдотуберкулез (инфекция, вызванная Yersinia pseudotuberculosis): основы практики, общие сведения, патофизиология
Автор
Дэвид Р. Хабурчак, доктор медицины, FACP Заслуженный профессор медицины, факультет медицины, отделение инфекционных болезней, Медицинский колледж Джорджии Университета Огаста; Ведущий преподаватель, Программа резидентуры по внутренним болезням Wellstar Kennestone, Wellstar Health System
Хабурчак, доктор медицины, FACP Заслуженный профессор медицины, факультет медицины, отделение инфекционных болезней, Медицинский колледж Джорджии Университета Огаста; Ведущий преподаватель, Программа резидентуры по внутренним болезням Wellstar Kennestone, Wellstar Health System
Дэвид Р. Хабурчак, доктор медицины, FACP является членом следующих медицинских обществ: Американского колледжа врачей, Американского общества Ослера, Американского общества микробиологии, Христианских медицинских и стоматологических ассоциаций , Общество инфекционных болезней Америки
Раскрытие информации: нечего раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие: Получил зарплату от Medscape за работу. для: Medscape.
Джозеф Ф. Джон, младший, доктор медицины, FACP, FIDSA, FSHEA Клинический профессор медицины, молекулярной генетики и микробиологии Медицинского колледжа Медицинского университета Южной Каролины; Заместитель начальника отдела образования, Медицинский центр по делам ветеранов Ральфа Х. Джонсона
Джон, младший, доктор медицины, FACP, FIDSA, FSHEA Клинический профессор медицины, молекулярной генетики и микробиологии Медицинского колледжа Медицинского университета Южной Каролины; Заместитель начальника отдела образования, Медицинский центр по делам ветеранов Ральфа Х. Джонсона
Джозеф Ф. Джон младший, доктор медицинских наук, FACP, FIDSA, FSHEA является членом следующих медицинских обществ: Медицинская ассоциация округа Чарлстон, Американское общество инфекционных болезней, Южная Общество инфекционных болезней Каролины
Раскрытие информации: нечего раскрывать.
Главный редактор
Марк Р. Уоллес, MD, FACP, FIDSA Врач-инфекционист, Госпиталь Скагит-Вэлли, Региональное здравоохранение Скагита
Раскрытие информации: Ничего не разглашать.
Дополнительные участники
Хари Поленаковик, доктор медицины, FACP, FIDSA Профессор медицины, Государственный университет Райта, Медицинская школа Буншофт
Хари Поленаковик, доктор медицины, FACP, FIDSA является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей , Американское общество микробиологов, Европейское общество клинической микробиологии и инфекционных заболеваний, Американское общество инфекционных болезней, Американское общество эпидемиологии здравоохранения
Раскрытие: нечего раскрывать.
Асим Яни, доктор медицины, магистр здравоохранения, FACP Клиницист-педагог и эпидемиолог, консультант и старший врач, Департамент здравоохранения Флориды; Дипломант, инфекционные заболевания, внутренняя медицина и профилактическая медицина
Асим А Яни, доктор медицинских наук, магистр здравоохранения, FACP является членом следующих медицинских обществ: Американской ассоциации врачей общественного здравоохранения, Американского колледжа врачей, Американского колледжа профилактической медицины, Американской медицины. Ассоциация, Американская ассоциация общественного здравоохранения, Американское общество инфекционных заболеваний
Раскрытие информации: нечего раскрывать.
Пол Чен Юго-западная медицинская школа Техасского университета
Раскрытие информации: раскрывать нечего.
Псевдотуберкулез (инфекция, вызванная Yersinia pseudotuberculosis) Клиническая картина: история болезни, физикальное состояние, причины
Автор
Дэвид Р. Хабурчак, доктор медицины, FACP Заслуженный профессор медицины, факультет медицины, отделение инфекционных болезней, Медицинский колледж Джорджии Университета Огаста; Ведущий преподаватель, Программа резидентуры по внутренним болезням Wellstar Kennestone, Wellstar Health System
Хабурчак, доктор медицины, FACP Заслуженный профессор медицины, факультет медицины, отделение инфекционных болезней, Медицинский колледж Джорджии Университета Огаста; Ведущий преподаватель, Программа резидентуры по внутренним болезням Wellstar Kennestone, Wellstar Health System
Дэвид Р. Хабурчак, доктор медицины, FACP является членом следующих медицинских обществ: Американского колледжа врачей, Американского общества Ослера, Американского общества микробиологии, Христианских медицинских и стоматологических ассоциаций , Общество инфекционных болезней Америки
Раскрытие информации: нечего раскрывать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие: Получил зарплату от Medscape за работу. для: Medscape.
Джозеф Ф. Джон, младший, доктор медицины, FACP, FIDSA, FSHEA Клинический профессор медицины, молекулярной генетики и микробиологии Медицинского колледжа Медицинского университета Южной Каролины; Заместитель начальника отдела образования, Медицинский центр по делам ветеранов Ральфа Х. Джонсона
Джон, младший, доктор медицины, FACP, FIDSA, FSHEA Клинический профессор медицины, молекулярной генетики и микробиологии Медицинского колледжа Медицинского университета Южной Каролины; Заместитель начальника отдела образования, Медицинский центр по делам ветеранов Ральфа Х. Джонсона
Джозеф Ф. Джон младший, доктор медицинских наук, FACP, FIDSA, FSHEA является членом следующих медицинских обществ: Медицинская ассоциация округа Чарлстон, Американское общество инфекционных болезней, Южная Общество инфекционных болезней Каролины
Раскрытие информации: нечего раскрывать.
Главный редактор
Марк Р. Уоллес, MD, FACP, FIDSA Врач-инфекционист, Госпиталь Скагит-Вэлли, Региональное здравоохранение Скагита
Раскрытие информации: Ничего не разглашать.
Дополнительные участники
Хари Поленаковик, доктор медицины, FACP, FIDSA Профессор медицины, Государственный университет Райта, Медицинская школа Буншофт
Хари Поленаковик, доктор медицины, FACP, FIDSA является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей , Американское общество микробиологов, Европейское общество клинической микробиологии и инфекционных заболеваний, Американское общество инфекционных болезней, Американское общество эпидемиологии здравоохранения
Раскрытие: нечего раскрывать.
Асим Яни, доктор медицины, магистр здравоохранения, FACP Клиницист-педагог и эпидемиолог, консультант и старший врач, Департамент здравоохранения Флориды; Дипломант, инфекционные заболевания, внутренняя медицина и профилактическая медицина
Асим А Яни, доктор медицинских наук, магистр здравоохранения, FACP является членом следующих медицинских обществ: Американской ассоциации врачей общественного здравоохранения, Американского колледжа врачей, Американского колледжа профилактической медицины, Американской медицины. Ассоциация, Американская ассоциация общественного здравоохранения, Американское общество инфекционных заболеваний
Раскрытие информации: нечего раскрывать.
Пол Чен Юго-западная медицинская школа Техасского университета
Раскрытие информации: раскрывать нечего.
Yersinia pseudotuberculosis — Инфекционные болезни и противомикробные препараты
Yersinia pseudotuberculosis вызывает зоонозную кишечную инфекцию у сельскохозяйственных животных, диких животных и птиц. Люди приобретают его, употребляя пищу или воду, загрязненную фекалиями животных. Он обычно вызывает легкие, самостоятельно купирующиеся заболевания мезентериального аденита, илеита и диареи, но может вызвать серьезный сепсис и абсцессы у пациентов с ослабленным иммунитетом.Эта инфекция встречается реже, чем инфекция, вызванная двумя другими возбудителями Yersinia Y. pestis и Y. enterocolitica . В последнее десятилетие его геном был выяснен благодаря интересу к этой бактерии как к предку бациллы чумы Y. pestis , с которой она имеет более 90% общих генов (1).
Люди приобретают его, употребляя пищу или воду, загрязненную фекалиями животных. Он обычно вызывает легкие, самостоятельно купирующиеся заболевания мезентериального аденита, илеита и диареи, но может вызвать серьезный сепсис и абсцессы у пациентов с ослабленным иммунитетом.Эта инфекция встречается реже, чем инфекция, вызванная двумя другими возбудителями Yersinia Y. pestis и Y. enterocolitica . В последнее десятилетие его геном был выяснен благодаря интересу к этой бактерии как к предку бациллы чумы Y. pestis , с которой она имеет более 90% общих генов (1).
МИКРОБИОЛОГИЯ
Характеристики
Ю.pseudotuberculosis — грамотрицательная палочка и факультативный анаэроб из семейства Enterobacteriaceae. Он является оксидазонегативным, не ферментирующим лактозу, положительным по уреазе, отрицательным цитратом и подвижным при выращивании при 25 0 ° C, но не подвижным при выращивании при 37 0 ° C. Оптимальная скорость роста составляет 30 0 ° C. C, и он будет расти в забуференном физиологическом растворе при 4 0 C. Было идентифицировано шесть серотипов (I-VI) и четыре подтипа, при этом группа O I составляет примерно 80% случаев заболевания людей.Он продуцирует липополисахаридный (ЛПС) эндотоксин с О-антигенной боковой цепью, который имеет биологическую активность, аналогичную активности других грамотрицательных бактерий.
Оптимальная скорость роста составляет 30 0 ° C. C, и он будет расти в забуференном физиологическом растворе при 4 0 C. Было идентифицировано шесть серотипов (I-VI) и четыре подтипа, при этом группа O I составляет примерно 80% случаев заболевания людей.Он продуцирует липополисахаридный (ЛПС) эндотоксин с О-антигенной боковой цепью, который имеет биологическую активность, аналогичную активности других грамотрицательных бактерий.
Генетика вирулентности
Y. pseudotuberculosis несет ту же плазмиду вирулентности 70 т.п.н., что и другой патогенный Yersiniae, pYV, который кодирует систему секреции типа III (TTSS), иерсиниальные внешние белки (Yops) и антиген V, которые продуцируются в культуре при 37 0 ° C в ограничивающих рост условиях низких концентраций кальция.TTSS использует игольчатую инъекцию для вставки Yops в клетки-хозяева. Основные эффекты Yops, которые являются различными ферментами, активаторами ферментов и цитотоксинами, заключаются в подавлении фагоцитоза путем подавления цитокинов и вызывая апоптоз макрофагов (9). Мутанты Y. pseudotuberculosis , которые были дефицитными по YopE и YopH у мышей, могли колонизировать кишечник и пятна Пейера, но не достигли селезенки и печени (16). Другие мутанты, дефицитные по Yops и TTSS, не могли выжить в кишечнике мышей после инокуляции орогастрия (17).YadA — это молекула адгезии, кодируемая плазмидой pYV, которая необходима для выживания и репликации в пятнах Пейера. С другой стороны, сообщалось о двух пациентах, в культурах которых были обнаружены pYV-отрицательные бактерии (27). Хромосомные гены, которые также важны для вирулентности, включают ген инвазина, который способствует проникновению бактерий в М-клетки, которые покрывают пятна Пейера (9). Мутанты с генами, дефектными для синтеза О-антигена в LPS, приводящие к появлению бактерий с грубой морфологией колоний, приводят к тому, что организмы не могут выжить в кишечнике мыши, а также не могут проникать в эпителиальные клетки (17).Было показано, что цитотоксический некротический фактор (CNF) секретируется растущими бактериями и может нацеливаться на GTPases клетки-хозяина (15).
Мутанты Y. pseudotuberculosis , которые были дефицитными по YopE и YopH у мышей, могли колонизировать кишечник и пятна Пейера, но не достигли селезенки и печени (16). Другие мутанты, дефицитные по Yops и TTSS, не могли выжить в кишечнике мышей после инокуляции орогастрия (17).YadA — это молекула адгезии, кодируемая плазмидой pYV, которая необходима для выживания и репликации в пятнах Пейера. С другой стороны, сообщалось о двух пациентах, в культурах которых были обнаружены pYV-отрицательные бактерии (27). Хромосомные гены, которые также важны для вирулентности, включают ген инвазина, который способствует проникновению бактерий в М-клетки, которые покрывают пятна Пейера (9). Мутанты с генами, дефектными для синтеза О-антигена в LPS, приводящие к появлению бактерий с грубой морфологией колоний, приводят к тому, что организмы не могут выжить в кишечнике мыши, а также не могут проникать в эпителиальные клетки (17).Было показано, что цитотоксический некротический фактор (CNF) секретируется растущими бактериями и может нацеливаться на GTPases клетки-хозяина (15). Кроме того, суперантигенный токсин YPMa, также называемый митогеном, производным от Y. pseudotuberculosis , присутствует в 20% европейских изолятов и обладает активностью при внутривенном инфицировании мышей, ускоряя смертность (3).
Кроме того, суперантигенный токсин YPMa, также называемый митогеном, производным от Y. pseudotuberculosis , присутствует в 20% европейских изолятов и обладает активностью при внутривенном инфицировании мышей, ускоряя смертность (3).
ЭПИДЕМИОЛОГИЯ
Зоонозная инфекция, Y.pseudotuberculosis имеет свои естественные резервуары в сельскохозяйственных животных, диких грызунах, кроликах, оленях и птицах, включая индеек, уток, гусей, голубей, фазанов и канареек. Передается среди животных фекально-оральным путем. Люди заражаются при употреблении свежих продуктов, зараженных фекалиями животных, зараженного мяса, особенно свинины, и непастеризованного молока или загрязненной воды. Инфекция встречается во всем мире, но большинство случаев зарегистрировано во Франции и Скандинавии.О вспышках болезней пищевого происхождения, связанных с тертой морковью и салатом айсберг, сообщалось из Финляндии (11, 23). Во время вспышек, связанных с морковью, продукты хранились в открытых контейнерах в течение зимних месяцев, обеспечивая доступ к грызунам, а также естественное холодное обогащение, и морковь не промывалась перед теркой для потребления в сыром виде (10, 20). Во время этих вспышек у более 500 школьников возникли лихорадка и боли в животе, а 5 были перенесены ненужные аппендэктомии. Инкубационный период составлял 4-18 дней, в среднем 8 дней.Прием пищи вне дома был фактором риска инфицирования в Финляндии (11). В исследовании финских свиней бактерии были изолированы от 17% выборки из 364 животных, причем больше инфекций было обнаружено у свиней, выращиваемых на органических фермах и на фермах с более чем 1000 свиней (14). Свиньи, являющиеся переносчиками этой инфекции, не проявляют признаков болезни. Миндалины кабанов в Швеции содержали этот организм примерно у 20% животных (21). Миндалины забитых свиней из бельгийских ферм содержали его у 2-10% животных (24). Установлено, что он является важной причиной смерти коз в Калифорнии (6).
Во время вспышек, связанных с морковью, продукты хранились в открытых контейнерах в течение зимних месяцев, обеспечивая доступ к грызунам, а также естественное холодное обогащение, и морковь не промывалась перед теркой для потребления в сыром виде (10, 20). Во время этих вспышек у более 500 школьников возникли лихорадка и боли в животе, а 5 были перенесены ненужные аппендэктомии. Инкубационный период составлял 4-18 дней, в среднем 8 дней.Прием пищи вне дома был фактором риска инфицирования в Финляндии (11). В исследовании финских свиней бактерии были изолированы от 17% выборки из 364 животных, причем больше инфекций было обнаружено у свиней, выращиваемых на органических фермах и на фермах с более чем 1000 свиней (14). Свиньи, являющиеся переносчиками этой инфекции, не проявляют признаков болезни. Миндалины кабанов в Швеции содержали этот организм примерно у 20% животных (21). Миндалины забитых свиней из бельгийских ферм содержали его у 2-10% животных (24). Установлено, что он является важной причиной смерти коз в Калифорнии (6).
КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ
Наиболее частыми проявлениями являются лихорадка и боль или спазмы в животе (2). Около половины пациентов испытывают боли в спине, а четверть пациентов страдают рвотой или диареей. Боль в животе часто возникает в правом нижнем квадранте, что соответствует клинической картине дистального илеита и регионарного лимфаденита, что дает основание для диагностического наименования «псевдоаппендицит». Этот диагноз в некоторых случаях приводит к аппендэктомии, но ультразвуковое исследование и компьютерная томография могут правильно выявить илеит и мезентериальный лимфаденит (27).Хотя в аппендэктомии нет необходимости, сообщалось, что Y. pseudotuberculosis вызывает редкую форму заболевания, называемую гранулематозным аппендицитом (13). Другой особенностью этой инфекции, встречающейся у половины пациентов, является узловатая эритема, которая обычно следует за появлением абдоминальных симптомов примерно через 10 дней (10). Узловатая эритема — это постинфекционная иммунологическая реакция, которая возникает в основном у детей (25). Точно так же реактивный артрит развивается у четверти пациентов и более вероятен у взрослых с аллелем главного комплекса гистосовместимости HLA-B27 (25).
Узловатая эритема — это постинфекционная иммунологическая реакция, которая возникает в основном у детей (25). Точно так же реактивный артрит развивается у четверти пациентов и более вероятен у взрослых с аллелем главного комплекса гистосовместимости HLA-B27 (25).
Инфекция может распространяться из брюшной полости через кровоток, особенно у лиц с ослабленным иммунитетом, вызывая сепсис, абсцессы печени или селезенки, остеомиелит и септический артрит. В сообщении о 27 случаях заболевания во Франции в 2004-2005 гг. У 22 человек были бактерии, выделенные из крови, а у 5 — из фекалий (26). Иммунодефицитные состояния присутствовали в 17 из этих случаев, включая сахарный диабет, рак, ВИЧ-инфекцию, цирроз и трансплантацию почки.Шесть из них погибли. Другие зарегистрированные случаи сепсиса также включали пациентов с инсулиннезависимым сахарным диабетом и ВИЧ-инфекцией (5, 18, 19).
Болезнь Кавасаки, самостоятельно купирующийся фебрильный васкулит у детей раннего возраста, как полагают, в некоторых случаях вызывается Y. pseudotuberculosis . В серии из 452 случаев в Японии 42 ребенка, у которых были положительные посевы стула или повышенные титры антител, с большей вероятностью демонстрировали потенциально серьезные последствия дилатации коронарных артерий и аневризм (22).
pseudotuberculosis . В серии из 452 случаев в Японии 42 ребенка, у которых были положительные посевы стула или повышенные титры антител, с большей вероятностью демонстрировали потенциально серьезные последствия дилатации коронарных артерий и аневризм (22).
ЛАБОРАТОРНАЯ ДИАГНОСТИКА
У . pseudotuberculosis может быть идентифицирован в культурах по признакам того, что он является грамотрицательной палочкой, которая является лактозонегативной, оксидазонегативной и уреазопозитивной. Он отличается от других кишечных патогенов дополнительными химическими реакциями: отрицательными для Фогеса-Проскауэра, цитрата, фенилаланиндезаминазы, орнитиндекарбоксилазы, ферментации сахарозы и целлобиозы, в то время как положительные для ферментации рамнозы и мелибиозы.В культурах стула рост на агаре MacConkey или SS приведет к образованию очень маленьких колоний через 24 часа при 37 0 ° C, но колонии будут видны через 48 часов. Извлечение из образцов стула или загрязненных образцов окружающей среды может быть увеличено за счет использования селективных сред. Одним из них является агар CIN (цефсулодин-иргасан-новобиоцин), содержащий антибиотики, к которым бактерии устойчивы. Образцы для культивирования также можно охладить, поместив их в бульон с фосфатным буфером и инкубируя при 4 0 ° C в течение 7 или 14 дней (14).ПЦР в реальном времени — альтернативный метод диагностики пищевых инфекций (12, 21).
Извлечение из образцов стула или загрязненных образцов окружающей среды может быть увеличено за счет использования селективных сред. Одним из них является агар CIN (цефсулодин-иргасан-новобиоцин), содержащий антибиотики, к которым бактерии устойчивы. Образцы для культивирования также можно охладить, поместив их в бульон с фосфатным буфером и инкубируя при 4 0 ° C в течение 7 или 14 дней (14).ПЦР в реальном времени — альтернативный метод диагностики пищевых инфекций (12, 21).
ПАТОГЕНЕЗ
Организмы попадают в организм с зараженными пищевыми продуктами, такими как салаты, содержащие морковь или салат, или свинину, или в воде. Во время инкубационного периода, который в среднем составляет 8 дней, бактерии достигают терминального отдела подвздошной кишки и проксимального отдела толстой кишки, где они проникают через эпителиальные клетки, покрывающие лимфоидные ткани, связанные с кишечником, включая пейеровские бляшки. Как внутриклеточная инфекция, бактерии захватываются макрофагами, где они выживают и размножаются. Используя TTSS и Yops, Y. pseudotuberculosis действует, чтобы ингибировать фагоцитоз, предоставляя организмам больший доступ к мезентериальным лимфатическим узлам и кровотоку. Результатом этой инфекции являются изъязвления слизистой оболочки в терминальном отделе подвздошной кишки, реже изъязвления восходящей толстой кишки, некротические поражения на участках Пейера и увеличение мезентериальных лимфатических узлов. Прогноз для пациентов с мезентериальным лимфаденитом и илеитом благоприятен для выздоровления от самоограничивающейся инфекции практически у всех ранее здоровых людей, но пациенты с септицемией, у которых часто есть сопутствующие иммунодефицитные заболевания, примерно в 27% случаев имеют смертельный исход. несмотря на противомикробную терапию в больнице (26).Хотя острый аппендицит не вызывается Yersinae , случаи гранулематозного аппендицита были отнесены к Y.
Как внутриклеточная инфекция, бактерии захватываются макрофагами, где они выживают и размножаются. Используя TTSS и Yops, Y. pseudotuberculosis действует, чтобы ингибировать фагоцитоз, предоставляя организмам больший доступ к мезентериальным лимфатическим узлам и кровотоку. Результатом этой инфекции являются изъязвления слизистой оболочки в терминальном отделе подвздошной кишки, реже изъязвления восходящей толстой кишки, некротические поражения на участках Пейера и увеличение мезентериальных лимфатических узлов. Прогноз для пациентов с мезентериальным лимфаденитом и илеитом благоприятен для выздоровления от самоограничивающейся инфекции практически у всех ранее здоровых людей, но пациенты с септицемией, у которых часто есть сопутствующие иммунодефицитные заболевания, примерно в 27% случаев имеют смертельный исход. несмотря на противомикробную терапию в больнице (26).Хотя острый аппендицит не вызывается Yersinae , случаи гранулематозного аппендицита были отнесены к Y. pseudotuberculosis , как показало применение ПЦР-зондов к хирургическим образцам (13). В этих тканях были обнаружены эпителиоидные гранулемы, трансмуральные лимфоидные агрегаты, гигантские клетки, изъязвления слизистой оболочки, криптит, ассоциированное поражение лимфатических узлов и в большинстве случаев отсутствие микроабсцессов. Хотя Y. pseudotuberculosis не является причиной болезни Крона, небольшой процент острых инфекций сопровождался хроническими симптомами, которые привели к диагнозу болезни Крона.Кроме того, у пациентов с болезнью Крона нарушен барьер слизистой оболочки, что может предрасполагать к иерсиниозу (8).
pseudotuberculosis , как показало применение ПЦР-зондов к хирургическим образцам (13). В этих тканях были обнаружены эпителиоидные гранулемы, трансмуральные лимфоидные агрегаты, гигантские клетки, изъязвления слизистой оболочки, криптит, ассоциированное поражение лимфатических узлов и в большинстве случаев отсутствие микроабсцессов. Хотя Y. pseudotuberculosis не является причиной болезни Крона, небольшой процент острых инфекций сопровождался хроническими симптомами, которые привели к диагнозу болезни Крона.Кроме того, у пациентов с болезнью Крона нарушен барьер слизистой оболочки, что может предрасполагать к иерсиниозу (8).
УСТОЙЧИВОСТЬ IN VITRO И IN VIVO
Изоляты Y. pseudotuberculosis проявили чувствительность к ампициллину, цефалоспоринам, тетрациклину, триметоприм-сульфаметоксазолу, хлорамфениколу, фторхинолонам и аминогликозидам. Организм устойчив к колистину. Будучи полностью чувствительным к ампициллину и цефалоспоринам первого поколения, он отличается от Y.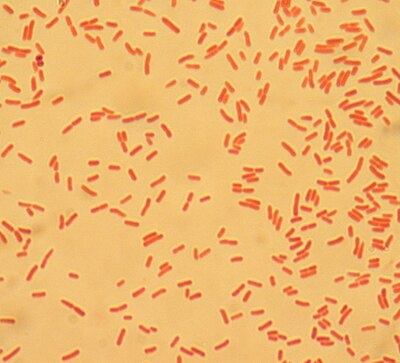 enterocolitica , несущая бета-лактамазу устойчивости к ампициллину и цефалоспоринам первого поколения.
enterocolitica , несущая бета-лактамазу устойчивости к ампициллину и цефалоспоринам первого поколения.
ПРОТИВОМИКРОБНАЯ ТЕРАПИЯ
Лечение нецелесообразно в большинстве случаев самоограничивающегося мезентериального лимфаденита и илеита, проявляющихся лихорадкой и болями в животе. Кроме того, диагноз не доступен по культуре во время острого заболевания. С другой стороны, пациентов с сепсисом необходимо лечить как можно быстрее, чтобы предотвратить летальный исход.К их преимуществу, большинство пациентов с сепсисом будут эмпирически начаты на антимикробной схеме лечения лихорадки до того, как будет установлен диагноз Y. pseudotuberculosis . Пациенты должны получать ампициллин (от 100 до 200 мг / кг / день внутривенно) или тетрациклин, доксициклин или аминогликозид в стандартных дозах при тяжелых инфекциях. Офлоксацин 400 мг / день и цефтриаксон 2 г / день были успешно использованы у пациента с септическим артритом (4). Ампициллин и гентамицин успешно применялись у пациента с абсцессами селезенки (19).Пациента с инфицированной аневризмой аорты вылечили хирургической резекцией с последующим введением цефтриаксона 1 г / день и ципрофлоксацина 200 мг 3 раза в день внутривенно (7).
Ампициллин и гентамицин успешно применялись у пациента с абсцессами селезенки (19).Пациента с инфицированной аневризмой аорты вылечили хирургической резекцией с последующим введением цефтриаксона 1 г / день и ципрофлоксацина 200 мг 3 раза в день внутривенно (7).
АДЪЮНКТИВНАЯ ТЕРАПИЯ
Пациентам с кишечным иерсиниозом выполнены ненужные аппендэктомии. Компьютерная томография брюшной полости может выявить мезентериальный лимфаденит, чтобы исключить острый аппендицит, что позволяет избежать операции у пациентов.С другой стороны, хирургическое вмешательство подходит пациентам с инфицированными аневризмами и абсцессом селезенки (7, 19). Пациентам с реактивным артритом полезно лечение нестероидными противовоспалительными средствами, внутрисуставные инъекции стероидов и физиотерапия.
КОНЕЧНЫЕ ТОЧКИ ТЕРАПИИ
Пациентам с сепсисом внутривенные противомикробные препараты вводятся в течение примерно 14 дней. В течение этого времени пациенты должны отложить лечение и устранить симптомы инфекции.Если используется гентамицин или другие аминогликозиды, следует измерять концентрацию антибиотика в сыворотке, чтобы гарантировать терапевтическую эффективность и избежать токсичности. Рекомендуются анализы крови на креатинин сыворотки и функции печени, а также общий анализ крови.
В течение этого времени пациенты должны отложить лечение и устранить симптомы инфекции.Если используется гентамицин или другие аминогликозиды, следует измерять концентрацию антибиотика в сыворотке, чтобы гарантировать терапевтическую эффективность и избежать токсичности. Рекомендуются анализы крови на креатинин сыворотки и функции печени, а также общий анализ крови.
ВАКЦИНЫ
В настоящее время вакцины отсутствуют.
ПРОФИЛАКТИКА
Эти инфекции передаются в основном через инфицированную пищу.Свежие продукты, такие как морковь и салат, перед употреблением следует мыть и не хранить в открытых контейнерах, доступных для грызунов. Следует избегать непастеризованных молочных продуктов и сырого или не полностью приготовленного мяса, особенно свинины. Продолжительное охлаждение продуктов перед употреблением не рекомендуется, потому что Yersiniae способны расти при температуре 4 0 C.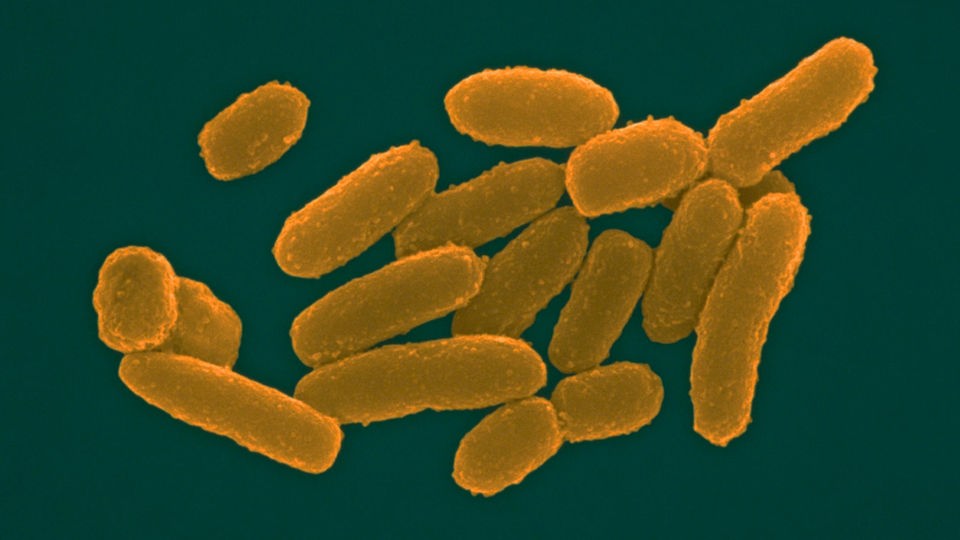
ССЫЛКИ
1.Achtman M, Zurth K, Morelli G, Torrea G, Guiyoule A, Carniel E. Yersinia pestis , вызывающая чуму, представляет собой недавно появившийся клон Yersinia pseudotuberculosis. PNAS 1999; 96: 14043-14048. [PubMed]
2. Бертелли Л., Мазетти Р., Бардаси Г., Маретти М., Гаргано Т., Корсини И., Мельчионда Ф., Тассинари Д., Каззато С., Лима М., Пессия А. Два случая боли в животе у детей с мезентериальным лимфаденитом из-за Yersinia pseudotuberculosis инфекция. Журнал Педиатр 2014; 165: 411.[PubMed]
3. Карной С., Кефаль С., Мюллер-Алуф Х., Летеуртр Э., Симонет М. Суперантиген YPMa усиливает вирулентность Yersinia pseudotuberculosis у мышей. Infect Immun 2000; 68: 2553-2559. [PubMed]
4. Кормье Г., Лукас В., Варин С., Хамелин Дж. П., Танги Г. Yersinia pseudotuberculosis Инфекция пояснично-фасеточного сустава. Костный сустав позвоночника 2007; 74: 110-111. [PubMed]
[PubMed]
5. Дикон А.Г., Хей Х., Дункан Дж. Септицемия, вызванная Yersinia pseudotuberculosis — отчет о болезни.Clin Microbiol Infect 2003; 9: 1118-1119. [PubMed]
6. Джаннитти Ф., Барр BC, Брито Б.П., Узал Ф.А., Вильянуэва М., Андерсон М. Yersinia pseudotuberculosis Инфекции коз и других животных, диагностированные в системе лабораторий по охране здоровья животных и безопасности пищевых продуктов Калифорнии: 1990-2012. J Vet Diagn Invest 2014; 26: 88-95. [PubMed]
7. Хаду Х., Эльфарра М., Алаузет С., Гине Ф., Лозневский А., Лион С. Аневризма брюшной аорты, инфицированная Yersinia pseudotuberculosis .J Clin Microbiol 2006; 44: 3457-3458. [PubMed]
8. Хоумвуд Р., Гиббонс С.П., Ричардс Д., Льюис А., Дуэйн П.Д., Гриффитс А.П. Илеит, вызванный Yersinia pseudotuberculosis при болезни Крона. J Infect 2003; 47: 328-332. [PubMed]
9. Hudson KJ, Bouton AH. Yersinia pseudotuberculosis адгезины регулируют тканеспецифическую колонизацию и локализацию иммунных клеток на мышиной модели системной инфекции. Infect Immun 2006: 74: 6487-6490. [PubMed]
Infect Immun 2006: 74: 6487-6490. [PubMed]
10.Ялава К., Хаккинен М., Валконен М., Накари Ю.М., Пало Т., Халланвуо С., Оллгрен Дж., Сийтонен А., Нуорти Дж. П. Вспышка желудочно-кишечного заболевания и узловатой эритемы из тертой моркови, зараженной Yersinia pseudotuberculosis . Журнал Infect Dis 2006; 194: 1209-1216. [PubMed]
11. Джалава К., Халланвуо С., Накари У. М., Рууту П., Кела Е., Хейнасмаки Т., Сийтонен А., Нуорти Дж. П.. Множественные вспышки случаев инфицирования Yersinia pseudotuberculosis в Финляндии. J Clin Microbiol 2004; 42: 2789-2791.[PubMed]
12. Lambertz ST, Nilsson C., Hallanvuo S. ПЦР в реальном времени на основе TaqMan для обнаружения Yersinia pseudotuberculosis в пище. Appl Environ Microbiol 2008; 74: 6465-6469. [PubMed]
13. Лампы LW, Мадхусудхан К.Т., Гринсон Дж.К., Пирс Р.Х., Массолл Н.А., Чили М.С., Дин П.Дж., Скотт М.А. Роль Yersinia enterocolitica и Yersinia pseudotuberculosis в гранулематозном аппендиците. Гистологическое и молекулярное исследование. Am J Surg Path 2001; 25: 508-515.[PubMed]
Гистологическое и молекулярное исследование. Am J Surg Path 2001; 25: 508-515.[PubMed]
14. Лаукканан Р., Мартинес П.О., Сиккинен К.-М., Ранта Дж., Майяла Р., Коркеала Х. Передача Yersinia pseudotuberculosis в цепочке производства свинины от фермы до бойни. Appl Envir Microbiol 2008; 74: 5444-5450. [PubMed]
15. Локман Х.А., Гиллеспи Р.А., Бейкер Б.Д., Шахнович Е. Yersinia pseudotuberculosis продуцирует цитотоксический некротический фактор. Infect Immun 2002: 70: 2708-2714. [PubMed]
16.Logsdon LK, Mecsas J. Провоспалительный ответ, индуцированный инфекцией Yersinia pseudotuberculosis дикого типа, ингибирует выживание мутантов yop в желудочно-кишечном тракте и пейеровских пятнах. Инфекция Иммун 2006; 74: 1516-1527. [PubMed]
17. Mecsas J, Bilis I, Falkow S. Идентификация аттенуированных штаммов Yersinia pseudotuberculosis и характеристика орогастральной инфекции у мышей BALB / c на 5-й день постинфекции с помощью сигнатурно-меченого мутагенеза. Infect Immun 2001; 67: 2779-2787. [PubMed]
Infect Immun 2001; 67: 2779-2787. [PubMed]
18. Палья М.Г., Д’Ареццо С., Феста А., Дель Борго С., Лойаконо Л., Антинори А., Антонуччи Г., Виска П. Yersinia pseudotuberculosis сепсис и ВИЧ. Emerg Infect Dis 2005; 11: 1128-1130. [PubMed]
19. Rathmell WK, Arguin P, Chan S, Yu A. Yersinia pseudotuberculosis бактериемия и абсцесс селезенки у пациента с инсулиннезависимым сахарным диабетом. West J Med 1999; 170: 110-112. [PubMed]
20.Rimhanen-Finne R, Niskanen T, Hallanvuo S, Makary P, Haukka K, Pajunen S, Siitonen A, Ristolainen R, Poyry H, Ollgren J, Kuusi M. Yersinia pseudotuberculosis , вызвавшая крупную вспышку моркови в Финляндии в 2006 г. Epidem Infect 2008; 4: 1-6. [PubMed]
21. Санно А., Аспан А., Хествик Г., Якобсон М. Присутствие Salmonella spp., Yersinia enterocolitica , Yersinia pseudotuberculosis и Escherichia coli 0157: H7 у диких кабанов.Epidemiol Infect 2014; 6: 1-6. [PubMed]
[PubMed]
22. Тахара М., Баба К., Ваки К., Аракаки Ю. Анализ болезни Кавасаки, показывающий повышенные титры антител Yersinia pseudotuberculosis . Acta Paediatr 2006; 95: 1661-1664. [PubMed]
23. Tauxe RT. Салат и псевдоаппендицит: Yersinia pseudotuberculosis как возбудитель пищевого происхождения. J. Infect Dis 2004; 189: 761-763. [PubMed]
24. Vanantwerpen G, Van Damme I, De Zutter L, Houf K.Распространенность внутри партии и количественная оценка патогенных для человека Yersinia enterocolitica и Y, pseudotuberculosis в миндалинах свиней при убое. Vet Microbiol 2014; 169: 223-227. [PubMed]
25. Васала М., Халланвуо С., Рууска П., Суокас Р., Сиитонен А., Хакала М. Высокая частота реактивного артрита у взрослых после вспышки Yersinia pseudotuberculosis 0: 1, вызванной зараженной тертой морковью. Ann Rheum Dis 2014; 73: 1793-1796. [PubMed]
26.Винсент П. , Леклерк А., Мартин Л., Дуэз Дж. М., Симоне М., Карниэль Э. Внезапное начало псевдотуберкулеза у людей, Франция, 2004–2005 гг. Emerg Infect Dis 2008; 14: 1119-1122. [PubMed]
, Леклерк А., Мартин Л., Дуэз Дж. М., Симоне М., Карниэль Э. Внезапное начало псевдотуберкулеза у людей, Франция, 2004–2005 гг. Emerg Infect Dis 2008; 14: 1119-1122. [PubMed]
27. Wunderink HF, Oostvogel PM, Frenay IHME, Notermans DW, Fruth A, Kuijper EJ. Трудности диагностики терминального илеита, вызванного Yersinia pseudotuberculosis . Eur J Clin Microbiol Infect Dis 2014; 33: 197-200. [PubMed]
Псевдотуберкулез | Британское общество иммунологии
Псевдотуберкулез, вызываемый Yersinia pseudotuberculosis , представляет собой зооноз, который может передаваться человеку через контакт с кожей инфицированных животных, загрязненную воду или употребление зараженной пищи или овощей. Y.pseudotuberculosis — это небольшая овальная грамотрицательная палочка, которая считается предком, от которого произошли другие патогенные Yersinia ( Y.pestis и Y.enterocolitica ); и, как и у Y. pestis , окрашивание по Граму происходит по биполярному типу на любом конце палочки. Y. pseudotuberculosis вызывает острый мезентериальный аденит (псевдотуберкулез), который может имитировать аппендицит. Псевдотуберкулез, как следует из названия, может вызывать симптомы, похожие на туберкулез, которые могут поражать печень, селезенку и лимфатические узлы, вызывая некроз тканей и гранулемы, сопровождающиеся лихорадкой и болями в животе.Иногда Y. pseudotuberculosis может вызывать тяжелое системное заболевание с высокой летальностью.
pestis , окрашивание по Граму происходит по биполярному типу на любом конце палочки. Y. pseudotuberculosis вызывает острый мезентериальный аденит (псевдотуберкулез), который может имитировать аппендицит. Псевдотуберкулез, как следует из названия, может вызывать симптомы, похожие на туберкулез, которые могут поражать печень, селезенку и лимфатические узлы, вызывая некроз тканей и гранулемы, сопровождающиеся лихорадкой и болями в животе.Иногда Y. pseudotuberculosis может вызывать тяжелое системное заболевание с высокой летальностью.
Штаммы Y. pseudotuberculosis можно разделить на 6 серотипов на основе ряда термостабильных соматических антигенов и термолабильных жгутиковых антигенов, которые присутствуют в культурах, выращиваемых при температуре 18–26 o C. Как и Y.pestis , Y. pseudotuberculosis экспрессирует укороченную форму поверхностного липополисахарида («грубый» LPS), которая позволяет ему уклоняться от распознавания TLR4 в хозяине, в то время как жгутиковые антигены сдерживают фагоцитоз .
Как и другие Yersinia, Y. pseudotuberculosis также содержит плазмиду pYV, кодирующую секрецию 3 типа (T3S), антиген V и другие внешние белки Yersinia. Антиген V регулирует T3S, а также обладает противовоспалительным действием. T3S позволяет Y. pseudotuberculosis образовывать полый игольчатый выступ при тесном контакте с клеткой-хозяином in vivo , через который эффекторные белки перемещаются непосредственно в клетку-хозяин.Эти эффекторы являются по-разному цитотоксическими, антифагоцитарными или противовоспалительными и обычно способствуют апоптозу клеток-хозяев и, таким образом, выживанию бактерий в организме-хозяине. С помощью всех этих средств, Y. pseudotuberculosis противодействует врожденной иммунной защите и достигает распространения в организме хозяина, вызывая потенциально серьезную бактериемию. V-антиген из Y. pseudotuberculosis имеет последовательность V03 и гомологичен антигену, секретируемому Y.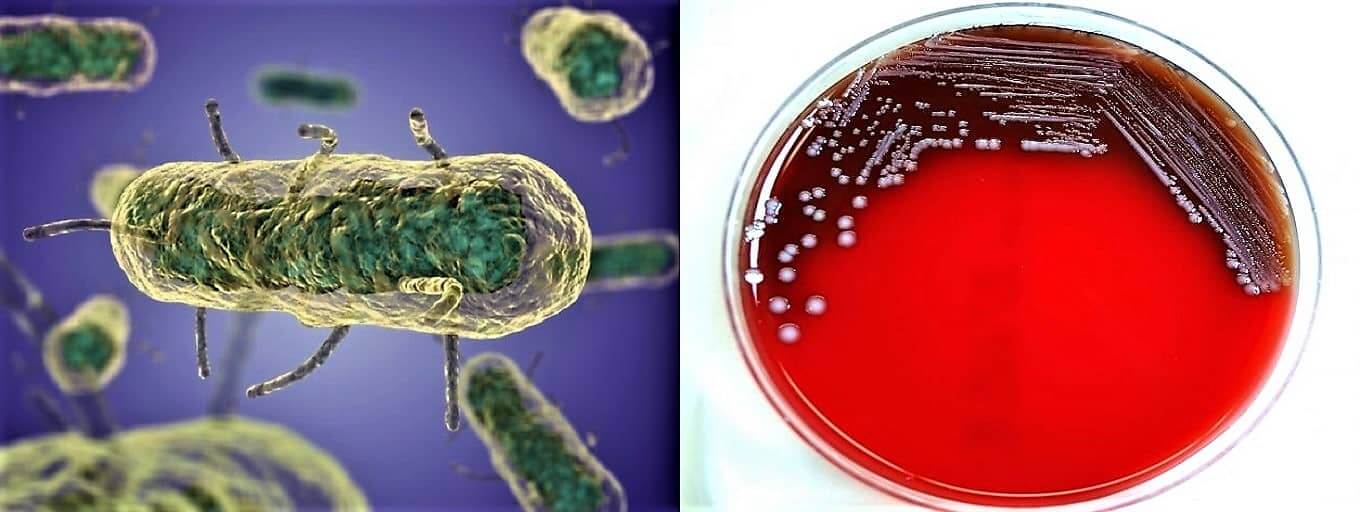 pestis . Это важно, потому что антиген V является основным защитным антигеном для вакцинации против чумы и, таким образом, имеет некоторую перекрестную защиту с Y.pseudotuberculosis возможно.
pestis . Это важно, потому что антиген V является основным защитным антигеном для вакцинации против чумы и, таким образом, имеет некоторую перекрестную защиту с Y.pseudotuberculosis возможно.
Y. pseudotuberculosis чувствителен к широкому спектру антибиотиков, включая пенициллин, ампициллин и тетрациклин.
© Авторские права на это произведение принадлежат автору
Редкие инфекции: Yersinia Enterocolitica и Yersinia Pseudotuberculosis
Yersinia enterocolitica и Yersinia pseudotuberculosis — это бактериальные инфекции, которые встречаются редко, но могут вызывать проблемы, когда они возникают. Y enterocolitica вызывает состояние, называемое энтероколитом, которое представляет собой воспаление тонкой и толстой кишки, которое возникает и часто рецидивирует, в основном у маленьких детей.
Эти инфекции, по-видимому, передаются в результате употребления в пищу зараженных продуктов, особенно сырых или недостаточно приготовленных из свинины, и употребления непастеризованного молока. Они также могут заразиться при прикосновении к инфицированному животному, питья зараженной колодезной воды или, в редких случаях, при переливании зараженной крови.Инфекции учащаются среди детей с ослабленной иммунной системой. Инкубационный период составляет от 4 до 6 дней.
Они также могут заразиться при прикосновении к инфицированному животному, питья зараженной колодезной воды или, в редких случаях, при переливании зараженной крови.Инфекции учащаются среди детей с ослабленной иммунной системой. Инкубационный период составляет от 4 до 6 дней.
Признаки и симптомы
Когда присутствует инфекция Y enterocolitica , она вызывает не только воспаление тонкой и толстой кишки, но и такие симптомы, как диарея и лихорадка. У ребенка с этой инфекцией стул может содержать кровь и слизь. Эти симптомы могут длиться от 1 до 3 недель, а иногда и дольше.
Наряду с этими более частыми симптомами, очень маленькие дети, у которых в организме накоплено слишком много железа, например, те, кто получает переливание крови или чья иммунная система уже подавлена или ослаблена из-за другого заболевания, могут быть восприимчивы к бактериемии ( распространение бактерий в кровь).У более старшего возраста также могут быть симптомы, имитирующие аппендицит (синдром псевдоаппендицита), с болью в животе справа и болезненностью. В редких случаях эта инфекция может быть связана с такими состояниями, как боль в горле, воспаление глаз, менингит и пневмония. У молодых людей старшего возраста после того, как инфекция ушла, может развиться боль в суставах или покраснение кожи (узловатая эритема) на голенях.
В редких случаях эта инфекция может быть связана с такими состояниями, как боль в горле, воспаление глаз, менингит и пневмония. У молодых людей старшего возраста после того, как инфекция ушла, может развиться боль в суставах или покраснение кожи (узловатая эритема) на голенях.
У детей с псевдотуберкулезом Y , вероятно, разовьется лихорадка, сыпь и боли в животе, включая синдром псевдоаппендицита.У некоторых детей также может быть диарея, сыпь и избыток жидкости в области груди или пространства вокруг суставов.
Когда звонить педиатру
Обратитесь к педиатру, если в стуле вашего ребенка прожилки крови. Обратите внимание на признаки обезвоживания, которые могут быть вызваны диареей вашего ребенка, включая сухость во рту, необычную жажду и снижение частоты мочеиспускания.
Как ставится диагноз?
Ваш педиатр может назначить анализы для определения наличия Yersinia организмов в стуле вашего ребенка.Доказательства инфекции также можно увидеть, взяв мазки из горла и оценив их в лаборатории, исследуя мочу или исследуя кровь на антитела к бактериям.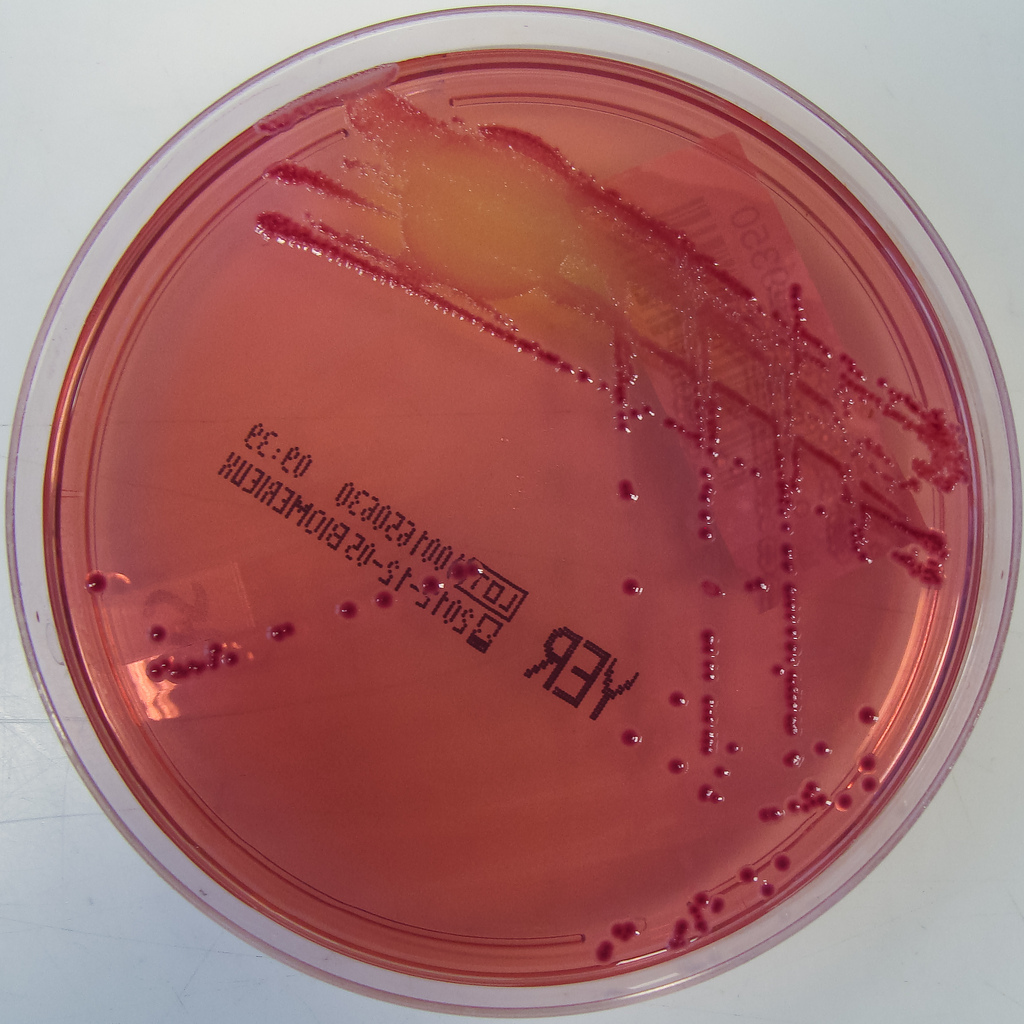
Поскольку это относительно редкие инфекции, большинство лабораторий обычно не проводят анализы на предмет Yersinia организмов в фекалиях.
Лечение
У большинства детей инфекция проходит сама по себе. В некоторых случаях инфекции Yersinia необходимо лечить антибиотиками.Как и во всех случаях диареи, жидкости назначают для предотвращения или лечения обезвоживания.
Профилактика
Убедитесь, что ваш ребенок не ест сырую или недоваренную свинину, непастеризованное молоко и загрязненную воду. Тщательно мойте руки водой с мылом после обработки сырых свиных кишок (детенышей).
Вакцины для предотвращения инфекции, вызванной Yersinia , не существует.
Информация, содержащаяся на этом веб-сайте, не должна использоваться вместо медицинской помощи и рекомендаций вашего педиатра.Ваш педиатр может порекомендовать различные варианты лечения в зависимости от индивидуальных фактов и обстоятельств.
Патогенез Y.
 enterocolitica и Y. pseudotuberculosis при иерсиниозе человека
enterocolitica и Y. pseudotuberculosis при иерсиниозе человека Иерсиниоз — это пищевое заболевание, которое стало более распространенным в последние годы из-за передачи от человека фекально-оральным путем и среди сельскохозяйственных животных. Иерсиниоз вызывается в первую очередь Yersinia enterocolitica и реже Yersinia pseudotuberculosis .Инфекция обычно характеризуется самоизлечивающейся острой инфекцией, которая начинается в кишечнике и распространяется на брыжеечные лимфатические узлы. Однако также могут возникать более серьезные инфекции и хронические состояния, особенно у людей с ослабленным иммунитетом. Y. enterocolitica и Y. pseudotuberculosis являются гетерогенными организмами, которые значительно различаются по степени патогенности, хотя некоторые обобщения можно отнести к патогенным вариантам. Молекулы адгезии и система секреции типа III имеют решающее значение для возникновения и развития инфекции.Кроме того, для выведения иерсиний необходимы как врожденный, так и адаптивный иммунные ответы. Несмотря на повсеместное распространение кишечных видов Yersinia и их ассоциацию в качестве важных причин пищевых отравлений во всем мире, немногие национальные программы надзора за кишечными патогенами включают иерсинии в качестве патогенов, подлежащих уведомлению. Более того, не существует стандарта, позволяющего эффективно сравнивать системы идентификации и отчетности и развивать глобальные тенденции. В этом обзоре обсуждаются факторы иерсиниальной вирулентности, механизмы заражения и реакции организма хозяина в дополнение к текущему состоянию эпиднадзора, обнаружения и профилактики иерсиниоза.
Несмотря на повсеместное распространение кишечных видов Yersinia и их ассоциацию в качестве важных причин пищевых отравлений во всем мире, немногие национальные программы надзора за кишечными патогенами включают иерсинии в качестве патогенов, подлежащих уведомлению. Более того, не существует стандарта, позволяющего эффективно сравнивать системы идентификации и отчетности и развивать глобальные тенденции. В этом обзоре обсуждаются факторы иерсиниальной вирулентности, механизмы заражения и реакции организма хозяина в дополнение к текущему состоянию эпиднадзора, обнаружения и профилактики иерсиниоза.
1. Введение
Иерсиниоз обычно является самоизлечивающимся желудочно-кишечным заболеванием, вызывающим озабоченность во всем мире. Однако, несмотря на известную связь возбудителей ( Y. enterocolitica , YE и очень редко Y. pseudotuberculosis , YPT) как с гастроэнтеритом, так и с внекишечными инфекциями, это заболевание остается плохо изученным. По-прежнему регистрируются единичные случаи, когда пища не считается источником инфекции, а изоляция от зараженных источников пищи часто является проблематичной.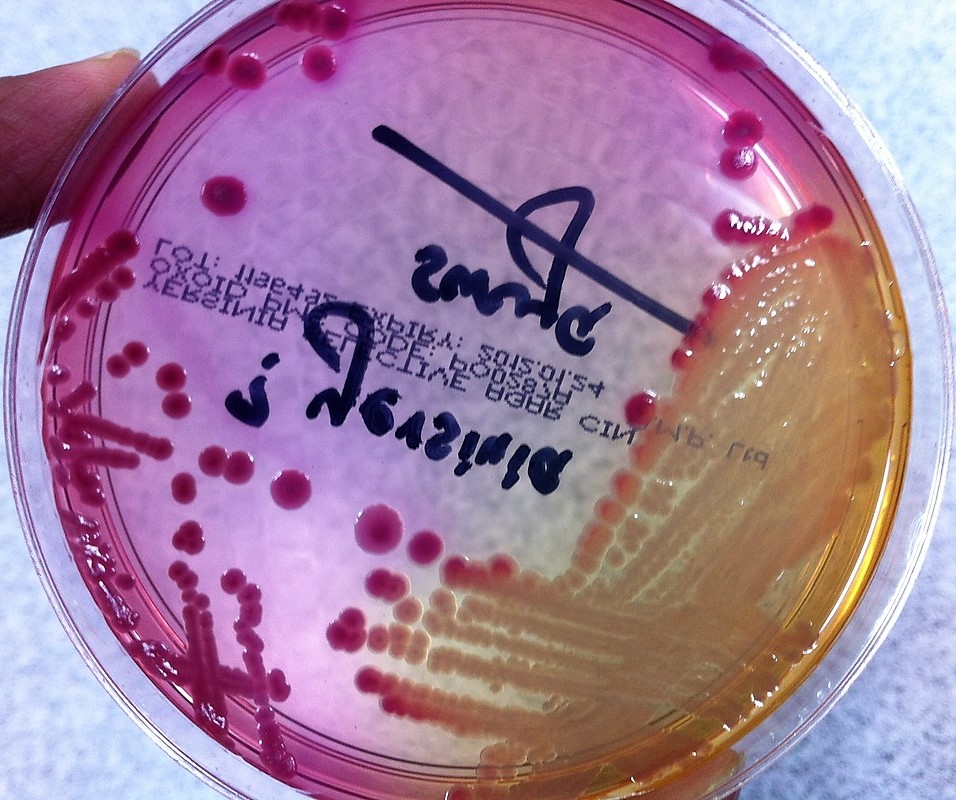 Поскольку иерсиниоз считается относительно редким, а YE и YPT распространены повсеместно, источники питания и воды не контролируются на предмет наличия этих бактериальных патогенов на регулярной основе. Однако способность иерсиний сохраняться в некультивируемом, но жизнеспособном состоянии в природных образцах [1], а также расти и процветать при температурах охлаждения (~ 4 ° C) предполагает, что их вклад в развитие болезни может быть недооценен.
Поскольку иерсиниоз считается относительно редким, а YE и YPT распространены повсеместно, источники питания и воды не контролируются на предмет наличия этих бактериальных патогенов на регулярной основе. Однако способность иерсиний сохраняться в некультивируемом, но жизнеспособном состоянии в природных образцах [1], а также расти и процветать при температурах охлаждения (~ 4 ° C) предполагает, что их вклад в развитие болезни может быть недооценен.
1.1. YE Инфекции
Основным возбудителем иерсиниоза является грамотрицательный зоонозный бактериальный патоген, YE, который обычно передается фекально-оральным путем [2].Близкородственный YPT также может вызывать иерсиниоз, но инфекции YPT у людей встречаются реже, чем инфекции, вызванные YE. Иерсиниоз наблюдается на всех континентах [3], но наиболее распространен в европейских странах. Некоторые из проблем, связанных с привязкой иерсиниоза к его источнику заражения, объясняются неоднородностью популяций иерсиний во множестве сред и водоемов, включая почву, воду и множество животных. Иерсиниоз является серьезной инфекцией у русских зайцев [4] и дополнительно обнаружен у канадских бобров, зайцев-снегоступов и ондатр [5].Кроме того, YE и YPT были изолированы от летучих мышей в Германии [6]. Более актуальным для человека является преобладание иерсиний в источниках корма для животных, особенно в свиньях и продуктах из свинины [7–9], а в последнее время и у домашних сельскохозяйственных собак в Китае [10]. Еще больше усложняет картину передачи болезни недавнее исследование, показавшее, что дикие грызуны на европейской свиноферме дали положительный результат на ЯЭ, предполагая, что грызуны могут служить межвидовыми переносчиками между резервуарами [11]. YE также был изолирован от мух, обнаруженных в свинарниках и на кухнях ферм [12], что позволяет предположить, что членистоногие-переносчики / насекомые могут играть роль в передаче кишечных иерсиний от животных к человеку.Мухи также могут способствовать распространению внутрибольничных инфекций, что вызывает особую озабоченность, поскольку есть по крайней мере одно сообщение о мухах в ливийских больницах, несущих устойчивые к антибиотикам штаммы бактерий, принадлежащих к семейству Enterobacteriaceae [13].
Иерсиниоз является серьезной инфекцией у русских зайцев [4] и дополнительно обнаружен у канадских бобров, зайцев-снегоступов и ондатр [5].Кроме того, YE и YPT были изолированы от летучих мышей в Германии [6]. Более актуальным для человека является преобладание иерсиний в источниках корма для животных, особенно в свиньях и продуктах из свинины [7–9], а в последнее время и у домашних сельскохозяйственных собак в Китае [10]. Еще больше усложняет картину передачи болезни недавнее исследование, показавшее, что дикие грызуны на европейской свиноферме дали положительный результат на ЯЭ, предполагая, что грызуны могут служить межвидовыми переносчиками между резервуарами [11]. YE также был изолирован от мух, обнаруженных в свинарниках и на кухнях ферм [12], что позволяет предположить, что членистоногие-переносчики / насекомые могут играть роль в передаче кишечных иерсиний от животных к человеку.Мухи также могут способствовать распространению внутрибольничных инфекций, что вызывает особую озабоченность, поскольку есть по крайней мере одно сообщение о мухах в ливийских больницах, несущих устойчивые к антибиотикам штаммы бактерий, принадлежащих к семейству Enterobacteriaceae [13]. Основным источником иерсиниоза являются свиньи, но также были зарегистрированы недавние изоляты из зараженных цыплят, молока, тофу и воды [8, 14].
Основным источником иерсиниоза являются свиньи, но также были зарегистрированы недавние изоляты из зараженных цыплят, молока, тофу и воды [8, 14].
У здоровых, иммунокомпетентных людей симптомы иерсиниоза варьируются от легкой, самоограничивающейся диареи до мезентериального лимфаденита.Однако у лиц с ослабленным иммунитетом также наблюдались хронические состояния, такие как реактивный артрит [15]. Инфекция YE обычно возникает при переваривании зараженной пищи или воды с последующим прикреплением бактерий к эпителиальным клеткам тонкого кишечника и возможным пересечением кишечного барьера через М-клетки [16]. Впоследствии YE-бациллы реплицируются в пятнах Пейера и иногда могут распространяться на более отдаленные лимфоидные ткани, такие как брыжеечные лимфатические узлы [16–18].Распространение от дистального отдела подвздошной кишки к селезенке и печени является относительно обычным явлением с последующей внеклеточной репликацией и образованием моноклональных микроабсцессов [19]. Наиболее распространенной инфекцией является острый гастроэнтерит, который в основном наблюдается у детей и младенцев из-за ослабленного иммунитета из-за незрелой иммунной системы. Однако у детей старшего возраста и взрослых может возникнуть множество других инфекций и осложнений, в том числе псевдоаппендикулярный синдром, микотические аневризмы [20–28] и, реже, сепсис как вторичное осложнение иерсиниоза или переливания крови.Также описано несколько хронических состояний, включая реактивный артрит, узловатую эритему, увеит, гломерулонефрит и миокардит [3, 29]. Хотя энтеропатогенный иерсиниоз обычно проходит самостоятельно у здоровых людей, уровень смертности у лиц с ослабленным иммунитетом может достигать 50% в результате системного распространения бактерий [30].
Наиболее распространенной инфекцией является острый гастроэнтерит, который в основном наблюдается у детей и младенцев из-за ослабленного иммунитета из-за незрелой иммунной системы. Однако у детей старшего возраста и взрослых может возникнуть множество других инфекций и осложнений, в том числе псевдоаппендикулярный синдром, микотические аневризмы [20–28] и, реже, сепсис как вторичное осложнение иерсиниоза или переливания крови.Также описано несколько хронических состояний, включая реактивный артрит, узловатую эритему, увеит, гломерулонефрит и миокардит [3, 29]. Хотя энтеропатогенный иерсиниоз обычно проходит самостоятельно у здоровых людей, уровень смертности у лиц с ослабленным иммунитетом может достигать 50% в результате системного распространения бактерий [30].
1.2. YPT-инфекции
YPT вызывает зоонозные инфекции у различных хозяев, включая как диких, так и домашних животных и птиц [31].YPT-инфекции человека, хотя и реже, чем вызванные YE, чаще всего передаются через зараженную пищу или воду [32]. Клинически инфекции YPT обычно проявляются в виде абсцессообразующего брыжеечного лимфаденита и диареи, но могут также приводить к вторичным осложнениям, таким как перфорация [33], синдром подострой обструкции [34], инвагинация кишечника [35] и острая почечная недостаточность [36], в редких случаях. случаи. Кроме того, сообщалось о пациентах с тяжелым желудочно-кишечным кровотечением в случаях YPT-колита [37–39].Подобно YE, наиболее частыми проявлениями YPT-инфекций у людей являются илеоколит и мезентериальный лимфаденит [40], последний из которых может поражать ткань аппендикса и быть ошибочно принят за аппендицит [41]. Инфекции YPT могут быть острыми или хроническими [42], с ретикулогранулоцитарной инфильтрацией, увеличенными фолликулами и некрозом с образованием абсцесса в мезентериальных лимфатических узлах [39, 43, 44]. Инфекция обычно проходит самостоятельно, но в редких случаях сепсис может привести к очень высокому уровню смертности (> 75%) [45].Помимо аппендицита, инфекции YPT путают с опухолевыми поражениями [46], терминальным илеитом и болезнью Крона [47].
Клинически инфекции YPT обычно проявляются в виде абсцессообразующего брыжеечного лимфаденита и диареи, но могут также приводить к вторичным осложнениям, таким как перфорация [33], синдром подострой обструкции [34], инвагинация кишечника [35] и острая почечная недостаточность [36], в редких случаях. случаи. Кроме того, сообщалось о пациентах с тяжелым желудочно-кишечным кровотечением в случаях YPT-колита [37–39].Подобно YE, наиболее частыми проявлениями YPT-инфекций у людей являются илеоколит и мезентериальный лимфаденит [40], последний из которых может поражать ткань аппендикса и быть ошибочно принят за аппендицит [41]. Инфекции YPT могут быть острыми или хроническими [42], с ретикулогранулоцитарной инфильтрацией, увеличенными фолликулами и некрозом с образованием абсцесса в мезентериальных лимфатических узлах [39, 43, 44]. Инфекция обычно проходит самостоятельно, но в редких случаях сепсис может привести к очень высокому уровню смертности (> 75%) [45].Помимо аппендицита, инфекции YPT путают с опухолевыми поражениями [46], терминальным илеитом и болезнью Крона [47].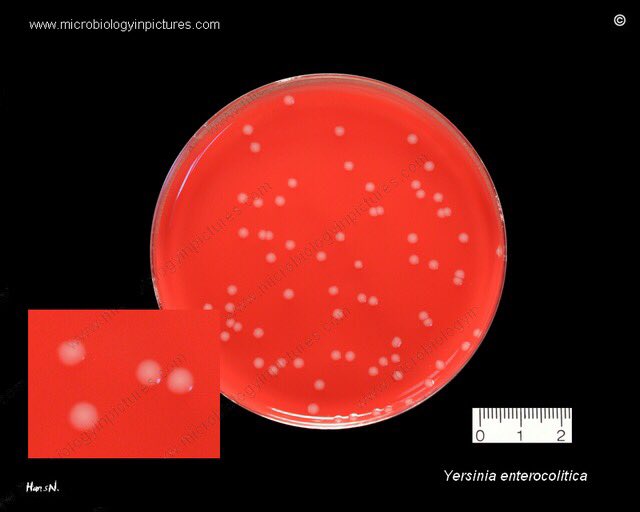 YPT также вовлечен в реактивный артрит, узловатую эритему и аутоиммунный синдром Квасаки [48].
YPT также вовлечен в реактивный артрит, узловатую эритему и аутоиммунный синдром Квасаки [48].
1.3. YE Epidemiology
Наблюдение за инфекциями YPT среди людей обычно не проводится, поэтому нет полных баз данных, из которых можно было бы использовать информацию для определения тенденций в отношении инфекций YPT среди людей. Однако существует несколько национальных сетей эпиднадзора, которые включают иерсиниоз в еженедельные, ежемесячные и ежегодные отчеты о случаях / выделениях кишечных заболеваний человека, особенно в тех, которые собираются государствами-членами Европейского Союза, США и Новой Зеландии.Потенциальные источники эпидемиологических данных включают клинические отчеты, лабораторные исследования, дозорные исследования на местах, зарегистрированные случаи и показатели, рассчитанные как случаи на 100 000 человек в зоне наблюдения за пораженным населением в год. Различия в методах отчетности, методах изоляции и доступности информации о штаммах значительно усложняют сравнения между странами, а иногда даже между различными регионами / штатами / территориями в пределах отдельной страны. Кроме того, иерсиниоз нечасто контролируется в развивающихся странах, где кишечные заболевания являются основной причиной младенческой и детской смертности.Например, Всемирная организация здравоохранения инициировала план по решению этой проблемы в Африке в 1998 году, работая с государствами-членами и техническими партнерами для реализации программы комплексного эпиднадзора и ответных мер (IDSR), но иерсиниоз не включен в качестве основной цели эпиднадзора. Точно так же Центр медицинских наук по контролю за заболеваниями (http://www.moh.gov.cn), подразделение Министерства здравоохранения Китая, еженедельно сообщает о заболеваемости инфекционными заболеваниями, но чума — единственное заболевание, связанное с иерсиниями. включены в их усилия по наблюдению.
Кроме того, иерсиниоз нечасто контролируется в развивающихся странах, где кишечные заболевания являются основной причиной младенческой и детской смертности.Например, Всемирная организация здравоохранения инициировала план по решению этой проблемы в Африке в 1998 году, работая с государствами-членами и техническими партнерами для реализации программы комплексного эпиднадзора и ответных мер (IDSR), но иерсиниоз не включен в качестве основной цели эпиднадзора. Точно так же Центр медицинских наук по контролю за заболеваниями (http://www.moh.gov.cn), подразделение Министерства здравоохранения Китая, еженедельно сообщает о заболеваемости инфекционными заболеваниями, но чума — единственное заболевание, связанное с иерсиниями. включены в их усилия по наблюдению.
Несмотря на отсутствие эпиднадзора во многих странах, включая Африку, Азию, Ближний Восток, острова Тихого океана, Латинскую Америку, Карибский бассейн и другие, в Северной Америке и Европе есть несколько национальных агентств, которые предоставляют ежегодные отчеты, включающие спорадический иерсиниоз. случаев, вспышек и заболеваемости как среди людей, так и среди животных. Как показано на Рисунке 1, имеется широкий спектр сообщений о случаях заболевания из Северной Америки (включая США и Канаду), Океании (включая Австралию и Новую Зеландию) и нескольких европейских стран.Например, Ирландия сообщила от 3 до 14 случаев выделения YE / YPT от людей в период с 2000 по 2009 год, в то время как Германия сообщила от 3906 до 7186 подтвержденных случаев иерсиниоза человека за тот же период времени (Рисунок 1). Хотя заболеваемость снизилась за последние 10 лет (Рисунок 2), случаи немецкого иерсиниоза составляют более половины всех зарегистрированных случаев иерсиниоза в Европе и ~ 90% случаев в странах Западной Европы, которые регулярно обследовали свое население на предмет инфекций, связанных с YE в течение вышеупомянутые десятилетние временные рамки (Рисунок 1).Причины резко более высокого уровня заболеваемости иерсиниозом в Германии по сравнению со всеми другими странами с активными программами надзора за YE / YPT неясны, но потенциальные факторы включают вариабельность процедур выделения иерсиний и систем отчетности, различия в частоте клинической диагностики, степень занижения данных, распространенность.
случаев, вспышек и заболеваемости как среди людей, так и среди животных. Как показано на Рисунке 1, имеется широкий спектр сообщений о случаях заболевания из Северной Америки (включая США и Канаду), Океании (включая Австралию и Новую Зеландию) и нескольких европейских стран.Например, Ирландия сообщила от 3 до 14 случаев выделения YE / YPT от людей в период с 2000 по 2009 год, в то время как Германия сообщила от 3906 до 7186 подтвержденных случаев иерсиниоза человека за тот же период времени (Рисунок 1). Хотя заболеваемость снизилась за последние 10 лет (Рисунок 2), случаи немецкого иерсиниоза составляют более половины всех зарегистрированных случаев иерсиниоза в Европе и ~ 90% случаев в странах Западной Европы, которые регулярно обследовали свое население на предмет инфекций, связанных с YE в течение вышеупомянутые десятилетние временные рамки (Рисунок 1).Причины резко более высокого уровня заболеваемости иерсиниозом в Германии по сравнению со всеми другими странами с активными программами надзора за YE / YPT неясны, но потенциальные факторы включают вариабельность процедур выделения иерсиний и систем отчетности, различия в частоте клинической диагностики, степень занижения данных, распространенность. YE и YPT в резервуарах для животных, различия в обработке пищевых продуктов и вариативность в потреблении мясных продуктов. Есть некоторые доказательства, подтверждающие идею о том, что более высокое потребление мяса, особенно свинины в Германии по сравнению с другими европейскими странами, может коррелировать с более высокой заболеваемостью иерсиниозом в Германии [49].
YE и YPT в резервуарах для животных, различия в обработке пищевых продуктов и вариативность в потреблении мясных продуктов. Есть некоторые доказательства, подтверждающие идею о том, что более высокое потребление мяса, особенно свинины в Германии по сравнению с другими европейскими странами, может коррелировать с более высокой заболеваемостью иерсиниозом в Германии [49].
1.4. YE Genomics
YE — гетерогенная группа организмов, характеризующаяся шестью биотипами и 60 серотипами. Биотипы можно различать по уровню патогенности, только один из которых не является патогенным (биотип 1A). «Старый Свет» YE включает биотипы 2–5, которые являются слабопатогенными. Наиболее вирулентным является биотип 1B «Нового Света», который является высокопатогенным для человека и летальным на мышиной модели инфекции [50]. Из шестидесяти серотипов YE только одиннадцать были связаны с заболеванием у людей, и большинство можно отнести только к трем обычно вирулентным серотипам: O: 3, O: 8 и O: 9. Эти три серотипа обычно считаются возбудителями иерсиниоза и различаются в зависимости от географического положения. Например, штамм 1B / O: 8 был преобладающей версией патогенного YE в Соединенных Штатах [15]; Напротив, штамм 3 / O: 9 является наиболее частой причиной иерсиниоза в Китае и Европе [51, 52].
Эти три серотипа обычно считаются возбудителями иерсиниоза и различаются в зависимости от географического положения. Например, штамм 1B / O: 8 был преобладающей версией патогенного YE в Соединенных Штатах [15]; Напротив, штамм 3 / O: 9 является наиболее частой причиной иерсиниоза в Китае и Европе [51, 52].
Изоляты этих двух патогенных штаммов были секвенированы [53, 54] и недавно сравнены для выявления общих и уникальных областей вирулентности [54]. Результаты этого анализа показали, что эти два штамма обладают значительной генетической консервацией / сходством, включая большинство известных детерминант вирулентности YE.Однако несколько ключевых областей вирулентности 1B / O: 8 отсутствовали в штамме 3 / O: 9 [54], в том числе остров высокой патогенности (HPI) [55], секреция Yersinia типа II 1 ( yts1 ) [56] и аппарат секреции Yersinia типа III ( ysa ). Аналогично, штамм 3 / O: 9 обладал областями патогенности, отсутствующими в высокопатогенном штамме 1B / O: 8. Области, специфичные для штамма 3 / O: 9, включали новую хромосомно-кодируемую систему секреции типа III (T3SS), систему переносчиков кассет, связывающих АТФ, кластеры генов, связанных с токсином, и кластер жгутиковых генов [54].Секвенирование дополнительных штаммов YE, таких как 4 / O: 3, который недавно стал важной причиной иерсиниоза в Соединенных Штатах [57], вероятно, будет способствовать лучшему пониманию взаимосвязи между специфичными для штамма факторами вирулентности и вариациями клинической картины. последствия.
Области, специфичные для штамма 3 / O: 9, включали новую хромосомно-кодируемую систему секреции типа III (T3SS), систему переносчиков кассет, связывающих АТФ, кластеры генов, связанных с токсином, и кластер жгутиковых генов [54].Секвенирование дополнительных штаммов YE, таких как 4 / O: 3, который недавно стал важной причиной иерсиниоза в Соединенных Штатах [57], вероятно, будет способствовать лучшему пониманию взаимосвязи между специфичными для штамма факторами вирулентности и вариациями клинической картины. последствия.
1.5. YPT Genomics
YPT можно разделить на 14 различных биотипов [58], пять из которых почти исключительно патогены (O1 – O5). Остальные девять биотипов (O6 – O14) были выделены из животных и окружающей среды, но никогда из клинических образцов человека [58–61].И патогенный, и непатогенный YPT можно подразделить на 21 серотип [62] на основании распределения около 30 различных O-факторов (O-специфический полисахарид липополисахарида [LPS]) внутри вида [58]. Эти серотипы различаются географически и по степени патогенности [63], обычно коррелируя с размером и наличием острова патогенности хромосом, HPI [63]. Только штаммы Biotype O1 содержат полный неповрежденный HPI. Биотип O3 содержит усеченную версию, а остров патогенности полностью отсутствует у всех других штаммов YPT, которые до сих пор исследованы [64–66].Патогенность YPT зависит от присутствия плазмиды вирулентности, кодирующей T3SS, pYV [67], YPMa [68] и HPI [69] (подробно описаны в следующем разделе), а клинические признаки тесно связаны с различными комбинациями. из этих трех факторов вирулентности. Например, pYV отсутствует в одной четверти известных вирулентных серотипов, которые вместо этого экспрессируют суперантигенный вариант YPMa и / или белки HPI [63]. Неоднородное распределение этих факторов объясняет различия в клинических проявлениях инфекций на Дальнем Востоке, в Европе и странах Запада [63, 66, 70–72].
Эти серотипы различаются географически и по степени патогенности [63], обычно коррелируя с размером и наличием острова патогенности хромосом, HPI [63]. Только штаммы Biotype O1 содержат полный неповрежденный HPI. Биотип O3 содержит усеченную версию, а остров патогенности полностью отсутствует у всех других штаммов YPT, которые до сих пор исследованы [64–66].Патогенность YPT зависит от присутствия плазмиды вирулентности, кодирующей T3SS, pYV [67], YPMa [68] и HPI [69] (подробно описаны в следующем разделе), а клинические признаки тесно связаны с различными комбинациями. из этих трех факторов вирулентности. Например, pYV отсутствует в одной четверти известных вирулентных серотипов, которые вместо этого экспрессируют суперантигенный вариант YPMa и / или белки HPI [63]. Неоднородное распределение этих факторов объясняет различия в клинических проявлениях инфекций на Дальнем Востоке, в Европе и странах Запада [63, 66, 70–72].
1,6. Факторы вирулентности YE и YPT
Геномы YE, YPT и YP идентичны на 97%, но эти три бактерии вызывают совершенно разные заболевания у людей, несмотря на общий тропизм к лимфатическим узлам [73–76]. Распределение их общих и уникальных факторов вирулентности играет решающую роль в различных путях заражения, типах инфекций и тяжести заболевания у людей. Как хромосомные, так и плазмидные факторы вирулентности играют роль в патогенезе иерсиний, а также в возникновении и прогрессировании иерсиниоза.Патогенность YE зависит от присутствия плазмиды размером 70 т.п.н., ассоциированной с вирулентностью Yersinia , pYV [67, 77–79]. Плазмида pYV отличает патогенные штаммы от непатогенных, поскольку она важна для вирулентности [79]. Высокопатогенный биотип 1B Y. enterocolitica также содержит хромосомный остров высокой патогенности (HPI), как и почти все европейские штаммы Y. pseudotuberculosis серотипа O1 [69]. HPI кодирует белки, которые участвуют в биосинтезе, регуляции и транспорте сидерофор иерсиниабактина [80, 81], и поэтому его называют «островком захвата железа» [63, 69].На этом острове есть пять основных генов ( psn , irp1 , irp2 , ybtP и ybtQ ), которые участвуют в системе иерсиниабактина [80, 82, 83]. Эта система позитивно регулируется с помощью YtbA, который сам по себе негативно регулируется с помощью регулятора, отвечающего за железо, Fur [84]. Гены psn и irp2 важны для фенотипа высокой патогенности YPT [69, 85].
Распределение их общих и уникальных факторов вирулентности играет решающую роль в различных путях заражения, типах инфекций и тяжести заболевания у людей. Как хромосомные, так и плазмидные факторы вирулентности играют роль в патогенезе иерсиний, а также в возникновении и прогрессировании иерсиниоза.Патогенность YE зависит от присутствия плазмиды размером 70 т.п.н., ассоциированной с вирулентностью Yersinia , pYV [67, 77–79]. Плазмида pYV отличает патогенные штаммы от непатогенных, поскольку она важна для вирулентности [79]. Высокопатогенный биотип 1B Y. enterocolitica также содержит хромосомный остров высокой патогенности (HPI), как и почти все европейские штаммы Y. pseudotuberculosis серотипа O1 [69]. HPI кодирует белки, которые участвуют в биосинтезе, регуляции и транспорте сидерофор иерсиниабактина [80, 81], и поэтому его называют «островком захвата железа» [63, 69].На этом острове есть пять основных генов ( psn , irp1 , irp2 , ybtP и ybtQ ), которые участвуют в системе иерсиниабактина [80, 82, 83]. Эта система позитивно регулируется с помощью YtbA, который сам по себе негативно регулируется с помощью регулятора, отвечающего за железо, Fur [84]. Гены psn и irp2 важны для фенотипа высокой патогенности YPT [69, 85].
Практически все дальневосточные штаммы YPT дополнительно продуцируют один из трех вариантов хромосомно-кодируемого нового суперантигенного токсина YPM (производный митоген YPT — ), кодируемого геном ypm [86, 87].Исходный YPM (переименованный в YPMa) кодируется ypmA [88] и играет более важную роль при системных инфекциях, чем при гастроэнтерите [68]. Два других варианта, YPMb и YPMc, кодируются генами ypmB и ypmC соответственно [88, 89].
Небольшой консервативный шаперонный белок РНК, Hfq, необходим для полной вирулентности множества патогенных бактерий, включая YE и YPT [90]. Hfq необходим для экспрессии термостабильного энтеротоксина Yst в YE [91].В YPT Hfq играет роль в регуляции подвижности, внутриклеточного выживания и продукции эффекторов T3SS [90].
Система PhoP / Q, кодируемая хромосомой YPT [92], регулирует выживание и рост макрофагов [93, 94] и ковалентные модификации LPS, которые снижают его стимулирующую способность [95], тем самым давая бактериям возможность избегать, минимизировать или задерживать активацию макрофагов. . В модели кишечной инфекции у мышей мутанты, лишенные PhoP, были в 100 раз аттенуированы по вирулентности из-за сниженной способности выживать и реплицироваться внутри клеток внутри макрофагов [93].Глобальный регулон PhoPQ также определяет снижение уровней Mg 2+ и, возможно, Mn 2+ , что характеризует внутриклеточную среду клеток-хозяев. MntH, предполагаемый переносчик Yersinia Mn 2+ , был недавно предложен для обеспечения выживания бактерий в фагоцитарных вакуолях, защищая их от активных форм кислорода [96].
1,7. Установление инфекции иерсиниозом
У многих патогенов факторы вирулентности тесно связаны с температурой, и это регулирование температуры особенно важно для возникновения инфекции.При температуре окружающей среды (менее 28 ° C) и в кислых условиях при 37 ° C кишечные иерсинии оптимально экспрессируют белок инвазин, который кодируется хромосомным локусом inv [17, 18]. При приеме внутрь инвазин связывается с интегринами B1 на клетках-хозяевах и способствует проникновению в эпителиальный слой (рис. 3). Постепенное повышение температуры в организме хозяина вызывает экспрессию факторов вирулентности, необходимых для закрепления в лимфатических тканях и избежания обнаружения иммунной системой.Экспрессия хромосомного ail ( инвазия прикрепления ) , локус , например, индуцируется при 37 ° C, и образующийся в результате белок Ail / OmpX дополнительно усиливает инвазию эпителиальных клеток. Установление инфекции также требует транслокации токсичных эффекторов через T3SS, а также «другие системы транспортеров» [97]. Регуляция адгезии и инвазии опосредуется регулятором вирулентности A (RovA), который положительно регулирует экспрессию inv , белка, модулирующего Yersinia (YmoA), и белка, структурирующего гистоноподобный нуклеоид (H-NS) [98– 103].
Yersinia адгезия Белок (YadA) также опосредует прикрепление слизи и эпителиальных клеток и, вместе с инвазином, способствует инвазии клеток-хозяев (рис. 3). YadA представляет собой многофункциональный фактор вирулентности, подвергающийся воздействию поверхности, кодируемый плазмидой вирулентности pYV, которая придает способность прикрепляться к белкам внеклеточного матрикса [104–106]. Индукция экспрессии YadA координируется с активацией Yops ( Yersinia, белков внешней мембраны) [107, 108].Вклад YadA в вирулентность для YE больше, чем для YPT, поскольку он играет важную роль в позитивной регуляции как адгезии, так и инвазии клеток-хозяев [105, 109]. YadA играет лишь второстепенную роль в YPT, обеспечивая просто адгезивный фенотип [110–112]. Подобно инвазину, YadA инициирует интернализацию путем связывания с внеклеточным фибронектином, который связан с интегрином 5b1 [105]. YadA из YPT и YE связывает фибронектин, коллаген I, II и IV и ламинин, хотя и с разной аффинностью, тем самым способствуя различным свойствам вирулентности [105].YadA вызывает воспалительную реакцию в эпителиальных клетках, индуцируя митоген-активированную протеинкиназу (MAPK-) зависимую продукцию интерлейкина (IL) -8, и вносит свой вклад в результирующий воспалительный каскад кишечника [113, 114]. Было высказано предположение, что взаимодействие YadA с коллагеном способствует развитию хронических инфекций иерсиниоза, таких как развитие реактивного артрита [113–116], что было продемонстрировано на модели на крысах [117–119].
Помимо ингибирования и инвазии клеток-хозяев, как Ail, так и YadA играют важную роль в сопротивлении комплемента и уклонении от иммунитета.Ail и YadA ингибируют альтернативный путь комплемента путем связывания фактора регулятора H и узурпируют его естественную функцию для предотвращения лизиса клеток-хозяев [120–123]. Ail и YadA аналогичным образом разрушают классический путь комплемента и лектина путем связывания с C4b-связывающим белком, тем самым способствуя деградации фактора комплемента C4b и предотвращая образование C3-конвертазы, которая в противном случае привела бы к лизису бактериальных клеток [123].
Другие факторы вирулентности YPT включают предполагаемую ДНК-аденинметилтрансферазу, YamA, которая необходима для полной вирулентности [124], и несколько белков, которые помогают выживанию бактерий в кислых условиях.Аспартат-зависимая система кислотного выживания была недавно описана для YPT, который играет роль в выживании бактерий и, таким образом, способствует возникновению инфекции [125]. Снижение pH индуцирует экспрессию гена аспертазы YPT ( aspA ); закодированный продукт гена, AspA, впоследствии производит аммиак, позволяя организмам, попавшим внутрь, выжить в кислой среде желудочно-кишечного тракта [125]. К другим бактериальным факторам, способствующим выживанию в кислых условиях, относятся уреаза [126], TatC [127], PhoP, OmpR и PmrA [128, 129].Кислый pH также вызывает подавление регуляции транскрипции Cra (репрессора / активатора катаболита), что увеличивает выживаемость бактериальной кислоты [130]. Предположительно Cra опосредует это действие посредством регуляции транскрипции, но механизм его действия остается неизвестным.
1.8. T3SS и Yop Effectors
T3SS, который кодируется на плазмиде вирулентности pYV и является общим для всех трех патогенных иерсиний, играет существенную роль как в возникновении, так и в исходе инфекции.Инъекция T3SS охватывает как внутреннюю, так и внешнюю бактериальные мембраны, а вирулентные эффекторные белки, называемые внешними белками Yersinia (Yops), транслоцируются через прикрепленную к хозяйской клетке иглу Yersinia секреционного белка F (YscF) непосредственно в мишень клетки-хозяева [131]. Белки YopB и YopD образуют поры в плазматической мембране клетки-хозяина, обеспечивая стыковку иглы YscF и возможную транслокацию эффекторов (Рисунок 3). Для правильной сборки стабильного комплекса инъектисомы также необходимы цитозольные шапероны YscE и YscG [132].Существует шесть эффекторных белков Yop (YopE, YopH, YopP / J, YopO / YpkA и YopM), которые опосредуют уклонение от иммунитета, вмешиваясь в пути передачи сигнала хозяина, разрушая актиновый цитоскелет хозяина и вызывая апоптоз клетки-хозяина (рисунок 3) [133, 134].
Доставка Yops требует тесного контакта между бактериальными клетками и клетками-хозяевами и опосредуется YadA и инвазином посредством их связывания с β 1-интегринами (рис. 3) [135, 136], которые при стимуляции вызывают активацию киназ Src. и RhoA, которые облегчают транслокацию Yop посредством модуляции полимеризации актина [137].В отсутствие Yops активация β 1-интегринов д. Вместо этого приводить к перестройкам актина, которые способствуют интернализации бактерий [138]. У каждого Yop есть обозначенный шаперон, называемый Syc-белком (для специфического шаперона Yop) (например, SycE для YopE), необходимый для секреции Yop [133]. Инъектисома T3SS запускается при контакте клетки-хозяина [139], а также in vitro при температуре (37 ° C) и условиях низкого содержания кальция (которые служат для имитации внутриклеточных условий клеток-хозяев) [140–142].Эффекторы Yop позволяют уклоняться от иммунных ответов, блокируя фагоцитарную функцию хозяина [133, 143, 144], которая жизненно важна для репликации бактерий и внутриклеточного выживания. Недавно было высказано предположение, что сама пора T3SS Yersinia запускает процессинг IL-1 β и IL-18 в макрофагах [75, 145] и последующее образование инфламмасомы, цитозольного комплекса врожденного иммунитета [146], который запускает воспаление и пироптоз в ответ на порообразование [147, 148].
Смерть клетки-хозяина опосредуется эффектором YopP / J, серин-треонинацетилтрансферазой, которая индуцирует апоптоз фагоцитов, модулируя действие ЛПС (рис. 3).При связывании с toll-подобным рецептором (TLR) -4, LPS индуцирует активацию проапоптотических факторов хозяина через TRIL (адаптер, содержащий домен рецептора Toll / IL-1, индуцирующий IFN- β ) [149, 150], при этом одновременно подавление провоспалительных генов и генов выживания клеток посредством инактивации MAPK и ядерного фактора, фактора транскрипции каппа B (NF- κ B) (рис. 3) [151–153]. YopP / J специфически ингибирует воспалительное действие и действие LPS на выживание клеток [154, 155], таким образом склоняя чашу весов в сторону апоптоза клеток-хозяев [150, 156].YopP / J-опосредованное ингибирование провоспалительных ответов клетки-хозяина включает ингибирование активации IKK β и, таким образом, активности NF- κ B (Рисунок 3) [157], что приводит к снижению высвобождения TNF- α за счет макрофаги [158], предотвращение секреции IL-8 эпителиальными клетками [155] и снижение презентации факторов адгезии ICAM-1 и E-селектина на поверхности эпителиальных клеток [159]. Совсем недавно было показано, что YopP / J также напрямую активирует каспазы (Рис. 3) независимо от вышестоящих рецепторов смерти [160–162].
После инъекции в цитоплазму клетки-хозяина YopE, -H, -P и -T совместно разрушают цитоскелет эпителиальных клеток, макрофагов и дендритных клеток, тем самым уменьшая их способность поглощать вторгающиеся бактерии. YopP / J может также способствовать уклонению от адаптивных иммунных ответов путем ингибирования способности дендритных клеток представлять антигены Т-клеткам CD8 + [163], либо напрямую, либо, возможно, путем уменьшения популяции дендритных клеток посредством индукции апоптоза [162, 164, 165].Похожая стратегия используется YPT с использованием белка, активирующего GTPase (GAP), YopE, для предотвращения фагоцитоза дендритными клетками [163, 166]. Помимо инъекционных и эффекторных белков Yersinia , для активности T3SS необходимы по крайней мере три адапторных белка YopB, YopD и VirF / LcrV (V-антиген с низким ответом на кальций) [133]. VirF / LcrV (также называемый V-антигеном) представляет собой член семейства множественных адаптационных ответов (MAR), который регулирует T3SS на уровне транскрипции и, когда секретируется во внеклеточную среду хозяина, способствует вирулентности, подавляя воспаление [167, 168].
YopE, YopT и YopO / YpkA противодействуют фагоцитозу клетки-хозяина, действуя на мономерные Rho GTPases, ответственные за регуляцию динамики цитоскелета [133]. YopE проявляет активность GAP, тем самым вызывая гидролиз GTP и, таким образом, инактивацию RhoA, Rac1 и Cdc42 (Рисунок 3) [169–171]. YopT, с другой стороны, действует как цистеиновая протеаза, которая инактивирует Rho, Rac и Cdc42 посредством расщепления [172, 173]. YopO / YpkA — серин-треониновая киназа с последовательностью и структурным сходством с RhoA-связывающими киназами, которая подвергается аутофосфорилированию при связывании с актином [174–176].YopO может также напрямую связываться с RhoA и Rac-1 с неизвестными в настоящее время последствиями [133].
Эффектор YopH, как недавно было показано, ингибирует воспалительные реакции хозяина посредством подавления хемоаттрактантного белка хемокинов моноцитов 1 (MCP-1) [177]. YopH из YPT ингибирует активацию фосфатидилинозитол-3-киназного пути, что приводит к предотвращению антиген-опосредованной активации лимфоцитов [177, 178]. YopH, протеинтирозинфосфатаза, нарушает активацию Т-клеток и В-клеток, вмешиваясь в события передачи сигналов фосфорилирования, что приводит к снижению экспрессии костимулирующих молекул B7.2 и CD69, а также митоген лейкоцитов IL-2 [178, 179]. О YopM известно очень мало, но его удаление приводит к резкому снижению вирулентности [180]. YopM, по-видимому, вводится в клетки-хозяева вместе с другими эффекторными белками T3SS [181], но есть также доказательства того, что YopM может связываться с внеклеточным белком острой фазы α 1-антитрипсином [182]. Совсем недавно было показано, что YopM образует комплекс с рибосомной киназой S6 (RSK) и протеазо-активируемой киназой (PKN) (рис. 3) [183], что приводит к устойчивой активации RSK и, возможно, способствует патогенности Yersinia [184 , 185].
1.9. Хромосомные T3SSs
Помимо pYV-кодированного T3SS, существуют два дополнительных хромосомно-кодируемых T3SSs в YE: жгутиковый T3SS и Ysa T3SS [186, 187]. Ysa T3SS оптимально экспрессируется при высоких концентрациях соли, 26 ° C и в стационарной фазе роста [186, 188, 189]. Чувствительность к соли опосредуется опероном sycByspBCDA, который регулируется YsaE и шапероном SycB [189]. Ysa T3SS играет роль в вирулентности [186] и важен для колонизации тонкого кишечника, несмотря на его оптимальную экспрессию при температурах, не относящихся к млекопитающим (26 ° C) [190].Известно 15 эффекторных белков Ysa (Ysps), которые, как полагают, действуют подобно эффекторам Yop в качестве модуляторов иммунных ответов хозяина [191]. Интересно, что жгутиковый T3SS, который функционирует в биогенезе жгутиков, секретирует эффекторы Fop, которые также играют роль в патогенезе YE [187]. YplA ( Yersinia, фосфолипаза A), например, представляет собой Fop, необходимый для колонизации пейеровских бляшек и брыжеечных лимфатических узлов, который способствует воспалительным ответам в этих тканях [192].
1.10. Система секреции типов VI и IV
T3SS — не единственные системы секреции, идентифицированные у иерсиний, которые способствуют бактериальной вирулентности. Фактически, система секреции типа VI (T6SS) была недавно идентифицирована в YPT, которая содержит четыре копии, одна из которых, как недавно было показано, регулируется температурой, фазой роста и N-ацилгомесерин-лактон-зависимым чувствительностью кворума. система [193]. YPT также несет кластер генов пилуса IV типа, который вносит вклад в патогенность [194].
1.11. Ответы хозяина на инфекцию YE и YPT
Инфекции, вызванные Yersinia , являются двухфазными и инициируются «тихим» 36–48-часовым периодом бактериальной репликации без измеримого ответа хозяина. За этой начальной «спокойной» фазой следует приток активированных фагоцитов в инфицированные ткани и лимфатические узлы, что вызывает острую воспалительную реакцию, характеризующуюся выработкой цитокинов и некрозом тканей [74, 76, 195–199]. Эффекторы T3SS Yop, вероятно, ответственны за начальное ингибирование фагоцитарных функций, но механизмы, лежащие в основе такой внезапной биполярной воспалительной реакции «выключено-включено», в настоящее время полностью не изучены.T3SS абсолютно необходим для эффективной колонизации системных органов, а инактивация T3SS приводит к быстрому удалению бактерий хозяином [200–202]. В результате иерсинии, лишенные функционального T3SS, становятся авирулентными и могут функционировать как живые аттенуированные вакцинные штаммы у мышей [200, 203, 204].
Недавние данные свидетельствуют о том, что макрофаги могут компенсировать YopE / YopH-опосредованное ингибирование эндосомного пути презентации антигена MHC класса II с помощью механизма, зависимого от аутофагии [205].Таким образом, аутофагия может служить альтернативным противодействующим путем, с помощью которого хозяин может вызывать Т-клеточный ответ CD4 + , ограниченный МНС класса II, против опосредованной Yersinia T3SS транслокации эффекторов вирулентности Yop [205]. Однако, в то время как Deuretzbacher et al. [206] продемонстрировали опосредованную аутофагией деградацию интернализованного макрофагами YE, было показано, что YPT узурпирует аутофагосомный путь для продолжения репликации внутри макрофагов в кишечном участке инфекции [207].
Исследования на мышах показали, что CD4 + и CD8 + Т-клетки необходимы для борьбы с инфекцией YE [196, 208], как и IFN- γ -опосредованные иммунные ответы Th2, включая продукцию макрофагами TNF, ИЛ-12 и ИЛ-18 [209–212]. Ингибирование пролиферации Т-клеток и функций дендритных клеток с помощью Yops являются первичными механизмами, с помощью которых иерсинии уклоняются как от врожденных, так и от адаптивных иммунных ответов [213]. Интересно, что иерсинии вызывают как апоптоз наивных макрофагов, так и гибель воспалительных клеток (пироптоз) активированных макрофагов, что согласуется с двухфазным инфекционным процессом [73, 75].Усиление воспаления, связанное с перенаправленной гибелью клеток-хозяев, первоначально может принести пользу иерсиний, но позже может способствовать генерализованному иммунному ответу и, в конечном итоге, избавлению от бактерий [73, 75].
1.12. Выявление и профилактика пищевого иерсиниоза
Клинические инфекции YE и YPT чаще всего возникают после попадания бактерий в загрязненную пищу или воду. Две вышеупомянутые иерсинии были выделены из мяса, свежих продуктов и молока, но их присутствие часто не очевидно из-за трудностей обнаружения.Различные штаммы YE чаще всего различают с помощью гель-электрофореза в импульсном поле (PFGE), но в настоящее время нет стандартизированного теста или базы данных для последовательной идентификации. Более того, энтеропатогенные виды Yersinia не включены в протоколы, которые используются лабораториями PulseNet, которые в сотрудничестве с Ассоциацией лабораторий общественного здравоохранения (APHL) координируют свои действия с лабораториями общественного здравоохранения для определения подтипов бактериальных патогенов пищевого происхождения [214]. Гетерогенность как YE, так и YPT затрудняет окончательное выявление, а PFGE дает множество полос, которые не особенно различимы в зависимости от серотипа [29, 215–217].В некоторых отчетах высказывается предположение, что современные методы обнаружения могут давать ложноотрицательные или ложноположительные результаты на основе вариабельности в присутствии факторов вирулентности Yersinia и их вариабельной корреляции с патогенностью [218, 219]. Предложения по улучшению обнаружения включают использование более чем одной рестрикционной нуклеазы в анализах PFGE [29] и применение недавно разработанного мультилокусного анализа тандемных повторов с переменным числом переменных (MLVA) для YE [220, 221].
Обнаружение — особенно важная проблема, потому что и YE, и YPT могут легко размножаться при температурах охлаждения (4 ° C) и даже при таких низких, как 0 ° C.Кроме того, энтеропатогенные иерсинии также могут адаптироваться и процветать в измененных атмосферных условиях, которые часто используются в сочетании с более низкими температурами в качестве обычных методов сохранения пищевых продуктов. Выживание и рост клеток при низких температурах достигаются за счет кратковременной реакции на холодовой шок, при которой продуцируются различные белки стрессовой реакции, которые обеспечивают адаптацию бактерий к внезапному падению температуры (см. Обзор [222]). И YE, и YPT также способны к более длительной адаптации к холоду, процессу, который требует полинуклеотидфосфорилазы (PNPase), экзорибонуклеазы холодового шока, которая усиливает как функцию T3SS, так и способствует росту в холодных условиях [223].
Патогенный YE продуцирует инсектицидные токсины, кодируемые генами tc (, подобные комплексу токсина ), локализованными на острове хромосомной патогенности [224, 225]. Эти инсектицидные токсины экспрессируются при низких температурах [226], но, тем не менее, считается, что они обладают функциями вирулентности у млекопитающих-хозяев [224, 225]. Возможно, присутствие этих инсектицидных токсинов предполагает, что нормальный жизненный цикл YE включает стадию насекомых, как предполагалось ранее [226], и эти токсины могут способствовать росту организмов в охлажденных пищевых продуктах.Белки Tc в YPT, с другой стороны, не обладают инсектицидной активностью, а скорее придают токсичность клеткам млекопитающих [227] и, следовательно, могут играть роль в заболеваниях человека.
Присутствие β -лактамаз, которые придают устойчивость к антибиотикам некоторым патогенным штаммам YE [228, 229], подчеркивает важность наблюдения за этими патогенными организмами. Хотя мониторинг этих организмов на национальном уровне не проводится, показатели заболеваемости иерсиниозом и демографические данные пациентов в Соединенных Штатах ежегодно собираются Сетью активного наблюдения за болезнями пищевого происхождения (FoodNet).FoodNet сообщила о 1355 и 18 случаях иерсиниоза человека с YE и YPT, соответственно, в США в период с 1996 по 2007 год. Однако, согласно оценкам FoodNet [230], случаи иерсиниоза, особенно вызванного YPT, вероятно, недооценены в США из-за отсутствия тестирования и трудностей, связанных с культивированием иерсиний на стандартных средах [231, 232].
2. Выводы
YE является основной причиной иерсиниоза у людей, хотя информация о распространенности YPT-ассоциированного заболевания, вероятно, занижена из-за отсутствия надзора и различий в применяемых стратегиях изоляции.Чрезвычайная неоднородность штаммов YE и YPT еще больше затрудняет попытки связать заражение с источником и единообразный мониторинг заболеваний человека, сравнимый с другими более тщательно изученными патогенами пищевого происхождения (например, Salmonella ). Хотя множество животных-хозяев служат резервуарами как для YE, так и для YPT, иерсинии, связанные с заболеваниями человека, наиболее распространены у свиней. У здоровых людей заболевание может проявляться в виде легкой, самоограничивающейся диареи, но у маленьких детей и лиц с ослабленным иммунитетом иерсиниоз может представлять собой значительный источник заболеваемости и смертности.Кроме того, у людей с ослабленным иммунитетом могут развиваться хронические заболевания, такие как реактивный артрит, и вторичные (или внутрибольничные) осложнения, такие как сепсис.
YE и YPT — гетерогенные организмы, различающиеся по геномному составу и степени патогенности. Два патогенных штамма (1B / O: 8 и 3 / O: 9) были секвенированы и сопоставлены [53, 54], чтобы получить представление о механизмах вирулентности, необходимых для инициирования инфекции и возникновения острых симптомов или хронических состояний у пациентов.Инфекция YE обычно возникает при употреблении зараженной пищи или воды и включает в себя присоединение к кишечному барьеру и перемещение через него через М-клетки [16]. Другие факторы вирулентности включают плазмиду pYV, которая кодирует T3SS, необходимый для патогенности YE [79], и хромосомный локус HPI, обнаруженный в высокопатогенных штаммах [69]. Патогенные штаммы YPT кодируют новый суперантигенный токсин, YPM, который способствует системным инфекциям [68], и систему PhoP / Q, важную для регуляции выживания и роста бактерий в макрофагах [93, 94].Гены пилуса IV типа [194] и недавно обнаруженный T6SS [193] также вносят вклад в вирулентность иерсиний. Несмотря на то, что большая часть молекулярных исследований внесла значительный вклад в лучшее понимание патогенности YE и YPT, многое можно извлечь из будущих исследований, особенно тех, которые направлены на анализ вклада различных комбинаций факторов вирулентности в патогенность, и возникающий в результате тип инфекции. и способность иммунной системы хозяина избавляться от бактерий. Очень мало известно об аутоиммунных заболеваниях, связанных с иерсиниями, и других хронических состояниях.Например, YPT гораздо менее изучен, чем YE, и поэтому его можно недооценивать как возбудителя иерсиниоза. Таким образом, усилия по надзору за иерсиниозом сосредоточены почти исключительно на YE, что делает практически невозможными попытки точно оценить заболеваемость YPT-ассоциированным гастроэнтеритом.
Энтеропатогенные YE и YPT вызывают иерсиниоз во всем мире и вызывают серьезную озабоченность в свиноводстве. Способность энтеропатогенных иерсиний размножаться и процветать при температурах охлаждения в сочетании с их, казалось бы, повсеместным характером, предполагает, что будущие и более единообразные меры надзора неизбежны и необходимы.В настоящее время случаи энтеропатогенных иерсиний, вероятно, недооценены; однако недавние профилактические меры в свиноводстве и повышенное внимание, как в исследовательских лабораториях, так и в клиниках, дадут столь необходимое понимание и лучшие стратегии для лечения иерсиниоза. Кроме того, более тщательные и единообразные меры эпиднадзора позволят нам более точно оценить национальные и глобальные тенденции иерсиниоза и лучше предсказать, какие сельскохозяйственные, гигиенические и клинические меры являются эффективными для снижения заболеваемости иерсиниозом среди населения в целом.
Благодарности
Работа над этим документом была поддержана соглашением о сотрудничестве NNX08B4A47A (JAR) Национального управления по аэронавтике и исследованию космического пространства (НАСА) и грантами NIH / NIAID AI064389 и N01 AI30065, присужденными Ашоку К. Чопре. Авторы также признают грант UC7, который способствовал их исследованиям в Национальной лаборатории Галвестона.
Инфекция Yersinia pseudotuberculosis — microbewiki
Университет Оклахомы, исследование микробиологии за рубежом в Ареццо, Италия [1] Изображение Yersinia psuedotuberculosis .Источник: tufts.edu [2]Этиология / бактериология
Таксономия
| Домен = Бактерии
| Тип = Proteobacteria
| Class = Гамма-протеобактерии
| Заказ = Энтеробактерии
| Семья = Enterobacteriaceae
| Род = Yersinia
| Вид = Псевдотуберкулез
| NCBI: Таксономия Геном: Геном |
Описание
Yersinia pseudotuberculosis — это грамотрицательная коккобацилла, не ферментирующая лактозу, способная инфицировать как людей, так и животных, но в первую очередь это зоонозная инфекция [1,8].Зарегистрированные случаи заболевания людей Y. pseudotuberculosis связаны с загрязнением пищевых продуктов и воды. Этот организм обладает высокой вирулентностью из-за секреции суперантигенного экзотоцина YPM. Боль в животе и жар — следующие симптомы этой инфекции, но это не единственные симптомы. Есть множество симптомов, которые могут возникнуть в результате заражения этими бактериями. Уровень смертности низкий, несмотря на большое количество осложнений, которые могут возникнуть от Y. pseudotuberculosis , таких как ненужные аппендэктомии или бактериемия, то есть присутствие микроорганизмов в кровотоке [3].Диагностика проводится путем анализа образцов кала, и Y. pseudotuberculosis может быть выделено с помощью агара МакКонки. Чтобы избежать заражения, вызываемого Y. pseudotuberculosis , следует избегать употребления неправильно приготовленного мяса, непастеризованного молока и загрязненной воды. Кроме того, правильное мытье рук может снизить воздействие.
Патогенез
Трансмиссия
Хотя Yersinia pseudotuberculosis — зоонозное заболевание, поэтому оно может передаваться людям.Иерсиниоз в первую очередь вызывается инфекциями, вызванными Yersinia enterocolitica , но в качестве причин были зарегистрированы зараженные пищевые продукты и инфекции, передаваемые через воду, вызванные Y. pseudotuberculosis . Некоторые примеры включают передаваемые через воду инфекции, обнаруженные в Чехословакии, а также в Окаяме, Япония. [2]
Заражение человека начинается с попадания зараженных пищевых продуктов в желудочно-кишечный тракт, начиная с кишечника и заканчивая брыжеечными лимфатическими узлами. Y. pseudotuberculosis может колонизировать ряд различных животных-резервуаров, таких как: собаки, кошки, крупный рогатый скот, лошади, кролики, олени, индейки, утки и многие другие.
Инфекционная доза и инкубационный период
Характеристика других инфекций Yersinia , Yersinia pseudotuberculosis требует дозы 10 9 организмов, чтобы вызвать заболевание. Инкубационный период Y. pseudotuberculosis составляет 5-10 дней; однако сообщалось о продолжительности эпизодических вспышек от 2 до 20 дней, при этом в среднем через 4 дня после контакта с бактерией наблюдались симптомы.
Эпидемиология
По данным FDA, на сегодняшний день в Соединенных Штатах не зарегистрировано случаев заражения Y. pseudotuberculosis из-за заражения пищевых продуктов. О спорадических вспышках болезни сообщалось в Северной Европе и Японии [3]. В апреле 2004 г. в Финляндии было зарегистрировано несколько случаев гастроэнтерита, вызванного инфекцией Y. pseudotuberculosis , у школьников [4], и в конечном итоге зараженная морковь была признана причиной инфекции.Многие другие задокументированные случаи связаны с употреблением нечистой питьевой воды или загрязненных колодцев [2]. Большинство случаев Y. pseudotuberculosis являются изолированными и необычными для людей, поскольку он часто вызывает заболевание у животного-хозяина. Y. pseudotuberculosis имеет низкий уровень смертности среди людей, если у пациента нет хронического заболевания печени. В этом случае летальность может превышать 75% [2]. Большинство случаев у людей происходит зимой из-за того, что повышенная сезонная заболеваемость поражает животных.Также наблюдаются улучшенные характеристики роста при низких температурах [13]. Y. pseudotuberculosis , по-видимому, не имеет каких-либо расовых особенностей, но в 3 раза чаще встречается у мужчин, чем у женщин.
Факторы вирулентности
Yersinia pseudotuberculosis имеет ряд факторов вирулентности, которые способствуют патогенности организма. Факторы вирулентности Yersinia pseudotuberculosis положительно коррелируют с температурой.В частности, следующие факторы вирулентности требуют кислой среды при высоких температурах для проникновения в клетки-хозяева. По мере повышения температуры хозяина токсичность факторов вирулентности увеличивается, позволяя им прочно связываться с лимфатической тканью хозяина.
Йопс
Y. pseudotuberculosis содержит плазмиду размером 70 кДа, которая кодирует систему секреции типа III, которая доставляет внешние белки Yersinia (Yops). Существует четыре основных белка Yops, которые необходимы для патогенности Y.pseudotuberculosis : YopE, YopJ, YopT и YopH. YopE активирует RhoGTPase GTP-связывающего белка, который играет роль в расположении актиновых филаментов, стимулировании округления клеток, предотвращении пор мембраны клетки-хозяина и ингибировании фагоцитоза [2]. YopE также играет роль в снижении провоспалительных сигналов клеток-хозяев за счет снижения выработки интерлейкина-8. YopJ связывается с протеинкиназами, которые блокируют фосфорилирование в клетке. В конечном итоге это приведет к снижению выработки интерлейкина-8, влияя на провоспалительный ответ хозяйских клеток.YopT нарушает расположение актиновых филаментов и предотвращает фагоцитоз клетки-хозяина. YopT не присутствует в патогенных штаммах Y. pseudotuberculosis . YopH также способствует нарушению фагоцитоза и расположения актиновых филаментов, а также снижает секрецию интерлейкина-8. Четыре основных внешних белка Yersinia работают вместе, чтобы нарушить иммунный ответ хозяина.
Экзотоксин-YPM
Некоторые штаммы Y. Pseudotuberculosis секретируют суперантигенный экзотоксин YPM, или Y.pseudotuberculosis -производный митоген. YPM предпочтительно стимулирует пролиферацию Т-лимфоцитов CD4, но некоторая экспрессия CD8 все же происходит. Наряду с пролиферацией YPM стимулирует гиперпродукцию интерлейкина-8, увеличивая воспалительную реакцию хозяина. Y. pseudotuberculosis. штаммов, связанных с FESLF, недавно были генетически секвенированы, что показало, что мобильные генные пулы содержат YPM. YPM включает 3 суперантигена — YPMa, YPMb и YPMc — все они имеют патогенное значение и отличаются от других бактериальных суперантигенов [13]
Молекулы адгезии
Молекулы адгезии Y.pseudotuberculosis связываются с клеткой-хозяином и облегчают ее колонизацию в организме-хозяине. Два основных белка этой группы включают инвазин и yadA. Инвазин связывается с интегринами М-клеток пейеровского пятна в тонком кишечнике, а также играет роль в интернализации бактерий через М-клетки. YadA связывается с ламинином, коллажем и фибронектином, которые связаны со своими рецепторами на поверхности клетки.
Остров высокой патогенности (HPI)
Остров высокой патогенности содержит ген, кодирующий иерсиниабактин, который используется для поглощения железа.
Путь двойной транслокации аргинина (tat)
Двойной путь транслокации аргинина важен для секреции белков, обеспечивающих подвижность и устойчивость к кислотам. Недавние геномные исследования показали, что этот путь подобен пути tat в E. coli . Вероятно, что оба пути tat произошли от общего промотора. При изучении пути tat в гораздо более известном организме, таком как E. coli , патогенность фактора вирулентности tat стала гораздо более изученной.Последующие открытия доказали, что белок tat не играет никакой роли в росте клеток. Скорее, фактор вирулентности tat остается наиболее связанным с подвижностью клеток.
Клинические особенности
Двумя наиболее распространенными симптомами, связанными с инфекциями Yersinia pseudotuberculosis , являются боль в животе, которая может варьироваться в зависимости от того, где бактерия поражает хозяина, и лихорадка. Не существует процесса определения стадии, связанного с инфекциями Y. pseudotuberculosis . Ряд клинических проблем может проявиться у Y.псевдотуберкулез , включая осложнения со стороны почек, желудочно-кишечного тракта и сильные кожные высыпания. Сопутствующие симптомы могут включать кожную сыпь, клубничный язык и лимфаденопатию. Наиболее распространенная форма инфекции Y. pseudotuberculosis возникает в результате употребления зараженных пищевых продуктов, особенно свежих. Прием зараженной пищи или воды, например, вызывает гастроэнтерит, мезентериальный лимфаденит (ссылка ниже) и даже узловатую эритему.Фактически, дифференциальный диагноз может включать узловатую эритему и ювенильный ревматоидный артрит [13]. Диарея встречается редко, и люди, у которых развивается лихорадка Идзуми, сопровождаются дополнительными сопутствующими симптомами. Хотя инфекции, вызываемые Y. pseudotuberculosis , широко распространены, инфекции обычно проходят самостоятельно с низким уровнем летальности. [5], поскольку Y. pseudotuberculosis не продуцирует железосвязывающие соединения, пациенты с состояниями перегрузки железом, такими как гемохроматоз, венозный застой, гемолитическая анемия или цирроз, подвержены риску сепсиса [13].
Диагностика
Yersinia pseudotuberculosis может быть трудно культивировать из-за наличия здоровой микробиоты. От пациента требуется образец кала, после чего можно выделить микроорганизм. Исследования показали, что обогащение при низких температурах эффективно использовалось для культивирования и изоляции микроорганизмов. [6] Затем можно использовать анализ полимеразной цепной реакции для идентификации бактерий и дальнейшего серотипирования организма. [7] Культуру также можно выделить и выращивать на агаре МакКонки благодаря ее способности ферментировать сорбит и ее способности продуцировать орнитиндекарбоксилазу.[8] Y. pseudotuberculosis был серотипирован с использованием иммуноферментного анализа вместе с тестами на агглютинацию, но результаты оказались неубедительными из-за возможности перекрестных реакций других патогенных антител. [8] Образцы крови могут быть взяты и протестированы для подтверждения присутствия микроорганизма, но образец фекалий является предпочтительным методом диагностического тестирования. [7]
Лечение
Серьезность инфекции напрямую определяет уровень лечения, необходимого для устранения колонизации Yersinia pseudotuberculosis .За многими случаями Y. pseudotuberculosis внимательно наблюдает врач, но никаких действий не требуется из-за самоограничивающей природы бактерий. [8] При необходимости, Y. pseudotuberculosis чувствителен к ампициллину, цефалоспоринам, аминогликозидам, тетрациклинам и хлорамфениколу. [9] Если у пациента есть основные факторы, такие как иммунодефицит или тяжелое обезвоживание, может потребоваться госпитализация, чтобы можно было назначить правильный уровень лечения.[8]
Профилактика
Могут возникать пищевые и водные эпидемии Y. pseudotuberculosis . Избегайте употребления сырого мяса и непастеризованного молока и помните о возможности заражения воды. Следует соблюдать осторожность, особенно при обращении со свиными кишками. Если вы когда-либо обращались со свининой подобным образом, необходимо применять надлежащие методы мытья рук. Будьте осторожны при обращении с фекалиями животных, особенно домашнего скота. Также рекомендуется правильное удаление фекалий животных, чтобы избежать загрязнения воды.Опять же, правильное мытье рук предотвратит распространение инфекции от животного к человеку-хозяину. [2]
Иммунный ответ хозяина
Y. pseudotuberculosis демонстрирует уникальные ответы на иммунную систему хозяина; он характеризуется факторами вирулентности, которые позволяют микроорганизму поддерживать жизнь в организме хозяина. Одной из характеристик, общих для всех видов Yersenia , является способность атаковать фагоцитарные клетки, что является важной частью ответа хозяина на патогенные инвазии [10].Несмотря на его внеклеточное пребывание во время патогенеза, исследования показали, что иммунный ответ хозяина компенсирует атаку фагоцитарных клеток CD8 + Т-клетками [10]. Эффекторная молекула Т-клеток, перфорин, играет не менее важную роль в гибели и фагоцитозе патогена [10]. Гибель клеток характеризуется апоптозом наивных клеток и пироптозом активированных макрофагов, которые являются невоспалительными и воспалительными, соответственно [11]. Y. pseudotuberculosis чаще всего встречается у животных, но при передаче обычно поражает детей и лиц с ослабленным иммунитетом [12].
Структура реагирования на повреждения
График реакции на повреждение для Y. pseudotuberculosisПринято характеризовать патогены на основе факторов вирулентности, способов передачи или типа систем органов, которые они инфицируют. Одна система классификации, называемая структурой реакции на повреждение, характеризует микроорганизмы на основе их взаимодействия с хозяином и причиненного ущерба. [14] Эта система классификации основана на том принципе, что микроорганизм и хозяин взаимодействуют друг с другом, и что эти взаимодействия могут быть полезными или вредными.Структура реакции на повреждение также основана на идее, что повреждение, которое проявляется в виде патогенных симптомов, может быть вызвано микроорганизмом или защитными механизмами хозяина в ответ на этот микроорганизм. [14] Основываясь на этом понимании, можно построить график течения болезни или любого другого взаимодействия между хозяином и микроорганизмом в зависимости от повреждения хозяина в зависимости от времени. Горизонтальная линия в середине графика представляет собой нейтральное взаимодействие между двумя факторами. Уменьшение в нижних областях графика означает, что взаимодействие выгодно для хоста, в то время как увеличение в верхних областях графика указывает на повреждение, даже потенциально смерть.[14] График, показанный здесь, иллюстрирует, как структура реакции на повреждение может быть применена к инфекции Yersinia pseudotuberculosis . В начальный момент заражения, обычно фекально-оральным путем, не наблюдается ни положительного, ни отрицательного воздействия на хозяина. [8] Инкубационный период Y. pseudotuberculosis может составлять от 5 до 10 дней. [8] В течение этого инкубационного периода хозяину практически не причиняется никакого ущерба, и, следовательно, реакция на повреждение не смещается из нейтрального положения.После инкубационного периода Y. pseudotuberculosis может иметь латентный период от 2 до 20 дней, в течение которого повреждения практически отсутствуют, поэтому график реакции на повреждения не изменяется [8]. Появление симптомов, таких как боль в животе, лихорадка, кожная сыпь, клубничный язык и лимфаденопатия, быстро ускоряет реакцию на повреждение, но поскольку инфекция является самоограничивающейся, реакция на повреждение спадает обратно в нейтральное положение между болезнью и комменсализмом . [8] Однако заболевание может вызывать хронические осложнения, и в этом случае реакция на повреждение остается повышенной из-за этого долгосрочного последствия взаимодействия хозяина и микроорганизма.В более серьезных случаях Y. pseudotuberculosis может вызвать сепсис у хозяина, который часто приводит к смерти [8]. Это представлено на временной шкале реакции на повреждение резким увеличением повреждений.
Номер ссылки
1. Лонг, К., Т.Ф. Джонс., Д.Дж. Vugia, J. Scheftel, N. Strockbine, P. Ryan, B. Shiferaw, R.V. Tauxe, L.H. Gould. Yersinia pseudotuberculosis и Y. enterocolitica Infections, FoodNet, 1996–2007. 2010. NCBI. 16 (3): 566.
2.Асим, Дж. А. «Псевдотуберкулез (иерсиния)».
3. http://www.fda.gov/Food/FoodborneIllnessContaminants/CausesOfIllnessBadBugBook/ucm070040.htm
4. « Yersinia pseudotuberculosis O: 1, произведенная в сырой моркови, Финляндия». Возникающие инфекционные заболевания. Vol. 14, № 12, декабрь 2008 г.
5. Лонг С., Джонс Т., Гулд Л. и др. Yersinia pseudotuberculosis и Y.enterocolitica инфекции, FoodNet, 1996-2007. Новые инфекционные заболевания [сериал онлайн]. Март 2010 г .; 16 (3): 566-567. Доступно по адресу: MEDLINE, Ипсвич, Массачусетс.
6. Абдулла З.А. и Канан Т.А. «Изоляция Yersinia spp. От случаев диареи у младенцев и детей Ирака». EMHJ — Eastern Mediterranean Health Journal, 15 (2), 276-284, 2009.
7. Nakajima, H .; Inoue, M .; Мори, Т .; Ито, К .; Аракава, Э.и Ватанабе, Х. «Обнаружение и идентификация Yersinia pseudotuberculosis и патогенных Yersinia enterocolitica с помощью усовершенствованного метода полимеразной цепной реакции». Журнал клинической микробиологии Vol. 30, №9. Сентябрь 1992 г.
8. Яни А. и Чен П. «Обследование псевдотуберкулеза (иерсинии)». Medscape. Ноябрь 2013 г.
9. «Yersinia pseudotuberculosis».Агентство общественного здравоохранения Канады. 2011.
10. Бергман М.А., В.П. Лумис, Дж. Мексас, М. Штарнбах и Р.Р.Исберг. CD8 + Т-клетки ограничивают инфекцию Yersinia pseudotuberculosis: обход антифагоцитоза путем нацеливания на антигенпрезентирующие клетки. 2009. NCBI. 5 (9).
11. Bergsbaken, T., and B.T. Куксон. Врожденный иммунный ответ во время инфекции Yersinia: критическая модуляция механизмов гибели клеток через активацию фагоцитов.2009. NCBI. 86 (5).
12. Хан, Т.Х., И.К. Пак, С.Дж. Ким. Молекулярная связь между изолятами Yersinia pseudotuberculosis от пациента и изолятом из воды из горных источников. 2002. NCBI. 18: 425.
13. Асим, А. Яни. Патофизиология Y. Pseudotuberculosis. 2013.
14.Касадевалл А., Пирофски Л. 2003. Структура реакции на повреждение микробного патогенеза. Nature Reviews 10: 17-24.
Создано Линдси Болдуин, Тарой Карлайл, Рэйчел Гаррисон и Тори Каппел, учениками доктора Тиррелла Конвея в Итальянском центре Университета Оклахомы
Последний раз редактировали Ханна Уилсон, Сабрина Во и К.С. По, 15 июля 2015 г.
.

 ), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала.
), и препаратов, влияющих на окраску кала (железо, висмут, сернокислый барий), в течение 72 часов до сбора кала. Еще одним недостатком серологических тестов является то, что антитела к иерсиниям (IgG-антитела) сохраняются в течение нескольких лет после инфицирования, что может препятствовать интерпретации результата. Следует помнить, что результат серологических тестов зависит от иммунного статуса организма.
Еще одним недостатком серологических тестов является то, что антитела к иерсиниям (IgG-антитела) сохраняются в течение нескольких лет после инфицирования, что может препятствовать интерпретации результата. Следует помнить, что результат серологических тестов зависит от иммунного статуса организма.