Трофобластическая болезнь в гинекологии: признаки, диагностика, лечение
Трофобластическая болезнь – патология, возникающая во время беременности и в ранний послеродовой период. Ее диагностируют в 1-2,5% случаев. Это тяжелое состояние, которое заканчивается гибелью плода.
Что такое трофобластическая болезнь
Патология развивается при наличии аномалий трофобласта – элемента тканей плодного яйца. Ворсины хориона разрастаются, начинается усиленное деление клеток плацентарного ложа. Обычно процесс приводит к смерти плода. В ряде случаев беременность удается сохранить, но тогда начинаются преждевременные роды. Ребенок появляется на свет с серьезными пороками развития и чаще всего погибает.
Трофобластическая болезнь в гинекологии приводит к усиленному делению клеток плацентарного ложаВыделяют несколько разновидностей трофобластической болезни:
- Пузырный занос. Составляет более 70% случаев патологии. Характеризуется трансформацией ворсин наружной зародышевой оболочки в пузыри, наполненные жидкостью.

- Хорионкарцинома. Злокачественная опухоль, состоящая из трансформированных эпителиальных клеток хориона, трофобласта и зародышевых клеток. Болезнь быстро дает метастазы и распространяется по всему организму. Она вызывает серьезные поражения плода, которые приводят к выкидышу или замиранию беременности.
- Эпителиоидно одноклеточная трофобластическая опухоль. Наиболее редкая трофобластическая опухоль. Формируется из скопления аномальных трофобластов. Вызывает обширный некроз окружающих тканей. Дает метастазы по всему организму вплоть до головного мозга.
- Трофобластическая опухоль плацентарного ложа. Некоторые ученые относят ее к разновидностям хорионкарциномы.
 Концентрируется в области плацентарной площадки. Отдаленные метастазы дает на поздних этапах.
Концентрируется в области плацентарной площадки. Отдаленные метастазы дает на поздних этапах.
Каждая из этих разновидностей обладает определенными симптомами. Методы терапии будут различаться.
В гинекологии выделяют 4 стадии поражения:
- Новообразование не выходит за пределы матки.
- Распространение патологических клеток на придатки и влагалище.
- Выход опухоли на границы гениталий.
- Метастазирование на другие органы: почки, печень, легкие, головной мозг.
Симптоматика, методы лечения и прогноз на каждой стадии отличаются.
Причины развития патологии
Точные причины болезни не установлены. Существует несколько теорий ее возникновения. Некоторые ученые считают, что виной всему перенесенные вирусные инфекции. Другие склоняются к тому, что проблема заключается в излишней активности ферментов, дефиците белка и ослабленном иммунитете.
Сторонники вирусной теории говорят, что клетки вируса, например, гриппа, вызывают мутацию яйцеклетки. Эмбрион погибает, а патогенные ткани разрастаются. Некоторые считают, что гормоны эстроген, прогестерон и хориогонадотропин, уровень которых растет при беременности, иногда имеют выраженное иммунодепрессивное действие. Женский организм воспринимает плодное яйцо как инородное тело. В этом случае случается выкидыш. Если иммунный ответ слабый, формируется пузырный занос.
Эмбрион погибает, а патогенные ткани разрастаются. Некоторые считают, что гормоны эстроген, прогестерон и хориогонадотропин, уровень которых растет при беременности, иногда имеют выраженное иммунодепрессивное действие. Женский организм воспринимает плодное яйцо как инородное тело. В этом случае случается выкидыш. Если иммунный ответ слабый, формируется пузырный занос.
Не менее распространенным является мнение о том, что виной всему фермент гиалуронидаза, разрушающий стенки сосудов. В подтверждение тому выступают результаты анализов больных: при пузырном заносе уровень фермента в 7 раз превышает норму, а при злокачественных новообразованиях – в 15 раз. Также популярна теория о том, что при дефиците протеинов в организме матери хромосомы мутируют. Зародыш становится неполноценным, а его клетки вызывают рост новообразований.
Спровоцировать развитие патологии могут следующие факторы:
- перенесенные аборты, выкидыши, роды;
- внематочная беременность;
- позднее половое созревание;
- трофобластическая болезнь в анамнезе;
- интоксикация;
- прием некоторых препаратов, алкоголя и наркотиков во время беременности;
- диагностированное воспаление внутреннего слоя матки.

Доказано, что эта гестационная патология поражает женщин старше 40 лет в 5 раз чаще. У представительниц западных народов риск заболеть меньше, чем у выходцев с Востока.
Признаки заболевания
- артериальная гипертензия;
- сильный токсикоз с неукротимой рвотой;
- тахикардия;
- повышение температуры тела;
- патологические выделения из сосков.
Если опухоль дает метастазы в легкие, возникает кашель и выделяется мокрота с прожилками крови. При поражении головного мозга ухудшается зрение, женщину мучают головные боли. Вовлечение в процесс желудочно-кишечного тракта сопровождается болями в животе, желудочно-кишечными кровотечениями. Метастазы в почках приводят к появлению крови в моче.
Метастазы в почках приводят к появлению крови в моче.
Диагностика патологии
Для выявления пузырного заноса проводят ультразвуковое исследование. В большинстве случаев матка оказывается больше, чем должна быть на данном сроке. Но иногда при частичном заносе детородный орган не увеличивается или даже становится меньше. УЗ картина специфическая, ее достаточно для постановки диагноза. Дополнительно назначают анализ мочи на уровень ХГЧ. При заболевании он может превышать норму в десятки раз. Признаки пузырного заноса на УЗИПри подозрении на хорионкарциному проводят гинекологический осмотр. Он должен показать цианоз слизистой влагалища и шейки матки, метастазы в виде темно-красных бугорков и сероватые узелки в некротических тканях. Матка увеличена, ее стенки более мягкие, в области придатков прощупываются кисты. Также необходимо УЗИ. Оно показывает локализацию новообразования.
Проводят анализы на наличие белков и уровень гормона ХГЧ. В ходе диагностического выскабливания берутся ткани для биопсии.
Лечение трофобластической болезни
Доброкачественную форму заболевания лечат путем удаления новообразований. Для этого используют выскабливание или вакуумную аспирацию. Также прописывают кровоостанавливающие препараты. После процедуры в течение 2 месяцев необходим постоянный врачебный контроль с периодической проверкой уровня хориогонадотропина и УЗИ органов малого таза. Клинические рекомендации включают в себя исследование ХГ каждые 2 недели в течение 3 месяцев, а затем раз в месяц в течение полугода, соблюдение контрацепции на протяжении года.
При удовлетворительных результатах исследований и нормализации менструального цикла в течение 8 недель дополнительное лечение не показано. Но если в течение этого срока симптомы болезни не пропали, а результаты ультразвукового исследования показывают патологические участки в матке, пациентке необходима химиотерапия.
При отсутствии положительных результатов терапии и возникновении маточного кровотечения проводят операцию. Она заключается в удалении матки и придатков или надвлагалищная ампутация. Пациенткам репродуктивного возраста может быть проведена органосберегающая операция с иссечением пораженных участков.
Показания к операции при трофобластической болезниИнвазивный пузырный занос, хорионкарциному и другие виды злокачественных новообразований лечат путем химиотерапии. Схема и длительность лечебных мероприятий зависит от точности диагноза и степени поражения внутренних органов. При отсутствии положительного результата от медикаментозного лечения проводят операцию по удалению матки. В обязательном порядке хирургическое вмешательство назначают больным старше 40 лет. Перед операцией проводят 1-2 курса химиотерапии.
Прогноз
При своевременной диагностике и своевременных лечебных мероприятиях болезнь проходит без осложнений.
- Новости
- Здоровье
- Семья и дети
- Питание и диеты
- Красота и мода
- Отношения
- Спорт
- О портале
Здоровье
- Диагностика
- Компьютерная томография
- МРТ диагностика
- Медицинские манипуляции
- Обследование организма
- Эндоскопия (эндоскопические исследования)
- Радионуклидная диагностика
- Рентген (рентгенологические исследования)
- Ультразвуковая диагностика (УЗИ)
- Лечение
- Операции
- Врачебные специальности
- Лечение болезней
- Обзор лекарственных средств
- Нетрадиционная медицина
- Стволовые клетки
- Физиотерапия
- Переливание крови
- Трансплантация
- Болезни
- Беременность, роды и послеродовой период
- Синдромы
- Хирургические болезни
- Болезни зубов (стоматология)
- Болезни молочных желез (маммология)
- Болезни суставов, мышц и соединительной ткани (ревматология)
- Рак (онкология)
- Болезни иммунной системы (иммунология)
- Болезни крови (гематология)
- Болезни сердца и сосудов (кардиология)
- Психическое здоровье (психиатрия)
- Травмы и отравления
- Болезни кожи и подкожной клетчатки (дерматология)
- Болезни легких, бронхов и плевры (пульмонология)
- Болезни уха, горла и носа (отоларингология)
- Болезни эндокринной системы и нарушения обмена веществ (эндокринология)
- Инфекции, передающиеся преимущественно половым путем (венерические болезни)
- Гинекологические болезни (гинекология)
- Болезни глаз (офтальмология)
- Болезни детей (педиатрия)
- Болезни печени и желчных путей
- Болезни прямой кишки и анальной области
- Болезни нервной системы (неврология)
- Болезни желудочно-кишечного тракта (гастроэнтерология)
- Инфекционные и паразитарные болезни
- Болезни мочеполовой системы
- Анализы
- Анализы на гормоны
- Гематологические исследования
- Генетические исследования
- Определение наркотиков
- Пренатальная диагностика
- ПЦР (Полимеразная цепная реакция, ПЦР-диагностика)
- Серологические исследования
- Токсикологические исследования
- Онкомаркеры
- Диагностика аутоиммунных заболеваний
- Иммунитет
MEDISON. RU — Инвазивная трофобластическая неоплазия — клинический случай 3D сонографии
RU — Инвазивная трофобластическая неоплазия — клинический случай 3D сонографии
УЗИ сканер WS80
Идеальный инструмент для пренатальных исследований. Уникальное качество изображения и весь спектр диагностических программ для экспертной оценки здоровья женщины.
Введение
Роль сонографии в диагностике трофобластических неоплазий возрастает в связи с участившимися в последние годы случаями атипических форм трофобластической болезни без повышения уровня специфического опухолевого маркера — β-ХГ в плазме крови. В литературе описаны случаи инвазивной трофобластической неоплазии при относительно низких или нормальных уровнях β-ХГ после внематочной беременности или трофобластической опухоли плацентарного ложа с преимущественной пролиферацией промежуточных клеток трофобласта, которые во время беременности отвечают за выработку плацентарного лактогена [1, 2]. В исследованиях P. Cavoretto и соавт. было продемонстрировано, что использование цифрового допплеровского картирования (ЦДК) позволяет значительно раньше выявлять инвазию ткани трофобласта в миометрий, а также проводить динамическое наблюдение за ответом опухоли на проводимое лечение, чем при рутинном ультразвуковом исследовании [1].
В исследованиях P. Cavoretto и соавт. было продемонстрировано, что использование цифрового допплеровского картирования (ЦДК) позволяет значительно раньше выявлять инвазию ткани трофобласта в миометрий, а также проводить динамическое наблюдение за ответом опухоли на проводимое лечение, чем при рутинном ультразвуковом исследовании [1].
Представлен случай инвазивной трофобластической опухоли, развившейся после выскабливания матки по поводу неразвивающейся беременности, не сопровождавшейся повышением уровня β-ХГ и диагностированной с помощью 3D/4D реконструкции полости матки.
Клиническое наблюдение
Пациентка С., 29 лет, повторнобеременная. В анамнезе одни роды живым доношенным плодом 2 года назад. Настоящая беременность вторая. При сроке 8 нед диагностирована замершая беременность, произведен медикаментозный аборт. На контрольном УЗИ после выкидыша диагности
ТРОФОБЛАСТИЧЕСКАЯ ОПУХОЛЬ (ТРОФОБЛАСТИЧЕСКАЯ БОЛЕЗНЬ) — Здоровье прежде всего!
ТРОФОБЛАСТИЧЕСКАЯ ОПУХОЛЬ (ТРОФОБЛАСТИЧЕСКАЯ БОЛЕЗНЬ)
Воспалительные изменения эндометрия
С. P. Manahan и соавт. (1961) указывают, что далеко нередко при установлении диагноза синцитиального эндометрита в дальнейшем возникали метастазы трофобластической опухоли и больные умирали. Гистологическая диагностика синцитиомы затруднительна, а диагностика по данным изучения материала, полученного при выскабливании не всегда достоверна [Wei P., Ouyang P., 1963]. Существует мнение, что данную патологию клинически, учитывая случаи злокачественного течения заболевания, можно рассматривать как хорионэпителиому in situ и подобно раку шейки матки in situ относить ее к злокачественным заболеваниям.
P. Manahan и соавт. (1961) указывают, что далеко нередко при установлении диагноза синцитиального эндометрита в дальнейшем возникали метастазы трофобластической опухоли и больные умирали. Гистологическая диагностика синцитиомы затруднительна, а диагностика по данным изучения материала, полученного при выскабливании не всегда достоверна [Wei P., Ouyang P., 1963]. Существует мнение, что данную патологию клинически, учитывая случаи злокачественного течения заболевания, можно рассматривать как хорионэпителиому in situ и подобно раку шейки матки in situ относить ее к злокачественным заболеваниям.
Синцитиома (синцитиальный эндометрит)
Синцитиома (синцитиальный эндометрит). Заболевание характеризуется воспалительными изменениями эндометрия и миометрия различной степени выраженности, а также инфильтрацией их трофобластическими элементами, однако с низкой злокачественностью. По мнению А. Т. Hertig и Mansell (1956), синцитиома иногда морфологически подобна хориокарциноме, поэтому нередко используют синоним «хорионэпителиома in situ» [Bagshawe К. D., 1969; Goldstein D. P., Berkowitz R. S., 1982]. Биологическая реакция при синцитиоме часто бывает отрицательной. R. J. Kurmann и соавт. (1976), изучая резко выраженный синцитиальный эндометрит у 12 больных, отметили в гистологическом аспекте значительное отличие синцитиомы от трофобластических опухолей, отсутствие У 8 из них положительных тестов на беременность. Однако в отношении злокачественности синцитиомы имеются также высказывания другого рода. У одной из 3 больных, наблюдавшихся К. D. Bagshawe (1969), после удаления пузырного заноса по данным гистологического исследования был установлен синцитиальный эндометрит, через 5 мес у них увеличилась экскреция ХГ и появились метастазы в легких. По данным Н. Acosta-Sison (1957), 5 больных, имевших синцитиому (обнаруженную при выскабливании матки), в дальнейшем умерли от хорионэпителиомы.
D., 1969; Goldstein D. P., Berkowitz R. S., 1982]. Биологическая реакция при синцитиоме часто бывает отрицательной. R. J. Kurmann и соавт. (1976), изучая резко выраженный синцитиальный эндометрит у 12 больных, отметили в гистологическом аспекте значительное отличие синцитиомы от трофобластических опухолей, отсутствие У 8 из них положительных тестов на беременность. Однако в отношении злокачественности синцитиомы имеются также высказывания другого рода. У одной из 3 больных, наблюдавшихся К. D. Bagshawe (1969), после удаления пузырного заноса по данным гистологического исследования был установлен синцитиальный эндометрит, через 5 мес у них увеличилась экскреция ХГ и появились метастазы в легких. По данным Н. Acosta-Sison (1957), 5 больных, имевших синцитиому (обнаруженную при выскабливании матки), в дальнейшем умерли от хорионэпителиомы.
Деление трофобластических опухолей
Определение степени злокачественности зависит от критерия
Для хорионэпителиомы характерно образование некроза в центре фокуса трофобластических элементов.
Дифференцировать деструирующий пузырный занос и хорионэпителиому без гистологического исследования пораженного органа невозможно. Иногда приходится проводить дифференциальную гистологическую диагностику хорионэпителиомы со светлоклеточной саркомой, клетки которой напоминают цитотрофобласт, а также с эндометриальной саркомой и аденоакантомои эндометрия [Goldstein D. P., Berkowitz R. S., 1982].
Данные литературы и собственный опыт свидетельствуют о том, что деление трофобластических опухолей на доброкачественные и злокачественные относительно, так как:
определение степени злокачественности зависит от критерия, используемого каждым специалистом при установлении диагноза. Бывают случаи, когда при исследовании одного и того же гистологического препарата несколькими специалистами они дают разноречивые заключения;
патоморфологический диагноз зависит от материала, взятого для исследования.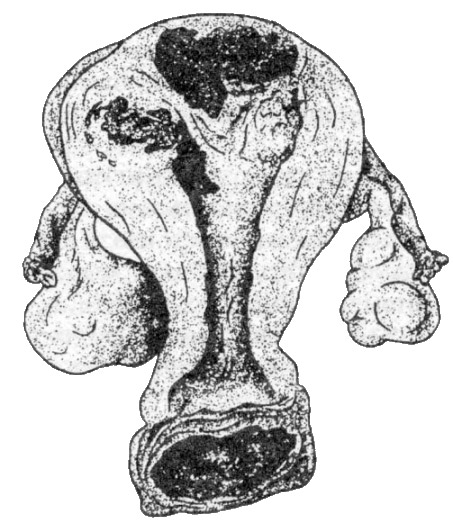 Исследование материала, полученного при выскабливании матки, не может считаться исчерпывающим, поскольку нет уверенности в том, что получен соскоб со всех участков слизистой оболочки матки
Исследование материала, полученного при выскабливании матки, не может считаться исчерпывающим, поскольку нет уверенности в том, что получен соскоб со всех участков слизистой оболочки матки
Деструирующий пузырный занос
Чаще всего заболеванию предшествуют аборты
При изучений влияния исхода предшествовавшей беременности на клиническое течение заболевания после удаления пузырного заноса установлено, что при завершении беременности родами злокачественные опухоли трофобласта развились у 53,1% больных. В тех же случаях, когда пузырному заносу предшествовали аборты, прогрессирование заболевания наблюдалось у 35,4% больных. Таким образом, злокачественные формы трофобластической болезни чаще развивались у больных, у которых пузырному заносу предшествовали роды.
При деструирующем пузырном заносе, по нашим данным, чаще всего заболеванию предшествовали аборты — у 67,6% больных (самопроизвольные — у 6,1%), роды наблюдались у 30,3% женщин. Хорионэпителиома чаще всего развивается после пузырного заноса, но может возникнуть и после абортов, родов, внематочной беременности. При анализе данных литературы [Новикова Л. А., Григорова Т. М., 1968] установлено, что частота того или иного исхода беременности, предшествовавшей хорионэпителиоме, была следующей.
При анализе данных литературы [Новикова Л. А., Григорова Т. М., 1968] установлено, что частота того или иного исхода беременности, предшествовавшей хорионэпителиоме, была следующей.
Из приведенных данных видно, что у больных в европейских странах, хорионэпителиома чаще всего возникает после родов, чем в странах Азии, но повсеместно это заболевание чаще наблюдается у больных, перенесших пузырный занос. В последующих публикациях, посвященных хорионэпителиоме, приводятся подобные же соотношения.
И. Д. Нечаевой и В. М. Дильман (1976) при анализе результатов наблюдений за 145 больными трофобластической болезнью отмечена существенная особенность данного заболевания, которая подтверждена в наших наблюдениях, значительно больших по численности: у больных с более злокачественными формами опухолей трофобласта им чаще всего предшествуют роды. Следовательно, наличие родов, предшествующих развитию трофобластических опухолей, следует считать неблагоприятным прогностическим фактором.
Деструирующий пузырный занос развивается только после пузырного заноса
Деструирующий пузырный занос. При деструирующем пузырном заносе обычно отмечается прорастание пузырной тканью всей толщи миометрия. На разрезе опухоль имеет вид рыхлой ткани от белесовато-желтого до темно-красного цвета, в которой имеются пузырьковидные образования. Микроскопически деструирующий пузырный занос характеризуется интенсивной пролиферацией хориального эпителия, его анаплазией, отеком стромы и распространением по венозным сосудам стенки матки.
При деструирующем пузырном заносе обычно отмечается прорастание пузырной тканью всей толщи миометрия. На разрезе опухоль имеет вид рыхлой ткани от белесовато-желтого до темно-красного цвета, в которой имеются пузырьковидные образования. Микроскопически деструирующий пузырный занос характеризуется интенсивной пролиферацией хориального эпителия, его анаплазией, отеком стромы и распространением по венозным сосудам стенки матки.
Патологоанатомическими критериями для диагностики деструирующего пузырного заноса, по мнению Novak и Woodruff, являются глубокое проникновение в толщу мышечного слоя, параметрий и прилежащие ткани пузырного заноса, который может иметь доброкачественное строение, а также выраженная пролиферация трофобластических клеток. При деструирующем пузырном заносе часто встречаются кровоизлияния, некроз и выраженная лимфоидная инфильтрация, окружающая опухоль. Отмечается глубокая инвазия клеток хориального эпителия в стенки сосудов. Деструирующий пузырный занос развивается только после пузырного заноса.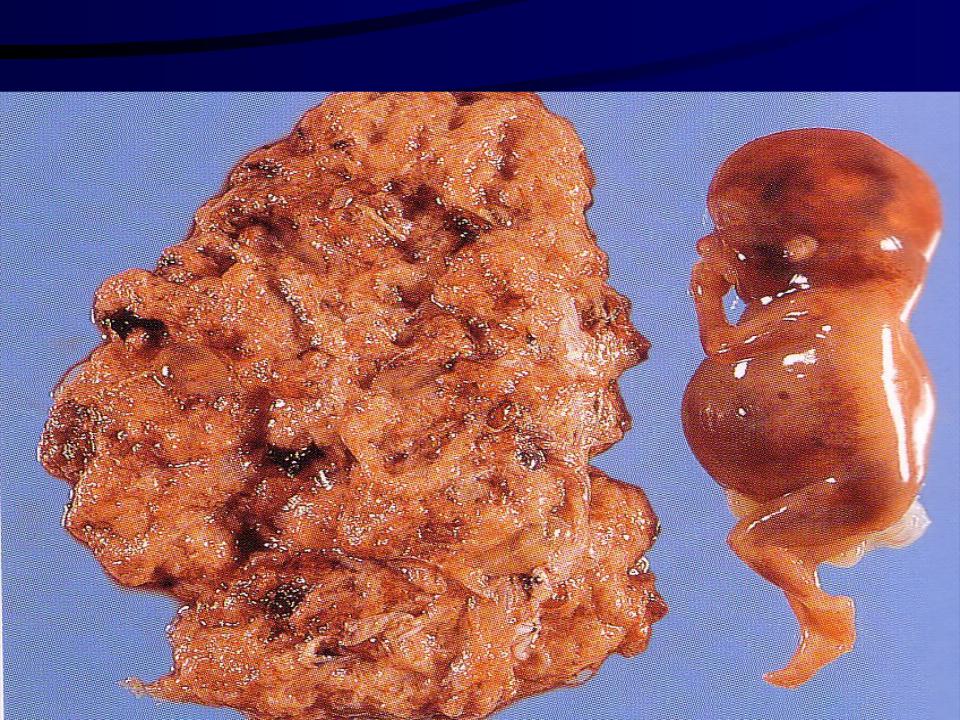
Некоторые опухоли имеют атипическое строение
Некоторые опухоли имеют атипическое строение: в них наблюдаются беспорядочное расположение и полиморфизм цитотрофобластических клеток, разные размеры клеток и их ядер, гиперхромия, наличие так называемых переходных форм между элементами цито- и синцитиотро-фобласта. Клетки «переходных форм» иногда встречаются крупнее клеток цитотрофобласта, ядра их более вытянутые, гиперхромные. Наличие «переходных форм» подтверждает точку зрения R. M. Wynn и J. С. Davies (1964) о происхождении синцитиотрофобласта из цитотрофобласта.
Дифференциальный диагноз между пузырным заносом с пролиферацией и полиморфизмом эпителия и хорион-эпителиомой труден, а в ряде случаев, вероятно, невозможен. Критериями злокачественности являются выраженная анаплазия клеточных элементов, наличие значительного количества митозов как в цитотрофобласте, так и в «переходных формах», участки некроза и кровоизлияний. Хотя долгое время многие авторы отвергали существование ворсин при хорионэпителиоме, наличие ворсин не противоречит диагнозу хорионэпителиомы.
Простой пузырный занос характеризуется наличием крупных ворсин хориона
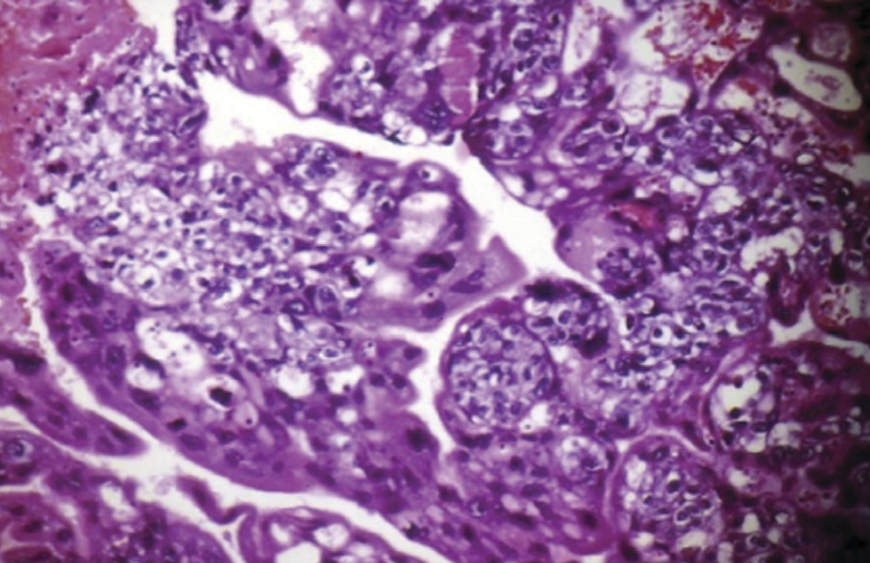
Основные морфологические признаки этого заболевания — значительное увеличение размеров ворсинок хориона с отеком и ослизнением их стромы и отсутствием сосудов, гиперплазия хориального эпителия, которая в равной степени охватывает как синцитий, так и трофобласт. Простой пузырный занос характеризуется наличием крупных ворсин хориона с отеком стромы и кистозной дегенерацией. Поверхность ворсин покрыта одним-двумя рядами клеток кубической или призматической формы с единичными клетками синцитиотрофобласта. Вокруг ворсин могут располагаться небольшие скопления клеток хориального эпителия. Пузырный занос с пролиферацией хориального эпителия имеет ворсины такого же строения. Иногда по периферии ворсины под эпителием имеется то или иное количество клеточно-волокнистой отечной стромы, эпителий кубический, иногда утолщен, располагается в несколько рядов, имеет участки фибриноидного некроза. Видны синцитиальные клетки, образующие как бы сосочковые структуры, цитоплазма этих клеток вакуолизирована. К ворсинам прилежат пласты хориального эпителия, состоящие из цитотрофобласта. Вокруг цитотрофобласта расположены синцитиальные элементы в виде протоплазматических масс, содержащих различное количество небольших ядер округлой формы.
К ворсинам прилежат пласты хориального эпителия, состоящие из цитотрофобласта. Вокруг цитотрофобласта расположены синцитиальные элементы в виде протоплазматических масс, содержащих различное количество небольших ядер округлой формы.
Хорионэпителиома встречается значительно реже пузырного заноса
Деструирующий пузырный занос возникает реже пузырного заноса и хорионэпителиомы. По материалам Л. Д. Заплавновой (1979), которая приводит данные литературы и наблюдения ВОНЦ АМН СССР, эта форма составляет всего 8% от всех случаев трофобластической болезни.
Хорионэпителиома встречается значительно реже пузырного заноса, но при этом также чаще наблюдается в восточных странах. Так, по данным A. Bremond (1977), во Франции одна хорионэпителиома зарегистрирована на 15 000 беременностей. P. Wie и P. Ouyang (1963) сообщают, что на о. Тайвань частота хорионэпителиомы по отношению к числу беременностей составляет 1:82. Однако из сообщений последних лет [Baltazar J. С, 1977] следует, что в городах Филлипин общая заболеваемость хорионэпителиомой значительно ниже по сравнению с ранее опубликованными данными— 1:5733 родов, или 1:6392 беременности.
Клиническое течение болезни
Разнообразие клинического течения трофобластической болезни
Разнообразие клинического течения трофобластической болезни многие авторы пытаются объяснить особенностями гистологического строения трофобластических новообразований.
Первая классификация трофобластических новообразований была предложена J. P. Ewing (1910). Автор пытался связать патогистологическую картину с клинической и предложил различать три группы опухолей: синцитиома, деструирующая хориоаденома, хориокарцинома (последнее название, подчеркивая близость с раковой опухолью, в сущности тождественно наименованию «хорионэпителиома»).
Прогноз заболевания
Пузырный занос, включая деструирующий пузырный занос, наиболее часто поражает женщин в начале детородного периода
По нашим данным, пузырный занос, включая деструирующий пузырный занос, наиболее часто поражает женщин в начале детородного периода — в возрасте 20— 24 лет, затем идет постепенное снижение частоты заболевания. Для деструирующего пузырного заноса отмечен второй пик в возрасте 40—49 лет, т. е. в период угасания детородной функции. Хорионэпителиома развивается преимущественно у женщин в возрасте 20—40 лет, чаще всего в 30—34 года.
Для деструирующего пузырного заноса отмечен второй пик в возрасте 40—49 лет, т. е. в период угасания детородной функции. Хорионэпителиома развивается преимущественно у женщин в возрасте 20—40 лет, чаще всего в 30—34 года.
Разноречивые мнения высказываются по вопросу о том, в каком возрасте возникновение пузырного заноса потенциально опаснее в отношении развития злокачественных форм опухолей трофобласта. Ряд авторов [Wagner D., 1968; Doehner H. G., 1969; Longfu S. et al., 1980] отметили, что хорионэпителиома после пузырного заноса у женщин старше 40 лет развивается почти в 3 раза чаще, чем у женщин моложе 30 лет. S. L. Curry и соавт. (1975), наблюдавшие 347 больных с пузырным заносом, подобной зависимости не установили. Из результатов нашего исследования также следует, что вероятность прогрессирования заболевания в значительной степени увеличивается, если пузырный занос возникает у женщин старше 40 лет, — 51,4%, а у женщин моложе 40 лет — 37%.
Клиническими критериями высокого риска пузырного заноса являются
Деление пузырного заноса на стадии 0—А и 0—В предусматривает возможную пролиферативную активность трофобласта. Клиническими критериями высокого риска пузырного заноса являются: размеры матки больше предполагаемого срока беременности, лютеиновые кисты яичников более 6 см в диаметре, возраст больной старше 40 лет, токсемия, предшествовавшая трофобластической опухоли, гипертиреоидизм и др.
Клиническими критериями высокого риска пузырного заноса являются: размеры матки больше предполагаемого срока беременности, лютеиновые кисты яичников более 6 см в диаметре, возраст больной старше 40 лет, токсемия, предшествовавшая трофобластической опухоли, гипертиреоидизм и др.
Большое количество классификаций трофобластической болезни свидетельствует о том, что до настоящего времени не изучены все особенности этого заболевания. Мы считаем гистологическую классификацию ВОЗ 1975 г. и клинико-анатомическую классификацию 1976 г. наиболее удобными для применения в клинической практике и для научных разработок. Эти классификации, на наш взгляд, дают возможность наиболее полно охарактеризовать патологический процесс при трофобластической болезни, четко выделить различные формы трофобластических опухолей и сопоставить с анатомическим распространением опухоли в организме больной, что позволяет применить адекватное лечение. Они отражают уровень знаний об этом заболевании на современном этапе исследований. Основываясь на собственном опыте диагностики и лечения трофобластической болезни, мы считаем целесообразным рекомендовать эти классификации для повсеместного применения в практике здравоохранения.
Основываясь на собственном опыте диагностики и лечения трофобластической болезни, мы считаем целесообразным рекомендовать эти классификации для повсеместного применения в практике здравоохранения.
Критерии для определения возможного озлокачествления трофобласта
Для того чтобы полно представить и документировать течение трофобластической болезни после удаления пузырного заноса, ряд исследователей [Bagshawe К. D., 1969; Hammond С. В., Parker R. Т., 1970; Hertz R., 1974, и др.] предлагали различные критерии для определения возможного озлокачествления трофобласта, которые послужили основой для новой классификации. В 1976 г. Международный комитет по изучению трофобластических опухолей принял классификацию, в которой сделана попытка сопоставить анатомическую распространенность опухолевого процесса с прогнозом заболевания.
Стадия 0 — пузырный занос;
А — низкий риск.
В — высокий риск. Стадия I — опухоль в пределах матки.
Стадия II — метастазы в органах малого таза и влагалище. Стадия III — метастазы в легких. Стадия IV — отдаленные метастазы (в мозге, печени и др.).
Стадия III — метастазы в легких. Стадия IV — отдаленные метастазы (в мозге, печени и др.).
Прогрессирование болезни
Прогрессирование трофобластической болезни происходило чаще у больных с поздним менархе
Раннее и позднее менархе встретилось почти в одинаковом проценте случаев. До наступления беременности, закончившейся развитием пузырного заноса, у 6,4% больных отмечались нарушения менструального цикла.
При изучении особенностей менструальной функции у больных с различными исходами заболевания после удаления пузырного заноса установлено, что прогрессирование трофобластической болезни происходило чаще у больных с поздним менархе (53,7%), по сравнению с больными, у которых оно наступало своевременно и рано. На основании этих данных мы пришли к заключению, что возникновение пузырного заноса у женщин, у которых менструации появились поздно — в возрасте 16 лет и старше, является прогностически неблагоприятным признаком, так как у них чаще развиваются злокачественные формы трофобластической болезни.
В настоящее время имеется довольно много работ, в которых отмечается влияние исхода предшествующей беременности на клиническое течение заболевания у больных со злокачественными формами трофобластических опухолей матки [Давиденко А. А., 1973; Нечаева И. Д., Дильман В. М., 1976; Bagschawe К. D., 1976, и др.]. Подобных исследований при пузырном заносе мы в литературе не встретили. В наших наблюдениях пузырному заносу наиболее часто предшествовали аборты — у 39,9% больных (искусственные — у 31,3%, самопроизвольные — у 8,6%), роды — у 24% больных, внематочная беременность — у 0,5% (2 больные).
Среди больных пузырны
Трофобластическая болезнь: виды, симптомы и лечение
Трофобластическая болезнь – термин, который обозначает патологические процессы, в результате которых в плаценте образуются доброкачественные или злокачественные образования. В данную группу входит простой пузырчатый занос, опухоли трофобластов эпителия, опухоли плацентарной площадки, хорионкарцинома.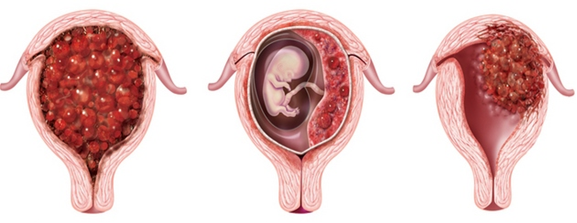
Четких ограничений относительно возрастной категории данное заболевание не имеет. Отмечается, что наиболее часто простой пузырчатый занос диагностируется у женщин до 24 лет, а инвазивная форма этого же заболевания свойственна женщинам после 40 лет.
Трофобластическая болезнь симптомы имеет неспецифического характера, поэтому своевременное лечение наблюдается крайне редко. Более того, медицине известны случаи, когда в латентной форме трофобластическая болезнь протекала несколько лет и была установлена случайно, путем диагностики другого заболевания. Необходимо отметить, что развитие такой патологии может происходить как после родоразрешения, так и во время беременности. В последнем случае болезнь приводит к гибели плода. Если патогенные клетки попадут в кровеносное русло, присутствует высокий риск летального исхода.
Лечение, как правило, операбельное или основывается на химиотерапии. В некоторых случаях совмещают два метода для повышения эффективности и снижения вероятности рецидива. Прогноз будет зависеть от природы образования. Если оно носит доброкачественный характер, то прогноз относительно положительный. В противном случае все зависит от тяжести течения патологии, возраста и общих показателей здоровья пациентки.
Прогноз будет зависеть от природы образования. Если оно носит доброкачественный характер, то прогноз относительно положительный. В противном случае все зависит от тяжести течения патологии, возраста и общих показателей здоровья пациентки.
Вне зависимости от того, какой именно патологический процесс имеет место, этиология различаться не будет. В гинекологии заболевания, которые входят в группу трофобластической болезни рассматриваются как единый этиопатогенетический процесс.
Предрасполагающими факторами для развития такого патологического процесса можно считать:
- вирусные заболевания затяжного характера или в хронической форме с частыми рецидивами;
- мутация яйцеклетки;
- иммунологические реакции организма;
- повышенное количество фермента гиалуронидазы;
- эндометрит;
- частые абортивные прерывания беременности;
- внематочная беременность;
- самопроизвольное прерывание беременности;
- зачатие ребенка в раннем возрасте;
- тяжелые роды в личном анамнезе;
- онкологические заболевания в семейном анамнезе;
- возраст младше 20 и старше 40 лет.

Кроме этого, ситуацию может усугубить курение, чрезмерное количество употребляемых спиртных напитков, бесконтрольный прием гормональных препаратов.
Женщинам, которые входят в группу риска, необходимо систематически проходить медицинский осмотр и ответственно относиться к зачатию ребенка – беременность нужно планировать.
Трофобластическая болезнь классифицируется по нескольким признакам. Так, в данное понятие, согласно международной классификации заболеваний, входят следующие патологии:
- пузырный занос – может быть частичным или полным;
- инвазивный пузырный занос;
- хориокарцинома;
- хориокарцинома, которая сочетается с тератомой;
- трофобластическая злокачественная тератома;
- трофобластическая опухоль плацентарной площадки.
Принимая во внимание клиническое течение заболевания, оно может быть доброкачественным или злокачественным.
Также патологические процессы такого типа классифицируют по степени тяжести:
- первая – метастазы отсутствуют или находятся только в пределах матки;
- вторая – метастазы присутствуют только в области влагалища или малого таза;
- третья – метастазирование происходит в легкие;
- четвертая – метастазирование происходит по всему организму.

Наиболее благоприятные прогнозы, если так можно говорить в данном случае, имеет 1-2 степень тяжести течения патологического процесса.
Трофобластическая болезнь
Клиническая картина этой группы заболеваний может проявляться как во время беременности, так и спустя 3-12 месяцев после родоразрешения. При этом следует отметить, что клиническая картина доброкачественной и злокачественной опухоли практически не различается.
Трофобластическая болезнь не имеет специфической клинической картины и может характеризоваться следующим образом:
- уровень ХГЧ существенно превышает норму, которая оптимальна для того или иного срока беременности;
- кровянистые выделения с пузырьками вне менструального цикла;
- тошнота, которая часто сопровождается рвотой;
- слабость, недомогание;
- отечность рук и ног, что будет наиболее ярко выражено в утреннее время;
- повышенное артериальное давление;
- тест на беременность может быть положительный, но никаких других достоверных признаков нет;
- судороги, парезы;
- боли тянущего, ноющего характера внизу живота;
- субфебрильная, повышенная температура тела;
- боль и дискомфорт во время мочеиспускания;
- симптоматика интоксикации организма;
- если есть хронические заболевания, то возможен рецидив.

Подобная клиническая картина, если не принимать во внимание результаты лабораторных анализов, может присутствовать и при других гинекологических заболеваниях, поэтому нужно немедленно обращаться за медицинской помощью.
Ввиду того что трофобластическая болезнь не имеет специфической клинической картины, диагностика должна проводиться максимально тщательно.
В первую очередь врач проводит физикальный осмотр, в ходе которого:
- выясняет характер текущей клинической картины;
- собирает личный и семейный анамнез;
- изучает историю болезни пациентки.
На основе полученной информации составляется диагностическая программа, которая может основываться на следующем:
- общий клинический и развернутый биохимический анализ крови;
- общий анализ мочи;
- тест на маркер трофобластической болезни;
- УЗИ мочеполовой системы;
- УЗИ органов брюшной полости;
- КТ, МРТ внутренних органов;
- ПЭТ головного мозга;
- рентгенография с контрастным веществом;
- биопсия новообразования для гистологического и цитологического исследования.

ПЭТ головного мозга
По результатам диагностики будет определено дальнейшее лечение.
Тактика терапии будет зависеть от того, какой именно тип патологического процесса имеет место. Как правило, используются радикальные методы лечения с последующей медикаментозной и химиотерапией. В ряде случаев удается сохранить репродуктивную функцию.
При пузырчатом заносе используют следующие методы:
- вакуумная эвакуация с последующим гистологическим исследованием содержимого и выскабливанием матки;
- иммуноглобулиновая терапия.
При других формах такого заболевания лечение может подразумевать максимально радикальные меры:
- удаление матки;
- удаление влагалищных связок;
- удаление маточных фрагментов.
Дополнительно назначают курс химиотерапии и восстановительные процедуры, которые могут подразумевать под собой медикаментозное лечение и физиотерапевтические методики.
Вне зависимости от того, какая тактика лечения будет иметь место, женщинам необходимо соблюдать следующие общие рекомендации:
- в течение 1,5 лет после проведения операции или курса химиотерапии нужно использовать контрацепцию;
- следует исключить курение и чрезмерное количество спиртных напитков;
- соблюдение диеты;
- исключение стрессов, нервного перенапряжения;
- тщательная профилактика инфекционных заболеваний мочеполовой системы.
Прогноз при таких заболеваниях довольно сложно назвать положительным. Трофобластическая болезнь лечение подразумевает сложное и комплексное, поэтому пациентке нужно быть готовой к этому как с физической, так и с моральной точки зрения.
Если образование было доброкачественным, то осложнений, которые бы представляли угрозу для жизни, можно избежать.
Во всех остальных случаях могут возникнуть следующие негативные факторы:
Риск рецидива болезни присутствует.
Специфических методов профилактики трофобластическая болезнь не имеет.
В данном случае снизить риск ее развития можно, придерживаясь общих правил:
- исключение абортов;
- использование только правильно подобранной контрацепции;
- профилактика гинекологических заболеваний;
- профилактические осмотры у гинеколога;
- планирование беременности.
Лицам, которые входят в группу риска, нужно проходить полное медицинское обследование не реже одного раза в год.
Поделиться статьей:
Все ли корректно в статье с медицинской точки зрения?
Ответьте только в том случае, если у вас есть подтвержденные медицинские знанияТрофобластическая болезнь — Симптомы и лечение. Журнал Медикал
Трофобластическая болезнь включает в себя родственные опухоли, развивающиеся из плацентарной ткани. К ней относятся: пузырный занос (частичный или полный), деструирующий пузырный занос, хориокарцинома и трофобластическая опухоль плацентарной площадки.
К ней относятся: пузырный занос (частичный или полный), деструирующий пузырный занос, хориокарцинома и трофобластическая опухоль плацентарной площадки.
Пузырный занос
Пузырный занос представляет собой измененный ворсинчатый слой хориона (изменения в виде пузырьков), который полностью (полный занос) или частично (частичный занос) вытесняет нормальную ткань плаценты. Распространенность пузырного заноса – полный 0,5 на 1000, частичный – 1,4 на 1000 беременностей.
Полный пузырный занос – возникает при оплодотворении поврежденной яйцеклетки, без хромосом. В результате происходит удвоение только отцовских хромосом, зигота является нежизнеспособной, эмбрион не образуется, происходит только рост ворсин. Кариотип при этом 46 XX, реже XY. Наиболее частой и доказанной причиной неполного пузырного заноса является оплодотворение яйцеклетки двумя сперматозоидами. В этом случае клетки содержат дополнительные хромосомы, что приводит к тому, что эмбрион не развивается. При этом наблюдается триплоидия – клетки несут 69 хромосом. У плода имеются признаки триплоидии: многочисленные пороки развития. Однако, следует отметить, что при неполном пузырном заносе все же возможно развитие жизнеспособного плода.
У плода имеются признаки триплоидии: многочисленные пороки развития. Однако, следует отметить, что при неполном пузырном заносе все же возможно развитие жизнеспособного плода.
Клиническая картина при пузырном заносе характеризуется:
• кровянистыми выделениями из половых путей (в 97% случаев) в первом триместре беременности в результате отслойки пузырного заноса от децидуальной оболочки;
• увеличением матки, не соответствующее сроку беременности – возможная причина скопление крови и патологический рост хориона;
• преэклампсия – у 27% беременных, при этом эклампсия развивается редко, характеризуется появлением белка в моче, повышением артериального давления, гиперрефлексией;
• токсикоз, неукротимая рвота беременных — возможны тяжелые электролитные нарушения;
• тиреотоксикоз
• эмболия ветвей легочной артерии
• кисты яичников
К основным методам диагностики относят:
• УЗИ – основной метод диагностики пузырного заноса
• Анализ крови на ХГЧ – выявление β-субъединицы ХГЧ более 100 000 МЕ/л и выше, в сочетании с другими факторами, может достоверно свидетельствовать об пузырном заносе
• Матка, на много больше предпалагаемого срока, в купе с кровянистыми выделениями в первом триместре – характерный симптом.
Лечение – сразу после постановки диагноза необходимо купирование тяжелых осложнений пузырного заноса. После стабилизации состояния занос необходимо эвакуировать. Наиболее щадящий метод при этом – вакуум-аспирация матки. Для больных, которые не планируют иметь детей – экстирпация матки.
После эвакуации пузырного заноса необходимо измерять уровень β-субъединицы ХГ, который должен прогрессивно уменьшаться и нормализоваться к 9 неделям после эвакуации. Беременность разрешается после завершения наблюдения.
Прогноз, как правило, благоприятный, однако у примерно 15% больных исходом является трофобластические опухоли, из них 4% метастазирующие. Особенно это важно для больных старшей возрастной группы (старше 40 лет – 37%). По последним данным применение адъювантной (направленной) химиотерапии снижает риск исхода в трофобластическую опухоль.
Трофобластические опухоли
Хорионкарцинома (синоним — хорионэпителиома) — злокачественная форма трофобластической болезни, возникающая после пузырного заноса, аборта (25%) или после родов (20%).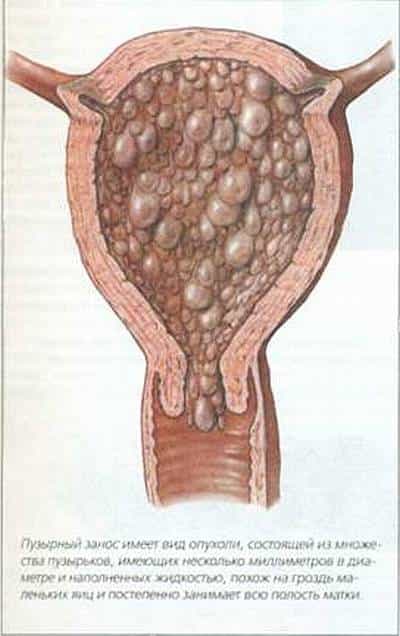 Встречается редко. Самое частое место расположения – полость матки, в месте имплантации плодного яйца.
Встречается редко. Самое частое место расположения – полость матки, в месте имплантации плодного яйца.
Редко встречается хорионкарцинома во время беременности. Хорионкарцинома при беременности зарактеризуется высокой степенью злокачественности, приводя к метастатическим поражениям в отдаленных органазх. Симптоматики долгое время может не быть. Прогноз как правило неблагоприятный.
Наиболее частой симптоматикой являются:
• Кровотечение из половых путей, которые могут не прекращаться после выскабливания, требуют повторной процедуры – необходимость повторных выскабливаний — характерный показатель.
• Гнойные и серозные выделения из половых путей – связаны с нагноением опухолевых узлов, что происходит не так уж и редко.
• Боли – характерны при прорастании органа.
Для диагностики хорионкарциномы основным методом остаестя УЗИ. Кроме него, также могут быть использованы: биохимическое исследование крови (можно определять плацентарный лактоген, эстриол, хорионический тиреотропина и т. д.), гистероскопия, МРТ, КТ и т.д., по усмотрению специалиста.
д.), гистероскопия, МРТ, КТ и т.д., по усмотрению специалиста.
Трофобластическая опухоль плацентарной площадки – редкая опухоль. Характеризуется инвазивным ростом (в стенку органа), метастазирование редко. Как правило химиотерапия при этом мало эффективна.
Стадии трофобластических опухолей (упрощенная схема):
Стадия I – опухоль ограничена маткой
Стадия II – поражения придатков матки, влагалища, параметрия
Стадия III – Метастазы в легкие (независимо от поражения половых органов)
Стадия IV – Отдаленные метастазы, кроме метастазов в легкие
На момент постановки диагноза у 80% пациенток имеются метастазы в легкие. Выявление на рентгенографии грудной клетки. Метастазы в печень наблюдаются в 10% случаев диссеминированных трофобластических опухолей.
Лечение трофобластических опухолей в основном зависит от стадии заболевания, от состояния больной и ее желания в дальнейшем иметь детей. В общих чертах лечение ведется по следующим схемам:
Стадия I – монохимиотерапия; экстирпация матки и адъювантная химиотерапия; полихимиотерапия при развитии резистентности
Стадия II – Ш – монохимиотерапия; полихимиотерапия; полихимиотерапия 2-й линии
Стадия IV – полихимиотерапия, лучевая терапия в суммарной дозе 30 Гр, хирургическое лечение осложнений; регионарная химиотерапия при метастазах в печень
Врач гинеколог Купатадзе Д. Д.
Д.
Трофобластическая опухоль в области плаценты | Гестационная трофобластическая болезнь (ГТД)
,00Трофобластические опухоли плацентарной зоны (ТППТ) возникают после беременности. Они чрезвычайно редки, медленно растут и обычно излечимы.
Что такое трофобластическая опухоль плацентарной локализации
Трофобластическая опухоль плацентарной локализации встречается очень редко. Ежегодно в Великобритании диагноз ТЗПТ диагностируется менее чем у 5 женщин.
Они являются частью группы состояний, называемых гестационной трофобластической болезнью (сокращенно GTD).Менее 1 из 100 (1%) GTD являются трофобластическими опухолями в области плаценты.
Важно понимать, что PSTT — это не то же самое, что рак матки. При раке матки рак развивается из клеток слизистой оболочки матки (эндометрия). При PSTT опухоль развивается из клеток, которые растут и образуют плаценту. Эти клетки называются клетками трофобласта.
Трофобластические опухоли плацентарной зоны (ТППТ) возникают после беременности. Они могут произойти после любого типа беременности, включая молярную беременность, выкидыш, аборт или полную нормальную беременность.Они могут возникать через несколько месяцев или даже лет.
Они могут произойти после любого типа беременности, включая молярную беременность, выкидыш, аборт или полную нормальную беременность.Они могут возникать через несколько месяцев или даже лет.
Эти опухоли развиваются в области соединения плаценты со слизистой оболочкой матки (матки). Они могут прорасти в мышечный слой матки. Они медленно растут и обычно излечимы.
У некоторых женщин ТЗПТ может распространяться за пределы матки. Скорее всего, он распространится на легкие или на структуры тела, окружающие матку.
Симптомы PSTT
Основным симптомом PSTT является нерегулярное кровотечение из влагалища, которое у некоторых женщин следует за потерей менструации (аменорея).
Диагностика PSTT
Если у вас вагинальное кровотечение или у вас прекратились месячные, ваш врач направит вас на анализы. У вас могут быть следующие тесты.
Диагностика PSTT
Если у вас вагинальное кровотечение или менструальный цикл прекратился, врач направит вас на анализы. У вас могут быть следующие тесты.
У вас могут быть следующие тесты.
У женщин с ТГПТ обычно повышен уровень гормона, называемого хорионическим гонадотропином человека (ХГЧ), в крови. Этот гормон вырабатывается клетками PSTT.
Ультразвуковое сканирование может показать аномальные участки слизистой оболочки матки. Особый тип сканирования, называемый ультразвуковым допплером, использует цвет для выявления структур тела. Допплеровское сканирование может показать, что в области опухоли больше кровеносных сосудов, чем обычно.
Вам в больнице делают операцию под общим наркозом. Когда вы засыпаете, хирург открывает (расширяет) вход в матку (шейку матки) и берет образцы любых аномальных участков. Врач использует небольшой инструмент, называемый кюреткой, для соскабливания слизистой оболочки матки.Они отправляют удаленную ткань в лабораторию. Под микроскопом патологоанатом может сказать, что клетки являются PSTT.
Лечение трофобластической опухоли в области плаценты
Если опухоль находится только в утробе матери, основным лечением является хирургическое вмешательство. У большинства женщин удаление матки (гистерэктомия). Если ваш врач может удалить всю опухоль таким образом, это должно вылечить состояние.
У большинства женщин удаление матки (гистерэктомия). Если ваш врач может удалить всю опухоль таким образом, это должно вылечить состояние.
У молодых женщин, которые хотят иметь больше детей, иногда возможно удалить хирургическим путем только ткань опухоли.Но ткань опухоли может вернуться. Таким женщинам необходимо регулярно сдавать анализы крови, чтобы проверять уровни гормонов, hPL и hCG.
Если уровень гормонов начнет повышаться или у женщины появятся другие симптомы рецидива опухоли, ей потребуется гистерэктомия.
Если PSTT распространился на другую часть вашего тела, например, область вокруг матки или легкие, вам понадобится химиотерапия после операции. Лечение обычно включает комбинацию химиотерапевтических препаратов.Используемые препараты могут включать:
- этопозид
- цисплатин
- метотрексат
- актиномицин D
- циклофосфамид
- винкристин
Лечение проводят до тех пор, пока уровень ХГЧ не станет нормальным, а затем в течение следующих 8 недель.
Последующее наблюдение после лечения
После лечения ваш специалист будет внимательно следить за вами. Вам может потребоваться ультразвуковое сканирование, сканирование МРТ, компьютерная томография и анализы мочи, чтобы проверить, насколько хорошо лечение работает, и отслеживать свой прогресс.
определение трофобластической опухоли и синонимов трофобластической опухоли (английский)
трофобластическая опухоль: определение трофобластической опухоли и синонимы трофобластической опухоли (английский)арабский болгарский китайский язык хорватский Чешский Датский Голландский английский эстонский Финский французкий язык Немецкий Греческий иврит хинди Венгерский исландский индонезийский Итальянский Японский корейский язык Латышский Литовский язык Малагасийский норвежский язык Персидский Польский португальский румынский русский сербский словацкий словенский испанский Шведский Тайский турецкий вьетнамский
арабский болгарский китайский язык хорватский Чешский Датский Голландский английский эстонский Финский французкий язык Немецкий Греческий иврит хинди Венгерский исландский индонезийский Итальянский Японский корейский язык Латышский Литовский язык Малагасийский норвежский язык Персидский Польский португальский румынский русский сербский словацкий словенский испанский Шведский Тайский турецкий вьетнамский
сообщить о проблеме
Трофобластическая опухоль (n.)
1. (MeSH) Трофобластический рост, который может быть гестационным или негестационным по происхождению. Трофобластная неоплазия, возникшая в результате беременности, часто описывается как гестационная трофобластическая болезнь, чтобы отличить ее от опухолей половых клеток, которые часто имеют трофобластические элементы, и от трофобластической дифференцировки, которая иногда встречается при большом разнообразии эпителиального рака. Рост гестационного трофобласта имеет несколько форм, в том числе ГИДАТИДИФОРМУ и ХОРИОКАРЦИНОМУ. (Из Голландии и др., Медицина рака, 3-е изд., Стр. 1691)
сообщить о проблеме
аналоговый словарь
Осложнения, Неопластическая беременность, Неопластические осложнения беременности, Беременность, Неопластические осложнения, Осложнения беременности, Неопластические — рак, Эмбриональные, Рак, Эмбриональные и смешанные, Эмбриональные новообразования, Зародышевые клетки и эмбриональные новообразования, Зародышевые клетки и зародышевые новообразования, Зародышевые клетки Клеточные новообразования, опухоли зародышевых клеток, новообразования, эмбриональные, новообразования, эмбриональные и смешанные, новообразования, зародышевые клетки, новообразования, половые клетки и эмбрионы, новообразования, зародышевые клетки и эмбриональные [Hyper.]
Трофобластическая опухоль (n.) [MeSH] ↕
Википедия — см. Также
Все переводы трофобластической опухоли
содержание сенсагента
- определения
- синонимов
- антонимов
- энциклопедия
Решение для веб-мастеров
Александрия
Всплывающее окно с информацией (полное содержание Sensagent), вызываемое двойным щелчком по любому слову на вашей веб-странице.Предоставьте контекстные объяснения и перевод с вашего сайта !
Попробуйте здесь или получите код
SensagentBox
С помощью SensagentBox посетители вашего сайта могут получить доступ к надежной информации на более чем 5 миллионах страниц, предоставленных Sensagent.com. Выберите дизайн, который подходит вашему сайту.
Бизнес-решение
Улучшите содержание своего сайта
Добавьте новый контент на свой сайт из Sensagent by XML.
Сканирование продуктов или добавление
Получите доступ к XML для поиска лучших продуктов.
Индексирование изображений и определение метаданных
Получите доступ к XML, чтобы исправить значение ваших метаданных.
Напишите нам, чтобы описать вашу идею.
Lettris
Lettris — любопытная игра-тетрис-клон, в которой все кубики имеют одинаковую квадратную форму, но разное содержание. На каждом квадрате есть буква. Чтобы квадраты исчезли и сэкономили место для других квадратов, вам нужно собрать английские слова (left, right, up, down) из падающих квадратов.
болт
Boggle дает вам 3 минуты, чтобы найти как можно больше слов (3 буквы и более) в сетке из 16 букв. Вы также можете попробовать сетку из 16 букв. Буквы должны располагаться рядом, и более длинные слова оцениваются лучше. Посмотрите, сможете ли вы попасть в Зал славы сетки!
Английский словарь
Основные ссылки
WordNet предоставляет большинство определений на английском языке. Английский тезаурус
в основном является производным от The Integral Dictionary (TID).
- Новости
- Здоровье
- Семья и дети
- Питание и диета
- Красота и мода
- Отношения
- Спорт
- О портале
Здоровье
- Диагностика
- КТ
- МРТ диагностика
- Медицинские манипуляции
- Осмотр тела
- Эндоскопия (эндоскопия)
- Радионуклидная диагностика
- Рентген (рентгеновские исследования)
- Ультразвуковая диагностика (УЗИ)
- лечение
- Операции
- Медицинские специальности
- Лечение болезней
- Обзор лекарственных средств
- Альтернативная медицина
- Стволовые клетки
- Физиотерапия
- Переливание крови
- Трансплантация
- Болезни
- Беременность, роды и послеродовой период
Что такое трофобласт? (с рисунками)
Трофобласт — это слой клеток, составляющий внешнюю оболочку бластоцисты, клеточный кластер, который в конечном итоге разовьется в эмбрион.Трофобласт играет важную роль в имплантации и развитии эмбриона, и содержащиеся в нем клетки одними из первых начинают дифференцироваться, когда оплодотворенная яйцеклетка начинает делиться с образованием эмбриона. В конечном итоге эти клетки развиваются в плаценту, интерфейс между плодом и матерью, предназначенный для обеспечения прохода питательных веществ и продуктов жизнедеятельности.
Наружная оболочка бластоцисты известна как трофобласт.В течение четырех-шести дней после оплодотворения начинает формироваться трофобласт. Эти клетки располагаются вдоль внешней стороны развивающейся бластоцисты и начинают секретировать гормоны, предназначенные для подготовки эндометрия, слизистой оболочки матки, к имплантации. Вначале бластоциста перемещается в матку, пока трофобласт не соединится со слизистой оболочкой матки и имплантатами. Трофобласт может начать делиться и дифференцироваться, чтобы создать плаценту.
Трофобласт — это слой клеток, составляющий внешнюю оболочку бластоцисты, клеточный кластер, который в конечном итоге разовьется в эмбрион.На ранних стадиях эмбрионального развития могут возникнуть некоторые проблемы.Клетки могут не делиться, что останавливает развитие, или могут произойти фатальные ошибки деления. Иногда бластоциста не может имплантироваться, и она перестает развиваться из-за отсутствия доступа к питательным веществам. После имплантации воздействие окружающей среды и множество других факторов могут помешать успешному развитию.
Клетки трофобласта выделяют гормоны, чтобы подготовить эндометрий к имплантации.После родов плацента отделяется, и ее можно выбросить. Важно полностью удалить плаценту из матки, чтобы снизить риск инфицирования и других осложнений, связанных с задержкой плацентарного материала. Также существуют опасения по поводу маточного кровотечения и других осложнений после родов, требующих повторного посещения врача для выявления признаков осложнений.
Изучение клеток, участвующих в эмбриональном развитии, может быть применено к проблемам бесплодия.Трофобластические клетки могут стать злокачественными. Иногда эмбрион не может развиваться, и трофобластические клетки продолжают делиться при молярной беременности, и если трофобластические клетки остаются после родов, они могут развиться в трофобластическую опухоль.Эти аномалии развития клеток, известные как гестационная трофобластическая болезнь, иногда являются доброкачественными, а иногда нет. Биопсия клеток необходима, чтобы узнать больше о происхождении роста и уровне их злокачественности.
После рождения ребенка из матки необходимо полностью удалить плаценту.Подобно другим клеткам, участвующим в эмбриональном развитии, трофобластические клетки представляют интерес для исследователей. Ученые заинтересованы в изучении того, как клетки передают сигнал между собой в процессе развития плода, а также изучают, что идет не так с эмбриональным развитием. Это исследование можно применить к бесплодию и множеству других медицинских проблем.
Для определения наличия рака необходима биопсия трофобластической опухоли.опухолей тела матки и гестационной трофобластической болезни Стивена Г. Сильверберга
- Домой
- Мои книги
- Обзор ▾
- Рекомендации
- Choice Awards
- Жанры
- Подарки
- Новые выпуски
- Списки
- Изучить
- Новости и интервью
- Новости и интервью
- Жанры 9000 Искусство
- Бизнес
- Детский
- Христиан
- Классика
- Комиксы
- Поваренные книги
- Электронные книги
- Фэнтези
- Художественная литература
- Графические романы
- Историческая фантастика
- История
- 13313
- Тайна
- Документальная литература
- Поэзия
- Психология
- Романтика
- Наука
- Научная фантастика
- Самопомощь
- Спорт
- Триллер
- Путешествия
- Молодые люди
- Больше 059
- Сообщество ▾
- Группы
- Обсуждения
- Цитаты
- Задать вопрос автору
- Войти
- Присоединиться
- Просмотреть профиль 90
- Друзья
- Группы
- Обсуждения
- Комментарии
- Задание по чтению
- Kindle Заметки и основные моменты
- Цитаты
- Любимые жанры
- Рекомендации друзей
- Настройки учетной записи
- Помощь
- Выйти
- Мои книги
- Обзор ▾
- Рекомендации
- Награды Choice
- Жанры
- Подарки
- Новые выпуски
- Списки
- Изучите
- Новости и интервью
Жанры
- Бизнес Биография 48
- Детская
- Христианская
- Классика
- Комиксы
- Поваренные книги
- Электронные книги
- Фэнтези
- Художественная литература
- Графические романы
- Историческая фантастика



 Концентрируется в области плацентарной площадки. Отдаленные метастазы дает на поздних этапах.
Концентрируется в области плацентарной площадки. Отдаленные метастазы дает на поздних этапах.
 RU — Инвазивная трофобластическая неоплазия — клинический случай 3D сонографии
RU — Инвазивная трофобластическая неоплазия — клинический случай 3D сонографии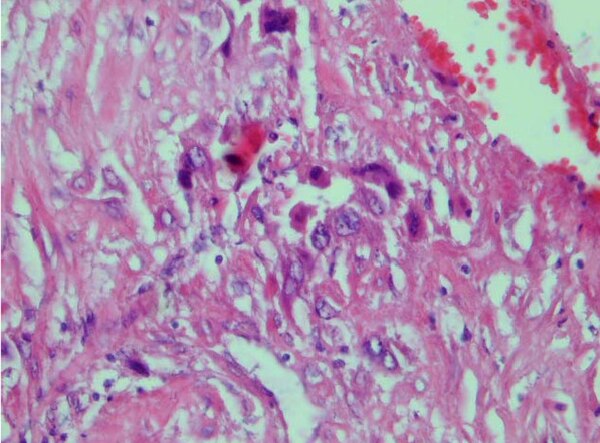


Leave a Comment