Киста почки — WMT клиника высоких технологий
Киста почки – новообразование, которое развивается из паренхимы почки и имеет полость, чаще всего заполненную жидкостью. Обычно кисты являются доброкачественными, располагаются одиночно и обнаруживаются случайно при обследовании по другому поводу.
КЛАССИФИКАЦИЯ КИСТЫ ПОЧКИ ПО BOSNIAK
Несмотря на то, что кисты в большинстве случаев имеют доброкачественный характер, встречаются и те, которые требуют повышенного внимания. С этой целью используется классификация по Bosniak:
I категория
Простые доброкачественные кисты почек, которые четко визуализируются ультразвуком, КТ или МРТ. Они часто встречаются и никак не проявляют себя, а также не требуют никакого лечения кроме наблюдения.
II категория
Доброкачественные кисты с минимальными изменениями. Отличаются от кист первой категории появлением перегородок, отложением кальция в стенках или перегородках. Данная категория кист практически не становится злокачественной и нуждается в динамическом УЗ- наблюдении.
IIF категория
Доброкачественные кисты, которые содержат большее количество тонких перегородок. Стенки и перегородки могут быть утолщены, часто содержат отложения кальция в виде узелков. Практически никогда не накапливают контраст, так как не содержат тканевого компонента. Размеры этих кист могут быть больше или равны 3 см и нуждаются в динамическом наблюдении. Как правило, не требуют оперативного лечения.
III категория
Группа более неопределенная и имеет тенденцию к малигнизации (приобретает злокачественные качества). Радиологические особенности включают нечеткий контур, утолщенные перегородки и неоднородные участки отложения кальция. При отсутствии травм почки или инфекционных заболеваний, как правило, требуют оперативного лечения.
IV категория
Образования имеют большой жидкостный компонент, неровный и даже бугристый контур и, что особенно важно, местами накапливают контрастное вещество за счет тканевого компонента.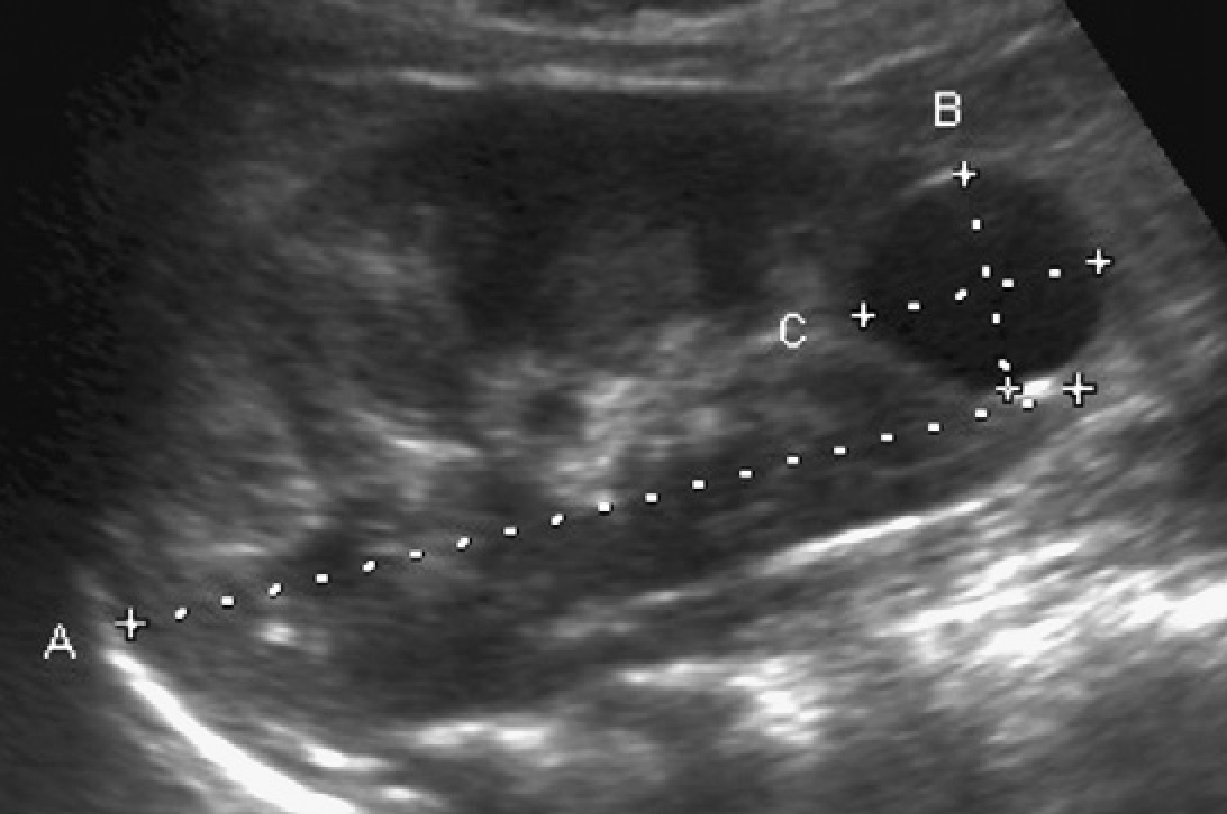
КАК ПРОЯВЛЯЮТСЯ КИСТЫ ПОЧЕК?
Чаще всего пациенты отмечают боли в пояснице, особенно при долгой ходьбе или тяжелой физической нагрузке, на примесь крови в моче. Поскольку почка участвует в регуляции артериального давления, при некоторых кистах отмечают стойкое высокое артериальное давление без видимых причин, не поддающееся лечению лекарственной терапией. При кистах больших размеров пациенты отмечают сильные боли даже в покое, а также могут прощупывать непонятное образование в животе. В редких случаях могут развиваться симптомы почечной недостаточности.
Здесь также стоит упомянуть о другом заболевании – поликистоз почек. Это врожденное наследственное заболевание, при котором появляются множественные кисты в паренхиме почки. Врожденный поликистоз прогрессирует медленно и проявляется аналогично классической кисте почки, однако возможность радикального лечения в этом случае сильно ограничена.
ДИАГНОСТИКА КИСТЫ ПОЧКИ
Для получения достоверного результата врачи проводят инструментальную диагностику: УЗИ, КТ с контрастированием или МРТ. Для диагностики функции почек выполняют радиоизотопное исследование – сцинтиграфию. Полное обследование обязательно для исключения опухоли почки, определения функций почки, исключения почечной недостаточности и определения показаний к операции.
ЛЕЧЕНИЕ КИСТЫ ПОЧКИ
В клинике WMT проводится тщательная оценка кисты на предмет ее сложности и дисфункции почки, вызванной кистозным новообразованием. При необходимости выполняется лапароскопическая резекция кисты почки – операция по удалению кисты через несколько проколов в области поясницы. Благодаря такой технике выполнения операции пациент может вернуться к привычной жизни уже через 2-3 дня.
Лечение кисты почки возможно только оперативным путем. При образованиях небольших размеров, которые не имеют признаков злокачественности, пациенты остаются под динамическим наблюдением.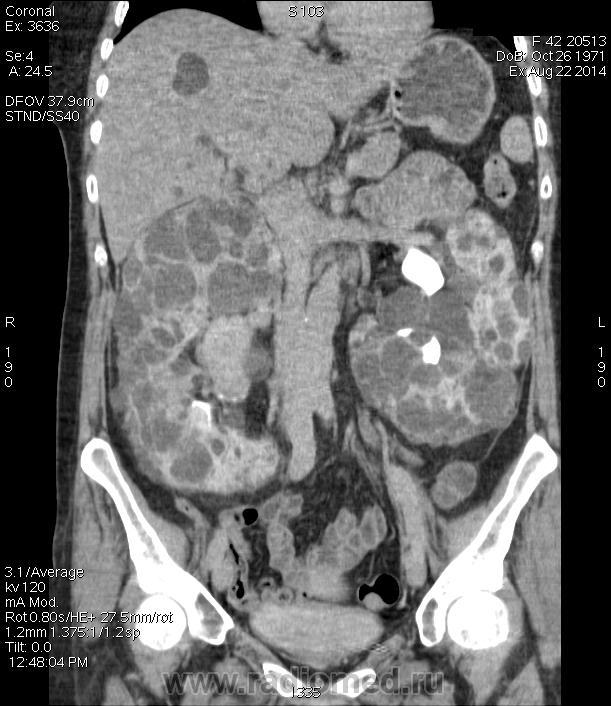
Операция показана пациентам при:
- Выраженных болевых синдромах при сдавлении кистой соседних органов
- Нарушениях мочеоттока, вызванных кистой
- Разрыве кисты или угрозе разрыва
- Наличии инфекционного очага в кисте
- Некупируемой артериальной гипертензии, а также при подозрении на злокачественный процесс
В некоторых случаях пациентам проводят введение специальных склерозантов в полость кисты с целью заполнения этой полости и снижения дальнейшего роста кисты. Однако этот метод не является радикальным, и у некоторых пациентов может возникнуть рецидив. В случае врожденного поликистоза оперативное лечение практически не показано. Таких пациентов ведут консервативно.
ЗАПИСЬ НА ПРИЁМ
Запишитесь на консультацию к урологу клиники WMT по телефону: 8 (861) 206-03-03 или оставьте заявку на сайте.
Поликистоз почек в Сочи — клиника УРО-ПРО — лечение урологических заболеваний
Поликистоз почек – наследственное заболевание, характеризующееся формированием многочисленных кист в полости почки. Даная аномалия встречается как у мужчин, так и у женщин по причине генетических нарушений, которые проявляются к 45-65 годам, когда ткани почки претерпевают многочисленные расширения, заполняющиеся жидкостью. При поликистозе почек нарушается функционирование почечных мембран.
Даная аномалия встречается как у мужчин, так и у женщин по причине генетических нарушений, которые проявляются к 45-65 годам, когда ткани почки претерпевают многочисленные расширения, заполняющиеся жидкостью. При поликистозе почек нарушается функционирование почечных мембран.
Поликистоз проявляется не только в области почек, кисты способны образовываться и в других органах:
- поджелудочной железе;
- яичниках;
- щитовидной железе;
- семенных пузырьках.
Данное заболевания может проявляться по-разному.
Возникают болевые ощущения в области поясницы и в боку в связи с растяжением ткани почки множественными образованиями. Кровоизлияния и примесь крови в моче – факторы, возникающие из-за кровотечения внутри кист, которые зачастую требуют оперативного вмешательства.
В связи с нарушением обмена веществ в тканях почки и затрудненным оттоком мочи могут формироваться камни. Движение камней провоцирует болевые ощущения в почках из-за чего может появляться кровь в моче.
Движение камней провоцирует болевые ощущения в почках из-за чего может появляться кровь в моче.
Появление гипертонии связано с тем, что ткани почки сдавливаются, а затем происходит химический синтез элементов, которые поддерживают и регулируют уровень артериального давления. Когда нарушается кровообращение определенных зон, происходит активный выброс элементов, поднимающих давление.
Инфекция в мочевыводящем канале появляется в связи с нарушением оттока мочи. Бактерии поднимаются по мочевыводящим путям и наносят удар по чашечно-лоханочной системе почки и по самой кисте.
Осложнение поликистоза почек, приводящее к летальному исходу, — это почечная недостаточность. В крови и тканях собираются азотистые вещества, отравляющие организм.
Диагностика
Для точного диагноза учитываются не только жалобы больного, но и наличие аналогичных заболеваний у ближайших родственников.
В клинике «УРО-ПРО» для диагностики поликистоза проводятся такие исследования как:
- УЗИ;
- внутривенная урография;
- КТ.

Лечение
В случае если заболевание вызвано генетическими изменениями, то остановить данный процесс невозможно. Зачастую терапия направлена на лечение осложнений заболевания. Так к примеру большие кисты, которые причиняют сильную боль лечатся путем хирургического вмешательства из них удаляется все содержимое. Если в почке происходит сильное нагноение, то ее следует удалить, но подобное вмешательство проводится только с условием, что вторая почка функционирует нормально. При инфицировании мочевыводящих путей проводится антибактериальная терапия. При гипертонии пациенту назначаются препараты, нормализующие давление. В случае диагностирования у пациента почечной недостаточности ему назначается очищение крови от продуктов обмена.
Поликистоз почек требует безотлагательного обращение к врачу-урологу. Специалисты клиники «УРО-ПРО» проведут все необходимые диагностические обследования, и назначат необходимое лечение.
УЗИ почек по доступной цене в Москве
УЗИ почек может проводиться самостоятельно или входить в ультразвуковое обследование органов брюшной полости.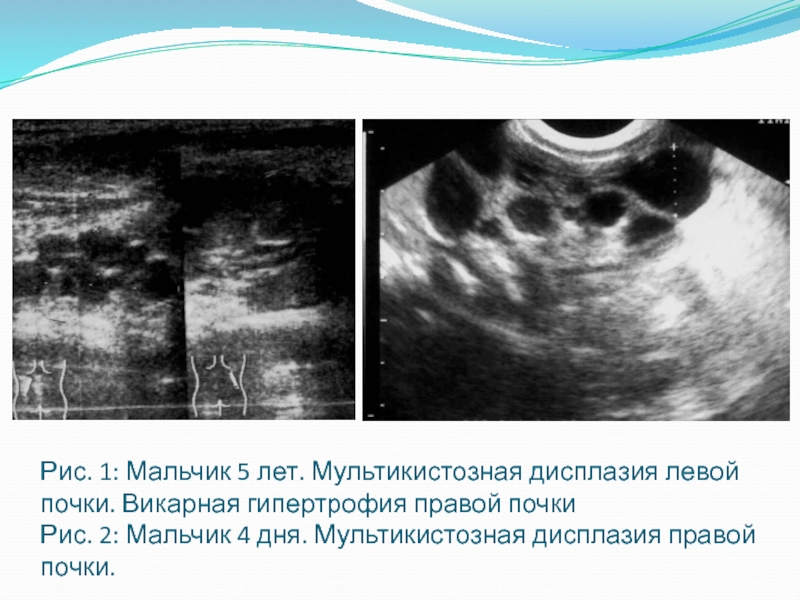
Ультразвук является одним из самых эффективных диагностических методов, включающих визуализацию органов с помощью ультразвуковых волн. Преимуществами диагностики являются:
- неинвазивность
- простота проведения
- безопасность и возможность повторения через короткие промежутки времени
- доступная цена
Особенности обследования
В нефрологии и урологии изучают мочевые пути, то есть почки, мочевой пузырь, а у мужчин также простату. УЗИ почек позволяет определить их размеры, форму, расположение и структуру и оценить правильность работы системы, а также наличие камней в почках, кист или опухолей.
Наиболее распространенные заболевания почек и мочевыводящих путей, при которых используется ультразвук:
- гломерулонефрит
- тубулоинтерстициальный нефрит
- поликистоз почек
- гидронефроз
- почечная тромбоэмболия
- заболевание простаты или мочевого пузыря
Подготовка к диагностике
-
За восемь часов до УЗИ почек воздерживайтесь от приема пищи или принимайте 6-8 таблеток активированного угля.
 Это поможет удалить газы из брюшной полости, которые являются акустическим барьером при использовании ультразвука.
Это поможет удалить газы из брюшной полости, которые являются акустическим барьером при использовании ультразвука. - Делайте УЗИ почек натощак.
- Не пейте газированные напитки в день теста.
- Воздержитесь от курения в день обследования.
Показания к обследованию
- патологический анализ мочи
- боли в пояснице
- колики, отдающие в пах
- гематурия
- нарушение функции почек
- гипертония
Что показывает ультразвуковой тест
Диагностика позволяет оценить расположение, форму почек, размер, толщину коры и ядра, а также эхогенность парного органа, которая может быть показательной при диагностике почечных паренхиматозных заболеваний. Нормальный размер почек составляет 9-13 см (продольный размер) и толщина коры 15-25 мм. В случае диагностики мочекаменной болезни в почечной лоханке визуализируются камни.
В случае диагностики мочекаменной болезни в почечной лоханке визуализируются камни.
Сделать УЗИ почек в Москве
Пройти качественную платную диагностику почек вы можете, записавшись на удобное время в ЦКБ РАН. Запись ведется в телефонном формате, а также с помощью онлайн формы. Убедитесь в том, что наше предложение является лучшим в столице – цены на ультразвуковые и другие аппаратные обследования представлены на сайте.
Поликистоз почек — симптомы и лечение у взрослых. МЦ «Здоровье» в Москве ЮАО (Варшавская и Аннино), ЦАО (Краснопресненская и Рижская).
Поликистоз почек — генетическая патология, при которой образуются множественные кисты. Выделяют две формы заболевания: аутосомно-доминантный и рецессивный. В первом случае все дети человека могут заболеть поликистозом, во втором 50–100% детей, но патология будет характеризоваться более тяжёлым течением.Мы подходим комплексно к диагностике и лечению поликистоза почек, чтобы вернуть пациентам комфорт здоровой жизни. Лечение включает подбор медикаментов, составление диеты и назначение физиотерапии при необходимости.
Причины развития поликистоза почек
Поликистоз — это наследуемое заболевание, возникающее из-за генетических особенностей. Даже если поликистоз есть только у одного из двух родителей, очень высока вероятность, что им будут страдать все их дети. Признаки поликистоза могут проявиться в раннем детстве, других заболевание настигает в среднем возрасте. Чем опасен поликистоз почек? Заболевание незаметно поглощает ткани почек, лишая их возможности нормально функционировать, что приводит к хронической почечной недостаточности. Стоит отметить, что поврежденные ткани почек легко поддаются заражению вторичной инфекцией.
Симптомы
Некоторое время болезнь развивается бессимптомно. После того, как почки будут значительно повреждены, появляются следующие симптомы:
- Имеющие тупой характер боли
- Больной теряет аппетит
- Общая слабость
- Снижение общей трудоспособности
- Постоянное ощущение «тяжёлой поясницы»
- Увеличение объёма мочи при мочеиспускании
- Постоянная жажда
- Кровь, выявляемая в моче
При пальпации определяются увеличенные в размерах почки. Если надлежащее лечение не производится, развивается хроническая почечная недостаточность. Почки перестают выполнять свою функцию, и к симптомокомплексу добавляются:
Если надлежащее лечение не производится, развивается хроническая почечная недостаточность. Почки перестают выполнять свою функцию, и к симптомокомплексу добавляются:
- Повышенное давление
- Кожный зуд
- Нарушение стула и тошнота
- Резкое снижение аппетита
- Нарушение сердечного ритма
- Повышенная температура
- Ознобы
Важно отметить, что патология более тяжело протекает у мужчин. Также к факторам, осложняющим течение заболевания, относят чрезмерное потребление кофе и курение.
Диагностика поликистоза почек
Диагностика поликистоза почек включает:
В отдельных случаях используют КТ, МРТ, контрастную урографию и другие методы, которые позволяют точно определить, какие части почек подверглись кистозным изменениям больше всего.
Лечение поликистоза почек
Что делать при поликистозе почек? Специальная диета, медикаменты, физиопроцедуры помогут вернуть вам качество жизни. Обратитесь в сеть МЦ «Здоровье», наши специалисты помогут вам в диагностике и лечении поликистоза почек.
Обратитесь в сеть МЦ «Здоровье», наши специалисты помогут вам в диагностике и лечении поликистоза почек.
НПЦ специализированной медицинской помощи детям им. Войно-Ясенецкого — НАУЧНО-ПРАКТИЧЕСКИЙ ЦЕНТР СПЕЦИАЛИЗИРОВАННОЙ МЕДИЦИНСКОЙ ПОМОЩИ ДЕТЯМ имени В.Ф.Войно-Ясенецкого
Впервые в России!
Отделение оториноларингологии спешит поделиться радостной новостью!
17 ноября 2021 года в нашем Центре в формате online + offline
будет проводиться однодневная научная конференция
«Эндоскопическая хирургия ЛОР — органов у детей».
Мероприятие пройдет при поддержке ведущих клинических и образовательных учреждений г. Москвы. В рамках конференции будут представлены доклады на различные темы ЛОР — патологии и эндоскопической ЛОР — хирургии у детей. В online-формате будет выполняться живая хирургия по эндоскопическому удалению ангиофибромы носоглотки у ребенка 12-ти лет и удалению новообразования гортани при помощи синего лазера Tru-Blue у ребенка 2-х лет.
В online-формате будет выполняться живая хирургия по эндоскопическому удалению ангиофибромы носоглотки у ребенка 12-ти лет и удалению новообразования гортани при помощи синего лазера Tru-Blue у ребенка 2-х лет.
Презентация инновационных технологий HIFU в НПЦ
HIFU-терапия расшифровывается как высокоинтенсивный сфокусированный ультразвук, или ещё её называют ультразвуковой абляцией.
Ультразвуковая абляция (HIFU) — самый современный в мире неинвазивный (дистанционный) метод локальной деструкции опухолей. Метод HIFU основан на генерации ультразвуковых лучей которые безвредно распространяются через здоровые ткани и фокусируются в заданной фокальной области для достижения лечебных целей. Энергия в фокальной области достаточно высока, чтобы вызвать немедленную термическую абляцию при температуре выше 56оС, что в свою очередь вызывает коагуляционный некроз. Лечение осуществляется без повреждения кожных покровов, окружающих здоровые ткани и органы.
О новой технологии в медицине рассказал заведующий отделением интервенционных методов диагностики и лечения из Самарского областного клинического диспансера, д.м.н., врач высшей категории, профессор Соловов Вячеслав Александрович. Он уже много лет занимается лечением пациентов, применяя данную методику, и как никто другой знает о ней всё.
Стоит отметить, что данная терапия используется уже в нескольких государственных учреждениях Москвы и, надеемся, что в будущем появится и в НПЦ.
Также во встрече приняли участие представители компании ООО»Интермедицина», которые занимаются снабжением частных и государственных медицинских учреждений диагностическим оборудованием.
Уважаемые родители наших пациентов!
У нас хорошая новость!
Открыта запись на амбулаторный приём к неврологам нашего Центра по субботам.
С 11 сентября мы рады предложить Вам консультации наших ведущих специалистов:
Лукьянова Екатерина Геннадьевна,
Сушко Лилия Марленовна,
Большакова Екатерина Сергеевна,
Фролова Анастасия Валентиновна.
Для записи и уточнения подробной информации просим Вас обращаться в кол-центр стационара по номеру: +7 (495) 638-36-45
День оториноларинголога
В оториноларингологическом отделении нашего Центра работают прекрасные специалисты, профессионалы своего дела, обеспечивающие оказание плановой хирургической и консервативной помощи детям с ЛОР-патологиями.
И сегодня, 29 сентября их профессиональный праздник – День оториноларинголога!
Мы с радостью спешим поздравить коллег с праздником и пожелать им крепкого здоровья, приятных рабочих будней и благодарных улыбок пациентов!
Спасибо за ваш труд!
СДЕЛАЙТЕ ПРИВИВКУ ОТ COVID-19!
УЧАСТВУЙТЕ В АКЦИИ!
22 апреля 2021 года в нашем Центре состоялась операция на печени по поводу
злокачественной опухоли у 3-х летней девочки, в ходе которой впервые была применена модульная станция нового поколения компании ERBE Elektromedizin VIO 3D, приобретенная для хирургов-онкологов НПЦ на деньги выделенного Департаментом здравоохранения г. Москвы гранта по онкологии в декабре 2020 г. Используемые в модульной станции инновационные технологии в области электро-, аргоноплазменной и водоструйной хирургии, позволяют выполнять операции на паренхиматозных органов у детей, больных злокачественными опухолями с минимальной кровопотерей, без интра- и послеоперационных осложнений. Более подробно об истории болезни ребёнка и ходе операции вы можете познакомиться на нашем сайте в разделе «Случаи из практики» в подразделе «опухоли печени».
Москвы гранта по онкологии в декабре 2020 г. Используемые в модульной станции инновационные технологии в области электро-, аргоноплазменной и водоструйной хирургии, позволяют выполнять операции на паренхиматозных органов у детей, больных злокачественными опухолями с минимальной кровопотерей, без интра- и послеоперационных осложнений. Более подробно об истории болезни ребёнка и ходе операции вы можете познакомиться на нашем сайте в разделе «Случаи из практики» в подразделе «опухоли печени».
http://npcmed.ru/images/2021/05/text7.pdf
Диагностика и лечение больных с поликистозом почек и инфицированными кистами
Трушкин Р.Н., Лубенников А.Е., Погодина К.С.
Поликистоз почек (ПП) или аутосомно-доминантная поликистозная болезнь — самое распространенное наследственное заболевание почек [1]. Основными осложнениями со стороны кист являются: инфицирование, кровоизлияние, реже наблюдается малигнизация [1-5]. По результатам одного моноцентрового исследования инфицирование кисты (ИК) оказалась относительно редким явлением и составило всего 0,01 пациент/эпизод/год..jpg) Предрасполагающими факторами были возраст, женский пол и предшествующие трансуретральные инструментальные пособия. Также отмечалось увеличение встречаемости их у пациентов, получающих программный диализ, в тоже время после пересадки почки такой закономерности не наблюдалось [2]. ИК представляет собой серьезную опасность для здоровья и жизни, особенно у больных терминальной стадией хронической почечной недостаточности (ТХПН), у которых риск развития сепсиса и летального исхода во много раз выше, в связи с чем, своевременная диагностика нагноения в кисте крайне актуальна [3]. Несмотря на кажущуюся простоту, постановка диагноза ИК представляет трудности, как для клиницистов, так и для врачей диагностических служб. Дифференциальная диагностика ИК проводится с кровоизлиянием и злокачественным новообразованием.
Предрасполагающими факторами были возраст, женский пол и предшествующие трансуретральные инструментальные пособия. Также отмечалось увеличение встречаемости их у пациентов, получающих программный диализ, в тоже время после пересадки почки такой закономерности не наблюдалось [2]. ИК представляет собой серьезную опасность для здоровья и жизни, особенно у больных терминальной стадией хронической почечной недостаточности (ТХПН), у которых риск развития сепсиса и летального исхода во много раз выше, в связи с чем, своевременная диагностика нагноения в кисте крайне актуальна [3]. Несмотря на кажущуюся простоту, постановка диагноза ИК представляет трудности, как для клиницистов, так и для врачей диагностических служб. Дифференциальная диагностика ИК проводится с кровоизлиянием и злокачественным новообразованием.
Достоверно можно говорить об ИК только после получения аспирата, содержащего лейкоциты и/или бактерии, во всех остальных случаях диагноз считается вероятным [4]. Лабораторное исследование аспирата является золотым стандартом диагностики, однако пункция кисты не всегда технически выполнима из-за больших размеров почек, трудности визуализации ИК и риска травмы органов брюшной полости [2-5].
КЛИНИЧЕСКАЯ КАРТИНА И ЛАБОРАТОРНЫЕ ДАННЫЕ
Вероятный диагноз ИК устанавливается при наличии: лихорадки, боли в проекции почек/почки, высокого уровня С-реактивного белка (СРБ), лейкоцитоза, положительных посевах мочи, крови [4,5]. M.A. Lantinga и соавт. проанализировали 70 работ, опубликованных с 1948 г. по 2014 г., в которых описано в общей сложности 119 случаев ИК. Авторы выявили, что медиана лихорадки была 390С, боль в проекции почек отмечали 59-88% больных, медиана СРБ составила 55-228 мг/л, медиана лейкоцитоза — 10,7-17,4х109, отрицательные посевы мочи отмечены у 46% больных, крови — у 61% пациентов, в 88% случаев посевы мочи соответствовали посеву содержимого из кисты [5]. Грамотрицательная флора — основная этиологическая причина, приводящая к нагноению в кисте, лидирующее положение занимает E. coli, выявляемая у трети пациентов, что позволяет заподозрить восходящий путь инфицирования кист [3,4,5,6].
УЛЬТРАЗВУКОВОЕ ИССЛЕДОВАНИЕ
На сегодняшний день, ультразвуковое исследование (УЗИ) нельзя рассматривать как скрининговый метод диагностики ИК.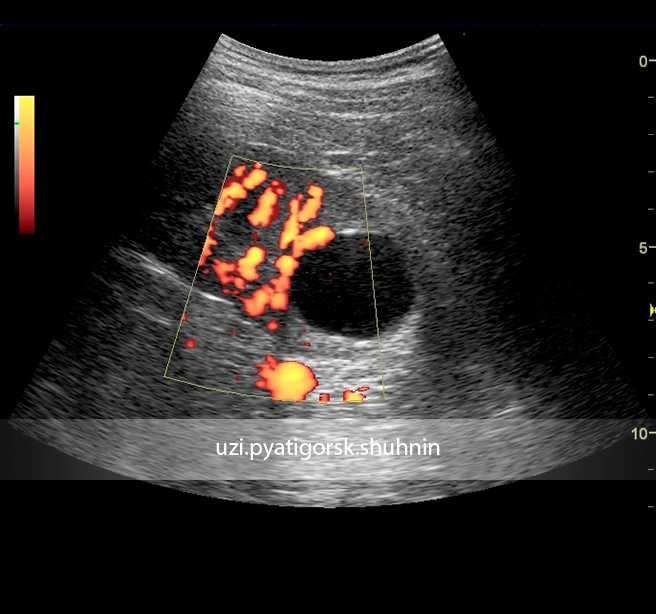 Во-первых, это связано с тем, что кровь и гной в полости кисты могут давать аналогичную эхо-картину, а во-вторых -большие размеры почек затрудняют визуализацию. Так в работе M. Sallee и соавт. данные УЗИ были положительны лишь у 6% больных с верифицированным диагнозом ИК [2].
Во-первых, это связано с тем, что кровь и гной в полости кисты могут давать аналогичную эхо-картину, а во-вторых -большие размеры почек затрудняют визуализацию. Так в работе M. Sallee и соавт. данные УЗИ были положительны лишь у 6% больных с верифицированным диагнозом ИК [2].
КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ
Компьютерная томография (КТ) обладает невысокой информативностью в диагностике ИК [2,5]. Заподозрить ИК можно по наличию утолщенной стенки, неоднородному гиперденсному содержимому внутри кисты (рис. 1 а). Однако содержимое высокой плотности в кисте
наблюдаться как при наличии гнойного субстрата, так и при кровоизлиянии [7,8]. Патогномоничным КТ-признаком ИК является динамическая оценка: увеличение размеров, изменение (повышение) денсито-метрической плотности, утолщение стенки в течение короткого времени [5]. Контрастирование значимо не увеличивает информативность КТ, так как повышение плотности стенки кисты может быть связано и с воспалительным процессом, и с оставшейся функциональной паренхимой и с наличием почечно-клеточного рака [9,10].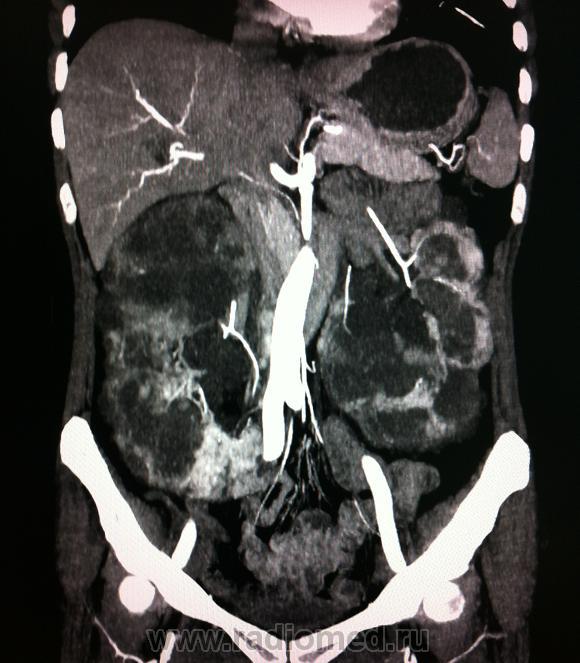 Так в ретроспективном 10-летнем исследовании M. Sallee и соавт. с помощью КТ диагноз был поставлен лишь у 18% больных с доказанной ИК [2], в работе F. Juret и соавт. — только у 15% [4].
Так в ретроспективном 10-летнем исследовании M. Sallee и соавт. с помощью КТ диагноз был поставлен лишь у 18% больных с доказанной ИК [2], в работе F. Juret и соавт. — только у 15% [4].
МАГНИТНО-РЕЗОНАНСНАЯ ТОМОГРАФИЯ
Магнитно-резонансная томография (МРТ) в режиме Т1, Т2 (рис. 1 в, г) более информативна по сравнению с КТ, но ложно-положительные результаты достигают 60% [2,4]. Предположить наличие ИК можно по усилению МР сигнала от стенки кисты после введения контрастного препарата [11,12]. Однако связь гадолиний-содержащего вещества с развитием нефрогенного системного фиброза ограничивает применение у больных с ХПН [5]. К другим недостаткам МРТ можно отнести длительную продолжительность исследования, влияние движений пациента на интерпретацию результатов, ограничение применение у больных с металлическими имплантантами и невозможность проведение исследования у пациентов с кардиостимулятором.
В последние годы все больше появляется публикаций, свидетельствующих о высокой информативности МРТ с использованием протоколов диффузионно-взвешенных изображений (ДВ-МРТ) (рис. 1б) [13-16]. ДВ-МРТ позволяет визуализировать и измерять случайное (броуновское) движение молекул воды. Интенсивность сигнала на диффузионно-взвешенном изображении (ДВИ) отражает диффузионную способность молекул воды исследуемого объекта [17]. Диффузия затруднена при повышении «клеточности» ткани — к примеру, при опухолях, фиброзе, абсцессах, цитотоксическом отеке [18-21], а также в структурах содержащих высокую концентрацию белка и продукты деградации гемоглобина [6]. Количественная оценка МР-диффузии достигается путем построения карт измеряемого коэффициента диффузии (ИКД) [22], однако в настоящее время достоверно не определены пороговые значения ИКД для ИК у пациентов с полики-стозом почек [5]. Тем не менее МР-диффузия является информативным дополнением к традиционным последовательностям, применяемым в МРТ. Ее использование позволяет в ряде случаев избежать введения дорогостоящих контрастных препаратов и не сопряжено с существенными временными или техническими затратами, повышая диагностическую эффективность метода [22].
Рис. 1. а — КТ без контрастирования: увеличение плотности кисты, утолщение стенок, б — МРТ – повышение интенсивности на ДВИ от этой кисты, в — Т1 взвешенное изображение, г — Т2 взвешенное изображение демонстрируют снижение MP-сигнала
ПОЗИТРОННО-ЭМИССИОННАЯ ТОМОГРАФИЯ, СОВМЕЩЕННАЯ С КТ
По мнению ряда авторов, наиболее чувствительным методом в диагностике ИК у пациентов в поликистозом почек в настоящее время считается позитронно-эмиссионная томография, совмещенная с КТ (ПЭТ-КТ), с 18-фтор-дезоксиглюкозой (18Б-ФДГ) (рис. 2), чувствительность которой составляет 77-90% [9,23-25].
Рис. 2. ПЭТ-КТ с 18F-ФДГ. Отмечается гиперфиксация 18ФДГ в кистах верхнего и нижнего сегментах левой почки, что говорит об их инфицировании, кроме этого видно накопление 18F-ФДГ в парааортальных лимфоузлах, некоторых кистах правой почки. Накопление 18F-ФДГ желудком — физиологическое состояние
Положительными моментами данного метода диагностики являются: отсутствие нефро- и гепато-токсичности, в том числе у пациентов с начальными формами ХПН, возможность пространственной визуализации, оценка динамики степени воспалительного процесса на фоне консервативного лечения, возможность идентификации воспалительного очага в брюшной полости экстраренальной локализации. Последний момент крайне актуален у больных с ПП и лихорадкой неясного генеза. F. Jouret и соавт. сообщают о том, что у 6 больных с поликистозом почек после
ПЭТ-КТ была изменена тактика лечения. Этим пациентам проводилось исследование в связи с подозрением на ИК, однако были выявлены: холангит, дивертикулит тонкого кишечника, дивертикулит восходящего отдала толстого кишечника, простатит, пиелонефрит трансплантированной почки, воспаление в стенки аневризмы брюшного отдела аорты [25]. В публикации G. Piccoli и соавт. отмечается, что у 4-х пациентов не подтверждена ИК, однако выявлено патологическое накопление радиофармпрепарата в перипанкреатических лимфатических узлах, что было связано с наличием мезенхимальных образований [9]. Недостатками метода является высокая стоимость, ограниченная доступность, трудности дифференцировки воспалительного процесса от злокачественного, а также недостаточно данных на сегодняшний день о вероятности ложноположительных результатов при кровоизлиянии в кисту [4,25].
ЛЕЧЕНИЕ
В подавляющем большинстве доступных публикаций отмечается, что фторхинолоны являются препаратами выбора в стартовой терапии, это связано с их липофильными свойствами и возможностью создавать высокие концентрации внутри кист [2,26,27]. К сожалению, консервативная терапия в подавляющем большинстве случаев обречена на провал. Так, в 2016 году M. Lintinga и соавт. приводят результаты анализа 60 публикаций, начиная с 1948 г., в которых описывается лечение 85 пациентов с ИК. Эффекта от антибактериальной терапии удалось добиться лишь у 25% [26].
При выявлении нагноившейся кисты показано ее дренирование, бактериологический анализ содержимого, проведение этиотропной антибактериальной терапии. В случае невозможности дренирования под УЗ наведением, целесообразно использовать КТ навигацию с учетом прежде полученных данных ДВ-МРТ. Эффективность такого подхода продемонстрирована в ряде публикаций [28,29].
Отсутствие эффекта от консервативного лечения, малоинвазивных вмешательств, является показанием к ревизии почки, в ряде случаев — к нефрэктомии [26,30].
Учитывая высокий риск сепсиса, летального исхода, побочных эффектов от антибактериальной терапии у больных, получающих программный диализ, при отсутствии возможности дренирования кисты, особенно при наличии множественных ИК, показано выполнение нефрэктомии [30].
ЗАКЛЮЧЕНИЕ
Лихорадка, боль в проекции почек/почки, высокий уровень лейкоцитоза, С-реактивного белка диктуют необходимость проведение диагностических мероприятий по выявлению инфицирования кисты у пациентов с поликистозом почек. Необходимо учитывать, что бактериологическое исследование крови и мочи почти у половины пациентов оказывается отрицательным. Учитывая низкую информативность УЗИ, КТ, первым этапом при отсутствии противопоказаний целесообразно проведение ДВ-МРТ, в случае технической доступности -ПЭТ-КТ.
При выявлении ИК показано ее дренирование под УЗ наведением, в сложных случаях целесообразно использовать КТ навигацию, ориентируясь на данные МРТ-DWI.
Вероятно,антибактериальную терапию необходимо рассматривать в качестве стартового лечения только у больных с ПП, сохраненной функцией почек, отсутствием явных признаков нагноения в кисте, без факторов осложненной мочевой инфекции.
У пациентов, получающих лечение диализом, выполнение нефрэктомии при наличии ИК необходимо рассматривать как основной вариант лечения.
ЛИТЕРАТУРА
1. Torres VE, Harris PC, Pirson Y. Autosomal dominant polycystic kidney disease. Lancet 2007;369(9569):1287-1301.
2. Sallee M, Rafat C, Zahar JR, Paulmier B, Grunfeld JP, Knebelmann B, et al. Cyst infections in patients with autosomal dominant polycystic kidney disease. Clin J Am Soc Nephrol 2009;4(7):1183-1189. doi: 10.2215/CJN.01870309.
3. Christophe JL, van Ypersele, de Strihou C, Pirson Y. Complications of autosomal dominant polycystic kidney disease in 50 haemodialysed patients. A case-control study. The U.C.L. Collaborative Group. Nephrol Dial Transplant 1996;11(7):1271-1276.
4. Jouret F, Lhommel R, Devuyst, Annet L, Pirson Y, Hassoun Z, et al. Diagnosis of cyst infection in patients with autosomal dominant polycystic kidney disease: attributes and limitations of the current modalities. Nephrol Dial Transplant 2012;27(10):3746-3751. doi: 10.1093/ndt/gfs352
5. Lantinga MA, Drenth JP, Gevers TJ.Diagnostic criteria in renal and hepatic cyst infection. Nephrol Dial Transplant 2015;30(5):744-751. doi: 10.1093/ndt/gfu227
6. Юхно Е.А. Трофименко И.А. Труфанов Г.Е. Малигнизация эндометриоидных кист в аспекте магнитно-резонансного исследования: семиотика и диагностические ошибки. Опухоли женской репродуктивной системы 2013;(3):72-80.
7. Gupta S, Seith A, Dhiman RK, Chawla YK, Sud K, Kohli HS, et al. CT of liver cysts in patients with autosomal dominant polycystic kidney disease. Acta Radiol 1999;40(4):444-448.
8. Gupta S, Seith A, Sud K, Kohli HS, Singh SK, Sakhuja V, et al. CT in the evaluation of complicated autosomal dominant polycystic kidney disease. Acta Radiol 2000;41(3):280-284.
9. Piccoli GB, Arena V, Consiglio V, Deagostini MC, Pelosi E, Douroukas A, et al. Positron emission tomography in the diagnostic pathway for intracystic infection in ADPKD and ‘cystic’ kidneys. A case series. BMC Nephrol 2011;12:12-48. doi: 10.1186/1471-2369-12-48.
10. Keith DS, Torres VE, King BF, Zincki H, Farrow GM. Renal Cell Carcinoma in Autosomal Dominant Polycystic Kidney Disease. J Am Soc Nephrol 1994;4(9):1661-9.
11. Wood cG, Stromberg LG, Harmath CB, Horowitz JM, Feng C, Hammond NA, et al. CT and MR imaging for evaluation of cystic renal lesions and diseases. Radiographics 2015;35(1):125-141. doi: 10.1148/rg.351130016.
12. Migali G, Annet L, Lonneux M, Devuyst O. Renal cyst infection in autosomal dominant polycystic kidney disease. Nephrol Dial Transplant 2008;23(1):404-405.
13. Ichioka K, Saito R, Matsui Y, Terai A. Diffusion-weighted magnetic resonance imaging of infected renal cysts in a patient with polycystic kidney disease. Urology 2007;70(6):1219.
14. Katano K, Kakuchi Y, Nakashima A, Takahashi S, Kawano M. Efficacy of diffusion-weighted magnetic resonance imaging in detecting infected cysts in a case of polycystic kidney disease. Clin Nephrol 2011;75:24-26.
15. Takase Y, Kodama K, Motoi I, Saito K. Cyst infection in unilateral renal cystic disease and the role of diffusion-weighted magnetic resonance imaging. Urology 2012;80(5):61-62. doi: 10.1016/j.urology.2012.07.022.
16. Suwabe T, Ubara Y, Sumida K, Hayami N, Hiramatsu R, Yamanouchi M et al. Clinical features of cyst infection and hemorrhage in ADPKD: new diagnostic criteria. Clin Exp Nephrol 2012;16(6):892-902. doi: 10.1007/s10157-012-0650-2.
17. Mascalchi M, Filippi M, Floris R, Fonda C, Gasparotti R, Villari N. Diffusion-weighted MR of the brain: methodology and clinical application. Radiol Med 2005;109( 3):155-97.
18. Bruegel M, Holzapfel K, Gaa J, Woertler K, Waldt S, Kiefer B, et al. Characterization of focal liver lesions by ADC sequence for detection of focal liver lesions. Invest. Radiol 2008;43:261-266.
19. Lowenthal D, Zeile M, Lim WY, Wybranski C, Fischbach F, Wieners G, et al. Detection and characterization of focal liver lesions in colorectal carcinoma patients: comparison of diffusion-weighted and Gd-EOB-DTPA enhanced MR imaging. Eur Radiol 2011;21(4):832-840. doi: 10.1007/s00330-010-1977-2.
20. Miller FH, Hammond N, Siddiqi AJ, Shroff S, Khatri G, Wang Y, et al. Utility of diffusion-weighted MRI in distinguishing benign and malignant hepatic lesions. J Magn. Res. Imaging 2010;32(1):138-147. doi: 10.1002/jmri.22235.
21. Coenegrachts K, Delanote J, Ter Beek L, Haspeslagh M, Bipat S, Stoker J, et al. Improved focal liver les ion detection: comparison of singleshot diffusion-weighted echoplanar and single shot T2 weighted turbo spin echo techniques. Brit J of Radiol 2007;80(955):524-531.
22. Берген Т.А. Трофименко И.А. Методика МР-диффузии и ее применение в исследовании опухолей малого таза у женщин. Бюллетень сибирской медицины 2012;(11):10-12.
23. Bobot M, Ghez C, Gondouin B, Sallee M, Fournier PE, Burtey S, et al. Diagnostic performance of (18)F fluorodeoxyglucos positron emission tomography-computed tomography in cyst infection in patients with autosomal dominant polycystic kidney disease. Clin Microbiol Infect 2016; 22(1):71-77. doi: 10.1016/j.cmi.2015.09.024
24. Paschali AN, Georgakopoulos AT, Pianou NK, Anagnostopoulos CD. (18)F-fluorodeoxyglucose positron emission tomography/computed tomography in infected polycystic kidneydisease. World JNuclMed 2015;14(1):57-59. doi: 10.4103/1450-1147.150553.
25. Jouret F, Lhommel R, Beguin C, Devuyst O, Pirson Y, Hassoun Z, et al. Positron-emission computed tomography in cyst infection diagnosis in patients with autosomal dominant polycystic kidney disease. Clin J Am Soc Nephrol 2011;6(7):1644-1650. doi: 10.2215/CJN.06900810
26. Lantinga MA, Casteleijn NF, Geudens A, de Sevaux RG, van Assen S, Leliveld AM, et al. Management of renal cyst infection in patients with autosomal dominant polycystic kidney disease: asystematic review. Nephrol Dial Transplant. 2016. first published online January 29.
27. Suwabe T, Araoka H, Ubara Y, Kikuchi K, Hazue R, Mise K, et al. Cyst infection in autosomal dominant polycystic kidney disease: causative microorganisms and susceptibilityto lipid-soluble antibiotics. Eur J Clin Microbiol Infect Dis 2015;34(7):1369-1379. doi: 10.1007/s10096-015-2361-6
28. Kale PG, Devi BV, Lakshmi AY, Sivakumar V. Use of diffusion-weighted magnetic resonance imaging in the management of infected renal cyst in polycystic kidney disease. Indian J Nephrol 2015;25(1):60-61. doi: 10.4103/0971-4065.
29. Kato S, Hotta H, Mineta M, Miyake M. Case of infected renal cyst in polycystic kidney disease. Nihon Hinyokika Gakkai Zasshi 2013;104(3):536-539.
30. Лысенко МА, Вторенко В.И., Трушкин Р.Н., Лубенников А.Е., Сысоев А.М., Соколов А.А. Билатеральная нефрэктомия у пациентов с терминальной стадией хронической почечной недостаточности и активным течением хронического пиелонефрита. Урология 2016;(1): 46-52
Журнал «Экспериментальная и клиническая урология» Выпуск №4 за 2016 год
| Стоимость программы | к-во | Цена | Сумма |
Прием нефролога первичный | 1 | 760 | 760,00 | |
Консультация уролога (при необходимости) | 1 | 700 | 700,00 | |
Общий анализ мочи | 1 | 140 | 140,00 | |
Забор крови из вены в два вакутейнера | 1 | 169 | 169,00 | |
Общий (клинический) анализ крови, б/х: креатинин, мочевина, К+ | 1 | 852 | 852,00 | |
УЗИ почек + печень | 1 | 765 | 765,00 | |
Расчет СКФ по MDRD (входит в консультацию) |
|
|
| |
Микробиологическое исследование мочи на аэробные и факультативно-анаэробные условно-патогенные микроорганизмы | 1 | 318 | 318,00 | |
Повторный прием нефролога | 1 | 760 | 760,00 | |
Персональное сопровождение пациента | 1 | 311 | 311,00 | |
ИТОГО |
|
| 4775,00 |
Оценка поликистозной болезни почек у грызунов: сравнение роботизированного 3D-ультразвукового исследования и магнитно-резонансной томографии
Резюме
Поликистоз почек (PKD) — наследственное заболевание, характеризующееся образованием почечных кист и увеличением почки. Степень тяжести PKD можно определить неинвазивно путем измерения общего объема почек (TKV), многообещающего биомаркера, недавно получившего нормативную квалификацию. В доклинических моделях мышей, где изучается заболевание и оцениваются потенциальные терапевтические средства, наиболее популярным неинвазивным методом измерения TKV является магнитно-резонансная томография (МРТ).Хотя МРТ обеспечивает превосходное трехмерное разрешение и контраст, эти системы дороги в эксплуатации, имеют длительное время сбора данных и, следовательно, не используются активно в доклинических исследованиях ДОК. В этом исследовании новый прибор для визуализации, основанный на роботизированном ультразвуке (УЗИ), был оценен как дополнительный подход к оценке поликлинической болезни на моделях грызунов. Цель заключалась в том, чтобы определить степень, в которой измерения TKV на роботизированном ультразвуковом сканере коррелировали с эталонными стандартами in vivo и ex vivo (МРТ и штангенциркуль Вернье, соответственно).Был реализован дизайн поперечного исследования, который включал как мышей, пораженных PKD, так и здоровых диких типов, с охватом пола и возраста для широкого диапазона объемов почек. Было обнаружено, что полученные в США измерения TKV и длина почек были тесно связаны как с измерениями in vivo MRI и ex vivo штангенциркулем ( R 2 = 0,94 и 0,90, соответственно). В дополнение к измерению TKV, плотность почечных сосудов оценивалась с помощью акустической ангиографии (АА), новой методики УЗИ с контрастированием.Было обнаружено, что интенсивность изображения AA, показывающая объемную васкуляризацию, имеет сильную отрицательную корреляцию с TKV ( R 2 = 0,82), что свидетельствует о нарушении функции сосудов почек у мышей с более крупными почками. Эти исследования демонстрируют, что роботизированная УЗИ может обеспечить быстрый и точный подход для неинвазивной оценки поликлинической болезни на моделях грызунов.
Введение
Поликистоз почек (PKD) — это наследственное заболевание, определяемое развитием множества кист в почках.Заболевание является генетическим заболеванием с аутосомно-рецессивной и аутосомно-доминантной формами. Аутосомно-доминантная форма встречается чаще и встречается примерно у одного человека из 2500 в развитых странах (1,2). Кисты имеют тенденцию увеличиваться в количестве и размере в течение жизни человека, в конечном итоге вызывая ХБП и возможную почечную недостаточность (3). На сегодняшний день только один препарат (толваптан) одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для лечения PKD и может только замедлить прогрессирование заболевания (4).Таким образом, продолжаются широкомасштабные исследования по созданию лучших лекарств от PKD.
Модели на грызунах играют решающую роль в поддержке исследований болезней и тестирования лекарств (5). Сегодня существует несколько различных моделей ПКД на мелких животных, и прогрессирование заболевания обычно окончательно измеряют гистологическими методами (5,6). Гистология обеспечивает разрешение клеток и может количественно определить наличие связанных с заболеванием процессов, таких как кистозный диаметр / распределение, воспаление и фиброз.Однако гистология занимает много времени и в конечном итоге деструктивна, ограничивая ее одной временной точкой для каждого субъекта. У людей рСКФ является обычным неинвазивным биомаркером, используемым для оценки функции почек. Однако при PKD рСКФ имеет тенденцию к снижению на поздних стадиях заболевания, когда кистозное бремя является значительным и трудно поддается лечению (7,8). Из-за ограничений рСКФ у пациентов в 2015 году FDA квалифицировало полученные с помощью изображений измерения общего объема почек (TKV) в качестве биомаркера для количественной оценки эффективности препаратов PKD в клинических испытаниях (9).В дополнение к более ранней чувствительности к прогрессированию заболевания, TKV позволяет оценивать почки на протяжении всего начала и прогрессирования PKD. В контексте доклинических исследований TKV может обеспечить улучшенную статистику между группами с меньшим количеством животных по сравнению с исследованиями, в которых используются только инвазивные методы измерения (10).
Наиболее распространенными методами неинвазивного измерения TKV являются магнитно-резонансная томография (МРТ) и ультразвук (УЗИ) из-за их превосходного контраста мягких тканей, глубины проникновения и отсутствия ионизирующего излучения (11).Между ними МРТ считается золотым стандартом из-за ее высокого разрешения, многопараметрического определения последовательности импульсов и считывания данных о прогрессировании PKD, таких как TKV и кистозная нагрузка (12–14), связанных с заболеванием. Однако временные точки МРТ могут быть дорогими из-за высоких эксплуатационных расходов, длительного времени сбора данных и ограниченного доступа из-за высокого спроса со стороны пользователей. УЗИ может стать рентабельной альтернативой МРТ для быстрого измерения размеров органов, плотности сосудов и жесткости тканей, но давно страдает от проблем воспроизводимости из-за портативного форм-фактора и зависимости от пользователя.Сбор высококачественных воспроизводимых измерений почек грызунов с помощью УЗИ требует опытных сонографистов и громоздких рабочих процессов, которые могут свести на нет затраты, время и эффективность, которые обещает метод.
Недавно был разработан доклинический роботизированный ультразвуковой сканер для решения этих проблем. Это устройство использует механизм автоматического сканирования для растрирования ультразвукового датчика по всему телу грызуна, создавая трехмерное (3D) изображение анатомии с широким полем поля (15).Предоставляя единое трехмерное изображение с целостным изображением обеих почек в контексте окружающей анатомии, мы предположили, что эта технология может обеспечить высокоточные измерения TKV в моделях болезней грызунов. Следующее исследование проверяет эту гипотезу в двух поперечных исследованиях с проверкой как in vivo, (, т.е.., МРТ), так и ex vivo (, т.е. ., Штангенциркуль). Кроме того, поскольку было показано, что PKD снижает плотность почечных сосудов на моделях грызунов (16,17), мы оценили, можно ли оценить это снижение плотности с помощью режима микрососудистой визуализации с контрастированием микропузырьков, обеспечиваемого роботизированным инструментом (акустическая ангиография [AA ]) (18).Наконец, была оценена и представлена информация о внутри- и межэкспертной надежности.
Материалы и методы
Исследования изображений
В этом исследовании использовались две разные когорты мышей: одна для сравнения роботизированного УЗИ прибора с эталонным стандартом in vivo системы визуализации , а третья — для сравнения роботизированной УЗИ системы с системой визуализации ex vivo стандарт (штангенциркуль с вернье). Роботизированные УЗИ (рис.1) были получены с помощью тепловизора Vega (SonoVol, Inc., Дарем, Северная Каролина) и сравнены с обоими МРТ (16.4T Avance DRX 700WB; Bruker BioSpin, Биллерика, Массачусетс) и стандартное доклиническое УЗИ (Vevo 3100; FUJIFILM VisualSonics Inc., Торонто, Канада). Все исследования были одобрены комитетами по уходу за животными и использованием животных Университета Северной Каролины в Чапел-Хилл (UNC) и клиники Мэйо. Более подробную информацию о параметрах сканирования можно найти в дополнительном материале, а пример роботизированного ультразвукового сканирования представлен в дополнительном видео 1.
Рисунок 1.Обзор рабочего процесса сбора данных для роботизированной ультразвуковой системы. (A) Получены множественные параллельные развертки, обычно три, в результате чего получаются тысячи отдельных двумерных изображений по всему телу животного. (B и C) Эти изображения затем сшиваются вместе для создания одного объемного трехмерного (3D) изображения с широким полем поля, которое можно просматривать в различных ориентациях. Трехмерные данные можно увидеть в (B1) фронтальной, (B2) поперечной и (B3) сагиттальной плоскостях соответственно. (C) Затем каждую почку можно сегментировать в 3D для оценки общего объема почки. Масштабная линейка, 1 см.
Когорта 1
Чтобы оценить точность роботизированного ультразвукового сканера по сравнению с эталонным стандартом визуализации in vivo , был использован дизайн поперечного сечения исследования, гарантирующий, что почки будут наблюдаться в диапазоне размеров. Самцы и самки мышей PKD ( N = 7) сначала были визуализированы в клинике Мэйо с помощью МРТ и обычного УЗИ в соответствии со стандартными протоколами, чтобы служить золотым стандартом. Затем эти животные были доставлены в UNC для получения изображений с помощью роботизированного ультразвукового прибора.Конкретные сведения о параметрах визуализации для МРТ и УЗИ можно найти в дополнительных методах. Кроме того, физические и генетические характеристики когорты 1 представлены в дополнительной таблице 1.
Когорта 2
Для оценки in vivo по сравнению с ex vivo измерений размера вторая когорта ( N = 8) здоровых Nu / Использовали мышей Nu (Charles River Laboratories, Wilmington, MA). Когорта включала мышей-самок и самцов двух разных возрастов (возрастом 4 недели и возрастом 16 недель).Изображения этих животных были получены исключительно с помощью роботизированного ультразвукового сканера в UNC, и их не перевозили ни в какое другое учреждение. После роботизированного ультразвукового исследования когорты 2 всех мышей умерщвляли для оценки размера почек с помощью штангенциркуля Вернье (Mitutoyo, Sakado, Japan) постнекропсии. Кроме того, извлеченные почки были визуализированы на роботизированном ультразвуковом сканере после измерений Вернье, чтобы подтвердить точность измерений in vivo при отсутствии окружающей анатомии. Иссеченные почки помещали в нагретый гель для УЗИ на тепловизоре Vega и сканировали в 3D с использованием тех же параметров визуализации, что и in vivo .
Анализ изображения
Для определения объема почек из трехмерного изображения почки были вручную сегментированы на основе данных. Быстрая сегментация роботизированных данных США была выполнена с помощью SonoEQ (SonoVol, Inc.), который использует серверную часть 3D Slicer с открытым исходным кодом (www.slicer.org) (19). Чтобы улучшить очерчивание границ почек в данных США, трехмерные объемы от обоих датчиков США (двухэлементный и линейный массив) были наложены друг на друга с альфа-смешением. Тома МРТ и обычные УЗИ были сегментированы двумя отдельными считывающими устройствами с использованием программного обеспечения для сегментации, разработанного в компании (20).На время анализа изображений все считыватели были не в курсе генотипов животных, пола, возраста и объема почек друг друга с помощью рандомизации мышей. Для оценки интермодальности (УЗИ по сравнению с МРТ) и оценки интрамодальности (УЗИ с роботом по сравнению с обычным УЗИ) сегменты от одного экспертного читателя сравнивались по всем трем категориям: УЗИ с роботом (R.C.G.), обычное УЗИ (HLH) и МРТ (M.E.E.). Чтобы определить точность определения размера почек роботизированной УЗИ-системой по сравнению с ex vivo измерениями, все почки в когорте 2 были оценены двумя способами: с помощью измерителей программного обеспечения и 3D-сегментации.Программные измерители представляют собой линейные объекты измерения, которые могут быть помещены в трехмерные изображения с помощью программного обеспечения SonoEQ, и использовались для измерения длины и ширины почек в той же ориентации, что и постнекропсия с помощью штангенциркуля Вернье. Чтобы оценить надежность роботизированного ультразвукового сканера между считывающими устройствами, четыре независимых считывателя (N.J.B., J.D.R., R.C.G. и T.J.C.), охватывающие широкий спектр исследований в области ультразвуковой визуализации, сегментировали почки в роботизированных ультразвуковых данных и сравнивали. Для оценки внутричерепной изменчивости один читатель (Н.J.B.) снова сегментировал те же объемы почек 67 дней спустя, не просматривая предыдущие сегменты. Чтобы количественно определить минимальный определяемый размер кисты, на одном коронковом срезе почек с множеством кист были проведены измерения с помощью цифрового штангенциркуля для 11 идентифицируемых кист.
Оценка взаимосвязи между васкуляризацией почек и размером почек
Для оценки взаимосвязи между размером и васкулярностью почек был проведен анализ интенсивности изображения на изображениях AA каждой почки. Сегментация США для каждой почки, описанная в предыдущем разделе, была применена к зарегистрированным объемам AA.Это позволило проанализировать воксели изображения в почке в виде гистограммы значений интенсивности. Поскольку яркость данного пикселя коррелирует с количеством контрастных веществ микропузырьков, присутствующих в этой локализованной области ткани, «процент положительности» или процент пикселей в интересующей области выше заданного порога является показателем васкулярности. Этот показатель сосудистой сети потребовал выбора порога интенсивности, выше которого пиксели были идентифицированы для представления сосудистой сети.Модулируя «порог васкулярности» по диапазону, можно оценить силу корреляции между размером почек и васкуляризацией. Этот анализ был выполнен в Matlab R2017a (Mathworks, Natick, MA).
Статистический анализ
Согласованность и корреляция между модальностями визуализации оценивалась в Matlab R2017a (Mathworks) с использованием инструментария Klein’s Bland – Altman и Correlation Plot версии 1.10. Сообщенные метрики включали коэффициент корреляции Пирсона ( r ), квадрат Пирсона ( r 2 ), коэффициент детерминации ( R 2 ), коэффициент корреляции Спирмена ( ρ ), уравнение наилучшего соответствия ( наименьших квадратов), коэффициент вариации и пределы согласия (LOA).Уравнение линейной регрессии решалось с граничным условием нулевого пересечения. Расхождение между измерениями оценивали с помощью анализа Бланда – Альтмана. P <0,05 считалось статистически значимым. Для количественной оценки надежности между читателями был вычислен коэффициент внутриклассовой корреляции (ICC) с использованием формулировки абсолютного согласия между измерениями («ICC [A, 1]») (21) для четырех считывателей изображений, а также коэффициент разница между измерениями в США для каждого TKV.
Результаты
Оценка точности измерения размера почек (
исследований in vivo )Почки можно легко визуализировать как на МРТ, так и на роботизированных наборах данных США. Как и ожидалось, наборы данных МРТ имели лучший контраст тканей, но требовали большего времени сбора данных на одно животное (5–10 минут против 26 секунд). При сравнении изображений МРТ и роботизированного УЗИ в каждом объеме были соответствующие анатомические ориентиры, такие как кисты и кровеносные сосуды (рис. 2). Множество кист, вплоть до 0.4 мм в диаметре, были идентифицированы в УЗИ, но кисты меньшего размера не были достоверно отличимы от спеклов УЗИ (дополнительный рисунок 1).
Рисунок 2.Параллельное сравнение УЗИ и МРТ почки. Срезы в одном месте в обоих режимах визуализации показывают кисты (желтые стрелки) в одних и тех же областях. Также видна нижняя полая вена (красная стрелка).
Чтобы оценить корреляцию между МРТ и роботизированным ультразвуковым сканером, сегментированные почки из когорты 1 сравнивали через , линейную регрессию и анализ Бланда – Альтмана (рис. 3).Корреляция между сегментацией между модальностями была очень сильной, со значением 0,94 R 2 . Анализ Бланда – Альтмана выявил среднюю ошибку занижения объема почек на 4,9 мм. 3 с роботизированным УЗИ; однако это не было значимым ( P = 0,62). Длина между двумя модальностями составляла 70 мм 3 . Кроме того, роботизированное УЗИ сравнивалось с обычным УЗИ (дополнительный рисунок 2) и обычное УЗИ с МРТ (дополнительный рисунок 3).При сравнении с обычным УЗИ роботизированное УЗИ продемонстрировало отличную корреляцию ( R 2 = 0,97) и даже меньший LOA (44 мм 3 ) по сравнению с МРТ. Обычные УЗИ и МРТ также показали высокую степень корреляции ( R 2 = 0,92), хотя и с большим LOA (90 мм 3 ).
Рис. 3.Регрессия и графики Бланда – Альтмана, сравнивающие результаты in vivo измерений объема почек на основе ультразвукового робота с in vivo МРТ. CV, коэффициент вариации; LOA, пределы соглашения; r , коэффициент корреляции Пирсона; r 2 , квадрат коэффициента Пирсона; R 2 , коэффициент детерминации; rho , коэффициент корреляции Спирмена.
Оценка точности измерения размера почек (
Ex vivo исследований)Для оценки взаимосвязи между in vivo измерениями размера почек, выполненными на роботизированном ультразвуковом сканере, и ex vivo методами определения размера почек с помощью штангенциркуля, a Сравнительное исследование было выполнено на когорте 2, включая измерения ширины и длины почек.Для набора данных роботизированного ультразвукового сканера 3D-изображения были получены как на почках in vivo, перед вскрытием (служит нормальным сценарием для измерения в продольном исследовании), так и при постнекропсии эксплантированной почки (служит наилучшим сценарием для производительности системы и измерения. точность). На рис. 4 показано размещение штангенциркулей (штангенциркуль Вернье на рис. 4A и штангенциркуль США на рис. 4, B и C для in vivo и ex vivo , соответственно). По измерениям штангенциркуля Вернье диапазон ширины почек для этого исследования составлял 5.42–8,03 мм, а длина почек — 7,47–11,75 мм. Размеры почек, измеренные ультразвуковыми штангенциркулями, in vivo и ex vivo , сильно коррелировали с измерениями штангенциркуля с вернье, с коэффициентами определения R 2 = 0,90 и R 2 = 0,95 соответственно. (Рисунок 4). Также наблюдались ожидаемые тенденции для возраста и пола: у старых мышей почки были больше, чем у более молодых мышей того же пола, а у самцов в среднем почки были больше, чем у самок для данного возраста (дополнительный рисунок 4).
Рис. 4.Штангенциркуль нониус и штангенциркуль США. (A) Изображение, показывающее, как штангенциркуль Вернье использовался для измерения длины почек (пунктирная линия) и ширины (сплошная линия). (B) Штангенциркуль для США, нарисованный в программном обеспечении на корональном изображении in vivo US. (C) Штангенциркуль, нарисованный на американском изображении ex vivo почек. Линии в (A, B и C) соответствуют одним и тем же осям. (D – F) графики Блэнда – Альтмана, сравнивающие (D) in vivo, штангенциркулей США, (E) ex vivo, штангенциркулей США и (F) ex vivo, штангенциркулям США.CV, коэффициент вариации; LOA, пределы соглашения; r , коэффициент корреляции Пирсона; r 2 , квадрат коэффициента Пирсона; R 2 , коэффициент детерминации; rho , коэффициент корреляции Спирмена.
Оценка согласованности между считывающими устройствами
На рисунке 5 показана изменчивость TKV между считывателями для когорты 1 мышей, сканированных с помощью роботизированной УЗИ, с сортировкой по размеру. Показаны среднее и стандартное отклонение измерений, а также значения каждого из четырех считывающих устройств.Диапазон значений TKV для этой когорты составлял 250,5–904,8 мм 3 . В среднем SD для измерения TKV на нескольких считывателях составляло 43,62 мм 3 , минимум 19,5 мм 3 и максимум 69,0 мм 3 для животных 603 и 60A, соответственно. Средний коэффициент вариации (SD / среднее) для этих мышей составлял 9%, с минимумом 3% и максимумом 18% для мышей 570B и 607, соответственно. ICC между четырьмя читателями был очень высоким — 0,93 (95% ДИ, 0,83: 0.97). Что касается внутрипользовательской вариабельности, тестируемый ридер имел ICC 0,96 (95% ДИ, 0,88–0,99) между двумя временными точками.
Рисунок 5.Вариабельность между считывателями для измерения общего объема почек для когорты 1. Считыватели обозначены маркером, на графике нанесены среднее значение и стандартные отклонения. ID, идентификатор.
Оценка взаимосвязи между васкуляризацией почек и размером почек
Была выдвинута гипотеза, что на изображениях AA будет корреляция между процентом ярких пикселей в почке (процент положительности, i.e ., сосудистость) и размер почки. Например, почка, заполненная большими неваскуляризированными кистами, будет содержать высокий процент пикселей низкой интенсивности внутри почки и, следовательно, низкий процент положительности. И наоборот, почка с высокой плотностью сосудов будет иметь высокий процент положительности. Оптимальным порогом, обеспечивающим максимальную силу корреляции между васкуляризацией и размером почек, было значение интенсивности AA, равное 46 (постпороговое изображение для этого значения можно увидеть на рисунке 6A).При этом пороговом значении значение R 2 для линейной регрессии между васкуляризацией и размером почек составляло 0,82. Этот анализ носил исследовательский характер, и необходимо провести дополнительные исследования, чтобы охарактеризовать стабильность этого оптимального порога в различных когортах животных, а также то, как его можно использовать для извлечения других значимых результатов из моделей ДОК, таких как кистозная нагрузка.
Рисунок 6.Корреляция между васкуляризацией и размером почек. (A) Морфология сосуда, визуализированная с помощью проекций максимальной интенсивности объемов акустической ангиографии (AA). Показан одиночный двумерный (2D) срез объема с типичной кистой (белая стрелка). После определения оптимального порога в 46 отсчетов, вокселы в кисте и в других местах были установлены на ноль и не включались в показатель процента положительности для васкулярности. (B) Средняя гистограмма всех объемов AA когорты 1. Стандартные отклонения бинов гистограммы показаны с планками ошибок.(C) Процент ярких вокселей в почке во время перфузии микропузырьков (позитивный процент) отрицательно коррелирует с объемом почки. На этом графике для почек было установлено 46 отсчетов. (D) Коэффициент детерминации линейной регрессии в (C) зависит от порогового уровня. Установление порога в 46 отсчетов дает наивысшее значение R 2 . Этот порог исключает кисты, но включает большую часть сосудистой сети (см. Справа на [A]).
Обсуждение
В этом исследовании было продемонстрировано, что роботизированное 3D УЗИ может производить точные и последовательные измерения in vivo TKV на моделях грызунов.Анализ корреляции между объемом почки, полученным с помощью УЗИ и МРТ, дал значение R 2 , равное 0,94, без статистически значимой ошибки. Кроме того, роботизированные измерения в УЗИ очень хорошо согласуются с обычными измерениями в УЗИ ( R 2 = 0,97) и требуют значительно меньше времени для получения. Это важный вывод, потому что он показывает, что новый американский прибор с роботизированным форм-фактором может использоваться в качестве высокопроизводительного метода скрининга на TKV, что позволяет проводить доклинические исследования большой когорты, выполнение которых в противном случае было бы недопустимо по стоимости и времени. МРТ или обычное УЗИ.Когда желательно более высокое пространственное разрешение, отдельных животных, прошедших ультразвуковой скрининг, всегда можно выборочно отправить на МРТ, аналогично целевому набору в клинических исследованиях. В дополнение к высокой корреляции измерений объема почек между модальностями, кисты диаметром до 0,4 мм были видны в обоих случаях (рисунок 2, дополнительный рисунок 1). Это говорит о том, что продольный мониторинг общего объема кисты, среднего размера кисты и процентного пространства кисты может быть возможным с помощью роботизированного УЗИ. Другие показатели для количественной оценки поликлинической болезни, такие как паренхиматозный фиброз и почечный кровоток, также можно измерить с помощью робота US с помощью визуализации эластографии сдвиговой волной и допплеровской визуализации, соответственно.Хотя эти показатели выходили за рамки нашего исследования с единовременной проверкой, они будут изучены более подробно в будущем.
Кроме того, было продемонстрировано, что размеры почек дикого типа, измеренные in vivo и с помощью роботизированной УЗ-системы, сильно коррелировали с размерами почек, измеренными ex vivo (Рисунок 4). Ex vivo Определение размеров органов — обычная практика в доклинических исследованиях, поскольку неинвазивная визуализация обычно не проводится. В частности, для почек это можно сделать с помощью подходов смещения объема или измерения каверномером по двум осям ( i.e ., длина и ширина) или три оси (, т.е. ., длина, ширина и высота), которые могут быть помещены в уравнение эллипсоида для получения объема (22). В этом исследовании измерений in vivo сравнивались с измерениями ex vivo , выполненными как ультразвуковыми, так и ручными средствами ( с помощью штангенциркуля). Во всех случаях измерения штангенциркуля точно совпадали, со значениями R 2 в диапазоне от 0,88 до 0,95.
Интересно, что при сравнении штангенциркуля in vivo US с штангенциркулем Вернье (0.87 мм, P = 5.0e-5; Рисунок 4D). Чтобы определить, было ли это артефактом того, что считыватель из США неправильно видит границу почки в пределах данных in vivo США, мы проанализировали измерения между штангенциркулем Вернье и штангенциркулем ex vivo США, где границы ткани имеют максимальный контраст по сравнению с связующий гель. В этом случае (рис. 4E) можно увидеть почти такое же завышение 0,88 мм по US ( P = 2,9e-10). Одним из объяснений этого может быть то, что штангенциркуль Вернье физически сжимал почки на это расстояние, что приводило к занижению этих данных, что является известной проблемой при использовании штангенциркуля Вернье для измерения образцов тканей.При сравнении штангенциркуля in vivo и ex vivo US, измерения были в высокой степени согласованы без существенной систематической ошибки (рис. 4F).
Это исследование показало, что васкуляризация почек, измеренная с помощью ярких вокселей с усиленным контрастом, имела сильную отрицательную корреляцию с объемом почек, измеренным с помощью УЗИ ( R 2 = 0,82) (Рисунок 6). Хотя микропузырьки обычно считаются безопасными как для клинических, так и для доклинических исследований (23), их использование вместе с высокоинтенсивными ультразвуковыми импульсами может привести к нежелательным биоэффектам и повреждению клеток.Было обнаружено, что в почках грызунов порог механического индекса (МИ), при котором происходит повреждение микропузырьками, зависит от частоты кадров и времени визуализации области. Одно исследование показало, что визуализация одного места в течение 60 секунд с одним кадром в секунду с ИМ> 0,6 может вызвать клубочковое кровоизлияние (24). Другое более крупное исследование не обнаружило клубочкового кровотечения при ИМ до 1,9, но обнаружило, что АМК увеличивалась с импульсами при ИМ 1,0 (25). Поскольку система Vega выполняет АА при МИ 0,54 и быстро перемещает датчик через почки, не ожидается, что значительные биоэффекты, как сообщалось в предыдущих исследованиях, возникнут при сканировании сосудистой сети почки; однако эту гипотезу следует тщательно проверить в будущих исследованиях.
PKD у людей обычно вызывает гипертензию (26, 27, 28), а сердечно-сосудистые заболевания являются наиболее частой причиной смерти пациентов с PKD (29). Помимо гипертонии, могут развиваться сердечно-сосудистые нарушения, такие как гипертрофия левого желудочка, диастолическая дисфункция бивентрикулов и нарушение резерва скорости коронарного кровотока (30). УЗИ обычно используется для быстрого измерения общих показателей сердечно-сосудистой системы, таких как фракция выброса, ударный объем и сердечный выброс. В будущих исследованиях можно будет измерить TKV вместе с этими сердечными показателями с помощью роботизированного ультразвукового сканера, оцениваемого здесь.
Одной из проблем, с которой часто возникают проблемы при визуализации in vivo , являются респираторные артефакты. В этом исследовании дыхание животных не вызывает значительных артефактов при сканировании почек в УЗИ. На Рисунке 1 (панель B1) горизонтальные линии видны на коже мыши, где происходило дыхание, но очень незначительны на почках. Это связано с тем, что, во-первых, животные лежали на спине, поэтому смещение почки из-за расширения легких было незначительным. Во-вторых, для сегментации было наложено сканирование высоких и низких частот, поэтому дыхательные линии стали менее резкими.Основываясь на этих результатах, не представляется, что активная синхронизация дыхания необходима для точного измерения TKV, что позволяет упростить рабочий процесс и повысить пропускную способность животных.
У этого исследования было несколько ограничений. Во-первых, МРТ и УЗИ не выполнялись в одном и том же учреждении, что требовало доставки и акклиматизации мышей, что приводило к временной задержке между методами визуализации. Хотя эта задержка была относительно короткой (20 дней), вполне вероятно, что размер почки мог измениться из-за естественного биологического прогрессирования и уменьшить согласие между МРТ и УЗИ.Во-вторых, наборы данных МРТ и УЗИ оценивались разными читателями с использованием разных пакетов программного обеспечения для сегментации, без явного обучения между ними. Ожидается, что с улучшенным обучением (, например, , разработка рубрики сегментации), корреляция между МРТ и УЗИ может увеличиться по сравнению с тем, о котором сообщалось в этом исследовании. В-третьих, ex vivo измерений объема почек имели временную зависимость от времени эвтаназии (дополнительная фигура 5). В этом исследовании все мыши в когорте 2 были умерщвлены посредством передозировки изофлурана с последующим смещением шейки матки, причем время извлечения почки варьировалось в зависимости от скорости техника, выполнявшего вскрытие.Первые извлеченные почки имели ex vivo объемов, которые были меньше, чем in vivo объемов, тогда как последние извлеченные почки (примерно через 30 минут после эвтаназии) имели на ex vivo объемов больше, чем in vivo объемов. Это указывает на то, что посмертные изменения могли повлиять на корреляцию между измерениями in vivo и ex vivo , и подчеркивает важность стандартизации аутопсии. В-четвертых, это исследование оценивало только небольшое количество мышей ( N = 30 почек между двумя когортами), поэтому более крупные исследования с более широким диапазоном размеров почек и патологий заболеваний ( e.g ., модели фиброза почек) должны быть проведены в будущем. Наконец, сывороточные и мочевые биомаркеры с прогнозом прогрессирования PKD, аналогичные TKV, такие как β 2 микроглобулин и моноцитарный хемоаттрактантный белок-1 (31), не измерялись в этом исследовании, но они предоставят более подробную стратификацию заболевания в будущих исследованиях.
Раскрытие информации
N. Beaumont, T. Czernuszewicz, P. Dayton, R. Gessner и J. Rojas либо наняты, имеют значительный финансовый интерес, либо являются соавторами патентов, лицензированных SonoVol, Inc.Авторы сообщают, что следующий грант Национального института здравоохранения (NIH) с SonoVol находится на рассмотрении: R43 DK126607 (Исследования инноваций в малом бизнесе / NIH; несколько главных исследователей [MPI]; главный исследователь SonoVol, Т. Чернушевич / Майо; Mayo MPI, T. Клайн и М. Ромеро), «Новая роботизированная платформа обработки изображений ИИ для улучшения исследований по заболеваниям почек и открытия новых лекарств». Это предложение основано на работе, представленной в этой рукописи, и расширяет ее.
Финансирование
Финансирование этой работы было предоставлено Фондом Мэйо, Фондом оксалоза и гипероксалурии и грантом Центра ДОК Мейо P30 DK0
Благодарности
Мы хотели бы поблагодарить г-на Брайана Веласко и Центр животных Северной Каролины за их помощь в обращении с животными во время экспериментов in vivo .
Вклад авторов
Н. Бомонт написал первоначальный черновик и отвечал за визуализацию; Н. Бомонт, Т. Чернушевич, П. Дейтон, Р. Гесснер, Х. Холмс, Т. Клайн, Дж. Рохас и М. Ромеро рецензировали и редактировали рукопись; Н. Бомонт, Т.Чернушевич, М. Эдвардс, Р. Гесснер, А. Грегори, Х. Холмс и Дж. Рохас отвечали за формальный анализ; Т. Чернушевич отвечал за методологию; Т. Чернушевич, П. Дейтон, Р. Гесснер, Т. Клайн и М. Ромеро отвечали за ресурсы и контроль; Т. Чернушевич, М. Эдвардс, А. Грегори и Х. Холмс отвечали за курирование данных; А. Грегори отвечал за программное обеспечение; Т. Чернушевич, Р. Гесснер, Т. Клайн и М. Ромеро концептуализировали исследование; Т. Чернушевич, Р.Гесснер и М. Ромеро отвечали за финансирование приобретения; и М. Ромеро отвечал за администрирование проекта.
- Получено 24 июня 2020 г.
- Принято 17 августа 2020 г.
- Copyright © 2020 Американское общество нефрологов
Поликистоз почек — Диагностика и лечение
Диагноз
При поликистозе почек с помощью определенных тестов можно определить размер и количество кист почек, а также оценить количество здоровой ткани почек, в том числе:
- УЗИ. Во время ультразвука на ваше тело помещается палочкообразное устройство, называемое датчиком. Он излучает звуковые волны, которые отражаются обратно на датчик, как сонар. Компьютер преобразует отраженные звуковые волны в изображения почек.
- Компьютерная томография. Когда вы лежите на подвижном столе, вас подводят к большому устройству в форме пончика, которое проецирует тонкие рентгеновские лучи через ваше тело. Ваш врач может увидеть изображения ваших почек в поперечном сечении.
- МРТ. Когда вы лежите внутри большого цилиндра, магнитные поля и радиоволны создают поперечный разрез ваших почек.
Дополнительная информация
Показать дополнительную информациюЛечение
Степень тяжести поликистоза почек варьируется от человека к человеку — даже среди членов одной семьи. Часто люди с PKD достигают терминальной стадии болезни почек в возрасте от 55 до 65 лет. Но некоторые люди с PKD имеют легкое заболевание и могут никогда не перейти в терминальную стадию болезни почек.
Лечение поликистоза почек включает устранение следующих признаков, симптомов и осложнений на ранних стадиях:
Рост кисты почки. Терапия толваптаном может быть рекомендована взрослым с риском быстрого прогрессирования ADPKD . Толваптан (Jynarque, Samsca) — это таблетка, которую вы принимаете внутрь, она замедляет скорость роста кисты почек и снижает эффективность работы почек.
При приеме толваптана существует риск серьезного повреждения печени, и он может взаимодействовать с другими лекарствами, которые вы принимаете.При приеме толваптана лучше всего обратиться к врачу, специализирующемуся на здоровье почек (нефрологу), чтобы отслеживать побочные эффекты и возможные осложнения.
Высокое кровяное давление. Контроль высокого кровяного давления может замедлить прогрессирование заболевания и замедлить дальнейшее повреждение почек. Сочетание диеты с низким содержанием натрия и жиров с умеренным содержанием белка и калорий с отказом от курения, увеличением физических нагрузок и снижением стресса может помочь контролировать высокое кровяное давление.
Однако для контроля высокого кровяного давления обычно необходимы лекарства. Лекарства, называемые ингибиторами ангиотензинпревращающего фермента (АПФ) или блокаторами рецепторов ангиотензина II (БРА), часто используются для контроля высокого кровяного давления.
- Снижение функции почек. Чтобы почки оставались здоровыми как можно дольше, специалисты рекомендуют поддерживать нормальную массу тела (индекс массы тела). Питьевая вода и жидкости в течение дня могут помочь замедлить рост кист почек, что, в свою очередь, может замедлить снижение функции почек.Следование диете с низким содержанием соли и употребление меньшего количества белка может позволить кистам почек лучше реагировать на увеличение жидкости.
- Боль. Вы можете контролировать боль при поликистозе почек с помощью безрецептурных лекарств, содержащих ацетаминофен. Однако у некоторых людей боль более сильная и постоянная. Ваш врач может порекомендовать процедуру с использованием иглы для извлечения жидкости из кисты и введения лекарства (склерозирующего агента) для уменьшения кисты почек. Или вам может потребоваться операция по удалению кист, если они достаточно большие, чтобы вызывать давление и боль.
- Инфекции мочевого пузыря или почек. Срочное лечение инфекций антибиотиками необходимо для предотвращения повреждения почек. Ваш врач может выяснить, есть ли у вас простая инфекция мочевого пузыря или более сложная киста или инфекция почек. При более сложных инфекциях может потребоваться более длительный курс антибиотиков.
- Кровь в моче. Вам нужно будет пить много жидкости, предпочтительно простой воды, как только вы заметите кровь в своей моче, чтобы ее разбавить.Разбавление может помочь предотвратить образование тромбов в мочевыводящих путях. В большинстве случаев кровотечение останавливается само. Если это не так, важно обратиться к врачу.
- Почечная недостаточность. Если ваши почки теряют способность удалять продукты жизнедеятельности и лишнюю жидкость из крови, вам в конечном итоге потребуется диализ или трансплантация почки. Регулярное посещение врача для мониторинга поликлинической болезни позволяет лучше всего провести трансплантацию почки. Возможно, вам удастся сделать превентивную трансплантацию почки, что означает, что вам не нужно будет начинать диализ, но вместо этого вам потребуется трансплантация.
Аневризмы. Если у вас поликистоз почек и в семейном анамнезе разорванные (внутричерепные) аневризмы головного мозга, ваш врач может порекомендовать регулярный скрининг на внутричерепные аневризмы.
При обнаружении аневризмы в зависимости от ее размера может быть вариантом хирургического клипирования аневризмы для снижения риска кровотечения. Нехирургическое лечение небольших аневризм может включать контроль высокого кровяного давления и высокого холестерина в крови, а также отказ от курения.
Раннее лечение дает наилучшие шансы замедлить прогрессирование поликистоза почек.
Клинические испытания
Изучите исследования клиники Mayo Clinic, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или контроля этого состояния.
Помощь и поддержка
Как и в случае с другими хроническими заболеваниями, поликистоз почек может казаться подавляющим.Поддержка друзей и семьи важна в борьбе с хроническим заболеванием. Кроме того, могут помочь консультант, психолог, психиатр или священнослужитель.
Вы также можете подумать о вступлении в группу поддержки. Хотя не для всех, группы поддержки могут предоставить полезную информацию о лечении и преодолении трудностей. А общение с людьми, которые понимают, через что вы проходите, может заставить вас чувствовать себя менее одиноким.
Спросите своего врача о группах поддержки в вашем районе.
Подготовка к приему
Скорее всего, вы начнете с посещения вашего основного лечащего врача. Однако вас могут направить к врачу, специализирующемуся на здоровье почек (нефрологу). Вам может быть полезно начать специализированное лечение на ранней стадии заболевания, даже если анализы крови показывают, что у вас все еще нормальная функция почек.
Вот некоторая информация, которая поможет вам подготовиться к встрече.
Что вы можете сделать
Когда вы записываетесь на прием, спросите, есть ли что-нибудь, что вам нужно сделать заранее, например, поститься перед определенным тестом.Составьте список из:
- Ваши симптомы, включая те, которые кажутся не связанными с причиной, по которой вы записались на прием, и когда они начались
- Все лекарства, витамины и другие добавки , которые вы принимаете, включая дозы
- Ваша история болезни и история болезни вашей семьи, особенно болезни почек
- Вопросы, которые следует задать своему врачу
По возможности возьмите с собой члена семьи или друга, чтобы они помогли вам запомнить полученную информацию.
При поликистозе почек вопросы, которые следует задать врачу, включают:
- Какая наиболее вероятная причина моих симптомов?
- Есть ли другие возможные причины моих симптомов?
- Какие тесты мне нужны?
- Это состояние временное или хроническое?
- Как лучше всего действовать?
- Какие альтернативы предлагаемому вами подходу?
- У меня другие проблемы со здоровьем. Как мне лучше всего управлять ими вместе?
- Нужно ли мне ограничивать свою диету или занятия?
- Могу ли я взять с собой брошюры или другие печатные материалы? Какие сайты вы рекомендуете?
Не стесняйтесь задавать другие вопросы.
Чего ожидать от врача
Ваш врач может задать вам такие вопросы, как:
- Были ли симптомы постоянными или случайными?
- Кажется, что-нибудь улучшает или ухудшает ваши симптомы?
- Знаете ли вы, какое у вас обычно артериальное давление?
- Измерялась ли у вас функция почек?
14 октября 2020 г.
Аутосомно-доминантная поликистозная болезнь почек — Диагноз
Аутосомно-доминантная поликистозная болезнь почек (АДПБП) обычно диагностируется у взрослых старше 30 лет, потому что симптомы обычно не проявляются раньше.
При постановке диагноза ваш терапевт спросит о ваших симптомах и истории болезни вашей семьи.
Если ваши почки увеличены, ваш терапевт может почувствовать их в вашем животе.
Ваш терапевт также может организовать проведение некоторых анализов.
Анализы мочи и крови
Ваш терапевт измерит ваше кровяное давление, чтобы убедиться, что оно выше нормы.
Они также могут проводить другие тесты, такие как:
- Анализы мочи для проверки крови или белка в моче
- анализов крови, чтобы можно было оценить скорость фильтрации крови почками
Анализ крови на СКФ
Эффективный способ оценить, насколько хорошо работают ваши почки, — это рассчитать скорость клубочковой фильтрации (СКФ).
СКФ — это показатель того, из скольких миллилитров (мл) крови ваши почки могут отфильтровать отходы за минуту.
Здоровая пара почек должна быть способна фильтровать более 90 мл крови в минуту.
Сканы
Ваш терапевт также назначит вам ультразвуковое сканирование для поиска кист в почках или других органах, например, в печени.
Ультразвуковое сканирование — это безболезненная процедура, при которой через кожу над почками проводят небольшой зонд.
Зонд излучает высокочастотные звуковые волны, которые используются для создания изображения изнутри вашего тела.
В некоторых случаях вам может потребоваться компьютерная томография или МРТ. На них будут более подробно показаны ваши почки.
МРТ будет рекомендовано, если у вас есть семейная история аневризм головного мозга.
Аневризма головного мозга — это выпуклость в кровеносном сосуде головного мозга, вызванная слабостью стенки кровеносного сосуда.
Узнайте больше о диагностике аневризм головного мозга
Скрининг
Скрининг людей, о которых известно, что они подвержены риску развития ADPKD, потому что у них есть семейный анамнез этого состояния, является спорным вопросом в медицинском сообществе.
Некоторые утверждают, что скрининг мало что дает, потому что в настоящее время нет лечения, чтобы остановить развитие ADPKD.
Сообщение человеку о том, что у него ADPKD и что у него может развиться почечная недостаточность в более позднем возрасте, также может вызвать у него стресс и беспокойство.
Другие утверждают, что, хотя вы не можете предотвратить ADPKD, скрининг может помочь выявить кисты, и можно вылечить высокое кровяное давление (гипертонию), связанное с ADPKD, что может снизить риск развития сердечно-сосудистых заболеваний.
Если диагноз известен, осложнения не станут неожиданностью, и их можно будет лечить быстро и надлежащим образом.
Также существует лечение под названием толваптан, которое может замедлить рост кист и в некоторых случаях может быть полезным.
Если вы планируете пройти обследование на ADPKD или обследовать своих детей, вам следует обсудить преимущества и недостатки скрининга со своим терапевтом, партнером и семьей.
Вы также можете попросить направление к специалисту по почкам.
Как проводится досмотр
Есть 2 метода, которые можно использовать для подтверждения диагноза ADPKD.
Это:
- с помощью УЗИ, КТ или МРТ для проверки аномалий почек
- в особых обстоятельствах, используя генетические анализы крови, чтобы определить, унаследовали ли вы один из генетических дефектов, которые, как известно, вызывают ADPKD в вашей семье, — но поскольку эти генетические тесты дороги и могут быть трудными для интерпретации, они обычно не проводятся в подарок
Важно знать, что ни один из тестов не является полностью точным и не всегда может обнаружить ADPKD, даже если у вас есть заболевание.
Визуализирующие тесты могут пропускать очень маленькие кисты у молодых людей, и их придется повторить в более позднем возрасте.
Генетическое тестирование является более чувствительным и точным при диагностике ADPKD, но может быть отрицательным у 10% людей с ADPKD.
Последняя проверка страницы: 11 апреля 2019 г.
Срок следующей проверки: 11 апреля 2022 г.
Поликистоз почек (PKD): признаки, симптомы и лечение
Обзор
Что такое поликистоз почек?
Поликистоз почек (PKD) вызывает образование кист (опухолей, заполненных жидкостью) в почках.PKD — это генетическое заболевание, то есть у вас должен быть мутировавший (измененный) ген, чтобы получить заболевание.
PKD — это не то же самое, что простые кисты почек, которые обычно безвредны. PKD — серьезный тип хронического заболевания почек. Кисты могут увеличивать почки и мешать им выводить отходы из крови. PKD может привести к почечной недостаточности.
Существуют ли разные типы поликистоза почек?
Существует два типа поликистоза почек:
- Аутосомно-доминантная поликистозная болезнь почек (ADPKD): ADPKD — наиболее распространенная форма PKD.Обычно это заболевание диагностируется в зрелом возрасте, в возрасте от 30 до 50 лет. ADPKD обычно диагностируется во взрослом возрасте, в возрасте от 30 до 50 лет, но может возникнуть в раннем детстве или подростковом возрасте.
- Аутосомно-рецессивная поликистозная болезнь почек (ARPKD): ARPKD — редкая форма PKD, также называемая детской PKD. Это вызывает аномальное развитие почек в утробе матери или вскоре после рождения.
Насколько распространен поликистоз почек?
Около 500000 человек в США.С. есть ДОК. Примерно 2% всех случаев почечной недостаточности являются результатом PKD.
Симптомы и причины
Что вызывает поликистоз почек?
Генетические мутации вызывают поликистоз почек. В большинстве случаев родители передают заболевание своим детям. Итак, вы унаследовали ДОК. Но иногда гены мутируют или изменяются случайным образом. У людей всех возрастов, рас и национальностей может быть ДОК. В равной степени встречается у женщин и мужчин.
Каковы симптомы аутосомно-доминантной поликистозной болезни почек (АДПБП)?
Симптомы ADPKD включают:
Каковы признаки аутосомно-рецессивной поликистозной болезни почек (ARPKD)?
Признаки того, что у плода (будущего ребенка) или новорожденного может быть АДПБП, включают:
- Увеличенные почки.
- Нарушение роста (маленький рост или низкая масса тела при рождении).
- Низкий уровень околоплодных вод, что может означать, что ребенок не вырабатывает достаточно мочи в утробе матери.
Всегда ли сразу проявляются признаки и симптомы поликистоза почек?
Нет. Это заболевание часто протекает бессимптомно, примерно половина случаев диагностируется при жизни человека.
Какие осложнения возникают при поликистозе почек?
PKD может вызвать серьезные осложнения для здоровья взрослых и детей.
Взрослые могут развиваться:
Младенцы могут иметь:
- Проблемы с дыханием из-за недоразвитых легких.
- Высокое кровяное давление.
- Почечная недостаточность.
- Проблемы с печенью.
Диагностика и тесты
Как диагностируется поликистоз почек?
Нефролог (поставщик медицинских услуг, специализирующийся на заболеваниях почек) диагностирует PKD. Они могут назначить следующие визуализационные исследования для проверки ваших почек:
Медицинский работник также может порекомендовать генетическое тестирование.Анализ крови или слюны может проверить наличие мутировавших генов, вызывающих поликлиническую болезнь.
Ведение и лечение
Как лечить поликистоз почек?
Наиболее распространенные методы лечения ДОК включают:
- Управление артериальным давлением: Ваш врач помогает вам контролировать артериальное давление с помощью лекарств, диеты и физических упражнений. Поддержание вашего кровяного давления в безопасном диапазоне снижает риск сердечных заболеваний и инсульта.
- Дыхательная поддержка: Младенцам с недоразвитыми легкими и проблемами с дыханием может потребоваться искусственная вентиляция легких.
- Диализ: Если у вас почечная недостаточность, вам может потребоваться диализ (процедура очистки крови). Гемодиализ использует машину для фильтрации крови вне тела. Перитонеальный диализ использует подкладку живота и специальную жидкость для фильтрации крови.
- Ростовая терапия: Младенцам с недостаточным весом или недоразвитию может потребоваться помощь в росте. Врач может порекомендовать диетическое питание или гормон роста человека.
- Пересадка почки: Пересадка почки может потребоваться, если ADPKD прогрессирует до терминальной стадии почечной недостаточности.Трансплантация — это операция по замене поврежденной почки донорской почкой.
- Обезболивание: Медицина может контролировать боль, вызванную инфекциями, камнями в почках или лопнувшими кистами. Ваш лечащий врач должен одобрить все принимаемые вами обезболивающие. Некоторые лекарства могут усугубить поражение почек.
Профилактика
Можно ли предотвратить поликистоз почек?
Поликистоз почек не поддается профилактике. Но вы можете замедлить развитие болезни или предотвратить почечную недостаточность, придерживаясь здорового образа жизни.
Перспективы / Прогноз
Каковы перспективы для человека с ДОК?
Люди с управляемым ADPKD могут вести полноценную жизнь. Примерно половине людей с ADKPD потребуется диализ или трансплантация почки из-за почечной недостаточности к 70 годам.
Перспективы для детей с АРПКБ не столь позитивны. Около трети всех младенцев, рожденных с ARPKD, не выживают. Выжившие младенцы, вероятно, будут нуждаться в лечении до конца своей жизни.
Жить с
Что я могу сделать, чтобы облегчить жизнь с ДОК?
Сохраняйте здоровье и предотвращайте осложнения по:
- Правильное питание.
- Тренировка.
- Похудение.
- Управление артериальным давлением.
- Бросить курить.
- Снижение стресса.
Когда мне следует позвонить врачу по поводу PKD?
Немедленно обратитесь к поставщику медицинских услуг, если у вас есть ДОК, а ваш номер:
- Запутался.
- Развитие опухших ног, лодыжек или ступней.
- Боль в груди.
- Одышка.
- Невозможно помочиться.
Записка из клиники Кливленда
Поликистоз почек (PKD) является генетическим и вызывает образование кист в почках.Кисты могут увеличивать почки и нарушать функцию почек. Большинство людей с ДОК — взрослые. Но в редких случаях у младенцев может быть опасная форма PKD. Лечение уменьшает симптомы и улучшает работу почек. Большинству людей с PKD потребуется диализ или трансплантация почки.
Визуализация при кистозной болезни почек
Термин «кистозные почки» используется для описания гетерогенной группы состояний, характеризующихся либо одиночными / множественными кистами, либо аномальными почками без очевидных кист, поскольку почка может казаться гиперэхогенной (твердой).Возникла путаница, потому что терминология временами бывает неточной, а множественные кисты не обязательно обозначают наследственное состояние или конкретный синдром. Заболевания охватывают все возрасты в детстве, и с момента введения рутинного дородового ультразвукового исследования многие из них выявляются антенатально.
Окончательный диагноз многих «кистозных почек» требует клинической, генетической, радиологической и патологической информации. Ошибки возникают при сборе и сопоставлении недостаточной информации. Точный диагноз важен для прогноза, лечения и генетического консультирования, хотя при предъявлении диагноза это может быть невозможно.1-3 Поскольку этиология, гистология и клинические проявления разнообразны, единой классификации «кистозной болезни почек» не существует; наиболее приемлемая классификация — генетическая и негенетическая (см. таблицу 1). Однако морфологическая классификация «кистозных почек» остается полезной для негенетических заболеваний. Классификация «кистозных почек» конкретного ребенка требует информации о любом соответствующем семейном анамнезе; родство родителей; соответствующая гистопатология, если таковая имеется, и ультразвуковое исследование родителей, братьев и сестер.Важны полная клиническая оценка, доказательства синдрома или дисморфических особенностей, оценка функции почек и любые результаты дородового ультразвукового исследования. Возникают внепочечные проявления и обязательно ультразвуковое исследование печени, поджелудочной железы и селезенки.
Таблица 1Классификация кистозной болезни почек
Ультразвук
Ультразвук является краеугольным камнем визуализации, и последовательные исследования описали естественное течение многих из этих заболеваний (см. Таблицу 2).Иногда для диагностики достаточно одного УЗИ, например, поликистоз почки; однако другие условия требуют интеграции многих методов визуализации при рассмотрении определенных условий.
Таблица 2Естественный анамнез кистозной болезни почек
Ультразвук определит, является ли аномалия односторонней или двусторонней; симметричный или асимметричный; размер почек; и наличие или отсутствие расширения собирающей системы. Необходимо указать точное расположение в почке, размер и количество кист; эхогенность коры необходимо сравнивать как с мозговым веществом, так и с печенью / селезенкой.По мере совершенствования ультразвукового оборудования анатомические детали коры почек стали лучше, и теперь стало возможным обнаруживать трансзвуковые поражения 1-2 мм, которые, вероятно, представляют собой крошечные кисты. Ожидается, что УЗИ позволит установить конкретный диагноз, но УЗИ почек не может различить определенные состояния, например, аутосомно-доминантную поликистозную болезнь почек (АДПБП) и туберозный склероз у маленьких детей. Кроме того, обычно требуется другая визуализация для поиска связанных аномалий, например кистозной дисплазии и пузырно-мочеточникового рефлюкса; вовлечение других систем, например, печени в болезнь Кароли и аутосомно-рецессивную поликистозную болезнь почек (ARPKD).
Негенетическая «кистозная почка»
Номенклатура сбивает с толку; «Кисты» могут быть обнаружены, но кисты могут быть просто частью другого состояния, однако они должны быть включены в дифференциальный диагноз «кистозная болезнь почек».
ДИСПЛАЗИЯ / КИСТИЧЕСКАЯ ДИСПЛАЗИЯ
Дисплазия почек — это аберрация метанефротического развития, при которой изменяется структура почек и нарушается дифференцировка клубочков и протоков. Сохраняется «фетальная» ткань почек в виде гнезд из метапластических хрящей, связанных с примитивными протоками.Патологически кистозная болезнь почек и дисплазия почек — две разные сущности. Это верно даже при том, что диспластические почки часто бывают кистозными, а при многих типах кистозных почек наблюдается некоторая дисплазия. Однако этот термин используется без гистологического подтверждения со стороны клинициста. Состояние может быть односторонним или двусторонним; при двусторонней почечной недостаточности у ребенка рано или поздно наступит почечная недостаточность, но конечная стадия почечной недостаточности варьирует и может проявиться только в более позднем возрасте. Все диспластические почки функционируют, хотя и плохо.5
Визуализация
Почечный ультразвуковой вид показывает небольшую почку (менее 3-го центиля для возраста) с яркой эхонефрограммой и потерей кортикомедуллярной дифференцировки. Кисты различаются по размеру и количеству, но обычно меньше 1 см. Иногда на ультразвуковом изображении преобладают эти маленькие кисты, обычно подкорковые по своему положению, даже если почка остается маленькой (рис. 1). Дилатация редко выявляется на УЗИ, если только она не связана с обструкцией, как при задних клапанах уретры (PUV) или пузырно-мочеточниковом рефлюксе 4–5 степени (VUR).
Рисунок 1Кистозная диспластическая почка. Продольное ультразвуковое исследование новорожденного мужского пола. Правая почка небольшая, гиперэхогенная, с потерей нормальной кортикомедуллярной дифференцировки и содержит множество мелких кист. Левая почка имела аналогичный вид. Мочевой пузырь был толстостенным, и у младенца были задние уретральные клапаны.
Радиологическое контрастное исследование — Наблюдается повышенная частота ПМР. Когда чашечки контрастно очерчены либо на цистограмме мочеиспускания (MCU) (рис. 2), либо на внутривенной урографии (IVU), их немного, и они показывают потерю сводов с притуплением; при рефлюксе почечная лоханка может быть расширена и скорее перпендикулярна, а мочеточник извит и расширен.
Рисунок 2Кистозная диспластическая почка. Цистоуретрограмма при мочеиспускании у младенца с диспластическими почками на УЗИ, показывающая пузырно-мочеточниковый рефлюкс в извитые мочеточники и аномальные чашечки с паренхиматозным наполнением и румянцем.
Радиоизотоп — сканирование с использованием DMSA технеция-99m показывает снижение функции при одностороннем или плохую визуализацию почек при двустороннем сканировании. Нормальные холодные пирамиды не видны, и часто наблюдаются очаговые дефекты почек, которые нельзя отличить от рубца, вторичного по отношению к инфекции мочевыводящих путей (ИМП).Эти очаговые дефекты наблюдаются у детей с дисплазией, у которых никогда не было ИМП.
Дисплазия может наблюдаться в связи с пороками развития почек, например, верхней частью дуплекса (рис. 3), задними уретерными клапанами, перекрещенной слитной почечной эктопией, подковообразной почкой или тазовой почкой. При многих синдромах и генетических нарушениях поражаются почки с кистами или без них; к ним относятся синдром Беквита – Вейдемана, синдром Лоуренса – Муна – Бейделя, синдром Опица – Леми, отобрахиально-цифровой синдром, синдром Меккеля и синдром Зеллвегера.5
Рисунок 3Диспластический верхний отдел дуплексной почки. Продольное ультразвуковое исследование правой почки. В верхнем полюсе небольшие подкорковые кисты (стрелка). Коллекторную систему нижнего полюса можно увидеть ниже (открытая стрелка).
МУЛЬТИКИСТИЧЕСКАЯ ПОЧКА (МУЛЬТИКИСТИЧЕСКАЯ ДИСПЛАСТИЧЕСКАЯ ПОЧКА)
Мультикистозная почка или мультикистозная диспластическая почка (MDK) вызывает путаницу с диспластической / кистозной диспластической почкой, как описано выше. При MDK наблюдается потеря дольчатой организации, хотя могут быть идентифицированы небольшие островки почечной ткани.Присутствуют примитивные хрящи и протоки, что указывает на аберрацию почечной дифференцировки, признак дисплазии. Некоторые считают, что MDK и кистозная дисплазия являются концами одного и того же спектра; однако все MDK не функционируют и имеют атретический мочеточник. Существуют противоречивые данные о частоте ПМР.
Антенатальное ультразвуковое исследование является наиболее частым проявлением. MDK чаще встречается у мужчин и имеет естественную историю инволюции. Есть несколько сообщений о случаях гипертонии или злокачественных новообразований, но эта связь не является общепринятой.Важные сопутствующие аномалии (30%) включают обструкцию лоханочно-мочеточникового перехода (PUJ), стеноз мочеточника противоположной почки и ПМР.
Визуализация
Ультразвуковые изображения варьируются от небольшой одиночной кисты до множественных кист разного размера с большой доминирующей кистой, расположенной на периферии без идентифицируемой почечной паренхимы (рис. 4). Последовательное ультразвуковое исследование показывает, что большинство МДК разворачивается, некоторые — во время внутриутробной жизни. Некоторые MDK прогрессивно увеличиваются, как правило, у тех, кто при рождении превышает 5–6 см.Иногда УЗИ может не отличить MDK от PUJ. В таких обстоятельствах рекомендуется изотопное исследование с использованием 99m Tc DMSA или MAG3. Если функция обнаружена, хотя и очень плохая, значит, вы имеете дело с PUJ; если нет функции, тогда нет смысла в процедуре дренирования, так как полностью нефункционирующая почка с PUJ никогда не функционирует после дренирования; тогда как плохо функционирующая почка с PUJ может выздороветь после дренирования. В редких случаях при проколе кисты с введением контраста можно отличить MDK от PUJ.
Рисунок 4Мультикистозная почка. Продольное ультразвуковое исследование правой поликистозной почки, показывающее классический вид множественных кист разного размера с очень небольшой окружающей паренхимой, занимающей всю правую почку.
На 99m Tc MAG3 изучает нет функции MDK; противоположная почка требует оценки для адекватного дренажа. Есть дебаты о необходимости MCU, если ультразвуковое сканирование мочевого пузыря в норме.
ПРОСТЫЕ КИСТЫ
Простые кисты у детей встречаются редко и обычно обнаруживаются случайно.В самой большой серии педиатрических ультразвуковых исследований (16 102 случая) кисты были обнаружены в 0,22% случаев. 6 Это не было связано с возрастом. Диагноз простой кисты почек следует исключать, особенно если поражен верхний полюс, когда следует подозревать дуплексную почку, кисту чашечки или часть другого «кистозного заболевания». Ультразвук не может отличить простую кисту от другой патологии; для этого требуется ВВУ или магнитно-резонансная урография. Рекомендуется повторное ультразвуковое исследование в подростковом возрасте, чтобы определить, развиваются ли другие кисты.
CALYCEAL CYSTS
Это не истинное «кистозное» состояние, а скорее наблюдение, сделанное на УЗИ и подтвержденное на ВВУ. Важность кисты чашечки чашечки заключается в возможности образования камня внутри или в теоретическом существовании туберкулеза как причины. В контексте кистозного заболевания это необходимо идентифицировать как отдельное.
МНОГОКУЛЯРНАЯ КИСТА / МНОГОКУЛЯРНАЯ КИСТИЧЕСКАЯ ОПУХОЛЯ ВИЛМА
Мультилокулярная кистозная нефрома — это редкое кистозное образование почек, возникающее из метанефической бластемы, наблюдаемое у детей.Гистология варьирует от полностью доброкачественной (мультилокулярная киста почек) до злокачественной (мультилокулярная кистозная опухоль Вильмса). Клинически у ребенка может наблюдаться образование в брюшной полости. Ультразвук показывает многоячеистую почечную массу с множественными кистами и перегородками, которая не работает на изотопе. Отличительным признаком является наличие капсулы вокруг кисты.7 Всем этим детям следует проводить компьютерную томографию (КТ) или магнитно-резонансную томографию (МРТ).
ЛОКАЛИЗОВАННАЯ ЦИСТИЧЕСКАЯ БОЛЕЗНЬ ПОЧКИ
Это недавно выявленное заболевание генетически, радиологически и морфологически отличается от аутосомно-доминантной поликистозной болезни почек (ADPKD).Пораженный сегмент увеличен и содержит несколько небольших кист, которые сливаются с нормальной паренхимой почек без резкой границы. При визуализации или гистологии окружающей капсулы нет. Это состояние отличается от ADPKD, поскольку оно локализуется в одной части одной почки. У некоторых из ранее описанных пациентов с односторонним ADPKD почти наверняка было это состояние. Клинически поражения не прогрессируют в нескольких зарегистрированных случаях; так как естественное течение болезни неясно, необходимо обследовать почку.Сообщалось о гипертонии.
МЕДУЛЛЯРНАЯ ГУБЧАТАЯ ПОЧКА
Губчатая медуллярная почка описывает внешний вид на ВВУ, при котором расширение собирающих протоков вызывает медуллярный покраснение в сочетании с камнями. Это может быть очаговое или генерализованное, и почка может быть увеличена; его редко можно увидеть в детстве. На IVU видимый румянец связан с чашечками, что наблюдается при ARPKD. Для описания этих изменений используется термин почечная канальцевая эктазия.
ПРИОБРЕТЕННАЯ КИСТИЧЕСКАЯ ПОЧКА
Кистозная почечная недостаточность отсутствует, другие органы не вовлечены.У детей с хронической почечной недостаточностью могут развиваться кисты; частота увеличивается с увеличением продолжительности диализа, и при диализе более 10 лет развиваются до 90% кист. После трансплантации кисты имеют тенденцию уменьшаться в размерах. Осложнения включают риск почечно-клеточного рака или кровотечения. Ультразвук подходит для диагностики и наблюдения.
Генетическая кистозная болезнь
Хотя ее удобно разделить на доминантную, рецессивную и кисты, связанные с синдромами, визуализация является более сложной.Подобные особенности изображения можно увидеть более чем в одном состоянии, и, кроме того, внешний вид может измениться со временем; эти два фактора подчеркивают необходимость комплексной визуализации как при презентации, так и при последующих действиях. Нельзя полагаться только на УЗИ при диагностике.
АВТОСОМНАЯ ДОМИНАНТНАЯ ПОЛИКИСТИЧЕСКАЯ БОЛЕЗНЬ ПОЧЕК
ADPKD характеризуется как почечными, так и внепочечными проявлениями. Обычно он проявляется после третьего десятилетия жизни, но регистрируется в детстве.Степень тяжести заболевания почек при обнаружении в младенческом или дородовом периоде может быть разной.9 Предполагаемая распространенность составляет не менее 1/1000. Были идентифицированы два и, возможно, три генетических локуса. В 90% семей ген находится на коротком плече хромосомы 16 (PKD1) 10; второй ген находится на хромосоме 4 (PKD2). Происходит спонтанная мутация, которая объясняет отсутствие семейного анамнеза. В семьях PKD1 у 64% пораженных детей в возрасте до 10 лет будут кисты; к 19 годам эта цифра возрастает до 90%.11 В детстве внепочечные проявления редки, но включают кисты в печени, поджелудочной железе или селезенке, 12 , 13 и субарахноидальное кровоизлияние, вызванное внутричерепной аневризмой. Врожденный фиброз печени обычно связан с ARPKD, но сообщается в связи с ADPKD.14
Ультразвук
Пренатальное ультразвуковое исследование может показать большие гиперэхогенные почки (рис. 5), но не является специфическим (см. ARPKD для дифференциальной диагностики). Это наблюдение неожиданно и привело к некоторой путанице.В младенчестве ультразвуковые признаки варьируются от нормальных до нескольких изолированных кист до почки, заполненной кистами. Чем больше кист, тем крупнее почки. Кисты обычно разбросаны как по коре, так и по мозговому веществу. Часто наблюдается неравномерное поражение почек, и промежуточная почечная ткань кажется нормальной. При обнаружении у детей (особенно очень маленьких) без семейного анамнеза необходимо учитывать диагноз туберозного склероза (СК).
Рис. 5Ультразвуковое исследование обеих почек, сделанное антенатально.Обе почки (отмечены знаком × и +) в целом гиперэхогенные и большие. Ультразвук чувствителен к обнаружению «светлых» почек, но не специфичен.
Внутривенная урография
Когда кисты видны на УЗИ, ВВУ покажет сдавление и смещение чашечек (рис. 6А), а контуры почек потеряны. Качество ВВУ обычно низкое из-за множества кист и проводится нечасто.
Рисунок 6(A) ADPKD. Внутривенная урограмма ребенку с АДПБП.Правая почка большая, а левая кажется нормальной, что свидетельствует об асимметричном характере заболевания. Чашечки справа смещены вокруг внутрипочечных кист. (B) 99m Tc DMSA сканирование того же пациента, показывающее нормальную левую почку. Справа имеется небольшое количество функционирующей паренхимы почек вокруг нефункционирующих кист почек.
Radionuclide
A 99m Tc DMSA сканирование даст информацию о дифференциальной функции и покажет области с дефицитом фотонов, занятые кистами с поглощением в промежуточной сжатой нормальной паренхиме (рис. 6B).
ТУБЕРОЗНЫЙ СКЛЕРОЗ
Туберозный склероз (TS) — это аутосомно-доминантное заболевание с зарегистрированной распространенностью 1 на 10 000 и характеризующееся множественными гамартомами в головном мозге, коже, сердце, почках, печени, легких и костях. Генетическая связь была установлена с хромосомами 9 и 16; последний расположен в том же районе, что и ген ADPKD1. Частота почечных проявлений колеблется от 47% до 73%. Ангиомиолипомы обнаруживаются у пожилых пациентов по мере их развития и роста в подростковом возрасте.Они могут возникать с кистами или без них. Кисты почек встречаются реже (18–53%) и у более молодых пациентов. В настоящее время никакие методы визуализации не могут отличить кисты TS почек от ADPKD (рис. 7). Эхокардиография и КТ / МРТ черепа должны быть частью рутинной диагностической работы. 15
Рисунок 7Туберозный склероз. Продольная и поперечная сонограмма правой почки. На УЗИ левая почка была похожа. На сонограмме видны множественные кисты разного размера, разбросанные по паренхиме почки.У матери этого ребенка были почки, которые выглядели очень похожими, и первоначально считалось, что у нее ADPKD, пока диагноз не стал очевидным с другими клиническими проявлениями туберозного склероза.
Ультразвук
Почки имеют два вида: множественные кисты или множественные маленькие округлые эхогенные очаги по всей паренхиме от ангиомиолипом. Иногда кисты и ангиомиолипомы могут сосуществовать, создавая смешанный вид. Редким осложнением может быть кровотечение.В более позднем возрасте встречается более высокая частота почечно-клеточного рака.
АУТОСОМНОЕ РЕЦЕССИВНОЕ ПОЛИКИСТИЧЕСКОЕ ЗАБОЛЕВАНИЕ ПОЧЕК
Это редкое генетическое заболевание с частотой примерно 1 из 55 000. Наследование рецессивное; ген находится на хромосоме 6. У всех детей поражены печень и почек. К тому времени, когда они достигнут позднего подросткового возраста, печень покажет фиброз печени у всех детей; может также наблюдаться застой желчных путей с изменениями, аналогичными тем, которые наблюдаются при болезни Кароли.Спленомегалия является результатом портальной гипертензии, вторичной по отношению к фиброзу печени. Дети с менее тяжелым поражением могут появиться в детстве или даже в подростковом возрасте.
Ультразвук
Пренатальный диагноз ставится уже на 14–17 неделе беременности. Появление двусторонних эхогенных почек во время плода не является специфическим для АРПКБП. Дифференциальный диагноз эхогенных почек, выявленных антенатально, включает ARPKD, ADPKD, дисплазию, синдромы пороков развития, связанные с дисплазией, и гломеруло-кистозную болезнь почек.
В раннем младенчестве обе почки одинаково задействованы и увеличены (> 95-го центиля). По мере роста ребенка почки «кажутся» менее увеличенными. Обычно имеется гиперэхогенная кора и мозговой слой; вариации включают в себя то, что мозговое вещество светлее коры. С помощью высокочастотных ультразвуковых датчиков можно обнаружить небольшие (1-2 мм) кисты в мозговом веществе (рис. 8A). Иногда могут обнаруживаться кисты размером более 2 см, особенно по мере роста ребенка. Есть хорошо описанные случаи, когда визуализация «характерна» для ARPKD в младенчестве, но к 5 годам визуализация сильно напоминает ADPKD.
Рисунок 8(A) ARPKD — ультразвуковое сканирование. Продольная сонограмма правой почки в положении лежа на спине. Это показывает значительно увеличенную почку (между + и +) с глобальной эхогенной эхонефрограммой. На мозговом веществе видны несколько эхогенных очагов (стрелка), которые представляют собой акустическое усиление за небольшими мозговыми кистами. (B) ARPKD — внутривенная урограмма. Две значительно увеличенные почки с типичным полосатым лучистым рисунком выделения контрастного вещества. (C) ARPKD — ультразвуковое исследование и сканирование 99m Tc DMSA.Левое изображение показывает типичную большую гиперэхогенную почку ARPKD. Правое изображение показывает сканирование 99m Tc DMSA того же пациента, показывая фокальные дефекты в основном в полярных областях почек. Дефекты не связаны с большими кистами, что видно на УЗИ. Этот ребенок не болел инфекциями мочевыводящих путей. (D) ARPKD — ультразвуковое исследование печени. Это продольное сканирование печени ребенка на (A) показывает множественные кистозные расширения желчных протоков в печени.Желчный пузырь обозначен стрелкой. (E) ARPKD — УЗИ печени и сканирование Hida. Левое изображение представляет собой продольное сканирование печени, показывающее «кисту» высоко в правой доле печени. Правое изображение — сканирование Хида того же пациента. Хида — радиофармпрепарат, который выделяется с желчью. На изображении показано скопление метки внутри «кисты», видимой на УЗИ (стрелка). Обратите внимание также на большую левую долю печени.
У большинства пораженных детей гепатоспленомегалия в той или иной степени развивается по мере взросления.Спектр печеночных аномалий может быть незаметен на УЗИ. У маленьких детей печень может быть нормальной или увеличенной с повышенной эхогенностью в перипортальной области из-за разрастания желчных протоков и фиброза. Могут присутствовать одиночные или множественные кисты, сообщающиеся и тесно связанные с билиарным деревом, вместе с билиарной эктазией. Крупная селезенка и признаки портальной гипертензии и варикозного расширения вен могут быть показаны при ультразвуковом и допплеровском обследовании.
Внутривенная урография
ВВУ по-прежнему считается обязательным для подтверждения диагноза АРПКБ.Это покажет двустороннее и симметричное увеличение почек и полосатую нефрограмму по мере исчезновения контраста в эктатических собирательных протоках. Для этого могут потребоваться отложенные изображения до 24 часов. ВВУ следует проводить в возрасте 3–6 месяцев, так как незрелость почек с или без сопутствующей почечной недостаточности до этого возраста может привести к невозможности визуализации почек (рис. 8B). Однако у младенцев с ADPKD, у которых в неонатальном периоде имеются большие гиперэхогенные почки, может наблюдаться «лужица» контраста, позволяющая отличить ARPKD от ARPKD.18
Радиоизотопы
Почечные
99m Tc DMSA исследования в ARPKD показывают неоднородное поглощение изотопа, особенно на полюсах. Отмеченные дефекты относительно большие и не связаны с какими-либо очаговыми аномалиями, наблюдаемыми на УЗИ. Эти изменения наблюдались у всех воспитанников этого учреждения. Изменения в 99m Tc DMSA не являются специфическими; однако в этой клинической обстановке без истории ИМП эти дефекты специфичны для ARPKD (рис. 8C).
Печень — 99m Tc HIDA — это гепатобилиарный агент, который после поглощения гепатоцитами секретируется с желчью.После 1 года сканирование 99m Tc HIDA показывает увеличенную левую долю печени с отсроченным прохождением изотопа через печень, иногда с областями скопления и выступа в системе протоков, даже когда УЗИ не показывает расширение желчные протоки (рис. 8D). Это представляет собой ценный неинвазивный метод для демонстрации субклинической билиарной эктазии, которая неизменно при АРПБП. Этот вид был описан при болезни Кароли (рис. 8E).
ЮВЕНИЛЬНЫЙ НЕФРОНОФТИЗ
Ювенильный нефронофтиз имеет аутосомно-рецессивную наследственность и в детстве проявляется как хроническая почечная недостаточность.Он характеризуется ранним дефектом концентрации, полиурией, полидипсией с задержкой роста и анемией.
МЕДуллярная цистическая болезнь
Медуллярная кистозная болезнь имеет аутосомно-доминантное наследование и проявляется до четвертого десятилетия жизни.
Визуализация при ювенильном нефронофтисе и кистозно-мозговом заболевании
Поскольку ультразвуковые изображения похожи, они будут описаны вместе. Ультразвук выявит две почки нормального размера с глобально гиперэхогенным внешним видом.Кисты не проявляются на поздних стадиях заболевания и обычно бывают кортикомедуллярными. ВВУ мало помогает из-за очень слабого помутнения почек. На ранних стадиях заболевания, когда канальцы поражены в большей степени, чем клубочки, сканирование 99m Tc DMSA может не показать почки, но сканирование 99m Tc DTPA (клубочковый агент) может почти обычный.
Экстраренальные проявления, о которых сообщалось при ювенильном нефронофтисе, включают аномалии скелета, врожденный фиброз печени и умственную отсталость.
Заключение
Кистозная болезнь почек — это широкий спектр заболеваний; визуализация формирует решающий аспект в оценке ребенка. Первичный метод визуализации — УЗИ. Однако почти во всех случаях требуется другая визуализация, чтобы гарантировать, что предлагаемый диагноз или дифференциальный диагноз является как можно более точным при обращении. Наблюдение за этими детьми имеет важное значение и включает визуализацию. Скрининг членов семьи с помощью УЗИ — полезная процедура, и ее можно проводить в соответствующих семьях.Каждый пациент уникален; визуализация должна быть исчерпывающей, а сопоставление всей информации имеет важное значение, чтобы иметь наилучшие шансы на постановку диагноза.
Визуализация плода позволяет поставить диагноз матери: аутосомно-доминантная поликистозная болезнь почек
С частотой от 1/500 до 1/1000 живорождений ADPKD является наиболее распространенным летальным заболеванием с доминантной наследственностью. 4 Существует большая межсемейная и внутрисемейная изменчивость с ADPKD, при этом признаки и симптомы заболевания обычно не проявляются до более позднего возраста. 2 Отсутствие известного семейного анамнеза у многих пораженных людей, продемонстрированное описанными здесь случаями, указывает на возможное легкое течение болезни.
Таким образом, многие люди не знают, что они или их дети могут быть затронуты или подвержены риску. В многоцентровой серии из 27 случаев 59% пациентов не знали, что они носители ADPKD до УЗИ плода. 5 Поскольку пренатальное ультразвуковое исследование стало стандартом лечения, все чаще выявляются возможные случаи АДПБП плода. 4 УЗИ плода, указывающие на ADPKD, представляют собой увеличенные гиперэхогенные почки с нормальным объемом околоплодных вод. Кисты почек встречаются в меньшинстве случаев у плода. 3, 5 Главный дифференциальный диагноз — аутосомно-рецессивная поликистозная болезнь почек (ARPKD) и ADPKD. При доминирующей форме почки плода умеренно увеличены, обычно на 1,5-2 раза в день. выше среднего 5 по сравнению с гораздо большим увеличением почек при ARPKD (на 4-6 s.d. выше среднего). Кисты почек плода и уменьшение количества околоплодных вод чаще связаны с АРПБП. 6 У взрослых с ADPKD результаты УЗИ почек включают нормальную эхогенность, увеличенные дискретные кисты и общее увеличение. 3 При известном семейном анамнезе ADPKD две или более почечных кист у пациентов моложе 30 лет или две кисты в каждой почке у пациентов старше 30 лет считаются диагностическими. 2 Нефромегалия наблюдается у всех пациентов и может быть причиной острой и хронической боли, которую испытывают некоторые пациенты. Гипертония может развиваться у 30% детей и до 60% взрослых до почечной недостаточности. 1
У женщин с ADPKD и нормальной функцией почек обычно протекает неосложненная беременность. И наоборот, женщины с нарушенной функцией почек до беременности нуждаются в тщательном наблюдении за гипертонией и преэклампсией. 7 Беременность может влиять на функцию почек у пациентов с ADPKD, поскольку некоторые данные предполагают, что три или более беременностей были связаны с более ранним возрастом начала почечной недостаточности. 1 До 50% пациентов с ADPKD имеют кисты печени с возрастной заболеваемостью.На кисты печени могут влиять женские стероидные гормоны; они чаще встречаются у повторнородящих женщин и часто больше у повторнородящих женщин или у тех, кто принимал оральные противозачаточные таблетки. 2 Внутричерепные аневризмы также могут возникать при ADPKD с частотой от 0 до 41%, и некоторые акушеры рассматривают возможность визуализации головного мозга, чтобы исключить церебральные аневризмы перед родами. 1
Таким образом, диагноз ADPKD всегда следует рассматривать при обнаружении эхогенных увеличенных почек при УЗИ плода, даже если мать не сообщает об отсутствии болезни в анамнезе.Мы представляем эти случаи как важное напоминание о том, что беременность может служить важной возможностью для выявления этого заболевания как для матери, так и для ребенка.
Сравнение ультразвуковой и магнитно-резонансной томографии показывает, что длина почки позволяет прогнозировать хроническое заболевание почек при аутосомно-доминантной поликистозной болезни почек
https://doi.org/10.1038/ki.2015.71 Получить права и содержаниеАутосомно-доминантная поликистозная болезнь почек (ADPKD) ) характеризуется постепенным увеличением кисты и почек и, в конечном итоге, почечной недостаточностью.Общий объем почек с поправкой на высоту, основанный на магнитном резонансе (htTKV) более 600 куб. Здесь мы сравнили одновременное ультразвуковое исследование и магнитно-резонансную томографию, чтобы определить, могут ли ультразвуковое исследование и длина почки (KL) предсказывать будущую стадию 3 стадии ХБП в течение более длительных периодов наблюдения. В общей сложности у 241 пациента с ADPKD в возрасте 15–46 лет с клиренсом креатинина 70 мл / мин и выше был проведен клиренс иоталамата, магнитно-резонансная и ультразвуковая оценки.Участники прошли в среднем пять повторных измерений клиренса в течение среднего периода наблюдения 9,3 года. TKV и KL на основе ультразвука и магнитного резонанса сравнивались с использованием графиков Бланда – Альтмана и внутриклассовых корреляций. Каждый показатель был протестирован для прогнозирования будущей стадии ХБП 3. Относительно сильные внутриклассовые корреляции между ультразвуком и магнитным резонансом были обнаружены как для htTKV, так и для KL (0,81 и 0,85 соответственно). HtTKV и KL на основе УЗИ и магнитного резонанса предсказывают будущую стадию 3 ХБП аналогичным образом (AUC 0.87, 0,88, 0,87 и 0,88 соответственно). Ультразвуковая длина почки более 16,5 см и htTKV более 650 мл / мин имели наилучшую точку отсечения для прогнозирования развития ХБП 3 стадии. Таким образом, одной длины почки достаточно, чтобы стратифицировать риск прогрессирования почечной недостаточности на ранней стадии АДПБП с использованием любого ультразвукового исследования.


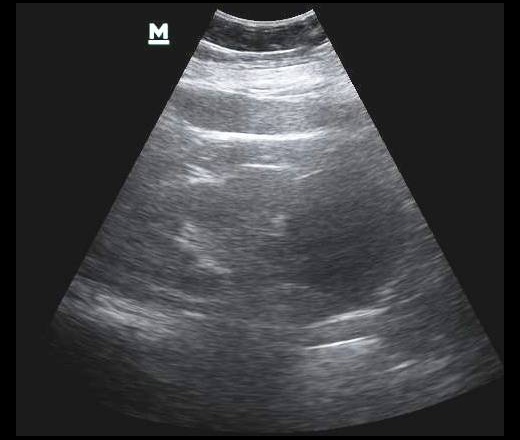
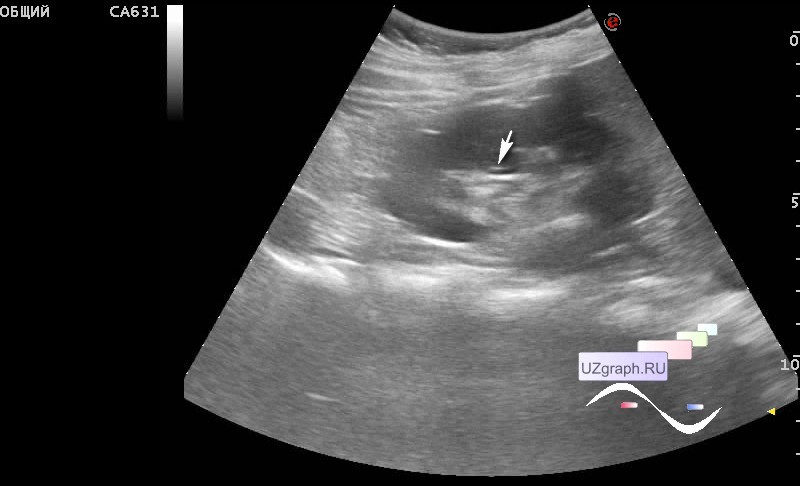 Это поможет удалить газы из брюшной полости, которые являются акустическим барьером при использовании ультразвука.
Это поможет удалить газы из брюшной полости, которые являются акустическим барьером при использовании ультразвука.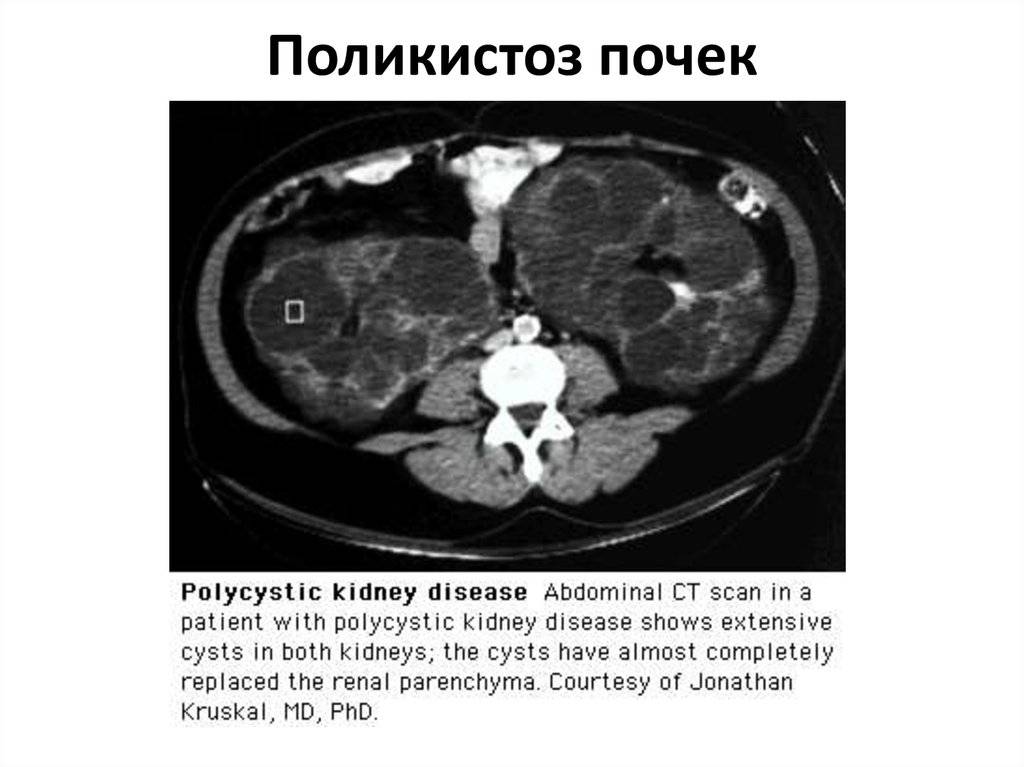 Мы подходим комплексно к диагностике и лечению поликистоза почек, чтобы вернуть пациентам комфорт здоровой жизни. Лечение включает подбор медикаментов, составление диеты и назначение физиотерапии при необходимости.
Мы подходим комплексно к диагностике и лечению поликистоза почек, чтобы вернуть пациентам комфорт здоровой жизни. Лечение включает подбор медикаментов, составление диеты и назначение физиотерапии при необходимости.