О методах тестирования на коронавирус
Москва сегодня является лидером среди мировых городов по тестированию горожан на выявление коронавирусной инфекции. Для этого в столице используются самые современные методы диагностики: ПЦР и ИФА (ИХЛА).
О ПЦР-диагностике
ПЦР (полимеразная цепная реакция) – метод, который позволяет выявить присутствие вируса в организме. Для исследования берется мазок из носа и ротоглотки.
Такое тестирование проводится всем жителям с симптомами ОРВИ, пациентам с пневмонией, проживающим с людьми, у которых уже был подтвержден диагноз «коронавирусная инфекция», а также всем пациентам некоронавирусных стационаров Москвы.
Анализ может быть взят врачом поликлиники на дому, в амбулаторном КТ центре или в стационаре.
Всего на сегодняшний день в Москве сделано  ПЦР-тестов.
ПЦР-тестов.
Согласно требованиям Роспотребнадзора, если у пациента выявлен коронавирус, для выписки и подтверждения выздоровления необходимо два отрицательных результата.
В соответствии с указом Мэра Москвы, работодатели обязаны ПЦР методом тестировать на коронавирус не менее 10% сотрудников, физически посещающих предприятия, каждые две недели.
Об ИФА-тестировании
ИФА (ИХЛА) (иммуноферментный и иммунохемилюминесцентный анализ) – это лабораторное исследование по крови из вены, с помощью которого выявляют иммунный ответ к вирусу.
Анализ показывает количество антител IgM и IgG. Иммуноглобулины М говорят об активном иммунном ответе, то есть о том, что человек сейчас болеет коронавирусом. Иммуноглобулины G говорят о том, что человек уже переболел, и у него выработался иммунитет к вирусу.
Всего с начала применения метода ИФА уже проведено более 235 тысяч исследований. Из них более 18 тысяч тестов были сделаны для пациентов нековидных отделений стационаров.
ИФА-исследования проходят:
- все сотрудники медицинских организаций Департамента здравоохранения – еженедельно,
- пациенты стационаров – в день госпитализации,
- пациенты дневных стационаров и КТ-центров – при первом обращении,
- пациенты поликлиник (по направлению врача),
Москва также дополнительно обеспечивает проведение ИФА-тестов пациентам медицинских организаций
С 15 мая на ИФА-тестирование в городские поликлиники приглашаются москвичи в рамках исследования формирования иммунитета к коронавирусу. Массовое ИФА-тестирование позволит выявить три категории людей:
Массовое ИФА-тестирование позволит выявить три категории людей:
- Бессимптомных носителей, у которых болезнь никак не проявляется, но они могут заражать других, не подозревая об этом.
- Пациентов с легкой и средней степенью течения болезни, у которых с момента заражения прошло две недели. За это время коронавирус мог опуститься в легкие, и обычный ПЦР-тест может его не обнаружить.
- Жителей столицы, которые переболели COVID-19 и выработали иммунитет к вирусу.
Пока принять участие в скрининге можно только по приглашению. Участники определяются методом случайной выборки среди всех возрастных групп и городских административных округов. Жителям, выбранным для исследования, приходит смс или e-mail. Тем, у кого подтвержден коронавирус, как и тем, кто болен ОРВИ, такие приглашения не приходят.
В сообщении указана ссылка для онлайн записи в пункт забора крови — запись доступна в течение 3 дней. Возможность сдачи теста всеми желающими в данный момент прорабатывается. Пока отрабатывается логистика и схема работы. Первоначально приглашение было направлено группе из 70 тысяч человек, на сегодняшний день приглашений было отправлено уже порядка 300 тыс.
Возможность сдачи теста всеми желающими в данный момент прорабатывается. Пока отрабатывается логистика и схема работы. Первоначально приглашение было направлено группе из 70 тысяч человек, на сегодняшний день приглашений было отправлено уже порядка 300 тыс.
Пришли и сдали анализ – более 27 тыс. человек,
Во всех 30 поликлиниках, на базе которых проходит тестирование, действуют строгие правила работы. Сдача крови проводится только по предварительной записи, что позволяет избежать очередей в медицинских учреждениях и не допустить распространения коронавирусной инфекции. Перед кабинетами установлены стойки, на которых администраторы печатают направления – это сокращает время ожидания внутри кабинета.
С начала распространения коронавируса в поликлиниках приняты все необходимые меры безопасности: установлены бактерицидные лампы закрытого типа для обеззараживания воздуха, антисептики для рук, не менее двух раз в сутки проводится дезинфекция всех помещений, нанесены отметки для соблюдения 1,5-метровой дистанции, по возможности оборудован отдельный вход для пациентов с признаками ОРВИ.
Также в рамках государственно-частного партнерства
Москва готова будет в ближайшее время в пределах имеющихся мощностей лабораторий предоставить их часть работодателям, которые в инициативном порядке захотят методом ИФА протестировать сотрудников на иммунитет. Работодатели должны будут самостоятельно организовать забор крови и ее доставку в установленный день в одну из лабораторий Департамента здравоохранения города Москвы (заранее определенную для работодателя). Предварительно необходимо будет подключиться к информационной системе «Реестр направлений и учет результатов исследований на COVID-19» для формирования электронных направлений на анализ, поскольку в городе данный процесс автоматизирован. Подробный порядок взаимодействия будет представлен Департаментом здравоохранения в ближайшее время.О совместном применении тестов
Два вида тестов наилучшим образом работают совместно. ПЦР-диагностика позволяет поймать заболевание  При этом ПЦР-тесты имеют немаленький процент ложных результатов при более поздних стадиях заболевания. В то же время ИФА-тестирование может служить как дополнительный инструмент. Такие тесты помогают выявить заболевания, когда с момента заражения уже прошло 2 недели и вирус опустился в легкие. В сочетании с КТ-диагностикой ИФА позволяет быстро определить наличие изменений в легких и применить необходимую терапию.
При этом ПЦР-тесты имеют немаленький процент ложных результатов при более поздних стадиях заболевания. В то же время ИФА-тестирование может служить как дополнительный инструмент. Такие тесты помогают выявить заболевания, когда с момента заражения уже прошло 2 недели и вирус опустился в легкие. В сочетании с КТ-диагностикой ИФА позволяет быстро определить наличие изменений в легких и применить необходимую терапию.
Что такое ПЦР диагностика кошек?
Современная ветеринария активно применяет на практике все передовые научные достижения. Это помогает добиться высоких результатов в диагностике инфекционных заболеваний у животных. Например, сегодня уже просто невозможно обойтись без такого передового метода, как ПЦР (полимеразная цепная реакция). Данная методика позволяет безошибочно выявить возбудителей целого ряда инфекций, которыми страдают кошки. Причем поставить диагноз в большинстве случаев удается на самых ранних этапах патологического процесса.
Зачем проводится такая диагностика
Чтобы понять, чем отличается ПЦР диагностика кошек, надо иметь представление об инфекциях, которые чаще всего поражают этих животных.
Среди всех патологий, вызываемых вирусами, чаще всего ветеринары сталкиваются со следующими болезнями:
- Вирусным иммунодефицитом
- Лейкозом, развитие которого провоцирует вирус
- Инфекционным перитонитом
Эти три заболевания считаются неизлечимыми, и нередко они приводят к смерти животного.
Но благодаря внедрению ПЦР-диагностики многим питомцам удалось продлить жизнь. И даже в случае обнаружения возбудителя одной из этих инфекций при правильной программе лечения животное может вести активный образ жизни, радуя своего владельца.
Что представляет собой данный метод исследования
ПЦР — диагностика является молекулярным методом выявления инфекций. Его специфические особенности позволяют обнаруживать в биологическом материале даже единичных представителей патогенной флоры. Данная методика появилась в конце прошлого века, а точнее — в 1983 году. Ее автор американский химик К. Мюллис за свою разработку был удостоен Нобелевской премии.
Его специфические особенности позволяют обнаруживать в биологическом материале даже единичных представителей патогенной флоры. Данная методика появилась в конце прошлого века, а точнее — в 1983 году. Ее автор американский химик К. Мюллис за свою разработку был удостоен Нобелевской премии.
Анализ ПЦР состоит из трех этапов:
- Сначала обрабатывается материал, подлежащий исследованию
- Затем из него выделяется наследственная основа (РНК, ДНК)
- Последняя фаза заключается в проведении амплификации (умножение выделенных участков ДНК)
Стоит заметить, что достоверный результат можно получить только в том случае, когда материал животного берется при соблюдении всех правил.
Какие материалы берутся на анализ
При проведении ПЦР диагностики кошек можно брать на анализ абсолютно любой материал:
- Каловые массы.
- Мочу.
- Слизистые выделения.
- Фрагменты пораженных органов и прочие биологические субстанции.
 Забор материала производится в специальные контейнеры, а затем направляются в лабораторию на исследование.
Забор материала производится в специальные контейнеры, а затем направляются в лабораторию на исследование.
Когда необходима ПЦР-диагностика
Данный вид исследования сегодня просто незаменим. Его возможности трудно переоценить, особенно в тех случаях, когда речь идет об инфекционном перитоните кошек. Это заболевание считается самым распространенным и коварным. Вот почему диагностика с применением метода ПЦР получила такое широкое распространение в ветеринарной практике. Тест на наличие инфекционных возбудителей этим методом следует проводить всем кошкам, которые регулярно бывают на улице.
Поскольку наша лаборатория располагает всем необходимым для проведения этого высокочувствительного теста, что позволяет проводить качественную диагностику. Если своевременно выявить источник болезни, можно составить адекватную для конкретной кошки программу терапии и профилактические мероприятия.
НПО «Вирион» — Медицинский Диагностический Центр
Подготовка пациента к сдаче крови.
Общие правила подготовки пациентов:
— Кровь забирается строго натощак, до приема и введения лекарственных препаратов и до рентгеновского, эндоскопического и ультразвукового обследования.
· Препараты, способные существенно влиять на результаты исследования, должны быть заранее отменены, кроме случаев контроля за лечением данным препаратом.
— Кровь для исследования на вещества, концентрация которых в крови изменяется циклически, должна забираться в строгом соответствии с физиологическими циклами. Например, концентрация ФСГ и ЛГ определяется на 5-7 день менструального цикла.
Просим соблюдать данные рекомендации для повышения точности исследования. Надеемся, что они помогут Вам правильно подготовится к исследованию и получить надежные результаты.
Ряд анализов делают натощак. Например, биохимические (глюкоза, холестерин ,билирубин и др.) и серологические тесты (сифилис, гепатит В), гормоны (ТТГ, паратгормон) и др. «Натощак» — это когда между последним приемом пищи и взятием крови проходит не менее 4 ч. (желательно — не менее 8 ч.). Сок, чай, кофе, тем более с сахаром, не допускаются. Можно пить воду.
(желательно — не менее 8 ч.). Сок, чай, кофе, тем более с сахаром, не допускаются. Можно пить воду.
Строго натощак (после 12-часового голодания) следует сдавать кровь для определения параметров липидного профиля: холестерин, ЛПВП, ЛПНП, триглицериды.
Содержание многих аналитов в крови подвержено суточным колебаниям, поэтому для ряда исследований кровь следует сдавать строго в определенное время суток. Так, кровь на некоторые гормоны (ТТГ и паратгормон), а также на железо сдают только до 10 утра.
При сдаче венозной крови нужно исключить факторы, влияющие на результаты исследований: физическое напряжение (бег, подъем по лестнице), эмоциональное возбуждение. Поэтому перед процедурой следует отдохнуть 10 — 15 минут, успокоиться.
Кровь на анализ сдают до начала приема лекарственных препаратов (например, антибактериальных и химиотерапевтических) или не ранее чем через 10 — 14 дней после их отмены. Исключение составляют случаи, когда хотят исследовать концентрацию лекарств в крови (например, вальпроевой кислоты, антиконвульсантов). Если вы принимаете лекарства, обязательно предупредите об этом лечащего врача. Для получения корректных результатов необходимо прекратить прием железосодержащих пищевых добавок или лекарственных препаратов или предупредить о приеме препаратов лечащего врача. Если пациенту было проведено переливание крови, исследование необходимо отложить на несколько дней.
Если вы принимаете лекарства, обязательно предупредите об этом лечащего врача. Для получения корректных результатов необходимо прекратить прием железосодержащих пищевых добавок или лекарственных препаратов или предупредить о приеме препаратов лечащего врача. Если пациенту было проведено переливание крови, исследование необходимо отложить на несколько дней.
Кровь не следует сдавать после рентгенографии, ректального исследования или физиотерапевтических процедур.
При гормональных исследованиях у женщин репродуктивного возраста (примерно с 12 — 13 лет и до наступления климактерического периода) на результаты влияют физиологические факторы, связанные со стадией менструального цикла. Поэтому при подготовке к обследованию на гормоны ФСГ, ЛГ, пролактин, эстриол, эстрадиол, прогестерон следует указать фазу цикла. При проведении исследования на половые гормоны строго придерживайтесь рекомендаций вашего лечащего врача о дне менструального цикла, в который необходимо сдать кровь.
При исследовании показателей системы гемостаза (фибриноген, ПТИ, МНО, АЧТВ, волчаночный антикоагулянт) отменить прием гепарина за 2 дня и отменить кумариновые препараты за 2 недели до взятия крови (эти препараты могут давать ложноположительные результаты). Исследование желательно проводить натощак. «Натощак» — это когда между последним приемом пищи и взятием крови проходит 4-8 часов.
Исследование желательно проводить натощак. «Натощак» — это когда между последним приемом пищи и взятием крови проходит 4-8 часов.
При выполнении исследований на наличие инфекций следует учитывать, что в зависимости от периода инфицирования и состояния иммунной системы у любого пациента может быть отрицательный результат. Но тем не менее отрицательный результат полностью не исключает инфекции. В сомнительных случаях рекомендуется провести повторный анализ.
1. Подготовка к забору крови на гормональные исследования.
1.1. ТЗ свободный, ТЗ общий, Т4 (тироксин общий), Т4 свободный, ТТГ.
Уровень этих гормонов необходимо проверять натощак, для исключения нарушения функции щитовидной железы. Сдается в любой день менструального цикла. Непосредственно перед взятием крови пациент должен находиться в состоянии покоя около 30 минут.
За 2 — 3 дня до сбора крови на анализ нужно предотвратить прием йодсодержащих препаратов, йода-131 и технеция-99m. За 1 мес. прекращается прием гормонов щитовидной железы (кроме как по специальным указаниям лечащего эндокринолога). Рекомендуется ограничить физические нагрузки и психоэмоциональный стресс.
Рекомендуется ограничить физические нагрузки и психоэмоциональный стресс.
1.2. Прогестерон.
Анализ проводится на 22 — 23 день менструального цикла, если другие сроки не указаны лечащим врачом. Взятие крови производится утром натощак, т.е. тогда, когда между последним приемом пищи и взятием крови проходит 8 — 12 часов. Можно пить воду. При отсутствии возможности прийти в лабораторию утром, можно выдержать перед забором крови период голодания не менее 6 часов, исключив при утреннем приеме пищи жиры.
1.3. Пролактин.
За 1 день исключить половое сношение и тепловые воздействия (сауну), за 1 час — курение. Т.к. на уровень пролактина большое влияние оказывают стрессовые ситуации, желательно исключить факторы, влияющие на результаты исследований: физическое напряжение (бег, подъем по лестнице), эмоциональное возбуждение. Поэтому перед процедурой следует отдохнуть 10 — 15 минут, успокоиться.
1.4. ЛГ, ФСГ, эстрадиол.
Накануне исследования исключить физические нагрузки (спортивные тренировки) и курение. У женщин репродуктивного возраста (примерно с 12 — 13 лет и до наступления климактерического периода) анализ производится на 6 — 7 день менструального цикла, если другие сроки не указаны лечащим врачом.
У женщин репродуктивного возраста (примерно с 12 — 13 лет и до наступления климактерического периода) анализ производится на 6 — 7 день менструального цикла, если другие сроки не указаны лечащим врачом.
1.5. Свободный тестостерон.
Между последним приемом пищи и взятием крови должно пройти не менее 8 часов (желательно — не менее 12 часов). Сок, чай, кофе (тем более с сахаром) не допускаются. Можно пить воду.
1.6. Соматотропный гормон.
За 3 дня до взятия крови необходимо исключить спортивные тренировки. За 1 час до взятия крови — курение. Исследование проводится натощак (через 12 часов после последнего приема пищи). Пациент должен находиться в полном покое в течение 30 минут перед взятием крови.
1.7. ХГЧ, ДГА-S.
Специальной подготовки к исследованию не требуется.
1.8. ПСА.
Анализ следует проводить до или не ранее чем после 6 — 7 дней после массажа или пальцевого ректального обследования простаты, трансректального УЗИ, биопсии, лазерной терапии, эргометрии, цисто- и колоноскопии, и после любых других механических воздействий на простату. Важно учитывать, что повышение уровня ПСА может быть в течение до 3 недель после биопсии, простатэктомии или массажа простаты. Для исключения ошибок определение свободного и общего иммунореактивного ПСА (с расчетом их соотношения) надо проводить одним методом и из одной пробы крови. Последующий мониторинг желательно проводить с использованием того же метода и желательно в той же лаборатории.
Важно учитывать, что повышение уровня ПСА может быть в течение до 3 недель после биопсии, простатэктомии или массажа простаты. Для исключения ошибок определение свободного и общего иммунореактивного ПСА (с расчетом их соотношения) надо проводить одним методом и из одной пробы крови. Последующий мониторинг желательно проводить с использованием того же метода и желательно в той же лаборатории.
1.9. АКТГ.
Накануне исследования необходимо исключить физические нагрузки (спортивные тренировки) и курение. У женщин анализ производится на 6 — 7 день менструального цикла, если другие сроки не указаны лечащим врачом. Сдавать кровь на анализ предпочтительно рано утром, если нет особых указаний эднокринолога. Дополнительные пробы, взятые поздно вечером, могут быть полезны при диагностике синдрома Кушинга. Для адекватной сравнительной оценки в динамике пробы крови следует брать в одни и те же периоды времени.
1.10. С-пептид.
Между последним приемом пищи и взятием крови проходит не менее 8 часов (желательно — не менее 12 часов). Сок, чай, кофе (тем более с сахаром) не допускаются. Можно пить воду.
Сок, чай, кофе (тем более с сахаром) не допускаются. Можно пить воду.
1.11. 17-ОН-прогестерон.
Подготовка к исследованию — по указаниям лечащего врача (у женщин обычно кровь для исследования берут на 3 — 5 день цикла).
РЕЖИМ РАБОТЫ ПРОЦЕДУРНОГО КАБИНЕТА КДП
1. Общий анализ крови.
Взятие капиллярной крови из пальца производится натощак, в утренние часы в процедурном кабинете с 7-45 до 09-30 с понедельника по субботу.
2. Биохимический анализ крови.
Взятие венозной крови производится натощак, в утренние часы в процедурном кабинете с 7-45 до 09-30 с понедельника по субботу.
3. Иммунограмма.
Взятие венозной крови производится строго натощак, в утренние часы в процедурном кабинете с 7-45 до 10-00 понедельник, вторник, среда.
4. Подготовка к ИФА-исследованиям крови.
Взятие венозной крови производится натощак, в утренние часы или спустя 4 часа после последнего приема пищи.Часть проб на исследование принимается в определенные дни недели, уточнять следует по телефону 905-898; 905-899.
5. Подготовка к ПЦР-исследованиям крови.
Взятие венозной крови производится в любое время и не зависит от приема пищи.
6. Исследование клеща на наличие клещевых инфекций (клещевой энцефалит, болезнь Лайма эрлихиозы, риккетсиозы)
Клеща берут на исследование в первые сутки после контакта (присасывание, наползание) с человеком. Спустя сутки на исследование принимается только венозная кровь. Клещ пригоден для исследования, если он неповрежден, желательно живой, не обработан бытовыми средствами или любыми химическими веществами.
Для сохранения клеща в живом состоянии до момента доставки в лабораторию необходимо поместить его в чистый флакон, закрытый ватно-марлевой пробкой. Во флакон надо поместить кусочек влажной ваты. Хранить флакон в холодильнике, на дверце или в нижнем ящике холодильника.
7. Рекомендации женщинам по подготовке к сдаче мазка на ПЦР.
· Нельзя сдавать данные исследования в период приема любых антибиотиков.
· Указанные исследования не сдаются в период менструации.
· Накануне визита в клинику (за 2-3 дня) следует прекратить использование любых влагалищных таблеток, шариков, свеч — как лечебных, так и противозачаточных (Фарматекс, Пантекс-Овал, клион Д, Полижинакс и все прочие).
· С утра до взятия мазка не следует подмываться и спринцеваться.
· ВАЖНО! Нельзя брать мазки на ПЦР после проведения кольпоскопических проб.
Забор материала производится в режиме работы врача гинеколога КДП.
8. Материал из цервикального канала, влагалища.
Особой подготовки не требуется.
Забор материала производится в режиме работы врача гинеколога КДП.
9. Материал из уретры на ПЦР.
Перед взятием материала пациенту рекомендуется воздержаться от мочеиспускания в течение 1,5-2 часов. При наличии гнойных выделений соскоб рекомендуется брать через 15-20 мин. после мочеиспускания.
Забор материала производится в режиме работы врача уролога КДП.
10. Секрет предстательной железы.
Особой подготовки не требуется.
Забор материала производится в режиме работы врача уролога КДП.
11. Материал с конъюнктивы глаз, задней стенки глотки.
Особой подготовки не требуется.
Взятие крови из вены у пациентов осуществляется в процедурном кабинете с 7:45 до 19:30часов.
12. Материал из носоглотки.
Взятие мазка проводится натощак или не ранее, чем через 2-4 часа после еды.
Взятие крови из вены у пациентов осуществляется в процедурном кабинете с 7:45 до 19:30часов.
13. Слюна.
За 12 часов до взятия (сбора) слюны исключается прием пищи, алкоголя и лекарственных препаратов. Перед тем, как собрать слюну, необходимо почистить зубы без зубной пасты, затем хорошо прополоскать рот без использования раздражающих средств. Удалить съемные зубные протезы.
ПЦР–диагностика в Кемерово — Консультация, цены
ПЦР–диагностика – современный лабораторный метод, позволяющий с максимальной точностью исследовать и выявить наличие возбудителя инфекций передающихся половым путем по пробе исследуемого материала.
ПЦР (полимеразная цепная реакция) – позволяет выявить ДНК клеток возбудителя инфекции в исследуемом образце, даже если их присутствие в организме минимально.
Для анализа используется различный материал – кровь, мокрота, кал, соскобы слизистых.
Когда стоит сдать анализ
Анализ методом ПЦР назначает лечащий врач при подозрении на определенный вид возбудителя или инфекцию. Качественное исследование дает доктору полную картину, на основании которой назначается эффективное лечение. Количественные пробы покажут активность возбудителя и помогут скорректировать дозировку назначаемого для лечения препарата.
Данный метод широко применяется в гинекологии, урологии и отоларингологии. Если у вас присутствуют следующие симптомы, следует посетить доктора и попросить об анализе методом ПЦР:
- частые тонзиллиты и риниты,
- наружный, острый и хронический отиты неясного генеза,
- не проходящий кандидоз с периодами явного обострения,
- частые циститы и осложнения связанные с ними,
- первичное бесплодие, не отягощенное другими заболеваниями.

Большинство современных докторов назначают данное исследование при малейших подозрениях на возможное присутствие возбудителя и по результатам назначают щадящие комплексное лечение, которое в минимальные сроки помогает пациенту вернуться в полноценному образу жизни, победив недуг.
Какие материалы подходят для ПЦР-диагностики
В зависимости от локации возбудителя для анализа принимается различный материал:
- соскобы со слизистых оболочек,
- моча,
- мокрота,
- кровь, сыворотка и плазма,
- биологические жидкости.
На Covid-19 посевы не осуществляются.
Сдать анализ на Молекулярная диагностика ПЦР в Перми
Молекулярная диагностика методом ПЦР помогает выявить наличие возбудителя инфекционного заболевания, а также определить концентрацию вируса, то есть узнать стадию развития болезни. При проведении исследования копируют фрагменты ДНК и РНК возбудителей заболевания, на основании полученных данных выясняется тип и концентрация бактерии, вируса или паразита в организме.
Главные преимущества ПЦР-анализа:
-
высокая чувствительность — возможность распознать заболевание на ранней стадии;
-
точность — отсутствие ложноположительных и ложноотрицательных результатов;
-
оперативность — простая технология проведения позволяет получить достоверный результат примерно за пять часов;
-
доступность — стоимость диагностики ПЦР часто не превышает цену инфекционных заболеваний методом ИФА.
Что мы предлагаем
В клинике «Философия красоты и здоровья» есть услуга молекулярной диагностики ПЦР в Перми. Современная лаборатория позволяет выполнять ПЦР-диагностику инфекций:
-
мочеполовой системы,
-
ЗППП (соскоб со слизистых),
-
гепатита,
-
герпеса,
-
ВИЧ, острых и скрытых инфекций,
-
туберкулеза,
-
микоплазмоза (ПЦР-исследование мокроты).

Для выявления некоторых инфекций может понадобиться другой биоматериал: биоптата, слюна, суставная, околоплодная, спинномозговая жидкость.
Как подготовиться к сдаче анализа?
Подготовки перед сдачей крови не требуется, достаточно отказаться от алкоголя накануне проведения диагностики и от пищи в день анализа. Об особенностях подготовки к исследованию при взятии другого биоматериала расскажет лечащий врач.
Вы можете обратиться в любой заборный пункт клиники и сдать ПЦР анализ в Перми.
Анализы: ПЦР-диагностика инфекций
Для обследования пациента на предмет наличия у него инфекционной болезни применяются две большие группы специфических методов:1) Прямые методы диагностики (микробиологические методы, ПЦР-диагностика, ИФА метод с определением антигенов возбудителей).
2) Непрямые методы (серологические реакции для обнаружения антител – ИФА, РА, РНГА, РПГА, РТГА, РН и прочие).
Прямые методы диагностики направлены на выявление возбудителей и их антигенов. Микробиологические исследования проводятся при подозрении на бактериальные и вирусные инфекции путем посева материала от больного на специальные питательные среды и своеобразного выращивания колоний патогенов в определенных комфортных для них условиях. Преимущество таких методов в выявлении самого возбудителя, однако ряд исследований проводится длительно – до 10 дней. В связи с этим на помощь пришла ПЦР-диагностика – определение антигенов возбудителей (ДНК, РНК). Преимущество ПЦР-диагностики в высокой специфичности метода с определением даже одной молекулы нуклеиновой кислоты (ДНК, РНК) в живом или погибшем материале.
Прямыми методами являются и паразитологические исследования материалов на обнаружение яиц простейших и гельминтов. Материалом для исследования при прямых методах является практически любой биологический материал: кровь, слизь носа и зева, моча, желчь, спинномозговая жидкость, биоптаты тканей и органов.
Результатом непрямых методов диагностики является обнаружение в крови специфических антител к какому-либо заболеванию — это иммуноглобулины, которые образуются в ответ на попадание в организм человека возбудителей инфекций. Это метод непрямого выявления возбудителя болезни по образовавшимся антителам, причем можно предполагать как острую инфекцию, так и обострение хронического заболевания. Реакции могут быть качественными и количественными, выражаемыми в титрах антител. Антитела IgM могут определяться как при остром процессе, так и обострении хронического. Антитела класса G свидетельствуют о хронической инфекции либо в стадии активации или ремиссии, реинфекции (повторной инфекции), периоде выздоровления (реконвалесценции), перенесенной инфекции в прошлом. IgG могут циркулировать пожизненно, формируя иммунитет к конкретной инфекции. Концентрация антител в сыворотке крови зависит от ряда факторов: времени с момента заражения, антигенных свойств возбудителя заболевания, состояния иммунной системы самого человека в момент заражения. Материалом для непрямых методов является преимущественно сыворотка крови больного, взятая натощак.
Материалом для непрямых методов является преимущественно сыворотка крови больного, взятая натощак.
диагностика — Государственное бюджетное учреждение здравоохранения Республики Тыва «Инфекционная больница»
МЕТОД ПЦР-ДИАГНОСТИКИ
Полимеразная цепная реакция (ПЦР) — экспериментальный метод молекулярной биологии, способ значительного увеличения малых концентраций определённых фрагментов нуклеиновой кислоты (ДНК) в биологическом материале (пробе).
В основе метода ПЦР лежит многократное удвоение определённого участка ДНК при помощи ферментов в искусственных условиях (in vitro). В результате нарабатываются количества ДНК, достаточные для визуальной детекции. При этом происходит копирование только того участка, который удовлетворяет заданным условиям, и только в том случае, если он присутствует в исследуемом образце.
Кроме простого увеличения числа копий ДНК (этот процесс называется амплификацией), ПЦР позволяет производить множество других манипуляций с генетическим материалом (введение мутаций, сращивание фрагментов ДНК), и широко используется в биологической и медицинской практике, например, для диагностики заболеваний (наследственных, инфекционных), для установления отцовства, для клонирования генов, введения мутаций, выделения новых генов.
ПЦР — метод молекулярной диагностики, ставший для ряда инфекций «золотым стандартом», проверен временем и тщательно апробирован клинически. Метод ПЦР позволяет определить наличие возбудителя заболевания, даже если в пробе присутствует всего несколько молекул ДНК возбудителя.
ПЦР позволяет диагностировать наличие долго растущих возбудителей, не прибегая к трудоёмким микробиологическим методам, что особенно актуально в гинекологии и урологии при диагностике урогенитальных инфекций, передающихся половым путем (ИППП).
Также, этим методом проводят диагностику вирусных инфекций, таких как гепатиты, ВИЧ и др. Чувствительность метода значительно превосходит таковую у иммунохомических и микробиологических методов, а принцип метода позволяет диагностировать наличие инфекций со значительной антигенной изменчивостью.
Специфичность ПЦР при использовании технологии PCR даже для всех вирусных, хламидийных, микоплазменных, уреаплазменных и большинства других бактериальных инфекций достигает 100%. Метод ПЦР позволяет выявлять даже единичные клетки бактерий или вирусов. ПЦР-диагностика обнаруживает наличие возбудителей инфекционных заболеваний в тех случаях, когда другими методами (иммунологическими, бактериологическими, микроскопическими) это сделать невозможно.
Метод ПЦР позволяет выявлять даже единичные клетки бактерий или вирусов. ПЦР-диагностика обнаруживает наличие возбудителей инфекционных заболеваний в тех случаях, когда другими методами (иммунологическими, бактериологическими, микроскопическими) это сделать невозможно.
Особенно эффективен метод ПЦР для диагностики трудно культивируемых, некультивируемых и скрыто существующих форм микроорганизмов, с которыми часто приходится сталкиваться при латентных и хронических инфекциях, поскольку этот метод позволяет избежать сложностей, связанных с выращиванием таких микроорганизмов в лабораторных условиях.
Применение ПЦР-диагностики также очень эффективно в отношении возбудителей с высокой антигенной изменчивостью и внутриклеточных паразитов. Методом ПЦР возможно выявление возбудителей не только в клиническом материале, полученном от больного, но и в материале, получаемом из объектов внешней среды (вода, почва и т. д.). В урологической и гинекологической практике — для выявления хламидиоза, уреаплазмоза, гонореи, герпеса, гарднереллёза, микоплазменной инфекции, ВПЧ — вирусов папилломы человека; в пульмонологии — для дифференциальной диагностики вирусных и бактериальных пневмоний, туберкулёза; в гастроэнтерологии — для выявления хеликобактериоза; в клинике инфекционных заболеваний — в качестве экспресс-метода диагностики сальмонеллёза, дифтерии, вирусных гепатитов В, С и G; в гематологии — для выявления цитомегаловирусной инфекции, онковирусов.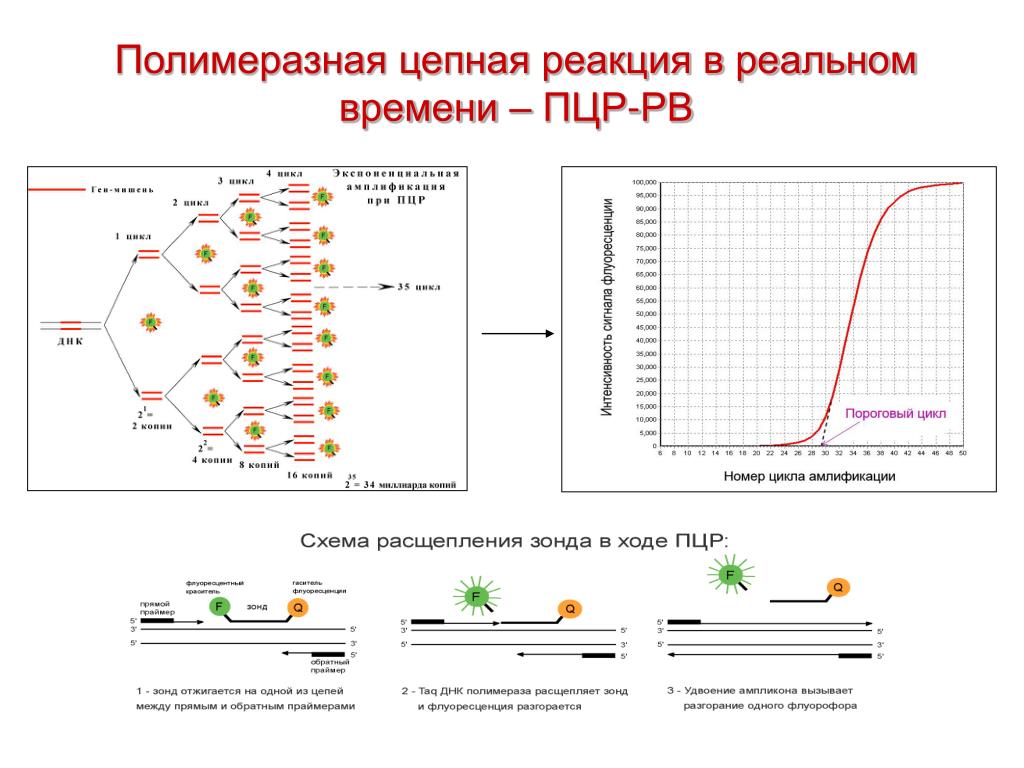
Специфичность ПЦР основана на образовании комплементарных комплексов между матрицей и праймерами — короткими синтетическими олигонуклеотидами длиной 18 — 30 букв. Каждый из праймеров сопоставим (комплементарен) с одной из цепей двуцепочечной матрицы, обрамляя начало и конец амплифицируемого участка.
После соединения (гибридизации) матрицы с праймером (отжиг), последний служит затравкой для ДНК-полимеразы при синтезе комплементарной цепи матрицы.
ПЦР-исследования выполняют на амплификаторе CFX-96 Touch – это многофункциональный высокоскоростной Real Time амплификатор, позволяющий проводить мультиплексный анализ до 5 мишеней в 96 пробах одновременно. Амплификатор CFX-96 создан на основе амплификатора С1000 Touch и шестиканального оптического реакционного модуля CFX-96.
Выявляемый микроорганизм | Вид биологического материала |
ДНК Бордетелла пертуссис (Bordetella pertussis) | Мазки с задней стенки глотки |
ДНК Вируса Эпштейна-Барр (EBV) | Слюна, моча, соскобы из уретры, цервикального канала, заднего свода влагалища, мононуклеарная фракция клеток периферической крови |
ДНК Цитомегаловируса (CMV) | Слюна, моча, соскобы из уретры, цервикального канала, заднего свода влагалища, мононуклеарная фракция клеток периферической крови |
РНК Энтеровирусов (Enterovirus) | Спинномозговая жидкость(ликвор), фекалии |
РНК Вирусного гепатита А (HAV) качественное исследование | Периферическая кровь (плазма крови) |
ДНК Вирусного гепатита В (HBV) качественное и количественное исследование | Периферическая кровь (плазма крови) |
РНК Вирусного гепатита С (HCV) качественное и количественное исследование | Периферическая кровь (плазма крови) |
РНК Вирусного гепатита С (HCV) Генотипирование вируса гепатита 1, 2 и 3 | Периферическая кровь (плазма крови) |
РНК Вирусного гепатита D (HDV) Качественное исследование | Периферическая кровь (плазма крови) |
РНК Вирусов гриппа А (Influenza А virus) Качественное исследование | Мазки и смывы из полости носа и ротоглотки, мокрота |
РНК Вирусов гриппа В (Influenza В virus) Качественное исследование | Мазки и смывы из полости носа и ротоглотки, мокрота |
РНК Вирусов гриппа А «свиной грипп» — Пан h2N1 (Influenza А virus (h2N1) Качественное исследование | Мазки и смывы из полости носа и ротоглотки, мокрота |
РНК Вирусов гриппа А «птичий грипп» субтипа H5N1 (Influenza А virus (subtypeH5N1) Качественное исследование | Мазки и смывы из полости носа и ротоглотки, мокрота |
РНК коронавирусов | Мазки со слизистой нижнего носового хода, мазки из ротоглотки, мокрота или аспират из трахеи, плазма крови, фекалии. |
ДНК парвовирусов В 19 | Смывы и мазки из ротоглотки, слюна, плазма крови |
Для получения корректных результатов большое значение имеет качество образца биоматериала для исследования, его хранение, транспортировка и предварительная обработка.
Исследование методом ПЦР относится к прямым методам лабораторного исследования, поэтому взятие биологического материала необходимо проводить из места локализации инфекционного процесса.
- Взятие образцов периферической крови. Взятие крови проводится в пластиковые пробирки объемом 2,5 мл с добавлением в качестве антикоагулянта динатриевой солью этилендиаминтетраацетата (сиреневые крышки – 6% ЭДТА) в конечной концентрации 2,0 мг/мл. Для перемешивания с антикоагулянтом пробирку переворачивают 2 – 3 раза. Время взятия материала до получения плазмы не должно превышать 6 часов.
- Особенности взятия мазков из полости носа.
 Зонд вводят легким движением по наружной стенки носа на глубину 2 – 3 см до нижней раковины. Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину, делают вращательное движение и удаляют вдоль наружной стенки носа. Перенесите зонд с биоматериалом в пробирку с транспортной средой и тщательно прополощите его, избегая разбрызгивания жидкости. Затем извлеките зонд из раствора, прижимая его к стенке пробирки, отожмите избыток жидкости и выбросьте. Время взятия материала до начала исследования не должно превышать 24 часов.
Зонд вводят легким движением по наружной стенки носа на глубину 2 – 3 см до нижней раковины. Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину, делают вращательное движение и удаляют вдоль наружной стенки носа. Перенесите зонд с биоматериалом в пробирку с транспортной средой и тщательно прополощите его, избегая разбрызгивания жидкости. Затем извлеките зонд из раствора, прижимая его к стенке пробирки, отожмите избыток жидкости и выбросьте. Время взятия материала до начала исследования не должно превышать 24 часов. - Особенности взятия мазков из ротоглотки. Мазки берут вращательным движением с поверхности миндалин, небных дужек и задней стенки глотки. Перенесите зонд с биоматериалом в пробирку с транспортной средой и тщательно прополощите его, избегая разбрызгивания жидкости. Затем извлеките зонд из раствора, прижимая его к стенке пробирки, отожмите избыток жидкости и выбросьте. Время взятия материала до начала исследования не должно превышать 24 часов.

- Особенности взятия смывов из ротоглотки. Перед взятием смывов из ротоглотки проводят предварительное полоскание полости рта водой. После этого проводят тщательное полоскание ротоглотки (в течение 10 – 15 секунд) 8,0 – 10 мл стерильного физиологического раствора. Жидкость собирают через воронку в стерильную пробирку. Не допускается повторное использование воронки без предварительного автоклавирования. Время взятия материала до начала исследования не должно превышать 24 часов.
- Особенности взятия смывов из полости носа. Взятие материала производят в положении больного сидя с отклоненной назад головой. Для получения смыва из полости носа в оба носовых хода поочередно с помощью зонда или одноразового шприца вводят по 3,0 – 5,0 мл теплого стерильного физиологического раствора. Промывную жидкость из обоих носовых ходов собирают через воронку в одну стерильную пробирку. Не допускается повторное использование воронки без предварительного автоклавирования. Время взятия материала до начала исследования не должно превышать 24 часов.

- Мокрота или аспират из трахеи. Мокроту собирают в стерильные герметичные одноразовые пластиковые контейнеры после предварительного полоскания полости рта водой. Аспираты из трахеи получают традиционным способом и помещают в стерильные герметичные одноразовые пластиковые контейнеры.
- Фекалии. Образцы забирают в стерильный горшок или подкладное судно. Затем в количестве 1 г (примерно) переносят в одноразовую герметичную емкость из полипропилена.
- Слюна. Слюну собирают в стерильную пробирку типа «Эппендорф» объемом 1,5 мл в количестве 0,2-1,0 мл после трехкратного полоскания рта кипяченной водой.
Интерпретация результатов количественного определения ДНК вируса гепатита Б (HBV) и РНК вируса гепатита С (HCV) методом ПЦР:
· если значение вирусной нагрузки находится в пределах 7,5 х 102 – 1,0 х 108 копий/мл, результат определяется как положительный с указанием вирусной нагрузки в образце (копий/мл.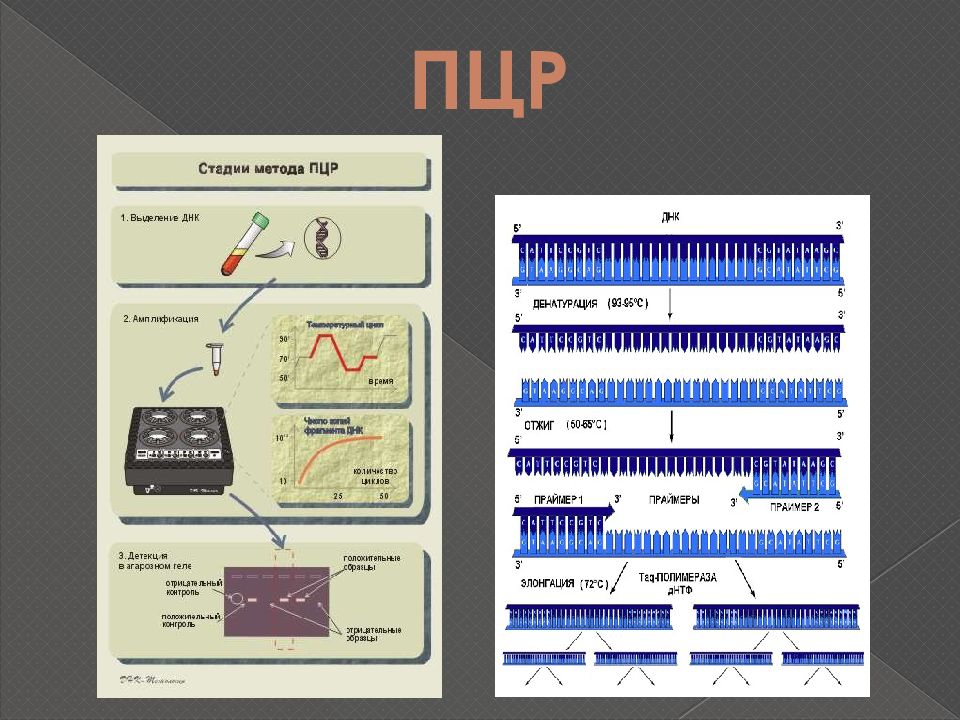 )
)
· если значение вирусной нагрузки выходит за рамки линейного диапазона, то для образцов с низкой вирусной нагрузкой (значение, определенное программой меньше 7,5 х 102 копий/мл) результат фиксируется как «менее 7,5 х 102 копий/мл». Для образцов с высокой вирусной нагрузкой (значение, определенное программой, больше 1,0 х 108 копий/мл) результат фиксируется как: «более 1,0 х 108 копий/мл»
Интерпретация результатов качественнного определения ДНК вируса гепатита Б (HBV) и РНК вируса гепатита С (HCV) методом ПЦР: обнаружена РНК HCV/ ДНК HBV, не обнаружена РНК HCV/ ДНК HBV, недостоверный результат.
Диагностическое тестирование COVID-19 — клиника Мэйо
Обзор
Диагностическое тестирование COVID-19 проводится, чтобы выяснить, инфицированы ли вы в настоящее время SARS-CoV-2, вирусом, вызывающим коронавирусную болезнь 2019 (COVID-19).
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) одобрило следующие типы тестов для диагностики инфекции COVID-19 :
ПЦР-тест. Этот тест COVID-19 , также называемый молекулярным тестом, выявляет генетический материал вируса с помощью лабораторного метода, называемого полимеразной цепной реакцией (ПЦР).Образец жидкости собирают путем введения длинного носового мазка (носоглоточного мазка) в ноздрю и взятия жидкости из задней части носа или с помощью более короткого носового мазка (мазок из средней носовой раковины) для получения образца.
В некоторых случаях длинный тампон вводится в заднюю часть горла (ротоглоточный мазок) или вы можете сплюнуть его в пробирку для получения образца слюны. Результаты могут быть доступны в считанные минуты, если они проанализированы на месте, или через несколько дней — или дольше в местах с задержками обработки тестов — если они будут отправлены во внешнюю лабораторию.
 Тесты PCR очень точны, если их правильно выполняет специалист в области здравоохранения, но в некоторых случаях экспресс-тест может пропустить.
Тесты PCR очень точны, если их правильно выполняет специалист в области здравоохранения, но в некоторых случаях экспресс-тест может пропустить.Тест на антиген. Этот тест COVID-19 обнаруживает определенные белки в вирусе. Используя длинный носовой мазок для взятия образца жидкости, некоторые тесты на антигены могут дать результаты за считанные минуты. Остальные могут быть отправлены в лабораторию для анализа.
Положительный результат теста на антиген считается точным при тщательном соблюдении инструкций, но есть повышенная вероятность ложноотрицательных результатов — это означает, что можно заразиться вирусом, но получить отрицательный результат.В зависимости от ситуации врач может порекомендовать тест PCR для подтверждения отрицательного результата теста на антиген.
Тест PCR , называемый Flu SC2 Multiplex Assay, может одновременно обнаружить любой из трех вирусов: вирус COVID-19 , грипп A и грипп B (грипп). Для проверки на все три вируса необходим только один образец, и это может быть полезно во время сезона гриппа. Но отрицательный результат не исключает возможности возникновения какой-либо из этих инфекций.Таким образом, диагностический процесс может включать больше шагов в зависимости от симптомов, возможных воздействий и клинической оценки вашего врача.
Для проверки на все три вируса необходим только один образец, и это может быть полезно во время сезона гриппа. Но отрицательный результат не исключает возможности возникновения какой-либо из этих инфекций.Таким образом, диагностический процесс может включать больше шагов в зависимости от симптомов, возможных воздействий и клинической оценки вашего врача.
Продукты и услуги
Показать больше продуктов от Mayo ClinicПочему это делается
В США диагностический тест COVID-19 необходим, если:
- У вас COVID-19 симптомов, таких как жар, кашель, усталость или одышка
- У вас нет симптомов, но у вас был тесный контакт с человеком, у которого положительный результат теста на вирус COVID-19 или у кого есть подозрение на наличие вируса.
 Тесный контакт означает, что вы были в пределах 6 футов (2 метров) от человека, у которого COVID-19 . Но если вы дали положительный результат на COVID-19 в течение последних трех месяцев, вам не нужно проходить тестирование. Если вы прошли полную вакцинацию и тесно общались с кем-то, у кого есть вирус COVID-19 , пройдите тестирование через 3-5 дней после контакта с ним.
Тесный контакт означает, что вы были в пределах 6 футов (2 метров) от человека, у которого COVID-19 . Но если вы дали положительный результат на COVID-19 в течение последних трех месяцев, вам не нужно проходить тестирование. Если вы прошли полную вакцинацию и тесно общались с кем-то, у кого есть вирус COVID-19 , пройдите тестирование через 3-5 дней после контакта с ним. - Вы участвовали в мероприятиях, повышающих риск заражения COVID-19 , и не оставались на расстоянии не менее 6 футов от других — например, путешествия, большие собрания или многолюдные помещения.
- Ваш врач, другой медицинский работник или отдел общественного здравоохранения рекомендует пройти тест
Определенные группы считаются высокоприоритетными для диагностического тестирования. К ним относятся люди с признаками и симптомами COVID-19 , которые:
- Работать в медицинском учреждении или оказывать первую помощь
- Живут или работают в учреждениях длительного ухода, таких как дома престарелых, или в других местах, где люди проживают вместе, например, в тюрьмах или приютах
- Находится на лечении в больнице
Другим людям может быть предоставлен приоритет для тестирования в зависимости от рекомендаций местного департамента здравоохранения по мониторингу COVID-19 в отдельных сообществах.
У некоторых людей, инфицированных вирусом COVID-19 , симптомы могут отсутствовать, то есть у них нет никаких признаков или симптомов. Но они все еще могут передавать вирус другим. В некоторых районах США тестирование доступно для бессимптомных людей. Если у людей без симптомов есть положительный результат теста, они должны следовать инструкциям по самоизоляции, чтобы сдержать распространение вируса.
Доступность диагностического тестирования COVID-19 и место проведения тестирования могут варьироваться в зависимости от того, где вы живете, и рекомендаций местных органов здравоохранения.
Получите самые свежие советы по здоровью от клиники Мэйо. в ваш почтовый ящик.
Зарегистрируйтесь бесплатно и будьте в курсе новостей
достижения, советы по здоровью и актуальные темы о здоровье,
например, COVID-19, плюс советы экспертов по поддержанию здоровья.
Получите более подробную консультацию специалиста.
Подпишитесь на специальные предложения на книги, продукты и услуги Mayo Clinic, разработан экспертами, чтобы помочь людям управлять своим здоровьем
Узнайте больше о нашем использовании данныхЧтобы предоставить вам наиболее актуальную и полезную информацию и понять, какие Информация выгодно, мы можем объединить вашу электронную почту и информацию об использовании веб-сайта с другими информация, которая у нас есть о вас.Если вы пациент клиники Мэйо, это может включать в себя защищенную медицинскую информацию (PHI). Если мы объединим эту информацию с вашей PHI, мы будем рассматривать всю эту информацию как PHI, и будет использовать или раскрывать эту информацию только в соответствии с нашим уведомлением о конфиденциальности. практики. Вы можете отказаться от рассылки по электронной почте. в любое время, нажав ссылку «Отказаться от подписки» в электронном письме.
Подписаться!
Спасибо за подписку
Наша электронная рассылка Housecall будет держать вас в курсе
на последней информации о здоровье.
Сожалеем! Наша система не работает. Пожалуйста, попробуйте еще раз.
Что-то пошло не так на нашей стороне, попробуйте еще раз.
Пожалуйста, попробуйте еще раз
Риски
Есть вероятность, что ваш диагностический тест COVID-19 может дать ложноотрицательный результат. Это означает, что тест не обнаружил вирус, даже если вы действительно им заражены.Вы рискуете неосознанно передать вирус другим, если не примете надлежащих мер предосторожности, таких как соблюдение правил социального дистанцирования и, при необходимости, ношение маски для лица. Также есть вероятность, что экспресс-тест на антиген COVID-19 может дать ложноположительные результаты — указывая на инфекцию, когда на самом деле ее нет — если инструкции не будут тщательно соблюдены.
Риск получения ложноотрицательных или ложноположительных результатов теста зависит от типа и чувствительности диагностического теста COVID-19 , тщательности сбора образцов и точности лабораторного анализа.
С осторожностью относитесь к предложениям о домашних тестах COVID-19 , которые FDA не разрешил для использования — они часто дают неточные результаты.
Как вы готовитесь
Независимо от того, есть ли у вас симптомы, планируйте носить маску для лица и обратно в кабинет врача или в центр тестирования, и пусть любой, кто идет с вами, тоже будет ее носить.
- Если вы считаете, что у вас может быть COVID-19 , позвоните в офис своего врача или в местный отдел здравоохранения, чтобы проверить свои симптомы и спросить о тестировании до вашего посещения, чтобы персонал мог подготовиться к вашему визиту, используя средства индивидуальной защиты.
- Если у вас нет симптомов, но вы были в тесном контакте с кем-то, у кого COVID-19 , следуйте советам по тестированию вашего врача или отдела общественного здравоохранения.
 Лучше всего пройти тест на COVID-19 через 5-7 дней после того, как вы были рядом с человеком с COVID-19 . Если вы пройдете тестирование слишком рано, тест может не обнаружить вирус.
Лучше всего пройти тест на COVID-19 через 5-7 дней после того, как вы были рядом с человеком с COVID-19 . Если вы пройдете тестирование слишком рано, тест может не обнаружить вирус.
Если вы считаете, что у вас может быть COVID-19 , позвоните своему врачу, чтобы проверить свои симптомы, если таковые имеются, и спросить о тестировании.Затем ваш врач и другой персонал могут подготовиться к вашему визиту, надеть средства индивидуальной защиты и проинструктировать вас о том, куда идти и как будет проводиться анализ. Планируйте носить маску для лица в центр тестирования и обратно, и пусть все, кто вас сопровождает, тоже будут носить ее.
Если у вас нет симптомов и вы сознательно не контактировали с кем-то, инфицированным вирусом COVID-19 , но хотите пройти тестирование, спросите своего поставщика медицинских услуг, доступно ли и где тестирование.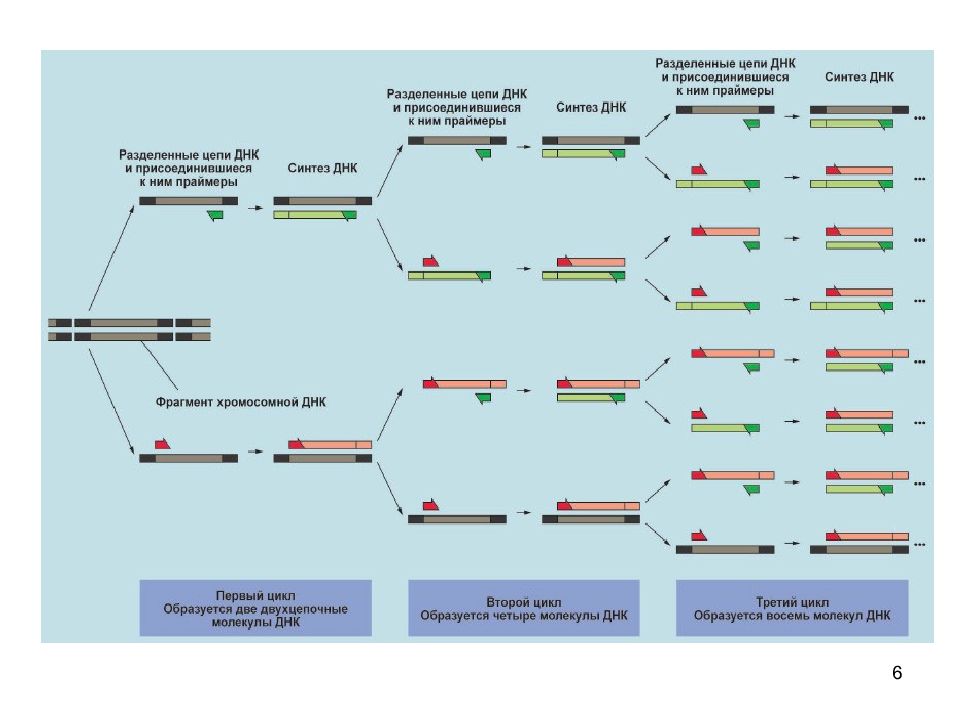 Или вы можете позвонить в департамент здравоохранения своего штата или в местный отдел здравоохранения или посетить их веб-сайт для получения информации о тестировании.
Или вы можете позвонить в департамент здравоохранения своего штата или в местный отдел здравоохранения или посетить их веб-сайт для получения информации о тестировании.
Что вас может ожидать
Для диагностического теста COVID-19 медицинский работник берет образец слизи из носа или горла или образец слюны. Образец, необходимый для диагностического тестирования, может быть собран в кабинете вашего врача, в медицинском учреждении или в центре тестирования.
Мазок из носа или зева. Рекомендуется использовать длинный мазок из носа (мазок из носоглотки), хотя допускается использование более короткого мазка из носа или горла. Ваш врач или другой медицинский работник вставляет вам в нос тонкую гибкую палочку с ватой на кончике или проводит тампоном по задней стенке горла, чтобы собрать образец слизи. Это может быть несколько неудобно.
В случае пробы из носа мазок может производиться из обеих ноздрей, чтобы собрать достаточно слизи для анализа.
 Тампон ненадолго остается на месте, прежде чем его осторожно повернуть при извлечении.Образец запечатывается в пробирку и отправляется в лабораторию для анализа.
Тампон ненадолго остается на месте, прежде чем его осторожно повернуть при извлечении.Образец запечатывается в пробирку и отправляется в лабораторию для анализа.- Образец слюны. В некоторых местах предлагают анализы слюны. Хотя образец слюны может быть немного менее чувствительным, чем образец слизи, взятый с помощью длинного носового мазка, анализ слюны сделать проще и часто менее неудобен. Вы несколько раз плюете в трубку, чтобы взять образец слюны для анализа. Пробирку герметично закрывают перед отправкой в лабораторию на анализ.
Если у вас продуктивный кашель, ваш врач может взять образец мокроты, которая содержит выделения из легких, части нижних дыхательных путей.Вирус больше концентрируется в носу и горле на ранних этапах развития инфекции. Но после более чем пяти дней появления симптомов вирус, как правило, больше концентрируется в нижних дыхательных путях.
В дополнение к диагностическому тесту COVID-19 ваш врач может также проверить другие респираторные заболевания, такие как грипп, которые имеют похожие симптомы и могут объяснить ваше заболевание.
FDA предоставило разрешение на использование в экстренных случаях некоторых наборов для тестирования на дому COVID-19 , включая тот, который предназначен для тестирования как на COVID-19, , так и на грипп.Большинство этих анализов требует рецепта врача. Вы собираете собственный образец носовой жидкости или слюны дома, а затем отправляете его в лабораторию для быстрого анализа. Один тест COVID-19 дает быстрые результаты дома, не отправляя образец в лабораторию. А FDA недавно разрешило купить тест на антиген без рецепта, хотя тесты на антигены не считаются такими же надежными, как тесты PCR .
Точность каждого из этих тестов различается, поэтому отрицательный тест не исключает полностью наличия вируса COVID-19 . Пройдите только домашний тест, разрешенный FDA или одобренный вашим врачом или местным отделом здравоохранения.
Пройдите только домашний тест, разрешенный FDA или одобренный вашим врачом или местным отделом здравоохранения.
Поддержка вашего ребенка во время исследования мазка из носа на COVID-19
Цель этого видео — подготовить детей к сдаче мазка из носа на COVID-19, чтобы облегчить некоторые из их потенциальных страхов и тревог. Когда дети готовы пройти медицинское обследование, они становятся более сговорчивыми и уступчивыми, что создает для них положительный опыт преодоления трудностей.Это видео предназначено для просмотра детьми в возрасте от 4 лет.
Покажите стенограмму видео в поддержку вашего ребенка во время тестирования мазка из носа на COVID-19Дженнифер Родемейер, менеджер программы «Детская жизнь», клиника Мэйо: Привет, я Дженнифер, я специалист по детской жизни в клинике Мэйо. Моя работа — помочь таким детям, как вы, подготовиться к медицинским обследованиям.
Возможно, вы слышали, что существует вирус, который может вызывать у людей тошноту. Вирус — это микроб, и он настолько крошечный, что вы его даже не видите.
Вирус — это микроб, и он настолько крошечный, что вы его даже не видите.
У некоторых людей, зараженных этим вирусом, может подниматься температура или кашель, они могут чувствовать слабость и усталость, в то время как некоторые люди могут быть заражены этим вирусом и совсем не чувствовать себя больным. Люди могут заразиться этим вирусом от прикосновения к вещам. Вот почему так важно часто мыть руки водой с мылом. Вирус также может передаваться через кашель или чихание. Поэтому важно всегда прикрывать кашель или чихание.
Сегодня, даже если вы чувствуете себя плохо или нет, нам нужно будет сделать вам тест, чтобы мы знали, как лучше всего продолжить лечение.Этот медицинский тест покажет нам, есть ли у вас вирус.
Когда вы пойдете на тест, врач будет носить специальную защитную одежду. Они носят эту одежду, чтобы обезопасить себя и вас от заражения микробами. Они будут носить маску, закрывающую нос и рот, и прозрачный пластиковый щит, защищающий глаза.
Самое важное, что вы можете сделать во время теста, — это сидеть совершенно неподвижно, как статуя. Чтобы вы не двигались, родители или опекун помогут вам сохранять спокойствие и спокойствие во время теста.Врач должен коснуться внутренней части задней части вашего носа длинным тонким ватным наконечником. Для этого вам нужно поднять подбородок, затем врач на короткое время вставит вам в нос ватную палочку, чтобы взять образец.
Чтобы вы не двигались, родители или опекун помогут вам сохранять спокойствие и спокойствие во время теста.Врач должен коснуться внутренней части задней части вашего носа длинным тонким ватным наконечником. Для этого вам нужно поднять подбородок, затем врач на короткое время вставит вам в нос ватную палочку, чтобы взять образец.
В то время как это происходит, вы можете почувствовать, что хотите отодвинуть ватную палочку, но действительно важно оставаться как можно более неподвижным, чтобы врач мог закончить тест. Ватная палочка будет входить и выходить из носа через несколько секунд.
Некоторые дети говорят мне, что счет до трех или глубокий вдох расслабляет их перед тестом, а некоторые говорят, что им нравится держаться за свою любимую мягкую игрушку или одеяло. Может быть, у вас есть свой способ расслабиться.
Помните, что во время теста самое главное — сохранять неподвижность тела.
Вы можете испытывать много чувств, когда видите, что врач носит другую одежду, но вы знаете, что этот человек заботится о вас и хочет вам помочь.
Спасибо за то, что помогли нам пройти этот тест, поэтому мы знаем, как продолжить лечение.
Результаты
В некоторых учреждениях есть экспресс-тесты для диагностического тестирования COVID-19 . В этом случае вы можете получить результаты менее чем за час или в тот же день, когда вы проходили тестирование. Другим предприятиям может потребоваться отправить образец для анализа в лабораторию за пределами лаборатории. Если им нужно отправить образец, ваши результаты могут быть доступны только через несколько дней.
Результат вашего диагностического теста COVID-19 может быть положительным или отрицательным.
Положительный результат. Это означает, что в настоящее время у вас есть активное заражение вирусом, вызывающим COVID-19 . Примите соответствующие меры, чтобы позаботиться о себе и избежать передачи вируса другим.
 Вам нужно будет изолировать себя до тех пор, пока: ваши симптомы не улучшатся, прошло 24 часа с тех пор, как у вас поднялась температура, и прошло не менее 10 дней с момента появления ваших симптомов.
Вам нужно будет изолировать себя до тех пор, пока: ваши симптомы не улучшатся, прошло 24 часа с тех пор, как у вас поднялась температура, и прошло не менее 10 дней с момента появления ваших симптомов.Если у вас серьезные симптомы COVID-19 или состояние здоровья, которое снижает вашу способность бороться с болезнью, ваш врач может порекомендовать вам оставаться в изоляции подольше. Если у вас положительный результат, но симптомы не проявились, изолируйте его в течение 10 дней после теста.
Отрицательный результат. Это означает, что вы, вероятно, не были заражены вирусом COVID-19 . Но ложноотрицательный результат теста может произойти в зависимости от времени и качества тестового образца.
Даже если ваш тест окажется отрицательным, вы можете заразиться в будущем, поэтому важно соблюдать правила социального дистанцирования, использования масок для лица и мытья рук, чтобы избежать потенциального распространения.
 Ваш врач может порекомендовать повторное обследование, если симптомы не исчезнут.
Ваш врач может порекомендовать повторное обследование, если симптомы не исчезнут.
Отслеживание контактов
Если вы дали положительный результат на вирус COVID-19 — или ваш врач подозревает, что у вас есть вирус, но у вас еще нет результатов — вас могут попросить принять участие в отслеживании контактов.Отслеживание контактов играет ключевую роль в ограничении распространения инфекционных заболеваний. Чем раньше начнется отслеживание контактов, тем эффективнее будет ограничение распространения вируса.
Для начала вы предоставляете список людей, с которыми вы тесно контактировали в то время, когда вы могли заразиться. Затем работники общественного здравоохранения связываются с этими близкими людьми, чтобы сообщить им о воздействии и возможности заражения. Ваша личность защищена во время этого обмена информацией.
Группа отслеживания контактов предоставляет информацию о том, что близкие контакты могут сделать, чтобы минимизировать риск распространения вируса. Эти шаги могут включать в себя прохождение теста COVID-19 , пребывание дома и вдали от других — так называемый карантин — после контакта, изучение признаков и симптомов и принятие других мер предосторожности.
Эти шаги могут включать в себя прохождение теста COVID-19 , пребывание дома и вдали от других — так называемый карантин — после контакта, изучение признаков и симптомов и принятие других мер предосторожности.
Рекомендации по карантину
Если у вас был тесный контакт с человеком, имеющим COVID-19 , и вы находились в пределах 6 футов (2 метров) от этого человека, лучше всего оставаться дома и подальше от других (карантин) в течение 14 через несколько дней после контакта, чтобы узнать, появятся ли у вас симптомы COVID-19 .Если у вас было COVID-19 или вы были полностью вакцинированы за последние три месяца, вам, как правило, не нужно помещать в карантин, если у вас был тесный контакт с COVID-19 .
Другие варианты могут включать прекращение карантина через 10 дней, если у вас нет симптомов и вы не прошли тестирование, или прекращение карантина через 7 дней, если вы получили отрицательный результат теста и у вас нет симптомов. Но продолжайте наблюдать за симптомами в течение полных 14 дней.
Но продолжайте наблюдать за симптомами в течение полных 14 дней.
Обратитесь к своему врачу или в местный отдел здравоохранения за советом по тестированию и рекомендациям по карантину.
Клинические испытания
Изучите исследования клиники Mayo, посвященные тестам и процедурам, которые помогают предотвратить, выявлять, лечить или контролировать состояния.
3 августа 2021 г.
Стандартный тест на коронавирус, если он доступен, работает хорошо, но могут ли новые методы диагностики помочь в этой пандемии? | Наука
Врач в Германии готовит мазок для проверки на коронавирусную инфекцию.
Дэниел Рейнхардт / фото альянс через Getty Images Автор Роберт Ф. Сервис
Сервис
По мере того, как Соединенные Штаты стремятся активизировать тестирование на пандемический коронавирус с использованием технологии, основанной на проверенной временем полимеразной цепной реакции (ПЦР), начинают внедряться альтернативные подходы, которые могут упростить и ускорить изучение людьми того, нужно ли они были инфицированы.Некоторые методы модифицируют стандартный тест ПЦР, который усиливает крошечные кусочки генетического материала для обнаружения, в то время как другие секвенируют вирус напрямую или используют редактор генома CRISPR.
«Грядут более быстрые и дешевые тесты», — говорит Эван Джонс, генеральный директор OpGen, компании по быстрой диагностике. Однако, добавляет он, разработка новых видов тестов «займет время». Некоторые из новых тестов уже поступают в онлайн, но для проверки других, вероятно, потребуются месяцы, и они будут готовы к широкому распространению.
«Тестирование, тестирование, тестирование» — это мантра, которую снова и снова повторяет Генеральный директор Всемирной организации здравоохранения Тедрос Адханом Гебрейесус. Диагностические тесты, выявляющие активные инфекции у людей, жизненно важны для усилий общественного здравоохранения, а не только для здоровья людей. Широко распространенное диагностическое тестирование, наряду с изоляцией инфицированных, отслеживанием контактов и помещением в карантин этих контактов, похоже, сыграло ключевую роль в работе Южной Кореи по подавлению распространения вируса.
Диагностические тесты, выявляющие активные инфекции у людей, жизненно важны для усилий общественного здравоохранения, а не только для здоровья людей. Широко распространенное диагностическое тестирование, наряду с изоляцией инфицированных, отслеживанием контактов и помещением в карантин этих контактов, похоже, сыграло ключевую роль в работе Южной Кореи по подавлению распространения вируса.
Связанные
В Соединенных Штатах медленное развертывание ПЦР-тестов на коронавирус широко объясняется сочетанием строгих правил, направленных на обеспечение их надежности, и сложной сети компаний и систем здравоохранения, ответственных за разработку, проведение и оплату тестов. Администрация Трампа заявляет, что тестирование ускоряется. 16 марта на пресс-конференции в Белом доме У.Заместитель секретаря по вопросам здравоохранения S. Health and Human Services Бретт Гироар сказал, что страна сможет обработать 1 миллион тестов к концу недели и 2 миллиона на следующей неделе. Но реальные цифры еще не близки к этому. Согласно данным, собранным в рамках проекта отслеживания COVID, некоммерческого сотрудничества представителей общественного здравоохранения и журналистов по подсчету тестов, проведенных в Соединенных Штатах, по состоянию на 22 марта была проведена 191 541 ПЦР-диагностика, 24 345 из которых оказались положительными на вирус.
Но реальные цифры еще не близки к этому. Согласно данным, собранным в рамках проекта отслеживания COVID, некоммерческого сотрудничества представителей общественного здравоохранения и журналистов по подсчету тестов, проведенных в Соединенных Штатах, по состоянию на 22 марта была проведена 191 541 ПЦР-диагностика, 24 345 из которых оказались положительными на вирус.
29 февраля Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) опубликовало новые правила, разрешающие экстренное использование тестов на коронавирус помимо тех, которые производятся и распространяются Центрами США по контролю и профилактике заболеваний. Академические вирусологические лаборатории, департаменты здравоохранения и компании начали создавать свои собственные тесты ПЦР. Сегодня около четырех десятков организаций получили одобрение FDA на свои тесты. Среди крупнейших — диагностические компании, такие как Roche Molecular Systems, получившая на этой неделе зеленый свет на проведение испытаний FDA. По словам Александра Валсамакис, главного медицинского директора компании, на начальном этапе она будет предоставлять около 400 000 тестов в неделю в США и 3 миллиона во всем мире. Другие крупные компании также недавно получили одобрение на свои тесты, в том числе Thermo Fisher Scientific и Abbott Laboratories.
По словам Александра Валсамакис, главного медицинского директора компании, на начальном этапе она будет предоставлять около 400 000 тестов в неделю в США и 3 миллиона во всем мире. Другие крупные компании также недавно получили одобрение на свои тесты, в том числе Thermo Fisher Scientific и Abbott Laboratories.
университетских вирусологических лабораторий также вскочили, чтобы помочь диагностировать случаи заболевания поблизости от них. Например, на прошлой неделе врачи Медицинского центра Университета Питтсбурга (UPMC) начали использовать самодельный ПЦР-тест для проверки на наличие инфекции в округе Аллегейни.На данный момент количество тестов остается небольшим, около 100 в неделю. «Нам определенно хотелось, чтобы мы начали это раньше, — говорит Алан Уэллс, возглавляющий клинические лаборатории UPMC.
ПЦР — это наиболее часто используемый тест для диагностики коронавируса, поскольку он очень точен. (См. Как работает наиболее распространенный тест на коронавирус?) Но другие проблемы ограничивают его. «Нам не удалось добиться необходимых результатов», — говорит Стивен Волински, врач-инфекционист Северо-Западного университета. Каждый тест занимает около 4 часов после того, как образец поступает в централизованную лабораторию тестирования, с разделением времени между подготовкой образца и фактическим тестом ПЦР.С транспортом и очередями получение результата может занять от 2 до 4 дней. За это время инфицированные люди могут передать вирус многим другим.
«Нам не удалось добиться необходимых результатов», — говорит Стивен Волински, врач-инфекционист Северо-Западного университета. Каждый тест занимает около 4 часов после того, как образец поступает в централизованную лабораторию тестирования, с разделением времени между подготовкой образца и фактическим тестом ПЦР.С транспортом и очередями получение результата может занять от 2 до 4 дней. За это время инфицированные люди могут передать вирус многим другим.
Самостоятельная тампона
В диагностический ландшафт коронавируса добавляется еще одно новое измерение: «домашние» тесты, которые включают отправку образца, взятого дома, в лабораторию. Например, завтра Everlywell планирует начать поставки комплектов на дом и в розничные аптеки. Эти тесты начнутся со скрининговых вопросов в Интернете или в магазине, чтобы определить, может ли человек подвергнуться воздействию вируса.Если да, они могут получить набор для отбора проб из носоглотки по почте или купить его у местного продавца. Человеку будут даны подробные инструкции по введению его собственного тампона, помещению его в защитный флакон и в ночное время по почте в одну из десятков диагностических лабораторий (которые сотрудничают с Everlywell и уже имеют одобрение FDA) для анализа ПЦР.
Человеку будут даны подробные инструкции по введению его собственного тампона, помещению его в защитный флакон и в ночное время по почте в одну из десятков диагностических лабораторий (которые сотрудничают с Everlywell и уже имеют одобрение FDA) для анализа ПЦР.
Фрэнк Онг, главный медицинский и научный директор Everlywell, говорит, что компания рассчитывает быстро вырасти с тысячи таких тестов в день до десятков тысяч.Хотя каждый тест, вероятно, потребует 4-дневного ожидания результатов, говорит Онг, эта стратегия домашнего отбора проб имеет серьезные преимущества: она защитит медицинских работников от воздействия потенциальной инфекции и высвободит их время. «Нам нужно убедиться, что мы даем им возможность позаботиться о пациентах», — говорит Онг. Другие компании, в том числе Nurx и Carbon Health, заявляют, что теперь поставляют ограниченные запасы собственных наборов для взятия проб в домашних условиях.
Большинство тестов ПЦР на новый вирус проводится на больших дорогих автоматизированных машинах, которые выполняют множество тестов одновременно. Они есть в крупных больницах или диагностических центрах, но сейчас начинает разворачиваться еще один вариант — меньшие по размеру и менее дорогие устройства, которые также выполняют амплификацию нуклеиновых кислот. Они могут использоваться небольшими больницами и даже отдельными врачебными кабинетами.
Они есть в крупных больницах или диагностических центрах, но сейчас начинает разворачиваться еще один вариант — меньшие по размеру и менее дорогие устройства, которые также выполняют амплификацию нуклеиновых кислот. Они могут использоваться небольшими больницами и даже отдельными врачебными кабинетами.
В пятницу, например, компания Cepheid, которая продает небольшие системы ПЦР для быстрого обнаружения вирусов гриппа, бактерий туберкулеза и других микробов, получила одобрение FDA на экстренное использование тестового картриджа на коронавирус 2 (SARS-CoV-2), который может экстренно использовать острый респираторный синдром. в систему GenXpert компании, устройство размером с кофемашину, которое может выдать диагностический результат всего за 45 минут.Официальные лица Cepheid говорят, что во всем мире установлено 23 000 таких систем, из них 5000 — в Соединенных Штатах. 19 марта GenMark получил одобрение FDA на экстренное использование собственных тестов на коронавирус, которые проводятся на машинах аналогичного размера, которые используют запатентованный электрохимический подход для обнаружения целевого генетического материала менее чем за 2 часа.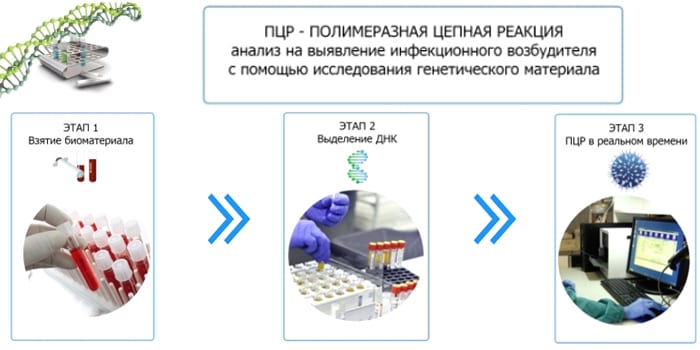 Другие компании, спешащие поставить диагностические аппараты для пунктов оказания медицинской помощи, включают Mesa Biotech, HiberGene, Mobidiag и QuantuMDx.
Другие компании, спешащие поставить диагностические аппараты для пунктов оказания медицинской помощи, включают Mesa Biotech, HiberGene, Mobidiag и QuantuMDx.
То же самое и с такими компаниями, как Oxford Nanopore и Fulgent Genetics, которые вместо использования ПЦР напрямую секвенируют любой генетический материал в образце, а затем ищут совпадения, скажем, с новым коронавирусом.Этот подход к высокоскоростному секвенированию генов может помочь охарактеризовать геном коронавируса, чтобы лучше понять, как вирус развивается, но он также может быть диагностическим в определенных ситуациях, таких как удаленные сайты без доступа к ПЦР. Портативные устройства Oxford Nanopore использовались во время вспышек лихорадки Эбола, и компания отправила их в Китай на ранних этапах пандемии.
CRISPR для тестирования
Самый быстрый способ тестирования на коронавирус в конечном итоге может быть предложен компаниями, использующими редактор генома CRISPR, более известный тем, что он добавляет или удаляет ДНК в клетках. Две американские компании, Mammoth Biosciences и Sherlock Biosciences, заявляют, что они создали тесты на основе CRISPR и в настоящее время проверяют их на образцах пациентов, прежде чем обращаться за разрешением на экстренное использование в FDA. Метод начинается с образца пациента, извлекается вирусная РНК и используется тест быстрой амплификации нуклеиновых кислот, называемый петлевой амплификацией, чтобы получить ровно столько РНК, чтобы тест мог ее обнаружить. Затем исследователи добавляют два компонента редактора генома CRISPR: белок под названием CAS12, который разрезает ДНК или РНК, и «направляющую» РНК, которая вставляется в CAS12 и помогает ему найти последовательность, соответствующую части генома коронавируса.Если CAS12 и его руководство находят совпадение в РНК, CAS12 связывается с этой совпадающей РНК, которая активирует CAS12, чтобы разрезать ее и продолжить разрезать любые другие короткие цепи РНК или ДНК поблизости, включая копии цепи, предназначенные для высвобождения цвета.
Две американские компании, Mammoth Biosciences и Sherlock Biosciences, заявляют, что они создали тесты на основе CRISPR и в настоящее время проверяют их на образцах пациентов, прежде чем обращаться за разрешением на экстренное использование в FDA. Метод начинается с образца пациента, извлекается вирусная РНК и используется тест быстрой амплификации нуклеиновых кислот, называемый петлевой амплификацией, чтобы получить ровно столько РНК, чтобы тест мог ее обнаружить. Затем исследователи добавляют два компонента редактора генома CRISPR: белок под названием CAS12, который разрезает ДНК или РНК, и «направляющую» РНК, которая вставляется в CAS12 и помогает ему найти последовательность, соответствующую части генома коронавируса.Если CAS12 и его руководство находят совпадение в РНК, CAS12 связывается с этой совпадающей РНК, которая активирует CAS12, чтобы разрезать ее и продолжить разрезать любые другие короткие цепи РНК или ДНК поблизости, включая копии цепи, предназначенные для высвобождения цвета. -заменяет молекулы, когда CAS12 отсекает их. Результатом может быть простое изменение цвета тест-полоски.
-заменяет молекулы, когда CAS12 отсекает их. Результатом может быть простое изменение цвета тест-полоски.
Этот метод отлично подходит для поиска небольших фрагментов генетического материала, — говорит Дженнифер Дудна, биохимик из Калифорнийского университета (UC), Беркли, пионер CRISPR, председатель научного консультативного совета Mammoth Biosciences.
В препринте, опубликованном 10 марта на medRxiv, исследователи из Mammoth Biosciences и Калифорнийского университета в Сан-Франциско сообщают, что тесты на клинических образцах дали результаты с точностью, сравнимой с ПЦР, всего за 30 минут. Он использует простую полосу, похожую на бумагу, с цветной линией, которая появляется с положительным результатом. По словам Тревора Мартина, генерального директора Mammoth, компания обсуждает с партнерами производство наборов для тестирования, которые позволят быстро и дешево диагностировать инфекцию SARS-CoV-2 в домашних условиях, не требуя медицинских знаний.
На завершение теста и получение одобрения регулирующих органов могут уйти месяцы, поэтому, скорее всего, он не будет готов в ближайшие решающие недели. Но он может быть готов, если распространение коронавируса продолжится. Некоторые предсказывают, что вирус тоже исчезнет, но осенью снова появятся инфекции. Мартин говорит, что для получения результатов не потребуются машины для ПЦР, управляемые обученными специалистами. «Это изменило бы правила игры» в нашей реакции на возникающие болезни, — говорит Мартин.
Проблемы со снабжением
Несмотря на то, что компании и академические лаборатории расширяют свои усилия по диагностике на основе ПЦР, больницы и центры тестирования по всей стране сообщают, что они столкнулись с более серьезным кризисом: у многих заканчиваются химические вещества и другие материалы, которые позволяют проводить тесты, такие как тампоны для сбора образцов у пациентов и реагенты, необходимые для ПЦР.Бенджамин Пински, патолог Стэнфордского университета, который разработал диагностический тест на основе ПЦР, используемый в Северной Калифорнии, говорит, что его лаборатория сталкивается с постоянной нехваткой различных материалов, в первую очередь наборов, используемых для извлечения РНК из вирусных образцов, прежде чем ее можно будет загрузить в ПЦР-машины.
«Это был большой вызов», — говорит Пинский. «Мы должны были быть очень ловкими, чтобы справиться с этим», постоянно меняя поставщиков или даже химические процедуры, которые должны быть проверены, прежде чем их можно будет использовать на образцах пациентов.Его команда даже разослала в Твиттере просьбы к сообществу Стэнфорда и региональным биотехнологическим компаниям с просьбой пожертвовать наборы реагентов, такие как наборы от Zymo и Qiagen. По словам Пинского, даже несмотря на то, что поступают пожертвования, запасов по-прежнему не хватает.
Реагентные компании пытаются ответить. Например, Qiagen, крупный поставщик наборов для экстракции РНК, объявил во вторник, что его сотрудники работают круглосуточно, чтобы увеличить производство с 1,5 миллиона наборов в месяц до 6.5 миллионов в месяц до конца апреля, а позже увеличится.
Пинский, например, говорит, что он готов к тому, чтобы компании полностью взяли на себя тестирование на коронавирус у таких ученых, как он сам. «Я надеюсь, что эти компании смогут провести обещанное тестирование», — говорит Пинский. «Это еще предстоит выяснить.»
Основы тестирования на коронавирусную болезнь 2019
Español 简体 中文 한국어 Tagalog Việt
Вы, наверное, много слышали о тестировании на коронавирусную болезнь (COVID-19).Если вы считаете, что заболели COVID-19 и нуждаетесь в тесте, немедленно обратитесь к своему врачу или в местный отдел здравоохранения. Вы также можете найти общественный центр тестирования в своем штате или купить домашний тест, разрешенный FDA. Некоторые домашние тесты, разрешенные FDA, дают результаты в течение нескольких минут. Другие требуют, чтобы вы отправили образец по почте в лабораторию для анализа.
Понимание тестирования COVID-19 — ключ к принятию обоснованного решения, отвечающего вашим потребностям.
Типы тестов
Существуют разные типы тестов — диагностических тестов и тестов на антитела .
Диагностические тесты могут показать, есть ли у вас активная инфекция COVID-19 и вам нужно принять меры для карантина или изоляции от других. Молекулярные тесты и на антиген — это типы диагностических тестов, с помощью которых можно определить, есть ли у вас активная инфекция COVID-19. Образцы для диагностических тестов обычно собираются с помощью мазка из носа или горла или слюны, выплевываемой в трубку.
Тесты на антитела ищут антитела в вашей иммунной системе, вырабатываемые в ответ на SARS-CoV-2, вирус, вызывающий COVID-19.Тесты на антитела не следует использовать для диагностики активной инфекции COVID-19 . Для выработки антител может потребоваться несколько дней или недель после заражения, и они могут оставаться в вашей крови в течение нескольких недель или более после выздоровления. Образцы для тестов на антитела обычно представляют собой кровь из пальца или кровь, взятую вашим врачом или другим медицинским персоналом.
Начало испытаний
Если вы прошли тестирование, вы должны изолировать себя дома до тех пор, пока вы не получите результаты теста и не будете следовать советам вашего поставщика медицинских услуг или специалиста в области общественного здравоохранения.
Когда мне следует пройти тест?
- Если у вас есть симптомы COVID-19, даже после вакцинации
- Если у вас был тесный контакт (в пределах 6 футов в общей сложности 15 минут или более) с кем-то с подтвержденным COVID-19, даже после вакцинации
- Если вы принимали участие в деятельности, которая подвергает вас повышенному риску заражения COVID-19 из-за того, что вы не могли социально дистанцироваться, как это было необходимо, например, путешествуя, посещая большие общественные или массовые собрания или находясь в переполненных помещениях
- Если вас попросили или направили пройти тестирование вашим поставщиком медицинских услуг, местным или государственным отделом здравоохранения
В вашей школе, на рабочем месте или в вашем районе также может быть установлена программа скрининга, в рамках которой они проверяют людей, входящих в группу (на работе, в школе), даже если нет оснований подозревать, что эти люди инфицированы COVID-19.FDA опубликовало дополнительную информацию о программах скрининга в этом информационном бюллетене.
Чтобы найти местный центр тестирования, вам следует обратиться к своему поставщику медицинских услуг или зайти на веб-сайт вашего штата или местного департамента здравоохранения.
Заказ теста
Многие тесты, в том числе некоторые домашние тесты и тесты на дому, требуют рецепта или заказа от поставщика медицинских услуг.
Тесты по рецепту — Поставщики медицинских услуг могут определить, нужен ли вам тест, и убедиться, что вы прошли наиболее подходящий тест и знаете, что означают результаты.Например, определенные тесты разрешены только для людей с подозрением на COVID-19 или для людей с симптомами COVID-19, которые начались в течение определенного количества дней. Поставщик медицинских услуг может помочь определить, какой тест лучше всего подходит для вашей ситуации. Домашний сбор только по рецепту и домашние тесты могут потребовать от вас ответа на некоторые вопросы в Интернете, чтобы поставщик медицинских услуг мог определить, назначить ли вам конкретный тест или заказать его.
Тесты без рецепта — Некоторые тесты доступны без рецепта.Домашние тесты и тесты на дому, доступные без рецепта, могут называться «напрямую потребителю» (DTC) или «без рецепта» (OTC). Тесты DTC и OTC можно приобрести в аптеке или в Интернете, но они могут быть доступны не везде.
Домашнее собрание и домашние тесты
Могу ли я пройти тест на дому? В чем разница между домашним сбором и домашним тестом? Какой комплект мне нужно заказать? Чтобы ответить на эти вопросы, важно понимать разницу между тестами на COVID-19 и домашними тестами по сравнению с домашними тестами.
Почему это важно? Эти различия определяют, где будет собираться образец, где проводится тест и насколько быстро вы узнаете результаты. Хотя домашние тесты могут быть самым быстрым и удобным вариантом, они могут не подходить для всех ситуаций.
Если вы хотите быть уверены, что приобретаемый вами тест одобрен FDA, посетите наши таблицы разрешений на использование в чрезвычайных ситуациях (EUA) по молекулярным, антигенам, серологии и адаптивному иммунному ответу.
Используя поле поиска в таблицах EUA, вы можете использовать ключевые слова для поиска и фильтрации типа теста или набора для сбора, который вы ищете. С помощью этого поиска, когда новые тесты разрешены для использования, потребители могут получить доступ к актуальной информации об авторизованных тестах и наборах для сбора.
Типы образцов
Разрешается использовать разные тесты с разными типами образцов. Наиболее распространенные типы образцов:
Образцы тампона используют тампон (аналогичный длинной ватной палочке) для взятия образца из носа или горла.Типы образцов включают:
- Передние ноздри (носовые) — образец берут прямо из ноздрей
- Средняя носовая раковина — проба берется изнутри носа
- Носоглотка — образец берется из глубины носа, достигая задней части глотки
- Ротоглотка — забор пробы из средней части глотки (глотки) сразу за ротовой полостью
Образцы слюны собирают путем сплевывания в пробирку, а не с помощью мазка из носа или горла.
Образцы крови используются только для тестирования на антитела, а не для диагностики COVID-19. Образцы венозной крови обычно берут в кабинете врача или в клинике. Некоторые тесты на антитела используют кровь из пальца.
Тестирование объединенной выборки
Один из способов для лабораторий проверить больше людей на COVID-19 — объединить образцы, полученные от нескольких человек, в один образец и протестировать их вместе, что также называется «объединением». Объединение наиболее полезно в тех областях, где ожидается, что большинство образцов будут отрицательными.Это экономит время и тестовые материалы, когда ожидается лишь очень небольшое количество положительных результатов, что позволяет лабораториям тестировать больше образцов.
Если тест отрицательный или не обнаруживает SARS-CoV-2, то ни один из людей, чьи образцы были включены в объединенную выборку, скорее всего, не болен активной инфекцией COVID-19.
Если тест положительный, показывая наличие вируса, вызывающего COVID-19, каждый проходит повторное тестирование отдельно, либо путем взятия нового образца, либо тестирования оставшейся части исходного образца, чтобы найти положительные образцы.
Анализ результатов теста
Как правило, для диагностических тестов отрицательный результат означает, что тест не обнаружил вирус SARS-CoV-2, а положительный результат означает, что тест действительно обнаружил вирус SARS-CoV-2, и у вас очень высока вероятность заражения COVID-19. .
Однако ни один тест не идеален. Всегда есть шанс, что тест вернет ложный результат. Для диагностических тестов ложноотрицательный результат означает, что у вас нет COVID-19, но вы инфицированы, а ложноположительный результат означает, что у вас есть COVID-19, но вы не инфицированы.
Из-за этого, даже если вы получили отрицательный результат, вы должны продолжать практиковать профилактические меры, такие как дистанцирование, мытье рук и ношение масок, чтобы снизить риск распространения COVID-19.
Если вы заболели, вам следует оставаться дома и изолироваться от других, даже если вы получите отрицательный результат теста. Поговорите со своим лечащим врачом, чтобы определить, следует ли вам пройти повторное обследование или получить совет по лечению симптомов.
Для серологических тестов отрицательный результат означает, что тест не обнаружил антител к вирусу, вызывающему COVID-19.Положительный результат означает, что тест действительно обнаружил антитела к вирусу, вызывающему COVID-19, и возможно, что у вас была недавняя или предыдущая инфекция COVID-19, и у вас развился адаптивный иммунный ответ на вирус.
Мы не знаем, как долго антитела остаются в организме после заражения вирусом, вызывающим COVID-19. Мы не знаем, дают ли антитела вам защитный иммунитет против вируса, поэтому результаты серологического теста не следует использовать для определения наличия у вас иммунитета от вируса.FDA предостерегает пациентов от использования результатов любого серологического теста в качестве указания на то, что они могут прекратить принимать меры для защиты себя и других, такие как прекращение социального дистанцирования или прекращение ношения масок.
Ключевые термины
- SARS-CoV-2 : вирус, вызывающий COVID-19
- COVID-19 : болезнь, вызванная вирусом SARS-CoV-2
- Тест домашней коллекции : образец собирается дома, но анализируется в лаборатории
- Тест напрямую к потребителю (DTC) : тесты для домашнего забора доступны без рецепта, но образец анализируется в лаборатории
- Тестирование на дому : потребитель завершает сбор образцов и тестирование дома
- Безрецептурный тест : потребитель завершает сбор и тестирование образцов дома без рецепта
- Диагностический тест : показывает, есть ли у вас активная инфекция COVID-19
- Молекулярный тест : диагностический тест, обнаруживающий генетический материал вируса
- Полимеразная цепная реакция с обратной транскрипцией (ОТ-ПЦР) : один тип молекулярного диагностического теста
- Тест на амплификацию нуклеиновых кислот (NAAT) : один тип молекулярного диагностического теста
- Antigen Test : диагностический тест, выявляющий специфические белки вируса
- Тест на антитела (серология) : обнаруживает антитела, которые вырабатываются вашей иммунной системой в ответ на угрозу, такую как определенный вирус; не используется для диагностики активной инфекции
- Тестирование объединенных образцов : совместное тестирование нескольких образцов
Сообщить о нежелательных явлениях
FDA рекомендует медицинским работникам и пациентам сообщать о нежелательных явлениях или побочных эффектах, а также о проблемах с производительностью, связанных с использованием тестов на COVID-19 или других медицинских продуктов, в Программу информации о безопасности и нежелательных явлениях FDA MedWatch:
- Заполните и отправьте отчет онлайн через сайт MedWatch FDA.
- Загрузите форму или позвоните по телефону 1-800-332-1088, чтобы запросить форму, затем заполните и верните по адресу, указанному в форме, или отправьте по факсу 1-800-FDA-0178.
Молекулярная диагностика — обзор
Введение
Молекулярная диагностика — это раздел лабораторной медицины или клинической патологии, который использует методы молекулярной биологии для диагностики заболевания, прогнозирования течения заболевания, выбора лечения и мониторинга эффективности терапии. Молекулярная диагностика связана практически со всеми клиническими специальностями и является жизненно важным дополнением к нескольким областям клинической и лабораторной медицины, но чаще всего связана с инфекционными заболеваниями, онкологией и генетикой.Предметом этой главы является молекулярная генетика, которая занимается анализом нуклеиновых кислот человека в их отношении к болезням.
С момента завершения первого рабочего проекта последовательности человеческого генома в 2000 году и завершения уточненной последовательности в 2003 году прогресс в молекулярной генетике был быстрым и не показывает никаких признаков ослабления. В конце 1990-х было клинически доступно относительно небольшое количество генетических тестов, тогда как сегодня доступно более 5000 тестов. Кроме того, молекулярно-генетическое тестирование оказалось достаточно полезным и надежным, чтобы его можно было расширить до популяционного скрининга.Молекулярное тестирование служит заключительным подтверждающим тестом для нескольких заболеваний, включенных в расширенные программы скрининга новорожденных, и в 2003 году Американский колледж медицинской генетики и Американский конгресс акушеров и гинекологов рекомендовали популяционный скрининг носителей кистозной болезни. фиброз с использованием молекулярного тестирования будет внедрен в Соединенных Штатах.
Молекулярная генетика как дисциплина и как клиническая лабораторная служба существует не на пустом месте.Скорее, это тесно связано с молекулярной и клеточной биологией и центральной парадигмой молекулярной биологии, согласно которой гены кодируют белки. Таким образом, понимание генезиса нарушения функции белка может быть достигнуто посредством анализа генов. Такое исследование, в частности, влечет за собой оценку того, как последовательность ДНК гена сравнивается с его последовательностью дикого типа или нормальной последовательностью. В конечном итоге нарушения функции белков, связанные с мутациями генов, приводят к дисфункции органов и болезненным состояниям. В этой главе будут рассмотрены основы молекулярной генетики и она разделена на пять разделов, в которых рассматриваются концепции, присущие молекулярной генетике.Первый раздел посвящен молекулярной структуре ДНК, транскрипции ДНК и трансляции белков. Второй раздел посвящен молекулярной патологии, репликации ДНК и механизмам восстановления ДНК. В третьем разделе представлен базовый обзор генетики передачи. Четвертый раздел подчеркивает взаимосвязь между генами, белками и фенотипом и включает обоснование молекулярно-генетического тестирования. В последнем разделе рассматривается аллельная гетерогенность и соответствующий выбор аналитической методологии.
Массовое и быстрое тестирование на COVID-19 возможно с помощью безэкстракционной ОТ-ПЦР SARS-CoV-2
Разработка SARS-CoV-2 hid-RT-PCR
Мы начали с изучения того, как транспортные среды используются для взятия мазков влияют на ОТ-ПЦР. Для этого мы добавили синтетическую полногеномную РНК SARS-CoV-2 (SKU102024-MN
7.3, Twist Biosciences) в серии разведений трех различных транспортных сред (Virocult MED-MW951S, Sigma; Transwab MW176S, Sigma и Eswab 482). C, COPAN), использованный для отбора клинических образцов во время и в месте исследования (больница Каролинского университета, Стокгольм, Швеция).Каждый ложный образец содержал 50 000 копий синтетической пРНК SARS-CoV-2 и 95-0,1% среды, что соответствует 47,5-0,05% среды в реакции RT-PCR. Мы провели однократную ОТ-ПЦР с использованием 10 мкл образца в 20 мкл реакции (TaqPath, Thermo, A15299) и набора праймер-зонд для нуклеокапсида CDC 1 (N1) (Таблица 1, Методы) и зарегистрированного порога цикла (C T ) значения для серии разбавлений среды. Мы наблюдали ингибирующие эффекты во всех трех средах и, что важно, выраженные различия между средами (рис.2а). Virocult и Transwab продемонстрировали сходные профили ингибирования, что привело к + 2-3 C T при наивысших концентрациях среды и минимальное ингибирование при концентрациях ниже 30% среды в реакции RT-PCR. Eswab полностью препятствовал обнаружению при высоких концентрациях, но достиг такого же низкого уровня ингибирования, как Virocult и Transwab при концентрации 25% в реакции. Чтобы проверить, что партия использованной синтетической РНК не содержала устаревшую ДНК-матрицу, мы дополнительно провели реакции ОТ и КПЦР в два отдельных этапа («Методы»), включая ОТ ± контроли, которые продемонстрировали отсутствие сигнала амплификации ДНК при использовании обратной транскриптазы. исключены из реакции (дополнительный рис.1а). Вместе эти результаты указывают на минимальное ингибирование или отсутствие ингибирования Virocult, Transwab и Eswab на уровне ≤25% в реакции RT-PCR, что соответствует ≤5 мкл образца в реакции RT-PCR SARS-CoV-2 на 20 мкл. Таблица 1 Праймеры и зонды, используемые для ОТ-ПЦР SARS-CoV-2. Рис. 2: SARS-CoV-2 hid-RT-PCR на замороженных образцах мазков из носоглотки.a C Значения T из RT-qPCR, выполненные в серии разведений транспортной среды (Virocult, Transwab и Eswab) с использованием 50000 копий синтетической полногеномной РНК SARS-CoV-2 и праймера-зонда N1 задавать.Линии представляют собой среднее значение дубликатов, показанных по отдельности в виде точек. НД: не обнаружено. b Столбчатые диаграммы C T из SARS-CoV-2 hid-RT-PCR на клинических мазках из носоглотки, инактивированных внешним буфером для лизиса MagNA Pure 96 (ELB) или нагреванием (65 ° C 30 мин). Точки указывают на C T дубликатов hid-RT-PCR, а крестики указывают на значения C T из диагностики, выполненной на свежей извлеченной РНК. Положительные контроли экстрагировали РНК из положительного образца (P) и плазмиды ДНК положительного контроля CDC (CDC +).Отрицательные контроли экстрагировали РНК из отрицательного образца (N) и воды (H 2 O). НД: не обнаружено. c Графики амплификации, показывающие нормализованное значение репортера (ΔRn, линейная шкала) как функция цикла кПЦР для эксперимента и образцов, описанных в ( b ). ( d ) Гистограммы значений C T для 11 положительных образцов мазков из носоглотки с использованием наборов праймер-зонды, нацеленных на ген E, N и RdRP SARS-CoV-2. и Коробчатые диаграммы различия C T в тех же образцах, что и в (d), при сравнении E и RdRP с набором праймер-зонд N1.Центральные линии обозначают медиану, петли обозначают межквартильный диапазон (IQR), а усы обозначают точки выбросов при максимальном 1,5 × IQR. f , g Линейные диаграммы C T из отдельных клинических образцов (цветные линии) с использованием переменного количества вводимых образцов. Показано как абсолютное значение C T ( f ) или C T относительно ввода 10 мкл (г). ч Диаграммы разброса значений C T из клинической диагностики, выполненной на извлеченной РНК ( y -ось) и hid-RT-PCR ( x -ось) 85 образцов мазков из носоглотки, показанных для разных праймеров-зондов установить сравнения.Ро указывает на корреляцию Спирмена положительных образцов. НД: не обнаружено. i Тепловая карта значений C T из диагностики, выполненной на 85 клинических образцах с использованием извлеченной РНК (E, RdRP) и hid-RT-PCR (N1, RdRP), ранжированных по гену E C T . Контроль целостности образца с помощью ОТ-ПЦР для РНКазы P в тех же образцах, что показаны справа. Два пациента, отмеченные звездочкой, были отрицательными при диагностике на основе экстракции, но положительными при hid-RT-PCR. Позднее пациенты были повторно протестированы с помощью клинической диагностики на основе экстракции, и было подтверждено, что они имеют SARS-CoV-2 положительный результат.Пациента, помеченного кольцом, повторное обследование не проводилось. Три образца, отмеченные решёткой, были признаны COVID-19-положительными с помощью стандартной диагностики, но не с помощью какого-либо набора праймеров в hid-RT-PCR. j Диаграмма разброса значений C T из 19 согласованных свежих ( x -ось) и замороженно-размороженных ( x -ось) экстрагированных образцов с использованием гена E (крест) и праймера RdRP (звездочка). наборы датчиков. НД: не обнаружено. Показанная на этом рисунке hid-RT-PCR была проведена на ранее диагностированных замороженных образцах.
Чтобы проверить, может ли прямая ОТ-ПЦР точно определить присутствие SARS-CoV-2 в клинических образцах, мы начали с получения пяти аликвот образцов мазков из носоглотки, хранящихся в транспортной среде при –20 ° C. Аликвоты тех же образцов ранее были клинически диагностированы с использованием стандартной экстракции РНК (MagNA Pure 96 DNA и Viral NA SV Kit, Roche Diagnostics 06543588001) с последующей ОТ-ПЦР, в которой три образца пациентов были признаны SARS-CoV-2 положительными, а два — отрицательными. к вирусу (Клиническая диагностика проводится в больнице Каролинского университета, Стокгольм).Мы инактивировали образцы носоглотки либо путем добавления буфера для внешнего лизиса MagNA Pure 96 (Roche, 06374
1), используемого при стандартной очистке РНК, либо путем нагревания при 65 ° C в течение 30 минут, и провели прямую ОТ-ПЦР с использованием 3 мкл образца. Мы наблюдали отсутствие амплификации в образцах, положительных по SARS-CoV-2, инактивированных внешним буфером для лизиса (рис. 2b, c и дополнительный рис. 1b). Однако ОТ-ПЦР, проведенная непосредственно на инактивированных нагреванием образцах, правильно выявила SARS-CoV-2 во всех положительных образцах и не содержала сигнала в отрицательных образцах и контролях (рис.2б, в). Это указывает на жизнеспособность дальнейшего изучения инактивированной нагреванием прямой ОТ-ПЦР (hid-RT-PCR) в качестве метода обнаружения SARS-CoV-2 в клинических образцах. Мы также протестировали двухэтапную ОТ и КПЦР для обнаружения SARS-CoV-2 на одних и тех же клинических образцах («Методы»), правильно определив присутствие и отсутствие вируса (дополнительный рисунок 1c).Затем мы проверили эффективность набора праймер-зонд в hid-RT-PCR с использованием образцов мазков из носоглотки и наборов праймеров-зондов, нацеленных на РНК-зависимую РНК-полимеразу (RdRP) генов SARS-CoV-2, оболочку (E) и нуклеокапсид. (N1) (Таблица 1).Мы получили дополнительные образцы носоглоточных мазков, инактивированных нагреванием (65 ° C, 30 мин), которые были названы положительными на SARS-CoV-2 в предыдущей клинической диагностике («Методы»). В наших условиях мы наблюдали умеренную разницу между N1 и RdRP в hid-RT-PCR (среднее и медианное отличие C T от N1: 0,63 и 0,27, P = 0,032, ранговый критерий Вилкоксона), в то время как Набор E-генов проявился при значительно более высоких значениях C T , чем другие наборы праймер-зонд (среднее и медианное отличие C T от N1: 2.9 и 1.7, P = 0,00098, знаковый ранговый критерий Вилкоксона) (рис. 2d, e), что соответствует предыдущим результатам 10 . Мы утверждаем, что использование коротких ампликонов-мишеней имеет решающее значение для hid-RT-PCR из-за ожидаемой фрагментации РНК во время нагревания, в то время как соображения по длине ампликона должны быть менее важны для амплификации ПЦР, выполняемой на извлеченной РНК из свежих образцов. Благодаря превосходным характеристикам N1 в hid-RT-PCR, мы сосредоточили внимание на этом наборе праймеров-зондов в углубленных анализах hid-RT-PCR.
Наши эксперименты по разбавлению среды и синтетической РНК SARS-CoV-2 показали ограниченное ингибирование при ≤25% среды в реакции (рис. 2а). Однако клинические образцы содержат дополнительный материал из мазка и другие неизвестные и потенциально ингибирующие агенты. Кроме того, из-за потенциально большой вариабельности между клиническими образцами важно охарактеризовать кривые ингибирования в нескольких отдельных клинических образцах, а не в усредненной смеси образцов. Оптимальное количество образца, вводимого в hid-RT-PCR, должно быть балансом между возможным ингибированием образца и количеством РНК, вступающей в реакцию.Чтобы определить оптимальный диапазон ввода пробы в клинические образцы, мы выполнили серии разведений (10–0,01 мкл) отдельных образцов носоглоточных мазков, инактивированных нагреванием, и обнаружили ввод 1–4 мкл образца в 20 мкл RT. -Реакция ПЦР должна быть оптимальной, избегая резкого ингибирующего эффекта при более высоких количествах вводимого образца, наблюдаемого в некоторых отдельных образцах, но при этом минимизируя C T (рис. 2f, g).
Чтобы начать исследовать, может ли прямая ОТ-ПЦР на инактивированных нагреванием образцах обеспечить эффективную диагностику COVID-19, мы выполнили тепловую инактивацию (65 ° C 30 мин) замороженных (-20 ° C) аликвот из 85 клинически диагностированных носоглоточных образцов. и провели скрытую ОТ-ПЦР вслепую для определения своего статуса COVID-19.Мы использовали входные 4 мкл и праймеры N1, RdRP, а также РНКазу P для оценки целостности образца. После этого мы объединили результаты hid-RT-PCR со значениями C T из клинической диагностики, выполненной на извлеченной РНК (MagNA Pure 96, Roche Diagnostics, 1: 1 объем вводимого элюата, тест, нацеленный на E и RdRP, Методы). Мы наблюдали сильную корреляцию между значениями C T извлеченных и инактивированных нагреванием образцов (рис. 2h) и общим соответствием вызовов SARS-CoV-2 (рис. 2i). Однако значения C T для hid-RT-PCR (65 ° C 30 мин) на замороженных образцах были выше, чем для элюатов свежей РНК тех же образцов (медиана 6.7 C T разница) (рис. 2h, i). Это ожидалось, учитывая, что (1) для элюатов было загружено больше РНК (2,5x, стандартный ввод 10 мкл против эквивалента объема 4 мкл в hid-RT-PCR), (2) экстракция РНК элюатов выполнялась на свежих образцах, в то время как аликвоты, используемые для hid-RT-PCR, были заморожены и хранились при –20 ° C перед тепловой инактивацией; (3) нагревание может разрушить РНК в присутствии РНКаз и / или ионов металлов (расщепление РНК на основе ионов металлов). Выполнив повторную экстракцию РНК из 19 аликвот, размороженных замораживанием и сравнив значения C T с элюатами соответствующих свежих аликвот тех же образцов из носоглотки, мы обнаружили, что эффект замораживания-оттаивания приводит к + 2-3 C T ( Инжир.2j).
Таким образом, наши данные из 85 клинически диагностированных замороженных образцов носоглотки показали, что hid-RT-PCR может быть рабочим вариантом для диагностики SARS-CoV-2 на основе экстракции, и что усилия по оптимизации протокола hid-RT-PCR для максимальная производительность будет стоить того.
Оптимизация SARS-CoV-2 hid-RT-PCR
Чтобы определить оптимальную программу тепловой инактивации, предшествующую hid-RT-PCR, мы подвергли 50 мкл свежих (незамороженных) аликвот тех же клинических образцов носоглотки в транспортной среде. различные температуры и время инкубации (65 ° C 30 мин; 95 ° C 5 мин; 95 ° C 10 мин; 95 ° C 15 мин; 98 ° C 5 мин; n ≥ 11 образцов пациентов).Мы наблюдали последовательное улучшение (снижение) значений hid-RT-PCR C T в аликвотах, инактивированных при 95 ° C 5 мин по сравнению с 65 ° C 30 мин (медиана изменения C T : -1,3, P = 1,1 × 10 -5 , критерий знакового ранга Вилкоксона, набор праймер-зонд N1) (рис. 3а). Интересно, что все другие испытанные высокотемпературные (≥95 ° C) условия привели к тому, что C T была аналогична 5-минутной обработке 95 ° C ( P > 0,05, тесты Вилкоксона с поправкой на FDR) (рис.3а). Таким образом, мы приходим к выводу, что инактивацию перед hid-RT-PCR следует проводить при 95–98 ° C. Этот результат является удачным и важным, поскольку инкубация при такой высокой температуре должна полностью инактивировать вирус 11 . Более того, стабильность в течение всего времени инкубации (5–15 мин) при высокой температуре демонстрирует замечательную надежность процедуры.
Рис. 3: Оптимизация условий тепловой инактивации для SARS-CoV-2 hid-RT-PCR. Значенияa C T для аликвот образцов мазков из носоглотки, инактивированных при различных температурных и временных условиях, показаны на абсолютной шкале (слева) и C T изменяются относительно 5-минутных условий 95 ° C (справа). P — значения, рассчитанные как двусторонние знаковые ранговые критерии Вилкоксона. * FDR исправлен для многократного тестирования. Медианные значения показаны красным. b Тепловые карты рангов на основе абсолютных значений C T для образцов мазков из носоглотки ( n = 20) с добавлением или без добавления поливинилсульфоновой кислоты (PVSA) и / или этилендиаминтетрауксусной кислоты (EDTA) перед проведением тепловой инактивации при 95 ° C в течение 5 мин. Для образцов, содержащих ЭДТА, в реакцию ОТ-ПЦР добавляли эквимолярную добавку MgCl 2 , как указано.Одни и те же образцы повторно оценивали с помощью RT-qPCR через разное количество дней хранения при 4 ° C после тепловой активации. Все условия перечислены в таблице 2. c Коробчатые диаграммы значений C T относительно состояния 95 ° C без добавок, упорядоченные по рангу в (b). Центральные линии обозначают медианное значение, петли обозначают IQR, а усы обозначают точки выброса при максимальном 1,5 × IQR. d Изменение ранга за дни хранения при 4 ° C. Цвета и порядок такие же, как в ( b , c ).Аннотации относятся к образцам, хранящимся 0 дней. e Изменение значений C T за дни хранения при 4 ° C в различных условиях. Толстая линия и лента обозначают подобранную кривую LOESS и доверительный интервал ± 95% соответственно. Пунктирная линия указывает на 95 ° C (без добавки).
Затем мы проверили, можно ли улучшить hid-RT-PCR путем добавления химического, термостабильного ингибитора РНКаз поливинилсульфоновой кислоты (PVSA) и / или хелатирующего агента этилендиаминтетрауксусной кислоты (EDTA) во время тепловой инактивации.PVSA вдвое снижает активность РНКазы A in vitro (50% ингибирование, IC 50 ) при концентрации 150 мкг / мл и вдвое снижает активность РНКазы лизата E. coli (IC 50 ) при 430 мкг / мл 12 . В то же время PVSA может ингибировать ОТ-ПЦР. Выполнив серии разведений PVSA с использованием синтетической РНК SARS-CoV-2 (SKU102024-MN
7.3, Twist Biosciences) в качестве матрицы, мы определили диапазон концентраций с предполагаемым ингибированием РНКазы в образце, но с ограниченным ингибированием RT-PCR (дополнительный рис.1г). Затем мы добавили свежие аликвоты из 20 клинических образцов носоглотки с диагнозом COVID-19 в транспортной среде с различными количествами PVSA и / или EDTA, а для условий, содержащих EDTA, мы дополнительно провели тесты с добавлением эквимолярных количеств MgCl 2 в RT- Смесь для ПЦР (12 условий и 20 образцов, n = 240) (таблица 2). Чтобы дополнительно проверить стабильность РНК при различных обработках с течением времени при хранении (4 ° C), мы определили изменение SARS-CoV-2 RT-PCR C T в тех же образцах за разное количество дней (0, 1, 4, и 7) после тепловой инактивации.Мы ранжировали обработки в каждом образце и в каждый день, и мы наблюдали, что 95 ° C 5 мин + 150 мкг / мл PVSA дали наивысший балл (самый низкий C T ), а затем 95 ° C 5 минут без добавок с 0 по 4 день. (Рис. 3b – d). Преимущество ЭДТА и более высоких концентраций PVSA стало очевидным только после 4-7 дней хранения (4 ° C) (рис. 3d, e). Интересно, что хотя значения C T со временем увеличивались, результаты временного ряда показали, что образцы, инактивированные нагреванием, неожиданно стабильны до одной недели при хранении при 4 ° C. Таблица 2 Условия тепловой инактивации, протестированные для оптимизации SARS-CoV-2 hid-RT-PCR.Учитывая хорошие характеристики условий 95 ° C в течение 5 минут без добавок (разница менее 1 ° C T по сравнению с 150 мкг / мл PVSA, рис. 3c), а также простоту обращения с образцами, мы выбрали это условие для дальнейшего использования. сравнительный анализ.
Наконец, чтобы экспериментально подтвердить эффективность процедуры термической инактивации, мы размножили SARS-CoV-2 in vitro («Методы») и подвергали активные собранные вирусные частицы (~ 2.5 миллионов бляшкообразующих единиц (БОЕ) в 500 мкл) для нагревания при 95 ° C в течение 5 мин. Затем мы провели анализ бляшек на клетках Vero E6, действительно продемонстрировав отсутствие образования бляшек на инактивированных нагреванием образцах (рис. 4).
Рис. 4: Тепловая инактивация SARS-CoV-2, подтвержденная анализом бляшек.Коробчатые диаграммы, показывающие количество бляшкообразующих единиц (БОЕ), наблюдаемых после тепловой инактивации (95 ° C 5 мин, слева) активного SARS-CoV-2, размноженного in vitro, а также для серии разведений SARS-CoV-2 без тепловой инактивации (справа), с кружками, обозначающими значения отдельных повторов.Центральные линии обозначают медианное значение, петли обозначают IQR, а усы обозначают точки выброса при максимальном 1,5 × IQR. Вирус добавляли в чашки размером 9,6 см. 2 , засеянные 1 миллионом клеток Vero E6, и анализы бляшек выполняли, как описано в разделе «Методы». Неразбавленные образцы содержали ~ 2,5 миллиона БОЕ SARS-CoV-2. Репрезентативные изображения показаны под каждым условием (шкала 5 мм).
Бенчмаркинг SARS-CoV-2 hid-RT-PCR
Оптимизировав условия тепловой инактивации, мы затем протестировали SARS-CoV-2 hid-RT-PCR (95 ° C 5 мин) с использованием системы cobas 6800 ( Roche Diagnostics; далее именуется cobas) и большой набор парных клинических образцов носоглоточных мазков в качестве эталона.Чтобы сначала проверить эффективность cobas по сравнению с обычной ОТ-ПЦР на элюированной РНК, мы определили значения C T для 21 очищенного клинического образца носоглоточного мазка и провели эксперимент по пределу обнаружения с тем же образцом (разведение от 1: 100 до 1: 100 000) в обеих системах и наблюдал более высокую скорость обнаружения и чувствительность кобаз (дополнительные таблицы 1, 2). Учитывая его производительность и тот факт, что cobas представляет собой стандартизированную и полностью автоматизированную систему (исключающую ручную обработку образцов), мы сочли ее подходящей системой для проверки SARS-CoV-2 hid-RT-PCR.Мы собрали аликвоты 597 клинических образцов мазков из носоглотки, диагностированных на анализаторе cobas в тот же день, с использованием двух мишеней (наборы праймер-зонд для ORF1 и E; «Цель 1» и «Цель 2» cobas SARS-CoV-2, P / N: 09175431190, Roche Diagnostics) и выполнили тепловую инактивацию (95 ° C, 5 мин), а затем SARS-CoV-2 hid-RT-PCR (набор праймер-зонд N1, ввод образца 4 мкл). Значения C T для hid-RT-PCR и cobas хорошо коррелировали и имели схожие распределения значений C T ( P = 0.11 и 0,88; N1 против ORF1 и E соответственно; Тест Колмогорова – Смирнова) (рис. 5а, б). В дополнение к 597 образцам, перекрестно сравниваемым с hid-RT-PCR, мы построили график 9437 исторических значений носоглоточного SARS-CoV-2 C T , собранных на той же машине cobas, и наблюдали, что распределение значений C T для 597 Образцы были репрезентативными для большей выборки ( P = 0,23 и 0,35; ORF1 и E, соответственно; тест Колмогорова-Смирнова) (рис. 5c – d). Наконец, мы классифицировали статус COVID-19 597 образцов мазков из носоглотки на кобах, требуя либо положительного сигнала ( C T ≤ 40) для обеих целей (ORF1 и E), либо любой цели (ORF1 и / или E), чтобы назвать образец SARS-CoV-2 положительным (рис.5д, крайние левые столбцы). Мы составили тепловую карту обнаружения SARS-CoV-2 (C T ) и наблюдали замечательное соответствие между cobas и hid-RT-PCR (рис. 5e – g). Используя диагностический вызов обеих мишеней cobas в качестве эталона, hid-RT-PCR имела точность, чувствительность и специфичность 98,8% (95% доверительный интервал, CI 95 : 97,5–99,5%), 96,0% и 99,8%. соответственно (таблица 3). Требуется только одна мишень cobas для вызова образцов, положительных на SARS-CoV-2, точность, чувствительность и специфичность hid-RT-PCR составила 97.5% (ДИ 95 : 95,9–98,6%), 91,4% и 99,8% соответственно. Мы наблюдали эффективность hid-RT-PCR (95 ° C, 5 мин) с использованием набора праймеров-зондов N1, чтобы быть похожими на мишень cobas ORF1 (таблица 3 и фиг. 5f-h). Затем мы рассчитали чувствительность hid-RT-PCR при различных порогах C T и C T (как обнаружено наиболее чувствительной мишенью E-гена cobas; предел обнаружения ORF1: 0,009 TCID 50 / мл. , E: 0,003 TCID 50 / мл; дополнительная таблица 2) и обнаружил, что hid-RT-PCR эффективно теряет чувствительность только для образцов, обнаруженных при C T 35–40 мишенью cobas E, т.е.е., близкой к пределу обнаружения (рис. 5i, j).
Рис. 5: Проверка SARS-CoV-2 hid-RT-PCR.a Графики разброса значений C T из клинической диагностики, выполненной на Roche Diagnostics cobas 6800 ( y -ось) и hid-RT-PCR ( x -ось) для 597 образцов носоглоточных мазков, показаны для сравнения различных наборов праймер-зонд. Ро указывает на корреляцию Спирмена положительных образцов. НД: не обнаружено. b Гистограммы значений C T из 597 парных образцов назофарингеальных мазков показаны для следующих наборов праймер-зонд и условий: cobas ORF1, cobas E и hid-RT-PCR N1.НД: не обнаружено. c Гистограммы значений C T из 9437 клинических образцов, проанализированных на cobas 6800, показаны для ORF1 (слева) и E (справа). d Диаграммы разброса значений C T из 9437 клинических образцов, проанализированных на cobas 6800. Rho указывает корреляцию Спирмена положительных образцов. НД: не обнаружено. e Тепловая карта значений C T по результатам диагностики, выполненной на 597 клинических образцах мазков из носоглотки с использованием cobas 6800 (наборы ORF1 и E праймер-зонд) и hid-RT-PCR (N1).Полосы слева указывают на клинический вызов от системы диагностики cobas с учетом обнаружения либо в обоих, либо только в одном (любом) наборе праймеров-зондов для диагностического вызова. f — h Матрица ошибок диагностического вызова от cobas 6000 и hid-RT-PCR (N1) для данных, показанных в ( e ). i Процентная чувствительность hid-RT-PCR (N1) с использованием наборов праймер-зонд cobas ORF1 и E в качестве эталона, показана как функция от порогового значения C T для того же образца, обнаруженного с помощью набора праймер-зонд cobas E .Красные линии обозначают совокупную чувствительность ниже заданного порогового значения C T , а полосы обозначают чувствительность в ячейках 5-C T . j То же, что ( i ), но с использованием наборов праймеров-зондов cobas ORF1 и / или E в качестве эталона для расчета чувствительности.
Таблица 3 Точность, чувствительность и специфичность SARS-CoV-2 hid-RT-PCR.Вместе эти данные демонстрируют, что простая программа тепловой инактивации с последующей прямой ОТ-ПЦР с использованием пары праймер-зонд CDC N1 выявляет SARS-CoV-2 с поразительной точностью, чувствительностью и специфичностью, учитывая простоту метода.В результате обнаружение SARS-CoV-2 без очистки РНК является жизнеспособным, обеспечивая дешевое, масштабируемое и быстрое тестирование COVID-19.
Общие транспортные буферы, оптимальные для прямого тестирования ОТ-ПЦР
Наша проверка продемонстрировала диагностический потенциал SARS-CoV-2 hid-RT-PCR для клинических образцов носоглотки, собранных в трех коммерческих транспортных средах (Virocult, Transwab и Eswab). Хотя ингибирование среды было успешно обойдено путем разбавления в реакции RT-PCR (фиг. 2), эта процедура уменьшала вводимое количество образца (вводимые 4 мкл на 20 мкл реакции).Дополнительные данные по ингибированию для широко используемой универсальной транспортной среды (копан, клинически не используемой в месте и во время исследования) доступны на дополнительном рисунке 2. Однако оптимально для метода ОТ-ПЦР без экстракции материал мазка будет собираются в транспортном буфере, который вообще не ингибирует ОТ-ПЦР, поскольку это позволит максимально увеличить вводимый объем образца, улучшая чувствительность анализа. Простой и универсальный состав транспортного буфера также может быть дешевой альтернативой коммерческим транспортным средам и, таким образом, подходить для массового тестирования.Чтобы идентифицировать такие буферы, мы добавили фиксированное количество активного расширенного in vitro SARS-CoV-2 в 17 различных универсальных буферов (50 000 БОЕ в объемах 100 мкл, выполненных в трех повторностях, «Методы») (буферы перечислены в дополнительной таблице 3). Затем мы выполнили тепловую инактивацию (95 ° C 5 мин) с последующей ОТ-ПЦР (набор праймеров-зондов N1) с использованием 4, 7, 10 или 13,5 мкл вводимых в 20 мкл реакции ОТ-ПЦР для характеристики ингибирования. Это позволило идентифицировать несколько хорошо действующих буферных составов без ингибирования при максимальном вводе (13.5 мкл на 20 мкл реакции RT-PCR), например, PVSA в воде, свободной от нуклеаз (50 мкг / мл), TE, Tris-буфере и даже воде, свободной от нуклеаз (рис. 6a) (обратите внимание, что буферы, обработанные DEPC, являются неподходящий, «Методы»). Интересно, что физиологический раствор (0,9% NaCl) и 100 мМ PBS показали заметное ингибирование при более высоких входных уровнях, причем профили ингибирования были аналогичны профилям Eswab (рис. 6a). Таким образом, физиологический раствор и 100 мМ PBS совместимы с SARS-CoV-2 hid-RT-PCR при меньших входных объемах (4 мкл на вход 20 мкл реакции RT-PCR), но явно неоптимальный выбор транспортного буфера для ОТ-ПЦР без экстракции.
Рис. 6. Идентификация общих транспортных буферов, оптимальных для SARS-CoV-2 hid-RT-PCR.a Линейные диаграммы значений C T ( y -ось) из hid-RT-PCR (пара праймер-зонд N1) для различного объема входного образца (13,5, 10, 7 или 4 мкл до реакция 20 мкл; x -ось), демонстрирующая профиль ингибирования различных транспортных буферов и сред. Эксперимент выполняли путем добавления равного количества расширенного in vitro SARS-CoV-2 к каждому условию буфера в трех экспериментальных повторностях (точки).Пунктирные черные линии обозначают PVSA в состоянии H 2 O, включенном для сравнения. Буферы заказываются в соответствии с минимальным C T . b Линейные диаграммы значений C T ( y -ось) из hid-RT-PCR (пара праймер-зонд N1, ввод 4 мкл для реакции 20 мкл) расширенного in vitro SARS-CoV-2, хранящегося в различные буферы на срок до 7 дней ( x -ось) в холодильнике (4 ° C, квадрат) или при комнатной температуре (21 ° C, треугольник) перед тем, как подвергнуть образцы тепловой инактивации (95 ° C 30 мин) и скрыть ОТ-ПЦР.Данные представлены в виде отдельных повторов (точки, n = 3) и медианы (линия).
Работоспособный транспортный буфер должен поддерживать обнаруживаемые уровни SARS-CoV-2 через несколько дней после сбора образца. Поэтому мы также охарактеризовали, как значения C T менялись с течением времени при хранении в различных буферах. Мы добавили активный SARS-CoV-2 в буферы (50 000 БОЕ в 100 мкл) и хранили аликвоты в холодильнике (4 ° C) и при комнатной температуре (21 ° C) в трех экземплярах для каждого условия.Мы собрали аликвоты через 1, 4 и 7 дней хранения и подвергли образцы тепловой инактивации (95 ° C 5 мин) и ОТ-ПЦР (набор праймер-зонд N1), используя 4 мкл образца, введенного в 20 мкл RT- ПЦР-реакция для каждого буферного состояния. Мы построили графики значений C T для каждого буфера, момента времени и температуры хранения и наблюдали изменение C T для буферов (рис. 6b). Интересно, что химический ингибитор РНКазы PVSA в воде (pH 6,5) или 10 мМ Трис-буфере (pH 7) продуцировал почти неизменный C T в течение недели при хранении в холодильнике, а также при комнатной температуре (рис.6б).
Таким образом, мы определили простые и доступные буферы, подходящие для SARS-CoV-2 hid-RT-PCR. Важно отметить, что буферы, идентифицированные без ингибирования RT-PCR, позволяют более чем в три раза увеличивать вводимый объем образца (13,5 против 4 мкл), дополнительно повышая чувствительность анализа SARS-CoV-2 hid-RT-PCR.
Прямая ОТ-ПЦР на лизированных образцах SARS-CoV-2
Оболочки коронавируса SARS представляют собой самособирающиеся частицы, в которых липидный бислой является слабым местом 13 , таким образом, вирусная оболочка может быть разорвана поверхностно-активными веществами и одновременно время вирусной РНК может быть высвобождено из аналогичным образом лизированных человеческих клеток в образце 14 .Прямым путем скрининга на SARS-CoV-2 может быть самотестирование с использованием мазков из носа и горла или даже слюны с последующим лизисом непосредственно перед ОТ-ПЦР на неочищенных образцах. Анализы ОТ-ПЦР непосредственно на образцах, инактивированных детергентом, потребуют анализа ОТ-ПЦР, устойчивого к высоким концентрациям детергента. Мы отслеживали влияние Triton X-100 и Tween-20 на ОТ-ПЦР SARS-CoV-2 с использованием 50 000 копий синтетической полногеномной РНК SARS-CoV-2 (SKU102024-MN
7.3, Twist Biosciences). и набор праймер-зонд N1.Значения C T изменялись незначительно (+ 1-2 C T ) при инкубации с 5% Triton X-100 или 10% Tween-20 в реакции RT-PCR (рис. 7a, b) . Мы наблюдали пониженные уровни флуоресценции в фазе плато в кПЦР при повышенных концентрациях детергента, не оказывая заметного влияния на C T (рис. 7c, d). Чтобы проверить, можно ли обнаружить реальную РНК SARS-CoV-2 после прямого лизиса, мы получили шесть аликвот слюны и шесть комбинированных мазков из носа и горла в PBS от шести деидентифицированных доноров («Методы»), четыре из которых были идентифицированы как COVID. -19 положительных и два отрицательных при рутинной диагностике на основе экстракции (аликвоты образцов получены из Агентства общественного здравоохранения Швеции).Примечательно, что эти образцы не были собраны медицинскими работниками с использованием флокированных пластиковых тампонов клинического качества, а образцы были собраны самостоятельно с использованием простых ватных тампонов (осаждение в PBS) и баночки без буфера для хранения слюны (методы). Кроме того, во время нашего эксперимента эти образцы были заморожены, разморожены и хранились при комнатной температуре в течение нескольких часов вместе. Мы протестировали эти образцы вслепую, смешав 5 мкл образца (слюна или мазок из носа + горла) с 5 мкл 10 или 20% Triton X-100, и выполнили ОТ-ПЦР SARS-CoV-2 с использованием набора праймер-зонд N1 напрямую. на эти лизаты (10 мкл образца и смесь Triton X-100 в реакциях RT-PCR на 20 мкл, «Методы»).Действительно, все четыре COVID-19-положительных донора были правильно названы SARS-CoV-2-положительными по крайней мере в одном состоянии или образце Triton X-100 (слюна и / или мазок из носа + горла), в то время как у отрицательного контроля отсутствовал сигнал (рис. 7д). Рис. 7. Прямое обнаружение ОТ-ПЦР SARS-CoV-2 из лизата.a , b Линейные диаграммы значений C T (ось y) из RT-qPCR, выполненных с разным процентом (об. / Об.) Triton X-100 ( a ) или Tween-20 ( b ) ( x -ось) в реакции. c , d Графики амплификации, показывающие нормализованное репортерное значение (ΔRn, линейная шкала) как функцию цикла кПЦР для экспериментов и образцов, описанных в ( a , b ). e Столбчатые диаграммы C T из SARS-CoV-2 RT-PCR с использованием набора праймер-зонд N1, выполненного непосредственно на лизированных донорских образцах после хранения и замораживания-оттаивания из самостоятельного отбора образцов (суспензии слюны или назального + горлового мазка, взятые с деревянные палочки с ватным наконечником) без очистки.Процент Triton X-100 указывает процентное содержание детергента в образце (половина концентрации в реакции RT-PCR). Крестиками обозначены значения C T по результатам диагностики, проведенной для экстрагированной РНК из свежих аликвот.
Эти первоначальные, но принципиальные результаты демонстрируют, что прямая ОТ-ПЦР SARS-CoV-2 также может применяться к инактивированным детергентами материалам, взятым самостоятельно, что открывает альтернативный путь для крупномасштабного скрининга населения.
Антиген и молекулярные тесты | Типы тестов на COVID-19
Набор инструментов для тестирования COVID-19> Основы тестирования> Типы тестов на COVID-19> Антигенные и молекулярные тестыДиагностические тесты используются для выявления текущих активных инфекций вируса SARS-CoV-2.Диагностические тесты могут быть основаны на антигенах (экспресс-тесты на антиген), которые ищут белковые маркеры вне вируса, или они могут быть молекулярными (включая ПЦР, LAMP, CRISPR), которые ищут вирусный геномный материал, специфичный для SARS. -CoV-2. Молекулярные тесты, которые усиливают генетический материал, также называются тестами амплификации нуклеиновых кислот (NAAT).
Антигенные и молекулярные диагностические тесты:
- Ищите активную инфекцию SARS-CoV-2 по:
- Обнаруживая определенные части последовательности генома SARS-CoV-2
- Обнаруживая специфические маркеры вне SARS- Вирус CoV-2
Подробнее об антигенных и молекулярных тестах:
Как работают антигенные и молекулярные тесты?
Вирусы требуют хоста для репликации.Вирус захватывает клетки хозяина, чтобы произвести больше вирусных копий самого себя. Геномным материалом для вируса SARS-CoV-2 является рибонуклеиновая кислота (РНК), которая остается в организме, пока вирус все еще реплицируется и воспроизводится. Диагностические тесты ищут доказательства этого процесса репликации — что создается больше вирусов — для диагностики активной инфекции COVID-19.
Диагностические тесты на антигены выявляют структурные особенности внешней части вируса, называемые антигенами, — небольшие белки, из которых состоит вирус, — которые могут присутствовать в образце пациента.
Антигенные диагностические тесты работают по:
- Поиск более крупных доказательств того, что вирус SARS-CoV-2 активно заражает человека
- Обнаружение специфических трехмерных антигенов вне SARS-CoV-2 вирус
Молекулярные тесты усиливают биты вирусной РНК, чтобы вирусную инфекцию можно было обнаружить с помощью специального теста. Эти тесты также называются тестами амплификации нуклеиновых кислот (NAAT). Процедура начинается с взятия пробы из носа или рта (слюны) потенциально инфицированного человека, где может быть обнаружен вирус.Если в образце присутствует SARS-CoV-2, то даже низкие уровни вирусного геномного материала можно амплифицировать до миллионов копий, обнаруженных в ходе молекулярного диагностического анализа. Если человек инфицирован, вирусная РНК будет обнаружена и даст положительный результат теста; если человек не инфицирован, вирусная РНК не будет скопирована или обнаружена, что приведет к отрицательному результату теста. Усиление сигнала позволяет обнаруживать даже небольшое количество вируса. Эта категория диагностических тестов включает в себя тесты полимеразной цепной реакции (ПЦР), петлевой изотермической амплификации (LAMP) и кластерные анализы на основе коротких палиндромных повторов с регулярными интервалами (CRISPR).Существует множество методов молекулярной диагностики, и некоторые из них обеспечивают более быстрые результаты, чем традиционные методы на основе ПЦР. Эти быстрые молекулярные тесты включают LAMP, которые могут дать результаты за минуты, а не за часы. Быстрые молекулярные тесты, в которых используются такие методы, как LAMP, очень специфичны, но также очень чувствительны, поскольку они усиливают геномный материал в образце пациента. Важно отметить, что не все быстрые диагностические тесты являются тестами на антигены — некоторые из них представляют собой быстрые молекулярные тесты, которые очень чувствительны, но дают результаты за считанные минуты.
Молекулярные диагностические тесты работают:
- Обнаружение того, что вирус SARS-CoV-2 активно заражает человека
- Создание миллионов копий небольших сегментов вируса SARS-CoV-2, если это так. присутствует в образце пациента, усиливая сигнал
- Обнаружение этих миллионов копий на специализированных машинах
Что необходимо для проведения антигенного или молекулярного теста?
Антигенные и молекулярные тесты требуют образцов, таких как клетки поверхности носоглотки или мокрота / слюна, которые могут содержать вирус.Вирусы и другие патогены также могут быть обнаружены в кале, моче или крови. Для респираторных заболеваний, таких как COVID-19, в большинстве доступных или разрабатываемых тестов используются образцы из носа человека (с использованием мазков из носоглотки или переднего носа) или изо рта (с использованием чашек для сбора слюны), чтобы облегчить тестирование как для медицинских работников, так и для медицинских работников. пациенты.
Большинство молекулярных тестов проводится в лабораторных условиях из-за сложности и чувствительности процесса тестирования.Для получения результатов некоторых лабораторных тестов может потребоваться 1 или более дней. Некоторые тесты, в том числе многие тесты на антигены, разрешено использовать в месте оказания медицинской помощи, что означает, что они могут быть выполнены в медицинских условиях, а результаты могут быть получены в течение примерно 30 минут. Разрабатывается больше диагностических тестов для домашнего использования, с медицинским наблюдением или без него.
Антигенные и молекулярные тесты:
- Для получения результатов может потребоваться от нескольких минут до дней, в зависимости от типа используемого теста
- Может проводиться в различных условиях (дома, в офисе поставщика медицинских услуг или в лаборатории)
Как молекулярные тесты обнаруживают SARS-CoV-2?
Большинство молекулярных тестов на SARS-CoV-2 используют процесс количественной полимеразной цепной реакции с обратной транскриптазой в реальном времени (rRT-PCR).На этом сайте большинство молекулярных наборов помечены как rRT-PCR. Включенные тесты называются так, как их перечислили производители, хотя в некоторых случаях они используют qPCR. Если тест предоставляет количественную информацию, а не только качественную (да / нет), это требует количественной (q) ПЦР в дополнение к ПЦР. Эти тесты основаны на тех же основных шагах:
- Обнаружение генетического материала (ДНК или РНК), специфичного для патогена
- Амплификация (создание большего количества копий) обнаруженной области генетического материала патогена
- Произвести результат измерения количества амплифицированного генетического материала, если он присутствует в образце. геном.Затем праймеры прикрепляются или «отжигаются» к конкретным областям вирусного генома и обеспечивают основу для амплификации этой области. При создании праймеров исследователи ищут определенные части вирусного генома, которые уникальны для рассматриваемого вируса. Поскольку вирусная РНК слишком мала для визуализации и обнаружения в таких малых количествах, необходимо усиление сигнала.
Для большинства вирусных геномов на основе РНК требуется еще один этап, называемый обратной транскрипцией. Геном SARS-CoV-2 состоит из РНК, которая менее стабильна и более чувствительна к УФ-излучению и разрушению ферментами, чем ДНК.Следовательно, извлечение РНК и ее использование в тестировании необходимо проводить осторожно, чтобы сохранить генетический материал. В обратной транскрипции используются белки, называемые ферментами обратной транскриптазы, для трансляции РНК в ДНК, которая является более стабильной молекулой.
На этапе 2 область, в которой праймеры прикрепляются или отжигаются, амплифицируется в повторяющихся циклах. Эти циклы разработаны, чтобы точно имитировать естественные процессы репликации ДНК во всех клетках человека. В большинстве ПЦР циклы амплификации основаны на запрограммированных изменениях температуры, которые побуждают двухцепочечную ДНК расщепляться, позволяют ферментам репликации создавать новую копию ДНК, а затем снова закрывать вновь образованные цепи.По этой причине большинство анализов ПЦР необходимо проводить в машинах, называемых «термоциклеры», которые позволяют регулировать время цикла, температуру и количество итераций. Исключением из этого процесса являются изотермические методы, такие как петлевой изотермической амплификации (LAMP), которые не требуют циклов нагревания для амплификации целевой ДНК. Шаг 2 продолжается до тех пор, пока исследователи не синтезируют достаточно генетического материала, чтобы они могли читать.
На этапе 3 изучается результат процесса амплификации, и исследователи могут визуализировать вирус в образце.В машинах RT-qPCR в реальном времени читаемый результат отображается в виде флуоресценции, которую испускает амплифицированный материал, когда его количество увеличивается после нескольких циклов амплификации.
Хотя не все тесты, перечисленные ниже, являются тестами rRT-qPCR, все молекулярные тесты разработаны для информирования исследователей о присутствии патогена путем идентификации его генетического материала или идентификации уникальных маркеров самого патогена. Этап амплификации имеет решающее значение для этих тестов, потому что в противном случае исследователи не смогли бы легко и быстро обнаружить присутствие таких небольших молекул.
Общие типы антигенных и молекулярных тестов, разрабатываемые для SARS-CoV-2
Краткий обзор этих тестов и методологий см. В таблице ниже.
Антиген
Экспресс-тест на антиген: Обнаруживает легко обнаруживаемые поверхностные маркеры на внешней стороне вируса и позволяет избежать этапов экстракции и амплификации. Исследователи или клиницисты собирают образцы в легкодоступных местах (например, в носовом проходе), где вирус имеет тенденцию к наибольшей репликации.
Плюсы: Может определять активное производство вирусных белков, довольно быстрые тесты (за считанные минуты до результатов), этапы экстракции РНК и амплификации не требуются.
Минусы: Требуется тщательная разработка и устранение неисправностей тестовых антител, которые будут реагировать на вирусные белки в образце, глубокое знание вирусных белков, продуцируемых в различных тканевых средах, и тест может дать ложноотрицательные результаты, если продукция вирусного белка низкая или если в исследуемой области недостаточно репликации вируса.
Как это работает:Эти тесты могут быть довольно быстрыми с использованием анализа бокового потока. Эти типы тестов распространены при диагностике таких заболеваний, как ангина. Они могут показаться похожими на серологические тесты, но они отличаются 3 важными способами: (1) они обнаруживают только активное заражение вирусом; (2) они обнаруживают не антитела, а вирусные белки (антигены), которые вирус производит в организме человека-хозяина; и (3) они обычно не основаны на крови или сыворотке.Основным принципом тестов на обнаружение антигенов является использование разработанных синтетических антител для проверки образца пациента на наличие вирусных белков. Во время инфекции часто образуются вирусные белки, которые могут быть обнаружены в крови, других тканях или выделениях. Образец пациента смешивают с буфером, реагентами и синтетическими антителами. Важно отметить, что эти антитела сконструированы таким образом, что они связываются только с определенными вирусными белками; они не связываются с вирусными белками других вирусов.Если белки присутствуют в образце пациента, тогда синтетические антитела будут связываться, и эти комплексы могут быть обнаружены на боковой полоске потока с помощью считывания на основе цвета или света. Используемые синтетические антитела должны быть очень тщательно спроектированы, чтобы они должным образом связывали белок, продуцируемый вирусом во время естественной инфекции, включая любые специальные фолдинг или модификации белка, которые могут присутствовать. Этот метод также зависит от наличия достаточного количества вирусных белков в тестируемом образце для их обнаружения.Другими словами, эти тесты иногда имеют проблемы с чувствительностью и могут быть менее чувствительными, чем методы RT-qPCR или RT-LAMP. Эти тесты также должны быть очень специфичными, чтобы аналогичные белки, продуцируемые другими патогенами (например, другими человеческими коронавирусами, гриппом и т. Д.), Не обнаруживались этими синтетическими антителами. Хотя чувствительность этого метода имеет некоторые недостатки, он быстрый и может использоваться в условиях стационара.
Molecular
Количественная полимеразная цепная реакция с обратной транскриптазой (rRT-qPCR): Идентифицирует и количественно определяет присутствие инфекционных агентов в образце в процессе обнаружения, амплификации и измерения выходного сигнала.
Плюсы: Высокая специфичность, возможность модификации по мере развития вируса для соответствия новым итерациям, сотни образцов могут запускаться одновременно и чрезвычайно чувствительны (низкий предел обнаружения).
Минусы: Требуется обученный персонал и специальное оборудование, конструкция праймера и зонда должна быть точной, образцы могут потребоваться доставить в лабораторию, а сам тест занимает от 1 до 3 часов. Образцы должны подвергнуться экстракции РНК перед запуском теста, добавив еще 1-2 часа, в зависимости от возможностей лаборатории.
Как это работает:Он может включать 1 или 2 этапа, в зависимости от используемых реагентов и наборов. Описанный выше процесс транскрибирует вирусную РНК в ДНК, если она присутствует в образце, для амплификации и визуализации. Эти тесты обычно занимают от 1 до 3 часов, и за один раз можно обработать сотни образцов. Результаты можно считать количественно или, проще говоря, их можно использовать для обозначения наличия или отсутствия инфекции. Как в количественных, так и в качественных итерациях, тесты rRT-qPCR требуют специального оборудования и обученных лаборантов для правильного получения и интерпретации результатов.Помимо лабораторного персонала и оборудования, для проведения теста необходимы специальные реагенты, называемые праймерами и зондами. Эти праймеры и зонды должны быть специально разработаны для связывания только с представляющей интерес вирусной РНК. Праймеры позволяют амплифицировать РНК, в то время как зонды позволяют амплифицированной РНК испускать флуоресцентный сигнал, который считывается и количественно определяется с помощью ПЦР-машины.
Изотермическая амплификация, опосредованная обратной транскрипцией (RT-LAMP): Быстрая амплификация вирусного геномного материала в сочетании со считыванием на основе цвета или света, и это может быть выполнено при одной температуре, в отличие от rRT-PCR .
Плюсы: Требуется только одна температура, быстрое (за считанные минуты до результатов), подходящее для оказания медицинской помощи, высокочувствительное и специфичное для определенных последовательностей SARS-CoV-2.
Минусы: Дизайн праймера должен быть точным, неправильно сложенные праймеры могут привести к появлению «мусора», который может помешать реакции, что затрудняет количественную оценку вируса. Образцы должны подвергнуться экстракции РНК перед запуском теста, добавив еще 1-2 часа, в зависимости от возможностей лаборатории.
Как это работает:Этот метод является более поздней разработкой в области диагностики в местах оказания медицинской помощи.В отличие от rRT-qPCR, который требует быстрой смены нескольких температур для амплификации нуклеиновых кислот, реакции LAMP происходят при одной изотермической температуре, от 63 ° C до 65 ° C. Это делает реакцию намного проще, быстрее и легче в условиях стационара. Кроме того, реакции LAMP обычно вызывают изменение цвета или помутнения реакционной смеси, которые часто видны глазу. Опять же, это упрощает протокол для использования в различных условиях.
Основным принципом RT-LAMP является этап обратной транскрипции (РНК в ДНК), за которым следует добавление 6 праймеров, которые связываются с интересующим геном.При правильной температуре эти 6 праймеров связывают ДНК-мишень, создают петли для создания кольцевых конструкций и удлиняют ДНК. Каждая «петля» открывает новый сайт для связывания праймеров, дополнительно усиливая ген. Этот процесс позволяет быстро экспоненциально увеличивать интересующий ген. Если в смесь включены зонды, красители или флуорофор, во время реакции может наблюдаться видимое изменение, которое можно измерить на глаз или с помощью специального оборудования.
Таким образом, реакция RT-LAMP на образец пациента, содержащий вирус, вызовет видимое изменение реакции в течение нескольких минут.RT-LAMP может быть в сотни раз более чувствительным, чем RT-qPCR, что означает, что он может улавливать даже меньшие концентрации вируса в образце, чем некоторые анализы RT-qPCR. Доступно программное обеспечение для разработки наборов праймеров для RT-LAMP, поскольку этот чувствительный и сложный процесс может быть легко сброшен из-за плохо разработанных праймеров. Обломки, которые могут мешать реакции, включают петли шпильки и димеры праймеров, которые могут образовываться, если праймеры случайно связываются сами. Исследователи также определили способы пометить образцы пациентов «штрих-кодами», а затем усилить их как одну объединенную выборку.Этот процесс, называемый LAMP-Seq, сокращает потребность в оборудовании за счет объединения большого количества образцов пациентов в 1 реакционную пробирку, которые впоследствии могут быть идентифицированы и разделены для анализа.
Амплификация рекомбиназной полимеразы (RPA): Обнаруживает последовательности ДНК посредством точных совпадений фермента, называемого рекомбиназой, который может расщеплять (смещать) цепи ДНК и затем амплифицировать определенные вирусные гены.
Плюсы: Требуется только одна температура, быстрый, требуется меньше оборудования, высокочувствительный и специфичный для определенных последовательностей SARS-CoV-2.
Минусы: Дизайн праймера должен быть точным, может быть трудно количественно определить вирус, а мусор может помешать реакции. Образцы должны подвергнуться экстракции РНК перед запуском теста, добавив еще 1-2 часа, в зависимости от возможностей лаборатории.
Как это работает:В случае SARS-CoV-2 это должно быть связано с этапом обратной транскриптазы, чтобы перевести вирусный ген из РНК в ДНК. Как и RT-LAMP, этот метод также является изотермическим, что означает, что для проведения реакции требуется только 1 температура.Реакция вызывает экспоненциальную амплификацию ДНК, протекает быстро, легко и требует небольшого количества реагентов.
Основная идея RPA зависит от связывания праймера с интересующей последовательностью ДНК, где затем может связываться фермент рекомбиназа. Эта рекомбиназа расщепляет две нити ДНК и затем стабилизируется специальными белками. Выполнив свою работу, рекомбиназа оставляет ДНК открытой для облегчения амплификации. В RPA праймеры спроектированы так, чтобы противостоять одному и тому же участку ДНК, так что каждый раз, когда завершается удлинение, возникают 2 результирующие копии ДНК.Это способствует быстрому усилению. Постоянное связывание праймеров и открытие рекомбиназой также способствует быстрой экспоненциальной амплификации.
Этот метод быстрой амплификации очень чувствителен и требует очень небольшого количества исходного материала ДНК. Однако праймеры должны быть тщательно разработаны и контролироваться температурой, чтобы ферменты могли правильно собирать и разбирать ДНК.
Диагностика на основе CRISPR: Использует высокоспецифичное целевое и расщепляющее действие систем CRISPR-Cas для обнаружения и отсечения определенной части последовательности РНК SARS-CoV-2.В результате расщепления появляется визуальный сигнал, указывающий на присутствие вируса.
Плюсы: Высокая специфичность для определенных последовательностей SARS-CoV-2, требуется меньше оборудования, очень быстрые результаты (минуты), очень чувствительны.
Минусы : Требуется точный дизайн праймера, может потребоваться поиск и устранение неисправностей и особый дизайн всех компонентов (ферментов, праймеров, репортеров). Образцы должны подвергнуться экстракции РНК перед запуском теста, добавив еще 1-2 часа, в зависимости от возможностей лаборатории.
Как это работает: Тесты на основеCRISPR могут быть более быстрыми, чем ПЦР, в сочетании с LAMP и не требуют специального оборудования, как ПЦР.
Система состоит из двух основных компонентов: последовательности CRISPR (кластеризованные палиндромные повторы с регулярными интервалами), которая предназначена для включения направляющих РНК, соответствующих частям вирусного генома, и фермента Cas, который разрезает РНК там, где последовательность CRISPR совпадает. Фермент Cas подобен строительной бригаде, готовой снести определенный участок.Направляющие РНК, разработанные исследователем, представляют собой GPS для экипажа, сообщающие ферменту, где нужно разрезать. Эти системы были впервые обнаружены у бактерий как своего рода бактериальный иммунный ответ на вирусные инфекции. Совсем недавно CRISPR был адаптирован для широкого круга применений, особенно для редактирования генов, из-за простоты использования, быстрого времени обработки и очень специфического расщепления последовательностей нуклеиновых кислот ферментом Cas. Различные ферменты Cas (Cas 9, Cas 13 и др.) Расщепляют разные типы нуклеиновых кислот.В диагностике CRISPR для COVID-19 они должны использовать Cas, который может распознавать и расщеплять РНК (а не ДНК). Cas12 является таким ферментом, и недавно он был использован в системе DETECTR для быстрой диагностики SARS-CoV-2 с ограниченной перекрестной реактивностью. Cas13 использовался при полевом обнаружении вируса денге с использованием системы SHERLOCK.
Чтобы использовать диагностику на основе CRISPR, исследователи создают следующее:
- Направляющие РНК, которые созданы для комплементарности вирусной РНК.Они направляют фермент Cas к вирусному гену, где он может расщеплять РНК. Это активирует фермент Cas.
- Специальный репортер, который имеет флуоресцентные молекулы или цвет и якорную молекулу, такую как биотин, или молекулу гашения, которая препятствует считыванию света. Если репортер останется нетронутым, то якорь / гаситель предотвратит обнаружение репортера. Если репортер расщепляется ферментом Cas, то может передаваться сигнал.
- Репортер смешан с ферментами, направляющими РНК и материалом образца пациента.Затем репортер расщепляется только после связывания направляющих РНК с соответствующей мишенью в вирусной РНК. Как только фермент Cas распознает вирусную мишень, он также может расщепить репортерную последовательность свидетеля. После этого расщепленный репортер может связать «тестовую» полоску, в то время как любой нерасщепленный репортер остается на контрольной полоске, закрепленной биотином. В случае тушащей молекулы, как только репортер расщеплен, может испускаться флуоресценция.
- Исследователь может прочитать результат на основе цвета или флуоресценции, который иногда находится на полосе бокового потока (аналогично тесту на беременность или серологическому тесту RDT).
Какие антигенные и молекулярные тесты есть на рынке? В чем разница между ними?
В настоящее время доступны пять распространенных типов антигенных и молекулярных тестов:
Тип теста Время до получения результатов Что он нам говорит Ограничения Ссылка Экспресс-тест на антиген (RAT) 15-30 минут Наличие активной инфекции путем выявления специфических вирусных белков, присутствующих в образце пациента.Обычно это сочетается с анализом бокового потока для отображения результатов, которые можно прочитать на глаз. Требует очень тщательного конструирования синтетических антител, глубоких знаний о вирусных белках, продуцируемых в различных тканевых средах, и может давать ложноотрицательные результаты, если продукция вирусного белка низка. RAT rRT-qPCR 2-4 часа Наличие активной инфекции путем нацеливания на специфические генные последовательности SARS-CoV-2. Это может быть количественное, но обычно качественное (да / нет).Обычно он имеет очень низкий предел обнаружения, около 100 вирусов / мл. Время, необходимое для завершения теста; обученный персонал и специальное оборудование для анализа результатов rRT-qPCR LAMP 15-60 минут Наличие активной инфекции путем нацеливания на определенные последовательности генов SARS-CoV-2. Обычно это качественный (да / нет). Он основан на специально разработанных праймерах, которые помогают создавать петлевые структуры, необходимые для амплификации.Это очень быстро и не всегда требует специального оборудования (в некоторых случаях его можно измерить на глаз). Он имеет очень низкий предел обнаружения 125 вирусов / мл. Создание необходимых праймеров может быть сложной задачей, и мусор может помешать реакции. Также сложно количественно оценить результаты (уровень вирусной инфекции). LAMP RPA 15-60 минут Наличие активной инфекции путем нацеливания на специфические генные последовательности SARS-CoV-2.Обычно это качественный (да / нет). Он полагается на фермент рекомбиназа. Это очень быстро и не всегда требует специального оборудования. Он имеет очень низкий предел обнаружения 125 вирусов / мл. Создание необходимых праймеров может быть сложной задачей, и мусор может помешать реакции. Также сложно количественно оценить результаты (уровень вирусной инфекции). RPA Диагностика на основе CRISPR 15-60 минут Наличие активной инфекции путем нацеливания на специфические последовательности генов SARS-CoV-2.Обычно это связано с LAMP, но это не всегда необходимо. Результаты обычно видны невооруженным глазом и не требуют специального оборудования. Требуется эксперт, специфический дизайн компонентов (ферменты, праймеры, репортеры). CRISPR Текущие антигенные и молекулярные тесты со статусом FDA EUA
Мы составили список коммерческих и лабораторных тестов, получивших разрешение FDA на экстренное использование. Есть 2 основных раздела:
- Коммерческие тесты : Эти тесты (иногда называемые наборами) были разработаны профессионалами отрасли в области биотехнологии.Эти наборы обычно доступны для покупки поставщиками медицинских услуг или исследователями, проходят внутреннюю проверку, и исследователи сами производят тесты. Эти тесты можно приобрести и провести в лабораториях и на объектах, отличных от производственных.
- Лабораторные тесты : Эти тесты были разработаны медицинскими специалистами и исследователями. Они предназначены для использования только в учреждении, в котором они были разработаны. Например, если тест был разработан в больнице, его можно использовать только в этой больнице.Лаборатория, разрабатывающая и проводящая тест, должна быть сертифицирована в соответствии с поправками о совершенствовании клинической лаборатории 1988 г. (CLIA), 42 U.S.C. §263a, для выполнения тестов высокой сложности. Эти комплекты не предназначены для коммерческой продажи; они проходят внутреннюю валидацию и перечисляют необходимые реагенты в протоколах.
Произошла ошибка при настройке пользовательского файла cookie
Этот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, нажмите кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.




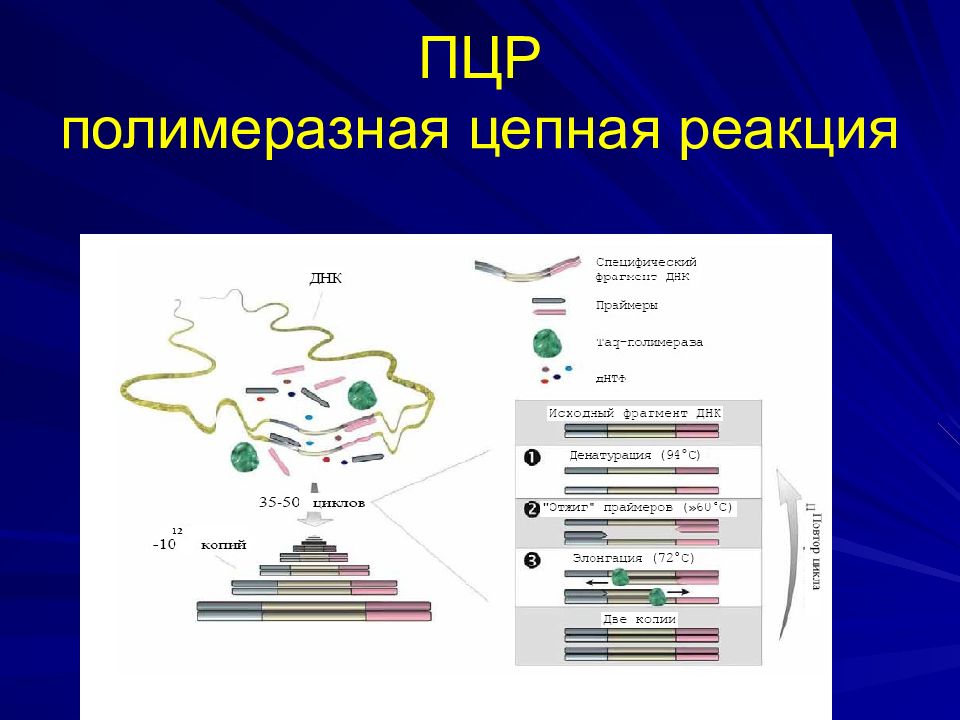
 Зонд вводят легким движением по наружной стенки носа на глубину 2 – 3 см до нижней раковины. Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину, делают вращательное движение и удаляют вдоль наружной стенки носа. Перенесите зонд с биоматериалом в пробирку с транспортной средой и тщательно прополощите его, избегая разбрызгивания жидкости. Затем извлеките зонд из раствора, прижимая его к стенке пробирки, отожмите избыток жидкости и выбросьте. Время взятия материала до начала исследования не должно превышать 24 часов.
Зонд вводят легким движением по наружной стенки носа на глубину 2 – 3 см до нижней раковины. Затем зонд слегка опускают книзу, вводят в нижний носовой ход под нижнюю носовую раковину, делают вращательное движение и удаляют вдоль наружной стенки носа. Перенесите зонд с биоматериалом в пробирку с транспортной средой и тщательно прополощите его, избегая разбрызгивания жидкости. Затем извлеките зонд из раствора, прижимая его к стенке пробирки, отожмите избыток жидкости и выбросьте. Время взятия материала до начала исследования не должно превышать 24 часов.

 Тесты PCR очень точны, если их правильно выполняет специалист в области здравоохранения, но в некоторых случаях экспресс-тест может пропустить.
Тесты PCR очень точны, если их правильно выполняет специалист в области здравоохранения, но в некоторых случаях экспресс-тест может пропустить.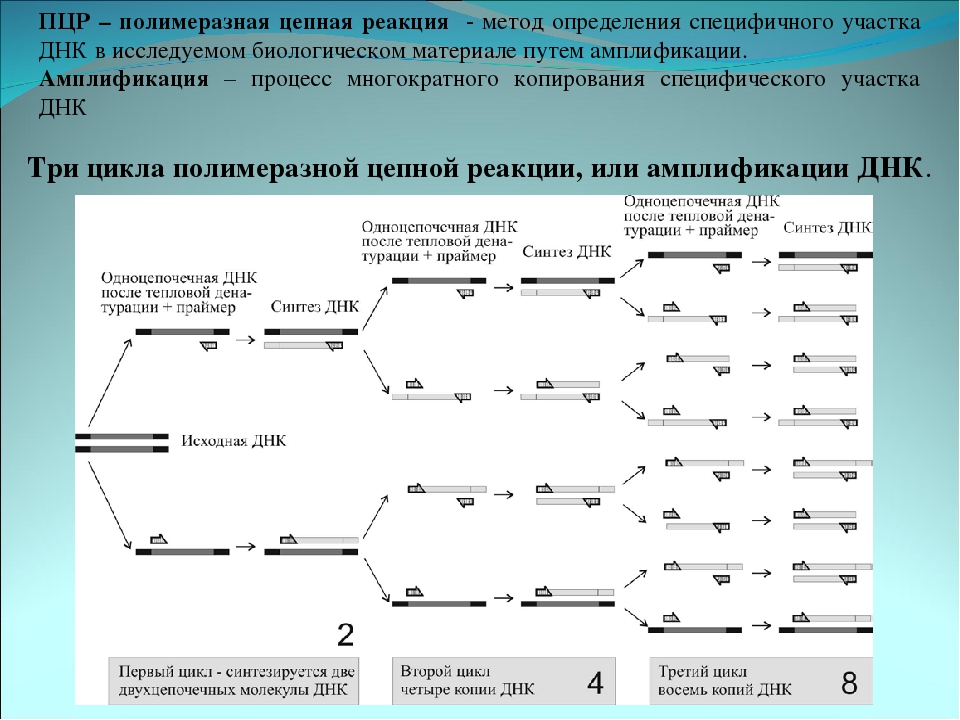 Тесный контакт означает, что вы были в пределах 6 футов (2 метров) от человека, у которого COVID-19 . Но если вы дали положительный результат на COVID-19 в течение последних трех месяцев, вам не нужно проходить тестирование. Если вы прошли полную вакцинацию и тесно общались с кем-то, у кого есть вирус COVID-19 , пройдите тестирование через 3-5 дней после контакта с ним.
Тесный контакт означает, что вы были в пределах 6 футов (2 метров) от человека, у которого COVID-19 . Но если вы дали положительный результат на COVID-19 в течение последних трех месяцев, вам не нужно проходить тестирование. Если вы прошли полную вакцинацию и тесно общались с кем-то, у кого есть вирус COVID-19 , пройдите тестирование через 3-5 дней после контакта с ним. Лучше всего пройти тест на COVID-19 через 5-7 дней после того, как вы были рядом с человеком с COVID-19 . Если вы пройдете тестирование слишком рано, тест может не обнаружить вирус.
Лучше всего пройти тест на COVID-19 через 5-7 дней после того, как вы были рядом с человеком с COVID-19 . Если вы пройдете тестирование слишком рано, тест может не обнаружить вирус. Тампон ненадолго остается на месте, прежде чем его осторожно повернуть при извлечении.Образец запечатывается в пробирку и отправляется в лабораторию для анализа.
Тампон ненадолго остается на месте, прежде чем его осторожно повернуть при извлечении.Образец запечатывается в пробирку и отправляется в лабораторию для анализа. Вам нужно будет изолировать себя до тех пор, пока: ваши симптомы не улучшатся, прошло 24 часа с тех пор, как у вас поднялась температура, и прошло не менее 10 дней с момента появления ваших симптомов.
Вам нужно будет изолировать себя до тех пор, пока: ваши симптомы не улучшатся, прошло 24 часа с тех пор, как у вас поднялась температура, и прошло не менее 10 дней с момента появления ваших симптомов. Ваш врач может порекомендовать повторное обследование, если симптомы не исчезнут.
Ваш врач может порекомендовать повторное обследование, если симптомы не исчезнут.