Термины и определения / КонсультантПлюс
Термины и определения
Острые лимфобластные лейкозы — это гетерогенная группа клональных заболеваний системы крови, возникающих вследствие мутации в T- или B-клетках-предшественницах.
Ph-негативные острые лимфобластные лейкозы — это группа, объединяющая несколько подтипов острых лимфобластных лейкозов, при которых не обнаруживается филадельфийская хромосома (Ph-t(9;22)). В нее включены все B-клеточные и T-клеточные острые лимфобластные лейкозы и лимфобластные лимфомы.
Ph-позитивный острый лимфобластный лейкоз — это вариант острого лимфобластного лейкоза, при котором методом стандартного цитогенетического исследования (G-banding) или методом FISH определяется транслокация t (9;22). Диагноз Ph-позитивного острого лимфобластного лейкоза не может быть основан только на методе молекулярной детекции химерного транскрипта. Цитогенетическое или FISH (метод флуоресцентной гибридизации in situ) исследования являются обязательными.
Полная ремиссия — это состояние кроветворной ткани, при котором в пунктате костного мозга обнаруживается 5% и менее бластных клеток при нормальном соотношении всех ростков кроветворения, при количестве нейтрофилов в периферической крови более 1,0 x 109/л, при количестве тромбоцитов более или равном 100 x 109/л, при отсутствии экстрамедуллярных очагов лейкемического роста. Констатация морфологически полной ремиссии (соответственно, оценка резистентности) осуществляется либо после первой фазы индукционной терапии, либо после второй. При отсутствии полной ремиссии после завершения двух этапов индукционной терапии регистрируется рефрактерная форма острого лимфобластного лейкоза. В этой связи необходимо подчеркнуть, что у ряда пациентов после завершения второй фазы индукционной терапии на фоне восстановления кроветворения после цитостатического воздействия в ранние сроки после его завершения может определяться увеличенный процент бластных клеток (до 10 — 12%).
Полная ремиссия подразделяется на три основных типа: 1) цитогенетическая, 2) молекулярная, 3) с неполным восстановлением показателей периферической крови, когда число нейтрофилов менее 1 x 109/л, а тромбоцитов менее 10 x 109/л. Последняя категория оговаривается специально, поскольку, по ряду данных, прогноз у таких пациентов несколько хуже. При этом эксперты не рекомендуют констатировать у таких пациентов полную ремиссию. Тем не менее вне клинических исследований эту формулировку ответа применяют редко.
Частичная ремиссия (частичный ответ) — этот термин рекомендуют использовать только в клинических исследованиях I — II фазы, оценивающих противоопухолевую эффективность, токсичность, переносимость новых препаратов и определяющих оптимальные дозы этих препаратов.
Резистентная форма — эта форма заболевания, которая констатируется при отсутствии полной ремиссии после завершения двух фаз индукционной терапии.
Ранняя смерть — это смерть пациента в период индукционной терапии (двух фаз индукции для острых лимфобластных лейкозов). Следует подчеркнуть, что этот критерий является обобщающим для понятия гибели пациента в процессе индукционной терапии. Чаще используют термин «смерть в период индукции», что более четко отражает ситуацию, поскольку в ряде случаев смерть пациента происходит на второй фазе индукционной терапии, при этом у них была зарегистрирована полная ремиссия после первой фазы индукционной терапии. В этих случаях смерть рассматривают как смерть в консолидации или смерть после достижения полной ремиссии.
Рецидив — это состояние констатируется при обнаружении в пунктате костного мозга более 5% бластных клеток. Рецидив заболевания не констатируется при обнаружении в очередном контрольном пунктате костного мозга более 5% бластных клеток, но менее 10%, в тех случаях, когда пункция костного мозга производится в ранние сроки после курса химиотерапии или использовались ростовые гемопоэтические факторы с целью сокращения периода нейтропении, при этом анализ периферической крови нормальный и отсутствуют экстрамедуллярные поражения. Вторая диагностическая пункция осуществляется через 7 — 10 дней после первой. Если сохраняется процент бластных клеток выше 5 или отмечается их увеличение (например, с 7 до 13%), то констатируется рецидив.
Вторая диагностическая пункция осуществляется через 7 — 10 дней после первой. Если сохраняется процент бластных клеток выше 5 или отмечается их увеличение (например, с 7 до 13%), то констатируется рецидив.
Ранний рецидив — эта форма рецидива называется в том случае, если он регистрируется раньше, чем через полгода от момента окончания поддерживающей терапии или на терапии после достижения ремиссии. Поздним считается тот рецидив, который возникает через полгода и более от окончания поддерживающей терапии. Рецидивом также является и внекостномозговое поражение (нейролейкемия, поражение яичек, увеличение селезенки и т.д.) даже при отсутствии изменений в крови и костном мозге. Внекостномозговые рецидивы (особенно поражение центральной нервной системы) при использовании современных протоколов лечения встречаются приблизительно в 4 — 8% случаев. Если констатирован изолированный внекостномозговой рецидив, то, кроме локальной терапии (лечение нейролейкемии, облучение/удаление яичка, удаление лейкемического очага в яичнике и т.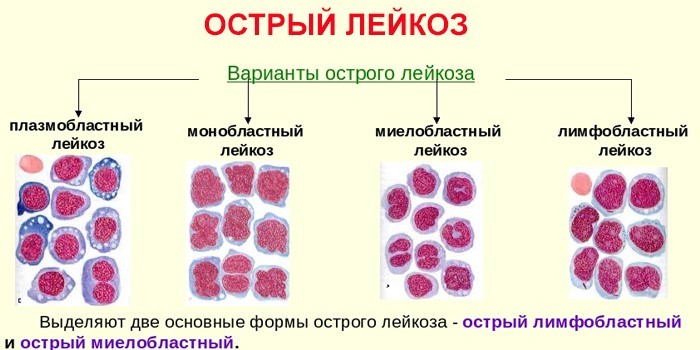
Минимальная остаточная болезнь, или минимальная резидуальная болезнь — это небольшая популяция опухолевых клеток, которая не может быть зафиксирована с помощью светового микроскопа, но обнаруживается более тонкими методами исследования, выявляющими 1 лейкемическую клетку на 104-6 исследуемых. Основными методами детекции минимальной остаточной болезни являются проточная цитометрия и полимеразная цепная реакция. Методы стандартного цитогенетического исследования и метод FISH не используются в целях оценки минимальной остаточной болезни.
Цитогенетическая ремиссия — это полная клинико-гематологическая ремиссия, при этом методами стандартной цитогенетики не выявляются исходные аномалии кариотипа; кариотип должен быть нормальным, а число проанализированных метафаз должно составлять не менее 20. Цитогенетическая ремиссия — новое понятие, появившееся при регулярном использовании методов цитогенетики для исследований пунктатов костного мозга в период полной ремиссии.
Цитогенетический рецидив — это рецидив, который констатируется при наличии в пунктате костного мозга митозов с хромосомными аберрациями, которые обнаружены в дебюте заболевания на фоне сохраняющейся клинико-гематологической ремиссии.
Молекулярная ремиссия — это полная клинико-гематологическая ремиссия при отсутствии в костном мозге исходно определявшихся методом полимеразной цепной реакции молекулярных маркеров острого лейкоза с чувствительностью метода 10-4. Это также новое понятие, ставшее в настоящее время ключевым. Следует отметить, что может быть достигнута цитогенетическая ремиссия, но при этом молекулярные маркеры могут еще определяться.
Молекулярный рецидив — это появление исходно определявшихся молекулярных маркеров острых лейкозов в двух повторных анализах (проведенных с коротким интервалом времени) на фоне сохраняющейся клинико-гематологической ремиссии.
Важным и одним из самых точных способов оценки эффективности терапии острых лейкозов являются применение статистических методов и построение кривых выживаемости пациентов, которым проводили то или иное лечение.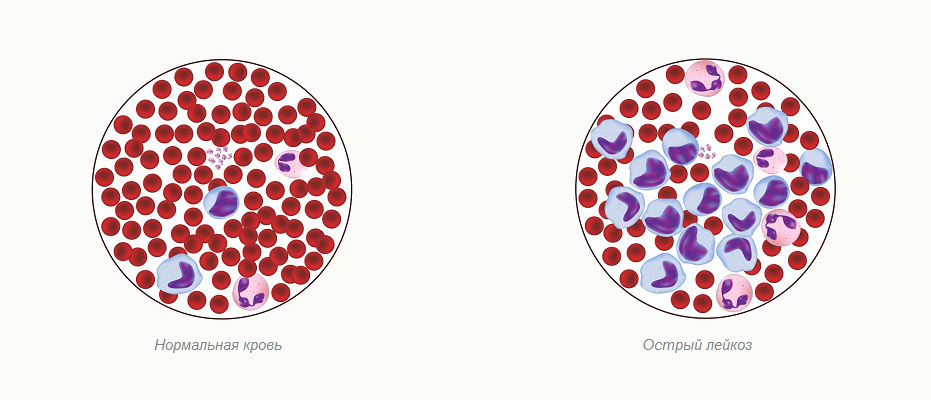 Чаще всего оценивают общую, безрецидивную, бессобытийную выживаемость и вероятность сохранения полной ремиссии (или обратное понятие — вероятность развития рецидива).
Чаще всего оценивают общую, безрецидивную, бессобытийную выживаемость и вероятность сохранения полной ремиссии (или обратное понятие — вероятность развития рецидива).
Общая выживаемость. Для оценки общей выживаемости анализируют временные параметры всех пациентов, включенных в исследование. Точкой отсчета является день начала терапии. Событием считается только смерть пациента от любой причины (ранняя летальность, смерть в период ремиссии от любой причины, смерть в период рецидива). Событие на кривой выживаемости графически отображается ступенькой, идущей вниз. Пациентов, живых во время проведения анализа, расценивают как случай и отмечают на кривой черточкой, т.е. цензурируют. Пациентов, судьба которых неизвестна, цензурируют в тот момент, когда было известно, что они живы. Больных, отказавшихся от лечения, цензурируют в день отказа от терапии.
Безрецидивная выживаемость. При оценке безрецидивной выживаемости учитывают данные только тех пациентов, у которых была достигнута полная ремиссия. Точкой отсчета считается дата достижения полной ремиссии. Событиями считаются рецидив или смерть от любой причины (в период консолидации или поддерживающего лечения, от рецидива, в период ремиссии от другой причины, например, суицида). Цензурируют только тех пациентов, которые были живы и находились в полной ремиссии в момент проведения анализа. Больных, судьба которых неизвестна, цензурируют в тот момент, когда было известно, что они живы в полной ремиссии. Пациентов, у которых была достигнута полная ремиссия, но они отказались от лечения в ремиссии, цензурируют в день отказа от терапии.
Точкой отсчета считается дата достижения полной ремиссии. Событиями считаются рецидив или смерть от любой причины (в период консолидации или поддерживающего лечения, от рецидива, в период ремиссии от другой причины, например, суицида). Цензурируют только тех пациентов, которые были живы и находились в полной ремиссии в момент проведения анализа. Больных, судьба которых неизвестна, цензурируют в тот момент, когда было известно, что они живы в полной ремиссии. Пациентов, у которых была достигнута полная ремиссия, но они отказались от лечения в ремиссии, цензурируют в день отказа от терапии.
Вероятность сохранения полной ремиссии (обратное от вероятности развития рецидива). При оценке вероятности сохранения полной ремиссии учитываются данные только тех пациентов, у которых достигнута полная ремиссия. При этом точкой отсчета служит дата достижения полной ремиссии. Событием считается только рецидив заболевания. Цензурируют всех больных, кто жив в полной ремиссии в момент проведения анализа.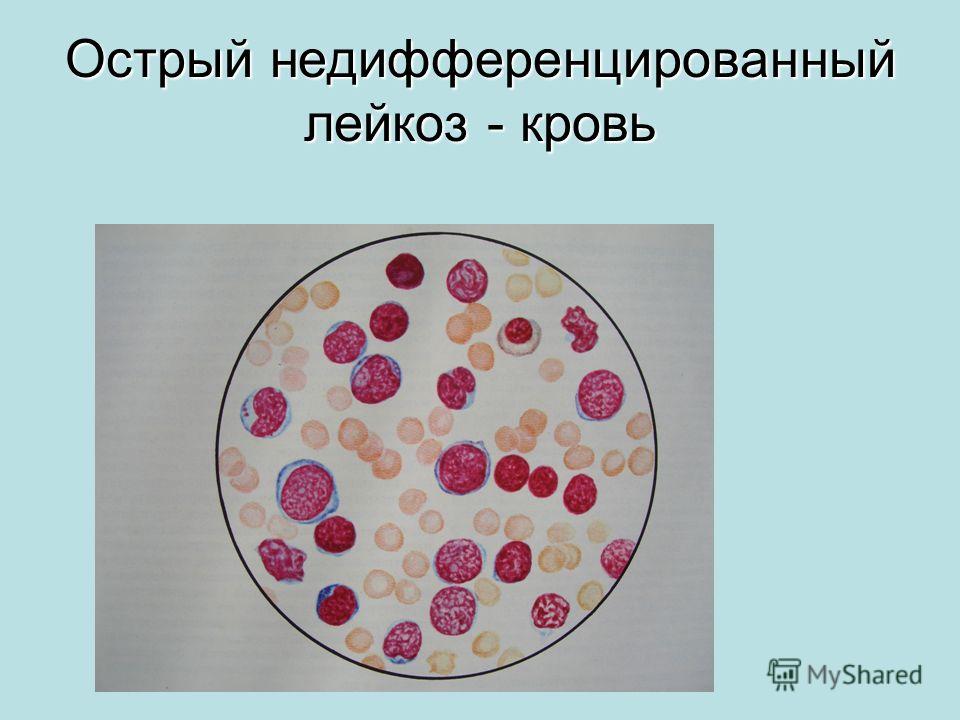 Пациенты, умершие в период полной ремиссии от осложнений, связанных с лечением, или от других причин, цензурируют в день смерти, как больных, находившихся в полной ремиссии. Пациентов, судьба которых неизвестна, цензурируют на тот момент, когда было известно, что они живы в полной ремиссии. Пациентов, у которых была достигнута полная ремиссия и которые отказались от лечения в период ремиссии, цензурируют в день отказа от терапии.
Пациенты, умершие в период полной ремиссии от осложнений, связанных с лечением, или от других причин, цензурируют в день смерти, как больных, находившихся в полной ремиссии. Пациентов, судьба которых неизвестна, цензурируют на тот момент, когда было известно, что они живы в полной ремиссии. Пациентов, у которых была достигнута полная ремиссия и которые отказались от лечения в период ремиссии, цензурируют в день отказа от терапии.
Вероятность сохранения полной ремиссии является тем показателем, который позволяет оценивать истинную противоопухолевую эффективность какой-либо терапии без учета таких субъективных моментов, как выхаживание пациентов от осложнений, связанных с самим лечением.
Бессобытийная выживаемость. Этот показатель оценивает выживаемость всех больных, включенных в анализ, с момента начала терапии. Событием считается ранняя летальность, факт недостижения полной ремиссии через два месяца от начала лечения, смерть в период ремиссии от осложнений химиотерапии или других причин, а также рецидив заболевания. Цензурируют только пациентов, у которых была достигнута полная ремиссия в течение первых двух курсов химиотерапии, и они остаются живыми, сохраняя полную ремиссию, на момент проведения анализа.
Цензурируют только пациентов, у которых была достигнута полная ремиссия в течение первых двух курсов химиотерапии, и они остаются живыми, сохраняя полную ремиссию, на момент проведения анализа.
Индукция — это период начального лечения, целью которого является максимально быстрое и существенное сокращение опухолевой массы и достижение полной ремиссии, называется периодом индукции (обычно 1 — 2 курса). Именно в этот период на фоне применения цитостатических средств количество лейкемических клеток в костном мозге уменьшается примерно в 100 раз, т.е. в момент констатации полной ремиссии в костном мозге морфологически определяется менее 5% опухолевых клеток.
Консолидация. Второй этап терапии острых лейкозов — закрепление достигнутого противоопухолевого эффекта (разное количество, в зависимости от протокола). Задачей этого периода является по возможности еще большее уменьшение числа остающихся после индукции лейкемических клеток.
Поддерживающее лечение — это продолжение цитостатического воздействия в меньших дозах, чем в период индукции ремиссии, на возможно остающийся опухолевый клон.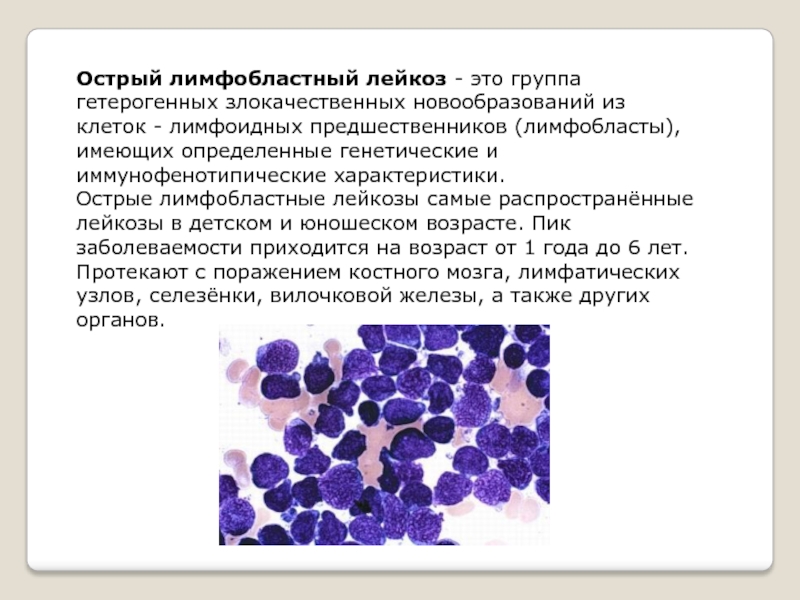
Лейкоз/лимфома Беркитта — это высокоагрессивное лимфопролиферативное заболевание из иммунологически зрелых В-клеток с преимущественно экстранодальной локализацией. Клинически выделяют 3 варианта лимфомы Беркитта: эндемический, спорадический и ВИЧ-ассоциированный.
Эндемический вариант лимфомы Беркитта — это вариант лимфомы Беркитта характерен для темнокожих детей-аборигенов экваториальной Африки и мигрантов из Африки в Новую Гвинею. В клинической картине часто наблюдается поражение лицевого скелета: верхней и нижней челюстей, орбиты, а также почек, яичек, яичников, слюнных, молочных желез и центральной нервной системы.
Спорадический вариант лимфомы Беркитта — это типичная лимфома Беркитта по морфологическим, иммунофенотипическим и цитогенетическим признакам, возникающая вне эндемичной зоны.
Иммунодефицит-ассоциированный вариант лимфомы Беркитта — это лимфома Беркитта, возникающая на фоне иммунодефицитных состояний (у пациентов с ВИЧ-инфекцией, после трансплантации органов, у пациентов с первичными иммунодефицитами). Чаще всего встречается у ВИЧ-инфицированных пациентов, причем на ранних этапах развития (до снижения CD4+-клеток).
Чаще всего встречается у ВИЧ-инфицированных пациентов, причем на ранних этапах развития (до снижения CD4+-клеток).
Лейкоз без слез: МРТ-диагностика заменит биопсию костного мозга | Статьи
Медики Центра детской гематологии, онкологии и иммунологии имени Дмитрия Рогачева в сотрудничестве со специалистами Philips Clinical Science впервые с помощью аппарата МРТ смогли оценить количественное соотношение жировых клеток и воды в костном мозге маленьких пациентов, страдающих острым лимфобластным лейкозом (ОЛЛ). МРТ-данные больных детей показали патологическое уменьшение доли жира в костном мозге. Планируется, что новая технология во многих случаях позволит отказаться от биопсии костного мозга, которая сейчас необходима для диагностики злокачественных заболеваний кроветворной системы, но при этом берется посредством болезненной пункции и порой чревата осложнениями. Эксперты, опрошенные «Известиями», отметили высокую точность и безопасность нового метода. Однако, по их словам, не всегда уменьшение доли жировой ткани может говорить об ОЛЛ.
Однако, по их словам, не всегда уменьшение доли жировой ткани может говорить об ОЛЛ.
Специалисты Национального медицинского исследовательского центра детской гематологии, онкологии и иммунологии (НМИЦ ДГОИ) имени Дмитрия Рогачева совместно с Philips Clinical Science первые в мире смогли на практике испытать разработанную ими технологию количественной оценки концентрации жира в костном мозге детей с диагнозом «острый лимфобластный лейкоз» (ОЛЛ) с помощью МРТ-аппарата. Предложенный учеными метод позволит обнаруживать и оценивать нарушения в работе кроветворной системы без необходимой сейчас биопсии, осуществляемой посредством болезненной пункции костного мозга. Это особенно важно при работе с детьми.
«Возможность минимизировать количество болезненных процедур с помощью неинвазивного метода визуализации является важной задачей, особенно для пациентов детского возраста», — пишут ученые в статье, посвященной результатам исследования.
Острый лимфобластный лейкоз — это злокачественное заболевание кроветворной системы. Его доля составляет около 30% от всех детских онкологических заболеваний. На 100 тыс. детей приходится до четырех случаев болезни. При этом самое большое количество заболевших таким видом лейкоза — в возрасте до пяти лет.
Фото: ТАСС/Сергей Бобылев
Сейчас для диагностики заболевания используется биопсия: делается пункция и непосредственно забирается ткань костного мозга, которая затем подвергается анализу. Если во взятом материале количество бластов — незрелых клеток — превышает 25%, это может говорить о развитии патологии.
При этом в тканях костного мозга происходит видимое изменение концентрации жировых клеток и воды. Стандартная МРТ-диагностика позволяет увидеть на снимках изменения костного мозга, однако для постановки диагноза необходимо определить количественное соотношение в нем жира и жидкости.
— Мы рассмотрели модель костного мозга, которая в трубчатых и губчатых костях отвечает за кроветворение. Модель состоит из трех частей: воды, жира и клеточного состава, — пояснила заведующая рентгенологическим отделением НМИЦ ДГОИ имени Дмитрия Рогачева Галина Терещенко. — Мы решили использовать современные методы МРТ для ее анализа — и смогли количественно определить объем жировой ткани и воды.
Модель состоит из трех частей: воды, жира и клеточного состава, — пояснила заведующая рентгенологическим отделением НМИЦ ДГОИ имени Дмитрия Рогачева Галина Терещенко. — Мы решили использовать современные методы МРТ для ее анализа — и смогли количественно определить объем жировой ткани и воды.
Для решения этой задачи ученые использовали различные методики МРТ-визуализации: магнитно-резонансную спектроскопию и визуализацию химического сдвига (изменение сигнала в зависимости от химического состава вещества). С их помощью был проанализирован костный мозг подвздошных костей и поясничных позвонков 20 маленьких пациентов с острым лимфобластным лейкозом, а также костный мозг их 20 здоровых сверстников. Исследование показало у больных снижение концентрации жира на 90–95% по сравнению с группой здоровых. При этом ученым в пяти случаях не удалось определить количество жира посредством магнитно-резонансной спектроскопии, так как его концентрация у этих пациентов оказалась слишком низкой. Из этого авторы работы сделали вывод, что применение технологии визуализации химического сдвига для отслеживания патологий в костном мозге дает более надежный результат.
Из этого авторы работы сделали вывод, что применение технологии визуализации химического сдвига для отслеживания патологий в костном мозге дает более надежный результат.
Фото: ТАСС/Валерий Шарифулин
— Мы не планируем ставить окончательный диагноз «острый лимфобластный лейкоз» по МРТ. Однако по результатам таких исследований мы в случае сильного понижения концентрации жира сможем утверждать, что костный мозг соответствует поражению при ОЛЛ. Также мы получим возможность наблюдать, есть ли положительные изменения в костном мозге в ходе лечения, — подчеркнула Галина Терещенко.
Она добавила, что зато в группе пациентов с таким гематологическим заболеванием, как врожденная и приобретенная анемия, МРТ сможет «полностью заменить биопсию костного мозга».
Безопасно и информативноОпределение количества жира по данным МРТ уже достаточно давно используется в мировой практике. Однако сотрудниками НМИЦ ДГОИ имени Дмитрия Рогачева впервые была проведена оценка жировой ткани в костном мозге у детей с острым лимфобластным лейкозом, пояснил заведующий отделением рентгенологии Пироговского центра Олег Бронов.
— Одна из основных задач в современной лучевой диагностике — это замена инвазивных процедур на неинвазивные, — отметил Олег Бронов. — Тем более когда речь идет о детях. После любого инвазивного вмешательства, даже незначительного, есть риск получить осложнение, что крайне нежелательно для пациентов с серьезными гематологическими заболеваниями.
По мнению специалиста, полученные данные показали убедительную корреляцию между снижением фракции жира в костном мозге и наличием острой фазы ОЛЛ. Поэтому необходимо проводить дальнейшие исследования, чтобы стандартизировать методику, минимизировать ошибки, а также сделать ее доступной для всех специалистов. При правильном развитии технологии возможно избежать биопсии костного мозга и снизить количество осложнений. Также со временем с помощью МРТ можно попытаться еще и оценить эффективность лечения, не прибегая к болезненной пункции, заявил эксперт.
Фото: ИЗВЕСТИЯ/Дмитрий Коротаев
Предложенный учеными из НМИЦ ДГОИ имени Дмитрия Рогачева метод диагностики острого лимфобластного лейкоза по МРТ очень удобен и информативен, уверен заведующий кафедрой лучевой диагностики Института повышения квалификации медицинских кадров Дмитрий Измалков. Но изменения, которые удалось зафиксировать с помощью томографии, могут происходить и при других заболеваниях.
— Точность количественной оценки жира в костном мозге оказалась очень высокой, что обеспечивает надежность диагноза, сопоставимую с биопсией, — сказал Дмитрий Измалков. — Однако выявленные изменения не говорят о причинах патологического состояния. Мы не знаем, произошли они из-за лейкоза — или, может быть, другой болезни. Поэтому метод лучше применять на первых этапах обследования, когда еще не ясны клиника и диагноз пациента.
Наблюдая с помощью нового метода за патологическим уменьшением доли жира в костном мозге, можно обнаружить у пациента наличие болезни, а уже на следующем этапе можно будет принимать решение о необходимости биопсии, резюмировал специалист.
Публикации в СМИ
Острый лейкоз — злокачественное заболевание кроветворной системы; морфологический субстрат — бластные клетки.
Частота. 13,2 случаев на 100 000 населения среди мужчин и 7,7 случаев на 100 000 населения среди женщин.
КЛАССИФИКАЦИЯ
FAB классификация (франко американо британская) основана на морфологии лейкемических клеток (строение ядра, соотношение размеров ядра и цитоплазмы) • Острый миелобластный (нелимфобластный) лейкоз (ОМЛ) •• М0 — без созревания клеток, миелогенная дифференцировка доказывается только иммунологически •• М1 — без созревания клеток •• М2 — ОМЛ с дифференцировкой клеток, •• М3 — промиелоцитарный •• М4 — миеломоноцитарный •• М5 — монобластный лейкоз •• М6 — эритролейкоз •• М7 — мегакариобластный лейкоз • Острый лимфобластный лейкоз (ОЛЛ): •• L1 — без дифференцировки клеток (морфологически гомогенные клетки) •• L2 — с дифференцировкой клеток (морфологически гетерогенная популяция клеток) •• L3 — беркеттоподобные лейкозы • Недифференцируемый лейкоз — к этой категории относят лейкозы, клетки которых невозможно идентифицировать как миелобластные или лимфобластные (ни химическими, ни иммунологическими методами) • Миелопоэтическая дисплазия •• Рефрактерная анемия без бластоза (в костном мозге бласты и промиелоциты <10%) •• Рефрактерная анемия с бластозом (в костном мозге бласты и промиелоциты 10 30%) •• Рефрактерная анемия с избытком бластов в трансформации •• Хронический миеломоноцитарный лейкоз.
REAL классификация (Revised Europian American classification of Lymphoid neoplasms), пересмотренная (Европейско Американская) классификация лимфоидных гемобластозов • Пре B клеточные опухоли •• Пре B лимфобластный лейкоз/лимфома • Пре T клеточные опухоли •• Пре T лимфобластный лейкоз/лимфома • Опухоли периферических B клеток •• хронический лимфолейкоз/лимфома из малых лимфоцитов •• Лимфоплазмоцитарная лимфома •• Лимфома из плащевых клеток •• Фолликулярная лимфома •• Лимфома из клеток краевой зоны •• Волосато клеточный лейкоз •• Плазмоцитома/миелома плазмоцитарная •• Диффузная лимфома из больших лимфоцитов•• Лимфома Беркетта • Опухоли периферических T клеток и NK клеток •• T клеточный хронический лимфолейкоз •• Лейкоз из крупных зернистых лимфоцитов •• Грибовидный микоз и синдром Сезари T клеточная лимфома •• Ангиоиммунобластическая T клеточная лимфома •• Ангиоцентрическая лимфома (лимфома из NK и T клеток) •• Кишечная T клеточная лимфома •• Лейкоз/лимфома T клеточная взрослых •• Анапластическая крупноклеточная лимфома
Варианты ОМЛ (классификация ВОЗ, 1999) • ОМЛ с t(8;21)(q22;q22) • ОМЛ с t(15;17) (q22;q11 12) • Острый миеломонобластный лейкоз • ОМЛ с патологической костномозговой эозинофилией (inv(16)(p13q22) или t(16;16) (p13;q11) • ОМЛ с 11q23 (MLL) дефектами • Острый эритроидный лейкоз • Острый мегакариоцитарный лейкоз • Острый базофильный лейкоз • Острый панмиелоз с миелофиброзом • Острые бифенотипические лейкозы • ОМЛ с мультилинейной дисплазией • Вторичный ОМЛ.
Иммуногистохимическое исследование (определение клеточного фенотипа) необходимо для уточнения иммунологического варианта лейкоза, влияющего на схему лечения и клинический прогноз
• Острый лимфобластный лейкоз (247640, , мутация соматических клеток) — 85% всех случаев, составляет до 90% всех лейкозов детского возраста У взрослых развивается достаточно редко. Цитохимические реакции: положительная на терминальную дезоксинуклеотидил трансферазу; отрицательные на миелопероксидозу, гликоген. Использование маркёров клеточной мембраны позволило выделить подвиды •• В-клеточные — 75% всех случаев •• С отсутствием розеткообразования •• Т-клеточые •• Другие варианты (редко). Дифференциальная диагностика подвидов важна для прогноза, т.к. Т-клеточные варианты плохо поддаются лечению.
• Острый миелобластный лейкоз чаще возникают у взрослых, подтип зависит от уровня дифференцировки клеток. В большинстве случаев клон миелобластов исходит из стволовых кроветворных клеток, способных к множественной дифференцировке в колониеобразующие единицы гранулоцитов, эритроцитов, макрофагов или мегакариоцитов, поэтому у большинства больных злокачественные клоны не имеют признаков лимфоидных или эритроидных ростков •• ОМЛ наблюдают наиболее часто; имеет четыре варианта (М0 — М3) •• М0 и М1 — острый лейкоз без дифференцировки клеток •• М2 — острый с дифференцировкой клеток •• М3 — промиелоцитарный лейкоз, характеризуется наличием аномальных промиелоцитов с гигантскими гранулами; часто сочетается с ДВС, обусловленным тромбопластическим эффектом гранул, что подвергает сомнению целесообразность применения гепарина при терапии. Прогноз при М3 менее благоприятен, чем при М0–М1 •• Миеломонобластный и монобластный лейкозы (соответственно М4 и М5) характеризуются преобладанием неэритроидных клеток типа монобластов. М4 и М5 составляют 5–10% всех случаев ОМЛ. Частый признак — образование внекостномозговых очагов кроветворения в печени, селезёнке, дёснах и коже, гиперлейкоцитоз, превышающий 50–100109/л. Чувствительность к терапии и выживаемость ниже, чем при других вариантах острых миелобластных лейкозов •• Эритролейкоз (М6). Вариант острого миелобластного лейкоза, сопровождающийся усиленной пролиферацией эритроидных предшественников; характерно наличие аномальных бластных ядросодержащих эритроцитов. Эффективность лечения эритролейкоза сходна с результатами терапии других подтипов или несколько ниже •• Мегакариобластный лейкоз (М7) — редкий вариант, сочетающийся с фиброзом костного мозга (острый миелосклероз). Плохо поддаётся терапии. Прогноз неблагоприятный.
Патогенез обусловлен пролиферацией опухолевых клеток в костном мозге и их метастазированием в различные органы. Угнетение нормального кроветворения связано с двумя основными факторами: • повреждение и вытеснение нормального ростка кроветворения низкодифференцированными лейкемическими клетками • выработка бластными клетками ингибиторов, подавляющих рост нормальных кроветворных клеток.
Стадии острого лейкоза • Первично-активная фаза • Ремиссия (при лечении) — полная клинико-гематологическая •• Содержание бластов в костном мозге менее 5% при нормальной клеточности •• В клинической картине отсутствует пролиферативный синдром • Рецидив (ранний и поздний) •• Изолированный костномозговой — содержание бластов в костном мозге более 25% •• Внекостномозговой ••• Нейролейкоз (неврологическая симптоматика, цитоз более 10 клеток, бласты в ликворе) ••• Тестикулярный (увеличение размеров одного или двух яичек, наличие бластов подтверждено цитологическим и гистологическим исследованиями) •• Смешанный • Терминальная фаза (при отсутствии лечения и резистентность к проводимой терапии)
Клиническая картина острых лейкозов определяется степенью инфильтрации костного мозга бластными клетками и угнетения ростков кроветворения • Угнетение костномозгового кроветворения •• Анемический синдром (миелофтизная анемия) •• Геморрагический синдром (вследствие тромбоцитопении отмечают кожные геморрагии — петехии, экхимозы; кровотечения из слизистых оболочек — носовые кровотечения, внутренние кровотечения) •• Инфекции (нарушение функции лейкоцитов) • Лимфопролиферативный синдром •• Гепатоспленомегалия •• Увеличение лимфатических узлов • Гиперпластический синдром •• Боли в костях •• Поражения кожи (лейкемиды), мозговых оболочек (нейролейкоз) и внутренних органов • Интоксикационный синдром •• Снижение массы тела •• Лихорадка •• Гипергидроз •• Выраженная слабость.
Диагноз острого лейкоза подтверждают наличием бластов в костном мозге. Для идентификации подтипа лейкоза применяют гистохимические, иммунологические и цитогенетические методы исследования.
Лабораторные исследования • В периферической крови уровень лейкоцитов может варьировать от выраженной лейкопении (ниже 2,0109/л) до гиперлейкоцитоза; анемия, тромбоцитопения; наличие бластных клеток вплоть до тотального бластоза • Гиперурикемия вследствие ускоренного жизненного цикла клеток • Гипофибриногенемия и повышение содержания продуктов разрушения фибрина вследствие сопутствующего ДВС. Влияние ЛС. ГК не следует назначать до постановки окончательного диагноза. Высокая чувствительность к преднизолону бластных клеток приводит к их разрушению и трансформации, затрудняющим диагностику.
Лечение комплексное; цель — достижение полной ремиссии. В настоящее время в гематологических центрах используют различные протоколы химиотерапии, основанные на принципах полихимиотерапии и интенсификации лечения.
• Химиотерапия состоит из нескольких этапов •• Индукция ремиссии ••• При ОЛЛ — одна из схем: комбинации винкристина в/в еженедельно, преднизолона внутрь ежедневно, даунорубицина и аспарагиназы в течение 1–2 мес непрерывно ••• При ОМЛ — сочетание цитарабина в/в капельно или п/к, даунорубицина в/в, иногда в сочетании с тиогуанином. Более интенсивная постиндукционная химиотерапия, уничтожающая оставшиеся лейкозные клетки, увеличивает длительность ремиссии •• Консолидация ремиссии: продолжение системной химиотерапии и профилактика нейролейкоза при ОЛЛ (эндолюмбальное введение метотрексата при ОЛЛ в сочетании с лучевой терапией на головной мозг с захватом спинного мозга [C1–C2]) •• Поддерживающая терапия: периодические курсы реиндукции ремиссии.
• При ОМЛ М3 проводят лечение препаратами ретиноевой кислоты (третиноин).
• Трансплантация костного мозга — метод выбора при острых миелобластных лейкозах и при рецидивах всех острых лейкозов. Главное условие для проведения трансплантации — полная клинико-гематологическая ремиссия (содержание бластов в костном мозге менее 5%, отсутствие абсолютного лимфоцитоза). Перед операцией можно провести химиотерапию в сверхвысоких дозах, изолированно или в сочетании с лучевой терапией (с целью полного уничтожения лейкозных клеток) •• Оптимальный донор — однояйцовый близнец или сибс; чаще используют доноров с 35%-совпадением по Аг HLA. При отсутствии совместимых доноров используют аутотрансплантацию костного мозга, взятого в период ремиссии •• Главное осложнение — реакция трансплантат против хозяина. Развивается вследствие пересадки Т-лимфоцитов донора, распознающих Аг реципиента как чужеродные и вызывающих иммунную реакцию против них. Острая реакция развивается в течение 20–100 дней после трансплантации, отсроченная — через 6–12 мес ••• Основные органы-мишени — кожа (дерматит), ЖКТ (диарея) и печень (токсический гепатит) ••• Лечение длительное, обычно ограничено назначением комбинаций преднизолона, циклоспорина и малых доз азатиоприна •• На течение посттрансплантационного периода влияют также подготовительные схемы лечения, развитие интерстициальной пневмонии, отторжение трансплантата (редко).
• Заместительная терапия •• Трансфузия эритроцитарной массы для поддержание уровня Hb не ниже 100 г/л. Условия трансфузий: неродственный донор, использование лейкоцитарных фильтров •• Трансфузия свежей тромбоцитарной массы (снижает риск кровотечений). Показания: содержание тромбоцитов менее 20109/л; геморрагический синдром при содержании тромбоцитов менее 50109/л.
• Профилактика инфекций — главное условие выживания пациентов с нейтропенией, возникшей вследствие химиотерапии •• Полная изоляция пациента •• Строгий санитарно-дезинфекционный режим — частые влажные уборки (до 4–5 р/сут), проветривание и кварцевание палат; использование одноразового инструментария, стерильной одежды медицинского персонала •• Профилактическое применение антибиотиков, противогрибковых и противовирусных препаратов (при содержании сегментоядерных нейтрофилов менее 0,5109/л показана профилактика пневмоцистной пневмонии) ••• При повышении температуры тела проводят клиническое и бактериологическое исследования и немедленно начинают лечение комбинациями бактерицидных антибиотиков широкого спектра действия: цефалоспоринов, аминогликозидов и полусинтетических пенициллинов ••• При вторичных подъёмах температуры тела, возникших после лечения антибиотиками широкого спектра действия, эмпирически применяют противогрибковые средства (амфотерицин В) •• Для профилактики и лечения нейтропении можно назначить колониестимулирующие факторы (например, молграмостим).
Прогноз • Прогноз у детей с острым лимфолейкозом хороший: у 95% и более наступает полная ремиссия. У 70–80% больных проявлений болезни нет в течение 5 лет, их считают излечившимися. При возникновении рецидива в большинстве случаев можно достичь второй полной ремиссии. Больные со второй ремиссией — кандидаты на трансплантацию костного мозга с вероятностью долговременного выживания 35–65% • Прогноз у больных острым миелобластным лейкозом неблагоприятный. 75% больных, получающих адекватное лечение с использованием современных химиотерапевтических схем, достигают полной ремиссии, 25% больных погибают (длительность ремиссии — 12–18 мес). Есть сообщения об излечении в 20% случаев при продолжении интенсивной терапии после ремиссии. Прогноз при М3-варианте ОМЛ улучшается при лечении препаратами ретиноевой кислоты. Больным моложе 30 лет после достижения первой полной ремиссии можно проводить трансплантацию костного мозга. У 50% молодых больных, подвергшихся аллогенной трансплантации, развивается длительная ремиссия. Обнадёживающие результаты получены и при пересадках аутологичного костного мозга.
Возрастные особенности
• Дети •• 80% всех острых лейкозов — ОЛЛ •• Неблагоприятные прогностические факторы при ОЛЛ ••• Возраст ребёнка младше 1 года и старше 10 лет ••• Мужской пол ••• Т-клеточный вариант ОЛЛ ••• Содержание лейкоцитов в момент диагностики более 20109/л ••• Отсутствие клинико-гематологической ремиссии на фоне проводимой индукции •• Прогноз и течение. 80% выхода в клинико-гематологическую ремиссию. 5-летняя выживаемость — 40–50%.
• Пожилые. Снижена толерантность к аллогенному костному мозгу. Максимальный возраст для трансплантации — 50 лет. Аутологичную трансплантацию можно проводить пациентам старше 50 лет при отсутствии органных поражений и общем соматическом благополучии.
Сокращения • МДС — миелодиспластический синдром • ОЛЛ — острый лимфобластный лейкоз • ОМЛ — острый миелобластный лейкоз.
МКБ-10 • C91.0 Острый лимфобластный лейкоз • C92 Миелоидный лейкоз [миелолейкоз] •• C93.0 Острый моноцитарный лейкоз
Острый лейкоз крови — симптомы, лечение, рекомендации
Общие сведения
Острый лейкоз – быстро развивающаяся форма рака, при которой патологически измененные лейкоциты накапливаются в крови и в костном мозге. Существует несколько видов острого лейкоза. Так называемый острый лимфобластный лейкоз чаще всего возникает у детей. Другой тип – острый гранулоцитарный лейкоз чаще встречается у взрослых.
При лимфобластном лейкозе патологически измененные лейкоциты образуются в лимфоузлах или костном мозге. Гранулоцитарный лейкоз затрагивает лейкоциты, которые продуцируются в костном мозге.
Причины возникновения острого лейкоза
Причины лейкоза до настоящего времени неизвестны. Считается, что определенные факторы повышают риск развития лейкемии: определенные генетические отклонения, заболевания иммунной системы, воздействие высоких доз радиации и химических веществ, которые подавляют костномозговое кроветворение.
Cимптомы острого лейкоза
- Высокая температура тела;
- Общая слабость и другие гриппоподобные симптомы;
- Увеличение лимфатических узлов, селезенки и печени;
- Боли в костях;
- Тенденция к кровоточивости и образованию синяков;
- Красные или пурпурные пятна на коже, вызванные кровотечением;
- Частые инфекции и прогрессирующая слабость.
Осложнения при остром лейкозе
Острый лейкоз часто возникает внезапно, особенно у детей. Сначала кажется, что это простуда или грипп, но симптомы быстро прогрессируют, состояние ухудшается и появляются патологические изменения со стороны крови.
Острая лейкемия – опасное заболевание. При отсутствии лечения болезнь быстро прогрессирует и приводит к летальному исходу.
Специальных мер профилактики нет.
Что можете сделать Вы
При подозрении на лейкоз следует обратиться к врачу как можно скорее. Лучше всего, чтобы лечение проводил специалист-онколог, имеющий опыт лечения соответствующего типа лейкоза.
Длительность лечения лейкоза обычно составляет 2 года. В течение этого времени необходимо особенно поддерживать свои жизненные силы, поскольку противоопухолевая терапия и лучевая терапия сопровождаются тошнотой.
Чем раньше начато лечение, тем выше вероятность выздоровления.
Что может сделать врач
Во-первых, врач должен определить, связаны ли имеющиеся у пациента симптомы с лейкозом, или они вызваны анемией, или инфекционным заболеванием. Если в крови и костном мозге обнаружены клетки, характерные для лейкемии, дальнейшие исследования проводятся для того, чтобы определить тип лейкоза и наметить программу лечения.
Диагноз острого лейкоза предполагается, когда при проведении нескольких анализов крови выявляется патологически повышенное количество лейкоцитов. Для подтверждения этого диагноза проводят биопсию костного мозга.
Для лечения острого лейкоза проводят химиотерапию, применяя различные комбинации противоопухолевых препаратов. Целью лечения является уничтожение опухолевых клеток.
Доза таких препаратов должна быть тщательно подобрана для того, чтобы опухолевые клетки были уничтожены, а здоровые клетки организма не пострадали. Первая фаза лечения — индукционная терапия. В этот период больной получает наиболее интенсивное лечение в течение 4-6 недель. Этот этап терапии, как правило, вызывает ремиссию заболевания, которая, однако, может оказаться лишь временной, если не продолжать терапию.
Вторая фаза лечения – закрепляющая терапия, целью которой является уничтожение патологических клеток, присутствующих на этот момент в организме. Препараты, которые получает пациент в этой фазе, необходимы для преодоления возможной устойчивости к терапии. Поддерживающая химиотерапия обычно продолжается 2-3 года.
Большинство пациентов остается в стационаре в течение первой фазы лечения, поскольку существует высокий риск инфицирования, а также развития тяжелого кровотечения. Поскольку эти препараты подавляют продукцию лейкоцитов возможно ухудшение самочувствия, могут потребоваться частые переливания крови.
Важной частью лечения может стать трансплантация костного мозга. Это сложная процедура, при которой все продуцируемые клетки крови вначале разрушаются облучением, а затем новые клетки от подходящего донора вводятся в костный мозг со здоровыми клетками. Для предотвращения вторжения опухолевых клеток из костного мозга возможно проведение лучевой терапии.
На сегодняшний день все более количество случаев острого лейкоза успешно поддается терапии, прогноз существенно улучшается, особенно у детей; все большее число пациентов вылечивается. В 90% случаев и более достигается ремиссия, половина пациентов выживает в течение 5 и более лет.
Хронический миелолейкоз: лечение, симптомы, диагностика
Хронический миелолейкоз (ХМЛ, хронический миелоидный лейкоз) занимает третье место среди онкогематологических заболеваний. Еще несколько десятилетий назад болезнь плохо поддавалась лечению, но современные препараты позволяют значительно продлить жизнь пациентов и при этом сохранить ее качество.
Чаще всего миелолейкоз развивается у взрослых, примерно в 90% случаев болезнь обнаруживается именно в хронической форме. Чаще диагностируется у мужчин. Фактор, увеличивающий риск заболевания, – воздействие ионизирующего излучения.
Хронический миелоидный лейкоз относится к группе миелопролиферативных заболеваний.
Болезнь развивается из-за случайной хромосомной поломки, которая происходит в стволовой клетке. Стволовые клетки способны дифференцироваться в различные виды клеток, которые выполняют свои функции в организме, в том числе и в форменные элементы крови. Поломка получила название «филадельфийской» хромосомы. В клетках с поломанной хромосомой образуется онкобелок – тирозинкиназа, обладающий повышенной активностью и нарушающий работу нормальных клеток костного мозга. Увеличивается количество «молодых» форм лейкоцитов, которые постепенно размножаются и заполняют костный мозг, а затем выходят в периферическую кровь, проникают в печень и селезенку.
Хронический миелолейкоз не относится к наследуемым патологиям. В отличие от острых форм лейкозов, болезнь развивается постепенно.
Стадии заболевания
В течении хронического миелолейкоза выделяют 4 фазы:
Хроническая фаза
Менее 10% клеток в крови и костном мозге являются патологическими. Клинические признаки в этот период отсутствуют, но могут наблюдаться слабость, утомляемость, чувство тяжести в животе. Фаза может длиться до пяти лет, поэтому при наличии данных симптомов очень важно проводить ежегодные исследования показателей крови, а при их отклонениях обязательно получить консультацию специалиста.
Фаза ускорения (акселерации)
От 10% до 19% клеток в крови и костном мозге являются патологическими. Появляются признаки анемии, из-за нехватки тромбоцитов развиваются кровотечения, повышается утомляемость и усиливается риск развития инфекционных заболеваний, возможно развитие неврологических и зрительных нарушений, может появиться боль в суставах. Пациент нуждается в госпитализации и лечении.
Бластный криз
Из-за резкого увеличения количества патологических клеток (более 20%) возникает бластный криз, который по клиническим признакам напоминает острый миелобластный лейкоз. Это быстро прогрессирующее состояние, сопровождающееся значительным повышением температуры тела, увеличением селезенки, слабостью. Бластный криз – угрожающее жизни и плохо поддающееся лечению состояние.
Фаза ремиссии
Благодаря эффективному лечению, пациенты достигают ремиссии. В этот период максимально уменьшается количество клеток с «филадельфийской» хромосомой, благодаря чему нормализуется количество лейкоцитов, гемоглобина и тромбоцитов. У пациента в этот период отсутствуют клинические симптомы болезни.
Симптомы ХМЛ
На начальном этапе симптомы заболевания отсутствуют.
Затем возникают и постепенно усиливаются вялость, утомляемость, повышенная потливость (особенно ночью), чувство тяжести в левом боку из-за увеличения селезенки. Пациенты теряют аппетит и вес. Из-за накопления патологических клеток может появиться боль в суставах, а также — повышаться температура. В связи с тем, что в крови увеличивается количество аномальных клеток и возникает дефицит «здоровых» клеток, снижается иммунитет и усиливается предрасположенность к инфекционным заболеваниям. Развивается анемия, бледность кожных покровов, на ногах и на слизистой оболочке полости рта появляется сыпь в виде мелких красных точек (петехии), могут появляться кровоподтеки или развиваться кровотечения.
Для установления точной причины обнаруженных симптомов следует обязательно пройти полное диагностическое обследование. Обратитесь в LISOD, чтобы быть уверенным в точности результатов и в высоком качестве диагностики.
Диагностика
Онкогематолог. Доктор медицинских наук. Заслуженный врач Украины.
Первый шаг — выполнение анализов крови. У пациентов с ХМЛ увеличивается количество «молодых» форм лейкоцитов. Однако для постановки окончательного диагноза обязательно должна быть проведена биопсия костного мозга с последующим гистологическим исследованием.
В Больнице израильской онкологии LISOD выполняют различные виды биопсий. Все они проводятся с высококлассным анестезиологическим обеспечением, что полностью исключает болевые ощущения при проведении данной процедуры. Полученный материал направляется на исследование, позволяющее выявить «филадельфийскую» хромосому и определить количество патологических клеток. Мы можем быть уверены в правильности и точности выполнения исследований, поскольку они выполняются в референтной патологической лаборатории Германии, являющейся одной из ведущих в этом направлении.
При необходимости дообследования пациентов в LISOD есть возможность проведения всех современных диагностических исследований (КТ, ПЭТ-КТ и т. д.).
Лечение
Команда специалистов LISOD руководствуется рекомендациями международных медицинских протоколов (NCCN, AHA, EHA, ESMO). Цель лечения — максимальное снижение количества атипичных клеток в крови и костном мозге. При этом возможно достичь долговременной ремиссии.
В LISOD определением тактики лечения для каждого пациента занимается консилиум специалистов. Это дает возможность учесть все нюансы заболевания и назначить наиболее эффективное лечение с учетом возраста пациента, общего состояния здоровья, фазы заболевания.
Основные препараты для лечения ХМЛ — ингибиторы тирозинкиназы. Пациенты, обратившиеся в LISOD, имеют возможность лечения препаратами последних поколений из этой группы. При развитии бластного криза лечение проводится по схеме лечения острых лейкозов.
Лечение хронического миелолейкоза в LISOD позволяет пациентам достичь длительной ремиссии и после лечения вернуться к привычной жизни. На всех этапах лечения специалисты больницы контролируют состояние здоровья пациента, при необходимости — меняют схему лечения и назначают сопроводительную терапию.
что это, каковы основные симптомы и как с ним справиться?
Лейкоз — самое распространенное онкологическое заболевание у детей и подростков. Но оно встречается и у взрослых людей. Так на 2020 год по распространенности в мире лейкоз находился на 13 месте среди других злокачественных образований. В этом материале разбираемся, что вызывает эту болезнь и на что она влияет.
Содержание
Что такое лейкоз
Часто лейкоз называют раком крови, но это не верно. Термин «рак» относится к злокачественным опухолям, которые развиваются из эпителиальной ткани, если следовать русскоязычной медицинской традиции. Но это не включает в себя мозг и кровь. А лейкоз как раз появляется в костном мозге (мягкой ткани в полостях костей, которая отвечает за создание крови) и нарушает нормальное производство различных клеток крови.
При этой болезни отдельные недоразвитые клетки, которые стали злокачественными, начинают занимать пространство костного мозга и вытесняют остальные зрелые клетки крови.
Из-за этого меньше нормальных клеток крови производится и высвобождается в кровь, их место занимают лейкозные клетки. В итоге органы и ткани тела начинают меньше получать кислорода, тело хуже борется с инфекциями или свертывает кровь, когда это необходимо.
В зависимости от того, какие клетки крови поражает лейкоз, вид заболевания будет отличаться. Например, некоторые лейкозы относят к хроническим, а некоторые к острым. Разница здесь в том, что при остром лейкозе изменяются незрелые клетки крови (бласты). Они перестают выполнять свои обычные функции и быстро размножаются, поэтому болезнь прогрессирует внезапно — может развиться в течение нескольких дней или недель.
При хроническом лейкозе страдают зрелые и созревающие клетки крови. Они размножаются и накапливаются в организме медленнее, поэтому могут нормально функционировать дольше по времени.
Некоторые формы хронического лейкоза бессимптомны какой-то период и могут оставаться недиагностированными в течение многих лет.
Еще объединить виды лейкоза можно по типу стволовых клеток крови, из которых они произошли. При миелобластном (миелоидном) лейкозе болезнь развивается из линии миелоидных клеток. Из них у здорового человека образуются потом эритроциты, лейкоциты и тромбоциты. При лимфобластном лейкозе изменения происходят в лимфоидных стволовых клетках. Из них получаются белые кровяные тельца (лимфоциты), которые являются важной частью иммунной системы организма.
К основным типам относят: острый лимфобластный лейкоз, острый миелобластный (миелоидный) лейкоз, хронический лимфоцитарный лейкоз и хронический миелоидный лейкоз. Кстати, лейкоз еще могут называть лейкемией или белокровием, но это устаревшие синонимы этой болезни.
Почему лейкоз возникает
Считается, что лейкоз появляется из-за мутаций в стволовых клетках. Но почему именно возникают эти мутации, пока точно не известно. Врачи выделяют некоторые факторы риска, которые увеличивают вероятность этой болезни. Среди них:
- предыдущее лечение рака с помощью химиотерапии и лучевой терапии;
- наличие генетического заболевания, например, нейрофиброматоза, синдрома Клайнфельтера, синдрома Швахмана-Даймонда или синдрома Дауна;
- воздействие определенных химических промышленных веществ, таких как бензол и формальдегид;
- курение и влияние на организм канцерогенов, содержащихся в табачном дыме;
- для некоторых типов лейкоза в факторах риска отдельно выделяют семейную историю болезни. Хотя большинство мутаций, связанных с лейкозом, не передаются от родственников, а приобретаются в течение жизни.
Нужно понимать, что большинство людей, которые подвержены этим факторам риска, не заболевают лейкозом. И напротив, у многих людей с этой болезнью нет ни одного фактора риска.
Какие симптомы вызывает эта болезнь
Симптомы различаются в зависимости от типа заболевания. К общим признакам относятся: жар, озноб, ночная потливость, частые кровоподтеки, не связанные с ушибами, медленно заживающие ранки, беспричинная потеря веса, сильная и постоянная слабость, боли в суставах и костях, частые инфекции, увеличение лимфатических узлов, печени и селезенки.
Многие из этих симптомов возникают и при менее серьезных болезнях, поэтому не всегда они будут сигнализировать именно о лейкозе. Но лучше проконсультироваться у специалиста, если какие-то из признаков у вас внезапно появились.
Лейкоз возникает из-за мутаций — могут ли генетические тесты как-то помочь с лечением этой болезни?
Доступные варианты лечения могут зависеть от того, есть ли у лейкоза определенные характеристики (например, мутации), обнаруженные при генетическом тестировании. Например, у хронического миелоидного лейкоза могут искать мутацию T315I в гене ABL1, которая позволяет использовать особый тип таргетной терапии. При остром миелобластном лейкозе некоторые клетки имеют мутацию в гене FLT3, а также в гене IDh2 или IDh3 — эти генетические нарушения также играют роль при подборе таргетной терапии.
Примерно у 1 из 4 взрослых пациентов с острым лимфобластным лейкозом в клетках обнаруживают филадельфийскую хромосому. Она приводит к созданию в клетках нового гена под названием BCR-ABL, который начинает вырабатывать аномальный белок, помогающий злокачественным клеткам расти. Чтобы бороться с ним, есть специальные препараты — ингибиторы тирозинкиназы.
Генетический анализ онкологии часто помогает в подборе терапии: особено, когда опухоль обнаружили на этапе метастазов. Узнать больше о том, как это работает можно на сайте Центра молекулярной онкологии ОнкоАтлас.
- American Cancer Society, What Causes Acute Lymphocytic Leukemia (ALL)?, 2021
- American Cancer Society, Leukemia in Children, 2021
- American Cancer Society, What Is Acute Lymphocytic Leukemia (ALL)?, 2021
- American Cancer Society, Targeted Therapy for Acute Lymphocytic Leukemia (ALL), 2021
- American Cancer Society, Targeted Therapy Drugs for Acute Myeloid Leukemia (AML), 2021
- American Cancer Society, Targeted Therapies for Chronic Myeloid Leukemia, 2021
- Cleveland Clinic, Leukemia, 2021
- Canadian Cancer Society, What is leukemia?, 2021
- Cancer Today, Estimated number of new cases in 2020, worldwide, both sexes, all ages, 2021
- Mayo Foundation for Medical Education and Research, Leukemia, 2021
- UpToDate, Patient education: Chronic lymphocytic leukemia (CLL) in adults, 2021
Насколько быстро развивается лейкоз — Doc. Theodore Ross
Теодор Росс, доктор медицинских наук, рассказывает о разнице между острым и хроническим лейкозом и описывает, как быстро они развиваются и прогрессируют.
Лейкемия — это рак крови. Это начинается, когда костный мозг начинает быстро производить аномальные лейкоциты, называемые лейкозными клетками. Они могут вытеснять нормальные лейкоциты, эритроциты и тромбоциты , мешая нормальным клеткам выполнять свою работу.
Существует четыре основных типа лейкемии:
- Острый лимфоцитарный лейкоз
- Хронический лимфолейкоз
- Острый миелоидный лейкоз
- Хронический миелолейкоз
Хронические и острые лейкемии — совершенно разные заболевания, и они прогрессируют с разной скоростью. То, как с ними обращаются, может быть совершенно другим.
Лейкемия у взрослых и другие заболевания крови
Лейкемия — это название нескольких видов рака, которые начинаются в ткани, которая создает клетки крови. Чтобы понять лейкемию, полезно знать, как образуются нормальные клетки крови.
Острый лейкоз: наиболее быстро прогрессирующий рак, о котором мы знаем
Острые лейкемии, которые невероятно редки, являются наиболее быстро прогрессирующим раком, о котором мы знаем. Белые клетки в крови растут очень быстро, в течение нескольких дней или недель. Иногда пациент с острым лейкозом не имеет симптомов или имеет нормальную работу крови даже за несколько недель или месяцев до постановки диагноза. Изменение может быть довольно драматичным.
Чрезвычайная усталость обычно является первым симптомом, который заставляет пациентов с острым лейкозом обращаться за медицинской помощью. Они устали без видимой причины. Они не могут двигаться и не могут ходить, и это происходит довольно быстро. Когда мы проверяем их анализ крови, их количество эритроцитов может быть вдвое меньше нормального. Вот почему они истощены — потому что они не получают достаточно кислорода.
Для этих пациентов также характерно развитие пневмонии или какой-либо инфекции. Они не поправляются после приема антибиотиков, поэтому они принимают все больше и больше, но они все равно не поправляются. Затем, наконец, кто-то проверяет свой анализ крови и обнаруживает, что он не отвечает, потому что его иммунная система очень низкая из-за острого лейкоза.
Эффекты слишком большого количества белых кровяных клеток
На момент постановки диагноза у пациентов может быть очень и очень высокое количество лейкоцитов. Как правило, у здорового человека количество лейкоцитов составляет около 4000-11000. Пациенты с острым или даже хроническим лейкозом могут войти с количеством лейкоцитов в диапазоне от 100 000 до 400 000.
Когда у вас в кровеносных сосудах столько белых клеток, это может ухудшить кровоток, потому что у вас в 20-40 раз больше нормального числа клеток в кровеносных сосудах. И это не нормальные клетки — это опухолевые клетки, поэтому они могут слипаться, а также могут прилипать к кровеносным сосудам.
Когда у пациентов очень высокое количество лейкоцитов, лейкозные клетки обычно перетекают из кровеносных сосудов в некоторые органы. Если поражены легкие, у пациента может быть дыхательная недостаточность. У пациентов могут быть инсульты из-за прерванного кровотока в мозге. У них могут быть сердечные приступы или неврологические изменения. Поэтому, когда кто-то приходит с очень высоким уровнем лейкоцитов, мы очень обеспокоены этими рисками. В этих случаях мы обычно стараемся быстро удалить аномальные клетки из крови и начать химиотерапию, чтобы как можно скорее убить их.
Лейкемия также может привести к уменьшению количества тромбоцитов в организме, что способствует свертыванию крови. Когда это происходит, у пациентов повышается риск кровотечения, поэтому они могут оказаться в отделении неотложной помощи или центре неотложной медицинской помощи после развития носового кровотечения, которое длится в течение двух часов. Поэтому, если у вас необычное кровотечение из-за небольшой травмы или вы проснулись с огромными ушибами и не помните, что получили травму, это может означать, что что-то не так с вашими тромбоцитами и вашей системой свертывания.
Низкие тромбоциты также могут вызывать петехии , небольшие разрывы в самых маленьких кровеносных сосудах, которые вызывают попадание крови в кожу. Петехии вызывают появление темно-красных пятен на коже, очень похожих на сыпь.
Примечания:
Острые лейкемии | CalvertHealth
Острый лейкоз — это рак крови и костного мозга, который является одним из наиболее распространенных видов рака у детей. Это также может произойти у взрослых. Лечение обычно более эффективно у детей. Формы острого лейкоза включают острый миелоидный лейкоз (ОМЛ) и острый лимфоцитарный лейкоз (ОЛЛ). Также существует несколько типов хронического лейкоза. Каковы симптомы острого лейкоза?
Некоторые общие симптомы включают: увеличение печени или селезенки, легкие синяки, кровоточивость десен, боль в костях или суставах, лихорадку и озноб, частые инфекции, кровотечения из носа, бледность кожи, одышку, общую слабость, ночную потливость и увеличение лимфатических узлов вокруг шея, подмышки, живот или пах.
Как диагностируется острый лейкоз?
Диагностика острого лейкоза проводится путем анализа крови и костного мозга.
Как лечить острый лейкоз?
Лечение зависит от множества факторов, включая возраст и состояние здоровья пациента, точную форму лейкемии и связанные с ней генетические мутации. Химиотерапия — это обычное лечение. Химиотерапия часто начинается с интенсивного режима перед переходом к более длительной поддерживающей фазе, которая может длиться около двух лет.В большинстве случаев это будет проводиться с помощью инфузионной терапии. Радиация иногда используется в определенных ситуациях, например, чтобы уменьшить опухоль, когда лейкемия распространилась на какой-либо орган. Иногда может потребоваться хирургическое вмешательство и пересадка стволовых клеток.
Каковы факторы риска развития острого лейкоза?
Люди, которые ранее перенесли химиотерапию, подверглись облучению или курению, или у которых есть определенные генетические нарушения, или у кого-то из близких родственников острый лейкоз, выше риск развития этого рака.Однако у большинства людей факторы риска неизвестны.
Какие дополнительные ресурсы можно узнать об остром лейкозе?
Если вы или ваш близкий человек страдаете острой лейкемией, CalvertHealth предлагает целый ряд услуг, призванных помочь вам, поэтому вы никогда не отправитесь в путь в одиночку. Пожалуйста, поговорите со своим поставщиком CalvertHealth, вашим медсестрой-навигатором или проверьте страницы услуг для получения информации о лечении, услугах и группах поддержки. Более подробная информация обо ВСЕМ доступна здесь: https: // www.nccn.org/patients/guidelines/all/index.html
Какие типы лейкемии?
Врачи классифицируют лейкоз в зависимости от типа лейкоцитов — лимфоцитов или миелоидных клеток — и от того, развивается ли болезнь очень быстро ( острое заболевание ) или медленно ( хроническое заболевание ).
Лимфоцитарные лейкозы развиваются из клеток, дающих начало Т-лимфоцитам (Т-клеткам), В-лимфоцитам (В-клетки) или естественным киллерам (NK).Каждый из этих типов клеток играет особую роль в иммунной системе; одни вырабатывают антитела, тогда как другие напрямую борются с другими иммунными клетками или направляют их на борьбу с инфекциями.
Миелоидные лейкозы развиваются из клеток, дающих начало лейкоцитам, называемым гранулоцитами и моноцитами. Гранулоциты получили свое название от гранул, содержащих ферменты, которые они несут внутри себя. Они высвобождают эти ферменты при встрече с бактериями или грибками. Моноциты в конечном итоге становятся макрофагами, которые поглощают и уничтожают бактерии и грибки.
При остром лейкозе, который развивается быстро, злокачественные клетки (называемые бластами ) являются незрелыми и неспособны выполнять свои функции иммунной системы. Хронические лейкозы развиваются в более зрелых клетках, которые могут выполнять некоторые из своих функций, но не очень хорошо. Эти аномальные клетки обычно размножаются медленнее, чем при остром лейкозе.
Из четырех распространенных типов лейкемии у взрослых наиболее часто встречаются острый миелоидный лейкоз (ОМЛ) и хронический лимфоцитарный лейкоз (ХЛЛ).Другие родственные виды рака крови включают миелопролиферативные новообразования и системный мастоцитоз.
- О волосатоклеточном лейкозе (HCL)
Волосатоклеточный лейкоз (HCL) — это редкий вид рака у взрослых, который обычно обнаруживается во время тестирования на низкое содержание крови. Узнайте больше о том, что врачи MSK ищут при диагностике HCL.
- Острый лимфоцитарный лейкоз (ОЛЛ)
Острый лимфоцитарный лейкоз (ОЛЛ) — редкая форма рака у взрослых, но наиболее распространенная форма лейкемии у детей. Узнайте больше о том, что врачи MSK ищут при постановке диагноза ВСЕ.
- Острый миелоидный лейкоз (ОМЛ)
Острый миелоидный лейкоз (ОМЛ) — один из наиболее распространенных лейкозов у взрослых.Узнайте больше о AML и способах его диагностики.
- Острый промиелоцитарный лейкоз (APL)
Острый промиелоцитарный лейкоз (APL) — это агрессивный тип острого миелоидного лейкоза. Узнайте больше об APL и способах его диагностики.
- Хронический лимфоцитарный лейкоз (ХЛЛ)
Хронический лимфолейкоз (ХЛЛ) является наиболее распространенным хроническим лейкозом у взрослых.Методы лечения ХЛЛ быстро улучшаются и меняются. Узнайте о методах лечения ХЛЛ.
- Хронический миелоидный лейкоз (ХМЛ)
Узнайте больше о том, какую роль хромосомы играют в развитии хронического миелоидного лейкоза (ХМЛ).
- Миелопролиферативные новообразования (MPN)
Узнайте, что делает костный мозг и как это может привести к развитию заболеваний, известных как миелопролиферативные новообразования.
- Системный мастоцитоз
Мастоцитоз возникает, когда в организме накапливается слишком много тучных клеток. Читайте о том, как диагностируется это заболевание и его отношения к аллергии.
Острый лейкоз — обзор
МОРФОЛОГИЯ И БИОЛОГИЯ
Острые лейкозы, определяемые как 20% или более бластов в крови или костном мозге в соответствии с критериями Всемирной организации здравоохранения (ВОЗ), классифицируются в соответствии с преобладающей линией опухолевых клеток и, следовательно, могут обозначается как лимфобластный или миелоидный.Классификация ВОЗ учитывает цитогенетические и молекулярные данные в дополнение к морфологическим и гистохимическим критериям (см. Таблицы 15.1 и 15.4). Примерно от 70% до 80% случаев можно классифицировать только на основании морфологии, в то время как дополнительные от 10% до 15% случаев требуют гистохимических определений для постановки конкретного диагноза. Примерно в 10% случаев для точной классификации необходимы поверхностные маркеры и цитогенетические исследования, особенно при «недифференцированных» острых лейкозах.Использование моноклональных антител показало, что около 20% случаев ОЛЛ имеют Т-клеточное происхождение; большая часть остальных имеет происхождение от В-клеток или пре-В-клеток (см. Таблицу 15.3).
Разработка методов анализа колоний и новых моноклональных антител привела к более четкому пониманию нормального онтогенеза миелоида. Установлены закономерности экспрессии различных антигенов во время нормальной миелоидной дифференцировки. Методы иммунофенотипирования продемонстрировали, что в некоторых случаях острого «недифференцированного» лейкоза или тех, которые по морфологии считаются ОЛЛ, обнаруживаются миелоидные маркеры.Улучшение цитогенетических исследований за счет использования новых методов группирования показало, что почти все острые лейкемии характеризуются хромосомными аномалиями, от гипоплоидии до полиплоидии. Были идентифицированы значительные цитогенетические дефекты, которые имеют прогностическое значение (например, наблюдаются только в определенных подгруппах), включая ОЛЛ, а также ОМЛ. Генетические аномалии при остром лейкозе могут влиять на гены, которые кодируют белки, участвующие в передаче сигналов, регуляции транскрипции, клеточной дифференцировке и апоптозе, а также в подавлении опухоли (антионкогены).
Примерно у 10% взрослых с ОЛЛ цитогенетические исследования покажут наличие филадельфийской хромосомы (t (9; 22) (q34; q11)), и частота случаев увеличивается с возрастом. Эти Ph-положительные пациенты, как правило, старше (средний возраст 46 лет против 35 лет) и имеют более низкую частоту анемии и более высокую частоту лейкоцитоза, чем Ph-отрицательные пациенты (Preti et al., 1994). Ph-положительные пациенты с ОЛЛ также могут иметь морфологию FAB-L2 (см. Таблицу 15.1), быть обычными антиген-положительными по ОЛЛ (CALLA-CD10-положительными) и CD34-положительными и иметь худший прогноз, чем Ph-отрицательный ОЛЛ. случаи.У некоторых пациентов с ОЛЛ и ОМЛ, которые являются Ph-отрицательными, молекулярные исследования (например, полимеразная цепная реакция) выявляют наличие транскриптов BCR-ABL, позволяющих диагностировать аномалию Ph-хромосомы, которые иначе не обнаруживаются из-за недостаточности метафаз (Kantarjian et al. ., 1994).
Острый лимфобластный лейкоз (ОЛЛ): основы практики, патофизиология, этиология
Гривз М. Причинный механизм острого лимфобластного лейкоза у детей. Нат Рев Рак .2018 21 мая. [Medline].
Нельсон Р. «Слишком чистый» может стать триггером острого лейкоза у детей. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/897242. 25 мая 2018 г .; Дата обращения: 29 мая 2018 г.
Curtis RE, Freedman DM, Ron E, Ries LAG, Hacker DG, Edwards BK и др. Новые злокачественные новообразования среди выживших после рака, Регистры рака SEER, 1973-2000 гг. . Номер публикации NIH 05-5302. Бетесда, Мэриленд: Национальный институт рака; 2006 г.
Тан М., Фонг Р., Ло М., Янг Р. Леналидомид и вторичный острый лимфобластный лейкоз: серия случаев. Гематол Онкол . 2017 марта. 35 (1): 130-134. [Медлайн].
Розенберг А.С., Брансон А., Паулюс Дж. К., Тоскано Дж., Вун Т., Киган Т.М. и др. Вторичный острый лимфобластный лейкоз — отдельная клиническая картина, имеющая прогностическое значение. Рак крови J . 2017 8 сентября. 7 (9): e605. [Медлайн].
Андерсен М.К., Кристиансен Д.Х., Йенсен Б.А., Эрнст П., Хауге Г., Педерсен-Бьергаард Дж.Связанный с терапией острый лимфобластный лейкоз с перестройками MLL после ингибиторов ДНК-топоизомеразы II, растущая проблема: сообщение о двух новых случаях и обзор литературы с 1992 года. Br J Haematol . 2001 сентябрь 114 (3): 539-43. [Медлайн].
Perez-Andreu V, Roberts KG, Xu H, et al. Полногеномное ассоциативное исследование восприимчивости к острому лимфобластному лейкозу у подростков и молодых людей. Кровь . 2015, 22 января. 125 (4): 680-6.[Медлайн].
Эрнандес-Гонсалес О, Ортис-Замудио Дж.Дж., Родригес-Пиналь С.Дж., Альварадо-Моралес I, Мартинес-Хименес В.Д.К., Салазар-Гонсалес РА и др. Генетический полиморфизм N-ацетилтрансфераз ариламина 1 и 2 и вероятность развития острого лимфобластного лейкоза у детей. Лимфома лейк . 2017 7 декабря. 1-8. [Медлайн].
Pei JS, Chou AK, Hsu PC, Tsai CW, Chang WS, Wu MF и др. Вклад генотипов матричной металлопротеиназы-7 в риск нетвердой опухоли, детской лейкемии. Противораковое лечение . 2017 г., 37 (12): 6679-6684. [Медлайн].
Gutierrez-Camino A, Martin-Guerrero I, García-Orad A. Генетическая предрасположенность при остром лимфобластном лейкозе у детей. Мед Онкол . 2017 13 сентября. 34 (10): 179. [Медлайн].
Программа эпиднадзора, эпидемиологии и конечных результатов. Национальные институты здоровья. Доступно по адресу https://seer.cancer.gov/statfacts/html/alyl.html. Дата обращения: 23 марта 2021 г.
Рак в фактах и цифрах 2021.Американское онкологическое общество. Доступно по адресу https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2021/cancer-facts-and-figures- 2021.pdf. Дата обращения: 23 марта 2021 г.
Игве И.Дж., Ян Д., Торговец А, Мерин Н., Ягмур Г., Келли К. и др. Наличие филадельфийской хромосомы не означает плохой прогноз при остром лимфобластном лейкозе до В у взрослых в эпоху ингибиторов тирозинкиназы — наблюдение, эпидемиология и анализ базы данных конечных результатов. Br J Haematol . 2017 ноябрь 179 (4): 618-626. [Медлайн].
Czuczman MS, Dodge RK, Stewart CC, Frankel SR, Davey FR, Powell BL и др. Значение иммунофенотипа при интенсивном лечении острого лимфобластного лейкоза взрослых: рак и лейкемия Исследование группы B 8364. Кровь . 1 июня 1999 г. 93 (11): 3931-9. [Медлайн].
Preti HA, Huh YO, O’Brien SM, Andreeff M, Pierce ST, Keating M и др. Миелоидные маркеры при остром лимфоцитарном лейкозе у взрослых.Корреляция с характеристиками пациента и заболевания и прогнозом. Рак . 1995, 1. 76 (9): 1564-70. [Медлайн].
Issa GC, Kantarjian HM, Yin CC, Qiao W., Ravandi F, Thomas D, et al. Прогностическое влияние цитогенетики до лечения при остром лимфобластном лейкозе с отрицательными хромосомами в Филадельфии в эпоху минимальной остаточной болезни. Рак . 2017 г. 1. 123 (3): 459-467. [Медлайн].
Берри Д.А., Чжоу С., Хигли Х., Мукундан Л., Фу С., Реаман Г.Х. и др.Связь минимальной остаточной болезни с клиническим исходом при остром лимфобластном лейкозе у детей и взрослых: метаанализ. JAMA Oncol . 2017 13 июля 3 (7): e170580. [Медлайн].
Patel S, Mason CC, Glenn MJ, Paxton CN, South ST, Cessna MH и др. Геномный анализ взрослого B-ALL определяет потенциальные маркеры более короткой выживаемости. Лейк Рес . 2017 май. 56: 44-51. [Медлайн].
Лю Й., Истон Дж., Шао Й. и др.Геномный ландшафт острого лимфобластного лейкоза Т-линии у детей и подростков. Нат Генет . 2017 августа 49 (8): 1211-1218. [Медлайн].
[Рекомендации] NCCN Клинические рекомендации по онкологии: острый лимфобластный лейкоз. Национальная всеобъемлющая онкологическая сеть. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/all.pdf. Версия 2.2020 — 23 октября 2020 г .; Дата обращения: 23 марта 2021 г.
Арбер Д.А., Орази А., Хассерджян Р., Тиле Дж., Боровиц М.Дж., Ле Бо М.М. и др.Пересмотр 2016 г. классификации миелоидных новообразований и острого лейкоза Всемирной организации здравоохранения. Кровь . 2016 19 мая. 127 (20): 2391-405. [Медлайн].
Робертс К.Г., Ли Ю., Пейн-Тернер Д. и др. Целевые поражения, активирующие киназу, при Ph-подобном остром лимфобластном лейкозе. N Engl J Med . 2014 11 сентября. 371 (11): 1005-15. [Медлайн].
Reshmi SC, Harvey RC, Roberts KG и др. Целевые слияния генов киназ при B-ОЛЛ высокого риска: исследование Детской онкологической группы. Кровь . 2017, 22 июня. 129 (25): 3352-3361. [Медлайн].
Heerema NA, Carroll AJ, Devidas M, Loh ML, Borowitz MJ, Gastier-Foster JM и др. Внутрихромосомная амплификация хромосомы 21 связана с худшими результатами у детей с острым лимфобластным лейкозом, леченных в современных исследованиях детской онкологической группы стандартного риска: отчет детской онкологической группы. Дж. Клин Онкол . 2013 20 сентября. 31 (27): 3397-402. [Медлайн].
Харрисон С.Дж., Мурман А.В., Шваб С.и др. Международное исследование внутрихромосомной амплификации хромосомы 21 (iAMP21): цитогенетическая характеристика и исход. Лейкемия . 2014 май. 28 (5): 1015-21. [Медлайн].
Coustan-Smith E, Mullighan CG, Onciu M, Behm FG, Raimondi SC, Pei D, et al. Ранний лейкоз-предшественник Т-лимфоцитов: подтип острого лимфобластного лейкоза с очень высоким риском. Ланцет Онкол . 2009 фев.10 (2): 147-56. [Медлайн].
Чжан Дж., Динг Л., Холмфельдт Л. и др. Генетическая основа раннего Т-клеточного предшественника острого лимфобластного лейкоза. Природа . 2012 г. 11 января. 481 (7380): 157-63. [Медлайн].
Кантарджан Х., Томас Д., О’Брайен С., Кортес Дж., Джайлс Ф., Джеха С. и др. Долгосрочные результаты наблюдения гиперфракционированного циклофосфамида, винкристина, доксорубицина и дексаметазона (Hyper-CVAD) в режиме интенсивной дозы при остром лимфолейкозе у взрослых. Рак . 2004 15 декабря. 101 (12): 2788-801. [Медлайн].
Ларсон Р.А., Додж Р.К., Бернс С.П., Ли Э.Дж., Стоун Р.М., Шульман П.и др. Схема индукции ремиссии с пятью препаратами с интенсивной консолидацией для взрослых с острым лимфобластным лейкозом: рак и лейкемия, исследование группы B 8811. Кровь . 1995 15 апреля. 85 (8): 2025-37. [Медлайн].
Dhédin N, Huynh A., Maury S, Tabrizi R, Beldjord K, Asnafi V и др. Роль аллогенной трансплантации стволовых клеток у взрослых пациентов с Ph-отрицательным острым лимфобластным лейкозом. Кровь . 2015 16 апреля. 125 (16): 2486-96; викторина 2586. [Medline].
Linker CA, Levitt LJ, O’Donnell M, Forman SJ, Ries CA. Лечение острого лимфобластного лейкоза у взрослых с помощью интенсивной циклической химиотерапии: отчет о наблюдении. Кровь . 1 декабря 1991 г. 78 (11): 2814-22. [Медлайн].
Rowe JM, Buck G, Burnett AK, Chopra R, Wiernik PH, Richards SM и др. Индукционная терапия для взрослых с острым лимфобластным лейкозом: результаты более чем 1500 пациентов из международного исследования ALL: MRC UKALL XII / ECOG E2993. Кровь . 2005 декабрь 1. 106 (12): 3760-7. [Медлайн].
Maury S, Chevret S, Thomas X, Heim D, Leguay T, Huguet F и др. Ритуксимаб при остром лимфобластном лейкозе у взрослых B-линии. N Engl J Med . 2016 15 сентября. 375 (11): 1044-53. [Медлайн].
Fiere D, Extra JM, David B, Witz F, Vernand JP, Gastaut JA, et al. Лечение 218 острых лимфобластных лейкозов у взрослых. Семин Онкол . 1987, 14 июня (2 приложение 1): 64-6.[Медлайн].
Hoelzer D, Thiel E, Löffler H, Bodenstein H, Plaumann L, Büchner T, et al. Интенсивная терапия острого лимфобластного и острого недифференцированного лейкоза у взрослых. Кровь . 1984 июл.64 (1): 38-47. [Медлайн].
Дуррант И.Дж., Прентис Х.Г., Ричардс С.М. Интенсификация лечения взрослых с острым лимфобластным лейкозом: результаты рандомизированного исследования UKALL XA. Рабочая группа Совета медицинских исследований по лейкемии у взрослых. Br J Haematol . 1997 Октябрь 99 (1): 84-92. [Медлайн].
Каттнер Дж., Мик Р., Будман Д. Р., Майер Р. Дж., Ли Э. Дж., Хендерсон Е. С. и др. Испытание фазы III кратковременного интенсивного лечения острого лимфоцитарного лейкоза у взрослых, сравнивающее даунорубицин и митоксантрон: исследование CALGB. Лейкемия . 1991 Май. 5 (5): 425-31. [Медлайн].
Dekker AW, van’t Veer MB, Sizoo W, Haak HL, van der Lelie J, Ossenkoppele G, et al. Интенсивная постремонтная химиотерапия без поддерживающей терапии у взрослых с острым лимфобластным лейкозом.Голландская исследовательская группа по гемато-онкологии. Дж. Клин Онкол . 1997 15 февраля (2): 476-82. [Медлайн].
Манделли Ф., Аннино Л., Ротоли Б. Испытание GIMEMA ALL 0183: анализ 10-летнего наблюдения. Кооперативная группа GIMEMA, Италия. Br J Haematol . 1996, март 92 (3): 665-72. [Медлайн].
Cortes J, O’Brien SM, Pierce S, Keating MJ, Freireich EJ, Kantarjian HM. Значение высоких доз системной химиотерапии и интратекальной терапии для профилактики центральной нервной системы в различных группах риска острого лимфобластного лейкоза у взрослых. Кровь . 1995 15 сентября. 86 (6): 2091-7. [Медлайн].
Hoelzer D, Ludwig WD, Thiel E, Gassmann W, Löffler H, Fonatsch C и др. Улучшение результатов при остром B-клеточном остром лимфобластном лейкозе. Кровь . 1996 15 января. 87 (2): 495-508. [Медлайн].
Thomas TA, Kantarjian H, Faderl S, et al. Обновление модифицированного режима гипер-CVAD с ритуксимабом или без него в качестве передовой терапии взрослых с острым лимфолейкозом (ALL) или лимфобластной лимфомой (LL) [аннотация]. Кровь . 2007. 110: 2824a. [Полный текст].
Томас Д.А., Фадерл С., Кортес Дж., О’Брайен С., Джайлс Ф.Дж., Корнблау С.М. и др. Лечение острого лимфоцитарного лейкоза с положительной хромосомой в Филадельфии с помощью гипер-CVAD и мезилата иматиниба. Кровь . 2004 15 июня. 103 (12): 4396-407. [Медлайн].
Дэвер Н., Томас Д., Раванди Ф., Кортес Дж., Гаррис Р., Джаббур Е. и др. Заключительный отчет фазы II исследования мезилата иматиниба с гипер-CVAD для первичного лечения взрослых пациентов с острым лимфобластным лейкозом, положительным по филадельфийской хромосоме. Haematologica . 2015 май. 100 (5): 653-61. [Медлайн].
Людвиг В.Д., Ридер Х., Бартрам С.Р., Хайнце Б., Шварц С., Гассманн В. и др. Иммунофенотипические и генотипические особенности, клинические характеристики и исход лечения острого лимфобластного лейкоза про-B у взрослых: результаты многоцентровых исследований GMALL 03/87 и 04/89 в Германии. Кровь . 1998 15 сентября. 92 (6): 1898-909. [Медлайн].
Филдинг А.К., Роу Дж. М., Бак Дж., Форони Л., Джеррард Дж., Литцов М. Р. и др.UKALLXII / ECOG2993: добавление иматиниба к стандартной схеме лечения улучшает долгосрочные результаты при остром лимфобластном лейкозе с положительным результатом в Филадельфии. Кровь . 2014 6 февраля. 123 (6): 843-50. [Медлайн].
Wetzler M, Watson D, Stock W, Koval G, Mulkey FA, Hoke EE, et al. Аутологичная трансплантация при остром лимфобластном лейкозе с положительной хромосомой в Филадельфии дает результаты, аналогичные аллогенной трансплантации: результаты исследования CALGB Study 10001 (Alliance). Haematologica . 2014 Январь 99 (1): 111-5. [Медлайн].
Танги-Шмидт А., Русселот П., Шаландон Ю., Кайуэла Дж. М., Хайетт С., Векеманс М.С. и др. Долгосрочное наблюдение за исследованием иматиниба GRAAPH-2003 у впервые диагностированных пациентов с острым лимфобластным лейкозом de novo, положительным по филадельфийской хромосоме: исследование GRAALL. Пересадка костного мозга Biol . 2013 января 19 (1): 150-5. [Медлайн].
Янада М., Такеучи Дж., Сугиура I, Акияма Х., Усуи Н., Ягасаки Ф. и др.Высокая частота полной ремиссии и многообещающий исход при комбинации иматиниба и химиотерапии для недавно диагностированного BCR-ABL-положительного острого лимфобластного лейкоза: исследование фазы II, проведенное Японской группой изучения лейкемии взрослых. Дж. Клин Онкол . 2006 20 января. 24 (3): 460-6. [Медлайн].
Бассан Р., Росси Г., Поглиани Э.М., Ди Бона Э., Ангелуччи Э., Каваттони И. и др. Импульсы иматиниба с фазой химиотерапии улучшают отдаленные результаты у взрослых пациентов с острым лимфобластным лейкозом, положительным по филадельфийской хромосоме: протокол группы лейкемии Северной Италии 09/00. Дж. Клин Онкол . 2010, 1. 28 (22): 3644-52. [Медлайн].
Kantarjian H, Giles F, Wunderle L, Bhalla K, O’Brien S, Wassmann B, et al. Нилотиниб при устойчивом к иматинибу ХМЛ и положительном по филадельфийской хромосоме ОЛЛ. N Engl J Med . 2006 15 июня. 354 (24): 2542-51. [Медлайн].
Kim DY, et al; Рабочая группа по острому лимфобластному лейкозу у взрослых Корейского общества гематологов. Нилотиниб в сочетании с мультиагентной химиотерапией при впервые выявленном филадельфийском остром лимфобластном лейкозе. Кровь . 2015 6 августа. 126 (6): 746-56. [Медлайн]. [Полный текст].
Talpaz M, Shah NP, Kantarjian H, Donato N, Nicoll J, Paquette R и др. Дазатиниб при устойчивых к иматинибу филадельфийских хромосомных лейкозах. N Engl J Med . 2006 15 июня. 354 (24): 2531-41. [Медлайн].
Foa R, Vitale A, Vignetti M, et al. Дазатиниб в качестве терапии первой линии для взрослых пациентов с острым лимфобластным лейкозом с положительной филадельфийской хромосомой. Кровь . 2011 15 декабря. 118 (25): 6521-8. [Медлайн].
Раванди Ф., О’Брайен С.М., Кортес Дж. Э., Томас Д.М., Гаррис Р., Фадерл С. и др. Долгосрочное наблюдение за фазой 2 исследования химиотерапии плюс дазатиниб для начального лечения пациентов с острым лимфобластным лейкозом с положительной филадельфийской хромосомой. Рак . 2015 г. 1. 121 (23): 4158-64. [Медлайн].
Rousselot P, Coudé MM, Gokbuget N, et al. Дазатиниб и низкоинтенсивная химиотерапия у пожилых пациентов с филадельфийским хромосомно-положительным ОЛЛ. Кровь . 2016 11 августа 128 (6): 774-82. [Медлайн].
Foà R, et al; Следователи GIMEMA. Дазатиниб-Блинатумомаб для Ph-положительного острого лимфобластного лейкоза у взрослых. N Engl J Med . 2020 22 октября. 383 (17): 1613-1623. [Медлайн].
Iclusig (понатиниб) [вкладыш в упаковке]. Кембридж, Массачусетс: Ariad Pharmaceuticals, Inc., декабрь 2013 г. Доступно на [Полный текст].
Sasaki K, Jabbour EJ, Ravandi F, Short NJ, Thomas DA, Garcia-Manero G, et al.Гипер-CVAD плюс понатиниб по сравнению с гипер-CVAD плюс дазатиниб в качестве терапии первой линии для пациентов с острым лимфобластным лейкозом с положительной филадельфийской хромосомой: анализ предрасположенности. Рак . 2016 г. 1. 122 (23): 3650-3656. [Медлайн].
Stock W, La M, Sanford B, Bloomfield CD, Vardiman JW, Gaynon P и др. Что определяет исходы для подростков и молодых людей с острым лимфобластным лейкозом, пролеченных по протоколам совместной группы? Сравнение исследований детской онкологической группы и рака и лейкемии группы B. Кровь . 2008 сен 1. 112 (5): 1646-54. [Медлайн]. [Полный текст].
Boissel N, Auclerc MF, Lhéritier V, Perel Y, Thomas X, Leblanc T. и др. Следует ли лечить подростков с острым лимфобластным лейкозом как детей старшего возраста или молодых людей? Сравнение французских испытаний FRALLE-93 и LALA-94. Дж. Клин Онкол . 2003 г., 1. 21 (5): 774-80. [Медлайн].
Ribera JM, Oriol A, Sanz MA, Tormo M, Fernández-Abellán P, del Potro E, et al.Сравнение результатов лечения подростков и молодых людей с острым лимфобластным лейкозом стандартного риска с помощью педиатрического протокола ALL-96. Дж. Клин Онкол . 2008 г., 10 апреля (11): 1843-9. [Медлайн].
ДеАнджело Д. Д., Стивенсон К. Э., Дальберг С. Е., Сильверман Л. Б., Кубан С., Супко Дж. Г. и др. Долгосрочный результат лечения, рекомендованного педиатрами, для взрослых в возрасте 18-50 лет с впервые диагностированным острым лимфобластным лейкозом. Лейкемия . 2015 29 марта (3): 526-34. [Медлайн].
Seftel MD, Neuberg D, Zhang MJ и др. Терапия, вдохновленная педиатром, по сравнению с аллотрансплантацией для Филадельфийского хромосомно-отрицательного ОЛЛ у взрослых в первой полной ремиссии. Ам Дж. Гематол . 2016 Март 91 (3): 322-9. [Медлайн].
Алабдулвахаб А.С., Эльсайед Х.Г., Шеришер М.А., Зинелдин А., Альгамди К., Эльбджейрами В.М. Протокол консорциума Даны Фарбер (DFCP) в сравнении с классическим Hyper-CVAD для лечения острого лимфобластного лейкоза у пациентов Leuk Res .2017 Сентябрь 60: 58-62. [Медлайн].
Rytting ME, Jabbour EJ, Jorgensen JL, Ravandi F, Franklin AR, Kadia TM, et al. Окончательные результаты опыта одного учреждения с педиатрической схемой расширенного режима Берлин-Франкфурт-Мюнстер у подростков и молодых людей с острым лимфобластным лейкозом и сравнение с режимом гипер-CVAD. Ам Дж. Гематол . 2016 август 91 (8): 819-23. [Медлайн].
Hunault M, Harousseau JL, Delain M, Truchan-Graczyk M, Cahn JY, Witz F и др.Лучший исход острого лимфобластного лейкоза у взрослых после ранней геноидентичной аллогенной трансплантации костного мозга (BMT), чем после поздней терапии высокими дозами и аутологичной BMT: исследование GOELAMS. Кровь . 2004 15 ноября. 104 (10): 3028-37. [Медлайн].
Attal M, Blaise D, Marit G, Payen C, Michallet M, Vernant JP и др. Консолидированное лечение острого лимфобластного лейкоза у взрослых: проспективное рандомизированное исследование, сравнивающее аллогенную и аутологичную трансплантацию костного мозга и проверяющее влияние рекомбинантного интерлейкина-2 после аутотрансплантации костного мозга.БГМТ Групп. Кровь . 1995 15 августа. 86 (4): 1619-28. [Медлайн].
Fiere D, Archimbaud E, Extra JM, Marty M, David B, Witz F и др. Лечение острого лимфобластного лейкоза у взрослых. Предварительные результаты исследования французской группы. Переливание крови гематол . 1987. 30: 125-9. [Медлайн].
Rowe JM, Buck G, Burnett AK, Chopra R, Wiernik PH, Richards SM и др. Индукционная терапия для взрослых с острым лимфобластным лейкозом: результаты более чем 1500 пациентов из международного исследования ALL: MRC UKALL XII / ECOG E2993. Кровь . 2005 декабрь 1. 106 (12): 3760-7. [Медлайн].
Мартино Р., Беллидо М., Брюне С., Суреда А., Пейрет М., Гуардия Р. и др. Аллогенная или аутологичная трансплантация стволовых клеток после химиотерапии для спасения взрослых с рефрактерным или рецидивирующим острым лимфобластным лейкозом. Пересадка костного мозга . 1998 Май. 21 (10): 1023-7. [Медлайн].
Weisdorf DJ, Billett AL, Hannan P, Ritz J, Sallan SE, Steinbuch M, et al.Сравнение аутологичной и неродственной донорской аллогенной трансплантации костного мозга при остром лимфобластном лейкозе. Кровь . 1997 15 октября. 90 (8): 2962-8. [Медлайн].
Mulcahy N. Исследование трансплантологии при раке крови, меняющее практику. Медицинские новости Medscape. 17 октября 2012 г. [Полный текст].
Anasetti C, Logan BR, Lee SJ, Waller EK, Weisdorf DJ, Wingard JR и др. Стволовые клетки периферической крови против костного мозга от неродственных доноров. N Engl J Med .2012 Октябрь 18, 367 (16): 1487-96. [Медлайн]. [Полный текст].
Джеха С., Гейнон П.С., Раззук Б.И., Франклин Дж., Кадота Р., Шен В. и др. Фаза II исследования клофарабина у педиатрических пациентов с рефрактерным или рецидивирующим острым лимфобластным лейкозом. Дж. Клин Онкол . 2006 20 апреля. 24 (12): 1917-23. [Медлайн]. [Полный текст].
Jeha S, Razzouk B, Rytting M, Rheingold S, Albano E, Kadota R и др. Фаза II исследования клофарабина у педиатрических пациентов с рефрактерным или рецидивирующим острым миелоидным лейкозом. Дж. Клин Онкол . 2009 10 сентября. 27 (26): 4392-7. [Медлайн]. [Полный текст].
Берг С.Л., Блейни С.М., Девидас М., Лампкин Т.А., Мурго А., Бернштейн М. и др. Фаза II исследования неларабина (соединение 506U78) у детей и молодых людей с рефрактерными Т-клеточными злокачественными новообразованиями: отчет Детской онкологической группы. Дж. Клин Онкол . 2005 20 мая. 23 (15): 3376-82. [Медлайн]. [Полный текст].
Marqibo (липосомальный винкристин) [вставка в упаковку].Южный Сан-Франциско, Калифорния: Talon Therapeutics, Inc., август 2012 г. Доступно на [Полный текст].
Topp MS, Gokbuget N, Zugmaier G, Klappers P, Stelljes M, Neumann S и др. Фаза II испытания блинатумомаба, биспецифического Т-клеточного активатора против CD19, демонстрирует гематологические и молекулярные ремиссии у пациентов с рецидивирующим или рефрактерным острым лимфобластным лейкозом, являющимся предшественником B. Дж. Клин Онкол . 2014 10 ноября [Medline].
Topp MS. Подтверждающее открытое, одноэтапное, многоцентровое исследование фазы 2 блинатумомаба антител к BiTE у пациентов (пациентов) с рецидивирующим / рефрактерным острым лимфобластным лейкозом B-предшественником (r / r ALL).Представлено на Ежегодном собрании ASCO 2014 г., 30 мая — 3 июня 2014 г .; Чикаго, Иллинойс. J Clin Oncol 32: 5s, 2014 (добавлено; резюме 7005). [Полный текст].
Kantarjian H, Stein A, Gökbuget N, Fielding AK, Schuh AC, et al. Блинатумомаб против химиотерапии при запущенном остром лимфобластном лейкозе. N Engl J Med . 2017 марта 2. 376 (9): 836-847. [Медлайн].
Goekbuget, N, Dombret, H, Bonifacio, M, et al. BLAST: подтверждающее, одноэтапное исследование фазы 2 блинатумомаба, конструкции антитела биспецифического активатора Т-клеток (BiTE®), у пациентов с острым лимфобластным лейкозом (ОЛЛ), предшественником B-предшественника минимальной остаточной болезни. Кровь . 2014. 124 (21): 379. [Полный текст].
Kantarjian HM, DeAngelo DJ, Stelljes M, et al. Инотузумаб Озогамицин в сравнении со стандартной терапией острого лимфобластного лейкоза. N Engl J Med . 2016. 375: 740-753. [Полный текст].
CAR Т-клетки: разработка иммунных клеток пациентов для лечения их рака. Национальный институт рака. Доступно по адресу https://www.cancer.gov/about-cancer/treatment/research/car-t-cells#option. 14 декабря 2017 г .; Дата обращения: 20 июня 2019 г.
Smith M, Goodman B. FDA одобрило первый в своем роде метод лечения рака. Медицинские новости Medscape. Доступно по адресу https://www.webmd.com/cancer/lymphoma/news/20170830/fda-approves-breakthrough-cancer-treatment. 30 августа 2017 г .; Дата обращения: 30 марта 2021 г.
Одобрение FDA дает первую генную терапию в Соединенных Штатах. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно на https://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm574058.htm. 30 августа 2017 г .; Дата обращения: 20 июня 2019 г.
Kymriah (tisagenlecleucel) [вкладыш в упаковке]. Восточный Ганновер, Нью-Джерси: Novartis Pharmaceuticals Corporation. Май 2018 г. Доступно по ссылке [Полный текст].
Geissler K, Koller E, Hubmann E, Niederwieser D, Hinterberger W, Geissler D, et al. Гранулоцитарный колониестимулирующий фактор в качестве дополнения к индукционной химиотерапии острого лимфобластного лейкоза у взрослых — рандомизированное исследование III фазы. Кровь . 1997 15 июля. 90 (2): 590-6. [Медлайн].
Ларсон Р.А., Додж Р.К., Линкер CA, Стоун Р.М., Пауэлл Б.Л., Ли Э.Дж. и др.Рандомизированное контролируемое исследование филграстима во время химиотерапии для индукции ремиссии и консолидации у взрослых с острым лимфобластным лейкозом: исследование CALGB 9111. Кровь . 1998 Сентябрь 1. 92 (5): 1556-64. [Медлайн].
Bassan R, Lerede T., Di Bona E, Rossi G, Pogliani E, Rambaldi A и др. Гранулоцитарный колониестимулирующий фактор (G-CSF, филграстим) после или во время интенсивной терапии для индукции ремиссии острого лимфобластного лейкоза у взрослых: эффекты, роль характеристик пациента до лечения и затраты. Лимфома лейк . 1997, 26 июня (1-2): 153-61. [Медлайн].
Ifrah N, Witz F, Jouet JP, François S, Lamy T., Linassier C, et al. Интенсивная краткосрочная терапия с поддержкой гранулоцитарно-макрофагально-колониестимулирующего фактора, аналогичная терапии острого миелобластного лейкоза, не улучшает общие результаты у взрослых с острым лимфобластным лейкозом. Группа ГОЭЛАМС. Рак . 1999 15 октября. 86 (8): 1496-505. [Медлайн].
Thomas X, Boiron JM, Huguet F, Reman O, Sutton L, Turlure P и др.Эффективность гранулоцитарных и гранулоцитарно-макрофагальных колониестимулирующих факторов в индукционной терапии острого лимфобластного лейкоза у взрослых: многоцентровое рандомизированное исследование. Гематол J . 2004. 5 (5): 384-94. [Медлайн].
Cortes J, Moore JO, Maziarz RT, Wetzler M, Craig M, Matous J, et al. Контроль мочевой кислоты в плазме у взрослых с риском синдрома лизиса опухоли: эффективность и безопасность только расбуриказы и расбуриказы с последующим применением аллопуринола по сравнению с одним аллопуринолом — результаты многоцентрового исследования III фазы. Дж. Клин Онкол . 2010 сен 20. 28 (27): 4207-13. [Медлайн].
Арбер Д.А., Боровиц М.Дж., Цессна М., Этцелль Дж., Фукар К., Хассерджян Р.П. и др. Первоначальное диагностическое исследование острого лейкоза: руководство Коллегии американских патологов и Американского общества гематологов. Arch Pathol Lab Med . 2017 22 февраля. [Medline]. [Полный текст].
[Рекомендации] Хельцер Д., Бассан Р., Домбрет Х., Филдинг А., Рибера Дж. М., Буск С. и др.Острый лимфобластный лейкоз у взрослых пациентов: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол . 2016 г. 7 апреля [Medline]. [Полный текст].
Олианский Д.М., Ларсон Р.А., Вайсдорф Д., Диллон Х., Ратко Т.А., Уолл Д. и др. Роль цитотоксической терапии с трансплантацией гемопоэтических стволовых клеток в лечении острого лимфобластного лейкоза у взрослых: обновление обзора, основанного на фактических данных, 2006 г. Пересадка костного мозга Biol .2012 18 января (1): 18-36.e6. [Медлайн].
Острый лимфобластный лейкоз (ВСЕ) (для родителей)
Что такое лейкемия?
Лейкоз — это рак, поражающий в основном белые кровяные тельца. Лейкоциты (также называемые лейкоцитами) борются с инфекциями.
Костный мозг — это губчатый материал внутри костей, который вырабатывает лейкоциты, эритроциты и тромбоциты. При лейкемии (loo-KEE-mee-uh) костный мозг вырабатывает белые кровяные тельца, которые не работают.Эти аномальные клетки не могут защитить организм от микробов. Они переполняют костный мозг, попадают в кровоток и могут распространяться на другие части тела, такие как лимфатические узлы, мозг или печень.
Лейкоз — это самый распространенный вид рака у детей. Он может быть острым (быстрорастущий) или хроническим (медленнорастущий). Большинство детей и подростков, лечившихся от лейкемии, излечились от болезни.
Что такое острый лимфобластный лейкоз?
Острый лимфобластный лейкоз (ОЛЛ) возникает, когда в организме вырабатывается слишком много белых кровяных телец, называемых лимфоцитами.Это наиболее распространенный тип лейкемии у детей. ОЛЛ также называют острым лимфолейкозом и острым лимфоидным лейкозом .
ALL может влиять на различные типы лимфоцитов, называемые B-клетками или T-клетками. Врачи маркировать типа основаны на которых пораженные клетки. Большинство детей с ОЛЛ имеют подтип В-клеток.
Острый лимфобластный лейкоз развивается и быстро ухудшается, поэтому важна ранняя диагностика. Большинство детей излечиваются с помощью лечения.
Каковы признаки и симптомы острого лимфобластного лейкоза?
Дети с ОЛЛ могут заболеть анемией, когда в организме слишком мало эритроцитов.Это происходит, когда костный мозг перестает вырабатывать обычное количество красных кровяных телец.
Дети с анемией могут:
- бледный
- Чувство сильной усталости или слабости
- одышка во время игры
Когда у них недостаточно тромбоцитов (PLATE-lits), дети с лейкемией могут легко получить синяки, кровотечение из носа или долгое кровотечение даже после небольшого пореза.
Другие симптомы лейкемии могут включать:
- Боль в костях или суставах, иногда вызывающая хромоту
- опухший лимфатические узлы (опухшие железы) на шее, паху или в другом месте
- Плохой аппетит и похудание
- лихорадка
- боль в животе
Поскольку их лейкоциты не могут бороться с инфекциями, дети с лейкемией более склонны к вирусным или бактериальным инфекциям.
Иногда лейкоз может распространяться или метастазировать (meh-TASS-tuh-size). Если он распространяется на мозг, симптомы могут включать головные боли, судороги, проблемы с равновесием или проблемы со зрением. Если он распространяется на лимфатические узлы в груди, симптомы могут включать проблемы с дыханием и боль в груди.
Что вызывает острый лимфобластный лейкоз?
Врачи точно не знают, что вызывает лейкемию. Но некоторые вещи могут повысить вероятность его получения детьми, например:
- имеет брата или сестру с лейкемией в анамнезе
- более ранняя лучевая терапия или химиотерапия для других видов рака
- прием лекарств для подавления иммунной системы после трансплантации органов
- генетические состояния, такие как:
- Синдром Ли-Фраумени
- Синдром Дауна
- нейрофиброматоз
- атаксия телеангиэктазия
- Анемия Фанкони
- с ненаследственным заболеванием, таким как синдром миелодисплазии (разновидность предлейкемии, которая препятствует нормальному росту клеток крови)
Как диагностируется острый лимфобластный лейкоз?
Врачи используют специальные тесты для проверки на лейкоз.К ним относятся:
- Анализы крови. Такие анализы, как общий анализ крови, функции печени и почек, а также биохимические анализы крови могут дать важную информацию о количестве нормальных клеток крови в организме и о том, насколько хорошо работают органы. Форму и размер клеток крови проверяют под микроскопом.
- Визуальные исследования. Это может быть рентген, компьютерная томография, МРТ или ультразвук. Врачи используют их, чтобы исключить другие причины симптомов или искать массу лейкозных клеток в груди, которые могут повлиять на дыхание или кровообращение.
- Аспирация и биопсия костного мозга. Для этой процедуры ребенку дают лекарство, чтобы он уснул и почувствовал себя комфортно. Затем врач вводит иглу в большую кость, обычно в бедро, и удаляет небольшое количество костного мозга. Лаборатория проводит следующие тесты на образце костного мозга:
- Тесты проточной цитометрии. Врачи внимательно изучают раковые клетки и определяют тип и подтип лейкемии. Это важно, потому что лечение зависит от разных типов лейкемии.
- Генетические тесты. Тщательно исследуя кровь или костный мозг, врачи проверяют наличие изменений в генах. Это может помочь врачам подобрать наилучшее лечение.
- Типирование тканей или HLA (человеческий лейкоцитарный антиген) типирование. Если ребенку нужна трансплантация стволовых клеток (иногда называемая трансплантацией костного мозга), этот тест помогает найти подходящего донора стволовых клеток. Он сравнивает белки на поверхности клеток крови ребенка с белками на клетках потенциального донора.Чем больше маркеров HLA используется у ребенка и донора, тем больше шансов, что трансплантация пройдет успешно.
- Спинальная пункция (люмбальная пункция). Врач использует полую иглу для удаления небольшого количества спинномозговой жидкости (жидкости, окружающей головной и спинной мозг). Жидкость проверяется на наличие раковых клеток. Это помогает врачам спланировать лечение.
Как лечится острый лимфобластный лейкоз?
Химиотерапия
Большинство детей с ОЛЛ будут проходить химиотерапию.Это специальные препараты, убивающие раковые клетки. Какие лекарства и в какой комбинации получает ребенок, зависит от подтипа ОЛЛ и от того, насколько быстро развивается болезнь. То, как раковые клетки реагируют на первое лечение, помогает врачам решить, как выбрать следующий тип химиотерапии.
Могут быть предоставлены различные виды химиотерапии:
- в вену (IV)
- в виде инъекции в мышцу
- внутрь в форме таблеток
- спинальной пункцией прямо в спинномозговую жидкость
Целью лечения является ремиссия, то есть когда анализы не обнаруживают раковых клеток в организме.Затем поддерживающая химиотерапия поддерживает ремиссию ребенка и предотвращает рецидив рака. Дети получают поддерживающую химиотерапию от 2 до 3 лет.
Трансплантаты стволовых клеток
Некоторым детям с быстрорастущим типом ОЛЛ может потребоваться пересадка стволовых клеток (иногда называемая трансплантацией костного мозга). В этом обращении участвуют:
- уничтожение раковых клеток, нормального костного мозга и клеток иммунной системы с помощью высокодозной химиотерапии и / или облучения
- Возвращение здоровых донорских стволовых клеток в организм
- восстановление здорового кровоснабжения и иммунной системы с помощью новых стволовых клеток
Другие процедуры могут включать:
- лучевая терапия: высокоэнергетические рентгеновские лучи, убивающие раковые клетки
- таргетная терапия: специальные препараты, которые находят и атакуют раковые клетки, не повреждая нормальные клетки
- иммунотерапия: лекарство, использующее собственную иммунную систему ребенка для избавления от раковых клеток
Клинические испытания
Клинические испытания — это исследования, которые предлагают новые многообещающие методы лечения, еще не доступные широкой публике.Доктора решат, подходит ли ребенок для клинического исследования.
Что еще мне нужно знать?
Лечение ребенка от рака может показаться сложной задачей для любой семьи. Но вы не одиноки. Чтобы найти поддержку, поговорите с кем-нибудь из группы по уходу за вашим ребенком или социальным работником больницы. Доступно множество ресурсов, которые помогут вам пережить это трудное время.
Вы также можете найти информацию и поддержку в Интернете по адресу:
Острый лимфолейкоз (ВСЕ) | Больницы и клиники Университета Айовы
Что такое острый лимфолейкоз (ОЛЛ)?
Острый лимфоцитарный лейкоз, также называемый острым лимфобластным лейкозом, — это тип рака, при котором в костном мозге слишком много лимфоцитов — ранней фазы белых кровяных телец.Лейкоз отличается от других видов рака тем, что он начинается в крови и костном мозге и может распространяться на другие части тела. Другие виды рака могут в конечном итоге распространиться на костный мозг, но они не перерастают в лейкоз.
Рак, который считается острым , может быстро прогрессировать и, если его не лечить, привести к летальному исходу всего за несколько месяцев. Острый лейкоз отличается от хронического лейкоза тем, что при остром лейкозе клетки костного мозга не созревают должным образом.Незрелые лейкозные клетки продолжают размножаться и накапливаться. При хроническом лейкозе клетки созревают частично, но не полностью, и они не борются с инфекцией так же хорошо, как нормальные белые кровяные тельца. Хронические лейкозы имеют тенденцию прогрессировать со временем, и большинство людей могут жить несколько лет, хотя эти виды лейкозов труднее лечить.
Каковы симптомы ВСЕГО?
Как и в случае с другими типами лейкемии, есть несколько симптомов, которые могут привести к диагностике ОЛЛ, но многие из этих признаков и симптомов также указывают на многие другие заболевания.Чаще всего ВСЕ обнаруживается, когда ваш врач проверяет вашу кровь по другой причине и видит нехватку нормальных клеток крови.
Эта нехватка может вызвать следующие симптомы:
- Усталость
- Чувство слабости или упадок сил
- Головокружение или дурноту
- Одышка
- Лихорадка
- Невозможность избавиться от инфекции
- Легко ушибается
- Кровотечение, такое как кровоточивость десен и сильное носовое кровотечение
Другие симптомы, которые могут испытывать ВСЕ пациенты, включают:
- Потеря веса
- Лихорадка
- Ночные поты
- Потеря аппетита
Клетки лейкемии также могут вызывать увеличение селезенки, что можно определить по вздутию живота; увеличенные лимфатические узлы; и боль в костях или суставах.Клетки иногда — хотя и не часто — распространяются на другие органы и могут вызывать там больше симптомов: головные боли, судороги и рвоту, если лейкоз распространился на головной или спинной мозг, или затрудненное дыхание, если оно распространилось на грудную полость, т. пример.
Как лечится ВСЕ?
Поскольку ОЛЛ не является отдельным заболеванием — это фактически группа связанных заболеваний, пациенты с разными подтипами ОЛЛ будут получать разные методы лечения и реакции на это лечение.
После того, как вам поставят диагноз, вы и ваша группа по уходу встретитесь, чтобы решить, какой вариант лечения лучше всего подходит для вас. Основные варианты лечения:
- Химиотерапия
- Таргетная терапия — ежедневное лечение, обычно принимаемое в виде таблеток.
- Пересадка стволовых клеток
Другие возможные формы лечения включают хирургическое вмешательство, лучевую терапию или использование моноклональных (искусственных) антител.
Лечение ВСЕХ обычно длится два года. Это может быть интенсивное лечение, поэтому хорошо находиться в центре с признанным опытом лечения этого заболевания.
Как диагностируется ВСЕ?
Многие люди с ОЛЛ не имеют никаких симптомов на момент постановки диагноза — обычно это обнаруживается, когда врач назначает анализы крови для чего-то совершенно не связанного с этим или во время обычного осмотра.
Некоторые люди могут быть подвержены более высокому риску ОЛЛ из-за определенных заболеваний крови, таких как миелодиспластический синдром, или наследственных заболеваний, таких как синдром Дауна, или из-за того, что они лечились определенными химиотерапевтическими препаратами или лучевой терапией. Врачи обычно рекомендуют этим людям проходить регулярные осмотры.
Если у вас есть признаки или симптомы ОЛЛ, или если физическое обследование показало, что у вас лейкемия, врач должен будет взять образцы вашей крови и костного мозга для проверки. Кровь в большинстве случаев берется из вены руки, но костный мозг извлекается двумя способами: путем аспирации и биопсии.
Костная аспирация и биопсия
Аспирация костного мозга и биопсия выполняются одновременно. Образцы обычно берутся из задней части тазовой кости (бедра) или иногда из грудины (грудины).Эти образцы отправляются в лабораторию, где они исследуются на лейкозные клетки.
Люмбальная пункция
ALL может иногда передаваться в головной и спинной мозг, и по этой причине вашему врачу может потребоваться взять образец спинномозговой жидкости для анализа. Жидкость будет извлечена с помощью люмбальной пункции, также известной как спинномозговая пункция. Этот тест используется только для пациентов, симптомы которых могут быть вызваны лейкемией, распространяющейся на головной и спинной мозг.
Анализы крови
Существует несколько лабораторных тестов, которые можно использовать, чтобы определить, есть ли у вас ОЛЛ и насколько далеко может быть заболевание.
Общий анализ крови и мазок периферической крови
Полный анализ крови (CBC) измеряет уровни различных клеток в крови: эритроцитов, лейкоцитов и тромбоцитов. Часть крови помещается на предметное стекло и исследуется под микроскопом: у большинства пациентов с ОМЛ слишком много незрелых лейкоцитов и недостаточно эритроцитов или тромбоцитов.
Биохимический анализ крови и тесты на коагуляцию
Эти тесты измеряют количество определенных химических веществ в крови, а также способность крови к свертыванию.Эти тесты не используются для диагностики лейкемии, но могут обнаруживать другие проблемы.
Тестирование хромосом
Обычно клетки человека содержат 23 пары хромосом или пучки ДНК. Однако у людей с лейкемией в клетках могут быть некоторые хромосомные изменения — иногда бывает делеция или отсутствует часть хромосомы.
Что чаще всего происходит при ОЛЛ, так это то, что две хромосомы «разделяют» часть своей ДНК — одна хромосома присоединяется к части другой хромосомы.Это называется транслокацией.
Информация об этих и других изменениях может помочь вашему врачу определить ваш прогноз и реакцию на лечение.
Визуальные тесты
Визуализирующие обследования, такие как рентген, компьютерная томография (КТ), магнитно-резонансная томография (МРТ) и ультразвук, могут использоваться, чтобы помочь врачам увидеть подробные изображения внутри вашего тела.
Каков прогноз для ВСЕХ?
Для многих людей с ОЛЛ лечение может избавить от рака, но даже после того, как вы закончили лечение, ваши врачи захотят наблюдать за вами.Важно придерживаться регулярного графика последующих посещений, как для ответа на любые вопросы, которые могут у вас возникнуть, так и для отслеживания любых побочных эффектов лечения.
ВСЕ факторы риска
Что вызывает ВСЕ?
При многих видах рака существуют факторы риска, которые можно контролировать, чтобы увеличить или уменьшить свои шансы заболеть. Фактор риска — это то, что влияет на ваши шансы заболеть, но не обязательно означает, что вы заразитесь этим заболеванием.
Есть лишь несколько известных факторов риска для ВСЕХ:
- Воздействие высоких уровней радиации
- Воздействие определенных химических веществ, таких как бензол и некоторые химиотерапевтические препараты
- Определенные вирусные инфекции, такие как:
- Вирус-1 Т-клеточной лимфомы / лейкемии (HTLV-1) в Японии и странах Карибского бассейна
- Вирус Эпштейна-Барра в Африке
- Унаследованные синдромы, такие как:
- Синдром Дауна
- Синдром Клайнфельтера
- Анемия Фанкони
- Синдром Блума
- Атаксия-телеангиэктазия
- Нейрофиброматоз
- Гонка
- ВСЕ чаще встречается у кавказцев, чем у афроамериканцев
- Пол
- ОЛЛ немного чаще встречается у мужчин, чем у женщин
Должен ли я пройти проверку на ВСЕ?
К сожалению, обычно не существует скрининговых тестов для выявления ОЛЛ на ранних стадиях.Однако ОЛЛ иногда обнаруживается, когда определенные симптомы обнаруживаются в обычных анализах крови, проводимых по другим причинам. Например, нормальное количество клеток крови человека может быть очень низким, даже если нет других симптомов. Это может привести к другим тестам, в которых можно будет найти ВСЕ.
Острый лейкоз — Knowledge @ AMBOSS
Последнее обновление: 2 августа 2021 г.
Резюме
Острые лейкозы — это злокачественные опухолевые заболевания, которые возникают в лимфоидной или миелоидной клеточной линии.Острый лимфолейкоз (ОЛЛ) является наиболее распространенным злокачественным новообразованием у детей, тогда как острый миелоидный лейкоз (ОМЛ) в первую очередь поражает взрослых. Основная причина острого лейкоза редко выявляется, но факторы риска включают предшествующую химиотерапию и лучевую терапию, а также наследственные синдромы, такие как синдром Дауна. ОМЛ также связан с ранее существовавшими гематологическими нарушениями (например, миелодиспластическим заболеванием, миелопролиферативными расстройствами). Острые лейкозы характеризуются разрастанием незрелых нефункциональных лейкоцитов (бластов) в костном мозге, что нарушает нормальный гемопоэз.Это приводит к панцитопении, которая проявляется симптомами и признаками анемии (снижение количества эритроцитов), нарушений свертывания крови (снижение количества тромбоцитов) и иммунодефицита (снижение полностью функциональных зрелых лейкоцитов). У пациентов с острым лейкозом, особенно с ОМЛ, может развиться чрезвычайно высокое количество лейкоцитов, что увеличивает риск лейкостаза и диссеминированного внутрисосудистого свертывания (ДВС). Лейкозные клетки также могут проникать в экстрамедуллярные органы, что приводит к гепатоспленомегалии, почечной недостаточности, менингеальному лейкозу и, реже, поражению кожи и / или яичек.Первые диагностические шаги включают общий анализ крови и мазок периферической крови для определения количества лейкоцитов у пациента и оценки наличия бластов. Аспирация костного мозга и биопсия обычно используются для подтверждения диагноза, а последующий цитогенетический анализ и иммунофенотипирование используются для выявления подтипов и специфических мутаций. Режим химиотерапии, состоящий из циклов высоких доз (индукция) и низких доз (консолидация и поддерживающая терапия), является основой лечения. Дополнительные меры, такие как трансплантация аллогенных стволовых клеток, могут быть показаны пациентам с плохими прогностическими факторами (например,g., неблагоприятная цитогенетика) или при неудачной начальной химиотерапии.
Эпидемиология
Эпидемиологические данные относятся к США, если не указано иное.
Этиология
- В большинстве случаев причина или факторы риска отсутствуют
- Ранее существовавшее нарушение кроветворения (наиболее частая идентифицируемая причина) [8]
- Факторы окружающей среды [2]
- Генетические или хромосомные факторы
Ссылки: [9] [10]
Классификация
- Франко-американо-британская (FAB) историческая классификация ВСЕХ
- L1 ALL с маленькими ячейками (20–30%)
- L2 ALL с гетерогенными большими ячейками (70%)
- L3 ALL с большими ячейками, т.е.е., лимфома Беркитта (1-2%)
- Текущая Классификация ВОЗ (2016 г.) классифицирует ОЛЛ на подтипы предшественников лимфобластной лейкемии / лимфомы на основе морфологических и генетических факторов:
- Классификация иммунофенотипа ОЛЛ: на основе происхождения (В-клетки или Т-клетки) и зрелости лейкозных клеток
- B-клеточный ОЛЛ (∼ 80–85% случаев) [11]
- Т-лимфоциты ALL (∼ 15–20% случаев)
- Французско-американо-британская классификация (FAB) различает восемь подтипов AML в соответствии с гистопатологическим внешним видом клеток.
- Классификация ВОЗ основана на различных факторах (например, наличии генетических аномалий или ассоциаций с предшествующей химиотерапией / лучевой терапией).
Каталожные номера: [8] [12]
Патофизиология
Ссылки: [8] [13] [14]
Клинические признаки
Клинические признаки связаны либо с недостаточностью костного мозга, инфильтрацией органов лейкемическими клетками, либо с сочетанием того и другого.
| Общие признаки острого лейкоза | |||||||||
|---|---|---|---|---|---|---|---|---|---|
| Клинические особенности ВСЕХ | Клинические особенности ОМЛ | ||||||||
| Общие агенты, используемые в схемах химиотерапии при остром лейкозе [18] [20] [25] [32] [33] | |
|---|---|
| ВСЕ |
|
| AML | |
| APL | |
Схема химиотерапии, обычно используемая для лечения ОЛЛ, — это гипер-CVAD: циклофосфамид, винкристин, даунорубицин (или адриамицин) и дексаметазон.
Если есть подозрение на APL, рано начните лечение дифференцирующим агентом (например, ATRA), не дожидаясь иммунотипа или генетического подтверждения. Лечение может быть скорректировано позже в зависимости от результатов. [25]
В APL транслокация t (15; 17) и последующее образование гибридного гена PML-RARA могут ингибировать дифференцировку миелобластов при физиологических уровнях ретиноевой кислоты. Высокие дозы ATRA (производного витамина А) могут вызывать дифференцировку миелобластов и способствовать ремиссии.
Лечение инфильтрации ЦНС
[32] [33] [34]Интратекальную профилактику следует начинать на ранней стадии, поскольку профилактика лейкемии ЦНС обычно эффективна. Пациенты с инфильтрацией ЦНС подвержены более высокому риску рецидива, чем пациенты без инфильтрации ЦНС.
Расширенные методы лечения
[25] [31]Лечение осложнений
[25]Осложнения
Мы перечисляем наиболее важные осложнения.Выбор не исчерпывающий.
Прогноз
5-летняя выживаемость после лечения
- ALL: 5-летняя выживаемость обычно выше по сравнению с AML (варьируется от ~ 20% у пожилых пациентов до ~ 80% у детей и подростков)
- ОМЛ: ~ 30%, но зависит от возраста пациента. В последнее время время выживания увеличилось благодаря улучшениям в лечении.
Неблагоприятные прогностические факторы
Благоприятные прогностические факторы
Чтобы помнить, что транслокация t (12; 21) обычно проявляется при детском B-ОЛЛ и обычно имеет благоприятный исход, подумайте: «Дети возвращаются к здоровью!» (число 12 — 21 перевернутое).
Каталожные номера: [41] [42] [43] [44] [45] [46]
.
