Аденоз » Рак Молочной Железы
Аденоз — доброкачественное (незлокачественное) заболевание груди, форма фиброзно-кистозной мастопатии, сопровождающаяся разрастанием железистой ткани молочной железы. Симптоматика аденоза схожа с симптоматикой мастопатии- вы можете ощущать нагрубание молочных желёз, чувствительность и болезненность. Аденоз нередко обнаруживается у женщин с фиброзом или кистами в молочных железах. Аденоз не является раком молочной железы и чаще встречается у женщин в возрасте 30-45 лет, у беременных в первом триместре и у девушек в период полового созревания и становления менструального цикла.
Склерозирующий аденоз
Склерозирующий аденоз — это тип аденоза, при котором происходит поражение долек молочной железы с быстрым разрастанием тканей фиброза, которые перемежаются с железистыми клетками. При склерозирующем аденозе проявляются мелкие уплотнения (узелки) небольшого размера, подвижные и плотные.
Диагностика
Для диагностики аденоза необходимо посетить маммолога, сделать УЗИ молочных желёз и маммографию.
При аденозе, склерозирующем аденозе и раке молочной железы могут формироваться кальцинаты молочных желёз – они формируются в одной либо обеих молочных железах и выявляются при плановой маммографии. В случае их выявления также необходимо проведение биопсии для подтверждения, вызвано ли изменение груди аденозом либо раком.
Лечение
В связи с повышением риска развития рака молочной железы, обычно рекомендуется лечение аденоза путем хирургического удаления образования. После удаления образования прогноз и риск развития злокачественных образований (чаще — карциномы) минимален. Тем не менее, если у вас был аденоз, прохождение более частных и плановых проверок молочных желез может быть полезным.
Риск развития рака молочной железы
Аденоз является индикатором увеличения риска последующего развития рака молочной железы. Объем риска зависит от индивидуальных факторов, размера образования и его типа.
Объем риска зависит от индивидуальных факторов, размера образования и его типа.
ФИБРОСКЛЕРОЗ И СКЛЕРОЗИРУЮЩИЙ АДЕНОЗ С МИКРОКАЛЬЦИНАТАМИ В МОЛОЧНОЙ ЖЕЛЕЗЕ. МОЛЕКУЛЯРНЫЙ ПАТОГЕНЕЗ, СВОЕВРЕМЕННАЯ ДИАГНОСТИКА И ЛЕЧЕНИЕ | Муйжнек
1. Рассказова Е. А., Рожкова Н. И. Скрининг для ранней диагностики рака молочной железы. Исследования и практика в медицине. 2014;1 (1):45—51. DOI: https://doi. org/10.17709/2409-2231-2014-1-1-45-51
2. Рожкова Н. И. Лучевая диагностика в маммологии. Руководство для врачей. М.: СИМК; 2014, 128 с.
4. Мазо М. Л., Рожкова Н. И., Прокопенко С. П., Бурдина И. И., Запирова С. Б., Якобс О. Э. Инвазивная лучевая диагностика рака молочной железы. Тонкоигольная биопсия или трепан-биопсия? Медицинская визуализация. 2015;4:79-86.
Л., Рожкова Н. И., Прокопенко С. П., Бурдина И. И., Запирова С. Б., Якобс О. Э. Инвазивная лучевая диагностика рака молочной железы. Тонкоигольная биопсия или трепан-биопсия? Медицинская визуализация. 2015;4:79-86.
5. Злокачественные новообразования в России в 2017 году (заболеваемость и смертность). Под ред. А. Д. Каприна, В. В. Старинского, Г. В. Петровой. М., 2018.263 с. Доступно по: http://www. oncology.ru/service/statistics/malignant_tumors/2017.pdf
6. Доброкачественные заболевания молочной железы. Этиопатогенез, диагностика, лечение, профилактика. Под ред. A. Д. Каприна, Н. И. Рожковой. М.: ГЭОТАР-Медиа; 2017, 283 с.
7. Рожкова Н. И., Подзолкова Н. М., Овсянникова Т. В. Молочная железа и пролактин: новые данные. StatusPraesens. 2016;4 (33):48-55.
8. Hartmann LC, Sellers TA, Frost MH, Lingle WL, Degnim AC, Ghosh K, et al. Benign breast disease and the risk of breast cancer. N Engl J Med. 2005 Jul 21;353 (3):229-37. DOI: 10.1056/NEJ- Moa044383
9. Dupont WD, Parl FF, Hartmann WH, Brinton LA, Winfield AC, Worrell JA, et al. Breast cancer risk associated with proliferative breast disease and atypical hyperplasia. Cancer. 1993 Feb 15;71 (4):1258-65.
10. Kabat GC, Jones JG, Olson N, Negassa A, Duggan C, Ginsberg MS, et al. A multi-center prospective cohort study of benign breast disease and risk of subsequent breast cancer. Cancer Causes Control. 2010 Jun;21 (6):821-8. DOI: 10.1007/s10552-010-9508-7
11. Pearlman MD, GriffinJL. Benign breast disease. ObstetGynecol. 2010 Sep;116 (3):747-58. DOI: 10.1097/A0G.0b013e3181ee9fc7.
Benign breast disease. ObstetGynecol. 2010 Sep;116 (3):747-58. DOI: 10.1097/A0G.0b013e3181ee9fc7.
12. Cote ML, Ruterbusch JJ, Alosh B, Bandyopadhyay S, Kim E, Albashiti B, et al. Benign breast disease and the risk of subse-quent breast cancer in African American women. Cancer Prev Res (Phila). 2012 Dec;5 (12):1375-80. DOI: 10.1158/1940-6207. CAPR-12-0175
13. Visscher DW, Nassar A, Degnim AC, Frost MH, Vierkant RA, Frank RD, et al. Sclerosing adenosis and risk of breast cancer. Breast Cancer Res Treat. 2014 Feb;144 (1):205-12. DOI: 10.1007/s10549-014-2862-5.
14. Castells X, Domingo L, Corominas JM, Tora-Rocamora I, Quintana MJ, Baré M, et al. Breast cancer risk after diagnosis by screening mammography of nonproliferative or proliferative benign breast disease: a study from a population-based screening program. Breast Cancer Res Treat. 2015 Jan;149 (1):237-44. DOI: 10.1007/s10549-014-3208-z
Breast Cancer Res Treat. 2015 Jan;149 (1):237-44. DOI: 10.1007/s10549-014-3208-z
15. Vorherr H. Fibrocystic breast disease: Pathophysiology, pathomorphology, clinical picture, and management. Am J Obstet Gynecol. 1986 Jan;154 (1):161-79.
16. Практическая маммология. Под ред. М. И. Давыдова, B. П. Летягина. М.: Практическая медицина; 2007, 272 c.
17. Bland KI, Kuhns JG, Buchanan JB, Dwyer P, Heuser L, O’Connor C, et al. Aclinicopathologic correlation of mammographic parenchymal patterns and associated risk factors for human mammary carcinoma. Ann Surg. 1982 May;195 (5):582-94. DOI: 10.1097/00000658-198205000-00007
18. Lisanti MP, Tsirigos A, Pavlides S, Reeves KJ, Peiris-Pagès M, Chadwick AL, et al.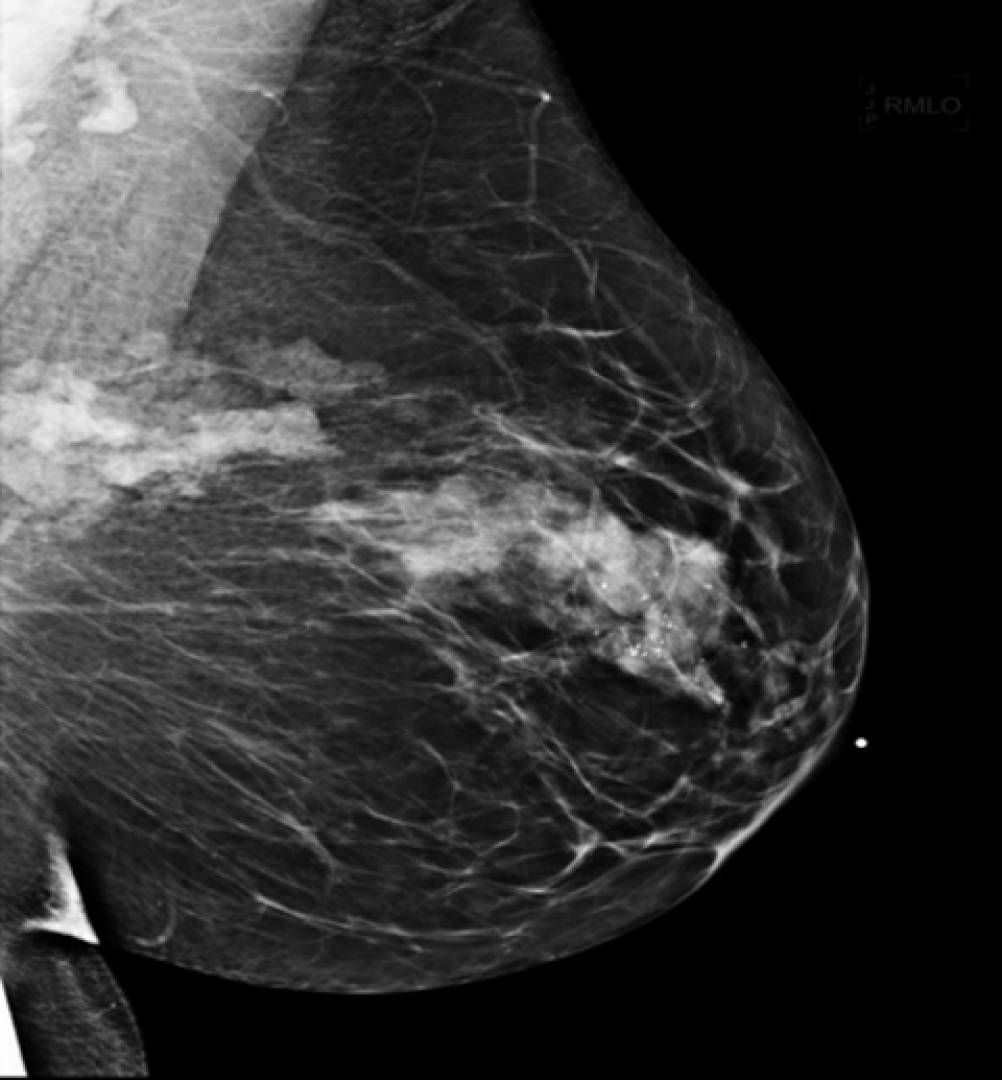 JNK1 stress signaling is hyper-activated in high breast density and the tumor stroma: œnnecting fibrosis, inflammation, and stemness for cancer prevention. Cell Cycle. 2014;13 (4):580-99. DOI: 10.4161/cc.27379.
JNK1 stress signaling is hyper-activated in high breast density and the tumor stroma: œnnecting fibrosis, inflammation, and stemness for cancer prevention. Cell Cycle. 2014;13 (4):580-99. DOI: 10.4161/cc.27379.
19. Salarieh A, Sneige N. Breast carcinoma arising in microglan-dular adenosis: a review of the literature. Arch Pathol Lab Med. 2007 Sep;131 (9):1397-9. DOI: 10.1043/1543-2165 (2007)131 [1397: BCAIMA]2.0.CO;2
20. Koenig C, Dadmanesh F, Bratthauer GL, Tavassoli FA. Carcinoma arising in microglandular adenosis: an immunohistochemical analysis of 20 intraepithelial and invasive neoplasms. Int J Surg Pathol. 2000 0ct;8 (4):303-315. DOI: 10.1177/106689690000800409
21. Khalifeh IM, Albarracin C, Diaz LK, Symmans F, Edgerton M, Hwang R, et al. Clinical, histopathologic, and immunohistochemical features of microglandular adenosis and transition into in situ and invasive carcinoma.
22. Geyer FC, Kushner YB, Lambros MB, Natrajan R, Mackay A, Tamber N, et al. Microglandular adenosis or microglandular ad-enoma? A molecular genetic analysis of a case associated with atypia and invasive carcinoma. Histopathology. 2009 Dec;55 (6):732-43. DOI: 10.1111/j.1365-2559.2009.03432.x.
23. Tavassoli FA, Norris HJ. Microglandular adenosis of the breast. A clinicopathologic study of 11 cases with ultrastructural observations. Am J Surg Pathol. 1983 Dec;7 (8):731-7.
24. Rosenblum MK, Purrazzella R, Rosen PP. Is microglandular adenosis a precancerous disease? A study of carcinoma arising therein. Am J Surg Pathol. 1986 Apr;10 (4):237-45.
25. Acs G, Simpson JF, Bleiweiss IJ, Hugh J, Reynolds C, Olson S, et al. Microglandlar adenosis with transition into adenoid cystic carcinoma of the breast. Am J Surg Pathol. 2003 Aug;27 (8):1052-60.
Acs G, Simpson JF, Bleiweiss IJ, Hugh J, Reynolds C, Olson S, et al. Microglandlar adenosis with transition into adenoid cystic carcinoma of the breast. Am J Surg Pathol. 2003 Aug;27 (8):1052-60.
26. Kay S. Microglandular adenosis of the female mammary gland: study of a case with ultrastructural observations. Hum Pathol. 1985 Jun;16 (6):637-41.
27. Rosen PP. Microglandular adenosis. A benign lesion simulat-ing invasive mammary carcinoma. Am J Surg Pathol. 1983 Mar;7 (2) :137-44.
28. Geyer FC, Lacroix-Triki M, Colombo PE, Patani N, Gauthier A, Natrajan R, et al. Molecular evidence in support of the neoplastic and precursor nature of microglandular adenosis. Histopathology. 2012 May;60 (6B): E115-30. DOI: 10.1111/j.1365- 2559.2012.04207.x.
29. Shin SJ, Simpson PT, Da Silva L, Jayanthan J, Reid L, Lakhani SR, et al. Molecular evidence for progression of microglandular adenosis (MGA) to invasive carcinoma. Am J Surg Pathol. 2009 Apr;33 (4):496-504. DOI: 10.1097/PAS.0b013e31818af361
Shin SJ, Simpson PT, Da Silva L, Jayanthan J, Reid L, Lakhani SR, et al. Molecular evidence for progression of microglandular adenosis (MGA) to invasive carcinoma. Am J Surg Pathol. 2009 Apr;33 (4):496-504. DOI: 10.1097/PAS.0b013e31818af361
30. Santen RJ, Mansel R. Benign breast disorders. N Engl J Med. 2005 Jul 21;353 (3):275-85.
31. Каприн А. Д., Рожкова Н. И. Маммология. Национальное руководство. 2-е изд. M.: ГЭОТАР-Медиа; 2016, 496 с.
32. Cichon MA, Degnim AC, Visscher DW, Radisky DC. Microenvironmental influences that drive progression from benign breast disease to invasive breast cancer. J Mammary Gland Biol Neoplasia. 2010 Dec;15 (4):389-97. DOI: 10.1007/s10911-010-9195-8.
33. Polyak K, Hu M. Do myoepithelial cells hold the key for breast tumor progression? J Mammary Gland Biol Neoplasia. 2005 Jul;10 (3) :231—47. DOI: 10.1007/s10911-005-9584-6
Polyak K, Hu M. Do myoepithelial cells hold the key for breast tumor progression? J Mammary Gland Biol Neoplasia. 2005 Jul;10 (3) :231—47. DOI: 10.1007/s10911-005-9584-6
34. Allinen M, Beroukhim R, Cai L, Brennan C, Lahti-Domenici J, Huang H, et al. Molecular characterization of the tumor micro-environment in breast cancer. Cancer Cell. 2004 Jul;6 (1):17-32. DOI: 10.1016/j.ccr.2004.06.010
35. Hilson JB, Schnitt SJ, Collins LC. Phenotypic alterations in ductal carcinoma in situ-associated myoepithelial cells: biologic and diagnostic implications. Am J Surg Pathol. 2009 Feb;33 (2):227-32. DOI: 10.1097/PAS.0b013e318180431d
36. Kalluri R, Zeisberg M. Fibroblasts in cancer. Nat Rev Cancer. 2006 May;6 (5):392-401. DOI: 10.1038/nrc1877
37. Hu M, Peluffo G, Chen H, Gelman R, Schnitt S, Polyak K. Role of COX-2 in epithelial-stromal cell interactions and progression of ductal carcinoma in situ of the breast. Proc Natl Acad Sci U S A. 2009 Mar 3;106 (9):3372-7. DOI: 10.1073/pnas.0813306106
Hu M, Peluffo G, Chen H, Gelman R, Schnitt S, Polyak K. Role of COX-2 in epithelial-stromal cell interactions and progression of ductal carcinoma in situ of the breast. Proc Natl Acad Sci U S A. 2009 Mar 3;106 (9):3372-7. DOI: 10.1073/pnas.0813306106
38. Visscher DW, Pankratz VS, Santisteban M, Reynolds C, Risti- maki A, Vierkant RA, et al. Association between cyclooxygenase-2 expression in atypical hyperplasia and risk of breast cancer. J Natl Cancer Inst. 2008 Mar 19;100 (6):421-7. DOI: 10.1093/jnci/djn036
39. Santisteban M, Reynolds C, Barr Fritcher EG, Frost MH, Vier-kant RA, Anderson SS, et al. Ki67: a time-varying biomarker of risk of breast cancer in atypical hyperplasia. Breast Cancer Res Treat. 2010 Jun;121 (2):431—7. DOI: 10.1007/s10549-009-0534-7
40. Kalluri R, Weinberg RA. The basics of epithelial-mesenchy-mal transition. J Clin Invest. 2009 Jun;119 (6):1420-8. DOI: 10.1172/JCI39104.
Kalluri R, Weinberg RA. The basics of epithelial-mesenchy-mal transition. J Clin Invest. 2009 Jun;119 (6):1420-8. DOI: 10.1172/JCI39104.
41. Scimeca M, Giannini E, Antonacci C, Pistolese CA, Spag- noli LG, Bonanno E. Microcalcifi ca ons in breast cancer: an ac ve phenomenon mediated by epithelial cells with mesenchymal characteris cs. BMC Cancer. 2014 Apr 23;14:286. DOI: 10.1186/1471–2407–14–286.
42. Горшков В. А., Рожкова Н. И., Прокопенко С. П. Аналитическая идентификация единичных микрокальцинатов на основе распределения атомного номера. Медицинская техника. 2017;3 (303):39–42.
43. Якобс О. Э., Рожкова Н. И., Каприн А. Д. Возможности соноэластографии в дифференциальной диагностике заболеваний молочной железы, сопровождающихся скоплением микрокальцинатов.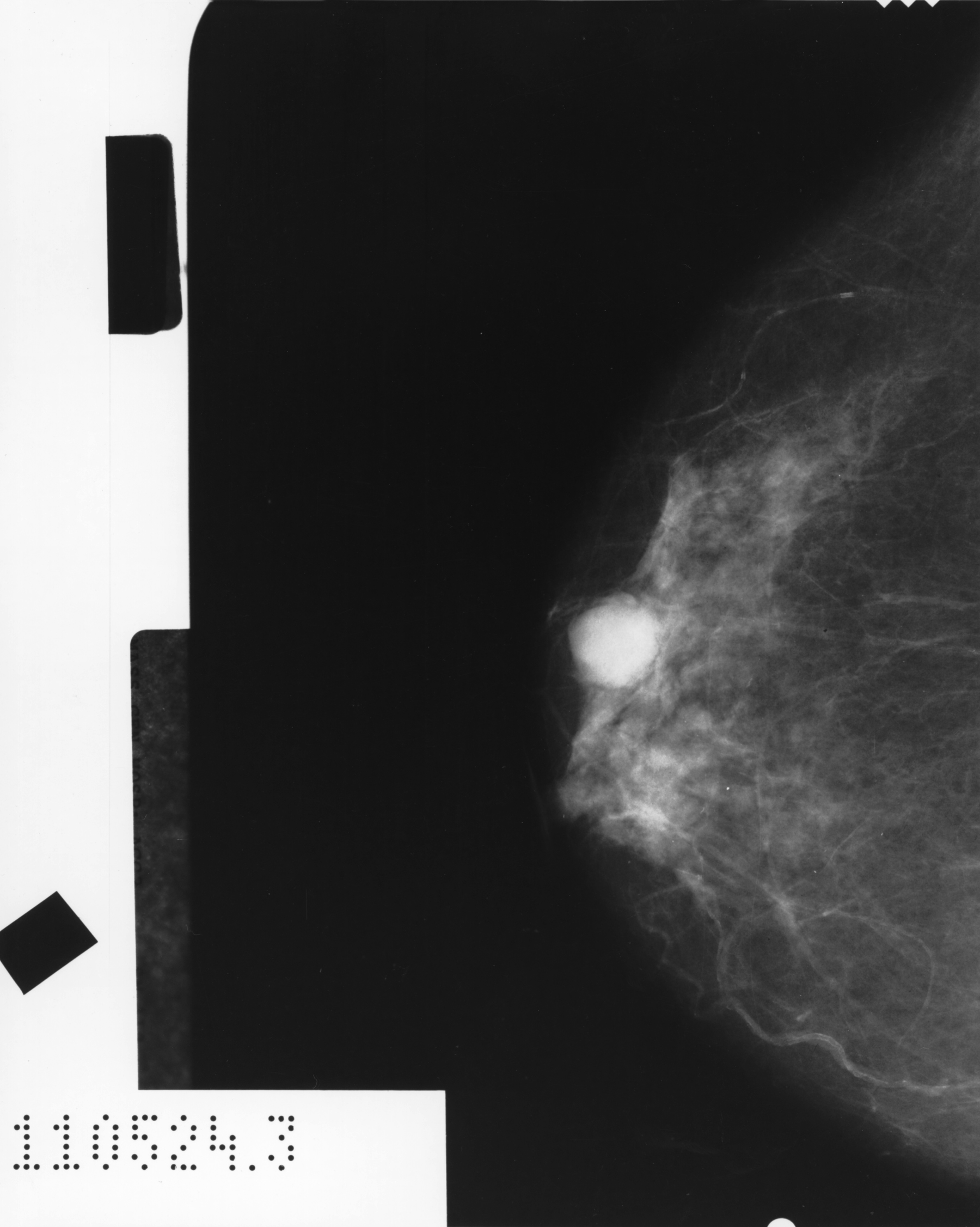 Акушерство и гинекология: Новости. Мнения. Обучение. 2017;1 (15):69–75.
Акушерство и гинекология: Новости. Мнения. Обучение. 2017;1 (15):69–75.
44. Якобс О. Э., Кудинова Е. А., Рожкова Н. И., Боженко В. К. Радиологические технологии и биогенетические маркеры в дифференциальной диагностике заболеваний молочной железы, сопровождающихся скоплениями микрокальцинатов. Вестник РНЦРР. 2017;17 (1):6.
45. Ferranti C, Coopmans de Yoldi G, Biganzoli E, Bergonzi S, Mariani L, Scaperrotia G, et al. Relationships between age, mammographic features and pathological tumour characteristics in non-palpable breast cancer. Br J Radiol. 2000 Jul;73 (871):698– 705. DOI: 10.1259/bjr.73.871.11089459
46. Gülsün M, Demirkazik FB, Ariyürek M. Evaluation of breast microcalcifi cations according to breast imaging reporting and data system criteria and Le Gal’s classifi cation. Eur J Radiol. 2003 Sep;47 (3):227–31.
Eur J Radiol. 2003 Sep;47 (3):227–31.
47. Мастопатии. Под ред. А. Д. Каприна, Н. И. Рожковой. М.: ГЭОТАР-Медиа; 2019, 320 с.
Что такое аденоз молочных желез? | Женское здоровье
Каждый четвертый случай возникновения злокачественных опухолей приходится на рак молочной железы. Этот недуг ежегодно уносит тысячи жизней. Однако во многих случаях его страшные последствия можно предупредить при своевременной диагностике и грамотном лечении заболеваний, являющихся предшественниками раковых образований. Среди недугов, влекущих за собой перерождение клеток в злокачественную опухоль, выделяют мастопатию. Она поражает как протоки грудных желез, так и их дольки. В зависимости от особенностей развития и расположения затронутых участков выделяют различные виды мастопатии.
Один из них — аденоз молочной железы. В 45-50 процентов случаев аденоз не приносит женщине болевых ощущений или дискомфорта.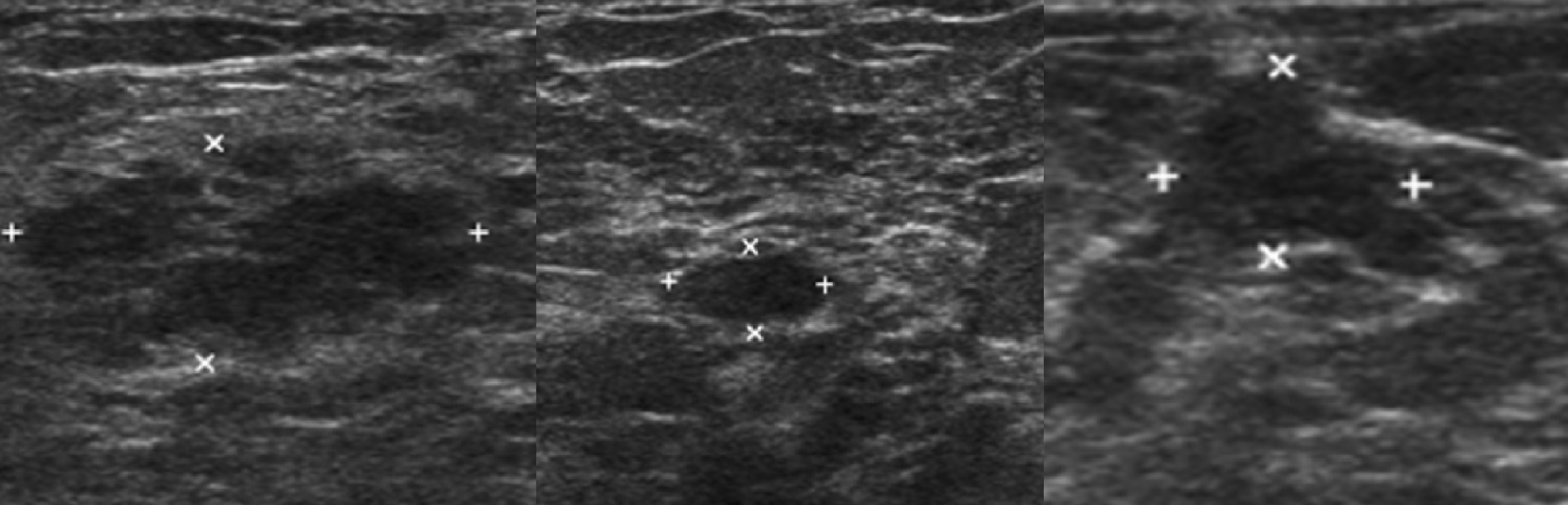 Это существенно усложняет процесс своевременной диагностики заболевания. Во избежание развития рака груди рекомендуется регулярное самообследование и посещение врача-маммолога минимум 1 раз в полгода или год.
Это существенно усложняет процесс своевременной диагностики заболевания. Во избежание развития рака груди рекомендуется регулярное самообследование и посещение врача-маммолога минимум 1 раз в полгода или год.
Что это такое?
Избыточное разрастание тканей и клеток в организме человека вне зависимости от природы и причин носит имя аденоз. Зачастую заболевания железистых структур и лимфоузлов носят аналогичное наименование. Аденоз молочной железы представляет собой подвид мастопатии и имеет фиброзную форму. Эта форма заболевания развивается на фоне избыточного разрастания клеток эпителия. Недуг поражает дольки железы, приводя к развитию отечности, застою и воспалению. В структуре доброкачественной опухоли превалируют железистые элементы. Наиболее распространен недуг среди:
- женщин среднего и старшего возраста;
- девушек в конце периода полового созревания;
- у беременных женщин в первые три месяца беременности.
Виды заболевания
Последующая терапия заболевания во многом определяется его принадлежностью к определенному виду.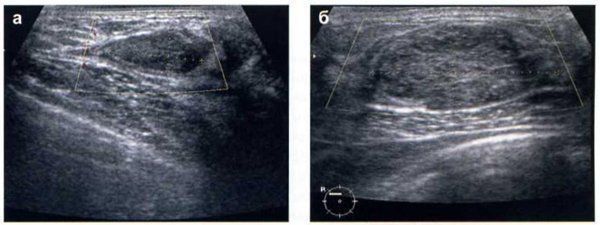 Существуют несколько типов заболевания, отличающихся по своим проявлениям. Выделяют:
Существуют несколько типов заболевания, отличающихся по своим проявлениям. Выделяют:
- Апокринный. Формируется за счет крупных узловатых образований, локализованных в дольках грудных железы. Зачастую они имеют одинаковые очертания и границы. Эпителиальные клетки при этом разрастаются, отмечается чрезмерное увеличение цитологического ядра и появление гранулированных образований.
- Протоковый. Опухоль в данном случае формируется из трубчатых образований, имеющих единые очертания с долькой молочной железы. В протоках происходит удвоение эпителиального слоя.
- Склерозирующий. Представляет собой самое маленькое из возможных образование и не ведет к повреждению эпителиального слоя. Однако в некоторых случаях характеризуется значительным разрастанием фиброзной ткани.
- Аденоэпителиальный. Поражает клетки эпителия молочных желез, вызывая их разрастание.
- Микрогландулярная. Редкая форма, которая лишена симптоматики и обнаруживается случайно.
Причины возникновения
Аденома молочной железы возникает по причинам, которые не установлены современной медициной наверняка.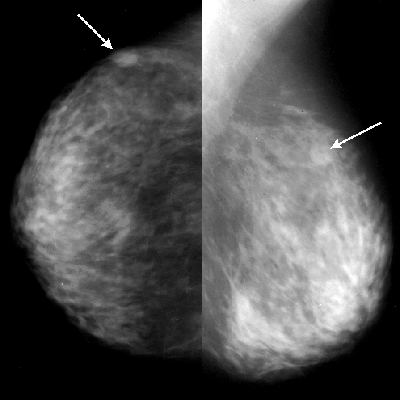 Известно, что основным фактором, приводящим к развитию болезни, относится нарушение гормонального фона в организме женщины. Подобная ситуация может быть вызвана следующими причинами:
Известно, что основным фактором, приводящим к развитию болезни, относится нарушение гормонального фона в организме женщины. Подобная ситуация может быть вызвана следующими причинами:
- колебания гормонального фона, спровоцированные началом пубертатного периода;
- перестройка гормонов, связанная с наступлением климатической паузы;
- беременность или роды;
- эмоциональное потрясение или перенапряжение;
- стрессовые ситуации, депрессия;
- избыточные физические нагрузки;
- работа в ночное время суток;
- прием оральных контрацептивов;
- прерывание беременности;
- гормонотерапия.
Механизм развития заболевания
Аденоз молочных желез развивается в связи с гормональным воздействием. Негативное влияние оказывают:
- Эстроген. Активно воздействует до начала периода полового созревания. Принимает участие в развитии и формировании тканей протоков молочных желез. Является одним из ведущих компонентов для соединительной ткани груди, оказывает благоприятное действие на рост ее клеток.

- В период действующей детородной функции воздействуют эстроген и прогестерон. Прогестерон служит регулятором при формировании тканей и альвеол молочной железы.
- Пролактин. Гормон необходим для производства железами молозива, оказывает стимулирующее воздействие на его секрецию и созревание. Стимулирует рост тканей груди и участвует в развитии ее клеток. Провоцирует возникновение рецепторов эстрогена.
В норме все эти гормоны не оказывают неблагоприятного влияния на здоровье женщины. Однако в случае чрезмерного разрастания рецепторного аппарата происходит развития аденоза молочной железы.
Симптомы
Проявляется аденома молочной железы следующим образом:
- появление болезненных ощущений или дискомфорта в области груди;
- тяжесть и отечность желез;
- набухание и одутловатость;
- покраснение;
- чрезмерная чувствительность сосков;
- выделение молозива;
- проявление сосудистой сетки;
- увеличение температуры груди;
- ухудшение общего самочувствия;
- слабость, потеря работоспособности;
- быстрая утомляемость;
- раздражительность.

В большинстве случаев симптомы отсутствуют или выражены крайне слабо.
Диагностика
Аденома молочной железы во многих случаях не обнаруживает себя. Это связано с тем, что болевые ощущения в половине случаев могут отсутствовать. Для обнаружения заболевания и принятия мер по его лечению применяют следующие типы исследований:
- Ультразвуковое исследование. Представляет собой диагностирование аденоза путем обнаружения образования, получения информации о размерах и границах доброкачественной опухоли. Однако УЗИ не всегда позволяет получить полноценную картину течения заболевания.
- Маммография. Приоритетный метод исследования не только аденоза, но и других заболеваний, поражающих молочные железы. Дает более глубокие и точные результаты. Позволяет оценить расположения доброкачественного образования, его размеры и границы. Кроме того, дает понимание о динамике развития опухоли.
- Гистологическое исследование. Представляет собой пробу тканей, позволяющей понять, что это такое – рак или доброкачественное образование.

- Лабораторные исследования. Преимущественно направлены на выявление уровня гормонального фона. Позволяют выявить и оценить отклонения от показателей нормы в целях назначения дальнейшей терапии.
Наиболее точные результаты дает применение комплексного обследования. Точный диагностический курс поможет подобрать врач-маммолог.
Лечение
Возможны следующие пути лечения:
- Хирургическое вмешательство. При обнаружении единичных узловых образований к радикальным оперативным вмешательствам, как правило, не прибегают. Однако пациентке необходимо в обязательном порядке регулярно наблюдаться у специалиста. Минимальное количество посещений маммолога в год – 2. Если выявляется склерозирующая форма, то ее необходимо иссечь хирургическим путем. Проведение операции возможно под местной и под общей анестезией, исходя из показаний. После удаления доброкачественного образования необходимо принимать обезболивающие препараты перорально.
- Во многих случаях положительные результаты дает применение гормональной терапии.
 Преимущественно рекомендуется прием оральных контрацептивов или гестагенных препаратов. В среднем положительные результаты отмечаются спустя 50-60 дней лечения.
Преимущественно рекомендуется прием оральных контрацептивов или гестагенных препаратов. В среднем положительные результаты отмечаются спустя 50-60 дней лечения. - Гомеопатические препараты. Эти лекарственные средства изготовлены из натуральных природных компонентов. Они способны оказать значительный терапевтический эффект.
- Витаминные комплексы. Назначаются с целью нормализации обмена веществ и усиления иммунитета. Не применяются без согласования с лечащим врачом.
- Диетическое питание. Правильная пища позволит не только выздороветь в кратчайшие сроки, но и окажет общее благотворное влияние на организм. Необходимо отказаться от употребления жареной, жирной, острой пищи. Не стоит увлекаться копченными или солеными продуктами. Они способны вызвать застой жидкости и спровоцировать отечность.
Заболевание причиняет женщине дискомфорт и может стать первой весточкой грозящего рака груди. Заболевание развивается без выраженной симптоматики. Для его предупреждения всем женщинам, начиная с самого раннего возраста, необходимо тщательно следить за своим здоровье. Однако стоит отметить, что аденоз крайне редко перерождается в злокачественное образование. Во многих случаях, например, при беременности, заболевание проходит самостоятельно.
Однако стоит отметить, что аденоз крайне редко перерождается в злокачественное образование. Во многих случаях, например, при беременности, заболевание проходит самостоятельно.
Диффузная фиброзно-кистозная мастопатия: как лечить фиброзно-кистозную мастопатию молочной железы?
Для женщин репродуктивного возраста характерна смена пролиферативных и регрессивных изменений эпителиальных и опорных тканей молочных желёз, Нарушение регуляции этих процессов может вызвать диффузную перестройку структуры молочных желёз, что наблюдают у 39% женщин. Такая перестройка проявляется в виде диффузных и диффузно-узловых изменений. Наиболее распространена фиброзно-кистозная мастопатия. Термин «фиброзно-кистшман мастопатия» имеет до 30 синонимов, например:
- кистозная десквамативная гиперплазия;
- хронический кистозный мастит;
- фиброаденоматоз простой;
- макрокистозный фиброаденоматоз;
- папиллярный фиброаденоматоз; • болезнь Реклю;
- болезнь Шиммельбуша;
- аденоз;
- мазоплазия;
- микрокистозный фиброаденоматоз;
- болезнь Вельяминова;
- мастодиния;
- аденофиброз;
- кистозный склероз;
- скларокистозный мастоз.

Разделение мастопатии по степени выраженности процесса имеет большое значение для дифференциальной диагностики и выбора оптимальных сроков повторных исследований.
Диффузная фиброзно-кистозная мастопатия с преобладанием железистого компонента (аденоз)Аденоз — состояние, пограничное между нормой у молодых женщин и патологией у женщин старше 22-25 лет (9,7%). Морфологическая основа аденоза — гиперплазия железистых долек. Клинически регистрируют болевые ощущения, особенно в предменструальный период, набухание молочных желёз, их уплотнение. При пальпации молочные Железы плотные, с отдельными диффузно расположенными узлами, нерезко отграниченными от окружающих тканей.
На рентгенограммах выявляют множественные тени неправильной фирмы с нечеткими, расплывчатыми контурами. Каждая тень соответствует участку лобулярной гиперплазии, совокупность теней образует неоднородную неравномерную тень, занимающую почти всю молочную железу.
Диффузная фиорозно-кистозная мастопатия с преобладанием фиброзного компонента.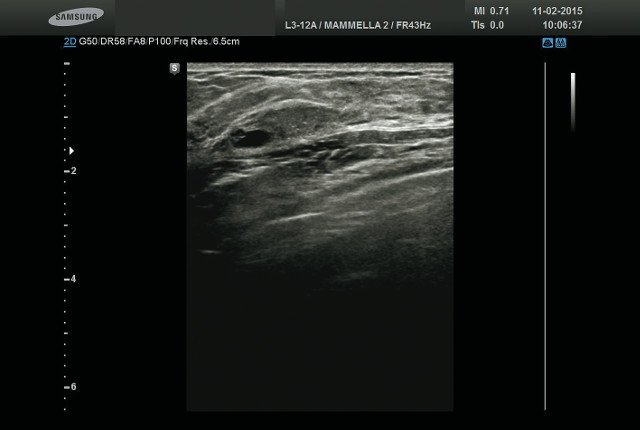
Клиническая картина и субъективные ощущения почти такие же. как при форме мастопатии, описанной выше. Рентгенологическая картина обеих форм также сходна. Вся молочная железа интенсивно затемнена, имеет узкую полоску просветления, образованную подкожно-жировой клетчаткой. В отличие от аденоза, при фиброзе контуры отдельных участков лобулярной гиперплазии подчёркнуты, а не разрыхлены. Эта форма мастопатии встречается в 30,7% случаев.
Диффузная фиброзно-кистозная мастопатия с преобладанием кистозного компонента.Встречается у 17,4% всех женщин с мастопатией. При морфологическом обследовании обнаруживают множественные кисты, расширение протоков, преобладание фиброза, атрофию долек.
Клиническая картина такая же, как у предыдущих форм мастопатии, но, в отличие от них, могут пальпироваться отдельные уплотнения округлой или овальной формы, эластической консистенции, отграниченные от окружающих тканей, если их размер превышает 2 см. Более мелкие уплотнения при пальпации не всегда обнаруживают вследствие мягкой консистенции, в этом случае помогает рентгенография. На рентгенограммах на фоне пёстрого неоднородного рисунка, обусловленного чередованием жировой, соединительной и железистой ткани, видны уплотнения — округлые, овальные или с вдавлениями от соседних кист. Размеры уплотнений колеблются от 0,3 до 6-8 см, их контуры чёткие, ровные, с ободком просветления, свидетельствующим об экспансивном росте. При наличии в кистах нескольких камер их контуры полицикличные, резкие. Наиболее информативный метод диагностики — УЗИ.
На рентгенограммах на фоне пёстрого неоднородного рисунка, обусловленного чередованием жировой, соединительной и железистой ткани, видны уплотнения — округлые, овальные или с вдавлениями от соседних кист. Размеры уплотнений колеблются от 0,3 до 6-8 см, их контуры чёткие, ровные, с ободком просветления, свидетельствующим об экспансивном росте. При наличии в кистах нескольких камер их контуры полицикличные, резкие. Наиболее информативный метод диагностики — УЗИ.
Встречается в 38,6% случаев. Морфологическая картина довольно пёстрая: избыточное развитие железистых долек, склерозирование внутридольковой и междольковой соединительной ткани, превращение альвеол в микрокисты.
Различают непролиферирующую и пролиферирующую формы мастопатии; на фоне последней рак встречается в 7-14 раз чаще. Клинически заболевание проявляется ощущением болей различной степени выраженности, даже при прикосновении одежды.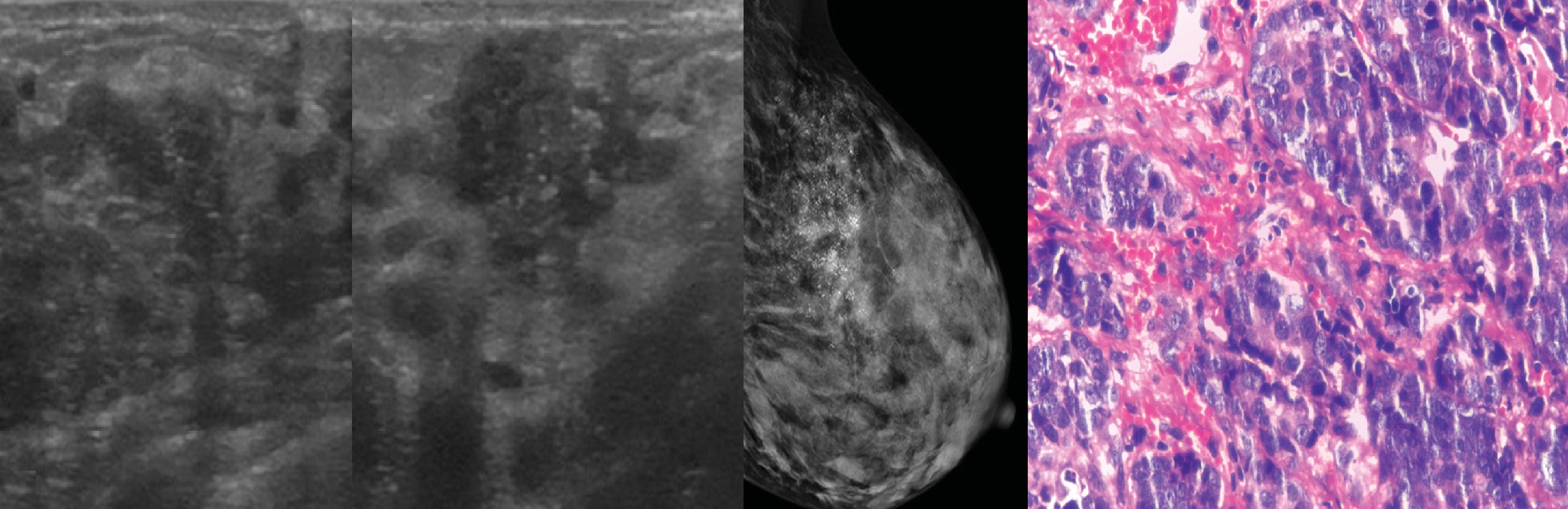 При пальпации выявляют либо диффузную мелкую зернистость, либо дисковидную тестоватость. В рентгенологическом изображении отмечается нарушение нормального структурного рисунка, выражающееся в чередовании просветлений и затемнений округлой, овальной или неправильной формы, сочетающихся с хаотически расположенными плотными фиброзными тяжами. Нередко УЗИ вносит ясность, уточняя, какие структуры преобладают.
При пальпации выявляют либо диффузную мелкую зернистость, либо дисковидную тестоватость. В рентгенологическом изображении отмечается нарушение нормального структурного рисунка, выражающееся в чередовании просветлений и затемнений округлой, овальной или неправильной формы, сочетающихся с хаотически расположенными плотными фиброзными тяжами. Нередко УЗИ вносит ясность, уточняя, какие структуры преобладают.
Чем раньше пациент получит квалифицированную помощь, тем меньше времени займет лечение, и оно будет более эффективным.
Лечение опухолей и опухолеподобных процессов в СПб больнице РАН на маммологическом отделении
Доброкачественная патология молочных желез (опухоли и опухолеподобные процессы): протоковая неоплазия, внутрипротоковые папилломы, кисты молочных желез, галактоцеле, аденома молочной железы, фиброаденома молочной железы, листовидная опухоль молочной железы, липома молочной железы, псевдоангиоматозная стромальная гиперплазия, очаговый фиброз (локализованный фиброаденоматоз), аденозы молочных желез ( склерозирующий аденоз, радиальный рубец), воспалительная псевдоопухоль молочной железы, гинекомастия.
Киста молочной железы
Киста молочной железы встречается у 50% женщин репродуктивного возраста, у мужчин встречается достаточно редко. Размеры могут меняться в зависимости от фазы менструального цикла.
При самостоятельном обследовании проявляется как округлое образование, подвижное, безболезненное.
В молодом возрасте с целью инструментальной диагностики предпочтение отдается УЗИ молочных желез. У пациенток с иволютивными изменениями, возможно проведение маммографии.
Принято различать простые (гомогенные) и сложные (гетерогенные) кисты молочных желез. Простые кисты небольших размеров могут наблюдаться в динамике и не имеют злокачественного потенциала. Хирургическое лечение показано в случаях неэффективности консервативной терапии.
простая киста молочной железы.
Сложные кисты обязательно подвергаются инвазивным методам диагностики с цитологическим или гистологическим исследованием материала. Вероятность озлокачествления сложной кисты равна 0.3%. При выявлениях сложных кист хирургическая тактика предлагается более активно.
Вероятность озлокачествления сложной кисты равна 0.3%. При выявлениях сложных кист хирургическая тактика предлагается более активно.
сложная киста молочной железы.
В настоящее время в СПб больнице РАН мы можем предложить безоперационные способы удаления сложных кист молочных желез, методом ваккуумно-аспирационной резекции.
Галактоцеле
Галактоцеле — это объемное образование с жидкостью молочного цвета. Данная патология развивается во время беременности или в период лактации.
При осмотре пальпируется плотный узел.
полость с густым содержимым.
Для лечения используется аспирация содержимого кистозной полости с консервативной терапией по показаниям.
В маммологическом отделении СПб больницы РАН пациентка может пройти качественное лечение при этой патологии.
Фиброаденома
Фиброаденома — доброкачественная опухоль молочных желез из компонентов соединительной ткани.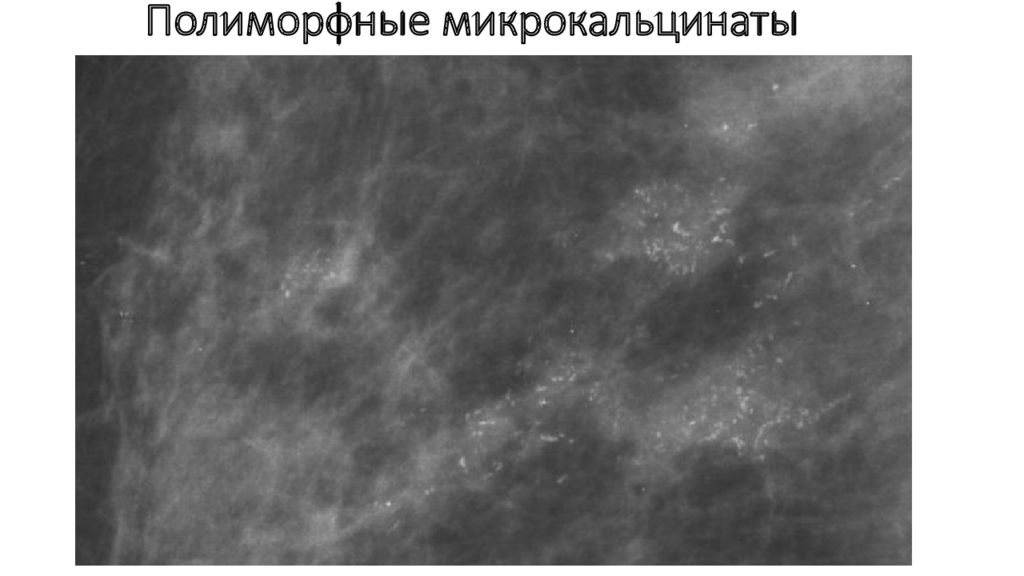 Это самый частый вариант доброкачественных опухолей молочных желез.
Это самый частый вариант доброкачественных опухолей молочных желез.
Наиболее часто встречается в возрасте 20-35 лет.
В 15% случаев процесс носит множественный характер.
При осмотре определяется в виде плотного узла, с четкими границами.
Для диагностики у пациенток до 30 лет, как правило, используется УЗИ, в старшем возрасте маммография. При сложных клинических случаях возможно проведение МРТ.
Необходимость биопсии зависит от клинических и лабораторных данных.
Переход в рак молочной железы наблюдается редко от 0.5 до 1.5% наблюдений.
При благоприятном течении процесса допускается динамический контроль за образованием.
Традиционно при выявлении фиброаденомы молочной железы пациентке предлагается проведение секторальной резекции молочной железы. При этом варианте оперативного лечения форма молочной железы не нарушается. Однако, после вмешательства остается п/о рубец.
Однако, после вмешательства остается п/о рубец.
В нашей клинике мы предлагаем безоперационный метод удаления фиброаденом при помощи вакуумно-аспирационной резекции. Доступ осуществляется через прокол кожи 2-3 мм, а сама ткань новообразования удаляется под УЗ контролем.
На рисунке показано подведение инструмента (тонкая стрелка) к образованию (короткая стрелка) молочной железы.
Методика безопасна, является альтернативно секторальной резекции при доброкачественных образованиях молочных желез, обладает низким процентом осложнений и хорошо переносится пациентами.
Липома молочной железы
Липома молочной железы — доброкачественное образование возникающее в 1% наблюдений.Чаще всего имеет узловую форму. Представлено мягким образованием овальной или дольчатой формы. Для диагностики чаще всего применяется УЗИ и маммография.
Основной лечебной опцией является динамическое наблюдение, а хирургическое лечение проводится при сомнении в диагнозе или из косметических целей.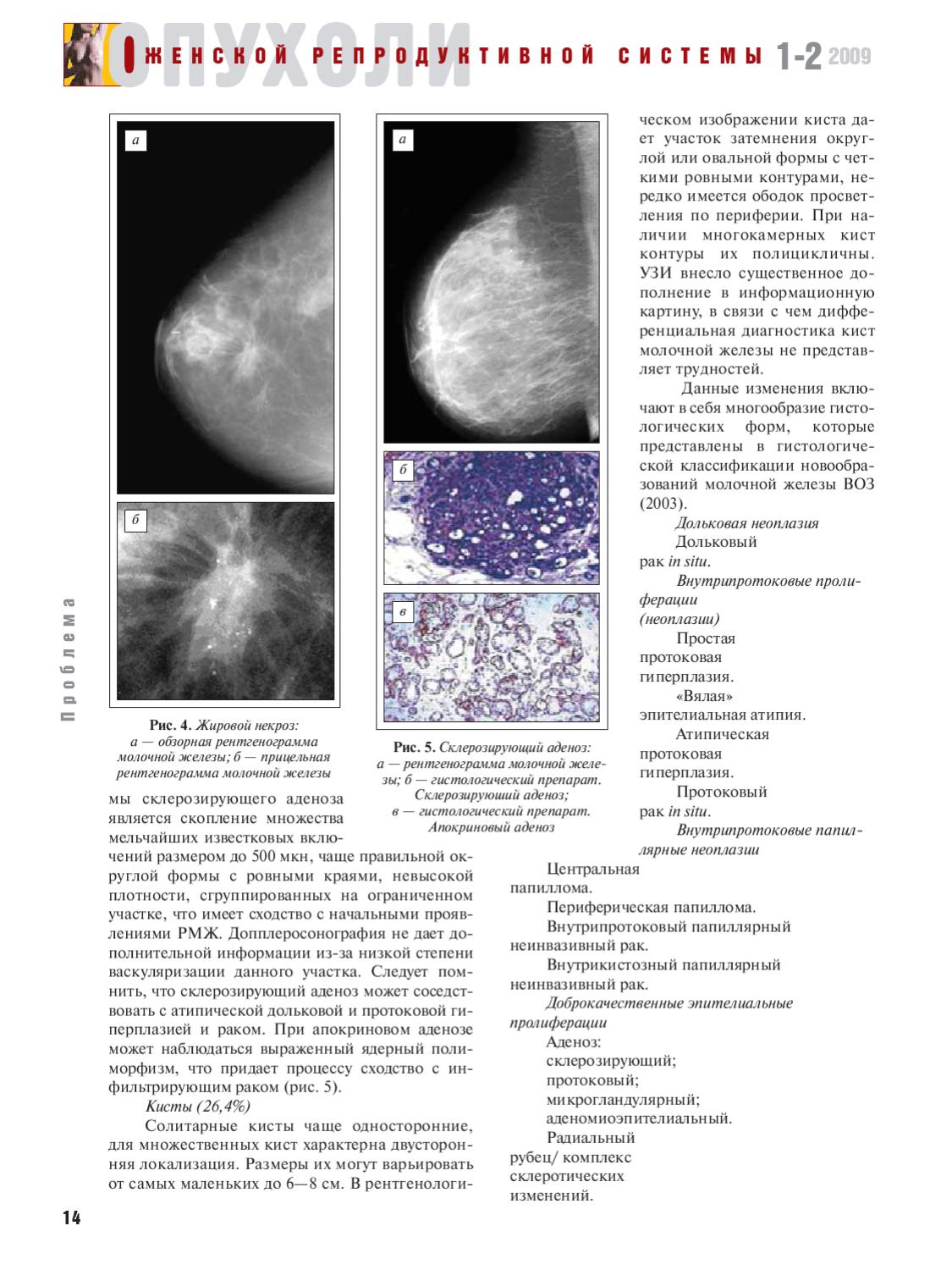
Малигнизации, как правило, они не подвергаются.
Листовидная опухоль
Листовидная опухоль -это редкая группа опухолей, с частотой встречаемости около 0.3% от всех новообразований молочных желез.
Средний возраст женщин страдающих данной патологией варьирует от 45 до 49 лет.
В 80% опухоль является доброкачественной. Около 5% составляет злокачественная форма. Остальные случаи относятся к пограничному типу.
Клиническое течение делится на 2 периода: период стабилизации и период интенсивного роста.
С целью инвазивной диагностики предпочтение отдается cor-биопсии.
Лечение в большинстве случаев хирургическое. При небольших опухолях проводится секторальная резекция молочной железы. Проведение энуклеации опухоли недопустимо из-за почти 100% риска рецидива образования.
При объемных злокачественных опухолях проводится мастэктомия без лимфаденэктомии с последующим динамическим контролем.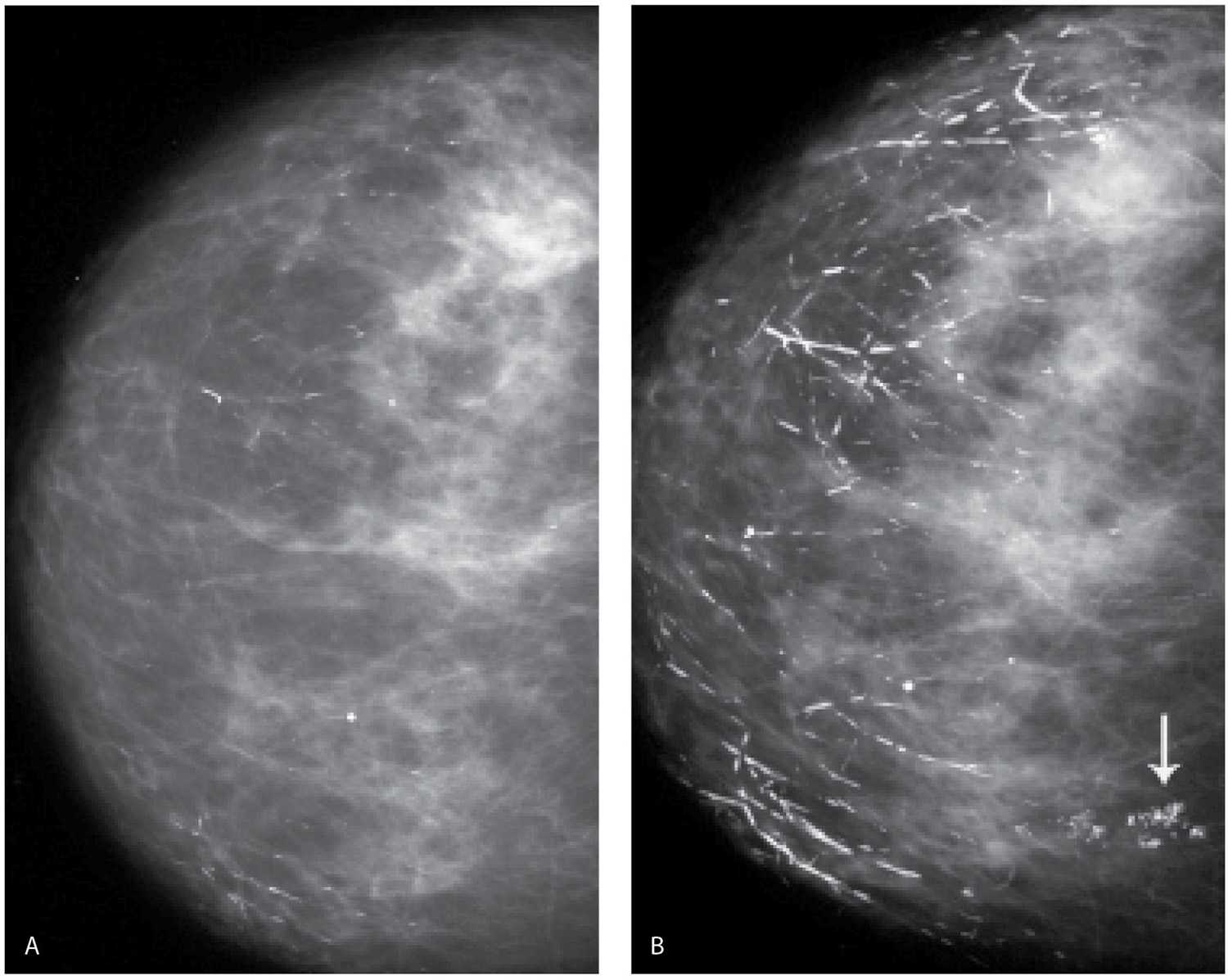
Прогноз — благоприятный.
Псевдоангиоматозная стромальная гиперплазия
Патология встречается редко. При пальпации определяется безболезненное образование с отеком кожи по типу «лимонной корки»
Для дообследования используют весь спектр инструментальной диагностики (маммография, УЗИ, МРТ).
При выявлении данной патологии, лечение хирургическое. Допустимо проведение вакуумно-аспирационной резекции, в ряде случаев, секторальной резекции молочной железы.
Прогноз — благоприятный.
Аденозы
Группа доброкачественных, узловых образований молочных желез с различными вариантами течения.
Варианты:
- склерозирующий аденоз
- радиальный рубец
- аденоз с расширением концевых отделов
- микрогландулярный аденоз
- апокриновый аденоз
- миоэпителиальный аденоз
Наиболее характерный интервал возникновения данных образований 35-50 лет. Наиболее часто встречается склерозирующий аденоз. С целью установки диагноза в большинстве случаев используется маммография, УЗИ является малоспецифичным методом.
Наиболее часто встречается склерозирующий аденоз. С целью установки диагноза в большинстве случаев используется маммография, УЗИ является малоспецифичным методом.
С целью лечения применяются все виды хирургического пособия (эксцизионная биопсия или секторальная резекция молочной железы).
Радиальный рубец.
Данный аденоз требует более пристального рассмотрения, так как обладает высоким риском перерождения в злокачественную опухоль. С целью установки правильного диагноза используется маммография. Оптимальной лечебной тактикой является проведение вакуумно-аспирационной биопсии( резекции). При выявлении фокусов атипической протоковой гиперплазии показано проведение секторальной резекции молочной железы.
Воспалительная псевдоопухоль
Воспалительная псевдоопухоль — это узловое доброкачественное образование молочных желез.
Данная патология может свидетельствовать о перенесенных травмах, воспалительных заболеваниях или внедрении инородного тела. Встречаемость достаточно редкая. Для диагностики используется маммография, реже — УЗИ.
Встречаемость достаточно редкая. Для диагностики используется маммография, реже — УЗИ.
С целью лечения применяется вакуумно-аспирационная резекция, либо секторальная резекция молочной железы.
Прогноз благоприятный.
Эктазия протоков
Эктазия протоков — прогрессирующее расширение протоков молочной железы, как правило, в подсосковой зоне. Часто сопровождается выделениями из молочных желез, разного характера.
Лечение симптоматическое.
Прогноз — благоприятный.
Гинекомастия
Гинекомастия — увеличение молочных желез у мужчин.
В настоящее время данная патология встречается у 1/3 взрослых мужчин.
Различают истинную и ложную гинекомастию.
Ложная гинекомастия формируется за счет отложения жира в области молочных желез и не связана с процессами гиперплазии.
Истинная гинекомастия возникает вследствие пролиферации стромы и протоковый молочных желез у мужчин.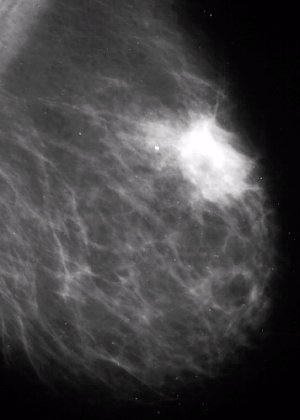
Причины возникновения гинекомастии разнообразны. К этому состоянию приводят различные эндокринные заболевания, генетические нарушения, патология нейроэндокринных процессов, паранеопластические процессы.
Клинически гинекомастия может быть узловой и диффузной, одно и/или двусторонней. Степень проявлений варьирует от 1 до 4.
Для диагностики используют УЗИ, реже маммографию.
С целью лечения возможно проведение лекарственной коррекции направленной на снижения содержания эстрогенов в организме.
Узловые формы гинекомастии подлежат хирургическому удалению.
В маммологическом отделении СПб больницы РАН проводится весь спектр хирургических вмешательств при данном заболевании, в том числе с применением методов коррекции сосково-ареолярного комплекса для профилактики его западения и нарушения эстетики груди.
Диффузный фиброаденоматоз молочных желёз | СПб ГБУЗ «Городская поликлиника №122»
Диффузный фиброаденоматоз молочных желёз | СПб ГБУЗ «Городская поликлиника №122»6
Фев
2016Диффузный фиброаденоматоз молочных желёз (ФАМ) – это доброкачественное заболевание молочной железы, которое может захватывать как одну, так и обе груди.Основополагающей причиной развития фиброаденоматоза считается дисбаланс гормональной системы в организме. Как правило, изменения в гормональном фоне женщины происходит в следующих случаях:
стрессовые ситуации – психическая нестабильность, психоэмоциональные срывы. Особенно, если человек находится в стрессовом состоянии постоянно или длительное время;
гинекологические заболевания, сопровождающиеся расстройством функциональной способности яичников, спровоцированные воспалительными процессами репродуктивных органов, нарушениями менструального цикла;
аборты, в том числе и медикаментозные.
отказ или раннее прекращение грудного вскармливания малыша – провоцирует застой в молочных железах. Грудное вскармливание следует практиковать как минимум в течение года после рождения ребенка;
сексуальные проблемы – практика прерванного полового акта, нерегулярный секс или отсутствие постоянного полового партнера, неудовлетворение сексуальных потребностей;
патологии щитовидной железы – недостаток или избыток гормонов щитовидной железы влияет и на баланс половых гормонов;
вредные привычки (курение, употребление алкоголя).
Фиброаденоматоз может протекать в различных формах:
диффузный
локализованный
очаговый
кистозный
фиброзный
узловой
Форму заболевания определяет врач-маммолог, онколог.
Симптомами заболевания могут быть:
часто повторяющиеся колющие боли в молочной железе;
нагрубание и уплотнение молочных желез за несколько дней до начала менструации или вне зависимости от цикла;
ощущение давления и жгучей боли в молочной железе;
выделения из молочных протоков, как самостоятельные, так и появляющиеся при сдавливании соска;
увеличение лимфатических узлов в подмышечной области (иногда).
Болезненность имеет свойство усиливаться после нервного или физического перенапряжения.
Обнаружив у себя хоть один из выше перечисленных признаков, стоит незамедлительно обратиться к врачу-маммологу или онкологу !Для того чтобы заметить изменения ткани молочной железы, необходимо проводить ежемесячное обследование!
Выполнить его может каждая женщина самостоятельно.
Для этого необходимо внимательно ощупать грудь по всей окружности, а потом более внимательно – в каждом квадранте.
В настоящее время широкое распространение получили рентгенологический (цифровая маммография) и ультразвуковой методы исследования.
Ультразвуковое исследование более предпочтительно для молодых женщин.
Уважаемые пациентки, обращаем Ваше внимание, что в условиях нашей поликлиники оба метода активно выполняются на современном оборудовании.
Женщинам старше 39 лет обязательно проходить маммографию, независимо от того, есть у них жалобы или нет.
Начиная с 39 до 50 лет, если нет жалоб, необходимо выполнять обследование 1 раз в 2 года, после 50 лет-1 раз в год.
Частота обследования, прежде всего, зависит от присутствия рисков, наследственности, а также при наличии каких-либо жалоб.
Кроме того, нужно избегать неблагоприятных факторов и переохлаждений, правильно питаться и носить удобное бельё.
Основные принципы терапии фиброаденоматоза
Для определения необходимой схемы терапевтических мероприятий важно установить и устранить причину патологии, а также сбалансировать работу гормональной системы.
Подбор лечения осуществляется в зависимости от возрастной категории пациента, стадии болезни, особенности метаболизма и гормонального фона, наличия каких-либо других смежных патологий в организме.
В настоящее время терапия данного заболевания предполагает назначение гормональных препаратов, гомеопатических средств, витаминов, антидепрессантов, адаптогенов. Для снятия болезненности могут быть назначены нестероидные противовоспалительные средства, однако это делается на непродолжительный период.
Метод обследования и схема лечения назначается врачом в индивидуальном порядке, учитывая особенности каждой женщины.
Хирургическое вмешательство требуется только если существует подозрение на рак. С целью сохранения женского здоровья рекомендуется ежегодно наблюдаться у гинеколога и маммолога!
Спасибо за отзыв!
Ваш отзыв был получен и отправлен администратору!
Признаки и лечение аденоза молочных желез — Портал о заболеваниях груди
Аденоз молочной железы – разновидность мастопатии. Предусловием для правильной работы молочных желез являются железистые дольки. Они обеспечивают выработку секрета, необходимого для появления молока в послеродовой период. Аденоз – это, по сути, гиперплазия и отсутствие лактации одновременно. В зону риска заболевания попадают нерожавшие женщины или же мамы, которые рано прекращают грудное вскармливание. Для девушек аденоз – это фактор полового созревания. У мужчин болезнь также может проявляться.
Предусловием для правильной работы молочных желез являются железистые дольки. Они обеспечивают выработку секрета, необходимого для появления молока в послеродовой период. Аденоз – это, по сути, гиперплазия и отсутствие лактации одновременно. В зону риска заболевания попадают нерожавшие женщины или же мамы, которые рано прекращают грудное вскармливание. Для девушек аденоз – это фактор полового созревания. У мужчин болезнь также может проявляться.
Причины
Причина возникновения аденоза грудных желез – нарушения гормонального фона. Вырабатывается избыток гормонов при беременности, после родов и во время полового созревания. Значительно превышается норма эстрогена и пролактина, а выработок пролактина снижается. Такие сбои провоцируют возникновения разных патологий.
Для точного выяснения причины и природы гормональных нарушений, нужно провести лабораторное исследование крови.
Часто предусловием к образованию уплотнения становится наличие других патологий:
- гипотиреоз, гипертиреоз (проблемы в области щитовидной железы)
- кистозное образование на яичниках
- гиперплазия эндометрия
- жировая дистрофия печени
Дополнительным фактором, сигнализирующим о возможных будущих проблемах в груди, является кальцинат — отложения кальция в молочных железах.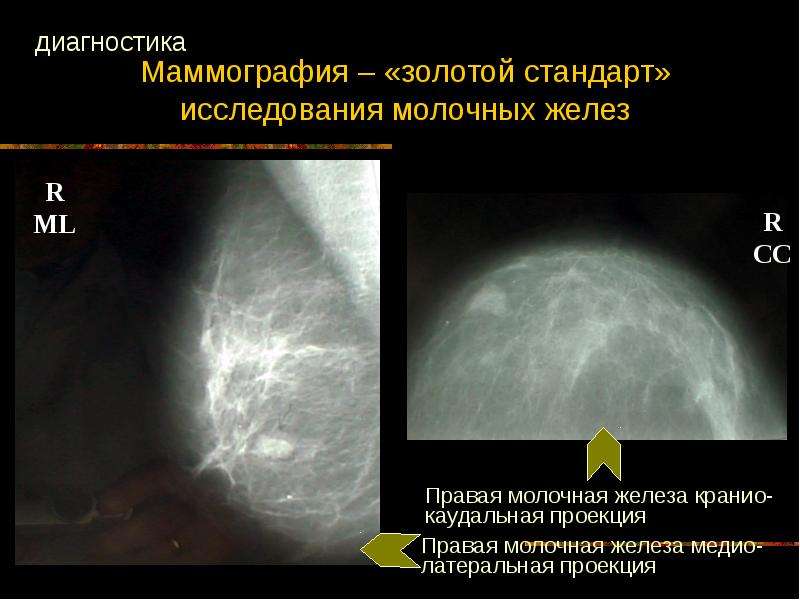 Кальцинаты бывают разных размеров, заметными становятся тогда, когда вырастают больше 1см. Сами по себе кальцинаты никак не проявляются, не наносят вреда организма.
Кальцинаты бывают разных размеров, заметными становятся тогда, когда вырастают больше 1см. Сами по себе кальцинаты никак не проявляются, не наносят вреда организма.
Часто за развитием патологии нужно просто наблюдать. Но сам факт образования кальцинатов свидетельствует о воспалительных процессах, развивающихся в тканях груди. Накапливаются молочная и пировиноградная кислоты, в результате чего кальций и его соли оседают. Данный сигнал организма не следует оставлять без внимания.
Факторы, способствующие развитию мастопатии:
- наследственность
- дисфункция (кистоз) яичников
- образ жизни (алкоголь, курение)
- плохая экология
Классификация
По степени роста количества клеток в грудной железе, их размещения, аденоз молочных желез делится на подвиды:
- Локальный аденоз грудных желез.
 Новообразования характеризуются четкой локализацией, дольчатой структурой. Хорошо ощущаются во время пальпации . Наблюдается рост подмышечных лимфоузлов. При прощупывании уплотнения очень болезненны.
Новообразования характеризуются четкой локализацией, дольчатой структурой. Хорошо ощущаются во время пальпации . Наблюдается рост подмышечных лимфоузлов. При прощупывании уплотнения очень болезненны. - Диффузный аденоз грудных желез — это первая стадия мастопатии. Нет четкой локализации, образуется в тканях железы, протоках, узлах. Мелкие новообразования могут перерасти в одну большую опухоль. В предменструальный период усиливается боль, грудь уплотняется и набухает. Страдают данным заболеванием нерожавшие женщины. Если игнорировать первые проявления, то последует длительное лечение болезни.
- Очаговый аденоз груди — образуется в протоках груди, выстилает их цилиндрической тканью. Становится основой для формирования узловой мастопатии. В этом случае беспокоят сильные предменструальные боли, тяжесть и плотность груди. Большие аденозные очаги желательно удалить, чтобы они не сформировали опухоль.
- Фиброзирующий аденоз груди типичен для женщин старшего возраста. С приближением климакса потребность в железистой ткани снижается, ее заменяет фиброзная .
 Патология характеризуется локальной периодичной болью в области желез. Прощупываются мелкие узелки на правой и левой железах, очаг эластичный, довольно мелкий. Выделения из сосков отсутствуют.
Патология характеризуется локальной периодичной болью в области желез. Прощупываются мелкие узелки на правой и левой железах, очаг эластичный, довольно мелкий. Выделения из сосков отсутствуют.
По характеру появления «лишних» клеток, аденоз грудных желез делится на:
- Склерозирующий аденоз груди. Особенность данного вида болезни — появляются не отдельные уплотнения, а вся грудь становится твердой, болезненной, ближайшие лимфоузлы увеличиваются. Типичен для больных, в возрасте от 35 лет. Природа недуга – гормональный сбой в результате возрастных изменений. Даная патология требует тщательного наблюдения.
- Аденомиоэпителиальный и тубулярный аденоз груди — когда клетки эпителия разбросаны хаотично по всей области груди.
- Апокринный аденоз груди набирает форму узлов, похожих на доли молочной железы. В таких случаях родные клетки замещаются иными клетками с подобной структурой.
- Протоковый аденоз груди препятствует правильному формированию протоков.
 Эта форма аденоза болезненна, симптомы четко выражены.
Эта форма аденоза болезненна, симптомы четко выражены. - Микрогландулярный аденоз груди характерен тем, что в млечных протоках разрастаются клетки эпителия. Проходит бессимптомно, боль и опухоль развивается постепенно.
- Опухолеподобный аденоз груди имеет форму подвижных болезненных новообразований.
Симптомы заболевания
При разных формах заболевания, симптомы аденоза молочной железы отличаются. Но есть один общий симптом, характеризирующий болезнь — это болевые ощущения, уплотнения и тяжесть в груди.
Один из первых симптомов – набухание, увеличение в молочной железы чаще всего во второй части менструального цикла. При локальном аденозе груди уплотняется болезненная, пораженная часть груди, выделения из соска практически всегда отсутствуют. При диффузном типе молочная железа набухает вся, выделения возможны, но только прозрачные или белые. Появление кровавых выделений – очень опасный признак – может сигнализировать о злокачественных новообразованиях. Склерозирующий аденоз грудных желез отличается плохим аппетитом, повышенной температурой тела, тошнотой, общей слабостью.
Склерозирующий аденоз грудных желез отличается плохим аппетитом, повышенной температурой тела, тошнотой, общей слабостью.
Диагностика
При появлении первых симптомов аденоза, нужно проконсультироваться у врача- маммолога. Он проведет опрос, осмотрит грудь, назначит дальнейшие методы исследования. На их основе сможет поставить остаточный диагноз.
Основные известные методы диагностики:
- маммография
- цитологическое исследование
- ультразвуковое исследование (УЗИ) молочной железы и лимфоузлов
- маммосцинтиграфия
- биопсия ткани
- томография (КТ, МРТ)
- аспирационная, эксцизионная биопсия (обязательная пункция новообразования)
- анализ крови для определения гормонального фона
Код по Международной классификации болезней 10-го пересмотра
По результатам исследований специалист определяет диагноз в форме кода МКБ-10. В основном маммолог может сделать определенные заключения:
- диффузная форма мастопатии — №1
- фиброаденоз железистой ткани груди — №2
- фибросклероз груди — №3
- неопределенная форма мастопатии (доброкачественная)
Лечение аденоза молочной железы
Известны два способа, чтобы лечить подобные заболевания молочной железы: консервативный и хирургический.
Консервативное лечение
На начальных этапах аденоз грудной железы практически всегда лечится медицинскими средствами. Но для этого заболевание нужно вовремя диагностировать и локализовать.
Самые распространенные методы и процедуры:
- витаминотерапия – прием витаминов в нужные периоды менструального цикла, наиболее актуальный для девушек
- гормонотерапия (для восстановления эндокринного баланса)
- успокоительные гомеопатические препараты
- фитопрепараты
- улучшение образа жизни (исключение вредных привычек, здоровое питание), диета
Диффузной аденоз лечится, как правило, с помощью гормональной терапии. Применяется комбинация «гестагены + контрацептивы (оральные). Если болезнь не запущена, такой метод используется на протяжении 6 месяцев.
Основные препараты, используемые при терапевтическом лечении:
- Линдинет 30 — устраняет клинические признаки мастопатии, нормализует менструальную функцию у пациенток
- Норколут
- Прегнин
- Дюфастон
- 1% масляный раствор Прогестерона
Средства назначаются в промежуток с 16 по 25 день менструального цикла. Применение препаратов снимает боль и устраняет уплотнения молочных желез, прекращаются выделения из сосков.
Применение препаратов снимает боль и устраняет уплотнения молочных желез, прекращаются выделения из сосков.
В некоторых случаях врач назначает контрацептивы Жаннин, Силуэт, основное вещество которых – диеногест. Этот гормон обладает такой же эффективностью, как и прогестерон, только он синтетический.
Популярностью пользуется также Мастодинон – гомеопатический препарат. Но специалисты утверждают, что явных положительных результатов лечение данным средством не приносит. Назначать его стоит в комплексе с гормонотерапией. Отдельно его могут применять молодые пациентки или при первых признаках мастодинии.
Хирургическое лечение
При очаговом аденозе необходимым становится хирургическое вмешательство. Узловой очаг не реагирует на традиционное лечение, откладывать операцию достаточно опасно. Процедура заключается в резекции поврежденного участка и удалении патологического узла. При малейшей возможности образования злокачественного образования, применяется гистологическое исследование. Для полноценного выздоровления назначаются витамины А, С, Е, Р, В1, В2, В9, препараты кальция и магния.
При малейшей возможности образования злокачественного образования, применяется гистологическое исследование. Для полноценного выздоровления назначаются витамины А, С, Е, Р, В1, В2, В9, препараты кальция и магния.
Средства народной медицины
Существуют методы народной медицины, дающие неплохие результаты в борьбе с аденозом. Но их можно использовать только при условии их одобрения врачом. Это, в основном, настои из корней лопуха, конского каштана и грецких орехов.
При лечении более серьезной, кистозной мастопатии хорошим плюсом к гормональной терапии могут стать компрессы в домашней обстановке. В основном применяются компрессы из поваренной соли, магнезии (английской соли) и капустных листьев. Составляющие данных веществ, владеют противоотечными и противовоспалительными свойствами и практически не имеют противопоказаний (кроме аллергии). Делать компрессы просто:
- 2-3 ложки соли развести в литре теплой воды
- ложку магнезии развести в небольшом количестве воды
- нанести на натуральную ткань, приложить к больной груди
- чистые листья капусты приложить к железе, все компрессы хорошо закрепить
Профилактика
Самой действенной профилактикой от заболеваний груди является выполнения ею природной функции – кормление малыша молоком.
Также положительное влияние оказывают:
- беременность, кормление грудью ребенка хотя бы до полугода
- отказ от абортов
- отказ от бесконтрольного применения противозачаточных препаратов
- регулярная половая жизнь
- правильный, щадящий образ жизни
- регулярное посещение маммолога
Аденоз грудной железы хорошо лечится при своевременном диагностировании. Но не стоит недооценивать серьезность заболевания. В результате развития болезни возможны тяжелые последствия, вплоть до возникновения рака груди. Надо проходить регулярный осмотр у специалиста (минимум раз в полгода) и при появлении первых признаков недуга. Такое простое правило поможет уберечь здоровье, а может, и жизнь женщин и мам!
Тубулярный аденоз груди. Характерное доброкачественное образование, имитирующее инвазивную карциному
Тубулярный аденоз, термин, впервые введенный Оберманом, представляет собой необычное доброкачественное поражение груди, которое может имитировать инвазивную карциному. В литературе нет формального описания этого состояния. Мы сообщаем о результатах шести образцов от пяти пациентов (один с двусторонним заболеванием), в том числе трех, которые показали канцеризацию внутрипротоковой карциномой (DCIS).Возраст пациентов от 40 до 82 лет. У одного пациента опухоль груди составляла 3 см, а у других были обнаружены образцы, удаленные по поводу инфильтрирующей протоковой карциномы (два образца) или DCIS (три образца). Гистологическим признаком аденоза канальцев было беспорядочное разрастание удлиненных канальцев, которые не были скученными, узкими, а иногда и ветвящимися. Не было дольчатого расположения или, в лучшем случае, нечеткой дольчатой группировки, при этом некоторые канальцы часто заходили в жир. Канальцы содержали базофильный или гранулярный эозинофильный секрет.Строма была от склеротической до отечной. Канальцы были выстланы мягкими на вид протоковыми клетками и окружены интактным миоэпителиальным слоем — феномен, хорошо выявленный с помощью иммуноокрашивания на мышечно-специфический актин (HHF-35) или белок S-100.
В литературе нет формального описания этого состояния. Мы сообщаем о результатах шести образцов от пяти пациентов (один с двусторонним заболеванием), в том числе трех, которые показали канцеризацию внутрипротоковой карциномой (DCIS).Возраст пациентов от 40 до 82 лет. У одного пациента опухоль груди составляла 3 см, а у других были обнаружены образцы, удаленные по поводу инфильтрирующей протоковой карциномы (два образца) или DCIS (три образца). Гистологическим признаком аденоза канальцев было беспорядочное разрастание удлиненных канальцев, которые не были скученными, узкими, а иногда и ветвящимися. Не было дольчатого расположения или, в лучшем случае, нечеткой дольчатой группировки, при этом некоторые канальцы часто заходили в жир. Канальцы содержали базофильный или гранулярный эозинофильный секрет.Строма была от склеротической до отечной. Канальцы были выстланы мягкими на вид протоковыми клетками и окружены интактным миоэпителиальным слоем — феномен, хорошо выявленный с помощью иммуноокрашивания на мышечно-специфический актин (HHF-35) или белок S-100. В трех образцах канальцевый аденоз был поражен некомедонией DCIS, создавая картину, сильно имитирующую инфильтрирующую карциному; природа карциномы in situ была подтверждена иммунореактивностью актина в остаточном миоэпителии, а также наличием в непосредственной близости архитектурно подобного канальцевого аденоза.Тубулярный аденоз демонстрирует инфильтративный рост, аналогичный микрогландулярному аденозу и аденомиоэпителиальному аденозу, но он отличается от них встречно-гребенчатой конфигурацией канальцев, а также отличается от микрогландулярного аденоза наличием миоэпителия. Тубулярный аденоз можно отличить от склерозирующего аденоза по отсутствию очевидной дольчатой архитектуры или завитушек, а также по более широкому разделению канальцев. Тубулярный аденоз сам по себе является доброкачественным поражением, но еще предстоит определить, имеет ли он предраковый потенциал.Важность распознавания этой сущности заключается в том, что ее можно ошибочно принять за инвазивную карциному, особенно на интраоперационной замороженной секции или когда поражение поражено раком DCIS.
В трех образцах канальцевый аденоз был поражен некомедонией DCIS, создавая картину, сильно имитирующую инфильтрирующую карциному; природа карциномы in situ была подтверждена иммунореактивностью актина в остаточном миоэпителии, а также наличием в непосредственной близости архитектурно подобного канальцевого аденоза.Тубулярный аденоз демонстрирует инфильтративный рост, аналогичный микрогландулярному аденозу и аденомиоэпителиальному аденозу, но он отличается от них встречно-гребенчатой конфигурацией канальцев, а также отличается от микрогландулярного аденоза наличием миоэпителия. Тубулярный аденоз можно отличить от склерозирующего аденоза по отсутствию очевидной дольчатой архитектуры или завитушек, а также по более широкому разделению канальцев. Тубулярный аденоз сам по себе является доброкачественным поражением, но еще предстоит определить, имеет ли он предраковый потенциал.Важность распознавания этой сущности заключается в том, что ее можно ошибочно принять за инвазивную карциному, особенно на интраоперационной замороженной секции или когда поражение поражено раком DCIS.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie. Вам необходимо сбросить настройки вашего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались.
Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.

- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie. Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie.Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу. Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файлах cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в cookie-файлах может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта. Например, сайт не может определить ваше имя электронной почты, пока вы не введете его. Разрешение веб-сайту создавать файлы cookie не дает этому или любому другому сайту доступа к остальной части вашего компьютера, и только сайт, который создал файл cookie, может его прочитать.
Доброкачественные заболевания груди
Циклическая боль
Большинство женщин в какой-то момент своей жизни испытали боль в груди. Обычно боль связана с гормональными колебаниями менструального цикла, развивается во второй половине месячного цикла и усиливается за несколько дней до начала менструации. Это известно как циклическая боль в груди, и обычно она снова проходит через несколько дней после менструации.
Циклическая боль в груди обычно возникает в обеих грудях, особенно в верхней внешней области, где находится наибольшая концентрация железистой ткани груди. Боль часто бывает тупой, тяжелой или ноющей, а иногда грудь может казаться опухшей и «бугристой».
Часто боль слабая, и до тех пор, пока нет других симптомов, лечение не требуется.Многие женщины обеспокоены тем, что боль может быть признаком основного рака, поэтому достаточно уверенности после клинического обследования груди. Сама по себе боль обычно не является признаком рака груди.
Ношение поддерживающего, хорошо подогнанного бюстгальтера без косточки в течение дня и, если необходимо, ночью, как правило, приносит некоторое облегчение. Во время тренировок следует использовать подходящий спортивный бюстгальтер.При умеренной боли могут помочь безрецептурные лекарства, такие как парацетамол или ибупрофен. Втирать в кожу противовоспалительные гели могут немного облегчить состояние. Если боль более сильная, следует вести дневник боли в течение одного-двух месяцев, чтобы помочь врачам увидеть, есть ли закономерности боли или триггеры, которых можно было бы избежать, прежде чем рассматривать возможность использования рецептурных препаратов.
Оральные контрацептивы, ЗГТ и некоторые антидепрессанты могут усилить боль в груди, поэтому обсудите это со своим врачом.Некоторым женщинам удается с успехом использовать масло примулы вечерней или масло звездоцвета в течение нескольких месяцев. Это может изменить баланс жирных кислот в организме, хотя клинические испытания явно не доказали, что это полезно.
Нециклическая боль в груди
Характер этой боли не имеет отношения к менструальному циклу. Он может присутствовать постоянно или приходить и уходить. Он может быть ограничен определенной областью или ощущаться на одной или обеих грудях, и чаще встречается у женщин старше 40 лет.
Причины:
- Боль в ткани груди иногда может возникать без какой-либо очевидной причины или основного отклонения.
- Указанная боль. Иногда боль, ощущаемая в груди, возникает где-то еще. Направленная боль в грудной стенке довольно распространена и может быть связана с травмой, растяжением мышц после многократных упражнений на верхнюю часть тела, инфекцией грудной клетки или реберно-хондрозом (синдром Титце). Костохондрит — это воспаление хряща грудной клетки, обычно в области прикрепления верхних ребер к грудины (грудины).Боль в груди также может исходить от шеи.
- Беременность. На ранних сроках беременности грудь часто набухает и становится болезненной. У некоторых женщин кормление грудью также может вызывать боль.
- Мастит. Это воспаление ткани груди, обычно вызванное инфекцией и чаще всего связанное с лактацией.
- Большая, отвисшая грудь может вызвать растяжение поддерживающих связок и причинить боль.
- Большие кисты груди могут вызывать боль, и для облегчения их может потребоваться дренирование.
Критерии выявления остаточных опухолей после неоадъювантной химиотерапии рака молочной железы: исследование магнитно-резонансной томографии
Пациенты
В этом исследовании оценивали МРТ в ретроспективной популяции и применяли полученные критерии в когорте проспективного пилотного исследования. Это исследование было одобрено институциональным наблюдательным советом Национального онкологического центра (NCC2017-0141, NCC2019-0276). Для ретроспективного анализа требование письменного информированного согласия было отклонено институциональным наблюдательным советом Национального онкологического центра.С ноября 2015 года по март 2019 года мы выявили 574 подходящих пациента, у которых был диагностирован односторонний инвазивный рак груди II или III стадии и которые перенесли операцию после завершения NAC. Из них 284 пациента были исключены по следующим причинам: подтип просвета (n = 230, HR + HER2-), сомнительный статус HER2 (n = 19), отсутствие МРТ после завершения NAC (n = 25) и рецидив молочной железы. рак (n = 10). Наконец, 290 пациентов составили ретроспективное исследование.
Проспективное пилотное исследование было разработано для применения предварительных диагностических критериев МРТ и определения любой дополнительной ценности предоперационной биопсии иглы (биопсии иглы после NAC и перед операцией) для обнаружения остаточной опухоли.Для этой предполагаемой части было получено письменное информированное согласие от всех участников. С июля 2017 г. по май 2018 г. в проспективное пилотное исследование были включены 15 пациентов. МРТ до и после НАК были обязательными. Пациенты могли выбирать, проходить ли дооперационную игольную биопсию. Пациентам была выполнена биопсия иглой 14 калибра под ультразвуковым контролем в ложе опухоли после завершения NAC. Данные МРТ, УЗИ и маммографии до и после лечения были всесторонне проанализированы для выбора наиболее подходящего места для биопсии.Один из двух опытных рентгенологов получил от четырех до шести ядер ткани. Пациенты были прооперированы в течение 2 недель с момента проведения предоперационной пункционной биопсии. Данные этих пациентов не были включены в ретроспективный анализ.
Анализ клинических и гистопатологических данных
Были изучены медицинские записи, включая возраст пациента, клиническую стадию TNM до лечения, режим NAC и записи об операции. Первоначальный диагноз рака груди был основан на биопсии стержневой иглы под контролем УЗИ.Стандартные гистопатологические отчеты включали гистологический тип и степень опухоли. Образцы биопсии иглы перед лечением использовались для иммуногистохимической оценки и группировки подтипов. Отрицательный статус рецептора эстрогена или прогестерона был определен как менее 1% иммунореактивных клеток, соответственно 24 . Положительность HER2 была определена как окрашивание мембраны на 3+, тогда как 1+ и 0 были определены как HER2-отрицательные. Амплификацию гена с использованием флуоресцентной гибридизации in situ или двухцветной серебряной гибридизации in situ проводили, когда оценка была неоднозначной (2+).Опухоли были разделены на три подтипа следующим образом: HR-HER2- (TN), HR-HER2 + и HR + HER2 +. Системное лечение назначалось по усмотрению врача. Патология после хирургического иссечения была эталоном для анализа. Мы определили pCR молочной железы как гистопатологическое отсутствие инвазивной опухоли в удаленных образцах молочной железы независимо от оставшихся повреждений in situ (ypT0 / is) 25 .
Получение и анализ МРТ
Были использованы следующие три сканера МРТ со специальными катушками на поверхности груди и пациентом в положении лежа: Signa HDxt 3.0 T (GE Healthcare, Милуоки, Висконсин), Achieva 3.0 T TX (Philips N.V., Эйндховен, Нидерланды) и Ingenia 3.0 T (Philips N.V.) 22 . Протоколы МРТ состояли из следующих последовательностей: Т2-взвешенная последовательность с аксиальным подавлением жира; динамическая последовательность Т1-взвешенной последовательности с аксиальным подавлением жира до и через 90, 180, 270 и 360 секунд после внутривенной инъекции гадотериновой кислоты (0,2 мл / кг веса тела, Dotarem; Guerbet, Aulnay-sous-Bois, France). Толщина среза T1-взвешенных изображений составляла 2 мм.Проекционные изображения с вычитанием и максимальной интенсивностью были созданы из динамической серии. Средний интервал между МРТ после NAC и операцией составлял 4 дня (от 0 до 26 дней).
Все изображения были просмотрены рентгенологом груди с 7-летним опытом. Радиолог не знал клинико-патологической информации, за исключением диагноза рака груди. Когда оценивали МРТ после НАК, МРТ до НАК и другие визуализационные исследования до НАК были проанализированы для сравнения. ДПЭ классифицировали как минимальную, легкую, среднюю и выраженную степень 26 .Размер поражения и интенсивность сигнала (SI) измеряли на ранних (первая фаза, 90 с после введения контрастного вещества) и поздних (последняя фаза, 360 с после инъекции контрастного вещества) постконтрастных T1-взвешенных изображениях. Размер поражения определялся как максимальный диаметр усиливающегося поражения. Размер был описан как 0 см, если не было поражения с контрастным усилением. Определение паренхиматозного SER между поражением и фоном было небольшой модификацией метода, использованного Kim et al. 15 . SER был определен как SI поражения, деленный на SI нормальной паренхимы контралатеральной груди.Две представляющие интерес круглые области со средним диаметром 2,2 мм (диапазон от 1,8 до 3,1 мм) были нарисованы вручную, чтобы включить наиболее активную часть опухоли и нормальную паренхиму. Когда усиливающееся поражение исчезло после NAC, SI поражения измеряли на участке исходной опухоли. Размер поражения и SER на изображениях ранней и поздней фазы определялись как ранний размер, поздний размер, ранний SER и поздний SER, соответственно.
Статистический анализ
Статистический анализ проводился с использованием SAS версии 9.4 (SAS Institute Inc., Кэри, Северная Каролина, США) и программное обеспечение R, версия 3.6.2 (проект R для статистических вычислений). Независимый t-критерий, критерий суммы рангов Вилкоксона, точный критерий Фишера или критерий хи-квадрат Пирсона использовались для сравнения между пациентами с pCR и без pCR, в зависимости от ситуации. Кривые рабочих характеристик приемника были построены в соответствии с размером поражения и SER на ранней и поздней фазах. Различия в AUC сравнивали с использованием метода Делонга. Были рассчитаны несколько параметров диагностической эффективности для идентификации остаточной опухоли, включая чувствительность, специфичность, точность, положительную прогностическую ценность (PPV) и NPV.Значения были получены в общей популяции и в подгруппах на основе иммуногистохимии. Значение p <0,05 считалось статистически значимым.
Пятнадцать пациентов соответствовали критериям проспективной оценки. Поскольку нашей основной задачей было выявление пациентов, которые могут безопасно пропустить операцию, требовались высокая чувствительность для обнаружения остаточных повреждений и высокий NPV (вероятность того, что пациенты с rCR действительно достигают pCR). Поэтому мы устанавливаем максимальные значения МРТ как точки отсечения, которые показывают более 90% чувствительности и NPV в этом исследовании.
Этическое разрешение
Все процедуры, выполненные в исследованиях с участием людей, соответствовали с этическими стандартами институционального исследовательского комитета Национального онкологического центра (IRB №: NCC2017-0141, NCC2019-0276) и с Хельсинкской декларацией 1964 года и более поздними поправками к ней или сопоставимыми этическими стандартами.
|
Карцинома in situ, вовлекающая склерозирующий аденоз при основной биопсии: диагностические жемчужины, помогающие практикующему врачу и предотвращающие чрезмерное лечение
Интерпретация биопсии стержневой иглой — надежный метод для сортировки маммографических аномалий.Однако диагностика DCIS или дольчатой неоплазии, включающей склерозирующее поражение при основной биопсии, может представлять сложные диагностические проблемы и часто может быть перепутана с инвазивной карциномой, что приводит к чрезмерному лечению, включая неправильное назначение химиотерапии или более обширное хирургическое вмешательство. Однако, когда кто-то знаком с этой диагностической ловушкой, диагноз становится намного более простым, и в большинстве случаев иммуногистохимические окрашивания не требуются для подтверждения диагноза.
Обзор английской литературы выявил четыре отчета об отдельных случаях и четыре отчета о сериях случаев, в целом описывающих 39 случаев DCIS и / или LN с участием SA. Наша серия случаев добавляет к литературе 31 дополнительный случай. В первой описанной серии из шести случаев LCIS с участием SA [1] Fechner et al. обнаружили, что архитектура поражения с помощью оценки с низким увеличением была ключом к правильному диагнозу, отметив, что инвазивная карцинома не должна иметь общей организационной структуры.Мы также обнаружили, что оценка с низким энергопотреблением является наиболее полезным признаком того, что мы имеем дело с SA. Склерозирующие поражения сохраняют организованный, дольчатый архитектурный узор. Если кого-то беспокоит инвазивная карцинома, но поражение сохраняет дольчатую архитектуру при низкой мощности, следует тщательно рассмотреть возможность DCIS / LN с участием SA.
В более поздней серии случаев, которые включали как протоковые, так и дольчатые случаи [2], Rasbridge et al. прокомментировал, что дольчатую архитектуру иногда трудно полностью оценить из-за искажения как SA, так и протоковой или дольчатой неоплазии, и что полезны как иммуногистохимические окрашивания, так и сравнение с соседним аденозом, не связанным с протоковой или дольчатой неоплазией.Мы также обнаружили, что лобулярную архитектуру иногда трудно оценить при основной биопсии, особенно если поражение, вызывающее озабоченность, находится на краях центральной биопсии. Один чрезвычайно полезный ключ в диагностике этих случаев — наличие SA, не вовлеченной в неоплазию, на других участках биопсии. Эта функция была обнаружена почти во всех случаях и обеспечивала обнадеживающий «внутренний контроль» процесса сравнения. Это открытие также является доказательством того, что в груди происходит склерозирующий процесс.Еще одна полезная подсказка возникает, когда неопластический процесс не полностью заполняет склерозирующее поражение. Когда это происходит, периферия дольки обычно показывает узнаваемую гистологию обычного склерозирующего поражения. По нашему опыту, если это открытие будет замечено, вторжение очень маловероятно.
В сложных случаях можно использовать иммуногистохимическое окрашивание на миоэпителиальные маркеры. Например, в некоторых из наших случаев наблюдались случайные единичные неопластические клетки, окруженные миоэпителиальными клетками (идентифицированными в центре дольки).В этих случаях следует заказывать подтверждающие миоэпителиальные маркеры, чтобы исключить инвазивную карциному. Другой случай, когда следует учитывать иммуногистохимические пятна, — это когда склерозирующее поражение связано с плотным воспалительным фоном. В этих случаях и миоэпителиальные маркеры, и окраска панцитокератина могут быть полезны для подтверждения диагноза карциномы in situ.
В меньшей серии смешанных случаев [3], Eusebi et al. отметили, что наличие PAS-положительной базальной пластинки и миоэпителиальных клеток было полезным дополнением к оценке с низким увеличением.Мы также отметили, что присутствие миоэпителиальных клеток по крайней мере в некоторых частях поражения было полезным признаком. Часто миоэпителиальные клетки тонкие или истонченные и не видны с первого взгляда. Может потребоваться фокусировка вверх и вниз на плоскости ткани (или иммуногистохимических пятнах).
Конечно, причина того, что эти поражения так важно учитывать, — это реальная возможность спутать их с инвазивной карциномой. В смешанной серии случаев [3], проведенной Eusebi et al., Двое пациентов подверглись мастэктомии, потому что им изначально был поставлен диагноз инвазивной карциномы путем замороженного разреза.Другие отчеты об отдельных случаях [4,5,6,7] были примечательны случаем LCIS / SA, который первоначально назывался инвазивной карциномой при биопсии. Некоторые из наших случаев продемонстрировали характеристики, которые обычно можно рассматривать как связанные с инвазивным процессом, если общие архитектурные ключи не распознаются. Десмоплазия наблюдалась в 19,4% случаев, которые, насколько нам известно, никогда не описывались в связи с этими поражениями. Кроме того, отдельные клетки, окруженные тонкими аттенуированными миоэпителиальными клетками, также присутствовали в центре склерозирующего поражения у 19.4% случаев. Во всех случаях внимание к другим критериям помогало предотвратить ошибочный диагноз, основанный на одной характеристике.
Данные о последующих действиях были предоставлены для некоторых из предыдущих тематических исследований. В шести случаях LCIS с участием SA [1] Fechner et al. обнаружили, что единственной инвазивной карциномой была случайная канальцевая карцинома, которая была расположена вдали от областей SA. В более поздней серии случаев, включающей как протоковые, так и дольчатые случаи [2], Rasbridge et al. не предоставили последующего наблюдения за пациентом, но отметили, что в трех случаях были небольшие очаги инвазивной карциномы в дополнение к протоковой или дольчатой неоплазии с участием SA.В смешанной серии случаев [3], проведенной Eusebi et al., Все пациенты были живы и здоровы после квадрантэктомии или мастэктомии в течение периода наблюдения от 23 месяцев до 10 лет. В небольшой серии смешанных случаев [8] Oberman et al. отдельные случаи DCIS / LCIS, которые проявлялись исключительно при склерозирующем аденозе, при отсутствии карциномы in situ за пределами склерозирующего поражения. Восемь пациентов наблюдались в среднем в течение 3 лет, и они были живы и здоровы. Как и ожидалось, наши последующие данные также показывают, что эти пациенты чувствуют себя очень хорошо.Из пациентов с инвазивной протоковой карциномой при иссечении один пациент ждал 3 года между постановкой диагноза и иссечением, в промежуточный период применяя только альтернативные методы лечения. Единственным неожиданным случаем инвазивной карциномы при последующем хирургическом наблюдении был очаг рака диаметром 1,8 мм, который был преимущественно канальцевого типа, и пациент был жив и здоров в течение 11 лет с момента постановки диагноза. Все пациенты с LCIS живы и здоровы (за исключением двух пациентов, у которых в анамнезе была первичная карцинома легких).Несмотря на известную повышенную частоту инвазивной карциномы у этих пациентов, ни у одного из пациентов с LCIS с участием SA, которые перенесли операцию, не было инвазивной карциномы в их иссечениях.
Ранее сообщалось о случаях 21 дольчатой, 15 протоковой и 3 комбинированных протоковой / дольчатой неоплазии. В наших случаях было обнаружено очень небольшое преобладание дольки (19 дольчатых, 12 протоковых), взаимосвязь, также описанная Кернером [9]. Можно было ожидать, что, поскольку склерозирующий аденоз является эстроген-зависимым лобулоцентрическим процессом, частота ассоциированной лобулярной неоплазии будет намного выше, но это не было продемонстрировано.Следует проявлять осторожность, чтобы не допустить, что низкосортная карцинома in situ, включающая склерозирующий аденоз, является лобулярной карциномой, поскольку канцеризация протоков встречается почти так же часто. Полезно оценить образование вторичного просвета (даже при аденозе) и поляризацию клеток. Окрашивание E-кадгерином может использоваться, чтобы помочь различить эти два объекта.
Ограничения этого исследования включают небольшой размер выборки пациентов с этим необычным, но клинически значимым диагнозом. Еще одним ограничением исследования является отсутствие обширного последующего наблюдения, хотя среди пациентов с DCIS, перенесших иссечение, 90% имели DCIS или DCIS с микроинвазией.Ограниченное количество случаев позволяет только описательное сравнение гистологии. Используя описательную статистику, три основных признака (лобулоцентрический узор, видимость миоэпителиальных клеток и отдельные области склерозирующего аденоза) статистически встречаются чаще, чем ожидалось случайным образом. Интерпретация маммографических аномалий с помощью стержневой биопсии является надежным методом оценки, и диагносты должны поддерживать широкий дифференциальный диагноз, который включает имитаторы инвазивной карциномы, чтобы предотвратить чрезмерный диагноз и чрезмерное лечение.
Радиологический вид и эффективность биопсии стержневой иглой
Склерозирующий аденоз груди • v
сегментарно-линейный, линейный или нерегулярный
Наблюдалосьпаттернов ветвления.
Фокальная архитектурная дисторсия и
лучевых склерозирующих поражений на мамографии
в основном связаны с
злокачественными новообразованиями. Склерозирующий аденоз, жировой некроз
, лучевые рубцы и хирургические рубцы
— это доброкачественные образования, в которых могут быть видны
этих спикулированных поражений.
Franquet et al. (16) обнаружили, что центральные части этих поражений были ra-
диоптрий в случаях злокачественных новообразований и на
менее радиоплотных или рентгенопрозрачных в более
очагах поражения. Однако в нескольких других исследованиях
(17, 18) сообщается, что этот результат
ненадежен для дифференциального диагноза
. Биопсия — единственный метод
, который может использоваться для дифференциального диагноза
архитектурного искажения
из-за большого совпадения между
доброкачественных и злокачественных образований.В нашем исследовании
было восемь поражений, которые
представляли как архитектурные искажения,
, три из которых были случаями чистого скле-
розового аденоза.
Роль ультразвукового исследования
в диагностике и описании поражений в
чрезвычайно плотных молочных железах (поскольку диагностика
массового поражения практически невозможна с помощью маммографии
) хорошо известна.
Фокусное акустическое затенение
описывается как фокальное затенение без массового поражения
на УЗИ.Поражение
должно быть видно по крайней мере в двух звуковых плоскостях ультра-
, и конфигурация поражения
должна быть одинаковой, когда пациент
находится в разных положениях. Фокальное акустическое затенение
— редкая, но полезная находка
для радиолога, а также
, описанная Gunhan-Bilgen et al. (9).
По нашему опыту, очаговая акустическая тень
не является специфическим критерием для
склерозирующего аденоза, поскольку эта находка может наблюдаться при различных доброкачественных
и злокачественных заболеваниях груди.
Согласно Stavros (19), различные
результатов ультразвукового исследования могут сопровождать
склерозирующий аденоз.
Ультрасонографически определяемые очаги
видны, когда диаметр конечной протоковой дольчатой единицы ex-
превышает 5 мм. Повреждения могут быть обнаружены как
микролобулированных, угловатых или спикулированных
массовых поражений. Опухолевый аденоз
может быть неопределенным из-за периферической фиброзной ткани
или может быть очевидным, если округление
округляется изоэхогенной жировой тканью.Ставрос
рекомендует использовать голосовой фремитус
, чтобы различать схожие эхогенности
, которые неотличимы друг от друга в
изоэхогенной области, открытие, которое может быть
связано с несколькими доброкачественными или злокачественными
состояниями. Этот тип оценки
не проводился в нашем исследовании.
Среди 35 пациентов в этом исследовании
со склерозирующим аденозом в качестве дополнительного диагноза
наиболее частыми доброкачественными состояниями были фибро-
кистозные изменения, фиброаденома и
внутрипротоковая папиллома.Фиброаденома
и внутрипротоковая папиллома также были
наиболее частыми доброкачественными диагнозами в серии
, о которых сообщали Gill et al. (10).
Фиброаденомы называются «сложными броаденомами
», если они содержат очаг склеро-
единственного аденоза. Dupont et al. (20)
сообщили о 3,1-кратном увеличении риска злокачественной опухоли у пациентов с фиброаденомой com-
plex. Клинико-клиническое наблюдение после биопсии
У этих пациентов не должно быть препятствий для наблюдения
и радиологического наблюдения.
Таким образом, склерозирующий аденоз — это доброкачественное состояние
, которое не имеет
каких-либо типичных признаков, помогающих в радиологической диагностике. Склерозирующий аденоз
может иногда имитировать in situ или инвазивную карциному
. Выбор методов биопсии
и постпроцедурный возраст очень важен из-за
гистопатологических вариаций тканей,
повышенной атипичной клеточности и
риска злокачественных новообразований.Насколько нам известно,
биопсий молочной железы часто выполняются
при поражениях BI-RADS 4, и
60–80% этих поражений фактически являются
доброкачественными поражениями (21). Следовательно, целью
биопсии должно быть получение
наилучшего образца поражения с помощью наименее инвазивного метода
. Биопсии стержневой иглой
должно быть достаточно, чтобы избежать пропуска возможных злокачественных изменений
.Тип биопсии, объем образца
и опыт оператора
могут повлиять на точность биопсии иглой
(21–24). Core nee-
биопсий dle может быть достаточным для диагностики
небольших спикулярных поражений
, таких как фокальные архитектурные искажения
или лучевые склерозирующие поражения (25, 26). В
этом исследовании все кластеры микрокальцификации —
уровня и большая часть очаговых архитектурных искажений
и спикулированные поражения
были хирургически иссечены после локализации проволоки иглой
, чтобы гарантировать адекватность образца
и предотвратить возможное
.проблемы, связанные с плохой локализацией.
Все образования, наиболее асимметричные помутнения
узлы и поражения с очаговым акустическим затенением
при ультразвуковом исследовании были взяты
при биопсии иглой. Во время наблюдения
ни одно из этих поражений не продемонстрировало никаких изменений, совместимых с
злокачественными новообразованиями, и повторных биопсий
не потребовалось.
Центральная игольная биопсия под визуальным контролем
груди — широко используемая процедура для диагностики новообразований или образований, обнаруженных при радиологической оценке
.Процедура обеспечивает надежные гистопатологические результаты
, а также является экономичной и минимально инвазивной на
.
В этом исследовании мы наблюдали 100% диагностическую точность биопсии иглой с сердечником 14 G
. Частота ложноотрицательных результатов при стержневой биопсии
варьируется от 0,3% до
3,2% (в среднем 2,8%) в литературе.
Процедуры локализации проводов имеют
аналогичных ложноотрицательных результатов (0% –8%; среднее значение
, 2%) (27–30).
Дальнейшая оценка в этих случаях была
, определенная в соответствии с коллективным
решением, принятым в ходе многопрофильных
личных встреч между хирургическим,
отделениями патологии и радиологии
в нашем учреждении. В результате нашего увеличенного опыта работы с этой технологией
, в настоящее время мы используем опсию с сердечником-иглой bi-
для кластеров микрокальцификации и
архитектурных искажений чаще, чем в прошлом.Наше исследование исключает возможность обобщения точности
биопсий стержневой иглой для диагностики
склерозирующего аденоза, потому что не все
пациентов были отобраны этим методом.
Тем не менее, мы можем констатировать, что биопсия стержневой иглой
минимизирует потребность в хирургическом удалении склерозирующего аденоза у отдельных пациентов. Биопсия иглой
может быть первым шагом к диагностике склерозирующего аденоза
.Как и в случае
других диагностических ситуаций, если злокачественная
не может быть исключена, если имеется
несоответствий между рентгенологическими и гистопатологическими данными
или если присутствуют атипичные
каловых клеток, следующей должна быть эксцизионная биопсия
. шаг для завершения
оценки.
Раскрытие конфликта интересов
Авторы заявляют об отсутствии конфликта интересов.
Ссылки
1. Tavassoli FA.Патология груди.
Норуолк: Эпплтон и Ланге, 1992; 93–
97.
2. Нильсен Н.С., Нильсен ББ. Маммографические
признаки склерозирующего аденоза, представляющие
как опухоль. Clin Radiol 1986; 37: 371–
373.
3. Расбридж С.А., Миллис Р.Р. Карцинома in situ
, вовлекающая склерозирующий аденоз: имитация инвазивной карциномы груди
. Гистопатология
1995; 27: 269–273.



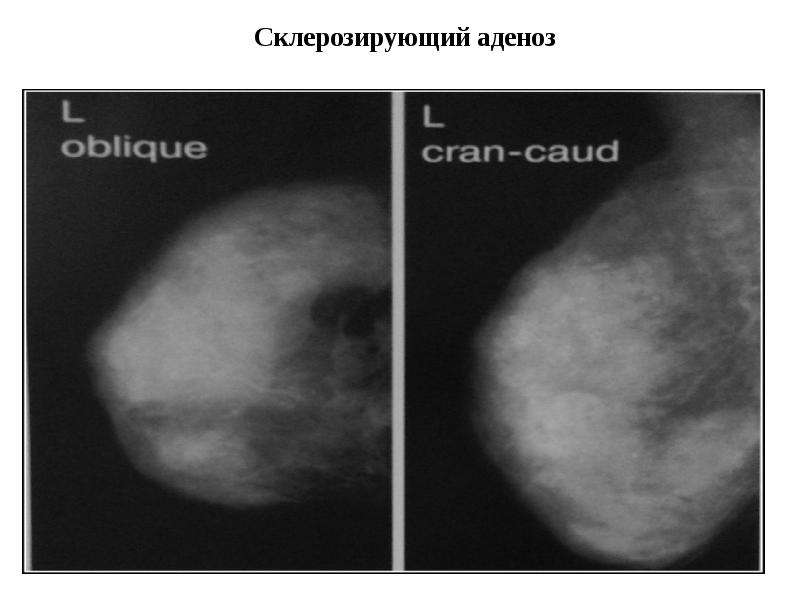

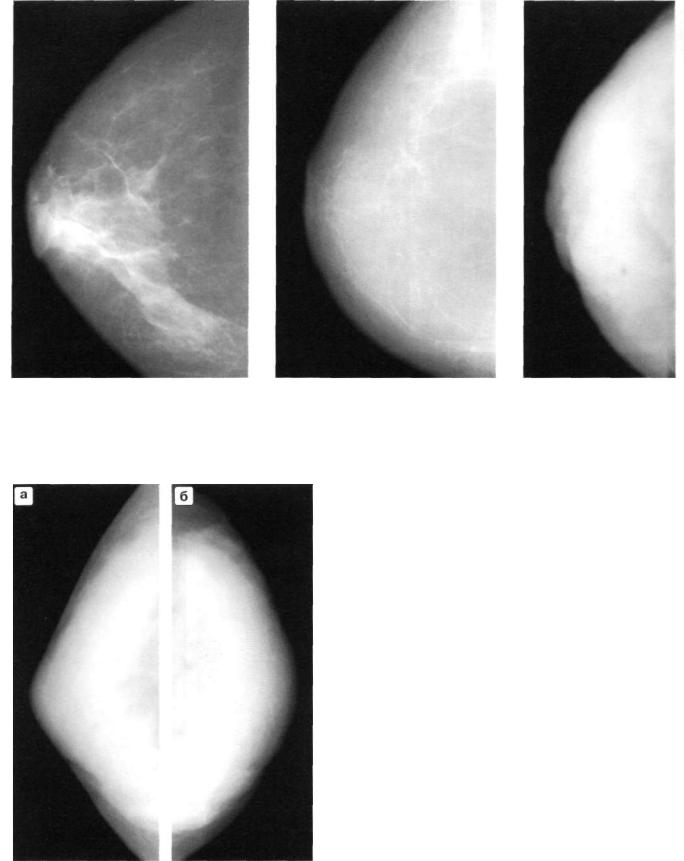 Преимущественно рекомендуется прием оральных контрацептивов или гестагенных препаратов. В среднем положительные результаты отмечаются спустя 50-60 дней лечения.
Преимущественно рекомендуется прием оральных контрацептивов или гестагенных препаратов. В среднем положительные результаты отмечаются спустя 50-60 дней лечения.

 Для этого необходимо внимательно ощупать грудь по всей окружности, а потом более внимательно – в каждом квадранте.
Для этого необходимо внимательно ощупать грудь по всей окружности, а потом более внимательно – в каждом квадранте.
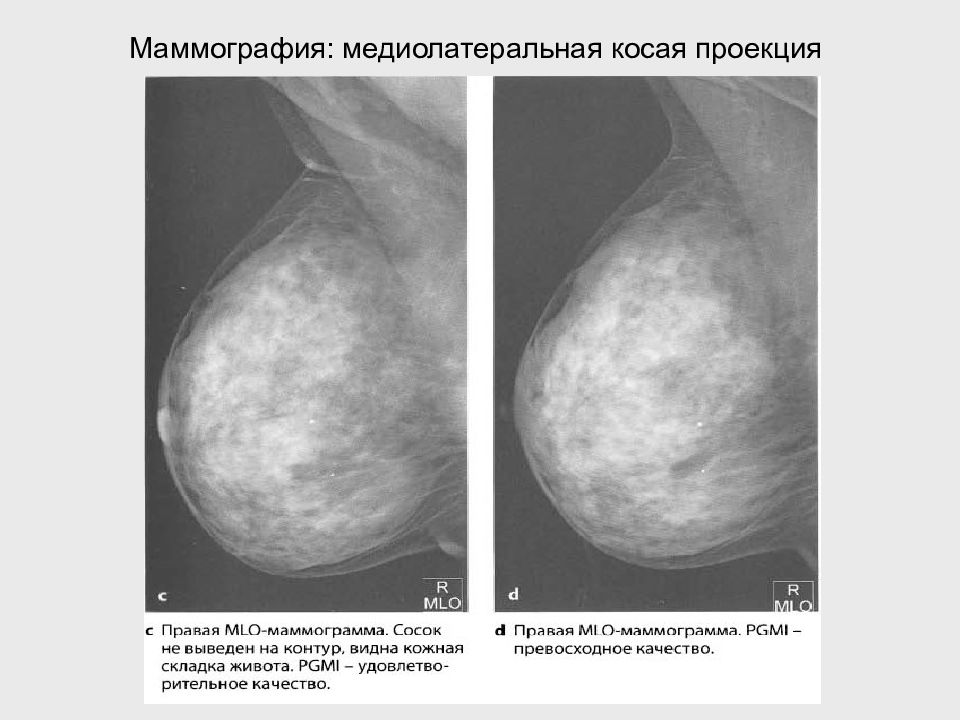 Новообразования характеризуются четкой локализацией, дольчатой структурой. Хорошо ощущаются во время пальпации . Наблюдается рост подмышечных лимфоузлов. При прощупывании уплотнения очень болезненны.
Новообразования характеризуются четкой локализацией, дольчатой структурой. Хорошо ощущаются во время пальпации . Наблюдается рост подмышечных лимфоузлов. При прощупывании уплотнения очень болезненны.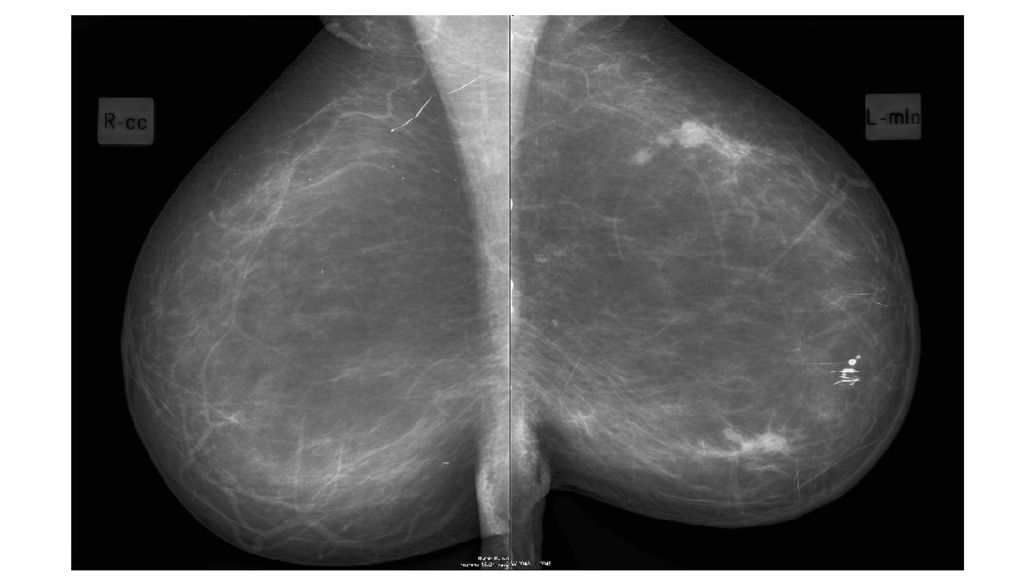 Патология характеризуется локальной периодичной болью в области желез. Прощупываются мелкие узелки на правой и левой железах, очаг эластичный, довольно мелкий. Выделения из сосков отсутствуют.
Патология характеризуется локальной периодичной болью в области желез. Прощупываются мелкие узелки на правой и левой железах, очаг эластичный, довольно мелкий. Выделения из сосков отсутствуют.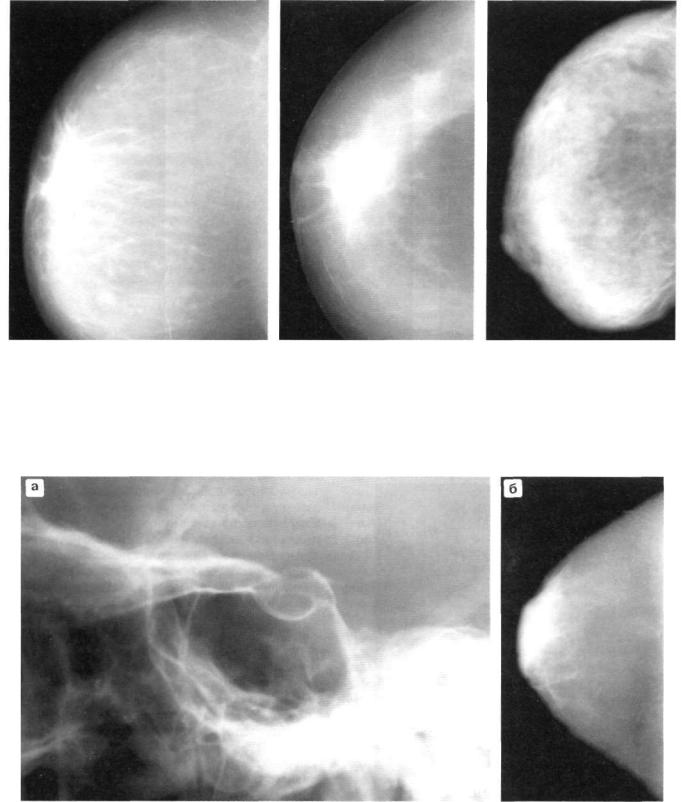 Эта форма аденоза болезненна, симптомы четко выражены.
Эта форма аденоза болезненна, симптомы четко выражены.
