НЕ-4 (онкомаркер яичников) – Медицинский центр Протос
HE4 (от англ. human epididymis protein 4) – небольшой протеин относящийся к семейству белков, содержащих 4 дисульфидных связи в коровой части. Первоначально он был обнаружен в дистальных отделах эпителия протока придатка яичника (эпидидимального протока), откуда и произошло название человеческий эпидидимальный протеин. Впоследствии стало известно, что HE4 также образуется во многих других тканях (железистый эпителий молочной железы, женской и мужской репродуктивных систем, дистальных почечных канальцев, толстой кишки, слюнных желез). Физиологическая роль HE4 до конца не ясна, вероятно, он необходим для нормального функционирования эпителия. Кроме того, он поддерживает систему врождённого иммунитета дыхательного тракта и ротовой полости.
Усиленный синтез HE4 характерен для некоторых злокачественных опухолей (мезотелиомы, рака легкого, почек, молочной железы, эндометрия, злокачественных образований желудочно-кишечного тракта), что позволяет использовать этот белок в качестве онкомаркера.
- HE4 для дифференциальной диагностики образований малого таза.
Одной из наиболее сложных диагностических задач является дифференциальная диагностика доброкачественных и злокачественных образований малого таза. Часто для этого используется онкомаркер CA-125. Существенным недостатком CA-125 является его недостаточная специфичность, так как он может быть повышен и при доброкачественных заболеваниях. По сравнению с CA-125 онкомаркер HE4 реже повышен при доброкачественных новообразованиях (в 8 % случаев против 29 %). СА 125 также повышен в 67 % случаев эндометриоза, тогда как HE4 – только в 3 %. Таким образом, преимуществом HE4 является более высокая специфичность в отношении злокачественных образований.
При использовании комбинации онкомаркеров СА 125 и HE4 удается более точно дифференцировать злокачественные и доброкачественные образования малого таза, чем при использовании каждого маркера в отдельности. Комбинация этих онкомаркеров в сочетании с менопаузальным статусом пациентки используется в алгоритме риска рака яичников ROMA.
Комбинация этих онкомаркеров в сочетании с менопаузальным статусом пациентки используется в алгоритме риска рака яичников ROMA.
- HE4 для скрининга рака яичников и эндометрия.
Показано, что HE4 может быть обнаружен в 32 % случаев рака яичника, отрицательных по СА 125 и, поэтому, дополняет СА 125.
HE4 входит в большинство панелей тестов, которые предлагается использовать для скрининга рака яичников. Наилучший результат показан при использовании комбинации HE4, CA-125, раково-эмбрионального антигена: комбинация этих онкомаркеров выявляет рак яичника на ранних стадиях с чувствительностью 86 % и специфичностью 98 %.
Важно подчеркнуть, что онкомаркер HE4, так же, как и онкомаркер CA-125, способен выявлять только злокачественные образования яичника эпителиального происхождения и не выявляет герминогенные опухоли или опухоли стромы полового тяжа.
В некоторых исследованиях также было показано, что HE4 может быть использован для скрининга рака эндометрия.
- HE4 для оценки прогноза рака яичников и эндометрия.
Повышенный уровень HE4 ассоциирован с более высокой степенью злокачественности и более выраженной стадией рака яичников по классификации FIGO. Высокий уровень HE4 чаще наблюдается при более агрессивных вариантах рака яичника и указывает на менее благоприятный прогноз.
Так же, как и при раке яичника, повышенный уровень HE4 ассоциирован с более агрессивным фенотипом рака эндометрия, а высокая концентрация этого онкомаркера говорит о плохом прогнозе заболевания.
- HE4 для контроля лечения и диагностики рецидива рака яичника и эндометрия.
Исследование на HE4 может быть использовано для оценки эффективности лечения. Так, концентрация HE4 существенно отличается у пациентов при постановке диагноза рака яичника и пациентов, достигших полной клинической ремиссии.
Анализ на HE4 также может применяться для диагностики рецидива рака яичника. Показано, что HE4 начинает определяться примерно за 4,5 месяца до возникновения клинических признаков рецидива этого заболевания. На этом основании анализ на HE4 используют для мониторинга эффективности лечения. В некоторых случаях повышение HE4 предшествует повышению CA-125. В одном из исследований показано, что онкомаркер HE4 способен выявлять рецидив рака яичника с чувствительностью 74 % и специфичностью 100 % при концентрации более 70 пикомоль/л. Использование комбинации онкомаркеров HE4 и CA-125 позволяет увеличить чувствительность до 76 %.
На этом основании анализ на HE4 используют для мониторинга эффективности лечения. В некоторых случаях повышение HE4 предшествует повышению CA-125. В одном из исследований показано, что онкомаркер HE4 способен выявлять рецидив рака яичника с чувствительностью 74 % и специфичностью 100 % при концентрации более 70 пикомоль/л. Использование комбинации онкомаркеров HE4 и CA-125 позволяет увеличить чувствительность до 76 %.
Анализ на рак яичников — онкомаркер СА-125
Диагностическое направление
Онкоскрининги
Общая характеристика
Антиген СА-125 – гликопротеин, который происходит из дериватов целомического эпителия тканей плода.СА-125 повышен у 80 % женщин с эпителиальным раком яичников. Однако, на первой стадии заболевания этот показатель увеличивается только 50% женщин. В ряде стран данный онкомаркер рекомендован для скрининга рака яичников (в комплексе с УЗИ) у женщин группы риска (с отягощенным семейным анамнезом по раку яичников и молочной железы, нерожавших, родивших первого ребенка (?35 лет), ранним менархе, принимавших гормональную терапию, воспалительными заболеваниями тазовых органов (PID), экстракорпоральной стимуляцией).
Показания для назначения
1. Мониторинг течения заболевания. 2. Доклиническая диагностика метастазирования и оценка эффективности проводимой терапии рака яичников. 3. Дифференциация злокачественного и доброкачественного процессов при новообразованиях в яичниках.
Маркер
Маркер рака яичников и его метастазов.
Клиническая значимость
1. Мониторинг терапии рака яичников. 2. Прогнозирование рецидива рака яичников.
Состав показателей:
Онкомаркер яичников СА-125
Метод:
Хемилюминесцентный иммуноанализ Диапазон измерений: 2-100000
Единица измерения: Единиц на миллилитр
Референтные значения:
ВозрастКомментарии
Выполнение возможно на биоматериалах:
Биологический материал
Условия доставки
Объем
Сыворотка
Условия доставки:
24 Час. при температуре от 2 до 8 градусов Цельсия
при температуре от 2 до 8 градусов Цельсия
Вакутейнер с разделительным гелем
Объем:
8.5 Миллилитров
Правила подготовки пациента
Стандартные условия: утром до 11. 00, натощак или перерыв не менее 6 часов после приема пищи (должна быть исключена жирная пища). Внимание: при наличии диагноза злокачественного заболевания сделать отметку в направлении.
00, натощак или перерыв не менее 6 часов после приема пищи (должна быть исключена жирная пища). Внимание: при наличии диагноза злокачественного заболевания сделать отметку в направлении.
Вы можете добавить данное исследование в корзину на этой странице
Интерференция:
- Не обнаружена.
- Не обнаружена.
Интерпретация:
- Эпителиальный рак яичников. Доброкачественные гинекологические опухоли, воспалительные процессы, с вовлечением придатков; опухоли желудочно-кишечного тракта; карцинома молочной железы, бронхов.
 I триместр беременности, цирроз печени, хронический гепатит, панкреатит, аутоиммунные заболевания.
I триместр беременности, цирроз печени, хронический гепатит, панкреатит, аутоиммунные заболевания.
CA 125 II: исследования в лаборатории KDLmed
СА-125 – это высокомолекулярный гликопротеин, который обнаруживается на опухолевых клетках эпителия яичников, а также в норме в клетках эндометрия, брюшины, плевры, перикарда и яичек. Присуствие данного гликопротеина в крови в очень высоких концентрациях часто указывает на онкологическую трансформацию яичников и реже некоторых других органов и тканей (эндометрия, толстого кишечника, лёгкого, молочной, поджелудочной железы).
Синонимы русские
Углеводный антиген – 125, онкомаркер рака яичника.
Синонимы английские
CA 125 tumor marker, Cancer Antigen – 125.
Метод исследования
Иммунохемилюминесцентный анализ.
Единицы измерения
Ед/мл (единица на миллилитр).
Какой биоматериал можно использовать для исследования?
Венозную кровь.
Как правильно подготовиться к исследованию?
- Не курить в течение 30 минут до сдачи крови.
Общая информация об исследовании
CA 125 – это белок, присутствующий на поверхности большинства клеток раковой опухоли яичников. Значительное увеличение концентрации CA 125 указывает на рак яичников. Этот анализ иногда назначают пациенткам с наследственной предрасположенностью к раку яичников.
В норме СА-125 содержится в ткани эндометрия и в серозной и муцинозной жидкости матки. В кровоток он попадает, например, при менструации, эндометриозе, в первый триместр беременности. Само по себе наличие CA 125 не всегда указывает строго на онкологию яичников – незначительные количества CA 125 вырабатываются различными тканями организма, а также раковыми опухолями другой этиологии (эндометрия, желудочно-кишечного тракта, фаллопиевых труб, лёгких и желудочно-кишечного тракта). Кроме того, повышение уровня CA 125 в крови может быть связано с воспалением органов малого таза. В связи с невысокой специфичностью анализа на CA 125 целесообразно вместе с ним проводить и другие тесты на опухоль яичников – комплексное исследование делает диагностику максимально точной.
Кроме того, повышение уровня CA 125 в крови может быть связано с воспалением органов малого таза. В связи с невысокой специфичностью анализа на CA 125 целесообразно вместе с ним проводить и другие тесты на опухоль яичников – комплексное исследование делает диагностику максимально точной.
Не все виды опухоли яичников проявляются увеличением количества CA 125 в крови – повышенный уровень CA 125 обнаруживается приблизительно у 80 % женщин, больных раком яичников.
Если среди ближайших родственников пациентки были больные раком яичника, риск заболеть у неё возрастает.
Для чего используется анализ?
- Для диагностики рака яичников и для контроля за течением заболевания.
- Чтобы оценить эффективность терапии опухоли яичников.
- Для выявления рецидива рака яичников.
Когда назначается исследование?
- До начала лечения рака яичников (чтобы затем сравнить полученные результаты с результатами анализов, сделанных после лечения).

- При уже диагностированном раке яичников.
- После завершения терапии рака яичников.
Что означают результаты?
Референсные значения: 0 — 35 Ед/мл.
Снижение уровня CA 125 в крови во время терапии свидетельствует о её положительном эффекте.
Если уровень CA 125 возрастает и остаётся высоким, значит, опухоль не реагирует на лечение.
Нарастание уровня CA 125 после терапии может указывать на рецидив заболевания.
В исключительных случаях у пациенток с диагнозом «рак яичников» уровень CA 125 находится в пределах нормы. Это связано с тем, что опухоль не производит CA 125, так что он не является подходящим маркёром, используемым при лечении болезни в данном случае.
Также рекомендуется
Онкомаркеры в Израиле | Ранняя диагностика рака, цены
Анализ на онкомаркеры выполняется для ранней диагностики онкологических заболеваний. Рентген, УЗИ, МРТ выявляют патологию на поздних стадиях, когда опухоль уже развилась.
Рентген, УЗИ, МРТ выявляют патологию на поздних стадиях, когда опухоль уже развилась.
Новейшее оборудование и качественные реактивы, используемые в израильских клиниках, позволяют своевременно выявить онкологию, определить степень злокачественности, стадию новообразования.
Онкомаркеры – вещества, которые содержатся в организме здорового человека в минимальном количестве и резко повышаются при развитии опухолей и ряде других заболеваний.
Они бывают:
- специфические – повышаются при определенном виде новообразований и указывают на его злокачественность.
- неспецифические – повышаются при росте всех типов опухолей.
Технически сдать кровь на онкомаркеры в клиниках Израиля не сложно – для этого достаточно записаться на процедуру, согласовать время проведения исследования, условия оплаты, прийти в назначенный день для забора крови. Для анализа берут венозную кровь предплечья в объеме 5-6 мл.
Для анализа берут венозную кровь предплечья в объеме 5-6 мл.
В каких случаях необходим тест на онкомаркеры
Основными показаниями для назначения анализа являются следующие:
- первичная диагностика онкозаболеваний,
- наблюдение за прошедшими курс лечения пациентами (для выявления рецидива),
- выявление рака при невозможности провести биопсию.

Маркеры очень эффективны для определения рецидива онкозаболеваний до начала первых симптомов, что позволяет провести раннее лечение болезни.
Раково-эмбриональный антиген (РЭА)
Это комплексное белково-углеводное соединение, которое вырабатывается в процессе внутриутробного развития у плода и служит для соединения клеток с субстратами (клеточной адгезии). У взрослых людей РЭА в крови почти отсутствует (норма РЭА– от 0 до 5 нг/мл).
Повышение РЭА бывает при состояниях, не связанных с онкозаболеваниями:
- курение – возрастает в несколько раз;
- язвенный колит;
- язва желудка;
- болезни желчевыводящих путей;
- цирроз печени;
- панкреатит;
- гипотиреоидизм.

РЭА показан для мониторинга рецидива и определения степени злокачественности опухоли.
Получить программу лечения из нескольких клиник
Онкомаркер молочной железы (СА 15-3)
Маркер СА 15-3 – это аналог СА 27.29. Он синтезируется в здоровых клетках грудных желез. С возникновением рака синтез ускоряется. Повышение СА 15-3 может свидетельствовать об:
- эндометриозе;
- хронических воспалениях репродуктивных органов;
- гепатите;
- доброкачественных опухолях яичников и молочных желез.
Норма для СА 15-3: от 0 до 22 ЕД/мл.
ОРГАНЫ МАЛОГО ТАЗА
Онкомаркер поджелудочной железы (СА 19-9)
Маркер СА 19-9 обычно секретируют клетки эпителия в ЖКТ. Норма для взрослого человека СА 19-9: от 0 до 35 ЕД/мл.
СА 19-9 используют как маркер для мониторинга рецидивов у пациентов, прошедших лечение по поводу злокачественных онкопроцессов поджелудочной железы.
Онкомаркер яичников (СА 125)
СА 125 продуцируется мембранами клеток злокачественных неопластических процессов в яичниках. Норма для СА 125: от 0 до 35 ЕД/мл. Этот маркер используют для определения эффективности лечения рака яичников 2-4 стадий.
Помимо онкозаболеваний, СА 125 возрастает при:
- беременности;
- злокачественных опухолях эндометрия;
Онкомаркер желудка (СА 72-4)
Этот гликопротеид продуцируют клетки плода на этапе антенатального развития. Норма для СА 72-4: от 0 до 35 ЕД/мл.
Склонностью к активной выработке СА 72-4 обладают:
Бета-хорионический гонадотропин (Бета-ХГЧ)
ХГЧ вырабатывается клетками предшественника плаценты – трофобласта. Он нужен для стимуляции секреции прогестерона в организме беременной женщины. Норма ХГЧ для небеременных : от 0 до 5 нг/мл.
Норма ХГЧ для небеременных : от 0 до 5 нг/мл.
Увеличение бета-ХГЧ может говорить о:
- раке яичек;
- опухолях из тканей трофобласта;
- хорионкарциноме.
Альфа-фетопротеин (АФП)
АФП временно выполняет роль альбумина в крови плода и вырабатывается внутриутробно: изначально – желточным мешком (до 10-12 недель), позднее – печенью плода (с 20 недели). Норма АФП у взрослых: 0-5 нг/мл.
Изменения АФП контролируют при беременности на 20 неделе как маркер аномалий развития плода:
- при синдроме Дауна уровень АФП снижен;
- дефекты нервной трубки и омфалоцеле сопровождаются резким повышением АФП.
Повышение АФП у мужчин, женщин, не вынашивающих плод, и детей от 500 нг/мл может указывать на:
Простатический специфический агент (ПСА)
ПСА – онкомаркер, применяющийся для диагностики и наблюдения за течением аденомы (доброкачественной опухоли) и рака предстательной железы. Нормальные показатели ПСА в крови человека: 2.5-6.5 нг/мл (в зависимости от возраста). При выявление повышенных значений ПСА необходимо провести биопсию предстательной железы для уточнения диагноза.
Нормальные показатели ПСА в крови человека: 2.5-6.5 нг/мл (в зависимости от возраста). При выявление повышенных значений ПСА необходимо провести биопсию предстательной железы для уточнения диагноза.
Цены на определение онкомаркеров в Израиле
Анализ на онкомаркеры имеет различную стоимость в лабораториях разных клиник. На стоимость влияет квалификация лаборантов, репутация клиники или медцентра, реактивы и оборудование для проведения анализов.
| Процедура | Стоимость, $ |
| Анализ на онкомаркеры | 300-600 |
Отправить запрос в израильские онкоцентры
Вы получите программы лечения и стоимость из нескольких израильских клиник
СА-125
СА-125
Что такое CA-125?
CA-125 (Cancer Antigen 125) – особое биологическое вещество (белково-углеводный комплекс, гликопротеин), которое вырабатывается клетками, выстилающими брюшную полость, поверхность между поверхностью легких и ребрами (плевральная полость), а также клетками некоторых других органов. CA-125 используется в современной клинической практике в качестве опухолевого маркера (онкомаркера). Его повышение наиболее часто наблюдается у пациенток с опухолями яичников, маточных труб или брюшины. Определение концентрации CA-125 в крови вошло в клиническую практику в 1980-ых годах, когда исследователи обнаружили, что изменение его концентрации может отражать течение заболевания у пациенток со злокачественными новообразованиями яичников. Для анализа используется венозная кровь.
CA-125 используется в современной клинической практике в качестве опухолевого маркера (онкомаркера). Его повышение наиболее часто наблюдается у пациенток с опухолями яичников, маточных труб или брюшины. Определение концентрации CA-125 в крови вошло в клиническую практику в 1980-ых годах, когда исследователи обнаружили, что изменение его концентрации может отражать течение заболевания у пациенток со злокачественными новообразованиями яичников. Для анализа используется венозная кровь.
Как СА-125 попадает в кровь и где он образуется?
На фоне наличия злокачественной опухоли яичников происходит активное размножение раковых клеток, которые способы вырабатывать СА-125, кроме того, их наличие вызывает значительное раздражение ткани, выстилающей брюшную полость (брюшины), что также приводит к повышению концентрации СА-125. Необходимо отметить, что повышение концентрации данного онкомаркера также возможно при других злокачественных опухолях, например, раке легкого, молочной железы, желудочно-кишечного тракта.
Здоровые ткани тоже могут продуцировать СА-125, поэтому в качестве диагностически значимого уровня было выбрано значение его концентрации ≥35 Ед/мл. У 99% здоровых женщин концентрация СА-125 в крови ниже указанного значения. Колебания концентрации СА-125 в пределах нормальных значений (0-35 Ед/мл) не являются признаком наличия патологии. Повышение концентрации СА-125 отмечается у 85% пациенток с диагнозом рака яичников, при этом менее, чем у 1% пациенток без наличия опухоли выявляются высокие уровни этого маркера. Необходимо, отметить, что на ранних стадиях рака яичников концентрация СА-125 не выходит за пределы нормальных значений. Это означает, что нормальная концентрация СА-125 не исключает диагноз рака яичников.
Все опухоли обладают различной способностью вырабатывать СА-125. По этой причине наиболее полезна оценка не отдельных значений концентрации СА-125, а динамика изменений концентрации этого онкомаркера в процессе лечения.
Ложно-положительные результаты определения концентрации СА-125
Кроме того, концентрация этого маркера в крови может повышаться при доброкачественных опухолях яичников, а также заболеваниях, сопровождающихся воспалением в плевральной или брюшной полости. Это связано с тем, что в норме небольшое количество СА-125 вырабатывается здоровыми клетками, выстилающими эти полости. Раздражение брюшины или плевры (оболочки, выстилающие брюшную и плевральную полости) вследствие наличия воспаления, проведенной хирургической операции, травмы, или воздействия других факторов может приводить к повышению концентрации СА-125 в крови. Необходимо учитывать, что при определении концентрации СА-125 возможно получение ложноположительных результатов, что означает высокую концентрацию этого маркера в крови при отсутствии злокачественной опухоли. Такое может наблюдаться следующих заболеваниях:
- Инфекционные и воспалительные заболевания органов брюшной полости: дивертикулит, перитонит, туберкулез, панкреатит, а также воспалительные заболевания кишечника (язвенный колит, болезнь Крона) и другие инфекции;
- Заболевания печени;
- Недавно проведенная хирургическое вмешательство на органах брюшной полости;
- Доброкачественные заболевания женских половых органов, включая фиброиды, эндометриоз, поликистоз яичников и т.
 д., а также при беременности.
д., а также при беременности.
По этой причине повышение концентрации СА-125 не означает диагноза онкологического заболевания. Интерпретировать результаты исследования должен только лечащий врач. Диагноз рака яичников устаналивается только на основании результатов гистологического заключения, сделанного в ходе изучения послеоперационного материала (удаленного яичника и/или других органов, подозрительных в отношении вовлечения в опухолевый процесс).
Для чего используется определение концентрации СА-125?
В настоящее время определение концентрации СА-125 используется в процессе обследования пациенток с подозрением на рак яичников, в процессе лечения этого новообразования для оценки динамики течения болезни и эффективности проводимой терапии, а также после завершения лечения для выявления рецидивов заболевания:
1. Прогнозирование дальнейшего течения заболевания.
В ряде исследований было показано, что если концентрация СА-125 после проведенного лечения возвращается в нормальные пределы, это может означать более благоприятный прогноз течения болезни. Необходимо отметить, что, как и любые другие статистические данные, это применимо только в отношении больших групп пациентов. Невозможно предугадать течение болезни у отдельно взятого пациента.
Необходимо отметить, что, как и любые другие статистические данные, это применимо только в отношении больших групп пациентов. Невозможно предугадать течение болезни у отдельно взятого пациента.
2. Выявление рецидивов болезни после проведенного лечения.
Рак яичников – хроническое заболевание. К сожалению, после первоначально проведенного лечения у многих пациенток развиваются рецидивы болезни, которые могут потребовать повторного проведения химиотерапии или хирургического лечения. Для выявления рецидивов в процессе наблюдения за пациентками регулярно проводится определение концентрации СА-125 в крови. Как правило, возрастающая концентрация СА-125, особенно в тех случаях, когда это подтверждается в нескольких исследованиях, выполненных с интервалом в несколько недель, означает рецидив болезни, что может потребовать более тщательного обследования и/или решения о начале лечения.
Необходимо отметить, что в тех случаях, когда отсутствуют какие-либо симптомы болезни и маловероятно их скорое появление, повышение концентрации СА-125 не требует немедленного начала терапии, так как было показано, что раннее начало лечения не приводит к улучшению его результатов. Решение о необходимости начала лечения должен принимать лечащий врач с учетом пожеланий пациентки. Необходимо отметить, что не всегда повышение концентрации СА-125 на фоне лечения означает прогрессирование заболевания. У пациенток, прошедших лечение по поводу рака яичников, повышение концентрации СА-125 может наблюдаться по вышеуказанным причинам.
Решение о необходимости начала лечения должен принимать лечащий врач с учетом пожеланий пациентки. Необходимо отметить, что не всегда повышение концентрации СА-125 на фоне лечения означает прогрессирование заболевания. У пациенток, прошедших лечение по поводу рака яичников, повышение концентрации СА-125 может наблюдаться по вышеуказанным причинам.
3. Оценка течения болезни во время лечения.
СА-125 используется вместе с инструментальными обследованиями (такими как УЗИ, рентгенография или компьютерная томография) для того, чтобы оценить эффективность терапии. Как правило, снижение концентрации СА-125 в процессе лечения тесно связано с уменьшением количества опухолевых клеток и эффективностью терапии. Важно заметить, что в некоторых случаях возможен кратковременный подъем концентрации СА-125 при эффективном лечении, например, возможен «всплеск» после проведения первого или второго курса терапии – данное явление отмечается примерно у 30% пациентов. Решения о продолжении или смене лечения должно основываться на ряде факторов, включая данные инструментальных обследований, самочувствие пациентки и должно приниматься лечащим врачом.
Решения о продолжении или смене лечения должно основываться на ряде факторов, включая данные инструментальных обследований, самочувствие пациентки и должно приниматься лечащим врачом.
4. Ранняя диагностика рака яичников.
Как и при других злокачественных опухолях, ранняя диагностика рака яичников, как правило, приводит к достижению наилучших результатов лечения. Отсутствие специфичных симптомов затрудняет раннюю диагностику заболевания, по этой причине CA-125 иногда используется с этой целью. Тем не менее, низкая информативность теста при небольших размерах опухоли, ограничивает его использование с этой целью.
В настоящее время предпринимаются активные попытки повысить информативность и целесообразность использования опухолевых маркеров для ранней диагностики злокачественных опухолей яичников. Наиболее широкое применение нашел диагностический тест, получивший название ROMA (Risk of Ovarian Malignancy Algorithm, алгоритм оценки риска наличия злокачественного новообразования). В его основе лежит оценка соотношения концентрации СА-125 и еще одного опухолевого маркера, повышение которого также наблюдается при раке яичников – HE4 (human epididymis protein 4). В случае выявления объемного образования в яичниках индекс ROMA позволяет оценить вероятность, с которой выявленная опухоль может являться злокачественной. Высокое значение индекса ROMA — веская причина для тщательного обследования и обращения к специалисту-онкогинекологу с целью решения вопроса о выполнении оперативного удаления выявленной опухоли.
В его основе лежит оценка соотношения концентрации СА-125 и еще одного опухолевого маркера, повышение которого также наблюдается при раке яичников – HE4 (human epididymis protein 4). В случае выявления объемного образования в яичниках индекс ROMA позволяет оценить вероятность, с которой выявленная опухоль может являться злокачественной. Высокое значение индекса ROMA — веская причина для тщательного обследования и обращения к специалисту-онкогинекологу с целью решения вопроса о выполнении оперативного удаления выявленной опухоли.
Описание анализа Онкомаркер яичников СА-125 в Енакиево
Код: 01-203
Цена: 590 руб
Описание
СА-125 — онкомаркер рака яичников. Это гликопротеин, который присутствует в эпителии яичников, поджелудочной железы, желчного пузыря, желудка, бронхов, почек, кишечника.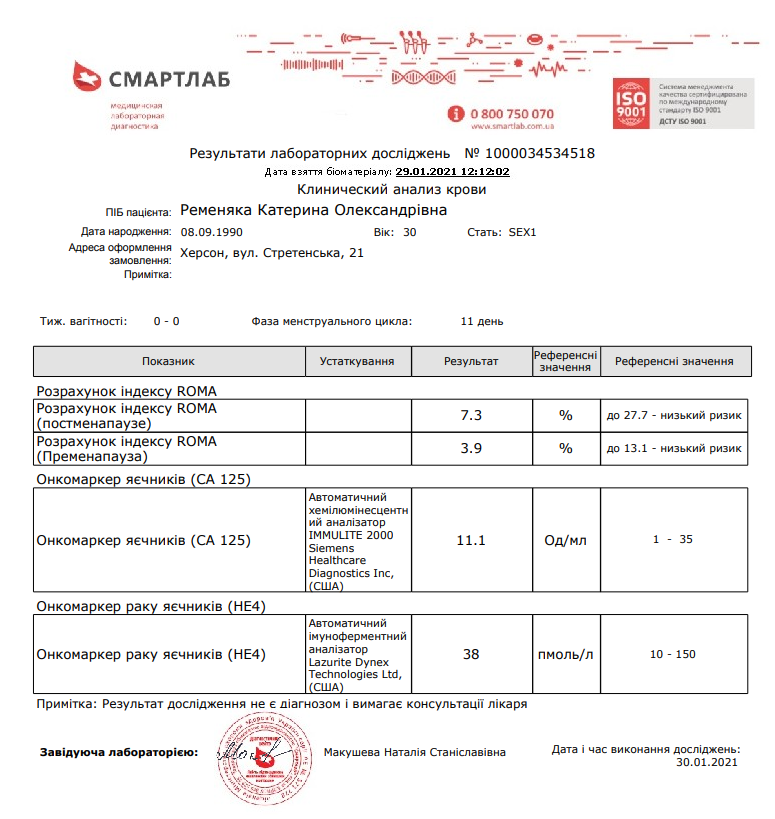
Главным образом исследование применяют для мониторинга рака яичников и диагностики его рецидивов. Повышение уровня СА-125 в крови связано с прогрессированием опухолевого процесса. Регрессия опухоли или удаление ее хирургическим путем сопровождается уменьшением лабораторного показателя.
СА-125 коррелирует с ремиссией заболевания при химио- и химиолучевом лечении.
CA-125 также может быть использован в качестве вторичного маркера при раке поджелудочной железы, после CA 19–9.
Значительное увеличение уровня СА-125 в крови наблюдается иногда при различных доброкачественных гинекологических опухолях, а также при воспалительных процессах, вовлекающих придатки.
Незначительный подъем уровня этого маркера выявляется в I триместре беременности, при различных аутоиммунных заболеваниях, гепатите, хроническом панкреатите и циррозе печени.
Подготовка к анализу
Кровь для исследования сдается утром натощак после 8-12 часового ночного периода голодания (можно пить воду). Накануне перед сдачей крови следует исключить из рациона жирную пищу.
Накануне перед сдачей крови следует исключить из рациона жирную пищу.
Требования
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом.
Референсные значения (норма):
| < 21.0 | женщины |
< 35.0 | пороговый уровень |
Повышение уровня CА-125:
Онкопатология:
- Рак яичников (в 80% случаев)
- Рак матки
- Рак эндометрия
- Рак фаллопиевых труб
- Рак молочной железы
- Рак поджелудочной железы
- Рак прямой кишки
- Рак желудка
- Рак легких
- Рак печени
Соматическая патология (незначительное повышение):
- Кистозные образования яичников
- Эндометриоз
- Воспалительные заболевания придатков, банальная гинекологическая инфекция
- Перитонит, плеврит
- Хронический гепатит, цирроз печени
- Хронический панкреатит
- Аутоиммунная патология
Медицинский центр «Консультант» — Иммунохимические исследования (гормоны и онкомаркеры)
В настоящее время остается актуальной проблема ранней диагностики рака яичников. Рак яичников стоит на 4 месте среди наиболее частых причин смерти женщин от злокачественных новообразований. Около 70% вновь выявленных случаев рака яичников представляют собой распространенный опухолевый процесс. Рак яичников не имеет ярко выраженных и специфичных симптомов, часто воспринимается как проявление аднексита и других неопухолевых заболеваний малого таза. В связи с этим , главная задача диагностических процедур при выявлении образований в малом тазу — определение злокачественной или доброкачественной природы заболевания. Несмотря на то, что большая часть выявленных случаев образований в малом тазу составляют доброкачественные опухоли, для правильного выбора тактики лечения очень важно до проведения оперативного вмешательства оценить риск наличия злокачественной опухоли.
Рак яичников стоит на 4 месте среди наиболее частых причин смерти женщин от злокачественных новообразований. Около 70% вновь выявленных случаев рака яичников представляют собой распространенный опухолевый процесс. Рак яичников не имеет ярко выраженных и специфичных симптомов, часто воспринимается как проявление аднексита и других неопухолевых заболеваний малого таза. В связи с этим , главная задача диагностических процедур при выявлении образований в малом тазу — определение злокачественной или доброкачественной природы заболевания. Несмотря на то, что большая часть выявленных случаев образований в малом тазу составляют доброкачественные опухоли, для правильного выбора тактики лечения очень важно до проведения оперативного вмешательства оценить риск наличия злокачественной опухоли.
До последнего времени в качестве основного онкомаркера при раке яичника рассматривалось определение в сыворотке крови маркера СА125. Значение его для мониторинга, а именно для оценки ответа на проводимое лечение и раннего выявления рецидивов, не вызывает сомнений. Уровень СА125 повышен у более 80% всех пациенток с эпителиальным раком яичников. Но его чувствительность на стадиях 1-2 невысока: повышенные значения СА125 установлены не более чем у 50% пациенток.
Значение его для мониторинга, а именно для оценки ответа на проводимое лечение и раннего выявления рецидивов, не вызывает сомнений. Уровень СА125 повышен у более 80% всех пациенток с эпителиальным раком яичников. Но его чувствительность на стадиях 1-2 невысока: повышенные значения СА125 установлены не более чем у 50% пациенток.
Кроме того, СА125 не является строго специфичным маркером рака яичников,он может повышаться при доброкачественных гинекологических заболеваниях, при злокачественных опухолях других локализаций, у здоровых женщин репродуктивного возраста.
Сравнительно недавно появился тест для определения опухолевого антигена НЕ4, который может дать дополнительную информацию о динамике опухолевого процесса при раке яичника. Именно повышенная концентрация белка НЕ4 сегодня является наиболее точным лабораторным предиктором злокачественного процесса.
НЕ4 (Human epididymis protein 4) — человеческий эпидидимальный секреторный белок 4. Первоначально он был идентифицирован в эпителии дистального эпидидимиса (придатка яичка) как предполагаемый протеазный ингибитор, вовлеченный в созревание спермы. С тех пор экспрессия НЕ4 была описана в различных тканях, включая эпителий репродуктивной системы. В норме его продукция сильно ограничена, но при раке яичника был показан высокий уровень секреции НЕ4 в крови у пациенток. На основании исследований последних лет НЕ4 рекомендован в качестве опухолевого маркера эпителиального рака яичников и обладает высокой чувствительностью и специфичностью даже на 1 стадии болезни.
Первоначально он был идентифицирован в эпителии дистального эпидидимиса (придатка яичка) как предполагаемый протеазный ингибитор, вовлеченный в созревание спермы. С тех пор экспрессия НЕ4 была описана в различных тканях, включая эпителий репродуктивной системы. В норме его продукция сильно ограничена, но при раке яичника был показан высокий уровень секреции НЕ4 в крови у пациенток. На основании исследований последних лет НЕ4 рекомендован в качестве опухолевого маркера эпителиального рака яичников и обладает высокой чувствительностью и специфичностью даже на 1 стадии болезни.
Однако, в связи с возможным повышением при доброкачественных заболеваниях,а также с тем, что некоторые, более редкие, типы рака яичников (например, муцинозный или герминативноклеточный) редко экспрессируют НЕ4, этот маркер нельзя использовать как единственное свидетельство наличия или отсутствия злокачественной патологии; он не рекомендован для общего скрининга. Результат исследования НЕ4 следует интерпретировать в комплексе с другими тестами и процедурами, он не заменяет утвержденных видов клинического обследования.
В настоящее время при наличии образований в малом тазу на основании многочисленных исследований предложено сочетанное использование НЕ4 и СА125 с расчетом прогностического индекса RОМА (Risk of Ovarian Malignancy Algorithm) . Метод одобрен ведущими мировыми экспертами в области медицины, валидирован в многоцентровых исследованиях и является высокоинформативным.
Индекс ROMA учитывает концентрации онкомаркеров НЕ4 и СА125, а также менопаузальный статус пациентки и позволяет с высокой вероятностью оценить наличие рака яичников, разделяя женщин в пре- и постменопаузе на группы с высоким и низким риском рака яичников.
Так для женщин в пременопаузе:
- Значение ROMA > 13.1% говорит о высоком риске обнаружения эпителиального РЯ
- Значение ROMA
Для женщин в постменопаузе:
- Значение ROMA > 27,7 % — говорит о высоком риске обнаружения эпителиального РЯ
- Значение ROMA
При заказе исследования «Оценка риска рака яичников по алгоритму ROMA» проводится определение концентрации онкомаркеров НЕ4 и СА125. Неоходимо обязательно указать менопаузальный статус пациентки (пре- или постменопауза). Без этих данных индекс рассчитан не будет.
Материалом для исследования является сыворотка крови. Специальной подготовки к исследованию не требуется. Необходимо соблюдать общие рекомендации при сдаче крови, приведенные в разделе Лабораторная диагностика.
Каков контрольный диапазон CA 125?
Ши М., Соколл Л., Чан DW. Рак яичников. Diamandis EP, Fritsche HA, Lilja H, Chan DW, Schwartz MK, ред. Онкомаркеры: физиология, патобиология, технология и клиническое применение . Вашингтон, округ Колумбия: AACC Press; 2002. 239-52.
Davelaar EM, van Kamp GJ, Verstraeten RA, Kenemans P. Сравнение семи иммуноанализов для количественной оценки антигена CA 125 в сыворотке. Clin Chem .1998 июл. 44 (7): 1417-22. [Медлайн].
Munkarah A, Chatterjee M, Tainsky MA. Обновленная информация о скрининге на рак яичников. Curr Opin Obstet Gynecol . 2007 февраля 19 (1): 22-6. [Медлайн].
Руководство по клинической практике в онкологии Национальной комплексной онкологической сети (NCCN). Рак яичников. Версия 3.2012 (проверено 6 сентября 2012 г.).
Джохари-Ахар М., Рашиди М.Р., Барар Дж., Агаи М., Мохаммаднеджад Д., Рамазани А. и др.Сверхчувствительный импедиметрический иммуносенсор для обнаружения сывороточного онкомаркера СА-125 у больных раком яичников. Наноразмер . 2015 28 февраля. 7 (8): 3768-79. [Медлайн].
Мемар Б., Аледавуд А., Шахидсалес С., Ахади М., Фарзадния М., Рази Х.Р. и др. Прогностическая роль опухолевого маркера CA-125 в В-клеточной неходжкинской лимфоме. Иран Дж. Рак. Предыдущая . 2015 янв-фев. 8 (1): 42-6. [Медлайн].
Мацукс р, Байдекална I, Донина С.Сравнение различных алгоритмов выявления рака яичников. евро J Gynaecol Oncol . 2011. 32 (4): 408-10. [Медлайн].
Определения CA125 согласованы с GCIG. http://www.gcig.igcs.org/CA125/respdef_nov2005.pdf (по состоянию на 6 сентября 2012 г.). Ноябрь 2005 г.
Potenza E, Parpinel G, Laudani ME, Macchi C, Fuso L, Zola P. Прогностическая и прогностическая ценность комбинированных биомаркеров HE-4 и CA-125 во время химиотерапии у пациентов с эпителиальным раком яичников. Int J Biol Маркеры . 2020 Декабрь 35 (4): 20-7. [Медлайн]. [Полный текст].
Fularz M, Adamiak P, Czepczyński R, Jarzbek-Bielecka G, Rewers A, Kędzia W, et al. Применение ПЭТ / КТ в диагностике рецидива рака яичников в зависимости от уровня СА 125 в сыворотке. Нуклеармедизин . 2015 3 августа. 54 (4): 158-62. [Медлайн].
Rustin G, Van der Burg ME. от имени сотрудников MRC и EORTC. Рандомизированное исследование рака яичников по раннему лечению рецидива, основанное только на уровне CA125, в сравнении с отсроченным лечением на основе общепринятых клинических показателей (испытания MRC OV05 / EORTC 55955) Раннее и отсроченное лечение рецидива рака яичников (MRC OV05 / EORTC 55955): рандомизированное испытание. Ланцет . Октябрь 2010 г. Том 376: выпуск 9747.1155: 1155-1163.
Jacobs I, Bast RC Jr. Антиген, связанный с опухолью CA 125: обзор литературы. Репродукция Человека . 1989, 4 (1): 1-12. [Медлайн].
Партридж EE, Барнс Миннесота. Эпителиальный рак яичников: профилактика, диагностика и лечение. CA Cancer J Clin . 1999 сентябрь-октябрь. 49 (5): 297-320. [Медлайн].
Лю LY. [Взаимосвязь между уровнем CA125 в сыворотке и результатами вторичного осмотра при раке яичников]. Чжунхуа Чжун Лю За Чжи . 1992 июля 14 (4): 287-9. [Медлайн].
Мейер Т, Растин ГДж. Роль онкомаркеров в мониторинге эпителиального рака яичников. Br J Рак . 2000 Май. 82 (9): 1535-8. [Медлайн].
Nasioudis D, Wilson E, Mastroyannis SA, Latif NA. Прогностическое значение повышенных уровней СА-125 в сыворотке до лечения у пациентов с опухолями стромы полового канатика яичника I стадии. евро J Obstet Gynecol Reprod Biol .2019 Июль 238: 86-9. [Медлайн].
Руководство по клинической практике в онкологии Национальной комплексной онкологической сети (NCCN). Генетическая / семейная оценка высокого риска: грудь и яичники. Версия 1.2012 (проверено 6 сентября 2012 г.).
Antoniou A, Pharoah PD, Narod S, Risch HA, Eyfjord JE, Hopper JL. Средние риски рака груди и яичников, связанные с мутациями BRCA1 или BRCA2, обнаруженными в серии случаев, не выбранных для семейного анамнеза: комбинированный анализ 22 исследований. Am J Hum Genet . 2003 май. 72 (5): 1117-30. [Медлайн].
Risch HA, McLaughlin JR, Cole DE, Rosen B, Bradley L, Kwan E. Распространенность и пенетрантность мутаций BRCA1 и BRCA2 зародышевой линии в популяционной серии из 649 женщин с раком яичников. Ам Дж Хам Генет . 2001 Mar.68 (3): 700-10. [Медлайн].
Консенсусная конференция NIH. Рак яичников. Скрининг, лечение и последующее наблюдение. Группа разработки консенсуса NIH по раку яичников. JAMA . 1995 8 февраля. 273 (6): 491-7. [Медлайн].
Руководство по клинической практике в онкологии Национальной комплексной онкологической сети (NCCN). Скрининг колоректального рака. Версия 2.2012 (проверено 6 сентября 2012 г.).
Fleisher M, Dnistrian A, Sturgeon C, Lamerz R, Witliff J. Практическое руководство и рекомендации по использованию онкомаркеров в клинике. Онкомаркеры. Физиология, патобиология, технология и клиническое применение .Вашингтон: AACC Press; 2002. 33–63.
Sturgeon CM, Duffy MJ, Stenman UH, Lilja H, Brunner N, Chan DW. Практическое руководство по лабораторной медицине Национальной академии клинической биохимии по использованию онкомаркеров при раке яичек, простаты, колоректального рака, молочной железы и яичников. Clin Chem . 2008 декабрь 54 (12): e11-79. [Медлайн].
Инь Б.В., Ллойд КО. Молекулярное клонирование антигена рака яичников CA125: идентификация как новый муцин, MUC16. Дж. Биол. Хим. . 2001. 20 июля. 276 (29): 27371-5. [Медлайн].
Bast RC Jr, Xu FJ, Yu YH, Barnhill S, Zhang Z, Mills GB. CA 125: прошлое и будущее. Int J Biol Маркеры . 1998 окт-дек. 13 (4): 179-87. [Медлайн].
Kenemans P, van Kamp GJ, Oehr P, Verstraeten RA. Гетерологический двухдетерминантный иммунорадиометрический анализ CA 125 II: надежный иммуноанализ второго поколения для определения CA 125 в сыворотке. Clin Chem .1993 Декабрь 39 (12): 2509-13. [Медлайн].
Даффи М.Дж., Бонфрер Дж. М., Кульпа Дж., Растин Дж. Дж., Солетормос Дж., Торре Дж. CA125 при раке яичников: Руководство Европейской группы по онкомаркерам для клинического использования. Int J Gynecol Cancer . 2005 сентябрь-октябрь. 15 (5): 679-91. [Медлайн].
Коломбо Н., Пейретти М., Парма Дж. И др. Недавно диагностированная и рецидивирующая эпителиальная карцинома яичников: Руководство ESMO по клинической практике по диагностике, лечению и последующему наблюдению. Энн Онкол . 2010 май. 21 Дополнение 5: ст. 23-30. [Медлайн].
Vasey PA, Herrstedt J, Jelic S ,. Минимальные клинические рекомендации ESMO по диагностике, лечению и наблюдению за эпителиальной карциномой яичников. Энн Онкол . 2005. 16 Suppl 1: i13-5. [Медлайн].
Michalak M, Gąsiorowska E, Markwitz EN. Диагностическая ценность CA125, HE4, ROMA и модели логистической регрессии в диагностике массы таза — наш опыт. Гинеколь Пол .2015 Апрель, 86 (4): 256-61. [Медлайн].
Buys SS, Partridge E, Black A, Johnson CC, Lamerato L, Isaacs C. Влияние скрининга на смертность от рака яичников: рандомизированное контролируемое исследование скрининга рака простаты, легких, толстой кишки и яичников (PLCO). JAMA . 2011 г. 8 июня. 305 (22): 2295-303. [Медлайн].
Валентин Л., Юркович Д., Ван Калстер Б. и др. Добавление одного измерения CA 125 к ультразвуковому изображению, выполненному опытным врачом, не улучшает предоперационное различение доброкачественных и злокачественных образований придатков. Ультразвуковой акушерский гинеколь . 2009 Сентябрь 34 (3): 345-54. [Медлайн].
Menon U, Gentry-Maharaj A, Hallett R, Ryan A, Burnell M, Sharma A. Чувствительность и специфичность мультимодального и ультразвукового скрининга на рак яичников, а также распределение по стадиям обнаруженного рака: результаты скрининга распространенности Совместного исследования Великобритании Испытание скрининга рака яичников (UKCTOCS). Ланцет Онкол . 2009 Апрель 10 (4): 327-40. [Медлайн].
Пал МК, Рашид М., Бишт М.Мультиплексные конъюгаты магнитных наночастиц и антител (MNPs-ABS) основаны на прогностическом обнаружении биомаркеров рака яичников, CA-125, β-2M и ApoA1 с использованием флуоресцентной спектроскопии со сравнением анализа поверхностного плазмонного резонанса (SPR). Биосенс Биоэлектрон . 2015 15 ноября. 73: 146-52. [Медлайн].
Choi HJ, Lee YY, Sohn I, et al. Сравнение одного CA 125 и алгоритма риска злокачественных новообразований яичников (ROMA) у пациентов с опухолью придатков: многоцентровое исследование. Curr Probl Cancer . 1 ноября 2019 г. 100508. [Medline].
Хан К.Х., Парк Н.Х., Ким Дж.Дж. и др. Сила алгоритма риска злокачественных новообразований яичников с учетом менопаузального статуса: сравнение с CA 125 и HE4. Дж Гинеколь Онкол . 2019 30 ноября (6): e83. [Медлайн]. [Полный текст].
Роль CA125 в прогнозировании выживаемости при раке яичников
Abstract
CA125 — это золотой стандарт опухолевого маркера при раке яичников.Уровень CA125 в сыворотке крови используется для мониторинга ответа на химиотерапию, рецидива и прогрессирования заболевания у пациентов с раком яичников. Таким образом, разумно исследовать, может ли CA125 использоваться в качестве прогностического индикатора также при раке яичников. На этот счет было проведено большое количество эпидемиологических исследований. В этом обзоре обобщена вся доступная эпидемиологическая литература о связи между уровнями CA125 и выживаемостью при раке яичников. Чтобы поместить эти исследования в контекст, мы приводим некоторую справочную информацию о CA125 и его роли в развитии рака яичников.
Введение
Рак яичников является основной причиной смертности от гинекологических онкологических заболеваний в Соединенных Штатах (США), приводя к примерно 14 500 смертельным случаям ежегодно [1]. Общий риск развития рака яичников в течение жизни для женщин в США составляет от 1,4% до 1,8%. Этот риск колеблется от 0,6% для женщин без семейного анамнеза, не менее трех доношенных беременностей и четырех и более лет использования оральных контрацептивов до 3,4% для первородящих женщин, не использующих оральные контрацептивы. Для женщин с семейным анамнезом пожизненный риск рака яичников оценивается в 9.4% [2]. Общий скорректированный по возрасту уровень заболеваемости для всех случаев рака яичников, по данным Программы эпиднадзора, эпидемиологии и конечных результатов (SEER) Национального института рака, составляет 16,23 случая на 100 000 женщин, стандартизованных для стандартной популяции США 2000 года [3]. Существуют заметные географические различия в стандартизированных по возрасту показателях заболеваемости и смертности от рака яичников, причем самые высокие показатели наблюдаются в Северной и Западной Европе, особенно в Скандинавии, и в Северной Америке [4].
Рак яичников на ранних стадиях часто протекает бессимптомно, поэтому на момент постановки диагноза у большинства пациентов наблюдается широко распространенное заболевание [5].К сожалению, большая часть эпителиального рака яичников остается клинически невыявленной до тех пор, пока у пациентов не разовьется поздняя стадия заболевания, и лишь 25% случаев рака выявляются как стадия I [6]. Однако при диагностировании на стадии I показатель излечения может приближаться к 90% с помощью доступной в настоящее время циторедуктивной хирургии и комбинированной химиотерапии [7]. Рак яичников остается заболеванием, которое оказывается фатальным для большинства пациентов, но химиотерапия считается лечением, улучшающим выживаемость.Меньшая часть пациентов достигает длительного выживания после такого лечения [8]. Несмотря на высокие показатели эффективности хирургического вмешательства с последующей химиотерапией [9–11], 75% женщин в конечном итоге умирают от осложнений, связанных с прогрессированием заболевания. После диагностики рака яичников стадии III и IV, который определяется перитонеальным и внебрюшинным метастатическим распространением, выживаемость снижается с 95% на стадии I примерно до 20-25% пятилетней выживаемости, несмотря на соответствующее лечение [12,13]. Следовательно, клинический исход и, возможно, выживаемость могут быть значительно улучшены путем выявления стадии I заболевания без необходимости изменения хирургических или химиотерапевтических подходов [14].Разработка специфичного для рака яичника биомаркера для раннего выявления заболевания может улучшить мрачную выживаемость [15].
Онкомаркеры при раке яичников
Потребность в разработке надежных сывороточных биомаркеров для раннего выявления и прогнозирования рака яичников, которые являются как чувствительными, так и специфическими, остается долгожданным приоритетом. Исследователи знают об этой необходимости, и Сеть исследований раннего обнаружения (EDRN), созданная Национальным институтом рака, предложила «руководящие принципы» для разработки скрининговых биомаркеров [16].При лечении рака яичников эти биомаркеры применялись для мониторинга реакции на лечение, для различения злокачественных и доброкачественных образований таза, для оценки прогноза, для прогнозирования ответа на отдельные лекарства и для выявления первичного заболевания на ранней стадии [17]. Несколько эпитопов на полиморфном эпителиальном муцине, происходящем из гена MUC1, были идентифицированы как мишени для семейства онкомаркеров, которые включают CA549, CASA (сывороточный антиген, связанный с раком), CA19-9, CA15-3, MCA, MOV-1 и TAG72. .Маркеры пролиферации цитокератина TPS и CYFRA21-1 также были исследованы при раке яичников [18]. Среди этих маркеров наиболее изученным является CA125.
CA125 при раке яичников
Наиболее широко используемым онкомаркером при раке яичников, который часто считается «золотым стандартом», является CA125 [19]. Впервые он был идентифицирован Бастом, Кнаппом и коллегами [20] в 1981 году. CA125 — это высокомолекулярный гликопротеин, который повышается примерно у 90% пациентов с распространенным эпителиальным раком яичников [21].CA125 экспрессируется амниотическим и целомическим эпителием плода, а во взрослых тканях происходит из целомического (мезотелиальные клетки плевры, перикарда и брюшины) и мюллерова (трубный, эндометриальный и эндоцервикальный) эпителий. CA125 содержит 2 основных антигенных домена, а именно A и B, которые связывают моноклональные антитела OC125 и M11 соответственно [22]. С момента своего создания измерение уровня антигена CA125 в сыворотке крови стало стандартным компонентом рутинного ведения женщин с распространенным раком яичников [23].Уровни CA125 менее 35 Ед / мл в настоящее время считаются нормой [21,24]. При стратификации по стадиям заболевания повышенные уровни были обнаружены более чем у 90% пациентов с поздней стадией рака яичников, но только у 50% пациентов с болезнью I стадии [22]. Кроме того, повышенные уровни CA125 сильнее связаны с серозными, а не муцинозными опухолями [25]. Общепринятые определения рецидива заболевания, основанные только на уровнях СА125 в сыворотке, указывают на удвоение уровня этого онкомаркера либо от верхнего предела нормы (35 Ед / мл) у пациентов с нормализацией этого маркера после первичного лечения, либо от нижних уровней в пациенты с повышенным уровнем сывороточного маркера, который никогда не нормализуется после первичного лечения [26,27].
Многочисленные исследования подтвердили полезность уровней CA125 для мониторинга прогресса пациентов с эпителиальным раком яичников [18,28-30]. В большинстве отчетов указывается, что повышение уровня CA125 предшествует клиническому обнаружению примерно на 3 месяца [31]. К сожалению, несколько проспективных исследований показали неадекватную чувствительность CA125 в условиях скрининга рака яичников в бессимптомных популяциях [32–34]. Несмотря на хорошо изученные ограничения в интерпретации одиночного значения CA125, этот биомаркер широко используется для проспективной оценки терапевтической эффективности и мониторинга статуса заболевания среди пациентов с раком яичников [35,36].Антиген CA125 — это сывороточный маркер, который достаточно хорошо валидирован для использования в повседневной клинической практике [18]. Таким образом, разумно попытаться определить, может ли CA125 использоваться в качестве прогностического индикатора и может ли он в будущем использоваться для индивидуального лечения пациентов с раком яичников [19]. Цель этого обзора — качественно обобщить научную литературу по сыворотке CA125 и выживаемости при раке яичников, а также дать рекомендации для будущих исследований.
Стратегия поиска и критерии выбора
Мы провели поиск в MEDLINE, чтобы выявить все исследования взаимосвязи между уровнем СА125 в сыворотке и выживаемостью при раке яичников, опубликованные между 1985 и 2009 годами.Мы провели поиск, используя термины «выживаемость / смертность / прогноз при раке яичников» в сочетании со следующими терминами: сыворотка до химиотерапии CA125, сыворотка после химиотерапии CA125, предоперационная сыворотка CA125, послеоперационная сыворотка CA125, период полувыведения CA125, уровень надира CA125, время достижения уровень надира, CA125 Площадь под кривой (AUC). Мы также провели поиск в библиографиях выбранных статей, чтобы выявить релевантные статьи, которые мы могли пропустить во время первичного поиска в MEDLINE. Для включения в обзор исследование должно: быть опубликовано на английском языке, содержать данные, собранные у людей с раком яичников, иметь CA125 в качестве одной из переменных-предикторов, измеренных следующим образом (абсолютное значение, период полувыведения, минимальное значение, время до достижения надира и AUC), выживаемость в качестве одного из критериев исхода (первичная или вторичная) и любой из следующих дизайнов исследования (случай-контроль, когортное, кросс-секционное, проспективное, ретроспективное, серии случаев, продольное, клиническое исследование , метаанализ).Не было ограничений по возрасту, этнической принадлежности, типу или стадии рака яичников. Все исследования, рассмотренные в этой статье, сведены в таблицы под отдельными заголовками и расположены в хронологическом порядке по годам публикации.
Оценка качества
Хотя мы официально не оценивали качество отчетов, мы записали и представили информацию о переменных, которые могут отражать качество отчетов. Переменные включали дизайн исследования (ретроспективное или проспективное), годы сбора данных, размер выборки и включение важных прогностических факторов в многомерный анализ.
Эпидемиологические исследования CA125 и выживаемости при раке яичников
Абсолютная сыворотка CA125 до химиотерапии и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между абсолютными уровнями CA125 до химиотерапии и выживаемостью при раке яичников. В исследовании оценивалась взаимосвязь между выживаемостью и ранними изменениями сывороточного уровня антигена CA125 при распространенном раке яичников. Хотя значения CA125 до лечения не коррелировали с выживаемостью, концентрация этого онкомаркера через 8 недель после начала терапии была мощным независимым прогностическим фактором.Средняя выживаемость пациентов (n = 51) с CA125 <35 U / мл по сравнению с пациентами (n = 50) с CA125> 35 U / ml в этот момент времени составила 26 месяцев и 15 месяцев соответственно. Кроме того, у женщин со значениями СА125 в сыворотке крови <50% от их концентрации до лечения через 8 недель средняя выживаемость составила 21 месяц, по сравнению с только 10 месяцами для лиц с уровнями опухолевых маркеров> 50% от исходного значения [37]. Многоцентровое исследование кинетики CA125 при индукционной химиотерапии, проведенное у 631 пациента с раком яичников, показало, что прехимиотерапия CA125, его период полувыведения, концентрация надира и время до надира имеют однофакторное прогностическое значение для безрецидивной и общей выживаемости [38].В другом проспективном исследовании изучалось значение предтерапевтического CA125 у 70 последовательных пациентов с рецидивирующим раком яичников до начала химиотерапии второй линии. Было обнаружено, что CA125 не был значительно связан с выживаемостью ни по одному из пороговых значений (35, 65, 132 и 339 Ед / мл) [39].
Таблица 1
Взаимосвязь между абсолютными уровнями CA125 в сыворотке до химиотерапии и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования | 9025Сравниваемые группы | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |
| USA Markman [ 37] | NA | Продольное исследование | 101 | ≤ 35 Ед / мл,> 35 — <100 Ед / мл, ≥ 100 Ед / мл | NA | Снижение концентрации CA-125 в сыворотке по сравнению с исходным 2 цикла химиотерапии были независимым предиктором выживаемости | NA |
| Riedinger JM, 2006, France [38] | 1988-1996 9025 6 | Многоцентровое ретроспективное исследование | 631 | ≤ 230 кЕд / л и> 230 кЕд / л | Одномерный анализ 0.77 (0,73-0,81), <0,0001 | Предварительная химиотерапия CA125 имела однофакторное прогностическое значение для выживаемости без болезни и общей выживаемости | NA |
| Gronlund B, 2005, Дания [39] | с декабря 1993 г. по сентябрь 1998 г. | Проспективное исследование | 70 | Множественные пороговые значения 35, 65, 132 и 339 Ед / мл | NA | Не было обнаружено, что уровень CA125 до лечения значимо связан с выживаемостью ни одним из отсечки | стадия FIGO, гистология, локализация рецидива опухоли, размер рецидива опухоли, уровень CASA |
| Gadducci A, 1995, Италия [40] | 1986–1992 | многоцентровое ретроспективное исследование | 225 | <500 Ед / мл, ≥ 500 Ед / мл | NA | Было обнаружено, что выживаемость в значительной степени зависит от сывороточного СА 125 перед третьим циклом | стадия FIGO, степень опухоли, повторная двусторонняя болезнь, период полувыведения CA125 |
| Ron IG, 1994, Израиль [41] | с февраля 1987 г. по декабрь 1990 г. | Проспективное исследование | 48 | 35-100 Ед / мл, 101-299 Ед / мл, 300-499 Ед / мл, ≥ 500 Ед / мл | NA, <0.0001 | Ранний ответ (норма CA125 к концу второго курса химиотерапии) был очень значимым предиктором безрецидивной выживаемости через 12 месяцев | Возраст, стадия FIGO, гистология, степень, остаточная опухоль, асцит |
| Дэвидсон Н.Г., 1991, [42] | С сентября 1985 г. по сентябрь 1987 г. | Удобный образец | 55 | <50 кЕд / л, 125 ≥ 50 кЕд / л | NA, <0,003 | Предварительная химиотерапия CA125 Уровень, полученный через 4 недели после операции по удалению опухоли, может прогнозировать выживаемость у пациентов с раком яичников, которые проходят курс химиотерапии | Возраст, гистология, стадия FIGO, степень опухоли, остаточная болезнь |
| Rustin GJ, 1989, U.K. [43] | Апрель 1985 г. — февраль 1987 г. | Проспективное исследование | 54 | ≥ 35 Ед / мл, <35 Ед / мл | NA, 0,001 | Существует очень значимая взаимосвязь между выживаемостью без прогрессирования время и изменение уровней CA125 непосредственно перед химиотерапией | NA |
| van der Burg ME, 1988, Нидерланды [44] | с сентября 1979 года по декабрь 1983 года | Серия последовательных случаев | 85 | ≤ 35 Ед / мл, 35-60 Ед / мл,> 60 Ед / мл | NA | Сам по себе уровень CA125 до химиотерапии сильно коррелирует со скоростью прогрессирования и вероятностью прогрессирования в течение 3 лет | стадия FIGO, гистология, гистологическая степень, размер послеоперационной опухоли |
Ретроспективное многоцентровое исследование, оценивающее прогностическую ценность сывороточного анализа CA125 у 225 пациентов с распространенным эпителиальным раком яичников, показало, что: urvival значимо связана со стадией, остаточным заболеванием, степенью опухоли, уровнем СА125 в сыворотке перед третьим циклом и периодом полужизни СА125 в сыворотке.Модель пропорциональных рисков Кокса показала, что остаточная болезнь, период полувыведения CA125 в сыворотке и степень опухоли сохраняют значительную ценность для прогнозирования выживаемости [40]. В другом исследовании оценивалась прогностическая ценность уровней СА125 в сыворотке как до химиотерапии, так и после каждого цикла из одного или двух курсов у 48 пациентов с запущенной аденокарциномой яичников. Пациенты со значениями СА125 в сыворотке ниже нормального значения 35 Ед / мл после двух курсов имели значительно более длительную медианную выживаемость и более длительную выживаемость без признаков заболевания, чем те пациенты, у которых уровни СА125 упали до нормального значения после третьего или более поздних курсов химиотерапии [41 ].В другом исследовании 55 пациентов с эпителиальной карциномой яичников, получавших химиотерапию на основе платины, наблюдались в течение как минимум 2 лет. Из этих 22 пациентов уровень CA125 до химиотерапии в сыворотке был ниже 50 kU / л, а у 33 пациентов уровень CA125 в сыворотке был больше или равен 50 kU / л. 5-летняя актуарная выживаемость в двух группах составила 75% и 10% соответственно [42]. Исследование, оценивающее прогностическую ценность измерений СА125 в сыворотке у 54 пациентов с распространенной аденокарциномой яичников, показало, что изменение уровней СА125 от до химиотерапии до 1 месяца спустя можно использовать для разделения пациентов на разные прогностические группы.Наилучшая дискриминация была обнаружена при разделении пациентов на тех, у кого было более чем семикратное снижение уровня CA125, и тех, у кого было отмечено меньшее изменение [43]. Наконец, исследование, проведенное с участием 85 пациентов с эпителиальным раком яичников, показало, что уровень CA125 до химиотерапии не имел прогностической ценности, если пациенты были стратифицированы по размеру опухоли [44].
Из восьми исследований, рассмотренных в рамках взаимосвязи между абсолютными уровнями СА125 в сыворотке до химиотерапии и выживаемостью, четыре были проспективными, одно ретроспективное, одно удобное исследование, одно последовательное исследование серии случаев.Шесть исследований [37,38,40-43] показали очень значимую взаимосвязь между изменениями уровня СА125 в сыворотке до химиотерапии и выживаемостью, тогда как одно исследование [39] не обнаружило такой взаимосвязи. В одном исследовании было обнаружено, что предварительная химиотерапия CA125 сильно коррелировала с вероятностью прогрессирования в течение 3 лет, но данные, предполагающие взаимосвязь между уровнем CA125 до химиотерапии и выживаемостью, не были предоставлены [44]. Следовательно, общие данные о взаимосвязи между уровнями СА125 в сыворотке до химиотерапии и выживаемостью при раке яичников предполагают обратную взаимосвязь между ними.
Абсолютная сыворотка СА125 после химиотерапии и выживаемость при раке яичников
В таблице приведены эпидемиологические исследования связи между абсолютными уровнями СА125 после химиотерапии и выживаемостью при раке яичников. Ретроспективное исследование оценило прогностическое значение уровня СА125 в сыворотке после 6 циклов системной адъювантной химиотерапии. Средняя выживаемость без прогрессирования составила 26, 14 и 10 месяцев, а средняя общая выживаемость составила 105, 42 и 37 месяцев в группе I (<10 Ед / мл), группе II (10-21 Ед / мл), и группа III (> 21 Ед / мл) соответственно [45].Одно исследование определило, является ли CA125 независимым предиктором общей выживаемости (ОВ) у пациентов с хирургически определенным статусом заболевания в конце первичной терапии перед внутрибрюшинной (IP) консолидационной химиотерапией. Если рассматривать как непрерывную переменную, CA125 был предсказателем ОС. Используя средний уровень CA125 в качестве порогового значения, OS была увеличена у пациентов с CA125 ≤ 12 Ед / мл (в среднем 5,8 лет) по сравнению с> 12 (3,7 года) [46].
Таблица 2
Взаимосвязь между абсолютными уровнями CA125 в сыворотке после химиотерапии и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Размер образца 9025 | Группы для сравнения | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | ||
| Kim HS, 2008 Kim HS, South Korea, 2008 45] | Январь 1997 г. — март 2007 г. | Ретроспективное исследование | 123 | <10 Ед / мл, 10-21 Ед / мл и> 21 Ед / мл | 2.51 (1,06-5,92), 0,027 3,13 (1,14-8,61), <0,001 | Уровень CA125 в сыворотке после 6 циклов первичной адъювантной химиотерапии паклитаксел / карбоплатин может быть хорошим прогностическим фактором для выживаемости у пациентов с полным ответом | Остаточная опухоль, химиотерапия циклов | |
| Juretzka MM, 2007, США [46] | 1984–1998 | Ретроспективное когортное исследование | 241 | CA125 ≤ 12 Ед / мл против> 12 Ед / мл 1 | 41 (1,05-1,91), 0,0248 | Уровень CA125 в конце первичной терапии был предиктором общей выживаемости и выживаемости без прогрессирования | стадия FIGO, гистология, степень | |
| Riedinger JM, 2007 , Франция [47] | 1988–1996 | Многоцентровое ретроспективное исследование | 494 | ≤ 35 кЕд / л,> 35 кЕд / л | Uni-2.7 (2.2-3.3), <0.0001 Multi-1.27 (0.94 -1.71), NS | Изменение CA125 после первого курса химиотерапии было независимым прогностическим фактором как для достижения полного патологического ответа, так и для общей выживаемости. | Возраст, гистология стадия FIGO, остаточная опухоль | |
| Бадулеску F, 2005, Румыния [48] | 2000–2002 | Проспективное исследование | 40 | NA | NA, NA | NA, NA | Критерии оценки ответа, основанные на вариациях уровней антигена CA125 в крови, являются лучшим инструментом для оценки сравниваемого прогноза с критериями RECIST | Возраст, стадия FIGO, критерии RECIST |
| Van Dalen A , 2000, Европа [5] | 1994–1997 | Проспективное многоцентровое исследование | 213 | ≤ 25 кЕд / л,> 25 кЕд / л | 5.6 (2,65-11,90), <0,0001 | Уровень CA125 25 kU / L по завершении трех курсов химиотерапии является хорошим показателем 2-летней общей выживаемости | стадия FIGO, гистология, степень, уровни TPS | |
| Рон И.Г., 1994, Израиль [41] | с февраля 1987 г. по декабрь 1990 г. | Проспективное исследование | 48 | ≤ 35 Ед / мл,> 35 Ед / мл | NA, <0,0001 | Пациенты с СА125 ниже 35 Ед / мл после 2 курсов имели значительно более длительную медианную выживаемость и выживаемость без признаков заболевания, чем пациенты, у которых СА125 упал до нормы после третьего или более позднего цикла | Возраст, стадия FIGO, гистология, степень, остаточная опухоль, асцит , прехимиотерапия CA125 | |
| Fisken J, 1993, UK [49] | NA | Ретроспективное исследование | 58 | 4 квартиля <55 Ед / мл, 58-221 Ед / мл, 228- 434 Ед / мл,> 450 Ед / мл | <0.0005 | CA125 был очень значимым предиктором как выживаемости без прогрессирования, так и общей выживаемости после первого цикла и на протяжении всей первичной химиотерапии | Остаточная болезнь, возраст, степень опухоли, статус работоспособности, асцит | |
| Redman CW, 1990, Великобритания [50] | Март 1986 г. — март 1988 г. | Серия последовательных случаев | 50 | ≤ 35 Ед / мл,> 35 Ед / мл | NA, 0,0009 | Сыворотка CA125 после двух курсов дала наибольшую дискриминацию между пациентами, живущими через 12 месяцев, и теми, кто не выжил в течение этого длительного периода | Возраст, стадия FIGO, гистология, степень, остаточное заболевание | |
Было проведено ретроспективное многоцентровое исследование для оценки прогностической ценности изменения CA125 после первый и второй курсы индукционной химиотерапии.Изменение CA125 после первого курса, остаточная опухоль, CA 125 перед вторым курсом и возраст пациентов были независимыми прогностическими факторами OS [47]. В исследовании сравнивали прогнозируемое значение вариаций уровня в крови антигена CA125 и имуногистохимической экспрессии CA125 с образными критериями оценки выживаемости пациенток с рецидивом рака яичников. В многофакторном анализе только вариация уровней CA125 в крови и интервал свободного заболевания от завершения химиотерапии первой линии были предикторами выживаемости, в то время как другие переменные, включая критерии RECIST, не влияли на выживаемость [48].В другом проспективном многоцентровом исследовании оценивалась прогностическая значимость уровней CA125 и TPS выше значения дискриминации (25 kU / L и 100 U / L, соответственно). Уровни опухолевых маркеров на стадии I и II не коррелировали с выживаемостью. Однако пациенты со стадией III и IV с повышенным уровнем CA125 или TPS после трех курсов химиотерапии имели худшую двухлетнюю выживаемость (69% против 26% и 57% против 20% соответственно), чем пациенты с нормальным уровнем маркеров [ 5].
В одном исследовании изучалась прогностическая ценность раннего анализа сывороточного CA125 у 58 пациентов с распространенным эпителиальным раком яичников.CA125 был очень значимым предиктором как выживаемости без прогрессирования, так и общей выживаемости после первого цикла и на протяжении всей первичной химиотерапии. Пациенты из верхнего квартиля (СА125> 450 Ед / мл) имели очень плохую медианную выживаемость, составляющую 7 месяцев, в то время как пациенты из нижнего квартиля (СА125 <55 Ед / мл) имели хорошую медианную выживаемость 23 месяца. Те в двух межквартильных группах, у которых уровни CA125 варьировались от 58 до 221 Ед / мл и 228-434 Ед / мл, имели относительно промежуточное среднее время выживания - 16 месяцев и 15 месяцев соответственно [49].Другое исследование показало, что пациенты со значениями СА125 в сыворотке ниже 35 Ед / мл после двух курсов химиотерапии значительно чаще достигают полной ремиссии и имеют значительно более длительную медианную выживаемость. В многофакторном анализе уровни CA125 в сыворотке после двух курсов были наиболее важным независимым прогностическим фактором [50].
Из восьми исследований, рассмотренных в этом разделе, три были ретроспективными, три проспективных и одна последовательная серия случаев. Из них семь исследований [41,45-50] продемонстрировали, что уровень CA125 в сыворотке после химиотерапии является хорошим прогностическим индикатором выживаемости.Эти исследования предполагают, что пациенты со значениями СА125 в сыворотке в пределах нормального диапазона после химиотерапии имели значительно более длительную общую выживаемость и безрецидивную выживаемость, чем те пациенты, у которых уровни СА125 оставались высокими после химиотерапии. В одном из исследований CA125 ниже 25 kU / l после 3 курсов химиотерапии не имел достоверной корреляции с общей выживаемостью у пациентов с I и II стадиями, хотя это было в подгруппе пациентов с III и IV стадиями заболевания [5]. В целом, существует множество доказательств того, что уровень CA125 после химиотерапии является хорошим предиктором общей выживаемости и выживаемости без прогрессирования при раке яичников.
Абсолютная сыворотка СА125 во время химиотерапии и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между абсолютными уровнями СА125 во время химиотерапии и выживаемостью при раке яичников. В ретроспективном исследовании оценивалась прогностическая ценность уровня СА125 в сыворотке до химиотерапии, кинетики СА125 и периода полувыведения СА125 при распространенном раке яичников во время индукционной полихимиотерапии цисплатином. Уровень CA125 до химиотерапии не имел прогностического значения для выживаемости.Однако среднее время выживания пациентов с уровнем CA125 ниже верхней границы нормы после двух курсов КТ составило 101 месяц по сравнению со средней продолжительностью жизни 21 месяц у пациентов без нормализации CA125 [51]. В другом ретроспективном многоцентровом исследовании оценивалась прогностическая ценность сывороточного анализа CA125 у 225 пациентов с распространенным эпителиальным раком яичников. Множественная логистическая регрессия показала, что остаточная болезнь, период полувыведения СА 125 в сыворотке, СА 125 в сыворотке до третьего цикла и СА 125 в сыворотке до первого цикла сохраняют значительную ценность для прогнозирования результатов второго обзора.Выживаемость была существенно связана со стадией, остаточным заболеванием, степенью опухоли, уровнем СА125 в сыворотке до третьего цикла и периодом полужизни СА125 в сыворотке [40]. В другом исследовании изучалась регрессия сывороточного CA125 после циторедуктивной хирургии и во время первых трех курсов химиотерапии у 60 пациентов с раком яичников. У пациентов со стадией III-IV наблюдалась значимая положительная корреляция между выживаемостью и (а) стадией III, (б) остаточной опухолью ≤ 1 см, (в) нормализацией СА125 после трех курсов и (г) периодом полувыведения СА125 ≤ 20 дней. .Среднее время выживания пациентов с нормализацией CA 125 и без него после трех курсов составляло 27 и 14 месяцев соответственно [52].
Таблица 3
Взаимосвязь между абсолютными уровнями СА125 в сыворотке во время химиотерапии и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования Размер | Сравниваемые группы | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |
| 51] | NA | Ретроспективное исследование | 222 | ≤ 35 Ед / мл &> 35 Ед / мл | <0.0001 | Время, необходимое для нормализации уровней CA125, может разделить пациентов на группы с хорошим и плохим прогнозом на ранних этапах химиотерапии | Терапевтический ответ Индекс Карновского, остаточная болезнь, степень опухоли, период полувыведения CA125, кинетика CA125 |
| Gadducci A, 1995, Италия [40] | 1986–1992 | Многоцентровое ретроспективное исследование | 225 | <35 Ед / мл и> 35 Ед / мл перед третьим курсом химиотерапии | NA | Сыворотка CA125 Период полувыведения во время ранней химиотерапии был независимым прогностическим фактором как для достижения полного патологического ответа, так и для выживаемости пациентов с запущенным эпителиальным раком яичников | стадия FIGO, степень опухоли, размер остаточного заболевания, сыворотка CA125 перед первым циклом химиотерапия и сыворотка Период полувыведения CA125 |
| Yedema CA, 1993, Нидерланды [52] 90 256 | июль 1984 — декабрь 1990 | Ретроспективное исследование | 60 | ≤ 35 Ед / мл &> 35 Ед / мл | 5.60 (1.16-27.1), 0,03 | Наблюдалась значимая взаимосвязь между уровнями СА125 в сыворотке после трех курсов химиотерапии и выживаемостью при раке яичников. | Стадия, гистология, степень, остаток опухоли |
Все три исследования, рассмотренные выше, были ретроспективными. В совокупности результаты этих исследований в сочетании с данными, приведенными в таблицах, предоставляют дополнительные доказательства, подтверждающие прогностическую роль CA125 во всем спектре химиотерапевтического лечения рака яичников.
Абсолютная предоперационная сыворотка CA125 и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между абсолютными предоперационными уровнями CA125 и выживаемостью при раке яичников. Ретроспективное исследование 75 пациентов с эпителиальной карциномой яичников показало, что предоперационные уровни CA125 существенно не коррелировали со стадией, степенью опухоли или выживаемостью. Снижение выживаемости было отмечено с увеличением возраста на момент операции и большей частью остаточной болезни в послеоперационном периоде [53].Другое исследование, оценивающее предоперационный CA125 как прогностический фактор при эпителиальном раке яичников I стадии, показало, что пациенты с предоперационным уровнем CA125 в сыворотке <65 Ед / мл имели значительно более длительную выживаемость по сравнению с пациентами с EOC I стадии с предоперационным уровнем CA125 в сыворотке ≥ 65 Ед / мл [54 ]. Другое исследование, оценивающее связь предоперационных уровней CA125 с исходом, показало, что после поправки на ковариаты существовала значимая связь между уровнями CA125 и выживаемостью при конкретном заболевании.Поскольку предоперационные уровни CA125 увеличивались, риск смерти увеличивался, за исключением самых высоких значений CA125 [55].
Таблица 4
Взаимосвязь между предоперационными абсолютными уровнями CA125 в сыворотке и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования Размер | Сравниваемые группы | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |||
| Осиманрик [2008, L Osimeman N ] | с января 2001 г. по декабрь 2005 г. | Ретроспективное исследование | 75 | ≤ 500 ед / мл,> 500 ед / мл | NA, 0.85 | Предоперационный уровень CA125 существенно не коррелировал со стадией, степенью опухоли или выживаемостью | Возраст, гистология, стадия FIGO, степень | ||
| Petri A, 2006, Дания [54] | Dec 1994 на май 1999 г. | Ретроспективное исследование | 118 | <65 Ед / мл, ≥ 65 Ед / мл | 3,4 (1,2-9,6), 0,01 | Пациенты с ЭРЯ I стадии и предоперационным уровнем СА125 в сыворотке <65 Ед / мл имели значительно более длительную выживаемость по сравнению с теми, у которых сыворотка CA125 ≥ 65 Ед / мл | Возраст, гистология Подстадия FIGO, степень, химиотерапия | ||
| Cooper BC, 2002, США [55] | 1990 до 1996 | Ретроспективное исследование | 142 | <160, 160-399, 400-924, 925-2399, 2400 Ед / мл | GI-Reference, GII-2, GIII-1.5, GIV-4, GV-2, 0,03 (для тенденции) | Обнаружена значимая связь между уровнями CA125 и выживаемостью, характерной для конкретного заболевания | Возраст, гистология, стадия FIGO, степень, асцит и оптимальная циторедукция | ||
| Buller R, 1996, США [56] | 1987-1982 | Ретроспективное исследование | 126 | ≤ 500 Ед / мл,> 500 Ед / мл, ≤ 3000 Ед / мл,> 3000 Ед / мл | I-HR-NA, 0,48 II-HR-NA, 0,65 | Предоперационные уровни CA125 не предсказывали преимущества в выживаемости в диапазоне точек отсечения (от 400 до 3000 Ед / мл) | Возраст, гистология, стадия FIGO, степень опухоли, остаточное заболевание, время до начальной химиотерапии | ||
| Geisler JP, 1996, США [57] | NA | Серия последовательных случаев | 82 | NA | NA, 0.047 | При эпителиальной карциноме яичников высокие предоперационные уровни CA125 в сыворотке предсказывают снижение продолжительности выживания | Гистология Подстадия FIGO, степень | ||
| Gadducci A, 1995, Италия [40] | Многоцентровое ретроспективное исследование | 225 | ≥ 500 Ед / мл, <500 Ед / мл | NA | Период полувыведения CA125 в сыворотке во время ранней химиотерапии был независимым прогностическим фактором выживаемости | стадия FIGO, степень опухоли, размер остаточной болезни и период полувыведения CA125 в сыворотке | |||
| Nagele F, 1995, Австрия [58] | Январь 1984 г. — июнь 1993 г. | Ретроспективное исследование | 201 | <65 Ед / мл, ≥ 65 Ед / мл | Uni-7.45 (2,83-19,65), <0,001 Мульти-6,37 (2,39-16,97), <0,001 | Предоперационный CA125 был самым сильным прогностическим фактором для выживаемости | Возраст, стадия FIGO, степень, | ||
| Макар А.П., 1992, Норвегия [59] | с 1983 по 1990 год | Проспективное исследование | 200 | ≤ 150 Ед / мл,> 150 Ед / мл | NA, 0,035 | Предоперационная CA125 не показала любое прогностическое значение при эпителиальном раке яичников | NA | ||
| Sevelda P, 1989, Австрия [60] | NA | Проспективное исследование | 163 | ≥ 35 Ед / мл, <35 Ед / мл мл | NA, 0.13 | Предоперационный CA125 не был предиктором выживаемости | Гистологический класс, стадия FOGO, остаточная опухоль | ||
| Moebus V, 1988, Германия [61] | NA | ≥ 65 Ед / мл, <65 Ед / мл | NA, 0,005 | Значительно более длительная выживаемость была отмечена у пациентов с дооперационными значениями ниже 65 Ед / мл, чем у пациентов со значениями выше 65 Ед / мл | NA | ||||
| Cruickshank D, 1987, Aberdeen [62] | NA | Проспективное исследование | 52 | ≥ 35 Ед / мл, <35 Ед / мл | NA | Не было обнаружено корреляции между концентрациями CA125 и выживаемость | NA | ||
Одно исследование определило важность скорости снижения CA125 по сравнению с обычными прогностическими факторами выживаемости при раке яичников и обнаружило, что после univa Рентгеновский анализ, наклон кривой экспоненциальной регрессии CA125, количество циклов до нормального уровня CA125, остаточная болезнь и интенсивность лечения платиной были наиболее важными предикторами выживаемости [56].В другом исследовании оценивалась взаимосвязь между степенью повышения предоперационного CA125 и продолжительностью выживания при раке яичников. Было обнаружено, что уменьшение продолжительности жизни связано со степенью повышения CA125 до начальной исследовательской лапаротомии. Среднее начальное значение CA125 для пациентов, живущих пять и более лет (15 пациентов), составляло 899 Ед / мл, со стандартным отклонением +/- 1880 Ед / мл, в то время как CA125 для пациентов, живущих менее пяти лет (67 пациентов), составляло 1978 Ед. / мл со стандартным отклонением +/- 1,852 Ед / мл [57].
Исследование, оценивающее прогностическое значение предоперационного CA125 у пациентов с эпителиальным раком яичников I стадии, показало, что при однофакторном анализе общая выживаемость значительно снизилась у пациентов, положительных на CA125 (≥ 65 Ед / мл). Многофакторный анализ выявил предоперационный CA125 как наиболее мощный прогностический фактор для выживаемости, риск смерти от болезни в 6,4 раза выше у CA125-положительных пациентов [58]. В ходе исследования прогностическая значимость уровня СА125 в сыворотке была оценена у 687 пациентов с инвазивными эпителиальными злокачественными новообразованиями яичников.Используя многомерный анализ Кокса, предоперационный уровень CA125 в сыворотке не показал независимой прогностической значимости, тогда как послеоперационный уровень показал [59]. В исследовании уровни CA125 в сыворотке, определенные до операции и через 3 месяца после операции, оценивались как независимые прогностические факторы выживаемости. CA125 не дал дополнительной информации относительно взаимосвязи прогноза выживаемости с гистологическим классом и диаметром остаточной опухолевой массы [60].
В исследовании оценивали, улучшает ли предоперационное и послеоперационное определение CA 125 прогностическую информацию во время первичной операции.У пациентов с дооперационными значениями ниже 65 Ед / мл выживаемость была значительно выше, чем у пациентов с уровнями выше 65 Ед / мл. Повышенные послеоперационные показатели также привели к плохому прогнозу. Исследование показало, что выживаемость в этой группе составила 5% через 5 лет по сравнению с 42% для пациентов с нормальными послеоперационными показателями. Наилучший прогноз был у пациентов с до- и послеоперационными значениями ниже 65 Ед / мл [61]. В проспективном исследовании 52 пациенток со злокачественными новообразованиями яичников, наблюдавшихся в течение 3-18 месяцев, оценивалась клиническая значимость предоперационного уровня СА125 в сыворотке как онкомаркера.Данные показали, что у 41 пациента с эпителиальным раком яичников уровень CA125 хорошо коррелировал с опухолевой нагрузкой, как показано стадией FIGO. Однако не было обнаружено корреляции между концентрацией CA125 и гистопатологической степенью, также уровень CA125 не имел никакого прогностического значения [62].
Из одиннадцати исследований, рассмотренных в рамках взаимосвязи между предоперационными абсолютными уровнями СА125 в сыворотке крови и выживаемостью, шесть исследований были ретроспективными, два проспективных и одно удобное.Четыре из шести ретроспективных исследований обнаружили значительную корреляцию между предоперационными уровнями СА125 в сыворотке и выживаемостью. Одно исследование показало, что CA125 является самым сильным независимым прогностическим фактором выживаемости. Два проспективных исследования не обнаружили значительной корреляции между предоперационным уровнем CA125 в сыворотке и выживаемостью. Наконец, исследование на основе удобной выборки также зафиксировало значительную корреляцию между предоперационными уровнями CA125 в сыворотке и выживаемостью при раке яичников. Общий обзор литературы в этом разделе предполагает сильную прогностическую роль предоперационных уровней СА125 в сыворотке при раке яичников.
Абсолютная послеоперационная сыворотка CA125 и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между абсолютными послеоперационными уровнями CA125 и выживаемостью при раке яичников. Исследование показало, что послеоперационный CA125 коррелирует со стадией FIGO, степенью опухоли и общей выживаемостью [53]. Другой ретроспективный анализ 85 пациентов с повышенным уровнем СА125 в сыворотке крови после операции по поводу рака яичников показал, что абсолютные уровни СА125 в сыворотке не могут служить ориентиром для прогноза [63].Исследование показало, что у пациентов без остаточного заболевания после первичной операции гистологический тип, послеоперационный уровень CA125 с пороговым значением 35 Ед / мл и степень опухоли были независимыми прогностическими факторами выживаемости. Для пациентов с остаточной опухолью после первичной операции независимыми прогностическими факторами были гистологический тип, послеоперационное лечение, размер остаточной болезни и послеоперационный уровень СА125 в сыворотке с 65 Ед / мл в качестве порогового значения [59]. В другом исследовании с участием 132 пациентов послеоперационный CA125 оказался самым сильным независимым прогностическим фактором выживаемости по сравнению с гистологической степенью, стадией FIGO и диаметром остаточной опухолевой массы [60].В исследовании оценивалось, улучшает ли до- и послеоперационное определение CA 125 прогностическую информацию во время первичной операции. Повышенные послеоперационные показатели привели к плохому прогнозу. Исследование показало, что выживаемость в этой группе составила 5% через 5 лет по сравнению с 42% для пациентов с нормальными послеоперационными показателями. Наилучший прогноз был у пациентов с до- и послеоперационными значениями ниже 65 Ед / мл [61].
Таблица 5
Взаимосвязь между послеоперационными абсолютными уровнями СА125 в сыворотке и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования Размер | Сравниваемые группы | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |
| Осиманрик [2008, L Osimeman N ] | Январь 2001 г. — декабрь 2005 г. | Ретроспективное исследование | 68 | ≤ 500 Ед / мл,> 500 Ед / мл | NA, <0.01 | Послеоперационный CA125 коррелировал со стадией FIGO, степенью опухоли и общей выживаемостью. Снижение выживаемости было отмечено с увеличением возраста на момент операции и большей частью остаточного заболевания в послеоперационном периоде. | Возраст, гистология, стадия FIGO, степень |
| Munstedt K, 1997, Германия [63] | 1987–1994 | Ретроспективное исследование | 85 | <60 Ед / мл,> 60 Ед / мл,> 480 Ед / мл | NA | Уровни CA125 в сыворотке в течение 4 недель после операции не имели существенного значения как показатели общей выживаемости | Возраст, стадия FIGO, гистология, степени |
| Макар А.П., 1992, Норвегия [59] | 1983–1990 | Проспективное исследование | 487 | ≤ 35 Ед / мл, 36-65 Ед / мл,> 65 Ед / мл | I-1.00, (Ссылка), II- 1,56 (0,82-2,80), NS, III- 2,40 (1,42-4,06), 0,0008 | У пациентов без остаточной болезни после первичной операции, гистологический тип, послеоперационный уровень CA125 с 35 Ед / мл как пороговое значение и степень опухоли были независимыми прогностическими факторами выживаемости | Размер остаточной болезни, гистология, стадия FIGO, степень опухоли |
| Sevelda P, 1989, Австрия [60] | NA | Проспективное исследование | 132 | ≥ 35 Ед / мл, <35 Ед / мл | NA, 0.0006 | Послеоперационный CA125 был самым сильным независимым прогностическим фактором для выживаемости | Гистологический класс, стадия FOGO, остаточная опухоль |
| Moebus V, 1988, Германия [61] | NA | образец удобства | 165 | ≥ 65 Ед / мл, <65 Ед / мл | NA, 0,001 | Значительно более длительная выживаемость была отмечена у пациентов с послеоперационными значениями ниже 65 Ед / мл, чем у пациентов с послеоперационными значениями выше 65 Ед / мл | NA |
Из пяти исследований, рассмотренных в рамках взаимосвязи между послеоперационными абсолютными уровнями СА125 в сыворотке и выживаемостью, два были ретроспективными, два проспективных и одно удобное.Четыре исследования [53,59-61] показали, что послеоперационные уровни CA125 в сыворотке крови являются сильным независимым прогностическим фактором выживаемости при раке яичников. В то время как только одно исследование показало, что послеоперационная сыворотка CA15 не имеет значительной прогностической ценности [63].
Период полураспада CA125 в сыворотке и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между периодом полураспада CA125 в сыворотке и выживаемостью при раке яичников. В одном исследовании было обнаружено, что концентрация надира, остаточный объем опухоли и количество курсов химиотерапии являются независимыми прогностическими факторами для DFS и OS.Групповая классификация CA125 оказалась независимым прогностическим фактором только для DFS [64]. В другом исследовании изучались период полураспада CA125, низшее значение CA125 и время до надира. Медиана (диапазон) для кинетики CA125 составляла: 263 kU / л (5-52000 kU / л) до 1 курса, 15,8 дней (4,5-417,9 дней) для периода полувыведения CA125, 16 kU / л (3-2610 kU / л). ) для надира и 85 дней (0-361 день) для времени до надира. В моделях Кокса период полувыведения CA125, остаточная опухоль, концентрация и стадия надира были наиболее сильными прогностическими факторами для DFS и OS [38].
Таблица 6
Взаимосвязь между периодом полужизни CA125 в сыворотке и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования | Размер выборки| Группы для сравнения | RR / HR, (95% ДИ), P-Value | Заключение | Переменные, скорректированные для | |
| Riedinger [JM], 2008, | 1996–2000 гг. | Многоцентровое ретроспективное исследование | 130 | Не поддающееся оценке, ≤ 14 дней и моноэкспоненциальный спад, ≤ 14 дней и двухэкспоненциальный спад,> 14 дней | NA | Групповая классификация CA125 была как независимый прогностический фактор только для надира DFS | CA125, курсов химиотерапии, остаточной опухоли |
| Riedinger JM, 2006, Франция [38] | 1988–1996 | Многоцентровое ретроспективное исследование | 553 | ≤ 14 дней,> 14 дней | 2.04 (1,58-2,63), <0,0001 | Среди хорошо установленных прогностических факторов при раке яичников период полувыведения CA125 и надирная концентрация имеют сильное и независимое прогностическое значение | стадия FIGO, остаточная опухоль, возраст, CA125 надир |
| Gadducci A, 2004, Италия [65] | 1996-2002 | Ретроспективное исследование | 71 | ≤ 14 дней,> 14 дней | 3,11 (1,22-7,98), 0,0181 | Сыворотка Период полувыведения CA125 был независимым прогностическим фактором для вероятности достижения полного ответа на лечение, а также для выживаемости без прогрессирования и общей выживаемости | Возраст, гистология стадия FIGO, остаточная болезнь, режим химиотерапии, процентное снижение CA125 после первый курс химиотерапии |
| Colakovic S, 2000, Югославия [51] | NA | Ретроспективное исследование | 222 | <20 дней,> 20 дней | NA, 0.007 | Период полувыведения CA125 может разделить пациентов на группы с хорошим и плохим прогнозом на ранних этапах химиотерапии | Терапевтический ответ Индекс Карновского, остаточное заболевание, степень опухоли, кинетика CA125 |
| Munstedt K, 1997, Германия [63] ] | 1987–1994 | Ретроспективное исследование | 85 | <20 дней,> 20 дней | 0,6184 | Период полувыведения CA125 в сыворотке не имел значительной корреляции с выживаемостью | Возраст, стадия FIGO, гистология, степени |
| Gadducci A, 1995, Италия [40] | 1986–1992 | Мультицентрическое ретроспективное исследование | 225 | <25 дней, ≥ 25 дней | 2.13 (1,23–3,68), 0,0073 | Период полувыведения CA125 в сыворотке во время ранней химиотерапии был независимым прогностическим фактором как для достижения полного патологического ответа, так и для выживаемости | стадия FIGO, степень опухоли, размер остаточной болезни, уровень CA125 |
| Rosman M, 1994, Коннектикут [66] | Июнь 1985 г. — июль 1989 г. | Ретроспективное исследование | 51 | ≤ 12 дней,> 12 дней | 3,6 (1.8-7.4), <0,001 | У тех пациентов, у которых остаточная болезнь малого объема после первичной операции указывает на хороший прогноз, минимальные значения CA125 и CA125 t1 / 2 во время химиотерапии могут дополнительно разделить пациентов на группы с благоприятным и неблагоприятным прогнозом | стадия FIGO, степень опухоли, остаточная болезнь, CA125 |
| Yedema CA, 1993, Нидерланды [52] | июль 1984 г. — декабрь 1990 г. | Ретроспективное исследование | 60 | ≤ 20 дней,> 20 дней | 9.17 (1,49-56,3), 0,01 | Период полувыведения CA125 является независимым прогностическим фактором выживаемости у пациентов со стадией III-IV в начале курса терапии | Стадия, гистология, степень, остаточная опухоль |
| Hogberg T, 1990, Швеция [67] | 1984-1987 | Проспективное исследование | 72 | ≤ 8 дней, 8 — ≤ 12 дней, 12 <- ≤ 16 дней,> 16 дней | NA, 0,003 | Пациенты с коротким периодом полувыведения CA125 в сыворотке имели значительно лучшую вероятность выживания | Возраст, гистология Стадия FIGO, остаточная опухоль, степень |
| Hunter VJ, 1990, Durham [68] | Март 1984 — январь 1989 | Проспективное исследование | 54 | ≤ 20 дней,> 20 дней | NA, <0.015 | Общая выживаемость была значительно выше у пациентов с периодом полураспада CA125 ≤ 20 дней | NA |
| Hawkins RE, 1989, Лондон [69] | NA | Проспективное исследование | 29 | <20 дней, 20-40 дней,> 40 дней | 3,7 (0,7-20,1), 0,001; 27,8 (4,0-193), 0,001 | Период полувыведения CA125 был независимым прогностическим показателем выживаемости | Остаточная опухоль, стадия, асцит |
| van der Burg ME, 1988, Нидерланды [44] | С сентября 1979 года по декабрь 1983 года | Последовательная серия случаев | 85 | <20 дней, ≥ 20 дней | NA | Период полувыведения CA125, по-видимому, достоверно и независимо коррелировал с частотой прогрессирования и выживаемостью без прогрессирования | Стадия FIGO, гистология, гистологический класс, размер послеоперационной опухоли |
В ретроспективном исследовании 25%, 50% и 75% квартили периода полувыведения CA125 в сыворотке во время ранней химиотерапии составляли 10, 14 и 20 дней, соответственно. .Принимая значение, соответствующее квинтилю 50% (т.е. 14 дней) в качестве порогового значения, период полувыведения CA125 в сыворотке был независимым прогностическим фактором для шанса достижения полного ответа на лечение, а также для выживаемости без прогрессирования и общей выживаемости. [65]. Другое ретроспективное исследование показало, что среднее время выживания пациентов с периодом полураспада CA125 <20 дней и> 20 дней составляло 101+ и 18 месяцев, соответственно. В анализе Кокса независимые прогностические переменные выживаемости включали терапевтический ответ, индекс Карновского, остаточную болезнь, степень опухоли, период полувыведения CA125 и кинетику CA125 [51].Другое исследование показало, что остаточная болезнь, период полувыведения CA125 в сыворотке и степень опухоли сохраняли значительную ценность в прогнозировании выживаемости у 225 пациентов с распространенным эпителиальным раком яичников [40].
В другом исследовании стадия, остаточное заболевание, минимум CA 125 и CA 125 t1 / 2 по отдельности позволяли прогнозировать персистирующее заболевание или рецидив в течение 3 лет после постановки диагноза с чувствительностью 97, 70, 34 и 49% соответственно, и специфичность 33, 83, 100 и 83% соответственно [66]. Другое ретроспективное исследование обнаружило значительную положительную корреляцию между выживаемостью и (а) стадией III, (б) остаточной опухолью ≤ 1 см, (в) нормализацией СА125 после трех курсов и (г) периодом полувыведения СА125 ≤ 20 дней.Период полувыведения CA125 <или = 20 дней против> 20 дней обеспечивает независимый прогностический фактор для выживаемости у пациентов со стадиями III-IV в начале курса терапии [52].
Исследование показало, что пациенты с периодом полураспада CA125 в сыворотке короче 16 дней во время индукционной химиотерапии имели расчетную выживаемость 68% по сравнению с 18% у 49 пациентов с периодом полураспада CA125 более 16 дней [67] . В другом исследовании период полураспада CA125 менее 20 дней был связан с увеличенной общей выживаемостью.У тех пациентов, у которых в конечном итоге было обнаружено, что у них нет заболевания при хирургических процедурах наблюдения, нормализация уровней СА125 в сыворотке до уровня менее 35 Ед / мл в течение 65 дней после первичной операции также свидетельствует об улучшении выживаемости [68]. Исследование показало, что период полураспада CA125 менее 20 дней, 20-40 дней и более 40 дней, по-видимому, выявляет пациентов с хорошим, промежуточным или плохим прогнозом, двухлетняя актуарная выживаемость составляет 76%, 48% и 0%. соответственно. Изменение достижения полной ремиссии составило 15% и 67% соответственно для пациентов с периодом полувыведения СА125 из сыворотки более 20 или менее 20 дней [69].В другом исследовании пациенты с периодом полураспада 20 дней и более имели в 3,2 раза более высокую скорость прогрессирования и значительно более короткое среднее время до прогрессирования, составляющее всего 11 месяцев, по сравнению с 43 месяцами для пациентов с периодом полураспада менее 20 дней [44].
Из двенадцати исследований, рассмотренных в рамках взаимосвязи между периодом полураспада CA125 в сыворотке и выживаемостью у женщин с раком яичников, восемь исследований были ретроспективными, одно проспективное и три последовательных серии случаев. Одиннадцать исследований показали, что период полураспада CA125 в сыворотке был независимым прогностическим показателем выживаемости.
Надир сыворотки СА125 и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между надирными уровнями СА125 в сыворотке и выживаемостью при раке яичников. В одном исследовании было обнаружено, что концентрация надира, остаточный объем опухоли и количество курсов химиотерапии являются независимыми прогностическими факторами для DFS и OS [64]. В другом исследовании изучали концентрацию СА125 в надире и время до надира. Медиана (диапазон) для кинетики CA125 составляла: 16 kU / л (3-2610 kU / л) для надира и 85 дней (0-361 день) для времени до надира.В моделях Кокса период полувыведения CA125, остаточная опухоль, концентрация и стадия надира были наиболее сильными прогностическими факторами для DFS и OS [38]. Совсем недавно Кроуфорд и Пис исследовали различия в надирных уровнях CA125 в пределах нормы как прогностический фактор как для общей выживаемости, так и для выживаемости без прогрессирования. Используя произвольно определенные группы <10 Ед / мл, 11-20 Ед / мл и 21-30 Ед / мл, они продемонстрировали статистически значимое увеличение общей выживаемости только между пациентами с СА125 <10 Ед / мл (медиана выживаемости 2436 дней. ) и пациенты с CA125> 11-20 Ед / мл или 21-30 (средняя выживаемость 537 дней для обеих групп).В многофакторном анализе надир оставался очень значимым [8]. В другом исследовании у 223 пациентов с эпителиальной карциномой яичников тренд CA125 был наиболее значимой переменной, за которой следовала стадия FIGO. Исходный уровень CA125 и надир CA125, хотя и значимы, если рассматривать их отдельно, не были значимыми независимыми переменными [70].
Таблица 7
Связь между надиром CA125 и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования | Сравниваемые группы | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |
| Riedinger JM, 2008, Франция | 1996-2000 гг. | Многоцентровое ретроспективное исследование | 130 | ≤ 20 kU / L,> 20 kU / L | 4.18 (2,65-6,62), <0,0001 | Концентрация надира, остаточный объем опухоли и количество курсов химиотерапии оказались независимыми прогностическими факторами выживаемости без болезни и общей выживаемости | Курсы химиотерапии, остаточная опухоль |
| Riedinger JM, 2006, Франция [38] | 1988-1996 | Многоцентровое ретроспективное исследование | 631 | ≤ 20 kU / L,> 20 kU / L | 1,65 (1.28-2.12), <0,0001 | Период полувыведения и минимальная концентрация CA125 являются важными независимыми прогностическими факторами. Концентрация надира CA125 и время достижения надира имели одномерное прогностическое значение для выживаемости без болезни и общей выживаемости | Возраст, стадия FIGO, остаточная опухоль, период полувыведения CA125 |
| Crawford SM, 2005, [8] | 1988 по 2000 год | Ретроспективное исследование | 79 | ≤ 10 Ед / мл, 11-20 Ед / мл, 21-30 Ед / мл | NA, <0.001 | Группа надира была единственным прогностическим фактором общей выживаемости, который оставался очень значимым (P <0,001) после того, как действие других факторов было разрешено для | Тип химиотерапии, уровень CA125 на третьем курсе |
| Gard GB, 1994, Австралия [70] | 1985–1991 | Ретроспективное исследование | 223 | > 35 Ед / мл, 15-35 Ед / мл, <15 Ед / мл | Uni- 3,23 ( 2.62-3.99), <0.0001 Мульти-0,85 (0,54-1,33), 0,476 | Начальный уровень CA125 и надир CA125, хотя и значимы, если рассматривать их отдельно, не были значимыми независимыми переменными | Типы опухолей, стадия FIGO, остаточная болезнь, CA125 |
Все четыре исследования, рассмотренных в рамках взаимосвязи между надиром CA125 и выживаемостью, были ретроспективными. Все исследования показали, что концентрация надира была независимым прогностическим фактором для выживаемости без болезней и общей выживаемости.Примечательно, что в одном из этих исследований [70] сообщается, что исходный уровень CA125 и надир CA125 были признаны значимыми, если рассматривать их отдельно, но не были значимыми как независимые переменные.
Время достижения надира CA125 и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между временем достижения надира CA125 и выживаемостью при раке яичников.
Таблица 8
Взаимосвязь между временем достижения надира CA125 уровней и выживаемостью при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования Размер | Сравниваемые группы | RR / HR, (95% ДИ), значение P | Заключение | Переменные, скорректированные для | |
| 38] | 1988–1996 | Многоцентровое ретроспективное исследование | 553 | ≤ 72 дней,> 72 дней | Одномерный анализ 0.67 (0,63-0,71) <0,0001 | Концентрация СА125 в надире и время до надира имели однофакторное прогностическое значение для выживаемости без болезни и общей выживаемости. В моделях Кокса концентрация надира была наиболее сильным прогностическим фактором выживаемости без болезней | NA |
| Frasci G, 1996, Италия [71] | 1985–1990 | Серия последовательных случаев | 54 | ≤ 1 мес.,> 1 мес. | 0.009 | Выживаемость пациентов с распространенным раком яичников можно точно спрогнозировать, учитывая вместе некоторые переменные перед лечением и время до нормализации CA125, без выполнения повторной лапаротомии | Остаточная опухолевая нагрузка после операции, статус работы Восточной кооперативной кооперативной Онкологической группы (ECOG) |
В одном исследовании изучали концентрацию СА125 в надире и время до надира. В моделях Кокса период полувыведения CA125, остаточная опухоль, концентрация и стадия надира были наиболее сильными прогностическими факторами для DFS и OS.Это исследование пришло к выводу, что среди хорошо установленных прогностических факторов рака яичников период полувыведения CA125 и концентрация надира имеют сильное и независимое прогностическое значение [38]. В другом исследовании оценивалось включение времени нормализации CA125 в прогностическую модель на основе переменных до лечения у пациентов с карциномой яичников, чтобы определить, могут ли они сделать повторную лапаротомию (SLL) избыточной. Время до нормализации уровней CA125 в сыворотке (анализируемое либо как непрерывная, либо как двухкатегориальная переменная) играло независимую прогностическую роль при включении в модель.Пациенты с хорошими прогностическими переменными до лечения и пациенты с промежуточным прогнозом в начале терапии, у которых была быстрая нормализация CA125, имели 80% 5-летнюю выживаемость по сравнению с 16% 5-летней выживаемостью у остальных пациентов [71].
CA125 Площадь под кривой (AUC) и выживаемость при раке яичников
В исследовании оценивалась полезность CA125, нормализованная по временной площади под кривой (CA125 AUC), для сигнализации рецидива эпителиального рака яичников. Данные 111 пациентов были представлены для двух разных подходов на основе значений увеличения AUC CA125 для прогнозирования рецидива у пациента.В Критерии A лучшая точность была достигнута с коэффициентом (F) 1,25 (увеличение на 25% от предыдущего статуса), в то время как в Критерии B лучшая точность была достигнута с порогами отсечки 25, 50, 75 и 100 МЕ / мл. Среднее время заблаговременности до рецидива, достигнутое с помощью критерия A, составило 181 день, а с критерием B — соответственно 131, 111, 63 и 11 дней. На основании результатов этого исследования был сделан вывод, что сопряжение и последовательное применение обоих критериев для выявления рецидивов у пациентов должно быть весьма целесообразным [72].В другом исследовании изучали полезность площади под кривой CA125 (AUC) в качестве нового кинетического параметра для прогнозирования общей выживаемости. У пациентов с полным ответом на первичную химиотерапию средняя AUC СА125 составляла 48,8, у пациентов с частичным ответом — в среднем 251,7 МЕ / мл * день, а у пациентов без ответа или прогрессирования заболевания — в среднем 316,5 МЕ / мл * дней. Наилучшие показатели AUC CA125 заключаются в прогнозировании полного ответа пациента на химиотерапию с пороговым значением 100 МЕ / мл * дней и точностью 82% [73].
Продольный уровень CA125 в сыворотке и выживаемость при раке яичников
В таблице обобщены эпидемиологические исследования связи между продольными уровнями CA125 и выживаемостью при раке яичников.
Таблица 9
Продольные исследования уровней CA125 в сыворотке и выживаемости при раке яичников
| Первый автор, год, место исследования | Сбор данных | Дизайн исследования | Размер выборки| Группы для сравнения | RR / HR, (95% CI), P-Value | Заключение | Переменные, скорректированные для | |
| Riedinger [JM], 2007, | 1988–1996 гг. | Многоцентровое исследование | 494 | ≥ 75% уменьшение, <75% уменьшение или увеличение | Одномерное — 1.92 (1,34-2,74), <0,0001 3,08 (2,10-4,50), <0,0001 Многовариантный-0,90 (0,59-1,39), NS 0,97 (0,59-1,59), NS | Изменение CA125 после первого курса Результаты КТ были независимыми прогностическими факторами как для достижения полного патологического ответа, так и для общей выживаемости. | Возраст, гистология Стадия FIGO, остаточная опухоль |
| Markman M, 2006, США [37] | NA | Продольное исследование | 291 | I> 100, ≤ 35 ед / мл II 36-99, ≤ 35 ед / мл III> 100, 36-99 ед / мл | I — 3.0 (1,7-8,6), 0,0001 II — 1,6 (0,9-2,8), 0,09 III-1,8 (1,0-3,5), 0,07 | В то время как значения CA125 до лечения не коррелировали с выживаемостью, концентрация CA125 8 Через несколько недель после начала терапии это был мощный независимый прогностический фактор. | Возраст, работоспособность, стадия заболевания, измеримое заболевание, лечение, некроз опухоли, склероз стромы |
Первое исследование было многоцентровым [47], проведенным для оценки прогностической ценности изменения CA125 после первого и вторые курсы индукционной химиотерапии.Определение CA125 у всех пациентов проводили перед каждым циклом химиотерапии (в среднем каждые 3 недели). Данные этого исследования показали, что раннее изменение CA125, вызванное первыми курсами химиотерапии, сильно коррелировало как с вероятностью достижения полного патологического ответа после химиотерапии, так и с продолжительностью выживания. В другом исследовании [37] оценивалась взаимосвязь между выживаемостью и ранними изменениями сывороточного уровня антигена CA125 у пациентов с распространенным раком яичников.В то время как значения CA125 до лечения не коррелировали с выживаемостью, концентрация CA125 через 8 недель после начала терапии была мощным независимым прогностическим фактором.
Обсуждение
Эпителиальный рак яичников довольно распространен с высокими показателями в Скандинавии, средними показателями в Западной Европе и Северной Америке и низкими показателями в развивающихся странах и Японии. Пятилетняя выживаемость составляет менее 40% [74]. Были разработаны различные биомаркеры для мониторинга роста рака яичников и выявления заболевания на ранней стадии [17].Среди них CA125 был наиболее широко изученным и клинически используемым сывороточным онкомаркером. В качестве клинического инструмента прогностические маркеры, такие как CA125, потенциально могут помочь индивидуализировать лечение внутри подгрупп пациентов. Уровни СА125 в сыворотке крови используются для мониторинга реакции на химиотерапию, рецидива и прогрессирования заболевания у пациентов с раком яичников [31,75]. Уровень CA125 может быть повышен в сыворотке до клинического развития первичной и рецидивирующей карциномы яичников [76]. В настоящее время широко признано, что онкомаркер CA125 является прогностическим и прогностическим фактором при CA125-положительном раке яичников.
В диагностике заболевания, прогнозе и мониторинге лечения концентрация CA125 в сыворотке была признана очень важным инструментом. Важной характеристикой CA125 является способность отражать изменения массы опухоли во время химиотерапии или в период наблюдения после завершения терапии [77]. Послеоперационный уровень CA125 в сыворотке крови является независимым прогностическим фактором у пациентов с инвазивным раком яичников [59], а период полураспада опухолевого маркера CA125 (t1 / 2) и время удвоения опухолевого маркера (DT) часто используются в качестве кинетических параметров для оценки клинический ответ и наблюдение за пациентами с раком яичников [78].Период полувыведения CA125 в сыворотке во время ранней химиотерапии является независимым прогностическим фактором как для достижения патологически полного ответа, так и для выживаемости пациентов с распространенным эпителиальным раком яичников [40], и в нескольких исследованиях сообщается, что наибольшая разница в скорости прогрессирования была обнаружена при t1 / 2 20 дней [44,51,68,69,73]. В то время как уровни CA125 на момент постановки диагноза имеют ограниченное прогностическое значение, измерения CA125 в настоящее время выполняются почти рутинно во время курса химиотерапии.Снижение уровней CA125 после циторедуктивной хирургии и во время начальных курсов химиотерапии использовалось в качестве индикатора клинического исхода [5]. Несмотря на всеобщее признание того, что CA125 является прогностическим маркером, остается неясным, насколько точно серийные измерения CA125 могут предсказать общую долгосрочную выживаемость у пациентов с распространенным раком яичников [79].
В настоящем обзоре обобщены результаты исследований, посвященных оценке взаимосвязи между уровнями СА125 в сыворотке крови и выживаемостью при раке яичников.В этот обзор были включены все исследования, в которых оценивалась взаимосвязь между прехимиотерапией, постхимиотерапией, во время химиотерапии, предоперационными, послеоперационными абсолютными уровнями СА125 в сыворотке, периодом полувыведения СА125, низкими уровнями СА125, временем достижения надира уровня и выживаемостью при раке яичников. Также были рассмотрены исследования, оценивающие взаимосвязь между новым кинетическим параметром AUC (площадь под кривой), а также продольные исследования CA125 и выживаемости при раке яичников.
Большинство рассмотренных исследований имели ретроспективный дизайн.На сегодняшний день было проведено только четыре проспективных исследования, из которых в двух [41,62] было очень мало случаев (n <55), что указывает на ограниченные возможности для выявления ассоциаций. Проспективные исследования являются предпочтительным дизайном исследований, поскольку они менее подвержены различным типам систематических ошибок и обеспечивают наилучшие оценки риска. Таким образом, необходимы дальнейшие проспективные исследования для четкого понимания взаимосвязи между уровнями СА125 в сыворотке и выживаемостью при раке яичников. Также в большинстве рассмотренных исследований отсутствует информация об оценках относительного риска, связанного с различными уровнями CA125.
Ранее были попытки Hogdall [19] и Gadducci et al. [80] для обзора литературы по CA125 и выживаемости при раке яичников. В обзоре Hogdall рассматривается недавно сообщенный прогресс в CA125 как прогностическом маркере у пациентов с раком яичников. Основное внимание в нем уделялось недавним публикациям по этой теме и исключены некоторые исследования уровней CA125 во время химиотерапии, времени достижения надира и уровней AUC CA125. Еще один очень информативный обзор Gadducci et al. были сосредоточены на всех сывороточных и тканевых биомаркерах рака яичников, а не только на CA125.Кроме того, в него не были включены все возможные исследования по CA125, потому что в центре внимания статьи была не только CA125. Мы полагаем, что настоящий обзор дает очень всестороннюю оценку существующей литературы о прогностической роли CA125 при раке яичников.
Мы пришли к выводу, что, хотя результаты различных исследований иногда противоречат друг другу, уровень CA125 в сыворотке является сильным прогностическим фактором для общей выживаемости и выживаемости без прогрессирования при раке яичников. Существует обратная зависимость между уровнем СА125 в сыворотке и выживаемостью при раке яичников.Снижение уровня обычно указывает на положительный ответ на терапию рака, в то время как повышение уровня указывает на рецидив опухоли и плохую выживаемость. Дальнейшие исследования по этой теме должны быть сосредоточены на проспективных лонгитюдных исследованиях, оценивающих влияние изменений сывороточных уровней СА125 на выживаемость.
Как проверить наличие рака яичников
Лишь около 20% случаев рака яичников обнаруживаются на ранней стадии. Когда рак яичников обнаруживается на ранней стадии, около 94% пациентов живут дольше 5 лет после постановки диагноза.
Способы ранней диагностики рака яичников
Регулярные медицинские осмотры женщин
Во время гинекологического осмотра медицинский работник проверяет яичники и матку на предмет размера, формы и консистенции. Осмотр органов малого таза может быть полезен, поскольку с его помощью можно обнаружить некоторые виды рака у женщин на ранней стадии, но большинство ранних опухолей яичников трудно или невозможно обнаружить. Однако обследование органов малого таза может помочь найти другие виды рака или женские заболевания. Женщинам следует обсудить необходимость этих обследований со своим врачом.
Скрининговые тесты, используемые для выявления рака шейки матки, такие как Пап-тест или тест на ВПЧ (вирус папилломы человека), не являются эффективными тестами на рак яичников. Изредка рак яичников выявляется с помощью мазка Папаниколау, но обычно он находится на поздней стадии.
При появлении симптомов обратитесь к врачу
Ранний рак яичников часто протекает бессимптомно. Симптомы рака яичников также могут быть вызваны другими, менее серьезными заболеваниями. К тому времени, когда рак яичников считается возможной причиной этих симптомов, он обычно уже распространился.Кроме того, некоторые виды рака яичников могут быстро распространяться на близлежащие органы. Своевременное внимание к симптомам может повысить шансы ранней диагностики и успешного лечения. Если у вас есть симптомы, похожие на симптомы рака яичников, почти ежедневно в течение более чем нескольких недель, немедленно сообщите о них своему врачу.
Скрининговые тесты на рак яичников
Скрининговые тесты и экзамены используются для выявления таких заболеваний, как рак, у людей без каких-либо симптомов. (Например, маммография часто позволяет обнаружить рак груди на самой ранней стадии, даже до того, как врач почувствует рак.)
Было проведено много исследований по разработке скринингового теста на рак яичников, но пока они не увенчались успехом. Два теста, которые наиболее часто используются (в дополнение к полному осмотру органов малого таза) для выявления рака яичников, — это трансвагинальное ультразвуковое исследование (TVUS) и анализ крови CA-125 .
- TVUS (трансвагинальное ультразвуковое исследование) — это тест, в котором используются звуковые волны для осмотра матки, маточных труб и яичников путем введения ультразвуковой палочки во влагалище.Он может помочь найти новообразование (опухоль) в яичнике, но на самом деле не может сказать, является ли новообразование злокачественным или доброкачественным. Когда он используется для скрининга, большинство обнаруженных новообразований не являются раком.
- Анализ крови CA-125 измеряет количество белка CA-125 в крови. Многие женщины с раком яичников имеют высокий уровень СА-125. Этот тест может быть полезен в качестве онкомаркера, чтобы помочь в лечении женщин с раком яичников, потому что высокий уровень часто снижается, если лечение работает.Но выяснилось, что проверка уровня CA-125 не так полезна, как скрининговый тест на рак яичников. Проблема с использованием этого теста для скрининга рака яичников заключается в том, что высокие уровни CA-125 чаще всего вызваны такими общими состояниями, как эндометриоз и воспалительные заболевания органов малого таза. Кроме того, не у всех больных раком яичников высокий уровень СА-125. Если у кого-то, у кого нет данных о раке яичников, наблюдается аномальный уровень CA-125, врач может повторить тест (чтобы убедиться, что результат правильный) и может рассмотреть возможность проведения трансвагинального ультразвукового исследования.
Изучаются более эффективные способы скрининга на рак яичников, но в настоящее время надежных скрининговых тестов нет. Надеемся, что улучшение скрининговых тестов в конечном итоге приведет к снижению смертности от рака яичников.
Если вы находитесь в группе среднего риска
Не существует рекомендуемых скрининговых тестов на рак яичников для женщин без симптомов и не подверженных высокому риску развития рака яичников. В исследованиях женщин со средним риском рака яичников использование TVUS и CA-125 для скрининга привело к большему количеству тестов, а иногда и большему количеству операций, но не снизило количество смертей, вызванных раком яичников.По этой причине ни одна крупная медицинская или профессиональная организация не рекомендует рутинное использование TVUS или анализа крови CA-125 для выявления рака яичников у женщин со средним риском.
Если вы в группе высокого риска
Некоторые организации заявляют, что TVUS и CA-125 могут быть предложены для скрининга женщин с высоким риском рака яичников из-за наследственного генетического синдрома, такого как синдром Линча, мутации гена BRCA или сильная семейная история рака груди и яичников.Тем не менее, даже у этих женщин не было доказано, что использование этих тестов для скрининга снижает их шансы умереть от рака яичников.
Скрининговые тесты на опухоли половых клеток / стромальные опухоли
Не существует рекомендуемых скрининговых тестов на опухоли половых клеток или стромальные опухоли. При некоторых злокачественных опухолях зародышевых клеток в кровь выделяются определенные белковые маркеры, такие как хорионический гонадотропин человека (ХГЧ) и альфа-фетопротеин (АФП). После того, как эти опухоли излечены хирургическим путем и химиотерапией, можно использовать анализы крови на эти маркеры, чтобы увидеть, работает ли лечение, и определить, возвращается ли рак.
CA125 анализ крови | Целевой рак яичников
Найдите ответы на часто задаваемые вопросы, связанные с анализом крови CA125. Если у вас есть вопросы, которых здесь нет, позвоните в нашу службу поддержки по телефону 020 7923 5475 или обратитесь к своему терапевту.
- Что такое анализ крови на CA125?
CA125 — это белок, который содержится в крови.
Небольшой образец крови будет взят из вашей руки и отправлен в лабораторию, где простой тест определит уровень CA125 в вашем образце крови.
У большинства здоровых женщин уровень CA125 обычно составляет менее 35 единиц на миллилитр (ед / мл). Однако у некоторых женщин в крови действительно высокий уровень СА125.
Помимо помощи в диагностике рака яичников, анализы крови CA125 иногда используются для наблюдения за лечением рака яичников или выявления признаков рецидива (если рак вернулся). Для получения дополнительной информации об использовании анализа крови CA125 вы можете поговорить с одним из наших медсестер-консультантов, связавшись с нашей линией поддержки по телефону 020 7923 5475.
- Когда мне следует запросить анализ крови на CA125?
Симптомы, включая стойкое вздутие живота, быстрое чувство сытости и / или потерю аппетита, боль в области таза или живота и необходимость мочиться чаще или срочно, чем обычно, иногда вызваны раком яичников.
Если у вас есть один или несколько из этих симптомов часто и постоянно, маловероятно, что у вас будет рак яичников, но ваш терапевт исключит такую возможность. Анализы крови CA125 — полезный способ собрать дополнительную информацию и помогут вашему терапевту решить, что делать дальше.
Если вас беспокоят эти симптомы, спросите своего терапевта о раке яичников и сдайте анализ крови на CA125.
- Как мне подготовиться к анализу крови на CA125?
Ваш терапевт может посоветовать вам не проходить тест, если у вас месячные, поскольку это может повлиять на результат. Если ваша кровь проверяется только на CA125, вы можете нормально есть и пить перед анализом и сразу же возобновить свою обычную деятельность.
- Означает ли результат CA125 выше 35 ед / мл, что у меня рак яичников?
№Уровень CA125 в крови может повышаться по многим причинам, включая эндометриоз, менструацию, кисты яичников, а иногда и рак яичников. Это одна из причин, по которой его нельзя точно использовать в качестве скринингового теста на рак яичников.
Если уровень CA125 в вашей крови составляет 35 ед / мл или выше, ваш терапевт должен организовать для вас ультразвуковое сканирование живота и таза. Ультразвуковое сканирование создаст снимки ваших яичников, чтобы их можно было проверить на предмет чего-либо необычного, и поможет вашему терапевту собрать больше информации.В некоторых районах Великобритании анализ крови на CA125 и ультразвуковое сканирование будут заказаны одновременно.
- Означает ли результат CA125 ниже 35 ед / мл, что у меня нет рака яичников?
У большинства женщин с результатом ниже 35 ед / мл не будет рака яичников. Однако у небольшого числа женщин с раком яичников результат теста CA125 будет ниже 35 ед / мл.
Если ваши симптомы продолжаются или ухудшаются, вы должны вернуться к своему терапевту, сообщить ему об этом и назначить встречу для проверки в течение одного месяца.
Следующие шаги
Как мне получить результат теста?
Ваш терапевт сообщит вам, через какое время ваш результат теста должен вернуться из лаборатории, а также расскажет, как узнать результат вашего теста. Однако, если вы ничего не услышите в течение двух недель, позвоните своему терапевту — иногда результаты теряются. Если вы получили результаты своего теста и не уверены, что они означают, вернитесь к своему терапевту и попросите разъяснений.
Если ваш результат анализа составляет около 35 ед / мл, ваш терапевт назначит дополнительные анализы или назначит повторный прием.
Что делать, если мои симптомы не исчезнут?
Если ваш уровень CA125 ниже 35 ед / мл, но симптомы продолжаются или ухудшаются, вы должны вернуться и сообщить об этом своему терапевту в течение месяца. Почему бы не вести дневник симптомов [PDF]? Ежедневно делайте быстрые записи о каждом симптоме и о том, насколько он серьезен. Это может помочь вашему терапевту определить причину ваших симптомов.
Для получения дополнительной информации о том, как получить максимум от посещения терапевта, ознакомьтесь с нашими главными советами.
Если после прочтения этой информации у вас возникнут дополнительные вопросы, обратитесь к своему терапевту или позвоните в нашу службу поддержки по телефону 020 7923 5475.
Эта информация регулярно проверяется и соответствует принятым национальным и международным нормам. Все наши публикации проходят экспертную рецензию и рецензируются женщинами с раком яичников, чтобы гарантировать, что мы предоставляем точную и качественную информацию. Чтобы узнать больше, ознакомьтесь с нашими информационными стандартами.
Повышенный СА 125 в СЛУЧАЕ утечки эндометриомы
Чрезвычайно повышенный СА 125, обычно указывающий на злокачественность яичников, может быть обнаружен при физиологических или доброкачественных состояниях, таких как эндометриоз.Мы представляем случай чрезвычайно повышенного уровня СА 125 в сыворотке у пациентки с эндометриозом четвертой стадии и двусторонними неразорвавшимися эндометриомами яичников с признаками односторонней утечки. Чтобы избежать дорогостоящих и излишне инвазивных тестов и процедур, важно рассмотреть возможность дифференциальной диагностики эндометриоза и / или протекающей эндометриомы у пациентов с сильно повышенным уровнем СА 125.
1. Введение
Раковый антиген (CA) 125 представляет собой высокомолекулярный гликопротеин, который происходит из целомического эпителия, который экспрессируется нормальными тканями, такими как эндометрий, брюшина, перикард и эпителиальная карцинома яичников (EOCs) [ 1].Чаще всего он используется в качестве биомаркера EOC для целей диагностики, мониторинга прогрессирования заболевания и ответа на лечение [2]. CA 125 также играет важную роль в дифференциации доброкачественных и злокачественных новообразований малого таза, особенно до операции, поскольку считается, что более высокие уровни CA 125 коррелируют с более высокой вероятностью злокачественного новообразования [2]. Однако уровни CA 125 в сыворотке могут быть повышены при других злокачественных новообразованиях, а также при различных физиологических и доброкачественных состояниях, таких как эндометриоз, миома матки, воспалительные заболевания органов малого таза, ранняя беременность и нормальная менструация [2, 3].Положительная прогностическая ценность CA 125 для рака яичников высока среди женщин в постменопаузе (96%) [4], но связана с более низкой специфичностью среди женщин в пременопаузе, учитывая различные доброкачественные состояния, которые могут приводить к повышению уровня CA 125 [2]. Следовательно, доброкачественные состояния, такие как эндометриоз, следует рассматривать как дифференциальный диагноз в контексте повышенного уровня СА 125, особенно среди женщин в пременопаузе. Сильно повышенный СА 125 при отсутствии злокачественных новообразований встречается редко; мы изучаем литературу по аналогичным случаям, чтобы помочь в оценке и ведении таких пациентов.
2. Изложение клинического случая
Нерожавшая женщина 27 лет поступила в отделение неотложной помощи с жалобами на боли в животе на фоне хронических болей в области таза.
При поступлении на УЗИ органов малого таза был продемонстрирован увеличенный правый яичник объемом 150 см3 с кистой размером 6,5 см и низким внутренним эхосигналом. Компьютерная томография (КТ) брюшной полости также показала кисту правого яичника плотностью 6,5 см с умеренным объемом свободной жидкости и без признаков аппендицита.Онкомаркеры, взятые во время острого проявления, продемонстрировали уровень СА 125 в сыворотке 8142 Ед / мл (референсный диапазон: <35 Ед / мл), который значительно увеличился с 115 Ед / мл при выполнении за 12 месяцев до этого. Уровни сывороточного альфа-фетопротеина (AFP) и хорионического гонадотропина человека (ХГЧ) были <2 Ед / мл.
Она была направлена в гинекологическую клинику при больнице Вестмид для дальнейшего неотложного обследования и лечения. Ультразвуковое сканирование при глубоком инфильтративном эндометриозе (DIE) подтвердило наличие кисты правого яичника (6.3 x 5,0 x 4,4 см) с кишечником, прилегающим к задней части матки. В это время было запрошено гинекологическое онкологическое заключение в свете значительного повышения CA 125, рекомендовавшего повторный уровень через 2 недели при предварительном диагнозе эндометриоза после просмотра ультразвуковых изображений и анамнеза пациента при первоначальном обращении. Повторное измерение уровня СА 125 в сыворотке, проведенное через две недели после ее первоначального обращения, продемонстрировало более низкий, но все же значительно повышенный уровень 2038 Ед / мл (день 12).Сывороточный карциноэмбриональный антиген (CEA) и CA 19.9 были <2 Ед / мл и 430 Ед / мл (референсный диапазон: <37 Ед / мл), соответственно.
Было проведено многопрофильное обсуждение с гинекологом-онкологом для определения дальнейшего лечения. Основываясь на изображениях и снижении уровня СА 125 в сыворотке, утечка эндометриоза из эндометриомы яичника была сочтена наиболее вероятной, а злокачественная опухоль яичников была основным дифференциальным и маловероятным диагнозом.
При лапароскопии на 58-е сутки были выявлены эндометриоз четвертой стадии и двусторонние неразорвавшиеся эндометриомы яичников с признаками одностороннего подтекания.Широко распространенные эндометриоидные отложения были обнаружены на верхней и передней брюшной стенке, сальнике и двусторонних маточно-крестцовых связках, вероятно, вторичных по отношению к протекающей эндометриоме (Рисунки 1 и 2). Были выполнены лапароскопическое удаление эндометриоза, двусторонний уретеролиз, двустороннее удаление эндометриомы и введение внутриматочной спирали Мирена © .
Гистопатологическое исследование подтвердило диагноз эндометриомы. Пациент выздоровел без осложнений и был выписан на третьи послеоперационные сутки.На третьей послеоперационной неделе состояние пациента оставалось стабильным, и было рекомендовано плановое наблюдение у терапевта.
3. Обсуждение
CA 125 был впервые идентифицирован как антиген рака яичников в 1981 году [19] и позже был разработан как биомаркер для EOC, когда уровни сыворотки> 35 U / мл были обнаружены более чем у 80% пациентов с EOC, но только 1% здоровых женщин [4]. Положительная прогностическая ценность CA 125 (> 95 МЕ / мл) для рака яичников высока среди женщин в постменопаузе (96%) [4] и связана с высокой чувствительностью и специфичностью, 69-97% и 81-93%. соответственно [20].Хотя чаще всего используется при EOC, уровни CA 125 в сыворотке могут быть повышены при других злокачественных новообразованиях и различных физиологических и доброкачественных состояниях, включая эндометриоз [2, 3]. Следовательно, CA 125 связан с более низкой специфичностью среди женщин в пременопаузе, учитывая различные доброкачественные состояния, которые могут приводить к повышенному уровню CA 125 [2, 21] и физиологическому периоду полувыведения из сыворотки приблизительно 6 дней [22]. Поэтому плановый уровень СА 125 не рекомендуется всем женщинам в пременопаузе с простой кистой яичника [23].
Пациенты с эндометриозом часто не имеют уровней СА 125> 100 Ед / мл [13, 16]. Тем не менее, эндометриоз — одно из наиболее распространенных доброкачественных состояний, связанных с повышенным уровнем СА 125 в сыворотке [14]. CA 125 широко изучался как биомаркер эндометриоза, и два метаанализа пришли к выводу, что он имеет ограниченную полезность в качестве диагностического маркера эндометриоза, учитывая его низкую чувствительность (20-50%) [1, 24, 25]. Это подтверждается международными рекомендациями по эндометриозу, которые не рекомендуют измерение уровня СА 125 в сыворотке как часть рутинного диагностического обследования [26].Связь между повышенным уровнем СА 125 и эндометриозом хорошо известна в литературе, причем уровни отражают как тяжесть, так и прогрессирование заболевания [3, 27, 28]. Повышенные уровни СА 125 в сыворотке часто связаны с эндометриомами яичников и эндометриозом более высокой степени тяжести, например с третьей и четвертой стадиями [3, 14, 23, 29]. Также было показано, что уровни CA 125 снижаются как после медикаментозного, так и после хирургического лечения эндометриоза [10, 29].
Сообщалось о чрезвычайно повышенных уровнях CA 125 при наличии как разорванных [5, 7, 9, 10, 12, 30], так и неразорвавшихся эндометриом [13–18] (таблицы 1 и 2).Самый высокий уровень СА 125, зарегистрированный при доказанном эндометриозе, составляет 9537 Ед / мл после острого разрыва эндометриомы [7]. В данном случае мы сообщаем о чрезвычайно повышенном уровне СА 125 в сыворотке 8142 Ед / мл у пациентки с эндометриозом четвертой стадии, двусторонними неразорвавшимися эндометриомами яичников с признаками одностороннего протекания и широко распространенными эндометриотическими отложениями при осмотре во время операции. Предыдущий наивысший уровень СА 125 в контексте неразорвавшейся эндометриомы составлял 7900 Ед / мл [16].Это имеет важное клиническое значение, так как повышенный уровень СА 125, особенно при наличии образования в тазу, может имитировать и вызывать подозрение на злокачественный процесс, ведущий к излишне инвазивным процедурам [15, 30]. Информирование пациента о значении повышенного маркера опухоли при отсутствии злокачественной опухоли имеет первостепенное значение, учитывая чувствительность к потенциальному эмоциональному стрессу, который могут вызвать такие слова. Решение о лечении как доброкачественного гинекологического состояния по сравнению с потенциально злокачественным заболеванием следует обсудить.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 I триместр беременности, цирроз печени, хронический гепатит, панкреатит, аутоиммунные заболевания.
I триместр беременности, цирроз печени, хронический гепатит, панкреатит, аутоиммунные заболевания.


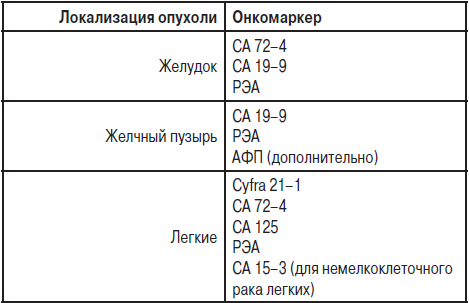 д., а также при беременности.
д., а также при беременности.