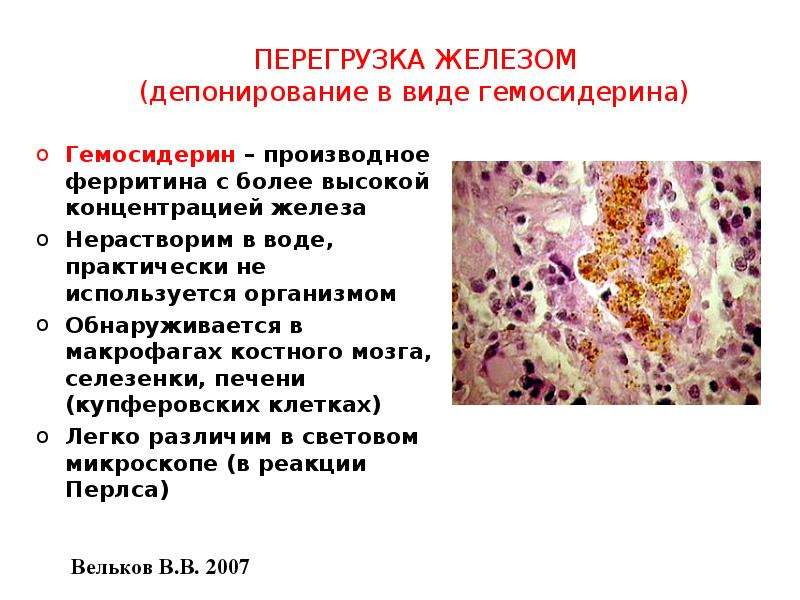
Гемосидероз — Справочник заболеваний
Гемосидероз — отложение гемосидерина в тканях организма из-за избыточного образования его макрофагами при усиленном распаде эритроцитов.
Общая информация
Заболевание возникает в результате нарушения утилизации гемосидерина в процессе эритроцитопоэза, он усиленно всасывается в кишечнике, нарушается обмен железосодержащих пигментов. В организме человека содержится 4-5 граммов железа, которое содержится в составе гемопротеидов, ферритина и гемосидерина. При избытке железа гемосидерин накапливается в тканях организма, что приводит к повреждению лизосом.
Гемосидероз обычно является симптомом какого-либо заболевания:
- наследственных гемолитических анемий — энзимопатии, гамоглобинопатии
- приобретенных гемолитических анемий — аутоиммунных
- при гипопластических и рефракторных анемиях
- инфекционных заболеваниях (бруцеллезе, возвратном тифе, малярии)
- отравлениях гемолитическими ядами
- частых гемотрансфузиях
- циррозе печени
В качестве самостоятельных заболеваний выделяют:
- эссенциальный легочный гемосидероз (поражается только легочная ткань)
- гемохроматоз (наследственное заболевание, нарушение всасывания железа в кишечнике, и накопление его в тканях)
- гемосидероз кожи (гемосидерин откладывается в коже нижних конечностей.
 Проявляется пятнами коричнево-красного цвета, не пропадающими при надавливании. Может быть спровоцировано расстройством кровообращения конечностей. Чаще всего встречается у мужчин.)
Проявляется пятнами коричнево-красного цвета, не пропадающими при надавливании. Может быть спровоцировано расстройством кровообращения конечностей. Чаще всего встречается у мужчин.)
Виды гемосидероза
Местный гемосидероз. Развивается при внесосудистом (экстраваскулярном) гемолизе в местах кровоизлияний. Накопление гемосидерина не повреждает ткань или орган, но если онсочетается со склерозом, то функция органа или ткани нарушается.
Общий гемосидероз. Развивается при избытке железа из-за внутрисосудистого (интраваскулярного) гемолиза или при повышении всасывания железа из пищи. Гемосидерин откладывается преимущественно в гепатоцитах, макрофагах печени, селезёнки, костного мозга и других органах. Как правило, пигмент не повреждает паренхиматозные клетки и не вызывает нарушений функций органа. В случае, если избыток железа сочетается с повреждением тканей с атрофией паренхимы, склерозом, снижением функции органа, то это называется гемохроматоз.
Лечение
Для диагностики проводится анализ крови для определения содержания железа и железосвязывающей способности крови. С помощью биопсии и трепанобиопсии получают ткани печени или костного мозга для гистологического исследования, в которых выявляют железо. Еще одним из методов диагностики является десфераловая проба: пациенту вводят внутримышечно десферал, а затем в течение 6-24 часов собирают мочу, в которой определяют количество железа.
С помощью биопсии и трепанобиопсии получают ткани печени или костного мозга для гистологического исследования, в которых выявляют железо. Еще одним из методов диагностики является десфераловая проба: пациенту вводят внутримышечно десферал, а затем в течение 6-24 часов собирают мочу, в которой определяют количество железа.
Лечение заключается в выявлении и терапии основного заболевания.
Диагностика гемосидероза | Российский аграрный портал
Гемосидерозом принято называть состояние тканей с патологически повышенным содержанием темно-желтого, коричневатого пигмента – гемосидерина, откладывающегося в толще цитоплазмы аморфными, сильно преломляющими свет зёрнами. Общее чрезмерное накопление гемосидерина в организме вызывает избыток железа при внутрисосудистом (интраваскулярном) гемолизе либо это связано с повышенным всасыванием железа из потребляемых продуктов питания. Гемосидероз бывает местный – очаговый (при гемолизе внесосудистом) и общий – генерализованный (гемолиз — внутрисосудистый).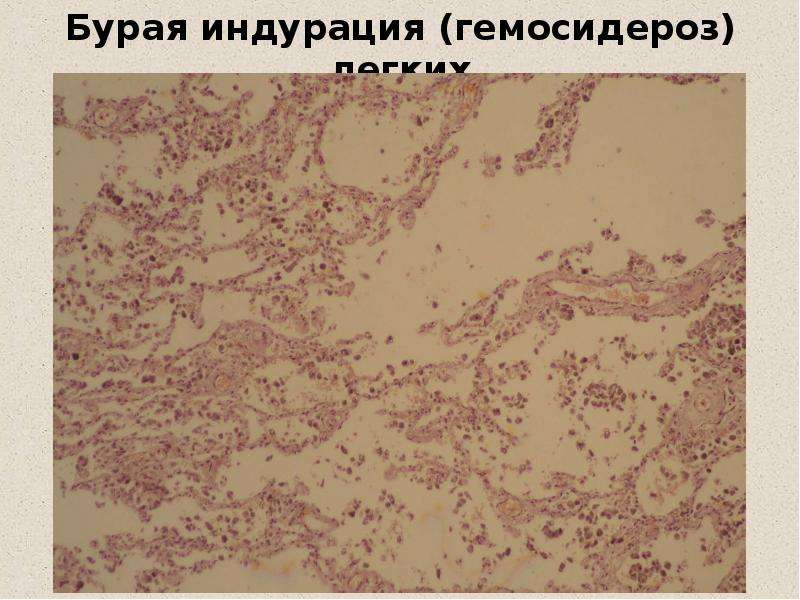 Гемосидерин возникает при расщиплении гема и образозовании коллоидной гидроокиси железа, которая соединяется с белками, мукопротеидами и липидами клетки. В патологических условиях наблюдается избыточное образование и отложение гемосидерина в органах и тканях. Распространенный гемосидероз наблюдается при внутрисосудистом разрушении эритроцитов, встречается при болезнях системы крови (анемии, лейкозы), интоксикациях, некоторых инфекционных заболеваниях. Местный гемосидероз возникает при внесосудистом разрушении эритроцитов (экстраваскулярный гемолиз).
Гемосидерин возникает при расщиплении гема и образозовании коллоидной гидроокиси железа, которая соединяется с белками, мукопротеидами и липидами клетки. В патологических условиях наблюдается избыточное образование и отложение гемосидерина в органах и тканях. Распространенный гемосидероз наблюдается при внутрисосудистом разрушении эритроцитов, встречается при болезнях системы крови (анемии, лейкозы), интоксикациях, некоторых инфекционных заболеваниях. Местный гемосидероз возникает при внесосудистом разрушении эритроцитов (экстраваскулярный гемолиз).
При гистологическом исследовании доставленного материала обнаружены изменения характерные для общего генерализованного гемосидероза и кожной лимфоидной гиперплазии. При микроскопическом исследовании срезов ткани пробы обнаружены изменения:
— в ткани печени: наблюдается нарушение архитектоники органа, избыточное отложение гемосидерина во всех срезах и тканях органа, скопление зерен буро-коричневого гемосидерина в толще ткани, цитоплазме, деформация стенок сосудов, распад эритроцитов.
 Признаков токсической дистрофии печени — не выявлено;
Признаков токсической дистрофии печени — не выявлено;— на ткани кожи: наблюдается нарушение архитектоники, вакуольная дегенерация разной степени выраженности, имеются срезы с гиперплазией капилляров и набухания эндотелия, наблюдаются ограниченные узелковые лимфоидные инфильтраты, содержащие гистиоциты с преобладающей популяцией малых зрелых лимфоцитов, а также наблюдаются отложения глыбок гемосидерина и деформация сосудов.
Сотрудники ФГБУ «Краснодарская МВЛ» готовы провести дифференциальную диагностику с целью постановки точного диагноза.
пресс-служба ФГБУ «Краснодарская МВЛ»
Гемосидероз
Гемосидероз — — избыточное отложение гемосидерина в тканях организма. Возможные причины гемосидероза — усиленный распад эритроцитов, нарушение утилизации этого пигмента в процессе эритроцитопоэза, усиленное всасывание его в кишечнике, нарушение обмена железосодержащих пигментов, ацерулоплазминемия, передозировка препаратов железа.
1.1. Виды гемосидероза Местный гемосидероз
Возникает при внесосудистом экстраваскулярном гемолизе в очагах кровоизлияний. Накопление гемосидерина не повреждает ткань или орган, но если гемосидероз сочетается со склерозом, функция нарушается. Бурая индурация лёгких — пример местного гемосидероза, вследствие венозного застоя в малом круге кровообращения при сердечной недостаточности. Синяк — тоже можно рассматривать как пример местного гемосидероза.
1.2. Виды гемосидероза Общий гемосидероз
Развивается при избытке железа из-за внутрисосудистого интраваскулярного гемолиза или при повышении всасывания железа из пищи.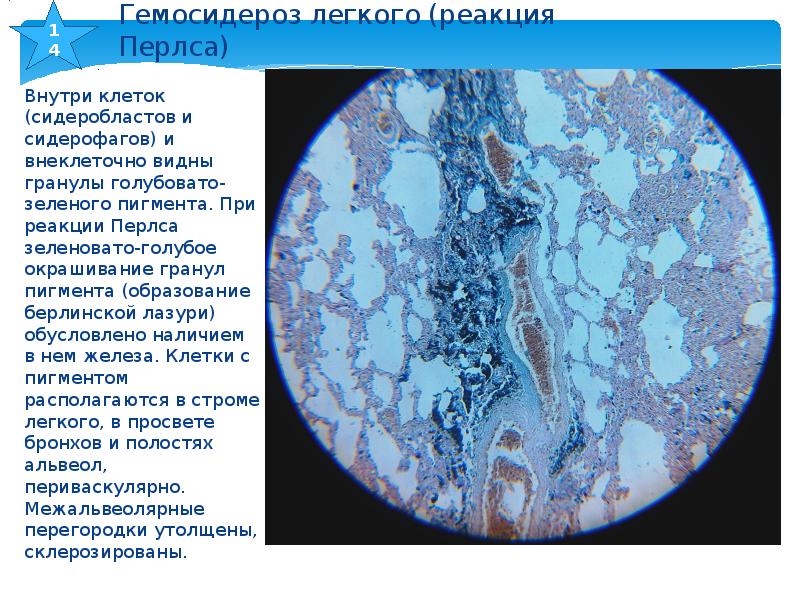 Причинами гемолиза, чаще всего бывают: переливание несовместимой крови, отравления гемолитическими ядами, инфекционные заболевания, наследственные гемолитические анемии. В этих случаях гемосидерин откладывается преимущественно в гепатоцитах, макрофагах печени, селезёнки, костного мозга и других органах. В большинстве случаев пигмент не повреждает паренхиматозные клетки и не вызывает нарушений функций органа. Если повышеное содержание железа сопровождается повреждением тканей с атрофией паренхимы, склерозом, снижением функции органа, такое состояние называется гемохроматоз.
Причинами гемолиза, чаще всего бывают: переливание несовместимой крови, отравления гемолитическими ядами, инфекционные заболевания, наследственные гемолитические анемии. В этих случаях гемосидерин откладывается преимущественно в гепатоцитах, макрофагах печени, селезёнки, костного мозга и других органах. В большинстве случаев пигмент не повреждает паренхиматозные клетки и не вызывает нарушений функций органа. Если повышеное содержание железа сопровождается повреждением тканей с атрофией паренхимы, склерозом, снижением функции органа, такое состояние называется гемохроматоз.
2. Диагностика
Гемосидерин выявляется в клетках в виде зёрен золотисто-жёлтого или золотисто-коричневого цвета, при реакции Перлса эти гранулы приобретают зеленовато-синее окрашивание за счёт образования железосинеродистого железа берлинской лазури.
3. Патогенез
Патогенез
В области мелких диапедезных кровоизляний начинается распад эритроцитов и гемолиз. Гемолиз в присутствиии кислорода ведёт к образованию гемосидерина, который синтезируется сидеробластами. В очагах крупных кровоизлияний, в центральных областях кислород отсутствует, поэтому на периферии образуется гемосидерин, а в центре — кристаллы гематоидина. К местному гемосидерозу, например, в лёгких бурая индурация лёгких ведёт патологический рост давления в легочных сосудах легочная гипертензия, формирование множества диапедезных кровоизлияний с последующим гемолизом.
Дата публикации:
05-16-2020
Дата последнего обновления:
05-16-2020гемосидероз местный — это.
 .. Что такое гемосидероз местный?
.. Что такое гемосидероз местный?- гемосидероз легких эссенциальный
- гемосидероз общий
Смотреть что такое «гемосидероз местный» в других словарях:
сидероз местный — (s. localis) 1) С. ограниченного участка ткани; 2) см. Гемосидероз местный … Большой медицинский словарь
Сидероз — I Сидероз (siderosis; Сидеро + оз) пневмокониоз, развивающийся в результате систематического вдыхания пыли железа или его соединений. Сидероз красный (s. rubra) С., характеризующийся бурым окрашиванием ткани легких окислами железа. Сидероз чёрный … Медицинская энциклопедия
Селезёнка — I Селезёнка (lien, splen) непарный паренхиматозный орган брюшной полости; выполняет иммунную, фильтрационную и кроветворную функции, принимает участие в обмене веществ, в частности железа, белков и др.
 Селезенка не принадлежит к числу жизненно… … Медицинская энциклопедия
Селезенка не принадлежит к числу жизненно… … Медицинская энциклопедияДистрофия — (от Дис… и греч. trophe питание) дегенерация, перерождение, патологический процесс, возникающий в связи с нарушением обмена веществ и характеризующийся появлением в тканях продуктов обмена веществ, изменённых количественно и качественно … Большая советская энциклопедия
Гемосидеро́з ме́стный — (haemosiderosis localis; син. сидероз местный) гемосидероз, возникающий в очагах кровоизлияний … Медицинская энциклопедия
Осмо́тр больно́го — Различают общий О. б. и специальный (местный), нередко осуществляемый специалистами (например, офтальмологом, гинекологом) с помощью инструментов. Общий О. б. является одним из основных методов обследования. Хотя он представляет собой лишь первый … Медицинская энциклопедия
ОСТИТ ФИБРОЗНЫЙ — (ostitis fibrosa), син. фиброзная остеодистрофия (osteodystrophia fibrosa), б нь костей, впервые точно очерченная Реклингаузеном (Recklinghausen) в 1891 г.

Местный гемосидероз. Выберите характерные признаки. — Студопедия
А. Развивается при внутрисосудистом гемолизе
Б. Связан с накоплением гемосидерина
В. Развивается при внесосудистом гемолизе
Г. Часто сопровождается желтухой
Д. Чаще всего поражаются печень, селезенка, костный мозг
Е. Часто поражаются легкие
Какие из перечисленных проявлений наиболее характерны для первичного гемохроматоза
А. Избирательное накопление меди в звездчатых ретикулоэндотелиоцитах, приводящее к циррозу
Б. Избирательное накопление меди в гепатоцитах, приводящее к циррозу
В. Кольца Кайзера—Флейшера
Г. Уменьшение процента насыщения плазменного трансферрина
Д. Увеличение риска развития цирроза печени и гепатоцеллюлярного рака
Выберите признаки, характерные для общего гемосидероза
А. Гемосидерин накапливается преимущественно в печени, селезенке, костном мозге
Гемосидерин накапливается преимущественно в печени, селезенке, костном мозге
Б. Гемосидерин накапливается преимущественно в печени, поджелудочной железе, миокарде
В. Часто сопровождается сахарным диабетом
Г. Наиболее частая причина смерти — печеночная недостаточность
Д. Часто возникает при пороках сердца
148. Конъюгированная гипербилирубинемия, положительные тесты на билирубин в моче и полное отсутствие уробилиногена в моче и каловых массах характерны для следующих заболеваний:
А. Рак головки поджелудочной железы
Б. Абсцесс печени
В. Тромбофлебит печеночных вен
Г. Вирусный гепатит А
Д. Наследственный сфероцитоз
Укажите морфологические признаки, которые могут быть обнаружены в биоптате печени при обструкции желчных путей.
А. Расширение желчных капилляров, переполнение их желчью
Б. Коричнево-зеленый пигмент в гепатоцитах, в звездчатых ретикулоэндотелиоцитах
В.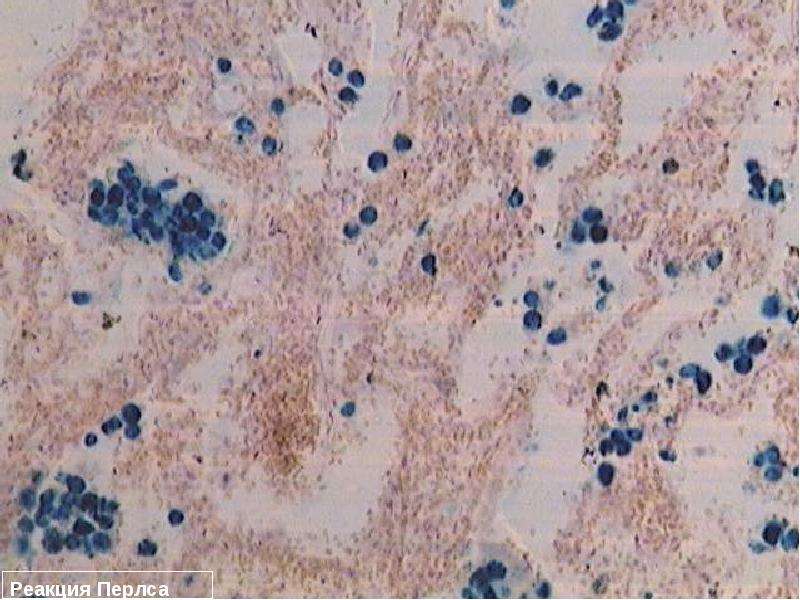 Отсутствие желчи в гепатоцитах и желчных капиллярах
Отсутствие желчи в гепатоцитах и желчных капиллярах
Г. Отек и рыхлая, преимущественно лейкоцитарная, инфильтрация портальной стромы, постепенно нарастающий перидуктальный склероз
Д. Очаговые некрозы гепатоцитов
У больного раком легкого с множественными гематогенными метастазами появились темно-коричневое окрашивание кожи, адинамия, гипотония. Смерть наступила от кахексии. Выберите положения, наиболее вероятные в данной ситуации.
А. Появившиеся симптомы можно объяснить метастазами в печень
Б. Темно-коричневая окраска кожи связана с меланином
В. В сердце обнаружена бурая атрофия
Г. Бурая окраска сердца обусловлена меланином
Д. В легких обнаружена бурая индурация
151. Все положения верны в отношении бурой атрофии сердца, за исключением:
А. Процесс развивается в старческом возрасте
Б. Процесс связан с накоплением липофусцина
В. Содружественно поражается печень
Г.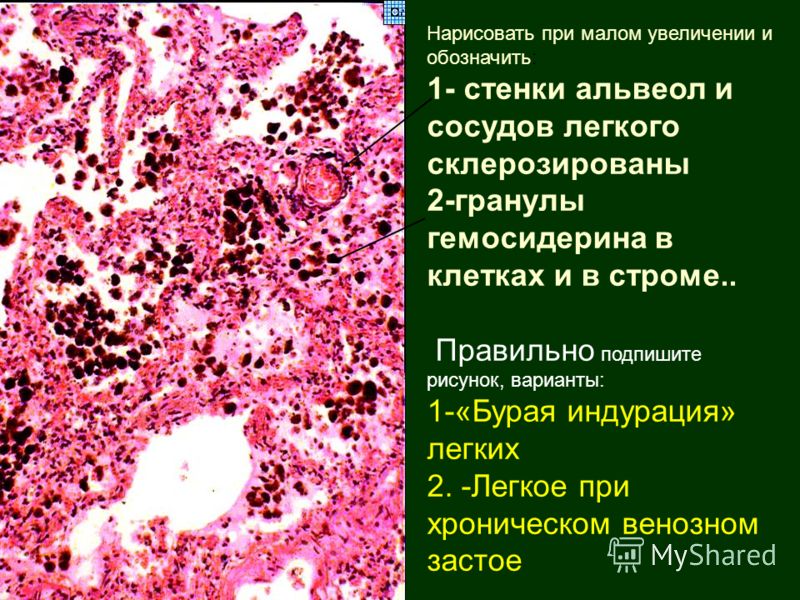 Содружественно поражаются легкие
Содружественно поражаются легкие
Д. Процесс часто развивается при злокачественных опухолях
На вскрытии в веществе головного мозга обнаружена киста с ржавыми стенками. С каким пигментом связан цвет кисты?
А. Билирубин
Б. Порфирин
В. Меланин
Г. Гемосидерин
Д. Солянокислый гематин
153. Больной, страдавший малярией, умер при явлениях малярийной комы. На вскрытии обнаружены желтушность кожных покровов, серо-аспидный цвет головного мозга, бурый оттенок ткани печени, селезенки. Все положения верны в отношении данной ситуации, за исключением:
А. Желтушность кожных покровов связана с билирубином
Б. Желтуху можно отнести к неконъюгированной
В. Цвет головного мозга обусловлен пигментом гемомеланином
Г. Цвет селезенки, печени обусловлен накоплением липофусцина
Д. Все образующиеся при малярии пигменты можно отнести к гемоглобиногенным
Больная 38 лет длительно страдала ревматическим пороком сердца (преобладание стеноза левого атриовентрикулярного отверстия). В течение последних месяцев — нарастающая одышка, кашель с ржавой мокротой. Смерть наступила внезапно от массивного желудочного кровотечения. На вскрытии в желудке — множественные эрозии и язвы. Выберите положения, верные в данной ситуации
В течение последних месяцев — нарастающая одышка, кашель с ржавой мокротой. Смерть наступила внезапно от массивного желудочного кровотечения. На вскрытии в желудке — множественные эрозии и язвы. Выберите положения, верные в данной ситуации
А. В легких обнаружена бурая индурация
Б. Цвет легких можно объяснить развитием местного гемосидероза
В. Идентифицировать пигмент в легких можно с помощью гистохимической реакции Перлса
Г. Дно эрозий и язв окрашено в зеленоватый цвет
Д. Цвет эрозий и язв связан с накоплением гемосидерина
Гемосидероз, что это за болезнь, симптомы у взрослых, лечение
Гемосидероз – это заболевание, характеризующееся сбоем в обменных процессах и повышенным содержанием пигмента гемосидерина в клетках. Этот пигмент является продуктом распада гемоглобина и участвует в доставке химических веществ в ткани.
Источник: https://medvisor.ru/articles/immunitet/gemosideroz/
Описание гемосидероза
Designed by pressfoto/freepik
Гемосидероз разделяется на следующие типы:
- локальный (местный), поражающий только кожу и легкие;
генерализованный (общий), поражающий различные внутренние органы: печень, костный мозг, почки и т.
 д.
д.
Симптомы обоих типов схожи между собой – это красноватая сыпь на коже, отхаркивание кровью, анемия и постоянная усталость.
Чаше всего данному заболеванию подвержены мужчины.
Известно, что к возникновению этого недуга могут приводить такие нарушения, как:
избыточное всасывание в кишечнике;
проблемы с метаболизмом;
чрезмерное разрушение эритроцитов.
В силу того, что в основе болезни лежат нарушения метаболизма и проблемы в работе различных органах организма лечение данного недуга представляет собой очень непростую задачу.
Для диагностирования заболевания требуется консультация нескольких врачей-специалистов:
дерматолог;
иммунолог;
гематолог;
пульминолог.
Местный гемосидероз возникает там, где есть очаг кровоизлияния.
При сердечной недостаточности может начаться местный гемосидероз, спровоцированный венозным застоем. Это приводит к бурой индурации легких.
Общий гемосидероз может быть вызван:
переливанием неподходящего типа крови;
отравлением гемолитическими ядами;
инфекциями;
наследственными гемолитическими анемиями.
Общий гемосиредоз наиболее сильно затрагивает печень и селезенку. При этом характерно изменение их цвета на более темный.
Существуют несколько форм гемосидероза:
поражающий легкие;
передающийся по наследству;
дерматологический;
печеночный;
неустановленной этиологии.
Причины возникновения гемосидероза
Designed by freepik
Медицина пока не выяснила точные причины развития данного заболевания, однако известно, что оно не является основной болезнью, а возникает в случае уже имеющихся недугов.
Этому заболеванию чаще всего подвержены люди, страдающие:
болезнями крови;
инфекционными заболеваниями;
нарушениями иммунной системы;
заболеваниями сосудов;
интоксикацией.
Кожный гемосиредоз может развиваться как под влиянием травм, так и после занесения кожных инфекций. В случае первичного заболевания причиной могут послужить эндокринные заболевания.
Симптомы гемосидероза
Designed by freepik
Симптоматика гемосидероза зависит от того, где находится очаг заболевания.
Если болезнь поразила кожу, то она выражается в кожном зуде, пигментации в виде красных пятен, которые могут сохраняться на коже в течение нескольких месяцев или лет.
При поражении легких характерны:
постоянная одышка;
влажный кашель;
кровавая мокрота;
высокая температура;
увеличение печени и селезенки;
анемия.

Приступы гемосидероза этого типа на начальном этапе заболевания имеют временный характер. Больной после того, как обострение проходит, начинает вновь чувствовать себя нормально и может вести полноценный образ жизни. Но если не проводить лечение, рецидивы заболевания случаются все чаще и продолжаются все большее количество времени.
В случае тяжелой формы заболевания может возникнуть пневмония, легочное сердце.
Для гемосидероза печени характерно:
увеличение этого внутреннего органа в размерах;
скопление асцитической жидкости;
повышение артериального давления;
пожелтение кожи;
увеличение селезенки;
пигментация на коже.
При почечном гемосидерозе этот орган покрывается коричневыми гранулами.
Течение заболевания напоминает нефрит и нефроз. Больной страдает отеками ног, болью в районе поясницы, у него пропадает аппетит. Вследствие этого недуга и при отсутствии надлежащего лечения развивается почечная недостаточность.
Больной страдает отеками ног, болью в районе поясницы, у него пропадает аппетит. Вследствие этого недуга и при отсутствии надлежащего лечения развивается почечная недостаточность.
Также гемосидероз может развиваться в:
Методы диагностики гемосидероза
Для точного диагностирования заболевания требуется:
общий анализ крови для определения уровня сывороточного железа;
биопсия соответствующего внутреннего органа и его гистологическое исследование;
десфераловая проба;
микроскопическое исследование кожного покрова больного при наличии высыпаний.
Также может потребоваться:
Лечение гемосидероза
При проведении лечения гемосидероза, как правило, рекомендуется:
соблюдать особую диету, не содержащую алкоголя и продуктов, способных вызвать аллергию;
избегать травм, переохлаждения или перегрева;
устранить очаги инфекции.

Кроме этого, медики выписывают такие медикаменты как:
гормональные стероидные средства;
противовоспалительные средства;
дезагреганты;
иммуносупрессивные препараты;
ноотропы;
противоаллергические средства;
витамины и минералы;
железосодержащие препараты.
В особых случаях может потребоваться переливания крови, либо удаление селезенки.
Профилактика гемосидероза
Заболевание в большей степени представляет косметический дефект и склонно к постепенному разрешению.
Предупреждению нарушения обмена гемосидерина может способствовать своевременная терапия кожных и общих инфекционных, сосудистых, гематологических и других заболеваний.
классификация и причины возникновения заболевания, клинические симптомы у взрослых и детей, диагностика патологии и тактика лечения, прогноз для жизни
Гемосидероз легких представляет собой тотальное поражение органа, вызванное чрезмерным поступлением в ткани эритроцитов. В группе риска находятся преимущественно дети и люди в возрасте до 30 лет.
В группе риска находятся преимущественно дети и люди в возрасте до 30 лет.
По половому признаку этот недуг не дифференцируется. Однако, несмотря на тяжесть течения и высокую вероятность развития осложнений, гемосидероз успешно поддается лечению. Главное — успеть начать его вовремя.
Тогда опасных осложнений наверняка удастся избежать.
Здесь нет места самолечению или медикаментам, которые присутствуют в домашней аптечке каждого человека. Успех в лечении — это залог кропотливого труда профессиональных медиков.
Достоверные причины, по которым в организме начинает прогрессировать гемосидероз, на данный момент медицине неизвестны. Основной из них призвано называть врожденную неполноценность волокон сосудов малого круга кровообращения, в результате чего и нарушается отток крови.
Однако, если имеется даже явная склонность, раньше времени переживать не стоит. Вероятность того, что болезнь действительно проявит себя — 50/50. И то лишь при ослаблении иммунитета или длительном стрессовом воздействии на организм. Именно поэтому, зная о таковых проблемах со здоровьем, лучше избегать перенапряжения.
Именно поэтому, зная о таковых проблемах со здоровьем, лучше избегать перенапряжения.
Гемосидероз легких может протекать как в острой, так и в хронической форме. Причем первая из них характерна преимущественно для детского возраста. Вторая форма же возникает исключительно на фоне первой, запущенной или недолеченной.
- кашель, иногда с выделением кровянистой массы;
- одышка, особенно при нагрузках;
- головокружение;
- проявление в глазах мушек;
- периодический шум в ушах.
Если пациент длительное время не получает квалифицированного лечения, у него может значительно ухудшиться общее состояние и наблюдаться значительная потеря веса.
Именно поэтому, заметив продолжительное ухудшение состояния и все симптомы «простуды», не проходящей несколько недель, нужно обязательно обратиться за помощью в больницу. Особенно это касается тех случаев, когда болезнь прогрессирует у детей. В столь нежном возрасте она является для организма сильным стрессом и может отразиться даже на дальнейшем развитии.
В противном случае при равнодушии или беспечности родителей к гемосидерозу может присоединиться инфаркт — пневмония, вероятность летального исхода при котором очень велика.
Как лечится заболевание
Гемосидероз легких в зависимости от формы диагностируется дерматологами, инфекционистами, пульмонологами и другими специалистами.
В первую очередь в него входят глюкокортикостероиды, однако их эффективность доказана всего лишь в 50% случаев. Для достижения более качественного результата активно применяются иммунодепрессанты по смешанной схеме.
Периодически во время лечения у пациента берутся контрольные анализы, КТ. И если положительная динамика наблюдается, некоторые медикаменты могут быть отменены. Не исключена и диаметрально противоположная ситуация, когда выбранная схема не дает положительного результата.
В таком случае необходимые препараты добавляются.
Кроме того, в схему лечения могут быть включены другие медикаменты, подавляющие другие неприятные симптомы. Однако каждый микропрепарат должен быть подобран исключительно специалистом.
Однако каждый микропрепарат должен быть подобран исключительно специалистом.
В целом, прогноз при гемосидерозе легких достаточно благоприятный. Однако для того чтобы окончательно побороть недуг, придется набраться терпения. Не исключено, что лечение займет до нескольких месяцев, но положительная динамика обычно наблюдается практически сразу в течение нескольких дней после начала приема таблеток.
Почти любую болезнь можно предотвратить, однако в случае с гемосидерозом сделать это практически невозможно. Единственное, что советуют специалисты, — это тщательно следить за собственным здоровьем и мониторить даже незначительные негативные изменения. Лучше лишний раз пройти обследование и убедиться, что со здоровьем все хорошо, чем запустить болезнь и направить все силы на ее устранение.
Источник: https://stronglung.ru/drugie/gemosideroz-legkix.html
Гемосидероз
Гемосидероз – это заболевание, которое относится к категории пигментных дистрофий, а также для него характерно скопление в тканях большого количества гемосидерина, который представляет собой железосодержащий пигмент. Механизм развития болезни остаётся до конца не известным, однако специалистами из области дерматологии установлено, что причины формирования могут отличаться в зависимости от формы протекания такого расстройства.
Механизм развития болезни остаётся до конца не известным, однако специалистами из области дерматологии установлено, что причины формирования могут отличаться в зависимости от формы протекания такого расстройства.
Симптоматическая картина также напрямую диктуется разновидностью недуга. Примечательно то, что гемосидероз может поражать как внутренние органы, так и кожный покров. Во втором случае пациенты очень редко предъявляют жалобы касательно ухудшения самочувствия.
Основу диагностики составляют лабораторные изучения крови, которые в обязательном порядке должны дополняться инструментальными процедурами и рядом манипуляций, выполняемых непосредственно клиницистом.
Лечение гемосидероза ограничивается применением консервативных методик терапии, в частности приёмом лекарственных препаратов. Однако при тяжёлом течении болезни может понадобиться такая процедура, как плазмаферез.
В международной классификации болезней десятого пересмотра такому заболеванию отведено несколько собственных шифров, отличающихся по варианту течения. Гемосидероз кожи имеет значение L 95.8. Гемосидероз лёгких код по МКБ-10 – J 84, а идиопатическая форма патологии — J 84.8.
Гемосидероз кожи имеет значение L 95.8. Гемосидероз лёгких код по МКБ-10 – J 84, а идиопатическая форма патологии — J 84.8.
Этиология
Поскольку подобный недуг у детей и взрослых может быть первичным и вторичным, то и предрасполагающие факторы будут отличаться.
В первом случае патогенез и этиология гемосидероза остаются до конца не выясненными, однако клиницисты выдвигают несколько предположений, среди которых:
- генетическая предрасположенность;
- иммунопатологический характер патологии;
- врождённые нарушения обменных процессов.
Что касается вторичного гемосидероза, то в качестве возможных причин могут выступать:
Спровоцировать манифестацию недуга можно такими причинами:
- длительное переохлаждение организма;
- физическое переутомление;
- стрессы и нервные перенапряжения;
- бесконтрольный приём некоторых групп лекарственных препаратов, в частности диуретиков, нестероидных противовоспалительных средств, а также парацетамола и ампициллина.

Не последнее место в формировании подобного патологического процесса занимают:
- избыток железа в организме – этого можно достичь путём потребления продуктов или медикаментов, в состав которых входит большое количество этого вещества;
- процедура переливания крови, в особенности если это проводится несколько раз в неделю. В таких случаях говорят про возникновение трансфузионного гемосидероза;
- повышенное всасывание гемосидерина органами пищеварительной системы;
- нарушение метаболизма гемосидерина;
- переохлаждение организма.
Классификация
По степени распространённости патологического процесса существует:
- генерализованный или общий гемосидероз – формируется на фоне какого-либо системного процесса. В таких ситуациях гемосидерин скапливается в селезёнке и печени, а также в красном костном мозге, отчего они меняют свой окрас и становятся ржавыми или бурыми;
- локальный, очаговый или местный гемосидероз – отличается тем, что накопление железосодержащего внутриклеточного пигмента может осуществляться как в небольших участках тела, например, в зоне гематом, так и в полости одного из внутренних органов.
 Наиболее часто это отмечается в лёгочных тканях.
Наиболее часто это отмечается в лёгочных тканях.
По этиологическому фактору гемосидероз бывает:
- первичным – причины на сегодняшний день остаются неизвестными;
- вторичным – развивается на фоне протекания какого-либо из вышеуказанных недугов.
К самостоятельным типам болезни стоит отнести:
- гемосидероз кожи;
- идиопатический лёгочный гемосидероз, который в медицинской сфере носит название бурая пурпура лёгких.
В случаях поражения кожного покрова заболевание может протекать в нескольких вариациях, отчего делится на:
- болезнь Шамберга;
- кольцевидную телеангиэктатическую пурпуру Майокки;
- старческий гемосидероз;
- лихеноидный пигментный или пурпурозный ангиодермит;
- охряный дерматит.
Вторичная форма патологии также имеет собственную классификацию:
- гемосидероз печени;
- гемосидероз почек;
- гемосидероз костного мозга;
- гемосидероз селезёнки;
- гемосидероз с поражением слюнных или потовых желез.

Симптоматика
Клиническая картина подобного заболевания у детей и взрослых напрямую диктуется разновидностью его протекания.
Таким образом, идиопатический гемосидероз лёгких представлен такими проявлениями:
- продуктивным кашлем, т. е. с выделением мокроты;
- кровохарканьем;
- одышкой;
- повышением температурных значений;
- болевым синдромом с локализацией в грудине;
- бледностью кожи;
- иктеричностью склер;
- синюшностью носогубного треугольника;
- сильнейшими головокружениями;
- слабостью и понижением работоспособности;
- отсутствием аппетита;
- учащением сердечного ритма;
- понижением АД;
- одновременным изменением объёмов печени и селезёнки в большую сторону.
На фоне того, что бурая индурация лёгких является тяжёлым недугом, подобный диагноз при жизни человека устанавливается достаточно редко.
Гемосидероз кожи прежде всего выражается в возникновении пигментных пятен, имеющих коричневый и в подавляющем большинстве случаев локализуется нижней части ног. Помимо этого, симптоматика такой вариации недуга также включает в себя:
Помимо этого, симптоматика такой вариации недуга также включает в себя:
- возникновение геморрагической сыпи или небольших пигментных пятен, которые в диаметре варьируются от одного миллиметра до 3 сантиметров;
- вовлечение в патологию голеней, предплечий и кистей;
- вариабельность оттенка высыпаний – они могут быть кирпично-красными, бурыми, тёмно-коричневыми или желтоватыми;
- незначительный кожный зуд;
- формирование на проблемных участках кожного покрова петехий, узелков, лихеноидных папул и бляшек.
Симптомы гемосидероза кожи
Гемосидероз печени выражается в:
- увеличении размеров и плотности поражённого органа;
- болезненности при пальпации проекции этого органа;
- скоплении большого количества жидкости в брюшине;
- повышении кровяного тонуса;
- желтушности кожных покровов, видимых слизистых и склер;
- пигментации верхних конечностей, лица и подмышечных впадин.
В случаях вовлечения в патологический процесс почек будет отмечаться присутствие:
- отёчности нижних конечностей и век;
- отвращения к пище;
- помутнения урины;
- болей в области поясницы;
- общей слабости и разбитости;
- диспепсии.

Всю вышеуказанную симптоматику целесообразно относить к ребёнку и взрослому.
Диагностика
Поскольку гемосидероз, прежде всего, характеризуется изменением состава крови, то вполне естественно, что основу диагностики будут составлять лабораторные исследования.
При возникновении характерной симптоматики стоит обратиться за помощью к терапевту, который проведёт манипуляции первичного диагностирования и назначит общие обследования, а при необходимости направит пациента на дополнительную консультацию к иным специалистам.
Первый шаг в установлении правильного диагноза направлен на:
- изучение истории болезни – для поиска патологических факторов, приводящих к вторичному гемосидерозу;
- ознакомление с анамнезом жизни человека – для установления возможных источников первичной формы недуга;
- тщательнейший физикальный осмотр больного, который обязательно должен включать в себя изучение состояния кожи, пальпацию передней стенки брюшной полости, измерение пульса и АД;
- детальный опрос пациента – для составления полной симптоматической картины протекания болезни.

Лабораторные исследования основываются на:
- общеклиническом анализе крови;
- биохимии крови;
- ПЦР-тестах;
- общем анализе урины;
- дисфераловой пробе;
- микроскопическом изучении мокроты.
Самыми ценными в плане диагностики выступают такие инструментальные процедуры:
- биопсия поражённого сегмента, т. е. кожного покрова, печени, почек, лёгкого, костного мозга и т. д.;
- спирометрия;
- бронхоскопия;
- сцинтиграфия;
- рентгенография грудины;
- КТ и МРТ.
Процедура спирометрия
Лечение
Вылечить подобное заболевание можно при помощи консервативных методик терапии, применяемых при любом варианте его протекания.
Лечение гемосидероза включает в себя:
- приём глюкокортикоидов;
- применение иммунодепрессантов и препаратов железа;
- осуществление плазмафереза;
- использование медикаментов для купирования симптомов;
- ингаляции кислорода;
- криотерапию;
- витаминотерапию;
- приём лекарств, содержащих кальций и ангиопротекторов;
- ПУВА-терапию – при кожном гемосидерозе.

Хирургическое вмешательство в терапии недуга не применяется.
Профилактика и прогноз
Поскольку в половине случаев не удаётся выяснить причину формирования такой болезни, то профилактические рекомендации будут не специфическими, а общими. К ним стоит отнести:
- правильное и сбалансированное питание;
- ведение здорового и активного образа жизни;
- недопущения каких-либо травм и переохлаждений;
- раннюю диагностику и полноценное лечение патологий, которые могут спровоцировать развитие вторичного гемосидероза;
- исключение лекарственных и химических интоксикаций;
- регулярное прохождение профилактического осмотра в медицинском учреждении.
На фоне того, что гемосидероз довольно сложно диагностировать, его прогноз будет относительно благоприятным – лучше всего переносится людьми кожная форма. Очень часто иные разновидности недуга приводят к инвалидности и развитию осложнений, которые иногда становятся причиной летального исхода пациента.
Источник: https://SimptoMer.ru/bolezni/other/2627-gemosideroz-simptomy
Гемосидероз легких идиопатический у детей
Идиопатический гемосидероз лёгких или синдром Целена-Геллерстедта является достаточно редким заболеванием, которое имеет волнообразное течение с частыми рецидивами, проявляет себя повторными кровоизлияниями в лёгкие, на фоне которых развивается гипохромная анемия.
Эпидемиология
Раньше данная патология диагностировалась в большинстве своём патологоанатомами. В настоящее время разработаны диагностические критерии, по которым удаётся поставить диагноз прижизненно.
Патология чаще всего выявляется в детском возрасте, причём представительницы прекрасного пола страдают чаще, чем мужчины.
Этиология
Истинные причины и механизмы развития данного заболевания всё ещё не установлены. Многочисленные данные свидетельствуют о роли врождённых аномалий, среди которых огромное значение имеет несостоятельность эластических волокон сосудов лёгких среднего и мелкого калибра, а также аномалии анастомозов между бронхиальными артериями и венами лёгких.
Определённая роль в развитии данного патологического состояния отводится наследственным нарушениям функции селезёнки, о чём свидетельствует выраженный гемолиз эритроцитов.
Клиническая картина
Первым симптомом идиопатического легочного гемосидероза может выступать легочное кровохарканье. Течение патологического процесса зависит от распространённости основных морфологических изменений и компенсаторных возможностей детского организма.
Среди наиболее характерных жалоб ребёнка и его родителей при данном состоянии следует отметить слабость, кашель, одышку, сердцебиение, боли в грудной клетке, повышение температуры тела.
При осмотре обращает на себя внимание желтизна и бледность кожных покровов, цианоз носогубного треугольника, умеренная иктеричность склер. Перкуторный звук над тканью лёгких укорочен. При аускультации над зонами его притупления выслушиваются влажные разнокалиберные или сухие хрипы. Может пальпироваться увеличенная селезёнка и печень.
Длительность рецидива может составлять от пары часов до нескольких недель.
Стадия ремиссии обычно продолжается год и более. По мере прогрессирования патологических изменений в лёгких выраженность и длительность кризов возрастает, а периоды ремиссии, соответственно, сокращаются.
Такое осложнение идиопатического легочного гемосидероза, как инфаркт-пневмония, становится причиной повышения степени сердечной и легочной недостаточности, увеличивая риск развития летального исхода. Для детского возраста характерно злокачественное течение данной патологии.
Диагностика
Характерная клиническая картина и симметричное поражение ткани лёгких, подтверждённое рентгенологически, позволяют диагностировать данную патологию на ранних стадиях.
К диагностическим рентгенологическим признакам синдрома Целена-Геллерстедта относятся плотные, диффузные сетевидные очаги затемнения легочной ткани, которые локализуются преимущественно в нижних и средних отделах лёгких.
Биохимический анализ крови позволяет выявить увеличение концентрации железа, признаки гипохромной анемии, пойкилоцитоз, повышение количества ретикулоцитов на фоне умеренного лейкоцитоза. Для общего анализа мочи характерна гематурия, альбуминурия, цилиндрурия.
Для общего анализа мочи характерна гематурия, альбуминурия, цилиндрурия.
Лечение
Существуют клинические данные о случаях самопроизвольного выздоровления. При установленном диагнозе лечение следует начинать с десферала, регулярно контролируя количество железа, выделяемого из организма с мочой. Показаны также кортикостероиды. Спленэктомия показана в ситуациях, когда нет возможности справиться с повышенным разрушением эритроцитов другими путями.
Источник: https://snovenie.ru/gemosideroz-legkih-idiopaticheskii-y-detei.html
Идиопатический гемосидероз легких
В основе болезни лежит кровоизлияние в альвеолы легких, которое носит обычно диффузный характер. Освобождающееся вследствие распада эритроцитов железо поглощается макрофагами, которые могут
быть обнаружены в мокроте больных (сидерофаги). Первичный ИГЛ чаще встречается в детском возрасте.
Этипатогенез остается малоизученным. Больше склоняются в пользу иммунопатологического характера
заболевания, в частности взаимодействию аллерген-антитело, реализующемуся в сосудах легких.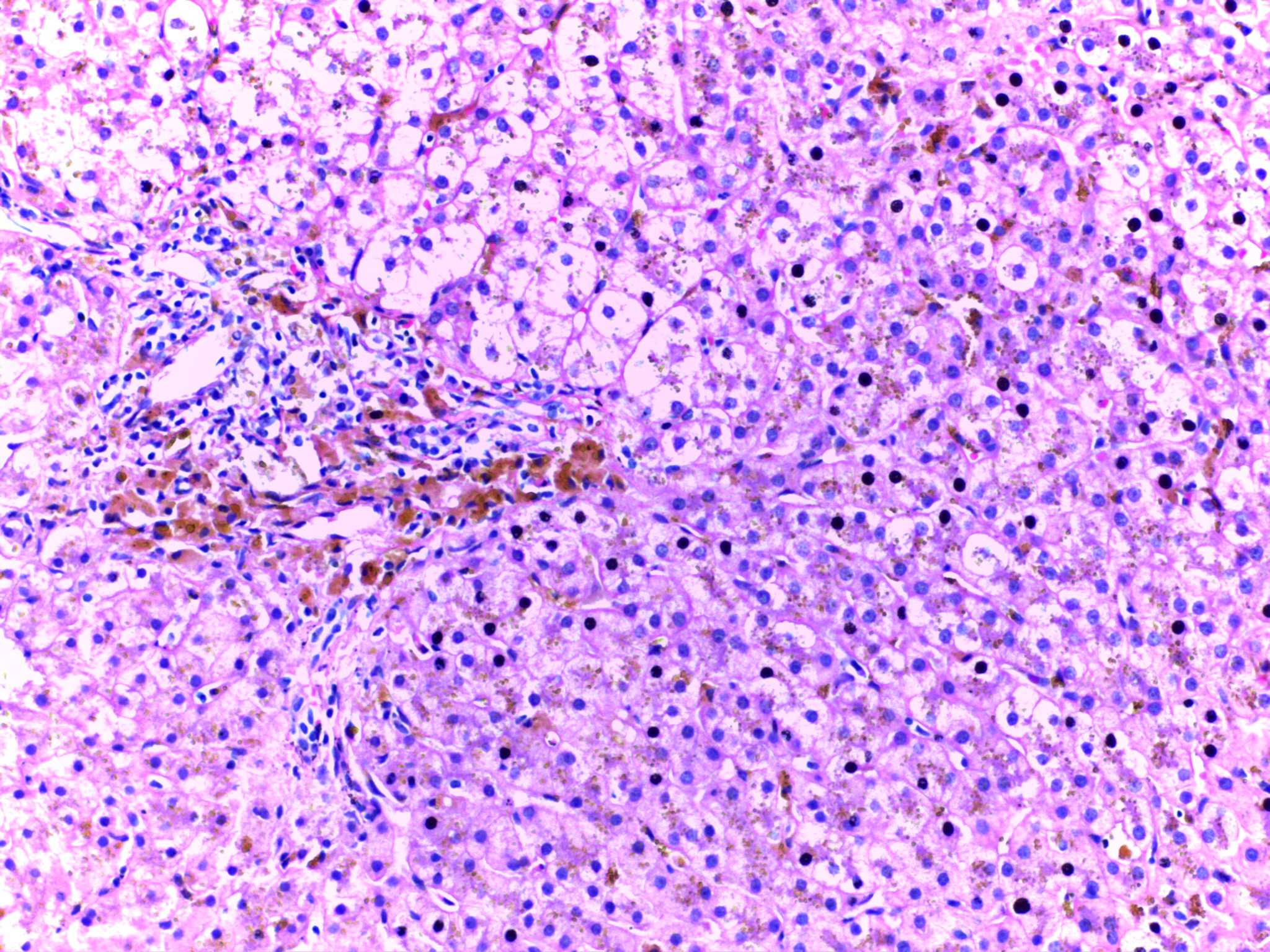
В пользу такого предположения свидетельствует наличие такой формы, как ИГЛ с повышенной
чувствительностью к коровьему молоку (синдром Гейснера). В этом в сыворотке крови обнаруживаются в большом количестве преципитины к ингредиентам коровьего молока.
Морфологически (по материалам открытой биопсии легких) обнаруживаются эритроциты в полости альвеол, гемосидерин- содержащие макрофаги (сидерофаги), интерстициальный диффузный фиброз,
склерозирование мелких сосудов легких.
Клиническая картина ИГЛ складывается из симптомов со стороны органов дыхания и гематологических
симптомов. При обострении появляется кашель, у детей старшего возраста сопровождающийся ровохарканием — появлением крови в мокроте. Маленькие дети мокроту не откашливают, заглатывают
ее.
При обильном легочном кровотечении у них может быть рвота с примесью в рвотных массах проглоченной крови.
Выраженность клинической картины со стороны легких зависит от количества излившейся крови в львеолы. Вместе с кашлем и повышением температуры появляемся одышка, цианоз. В легких выслушиваются хрипы.
Вместе с кашлем и повышением температуры появляемся одышка, цианоз. В легких выслушиваются хрипы.
Появляются рентгенологические изменения в виде крупнопятнистых теней в обоих легких. Заболевание нередко принимается за пневмонию, что приводит к назначению неадекватного лечения и ухудшает состояние больного. Особенность рентгенологически выявляемых изменений при ИГЛ является быстрое обратное развитие очагов затемнения.
В ряде случаев на рентгенограммах грудной клетки отмечаются рассеянные мелкие тени в обоих легких, что служит причиной ошибочной диагностики милиарного туберкулеза легких.
Изменения в легких, выявляемые при рентгенографии могут варьировать в широких пределах: от
небольших инфильтратов до массивных тенеобразований, сопровождающихся ателектазами, эмфиземой и реакцией со стороны лимфатических узлов корней легких. Сразу после обострения, которое длится 3-5 дней, отмечается анемия — микроцитарная и гипохромная.
Уровень сывороточного железа падает.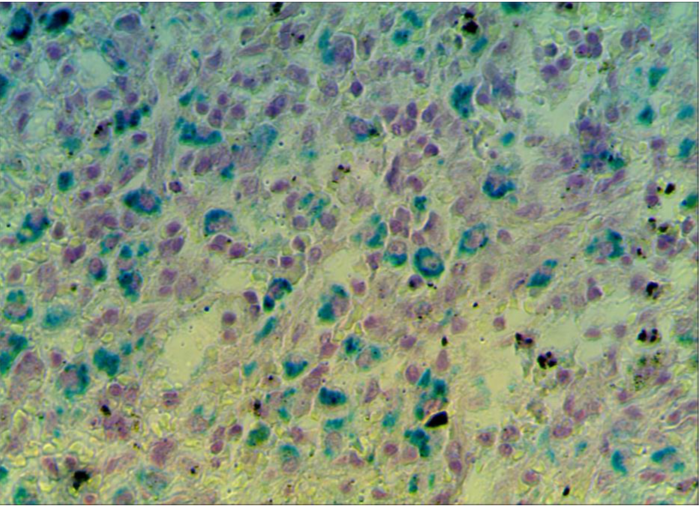 В биохимическом анализе крови может отмечаться повышенный уровень билирубина.
В биохимическом анализе крови может отмечаться повышенный уровень билирубина.
Поскольку регенераторная функция костного мозга не страдает, в периферической крови появляются ретикулоциты. У маленьких детей анализ кала на скрытую кровь может оказаться положительным
(проглоченная при кашле мокрота с кровью). Часто отмечается гепатоспленомегалия.
Условно выделяют острое и подострое течение.
При острой форме ИГЛ отмечается значительное ухудшение состояния, слабость, выраженная одышка, старшие дети жалуются на боли в груди, кашель со скудной мокротой, в легких выслушиваются ослабленное
дыхание и влажные хрипы. Возможно повышение температуры до фебрильных цифр. Быстро нарастает анемия.
При подостром варианте ИГЛ постепенно развивается бледность кожных покровов, симптомы интоксикации. Обострения заболевания протекают более тяжело. Диагностически значимым является
обнаружение в мокроте или трахеальном аспирате, а также в ряде случаев в промывных водах желудка, сидергофагов.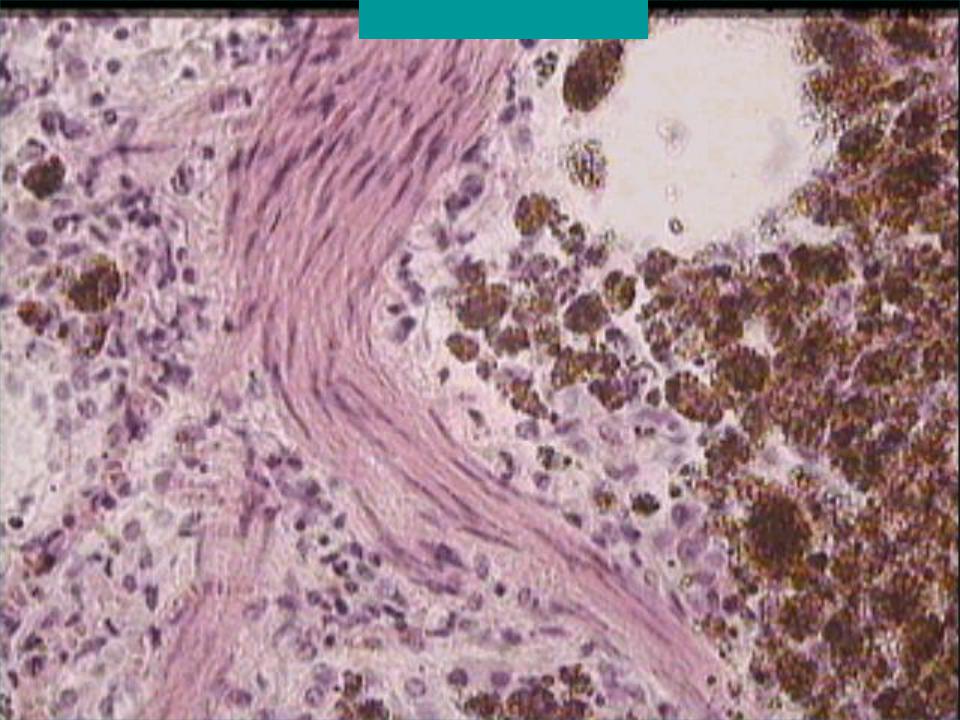
Пункционная биопсия легких чревата серьезными осложнениями.
Исследование функции внешнего дыхания обнаруживает или нормальные показатели вентиляции, если длительность заболевания небольшая, или выраженные рестриктивные нарушения, снижение диффузионной способности легких, если заболевание протекает длительно с тяжелыми обострениями.
Если повторные респираторные заболевания протекают всякий раз с анемией, необычной рентгенологической картиной в легких и плохо поддаются противовоспалительной терапии, необходимо обследовать такого больного на наличие ИГЛ.
Прогноз заболевания серьезный. Половина детей погибает в первые пять лет от начала заболевания. Непосредственной причиной смерти чаще всего служат острое массивное легочное кровотечение или прогрессирующая легочно-сердечная недостаточность. Причем предсказать вероятность острого
легочного кровотечения не представляется возможным.
Лечение больных с ИГЛ предполагает назначение кортикостероидных препаратов и
симптоматическое лечение.
Некоторые авторы рекомендуют до определения преципитинов в сыворотке крови больных
исключить из рациона питания коровье молоко.
Преднизолон назначается из расчета 1 -1,5 мг/кг до достижения клинико-лабораторной ремиссии. Имеются
сообщения о том, что после спленэктомии наступает стойкая длительная ремиссия.
Источник: https://StudFiles.net/preview/6008568/page:9/
Идиопатический Гемосидероз легких
Идиопатический гемосидероз легких (синонимы: бурая ин- дурация легких, легочная гемосидеротическая анемия, синдром Целена-Геллерстедта -характеризующееся повторными кровоизлияниями в легкие, гипохромной анемией и волнообразным рецидивирующим течением.
Патомофологическая картина идиопатического гемосидероза легких описана И. Virchow (1864) под названием «бурая индурация легких».
Заболевание принято считать редким, еще реже диагностируемым прижизненно. Однако в последние годы идиопатический гемосидероз легких встречается чаще, что, возможно, связано как с лучшей диагностикой, так и со значительным ростом сенсибилизирующих факторов, воздействующих на человека, что косвенно может подтверждать иммуноаллергический генез заболевания.
Болеют преимущественно дети. Среди взрослых чаще болеют женщины (2:1).
Одной из первых теорий, объясняющих причину возникновения идиопатического гемосидероза легких, является гипотеза о врожденной неполноценности эластических волокон мелких и средних сосудов легких, что ведет к их расширению, стазу крови и проникновению эритроцитов через стенку сосуда.
Избирательное отложение гемосидерина только в легочной ткани косвенно подтверждает теорию врожденного дефекта эластических волокон легких.
Существуют и другие гипотезы, объясняющие этиологию заболевания: врожденная аномалия анастомозов, соединяющих бронхиальные артерии с легочными венами; патологическая функция селезенки, приводящая к гемолизу эритроцитов, и др.
Нередкое возникновение идиопатического гемосидероза легких после острых респираторных и других инфекционных заболеваний (кори, коклюша) указывают на возможную этиологическую роль инфекций и интоксикаций.
Большинство авторов в настоящее время придерживаются гипотезы об иммуноаллергической природе идиопатического гемосидероза легких.
Образование аутоантител в ответ на воздействие сенсибилизирующего агента и реакция антиген — антитело, шоковым органом для которой являются легкие, приводит к расширению капилляров, стазу и диапедезу эритроцитов в легочную ткань с отложением в ней гемосидернна.
Косвенным подтверждением этой гипотезы является сочетание идиопатического гемосидероза легких с обструктивным синдромом, аллергическими высыпаниями на коже, эозинофилией периферической крови и др., а также положительный лечебный эффект при назначении кортикостероидов.
Патологическая анатомия. В альвеолах и межальвеолярных перегородках выявляются свежие кровоизлияния с гемолизом эритроцитов и значительные отложения гемосидерина.
Протоплазма альвеолярных макрофагов также содержит глыбки гемосидерина. Эластические и коллагеновые волокна импрегни- рованы железом, что приводит к их истончению, фрагментации и гиалиновой дегенерации коллагена.
Гемосидерин находится и внеклеточно. Характерен прогрессирующий пневмосклероз.
Характерен прогрессирующий пневмосклероз.
Наиболее типичными симптомами являются кровохарканье (может быть и легочное кровотечение), гипохромная анемия и, как правило, двусторонние симметричные мелкоочаговые изменения в легких, выявляемые при рентгенологическом исследовании.
Болезнь может протекать остро или приобретать волнообразный, рецидивирующий характер.
При обострении болезни (кризе) больные жалуются на одышку, кашель, кровохарканье, слабость, сердцебиение, может повышаться температура тела (особенно при развитии инфарктпневмонии), боли в грудной клетке, в брюшной полости.
При осмотре больных выявляются бледность и желтизна кожных покровов, иктеричность склер, цианоз. При перкуссии легочный звук укорочен.
Над участками притупления могут выслушиваться сухие и (или) разнокалиберные влажные хрипы.
Присоединение обструктивного синдрома или инфарктпневмонии вносит соответствующие изменения в клиническую картину болезни. Нередко пальпируются увеличенные печень и селезенка.
Нередко пальпируются увеличенные печень и селезенка.
Рецидив болезни (криз) может продолжаться от нескольких часов до 1-2 нед. Длительность ремиссии также может быть различной, 1 год и более. В этот период больные сохраняют работоспособность. Состояние относительного благополучия может сменяться бурным прогрессированием болезни, кровохарканьем, рецидивирующими легочными кровотечениями, а также рецидивирующим пневмотораксом.
Обострение болезни может сопровождаться аллергическими реакциями (бронхоспастический синдром, эозинофилия и др.). По мере прогрессирования болезни тяжесть кризов нарастает, а присоединение инфарктпневмонии резко усугубляет имеющуюся легочную и сердечную недостаточность, приводя к летальному исходу. Злокачественное течение заболевания более характерно для детского возраста.
Исследование крови выявляет, как правило, гнпохром- ную анемию, анизоцитоз, пойкилоцитоз, ретикулоцитоз.
Во время криза, а также при присоединении пнфарктппев- монии выявляются лейкоцитоз, сдвиг лейкоцитарной формулы влево, увеличение СОЭ. Непрямой билирубин в сыворотке крови повышен.
Непрямой билирубин в сыворотке крови повышен.
Количество железа в плазме крови может быть повышенным, а в легочной ткани увеличено в 100 — 200 раз. В мокроте находят сидерофаги. Миелограмма указывает на усиленный эритропоэз.
Рентгенологическая картина вариабельна: от вуалеподоб- ного понижения прозрачности легочных полей, появления множественных мелкоочаговых (1-2 мм) теней, покрывающих равномерно все легочные поля или локализующихся преимущественно в средних и нижних отделах легких до возникновения более крупных полициклических очагов (инфильтратов), местами сливающихся между собой. Характерной особенностью их является не только внезапное возникновение, но и сравнительно быстрая обратная динамика, изменение их локализации.» Частые кризы приводят к развитию пневмосклероза.
Исследование функции легких, наряду с рестриктивными нарушениями, нередко выявляет и нарушения бронхиальной проходимости.
Идиопатический гемосидероз легких следует дифференцировать с гемосидерозом, возникающим вследствие застоя крови в легких при пороках сердца, профессиональным сидерозом, мп- лиарным (в том числе гематогенно-диссеминированным) туберкулезом легких, гемохроматозом, диссемииированным карцино- матозом, силикозом, саркоидозом, синдромом Гудпасчера. Нахождение сидерофагов в мокроте не является патогномоннчным признаком, так как может иметь место и при многих других заболеваниях (туберкулез легких, рак бронха, болезнь Рендю — Ослера, аспергиллез, пороки сердца и др.), сопровождающихся кровохарканьем или легочным кровотечением.
Нахождение сидерофагов в мокроте не является патогномоннчным признаком, так как может иметь место и при многих других заболеваниях (туберкулез легких, рак бронха, болезнь Рендю — Ослера, аспергиллез, пороки сердца и др.), сопровождающихся кровохарканьем или легочным кровотечением.
Для лечения больных идионатическим гемосидерозом легких в последние годы широко применяются кортикостероидные препараты. Спленэктомия на фоне кортикостероидной терапии, по мнению многих авторов, дает обнадеживающие результаты.
В литературе отсутствуют данные об эффективности применения иммуносупрессантов, хотя такие попытки имели место. Показана также симптоматическая терапия (препараты железа, гемотрансфузии и др.).
Применяется также десферал в дозе 50-70 мг на 1 кг массы тела (связывает железо и выводит его через почки).
Прогноз, как, правило, неблагоприятный. Средняя продолжительность жизни 3-5 лет. При комплексном целенаправленном лечении, адекватном диспансерном наблюдении — до 10 и более лет.
Основные причины летального исхода — профузное легочное кровотечение, острая дыхательная недостаточность вследствие закупорки бронхов сгустками крови или прогрессирующая правожелудочковая недостаточность с развитием де- компенснрованного легочного сердца.
Источник: https://www.eurolab.ua/diseases/1517/
Гемосидероз у детей: симптомы, причины, лечение, профилактика, осложнения
Причины
В организме каждого человека и ребенка в том числе содержится железо, оно участвует во многих процессах и примерное его содержание составляет 4-5 грамм.
Гемоглобин – это основной показатель количества железа и его соединений в организме у ребенка. Когда железа становится слишком много и показатель гемоглобина высокие, то пигмент гемосидерин накапливается в тканях организма ребенка.
Этот пигмент является составляющим гемоглобина. Рассмотрим причины появления гемосидероза у ребенка:
- Врожденные заболевание и особенности организма ребенка
- Аутоимунные заболевания, которые не лечатся, со временем только прогрессируют и ухудшают состояние ребенка
- Цирроз печени и другие ее заболевания
- Инфекционные заболевания, такие как мононуклеоз, гепатиты, бруцеллез
- Гепатоз
- Сепсис
- Отравления свинцом и другими железосодержащими ядами
- Процессы нарушения обмена веществ
- Гормональные нарушения, чаще всего в период полового созревания у детей
- Болезни крови
- Раковые заболевания. Лейкемия очень часто приводит к появлению гемосидероза
- Пороки сердца и проблемы с серднечно сосудистой системой
У детей очень часто встречается идиопатический гемосидероз. Также может быть гемосидероз легких, печени, кожи и других почти всех внутренних органах.
Симптомы
Симптомы гемосидероза у ребенка зависят от того, какой орган поражен. Самый часто встречающийся идиопатический гемосидероз у детей характеризуется следующими симптомами:
- Нарушение в работе легких
- Ребенок жалуется на то, что не может полноценно вздохнуть или выдохнуть
- Появляется одышка
- Кашель, который усиливается по ночам. Часто наступают острые приступы кашля.
- Мокрота, которая может быть с примесями крови или ржавого цвета
- В острый период заболевания у ребенка очень высокая температура, бледные покровы, предобморочное состояние
- Анализы крови показывают очень низкое содержание гемоглобина, ниже 20-30 г/л.
- Заболевание длиться от недели до трех
Для гемосидероза кожи у ребенка характерны следующие признаки:
- Отложение пигмента гемосидерина в кожи, в ее дерме.
- Геморрагическая сыпь, которая может локализовываться по всему телу, либо отдельными участками. Чаще всего поражаются ноги и руки
- Новые высыпания на коже сначала имеют желтый или коричневый цвет. Ребенок может жаловаться на зуд и жжение в местах высыпаний
- Со временем все высыпания приобретают характер бляшек и узелков и становятся ярко красными
Диагностика гемосидероза у ребенка
Диагностируется гемосидероз у детей врачом педиатром. При первых симптомах следует сразу обратиться к врачу для обследования. Оно может включать в себя следующее:
- Общий осмотр ребенка, анализ жалоб и анамнеза заболевания
- Опрос родителей или близких ребенка на наследственность, возможно гемосидероз является наследственным заболеванием
- Биохимический и клинический анализ крови
- Анализ крови на содержание железа
- Определение железосвязывающей способности крови
Для диагностики гемогосидероза легких проводится биопсия и бронхоскопия. Берутся ткани для гистологического исследования и проводится биопсия тканей (кожи, легких, печени, в некоторых случаях костного мозга) у детей. Понадобится консультация таких специалистов как дерматолог, эндокринолог и инфекционист. Также Ребенку могут быть назначены следующие исследования:
- Рентген легких и грудной клетки
- Флюорография легких
- Компьютерная томография
- Исследование мокроты под микроскопом для того, чтобы определить наличие бактерий
- Исследование промывных вод при проведении бронхоскопии
Осложнения
Основной опасностью гемосидероза является легочное кровотечение. Прогноз у данного заболевания неблагоприятный. Однако при своевременной и поддерживающие терапии люди живут довольно долго.
Гемосидероз кожи не представляет собой какой-то угрозы, а осложнением является визуальные изменения кожи. Однако этот тип гемосидероза не являются угрозой для жизни, в отличие от гемосидероза легких и каких-то других внутренних органов.
Гемосидероз легких чаще всего приводит к легочной недостаточности и инвалидности ребенка.
Лечение
Никакого домашенго самолечения гемосидероза у детей проводится не может. Не в коем случае нельзя рисковать. При первых симптомах или ухудшении состояния ребенка следует сразу обратиться к врачу.
Если у ребенка поднялась температура, то необходимо давать ему много пить. Больше всего подойдут регидратационные растворы, минеральная вода без газа.
Также надо дать ребенку жаропонижающие лекарства и сразу вызвать врача.
Что делает врач
После проведения обследования и постановки диагноза врачи назначат лечение. Оно зависит от того какая форма гемосидероза у ребенка. Для лечения легочного гемосидероза и гемосидероза каких-то других внутренних органов применятся гормональная терапия. Лечение чаще всего проводится в стационаре и включает в себя следующее:
- Инфузионную терапию
- Терапию, предназначенную на нормализацию уровня железа в организме
- Кровоостанавливающие средства
- Бронхолитики, которые улучшают отхождение мокроты
- Терапия иммунодепрессантами
- Применение аскорбиновой кислоты в больших количествах и препаратов кальция
При гемосидирозе кожи у ребенка проводится подобная терапия вместе с местной терапией. На кожу наносятся гормональные мази, также может проводиться криотерапия и ультрафиолетовое облучение ребенка. Также следует соблюдать безмолочную диету и вести правильный образ жизни.
Профилактика
Никакой специфической профилактики гемосидероза у детей в настоящее время не имеется. Следует вести правильный образ жизни. Периодически применять витаминные комплексы и препараты железа.
Также раз в пол года ребенку необходимо сдавать анализы крови и мочи и следить за состоянием здоровья. Своевременно проводить лечение кожных инфекций и заболеваний, ОРВИ и сердечно-сосудистых болезней.
Источник: https://DetStrana.ru/service/disease/children/gemosideroz/
Гемосидероз — обзор | Темы ScienceDirect
ПЕРЕГРУЗКА ЖЕЛЕЗА
Перегрузка железом, приводящая к гемосидерозу, является серьезным долгосрочным осложнением хронического переливания крови у пациентов с ВСС. Наиболее информативные сообщения о перегрузке железом, связанной с переливанием крови, были описаны у пациентов с талассемией; см. «Талассемии» для обсуждения патофизиологии перегрузки железом. Пациентам, у которых развивается перегрузка железом, можно назначать длительную хелатную терапию в форме дефероксамина; тем не менее, эта терапия является дорогостоящей, и из-за множества побочных эффектов и сложностей с введением препарата в анамнезе пациенты плохо соблюдают режим лечения. 113 Однако с одобрением FDA в ноябре 2005 г. первого перорального хелатора железа, доступного в Соединенных Штатах, соответствие 114 длительной хелатной терапии может улучшиться в результате повышения простоты использования.
Одной из возможных методик переливания крови для предотвращения перегрузки железом, которая в настоящее время изучается у пациентов с ВСС, является хронический эритроцитаферез. Процедуры хронического эритроцитафереза можно проводить с интервалом в 3-4 недели. В отличие от простых переливаний, серповидные эритроциты пациента удаляются, в то время как вводится равный объем нормальных донорских эритроцитов.Очевидное потенциальное преимущество хронического эритроцитафереза по сравнению с простым переливанием — предотвращение длительного накопления железа и гемосидероза.
Хотя хронический эритроцитаферез не получил повсеместного применения, он, по-видимому, клинически эффективен для снижения перегрузки железом у пациентов с хроническим переливанием крови. Четыре исследовательские группы 19–22 описали свой индивидуальный опыт использования протоколов переливания крови для хронического эритроцитафереза пациентам с ВСС.Все предположили, что эритроцитаферез ограничивает накопление железа у пациентов с ВСС, но три из четырех групп сообщили, что эритроцитаферез не устраняет необходимости в хелатной терапии у пациентов с ранее накопленным железом. 20–22 В целом уровни ферритина снизились у пациентов, подвергающихся хроническому эритроцитаферезу, которые получали одновременную хелатную терапию, и они либо слегка снизились, либо стабилизировались у пациентов, которые не получали хелатную терапию. Тем не менее, у пациентов из группы риска, которые начали эритроцитаферез без длительной истории предыдущих хронических простых переливаний, сохранялись очень низкие уровни ферритина в сыворотке, не требующие хелатной терапии. 20–22
Таким образом, оказывается, что хронический эритроцитаферез может быть наиболее эффективным, если его начинать на ранних этапах курса хронической трансфузионной терапии, до того, как произойдет значительное накопление железа. Тем не менее, хронический эритроцитаферез, по-видимому, стабилизирует или снижает уровень ферритина в сыворотке крови у пациентов, у которых уже развилась значительная перегрузка железом и которые продолжают хелатную терапию. 20–22
Основные потенциальные проблемы с протоколом переливания хронического эритроцитафереза (по сравнению с протоколами простого хронического переливания) — это повышенное воздействие продуктов крови с сопутствующим повышенным риском аллоиммунизации к эритроцитам и тромбоцитам и инфекции, передаваемой при переливании крови, а также повышенная стоимость (т.е., увеличенное количество используемых продуктов крови, увеличенная стоимость фенотипически сходных единиц, если они выбраны для переливания, и добавленная стоимость самих автоматизированных процедур).
Четыре опубликованных отчета 19–22 показали, что воздействие продуктов крови пациентов с ВСС увеличивается в протоколах хронического эритроцитафереза, при этом сообщается об увеличении коэффициента использования крови в диапазоне от 52% до почти 100% (т. Е. В 1-2 раза больше единиц эритроцита. переливали, чем при предыдущих простых переливаниях тем же пациентам).Однако из 43 обследованных пациентов только у 1 в период лечения эритроцитаферезом развилось аллоантитело 20 . Три из этих центров использовали антиген-соответствующие эритроциты для процедур эритроцитафереза: Singer and associates 22 , сопоставленные по C, E и K; Хиллиард и его коллеги 21 для C, E, K, Fy a и Jk b ; и Адамс и партнеры 20 для C, E, K и Jk b . При оценке очень низких показателей аллоиммунизации, которые были зарегистрированы для протоколов хронического эритроцитафереза, важно понимать, что большинство исследованных пациентов с SCD получали единицы эритроцитов, соответствующие по крайней мере антигенам C, E и K.
Высокая стоимость эритроцитафереза - важный вопрос. Хиллиард и его коллеги 21 сравнили общую стоимость 1 года эритроцитафереза (36 085 долларов США) с общей годовой стоимостью простого переливания крови (26 058 долларов США) и обнаружили экономически значимую разницу. Они предположили, что добавленная стоимость хелатной терапии (29 480 долларов США) с простым переливанием крови (всего 62 143 доллара США) делает эритроцитаферез без хелатирования гораздо менее дорогой альтернативой. Однако для пациентов, у которых на момент начала терапии эритроцитафереза наблюдается значительное накопление железа, хелатную терапию необходимо продолжать для достижения снижения или стабилизации уровня ферритина в сыворотке. 19–21 Это сравнение затрат является дополнительным доказательством того, что, если это технически осуществимо, раннее начало хронического эритроцитафереза у пациентов с ВСС до того, как произойдет значительное накопление железа, может быть предпочтительнее длительной хронической простой трансфузии и связанных с этим осложнений в виде перегрузки железом и необходимость хелатной терапии.
Гемосидероз печени — обзор
Первичные митохондриальные нарушения
Митохондриальные нарушения включают широкий спектр заболеваний, поражающих многие системы органов. 1015–1018 Многие из этих заболеваний поражают нервно-мышечную систему без поражения печени. Митохондриопатия, определяемая как нарушение функции или структуры митохондрий, может приводить к сочетанию множества разнообразных симптомов, включая печеночную недостаточность или холестаз с сохраненной функцией печени, кардиомиопатию, пигментную ретинопатию, миоклонические судороги, гипотонию, нарушение проксимальных канальцев, эндокринопатии или панцитопению. . Тяжесть заболевания сильно различается, как и время проявления и скорость прогрессирования заболевания.Унаследованные митохондриопатии печени, как правило, клинически проявляются в младенчестве или детстве; позднее поражение печени встречается реже.
Классификация митохондриопатий также является сложной задачей, особенно с учетом того, что количество известных митохондриальных цитопатий продолжает расти. Заболевания можно классифицировать по генетическому дефекту (аутосомный или митохондриальный) или по пораженной ферментной системе (окислительное фосфорилирование или окисление жирных кислот). Недавно была предложена комплексная классификация митохондриальных заболеваний 1019 , а также классификация поражений печени. 1020 В этом разделе мы сосредоточимся на митохондриальных нарушениях, при которых заболевание печени является важной клинической особенностью. Большинство из них генетические. Приобретенные митохондриальные нарушения печени, например, связанные с токсичностью ретровирусных препаратов аналогов нуклеозидов или с хроническим вирусным гепатитом, обсуждаются в других главах.
Митохондрии производят в клетках АТФ и, по совпадению, активированные формы кислорода; в гепатоцитах митохондрии играют важную роль в β-окислении.Митохондрии уникальны среди клеточных органелл тем, что имеют собственный набор ДНК, который кодирует некоторые белки дыхательной цепи, ответственные за окислительное фосфорилирование, а также специфические РНК, критические для синтеза белка в митохондриях. Наследование митохрондриальной ДНК (мтДНК) происходит по материнской линии. Митохондрии происходят почти исключительно из яйцеклетки, поскольку сперматозоиды содержат очень мало митохондрий. Митохондрии имеют собственную ДНК-полимеразу, полимеразу γ (POLG или POLγ) для производства мтДНК.Возможности проверки и восстановления ДНК в митохондриях крайне ограничены. Тканевая экспрессия аномалий мтДНК сложна и зависит от популяции митохондрий в каждой клетке. Локализация генов и определение конкретных генетических дефектов доступны для некоторых митохондриопатий. Отсутствие простого однозначного соответствия определенной мутации мтДНК клинической картине заболевания затрудняет корреляцию генотип-фенотип.
Дефекты, происходящие из мутаций в ядерной ДНК, наследуются как аутосомные признаки, тогда как дефекты митохондриальной ДНК наследуются по материнской линии.Митохондриальные нарушения встречаются редко, но их точная частота не определена, главным образом потому, что до сих пор точный диагноз был затруднен. Генетические митохондриальные нарушения можно классифицировать на основе того, влияет ли мутация на отдельный белок в митохондрии или на продукцию мтДНК. Подробно описаны мутации, затрагивающие отдельные белки дыхательной цепи. Обычными клиническими признаками являются тяжелый синдром неонатального гепатита или печеночная недостаточность новорожденных. 1021–1028 Дети с дефектами митохондриальной дыхательной цепи могут подвергаться повышенному риску развития гепатоцеллюлярной карциномы. 1029 Дефицит цитохром с оксидазы, обнаруженный у родственников из Квебека, может быть связан с ожирением печени. 1030 Нарушения белков, жизненно важных для сборки белков дыхательной цепи, также могут вызывать заболевание печени: важным примером является неонатальная печеночная недостаточность, связанная с мутациями в SCO1, белке, жизненно важном для сборки комплекса IV (цитохром с оксидазы) в митохондриальном окислении. цепь фосфорилирования. 1031 Синдром GRACILE — тяжелое мультисистемное аутосомно-рецессивное заболевание с такими особенностями, как холестаз, перегрузка печеночным железом и лактоацидоз; мутация находится в гене белка BCS1L, который необходим для сборки комплекса III. 1032 Описана также печеночная недостаточность из-за мутаций BCS1L. 1033 Другая важная группа митохондриальных нарушений демонстрирует истощение мтДНК. 1034 Как следствие, может возникнуть нарушение функции дыхательной цепи. Инфантильная атрофия ворсинок, проявляющаяся в виде трудноизлечимой диареи с митохондриальными аномалиями в мышцах или печени, может быть примером такого болезненного процесса. 1035,1036 Известно, что два специфических генных дефекта связаны с истощением мтДНК; Из этих мутаций в дезоксигуанозинкиназе (dGK или DGOUK) аномалия, более часто связанная с заболеванием печени. 1037–1041 Синдром Альперса, который обычно имеет относительно более хроническое течение, связан с мутациями ДНК-полимеразы γ. 1042–1045 Мутации в полимеразе γ могут приводить к разнообразному спектру клинических заболеваний, и этим может объясняться некоторая гетерогенность синдрома Альперса. 1046
Клинически митохондриальные цитопатии с заболеванием печени проявляются одним из двух способов. 1027 Во-первых, тяжелое заболевание печени может проявляться в течение первой недели жизни.Такие пациенты умирают внезапно или кажутся зараженными. Типичные пациенты имеют преходящую гипогликемию, тяжелые неврологические нарушения (гипотония, миоклонические судороги и задержка развития) и печеночную недостаточность с быстро летальным клиническим течением. 1027,1047,1048 В качестве альтернативы, появление симптомов откладывается, так что клиническая картина наступает в возрасте от 2 до 18 месяцев. Заболевание печени первоначально протекает менее серьезно (хотя печеночная недостаточность прогрессирует), неврологические нарушения варьируют, и некоторые пациенты выживают в течение длительного периода.Эта вторая группа включает прогрессирующую детскую полиодистрофию Альперса, теперь известную как синдром Альперса (или, взаимозаменяемо, синдром Альперса – Хаттенлохера) с клинической триадой рефрактерных приступов, психомоторной регрессии и гепатопатии. 1034 Пациенты с синдромом Альперса имеют диффузную церебральную дегенерацию и прогрессирующее нервно-мышечное ухудшение, включая атаксию, которая приводит к смерти, часто в первые 2 года жизни. 1049,1050 Первоначальное проявление обычно неврологическое, с миоклоническими припадками и задержкой развития; Поражение печени варьируется, но может прогрессировать до печеночной недостаточности в течение месяцев и, таким образом, часто предвещает смерть.Редко клинические проявления — острая печеночная недостаточность без судорожного расстройства. Спектр детской миоцереброгепатопатии ( MCHS ) представляет собой другую группу детских расстройств с мутациями POLG, при которых может возникать печеночная недостаточность, а также задержка развития, задержка развития, лактоацидоз и миопатия. 1051 Митохондриальные цитопатии, особенно синдром Альперса, являются фактором риска фульминантной печеночной недостаточности, вызванной вальпроатом, которая может скрыть основной диагноз. 1052–1056
Нарушения окисления жирных кислот представляют собой широкий спектр нарушений β-окисления. 1057 Гепатоцеллюлярный метаболизм жирных кислот включает сложные процессы, которые происходят как в цитоплазме, так и в митохондриях. Сложные эфиры длинноцепочечного ацилкофермента A (CoA) транспортируются в митохондрии через карнитин-зависимый механизм; эти сложные эфиры затем метаболизируются путем β-окисления в митохондриях. Некоторые из этих процессов происходят на внутренней мембране митохондрий, а другие — в матриксе митохондрий.Дефекты окисления жирных кислот снижают выработку энергии и препятствуют образованию кетоновых тел; производство дикарбоновых кислот становится доминирующим альтернативным путем. Клинические проявления со стороны печени часто имитируют синдром Рея. 1058 Заболевания, которые с особой вероятностью вызывают заболевание печени, включают: дефекты в обращении с карнитином, особенно дефекты поглощения карнитина ( OCTN2 ) и карнитин-пальмитоилтрансферазы ( CPT1 , CPT2 ); дефицит среднецепочечной ацил-КоА-дегидрогеназы (MCAD); Дефицит LCHAD в этой жировой печени во время беременности возникает у гетерозиготной матери, несущей плод, пораженный гомозиготой, и потому, что у пораженных людей может развиться неонатальная печеночная недостаточность или отложенная печеночная картина с холестатической болезнью печени или циррозом. 1059 Диагностика и лечение этих заболеваний затруднены. 1057,1058 Добавки карнитина могут быть эффективными при некоторых из этих расстройств и действительно могут спасти жизнь при дефиците поглощения карнитина ( дефектов OCTN2 ). Избегать длительного голодания критически важно для всех.
Скрининг митохондриального заболевания включает в себя тщательный сбор анамнеза и физикальное обследование для выявления любых неуловимых поддерживающих признаков и симптомов. Лактоацидоз — важное открытие.Гипогликемия может быть единственным признаком митохондриального нарушения. 1060 Лабораторные данные, подтверждающие диагноз дефекта митохондриальной дыхательной цепи, включают повышенный уровень лактата в плазме, соотношение лактат / пируват в артериальной плазме и соотношение α-гидроксибутират / ацетоацетат в артериальной плазме. Эти отклонения могут усиливаться после еды или пероральной глюкозной нагрузки. Органические кислоты в моче, уровни карнитина в сыворотке или функция почечных канальцев также могут быть аномальными при нарушениях окисления жирных кислот. Подтверждение диагноза митохондриопатии может потребовать технических средств.Гистопатологическое исследование печени и мышц с помощью электронной микроскопии может выявить характерные отклонения. Критерии диагностики поражения печени при синдроме Альперса были предложены и включают микровезикулярный стеатоз и онкоцитарные изменения, но в остальном эти критерии не особенно различимы. 1061 Гистохимическое исследование цитохромоксидазы в печени и мышцах может быть очень информативным. 1062 Некоторые субъединицы дыхательной цепи можно обнаружить с помощью иммуногистохимии.Молекулярно-биологические методы позволяют количественно определять мтДНК, а также обнаруживать некоторые делеции и / или мутации в ядерной или митохондриальной ДНК. Некоторые центры разработали полярографические или ферментативные методы измерения активности дыхательной цепи. Эти и новые методы диагностики были рассмотрены. 1063–1065 Если для этих исследований требуются свежие ткани, пациентам может потребоваться обратиться в центры, специализирующиеся на митохондриальных нарушениях. Анализы окисления жирных кислот можно проводить в фибробластах кожи либо ферментативно, либо функционально. 1015 Биопсия печени может быть информативной в отношении дефектов дыхательной цепи даже при отсутствии очевидного заболевания печени. 1066
Гистопатологические изменения дефектов митохондриального окислительного фосфорилирования были описаны многочисленными исследователями. 1021,1024,1026,1028,1047,1067-1071 Все они характеризовались микровезикулярным стеатозом (рис. 4.72), вариабельным холестазом и протоковой реакцией, вариабельным, а иногда и прогрессирующим фиброзом, а в некоторых случаях циррозом (рис. 4.73, 4.74). Наиболее подробные описания, включая ультраструктурные исследования, были представлены в серии из 10 случаев Bioulac-Sage et al. 1067 и в другой серии из пяти случаев Morris et al. 1069 Дополнительные гистопатологические признаки включают гемосидероз и онкоцитарный вид клеток печени (из-за увеличения количества митохондрий) (рис. 4.74). 1070 Изменения на ультраструктурном уровне включают плеоморфные митохондрии с небольшим количеством крист или без них и зернистый пушистый матрикс (рис.4.75). 1024,1067 Морфологические находки при синдроме Альперса очень похожи на таковые при других митохондриальных цитопатиях (рис. 4.76, 4.77). Может быть полезна корреляция изменений печени с изменениями в других системах органов. 1072
В девяти случаях нарушений окисления жирных кислот , включая ацил-КоА дегидрогеназу со средней длиной цепи (MCAD) и длинной цепью (LCHAD), гистопатологические находки были в основном микровезикулярным стеатозом. 1073 В случае, описанном Амирханом 1068 , наблюдалась тяжелая баллонная дегенерация клеток печени, умеренный холестаз и выраженный мостовидный фиброз.В ультраструктурном отношении были отмечены большие овальные мембраносвязанные везикулы, содержащие рыхлый хлопьевидный материал и неправильные профили внутренней мембраны.
Терапия митохондриальных нарушений зависит от заболевания. Новорожденному с печеночной недостаточностью требуется интенсивная поддерживающая терапия, особенно для точного диагноза и тщательной глобальной оценки внепеченочного поражения. Пациентам с более отсроченной формой заболевания печени проводится поддерживающее лечение, включая стратегии питания и метаболизма; неврологические особенности могут потребовать приема противоэпилептических препаратов, которые необходимо специально подбирать и контролировать, чтобы избежать обострения заболевания печени.В некоторых случаях использование «митохондриального коктейля» улучшило клиническое состояние пациента. 1074 Лечение нарушений окисления жирных кислот адаптируется к конкретному дефекту. 1058,1075 Трансплантация печени вызывает споры. Несколько авторов сообщили об успешном излечении заболевания печени с помощью трансплантации. Однако у пациентов с синдромом Альперса или другими митохондриопатиями с неврологическим поражением трансплантация не замедляет прогрессирование неврологического заболевания.Тщательный отбор пациентов имеет решающее значение: трансплантация печени не показана пациентам с клинически клинически очевидным заболеванием. 1076,1077
Накапливающиеся данные показывают, что многие младенцы с митохондриальными нарушениями обнаруживают аномалии еще до рождения. 1078 Пренатальная диагностика зависит от идентификации и клонирования мутантных генов или прямого измерения митохондриального метаболизма в культивируемых клетках ворсинок хориона или амниоцитах. 1079 Если ген, участвующий в митохондриопатии ранее пораженного брата или сестры, был идентифицирован, семья может получить пользу от пренатальной диагностики.Если семья с известным митохондриальным заболеванием желает пренатальной диагностики, следует связаться с центром, специализирующимся на этих заболеваниях, чтобы определить статус пренатальной диагностики конкретного заболевания.
Синдром Пирсона
Этот синдром состоит из рефрактерной сидеробластной анемии с вакуолизацией предшественников костного мозга и внешнесекреторной дисфункции поджелудочной железы. 1080 У пациентов наблюдаются большие делеции или перестройки митохондриального генома. 1081 У недавно зарегистрированного пациента были преимущественно печеночные проявления, такие как микровезикулярный стеатоз, массивный гемосидероз и быстро развивающийся цирроз. 1082 У этого пациента была делеция митохондриального генома 7436 п.н. во всех исследованных тканях, совместимая с синдромом Пирсона. Он умер в течение 3 месяцев после рождения от печеночной недостаточности. Гемосидероз у этого пациента мог быть вызван сложной гетерозиготностью (C282Y и H63D) в отношении мутаций гена наследственного гемохроматоза HFE, но у других младенцев с синдромом Пирсона также был гемосидероз печени, один из которых был гетерозиготным по мутации C282Y. 1083,1084
Нейрогепатопатия навахо
Это аутосомно-рецессивное заболевание представляет собой сенсомоторную нейропатию у полнокровных детей индейцев навахо (юго-запад США), которая была впервые описана Appenzeller et al. 1085 в 1976 г., и далее охарактеризован Singleton et al. в 1990 г. 1086 и Holve et al. в 1999; 1087 последние авторы предложили изменить название с невропатии на нейрогепатопатию, поскольку поражение печени является важным компонентом заболевания. Они описали три клинических фенотипа в зависимости от возраста на момент обращения и течения: инфантильный тип , проявляющийся в возрасте до 6 месяцев с желтухой и задержкой развития; детский тип в возрасте от 1 до 5 лет с дисфункцией печени, которая прогрессировала до печеночной недостаточности и смерти в течение 6 месяцев; и классический тип с вариабельным началом заболевания печени, но прогрессирующим неврологическим ухудшением.
Гистопатологические данные печени характеризуются многоядерными гигантскими клетками, смешанным макро- и микровезикулярным стеатозом, псевдоацинами, холестазом, воспалением, мостовидным фиброзом и в некоторых случаях циррозом. Ультраструктурные данные у четырех пациентов включали аномалии митохондрий (кольцевидные кристы, набухание и потеря крист, плеоморфный контур), стирание канальцевых микроворсинок и накопление внутриклеточных желчных пигментов и жиросодержащих пузырьков. 1087
Патогенез нейрогепатопатии навахо остается плохо изученным; однако выявлен генетический дефект.Мутации были идентифицированы в гене, кодирующем MPV17, белок внутренней митохондриальной мембраны, который способствует поддержанию мДНК. 1088,1089 Хотя детская форма имеет некоторое сходство с семейными расстройствами внутрипеченочного холестаза, детская форма предполагает митохондриальное расстройство, 1087 и фактически, по-видимому, относится к спектру расстройств истощения мтДНК.
Синдромы перегрузки железом и печень
Feder JN, Gnirke A, Thomas W, et al .Новый ген, подобный MHC класса 1, мутирован у пациентов с наследственным гемохроматозом. Nat Genet 1996; 14 : 399–408.
Артикул Google Scholar
Edwards CQ, Ajioka RS, Kushner JP. Гемохроматоз: генетическое определение. В: Barton JC, Edwards CQ (ред.). Гемохроматоз. Генетика, патофизиология, диагностика и лечение . Издательство Кембриджского университета: Кембридж, 2000, стр. 8–11.
Глава Google Scholar
Yen AW, Fancher TI, Bowlus CL.Возвращаясь к наследственному гемохроматозу: современные концепции и прогресс. Am J Med 2006; 119 : 391–399.
CAS Статья PubMed Central Google Scholar
Wessling-Resnic M. Импорт железа III. Перенос железа из слизистой в кровоток. Am J Physiol Gastrointest Liver Physiol 2006; 290 : G1 – G6.
Артикул Google Scholar
Ганц Т., Немет Э.Импорт железа IV. Гепсидин и регуляция метаболизма железа в организме. Am J Physiol Gastrointestinal Liver Physiol 2006; 290 : G199 – G203.
CAS Статья Google Scholar
Пьетранджело А, Траутвайн С. Механизмы заболевания: роль гепсидина в гомеостазе железа — последствия для гемохроматоза и других нарушений. Nat Clin Prac Gastroenterol Hepatol 2004; 1 : 39–45.
CAS Статья Google Scholar
von Recklinghausen FD.Убер-гемохроматоза. Tagelb Versamml Natur Artze Heidelberg 1889; 62 : 324–325.
Google Scholar
Шелдон Дж. Х. Гемохроматоз . Издательство Оксфордского университета: Лондон, 1935.
Google Scholar
Дэвис В.Д., Эрроусмит В. Эффект от повторных флеботомий при гемохроматозе; отчет о трех случаях. J Lab Clin Med 1952; 39 : 526–532.
PubMed PubMed Central Google Scholar
Scheuer PJ, Williams R, Muir AR. Патология печени у родственников больных гемохроматозом. J Pathol Bacteriol 1962; 84 : 53–64.
CAS Статья PubMed Central Google Scholar
Саймон М., Павлоцкий Ю., Бурель М., и др. . Идиопатическая гемохроматоза: заболевание, связанное с тканевым антигеном HLA 3. Nouv Presse Med 1975; 19 : 1432.
Google Scholar
Fleming RE, Britton RS, Waheed A, и др. . Патогенез наследственного гемохроматоза. Clin Liver Dis 2004; 8 : 755–773.
Артикул PubMed Central Google Scholar
Roetto A, Camaschella C. Новое понимание гомеостаза железа стало возможным благодаря изучению наследственного гемохроматоза, не связанного с HFE. Best Practice Res Clin Haematol 2005; 18 : 235–250.
CAS Статья Google Scholar
Фэрбенкс В.Ф. Популяционная генетика. В: Barton JC, Edwards CQ (ред.). Гемохроматоз. Генетика, патофизиология, диагностика и лечение . Издательство Кембриджского университета: Кембридж, 2000, стр. 42–50.
Глава Google Scholar
Pointon JJ, Wallace D, Merryweather-Clarke AT, и др. .Необычные мутации и полиморфизмы в гене гемохроматоза. Генетический тест 2000; 4 : 151–161.
CAS Статья Google Scholar
Гочи П.А., Пауэлл Л.В., Клаллен Д.Д., и др. . Популяционное исследование биохимических и клинических проявлений мутации гемохроматоза H63D. Гастроэнтерология 2002; 122 : 646–651.
CAS Статья PubMed Central Google Scholar
Акилар-Мартинес П., Швед Дж. Ф., Бриссо П.Оценка гиперферритинемии: обновленная стратегия, основанная на достижениях в обнаружении генетических аномалий. Am J Gastroenterol 2005; 100 : 1185–1194.
Артикул Google Scholar
Levy JE, Montross LK, Andrews NC. Гены, изменяющие фенотип гемохроматоза у мышей. Дж. Клин Инвест 2000; 105 : 1209–1216.
CAS Статья PubMed Central Google Scholar
Brissot P, Troadec MB, Loreal O.Клиническая значимость новых открытий в области транспорта и метаболизма железа. Curr Haematol Rep 2004; 3 : 107–115.
Google Scholar
Waalen J, Nordestgaard BG, Beutler E. Пенетрантность наследственного гемохроматоза. Best Practice Res 2005; 18 : 203–220.
CAS Google Scholar
Beutler E, Felitti VJ, Koziol JA, и др. .Проникновение мутации наследственного гемохроматоза 845G-A (282Y) HFE в США. Lancet 2002; 359 : 211–218.
Артикул PubMed Central Google Scholar
DeDomenico I, Ward DM, Musci G, и др. . Перегрузка железом из-за мутаций ферропортина. Haemoatologica 2006; 91 : 92–95.
CAS Google Scholar
Celec P.Гемоювелин: предполагаемая роль в метаболизме железа через год после его открытия. J Mol Med 2005; 83 : 521–525.
CAS Статья PubMed Central Google Scholar
Whitington PF. Гемохроматоз плода и детский. Гепатология 2006; 43 : 654–660.
CAS Статья PubMed Central Google Scholar
Брант Е.М., Олиник Дж. К., Бриттон Р.С., и др. .Гистологическая оценка железа в биоптатах печени: связь с мутациями HFE. Am J Gastroenterol 2000; 95 : 1788–1893.
CAS PubMed PubMed Central Google Scholar
Deugnier YM, Loreal O, Turlin B, et al . Патология печени при генетическом гемохроматозе: обзор 135 гомозиготных случаев и их биохимические корреляции. Гастроэнтерология 1992; 102 : 2050–2059.
CAS Статья PubMed Central Google Scholar
Пауэлл Э., Али А., Клустон А.Д., и др. . Стеатоз является кофактором поражения печени при гемохроматозе. Am J Gastroenterol 2005; 129 : 1937–1943.
CAS Google Scholar
Лайне Ф., Жуаннолле А.М., Морсет Дж., и др. . Фенотипическая экспрессия у выявленных гомозиготных женщин по C282Y зависит от индекса массы тела. J Hepatol 2005; 43 : 1055–1059.
CAS Статья PubMed Central Google Scholar
Deugnier YM, Guyader D, Crantock L, et al . Первичный рак печени при генетическом гемохроматозе: клиническое, патогенетическое исследование 54 случаев. Гастроэнтерология 1993; 104 : 228–234.
CAS Статья PubMed Central Google Scholar
Нидерау К., Фишер Р., Пуршель А, и др. .Долгосрочная выживаемость пациентов с наследственным гемохроматозом. Гастроэнтерология 1996; 110 : 1107–1119.
CAS Статья PubMed Central Google Scholar
Людвиг Ж.Л., Хашимото Э., Порайко М.К., и др. . Гемосидероз при циррозе: исследование 447 местной печени. Гастроэнтерология 1997; 112 : 882–888.
CAS Статья PubMed Central Google Scholar
Фил М.И., Скиано Т.Д., Боденхаймер Х.С., и др. .Наследственный гемохроматоз при трансплантации печени. Хирургическая трансплантология печени 1999; 5 : 50–56.
CAS Статья Google Scholar
Дуэйн П., Раджа КБ, Симпсон Р.Дж., и др. . Абсорбция железа в кишечнике у хронических алкоголиков. Alcohol Alcoholism 1992; 27 : 539–544.
CAS PubMed PubMed Central Google Scholar
Пауэлл Л.В., Флетчер Л.М., Холлидей Дж.Различие между гемохроматозом и алкогольным сидерозом. В: Hall P (ed). Алкогольная болезнь печени , 2-е изд. Эдвард Арнольд: Лондон, 1995, стр. 199–216.
Google Scholar
Fabris C, Toniutto P, Scott CA, и др. . Индексы сывороточного железа как мера отложений железа при хроническом гепатите D. Clin Chim Acta 2001; 304 : 49–55.
CAS Статья PubMed Central Google Scholar
Яно М., Хаяси Х., Ваксава С., и др. .Долгосрочные эффекты флеботомии на биохимические и гистологические параметры хронического гепатита С. Am J Gastroenterol 2002; 97 : 133–137.
CAS Статья PubMed Central Google Scholar
Hofer H, Osterreicher C, Jessner W, и др. . Концентрация железа в печени не предсказывает ответ на терапию стандартным и пгилированным IFN / рибавирином у пациентов с хроническим гепатитом C. J Hepatol 2004; 40 : 1018–1022.
CAS Статья PubMed Central Google Scholar
Бассет М.Л., Холлидей Дж. У., Пауэлл Л. В.. Значение измерения железа в печени при раннем гемохроматозе и определение критического уровня железа, связанного с фиброзом. Hepatology 1986; 6 : 24–29.
CAS Статья PubMed Central Google Scholar
LeSage GD, Baldus WP, Fairbanks VF, и др. .Гемохроматоз: генетический или вызванный алкоголем? Гастроэнтерология 1983; 84 : 1471–1477.
CAS PubMed PubMed Central Google Scholar
Адамс ПК, Агнью С. Возвращение к алкоголизму при наследственном гемохроматозе; распространенность и клинические последствия среди гомозиготных братьев и сестер. Hepatology 1996; 23 : 724–727.
CAS Статья PubMed Central Google Scholar
Ирвинг М.Г., Холлидей Дж. У., Пауэлл Л. В..Связь между алкоголизмом и увеличением запасов железа в печени. Алкоголь: Clin Exp Res 1988; 12 : 7–13.
CAS Статья Google Scholar
Deugnier YM, Turlin B, Powell LW, и др. . Дифференциация гетерозигот и гомозигот при генетическом гемохроматозе с помощью гистологического индекса железа в печени: исследование 192 случаев. Hepatology 1993; 19 : 30–34.
Артикул Google Scholar
Олиник Дж., Холл П., Салли Р., и др. . Компьютерное измерение железа в биопсиях печени: сравнение с биохимическим измерением железа. Hepatology 1990; 12 : 26–30.
CAS Статья PubMed Central Google Scholar
Гемохроматоз и вождение автомобиля — Fundación MAPFRE
Гемосидероз
Гемосидероз характеризуется локальным или генерализованным отложением железа в тканях выше нормы.Гемохроматоз возникает при повреждении тканей.
Симптомы гемохроматоза вызваны циррозом печени, сахарным диабетом, миокардиопатией, сердечной недостаточностью, аритмией и, реже, болями в животе и артритом.
Переливание крови — это форма трансплантации клеточных компонентов крови от донора реципиенту, при которой иногда могут возникать следующие осложнения.
Гемолитическая реакция обычно имеет острое начало и возникает во время переливания или сразу после него, с переменным исходом, но это всегда серьезное заболевание.
Пациент замечает дискомфорт и беспокойство, начинается с одышки, головной боли, сильной боли в шее, груди и нижней части спины, сжатия груди и рвоты.
- Фебрильная реакция связана с ознобом, лихорадкой, головной болью и болью в пояснице.
- Аллергическая реакция обычно легкая, с крапивницей, отеком, головокружением и головной болью во время переливания или сразу после него, а иногда могут возникать бронхоспазм и недержание мочи.В зависимости от симптомов и их тяжести будут назначены антигистаминные препараты, кортикоиды или адреналин.
- Перегрузка кровообращения возникает у пациентов с анемией и сердечными заболеваниями, когда переливание крови вызывает застойную сердечную недостаточность, требующую специального лечения.
Консультации по гемосидерозу
- Способность управлять автомобилем будет зависеть от стадии заболевания, поскольку поражение многих органов встречается часто.
- Врач укажет на дополнительные риски, вызванные гемохроматозом при вождении, а также на благоприятное или стабильное развитие, которое в каждом случае позволяет управлять автомобилем.
- В необходимых случаях врач посоветует не водить машину.
- Желательно взять с собой в машину на видном месте отчет с данными о заболевании и лечении, если потребуется помощь на дороге в случае возникновения осложнений во время вождения или в случае аварии.
Миелопролиферативные заболевания
Истинная полицитемия характеризуется повышенной концентрацией гемоглобина, объемом, вязкостью крови и эритроцитозом.У половины пациентов также наблюдается повышенная продукция лейкоцитов и тромбоцитов.
Это проявляется слабостью, зудом, головной болью, головокружением, нарушениями зрения, астенией или одышкой, а также частыми желудочно-кишечными кровотечениями и носовыми кровотечениями. Часто наблюдаются гепатомегалия и спленомегалия, которые могут стать массивными.
Характерны ранние атеросклеротические и тромботические заболевания, сопровождающиеся инсультом, инфарктом миокарда и заболеваниями периферических сосудов. Позже возникают подагра и нефролитиаз.
Это может быть связано с язвенной болезнью, тромбозом и болями в костях. Наиболее частой причиной смерти является тромбоз, за которым следуют осложнения в виде миелоидной метаплазии и кровоизлияния.
Вторичный эритроцитоз возникает из-за артериальной гипоксемии при хронической болезни легких, курении, некоторых новообразованиях или нарушениях гемоглобина.
Миелофриброз или миелоидная метаплазия в процессе развития вызывает астению, анемию, потерю веса, спленомегалию и в половине случаев гепатомегалию.
Часто возникает тромбоз и нечасто кровотечение.
Лечение направлено на борьбу с осложнениями, включая переливание крови при тяжелой анемии, спленэктомию и паллиативную терапию.
Первичная тромбоцитемия часто сопровождается слабостью, желудочно-кишечным кровотечением, носовыми кровотечениями, экхимозом, головной болью, парестезией кистей и стоп, ишемией пальцев рук и головокружением. Часты анемии.
Лечение направлено на снижение количества тромбоцитов, геморрагических и тромботических осложнений.
Хронический миелоидный лейкоз характеризуется спленомегалией и лейкоцитозом, и сначала проявляется хроническая фаза с небольшими симптомами, а затем бластная фаза, аналогичная острому лейкозу с фатальным прогнозом.
Консультации по переливанию крови
- Пациент не может управлять автомобилем до тех пор, пока его клиническое состояние полностью не вернется к норме и не будет предоставлен отчет специалиста, в котором это уточняется и указывается.
Консультации по фебрильной реакции
- Пациенту не следует садиться за руль с лихорадкой, головной болью и отсутствием концентрации внимания.
Консультации по аллергическим реакциям
- Пациент не может водить машину до тех пор, пока его клиническое состояние полностью не вернется к норме, и врач предупредит пациента о риске.
- Пациент будет предупрежден о побочных эффектах некоторых лекарств, которые могут мешать управлению автомобилем, например о сонливости.
Рекомендации по перегрузке кровообращения
- Пациент не может водить машину до тех пор, пока его клиническое состояние полностью не вернется к норме, и пациента следует предупредить об этом.
- Специалист сообщит о полном кардиологическом выздоровлении пациента без каких-либо симптомов или нарушений, о том, когда он может управлять автомобилем.
Консультации по миелопролиферативным заболеваниям
- Истинная полицитемия — это заболевание, которое мешает вождению автомобиля из-за риска возникновения осложнений, связанных с повышенной вязкостью и повышенным объемом кровообращения.
- Специалист посоветует пациенту не садиться за руль в случае возможного или наличия осложнений заболевания, предоставив в рекомендациях отчета совет не садиться за руль.
- Исходя из развития каждого пациента, эксперт порекомендует способность управлять автомобилем в легких случаях.
Консультации по эритроцитозу
- Не мешает управлять автомобилем.
- Симптомы основного заболевания — это те, которые ограничивают вождение автомобиля.
Консультации по миелофриброзу или миелоидной метаплазии
- В запущенных случаях способность управлять автомобилем ограничена из-за головокружения, сонливости и недостатка внимания, вызванных анемией.
- Приступы тромбоза приводят к инвалидности при вождении, о чем следует предупредить пациента.
- Спленэктомия требует послеоперационного периода восстановления без вождения, пока специализированный врач не сообщит о полном выздоровлении пациента как в гематологии, так и в заживлении ран.
Консультации по первичной тромбоцитемии
- Наличие кровотечения, симптоматической анемии и тромбоза препятствует управлению автомобилем.
- Благоприятный ответ на лечение и его стабилизация с течением времени позволят управлять автомобилем, всегда с заключением врача-эксперта по этому поводу.
Консультации по миелоидному лейкозу
- Вождение автомобиля разрешено во время бессимптомной хронической фазы.
- Неблагоприятное естественное течение болезни не позволяет управлять автомобилем в определенное время, и пациента должен предупредить об этом лечащий врач.
Педиатрия по случаям болезни Глава
Это 8-месячный мужчина, направленный в Детскую легочную клинику с основной жалобой на хронический кашель. Кашель присутствует 7 недель.Первоначально это было связано с вирусным заболеванием, но вирусные культуры и скрининг на RSV были отрицательными. Кашель уменьшился, но не исчез с помощью бронходилататоров и короткого агрессивного курса пероральных кортикостероидов, которые были назначены при подозрении на астму. Симптомы снова ухудшились после прекращения приема бронходилататоров и стероидов. Лихорадка невысокая, но признаков новой инфекции верхних дыхательных путей нет. Рентгенограммы грудной клетки, выполненные лечащим врачом пациента, показывают ухудшение диффузных пятнистых уплотнений с гиперэкспандированием.Обзор систем показывает замедление роста от 4-месячного обычного посещения ребенка до настоящего времени. В семейном анамнезе отсутствуют какие-либо респираторные заболевания, хронические или серьезные заболевания.
Экзамен: VS T 37.0, P 140, R 50, BP 100/60, пульсоксиметрия показала насыщение кислородом 86% в воздухе помещения. Его вес находится на 5-м процентиле. Он худой, слегка бледный, тахипноэ с легким затрудненным дыханием. Экзамен HEENT — это нормально. Его грудь имеет симметричное расширение. Имеются незначительные ретракции подреберья, но не межреберные или надключичные ретракции.Его сердце тахикардическое, но ровное, без шума. Звуки его дыхания грубые на вдохе и выдохе. Фаза выдоха немного удлиняется. Хороший воздухообмен. Его живот мягкий, не растянутый, с нормальными звуками кишечника и без гепатоспленомегалии.
Кислород запускается через маску, и он поступает в больницу. Назначены бронходилататоры и антибиотики и возобновлены кортикостероиды. Его насыщение кислородом лишь незначительно улучшается при добавлении кислорода.Газы артериальной крови показывают pH 7,35, pCO2 34, pO2 55 на 2 литрах в минуту дополнительного кислорода. Его общий анализ крови показывает умеренное повышение количества лейкоцитов, нормальное количество тромбоцитов и анемию с гематокритом 26, средним корпускулярным объемом 76 и шириной распределения красных кровяных телец 15. Количество эозинофилов умеренно повышено. Исследования железа показывают истощение запасов железа. Рентгенограмма его грудной клетки все еще показывает интерстициальные инфильтраты.
Его улучшение в течение следующих трех дней постепенное, и на рентгенограмме грудной клетки все еще видны интерстициальные паттерны.Проведена бронхоскопия. Бронхоальвеолярный лаваж демонстрирует большое количество макрофагов, нагруженных гемосидерином. Культуры и макрофаги с липидами отрицательны.
После дальнейшего изучения его истории, он страдал запором на смеси в течение первых нескольких месяцев жизни, поэтому его перевели на обычное коровье молоко и сок в возрасте 3 месяцев. Преципитаты сывороточного IgG к белку коровьего молока сильно положительны. Поставлен диагноз «Легочный гемосидероз по синдрому Хайнера».Все коровье молоко и молочные продукты не выдаются. Его клиническое состояние стремительно улучшается. Его последующая рентгенограмма грудной клетки проясняется только с сохраняющимися полосатыми уплотнениями. После недели приема кортикостероидов их отменяют. Он продолжает принимать препараты железа, и его анемия постепенно проходит. Рост также нормализуется в течение следующих 3 месяцев.
Любое кровотечение из или в легкое приведет к отложению гемосидерина в макрофагах легких. Легочный гемосидероз (ЛГ) — это термин, который следует использовать для обозначения хронических постоянных или повторяющихся кровотечений.Это сложная тема, охватывающая спектр различных состояний и болезненных состояний. Клинические проявления и течение очень разнообразны. Кровотечение может быть очаговым или диффузным. Это может произойти в дыхательных путях, альвеолах или паренхиме. Это может быть легочный (более низкое давление) или бронхиальный (более высокое давление) кровоток. Он может быть легким или опасным для жизни. Хотя универсального согласия в классификации нет, полезно разделить ЛГ на первичную или вторичную (1-3). В следующей таблице перечислены этиологии легочного гемосидероза у детей с точки зрения того, является ли поражение легких первичным или вторичным:
1.Первичный легочный гемосидероз (ПРК)
. . . А. Идиопатический (IPH).
. . . B. Связан с некоторыми плесневыми грибами или грибами (Stachybotrys atra) (4).
. . . C. Связано с аллергией на коровье молоко (синдром Хайнера) (5).
. . . D. Ассоциируется с антителами к базальной мембране легких (гранулематоз Вегенера) и почек (синдром Гудпасчера).
. . . E. Травма, включая аспирацию инородного тела.
. . . F. Бронхоэктазы и другие хронические инфекции легких.
2. Вторичный гемосидероз легких
. . . A. Заболевания легочных сосудов, включая сердечные заболевания, легочную гипертензию и артериовенозные мальформации.
. . . Б. Генерализованное системное воспалительное заболевание.
. . . C. Генерализованные нарушения свертываемости крови, включая пурпурные синдромы и коагулопатии, связанные с сепсисом.
. . . D. Проглатывание лекарств или химических веществ, таких как ангидрид тримеллитовой кислоты или D-пеницилламин.
Патофизиология легочного кровотечения зависит от этиологии.Кровотечение может быть результатом наследственной или приобретенной слабости, воспаления или закупорки легочных кровеносных сосудов; иммунные реакции или отложение комплекса антиген-антитело в легких; инвазивные или хронические инфекции или токсические реакции. Независимо от этого, любые клетки крови в альвеолах, дыхательных путях или паренхиме разрушаются, и гемоглобин поглощается местными макрофагами. При попадании внутрь гемоглобин превращается в гемосидерин путем лизосомной деградации. Он также может активировать местные макрофаги, за которыми следует воспалительный каскад, включая привлечение клеток и выработку цитокинов.Эти события могут вызвать все типы заболеваний легких, легочные уплотнения и лимфаденопатию.
Обструктивное заболевание проявляется в сужении дыхательных путей с увеличением отека, слизи и попадания эпителиальных клеток в дыхательные пути. Виден бронхоспазм (сокращение гладких мышц, окружающих дыхательные пути). Хроническое накопление отложений фибрина и коллагена может привести к фиброзу легких с пониженной эластичностью легких. Это может проявляться в виде рестриктивного заболевания легких.
Легочный гемосидероз — необычная находка, но истинная частота неизвестна. Первичная ЛГ чаще встречается у детей. Пик заболеваемости ИЛГ (идиопатической) приходится на возраст от 1 до 7 лет на момент постановки диагноза, но примерно 15% диагностируются после 16 лет. В возрасте до 10 лет заболеваемость поровну распределяется между полами. После 10 лет соотношение мужчин и женщин составляет 2: 1 (7). Сообщается о редких случаях семейных кластеров. У взрослых ЛГ чаще носит вторичный характер.
Классическая триада результатов включает легочные инфильтраты, железодефицитную анемию и кровохарканье (хотя кровохарканье у детей встречается реже). Примерно 50% детей младшего возраста не жалуются на легочные заболевания. Жалобы при наличии включают жар, бледность, одышку, кашель, непереносимость физических упражнений и задержку роста. Распространенными симптомами являются тахипноэ, тахикардия, цианоз, дубинки, мелкие или грубые хрипы, хрипы и гипоксемия. У детей со значительным кровотечением может быть трудно определить, идет ли кровь из верхних дыхательных путей, нижней легочной системы или желудочно-кишечного тракта.У многих пациентов будет мелена из проглоченной легочной крови.
Рентгенологический вид может варьироваться в зависимости от степени поражения и хронического характера. Простые рентгенограммы грудной клетки могут варьироваться от нормальных до демонстрации очаговой лимфаденопатии или консолидации, или обширного двустороннего интерстициального заболевания. Функциональное исследование легких может выявить обструктивный, ограничительный или смешанный характер.
У пациентов с ЛГ обычно задерживается постановка диагноза.Инфекционная пневмония, бронхит, аспирация, астма и кистозный фиброз чаще наблюдаются со многими схожими жалобами и симптомами. Для постановки диагноза необходимо наличие высокого клинического подозрения. Хотя обнаружение в бронхоальвеолярном лаваже большого количества макрофагов, нагруженных гемосидерином, является диагностическим, это не конец оценки. Для оценки этиологии необходимы последующие исследования. IPH — это диагноз исключения, который уместен только после завершения тщательного исследования.
Полный анализ крови, исследования железа и определение функции почек помогут оценить текущее состояние пациента. ANA, ревматоидный фактор, скорость оседания эритроцитов, уровни комплемента, иммуноглобины, антитела против базальной мембраны и преципитины сыворотки к белку коровьего молока также должны быть включены в оценку этиологии. Следует включить кардиологическое обследование, включая физикальный осмотр, оценку ЭКГ и рентгенографии. Следует рассмотреть возможность направления к кардиологу, ревматологу или гематологу.Некоторые эксперты рекомендуют проводить биопсию легких для всех пациентов, включая исследования с использованием иммунофлуоресценции и электронной микроскопии. Другие оставляют это для отдельных случаев.
Каждому пациенту должны быть назначены поддерживающие меры в соответствии с его представлением, включая дополнительный кислород, переливание крови и антибиотики в случаях вторичной инфекции или подозрения на инфекцию. Респираторная поддержка включает физиотерапию грудной клетки, помогающую избавиться от лишнего секрета, бронходилататоры, CPAP или механическую вентиляцию легких.Пациентам с продолжающимся кровотечением может быть полезно положительное давление в конце выдоха (ПДКВ).
Лечение следует рассматривать в свете этиологии. Для людей с ЛГ от воздействия и токсинами от Stachybotrys основным лечением является устранение возбудителя. Ограничение диеты, особенно для тех, у кого обнаружены преципитаты сыворотки к молочным продуктам, имеет важное значение. Для пациентов с вторичной ЛГ критически важно лечение первичной этиологии.
Медикаментозная терапия обычно направлена на контроль воспалительной реакции.Кортикостероиды являются основой, но исследований, сравнивающих стратегию дозирования, не проводилось. Дозу обычно начинают с 2-5 мг / кг / день преднизона или его эквивалента. Эта доза используется в течение нескольких недель или до тех пор, пока кровотечение не будет хорошо куплено. Затем доза уменьшается, и существует множество различных протоколов. Другие иммунодепрессанты использовались в попытке уменьшить пролонгированные эффекты кортикостероидов, включая азатиоприн, хлорохин и циклофосфамид.
Если у пациента продолжающееся сильное кровотечение, можно провести исследование ядерной медицины с использованием меченых эритроцитов, чтобы определить местонахождение этого места.При опасном для жизни кровотечении или пациентах, которые не реагируют на медикаментозное лечение, может потребоваться эмболизация бронхиальной артерии. В крайних случаях может потребоваться удаление пораженного сегмента или доли.
Тщательный мониторинг должен включать в себя рост, мониторинг насыщения кислородом, исследования гемоглобина и железа, рентгенограммы грудной клетки, исследование функции легких (если он достаточно взрослый) и исследования функции почек в период выздоровления. Восстановление агрессивных кортикостероидов или иммуносупрессивной терапии типично для обострений прорыва.
Прогноз варьируется в зависимости от причины. В случае вторичной ЛГ он должен включать естественную историю основного заболевания. Задержка с диагностикой ухудшит прогноз. Ранние исследования показали очень плохой прогноз ИЛГ. В среднем от постановки диагноза до смерти прошло около 2 лет. Более поздние отчеты предполагают улучшение этой статистики при более агрессивном ведении (8,9). Кроме того, новые технологии предоставили средства для более обширной оценки, облегчая конкретное диагностическое определение (т.е., меньшее количество диагнозов ИЛГ). Многие пациенты могут достичь стойкой или полной ремиссии с помощью новых методов лечения. Хотя рубцевание и фиброз могут быть постоянными, возможна полная компенсация, особенно у молодых пациентов.
Вопросы
1. Какие из следующих результатов обычно не наблюдаются у пациентов с легочным гемосидерозом?
. . . . . а. Жар
. . . . . б. Паренхиматозные уплотнения
. .. . . c. Гиперкарбия
. . . . . d. Гипоксемия
. . . . . е. Кашель
2. Почему важно классифицировать гемосидероз как первичный или вторичный?
3. Какое заболевание легких проявляется при легочном гемосидерозе?
. . . . . а. Обструктивная болезнь
. . . . . б. Рестриктивное заболевание
. . . . . c. Смешанные обструктивные и ограничительные
. . . . . d. Любой из вышеперечисленных
4.Что из перечисленного не входит в классическую триаду симптомов легочного гемосидероза?
. . . . . а. Легочное кровотечение
. . . . . б. Анемия
. . . . . c. Кровохарканье
. . . . . d. Легочные инфильтраты
. . . . . е. Ни один из вышеперечисленных
5. Верно / неверно: Биопсия легкого — это предпочтительный диагностический тест при идиопатическом гемосидерозе легких.
Связанные рентгеновские снимки
Дело о болезни Гудпасчера: Накамура CT.Кровохарканье и анемия у 12-летнего ребенка. В: Ямамото Л.Г., Инаба А.С., ДиМауро Р. (ред.). Радиологические случаи в педиатрической неотложной медицине, 1995, том 3, случай 7. Доступно в Интернете по адресу: www.hawaii.edu/medicine/pediatrics/pemxray/v3c07.html
Список литературы
1. McCoy KS. Глава 54-Гемосидероз. В: Taussig LM, Landau LI (ред.). Детская респираторная медицина. 1999, Сент-Луис: Мосби, стр. 835-841.
2. Heiner DC. Глава 36 — Легочный гемосидероз.В: Черник В., Кендиг Е.Л. (ред.). Заболевания дыхательных путей у детей Кендига, пятое издание. 1990, Филадельфия: W.B. Сондерс, стр. 498-509.
3. Авиталь А., Спрингер С., Годфри С. Редкое хроническое заболевание легких: легочные геморрагические синдромы у детей. Ped Resp Rev 2000; 1 (3): 1-9.
4. Элидемир О., Джузеппе Н. С., Россманн С. Н., Фан Л. Изоляция стахиботридов из легкого ребенка с легочным гемосидерозом. Педиатрия 1999; 104 (4): 964-966.
5. Пищевой гемосидероз легких (синдром Хайнера). Миддлтон Э. и др. (Ред.). Аллергия: принципы и практика, пятое издание. 1998, Сент-Луис: Ежегодник Мосби, стр. 1173.
6. Дирборн Д.Г. Глава 402 — Легочный гемосидероз (легочное кровотечение). В: Behrman RE, Vaughan VC (ред.). Учебник педиатрии Нельсона, 16-е издание. 2000, Филадельфия: W.B. Сондерс, стр. 1295–1297.
7. Кьельман Б., Элиндер АГ, Гарвич С., Свон Х.Идиопатический гемосидероз легких у шведских детей. Acta Pediatr Scand 1984; 73: 584-588.
8. Le Clainche L, et al. Отдаленные последствия идиопатического легочного гемосидероза у детей. Медицина 2000; 79 (5): 1-14.
9. Саид М.М., Ву М.С. и др. Прогноз при педиатрическом идиопатическом легочном гемосидерозе. Chest 1999; 116 (3): 721-725.
Ответы на вопросы
1. c. Гиперкарбия обычно не наблюдается, потому что компенсаторные механизмы обычно преодолевают проблемы снижения газообмена за счет увеличения минутной вентиляции (либо за счет увеличения скорости или глубины вентиляции).
2. Это одна из схем, помогающих определить этиологию состояния с множеством причин. Лечение, скорее всего, будет успешным после выявления и лечения основной причины.
3. г. Бронхоспазм, отек и слизь могут сужать дыхательные пути, вызывая обструктивное заболевание, подобное астме. Хроническое воспаление может увеличивать интерстициальные отложения фибрина и коллагена, которые затем снижают комплаентность, что приводит к развитию рестриктивного заболевания. Возможна любая их комбинация.
4. а. Классическая триада — железодефицитная анемия, легочные инфильтраты и кровохарканье, хотя кровохарканье у детей встречается реже. «Легочное кровотечение» действительно приводит к гемосидерозу, но это не часть классической триады.
5. Неверно. Существуют разногласия по поводу того, следует ли проводить биопсию легкого всем пациентам со значительной ЛГ. Можно утверждать, что всем пациентам с ЛГ без известной этиологии (подозрение на ИЛГ) следует делать биопсию легкого.Но поскольку IPH является диагнозом исключения, биопсия легкого не исключает других частей оценки, включая анамнез, осмотр, радиологию и лабораторные исследования. Патология, полученная при биопсии легкого, редко является диагностической самостоятельно и может быть интерпретирована только в свете другой информации.
Вернуться к содержанию
Домашняя страница факультета педиатрии Гавайского университета
Инфекция легочной нокардии у ребенка с идиопатическим легочным гемосидерозом | BMC Pulmonary Medicine
16 мая 2019 года в нашу больницу поступила девочка 7 лет с основными жалобами на бледность кожи, сохраняющуюся в течение 1 года и кашель в течение 20 дней.У нее был кашель, гнойная мокрота, эпизодическая боль в груди и профилактическое применение вориконазола. Ей ранее поставили диагноз ЖДА в местной больнице из-за головокружения и жалоб на боль в животе при обращении в апреле 2018 г. 25 февраля 2019 г. в нашей больнице ей поставили диагноз ИГБ на основании проявления диффузных мелких зернистых теней в обоих легких на Компьютерная томография грудной клетки (КТ), наличие в желудочном соке макрофагов, нагруженных гемосидерином, ухудшение ее бледного цвета лица, апатия, плохой аппетит, периодическая рвота желудочным содержимым без желчи и крови, отсутствие гематурии и наличие черного стула ( Инжир.1а). С этого момента вводили непрерывные дозы кортикостероидов (метилпреднизолон, 2 мг / кг в день в течение 20 дней, затем 1,54 мг / кг в день в течение 2 месяцев). Перед госпитализацией 2 мая 2019 г. на КТ были обнаружены диффузные зернистые тени в обоих легких и округлые узловатые тени высокой плотности в правом легком (рис. 1б). Пациентка является вторым ребенком здоровой пары, ей 16 лет. летняя сестра была здорова.
Рис. 1Изменения в визуализации грудной клетки пациента. a В обоих легких наблюдались диффузные мелкозернистые тени (за 2 месяца до поступления). b Диффузные зернистые тени в обоих легких и круглые узловатые тени высокой плотности в правом легком (за 14 дней до поступления). c — d Передача болезни в двустороннее легкое снизилась неравномерно, и в легких все еще оставались мелкие частицы. Правое легкое содержало рассеянные круглые очаги поражения, границы были четкими, на дугах видны два больших очага поражения, более крупное — около 30 × 42 × 27 мм (в день поступления). e , f Поражения в нижней доле правого легкого улучшились, но наблюдались образование полости, новые поражения в левом легком и двустороннее утолщение плевры (на 9-й день госпитализации). g , h Поражения в нижней доле правого легкого с полостью были значительно уменьшены, а изменения обоих легких улучшились (на 16-й день выписки)
Физикальное обследование показало артериальное давление 111/68 мм рт. ст., частота дыхания 31 уд / мин, пульс 100 уд / мин и вес 31,5 кг. Отмечались бледный цвет лица и округлое лицо. У больного был приступообразный непрерывный кашель, при аускультации легкие грубые звуки дыхания, печень расположена на 2 см ниже ребер, селезенка ниже реберной области не пальпируется.Влажные хрипы, хрипы, кровохарканье, боли в груди и одышка отсутствовали. Неврологическое обследование явных отклонений не выявило. Не было ни сыпи, ни булавленных пальцев, ни синяков на губах и конечностях.
Лабораторные исследования показали, что количество лейкоцитов составляет 20,62 × 10 9 / л (контрольный диапазон, 4–10 × 10 9 / л), количество тромбоцитов 310 × 10 9 / л (контрольный диапазон, 100–400 × 10 9 / л), уровень гемоглобина 152 г / л (референсный диапазон 110–155 г / л), средний объем эритроцитов 85.3 мкл (контрольный диапазон, 75–92 мкл), среднее содержание гемоглобина 25,4 пг (контрольный диапазон, 26–31 пг) и ретикулоцитов 1,36% (контрольный диапазон, 0,5–1,5%). IgG, IgA и IgM составляли 5,40 г / л, 0,81 г / л и 1,87 г / л соответственно. Правое легкое содержало рассеянные круглые очаги поражения, а границы были четкими на КТ грудной клетки, выполненной в день госпитализации (рис. 1c, d). Биопсия костного мозга выявила активную гиперплазию эритроидов, в первую очередь в поздних ювенильных эритроцитах, а центральный бледный шар некоторых зрелых эритроцитов был увеличен, что соответствовало миелограмме железодефицитной анемии (рис.2а). Тест на антитуберкулезные антитела, твердофазный иммуноферментный анализ, туберкулиновый тест, ВИЧ-Ig, ANA, P-ANCA, C-ANCA, MPO + PR3, СОЭ и анти-GBM были отрицательными. Вирусные мазки из носоглотки, тест на Mycoplasma pneumonia, РНК в мокроте, тесты на антитела к Mycoplasma pneumonia, и Chlamydia pneumonia, , скрининг 16S рРНК на наличие грамположительных и грамотрицательных бактерий, а также несколько культур крови ( например, для обнаружения бактерий L-формы, анаэробных бактерий, грибков и т. д.) были отрицательными.
Рис. 2Патологический анализ. a Наблюдалась активная гиперплазия эритроидов, в первую очередь в поздних ювенильных эритроцитах, а центральный бледный шар некоторых зрелых эритроцитов был увеличен. b Обнаружены множественные эритроциты и большое количество макрофагов, нагруженных гемосидерином.
Для дальнейшего анализа патогенов на третий день госпитализации была проведена фибробронхоскопия. Количество лимфоцитов, нейтрофилов и макрофагов в жидкости бронхоальвеолярного лаважа (ЖБАЛ) составляло приблизительно 3, 2 и 95% соответственно.Эозинофилы отсутствовали. Наблюдались множественные эритроциты и большое количество нагруженных гемосидерином макрофагов (рис. 2b). Культура BALF была отрицательной. Секвенирование следующего поколения (NGS) (BGISEQ-50) было выполнено для обнаружения присутствия патогенов в ЖБАЛ. Результаты секвенирования сравнивали с последовательностями патогенов в четырех базах данных микробного генома, включая 3446 видов бактерий, 206 видов грибов, 4152 вируса и 140 видов паразитов. Было обнаружено 96% совпадение с эталонной последовательностью N.Абсцесс .
Сульбактам и цефоперазон применялись внутривенно. Тест на галактоманнан и тест (1, 3) β-D глюкана предполагал грибковую инфекцию, и на второй день после госпитализации был назначен пероральный вориконазол в качестве антибактериального и противогрибкового лечения. Однако никаких улучшений отмечено не было. Поражение нижней доли правого легкого было лучше, наблюдалось образование полости, новые очаги поражения в левом легком, двустороннее утолщение плевры (рис. 1д, е) 29 мая 2019 г. (14-й день поступления).После того, как 21 мая 2019 г. была диагностирована инфекция N. abscessus, был назначен линезолид в дозе 0,04 г / кг · сут (рис. 3). Наконец, 3 июня 2019 г. пациент был выписан.
Рис. 3Схематическое изображение лечения и результатов
Рентгенография грудной клетки, выполненная через 1, 15 и 21 месяц после выписки (рис. 4), показала значительное улучшение состояния. Поражение легких по сравнению с таковым на момент приема небольшой дозы метилпреднизолона (0.25 мг / кг · сут). Пероральный линезолид в дозе 0,03 г / кг · день в течение 7 дней был отменен через неделю после выписки. Симптомы пациента и легочные поражения восстановились, и IPH, по-видимому, хорошо контролировался (рис. 1g, h).
Рис. 4Рентгенография грудной клетки, выполненная через 1, 15 и 21 месяц после выписки. Поражения легких были значительно улучшены.
Инфекция легочной нокардии у ребенка с идиопатическим легочным гемосидерозом: клинический случай и обзор литературы
Предпосылки
Идиопатический легочный гемосидероз (IPH) включает редкую и агногенную группу диффузных заболеваний альвеолярных капилляров.Лечение кортикостероидами — это глобально предпочтительная терапевтическая стратегия при ИЛГ. Однако его длительное применение может вызвать иммунодефицит. Nocardia Инфекция часто встречается у пациентов с ослабленным иммунитетом и в первую очередь поражает плевру и легкие. Здесь мы описываем случай детской легочной инфекции Nocardia , осложненной ИЛГ.
История болезни
Девочка 7 лет обратилась с основными жалобами на бледность кожи, сохраняющуюся в течение 1 года и кашель в течение 20 дней.Обильные макрофаги, нагруженные гемосидерином, были обнаружены в желудочном соке во время последней госпитализации. Для лечения ИГБ пациенту непрерывно вводили небольшие дозы кортикостероидов (1-2 мг / кг / день). После почти двух месяцев терапии кортикостероидами у детей начался кашель. Секвенирование следующего поколения образца жидкости бронхоальвеолярного лаважа (ЖБАЛ) выявило присутствие ДНК Nocardia abscessus ( N. abscessus ) и снова подтвердило IPH. Линезолид применялся для лечения N.abscessus инфекция. Она выздоровела и была выписана через 18 дней госпитализации. Через 1 месяц наблюдения ее легочные поражения постепенно рассасывались, железодефицитная анемия исчезла, и IPH, по-видимому, хорошо контролировался.


 Проявляется пятнами коричнево-красного цвета, не пропадающими при надавливании. Может быть спровоцировано расстройством кровообращения конечностей. Чаще всего встречается у мужчин.)
Проявляется пятнами коричнево-красного цвета, не пропадающими при надавливании. Может быть спровоцировано расстройством кровообращения конечностей. Чаще всего встречается у мужчин.)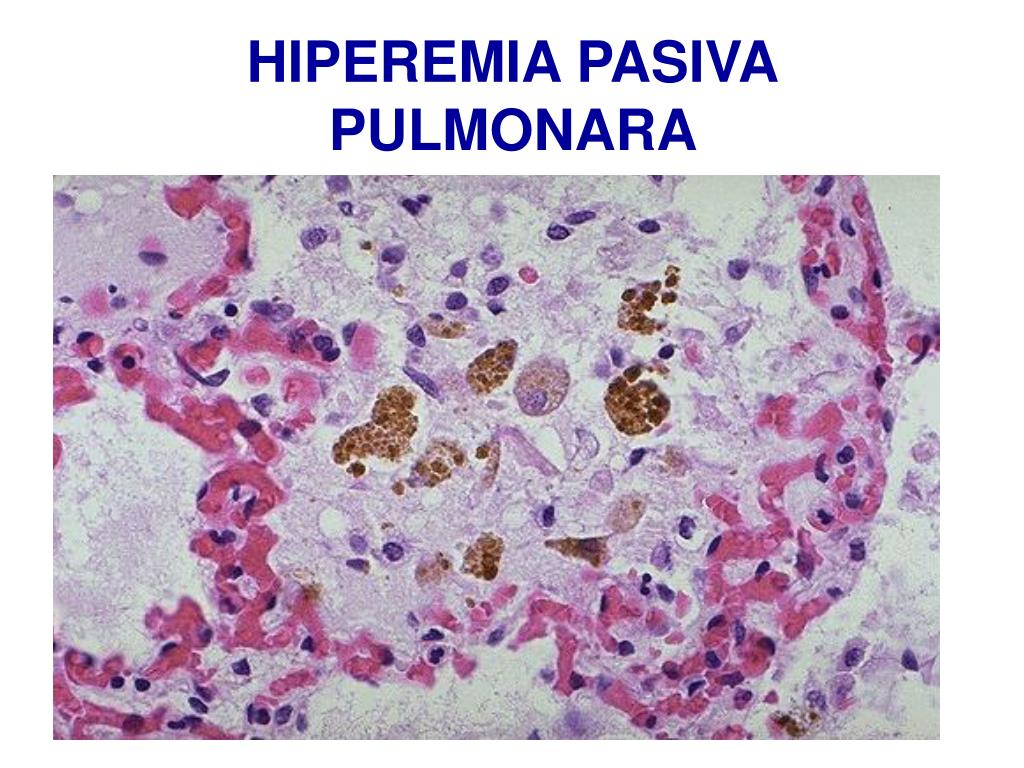 Селезенка не принадлежит к числу жизненно… … Медицинская энциклопедия
Селезенка не принадлежит к числу жизненно… … Медицинская энциклопедия
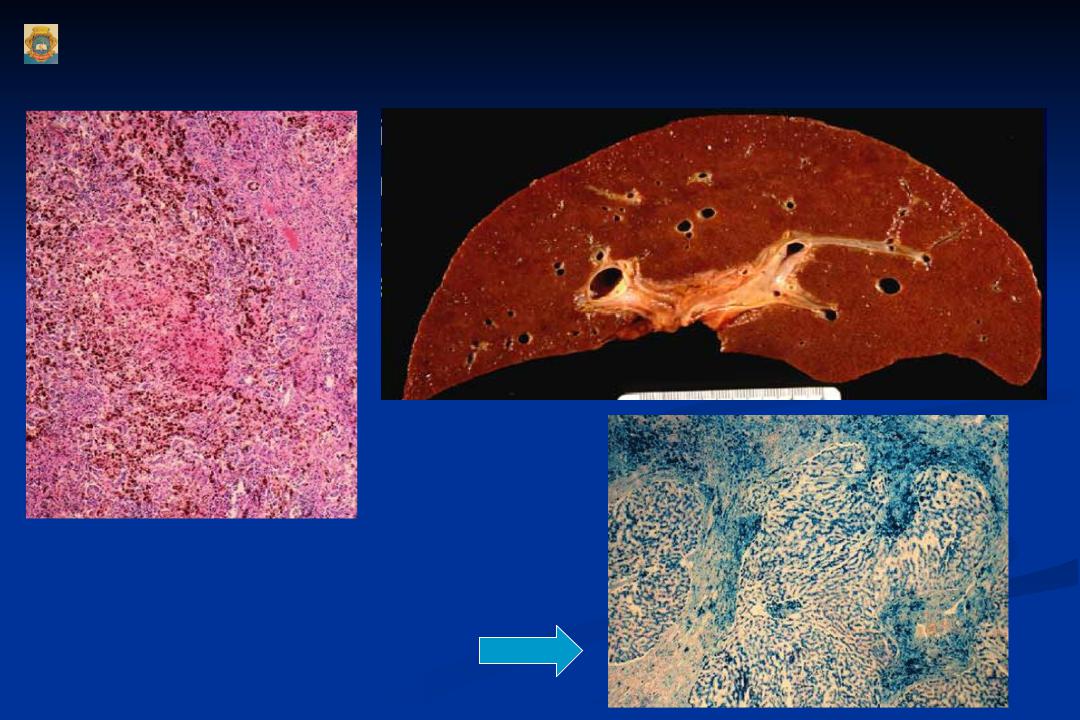 д.
д.

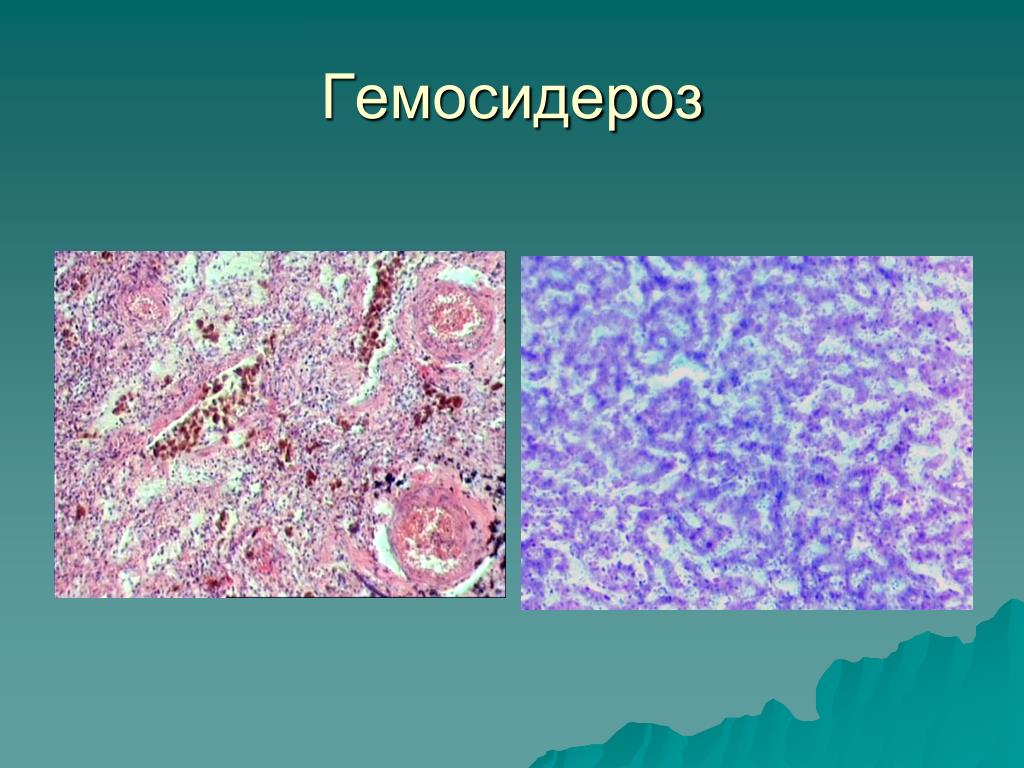

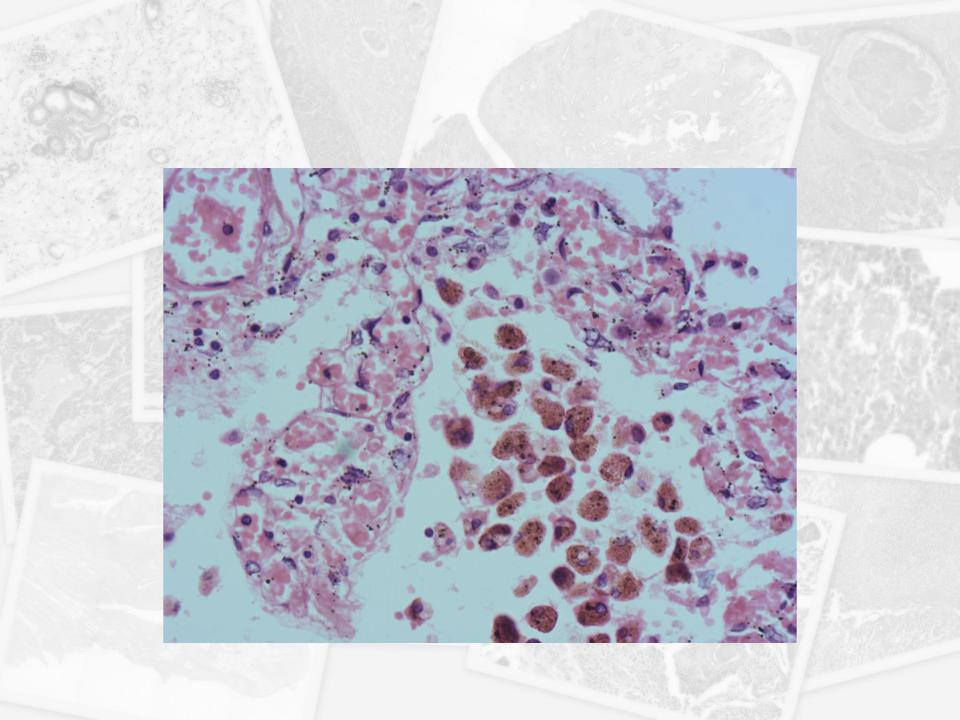 Наиболее часто это отмечается в лёгочных тканях.
Наиболее часто это отмечается в лёгочных тканях.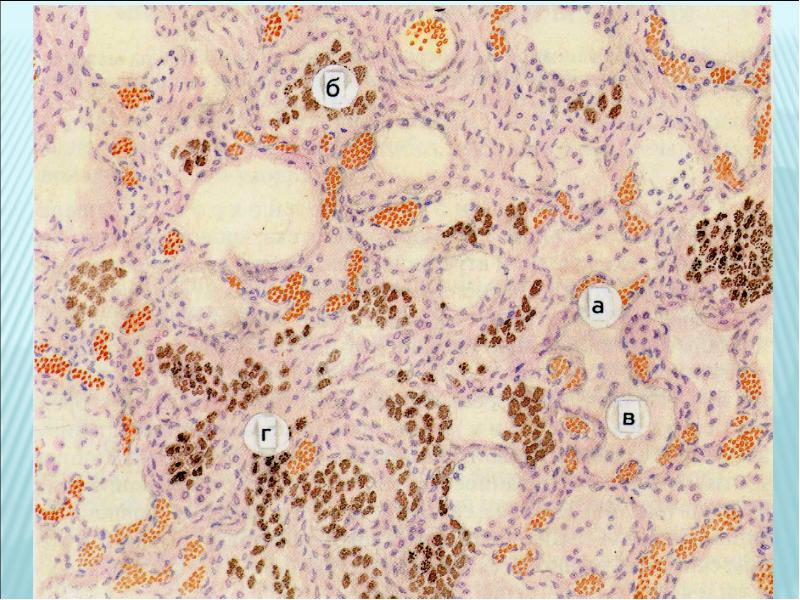



 Стадия ремиссии обычно продолжается год и более. По мере прогрессирования патологических изменений в лёгких выраженность и длительность кризов возрастает, а периоды ремиссии, соответственно, сокращаются.
Стадия ремиссии обычно продолжается год и более. По мере прогрессирования патологических изменений в лёгких выраженность и длительность кризов возрастает, а периоды ремиссии, соответственно, сокращаются.