Серологический анализ методом РНГА с сыпнотифным диагностикумом (anti-Ricketsia prowazeki) в медицинской лаборатории \»Оптимум\»
РНГА с сыпнотифным диагностикумом (anti-Ricketsia prowazeki)
Исследование предназначено для определения наличия в крови пациента специфических антител к Ricketsia prowazeki — возбудителю сыпного тифа. Анализ является серологическим маркером болезни Брилла-Цинссера (спорадического сыпного тифа).
Серологический анализ проводится методом РНГА (реакцией непрямой гемагглютинации). В лунках лабораторной планшетки серолог разводит исследуемую сыворотку с поэтапным удвоением. Затем добавляет в образцы стандартные эритроциты, сенсибилизированные риккетсиями. При наличии в пробах иммунных антител к антигену возбудителя инфекции, эритроциты слипаются и равномерно покрывают все дно лунки – реакция считается положительной, при отрицательной реакции эритроциты располагаются на дне в виде маленькой пуговки.
Подготовка к исследованию:
- Анализ проводится утром, натощак.

- С последнего приема пищи должно пройти не менее 8 часов.
- Исключить прием алкоголя не менее чем за 24 часа до взятия биоматериала.
- Не рекомендуется сдавать кровь на серологию после флюорографии, рентгена, физиотерапевтических процедур.
Тип биоматериала: венозная кровь
Синонимы (rus): Серодиагностика с эритроцитарным сыпнотифозным (риккетсиозным Провачека) диагностикумом
Синонимы (eng): Detection of anti-typhus Рrowazeki antibodies in patient serum
Методы: Реакция непрямой гемагглютинации (РНГА)
Сроки выполнения: 7-8 дней
Сыпным или вшивым тифом называют острую инфекцию, вызываемую внутриклеточными паразитами — риккетсиями провачека (Ricketsia prowazeki). Это название мелкая грамотрицательная бактерия, унесшая миллионы жизней, получила по фамилиям двух ученых, разгадавших тайну смертельного заболевания — американского биолога Говарда Тейлора Риккетса и чешского естествоиспытателя Станислава Провачека.
Источник инфекционного процесса — больной человек, от которого заражение передается здоровому человеку платяными и головными вшами. Расчесывая укусы этих специфических паразитов, человек втирает их экскременты, содержащие риккетсии, в клетки кожных покровов. Сыпной тиф распространяется из-за плохих социальных условий, скученности, тесноты. Именно поэтому наиболее страшные эпидемии инфекции возникали в военное время и при стихийных катастрофах.
После выздоровления у человека вырабатывается иммунный барьер к возбудителю, однако он способен сохраняться в организме длительный период и спустя много лет рецидивировать. Повторный сыпной тиф имеет те же клинические проявления, но в более легкой форме. При заражении риккетсиями в организме продуцируются специфические антитела, концентрация которых нарастает с каждой неделей заболевания и остается повышенной длительный период. Для эндогенной рецидивирующей инфекции (болезни Брилла) также характерно выраженное повышение уровня иммунных антител.
Серологический анализ с эритроцитарным сыпнотифозным диагностикумом необходим для диагностирования этих серьезных инфекционных патологий.
Опытные инфекционисты проводят серологическое исследование при наличии у пациента:
Негативная РНГА считается отрицательным результатом — заражения риккетсиями нет. Положительным результатом считается диагностический титр 1:640 — текущий или перенесенный в прошлом риккетсиоз (сыпной или спорадический тиф).
Рекомендовано проводить РНГА — исследование в парных образцах биоматериала: первое — на седьмой день инфекционного процесса, второе — спустя две недели.
РНГА — это… Что такое РНГА?
РНГА — РИГА РНГА реакция непрямой гемагглютинации мед. РНГА Словарь: С. Фадеев. Словарь сокращений современного русского языка. С. Пб.: Политехника, 1997. 527 с. РНГА русский нефтегазовый альянс энерг … Словарь сокращений и аббревиатур
РНГА — см.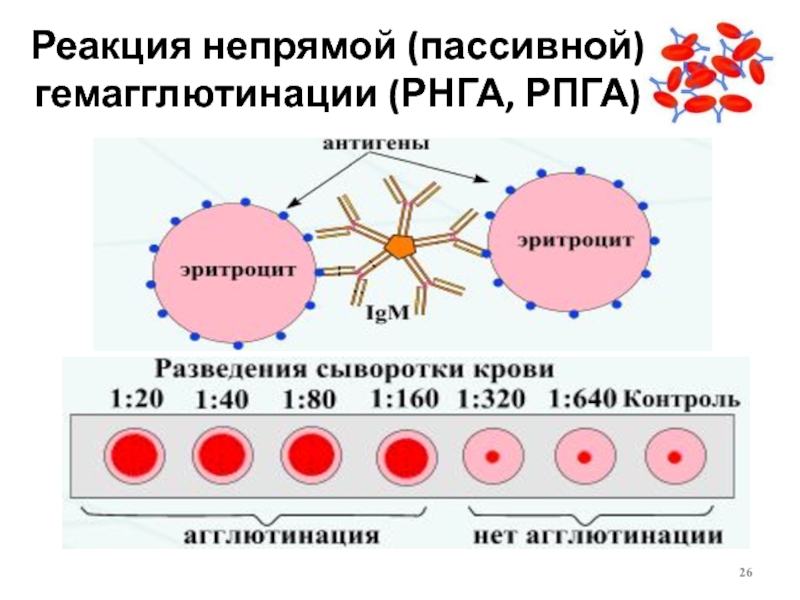 Реакция непрямой гемагглютинации … Большой медицинский словарь
Реакция непрямой гемагглютинации … Большой медицинский словарь
РНГА — реакция непрямой ремагглютинации … Словарь сокращений русского языка
реакция непрямой гемагглютинации — (РНГА; син. реакция пассивной гемагглютинации) метод обнаружения и идентификации антигенов или антител, основанный на возникающем в их присутствии феномене агглютинации эритроцитов, на поверхности которых были предварительно адсорбированы… … Большой медицинский словарь
БРЮШНОЙ ТИФ — – инфекционная болезнь из группы кишечных инфекций, характеризующаяся язвенным поражением лимфатического аппарата тонкой кишки, циклическим течением, бактериемией, симптомами интоксикации, сыпью на коже. Возбудитель – Salmonella typhi,… … Энциклопедический словарь по психологии и педагогике
ГЕМАГГЛЮТИНАЦИЯ — (от греч. háima кровь и лат. agglutinatio склеивание), склеивание и выпадение в осадок эритроцитов под воздействием бактерий, вирусов, токсинов и др. , способных адсорбироваться на поверхности эритроцитов, а также гемагглютининов.… … Ветеринарный энциклопедический словарь
, способных адсорбироваться на поверхности эритроцитов, а также гемагглютининов.… … Ветеринарный энциклопедический словарь
реакция непрямой гемагглютинации — РНГА Лабораторный тест с использованием эритроцитарных диагностикумов. [Англо русский глоссарий основных терминов по вакцинологии и иммунизации. Всемирная организация здравоохранения, 2009 г.] Тематики вакцинология, иммунизация Синонимы РНГА EN… … Справочник технического переводчика
РИГА — РНГА реакция непрямой гемагглютинации мед. РНГА Словарь: С. Фадеев. Словарь сокращений современного русского языка. С. Пб.: Политехника, 1997. 527 с … Словарь сокращений и аббревиатур
Гельминтологи́ческие ме́тоды иссле́дований — Методы диагностики гельминтозов разделяют на прямые, основанные на непосредственном выявлении самих гельминтов или их фрагментов, а также личинок и яиц гельминтов (методы исследования фекалий, мочи, желчи и дуоденального содержимого, мокроты,… … Медицинская энциклопедия
Иммунологи́ческие ме́тоды иссле́дования — диагностические методы исследования, основанные на специфическом взаимодействии антигенов и антител. Широко используются для лабораторной диагностики инфекционных и паразитарных болезней, определения групп крови, тканевых и опухолевых антигенов,… … Медицинская энциклопедия
Широко используются для лабораторной диагностики инфекционных и паразитарных болезней, определения групп крови, тканевых и опухолевых антигенов,… … Медицинская энциклопедия
РПГА с Yersinia pseudotuberculosis (Y. pseudotuberculosis IHA)
Интерпретация результатов
Интерпретация результатов исследований содержит информацию для лечащего врача и не является диагнозом. Информацию из этого раздела нельзя использовать для самодиагностики и самолечения. Точный диагноз ставит врач, используя как результаты данного обследования, так и нужную информацию из других источников: анамнеза, результатов других обследований и т.д.
Единицы измерения и коэффициенты пересчёта: тест полуколичественный.
Результат предоставляется в форме «отрицательно» или «положительно» (в последнем случае с приведением титра – последнего разведения сыворотки дающего положительный результат). Диагностически достоверным считают прирост титров в 4 и более раз за 7-10 дней.
Условно-диагностический титр – 1:100. При групповых вспышках псевдотуберкулёза для детей до 5 лет условно-диагностический титр может быть снижен до 1:50.
Референсные значения: отрицательно.
Интерпретация результата
Положительно:
- текущая или перенесённая в прошлом инфекция. Рекомендовано обследовать больного не менее 2 раз – в начале заболевания и с интервалом в 7-10 дней, диагностически достоверным считают 4-кратный и более прирост титров антител. При необходимости оценивать одиночные результаты или отсутствии выраженной динамики титров допустимо использовать минимальный условно-диагностический титр 1:100. При групповых вспышках псевдотуберкулёза для детей до 5 лет условно диагностический титр может быть снижен до 1:50. Результат следует оценивать в комплексе с эпидобстановкой, формой и сроками болезни;
- редко — перекрёстные реакции (другие виды Yersinia,Vibrio, Salmonella, Brucella, Rickettsia).
Отрицательно:
- отсутствие инфекции данным сероваром Yersinia pseudotuberculosis;
- низкая концентрация или отсутствие антител в ранний период инфекции.

Брюшной тиф (антитела к Salmonella typhi (РПГА-тест)
Брюшной тиф — острое инфекционное заболевание с циклическим течением с фекально-оральным механизмом передачи. Инкубационный период длится в среднем 9-14 дней. Выраженность клинических проявлений инфекции варьирует, характеризуется поражением кишечника и лимфатических узлов, бактериемией, выраженной интоксикацией, увеличением печени и селезёнки, розеолёзной сыпью. При отсутствии лечения заболевание потенциально опасно для жизни в связи с возможностью развития ряда осложнений, включая кишечное кровотечение или перфорацию кишки вследствие некроза пейеровой бляшки.
Возбудитель брюшного тифа — Salmonella typhi (S. typhi), грамотрицательная подвижная палочка рода Salmonella семейства Enterobacteriaceae
Источник инфекции – больной человек или бактерионоситель. Бактерия начинает выделяться с калом с первых дней заболевания. С этого момента человек считается опасным для окружающих. На 3-4 неделе болезни выделение бактерий происходит в более активной форме с испражнениями, мочой, потом; также бактерии можно обнаружить в грудном молоке и носоглотке. После выздоровления выделение бактерий обычно прекращается. Бактерионосительство может быть острым, хроническим или транзиторным. Но в отличие от других острых кишечных инфекций, после перенесенного заболевания брюшного тифа в 2-5% случаев может формироваться хроническое бактерионосительство (более 3-х месяцев), которое сопровождается выделением возбудителя (с фекалиями и мочой) и наличием в сыворотке крови иммуноглобулинов (антител) к Vi-антигену возбудителя. Последний признак считают индикатором хронической формы инфекции или бессимптомного носительства. Носительство может быть кратковременным или продлиться всю жизнь. Бактерионосители опасны, как источники инфекции.
Бактерия начинает выделяться с калом с первых дней заболевания. С этого момента человек считается опасным для окружающих. На 3-4 неделе болезни выделение бактерий происходит в более активной форме с испражнениями, мочой, потом; также бактерии можно обнаружить в грудном молоке и носоглотке. После выздоровления выделение бактерий обычно прекращается. Бактерионосительство может быть острым, хроническим или транзиторным. Но в отличие от других острых кишечных инфекций, после перенесенного заболевания брюшного тифа в 2-5% случаев может формироваться хроническое бактерионосительство (более 3-х месяцев), которое сопровождается выделением возбудителя (с фекалиями и мочой) и наличием в сыворотке крови иммуноглобулинов (антител) к Vi-антигену возбудителя. Последний признак считают индикатором хронической формы инфекции или бессимптомного носительства. Носительство может быть кратковременным или продлиться всю жизнь. Бактерионосители опасны, как источники инфекции.
Бактерии Salmonella typhi умеренно устойчивы во внешней среде — в почве и воде могут сохраняться до 1-5 месяцев, в испражнениях — до 25 дней, на белье — до 2 недель, на пищевых продуктах — от нескольких дней до недель. Особенно опасно купаться в водоемах, которые могут быть заражены сточными водами. Самый высокий риск заражения связан с молочными и мясными продуктами, в них бактерия при температуре +18 С начинает активно размножаться. При нагревании возбудитель достаточно быстро погибает, дезинфицирующие растворы в обычных концентрациях действуют на него губительно.
Особенно опасно купаться в водоемах, которые могут быть заражены сточными водами. Самый высокий риск заражения связан с молочными и мясными продуктами, в них бактерия при температуре +18 С начинает активно размножаться. При нагревании возбудитель достаточно быстро погибает, дезинфицирующие растворы в обычных концентрациях действуют на него губительно.
К антигенной структуре Salmonella typhi относятся:
• термостабильный соматический О-антиген,
• термолабильный жгутиковый Н-антиген,
• термолабильный соматический Vi-антиген и др.
Безусловным лабораторным подтверждением диагноза служит выделение брюшнотифозных бацилл микробиологическим методом при серийных посевах крови (начиная с первой недели болезни) или кала – на второй неделе. Выявление возбудителя микробиологическими методами зависит от концентрации возбудителя в материале и влияния терапии антибиотиками.
В настоящее время наибольшее распространение получил серологический метод исследования, к числу которых относится исследование крови на антитела к Salmonella typhi с помощью реакции пассивной гемагглютинации (РПГА-тест), результат которой бывает положительным ко второй неделе заболевания.
Показания к назначению:
• для диагностики острой инфекции,
• дифференциальной диагностики у длительно лихорадящих
• обследования реконвалесцентов (выздоравливающих)
Референсные значения:
«отрицательный» — отсутствие антител к антигенам Salmonella typhi
Интерпретация результатов:
положительный
• наличие инфицирования S. typhi
отрицательный результат
• отсутствие инфицирования S. typhi
Возможны ложноположительные перекрёстные реакции с другими типами сальмонелл.
Необходимо воздержаться от приема пищи в течение 2-3 часов.
| Treponema pallidum | ||
| ПЦР | на следующий день | 250 |
| ИФА суммарные антитела к Treponema pallidum | 2 рабочих дня | 350 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ИФА Ig G титр (антитела класса G) | 4-5 рабочих дней | 350 |
| РПГА | 2 рабочих дня | 250 |
| Микрореакция | 4-5 рабочих дней | 250 |
| РИТ | 4-5 рабочих дней | 1 500 |
| РИФ абс | 4-5 рабочих дней | 1 000 |
| РИФ количественная | 4-5 рабочих дней | 1 000 |
| ВИЧ | ||
| Ф-50 АнтиВИЧ1,2 ат/аг | 3-4 дня | 300 |
| Гепатиты | ||
| Гепатит А (HAV): | ||
| ИФА anti-HAV IgM | 4-5 рабочих дней | 300 |
| ИФА anti-HAV IgG | 4-5 рабочих дней | 300 |
| Гепатит В (HВV): | ||
| ИФА HBsAg (для госпитализации) | 4-5 рабочих дней | 300 |
| ИФА anti-HBsAg | 4-5 рабочих дней | 300 |
| ИФА anti-HBc (общ) | 4-5 рабочих дней | 350 |
| ИФА anti-HBc IgM | 4-5 рабочих дней | 350 |
| ИФА HBе Ag | 4-5 рабочих дней | 350 |
| ИФА anti-HBе IgG | 4-5 рабочих дней | 350 |
| ПЦР HВV (качественно) | 4-5 рабочих дней | 450 |
| Количественная вирусная нагрузка HBV | 25-30 рабочих дней | 2 900 |
| Гепатит С (HСV): | ||
| ИФА anti-HCV IgM | 4-5 рабочих дней | 350 |
| ИФА anti-HCV IgG+М(для госпитализации) | 4-5 рабочих дней | 300 |
| ИФА anti-HCV cor_NS | 4-5 рабочих дней | 350 |
| ПЦР HСV (качественно) | 4-5 рабочих дней | 450 |
| Генотипирование HСV | 4-5 рабочих дней | 1 000 |
| Количественная вирусная нагрузка HСV | 25-30 рабочих дней | 2 900 |
| Гепатит D (HDV): | ||
ИФАanti-HDV. AB(общ) AB(общ) | 4-5 рабочих дней | 350 |
| ИФА anti-HDV IgM | 4-5 рабочих дней | 350 |
| Урогенитальные инфекции и пр. | ||
| Микроскопическое исследование урогинекологической микрофлоры на микробиоценоз | 1(один) рабочий день | см. раздел общеклинические исследования |
| Андрофлор | 5 рабочих дней | 3000 |
| Фемофлор 8 | 5 рабочих дней | 1600 |
| Фемофлор 16 | 5 рабочих дней | 3000 |
| Фемофлор Скрин | 5 рабочих дней | 2100 |
| Комплексное исследование на микробиоценоза влагалища (ПЦР+микроскопия) | 1-2 рабочих дня | 1 200 |
| Lactobacillus spp. (лактобактерии) | ||
| ПЦР | на следующий день | 250 |
Bacteroides spp. (бактероиды) (бактероиды) | ||
| ПЦР | на следующий день | 250 |
| Mobiluncus curtisii (мобилюнкусы): | ||
| ПЦР | на следующий день | 250 |
| E.coli (кишечная палочка): | ||
| ПЦР | на следующий день | 250 |
| Chlamidia trachomatis | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| ПЦР | на следующий день | 250 |
| ИФА Ig A (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Посев на культуральные среды с а/б чувствительностью | 7-10 рабочих дней | 700 |
| Chlamidia pneumoniaе | ||
| ПЦР | на следующий день | 250 |
| ИФА Ig A (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Mycoplasma hominis | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР(REAL TIME) | на следующий день | 380 |
| ПЦР | на следующий день | 250 |
| ИФА Ig А (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Посев на культуральные среды с а/б чувствительностью | 7-10 рабочих дней | 800 |
| Mycoplasma genitalium | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| ПЦР | на следующий день | 250 |
| Mycoplasma pneumoniaе | ||
| ПЦР | на следующий день | 250 |
| ИФА Ig A (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
Ureaplasma spp. | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| ПЦР | на следующий день | 250 |
| ИФА Ig А (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Посев на культуральные среды с а/б чувствительностью | 7-10 рабочих дней | 800 |
| Ureaplasma Раrvo/urealyticum (ПЦР) | на следующий день | 250 |
| Ureaplasma Раrvo КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| Ureaplasma urealyticum КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| Toxoplasma gondii | ||
| ПЦР | на следующий день | 250 |
| ИФА АВИДНОСТЬ Ig G | на следующий день | 400 |
| ИФА Ig A (антитела класса А) | на следующий день | 300 |
| ИФА Ig М (антитела класса М) | на следующий день | 300 |
| ИФА Ig G (антитела класса G) | на следующий день | 300 |
| Trihomonas vaginalis | ||
| ПЦР | на следующий день | 250 |
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| ИФА Ig А (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Посев на культуральные среды с а/б чувствительностью | 10-14 рабочих дней | 600 |
| Candida albicans | ||
| ПЦР | на следующий день | 250 |
| ИФА Ig А (антитела класса А) | 4-5 рабочих дней | 300 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Посев на культуральные среды | 10-14 рабочих дней | 600 |
Комплексное обследование на Кандидоз – C. albicans, C.glabrata, C.crusei, C.parapsilosis, C.tropicalis albicans, C.glabrata, C.crusei, C.parapsilosis, C.tropicalis | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 2-3 рабочих дней | 900 |
| Candida glabrata | ||
| ПЦР | на следующий день | 250 |
| Candida crusei | ||
| ПЦР | на следующий день | 250 |
| Candida parapsilosis | ||
| ПЦР | на следующий день | 250 |
| Rubella (краснуха) | ||
| ИФА АВИДНОСТЬ Ig G | 4-5 рабочих дней | 400 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Gardnerella vaginalis | ||
| ПЦР | на следующий день | 250 |
Комплексное обследование на – Gardnerella vaginalis, Lactobacillus spp. , Atopobium vaginae , Atopobium vaginae | 2-3 рабочих дней | |
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 900 | |
| Neisseria gonorrhoeae | ||
| ПЦР | на следующий день | 250 |
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
| Streptococcus pyogenes (гр А) | ||
| ПЦР | на следующий день | 250 |
| Streptococcus agalactiae (гр В) | ||
| ПЦР | на следующий день | 250 |
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | на следующий день | 380 |
Комплексное обследование на – Staphylococcus spp., Streptococcus spp. , Enterobacteriaceae , Enterobacteriaceae | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 3-5 рабочих дней | 900 |
| Streptococcus spp. | ||
| ПЦР | на следующий день | 250 |
| Staphylococcus aureus | ||
| ПЦР | на следующий день | 250 |
| Папиломовирусы | ||
| HPV скрининг ПЦР (16,18,31,33,35,39, 52,53,56,58,59,66,70) | на следующий день | 350 |
| HPV генотип ПЦР (16,18,31,33,35,39, 45,52,56,58,59) | на следующий день | 800 |
| HPV КОЛИЧЕСТВЕННЫЙ ПЦР HPV –скрининг (REAL TIME) | 2-3 рабочих дня | 1 300 |
| HPV скрининг количественно +ОНКОГЕНЫ Е6 HPV 16,18,45 | 3-5 рабочих дней | 1 500 |
| HPV 16 (вирус папиломы) ПЦР | на следующий день | 250 |
| HPV 16 КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 3-5 рабочих дней | 380 |
| HPV 18 (вирус папиломы) ПЦР | на следующий день | 250 |
| HPV 18 КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 3-5 рабочих дней | 380 |
| HPV 31/33 (вирус папиломы) ПЦР | на следующий день | 250 |
| HPV 6/11 (вирус папиломы) ПЦР | на следующий день | 250 |
| HSV 1,2 (вирус герпеса) | ||
| ПЦР | на следующий день | 250 |
| ИФА АВИДНОСТЬ Ig G | 4-5 рабочих дней | 400 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ИФА Ig G титр (антитела класса G) | 4-5 рабочих дней | 350 |
| HSV 1 (вирус герпеса) | ||
| ПЦР | на следующий день | 250 |
| HSV 2 (вирус герпеса) | ||
| ПЦР | на следующий день | 250 |
| ИФА АВИДНОСТЬ Ig G | 4-5 рабочих дней | 400 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ИФА Ig G титр (антитела класса G) | 4-5 рабочих дней | 350 |
| VZV (вирус варицеллы зостер – HHV3) | ||
| ПЦР | на следующий день | 250 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ЕВV (вирус Эпштейн-Барра – HHV4): | ||
| ПЦР | на следующий день | 250 |
| ИФА АВИДНОСТЬ Ig G | 4-5 рабочих дней | 400 |
| ИФА а/т к ядерному антигену | 4-5 рабочих дней | 300 |
| ИФА а/т к раннему антигену | 4-5 рабочих дней | 300 |
| ИФА Ig М (антитела класса М к капсидному антигену) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G к капсидному антигену) | 4-5 рабочих дней | 300 |
| СМV (цитомегаловирус – HHV5) | ||
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 3-5 рабочих дней | 380 |
| ПЦР | на следующий день | 250 |
| ИФА АВИДНОСТЬ Ig G | 4-5 рабочих дней | 400 |
| ИФА антитела к предраннему белку | 4-5 рабочих дней | 350 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ИФА Ig G титр (антитела класса G) | 4-5 рабочих дней | 350 |
| HHV 6 (вирус герпеса человека 6 типа) | ||
| ПЦР | на следующий день | 250 |
| КОЛИЧЕСТВЕННЫЙ ПЦР (REAL TIME) | 3-5 рабочих дней | 380 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| HHV 8 (вирус герпеса человека 8 типа) | ||
| ПЦР | на следующий день | 250 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Вирус гриппа А | ||
| ПЦР | на следующий день | 500 |
| Вирус гриппа В | ||
| ПЦР | на следующий день | 500 |
| Вирус гриппа А пан h2N1 (свиной грипп) | ||
| ПЦР | на следующий день | 500 |
| Helicobacter pylory | ||
| ПЦР | на следующий день | 250 |
| ИФА (суммарные антитела) | 4-5 рабочих дней | 300 |
| Антиген в кале | на следующий день | 650 |
| Mycobacterium tuberculosis | ||
| ПЦР | на следующий день | 250 |
anti-MycobacteriumTuberculos. (IgА,М,G) (IgА,М,G) | 4-5 рабочих дней | 300 |
| Аскаридоз | ||
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Аспергиллез | 10-14 рабочих дней | 700 |
| Бруцеллез (суммарные а/т) | 10-14 рабочих дней | 350 |
| Боррелиоз (болезнь Лайма) | ||
| ПЦР | 4-5 рабочих дней | 600 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 350 |
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 350 |
| Клещевой энцефалит | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 350 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 350 |
| Комплексное обследование на выявления РНК/ДНК возбудителей инфекций, передающихся ИКСОДОВЫМИ КЛЕЩАМИ – Клещевой энцефалит, Боррелиоз, Эрлихиоз, Анаплазмоз | ||
| ПЦР | 4-5 рабочих дней | 1 200 |
| Корь | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| ИФА Ig G титр (антитела класса G) | 4-5 рабочих дней | 350 |
| Лямблиоз | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА суммарные антитела | 4-5 рабочих дней | 300 |
| Описторхоз | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 300 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Паротит | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 350 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 350 |
| Токсокароз | ||
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 300 |
| Трихинеллез | ||
| ИФА Ig М (антитела класса М) | 4-5 рабочих дней | 350 |
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 350 |
| Эхинококкоз | ||
| ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 350 |
| А/т к 4-м паразитам: описторхисов, токсокар, трихинел, эхинококков ИФА Ig G (антитела класса G) | 4-5 рабочих дней | 500 |
| Брюшной тиф | ||
| РПГА | 2-3 рабочих дня | 350 |
| Дизентерия | ||
| РПГА | 2-3 рабочих дня | 350 |
| Дифтерия | ||
| РПГА | 2-3 рабочих дня | 400 |
| ПЦР | на следующий день | 250 |
| Кишечный иерсиниоз, псевдотуберкулез | ||
| РНГА | 2-3 рабочих дня | 300 |
| Bordеtella pertussis-коклюш | ||
| ПЦР | на следующий день | 250 |
| РА | 1-2 рабочих дня | 400 |
| Сальмонеллез | ||
| РНГА | 2-3 рабочих дня | 350 |
| Enterovirus (энтеровирусы) | ||
| ПЦР | на следующий день | 600 |
| Комплексное обследование на кишечные инфекции – Rotavirus (ротавирусы группы А), Norovirus (норовирус) 2 генотип, Astrovirus (астровирус) | ||
| ПЦР | на следующий день | 900 |
Анализы на инфекции в Москве,цены,запись,отзывы
Инфекционные заболевания – обширная группа патологий. Их причиной становятся проникшие в организм вирусы, бактерии, грибки, простейшие или гельминты. Эффективность лечения зависит от вовремя установленного диагноза и правильно подобранных препаратов. Именно поэтому при подозрении на патологию инфекционного характера врач назначает пациенту сдать ряд лабораторных анализов.
Их причиной становятся проникшие в организм вирусы, бактерии, грибки, простейшие или гельминты. Эффективность лечения зависит от вовремя установленного диагноза и правильно подобранных препаратов. Именно поэтому при подозрении на патологию инфекционного характера врач назначает пациенту сдать ряд лабораторных анализов.
Виды анализов на инфекции
Существуют две большие группы лабораторных методов диагностики инфекционных заболеваний.
- Прямые методы (ПЦР-диагностика, ИФА, микробиологический способ). Это анализы по определению вируса и других возбудителей, а также их антигенов. Микробиологический способ исследования – это посев биологического материала на питательные среды. Это достоверный метод, однако результатов анализа приходится ждать около недели. Его усовершенствованной альтернативой является анализ методом ПЦР-диагностики, позволяющий определить антигены возбудителей (ДНК, РНК) даже в небольшом количестве биоматериала. Все паразитологические исследования также являются прямыми методами диагностики.
 Сюда относятся исследования биоматериала на простейшие и яйца глистов.
Сюда относятся исследования биоматериала на простейшие и яйца глистов. - Непрямые методы (различные серологические реакции – РА, РНГА, РПГА и пр.). Их используют для обнаружения в крови специфических антител к возбудителю, например на антитела к вирусу кори. Это особая группа иммуноглобулинов, синтез которых запускается при попадании инфекции в организм. Материал для исследования – преимущественно сыворотка крови.
Когда и кому назначают анализы на инфекции
- В первую очередь сдать кровь или другой биоматериал назначают пациентам с подозрением на инфекционное заболевание.
- При планировании беременности и во время наблюдения при вынашивании ребенка женщина должна сдать анализ на инфекции, которые могут негативно сказаться на течении беременности и самом ребенке.
- В ходе ежегодной диспансеризации организованные (посещающие учреждения) дети и подростки, а также определенные категории взрослых не только обходят основных специалистов, но и сдают ряд лабораторных тестов.

- Оформление санитарной книжки при приеме на работу и ее продление требует сдачи анализов на инфекции. Их перечень может несколько варьировать в зависимости от сферы деятельности соискателя.
- При оформлении детей в школу и детский сад требуется сдать обязательный минимум анализов.
Анализы на инфекции в лаборатории медицинского центра «Медлайн-Сервис»
Анализы на инфекции, в том числе скрытые и ИППП, недорого сдать в Москве можно в клинико-диагностической лаборатории медицинского центра «Медлайн-Сервис».
Наши лаборанты в кратчайшие сроки сделают такие сложные тесты, как анализы на КО-инфекции, на СПИД и гепатит, герпес. Полный список лабораторных исследований есть на сайте клиники. Уточняющие вопросы по поводу цены и подготовки к анализам можно задать по телефону администратору.
Иерсиниоз и псевдотуберкулез — Кабинет инфекционных заболеваний — Отделения
Иерсиниоз и псевдотуберкулез – это кишечные сапрозоонозы, вызываемые иерсиниями, характеризующиеся поражением желудочно-кишечного тракта, выраженной токсико-вазарной симптоматикой и наклонностью (наиболее выраженной при псевдотуберкулезе) к генерализованному течению. Оба заболевания имеют отчетливо выраженную тенденцию индуцировать развитие иммунопатологии.
Оба заболевания имеют отчетливо выраженную тенденцию индуцировать развитие иммунопатологии.
Этиология
Возбудители иерсиниоза (Y. enterocolitica) и псевдотуберкулеза (Y. pseudotuberculosis) относятся к семейству кишечных бактерий. Иерсинии представляют собой грамотрицательные палочки, которые растут как на обычных, так и на обедненных питательными веществами средах. Последние используются при бактериологическом исследовании по методу Петерсона и Кука (1963).
Иерсинии содержат О- и Н-антигены. Различия в строении 0-антигенов позволили выделить более 50 сероваров Y. enterocolitica. Наибольшее значение в патологии человека имеют серовары 03; 05,27; 07,8 и 09. У возбудителя псевдотуберкулеза — установлено наличие 8 сероваров. Наиболее часто заболевания у людей вызываются 1-м сероваром.
Многие штаммы иерсиний продуцируют экзотоксин (термостабильный энтеротоксин). При разрушении бактерий выделяется эндотоксин. Иерсинии обладают также способностью кадгезии, инвазии и внутриклеточному размножению. Инвазивные свойства у Y. pseudotuberculosis выражены в большей степени, чем у Y. entero-colitica.
Инвазивные свойства у Y. pseudotuberculosis выражены в большей степени, чем у Y. entero-colitica.
Иерсинии относятся к психрофилам. При температуре холодильника (4-8 °С) они способны длительно сохраняться и размножаться на овощах, корнеплодах и других пищевых продуктах. В то же время, некоторые из штаммов бактерий обладают повышенной термоустойчивостью к высокой температуре и способны выдержать режим пастеризации. При кипячении (100°С) все штаммы иерсиний погибают через несколько секунд. Чувствительны к действию обычных дезинфектантов.
Эпидемиология
Иерсинии (Y. enterocolitica и Y. pseudotuberculosis) широко распространены в природе. Их обнаруживали в почве, воде, выделяли из организма многих видов животных. Однако основным резервуаром возбудителя в природе, очевидно, являются мелкие грызуны, которые, обсеменяя различные объекты внешней среды, пищевые продукты, воду, способствуют распространению инфекции среди других животных. Другим резервуаром иерсиний является почва. Частое обнаружение в ней возбудителей болезней связано не только с загрязнением испражнениями животных, но и с наличием у иерсиний сапрофитических свойств. На основании этого заболевание может быть отнесено к сапрозоонозам.
Частое обнаружение в ней возбудителей болезней связано не только с загрязнением испражнениями животных, но и с наличием у иерсиний сапрофитических свойств. На основании этого заболевание может быть отнесено к сапрозоонозам.
Основным источником инфекции для человека при иерсиниозе являются сельскохозяйственные животные, реже – синантропные грызуны. Больной человек как источник инфекции имеет несравненно меньшее значение. При псевдотуберкулезе основными источниками инфекции являются синантропные и дикие грызуны. Человек, как правило, источником псевдотуберкулеза не является.
Основной путь распространения обеих инфекций – пищевой. Факторами передачи Y. enterocolitica чаще всего являются инфицированные мясные продукты, молоко, овощи, корнеплоды, вода. К факторам передачи Y. pseudotuberculosis относятся овощные блюда (салаты из капусты, моркови и др.) и молочные продукты, употребляемые в пищу без предварительной термической обработки. Водный путь передачи имеет при обеих инфекциях несравненно меньшее значение. Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи не имеют существенного значения в эпидемиологии иерсиниозов.
Он обычно реализуется при употреблении воды из открытых водоемов. Другие пути передачи не имеют существенного значения в эпидемиологии иерсиниозов.
Заболевание встречается во всех возрастных группах, но чаще у детей первых лет жизни. Сезонный подъем заболеваемости иерсиниозом отмечается в холодное время года с пиком в ноябре. В некоторых регионах наблюдается два сезонных подъема — осенью и весной. Пик заболеваемости псевдотуберкулезом приходится на весенние месяцы (март-май). Иерсиниоз и псевдотуберкулез протекают в виде спорадических и групповых заболеваний.
Патогенез
Входными воротами для возбудителей иерсиниоза и псевдотуберкулеза служит желудочно-кишечный тракт. Максимально выраженная местная реакция в ответ на инвазию иерсиний регистрируется со стороны слизистой оболочки подвздошной кишки и ее лимфоидных образований. В подвздошной кишке развивается различной выраженности воспалительный процесс – терминальный илеит. По лимфатическим сосудам иерсиний проникают в мезентериальные лимфатические узлы и вызывают мезаденит. В патологический процесс могут быть вовлечены червеобразный отросток и слепая кишка.
В патологический процесс могут быть вовлечены червеобразный отросток и слепая кишка.
На фоне инфекционно-воспалительных изменений развиваются токсический и токсико-вазарный (парез вазамоторов) процессы, связанные с токсинемией. На этом этапе инфекционный процесс, приобретая черты локализованной формы, может завершиться.
В случае прорыва лимфатического барьера кишечника, возникает бактериемия, обусловливающая развитие генерализованных форм заболевания. Наблюдается бактериально-токсическое поражение многих органов и систем, в первую очередь печени и селезенки, возможно развитие полилимфаденита, полиартрита, миозита, нефрита, уретрита, менингита и др.
При длительном нахождении иерсиний и их токсинов в крови и органах больного происходит сенсибилизация организма. У части больных, как правило, с фенотипом HLA-B27, иерсиниоз и псевдотуберкулез могут явиться толчком к возникновению иммунопатологических реакций и состояний.
Заключительное звено патогенеза – освобождение организма от возбудителя, ведущее к выздоровлению.
Развитие специфического иммунитета при иерсиниозе и псевдотуберкулезе происходит медленно и он не является достаточно прочным, с чем связано нередкое развитие обострений и рецидивов болезни.
Клиника
Продолжительность инкубационного периода при иерсиниозе колеблется от 1 до 7 дней, а псевдотуберкулезе – от 3 до 21 дня.
На основе общих патогенетических закономерностей кишечных зоонозов и клинико-патогенетических особенностей иерсиниоза и псевдотуберкулеза могут быть выделены локализованная (гастро-интестиномезентериальная) и генерал и зеванная формы. Они могут иметьманифестноеили (реже) бессимптомное течение.
Локализованная (гастроинтестиномезентериальная) форма манифестного течения включает следующие варианты: гастроэнтеро-колит, гастроэнтерит, энтероколит, энтерит, острый терминальный илеит, мезаденит, аппендицит. Бессимптомное течение локализованной (гастроинтестиномезентериальной) формы включает субклинический и реконвалесцентный варианты. Последний не характерен для псевдотуберкулеза.
Последний не характерен для псевдотуберкулеза.
Генерализованная форма манифестного течения может иметь две разновидности: токсикобактериемическая и септическая. В зависимости от преобладания той или иной симптоматики токсикобактериемическая разновидность генерализованной формы может протекать в следующих вариантах: экзантематозном, артритическом, желтушном (иерсиниозный гепатит), менингеальном, катаральном, смешанном и в виде иерсиниоза (псевдотуберкулеза) редких локализаций. В редких случаях (например, у иммунокомпрометированных лиц с хронической патологией печени и признаками тезауризмоза железа) развивается иерсиниозный сепсис. Бессимптомное течение при генерализованной форме может быть представлено реконвалесцентным вариантом. Последний обычно не характерен для псевдотуберкулеза.
По тяжести манифестного течения заболевания выделяют легкое, среднетяжелое и тяжелое течение. По характеру течения — гладкое и осложненное, в том числе с обострениями и рецидивами. По продолжительности заболевания и его исходам – острое (до 3 мес. ), хроническое (более 3 мес.) и клиника последствий (резидуальная фаза).
), хроническое (более 3 мес.) и клиника последствий (резидуальная фаза).
Локализованная (застроинтестиномезентериальная) форма встречается в 70% случаев иерсиниоза и почти 30% псевдотуберкулеза. Наиболее частыми проявлениями данной формы являются гастроэнтероколитический, гастроэнтеритический, энтероколитический и энтеритический варианты течения болезни. Они регистрируются во всех возрастных группах, но в основном у детей в возрасте до 10 лет.
Клиническая картина указанных вариантов характеризуется наличием интоксикационного синдрома и симптомов поражения желудочно-кишечного тракта на том или ином его уровне. Заболевание начинается остро: возникают озноб, повышение температуры тела до 38-38,5°С. Больных беспокоит головная боль, слабость, миалгии и артралгии. Одновременно с интоксикационным синдромом возникают тошнота, у части больных — рвота, боли в животе, которые носят схваткообразный или постоянный характер.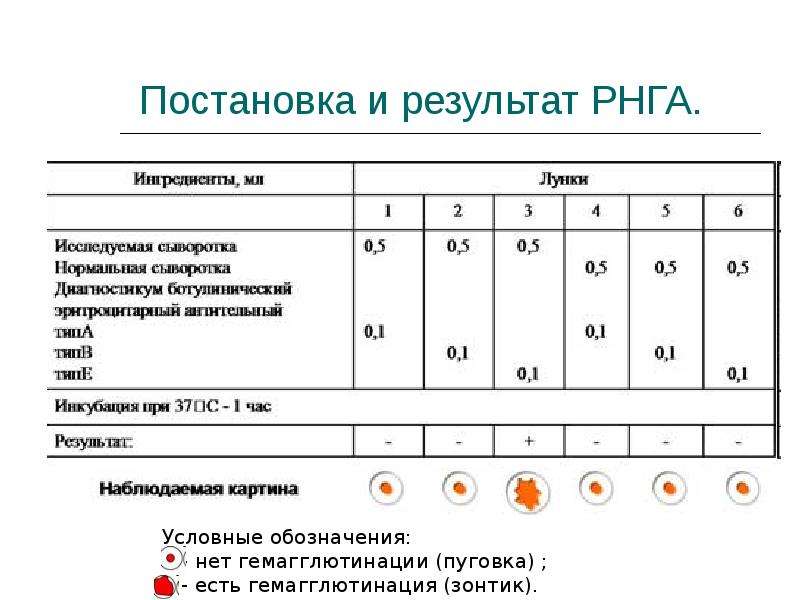 Локализация болей – в эпигастрии, вокруг пупка, в правой подвздошной области, иногда в правом подреберье. Стул жидкий, вязкий, с резким запахом. У некоторых больных при вовлечении в патологический процесс толстой кишки в стуле обнаруживают примесь слизи, реже крови. Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Локализация болей – в эпигастрии, вокруг пупка, в правой подвздошной области, иногда в правом подреберье. Стул жидкий, вязкий, с резким запахом. У некоторых больных при вовлечении в патологический процесс толстой кишки в стуле обнаруживают примесь слизи, реже крови. Частота стула от 2-3 до 15 раз в сутки. Продолжительность заболевания от 2 до 15 сут. Наряду с доброкачественным течением встречаются тяжелые формы болезни с резко выраженной интоксикацией, обезвоживанием организма.
Острый терминальный илеит сопровождается повышением температуры тела до 38-39°С, интенсивными болями в илеоцекальной области и диареей. Больные, как правило, описывают два вида болей: постоянного и на их фоне – схваткообразного типов. При рентгенологическом исследовании пораженная часть подвздошной кишки резко сужена и имеет сглаженный рельеф слизистой оболочки («симптом шнура»). Терминальный илеит имеет длительное и нередко осложненное течение. Среди возможных осложнений: инфарцирование и некроз слизистой оболочки с последующим ограниченным или (редко) разлитым перитонитом, спаечный процессе развитием кишечной непроходимости и др. Возможно развитие клиники последствий в виде хронического гранулематозно-язвенного поражения подвздошной кишки, морфологически не отличимого от болезни Крона.
Возможно развитие клиники последствий в виде хронического гранулематозно-язвенного поражения подвздошной кишки, морфологически не отличимого от болезни Крона.
Острый мезаденит характеризуется умеренно выраженной интоксикацией, субфебрильной температурой, меньшей, чем при терминальном илеите силой схваткообразных и постоянного типа болей. В дебюте заболевания может иметь место тошнота, рвота, жидкий стул до 3-5 раз за сутки. В дальнейшем у значительной части больных наблюдается развитие (за 4-6 дней) «инфильтрата» в илеоцекальной области, представляющего собой группу увеличенных мезентериальных узлов, и перитонеальной симптоматики. Выявляют положительные симптомы Мак-Фаддена, Клейна, Падалки, «перекрестный» симптом Штернберга. Течение острого мезаденита нередко сопровождается обострениями и рецидивами. Возможен переход заболевания в затяжное и хроническое течение. Часть больных подвергаются оперативному вмешательству.
Острый иерсиниозный (псевдотуберкулезный) аппендицит в отличие от вульгарного имеет более медленный темп развития от катаральной до деструктивной форм. Как следствие этого – большая частота обнаружения катарально измененного червеобразного отростка в ходе оперативного вмешательства, чем при вульгарном аппендиците. Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Как следствие этого – большая частота обнаружения катарально измененного червеобразного отростка в ходе оперативного вмешательства, чем при вульгарном аппендиците. Однако и этот вариант не отличается гладким течением. Нередко после хирургического вмешательства развиваются признаки генерализации: высокая лихорадка, полилимфаденит, гепатоспленомегалия, экзантема.
Всем вариантам локализованной формы свойственна не только абдоминальная (желудочно-кишечная), но и внеабдоминальная симптоматика, обусловленная действием токсина и избыточной продукцией простагландинов на вазомоторы и эндотелий сосудов: инъекция сосудов склер и гиперемия конъюнктив, «малиновый» язык, гиперемия мягкого неба, артралгии, миалгии и др.
В периферической крови наблюдается лейкоцитоз, нейтрофилез, палочкоядерный сдвиг, увеличение СОЭ, иногда эозинофилия.
Генерализованная форма встречается примерно в 30% случаев манифестного течения иерсиниозаи 70% случаев псевдотуберкулеза. Она имеет две разновидности течения :токсикобактериемическая и септическая. Как при иерсиниозе, так и при псевдотуберкулезе обычно наблюдается токсикобактериемическое течение генерализованной формы. Септическое течение при обоих заболеваниях встречается крайне редко.
Как при иерсиниозе, так и при псевдотуберкулезе обычно наблюдается токсикобактериемическое течение генерализованной формы. Септическое течение при обоих заболеваниях встречается крайне редко.
Токсикобактериемическое течение генерализованной формы наиболее хорошо изучено при экзантем атозном варианте псевдотуберкулеза, описанном ранее как дальневосточная скарлати неподобная лихорадка. Заболевание характеризуется острым началом. Больные жалуются на озноб, головную боль, миалгии и артралгии. Температура тела повышается до 38-40°С и держится на этом уровне в течение 5-7 сут, а при тяжелой форме и дольше. В первые дни болезни отмечаются тошнота, иногда рвота, жидкий стул, боли в животе. Нередко наблюдаются катаральные симптомы со стороны верхних дыхательных путей: першениеи умеренные боли при глотании, покашливание, насморк.
При объективном обследовании в 1-ю неделю заболевания кожа больных сухая, горячая, лицо одутловатое. Отмечается гиперемия конъюнктив, инъекция сосудов склер. Нередко, особенно у детей, определяется бледный носогубный треугольник. Слизистая оболочка ротоглотки диффузно гиперемирована. У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
Нередко, особенно у детей, определяется бледный носогубный треугольник. Слизистая оболочка ротоглотки диффузно гиперемирована. У части больных на мягком небе обнаруживается точечная энантема. К числу кардинальных признаков этого заболевания относятся точечная скарлатиноподобная экзантема в сочетании с симптомами «капюшона» (гиперемия лица и шеи), «перчаток» и «носков» (ограниченная гиперемия кистей и стоп). Эти кардинальные симптомы появляются чаще всего на 2-4-й день болезни. Продолжительность существования сыпи – 1-7 дней. После ее исчезновения, со 2-й недели болезни, у большинства больных появляется отрубевидное шелушение кожи туловища, лица и шеи и пластинчатое (листовидное) – кожи ладоней и стоп.
Следует заметить, что подобный тип экзантемы практически не встречается при иерсиниозе. Для него более характерна мелкопятнистая сыпь на симметричных участках кожи туловища и/или конечностей, которая исчезает в срок от нескольких часов до 3-4 сут.
При пальпации находят умеренно увеличенные и болезненные периферические лимфоузлы. Определяются лабильность и учащение пульса, соответствующее температуре тела. Артериальное давление несколько снижено.
Определяются лабильность и учащение пульса, соответствующее температуре тела. Артериальное давление несколько снижено.
Органы пищеварительной системы закономерно вовлекаются в патологический процесс. Язык, обложенный в первые дни болезни белым налетом, часто к 5-7-му дню очищается и становится «малиновым». При пальпации живота отмечают болезненность и урчание в илеоцекальной области, с меньшим постоянством в эпи- и мезогастрии. Выявляются положительные симптомы Падалки, «перекрестный» Штернберга. У больных с пониженным питанием можно прощупать увеличенные и болезненные мезентериальные лимфатические узлы. Обычно в патологический процесс вовлекается печень. Она увеличивается, становится доступной для пальпации к концу 1-й недели заболевания. У некоторых больных поражение паренхимы печени приводит к появлению иктеричности склер и кожи, гипербилирубинемии, уробилин- и билирубинурии, умеренно выраженной гипертрансаминаземии.
В части случаев имеет место спленомегалия. В периферической крови – нейтрофильный лейкоцитоз Ю-ЗОхЮ^л, палочкоядерный сдвиг, иногда эозинофилия, увеличение СОЭ до 25-50 мм/ч.
Заболевание нередко сопровождается развитием признаков инфекционно-токсического интерстициального нефрита. В некоторых случаях тяжелого течения болезни наблюдаются признаки серозного менингита.
У части больных 2-я и 3-я недели болезни характеризуются появлением симптомов, свидетельствующих об иммунопатологической перестройке. В это тпериод нередко появляются уртикарные, макулезные и макулопапулезные высыпания с локализацией на туловище и конечностях, чаще в области крупных суставов. Возникает узловатая эритема. У некоторых больных развивается реактивный полиартрит, болезнь Рейтера.
Иногда в этот период заболевания выявляют миокардит, нефрит, уретрит, цистит, конъюнктивит, иридоциклит и другие поражения внутренних органов.
По преобладанию той или иной симптоматики в пределахтокси-кобактериемического течения генерализованной формы заболевания выделяют следующие варианты: экзантематозный, артритический, желтушный (иерсиниозный/псевдотуберкулезный гепатит), менингеальный, катаральный и иерсиниоз (псевдотуберкулез) редких локализаций.
Обострения и рецидивы часто осложняют течение иерсиниоза и псевдотуберкулеза. Они встречаются у 1/ больных и характеризуются повторной волной лихорадки и симптомами локальных поражений.
В период реконвалесценции температура тела снижается до нормальной, симптомы интоксикации исчезают, нормализуются функции внутренних органов.
Тяжесть течения иерсиниоза и псевдотуберкулеза определяется выраженностью интоксикационного синдрома и степенью вовлечения в патологический процесс внутренних органов. Чаще заболевание протекает в легкой и среднетяжелой формах.
Септическое течение генерализованной формы иерсиниоза и псевдотуберкулеза встречается очень редко. Оно, как правило, развивается при выраженном иммунодефиците, у лиц с хронической патологией печени и признаками тезауризмоза железа. Течение заболевания характеризуется тяжелой интоксикацией, микроабсцедированием внутренних органов, гепатоспленомегалией, нередко диареей, длительным рецидивирующим течением и, несмотря на лечение, высокой летальностью.
При всех формах манифестного течения иерсиниозной инфекции продолжительность заболевания обычно не превышает 1,5 мес. Однако иногда встречается затяжное течение болезни (от 1,5 до 3 мес) и в редких случаях хроническое (более 3 мес). Наличие заболевания, этиологически связанного с перенесенным иерсиниозом, но при доказанном бактериологически и серологически отсутствии возбудителя в организме больного должно расцениваться как клиника последствий иерсиниоза (резидуальная фаза).
Бессимптомное течение может быть острым (до 3 мес) и хроническим (более 3 мес). Последнее не характерно для псевдотуберкулеза. Кроме того, при иерсиниозев отличие от псевдотуберкулеза наблюдается не только субклиническое, но и реконвалесцентное бактериовыделение возбудителей болезни. Лица, имеющие бессимптомное течение заболевания, выявляются активно при обследовании работников пищевых предприятий и контактных – в очагах.
Прогноз в большинстве случаев, за исключением септического течения болезни, благоприятный.
Диагностика
Из клинических признаков наибольшее диагностическое значение имеет сочетание синдрома поражения желудочно-кишечного тракта и «внекишечной» токсико-вазарной симптоматики. Данные эпидемиологического анамнеза, особенно при групповом характере заболеваемости, также имеют большое значение в распознавании иерсиниоза и псевдотуберкулеза. Однако решающим в установлении окончательного диагноза являются специфические методы диагностики – бактериологический и серологический.
Основными материалам и для бактериологического исследования служат испражнения, кровь, цереброспинальная жидкость, резецированные лимфатические узлы и червеобразный отросток. Для определения присутствия псевдотуберкулезных антигенов в фекалиях и другом материале используют иммуноферментный анализ (ИФА).
Серологическая диагностика имеет большое значение для подтверждения не только клинического диагноза, но и этиологической роли выделенных иерсиний. Она осуществляется с помощью РА и РНГА методом парных сывороток.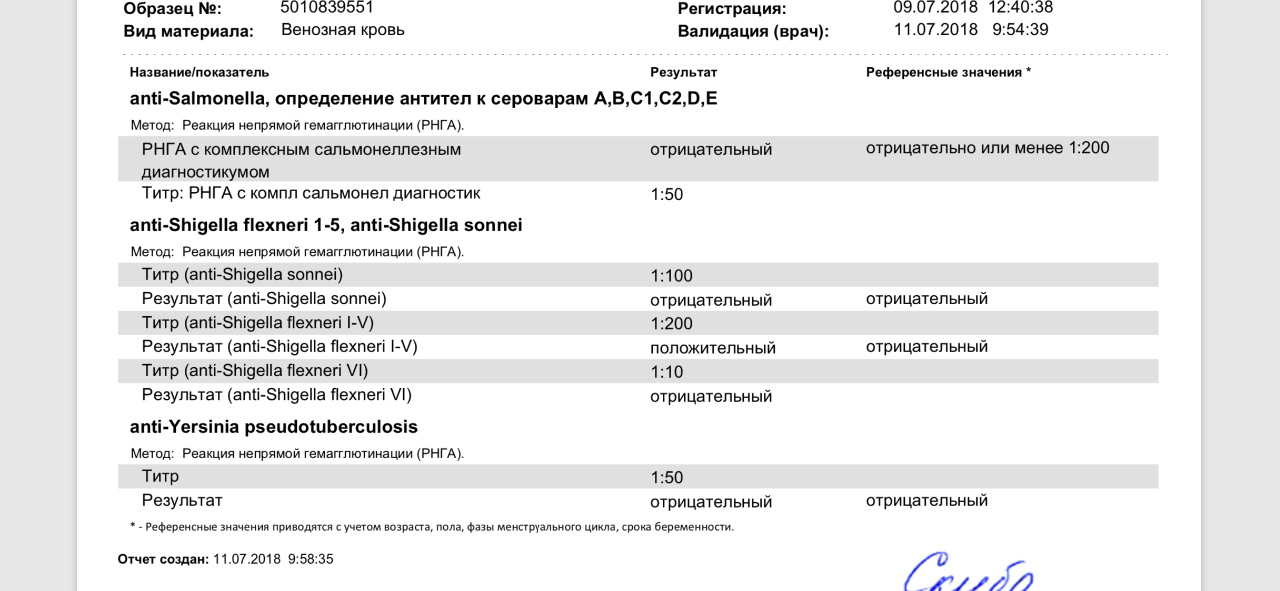 Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
Исследуют сыворотки крови, взятые в начале и на 3-й неделе болезни. Диагностическим для РА считается титр антител 1:80 и выше, а для РНГА-1:160 и выше.
В экспресс-диагностике иерсиниоза используют РНГА с иммуноглобулиновыми диагностикумами и МФА.
Определенное значение в диагностике имеет также гистологическое исследование биоптатов лимфатических узлов и других органов.
Дифференциальная диагностика иерсиниоза и псевдотуберкулеза зависит от клинического варианта болезни. Наиболее часто возникает необходимость дифференцировать эти заболевания с острыми кишечными инфекциями, аппендицитом, различными заболеваниями суставов, вирусным гепатитом, сепсисом иной этиологии и др.
Лечение
В качестве этиотропных средств применяют антибиотики, сульфаниламиды и химиопрепараты. К препаратам выбора при генерализованной форме заболеваний относятся фторхинолоны. К препаратам резерва — цефалоспорины 3-го поколения, тетрациклины и левомицетин. Аминогликозиды обычно используют при лечении больных с иерсиниозным (псевдотуберкулезным) гепатитом. Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Для лечения больных с гастроинтестиномезентериальной формой (варианты: гастроэнтероколит, гастроэнтерит, энтероколит, энтерит) могут быть использованы препараты из группы котримоксазола и нитрофурана. Продолжительность этиотропной терапии зависит от формы заболевания. При локализованной форме она составляет 7-10 дней, при генерализованной – не менее 12-14 дней.
Патогенетическая терапия предусматривает назначение дезинтоксикационных, общеукрепляющих и стимулирующих, а также десенсибилизирующих средств. В некоторых случаях используют глюкозоэлектролитныеи полиионные растворы для регидратации.
Больных с септическим течением заболевания лечат в соответствие с принципами лечения сепсиса, используя 2-3 антибиотика (фторхинолоны, аминогликозиды, цефалоспорины) внутривенно в сочетании с интенсивной патогенетической терапией.
Больные с бессимптомным течением получают терапию в зависимости от варианта (субклинический или реконвалесцентный) и продолжительности бактериовыделения. Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
Лечение острого субклинического варианта соответствует терапии легкого течения локализованной формы. В терапии хронического субклинического и реконвалесцентного вариантов используют фторхинолоны, аминогликозиды, рифампицин в комплексе с иммуноориентированными средствами.
По показаниям проводится оперативное лечение.
Профилактика
Контроль за состоянием овощехранилищ, борьба с грызунами.
Причины, факторы риска, диагностика и лечение
Кровь в моче — ваш врач может назвать это гематурией — обычно не является поводом для серьезной тревоги.
Но не стоит игнорировать это, потому что это также может быть признаком серьезного заболевания. Расскажите об этом своему врачу; они могут заказать тесты для поиска причины.
Гематурия — это всего лишь симптом, поэтому лечение будет сосредоточено на состоянии, вызвавшем ее.
Откуда может поступать кровь в моче
Кровь в моче может поступать из почек, которые производят мочу. Он также может поступать из других частей мочевыводящих путей, таких как:
Он также может поступать из других частей мочевыводящих путей, таких как:
- Мочеточники (трубки, идущие от почек к мочевому пузырю)
- Мочевой пузырь (в котором хранится моча)
- Уретра (трубка, ведущая из мочевого пузыря наружу. вашего тела)
Симптомы, связанные с гематурией
Вместо обычного бледно-желтого цвета ваша моча может быть розовой, красной, коричневато-красной или чайного цвета. Это то, что врачи называют макрогематурией.
Иногда кровь в моче не видна.Только лабораторный анализ может обнаружить эритроциты. Врачи называют это микроскопической гематурией.
У вас может не быть других симптомов. Но некоторые из возможных причин могут иметь и другие признаки. К ним относятся:
- Инфекции мочевого пузыря (острый цистит). У взрослых инфекции мочевого пузыря обычно вызывают жжение или боль при мочеиспускании. У младенцев с инфекциями мочевого пузыря может подниматься температура, они могут быть сварливыми и плохо питаться.
 У детей более старшего возраста могут быть жар, боль и жжение при мочеиспускании, сильное желание в туалет и боль в нижней части живота.
У детей более старшего возраста могут быть жар, боль и жжение при мочеиспускании, сильное желание в туалет и боль в нижней части живота. - Инфекции почек (пиелонефрит). Симптомы могут включать жар, озноб и боль в пояснице (боку).
- Камни в почках. Они вызывают сильную боль в животе или тазу.
- Рак почки. Вы можете похудеть, потерять аппетит, утомиться или почувствовать боль в боку.
- Заболевания почек. Симптомы включают слабость, высокое кровяное давление и отечность тела, в том числе отечность вокруг глаз.
Причины гематурии и факторы риска
У вас может быть кровь в моче из-за:
Цвет вашей мочи также может измениться из-за красных пигментов от таких вещей, как пищевые красители, лекарства или употребление большого количества свеклы.Врачи иногда называют это «бетурией».
Диагностика гематурии
Ваш врач спросит о вашей истории болезни и отправит образец вашей мочи для лабораторных анализов. Это называется анализом мочи. Тесты могут включать цитологию, в которой техник использует микроскоп для поиска необычных клеток.
Это называется анализом мочи. Тесты могут включать цитологию, в которой техник использует микроскоп для поиска необычных клеток.
Ваш врач может назначить анализы крови для выявления шлаков, которые должны вывести ваши почки. Это может быть признаком заболевания почек.
Вам также могут понадобиться другие тесты, в том числе:
- Компьютерная томография. Особый вид рентгеновского сканирования может помочь обнаружить камни, опухоли и другие проблемы в мочевом пузыре, почках и мочеточниках.
- УЗИ почек. В этом тесте используются звуковые волны для создания изображения вашей почки.
- Цистоскопия. Ваш врач вставляет небольшую трубку с камерой в мочевой пузырь через уретру. Они могут взять образцы ткани (биопсия), чтобы проверить наличие необычных или злокачественных клеток.
- Биопсия почки. Техник рассматривает образец ткани почек под микроскопом на предмет выявления признаков заболевания почек.

Лечение гематурии
Ваш врач лечит состояние, при котором в вашей моче появляется кровь. Затем они снова проверит вас, чтобы увидеть, не ушла ли кровь. Если у вас все еще есть кровь в моче, вам могут потребоваться дополнительные анализы или вы можете обратиться к специалисту, называемому урологом или нефрологом.
Если ваш врач не может найти причину во время первой оценки, он может посоветовать вам проводить контрольный анализ мочи и мониторинг артериального давления каждые 3–6 месяцев, особенно если у вас есть факторы риска рака мочевого пузыря.К ним относятся возраст от 50 лет, курение сигарет и контакт с некоторыми промышленными химическими веществами.
Титр — обзор | Темы ScienceDirect
Disease Association
Изотип антител также может различаться в зависимости от состояния заболевания. У пациентов со следующими заболеваниями титр антител сильно повышен.
Болезнь Грейвса
Титры анти-Galα1,3Gal сильно повышены у пациентов с гипертироидной болезнью Грейвса (БГ) [4]. Анти-Galα1,3Gal специфически связывается с тироцитами GD и индуцирует увеличение синтеза цАМФ, захвата 125 I и синтеза ДНК в этих клетках. Кроме того, стимулирующие эффекты аутологичных сывороток на тироциты GD были значительно снижены после специфического истощения анти-α-gal из этих сывороток. Никакого связывания и стимулирующих эффектов анти-αGal не наблюдалось с нормальными тироцитами человека. Эти стимулирующие in vitro эффекты анти-αGal на тироциты GD предполагают, что это антитело может вносить вклад в непрерывную стимуляцию тироцитов in vivo у пациентов с GD [5].В недавнем исследовании [6] сообщается, что пациентов с гипертиреозом (n = 20) имели значительно более низкие уровни анти-Gal IgG, чем нормальные ( n = 36; p <0,05). У пациентов с гипертиреозом без клинической офтальмопатии уровни IgG anti-Gal были ниже, чем у эутиреоидных пациентов с офтальмопатией ( p = 0,1). Был сделан вывод, что гипертиреоз значительно снижает уровень анти-Gal, но возможное повышение уровня анти-Gal у пациентов с офтальмопатией предполагает, что анти-Gal может играть роль в офтальмопатии или может отражать эутиреоидный статус этих пациентов.
Анти-Galα1,3Gal специфически связывается с тироцитами GD и индуцирует увеличение синтеза цАМФ, захвата 125 I и синтеза ДНК в этих клетках. Кроме того, стимулирующие эффекты аутологичных сывороток на тироциты GD были значительно снижены после специфического истощения анти-α-gal из этих сывороток. Никакого связывания и стимулирующих эффектов анти-αGal не наблюдалось с нормальными тироцитами человека. Эти стимулирующие in vitro эффекты анти-αGal на тироциты GD предполагают, что это антитело может вносить вклад в непрерывную стимуляцию тироцитов in vivo у пациентов с GD [5].В недавнем исследовании [6] сообщается, что пациентов с гипертиреозом (n = 20) имели значительно более низкие уровни анти-Gal IgG, чем нормальные ( n = 36; p <0,05). У пациентов с гипертиреозом без клинической офтальмопатии уровни IgG anti-Gal были ниже, чем у эутиреоидных пациентов с офтальмопатией ( p = 0,1). Был сделан вывод, что гипертиреоз значительно снижает уровень анти-Gal, но возможное повышение уровня анти-Gal у пациентов с офтальмопатией предполагает, что анти-Gal может играть роль в офтальмопатии или может отражать эутиреоидный статус этих пациентов.
Scleroderma
Сыворотки 224 пациентов с системным склерозом (склеродермией) были проанализированы на антитела против Galα1,3Gal [7]. Средний уровень антител у пациентов был значительно ( p < 0,001) выше, чем у здоровых субъектов. Средний уровень анти-α-галлонов коррелировал со степенью поражения кожи и внутренних органов, а также с наличием прогрессирования или воспаления.
Миелофиброз
Пациенты с миелофиброзом также имеют титры антител против αGal выше контрольных значений.Средний титр антител был значительно выше, чем значение, обнаруженное в нормальном контроле, но не было обнаружено различий между пациентами с идиопатическим миелофиброзом и пациентами с миелофиброзом, связанным с хроническим миелопролиферативным заболеванием [8].
Анти-Galα 1,3Gal-антитела у пациентов с простейшими инфекциями
Паразиты эритроцитарной стадии Plasmodium falciparum экспрессируют детерминанты Galα1,3Gal. Anti-Galα1,3Gal IgG3 преобладает у P. falciparum , инфицированная сыворотка пациентов, в то время как IgG2 оказался доминирующим в неэндемичной контрольной сыворотке. В сыворотках крови пациентов с болезнью Шагаса и инфекцией Leishmania титры анти-Galα1,3Gal антител в 10 и 16 раз выше, чем у здоровых или инфицированных бактериями людей. Это увеличение титра антител, по-видимому, является результатом специфического иммунного ответа на паразитические эпитопы Galα1,3Gal. Паразиты Trypanosoma cruzi и American Leishmania действительно продемонстрировали присутствие на этих паразитах эпитопов Galα1,3Gal.Естественно высокий уровень антитела против Galα1,3Gal у человека и его связывание с T. cruzi и Leishmania предполагают, что это антитело может вносить вклад в естественную защиту от вторжения таких паразитов [9].
falciparum , инфицированная сыворотка пациентов, в то время как IgG2 оказался доминирующим в неэндемичной контрольной сыворотке. В сыворотках крови пациентов с болезнью Шагаса и инфекцией Leishmania титры анти-Galα1,3Gal антител в 10 и 16 раз выше, чем у здоровых или инфицированных бактериями людей. Это увеличение титра антител, по-видимому, является результатом специфического иммунного ответа на паразитические эпитопы Galα1,3Gal. Паразиты Trypanosoma cruzi и American Leishmania действительно продемонстрировали присутствие на этих паразитах эпитопов Galα1,3Gal.Естественно высокий уровень антитела против Galα1,3Gal у человека и его связывание с T. cruzi и Leishmania предполагают, что это антитело может вносить вклад в естественную защиту от вторжения таких паразитов [9].
Ксенотрансплантация
Естественное присутствие активирующих комплемент анти-Galα1,3Gal-антител в сыворотке крови человека считается основным препятствием для ксенотрансплантации. Пациенты, чья кровь была перфузирована через печень свиньи для лечения печеночной недостаточности, имеют природные антитела, специфичные для Gal1-3Gal.Антитела против Gal1-3Gal представлены преимущественно IgM и IgG2 у всех несенсибилизированных индивидуумов; это IgM, IgG2 и IgG1 после сенсибилизации. Измеряли активацию комплемента анти-Gal1-3Gal на микрограмм антитела. Отложение фактора комплемента C3bi коррелировало с концентрациями IgG1 и IgM, но не IgG2 против Gal1-3Gal. В соответствии с этим открытием, очищенный IgG1, но не IgG2, фиксированный комплемент анти-Gal1-3Gal на клетках свиньи. Эти результаты демонстрируют, что свойства антиуглеводных антител развиваются после сенсибилизации, чтобы увеличить фиксацию комплемента на потенциальных мишенях [10].
Пациенты, чья кровь была перфузирована через печень свиньи для лечения печеночной недостаточности, имеют природные антитела, специфичные для Gal1-3Gal.Антитела против Gal1-3Gal представлены преимущественно IgM и IgG2 у всех несенсибилизированных индивидуумов; это IgM, IgG2 и IgG1 после сенсибилизации. Измеряли активацию комплемента анти-Gal1-3Gal на микрограмм антитела. Отложение фактора комплемента C3bi коррелировало с концентрациями IgG1 и IgM, но не IgG2 против Gal1-3Gal. В соответствии с этим открытием, очищенный IgG1, но не IgG2, фиксированный комплемент анти-Gal1-3Gal на клетках свиньи. Эти результаты демонстрируют, что свойства антиуглеводных антител развиваются после сенсибилизации, чтобы увеличить фиксацию комплемента на потенциальных мишенях [10].
Рак желудочно-кишечного тракта и молочной железы
Аутоантиген antiGalα1,3Gal IgG может экспонироваться в злокачественных клетках, включая карциному молочной железы, и в плоских клетках шейки матки, инфицированных вирусом папилломы человека. Анализ сывороток на antiGalα1,3Gal у пациентов с раком желудка показал, что уровень IgG был выше на стадиях III и IV (p = 0,059) и значительно выше у пациентов с объемом опухоли T2 + T3 по сравнению с T1 (p = 0,024). ). У пациентов с раком груди был отмечен более низкий уровень антиGalα1,3Gal IgG для большего объема опухоли (p = 0.024). Более низкий уровень antiGalα1,3Gal IgG также был связан с низкодифференцированными карциномами у пациентов с раком груди (p = 0,036). Различия, обнаруженные у онкологических больных, указывают на участие антител антиGalα1,3Gal IgG в прогрессировании опухоли и патологии [11].
Анализ сывороток на antiGalα1,3Gal у пациентов с раком желудка показал, что уровень IgG был выше на стадиях III и IV (p = 0,059) и значительно выше у пациентов с объемом опухоли T2 + T3 по сравнению с T1 (p = 0,024). ). У пациентов с раком груди был отмечен более низкий уровень антиGalα1,3Gal IgG для большего объема опухоли (p = 0.024). Более низкий уровень antiGalα1,3Gal IgG также был связан с низкодифференцированными карциномами у пациентов с раком груди (p = 0,036). Различия, обнаруженные у онкологических больных, указывают на участие антител антиGalα1,3Gal IgG в прогрессировании опухоли и патологии [11].
Распространенность заболевания
При измерении antiGalα1,3Gal в сыворотке 200 здоровых добровольцев (100 мужчин, 100 женщин) разных возрастных групп с использованием специфичного для изотипа IgG и IgM ELISA и теста прямой гемагглютинации (HA) с эритроцитами кролика было отмечено, что значения antiGal IgM значительно выше (p < 0.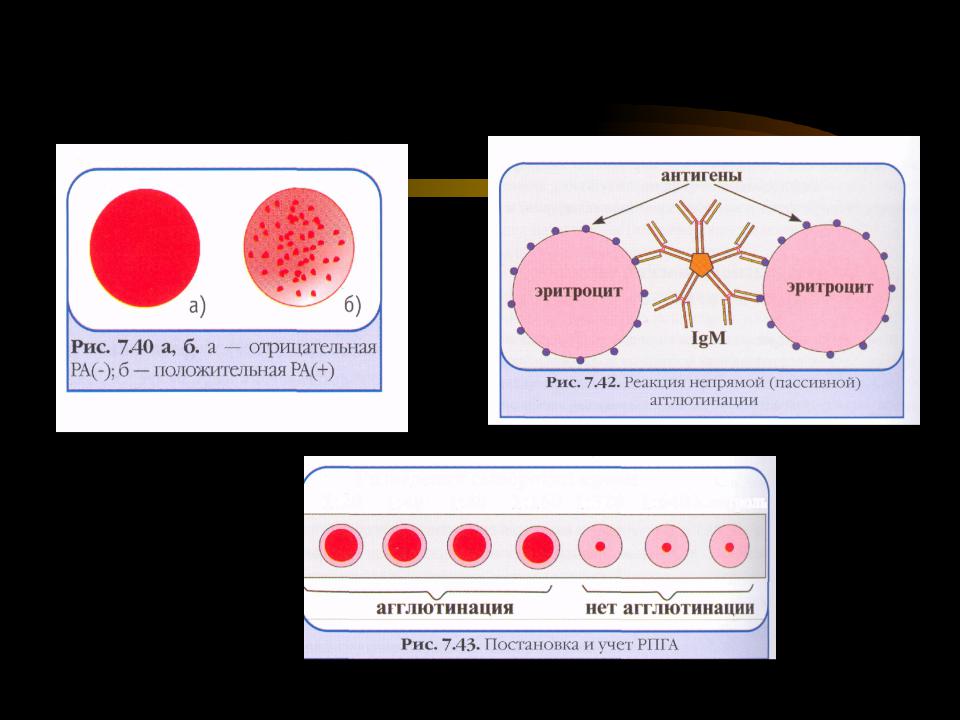 005) у женщин, чем у мужчин, тогда как гендерные различия в титрах анти-Galα1,3Gal IgG или HA не были значительными. Высокий титр антител antiGalα1,3Gal, наблюдаемый у женщин, объясняется предрасположенностью женщин к аутоиммунным нарушениям, болезни Грейвса и склеродермии.
005) у женщин, чем у мужчин, тогда как гендерные различия в титрах анти-Galα1,3Gal IgG или HA не были значительными. Высокий титр антител antiGalα1,3Gal, наблюдаемый у женщин, объясняется предрасположенностью женщин к аутоиммунным нарушениям, болезни Грейвса и склеродермии.
Диагностическая ценность
У пациентов с ранним началом склеродермии уровни антиGalα1,3Gal-антител были высокими среди пациентов с прогрессированием или воспалением, но не среди пациентов со стабильным заболеванием. Иммунный ответ на Galα1,3Gal может быть важным ранним патогенетическим признаком склеродермии и может обеспечить более чувствительный инструмент для выявления активности заболевания.
Установлено, что определение сывороточных антител к Ga1,3Gal является чувствительным и специфическим параметром у пациентов с миелофиброзом. Антитела Anti-Galα1,3Gal коррелировали с активностью заболевания и количеством тромбоцитов. Гуморальный иммунитет против Galα1,3Gal может служить чувствительным инструментом для выявления активности заболевания у пациентов с идиопатическим миелофиброзом и может быть важным для понимания его патогенеза.
Клиническая применимость различных методов обнаружения
Анализ гемагглютинации с кроличьими эритроцитами и непрямой ИФА с Galα1,3Gal-содержащими олигосахаридами обычно используются для определения титров изотипов антител против Galα1,3Gal.Анализ ELISA требует оценки фоновых значений сывороток, протестированных против лунок, не покрытых антигеном, положительного контроля с высоким титром антител против Galα1,3Gal и отрицательного контроля (здоровые доноры с группами крови A или O). Титры могут быть преобразованы в натуральный логарифм для статистических сравнений. Необходимо установить титры антител против αGal у здоровых людей с разными группами крови. При сравнении титров, обнаруженных у здоровых добровольцев с пациентами, было бы более целесообразно сопоставить пол и группы крови.
(PDF) Гомеостаз химического состава крови во время длительного голодания у северных морских слонов
R594
DP COSTA AND CL ORTIZ
обнаружил физическое насилие при попытках кормления грудью, тогда как самое низкое значение, полученное в этом исследовании у
инопланетных самок (13 ). натощак был 273 мгдл-‘. Интересно отметить, что в
натощак был 273 мгдл-‘. Интересно отметить, что в
Постепенное снижение уровня глюкозы в сыворотке и мочевины у кроликов натощак, несмотря на повышение уровня холестерина в сыворотке, содержащего
азота (рис.1 и 2) характерно для других концентраций натощак, в которых не происходило чистого синтеза или деградации,
млекопитающих, включая человека (4). Эти наблюдения почти всегда были связаны с высвобождением накопленного холестерина
, скорее всего, отражают
и увеличенное снижение содержания белка
.
— —
показывают, что оборот глюкозы
детенышей существенно ниже, чем
глюконеогенной активности
Предварительные исследования (10)
натощак
, которые наблюдались у людей
(27) и собак (5). ) во время длительных постов.Что такое —
жирных диет(32, 33). Более того, похоже, что
выдвинули правдоподобные гипотезы, относящиеся к водным организмам
Что парадоксально в случае морского слона, так это то, что
среда, физиология дайвинга и низкоуглеводная
концентрация глюкозы в сыворотке остается примерно в два раза
морские млекопитающие в целом, голодные или кормящиеся,
dieti ‘(25, 30).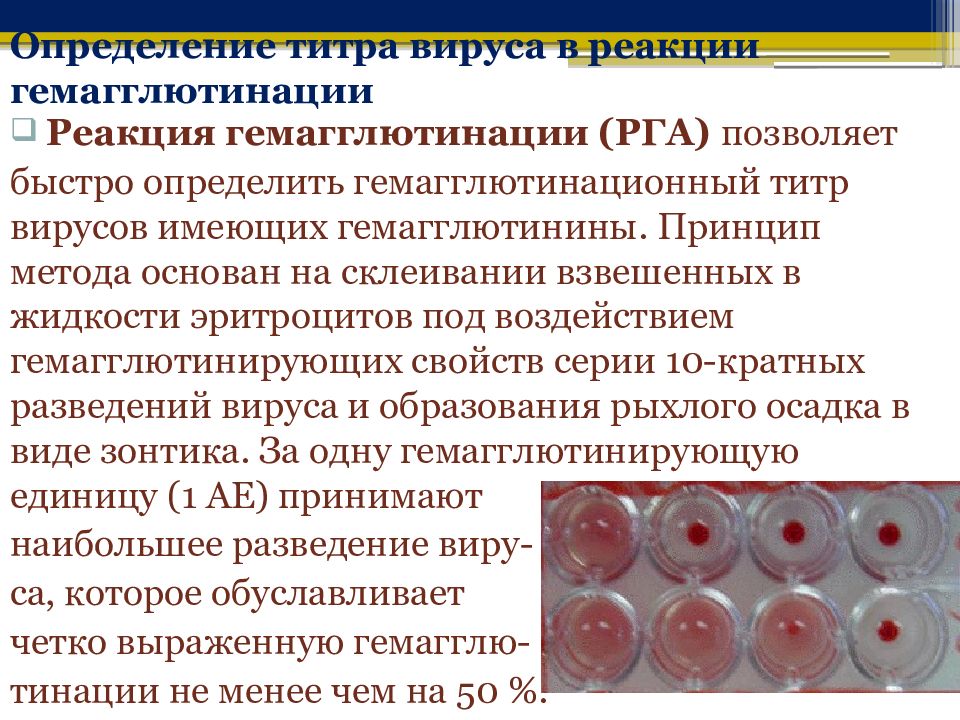 Поскольку уровни глюкозы и инсулина в
Поскольку уровни глюкозы и инсулина в
выше, чем прогнозировалось для млекопитающих его массы и
,«клинически нормальных» морских млекопитающих напоминают наблюдаемые
скорости метаболизма (29), несмотря на длительное голодание. Эти
демонстрируют концентрации глюкозы в сыворотке, превышающие эти
«гипергликемия натощак» может быть результатом
с высоким содержанием жира, предсказанного размером тела (30). Адаптивное значение рациона
, потребляемого во время кормления грудью (24).Гипергликемия, повторное снижение толерантности к глюкозе и нарушение чувствительности к инсулину наблюдались у голодающих крыс после высокого уровня
, этот результат неясен, но другие исследователи имели до
в липидной капле (28). . Повышенный уровень холестерина до
характерен для нескольких голодающих ластоногих [калифорнийский морской лев
(25), южный морской слон (Zl) и северный морской котик
(9)], а также зимующие медведи ( 17). Было бы поучительно узнать, наблюдается ли динамика холестерина «закрытая система
Было бы поучительно узнать, наблюдается ли динамика холестерина «закрытая система
tem», наблюдаемая в битах принудительного голодания кролика
, также для млекопитающих, подвергающихся естественному голоданию.
без серьезных, а иногда и необратимых
физиологических повреждений. Дальнейшие исследования могут выявить дополнительные
адаптации, которые позволяют молодым морским слонам
Хотя мы подчеркнули физиологические и
метаболические адаптации, лежащие в основе гомеостаза во время голодания
, следует признать, что эти голодания
не только выживают. но остаются устойчивыми перед лицом
неотъемлемая часть раннего развития молодых слонов
полная длительная недостаточность питания.
тюленей, резко контрастирующих с большинством млекопитающих. Действительно,
неполовозрелых млекопитающих неспособны к длительному голоданию.
Данные по углеводному обмену и его гормональному положению
у морских млекопитающих представляют значительный интерес.
Сывороточный холестерин
Концентрация
у морских слонов
при нескольких формах диабета человека (25, 31) дополнительно
Грант программы биомедицинской поддержки меньшинств SO6-RR0813244 и
Стипендия для докторантов 06 AM-3%: 0-OX в D.П. Коста и
Мы благодарим Департамент парков и отдыха Калифорнии по адресу
Государственный заповедник Афро Нуэво за их сотрудничество и техническую поддержку.
Факультетский исследовательский грант и патентные фонды Университета
Калифорния, Санта-Крус. Полевые работы были разрешены на основании разрешения 277,
, Национальная служба рыболовства США.
Эта работа была частично поддержана Национальными институтами здравоохранения,
, хотя несколько вариабельная была значительно выше, чем
Текущий адрес Д.П. Коста: Лаборатория физиологических исследований,
, который наблюдался у голодных кроликов (28). Эти авторы сообщили о
Институте океанографии Скриппса, Калифорнийский университет, Сан
, что уровни холестерина выросли примерно с 30 мкг / год
Диего, Калифорния 92093.
дл-‘до более чем 100 мг * дл-л в течение 32 дней применения. пост,
Поступила 8 марта 1981 г .; принята в окончательной форме 29 сентября 1981 г.
СПИСОК ЛИТЕРАТУРЫ
1.БАРФОЛОМЕВ, Г. А. Модель эволюции ластоногих
полигиния. Euoiution 24: 546-559, 1970.
2, BONNELL, M. IL., AND R.K.SELANDER. Морские слоны: генетическая вариация
, близкая к исчезновению. Science lt34: 908-909, 1974.
3. Кэхилл, Дж. Ф., младший, М. Г. ХЕРРЕРА, А. П. МОРГАН, Дж. С. СОЕЛДНЕР,
Дж. Штейн, П. Л. Леви, Г. А. Рейчард, младший, Д. М. Кипнис.
Гормонально-топливные взаимосвязи во время голодания.J. CZin. fnuest. 45:
1751-1769, 1966.
4, CAHILL, G. F., E. B. MARLISS, T. T. AOKI. Жиры и азот
Обмен веществ у голодающего человека. В: Жировая ткань: Регуляция arzd
Метаболическая функция. Нью-Йорк: Academic, 1970, стр. М-185.
5. КОУАН Дж., М. Врэник и Г. А. Реншолл. Влияние предшествующей диеты
и голодания на обмен глюкозы у нормальных собак. IMetaboLism
18: 319-330, 1969.
6. ФРЕЙ, E3. M., R. MORDASINI, F. J. FREY, E. WEGMULLER, G.
,SCHLIERF, J. HODLER. Диспротеинемия при полном голодании.
Metabolism 28: 363-369, 1979.
7. GERACI, J. R., AND D. J. ST. Обен. Тканевые источники и диагностика
Значение циркулирующих ферментов у китообразных. J. Fish. Res. Доска Can.
36: 158-163, 1979.
8. HARRISON, R.J., AND G.L. KOOYMAN. Общая физиология ластоногих
.В: Поведение и физиология ластоногих, отредактированный Р. Дж. Харрисоном
. Нью-Йорк: Appleton-Crofts, 1968, стр. 211-296.
9. ХАНТЕР Л. И С. Х. МАДИН. Клинические показатели крови северного морского котика
. J. WiZdZ. Дис. 12: 526-530, 1976.
10. КИТ, Э. О., С. ПЕРНИЯ, Р. КОНДИТ, И К. Л.,
ORTIZ.
Метаболизм
и переработка глюкозы у северных морских слонов.Bienn. Con /
Biol. Март. Млекопитающие, 3-й Сиэтл, Вашингтон, 1979.
11. ЛЕЙН, Р. А. Б., Р. Дж. Х. МОРРИС, И Дж. У. ШИДИ. Гемото-
логическое исследование южного морского слона. Комп. Biochem. Phys-
ioL. A 42: 841-850, 1972.
12. LE BOEUF, B.J. Конкуренция самцов и самцов и репродуктивный успех
морских слонов. Являюсь. 2002. 14: 163-176, 1974.
13. LE BOEUF, B.J., AND K.Т. БРИГГС. Стоимость проживания тюленя в гареме
. Mammalia 41: 167-195, 1977.
14. LE ~ OEUF, B.J., AND R.S. PETERSON. Социальный статус и спаривание
активность слоновьих слонов. Science 163: 91-93, 1969,
15. LE BOEUF, B.J., R.J. WHITING, R.F. GANTT. Perinati
Поведение самок северного морского слона и их детенышей. Be-
haviour 43: 121-156, 1972.
16.МРОСОВСКИЙ Н., И Д. Ф. ШЕРРИ. Анорексия животных. Science
207: 837-842, 1980.
17. НЕЛЬСОН, Р. А., Дж. Д. ДЖОНС, Х. У. ВАНЕР, Д. Б. МАКГИЛЛ, И
К. Ф. КОД. Метаболизм азота у медведей: метаболизм мочевины в
летнем и зимнем сне и роль мочевого пузыря в воде
и сохранение азота. Mayo Clin, Proc. 50: 141-146, 1975.
18. НЕЛЬСОН Р. А., Х. В. ВАНЕР, Дж.Д. ДЖОНС, Р. Д. ЭЛЛЕФСОН, И
П. Э. ЗОЛЬМАН. Метаболизм медведей до, во время и после зимнего сна. Являюсь. J. Physiol. 224: 491-496, 1973.
19. ORTIZ, C. L., II. П. КОСТА, И Б. Ж. ЛЕ БОФ. Вода и энергия
Поток у детенышей морского слона натощак и в естественных условиях.
Physiol. Zool. 51: 166-178, 1978.
20. ПЕРНИЯ, С. Д., А. ХИЛЛ, Э. К. Л, ОРТИЗ. Оборот мочевины при длительном голодании
северного морского слона.Лагерь. Biochem.
Physiol. B 65: 731-734, 1980.
21. PFEIFFER, E. W., L. N. REINKING, AND J. II. ГАМИЛЬТОН. Примерно
эффектов пищевого и водного лишения метаболизма у чернохвостых
луговых собачек, Cynomys ludovicianus. Лагерь. Biochem. Physiol. A
от 1 ноября 2005 г. ajpregu.physiology.orgЗагружено с сайта
Frontiers | Сибирская язва северного оленя в Российской Арктике, 2016: климатические детерминанты вспышки и эффективность вакцинации
Введение
Сибирская язва — это бактериальное заболевание, поражающее людей и других млекопитающих, вызываемое грамположительной спорообразующей палочковидной бактерией Bacillus anthracis .Основной особенностью этого микроорганизма, во многом определяющей его эпидемиологический потенциал и популяционную структуру, является способность образовывать эндоспоры, чрезвычайно устойчивые к неблагоприятным условиям окружающей среды и способные сохранять жизнеспособность в течение длительного времени (1–3). Споры сибирской язвы долго сохраняются в почве и не только выживают, но и становятся частью почвенного биоценоза благодаря сочетанию природных условий. К ним относятся структура естественного почвенного покрова, химические свойства почвы и ее слоев, а также чередование наводнений и засух, которые увеличивают вымывание из почвы, высыхание и распространение спор.Время выживания спор непредсказуемо, что создает благоприятные условия для образования природных очагов (3–5).
Зоонозный потенциал сибирской язвы хорошо известен во всем мире. Овцы, козы, крупный рогатый скот, буйволы, лошади, олени, ослы и другие животные, включая дикие виды, как известно, очень восприимчивы к сибирской язве, в то время как свиньи менее восприимчивы. В естественных условиях заболеванием могут заразиться и грызуны (5). В настоящее время случаи сибирской язвы крайне редки в большинстве европейских стран, но болезнь остается эндемической в России, где она вызывает спорадические случаи у животных и редкие случаи у людей.Эпидемический процесс обычно связан с заражением пастбищного скота пищевым путем, путем проглатывания спор B. anthracis при поедании растений, загрязненных почвой, или при питье из источников воды с высокой концентрацией спор (3, 4, 6, 7). Эпидемиология сибирской язвы характеризуется летне-осенней сезонностью, вызванной выпасом животных на пастбищах, обычно с редкой и сухой травой. В зимне-весенний (стойловый) период заражение связано с употреблением зараженных кормов.
Предпосылками для функционирования биосистемы сибирской язвы являются постоянно высокий уровень загрязнения почвы спорами B. anthracis , свободный выпас скота, а также практика отгонного и полукочевого выпаса животных, что характерно для оленеводства Крайнего Севера России. Россия (3). В России наличие больших территорий, населенных популяциями диких животных и домашнего скота, создает благоприятные условия для вспышек эпидемических заболеваний, а низкая плотность населения на большей части территории страны затрудняет проведение противоэпидемических мероприятий и учет мест захоронения животные, умершие от сибирской язвы правильно.Исторические захоронения сибирской язвы часто не документируются, а иногда трупы не хоронят должным образом. Эти могильники, а также целые территории исторических эпидемий могут быть вовлечены в хозяйственную деятельность, что может привести к новым вспышкам болезней, учитывая заметную сохранность спор в холодном климате.
Особый интерес в этом отношении представляет тундровая зона России, расположенная между 55 и 68 градусами северной широты. Предпоследняя вспышка сибирской язвы в 1941 г. в популяции северных оленей полуострова Ямал привела к гибели 6700 оленей.Последняя вспышка в 2016 г. убила более 2000 оленей и привела к госпитализации 90 местных жителей, а также к гибели одного ребенка (8–10).
В настоящее время в северных регионах России существует опасность возникновения (возрождения) почвенных очагов сибирской язвы из-за затопления пастбищ и населенных пунктов рек Яна, Индигирка, Колыма, а также масштабных земляных работ (добыча алмазов, золото, нефть, газ; другие виды недропользования). Это требует постоянных профилактических мер среди сельскохозяйственных животных независимо от текущего состояния известных очагов сибирской язвы, особенно в условиях, когда изменения климата влияют на среду обитания макро- и микроорганизмов.
Одним из важных компонентов таких профилактических мер является ежегодная вакцинация восприимчивых животных, которая направлена на формирование коллективного иммунитета против болезни у поголовья сельскохозяйственных животных, включая северных оленей. Эффективность активной иммунизации контролируется путем оценки титра антител против сибирской язвы (10–14). В 2007 году вакцинация северных оленей на полуострове Ямал была отменена, что могло привести к увеличению восприимчивости популяции. В ответ на вспышку 2016 г. была возобновлена тотальная вакцинация всех восприимчивых животных.
Цели настоящего исследования заключались в (1) оценке эффективности вакцинации оленей против сибирской язвы, проведенной в ответ на вспышку 2016 г. на полуострове Ямал, (2) для изучения климатических условий летом 2016 г. и их потенциальной роли в этой вспышке. и (3) оценить ожидаемое изменение климата на полуострове Ямал и его потенциальное влияние на риск возобновления сибирской язвы.
Материалы и методы
В соответствии с местным и национальным законодательством для этого исследования не требовалось этической экспертизы, поскольку эта работа не содержит никаких экспериментов на животных.Образцы крови для исследования иммунитета к сибирской язве собирали сертифицированные ветеринары с использованием стандартных процедур, позволяющих избежать страданий животных, и в соответствии с рекомендациями Государственной ветеринарной службы Российской Федерации.
Область исследования
В нашем исследовании оценивалась эпидемическая ситуация с сибирской язвой в Ямало-Ненецком автономном округе (ЯНАО), который входит в 85 регионов Российской Федерации. ЯНАО находится в арктической зоне России, частично на полуострове Ямал.Большая часть его территории находится за Полярным кругом (рис. 1). Площадь составляет 769 250 км, 2 , плотность населения около 0,7 человек / км 2 . Для региона характерны вечная мерзлота, большое количество рек и озер, а также арктический и субарктический климат на большей части территории. Общее поголовье оленей в ЯНАО оценивается более чем в 700 000 голов (15).
Рисунок 1 . Район исследования, вспышки сибирской язвы в 2016 г. и территория мониторинга иммунитета к сибирской язве у северных оленей.
Источники данных и методы
Данные сибирской язвы
Эпидемиологический анализ вспышки сибирской язвы среди северных оленей в ЯНАО в 2016 г. был основан на официальных данных Федеральной службы по ветеринарному и фитосанитарному надзору («Россельхознадзор», https://fsvps.gov.ru/fsvps/iac/rf/operative -messages.html), о которых Россия уведомила МЭБ (https://wahis.oie.int/#/dashboards/country-or-disease-dashboard). Данные содержали информацию о зараженных видах, точном местонахождении вспышек и количестве инфицированных и мертвых животных.Эта информация была представлена в виде шейп-файла для картографирования и пространственного анализа в географической информационной системе (ГИС).
Климатические данные
Метеорологические данные для оценки среднемесячных и максимальных температур воздуха в районе исследований (Тазовский район ЯНАО) за 1987–2016 гг. Взяты с официального сайта Федеральной службы по гидрометеорологии и мониторингу окружающей среды (16) и из Интернет-портал «Архив погоды» (http: // погода-сервис.ru / archive_gsod.php) для стационарной метеостанции Антипаюта (синоптический индекс 23058; географические координаты 69 ° 6′13 ′ ′ N, 76 ° 51′28 ′ ′ E). Мы сравнили среднемесячные и максимальные температуры воздуха в мае, июне, июле и августе 2016 года (2 месяца с зарегистрированными вспышками сибирской язвы и два предыдущих месяца) с соответствующими показателями за весь 30-летний период. Оценка статистической значимости различий температурных диапазонов проводилась с помощью двухвыборочного теста t с неравными дисперсиями.
Ожидаемое будущее изменение климатического режима исследуемой территории было оценено путем сравнения средней годовой температуры воздуха и среднего годового количества дней с температурой воздуха выше 0 ° C для текущего климата и для прогнозируемого климата на период 2081–2100 гг. . Чтобы количественно оценить ожидаемые изменения обоих показателей, мы усреднили рассчитанные различия по всей исследуемой области.
В качестве «текущего» климата использовались показатели, полученные при усреднении суточных наблюдений за температурой воздуха на метеостанциях в Арктической зоне России с 1981–2015 гг. (17), которые были интерполированы с помощью метода кригинга (18–20) с пространственным разрешением 1 км 2 .
Прогнозируемые индикаторы на период 2081–2100 гг. Были рассчитаны с помощью ансамбля из 13 климатических моделей, включенных в международный проект взаимного сравнения связанных моделей 5 (21) в соответствии с экспериментальным сценарием RCP8.5 (22). Сценарий RCP8.5 учитывает высокий уровень воздействия на климат, связанный с парниковыми газами, и предполагает «отсутствие изменений» в текущем поведении людей в отношении антропогенных выбросов в атмосферу. Этот сценарий обеспечивает наиболее статистически значимую реакцию моделей на воздействие климата и может использоваться как «наихудший случай», но все же правдоподобный сценарий изменения климата.
Обработка климатических данных и визуализация результатов выполнялись с помощью программного обеспечения ArcMap 10.8.1, включая расширение Spatial Analyst (Esri, США).
Исследование поствакцинального иммунитета
оленей были иммунизированы в Тазовском районе ЯНАО в сентябре-октябре 2016 г. сухой живой вакциной против сибирской язвы животных из штамма 55-ВНИВВИМ производства Орловского биологического завода (Орел, Россия) согласно инструкции (http : //www.biofabrika.com / catalog.html? cid = 13). Было вакцинировано около 15 000 голов.
Затем ветеринары взялипроб крови у 913 привитых оленей в июле 2017 года в рамках стандартных ветеринарных процедур. Забор крови производился из яремной вены, и образцы собирались в одноразовые стерильные пробирки. Сыворотку крови получали путем осаждения крови с последующим внесением аликвот 1-2 мл сыворотки в пробирки Эппендорфа. Сыворотка крови стабилизирована борной кислотой.
Обнаружение специфических антител к сибирской язве в сыворотке крови животных проводили с помощью тестовой реакции непрямой гемагглютинации (IHA) с помощью диагностического набора на эритроциты сибирской язвы.В связи с отсутствием коммерческих тест-систем в России (14) мы изготовили набор для диагностики антигенных эритроцитов в соответствии с «Временной инструкцией по изготовлению и контролю набора для диагностики антигенных эритроцитов для реакции непрямого теста гемагглютинации (тест-реакция IHA)» ( 1979) »(23). Методика создания набора была получена в Государственном научном учреждении ветеринарной вирусологии и микробиологии Россельхозакадемии, эффективность набора подтверждена аналогичными исследованиями (14, 24, 25).
Тест-реакцию IHA проводили по общепринятой методике (26). Исходную сыворотку крови разводили в соотношении 1:40 физиологическим раствором (принятым в качестве первого разведения сыворотки), после чего делали двойные разведения и анализировали с помощью диагностического набора для эритроцитов. Предварительную регистрацию реакции проводили через 2–3 ч, окончательную — через 18 ч. Результат реакции оценивали визуально по схеме:
++++: эритроциты покрывают все дно лунки ровным слоем; иногда наблюдается «зонтик» с неровными краями;
+++: эритроциты покрывают 3/4 дна лунки, а «зонтик» меньше;
++: «зонт» небольшой, находится в самом центре колодца;
+: в центре небольшого «зонтика» хорошо виден осадок эритроцитов («пуговицы»).
-: реакция отрицательная, эритроциты оседают на дне лунки в виде «пуговицы» или небольшого кольца с ровными, четко очерченными краями.
Результаты реакции считались положительными при обнаружении агглютинации эритроцитарного антигена, начиная с разведения 1:80 и выше на 3–4 скрещивания.
Для оценки доли всей популяции оленей со специфическим иммунитетом тестирование рассматривалось как гипергеометрический процесс, при котором было взято n проб из популяции M с уровнем защиты p , из которых s были положительный (т.е., с обнаруженным защитным титром выше 1:80). Поскольку размер выборки n был намного меньше, чем размер всей генеральной совокупности M , использовалось биномиальное приближение гипергеометрического процесса, а ожидаемый уровень защиты p был рассчитан с использованием бета-распределения: p = Beta ( s + 1; n — s + 1) (27). Расчеты были выполнены с использованием 10 000 симуляций Монте-Карло в надстройке Microsoft Excel @RISK v.4.5 (www.palisade.com).
Результаты
Описательный анализ вспышки сибирской язвы в ЯНАО
Эпидемия сибирской язвы в российской Арктике произошла в июле – августе 2016 г. на трех территориях: в районе озера Писото, в Новопортовской тундре и в районе реки Еваяха. Районы расположены на расстоянии до 250 км друг от друга и включают в себя две водные преграды: Обскую губу (ширина 30–80 км) и устье реки Таз (средняя ширина 25 км). Были определены границы шести очагов (рис. 1), а уязвимая популяция северных оленей оценивалась в 41 001 голов.Из общего количества животных у 2650 (6,46%) животных развились клинические признаки, из которых 2350 умерли (летальность 88,67%). Вспышка характеризовалась вовлечением населения в эпидемический процесс, что проявилось в заражении 36 человек с одним предполагаемым летальным исходом (28).
Анализ официальных отчетов и директив показал, что животные не вакцинировались в регионе происхождения сибирской язвы с 2007 года.
Анализ климатических данных
Анализ среднемесячных и максимальных месячных температур воздуха в весенние и летние месяцы 2016 г. не выявил статистически значимых различий между температурами в мае с соответствующими значениями 1987–2016 гг., А средние температуры июня, июля и августа оказались равными На 16–100% выше в 2016 году (таблица 1).В целом в 2007–2016 гг. Наблюдалось повышение летних температур воздуха, достигнув пиковых значений 15,4, 22,1 и 15,0 ° C в июне, июле и августе 2016 г. соответственно.
Таблица 1 . Результаты сравнения температуры воздуха в мае, июне, июле и августе 2016 г. с соответствующими показателями за 1987–2016 гг. По данным метеостанции Антипаюта.
Моделирование текущих и прогнозируемых климатических индикаторов показало, что при «худшем» сценарии потепления к 2100 году ожидается повышение средней годовой температуры воздуха в пределах исследуемой территории на 8.3 ± 0,5 ° C и будет положительным на большей части территории ЯНАО, а годовое количество дней с температурой воздуха выше 0 ° C может увеличиться на 49 ± 6 дней (рис. 2). Такие климатические изменения могут привести к дальнейшему оттаиванию вечной мерзлоты на всей территории исследования и могут усугубить ситуацию с оттаиванием почвы, содержащей споры сибирской язвы.
Рисунок 2 . Результаты моделирования среднегодовой температуры воздуха (вверху) и количества дней в году с температурой воздуха выше 0 ° C (внизу) на территории Ямало-Ненецкого автономного округа для текущего и прогнозируемого климата (2081 г. –2100) согласно RCP8.5 сценарий.
Оценка эффективности вакцинации
В 2007 году правительство прекратило плановую вакцинацию оленей на полуострове Ямал, который считался свободным от сибирской язвы. Учитывая промежуток времени между последней вакцинацией в 2007 году и вспышкой в 2016 году, вполне вероятно, что подавляющее большинство животных не были вакцинированы до контакта с бактерией сибирской язвы в 2016 году. Такая наивная популяция является благодатной почвой для распространения инфекции. инфекционный агент, поскольку все или большинство животных не имели иммунитета к сибирской язве.
Сила иммунитета против сибирской язвы после возобновления вакцинации в 2016 году была определена по результатам анализа сыворотки крови IHA (Рисунок 3). Скрининг 913 образцов сыворотки крови северного оленя на антитела к сибирской язве с помощью этого анализа показал, что 1,97% образцов (18 голов) не содержали антител к сибирской язве. В 8,87% проб (81 голова) антитела к сибирской язве были обнаружены с титром 1:80, что ниже защитного уровня. В 89,16% проб (814 голов) уровень специфических антител через 9 месяцев после вакцинации был ≥1: 80, из них 9.0% образцов (82 головы) имели титр сывороточных антител против сибирской язвы ≥1: 640. Полученные данные свидетельствуют о создании иммунной доли у 89% (доверительный интервал 95%: 87–91%) популяции северных оленей Тазовского района ЯНАО.
Рисунок 3 . Результаты анализа образцов сыворотки крови в пробе непрямой гемагглютинации.
Обсуждение
В этом исследовании мы оценили эффективность вакцинации северных оленей против сибирской язвы, проведенной в ответ на вспышку 2016 г. на полуострове Ямал, изучили влияние климатических условий летом 2016 г. на эту вспышку и оценили ожидаемое изменение климата в этот регион и его потенциальное влияние на риск повторного появления сибирской язвы.Мы обнаружили, что вакцинация дала уровень защиты 89% всей популяции северных оленей. Кроме того, аномально высокая температура окружающей среды летом 2016 г. способствовала таянию вечной мерзлоты и реактивации почвенных резервуаров B. anthracis . Используя прогнозируемые климатические данные на 2081–2100 годы в соответствии со сценарием «худшего случая» RCP8.5, мы продемонстрировали, что ожидаемое изменение климата создаст условия для реактивации резервуаров почвенной сибирской язвы.
Профилактика сибирской язвы на основе вакцинации во многих развитых странах привела к снижению количества зарегистрированных случаев заболевания (29–36).Однако риск заражения сибирской язвой остается высоким в странах Африки к югу от Сахары, Юго-Восточной Азии, а также в некоторых регионах России и странах бывшего Советского Союза (37–40). Серологическое тестирование необходимо для определения эффективности программ вакцинации и получения эпидемиологической информации в районах, эндемичных по сибирской язве. В России эффективность вакцинации оленей против сибирской язвы ранее не оценивалась; поэтому данных об уровнях антител у северных оленей в 2007–2017 гг. нет. Насколько нам известно, данное исследование является первым в данной области, посвященным изучению этого явления конкретно на оленях.Однако данные исследований эффективности вакцинации против сибирской язвы у сельскохозяйственных животных продемонстрировали высокие уровни антител у коров и овец в течение примерно 1,5 лет (41). Это говорит о том, что во время вспышки 2016 г. у северных оленей не могло быть иммунитета. В этом исследовании мы продемонстрировали полезность вакцинации против сибирской язвы, проверив стада оленей в Тазовском районе ЯНАО на антитела к сибирской язве с помощью ИНА. В 89,16% образцов уровень специфических антител к 9 месяцам после вакцинации был ≥1: 80, из них 9.0% образцов имели титр сывороточных антител против сибирской язвы ≥1: 640. Это свидетельствует об установлении иммунитета у 89% оленей. С 2016 г. новых вспышек сибирской язвы в ЯНАО не наблюдалось. Исходя из концепции коллективного иммунитета, количество иммунных особей в популяции, необходимое для предотвращения распространения инфекции, должно быть не менее 1 — 1 / R 0 , где R 0 — базовый репродуктивный коэффициент заболевания (42). Принятие значения R 0 для сибирской язвы как 1.251–1.292 согласно предыдущим исследованиям (43, 44), мы получили минимальный порог коллективного иммунитета 20–23%. Таким образом, уровень иммунитета, достигнутый в результате вакцинации, можно считать достаточным для предотвращения распространения сибирской язвы в популяции северных оленей. Отсутствие или низкий уровень антител к сибирской язве у части населения может указывать на невыполнение вакцинации против сибирской язвы или нарушение правил вакцинации (вакцинация беременных, ослабленных и истощенных животных и т. Д.), Либо это может быть связано с характеристиками некоторых частные лица.
В настоящее время изменение климата более выражено в российской Арктике, чем в любой другой части страны. В этом регионе наблюдаются самые быстрые темпы экологических изменений на Земле, включая уменьшение площади морского льда, таяние ледников и ледяных щитов, удлинение вегетационного периода, таяние вечной мерзлоты и усиление гидрологического цикла. Среднегодовая температура воздуха на Русском Севере повысилась на 1,28 ° C с 1905 по 2000 год (40). Глобальная температура поверхности Земли, нагретой на 0.89 ° C с 1901 по 2012 г. (45). Вечная мерзлота — это любой грунт, который остается полностью замерзшим при температуре ниже 0 ° C не менее 2 лет подряд (46). Вечная мерзлота может достигать глубины основания более 1000 м и оставаться замерзшей в течение тысяч лет.
В условиях вечной мерзлоты микроорганизмы хорошо сохраняются, а вечная мерзлота действует как аккумулятор микробиоты. Сохранность спор B. anthracis в условиях вечной мерзлоты не вызывает сомнений (10). Температура вечной мерзлоты повысилась на 0,29 ± 0.12 ° C во всем мире после повышения температуры воздуха в Арктике (47). Таким образом, вечная мерзлота в российской Арктике превратилась в резервуар сибирской язвы, способный сохранять жизнеспособные споры в течение длительного времени. Высокая температура воздуха в исследуемом регионе могла привести к таянию вечной мерзлоты и открытию почвенных резервуаров сибирской язвы, а также к увеличению числа кровососущих насекомых, которые могут быть переносчиками возбудителя сибирской язвы (10, 48). Следовательно, глобальное потепление в Арктике может стать одним из факторов риска возникновения и распространения сибирской язвы из-за таяния вечной мерзлоты (49, 50).В изменившихся климатических и почвенно-гидрологических условиях эти споры могли появиться на поверхности почвы и, как следствие, инфицировать животных. Проведенное моделирование показало, что при неблагоприятном сценарии изменения климата среднегодовая температура воздуха на территории ЯНАО превысит 0 ° C, что создаст условия для широкомасштабного таяния вечной мерзлоты.
Вторым фактором риска эпидемии сибирской язвы является прекращение вакцинации. Ямальская тундра — крупнейший центр оленеводства в Арктике; Например, в 2015 г. в Ямальском районе ЯНАО выпасалось 254 тыс. голов оленей (51).Таким образом, эпидемические и экономические риски в этом регионе очень высоки. Ретроспективный анализ климатических данных и моделирование показали эффективность профилактики сибирской язвы путем ежегодной вакцинации северных оленей.
Для оценки степени охвата популяции животных и эффективности вакцинации необходимо проводить серологический мониторинг, включая использование диагностического набора IHA для выявления антигенов эритроцитарной сибирской язвы.
Выводы
Это исследование показало, что к факторам, вызвавшим эпидемию сибирской язвы в 2016 г. в российской Арктике, могут относиться повышение летних температур воздуха, таяние вечной мерзлоты, вызванное изменением климата, и прекращение вакцинации оленей против сибирской язвы.Это привело к созданию цепочки эпидемий сибирской язвы. Более того, ожидаемое изменение климата по самому неблагоприятному сценарию может способствовать заметному потеплению на территории ЯНАО, создавая условия для повсеместного таяния вечной мерзлоты и реактивации очагов сибирской язвы в почве. Выявленный в нашем исследовании уровень поствакцинального иммунитета у северных оленей можно считать достаточным для предотвращения вспышек сибирской язвы, в том числе в условиях таяния вечной мерзлоты в российской Арктике. В период 2017–2020 годов на полуострове Ямал не было зарегистрировано новых вспышек сибирской язвы, что можно отнести к традиционной практике ежегодной вакцинации против сибирской язвы.Более того, разработанная здесь IHA является эффективным инструментом, который будет полезен для мониторинга эффективности вакцинации северных оленей в контексте возрастающего эпидемического риска сибирской язвы в Арктике.
Заявление о доступности данных
Данные, проанализированные в этом исследовании, подлежат следующим лицензиям / ограничениям: Наборы данных климатических переменных, а также данные образцов крови оленей не могут быть общедоступными из-за конфиденциальности. Их можно получить по разумному запросу у соответствующих авторов.Запросы на доступ к этим наборам данных следует направлять Елене Александровне Лисковой, [email protected].
Взносы авторов
EL, AB и FK: концептуализация, проверка и формальный анализ. IE, EL, AB, GS и SM: методология. ФК и ОЗ: программное обеспечение. IR, OZ и NT: расследование. NG, OB и GS: ресурсы. EL и AB: курирование и контроль данных. EL, IR, OZ и AB: написание — подготовка первоначального черновика. EL, YS, FK и AB: написание — просмотр и редактирование. ОЗ и ФК: визуализация. IE и II: управление проектом.Все авторы прочитали и согласны с опубликованной версией рукописи.
Финансирование
Работа поддержана Федеральным исследовательским центром вирусологии и микробиологии (FRCVM) по государственному заказу.
Конфликт интересов
Авторы заявляют, что исследование проводилось при отсутствии каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Сноски
Список литературы
1.Гомес Дж. П., Некорчук Д. М., Мао Л., Райан С. Дж., Пончиано Дж. М., Блэкберн Дж. Разделение экологических эффектов и динамики популяции хозяев для сибирской язвы, классической болезни, вызываемой резервуаром. PLoS ONE. (2018) 13: e0208621. DOI: 10.1371 / journal.pone.0208621
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Ровид Спиклер А. Сибирская язва . (2003). Доступно на сайте: www.cfsph.iastate.edu (по состоянию на 1 октября 2020 г.).
4. Диксон Т.С., Мезельсон М., Гийемин Дж., Ханна П.С.Сибирская язва. N Engl J Med. (1999) 341: 815–26. DOI: 10.1056 / NEJM1993411107
CrossRef Полный текст | Google Scholar
7. Еременко Е.И., Рязанова А.Г., Буравцева Н.П. Текущая ситуация по сибирской язве в России и в мире основные тенденции и особенности. Probl Деталь Опасно Заражение. (2017) 1: 65–71. DOI: 10.21055 / 0370-1069-2017-1-65-71
CrossRef Полный текст
10. Тимофеев В., Бахтеева И., Миронова Р., Титарева Г., Лев И., Кристиани Д. и др.Выводы по штамму Bacillus anthracis , выделенному из вечной мерзлоты в тундровой зоне России. PLoS ONE. (2019) 14: e0209140. DOI: 10.1371 / journal.pone.0209140
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11. Петерсон MJ, Дэвис Д.С., Темплтон JW. Иммуноферментный анализ для выявления антител к сибирской язве у белохвостого оленя (Odocoileus virginianus): оценка вакцинации против сибирской язвы и сыворотки оленей, находящихся на свободном выгуле. J Wildl Dis. (1993) 29: 130–5. DOI: 10.7589 / 0090-3558-29.1.130
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Казановский ЭС. Ветеринарные проблемы северного оленеводства и совершенствование технологии проведения массовых лечебно-профилактических мероприятий. Сельское хозяйство Евро-Северо-Восток. (2017) 59: 44–8. DOI: 10.30766 / 2072-9081.2017.59.4.44-48
CrossRef Полный текст | Google Scholar
13. Барков А.М., Баркова И.А., Алексеев В.В., Липницкий А.В., Кулаков М.Ю.Обнаружение антител к защитному антигену бациллы сибирской язвы с использованием теста непрямой гемагглютинации и иммуноферментного анализа. Probl Деталь Опасно Заражение. (2010) 52: 42–5. DOI: 10.21055 / 0370-1069-2010-3 (105) -42-45
CrossRef Полный текст
14. Васина Н.К., Сельянинов Ю.О., Егорова И.Ю. Серологический мониторинг эффективности специфической профилактики сибирской язвы в Cfd Rf . (2012). Доступно в Интернете по адресу: https://booksc.org/book/36540006/ee6fa4 (по состоянию на 7 октября 2020 г.)
15.Южаков А.А. Северное оленеводство в XXI веке: генетические ресурсы, культурное наследие и бизнес. Arct Ecol Econ. (2017) 4: 131. DOI: 10.25283 / 2223-4594-2017-2-131-137
CrossRef Полный текст
18. Оливер MA. Кригинг: метод интерполяции для географических информационных систем. Int J Geographic Inform Syst. (1990) 4: 313–32. DOI: 10.1080 / 026937941549
CrossRef Полный текст | Google Scholar
19.Оливер М.А. Вариограмма и кригинг. В: Фишер М.М., Венский бизнес-университет экономики и геофизических наук, редакторы. Справочник по прикладному пространственному анализу . Берлин; Гейдельберг: Springer (2010). п. 319–52. DOI: 10.1007 / 978-3-642-03647-7_17
CrossRef Полный текст | Google Scholar
20. Хофстра Н., Хейлок М., Джонс М.Н.П., Фрей К. Сравнение шести методов интерполяции ежедневных европейских климатических данных. J Geophys Res Atmos. (2008) 113: D21110. DOI: 10.1029 / 2008JD010100
CrossRef Полный текст | Google Scholar
21. Тейлор К.Е., Стоуфер Р.Дж., Мил Г.А. Обзор CMIP5 и план эксперимента. Bull Am Meteorol Soc. (2012) 93: 485–98. DOI: 10.1175 / BAMS-D-11-00094.1
CrossRef Полный текст | Google Scholar
23. Временные инструкции по производству и контролю сибирской язвы для диагностики сухих антигенных эритроцитов для определения стадии реакции непрямой гемагглютинации (RNGA). ВНИИВВиМ (Покров).Покрова (1979). Протокол № 16 от 19 сентября 1979 г.
24. Бакулов И.А., Гаврилов В.А., Селиверстов В.В. Сибирская язва. Новые страницы в изучении «старой болезни». Посад . Владимир (2001).
25. Иванова С.В., Мельникова Л.А., Родионов А.П., Макаев ХН. Использование диагностики эритроцитов в оценке эффективности иммунопрофилактики крупного рогатого скота против сибирской язвы. Ветеринария. (2019) 11: 25–8. DOI: 10.30896 / 0042-4846.2019.22.11.25-29
CrossRef Полный текст
26.Биргер МО. Справочник по микробиологическим и вирусологическим методам исследования . Москва: Медицина Москва. (1982). 133–135.
27. Восе Д. Анализ рисков — количественное руководство . Чичестер: Джон Вили и сыновья (2008). п. 729.
Google Scholar
28. Рязанова А.Г., Семенова О.В., Еременко Е.И., Аксенова Л.Ю., Буравцева Н.П., Головинская Т.М. и др. Эпидемиологическая и эпизоотологическая ситуация по сибирской язве в 2017 году, прогноз на 2018 год. Probl Part Danger Infect. (2018) 1: 63–5. DOI: 10.21055 / 0370-1069-2018-1-63-65
CrossRef Полный текст
29. Карлсон CJ, Getz WM, Kausrud KL, Cizauskas CA, Blackburn JK, Bustos Carrillo FA, et al. Споры и почва с шести сторон: междисциплинарность и экологическая биология сибирской язвы ( Bacillus anthracis ). Biol Rev. (2018) 93: 1813–31. DOI: 10.1111 / brv.12420
PubMed Аннотация | CrossRef Полный текст | Google Scholar
30. Кросс А.Р., Болдуин В.М., Рой С., Эссекс-Лопрести А.Е., Прайор Дж. Л., Хармер, штат Нью-Джерси.Зоонозы под носом. Microbes Infect. (2019) 21: 10–19. DOI: 10.1016 / j.micinf.2018.06.001
CrossRef Полный текст | Google Scholar
31. Dragon DC, Bader DE, Mitchell J, Woolen N. Естественное распространение спор Bacillus anthracis в Северной Канаде. Appl Environ Microbiol. (2005) 71: 1610–5. DOI: 10.1128 / AEM.71.3.1610-1615.2005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
32. Гейтс СС, Элкин Б.Т., Дракон, округ Колумбия.Изучение, контроль и эпизоотология сибирской язвы в географически изолированной свободно бродящей популяции бизонов на севере Канады. Can J Vet Res. (1995) 59: 256–264.
PubMed Аннотация | Google Scholar
33. Леверин С.С., Эльвандер М., Вестермарк Т., Хартцелл Л.Н., Норстрём А.К., Эрс С. и др. Вспышка сибирской язвы в шведском стаде мясного скота — первый случай за 27 лет: отчет о случае. Acta Vet Scand. (2010) 52: 7. DOI: 10.1186 / 1751-0147-52-7
PubMed Аннотация | CrossRef Полный текст | Google Scholar
37.Fasanella A, Garofolo G, Galante D, Quaranta V, Palazzo L, Lista F и др. Тяжелые вспышки сибирской язвы в Италии в 2004 году: рассмотрение факторов, влияющих на распространение инфекции. New Microbiol. (2010) 33: 83–86.
PubMed Аннотация | Google Scholar
38. Касрадзе А., Эчеверрия Д., Захашвили К., Баутиста С., Хейер Н., Имнадзе П. и др. Частота и факторы риска кожной сибирской язвы человека в Грузии: данные национального эпиднадзора, 2008–2015 гг. PLoS ONE. (2018) 13: e0192031. DOI: 10.1371 / journal.pone.0192031
PubMed Аннотация | CrossRef Полный текст | Google Scholar
39. Кракалик И., Абдуллаев Р., Асадов К., Исмаилова Р., Багирова М., Устун Н. и др. Изменение характера распространения сибирской язвы в Азербайджане в постсоветскую эпоху и в эпоху превентивной вакцинации домашнего скота. PLoS Negl Trop Dis. (2014) 8: e2985. DOI: 10.1371 / journal.pntd.0002985
PubMed Аннотация | CrossRef Полный текст | Google Scholar
41.Ипатенко Н.Г., Гаврилов В.А., Маничев А.А. Опыт профилактики сибирской язвы у животных в России. Ветеринария . (1995) 5: 27–30.
42. Anderson RM, May RM. Инфекционные болезни человека: динамика и контроль . Оксфорд: Издательство Оксфордского университета (1992). 757. с.
Google Scholar
44. Саад-Рой С.М., ван ден Дрише П., Якубу А.А. Математическая модель передачи сибирской язвы в популяциях животных. Bull Math Biol. (2017) 79: 303–24.DOI: 10.1007 / s11538-016-0238-1
PubMed Аннотация | CrossRef Полный текст | Google Scholar
45. Zhou Z, Shi H, Fu Q, Li T, Gan TY, Liu S, et al. Становится ли холодный регион на северо-востоке Китая все еще теплее под воздействием изменения климата? Atmos Res. (2020) 237: 104864. DOI: 10.1016 / j.atmosres.2020.104864
CrossRef Полный текст | Google Scholar
46. Олива М., Фриц М. Деградация вечной мерзлоты на более теплой Земле: проблемы и перспективы. Curr Opin Environ Sci Heal. (2018) 5: 14–18. DOI: 10.1016 / j.coesh.2018.03.007
CrossRef Полный текст | Google Scholar
47. Бискаборн Б.К., Смит С.Л., Ноецли Дж., Маттес Х., Виейра Г., Стрелецкий Д.А. и др. Вечная мерзлота нагревается в глобальном масштабе. Nat Commun. (2019) 10: 264. DOI: 10.1038 / s41467-018-08240-4
CrossRef Полный текст
48. Турелл М.Дж., Кнудсон Г.Б. механическая передача Bacillus anthracis устойчивыми мухами (Stomoxys calcitrans) и комарами (Aedes aegypti и Aedes taeniorhynchus). Заражение иммунной . (1987) 55: 1859–61. DOI: 10.1128 / IAI.55.8.1859-1861.1987
PubMed Аннотация | CrossRef Полный текст | Google Scholar
49. Парк Х, Шерстюков А.Б., Федоров А.Н., Поляков И.В., Уолш Дж. Э. Оценка влияния температуры воздуха и высоты снежного покрова на температуру почвы в России на основе наблюдений. Environ Res Lett. (2014) 9: 064026. DOI: 10.1088 / 1748-9326 / 9/6/064026
CrossRef Полный текст | Google Scholar
51.Богданов В., Головатин М. Сибирская язва на Ямале: экологический взгляд на традиционное оленеводство. Экология. (2017) 2: 1–6. DOI: 10.1134 / S1067413617020059
CrossRef Полный текст | Google Scholar
Amazon.com: Гематитовые кольца для культурных товаров Луоса — широкополосные, плоские и закругленные, аксессуары для пальцев, полированная отделка, удобная посадка, различные размеры, толщина 6 мм, 20 в упаковке: все остальное
Красиво, именно то, что я искал. Я читал много обзоров о том, что «эти гематитовые кольца не магнатизированы», поэтому я добавляю краткую историю, полученную из (онлайн-таблицы происхождения минералов) […]: Формула: Fe2O3Система: Тригональная Цвет: От стального серого до черного в … Блеск: Металлический, Субметаллический, Тусклый, Землистый Твердость: 5 — 6 Член группы: Гематит Имя: Первоначально назван Феофрастом около 300-325 гг. До н.э. греческое «αιματίτις λίθος» («aematitis lithos») означает «кровавый камень». Возможно, это первый минерал, когда-либо названный с суффиксом «-ит». В 79 г. Плиний Старший перевел гематит, «кровоподобный», имея в виду ярко-красный цвет порошка. Современная форма, разработанная авторами, часто упрощает написание, исключая «а», в некоторой степени параллельно с другими словами, изначально использующими корень «haeme».Диморф: Маггемит
Группа гематита. Железный аналог корунда, эсколаита и карелианита.
Гематит довольно разнообразен по внешнему виду — он может быть красновато-коричневыми, охристыми массами, темно-серебристо-серыми чешуйчатыми массами, кристаллами от серебристо-серого до черного и темно-серыми массами, и это лишь некоторые из них. Их всех объединяет ржаво-красная полоса.
Черные кристаллы можно спутать с ильменитом.
ПРИМЕЧАНИЕ. «Гематит», используемый в ювелирных изделиях и часто продаваемый как намагниченные предметы, не имеет ничего подобного и является искусственно созданным материалом, см. Магнитный гематит.
В экспериментальной конденсации вулканического газа, проведенной Africano et al. (2002) он осаждался в условиях высокого fO2 во время охлаждения от ок. От 800oC до прибл. 650oC.
Итак, как многие могут прочесть, если вы не хотите «гематит», который намагничен, вам следует выбрать «имитированный» гематит, поскольку НАСТОЯЩИЙ гематит не магнатизирован.
Мой заказ был отправлен исключительно быстро, ни одно из колец не было сломано, в упаковке было много разных размеров, и все они были правильного размера 6 мм, как было указано в рекламе.Я не получил НИКАКОЙ компенсации за этот обзор, поэтому мой обзор, включая минеральный состав гематита, полностью объективен.
Сквозь темный континент — Зритель — Mировая цифровая библиотека
Режим «Чтение» разработан так, чтобы быть максимально быстрым.
Режим «Масштаб» позволяет просматривать наиболее подробные сведения.
Режим «Сетка» отображает сразу несколько страниц для быстрой навигации
Навигация с помощью клавиатуры
| Перейти на следующую страницу | Page Down , пробел , j |
|---|---|
| Перейти на предыдущую страницу | Page Up , сдвиг + пробел , к |
| Повернуть влево | alt + стрелка влево |
| Повернуть вправо | alt + стрелка вправо |
| Перейти к представлению сетки | г |
| Увеличить текущую страницу | z |
| Войти в полноэкранный режим | из |
| Показать справку | ? |
Сенсорное управление
| Перейти на следующую страницу | Проведите по экрану вправо Коснитесь правого края экрана |
|---|---|
| Перейти на предыдущую страницу | Проведите по экрану влево Коснитесь левого края экрана |
| Перейти к представлению сетки | Нажмите «Сетка» |
| Увеличить текущую страницу | Нажмите «Масштаб» |
Кровотечение из верхних отделов желудочно-кишечного тракта: что должны знать медики
Это долгий путь от рта до ануса, и во время путешествия требуется много времени, чтобы извлечь питательные вещества, необходимые для выживания, и избавиться от непитательных остатков.Очевидно, что эта система требует обширного кровоснабжения для выполнения своей миссии, но иногда этот кровоток отклоняется.
Краткая анатомия
Желудочно-кишечная система в основном представляет собой одну длинную трубку с отверстиями на каждом конце, с переменным внутренним диаметром трубки в зависимости от функции. Система следует несколько извилистой траектории, поэтому большая ее часть может находиться в брюшной полости.Трубка разделена на верхний и нижний желудочно-кишечный тракт (ЖКТ). Точка разделения находится в связке Treitz, связке из мышечной и соединительной ткани, которая прикрепляет последний отдел двенадцатиперстной кишки к диафрагме. 1 Все, что к северу от связки, является верхним отделом желудочно-кишечного тракта: двенадцатиперстная кишка, желудок, пищевод и рот. Все, что к югу от связки — это нижний отдел желудочно-кишечного тракта: остальная часть тонкой кишки (тощая кишка, подвздошная кишка), слепая кишка, толстая и прямая кишка. Верхние отделы желудочно-кишечного тракта в значительной степени отвечают за потребление и пищеварение, а нижние отделы желудочно-кишечного тракта — за абсорбцию и выведение.
УГИБ
Кровотечение из верхних отделов желудочно-кишечного тракта делится на варикозные и не варикозные источники. Варикозное кровотечение возникает из расширенных и чрезмерно растянутых вен (варикозно расширенных вен) в пищеводе и желудке, что может вызвать чрезмерное натяжение стенки сосуда и потенциально разорвать вену и кровоточить. Повышенное давление в этих венах связано с портальной гипертензией. Система воротной вены перемещает богатую питательными веществами кровь из желудочно-кишечного тракта в печень для обработки. 2 Если печень повреждена чрезмерным употреблением алкоголя или таким заболеванием, как гепатит, возникает рубцевание, которое может вызвать цирроз печени. Это приводит к сужению печеночных вен и увеличению обратного давления в портальной системе, что вызывает портальную гипертензию, которая расширяет вены пищевода и желудка, что может привести к разрыву и кровотечению. 3
Больная печень может представлять вторую угрозу для жизни, вырабатывая недостаточное количество факторов свертывания крови, что препятствует образованию тромбов.Этим пациентам может потребоваться замена факторов свертывания крови путем переливания цельной крови или вливания свежезамороженной плазмы при использовании упакованных эритроцитов. Кроме того, чрезмерное употребление алкоголя может привести к аномальному снижению количества тромбоцитов и добавить третью угрозу жизни в результате кровотечения.
НВУГИБ
Неварикозное кровотечение из верхних отделов желудочно-кишечного тракта или НВУГИБ чаще всего возникает из-за язвы желудка, которая часто вызвана инфекцией бактериями H.Pylori или чрезмерное употребление нестероидных противовоспалительных препаратов, НПВП, таких как аспирин, ибупрофен, напроксен и т. Д. Менее распространенными причинами НВУГИБ являются язвы пищевода, слезы Мэллори-Вейсса, которые возникают вокруг желудочно-пищеводного перехода из-за сильной рвоты, эрозии желудка или пищевода в результате чрезмерного употребления алкоголя или НПВП. 4
Догоспитальная помощь
Лечение кровотечения из UGI в полевых условиях такое же, как лечение любого внутреннего кровотечения или внешнего кровотечения, которое невозможно контролировать с помощью давления, гемостатических повязок / прокладок / марли или жгута.Лечение включает: своевременную транспортировку, дополнительный кислород, разумную инфузионную терапию и частую переоценку. Если вы можете дать противорвотное средство, то уменьшение рвоты может предотвратить разрушение образовавшихся сгустков.
Первичная медицинская помощь в учреждении
Принимающее учреждение повторно осмотрит пациента на предмет признаков и симптомов недостаточной перфузии и определит, требуется ли переливание крови. Введение назогастрального зонда или зонда NG обеспечит визуальное представление кровотечения.Ярко-красный аспират (или рвота) из пробирки NG из НВУГИБ или темный венозный аспират (или рвота) из варикозного кровотечения указывает на недавнее кровотечение. Если всасывающая канистра для трубки NG продолжает заполняться кровью любого оттенка, значит, идет активное кровотечение. Если аспират из трубки (или рвота) выглядит как кофейная гуща, значит, кровотечение произошло в недавнем прошлом и оно частично переварено.
Иногда у пациентов с UGIB может наблюдаться обильное ректальное кровотечение из-за обильного кровотечения UGI, которое слишком быстро выталкивает кровь через кишечник, чтобы ее разложить или смешать с калом.К счастью, это случается нечасто. Большинство случаев ректального кровотечения легкие и вызваны не опасными для жизни проблемами, такими как геморрой. Мелена — это черный, дегтеобразный, липкий, вонючий стул, который образуется, когда кровь движется с нормальной скоростью по кишечнику, позволяя крови перевариваться и хорошо перемешиваться со стулом до попадания в конец линии. Но все черное — это не кровь. Проглатывание железа, висмута или черной лакрицы может вызвать черный стул, хотя он не такой стойкий и пахучий, как его кузина мелена.
У пациентов с подозрением на НВУГИБ использование ингибиторов протонной помпы (ИПП), таких как омепразол, пантопразол или лансопразол, может помочь замедлить кровотечение за счет уменьшения продукции кислоты в желудке и повреждения кислотой открытых кровеносных сосудов. 4 ИПП могут также препятствовать тому, чтобы избыток кислоты разрушал тромбы, уже образовавшиеся в желудке. 5
У пациента с подозрением на кровотечение из варикозно расширенных вен часто наблюдаются признаки и симптомы, связанные с тяжелым поражением печени, такие как асцит, отек, желтуха и синяки.Октреотид, коммерческая форма гормона соматостатина, вводится внутривенно для сужения артериального кровоснабжения желудочно-кишечного тракта. Это уменьшает венозный кровоток в портальной системе, что снижает обратное давление в варикозно расширенных венах желудочно-кишечного тракта, что снижает вероятность кровотечения. 3 Неясно, эффективен ли октреотид при НВУГИБ, но если источник кровотечения неизвестен, начальный поставщик медицинских услуг может предпочесть введение октреотида после ИПП.
Специализированная помощь
В конечном итоге пациентам с кровотечением из UGI потребуется помощь гастроэнтеролога, а иногда и хирурга. Гастроэнтерологи используют эзофагогастродуоденоскопию (EGD) для осмотра тракта UGI. Это достигается с помощью длинной гибкой оптоволоконной трубки диаметром с ваш мизинец, которая подсоединяется к видеокамере и обеспечивает прямую визуализацию пищевода, желудка и первой части двенадцатиперстной кишки.Очевидно, что способность визуализировать верхние отделы желудочно-кишечного тракта обычно ставит диагноз. Если отмечается активный кровоток, можно предпринять различные терапевтические воздействия на источник кровотечения с помощью прицела EGD. Через дополнительные каналы, встроенные в трубку EGD, можно вводить различные устройства, чтобы достичь пищевода, желудка и двенадцатиперстной кишки. Деловая сторона этих инструментов с длинной ручкой может обеспечить прижигание мест кровотечения или возможность перевязать или перерезать кровоточащие сосуды, или ввести в области кровотечения вазоконстрикторы, такие как адреналин или вазопрессин, или ввести склерозирующие агенты (раздражители) в варикозные узлы, чтобы вызвать свертывание крови. и рубцы, чтобы закрыть утечку.
Операция по контролю UGIB требуется нечасто и обычно требуется только после того, как вмешательства EGD не могут остановить кровотечение.
Сводка
У пациентов с кровотечением из мочевого тракта следует начать транспортировку на ранней стадии и, если пациенту необходимо лежать на спине, принять положение на боку, чтобы снизить риск аспирации.Убедитесь, что у вас есть халат, маска и защитная маска для лица, так как таких пациентов может рвать, а в задней части машины скорой помощи они могут быть направлены в вашу сторону. Получите внутривенный или внутрикостной доступ в пути и поддерживайте систолическое артериальное давление в диапазоне 80-90 мм рт.ст., чтобы поддерживать жизненно важные органы в живых без увеличения кровопотери. И заранее уведомить принимающую организацию — предупрежден, значит вооружен.
Каталожные номера:
1.Серый H, Льюис WH. Анатомия человеческого тела Грея . 20-е изд. Нью-Йорк, Нью-Йорк: Бартлби; 2000
2. Витмер Л.М. Клиническая анатомия портальной системы в контексте портальной гипертензии. Доступно по адресу http://www.oucom.ohiou.edu/dbms-witmer/downloads/portal.pdf. Доступ 23 сентября 2011 г.
3. Гарсиа-Цао Г., Саньял А.Дж., Грейс Н.Д., Кэри В. Профилактика и лечение варикозно-расширенных вен пищевода и варикозного расширения вен при циррозе. Гепатология 2007; 46 (3): 922-937.
4. Каппелл М.С., Фридель Д. Начальное лечение острого кровотечения из верхних отделов желудочно-кишечного тракта: от первоначальной оценки до эндоскопии. Med Clin N Am 2008; 92: 491-509
5. Грин Ф. В., Каплан М. М., Кертис Л. Е., Левин PH. Влияние кислоты и пепсина на свертывание крови и агрегацию тромбоцитов. Возможный фактор длительного гастродуоденального кровотечения слизистой оболочки. Гастроэнтерология . 1978; 74 (1): 38-43


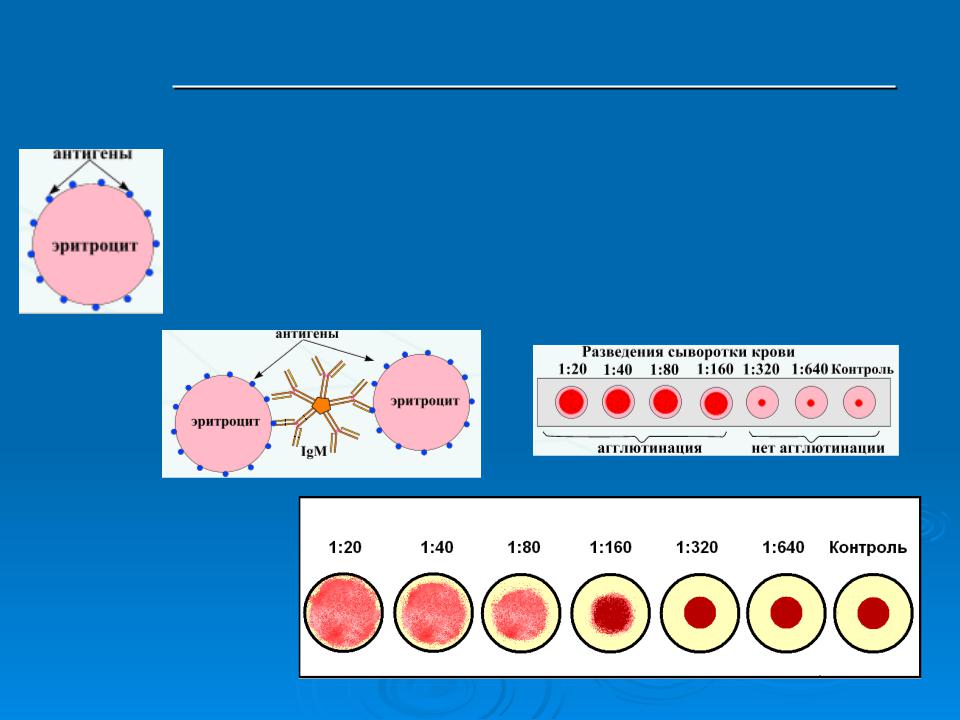

 Сюда относятся исследования биоматериала на простейшие и яйца глистов.
Сюда относятся исследования биоматериала на простейшие и яйца глистов.
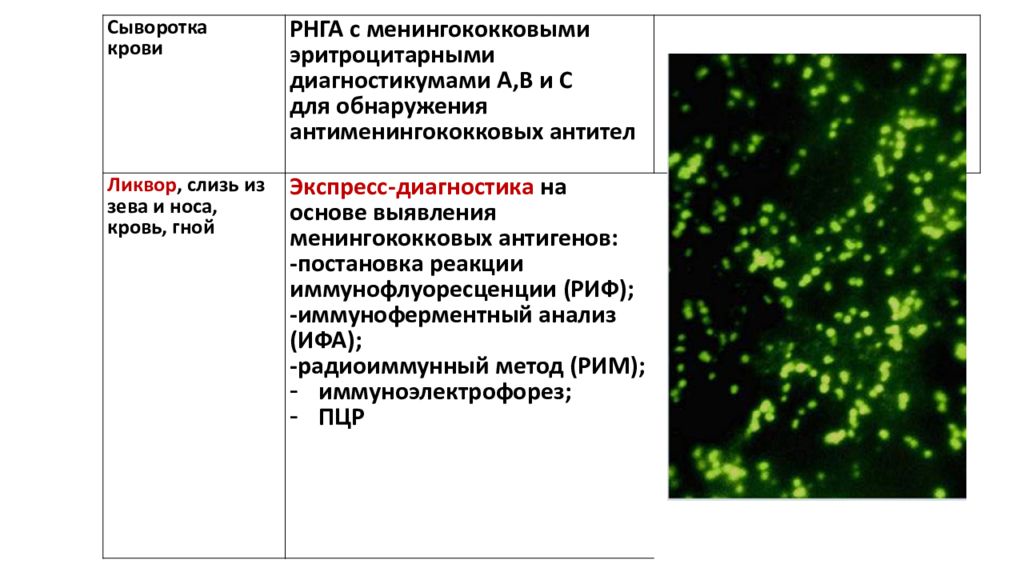 У детей более старшего возраста могут быть жар, боль и жжение при мочеиспускании, сильное желание в туалет и боль в нижней части живота.
У детей более старшего возраста могут быть жар, боль и жжение при мочеиспускании, сильное желание в туалет и боль в нижней части живота.