Корь: 8 мифов о вакцинации, которые способствуют нарастанию заболеваемости
Автор фото, Getty Images
Підпис до фото,Отказ от прививки — основная причина роста заболеваемости корью
Последние вспышки кори в США, на Филиппинах, а также в Украине, объясняются тем, что все больше людей отказываются от прививки, заявляют специалисты в сфере здравоохранения.
Последними о вспышке кори объявили Филиппины. 7 февраля руководство местных органов здравоохранения сообщило, что в этом году количество случаев заболевания возросло на 74% по сравнению с 2018 годом.
По данным ВОЗ, в 2017 году это высокозаразное вирусное заболевание унесло жизни 111 тысяч человек по всему миру.
В своем последнем отчете, датированным ноябрем 2018 года, ВОЗ называет главные причины вспышки кори: халатность и распространение ложных новостей о вакцинах, а также неэффективность систем здравоохранения в отдельных государствах. Сообщается, что в 2016-2017 гг. число заболевших корью по всему миру выросло на 30%.
Сообщается, что в 2016-2017 гг. число заболевших корью по всему миру выросло на 30%.
По оценке ВОЗ, наибольшие вспышки заболеваемости корью произошли в пяти из шести регионов. В том числе, в Северной и Южной Америке, Европе и Восточном Средиземноморье.
Разбираем популярные заблуждения о вакцинах. Имеено они являются причиной снижения охвата вакцинацией, несмотря на все научные доказательства ее пользы.
Автор фото, Getty Images
Підпис до фото,Ученые доказали отсутствие причинно-следственной связи между вакциной против кори, паротита и краснухи (КПК) и аутизмом
1. «Вакцины могут вызвать аутизм»
Решение родителей отказаться от прививок чаще всего связывают с опубликованным в 1998 году исследованием британского гастроэнтеролога Эндрю Уэйкфилда, который предположил, что вакцина от кори КПК может способствовать развитию у детей аутизма. Статью противника вакцинации опубликовал авторитетный медицинский журнал Lancet.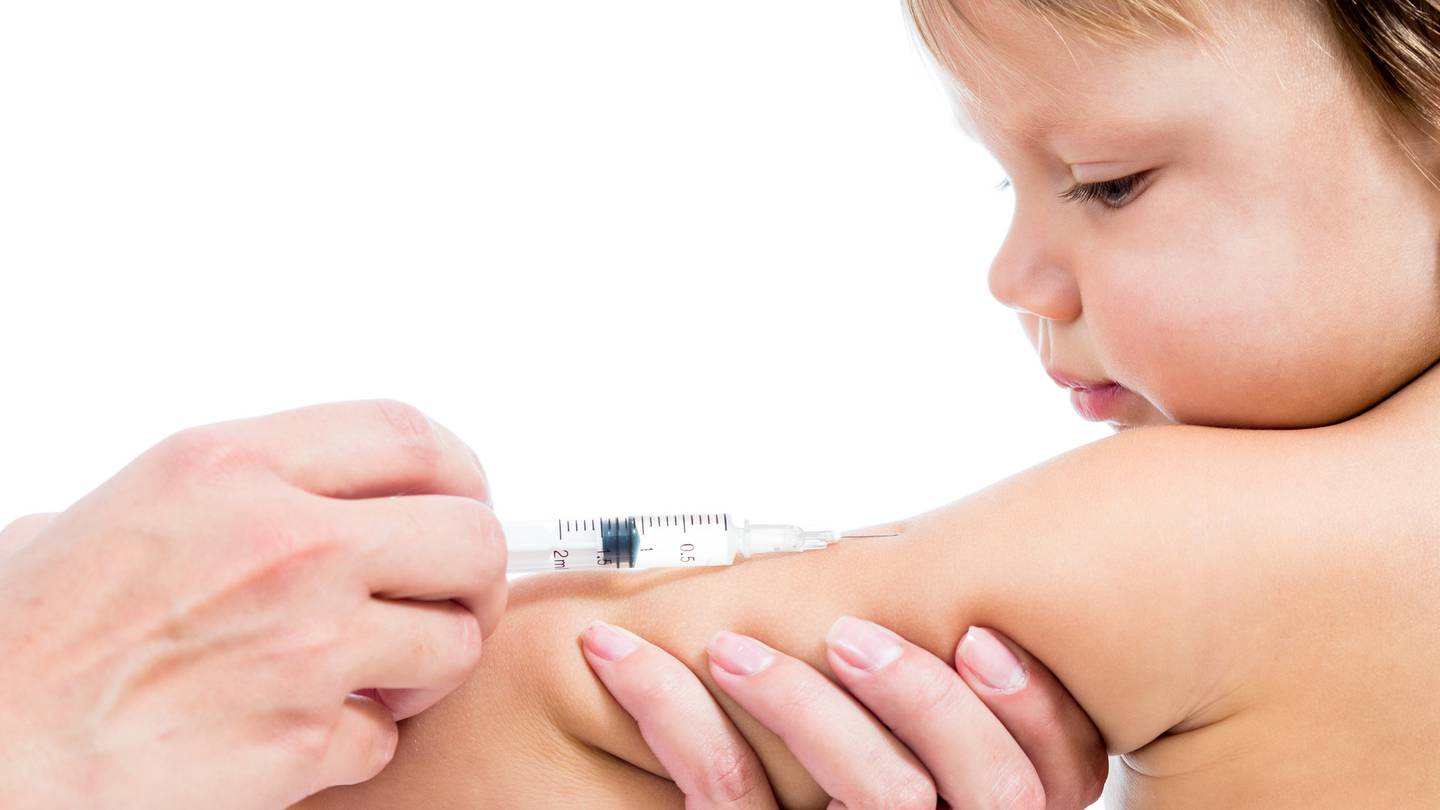
Предположения ученого не нашли подтверждения, публикация была отозвана из журнала, а сам Уэйкфилд — исключён из реестра практикующих врачей.
Однако эта теория до сих пор остается популярной в развитых странах.
В часности, уровень охвата прививками вакциной КПК в Великобритании снизился с 92% в 1996 году до 84% в 2002-м. Впоследствии этот показатель вновь увеличился примерно до 91%, одако пока так и не достиг рекомендованных ВОЗ 95%.
Автор фото, Getty Images
Підпис до фото,Эндрю Уэйкфилда, который связал применение вакцины против кори, паротита и краснухи (КПК) с развитием аутизма, исключили из реестра практикующих врачей после научного опровержения его идей
2. «Детская иммунная система не способна справиться с таким количеством вакцин»
Грудничкам и детям до 2 лет рекомендовано по меньшей мере 11 вакцин. Некоторые родители волнуются, что такое количество вакцин перегружает детскую иммунную систему.
Бытует мнение, что вакцина — это введение в организм вирусов или бактерий, которые могут вызывать определенные болезни.
На самом деле в вакцине содержатся ослабленные микробы, которых не стоит боятся.
Используя естественные защитные реакции организма, они помогают выработать иммунитет к болезни.
«Дети развивают способность реагировать на посторонние антигены (вещества, стимулирующие иммунную реакцию) еще до своего рождения», — пишет американский педиатр Пол Оффит в одной из самых известных своих работ, посвященной связи между множественными вакцинами и иммунной системой новорожденных.
«Спустя считанные часы после рождения, получив прививку, они начинает формировать свою защиту», — добавляет он.
Автор фото, Getty Images
Підпис до фото,Улучшение условий жизни, переселение из трущоб в современные дома позволили снизить уровень заболеваемости
3. «Болезни исчезали сами по себе, когда стали вводить вакцины»
Суть этого аргумента в том, что улучшение социоэкономических условий — в частности, питания и гигиены — сыграло не меньшую роль в лечении болезней, чем вакцинация.
Действительно, благодаря прогрессу смертность от некоторых заболеваний снизилась еще до того, как появились вакцины. Однако невысокие темпы снижения инфекции свидетельствуют скорее о пользе вакцинации.
В частности, в США, по данным Центров контроля и профилактики заболеваний США, годовой показатель смертности от кори снизился с 5 300 в 1960 году до 450 в 2012 году. Первая вакцина от кори появилась в 1963 году.
Только за пять лет использования прививок (1963-1968) вакцинация не только радикально повысила выживаемость, но и не менее радикально сократила количество случаев заболевания.
Кроме того, существуют веские причины считать, что массовые отказы от вакцинации могут привести к новому витку болезни. Например, в 1970-е годы в Японии и Швеции резко возросло количество случаев заболевания коклюшем, а также — смертей от него. Причиной тому было знижение количества привитых детей.
Автор фото, Getty Images
Підпис до фото,Витамины не всегда помогают предотвратить болезнь
4.
Этим аргументом часто пользуются те, кто выступает против иммунизации.
Дело в том, что ни одна вакцина не дает стопроцентную защиту. По данным ВОЗ, прививка защищает от заболевания примерно на 85-95%.
Каждый организм реагирует на прививки по-своему, а это значит, что иммунитет вырабатывается не у всех.
И единственная причина, почему среди больных больше привитых, чем непривитых — это то, что первых просто намного больше.
Среди невакцинированных уровень заболеваемости значительно выше.
Автор фото, Getty Images
Підпис до фото,Вакцины до сих пор составляют очень небольшую долю прибыли для мировой фармацевтической промышленности
5. «Фармацевтические гиганты заинтересованы в продаже вакцин»
Экономист ВОЗ Милуд Кадар, сообщил, что в 2013 году объем мирового рынка вакцин составил 24 млрд долларов.
В минувшем году это составило менее 3% глобального фармацевтического рынка.
В последние годы рынок вакцин набирает обороты; основные факторы роста — расширение программ иммунизации в странах-лидерах мирового промышленного производства, таких как Китай, а также финансирование исследований и разработки вакцин состоятельными людьми (среди них — руководитель компании Microsoft Билл Гейтс).
Впрочем, на самом деле заинтересованная сторона — это население Земли, ведь болеть — гораздо дороже.
Согласно исследованию, проведенному в 2016 году Университетом Джона Хопкинса, в 94 беднейших странах мира, каждый доллар, вложенный в вакцинацию, прогнозируемо экономит 16 долларов расходов, связанных с лечением, оплатой труда, утраченной работоспособностью и смертью.
Автор фото, Getty Images
Підпис до фото,Заболевания, находящихся под контролем в развитых странах, все еще распространены или даже эндемичны в других частях мира
6. «Моя страна практически победила эту болезнь, поэтому мне не нужна вакцинация»
Во многих странах болезни, которые можно предотвратить, действительно случаются значительно реже благодаря вакцинации. Впрочем, на мировом уровне эти болезни до сих пор не научился побеждать.
Впрочем, на мировом уровне эти болезни до сих пор не научился побеждать.
Некоторые из них, наоборот, очень распространены и даже эндемичны в некоторых странах мира. Благодаря глобализации они легко распространяются и вспыхивают с новой силой в странах, где уровень иммунизации снижается.
Заболеваемость корью в Европе в 2018 году выросла в три раза (по сравнению с 2017 годом) и составила 83 тысяч случаев — самый высокий показатель в текущем десятилетии.
7. «Вакцины содержат опасные токсины»
Родителей, которые зачастую сомневаются, стоит ли делать своим детям прививки, беспокоит содержание в вакцинах таких веществ, как формальдегид, ртуть и алюминий.
Эти вещества действительно вредны, но доза этих химических соединений в вакцине настолько мала, что не может считаться токсичной.
По данным Управления продовольствия и медикаментов США, в стандартной вакцине токсическая доза ртути составляет 25 микрограммов на 0,5 мл дозу.
Столько же ртути содержится в 85-граммовой жестяной банке консервированного тунца, говорят специалисты из Управления.
Автор фото, Getty Images
Підпис до фото,Безопасность медиков, которые делают вакцинации в Нигерии, Пакистане или Афганистане — под угрозой. Они должны работать с вооруженной охраной
8. «Вакцины — это заговор Запада»
Уверенность в том, что вакцины являются частью заговора, направленного против мирного населения, — еще не редкость.
На севере Нигерии борьбе с полиомиелитом мешает убеждение, что вакцины якобы намеренно разработаны для того, чтобы сделать женщин бесплодными и распространить ВИЧ. Медработники часто становятся жертвами нападений.
Такие же мифы существуют в Афганистане и Пакистане; вместе с Нигерией, это единственные страны в мире, где вирус полиомиелита остается эндемическим.
К сожалению, сомнения в мотивах вакцинации не совсем беспочвенны: в марте 2011 года ЦРУ провело в Пакистане подставную прививочную кампанию в попытке получить ДНК лидера Аль-Каиды Усамы бен Ладена и, соответственно, установить его местонахождение.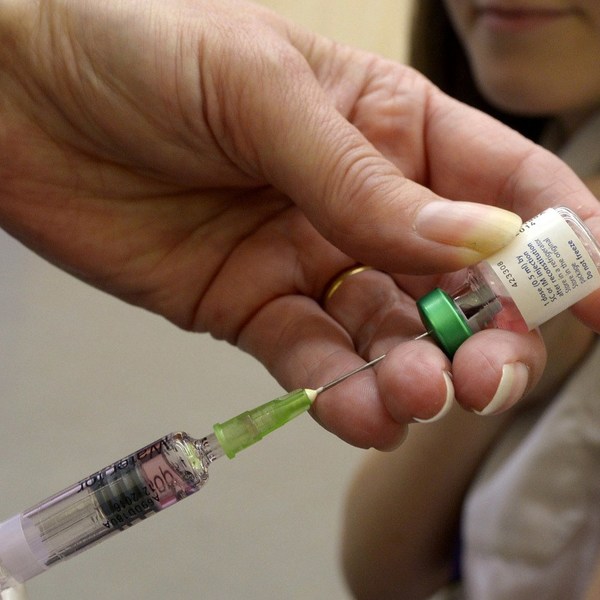
Этот заговор был раскрыт, и это только усилило недоверие к прививкам в стране, где охват вакцинации и без того низкий.
Подготовка к вакцинации — Детский медицинский центр
Для решения вопроса о необходимости вакцинации, определения, в какой последовательности и какими вакцинами прививать ребёнка, потребности в подготовке к прививке и наблюдения после неё нужно обращаться к врачу.
Сведения о проведённых профилактических прививках вносятся в медицинскую документацию (карта профилактических прививок-ф063\у, история развития ребёнка-ф112\у, медицинская карта ребёнка-ф026\у), которые хранятся в медицинском учреждении, производящем вакцинацию, а также в сертификат профилактических прививок (ф156\у-93), который находится у родителей вакцинируемого ребёнка. Выдача сертификата профилактических прививок при его отсутствии у ребёнка регламентируется приказом Минздрава РФ от 17 сентября 1993 г. N220 «О мерах по развитию и совершенствованию инфекционной службы в Российской Федерации».
Профилактические прививки проводят здоровым детям после осмотра их врачом, проведения термометрии. Родители ребёнка (или опекуны) заполняют добровольное информированное согласие на вакцинацию. Необходимость дополнительного лабораторного и инструментального обследования, консультаций узких специалистов определяет врач, направляющий ребёнка на вакцинацию. Вакцинацию не проводят если ребёнок болен острым инфекционным заболеванием или у него имеет место обострение хронического заболевания.
Здоровые дети не требуют специальной подготовки перед вакцинацией.
Необходимость и объём подготовки к вакцинации детей с хронической патологией или аллергическими реакциями определяется лечащим врачом совместно с узкими специалистами.
В момент прививки постарайтесь подержать ребенка и успокоить его после инъекции. Обычно дети грудного возраста быстро успокаиваются, если их приложить к груди (после применения живой оральной вакцины против полиомиелита нельзя кормить или поить ребенка в течение 45 мин), а дети постарше – если им предложить игрушку (игрушкой лучше запастись из дому).
Сразу после прививки не спешите покидать поликлинику или центр вакцинации. Вам следует вместе с ребёнком остаться в поликлинике еще на 30 минут. Такая предосторожность связана с возможностью возникновения коллапса или сильной аллергической реакции на прививку (анафилактический шок).
Несмотря на то, что такие реакции возникают исключительно редко, возможность их развития всегда следует иметь в виду.
После прививки рекомендуется придерживаться обычной диеты, в течение 3 дней не вводить в питание ребёнка новые продукты. Если прививка проводилась в виде инъекции, то в день прививки не рекомендуют ребёнка купать. После прививки возможны небольшое повышение температуры тела, некоторое беспокойство ребёнка, уплотнение в месте инъекции (при внутримышечном введении вакцины), которые характерны для течения поствакцинального периода и не требуют специального лечения. После введения вакцины против кори и краснухи на 7-10-й дни возможно появление необильной сыпи на туловище и конечностях, которая проходит самостоятельно через 2-3 дня.
При значительном повышении температуры тела или невысокой температуре, сохраняющейся длительное время, необычном поведении ребёнка (выраженная вялость или беспокойство, пронзительный крик), появлении других симптомов необходимо обратиться к врачу.
Особенности вакцинации БЦЖ-М на платной основе
Вакцинация против кори, краснухи, паротита к клинике МедиАрт
Вакцинация от кори, краснухи, паротита
Корь, краснуха и паротит крайне заразны, передаются воздушно-капельным путем – при кашле, разговоре, чихании, плаче. В детских коллективах (садах, школах) они могут распространяться и через посуду, грязные руки, общие игрушки. Особенно опасны эти инфекции для малышей, у которых иммунитет только формируется, а также детей с хроническими заболеваниями. Краснуха опасна и для матерей заболевших детей, если они не имеют иммунитета или прививки, и на момент заражения находятся на раннем сроке беременности.
Зачем прививать ребенка от кори
Корь – одно из самых опасных «детских» заболеваний. Во-первых, она крайне заразна: шансы заболеть после контакта с больным корью приближаются к 100%. Снижение процента вакцинированных детей даже ненамного немедленно дает всплеск заболеваемости корью. Уже в 2000-х годах были зафиксированы эпидемии в таких благополучных странах, как Ирландия и США: причины – доступность авиаперелетов и отказы от вакцинации. Во-вторых, корь обладает высокой летальностью (хотя и не такой высокой, как столбняк и дифтерия), и особенно подвержены ей дети до 5 лет.
Корь до сих пор не имеет специфического лечения – только симптоматическое. Кроме того, она дает тяжелейшие осложнения на дыхательную систему, включая бронхит и пневмонию, а также может привести к частичной потере ребенком слуха или зрения.
Зачем прививать ребенка от краснухи
Известно, что краснуха наиболее опасна для беременных женщин, так как она крайне негативно влияет на плод: более чем у половины новорожденных наблюдается глухота, часто встречаются также слепота и порок сердца. Поэтому целесообразность прививки от краснухи для женщин, планирующих беременность, вроде бы не вызывает сомнений.
Поэтому целесообразность прививки от краснухи для женщин, планирующих беременность, вроде бы не вызывает сомнений.
Однако родители часто задают вопрос: зачем прививать от краснухи годовалую девочку или, тем более, мальчика? Ведь известно, что в большинстве случаев краснуха протекает достаточно легко?
Как и в случае с паротитом, самое известное в народе осложнение – далеко не единственное и даже, увы, не самое ужасное. Прогрессирующий краснушный панэнцефалит – редкое, но страшное осложнение – чаще всего поражает как раз мальчиков в возрасте от 8 до 19 лет. При этом осложнении у человека постепенно угасает интеллект и отмирают моторные функции, а заканчивается оно слабоумием и смертью. Из других осложнений от краснухи, не делающих половых различий, встречаются артрит, пневмония и гепатит.
Зачем прививать ребенка от паротита
Эпидемический паротит (свинка) не относится к смертельно опасным заболеваниям, однако может дать крайне неблагоприятные осложнения. Известность он приобрел благодаря тому, что является довольно частой причиной бесплодия у мужчин, развившегося в результате орхита – воспаления яичек. Дело в том, что вирус паротита поражает железистые ткани и не ограничивается заушными слюнными железами (хотя они, действительно, как правило, поражаются первыми), а может развиться в тканях щитовидной железы, поджелудочной железы, яичек у мальчиков или яичников у девочек. С этой особенностью паротита связаны два самых распространенных мифа о вакцине против него.
Известность он приобрел благодаря тому, что является довольно частой причиной бесплодия у мужчин, развившегося в результате орхита – воспаления яичек. Дело в том, что вирус паротита поражает железистые ткани и не ограничивается заушными слюнными железами (хотя они, действительно, как правило, поражаются первыми), а может развиться в тканях щитовидной железы, поджелудочной железы, яичек у мальчиков или яичников у девочек. С этой особенностью паротита связаны два самых распространенных мифа о вакцине против него.
Первый: прививка вызывает бесплодие у мальчиков. Разумеется, это не так. При прививке ткани яичек не поражаются.
Второй: нет смысла прививать мальчиков до наступления полового созревания. И это не так – бесплодие вызывают не низкокачественные сперматозоиды, а атрофия тканей яичка, что от возраста, к сожалению, не зависит. Да и качественный иммунитет формируется после ревакцинации, и можно просто не успеть привить ребенка до того, как он заболеет.
Второй вопрос, не менее частый: если свинка опасна только для мальчиков, зачем прививать девочек? Только ради пресловутого популяционного иммунитета? Конечно, нет. Дело в том, что, помимо орхита, партотит может вызывать панкреатит, и это пожизненно, ведь ткани поджелудочной железы не восстанавливаются; а также энцефалит и менингоэнцефалит – опаснейшие разновидности воспаления мозга. Не очень часто, но все же бывает, что перенесенный паротит заканчивается глухотой.
Национальный календарь прививок
Национальный календарь прививок предусматривает первую вакцинацию ребенка против кори, краснухи и паротита, когда ребенок достигает 12 месяцев.
Ревакцинация делается в 6 лет.
Таким образом, до достижения ребенком совершеннолетия ему предстоит только дважды прививаться Вактривиром, Приориксом или аналогичной вакциной.
ЕРБ ВОЗ | Вакцинация во время пандемии COVID-19 в вопросах и ответах
Безопасно ли проводить вакцинацию детей во время пандемии COVID-19?
ВОЗ рекомендует проводить все плановые профилактические прививки в соответствии с графиком – даже во время пандемии COVID-19. В настоящее время у нас нет данных, свидетельствующих о том, что пандемия COVID-19 привела к появлению каких-либо особых рисков, связанных с вакцинацией. Следовательно, мы пользуемся теми же данными, что и в случае с другими инфекционными болезнями. Эти данные говорят о том, что возможный контакт с источником инфекции не является противопоказанием для проведения плановой иммунизации (1). По мере возможности странам следует продолжать плановую иммунизацию на базе медицинских учреждений, насколько позволяют местные условия и меры по борьбе с COVID-19. Однако при этом необходимо соблюдать стандартные правила профилактики инфекций, чтобы свести к минимуму риск передачи COVID-19 персоналу и посетителям медицинских учреждений.
В настоящее время у нас нет данных, свидетельствующих о том, что пандемия COVID-19 привела к появлению каких-либо особых рисков, связанных с вакцинацией. Следовательно, мы пользуемся теми же данными, что и в случае с другими инфекционными болезнями. Эти данные говорят о том, что возможный контакт с источником инфекции не является противопоказанием для проведения плановой иммунизации (1). По мере возможности странам следует продолжать плановую иммунизацию на базе медицинских учреждений, насколько позволяют местные условия и меры по борьбе с COVID-19. Однако при этом необходимо соблюдать стандартные правила профилактики инфекций, чтобы свести к минимуму риск передачи COVID-19 персоналу и посетителям медицинских учреждений.
Особенно важно обеспечить своевременное получение всех плановых профилактических прививок детьми при рождении и в первые два года жизни (2). Перечень этих прививок может быть разным в зависимости от национальных рекомендаций. В случае если проведение иммунизации в какой-либо возрастной группе было прервано, этот процесс необходимо будет возобновить, чтобы как можно скорее наверстать график вакцинации (2).
K началу страницы
Повышает ли вакцинация риск инфицирования COVID-19 или развития этого заболевания у ребенка?
COVID-19 – это новое заболевание, процесс накопления информации о котором все еще продолжается. Однако, опираясь на опыт борьбы с другими инфекционными болезнями, мы знаем, что вакцинация против одного заболевания не ослабляет иммунную реакцию организма на другое заболевание (3), (4), (5). В настоящее время у нас нет данных, которые свидетельствовали бы о том, что вакцинация может увеличить риск инфицирования ребенка COVID-19 или повлиять на характер течения этого заболевания у детей, которые по незнанию были привиты во время бессимптомной стадии или инкубационного периода.
Более того, продолжение плановой вакцинации детей во время пандемии COVID-19 позволит защитить их от вакциноуправляемых инфекций (ВУИ). Позаботившись о том, чтобы иммунизация проводилась в учреждениях, где действуют надлежащие меры профилактики инфекций, вы сведете к минимуму потенциальный риск инфицирования ребенка COVID-19.
K началу страницы
Почему особенно важно проводить вакцинацию во время пандемии COVID-19?
Любой сбой в предоставлении услуг иммунизации, даже продолжающийся в течение короткого периода, будет подвергать всех членов общества и особенно детей прямому риску заражения ВУИ (6). Увеличивая число восприимчивых к этим инфекциям индивидов, которые и так уже присутствуют среди населения, мы рискуем утратить коллективный иммунитет, защищающий все общество, и увеличиваем вероятность возникновения вспышек ВУИ. Такие вспышки могут приводить к связанным с ВУИ случаям заболевания и смерти, а также к увеличению нагрузки на системы здравоохранения, которые и без того вынуждены работать на пределе возможностей в связи со вспышкой COVID-19.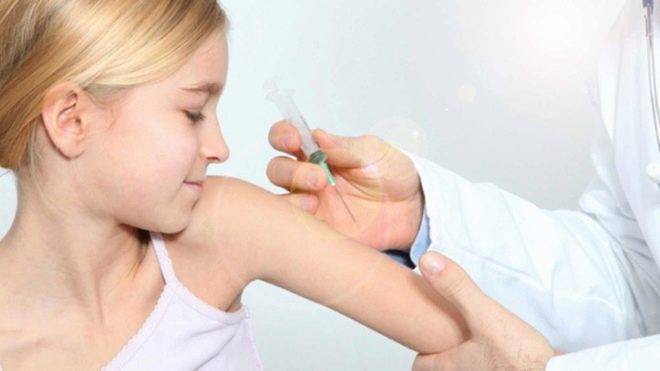
K началу страницы
Опасно ли вакцинировать ребенка во время инкубационного периода COVID-19?
В настоящее время у нас нет каких-либо особых данных, касающихся COVID-19 и вакцинации, поэтому в данном контексте медработникам необходимо следовать общим принципам вакцинации пациентов с инфекционными заболеваниями. Согласно этим принципам, вакцинация не повлияет на течение другого инфекционного заболевания у ребенка, который, возможно, уже им инфицирован, но на момент проведения вакцинации еще не демонстрирует каких-либо симптомов, или же у ребенка, который, возможно, инфицируется им вскоре после вакцинации. Аналогичным образом, такая инфекция не повлияет на безопасность или эффективность сделанной ребенку прививки (1), (7).
K началу страницы
Является ли инфекция COVID-19 противопоказанием для вакцинации?
Легкие симптомы, такие как повышенная температура тела и/или кашель, не обязательно являются противопоказанием для проведения вакцинации (1). В соответствии со стандартными процедурами, поставщики услуг здравоохранения должны давать своим пациентам соответствующие рекомендации, опираясь на анализ соотношения рисков и пользы (например, тяжесть имеющихся у пациента симптомов, а также риски и тяжесть течения ВУИ). Если медицинский специалист решит не делать ребенку прививку в этот день, плановую вакцинацию этого ребенка необходимо будет возобновить сразу же после его выздоровления.
В соответствии со стандартными процедурами, поставщики услуг здравоохранения должны давать своим пациентам соответствующие рекомендации, опираясь на анализ соотношения рисков и пользы (например, тяжесть имеющихся у пациента симптомов, а также риски и тяжесть течения ВУИ). Если медицинский специалист решит не делать ребенку прививку в этот день, плановую вакцинацию этого ребенка необходимо будет возобновить сразу же после его выздоровления.
Важно, чтобы любой человек, получивший положительный результат теста на COVID-19, находился на карантине в соответствии с национальными рекомендациями; таким образом он не инфицирует других и не будет способствовать дальнейшему распространению вируса.
K началу страницы
Есть ли какие-то конкретные прививки, которые рекомендуется получить медицинским работникам в условиях пандемии COVID-19?
В настоящее время вакцины против COVID-19 не существует. Более 100 вакцин-кандидатов проходят клинические исследования или находятся на стадии доклинической оценки (8). ВОЗ работает со всеми заинтересованными сторонами, чтобы гарантировать, что после появления безопасной и эффективной вакцины ее распределение будет осуществляться на справедливой основе. Сейчас, как никогда прежде, всем медицинским работникам необходимо позаботиться о прохождении рекомендованной им вакцинации в соответствии с их национальными календарями профилактических прививок (9).
ВОЗ работает со всеми заинтересованными сторонами, чтобы гарантировать, что после появления безопасной и эффективной вакцины ее распределение будет осуществляться на справедливой основе. Сейчас, как никогда прежде, всем медицинским работникам необходимо позаботиться о прохождении рекомендованной им вакцинации в соответствии с их национальными календарями профилактических прививок (9).
K началу страницы
Через сколько дней после получения пациентом отрицательного результата теста на COVID-19 ему можно проводить прививку?
В данный момент у нас нет конкретных данных о возможном влиянии COVID-19 на иммунный ответ организма на вакцину и наоборот. Проведение систематического тестирования на COVID-19 перед плановой вакцинацией в настоящее время не является обязательным требованием или рекомендацией. Любой пациент с отрицательным результатом теста на COVID-19 может пройти вакцинацию в любой момент, если его клиническое состояние позволяет это сделать.
K началу страницы
Через сколько дней после получения пациентом отрицательного результата теста на COVID-19 ему можно проводить туберкулиновую пробу?
У нас нет данных о том, что результат теста на COVID-19 или сама инфекция COVID-19 каким-либо образом влияют на туберкулиновую пробу.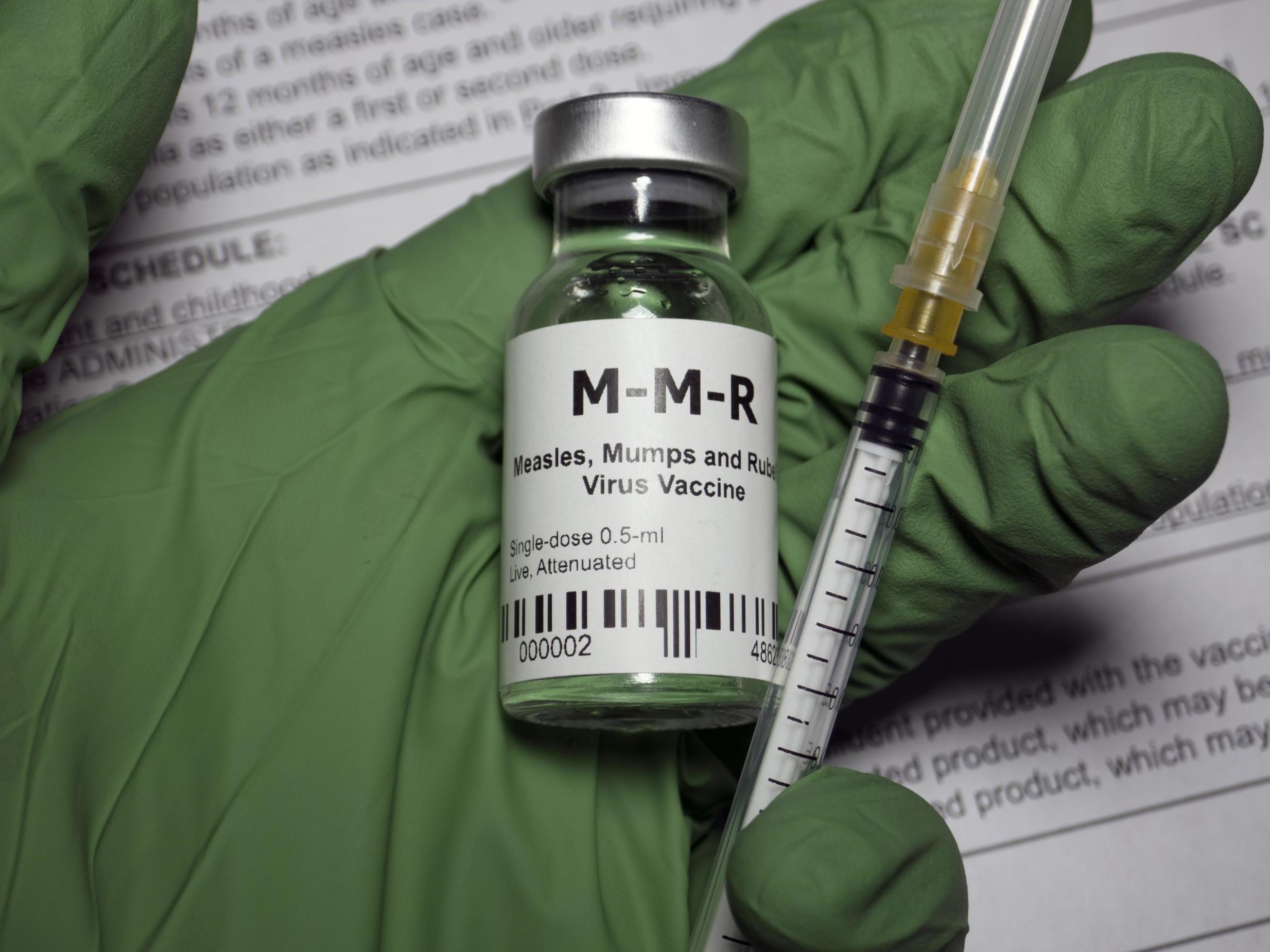
K началу страницы
Защищает ли вакцина БЦЖ от COVID-19?
Помимо профилактики туберкулезной инфекции, вакцина БЦЖ (бацилла Кальмета-Герена) оказывает положительное воздействие на иммунную систему, которое защищает организм человека от целого ряда других инфекций; эта вакцина также регулярно используется для лечения рака мочевого пузыря. В настоящее время проводятся два исследования, посвященных тому, может ли вакцина БЦЖ сыграть определенную роль в защите медицинских работников и других уязвимых лиц от развития у них тяжелой формы COVID-19, но на сегодняшний день у нас нет данных, свидетельствующих о том, что вакцина БЦЖ защищает людей от заражения новым коронавирусом. Следовательно, ВОЗ не рекомендует проводить вакцинацию БЦЖ с целью профилактики COVID-19. ВОЗ по-прежнему рекомендует проводить иммунизацию новорожденных вакциной БЦЖ в странах и регионах с высоким уровнем заболеваемости туберкулезом.
K началу страницы
Библиография
(1) Безопасность вакцин и ложные противопоказания к вакцинации. Учебное руководство. Копенгаген: Европейское региональное бюро ВОЗ; 2017 (http://www.euro.who.int/__data/assets/pdf_file/0009/351927/WHO-Vaccine-Manual.pdf, по состоянию на 10 июня 2020 г.).
Учебное руководство. Копенгаген: Европейское региональное бюро ВОЗ; 2017 (http://www.euro.who.int/__data/assets/pdf_file/0009/351927/WHO-Vaccine-Manual.pdf, по состоянию на 10 июня 2020 г.).
(2) Руководство по плановой иммунизации во время пандемии COVID-19 в Европейском регионе ВОЗ. Копенгаген: Европейское региональное бюро ВОЗ; 2020 (http://www.euro.who.int/en/health-topics/communicable-diseases/hepatitis/publications/2020/guidance-on-routine-immunization-services-during-covid-19-pandemic-in-the-who-european-region-2020, по состоянию на 10 июня 2020 г.).
(3) Offit P, Quarles J, Gerber MA, Hackett CJ, Marcuse EK, Kollman TR et al. Addressing parents’ concerns: do multiple vaccines overwhelm or weaken the infant’s immune system? [Ответы на вопросы, волнующие родителей: может ли применение многочисленных вакцин оказать чрезмерную нагрузку на иммунную систему младенца или ослабить ее?] Pediatrics. 2002;109:124–9.
(4) Глобальный консультативный комитет по безопасности вакцин, 6–7 июня 2006 г. Ежемесячный эпидемиологический бюллетень. 2006: 28(81):273–84 (https://www.who.int/vaccine_safety/committee/reports/wer8128.pdf?ua=1, по состоянию на 10 июня 2020 г.).
Ежемесячный эпидемиологический бюллетень. 2006: 28(81):273–84 (https://www.who.int/vaccine_safety/committee/reports/wer8128.pdf?ua=1, по состоянию на 10 июня 2020 г.).
(5) Miller E, Andrews N, Waight P, Taylor B. Bacterial infections, immune overload, and MMR vaccine. [Бактериальные инфекции, избыточная нагрузка на иммунную систему и вакцина КПК.] Arch Dis Child. 2003;88:222–3.
(6) Takahashi S, Metcalf CJ, Ferrari MJ, Moss WJ, Truelove SA, Tatem AJ et al. Reduced vaccination and the risk of measles and other childhood infections post-Ebola. [Снижение охвата вакцинацией и риск появления кори и других детских инфекций в период после вспышки эболы.] Science. 2015;347(6227):1240-2.
(7) Rubin LG, Levin MJ, Ljungman P, Davies G, Avery R, Tomblyn M et al. 2013 IDSA clinical practice guideline for vaccination of the immunocompromised host. [Руководство Американского общества инфекционных болезней по клинической практике в области вакцинации людей с ослабленной иммунной системой (2013 г. )] Clin Infect Dis. 2014;58(3):309-18.
)] Clin Infect Dis. 2014;58(3):309-18.
(8) Предварительный список вакцин-кандидатов против COVID-19 (на англ. яз.). Женева: ВОЗ; 2020 (https://www.who.int/who-documents-detail/draft-landscape-of-covid-19-candidate-vaccines, по состоянию на 10 июня 2020 г.).
(9) Сводный перечень документов с изложением позиции ВОЗ по вопросу иммунизации медицинских работников (на англ. яз.). Женева: ВОЗ; 2020 (https://www.who.int/immunization/policy/Immunization_routine_table4.pdf, по состоянию на 10 июня 2020 г.).
K началу страницы
Вакцинация детей от кори, онлайн-запись на консультацию к специалисту – сеть клиник МЕДСИ
Вакцинация от кори детям осуществляется с 60-х годов прошлого века. Она безопасна, эффективна и входит в национальный календарь прививок России.
Проводится прививка от кори детям в год и в 6 лет, согласно национальному календарю профилактических прививок. Введение всем детям двух доз вакцины от кори (при отсутствии противопоказаний) является обязательным. Наличие или отсутствие противопоказаний от вакцинации против кори определяет ваш личный врач.
Введение всем детям двух доз вакцины от кори (при отсутствии противопоказаний) является обязательным. Наличие или отсутствие противопоказаний от вакцинации против кори определяет ваш личный врач.
Сделать прививку от кори в Москве ребенку можно в МЕДСИ. В клинике проводится вакцинация против кори детям с использованием сертифицированных вакцин. Опытные детские специалисты проведут осмотр ребенка перед прививкой.
Как происходит заражение корью
Корь – это высококонтагиозная вирусная инфекция, которая является одной из основных причин смертности среди детей раннего возраста.
По оценкам Всемирной организации здравоохранения, в 2017 году в мире от кори погибло около 110 тысяч человек, 92 тысячи из них – дети в возрасте до пяти лет. В России заболеваемость корью в 2018 году возросла в 20 раз по сравнению с 2010 годом и составила 1,7 случаев на 100 000 человек.
Корь передается воздушно-капельным путем от зараженного человека, контагиозность составляет 90 %, то есть каждый больной заражает 9 из 10 контактировавших с ним невакцинированных людей.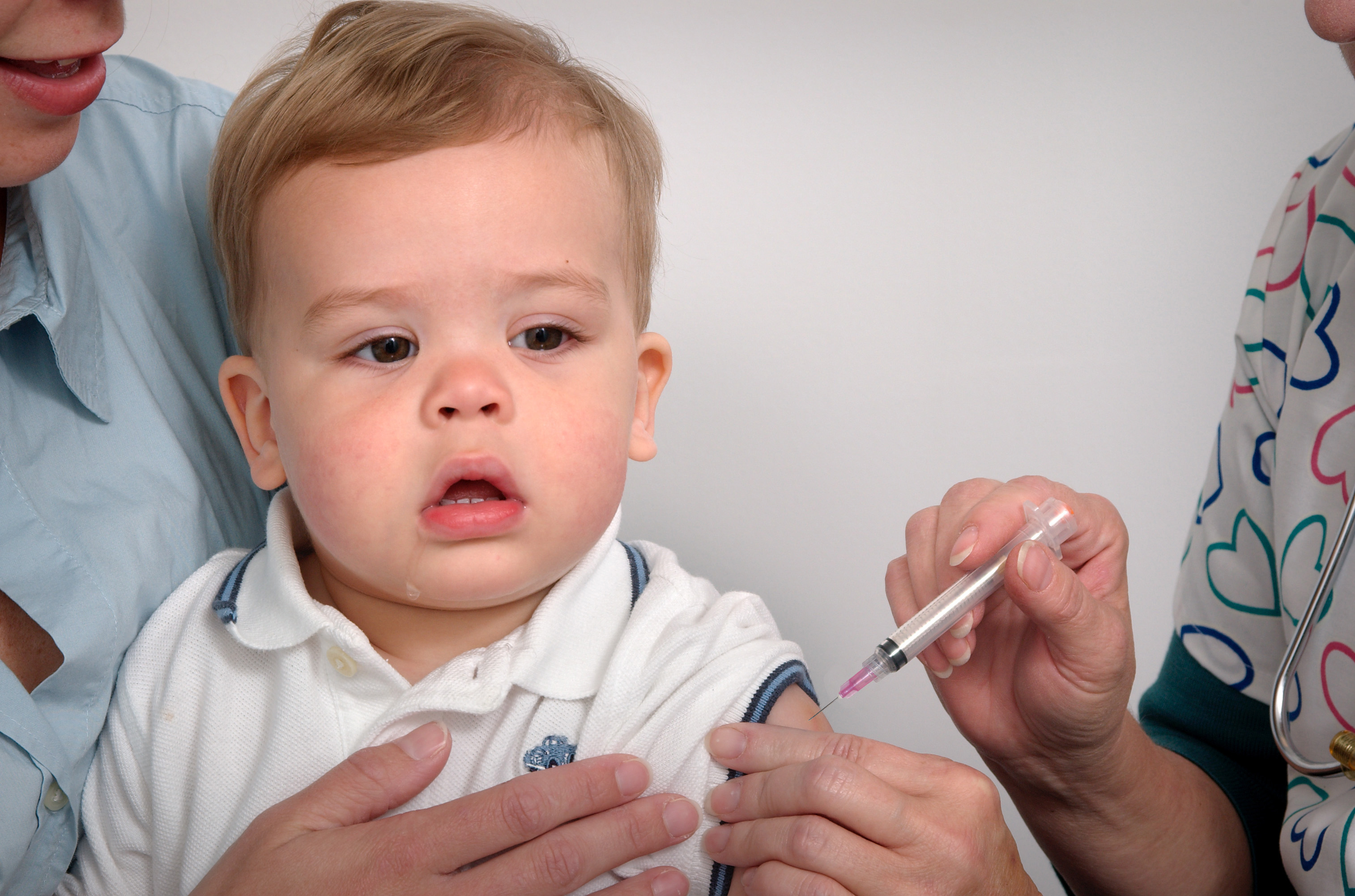 Прививки от кори ребенку в год и в шесть лет предотвратят возможность заражения заболеванием.
Прививки от кори ребенку в год и в шесть лет предотвратят возможность заражения заболеванием.
Вакцинопрофилактика
Для снижения уровня смертности от кори по всему миру проводится плановая иммунизация детей. Своевременная прививка против кори детям защищает от развития заболевания, возникновения тяжелых осложнений и летального исхода.
Прививка детям от кори в клиниках МЕДСИ проводится после профилактического осмотра и консультации педиатра.
Плановая вакцинация включает:
- Прививку от кори ребенку в 1 год
- Прививку от кори ребенку в 6 лет
Вакцину вводят под лопатку либо в верхнюю треть плеча.
Сделать прививку от кори детям в Москве можно в любое время года. Иммунизация не проводится только при наличии определенных противопоказаний, среди которых:
- Непереносимость куриного белка или других компонентов препарата
- Первичный или приобретенный иммунодефицит
- Осложнения на предыдущую прививку
- Наличие злокачественных опухолей
При тяжелых ОРВИ, гриппе, хронических заболеваниях в стадии обострения иммунизацию переносят на один месяц.
Корь – очень заразное вирусное заболевание
Корь — вирусное заболевание, чрезвычайно заразное. При контакте с больным корью заболевают 98% не привитых или не имеющих иммунитета людей. Вакцина готовится из живых ослабленных вирусов кори. В настоящее время широко используются тривакцины (против кори, краснухи, паротита), что позволяет за одну инъекцию ввести сразу три вакцины. Все эти вакцины вводятся подкожно или внутримышечно в область плеча.
План вакцинации
Вакцинация против кори является обязательным условием при устройстве ребенка в детский сад. Вакцинация проводится два раза:
- в 12 месяцев
- и перед школой в 7 лет.
Подростков и взрослых, получивших вакцину 1 раз в детстве, а также с неизвестным прививочным анамнезом, рекомендуется привить еще раз в любом возрасте.
Вакцинация детей согласно календарю прививок:
| Что делать? | Возраст |
|---|---|
| Вакцинация | 12 месяцев |
| Ревакцинация | 7 лет |
» src=»//www.youtube.com/embed/W0mbGmUzPqg?feature=oembed» allow=»accelerometer; autoplay; encrypted-media; gyroscope; picture-in-picture» allowfullscreen=»» frameborder=»0″>
Побочные эффекты
У большинства детей никаких побочных явлений после вакцинации нет. Может быть повышение температуры тела (как правило, не выше 37-38 С), легкое недомогание в течение 2-3 дней. У детей, склонных к аллергическим реакциям, может быть сыпь с 4 по 15 день после вакцинации. Серьезные осложнения, крайне редки.
Когда вакцинация откладывается
Противопоказания к вакцинации:
- иммунодефицитные состояния, онкологические заболевания
- аллергия на аминогликозиды (канамицин, мономицин)
- куриные яйца
Если ребенок получал препараты содержащие иммуноглобулины или плазму крови, то вакцинация проводится не ранее, чем через 2-3 месяца.
О прививках.
 Как подготовить ребёнка к прививке? Главная » Здоровье » О прививках. Как подготовить ребёнка к прививке?
Как подготовить ребёнка к прививке? Главная » Здоровье » О прививках. Как подготовить ребёнка к прививке?Родители знают: уберечь свое чадо от инфекционных заболеваний в большом детском коллективе, будь то ясли, детский садик или школа, практически невозможно. Единственным средством защиты детей остаются прививки.
Цифры в календаре прививок означают лишь приблизительный возраст, с которого можно начинать вакцинацию. Но родителям всегда стоит помнить, что нужный момент подбирается индивидуально. Если у малыша есть отклонения в развитии (не только отставание, но и опережение) или противопоказания (аллергия и т.п.) лечащий врач может отойти от строгого графика.
Раньше срока делаются лишь прививки в случаях, если в группе детского садика или семье кто-то заболел заразной болезнью.
Отложить прививку необходимо, если ребенок только что перенес какое-либо инфекционное или вирусное заболевание. Нужно хорошенько долечить его и только тогда отправляться на прививку. Врачи советуют переждать как минимум месяц после выздоровления, а также воздержаться от плановых прививок во время эпидемий гриппа и ОРЗ.
Нужно хорошенько долечить его и только тогда отправляться на прививку. Врачи советуют переждать как минимум месяц после выздоровления, а также воздержаться от плановых прививок во время эпидемий гриппа и ОРЗ.
Количество плановых прививок рассчитано на самый слабый иммунитет. Потому что практически у всех наших детей сегодня он именно такой. И даже еще слабее, потому что участились случаи заболевания привитых детей, чей организм не способен выработать необходимые антитела даже будучи специально спровоцированным вакциной. Правда, в случае заболевания привитый ребенок переносит его в несравнимо более легкой форме и никогда не погибает.
Вакцины не оказывают на организм ребенка по-настоящему вредного воздействия. Реакция на внесение в организм «заразы» хотя часто и пугает родителей (повышение температуры, краснота, припухлость и болезненность в месте прививки), но неизмеримо легче самой инфекции, против которой делается прививка.
Чем мы можем помочь нашему малышу, чтобы прививка подействовала с максимальной пользой? Уже за 5-7 дней до прививки постарайтесь отгородить ребенка от многочисленных сборищ – и не только детских. Не стоит вести его на рынок, запихивать в переполненный автобус и идти с ним на юбилей к любимой троюродной бабушке. Если ребенок часто страдает пищевой аллергией, придется несколько дней соблюдать диету, отказавшись от всех «запретных» лакомств. Накануне искупайте ребенка, ведь, как правило, несколько следующих дней ему придется обойтись без ванны. В день прививки измерьте ребенку температуру.
Не стоит вести его на рынок, запихивать в переполненный автобус и идти с ним на юбилей к любимой троюродной бабушке. Если ребенок часто страдает пищевой аллергией, придется несколько дней соблюдать диету, отказавшись от всех «запретных» лакомств. Накануне искупайте ребенка, ведь, как правило, несколько следующих дней ему придется обойтись без ванны. В день прививки измерьте ребенку температуру.
После прививки будьте повнимательнее к малышу. Его «обычные» капризы на этот раз могут быть вызваны недомоганием: побалуйте его ласками, но не лакомствами. Контролируйте температуру – ее повышение до38,5 градусов можно считать нормой. Она держится не дольше 2-3 дней и снижается без применения каких-либо лекарственных препаратов. Если состояние ребенка выходит за рамки обычного легкого недомогания, побалуйте его ласками, но не лакомством.
О профилактике поствакцинальных осложненийКогда подходит время делать ребенку плановую прививку, у родителей возникает масса опасений и подозрений, касающихся ее безопасности. Как подготовить ребенка к вакцинации и в последствии отличить нормальную реакцию детского организма от негативной? Особенно эти вопросы волнуют родителей детей, страдающих хроническими заболеваниями.
Как подготовить ребенка к вакцинации и в последствии отличить нормальную реакцию детского организма от негативной? Особенно эти вопросы волнуют родителей детей, страдающих хроническими заболеваниями.Вакцинация — единственный способ защиты от ряда заболеваний, которые невозможно вылечить другими средствами или само лечение может вызвать осложнение (например, корь, дифтерия и пр.). Врожденной невосприимчивости к инфекционным заболеваниям, от которых существуют прививки — нет. Если мама ребенка когда-то болела ими, то первые 3—6 месяцев жизни доношенный ребенок может быть защищен материнскими антителами, которые попали к нему через плаценту во время беременности и через грудное молоко. У недоношенных детей и детей на искусственном вскармливании такой защиты нет. Поскольку возможность заболеть из-за контактов с другими людьми велика, очень важно прививать малышей с самого раннего возраста.
Как же подготовить малыша к прививке и попытаться свести к минимуму риск возникновения осложнений?
Сразу отметим, что здоровых детей не требуется специально готовить к прививке, нужно лишь предварительно измерить температуру тела (она должна быть нормальной, чаще 36,6 градусов С; у детей до 1 года нормальной температурой может быть 37,1—37,2 градусов за счет особенностей теплообмена, он повышен, не зря детей, которые уже ходят, бегают, рекомендуется одевать чуть холоднее, чем взрослых), привести ребенка к специалисту и ответить на его вопросы.
Некоторые врачи прибегают к практике назначения всем детям перед прививкой, так сказать профилактически, приема противоаллергических препаратов, например ТАВЕГИЛА, КЛАРИТИНА, ЗИРТЕКА. В действительности такой «поголовной» необходимости нет. Не все дети предрасположены к аллергии и соответственно не все нуждаются в таких лекарствах. Скорее это происходит из-за желания врача лишний раз подстраховаться или из-за того, что выявление детей группы риска по аллергии это более трудоемкий процесс. Но если ребенок склонен к аллергическим реакциям, то профилактическое применение противоаллергических препаратов оправдано. Например, такая ситуация, ребенок первого года жизни, ранее аллергия не проявлялась, прививается против коклюша, дифтерии, столбняка (АКДС).
Первая прививка (на первом году АКДС делается трижды) прошла без особенностей, но после второй прививки ребенку начали вводить новое питание, и у малыша появилась впервые аллергическая сыпь, значит, перед третьей прививкой следует профилактически дать ребенку противоаллергический препарат, чтобы высыпания не повторились. Для профилактики поствакцинальных осложнений врач должен, в первую очередь, оценить состояние здоровья ребенка перед прививкой. Выявить противопоказания к ней — временные и постоянные (например, выраженная аллергическая реакция на предыдущее введение подобной вакцины), и решить вопрос о необходимости назначения каких-либо предварительных дополнительных обследований и лекарственных препаратов. Перед прививкой врач (фельдшер) осматривает ребенка, измеряет температуру (она должна быть нормальной — 36,6 градусов С), подробно расспрашивает родителей о жизни ребенка, перенесенных им заболеваниях и прочее. Родители, в свою очередь, должны проинформировать врача о всех особенностях и проблемах здоровья своего малыша.
Для профилактики поствакцинальных осложнений врач должен, в первую очередь, оценить состояние здоровья ребенка перед прививкой. Выявить противопоказания к ней — временные и постоянные (например, выраженная аллергическая реакция на предыдущее введение подобной вакцины), и решить вопрос о необходимости назначения каких-либо предварительных дополнительных обследований и лекарственных препаратов. Перед прививкой врач (фельдшер) осматривает ребенка, измеряет температуру (она должна быть нормальной — 36,6 градусов С), подробно расспрашивает родителей о жизни ребенка, перенесенных им заболеваниях и прочее. Родители, в свою очередь, должны проинформировать врача о всех особенностях и проблемах здоровья своего малыша.
О чем необходимо сказать врачу:
- Не повышалась ли температура в дни, предшествующие вакцинации? Не было ли каких-либо других признаков нездоровья, например, кашля, чихания, насморка, которые могут свидетельствовать о начале заболевания?
- Имеются ли у ребенка какие-либо хронические заболевания и не получает ли он в связи с этим постоянно лекарственные препараты, если да, то какие?
- Не было ли ранее судорог, выраженных аллергических реакций на пищу, лекарства и пр.?
- Необходимо рассказать, как ребенок переносил предыдущие прививки, повышалась ли у него температура, ухудшалось ли самочувствие и др.
- Не рекомендуется делать прививки сразу после возвращения из длительной поездки, особенно, если резко менялся климат, так как это создает условия для заболеваний.
- Необходимо сказать, получал ли ребенок в последние три месяца препараты, изготовленные на основе крови, или производилось ли переливание крови. Это влияет на сроки последующей вакцинации против кори, краснухи и паротита, они увеличиваются, т.к. препараты крови содержат готовые антитела — специфические защитные белки крови против указанных инфекций, которые «мешают» ребенку активно выработать иммунитет самому.
Если при осмотре перед прививкой врач делает заключение, что ребенок практически здоров, проводится прививка.
Когда и как прививают больных детей?Если у ребенка имеются заболевания, находящиеся в настоящее время вне обострения и ему нужно сделать прививку, то к мерам профилактики, проводимым у здоровых детей, добавляются предварительные обследования. Решается вопрос о необходимости назначения различных препаратов за 3—4 дня до проведения прививки и на весь период после процесса: 3—5 дней после введения неживых, химических вакцин и т.д., и 14 дней при использовании живых вакцин. В своих прошлых публикациях мы указывали на возможность развития осложнений после прививок . Их профилактика включает еще целый комплекс мероприятий, к которым относится соблюдение техники вакцинации, назначение в ряде случаев до прививки и после лекарственных средств, помогающих избежать осложнений, определенный режим и питание ребенка, патронаж (специальное наблюдение) после вакцинации. Медицинские работники навещают привитого ребенка на дому или узнают о состоянии его здоровья по телефону, чтобы не пропустить ситуации осложнения, развившиеся после прививки.
Какие признаки могут указать на неврологические проблемы ребенка при осмотре перед прививкой?У маленьких детей — напряжение, выбухание большого родничка в вертикальном положении, расширение подкожных вен головы, частые срыгивания, излишние движения языка, повышение мышечного тонуса рук и ног, тремор (мелкое дрожание) подбородка и рук в спокойном состоянии, нарушение сна и пр. Перечисленные признаки могут свидетельствовать о повышенном внутричерепном давлении. Чрезмерно быстрый рост головы, увеличение размеров большого родничка, вместо его сокращения и другие признаки могут свидетельствовать о гидроцефальном синдроме — избыточном накоплении мозговой жидкости в желудочках мозга и других внутричерепных пространствах. Эти и другие заболевания нервной системы выявляет и описывает при плановом осмотре детей до 3-х месяцев невролог.
Для подтверждения или исключения патологии проводят дополнительные исследования, например, ультразвуковое исследование головного мозга — нейросонографию, когда датчик аппарата устанавливается на большом родничке и на экране отображается картина строения мозга. Многие педиатры, неврологи склонны настороженно относиться к вакцинации детей с неврологическими проблемами из-за боязни усугубить течение патологии в поствакцинальном периоде. Это не правильно, так как инфекция, от которой проводится прививка, гораздо более опасна для ребенка с поражением нервной системы. Например, коклюш у таких детей, особенно в возрасте до года может вызывать тяжелые поражения мозга, судороги и прочее. К сожалению, иногда о поражении нервной системы начинают думать уже после прививки, которая спровоцировала временные ухудшения в работе этой системы. Поэтому основным средством предупреждения поствакцинальных осложнений со стороны нервной системы является своевременное выявление неврологической патологии у новорожденного, ее лечение и проведение прививок на фоне медикаментозной терапии или по ее окончании.
Какие медикаментозные средства обычно применяют при подготовке к иммунизации детей с неврологическими проблемами?
Детям с повышенным внутричерепным давлением и гидроцефальным синдромом, назначают мочегонные средства (в том числе травы), препараты, улучшающие кровоток и обмен веществ в мозговой ткани. Курсы терапии повторяют 2-3 раза в год, в эти же периоды может быть проведена иммунизация ребенка. Если прививкуделают после завершения лечения, то желательно в момент иммунизации снова провести короткий курс ранее применявшихся средств (мочегонных, успокоительных и т.п.). Если у ребенка были судороги, вызванные повышенной температурой, прививкиможно проводить не ранее, чем через 1 месяц после приступа. До и после прививки назначают противосудорожные, и иногда мочегонные лекарства. Детям, перенесшим судороги, причиной которых являлась температура выше 38,0 градусов С, в дальнейшем можно делать все прививки. Если судороги были на фоне температуры менее 38,0 градусов С, то не вводят коклюшную вакцину, входящую в состав комплексной вакцины против коклюша, дифтерии, столбняка (АКДС). Остальные вакцины могут быть использованы. Всем детям, ранее имевшим судороги или предрасположенным к ним, после прививки назначают и жаропонижающие препараты, так как вакцины могут вызвать высокую температуру и снова провоцировать судороги.
При наличии у ребенка эпилепсии, вакцинация также осуществляется не ранее, чем через 1 месяц после приступа, без коклюшной вакцины, на фоне противосудорожной терапии. При тяжелых формах эпилепсии вопрос о прививках решается индивидуально с врачом невропатологом. Дети с непрогрессирующими поражениями нервной системы (хромосомные, генетические заболевания, врожденные аномалии развития, детский церебральный паралич и т.п.), психическими заболеваниями вне острого периода, с умственной отсталостью и перенесшие воспалительные заболевания нервной системы не имеют противопоказаний к прививкам. Их вакцинируют с использованием симптоматической (применяемой при лечении конкретного заболевания) терапии или не назначают лекарств совсем.
Прививки и аллергические заболеванияДостаточно частой патологией на первом году жизни и в более старшем возрасте являются аллергические заболевания: пищевая аллергия, бронхиальная астма и т.п. Прививки в таком случае проводят не ранее 1 месяца после завершения обострения. Основными принципами профилактики осложнений после вакцинации у этой группы детей является — режим питания (особенно для детей с пищевой аллергией), исключающий введение новых продуктов за 5-7 дней до и после прививки. На новую пищу у них возможна аллергическая реакция, которую родители и врач ошибочно будут трактовать как реакцию на вакцину. Так же исключаются аллергены, на которые ребенок заведомо дает аллергические реакции. Например, ребенка с аллергией на пыльцу какого-либо растения не прививают, когда оно цветет.
До и после прививки могут быть назначены противоаллергические препараты, препараты, содержащие бифидо- и лактобактерии. Они благотворно влияют на микрофлору кишечника, так как при аллергических заболеваниях часто происходит ее нарушение. Детям с бронхиальной астмой, постоянно получающим ингаляционные препараты, в том числе и гормональные, это лечение не отменяется, а продолжается.
Вакцинация часто болеющих детейПри иммунизации детей, страдающих частыми респираторными заболеваниями, хроническими заболеваниями ЛОР — органов (уши, гортань, нос), повторными бронхитами, пневмониями, наиболее частой проблемой является развитие респираторных и других инфекций в поствакцинальном периоде. Предрасполагают к возникновению частых заболеваний особенности иммунной системы ребенка. Не у всех детей в одно время «созревают» иммунные реакции, поэтому одни являются более, а другие — менее восприимчивыми к инфекциям. Способствует заболеваниям и стрессовая ситуация, например, когда ребенок не комфортно себя чувствует в детском учреждении и находится в состоянии хронического стресса.
В какой-то мере к стрессу можно отнести и прививку. Для профилактики таких заболеваний до и после вакцинации назначают общеукрепляющие средства (витамины, растительные и гомеопатические средства) или противовирусные препараты, изготовленные на основе крови человека (ИНТЕРФЕРОН) или синтетический интерферон (ВИФЕРОН) и пр., а также, препараты, способные моделировать иммунитет (РИБОМУНИЛ, ПОЛИОКСИДОНИЙ и др.).
Как готовят к прививке старших дошкольников с хроническими заболеваниями?У более старших детей после прививки могут обостриться уже диагностированные хронические заболевания эндокринной системы, соединительной ткани, крови и кроветворных органов, почек, печени, сердца и др. Основной принцип иммунизации таких детей — прививать не ранее, чем через 1 месяц после окончания обострения и осуществлять профилактику обострений после прививки. Детям с хроническими заболеваниями проводят минимальное лабораторное обследование (например, анализы мочи при болезнях почек). Если анализы в норме, то ребенка прививают на фоне противорецидивной терапии, которую назначают за 3-5 дней до и на 7-14 дней после прививки. Рекомендуется провести контрольные лабораторные обследования через 7, 14 и 30 дней после прививки (анализы мочи, крови и др.). Такое обследование позволяет быть уверенным в достаточности медикаментозной терапии, которую получал ребенок в момент прививок. Если в анализах выявляются изменения, характерные для обострения хронического заболевания, то последующие прививки проводят после нормализации состояния на фоне более интенсивного лечения. Вот такая непростая последовательность комбинаций требуется для прививания заведомо нездорового малыша.
Но все же следует помнить о том, что инфекция, в плане обострения хронического заболевания много опаснее, чем возможность минимальных, крайне редко встречающихся, контролируемых обострений при вакцинации. Кроме того, детям с любыми хроническими заболеваниями рекомендуется проводить дополнительные прививки (помимо плановых) против гемофильной инфекции типа В, менингококковой, пневмококковой инфекций, гриппа. После прививки, и в последующие дни, родителям следует обращать внимание на состояние ребенка.
Первые три дня рекомендуется измерять температуру, особенно после прививкипротив коклюша, дифтерии и столбняка (АКДС, Тетракок). Если состояние не изменилось и не ухудшилось, т.е. малыш весел, бодр, у него хороший аппетит, спокойный сон и пр., то его режим жизни менять не нужно. Продолжайте как обычно, кормить, купать ребенка, гулять с ним. Единственно — следует ограничить общение с чихающими, кашляющими людьми, и детьми, чтобы ребенок не имел шансов заразиться. С этой же точки зрения не желательно путешествовать с ребенком сразу после прививки.
Если родителям необходимо куда-то уезжать с малышом, следует подумать о прививках заранее, за 1-2 недели до отъезда. За это время успеют выработаться антитела на введенную вакцину и успеют проявиться нежелательные эффекты от прививки, если им суждено быть. В дороге или в чужом городе может оказаться сложнее оказать медицинскую помощь ребенку.
Что же делать, если после прививки повысилась температура, ухудшилось общее состояние малыша?Следует воздержаться от купания и прогулок. Сообщите о нарушении состояния ребенка медицинской сестре, которая проводит патронаж после прививки или врачу. Дайте жаропонижающие средства в возрастной дозировке: для детей, перенесших ранее судороги — сразу же при любой повышенной температуре (даже если это 37,1 градусов С), для остальных — при температуре выше 38,5 градусов С. Своевременное обращение к врачу позволит выяснить, с чем связана температура — с обычной реакцией на вакцину, случайным заболеванием или с чем-либо еще.
Правильно поставленный диагноз — залог безопасности дальнейшей вакцинации. Помните, что в месте введения всех вакцин может появиться краснота и уплотнение, которые должны пройти через 1-3 дня. Если уплотнение, покраснение держится дольше 4 дней или его размеры более 5-8 см, необходимо обязательно проконсультироваться у врача.
Можно ли делать прививку в специальном центре?Любого ребенка, а тем более, страдающего каким-либо заболеванием можно прививать в специализированных центрах иммунопрофилактики (филиалы таких центров могут существовать и в участковых поликлиниках), под наблюдением врачей иммунологов. Они составят индивидуальный график прививок, подберут оптимальный тип вакцины для конкретного малыша и пр. Такие меры позволят свести к минимуму риск развития поствакцинальных осложнений и создать эффективную защиту организма от тяжелых и опасных инфекций.
Исключение из правилИзвестно, что детям во время острого заболевания или обострения хронического, плановые прививки не проводят. Вакцинацию откладывают до выздоровления или завершения обострения хронического процесса. Однако, если возникает экстренная ситуация, когда нужно привить нездорового ребенка, это может быть сделано (вакцинация по экстренным показаниям). Например, ребенок болен ОРВИ, или у него обострилось хроническое заболевание, и при этом он общался с больным дифтерией или его укусила собака и т.д. В таких случаях противопоказаниями к вакцинации можно пренебречь, чтобы по жизненно важным обстоятельствам срочно привить ребенка.
Обновление политики в области здравоохранения и безопасности
Политика КПК в области здравоохранения и безопасности
По мере того, как мы возвращаемся к живым выступлениям, Kirkland Performance Center продолжает уделять приоритетное внимание здоровью и безопасности нашего сообщества, артистов и персонала. В дальнейшем нам потребуется подтверждение полной вакцинации для всех участников мероприятия. Кроме того, маскировка потребуется для посетителей, арендаторов и сотрудников внутри объекта, независимо от статуса вакцинации.
СотрудникиKPC проверит у дверей наличие доказательств вакцинации или отрицательного результата теста на COVID-19 в качестве условия въезда.Те, у кого нет документации, к спектаклю не допускаются.
Невакцинированные дети младше 12 лет должны предоставить доказательство отрицательного результата ПЦР на COVID-19 или теста на антиген в течение 48 часов до начала выступления. Отрицательные результаты тестов, о которых сообщают сами пациенты, которые получены не от поставщика услуг тестирования, лаборатории или поставщика медицинских услуг, не могут быть приняты.
Следующие данные принимаются в качестве доказательства полной вакцинации (для лиц старше 12 лет) с подтверждением идентификации.Дата въезда должна быть как минимум через 14 дней после второй дозы двухдозовой вакцины COVID-19 или как минимум через 14 дней после однократной дозы вакцины COVID-19:
- Карта вакцинации (которая включает имя вакцинированного лица, тип вакцины и дату введения последней дозы)
- Фотография карты прививок отдельным документом
- Фотография карты вакцины участника, хранящаяся на телефоне или электронном устройстве
- Документация о вакцинации из электронной медицинской карты поставщика медицинских услуг или государственной записи в информационной системе иммунизации
В качестве доказательства отрицательного результата теста на COVID-19 (для детей до 12 лет и детей, не имеющих медицинских или религиозных льгот) приемлемы следующие документы с соответствующим идентификатором:
- Печатный документ (от провайдера тестирования или лаборатории)
- Электронное письмо или текстовое сообщение, отображаемое на телефоне или электронном устройстве от провайдера тестирования или лаборатории.Предоставляемая информация должна включать имя тестируемого человека, тип проведенного теста и дату отрицательного результата теста.
Мы ожидаем, что положения о вакцинации и маскировке останутся в силе в обозримом будущем, но будем постоянно пересматривать эту политику, изменяя ее по мере необходимости. Эти правила могут быть изменены в любое время без предварительного уведомления.
Если у вас есть какие-либо вопросы о наших мерах безопасности и их потенциальном влиянии на ваш опыт работы с KPC, обращайтесь в кассу по телефону 425.893.9900, со вторника по субботу с 12:00 до 18:00.
Психиатрический центр Кингсборо
Адрес:
681 Кларксон Авеню
Brooklyn, NY 11203
Схема проезда
Телефон: (718) 221-7700 / 7259
Факс: (718) 221-7206
Электронная почта: Психиатрический центр Кингсборо
Возможности трудоустройства
Миссия психиатрической больницы — оказывать компетентную и сострадательную психиатрическую помощь людям с серьезными психическими заболеваниями с целью их реинтеграции в общество.
Оказанные услуги
Предоставляем:
- Комплексные комплексные услуги 24 часа в сутки для госпитализированных пациентов,
- Кризисное общежитие на 24 койки для пациентов, которые были выписаны, но нуждаются в завершении договоренностей для размещения в общежитии,
- 48-местная переходная резиденция,
- Программа семейного ухода на 65 коек с сертифицированными домами по месту жительства.
- Наши общинные амбулаторные клиники, расположенные в районах Канарси и Вильямсбург, предоставляют: оценку и планирование лечения; проверка здоровья и направления к специалистам; планирование выписки; словесная терапия; медикаментозная терапия; медикаментозное образование; управление симптомами; определение готовности к психиатрической реабилитации; управление делом; кризисное управление; клиническая поддержка; мобильная связь; служба поддержки семьи.
Расположение поликлиники
Клиника Канарси
9801 Foster Ave
Бруклин, Нью-Йорк 11236
(718) 257-7780
Клиника Вильямсбург
10 Манхэттен-авеню
Бруклин, Нью-Йорк 11206-3950
(718) 388-3075 X301
Обслуживаемая территория
Округ Кингс (Бруклин) и регион Большого Нью-Йорка
Обслуживаемые возрастные группы
Взрослые от 18 лет и старше.
Общественный транспорт.
Метро:
Interborough Rapid Transit (IRT) № 2 или 5 до станции Winthrop Street. Больница находится на Кларксон-авеню между Олбани и Ютикой.
IRT № 3 или 4 до Ютика-авеню и Восточного бульвара. Затем следуйте указаниям автобуса ниже или дойдите до Ютики и Кларксона.
Автобус:
Utica Avenue Автобус № 46 до Кларксон-авеню.
Автобус №14 от Eastern Parkway до авеню Ютика и пересадка на автобус №46.
Church Avenue Автобус № 35 до Utica Avenue и пересадка на автобус № 46.
Почти четверть медицинских работников в больницах Южной Калифорнии не получили вакцину от COVID-19, по федеральным данным
ЛОС-АНДЖЕЛЕС (KABC) — Почти четверть медицинских работников в Южной Калифорнии до сих пор не сделали прививку от COVID-19. , по федеральным данным.Федеральные данные, предоставленные 98 больницами региона, показывают, что 22% их медицинского персонала остаются непривитыми.
Это произошло после того, как Kaiser Permanente, крупнейшая в стране некоммерческая организация здравоохранения, заявила, что сделает вакцины против COVID-19 обязательными для всех своих сотрудников и врачей.
Примерно 22% медицинских работников в больницах Kaiser Permanente в Южной Калифорнии до сих пор не получили вакцину COVID-19 по состоянию на последнюю неделю июля, согласно последним федеральным данным и подтвержденным официальными лицами Kaiser. .
«Мы ожидаем, что к 30 сентября этого года все наши врачи и персонал будут вакцинированы», — сказала д-р Нэнси Джин, региональный медицинский директор по качеству Kaiser Permanente Southern California.
Сообщать эти числа необязательно, согласно U.S. Документ Министерства здравоохранения и социальных служб. Термин «медицинский персонал» включает «всех оплачиваемых и неоплачиваемых лиц, работающих в медицинских учреждениях, которые могут напрямую или косвенно контактировать с пациентами или инфекционными материалами». Это может быть интерпретировано отдельными больницами.
Как в округах Лос-Анджелес, так и в округах Риверсайд 24% медицинских работников в больницах, заявивших о болезни, остаются непривитыми.
В Вентуре 21%; в Сан-Бернардино — 18%; и 14% в округе Ориндж.
Больницы в Южной Калифорнии с самым высоким уровнем невакцинированных медицинских работников включают Глобальный медицинский центр Menifee и Глобальный медицинский центр Hemet в округе Риверсайд.
Оба являются частью здоровья KPC. Доктор Суманта Чаудхури, главный научный сотрудник KPC Health, выступил с заявлением в ответ на федеральные данные:
«Многие из наших сотрудников выбрали вакцинацию. Мы продолжаем призывать тех, кто не был вакцинирован, серьезно подумать о том, чтобы сделать это.«Вакцина является самой надежной защитой от заражения COVID-19», — написал Чаудхури.
Но, по данным HHS, глобальный медицинский центр округа Ориндж (KPC) входит в число больниц с самым высоким уровнем вакцинированных медицинских работников.
Потому что данные самооценка и необязательность, не все больницы представили данные о вакцинации, а некоторые оспорили эти цифры.
Федеральные данные также показывают, что около половины персонала, работающего в больнице Cedars-Sinai Marina Del Rey, не были вакцинированы.Но представитель Cedars-Sinai сказал, что среди непривитых есть независимые подрядчики и волонтеры, которые не работали там довольно долгое время. Их собственные данные показывают, что 78% их сотрудников полностью вакцинированы.
Графика отображается неправильно? Щелкните здесь, чтобы открыть карту в новом окне. Щелкните здесь, чтобы открыть таблицу в новом окне.Несмотря на расхождения в некоторых отчетах, администраторы заявили, что цифры показывают, что даже медицинские работники, которые лично видели страдания, могут колебаться после того, как попали под влияние дезинформации.
«Эта культура, основанная на взглядах на вакцинацию, влияет на людей. Даже на людей, которые занимаются наукой», — сказал Гин.
Больницы с более высоким уровнем вакцинации включают региональный медицинский центр Лейквуда, медицинский центр MemorialCare Orange Coast и медицинский центр Long Beach Memorial.
Доктор Гин сказал, что Kaiser Permanente работает со своими партнерами по работе, чтобы определить, какие будут последствия, если рабочие не будут вакцинированы. Она сказала, что цель — защитить пациентов, но в конечном итоге положить конец этой пандемии.
«Мы знаем, что это будет не последний вариант, который появится. Будут и другие. Мы просто не знаем, когда это будет, но они придут», — сказал Гин. «И поэтому мы хотим быть настолько подготовленными и защищенными, насколько это возможно в нашем сообществе».
Авторские права © 2021 KABC Television, LLC. Все права защищены.
Вакцина против листерий и истощение Т-регуляторных клеток активируют иммунитет против ранней стадии внутриэпителиальных новообразований поджелудочной железы и продлевают выживание мышей
Гастроэнтерология.Авторская рукопись; доступно в PMC 2015 1 июня.
Опубликован в окончательной отредактированной форме как:
PMCID: PMC4035450
NIHMSID: NIHMS576160
, 1, 2 , 3 , 1 9017 4 , 5 , 1 , 6 , 6 , 4 , 4 , 7 , 1 и 1Бриджит П. Кинан
72
Онкологический центр Сидни Киммела, Центр клинических исследований рака поджелудочной железы им. Скип Вирага и Центр рака поджелудочной железы Сола Голдмана в Джонс Хопкинс, Балтимор, Мэриленд2 Программа аспирантуры по иммунологии, Школа медицины Университета Джонса Хопкинса, Балтимор, Мэриленд
Yvonne Saenger
3 Отделение гематологии и онкологии, Институт рака Тиша и отделение дерматологии, Медицинская школа Маунт-Синай, Нью-Йорк, Нью-Йорк
Мишель И.Кафруни
1 Онкологический центр Сидни Киммела, Центр клинических исследований рака поджелудочной железы им. Скипа Вирага и Центр рака поджелудочной железы Сола Голдмана в Джонс Хопкинс, Балтимор, Мэриленд
Эшли Лейбнер
1 Центр рака Сиднея Киммела , Центр клинических исследований рака поджелудочной железы имени Скип Вирага и Центр рака поджелудочной железы Сола Голдмана в Джонс Хопкинс, Балтимор, Мэриленд
Питер Лауэр
4 Aduro BioTech, Inc, Беркли, Калифорния
Анирбан
5 Отделение патологии и трансляционной молекулярной патологии, Онкологический центр доктора медицины Андерсона Техасского университета, Хьюстон, ТехасAgnieszka A.Rucki
1 Онкологический центр Сидни Киммела, Центр клинических исследований рака поджелудочной железы им. Скипа Вирага и Центр рака поджелудочной железы Сола Голдмана в Джоне Хопкинсе, Балтимор, Мэриленд
Эндрю Дж. Гандерсон
6 Отделение клеток и биологии развития, Knight Cancer Institute, Орегонский университет здоровья и наук, Портленд, Орегон
Lisa M. Coussens
6 Департамент клеточной биологии и биологии развития, Knight Cancer Institute, Орегонский университет здравоохранения и наук, Портленд, Орегон
Дирк Г.Brockstedt
4 Aduro BioTech, Inc, Беркли, Калифорния
Thomas W. Dubensky, Jr
4 Aduro BioTech, Inc, Беркли, Калифорния
Raffit Hassan Молекулярная биология, Центр исследований рака, Национальный институт рака, Национальные институты здравоохранения, Бетезда, Мэриленд
Тодд Д. Армстронг
1 Онкологический центр Сидни Киммела, Центр клинических исследований рака поджелудочной железы имени Скип Вирага и Сол Центр рака поджелудочной железы Голдмана при Джоне Хопкинсе, Балтимор, Мэриленд
Элизабет М.Jaffee
1 Онкологический центр Сидни Киммела, Центр клинических исследований рака поджелудочной железы им. Скипа Вирага и Центр рака поджелудочной железы Сола Голдмана в Джоне Хопкинсе, Балтимор, Мэриленд
1 Онкологический центр Сидни Вираг, Скип Вираг Центр клинических исследований рака поджелудочной железы и Центр рака поджелудочной железы Сола Голдмана в Джонс Хопкинс, Балтимор, Мэриленд
2 Программа для аспирантов по иммунологии, Школа медицины Университета Джона Хопкинса, Балтимор, Мэриленд
3 Отдел гематологии и Онкология, Институт рака Тиша и Отделение дерматологии, Медицинская школа Маунт-Синай, Нью-Йорк, Нью-Йорк
4 Aduro BioTech, Inc, Беркли, Калифорния
5 Отделение патологии и трансляционной молекулярной патологии, Университет из Техасского онкологического центра доктора медицины Андерсона, Хьюстон, Техас
6 Отделение клеток и биологии развития, Knight Cancer Institute, Орегонский университет здоровья и наук, Портленд, Орегон
7 Лаборатория молекулярной биологии, Центр исследований рака, Национальный институт рака, Национальные институты здравоохранения, Бетесда, Мэриленд
Запросы на перепечатку направляйте по адресу : Элизабет М.Джеффи, доктор медицины, Онкологический центр Сидни Киммела, Джонс Хопкинс, 1650 Орлеан-стрит, 4M07 Бантинг Блаустейн, Центр исследования рака, Балтимор, Мэриленд 21231. ude.imhj@eeffaje; факс: (410) 614-8216. Окончательная отредактированная версия этой статьи издателем доступна в Gastroenterology. См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
ИСТОРИЯ И ЦЕЛИ
Предраковые поражения и опухоли на ранних стадиях содержат иммуносупрессивные микросреды, которые создают барьеры для противораковых вакцин. Kras G12D / + ; Trp53 R172H / + ; У мышей Pdx-1-Cre (KPC), которые экспрессируют активированную форму Kras в тканях поджелудочной железы, развиваются интраэпителиальные новообразования поджелудочной железы (PanIN), которые прогрессируют до протоковой аденокарциномы поджелудочной железы (PDA). Мы использовали этих мышей для изучения иммуносупрессии КПК.
МЕТОДЫ
Мы иммунизировали KPC и Kras G12D / + ; Pdx-1-Cre мышей с ослабленными внутриклеточными Listeria моноцитогенами (которые индуцируют Т-клеточный иммунитет CD4 + и CD8 + ), сконструированные для экспрессии Kras G12D (LM-Kras).Вакцину вводили отдельно или в последовательности с антителом к CD25 (РС61) и циклофосфамидом для истощения Т-регуляторных (Treg) клеток. Было измерено время выживания; Ткани поджелудочной железы и селезенки собирали и анализировали с помощью гистологического, проточного цитометрии и иммуногистохимического анализа.
РЕЗУЛЬТАТЫ
Интерферон γ-опосредованный, CD8 + Т-клеточные ответы наблюдались у KPC и Kras G12D / + ; Pdx-1-Cre мышам, получавшим LM-Kras, но не невакцинированным мышам.Введение LM-Kras мышам KPC в возрасте 4–6 недель (с PanIN на ранней стадии), лишенным Treg-клеток, значительно увеличило выживаемость и снизило прогрессирование PanIN (средняя выживаемость, 265 дней) по сравнению с невакцинированными мышами (средняя выживаемость, 150 дней). ; P = 0,002), мыши, получавшие только LM-Kras (средняя выживаемость, 150 дней; P = 0,050), и невакцинированные мыши, лишенные Treg-клеток (медиана (выживаемость в среде, 170 дней; P = У 8-12-недельных мышей (с поздними стадиями PanIN) LM-Kras, отдельно или в комбинации с истощением Treg-клеток, не увеличивал время выживания или не замедлял прогрессирование PanIN.Комбинация LM-Kras и истощения клеток Treg уменьшила количество Foxp3 + CD4 + Т-клеток в лимфатических узлах поджелудочной железы, увеличила количество CD4 + Т-клеток, которые секретируют интерлейкин 17 и интерферон g, и вызвала CD11b + Gr1 + клеток поджелудочной железы для приобретения иммуностимулирующего фенотипа.
ВЫВОДЫ
Иммунизация мышей KPC с помощью Listeria monocytogenes , сконструированных для экспрессии Kras G12D , наряду с истощением Treg-клеток, снижает прогрессирование PanIN на ранней, но не поздней стадии.Такой подход увеличивает инфильтрацию поражения воспалительными клетками. Возможно, удастся разработать иммунотерапию против предраковых поражений поджелудочной железы, чтобы замедлить или предотвратить прогрессирование до PDA.
Ключевые слова: Рак поджелудочной железы, вакцина против листерий, микросреда опухоли, иммунитет
Аденокарцинома протока поджелудочной железы (PDA) клинически трудно поддается лечению из-за ее позднего выявления и устойчивости к традиционным методам лечения. Однако недавние исследования показали, что процесс развития ОАП от инициации опухоли до метастазов требует от многих лет до десятилетий, обеспечивая окно возможностей для предотвращения предракового прогрессирования на стадии, когда преобладают предраковые поражения, известные как интраэпителиальные новообразования поджелудочной железы (PanINs). . 1 Один из возможных подходов к лечению включает разработку стратегий иммунизации, направленных на ранние генетические изменения (гены-драйверы), которые инициируют формирование предраковых поражений.
Механизмы иммунной толерантности к аутоантигенам являются серьезными препятствиями на пути противоопухолевой иммунотерапии, особенно после развития КПК. 2–4 Лечения, которые обходят толерантность и вызывают специфический противоопухолевый иммунный ответ на периферии, все еще неэффективны из-за иммуносупрессивного микроокружения опухоли (TME), которое включает T-регуляторные клетки (Tregs), толерогенные антигенпредставляющие клетки, миелоидные клетки. производные супрессорные клетки (MDSC), иммунорегуляторные молекулы и иммуносупрессивные цитокины. 5–8 Из этих барьеров было показано, что Treg и MDSC увеличиваются в опухолях мышей и пациентов 3,5,9,10 , ингибируя защитные ответы Т-клеток CD8 + и способствуя росту PDA. 11–13 Стратегии лечения, нацеленные на эти подавляющие группы населения, усиливают активацию раковых Т-клеток в доклинических и клинических исследованиях. 12,14 Истощение Treg способствует эрадикации опухоли за счет увеличения отношения эффекторных Т-лимфоцитов к Treg в опухоли и лимфатических узлах, дренирующих опухоль, ключевых местах накопления и активации Treg. 8,12,15
Генно-инженерные мыши, имитирующие генетическую индукцию и прогрессирование опухолей в естественном органе, позволяют изучать иммунные ответы на рак и его предшественники в контексте естественных механизмов толерантности. 10 Kras G12D / + ; Pdx-1-Cre (KC) и Kras G12D / + ; Trp53 R172H / + ; Мыши Pdx-1-Cre (KPC) генетически запрограммированы таким образом, чтобы имитировать прогрессирование от нормальной ткани через все стадии предраковых PanIN к полностью развитому PDA, который генетически и гистологически повторяет болезнь человека. 16,17 Здесь мы сообщаем о наблюдении, что инфильтрация Treg происходит уже на стадии 1 PanIN. Учитывая раннее присутствие супрессивных клеток в месте развития опухоли, мы предположили, что иммунизация ослабленным внутриклеточным Listeria monocytogenes (LM ) вакцина, генетически модифицированная для экспрессии продукта гена драйвера Kras G12D (LM-Kras), потребует сопутствующей модуляции одного или нескольких иммунных ингибирующих механизмов для эффективного замедления прогрессирования PanIN.Мы показываем, что вакцинация LM-Kras и истощение Treg замедляют прогрессирование до PDA при введении на стадии PanIN 1, но не после того, как развиваются стадии 2–3 PanIN. Кроме того, истощение LM-Kras и Treg изменяет фенотип клеток CD11b + Gr-1 + в поджелудочной железе и рекрутирует эффекторные лимфоциты типа Т-хелперные клетки (Th) / Tc-17, способные останавливать раннюю прогрессию PanIN. Таким образом, вакцинационная первичная профилактика рака поджелудочной железы возможна, но требует одновременной иммунной модуляции.
Материалы и методы
Мыши
Lox-STOP-Lox Trp53 R172H / + ; Lox-STOP-Lox Kras G12D / + ; и штаммы Pdx-1-Cre на смешанном фоне 129 / SvJae / C57BL / 6 были подарком доктора Дэвида Тувсона (Лаборатория Колд-Спринг-Харбор, Колд-Спринг, Нью-Йорк). 16,17 Этих мышей подвергали обратному скрещиванию с генетическим фоном C57BL / 6 в течение 12 поколений и скрещивали для получения мышей KC и KPC. Животных содержали в условиях, свободных от патогенов, и лечили в соответствии с политикой, утвержденной Комитетом по уходу и использованию животных и Американской ассоциацией комитета лабораторных животных.
Пациенты и образцы опухолей
Образцы биопсии мезотелиомы были собраны у субъекта в исследовании ADU-CL-02, исследовании фазы I, оценивающем безопасность и индукцию иммунного ответа CRS-207, вакцины LM, нацеленной на мезотелин, в сочетании с химиотерапия у больных злокачественной мезотелиомой плевры. 18 Пациенты предоставили подписанное информированное согласие после утверждения исследования наблюдательным советом учреждения.
LM Construct
Вакцина LM-Kras была сконструирована на штамме с двойной делецией actA и inlB . 19 Кассета экспрессии 12 ras была сконструирована in silico для слияния 25 аминокислот активирующих мутаций V и D (в положении 12) в синтетическом гене, клонированном ниже промотора actA , как описано ранее. 19,20
Эксперименты по выживанию
LM-Kras (5 × 10 5 колониеобразующих единиц) в 0,2 мл фосфатно-солевого буфера вводили внутривенно на основании титрования доз для каждой партии вакцины. Мышам KPC в возрасте 4-6 недель или 8-14 недель вводили PC61 (50 мкг / мышь) 12 и циклофосфамид (Cy) (100 мг / кг; Bristol-Myers Squibb, New York, NY) путем внутрибрюшинной инъекции, За 1 день до вакцинации согласно плану эксперимента.Этот режим повторялся каждые 4 недели, а выживаемость контролировалась еженедельно.
Анализы внутриклеточных цитокинов и проточная цитометрия
CD8 + селезенки Т-клетки отбирали отрицательно и инкубировали с клетками T2K b и пептидами с последующим окрашиванием внутриклеточных цитокинов, как описано ранее. 15 Pancreata получали путем инкубации с 1 мг / мл коллагеназы и 25 мг / л гиалуронидазы в течение 30 минут при 37 ° C с последующей очисткой в градиенте Percoll.Лимфоциты стимулировали T-Activator CD3 / CD28 Dynabeads Mouse (Life Technologies, Grand Island, NY) в течение ночи при 37 ° C в соответствии с инструкциями производителя. Лимфоциты от 3 поджелудочной железы мыши были объединены и окрашены как один образец проточной цитометрии из-за небольшого числа клеток. Проточную цитометрию проводили с указанными антителами (дополнительная таблица 1) с использованием LSR II и анализировали с использованием программного обеспечения FACSDiva (BD Biosciences, Сан-Хосе, Калифорния).
Иммуногистохимия
Иммуногистохимия (ИГХ) была проведена с указанными антителами в соответствии со стандартными протоколами, если не указано иное (дополнительные материалы и методы и дополнительная таблица 2). 21 Все слайды получали с помощью камеры Eos Rebel T2i (Canon USA, Мелвилл, Нью-Йорк) и микроскопа Eclipse TS100 (Nikon, Inc, Мелвилл, Нью-Йорк).
Гистологический анализ поражений поджелудочной железы
Панкреату фиксировали формалином и залили парафином, разрезали на толщину 4- мкм мкм и окрашивали с использованием стандартных протоколов окрашивания H&E в лаборатории тканевых микрочипов Johns Hopkins. Для анализа вакцины и эффекта (-ов) истощения Treg, 2 предметных стекла от каждой поджелудочной железы, расположенных на расстоянии 400- мкм друг от друга м, были оценены на основе наивысшей стадии PanIN (или PDA), представленной патологом, не имеющим отношения к группе лечения.
Массив цитокинов
Панкреату мышей KPC в каждой группе лечения объединяли и выделяли клетки Gr-1 + с помощью флюоресцентно-активированной сортировки клеток из CD45 + CD11b + Gr-1 + популяции с использованием FACSAria II (BD Biosciences). Клетки лизировали в соответствии с инструкциями, и лизат подвергали блоттингу с использованием массива мышиных цитокиновых антител, панель A (R&D Systems, Миннеаполис, Миннесота). Полученный дот-блот сканировали и анализировали с использованием VisionWorks Q23 LS (UVP, LLC, Upland, CA) для расчета плотности на пиксель и кратного изменения экспрессии обработанных клеток по сравнению с необработанными клетками.
Статистический анализ
Данные были выражены как среднее значение ± стандартная ошибка среднего, и все эксперименты были повторены 3 раза, если не указано иное. Статистическую значимость анализировали с помощью GraphPad Prism (GraphPad Software, Inc, Ла-Хойя, Калифорния) и оценивали с помощью двустороннего критерия Стьюдента t . Поправка Уэлча использовалась, когда предполагалось, что дисперсия неравна. Для анализа выживаемости использовали критерий лог-ранга (Мантела – Кокса).
Результаты
LM-Kras индуцирует систематические CD8
+ Т-клеточные ответы в Kras G12D / + — экспрессирующие мышиМы выбрали мутант Kras (Kras G12D ) в качестве мишени для вакцинации, потому что он распространенный и самый ранний онкоген, вовлеченный в развитие КПК человека. 22 Бактериальный вектор, LM, был выбран, потому что вакцины на основе LM индуцируют устойчивый антиген-специфический Т-клеточный иммунитет CD4 + и CD8 + . 23,24 Доказано, что вакцина LM безопасна для лечения пациентов с КПК. 18 Сначала мы идентифицировали специфические пептиды из 9 аминокислот (9-мер), представленные аллелем главного комплекса гистосовместимости (MHC) I, H-2K b , путем скрининга перекрывающихся пептидов на распознавание активированными иммунизированными лимфоцитами, выделенными от вакцинированных мышей. с LM-Kras (). 25 Вакцинированные, нетолерантные, соответствующие MHC мыши несут интерферон (IFN) γ-секретирующие CD8 + Т-клетки, ответственные на множественные мутантные эпитопы Kras (Kras B – G) по сравнению с контрольным белком 2, связанным с тирозиназой (Trp2) эпитоп, который также связывается с MHC IK b (). Вакцина LM-Kras индуцировала Kras-специфические Т-клеточные ответы IFNγ CD8 + у мышей, экспрессирующих мутантный аллель Kras G12D , тогда как Krass-специфические Т-клеточные ответы CD8 + не были обнаружены у невакцинированных мышей KC и KPC, что позволяет предположить, что сама мутация не является иммуногенной по своей природе (и дополнительный рисунок 1).Удивительно, но эти исследования не смогли выявить различий в величине системных Krass-специфических Т-клеточных ответов CD8 + у нетолерантных родительских мышей по сравнению с трансгенными мышами, экспрессирующими мутацию Kras G12D (). Таким образом, LM-Kras может индуцировать значительный системный Т-клеточный ответ CD8 + против мутантного Kras как у родительских, так и у потенциально толерантных мышей KC и KPC.
Иммуногенность ЛМ-Крас. ( A ) 25меры мутантных аллелей Kras были клонированы ниже и в рамке считывания с аминоконцом ActA и помечены иммунологическими позитивными контрольными Т-клеточными эпитопами для мышей Balb / c (A, SYIPSAEKI) и мышей C57BL / 6 ( B, SIINFEKL), а также эпитоп С-концевого антитела (C, Myc).( B ) Последовательность эпитопов, используемых для тестирования иммуногенности LM-Kras, с мутантным остатком 12, выделенным жирным шрифтом . (C) CD8 + Т-клеточные ответы селезенки однопометных мышей KPC дикого типа (n = 5) оценивали через 7 дней после LM-Kras путем инкубации с указанным пептидом и клетками T2K b и внутриклеточного окрашивания на IFNγ. . ( D ) Через 7 или 14 дней после вакцинации секрецию IFNγ Т-клетками CD8 + селезенки мышей KC, вакцинированных LMKras или необработанных, оценивали, как в панели C .( E ) Совокупные результаты 5 экспериментов, сравнивающих величину Т-клеточного ответа CD8 + на KrasF у мышей, экспрессирующих мутацию Kras G12D , по сравнению с однопометниками дикого типа. * P <.05, ** P <.01, *** P <.001.
Для подавления прогрессирования PanIN требуется как истощение Treg, так и LM-Kras
Поскольку в предыдущих исследованиях сообщалось, что Treg присутствуют в PanIN и КПК мышей KPC, 10 , мы дополнительно оценили кинетику инфильтрации Treg и обнаружили, что Foxp3 + клетки присутствуют даже на самой ранней стадии развития PanIN, PanIN 1, и продолжают увеличиваться при прогрессировании до злокачественного новообразования ().Комбинация мышиного анти-CD25-антитела, PC61, и низких доз Cy приводит к наиболее полному истощению Treg в КПК, когда комбинация вводится за 1 день до вакцинации. 12 Мы использовали мышей KPC, а не KC, чтобы проверить способность LM-Kras, вводимого отдельно или с истощением Treg, ингибировать опухоли, поскольку мутация Trp53 R172H / + вызывает развитие опухоли с предсказуемой скоростью, что облегчает анализ выживаемости. . На выживаемость оценивали две возрастные группы: мышей в возрасте 4–6 или 8–12 недель, что соответствует ранней или поздней стадии PanIN соответственно.LM-Kras и Treg-истощающие агенты, вводимые отдельно, не влияли на выживаемость в обеих возрастных группах по сравнению с необработанными мышами. Однако комбинированное истощение LM-Kras и Treg давало значительное преимущество в выживании животным, получавшим лечение во время развития PanIN 1, но не мышам, начинающим лечение во время PanIN 2 и 3 (2). Системный Т-клеточный ответ CD8 + на LM-Kras существенно не отличался у мышей KPC в возрасте от 4 до 6 недель и мышей от 8 до 12 недель (дополнительная фигура 2 A ).Кроме того, у мышей с PanIN на ранней стадии, получавших 2 цикла LM-Kras и истощения Treg, было меньше PanIN и PDA на поздней стадии по сравнению с другими группами лечения (2). Таким образом, общая более низкая стадия развития PDA у мышей, получавших комбинированное истощение LMKras и Treg, согласуется с улучшенной выживаемостью, наблюдаемой в.
Эффект вакцинации и истощение Treg на мышей KPC. ИГХ для Foxp3 в поджелудочной железе мышей KPC, содержащих ( A ) PanIN 1 на ранней стадии, ( B ) PanIN 2 средней стадии и ( C ) PDA при 40-кратном увеличении.( D ) Мышей KPC моложе 2 месяцев лечили LM-Kras, истощением Treg, комбинацией LM-Kras и истощения Treg или оставляли без лечения (без лечения). Ревакцинация проводилась ежемесячно с предварительной обработкой PC61 / Cy или без нее в соответствии с назначением группы. Логранговый анализ (Mantel – Cox) показал значительное улучшение выживаемости в группе комбинированной терапии по сравнению с отсутствием лечения ( P = 0,002) и истощением Treg или только LM-Kras ( P =.048 и P = 0,050 соответственно). Не было статистически значимой разницы в выживаемости между необработанной группой и животными, получавшими истощение Treg, или между необработанной и LM-Kras. ( E ) Мышей старше 2 месяцев лечили и наблюдали, как в панели D . Статистически значимой разницы в выживаемости между группами с использованием анализа Мантела – Кокса не было отмечено. ( F ) Мышей KPC в возрасте от 4 до 6 недель (n = 4-6 на группу) лечили, как в панели C , до 5 недели, когда животных умерщвляли и оценивали гистологию поджелудочной железы.
LM-Kras и Treg-истощение рекрутируют эффекторные Т-клетки на предраковый TME
Системный иммунный ответ на один мутантный пептид Kras, KrasF, и на овальбумин H-2K b -связывающий пептид, SIINFEKL (Ova), был оценивали через 1 неделю после 2 циклов иммунотерапии (конструкция LM-Kras содержит иммуногенный пептид Ova для подтверждения эффективности вакцины). Истощение Treg за 1 день до LM-Kras уменьшало системный ответ на пептид KrasF по сравнению с одним LM-Kras ().Напротив, не было существенной разницы между ответами Т-клеток CD8 + спленоцитов, измеренными против Ova у мышей, получавших LM-Kras и истощение Treg по сравнению с LM-Kras (). Хотя общее количество системных респондеров CD8 + и CD4 + было уменьшено с истощением LM-Kras и Treg по сравнению с одним LM-Kras, это не было значительным, что позволяет предположить, что это нельзя полностью отнести к генерализованной делеции Т-клеток. PC61 и Cy, и что нацеленные на Kras CD8 + Т-клетки на периферии специфически были затронуты истощением Treg (дополнительная фигура 3).Проточно-цитометрический анализ популяций Т-клеток CD4 + показал статистически значимое снижение Т-клеток CD4 + Foxp3 — по сравнению с Т-лимфоцитами CD4 + Foxp3 — в дренирующих поджелудочную железу лимфатических узлах и тенденция к меньшему количеству CD4 + Foxp3 + Т-клеток в поджелудочной железе мышей с PanIN на ранней стадии, получающих LM-Kras и истощение Treg, по сравнению с одним LM-Kras (). IHC для Foxp3 показал меньшее количество Treg в поджелудочной железе мышей KPC, получавших LM-Kras и истощение Treg ().
Системные и локальные Т-клеточные ответы с истощением Treg и LM-Kras. Мышей KPC лечили, начиная с возраста 4-6 недель, и собирали после 2 циклов обработки LM-Kras с истощением Treg или без него. ( A ) Процент CD8 + клеток селезенки, продуцирующих IFNγ в ответ на пептиды KrasF и Ova, нормализовали по ответу на пептид отрицательного контроля (Trp2) (n = 6-9 на группу обработки). ( B ) Отношение CD4 + Foxp3 + к CD4 + Foxp3 — клеток в лимфатическом узле поджелудочной железы и поджелудочной железе было измерено с помощью проточной цитометрии (n = 5–10 на группу лечения) и соответствует с окрашиванием Foxp3 в поджелудочной железе KPC (увеличение, 40 ×).( C ) Общее количество CD8 + и CD4 + Foxp3 — клеток на миллиграмм поджелудочной железы и процентное содержание CD44 высокий CD62L низкий было измерено с помощью проточной цитометрии (n = 7-8 на каждый группа). ИГХ для CD4 и CD8 показан при 20-кратном увеличении. ( D и E ) Лимфоциты поджелудочной железы рестимулировали с помощью гранул активации CD3 / CD28 в течение ночи и стробировали по CD3 + и CD4 + или CD8 + (n = 4 образца на группу).Показаны репрезентативные графики проточной цитометрии, а также общее количество каждой популяции. Общее количество клеток Tbet + и RORγt + CD4 + и CD8 + измеряли с помощью проточной цитометрии. Все данные представляют 2 или более независимых экспериментов. Популяции клеток, положительных по маркерам клеточной поверхности и цитокинам, регистрировали с использованием изотипических контролей и нестимулированных контролей для каждого образца. * P <.05, ** P <.01, *** P <.001.
Поскольку Т-клетки CD8 + исключены из поджелудочной железы у нелеченых мышей KPC, 10 мы оценили, привлекала ли терапия, истощающая Treg, введенная LM-Kras, преимущественно эффекторные Т-клетки в предраковую поджелудочную железу. В поддержку этой гипотезы мы наблюдали значительное увеличение количества CD8 + и CD4 + Foxp3 — Т-клеток в поджелудочной железе мышей, получавших LM-Kras и истощение Treg, по сравнению с одним LM-Kras– обработанных мышей, как измерено с помощью проточной цитометрии и подтверждено IHC ().Более высокий процент CD4 þ Foxp3 — и CD8 + Т-клеток, обнаруженных в PanIN мышей, получавших терапию, истощающую Treg, и LM-Kras: CD62L низкий CD44 высокий , что указывает на наличие антигена. фенотип по сравнению с мышами, получавшими только вакцину (). Несмотря на попытки, небольшое количество клеток в поджелудочной железе ограничивало возможность оценки Т-клеточного ответа на KrasF непосредственно ex vivo. Однако гранулы анти-CD3 / CD28 использовали для стимуляции лимфоцитов, выделенных из поджелудочной железы мышей KPC, впервые вакцинированных в возрасте 4-6 недель, что позволяет оценить цитокиновый профиль всех Т-клеток, инфильтрирующих PanIN.Истощение как LMKras, так и комбинированного LM-Kras и Treg привело к продукции эффекторных цитокинов, включая IFNγ, фактор некроза опухоли α и интерлейкин (IL) 17, в инфильтрирующих Т-лимфоцитах CD4 + и CD8 + , что коррелирует с экспрессией Tbet и RORγt. Важно отметить, что мыши, получавшие LM-Kras и истощение Treg, имели большее общее количество цитокин-продуцирующих Т-клеток CD4 + и CD8 + (). Мы подтвердили, что как Т-клетки CD8 + , так и клетки, секретирующие IL17, важны для задержки прогрессирования PanIN, потому что защитный эффект отменяется, когда клетки CD8 + истощаются и когда IL17 нейтрализуется во время истощения LM-Kras и Treg (дополнительный рисунок). 4).
Чтобы дополнительно проверить нашу гипотезу относительно индукции фенотипов Th27 с помощью вакцины Listeria , мы оценили ткань одного пациента в клиническом испытании CRS-207, вакцины, использующей тот же ослабленный вектор LM для нацеливания на мезотелин, без Treg. истощающая терапия. 18 Окрашивание на RORγt показало усиленное окрашивание в момент времени после LM по сравнению с биопсией до LM (дополнительная фигура 5 A ). Окрашивание серийных срезов из каждой временной точки анти-CD3 показало, что внутриядерное окрашивание RORγt коррелировало с клетками CD3 + в биопсии после LM, тогда как клетки CD3 + в биопсии перед LM были отрицательными для RORγt (дополнительные Фиг.5 ( B )), предполагая, что экспрессия IL17 в лимфоцитах, инфильтрирующих опухоль, может управляться с помощью вектора Listeria .
Истощение LM-Kras и Treg усиливает рекрутирование клеток Gr-1 поджелудочной железы
Ранее было показано, чтоMDSC инфильтрируют PanIN и PDA у необработанных мышей KPC, способствуя онкогенезу и ингибируя эффекторные Т-клетки. 10,11 Мы обнаружили, что общее количество клеток Gr-1 + (Ly6G — Ly6C high и Ly6G + Ly6C low ) увеличивалось у мышей, получавших истощение LM-Kras и Treg. при сравнении с только LM-Kras или нелеченными мышами того же возраста ().Ly6G + Клетки Ly6C low были преобладающей популяцией Gr-1 + , идентифицированной с помощью проточной цитометрии. Анализ IHC показал, что клетки Ly6G + начинают инфильтрировать PanIN на средней стадии, увеличиваются с прогрессированием до PDA у необработанных мышей KPC и являются многочисленными независимо от группы лечения (). Макрофаги F4 / 80 + были менее многочисленными, но демонстрировали аналогичную повышенную инфильтрацию с прогрессированием от PanIN на ранней стадии к PDA у обработанных и необработанных мышей KPC ().
Инфильтрация миелоидных клеток в необработанные и обработанные PanIN и КПК. ( A ) Панкреату мышей KPC, получавших 2 цикла LM-Kras с PC61 / Cy или без него, начиная с возраста 4-6 недель или оставленных без лечения в течение того же периода времени, анализировали с помощью проточной цитометрии (n = 4-6 мышей на группа). Представитель 2 экспериментов. * P <.05, ** P <.01. Панкреату собирали у необработанных мышей KPC разного возраста или мышей KPC в возрасте от 4 до 6 недель, получавших 2 цикла LM-Kras с истощением Treg или без него, и слайды окрашивали ( B ) Ly6G или (). C ) F4 / 80 антитела.( B и C ) Увеличение, 20 ×.
LM-Kras и истощение Treg реполяризуют PanIN-инфильтрирующие клетки Gr-1
+Поскольку количество миелоидных клеток Gr-1 + и макрофагов F4 / 80 + в PanIN не уменьшалось при иммунотерапии, мы предположили, что клетки с этими поверхностными маркерами представляют собой менее подавляющие популяции мышей Q28 с истощением LM-Kras и Treg. 26 Мы исследовали продукцию IL12 и IL10 клетками CD11b + Gr-1 + и F4 / 80 + из поджелудочной железы мышей, получавших 2 цикла терапии, и обнаружили, что LM-Kras вводился с или без Истощение Treg индуцировало секрецию IL12 клетками Gr-1 + , что приводило к увеличению общего количества IL12-секретирующих клеток Gr-1 + в поджелудочной железе мышей, которым вводили LM-Kras и истощение Treg ().Панин-инфильтрирующие макрофаги, обработанные LM-Kras или LM-Kras, и истощение Treg также продуцировали повышенное количество IL12 (). Не было существенной разницы в продукции IL10 макрофагами F4 / 80 + или клетками Gr-1 + (). Клетки CD11b + Gr-1 + из поджелудочной железы обработанных мышей секретировали более высокие уровни многих иммуностимулирующих цитокинов, чем необработанные мыши, включая хемокины, ответственные за набор миелоидных и лимфоидных клеток и M1 / N1-ассоциированные цитокины, ответственные за продвижение IFNγ и IL17. ответы в Т-клетках, при этом самые высокие уровни продуцируются клетками Gr-1 + от мышей, которым вводили LM-Kras и истощение Treg ().
Фенотип врожденных популяций поджелудочной железы мышей KPC. ( A ) Типичные графики проточной цитометрии показаны для мышей, получавших в возрасте 4-6 недель LM-Kras с истощением Treg или без него или оставленных без лечения. ( B ) Средние проценты и общее количество клеток Gr-1, экспрессирующих IL12 и IL10 + или F4 / 80 + на мг поджелудочной железы, показаны из тех же экспериментов, что и на панели A (n = 4-6 мышей на группу). Представитель 2 экспериментов. * P <.05. ( C ) Данные массива цитокинов с использованием клеточного лизата из объединенных клеток CD11b + Gr-1 + показаны в виде кратного изменения экспрессии для обработанных мышей по сравнению с необработанными мышами (n = 2 технических повтора на группу).
Обсуждение
Мы сообщаем здесь о новой модели разработки иммунотерапии для предотвращения предракового развития рака, которая нацелена на самый ранний драйверный ген в КПК, мутант Kras. Инактивация мутанта Kras обращает дисплазию на ранних стадиях Pan-IN и вызывает апоптоз более продвинутых PanINs и PDA у мышей KPC, обеспечивая дополнительное обоснование для воздействия на эту мутацию в PDA. 27 Кроме того, мы показываем, что вакцина Listeria может усиливать раннюю инфильтрацию воспалительных клеток, изменяя предзлокачественное микроокружение в пользу ингибирования прогрессирования поражения, когда вводится в сочетании с агентами для модификации TME. Кроме того, мы определили популяции CD8 + и Th27 Т-клеток как критические эффекторы предотвращения PDA.
Рак прогрессировал, когда мышей KPC лечили только LM-Kras, даже несмотря на то, что вакцина вызывала значительный периферический Т-клеточный ответ CD8 + , направленный против эпитопов мутантного аллеля Kras, показывая, что индукция системного антиген-специфического T клетки не составляют эффективного противодействующего иммунитета.Эти данные согласуются с предыдущими выводами о том, что повышенные уровни системных Т-клеточных ответов на вирусный антиген вируса папилломы человека, кодируемые вакцинами LM, не коррелируют с эффективностью в ортотопической модели рака шейки матки 28 , несмотря на хорошо задокументированную потребность в CD8. + Т-клеток для оценки эффективности вакцины. 23 Даже когда Т-клетки CD8 + способны проникать в опухоли, приток противоопухолевых эффекторных клеток может включать механизмы иммунной толерантности, включая рекрутирование Treg. 29
Модель мыши KPC имитирует естественно развивающийся КПК человека, характеризующийся гиповаскулярностью и плотным фиброзным стромальным ответом. 30,31 В отличие от трансплантируемого КПК, спонтанно развивающийся КПК у мышей устойчив к гемцитабину, если не подавляется строма. 32,33 PanINs и PDA у мышей KPC также могут различаться по чувствительности к проникновению других химиотерапевтических агентов, включая Cy, что объясняет статистически значимое истощение Treg в дренирующих лимфатических узлах, но не в опухоли.Возможно, что усиленное истощение опухоли Treg еще больше усилило бы эффекты LM-Kras и истощения Treg. С другой стороны, лимфатические узлы, дренирующие опухоль, являются решающим местом для управления толерантностью к опухолевым антигенам против развивающихся опухолей 8 , и истощение Tregs в дренирующем лимфатическом узле может быть достаточным для активации CD8 + и CD4 + эффекторных Т-клеток и инфильтрация в поджелудочную железу. Роль IL17-секретирующих клеток в предраковом микроокружении остается спорной.В модели трансплантируемой меланомы адоптивно перенесенные Т-клетки Th27 CD4 + превосходили Т-клетки Th2 CD4 + в эрадикации опухоли, возможно, благодаря способности клеток Th27 сохраняться и развиваться в другие субпопуляции Th in vivo. 34,35 Все больше данных подтверждают концепцию пластичности среди различных субпопуляций CD4 + Т-клеток и существование патогенных и непатогенных популяций даже в пределах одной субпопуляции Th. 36,37 Клетки Tc1 и Tc17, как было показано, эффективны на моделях опухолей мышей; Tc1 непосредственно за счет экспрессии цитотоксического опухолевого IFNγ и Tc17 за счет способности секретировать IFNg и IL17, а также поддерживать фенотип центральной памяти. 38-40 Хотя IL17 участвует в рекрутировании нейтрофилов и MDSC, которые могут способствовать прогрессированию рака, рекрутируемые IL17 нейтрофилы также могут способствовать противораковому ответу, в зависимости от контекста и типа опухоли. 41,42 Клетки как нейтрофилов, так и макрофагов накапливаются с возрастающей частотой по мере прогрессирования PanIN, что подчеркивает концепцию, согласно которой воспаление, вызванное острым и хроническим панкреатитом, связано с развитием рака поджелудочной железы. 43,44 Неожиданно мы обнаружили, что истощение LM-Kras и Treg, вводимое на ранних стадиях PanIN, на самом деле увеличивало распространенность клеток CD11b + Gr-1 + , включая как гранулоцитарные Ly6G + Ly6C low , так и моноцитарные Ly6G — Ly6C high клеток. Однако мы также обнаружили, что добавление LM-Kras, с истощением Treg или без него, привело к более высокому проценту клеток Gr-1 + , продуцирующих IL12 и другие противораковые цитокины в предзлокачественном микроокружении.Одним из возможных объяснений этого изменения функции является меньшее количество иммуносупрессивных сигналов от Treg и большее количество провоспалительных цитокинов, секретируемых после инфицирования антигенпрезентирующих клеток LM, включая IL12. 24 Совместное введение IL12 и Cy, как было показано, переключает фенотип клеток, инфильтрирующих опухоли, с MDSC на менее супрессивные незрелые миелоидные клетки. 45 В нашем исследовании, несмотря на сочетание провоспалительных и противовоспалительных цитокинов и хемокинов, секретируемых популяцией Gr-1 + у мышей, получавших LM-Kras и PC61 / Cy, общая тенденция была в направлении более иммуностимулирующий фенотип.Поляризация этих клеток в направлении противоопухолевого фенотипа должна служить терапевтической целью при лечении PDA как на ранних, так и на поздних стадиях.
Вакцины Listeria представляют собой эффективную стратегию индукции иммунного ответа на опухолевые антигены. CRS-207, вакцина LM, нацеленная на мезотелин, оказалась одновременно безопасной и способной индуцировать мезотелин-специфические Т-клетки CD8 + у пациентов с КПК. 18 Хотя интерпретация наших данных относительно индукции клеток типа Th27 / Tc17 при раке человека была ограничена доступностью образцов и использованием только вакцины LM без дополнительных иммунотерапевтических агентов в этом конкретном клиническом испытании, это предполагает, что LM-вакцины могут быть особенно эффективными в индукции сильных противораковых фенотипов в лимфоцитах, инфильтрирующих опухоль.Несмотря на эффективную индукцию иммунных ответов у мышей KPC с помощью LM-Kras, одной вакцины было недостаточно для защиты от PDA и задержки прогрессирования PanIN даже в возрасте, характерном для самых ранних стадий PanIN. Одним из ограничений модели KPC является то, что индукция мутировавших Kras и p53 является спонтанной и, следовательно, несколько гетерогенной, поэтому нам пришлось обобщить стадию PanIN по возрасту (в неделях) на основе предыдущих характеристик необработанных мышей KPC. Мы не можем установить, могли ли другие факторы, связанные с возрастом (помимо системных ответов Т-лимфоцитов CD8 + на Kras, которые существенно не различались), способствовать различиям в прогрессировании PanIN в группах PanIN на ранней и поздней стадиях.Однако было очевидно, что раннее вмешательство с комбинированным истощением LM-Kras и Treg было необходимо для перенаправления потенциально проонкогенного воспалительного ответа на эффективный противоопухолевый иммунный ответ. Поэтому будущие стратегии вакцинации потребуют включения агентов, предназначенных для изменения воспалительной среды в микросреде развивающейся опухоли, даже если они предназначены для профилактического лечения пациентов с предраковыми поражениями или с генетической предрасположенностью к развитию рака.
Благодарности
Авторы благодарят Т. Корниша (Медицинский факультет Университета Джона Хопкинса, Балтимор, Мэриленд) за предоставление программного обеспечения для анализа гистопатологии поджелудочной железы и Э. Шугара (Школа общественного здравоохранения Джона Хопкинса, Балтимор, Мэриленд) за предоставление советы по статистическому тестированию и анализу данных. Авторы также благодарят L. Zheng и A. Wu (медицинский факультет Университета Джона Хопкинса) за техническую помощь в области иммуногистохимии и A. Tam и L. Blosser за помощь в проточной цитометрии (Johns Hopkins SKCCC Flow Cytometry Core, Балтимор, Мэриленд).
Бриджит Кинан, Ивонн Сэнгер, Мишель Кафруни, Питер Лауэр, Дирк Брокштедт, Томас Дубенски-младший, Раффит Хассан, Тодд Армстронг и Элизабет Джаффи отвечали за концепцию и дизайн исследования; Бриджит Кинан, Ивонн Сэнгер, Мишель Кафруни, Эшли Лойбнер, Агнешка Раки, Эндрю Гандерсон и Тодд Армстронг отвечали за сбор данных; Бриджит Кинан, Ивонн Сэнгер, Мишель Кафруни, Анирбан Майтра, Агнешка Раки, Эндрю Гандерсон, Лиза Кусенс, Тодд Армстронг и Элизабет Джаффи отвечали за анализ и интерпретацию данных; Бриджит Кинан, Ивонн Сэнгер, Тодд Армстронг и Элизабет Джаффи подготовили рукопись; Бриджит Кинан, Тодд Армстронг и Элизабет Джеффи отвечали за критический пересмотр рукописи на предмет важного интеллектуального содержания; Бриджит Кинан, Ивонн Сэнгер и Мишель Кафруни отвечали за статистический анализ; и Элизабет Джаффи получила финансирование и отвечала за руководство исследованиями.
Финансирование
При поддержке грантов Национального института рака, Национальных институтов здравоохранения (P50CA062924, R01CA122081 и U19CA113341 для EMJ) и при частичной поддержке Программы внутренних исследований Национальных институтов здравоохранения, Национального института рака, Центр для исследования рака.
Аббревиатуры, использованные в этой статье
| Cy | циклофосфамид | |||
| IFN | интерферон | |||
| IHC | ILHC | |||
| LM-Kras | Listeria monocytogenes бактериальная вакцина, нацеленная на мутантную Kras | |||
| KC | Kras G12D / D , Pdx-1-Cre | |||
| KPC Trp53 R172H / D , Pdx-1-Cre | ||||
| MDSC | миелоидная супрессорная клетка | |||
| MHC | главный комплекс гистосовместимости | |||
| эпителия поджелудочной железы | ||||
| ПДН | ||||
| PanIN | протоковая аденокарцинома поджелудочной железы | |||
| RORγt | __________________________ | |||
| TME | микросреда опухоли | |||
| Treg | Т-регуляторная клетка | |||
| Trp2 | 0 Примечания 9102 9103 9103 : Чтобы получить доступ к дополнительным материалам, сопровождающим эту статью, посетите онлайн-версию Gastroenterology на сайте www.gastrojournal.org и http://dx.doi.org/10.1053/j.gastro.2014.02.055.

