Аутоиммунная гемолитическая анемия: лечение заболевания
Быстрый переходАутоиммунная гемолитическая анемия (АИГА) — группа редких приобретенных гематологических болезней и синдромов, характеризующихся гемолизом (разрушением) эритроцитов, вследствие образования аутоантител к антигенам этих компонентов крови.
АИГА может возникнуть в любом возрасте, чаще ей подвержены женщины (60%). Патология развивается постепенно или внезапно.
Выделяют два основных типа АИГА: тепловую (аутоантитела наиболее активны/атакуют эритроциты при температуре 37-40 °C) и холодовую — с холодовыми гемолизинами (аутоантитела наиболее активны при температуре менее 30 °C, эритроциты разрушаются даже при локальном воздействии холода, например, когда человек пьет холодную воду или моет руки в холодной воде).
Распространенность АИГА составляет 1 случай на 70-80 тысяч человек в год.
Причины
Причины возникновения заболевания изучены недостаточно.
Симптомы
У некоторых людей заболевание может протекать бессимптомно, особенно если АИГА развивается постепенно (разрушение эритроцитов не настолько масштабно). В основном же симптомы АИГА схожи с клиническими проявлениями других типов анемии (слабость, повышенная утомляемость, бледность кожных покровов).
Симптомы при более тяжелом течении заболевания (быстром разрушении эритроцитов) включают желтушность кожных покровов и видимых слизистых оболочек, слабость, повышенную утомляемость с тахикардией и одышкой при физической нагрузке, ощущение дискомфорта в животе, чувство переполнения, холодные конечности и периферический цианоз (при холодовой АИГА). При физикальном осмотре выявляется спленомегалия (патологическое увеличение размеров селезенки) различной степени.
При физикальном осмотре выявляется спленомегалия (патологическое увеличение размеров селезенки) различной степени.
Если АИГА развивается на фоне другой патологии, преобладать могут симптомы основного заболевания, например: увеличение и болезненность лимфатических узлов, лихорадка, сильные боли в спине и ногах, головные боли, рвота, диарея, изменение цвета мочи на темно-коричневый.
Диагностика
Диагностика АИГА включает физикальный осмотр, общий и биохимический анализы крови, морфологическое исследование эритроцитов. Основным критерием диагностического поиска является определение аутоантител с помощью прямого антиглобулинового теста (прямой пробы Кумбса).
Лечение аутоиммунной гемолитической анемии
Первой линией терапии тепловой аутоиммунной гемолитической анемии являются глюкокортикостероиды. Высокодозная монотерапия преднизолоном может назначаться в течение 3-6 недель с постепенным снижением дозы или отменой в дальнейшем. Однако из-за сильно выраженных побочных эффектов такого лечения все чаще используют краткосрочную пульс-терапию метилпреднизолоном или дексаметазоном. Примерно треть пациентов достигают ремиссии, остальным же необходима поддерживающая терапия ГКС.
Однако из-за сильно выраженных побочных эффектов такого лечения все чаще используют краткосрочную пульс-терапию метилпреднизолоном или дексаметазоном. Примерно треть пациентов достигают ремиссии, остальным же необходима поддерживающая терапия ГКС.
При неэффективности стероидной терапии рассматривается возможность проведения спленэктомии (хирургическое удаление селезенки), биологической терапии (ритуксимаб) или иммуносупрессивной терапии (циклоспорин, азатиоприн и др.).
Прогноз зависит от первопричины заболевания, своевременно начатого и правильно подобранного лечения. Благоприятный прогноз (достижение ремиссии, длительная ремиссия) полностью связан с положительным терапевтическим ответом у пациента и отсутствием осложнений.
Пациентам с холодовой аутоиммунной гемолитической анемией рекомендуется избегать триггеров (холода, в том числе инфузий холодных растворов), а также пройти лечение основного заболевания (например, лимфомы), если с ним связано развитие х-АИГА. Терапия первой линии при х-АИГА — ритуксимаб. ГКС не является терапией выбора из-за низкого терапевтического ответа у пациентов. Также неэффективна и спленэктомия. В тяжелых случаях рекомендован плазмоферез.
Терапия первой линии при х-АИГА — ритуксимаб. ГКС не является терапией выбора из-за низкого терапевтического ответа у пациентов. Также неэффективна и спленэктомия. В тяжелых случаях рекомендован плазмоферез.
Особенности и преимущества лечения аутоиммунной гемолитической анемии в клинике Рассвет
Аутоиммунная гемолитическая анемия достаточно редкое заболевание крови, по мере его изучения критерии диагностики и лечения дорабатываются и обновляются.
Гематологи клиники Рассвет придерживаются стандартизированных диагностических критериев и терапевтических подходов, разработанных Международной консенсусной группой по АИГА. Мы осознаем важность точного диагностического поиска у таких пациентов, поскольку течение заболевания и эффективное лечение зависят от типа задействованных антител. Для диагностики первичной АИГА мы используем моноспецифический прямой антиглобулиновый тест, обязательно выясняем причины манифестации вторичной АИГА, т. е. выявляем основное заболевание, с которым связано развитие гемолитической анемии.
При лечении т-АИГА мы используем глюкокортикостероиды. Ритуксимаб назначаем только на раннем этапе тяжелого течения заболевания, а также при отсутствии быстрого терапевтического ответа на стероиды. Ритуксимаб в сочетании с антинеопластическим препаратом назначаем пациентам с х-АИГА в случаях, если их состояние требует лечения по клиническим признакам.
Гематология Рассвета представлена врачами высокой квалификации, имеющими большой опыт в выявлении и лечении сложнодиагностируемых и редких болезней. В своей работе наши специалисты используют международные протоколы лечения, применяют только безопасные, доказанные и эффективные методы.
Иммунные гемолитические анемии — причины, симптомы, диагностика и лечение
Иммунные гемолитические анемии – группа заболеваний, обусловленных повышенным разрушением эритроцитов вследствие выработки антител против неизмененных красных кровяных телец или гаптенов, появившихся на мембране эритроцита. Различают изоиммунные, трансиммунные, гетерогенные и аутоиммунные гемолитические анемии. Клинические признаки: бледность или желтушность кожных покровов, умеренное увеличение печени и селезенки, боли в поясничной области, одышка и другие симптомы. Диагностика основана на изучении клинических данных, результатов лабораторных и инструментальных исследований. Лечение: гемотрансфузии, введение препаратов крови и кортикостероидов, иногда – спленэктомия.
Различают изоиммунные, трансиммунные, гетерогенные и аутоиммунные гемолитические анемии. Клинические признаки: бледность или желтушность кожных покровов, умеренное увеличение печени и селезенки, боли в поясничной области, одышка и другие симптомы. Диагностика основана на изучении клинических данных, результатов лабораторных и инструментальных исследований. Лечение: гемотрансфузии, введение препаратов крови и кортикостероидов, иногда – спленэктомия.
Общие сведения
Иммунные гемолитические анемии – группа заболеваний, характеризующихся повреждением и преждевременной гибелью эритроцитов или эритрокариоцитов в связи с развитием иммунной реакции с участием IgG и IgM или иммунных лимфоцитов. Основные факторы, вызывающие разрушение эритроцитов – аутоиммунный процесс, гемотрансфузионные осложнения, эритробластоз плода и гемолиз, обусловленный действием некоторых лекарственных средств.
Гемолиз может происходить в самом кровеносном русле или вне сосудов: в печени, селезенке, костном мозге. В результате массовой гибели красных кровяных телец развиваются анемический и желтушный синдромы, свидетельствующие о нарушении функции печени, почек, дыхательной системы, системы кровообращения, других органов и систем организма. По данным статистики, распространенность иммунных гемолитических анемий составляет примерно 1 случай на 70-80 тысяч населения.
В результате массовой гибели красных кровяных телец развиваются анемический и желтушный синдромы, свидетельствующие о нарушении функции печени, почек, дыхательной системы, системы кровообращения, других органов и систем организма. По данным статистики, распространенность иммунных гемолитических анемий составляет примерно 1 случай на 70-80 тысяч населения.
Иммунные гемолитические анемии
Причины иммунных гемолитических анемий
Возникновение этой группы заболеваний связано с воздействием различных неблагоприятных факторов внешней и внутренней среды, приводящих к развитию иммунных реакций против собственных эритроцитов. Чаще всего встречается аутоиммунный механизм, при котором происходит выработка антител против неизмененных естественных антигенов мембраны эритроцитов, находящихся в кровяном русле, или их предшественников – эритрокариоцитов костного мозга. Первичный причинный фактор, вызывающий разрушение эритроцитов, неизвестен (идиопатическая форма).
При вторичных анемиях патологический процесс развивается на фоне хронического лимфолейкоза, лимфомы, антифосфолипидного синдрома или иммунодефицитных состояний. Чаще встречается тепловая форма аутоиммунной анемии, при которой внутренняя среда организма имеет нормальные температурные параметры, а на эритроцитах располагаются иммуноглобулины класса G и компоненты комплемента C3 и C4. Красные кровяные тельца разрушаются макрофагами в печени и селезенке. Менее распространенная холодовая форма может быть идиопатической или вторичной, связанной с инфекцией (инфекционным мононуклеозом и микоплазменной пневмонией), переохлаждением и лимфопролиферативными заболеваниями у больных старше 60 лет. Реакция антиген-антитело с гемолизом развивается в периферическом кровяном русле, где температура опускается ниже 32 градусов.
Чаще встречается тепловая форма аутоиммунной анемии, при которой внутренняя среда организма имеет нормальные температурные параметры, а на эритроцитах располагаются иммуноглобулины класса G и компоненты комплемента C3 и C4. Красные кровяные тельца разрушаются макрофагами в печени и селезенке. Менее распространенная холодовая форма может быть идиопатической или вторичной, связанной с инфекцией (инфекционным мононуклеозом и микоплазменной пневмонией), переохлаждением и лимфопролиферативными заболеваниями у больных старше 60 лет. Реакция антиген-антитело с гемолизом развивается в периферическом кровяном русле, где температура опускается ниже 32 градусов.
Иммунная гемолитическая анемия может возникать при фиксации на мембране эритроцита фрагмента, имеющего лекарственное, вирусное или бактериальное происхождение (гетероиммунная форма). Образовавшиеся гаптены превращают красные кровяные тельца в чужеродные клетки-мишени для иммунной системы, что в итоге приводит к гемолизу. Чаще всего такую реакцию вызывают антибиотики из группы пенициллинов, цефалоспоринов и тетрациклинов, противотуберкулезные препараты, анальгетики и антиаритмические средства.
Чаще всего такую реакцию вызывают антибиотики из группы пенициллинов, цефалоспоринов и тетрациклинов, противотуберкулезные препараты, анальгетики и антиаритмические средства.
Изоиммунная форма встречается при несовместимости крови матери и плода по группе крови или резус-фактору. При этом антиэритроцитарные антитела матери через плаценту проникают к плоду и вызывают разрушение эритроцитов. Подобный механизм наблюдается и при переливании (гемотрансфузии) несовместимой крови от донора пациенту.
Классификация иммунных гемолитических анемий
Выделяют изоиммунные, трансиммунные, гетерогенные и аутоиммунные гемолитические анемии.
- К изоиммунным вариантам заболевания относятся посттрансфузионные осложнения, связанные с непереносимостью крови донора или неправильным соблюдением процедуры трансфузии, а также гемолитическая болезнь новорожденных.
- При трансиммунных анемиях гемолиз возникает при попадании к плоду через плаценту антител от матери, болеющей аутоиммунной анемией.

- Гетероиммунная (гаптеновая) анемия – результат изменения мембраны эритроцита при воздействии вирусов или лекарственных препаратов.
- Аутоиммунные гемолитические анемии (с тепловыми и холодовыми агглютининами).
Симптомы иммунных гемолитических анемий
Болезнь чаще начинается остро: повышается температура тела, появляется озноб, головная боль и головокружение, одышка, боли в эпигастральной области и пояснице. Кожные покровы становятся бледными, затем желтушными, могут появиться геморрагии, увеличивается селезенка, печень, цвет мочи становится темным.
При холодовой форме иммунной гемолитической анемии нередко нарушается периферическое кровообращение с развитием синдрома Рейно, посинением и отечностью кожных покровов кистей рук, лица, ушных раковин. В некоторых случаях нарушение кровоснабжения тканей конечностей может привести к развитию гангрены пальцев стоп.
Тяжелое течение эритробластоза плода характеризуется развитием ядерной желтухи с поражением центральной нервной системы – билирубиновой энцефалопатии. При этом отмечается вялость, заторможенность, снижение аппетита, частые срыгивания, судорожный синдром. При пальпации обнаруживают увеличение селезенки, печени, периферических лимфоузлов.
При этом отмечается вялость, заторможенность, снижение аппетита, частые срыгивания, судорожный синдром. При пальпации обнаруживают увеличение селезенки, печени, периферических лимфоузлов.
Диагностика иммунных гемолитических анемий
Чтобы установить правильный диагноз, определить форму заболевания, необходимо тщательное обследование пациента со сбором анамнеза, проведением клинического физикального осмотра врачом-гематологом, аллергологом-иммунологом, инфекционистом, ревматологом и другими специалистами. Уже на этапе осмотра можно обнаружить бледность, желтушность кожных покровов и слизистых, пропальпировать увеличенную селезенку и печень. Выраженность спленомегалии и гепатомегалии уточняется при проведении ультразвукового исследования (УЗИ печени и селезенки).
Лабораторная диагностика подтверждает наличие нормо- или гипохромной (реже – гиперхромной) анемии, ретикулоцитоза, увеличение СОЭ, гипербилирубинемию. В анализе мочи может выявляться протеинурия, уробилинемия, гемоглобинурия. При исследовании пунктата костного мозга обнаруживаются признаки гиперплазии за счет активации эритропоэза. При гемолитической болезни новорожденных выявляется выраженный эритробластоз (100-150 тысяч в 1 мкл).
При исследовании пунктата костного мозга обнаруживаются признаки гиперплазии за счет активации эритропоэза. При гемолитической болезни новорожденных выявляется выраженный эритробластоз (100-150 тысяч в 1 мкл).
Диагноз аутоиммунной гемолитической анемии подтверждается положительной прямой пробой Кумбса (прямым антиглобулиновым тестом) или полибреновым тестом (сенсибилизированная проба Кумбса). Дифференциальная диагностика проводится с другими иммунными болезнями, различными формами анемий, гемобластозами, тяжелыми отравлениями, болезнями печени и почек.
Лечение иммунных гемолитических анемий
Лечебная тактика различается при различных формах болезни. При аутоиммунном характере гемолиза с тепловыми антигенами проводится введение высоких доз иммуноглобулина, кортикостероидов, иногда — циклофосфамида и других иммуносупрессивных препаратов. Возможно применение плазмафереза. При неэффективности консервативной терапии рекомендуется проведение спленэктомии. При холодовой иммунной гемолитической анемии используется введение моноклональных антител (ритуксимаба), плазмаферез, трансфузия индивидуально подобранных, отмытых и подогретых эритроцитов.
При холодовой иммунной гемолитической анемии используется введение моноклональных антител (ритуксимаба), плазмаферез, трансфузия индивидуально подобранных, отмытых и подогретых эритроцитов.
Лечение первичной аутоиммунной гемолитической анемии
Что такое первичная аутоиммунная гемолитическая анемия (АИГА)?
Красные кровяные клетки (эритроциты) доставляют кислород ко всем частям тела. У здоровых людей продолжительность жизни эритроцитов составляет около 120 дней. При АИГА иммунная система не работает должным образом и разрушает эритроциты быстрее, чем организм может их выработать. АИГА считается первичной, когда у пациента нет иной причины или иного состояния, вызвавшего АИГА.
Первичная АИГА развивается по-разному у разных людей. Таким людям часто необходимы повторные переливания крови, чтобы поддерживать уровень эритроцитов в норме. Это заболевание может быть смертельно опасным для некоторых людей.
Какова цель этого обзора и в чем его важность?
Цель этого обзора — выяснить, что говорят исследования о безопасности и эффективности лечения первичной АИГА иммуномодулирующими средствами. Иммуномодулирующие агенты изменяют работу вашей иммунной системы. Они не являются средством излечения, но они могут замедлить прогрессирование АИГА
Но насколько хорошо они работают? Являются ли некоторые их них более безопасными, чем другие? Ответы на эти вопросы важны для того,чтобы помочь врачам и пациентам принимать решение о терапии на основании доказательств.
Какие исследования были найдены в обзоре?
Мы изучили исследования, которые были завершены к 7 марта 2021 года.
В исследованиях сравнили две группы взрослых с первичной АИГА, которых лечили:
— ритуксимабом и стероидами
— только стероидами
Важно отметить, что эти исследования были очень небольшими (малыми), в общем счете включили 96 человек. Дизайн одного из исследований имел проблему, которая могла повлиять на результаты.
Восстановление после лечения
· Через 12 месяцев после начала лечения ритуксимаб и стероиды помогают большему числу людей восстановиться после первичной АИГА, чем только стероиды. Исследователи считают, что качество этого исследования низкое. Они считают, что будущие исследования, скорее всего, изменят эти результаты.
· Через шесть месяцев после начала лечения не было какой-либо разницы в выздоровлении между взрослыми, которых лечили ритуксимабом и стероидом, и теми, кого лечили только стероидом.
Побочные эффекты от лечения
· Побочные эффекты в обеих группах были одинаковыми.
Какова основная мысль этого обзора?
Ритуксимаб и стероиды могут помочь большему числу людей полностью восстановиться при впервые диагностированной (выявленной) первичной АИГА, чем только стероиды. Побочные эффекты кажутся примерно одинаковыми для обоих вариантов лечения. Но нужно больше исследований, чтобы знать наверняка.
Врачи предлагают другие методы лечения первичной АИГА, которые могут быть полезны, но не хватает исследований об их эффективности. Пока, основываясь на ограниченной информации, которой мы располагаем, пациент и врач должны будут вместе тщательно принимать решения о лечении первичной АИГА.
причины, симптомы, диагностика, лечение, профилактика
Представляет собой группу заболеваний, характеризующихся усиленным разрушением эритроцитов, что обусловлено выработкой антител против неизмененных красных кровяных телец или гаптенов, сформировавшихся на мембране эритроцитов.
Развитие иммунной гемолитический анемии связано с влиянием самых разных неблагоприятных экзогенных и эндогенных факторов, которые могут вызывать развитие иммунных реакций против собственных эритроцитов. В большинстве случаев аутоиммунный механизм, при котором отмечается выработка антител против неизмененных естественных антигенов мембраны эритроцитов, находящихся в кровяном русле, или их предшественников – эритрокариоцитов происходит в костном мозге. Первичный фактор, который может вызывать разрушение эритроцитов не установлен.
Вторичные анемии возникают на фоне хронического лимфолейкоза, лимфомы, антифосфолипидного синдрома либо иммунодефицитных состояний. В большинстве случаев выявляется тепловая форма аутоиммунной анемии, при которой температурные параметры не изменяются, а на эритроцитах располагаются иммуноглобулины класса G и компоненты комплемента C3 и C4. Разрушение красных кровяных телец макрофагами происходит в печени и селезенке. Намного реже встречается холодовая форма, которая возникает на фоне инфекционных заболеваний, переохлаждения и лимфопролиферативных нарушений у лиц старше 60 лет. Реакция антиген-антитело с гемолизом возникает в периферическом кровяном русле, где температура снижается до показателей менее 32 градусов.
Намного реже встречается холодовая форма, которая возникает на фоне инфекционных заболеваний, переохлаждения и лимфопролиферативных нарушений у лиц старше 60 лет. Реакция антиген-антитело с гемолизом возникает в периферическом кровяном русле, где температура снижается до показателей менее 32 градусов.
Иммунная гемолитическая анемия развивается при фиксации на мембране фрагмента эритроцита, имеющего медикаментозное, вирусное или бактериальное происхождение. Сформировавшиеся гаптены трансформируются в красные кровяные тельца в чужеродные клетки-мишени для иммунной системы, что и вызывает гемолиз. В большинстве случаев такие процессы развиваются при антибактериальной терапии препаратами пенициллинового, цефалоспоринового и тетрациклинового ряда, а также противотуберкулезных средств, анальгетиков и антиаритмических средств.
Изоиммунная форма заболевания возникает при несовместимости крови матери и плода по группе крови или резус-фактору. В этом случае антиэритроцитарные антитела матери через плацентарный барьер проникают к плоду и вызывают разрушение эритроцитов. Подобные патологические процессы наблюдается и при переливании несовместимой крови от донора реципиенту.
Подобные патологические процессы наблюдается и при переливании несовместимой крови от донора реципиенту.
В большинстве случаев наблюдается острая манифестация заболевания. В этом случае у больного отмечается повышение температуры тела, озноб, головные боли, головокружение, одышка, боли в области желудка и поясницы. У больного кожные покровы становятся бледными, а с течением времени желтушными, иногда возникают геморрагии, увеличение в размерах печени и селезенки и потемнение мочи.
При холодовой форме заболевания отмечается нарушение периферического кровообращения с развитием синдрома Рейно, возникновение синюшного окраса и отека кожных покровов кистей рук, лица, ушных раковин. В тяжелых случаях нарушение кровоснабжения тканей конечностей может стать причиной развития гангрены пальцев стоп.
При тяжелом течении эритробластоза плода происходит развитие ядерной желтухи с поражением центральной нервной системы, обусловленной развитием билирубиновой энцефалопатии.
Для постановки диагноза и определения формы заболевания потребуется тщательное обследование пациента со сбором анамнеза, проведением клинического физикального осмотра гематологом, аллергологом-иммунологом, инфекционистом и ревматологом. Также больному потребуется проведение ультразвукового исследования печени и селезенки, биохимического и общего анализа крови и пробы Кумбса.
ЛечениеВыбор лечебной тактики зависит от типа заболевания. При аутоиммунном характере гемолиза с тепловыми антигенами назначается введение высоких доз иммуноглобулина, кортикостероидов, циклофосфамида и других иммуносупрессивных препаратов. Иногда обоснованным является назначение плазмафереза. В случае неэффективности консервативной терапии проводится спленэктомия. При холодовой иммунной гемолитической анемии используется введение моноклональных антител и плазмаферез.
ПрофилактикаНа данный момент специальных методов, позволяющих предупредить иммунные гемолитические анемии, не разработано.
| Подробное описание | Гемолиз — это преждевременное разрушение эритроцитов. Гемолитическая анемия разовьется, если активность костного мозга не может компенсировать потерю эритроцитов. тяжесть анемии зависит от того, постепенное или внезапное начало гемолиза и от степени разрушение эритроцитов Гемолиз может быть следствием наследственных и приобретенных нарушений. причины гемолиза включают иммунные нарушения, токсичные химические вещества и лекарства, противовирусные средства и Физический ущерб . Аутоиммунная гемолитическая анемия (АИГА) обладает двумя важными характеристиками: укороченный красный цвет. выживаемость клеток крови (эритроцитов) и наличие аутоантител, направленных к аутологичным эритроцитам, обычно подтверждается положительным прямым тестом на антиглобулин (Кумбса) (DAT). классифицируется по температуре, при которой аутоантитела оптимально связываются с эритроцитами. |
|---|
Холодовая аутоиммунная гемолитическая анемия отвечает на терапию моноклональным антителом
Холодовая аутоиммунная гемолитическая анемия (Х-АИГА) — заболевание, связанное с вялотекущей патологической лимфопролиферацией, которая вызывается вирусом Эпштейна — Барр и другими инфекциями либо злокачественным перерождением B-лимфоцитов. В организме больного формируется клон лимфоцитов, секретирующий антитела IgM против эритроцитарного антигена. Антитела этого класса, находясь в крови в высокой концентрации, вызывают агглютинацию эритроцитов на холоду — это один из важных диагностических признаков. Связывание клональных IgM с эритроцитами приводит к комплемент-зависимому лизису и развитию анемии, зачастую угрожающей жизни. Многим пациентам необходимы постоянные переливания крови.
Антитела этого класса, находясь в крови в высокой концентрации, вызывают агглютинацию эритроцитов на холоду — это один из важных диагностических признаков. Связывание клональных IgM с эритроцитами приводит к комплемент-зависимому лизису и развитию анемии, зачастую угрожающей жизни. Многим пациентам необходимы постоянные переливания крови.
До настоящего времени специфическая терапия заболевания отсутствовала, терапевтическое антитело, элиминирующее В-лимфоциты, давало лишь временный эффект у части пациентов. Австрийские исследователи предложили другую концепцию, основой которой стала блокировка начальной стадии каскада активации комплемента. Для этого было создано антитело сутимлимаб, ингибирующее протеолитический компонент комплемента C1s.
Работа, опубликованная в журнале Blood, описывает клиническое испытание сутимлимаба на небольшой когорте пациентов (10 человек от 56 до 75 лет), которым вначале вводили тестовую дозу антитела для выявления побочных реакций, а затем четыре терапевтические дозы. Терапевтическая доза сутимлимаба составила 60 мг/кг веса, таким образом, за один раз пациенту вводили несколько граммов антитела. Сутимлимаб —это химерное антитело мышь-человек. Чтобы предотвратить побочные эффекты, в частности, антитело-зависимую цитотоксичность, константная часть антитела взята от человеческого IgG4, известного отсутствием эффекторных функций.
Терапевтическая доза сутимлимаба составила 60 мг/кг веса, таким образом, за один раз пациенту вводили несколько граммов антитела. Сутимлимаб —это химерное антитело мышь-человек. Чтобы предотвратить побочные эффекты, в частности, антитело-зависимую цитотоксичность, константная часть антитела взята от человеческого IgG4, известного отсутствием эффекторных функций.
Испытание дало весьма обнадеживающие результаты. Хотя антитело химерное, лишь у одного пациента детектировали антитела к сутимлимабу, причем в крайне низкой (нанограммы на мл) концентрации. Введение сутимлимаба эффективно удаляло C1s из кровотока и блокировало снижение гемоглобина у 6 пациентов из 10. У пациентов, не отвечавших на терапию или отвечавших частично, была диагностирована либо лимфома, либо аутоиммунная гемолитическая анемия смешанного типа (то есть вызванная не только описанными IgM, но и другими причинами).
Для шестерых пациентов, положительно отреагировавших на терапию, провели контрольное испытание с отменой антитела. При этом у всех пациентов возвращались симптомы заболевания, что свидетельствует об отсутствии спонтанной реверсии болезни на фоне приема сутимлимаба. Пациенты оставались бессимптомными на протяжении 18 месяцев терапии.
При этом у всех пациентов возвращались симптомы заболевания, что свидетельствует об отсутствии спонтанной реверсии болезни на фоне приема сутимлимаба. Пациенты оставались бессимптомными на протяжении 18 месяцев терапии.
Руководитель исследования, профессор Медицинского университета Вены Бернд Джилма оценил перспективы терапии с осторожным оптимизмом: «Если данные по безопасности останутся позитивными, сутимлимаб может стать первым одобренным препаратом для лечения холодовой гемолитической анемии. Очевидно, что лекарство занимает пустующую клиническую нишу, поскольку мы наблюдаем быстрый и сильный ответ у пациентов, которым ранее не помогли многие варианты терапии».
Гемолитическая анемия у детей > Клинические протоколы МЗ РК
Сокращения, используемые в протоколе:
| АГ | артериальная гипертензия; |
| АД | артериальное давление; |
| АЛТ | аланинаминотрансфераза |
| АСТ | аспартатаминотрансфераза |
| ВВИГ | внутривенная высокодозная иммуноглобулинтерапия |
| ГА | гемолитическая анемия |
| ГГТП | гаммаглютамилтранспептидаза |
| ГУС | гемолитико-уремический синдром |
| Г-6-ФД | глюкозо-6-фосфатдегидрогеназа |
| ДВС-синдром | диссеминированное внутрисосудистое свёртывание |
| ЖКБ | желчекаменная болезнь |
| ИВБДВ | интегрированное ведение болезней детского возраста |
| ИВЛ | искусственная вентиляция легких |
| ИТП | иммунная тромбоцитопения |
| КТ | компьютерная томография |
| КЩС | кислотно-щелочное состояние |
| ЛДГ | лактатдегидрогеназа |
| МАГА | микроангиопатическая гемолитическая анемия |
| МНН | международное непатентованное название |
| МРТ | магнитно-резонансная томография |
| НПВП | нестероидные противовоспалительные препараты |
| НС | наследственный сфероцитоз |
| ОАК | общий анализ крови |
| ОАМ | общий анализ мочи |
| ОРЭ | осмотическая резистентность эритроцитов |
| ОНМК | острое нарушение мозгового кровообращения |
| ОРЭ | осмотическая резистентность эритроцитов |
| ПАТ | прямой антиглобулиновый тест (реакция Кумбса) |
| ПНГ/ПГА | пароксизмальная ночная гемоглобинурия |
| ПВ/ТВ | протромбиновое время/тромбиновое время |
| СКБ | серповидно-клеточная болезнь |
| ТГР | трансфузионная гемолитическая реакция |
| ТКА | трансзиторная клеточная аплазия |
| УЗИ | ультразвуковое исследование |
| УД | уровень доказательности |
| ХЗ | хроническое заболевание |
| ЛДГ | лактатдегидрогеназа |
| ЧД | частота дыхания; |
| ЧСС | частота сердечных сокращений; |
| ЩФ | щелочная фосфатаза |
| ЭКГ | электрокардиография; |
| ЭМА-тест | тест с флюоресцентным красителем эозин-5-малеимид |
| ЭхоКГ | эхокардиография; |
| ЭЭГ | электроэнцефалография |
| Ig | иммуноглобулин |
| G6PD | глюкозо-6-фосфатдегидрогеназа |
| Hb | гемоглобин |
| HbА2 | взрослый тип гемоглобина |
| HbF | фетальный гемоглобин |
| HbSS | аномальный вид гемоглобина при серповидно-клеточной анемии |
| HbSC | аномальный вид гемоглобина при серповидно-клеточной анемии |
| HbSD | аномальный вид гемоглобина |
| HPP | аномальный вид гемоглобина |
| MSCV | средний объем сферического эритроцита |
| MCHC | средняя концентрация гемоглобина в эритроците |
| MCV | средний объём эритроцитов |
ОРГАНИЗАЦИОННЫЕ АСПЕКТЫ ПРОТОКОЛА
Список разработчиков:
1) Кыздарбекова Забира Нурахметовна – заведующая отделением онкологии №2, первая категория, Корпоративного фонда «UMC» ННЦМД, г.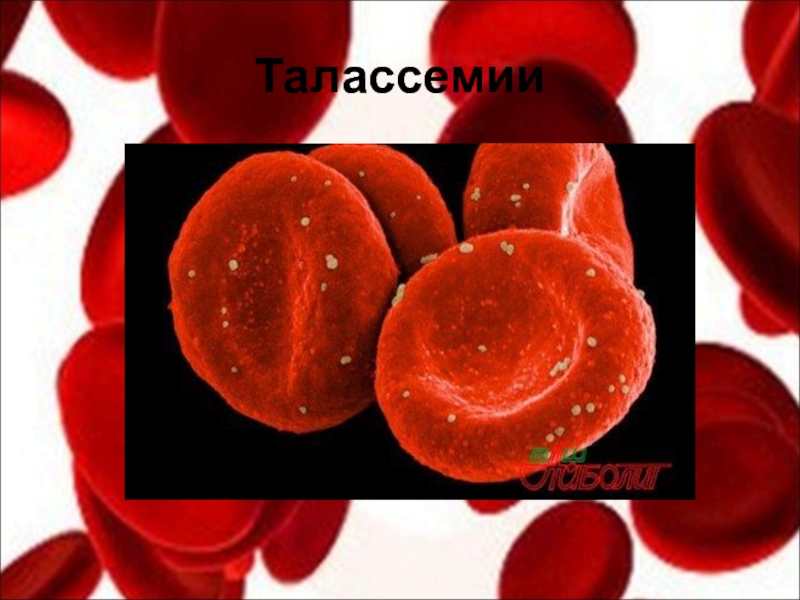 Астана;
Астана;
2) Тастанбекова Венера Булатовна – детский врач гематолог/онколог, Корпоративного фонда «UMC» ННЦМД, г. Астана;
3) Нургалиев Даир Жванышевич – д.м.н., заведующая отделением онкологии №1, высшая категория, Корпоративного фонда «UMC» ННЦМД, г. Астана;
4) Манжуова Ляззат Нурпапаевна – кандидат медицинских наук, медицинский директор РГКП «Национальный центр педиатрии и детской хиургии», г.Алматы;
4) Калиева Шолпан Сабатаевна – кандидат медицинских наук, доцент, заведующая кафедрой клинической фармакологии и доказательной медицины, РГП на ПХВ «Карагандинский государственный медицинский университет».
Указание на отсутствие конфликтов: нет.
Список рецензентов:
1) Кемайкин Вадим Матвеевич – кандидат медицинских наук, врач гематолог высшей квалификационной категории, онкогематолог Министерства здравоохранения и социального развития Республики Казахстан, г. Астана, «Национальный научный центр онкологии и трансплантологии», руководитель департамента онкогематологии и трансплантации костного мозга.
Указание условий пересмотра протокола: Пересмотр протокола через 5 лет после его опубликования и с даты его вступления в действие или при наличии новых методов с уровнем доказательности.
Приложение №1
Приложение №2
Приложение №3
Приложение №4
Приложение 5
Алгоритм действий при неотложных ситуациях:
Приложение 6
Рекомендуемый график вакцинопрофилактики детей с СКБ (уровень убедительности доказательства В, С)
| Вакцина | Возраст введения |
| Вакцина против дифтерии, столбняка, коклюша, полиомиелита, гемофильной тип В инфекции + коньюгированная вакцина против 13 серотипов пневмококка | 3 мес. |
| Вакцина против дифтерии, столбняка, коклюша, полиомиелита, гемофильной тип В инфекции + вакцина против менингококковой инфекции тип С | 4 мес. |
| Вакцина против дифтерии, столбняка, коклюша, полиомиелита, гемофильной тип В инфекции + коньюгированная вакцина против 13 серотипов пневмококка + вакцина против менингококковой инфекции тип С | 5 мес. |
| Вакцина против гепатита В* + вакцина против гемофильной тип В инфекции + вакцина против менингококковой инфекции тип С | 12 мес. |
| Вакцина против кори, краснухи и паротита + вакцина против гепатита В* + коньюгированная вакцина против 13 серотипов пневмококка | 13 мес. |
| Вакцина против дифтерии, столбняка, коклюша, полиомиелита, гемофильной тип В инфекции + Вакцина против гепатита В* | 18 мес. |
| Вакцина против полиомиелита + 23 валентная полисахаридная пневмококковая вакцина | 2 года |
| Вакцина против полиомиелита, дифтерии, столбняка | 6 лет |
| 23 валентная полисахаридная пневмококковая вакцина | 7 лет |
| Вакцина против дифтерии, столбняка | 11 лет |
| 23 валентная полисахаридная пневмококковая вакцина | 12 лет |
| Вакцина против дифтерии, столбняка** + 23 валентная полисахаридная пневмококковая вакцина*** | 17 лет |
| Вакцина против гриппа | Ежегодно, начиная с 6 мес. |
* если вакцинация не проведена на первом году жизни;
** далее каждые 10 лет жизни;
*** далее каждые 5 лет жизни.
Аутоиммунная гемолитическая анемия: симптомы, причины, диагностика, лечение
Аутоиммунная гемолитическая анемия, или АИГА, является редким типом анемии. Когда у вас анемия, ваш костный мозг не производит достаточно красных кровяных телец. Или эти клетки не работают так, как должны.
Красные кровяные тельца переносят кислород в ваше тело. Когда у вас слишком мало эритроцитов, ваше тело не может получать достаточно кислорода, из-за чего вы чувствуете усталость или одышку.
Что такое АМСЗ?
Красные кровяные тельца образуются в губчатом материале, называемом костным мозгом, глубоко внутри ваших костей.Эти клетки крови обычно живут около 120 дней.
Если у вас аутоиммунная гемолитическая анемия, иммунная система вашего организма атакует и разрушает эритроциты быстрее, чем костный мозг может создавать новые. Иногда эти эритроциты живут всего несколько дней.
Иногда эти эритроциты живут всего несколько дней.
Большинство людей, получающих АМСЗ, — это люди среднего и старшего возраста. Это редко встречается у детей, обычно проявляется вскоре после вирусного заболевания и проходит само по себе. Если ваш подросток заболел, это может быть признаком других проблем со здоровьем.
Типы АМСЗ
Аутоиммунная гемолитическая анемия подразделяется на несколько различных категорий:
- Первичный АМСЗ: проявляется сам по себе
- Вторичный АМСЗ: влияет на вас, потому что у вас другое заболевание.
Болезнь также классифицируется по температуре, при которой повреждаются эритроциты:
- Гемолитическая анемия с теплыми антителами: Иммунная реакция протекает при нормальной температуре тела или выше.
- Гемолитическая анемия с антителами к холоду: Эритроциты разрушаются при воздействии холода.
Признаки и симптомы аутоиммунной гемолитической анемии
Многие симптомы АИГА такие же, как и при других формах анемии. У вас могут быть:
У вас могут быть:
- Озноб
- Учащенное сердцебиение, известное как тахикардия
- Бледная кожа, которая может начать желтеть
- Одышка
- Слабость и усталость
- Боль в груди
- Желтая кожа или белки глаз (желтуха )
- Темная моча
- Ощущение переполнения живота, связанное с увеличением селезенки
Некоторые симптомы могут различаться в зависимости от того, какой у вас тип АМСЗ.При гемолитической анемии холодовых антител вы также можете заметить:
- Холодные руки и ноги
- Синеватый или красноватый цвет кистей и стоп
- Головная боль
- Проблемы с пищеварением
- Боль в спине и ногах
AIHA Причины
Вы можете получить аутоиммунную гемолитическую анемию, если у вас аутоиммунное заболевание, такое как волчанка. Обычно, когда ваша иммунная система обнаруживает чужеродных захватчиков, таких как бактерии и вирусы, она заставляет белки, называемые антителами, атаковать их. Когда у вас есть АИГА, ваша иммунная система вырабатывает антитела, которые по ошибке атакуют ваши собственные эритроциты.
Когда у вас есть АИГА, ваша иммунная система вырабатывает антитела, которые по ошибке атакуют ваши собственные эритроциты.
Другие болезни и лекарства также могут вызывать аутоиммунную гемолитическую анемию. Вот некоторые из них:
Диагноз АМСЗ
Если вы считаете, что у вас может быть какой-либо тип анемии, вам следует поговорить со своим врачом. Они могут направить вас к гематологу, врачу, специализирующемуся на заболеваниях крови. Скорее всего, они обсудят вашу прошлую историю болезни, лекарства, которые вы принимаете, и расскажут о ваших симптомах.
Они также запросят анализ крови, называемый полным анализом крови, или CBC, для выявления признаков анемии. Этот тест измеряет:
- Количество эритроцитов, лейкоцитов и тромбоцитов
- Размер ваших красных кровяных телец
- Белок в ваших красных кровяных тельцах, переносящий кислород (гемоглобин)
- Сколько красного пространства кровяные клетки поглощаются вашей кровью (гематокрит)
Низкое количество эритроцитов и низкий уровень гемоглобина и гематокрита являются признаками анемии.
Если результаты вашего общего анализа крови указывают на анемию, врач может захотеть провести дополнительные анализы. Вы можете получить одно из следующих значений:
- Число ретикулоцитов. Это количество молодых эритроцитов в вашем теле. Высокое количество ретикулоцитов означает, что ваш костный мозг производит гораздо больше клеток, чтобы заменить те, которые разрушило ваше тело.
- Тест Кумбса. Врач проведет этот тест, чтобы узнать, вырабатывает ли ваше тело антитела против эритроцитов.
- Периферический мазок. Ваш врач проверит ваши эритроциты под микроскопом на наличие признаков разрушения кровяных телец.
- Тест на билирубин. Уровень этого вещества повышается при разрушении клеток крови.
- Тест на гаптоглобин. Этот белок очищает кровь от остатков поврежденных эритроцитов. При интенсивном использовании уровни будут низкими.
- Титр холодных агглютининов.
 Врач может проверить ваш уровень этих антител, которые атакуют эритроциты при низких температурах.
Врач может проверить ваш уровень этих антител, которые атакуют эритроциты при низких температурах.
Лечение аутоиммунной гемолитической анемии
Если у вас есть такое заболевание, как волчанка, которое вызывает вашу анемию, ваш врач сначала лечит его. Если причиной является лекарство, вам, вероятно, придется прекратить его прием. Если ваш АМСЗ мягкий, лечение может не потребоваться.
Врачи обычно сначала назначают стероиды, такие как гидрокортизон или преднизон, чтобы ваша иммунная система не атаковала эритроциты. Лекарство под названием ритуксимаб может улучшить действие стероидов.
Если вы не поправитесь, вам может потребоваться операция по удалению селезенки. Именно здесь происходит большая часть разрушения красных кровяных телец.
Другие лекарства, такие как азатиоприн (Имуран) и циклофосфамид (Цитоксан), могут использоваться для подавления иммунной системы.
Возможно, вам понадобится переливание крови.
Анемия, гемолитическая, приобретенная аутоиммунная — NORD (Национальная организация редких заболеваний)
УЧЕБНИКИ
Petz LD. Аутоиммунные гемолитические анемии.В: Справочник НОРД по редким заболеваниям. Липпинкотт Уильямс и Уилкинс. Филадельфия, Пенсильвания. 2003: 367.
Аутоиммунные гемолитические анемии.В: Справочник НОРД по редким заболеваниям. Липпинкотт Уильямс и Уилкинс. Филадельфия, Пенсильвания. 2003: 367.
Берков Р., изд. Руководство Merck — домашнее издание, 2-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 2003: 991-92.
Beers MH, Berkow R, ред. Руководство Merck, 17-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 1999: 872-74.
Hoffman R, Benz Jr EJ, Shattil SJ и др., Ред. Гематология: основные принципы и практика. 2-е изд. Черчилль-Ливингстон, Инк. Нью-Йорк, штат Нью-Йорк; 1995: 715-29.
СТАТЬИ ИЗ ЖУРНАЛА
Свенссон А.М., Бушор С., Фунг МК. История болезни: обострение гемолитической анемии, требующее множественных переливаний несовместимых эритроцитов. Иммуногематол. 2004; 20: 177-83.
Эльхадж II, Шарара AI, Taher AT. Хронический гепатит С, связанный с Кумбс-положительной гемолитической анемией. Hematol J. 2004; 5: 364-66.
Какайя Р., Чери Дж. , Смит С. и др. Случай острого гемолиза после цефтриаксона: механизм иммунного комплекса, продемонстрированный проточной цитометрией. Arch Path Lab Med.2004; 128: 905-07.
, Смит С. и др. Случай острого гемолиза после цефтриаксона: механизм иммунного комплекса, продемонстрированный проточной цитометрией. Arch Path Lab Med.2004; 128: 905-07.
Ли Джм, Чан К., Кан Ю.В. и др. Целенаправленное нарушение Nrf2 вызывает регенерированную иммуноопосредованную гемолитическую анемию. Proc Natl. Академия наук США, 2004; 101: 9751-56.
Berentsen S, Ulvestad E, Gjertsen BT, et al. Ритуксимаб при первичной хронической болезни холодовых агглютининов: проспективное исследование 37 курсов терапии у 27 пациентов. Кровь. 2004; 103: 2925-28.
Вебстер Д., Ричи Б., Мант М.Дж. Быстрый ответ на ритуксимаб при тяжелой гемолитической анемии с применением как холодных, так и теплых аутоантител.Am J Hematal. 2004; 75: 258-59.
Petz LD. Руководство для врача по переливанию крови при аутоиммунной гемолитической анемии. Br J Haematol. 2004; 124: 712-16.
Ла Спина М., Руссо Г. Новые лекарства от детской анемии. Минерва Педиатр. 2003; 55: 483-98.
Buetens EW, Ness PM. Переливание эритроцитов при аутоиммунной гемолитической анемии. Curr Opin Hematol. 2003; 10: 429-33.
Переливание эритроцитов при аутоиммунной гемолитической анемии. Curr Opin Hematol. 2003; 10: 429-33.
ИНТЕРНЕТ
Медицинская энциклопедия: идиопатическая аутоиммунная гемолитическая анемия. MedlinePlus. Дата обновления: 05.06.2003.2 стр.
www.nlm.nih.gov/medlineplus/ency/article000579.htm
Медицинская энциклопедия: иммунная гемолитическая анемия. MedlinePlus. Дата обновления: 02.05.2003. 2 стр.
www.nlm.nih.gov/medlineplus/ency/article000576.htm
Медицинская энциклопедия: гемолитическая анемия. MedlinePlus. Дата обновления: 02.05.2003. 3 стр.
www.nlm.nih.gov/medlineplus/ency/article000571.htm
Анемия. Клиника Майо. 02 июня 2003 г. 7 стр.
www.mayoclinic.com/invoke.cfm?id=DS00321
Теплая аутоиммунная гемолитическая анемия — NORD (Национальная организация редких заболеваний)
TEXTBOOKS
Packman, CH.Гемолитическая анемия в результате повреждения иммунной системы. В Каушанский К; Lichtman MA, Prchal JT, Levi MM, Press OW, Burns LJ, Caligiuri MA, eds. Гематология Вильямса, 9-е изд. Нью-Йорк, штат Нью-Йорк: Макгроу Хилл; 2016: 823-845.
Гематология Вильямса, 9-е изд. Нью-Йорк, штат Нью-Йорк: Макгроу Хилл; 2016: 823-845.
Petz LD. Гемолитическая анемия с теплыми антителами. В: Справочник НОРД по редким заболеваниям. Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 2003: 371-372.
Берков Р., изд. Руководство Merck — домашнее издание, 2-е изд. Станция Уайтхаус, Нью-Джерси: Исследовательские лаборатории Мерк; 2003: 991-992.
СТАТЬИ ИЗ ЖУРНАЛА
Бродский Р.А.Теплая аутоиммунная гемолитическая анемия. N Engl J Med. 2019; 381 (7): 647-654.
Go RS, Винтерс JL, Кей NE. Как я лечу аутоиммунную гемолитическую анемию. Кровь. 2017; 129 (22): 2971-2979.
Барчеллини В., Фаттиццо Б., Занинони А. и др. Клиническая гетерогенность и предикторы исхода при первичной аутоиммунной гемолитической анемии: исследование GIMEMA с участием 308 пациентов. Кровь. 2014; 124 (19): 2930-2936.
Лехнер К., Ягер У. Как я лечу аутоиммунные гемолитические анемии у взрослых. Кровь. 2010; 116 (11): 1831-8.
Packman CH. Гемолитическая анемия, вызванная теплыми аутоантителами. Кровь Rev.2008; 22: 17-31.
D’Arena G, Califano C, Annunziata M, et al. Ритуксимаб идиопатическая аутоиммунная гемолитическая анемия теплого типа: ретроспективное исследование 11 взрослых пациентов. Eur J Haematol. 2007; 79: 53-58.
King KE, Ness PM. Лечение аутоиммунной гемолитической анемии. Semin Hematol. 2005; 42: 131-136.
Раманатан С., Куттс Дж., Герцберг М.С. Два случая рефрактерной теплой аутоиммунной гемолитической анемии, леченной ритуксимабом.Am J Hematol. 2005; 78: 123-126.
ИНТЕРНЕТ
Бругнара С., Бродский Р.А., Теплая аутоиммунная гемолитическая анемия (АИГА) у взрослых, UpTodate. Последнее обновление: 7 августа 2020 г. https://www.uptodate.com/contents/warm-autoimmune-hemolytic-anemia-aiha-in-adults Доступно 17 ноября 2020 г.
Brugnara C, Barcellini W, Пароксизмальная холодовая гемоглобинурия , Своевременно. Последнее обновление: 21 мая 2020 г. https://www. uptodate.com/contents/paroxysmal-cold-hemoglobinuria По состоянию на 17 ноября 2020 г.
uptodate.com/contents/paroxysmal-cold-hemoglobinuria По состоянию на 17 ноября 2020 г.
Schick P.Гемолитическая анемия. Medscape. Последнее обновление: 6 марта 2019 г. http://emedicine.medscape.com/article/201066-overview По состоянию на 17 ноября 2020 г.
Типы гемолитической анемии | Сотрудник гематологии-онкологии CNY
Существует много типов гемолитической анемии. Состояние может быть унаследованным или приобретенным. «Унаследовано» означает, что ваши родители передали вам ген этого заболевания. «Приобретенный» означает, что вы не родились с этим заболеванием, но у вас оно развивается.
Наследственные гемолитические анемии
При наследственной гемолитической анемии один или несколько генов, контролирующих выработку эритроцитов, являются дефектными.Это может привести к проблемам с гемоглобином, клеточной мембраной или ферментами, которые поддерживают здоровые эритроциты.
Аномальные клетки могут быть хрупкими и разрушаться при движении с кровотоком. Если это произойдет, орган, называемый селезенкой, может удалить остатки клеток из кровотока.
Если это произойдет, орган, называемый селезенкой, может удалить остатки клеток из кровотока.
Серповидно-клеточная анемия
Серповидно-клеточная анемия — серьезное наследственное заболевание. При этом заболевании в организме вырабатывается аномальный гемоглобин. Это приводит к тому, что красные кровяные тельца имеют форму серпа или полумесяца.
Серповидные клетки не живут так долго, как здоровые эритроциты. Обычно они умирают примерно через 10-20 дней. Костный мозг не может производить новые эритроциты достаточно быстро, чтобы заменить умирающие.
В Соединенных Штатах серповидноклеточная анемия поражает в основном афроамериканцев.
Талассемии
Талассемии (thal-a-SE-me-ahs) — это наследственные заболевания крови, при которых организм не вырабатывает достаточное количество определенных типов гемоглобина. Это заставляет организм вырабатывать меньше здоровых эритроцитов, чем обычно.
Талассемии чаще всего поражают людей юго-восточноазиатского, индийского, китайского, филиппинского, средиземноморского или африканского происхождения или происхождения.
Наследственный сфероцитоз
В этом состоянии дефект поверхностной мембраны (внешнего покрытия) красных кровяных телец приводит к тому, что они имеют сферическую или шарообразную форму. Эти клетки крови имеют продолжительность жизни короче, чем обычно.
Наследственный сфероцитоз (SFER-o-si-to-sis) является наиболее частой причиной гемолитической анемии среди людей североевропейского происхождения.
Наследственный эллиптоцитоз (овалоцитоз)
Подобно наследственному сфероцитозу, это состояние также связано с проблемами с клеточной мембраной. В этом состоянии эритроциты имеют эллиптическую (овальную) форму. Они не так гибки, как нормальные эритроциты, и имеют более короткую продолжительность жизни.
Дефицит глюкозо-6-фосфатдегидрогеназы (G6PD)
При дефиците G6PD в красных кровяных тельцах отсутствует важный фермент, называемый G6PD. G6PD является частью нормальной химии эритроцитов.
При дефиците G6PD, если красные кровяные тельца вступают в контакт с определенными веществами в кровотоке, недостающий фермент вызывает разрыв (взрыв) и гибель клеток.
Многие факторы могут вызвать распад красных кровяных телец. Примеры включают прием сульфамидных или противомалярийных препаратов; воздействие нафталина, вещества, содержащегося в некоторых шариках моли; есть фасоль; или есть инфекция.
ДефицитG6PD в основном поражает мужчин африканского или средиземноморского происхождения.В Соединенных Штатах это заболевание чаще встречается среди афроамериканцев, чем среди кавказцев.
Дефицит пируваткиназы
В этом состоянии в организме отсутствует фермент под названием пируват (PI-руват) киназа. Недостаток этого фермента приводит к легкому разрушению красных кровяных телец.
Это заболевание чаще встречается среди амишей, чем среди других групп.
Приобретенные гемолитические анемии
При приобретенной гемолитической анемии ваши эритроциты могут быть в норме.Однако какое-то другое заболевание или фактор заставляет организм разрушать эритроциты и удалять их из кровотока.
Разрушение красных кровяных телец происходит в кровотоке или, чаще, в селезенке.
Иммунная гемолитическая анемия
При иммунной гемолитической анемии ваша иммунная система разрушает ваши эритроциты. Три основных типа иммунной гемолитической анемии — это аутоиммунная, аллоиммунная и лекарственная.
Аутоиммунная гемолитическая анемия (АИГА). В этом состоянии ваша иммунная система вырабатывает антитела (белки), которые атакуют ваши эритроциты. Почему это происходит, неизвестно.
НаАМСЗ приходится половина всех случаев гемолитической анемии. АМСЗ может очень быстро развиться и стать серьезным.
Наличие определенных заболеваний или инфекций может повысить риск АМСЗ. Примеры включают:
- Аутоиммунные заболевания, такие как волчанка
- Хронический лимфолейкоз
- Неходжкинская лимфома и другие виды рака крови
- Вирус Эпштейна-Барра
- Цитомегаловирус
- Микоплазменная пневмония
- Гепатит
- ВИЧ
АМСЗ также может развиться после трансплантации стволовых клеток крови и костного мозга.
При некоторых типах АИГА антитела, вырабатываемые организмом, называются теплыми антителами. Это означает, что они активны (то есть разрушают эритроциты) при высоких температурах, таких как температура тела.
При других типах АИГА организм вырабатывает холодовые антитела. Эти антитела активны при низких температурах.
Холодно-реактивные антитела могут стать активными, когда части тела, такие как руки или ноги, подвергаются воздействию температур ниже 32–50 градусов по Фаренгейту (от 0 до 10 градусов Цельсия).
Теплые антитела АИГА встречаются чаще, чем холодные антитела АИГА.
Аллоиммунная гемолитическая анемия. Этот тип гемолитической анемии возникает, если ваш организм вырабатывает антитела против эритроцитов, которые вы получаете при переливании крови. Это может произойти, если переливаемая кровь отличается от вашей.
Этот тип гемолитической анемии также может возникнуть во время беременности, если у женщины
резус-отрицательная кровь, а у ее ребенка резус-положительная кровь. «Резус-отрицательный» и «резус-положительный» относятся к тому, есть ли в вашей крови резус-фактор.Резус-фактор — это белок красных кровяных телец.
Для получения дополнительных сведений перейдите к статье о несовместимости с Rh-фактором здравоохранения.
Лекарственная гемолитическая анемия. Некоторые лекарства могут вызывать реакцию, которая перерастает в гемолитическую анемию. Некоторые лекарства, такие как пенициллин, связываются с поверхностью эритроцитов и могут вызывать образование антител.
Другие лекарства вызывают гемолитическую анемию другими путями. Примеры этих лекарств включают химиотерапию, ацетаминофен, хинин и противомалярийные лекарства, противовоспалительные лекарства и леводопу.
Механические гемолитические анемии
Физическое повреждение мембран эритроцитов может привести к их более быстрому разрушению, чем обычно. Повреждение может быть вызвано:
- Изменения мелких кровеносных сосудов.
- Искусственный клапан сердца или другое устройство, используемое в кровеносных сосудах.
- Гемодиализ (HE-mo-di-AL-ih-sis). Это лечение почечной недостаточности удаляет продукты жизнедеятельности из крови.
- Аппарат искусственного кровообращения, который можно использовать во время операций на открытом сердце.
- Преэклампсия (pre-e-KLAMP-se-ah) или эклампсия. Преэклампсия — это повышенное артериальное давление во время беременности. Эклампсия, которая следует за преэклампсией, является серьезным заболеванием, вызывающим судороги у беременных.
- Злокачественная гипертензия (Hi-per-TEN-shun). Это состояние, при котором ваше кровяное давление внезапно и быстро повышается.
- Тромботическая тромбоцитопеническая пурпура (throm-BOT-ik throm-bo-cy-toe-PEE-nick PURR-purr-ah). Это редкое заболевание крови вызывает образование тромбов в мелких кровеносных сосудах по всему телу.
Повреждение клеток крови также может произойти в конечностях в результате выполнения напряженной деятельности, например, участия в марафонах.
Пароксизмальная ночная гемоглобинурия
Пароксизмальная ночная гемоглобинурия (HE-mo-GLO-bih-NYU-re-ah) или ПНГ — это заболевание, при котором эритроциты повреждены из-за недостатка определенных белков. Организм разрушает эти клетки быстрее, чем обычно.
Люди с ПНГ подвержены повышенному риску образования тромбов в венах и низкого уровня лейкоцитов и тромбоцитов.
Другие причины повреждения эритроцитов
Некоторые инфекции и вещества также могут повреждать эритроциты и приводить к гемолитической анемии. Примеры включают малярию и черноводную лихорадку, клещевые заболевания, змеиный яд и токсичные химические вещества.
Источник: Национальный институт сердца, легких и крови, Национальные институты здравоохранения.
Гемолитическая анемия: основы практики, патофизиология, этиология
Шах А.Приобретенная гемолитическая анемия. Индийский журнал J Med Sci . 2004 декабрь 58 (12): 533-6. [Медлайн]. [Полный текст].
Хейли К. Врожденная гемолитическая анемия. Мед Клин Норт Ам . 2017 Март 101 (2): 361-374. [Медлайн].
Coetzer TI. Нарушения мембран эритроцитов. Каушанский К., Лихтман М.А., Прчал Дж.Т., Леви М.М., Пресс О.В., Бернс Л.Дж., Калиджури М.А., ред. Гематология Вильямса . 9 изд. Нью-Йорк, Нью-Йорк: образование Макгроу-Хилл; 2016 г.661-88.
Jacobs J, Eichbaum Q. COVID-19, связанный с тяжелой аутоиммунной гемолитической анемией. Переливание крови . 2021 г., 61 (2): 635-640. [Медлайн]. [Полный текст].
Альгассим А.А., Эльгазали А.А., Алнахди А.С., Мохаммед-Рахим О.М., Аланази А.Г., Альдхувайхи Н.А. и др. Прогностическое значение уровня гемоглобина и аутоиммунной гемолитической анемии при инфекции SARS-CoV-2. Энн Гематол . 2021 января 100 (1): 37-43. [Медлайн]. [Полный текст].
Lichtman MA. Гемолитическая анемия в результате заражения микроорганизмами. Каушанский К., Лихтман М.А., Прчал Дж.Т., Леви М.М., Пресс О.В., Бернс Л.Дж., Калиджури М.А., ред. Гематология Вильямса . 9 изд. Нью-Йорк, Нью-Йорк: образование Макгроу Хилл; 2016. 815-22.
Herrmann PC. Заболевания эритроцитов в результате действия химических и физических агентов. Каушанский К., Лихтман М.А., Прчал Дж.Т., Леви М.М., Пресс О.В., Бернс Л.Дж., Калиджури М.А., ред. Гематология Вильямса .9 изд. Нью-Йорк, Нью-Йорк: образование Макгроу-Хилл; 2016. 809-14.
Сингх А., Мандал А., Патель А., Мишра С. Аутоиммунная гемолитическая анемия — спектр проявления у детей. J Clin Диагностика . 2017 11 (9) сентября: SR01-SR02. [Медлайн]. [Полный текст].
Kong JT, Schmiesing C. Скрытое злоупотребление нафталином перед анестезией: нафталиновые шарики, ингалянты и их лечение. Acta Anaesthesiol Scand . 2005 Январь 49 (1): 113-6. [Медлайн].
Lane DR, Youse JS. Кумбс-положительная гемолитическая анемия, вторичная по отношению к укусу паука-отшельника: обзор литературы и обсуждение лечения. Кутис . 2004 декабрь 74 (6): 341-7. [Медлайн].
Packman CH, Leddy JP. Приобретенная гемолитическая анемия из-за аутоантител, реагирующих на тепло. Beutler E, Lichtman MA, Coller BS, Kipps TJ, eds. Гематология Вильямса . 5-е изд. Нью-Йорк, штат Нью-Йорк: Макгроу Хилл; 1995. 667-84.
Gallagher PG.Нарушения мембран эритроцитов. Hoffman R, Benz EJ Jr, Silberstein LE, Heslop H, Weitz J, Anastasi J, ред. Гематология: основные принципы и практика . 6-е изд. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2013. 592-613.
Цена EA, Schrier SL. Внешние неиммунные гемолитические анемии. Hoffman R, Benz EJ Jr, Silberstein LE, Heslop H, Weitz J, Anastasi J, ред. Гематология: основные принципы и практика . 6-е изд. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2013.628-38.
Ягер У., Лехнер К. Аутоиммунная гемолитическая анемия. Hoffman R, Benz EJ Jr, Silberstein LE, Heslop H, Weitz J, Anastasi J, ред. Гематология: основные принципы и практика . 6-е изд. Нью-Йорк, Нью-Йорк: Черчилль Ливингстон; 2013. 614-17.
Berentsen S, Randen U, Tjønnfjord GE. Аутоиммунная гемолитическая анемия, опосредованная холодовыми агглютининами. Гематол Онкол Клин Норт Ам . 2015, 29 июня (3): 455-71. [Медлайн].
Rink BD, Gonik B, Chmait RH, O’Shaughnessy R.Гемолиз матери после внутривенного введения иммуноглобулинов при аллоиммунной тромбоцитопении у плода и новорожденного. Акушерский гинекол . 2013 февраль 121 (2, часть 2, приложение 1): 471-3. [Медлайн].
Майер Б., Лео А., Херцигер А., Хубен П., Шеммер П., Салама А. Внутрисосудистый иммунный гемолиз, вызванный контрастным веществом иомепролом. Переливание крови . 2013 24 января [Medline].
Ачарья Д., Макгиффин, округ Колумбия. Гемолиз после восстановления митрального клапана. J Card Surg . 2013 13 января. 1-4. [Медлайн].
Renard D, Rosselet A. Лекарственная гемолитическая анемия: фармакологические аспекты. Трансфус Клин Биол . 2017 Сентябрь 24 (3): 110-114. [Медлайн].
Chiao EY, Engels EA, Kramer JR, Pietz K, Henderson L, Giordano TP и др. Риск иммунной тромбоцитопенической пурпуры и аутоиммунной гемолитической анемии среди 120 908 ветеранов США с вирусной инфекцией гепатита С. Arch Intern Med .2009 23 февраля. 169 (4): 357-63. [Медлайн]. [Полный текст].
Zamvar V, McClean P, Odeka E, Richards M, Davison S. Инфекция вируса гепатита E с неиммунной гемолитической анемией. J Педиатр Гастроэнтерол Нутр . 2005 Февраль 40 (2): 223-5. [Медлайн].
Найк Р. Теплая аутоиммунная гемолитическая анемия. Гематол Онкол Клин Норт Ам . 2015 июн.29 (3): 445-53. [Медлайн].
Mayer B, Yürek S, Kiesewetter H, Salama A.Аутоиммунная гемолитическая анемия смешанного типа: дифференциальный диагноз и критический обзор зарегистрированных случаев. Переливание крови . 2008 окт. 48 (10): 2229-34. [Медлайн].
Hill A, Hill QA. Аутоиммунная гемолитическая анемия. Hematology Am Soc Hematol Educational Program . 2018 30 ноября 2018 (1): 382-389. [Медлайн].
Sanz J, Arriaga F, Montesinos P, Ortí G, Lorenzo I, Cantero S и др. Аутоиммунная гемолитическая анемия после трансплантации аллогенных гемопоэтических стволовых клеток у взрослых пациентов. Пересадка костного мозга . 2007 май. 39 (9): 555-61. [Медлайн].
Морейра М., Брас Р., Гонсалвес Д., Аленкоао И., Иноченсио Г., Родригес М. и др. Фетальная спленомегалия: обзор. Ультразвук Q . 2017 29 ноября. [Medline].
Джордж Дж. Тромботическая тромбоцитопеническая пурпура и гемолитико-уремические синдромы: обзор патогенеза (Опыт Оклахомского реестра TTP-HUS, 1989-2007). Почки Int Suppl .2009 Февраль S8-S10. [Медлайн].
Lechner K, Obermeier HL. Микроангиопатическая гемолитическая анемия, связанная с раком: клинические и лабораторные особенности в 168 зарегистрированных случаях. Медицина (Балтимор) . 2012 июл.91 (4): 195-205. [Медлайн].
Либман HA, Weitz IC. Аутоиммунная гемолитическая анемия. Мед Клин Норт Ам . 2017 Март 101 (2): 351-359. [Медлайн].
Тарик Т., Карабон П., Ирфан Ф. Б., Сиелофф Е. М., Паттерсон Р., Десаи А. П..Национальные тенденции и результаты неаутоиммунной гемолитической анемии при алкогольной болезни печени: анализ общенациональной стационарной выборки. Дж Клин Гастроэнтерол . 2021 г. 1. 55 (3): 258-262. [Медлайн].
Audia S, Bach B, Samson M, Lakomy D, Bour JB, Burlet B и др. Венозные тромбоэмболические события при теплой аутоиммунной гемолитической анемии. PLoS One . 2018.13 (11): e0207218. [Медлайн]. [Полный текст].
Серегина Е.А., Полетаев А.В., Бондарь Е.В., Вуймо Т.А., Атауллаханов Ф.И., Сметанина Н.С.Система гемостаза у детей с наследственным сфероцитозом. Тромб Рес . 2019 5 февраля. 176: 11-17. [Медлайн].
Quintanilla-Bordás C, Castro-Izaguirre E, Carcelén-Gadea M, Marín M. Первый зарегистрированный случай лекарственно-индуцированной гемолитической анемии, вызванной диметилфумаратом, у пациента с рассеянным склерозом. Переливание крови . 2019 31 января. [Medline].
Фелан М.П., Рейнекс Э.З., Берриочоа Дж. П., Шольд Д. Д., Хусти Ф. М., Чемберлин Дж. И др.Влияние использования меньшего объема, меньших вакуумных пробирок для забора крови на гемолиз в образцах крови из отделения неотложной помощи. Ам Дж. Клин Патол . 2017 г. 1. 148 (4): 330-335. [Медлайн].
Дхингра К.К., Джайн Д., Мандал С., Хурана Н., Сингх Т., Гупта Н. Синдром Эванса: исследование шести случаев с обзором литературы. Гематология . 2008 г., 13 (6): 356-60. [Медлайн].
Гарратти Г. Иммунная гемолитическая анемия, связанная с отрицательными стандартными серологическими исследованиями. Семин Гематол . 2005 июл. 42 (3): 156-64. [Медлайн].
Kamesaki T, Oyamada T., Omine M, Ozawa K, Kajii E. Пороговое значение IgG, связанного с эритроцитами, для диагностики аутоиммунной гемолитической анемии, отрицательной по Кумбсу. Ам Дж. Гематол . 2009 Февраль 84 (2): 98-101. [Медлайн]. [Полный текст].
Kamesaki T, Toyotsuji T, Kajii E. Характеристика прямой отрицательной антиглобулиновой аутоиммунной гемолитической анемии: исследование 154 случаев. Ам Дж. Гематол . 2013 Февраль 88 (2): 93-6. [Медлайн].
Moraes ML, Lima LR, Vicentini-Oliveira JC, de Souza AVG, Oliveira ON, Deffune E, et al. Иммуносенсор для диагностики аутоиммунной гемолитической анемии (AIHA) на основе иммобилизации моноклональных антител на слое фиброина шелка. Дж. Наноси Нанотехнологии . 1 июля 2019 г. 19 (7): 3772-3776. [Медлайн].
Феррер Г., Наварро А., Ходжсон К. и др. Экспрессия микроРНК при хроническом лимфолейкозе с развитием аутоиммунной гемолитической анемии. Лимфома лейк . 2013 29 января. [Medline].
Berentsen S, Tjønnfjord GE. Диагностика и лечение аутоиммунной гемолитической анемии, опосредованной холодовыми агглютининами. Кровь Ред. . 2012 май. 26 (3): 107-15. [Медлайн].
Юбинский П.Т., Рашид Н. Успешное лечение пациента с синдромом Эванса, опосредованным смешанными теплыми и холодными антителами, и непереносимостью глюкозы. Рак крови у детей . 2005 Сентябрь 45 (3): 347-50. [Медлайн].
Birgens H, Frederiksen H, Hasselbalch HC, Rasmussen IH, Nielsen OJ, Kjeldsen L, et al. Рандомизированное исследование фазы III, сравнивающее монотерапию глюкокортикоидами с глюкокортикоидами и ритуксимабом у пациентов с аутоиммунной гемолитической анемией. Br J Haematol . 2013 ноябрь 163 (3): 393-9. [Медлайн].
Go RS, Винтерс JL, Кей NE. Как я лечу аутоиммунную гемолитическую анемию. Кровь . 1 июня 2017 г. 129 (22): 2971-2979. [Медлайн].
Dierickx D, Kentos A, Delannoy A. Роль ритуксимаба у взрослых с аутоиммунной гемолитической анемией с тепловыми антителами. Кровь . 2015 21 мая. 125 (21): 3223-9. [Медлайн]. [Полный текст].
Jäger U, Barcellini W, Broome CM, Gertz MA, Hill A, Hill QA и др. Диагностика и лечение аутоиммунной гемолитической анемии у взрослых: рекомендации Первого международного консенсусного совещания. Кровь Ред. . 2020 май. 41: 100648.[Медлайн].
Барчеллини В., Фаттиццо Б. Как я лечу сердечную аутоиммунную гемолитическую анемию. Кровь . 2021 11 марта. 137 (10): 1283-1294. [Медлайн].
Маклеод К., Флиман Н., Киркхэм Дж., Багуст А., Боланд А., Чу П. и др. Деферасирокс для лечения перегрузки железом, связанной с регулярными переливаниями крови (трансфузионный гемосидероз) у пациентов, страдающих хронической анемией: систематический обзор и экономическая оценка. Оценка медицинских технологий .2009 13 января (1): iii-iv, ix-xi, 1-121. [Медлайн]. [Полный текст].
Берк-младший. Низкие дозы подкожного рекомбинантного эритропоэтина у детей с хронической почечной недостаточностью. Ассоциация педиатрической нефрологии Австралии и Новой Зеландии. Педиатр Нефрол . 1995 Октябрь 9 (5): 558-61. [Медлайн].
Арбах О., Функ Р., Зейбт Ф., Салама А. Эритропоэтин может улучшить анемию у пациентов с аутоиммунной гемолитической анемией, связанной с ретикулоцитопенией. Transfus Med Hemother . 2012 июн. 39 (3): 221-223. [Медлайн]. [Полный текст].
Schettler V, Wieland E. Сообщение о случае лечения дарбэпоэтином у пациента с серповидноклеточной анемией и хронической почечной недостаточностью, подвергающегося регулярным процедурам гемодиализа, которые вызывают дозозависимое увеличение интервалов переливания крови. Циферблат Тер Афера . 2009 Февраль 13 (1): 80-2. [Медлайн].
Болл AM, Уинстед ПС. Терапия рекомбинантным человеческим эритропоэтином у тяжелобольных Свидетелей Иеговы. Фармакотерапия . 2008 28 ноября (11): 1383-90. [Медлайн].
Tchernia G, Delhommeau F, Perrotta S, Cynober T., Bader-Meunier B, Nobili B и др. Терапия рекомбинантным эритропоэтином как альтернатива переливанию крови младенцам с наследственным сфероцитозом. Гематол Дж . 2000. 1 (3): 146-52. [Медлайн].
Хосоно С., Хосоно А., Мугишима Х, Накано И., Минато М., Окада Т. и др. Успешная терапия рекомбинантным эритропоэтином для новорожденных с анемией и наследственным сфероцитозом. Педиатр Инт . 2006 апр. 48 (2): 178-80. [Медлайн].
Моррисон Дж. Ф., Нойфельд Э. Дж., Грейс РФ. Использование средств, стимулирующих эритропоэтин, по сравнению с поддерживающей терапией у новорожденных с наследственным сфероцитозом: опыт единого центра. Eur J Haematol . 2014 августа 93 (2): 161-4. [Медлайн]. [Полный текст].
Balestracci A, Martin SM, Toledo I, Alvarado C, Wainsztein RE. Ранний эритропоэтин при постдиарейном гемолитико-уремическом синдроме: исследование случай-контроль. Педиатр Нефрол . 2014 21 августа [Medline].
Nairz M, Sonnweber T, Schroll A, Theurl I, Weiss G. Плейотропные эффекты эритропоэтина при инфекции и воспалении. Микробы заражают . 2012 марта 14 (3): 238-46. [Медлайн]. [Полный текст].
Бьенвену А.Л., Пико С. Церебральная малярия: защита эритропоэтином. Методы Мол Биол . 2013. 982: 315-24. [Медлайн].
Гамильтон Дж. У., Джонс Ф. Г., МакМуллин М Ф.Глюкозо-6-фосфатдегидрогеназа Гвадалахара — случай хронической несфероцитарной гемолитической анемии в ответ на спленэктомию и роль спленэктомии в этом заболевании. Гематология . 2004 г., 9 (4): 307-9. [Медлайн].
Reynaud Q, Durieu I., Dutertre M, Ledochowski S, Durupt S, Michallet AS, et al. Эффективность и безопасность ритуксимаба при аутоиммунной гемолитической анемии: метаанализ 21 исследования. Аутоиммунная Ред. . 2015 14 апреля (4): 304-13. [Медлайн].
Раджапаксе П., Бакирхан К. Аутоиммунная гемолитическая анемия, связанная с бабезиозом человека. Дж Гематол . 2021 Апрель 10 (2): 41-45. [Медлайн]. [Полный текст].
Гемолитическая анемия: оценка и дифференциальный диагноз
1. Mentzer WC, Schrier SL. Внешние неиммунные гемолитические анемии. В: Hoffman R, Benz EJ Jr., Silberstein LE, et al., Eds. Гематология: основные принципы и практика. 7-е изд. Филадельфия, Пенсильвания: Эльзевир; 2018: 663–672….
2. Мармит BJ. Диагностика по мазку крови. N Engl J Med . 2005. 353 (5): 498–507.
3. Дхаливал Г, Корнетт PA, Тирни Л. М. мл. Гемолитическая анемия. Ам Фам Врач . 2004. 69 (11): 2599–2606.
4. Мишель М., Ягер У. Аутоиммунная гемолитическая анемия. В: Hoffman R, Benz EJ Jr., Silberstein LE, et al., Eds. Гематология: основные принципы и практика. 7-е изд. Филадельфия, Пенсильвания: Эльзевир; 2018: 648–662.
5. Шарма С., Шарма П., Тайлер Л.Н. Переливание крови и продуктов крови: показания и осложнения. Ам Фам Врач . 2011; 83 (6): 719–724.
6. Гарратти Г. Лекарственная иммунная гемолитическая анемия. Hematology Am Soc Hematol Educational Program . 2009: 73–79.
7. Johnson ST, Fueger JT, Gottschall JL. Опыт одного центра: серология и препараты, связанные с лекарственной иммунной гемолитической анемией — новая парадигма. Переливание крови . 2007. 47 (4): 697–702.
8. Джордж Дж. Н., Нестер СМ. Синдромы тромботической микроангиопатии. N Engl J Med . 2014. 371 (7): 654–666.
9. Бломбери П., Скалли М. Лечение тромботической тромбоцитопенической пурпуры: современные перспективы. Дж. Кровавая медицина . 2014; 5: 15–23.
10. Бендапуди П.К., Ли А, Хамдан А, и другие. Получение и проспективная проверка прогностической оценки для быстрой диагностики тромботической тромбоцитопенической пурпуры: Plasmic Score. Кровь . 2014; 124 (21): 231.
11. Рок GA, Шумак Х., Бускард Н.А., и другие.; Канадская группа по изучению афереза. Сравнение плазмафереза с инфузией плазмы при лечении тромботической тромбоцитопенической пурпуры. N Engl J Med . 1991. 325 (6): 393–397.
12. Ардиссино Г, Саларди С, Коломбо Э, и другие. Эпидемиология гемолитико-уремического синдрома у детей.Данные из сети HUS Северной Италии. Eur J Pediatr . 2016; 175 (4): 465–473.
13. Брандт Дж., Вонг С, Михм С, и другие. Инвазивная пневмококковая инфекция и гемолитико-уремический синдром. Педиатрия . 2002. 110 (2 ч. 1): 371–376.
14. Йокиранта TS. ГУС и атипичный ГУС. Кровь . 2017; 129 (21): 2847–2856.
15. Вонг CS, Елачич С, Хабиб Р.Л., Уоткинс С.Л., Tarr PI.Риск гемолитико-уремического синдрома после лечения антибиотиками инфекций, вызванных Escherichia coli O157: H7. N Engl J Med . 2000; 342 (26): 1930–1936.
16. Pourrat O, Coudroy R, Пьер Ф. Дифференциация тяжелого HELLP-синдрома и тромботической микроангиопатии, тромботической тромбоцитопенической пурпуры и других имитаторов. Eur J Obstet Gynecol Reprod Biol . 2015; 189: 68–72.
17. Кейзер С.Д., Бойд К.В., Реберг Дж. Ф., и другие.Высокое соотношение ЛДГ и АСТ помогает дифференцировать тромботическую тромбоцитопеническую пурпуру (ТТП), связанную с беременностью, от синдрома HELLP. J Matern Fetal Neonatal Med . 2012. 25 (7): 1059–1063.
18. Вада Х, Мацумото Т, Ямасита Ю. Диагностика и лечение диссеминированного внутрисосудистого свертывания (ДВС) в соответствии с четырьмя рекомендациями по ДВС. J Интенсивная терапия . 2014; 2 (1): 15.
19. Риз Дж. А., Буги DW, Кертис Б.Р., и другие.Тромботическая микроангиопатия, вызванная лекарственными средствами: опыт реестра Оклахомы и Центра крови Висконсина. Ам Дж. Гематол . 2015; 90 (5): 406–410.
20. Аль-Нури З.Л., Риз Дж. А., Террелл Д.Р., Веселый СК, Джордж Дж. Лекарственная тромботическая микроангиопатия: систематический обзор опубликованных отчетов. Кровь . 2015; 125 (4): 616–618.
21. Шварц Дж., Падманабхан А, Aqui N, и другие.Руководство по использованию терапевтического афереза в клинической практике, основанное на доказательствах, от Авторского комитета Американского общества афереза: седьмой специальный выпуск. Дж. Клин Апер . 2016; 31 (3): 149–162.
22. Бейтлер Э. Дефицит G6PD. Кровь . 1994. 84 (11): 3613–3636.
23. Франк Дж. Э. Диагностика и лечение дефицита G6PD. Ам Фам Врач . 2005. 72 (7): 1277–1282.
24.Грегг XT, Прчал JT. Энзимопатии эритроцитов. В: Hoffman R, Benz EJ Jr., Silberstein LE, et al., Eds. Гематология: основные принципы и практика. 7-е изд. Филадельфия, Пенсильвания: Эльзевир; 2018: 616–625.
25. Сикка П., Биндра ВК, Капур С, Джайн V, Saxena KK. Синий лечит синий, но будьте осторожны. J Pharm Bioallied Sci . 2011. 3 (4): 543–545.
26. Джонсон Л, Бутани ВК, Карп К, Сивиери Э.М., Шапиро С.М.Клинический отчет пилотного реестра Kernicterus в США (1992–2004 гг.). Дж Перинатол . 2009; 29 (приложение 1): S25 – S45.
27. Каплан М, Гершель М, Хаммерман С, Хойер Дж. Д., Стивенсон ДК. Гипербилирубинемия среди афроамериканцев, новорожденных с дефицитом глюкозо-6-фосфатдегидрогеназы. Педиатрия . 2004; 114 (2): e213 – e219.
28. Подкомитет Американской академии педиатрии по гипербилирубинемии. Ведение гипербилирубинемии у новорожденного на сроке 35 недель и более [опубликованные поправки опубликованы в Pediatrics.2004; 114 (4): 1138]. Педиатрия . 2004. 114 (1): 297–316.
29. Christensen RD, Yaish HM, Галлахер П.Г. Практическое руководство педиатра по диагностике и лечению наследственного сфероцитоза у новорожденных. Педиатрия . 2015; 135 (6): 1107–1114.
30. Зевать Б.П., Джон-Сова Дж. Управление серповидно-клеточной анемией: рекомендации из отчета экспертной комиссии 2014 г. Ам Фам Врач . 2015; 92 (12): 1069–1076.
31. Манси Х.Л. младший, Кэмпбелл Дж. Альфа- и бета-талассемия. Ам Фам Врач . 2009. 80 (4): 339–344.
Новые взгляды на патогенез аутоиммунной гемолитической анемии — FullText — Transfusion Medicine and Hemotherapy 2015, Vol. 42, № 5
Сводка
Аутоиммунная гемолитическая анемия (АИГА) вызывается усиленным разрушением эритроцитов (эритроцитов) аутоантителами против эритроцитов с активацией комплемента или без нее.Разрушение эритроцитов может происходить как путем прямого лизиса через последовательную активацию конечных компонентов каскада комплемента (комплекс мембранной атаки), так и за счет антителозависимой клеточно-опосредованной цитотоксичности (ADCC). Патогенная роль аутоантител зависит от их класса (наиболее часто встречаются IgG и IgM), подкласса, тепловой амплитуды (теплая и холодная формы), а также от аффинности и эффективности активации комплемента. Некоторые цитокины и цитотоксические механизмы (CD8 + T и естественные клетки-киллеры) также участвуют в разрушении эритроцитов.Более того, активированные макрофаги, несущие Fc-рецепторы, могут распознавать эритроциты и фагоциты опсонизируются аутоантителами и комплементом. Прямой комплемент-опосредованный лизис происходит в основном в кровообращении и в печени, тогда как ADCC, цитотоксичность и фагоцитоз возникают преимущественно в селезенке и лимфоидных органах. Степень внутрисосудистого гемолиза в 10 раз выше внесосудистого. Наконец, эффективность компенсаторного ответа эритробластов может сильно влиять на клиническую картину АИГА.Взаимодействие и относительное бремя всех этих патогенных механизмов объясняют большую клиническую неоднородность АМСЗ, от полностью компенсированных до быстро развивающихся смертельных случаев.
© 2015 S. Karger GmbH, Фрайбург
Введение
Аутоиммунная гемолитическая анемия (АИГА) определяется как повышенное разрушение эритроцитов (эритроцитов) в присутствии аутоантител против эритроцитов с активацией комплемента или без нее.Аутоантитела продуцируются как тканевыми, так и циркулирующими аутореактивными В-лимфоцитами после взаимодействия с Т-хелперными лимфоцитами. Третьим ключевым участником аутоиммунитета против эритроцитов является система комплемента, которая способна индуцировать прямой осмотический лизис эритроцитов посредством последовательной активации комплекса мембранной атаки (MAC). Более того, аутоантитела способны разрушать эритроциты за счет антителозависимой клеточно-опосредованной цитотоксичности (ADCC), которая опосредуется цитотоксическими CD8 + T-клетками и естественными киллерами (NK), которые несут мембранные рецепторы для Fc-части иммуноглобулина G (IgG).Наконец, активированные макрофаги, несущие Fc-рецепторы, могут распознавать эритроциты и фагоциты опсонизируются аутоантителами и комплементом. В то время как прямой комплемент-опосредованный лизис происходит в основном в кровообращении и в печени, ADCC и фагоцитоз происходят преимущественно в селезенке и лимфоидных органах [1].
AIHA можно выделить на основе класса аутоантител Ig и тепловых характеристик, т. Е. Оптимальной температуры реакции с аутологичными эритроцитами в теплой (wAIHA), холодной (холодовая болезнь агглютининов; ИБС) и смешанных формах, хотя и нетипичных сложной диагностической классификации сообщается все чаще [1,2,3].Более того, АМСЗ классифицируются на первичные (идиопатические), при которых гемолиз доминирует в клинической картине при отсутствии любого другого сопутствующего расстройства, и на вторичные формы, сопровождающие и осложняющие основное заболевание. Большинство сердечных форм являются идиопатическими или связаны с другими аутоиммунными заболеваниями; острые формы простуды в основном являются вторичными по отношению к инфекциям, тогда как хронические ИБС часто связаны с лимфопролиферативными или опухолевыми заболеваниями [1,2,3]. Все эти факторы объясняют большую клиническую неоднородность АМСЗ — от компенсированных форм без анемии до молниеносной болезни.В таблице 1 приведены основные характеристики АМСЗ.
Таблица 1
Обычно считается, что аутоиммунитет является результатом взаимодействия генетической предрасположенности и факторов окружающей среды. Хотя сообщалось о нескольких ассоциациях HLA для различных органов и системных аутоиммунных заболеваний (инсулинозависимый диабет 1 типа, тиреоидит Хашимото, болезнь Грейвса, рассеянный склероз, миастения гравис, вульгарная пузырчатка, системная красная волчанка, ревматоидный артрит и анкилозирующий спондилит), Для АМСЗ обнаружена четкая связь с HLA.Более того, механизмы, участвующие в нарушении как центральной, так и периферической толерантности при развитии АИГА, все еще в значительной степени неизвестны. Центральная толерантность возникает во время ранней дифференцировки В-клеток в костном мозге и Т-клеток в тимусе, где аутореактивные клетки подвергаются апоптозу при связывании с аутоантигенами (отрицательный отбор). Периферическая толерантность — это активный процесс, при котором анергия или подавление аутоантигенов запускается специфическими регуляторными T-клетками CD4 + / CD25 + (Treg) и супрессорными T-лимфоцитами CD8 + [4].
Молекулярная мимикрия между аутоантигенами и чужеродными антигенами является одним из нескольких механизмов, с помощью которых патогены могут участвовать в инициации и / или ускорении аутоиммунитета. Вероятно, это преобладающий механизм АИГА, вторичный по отношению к различным бактериальным, микоплазменным или вирусным инфекциям, вероятно, из-за наличия общих антигенных эпитопов на белках или углеводах эритроцитов. Дополнительными механизмами, участвующими в неспособности поддерживать самотолерантность, являются активация поликлональных лимфоцитов, снова вызванная несколькими вирусными инфекциями, и появление «запрещенных клонов», что наблюдается при лимфопролиферативных заболеваниях.Эта гипотеза, предложенная более 60 лет назад Бернетом и основанная на сохранении самореактивных клонов лимфоцитов, которые должны были быть удалены из-за иммунной толерантности, вызвала новый интерес в связи с успехом терапии, истощающей В-клетки при некоторых аутоиммунных заболеваниях. болезни [5]. Конкретное состояние связано с генерацией неоантигенов агентами окружающей среды или лекарствами, как это наблюдается при лекарственно-индуцированном AIHA, где аутоиммунный ответ сохраняется до тех пор, пока они не будут разрушены и устранены [6,7].Более того, в большом исследовании 717 пациентов, демонстрирующих аутоантитела к эритроцитам, около одной трети были признаны положительными по аллоантителам, а переливание эритроцитов было идентифицировано как основная причина аутоиммунизации [8]. В последнее время внимание было сосредоточено на аутоиммунном / воспалительном синдроме, вызванном адъювантами, который включает несколько еще не определенных заболеваний, таких как силиконоз, синдром войны в Персидском заливе, синдром испанского токсического масла, синдром Ардистила и поствакцинация [9]. Прежде всего, это потеря супрессорных механизмов и изменение регуляторных клеток и сети цитокинов, участвующих в контроле самотолерантности [4].
Аутоантитела в патогенезе AIHA
Наиболее частыми аутоантителами против эритроцитов являются IgG, которые в основном определяют внесосудистый гемолиз через ADCC в ретикулоэндотелиальной системе (селезенка и, в меньшей степени, печень). Подкласс IgG влияет на степень, в которой эти антитела сокращают выживаемость эритроцитов: IgG1 является наиболее часто встречающимся подклассом и вместе с IgG3 сокращает период полужизни более эффективно, чем IgG2 и IgG4. Аутоантитела этого класса в основном направлены против эпитопов системы Rh.Обычно они реагируют при 37 ° C и, следовательно, ответственны за теплые формы АИГА [1]. IgG способны активировать каскад комплемента, за исключением подклассов IgG2 и IgG4. Аутоантитела IgA обычно связаны с IgG и лишь изредка сообщаются как единственный возбудитель АИГА.
IgM представляют собой пентамерные аутоантитела, способные значительно фиксировать комплемент по сравнению с другими изотипами, таким образом, преимущественно вызывая внутрисосудистый гемолиз и в меньшей степени C3d-опосредованный внесосудистый лизис (в основном в печени).Аутоантитела этого класса направлены против системы I / i. Их оптимальная температура реакции составляет 4 ° C, и, таким образом, они ответственны за холодные формы AIHA [1,2]. Однако тепловая амплитуда аутоантител IgM колеблется от 0 до 34 ° C, а те, у которых тепловая активность близка к физиологическим температурам (теплый IgM), являются наиболее вредными аутоантителами, способными вызывать тяжелые формы АИГА с зарегистрированным уровнем смертности около 20% [6]. Фактически, стоит напомнить, что количество разрушения эритроцитов при внутрисосудистом гемолизе рассчитано в 200 мл эритроцитов за 1 ч, тогда как при внесосудистом гемолизе оно в 10 раз меньше (0.25 мл эритроцитов / кг / ч, т.е. для пациента с массой тела 70 кг = 17,5 мл эритроцитов / ч = 420 мл эритроцитов / 24 ч) [1,2].
Антитела к эритроцитам обычно выявляются с помощью прямого теста на антиглобулин (DAT) или теста Кумбса, обычно выполняемого с помощью традиционной техники агглютинации пробирки с полиспецифической антисывороткой. В настоящее время рекомендуется использовать моноспецифические анти-IgG, анти-IgM и анти-C3 антисыворотки для определения класса аутоантител и его тепловой амплитуды. Стоит упомянуть простой тест, спонтанную агглютинацию эритроцитов при 20 ° C, характерную особенность, указывающую на наличие холодных аутоантител IgM.Согласно результатам DAT и тепловым характеристикам аутоантител АИГА обычно делятся на две основные группы: wAIHA (~ 70% случаев), которые отображают только IgG или IgG плюс C3d на эритроцитах, и ИБС (~ 20% пациентов). ), который показал только C3d, а также высокий сывороточный титр холодовых агглютининов со специфичностью I. В единичных случаях (7–8% всех АИГА) были обнаружены положительные результаты DAT на IgG и C3d при одновременном существовании теплых аутоантител и холодных агглютининов с высоким титром (смешанный АИГА).Однако появляется все больше свидетельств атипичных случаев сложной классификации — в основном DAT-отрицательных — которые часто бывают тяжелыми и рефрактерными / рецидивируют после нескольких линий терапии и могут иметь летальный исход [10,11]. DAT-отрицательные случаи могут быть вызваны теплыми аутоантителами IgM, которые могут быть идентифицированы с помощью двойного прямого антиглобулинового теста (DDAT) [12,13]. Стоит упомянуть аутоантитело Доната-Ландштейнера, битермический гемолизин, способный фиксировать комплемент при низких температурах и определять лизис эритроцитов при 37 ° C, которое направлено против антигена эритроцита P и вызывает пароксизмальную холодовую гемоглобинурию, которая довольно часто встречается при дети (30% случаев), но редко у взрослых (<1% всех случаев AIHA) [1,2].
Наконец, положительный результат DAT может быть также связан с лекарственными антителами, которые связаны с различными лекарствами (противомикробные препараты: 42% случаев, противовоспалительные препараты: 15% и противоопухолевые препараты: 11%), но встречаются редко. (примерно 1 из 1 миллиона населения). Лекарственно-зависимые антитела реагируют in vitro только в присутствии лекарства, связанного с эритроцитами или добавленного в сыворотку крови пациента в тест-системах (типичный пример пенициллина и цефотетана). Лекарственно-независимые антитела могут быть обнаружены in vitro без добавления какого-либо лекарства, поэтому их характеристики идентичны классическим аутоантителам.Типичным примером является метилдопа, которая вызывает выработку аутоантител к эритроцитам примерно у 15% пациентов, принимающих препарат, но только у 1% развивается АИГА [1,6,7,14,15].
Роль комплемента в патогенезе АМСЗ
Система комплемента играет важную роль как в «теплом» АМСЗ, так и в ИБС. В первых случаях IgG, связанный с эритроцитами, способен фиксировать белковый комплекс комплемента C1 и, таким образом, активировать классический путь комплемента; Подкласс IgG3 является более эффективным, за ним следует IgG1, тогда как IgG2 и IgG4 менее активны или неактивны.Теплые аутоантитела IgM являются мощными активаторами комплемента, но их обычно не обнаруживают в эритроцитах. Фактически, они временно связываются, активируют комплемент, а затем отделяются от мембраны, где могут быть продемонстрированы только факторы комплемента. После активации комплемента фагоцитоз C3b-опсонизированных эритроцитов происходит в основном в печени, хотя также может происходить полный внутрисосудистый гемолиз, опосредованный терминальным литическим комплексом [12,16,17,18]. Положительность DAT для фрагментов C3 является маркером участия комплемента в wAIHA.
Роль системы комплемента в ИБС также значительна, при условии, что тепловая амплитуда аутоантитела IgM близка к значениям, обнаруженным на поверхности участков тела, подвергнутых воздействию низких температур. IgM-холодное аутоантитело связывает C1 и тем самым инициирует классический путь комплемента [19]: C1 эстераза активирует C4 и C2, генерируя конвертазу C3, что приводит к расщеплению C3 на C3a и C3b. Когда эритроциты возвращаются в центральные части тела с температурой 37 ° C, аутоантитела IgM отделяются от поверхности клетки, в то время как C3b остается связанным.Часть эритроцитов, покрытых C3b, секвестрируется в печени, тогда как другие эритроциты лизируются за счет активации C5 с помощью C3b. Окончательное образование МАК определяет внутрисосудистый гемолиз [20,21,22]. Это происходит при тяжелых обострениях и у некоторых пациентов с тяжелым гемолитическим заболеванием, о чем свидетельствует обнаруженная гемоглобинурия, типичная картина пароксизмальной ночной гемоглобинурии (ПНГ). Этот патогенетический механизм в некоторых случаях объясняет положительный эффект ингибирования C5 моноклональным антителом экулизумабом [23,24].Дополнительным доказательством потенциального использования ингибиторов комплемента в лечении АИГА является открытие, что TNT003, мышиное моноклональное антитело, нацеленное на белок комплемента C1s, предотвращает индукцию гемолиза in vitro холодовыми агглютининами [25]. Более того, было обнаружено, что концентрат ингибитора С1-эстеразы защищает эритроциты от разрушения, опосредованного комплементом, при АИГА [26]. Другие ингибиторы комплемента, такие как компстатин Cp40, низкомолекулярный пептид, предотвращающий расщепление C3, и TT30, который предотвращает активацию C3-конвертазы, показали многообещающие эффекты на опосредованный комплементом лизис эритроцитов при ПНГ [27,28] и могут быть потенциальными методами лечения острого гемолиза при АИГА.
Следует напомнить, что холодовые IgM-антитела часто являются моноклональными и более чем у 90% пациентов обнаруживают ограничение легкой цепи [29]. Более того, пациенты с ИБС часто имеют ассоциированное клональное В-клеточное лимфопролиферативное заболевание (лимфоплазмоцитарная лимфома, лимфома маргинальной зоны) или, по крайней мере, неклассифицированную клональную лимфопролиферацию или реактивный лимфоцитоз [20,21]. Эти результаты объясняют обоснование лечения рефрактерных и тяжелых случаев ИБС ритуксимабом [30], отдельно или в комбинации с флударабином [31] или бендамустином, особенно в сочетании с хроническим лимфолейкозом [32] или бортезомибом [33].Поскольку большая часть разрушения эритроцитов происходит не в селезенке, неудивительно, что спленэктомия обычно неэффективна при ИБС [20,21,22].
Т-лимфоциты и иммунорегуляторные цитокины в патогенезе АИГА
Было показано, что Т-клеточная регуляция гуморальной иммунной системы играет решающую роль в потере самотолерантности при АИГА. В последние годы в AIHA было описано усиление пролиферативного ответа Т-клеток in vitro и повышенная цитотоксичность естественных клеток-киллеров в отношении аутологичных эритроцитов [34,35].Еще несколько лет назад CD4 + Т-хелперные клетки подразделялись на два основных подмножества Т-клеток, называемых подмножествами Th2 и Th3. Совсем недавно клетки Th27, которые характеризуются секрецией IL-17, были идентифицированы как ключевые эффекторы в развитии многих аутоиммунных заболеваний, включая АИГА [40]. Было обнаружено, что повышенная частота клеток Th27 и повышенная секреция IL-17 тесно связаны с активностью заболевания у пациентов с АИГА. Соответственно, в модели АИГА на крысах адоптивный перенос клеток Th27 усиливал реакцию антител против эритроцитов и увеличивал начало АИГА, в то время как начало заболевания отменялось нейтрализацией IL-17 in vivo [36].
Более того, CD4 + CD25 + Treg теперь признаны ключевыми игроками в иммунологической толерантности и, таким образом, в предотвращении AIHA и других поликлональных аутоиммунных заболеваний. Ward et al. [37] впервые описали аутоантиген-специфические клоны Treg, секретирующие ИЛ-10, выделенные ex vivo у пациента с АИГА. Эти клоны распознали пептид 72H-86L, происходящий из аутоантигена Rh RBC, и экспрессировали различные регуляторные Т-маркеры в зависимости от состояния активации: высокие уровни CD25 и LAG-3 при неспецифической экспансии, но FoxP3 после активации аутоантигеном, который они распознают [38 ].Совсем недавно было обнаружено, что циркулирующие Treg CD4 + снижены у пациентов с АИГА, наряду с высокими уровнями IL-10 и IL-12 [39]. Известно, что Treg продуцируют IL-10 и трансформирующий фактор роста β (TGF-β), и дисбаланс IL-10 / IL-12 может, таким образом, играть важную роль в возникновении и / или поддержании AIHA. При АМСЗ сообщалось о нескольких других нарушениях иммунорегуляторных цитокинов: было обнаружено повышение сывороточных уровней IL-1α, IL-2 / IL-2R, IL-6 и IL-21; в экспериментах с культивированием сообщалось о повышении Th2 цитокинов IL-2 и IL-12, тогда как было обнаружено снижение уровня IFN-γ.Более того, сообщалось об увеличении Th3 цитокинов IL-4 и IL-13, вместе с повышенной продукцией IL-6, IL-10 и IL-17 [36,40,41]. У пациентов с активным гемолизом наблюдалось дальнейшее снижение IFN-γ и повышение секреции TGF-β. Более того, добавление IL-4, IL-6, IL-10, IL-13 и TGF-β увеличивало секрецию аутоантител в культуре [40]. Все эти данные свидетельствуют в пользу пониженного Th2- и преобладающего Th3-подобного профиля в иммунопатогенезе АИГА, в отличие от преобладающей роли цитотоксических Т-клеток, секретирующих CD8 + IFN-γ, в органоспецифическом аутоиммунитете (т.е.e рассеянный склероз, экспериментальный аутоиммунный энцефаломиелит, диабет 1 типа и аутоиммунный тиреоидит). Более того, повышенные уровни TGF-β способствуют дифференцировке подмножества Th27, что усиливает провоспалительный и аутоиммунный ответ. Напротив, снижение уровней как IFN-γ, так и Tregs привело к снижению ингибирования ответа Th3, то есть к усилению аутоиммунного заболевания, опосредованного аутоантителами (рис. 1). Несмотря на эти цитокиновые нарушения, не было зарегистрировано различий в фенотипическом распределении полиморфизмов TNF-α, IL-10, IL-12 и CTLA-4 между пациентами AIHA и контрольной группой.Что касается терапии, иммунорегуляторные цитокины оценивали после приема низких доз ритуксимаба (фиксированная доза 100 мг на 4 еженедельных инфузии) [42]. Клинический ответ коррелировал с увеличением IFN-γ и снижением IL-4 и IL-17, что позволяет предположить, что лекарство проявляет иммуномодулирующую активность вместе с хорошо известным B-истощающим эффектом. Наконец, недавние неопубликованные наблюдения сообщают об увеличении сывороточных значений BAFF и APRIL при АМСЗ, открывая в будущем терапевтические возможности с использованием моноклональных антител, направленных против этих факторов, например.г. белимумаб. В таблице 2 приведены основные иммунологические аномалии, влияющие на патогенез АИГА.
Таблица 2
Основные иммунологические аномалии, участвующие в патогенезе АИГА
Рис. 1
Субпопуляции Т-лимфоцитов и цитокиновые взаимодействия при АИГА. Повышенное содержание цитокинов выделено желтым цветом: IL-2 и IL-12, которые индуцируют дифференцировку CD4 + наивных Т-клеток в подмножество Th2, и IL-4, который способствует переключению Th3. Повышенные уровни TGF-β способствуют дифференцировке подмножества Th27, что усиливает провоспалительный и аутоиммунный ответ.Напротив, были обнаружены пониженные уровни как IFN-γ, так и Treg (выделены зеленым). Первое привело к снижению ингибирования ответа Th3, то есть к усилению аутоиммунного заболевания, опосредованного аутоантителами, а второе может вызвать отсутствие подавления воспалительных и аутоиммунных путей.
Роль селезенки в патогенезе AIHA
Селезенка является основным органом синтеза антител и иммунного разрушения эритроцитов, покрытых IgG. Это причина того, что он считается наиболее эффективным традиционным методом лечения АИГА теплой второй линии [43].Однако спленэктомия неэффективна примерно в 30% случаев, предположительно потому, что все еще наблюдается повышенный синтез аутоантител в других лимфоидных органах, а печень заменяет функцию селезенки по разрушению эритроцитов. К сожалению, степень секвестрации селезенки, оцениваемая с помощью радиоактивно меченных эритроцитов, а также продолжительность заболевания и ответ на стероиды не являются надежными предикторами его эффективности [44]. Частота спленэктомии составляет около 10–15% всех случаев АМСЗ, но в настоящее время она снижается, учитывая доступность не менее эффективных препаратов второго ряда, в первую очередь ритуксимаба.Стоит напомнить, что спленэктомия обычно неэффективна при ИБС, поскольку большая часть разрушения эритроцитов происходит в печени [20,21]. Интересным недавно опубликованным открытием является появление долгоживущих аутореактивных плазматических клеток в селезенке у пациентов с первичным wAIHA, получавших ритуксимаб [45]. Селезенку получали после операции по поводу рецидива или неэффективности ритуксимаба и анализировали с помощью микроскопии и проточной цитометрии, показывая присутствие Bcl6 + В-клеток зародышевого центра. Остаточная популяция CD19 + B-клеток включает непролиферативные B-клетки памяти и плазматические клетки, которые секретируют анти-RBC IgG in vitro.Кроме того, цитокин BAFF был увеличен в супернатантах культур клеток селезенки, что позволяет предположить, что он может играть роль в дифференцировке короткоживущих плазматических клеток в долгоживущие. Авторы приходят к выводу, что наличие долгоживущих аутореактивных плазматических клеток селезенки может объяснить, почему некоторые пациенты с wAIHA не могут достичь ответа после ритуксимаба. Истощение В-клеток, вызванное самим ритуксимабом, способствует созданию подходящей среды для созревания аутоиммунных долгоживущих плазматических клеток в селезенке.Целенаправленное воздействие на некоторые факторы, такие как BAFF сразу после инъекции ритуксимаба, может стать интересным терапевтическим вариантом в будущем.
Дополнительные факторы, влияющие на клинические характеристики АМСЗ
Основными детерминантами клинической тяжести АИГА являются патогенность аутоантител (связанная с их классом, подклассом, термической амплитудой, а также сродством и эффективностью активации комплемента) и активность ретикулоэндотелиальная система. Однако есть и другие факторы, влияющие на клиническую картину АИГА, в частности эффективность компенсаторного ответа эритробластов, представленного абсолютным количеством ретикулоцитов в периферической крови.Ретикулоцитопения нередко встречается при АИГА, особенно у детей и в тяжелых случаях [46, 47, 48], и может быть вызвана аутоиммунной реакцией на предшественников эритроидов костного мозга. Появляются доказательства того, что введение эритропоэтина может быть полезным для преодоления временной недостаточности костного мозга при компенсации гемолиза [49], что согласуется с эффективностью агонистов тромбопоэтина при первичной иммунной тромбоцитопении [50]. Более того, использование эритропоэтина может снизить потребность в переливании крови и избежать гемолиза, связанного с переливанием крови.
Относительный вес всех факторов, вовлеченных в патогенез АИГА, может объяснить большую неоднородность заболевания. Недавнее крупное многоцентровое исследование 308 случаев АМСЗ показало, что 60% были wAIHA, 27% — ИБС, 8% — смешанными и 5% — атипичными (в основном DAT-отрицательными). Тяжелое проявление (уровень гемоглобина <6 г / дл) наблюдалось примерно в одной трети случаев, в основном это были теплые IgG + C, смешанные и атипичные формы с часто ассоциированной ретикулоцитопенией [10]. Что касается терапии, большинство пациентов wAIHA получали только стероидную терапию первой линии, тогда как пациенты со смешанными и атипичными формами имели повышенный риск рецидива и чаще получали лечение двумя или более линиями терапии.Тромботические события были связаны с тяжелым началом, внутрисосудистым гемолизом и предыдущей спленэктомией, а предикторами летального исхода были тяжелые инфекции, особенно в случаях спленэктомии, острая почечная недостаточность, синдром Эванса и комплексное лечение (4 или более линий) [10] .
Более того, мы недавно описали 13 острых и очень тяжелых случаев АМСЗ, демонстрирующих резистентность к нескольким лекарствам и связанные с ними осложнения, 7 из которых закончились смертельным исходом. Эти сложные АМСЗ продемонстрировали крайне непредсказуемое клиническое течение, что свидетельствует о том, что быстро развивающиеся случаи заслуживают скрупулезного внимания со стороны опытных клиницистов, чтобы избежать отсрочки в реализации потенциально жизненно важных стратегий.В частности, наличие внутрисосудистого гемолиза, гемоглобинурии, положительности DAT для IgG + C, ретикулоцитопении и / или синдрома Эванса должно настораживать клиницистов на необходимость щедрого введения болюсов стероидов, раннего применения ритуксимаба и рассмотрения плазмафереза в критических состояниях. Мы также предлагаем выполнять спленэктомию вскоре после неэффективности ритуксимаба из-за плохого прогноза операции после нескольких иммуносупрессивных терапий. Более того, мы предлагаем использовать эритропоэтин для уменьшения чрезмерной трансфузии и антитромботической профилактики, особенно у пациентов с удаленной спленэктомией [11].В настоящее время мы используем низкомолекулярные гепарины в профилактических дозах, т.е. 30-50% от дозы антикоагулянта, пока идет гемолитический процесс [51].
Дополнительным фактором, влияющим на клиническую картину АИГА, является связь с лимфопролиферативными заболеваниями. Известно, что приблизительно у 10% пациентов с хроническим лимфолейкозом и у 2-3% пациентов с неходжкинской лимфомой развивается АИГА. Более того, в популяционном исследовании 86 пациентов с ИБС клональная лимфопролиферация костного мозга была продемонстрирована у 75% и 90% пациентов с помощью биопсии костного мозга и проточной цитометрии, соответственно [20].Более того, появляется все больше доказательств того, что тяжелая и смертельная форма АИГА может быть осложнением трансплантации гемопоэтических стволовых клеток. Недавнее крупное исследование в больнице Кингс-Колледжа [52] описало общую частоту 3,6% и связь с трансплантацией гемопоэтических стволовых клеток от неродственных доноров. Около двух третей случаев потребовалось многократного лечения, но только в половине случаев АМСЗ удалось полностью избавиться от него. Десять случаев закончились смертельным исходом, а в 4 случаях смерть напрямую связана с АМСЗ, что указывает на более высокую общую смертность от АМСЗ после трансплантации (HR 2.48), чем первичный АМСЗ.
Наконец, стоит вспомнить синдром пассажирских лимфоцитов, который возникает из-за выработки антител, направленных против эритроцитов реципиента пассивно перенесенными лимфоцитами, перелитыми стволовыми клетками, что чаще всего наблюдается, когда донором является группа O и группа пациентов A. Преходящий иммунный гемолиз также был связан с трансплантацией твердых органов, при этом риск и степень гемолиза, пропорциональные массе пересаженных лимфоцитов, были самыми низкими в почках (антитела в 17%, гемолиз в 9%), затем выше в печени (антитела в 40% случаев, гемолиз в 29%) и самый высокий при трансплантации сердце-легкие (антитела в 70%, гемолиз в 70%) [53,54].
Выводы
АМСЗ — это гетерогенное заболевание, включающее теплые, холодные и смешанные формы, а также атипичные случаи сложной диагностической классификации (DAT-отрицательные, теплые IgM), о которых сообщается все чаще. Он может быть первичным или вторичным по отношению к лимфопролиферативным синдромам, инфекциям, иммунодефициту и опухолям. Более того, АИГА описывается все чаще после трансплантации гемопоэтических стволовых клеток и у реципиентов трансплантатов твердых органов.Клинические проявления первичного АИГА могут варьироваться от легких до очень тяжелых форм, при этом сообщаемая летальность составляет 11% в более ранних исследованиях и 4% в более поздних исследованиях; вторичные формы обычно более тяжелые, с повышенной смертностью, особенно при посттрансплантационных формах. В патогенез АИГА вовлечены несколько иммунологических механизмов: аутоантитела, ADCC, фагоциты, В- и Т-лимфоциты, Treg, цитокины и система комплемента. Новое понимание этого сложного сценария может дать подсказки для будущих терапевтических вариантов, специально нацеленных на коррекцию основного патогенного механизма, задействованного в различных формах АИГА.
Выражение признательности
Эта работа была поддержана исследовательским финансированием Fondazione IRCCS Ca ‘Granda Ospedale Maggiore Policlinico, номер гранта RC 2014 и Министерством здравоохранения, грант RF 2010, конвенция No. 141 / RF-2010-2303934.
Заявление о раскрытии информации
Автор не заявляет о конфликте интересов.
Список литературы
- Петц Л.Д., Гарратти Г.: Иммунные гемолитические анемии, 2-е изд.Филадельфия, Черчилль Ливингстон, 2004.
- Берентсен С: Как я справляюсь с болезнью холодовых агглютининов. Br J Haematol 2011; 153: 309-317.
- Герс BC, Фридберг RC: Аутоиммунная гемолитическая анемия.Am J Hematol 2002; 69: 258-271.
- Аббас А.К., Лихтман А.Х., Пиллай С.: Клеточная и молекулярная иммунология, Филадельфия, Сондерс, 2012.
- Маккуин Ф .: B-клеточное объяснение аутоиммунного заболевания: возвращение запрещенного клона.Postgrad Med J. 2012; 88: 226-233.
- Garratty G, Arndt PA: Лекарства, которые, как было доказано, вызывают лекарственную иммунную гемолитическую анемию или положительные прямые тесты на антиглобулин: некоторые интересные результаты с 2007 года. Иммуногематология 2014; 30: 66-79.
- Салама А. Иммунная гемолитическая анемия, вызванная лекарствами.Мнение эксперта Drug Saf 2009; 8: 73-79.
- Аренс Н., Прусс А., Кане А., Кизеветтер Н., Салама А. Сосуществование аутоантител и аллоантител к эритроцитам в результате переливания крови. Переливание 2007; 47: 813-816.
- Алижотас-Рейг J: синдром, связанный с адъювантом человека, или аутоиммунный / воспалительный синдром, индуцированный адъювантами.Откуда мы пришли? Куда мы идем? Предложение по новым диагностическим критериям. Волчанка 2015; 2015, DOI: 10,1177 / 0961203315579092.
- Барчеллини В., Фаттиццо Б., Занинони А., Радис Т., Нишель I, Ди Бона Е., Лунги М., Тассинари С., Альфинито Ф, Феррари А, Лепораче А. П., Нискола П., Карпенедо М., Боскетти С., Ревелли Н., Вилла М. А., Консонни D, Scaramucci L, De Fabritiis P, Tagariello G, Gaidano G, Rodeghiero F, Cortelezzi A, Zanella A: Клиническая гетерогенность и предикторы исхода при первичной аутоиммунной гемолитической анемии: исследование GIMEMA с участием 308 пациентов.Кровь 2014; 124: 2930-2936.
- Fattizzo B, Zaninoni A, Nesa F, Sciumbata VM, Zanella A, Cortelezzi A, Barcellini W: Уроки очень тяжелых, рефрактерных и фатальных первичных аутоиммунных гемолитических анемий. Am J Hematol 2015; 90: E149-151.
- Arndt PA, Leger RM, Garratty G: Серологические данные при аутоиммунной гемолитической анемии, связанной с переливанием теплых аутоантител к иммуноглобулину M, 2009; 49: 235-242.
- Бартолмас Т., Салама А. Двойной антиглобулиновый тест для обнаружения теплых аутоантител слабого или неагглютинирующего иммуноглобулина М. Переливание 2010; 50: 1131-1134.
- Bass GF, Tuscano ET, Tuscano JM: Диагностика и классификация аутоиммунной гемолитической анемии.Autoimmun Rev 2014; 13: 560-564.
- Гарратти G: Иммунная гемолитическая анемия, вызванная лекарствами. Мнение эксперта Drug Saf 2012; 11: 635-642.
- Packman CH: Гемолитическая анемия, вызванная теплыми аутоантителами.Кровь Rev 2008; 22: 17-31.
- Дейси Дж .: Аутоиммунная гемолитическая анемия [АМСЗ]: патогенез; в Dacie J (ed): гемолитические анемии. Vol. 3. Лондон, Черчилль Ливингстон, 1992, стр. 392-451.
- Курландер Р.Дж., Росс В.Ф., Лог Г.Л.: Количественное влияние антител и комплементарного покрытия эритроцитов на лизис клеток, опосредованный моноцитами.Дж. Клин Инвест 1978; 61: 1309-1319.
- Berentsen S, Beiske K, Tjønnfjord GE: Первичная хроническая болезнь холодовых агглютининов: обновленная информация о патогенезе, клинических особенностях и терапии. Гематология 2007; 12: 361-370.
- Berentsen S, Ulvestad E, Langholm R, Beiske K, Hjorth-Hansen H, Ghanima W., Sørbø JH, Tjønnfjord GE: Первичная хроническая болезнь холодовых агглютининов: популяционное клиническое исследование с участием 86 пациентов.Haematologica 2006; 91: 460-466.
- Свечицкий П.Л., Хегерова Л.Т., Герц М.А.: Болезнь холодовых агглютининов. Кровь 2013; 122: 1114-1121.
- Ulvestad E, Berentsen S, Mollnes TE: гемолиз в острой фазе при хронической болезни холодовых агглютининов.Scand J Immunol 2001; 54: 239-242.
- Рот А., Хаттманн А., Ротер Р.П., Дурсен Ю., Филипп Т.: Долгосрочная эффективность ингибитора комплемента экулизумаба при болезни холодовых агглютининов. Кровь 2009; 113: 3885-3886.
- Хилл А., Ротер Р.П., Арнольд Л., Келли Р., Каллен М.Дж., Ричардс С.Дж., Хиллмен П. Экулизумаб предотвращает внутрисосудистый гемолиз у пациентов с пароксизмальной ночной гемоглобинурией и демаскирует низкоуровневый внесосудистый гемолиз, происходящий из-за опсонизации С3.Haematologica 2010; 95: 567-573.
- Shi J, Rose EL, Singh A, Hussain S, Stagliano NE, Parry GC, Panicker S: TNT003, ингибитор сериновой протеазы C1s, предотвращает активацию комплемента, вызванную холодовыми агглютининами. Кровь 2014; 123: 4015-4022.
- Wouters D, Stephan F, Strengers P, de Haas M, Brouwer C, Hagenbeek A, van Oers MH, Zeerleder S: концентрат ингибитора C1-эстеразы спасает эритроциты от разрушения, опосредованного комплементом, при аутоиммунной гемолитической анемии.Кровь 2013; 121: 1242-1244.
- Risitano AM, Notaro R, Pascariello C, Sica M, del Vecchio L, Horvath CJ, Fridkis-Hareli M, Selleri C, Lindorfer MA, Taylor RP, Luzzatto L, Holers VM: слитный белок рецептор 2 / фактор H TT30 защищает пароксизмальная ночная гемоглобинурия, эритроциты в результате комплемент-опосредованного гемолиза и фрагмент C3.Кровь 2012; 119: 6307-6316.
- Risitano AM1, Ricklin D, Huang Y, Reis ES, Chen H, Ricci P, Lin Z, Pascariello C, Raia M, Sica M, Del Vecchio L, Pane F, Lupu F, Notaro R, Resuello RR, DeAngelis RA, Lambris JD: Пептидные ингибиторы активации C3 как новая стратегия ингибирования комплемента для лечения пароксизмальной ночной гемоглобинурии.Кровь 2014; 123: 2094-2101.
- Harboe M, van Furth R, Schubothe H, Lind K, Evans RS: Исключительное появление цепей K в изолированных холодных гемагглютининах. Scand J Haematol 1965: 2: 259-266.
- Berentsen S, Tjønnfjord GE: Диагностика и лечение аутоиммунной гемолитической анемии, опосредованной холодовыми агглютинином.Кровь Rev 2012; 26: 107-115.
- Berentsen S, Randen U, Vågan AM, Hjorth-Hansen H, Vik A, Dalgaard J, Jacobsen EM, Thoresen AS, Beiske K, Tjønnfjord GE: высокая частота ответа и стойкие ремиссии после комбинированной терапии флударабином и ритуксимабом при хронической болезни холодовых агглютининов.Кровь 2010; 116: 3180-3184.
- Quinquenel A, Willekens C, Dupuis J, Royer B, Ysebaert L, De Guibert S, Michallet AS, Feugier P, Guieze R, Levy V, Delmer A: комбинация бендамустина и ритуксимаба в лечении хронической аутоиммунной гемолитической анемии, связанной с лимфолейкозом : многоцентровое ретроспективное исследование французской интергруппы ХЛЛ (GCFLLC / MW и GOELAMS).Am J Hematol 2015; 90: 204-207.
- Carson KR, Beckwith LG, Mehta J: Успешное лечение IgM-опосредованной аутоиммунной гемолитической анемии бортезомибом. Кровь 2010; 115: 915.
- Fagiolo E: потеря иммунологической толерантности vs.аутоантигены эритроцитов и нарушение регуляции цитокиновой сети при аутоиммунной гемолитической анемии. Autoimmun Rev 2004; 3: 53-59.
- Gilsanz F, de La Serna J, Moltó L, Alvarez-Mon M: Гемолитическая анемия при хроническом крупнозернистом лимфоцитарном лейкозе естественных клеток-киллеров: цитотоксичность естественных клеток-киллеров против аутологичных эритроцитов связана с гемолизом.Переливание 1996; 36: 463-466.
- Xu L, Zhang T, Liu Z, Li Q, Xu Z, Ren T: критическая роль клеток Th27 в развитии аутоиммунной гемолитической анемии. Exp Hematol 2012; 40: 994-1004.
- Ward FJ, Hall AM, Cairns LS, Leggat AS, Urbaniak SJ, Vickers MA, Barker RN: Клональные регуляторные Т-клетки, специфичные для аутоантигена эритроцитов при аутоиммунной гемолитической анемии человека.Кровь 2008; 111: 680-687.
- Сакагути С., Оно М., Сетогучи Р., Яги Х., Хори С., Фехервари З., Симидзу Дж., Такахаши Т., Номура Т.: Foxp3 + CD25 + CD4 + естественные регуляторные Т-клетки при доминантной самотолерантности и аутоиммунных заболеваниях. Immunol Rev 2006; 212: 8-27.
- Ахмад Э., Элгохари Т., Ибрагим Х: естественные регуляторные Т-клетки и интерлейкины 10 и 12 в патогенезе идиопатической теплой аутоиммунной гемолитической анемии.Исследование J Allergol Clin Immunol 2011; 21: 297-304.
- Барчеллини В., Клеричи Дж., Монтесано Р., Тайоли Е., Морелати Ф., Ребулла П., Занелла А. Количественная оценка выработки антител к эритроцитам при идиопатической аутоиммунной гемолитической анемии in vitro: эффект стимуляции митогенов и цитокинов.Br J Haematol 2000; 111: 452-460.
- Toriani-Terenzi C, Fagiolo E: IL-10 и сеть цитокинов в патогенезе аутоиммунной гемолитической анемии человека. Энн Н. И. Акад. Наук 2005; 1051: 29-44.
- Barcellini W, Zaja F, Zaninoni A, Imperiali FG, Battista ML, Di Bona E, Fattizzo B, Consonni D, Cortelezzi A, Fanin R, Zanella A: низкие дозы ритуксимаба у взрослых пациентов с идиопатической аутоиммунной гемолитической анемией: клиническая эффективность и биологические исследования.Кровь 2012; 119: 3691-3697.
- Lechner K, U Jager U: Как я лечу аутоиммунные гемолитические анемии у взрослых. Кровь 2010; 16: 1831-1838.
- Crowther M, Chan YL, Garbett IK, Lim W, Vickers MA, Crowther MA: Основанный на фактах сфокусированный обзор лечения идиопатической теплой иммунной гемолитической анемии у взрослых.Кровь 2011; 118: 4036-4040.
- Mahévas M, Michel M, Vingert B, Moroch J, Boutboul D, Audia S, Cagnard N, Ripa J, Menard C, Tarte K, Mégret J, Le Gallou S, Patin P, Thai L, Galicier L, Bonnotte B, Godeau B, Noizat-Pirenne F, Weill JC, Reynaud CA: Появление долгоживущих аутореактивных плазматических клеток в селезенке у пациентов с первичной теплой аутоиммунной гемолитической анемией, получавших ритуксимаб.J Autoimmun 2015; DOI: 10.1016 / j.jaut.2015.05.006.
- Конли С.Л., Липпман С.М., Несс П.: Аутоиммунная гемолитическая анемия с ретикулоцитопенией. Неотложная медицинская помощь. JAMA 1980; 244: 1688-1690.
- Liesveld JL, Rowe JM, Lichtman MA: Вариабельность ответа эритроцитов при аутоиммунных гемолитических анемиях: анализ 109 случаев.Кровь 1987; 69: 820-826.
- Aladjidi N, Leverger G, Leblanc T, Picat MQ, Michel G, Bertrand Y, Bader-Meunier B, Robert A, Nelken B, Gandemer V, Savel H, Stephan JL, Fouyssac F, Jeanpetit J, Thomas C, Rohrlich P, Баручель А., Фишер А., Чене Дж., Перель Ю. Национальный центр аутоиммунных иммунитетов Cytopénies de l’Enfant (CEREVANCE): новый взгляд на аутоиммунную гемолитическую анемию у детей: национальное обсервационное исследование 265 детей во Франции.Haematologica 2011; 96: 655-663.
- Арбах О., Фанк Р., Зейбт Ф., Салама А. Эритропоэтин может улучшить анемию у пациентов с аутоиммунной гемолитической анемией, связанной с ретикулоцитопенией. Transfus Med Hemother 2012; 39: 221-223.
- Кутер DJ: Биология тромбопоэтина и агонистов рецепторов тромбопоэтина.Int J Hematol 2013; 98: 10-23.
- Akl EA, Ramly EP, Kahale LA, Yosuico VE, Barba M, Sperati F, Cook D, Schünemann H: Антикоагуляция для людей с раком и центральные венозные катетеры. Кокрановская база данных Syst Rev 2014; 10: CD006468.
- Wang M, Wang W, Abeywardane A, Adikarama M, McLornan D, Raj K, de Lavallade H, Devereux S, Mufti GJ, Pagliuca A, Potter VT, Mijovic A: Аутоиммунная гемолитическая анемия после трансплантации аллогенных гемопоэтических стволовых клеток: анализ 533 взрослые пациенты, перенесшие трансплантацию в больнице Королевского колледжа.Biol Blood Marrow Transplant 2015; 21: 60-66.
- Hoffman PC: Иммунная гемолитическая анемия — избранные темы. Образовательная программа Hematology Am Soc Hematol 2009: 80-86.
- ElAnsary M, Hanna MO, Saadi G, ElShazly M, Fadel FI, Ahmed HA, Aziz AM, ElSharnouby A, Kandeel MM: синдром пассажирских лимфоцитов при несоответствующей трансплантации печени и почек ABO и резус D минор: проспективный анализ.Hum Immunol 2015; 76: 447-452.
Автор Контакты
Доктор Вильма Барчеллини
U.O. Онкоематология, Padiglione Granelli
Fondazione IRCCS Ca ‘Granda Ospedale Maggiore Policlinico
Via F. Sforza, 35, 20122 Милан, Италия
wbarcel @ policlinico.mi.it
Подробности статьи / публикации
Предварительный просмотр первой страницы
Получено: 29 мая 2015 г.
Принято: 28 июля 2015 г.
Опубликовано онлайн: 7 сентября 2015 г.
Дата выпуска: сентябрь 2015 г.
Количество страниц для печати: 7
Количество рисунков: 1
Количество столов: 2
ISSN: 1660-3796 (печатный)
eISSN: 1660-3818 (онлайн)
Для дополнительной информации: https: // www.karger.com/TMH
Авторские права / Дозировка препарата / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме или любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование, или с помощью какой-либо системы хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарств: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарств, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю настоятельно рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новый и / или редко применяемый препарат.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, нанесенный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.



 антитела AIHA, которые составляют около 80-90% случаев у взрослых, гемолиз опосредуется антитела, которые связываются с эритроцитами при 37 ° C (98,6 ° F при криопатических гемолитических синдромах, холодореактивные аутоантитела проявляют сродство к эритроцитам оптимально при температурах ниже тела У взрослых большинство холодореактивных антител представляют собой агглютинины изотип иммуноглобулина M (IgM). У детей чаще всего встречаются холодовые гемолизины (как правило, IgG). У необычных пациентов со смешанным AIHA обнаруживаются аутоантитела, реагирующие как на холод, так и на тепло. . Каждый из этих типов АМСЗ может быть подразделен на подклассы в зависимости от наличия или отсутствия основные заболевания.При отсутствии основного заболевания АМСЗ называют первичным или идиопатический. Когда АИГА возникает как проявление или осложнение другого заболевания, термин используется вторичный АИГА. Хронический лимфолейкоз (ХЛЛ) и лимфомы составляют около половина всех вторичных случаев АИГА.
антитела AIHA, которые составляют около 80-90% случаев у взрослых, гемолиз опосредуется антитела, которые связываются с эритроцитами при 37 ° C (98,6 ° F при криопатических гемолитических синдромах, холодореактивные аутоантитела проявляют сродство к эритроцитам оптимально при температурах ниже тела У взрослых большинство холодореактивных антител представляют собой агглютинины изотип иммуноглобулина M (IgM). У детей чаще всего встречаются холодовые гемолизины (как правило, IgG). У необычных пациентов со смешанным AIHA обнаруживаются аутоантитела, реагирующие как на холод, так и на тепло. . Каждый из этих типов АМСЗ может быть подразделен на подклассы в зависимости от наличия или отсутствия основные заболевания.При отсутствии основного заболевания АМСЗ называют первичным или идиопатический. Когда АИГА возникает как проявление или осложнение другого заболевания, термин используется вторичный АИГА. Хронический лимфолейкоз (ХЛЛ) и лимфомы составляют около половина всех вторичных случаев АИГА. системная красная волчанка (СКВ) и другие аутоиммунные болезни также являются причиной большого числа вторичных случаев АМСЗ. иммунное повреждение эритроцитов. Известно три механизма, два из которых включают элементы аутоиммунитет, при котором аутоантитела распознают и связываются со специфическими эпитопами эритроцитов одновременно с лекарствами или их метаболитами или в которых аутоантитела связываются с эпитопами эритроцитов без наличие препарата Диагноз Признаки и симптомы АИГА неспецифичны и характерны для всех типов анемии. Первичные симптомы включают одышку при физической нагрузке, одышку в покое, утомляемость различной степени, а также признаки и симптомы гипердинамического состояния, такие как скачкообразный пульс, сердцебиение и т. д. Результаты лабораторных исследований АИГА, вызванного лекарственными препаратами, могут напоминать результаты АИГА с теплыми антителами или криопатический гемолитический синдром в зависимости от механизма индукции аутоантител и антиген-мишень. Высокий показатель подозрительности со стороны врача и дискуссий.
системная красная волчанка (СКВ) и другие аутоиммунные болезни также являются причиной большого числа вторичных случаев АМСЗ. иммунное повреждение эритроцитов. Известно три механизма, два из которых включают элементы аутоиммунитет, при котором аутоантитела распознают и связываются со специфическими эпитопами эритроцитов одновременно с лекарствами или их метаболитами или в которых аутоантитела связываются с эпитопами эритроцитов без наличие препарата Диагноз Признаки и симптомы АИГА неспецифичны и характерны для всех типов анемии. Первичные симптомы включают одышку при физической нагрузке, одышку в покое, утомляемость различной степени, а также признаки и симптомы гипердинамического состояния, такие как скачкообразный пульс, сердцебиение и т. д. Результаты лабораторных исследований АИГА, вызванного лекарственными препаратами, могут напоминать результаты АИГА с теплыми антителами или криопатический гемолитический синдром в зависимости от механизма индукции аутоантител и антиген-мишень. Высокий показатель подозрительности со стороны врача и дискуссий. Персонал банка крови обычно может раскрыть роль препарата. общий анализ крови Мазок периферической крови: этот тест может выявить анемию, панцитопению, и инфекции. Наряду с дифференциальным подсчетом, общий анализ крови может помочь диагностировать гематологические злокачественные новообразования и другие гематологические нарушения. Количество тромбоцитов обычно составляет нормальный при большинстве гемолитических анемий. Повышенное количество ретикулоцитов свидетельствует об увеличении продукции эритроцитов и является критерием гемолиз, но не специфичен для гемолиза. Тромбоцитопения, связанная с положительным прямым Кумбса возникают при синдроме Эванса. Исследование сывороточной лактатдегидрогеназы (ЛДГ): повышение уровня ЛДГ в сыворотке крови является критерием гемолиза, но не конкретно Гаптоглобин в сыворотке: низкий уровень гаптоглобина в сыворотке является критерием от средней до тяжелой степени. гемолиз. Непрямой билирубин: неконъюгированный билирубин является критерием гемолиза, но это не так.
Персонал банка крови обычно может раскрыть роль препарата. общий анализ крови Мазок периферической крови: этот тест может выявить анемию, панцитопению, и инфекции. Наряду с дифференциальным подсчетом, общий анализ крови может помочь диагностировать гематологические злокачественные новообразования и другие гематологические нарушения. Количество тромбоцитов обычно составляет нормальный при большинстве гемолитических анемий. Повышенное количество ретикулоцитов свидетельствует об увеличении продукции эритроцитов и является критерием гемолиз, но не специфичен для гемолиза. Тромбоцитопения, связанная с положительным прямым Кумбса возникают при синдроме Эванса. Исследование сывороточной лактатдегидрогеназы (ЛДГ): повышение уровня ЛДГ в сыворотке крови является критерием гемолиза, но не конкретно Гаптоглобин в сыворотке: низкий уровень гаптоглобина в сыворотке является критерием от средней до тяжелой степени. гемолиз. Непрямой билирубин: неконъюгированный билирубин является критерием гемолиза, но это не так. В частности, уровень непрямого билирубина обычно составляет менее 3 мг / дл. Прямой антиглобулиновый тест (DAT): Результат DAT обычно положительный при аутоиммунной гемолитической анемии (АИГА), но может иногда дает отрицательный результат при этом заболевании. ДАТ-отрицательные АМСЗ были рассмотрены. От 5 до 10% всех АМСЗ имеют DAT-отрицательный тест. Полибреновый тест позволяет обнаружить DAT-отрицательный AIHA. Лечение Все препараты, используемые для лечения АИГА, в значительной степени или частично направлены против естественной иммунной системы пациента, что, в свою очередь, может серьезно подорвать иммунная система из-за лечения .. Первая линия терапии АИГА — кортикостероиды, которые эффективны у 70-85% пациентов и должны постепенно снижаться в течение периода времени. 6-12 месяцев.Для рефрактерных / рецидивирующих случаев текущая последовательность терапии второй линии спленэктомия (эффективна примерно в 2 из 3 случаев, но с предполагаемой скоростью излечения до 20%), ритуксимаб (эффективен при ок.
В частности, уровень непрямого билирубина обычно составляет менее 3 мг / дл. Прямой антиглобулиновый тест (DAT): Результат DAT обычно положительный при аутоиммунной гемолитической анемии (АИГА), но может иногда дает отрицательный результат при этом заболевании. ДАТ-отрицательные АМСЗ были рассмотрены. От 5 до 10% всех АМСЗ имеют DAT-отрицательный тест. Полибреновый тест позволяет обнаружить DAT-отрицательный AIHA. Лечение Все препараты, используемые для лечения АИГА, в значительной степени или частично направлены против естественной иммунной системы пациента, что, в свою очередь, может серьезно подорвать иммунная система из-за лечения .. Первая линия терапии АИГА — кортикостероиды, которые эффективны у 70-85% пациентов и должны постепенно снижаться в течение периода времени. 6-12 месяцев.Для рефрактерных / рецидивирующих случаев текущая последовательность терапии второй линии спленэктомия (эффективна примерно в 2 из 3 случаев, но с предполагаемой скоростью излечения до 20%), ритуксимаб (эффективен при ок. 80-90% случаев), а затем любой из иммунодепрессанты (азатиоприн, циклофосфамид, циклоспорин, микофенолятмофетил). Дополнительные методы лечения включают внутривенное введение иммуноглобулинов, даназол, плазмаферез и алемтузумаб и высокие дозы циклофосфамида в качестве последнего средства. ритуксимаб развивается, вероятно, что этот препарат будет обнаружен на более ранней стадии терапии теплого АИГА, перед применением более токсичных иммунодепрессантов и вместо спленэктомии в некоторых случаях В настоящее время ритуксимаб рекомендуется при ишемической болезни сердца в качестве терапии первой линии.
80-90% случаев), а затем любой из иммунодепрессанты (азатиоприн, циклофосфамид, циклоспорин, микофенолятмофетил). Дополнительные методы лечения включают внутривенное введение иммуноглобулинов, даназол, плазмаферез и алемтузумаб и высокие дозы циклофосфамида в качестве последнего средства. ритуксимаб развивается, вероятно, что этот препарат будет обнаружен на более ранней стадии терапии теплого АИГА, перед применением более токсичных иммунодепрессантов и вместо спленэктомии в некоторых случаях В настоящее время ритуксимаб рекомендуется при ишемической болезни сердца в качестве терапии первой линии. Врач может проверить ваш уровень этих антител, которые атакуют эритроциты при низких температурах.
Врач может проверить ваш уровень этих антител, которые атакуют эритроциты при низких температурах.