Рецидив рака груди, прогнозы и наблюдение
Факторы, указывающие на возможный рецидив рака груди
Выбор тактики лечения и прогнозы для конкретной пациентки зависят от степени распространенности рака. Риск повторного возникновения заболевания можно вычислить по определенным характеристикам заболевания. Самым основным фактором, повышающим риск повторного возникновения, является наличие метастазов в подмышечных лимфоузлах.
После проведения оперативного удаления рака молочной железы патологи очень точно исследуют удаленную злокачественную опухоль и определяют тип рака. При выборе терапии и определении риска рецидива рака груди значимыми свойствами являются: степень злокачественности опухоли (градусы), гормональный статус, скорость деления клеток, а также наличие рецепторов HER-2. Кроме того, фактором, повышающим риск рецидива рака груди, является молодой возраст пациентки.
Иногда рак груди появляется повторно в том же месте, где и первичное образование (местный рецидив рака груди).
Шкала злокачественности рака груди
По злокачественности рак груди дифференцируется на три степени (по шкале градусов от 1 до 3). Чем лучше дифференцируется клетка, тем больше она напоминает здоровую ткань и тем медленнее она растет и распространяется. Градус 1 означает форму рака груди с хорошим прогнозом, и наоборот градус 3 говорит о форме рака с плохим прогнозом. Шкала градуса используется когда оценивается необходимость послеоперационного медикаментозного лечения.
После прохождения лечения возрастает роль систематического наблюдения заболевания
В клинике Дократес пациенткам составляется индивидуальный план наблюдения.
Хорошее самочувствие пациентки с раком груди
Для поддержания хорошего качества жизни женщины, заболевшей раком груди, нужно комплексно заботиться о ее здоровье и хорошем самочувствии. Именно для достижения этих целей в Дократес работает целая команда специалистов Центра восстановления здоровья. Специалисты центра составляют для пациентки программу, с учетом специфики заболевания и индивидуальных потребностей женщины. К самым распространенным поддерживающим и восстановительным процедурам при раке груди относятся лимфатерапия, консультации сексолога и специалиста по питанию.
Виды рака груди
Onko.lv Рак груди О болезни Виды рака грудиОткрыт целый ряд биологических признаков рака груди, но наиболее важны два, обнаруживаемых посредством анализов.
- Состояние гормональных рецепторов: если в клетках опухоли констатировано большое количество гормональных рецепторов (рецепторов эстрогена, или ER и/или рецепторов прогестерона, или PgR), такая опухоль называется гормонально-позитивной – соответственно – ER-позитивной и/или PgR-позитивной – опухолью. Примерно в двух третях случаев рак груди является гормонально-позитивным. Гормонально-позитивные опухоли очень хорошо реагируют на лечение, уменьшающее количество гормонов.
- Присутствие рецептора эпидермального фактора роста 2 (HER2): рецептор HER2 располагается на поверхности многих клеток и участвует в ответной реакции клетки на целый ряд факторов роста. В некоторых клетках рака груди содержание рецепторов HER2 патологически велико, что заставляет эти клетки делиться и размножаться намного стремительнее – такие клетки называются HER2 позитивными. До 30% случаев рака груди являются HER2 позитивными, что существенно влияет на прогноз и лечение заболевания.
 HER2 позитивные опухоли представляют собой отдельную, стремительно прогрессирующую форму болезни, требующую особых и неотложных действий. Поэтому важно определить состояние HER2 по возможности раньше – как только обнаружен рак груди, не дожидаясь рецидива или прогресса опухоли. На наличие HER2 исследуются раковые клетки, полученные любым из методов биопсии. Если врач не провел проверку HER2 по время биопсии, образцы тканей могут быть сохранены и исследованы в любое время.
HER2 позитивные опухоли представляют собой отдельную, стремительно прогрессирующую форму болезни, требующую особых и неотложных действий. Поэтому важно определить состояние HER2 по возможности раньше – как только обнаружен рак груди, не дожидаясь рецидива или прогресса опухоли. На наличие HER2 исследуются раковые клетки, полученные любым из методов биопсии. Если врач не провел проверку HER2 по время биопсии, образцы тканей могут быть сохранены и исследованы в любое время.
Внимание!
Всем женщинам с подтвержденным диагнозом рака груди необходимо точно определить состояние HER2. Без проверки врач не сможет определить точный прогноз заболевания и назначить правильное лечение.
Рак груди лечится, но чем раньше выявлен диагноз, тем больше шансов на благоприятный исход
Чем опасна онкология молочной железы и как проходит лечение рассказала онкомаммолог Людмила Гильмутдинова
21 августа, AmurMedia. Согласно статистике, заболеваемость онкологией молочной железы растет год от года — ежегодно в мире регистрируется более 1 миллиона впервые заболевших женщин, из них порядка 30% случаев — рак в запущенной стадии. Что такое рак груди, каковы факторы риска и симптомы заболевания корр. ИА AmurMedia поведала председатель регионального общества «Российское общество онкомаммологов» Людмила Гильмутдинова.
Согласно статистике, заболеваемость онкологией молочной железы растет год от года — ежегодно в мире регистрируется более 1 миллиона впервые заболевших женщин, из них порядка 30% случаев — рак в запущенной стадии. Что такое рак груди, каковы факторы риска и симптомы заболевания корр. ИА AmurMedia поведала председатель регионального общества «Российское общество онкомаммологов» Людмила Гильмутдинова.
— Что такое рак груди, почему он возникает?
— Для того, чтобы осознать всю опасность рака груди, необходимо понимать, всю важность этого органа. Условно грудь «принадлежит» не одной лишь женщине. Она необходима ребенку, как источник питания, является предметом внимания мужчин, а кроме того, грудь выполняет не только эстетическую и физиологическую, но и психологическую функции – влияет на самооценку женщины. К сожалению, при этом она еще и один из наименее защищенных органов женского тела, который очень подвержен онкологическим заболеваниям.
Но вернемся к вашему вопросу: что такое рак молочной железы? Это злокачественная опухоль, которая развивается из эпителия молочной железы. Согласно статистике, заболеваемость растет год от года — ежегодно в мире регистрируется более 1 миллиона впервые заболевших женщин. Из них порядка 30% случаев — рак в запущенной стадии, который хоть и лечится, но выживаемость при нем невероятно низкая. В России картина похожа на общемировую, в 2015 году в стране было зарегистрировано 68547 женщин с онкологией молочной железы. Это очень много, учитывая, что зачастую подвержены этому женщины в самом активном возрасте – от 40 до 55 лет.
— Не так давно рак груди считался, да и был возрастным заболеванием, а сегодня он отмечается даже у очень юных девушек. С чем это связано?
— В последние десятилетия рак молочной железы заметно «помолодел» — заболеваемость до 30 лет увеличилась на 13%. Выделить какую-то одну о причину этого попросту невозможно, потому что такой рост в принципе обусловлен современным невероятно интенсивным образом жизни.
— Каковы первые симптомы этого заболевания? Что должно насторожить женщину?
Проблема в том, что как таковых первых симптомов нет. Есть лишь предпосылки по которым можно догадаться, что не все в порядке. Например, есть такое понятие, как предменструальный синдром. В это время происходит напряжение молочных желез и если при этом ощущается болезненность, то это уже «звоночек» для того, чтобы обратиться к гинекологу, а также обследовать грудь.
— Как часто необходимо обследоваться?
— Молодые женщины до 35 лет должны ежегодно делать ультразвуковое исследование независимо от того, есть у них «сбои в работе» молочной железы или нет. Это профилактика. Желательно выбрать определенное время, например, пятый — десятый день с начала месячных и отправиться на УЗИ. В Хабаровске это весьма доступно, а к тому же процедуру можно провести бесплатно. Дальше уже на усмотрение врача: если есть какая-то патология, то возможно придется делать УЗИ чаще – раз в полгода, а то и раз в три месяца. Помните, что главная задача – выявить заболевание на ранней стадии, а сделать это можно только одним способом – как можно чаще обращаться к врачу и проходить диагностику. При раке молочной железы первой степени выживаемость составляет в среднем 95%, а в некоторых развитых европейских странах доходит и до 100%. Однако порядка 20% женщин обращаются за помощью только на третьей стадии, при которой уже смертность достигает 75%.
— А все-таки, можно ли обнаружить проблему самостоятельно?
— Самообследование, конечно, играет свою роль. По большей части женщины приходят к нам именно после того, как обнаружат новообразование самостоятельно. Но эффективно оно не всегда, чаще всего находят проблему девушки с маленькой грудью, которые могут самостоятельно себя пропальпировать, обнаружить уплотнения и обратиться к врачу. Из общих советов — обращать внимание нужно на все: покраснение, изменение формы молочной железы, формы соска (втягивается ли он, когда вы поднимаете руки кверху). Также сюда можно отнести и выделения из сосков, которые могут быть прозрачными, а могут и коричневыми и т.п. Все это — начальные тревожные признаки, при обнаружении которых женщина должна не задумываясь обратиться к врачу.
По большей части женщины приходят к нам именно после того, как обнаружат новообразование самостоятельно. Но эффективно оно не всегда, чаще всего находят проблему девушки с маленькой грудью, которые могут самостоятельно себя пропальпировать, обнаружить уплотнения и обратиться к врачу. Из общих советов — обращать внимание нужно на все: покраснение, изменение формы молочной железы, формы соска (втягивается ли он, когда вы поднимаете руки кверху). Также сюда можно отнести и выделения из сосков, которые могут быть прозрачными, а могут и коричневыми и т.п. Все это — начальные тревожные признаки, при обнаружении которых женщина должна не задумываясь обратиться к врачу.
— Есть ли установленные риски, факторы развития онкологии?
— Мы не можем назвать основную причину возникновения рака молочной железы, да и рака в принципе. Но факторов риска много. В 30% случаев женщина под эти риски не подпадает, однако это не значит, что она не заболеет – обследоваться нужно обязательно. Основной фактор — генетика, если у близких родственников по женской линии есть злокачественные образования молочной железы, яичников, кишечника. Все это является поводом к тому, чтобы обратить внимание на собственное здоровье. Менструальная функция – чем раньше начинаются месячные и чем позже заканчиваются, тем выше риск заболевания. Да те же эстрогены, которые поддерживают молодость женского организма, в конечном итоге могут привести к появлению злокачественной опухоли. К риску можно отнести отсутствие родов вообще, поздние первые роды, отказ от кормления грудью, неправильный образ жизни, наличие вредных привычек и даже неправильное питание, в котором превалирует употребление животных жиров. Но какой бы из рисков мы не назвали все они связаны тем, что опосредовано влияют на гормональный уровень женщины. Отдельный блок – радиация. Женщина в группе риска, если получала лучевое лечение в детском возрасте. Не забывайте и про такую вещь, как солярий, а также модную тенденцию загорать топлес: ткань покрывающая молочные железы гораздо нежнее, чем кожа на остальной части тела и потому УФ-лучи проникают гораздо глубже в тело и могут способствовать развитию рака в ней.
Основной фактор — генетика, если у близких родственников по женской линии есть злокачественные образования молочной железы, яичников, кишечника. Все это является поводом к тому, чтобы обратить внимание на собственное здоровье. Менструальная функция – чем раньше начинаются месячные и чем позже заканчиваются, тем выше риск заболевания. Да те же эстрогены, которые поддерживают молодость женского организма, в конечном итоге могут привести к появлению злокачественной опухоли. К риску можно отнести отсутствие родов вообще, поздние первые роды, отказ от кормления грудью, неправильный образ жизни, наличие вредных привычек и даже неправильное питание, в котором превалирует употребление животных жиров. Но какой бы из рисков мы не назвали все они связаны тем, что опосредовано влияют на гормональный уровень женщины. Отдельный блок – радиация. Женщина в группе риска, если получала лучевое лечение в детском возрасте. Не забывайте и про такую вещь, как солярий, а также модную тенденцию загорать топлес: ткань покрывающая молочные железы гораздо нежнее, чем кожа на остальной части тела и потому УФ-лучи проникают гораздо глубже в тело и могут способствовать развитию рака в ней.
— Излечим ли рак груди? Какие для этого применяются методы и как это сложно?
— Выживаемость при раке молочной железы в последнее десятилетие увеличилась благодаря ряду федеральных программ по диагностике данного заболевания. Сейчас вообще идет тенденция на улучшение диагностики и выявление рака на максимально ранних стадиях. В настоящее время основным методом лечения является хирургический — на ранних стадиях онкологии операция очень щадящая, но чем более запущен случай, тем тяжелее последствия в том числе и косметические. Именно поэтому лечение тесно переплетается и с пластической хирургией, позволяющей свести визуальные последствия удаления опухоли к минимуму. Конечно же в ход идут лучевая, гормональная и химотерапия. Кроме того, сегодня существует множество таргетных препаратов, которые воздействуют не на весь организм, а на конкретные клетки, влияющие на развитие опухоли, рассматривается вопрос о создании в Хабаровске протонного центра. Данный метод лечения отличается большей эффективностью, меньшим воздействием на организм пациента.
Но главное всегда держать в уме одну вещь — все методы лечения хороши на начальной стадии развития онкологии.
— И помните, что рак молочной железы не излечим окончательно. Мы можем увести его в ремиссию, которая будет длиться годами и больные могут умереть от совершенно другого заболевания, но сам диагноз останется с человеком на всю жизнь и в ряде моментов необходимо будет себя ограничивать, чтобы онкология не вернулась.
Подробнее:
https://amurmedia.ru/news/725271/?from=31
Лечение рака груди (молочной железы). Стадии рака груди, как вылечить
27 апреля 2018Лечение рака груди на разных стадиях
Лечение рака молочной железы проводится опытными маммологами-онкологами. Программа подбирается для каждой пациентки отдельно в зависимости от особенностей развития опухоли. При малейших подозрениях на рак груди обратитесь к нашему врачу и пройдите обследование. При раннем обнаружении присутствуют более высокие шансы на выздоровление.
Стадии рака молочной железы
Ответ на вопрос о том, можно ли полностью вылечить рак молочной железы, зависит от того, на какой стадии он был обнаружен. Медики выделяют следующие стадии:
- 0 стадия. Характеризуется тем, что опухоль неинвазивная, то есть не распространяется на здоровые клетки. Диагностируется крайне редко и случайно, поскольку патология еще не имеет явных симптомов. Излечивают от рака на этом этапе полностью.
- 1 стадия. Опухоль не превышает 2 см, но раковые клетки распространяются на ткани молочной железы. На начальной степени инвазивный рак имеет особенность – отсутствие злокачественных клеток в лимфоузлах.
- 2 стадия. Размер новообразования колеблется в пределах от 2 до 5 см. В большинстве случаев есть патологические изменения в лимфатических узлах подмышечных впадин.
- 3 стадия. Размеры опухоли превышают 5 см. Злокачественные клетки имеют большое распространение на кожу, внутригрудные лимфатические узлы, мышцы.
- 4 стадия.
 Опухоль может быть любых размеров. Характерная особенность – метастазы в печени, легких, головном мозге и других органах. Излечиться от патологии полностью практически невозможно, а медицинская помощь направлена на обеспечение качества жизни.
Опухоль может быть любых размеров. Характерная особенность – метастазы в печени, легких, головном мозге и других органах. Излечиться от патологии полностью практически невозможно, а медицинская помощь направлена на обеспечение качества жизни.
В нашем маммологическом центре получить профессиональную помощь можно при любой стадии рака. Помните, что на начальных этапах патология легче поддается лечению и есть возможность полного выздоровления. Чтобы не упустить начало развития опухоли, регулярно проводите самодиагностику и посещайте врача для профилактических осмотров, даже если отсутствуют симптомы заболевания.
Чего боится рак молочной железы: основные методы
Сегодня применяются разные методы борьбы со злокачественными опухолями грудей. Как правило методики комбинируют для большей эффективности. Программа лечения для каждой пациентки в нашем медицинском центре составляется персонально после проведения комплексного обследования согласно международным стандартам. Ниже перечислены методы борьбы с раком.
Хирургическое вмешательство
Радикальный подход дает высокие шансы на излечение, особенно на ранних стадиях. Если карцинома молочной железы имеет размеры не более 2-2,5 см, первым этапом проводится органосохраняющая операция. Во время оперативного вмешательства удаляется опухоль и близлежащие ткани. Всегда проводится удаление лимфатических узлов в подмышечных впадинах для предупреждения рецидива, количество удаленных л/у зависит от стадии болезни и опыта хирурга. При опухоли занимающей больше 1/3 груди проводится мастэктомия, но женщинам не стоит бояться операции. Современная медицина решает эстетическую проблему путем пластической хирургии. Восстановительное хирургическое вмешательство проводится одномоментно с удалением опухоли или отстрочено (на 1 год )
Лучевая терапия
Радиотерапия или лучевая терапия проводится после операции для уничтожения оставшихся раковых клеток. Облучение при помощи современных линейных ускорителей снижает вероятность рецидива рака груди.
Химиотерапия
Лекарственное лечение заключается в применении специальных препаратов, которые воздействуют на раковые клетки. Они разрушают их, и тем самым подавляют рост.
Лечение рака молочной железы без операции проводится крайне редко. Если у пациентки имеются противопоказания для хирургического вмешательства, ключевой момент отводится химиотерапии.
Таргетная терапия
Главная особенность этого метода заключается в том, что применяются препараты, которые оказывают прицельное воздействие на злокачественные клетки, но при этом не затрагивают здоровые ткани. Таргетная терапия относится к специальным способам лечения,дающим найлучший результат.
Гормональная терапия
Лечение такими гормональными препаратами используется не всегда. Если диагностирован гормонозависимый рак груди, без применения препаратов, блокирующих гормоны — не обойтись. В остальных случаях, при отсутствии в опухоли, эстрогенных и прогестероновых рецепторов, они никак не будут влиять на развитие опухоли.
Важно! Категорически запрещено самостоятельно принимать гормональные препараты даже по совету пользователей в интернете. эСамолечение способно спровоцировать рост злокачественного новообразования и вызвать серьезные осложнения.
Помимо перечисленных методов, которые часто комбинируют, дополнительно применяется симптоматическая терапия и иммунотерапия. Повышение собственных защитных сил организма позволяет ему бороться с раковыми клетками и приостановить их распространение.
Методы лечения рака груди на различных стадиях
Несмотря на то, что лечение составляется индивидуально, основные принципы применимы для всех пациенток. Методы подбираются в зависимости от стадии, симптомов, сопутствующих болезней, распространения метастазов и прочих факторов:
- При опухоли нулевой стадии проводится щадящая операция, при которой удается сохранить грудь. Дополнительно может назначаться курс химиотерапии или гормонотерапия. Некоторые пациентки используют компрессы и другие народные средства, но рак нетрадиционная медицина не способна вылечить. Промедление может стоить жизни.
- Если обнаружена первая стадия опухоли, нужно начинать только с хирургического метода. Так как злокачественное новообразование имеет небольшие размеры, в большинстве случаев удается сохранить грудь. Иногда молочная железа удаляется полностью. Для предупреждения рецидива могут применяться гормональная и лучевая терапия, лечение химиопрепаратами.
- Лечение рака молочной железы на второй стадии базируется на квадрантоктемии или мастэктомии. Методика оперативного вмешательства подбирается в зависимости от размеров и расположения опухоли. Удаляются и подмышечные лимфатические узлы. Обязательно назначается облучение, лечение гормональными при необходимости и химическими препаратами.
- Так как третья стадия часто сопровождается метастазами, удаления опухоли недостаточно для борьбы с патологией. Чтобы уничтожить раковые клетки назначается химиотерапия. Лечение медикаментами проводится до и после операции, а также проводится лучевая и гормонотерапия.
- На четвертой стадии рак полностью не излечивается из-за распространенных метастазов. Лечение направлено на предупреждение развития осложнений. Решение о проведении любого лечения принимается индивидуально. Иногда назначаются гормональные средства. Поскольку четвертая стадия рака груди сопровождается сильными болями и другими неприятными признаками, подбирается симптоматическое лечение.
Помните, что ранняя диагностика дает шанс на выздоровление. Пройдите обследование в нашем центре, чтобы убедиться в отсутствии патологии. Записаться к маммологу можно на удобное для вас время.
Прогнозы
Часто пациентки спрашивают, сколько живут с раком груди. Ответить на этот вопрос однозначно сложно. Прогноз напрямую зависит от стадии развития опухоли. При нулевой и первой стадии есть высокие шансы на полное излечение- 95%. При второй стадии пятилетняя выживаемость достигает 80%, а при третьей – 50% при условии прохождения комплексного лечения и соблюдения всех рекомендаций врача.
Четвертая стадия имеет менее утешительные прогнозы – около 15%, а при расчете десятилетней выживаемости показатели становятся еще ниже. Связано это с тем, что метастазы поражают жизненно важные органы. Кроме этого, запущенный рак груди у женщин доставляет серьезные страдания, что отражается на качестве жизни.
Не откладывайте лечение рака молочной железы. Патология будет прогрессировать. Если нужна медицинская помощь, обратитесь в наш маммологический центр. Квалифицированные врачи подберут оптимальное решение после проведения комплексной диагностики.
Запись возможна по телефону или через онлайн-форму на нашем сайте.
Рак груди: причины возникновения, группы риска и профилактика
Почему молочная железа больше других органов подвержена злокачественным процессам, ведь неблагоприятная экология, стрессы воздействуют на весь организм? Дело в том, что молочная железа — самый гормонозависимый орган в организме женщины. А на гормональный статус влияет абсолютно все: магнитные бури, солнечная радиация, образ жизни, душевный покой.
Родив единственного ребенка, большинство женщин спешат выйти на работу, в то время как природой им предназначено рожать и вскармливать грудью нескольких детей. Эндокринная система не зависит от карьерных планов, она работает в ритме, заложенном природой. Раньше женщина на протяжении всего репродуктивного возраста вынашивала детей, кормила их грудью. Причем, чтобы не забеременеть вновь, кормила долго, прикладывая к груди ребенка до 2-3 лет, молочная железа постоянно работала. Грудное вскармливание младенца хотя бы до полугода, а лучше — до 9-10 месяцев — просто необходимо.
Современные девушки занимаются спортом, в том числе и экстремальным. На первый взгляд незначительная травма может дать знать о себе спустя десятки лет, поэтому грудь необходимо оберегать от ударов и повреждений.
Врачи советуют женщинам ограждать себя от хронических стрессовых ситуаций. Вызванный душевными переживаниями цейтнот снижает иммунитет, а это значит, что организм может и не справиться с раковыми клетками, которые образуются в организме ежесекундно тысячами.
Одно из модных веяний последних лет — отдых на пляже топлесс — также вызывает опасения врачей. Они рекомендуют женщинам сократить пребывание на солнце: если в организме есть крохотное новообразование, ультрафиолет, проникая в железистую ткань, может стимулировать его рост. Поэтому лучше загорать в тени и обязательно в купальнике.
Чем старше — тем внимательнее к себе
Но стоит помнить, что даже при соблюдении всех этих правил женщинам старше 35 лет с целью профилактики все-таки рекомендуется выполнять УЗИ и/или маммографию не реже одного раза в год, женщинам от 50 до 70 лет следует проходить обследование раз в два года.
Вероятность возникновения рака молочной железы увеличивается пропорционально возрасту: в 20-25 лет такой диагноз — редчайший случай, заболевших до 30 лет — единицы, а после 35 лет риск возрастает каждые 5 лет почти вдвое.
В группе повышенного риска — женщины, у которых менструация началась раньше девяти лет и те, у которых менопауза наступила после 55 лет. Из-за высокого уровня половых гормонов эти женщины активны, прекрасно выглядят, но именно они должны особенно внимательно следить за состоянием груди.
Самый верный способ профилактики – ежемесячное самообследование. Никто не знает вашу грудь лучше, чем вы сами. Если врач осматривает женщину в первый раз, даже он может не увидеть того, что способна обнаружить сама женщина.
Для осмотра нужно выбрать время в течение недели после окончания менструации, в это время грудь мягче. Лучше всего — во время купания. Намыльте руки, встаньте прямо и, подняв правую руку вверх, левой ладонью прощупайте правую грудь от подмышки до солнечного сплетения. Затем то же самое проделайте с левой грудью. Не забудьте обследовать также подмышечные впадины, области над ними и над ключицами. Если вы обнаружите уплотнения, узелки, болезненность или выделения из соска, срочно обратитесь к врачу. При самообследовании также должны насторожить изменения формы груди, отеки, при которых кожа напоминает пористую лимонную корку, изменение формы соска, увеличение лимфатических узлов в подмышечной впадине.
Наследственный фактор
Учеными установлено, что среди заболеваний раком молочной железы 20-25% носят наследственный характер, причем в 5-10% случаев заболевание вызывает один ген, а в 15-20% случаев – совокупность различных генов и влияние окружающей среды.
В группу риска в первую очередь попадают женщины, в семье которых три или более близких родственников перенесли один и тот же вид рака молочной железы. Именно из-за наследственного характера заболевания специалисты выступают за отказ от брака при так называемой обоюдной онкологической отягощенности, чтобы не было развития наследственного рака груди.
Очень важно и питание. Согласно многочисленным исследованиям, риск заболеть снижается, если человек поддерживает здоровый вес, ест много свежих овощей и фруктов, богатых клетчаткой, не злоупотребляет алкоголем.
Ученые установили, также вероятность заболевания снижается при умеренной физической активности. Плавание, пеший туризм, бег трусцой – эффективные средства профилактики рака груди.
Стоит заметить, что рак молочной железы встречается и у мужчин, но гораздо реже (1% всех случаев заболевания). Причины те же: мутация в генах предрасположенности, ожирение, гормональные нарушения.
Материал подготовлен интернет-редакцией www.rian.ru на основе информации открытых источников
Найден способ лечения самого агрессивного вида рака груди
Британские онкологи нашли способ лечения самого агрессивного вида рака груди. Совместное использование химиотерапии и иммунотерапии снижает риск рецидива опухоли и повышает выживаемость. Хотя результаты пока предварительные, исследователи надеются, что такое лечение станет новым стандартом.
Совместное применение химиотерапии и иммунотерапии может значительно повысить шансы женщин на излечение от одного из самых опасных и агрессивных видов рака груди — трижды негативного рака. Своими выводами специалисты из Лондонского университета королевы Марии поделились на конгрессе Европейского общества медицинской онкологии в Барселоне.
Зачастую рак молочной железы можно подавить гормональной терапией. Опухолевые клетки обычно несут на себе рецепторы к гормонам прогестерону и эстрогену – оба гормона побуждают клетки делиться, что способствует развитию опухоли. Используя препараты, блокирующие действие гормонов, можно подавить рост опухоли.
Также можно задействовать рецептор HER2, взаимодействующий с эпидермальным фактором роста. Все факторы роста запускают деление клеток, в том числе и опухолевых. Для HER2 разработаны специальные препараты, останавливающие деление.
Однако в 12-20% случаев встречается тройной отрицательный рак молочной железы — у таких опухолей нет рецепторов ни к эстрогену, ни к прогестерону, ни к эпидермальному фактору роста.
Прогноз у трижды негативного рака куда хуже, а для лечения приходится применять менее точечные методики, чреватые осложнениями.
Чаще всего для лечения трижды негативного рака используется химиотерапия с последующим хирургическим вмешательством. Однако если все опухолевые ткани удалить не выходит, в 40-50% случаев опухоль снова возвращается в течение следующих трех лет.
С марта 2017 по сентябрь 2018 года в 124 городах 21 страны 1174 женщины с тройным отрицательным раком груди прошли через химиотерапию и операцию по удалению опухоли. 784 из них получали иммунотерапевтический препарат пембролизумаб до и после операции, а остальные — плацебо. Пембролизумаб рекомендован к применению также при меланоме и немелкоклеточном раке легкого.
Рецидивов не было у 64,8% женщин, получавших иммунотерапию. У тех, кто получал плацебо, частота рецидивов была на 13,6% выше.
Побочные эффекты во время лечения были связаны в основном с химиотерапией. Осложнения, которые можно было бы приписать иммунотерапии, встречались у 42% участниц из группы, получавшей пембролизумаб, и у 21% получавших плацебо. Серьезных проблем, угрожавших бы здоровью, исследователи не зарегистрировали.
Также исследователи отмечают возросшую выживаемость среди получавших иммунотерапию, но небольшая продолжительность исследования не позволяет делать выводы о дальнейших перспективах.
«Трижды негативный рак молочной железы — особенно агрессивная форма рака, отравляющая жизнь, — говорит ведущий автор исследования профессор Питер Шмид. — Мы искали лучшие варианты лечения. Эти ранние результаты свидетельствуют о том, что добавление иммунотерапии к химиотерапии приводит к значительному снижению рецидивов этой формы рака молочной железы».
Несмотря на то, что результаты пока предварительные, исследователи возлагают на них большие надежды.
«Если мы не допустим рецидива рака, мы вылечим больше пациентов, но нам нужны более долгосрочные данные, чтобы подтвердить это», — говорит Шмид.
Это лишь первый этап исследования. Ученые рассчитывают, что дальнейшая работа даст им больше оснований рекомендовать иммунотерапию как эффективный метод борьбы с трижды отрицательным раком. Если результаты подтвердятся, совмещение иммунотерапии с химиотерапией может стать новым стандартом лечения.
Ранее американские ученые предложили новый способ лечения рака груди. Они предложили использовать специально разработанный прибор, замораживающий раковые клетки с помощью углекислого газа. Эксперты рассказали, что уже успешно протестировали свою усовершенствованную технологию на животных.
Кроме того, новый способ лечения может стать спасением для большего количества людей, поскольку он не требует ни хирургического вмешательства, ни специальных палат, ни анестезий, ни лекарств. Изобретение американских специалистов способно убивать до 80% раковых клеток.
Комплексное гистологическое и иммуногистохимическое исследование с определением рецепторного статуса рака молочной железы (PR, ER, ki67, Her2 neu)
Данное исследование позволяет обнаружить отклонения от нормального строения тканей, выявить наличие злокачественных клеток или их предшественников, определить гистологический вариант изменений, рецепторный статус опухоли и её пролиферативный потенциал. Полученные данные позволяют максимально эффективно подобрать лечение и позволяют дать прогноз заболевания.
Состав исследования:
- Гистологическое исследование с определением рецепторного статуса рака молочной железы (PR, ER, ki67, Her2 neu)
- Иммуногистохимическая диагностика рецепторного статуса рака молочной железы (PR, ER, ki67, Her2 neu)
Синонимы русские
Определение рецепторного статуса рака молочной железы.
Метод исследования
Гистологический метод.
Какой биоматериал можно использовать для исследования?
Образец ткани (биоптат) опухолевого образования молочной железы.
Общая информация об исследовании
Гистологическое исследование любого органа позволяет оценить морфологию ткани, выявить характер роста опухоли, степень инвазии (прорастания), определить стадию, прогноз и тактику лечения заболевания. Но для эффективного лечения рака молочной железы (РМЖ) также важны результаты иммуногистохимического исследования, которое позволяет оценить рецепторный статус и пролиферативный потенциал опухолевых клеток. Особенно это актуально при карциноме молочной железы.
На поверхности клеток опухоли существуют специальные белки – рецепторы, стимуляция которых запускает рост новообразования. Различные комбинации этих рецепторов называются рецепторным статусом опухоли. Так, при раке молочной железы могут встречаться следующие рецепторы:
- Рецепторы к гормонам – эстрогенам и прогестерону (ER, PR).
Значительная часть опухолей молочной железы является гормонально-зависимыми, то есть их рост поддерживается и стимулируется эстрогенами и прогестероном. Как правило, они хорошо отвечают на терапию аналогами гормонов (тамоксифен), которые конкурентно связываются с соответствующими ядерными рецепторами, не вызывая активации внутриклеточных процессов. Таким образом, исследование продукции опухолью ER и PR позволяет определить ее чувствительность к этим препаратам. Но наличие данных рецепторов слабо влияет на прогноз заболевания. - Рецептор второго типа к человеческому эпидермальному фактору роста (human epidermal growth factor receptor 2 – HER2/neu).
Для клеток некоторых опухолей молочной железы может быть характерна повышенная выработка HER2/neu, который, соединяясь с естественным фактором роста, запускает в них процесс неконтролируемого деления. Наличие на клеточной мембране данного рецептора связано с плохим прогнозом (агрессивное течение, высокий риск рецидива) и позволяет предположить хороший терапевтический эффект от назначения антрациклиновой и таксановой химиотерапии и моноклональных антител к рецептору HER2 – трастузумаб (герцептин), лапатиниб (Tykerb), пертузумаб (Perjeta). При этом не рекомендуется гормональная терапия, так как такие опухоли резистентны к тамоксифену.
По данным исследований, общее число пациенток с HER2-положительным раком молочной железы составляет от 15 до 25% и некоторые раковые заболевания молочной железы, которые являются HER2-положительными, со временем могут стать HER2-негативными. Аналогично HER2-отрицательный рак молочной железы может стать HER2-положительным с течением времени. В случае рецидива заболевания рекомендуется повторное определение статуса HER2.
Кроме определения рецепторного статуса, важно знать пролиферативную активность – способность опухолевых клеток к неограниченному делению. Процесс деления сопровождается появлением в клетке определенных белков, один из которых – Ki-67. Это ядерный белок, который кодируется геном MK167 и экспрессируется только в пролиферирующих клетках, не выделяясь, если клетка в состоянии покоя. Это позволило использовать его как маркер пролиферативной активности опухоли. Определение уровня Ki-67 имеет важное прогностическое значение, так как наибольшей пролиферативной активностью обладают опухоли из наименее зрелых и дифференцированных клеток.
Существующие принципы Американского общества клинической онкологии не включают Ki-67 в список необходимых рутинных биологических маркеров. Однако появление новых генетических тестов подчеркивает роль пролиферативных генов, включая Ki-67, в качестве прогностических маркеров. Наиболее часто используемым методом определения Ki-67 является окрашивание антителом MIB-1. Но стандартизация патологической оценки Ki-67 еще не завершена.
На основании статуса гормональных рецепторов, HER2/neu, Ki-67 выделяют четыре иммунофенотипа рака молочной железы:
– Люминальный тип A или ER+, PR+, HER2-.
При этом типе рака обнаруживаются гормональные рецепторы (ER и PR), но нет HER2/neu и/или низкий индекс Ki-67. Около 80% рака молочной железы составляют ER+, и около 65% из них также являются PR+. Около 15% таких опухолей имеют мутации гена р53, которые имеют плохой прогноз.
– Люминальный тип B или тройной положительный (ER+, PR+, HER2+ или с высоким индексом Ki-67).
Чаще всего такой тип встречается при внутрипротоковых опухолях молочной железы.
– HER2-положительный (ER-, PR-, HER2+).
К данному типу относится около 20% раковых образований молочной железы. Как правило, они очень агрессивны, быстро растут и чаще встречаются у женщин в более раннем возрасте, чем типы A и B.
– Базальноподобный или тройной отрицательный фенотип (трижды негативный) (ER-, PR-, HER2-).
К данному типу относится примерно 10-20% случаев рака молочной железы. Он называется базальноподобными, так как опухолевые клетки имеют признаки, сходные с базальными клетками, окружающими протоки молочных желез. Большинство случаев рака молочной железы, связанных с геном BRCA-1, являются трижды негативными, и более половины их них содержат мутации гена p53. Такой рак не реагирует на гормональную терапию или методы лечения, которые направлены на рецепторы HER2. В таких случаях используют комбинацию методов лечения (оперативное вмешательство, лучевая терапия и химиотерапия). Базальноподобные раковые опухоли, как правило, более агрессивны, с более низкой, пятилетней выживаемостью, с более высокой частотой рецидивов. Чаще такой тип РМЖ встречается до 40-50 лет и особенно характерен для женщин со смуглой и темной кожей.
При комплексном гистологическом и иммуногистохимическом исследовании в первую очередь осуществляется морфологический анализ тканей под световым микроскопом с использованием специальных гистологических красителей. После верификации патологического процесса, определения степени инвазии и наличия фоновых процессов проводится иммуногистохимическое исследование. Оно позволяет определить все указанные выше маркеры. Срезы тканей окрашиваются растворами антител, специфичными к одному из исследуемых маркеров и меченными флюоресцирующими метками. Если в опухолевой клетке присутствует искомый рецептор, антитела связываются с ним и с помощью микроскопа можно увидеть флюоресценцию (свечение). Это будет свидетельствовать о положительном результате теста. Также врач-морфолог сможет определить, где именно располагается окрашенный маркер.
Для чего используется исследование?
- Для дифференциальной диагностики патологического процесса;
- для определения вида и подвида опухоли, степени ее злокачественности и распространенности онкологического процесса;
- для определения рецепторного статуса опухоли и ее пролиферативного потенциала;
- для подбора адекватной терапии, в том числе с учетом полученных результатов иммуногистохимического анализа;
- для контроля эффективности лечения;
- для верификации метастазов;
- для динамического контроля и прогноза у лиц, находящихся под наблюдением.
Когда назначается исследование?
- При первичной верификации образования молочной железы, особенно если велика вероятность, что оно злокачественное;
- при рецидивах рака молочной железы;
- при верификации метастатических опухолей.
Что означают результаты?
При гистологическом исследовании даётся подробное макро- и микроскопическое описание исследуемого образца тканей, заключение с указанием гистологической формы рака, степени его злокачественности или дифференцировки, наличия или отсутствия инфильтрации в самом узле и по периферии, степени распространенности, наличия фоновых процессов.
В заключении иммуногистохимического анализа указывается гистологический вариант опухоли и один из четырех возможных иммунофенотипов.
При интерпретации результатов рецепторного статуса к стероидным гормонам (эстрогену и прогестерону) следует оценивать не только процент окрашенных антителами клеток, но и интенсивность окрашивания. Эти параметры учитываются в шкале Allred, где процент позитивных клеток оценивается от 0 до 5 баллов, а интенсивность окрашивания от 0 до 3. Сумма двух показателей является итоговым баллом, по которому определяется позитивность опухоли по рецепторному статусу: 0-2 негативная, 3-8 позитивная. Общий балл 3 по этой шкале соответствует 1-10% окрашенных клеток и является минимальным позитивным результатом, когда назначение гормональной терапии может быть эффективным.
Иногда рецепторный статус определяется исключительно по проценту клеток с окрашенными ядрами. В таких случаях NCCN рекомендует считать позитивными все опухоли, где есть более 1% флюоресцирующих клеток. Учитывая, что окрашивание ER/PR может быть и в нормальных эпителиальных клетках молочной железы, следует оценивать только инвазивные опухолевые клетки.
Любой положительный результат теста, будь то только ER, PR или оба, означает, что рак молочной железы считается «гормон-рецептор-положительным» и оправдано назначение гормональной терапии.
При интерпретации окраски на рецептор HER2/neu учитывают только окрашивание клеточной оболочки, которое оценивают по шкале от 0 до +3:
- результат 0 и +1 считается HER2-негативным;
- +2 – пограничный результат, нельзя достоверно судить о наличии на поверхности клеток рецептора HER2-neu, необходимо проведение FISH- или CISH-исследования; при недоступности этих исследований допускается повторное иммуногистохимическое исследование, но на другом образце опухолевой ткани;
- +3 – положительный результат – таргетная терапия анти-HER2-препаратами будет эффективна.
Оценка маркера индекса пролиферации определяется как процент клеток с ядерным окрашиванием от общего числа опухолевых клеток. Согласно классификации St. Gallen Consensus (2009), низким индексом пролиферативной активности считается уровень Ki-67 менее 15%, средним – 16-30%, а высоким – более 30%.
Существует несколько шкал оценки рецепторного статуса рака молочной железы, в лабораторном отчете должно быть указано, какая из них использовалась, а также дана описательная характеристика количества позитивных клеток, особенностей окрашивания клеточных структур и морфологических особенностей клеток.
Статус эстрогеновых рецепторов и прогноз рака молочной железы
Введение: Статус рецептора эстрогена помогает в лечении рака груди.
- Рецепторы эстрогена (ER-позитивные) опухоли экспрессируют рецепторы эстрогенов. Это означает, что у них много рецепторов эстрогена.
- Эстроген-отрицательные (ER-отрицательные) опухоли не экспрессируют эстрогеновые рецепторы. Это означает, что у них мало или совсем нет рецепторов эстрогена.
ER-положительный рак молочной железы можно лечить с помощью гормональной терапии, такой как тамоксифен, ингибиторы ароматазы и подавление функции яичников.
Прогноз (шанс на выживание)
Люди с ER-положительным ранним раком груди, как правило, имеют лучшую выживаемость, чем люди с ER-отрицательным ранним раком груди [1].
Как показывают исследования, приведенные ниже, 5-летняя выживаемость после постановки диагноза примерно на 10 процентов лучше для женщин с ER-положительным раком груди на ранней стадии, чем для женщин с ER-отрицательным раком груди на ранней стадии.
Примерно через 5 лет эта разница в выживаемости начинает уменьшаться и со временем уходит [1].
Узнайте о сильных и слабых сторонах различных типов исследований.
Критерии отбора исследования: Проспективные когортные исследования с участием не менее 1500 участников и продолжительностью наблюдения не менее 5 лет.
Проспективные когортные исследования | |||||
SEER [4] | 111 993 | I, II или III этап * | 8 | Женщины моложе 40 лет: Женщины 40-49 лет: Женщины 50-59 лет: Женщины 60-69: Женщины 70-74: | Женщины моложе 40 лет: Женщины 40-49 лет: Женщины 50-59 лет: Женщины 60-79: Женщины 70-74: |
Датская кооперативная группа по раку груди [2] | 26 944 | Степень I, II или III | 5 | 85% ‡ | 69% ‡ |
Truong et al.[5] | 8 038 | T1-2 Степень I, II или III | 4-6 | Выше | Нижняя |
Сопик и др. [6] | 1,910 | I, II или II этап * | 15 | 95% †, § | 80% †, § |
Jayasekara et al.[7] | 1,196 | I, II или III этап * | 15 | 89% ¶ | 78% ¶ |
Sig = статистически значимая разница в выживаемости
NS = Нет статистически значимой разницы в выживаемости
см = сантиметр
* Стадия рака молочной железы по классификации до 2018 г.
† Показатели указаны для выживаемости при раке груди (смерть от рака груди), а не для общей выживаемости (смерти от любой причины).
‡ Для 3591 женщины, для которых были доступны данные о 10-летней выживаемости, 10-летняя выживаемость составила 68% для женщин с ER-положительными опухолями и 57% для женщин с ER-отрицательными опухолями.
§ Ставки рассчитаны от цифры. Выживаемость рака груди через 15 лет составила 77% для женщин с ER-положительными опухолями и 70% для женщин с ER-отрицательными опухолями.
¶ Общая выживаемость через 10 лет составила 77% для женщин с ER-положительными опухолями и 68% для женщин с ER-отрицательными опухолями.
Список литературы
- Moffat FL.Глава 28: Клинические и патологические прогностические и прогностические факторы, Harris JR, Lippman ME, Morrow M, Osborne CK. Болезни груди, 5-е издание, Lippincott Williams & Wilkins, 2014.
- Carey LA, Perou CM, Livasy CA, et al. Раса, подтипы рака груди и выживаемость в исследовании рака груди в Каролине. ДЖАМА. 295 (21): 24922502, 2006.
- Yu KD, Wu J, Shen ZZ, Shao ZM. Риск смертности от рака молочной железы среди женщин с эстроген-рецептор-положительным раком молочной железы через пять лет после постановки диагноза: значение для расширенной эндокринной терапии.J Clin Endocrinol Metab. 97 (12): E2201-9, 2012.
- Truong PT, Bernstein V, Wai, E, et al. Возрастные различия в использовании подмышечной диссекции: анализ выживаемости 8038 женщин с раком груди T1-ST2. Int J Radiat Oncol Biol Phys. 54 (3): 794-803, 2002.
- Сопик В., Сун П., Народ С.А. Прогностический эффект статуса рецептора эстрогена отличается для молодых и пожилых пациентов с раком молочной железы. Лечение рака груди Res. 165 (2): 391-402, 2017.
- Jayasekara H, MacInnis RJ, Chamberlain JA, et al.Смертность после рака груди как функция времени с момента постановки диагноза по статусу рецепторов эстрогена и возрасту на момент постановки диагноза. Int J Cancer. 145 (12): 3207-3217, 2019.
Обновлено 21.08.
Тройной отрицательный рак груди: обзор, лечение и многое другое
Тройной отрицательный рак груди — это рак, при котором тесты на рецепторы эстрогена, рецепторы прогестерона и избыток белка HER2 отрицательны.
Эти результаты означают, что рост рака не поддерживается гормонами эстрогеном и прогестероном или белком HER2.Таким образом, тройной отрицательный рак молочной железы не реагирует на гормональные терапевтические препараты или лекарства, нацеленные на рецепторы белка HER2. Тем не менее, другие лекарства используются для успешного лечения тройного отрицательного рака груди.
Около 10-20% случаев рака молочной железы являются тройными отрицательными формами рака молочной железы. Врачи и исследователи проявляют большой интерес к поиску новых лекарств, которые могут лечить этот вид рака груди. Исследования пытаются выяснить, могут ли определенные лекарства влиять на процессы, вызывающие рост тройного отрицательного рака груди.
Что такое тройной отрицательный рак груди?
Клеточные рецепторы — это особые белки, находящиеся внутри и на поверхности клеток. Эти рецепторные белки являются «глазами» и «ушами» клеток, они получают сообщения от веществ в кровотоке и затем говорят клеткам, что им делать.
Рецепторы гормонов внутри и на поверхности здоровых клеток груди получают сообщения от гормонов эстрогена и прогестерона. Гормоны прикрепляются к рецепторам и дают инструкции, которые помогают клеткам продолжать расти и хорошо функционировать.Большинство, но не все, клетки рака груди также имеют эти рецепторы гормонов. Примерно два из трех случаев рака груди дают положительный результат на один или оба этих гормональных рецептора. (Более полное объяснение см. На странице статуса гормональных рецепторов.)
Меньший процент рака груди — около 20% — вырабатывает слишком много белка HER2. В нормальных здоровых клетках груди HER2 стимулирует рост клеток. Однако, когда в клетках рака груди содержится слишком много белка HER2, клетки растут и делятся слишком быстро.(Более полное объяснение см. На странице статуса HER2.)
Гормональная терапия и терапия, нацеленная на HER2, нарушают действие эстрогена, прогестерона и белка HER2 на рак груди, что может помочь замедлить или даже остановить рост клеток рака груди.
Около 10-20% случаев рака груди отрицательны как на рецепторы гормонов, так и на избыток HER2 в лаборатории, что означает тройной отрицательный результат. Поскольку гормоны не способствуют росту рака, рак вряд ли поддастся лечению гормональными терапевтическими препаратами, включая тамоксифен и ингибиторы ароматазы.Тройной отрицательный рак груди также вряд ли подействует на лекарства, нацеленные на белок HER2, такие как Enhertu (химическое название: fam-trastuzumab-deruxtecan-nxki), Herceptin (химическое название: trastuzumab), Kadcyla (химическое название: T-DMA. или адо-трастузумаб эмтанзин), Nerlynx (химическое название: нератиниб), Perjeta (химическое название: пертузумаб) или Tykerb (химическое название: лапатиниб).
Три общих признака тройного отрицательного рака груди
- Тройной отрицательный рак груди считается более агрессивным и имеет худший прогноз, чем другие виды рака груди , главным образом потому, что существует меньше целевых лекарств, которые лечат тройной отрицательный рак груди.Исследования показали, что тройной отрицательный рак груди с большей вероятностью распространится за пределы груди и с большей вероятностью вернется (вернется) после лечения.
- Это, как правило, более высокая степень злокачественности, чем другие типы рака груди. Чем выше оценка, тем меньше раковые клетки похожи на нормальные здоровые клетки груди по внешнему виду и характеру роста. По шкале от 1 до 3 тройной отрицательный рак груди часто имеет 3 степень.
- Это обычно клеточный тип, называемый «базальным». «Базальные» означает, что клетки напоминают базальные клетки, выстилающие протоки молочной железы. Базальный рак, как правило, является более агрессивным, более высоким уровнем рака — точно так же, как рак молочной железы с тройным отрицательным результатом. Большинство, но не все базальные виды рака молочной железы являются тройными отрицательными, и большинство, но не все тройные отрицательные виды рака молочной железы являются базальными.
Кто заболевает тройным отрицательным раком груди?
У любого человека может быть диагностирован рак груди с тройным отрицательным результатом. Тем не менее, исследователи обнаружили, что это чаще встречается в:
- Молодежь. Тройной отрицательный рак груди чаще диагностируется у людей моложе 50 лет. Другие типы рака груди чаще диагностируются у людей в возрасте 60 лет и старше.
- Черные и латиноамериканские женщины. Тройной отрицательный рак груди чаще диагностируется у чернокожих и латиноамериканских женщин. Азиатские женщины и белые женщины неиспаноязычного происхождения с меньшей вероятностью будут иметь диагноз этого типа рака.
- Люди с мутацией BRCA1 . Около 70% случаев рака груди, диагностированных у людей с наследственной мутацией BRCA , особенно BRCA1 , являются трижды отрицательными.
Если вам поставили диагноз «тройной отрицательный рак груди»
Может быть неприятно и страшно узнать, что вам поставили диагноз рака груди, который часто бывает более агрессивным, чем другие типы, и не подходит для лечения, направленного на рецепторы гормонов или белок HER2.
Тем не менее, важно помнить, что отсутствие рецепторов гормонов и избыток белка HER2 — это всего лишь два фактора, которые вы и ваш врач будете учитывать при выборе плана лечения. Стадия и степень рака также имеют решающее значение для вашего прогноза.
Также важно помнить, что существуют методы лечения тройного отрицательного рака груди.
Вернуться к началу
Пэт Приятел, которой в мае 2006 года был поставлен диагноз «тройной отрицательный рак груди» на ранней стадии, и автор книги « Surviving Triple Negative Cancer », обсуждает, что для нее значил этот диагноз; почему она начала свой блог «Положительные стороны отрицательного»; и совет, который она дала бы человеку с новым диагнозом.
Лечение тройного отрицательного рака груди
Тройной отрицательный рак груди обычно лечится с помощью комбинации хирургического вмешательства, лучевой терапии и химиотерапии.
Неоадъювантная химиотерапия
Исследования показали, что когда тройной отрицательный рак груди лечится химиотерапией перед операцией — то, что врачи называют неоадъювантной химиотерапией — и наблюдается полный патологический ответ, выживаемость без болезней и общая выживаемость лучше.
Один из способов, которым врачи могут судить об эффективности неоадъювантного лечения, — это посмотреть на ткань, удаленную во время операции, чтобы увидеть, присутствуют ли какие-либо активные раковые клетки. Если отсутствуют активные раковые клетки, врачи называют это «полным патологическим ответом» или pCR.
Выживаемость без болезней — это продолжительность жизни человека без рецидива рака. Общая выживаемость — это продолжительность жизни человека независимо от того, рецидивирует ли рак.
Ингибиторы PARP
Ингибиторы PARP, такие как Lynparza (химическое название: олапариб) и Talzenna (химическое название: талазопариб), были одобрены для лечения HER2-негативного рака груди на поздней стадии у людей с мутацией BRCA1 или BRCA2 .
Фермент поли-АДФ-рибозо-полимераза (PARP) фиксирует повреждение ДНК как в здоровых, так и в раковых клетках. Исследования показали, что лекарства, которые мешают или ингибируют фермент PARP, еще больше затрудняют исправление повреждений ДНК раковым клеткам с мутацией BRCA1 или BRCA2 . Это затрудняет выживание раковых клеток. Другими словами, ингибитор PARP снижает вероятность выживания некоторых раковых клеток после повреждения ДНК.
Иммунотерапия
Лекарства для иммунотерапии используют силу иммунной системы вашего тела для атаки раковых клеток.
Иммунотерапевтический препарат Кейтруда (химическое название: пембролизумаб) используется для лечения тройного отрицательного рака груди.
Кейтруда используется в сочетании с химиотерапией для лечения неоперабельного местнораспространенного или метастатического тройно-отрицательного, PD-L1-положительного рака молочной железы.
Неоперабельный означает, что рак нельзя удалить хирургическим путем.
Кейтруда также используется в сочетании с химиотерапией перед операцией, а затем самостоятельно после операции для лечения ранней стадии тройного отрицательного рака молочной железы с высоким риском рецидива (возврат рака).
Посетите раздел «Лечение и побочные эффекты», чтобы получить дополнительную информацию об операции, лучевой терапии, химиотерапии, таргетных методах лечения, таких как ингибиторы PARP, и иммунотерапии.
Клинические испытания с использованием этих и других методов лечения могут сыграть ключевую роль в улучшении лечения тройного отрицательного рака груди. Поговорите со своим врачом, если считаете, что можете быть заинтересованы в участии в клиническом исследовании.
Вернуться к началу
Эта статья была полезной? Да / Нет Эта статья была полезной?
Вы знали о раке груди.org некоммерческая организация? Пожертвования частных лиц позволяют нам публиковать самую надежную, полную и актуальную информацию о раке груди. Сделайте пожертвование онлайн сегодня или отправьте сообщение HELPBCO на номер 243725 , чтобы сделать пожертвование через мобильное устройство. Могут применяться тарифы на передачу сообщений и данных.
Последнее изменение 28 августа 2021 г. в 8:59
Статус гормональных рецепторов, характеристики опухоли и прогноз: проспективная когорта пациентов с раком груди
Фон: Пациенты с раком груди с опухолями, которые являются рецепторами эстрогена (ER) и / или рецепторами прогестерона (PR), имеют более низкий риск смерти после постановки диагноза по сравнению с женщинами с ER- и / или PR-отрицательными заболеваниями.Однако в нескольких исследованиях оценивались различия в рисках смертности от рака молочной железы в зависимости от статуса ER / PR по демографическим или клиническим характеристикам.
Методы: Используя данные из 11 популяционных онкологических регистров, которые участвуют в программе SEER (Наблюдение, эпидемиология и конечные результаты), в исследование были включены 155 175 женщин в возрасте не менее 30 лет с первичным диагнозом инвазивной карциномы молочной железы с 1990 по 2001 годы.Связь между статусом рецепторов гормонов суставов и риском смертности от рака молочной железы в категориях возраста постановки диагноза, года постановки диагноза, расы / этнической принадлежности, гистологического типа опухоли, стадии, степени, размера и статуса подмышечных лимфатических узлов оценивалась с использованием модели пропорциональных рисков Кокса.
Полученные результаты: По сравнению со случаями ER + / PR +, повышение риска смертности наблюдалось во всех подкатегориях возраста на момент постановки диагноза, начиная с 1.Различия в 2–1,5 раза для случаев ER + / PR-, различия в 1,5–2,1 раза для случаев ER- / PR + и в 2,1–2,6 раза для случаев ER- / PR-. Более значительные различия наблюдались в анализах, стратифицированных по классам; среди женщин с поражениями низкой степени злокачественности, пациенты ER- / PR- имели от 2,6 раза (95% доверительный интервал [ДИ] 1,7–3,9) до 3,1 раза (95% ДИ 2,8–3,4) повышенный риск смерти по сравнению с ER + / PR +, но среди женщин с поражениями высокой степени у них был от 2,1 раза (95% ДИ от 1,9 до 2,2) до 2,3 раза (95% ДИ 1.8-2,8) повышенный риск.
Заключение: По сравнению с женщинами с опухолями ER + / PR +, женщины с опухолями ER + / PR-, ER- / PR + или ER- / PR- испытали более высокий риск смерти, который в значительной степени не зависел от различных демографических и клинических характеристик опухоли, оцененных в этом исследовании. . Более высокие относительные риски смертности, выявленные среди ER- / PR-пациентов с небольшими или низкосортными опухолями, поднимают вопрос о том, может ли адъювантная химиотерапия играть положительную роль в этой популяции.
настоящих и будущих клинических решений
Ther Adv Med Oncol. 2012 May; 4 (3): 127–137.
Профессор и консультант-онколог отделения онкологии Медицинского института Бергенского университета; Отделение онкологии, университетская больница Хаукеланд, N-5021, Берген, Норвегия
Автор, отвечающий за переписку. Эта статья цитируется в других статьях в PMC.Abstract
Использование химиотерапии для пациентов с раком молочной железы, положительным по рецепторам эстрогена (ER), было противоречивым вопросом.Недавние исследования определили прогностические маркеры, позволяющие идентифицировать ER-положительный рак молочной железы с плохим прогнозом, нуждающийся в более агрессивной терапии. В целом, опухоли, принадлежащие к так называемому люминальному классу B, опухоли, экспрессирующие высокий уровень Ki67, гиперэкспрессию рецептора 2 эпидермального фактора роста человека (HER-2) или высокий балл по профилю экспрессии гена Oncotype DX, показывают плохой прогноз по сравнению с ER. -богатые опухоли просвета А класса. Напротив, недавние исследования показали, что эти опухоли, контрастирующие с опухолями люминального класса А, получают пользу от более агрессивной химиотерапии, содержащей антрациклин, включая таксан.В случае метастатического заболевания пациентам с HER-2-положительными, ER-положительными опухолями может быть полезна комбинированная эндокринная терапия и анти-HER-2 агент.
Ключевые слова: рак молочной железы, химиотерапия, эндокринная терапия, рецептор эстрогена, рецептор 2 эпидермального фактора роста человека, прогноз
Введение
Термин «неблагоприятное для прогноза рецептор эстрогена (ER) заболевание» может охватывать различные виды рака молочной железы. категории. Важно отметить, что традиционные прогностические факторы, такие как положительность лимфатических узлов, указывают на худший прогноз среди всех видов рака молочной железы, независимо от статуса ER.Однако с терапевтической точки зрения множественные метастазы в лимфатические узлы вызывают мало споров, поскольку статус лимфатических узлов не позволяет прогнозировать чувствительность ни к эндокринному лечению, ни к химиотерапии.
Напротив, оптимальное лечение ER-положительных опухолей с плохим прогнозом, основанным на биологических характеристиках, представляет собой другой сценарий. Среди таких параметров многие прогностические параметры позволяют прогнозировать эффективность терапии [Lønning et al . 2007]. Принято считать, что ответ на эндокринную терапию при метастатических и адъювантных ситуациях зависит от уровней экспрессии ER.Таким образом, Harvey и его коллеги обнаружили преимущество тамоксифена по сравнению с без эндокринного лечения в адъювантной среде для опухолей, экспрессирующих всего 3 балла Allred ER [Harvey et al . 1999]. Однако они обнаружили линейную корреляцию между уровнями баллов ER и риском рецидива; самый высокий балл был связан с лучшим прогнозом. В соответствии с этим исследования, проведенные три десятилетия назад, выявили более высокий уровень ответа на эндокринную терапию среди пациентов с метастатическим раком молочной железы с опухолями, экспрессирующими высокие уровни ER по сравнению с опухолями, экспрессирующими умеренные и низкие уровни ER, как измерено с помощью анализа связывания лиганда [McGuire, 1978] .Аналогичным образом, сверхэкспрессия рецептора 2 эпидермального фактора роста человека (HER-2), как было показано, связана с более высокой частотой рецидивов среди ER-положительных опухолей, независимо от того, лечили ли тамоксифеном или ингибитором ароматазы, по сравнению с HER-2-отрицательными опухолями [Dowsett et al. . 2008; Расмуссен и др. . 2008]. Кроме того, хотя объединение доказательств указывает на отсутствие пользы от добавления таксана к антрациклин-содержащей химиотерапии или даже от использования антрациклин-содержащей химиотерапии среди ER-богатых просветных опухолей класса A [Albain et al .2010; Хью и др. . 2009; Penault-Llorca и др. . 2009], преимущество «более агрессивной» химиотерапии при ER-положительных опухолях, принадлежащих к классу просвета B, ER-положительных опухолях со сверхэкспрессией HER-2 или ER-положительных опухолях с высокой скоростью пролиферации (в целом принадлежащих к luminal B или класс HER-2) является более сложной проблемой.
В этом обзоре обсуждаются современные данные об оценке ответа на химиотерапию и эндокринное лечение у пациентов с ER-положительными опухолями, выявляя фенотип с неблагоприятным прогнозом на основе биологических характеристик.Кроме того, рассматривается польза от использования лечения анти-HER-2 с эндокринной терапией в ER-положительных опухолях, выявляющих сверхэкспрессию HER-2.
Использование химиотерапии
Долгосрочные преимущества адъювантной химиотерапии, предотвращающие рецидив рака груди и улучшающие общую выживаемость, хорошо документированы с помощью оксфордского метаанализа [Abe et al . 2005]. Хотя адъювантная химиотерапия в среднем может улучшить долгосрочную выживаемость примерно на 30%, противоречивые данные указывают на то, что отношение рисков (HR) может быть различным для разных групп пациентов.Хотя обзорный анализ 2005 года показал более высокую пользу от химиотерапии среди пациентов с ER-отрицательными опухолями, чем у пациентов с ER-положительными опухолями, и более высокую пользу среди пациентов в возрасте до 50 лет, чем у пациентов в возрасте 50-69 лет, недавний обзор 2011 года показал, что пользу от химиотерапии не зависит от возраста пациента, а также от статуса рецепторов ER [группа специалистов по раннему исследованию рака молочной железы, 2011]. Данные, указывающие на то, что химиотерапия в сочетании с эндокринной терапией имеет сходное преимущество среди пациентов с ER-положительными опухолями и пациентов с ER-отрицательными опухолями, удивительны, в частности, поскольку эти данные контрастируют с данными нескольких крупных контролируемых исследований (см. Ниже).Полное объяснение этого несоответствия в настоящее время недоступно. Однако метаанализ включал различные многоцентровые исследования, многие из которых не включали централизованную оценку статуса ER. В этом обзоре обобщены и обсуждаются данные, полученные в отдельных исследованиях, показывающие потенциальную прогностическую роль статуса ER и других биохимических параметров в измерении ответа на терапию. Однако при обобщении доказательств следует принимать во внимание результаты недавнего обзора.
Потенциальное влияние возраста пациента на пользу от химиотерапии представляет интерес для нашего понимания эффектов эндокринной терапии.Таким образом, возможным объяснением того, почему химиотерапия может быть особенно полезной для молодых женщин, является вызванная химиотерапией потеря функции яичников у женщин в пременопаузе. Большинство пациентов, участвовавших в более ранних исследованиях, получали лечение обычными циклофосфамидом, метотрексатом и химиотерапией с 5-фторурацилом (5-FU) (CMF) с более высокой склонностью к необратимой потере функции яичников по сравнению с современными схемами, содержащими антрациклин [Petrek et al . 2006]. Тем не менее, существует несколько противоречивых наблюдений о потенциальной пользе аменореи для разных групп пациентов и в отношении результатов терапии.Так, Swain и его коллеги недавно сообщили, что аменорея, длящаяся более 6 месяцев, связана с улучшением результатов у пациентов с ER-положительным, а также ER-отрицательным раком молочной железы, получавших различные схемы лечения доксорубицином и доцетакселом [Swain et al . 2010]. Принимая во внимание подавление функции яичников у пациентов, впоследствии получавших тамоксифен, общепринятое мнение считало, что эффект тамоксифена не зависит от уровней циркулирующего эстрогена. Однако эта гипотеза не получила должной оценки в рандомизированных исследованиях III фазы.В то время как австрийский протокол ABCSG-12 рандомизировал женщин в пременопаузе для приема гозерелина в комбинации с анастрозолом или тамоксифеном, не было контрольной группы с пациентами, получавшими монотерапию тамоксифеном [Gnant et al . 2009]. Данные некоторых небольших исследований метастатического рака молочной железы показали преимущество удаления яичников в сочетании с тамоксифеном по сравнению с монотерапией тамоксифеном [Klijn et al . 2000, 2001], но пока этот комбинированный подход не получил всеобщего признания.
Анализ результатов трех крупных исследований рака и лейкемии группы B (CALGB) — оценка важности интенсивности дозы антрациклина, добавления паклитаксела или плотной дозы (2 раза в неделю) по сравнению с обычной 3-недельной дозой [Berry и др. . 2006] — для каждой стратегии польза была выше среди пациентов с ER-отрицательными опухолями по сравнению с пациентами с ER-положительными опухолями, которые также получали тамоксифен (). Степень, в которой это взаимодействие может быть связано с сопутствующим введением тамоксифена или внутренней биологией ER-положительных опухолей, трудно измерить, поскольку текущие руководящие принципы рекомендуют эндокринную терапию для всех пациентов с ER-положительными опухолями, которые считаются подходящими для химиотерапии.
Таблица 1.
Ключевые исследования, сообщающие о различных параметрах, предсказывающих преимущества добавления химиотерапии, дозы / плотности лекарственного средства или добавления таксанов к антрациклин-содержащей химиотерапии при раке молочной железы с положительным рецептором эстрогена (ER), получавшем эндокринную терапию.
| Схема протестирована | Тип опухоли | Прогнозирующий фактор | Результат | Ссылка |
|---|---|---|---|---|
| Tam +/− anthra-pred cont chemo | ER + | c905 Оценка по гену DX (On) эффективность химиотерапии | [Albain et al .2010] | |
| Доза Anthra | ER +/− | ER + по сравнению с ER− | Выгода для ER−, а не ER + tum | [Berry et al . 2006] |
| Добавьте pacl к антре | ER +/− | ER + по сравнению с ER− | Выгода для ER−, а не ER + tum | [Berry et al . 2006] |
| DD anthra / tax Chemo | ER +/− | ER + по сравнению с ER− | Выгода для ER−, а не ER + tum | [Berry et al .2006] |
| Добавьте pacl к антре | ER + | Избыточная экспрессия HER-2 | Получите пользу от pacl в HER2 + tum | [Hayes et al . 2007] |
| TAC по сравнению с режимом FAC | ER + | Избыточная экспрессия HER-2 | Преимущество TAC в HER2 + tum | [Hugh et al . 2009] |
| TAC по сравнению с режимом FAC | ER + | «Класс опухоли» | Некоторые преимущества TAC в опухоли Lum B | [Hugh et al .2009] |
| Добавить doce в FEC 100 | ER + | Ki67 | Преимущество добавления doce с высоким значением Ki67 | [Penault-Llorca et al . 2009] * |
| Добавить doce в FEC 100 | ER + | Избыточная экспрессия HER-2 | Нет преимуществ от добавления doce HER-2 + | [Penault-Llorca et al . 2009] * |
В нескольких испытаниях в неоадъювантных и адъювантных условиях сообщалось о преимуществах повышения дозы антрациклина, но до определенного «порогового» уровня в HER-2-положительных опухолях [Henderson et al .2003; Muss и др. . 1994; Пайк и др. . 1998; Пети и др. . 2001; Притчард и др. . 2006]. Совсем недавно это было связано с коамплификацией топоизомеразы II [Knoop et al . 2005; Press et al . 2011; Таннер и др. . 2006], антрациклиновая мишень, ген которой расположен рядом с геном HER-2 на хромосоме 17.
Работа Perou, Sørlie и его коллег [Sørlie et al . 2001], обнаружение, что рак груди можно разделить на отдельные классы на основе профилей экспрессии генов (), сильно повлияло на наши размышления о влиянии биологии рака груди на лечение.Анализ результатов лечения пациентов для FAC (фторурацил 500 мг / м 2 , доксорубицин 50 мг / м 2 и циклофосфамид 500 мг / м 2 ) по сравнению с TAC (доцетаксел 75 мг / м 2 , доксорубицин 50 мг / м 2 и циклофосфамид 500 мг / м 2 ) каждые 3 недели в течение шести циклов в исследовании 001 Международной исследовательской группы по раку молочной железы (BCIRG), Хью и его коллеги [Hugh et al . 2009] оценили потенциальную прогностическую роль профилей экспрессии генов [Sørlie et al .2001], определенный с помощью иммуногистохимии, и влияние сверхэкспрессии HER-2 и лечения тамоксифеном в подгруппе пациентов с ER-положительными опухолями (). Примечательно, что в то время как большинство ER-положительных опухолей не сверхэкспрессируют HER-2, 50% всех HER-2-положительных опухолей действительно ER-положительны, но в среднем на низких уровнях (см. Ссылки в Kaufman et al [2009]. ]).
Паттерны экспрессии генов 85 экспериментальных образцов из 78 видов рака молочной железы, трех доброкачественных опухолей и четырех доброкачественных тканей.Рисунок слева, полная диаграмма кластера. Буквы C – G относятся к кластеру ампликона рецептора 2 эпидермального фактора роста человека (HER-2) (C), кластеру неизвестного значения (D), кластеру, обогащенному базальными эпителиальными клетками (E), нормальному кластеру, подобному груди (F). ), и кластер генов люминального эпителия, содержащий рецепторы эстрогена (G). Адаптировано из [Sørlie et al . 2001] с разрешения. Люм, просвет.
Результаты исследования BCIRG [Hugh et al . 2009] предоставляют интересную информацию о сложных взаимодействиях между эффектами химиотерапии, антигормонального лечения и внутренней биологией опухоли.Как упоминалось выше, невозможно дать полное биологическое объяснение, потому что почти все пациенты с ER-положительными опухолями не будут получать адъювантную химиотерапию, не получая также эндокринного лечения. Глядя на безрецидивную или общую выживаемость в общей популяции исследования, пациенты, классифицированные как имеющие опухоли просвета А, имели лучший прогноз. Пациенты с опухолями, классифицированными как просвет B, имели «промежуточный» исход, в то время как пациенты с опухолями с тройным отрицательным и сверхэкспрессией HER-2 имели низкие показатели безрецидивной и общей выживаемости.Таким образом, исследование Хью и его коллег воспроизвело оригинальные наблюдения Сорли и его коллег [Sørlie et al . 2001, 2003], что свидетельствует о прогностическом влиянии этой классификации независимо от того, применялась адъювантная терапия или нет (). Сравнивая две группы лечения, можно увидеть явную пользу от добавления доцетаксела у пациентов с опухолями со сверхэкспрессией HER-2 или тройными отрицательными опухолями, с ограниченным преимуществом для опухолей просвета B и без преимущества для опухолей просвета A ().Для подгруппы ER-положительных опухолей польза от доцетаксела наблюдалась в опухолях, сверхэкспрессирующих HER-2. Интересно, что включение тамоксифена значительно улучшило результат у пациентов с ER-положительными, HER-2-отрицательными опухолями, получавших TAC или FAC. Напротив, никакого преимущества от TAC по сравнению с FAC не наблюдалось среди ER-положительных и HER-2-отрицательных опухолей. У пациентов со сверхэкспрессией HER-2 умеренная польза от тамоксифена наблюдалась среди пациентов, получавших химиотерапию FAC. Напротив, у пациентов с опухолями со сверхэкспрессией HER-2, получавших TAC, пользы от тамоксифена не наблюдалось.Примечательно, что эти анализы подгруппы необходимо интерпретировать осторожно из-за ограниченного числа пациентов с ER-положительными опухолями, сверхэкспрессирующими HER-2, и потому, что количество пациентов с ER-положительными опухолями, не получающих эндокринную терапию, было небольшим. В исследовании CALGB 9344 / INT0148 было также обнаружено преимущество добавления таксана к антрациклин-содержащей химиотерапии в ER-положительных опухолях, сверхэкспрессирующих HER-2 (но не в HER-2-отрицательных, ER-положительных опухолях) [Hayes et al . 2007].
Прогностическое влияние различных классов опухолей среди пациентов, не получающих какого-либо системного адъювантного лечения (A), и пациентов с раком молочной железы III стадии, получавших в нашей клинике неоадъювантную химиотерапию (доксорубицин еженедельно или 3-недельный 5-фторурацил с митомицином) с тамоксифеном для эстрогеновые рецепторы (ER) -положительные опухоли (B).На рисунке (A) показана выживаемость без рецидивов, а на рисунке (B) — общая выживаемость. Воспроизведено с разрешения [Sørlie et al . 2003]. Adj endo, адъювантная эндокринная терапия; Адъювант тамоксифен.
Оценка прогностических факторов у пациентов с ER-положительными опухолями, рандомизированных для лечения либо FEC (5-FU, эпирубицин и циклофосфамид) 100 в течение шести циклов, либо FEC100 в течение трех циклов с последующим введением доцетаксела (100 мг / м) 2 для трех циклов ), Penault-Llorca и его коллеги обнаружили повышенную экспрессию Ki67 (определяемую как> 20% опухолевых клеток, показывающих положительное окрашивание), чтобы предсказать пользу от добавления доцетаксела в схему () [Penault-Llorca et al .2009]. В отличие от данных Хью и его коллег [Hugh et al . 2009] это исследование выявило незначительный вредный эффект добавления доцетаксела к лечению пациентов с опухолями со сверхэкспрессией HER-2. Этому открытию может быть несколько объяснений. Здесь, как и в исследовании Хью и его коллег, количество ER-положительных опухолей со сверхэкспрессией HER-2 было низким, и расхождение могло быть вызвано только случайностью. Однако в исследовании Penault-Llorca и его коллег, в отличие от исследования Hugh и коллег, количество циклов, содержащих антрациклин, было уменьшено с шести до трех в группе доцетаксела.Принимая во внимание пользу увеличения дозы антрациклина в HER-2-положительных опухолях (см. Выше), дизайн исследования вполне мог способствовать этому результату. Следует отметить, что оба эти испытания были проведены до применения трастузумаба в качестве адъюванта. Принимая во внимание пользу одновременной химиотерапии и трастузумаба, результаты этих исследований могли быть разными, если трастузумаб вводился в комбинации [Gianni et al .2011; Perez и др. . 2011].
Наконец, анализируя образцы опухолей из исследования South West Oncology Group (SWOG) -8814, оценивающего добавление CAF (циклофосфамида, доксорубицина и 5-FU) к адъюванту тамоксифена для ER-положительного рака молочной железы, Альбаин и его коллеги оценили прогностическую роль 21-гена или сигнатуры Oncotype DX () [Albain et al . 2010]. Эта сигнатура была впервые разработана как прогностический параметр у пациентов с ER-положительными опухолями, получавших тамоксифен [Paik et al .2004]; здесь низкий балл был связан с хорошим прогнозом. Впоследствии было также показано, что он предсказывает пользу от химиотерапии CMF в той же популяции пациентов с ER-положительными опухолями, получающих лечение тамоксифеном [Paik et al . 2006]. При добавлении химиотерапии к тамоксифену польза была ограничена пациентами с высокими показателями по сигнатуре 21 гена, что указывает на пользу химиотерапии среди пациентов с плохим прогнозом при монотерапии тамоксифеном. В своем анализе исследования SWOG-8814 Олбэйн и его коллеги подтвердили пользу от добавления антрациклин-содержащей химиотерапии к лечению пациентов с высоким показателем по сигнатуре 21 гена.Напротив, не было зарегистрировано никаких улучшений среди пациентов с низким баллом по сигнатуре 21 гена.
Взятые вместе, эти данные исследования показывают улучшенное преимущество химиотерапии у пациентов с ER-отрицательными опухолями по сравнению с пациентами с ER-положительными опухолями. Ясно, что существует дифференциальный эффект среди ER-положительных опухолей, что обнаруживается такими маркерами, как сверхэкспрессия HER-2, экспрессия Ki67, классификация по иерархической кластеризации и сигнатуры 21 гена. Помимо сверхэкспрессии HER-2, которая вместе с экспрессией топоизомеразы II должна считаться прогностическим маркером для идентификации лекарственной мишени, классификация ER-положительных опухолей в просвет A по сравнению с классом B, опухоли, обнаруживающие низкую экспрессию против высокой экспрессии Ki67 или опухоли, показывающие низкий балл по сравнению с высоким показателем по сигнатуре 21 гена, в значительной степени предоставляют перекрывающуюся информацию.Сигнатура из 21 гена измеряет пролиферацию опухоли, и опухоли просвета В в среднем выявляют более высокий Ki67 по сравнению с опухолями просвета А [Cheang et al . 2009]. Следовательно, любой из этих методов может характеризовать ER-положительные опухоли с хорошим прогнозом, вероятно, без необходимости в химиотерапии по сравнению с для тех, которые имеют более высокий риск рецидива и могут получить пользу от химиотерапии в сочетании с эндокринным лечением.
Использование эндокринной терапии
В то время как эндокринная терапия, как сообщается, приносит пользу при опухолях, экспрессирующих иммуноокрашивание ER только в нескольких процентах их клеток [Hammond et al .2010], эндокринная терапия в адъюванте () и на поздних стадиях более эффективна для опухолей, экспрессирующих высокие уровни рецепторов, по сравнению с опухолями, экспрессирующими низкие уровни [Harvey et al . 1999; Макгуайр, 1978]. Среди ER-положительных опухолей низкие уровни экспрессии ER и высокий Ki67 в целом характеризуют опухоли, принадлежащие к просвету B, а не к люминальному классу A (см. Обсуждение в Lønning et al . [2005]). положительные опухоли обнаруживают сверхэкспрессию HER-2 [Penault-Llorca et al .2009], среди подгруппы (15–20% всех случаев рака молочной железы), у которых выявлены амплификации или сверхэкспрессия HER-2, около половины являются ER-положительными [Perez et al . 2011; Untch и др. . 2008]. Таким образом, эндокринная терапия остается потенциальным вариантом лечения примерно половины опухолей, амплифицированных HER-2. Подобно опухолям, принадлежащим к люминальному классу B [Sørlie et al . 2001, 2003], ER-положительные опухоли, сверхэкспрессирующие HER-2, обычно экспрессируют ER на более низком уровне по сравнению с ER-положительными опухолями люминального класса A [Konecny et al .2003]. Таким образом, следует тщательно изучить потенциальное влияние статуса Ki67 и амплификации или сверхэкспрессии HER-2 на чувствительность к эндокринной терапии.
Таблица 2.
Ключевые исследования, сообщающие о различных параметрах, прогнозирующих преимущества эндокринной адъювантной / неоадъювантной терапии при эстроген-рецептор-положительном (ER +) раке молочной железы.
| Схема | Настройка | Прогнозирующий фактор | Результат | Ссылка | |||
|---|---|---|---|---|---|---|---|
| Тамоксифен | адъювант | Уровень ER по уровню IHC | Корреляция | между уровнем ER и уровнем ER | Корреляция между эффектом | и корреляцией и др., .1999] | |
| Тамоксифен | адъювант | Уровень ER по IHC | Корреляция между уровнем ER + и эффектом терапии | [Dowsett et al . 2008] | |||
| Анастрозол | адъювант | Уровень ER по IHC | Корреляция между уровнем ER + и эффектом терапии | [Dowsett et al . 2008] | |||
| Тамоксифен | адъювант | HER-2 +/- по IHC | Сверхэкспрессия HER-2 снижает эффективность терапии | [Dowsett et al .2008] | |||
| Анастрозол | адъювант | HER-2 +/- по IHC | Сверхэкспрессия HER-2 снижает эффективность терапии | [Dowsett et al . 2008] | |||
| Тамоксифен | адъювант | HER-2 +/- по IHC | Сверхэкспрессия HER-2 снижает эффективность терапии | [Rasmussen et al . 2008] | |||
| Летрозол | адъювант | HER-2 +/- по IHC | Сверхэкспрессия HER-2 снижает эффективность терапии | [Rasmussen et al .2008] | |||
| Тамоксифен | неоадъювант | Ki67 падение через 2 недели | Ki67 снижение прогнозируемый результат | [Dowsett et al . 2007] | |||
| Летрозол | неоадъювант | Ki67 падение через 2 недели | Ki67 снижение прогнозируемый результат | [Dowsett et al . 2007] |
Неоадъювантные исследования, проведенные Доусеттом и его коллегами, показали низкий Ki67, в частности, при определении через 2 недели эндокринной терапии, для прогнозирования хорошего долгосрочного результата для пациентов, получающих неоадъювантное лечение тамоксифеном или ингибитором ароматазы. () [Dowsett et al .2007]. В своем первоначальном отчете о профиле экспрессии гена Oncotype DX, содержащего 21 ген, Пайк и его коллеги сообщили о низком балле, позволяющем прогнозировать хороший прогноз у пациентов, получавших адъювантное лечение тамоксифеном [Paik et al . 2004]. Таким образом, низкая оценка пролиферации, независимо от того, оценивается ли она по экспрессии Ki67 или по шкале Oncotype DX, по-видимому, предсказывает пользу от эндокринного лечения, но меньшую пользу от более «агрессивной» химиотерапии по сравнению с высокой оценкой пролиферации.
Исследования, проведенные более десяти лет назад, показали, что избыточная экспрессия HER-2 снижает ответ на эндокринную терапию тамоксифеном [Berns et al .1995; Хьюстон и др. . 1999], но также к другим вариантам эндокринного лечения, таким как дролоксифен, мегестрола ацетат и ингибитор ароматазы второго поколения, фадрозол [Leitzel et al . 1995; Ямаути и др. . 1997] при метастатическом заболевании. Интересно, что данные двух неоадъювантных исследований показали пользу летрозола [Ellis et al . 2001] и анастрозол [Smith et al . 2005] по сравнению с тамоксифеном, чтобы быть особенно высоким в опухолях со сверхэкспрессией HER-2.Однако более свежие данные исследования TransAtac [Dowsett et al . 2008] и исследование BIG 1-98 [Rasmussen et al . 2008] указывают на то, что ингибиторы ароматазы могут снижать ЧСС рецидива по сравнению с тамоксифеном в адъювантном режиме примерно в той же степени у пациентов с HER-2-положительными и HER-2-отрицательными опухолями (2).
Недавние исследования показали, что неоадъювантное лечение HER-2-положительных опухолей различными схемами химиотерапии, содержащими антрациклин и таксан, включая трастузумаб, дает частоту патологического полного ответа (pCR) в диапазоне 30-40% [Gianni et al .2010; Untch и др. . 2010, 2011], что примерно вдвое превышает частоту ответа, обычно сообщаемую среди пациентов с опухолями с нормальным статусом HER-2. Пока что данные неубедительны относительно того, может ли pCR в HER-положительных, ER-положительных опухолях отличаться от ответа в HER-2-положительных, ER-отрицательных опухолях [Untch et al . 2010, 2011]. Однако тот факт, что клинические и патологические полные ответы превышают то, что может наблюдаться у пациентов с ER-положительными опухолями, получающих неоадъювантную эндокринную терапию, дает мало возможностей для исследований рандомизации ER-положительных HER-положительных пациентов между неоадъювантной эндокринной терапией и химиотерапией.Однако, поскольку у большинства этих пациентов не достигается оптимальный ответ на химиотерапию трастузумабом, требуются альтернативные растворы второй линии. Некоторым пациентам с субоптимальным ответом на химиотерапию может помочь эндокринная терапия в сочетании с лечением анти-HER-2. Чтобы продолжить в этой области, необходимо определить маркеры, позволяющие прогнозировать pCR при химиотерапии трастузумабом. Такие маркеры могут позволить выбрать пациентов с опухолями, нечувствительными к химиотерапии, которым следует оценить первичную эндокринную терапию тратузумабом.
По общему мнению, опухоли с избыточной экспрессией HER-2 или амплифицированные опухоли имеют более низкий ответ на эндокринную терапию по сравнению с HER-2-положительными опухолями. Однако степень, в которой это связано со сверхэкспрессией HER-2 per se , более высоким уровнем KI67 по сравнению с HER-2-отрицательными опухолями или тем фактом, что эти опухоли в среднем экспрессируют ER в более низкой концентрации по сравнению с HER -2-отрицательные опухоли до конца не изучены.
Сочетание анти-HER-2 и эндокринной терапии
Два рандомизированных исследования изучали влияние добавления трастузумаба к анастрозолу [Kaufman et al .2009] или лапатиниба на летрозол [Johnston et al . 2009] у пациентов с ER-положительным, HER-2-положительным метастатическим раком молочной железы. Оба исследования показали значительную пользу от комбинации анти-HER-2 агента с ингибитором ароматазы. Интересно, что в исследовании Джонстона и его коллег также были включены пациенты с ER-положительными, но HER-2-отрицательными опухолями [Johnston et al . 2009]. В то время как никакой пользы от лапатиниба не было зарегистрировано для всей группы пациентов с HER-2-отрицательными опухолями, предварительно определенный субанализ выявил незначительную пользу от приема лапатиниба в группе пациентов, у которых был рецидив менее чем через 6 месяцев после отмены адъювантного тамоксифена.Гипотеза, лежащая в основе этого исследования, заключается в том, что активация HER-2 может также придавать устойчивость к эндокринной терапии в подгруппе ER-положительных опухолей, не сверхэкспрессирующих HER-2, и это получило поддержку в экспериментальных и трансляционных исследованиях. Таким образом, трастузумаб, как было показано, противодействует устойчивости к летрозолу в клетках и ксенотрансплантатах, не сверхэкспрессирующих HER-2 [Sabnis et al . 2009]. Кроме того, в недавнем исследовании было обнаружено, что неоадъювантное лечение ингибиторами ароматазы повышает уровень экспрессии мРНК HER-2 в опухолях, не амплифицированных для HER-2 [Flageng et al .2009]. Представляет существенный интерес подтвердить результаты, полученные Джонстоном и его коллегами в независимых исследованиях.
Совсем недавно были опубликованы результаты двух небольших исследований по оценке комбинированного эндокринного и анти-HER-2 лечения ER-положительного, HER-2-положительного метастатического рака молочной железы. Исследование эффективности и безопасности летрозола в сочетании с трастузумабом у пациентов с метастатическим раком молочной железы (исследование eLETRA) [Huober et al . 2009] был досрочно закрыт из-за плохого начисления.С учетом 92 пациентов, рандомизированных для приема летрозола по сравнению с летрозолом в сочетании с трастузумабом, среднее время до прогрессирования было увеличено с 3,3 до 14,1 месяцев, но не достигло статистической значимости из-за небольшого числа пациентов. Наконец, показав 8 из 11 пациентов, у которых ранее обнаружилась резистентность к монотерапии анастрозолом и трастузумабом, чтобы получить пользу (показать ответ или стабильное заболевание после 6 месяцев) от двух соединений, вводимых в комбинации, исследование Koeberle и его коллег подтверждает гипотезу о том, что может быть положительный синергизм между этими соединениями [Koeberle et al .2011].
Резюме
Учитывая адъювантное лечение, теперь у нас есть возможность идентифицировать пациентов с ER-положительными опухолями, которым может помочь химиотерапия на основе антрациклинов и последовательное добавление таксана. Опухоли со сверхэкспрессией или амплификацией HER-2, по-видимому, демонстрируют улучшенное преимущество от добавления таксана к схеме лечения. Тот факт, что ER-положительные опухоли со сверхэкспрессией HER-2, по-видимому, получают меньшую пользу от эндокринной терапии по сравнению с ER-положительными, HER-2-отрицательными опухолями, еще раз подчеркивает, что эти пациенты нуждаются в химиотерапии и не должны быть лишены такого лечения в адъюванте. параметр.Единственным исключением могут быть пациенты, состояние здоровья которых исключает использование химиотерапии.
Вторая группа пациентов с ER-положительными опухолями, которые, вероятно, получат пользу от химиотерапии, — это пациенты с «высоким» баллом Ki67, выражением уровня ER от умеренного до низкого, обнаружением сигнатуры экспрессии гена B в просвете или с высоким баллом рецидива в соответствии с Анализ онкотипа DX [Paik et al . 2004]. В значительной степени эти группы пересекаются. Однако некоторые пациенты могут претендовать на химиотерапию на основании значения одного или, возможно, двух из этих параметров.
Неоадъювантная (первичная медикаментозная) терапия — область для дальнейших исследований. Первой целью должно быть определение прогностических маркеров pCR для химиотерапии (в целом) и химиотерапии в сочетании с трастузумабом при HER-2-положительных опухолях. После этого пациенты с ER-положительными опухолями, которые вряд ли достигнут pCR к химиотерапии, могут быть предметом дальнейших исследований по изучению оптимального антигормонального лечения в первичных условиях.
Что касается метастазов, то здесь сценарий другой.Метастатический рак груди остается неизлечимым заболеванием, и любой вариант лечения является паллиативным. Что касается качества жизни, эндокринная терапия выгодно отличается от цитотоксических соединений, а лечение анти-HER-2 обычно хорошо переносится. Хотя HER-2-положительные опухоли обычно имеют более низкий уровень ответа на эндокринную терапию по сравнению с HER-2-отрицательными опухолями, результаты недавних исследований, показывающие пользу от добавления тратузумаба или лапатиниба к лечению ингибитором ароматазы, предоставляют варианты эндокринной терапии, включая лечение этих пациентов анти-HER-2.Пациенты с эндокринно-чувствительными опухолями могут реагировать на несколько агентов, вводимых последовательно [Lønning, 2004, 2009]. Точно так же, по-видимому, отсутствует перекрестная резистентность между анти-HER-2 агентами, такими как трастузумаб и лапатиниб или пертузумаб. Кроме того, пациенты, прогрессирующие на лечении трастузумабом и химиотерапией, похоже, выиграют от продления лечения трастузумабом до следующего режима химиотерапии [Baselga et al . 2010; Блэквелл и др. . 2009; фон Минквитц и др. .2009]. Интересно, что пациенты, у которых ранее наблюдалось прогрессирование трастузумаба, получавшего лапатиниб, улучшалось время до прогрессирования, если трастузумаб добавлялся в комбинации [Blackwell et al . 2010]. Поскольку отсутствует полная перекрестная резистентность среди различных методов лечения анти-HER-2, оптимальное последовательное или комбинированное использование антиэндокринных и анти-HER-2 агентов может значительно улучшить терапию пациентов с метастатической ER-положительной, HER-2-положительной молочной железой. рак.
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Автор заявляет об отсутствии конфликта интересов при подготовке статьи.
Список литературы
- Абе О., Абе Р., Эномото К., Кикучи К., Кояма Х., Масуда Х. и др. (2005) Влияние химиотерапии и гормональной терапии при раннем раке груди на рецидив и 15-летнюю выживаемость: обзор рандомизированных исследований. Ланцет 365: 1687–1717 [PubMed] [Google Scholar]
- Албайн К.С., Барлоу У.Э., Шак С., Хортобадьи Г.Н., Ливингстон Р.Б., Йе И.Т. и др. (2010) Прогностическая и прогностическая ценность анализа рецидива 21 гена у женщин в постменопаузе с лимфоузловым и эстроген-рецепторно-положительным раком молочной железы при химиотерапии: ретроспективный анализ рандомизированного исследования.Ланцет Онкол 11: 55–65 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Базельга Дж., Гельмон К.А., Верма С., Уордли А., Конте П., Майлз Д. и др. (2010) Фаза II испытания пертузумаба и трастузумаба у пациентов с метастатическим раком молочной железы, положительным по рецептору эпидермального фактора роста 2, который прогрессировал во время предшествующей терапии трастузумабом. Дж Клин Онкол 28: 1138–1144 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Бернс Э., Фокенс Дж.А., Ванставерен И.Л., Ванпуттен В.Л.Дж., Деконинг Х., Портенген Х., Клин Дж. Г. М. (1995) Амплификация онкогенов и прогноз при раке груди — взаимосвязь с системным лечением. Ген 159: 11–18 [PubMed] [Google Scholar]
- Берри Д.А., Чирринчионе К., Хендерсон И.С., Цитрон М.Л., Будман Д.Р., Гольдштейн Л.Дж. и др. (2006) Статус эстрогеновых рецепторов и результаты современной химиотерапии для пациентов с раком молочной железы с положительным лимфоузлом. JAMA 295: 1658–1667 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Блэквелл К.Л., Бурштейн Х.Дж., Сторниоло А.М., Руго Х., Следж Г., Кёлер М. и др. (2010) Рандомизированное исследование лапатиниба или его комбинации с трастузумабом у женщин с ErbB2-положительным, рефрактерным к трастузумабом метастатическим раком молочной железы. Дж Клин Онкол 28: 1124–1130 [PubMed] [Google Scholar]
- Блэквелл К.Л., Пеграм М.Д., Тан-Чиу Э., Шварцберг Л.С., Арбушитес М.С., Мальцман Д.Д. и др. (2009) Монотерапия лапатинибом для лечения прогрессирующего или метастатического рака молочной железы со сверхэкспрессией HER2, который прогрессировал на схемах, содержащих трастузумаб первой или второй линии.Энн Онкол 20: 1026–1031 [PubMed] [Google Scholar]
- Cheang M.C.U., Chia S.K., Voduc D., Gao D.X., Leung S., Snider J. и др. (2009) Индекс Ki67, статус HER2 и прогноз пациентов с раком молочной железы в просвете B. J Natl Cancer Inst 101: 736–750 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Dowsett M., Allred C., Knox J., Quinn E., Salter J., Wale C., et al. (2008) Связь между количественной экспрессией рецептора эстрогена и прогестерона и статусом рецептора 2 эпидермального фактора роста человека (HER-2) с рецидивом в исследовании аримидекса, тамоксифена, отдельно или в комбинации.Дж Клин Онкол 26: 1059–1065 [PubMed] [Google Scholar]
- Доусетт М., Смит И.Е., Эббс С.Р., Диксон Дж. М., Скин А., А’Херн Р. и др. (2007) Прогностическое значение экспрессии Ki67 после краткосрочной предоперационной эндокринной терапии первичного рака молочной железы. J Natl Cancer Inst 99: 167–170 [PubMed] [Google Scholar]
- Совместная группа исследователей раннего рака молочной железы (2011) Сравнение различных режимов полихимиотерапии для метаанализа отдаленных результатов лечения раннего рака молочной железы среди 100.000 женщин в 123 рандомизированных исследованиях. Ланцет 379: 432–444 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Эллис М.Дж., Куп А., Сингх Б., Мориак Л., Лломберт Кассак А., Янике Ф. и др. (2001) Летрозол является более эффективной неоадъювантной эндокринной терапией, чем тамоксифен, для ErbB-1- и / или ErbB-2-положительного, эстроген-рецептор-положительного первичного рака молочной железы: данные рандомизированного исследования фазы III. Дж Клин Онкол 19: 3808–3816 [PubMed] [Google Scholar]
- Флагенг М.Х., Мои Л.Л.Х., Диксон Дж.M., Geisler J., Lien E.A., Miller W.R. и др. (2009) Коактиваторы ядерных рецепторов и HER-2 / neu активируются у пациентов с раком груди во время неоадъювантного лечения ингибиторами ароматазы. Br J Рак 101: 1253–1260 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Джанни Л., Дафни У., Гелбер Р.Д., Азамбуджа Э., Мюльбауэр С., Голдхирш А. и др. (2011) Лечение трастузумабом в течение 1 года после адъювантной химиотерапии у пациентов с HER2-положительным раком молочной железы на ранней стадии: 4-летнее наблюдение в рандомизированном контролируемом исследовании.Ланцет Онкол 12: 236–244 [PubMed] [Google Scholar]
- Джанни Л., Эйерманн В., Семиглазов В., Манихас А., Ллуч А., Тюландин С. и др. (2010) Неоадъювантная химиотерапия трастузумабом с последующей адъювантной химиотерапией трастузумабом по сравнению с одной неоадъювантной химиотерапией у пациентов с HER2-положительным местнораспространенным раком молочной железы (исследование NOAH): рандомизированное контролируемое исследование превосходства с параллельной HER2-отрицательной когортой. Ланцет 375: 377–384 [PubMed] [Google Scholar]
- Гнант М., Млинерич Б., Schippinger W., Luschin-Ebengreuth G., Postlberger S., Menzel C., et al. (2009) Эндокринная терапия плюс золедроновая кислота при пременопаузальном раке молочной железы. N Engl J Med 360: 679–691 [PubMed] [Google Scholar]
- Hammond M.E.H., Hayes D.F., Dowsett M., Allred D.C., Hagerty K.L., Badve S. и др. (2010) Американское общество клинической онкологии / Колледж американских патологов дают рекомендации по иммуногистохимическому тестированию рецепторов эстрогена и прогестерона при раке груди. Дж Клин Онкол 28: 2784–2795 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Харви Дж.M., Clark G.M., Osborne C.K., Allred D.C. (1999) Статус рецептора эстрогена с помощью иммуногистохимии превосходит анализ связывания лиганда для прогнозирования ответа на адъювантную эндокринную терапию при раке груди. Дж Клин Онкол 17: 1474–1481 [PubMed] [Google Scholar]
- Хейс Д.Ф., Тор А.Д., Дресслер Л.Г., Уивер Д., Эджертон С., Коуэн Д. и др. (2007) HER2 и ответ на паклитаксел при лимфоузловом раке молочной железы. N Engl J Med 357: 1496–1506 [PubMed] [Google Scholar]
- Хендерсон И.К., Берри Д.А., Деметри Г.Д., Чирринчионе С.Т., Гольдштейн Л.Дж., Мартино С. и др. (2003) Улучшение результатов при последовательном добавлении паклитаксела, но не при увеличении дозы доксорубицина в режиме адъювантной химиотерапии для пациентов с первичным раком молочной железы с положительным лимфоузлом. Дж Клин Онкол 21: 976–983 [PubMed] [Google Scholar]
- Хьюстон С.Дж., Планкетт Т.А., Барнс Д.М., Смит П., Рубенс Р.Д., Майлз Д.В. (1999) Сверхэкспрессия c-erbB2 является независимым маркером устойчивости к эндокринной терапии при распространенном раке молочной железы.Br J Рак 79: 1220–1226 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Хью Дж., Хэнсон Дж., Ченг М.С., Нильсен Т.О., Перу К.М., Дюмонте К. и др. (2009) Подтипы рака молочной железы и ответ на доцетаксел при лимфоузловом раке молочной железы: использование иммуногистохимического определения в исследовании BCIRG 001. Дж Клин Онкол 27: 1168–1176 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Huober J., Fasching PA, Paepke S., Kubista E., Barsoum M., Wallwiener D., Harbeck N. (2009) Летрозол в сочетании с трастузумабом превосходит монотерапию летрозолом в качестве лечения первой линии у пациентов с гормонально-рецепторными заболеваниями. положительный HER2-положительный метастатический рак молочной железы (MBC) — результаты исследования eLEcTRA.Рак Res 69: 737S – 738S [PubMed] [Google Scholar]
- Johnston S., Pippen J., Pivot X., Lichinitser M., Sadeghi S., Dieras V., et al. (2009) Лапатиниб в сочетании с летрозолом по сравнению с летрозолом и плацебо в качестве терапии первой линии при метастатическом раке молочной железы, положительном по рецепторам гормонов в постменопаузе. Дж Клин Онкол 27: 5538–5546 [PubMed] [Google Scholar]
- Кауфман Б., Макки Дж. Р., Клеменс М. Р., Бапси П. П., Вайд А., Уордли А. и др. (2009) Трастузумаб плюс анастрозол в сравнении с одним анастрозолом для лечения женщин в постменопаузе с положительным по рецептору эпидермального фактора роста 2 человека и положительным по рецептору гормона метастатическим раком молочной железы: результаты рандомизированного исследования III фазы TAnDEM.Дж Клин Онкол 27: 5529–5537 [PubMed] [Google Scholar]
- Klijn J.G.M., Beex L.V.A.M., Mauriac L., vanZijl J.A., Veyret C., Wildiers J. и др. (2000) Комбинированное лечение бусерелином и тамоксифеном при пременопаузальном метастатическом раке молочной железы: рандомизированное исследование. J Natl Cancer Inst 92: 903–911 [PubMed] [Google Scholar]
- Klijn JGM, Blamey RW, Boccardo F., Tominaga T., Duchateau L., Sylvester R. (2001) Комбинированный агонист тамоксифена и рилизинг-гормона лютеинизирующего гормона (LHRH) по сравнению с агонистом LHRH отдельно при распространенном раке молочной железы в пременопаузе: метаанализ из четырех рандомизированных испытаний.Дж Клин Онкол 19: 343–353 [PubMed] [Google Scholar]
- Кноп А.С., Кнудсен Х., Балслев Э., Расмуссен Б. Б., Овергаард Дж., Нильсен К. В. и др. (2005) Ретроспективный анализ амплификаций и делеций топоизомеразы IIa как прогностических маркеров у пациентов с первичным раком молочной железы, случайным образом отнесенных к циклофосфамиду, метотрексату и фторурацилу или циклофосфамиду, эпирубицину и фторурацилу: Датская кооперативная группа по раку молочной железы. Дж Клин Онкол 23: 7483–7490 [PubMed] [Google Scholar]
- Кёберле Д., Рухсталлер Т., Йост Л., Пагани О., Заман К., фон Моос Р. и др. (2011). Комбинация трастузумаба и летрозола после устойчивости к последовательной монотерапии трастузумабом и ингибиторами ароматазы у пациентов с эстроген-рецептор-положительным, HER-2-положительным распространенным раком молочной железы: испытание, подтверждающее концепцию (SAKK 23/03). Конец Rel Рак 18: 257–264 [PubMed] [Google Scholar]
- Конечны Г., Паулетти Г., Пеграм М., Унч М., Дандекар С., Агилар З. и др. (2003) Количественная связь между HER-2 / neu и рецепторами стероидных гормонов при первичном раке молочной железы, положительном по рецепторам гормонов.J Natl Cancer Inst 95: 142–153 [PubMed] [Google Scholar]
- Лейтцель К., Терамото Ю., Конрад К., Чинчилли В.М., Волас Г., Гроссберг Х. и др. (1995) Повышенные уровни антигена c- erb B-2 в сыворотке и снижение ответа на гормональную терапию рака груди. Дж Клин Онкол 13: 1129–1135 [PubMed] [Google Scholar]
- Лённинг П.Э. (2004) Ингибиторы ароматазы при раке груди. Конец Rel Рак 11: 179–189 [PubMed] [Google Scholar]
- Лённинг П.Э. (2009) Отсутствие полной перекрестной резистентности между различными ингибиторами ароматазы; настоящая находка в поисках объяснения? Eur J Рак 45: 527–535 [PubMed] [Google Scholar]
- Лённинг П.E., Knappskog S., Staalesen V., Chrisanthar R., Lillehaug J.R. (2007) Прогнозирование и прогнозирование рака груди в постгеномную эпоху. Энн Онкол 18: 1293–1306 [PubMed] [Google Scholar]
- Lønning P.E., Sørlie T., Børresen-Dale A.-L. (2005). Геномика при раке груди — терапевтическое значение? Нат Клин Прак Онкол 2: 26–33 [PubMed] [Google Scholar]
- Макгуайр У.Л. (1978) Стероидные рецепторы при раке груди человека. Рак Res 38: 4289–4291 [PubMed] [Google Scholar]
- Мусс Х.Б., Тор А.Д., Берри Д.А., Куте Т., Лю Э.Т., Кёрнер Ф. и др. (1994) экспрессия c-erB-2 и ответ на адъювантную терапию у женщин с лимфоузловым раком груди на ранней стадии. N Engl J Med 330: 1260–1266 [PubMed] [Google Scholar]
- Пайк С., Шак С., Тан Г., Ким К., Бейкер Дж., Кронин М. и др. (2004) Мультигенный анализ для прогнозирования рецидива рака молочной железы без лимфоузлов после лечения тамоксифеном. N Engl J Med 351: 2817–2826 [PubMed] [Google Scholar]
- Пайк С., Тан Г., Шак С., Ким С., Бейкер Дж., Ким В. и др. (2006) Экспрессия генов и польза химиотерапии у женщин с раком молочной железы с отрицательными узлами и положительными рецепторами эстрогена. Дж Клин Онкол 24: 3726–3734 [PubMed] [Google Scholar]
- Пайк С.М., Брайант Дж., Парк К.Х., Фишер Б., ТанЧиу Э., Хьямс Д. и др. (1998) erbB-2 и ответ на доксорубицин у пациентов с раком молочной железы, положительным по подмышечным лимфатическим узлам и отрицательным по рецепторам гормонов. J Natl Cancer Inst 90: 1361–1370 [PubMed] [Google Scholar]
- Пено-Льорка Ф., Андре Ф., Саган К., Лакруа-Трики М., Дену Й., Верриэль В. и др. (2009) Экспрессия Ki67 и эффективность доцетаксела у пациентов с раком молочной железы, положительным по рецепторам эстрогена. Дж Клин Онкол 27: 2809–2815 [PubMed] [Google Scholar]
- Перес Э.А., Ромонд Э.Х., Суман В.Дж., Чон Дж.Х., Дэвидсон Н.Э., Гейер С.Э. и др. (2011) Четырехлетнее наблюдение за терапией трастузумабом плюс адъювантной химиотерапией для функционального рака молочной железы с положительным рецептором 2 эпидермального фактора роста человека: совместный анализ данных NCCTG N9831 и NSABP B-31.Дж Клин Онкол 29: 3366–3373 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Пети Т., Борель К., Гнасия Ж.-П., Родье Ж.-Ф., Эсканде А., Морс Р., Хегеле П. (2001). Ответ на химиотерапию рака молочной железы зависит от HER-статуса и интенсивности дозы антрациклина в условиях неоадъювантной терапии. Clin Cancer Res 7, 1577–1581 [PubMed] [Google Scholar]
- Петрек Дж.А., Нотон М.Дж., Кейс Л.Д., Паскетт Е.Д., Нафталис Е.З., Синглетари С.Е., Сукумванич П. (2006) Частота, время и факторы, определяющие менструальное кровотечение после лечения рака груди: перспективное исследование.Дж Клин Онкол 24: 1045–1051 [PubMed] [Google Scholar]
- Press M.F., Sauter G., Buyse M., Bernstein L., Guzman R., Santiago A., et al. (2011) Изменение гена топоизомеразы II-альфа при раке груди человека: связь с реакцией на химиотерапию на основе антрациклинов. Дж Клин Онкол 29: 859–867 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Причард К.И., Шеперд Л.Э., О’Мэлли Ф.П., Андрулис И.Л., Ту Д., Брамвелл В.Х., Левин М.Н. (2006) HER2 и реакция рака груди на адъювантную химиотерапию.N Engl J Med 354: 2103–2111 [PubMed] [Google Scholar]
- Расмуссен Б. Б., Реган М. М., Ликкесфельдт А. Э., Делл’Орто П., Дель Курто Б., Хенриксен К. (2008) Адъювантный летрозол по сравнению с тамоксифеном в соответствии с централизованно оцененным статусом ERBB2 для женщин в постменопаузе с эндокринно-чувствительным раком молочной железы на ранней стадии: дополнительные результаты рандомизированного исследования BIG 1-98. Ланцет Онкол 9: 23–28 [PubMed] [Google Scholar]
- Сабнис Г., Шайовиц А., Голубьева О., Маседо Л., Броди А.(2009) Трастузумаб обращает вспять резистентность к летрозолу и усиливает чувствительность клеток рака груди к эстрогену. Рак Res 69: 1416–1428 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Smith I.E., Dowsett M., Ebbs S.R., Dixon J.M., Skene A., Blohmer J.U. и др. (2005). Неоадъювантное лечение рака молочной железы в постменопаузе с применением анастрозола, тамоксифена или обоих в комбинации: немедленное предоперационное лечение анастрозолом, тамоксифеном или комбинацией с тамоксифеном (IMPACT) в многоцентровом двойном слепом рандомизированном исследовании.Дж Клин Онкол 23: 5108–5116 [PubMed] [Google Scholar]
- Сорли Т., Перу К.М., Тибширани Р., Аас Т., Гейслер С., Йонсен Х. и др. (2001) В паттернах экспрессии генов карциномы молочной железы различаются подклассы опухолей с клиническими последствиями. Proc Nat Acad Sci U S A 98: 10869–10874 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Сорли Т., Тибширани Р., Паркер Дж., Хасти Т., Маррон Дж. С., Нобель А. и др. (2003) Повторное наблюдение подтипов опухолей молочной железы в независимых наборах данных по экспрессии генов.Proc Natl Acad Sci U S A 100: 8418–8423 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Суэйн С.М., Чон Дж.Х., Гейер С.Э., Константино Дж.П., Паджон Е.Р., Ференбахер Л. и др. (2010) Более длительная терапия, ятрогенная аменорея и выживаемость при раннем раке груди. N Engl J Med 362: 2053–2065 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Таннер М., Изола Дж., Виклунд Т., Эрикштейн Б., Келлокумпу-Лехтинен П., Мальмстрем П. и др. (2006) Амплификация гена альфа топоизомеразы II предсказывает благоприятный ответ на лечение индивидуализированной и увеличенной дозой адъювантной химиотерапии на основе антрациклина при HER-2 / neu-амплифицированном раке молочной железы: исследование скандинавской группы груди 9401.Дж Клин Онкол 24: 2428–2436 [PubMed] [Google Scholar]
- Untch M., Fasching P.A., Konecny G.E., Hasmuller S., Lebeau A., Kreienberg R., et al. (2011) Патологический полный ответ после неоадъювантной химиотерапии в сочетании с трастузумабом предсказывает благоприятное выживание при раке груди, сверхэкспрессирующем рецептор 2 эпидермального фактора роста: результаты исследования TECHNO, проведенного исследовательскими группами AGO и GBG. Дж Клин Онкол 29: 3351–3357 [PubMed] [Google Scholar]
- Untch M., Gelber R.D., Jackisch C., Procter M., Baselga J., Bell R., et al. (2008) Оценка величины эффектов трастузумаба в подгруппах пациентов в исследовании HERA. Энн Онкол 19: 1090–1096 [PubMed] [Google Scholar]
- Untch M., Rezai M., Loibl S., Fasching P.A., Huober J., Tesch H., et al. (2010) Неоадъювантное лечение трастузумабом при HER2-положительном раке молочной железы: результаты исследования GeparQuattro. Дж Клин Онкол 28: 2024–2031 [PubMed] [Google Scholar]
- фон Минквиц Г., дю Буа А., Шмидт М., Маасс Н., Куфер Т., де Йонг Ф. Э. и др. (2009) Трастузумаб выходит за рамки прогрессирования в 2-положительном распространенном раке молочной железы, положительном по рецептору эпидермального фактора роста человека: исследование 26 немецкой группы груди / международной группы груди 03-05. Дж Клин Онкол 27: 1999–2006 [PubMed] [Google Scholar]
- Ямаути Х., Онейл А., Гельман Р., Карни В., Тенни Д.Ю., Хош С., Хейс Д.Ф. (1997) Прогнозирование ответа на терапию антиэстрогенами у пациентов с распространенным раком молочной железы путем предварительной обработки циркулирующих уровней внеклеточного домена белка HER-2 / c-neu.Дж Клин Онкол 15: 2518–2525 [PubMed] [Google Scholar]
Типы рака молочной железы: тройной отрицательный, ER-положительный, HER2-положительный
Рак молочной железы, положительный по рецепторам гормонов
Около 80% всех случаев рака молочной железы являются «ER -положительно ». Это означает, что раковые клетки растут в ответ на гормон эстроген. Около 65% из них также являются «PR-позитивными». Они растут в ответ на другой гормон — прогестерон.
Если ваш рак груди имеет значительное количество рецепторов либо к эстрогену, либо к прогестерону, он считается положительным по рецепторам гормонов.
Опухоли, которые являются ER / PR-положительными, с гораздо большей вероятностью будут реагировать на гормональную терапию, чем опухоли, которые являются ER / PR-отрицательными.
Возможно, вам назначат гормональную терапию после операции, химиотерапии и лучевой терапии. Эти методы лечения могут помочь предотвратить возвращение болезни, блокируя действие эстрогена. Они делают это одним из нескольких способов.
Узнайте больше о гормональной терапии рака груди.
HER2-положительный рак молочной железы
Примерно в 20% случаев рака молочной железы клетки вырабатывают слишком много белка, известного как HER2.Эти виды рака имеют тенденцию быть агрессивными и быстрорастущими.
Было показано, что для женщин с HER2-положительным раком молочной железы целевой препарат трастузумаб (Герцептин) значительно снижает риск рецидива рака. Стандартным лечением является введение этого лекарства вместе с химиотерапией после операции людям с раком груди, который распространился на другие области. Его также можно использовать при раке груди на ранней стадии. Но есть небольшой, но реальный риск повреждения сердца и возможного повреждения легких.
Существует несколько других таргетных методов лечения, которые иногда используются при лечении HER2-положительного рака груди. К ним относятся:
Подробнее о причинах, симптомах и лечении HER2-положительного рака груди.
Тройной отрицательный рак молочной железы
Некоторые виды рака молочной железы — от 10% до 20% — известны как «тройно-отрицательные», потому что они не имеют рецепторов эстрогена и прогестерона и не сверхэкспрессируют белок HER2. Многие виды рака груди, связанные с геном BRCA1, являются тройными отрицательными.Их часто лечат хирургическим вмешательством, химиотерапией и лучевой терапией.
- Олапариб (Линпарза) и талазопариб (Талзенна) являются лекарственными средствами для таргетной терапии, которые могут использоваться для лечения женщин с мутацией BRCA, у которых есть метастатический HER2-отрицательный рак молочной железы. Эти препараты блокируют белок, называемый PARP.
- Атезолизумаб (Тецентрик) — это иммунотерапевтический препарат, который используется в комбинации с химиотерапевтическим наб-паклитакселом (Абраксан) для блокирования белка PD-L1 при некоторых формах рака молочной железы, которые имеют тройной отрицательный результат.
Получите обзор симптомов и методов лечения тройного отрицательного рака груди.
Границы | Прогноз рака молочной железы с положительным рецептором гормона, стратифицированный по статусу HER2
Введение
Рак молочной железы — это гетерогенное злокачественное новообразование, которое можно разделить на несколько молекулярных подтипов в зависимости от рецептора эстрогена (ER), рецептора прогестерона (PR) и эпидермального рака человека. фактор роста 2 (HER2). ER и PR называются рецепторами гормонов (HR). Четыре основных молекулярных подтипа — это просвет A, просвет B, HER2 + и тройной отрицательный рак молочной железы.Эта классификация обеспечивает хороший биомаркер прогноза и основу для таргетной терапии.
Отдельные подтипы ER + и PR + составляли около 10% всех молекулярных подтипов рака молочной железы (1). Некоторые исследования показали, что не было различий в прогнозе между пациентами ER + PR- и ER-PR + (2, 3). Другие обнаружили, что пациенты с ER-PR + имели худший прогноз по сравнению со случаями ER + PR- (1, 4). Исследования Национальной базы данных по раку и программы эпиднадзора, эпидемиологии и конечных результатов (SEER) показали тот же вывод, что одиночные опухоли HR + имели худший прогноз, чем опухоли ER + PR +, а подтип ER-PR + имел аналогичный прогноз относительно ER-PR- (5, 6).Однако статус HER2, важный предиктор прогноза рака молочной железы, не был включен для анализа в эти исследования. Недавно одноцентровое исследование показало, что клинико-патологические характеристики и прогноз были схожими между ER + PR +, ER-PR + и ER + PR- у пациентов с HER2 + (7). Из-за ограниченного размера выборки отдельных случаев HR + и дисбаланса между группами они получили бессмысленный и широкий доверительный интервал, что может снизить надежность результатов (7). Насколько нам известно, исследования прогнозов одиночных ER + и PR +, стратифицированных статусом HER2, очень ограничены.
Для того, чтобы лучше различать и лечить пациентов с одиночным HR +, мы сравнили прогноз между одиночными ER + и PR + опухолями и сравнили их с другими молекулярными подтипами, стратифицированными по статусу HER2. В отличие от предыдущих исследований, мы впервые сбалансировали переменные между группами, используя сопоставление оценок предрасположенности (PSM), и мы обнаружили некоторые новые результаты прогноза единичных опухолей HR + после введения HER2.
Пациенты и методы
Заявление об этике
Исследуемая популяция была получена из базы данных SEER с 2010 по 2016 год (имя пользователя SEERStat: 10561-ноябрь 2019).Это исследование было освобождено от утверждения институциональным наблюдательным советом в отношении его деидентифицированной информации в общедоступной базе данных.
Исследуемая популяция
Статус ER и PR определяли иммуногистохимическим методом. Если 1% или более клеток окрашиваются положительно, результаты теста считаются положительными. Статус HER2 был доступен с 2010 года в базе данных SEER, поэтому мы включаем пациентов с 2010 года. Из базы данных были извлечены следующие клинико-патологические характеристики: возраст пациента, год постановки диагноза, раса, семейное положение, страховка, типы патологии, степень опухоли, стадия опухоли, Стадия T / N / M, количество метастатических подмышечных лимфатических узлов, операция, лучевая терапия, химиотерапия, общая выживаемость (OS), выживаемость при раке молочной железы (BCSS) и месяцы выживаемости.Семейное положение включает холост, женат, разведен / проживает отдельно / вдовец (DSW) и др. Патология была разделена на инвазивную протоковую карциному, инвазивную лобулярную карциному и инвазивную протоковую и лобулярную карциному. Плохо дифференцированная и анапластическая гистология была определена как III степень. Стадия опухоли и стадия T / N / M была основана на стадии 6-го издания Американского объединенного комитета по раку (AJCC). Хирургия была разделена на частичную мастэктомию, полную мастэктомию и модифицированную радикальную мастэктомию.В исследование были включены только пациенты женского пола с одной первичной опухолью, положительной гистологией и возрастом ≥ 18 лет. Данные с неизвестной информацией были исключены.
Статистический анализ
Переменные категории были проанализированы с помощью критерия χ 2 . Возраст и год постановки диагноза анализировались с помощью теста Манна – Уитни U . Количество метастатических подмышечных лимфатических узлов сравнивали с помощью теста Стьюдента t . ОВ определялась как время от даты постановки первоначального диагноза до смерти от любых причин или последнего наблюдения.BCSS был определен как время от постановки диагноза до смерти от рака груди. Кривые Каплана – Мейера OS и BCSS были проанализированы с помощью лог-рангового критерия. Для оценки отношения рисков (HR) и 95% доверительного интервала (CI) для OS и BCSS была установлена многовариантная регрессия пропорциональных рисков Кокса.
Чтобы минимизировать дисбаланс переменных между группами, PSM выполняли с использованием программного обеспечения R (версия 3.3.3, https://www.r-project.org/) пакета MatchIt. Возраст, год постановки диагноза, раса, семейное положение, страховка, гистология, степень, стадия опухоли, стадия T / N / M, метастатические подмышечные лимфатические узлы, хирургическое вмешательство, лучевая терапия и химиотерапия были сопоставлены между группами.Соответствие один-к-одному с толщиной 0,1 использовалось для уравновешивания демографических, патологических и лечебных переменных, как описано ранее (8). Другие статистические анализы были выполнены с помощью Stata / MP (версия 14.2, StataCorp., College Station, TX) и GraphPad Prism (версия 7.0, GraphPad Software, Inc). Двустороннее значение P <0,05 считалось статистически разным.
Результаты
Клинико-патологические характеристики исследуемой популяции
Блок-схема процесса отбора показана на дополнительном рисунке 1.Всего было включено 203406 пациентов, в том числе 133662 пациента (65,7%) для ER + PR + HER2-, 16906 (8,3%) для ER + PR-HER2-, 1395 (0,7%) для ER-PR + HER2-, 21439 (10,5%) для ER-PR-HER2-; и 15646 (7,7%) для ER + PR + HER2 +, 5381 (2,6%) для ER + PR-HER2 +, 537 (0,3%) для ER-PR + HER2 + и 8440 (4,1%) для ER-PR-HER2 +. Средняя продолжительность наблюдения в исследуемой популяции составила 35 месяцев (диапазон: 1-83 месяца). Клинико-патологические характеристики каждого подтипа обобщены в таблице 1.
Таблица 1 Клинико-патологические характеристики исследуемой популяции ( n = 203 406).
Предикторы для ОС и BCSS с помощью многомерного регрессионного анализа Кокса
По сравнению с ER + PR + HER2-, пациенты с ER + PR-HER2-, ER-PR + HER2- и ER-PR-HER2- были связаны с скомпрометированным ОС с ЧСС (95% ДИ) 1,67 (1,58–1,77), 2,36 (2,02–2,75) и 2,72 (2,59–2,87), соответственно. Кроме того, ER + PR-HER2 + и ER-PR-HER2 + были связаны с нарушенной ОС по сравнению с ER + PR + HER2- с HR (95% ДИ) 1,20 (1,09–1,34) и 1,27 (1,17–1,38), соответственно. . Однако пациенты с ER + PR + HER2 + показали немного лучшую OS, чем пациенты с ER + PR + HER2-с HR (95% CI) 0.93 (0,86-1,01). Между пациентами с ER + PR + HER2- и ER-PR + HER2 + существенной разницы в OS не наблюдалось (таблица 2). BCSS показал ту же тенденцию, что и ОС. Кроме того, пациенты с ER + PR + HER2 + показали улучшенный BCSS по сравнению с ER + PR + HER2- случаями с HR (95% ДИ) 0,89 (0,80-0,99) (дополнительная таблица 1).
Таблица 2 Общая выживаемость по многомерному пропорциональному анализу Кокса.
Кривые Каплана – Мейера ОС и BCSS до PSM
Для подтипа HER2-, ER + PR + имел лучшую ОС по сравнению с ER + PR-, ER-PR + и ER-PR- (логарифмический ранг p <0 .001 для всех). Кроме того, ER + PR- показал лучшую ОС, чем ER-PR + и ER-PR- (лог-ранг p <0,001 для обоих). Кроме того, ER-PR + показал лучшую ОС, чем ER-PR- (лог-ранг p = 0,021) перед PSM (рисунки 1A, B).
Рис. 1 Общая выживаемость пациентов, стратифицированных по статусу рецептора эстрогена (ER), рецептора прогестерона (PR) и рецептора 2 эпидермального фактора роста человека (HER2) до сопоставления оценок предрасположенности. (A) Кривые выживаемости Каплана-Мейера для общей выживаемости. (B) Рейтинговая таблица сравнения по лог-ранговому тесту.
Для подгруппы HER2 + ER + PR + показал лучшую ОС, чем ER + PR- и ER-PR- (логарифмический ранг p <0,001 для обоих), в то время как ER + PR + имел аналогичную OS относительно ER-PR + (log- ранг р = 0,085). Кроме того, ER + PR- показал лучшую ОС, чем ER-PR- (лог-ранг p = 0,024). Однако не наблюдалось существенной разницы в OS между ER + PR- и ER-PR + (лог-ранг p = 0,370). Более того, ER-PR + показал аналогичную ОС по сравнению с ER-PR- (log-rank p = 0.082) (Рисунки 1A, B). BCSS показал ту же тенденцию, что и ОС. Кроме того, пациенты ER-PR + показали лучший BCSS, чем пациенты ER-PR- до PSM (логарифмический ранг p = 0,045) (дополнительный рисунок 2).
Кривые Каплана – Мейера OS и BCSS после PSM
Для минимизации дисбаланса исходных клинико-патологических характеристик между группами выполняли PSM. Абсолютные значения стандартизованных различий согласованных переменных были <0,1, что указывает на то, что переменные были хорошо сбалансированы между группами после сопоставления.Кроме того, статистические различия в исходных характеристиках между группами были уменьшены после PSM.
Для подгруппы HER2- не было различий в OS между ER-PR + и ER-PR- с HR (95% ДИ) 0,95 (0,77-1,18) в подобранной когорте из 1395 парных случаев (рисунок 2A и дополнительная таблица. 2). Однако ER + PR- показал лучшую OS, чем ER-PR- с HR (95% ДИ) 1,44 (1,31–1,55) в подобранной когорте из 9626 парных случаев (рисунок 2B и дополнительная таблица 3). Пациенты с ER + PR- показали лучшую OS, чем пациенты с ER-PR + ( n = 1394 пары) с HR (95% CI) 1.32 (1.06-1.65) (рисунок 2C и дополнительная таблица 4). ER + PR + показал лучшую ОС, чем ER + PR- с HR (95% ДИ) 1,52 (1,41-1,64) ( n = 16906 пар) (рисунок 2D; дополнительная таблица 5), и лучшую OS, чем ER-PR + ( n = 1395 пар) с HR (95% ДИ) 2,25 (1,76–2,88) (рисунок 2E и дополнительная таблица 6). Мы также обнаружили, что не было никакой разницы в OS между ER + PR + HER2 + и ER + PR + HER2 — с HR (95% CI) 0,99 (0,89-1,09) ( n = 15640 пар) (рисунок 2F и дополнительные Таблица 7).BCSS показал ту же тенденцию, что и ОС. Однако пациенты с ER + PR + HER2 + предсказывали BCSS лучше, чем пациенты с ER + PR + HER2- с HR (95% ДИ) 0,86 (0,76-0,98) (дополнительный рисунок 3).
Рис. 2 Кривые Каплана – Мейера общей выживаемости после сопоставления оценок предрасположенности в подгруппе HER2-. (A) Сравнение ER-PR + и ER-PR-. (B) Сравнение ER + PR- и ER-PR-. (C) Сравнение ER-PR + и ER + PR-. (D) Сравнение между ER + PR + и ER + PR-. (E) Сравнение ER + PR + и ER-PR +. (F) Сравнение между ER + PR + HER2- и ER + PR + HER2 +. ER, рецептор эстрогена; PR, рецептор прогестерона; HER2, рецептор 2 эпидермального фактора роста человека
Для подгруппы HER2 + пациенты с ER-PR- показали аналогичную OS по сравнению с ER-PR + ( n = 536 пар) (Рисунок 3A и дополнительная таблица 8) и ER + PR — ( n = 4984 пары) (рисунок 3B и дополнительная таблица 9). ER + PR + показал лучшую OS, чем ER-PR- с HR (95% CI), равным 1.37 (1,22–1,44) ( n = 8143 пары) (рисунок 3C и дополнительная таблица 10). Никаких значительных различий в OS не наблюдалось между пациентами с ER + PR + и ER-PR + ( n = 535 пар) (рисунок 3D и дополнительная таблица 11). Пациенты с ER + PR + имели лучшую OS, чем пациенты с ER + PR- с HR (95% ДИ) 1,26 (1,09–1,45) ( n = 5376 пар) (рисунок 3E и дополнительная таблица 12). Не было существенной разницы в OS между пациентами с ER + PR- и ER-PR + с HR (95% CI), равным 1.10 (0,68–1,80) ( n = 537 пар) (рисунок 3F и дополнительная таблица 13). BCSS показал ту же тенденцию, что и OS (дополнительный рисунок 4).
Рисунок 3 Кривые Каплана – Мейера общей выживаемости в подгруппе HER2 + после сопоставления показателей склонности. (A) Сравнение ER-PR + и ER-PR-. (B) Сравнение ER + PR- и ER-PR-. (C) Сравнение ER-PR- и ER + PR +. (D) Сравнение ER + PR + и ER-PR +. (E) Сравнение между ER + PR + и ER + PR-. (F) Сравнение ER + PR- и ER-PR +. ER, рецептор эстрогена; PR, рецептор прогестерона; HER2, рецептор 2 эпидермального фактора роста человека
Обсуждение
В этом исследовании мы обнаружили, что одиночный HR + показал различное влияние на прогноз опухолей молочной железы HER2- и HER2 +. ER + PR- имел лучший прогноз, чем ER-PR + в случаях HER2-. Однако ER + PR- показал аналогичный прогноз по сравнению с ER-PR + в случаях HER2 +. Кроме того, в случаях ER + PR- и ER-PR + общая смертность была выше, чем у пациентов с ER + PR + подтипом HER2-.Для подтипа HER2 + ER-PR + показал аналогичный прогноз по сравнению с ER + PR +. Пациенты с ER + PR + HER2 + имели аналогичную OS и лучший BCSS по сравнению с пациентами с ER + PR + HER2-.
Недавнее исследование показало, что ER + PR- и ER-PR + имели сходную выживаемость без признаков заболевания и общую выживаемость по сравнению с ER-PR- в подгруппах как HER2 +, так и HER2- (7). Однако мы обнаружили, что ER + PR- показал лучшую OS и BCSS, чем ER-PR- в подгруппе HER2-. Это несоответствие может быть результатом размера выборки, статистических методов и скорректированных переменных.Кроме того, в этом исследовании не удалось сравнить разницу в выживаемости между ER + PR- и ER-PR + (7). Мы обнаружили, что не было различий в прогнозах между ER + PR- и ER-PR + и ER-PR- после PSM в подгруппе HER2 +. Это указывало на то, что пациенты с одиночным ER + или PR + могут получить ограниченное преимущество выживания от эндокринной терапии при столкновении с HER2 +. Для ограниченного размера выборки они не смогли полностью исследовать различия выживаемости ER + PR + ( n = 518) и ER-PR + ( n = 30) и ER + PR- ( n = 159) в HER2 +. подтип.Мы обнаружили, что пациенты с ER + PR + ( n = 15646) имели аналогичный прогноз относительно пациентов с ER-PR + ( n = 537), но имели лучший прогноз, чем пациенты с ER + PR- ( n = 5381 ) и ER-PR- ( n = 8840) в подтипе HER2 + после PSM.
Клинико-патологические характеристики между ER-PR + HER2 + и ER-PR-HER2 + очень согласовывались. Однако пациенты с ER + PR-HER2 + были старше, имели более низкую степень опухоли и стадию опухоли по сравнению с ER-PR-HER2 +.Казалось, что пациенты с ER-PR + HER2 + с большей вероятностью получат выгоду от эндокринной терапии или HER2-таргетной терапии, чем пациенты с ER + PR-HER2 +. Это указывает на то, что уровни PR могут отражать активность фактора роста в опухоли. Низкая или отсутствующая экспрессия PR в некоторых опухолях указывает на высокую активность HER2. Повышенная передача сигналов фактора роста может снизить способность тамоксифена действовать как антагонист, что приводит к селективной резистентности к модуляторам ER (9).
В отличие от роли ER + PR- в опухолях HER2 +, пациенты с ER + PR- показали лучшие прогнозы по сравнению с пациентами с ER-PR + и ER-PR- в подтипе HER2- после PSM.Мы обнаружили, что ER-PR + HER2- показали аналогичный прогноз по сравнению с ER-PR-HER2-. Кроме того, ER + PR + HER2- показал лучшую ОС и BCSS, чем ER + PR-HER2-. Принимая во внимание различия в выживаемости между ER + PR- и ER-PR- в подтипах HER2 + и HER2-, мы можем предположить, что существовала перекрестная передача сигналов между ER / PR и HER2. Фактор роста может напрямую модулировать активность ER посредством фосфорилирования самого ER или посредством фосфорилирования корегуляторов, он также снижает уровень PR независимо от уровней или активности ER (9).В этом исследовании доля опухолей ER + PR- и ER-PR + составляла 11,9%. Статус ER и PR может измениться во время развития рака груди (10, 11). Следовательно, преобразование из ER + PR + в одиночный ER + или PR + или в ER-PR- может указывать на прогрессирование заболевания.
Доля фенотипа ER-PR + составляет 1,0% от общего числа пациентов в нашем исследовании. В исследовании была проведена повторная оценка 43 из 2432 (1,8%) пациентов, у которых в референс-лаборатории была указана ER-PR +. Однако ни один из случаев не был первоначальной ER-PR + (12). В другом исследовании была проведена переоценка 27 из 9844 (0.3%) пациентов, которым изначально был поставлен диагноз карциномы молочной железы ER-PR +, и 7 пациентов остались ER-PR + (13). Однако другое исследование показало, что карцинома молочной железы ER-PR + существует, хотя и редко (1,1% всех фенотипов), и имеет отчетливые клинико-патологические характеристики (14). Состояние ER-PR + следует тщательно оценивать, чтобы избежать технических артефактов (15).
Вопреки нашему общепринятому мнению, что ER + PR + HER2- предсказывает лучшую выживаемость и низкий риск местного или регионального рецидива (16, 17), мы обнаружили, что пациенты с ER + PR + HER2 + демонстрировали аналогичную ОС и даже лучший BCSS по сравнению с теми, у кого ER + PR + HER2-.Предыдущее исследование показало, что подтип HR + HER2 + испытал лучший BCSS, чем подтипы с HR + HER2- при раке груди IV стадии (16). Введение терапии трастузумабом может способствовать улучшению прогноза пациентов с HER2 +. Трастузумаб плюс адъювантная химиотерапия ассоциировалась со снижением риска смертности на 33% по сравнению с одной химиотерапией при операбельном раке молочной железы HER2 + (18). В исследовании CLEOPATRA двойное ингибирование передачи сигналов HER2 пертузумабом и трастузумабом значительно улучшило ОС по сравнению с одним трастузумабом при метастатическом раке молочной железы HER2 + (медиана ОС: 56.5 месяцев против 40,8 месяца) (19). С развитием ингибиторов HER2 пациенты с ER + PR + HER2 + могут получить лучший прогноз, чем пациенты с ER + PR + HER2-.
Необходимо признать ограничения этого исследования. Во-первых, при ретроспективном дизайне предвзятость отбора была неизбежна. Однако статистические различия в исходных переменных были значительно уменьшены после выполнения PSM, что может повысить надежность результатов. Кроме того, эндокринная терапия и терапия HER2 не были зарегистрированы в базе данных.Поэтому они не были включены в анализ. Кроме того, точные уровни экспрессии ER и PR были недоступны. Мы не можем переоценить единый статус ER + и PR +.
В заключение, это крупнейшее известное исследование, изучающее прогноз рака груди, стратифицированный по статусу ER, PR и HER2. Мы обнаружили, что отдельные подтипы ER + и PR + показали разные роли в прогнозе рака груди в зависимости от статуса HER2. Для подгруппы HER2- наилучший прогноз показали ER + PR +, затем ER + PR- и худший для подтипов ER-PR + и ER-PR-.Для подгруппы HER2 + ER + PR + показал аналогичный прогноз относительно ER-PR +, но лучший прогноз, чем подтипы ER + PR- и ER-PR-. Статус HER2 не уменьшал выживаемость пациентов с ER + PR +. Несмотря на то, что мы строго включили случаи и сбалансировали переменные между группами с большой популяцией, результаты следует осторожно интерпретировать при работе с единичными случаями рака молочной железы ER + или PR +.
Заявление о доступности данных
Исходные материалы, представленные в исследовании, включены в статью / дополнительные материалы.Дальнейшие запросы можно направить соответствующему автору.
Вклад авторов
Гц: концепция, сбор данных. HZ и YG: анализ данных и написание статьи. HZ и YG: критически пересмотрены на предмет важного интеллектуального содержания. HZ: расследование, администрирование проекта и надзор. Все авторы внесли свой вклад в статью и одобрили представленную версию.
Финансирование
Работа поддержана фондами фундаментальных исследований для центральных университетов (грант № 2042020kf0063).
Конфликт интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Дополнительные материалы
Дополнительные материалы к этой статье можно найти в Интернете по адресу: https://www.frontiersin.org/articles/10.3389/fonc.2021.643956/full#supplementary-material
Ссылки
1. Li Y , Ян Д., Инь Х, Чжан Х, Хуанг Дж, Ву И и др.Клинико-патологические характеристики и выживаемость больных раком молочной железы с положительным рецептором одного гормона раком молочной железы. JAMA Netw Open (2020) 3: e1918160. doi: 10.1001 / jamanetworkopen.2019.18160
PubMed Аннотация | CrossRef Полный текст | Google Scholar
2. Ракха Е.А., Эль-Сайед М.Э., Грин А.Р., Пайш Е.С., Пауэ Д.Г., Джи Дж. И др. Биологические и клинические характеристики рака молочной железы с позитивным фенотипом по одному гормональному рецептору. J Clin Oncol (2007) 25: 4772–8.doi: 10.1200 / JCO.2007.12.2747
PubMed Аннотация | CrossRef Полный текст | Google Scholar
3. Шен Т., Брандвайн-Генслер М., Хамид О, Сигал Г.П., Вей С. Характеристика рака груди, отрицательного по рецепторам эстрогена / положительного по рецепторам прогестерона. Хум Патол (2015) 46: 1776–84. doi: 10.1016 / j.humpath.2015.07.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
4. Li Z, Tu Y, Wu Q, Wang Z, Li J, Zhang Y, et al. Клинические характеристики и исходы рака молочной железы, положительного по сравнению с одним и двумя гормональными рецепторами, в 2 больших базах данных. Clin рака груди (2020) 20: e151 – e63. doi: 10.1016 / j.clbc.2019.07.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
5. Дофин С., Моаззез А., Нил Дж. К., Хлебовски Р. Т., Озао-Чой Дж. Рак молочной железы, положительный по одному гормональному рецептору, имеет разные характеристики и выживаемость. Ann Surg Oncol (2020) 27: 4687–94. doi: 10.1245 / s10434-020-08898-5
PubMed Аннотация | CrossRef Полный текст | Google Scholar
6. Lv M, Mao Y, Song Y, Wang Y, Liu X, Wang X и др.Клинические особенности и выживаемость при раке молочной железы с положительным рецептором гормона: популяционное исследование с участием 531 605 пациентов. Clin рака груди (2020) 20: e589 – e99. doi: 10.1016 / j.clbc.2020.04.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
7. Пэ Си, Ким С., Ли Дж. Х., Ли Х. К., Ли С. К., Кил У. и др. Плохой прогноз рака молочной железы с положительным рецептором гормона: результат такой же, как и при тройном отрицательном раке молочной железы. BMC Cancer (2015) 15: 138.doi: 10.1186 / s12885-015-1121-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
8. Чжао Х. Прогноз инвазивной протоковой карциномы, дольчатой карциномы и смешанной протоковой и дольчатой карциномы в соответствии с молекулярными подтипами молочной железы. Рак молочной железы (2020) 28: 187–95. doi: 10.1007 / s12282-020-01146-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
9. Цуй X, Шифф Р., Арпино Дж., Осборн К. К., Ли А. В.. Биология потери рецепторов прогестерона при раке молочной железы и ее значение для эндокринной терапии. J Clin Oncol (2005) 23: 7721–35. doi: 10.1200 / JCO.2005.09.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
10. Фуджи К., Ватанабе Р., Андо Т., Кусака Дж., Моури Ю., Йошида М. и др. Изменения в трех биомаркерах (рецептор эстрогена, рецептор прогестерона и эпидермальный фактор роста человека 2) и индекс Ki67 между первичным и метастатическим поражением рака молочной железы. BioMed Rep (2017) 7: 535–42. doi: 10.3892 / br.2017.1003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
11.Ли MH, Хоу CL, Wang C, Sun AJ. Her-2, ER, PR Соответствие статуса при первичном раке молочной железы и соответствующем метастатическом поражении лимфатического узла у китайских женщин. Pathol Res Pract (2016) 212: 252–7. doi: 10.1016 / j.prp.2015.11.019
PubMed Аннотация | CrossRef Полный текст | Google Scholar
12. Малеки З., Шариат С., Мокри М., Атри М. ER-отрицательный / PR-положительный рак груди или технические артефакты в иммуногистохимии? Arch Iran Med (2012) 15: 366–9. DOI: 012156 / AIM.0010
PubMed Аннотация | Google Scholar
13. Курода Х., Мурои Н., Хаяси М., Харада О, Хоши К., Фукума Э. и др. Фенотип инвазивной карциномы молочной железы в Японии: повторная оценка с использованием иммуногистохимического окрашивания. Рак молочной железы (2019) 26: 249–54. doi: 10.1007 / s12282-018-0898-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
14. Ахмед С.С., Тике А.А., Чжан К., Лим Дж. К., Тан PH. Клинико-патологические характеристики рака молочной железы с отрицательным рецептором эстрогена и положительным по рецептору прогестерона: повторная оценка подмножеств в этой группе. J Clin Pathol (2017) 70: 320–26. doi: 10.1136 / jclinpath-2016-203847
PubMed Аннотация | CrossRef Полный текст | Google Scholar
15. Кунч М., Бирнат В., Сенкус-Конефка Э. Рак молочной железы, отрицательный по рецепторам эстрогена, положительный по рецепторам прогестерона — «ничья земля» или просто артефакт? Лечение рака Ред. (2018) 67: 78–87. doi: 10.1016 / j.ctrv.2018.05.005
PubMed Аннотация | CrossRef Полный текст | Google Scholar
16. Howlader N, Cronin KA, Kurian AW, Andridge R.Различия в выживаемости при раке молочной железы по молекулярным подтипам в США. Эпидемиологические биомаркеры рака. Пред. (2018) 27: 619–26. doi: 10.1158 / 1055-9965.EPI-17-0627
PubMed Реферат | CrossRef Полный текст | Google Scholar
17. Водук К.Д., Ченг М.К., Тилдесли С., Гельмон К., Нильсен Т.О., Кеннеке Х. Подтипы рака груди и риск местного и регионального рецидива. J Clin Oncol (2010) 28: 1684–91. doi: 10.1200 / JCO.2009.24.9284
PubMed Аннотация | CrossRef Полный текст | Google Scholar
18.Romond EH, Perez EA, Bryant J, Suman VJ, Geyer CE Jr., Davidson NE, et al. Трастузумаб плюс адъювантная химиотерапия для оперативного HER2-положительного рака молочной железы. N Engl J Med (2005) 353: 1673–84. doi: 10.1056 / NEJMoa052122
PubMed Аннотация | CrossRef Полный текст | Google Scholar
19. Свейн С.М., Базельга Дж., Ким С.Б., Ро Дж., Семиглазов В., Кампоне М. и др. Пертузумаб, трастузумаб и доцетаксел при HER2-положительном метастатическом раке молочной железы. N Engl J Med (2015) 372: 724–34.doi: 10.1056 / NEJMoa1413513
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Тройной отрицательный рак груди | Johns Hopkins Medicine
Грудь Рак молочной железы БиопсииРекомендуемые эксперты:
Тройной отрицательный рак молочной железы лечить сложно, но во многих случаях лечение помогает. Бонни Сан, доктор медицины, хирург, специализирующийся на лечении рака груди, объясняет тройной отрицательный рак груди, перспективы для пациентов и причины для надежды.
Что нужно знать
- Тройной отрицательный рак груди составляет от 10% до 20% всех случаев рака груди.
- Каждый диагноз рака уникален, но в целом тройной отрицательный рак молочной железы — это более агрессивный тип опухоли с более высокой скоростью роста, более высоким риском метастазирования и риском рецидива.Поэтому часто требуется химиотерапия как часть лечения.
- Хирургия также является важной частью лечения, но если опухоль небольшая и локализованная, мастэктомия может не потребоваться. Химиотерапия может уменьшить тройные отрицательные опухоли груди, и пациенты могут стать кандидатами на менее обширную операцию.
- Трижды отрицательный рак чаще встречается у пациентов с наследственными генетическими мутациями, поэтому следует рассмотреть возможность генетического консультирования и тестирования.
Что означает «тройной отрицательный» с точки зрения рака груди?
Нормальные клетки груди имеют рецепторы, которые реагируют на гормоны, такие как эстроген и прогестерон, что позволяет им расти и регрессировать в ответ на уровень гормонов.Рецепторы гормонов могут присутствовать или не присутствовать при раке груди. Около двух третей случаев рака груди являются «положительными» и содержат эти рецепторы, как и нормальные клетки груди. Это менее агрессивные виды рака, которые с меньшей вероятностью нуждаются в химиотерапии и часто лечатся гормональной терапией и хирургическим вмешательством. Радиация может понадобиться, а может и не потребоваться.
HER2 / neu (рецептор 2 гормона эпидермального фактора роста) представляет собой белковую молекулу, которая играет роль в пролиферации клеток в нормальных клетках. При некоторых формах рака молочной железы этот белок вырабатывается чрезмерно или является «положительным».«Для HER2-положительных опухолей существует специальный препарат, нацеленный на этот белок.
Тройной отрицательный рак молочной железы не является положительным по рецепторам эстрогена, рецепторам прогестерона или белку HER2. «Поскольку эти мишени (рецепторы гормонов и HER2) отсутствуют при тройном отрицательном раке груди, необходима химиотерапия», — говорит Сан. «Тройной отрицательный рак груди часто очень чувствителен к химиотерапии, которая, несмотря на побочные эффекты, является эффективным лечением, которое может спасти жизни. Поскольку это агрессивный рак, лечение также является агрессивным.Но есть несколько способов решить эту проблему ».
Каков риск тройного отрицательного рака груди?
Болезнь может поразить любого, но чаще проявляется у тех, кто:
- Моложе 50 лет (большинство рецепторно-положительных форм рака груди обнаруживаются у людей в возрасте 60 лет и старше).
- Черный или Латинский.
- Жить с генетическим заболеванием, называемым мутацией BRCA, которое увеличивает риск рака груди и других форм рака.Большинство видов рака, диагностированных у людей с мутацией BRCA1, имеют тройной отрицательный результат.
Как лечить тройной отрицательный рак груди?
Химиотерапия. «Химиотерапия требуется почти всегда», — говорит Сан. «Химиотерапия может снизить стадию опухолей (уменьшить их или сделать менее агрессивными)». В то время как Сан говорит, что химиотерапия при тройном отрицательном раке груди может быть интенсивной, она добавляет, что режим может быть адаптирован к индивидууму и адаптирован для пожилых или более слабых пациентов.
«В тех случаях, когда мы получаем полный ответ, мы знаем, что дали вам правильное лекарство, и у вас хороший прогноз», — говорит Сан.
Операция позволяет удалить большую часть опухоли. «Операция по поводу тройного отрицательного рака груди не всегда должна быть мастэктомией», — говорит Сан. «Эффективная химиотерапия, проводимая в первую очередь, открывает возможности для менее инвазивных хирургических вмешательств, которые не являются тяжелым испытанием для пациента. Если после химиотерапии опухоль достаточно мала, возможны амбулаторные процедуры или лампэктомия.”
Хирургические образцы раковых тканей, взятые во время операции, могут предоставить больше информации о раке и его поведении, поэтому химиотерапия может быть адаптирована соответствующим образом.
Лучевая терапия включает использование пучков излучения для уничтожения раковых клеток с использованием различных методов для предотвращения повреждения здоровых окружающих тканей.
Лечебные процедуры проходят клинические испытания на опухолях молочной железы с тройным отрицательным результатом.
- Новые лекарства, называемые ингибиторами поли (АДФ-рибозы) полимеразы или ингибиторами PARP , могут разрушать раковые клетки, и теперь они одобрены FDA для лечения тройного отрицательного рака груди.
- Иммунотерапия помогает вашему организму рассматривать злокачественные клетки как вредных захватчиков, чтобы ваша иммунная система могла бороться с раком. «Хотя иммунотерапия обычно не является лечением первой линии для этого типа рака, она может помочь некоторым пациентам в очень специфических ситуациях», — отмечает Сан.
«Иммунотерапия и ингибиторы PARP очень интересны, и сейчас проводится множество исследований, в том числе здесь, в Johns Hopkins», — говорит Сан.
Каков прогноз при тройном отрицательном раке груди?
Хороший результат лечения зависит от нескольких факторов.«Химиотерапия — это то, что действительно может повлиять на результат. Размер инвазивной части опухоли и количество пораженных лимфатических узлов также могут сильно повлиять на ваш прогноз », — говорит Сан, но добавляет, что если рак распространился (метастазировал), прогноз менее определен.
«Есть надежда даже при таком серьезном диагнозе, и очень важно сохранять оптимизм. Прохождение химиотерапии может быть стрессовым и страшным, но позитивное мышление может иметь значение. Вы должны верить, что это приносит вам пользу, и для большинства людей так и есть.”
Лечение рака груди в Johns Hopkins
Программа по лечению рака груди в Johns Hopkins состоит из разнообразной группы признанных на национальном уровне специалистов по исследованию и лечению рака груди.


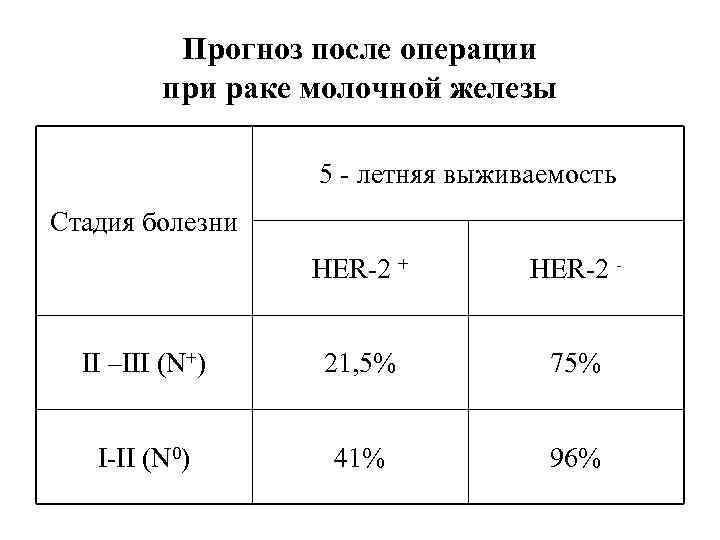 HER2 позитивные опухоли представляют собой отдельную, стремительно прогрессирующую форму болезни, требующую особых и неотложных действий. Поэтому важно определить состояние HER2 по возможности раньше – как только обнаружен рак груди, не дожидаясь рецидива или прогресса опухоли. На наличие HER2 исследуются раковые клетки, полученные любым из методов биопсии. Если врач не провел проверку HER2 по время биопсии, образцы тканей могут быть сохранены и исследованы в любое время.
HER2 позитивные опухоли представляют собой отдельную, стремительно прогрессирующую форму болезни, требующую особых и неотложных действий. Поэтому важно определить состояние HER2 по возможности раньше – как только обнаружен рак груди, не дожидаясь рецидива или прогресса опухоли. На наличие HER2 исследуются раковые клетки, полученные любым из методов биопсии. Если врач не провел проверку HER2 по время биопсии, образцы тканей могут быть сохранены и исследованы в любое время. Опухоль может быть любых размеров. Характерная особенность – метастазы в печени, легких, головном мозге и других органах. Излечиться от патологии полностью практически невозможно, а медицинская помощь направлена на обеспечение качества жизни.
Опухоль может быть любых размеров. Характерная особенность – метастазы в печени, легких, головном мозге и других органах. Излечиться от патологии полностью практически невозможно, а медицинская помощь направлена на обеспечение качества жизни.