Гидроторакс | Клиника «Оберіг»
Гидроторакс – это скопление жидкости между плевральными листками – в плевральной полости. Плевральные листки покрывают легкие и выстилают внутреннюю поверхность грудной клетки. В норме между ними содержится всего несколько миллилитров жидкости, которая выполняет функцию смазки.
Если легкие воспаляются, между плевральными листками скапливается экссудат. Это жидкость, которая выделяется из мелких кровеносных сосудов. В плевральной полости может появиться также транссудат. Он накапливается вследствие нарушения крово- и лимфообращения.
В отличие от экссудата, образование транссудата не связано с воспалительными процессами. Экссудат характерен для другого заболевания – плеврита. В этой статье мы рассмотрим накопление транссудата.
Причины гидроторакса легких могут быть различными. Это сердечная недостаточность, заболевания почек, цирроз печени и портальная гипертензия, тромбоэмболия легочной артерии и др.
Гидроторакс также сопровождает онкологические заболевания.
СИМПТОМЫ И ПРИЗНАКИ ГИДРОТОРАКСА
Симптомы гидроторакса вызываются сдавливанием легких скопившейся жидкостью. Пациентов беспокоит чувство тяжести, давления в груди, сухой кашель, одышка. Если в плевральной полости накапливается большое количество транссудата, затрудняется отток крови из шейных вен. Тогда становится заметным их набухание.
Классификация гидроторакса основывается на объеме и расположении жидкости. Выделяют малый и большой, правосторонний и левосторонний, тотальный и осумкованный гидроторакс. В большинстве случаев гидроторакс охватывает обе плевральные полости, а при метастатическом его характере чаще наблюдается одностороннее поражение.
ДИАГНОСТИКА ГИДРОТОРАКСА
Проводится рентгенологическое обследование органов грудной клетки, которое позволяет выявить наличие жидкости в плевральной полости. При подозрении на опухолевый гидроторакс показана компьютерная томография для выявления метастазов в органах грудной клетки.
При подозрении на опухолевый гидроторакс показана компьютерная томография для выявления метастазов в органах грудной клетки.
Окончательный диагноз при гидротораксе можно поставить только после лабораторного исследования жидкости в плевральной полости. Для ее забора проводится плевральная пункция. Жидкость отсасывается через небольшой прокол в грудной клетке. Лабораторный анализ показывает, является он экссудатом или транссудатом.
Тем не менее, в ряде случаев путем лабораторного анализа жидкости не удается установить причину развития гидроторакса, и для окончательной установки диагноза может быть рекомендована видеоторакоскопия. Этот эндоскопический метод позволяет осмотреть плевральную полость и произвести биопсию подозрительного участка.
ЛЕЧЕНИЕ ГИДРОТОРАКСА
Небольшой гидроторакс не требует специального лечения. Жидкость рассасывается самостоятельно при успешной терапии основного заболевания.
При значительном накоплении транссудата плевральная пункция используется в качестве не только диагностического, но и лечебного метода. Полное удаление жидкости называется плевроцентезом. Процедура проводится в условиях операционной торакальным хирургом под местной анестезией.
Полное удаление жидкости называется плевроцентезом. Процедура проводится в условиях операционной торакальным хирургом под местной анестезией.
Лечение гидроторакса легких с помощью плевроцентеза улучшает состояние пациента, уменьшает одышку и неприятные ощущения. Но поскольку гидроторакс – вторичное заболевание, последующее лечение должно быть направлено на причину его развития.
При персистирующем гидротораксе, в особенности – метастатического характера, может быть выполнен видеоторакоскопический плевродез. Хирург под контролем эндовидеокамеры вводит в плевральную полость различные агенты, чаще химические (тальковый плевродез). Процедура вызывает спаечный процесс между листками плевры, который препятствует дальнейшему накоплению жидкости.
В Торакопульмонологическом центре Универсальной клиники «Оберіг» имеется все необходимое для диагностики и лечения гидроторакса. Плевральная пункция, а также видеоторакоскопия, осуществляется с помощью современного высокотехнологичного оборудования.
В Универсальной клинике «Оберіг» работает собственный патогистологический центр, в котором проводится исследование плевральной жидкости. Точная диагностика причины гидроторакса – основа правильной стратегии лечения пациента.
Запишитесь на прием к специалистам Торакопульмонологического центра, позвонив по телефону:
(044) 521 30 03
Гидроторакс. Клиническая картина и диагностика гидроторакса!
1.Что такое гидроторакс
Так называемая «плевральная полость», расположенная между париетальными и висцеральными листками плевры лёгких, в норме содержит некоторый объём жидкости. Данная анатомическая особенность обеспечивает скольжение плевральных листков относительно друг друга в процессе дыхания. Объём этой жидкости не должен превышать 1-2 мл, однако в некоторых случаях происходит избыточное накопление транссудата в плевральной полости.
В отличие от экссудата, содержащего в своём составе значительное количество белков (до 30%) и ферментов, транссудат является более водянистой жидкостью. Он чаще всего прозрачен, почти не содержит свойственных плазме ферментов, а белка в нём обнаруживается не более 3%.
Накопление жидкости в плевральной полости в подавляющем большинстве случаев развивается как осложнением других заболеваний. Гидроторакс неясной этиологии – редкое явление, относимое, скорее, к погрешностям диагностики.
Хотя гидроторакс локализуется в лёгких, он чаще всего имеет симптоматику сердечнососудистых нарушений. Проблемы с дыханием самим больным ощущаются реже. Накопление жидкости происходит постепенно. На протяжении значительного периода жидкость пропотевает через сосудистые стенки капиллярной сети и наполняет плевральную полость.
Обязательно для ознакомления!
Помощь в госпитализации и лечении!
2.
 Причины гидроторакса
Причины гидротораксаЭтиопатогенетической причиной гидроторакса чаще всего выступает хроническая сердечнососудистая недостаточность, для которой характерны застойные явления в тканях и органах всего организма. К примеру, перикардит и серьёзные пороки сердца в большинстве случаев сопровождаются нарушениями, связанными с задержкой жидкости и капиллярной недостаточностью.
Одной из распространённых причин также являются заболевания почек. Нарушения в чашечно-лоханочном аппарате мочевыделительной системы приводят к гиперпротеинемии. Развивающаяся почечная недостаточность приводит к двустороннему гидротораксу при амилоидозе и на фоне нефротического синдрома.
Правосторонний гидроторакс характерен при циррозе печени. У 10 пациентов их ста, имеющих этот диагноз, жидкость из брюшины проникает в правую часть плевральной полости лёгких вследствие изменений, затрагивающих ткани диафрагмы в области печени.
Опухолевые заболевания органов средостения в ряде случаев также сопровождаются накоплением транссудата в лёгких.
Запись на консультацию
Посетите нашу страницу
Пульмонология
3.Клиническая картина и диагностика гидроторакса
Гидроторакс часто сочетается с признаками накопления жидкости в подкожно-жировой клетчатке и других полостях тела (перикардиальной, брюшной).
Транссудат в объёме 100-150 мл при малом гидротораксе не имеет выраженной клинической картины. Компрессия органов грудной клетки начинает проявляться лишь при большом скоплении лимфы в плевральной полости. Дебют этого состояния обычно не острый – симптоматика усугубляется постепенно.
Прогрессирующее течение гидроторакса характеризуется следующими нарастающими симптомами:
- одышка;
- тяжесть в области диафрагмы;
- неудовлетворённость вдохом и другие проявления затруднённого дыхания.

В дифференциальной диагностике гидроторакса важно исключить пневмоторакс, признаками которого является выраженный болевой синдром и проявления воспалительного характера (повышение температуры, общее недомогание, слабость).
Визуальный осмотр может выявить акроцианоз кожных покровов (синюшность кожи) со стороны скопления транссудата. Больной, как правило, стремится принять вынужденную полусидячую позу. Осмотр проводится путём пальпации, перкуссии границ сердца и лёгочного звука. Также прибегают к их аускультации (анализу звуков сердечной деятельности и дыхания).
Для уточнения диагноза могут быть назначены следующие диагностические мероприятия:
- компьютерная томография;
- рентгеноскопия;
- ультразвуковая диагностика;
- плевральная пункция с целью последующего микробиологического и цитологического исследования.
Также показан общий и биохимический анализ крови и проведение пробы Ривальта, которая при наличии гидроторакса даёт отрицательный результат.
Запись на консультацию
О нашей клинике
м. Чистые пруды
Страница Мединтерком!
4.Лечение гидроторакса
Лечение гидроторакса, исходя из того, что данная патология не является самостоятельной нозологической единицей, заключается в устранении первопричин, спровоцировавших скопление жидкости.
Если этиопатогенетически гидроторакс связан с сердечнососудистой недостаточностью, комплексная терапия включает не только препараты, поддерживающие работу сердца, но и сочетается с мерами, направленными на коррекцию образа жизни больного. Рекомендуется внести изменения в режим труда и отдыха, сон, диету, физическую активность. Для вывода жидкости необходимо ограничить приём поваренной соли. Из лекарственных препаратов могут быть назначены:
- гликозиды;
- ингибиторы фосфодиэстеразы;
- диуретики;
- ингибиторы АПФ;
- периферические вазодилататоры.

При связи гидроторакса с почечной недостаточностью отёчно-нефрофитовый синдром требует постельного режима, полного исключения соли в питании, контроля диуреза. Лечебная тактика опирается на результаты диагностики – препараты назначаются в зависимости от первопричин и динамики заболевания почек.
Оперативная помощь может потребоваться при неэффективности консервативного лечения, а также в случаях развития острых дыхательных расстройств и сердечнососудистой недостаточности.
Запись на консультацию
Правосторонний и левосторонний гидроторакс | Запись на приём к онкологу
Правосторонний и левосторонний гидроторакс Заболевания органов грудной клетки могут нарушать дыхательную функцию легких. Так, тотальный гидроторакс характеризуется скоплением большого количества жидкости в плевральной полости, что приводит к гипоксии и другим нарушениям. Это может быть самостоятельное заболевание или осложнение других патологических состояний.
Правосторонний гидроторакс – это патологическое состояние, при котором в плевральной полости скапливается жидкость невоспалительного происхождения. Отечность плевры становится причиной нарушения дыхания, гипоксии и других осложнений. Обычно заболевание возникает при метаболических нарушениях и злокачественных новообразованиях грудной клетки, однако в редких случаях диагностируется идиопатическая форма гидроторакса.
Иногда правосторонний гидроторакс относят к разновидностям плеврального выпота. В сущности, проявления этой болезни схожи со скоплением крови в плевральной полости (гемотораксом), экссудативным воспалением плевры и нарушением лимфатического оттока в средостении. Основная разница связана с происхождением патологии: при гидротораксе в плевральной полости скапливается транссудат, не связанный с воспалением или инфекцией.
Левосторонний или правосторонний гидроторакс часто диагностируется вместе с другими проявлениями заболеваний сердца, почек и печени. Помимо скопления жидкости в плевре у пациентов обнаруживают отеки нижних конечностей, асцит и симптомы органной недостаточности. При этом первопричина отека плевральной полости может быть гораздо более опасной, чем сам гидроторакс.
8 (495) 320-19-03
Круглосуточно без выходных
Анатомические особенностиПлевра является своеобразным соединительнотканным «мешком», изолирующим легкие от других органов грудной клетки. При этом париетальный слой плевры выстилает внутреннюю поверхность грудной клетки, а висцеральная плевра плотно прилегает к легочной ткани, бронхам и связанным с ним сосудам. Пространство между двумя листками плевры называют плевральной полостью. В норме эта полость содержит небольшое количество серозной жидкости, облегчающей трение легких во время дыхания.
Основные функции плевры:
- Поддержание герметичности плевральной полости, что является необходимым условием работы легких.
 Благодаря низкому давлению в плевральной полости легкие расправляются во время вдоха.
Благодаря низкому давлению в плевральной полости легкие расправляются во время вдоха. - Защита легочной ткани от трения.
- Выделение серозной жидкости.
В плевральной полости поддерживается постоянный объем жидкости, примерно равный 10 миллилитрам. Такого количества серозной жидкости достаточно для уменьшения трения и защиты легких. Внутренний механизм обратного оттока предотвращает скопление большого объема жидкости. Тем не менее при патологических состояниях возможно возникновение отека плевральной полости. Чем больше скапливается жидкости, тем сильнее нарушение функций легких.
Правосторонний гидроторакс встречается реже двухстороннего отека плевральной полости, поскольку основные причины заболевания связаны с расстройством функций сердца, почек или печени. В редких случаях также диагностируют левосторонний гидроторакс, который может возникать из-за травмы или онкологического процесса в левом легком.
Причины возникновения Невоспалительное происхождение жидкости исключает плеврит и другие воспалительные процессы, однако без данных лабораторной диагностики врачи ориентируются на симптоматику пациента. При гидротораксе у больных обычно обнаруживают признаки заболеваний сердца, легких, печени и почек.
При гидротораксе у больных обычно обнаруживают признаки заболеваний сердца, легких, печени и почек.
Основные причины и факторы риска:
- Почечная недостаточность или другое заболевание органа, при котором с мочой выделяется белок. Постепенное развитие гипоальбуминемии нарушает ток крови и обуславливает отек тканей. Такой же механизм возникает и при алиментарной дистрофии.
- Застойная сердечная недостаточность. При этом неэффективная работа сердца становится причиной депонирования крови в венозном звене. Из-за увеличения гидростатического давления крови возникает правосторонний гидроторакс.
- Нарушение оттока лимфы от органов грудной клетки.
- Отек брюшной полости (асцит), сопровождающийся резким увеличением внутрибрюшного давления. Через диафрагму жидкость из брюшной полости может перемещаться в плевру.
- Заболевания печени, при которых возникает нарушение функций органа. Недостаток белка альбумина в крови является распространенным осложнением цирроза печени.
 Дальнейший механизм развития отека плевральной полости схож с заболеваниями почек.
Дальнейший механизм развития отека плевральной полости схож с заболеваниями почек. - Осложнения злокачественных новообразований органов средостения.
- Закупорка легочной артерии – патологическое состояние, сопровождающееся гемодинамическими нарушениями.
Точное определение причины отека плевральной полости важно для назначения лечения.
СимптомыЛевосторонний или правосторонний гидроторакс может характеризоваться разными симптомами. От плеврита, при котором в плевральной полости также скапливается жидкость, заболевание отличается отсутствием инфекционного или воспалительного процесса. Выраженность симптомов зависит от объема жидкость. Незначительный отек (до 200 мл) может протекать в бессимптомной форме.
8 (495) 320-19-03
Круглосуточно без выходных
Возможные признаки заболевания:
- Прогрессирующая одышка, возникающая при постепенном скоплении жидкости в плевре.
- Боль во время вдоха.

- Поверхностное дыхание, обусловленное давлением в плевральной полости.
- Бледность кожных покровов.
- Головокружение.
Некоторые пациенты не сразу обращают внимание на признаки заболевания из-за наличия других патология легких, вызывающих дыхательную недостаточность.
Способы диагностикиПри обнаружении симптомов гидроторакса необходимо обратиться к врачу общей практики или пульмонологу. Во время приема врач спросит пациента о жалобах, изучит анамнестические данные и проведет физическое обследование. Часто гидроторакс слева или справа обнаруживается во время обследования пациентов с заболеваниями сердечно-сосудистой системы и почек, обратившихся к врачу из-за ухудшения симптомов. При аускультации (прослушивании) легких выявляются необычные шумы. Для постановки окончательного диагноза требуются данные инструментальной и лабораторной диагностики.
Специальные методы обследования:
- Плевральная пункция – основной метод обследования.
 Врач удаляет жидкость из плевры для проведения лабораторной диагностики. Для гидроторакса характерно отсутствие признаков инфекции или воспаления в образце.
Врач удаляет жидкость из плевры для проведения лабораторной диагностики. Для гидроторакса характерно отсутствие признаков инфекции или воспаления в образце. - Анализ крови для оценки функции почек, сердца и печени.
- Электрокардиография – исследование электрической активности сердца. Для проведения этого теста врач помещает специальные электроды на тела пациента. Результаты ЭКГ могут указать на первопричину отека плевры.
- Эхокардиография – ультразвуковое обследование сердца. Во время обследования врач может наблюдать работу сердца на мониторе. Эхокардиография также назначается для поиска первичных заболеваний сердца.
- Рентгенография грудной клетки – метод первичной диагностики, с помощью которого выявляют скопление жидкости в плевральной полости.
- Компьютерная и магнитно-резонансная томография – высокоточные методы сканирования, необходимые для диагностики первичных заболеваний органов грудной клетки.
- Эндоскопическое исследование органов грудной клетки для обнаружения причин гидроторакса.

- Биопсия плевры и легочной ткани с последующим гистологическим изучением тканевого образца. С помощью биопсии диагностируют онкологические заболевания, нарушающие отток лимфы в грудной клетке.
Врачам не нужно назначать все перечисленные процедуры, однако для постановки точного диагноза важно получить снимки и провести лабораторное исследование жидкости.
ЛечениеОсновной целью является лечение первичного заболевания, ставшего причиной отека плевральной полости. При тяжелых заболеваниях сердца, почек и печени может потребоваться трансплантация, однако в большинстве случаев медикаментозного лечения достаточно для устранения осложнений.
Основным методом облегчения симптомов гидроторакса является плевроцентез или пункция плевральной полости. Эта процедура проводится не только для диагностики, но и для облегчения дыхания у пациентов с тяжелым отеком плевральной полости.
Этапы проведения пункции:
- Получение данных рентгенодиагностики для определения места прокола.

- Обработка кожи в месте прокола антисептическим средством.
- Обезболивание тканей местным анестетиком (новокаин, лидокаин или другое средство).
- Введение иглы в межреберную область по лопаточной или задней подмышечной линии. Проникновение в плевральную полость сопровождается появлением пузырьков в шприце.
- Медленное удаление жидкости. Слишком быстрое проведение пункции может спровоцировать дыхательную недостаточность или расстройство деятельности сердца.
- Удаление иглы и повторная обработка места прокола антисептиком.
- Накладывание стерильной повязки.
Пункция может быть проведена при экстренном или плановом лечении. Как правило, такая процедура полностью избавляет пациента от симптомов болезни.
Таким образом, левый или правый гидроторакс может возникать как осложнение онкологических и функциональных заболеваний. Важно вовремя обратиться к пульмонологу при возникновении симптомов этой патологии.
8 (495) 320-19-03
Круглосуточно без выходных
Recurrent hepatic hydrothorax in a patient with liver cirrhosis.
 Рецидивирующий печеночный гидроторакc у больного циррозом печени
Рецидивирующий печеночный гидроторакc у больного циррозом печениНАБЛЮДЕНИЕ ИЗ ПРАКТИКИ
Клиническая гепатология, 2009, 4 33
эмфиземой, развитием гнойного плеврита [2,3]. Необ-
ходимость проведения частых торакоцентезов (на-
пример, каждые 2 недели) обусловливает поиск
альтернативных методов лечения, в частности, тран-
съюгулярного порто-системного шунтирования
(ТИПШ), которое позволяет предотвратить рецидив
гидроторакса у 60-80% больных [13,14]. У нашего
больного имелся ряд неблагоприятных факторов про-
гноза при ТИПШ (табл. 3), поэтому от данного метода
лечения решено воздержаться.
Имеются сообщения об эффективном использова-
нии неинвазивной вентиляции легких с постоянно по-
вышенным давлением в дыхательных путях с помощью
назальной маски во время сна (метод приводит к повы-
шению внутригрудного давления и уменьшению по-
ступления жидкости из брюшной полости в грудную
клетку через диафрагмальные дефекты). Однако для
Однако для
широкого внедрения данного метода в клиническую
практику необходимы дальнейшие исследования [15].
В последние годы появились сообщения о возмож-
ности локализации дефектов диафрагмы во время
торакоскопии с последующим закрытием их посредст-
вом биологического клея или ушивания, после чего
возможно проведение плевродеза тальком. Эта проце-
дура эффективна в 40-75% случаев [2,12]. В случае на-
растания гидроторакса и усиления дыхательной
недостаточности у представленного больного планиру-
ется обсуждение тактики лечения с торакальными хи-
рургами с возможным применением вышеуказанных
методов.
Таким образом, течение цирроза печени у обсуж-
даемого пациента было осложнено развитием пра-
востороннего гидроторакса, а затем и спонтанной
бактериальной эмпиемой (инфицирование плевраль-
ного выпота при циррозе печени), которая наблюдает-
ся в 13% случаев плеврального выпота, как правило,
вследствие проникновения бактерий, прежде всего E.
coli, Streptococcus spр., Enterococcus и Klebsiella, из
брюшной полости. Развитие спонтанной бактериаль-
ной эмпиемы следует предполагать при появлении у
больного с гидротораксом лихорадки, болей в грудной
клетке и/или энцефалопатии. Своевременная диагно-
стика и лечение бактериальной эмпиемы крайне
важна, так как летальность при развитии данного ос-
ложнения достигает 20%. Для профилактики реци-
дивов, по аналогии со спонтанным бактериальным
перитонитом, рекомендуется длительное лечение нор-
флоксацином [2,7], что и было применено в нашем на-
блюдении.
Таким образом, печеночный гидроторакс представ-
ляет собой одно из серьезных осложнений цирроза пе-
чени, в лечении которого, наряду со стандартной
диуретической терапией, применением октреотида и
терлипрессина возможно использование различных
хирургических пособий. Печеночный гидроторакс тре-
бует проведения дифференциального диагноза для ис-
ключения других возможных его причин.
Литература
1. Ивашкин В.Т. Осложнения портальной гипертензии при циррозе пече-
ни. Российский физиологический журнал им.И.М. Сеченова, 2009, 95,
10. 1074-1092
2. Lazaridis K.N., Frank J.W., Krowka M.J., et al. Hepatic hydrothorax: patho-
genesis, diagnosis, and management. Am J of Med, 1999, 107, 262-7.
3. Strauss R.M., Boyer T.D. Hepatic hydrothorax. Sem Liver Dis., 1997, 17,
227-232.
4. Garsia N., Mihas A.A. Hepatic hydrothorax: pathophysiology, diagnosis,
and management. J Clin Gastroenterol., 2004, 38, 52-58.
5. Kakizaki T., Yoshinaga T., Higuchi T., et al. Hepatic hydrothorax in the
absence of ascites. Liver, 1998, 18, 216-20.
6. Kirsch C.M., Chui D.W., Yenokida G.G., et al. Case report: hepatic
hydrothorax without ascites. Am J Med Sci., 1991, 302, 103-6.
7. Roussos A., Philippou N., Mantzaris G.J., et al. Hepatic hydrothorax: patho-
physiology, diagnosis, and management. J Gastroenterol Hepatol., 2007,
J Gastroenterol Hepatol., 2007,
22, 1388-1393.
8. Emerson PA, Davies JH. Hydrothorax complicating ascites. Lancet, 1955,
268, 487-8.
9. Huang P., Chang Y., et al. The morphology of diaphragmatic defects in
hepatic hydrothorax: Thoracoscopic finding s. J Thoracic Cardiovasc
Surgery, 2005, 130, 141-145.
10. Lau K.K., Arkles B., McKenzie A. A Case of Hepatic Hydrothorax Due to a
Large Diaphragmatic Defect. Australas Radiol., 1992, 36, 160-162.
11. Xiol X., Cortes R., Castellote J. Utility and complications of thoracocentesis
in cirrhotic patients. Am. J. Med., 2001, 111, 67-9.
12. Mouroux J., Perrin C., Venissac N., et al. Management of pleural effusion of
cirrhotic origin. Chest, 1996, 109, 1093-1096.
13. Jeffries M.A., Kazanjian S., Wilson M., et al. Transjugular intrahepatic por-
tosystemic shunts and liver transplantation in patients with refractory
hepatic hydrothorax. Liver Transpl Surg. , 1998, 4, 416-23.
, 1998, 4, 416-23.
14. Siegerstetter V., Deibert P., Ochs A., et al. Treatment of refractory hepatic
hydrothorax with transjugular intrahepatic portosystemic shunts: long-
term results in 40 patients. Eur J Gastroenterol Hepatol., 2001, 13, 529-34.
15. Takahashi K., Chin K., Sumi K., et al. Resistant hepatic hydrothorax: a suc-
cessful case with treatmrnt by nCPAP. Respiratory Med., 2005, 99, 262-64.
16. Pfammatter R., Quattropani C., Reichen J., et al. Treatment of hepatic
hydrothorax and reduction of chest tube output with octreotide. Eur J
Gastroenterol Hepatol., 2001, 13, 977-80.
17. Dumortier D., Lepretre J., Scalone O., et al. Successful treatment of hepat-
ic hydrothorax with octreotide. Eur J Gastroenterol Hepatol., 2000, 12, 817-
20.
18. Barreales M., Saenz-Lopes S., Igarzabal A., et al. Refractory hepatic
hydrothorax: successful treatment with octreotide. Rev Esp Enferm Dig.,
2005, 97, (11), 830-835.
19. Парсонз П.Э., Хеффнер Д.Э., Секреты пульмонологии. Под ред. Колод-
киной О.Ф. Москва, 2004г. С.79.
Таблица 3. Факторы плохого прогноза при ТИПШ
— возраст >60 лет
— экстренное ТИПШ
— АЛТ >100 ед/л
— билирубин >3 мг/дл
— предшествующая энцефалопатия
Страница не найдена |
Страница не найдена |404. Страница не найдена
Архив за месяц
ПнВтСрЧтПтСбВс
12
12
1
3031
12
15161718192021
25262728293031
123
45678910
12
17181920212223
31
2728293031
1
1234
567891011
12
891011121314
11121314151617
28293031
1234
12
12345
6789101112
567891011
12131415161718
19202122232425
3456789
17181920212223
24252627282930
12345
13141516171819
20212223242526
2728293031
15161718192021
22232425262728
2930
Архивы
Мар
Апр
Май
Июн
Июл
Авг
Сен
Окт
Ноя
Дек
Метки
Настройки
для слабовидящих
Лечение пациентки с гигантской склерозирующей гемангиомой левого легкого
Склерозирующая гемангиома легких является доброкачественной опухолью со злокачественным потенциалом.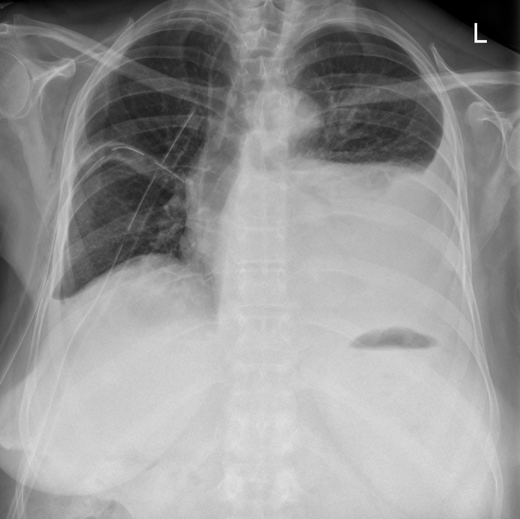 Впервые опухоль была описана в 1956 г. A. Libow и D. Hubbel [1, 2]. Чаще всего заболевание протекает бессимптомно и обнаруживается случайно при выполнении рентгенографии органов грудной клетки. Преимущественно поражаются нижние доли легких. Иногда опухоль может быть принята за опухоль средостения, плевральной полости, эхинококковую кисту [1, 3—5].
Впервые опухоль была описана в 1956 г. A. Libow и D. Hubbel [1, 2]. Чаще всего заболевание протекает бессимптомно и обнаруживается случайно при выполнении рентгенографии органов грудной клетки. Преимущественно поражаются нижние доли легких. Иногда опухоль может быть принята за опухоль средостения, плевральной полости, эхинококковую кисту [1, 3—5].
По патоморфологическому строению она в основном состоит из эпителиальных клеток (пневмоцитов типа II), выровненных в разных направлениях и сопровождающихся пролиферацией и реакцией других компонентов [1, 2]. В ряде случаев возможно наличие таких клинических проявлений, как кровохарканье и боли в грудной клетке [2, 5, 6]. В литературе встречаются публикации о выявлении метастатического поражения лимфатических узлов средостения у пациентов со склерозирующей гемангиомой [7—9].
Представляем клинический случай лечения пациентки с гигантской склерозирующей гемангиомой нижней доли левого легкого.
Клинический случайПациентка Н. , 62 лет. Поступила в клинику кафедры госпитальной и детской хирургии лечебного факультета НГМУ 16.10.17. Жалоб при поступлении нет. Из анамнеза: при прохождении флюорографии органов грудной клетки выявлено объемное образование левой плевральной полости с наличием жидкости в плевральной полости и компрессией нижней доли левого легкого. Госпитализирована в отделение для дообследования и лечения.
, 62 лет. Поступила в клинику кафедры госпитальной и детской хирургии лечебного факультета НГМУ 16.10.17. Жалоб при поступлении нет. Из анамнеза: при прохождении флюорографии органов грудной клетки выявлено объемное образование левой плевральной полости с наличием жидкости в плевральной полости и компрессией нижней доли левого легкого. Госпитализирована в отделение для дообследования и лечения.
При поступлении состояние удовлетворительное. Грудная клетка обычной формы. Обе половины участвуют в акте дыхания. При пальпации болезненности нет. При перкуссии слева в задних и нижнебоковых отделах притупление перкуторного звука. При аускультации там же резкое ослабление везикулярного дыхания.
По данным рентгенокомпьютерной томографии органов грудной клетки (рис. 1): Рис. 1. Мультиспиральная компьютерная томография органов грудной клетки пациентки. а — определяется негомогенный субстрат, размером 10,9×7,2×13,2 см по задней поверхности в левой плевральной полости; б — при контрастировании опухоль негомогенно накапливает контрастное вещество, определяется уплотнение и компрессия нижней доли левого легкого. в левой плевральной полости по дорсальной поверхности, на уровне нижней доли определяется негомогенный субстрат, размерами 10,9×7,2×13,2 см, негомогенно накапливающий контраст. По наддиафрагмальному отделу этого субстрата определяется жидкость, максимальной толщиной 14 мм. Определяются уплотнение и компрессия нижней доли левого легкого.
в левой плевральной полости по дорсальной поверхности, на уровне нижней доли определяется негомогенный субстрат, размерами 10,9×7,2×13,2 см, негомогенно накапливающий контраст. По наддиафрагмальному отделу этого субстрата определяется жидкость, максимальной толщиной 14 мм. Определяются уплотнение и компрессия нижней доли левого легкого.
Заключение: признаки объемного образования плевры. Гидроторакс слева.
С целью верификации диагноза проводилась пункция левой плевральной полости и пункционная биопсия образования. В обеих случаях атипичных клеток не получено.
03.11.17 пациентка оперирована (торакоскопия слева, удаление опухоли). Выполнен разрез кожи по VI межреберью длиной 6 см ближе к передней аксиллярной линии. Дополнительно в V межреберье по задней аксиллярной линии установлен троакар. В плевральной полости выпота нет. Определяется объемное образование, исходящее из S6, на широком основании, интенсивно кровоснабжающееся, размером 13×8×11 см, с гладкой поверхностью (рис. 2). Рис. 2. Интраоперационное фото. Определяется объемное образование, исходящее из S6, на широком основании, интенсивно кровоснабжающееся, размером 13×8×11 см, с гладкой поверхностью. На ножку опухоли наложены зажимы (рис. 3). Рис. 3. Интраоперационное фото. Этап операции. На ножку опухоли наложены зажимы. Ножка пересечена, опухоль отсечена и извлечена из плевральной полости. Ткань легкого ушита одиночными швами (рис. 4). Рис. 4. Интраоперационное фото. После удаления опухоли и ушивания легочной ткани. Аэрогемостаз. Сухо. Дренирование плевральной полости двумя дренажами. Послойное ушивание ран. Дренажи удалены из плевральной полости на 3-и сутки послеоперационного периода.
2). Рис. 2. Интраоперационное фото. Определяется объемное образование, исходящее из S6, на широком основании, интенсивно кровоснабжающееся, размером 13×8×11 см, с гладкой поверхностью. На ножку опухоли наложены зажимы (рис. 3). Рис. 3. Интраоперационное фото. Этап операции. На ножку опухоли наложены зажимы. Ножка пересечена, опухоль отсечена и извлечена из плевральной полости. Ткань легкого ушита одиночными швами (рис. 4). Рис. 4. Интраоперационное фото. После удаления опухоли и ушивания легочной ткани. Аэрогемостаз. Сухо. Дренирование плевральной полости двумя дренажами. Послойное ушивание ран. Дренажи удалены из плевральной полости на 3-и сутки послеоперационного периода.
По результатам патоморфологического исследования удаленной опухоли (101916−934): опухоль представлена фиброзной тканью различной степени зрелости, содержащей толстостенные сосуды или сосудистые щели, что соответствует склерозирующей гемангиоме.
Полученные данные указывают на сложность диа-гностики данного заболевания и широкие возможности торакоскопии для удаления опухолей легких гигантских размеров.
Авторы заявляют об отсутствии конфликта интересов.
Сведения об авторах
Дробязгин Евгений Александрович — д.м.н., проф., доцент, профессор кафедры госпитальной и детской хирургии ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России, зав. отделением эндоскопии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница», ведущий научный сотрудник центра онкологии ФГБУ «Национальный медицинский исследовательский центр им. акад. Е.Н. Мешалкина» Минздрава России; e-mail: [email protected]; https://orcid.org/0000-0002-3690-1316
Чикинев Юрий Владимирович — д.м.н., проф., зав. кафедрой госпитальной и детской хирургии ФГБОУ ВО «Новосибирский государственный медицинский университет» Минздрава России, торакальный хирург отделения торакальной хирургии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница»; e-mail: [email protected]
Коробейников Александр Владимирович — зав. отделением торакальной хирургии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница»
отделением торакальной хирургии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница»
Бобылев Евгений Николаевич — торакальный хирург отделения торакальной хирургии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница»
Щербина Константин Игоревич — торакальный хирург отделения торакальной хирургии ГБУЗ НСО «Государственная Новосибирская областная клиническая больница»
*e-mail: [email protected]; https://orcid.org/0000-0002-3690-1316
Возможности УЗИ в диагностике и лечении плевральных выпотов Текст научной статьи по специальности «Клиническая медицина»
позвоночника был значимым. Через 2—3 года после операции в связи с рецидивом болевого синдрома 3 пациента были оперированы повторно; 3 пациентам в сроки от 1 до 3 лет после нейрохирургического вмешательства были имплантированы эндопротезы тазобедренного сустава.
У пациентов группы !Б (деформация во фронтальной плоскости) при исследовании функциональной разницы длин нижних конечностей определялся наклон таза в горизонтальной плоскости. Установлено, что у человека наклон таза на 10 градусов наблюдается при укорочении ноги на 3,5 см. В нашем клиническом исследовании на 37 больных (в двух позициях — стоя и в положении наклона на 90 градусов) с помощью механических и электронных устройств установлена зависимость: 1 см укорочения конечности приводит к наклону таза в 3 градуса.
Установлено, что у человека наклон таза на 10 градусов наблюдается при укорочении ноги на 3,5 см. В нашем клиническом исследовании на 37 больных (в двух позициях — стоя и в положении наклона на 90 градусов) с помощью механических и электронных устройств установлена зависимость: 1 см укорочения конечности приводит к наклону таза в 3 градуса.
ВЫВОДЫ
• Для выявления доминирующей патологии
у пациента с синдромом hip-spine целесообразно применять диагностическую блокаду.
Обследование пациентов с синдромом hip-spine должно быть комплексным и определять не только анатомическую разницу длин конечностей, но и функциональную. Учитывая тот факт, что кососуженный таз, по нашим данным, встретился в 7% случаев у пациентов с патологией тазобедренного сустава, необходимо исследовать латеральную конъюгату. Для определения истинного укорочения и исследования комфортной компенсации конечности необходимо проводить исследования в динамике, с уменьшением неравенства функционального укорочения конечности. Для оценки имеющегося укорочения конечности и соответствующей коррекции при будущем эндопротезировании необходимо оценивать сколиометром и наклон таза, исходя из того факта, что 1 см укорочения приводит к наклону таза в 3 градуса.
Для определения истинного укорочения и исследования комфортной компенсации конечности необходимо проводить исследования в динамике, с уменьшением неравенства функционального укорочения конечности. Для оценки имеющегося укорочения конечности и соответствующей коррекции при будущем эндопротезировании необходимо оценивать сколиометром и наклон таза, исходя из того факта, что 1 см укорочения приводит к наклону таза в 3 градуса.
ЛИТЕРАТУРА
1. Matsuyama Y., Hasegawa Y., Yoshihara H. et al. Hip-spine syndrome // Spine. — 2004. — Vol. 29. — №21. — P. 2432—2437.
2. Offierski C. M., Macnab I. Hip-spine syndrome // Spine. — 1983. — Vol. 8. — №3. — P. 316—321.
3. Руководство по эндопротезированию тазобедренного сустава / Под ред. Р. М. Тихилова, В. М. Шаповалова. — СПб., 2008. — 324 с.
4. Шильников В. А., Тихилов Р. М., Денисов А. О. Болевой синдром после эндопротезирования тазобедренного сустава // Травматология и ортопедия России. — 2008. — №2. — С. 106—109.
5. Денисов А. О. Болевой синдром после эндопротезирования тазобедренного сустава / Автореф. дисс. … к.м.н. — СПб., 2010. — 25 с.
6. Klein K. K. A study of the progression of lateral pelvice asymmetry in 585 elementary, junior and senior high school boys // Am. Correct. Ther. J. — 1969. — Vol. 23. — P. 171—173.
ВОЗМОЖНОСТИ УЗИ
В ДИАГНОСТИКЕ И ЛЕЧЕНИИ ПЛЕВРАЛЬНЫХ ВЫПОТОВ
Ш. Г. Авакян, Т. Д. Джанелидзе, О. П. Боженко, О. А. Кашаев, Е. В. Пуличева;
ФГКУ «1602 ВКГ» МО РФ, г. Ростов-на-Дону
Ростов-на-Дону
Под плевральным выпотом понимается патологическое скопление жидкости в полости плевры. Это один из синдромов, наиболее часто встречающийся при патологии органов грудной клетки, после пневмоний. Количество больных плевритами имеет тенденцию к увеличению в периоды вспышек острых респираторных заболеваний.
В основе любого плеврального выпота лежит нарушение равновесия между выделением и всасыванием плевральной жидкости. Доминирующее количество плевритов, как правило, имеет вторичный характер. Первичные плевриты у практически здоровых лиц встречаются только при травмах грудной клетки, а также в случаях туберкулеза и опухолей плевры.
Большое диагностическое и прогностическое значение имеет возможность исключить наличие выпота в плевральной полости при наличии клинической симптоматики. В диагностическом отношении важен биохимический и цитологический состав жидкости (транссудат или экссудат), что отражается на эхокартине выпота. В широком кругу врачей традиционным методом диагностики плевритов до сих пор остаются рентгенологические методы — полипозиционная рентгеноскопия, многопроекционная рентгенография, флюорография (в том числе цифровая), послойная линейная томография, а также компьютерная томография (КТ) и спиральная компьютерная томография (СКТ).
В широком кругу врачей традиционным методом диагностики плевритов до сих пор остаются рентгенологические методы — полипозиционная рентгеноскопия, многопроекционная рентгенография, флюорография (в том числе цифровая), послойная линейная томография, а также компьютерная томография (КТ) и спиральная компьютерная томография (СКТ).
Наряду с высокой диагностической возможностью рентгеновский метод имеет ряд недостатков. Прежде
всего, это лучевая нагрузка на больного и персонал, особенно в случаях неоднократного его применения для контроля по ходу лечения. Рентгенологически при оптимальном (вертикальном) положении больного можно выявить жидкость в плевральной полости в количестве 150—200 мл и более. Данный метод не позволяет оценить характер самого выпота, а также состояние прилегающих отделов легочной ткани, органов брюшной полости, полости перикарда и мягких тканей грудной клетки.
Наш многолетний опыт применения УЗИ для выявления плевральных выпотов позволяет считать УЗИ органов грудной клетки ценным методом диагностики данной патологии — не только в качестве альтернативы рентгеновскому, а как разумное сочетание этих методов визуализации, оптимально дополняющих друг друга.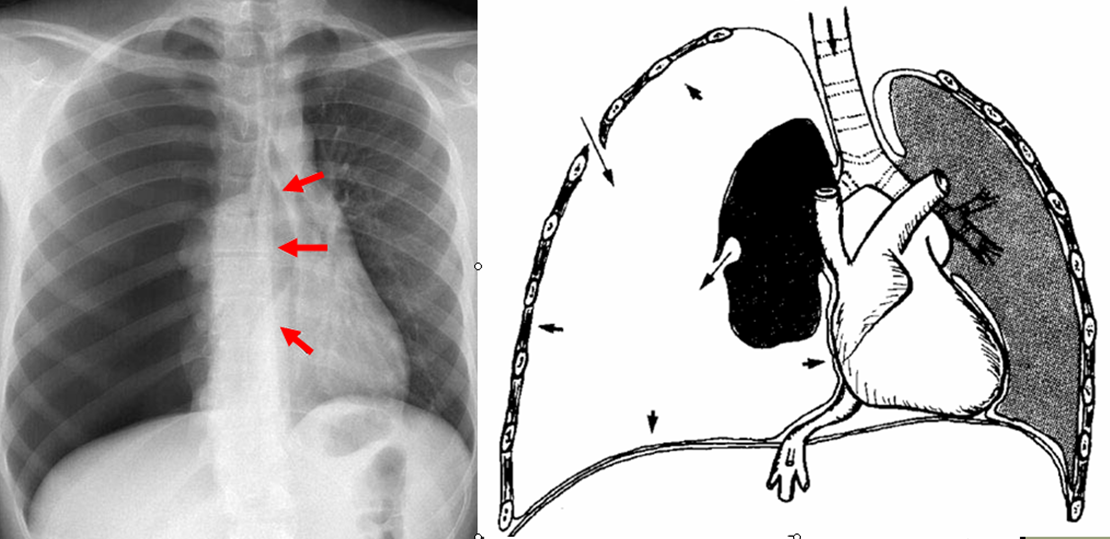 Наличие жидкости в плевральной полости создает хорошие условия, своего рода акустическое окно, для выявления изменений в легочной ткани, прилежащей к выпоту, особенно в базальных сегментах нижних долей легких и их кортикальных зон. Однако анатомическое строение грудной клетки (массивный костный каркас, воздушность легких) не дает возможности при УЗИ четко визуализировать медиальные зоны легких, органы средостения, глубокие участки междолевых щелей и выявить скопления жидкости в виде осумкованных плевритов. В этих случаях данные, полученные при рентгенологическом исследовании, являются основными.
Наличие жидкости в плевральной полости создает хорошие условия, своего рода акустическое окно, для выявления изменений в легочной ткани, прилежащей к выпоту, особенно в базальных сегментах нижних долей легких и их кортикальных зон. Однако анатомическое строение грудной клетки (массивный костный каркас, воздушность легких) не дает возможности при УЗИ четко визуализировать медиальные зоны легких, органы средостения, глубокие участки междолевых щелей и выявить скопления жидкости в виде осумкованных плевритов. В этих случаях данные, полученные при рентгенологическом исследовании, являются основными.
ПУЛЬМОНОЛОГИЯ
швниц
шч
Для выполнения УЗИ грудной клетки при наличии жидкости в плевральной полости для ультразвукового сканера не требуется специального технического или программного обеспечения. Данное исследование может выполняться на любых ультразвуковых аппаратах, в том числе и портативных, в режиме абдоминального сканирования с использованием конвексного датчика. Также для УЗИ грудной клетки пациент не нуждается в специальной подготовке. Сама методика УЗИ для диагностики плевральных выпотов достаточно проста: исследование проводится при свободном дыхании больного, при необходимости — в положении глубокого вдоха или выдоха, а также с пробой на дыхательную подвижность зоны интереса. Мы выполняем исследование в вертикальном положении больного, который сидит на кушетке спиной к врачу, поворачиваясь при необходимости.
Данное исследование может выполняться на любых ультразвуковых аппаратах, в том числе и портативных, в режиме абдоминального сканирования с использованием конвексного датчика. Также для УЗИ грудной клетки пациент не нуждается в специальной подготовке. Сама методика УЗИ для диагностики плевральных выпотов достаточно проста: исследование проводится при свободном дыхании больного, при необходимости — в положении глубокого вдоха или выдоха, а также с пробой на дыхательную подвижность зоны интереса. Мы выполняем исследование в вертикальном положении больного, который сидит на кушетке спиной к врачу, поворачиваясь при необходимости.
Для выявления выпота в плевральной полости и измерения его количества оптимальным положением пациента является вертикальное. Однако во многих случаях, особенно у тяжелых больных и пострадавших, находящихся на ИВЛ, проводить такое исследование становится невозможным. В таких случаях УЗИ в латеропозиции (что необходимо отметить в протоколе исследования) дает возможность получить информацию о наличии и количестве выпота в плевральной полости. При этом печень, селезенка, гиперэхогенная полоска диафрагмы являются маркерами и хорошими акустическими окнами для определения границы, количества плеврального выпота над ними, точки пункции.
При этом печень, селезенка, гиперэхогенная полоска диафрагмы являются маркерами и хорошими акустическими окнами для определения границы, количества плеврального выпота над ними, точки пункции.
Эффективность УЗИ зависит не только от технических характеристик ультразвукового сканера и квалификации врача ультразвуковой диагностики, но и от четкого взаимодействия с лечащим врачом и врачом-рентгенологом, что позволяет составить наиболее рациональный план инструментальных методов диагностики в каждом конкретном случае.
С 2005 по 2015 год в нашем многопрофильном лечебном учреждении проведено 9878 УЗИ плевральной полости, что составляет 2,7% от общего количества ультразвуковых исследований. Этот показатель в течение ряда лет достаточно стабилен, что свидетельствует о хорошей осведомленности врачей лечебных отделений об информативности УЗИ плевральной полости в диагностике и лечении плевральных выпотов. Наиболее часто за отчетный период УЗИ плевральной полости в нашем ЛПУ выполнялось больным, находящимся в отделении реанимации и палатах интенсивной терапии.
Наиболее часто за отчетный период УЗИ плевральной полости в нашем ЛПУ выполнялось больным, находящимся в отделении реанимации и палатах интенсивной терапии.
Наш большой опыт применения УЗИ для исследования плевральной полости и органов грудной клетки дает возможность определить алгоритм обследования различных групп больных (рис. 1).
При травмах грудной клетки применение УЗИ показано для исключения гемоторакса, особенно при малых количествах жидкости в плевральной полости в тех случаях, когда при рентгенографии при высоком стоянии диафрагмы не удается выявить небольшое количество крови в синусах плевральной полости и над диафрагмой на стороне поражения (рис. 2).
Обзорная рентгенография органов грудной клетки в прямой и боковой проекциях
Подозрение на малый выпот
Характеристика выпота: свободный/осумкованный
Обнаружен плевральный выпот (средний, большой, массивный)
Линейная томография или КТ
легких и средостения. Обследование других органов и систем
Обследование других органов и систем
Пункция плевральной полости
■ под контролем эхографии (эвакуация жидкости)
По клиническим показаниям плевроскопия и/или трансторакальная пункционная биопсия плевры под контролем УЗИ
Эхография плевральной полости
Определение характера выпота и его объема
Гистологическое, цитологическое, бактериологическое, биохимическое, иммунологическое исследование тканевого материала (аспирата,
При туберкулезном поражении легких и плевры (рис. 3) с помощью УЗИ определяем количество жидкости, ее характер и отмечаем место пункции. УЗИ позволяет контролировать процесс разрешения плеврита до его исхода — полное отсутствие жидкости, появление плевро-диафрагмальных и плевро-костальных наслоений — в процессе лечения. Такие больные требуют неоднократного обследования, что с применением УЗИ плевральной полости уменьшает лучевую нагрузку на пациента (рис. 4 а, б).
Такие больные требуют неоднократного обследования, что с применением УЗИ плевральной полости уменьшает лучевую нагрузку на пациента (рис. 4 а, б).
При заболеваниях сердца, печени, почек с признаками их декомпенсации УЗИ позволяет исключить наличие жидкости не только в плевральной полости, но и в брюшной полости, малом тазу, полости перикарда (рис. 5 а, б).
При заболеваниях легких неспецифического характера, особенно при пневмониях, на рентгенограммах в вертикальном положении на фоне инфильтрации базаль-ных отделов легких невозможно дифференцировать «малый» парапневмонический выпот (рис. 6 а, б, в). УЗИ помогает решить эту проблему. В некоторых случаях затруднена рентгенологическая дифференциация массивного инфильтрата, ателектаза опухолевого поражения с плевральным выпотом (рис. 7, 8).
При выявлении на рентгенограммах или флюорограммах деформации диафрагмы или ее высокого стояния (релаксация) для исключения наличия жидкости над диафрагмой, в плевральных синусах (рис. 9, 10), а также изменений
9, 10), а также изменений
поддиафрагмальных органов (печень, селезенка, хвост поджелудочной железы) проводится УЗИ (рис. 11 а, б).
Мы проводим УЗИ плевральной полости во всех случаях перед пункцией плевральной полости для определения точки проведения пункции, а также после эвакуации жидкости для определения объема оставшейся жидкости. Для определения оптимальной точки пункции мы отмечаем место наибольшего скопления выпота в соответствующем межреберье.
Обязательным является УЗИ плевральной полости в динамике лечения основного заболевания, которое явилось причиной вторичного плеврита (см. рис. 4 а, б и рис. 11 а, б).
Контрольное УЗИ плевральной полости проводится в нашем ЛПУ больным, перенесшим обширные оперативные вмешательства на органах брюшной полости или травмы, а также при перитонитах и больным на ИВЛ.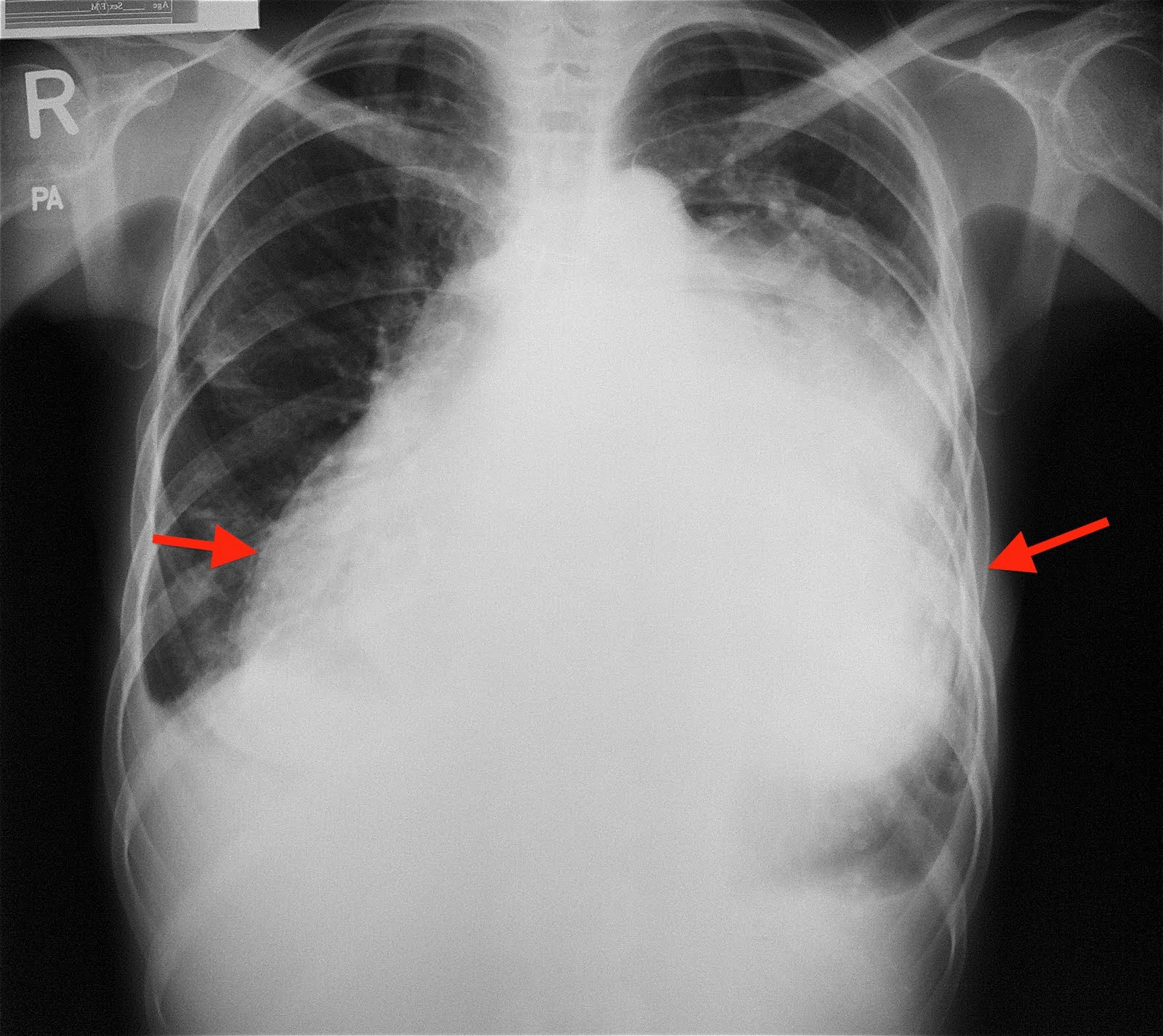
Важное значение имеет определение наличия жидкости в плевральной полости, ее локализация, определение оптимальной точки пункции и приблизительного объема жидкости в данном участке плевральной полости. Самым простым методом измерения объема плеврального выпота, по нашему мнению, является метод измерения толщины слоя жидкости от диафрагмы до наиболее удаленной точки грудной стенки. Примерный расчет в этом случае следующий:
Рис. 2. Травма грудной клетки слева с переломом заднего отрезка 9—10 ребер, гемоторакс слева.
Рис. 3. Очаговый туберкулез легких, плеврит справа.
Рис. 4. Рак левой молочной железы, левосторонняя радикальная мастэктомия, гидроторакс слева:
а) до пункции количество жидкости около 1,0 литра; б) после пункции количество жидкости около 500 мл.
— нвнииппап
ПУЛЬМОНОЛОГИЯ
Рис. 5. Двустронний гидроторакс при декомпенсации ХСН:
а) количество жидкости в правой плевральной полости до 800 мл; б) количество жидкости в левой плевральной полости около 400 мл.
Рис. 6а. Малый туберкулезный плеврит не дифференцированный при рентгенографии, Рис. 6в. Малый гидроторакс
количество жидкости около 60 мл (б — в вертикальном положении). при декомпенсации ХСН, количество
жидкости около 70 мл.
• при толщине слоя жидкости до 5,0 см каждый сантиметр равен 100 мл;
• при толщине слоя жидкости более 5,0 см каждый сантиметр равен 150 мл.
Для точного определения объема жидкости в плевральной полости приводятся различные формулы расчета. Но в практической работе метод измерения толщины
/¿чш<и и г*
■ :
Рис. 7. Внебольничная полисегментарная левосторонняя пневмония, парапневмонический плеврит с признаками организации и количеством жидкости около 800 мл.
жидкости, используемый нами, мы считаем наиболее простым и удобным. Тем более что точное определение объема плеврального выпота большого клинического значения не имеет. Наш опыт показывает, что определяемый нами предварительный объем жидкости и полученное при пункции количество жидкости совпадают в 60 —70% случаев, так как при большом количестве плеврального выпота, как правило, весь объем эвакуируют не всегда,
Рис. 8. Опухоль правого реберно-позвоночного угла, исходящая из позвоночника, с плевральным выпотом.
8. Опухоль правого реберно-позвоночного угла, исходящая из позвоночника, с плевральным выпотом.
www.akvarel2002.ru
МВРАЧ
■ ги риш
ПУЛЬМОНОЛОГИЯ
Рис. 11. Крупный абсцесс правой доли печени, реактивный плеврит справа:
а) до пункции абсцесса, количество жидкости до 200 мл; б) после пункции абсцесса.
жидкость на уровне синуса остается. Здесь важно отсутствие повторного накопления жидкости, которое часто является прогностически неблагоприятным и указывает на активность процесса (опухолевое поражение, туберкулез), продолжающееся кровотечение при травмах (особенно при поражении крупного сосуда), глубокую декомпенсацию основного заболевания.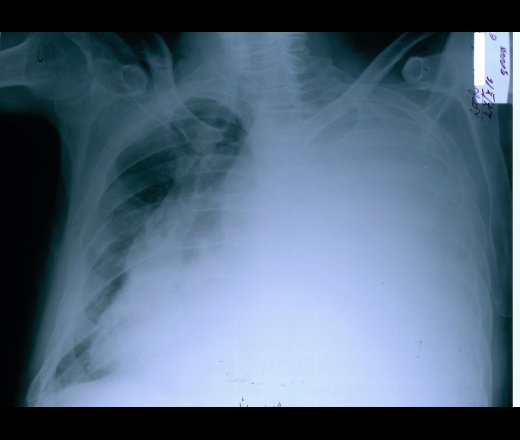
Протокол УЗИ, принятый в нашем ЛПУ, отражает факт наличия жидкости, ее локализацию, ее характер, наличие осумкования, признаков организации (плевро-диафрагмальные и плевро-костальные спайки), свободное перемещение жидкости при изменении положения тела больного, приблизительный объем выпота, точки на коже для проведения плевральной пункции.
Наш многолетний опыт позволяет определить следующие показания к УЗИ плевральной полости:
• клинические признаки (боли в грудной клетке при дыхании, субфебрилитет, одышка, шум трения плевры, воспалительные изменения в общем анализе крови и т. п.), свидетельствующие
о возможном плеврите и/или пневмонии, поражении легких специфического характера;
• травмы грудной клетки с переломом ребер или без них, сочетанные травмы грудной клетки и органов брюшной полости, особенно в случае высокого стояния диафрагмы, когда затруднительно
рентгенологическое определение наличия жидкости в плевральной полости;
• декомпенсация основного заболевания (хронической сердечной недостаточности, цирроза печени, нефротического синдрома и т. д.), что может привести к накоплению жидкости
д.), что может привести к накоплению жидкости
в плевральной полости;
• опухоли плевры и легких, как первичные, так и метастатические;
• оперативные вмешательства на органах грудной клетки, при болезнях крови и терапии антикоагулянтами для исключения гемоторакса.
ВЫВОДЫ
1. Метод УЗИ плевральной полости — разумная альтернатива рентгеновским методам для диагностики наличия жидкости в плевральной полости, обладающий рядом преимуществ, что позволяет широко использовать его в клинической практике.
2. При клиническом подозрении на наличие жидкости в плевральной полости и при травмах грудной клетки для исключения гемоторакса УЗИ среди методов визуализации должно выполняться как обязательное обследование..docx_html_4b59e7a014d99a86.jpg)
3. УЗИ плевральной полости в качестве контроля по ходу лечения должно рассматриваться как метод выбора.
www.akvarel2002.ru
Заболевание плевры: гидроторакс и гемоторакс печени
Болезнь плевры: гидроторакс и гемоторакс печени
1. Описание проблемы
Что нужно знать каждому врачу
Гидроторакс печени
Печеночный гидроторакс — это плевральный выпот, обычно более 500 мл, у пациента с циррозом без признаков первичного заболевания плевры, легких или сердца. Обычно эти излияния правосторонние, однако двусторонние или левосторонние излияния не редкость.У небольшого процента пациентов развивается гидроторакс при отсутствии асцита.
Гемоторакс
Гемоторакс определяется как кровь в плевральной полости.
Клинические особенности
Гидроторакс печени
Имеющиеся симптомы и признаки гидроторакса печени связаны с прямым сдавлением соседнего легкого. К ним относятся кашель, одышка, гипоксемия, боль в груди и утомляемость. Если она сопровождается лихорадкой и недомоганием, следует учитывать вторичную инфекцию плевральной жидкости, которая связана с повышенной смертностью.
К ним относятся кашель, одышка, гипоксемия, боль в груди и утомляемость. Если она сопровождается лихорадкой и недомоганием, следует учитывать вторичную инфекцию плевральной жидкости, которая связана с повышенной смертностью.
Гемоторакс
Имеющиеся симптомы и признаки гемоторакса связаны с прямым сдавлением соседнего легкого. К ним относятся кашель, одышка, гипоксемия, боль в груди и утомляемость. Кроме того, если плевральное кровотечение быстрое, у пациента могут наблюдаться симптомы и признаки острой кровопотери, включая шок. Если она сопровождается лихорадкой и недомоганием, следует учитывать вторичную инфекцию плевральной жидкости, которая связана с повышенной смертностью.
2.Управление в чрезвычайных ситуациях
Гидроторакс печени
Большой выпот может вызвать острые симптомы и признаки, требующие неотложной помощи. В некоторых случаях выпот даже средней величины может стать критическим из-за плохого сердечно-легочного резерва или из-за наличия другого острого процесса. В любом случае плевроцентез представляет собой необходимое первичное вмешательство.
В любом случае плевроцентез представляет собой необходимое первичное вмешательство.
Как правило, во время процедуры следует удалять не более 2 литров жидкости, чтобы избежать риска повторного расширения отека легких, потенциально опасного для жизни осложнения.В большинстве случаев удаление этого объема улучшит имеющиеся симптомы и признаки. Хотя плевроцентез считается безопасным, возникают осложнения, включая гемоторакс, пневмоторакс, воздушную эмболию, эмпиему и кровохарканье.
ОИТ Гемоторакс
При подозрении на гемоторакс рекомендуется ранняя хирургическая консультация. Параметры коагуляции следует измерить немедленно и скорректировать в случае отклонения от нормы. Важно убедиться, что у пациента есть упакованные эритроциты.Первоначальное лечение гемоторакса обычно включает введение плевральной трубки с целью эвакуации крови, повторного расширения легких и оценки дальнейшего кровотечения. Следует использовать плевральную дренажную трубку French 32-36 или больше, поскольку она обеспечивает лучший дренаж у взрослых; катетеры малого диаметра не рекомендуются.
После установки дренажной трубки необходимо получить повторную рентгенограмму грудной клетки, чтобы подтвердить положение трубки и оценить полноту эвакуации гемоторакса. Решение о хирургическом вмешательстве основывается как на скорости, так и на объеме кровотечения, измеряемом по выходу дренажной трубки и потребностям в переливании крови.Показания к последующему хирургическому вмешательству включают дренаж из грудной клетки 1500 мл за 24 часа, накопление> 200 мл кровянистого дренажа в час в течение 2-4 часов и / или постоянные потребности в переливании крови для поддержания гемодинамической стабильности.
В зависимости от имеющегося опыта и ожидаемого источника кровотечения, проблему можно решить торакоскопически. Однако, как правило, торакотомия является распространенным подходом при наличии стойкого кровотечения, массивном гемотораксе или, конечно, если предполагается серьезное повреждение сосуда как источник кровотечения.
3.
 Диагностика
ДиагностикаУстановление диагноза
Гидроторакс печени
У всех пациентов с плевральным выпотом следует исключить сердечную или легочную этиологию. Эхокардиография полезна для диагностики правожелудочковой недостаточности или перикардиального выпота. Всем пациентам с подозрением на гидроторакс печени следует проводить компьютерную томографию грудной клетки для выявления заболеваний легких, плевры или средостения, которые могут быть причиной скопления жидкости.
КТ также может выявить асцит, который, если он присутствует, может помочь в диагностике гидроторакса печени.Ультразвук печени полезен для выявления новообразований, а допплеровское исследование воротной и печеночной вен используется для оценки проходимости.
Торакоцентез — это диагностический тест выбора у пациентов с подозрением на гидроторакс печени. Анализ плевральной жидкости обычно выявляет транссудат. Хотя плевральная жидкость накапливается из перенесенного асцита, она может отличаться по концентрации общего белка и альбумина по сравнению с асцитом, вероятно, из-за различных абсорбционных свойств грудной плевры.
При подозрении на злокачественное новообразование следует провести цитологический анализ плевральной жидкости. У пациентов с лихорадкой, плевритной болью и / или энцефалопатией необходимо получить окраску жидкого грамм и посев, а также заподозрить парапневмонический выпот или инфекцию гидроторакса печени (спонтанная бактериальная эмпиема [SBEM]).
Критерии диагностики SBEM включают градиент сыворотки / плевральной жидкости> 1,1 г / дл, количество полиморфноядерных (PMN) лейкоцитов> 500 мм. 3 или положительный результат посева жидкости при отсутствии пневмонии или сопутствующей инфекции.
Бактерии, обычно связанные со спонтанным бактериальным перитонитом (SBEM), аналогичны бактериям, обнаруживаемым при SBEM, и включают E. Coli, виды Streptococcus, Enterococcus, Klebsiella или Pseudomonas, и примерно 50% эпизодов SBEM связаны со спонтанным бактериальным перитонитом.
Внутрибрюшинная инъекция коллоида 99mTc-сульфер или 99mTc-сывороточного альбумина человека — это описанный метод, используемый для подтверждения диагноза гидроторакса печени. Пациентам проводят терапевтический торакоцентез с последующей внутрибрюшинной инъекцией радиоизотопа.Обнаружение маркера в плевральной полости подтверждает. Это редко бывает необходимо.
Пациентам проводят терапевтический торакоцентез с последующей внутрибрюшинной инъекцией радиоизотопа.Обнаружение маркера в плевральной полости подтверждает. Это редко бывает необходимо.
ОИТ Гемоторакс
Гемоторакс обычно диагностируется с использованием клинических и радиологических методов. Небольшой гемоторак может быть трудно распознать клинически, а при аускультации грудной клетки можно не примечать. При большом или расширяющемся гемотораксе аускультация легких демонстрирует снижение звуков дыхания над пораженным полем легкого с ассоциированной тупостью при перкуссии.
Сердечно-легочная нестабильность может развиться частично из-за уменьшения объема циркулирующей крови и эффективного гематокрита.Сжатие легких и сердца может привести к увеличению объема крови в грудной клетке, что способствует сердечно-легочной нестабильности.
Рентген грудной клетки в вертикальном положении остается методом выбора при острой диагностике гемоторакса. Для выявления гемоторакса на рентгенограмме грудной клетки в плевральной полости должно присутствовать 400-500 мл жидкости. Пленки на спине менее полезны для оценки количества жидкости в груди из-за наслоения жидкости. Практически всегда легче оценить накопление жидкости (или воздуха) на пленке в отделении интенсивной терапии, если рентгеновский снимок проводится в вертикальном, а не в положении лежа на спине пациента.
Пленки на спине менее полезны для оценки количества жидкости в груди из-за наслоения жидкости. Практически всегда легче оценить накопление жидкости (или воздуха) на пленке в отделении интенсивной терапии, если рентгеновский снимок проводится в вертикальном, а не в положении лежа на спине пациента.
Боковые снимки на спине могут помочь отличить наслоенный выпот от ушиба легких или другого внутрипаренхиматозного процесса. У клинициста должен быть высокий индекс подозрения на гемоторакс, если на рентгенограмме грудной клетки после грудного вмешательства виден новый выпот.
Ультразвук может быть полезен для определения наличия и количественного определения объема плевральной жидкости.
Компьютерная томография грудной клетки — это высокоточное исследование для выявления и характеристики жидкости в плевральной полости.КТ позволяет различать паренхиматозный и плевральный отростки и может быть полезна для оценки стойких помутнений на рентгенограмме грудной клетки после торакостомии через зонд.
Нормальные лабораторные значения
Типичные результаты для плевральной жидкости при гидротораксе печени включают:
1. Количество клеток <1000 / см 3
2. Концентрация белка <2,5 г / дл
3. Количество полиморфноядерных лейкоцитов (ПЯН) <250 / мм 3
4. Соотношение общего белка в плевральной жидкости и сыворотке <0.5
5. Отношение лактатдегидрогеназы плевральной жидкости к сыворотке <0,6
6. Градиент плевральной жидкости / сывороточного альбумина> 1,1
7. pH> 7,4
8. Уровень глюкозы в плевральной жидкости на уровне сыворотки
Как мне узнать, что у пациента?
Гидроторакс печени следует подозревать у пациентов с портальной гипертензией и / или циррозом в анамнезе с плевральным выпотом. Асцит обычно присутствует наряду с другими признаками цирроза печени.
Дифференциальная диагностика
Необходимо рассмотреть альтернативные диагнозы при одностороннем или двустороннем плевральном выпоте.
Когда излияние одностороннее, Если у пациента наблюдается острая форма лихорадки и / или повышение уровня лейкоцитов, необходимо учитывать эмпиему или парапневмонический выпот, связанные с основной пневмонией. Если выпот находится слева, при лихорадке, особенно у алкоголиков, следует рассмотреть синдром Борхаве (разрыв пищевода).
После подтверждения транссудата наиболее вероятной альтернативной этиологией является ЗСН или низкий уровень альбумина.Другие причины транссудативного выпота включают легочную эмболию, гипотиреоз и раннюю лимфатическую обструкцию. Дифференциация экссудативного выпота намного больше и включает воспалительные и злокачественные процессы.
4. Специальное лечение
Гидроторакс печени
Торакоцентез представляет собой первичное вмешательство, необходимое, когда симптомы или признаки срочно нуждаются в лечении. Если симптомы или признаки легкие и переносимые, то первым вмешательством должна быть медикаментозная терапия. Медикаментозное лечение гидроторакса печени должно в основном сосредоточиваться на контроле асцита. Это достигается за счет постепенного уменьшения объема внеклеточной жидкости, но не за счет перфузии тканей.
Медикаментозное лечение гидроторакса печени должно в основном сосредоточиваться на контроле асцита. Это достигается за счет постепенного уменьшения объема внеклеточной жидкости, но не за счет перфузии тканей.
Пациенты соблюдают диету с ограничением натрия, пытаясь достичь отрицательного водного баланса с помощью диуретиков, включая спиронолактон и петлевой диуретик (фуросемид). Нестероидных противовоспалительных средств следует избегать из-за их активности по удержанию натрия и повышенного риска ОПН у этой популяции пациентов.Окончательное лечение гидроторакса печени требует лечения основной печеночной недостаточности, включая медикаментозное лечение трансплантации печени.
Когда медикаментозная терапия не контролирует выпот и он возвращается, показан торакоцентез. Если печеночный гидроторакс невосприимчив к медикаментозной терапии, обычно требуется повторное торакоцентез, однако продолжительность положительного эффекта может быть разной. Перед выполнением торакоцентеза полезно сделать рентген грудной клетки или компьютерную томографию, чтобы определить количество присутствующей жидкости.
Как правило, во время процедуры следует удалять не более 2 литров жидкости, чтобы избежать риска повторного расширения отека легких, потенциально опасного для жизни осложнения. Хотя плевроцентез считается безопасным, возникают осложнения, включая гемоторакс, пневмоторакс, воздушную эмболию, эмпиему и кровохарканье.
Гемоторакс
См. Раздел «Экстренное лечение» для начального лечения гемоторакса.
Устойчивая кровь, обнаруженная на рентгенограммах грудной клетки и компьютерной томографии после зондовой торакостомии, является независимым предиктором развития эмпиемы и требует лечения ранним ВАТС в течение 3-7 дней после госпитализации.
Кровь имеет тенденцию к формированию со временем и образует толстую корку, которая может привести к «застреванию» нерасширяющегося легкого. На этом этапе требуется хирургическое вмешательство (видео-торакоскопия или торакотомия) для удаления кожуры для облегчения расширения легких. Ранняя торакоскопия (до 3-го дня) при задержке гемоторакса была связана со снижением сложности операции, контаминации / инфицирования сгустка и продолжительности пребывания в больнице по сравнению с теми, которые выполнялись позже. Дополнительные преимущества включают меньшее количество легочных осложнений, более короткое время до выздоровления и менее длительную нетрудоспособность.
Дополнительные преимущества включают меньшее количество легочных осложнений, более короткое время до выздоровления и менее длительную нетрудоспособность.
VATS может быть предпринята позже при ретеншном гемотораксе; тем не менее, процент перехода к открытой торакотомии увеличивается с более длительными задержками. Должен быть низкий порог для раннего направления к специалисту по очистке VATS, если у пациента остается кровь, несмотря на адекватный дренаж через дренаж через дренажную трубку.
Сообщалось об использовании тромболитиков для лечения подострых (6-13-дневных) скоплений у пациентов с высоким риском торакотомии; однако хирургическое вмешательство является методом выбора, когда это возможно.
Огнеупорные футляры
Гидроторакс печени
У пациентов, которым требуется повторный плевроцентез, несмотря на максимальную медикаментозную терапию с частотой более чем каждые 2 недели, следует рассмотреть возможность проведения процедуры трансъюгулярного внутрипеченочного портосистемного шунта (TIPS). Процедура TIPS включает рентгеноскопическое размещение металлического стента в печени между воротной вене и печеночной венозной системой. Это приводит к снижению портального давления и последующему уменьшению образования асцита.
Процедура TIPS включает рентгеноскопическое размещение металлического стента в печени между воротной вене и печеночной венозной системой. Это приводит к снижению портального давления и последующему уменьшению образования асцита.
Симптоматическое улучшение отмечается у 70-80% пациентов с рефрактерным гидротораксом печени. Осложнения TIPS включают тромбоз шунта, печеночную энцефалопатию и обострение легочной гипертензии. Хотя TIPS может облегчить симптомы гидроторакса печени, его обычно считают «мостом» к трансплантации.
Следует ли ставить грудную трубку?
Нет, только не при неосложненном гидротораксе печени! Важно подчеркнуть, что, хотя дренаж плеврального дренажа может обеспечить немедленное облегчение симптомов одышки у пациентов с гидротораксом печени, всегда следует избегать установки дренажного дренажа.Это связано с последующим постоянным выводом через дренажную трубку большого объема, что приводит к значительному сдвигу жидкости, истощению белков и электролитов, риску инфицирования и кровотечения.
Является ли установка дренажной трубки после склероза вариантом лечения?
Нет! Установка грудной трубки с последующим введением склерозирующего агента (например, талька, тетрациклина) имеет ограниченный успех из-за быстрого накопления жидкости в плевральной полости, что препятствует висцерально-париетальной коаптации плевры и симфизу.Большой объем этих излишеств, обеспечивающий легкий путь выхода асцита, делает эти излияния невосприимчивыми к плевродезу. Поэтому ошибочно предполагать установку плевральной дренажной трубки с целью последующего выполнения плевродеза.
Если у пациента наблюдается одышка из-за выпота, временное облегчение может быть достигнуто с помощью плевроцентеза, так как начинается дальнейший контроль асцита, но установка дренажной трубки почти всегда является ошибкой.
Есть ли разумные варианты хирургического вмешательства?
Да.Сообщалось об успешных результатах использования талькового плевродеза с помощью видео-торакоскопии (VATS), хотя часто необходимы повторные процедуры. Сообщалось об успешном хирургическом лечении дефектов диафрагмы с хирургическим плевродезом или без него. Используя подход VATS, дефекты диафрагмы выявляются и закрываются с помощью швов. Другие описанные методы включают восстановление ВАТС с использованием плеврального лоскута или армирования только сеткой.
Сообщалось об успешном хирургическом лечении дефектов диафрагмы с хирургическим плевродезом или без него. Используя подход VATS, дефекты диафрагмы выявляются и закрываются с помощью швов. Другие описанные методы включают восстановление ВАТС с использованием плеврального лоскута или армирования только сеткой.
Эти процедуры следует считать паллиативными и их можно попробовать как альтернативу частым торакоцентезам и TIPS.Плевродез и / или хирургическая пластика диафрагмы должны быть зарезервированы для пациентов, которым не удалось принять консервативные меры, и следует учитывать повышенную заболеваемость и смертность при операциях у пациента с печеночной недостаточностью, прежде чем рассматривать любой из этих подходов в качестве рационального варианта.
Сообщалось о случаях установки туннельного плеврокутанного катетера для лечения симптоматического гидроторакса печени. К преимуществам этого метода относятся простота введения и предотвращение повторного плевроцентеза и связанных с ним осложнений. Основной риск постоянного катетера связан с риском инфицирования, который может быть связан с повышенной смертностью в этой популяции пациентов.
Основной риск постоянного катетера связан с риском инфицирования, который может быть связан с повышенной смертностью в этой популяции пациентов.
Перитонеовенозный шунт (шунт Ле Вина) отводит асцит из брюшной полости в венозную систему и использовался в прошлом для лечения гидроторакса печени. Из-за их ограниченной эффективности и высокой частоты осложнений шунты Ле Вина больше не используются для лечения гидроторакса печени.
5. Мониторинг, наблюдение и лечение
Гидроторакс печени
После обследования гидроторакса печени за пациентом следует внимательно наблюдать в течение 24 часов на предмет повторения симптомов и признаков и осложнений, связанных с плевроцентезом.Что наиболее важно, рентгенографию следует проводить вскоре после завершения процедуры, чтобы исключить пневмоторакс и оценить влияние удаления жидкости. HgB следует контролировать в течение 6-24 часов, чтобы убедиться в отсутствии внутреннего кровотечения. Наконец, необходимо назначить медикаментозную терапию для контроля асцита, иначе излияние будет повторяться.
Наконец, необходимо назначить медикаментозную терапию для контроля асцита, иначе излияние будет повторяться.
Гемоторакс
После установки плевральной трубки за пациентом следует внимательно наблюдать в течение 24 часов для оценки продолжающегося кровотечения и повторения сопутствующих симптомов и признаков.Вскоре после процедуры следует провести рентгенографию, чтобы оценить правильность размещения трубки и влияние удаления жидкости. Выход из грудной трубки следует определять каждые 1-2 часа, а уровень HgB следует проверять каждые 6-8 часов. Тщательное наблюдение должно продолжаться не менее 12-24 часов в зависимости от этиологии, объема и скорости кровотечения.
Последующие рентгеновские снимки грудной клетки и компьютерная томография должны быть выполнены для оценки очистки плевральной полости от крови, поскольку остаточная кровь, которая не может оттекать после торакостомии через зонд, является независимым предиктором развития эмпиемы и требует лечения раннее ВАТС, в течение 3-7 дней после госпитализации.
Кровь имеет тенденцию к формированию со временем и образует толстую корку, которая может привести к «застреванию» нерасширяющегося легкого. На этом этапе требуется хирургическое вмешательство (видео-торакоскопия или торакотомия) для удаления кожуры для облегчения расширения легких. Ранняя торакоскопия (до 3-го дня) при задержке гемоторакса была связана со снижением сложности операции, контаминации / инфицирования сгустка и продолжительности пребывания в больнице по сравнению с теми, которые выполнялись позже. Дополнительные преимущества включают меньшее количество легочных осложнений, более короткое время до выздоровления и менее длительную нетрудоспособность.
VATS может быть предпринята позже при ретеншном гемотораксе; тем не менее, процент перехода к открытой торакотомии увеличивается с более длительными задержками. Должен быть низкий порог для раннего направления к специалисту по очистке VATS, если у пациента сохраняется кровь, несмотря на адекватный дренаж через дренаж через дренажную трубку.
Сообщалось об использовании тромболитиков для лечения подострых (6-13-дневных) скоплений у пациентов с высоким риском торакотомии; однако хирургическое вмешательство является методом выбора, когда это возможно.
Патофизиология
Гидроторакс печени
Гидроторакс печени возникает в результате прямого прохождения асцита через небольшие дефекты диафрагмы, называемые фенестрациями. Эти фенестрации видны микроскопически как разрывы пучков коллагена в сухожильной диафрагме. Асцит проталкивается через эти отверстия в плевральную полость вниз по градиенту давления от более высокого внутрибрюшного давления к более низкому внутриплевральному давлению.
Как только абсорбционная способность поверхности плевры нарушена, жидкость накапливается, что приводит к плевральному выпоту.Считается, что накоплению плевральной жидкости при гидротораксе печени способствуют дополнительные механизмы, включая гипоальбуминемию (снижение коллоидно-осмотического давления), перито-плевральный лимфатический дренаж и гипертензию из асиготных вен с утечкой плазмы, поскольку не у всех пациентов с этим заболеванием имеется сосуществующий асцит.
Гемоторакс
Помимо травмы, большинство случаев гемоторакса в отделении интенсивной терапии связано с вмешательствами, включая торакоцентез, введение плевральной дренажной трубки, установку катетера по центральной линии или правому отделу сердца, а источник кровотечения обычно имеет венозное происхождение.Гемоторакс также возникает после торакальных и кардиохирургических вмешательств.
Торакоцентез часто выполняется у пациентов в отделении интенсивной терапии для оценки плевральной жидкости, а кровотечение, связанное с плевральным кровотечением, обычно незначительное и проходит без дополнительных вмешательств. Сильное кровотечение может возникнуть в результате разрыва межреберного сосуда.
Сообщалось о травмах селезенки и печени во время торакоцентеза; однако у этих пациентов чаще встречается внутрибрюшное кровотечение. Наличие в анамнезе нарушений свертываемости крови, приема антикоагулянтов и почечной недостаточности может увеличить риск кровотечения у пациентов, перенесших плевроцентез и другие инвазивные торакальные процедуры.
Гемоторакс после введения дренажной трубки — известное осложнение. Отток крови из плевральной дренажной трубки обычно является первым признаком осложнения вставочного кровотечения. Всегда следует получать рентгенограммы после установки дренажной трубки, чтобы подтвердить положение трубки и определить, были ли приняты во внимание показания к установке. Новое помутнение после установки трубки должно предупредить врача о повреждении паренхимы легкого или о возможном развитии гемоторакса.
Чтобы избежать гемоторакса, связанного с грудной клеткой, антикоагулянтную терапию следует прекратить в надлежащее время, а коагулопатию — по возможности обратить вспять. Пневматическая трубка должна быть проложена прямо поверх желаемого ребра. Это снижает риск повреждения межреберной вены и артерии, лежащих в нижней части ребер. Может возникнуть мышечное кровотечение, которое обычно проходит самостоятельно; однако повреждение мышечных артериальных и венозных ветвей может привести к стойкому кровотечению, требующему хирургического вмешательства.
Установка центрального венозного катетера — это часто выполняемая процедура в ОИТ. Подключичная вена расположена на вершине грудной клетки, рядом с плеврой, и проникновение вены через свободную стенку может вызвать гемоторакс. Сообщалось о травмах яремной вены, подключичной артерии и правого предсердия, приводящих к гемотораксу. Венозное повреждение в месте соединения левой брахиоцефальной верхней полой вены иногда происходит при вставке левых внутренних яремных или подключичных линий.
Осложнения, связанные с введением катетера в легочную артерию, включают сердечную аритмию, пункцию сонной и подключичной артерий, катетер-ассоциированный сепсис и катетер-индуцированный разрыв легочной артерии (PA).Гемоторакс после разрыва ЛА, вызванного катетером, представляет собой опасное для жизни осложнение, связанное с высокой смертностью. Оптимальна экстренная торакотомия с восстановлением прямой травмы; однако для остановки кровотечения может потребоваться лобэктомия или пневмонэктомия.
Попытки избежать разрыва ЛА включают надувание баллона в крупные артерии перед продвижением катетера, минимизацию времени, проведенного в положении клина, и удаление воздуха из баллона до извлечения катетера.
Эпидемиология
NA
Прогноз
Гидроторакс печени
Прогноз пациентов с гидротораксом печени во многом зависит от основного заболевания печени.
Гемоторакс
Прогноз гемоторакса во многом зависит от причины. В случае травмы прогноз отличный. Если причиной гемоторакса является злокачественное новообразование, то прогноз мрачный и четко определяется злокачественным новообразованием.
Особые рекомендации для медсестер и смежных медицинских работников.
NA
Какие доказательства?
Гурунг, П., Голдблатт, М., Хаггинс, Дж. Т., Доелкен, П., Нитерт, П.Дж., Сан, С.А. «Анализ плевральной жидкости и рентгенографические, сонографические и эхокардиографические характеристики гидроторакса печени». Сундук. об. 140. 2011. С. 448-53. (В статье представлен подробный анализ жидкости пациентов, перенесших плевроцентез по поводу гидроторакса печени.)
Mercky, P, Sakr, L, Heyries, L. «Использование туннельного плеврального катетера для лечения рефрактерного гидроторакса печени: новый терапевтический вариант». Дыхание. об. 80. 2010. С. 348-352. (Авторы описывают успешное ведение пациента с гидротораксом печени с помощью туннельного катетера плеврекса)
Алонсо, JC.«Плевральный выпот при заболеваниях печени». Семинары по респираторной медицине и реанимации. об. 31. 2010. С. 698-705.
Гурунг, П., Голдблатт, М., Хаггинс, Дж. Т., Доелкен, П., Нитерт, П.Дж., Сан, С.А. «Анализ плевральной жидкости и рентгенографические, сонографические и эхокардиографические характеристики гидроторакса печени». Сундук. об. 140. 2011. С. 448-53.
Roussos, A, Philippou, N, Mantzaris, GJ, Gourgouliannis, KI. «Гидроторакс печени: патофизиологическая диагностика и лечение». Журнал гастроэнтерологии и гепатологии. об. 22. 2007. С. 1388–93. (Обзорная статья, посвященная патогенезу, клиническим проявлениям, диагностике и лечению гидроторакса печени).
Cerfolio, RJ, Bryant, AS. «Эффективность видеоассистированной торакоскопической хирургии с тальковым плевродезом при синдроме пористой диафрагмы у пациентов с рефрактерным гидротораксом печени». Анналы торакальной хирургии. об. 82. 2006. С. 457-9. (Авторы описывают хирургический подход с использованием видеоторакоскопии с тальковым плевродезом для лечения рефрактерного гидроторакса печени, который оказался успешным в борьбе с выпотом у 3/4 пациентов.)
ДюБозе, Дж., Инаба, К., Деметриадес, Д., Скалея, Т.М., О’Коннор, Дж., Менакер, Дж., Моралес, К., Константинидис, А., Шифлетт, А., Копвуд, Б. «Группа исследования сохраненного гемоторакса AAST. Ведение посттравматического ретинированного гемоторакса: проспективное обсервационное многоцентровое исследование AAST ». Журнал травматологической и неотложной хирургии. об. 72. 2012. С. 11–22. (В статье рассматриваются практические модели и факторы, влияющие на успешное ведение посттравматического ретинированного гемоторакса, и определяются предикторы необходимости торакотомии у этих пациентов).
Мауэри, Н.Т., Гюнтер, О.Л., Коллиер, Б.Р., Диас, Дж.Дж., Хаут, Э., Хилдрет, А., Холевар, М., Мэйберри, Дж., Стрейб, Э. «Практическое руководство по лечению гемоторакса и скрытого пневмоторакса». Журнал травм, травм, инфекций и интенсивной терапии. об. 70. 2011. С. 510-8.
Пневматикос, И., Бурос, Д. «Плевральные выпоты у тяжелобольных». Дыхание. об. 76. 2008. С. 241-8. (Авторы описывают оценку и лечение плеврального выпота у пациентов в критическом состоянии, уделяя особое внимание начальному и последующему лечению гемоторакса у этих пациентов).
Copyright © 2017, 2013 ООО «Поддержка принятия решений в медицине». Все права защищены.
Ни один спонсор или рекламодатель не участвовал, не одобрял и не платил за контент, предоставляемый Decision Support in Medicine LLC. Лицензионный контент является собственностью DSM и защищен авторским правом.
Плевральный выпот — причины, симптомы, типы и лечение
Плевральный выпот — это необычное количество жидкости вокруг легкого. Многие медицинские условия могут привести к этому, поэтому, даже если ваш плевральный выпот, возможно, придется удалить, ваш врач, скорее всего, нацелит лечение на то, что вызвало его.
Плевра — это тонкая мембрана, выстилающая поверхность легких и внутреннюю часть грудной клетки. Когда у вас плевральный выпот, жидкость накапливается в пространстве между слоями плевры.
Обычно в плевральной полости находятся только чайные ложки водянистой жидкости, что позволяет вашим легким плавно перемещаться в грудной полости, когда вы дышите.
Причины
Плевральный выпот может быть вызван множеством факторов. Вот некоторые из наиболее распространенных:
Утечка из других органов. Это обычно случается, если у вас застойная сердечная недостаточность, когда ваше сердце не перекачивает кровь к вашему телу должным образом. Но это также может быть связано с заболеванием печени или почек, когда жидкость накапливается в вашем теле и просачивается в плевральную полость.
Продолжение
Рак. Обычно проблемой является рак легких, но другие виды рака, распространившиеся на легкие или плевру, также могут вызывать ее.
Инфекции. Некоторые болезни, которые приводят к плевральному выпоту, — это пневмония или туберкулез.
Аутоиммунные состояния. Волчанка или ревматоидный артрит — это некоторые заболевания, которые могут его вызывать.
Тромбоэмболия легочной артерии. Это закупорка артерии одного из легких, которая может привести к плевральному выпоту.
Признаки
У вас их может не быть. Вероятность появления симптомов выше при плевральном выпоте среднего или большого размера, а также при воспалении.
Если у вас есть симптомы, они могут включать:
- Одышку
- Боль в груди, особенно при глубоком вдохе (это называется плевритом или плевритной болью.)
- Лихорадка
- Кашель
Диагноз
Ваш врач расскажет вам о ваших симптомах и проведет медицинский осмотр. Они постучат вам по груди и послушают с помощью стетоскопа.
Чтобы подтвердить, что у вас плевральный выпот, вам необходимо пройти визуализацию, например:
Рентген грудной клетки. Плевральный выпот на рентгеновских снимках выглядит белым, а воздушное пространство — черным. Если вероятен плевральный выпот, вы можете сделать больше рентгеновских снимков, лежа на боку.Они могут показать, свободно ли течет жидкость в плевральной полости.
Продолжение
Компьютерная томография (компьютерная томография). КТ-сканер быстро принимает множество рентгеновских снимков, а компьютер создает изображения всей грудной клетки — внутри и снаружи. КТ показывает больше деталей, чем рентген грудной клетки.
Ультразвук. Датчик на груди создает изображения внутренней части вашего тела, которые отображаются на видеоэкране. Ваш врач может использовать ультразвук, чтобы определить местонахождение жидкости и взять образец для анализа.
Кроме того, ваш врач может провести процедуру, называемую торакоцентез. Для проверки возьмут немного жидкости. Для этого они вводят иглу и трубку, называемую катетером, между ребрами в плевральную полость.
Типы
Вы можете слышать, как ваш врач использует термины «транссудативный» и «экссудативный» для описания двух основных типов плевральных выпотов.
Транссудативный. Эта жидкость из плеврального выпота похожа на жидкость, которая обычно содержится в плевральной полости.Он образуется из жидкости, протекающей через нормальную плевру. Этот тип редко нужно сливать, если он не очень большой. Застойная сердечная недостаточность — наиболее частая причина этого типа.
Экссудативный. Он образуется из лишней жидкости, белка, крови, воспалительных клеток или иногда бактерий, которые проникают через поврежденные кровеносные сосуды в плевру. Возможно, вам потребуется его дренировать, в зависимости от его размера и степени воспаления. Причины этого типа включают пневмонию и рак легких.
Лечение
Вашему врачу может потребоваться лечение только того заболевания, которое вызвало плевральный выпот. Например, вы получите антибиотики от пневмонии или диуретики от сердечной недостаточности.
Большие, инфицированные или воспаленные плевральные выпоты часто необходимо дренировать, чтобы улучшить самочувствие и предотвратить появление новых проблем.
Процедуры лечения плеврального выпота включают:
Торакоцентез. Если выпот большой, врач может выпить больше жидкости, чем нужно для анализа, просто для облегчения симптомов.
Торакостомия через трубку (грудная трубка). Врач делает небольшой разрез в грудной стенке и вводит пластиковую трубку в плевральную полость на несколько дней.
Плевральный дренаж. Если плевральный выпот продолжает возвращаться, врач может ввести катетер длительного действия через кожу в плевральную полость. После этого вы сможете удалить плевральный выпот в домашних условиях. Ваш врач скажет вам, как и когда это делать.
Продолжение
Pleurodesis .Ваш врач вводит раздражающее вещество (например, тальк или доксициклин) через дренажную трубку в плевральную полость. Вещество вызывает воспаление плевры и грудной клетки, которые затем плотно связываются друг с другом по мере заживления. Во многих случаях плевродез может предотвратить повторение плеврального выпота.
Декортикация плевры. Хирурги могут работать внутри плевральной полости, удаляя потенциально опасные воспаления и нездоровые ткани. Для этого хирург может сделать небольшие надрезы (торакоскопия) или большие (торакотомия).
Плевральный выпот: причины, диагностика и лечение
Плевральный выпот — это скопление жидкости в пространстве между легкими и грудной полостью. Это может быть результатом пневмонии и многих других заболеваний. Это также может быть опасно для жизни.
Плевральный выпот, или «вода в легких», может напоминать респираторную инфекцию. Иногда причина может быть респираторной, но есть и другие возможные причины. Медицинскому работнику необходимо будет диагностировать первопричину, чтобы назначить соответствующее лечение.
Симптомы плеврального выпота могут включать кашель, боль в груди и затрудненное дыхание.
В этой статье будет рассмотрено, что происходит при плевральном выпоте, почему он возникает, и некоторые варианты решения этой проблемы.
Когда у человека наблюдается плевральный выпот, это означает, что жидкость собралась в пространстве между легкими и грудной полостью или плевральной полостью. И легкие, и грудная полость имеют слизистую оболочку, состоящую из плевры, которая представляет собой тонкую мембрану.
В здоровых легких эти мембраны обеспечивают наличие небольшого количества жидкости между легкими и грудной клеткой.Это предотвращает трение, поскольку легкие расширяются и сжимаются во время дыхания.
Однако у человека с плевральным выпотом в плевральной полости слишком много жидкости.
Любому, у кого может быть плевральный выпот, требуется немедленная медицинская помощь, поскольку без лечения это может быть опасно для жизни.
Плевральный выпот всегда является результатом другого заболевания. Это может быть вызвано многими условиями. Вот некоторые из наиболее частых причин:
Некоторые медицинские процедуры также могут вызвать плевральный выпот.Примеры из них:
- операция на открытом сердце или другая операция на грудной клетке
- определенные лекарства, включая метотрексат, амиодарон и фенитоин
- лучевая терапия
- гиперстимуляция яичников
У некоторых людей нет симптомов плеврального выпота . Если симптомы все же возникают, они обычно начинают появляться по мере того, как жидкость заполняет грудную полость.
Некоторые возможные симптомы включают:
- сухой или непродуктивный кашель
- затрудненное дыхание, особенно в положении лежа
- лихорадка и симптомы гриппа
- боль в груди
- резкая, сильная боль при глубоком вдохе
Постоянная икота также может быть признаком плеврального выпота.
Некоторые люди узнают, что у них плевральный выпот, только когда проходят тест на другое заболевание.
Также важно отметить, что симптомы плеврального выпота могут напоминать симптомы других заболеваний легких. Человеку требуется срочная медицинская помощь, если он испытывает какие-либо из этих симптомов.
Ниже представлена трехмерная модель плеврального выпота. Он полностью интерактивен.
Изучите модель с помощью коврика для мыши или сенсорного экрана, чтобы узнать больше об этом состоянии.
Диагностировать плевральный выпот может быть сложно, поскольку симптомы могут частично совпадать с симптомами многих других состояний.
Чтобы поставить диагноз, медицинский работник:
- спросит человека об его симптомах
- спросит его об общем состоянии его здоровья и истории болезни
- проведет физический осмотр
- предложит визуализирующие тесты, такие как X- лучевая, ультразвуковая или компьютерная томография
Медицинскому работнику также необходимо определить, является ли выпот транссудатом или экссудатом.В следующих разделах эти типы рассматриваются более подробно.
Выпот транссудата
Выпот транссудата обычно возникает, когда другое состояние вызывает дисбаланс давления в кровеносных сосудах. В результате жидкость просачивается обратно в грудную клетку. Жидкость в выпоте, вероятно, будет состоять из соединений из плазмы крови.
Выпот экссудата
Выпот экссудата обычно возникает в результате:
- воспалительных состояний
- инфекции
- рака
- травматического повреждения
- закупорки кровеносных или лимфатических сосудов в этой области
Медицинский работник может взять образец жидкость из плевральной полости путем введения иглы между ребрами.
Эти образцы могут помочь обнаружить признаки инфекции, уровень белка и раковые клетки. Они также могут помочь определить, есть ли у человека осложненный или неосложненный плевральный выпот.
При осложненном плевральном выпоте в жидкости будут присутствовать признаки воспаления или инфекции. Человеку может потребоваться немедленное лечение, чтобы предотвратить потенциально серьезные осложнения.
При неосложненном выпоте в жидкости не будет никаких признаков инфекции или воспаления.Неосложненный выпот может протекать легче и с меньшей вероятностью приведет к необратимому повреждению легких.
Некоторые другие тесты могут помочь определить причину выпота. К ним относятся:
- функциональные тесты почек
- функциональные тесты печени
- биопсия легких
- бронхоскопия
- ультразвуковое исследование сердца для оценки сердечной недостаточности
Эти тесты помогают медицинскому работнику сузить причину плеврального выпота и обеспечить соответствующее лечение.
Лечение будет зависеть от основной причины. Помимо лечения основного заболевания, медицинскому работнику может потребоваться слить жидкость из груди.
Слив из грудной клетки
Чтобы опорожнить грудную клетку, врач вставит трубку в плевральную полость и позволит жидкости покинуть тело.
Они будут использовать местные анестетики, чтобы обезболить боль в месте проникновения иглы в тело. Когда действие анестетиков прекратится, эта область может болеть.
Им также может потребоваться повторить процесс, если жидкость продолжает собираться в плевральной полости.
Существует небольшой риск осложнений, связанных с дренированием грудной клетки. К ним относятся:
- инфекция
- кровотечение
- коллапс легкого
- жидкость, попадающая в легкие
Однако эти осложнения возникают редко.
Другие методы лечения
В некоторых случаях могут потребоваться другие методы лечения.
При плевродезе, например, хирург закрывает зазор между плеврой легкого и грудной полостью, чтобы предотвратить скопление жидкости между ними.
В более тяжелых случаях хирург может направить жидкость из грудной полости в брюшную полость. В некоторых случаях они могут также удалить часть плевральной оболочки.
Плевральный выпот — признак основного заболевания. И основное заболевание, и сам плевральный выпот могут быть опасными для жизни.
Перспектива и время, необходимое для выздоровления, будут зависеть от причины излияния, общего состояния здоровья человека и тяжести его симптомов.
Человеку, возможно, потребуется провести время в больнице, где он может пройти обследования и наблюдение.Лечение часто может устранить плевральный выпот, хотя не всегда возможно вылечить его первопричину.
|
Диагностический подход к плевральному выпоту у взрослых
1.Легкая RW. Клиническая практика. Плевральный выпот. N Engl J Med . 2002; 346: 1971-7 ….
2. Эфрати О, Барак А. Плевральные выпоты в педиатрической популяции. Педиатр Ред. . 2002; 23: 417–26.
3. Легкая RW. Заболевания плевры. 4-е изд. Филадельфия: Lippincott Williams & Wilkins, 2001.
4. Porcel JM, Вивес М. Этиология и характеристика плевральной жидкости больших и массивных выпотов. Сундук .2003. 124: 978–83.
5. Фарфор JM, Light RW. Торакоцентез. PIER, Американский колледж врачей, 2004. Доступно онлайн 28 октября 2004 г. по адресу: http: //pier.acponline.org. Требуется подписка.
6. Джонс П. В., Мойерс Дж. П., Роджерс Дж. Т., Родригес Р.М., Ли YC, Легкая RW. Торакоцентез под ультразвуковым контролем: безопаснее ли это? Сундук . 2003; 123: 418–23.
7. Виллена В., Лопес-Энкуентра А, Гарсия-Лухан Р., Echave-Sustaeta J, Мартинес CJ.Клинические последствия появления плевральной жидкости при плевроцентезе. Сундук . 2004; 125: 156–9.
8. Фарфор JM, Вивес М, Висенте де Вера MC, Цао Г, Рубио М, Rivas MC. Полезные анализы плевральной жидкости, позволяющие отличить транссудаты от экссудата. Энн Клин Биохим . 2001; 38: 671–5.
9. Romero-Candeira S, Фернандес К, Мартин С, Санчес-Пайя J, Эрнандес Л.Влияние диуретиков на концентрацию белков и других компонентов плевральных транссудатов у пациентов с сердечной недостаточностью. Am J Med . 2001; 110: 681–6.
10. Romero-Candeira S, Эрнандес Л. Разделение транссудатов и экссудатов с особым упором на градиент белка. Curr Opin Pulm Med . 2004; 10: 294–8.
11. Хеффнер Дж. Э., Хайленд К, Коричневый LK. Вывод метаанализа непрерывных отношений правдоподобия для диагностики экссудата плевральной жидкости. Am J Respir Crit Care Med . 2003. 167: 1591–9.
12. Barnes TW, Олсон Э.Дж., Моргенталер Т.И., Эдсон Р.С., Деккер П.А., Ryu JH. Низкие результаты микробиологических исследований образцов плевральной жидкости. Сундук . 2005; 127: 916–21.
13. Сан С.А., Хеффнер Дж. Э. Анализ плевральной жидкости. В: Light RW, Гэри Ли YC. Учебник по болезням плевры. Лондон: Арнольд, 2003: 191–209.
14. Colice GL, Кертис А, Deslauriers J, Хеффнер Дж. Свет R, Литтенберг Б, и другие.Медикаментозное и хирургическое лечение парапневмонических выпотов: научно обоснованное руководство. Сундук . 2000; 118: 1158–71.
15. Дэвис К. В., Глисон FV, Дэвис Р.Дж., Группа заболеваний плевры. Комитет по стандартам ухода, Британское торакальное общество. Руководство BTS по лечению плевральной инфекции. Грудь . 2003; 58 (добавление 2): ii18–28.
16. Виллена В., Перес V, Посо Ф, Лопес-Энкуентра А, Echave-Sustaeta J, Arenas J, и другие.Уровни амилазы в плевральных выпотах: последовательная неизбирательная серия из 841 пациента. Сундук . 2002; 121: 470–4.
17. Виллена В., Лопес-Энкуентра А, Посо Ф, Echave-Sustaeta J, Ортуо-де-Соло B, Эстеноз-Альфаро Дж., и другие. Уровни гамма-интерферона в плевральной жидкости для диагностики туберкулеза. Am J Med . 2003; 115: 365–70.
18. Фарфор JM, Вивес М, Цао Г, Эскерда А, Рубио М, Ribas MC.Измерение натрийуретического пептида пробрена в плевральной жидкости для диагностики плеврального выпота из-за сердечной недостаточности. Am J Med . 2004; 116: 417–20.
19. Фарфор JM. Использование натрийуретического пептида пробрена в плевральной жидкости для диагностики плевральных выпотов в результате сердечной недостаточности. Curr Opin Pulm Med . 2005; 11: 329–33.
20. Фальгера М, Лопес А, Nogués A, Фарфор JM, Рубио-Кабальеро М.Оценка метода полимеразной цепной реакции для обнаружения ДНК Streptococcus pneumoniae в образцах плевральной жидкости. Сундук . 2002; 122: 2212–6.
21. Пай М, Флорес LL, Хаббард А, Райли Л.В., Колфорд Дж. М. мл. Тесты амплификации нуклеиновых кислот в диагностике туберкулезного плеврита: систематический обзор и метаанализ. BMC Infect Dis . 2004; 4: 6
22. Дикмен Г., Дикмен Э, Кара М, Сахин Э, Доган П, Оздемир Н.Диагностические значения активности теломеразы в плевральных выпотах. Eur Respir J . 2003. 22: 422–6.
23. Фарфор JM, Вивес М, Эскерда А, Салуд А, Перес Б, Родригес-Панадеро Ф. Использование панели онкомаркеров (карциноэмбриональный антиген, раковый антиген 125, углеводный антиген 15–3 и фрагменты цитокератина 19) в плевральной жидкости для дифференциальной диагностики доброкачественных и злокачественных выпотов. Сундук .2004; 126: 1757–63.
24. Фарфор JM, Салуд А, Вивес М, Эскерда А, Родригес-Панадеро Ф. Растворимый онкопротеин 185 (HER-2) в плевральной жидкости имеет ограниченную полезность для диагностической оценки злокачественных выпотов. Clin Biochem . 2005; 38: 1031–3.
25. Коннер Б.Д., Ли YC, Бранка П., Роджерс Дж. Т., Родригес Р.М., Легкая RW. Различия в количестве лейкоцитов в плевральной жидкости и дифференциальном подсчете для разных контейнеров для образцов и разных методов. Сундук . 2003; 123: 1181–7.
26. Фарфор JM, Вивес М. Дифференциация туберкулеза от злокачественного плеврального выпота: оценочная модель. Медицинский Научный Монит . 2003; 9: CR175–80.
27. Goto M, Ногучи Ы, Кояма Х, Хира К, Шимбо Т, Фукуи Т. Диагностическое значение аденозиндезаминазы при туберкулезном плевральном выпоте: метаанализ. Энн Клин Биохим . 2003. 40: 374–81.
28.Греко S, Жирарди Э, Masciangelo R, Capoccetta GB, Сальтини К. Измерения аденозиндезаминазы и гамма-интерферона для диагностики туберкулезного плеврита: метаанализ. Int J Tuberc Lung Dis . 2003; 7: 777–86.
29. Фарфор JM, Вивес М. Уровни аденозиндезаминазы в нетуберкулезных лимфоцитарных плевральных выпотах. Сундук . 2002; 121: 1379–80.
30. Хименес Кастро Д, Диас Нуэво G, Перес-Родригес Э., Легкая RW.Диагностическое значение аденозиндезаминазы при нетуберкулезных лимфоцитарных плевральных выпотах. Eur Respir J . 2003. 21: 220–4.
31. Дэвис П.Д. Туберкулезный плеврит. В: Bouros D, ed. Заболевание плевры. Нью-Йорк: Марсель Деккер, 2004: 677–97.
32. Хасанин Н.А., Заки МЭ, Шалабы Х.М., Эль-Морси А.С. Полимеразная цепная реакция биопсии плевры — быстрый и чувствительный метод диагностики туберкулезного плеврального выпота. Сундук .2003. 124: 2105–11.
33. Маскелл Н.А., Батленд Р.Дж., Группа заболеваний плевры, Комитет по стандартам лечения, Британское торакальное общество. Руководство BTS по исследованию одностороннего плеврального выпота у взрослых. Грудь . 2003; 58 (приложение 2): ii8–17.
34. Саллах С.М., Саллах Ж.А., Васкес Э, Шульц Л, Квале П. Объем плевральной жидкости, необходимый для диагностики злокачественного образования плевры. Сундук .2002; 122: 1913–7.
35. Аренас-Хименес Дж., Алонсо-Чартерина С, Санчес-Пайя J, Фернандес-Латорре Ф, Хиль-Санчес С, Льорет-Льоренс М. Оценка результатов КТ для диагностики плеврального выпота. Eur Radiol . 2000; 10: 681–90.
36. Duysinx B, Нгуен Д, Луи Р, Катальдо Д., Белхоцин Т, Бартч П., и другие. Оценка поражения плевры с помощью позитронно-эмиссионной томографии с 18-фтордезоксиглюкозой. Сундук . 2004; 125: 489–93.
37. Пракаш УБ, Reiman HM. Сравнение игольной биопсии с цитологическим анализом для оценки плеврального выпота: анализ 414 случаев. Mayo Clin Proc . 1985; 60: 158–64.
38. Маскелл Н.А., Глисон FV, Дэвис Р.Дж. Стандартная биопсия плевры в сравнении с биопсией с режущей иглой под контролем КТ для диагностики злокачественных опухолей плеврального выпота: рандомизированное контролируемое исследование. Ланцет .2003; 361: 1326–30.
39. Антоний В.Б., Loddenkemper R, Астул П, Бутин С, Золотая солома П, Хотт Дж, и другие. Лечение злокачественных плевральных выпотов. Eur Respir J . 2001; 18: 402–19.
40. Легкая RW. Обновление: лечение трудно диагностируемого плеврального выпота. Клин Пульм Мед . 2003; 10: 39–46.
41. Венекамп Л.Н., Велкенирс Б, Ноппен М.Существует ли «идиопатический плеврит»? Естественное течение неспецифического плеврита, диагностированного после торакоскопии. Дыхание . 2005. 72: 74–8.
Жидкость в грудной клетке (плевральный выпот)
Что такое плевральный выпот?
Плевральный выпот, также называемый водой в легких, — это чрезмерное скопление жидкости в пространстве между легкими и грудной полостью.
Тонкие оболочки, называемые плеврой, покрывают внешнюю часть легких и внутреннюю часть грудной полости.Внутри этой подкладки всегда есть небольшое количество жидкости, которая помогает смазывать легкие, поскольку они расширяются в груди во время дыхания.
Некоторые заболевания могут вызывать плевральный выпот.
По данным Американского торакального общества, плевральный выпот является обычным явлением, ежегодно в США диагностируется около 1 миллиона случаев. Это серьезное заболевание, связанное с повышенным риском смерти. В одном исследовании 15 процентов госпитализированных людей с диагнозом плевральный выпот умерли в течение 30 дней.
Плевра выделяет слишком много жидкости, когда она раздражена, воспалена или инфицирована. Эта жидкость накапливается в грудной полости за пределами легких, вызывая так называемый плевральный выпот.
Определенные виды рака могут вызывать плевральный выпот, наиболее распространенными являются рак легких у мужчин и рак груди у женщин.
Другие причины плеврального выпота включают:
Существует несколько типов плевральных выпотов, каждый из которых имеет разные причины и варианты лечения. Первая классификация плевральных выпотов бывает транссудативной или экссудативной.
Транссудативный плевральный выпот
Этот тип вызывается утечкой жидкости в плевральную полость в результате либо низкого количества белка в крови, либо повышенного давления в кровеносных сосудах. Наиболее частая причина — застойная сердечная недостаточность.
Экссудативный выпот
Этот тип вызван:
- блокировкой лимфы или кровеносных сосудов
- воспалением
- опухолями
- травмой легких
Общие состояния, которые могут привести к этому типу плевральной инфузии, включают легочную эмболию, пневмонию и грибковые инфекции.
Осложненные и неосложненные плевральные выпоты
Есть также сложные и неосложненные плевральные выпоты. Неосложненные плевральные выпоты содержат жидкость без признаков инфекции или воспаления. У них гораздо меньше шансов вызвать необратимые проблемы с легкими.
Осложненные плевральные выпоты, однако, содержат жидкость со значительной инфекцией или воспалением. Они требуют немедленного лечения, которое часто включает дренирование грудной клетки.
У некоторых людей симптомы плеврального выпота отсутствуют.Эти люди обычно узнают о своем заболевании на рентгеновском снимке грудной клетки или при физическом обследовании по другой причине.
Общие симптомы плеврального выпота включают:
Немедленно обратитесь к врачу, если у вас есть симптомы плеврального выпота.
Ваш врач проведет медицинский осмотр и послушает ваши легкие с помощью стетоскопа. Они также могут заказать рентген грудной клетки, чтобы диагностировать плевральный выпот. Другие возможные тесты включают:
При анализе плевральной жидкости ваш врач удалит жидкость из области плевральной мембраны, введя иглу в грудную полость и всасывая жидкость шприцем.Процедура называется плевроцентез. Это также обычная процедура для слива лишней жидкости из грудной полости. Затем жидкость будет проверена для определения причины.
Ваш врач может также выбрать биопсию плевры, которая включает взятие образца ткани плевры. Это можно сделать, введя небольшую иглу снаружи грудной клетки в грудную полость.
Если они обнаруживают, что у вас плевральный выпот, но не могут определить, какой тип, ваш врач может назначить торакоскопию.Это хирургическая процедура, которая позволяет врачу заглянуть внутрь грудной клетки с помощью оптоволоконной камеры.
Для этой процедуры ваш врач сделает несколько небольших разрезов в области груди, пока вы находитесь под общей анестезией. Затем они вставляют камеру через один разрез, а хирургический инструмент — через другой, чтобы извлечь небольшое количество жидкости или ткани для анализа.
Основная причина состояния и тяжесть выпота будут определять лечение.
Слив жидкости
Как правило, лечение заключается в сливе жидкости из грудной полости с помощью иглы или небольшой трубки, вставленной в грудную клетку.
Перед процедурой вам сделают местную анестезию, что сделает процедуру более комфортной. Вы можете почувствовать боль или дискомфорт в месте разреза после того, как действие анестетика закончится. Большинство врачей пропишут лекарства, чтобы облегчить боль.
Эта обработка может потребоваться более одного раза, если жидкость снова накапливается.
Другие методы лечения могут потребоваться для предотвращения скопления жидкости, если рак является причиной плеврального выпота.
Плевродез
Плевродез — это лечение, при котором возникает легкое воспаление между легким и плеврой грудной полости. После извлечения лишней жидкости из грудной полости врач вводит в эту область лекарство. Препарат часто представляет собой смесь талька. Это лекарство заставляет два слоя плевры слипаться, что предотвращает накопление жидкости между ними в будущем.
Хирургия
В более серьезных случаях врач хирургическим путем вводит шунт или небольшую трубку в грудную полость. Это помогает перенаправить жидкость из груди в брюшную полость, где ее легче удалить. Это может быть вариант для тех, кто не отвечает на другие виды лечения. Плеврэктомия, при которой часть плевральной оболочки удаляется хирургическим путем, также может быть вариантом в определенных случаях.
В некоторых случаях плевральный выпот можно лечить с помощью лекарств и другой поддерживающей терапии.Большинство людей выздоравливают в течение нескольких дней или недель. Незначительные осложнения от более инвазивных методов лечения могут включать легкую боль и дискомфорт, которые часто проходят со временем. В некоторых случаях плевральный выпот может иметь более серьезные осложнения в зависимости от тяжести состояния, причины и применяемого лечения.
К серьезным осложнениям могут относиться:
- отек легких или жидкость в легких, которые могут возникнуть в результате слишком быстрого оттока жидкости во время плевроцентеза
- частичное коллапсирование легкого
- инфекция или кровотечение
Эти серьезные осложнения очень редки. .Ваш врач поможет определить наиболее эффективный вариант лечения и обсудит преимущества и риски каждой процедуры.
Плевральный выпот может быть результатом распространения раковых клеток на плевру. Они также могут быть результатом того, что раковые клетки блокируют поток нормальной жидкости в плевре. Жидкость также может накапливаться в результате определенных методов лечения рака, таких как лучевая терапия или химиотерапия.
Некоторые виды рака с большей вероятностью вызывают плевральный выпот, чем другие, в том числе:
Признаки и симптомы часто включают:
- одышку
- кашель
- боль в груди
- потеря веса
Плевродез часто используется как средство противодействия. лечение злокачественных плевральных выпотов, вызванных раком.Ваш врач может назначить антибиотики, если у вас есть инфекция или вы подвержены ей. Стероиды или другие противовоспалительные препараты могут уменьшить боль и воспаление.
В дополнение к лечению плеврального выпота ваш врач лечит вызвавший его рак. Плевральный выпот обычно является результатом метастатического рака.
Люди, проходящие лечение от рака, также могут иметь ослабленную иммунную систему, что делает их более подверженными инфекциям или другим осложнениям.
Плевральный выпот может быть серьезным и опасным для жизни. Большинству из них требуется госпитализация, а некоторым — операция. Время, необходимое для восстановления после плеврального выпота, зависит от причины, размера и тяжести выпота, а также от вашего общего состояния здоровья.
Вы начнете выздоровление в больнице, где вам будут предоставлены необходимые лекарства и помощь, которые помогут вам начать выздоровление. Многие люди сообщают о чувстве усталости и слабости в первую неделю после выписки из больницы.В среднем вы увидите, что места разрезов после операции заживают в течение двух-четырех недель. Когда вы вернетесь домой, вам потребуется постоянный уход и наблюдение.
Гидроторакс CSF — The Western Journal of Emergency Medicine
]]>| Автор | Принадлежность |
|---|---|
| Николас Теста, MD | Отделение неотложной медицины Медицинской школы Кека Медицинского центра Университета Южной Калифорнии |
| Шон О.Хендерсон, Мэриленд | Отделение неотложной медицины Медицинской школы Кека Медицинского центра Университета Южной Калифорнии |
30-летняя афроамериканка обратилась в отделение неотложной помощи с жалобой на кашель в течение двух месяцев. У пациента в анамнезе была задержка развития, судорожные расстройства и вентрикуло-перитонеальный (ВП) шунт. Физическое обследование было значимым для артериального давления 101/71 мм рт.ст., частоты сердечных сокращений 111 ударов в минуту, частоты дыхания 18 вдохов в минуту и температуры 98 ° F.Она была хорошо развитой женщиной, у которой не было явных проблем с шунтом, пальпируемым на левой стороне черепа, и при нормальном осмотре легких, за исключением слегка ослабленного дыхания в основании левого края. Во время обследования на рентгенограмме грудной клетки был выявлен большой левосторонний плевральный выпот (рис. 1). Пациенту сделали торакоцентез, и первоначально считалось, что жидкость является транссудатом.
Рис. 1Рентген грудной клетки, демонстрирующий левосторонний плевральный выпот.
Последующее компьютерное сканирование грудной клетки выявило кончик VP-шунта в левой части грудной клетки, прилегающий к аорте, что привело к гидротораксу спинномозговой жидкости (рис. 2).Миграция перитонеальных катетеров в грудную клетку, вызывающая гидроторакс, является редким осложнением шунтирования ВП. 1 В некоторых случаях смещение катетера приводит к неисправности и неврологическим нарушениям, чего не было у нашего пациента. 2
Рисунок 2Компьютерная томография грудной клетки, демонстрирующая кончик вентрикуло-перитонеального шунтирующего катетера, прилегающий к аорте.
Сноски
История поступления: Поступила 24 мая 2007 г .; Принята к печати 7 июня 2007 г.
Полный текст доступен в открытом доступе по адресу http: // escholarship.org / uc / uciem_westjem
Адрес для корреспонденции: Шон О. Хендерсон, доктор медицины Департамента неотложной медицины LAC + USC Медицинский центр № 1, комната 1011 1200 N. State St. Los Angeles, CA
Конфликты интересов: Согласно соглашению о представлении статей JEM West , все авторы обязаны раскрывать информацию обо всех аффилированных лицах, источниках финансирования, финансовых или управленческих отношениях, которые могут быть восприняты как потенциальные источники предвзятости. Авторы не раскрывают.
ССЫЛКИ
1. Хадзикарич Н., Массер М., Машани А., Аммар А. Гидроторакс спинномозговой жидкости — В. П. Осложнение шунта без смещения перитонеального катетера. Child’s Nerv Syst, 2002; 18: 179–182.
2. Ган Ю.К., Стейнбок П. Миграция кончика брюшины вентрикулоперитонеального катетера, вызывающая нарушение работы шунта. J Neurosurg. (2 Доп. Педиатрия) 2006; 105: 153.
.



 Благодаря низкому давлению в плевральной полости легкие расправляются во время вдоха.
Благодаря низкому давлению в плевральной полости легкие расправляются во время вдоха. Дальнейший механизм развития отека плевральной полости схож с заболеваниями почек.
Дальнейший механизм развития отека плевральной полости схож с заболеваниями почек.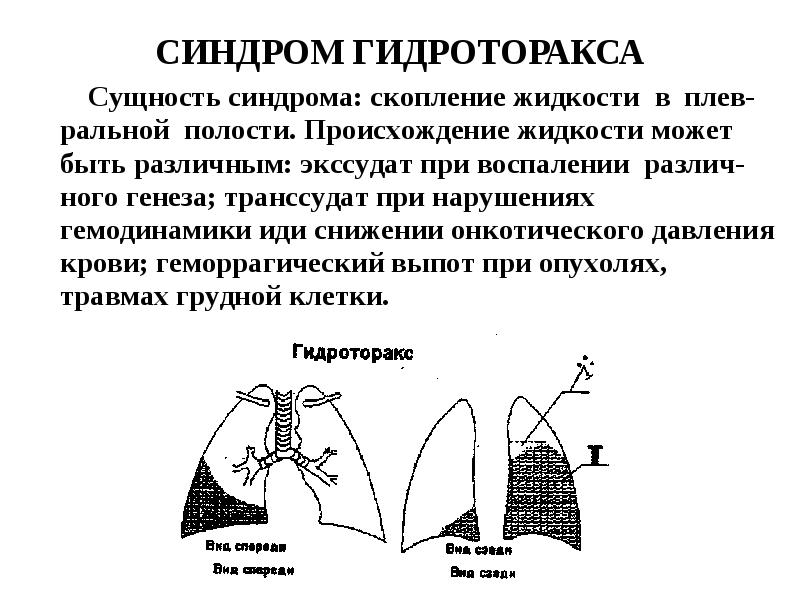
 Врач удаляет жидкость из плевры для проведения лабораторной диагностики. Для гидроторакса характерно отсутствие признаков инфекции или воспаления в образце.
Врач удаляет жидкость из плевры для проведения лабораторной диагностики. Для гидроторакса характерно отсутствие признаков инфекции или воспаления в образце.