Эндоскопия: история и современность
16 Сентября 2019
Эндоскопия: история и современность
Непреодолимое желание врачей заглянуть внутрь больного организма и выявить причину болезни старо, как вся история врачевания. Кто и когда выполнил первую эндоскопию, наверняка сказать невозможно. Но уже в IV веке до н.э. в трудах Гиппократа встречается описание манипуляции похожей на ректоскопию, а при раскопках Помпеи, пострадавшей от извержения Везувия в 79 году н.э., были обнаружены приспособления, напоминающие современные вагинальные зеркала.
Достоверно известно, что первый прибор, который можно назвать «эндоскопом», был разработан в 1805 году итальянцем из Франкфурта-на-Майне Филиппом Боццини (Ph.Bozzini). С помощью «светопроводника», как его назвал изобретатель, можно было осмотреть носовую полость и ректогенитальное пространство. В качестве источника света в приборе использовалась свеча, но копоть и ожоги не позволили использовать его по назначению. Более того, научные изыскания Боццини не были поняты коллегами, и вскоре он был наказан медицинским факультетом города Вены «за любопытство».
К середине XIX века идеи научно-технического прогресса все активнее обсуждались европейским сообществом, и идея Боццини нашла своего продолжателя. В 1853 году французский хирург Антуан Дезормо (A.J. Desormeaux) представил оригинальный прибор собственной конструкции, снабженный системой линз и зеркал-рефлекторов для направленного отражения света. Однако конструкция оказалась достаточно громоздкой и сложной для использования. Кроме того, источником света по-прежнему служила спиртовая горелка, и исследования нередко заканчивались ожогами. В 1873 году австрийский врач Густав Труве (Gustav Trouve) продемонстрировал коллегам созданный им «полископ», в котором источником света служила ярко светящаяся от проходящего по ней электрического разряда платиновая нить. Однако разогрев нити происходил так сильно и быстро, что исследование приходилось ограничивать 20 секундами.
Изобретение Томасом Эдисоном (T. Edison) в 1879 году лампы накаливания не могло не отразится на создании эндоскопов с электрическим освещением. Использование альтернативного источника света и прогрессивное развитие оптики изменило конструкцию эндоскопов, уменьшив их в размерах и сделав процедуру более безопасной.
Радикальное изменение конструкции прибора произошло после демонстрации волоконно-оптического эндоскопа в 1958 году, когда Б. Гиршович (B.I. Hirschowitz) с соавторами опубликовали ряд работ по использованию гибкого фиброэндоскопа, в основе которого лежал принцип передачи света по пучку гибкого световолокна. Революционный эндоскоп обладал несравнимо большими разрешающими возможностями, а главное — превосходной гибкостью и легкой управляемостью. Использование гибких эндоскопов сделало процедуру существенно проще, гуманнее и безопаснее.
Новейший этап в истории эндоскопии связан с развитием и внедрением в практическую медицину цифровых технологий. В 1969 году американские ученые разработали ПЗС-матрицу, способную преображать оптическое изображение в цифровой сигнал. Наличие алгоритма цифровой обработки позволило создать яркое контрастное изображение с четкой цветопередачей на экране HD-монитора и компьютера. Фотовидеофиксация, архивирование изображений, использование узкоспектральных и микроскопических технологий — вот лишь немногое из того, что умеют современные цифровые видеоэндоскопы.
Одной из наиболее серьезных проблем современной гастроэнтерологии является хеликобактериоз, что связано с прогрессивным возрастанием числа инфицированных Helicobacter pylori, который все чаще выявляется у молодых людей.
Долгое время считалось, что слизистая оболочка желудка практически стерильна, а бактерии, попадающие в желудок вместе с пищей и слюной, быстро погибают под воздействием соляной кислоты. В конце XIX века G. Bizzozero и H. Salomon впервые описали спиральные микроорганизмы, располагающиеся в толще слизи и на поверхности слизистой оболочки желудка кошек и собак, которых они назвали «желудочными спириллами».
Перелом во взглядах на природу воспалительных заболеваний желудка произошел после публикации в 1983 году результатов исследований австралийских ученых B. J. Marshall и J. R. Warren. Они сумели выделить и культивировать спиралевидные микроорганизмы со слизистой оболочки желудка пациента с гастритом. Для подтверждения своей теории о связи бактерий с развитием антрального гастрита, Барри Маршалл провел сознательное самозаражение культурой бактерий и наблюдал у себя развитие болезни. Уже на седьмой день появились первые признаки диспепсии, а на десятый день он описывал все признаки гастрита, который был подтвержден эндоскопически и гистологически.
Дальнейшие исследования свойств открытого ими микроорганизма позволили отнести его к роду Campylobacter и включить в международную таксономию бактерий в 1985 году под именем Campylobacter pyloridis. Позднее, в 1989 году Goodwin C.S. с соавторами продемонстрировали, что эта бактерия генетически не принадлежит к роду Campylobacter и назвали ее Helicobacter pylori —небольшой извитой бактерии, обитающей только в желудке человека. В 1994 году Международное агентство по изучению рака IARK отнесло хеликобактерную инфекцию к канцерогенам первого порядка.
Несмотря на существование множества различных методов диагностики H.pylori, универсального пока не существует. В рекомендациях пятого Маастрихтского/Флорентийского консенсуса указывается, что быстрый уреазный тест может быть использован как диагностический тест первой линии в тех случаях, когда есть показания для эндоскопии и нет противопоказаний для биопсии.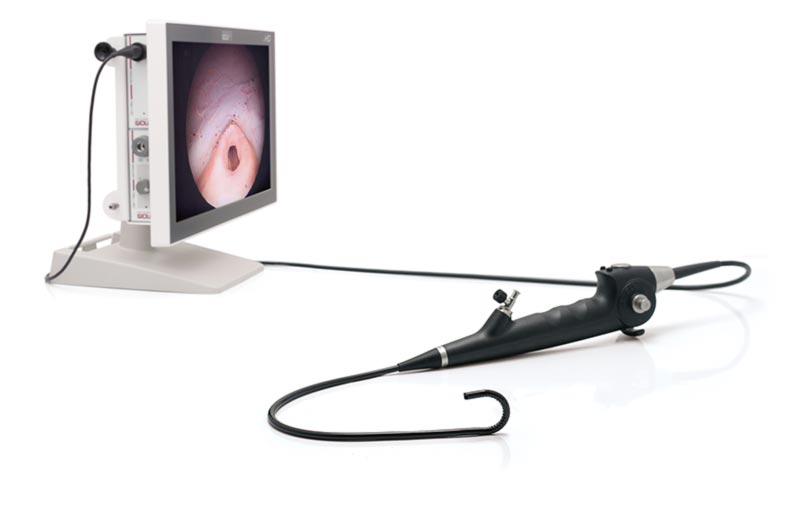 Положительный результат теста позволяет начать немедленное лечение. Для подтверждения эрадикации H.pylori лучшим вариантом признается уреазный дыхательный тест или тест с моноклональными антителами для выявления антигенов H.pylori в кале.
Положительный результат теста позволяет начать немедленное лечение. Для подтверждения эрадикации H.pylori лучшим вариантом признается уреазный дыхательный тест или тест с моноклональными антителами для выявления антигенов H.pylori в кале.
В процессе своей жизнедеятельности бактерия продуцирует большое количество ферментов и токсинов, которые способствуют быстрой деструкции эпителиальных клеток с последующим разрушением субэпителиальных тканей и экстрацеллюлярного матрикса. Для выявления накопленной в слизистой оболочке желудка уреазы, наличие которой свидетельствует о присутствии H.pylori, гастробиоптат помещают в диагностическую среду, содержащую мочевину и кислотно-щелочной индикатор. Реакция гидролиза мочевины уреазой приводит к появлению ионов аммония, которые изменяют рН среды и, соответственно, окраску индикатора. Быстрый уреазный тест прост, относительно недорог и позволяет получить ответ за несколько минут.
Нам показались интересными результаты сравнительной оценки двух самых популярных в нашей стране экспресс-тестов для определения уреазной активности H.pylori в гастробиоптате отечественного и финского производителя. В исследование вошли пациенты с H.pylori-ассоциированным гастродуоденитом и различными вариантами течения язвенной болезни12-перстной кишки, которым проводилась диагностика H.pylori в биоптате до и после проведения эрадикационной терапии. Результаты исследования показали сравнительно низкую диагностическую точность Ас = 67,2% отечественного теста и достаточно высокую Ас = 95,3% у финского. Имея возможность выполнять быстрый уреазный тест обоих производителей, мы отдаем предпочтение последнему.
Одним из наиболее обсуждаемых вопросов современной гастроэнтерологии является диагностика заболеваний тонкой кишки, в том числе связанных с лактазной недостаточностью. Лактаза — это фермент, который вырабатывается клетками тонкой кишки и участвует в гидролизе дисахарида лактозы с образованием моносахаридов глюкозы и галактозы. Гиполактазия приводит к тому, что нерасщепленная, осмотически активная лактоза накапливается в просвете кишечника и удерживает там жидкость, способствуя развитию диареи, образованию большого количества газа и появлению спастических болей в животе.
Гиполактазия приводит к тому, что нерасщепленная, осмотически активная лактоза накапливается в просвете кишечника и удерживает там жидкость, способствуя развитию диареи, образованию большого количества газа и появлению спастических болей в животе.
Первичная лактазная недостаточность, связанная с врожденным дефицитом фермента лактазы, имеет большое значение в педиатрии (у детей грудного возраста). При первичной гиполактазии у взрослых, на фоне морфологически сохранного энтероцита, происходит постепенное угасание ферментативной активности лактазы после прекращения грудного вскармливания.
Для гастроэнтерологов наибольший интерес представляет вторичная лактазная недостаточность, обусловленная снижением активности фермента за счет повреждения самого энтероцита, что может наблюдаться при хронических воспалительных заболеваниях кишечника и целиакии. Следует отметить, что значительную долю лактазы (до 80%) вырабатывают бактерии нормальной кишечной амилолитической микрофлоры, к которой относятся бифидо- и лактобактерии. Таким образом, наличие и выраженность клинических проявлений непереносимости лактозы часто не коррелирует со степенью снижения активности фермента, так как связана и с количеством ферментирующих лактозу бактерий.
Кроме того, результаты исследований последних лет говорят о том, что анамнестические данные не позволяют достоверно говорить о наличии или отсутствии лактазной недостаточности. Так, у пациентов, указывающих на хорошую переносимость молока и молочных продуктов, в половине случаев были выявлены проявления гиполактазии разной степени выраженности. В нашей клинике используется экспресс-тест с забором биоптата из залуковичных отделов 12-перстной кишки во время видеоэндоскопии, что не требует дополнительной подготовки и не увеличивает время обследования.
Полиглоттов Олег Владимирович, врач-эндоскопист
Список, использованной литературы:
-
Назаров В.
 Е. «Причины безуспешной эрадикационной терапии, не связанные с антибиотикорезистентностью Helicobacter pylori, и пути их преодоления», РМЖ, Медицинское обозрение, №3/2018.
Е. «Причины безуспешной эрадикационной терапии, не связанные с антибиотикорезистентностью Helicobacter pylori, и пути их преодоления», РМЖ, Медицинское обозрение, №3/2018.
Malfertheiner P., Megraud F., O’Morain C.A. et al. Management of Helicobacter pylori infection — the Maastricht V/Florence Consensus Report // Gut. 2017. Vol. 66 (1).
-
Бельмер С.В. и соавт., «История открытия H.pylori», Детская Гастроэнтерлогия на компакт-диске, II издание Под редакцией проф. С.В. Бельмера и проф. А.И. Хавкина.
-
Барышникова Н.В., «Актуальные проблемы диагностики хеликобактериоза», «Экпериментальная и клиническая гастроэнтерология», №2/2009.
-
Щербаков П.Л. и соавт., «Лактазная недостаточность у больных с постинфекционным синдромом раздраженного кишечника и роль микрофлоры кишечника в ее развитии (результаты рандомизированного двойного слепого контролируемого исследования)», «Экспериментальная и клиническая гастроэнтерология», №05/2012.
-
Асанина Л. М. и соавт., «Возможности эндоскопии верхних отделов желудочно-кишечного тракта в диагностике синдрома лактазной недостаточности», г. Санкт – Петербург.
ЭТАПЫ РАЗВИТИЯ ЭНДОСКОПИИ. ПУТИ РАЗВИТИЯ ТЕХНОЛОГИЙ.
1874 г.- первые попытки фотографий эндоскопий Stein photo endoscopy
1879 г.- Thomas Edison изобрёл лампочку накаливания и в этот же год Maximillian Nitze (Berlin) изобретает жёсткий цистоскоп 1881 г. – Mikulicz and Leiter активно занимаются эзофагогастроскопией
1883 г.- Newman (England) – электрическое освещение в цистоскопе
1890 г. G.Kelling – управляемый гастроскоп (20 лет)
1939 г. F. FRONCHER и P. CRAFOORD впервые выполнили эндоскопические лечебные вмешательства, разработали МЕТОД СКЛЕРОЗИРУЩЕЙ ТЕРАПИИ ПРИ ВАРИКОЗНО РАСШИРЕННЫХ ВЕНАХ ПИЩЕВОДА
1895 г. — Альфред Кирштейн во время выполнения эзофагоскопии случайно интубировал трахею и, сделав соответствующие выводы, предложил метод, позволяющий выполнить прямую ларингоскопию
— Альфред Кирштейн во время выполнения эзофагоскопии случайно интубировал трахею и, сделав соответствующие выводы, предложил метод, позволяющий выполнить прямую ларингоскопию1898 г. — F. LANGE и D. MELTZING Гастрокамера для фотографирования желудка без визуального осмотра
1901 г. Дмитрий Оскарович Отт (Санкт-Петербург) и 1902 г. G.Kelling провели celioscopy
1902 г. J. Turtle (1902) впервые использовал электрическую лампочку при ректоскопии
1907 г. W.Brunnings –эзофагоскоп с лампочкой на конце (электроскоп)
1911 г. Jacobeus – laparothoracoscopy (появляется терминология)
1912 г. Darwin Lespinasse (Chicago) –первые нейроэндоскопические операции
1920 г. R.Shindler проектирует канал для инсуффляции воздуха в гастроскопе
1924 г. Zolikofer выполняет серию лапароскопических операций на углекислом газе
1928 г. Первая в мире успешная попытка получения эндофотографии Фельдштейн Г.Д.
1929 г. Heinz Kalk (Germany) – предлагает углы обзора эндоскопов
1932 г. R.Shindler – полугибкий линзовый гастроскоп (длина 78 см, гибкая часть 24 см., диаметр 12 мм) . Считается отцом клинической гастроскопии
1937 – Jonh Ruddock (USA) – более 500 клинических случаев лапароскопии
1929-1946 гг. Harold Hopkins конструрирует жёсткий эндоскоп
1941 г. Н. TAYLOR создал гастроскоп с гибкой нижней частью
1948 г. E.B.Benidict – операционный гастроскоп с биопсионным каналом
1950 г. — Разработка первой в мире гастрокамеры для применения в практической медицине (компания Olympus)
1956 г. разработана фотографическая система с электронной вспышкой, позволявшей делать снимки эндоскопических изображений высокого качества.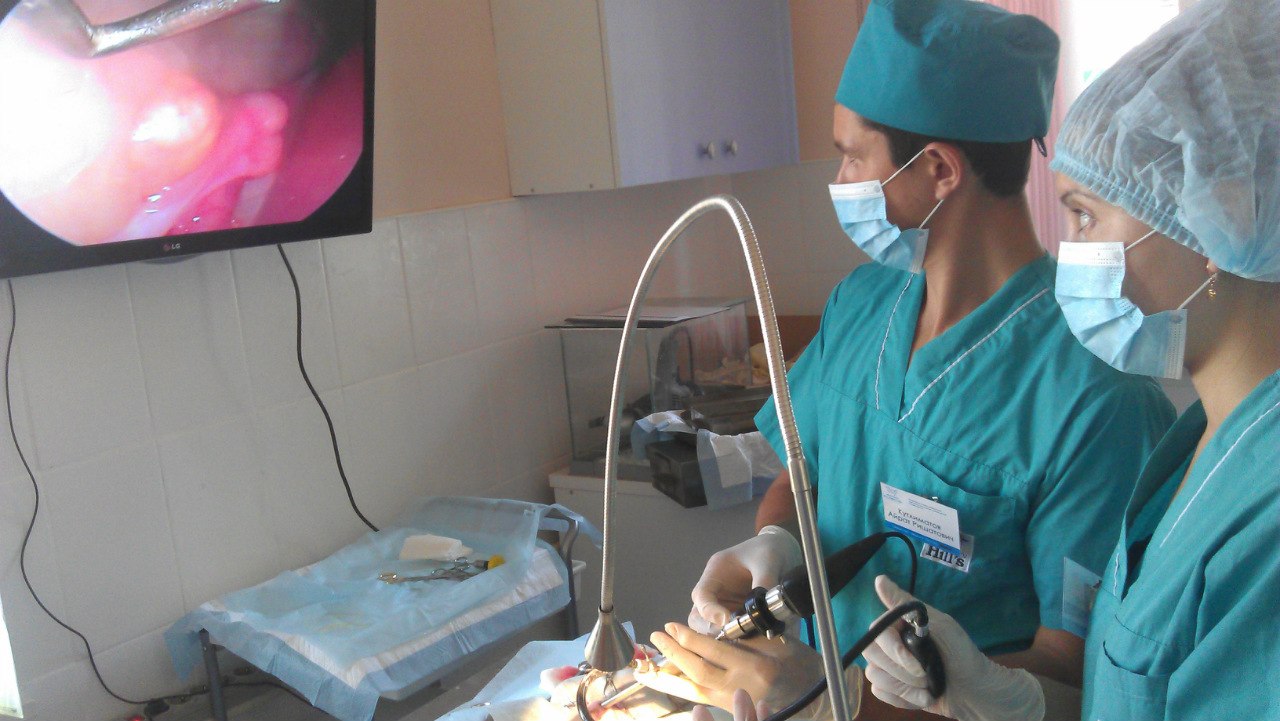
1958 г. S.Tasaka, S.Achizava – гастрокамера (внутрижелудочное фотографирование)
Третий этап (ВОЛОКОННО-ОПТИЧЕСКИЙ ПЕРИОД) в гастроинтестинальной эндоскопии начался после публикации
[Hirschowitz В. et al., 1958] работ, посвященных практическому применению гибкого фиброгастроскопа. Это был прибор длиной 90 см, диаметром 11 мм и углом зрения 34?. Он состоял из 150 000 волокон диаметром 11 мкм каждое. В создании первого фиброгастроскопа приняли участие Hirschowitz, Curtiss и Peters.
1958 году Ларри Кертисс и Бэзил Хиршовиц изобрели первый гибкий волоконно-оптический эндоскоп
В 1963-1966 гг. японские фирмы Machida Seisakusho, Olympus и Fuji Photo Optical разработали опытные модели фиброгастроскопа и фиброколоноскопа
1964 г- Jackson (Canada) первые артроскопические операции у людей
1964 г. фирма Karl Storz запатентовала один из первых экстракорпоральных источников холодного света, от которых световой поток передавался по оптическим волокнам.
1965 г. — успешная канюляция Фатерова сосочка Rabinov and Simon
1965 г. — Впервые чрезбронхиальная биопсия легкого была описана Andersen H. А. и соавт. и применена в клинике Мейо (США) с использованием ригидного бронхоскопа и ригидных щипцов у тринадцати пациентов с интерстициальными заболеваниями легких.
1968 г. Ikeda и соавт. создали первый фибробронхоскоп
1968 г. — была разработана методика ЭРХПГ W. McCUNE и соавт.
1960-1985 гг. Kurt Semm активная лапароскопическая деятельность
1970 г. — С. YOUMANS и Т. КОZU (1971) первыми выполнили электрокоагуляцию кровоточащего сосуда СО желудка через гибкий эндоскоп
1970 г. — К.TSUNEOKA и Т.UCHIDA первыми осуществили через эндоскоп с помощью металлической петли удаление полипов желудка
1971 год одновременно M. CLASSEN, L.DEMLING и R.OTTENJANN разработали методику эндоскопического удаления полипов петлей с использованием тока высокой частоты (электроэксцизия опухоли)
CLASSEN, L.DEMLING и R.OTTENJANN разработали методику эндоскопического удаления полипов петлей с использованием тока высокой частоты (электроэксцизия опухоли)
1974 г. — Р.CULLEN и D.MINICHRAN лигирование резиновыми кольцами для эндоскопической полипэктомии
1975 г. T.HAYASHI описал использование эндоклипс, а Н.HACHISU создал ротационный клипатор
1976 г. Р.FRUHMORGEN успешная фотокоагуляция
1978 г. — R.PROTELL и D.GILBERT (1979) доказали возможность эндоскопического гемостаза путем термокоагуляции с помощью зонда с алюминиевым дистальным наконечником, разогретым до 160-180 °С
1983 г. – чип камера на дистальный конец фиброскопа
1986 г. – видеоэндоскопия 1980 г. В.Т. ЗАЙЦЕВ и соавт. сообщили об успешном применении с целью эндоскопического гемостаза криоэлектрокоагуляции.
1982 г., благодаря работам T. TAYLOR, впервые появилась возможность эндоскопической денервации (по типу ваготомии) кислотопродуцирующей зоны желудка.
1983 г. M. TADA была выполнена первая эндоскопическая резекция СО желудка при раннем раке.
1987 г. разработан, а затем внедрен в клиническую практику метод аргоноплазменной коагуляции.
1995 г. C. MARCO для остановки кровотечения впервые применил радиоволновую коагуляцию.
1995 г. – эра роботизированной техники
1988 г. — Первый в мире видеобронхоскоп (компания Pentax)
1990 г. — Первый в мире ультразвуковой фиброэндоскоп для верхних отделов ЖКТ (Electronic Convex) (компания Pentax)
1993 г. — Первый в мире видеоназофаринголларингоскоп (компания Pentax)
1999-2001 г. — Гавриэль Иддан, а так же доктор Пол Свайн и доктор Аркадий Глуховски разработали видеокапсулы
2001 г. — Первый в мире ультразвуковой видеоэндоскоп для верхних отделов ЖКТ (Electronic radial array type) (компания Pentax)
2002 г. выпуск первой в мире эндоскопической видеосистемы высокой четкости (компания Olympus)
выпуск первой в мире эндоскопической видеосистемы высокой четкости (компания Olympus)
2004 г.- A.Kalloo (USA), транслюминарная эндохирургия
2006 г.- Конфокальный гастроэнтерологический эндомикроскоп―Первая в мире конфокальная система изображения (гибкий эндомикроскоп)
2008 г. – появление системы single port
2009 г. – миниатюризация эндоскопических приборов
2009 — первое использование криозондов для биопсии — «криобиопсия» (Babiak A. соавт. )
2010 Первый в мире HD Видеоназофаринголарингоскоп
Ригидный этап (1795-1939 гг.). В 1806 г. Phlip Bozzini сконструировал аппарат для исследования прямой кишки и матки, используя в качестве источника света свечу (Lichtleiter). В 1853 г. Antoine Jean Desormeaux применил для освещения во время исследования спиртовую лампу. Инструмент совмещал в себе систему зеркал и линз и использовался, главным образом, для осмотра урогенитального тракта. В 1868 г. Kussmaul ввел в практику методику гастроскопии с помощью металлической трубки с гибким обтураторомПолугибкий период (1932-1958 гг.). В 1932 г. Schindler разработал конструкцию полугибкого линзового гастроскопа. Этот гастроскоп представлял собой трубку длиной 78 см, его гибкая часть имела 24 см длины и содержала большое число короткофокусных линз, обеспечивающих воз-можность обследовать 4/5 слизистой оболочки желудка (рис. 3). В 1948 г. Е. В. Benedict создал операционный гастроскоп, имевший биопсийный канал. В 1958 г. S. Tasaka и S. Achizawa представили фотографии, выпол¬ненные при гастроскопии.
Волоконно-оптический период (1958-1981 гг.). В 1954 г. Хопкинс предложил принцип передачи света по гибким стеклянным волокнам и использование когерентного оптического пучка, а Curtiss, Hirschowitz,
Peters создали первый в мире фиброгастроскоп
Цифровой период (1981-2003 гг. ). В 1969 г. Boyle и Smith создали прибор с зарядовой связью (ПЗС), преобразующий оптические сигналы в электрические импульсы. В 1979 г. компанией Welch Allyn был создан первый электронный эндоскоп
). В 1969 г. Boyle и Smith создали прибор с зарядовой связью (ПЗС), преобразующий оптические сигналы в электрические импульсы. В 1979 г. компанией Welch Allyn был создан первый электронный эндоскоп
Телемедицинские технологии. Современная скорость передачи информации позволяет передавать видеоизображение на любые расстояния. Врач может контролировать ход выполнения операций из любой точки мира. С помощью эндоскопии возможно выполнение операций в любой сфере медицины
Пути развития эндоскопии
УЛУЧШЕНИЕ КАЧЕСТВА ИЗОБРАЖЕНИЯ1950-1960 гг. — появление цветного телевидения и 2 основных форматов PAL и NTSC («secam»). Максимальная разрешающая способность — 576 строк.
С 2006 г. применяется электронная эндоскопия (HD формат), позволяющая увеличить максимальную разрешающую способность до 1080 пикселей Превосходная четкость изображения, позволяющая рассматривать мельчайшие изменения слизистой толстой кишки
Конвенциональная эндоскопия Conventional Whaite Light Endoscopy [лат. conventionalis – соответствующий условию] — условный, принятый, соответствующий установившимся традициям – исследование в белом свете
Хромоэндоскопия (применение красителей для улучшения визуализации поверхности слизистой оболочки) Эндоскопия высокого разрешения (HRE) – технология получения изображения высокой четкости, количество телевизионных строк – 1080, против 576 строк в системе PAL) МАГНИФИКАЦИОННАЯ ZOOM-ЭНДОСКОПИЯМетод основан на изменении фокусного расстояния между линзами на дистальном конце аппарата. Современные эндоскопы позволяют получить изображение с увеличением в 115 раз (до х 115)
ОСМОТР В УЗКОМ СПЕКТРЕ СВЕТА (ВИРТУАЛЬНАЯ ХРОМОГРАФИЯ) Narrow-Band Imaging Endoscopy (NBI) «Виртуальная» хромография
Позволяет в узкоспектральной зоне проявлять кровеносные сосуды и другие тканевые структуры без нанесения красителей. Принцип основан на преимущественном поглощении света определенной длины волны гемоглобином. В результате появляется возможность контрастного выделения капилляров и других структур. При обследовании в режиме узкополосного освещения капилляры собственной пластинки имеют коричневую окраску, а вены подслизистого слоя — голубую
Принцип основан на преимущественном поглощении света определенной длины волны гемоглобином. В результате появляется возможность контрастного выделения капилляров и других структур. При обследовании в режиме узкополосного освещения капилляры собственной пластинки имеют коричневую окраску, а вены подслизистого слоя — голубую
При обычном спектре света удается определить только изъязвление. В узкополосном свете можно четко установить границы метаплазии слизистой пищевода с изьязвлением в центре (C-r in situ).
КОНФОКАЛЬНАЯ ЛАЗЕРНАЯ ЭНДОМИКРОСКОПИЯ
Разрешающая способность аппарата доходит до 0,7 мкм, а глубина излучения ткани достигает 250 мкм.
Конфокальная эндомикроскопия уменьшает количество последующих диагностических биопсий в 7 раз
АВТОФЛУОРЕСЦЕНТНАЯ ЭНДОСКОПИЯ
Метод основан на способности флуоресцентных веществ в подслизистом слое автофлуоресцировать при попадании на них возбуждающего света. На нормальных здоровых участках автофлуоресценция более сильная по сравнению с участками, пораженными опухолью.
Специальный фильтр «урезает» возбуждающий свет, позволяя захватить только автофлуоресценцию (избирательность накопления фотосенсибилизатора в опухоли и возможность его обнаружения по флуоресценции при освещении светом определенной длины волны, совпадающей с пиком поглощения препарата)
ИНТЕСТИНОСКОПИЯ
Метод основан на продвижении эндоскопа по тонкой кишке с поочередной фиксацией устройства и наружной силиконовой трубки в просвете тонкой кишки при помощи одного или двух баллонов
КАПСУЛЬНАЯ ЭНДОСКОПИЯ
Принцип основан на использовании видеокапсулы, которая при пассивном продвижении по ЖКТ осуществляет видеосъемку и посылает слабый сигнал, улавливаемый датчиками, прикрепленными на коже передней брюшной стенки
Пациент проглатывает видеоэндокапсулу самостоятельно. Через желудок и тонкий кишечник капсула проходит в течение 12-18 часов. Заряда батареи хватает на 3 суток непрерывной подачи сигнала на считывающее устройство Запись производится в режиме реального времени.
Через желудок и тонкий кишечник капсула проходит в течение 12-18 часов. Заряда батареи хватает на 3 суток непрерывной подачи сигнала на считывающее устройство Запись производится в режиме реального времени.
Недостатки данного метода диагностики:
1. Длина видеоэндокапсулы — 2,5 см. Некоторым пациентам трудно проглотить ее целиком.
2. При передаче изображения возможны «слепые» участки тонкой кишки.
3. Нет возможности манипулировать и изменять угол поворота видеоэндокапсулы в просвете кишки.
ЭНДОСКОПИЧЕСКАЯ УЛЬТРАСОНОГРАФИЯ
Метод основан на ультразвуковом сканировании при непосредственном контакте датчика со стенкой полого органа. Датчик расположен на дистальном конце эндоскопа. Можно использовать УЗ-датчики — зонды, вводимые через биопсийный канал.
Расположение датчика в просвете исследуемых органов исключает экранирование УЗ-волн воздухом при раздувании силиконового пузыря, заполненного водой до момента касания стенок полого органа.
ЭНДОЦИТОСКОПИЯ
Эндоцитоскопия является одним из наиболее новых методов эндоскопической диагностики, обеспечивающим исследование слизистой оболочки полых органов желудочно-кишечного тракта, дыхательных путей и ряда других полых органов с увеличением до 1150 раз, что позволяет оценивать ее тканевую и клеточную структуру непосредственно в процессе эндоскопического исследования. Данный метод, наряду с конфокальной лазерной эндомикроскопией, можно считать прижизненным морфологическим исследованием — «оптической биопсией». В настоящее время все возможности эндоцитоскопии еще не исследованы, эндоцитоскопическое оборудование находится на стадии совершенствования прототипов.
История отделения (эндоскопия)
История отделения эндоскопии
Эндоскопическая служба существовала в институте с 1968 года в составе отделения амбулаторной диагностики и терапии опухолей. У её истоков стояли руководитель этого отделения К.А. Павлов, сотрудники отделения Ю.Ф. Стефаненко, Д.П.Волков, В.Г. Черномордиков, А.М. Щербаков. На начальном этапе (70-80-е годы прошлого столетия) основной акцент делался на изучении возможностей использования эндоскопического метода в амбулаторных условиях. По результатам этих исследований были защищены кандидатские диссертации Ю.Ф. Стефаненко «Значение фиброгастроскопии в комплексной диагностике рака желудка в амбулаторных условиях» (1975 г.), Д.П.Волкова «Фиброгастроскопия в диагностике новообразований (рецидива и первичного рака) культи желудка» (1978 г.), В.Г. Черномордикова «Роль эндоскопии в комплексной диагностик полипов желудка в амбулаторных условиях» (1985 г.). Активно развивались методы лечебной эндоскопии, такие как эндоскопическая полипэктомия, что нашло отражение в кандидатской диссертации А.М.Щербакова «Электрохирургическая полипэктомия при фиброколоноскопии в условиях поликлиники и стационара» (1983 г.)
Существенное расширение потребностей поликлиники и института в эндоскопических исследованиях поставило задачу создания эндоскопической службы как самостоятельного структурного подразделения, которая была решена путем организации в октябре 1992 года кабинета эндоскопии в составе поликлинического отделения. 1 июля 1993 года в соответствии с приказом директора института К.П. Хансона было основано отделение эндоскопии как самостоятельное структурное подразделение.
Заведующим отделения с момента его организации, а в настоящий момент научным руководителем отделения эндоскопии, является д. м.н., профессор, заместитель директора института Александр Михайлович Щербаков.
м.н., профессор, заместитель директора института Александр Михайлович Щербаков.
Помимо повседневной клинической работы по обследованию поликлинических и стационарных больных на отделении были развернуты научные исследования по разработке новых эндоскопических методик в диагностике доброкачественных и злокачественных опухолей, оценке их эффективности. С появлением в начале 2000-х годов таких новых эндоскопических технологий, как аргоноплазменная и лазерная коагуляция, фотодинамическая терапия, широкое развитие в отделении получила лечебная эндоскопия. Основным направлением её стала разработка методов комбинированной реканализации пищевода, желудка, пищеводно-желудочных и пищеводно-кишечных анастомозов, трахеи и бронхов при стенозирущих злокачественных опухолях. В результате удалось создать оригинальную технологию эндоскопических операций при раке пищевода с использованием метода аргоноплазменной коагуляции в самостоятельном варианте или в сочетании с высокочастотной электрохирургией, применение которой обеспечивает полное или частичное восстановление просвета органа более чем в 90% случаев. Также была предложена уникальная тактика лечения неоперабельных больных раком пищевода в виде последовательного применения внутрипросветной эндоскопической хирургии и сочетанной лучевой терапии (внутрипросветная брахитерапия высокой мощности дозы излучения+дистанционная лучевая терапия, что позволило добиться выраженного местного эффекта в 80% случаев. По итогам проведенных исследований защищена кандидатская диссертация А.А.Аванесян «Возможности применения метода аргоноплазменной коагуляции в «гибкой» эндоскопии при лечении новообразований желудочно-кишечного тракта и трахеобронхиальной системы» (2006 г.), докторская диссертация А.М. Щербакова «Клиническое значение внутрипросветной эндоскопической хирургии в лечении неоперабельных больных раком пищевода» (2006 г.).
В сотрудничестве с отделением торакальной хирургии были разработаны комбинированные методы выполнения эндотрахеобронхиальных операций в условиях ригидной бронхоскопии при местнораспространенном и метастатическом немелкоклеточном раке легкого с опухолевой обструкцией центральных бронхов и трахеи. Предложенные методы позволяют в 30% случаев добиться полного и в 70% случаев частичного восстановления просвета дыхательных путей с полным или частичным устранением дыхательной недостаточности при значительном улучшении качества жизни пациентов. Результатом исследований явилась докторская диссертация А.И. Арсеньева «Оптимизация методов лечения распространенного немелкоклеточного рака легкого» (2007 г).
Предложенные методы позволяют в 30% случаев добиться полного и в 70% случаев частичного восстановления просвета дыхательных путей с полным или частичным устранением дыхательной недостаточности при значительном улучшении качества жизни пациентов. Результатом исследований явилась докторская диссертация А.И. Арсеньева «Оптимизация методов лечения распространенного немелкоклеточного рака легкого» (2007 г).
Результаты изучения клинической ценности методов автоматизированной количественной цитометрии и флоуресцентной бронхоскопии со встроенной спектрометрией при диагностике рака легкого нашли отражение в кандидатской диссертации А.А. Барчука, защищенной в 2010 году. В ней доказана принципиальная возможность эффективного использования многокомпонентных систем для ранней диагностики рака легкого.
Расширение показаний к эндоскопическим исследованиям желудочно-кишечного тракта, увеличение числа больных с сопутствующей патологией и старших возрастных групп делало актуальным проблему разработки анестезиологического обеспечения эндоскопических процедур. Результаты предпринятого в этом направлении исследования были оформлены в виде кандидатской диссертации О.Я. Замираловой «Анестезиологическое обеспечение эндоскопических вмешательств на желудочно-кишечном тракте у онкологических больных» (2002 г.)
В 2012 году отделение эндоскопии возглавил Олег Борисович Ткаченко, врач-эндоскопист 1-й категории, действующий член Российского эндоскопического Общества (РоЭндО), Европейского общества Гастроинтестинальной Эндоскопии (ESGE), практикующий хирург с более чем 10-летним стажем и опытом работы в ведущих клиниках города. О.Б. Ткаченко проходил длительную стажировку в клинических центрах Японии, США, Европы. С его приходом на отделение стала активно развиваться оперативная эндоскопия, а именно такие её направления, как эндоскопическое лечение раннего рака пищевода, желудка, толстой кишки, эндоскопическое удаление подслизистых образований желудочно-кишечного тракта. Расширение объема оперативной деятельности продиктовало необходимость совершенствования методики и техники диагностических процедур, внедрения в практику дополнительных уточняющих методик в виде хромоскопии, осмотра слизистой органов в узкоспектральном свете. Активное выявление ранних форм рака сопровождается необходимостью точного стадирования опухоли для определения дальнейшей тактики ведения пациента. Для эндоскопического удаления подслизистых образований на дооперационном этапе требуется установление не только природы образования, но и его истинных размеров и расположения относительно стенки органа. Владение сотрудниками отделения сложной методикой эндоскопической ультрасонографии позволяет успешно решить перечисленные задачи.
Расширение объема оперативной деятельности продиктовало необходимость совершенствования методики и техники диагностических процедур, внедрения в практику дополнительных уточняющих методик в виде хромоскопии, осмотра слизистой органов в узкоспектральном свете. Активное выявление ранних форм рака сопровождается необходимостью точного стадирования опухоли для определения дальнейшей тактики ведения пациента. Для эндоскопического удаления подслизистых образований на дооперационном этапе требуется установление не только природы образования, но и его истинных размеров и расположения относительно стенки органа. Владение сотрудниками отделения сложной методикой эндоскопической ультрасонографии позволяет успешно решить перечисленные задачи.
За время существования отделения эндоскопии в нем защищено 3 докторские и 9 кандидатских диссертаций. Его сотрудниками выпущено более 300 работ в виде монографий, сборников, глав в книгах, методических рекомендаций, статей в научных журналах, тезисов докладов на съездах, конференциях. Получено более 14 патентов на изобретения.
История развития эндоскопии
Врачи всегда хотели заглянуть внутрь тела человека и изучать происходящие там процессы. Многие врачи, инженера и изобретатели приняли участие в создании устройств позволявших ввести свет в организм человека и получить изображение внутренних полостей. По мере развития технологий и медицинской техники в эндоскопии выделяют четыре этапа развития:
- Ригидный 1795 — 1932 года
- Полугибкий 1932 — 1958 года
- Волоконно-оптический 1958 — 1981 года
- Электронный 1981 год и по наше время
Ригидная эндоскопия
История эндоскопии берет своё начало с изобретения Филиппа Боззини (1773-1808). Он был итальянским врачом, выросшим в Германии. Свой аппарат для эндоскопии он назвал «Lichtleiter» (в переводе с немецкого – световод). Аппарат представлял из себя систему трубок и держателя для свечи. Свет от свечи направлялся посредством трубок в полости тела, но недостатком были тепло и дым от свечи. Широкого применения среди врачей того времени это «революционное» изобретение не получило.
Широкого применения среди врачей того времени это «революционное» изобретение не получило.
Отцом же эндоскопии принято считать Антуана Жан Десормо (1815-1882), который заменил в аппарате Боззини свечу на источник света из смеси спирта и скипидара, чтобы увеличить освещенность и добавил конденсаторные линзы для концентрации освещения на одном месте. Он один из первых кто проводил удачные исследования на своих пациентах. Позже в жестких инструментах совершенствовался набор линз, а источник света был заменен на электрические лампочки. Лампочки встраивались в конец эндоскопа, но проблема нагрева так и не была решена, пациенты очень часто получали ожоги.
Свой вклад в развитие эндоскопи на этом этапе внесли:
Юлием Брук (1840-1902) — первым предложил вводит источник света внутрь полости усовершенствовал сам источник света (платиновая проволока в резервуаре с водой).
Макс Нитце (1848-1906) — будучи терапевтом изобрел инструмент для обследования мочевого пузыря. Он был первым кто создал эндоскоп с источником света на конце. Усовершенствовав источник света, он создал первый цистоскоп в 1877 году. Позже к своему цистоскопу он добавил возможность фиксировать изображения на фотопластинах.
Йоханн фон Микулич-Радецкий (1850-1905) усовершенствовал идею Нитце и внедрил в устройство своего эндоскопа зеркало, чтобы создать угловое поле зрения и добавил воздушный канал, который использовался исследователем для раздувания осматриваемой полости. Это существенно расширило поле зрения и позволило осматривать спавшиеся полости. Его жесткий гастроскоп имел длину 650 мм и диаметр 13 мм.
Полугибкий
Этот этап начинается с усовершенствования Шиндлером эзофагоскопа Келлинга сконструированного в 1898 году (нижняя треть этого эндоскопа могла изгибаться на 45 градусов). В 1932 году Шиндлер предложил гастроскоп состоящий из жесткой трубки 12 мм в диаметре и гибкой спирали с системой из 48 линз. Освещение осуществлялось электрической лампой, гастроскоп мог изгибаться на 30 градусов.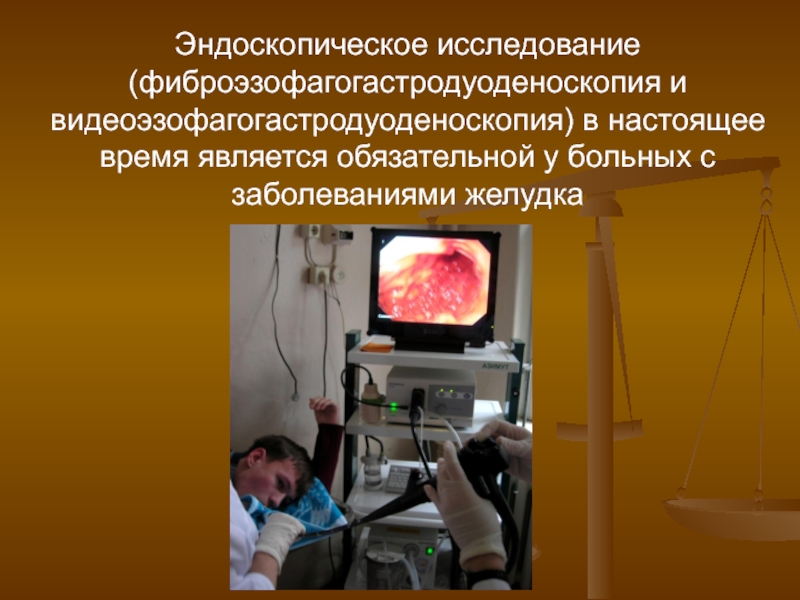 Но все равно еще оставались «слепые зоны», которые не могли быть осмотрены, (осмотру было доступно 4/5 желудка).
Но все равно еще оставались «слепые зоны», которые не могли быть осмотрены, (осмотру было доступно 4/5 желудка).
Е. В. Benedict в 1948 году конструирует эндоскоп с биопсийным каналом, который позволял производить манипуляции внутри желудка.
В эти же годы появляется «гастрокамера», аппарат состоял из жесткой трубки, камеры и кассеты с рулоном пленки, для освещения использовалась электрическая лампочка, имелся канал подачи воздуха. Но недостатком было то, что изображения получались только после проявки пленки и не всегда были диагностически ценными.
Волоконно-оптический
Этот этап берет свое начало с публикации В. I. Hirschowitz в 1958 году работ, посвященных применению гибкого фиброгастроскопа. В основе нового эндоскопа лежал принцип передачи света по гибким стеклянным волокнам (впервые идея предложена в 1927 году), а передача изображения обратно осуществлялась по пучку строго упорядоченных стеклянных волокон (применялся принцип когерентного оптического пучка предложенного Хопкинсом в 1954 году). Первый фиброгастроскоп создавался при участии Curtiss, Hirschowitz и Peters.
Новый гастроскоп обладал большими разрешающими возможностями по сравнению с предыдущими эндоскопами, но главной отличительной особенностью была гибкость и управляемость аппарата. Что в совокупности позволяло детально осматривать все отделы желудка, а исследование значительно легче переносилось пациентами, в сравнении с полугибкими эндоскопами.
В это период широко стали применятся различные эндоскопические манипуляции, что позволило эндоскопии желудочно кишечного тракта из диагностической методики стать и лечебной, стала развиваться эндоскопическая хирургия.
Электронный период
Предпосылками для начала «цифровой эры» в эндоскопии было изобретение в лаборатории Bell Laboratories (AT&T), инженерами Boyle и Smith прибора с зарядовой связью (ПЗС) в 1969 году. Появилась возможность переводить оптические сигналы в электронные импульсы. Через 10 лет инженеры компании Welch Allyn создали первый видеоэндоскоп использующий ПЗС матрицу для передачи изображения на монитор.
С 1981 года электронные видеоэндоскопы вошли в серийное производство и стали широко применятся в медицинской практике. Так началась «цифровая эра» в эндоскопии.
Новое эндоскопическое оборудование позволяло получать изображение высокой четкости, сохранять полученные видео- и фотоматериалы, теперь за эндоскопическим исследованием на мониторе могли наблюдать несколько специалистов. Позже появляются видеокапсулы и новое направление — капсульная эндоскопия. Параллельно развиваются прикладные эндоскопические методики: ЭРХПГ, лечебная эндоскопия и эндоскопическая ультрасонография.
Обо всех современных эндоскопических методиках будет рассказано в следующих статьях.
Современное состояние и перспективы развития эндоскопии | #06/04
Прежде чем достичь современного состояния, эндоскопия прошла длительный путь развития, связанный с совершенствованием эндоскопической аппаратуры и подсобного эндоскопического инструментария. Попытки увидеть внутреннюю поверхность пищевода предпринимались в 1795 г. Bozzini в Германии (Schindler, 1950). Благодаря работам Desormeaux (1853) был создан эндоскоп, с помощью которого можно было осмотреть пищевод, мочевой пузырь и прямую кишку. Однако первую эзофагоскопию им произвел не автор изобретения, а Kussmaul, доложивший в 1868 г. на заседании Общества естествоиспытателей во Фрейбурге о первых итогах эзофагоскопии (Killian, 1901).
История развития эндоскопии пищевода и желудка началась в 1868 г., когда Kussmaul ввел в желудок профессионального шпагоглотателя прямую металлическую трубку диаметром 13 мм и длиной 47 см с целью осмотра слизистой оболочки желудка. Из-за крайнего несовершенства аппаратуры и недостаточности освещения эта попытка оказалась неудачной.
В 1879 г. Nitze и Leiter сконструировали эндоскоп, состоящий из ряда подвижных колец, придававших прибору гибкость. Авторы использовали для освещения платиновую спираль, раскаляемую электрическим током, которую вводили через аппарат при исследовании. От раскаляемой током спирали, окруженной специальным колпачком, выделялось большое количество тепла, что требовало приспособления для охлаждения инструмента. Последнее достигалось постоянной циркуляцией холодной воды. Все устройство для тока воды делало эндоскоп настолько сложным в употреблении, что он не нашел практического применения. Однако Nitze впервые удалось через эндоскоп увидеть границу между слизистой оболочкой пищевода и желудка (Schindler, 1937).
От раскаляемой током спирали, окруженной специальным колпачком, выделялось большое количество тепла, что требовало приспособления для охлаждения инструмента. Последнее достигалось постоянной циркуляцией холодной воды. Все устройство для тока воды делало эндоскоп настолько сложным в употреблении, что он не нашел практического применения. Однако Nitze впервые удалось через эндоскоп увидеть границу между слизистой оболочкой пищевода и желудка (Schindler, 1937).
Основателем эзофагогастроскопии как метода исследования следует считать Mikulicz, создавшего в 1881 г. свою модель эндоскопа и опубликовавшего ряд работ по исследованию пищевода и желудка в норме и при некоторых заболеваниях этих органов. Для более легкого проникновения в желудок и удобства осмотра инструмент был согнут в нижней трети под углом 150°. Мikulicz первым применил при гастроскопии раздувание желудка воздухом. Он осмотрел слизистую оболочку желудка и диагностировал раковую опухоль. Аппарат Микулича был весьма несовершенен и небезопасен для применения, а поэтому не использовался в клинике.
В зависимости от конструкции приборов, в истории развития эндоскопии можно выделить 4 периода.
В первый период (1881–1932 гг.) для осмотра желудка использовались жесткие негнущиеся линзовые эндоскопы Kelling, Schindler, Elsner. Второй период (1932–1958 гг.) характеризовался применением полужестких гнущихся линзовых приборов Wolf, Schindler, Benedict, Palmer. В 1938 г. Henning впервые сфотографировал желудок через гастроскоп. В этот период нашли применение отечественные гастроскопы, созданные ВНИИ МиО. Большой вклад в развитие эндоскопии внесли Г. С. Беленький, А. Н. Тагман, В. Н. Добротворский, Н. С. Смирнов. В 1950 г. Uji изобрел гастрокамеру.
Третий период (1958–1984 гг.) отмечен тем, что в клинической практике нашли применение гибкие эндоскопы с волоконной оптикой. Идея светопередачи с помощью волоконной оптики связана с именем Baird и относится к 1928 г. , а практическое использование фиброоптики стало возможным благодаря исследованиям Van Heel (1954), который открыл материал с низким индексом рефракции для покрытия стекловолокна. Принцип передачи света по волокну — световоду диаметром несколько десятков микрон — заключается в его полном внутреннем отражении: свет, попавший на конец длинного тонкого волокна, последовательно отражается от его внутренних стенок и полностью выходит на противоположном конце. Светопередача осуществляется при любом изгибе прибора.
, а практическое использование фиброоптики стало возможным благодаря исследованиям Van Heel (1954), который открыл материал с низким индексом рефракции для покрытия стекловолокна. Принцип передачи света по волокну — световоду диаметром несколько десятков микрон — заключается в его полном внутреннем отражении: свет, попавший на конец длинного тонкого волокна, последовательно отражается от его внутренних стенок и полностью выходит на противоположном конце. Светопередача осуществляется при любом изгибе прибора.
О первом эндоскопическом приборе со стекловолоконной оптикой — гастродуоденоскопе фирмы А.К.М.I. — сообщил Hirshowitz в 1958 г. Это был прибор длиной 90 см, диаметром 11 мм и углом зрения 34°. Он состоял из 150 тыс. волокон диаметром 11 мк каждое.
В 1963–1966 гг. японские фирмы Machida Seisakusho, Оlympus и Fuji Photo Optical разработали фиброгастроскоп и фиброколоноскоп, а в 1966 г. было налажено их серийное производство. В 1968 г. Ikeda и соавт. создали первый фибробронхоскоп.
Недостатком фиброэндоскопов является то, что сильное сдавление прибора, например зубами, приводит к разрушению стекловолокон, появлению черных точек в поле зрения и ухудшению изображения. Этого недостатка лишен видеоэндоскоп.
Четвертый период (с 1984 г. по настоящее время) ознаменован применением в клинической практике видеоэндоскопов. Первые видеоэндоскопы EVF-F, EVD-XL, EVC-M были созданы в США. В современных видеоэндоскопах благодаря использованию высокоэффективных линз и точных систем цифровой обработки сигнала с помощью мегапиксельных ПЗС-матриц удается получить четкое высококачественное изображение, увеличенное примерно в 100 раз, при этом цветопередача не ухудшается.
Видеоэндоскопы более надежны в работе, так как их можно изгибать под любым углом и даже завязывать узлом, не боясь повредить прибор. Значительно уменьшилась нагрузка на глаза врача-эндоскописта. Благодаря использованию видеоэндоскопов удается выявить мельчайшие изменения слизистой оболочки пищевода, желудка, двенадцатиперстной и толстой кишки, а также трахеи и бронхов, что позволяет диагностировать рак этих органов на ранней стадии развития.
В нашей стране наибольшей популярностью пользуются фиброэндоскопы и видеоэндоскопы японских фирм Fujion и Olimpus. Они надежны в эксплуатации, имеют небольшой наружный диаметр и большой диаметр биопсийного канала, что очень важно при выполнении лечебно-оперативных исследований.
В настоящее время невозможно себе представить клиники без эндоскопических исследований. Эндоскопические исследования, возникшие вначале как диагностический метод, очень скоро превратились в лечебно-оперативные, нередко соперничая с полостными операциями.
В нашей стране эндоскопия была выделена в самостоятельную специальность в 1976 г., была введена должность врача-эндоскописта. Обучение врачей эндоскопическим методам диагностики было начато на 1-й кафедре хирургии Центрального института усовершенствования врачей в 1977 г., а в 1985 г. в ЦОЛИУв была создана кафедра эндоскопии, которую возглавил профессор В. Н. Сотников. В настоящее время обучение врачей проводится по унифицированной программе и включает цикл первичной переподготовки продолжительностью 4 мес и циклы тематического усовершенствования (сертификационный и аттестационный) продолжительностью 1 мес (144 ч).
Показаниями к диагностическим эндоскопическим исследованиям желудочно-кишечного тракта является подозрение на заболевания пищевода, желудка, двенадцатиперстной или толстой кишки. В настоящее время любое эндоскопическое исследование желудочно-кишечного тракта выполняется без предварительного рентгенологического исследования, так как при эзофагогастродуоденоскопии или колоноскопии можно увидеть мельчайшие изменения слизистой оболочки, особенно с помощью видеоэндоскопов, которые увеличивают изображение в 50–100 раз. Во время эндоскопического исследования берется биопсия из подозрительного участка (перестроенный рельеф слизистой оболочки, язва, опухоль) и выполняются цитологическое и гистологическое исследования биопсийного материала. Точность диагностики при этом приближается к 100%. В настоящее время во всем мире признан тот факт, что увеличившееся количество холецистэктомий приводит к раку толстой кишки, поэтому всем пациентам, перенесшим удаление желчного пузыря, следует 1 раз в год выполнять колоноскопию. Больным, страдающим язвенной болезнью желудка, ахилическим гастритом необходимо 1 раз в год проводить гастроскопию (оборудование Olimpus, LOMO, Pentax, Fujinon), так как рак желудка развивается на фоне существующей или зарубцевавшейся язвы желудка, а также на фоне гастрита с пониженной секрецией. Диагностика рака желудка на ранней стадии развития возможна лишь при массовых выполнениях гастроскопии больным группы риска, а также пациентам старше 50 лет.
В настоящее время во всем мире признан тот факт, что увеличившееся количество холецистэктомий приводит к раку толстой кишки, поэтому всем пациентам, перенесшим удаление желчного пузыря, следует 1 раз в год выполнять колоноскопию. Больным, страдающим язвенной болезнью желудка, ахилическим гастритом необходимо 1 раз в год проводить гастроскопию (оборудование Olimpus, LOMO, Pentax, Fujinon), так как рак желудка развивается на фоне существующей или зарубцевавшейся язвы желудка, а также на фоне гастрита с пониженной секрецией. Диагностика рака желудка на ранней стадии развития возможна лишь при массовых выполнениях гастроскопии больным группы риска, а также пациентам старше 50 лет.
Бронхоскопия (оборудование Pentax, Karl Storz, Olimpus, Fujinon) выполняется обязательно после предварительного рентгенологического исследования органов грудной полости в прямой и боковой проекциях, так как во время бронхоскопии можно осмотреть бронхи до V–VI порядков включительно и нельзя увидеть периферические отделы легких. Показаниями к бронхоскопии являются центральные или периферические, доброкачественные или злокачественные опухоли легких, выявленные рентгенологически, хронический бронхит, бронхоэктатическая болезнь, длительно текущая пневмония, муковисцидоз, абсцесс легкого, кровохарканье и легочное кровотечение неясной этиологии, опухоли средостения и патология плевры, инородные тела, подозрение на туберкулез.
При наличии у больного кровохарканья или длительно текущего кашля на фоне проводимого лечения при отрицательных рентгенологических данных, а также при изменении характера кашля у курильщика показания к бронхоскопии абсолютные.
Абсолютными противопоказаниями к плановым эндоскопическим исследованиям являются инфаркт миокарда в острой стадии, инсульт в острой стадии, сердечно-сосудистая и сердечно-легочная недостаточность III степени, пароксизмальная тахикардия и мерцательная аритмия.
Несмотря на то что эндоскопические исследования с каждым годом все шире внедряются в клиническую практику, многие врачи, особенно поликлинической сети, мало знакомы с возможностями диагностической и тем более лечебно-оперативной эндоскопии, а также преувеличивают опасность эндоскопических исследований, особенно бронхоскопии.
Конечно, при использовании инструментальных методов исследования не может не быть осложнений, но в связи с усовершенствованием эндоскопических приборов (уменьшение диаметра и увеличение гибкости аппарата) количество осложнений минимально, и обусловлены они, как правило, не небрежностью или низким уровнем подготовки врача-эндоскописта, а основным или сопутствующими заболеваниями пациента.
В настоящее время большинство лечебных учреждений оснащено современной дорогостоящей эндоскопической аппаратурой, и не использовать ее —большая ошибка.
Диагностическое эндоскопическое исследование позволяет установить диагноз, верифицировать его морфологически, оценить распространенность процесса и выработать оптимальную лечебную тактику. Благодаря постоянному усовершенствованию эндоскопической аппаратуры и подсобного эндоскопического инструментария, а также разработке и внедрению новых способов лечения, многие заболевания можно лечить через эндоскоп.
Показаниями к лечебно-оперативным эндоскопическим исследованиям являются:
- язвенная болезнь желудка и двенадцатиперстной кишки в стадии обострения заболевания;
- желудочно-кишечное и легочное кровотечение;
- доброкачественные эпителиальные и неэпителиальные опухоли пищевода, желудка, двенадцатиперстной и толстой кишки, трахеи и бронхов;
- инородные тела желудочно-кишечного тракта и трахеобронхиального дерева;
- воспалительные и нагноительные заболевания трахеобронхиального дерева и легких.
Противопоказаниями к лечебно-оперативным эндоскопическим исследованиям служат:
- инфаркт миокарда в острой стадии;
- инсульт в острой стадии;
- легочно-сердечная и сердечно-сосудистая недостаточность III степени;
- нарушения свертывающей системы крови;
- профузное артериальное желудочно-кишечное кровотечение;
- профузное легочное кровотечение;
- инородные тела верхних или нижних отделов желудочно-кишечного тракта с явлениями перитонита;
- инородные тела трахеи или бронха с явлениями медиастинита;
- крайне тяжелое состояние больного, когда невозможно выполнить диагностическое эндоскопическое исследование.
Язвенная болезнь желудка и двенадцатиперстной кишки, развивающаяся у лиц молодого и среднего возраста, является наиболее распространенной патологией в практике гастроэнтерологов. Это часто рецидивирующее заболевание (в течение года рецидив возникает у 60– 80% пациентов), которому сопутствуют тяжелые осложнения. Поэтому язвенная болезнь остается основной причиной потери трудоспособности больных.
Известно, что более 95% больных язвенной болезнью инфицированы Нр. Нр тормозит миграцию эпителиоцитов, необходимых для закрытия дефекта слизистой оболочки. На большом клиническом материале доказано, что Нр стимулирует апоптозы, тем самым усиливает гибель клеток в краях язвы, что и затрудняет их заживление.
Для эрадикации Нр со слизистой оболочки желудка и двенадцатиперстной кишки применяют различные антибактериальные препараты (антибиотики, сульфаниламиды), причем часто в больших дозах. Действие этих препаратов на организм человека, в частности на слизистую оболочку пищеварительного тракта, неоднозначно. Антибиотики отрицательно влияют на нормальную функцию кишечника, возможны осложнения в виде индивидуальной непереносимости препаратов, а также у Нр может возникнуть резистентность к определенным антибиотикам в процессе эрадикационной терапии. У пожилых больных эффективность лечения низкая вследствие изменения реактивности, выраженных дегенеративных и атрофических изменений слизистой оболочки гастродуоденальной зоны. Наконец, лечение является длительным и дорогостоящим.
В последние годы появились сообщения об универсальном лечебном действии озона. Установлено, что озон в терапевтических дозах действует как бактерицидное, аналгезирующее и иммуномодулирующее средство, а также улучшает метаболические и репаративные процессы, стимулирует антиоксидантную защиту, микроциркуляцию. Мы использовали масло «Озонид», которое производит фирма «Медозон», для лечения 275 больных с эрозивно-язвенными поражениями желудка и двенадцатиперстной кишки, у которых заболевание сопровождалось выраженным болевым синдромом, а при цитологическом исследовании биопсийного материала был выявлен Нр в значительном количестве (+++). Язвенный анамнез у большей части больных составлял свыше 5 лет, при этом рецидивы имели место ежегодно, по 2–3 раза в год. Аппликации масла «Озонид» выполняли во время эзофагогастродуоденоскопии. На язву наносили 3–4 мл масла, вводя его по длинному катетеру, проведенному через биопсийный канал эндоскопа. Процедуру повторяли через день, всего от 3 до 6 сеансов на курс лечения. Осложнений в процессе лечения не было. Больные группы сравнения (30 человек) получали традиционную противоязвенную терапию.
В процессе местного лечения маслом «Озонид» наблюдается ранний и стойкий обезболивающий эффект в 100% случаев (после 1–2 сеансов лечебных гастродуоденоскопий). Начальные признаки эпителизации появляются уже после первой лечебной процедуры: язва становится более плоской за счет уменьшения воспаления и развития сочных грануляций. После 3–6 сеансов язвы полностью эпителизировались у всех пациентов. При этом в группе сравнения (традиционное лечение) процесс эпителизации длился 24±0,2 дней, а в группе, получавшей масло «Озонид», — 10±0,3 дней. Большинство больных получали лечение амбулаторно. Возникший на месте язвы рубец — нежный, эластичный, незначительно деформирующий стенку органа. До лечения Нр был выявлен в значительном количестве у 91,3% больных, после лечения он определялся у 2,2% пациентов. Ремиссия длится свыше 5 лет у 90,2% пациентов.
Наиболее актуальной проблемой хирургии является кровотечение из острых и хронических язв желудка и двенадцатиперстной кишки в связи с тяжелыми послеоперационными осложнениями и высокой летальностью, достигающей 8–25% (С. Г. Григорьев и соавт., 1999).
Первое упоминание об эндоскопическом исследовании при кровотечении из пищеварительного тракта принадлежит Killian (1900). Уже в середине 20-х гг. XX в. некоторые авторы (Jackson, Korbsch и др.) применяли эзофагогастроскопию у больных с желудочно-кишечными кровотечениями. Однако эти наблюдения были немногочисленны из-за несовершенства аппаратуры и отсутствия гибких эндоскопов.
Потребовались годы, чтобы метод эндоскопии получил широкое распространение для диагностики причин желудочно-кишечных кровотечений. Наибольшая заслуга в этом принадлежит Palmer, который занимался вопросами эндоскопической диагностики причин желудочно-кишечных кровотечений с 1945 г. Palmer пропагандировал раннее эндоскопическое исследование, которое он называл «энергичный диагностический метод». Применение экстренной эзофагогастроскопии позволило автору поставить правильный диагноз в 87,1% случаев против 34,9%, когда больные обследовались «классическим» методом. Широкое внедрение в клиническую практику эндоскопических методов исследования помогло решить вопросы экстренной диагностики локальной причины кровотечений из верхних отделов пищеварительного тракта. Диагностическая ценность ЭГДС при остром кровотечении составляет 75–98% (М. И. Кузин, 2001; А. А. Курыгин и соавт., 2001). Однако применение разнообразных способов остановки кровотечения, в том числе и эндоскопических, существенно не повлияло на общую летальность при этом осложнении (В. Н. Чернов и соавт., 1999; T. R. Pollard и соавт., 1996).
Первые попытки остановки желудочного кровотечения через эндоскоп путем термического воздействия были предприняты C. R. Youmans и соавт. в 1970 г. Начиная с 1971 г. в литературе стали появляться отдельные сообщения о проведении диатермокоагуляции через фиброэндоскоп при кровотечениях из верхних отделов пищеварительного тракта. Первые отечественные работы по лечебной эндоскопии путем диатермокоагуляции относятся к 1975 г. (В. И. Кукош, Ю. М. Корнилов, Р. Т. Панченков и др.).
В настоящее время всем больным, поступающим в клинику с диагнозом желудочно-кишечное кровотечение, выполняют экстренную ЭГДС для определения локализации и источника кровотечения и проведения местной гемостатической терапии. ЭГДС проводят в отделении реанимации или в эндоскопическом кабинете под местной анестезией гастрофиброскопом (Olimpus, LOMO, Pentax, Fujinon) или видеогастроскопом фирмы Fujinon или Olumpus. Если не удается визуализировать источник кровотечения из-за большого количества крови, больному промывают желудок «ледяной» водой (4°C) с помощью толстого желудочного зонда и проводят повторное эндоскопическое исследование. Благодаря внедрению современных эндоскопических технологий, все меньшее количество больных оперируется по поводу желудочно-кишечного кровотечения, так как кровотечение удается остановить во время эндоскопического исследования с помощью обкалывания кровоточащего сосуда с последующим введением сосудосуживающих лекарственных препаратов, аргоноплазменной коагуляции, радиоволновой коагуляции с помощью прибора «Сургитрон™» фирмы «Эллман Рус» (США) и др.
Первыми удаление полипов из желудка через эндоскоп выполнили японские врачи K. Tsuneoka и T. Uchida в 1970 г. Способ заключался в механическом отсечении опухоли на ножке с помощью металлической петли. В 1971 г.
M. Classen, L. Demling и R. Ottenjann разработали методику удаления полипов через эндоскоп диатермической петлей с использованием тока высокой частоты. В СССР первую эндоскопическую полипэктомию выполнили
В. С. Савельев и соавт. в 1973 г. В дальнейшем эндоскопические вмешательства стали применяться не только при полипах, но и для удаления на ранних стадиях раковых опухолей желудка типа I и IIa и подслизистых опухолей. Удалять полипы из желудка можно в амбулаторных условиях, тогда как из толстой кишки — только в условиях стационара из-за опасности развития осложнений.
Методика удаления полипов и подслизистых опухолей с помощью радиоволновой коагуляции безопасна, так как на месте отсеченной опухоли не образуется коагуляционный струп, как при электрокоагуляции, который может отторгнуться на третьи–седьмые сутки и вызвать кровотечение. Пассивный электрод накладывают на эпигастральную область. Петлю набрасывают на полип, затягивают у основания и на смешанном режиме «коагуляция–резание» полип отсекают, извлекают и направляют на гистологическое исследование. На месте удаленного полипа остается язва, покрытая белесоватой пленкой.
Использование метода радиоволновой хирургии при удалении полипов и доброкачественных неэпителиальных опухолей позволяет практически избежать послеоперационных кровотечений, так как при воздействии радиоволной на месте удаленного полипа не образуется струпа, а остается поверхностное изъязвление, которое эпителизируется в течение 5–7 дней.
Диагностика таких инородных тел, как безоары желудка и двенадцатиперстной кишки, чрезвычайно трудна, так как они не имеют характерной клинической картины. Клиническими признаками безоаров являются боли в эпигастральной области, тошнота, рвота, отрыжка тухлым содержимом, плохой аппетит, похудание, т. е. те симптомы, которые встречаются при язвенной болезни желудка и двенадцатиперстной кишки или при раке желудка.
Чаще других выявляются фитобезоары, которые формируются из растительной клетчатки, кожицы, семян и косточек плодов и фруктов (хурмы, сливы, винограда, инжира, черемухи). Трихобезоары образуются при попадании в желудок волос и встречаются чаще у людей с неуравновешенной психикой, которые испытывают непреодолимое желание кусать волосы, а также у лиц, работающих с волосом. Трихобезоары желудка иногда достигают 3,5 кг. Шеллакобезоары образуются в основном у алкоголиков. Причиной образования безоаров является прием внутрь спиртового лака, нитролака и политуры. Пиксобезоары образуются у лиц, имеющих привычку жевать смолу, вар. Себобезоары образуются при уплотнении животного жира. Возникновение себобезоаров связано с тем, что точка плавления животного жира выше внутрижелудочной температуры и происходит кристаллизация триглицеридов с образованием жировых камней.
Себо- и фитобезоары способствуют образованию язв в желудке и двенадцатиперстной кишке у 10–25% больных. Перфорация язвы желудка и кровотечение чаще наблюдаются при трихобезоаре. Тогда безоар случайно обнаруживают во время операции. При длительном нахождении безоара в желудке возможна малигнизация язвы. Описаны случаи сочетания безоаров желудка с карциномой. Кроме перфорации и малигнизации язв безоары могут вызывать непроходимость желудка, двенадцатиперстной и тонкой кишки.
При рентгенологическом исследовании безоар нередко принимают за доброкачественную или злокачественную опухоль. Установить точный диагноз возможно лишь во время эндоскопического исследования.
Все безоары, как правило, имеют размеры свыше 3 см в диаметре, поэтому во время гастроскопии перед удалением их необходимо рассечь петлей или раздробить каким-либо инструментом. Для того чтобы ускорить процесс дробления безоара, на него наносят несколько миллилитров трипсина, химотрипсина или химопсина во время первого исследования. Повторный осмотр выполняют через 2–3 дня. За это время мелкие части безоара отходят естественным путем, а более крупные следует раздробить на более мелкие части и удалить с помощью различных инструментов, проведенных через биопсийный канал эндоскопа. Иногда, при очень больших безоарах, для их удаления требуется провести до 10 эндоскопических исследований.
Среди всех эндоскопических методов исследования бронхоскопия давно занимает особое место, являясь не только одним из первых диагностических методов, но и важнейшим и эффективным способом лечения больных хроническими воспалительными и нагноительными заболеваниями легких.
Как показал наш многолетний опыт, единичные курсы лечебных бронхоскопий эффективны при пневмонии, абсцедирующей пневмонии или абсцессе легкого, а при хроническом бронхите, муковисцидозе, бронхоэктатической болезни необходимо проводить лечебные бронхоскопии курсами. Основными лекарственными веществами, которые используют во время лечебных бронхоскопий, являются антисептики, антибиотики, муколитики и иммуномодуляторы. Во время лечебной бронхоскопии удается восстановить дренажную функцию бронхов, удаляя гнойное содержимое из бронхиального дерева, проводить целенаправленное воздействие на микрофлору бронхов и вводить препараты, снижающие вязкость секрета. Санационные бронхоскопии выполняют через день. При этом лечение можно проводить в амбулаторных условиях. В зависимости от степени интенсивности воспалительного процесса в бронхах, выполняют от 5–6 до 8–10 санационных бронхоскопий на курс лечения.
Из оперативных методов лечения во время бронхоскопии наиболее часто применяют удаление доброкачественных опухолей и извлечение инородных тел. Особенно актуальна проблема диагностики и удаления инородных тел в педиатрии.
В заключение следует подчеркнуть, что будущее эндоскопии — это повышение возможностей диагностической эндоскопии за счет усовершенствования эндоскопических приборов с увеличением изображения в 100 и более раз, а также расширение показаний к раннему применению лечебно-оперативных эндоскопических способов во избежаниe осложнений и в целях сокращения количества открытых оперативных вмешательств.
Н. Е. Чернеховская, доктор медицинских наук, профессор
РМАПО, Москва
История появления эндоскопического оборудования
История появления эндоскопического оборудования
До определенного периода в истории медицины обследование внутренних органов пациента являлось абсолютно невозможным. Доктор мог прибегнуть только к неинвазивным диагностическим методикам – пальпация, перкуссия и аускультация. Это затрудняло постановку диагноза, а иногда и делало этот процесс вовсе невозможным. Ситуация кардинально изменилась с появлением хоть и примитивного, но уже достаточно эффективного эндоскопического оборудования, которое постоянно совершенствуется.
Современные эндоскопы это не просто оптико-механические конструкции, как было ещё всего несколько десятилетий назад. Сегодня эндоскопическое оборудование превратилось в высокотехнологичные приборы, позволяющие не только искать источник заболевания с помощью микрокамер высокого разрешения и диодных ламп, но и проводить сложнейшие хирургические операции изнутри пациента.
Первый эндоскоп никогда не применялся для обследования людей
История создания эндоскопа уходит в далекий 1805 год. Именно в этот период врачом из Франкфурта-на-Майне по имени Филипп Боззини был создан первый диагностический прибор, предназначенный для обследования полостей и каналов внутри человеческого организма. Уже тогда он был укомплектован светопроводником, роль которого играла обычная восковая свеча. Однако такой эндоскоп не нашел практического применения и даже был осмеян докторами из медицинского факультета города Вена.
Свое признание эндоскоп получил только в 1853 году благодаря доктору Дезормо, который использовал его при проведении цистоскопии. Инструмент состоял из нескольких трубок различного диаметра и спиртовой лампы с набором отражателей, для подвода света к обследуемой зоне.
Проведение гастроскопии с использованием эндоскопа впервые опробовали в 1868 году. Автором методики стал доктор по фамилии Куссмауль. Именно она в дальнейшем была положена в основу многих методов диагностики желудка гибкими и жесткими эндоскопами.
Первое обследование мочевого пузыря с использованием эндоскопа провели в 1876 году. Вариант прибора, который можно было ввести в его полость вместе с источником света, ссорудил Макс Нитце. Это был катетер из металла, загнутый в передней части. Источник света располагался внутри него и представлял собой очень тонкую платиновую петлю, изолированную в гусиное перо. Из-за нагревания её приходилось охлаждать потоком проточной воды.
Изобретение инновационной лампы накаливания – прорыв в эндоскопии
Первый цистоскоп со встроенной лампой накаливания в конструкции был разработан Ньюманом в 1883 году. Он использовался для осмотра мочевого пузыря. В 1901 году Лео Буэргер существенно модифицировал его линзовую систему, предложив вариант панорамного обзора.
Созданию полугибкого линзового эндоскопа медицина обязана Р. Шиндлеру. Он представлял собой трубку приблизительно длиной 78 см, которая имела гибкий наконечник 24 см и диаметр 12 мм. Внутри неё размещалось большое количество разнофокусных линз. Эндоскоп был оснащен вспышкой и камерой, которые способствовали получению изображений обследуемой области в относительно высоком разрешении.
С 1960 года эндоскопы оснащаются автономным источником холодного света. В моделях с жесткой трубкой начато применение стержневидных линз, разработанных физиком Хопкинсом.
Первые видеоэндоскопы появились только в 1986 году после изобретения приборов с зарядовой связью. Стеклянные световоды значительно расширили возможности эндоскопии. К осмотру стали доступны практически все органы, появились оптимальные условия для фотографирования и видеосъемки внутренних тканей.
Современная эндоскопия
Современные эндоскопические устройства получили множество дополнительных функций. Например, с их помощью можно не только обследовать орган, но и сделать биопсию или точечно ввести лекарственный препарат. С появлением микроскопического инструмента начало развиваться и новое направление в медицине – эндоскопическая хирургия (тут будет ссылка на след статью). При выполнении таких операций в брюшную полость или полые органы вводится эндоскоп и инструменты манипуляторы, которые управляются хирургом, наблюдающим за ходом хирургического вмешательства на внешнем дисплее.
С уважением, команда «Невские Технологии»
История пациента: эндоскопия без боли для таксы Арчи
Главная > Блог ветиринарного центра «ДокВет» > История пациента: эндоскопия без боли для таксы Арчи
История пациента: эндоскопия без боли для таксы Арчи
Любой хозяин будет волноваться, если питомец потеряет аппетит. В чем причина необычного поведения животного?
Сегодня врачи нашей клиники столкнулись с интересным случаем. Такса Арчи не испытывая проблем с аппетитом начала терять вес. Один из симптомов болезни – частая рвота. После диагностики (ссылка диагностика, прием у терапевта) врачи клиники решили: необходима гастроскопия.
Гастроскопией называют осмотр пищевода, желудка и двенадцатиперстной кишки при помощи специального прибора – гастроскопа. Цель гастроскопии «заглянуть» внутрь желудка животного не прибегая к помощи скальпеля.
Первый этап процедуры – наркоз. В результате Арчи расслаблен и не чувствует боли. А врачи могут не опасаться укуса «благодарного» пациента.
Анестезиолог Попова Анастасия Алексеевна помещает в трахею собаки дыхательную трубку. Это поможет избежать ситуации, когда голосовая щель спазмирует и животное не может дышать. Анастасия Алексеевна следит за уровнем кислорода в крови и сердцебиением Арчи. Все показатели в норме: пациент лежит стабильно, дышит самостоятельно, сердцебиение хорошее.
Чтобы определить причину болезни эндоскопист Степанова Наталья Анатольевна берет материал слизистой для гистологического исследования (ссылка анализы, гистология). Кусочки материала кишечника настолько маленькие, что животное никак не отреагирует и не испытает дискомфорта.
В результате эндоскопического исследования инородных предметов в желудочно-кишечном тракте не обнаружено. Отмечено изменение слизистых отделов желудка и двенадцатиперстной кишки. Такие изменения могут быть связаны с:
- ранее присутствовавшими инородными предметами;
- грубой пищей;
- инфекционными заболеваниями.
Результаты гистологического исследования помогут нам поставить более точный диагноз.
После необходимых процедур кислородная трубка извлекается, и пациент дышит сам. В течение часа Арчи сможет стоять на лапках и отправится домой. Проснется животное в нашем стационаре под присмотром профессионалов.
Ваш питомец ведет себя необычно? У него пропал аппетит? Бедняга проглотил любимую игрушку? Профессионально подобранная в «ДокВет» процедура избавит ваше животное от беспокойства.
История инструментов и методов желудочно-кишечной эндоскопии
- Charles SpurrJr.
Первый онлайн:
- 1 Цитаты
- 1,4 км Загрузки
Abstract
Визуализация кишечного тракта предпринималась с ограниченным успехом за много лет до современной эры эндоскопии.Самые ранние эндоскопические инструменты относятся к грубым зеркалам, найденным в пепле Помпеи (рис. 1.1). Прошли столетия без разработки эффективных инструментов из-за множества препятствий для визуализации кишечного тракта, включая темноту, глубину, углы и содержимое кишечника. Современная эндоскопия не могла бы развиваться без трех основных параллельных изобретений: (1) лампы накаливания Эдисона, (2) волоконной оптики и (3) устройства с заряженной парой (ПЗС) (Hirschowitz, Gastroenterology 104: 337–342, 1993).Описывается роль этих изобретений в развитии эндоскопии до ее современного состояния.
Ключевые слова
История Инструменты Hirschowitz Incandescent Fiber optic VideoЭто предварительный просмотр содержания подписки,
войдите в систему, чтобы проверить доступ.
Ссылки
1.
Шон Н. Помпей Хирургия и хирургические инструменты: The Medical News; 1895.
Google Scholar2.
Hirschowitz B I., Развитие и применение эндоскопии, Гастроэнтерология, 1993, февраль; 104 (2): 337–342.
Google Scholar3.
Эдмонсон Дж. История инструментов для эндоскопии желудочно-кишечного тракта. Gastrointest Endosc. 1991. 37 (2): S27–56.
CrossRefPubMedGoogle Scholar4.
Rathert WL, Lutzmeyer W., Goddwin WE. Филип Боззини (1793–1809) и Лихтлейтер. Урология. 1974; 3: 113–8.
CrossRefPubMedGoogle Scholar5.
Desormeaux (перевод).Эндоскоп и его применение для диагностики и лечения заболеваний мочевыводящих путей — уроки, проводимые в больнице Неккер. Чикагский медицинский журнал. 1867; 24: 184.18.
Google Scholar6.
Walk L. История гастроскопии. Clio Medica. 1966; 1: 209–22.
Google Scholar7.
Bevan JA. Эзофагоскоп. Ланцет I. 1868; 91: 470–1.
CrossRefGoogle Scholar8.
Newell OK. Эндоскопические инструменты Йозефа Лейтера из Вены и современное развитие эндоскопии.Boston Med Surg J. 1887; 117: 528–30.
CrossRefGoogle Scholar9.
Schindler R. Гастроскопия: 9.
Google Scholar10.
Шиндлер Р. Гастроскопия. Эндоскопическое исследование патологии желудка. 2-е изд. Чикаго: Чикагский университет; 1950.
Google Scholar11.
Benedict EB. Обследование желудка с помощью гибкого гастроскопа: предварительный отчет. NEJM. 1934; 210: 669.
CrossRefGoogle Scholar12.
Герстнер П. Американское общество эндоскопии желудочно-кишечного тракта: история. Gastrointest Endosc. 1991; 37: S1 – S26.
CrossRefPubMedGoogle Scholar13.
Haubrich WS. История эндоскопии. В: Сивак-младший М.В., редактор. Эндоскопия желудочно-кишечного тракта; 1987. с. 6.
Google Scholar14.
Ray Hufford A. Новый легкий, сверхгибкий гастроскоп. Rev Gastroenterol. 1946; 13: 381.
Google Scholar15.
Дональд Т.Чемберлен. Описание нового гастроскопа. Гастроэнтерология. 1949; 12: 209–11.
Google Scholar16.
Рэй Хаффорд А. Интегративная эзофагогастроскопия. Am J Gastroenterol. 1954; 22: 116–25.
Google Scholar17.
Segal HL, Watson JS. Цветная фотография с помощью гибкого гастроскопа. Гастроэнтерология. 1948; 10: 575–85.
PubMedGoogle Scholar18.
История эндоскопии и Olympus.
Google Scholar19.
Hopkins HH, Капаны NS. Гибкий фиброскоп со статическим сканированием. Природа. 1954. 173: 39–41.
CrossRefGoogle Scholar20.
Van Heel ACS. Новый метод передачи оптических изображений без аберраций. Природа. 1954; 173: 39.
CrossRefGoogle Scholar21.
Hirschowitz B. Эндоскопическое исследование желудка и двенадцатиперстной кишки с помощью фиброскопа. Ланцет. 1961; 277: 1074–8.
CrossRefGoogle Scholar22.
Ахорд JL. История эндоскопии желудочно-кишечного тракта в Гинзберге. В: Грегори Г. и др., Редакторы. Клиническая эндоскопия желудочно-кишечного тракта. п. 6.
Google Scholar23.
Haubrich WS. Сивак Младший М.В., редактор. Эндоскопия желудочно-кишечного тракта. п. 13.
Google Scholar24.
Kelly HA. Новый метод обследования и лечения заболеваний прямой кишки и сигмовидного изгиба. Ann Surg. 1895; 21: 468–78.
CrossRefPubMedPubMedCentralGoogle Scholar25.
Overholt BF. Гибкие оптоволоконные сигмоидоскопы. CA. 1969; 19: 80–4.
Google Scholar26.
Вольф В.И., Шинья Х. Колонофибероскопия. ДЖАМА. 1971; 217: 1509–12.
CrossRefPubMedGoogle Scholar27.
Вольф В.И., Шинья Х. Полипэктомия с помощью оптоволоконного колоноскопа: удаление новообразований, недоступных для сигмоидоскопа. N Engl J Med. 1973; 288: 329–32.
CrossRefPubMedGoogle Scholar28.
McCune WS, Shorb PE, Moscovitz H.Эндоскопическая канюляция ампулы Фатера: предварительный отчет. Ann Surg. 1968. 167: 752–6.
CrossRefPubMedPubMedCentralGoogle Scholar29.
Oi I, Takemoto T, Kendo T. Волоконный дуоденоскоп, прямое наблюдение за сосочком воды: предварительный отчет. Эндоскопия. 1970; 3: 101–3.
Google Scholar30.
Такаги К., Икеда С., Накагава И. и др. Ретроградная панкреатография и холангиография с помощью волоконного дуоденоскопа. Гастроэнтерология.1970; 59: 445–52.
PubMedGoogle Scholar31.
Огоши К., Тобита Ю., Хара Ю. Эндоскопическое наблюдение двенадцатиперстной кишки и панкреатохоледохография с использованием дуоденофиброскопа под прямым зрением. Gastrointest Endosc. 1970; 12: 83–96.
Google Scholar32.
Classen M, Koch H, Fruhmorgen P, et al. Результаты ретроградной панкреатикографии. Acta Gastroenterol Jpn. 1972; 7: 131–6.
Google Scholar33.
Vennes JA, Silvis SE.Эндоскопическая визуализация желчных и панкреатических протоков. Gastrointest Endosc. 1972; 18: 149–52.
CrossRefPubMedGoogle Scholar34.
Каваи К., Акасака Ю., Мураками К., Тада М. и др. Эндоскопическая сфинктеротомия ампулы Фатера. Gastrointest Endosc. 1974; 20: 148–51.
CrossRefPubMedGoogle Scholar35.
Соехендра Н., Рейджиндерс-Фредерикс В. Паллиативное дренирование желчных протоков. Новый эндоскопический метод введения транспапиллярного дренажа.Эндоскопия. 1980; 12: 8–11.
CrossRefPubMedGoogle Scholar36.
Lutz H, Rosch W. Трансгастроскопическое ультразвуковое исследование. Эндоскопия. 1976; 8: 203–5.
CrossRefPubMedGoogle Scholar37.
DiMagno EP, Buxton JL, Regan PT, et al. Ультразвуковой эндоскоп. Ланцет. 1980; 1: 629–31.
CrossRefPubMedGoogle Scholar38.
Сивак М.В., Джордж К. Эндоскопическая ультрасонография: предварительный опыт. Gastrointest Endosc. 1983; 29: 187A.
CrossRefGoogle Scholar39.
Wiersema MJ, Hawes RH, Wiersema LM, et al. EUS в качестве дополнения к цитологическому исследованию тонкоигольной аспирации верхних и нижних отделов желудочно-кишечного тракта. Gastrointest Endosc. 1992; 38: 35–9.
CrossRefPubMedGoogle Scholar40.
Rex RK, Tarver RD, Wiersema M, et al. Эндоскопический чреспищеводный тонкоигольный аспират новообразований средостения. Gastrointest Endosc. 1991; 37: 465–8.
CrossRefPubMedGoogle Scholar41.
Сивак М.В., Флейшер Д.Е. Желудочно-кишечный тракт. Эндоскопия. 1984; 30: 1–5.
Google Scholar42.
Тада М., Каваи К. Эндоскопия тонкой кишки. Сканд Дж Гастроэнтерол. 1984; 19: 39–52.
Google Scholar43.
Yamamoto H, Sekine Y, Saito Y. Тотальная энтероскопия с нехирургическим управляемым методом двойного баллона. Gastrointest Endosc. 2001; 53: 216–20.
CrossRefPubMedGoogle Scholar44.
Akerman PA, Agrawal D, Cantero D, Pangtay J.Спиральная энтероскопия с новой увертюрой DSB: новая техника для глубокой перфоративной интубации тонкой кишки. Эндоскопия. 2008; 40: 974.
CrossRefPubMedGoogle Scholar45.
Хашаб М.А., Леннон А.М., Каллоо А.Н. и др. Эндоскопия желудочно-кишечного тракта. 2010; 72 (4): 766. Спиральная эндоскопия против одиночного баллона
CrossRefPubMedGoogle Scholar46.
Беспроводная капсульная эндоскопия. Отчет об оценке состояния технологии. Gastrointest Endosc. 2013. 78 (6): 805–15.
CrossRefGoogle Scholar47.
Капсульная эндоскопия толстой кишки. Отчет о новых технологиях. Gastrointest Endosc. 2008. 68 (4): 621–3.
CrossRefGoogle Scholar48.
Crafoord C. Хирургическое лечение варикозного расширения вен пищевода. Acta Otolaryngol Stockh. 1939; 27: 422–9.
CrossRefGoogle Scholar49.
Паттерсон С., Роуз М. Инъекционное лечение варикозного расширения вен пищевода. ДЖАМА. 1946. 130 (7): 384–6.
CrossRefGoogle Scholar50.
Van Stiegman NG, Cambre T, Sun JH. Новое устройство для перевязки эндоскопической эластичной ленты. Gastrointest Endosc. 1986; 32: 230.
CrossRefGoogle Scholar51.
Barron J. Офисное лигирование геморроя. Am J Surg. 1963; 195: 563.
CrossRefGoogle Scholar52.
Hayashi T, Yonezawa M, Kawabara T. Исследование прочного зажима для эндоскопического лечения. Эндоскопия. 1975; 17: 92.
Google Scholar53.
Gauderer MW, Ponsky JL, Kzant RJ.Гастростомия без лапаротомии: чрескожная эндоскопическая техника. J Pediatr Surg. 1980. 15 (6): 872–5.
CrossRefPubMedGoogle Scholar54.
Pasricha PJ. Эндоскопия на 20 лет в будущее. Клин Гастроэнтерол Гепатол. 2013; 11: 119–22.
CrossRefPubMedGoogle Scholar
Информация об авторских правах
© Springer International Publishing AG 2018
Авторы и аффилированные лица
- 1. Госпиталь для ветеранов Чарли Норвуда и отделение гастроэнтерологии и гепатологии, Медицинский колледж Джорджии, Университет Августа США
Abstract
В начале 19 века были предприняты элементарные попытки наблюдать гортань, прямую кишку, влагалище и мочевыводящие пути с помощью примитивных эндоскопов.В 1868 году Куссмауль попытался наблюдать внутреннюю часть желудка с помощью жесткой прямой трубки, но безуспешно. Примерно в это же время было обнаружено, что яркий свет получается путем подачи электричества на платиновый провод при охлаждении проточной водой. После этого было разработано множество различных типов жестких гастроскопов с использованием этой недавно открытой системы в качестве источника света, который сначала представлял собой платиновую проволоку накаливания, а затем миниатюрные лампочки. В 1932 году Шиндлер разработал гибкий гастроскоп с функцией изгиба на конце.Было также проведено несколько экспериментов для постановки диагноза по фотографиям, сделанным с помощью миниатюрной камеры, вставленной в желудок. Lange et al. и другие исследователи, участвовавшие в этом подходе, но ни один из их аппаратов не выдержал практического клинического использования. В 1950 году, совершенно отдельно от эксперимента Ланге, Uji et al. разработали гастрокамеру. Хотя гастрокамера Удзи также не выдерживала практического использования, группа Тасаки на первом отделении внутренней медицины медицинского факультета Токийского университета начала клинические эксперименты с гастрокамерой в 1953 году и внесла различные улучшения, чтобы сделать ее действительно практичным медицинским устройством.В 1957 году Хиршовиц сделал фиброскоп. На основе этой технологии была разработана и широко распространена по всей Японии гастрокамера, оснащенная фиброскопом. По мере развития технологии фиброскопов были разработаны эндоскопы для толстой кишки, пищевода и двенадцатиперстной кишки. Видеоскоп, который сегодня стал основным направлением эндоскопов, был разработан по мере развития телевизионных технологий. Улучшение изображения, анализ изображений и технология узкополосной визуализации являются сегодня горячими темами в эндоскопии.Автофлуоресцентная визуализация также является одной из последних тем в эндоскопии. В этой главе автор предвидит будущее эндоскопии.
Ключевые слова
Жесткий гастроскоп Внутрижелудочная фотография Фиброскоп Видеоэндоскоп Узкополосная визуализация (NBI) Автофлуоресцентная визуализация (AFI)Это предварительный просмотр содержимого подписки,
войдите в, чтобы проверить доступ.
Предварительный просмотр
Невозможно отобразить предварительный просмотр. Скачать превью PDF.
Для дополнительной информации
1.
Niwa H (1997) История желудочно-кишечной эндоскопии. Медицинский центр Нихон, Токио
Google Scholar2.
Эдмонсон Дж. М. (1991) История инструментов для эндоскопии желудочно-кишечного тракта. Gastrointest Endosc 37: 27–56
CrossRefGoogle Scholar3.
Vilardell F (2006) Эндоскопия пищеварительной системы во втором тысячелетии. Thieme, Stuttgart
Google Scholar4.
Schindler R (1950) Гастроскопия: эндоскопическое исследование патологии желудка, 2-е изд.University of Chicago Press, Чикаго
Google Scholar5.
Lange F, Meltzing (1898) Die Photographie des Mageninnern. Münch Med Wochenschr 45: 1585–1588
Google Scholar6.
Heilpern J, Porges O (1930) Ber die Gastrophotogrraphie, eine neue Untersuchungs-method. Klin Wochenschr 9: 15–17
CrossRefGoogle Scholar7.
Niwa H (1996) История и перспективы развития эндоскопической медицины пищеварительной системы в Японии.Третий бюллетень. Азиатско-Тихоокеанское общество эндоскопии пищеварительной системы, Токио, Япония, стр. 69–80
Google Scholar8.
Ашизава С., Сакита Т., Нива Х. и др. (1959) Gastrocamera., Огата-шотен, Токио
Google Scholar9.
Niwa H, Kaneko E, Umeda N (1975) Эндоскопическая диагностика заболеваний желудка. Nankodo, Tokyo
Google Scholar10.
Niwa H, Utsumi Y, Nakamura T. и др. (1966) Эндоскопия толстой кишки. Труды Первого Конгресса Международного общества эндоскопии, 16–18 сен., Tokyo, pp. 425–431
Google Scholar11.
Niwa H, Fujino M, Yoshitoshi Y (1972) Фиброскопия толстой кишки для повседневной практики. Достижения в эндоскопии желудочно-кишечного тракта. Piccin, Padua, pp 549–555
Google Scholar12.
Niwa H, Sakai Y, Williams CB (2003) История эндоскопии прямой и толстой кишки. В: Waye JD, Rex JK, Williams CB (eds) Колоноскопия: принципы и практика. Blackwell, Malden, pp 1–20
Google Scholar13.
Classen M, Phillip J (1984) Электрическая эндоскопия желудочно-кишечного тракта. Первый опыт работы с новым типом эндоскопа без волоконно-оптического пучка для визуализации. Эндоскопия 16: 16–19
PubMedCrossRefGoogle Scholar14.
Niwa H, Kawaguchi A, Miyahara T. и др. (1992) Клиническое использование новых видеоэндоскопов (EVIS 100 и 200). Эндоскопия 24: 187–238
CrossRefGoogle Scholar
Информация об авторских правах
Авторы и аффилированные лица
- 1.Японское общество гастроэнтерологической эндоскопии, Токио, Япония,
- 2.St. Медицинский факультет Университета Марианны, Кавасаки, Япония
История гибких эндоскопических устройств
Гибкие эндоскопические устройства в настоящее время широко используются членами медицинского сообщества. Но как мы сюда попали? История гибких эндоскопических устройств и их жестких аналогов довольно длинна! Давайте посмотрим на историю этих замечательных современных медицинских устройств.
Некоторые историки медицины предполагают, что инструменты, позволяющие врачам заглядывать внутрь человеческого тела, могли быть разработаны еще в древнеримский период.Хотя есть некоторые споры относительно точной даты, археологи обнаружили нечто похожее на эндоскоп в руинах Помпеи — города, разрушенного в 79 году нашей эры извержением Везувия, так называемого «стратовулкана». в Неаполитанском заливе в Италии.
Однако настоящее изобретение эндоскопа приписывается большинством историков медицины человеку по имени Филип Боззини в 1805 году. Боззини, который оказался немцем, использовал созданную им специальную трубку, получившую название «Lichtleiter» (световод. инструмент), чтобы исследовать мочевыводящие пути.Название «эндоскоп» было придумано Антуаном Жаном Десормо — французским хирургом, который регулярно использовал изобретение Боззини.
Согласно авторитетным медицинским источникам, человек по имени Адольф Куссмаул был первым, кто использовал эндоскоп для исследования внутренней части живота. Это произошло в 1868 году. Десятилетием позже пара врачей — Макс Нитце и Йозеф Лейтер — изобрели тип эндоскопа, который использовался специально для осмотра мочевыводящих путей и мочевого пузыря.
В 1881 году известный польско-австрийский хирург Иоганн фон Микулич создал первый в истории гастроскоп, который использовался для лечения тонкой кишки, желудка и пищевода.Рудольф Шиндлер, немецкий гастроэнтеролог, усовершенствовал изобретение Иоганна фон Микулича, создав гибкий гастроскоп в 1932 году. В 1950-х годах группа врачей и инженеров-оптиков создала миниатюрную версию гастроскопа с камерой, которую они назвали «гастрокамерой». ” Удивительно, не правда ли?
В то же десятилетие, когда была изобретена гастрокамера, Гарольд Хопкинс (известный британский физик) сыграл центральную роль в создании устройства, получившего название «фиброскоп». Он состоял из пучка гибких стекловолокон.Фиброскоп давал лучшее качество изображения, чем его предшественники, за счет более точной фокусировки света на проверяемых областях.
Гибкие эндоскопические устройства, которые составляют основу современной медицины, обязаны своим существованием новаторским идеям и изобретениям людей, о которых мы только что говорили. История гибких эндоскопических устройств поистине замечательна, и инновации никогда не прекращаются. Даже сегодня исследователи-медики придумывают новые и лучшие способы сделать гибкие эндоскопические устройства более безопасными и эффективными, чем когда-либо прежде.
Эндоскопия | медицинская процедура | Britannica
Эндоскопия , медицинское обследование внутренней части тела, обычно через естественное отверстие тела, путем введения гибкого оптического стержня с подсветкой или открытой трубки. Используемые инструменты включают эндоскоп, гибкую трубку для исследования пищевода, желудка и двенадцатиперстной кишки и бронхоскоп, гибкую трубку для исследования бронхов. Они передаются через рот в соответствующие органы.Обследования обычно проводятся в больнице или кабинете врача под местной анестезией. Колоноскоп, гибкая трубка, используемая для исследования толстой кишки, и проктосигмоидоскоп, аналогичный инструмент, используемый для исследования прямой кишки и нижней части толстой кишки, пропускаются через анальное отверстие; Во время этих процедур обычно вводятся легкие седативные и обезболивающие. Цистоскоп, стержень с подсветкой, вводится через уретру для исследования мочевого пузыря под местной, спинальной или общей анестезией.Сегодня эти процедуры обычно сопровождаются использованием камеры или видеотехники для получения изображений исследуемых тканей. Кроме того, эндоскопы могут быть разработаны с цифровыми модификациями, которые облегчают визуализацию тканей.
двенадцатиперстная кишкаЭндоскопическое изображение двенадцатиперстной кишки.
SamirТри эндоскопических процедуры требуют разрезов для введения освещенного стержня. Торакоскоп позволяет исследовать грудную полость и поверхность легких через небольшой разрез между ребрами.Перитонеоскоп позволяет исследовать брюшную полость и нижние поверхности печени и желчного пузыря через небольшой разрез в брюшной стенке. Кульдоскоп позволяет исследовать женские тазовые органы через небольшой вагинальный разрез.
Волоконно-оптические эндоскопы — это гибкие, высокоманевренные инструменты, которые обеспечивают доступ к каналам в организме, к которым более старые полужесткие инструменты не имеют доступа вообще или могут получить доступ только с большим дискомфортом для пациента. Эти инструменты, состоящие из нескольких связанных вместе волосовидных стеклянных стержней, легче сгибать и скручивать, а интенсивный свет позволяет эндоскописту видеть вокруг углов, а также вперед и назад.К инструменту могут быть добавлены аксессуары, позволяющие получать образцы клеток и тканей, удалять полипы и небольшие опухоли, а также удалять инородные предметы.
Хотя оптоволоконные эндоскопы можно использовать для визуализации желудка и двенадцатиперстной кишки, они не могут проникнуть дальше в тонкий кишечник. В результате обследование тонкой кишки может потребовать использования беспроводной капсульной эндоскопии (эндоскопии с видеокапсулой), которая состоит из камеры размером с таблетку, которую можно проглотить. Камера передает данные на датчики, прикрепленные к брюшной полости с помощью клея, а регистратор данных, в котором хранится информация об изображении, собранная камерой, прикреплен к ремню, который надевается на талию.В большинстве случаев датчики и пояс носят в течение восьми часов, в течение которых капсула камеры получает изображения почти всей длины тонкой кишки. Изображения, хранящиеся в регистраторе данных, загружаются в компьютер для анализа. В конечном итоге капсула проходит по желудочно-кишечному тракту и выводится с дефекацией.
Получите подписку Britannica Premium и получите доступ к эксклюзивному контенту. Подпишись сейчас(PDF) История желудочно-кишечной эндоскопии и педиатрической эндоскопии
2 ПЕДИАТРИЧЕСКАЯ Гастроинтестинальная эндоскопия: Учебник и атлас
THE FIBERSCOPE
В гибридном полугибком гастроскопе, созданном немецким производителем
, использовались
линз для гастроскопа
. визуализация, но электрическая лампочка
заменена световодами из стекла или пластика.
tic.Пластиковые волокна были более гибкими и прочными, чем стекло
; однако стеклянные оптические волокна можно было изготавливать с диаметром меньше, чем их пластмассовые аналоги, а качество светопропускания было на
выше, чем у стеклянных оптических волокон. Ламм, молодой студент-медик
из Мюнхена, посещавший эндоскопию Шиндлера
. Он был первым, кто придумал применение оптоволоконных средств
в медицине, но не смог продолжить свои исследования
, когда иммигрировал в Соединенные Штаты, спасаясь от преследований нацистов в начале 1930-х годов.19 Следующие
усовершенствований в оптоволоконной технологии были сделаны благодаря
инженерам-оптикам, таким как Хольгер Молл-Хансен из
Дания и американец Брайан О’Брайен, который рассматривал возможность
оптоволоконной оптики, передающей не только свет, а
. В 1953 году в конфиденциальном голландском обзоре
De Ingenieur Абрахам ван Хил из
Delft сообщил о своем опыте передачи изображений
с использованием оптоволокна. В следующем году в журнале опубликованы две статьи
в том же номере журнала Nature — краткая заметка
ван Хила о «переносе изображений» и расширенная статья о гибком фиброскопе Гарольда Хопкинса
из Лондона и его коллеги Нариндер Сингх
Капани.20,21 Хопкинс и Капани использовали большое количество
очень тонких волокон, в то время как Ван Хил использовал меньшее количество
более крупных волокон, покрытых защитным слоем. Хопкинс
(хорошо известный своим изобретением зум-линзы
1949) также получил признание за его вклад в разработку
«холодного света».
Клиническое применение фиброоптики в гастроинтестике
nal (GI) эндоскопия началось в результате сотрудничества
между Бэзилом Хиршовицем и физиком Ларри
Кертисс.С помощью Corning Glass
им удалось произвести высококачественные оптоволоконные средства, в результате чего была опубликована первая клиническая публикация
по гастроскопии в гастроэнтерологии
в 1958 г. 22
Прототип фиброскопов были изготовлены американской компанией
Cystoscope Makers (ACMI) в 1960 году. и коммерческая модель
была выпущена в 1961 году с первыми цветными
изображений, опубликованными в Lancet.23 Из-за высокой распространенности рака желудка
в Японии компания Machida
разработала фиберэндоскопию и вскоре Технические специалисты компании Olympus во главе с инженером Кавахара,
, произвели множество прекрасных моделей с высоким оптическим качеством с
боковым и фронтальным обзором.24
Макс Эпштейн и его коллеги из Северо-западного
университета изучили многие технические аспекты тиковой эндоскопии fiberop-
. Они узнали, что пучок оптических волокон
можно протянуть в печи таким образом, чтобы
сохраняли свое выравнивание. Результирующая структура формирования изображения является жесткой, поскольку отдельные волокна
сплавлены вместе. Разрешение совмещенной волоконно-оптической структуры определяется диаметром волокна, а
обычно меньше 1
—
.2d, где — диаметр волокна.Сплавленное многоволокно
покрыто полимером
, отверждаемым ультрафиолетом, что делает структуру достаточно гибкой. Эта технология
аналогична той, которая используется в производстве оптических волокон, используемых в коммуникационной технике. Диаметр отдельных волокон составляет порядка
порядка 10 мкм. В процессе наматывания они пропитываются связывающей эпоксидной смолой
. Диаметр мультиволоконного изображения
составляет от 1 до 2 мм для эндоскопов mini-
, таких как ангиоскопы или детские бронхоскопы
и 6 мм для больших колоноскопов с
длиной более 2 м.Большие мультиволокна могут содержать от
от 200000 до 300000 отдельных волокон, каждое из которых
обеспечивает одну точку разрешения или пиксель.25,26
Гастроэнтеролог, практикующий 30 лет назад, имел
доступ к терапевтическому и диагностическому фиберэндоскопическому инструменту
. . Тем временем в эндоскопии
использовались компьютерные технологии, и сегодня большинство
отделений эндоскопии оснащены видеоэндоскопическим оборудованием
(см. Главу 2 «Эндоскопическое оборудование»).Тем не менее,
панендоскопия и энтероскопия (см. Главу 8
«Энтероскопия») не позволяют легко обследовать
более мелкого дистального отдела тонкой кишки. Недавно разработка видеокапсулы
(см. Главу 11 «Беспроводная капсула
для эндоскопии») позволила визуализировать весь тракт
GI.
ФИБЕРЕНДОСКОПИЧЕСКИЕ ИНПЕДИАТРИКИ
После адаптации волоконно-оптических приборов для медицинских инструментов
в конце 1960-х годов эндоскопия тракта GI
стала рутинным диагностическим и терапевтическим инструментом
в отделениях гастроэнтерологии по всему миру.
Иногда в таких отделениях обследовались дети,
, но диагностика заболеваний органов пищеварения у детей была
в основном на основе контрастной радиологии. 27,28 с техническими
улучшениями, особенно уменьшением диаметра инструмента
, обследованием желудочно-кишечного тракта в дети
стало возможным в 1970-х годах.29,30 Афеведиатры
начали использовать эту новую исследовательскую технологию у
детей.31–38 Вначале было необходимо сотрудничество с
эндоскопистов, прошедших обучение взрослых, но в пределах
несколько у педиатрических гастроэнтерологов было
волоконно-оптических эндоскопов Hirschowitz, 1960 — Центр медицинской истории Диттрика
Волоконно-оптическая эндоскопия вошла в сферу практического применения в феврале 1957 года, когда Бэзил Хиршовиц пропустил первый прототип инструмента себе в глотку, а через несколько дней — в горло пациента.Хиршовиц начал работу над «фиброскопом» в 1954 году, когда он работал с Марвином Поллардом в Мичиганском университете. Прочитав статью Хопкинса и Капани, описывающую последние достижения в области волоконной оптики, Хиршовиц посетил авторов в Великобритании и обсудил применение волоконной оптики в эндоскопии. В течение следующих трех лет Хиршовиц и его сотрудники в Анн-Арборе, физик К. Уилбур Петерс и его ученик Ларри Кертисс разработали временный, но эффективный метод вытягивания собственных стеклянных волокон.В конце 1956 года Кертиссу удалось произвести стекловолокно с оптическими качествами, необходимыми для жгута волокон гастроскопа. После демонстрации нового фиброскопа, включающего это достижение в 1957 году, Хиршовиц сотрудничал с ACMI (American Cystoscope Manufacturing Inc.) для создания практического инструмента. Наконец, в октябре 1960 года Хиршовиц получил первую серийную модель и представил ее в виде Lancet , уверенно заявив, что «обычный гастроскоп устарел по всем пунктам.”
Бэзил Хиршовиц осматривает |
Этот инструмент уменьшил дискомфорт пациента за счет повышения гибкости и уменьшения объема. Заметные усовершенствования эндоскопов в конце 1960-х — начале 1970-х годов включали изменение положения линз для более широкого поля зрения, добавление каналов для биопсийных щипцов, аспирации, воздуха или воды и четырехстороннее контролируемое отклонение наконечника.
Волоконно-оптическая технология изменила эндоскопию желудочно-кишечного тракта гораздо глубже, чем могли представить ее самые ярые сторонники. Эндоскопические процедуры становятся более безопасными и, следовательно, более распространенными, и практически ни одна область желудочно-кишечного тракта не остается неисследованной. Уильям Хаубрих, редактор журнала Gastrointestinal Endoscopy , вспоминал, что «улучшения в дизайне эндоскопов были настолько многочисленными и быстрыми в начале 1970-х годов, что едва ли можно было купить новый инструмент и познакомиться с его использованием до того, как этот инструмент устарел новой моделью .Расширяющиеся диагностические возможности эндоскопии вскоре были дополнены новыми терапевтическими применениями, включая полипэктомию толстой кишки с петлей из проволоки (1971), канюляцию протока поджелудочной железы (1972), удаление желчных камней (1975) и установку питательных трубок с помощью гастростомия (1979). Диапазон технических достижений в эндоскопии желудочно-кишечного тракта был настолько обширен, что Джон Ф. Моррисси заявил: «Я думаю, что мы приближаемся к плато в разработке инструментов.Этот вывод оказался преждевременным, но, тем не менее, он передает изумление, которое испытывали Моррисси и его коллеги-эндоскописты желудочно-кишечного тракта, изучая недавнее развитие инструментальной техники в своей области. Действительно, волоконно-оптические технологии быстро распространились от гастроскопии до колоноскопии, бронхоскопии и других эндоскопических областей.
Вернуться к выбору артефактов
История— Европейское общество эндоскопии желудочно-кишечного тракта (ESGE)
ESGE была официально учреждена и получила свое название и устав на 7-м заседании A.S.N.E.M.G.E. («Ассоциация национальных европейских обществ и средиземноморских гастроэнтерологов») Конгресс, Брюссель, 1964 год. Однако, чтобы признать фактическое развитие общества, необходимо сделать краткий исторический взгляд на формирование тех обществ и конгрессов, из которых возникла ESGE.
В 1954 году было основано всемирное общество гастроэнтерологов взамен S.I.G.E. («Societé Internationale de Gastroentérologie»), которое было обществом индивидуальных членов.Также на Парижской конференции в 1954 году было решено провести всемирный конгресс гатстроэнтерологов в Вашингтоне в 1958 году. Этот конгресс оказался чрезвычайно посещаемым и успешным, и хотя не было представлено никаких конкретных докладов по эндоскопии, были презентации по фотографии желудка. и гастрокамера: был очевиден живой интерес к эндоскопическим темам.
К началу 1960-х эндоскопия играла все более важную роль на встречах, и в результате в больнице A.S.N.E.M.G.E. Конгресс в Лейдене в 1960 году прошел симпозиум по различным вопросам эндоскопии, где группа эндоскопистов собралась и решила создать клуб, который сосредоточился на продвижении эндоскопии. «Европейский эндоскопический клуб» был основан Адольфом Вибенга (Амстердам), Эдуардом Якобсом (Брюссель), Зденеком Мараткой, Сашей Сегал (Реймс) и Санду Стоичита (Бухарест). Всего четыре года спустя на вышеупомянутом конгрессе в Брюсселе члены клуба собрались с другими заинтересованными эндоскопистами и вместе договорились создать Европейское общество эндоскопии желудочно-кишечного тракта (ESGE).Шарль Дебре из Франции был первым президентом, в состав правления которого вошли три вице-президента, секретарь, казначей, редактор и почетный президент.
С этого времени ESGE неуклонно становился сильнее и активнее. Многочисленные семинары, грантовые программы, а также работа образовательных, руководящих принципов и исследовательских комитетов, разработка ежегодного конгресса ESGE Days и участие в Единой европейской гастроэнтерологической неделе (UEG Week) успешно достигли первой и главной цели общество: продвигать качество в эндоскопии
.

 Е. «Причины безуспешной эрадикационной терапии, не связанные с антибиотикорезистентностью Helicobacter pylori, и пути их преодоления», РМЖ, Медицинское обозрение, №3/2018.
Е. «Причины безуспешной эрадикационной терапии, не связанные с антибиотикорезистентностью Helicobacter pylori, и пути их преодоления», РМЖ, Медицинское обозрение, №3/2018.