польза и вред / bwell-swiss.ru
Помните, как наши мамы и бабушки заставляли нас дышать над картошкой?
Сейчас нам и в голову не придет такое, а тогда, в нашем детстве, так лечили любую простуду. На смену «картошке» пришли ингаляторы (небулайзеры). Но всегда ли оправдано их применение? Давайте разберемся.
С помощью современных медицинских ингаляторов проводятся, так называемые «холодные» ингаляции. Раствор с их помощью доставляется непосредственно в место назначения: трахею, бронхи, и даже бронхиолы . Ингаляторы могут отличаться по способу и механизму «измельчения» крупных молекул лекарственных веществ, однако цель у них одна — вылечить кашель, главный спутник большинства ОРЗ.
Но всегда ли ингаляционная терапия полезна?
Что нужно знать родителям, чтоб не навредить себе и ребенку:
Во-первых :
Ингаляции назначаются врачом! Доктор при осмотре обязательно выслушает легкие, определит локализацию источника кашля и после этого рекомендует то или иное лекарственное средство, которое с помощью современных приборов будет доставляться точно по назначению.
Во-вторых:
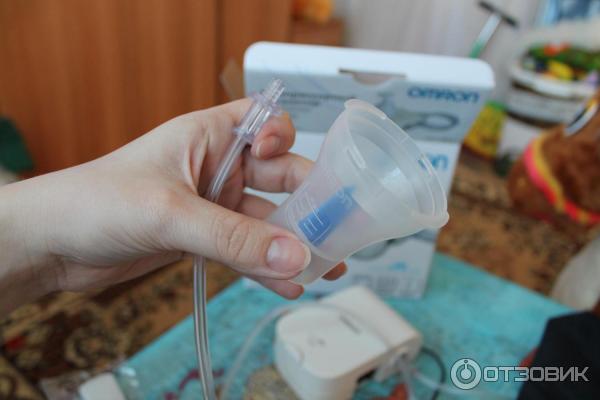
Нужно выбрать правильный ингалятор. И это желательно сделать заранее, не дожидаясь эпидемии. Иначе будете покупать то, что есть в наличии. И, возможно, даже по заоблачным ценам. Большинство врачей рекомендуют для домашней аптечки приобрести именно компрессорный небулайзер, например PRO-115 или PRO-110. Они не имеют ограничений по видам используемых лекарств для ингаляционной терапии. В комплекте с прибором обычно идут как взрослая, так и детская маски. А в комплекте к небулайзерам В.Well идут одна взрослая, две детские маски разных размеров, мундштук и насадка для носа, поэтому они прекрасно подходят для всех членов семьи, в том числе для самых маленьких.
В-третьих:
Есть лекарства, направленные на разжижение трудно отделяемой вязкой мокроты, и их нельзя применять детям младше 2 лет, а так же нельзя вдыхать слишком глубоко (их задача действовать в трахеях и крупных бронхах, не ниже). Ни в коем случае не занимайтесь самолечением, всегда доверяйте выбор лекарственного препарата сильнее физраствора доктору.
Кроме того, лекарства на основе трав в небулайзерах применять так же опасно, как и масляные растворы. Травы способны вызвать острую аллергическую реакцию, сопровождаемую резким спазмом дыхательных путей, а масляные растворы, образуя пленку в бронхиолах, нарушают газообмен что может спровоцировать «масляную» пневмонию.
Применение травяных отваров и масляных растворов допустимо лишь в ингаляторах, таких, как «Чудо Пар»
Так же стоит помнить:
Ингаляцию можно начинать если температура тела ребенка ниже 37,5 С.
При правильном , а главное разумном, применении ингаляционная терапия значительно облегчает и сокращает время течения большинства респираторных заболеваний.
Поделитесь статьёй с друзьями
ГБУЗ СО «Тольяттинская городская клиническая больница №5»
Ингаляция – хороший способ лечения дыхательных путей.
Лекарственные вещества в ингаляторах охватывают всю слизистую и быстрее таблеток всасывается в кровь. Однако у ингаляторов есть некоторые противопоказания и свои особенности. Мы рассказажем, как правильно использовать ингаляторы, чтобы еще больше не навредить своему здоровью.
Современная медицина может предложить три вида ингаляторов: небулайзерный, компрессорный и ультразвуковой.
Небулайзерный поможет избавиться от воспаления в бронхах, трахеях и проблем с легкими.
Компрессор – не самый эффективный, однако самый простой в обращении.
Ультразвуковой – неплохой вариант, но если у вас проблемы с задней стенкой горла и носоглоткой, лучше выбрать набулайзерный ингалятор. Он лучше других вылечивает бронхи и трахеи.
Он лучше других вылечивает бронхи и трахеи.
Ингалятор стоит держать в каждом доме из-за большого количества показаний. Во-первых, это заболевания лор-органов: для задней стенки глотки, для нёбных миндалин, при хроническом тонзиллите, для носоглотки, для слизистой оболочки полости носа, при воспалении слизистой, при аденоидах у детей, при синуситах – тоже назначаются для того, чтобы разжижить слизь в носу, при ларингитах. Также для бронхолегочной системы. Это заболевания трахеи – трахеиты, бронхов – бронхиты, и заболевания легких – это пневмония и воспаление легких.
Ингалятор необходим детям, у которых по ночам происходит острое воспаление гортани. Оно проявляется сухим кашлем или хрипом. Ингалятор в этом случае увлажнит слизистую и снимет симптомы. А если добавить кортикостероидные ингаляционные препараты и подышать ими, то отек и воспаление быстро будут купированы.
При сухом воздухе возникает огромное желание кашлянуть. В таком случае ингаляторы помогут увлажнить слизистую, которая страдает от сухости.
Однако есть случаи, когда ингаляторы использовать категорически нельзя!
Если у вас поднялась температура выше 38,5 градусов, появился отек и на лицо явные признаки ангины, то ингаляторы использовать вредно. В обострении хронического тонзиллита тоже запрещено. При температуре от 38,9 ингаляция может привести к отеку и удушению.
Кроме того, ингаляции противопоказаны при грибковой флоре. Потому что это может привести к распространению грибков со слизистой в гортань и бронхи и вызвать серьёзные последствия.
Применение ингалятора обязательно нужно согласовывать с врачом. Только он сможет рассчитать для вас конкретный тип и точную дозировку.
Есть исключения: если речь идет о ложном крупе у детей, то ингаляторы можно применить самостоятельно, – пояснил врач. – Здесь нужно применять ингалятор с физраствором, а затем вызвать скорую помощь. Если ребенку нужно отхаркивающее, используйте физраствор, а затем добавьте препарат, который разжижает мокроту (соотношение: 1 мл препарата, 10 мл физраствора).
Если ребенку нужно отхаркивающее, используйте физраствор, а затем добавьте препарат, который разжижает мокроту (соотношение: 1 мл препарата, 10 мл физраствора).
Небулайзер: вред и польза — Врач общей практики Сергей Макаров, Винница
«Доктор, знакомая купила ингалятор, нужно ли и нам его приобрести?».
«У ребенка начался насморк и покраснело горлышко, а у нас есть небулайзер, чем можно подышать?»
«А разве можно делать ингаляции при повышении температуры? Нам сказали, что это опасно».
«И что, этот аппарат правда лечит? Я вот слышала, что это очень вредно…».
Подобные вопросы довольно часто задают родители на приеме у врача. И если Вы, уважаемый читатель, заинтересовались заголовком данной публикации, значит, для Вас данная тема тоже является актуальной. Спешим уверить, что Вы на верном пути, потому что после прочтения этой статьи многое прояснится.
Итак, для чего же нужен этот аппарат и нужен ли он вообще? Давайте попробуем разобраться.
При заболеваниях глотки и полости рта – можно оказывать лечебное воздействие путем орошения или смазывания слизистой препаратом, либо просто рассасывая пастилки и леденцы с лекарственными веществами. То есть эти зоны достаточно легкодоступны и местное лечение не составляет практически никакого труда.
Когда же речь идет о слизистой гортани и нижних дыхательных путей – то добраться до них сложно и местное лечение в таком случае возможно только при наличии специальных приспособлений. Вот таким приспособлением и является небулайзер, который преобразует жидкое лекарство в аэрозоль, состоящий из очень маленьких и летучих капелек, который при вдыхании поступает глубоко в дыхательные пути и там оседает. Такой подход имеет ряд неоспоримых преимуществ, потому что позволяет создать на слизистой оболочке высокую концентрацию действующего вещества (и получить выраженный лечебный эффект) с минимальным риском развития системных побочных реакций, потому что в кровь при этом всасывается лишь ничтожная часть препарата.
Кстати, из вышесказанного можем сделать первый вывод: небулайзер предназначен для доставки лекарств в нижние дыхательные пути, а не в нос или глотку, поэтому, как говорит один знакомый доктор, попытки использовать его при насморке или фарингите равносильны забиванию гвоздей микроскопом. Справедливо это еще и потому, что на слизистой носа и глотки во время ингаляции оседает мало лекарства, гораздо меньше, чем могло быть нанесено с помощью того же спрея. Поэтому, во всем цивилизованном мире небулайзерная терапия назначается при довольно ограниченном перечне заболеваний и все подряд им лечить не следует. А верить мировому опыту мы можем спокойно, так как небулайзеры используют в медицинской практике уже больше ста лет, поэтому накоплен огромный опыт их применения, который нам остается только перенять.
Какие же существуют показания для использования небулайзеров? Их, на самом деле очень немного. Из того, что встречается чаще всего – это ложный круп (он же стенозирующий ларинготрахеит, он же стеноз гортани) и бронхообструктивный синдром (обструктивный бронхит и обострение бронхиальной астмы). В первом случае используют ингаляционные стероиды, которые быстро уменьшают отек слизистой оболочки гортани, расширяя ее просвет и устраняя проблемы с дыханием, во втором – бронхолитики (средства, снимающие бронхоспазм) и все те же стероиды, которые оказывают мощный противовоспалительный эффект. Иные ингаляционные препараты (например, разжижающие мокроту или антибиотики) используют очень редко и только при весьма специфических заболеваниях (упомянем их для самых любознательных читателей – это муковисцидоз, бронхоэктатическая болезнь и некоторые другие). Как видите, несмотря на вековой опыт применения небулайзеров, в мировой клинической практике используется довольно скудный перечень лекарств, употребляемых для ингаляционной терапии.
В первом случае используют ингаляционные стероиды, которые быстро уменьшают отек слизистой оболочки гортани, расширяя ее просвет и устраняя проблемы с дыханием, во втором – бронхолитики (средства, снимающие бронхоспазм) и все те же стероиды, которые оказывают мощный противовоспалительный эффект. Иные ингаляционные препараты (например, разжижающие мокроту или антибиотики) используют очень редко и только при весьма специфических заболеваниях (упомянем их для самых любознательных читателей – это муковисцидоз, бронхоэктатическая болезнь и некоторые другие). Как видите, несмотря на вековой опыт применения небулайзеров, в мировой клинической практике используется довольно скудный перечень лекарств, употребляемых для ингаляционной терапии.
В нашей же стране, к сожалению, наблюдается иная тенденция – «заливать» в небулайзер пытаются всё, что попадается под руку: начиная от минеральной воды и отваров трав, заканчивая масляными растворами и препаратами, явно не предназначенными для ингаляционного введения. Кроме того, некоторые весьма ловкие и предприимчивые отечественные фармпроизводители наладили выпуск препаратов, даже в инструкции к которым обозначено, что они пригодны для применения в виде ингаляций, а между тем, не существует никаких убедительных доказательств как их эффективности, так и безопасности. То есть никто и никогда всерьез не занимался изучением влияния этих лекарств на организм, а все выводы об их якобы «эффективности» — не более, чем ничем не обоснованные утверждения производителя. Следует подчеркнуть, что подобные препараты не используют больше нигде в мире. Но такая «эксклюзивность», на наш взгляд, должна отнюдь не радовать, а настораживать и врачей, и пациентов.
Кроме того, некоторые весьма ловкие и предприимчивые отечественные фармпроизводители наладили выпуск препаратов, даже в инструкции к которым обозначено, что они пригодны для применения в виде ингаляций, а между тем, не существует никаких убедительных доказательств как их эффективности, так и безопасности. То есть никто и никогда всерьез не занимался изучением влияния этих лекарств на организм, а все выводы об их якобы «эффективности» — не более, чем ничем не обоснованные утверждения производителя. Следует подчеркнуть, что подобные препараты не используют больше нигде в мире. Но такая «эксклюзивность», на наш взгляд, должна отнюдь не радовать, а настораживать и врачей, и пациентов.
Ведь легкомысленно относиться к ингаляционной терапии нельзя ни в коем случае.
Одной из наиболее частых ошибок является применение для ингаляций нестерильных растворов, в частности – минеральной воды. Это довольно рискованно, а все по одной простой причине. Нижние дыхательные пути в норме стерильны и организм постоянно прикладывает значительные усилия, чтобы эту стерильность поддерживать. Небулайзер же, как упоминалось ранее, создает очень летучий мелкодисперсный аэрозоль, который проникает глубоко в дыхательные пути и, если в используемом растворе содержатся бактерии, способные вызвать воспалительный процесс – это может привести к развитию пневмонии и других инфекционных осложнений. Конечно же, это происходит далеко не каждый раз, когда ребенку дают «подышать» минералкой или другими нестерилизованными растворами, но риск абсолютно реальный, поэтому такой практики следует избегать. Впервые на подобные результаты применения нестерильных растворов для ингаляций обратили внимание больше сорока лет назад (существует немало научных публикаций на этот счет) и с тех пор все современные международные рекомендации по небулайзерной терапии содержат указание на то, что все лекарства, применяемые с целью ингаляций должны быть стерильными.
Нижние дыхательные пути в норме стерильны и организм постоянно прикладывает значительные усилия, чтобы эту стерильность поддерживать. Небулайзер же, как упоминалось ранее, создает очень летучий мелкодисперсный аэрозоль, который проникает глубоко в дыхательные пути и, если в используемом растворе содержатся бактерии, способные вызвать воспалительный процесс – это может привести к развитию пневмонии и других инфекционных осложнений. Конечно же, это происходит далеко не каждый раз, когда ребенку дают «подышать» минералкой или другими нестерилизованными растворами, но риск абсолютно реальный, поэтому такой практики следует избегать. Впервые на подобные результаты применения нестерильных растворов для ингаляций обратили внимание больше сорока лет назад (существует немало научных публикаций на этот счет) и с тех пор все современные международные рекомендации по небулайзерной терапии содержат указание на то, что все лекарства, применяемые с целью ингаляций должны быть стерильными. Конечно, требования к стерильности в данном случае не настолько жесткие, как к растворам, применяемым для внутривенных вливаний и инъекций (после вскрытия многодозового флакона ингаляционный препарат теряет свою строгую стерильность, но может храниться и применяться какое-то время, так как микробное обсеменение незначительное). Но изначально, препарат для ингаляции стерилизуется в производственных условиях и хранится в герметичной емкости. Понятное дело, минеральная вода, отвары трав и другие «домашние» средства могут содержать непредсказуемо большое количество потенциально опасных бактерий, поэтому использоваться не должны.
Конечно, требования к стерильности в данном случае не настолько жесткие, как к растворам, применяемым для внутривенных вливаний и инъекций (после вскрытия многодозового флакона ингаляционный препарат теряет свою строгую стерильность, но может храниться и применяться какое-то время, так как микробное обсеменение незначительное). Но изначально, препарат для ингаляции стерилизуется в производственных условиях и хранится в герметичной емкости. Понятное дело, минеральная вода, отвары трав и другие «домашние» средства могут содержать непредсказуемо большое количество потенциально опасных бактерий, поэтому использоваться не должны.
Еще более грубой ошибкой является применение масляных растворов, так как жиры могут оседать на стенках бронхов и даже альвеол, что способно привести к нарушению газообмена с самыми непредсказуемыми последствиями. Также некоторые авторы указывают на возможность развития так называемого жирового пульмонита в случае применения масел для ингаляций с помощью небулайзера.
Бытует мнение, будто небулайзер нельзя применять при повышении температуры тела. Вместе с тем, невозможно найти хоть сколь-нибудь логичное и разумное объяснение данному высказыванию, как нет и подтверждений этому ни в инструкциях к ингаляционным препаратам, ни в руководствах по эксплуатации небулайзеров. Более того, никакого упоминания о вреде ингаляций при лихорадке нет ни в одних международных рекомендациях по использованию небулайзера (например, в таких, как European Respiratory Society Guidelines on the use of nebulizers, 2001), это при том, что, как мы уже говорили, за рубежом подобные аппараты используют больше ста лет. На самом деле, во всем цивилизованном мире ингаляционную терапию проводят при любой температуре тела пациента, если для этого есть показания. А все потому, что в действительности температура тела в этом отношении не имеет никакого значения. Это не влияет ни на свойства препарата, ни на реакцию организма. Некоторые утверждают, будто повышенная температура от ингаляции может еще больше вырасти, но ведь это не паровая ингаляция, при которой пациент дышит горячим паром! Аэрозоль, образуемый небулайзером, имеет комнатную температуру, поэтому никак не влияет течение лихорадки.
Итак, подытожим.
- Небулайзер – это средство доставки лекарственного средства в гортань и нижние дыхательные пути, использование его для лечения верхних отделов, таких, как носовая полость и глотка – нецелесообразно.
- Существует очень ограниченный перечень показаний и лекарств для ингаляционной терапии, не следует пытаться лечить при помощи небулайзера любой кашель, а тем более – насморк или боль в горле, а также использовать для ингаляций минералку, отвары трав, масляные растворы или сомнительные препараты.
- Наличие лихорадки не является препятствием к применению ингаляционной терапии, так как повышение температуры тела на 2-3 градуса никак не сказывается ни на эффективности, ни на безопасности такого лечения.
И последнее – лечит не небулайзер, а ингалируемое лекарство. Поэтому, поможет или навредит ингаляция – зависит от правильности выбора препарата и наличия обоснованных показаний к его применению. Соблюдение этих условий возможно только в том случае, если ингаляционная терапия назначается грамотным специалистом.
Соблюдение этих условий возможно только в том случае, если ингаляционная терапия назначается грамотным специалистом.
С пожеланием крепкого здоровья
Сергей и Ольга Макаровы
Вступайте в наши группы в фейсбуке и вконтакте!
Примечание: данная статья не претендует на исчерпывающую полноту, некоторые аспекты были умышленно опущены, чтобы не перегружать информацией, сложной для неподготовленного читателя.
ГБУЗ СО «Тольяттинская городская клиническая больница №5»
Ингаляция – хороший способ лечения дыхательных путей.
Лекарственные вещества в ингаляторах охватывают всю слизистую и быстрее таблеток всасывается в кровь. Однако у ингаляторов есть некоторые противопоказания и свои особенности. Мы рассказажем, как правильно использовать ингаляторы, чтобы еще больше не навредить своему здоровью.
Современная медицина может предложить три вида ингаляторов: небулайзерный, компрессорный и ультразвуковой.
Небулайзерный поможет избавиться от воспаления в бронхах, трахеях и проблем с легкими.
Компрессор – не самый эффективный, однако самый простой в обращении.
Ультразвуковой – неплохой вариант, но если у вас проблемы с задней стенкой горла и носоглоткой, лучше выбрать набулайзерный ингалятор. Он лучше других вылечивает бронхи и трахеи.
Ингалятор стоит держать в каждом доме из-за большого количества показаний. Во-первых, это заболевания лор-органов: для задней стенки глотки, для нёбных миндалин, при хроническом тонзиллите, для носоглотки, для слизистой оболочки полости носа, при воспалении слизистой, при аденоидах у детей, при синуситах – тоже назначаются для того, чтобы разжижить слизь в носу, при ларингитах. Также для бронхолегочной системы. Это заболевания трахеи – трахеиты, бронхов – бронхиты, и заболевания легких – это пневмония и воспаление легких.
Ингаляции можно использовать с препаратами или антистатиком, разжижающие слизь. При сильно кашле они тоже хорошо помогают, потому что снижают напряжение слизистой.
При сильно кашле они тоже хорошо помогают, потому что снижают напряжение слизистой.
Ингалятор необходим детям, у которых по ночам происходит острое воспаление гортани. Оно проявляется сухим кашлем или хрипом. Ингалятор в этом случае увлажнит слизистую и снимет симптомы. А если добавить кортикостероидные ингаляционные препараты и подышать ими, то отек и воспаление быстро будут купированы.
При сухом воздухе возникает огромное желание кашлянуть. В таком случае ингаляторы помогут увлажнить слизистую, которая страдает от сухости.
Однако есть случаи, когда ингаляторы использовать категорически нельзя!
Если у вас поднялась температура выше 38,5 градусов, появился отек и на лицо явные признаки ангины, то ингаляторы использовать вредно. В обострении хронического тонзиллита тоже запрещено. При температуре от 38,9 ингаляция может привести к отеку и удушению.
Кроме того, ингаляции противопоказаны при грибковой флоре. Потому что это может привести к распространению грибков со слизистой в гортань и бронхи и вызвать серьёзные последствия.
Применение ингалятора обязательно нужно согласовывать с врачом. Только он сможет рассчитать для вас конкретный тип и точную дозировку.
Есть исключения: если речь идет о ложном крупе у детей, то ингаляторы можно применить самостоятельно, – пояснил врач. – Здесь нужно применять ингалятор с физраствором, а затем вызвать скорую помощь. Если ребенку нужно отхаркивающее, используйте физраствор, а затем добавьте препарат, который разжижает мокроту (соотношение: 1 мл препарата, 10 мл физраствора).
Солевые орошения при хроническом риносинусите
Вопрос обзора
Мы рассмотрели доказательства о пользе и вреде назального солевого орошения у пациентов с хроническим риносинуситом.
Актуальность
Хронический риносинусит — это распространенное состояние, которое характеризуется воспалением слизистой носа и околоносовых пазух (группа наполненных воздухом пространств позади носа, глаз и щек). Пациенты с хроническим риносинуситом испытывают по крайней мере, два или более из следующих симптомов по меньшей мере в течение 12 недель: заложенность носа, выделения из их носа или насморк, боль или чувство давления в области лица и/или пониженное обоняние (гипосмия). У некоторых людей также бывают полипы в носу, представляющие собой похожие на виноград набухания нормальной слизистой оболочки внутри носовых ходов и носовых пазух.
У некоторых людей также бывают полипы в носу, представляющие собой похожие на виноград набухания нормальной слизистой оболочки внутри носовых ходов и носовых пазух.
Назальная ирригация (также известная, как назальный душ, ополаскивание или промывание) является процедурой, при котором полость носа промывают изотоническим или гипертоническим солевыми (соленой водой) растворами. Пациент проводит инстиляцию (введение) солевого (физиологического) раствора в одну ноздрю и позволяет ему вытекать из другой ноздри, промывая тем самым носовую полость. Солевое назальное орошение может быть выполнено при низком положительном давлении из пульверизатора, насоса или шприца-бутылки, с помощью небулайзера или при гравитационном давлении с использованием сосуда со специальным носиком (‘neti pot’). Эта терапия доступна без рецепта, и используется как отдельное, так и дополнительное лечение многими пациентами с хроническим риносинуситом.
Характеристика исследований
В этот обзор мы включили два рандомизированных контролируемых клинических испытания с участием в общей сложности 116 взрослых. В одном сравнивали орошения гипертоническим раствором большого объема (150 мл) с обычным лечением в течение шести месяцев. В другом сравнивали солевой раствор, распыляемый небулайзером в объеме 5 мл, используемый два раза в день, с интраназальными кортикостероидами. Лечение участников продолжалось в течение трех месяцев, оценку эффекта проводили по завершении лечения и спустя три месяца. Оба эти исследования имели существенные ограничения в методологии, и мы посчитали, что они имеют высокий риск смещения.
В одном сравнивали орошения гипертоническим раствором большого объема (150 мл) с обычным лечением в течение шести месяцев. В другом сравнивали солевой раствор, распыляемый небулайзером в объеме 5 мл, используемый два раза в день, с интраназальными кортикостероидами. Лечение участников продолжалось в течение трех месяцев, оценку эффекта проводили по завершении лечения и спустя три месяца. Оба эти исследования имели существенные ограничения в методологии, и мы посчитали, что они имеют высокий риск смещения.
Основные результаты и качество доказательств
Гипертонический солевой раствор в большом объеме (в носовую полость) в сравнении с обычным лечением
В небольшом испытании (76 участников) по нашему основному исходу «качество жизни, связанное со здоровьем по конкретному заболеванию» результаты были представлены с помощью шкалы от 0 до 100 баллов. По окончании трех месяцев лечения, пациентам в группе солевого орошения было лучше, чем в группе плацебо, а через шесть месяцев эффект от лечения был ещё `больший. Мы оценили качество доказательств по трем месяцам наблюдения как низкое, и как очень низкое — по шести месяцам.
Мы оценили качество доказательств по трем месяцам наблюдения как низкое, и как очень низкое — по шести месяцам.
Также сообщалось о тяжести заболевания по оценкам пациентов, но проводившие испытание не указали диапазон или счет баллов, которые они использовали, что сделало невозможным для нас определить значение представленных данных.
Данные о побочных эффектах не были собраны в контрольной группе, но 23% участников в группе солевого орошения испытывали побочные эффекты, включая кровотечение из носа (носовое кровотечение).
В этом исследовании также измеряли качество жизни, связанное с общим состоянием здоровья. Не было обнаружено различий после трех месяцев лечения, но через шесть месяцев была небольшая разница (хотя результат является неопределенным). Мы оценили качество доказательств как низкое.
Солевой раствор, распыленный небулайзером, в малом объёме (5 мл), в сравнении с интраназальными кортикостероидами
Одно небольшое исследование сравнило 20 пациентов в каждой из двух групп. Результаты по нашему основному исходу «качество жизни, связанное со здоровьем по конкретному заболеванию» не были представлены. В конце лечения (через три месяца) наблюдалось улучшение в симптоматике.
Результаты по нашему основному исходу «качество жизни, связанное со здоровьем по конкретному заболеванию» не были представлены. В конце лечения (через три месяца) наблюдалось улучшение в симптоматике.
Выводы
Эти два исследования были очень разные с точки зрения включенных групп населения, вмешательств и сравнений, и поэтому трудно сделать выводы для практики. Данные свидетельствуют о том, что нет пользы от солевого раствора, распыленного в небольшом объеме небулайзером (5 мл), по сравнению с интраназальными кортикостероидами, но может быть некоторая польза от орошения солевым раствором в большом объеме (150 мл) по сравнению с плацебо, хотя качество доказательств была низким в отношении длительности лечения в течение трех месяцев и очень низким — в течение шести месяцев.
«Юлайзер» и «Декасан» помогут в борьбе с респираторными вирусами – Газета.uz
За окном весна, дни становятся все жарче, но вероятность подхватить ОРВИ или по-народному простуду, совершенно не снижается. Многие и вовсе говорят о том, что заболевают простудой весной даже чаще, чем зимой. В чем причины этого парадокса?
Многие и вовсе говорят о том, что заболевают простудой весной даже чаще, чем зимой. В чем причины этого парадокса?
Причин несколько. В первую очередь это уменьшение запасов витаминов, что в итоге приводит к снижению иммунитета и местной защиты дыхательных путей. Также в межсезонье отмечается повышенная вирусная активность. Статистика подтверждает эти данные. Причинами острых респираторных инфекций в 80% случаев становятся вирусы, и только в 20% случаев — бактерии. Именно поэтому для лечения простуды нужно выбрать препарат, который будет действовать как против вирусов, так и против бактерий.
Также важно выбрать правильный способ доставки препаратов в дыхательные пути.
В настоящее время является возможным вылечить ОРВИ при помощи местных лекарств и таких умных устройств, как небулайзеры «Юлайзер». При ОРВИ «Юлайзер» свободно доставляет лекарственный препарат прямо в пораженный орган — в дыхательные пути, тем самым обеспечивает быстрый терапевтический эффект. В связи с тем, что лекарство практически не всасывается в системный кровоток, предупреждается развитие системных побочных эффектов.
В связи с тем, что лекарство практически не всасывается в системный кровоток, предупреждается развитие системных побочных эффектов.
Конечно же, без лекарственных средств «Юлайзер» один не справится с задачей. Для этого необходим препарат, который при ингаляции будет одновременно влиять как на вирусы, так и на бактерии. Одним из таких препаратов является ингаляционный антисептик «Декасан».
«Декасан» с помощью «Юлайзера» попадает прямо в дыхательные пути и действует как против вирусов, так и против бактерий. Он выпускается в стерильных однодозовых контейнерах, что обеспечивает удобство для использования и стерильность.
Антисептик «Декасан» в ингаляциях устраняет причину заболевания, а не только симптомы.
«Декасан» рекомендуется использовать через «Юлайзер» по 2−4 мл два раза в день в течение 5−7 дней.
Дополнительную информацию можно узнать на сайте и по телефону: (+998) 71−200−00−11.
«Декасан». Регистрационное удостоверение РУз: DV/X 06140/05/19. Состав: декаметоксин, 2 мл №10. Производитель: ООО «Юрия-Фарм», Украина.
Регистрационное удостоверение РУз: DV/X 06140/05/19. Состав: декаметоксин, 2 мл №10. Производитель: ООО «Юрия-Фарм», Украина.
Компрессорный небулайзер. Регистрационное удостоверение РУз: ТB/X 02332/02/19. Производитель: Vega Technologies Inc.
Имеются противопоказания. Перед применением следует ознакомиться с полной инструкцией или проконсультироваться со специалистом.
На правах рекламы.
Зачем капать аминокапроновую кислоту в нос для профилактики ОРВИ: 8 доказательств эффективности
Аминокапроновая кислота детям для профилактики гриппа предписывается врачом в виде капель или ингаляций 5% раствором этого вещества. Это готовый продукт для процедур. А за неимением такого можно использовать небулы (чистую кислоту в ампулах), но нужно обязательно разбавлять содержимое ампул с физраствором (в пропорции 1:1).
Аминокапроновая кислота детям для ингаляций: как разводить содержимое ампул с физраствором и по какой схеме проводить процедуры?
Для профилактики ОРВИ и гриппа | 0,5-1 мл + 0,5-1 мл физраствора | 1-2 процедуры в день по 3-5 минут, в течение 5-14 дней, за 3-4 месяца до начала эпидемиологического сезона Курс желательно повторить непосредственно перед началом сезона ОРВИ |
Для лечения | 1-2 мл + 1-2 мл физраствора | 2-3 процедуры ингаляции в день по 5-7 минут в течение недели |
Обратите внимание! Существует чистая аминокапроновая кислота в ампулах и уже разведенная с физраствором. По внешнему виду оба варианты похожи, но состав разный.
По внешнему виду оба варианты похожи, но состав разный.
Для разведения аминокапроновой кислоты из небул нужно использовать стерильный физраствор. Он продается не только в бутылках. Натрия хлорид 0,9% раствор также бывает в небольших ампулах, что чрезвычайно удобно. Дышать аминокапроновой кислотой можно через небулайзер, а ингаляции делают классическим компрессорным, ультразвуковым или же МЕШ-ингалятором. Перед процедурой обязательно промойте нос ребенка физраствором.
Для профилактических мер в основном назначают 1-2 сеанса в день по 5 минут, в течение 7-14 дней. Первый такой курс желательно пройти за 3-4 месяца до предполагаемого сезона обострения ОРВИ, а второй — непосредственно перед его началом.
Для лечения ОРВИ или гриппа предписывается в других дозах. Обычно, когда вирусная инфекция в организме ребенка уже обнаружена, назначают 2-3 процедуры ингаляции в день по 5-7 минут в течение недели и, конечно же, увеличивая дозу аминокапроновой кислоты до 2 мл.
Аминокапроновая кислота: ингаляции для профилактики ОРВИ будут максимально эффективными, если придерживаться некоторых правил терапии:
- ингаляции нельзя проводить сразу перед или после приема пищи;
- не делайте ингаляцию, если заметили, что температура вашего тела выше нормы;
- перед тем, как вылить раствор в емкость и выбросить бутылку в мусорное ведро (т.е. до того, как вы приступите к ингаляции), обязательно прочтите инструкцию к препарату и при необходимости свяжитесь с врачом;
- никогда не экспериментируйте с дозировками аминокапроновой кислоты или других лекарств, точные дозы вам должен сообщить врач;
- не включайте небулайзер до тех пор, пока не наполнили его сосуд лекарственным средством;
- во время ингаляции нужно следить за тем, чтобы маска небулайзера максимально плотно прилегала к вашему лицу;
- если вы собираетесь делать ингаляцию своему ребенку, постарайтесь заранее его подготовить к этой процедуре и найти способ, чтобы отвлечь внимание непоседы;
- чтобы поскорее избавиться от отека носоглотки и насморка, нужно вдыхать лекарство через нос, а выдыхать ртом.
 Вообще, вдохи во время процедуры должны быть достаточно глубокими;
Вообще, вдохи во время процедуры должны быть достаточно глубокими; - используйте хорошие небулайзеры и выбирайте всегда только качественные лекарственные препараты и растворы;
- после того, как вы закончите сеанс терапии, обязательно помойте стаканчик и маску небулайзера, чтобы на нем не скапливались болезнетворные микроорганизмы.
Обратите внимание! Время ингаляционной профилактики и терапии должен определять исключительно ваш лечащий врач. Если концентрация тромбоцитов в крови пациента превышает норму, аминокапроновую кислоту в нос закапывать или делать ингаляции с ней запрещено, поскольку это может вызвать осложнения.
Наличие небулайзера в домашней аптечке или специального ингалятора облегчает задачу родителям и ускоряет процесс выздоровления ребенка. Но что же делать, если малыш еще совсем маленький или боится дышать через такие аппараты?
В виде 5% раствора можно закапывать в нос аминокапроновой кислотой, как обычные капли. В течение всего сезона ОРВИ целесообразно ежедневное использование этого препарата в профилактических целях, даже самым маленьким членам семьи.
В течение всего сезона ОРВИ целесообразно ежедневное использование этого препарата в профилактических целях, даже самым маленьким членам семьи.
Аминокапроновая кислота грудничку назначается лечащим врачом, обычно по 1-2 капли 5% раствора в каждую ноздрю 2 раза в день, в течение недели. Данных об ограничении применения препарата детям нет, то есть его можно давать малышам любого возраста. Однако редкие исключения все же бывают, поэтому не поленитесь уточнить у своего врача: какое именно количество аминокапроновой кислоты грудничку давать для профилактики ОРВИ и как часто?
Является ли распыленный физиологический раствор плацебо при ХОБЛ? | BMC Pulmonary Medicine
Обследовано 40 пациентов во время госпитализации по поводу обострения ХОБЛ. Пациентов набирали в то время, когда их состояние стабилизировалось перед запланированной выпиской из больницы. Клинические данные пациентов приведены в таблице 1. Шесть пациентов прошли обе конечности исследования (частичный перекрестный дизайн)./GettyImages-835935056-59b5d4f5aad52b0011821cbe.jpg)
Пациенты были рандомизированы для получения 4 мл 0.9% физиологический раствор с использованием эффективной системы распылителя (активная группа) или неэффективной системы распылителя (группа плацебо). Активным небулайзером был небулайзер System 22 Acorn (Medic-Aid, Bognor Regis UK Ltd), приводимый в действие системой подачи кислорода по трубопроводу больницы со скоростью потока 9 л / мин в течение 10 минут. Было обнаружено, что эта распылительная система доставляет 95% частиц размером от 2,5 до 2,8 микрон с использованием лазерной системы Malvern. (Измерения любезно предоставлены доктором Стивом Ньюманом, главным физиком Королевской бесплатной больницы, Лондон, Великобритания).Этот небольшой размер частиц был выбран для достижения эффективной доставки в дыхательные пути. Небулайзер для плацебо представлял собой небулайзер Bard Inspiron старой модели (1980-е гг.) (Больше не производился), приводимый в действие кислородом со скоростью потока 3 л / мин. Эта система распылителя доставляла 95% частиц размером от 9,5 до 9,9 микрон. Этот размер частиц был выбран для достижения эффекта плацебо с отложением в трубках системы и в глотке, но с небольшим проникновением в дыхательные пути [12]. Оба препарата с распылителем вводились через мундштук, чтобы избежать осаждения капель физиологического раствора в носу и снизить вероятность того, что пациенты заметят, что результат от системы плацебо отличается от предыдущего лечения с помощью распыления, которое они получали.
Эта система распылителя доставляла 95% частиц размером от 9,5 до 9,9 микрон. Этот размер частиц был выбран для достижения эффекта плацебо с отложением в трубках системы и в глотке, но с небольшим проникновением в дыхательные пути [12]. Оба препарата с распылителем вводились через мундштук, чтобы избежать осаждения капель физиологического раствора в носу и снизить вероятность того, что пациенты заметят, что результат от системы плацебо отличается от предыдущего лечения с помощью распыления, которое они получали.
Исследование проводилось слепым методом. 40 листов бумаги были помечены как «Обработка A» или «Обработка B» и помещены в непрозрачные коричневые конверты. Они были перемешаны в случайном порядке, и каждому пациенту было предложено выбрать один конверт. Затем исследователь открыл его и назначил соответствующее лечение (активный А, плацебо В). Для шести пациентов, которые принимали участие в исследовании дважды, второе лечение состояло из того лечения, которое они не получали ранее.
Пациентам сказали, что мы хотели «наблюдать эффекты небулайзерного лечения, которое не является новым или экспериментальным лекарством». Они не были проинформированы о точном характере лечения с помощью распыления, поскольку это могло побудить пациентов попытаться угадать, было ли полученное лечение «плацебо». Комитет по этике согласился с тем, что было бы невозможно измерить истинный эффект плацебо, если бы пациенты знали, что оба препарата были физиологическим раствором (не бронходилататором), а один из небулайзеров был намеренно сделан неэффективным.
Пациенты были набраны в респираторные отделения университетской больницы. Мы набрали пациентов, у которых диагноз ХОБЛ был подтвержден консультантом по респираторным заболеваниям (пациенты с астмой или бронхоэктазами были исключены из исследования). К пациентам обратился один из исследователей, когда они находились в относительно стабильной фазе перед выпиской из больницы после госпитализации с обострением ХОБЛ. Все тесты проводились между 12. 00 и 16.00, по крайней мере, через четыре часа после лечения бронходилататорами.
00 и 16.00, по крайней мере, через четыре часа после лечения бронходилататорами.
Перед участием в исследовании пациенты дали информированное согласие и провели базовое измерение ОФВ1 и ФЖЕЛ, используя лучший из трех ударов на спирометре Microlab 3300 (Micro-Medical LTD, Рочестер, Великобритания. Измеряли пиковую скорость выдоха (PEF) с использованием пикового расходомера Райта. Каждый пациент также записывал оценку своего воспринимаемого уровня одышки с использованием модифицированной семибалльной шкалы Лайкерта (1 = не одышка, 2 = очень легкая одышка, 3 = легкая одышка, 4 = умеренная одышка, 5 = Сильная одышка, 6 = очень сильная одышка, 7 = наихудшая возможная одышка).
Через десять минут после завершения небулайзерной терапии были повторены измерения FEV1, FVC и PEF, а также субъективная оценка одышки. Пациенты также регистрировали субъективную оценку пользы, используя следующую модифицированную шкалу Лайкерта. (1 = Нет пользы от этого лечения, 2 = Очень незначительное улучшение, 3 = Незначительное улучшение, 4 = Умеренное улучшение, 5 = Хорошая польза, 6 = Очень хорошая польза, 7 = Максимально возможная польза).
Затем пациенты получили 4 вдоха сальбутамола (400 мкг) с использованием дозированного ингалятора и 750 мл спейсера Volumatic (Glaxo Smith Kleine UK).
Через пятнадцать минут были повторены измерения FEV1, FVC и PFR, а также баллы субъективной одышки и баллы облегчения симптомов.
Все данные были введены в статистический пакет SPSS версии 9. U-критерий Манна-Уитни использовался для сравнения тестов функции легких и оценки облегчения симптомов. Знаковый ранговый тест Вилкоксона использовался для сравнения изменения показателей одышки для согласованных пар до и после распыления физиологического раствора.
Исследование было одобрено Комитетом по этике исследований Салфорда и Траффорда.Все пациенты дали письменное информированное согласие на участие в исследовании и на получение однократной дозы распыленного препарата (в дополнение ко всему обычному лечению).
Преимущества небулайзерной терапии — PARI
Мягкое, естественное и эффективное — ингаляция
На протяжении веков было известно, что соленый воздух, как и морской воздух, оказывает успокаивающее и успокаивающее действие на наши дыхательные пути. Он стимулирует естественную функцию очистки наших дыхательных путей и помогает разжижить слизь в носу и легких. Благодаря современным ингаляционным аппаратам и солевым растворам для ингаляций вы можете принести пользу морского воздуха в собственный дом.Кроме того, после консультации с врачом можно вдыхать смеси лекарств или лекарств и изотонические солевые растворы (раствор-носитель).
Он стимулирует естественную функцию очистки наших дыхательных путей и помогает разжижить слизь в носу и легких. Благодаря современным ингаляционным аппаратам и солевым растворам для ингаляций вы можете принести пользу морского воздуха в собственный дом.Кроме того, после консультации с врачом можно вдыхать смеси лекарств или лекарств и изотонические солевые растворы (раствор-носитель).
Одно преимущество ингаляционной терапии? Это детская игра!
Для ингаляции с помощью ингаляционных аппаратов и небулайзеров PARI вам не нужно ни уметь интенсивно дышать, ни каких-либо особых навыков. Это особенно полезно для детей, людей с ограниченной подвижностью рук или пожилых людей. Это означает, что для ингаляции с помощью небулайзера достаточно спокойствия и расслабления.Многие пациенты думают, что при использовании ингаляционного аппарата нужно делать быстрый и сильный вдох. Это относится только к ингаляторам с сухим порошком. А когда вы вдыхаете с помощью дозированного ингалятора, вы должны глубоко вдохнуть, нажимая на ингалятор, потому что в противном случае лекарство вообще не высвободится. Использование небулайзера проще: сядьте прямо и расслабьтесь. Спокойно вдыхайте и выдыхайте. В идеале дышите как обычно. Таким образом, меньше лекарства попадает в горло и попадает в легкие туда, где оно необходимо.
Использование небулайзера проще: сядьте прямо и расслабьтесь. Спокойно вдыхайте и выдыхайте. В идеале дышите как обычно. Таким образом, меньше лекарства попадает в горло и попадает в легкие туда, где оно необходимо.
Вы можете научиться дышать расслабленно.
Чтобы солевые растворы или лекарства достигли легких, вы должны дышать как можно более расслабленно. Но что на самом деле означает расслабленное дыхание? Как я узнаю, что дышу правильно? С PARI PIF Control (PIF означает пиковый поток вдоха) вам не нужно об этом беспокоиться. Это дает вам надежную обратную связь, если вы слишком быстро вдохнете, «заблокировав» небулайзер. Если вы заметили эту закупорку, просто дышите немного медленнее.PIF-контроль интегрирован во многие устройства семейства PARI BOY и во все небулайзеры PARI LC SPRINT для нижних дыхательных путей. Исключения: медицинские наборы PARI LC SPRINT, PARI LC SPRINT Tracheo и PARI LC SPRINT CENTRAL. Пациенты с ХОБЛ могут использовать PIF-контроль, чтобы предотвратить коллапс мелких бронхов. Если чувствуете сопротивление, спокойно выдохните и на следующем вдохе сделайте медленный вдох.
Если чувствуете сопротивление, спокойно выдохните и на следующем вдохе сделайте медленный вдох.
Экономьте время: ингаляция плюс физиотерапия
Системы PARI PEP также помогают при дыхании.Как и в случае с физиотерапией, вы можете разжижить даже слизь, которая прочно застряла в бронхах. Различные системы PARI PEP могут быть очень легко прикреплены к небулайзерам PARI, так что ингаляционная терапия и дыхание PEP могут выполняться одновременно. Как это работает? Сопротивление систем PEP создает противодавление при выдохе. Это позволяет большему количеству лекарства попадать в периферические дыхательные пути при вдохе. Легче откашлять слизь и выдохнуть больше воздуха из легких.С PARI O-PEP вибрации, создаваемые O-PEP при выдохе, разжижают даже густую слизь со стенок бронхов, что облегчает откашливание.
Кстати, Deutsche Atemwegsliga (Немецкая лига респираторного здоровья) также включает ингаляцию физиологического раствора и терапию PEP в своих рекомендациях по респираторной физиотерапии.
Распыленный 5% или 3% гипертонический или 0,9% физиологический раствор для лечения острого бронхиолита у младенцев
Задача: Чтобы сравнить эффективность и безопасность 5%, 3% и 0.9% физиологический раствор для лечения острого бронхиолита на догоспитальном этапе.
Дизайн исследования: Это было двойное слепое испытание, в котором последовательно участвовали младенцы в возрасте <18 месяцев, получавшие лечение в городских условиях оказания неотложной помощи. В общей сложности 165 пациентов были рандомизированы для получения 5%, 3% или 0,9% (нормального) физиологического раствора с адреналином каждые 4 часа. Первичным результатом эффективности было улучшение оценки тяжести бронхиолита через 48 часов (анализ chi2).Для оценки безопасности записывались баллы и насыщение кислородом непосредственно до и после каждого лечения.
Полученные результаты: В исследование были включены 187 ранее здоровых младенцев (средний возраст 3,1 месяца) с диагнозом бронхиолит. Положительность в отношении респираторно-синцитиального вируса была аналогичной в 3 группах лечения (в среднем 56%). Через 48 часов средний балл тяжести для группы с 5% физиологическим раствором составлял 3.69 +/- 1,09, а для группы с 0,9% физиологическим раствором — 4,12 +/- 1,11 (P = 0,04; разница 0,43, 95% доверительный интервал для разницы 0,02-0,88). Средняя оценка тяжести для группы с 3% физиологическим раствором была промежуточной и составила 4,00 +/- 1,22. Частота повторных посещений после выписки была аналогичной в 3 группах лечения. Побочных реакций или других проблем безопасности выявлено не было.
Выводы: Распыление 5% -ным гипертоническим раствором безопасно, может быть широко распространено и может превосходить текущее лечение для раннего амбулаторного лечения бронхиолита.
Физиологический раствор для небулайзера (хлорид натрия 0,9% масс. / Об.) (Стрелка) — Сводка характеристик продукта (SmPC)
Эта информация предназначена для медицинских работников
Солевой раствор для небулайзера
(хлорид натрия 0,9% мас. / Об.)
Каждый 1 мл раствора содержит 9 мг хлорида натрия
Полный список вспомогательных веществ см. В разделе 6.1.
Раствор для распыления
Прозрачный бесцветный раствор в прозрачной пластиковой ампуле для однократного приема
Для разбавления растворов для распыления.
Взрослые, дети и пожилые люди: использовать по назначению врача.
Физиологический раствор для небулайзера должен использоваться только в качестве разбавителя для разбавления продуктов для небулайзера и не должен использоваться сам по себе. Его нельзя принимать перорально или парентерально.
Каждая ампула содержит 2,5 мл раствора.
Подробные инструкции по использованию этого раствора в качестве разбавителя см. В информационном бюллетене для пациента распыляемого продукта для разбавления, который вам прописал врач.Для обеспечения точного дозирования рекомендуется при необходимости использовать дозирующий шприц.
В информационном бюллетене для пациента распыляемого продукта для разбавления, который вам прописал врач.Для обеспечения точного дозирования рекомендуется при необходимости использовать дозирующий шприц.
Способ введения: Путем ингаляции из подходящего небулайзера или аппарата искусственной вентиляции легких с периодическим положительным давлением после того, как ампула с однократной дозой была открыта и ее содержимое перенесено в камеру небулайзера. Администрация должна осуществляться в соответствии с инструкциями производителя устройства.
1. Подготовьте небулайзер, следуя инструкциям производителя и советам врача.
2. Продукт, который нужно развести в небулайзере, следует ввести в камеру небулайзера в соответствии с инструкциями в соответствующем информационном буклете для пациента.
3. Осторожно отделите новую ампулу физиологического раствора от полоски. Никогда не используйте уже открытую ампулу.
3. Откройте ампулу, просто открутив верхнюю часть, всегда стараясь удерживать ее в вертикальном положении.
4. Выдавите содержимое пластиковой ампулы или используйте дозирующий шприц, если требуется, в камеру небулайзера и осторожно покрутите, чтобы перемешать.
5. Соберите небулайзер и используйте его в соответствии с указаниями врача.
6. После распыления очистите распылитель в соответствии с инструкциями производителя. Важно, чтобы небулайзер был чистым.
Поскольку единичные дозы не содержат консервантов, важно, чтобы их содержимое использовалось сразу после открытия, а при каждом введении использовалась свежая ампула, чтобы избежать микробного заражения. Частично использованные, открытые или поврежденные единичные дозы следует выбросить.
Любой раствор, оставшийся в камере небулайзера, следует выбросить.
Раствор нельзя вводить перорально или парентерально.
Не используйте, если продукт не прозрачный и упаковка не повреждена. Выбросьте излишки после использования. Физиологический раствор небулайзера следует использовать с небулайзером только под руководством врача. Пациентов, использующих растворы небулайзера в домашних условиях, следует предупредить, что если обычное облегчение уменьшится или обычная продолжительность действия уменьшится, им следует проконсультироваться со своим врачом.
Пациентов, использующих растворы небулайзера в домашних условиях, следует предупредить, что если обычное облегчение уменьшится или обычная продолжительность действия уменьшится, им следует проконсультироваться со своим врачом.
Как и в случае с большинством лекарств, сначала проконсультируйтесь с врачом, если вы беременны или кормите грудью.
Не ожидается, чтосолевой раствор небулайзера вызовет какие-либо нежелательные эффекты при нормальном использовании.
Сообщение о предполагаемых побочных реакциях
Важно сообщать о предполагаемых побочных реакциях после получения разрешения на лекарственный препарат. Это позволяет непрерывно контролировать соотношение польза / риск лекарственного средства. Профессионалов здравоохранения просят сообщать о любых предполагаемых побочных реакциях через схему желтых карточек; сайт: www.mhra.gov.uk/yellowcard
При обильном пероральном приеме может потребоваться использование мочегонного средства для удаления избытка натрия.
Изотонический (0,9% мас. / Об.) Раствор хлорида натрия широко используется для разбавления.
Нет никаких выводов, относящихся к лицу, выписывающему рецепт, кроме тех, которые уже упомянуты в другом месте в SPC. Пожалуйста, обратитесь к восстанавливаемому продукту.
24 месяца
Ампулы, снятые с фольги, следует использовать в течение 90 дней.
Использовать сразу после первого открытия ампулы. Выбросьте все неиспользованное содержимое.
Не хранить при температуре выше 25 ° C.
Не охлаждать и не замораживать.
Единичная доза, формованная раздувом, герметично запаянная ампула из полиэтилена низкой плотности, содержащая 2,5 мл раствора. Полоски из десяти ампул завернуты в упаковку из алюминиевой фольги. Солевой раствор небулайзера доступен в коробках, содержащих 20, 60 или 100 ампул.
Accord Healthcare Limited
Дом мудрецов
319 Пиннер Роуд
Северная борона
Миддлсекс
HA1 4HF
Соединенное Королевство
Дата первого разрешения: 23 от Октябрь 2009 г.
Дата последнего обновления: 14 -е Сентябрь 2014 г.
Оценка статуса плацебо распыленного физиологического раствора у пациентов с острым вирусным бронхиолитом: систематический обзор и метаанализ | Неотложная медицина | JAMA Педиатрия
Ключевые моментыВопрос Связан ли распыленный физиологический раствор с физиологическими показателями респираторного статуса у пациентов с острым вирусным бронхиолитом?
Выводы Этот систематический обзор и метаанализ показали, что пациенты с бронхиолитом, получавшие небулайзерный физиологический раствор, показали значительное улучшение частоты дыхания и респираторных показателей после терапии, хотя сатурация кислорода оставалась неизменной.Кроме того, по сравнению с пациентами, получавшими другие плацебо, пациенты, получавшие небулайзерный физиологический раствор, показали большее улучшение респираторных показателей после лечения.
Значение Распыленный физиологический раствор не может быть инертным плацебо для пациентов с бронхиолитом и должен быть дополнительно изучен, чтобы установить клиническую значимость любого потенциального результата лечения.
Важность В терапевтических испытаниях острого вирусного бронхиолита постоянное клиническое улучшение в группах, получавших небулайзерный физиологический раствор (НС) в качестве плацебо, поднимает вопрос о том, действуют ли распыленные НС в качестве лечения, а не плацебо.
Объектив Измерить краткосрочную связь распыленных NS с физиологическими показателями респираторного статуса у детей с бронхиолитом путем анализа изменений этих показателей между использованием распыленных NS и использованием других плацебо, а также изменений до и после лечения небулайзерами NS.
Источники данных В течение марта 2019 г. проводился поиск в MEDLINE и Scopus, а также в библиографиях включенных исследований и соответствующих систематических обзорах для рандомизированных клинических испытаний, оценивающих небулайзерную терапию при бронхиолите.
Выбор исследования Были включены рандомизированные клинические испытания, сравнивающие детей 2 лет и младше с бронхиолитами, получавших небулайзерные НП. Исследования с участием группы лечения, получавшей альтернативное плацебо, были включены для сравнения NS с другими плацебо.
Исследования с участием группы лечения, получавшей альтернативное плацебо, были включены для сравнения NS с другими плацебо.
Извлечение и синтез данных Извлечение данных было выполнено в соответствии с рекомендациями PRISMA. Были использованы метааналитические модели с фиксированными и случайными эффектами, взвешенные по дисперсии.
Основные результаты и мероприятия Объединенные оценки связи с респираторными баллами, частотой дыхания и насыщением кислородом в течение 60 минут после лечения были получены для распыленных NS по сравнению с другим плацебо и для изменений до и после получения распыленных NS.
Результаты Всего было включено 29 исследований с участием 1583 пациентов. Стандартизованные средние различия респираторных баллов для распыленных NS по сравнению с другим плацебо (3 исследования) благоприятствовали небулайзированным NS на -0.9 баллов (95% ДИ, от -1,2 до -0,6 балла) через 60 минут после лечения ( P <0,001). Не было различий в частоте дыхания или насыщении кислородом при сравнении распыленных NS с другими плацебо. Стандартизированная средняя разница респираторных баллов (25 исследований) после распыления NS составила -0,7 (95% ДИ, от -0,7 до -0,6; I 2 = 62%). Средневзвешенная разница в респираторных показателях с использованием согласованной шкалы (13 исследований) после распыления NS составила -1,6 балла (95% ДИ, -1.От 9 до -1,3 балла; I 2 = 72%). Средневзвешенная разница в частоте дыхания (17 исследований) после распыления NS составила -5,5 вдохов в минуту (95% ДИ, от -6,3 до -4,6 вдохов в минуту; I 2 = 24%). Средневзвешенная разница в насыщении кислородом (23 исследования) после распыления NS составила -0,4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%).
Выводы и значимость Распыленные NS могут быть активным средством лечения острого вирусного бронхиолита.Следует провести дополнительную оценку, чтобы установить, действительно ли это плацебо.
Острый вирусный бронхиолит, одно из наиболее распространенных детских болезней, насколько нам известно, не имеет надежной, научно обоснованной небулайзерной терапии. 1 -8 В большинстве рандомизированных клинических испытаний распыленный физиологический раствор (NS) используется в качестве плацебо, что логично, учитывая, что NS также используется в качестве носителя для распыления активного лечения.Однако в исследованиях бронходилататоров было отмечено последовательное улучшение показателей, превышающих ожидаемые, у пациентов, получавших плацебо. 9 Нарастающий и убывающий характер бронхиолита может объяснить эти результаты, но, учитывая сильную тенденцию к улучшению, также возможно, что распыленные НП действуют как эффективное лечение.
Распыленный NS исторически использовался в качестве плацебо и при других состояниях, обычно в исследованиях, посвященных изучению бронхолитических препаратов и отхаркивающих средств для мокроты. 10 Существует небольшое количество доказательств того, что распыленные NS могут быть активным средством лечения взрослых с хронической обструктивной болезнью легких. В рандомизированном клиническом исследовании 40 пациентов с хронической обструктивной болезнью легких исследователи использовали метод «неэффективного» распыления, чтобы скрыть участников от назначения лечения, и продемонстрировали значительное улучшение показателей одышки в пользу NS, распыленных через эффективный распылитель, по сравнению с неэффективным распылителем. 10 Рандомизированные клинические испытания, сравнивающие распыленные NS с ингаляционным тербуталином и с ингаляционным фуросемидом среди пациентов с одышкой, также обнаружили аналогичное улучшение показателей одышки среди групп, получающих активное лечение, и тех, кто получал NS. 11 , 12 Однако в другом очень небольшом исследовании лабораторно-индуцированной одышки у 5 здоровых добровольцев, которое было специально разработано для снижения ожидания облегчения одышки, только 1 из 5 пациентов испытали облегчение, которое исследователи приписали эффекту плацебо. 12
Концепция эффекта плацебо недавно подверглась пересмотру и уточнению. Статья Бичера 1955 года 13 , в которой впервые была сформулирована идея примерно 30% -ного ответа на плацебо, была подвергнута критической переоценке, предполагая, что на полученные результаты повлияли естественные колебания изучаемых заболеваний. 14 , 15 Кроме того, 2 больших метаанализа рандомизированных клинических испытаний, сравнивающих плацебо с отсутствием лечения, не смогли выявить значительных эффектов плацебо во многих типах исследований.В частности, чем объективнее оценка результатов, тем меньше вероятность того, что будет обнаружен какой-либо измеримый эффект плацебо. 15 , 16 Меньше известно о влиянии плацебо на младенцев, у которых любое улучшение обязательно определяется внешней оценкой, а не самооценкой.
В этом контексте мы стремились проверить гипотезу о том, что распыленные NS могут быть активным лечением, а не плацебо для пациентов с острым вирусным бронхиолитом.Мы провели систематический обзор и метаанализ рандомизированных клинических исследований острого вирусного бронхиолита с использованием небулайзированных НП с 2 целями: сравнить небулайзированные НП с другими формами плацебо (например, ненабулизованное плацебо или фиктивное распыление) и оценить связь небулайзированных НП. с краткосрочными физиологическими измерениями респираторного статуса в рандомизированных клинических испытаниях, в которых он использовался в качестве плацебо.
Исследования рассматривались для включения, если они сообщали о результатах клинических испытаний пациентов в возрасте 2 лет и младше с первичным диагнозом острого вирусного бронхиолита, которые лечились небулайзерами NS.Для испытаний, сравнивающих небулайзерные NS с другим плацебо, дополнительно требовалось включение по крайней мере 1 группы лечения, получавшей только альтернативную форму плацебо. В этом обзоре учитывались только опубликованные исследования.
Источники информации и стратегия поиска
Это исследование было проведено в соответствии с Руководством по отчетности «Предпочтительные элементы отчетности для систематических обзоров и метаанализов» (PRISMA).Мы выполняли поиск в MEDLINE с 1946 по март 2019 года и в Scopus с 1976 по март 2019 года. Условия поиска показаны на электронном рисунке 1 в Приложении. Библиографии квалификационных исследований и соответствующие систематические обзоры также были просмотрены вручную на предмет дополнительных исследований кандидатов. Протокол обзора не был зарегистрирован до завершения исследования.
Исследования, выявленные на основе первоначальных результатов поиска, прошли проверку заголовков и аннотаций, проведенную двумя независимыми рецензентами (S.А.Х. и С.Л.Р.). Любые разногласия относительно включения разрешались консенсусом. Затем исследования исключались посредством полнотекстового обзора, если в них не предоставлялась информация о краткосрочных физиологических показателях респираторного статуса, которые определялись как совокупный респираторный балл, частота дыхания и / или значения сатурации кислорода в течение первого часа после лечения. Другими критериями исключения были включение детей старше 2 лет и получение другого небулайзерного лекарства в группу NS в течение 1 часа после включения в исследование.Для исследований с неполными данными и тех, которые были исключены из-за отсутствия отчетов о краткосрочных физиологических исходах, в которых протокол исследования предполагал, что эти данные были собраны, с соответствующими авторами связались по электронной почте, чтобы определить, доступны ли эти дополнительные данные. Исследования иностранных языков были переведены на английский язык.
Извлечение данных было выполнено независимо двумя исследователями (S.A.H. и S.L.R.) с использованием стандартизированной таблицы извлечения данных, проведена перекрестная проверка на предмет согласия и передана третьему исследователю (A.М.Г.) при любых разногласиях. Извлеченные элементы данных включали условия исследования и географическое положение, типы вмешательств, средний или средний возраст пациентов, критерии тяжести заболевания для включения в исследование, респираторные баллы, частоту дыхания и насыщение кислородом. Для всех показателей результатов собирались среднее значение и стандартное отклонение исходных значений и значений после лечения, когда они были доступны, и рассчитывались или условно рассчитывались на основе представленных данных, если они не доступны напрямую, с использованием методов, представленных в Кокрановском справочнике. 17 Предпочтительно использовались 60-минутные посттерапевтические меры; Когда 60-минутные измерения были недоступны, использовались 20-30-минутные меры постобработки.
Оценка качества и риск предвзятости
Пересмотренный Кокрановский инструмент риска систематической ошибки для рандомизированных клинических испытаний был использован для скрининга общего риска систематической ошибки в каждом включенном исследовании на уровне результатов, изученных в нашем метаанализе. Два исследователя (S.A.H. и S.L.R.) оценивали каждое исследование, используя этот инструмент; расхождения были отнесены к третьему автору исследования (А.M.G.) для разрешения.
Сводные показатели и синтез данных
Для исследований, оценивающих небулайзерные NS по сравнению с другим плацебо, рассчитывались средневзвешенные различия результатов между группами лечения. Для исследований, предоставляющих данные о лечении небулайзерами NS в динамике, рассчитывались средневзвешенные различия результатов в течение первых 60 минут исследования по сравнению с исходным уровнем исследования.Стандартизированные средние различия использовались при объединении респираторных баллов для всей когорты исследования, потому что для конкретных исследований используются разные шкалы; однако шкала была сохранена при анализе исследований подгрупп с использованием согласованной оценки. Точечные оценки и 95% доверительный интервал были рассчитаны с помощью взвешенных с обратной дисперсией моделей с фиксированными и случайными эффектами с использованием Комплексного метаанализа 2.0. Неоднородность оценивалась с использованием статистики I 2 .
Предварительно запланированные анализы подгрупп проводились на основании того, была ли исследуемая популяция амбулаторными или стационарными пациентами, и в исследованиях с использованием одного и того же инструмента респираторной оценки, когда этому критерию соответствовали более 5 исследований.Анализы чувствительности были выполнены путем последовательного удаления одного исследования, удаления выбросов, как определено из-за того, что ДИ отдельного исследования не перекрывает любой конец ДИ, созданных для точечных оценок, и путем удаления исследований с высоким риском систематической ошибки на основе пересмотренного Кокрановского риска инструмент смещения для рандомизированных исследований. 18
Всего в ходе первоначального поиска в базе данных было обнаружено 1084 цитаты.Обзор библиографии включенных исследований и соответствующих метаанализов привел к дополнительным 26 кандидатским исследованиям. После удаления дубликатов было проанализировано 874 исследования, 118 из которых потенциально соответствовали критериям включения после проверки заголовка и аннотации. Восемьдесят девять исследований были исключены при полнотекстовом обзоре. Наиболее частой причиной исключения исследования из полнотекстового обзора было то, что в исследовании не были представлены данные по интересующим исходам. Двадцать девять исследований соответствовали критериям включения, основанным на опубликованных результатах. 19 -47 Дополнительные данные были запрошены по электронной почте от 5 авторов, и 3 ответили неопубликованными данными по 4 включенным исследованиям. 26 , 27,46 , 47 Выбор исследования показан на электронном рисунке 1 в Приложении. Было выявлено три исследования, в которых участвовала группа, получавшая плацебо без ингаляции. 26 , 27,32
В таблице представлена подробная информация о включенных исследованиях.Эти 29 испытаний были проведены во многих странах и оценивали ряд активных методов лечения, включая распыленный адреналин, альбутерол, гипертонический раствор, тербуталин, ипратропиум и фуросемид. Пятнадцать исследований были проведены в условиях стационара, 20 , 22 , 23,25 , 28 -30,33 , 37 , 38,40 , 41,44 — 46 и 14 были проведены в амбулаторных условиях. 19 , 21 , 24 , 26 , 27,31 , 32,34 -36,39 , 42 , 43,47 Всего было 1477 пациентов которые получали небулайзированные NS и 106 пациентов, получавших плацебо без ингаляции.Индекс оценки респираторного дистресса (RDAI) 48 был наиболее часто используемой системой оценки в 14 исследованиях. 20 , 21,23 , 24,28 , 33 , 34,36 , 38 -40,44 , 46 , 47 Около половины испытаний указали минимальный уровень тяжести заболевания для включения в исследование. 21 , 25 , 29 , 30,32 -37,39 -41,43 , 45 , 47
Большинство исследований были отнесены к категории имеющих некоторую озабоченность по поводу систематической ошибки, хотя было обнаружено, что 8 исследований имеют высокий риск систематической ошибки 20 , 23 , 25 , 29 , 31 , 32,41 , 44 (см. Рисунок 2 в приложении).
Небулизированные NS по сравнению с другим плацебо
В трех исследованиях сравнивали небулайзированные NS с плацебо, в том числе 2 с пероральным плацебо и 1 с использованием тумана. 26 , 27,32 Стандартизованные средние различия в баллах для группы NS (n = 102) по сравнению с другой группой плацебо (n = 106) благоприятствовали NS на -0.9 баллов (95% ДИ, от -1,2 до -0,6 балла) через 60 минут после терапии ( P < 0,001). Протоколы исследований в двух исследованиях, сравнивающих NS с пероральным плацебо, были идентичны, потому что они были выполнены одной и той же командой исследователей в 2 разных странах; Таким образом, мы проанализировали эти данные с сохранением респираторной шкалы. 26 , 27 Средневзвешенные различия в баллах для группы NS (n = 50) и группы перорального плацебо (n = 54) благоприятствовали NS на -1,6 балла (95% ДИ, -0.От 8 до -0,03 балла) по респираторной шкале для конкретного исследования (шкала от 0 до 20) через 60 минут после терапии ( P = 0,04). Не было различий в частоте дыхания или насыщении кислородом между группой, получавшей распыленный NS, и группой, получавшей другие плацебо.
Ассоциация небулайзированных НП с респираторными оценками
Всего в 25 исследованиях сообщалось о совокупных респираторных показателях с течением времени для пациентов, получавших небулайзерные NS. 20 , 21,24 -29,31 -47 Стандартизированная средняя разница в баллах в течение 60 минут после распыления NS уменьшилась на -0,7 (95% ДИ, от -0,7 до -0,6; I 2 = 62%; P <0,001) (Рисунок 1). Моделирование случайных эффектов и анализ подгрупп по условиям исследования существенно не изменили точечные оценки; однако гетерогенность оказалась связана с несогласованностью в подгруппе стационарных пациентов (амбулаторный I 2 = 4%; стационарный I 2 = 79%).
Ассоциация небулайзированных НП с оценкой RDAI
RDAI (шкала, 0–17 баллов) была единственной оценкой, использованной в достаточном количестве исследований для выполнения анализа подгруппы с сохранением шкалы. Всего в 13 исследованиях представлены данные RDAI 20 , 21,24 , 28 , 33 , 34,36 , 38 -40,44 , 46 , 47 ; В 1 исследовании использовалась эта система баллов, но исходные баллы не могли быть установлены, и поэтому баллы в этом исследовании не анализировались. 23 Средневзвешенная разница в баллах в течение 60 минут после распыления NS уменьшилась на -1,6 балла (95% ДИ, -1,9 до -1,3 балла; I 2 = 72%; P <0,001) ( Фигура 2). Анализ подгрупп продемонстрировал снижение на -2,0 балла (95% ДИ, от -2,3 до -1,6 балла) в амбулаторной подгруппе по сравнению с уменьшением на -0,9 балла (95% ДИ, от -1,4 до -0,4 балла) в подгруппе стационарных пациентов. Моделирование случайных эффектов существенно не изменило точечные оценки, в то время как неоднородность, по-видимому, была связана с несогласованностью в подгруппе стационарных пациентов (амбулаторный I 2 = 42%; стационарный I 2 = 72%).
Связь небулайзированных НП с частотой дыхания
В 17 исследованиях, предоставляющих данные о частоте дыхания, 19 -21,23 , 24,26 -28,30 , 33 -35,38 -40,43 , 47 , средневзвешенная разница в течение 60 минут после распыления NS уменьшилась на -5.5 вдохов в минуту (95% ДИ, от -6,3 до -4,6 вдохов в минуту; I 2 = 24%; P <0,001) (Рисунок 3). Моделирование фиксированных эффектов и случайных эффектов и анализ подгрупп по условиям исследования существенно не изменили точечные оценки, и неоднородность в общем анализе была низкой.
Связь небулайзированных НП с насыщением кислородом
В 23 исследованиях, предоставляющих данные о насыщении кислородом, 19 -28,30 , 32 -40,42 , 43,47 средневзвешенная разница в течение 60 минут после распыления NS уменьшилась на -0. .4% (95% ДИ, от -0,6% до -0,2%; I 2 = 79%; P <0,001) (Рисунок 4). Моделирование случайных эффектов существенно изменило общую точечную оценку в сторону незначительности (средняя разница, -0,3%; P = 0,10). Анализ подгрупп также дал незначительную точечную оценку в амбулаторной подгруппе (средняя разница 0,3%; P = 0,38). Кроме того, гетерогенность была высокой в подгруппе амбулаторных пациентов ( I 2 = 83%) по сравнению с подгруппой стационарных пациентов ( I 2 = 49%).
Анализ чувствительности с удалением одного исследования не повлиял на общие точечные оценки ни для одного из анализов. Для RDAI анализ чувствительности, удаляющий выбросы 46 , снизил неоднородность до приемлемых уровней ( I 2 = 42%) при получении аналогичной точечной оценки (средняя разница, -1,9; 95% ДИ, от -2,2 до -1,6) . Что касается частоты дыхания, анализ чувствительности, удаляющий выбросы 19 , существенно не изменил результатов.Для насыщения кислородом анализ чувствительности с удалением выбросов 23 , 32 , 35 , 47 дал общую точечную оценку -0,2%, что не было статистически значимым ( P = 0,10) с приемлемой неоднородностью. ( I 2 = 24%).
Анализ чувствительности, исключающий исследования с высоким риском систематической ошибки в анализе респираторных баллов 20 , 25 , 29 , 31 , 32,41 , 44 существенно не изменил точечную оценку, хотя пониженная неоднородность ( I 2 = 47%).Удаление исследований с высоким риском систематической ошибки в анализе RDAI 20 , 44 существенно не изменило точечную оценку или меры неоднородности. Удаление исследований с высоким риском систематической ошибки из анализа частоты дыхания 20 , 23 существенно не изменило точечную оценку или меры неоднородности. Удаление исследований с высоким риском систематической ошибки из анализа насыщения кислородом 20 , 23 , 25 , 32 существенно не изменило точечные оценки, хотя и привело к небольшому снижению неоднородности ( I 2 = 60%).
В этом систематическом обзоре рандомизированных клинических испытаний с использованием распыленных НП в качестве плацебо мы обнаружили прямые и косвенные доказательства того, что НП может быть активным лечением, а не плацебо. Прямые доказательства получены из 3 исследований с участием более 200 пациентов, в которых распыленные NS оценивались по сравнению с другими плацебо и значительно улучшили респираторные показатели. Косвенные доказательства получены из значительно улучшенных оценок респираторных показателей и частоты дыхания до и после распыления NS в нескольких рандомизированных клинических испытаниях.Хотя качество этих доказательств невысокое из-за небольшого количества исследований в первом анализе и отсутствия группы сравнения во втором, оно согласуется с широким спектром исследований и согласуется. Наконец, в метаанализе была отмечена двусмысленная связь с насыщением кислородом с высокой неоднородностью в широкой выборке; Анализ подгрупп и анализ чувствительности, разрешающий эту неоднородность, позволяют предположить, что распыленные NS не связаны с насыщением кислородом.
Есть несколько возможных объяснений наших выводов. Возможно, что распыленный NS действительно не плацебо; то есть он оказывает небольшое положительное влияние на маленьких детей с острым вирусным бронхиолитом за счет улучшения гидратации поверхностей дыхательных путей и слизистого просвета, а также снижения сопротивления верхних дыхательных путей. Также возможно, что клиническое течение бронхиолита усиливается и ослабевает независимо от оценки небулайзированных НП или других методов лечения. Пациентам могут быть назначены жаропонижающие средства или назальное отсасывание, или они могут просто успокоиться после начальной фазы оценки, таким образом улучшившись.В нескольких исследованиях было отмечено, что частота дыхания и оценка дыхания коррелируют с состоянием пациента (например, бодрствование, сон или плач). 25 -27,33 Невозможно изолировать относительный эффект дополнительных симптоматических методов лечения или состояния пациента по сравнению с небулайзированным NS на исходы, оцениваемые в этом наборе данных. Третья возможность состоит в том, что основной метод оценки (респираторный балл) — это необъективный инструмент, который подвержен психологическим воздействиям на оценщика, и что эти повторяющиеся измерения имеют тенденцию регрессировать к среднему значению.Современное понимание эффекта плацебо стало более тонким, и кажется, что любой потенциально субъективный инструмент измерения симптомов (например, шкалы боли или депрессии) с большей вероятностью продемонстрирует эффект плацебо, чем объективные результаты. 15 Этот феномен также может быть связан с результатами, полученными с помощью инструментов респираторной оценки в нашем исследовании.
Мы не можем сделать однозначных выводов относительно лечения на основании наших результатов из-за большого количества описанных возможных объяснений и врожденной систематической ошибки, связанной с оценкой до и после лечения.Наши данные не должны влиять на существующее мнение о том, что активные методы лечения острого вирусного бронхиолита не изменяют течение болезни. Хотя наличие лечебного эффекта от лекарственного средства, назначенного в качестве вспомогательного средства обеим группам лечения в рандомизированном клиническом исследовании (в качестве плацебо-терапии или средства активной терапии), может усложнить анализ мощности исследования, нет никаких веских оснований полагать что это может повлиять на лечебный эффект от других активных лекарств.Как минимум, наши данные должны подчеркивать необходимость будущих рандомизированных клинических испытаний этого заболевания, чтобы учесть тот факт, что краткосрочные физиологические показатели будут иметь тенденцию к улучшению. Таким образом, анализ мощности должен будет учитывать снижение чувствительности к изменениям этих показателей.
Этот метаанализ имеет некоторые ограничения, в том числе неоднородность включенных испытаний с различными максимальными возрастами, популяциями и критериями тяжести заболевания для включения в исследование.Неоднородность исследования была чрезмерной для некоторых из наших совокупных анализов, хотя нам удалось разрешить ее до приемлемого уровня с помощью анализа подгрупп и чувствительности без изменения общих выводов. Весьма вероятно, что тяжесть заболевания будет иметь значительную связь с результатами нашего исследования, потому что пациенты с легкой формой заболевания могут иметь небольшой запас для улучшения, учитывая их относительно нормальные жизненные показатели и низкие показатели дистресса на исходном уровне. Кроме того, неясна клиническая значимость краткосрочных физиологических результатов, которые мы предлагаем от лечения небулайзерами NS.Хотя снижение респираторной оценки и частоты дыхания может сигнализировать о краткосрочном клиническом улучшении, мы не оценивали другие соответствующие клинические исходы, более отражающие общее течение и тяжесть заболевания, такие как частота госпитализаций или продолжительность пребывания в больнице. Наконец, мы не приложили усилий для включения неопубликованных рефератов; таким образом, возможно, что недостающие данные могут изменить наши выводы, хотя такая возможность маловероятна с учетом количества пациентов и включенных исследований.
Этот метаанализ предполагает, что распыленные NS могут быть активным средством лечения острого вирусного бронхиолита, а не инертным плацебо.Следует провести дополнительную оценку распыленных НП по сравнению с имитацией распыления и / или пероральным плацебо, чтобы установить, является ли распыленный НП истинным плацебо. Планы будущих исследований должны учитывать потенциальный лечебный эффект распыленных НП на краткосрочные исходы.
Принято к публикации: 9 сентября 2019 г.
Автор для корреспонденции: Шон Л. Ральстон, доктор медицинских наук, кафедра педиатрии, Медицинская школа Джонса Хопкинса, 1800 Орлеан Авеню, Блумберг 8470, Балтимор, Мэриленд 21287 (sralsto3 @jhmi.эду).
Опубликован онлайн: 6 января 2020 г. doi: 10.1001 / jamapediatrics.2019.5195
Вклад авторов: Доктор Хаус и Ральстон имели полный доступ ко всем данным в исследовании и несут ответственность за целостность данных и точность анализа данных.
Концепция и дизайн: Все авторы.
Сбор, анализ или интерпретация данных: Все авторы.
Составление рукописи: Все авторы.
Критический пересмотр рукописи на предмет важного интеллектуального содержания: Все авторы.
Статистический анализ: Все авторы.
Административная, техническая или материальная поддержка: House, Gadomski.
Раскрытие информации о конфликте интересов: Не сообщалось.
Дополнительные материалы: Пейдж Н. Скаддер, MLIS, биомедицинские библиотеки, Дартмутский колледж, оказала помощь в первоначальном поиске литературы.За свой вклад она не получила компенсации.
1.Хартлинг L, Бялы Л. М., Вандермейер B, и другие. Адреналин при бронхиолите. Кокрановская база данных Syst Rev . 2011; (6): CD003123.PubMedGoogle Scholar4.Gadomski AM, Скрибани МБ. Бронходилататоры при бронхиолите. Кокрановская база данных Syst Rev . 2014; (6): CD001266.PubMedGoogle Scholar8.Harrison. W, Ангулвант F, дом S, Гайдос V, Ралстон SL.Гипертонический раствор при бронхиолите и ошибка I типа: пробный последовательный анализ. Педиатрия . 2018; 142 (3): e20181144. DOI: 10.1542 / peds.2018-1144PubMedGoogle Scholar17.Higgins JPT, Green S, eds. Справочник по систематическим обзорам вмешательств . Версия 5.1.0. Кокрановское сотрудничество .. http://handbook-5-1.cochrane.org/. Обновлено в марте 2011 г. Проверено 7 июля 2018 г. 188. Хиггинс JPT, Стерн JAC, Савович J, и другие. Пересмотренный инструмент для оценки риска систематической ошибки в рандомизированных исследованиях. Кокрановская база данных Syst Rev . 2016; 10 (приложение 1): 29-31.Google Scholar20.Lines DR, Каттампаллил JS, Листон P. Эффективность распыления сальбутамола при бронхиолите. Pediatric Rev Commun. 1990; 5: 121-129.Google Scholar 23.Lines ДР, Бейтс М.Л., Рехтман АР, Саммартино LP. Эффективность распыления бромида ипратропия при остром бронхиолите. Педиатрическая Революция . 1992; 6: 161-167.Google Scholar, 25, Кристьянссон. С, Лёдруп Карлсен KC, Веннергрен G, Страннегард Иллинойс, Карлсен KH.Распыленный рацемический адреналин в лечении острого бронхиолита у младенцев и детей ясельного возраста. Арка Дис Детский . 1993; 69 (6): 650-654. DOI: 10.1136 / adc.69.6.650PubMedGoogle ScholarCrossref 27.Gadomski AM, Лихенштейн Р., Хортон L, король Джей, Кин V, Пермутт Т. Эффективность альбутерола при лечении бронхиолита. Педиатрия . 1994; 93 (6, pt 1): 907-912.PubMedGoogle Scholar35.Khashabi J, Салари S, Карамияр М, Муссави ЧАС.Сравнение эффективности распыленного l-адреналина, сальбутамола и физиологического раствора при остром бронхиолите: рандомизированное клиническое испытание. Med J Islam Repub Iran . 2005; 19 (2): 119-125.Google Scholar, 36. Ralston. S, Хартенбергер C, Анайя Т, Куоллс C, Келли HW. Рандомизированное плацебо-контролируемое исследование альбутерола и адреналина в равных дозах бета-2-агонистов при остром бронхиолите. Пульмонол Педиатр . 2005; 40 (4): 292-299. DOI: 10.1002 / ppul.20260PubMedGoogle ScholarCrossref 37.Karadag B, Ceran О, Гювен ГРАММ, и другие. Эффективность сальбутамола и ипратропия бромида в лечении острого бронхиолита — клинические испытания. Дыхание . 2008; 76 (3): 283-287. DOI: 10.1159 / 000111817PubMedGoogle ScholarCrossref 38.Bar А, Сруго Я, Амирав Я, Цверлинг C, Нафтали Г, Кугельман A. Ингаляционный фуросемид у госпитализированных младенцев с вирусным бронхиолитом: рандомизированное двойное слепое плацебо-контролируемое пилотное исследование. Пульмонол Педиатр . 2008; 43 (3): 261-267. DOI: 10.1002 / ppul.20765PubMedGoogle ScholarCrossref 40.Tinsa F, Бен Рума А, Гаффари ЧАС, и другие. Рандомизированное контролируемое исследование распыленного тербуталина при первом остром бронхиолите у детей младше 12 месяцев. Тунис Мед . 2009; 87 (3): 200-203.PubMedGoogle Scholar42.Anil AB, Анил М, Саглам AB, Цетин Н, Бал А, Аксу N. Большой объем физиологического раствора такой же эффективен, как распыленный сальбутамол-физиологический раствор, адреналин-физиологический раствор и 3% -ный физиологический раствор при легком бронхиолите. Пульмонол Педиатр . 2010; 45 (1): 41-47. DOI: 10.1002 / ppul.21108PubMedGoogle ScholarCrossref 43.Ipek И.О., Ялчин ЕС, Сезер РГ, Бозайкут A. Эффективность распыления сальбутамола, гипертонического раствора и комбинации сальбутамол / гипертонический раствор при умеренном бронхиолите. Пульм Фармакол Тер . 2011; 24 (6): 633-637. DOI: 10.1016 / j.pupt.2011.09.004PubMedGoogle ScholarCrossref 44.Scarlett EE, Уокер S, Ровителли А, Рен CL.Ответы приливного дыхания на альбутерол и физиологический раствор у младенцев с вирусным бронхиолитом. Pediatr Allergy Immunol Pulmonol . 2012; 25 (4): 220-224. DOI: 10.1089 / ped.2012.0141Google ScholarCrossref 45.Tinsa Ф, Абделькафи С, Бель Хадж Я, и другие. Рандомизированное контролируемое исследование распыленного 5% гипертонического раствора и смешанного 5% гипертонического раствора с адреналином при бронхиолите. Тунис Мед . 2014; 92 (11): 674-677.PubMedGoogle Scholar47.Angoulvant F, Bellêttre X, Милсент K, и другие; Эффективность 3% гипертонического раствора в группе исследования острого вирусного бронхиолита (ГЕРАНДИЯ).Влияние небулайзерного гипертонического солевого раствора в отделениях неотложной помощи на частоту госпитализаций по поводу острого бронхиолита: рандомизированное клиническое исследование. Педиатр JAMA . 2017; 171 (8): e171333. DOI: 10.1001 / jamapediatrics.2017.1333PubMedGoogle Scholar48.Lowell DI, Lister G, фон Косс H, Маккарти П. Свистящее дыхание у младенцев: ответ на адреналин. Педиатрия . 1987; 79 (6): 939-945.PubMedGoogle ScholarОтвет дыхательных путей на вдыхаемый гипертонический раствор у пациентов с умеренной и тяжелой хронической обструктивной болезнью легких
Ключевые слова: гиперреактивность бронхов; обструкция дыхательных путей; гиперинфляция легких; одышка; бронхиальный вызов
Вдыхание гипертонического солевого раствора широко используется у пациентов с астмой в качестве метода бронхиального заражения (1).Это также часть процедуры получения мокроты, которая вызывает большой интерес у пациентов с заболеваниями дыхательных путей, в том числе с хронической обструктивной болезнью легких (ХОБЛ). Хотя предварительная ингаляция β 2 -агониста является обязательной при выделении мокроты, у пациентов может наблюдаться ухудшение функции легких после ингаляции физиологического раствора (2-4).
Однако надлежащая оценка функциональных реакций легких у пациентов с тяжелой ХОБЛ затруднена из-за сложностей механики легких, характеризующих заболевание, включающих уменьшение прикрепления альвеол (5) и изменения морфологии и функции дыхательных путей (6).До сих пор реакции на гипертонический раствор изучались только с помощью маневров форсированного выдоха, тогда как роль гиперинфляции легких по сравнению с обструкцией дыхательных путей, чувствительность различных индексов при обнаружении ответов и их связь с одышкой в настоящее время неизвестны. Это особенно верно ввиду доказательств того, что параметры вдоха могут превосходить параметры выдоха при исследовании тонуса дыхательных путей и одышки при ХОБЛ (7, 8).
Анализ реакции на гипертонический раствор также может иметь значение для оценки неспецифической гиперчувствительности дыхательных путей, которая присутствует у двух третей пациентов с ХОБЛ (9) и считается предиктором снижения функции легких с течением времени ( 10).Вдыхание физиологического раствора во время отхождения мокроты считается приемлемым при умеренной или тяжелой обструкции дыхательных путей (2), в отличие от проблем с метахолином или гистамином (11). Кроме того, такие косвенные проблемы могут представлять больший интерес в отношении стимулов, встречающихся в среде пациентов, чем фармакологические агонисты.
Помимо полезности в качестве проблемы, ингаляция солевого раствора имеет то преимущество, что индуцированная мокрота может дать ключ к разгадке задействованных механизмов.Это представляет особый интерес с учетом того факта, что β 2 -агонистов неспособны полностью предотвратить неблагоприятный ответ. Полученная информация также может иметь значение для будущих улучшений в отношении безопасности отведения мокроты.
Поэтому мы проанализировали реакцию дыхательных путей на вдыхание гипертонического и изотонического физиологического раствора у пациентов с умеренной и тяжелой ХОБЛ путем мониторинга различных показателей функции легких, включая форсированные маневры вдоха и выдоха.Мы дополнительно сравнили состав мокроты между испытаниями, чтобы получить информацию о механизмах, опосредующих ответ.
МЕТОДЫ
Раздел:
ВыбратьВверх страницыАннотация МЕТОДЫ << РЕЗУЛЬТАТЫ ОБСУЖДЕНИЕ Ссылки ЦИТИРУЮЩИЕ СТАТЬИПациенты
Были изучены 20 пациентов со стабильной ХОБЛ в соответствии с рекомендациями ATS (12) и FEV 1 ≤ 60% ранее. Протокол был одобрен местным этическим комитетом, и все пациенты дали свое письменное информированное согласие.
| Пол, ж / м | 5/15 | |||||||
| Высота, см | 173 ± 6 | |||||||
| ИМТ, кг · м −2 | 25,0 ± 3,3 | |||||||
| Курильщик, бывший / текущий | 15/5 | Пакет | ||||||
| 57 ± 17 | ||||||||
| IVC, L | 3.32 ± 0,73 | |||||||
| ОФВ 1 , L | 1,28 ± 0,33 | |||||||
| ОФВ 1 ,% перед | 42 ± 9,5 | |||||||
| 903 903 L | ||||||||
| 903 1 ± 0,84 | ||||||||
| PEF, л с −1 | 4,01 ± 1,34 | |||||||
| PIF, л с −1 | 5,1 ± 1,79 | |||||||
| H см см SRaw 2 О · с | 37.12 ± 19,21 | |||||||
| SRaw дюйм , см H 2 O · s | 20,46 ± 8,62 | |||||||
| TLC, L | 7,27 ± 1,09 | |||||||
| 77 | ||||||||
| 77 | 77 ± 0,79 | |||||||
| ITGV,% до | 150 ± 15,9 | |||||||
| RV, L | 4,04 ± 0,71 | |||||||
| IC, L | 2,20 ± 0,55 | 2,20 ± 0,55 | , ммоль (мин · кПа) −1 | 4.75 ± 1,49 | ||||
| Tl co ,% пред | 52,7 ± 14,7 | |||||||
| P 0,1 , кПа | 0,328 ± 0,128 | |||||||
| Pi макс. ± 2,52 |
Протокол исследования
Исследование состояло из одного дня скрининга и двух дней исследования, разделенных на ≥ 72 часа и ≤ 10 дней. Ингаляционные бронходилататоры короткого (длительного) действия были отменены в течение ≥ 6 (12) часов, тогда как другие препараты не были изменены.В день скрининга история болезни и клиническое состояние, общий иммуноглобулин E (IgE), функция легких, фактор переноса монооксида углерода (Tl co ), давление на вдохе через 0,1 с (P 0,1 ) и максимальное давление на вдохе (Pi макс ).
В дни исследования пациенты проходили тестирование функции легких, вдыхали 200 мкг сальбутамола через ингалятор с отмеренной дозой (MDI) и измеряли снова через 15 минут. Изменение одышки по визуальной аналоговой шкале (ВАШ) (13) оценивали непосредственно перед тестированием функции легких.Затем пациенты вдыхали рандомизированным двойным слепым методом либо изотонический (0,9%), либо гипертонический (3%) физиологический раствор из ультразвукового распылителя (NE-U12; Omron, Токио, Япония; производительность 1,7 мл / мин [14]) для до 4 × 5 мин. Функцию легких и ВАШ измеряли после каждого из 5-минутных периодов ингаляции. Когда ОФВ –1 упал на ≥ 20% от постбронходилатирующего значения, индукцию прекращали. Если это произошло после первого периода, мокрота собиралась после этого периода, в противном случае — после второго периода.Через пятнадцать минут после последней ингаляции снова оценивали ВАШ и функцию легких.
Жизненная емкость легких на вдохе (IVC), на выдохе (SRaw ex ) и на вдохе (SRaw в ), удельное сопротивление дыхательных путей, общая емкость легких (TLC), внутригрудной объем газа (ITGV), остаточный объем (RV) и вдох Емкость (IC) измеряли на боди-плетизмографе (Masterlab; Jaeger, Würzburg, Германия) (15, 16). Затем определяли ОФВ 1 , ФЖЕЛ, пиковую скорость выдоха и пиковую скорость вдоха (PEF, PIF) и FIV 1 по кривым максимального объема выдоха и вдоха (8).Рейтинги по ВАШ использовались для оценки изменений одышки (13, 17) в диапазоне от –100% («намного хуже») до + 100% («гораздо лучше»).
Мокроту обрабатывали сразу после индукции путем отбора пробок (3, 14), и подсчет клеток из кодированных препаратов цитоспина, окрашенных по Гимзе, выражали в процентах от не плоских клеток. Концентрации IL-8 (CLB, Амстердам, Нидерланды), гистамина (IBL, Гамбург, Германия), а также MMP-9 и TIMP-1 (Amersham Pharmacia, Фрайбург, Германия) в супернатантах измеряли с помощью ELISA.Уровни триптазы определялись FEIA (Pharmacia & Upjohn, Фрайбург, Германия) после 4-кратного концентрирования образцов. Концентрацию лейкотриенов C / D / E 4 оценивали с помощью ELISA (Biotrak, Amersham Pharmacia) после экстракции (18) и дополнительного добавления 0, 5 и 10 пг.
Статистический анализ
Вычисляли средние значения и стандартные отклонения (SD) (таблица 1) или стандартные ошибки среднего (SEM) (в противном случае). Значения, измеренные до и в конце ингаляционного заражения, сравнивали друг с другом с использованием парного теста t .Аналогичным образом сравнивались абсолютные и процентные изменения между двумя днями исследования. Корреляционный анализ проводился с использованием ANCOVA и коэффициентов линейной корреляции. Значимость была принята для p <0,05.
РЕЗУЛЬТАТЫ
Раздел:
ВыбратьВверх страницыАннотацияМЕТОДЫ РЕЗУЛЬТАТЫ << ОБСУЖДЕНИЕ Ссылки ЦИТИРУЮЩИЕСЯ СТАТЬИИз 20 исследованных пациентов 9 показали значения ОФВ 1 ≤ 50% до и 7 из ≤ 35% (Таблица 1). Все пациенты получали ингаляционные β 2 -агонисты и холинолитики; 9 из них дополнительно получали теофиллин и 11 — ингаляционные кортикостероиды.
Функция легких
Исходная функция легких существенно не различалась между двумя днями исследования. Вдыхание сальбутамола привело к увеличению IVC, FVC, FEV 1 , FIV 1 , IC, PIF и PEF, тогда как RV, SRaw ex и SRaw в снизились (p <0,001, каждый; Таблица 2). В TLC и ITGV значительных изменений не произошло. Ни абсолютные значения, ни абсолютные, ни процентные изменения, вызванные сальбутамолом, не различались между двумя днями.То же самое справедливо и для баллов по ВАШ, которые были отличны от нуля в оба дня (p <0,01, каждый).
| Сальбутамол | 0,9% солевой раствор † † | |||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Время вдоха, мин | — | 16.5 ± 1,3 | — | 8,8 ± 0,8 § | ||||||||||||||
| ΔFEV 1 , мл | 138 ± 20 | −202 ± 37 | −2016 ± 283 ± 38 ‖ | |||||||||||||||
| ΔFIV 1 , мл | 291 ± 45 | −606 ± 79 | 338 ± 56 | −1001 ± 60 | −1001 ± 60 мл | 313 ± 43 | −653 ± 77 | 341 ± 53 | −1076 ± 63 ‖ | |||||||||
| ΔPEF, мл с −1 | −362 ± 136 | 564 ± 87 | −993 ± 192 ‖ | |||||||||||||||
| ΔPIF, мл с −1 | 309 ± 106 | −7672 | −1 ± 186 | −883 ± 197 ‡ | ||||||||||||||
| ΔSRaw дюйм , см H 2 O · s | −6.3 ± 1,2 | 10,7 ± 1,7 | -6,4 ± 1,4 | 17,7 ± 1,7 § | ||||||||||||||
| ΔSRaw ex , см H 2 O · s | 22,9 ± 3,2 | −14,1 ± 3,1 | 38,2 ± 4,1 § | |||||||||||||||
| ΔTLC, мл | −17 ± 68 | −4 ± 79 | −80 ± 119 | |||||||||||||||
| ΔITGV, мл | −125 ± 67 | 400 ± 107 | −117 ± 81 | 623 ± 107 ‡ | −313 ± 86 | 662 ± 106 | −263 ± 100 | 959 ± 133 ‡ | ||||||||||
| ΔIC, мл | 109 ± 49 | 80740 | −40 184 ± 62 | −703 ± 77 ‡ 9 0741 | ||||||||||||||
| VAS, оценка | 19.6 ± 4 | −27,5 ± 4,7 | 19,4 ± 3,3 | −46,2 ± 3,8 ‖ |
Влияние ингаляционного физиологического раствора на FEV 1 и FIV 1 показано на рисунке 1. Во время ингаляции 0,9% физиологического раствора было остановлено 9 заражений из-за падения ОФВ на ≥20% 1 . FIV 1 снизился более чем на 20% у 10 пациентов. Среднее время ингаляции составило 16,5 мин (11,3 мин для тех, кто был остановлен). По сравнению с показателями постбронходилататора наблюдалось снижение VC, FVC, FEV 1 , FIV 1 , PEF, PIF и IC (p <0.05, каждый) и увеличение ITGV, RV, SRaw в и SRaw ex (p <0,01, каждое; Таблица 2). В среднем FEV 1 снизился на 202 мл после прекращения заражения, и это значение было меньше (p <0,001), чем соответствующее уменьшение FIV 1 на 606 мл.
Во время ингаляции 3% физиологического раствора всем пациентам, кроме двух, приходилось устранять проблемы из-за падения ОФВ более чем на 20%. 1 . Эти пациенты не могли продолжить заражение через 10 минут из-за сильной одышки, хотя их снижение ОФВ 1 было <20%.У всех пациентов FIV 1 снизился на 20%. Среднее время ингаляции составило 8,8 мин. VC, FVC, FEV 1 , FIV 1 , PEF, PIF и IC снизились, а ITGV, RV, SRaw в и SRaw ex увеличились во время ингаляции (p <0,01 для каждого; Таблица 2). В конце заражения FEV 1 упал на 363 мл, что было меньше (p = 0,006), чем соответствующее изменение FIV 1 на 1005 мл (таблица 2). Кроме того, средний балл по ВАШ был ниже нуля (p = 0.01).
Изменения FEV 1 , FIV 1 , PEF (p <0,001, каждый), PIF, IC, ITGV, RV (p <0,05, каждый) и SRaw в и SRaw ex (p <0,01, оба) были больше после ингаляции 3% по сравнению с 0,9% физиологическим раствором. Кроме того, баллы по ВАШ (p <0,001) и время ингаляции (p <0,01) были ниже после 3% физиологического раствора.
Чтобы оценить, вызывает ли установка, используемая для ингаляции через мундштук, саму реакцию дыхательных путей, подгруппа из 6 пациентов (6 м; FEV 1 , 39 ± 4% пред.) Дополнительно выполнила имитацию ингаляции в течение 20 мин. небулайзер наполнился, но выключился.Функция легких и ВАШ не изменились, среднее (± SEM) ОФВ 1 составляло 1,43 ± 0,21 л до и 1,44 ± 0,22 л после теста, FIV 1 составляло 3,48 ± 0,40 и 3,40 ± 0,37 л, а ВАШ -1,83. ± 1,83.
Корреляция между изменениями функции легких и одышкой
Ингаляция сальбутамола привела к значительной корреляции между ВАШ и абсолютными изменениями FIV 1 (r = 0,64, p = 0,021; см. Рисунок 2B), в то время как не было корреляция между ВАШ и изменениями ОФВ 1 (r = 0.19; Рисунок 2A) или IC (r = 0,18; Рисунок 2C). Эти анализы были выполнены ANCOVA с использованием данных за оба дня исследования. Напротив, при объединении данных, полученных после ингаляции 0,9 и 3% физиологического раствора с помощью ANCOVA, корреляции с ВАШ составили r = 0,62 для FEV 1 (p <0,0001; рисунок 2D), r = 0,73 для FIV 1 (p < 0,0001; рисунок 2E) и r = 0,67 для IC (p <0,0001; рисунок 2F). Соответствующие корреляции между процентными изменениями и ВАШ составили r = 0,70 (p <0.0001), r = 0,78 (p <0,0001) и r = 0,69 (p <0,0001). Аналогичные данные, что и для IC, были получены для ITGV.
Индуцированная мокрота
Не было обнаружено значительных различий в общем количестве клеток и процентном содержании макрофагов, нейтрофилов, эозинофилов и лимфоцитов при сравнении 0,9% физиологического раствора и 3% физиологического раствора (Таблица 3). Кроме того, не было значительных различий в отношении концентраций растворимой фазы IL-8, MMP-9, TIMP-1, отношения MMP-9 / TIMP-1 и лейкотриенов C / D / E 4 .Однако концентрации гистамина были повышены после ингаляции на 3% по сравнению с ингаляцией 0,9% физиологического раствора (p = 0,007, критерий согласованных пар Уилкоксона). Триптаза была обнаружена у 6 пациентов после хотя бы одной из двух ингаляций; у 5 из 6 пациентов его концентрация была выше через 3% по сравнению с 0,9% физиологическим раствором (p = 0,09, точный критерий Фишера, односторонний). Кроме того, не было значимой корреляции между уровнями растворимых медиаторов и исходной функцией легких или ее изменениями.
| 0,9% физраствор | 3% физиологический раствор | ||||||
|---|---|---|---|---|---|---|---|
| Общее количество клеток 41157 907/6 ÷ 1,23 | 4,88 ÷ 1,21 | ||||||
| Макрофаги,% | 26,8 ± 3,2 | 26,5 ± 2,7 | |||||
| Нейтрофилы,% | 69,1 ± 3,3 | 2 ± 3,1 | |||||
| Эозинофилы,% | 1,09 ÷ 1,36 | 1,25 ÷ 1,35 | |||||
| Лимфоциты,% | 0,71 ± 0,11 | 0,98 ± 0,1 на мл | 2700 ÷ 1,23 | 2379 ÷ 1.18 | |||
| MMP-9 / TIMP-1 | 0,13 ÷ 1,30 | 0,11 ÷ 1,38 | |||||
| Гистамин, нг / мл | 29,8 ÷ 1,23 | 38,9 † | |||||
| Лейкотриены C / D / E 4 , нг / мл | 1,95 ÷ 1,19 | 2,09 ÷ 1,16 |
ОБСУЖДЕНИЕ
Раздел:
Публикация статьи мы наблюдали значительное снижение функции легких при вдыхании физиологического раствора у пациентов с ХОБЛ.Ответы были сильнее после 3% по сравнению с 0,9% физиологическим раствором и включали усиление обструкции дыхательных путей, а также гиперинфляцию легких. Изменения FIV 1 были больше, чем изменения FEV 1 . Кроме того, ответ на гипертонический раствор, по-видимому, связан с активацией тучных клеток при ХОБЛ от умеренной до тяжелой, на что указывает повышение уровня гистамина в индуцированной мокроте.Наше исследование было направлено на оценку характера функциональных реакций легких после ингаляции физиологического раствора, стимула, регулярно используемого для отведения мокроты.Согласно действующим рекомендациям пациенты перед нагрузкой принимали сальбутамол ингаляциями (2). Подобно предыдущим данным (8), сопутствующий ответ на бронходилататоры показал снижение одышки, которое было связано с улучшением FIV 1 , но не FEV 1 , IC или ITGV. Эти данные подтверждают утверждение о том, что принудительное вдохновение действительно информативно для определения эффектов бронходилататоров при ХОБЛ.
В предыдущих исследованиях уже сообщалось о падении ОФВ 1 после ингаляции изотонического (3, 4) или гипертонического (4) физиологического раствора у пациентов с тяжелой ХОБЛ, несмотря на предварительное лечение β 2 -агонистом.По нашим данным, 0,9% физиологический раствор приводил к снижению ОФВ 1 на 20% почти у 50% пациентов; после введения 3% физиологического раствора все пациенты должны были прекратить ингаляцию менее чем через 20 мин. Независимо от этой разницы, характер ответа функции легких с точки зрения обструкции дыхательных путей и гиперинфляции легких оказался одинаковым для 0,9 и 3% физиологического раствора.
Из-за сложной взаимосвязи между бронхоспазмом и гиперинфляцией легких при ХОБЛ, которая затрудняет интерпретацию функциональных параметров, мы оценили панель показателей, позволяющую идентифицировать как гиперинфляцию, так и обструкцию.В качестве предварительного условия испытание с выключенным небулайзером продемонстрировало, что функциональные изменения вызваны не изменением характера дыхания через аппарат.
ТСХ не изменилась при вдыхании сальбутамола или физиологического раствора. Мы пришли к выводу, что пациенты, вероятно, выполняли дыхательные маневры с одинаковым максимальным усилием при наличии бронходилатации или бронхоспазма. Снижение IC и увеличение ITGV и RV указывало на усиление гиперинфляции легких, которое было наиболее выражено после ингаляции гипертонического солевого раствора.Кроме того, изменения ITGV и IC имели одинаковую величину, что указывает на согласованность измерений. Изменения в НПВ и ПЖ также были противоположны друг другу, небольшие расхождения, вероятно, были связаны с разными критериями отбора окончательных значений, сформулированными в рекомендациях по измерению функции легких (15).
Повышение удельного сопротивления дыхательных путей, как на вдохе, так и на выдохе, свидетельствует об увеличении бронхоспазма, в частности, поскольку считается, что удельное сопротивление дыхательных путей в значительной степени не зависит от объема легких.Если принять во внимание постоянную TLC, падение FEV -1 и PEF дополнительно подтвердило вывод о том, что физиологический раствор вызывал бронхоспазм.
Интересно, что изменения в FIV 1 были аналогичны изменениям в IVC, что указывает на важную роль гиперинфляции во время ингаляции физиологического раствора. Хотя наблюдалось ухудшение как FEV 1 , так и FIV 1 , FIV 1 , по-видимому, имеет преимущество перед FEV 1 , поскольку меньше подвержен разрушению дыхательных путей (8).Хотя трудно количественно оценить влияние бронхоспазма на снижение FIV 1 при повышенной гиперинфляции легких, вполне вероятно, что FIV 1 отражал как обструкцию, так и гиперинфляцию. При бронходилатации изменения функции легких и одышка были меньше, чем при использовании физиологического раствора, но изменения в FIV 1 также были аналогичны изменениям в IVC.
Мы также проанализировали взаимосвязь между изменениями функции легких и одышкой во время острого бронхоспазма, вызванного солевым раствором, в отличие от бронходилатации (8).Предыдущее исследование обнаружило только слабую корреляцию между изменениями ОФВ -1 и одышкой, количественно оцененной по шкале Борга, когда аденозин-5′-монофосфат и метахолин использовались в качестве бронхоконстрикторов (19). Мы выбрали ВАШ, так как сообщалось, что эта шкала более чувствительна, чем шкала Борга в условиях покоя (17, 20). Острый бронхоспазм, вызванный физиологическим раствором, отражался в значимых и аналогичных корреляциях ВАШ по сравнению с ОФВ 1 , FIV 1 и IC (рис. 1D – 1F).Корреляция оказалась наиболее сильной для FIV 1 и IC. Эти результаты согласуются с данными Noseda и его коллег, которые также изучали бронхоспазм и бронходилатацию; они обнаружили, что связь между ВАШ и изменениями инспираторных параметров, таких как IVC, MIF 50 и SRaw в , сильнее, чем связь между ВАШ и ОФВ 1 (7).
Вдыхание гипертонического раствора хорошо используется для оценки гиперчувствительности дыхательных путей при астме (1).Считается, что основным причинным фактором является скорость изменения осмолярности, при которой объем аэрозоля, вызывающий 20% -ное падение ОФВ 1 , уменьшается с увеличением концентрации (1). Как следствие высвобождения медиатора из эпителиальных клеток, сенсорных нервов и тучных клеток (21) происходит сокращение гладких мышц и отек дыхательных путей. Ответ на гипертонический раствор при астме может быть заблокирован антагонистами гистамина (22, 23), а тучные клетки легких человека in vitro продемонстрировали высвобождение гистамина в течение нескольких секунд, которое сохранялось после удаления стимула (24).Также могут быть задействованы лейкотриены, простагландины и сенсорные нейропептиды (25).
Действительно, по сравнению с некурящими, у пациентов с хроническим бронхитом наблюдается большее количество тучных клеток в больших (26) и дистальных дыхательных путях (27), а количество тучных клеток увеличивается с увеличением степени обструкции дыхательных путей (28). Кроме того, было обнаружено повышение уровня гистамина в мокроте (29) и моче (30). Настоящее исследование выявило повышение уровня гистамина в мокроте после ингаляции на 3% по сравнению с 0.9% физиологический раствор; кроме того, наблюдается тенденция к повышению уровня триптазы. Это говорит о том, что тучные клетки участвуют в ответе на гипертонический раствор при ХОБЛ. Тучные клетки также являются мощным источником цистеиниловых лейкотриенов, которые, однако, не были повышены в течение в среднем 8,8-минутного периода ингаляции гипертонического солевого раствора.
Роль тучных клеток при ХОБЛ дополнительно подтверждается открытием того факта, что бронхоспазм, вызванный AMP, который, как считается, опосредуется активацией тучных клеток (31), может быть заблокирован антигистаминным, но не холинолитическим действием (32).В качестве альтернативы была предложена активация сенсорных нервных окончаний с помощью AMP (33). Также могут быть задействованы нервные окончания, так как уровень вещества P в мокроте повышается при вдыхании гипертонического раствора (34).
Бронхоспазм, вызванный как изотоническим, так и гипертоническим физиологическим раствором, можно рассматривать как следствие вдыхания жидкости и попадания воды в просвет дыхательных путей. Однако, допуская чистый объемный эффект, следовало бы ожидать уменьшения количества ячеек и концентраций параметров жидкой фазы с более сильным откликом.Напротив, количество клеток и дифференциация клеток оставались постоянными, а уровни гистамина и триптазы даже увеличивались. Следовательно, каким бы ни был (осмотический) механизм ответа на гипертонический раствор, он, по-видимому, включает высвобождение медиаторов воспаления. На наличие «истинной» гиперреактивности дыхательных путей также указывает высокий процент положительных ответов на бронходилататоры, когда осмотические и / или объемные эффекты не играют роли.
Можно утверждать, что предварительная обработка 200 мкг ингаляционного сальбутамола исказила наши результаты, поскольку ингаляция сальбутамола имела тенденцию приводить к более низким уровням гистамина в мокроте у пациентов с астмой (35).В нашем исследовании сальбутамол не предотвращал разницу в концентрациях гистамина и не обеспечивал полную защиту, о чем свидетельствуют побочные реакции после ингаляции физиологического раствора.
У всех пациентов включенный анализ клеточных дифференциалов подтвердил диагноз ХОБЛ, показав высокое количество нейтрофилов и низкое количество эозинофилов. Значения не были изменены провокационными испытаниями, как и концентрации IL-8, MMP-9, TIMP-1 и лейкотриенов. При ХОБЛ состав мокроты не меняется в течение последовательных периодов индукции (3), в отличие от здоровых субъектов (14).Хотя гипертонические стимулы могут вызывать высвобождение IL-8 (36) и увеличивать хемотаксическую активность нейтрофилов (37), время, включенное в наш протокол, казалось, было слишком коротким, чтобы выявить различия в высвобождении или индуцировать синтез. Что наиболее важно, данные показывают, что не было заметной разницы в разжижении мокроты между двумя ингаляциями с физиологическим раствором, гарантируя, что разница в уровнях гистамина не была артефактом. В отличие от предыдущих данных (38), мы не обнаружили взаимосвязи между MMP-9, TIMP-1 или их соотношением и обструкцией воздушного потока на исходном уровне, вероятно, из-за того, что мы включили только пациентов с выраженной обструкцией, что привело к гораздо более узкому диапазон ОФВ 1 .
Таким образом, настоящие данные предполагают, что ответ функции легких на вдыхание гипертонического раствора у пациентов с умеренной и тяжелой ХОБЛ включает как бронхоспазм, так и гиперинфляцию легких. Ощущение одышки, вызванное провокацией, было связано с изменениями объемов форсированного вдоха и выдоха, а также с гиперинфляцией (IC, ITGV), в отличие от ответов бронходилататоров, где важными были только параметры форсированного вдоха (FIV 1 ). Более сильный ответ на гипертонический раствор по сравнению с изотоническим физиологическим раствором может быть опосредован, по крайней мере частично, активацией тучных клеток.
5 Преимущества использования распылителя | Аптека для ухода на дому Simi Valley
Есть несколько способов эффективно доставить лекарства в ваш организм. В зависимости от ваших обстоятельств, потребностей здоровья и характера вашего заболевания ваш врач мог дать вам небулайзер для лечения. В них нуждаются многие люди, например, страдающие бронхитом или астмой. Вот основные преимущества небулайзеров.
1. Эффективная доставка лекарств
Небулайзеры— это медицинские принадлежности, которые направляют лекарства прямо в легкие, где они вам больше всего нужны.В отличие от системных лекарств, которым требуется время, чтобы пройти через желудочно-кишечный тракт в кровоток, небулайзеры работают очень быстро, принося прямую пользу дыхательным путям. Альбутерол — популярный бронходилататор, который начинает действовать примерно через пять минут в форме небулайзера по сравнению с получасовым при пероральном приеме. Как видите, скорость здесь — большое преимущество.
2. Профилактика
Использование небулайзера предотвращает первоначальное развитие или ухудшение респираторных заболеваний.Они также эффективны при лечении неотложных состояний дыхания. Например, бронходилататоры длительного действия, которые вы используете каждый день, могут держать бронхи открытыми. Стероиды уменьшают воспаление и образование слизи в легких, что может препятствовать притоку кислорода.
3. Простота использования
Распылителиочень просты в использовании. В отличие от ингаляторов, которые требуют от человека вдоха при выпуске лекарства, лекарство, содержащееся в небулайзере, будет течь непрерывно. Это означает, что вы можете нормально дышать во время лечения. Новые модели небулайзеров достаточно малы, чтобы их можно было переносить, хотя и не на таком уровне портативности, как ингаляторы, которые могут поместиться прямо в кармане. Небулайзеры обычно питаются от батареи или электричества, и вам требуется от пяти до 10 минут, чтобы дать вам полную дозу лекарства.
4. Адаптивность
Небулайзер может использовать любой — даже младенцы, пожилые люди и люди с тяжелыми формами инвалидности.
5. Меньше побочных эффектов
Небулайзерная терапия снижает риск побочных эффектов по сравнению с пероральными версиями тех же лекарств. Небулайзеры также снижают риск краткосрочных побочных эффектов, таких как тремор, головная боль или учащенное сердцебиение. Кроме того, они снижают риск долгосрочных осложнений из-за стероидов, таких как высокое кровяное давление, высокий уровень глюкозы в крови, увеличение веса, потеря костной массы или риск инфицирования.
Связаться с аптекой на дому
Чтобы узнать больше о небулайзерах и их преимуществах, свяжитесь с нами по телефону 805-527-9600.В аптеке Home Care можно заказать любой аппарат, фильтр, трубку или мундштук, необходимые для дополнения вашей небулайзерной системы. Кроме того, наши фармацевты прошли обучение по многим легочным заболеваниям и могут посоветовать вам, как лучше всего использовать ваш небулайзер.
.

 Вообще, вдохи во время процедуры должны быть достаточно глубокими;
Вообще, вдохи во время процедуры должны быть достаточно глубокими;