Препараты для внутримышечных инъекций в туристическом походе
В этой статье мы подробно остановимся на тех препаратах из нашей аптечки, которые предназначены для внутримышечных инъекций. Это отдельный подраздел общественной аптечки, который отдельные группы туристов могут и не укомплектовывать либо в случае несложности или не большой длительности похода, либо в случае отсутствия в группе участников с навыками обращения подобными препаратами. Кроме этого, эти препараты также есть и в главе «Домашняя аптечка параноика\выживальщика».
Внимание! Данная информация является рекомендательной и предоставлена исключительно с ознакомительной целью и не должна быть использована как руководство к самолечению. Только врач может принять решение о назначении какого-либо препарата, а также определить дозы и способы его применения.
Кеторол, он же кеторолак, относится к нестероидным противовоспалительным препаратам и обладает достаточно сильным обезболивающим эффектом, самым сильным в этой группе.
Кеторол для внутримышечных инъекций обычно поставляется в ампулах, по 1 мл раствора, 30 мг\1мл. Т.е., одна доза содержит 30 мг действующего вещества — кеторолака трометамола.
В туристической аптечке основным назначением кеторола является снижение болевого синдрома в случае травм. По силе анальгезирующего эффекта этот препарат значительно превосходит другие НПВП. Некоторые источники даже сопоставляют его по силе действия с морфином. При всём при этом, это не означает того, что он является волшебной жидкостью, которая поставит обратно на лапы поломанного туриста\альпиниста и доведёт его до больницы. Так не бывает, по крайней мере, пока.
Нужно чётко очертить границы его использования: инъекции с кеторолом имеет смысл использовать только тогда, когда травма такова, что пострадавший не способен передвигаться самостоятельно и его либо требуется транспортировать силами группы, либо оставлять на лагере до прибытия помощи. Отдельно можно выделить случаи жёстких травм верхних конечностей, когда самостоятельное передвижение в сторону эвакуации всё же возможно – несложный перелом, разрыв связок и прочее подобное, когда полностью разгруженный участник группы способен перемещаться самостоятельно и с адекватной скоростью.
Анальгезирующий эффект наблюдается не сразу после введения, а начинает ощущаться только через полчаса, а максимум достигается через два часа. При этом у кеторола отсутствуют эффекты эйфории и снятия травматического стресса. Вводить препарат рядом с раной или местом травмы смысла никакого нет – схема его действия не зависит от места инъекции, поэтому, если есть возможность, лучше ставить укол «классически» (в отдельной статье я коснусь темы, как правильно вводить уколы в походных условиях).
По дозировке: категорически запрещается вводить более 90 мг кеторола в сутки. Т.е., не более трёх уколов. Промежуток между инъекциями должен быть не менее 6 часов. Как правило, первая инъекция будет утром, последняя перед сном, вторая где-то между ними. Если масса тела участника менее 50 кг, то суточная доза кеторола должна снижаться до 60 мг в сутки.
В случае превышения дозировки будем иметь целый букет последствий: нарушение функции почек, язвенное поражение ЖКТ, сильная слабость, диарея, рвота и резь в животе. В условиях дикой местности это будет означать с большей долей вероятности гибель участника.
По идее, применение кеторола должно продолжаться не более трёх суток. 10 ампул в общественной аптечке на то и рассчитаны. При повышении продолжительности курса будет ощущаться накапливание эффектов угнетения внутренних органов и всё равно, в конце концов, получим те же симптомы, что и при суточной передозировке.
Что делать, если пострадавших двое, а кеторола всего 10 ампул? Чередовать инъекции кеторола с принятием таблеток со спазмалгоном. Например, если участник «ходячий», то утром и днём используются таблетки, а вечером инъекция. Если «лежачий», то схема такая же. Почему именно на ночь? Сон очень важен, так как во сне происходит львиная доля процесса анаболизма, когда происходит строительство новых клеток и межклеточного вещества. Другими словами, наш организм выздоравливает от травм, пока спит. Если же говорить о сочетании кеторола и таблеток, то, к сожалению, использование этого анальгетика со спазмалгоном и подобными средствами будет усугублять побочные эффекты обоих препаратов, так что в любом случае более чем трёхдневное использование крайне нежелательно.
Применение кеторола также будет снижать воспаление, что может существенно облегчать общее состояние при травмах, но эффект достигается только при использовании, как только приём кеторола прекращается, воспаление возвращается – как и боль, впрочем.
Кеторол сам по себе препятствует образованию тромбов, поэтому совместное его использование с другими антикоагулянтами запрещается, так как может вызвать риск развития кровотечений. В нашем походном случае нельзя совмещать приём кеторола и ацетилсалициловой кислоты или тромбо АСС.
Кеторол бессмысленно использовать как препарат для анестезии.
Супрастин, он же хлоропирамин. Является антигистаминным препаратом Н1 группы и применяется при терапии аллергических заболеваний. В одной ампуле 20 мг действующего вещества, 1 мл раствора.
Показанием к применению на маршруте служат:
- Аллергическая крапивница. Выглядит как плоско-приподнятые бледно-розовые волдыри, похожи на ожог крапивой – отсюда название. Как правило, сопровождается насморком, может также проявляться учащённое дыхание. Как правило, достаточно одной инъекции супрастина в день, при более тяжёлых формах две инъекции в сутки. В некоторых случаях может сопровождаться анафилактическим шоком, при котором в большинстве случаев сам по себе супрастин бесполезен.

- Поллиноз (сенная лихорадка) – аллергическая реакция на пыльцу растений. Появляется насморк, покраснение глаз (конъюнктивит), першение в горле, кашель, иногда приступы удушья, редко — кожные проявления. При этом аллергия может быть на пыльцу определённых растений и до приезда на маршрут участник мог и не знать о своей возможной реакции. Тем не менее, обычно участник осведомлён по опыту жизни о возможности такой реакции и носит с собой соответствующие таблетки в личной аптечке, поэтому инъекция супрастина применяется только в тяжёлом случае.
- Аллергическая реакция на укусы насекомых – имеется в виду реакция, отличная от анафилактического шока.
Обычно при указанных выше случаях достаточно вводить 20 мг супрастина в сутки, на ночь, так как часто побочным эффектом является сонливость. Детям же до 14 лет и пожилым введение раствора супрастина в походных условиях противопоказано.
Сделаем теперь небольшое отступление и рассмотрим такую аллергическую реакцию, как отёк Квинке. Под отеком Квинке понимается внезапный и выраженный отек кожи, жировой клетчатки и/или слизистой оболочки. Отек Квинке иногда называют гигантской крапивницей, ангионевротическим отеком, ангиоотеком. Данная болезнь хотя бы раз в жизни отмечается до 10% населения. Почти в половине случаев отек Квинке сочетается с крапивницей. Основным проявлением является, как правило, безболезненный ограниченный отек кожи, подкожной жировой ткани и/или слизистой оболочки, иногда сопровождающийся чувством распирания кожи. Отек плотный и при надавливании на него пальцем не оставляет следов, кожа над отеком сохраняет свой первоначальный цвет. Чаще всего отек Квинке возникает в области губ, век, языка, мягкого неба, ушных раковин, кистей, стоп, половых органов. У 20-25% людей может отмечаться отек гортани, трахеи и крупных бронхов, в таких случаев отмечается сиплость голоса, ощущение нехватки воздуха, «лающий кашель». Приблизительно 20-25% случаев приходится на наследственную форму отека Квинке, которая связана с недостаточностью специфического С1-ингибитора крови.
Под отеком Квинке понимается внезапный и выраженный отек кожи, жировой клетчатки и/или слизистой оболочки. Отек Квинке иногда называют гигантской крапивницей, ангионевротическим отеком, ангиоотеком. Данная болезнь хотя бы раз в жизни отмечается до 10% населения. Почти в половине случаев отек Квинке сочетается с крапивницей. Основным проявлением является, как правило, безболезненный ограниченный отек кожи, подкожной жировой ткани и/или слизистой оболочки, иногда сопровождающийся чувством распирания кожи. Отек плотный и при надавливании на него пальцем не оставляет следов, кожа над отеком сохраняет свой первоначальный цвет. Чаще всего отек Квинке возникает в области губ, век, языка, мягкого неба, ушных раковин, кистей, стоп, половых органов. У 20-25% людей может отмечаться отек гортани, трахеи и крупных бронхов, в таких случаев отмечается сиплость голоса, ощущение нехватки воздуха, «лающий кашель». Приблизительно 20-25% случаев приходится на наследственную форму отека Квинке, которая связана с недостаточностью специфического С1-ингибитора крови.
На маршруте у нас минимальный набор медикаментов, поэтому для снятия отёка Квинке сразу вводится ударная доза препаратов: 12 мг дексаметазона (3 ампулы) и 20 мг супрастина (1 ампула).
В тяжёлых случаях в больницах при отёке Квинке так же вводят адреналин, по ряду причин не применяющийся в аптечках у туристов – рецептурный отпуск, широкий спектр побочных эффектов и необходимость применения только при наблюдении врача (впрочем, как и вообще всё лечение).
Теперь коснёмся анафилактического шока. Под названием анафилактический шок подразумевают острую системную аллергическую реакцию, вовлекающую более одного органа, на повторный контакт с аллергеном. Часто анафилактический шок угрожает жизни в результате выраженного падения давления и возможного развития удушья. Анафилактический шок является наиболее опасным осложнением лекарственной аллергии, заканчивающееся примерно в 10-20 % случаев летально. Скорость возникновения анафилактического шока — от нескольких секунд или минут до 2 часов от начала контакта с аллергеном. В развитии анафилактической реакции у больных с высокой степенью сенсибилизации ни доза, ни способ введения аллергена не играют решающей роли
Анафилактический шок является наиболее опасным осложнением лекарственной аллергии, заканчивающееся примерно в 10-20 % случаев летально. Скорость возникновения анафилактического шока — от нескольких секунд или минут до 2 часов от начала контакта с аллергеном. В развитии анафилактической реакции у больных с высокой степенью сенсибилизации ни доза, ни способ введения аллергена не играют решающей роли
Традиционно в клинической картине анафилактического шока выделяют три формы:
- Стремительная форма наступает через 1-2 секунды после введения аллергена. Происходит потеря сознания, судороги, расширение зрачков (миоз), отсутствие реакции зрачков не свет. Снижается артериальное давление, нарушается дыхание, тоны сердца не выслушиваются. Смерть при этой форме наступает через 8-10 минут
- Тяжелая форма возникает через 5-7 минут после введения аллергена. Характерно ощущение жара, нарушение дыхания, расширение зрачков. Беспокоит головная боль, наблюдается падение артериального давления.

- Средняя форма анафилактического шока развивается через 30 минут после введения аллергена. Имеет место аллергическая сыпь на коже, кожный зуд.
Для средней формы характерны следующие варианты:
А. Кардиогенный с отеком легких
Б. Астмоподобный с бронхоспазмом, ларингоспазмом, отеком гортани.
В. Церебральный, для которого характерно психомоторное возбуждение, нарушение сознания, судороги.
Г. Абдоминальный с симптоматими «острого живота».
Причины летального исхода при анафилактическом шоке:
- Острая сердечная и дыхательная недостаточность
- Острая почечная недостаточность
- Отек головного мозга
- Кровоизлияние в головной мозг, надпочечники.
Лечение анафилактического шока в полевых условиях затруднено. Внутримышечно вводим 8 мг дексаметазона (2 ампулы) и 20 мг супрастина (1 ампула). Если аллерген попал в организм через желудок, то требуется его промывка.
Дексаметазон — глюкокортикостероидный препарат, оказывающий противовоспалительное, противоаллергическое, десенсибилизирующее, иммунодепрессивное, противошоковое и антитоксическое действие. В ампуле 4 мг действующего вещества, раствора 1 мл.
В ампуле 4 мг действующего вещества, раствора 1 мл.
Дексаметазон на маршруте применяют в следующих случаях:
- шок – травматический, анафилактический, ожоговый, токсический;
- черепно-мозговая травма;
- тяжёлые аллергические реакции;
- тяжёлые инфекционные заболевания (в сочетании с антибиотиками)
При болевом шоке вводить 4 мг (1 ампулу) за раз, в тяжёлых случаях 8 мг (2 ампулы), затем по одной ампуле каждые 4-5 часов, если такая необходимость есть. При черепно-мозговой травме вводить сразу 2 ампулы, затем продолжать вводить по 1 ампуле каждые два часа – так как всего ампул у нас 10, то их хватит, в общей сложности, на 16 часов, что должно, по идее, снизить вероятность смертности от отёка мозга. Тут следует отметить следующую вещь – дексаметазон показан при черепно-мозговых травмах, то максимальный эффект достигается в комплексе с другими мероприятиями, которые мы на маршруте обеспечить не можем. Есть ли у пострадавшего отёк мозга или нет, диагноз, казалось бы, поставить в теории несложно, но в условиях маршрута и развивающейся аварийной ситуации сделать это сложнее. Если травма изолирована, не происходит кровотечения изо рта, носа и ушей, и при этом вместе с кровью не происходит вывод жидкости (смотрим разводы крови на светлой ткани), то прогноз по отёку мозга лучше считать неблагоприятным. Вместе с введением дексаметазона нужно немедленно начинать эвакуацию.
Если травма изолирована, не происходит кровотечения изо рта, носа и ушей, и при этом вместе с кровью не происходит вывод жидкости (смотрим разводы крови на светлой ткани), то прогноз по отёку мозга лучше считать неблагоприятным. Вместе с введением дексаметазона нужно немедленно начинать эвакуацию.
При тяжёлых инфекционных заболеваниях дексаметазон также вводится по 4 мг (1 ампула) одновременно вместе с приёмом антибиотиков.
Дицинон, он же этамзилат. Этот препарат обладает кровоостанавливающим действием и показан при травмах с обильным капиллярным кровотечением. После введение инъекции эффект наступает примерно через 45 минут.
Основное применение на маршруте – глубокие резаные раны, как правило либо на биваке, либо при рассечении о камень. Дицинон следует применять через несколько часов после нанесения раны и только при непрекращающемся кровотечении капиллярного характера, так как сосудистое кровотечение, обширную рану или размозжение им не остановить. Если процесс кровотечения (при перевязке, естественно) сходит на нет сам по себе, то применять препарат нельзя, так как это чревато образование тромбов. При необходимости следует вводить за раз 2 ампулы по 1 мл (в каждой ампуле 0,125 мг действующего вещества).
Если процесс кровотечения (при перевязке, естественно) сходит на нет сам по себе, то применять препарат нельзя, так как это чревато образование тромбов. При необходимости следует вводить за раз 2 ампулы по 1 мл (в каждой ампуле 0,125 мг действующего вещества).
Информация о дозировках и специфике применения всех перечисленных препаратов должна храниться распечатанной в соответствующем отделении аптечки, чтобы в случае необходимости применения можно было сразу всё это посмотреть, а не лихорадочно вспоминать.
Я считаю необходимыми эти препараты для групповой аптечки в длительных и сложных походах. Они являются дополнительной страховкой для хорошо подготовленной группы. В свою очередь, плохо подготовленную к тяготам маршрута группу, никакая навороченная аптечка спасти не сможет, так как, как и любое снаряжение, является в первую очередь инструментом, который должен прилагаться к здравомыслящей голове, физически развитому телу и умению этим самым инструментом пользоваться.
Статья написана в соавторстве с Димой Савцовым (Гоплит), медиком и туристом.
Дополнительные ссылки:
Всё о медицине.
ОТЕК КВИНКЕ — Школа здоровья — ГБУЗ Городская поликлиника 25 г. Краснодара МЗ КК
15 мая 2017 г.
Причины отека Квинке
Причины такие же, как у любой другой аллергической реакции. Такое состояние может возникнуть в результате контакта с любым аллергеном, будь то пищевой продукт, лекарственный препарат, пыльца растения или укус насекомого. Предрасполагающими факторами к развитию гигантской крапивницы могут служить вирусные и паразитарные инфекции, заболевания крови и эндокринной системы.
Отдельно выделяется ангиоотек, имеющий псевдоаллергическую природу. В этом случае заболевание протекает в виде обострений, к которым могут приводить различные факторы: стрессы, травмы, острые заболевания и т.д. Примерно в 30% случаях гигантской крапивницы причина болезни остается неустановленной.
Симптомы и признаки
Главные симптомы отека Квинке – это отеки, чаще всего наблюдаемые на местах с рыхлой клетчаткой. При нажатии на отек поверхность кожи не продавливается, что связано с тем, что в отечной жидкости содержится много белка. В отличие от обычной крапивницы, при данном заболевании отсутствует зуд.
При нажатии на отек поверхность кожи не продавливается, что связано с тем, что в отечной жидкости содержится много белка. В отличие от обычной крапивницы, при данном заболевании отсутствует зуд.
Особую тревогу должны вызывать такие признаки отека Квинке, как охриплость голоса, шумное дыхание, лающий кашель и усиливающаяся одышка. Кожа на лице становится синюшного оттенка, далее резко бледнеет. Все это свидетельствует о развитии такого грозного осложнения, как отек гортани, который без экстренного медицинского вмешательства может привести к смерти от удушья.
Первая помощь
Что делать при отеке Квинке? Правильный ответ — немедленно вызывать скорую! А до приезда врачей больному должна быть оказана первая помощь при отеке Квинке, которая заключается в приеме 1-2 таблеток любого антигистаминного препарата (супрастин, кларитин, кларотадин, тавегил и др.). Чтобы быстрее вывести аллерген из организма, дайте больному сорбент (активированный уголь, смекту, лактофильтрум) и обильное щелочное питье («Боржоми», «Нарзан» или 1-2%-ный раствор пищевой соды).
Если аллергическая реакция была вызвана укусом насекомого или инъекцией, выше пораженного места наложите жгут, а на место укуса или инъекции – прохладный компресс. Далее помогите больному принять удобное положение и ожидайте приезда медиков.
Лечение отека Квинке
Ввиду высокой опасности удушья лечение отека Квинке проводят только в стационаре. При поступлении в медицинское учреждение больному назначают внутривенные инъекции гормональных препаратов (преднизалона, гидрокортизона или дексаметазона) и внутримышечные инъекции антигистаминных препаратов. Кроме того, больному дают ферментные препараты, которые помогают подавить чувствительность к действию аллергена.
В случае развития асфиксии проводится процедура интубации трахей с введением миорелаксантов. При таком ходе событий к основным противоаллергическим препаратам добавляются катехоламины (адреналин и эфедрин).
Говоря о том, как лечить отек Квинке, нельзя обойти вниманием важность соблюдения гипоаллергенной диеты. Из рациона больного исключаются цитрусовые, кофе, шоколад, алкогольные напитки и острая пища.
Из рациона больного исключаются цитрусовые, кофе, шоколад, алкогольные напитки и острая пища.
Для выведения аллергена из организма используйте сорбенты: растолченный активированный уголь из расчета 5 таблеток на стакан воды, 1-2 пакетика смекты или 1-2 чайной ложки энтеросгеля.
Помните, что однажды развившись, ангионевротический отек может проявиться вновь. Поэтому после нормализации состояния обязательно посетите аллерголога, чтобы выяснить причину подобной реакции и при необходимости пройти дополнительное лечение.
Лекарство от шока. Что нужно знать о препарате дексаметазон
26 октября 2019, 02:27
Цей матеріал також доступний українськоюДексаметазон известен своим противовоспалительным, противоаллергическим и иммунодепрессивным действием.
Дексаметазон — лекарственный препарат, который содержит искусственный гормон-глюкокортикостероид.
Используют лекарство для лечения больных с отеком мозга, при различных воспалительных заболеваниях глаз, ревматологических и кожных заболеваниях.
Препарат также применяют при аллергии, болезнях дыхательных путей, онкологии и шоковых состояниях.
В аптеках препарат представлен в различных формах выпуска — дексаметазон в ампулах, дексаметазон в таблетках, дексаметазон в каплях.
Дексаметазон — инструкция. Кому назначают?
Дексаметазон оказывает противовоспалительное, антитоксическое, противоаллергическое и иммунодепрессивное действие (снижает активность клеток имунной системы).
Препарат назначают при таких заболеваниях:
- Отек головного мозга
- Болезнь Аддисона-Бирмера
- Бронхиальная астма
- Аллергические реакции (отек Квинке, дерматоз, бронхоспазм, острая анафилактическая реакция на лекарства)
- Тяжелые инфекционные заболевания
- Острая недостаточность коры надпочечников
- Различные заболевания суставов (бурсит, остеоартроз, остеохондроз, артриты различной этиологии)
- Заболевания глаз (негнойный и аллергический конъюнктивит, кератит, ирит, блефарит, эписклерит, склерит)
- Шок (токсический, ожоговый, травматический, операционный)
- Злокачественные заболевания (паллиативное лечение лейкоза и лимфомы у взрослых пациентов; острая лейкемия у детей).

Дексаметазон — применение
Режим дозировки зависит от вида и степени заболевания. При тяжелых заболеваниях назначают до 10−15 мг/сут, поддерживающая доза — 2−4,5 мг в сутки. Суточную дозу разделяют на пару приемов.
При различных глазных заболеваниях закапывают по 2 капли каждые 1−2 часа, затем — каждые 4−6 часов.
Дексаметазон — побочные действия
Могут возникать такие побочные действия от приема лекарственного препарата дексаметазон:
Со стороны пищеварительной системы — тошнота, рвота, кровотечения и перфорация ЖКТ, метеоризм, повышение или снижение аппетита.
Со стороны сердечно-сосудистой системы — аритмия, брадикардия, тромбозы, повышение артериального давления.
Со стороны нервной системы — дезориентация, галлюцинации, депрессия, паранойя, маниакально-депрессивный психоз, бессонница, нервозность или беспокойство, головокружение, головная боль.
Со стороны органов чувств — потеря зрения, повышение внутриглазного давления, развитие вторичных бактериальных, грибковых или вирусных инфекций глаз.
Со стороны кожных покровов — замедленное заживление ран, угри, стрии, склонность к развитию пиодермии и кандидозов.
Как долго выводится дексаметазон из организма? Период полувыведения препарата из плазмы составляет около 3—5 часов.
Дексаметазон — противопоказания
Повышенная чувствительность к дексаметазону или компонентам препарата является единственным серьезным противопоказанием для применения лекарства.
С осторожностью нужно применять препарат у детей в период роста.
Во время беременности дексаметазон назначают только в тех случаях, когда лечебный эффект будет превышать потенциальный риск для плода.
Купить препарат дексаметазон в аптеках
Сравнить цены и приобрети дексаметазон в аптеках:
Дексаметазон
Дексаметазон 4 мг 1 мл № 25 раствор
Дексаметазон КРКА 4 мг № 30 таблетки
Дексаметазон-Биофарма 0.1% 10 мл глазные капли
Дексаметазон
Дексаметазон 0,5 мг таблетки № 10
Дексаметазон 4 мг раствор 1 мл № 25
Дексаметазон 0,1% глазные капли 10 мл
Правовая информация. Эта статья содержит общие сведения справочного характера и не должна рассматриваться в качестве альтернативы рекомендациям врача. НВ не несет ответственности за любой диагноз, поставленный читателем на основе материалов сайта. НВ также не несет ответственности за содержание других интернет-ресурсов, ссылки на которые присутствуют в этой статье. Если вас беспокоит состояние вашего здоровья, обратитесь к врачу.
Эта статья содержит общие сведения справочного характера и не должна рассматриваться в качестве альтернативы рекомендациям врача. НВ не несет ответственности за любой диагноз, поставленный читателем на основе материалов сайта. НВ также не несет ответственности за содержание других интернет-ресурсов, ссылки на которые присутствуют в этой статье. Если вас беспокоит состояние вашего здоровья, обратитесь к врачу.
Раздел для практикующего врача аллерголога
Раздел только для специалистов в сфере медицины, фармации и здравоохранения!
Медицинский совет, № 7, 2015
Е.Н. МЕДУНИЦЫНА, к.м.н., старший научный сотрудник отделения Иммунодефицитов ФГБУ «ГНЦ Институт иммунологии» ФМБА России
Лечение обострения аллергических заболеваний — задача, которая решается комплексом мероприятий медикаментозного и немедикаментозного характера. Несмотря на достаточно широкий спектр лекарственных средств, использующихся для лечения обострения аллергических заболеваний с поражением различных органов и систем, наиболее часто применяющимися препаратами остаются антигистаминные препараты и глюкокортикостероиды. Эти группы препаратов оказывают наиболее выраженный клинический эффект, связанный с фармакологическими особенностями указанных лекарственных средств, позволяющими достаточно быстро воздействовать практически на все стадии аллергической реакции. В аллергологической практике также находят достаточно широкое применение другие противоаллергические препараты — антагонисты лейкотриеновых рецепторов, стабилизаторы мембран тучных клеток и др. Основная задача аллерголога-иммунолога состоит в выборе правильной тактики ведения больного в период обострения, подбор адекватной противоаллергической терапии с учетом индивидуальных особенностей пациента, характера течения и тяжести обострения заболевания.
Эти группы препаратов оказывают наиболее выраженный клинический эффект, связанный с фармакологическими особенностями указанных лекарственных средств, позволяющими достаточно быстро воздействовать практически на все стадии аллергической реакции. В аллергологической практике также находят достаточно широкое применение другие противоаллергические препараты — антагонисты лейкотриеновых рецепторов, стабилизаторы мембран тучных клеток и др. Основная задача аллерголога-иммунолога состоит в выборе правильной тактики ведения больного в период обострения, подбор адекватной противоаллергической терапии с учетом индивидуальных особенностей пациента, характера течения и тяжести обострения заболевания.
Лечение аллергических заболеваний — это целый комплекс профилактических и терапевтических мероприятий, направленных на купирование обострения, а также предотвращение рецидивов и прогрессирования заболевания.
Аллергия (греч. аllos — другой и ergon — действие) — состояние измененной реактивности организма, проявляющееся повышением его иммунологически опосредованной чувствительности к различным веществам экзогенного и эндогенного происхождения — аллергенам (веществам, вызывающим сенсибилизацию организма и аллергические реакции — чужеродные белки, липиды, мукополисахариды, соединения небелковой природы, некоторые низкомолекулярные вещества — гаптены). Первичный контакт организма с аллергеном, который может осуществляться разными путями — парентерально, ингаляционно, энтерально, через кожу или слизистые, при наличии генетической предрасположенности к подобному способу реагирования, приводит к сенсибилизации, которая в свою очередь сопровождается образованием антител или сенсибилизированных лимфоцитов. При повторном попадании аллергена развивается аллергическая реакция по немедленному или замедленному типу, включающая 3 стадии. В иммунологической стадии повторное попадание аллергена в организм приводит к реакции аллергических антител или сенсибилизированных лимфоцитов с аллергеном. В патохимической стадии происходит ряд биохимических реакций, приводящих к высвобождению медиаторов из клеток. Патофизиологическая стадия характеризуется наличием клинических проявлений замедленного и немедленного типа. Основными патофизиологическими изменениями при аллергической реакции являются сокращение гладкой мускулатуры, расширение мелких сосудов и капилляров, выход жидкости во внесосудистое пространство.
Первичный контакт организма с аллергеном, который может осуществляться разными путями — парентерально, ингаляционно, энтерально, через кожу или слизистые, при наличии генетической предрасположенности к подобному способу реагирования, приводит к сенсибилизации, которая в свою очередь сопровождается образованием антител или сенсибилизированных лимфоцитов. При повторном попадании аллергена развивается аллергическая реакция по немедленному или замедленному типу, включающая 3 стадии. В иммунологической стадии повторное попадание аллергена в организм приводит к реакции аллергических антител или сенсибилизированных лимфоцитов с аллергеном. В патохимической стадии происходит ряд биохимических реакций, приводящих к высвобождению медиаторов из клеток. Патофизиологическая стадия характеризуется наличием клинических проявлений замедленного и немедленного типа. Основными патофизиологическими изменениями при аллергической реакции являются сокращение гладкой мускулатуры, расширение мелких сосудов и капилляров, выход жидкости во внесосудистое пространство.
Существует целый ряд заболеваний, в основе который лежит аллергический процесс. Аллергические болезни — (греч. аllos — другой и ergon — действие) — группа заболеваний человека, обусловленных повышением чувствительности к экзоаллергенам: аллергический ринит, аллергический конъюнктивит, бронхиальная астма, атопический и контактный аллергический дерматит, аллергическая крапивницы и отек Квинке, лекарственная аллергия, пищевая и инсектная аллергия и др. Существуют аллергические нозологии, в генезе которых участвует несколько типов аллергической реакции, а также группа заболеваний, в которых аллергический процесс является компонентом основного заболевания. Клиническая картина аллергии зависит от пути попадания аллергена в организм, типа аллергической реакции и локализации аллергического воспаления. Аллергические заболевания протекают с поражением дыхательного тракта, кожи и слизистых, сердечно-сосудистой и других систем организма. Степень тяжести состояния при обострении аллергических заболеваний может варьировать от легкой до крайне тяжелой. Острые реакции, в т. ч. при лекарственной аллергии, могут приводить к тяжелой полиорганной недостаточности.
Острые реакции, в т. ч. при лекарственной аллергии, могут приводить к тяжелой полиорганной недостаточности.
Лечение
Воздействие на аллергическое воспаление предполагает не только применение фармакотерапии, но и выполнение ряда профилактических мер. В случае легких обострений, не требующих госпитализации в стационар, лечение проводится амбулаторно под динамическим наблюдением аллерголога-иммунолога с коррекцией терапии по результатам оценки состояния больного в динамике. При более тяжелых обострениях аллергического заболевания пациенту показана госпитализация в аллергологический стационар или, в случаях развития острой анафилактической реакции, астматического статуса и др. жизнеугрожающих состояний — в отделение реанимации и интенсивной терапии.
К немедикаментозным методам лечения аллергических заболеваний относятся мероприятия, направленные на элиминацию причинно-значимого аллергена и провоцирующих факторов. Элиминация аллергена — основополагающая мера, которая применяется как на этапе купирования обострения заболевания, так и в последующий период, и должна осуществляться при любой форме аллергии. В каждом отдельном случае рассматривается комплекс элиминационных мероприятий: назначение гипоаллергенной диеты, проведение мероприятий, направленных на исключение или минимизацию контакта с лекарственными, ингаляционными, инсектными, пищевыми и другими аллергенами. От своевременности выполнения элиминационных мероприятий во многом зависит длительность и эффективность лечения [1].
В каждом отдельном случае рассматривается комплекс элиминационных мероприятий: назначение гипоаллергенной диеты, проведение мероприятий, направленных на исключение или минимизацию контакта с лекарственными, ингаляционными, инсектными, пищевыми и другими аллергенами. От своевременности выполнения элиминационных мероприятий во многом зависит длительность и эффективность лечения [1].
Фармакотерапия обострения аллергического заболевания
В период обострения аллергического заболевания первостепенным является правильный выбор тактики ведения пациента. Купирование обострения или острого состояния и контроль над симптомами аллергии осуществляется целым рядом лекарственных средств, относящихся к разным фармакологическим группам. Разработка индивидуального комплекса противоаллергических средств должна осуществляться с учетом клинической картины заболевания, антропометрических данных и физиологических особенностей пациента и других параметров.
Существует основной перечень лекарственных препаратов, использующихся для лечения обострения аллергических заболеваний. Но надо учитывать и тот факт, что при тяжелых обострениях, как правило, применяется более широкий спектр лекарственных средств, как симптоматических, так и направленных на борьбу с системными нарушениями, септическими и иными осложнениями. В случае развития тяжелых обострений с признаками полиорганной недостаточности (в т. ч. при тяжелых реакциях на лекарственные средства) применяются различные средства и методы дезинтоксикационной терапии, лечение метаболических нарушений. При наличии инфекционных осложнений применяются антибактериальные, антимикотические препараты, проводятся санационные мероприятия. При выборе препарата, его дозы и длительности курса лечения оценивается эффективность и переносимость лекарственного средства, физиологические и антропометрические данные больного, его возраст и пр. При лечении обострения аллергического заболевания у детей и беременных женщин также учитывается профиль безопасности препаратов, уделяется особое внимание форме препарата и его дозировке [2].
Но надо учитывать и тот факт, что при тяжелых обострениях, как правило, применяется более широкий спектр лекарственных средств, как симптоматических, так и направленных на борьбу с системными нарушениями, септическими и иными осложнениями. В случае развития тяжелых обострений с признаками полиорганной недостаточности (в т. ч. при тяжелых реакциях на лекарственные средства) применяются различные средства и методы дезинтоксикационной терапии, лечение метаболических нарушений. При наличии инфекционных осложнений применяются антибактериальные, антимикотические препараты, проводятся санационные мероприятия. При выборе препарата, его дозы и длительности курса лечения оценивается эффективность и переносимость лекарственного средства, физиологические и антропометрические данные больного, его возраст и пр. При лечении обострения аллергического заболевания у детей и беременных женщин также учитывается профиль безопасности препаратов, уделяется особое внимание форме препарата и его дозировке [2].
Основные противоаллергические средства, использующиеся в период обострения аллергического заболевания:
1. Блокаторы Н1-рецепторов к гистамину.
2. Глюкокортикостероидные препараты.
3.Другие лекарственные средства (антихолинолитики, блокаторы лейкотриеновых рецепторов, антигистаминные препараты, обладающие мембраностабилизирующим действием).
Блокаторы Н1-рецепторов к гистамину (антигистаминные препараты)
Антигистаминные препараты — группа лекарственных средств, действие которых опосредуется их взаимодействием с рецепторами гистамина на клетках и различных тканях.
Одним из самых важных медиаторов аллергии является гистамин. Антагонисты Н1-рецепторов гистамина имеют структурное сходство с гистамином и блокируют указанные рецепторы по принципу конкуренции с гистамином. Действие антагонистов носит обратимый характер.
Гистамин — 5[2-аминоэтил] имидазол — образуется из аминокислоты гистидин при действии на нее фермента клеточной цитоплазмы — гистидиндекарбоксилазы. Гистамин депонируется в гранулах базофилов, тучных клеток, локализующихся в органах-мишенях, и находится в связанном состоянии с белковым и протеогликановым матриксом гранул, имеет сродство к гепарино-белковому комплексу гранул соединительно-тканных тучных клеток. При аллергической реакции активация тучных клеток и базофилов приводит к вытеснению гистамина из гранул. Фармакологическое действие гистамина на организм опосредуется через четыре типа гистаминовых рецепторов (Н1, Н2, Н3, Н4). Локализация Н1-рецепторов — гладкие мышцы бронхов, артерий, пищеварительной системы и мочевого пузыря, сердце и головной мозг. Через Н1-рецепторы гистамин вызывает сокращение гладкой мускулатуры бронхов, желудка, кишечника, желчного и мочевого пузыря, сосудов малого круга кровообращения, повышает проницаемость сосудов, увеличивает внутриклеточное содержание цГМФ, усиливает секрецию слизи слизистыми железами носа, вызывает хемотаксис эозинофилов, нейтрофилов и усиливает образование простаноидов (простагландинов F2, F2, D2, тромбоксана, простациклина).
Гистамин депонируется в гранулах базофилов, тучных клеток, локализующихся в органах-мишенях, и находится в связанном состоянии с белковым и протеогликановым матриксом гранул, имеет сродство к гепарино-белковому комплексу гранул соединительно-тканных тучных клеток. При аллергической реакции активация тучных клеток и базофилов приводит к вытеснению гистамина из гранул. Фармакологическое действие гистамина на организм опосредуется через четыре типа гистаминовых рецепторов (Н1, Н2, Н3, Н4). Локализация Н1-рецепторов — гладкие мышцы бронхов, артерий, пищеварительной системы и мочевого пузыря, сердце и головной мозг. Через Н1-рецепторы гистамин вызывает сокращение гладкой мускулатуры бронхов, желудка, кишечника, желчного и мочевого пузыря, сосудов малого круга кровообращения, повышает проницаемость сосудов, увеличивает внутриклеточное содержание цГМФ, усиливает секрецию слизи слизистыми железами носа, вызывает хемотаксис эозинофилов, нейтрофилов и усиливает образование простаноидов (простагландинов F2, F2, D2, тромбоксана, простациклина). Клиническими проявлениями действия гистамина являются: зуд кожи и слизистых, волдырная реакция, формирование отека слизистых и гиперсекреция слизи в дыхательных путях, бронхоспазм, боли, усиление продукции пепсина, соляной кислоты в желудке, падение артериального давления, нарушение сердечного ритма и ряд других нарушений. Существующие на данный момент антигистаминные лекарственные средства подразделяют на препараты I и II поколения. По форме лекарственного средства антигистаминные подразделяются на препараты системного (пероральные и парентеральные формы) и местного (в виде средств для нанесения на кожу, а также интраназальных средств и капель для глаз).
Клиническими проявлениями действия гистамина являются: зуд кожи и слизистых, волдырная реакция, формирование отека слизистых и гиперсекреция слизи в дыхательных путях, бронхоспазм, боли, усиление продукции пепсина, соляной кислоты в желудке, падение артериального давления, нарушение сердечного ритма и ряд других нарушений. Существующие на данный момент антигистаминные лекарственные средства подразделяют на препараты I и II поколения. По форме лекарственного средства антигистаминные подразделяются на препараты системного (пероральные и парентеральные формы) и местного (в виде средств для нанесения на кожу, а также интраназальных средств и капель для глаз).
Антигистаминные препараты I поколения
Основные представители I поколения АГ — хлоропирамин, клемастин, дифенгидрамин, ципрогептадин, гидроксизин, хифенадин, мебгидролин, диметинден, и др. Препараты могут оказывать блокирующее действие не только на Н1-рецепторы, но и на рецепторы других медиаторов, в т.ч. холинорецепторы и адренорецепторы, чем определяется различие их клинических эффектов. Некоторые лекарственные средства обладают антисеротониновой (пиперидины) и антидопаминовой (фенотиазины) активностью. Некоторые антигистаминные препараты обладают свойствами местных анестетиков, оказывают стабилизирующее действие на мембраны, хинидиноподобные эффекты на сердечную мышцу, что может проявляться уменьшением рефрактерной фазы и развитием желудочковой тахикардии [3, 4]. Антигистаминные препараты I поколения обладают липофильностью и способностью проникать через гематоэнцефалический барьер. Этим обусловлен их седативный эффект. Помимо этого, они могут затруднять отхождение вязкой мокроты из бронхов при наличии сопутствующих бронхолегочных заболеваний, в т. ч. бронхиальной астмы. Действие Н1-блокаторов I поколения кратковременное, в связи с чем необходимо неоднократное применение препаратов в течение суток, а развитие тахифилаксии диктует необходимость чередования разных групп препаратов каждые 2—3 недели.
Некоторые лекарственные средства обладают антисеротониновой (пиперидины) и антидопаминовой (фенотиазины) активностью. Некоторые антигистаминные препараты обладают свойствами местных анестетиков, оказывают стабилизирующее действие на мембраны, хинидиноподобные эффекты на сердечную мышцу, что может проявляться уменьшением рефрактерной фазы и развитием желудочковой тахикардии [3, 4]. Антигистаминные препараты I поколения обладают липофильностью и способностью проникать через гематоэнцефалический барьер. Этим обусловлен их седативный эффект. Помимо этого, они могут затруднять отхождение вязкой мокроты из бронхов при наличии сопутствующих бронхолегочных заболеваний, в т. ч. бронхиальной астмы. Действие Н1-блокаторов I поколения кратковременное, в связи с чем необходимо неоднократное применение препаратов в течение суток, а развитие тахифилаксии диктует необходимость чередования разных групп препаратов каждые 2—3 недели.
Фармакологические особенности этой группы препаратов хоть и ограничивают возможность их назначения, однако, несмотря на существующие побочные эффекты, антигистаминные препараты I поколения по-прежнему широко используются в аллергологической практике, в том числе их парентеральные формы (клемастин, хлоропирамин, дифенгидрамин). Показанием к парентеральному введению указанных средств являются острые аллергические реакции, требующие немедленного медикаментозного вмешательства. Парентеральный путь введения обеспечивает хорошую биодоступность и быстрое начало действия препарата. Это особенно актуально при лечении острых проявлений аллергии: крапивницы, отека Квинке, аллергического дерматита, острых тяжелых форм ринита/конъюнктивита, различных форм лекарственной, пищевой и инсектной аллергии и пр. Однако необходимо учитывать и тот факт, что при развитии острых аллергических реакций, сопровождающихся значимым снижением артериального давления (анафилактический шок), применение системных антигистаминных препаратов может усугубить гипотонию. Н1-блокаторы I поколения благодаря своей способности блокировать рецепторы других медиаторов также находят свое применение у пациентов с аллергическими заболеваниями, чаще аллергодерматозами, сопровождающимися выраженным зудом, у которых избирательное воздействие на Н1-рецепторы не приводит к формированию достаточного клинического ответа.
Показанием к парентеральному введению указанных средств являются острые аллергические реакции, требующие немедленного медикаментозного вмешательства. Парентеральный путь введения обеспечивает хорошую биодоступность и быстрое начало действия препарата. Это особенно актуально при лечении острых проявлений аллергии: крапивницы, отека Квинке, аллергического дерматита, острых тяжелых форм ринита/конъюнктивита, различных форм лекарственной, пищевой и инсектной аллергии и пр. Однако необходимо учитывать и тот факт, что при развитии острых аллергических реакций, сопровождающихся значимым снижением артериального давления (анафилактический шок), применение системных антигистаминных препаратов может усугубить гипотонию. Н1-блокаторы I поколения благодаря своей способности блокировать рецепторы других медиаторов также находят свое применение у пациентов с аллергическими заболеваниями, чаще аллергодерматозами, сопровождающимися выраженным зудом, у которых избирательное воздействие на Н1-рецепторы не приводит к формированию достаточного клинического ответа. В ряде случаев также возможно местное применение антигистаминных препаратов I поколения в составе местных лекарственных средств, в частности, в виде геля. Некоторые препараты (антазолин, диметинден и дифенгидрамин) применяются в виде интраназальных средств и средств для нанесения на кожу в качестве моно- или комбинированной терапии у пациентов с аллергическим ринитом и зудящими дерматозами.
В ряде случаев также возможно местное применение антигистаминных препаратов I поколения в составе местных лекарственных средств, в частности, в виде геля. Некоторые препараты (антазолин, диметинден и дифенгидрамин) применяются в виде интраназальных средств и средств для нанесения на кожу в качестве моно- или комбинированной терапии у пациентов с аллергическим ринитом и зудящими дерматозами.
Антигистаминные препараты II поколения
Антигистаминные препараты II поколения обладают избирательным действием на Н1-рецепторы и не блокируют рецепторы других медиаторов (в частности, ацетилхолина, катехоламинов, дофамина) и, вследствие этого, не дают многих побочных эффектов, свойственных Н1-антагонистам I поколения [3, 4]. По сравнению с антигистаминными препаратами I поколения они обладают значительно меньшей способностью проникать через гематоэнцефалический барьер и, соответственно, не вызывают или вызывают крайне незначительное седативное действие. В связи с более продолжительным действием антигистаминные препараты II поколения отличаются более удобным режимом приема и могут применяться один раз в сутки. Тахифилаксии при приеме этой группы препаратов также не возникает.
Тахифилаксии при приеме этой группы препаратов также не возникает.
Представители антигистаминных препаратов II поколения: акривастин, азеластин, эбастин, меквитазин, мизоластин, рупатадин, лоратадин, левоцетиризин, цетиризин, фексофенадин и дезлоратадин. Последние три из указанных препаратов некоторые специалисты относят к III поколению АГ препаратов, не имеющих тех побочных эффектов, которые присутствуют у АГ I и II поколения. Они являются фармакологически активными метаболитами Н1-блокаторов и могут подавлять как раннюю, так и позднюю фазу аллергического ответа [4].
Инструкция к некоторым антигистаминным препаратам II поколения также содержит информацию о предостережениях, связанных с приемом этих препаратов. Согласно рекомендациям Экспертов Европейской академии аллергологии и клинической иммунологии по безопасному применению антигистаминных средств следует избегать одновременного назначения препаратов, которые конкурируют с Н1-блокаторами, вовлекающие в метаболизм цитохром Р450. В конечной биотрансформация активных метаболитов препаратов II поколения изофермент CYP3А4 цитохрома Р450 не участвует, поэтому эта группа лекарственных средств характеризуются высоким профилем безопасности.
В конечной биотрансформация активных метаболитов препаратов II поколения изофермент CYP3А4 цитохрома Р450 не участвует, поэтому эта группа лекарственных средств характеризуются высоким профилем безопасности.
Топические антигистаминные препараты азеластин, левокабастин относятся к препаратам II поколения. Они обладают антигистаминным, мембраностабилизирующим и противовоспалительным действием. Для местных антигистаминных препаратов характерно достижение достаточно высоких локальных концентраций препарата при низкой дозе и быстрое начало терапевтического эффекта (через 15 мин после применения). Препараты могут использоваться как в монотерапии, так и в сочетанной терапии легких форм аллергического ринита/конъюнктивита.
Глюкокортикостероидные препараты
Глюкокортикостероиды (ГКС) воздействуют на разные фазы аллергического воспаления. Противовоспалительный эффект обусловлен целым комплексом воздействия на аллергическое воспаление: снижением проницаемости сосудистой стенки, торможением миграции лимфоцитов, эозинофилов, моноцитов в очаг воспаления. ГКС стабилизируют клеточные мембраны, тормозят пролиферативный процесс, повышают чувствительность к -агонистам, а также обладают иммуносупрессивным действием, проявляющимся в угнетении Т и В–лимфоцитов.
ГКС стабилизируют клеточные мембраны, тормозят пролиферативный процесс, повышают чувствительность к -агонистам, а также обладают иммуносупрессивным действием, проявляющимся в угнетении Т и В–лимфоцитов.
Глюкокортикостероиды применяются в разных формах — парентерально, перорально, а также в виде средств для ингаляционного введения, интраназально, конъюнктивально, местно с нанесением на кожные покровы.
Основные группы системных глюкокортикостероидов, использующиеся в клинической практике: гидрокортизоновая, преднизолоновая, триамцинолоновая, дексаметазоновая группы. По продолжительности угнетения адренокортикотропного гормона после разовой дозы глюкокортикостероиды подразделяются на препараты:
— короткого действия (24—36 часов) — гидрокортизон, преднизолон, преднизон, метилпреднизолон;
— промежуточного действия (до 48 часов) — триампцинолон;
— длительного действия (свыше 48 часов) — бетаметазон, дексаметазон.
Фармакокинетика глюкокортикостероидов представлена в таблице 1.
|
Таблица 1. Фармакокинетика глюкокортикостероидов |
|||||
| Препарат |
Эквивалентная доза, мг |
Время максимального содержания в плазме, ч |
Время наступления максимального эффекта, ч | Т ½ в плазме, ч | Т ½ глюкокортикоидной активности, ч |
|
Кортизон |
25 | 1—2 | 2—3 |
1 |
4—6 |
| Гидрокортизон | 20 | 1 | 2—8 | 1,5 | 8—12 |
| Преднизон | 5 | 1 | 2—8 | 1,5—3 | 12—36 |
| Преднизолон |
5 |
1—2 | 2—8 | 2,5—3 | 12—36 |
|
Метилпреднизолон |
4 |
1 | 2—6 | 2,5—3 | 12—36 |
| Триамцинолон |
0,75 |
1—2 | 6—24 |
3,5 |
36—72 |
| Дексаметазон | 0,5 | 1—2 | 6—24 | 3—4,5 | 36—72 |
Системные глюкокортикостероиды могут применяться для лечения обострения практически любого аллергического заболевания: бронхиальной астмы, атопического дерматита, крапивницы, отека Квинке, различных проявлени лекарственной, пищевой и инсектной аллергии. Однако при длительном применении ГКС возможно развитие ряда нежелательных явлений: нарушение электролитного обмена, повышение артериального давления, прибавка в весе, формирование остеопороза, миопатия, атрофия надпочечников, нарушение углеводного обмена и др. Поэтому, решение о применении системных глюкокортиостероидов должно быть обоснованным. В период терапии важен мониторинг состояния пациента, своевременная профилактика инфекционных, метаболических и других осложнений, связанных с применением указанной группы препаратов. Применение системных ГКС при аллергическом рините и конъюнктивита нежелательно в связи с большим количеством побочных эффектов, развивающихся вследствие их применения. Препараты могут быть назначены только при тяжелом течении аллергического ринита (конъюнктивита) коротким курсом и при полном отсутствии эффекта комплексной противоаллергической терапии, включающей топические ГКС.
Однако при длительном применении ГКС возможно развитие ряда нежелательных явлений: нарушение электролитного обмена, повышение артериального давления, прибавка в весе, формирование остеопороза, миопатия, атрофия надпочечников, нарушение углеводного обмена и др. Поэтому, решение о применении системных глюкокортиостероидов должно быть обоснованным. В период терапии важен мониторинг состояния пациента, своевременная профилактика инфекционных, метаболических и других осложнений, связанных с применением указанной группы препаратов. Применение системных ГКС при аллергическом рините и конъюнктивита нежелательно в связи с большим количеством побочных эффектов, развивающихся вследствие их применения. Препараты могут быть назначены только при тяжелом течении аллергического ринита (конъюнктивита) коротким курсом и при полном отсутствии эффекта комплексной противоаллергической терапии, включающей топические ГКС.
Ингаляционные глюкокортикостероиды (ИГКС) применяются для базисной терапии бронхиальной астмы средней и тяжелой степени, а также для купирования обострения бронхиальной астмы. К ингаляционным глюкокортикоидам относятся беклометазон, будесонид, флутиказон, мометазон, триамцинолон. Ингаляционные глюкокортикостероиды действуют в минимальных дозах, отличаются выраженным местным противовоспалительным действием, быстро инактивируются. ИГКС снижают бронхиальную реактивность и бронхиальную секрецию, потенциируют действие бета2-адреномиметиков, характеризуются низкой системной биодоступностью. Системное действие у ИГКС минимальное, однако, оно может иметь клиническое значение в случае длительного применения препаратов в высоких дозах. Как правило, в случае обострения бронхиальной астмы применяется будесонид в виде раствора для небулайзера (удобной и эффективной системы доставки препарата в легкие). При обострении бронхиальной астмы ИГКС можно сочетать с применением системных ГКС, особенно при существенной бронхиальной обструкции, затрудняющей попадание препарата в нижние отделы дыхательных путей. Однако при отсутствии показаний к дальнейшему введению системных ГКС, пациент переводится на ингаляционные препараты.
К ингаляционным глюкокортикоидам относятся беклометазон, будесонид, флутиказон, мометазон, триамцинолон. Ингаляционные глюкокортикостероиды действуют в минимальных дозах, отличаются выраженным местным противовоспалительным действием, быстро инактивируются. ИГКС снижают бронхиальную реактивность и бронхиальную секрецию, потенциируют действие бета2-адреномиметиков, характеризуются низкой системной биодоступностью. Системное действие у ИГКС минимальное, однако, оно может иметь клиническое значение в случае длительного применения препаратов в высоких дозах. Как правило, в случае обострения бронхиальной астмы применяется будесонид в виде раствора для небулайзера (удобной и эффективной системы доставки препарата в легкие). При обострении бронхиальной астмы ИГКС можно сочетать с применением системных ГКС, особенно при существенной бронхиальной обструкции, затрудняющей попадание препарата в нижние отделы дыхательных путей. Однако при отсутствии показаний к дальнейшему введению системных ГКС, пациент переводится на ингаляционные препараты. ИГКС нередко применяются в комбинации с другими ингаляционными препаратами (чаще, β2-агонистами), а также другими группами лекарственных средств, обладающих бронхолитической и противовоспалительной активностью. Интраназальные ГКС являются самыми эффективными средствами в лечении обострения аллергического ринита [5]. Основными представителями интраназальных ГКС являются беклометазона дипропионат, будесонид, мометазона фуроат, флутиказона пропионат. Препараты обладают высокой местной активностью, значительно уменьшают назальную обструкцию, секрецию желез слизистой оболочки и тканевой отек, снижают чувствительность к неспецифическим раздражителям и превосходят по своей эффективности интраназальные антигистаминные и кромогликаты. Системный эффект ГКС при интраназальном применении незначительный. Интраназальные ГКС нередко используются в комбинации с препаратами других фармакологических групп, в т.ч. в виде назальных спреев. ГКС могут применяться и при лечении аллергических конъюнктивитов в виде глазных капель или мазей (дексаметазон, гидрокортизон) коротким курсом с проведением мониторинга возможных осложнений, в т.
ИГКС нередко применяются в комбинации с другими ингаляционными препаратами (чаще, β2-агонистами), а также другими группами лекарственных средств, обладающих бронхолитической и противовоспалительной активностью. Интраназальные ГКС являются самыми эффективными средствами в лечении обострения аллергического ринита [5]. Основными представителями интраназальных ГКС являются беклометазона дипропионат, будесонид, мометазона фуроат, флутиказона пропионат. Препараты обладают высокой местной активностью, значительно уменьшают назальную обструкцию, секрецию желез слизистой оболочки и тканевой отек, снижают чувствительность к неспецифическим раздражителям и превосходят по своей эффективности интраназальные антигистаминные и кромогликаты. Системный эффект ГКС при интраназальном применении незначительный. Интраназальные ГКС нередко используются в комбинации с препаратами других фармакологических групп, в т.ч. в виде назальных спреев. ГКС могут применяться и при лечении аллергических конъюнктивитов в виде глазных капель или мазей (дексаметазон, гидрокортизон) коротким курсом с проведением мониторинга возможных осложнений, в т. ч. присоединения вторичной инфекции. Топические ГКС применяются активно для лечение аллергических дерматитов. Наружная терапия ГКС проводится в случаях обострения кожного процесса, сопровождающегося признаками выраженного воспаления, и при отсутствии достаточной эффективности применения препаратов других фармакологических групп. Существуют различные лекарственные формы топических ГКС — лосьоны, эмульсии, кремы, мази. Выбор формы препарата зависит от зоны нанесения, тяжести и характера поражения кожи. При назначении топических ГКС необходимо учитывать не только показания, но и противопоказания или ограничения к их назначению — местный инфекционный процесс любой этиологии, трофические изменения кожи и др. Также необходимо мониторировать побочные эффекты топических ГКС, которые могут носить как местный, так и системный характер. Топические кортикостероиды классифицируют по составу действующих веществ, а также по содержанию или отсутствию фтора, по силе противовоспалительной активности.
ч. присоединения вторичной инфекции. Топические ГКС применяются активно для лечение аллергических дерматитов. Наружная терапия ГКС проводится в случаях обострения кожного процесса, сопровождающегося признаками выраженного воспаления, и при отсутствии достаточной эффективности применения препаратов других фармакологических групп. Существуют различные лекарственные формы топических ГКС — лосьоны, эмульсии, кремы, мази. Выбор формы препарата зависит от зоны нанесения, тяжести и характера поражения кожи. При назначении топических ГКС необходимо учитывать не только показания, но и противопоказания или ограничения к их назначению — местный инфекционный процесс любой этиологии, трофические изменения кожи и др. Также необходимо мониторировать побочные эффекты топических ГКС, которые могут носить как местный, так и системный характер. Топические кортикостероиды классифицируют по составу действующих веществ, а также по содержанию или отсутствию фтора, по силе противовоспалительной активности. Выделяют фторированные (содержащие фтор) и нефторированные препараты. К нефторированным ГКС относятся: гидрокортизон и его производные, преднизолон и его производные, мометазона фуроат, мезипредон, метилпреднизолона ацепонат. К фторированным ГКС относят: дексаметазон, бетаметазон, флуметазон, флутиказон, триамцинолон, клобетазол. Нередко характер кожного процесса требует назначения комбинированного лечения. Комбинированные ГКС имеют в своем составе антибактериальные и/или противомикотические компоненты и применяются при наличии признаков вторичного инфицирования.
Выделяют фторированные (содержащие фтор) и нефторированные препараты. К нефторированным ГКС относятся: гидрокортизон и его производные, преднизолон и его производные, мометазона фуроат, мезипредон, метилпреднизолона ацепонат. К фторированным ГКС относят: дексаметазон, бетаметазон, флуметазон, флутиказон, триамцинолон, клобетазол. Нередко характер кожного процесса требует назначения комбинированного лечения. Комбинированные ГКС имеют в своем составе антибактериальные и/или противомикотические компоненты и применяются при наличии признаков вторичного инфицирования.
Другие противоаллергические лекарственные средства
Антигистаминные препараты, обладающие мембраностабилизирующим эффектом, тормозят как раннюю, так и позднюю фазы аллергической реакции, снижают гиперреактивность слизистых. Препараты показаны для профилактики и лечения обострения легких форм аллергических заболеваний. Представителем системных препаратов этой группы является кетотифен, который ингибирует выделение гистамина, лейкотриенов и медленно реагирующей субстанции анафилаксии из базофилов и нейтрофилов. Терапевтический эффект развивается медленно в течение 1—2 недель, препарат обладает седативным эффектом. Применение кетотифена возможно при легких формах аллергического ринита, конъюнктивита, атопического дерматита, крапивницы. Кромоглициевая кислота также применяется с целью купирования обострения легких форм бронхиальной астмы, аллергического ринита и конъюнктивита/кератоконъюнктивита, а также для лечения пищевой аллергии. Препарат стабилизирует мембраны тучных клеток, тормозит дегрануляцию и высвобождение из них гистамина, брадикинина, лейкотриенов, постагландинов и др. активных веществ, блокирует рецепторы, специфичные для медиаторов воспаления. Кромоглициевая кислота может использоваться ингаляционно при лечении бронхиальной астмы, применяться в интраназальной и конъюнктивальной формах, а также перорально (при наличии пищевой аллергии). Указанное лекарственное средство предназначено для лечения легких форм заболевания, однако являются безопасными и практически полностью лишено побочных эффектов.
Терапевтический эффект развивается медленно в течение 1—2 недель, препарат обладает седативным эффектом. Применение кетотифена возможно при легких формах аллергического ринита, конъюнктивита, атопического дерматита, крапивницы. Кромоглициевая кислота также применяется с целью купирования обострения легких форм бронхиальной астмы, аллергического ринита и конъюнктивита/кератоконъюнктивита, а также для лечения пищевой аллергии. Препарат стабилизирует мембраны тучных клеток, тормозит дегрануляцию и высвобождение из них гистамина, брадикинина, лейкотриенов, постагландинов и др. активных веществ, блокирует рецепторы, специфичные для медиаторов воспаления. Кромоглициевая кислота может использоваться ингаляционно при лечении бронхиальной астмы, применяться в интраназальной и конъюнктивальной формах, а также перорально (при наличии пищевой аллергии). Указанное лекарственное средство предназначено для лечения легких форм заболевания, однако являются безопасными и практически полностью лишено побочных эффектов. В качестве антихолинергического средства достаточно широко применяется ипратропиум бромид, который представляет собой М-холиноблокатор. Может применяться ингаляционно и интраназально. Подавляет бронхоконстрикцию при бронхиальной астме, уменьшает секрецию желез слизистой оболочки носа и бронхов. Практически не обладает системной антихолинергической активностью. Возможно как кратковременное, так и длительное применение ипратропиум бромида. Антагонисты лейкотриеновых рецепторов — группа препаратов, основными представителями которой являются монтелукаст и зафирлукаст. Действие антагонистов лейкотриеновых рецепторов состоит в угнетении лейкотриенов, участвующих в формировании воспалительных реакций у пациентов с бронхиальной астмой, в т.ч. у больных с непереносимостью нестероидных противовоспалительных препаратов, а также лечении сезонного и круглогодичного ринита. Препараты переносятся достаточно хорошо и могут использоваться длительно уже после прекращения симптоматики в качестве базисной терапии.
В качестве антихолинергического средства достаточно широко применяется ипратропиум бромид, который представляет собой М-холиноблокатор. Может применяться ингаляционно и интраназально. Подавляет бронхоконстрикцию при бронхиальной астме, уменьшает секрецию желез слизистой оболочки носа и бронхов. Практически не обладает системной антихолинергической активностью. Возможно как кратковременное, так и длительное применение ипратропиум бромида. Антагонисты лейкотриеновых рецепторов — группа препаратов, основными представителями которой являются монтелукаст и зафирлукаст. Действие антагонистов лейкотриеновых рецепторов состоит в угнетении лейкотриенов, участвующих в формировании воспалительных реакций у пациентов с бронхиальной астмой, в т.ч. у больных с непереносимостью нестероидных противовоспалительных препаратов, а также лечении сезонного и круглогодичного ринита. Препараты переносятся достаточно хорошо и могут использоваться длительно уже после прекращения симптоматики в качестве базисной терапии.
Заключение
Таким образом, лечение обострения аллергических заболеваний — это комплекс мероприятий, направленных на лечение аллергического воспаления и относящихся к медикаментозным и немедикаментозным методам воздействия. Применение тех или иных препаратов должно быть взвешенным и обоснованным. Противоаллергические лекарственные средства в случае необходимости необходимо сочетать с другими группами фармакологических средств, позволяющих усилить терапевтический эффект, а также купировать инфекционные, метаболические и иные осложнения аллергического заболевания. При проведении терапии должны учитываться степень тяжести обострения, эффективность и индивидуальная переносимость препаратов, наличие осложнений и сопутствующих заболеваний у пациента, физиологические особенности больного. Только комплексный подход к ведению пациентов с аллергическими заболеваниями может обеспечить наилучший эффект от проводимой терапии [6].
Литература
1. Аллергология. Клинические рекомендации. Под редакцией Р.М. Хаитова, Н.И.Ильиной. — Москва, издательская группа ГЭОТАР-Медиа, — 2006, — 227 с., тираж 3000 экз.,15 п.л.
Аллергология. Клинические рекомендации. Под редакцией Р.М. Хаитова, Н.И.Ильиной. — Москва, издательская группа ГЭОТАР-Медиа, — 2006, — 227 с., тираж 3000 экз.,15 п.л.
2. Курбачева О.М., Швец С.М. Аллергический ринит и беременность: возможности современной терапии. Эффективная фармакотерапия, 2013, 18: 74–80.
3. Гущин И. С. Аллергическое воспаление и его фармакологический контроль. — М.: Фармарус Принт, 1998. — 251 с.
4. Гущин И.С., Курбачева О.М. Лечение аллергического круглогодичного ринита антигистаминными препаратами. Лечащий врач, 2004, 8: 20-23.
5. Российская ассоциация аллергологов и клинических иммунологов. Федеральные клинические рекомендации по диагностике и лечению аллергического ринита, 2013 г.
6. Аллергология и иммунология. Национальное руководство. АСМОК. РААКИ. «Геотар-Медиа». — 2009. — С. 245-250.
Препараты при отеке Квинке: таблетки, укол, мазь
Опухание лица, непрерывный кашель, покраснение и зуд – все это симптомы, характерны для аллергии, которая может развиваться при контакте с раздражителем. Данное патологическое состояние требует немедленного медицинского вмешательства. Несвоевременно оказанная первая помощь может стать причиной инвалидности и даже летального исхода. Многие врачи рекомендуют применять Дексаметазон при отеке Квинке для устранения неприятных признаков патологии, но порой одного препарата недостаточно и необходима комбинированная терапия.
Данное патологическое состояние требует немедленного медицинского вмешательства. Несвоевременно оказанная первая помощь может стать причиной инвалидности и даже летального исхода. Многие врачи рекомендуют применять Дексаметазон при отеке Квинке для устранения неприятных признаков патологии, но порой одного препарата недостаточно и необходима комбинированная терапия.
Положительное действие лекарства обусловлено его составом. Препарат Дексаметазон при отеке Квинке дает противовоспалительный, антишоковый и противоаллергический эффект. Он содержит глюкокортикостероид − гормон, добытый искусственным путем. Главный компонент лекарства − дексаметазон натрия фосфат снижает активность клеток иммунитета, соответственно притупляет проявление симптомов. Врачи назначают Дексаметазон при всех видах аллергических реакций.Эффективно это лекарство от отека Квинке на лице, при опухании мозговой оболочки, при асфиксии, астматическом бронхите и астме.
В аптеках препарат предложен в форме ампул. Чтобы ввести средство в организм делают укол при отеке Квинке внутрисуставно, в мышцу или в вену. Людям с астмой рекомендовано вдыхание испарений препарата через небулайзер. Средство отлично переноситься пациентами всех возрастных групп, единственным противопоказанием выступает личная непереносимость вещества − дексаметазона.
Чтобы ввести средство в организм делают укол при отеке Квинке внутрисуставно, в мышцу или в вену. Людям с астмой рекомендовано вдыхание испарений препарата через небулайзер. Средство отлично переноситься пациентами всех возрастных групп, единственным противопоказанием выступает личная непереносимость вещества − дексаметазона.
Эффективные противоаллергические лекарства
Врачи, помимо Дексаметазона, назначают и другие препараты при отеке Квинке. Большинство из медикаментов направлено на купирование проявлений аллергической реакции, а также на притуплениеиммунных сил организма.
Хорошо себя зарекомендовал Преднизолон при отеке Квинке. Он оказывает быстрое противошоковое действие,стимулирует функциональность костного мозга, увеличивая в крови содержание эритроцитов и тромбоцитов. Подобное воздействие позволяет понизить проницаемость капилляров и предупредить выливание лимфы в рядом находящиеся ткани. Именно отток жидкой части крови в ткани и провоцирует опухоль.
Дозировка Преднизолона при отеке Квинке определяется врачом в зависимости от возраста, веса пациента, а также характера проявления аллергии. Способы введения активного вещества тоже решаются индивидуально. В случаях патологии гортани или лица гормональные средства, такие как Гидрокортизон и Преднизолон колят при отеке Квинке под язык. Там локализуются вены, которые позволяют быстро распространить лекарство и снять симптоматику.
Способы введения активного вещества тоже решаются индивидуально. В случаях патологии гортани или лица гормональные средства, такие как Гидрокортизон и Преднизолон колят при отеке Квинке под язык. Там локализуются вены, которые позволяют быстро распространить лекарство и снять симптоматику.
Гидрокортизон, Преднизолон и Дексаметазон предложены также в виде таблеток, но эта форма лекарства усваивается организмом длительное время. В случае со стремительным развитием реакции и шоком, нужно действовать как можно быстрее.
Иногда для терапии врачи назначают препараты при отеке Квинке на основе андрогенов (естественных мужских гормонов): Аназол, Станазол, Метилтестестерон. Они положительно сказываются на состоянии аллергика, но противопоказаны для употребления детям и беременным женщинам.
Десенсибилизирующие лекарства
Десенсибилизирующие таблетки от отека Квинке необходимы для того, чтобы ткани и клетки аллергика учились противостоять патогену без выделения гистамина. Самыми безопасными лекарствами врачи считают такие антигистаминные препараты при отеке Квинке:
Самыми безопасными лекарствами врачи считают такие антигистаминные препараты при отеке Квинке:
- Супрастин −обладает противозудным, седативным и снотворным действием. Супрастин при отеке Квинке снижает выраженность аллергической реакции,
- Тавегил −уменьшает проницаемость сосудов, тормозит процесс формирования опухоли,
- Пипольфен − подходит для использования при шоковом состоянии и опухании гортани в качестве первой медицинской помощи,
- Зиртрек − блокирует высвобождение гистамина. Зиртек при отеке Квинке снижает спазмы гладкой мускулатуры, устраняет кожные реакции и кашель при астматическом бронхите. Зиртек от отека Квинке может использоваться в терапии взрослых аллергиков и маленьких пациентов,
- Димедрол − угнетает гистаминные рецепторы, предупреждает эпилептические припадки, судороги, обладает расслабляющим и снотворным действием.
В терапии маленьких гиперчувствительных пациентов рекомендовано использовать Лоратадин при отеке Квинке, а также Фенистил, Цитиризин и Эриус. Они обладают минимальным токсическим действием и практически не имеют противопоказаний. Эти же лекарства при отеке Квинке можно использовать женщинам в период беременности и лактации.
Они обладают минимальным токсическим действием и практически не имеют противопоказаний. Эти же лекарства при отеке Квинке можно использовать женщинам в период беременности и лактации.
Купирование симптомов
Для лечения отека Квинке назначают не только препараты, действие которых направлено на снижение активности гистамина. Часто пациентов больше пугает симптоматика реакции, нежели ее развитие в целом и продолжительность. В процессе формирования патологии больной может испытывать болезненные ощущения и спазмы, отмечать на коже зуд, воспаление и сыпь. Для купирования этих признаков назначают препараты:
- спазмолитики (Но-шпа, Папазол, Риабал),
- обезболивающие лекарства (Парацетамол, Ибупрофен, Анальгин, Нимесулид),
- противовоспалительные (Диклоберил, Найз, Кеторол),
- против отечные (Фуросемид, Веноплант, Верошпирон),
- противозудные (Адвантан, Лотарен, Нафтадерм).
Для местного применения могут назначать мази от отека Квинке, такие как Элоком, Незулин, Псило-бальзам, Мезодерм, Целестодерм и др.
Если отмечается тошнота и рвота вполне вероятно, что раздражитель попал в организм с пищей. Соответственно следует уменьшить действие токсина на внутренние органы. Добиться этого можно применяя сорбенты, такие как Сорбекс, белый уголь, Полисорб и Энтерос-гель.
Зачем больному вводят Адреналин?
Очень часто людям, склонным к рецидивирующим аллергическим состояниям рекомендуют носить всегда с собой ампулку Адреналина. Этот препарат водят регулярно, если есть угроза для жизни. Обычно делают инъекцию в верхнюю часть бедра, так вещество быстрее попадает в кровь и наступает требуемый эффект.
Вводят Адреналин при отеке Квинке с целью снижения выработки гистамина. Вещество купирует аллергию еще на раннем этапе ее развития. У пациента стремительно повышается артериальное давление, соответственно активируются скрытые резервы и организм направляет свои силы на устранение шокового состояния, нормализацию работы всех органов и систем.Адреналин при отеке Квинке — это как разряд тока для человека, находящегося в коме. Все внутренние органы получают толчок для «перезагрузки».
Все внутренние органы получают толчок для «перезагрузки».
Дозировка препарата для купирования патологического синдрома − стандартная. Сегодня существуют даже специальные приспособления для того, чтобы больные могли сами себе оказывать первую помощь, вводя Адреналин внутримышечно.
Аллергия стала постоянной спутницей жизни огромного количества людей в современном обществе. Поэтому вместо того, чтобы искать причины этой неприятной ситуации, важно проходить профилактику шоковых состояний и учиться жить с гиперчувствительностью. Если вы будете знать, что принимать при отеке Квинке и как предоставлять первую помощь, то сможете вести нормальную жизнь без ограничений и пребывания в условиях стационара. Использование народных методик лечения при такой серьезной патологии, как синдром Квинке не только опасно, но и неразумно. Настойки и травяные отвары могут улучшить действие синтетических препаратов, но в качестве основного средства для терапии недопустимы. Устранять аллергию можно исключительно традиционными препаратами, назначенными квалифицированным врачом.
Крапивница, отек Квинке…
21.09.2019Крапивница, отек Квинке
Крапивница и ангионевротический отек (отек Квинке) широко распространены. Статистика утверждает, что их испытывал хотя бы один раз в жизни каждый пятый человек на Земле. Крапивница и отек Квинке могут встречаться порознь и сочетаться.
У нас есть товары, помогающие справиться и предотвратить это заболевание. Интернет-магазин «Доктор Аль» обладает огромной базой антиаллергенных и антиастматических товаров. Наш онлайн магазин работает с 2000 года и мы за это время помогли очень многим людям, страдающим от аллергии и астмы. Наши приборы проходят тщательное тестирование и обладают высокой эффективностью. Убедитесь в этом сами, ознакомившись с нашим каталогом товаров для здоровья, интернет-магазин «Доктор Аль» ждет своих покупателей. Если Вы в чем-то сомневаетесь или не можете определиться с выбором, наши высококвалифицированные специалисты-врачи всегда ответят на Ваш вопрос. Вы можете заказать обратный звонок (внизу экрана) и мы сразу Вам перезвоним или же свяжитесь с нами по телефону 8 (495) 950-53-53. Наши эксперты на связи.
Если Вы в чем-то сомневаетесь или не можете определиться с выбором, наши высококвалифицированные специалисты-врачи всегда ответят на Ваш вопрос. Вы можете заказать обратный звонок (внизу экрана) и мы сразу Вам перезвоним или же свяжитесь с нами по телефону 8 (495) 950-53-53. Наши эксперты на связи.
Крапивница
Свое название это заболевание получило за свои характерные проявления: волдыри, как будто оставшиеся после ожога крапивой. Эти волдыри сопровождаются покраснением, отеком, кожным зудом. Возможно повышение температуры тела которое можно узнать с помощью термометров, слабость, недомогание, головная боль.
Крапивница может быть локализованной и генерализованной (т.е. поражать определенный участок кожи или распространяться по всему телу), острой и хронической. Это общее название группы заболеваний со сходными проявлениями, но разными механизмами развития. Она может быть симптомом самых разных заболеваний.
В зависимости от причины возникновения, говорят о физической (тепло, холод, давление, солнечная радиация), дермографической (или механической — в месте раздражения кожи, например, расчесами), лекарственную, пыльцевую и т. д. Когда причину найти не удается, крапивницу именуют идиопатической.
д. Когда причину найти не удается, крапивницу именуют идиопатической.
Но чаще всего используется классификация крапивницы по механизму развития (патогенезу): на аллергическую (пыльцевую, пищевую и т.д.) и неаллергическую. Выделяют наследственные формы (синдром Шнитлера, пигментная крапивница и системный мастоцитоз, дефицит одного из компонентов системы комплемента — С3b-активатора и др.).
Острая крапивница чаще всего имеет аллергическую природу, при хронической рецидивирующей редко выявляется связь с причинно-значимым аллергеном, и вообще установить какую-либо причину удается у 5-30% больных.
Отек Квинке
Ангионевротический отек, иначе отек Квинке или гигантская крапивница, отличается от обычной крапивницы лишь глубиной поражения кожи. Впервые он был описан в 1882 г. Отек значительных размеров чаще всего появляется в местах с рыхлой клетчаткой — на губах, веках, щеках, слизистой рта, половых органов. В типичных случаях он бесследно исчезает через несколько часов (до 2-3 суток). Больные со среднетяжелыми и тяжелыми реакциями должны быть госпитализированы.
Больные со среднетяжелыми и тяжелыми реакциями должны быть госпитализированы.
Выделяется особая форма: наследственный ангионевротический отек, связанный с недостаточностью С1-ингибитора. Чаще болеют мужчины, характерен семейный анамнез, развитие отека провоцируется микротравмами и стрессом. Часто развивается отек гортани. Лечится заболевание по другим принципам. Перед хирургическими вмешательствами необходимо принимать профилактические меры.
Причины возникновения
Острая крапивница часто является симптомом пищевой и лекарственной аллергии. Из пищевых продуктов наибольшее значение имеют яйца, арахис, соя, свинина, молоко, пшеница, говядина, курица, рыба, орехи, морепродукты. Кроме того, следует учитывать возможность перекрестных аллергических реакций пищевых продуктов с пыльцевыми аллергенами и латексным аллергеном. Из лекарств могут быть антибиотики (например, пенициллин), сульфаниламидные препараты, аспирин и другие нестероидные противовоспалительные препараты, кодеин. Аспирин достаточно редко вызывает крапивницу, но часто при хронической крапивнице высыпание волдырей усиливается при приеме аспирина. Те же пациенты нередко принимают аспирин, когда высыпаний нет.
Аспирин достаточно редко вызывает крапивницу, но часто при хронической крапивнице высыпание волдырей усиливается при приеме аспирина. Те же пациенты нередко принимают аспирин, когда высыпаний нет.
С возникновением крапивницы может быть связано также введение препаратов крови, рентгеноконтрастных веществ. Для отека Квинке характерна связь с приемом ингибиторов ангиотензинпревращающего фермента (распространенная группа препаратов для лечения сердечной недостаточности и гипертонической болезни; к ним относятся такие известные препараты, как капотен, ренитек, энап, престариум и др.), причем частой локализацией бывают язык и губы. Частой причиной крапивницы бывают ужаления перепончатокрылых насекомых.
Одной из причин крапивницы могут быть вирусные и паразитарные инфекции, в том числе лямблиоз, гепатит, глистные инвазии. У части больных крапивницей имеются проблемы со щитовидной железой. Не исключена связь хронической рецидивирующей крапивницы с особым микроорганизмом — Helicobacter pillory — который обитает в желудке и 12-перстной кишке при хроническом гастрите и язвенной болезни. Неспецифические провоцирующие факторы — лихорадка, употребление алкоголя, физическая нагрузка, тепло, эмоциональные факторы, менструации.
Неспецифические провоцирующие факторы — лихорадка, употребление алкоголя, физическая нагрузка, тепло, эмоциональные факторы, менструации.
Одним из важнейших медиаторов, ответственных за развитие клинических симптомов крапивницы, является гистамин. При введении гистамина внутрикожно возникает типичный элемент — волдырь. Зуд, отек кожи и слизистых, появление волдырей — типичные проявления его действия. Именно поэтому при лечении крапивницы так важны антигистаминные препараты. В развитии крапивницы играют роль и другие медиаторы. Основные задействованные типы клеток — лимфоциты, тучные клетки и эозинофилы.
Тепловая крапивница. Холодовая крапивница. Пигментная крапивница.
Холинергическая крапивница — одна из часто встречающихся форм заболевания. Она проявляется мелкоточечной, сильно зудящей волдырной сыпью на верхней части груди и шеи (может затем стать генерализованной), характеризуются выраженной краснотой. При этой форме крапивницы одного вида волдырей достаточно для установления диагноза. Часто появление такой реакции провоцирует горячий душ, физические упражнения и эмоциональные переживания.
Часто появление такой реакции провоцирует горячий душ, физические упражнения и эмоциональные переживания.
У пациентов с приобретенной холодовой крапивницей пребывание в холодной воде может вызвать массивное высвобождение медиаторов. При этом у больного не исключено развитие шока, в результате которого он может утонуть. Но чаще всего волдыри при холодовой крапивнице появляются не в момент действия холода, а отсрочено.
Пигментная крапивница — частое проявление мастоцитоза (от слова «мастоцит» — тучная клетка). На коже больного появляются множественные пятна желтовато-коричневого или красновато-коричневого цвета, содержащие повышенное количество тучных клеток. Щелчок по коже в области пигментного пятна вызывает образование волдыря в пределах участка пигментации. При расчесывании пятна они также становятся волдырями.
Диагностика
Как и при всех заболеваниях, врач собирает анамнез (выясняет все, что уже случилось с Вами), далее осмотр и обязательные методы обследования, в том числе реакция Вассермана; рентген, аллергологические и иммунологические методы.
Обследование проводится тщательно, т.к. необходимо исключить самые различные заболевания. В том случае, когда анамнез или осмотр подразумевает возможность какой-либо инфекции, проводятся соответствующие исследования. Кроме того, упорное рецидивирование крапивницы может быть связано с наличием очагов инфекции: хронического тонзиллита, кариеса, холецистита, остеомиелита, патологией желудочно-кишечного тракта, эндокринными заболеваниями (сахарный диабет, заболевания щитовидной железы, дисфункция яичников), сывороточной болезнью, аутоиммунными заболеваниями, диспротеинемиями, саркоидозом и даже новообразованиями.
Возможности кожных проб при крапивнице ограничены из-за частых ложно-положительных и ложноотрицательных результатов. Дермографизм — противопоказание для кожного тестирования, т.к. приводит к ложноположительным реакциям. Характер аллергологического обследования определяется клинической ситуацией.
Причиной возникновения крапивницы и отека Квинке могут быть лекарственные препараты. За исключением пенициллина, чужеродных сывороток и инсулина, надежных тестов нет, и единственным надежным способом оценки причинной значимости лекарства служит его отмена.
За исключением пенициллина, чужеродных сывороток и инсулина, надежных тестов нет, и единственным надежным способом оценки причинной значимости лекарства служит его отмена.
Простейший метод диагностики холодовой крапивницы — холодовая проба. К предплечью на 4 минуты прикладывают кубик льда, затем 10 минут наблюдают. При положительном тесте образует типичный волдырь.
Холинергическую крапивницу можно подтвердить с помощью метахолинового кожного теста или погружением в горячую ванну (42о).
Вибрационную подтверждают, прикладывая к предплечью больного лабораторный вибратор на 4 минуты.
Дифференциальный диагноз: с чем можно спутать крапивницу и как отличить?
Достаточно сложно отличить хроническую крапивницу от уртикарного васкулита. Для этого нужно гистологическое исследование (изучение образца тканей). Сами волдыри более стойкие и оставляют после себя участок кровоизлияния. Часто васкулит сопровождается болью в суставах и мышщах, увеличением СОЭ, возможно поражение почек.
Основным отличительным признаком многоформной эритемы является полиморфность высыпаний (пятна, папулы, элементы-«мишени», пузыри и иногда волдыри). Они чаще бывают на конечностях и сопровождаются скорее жжением, чем зудом. Но для уточнения может понадобиться биопсия (взятие образца тканей).
Буллезный пемфингоид только при ограниченной форме и в ранней стадии может напоминать крапивницу, а потом образуются пузыри-буллы. В спорных случаях может помочь биопсия.
То же самое можно сказать и о герпетиформном дерматите: только ранние высыпания напоминают крапивницу. Они полиморфны, сопровождаются сильным зудом, сгруппированы и эволюционируют в везикулы и пустулы, а затем и вторичные элементы.
При хронической крапивнице во многих случаях (в общем, за исключением физической крапивницы и небольшого процента аллергической) обследование заканчивается диагнозом: идиопатическая крапивница, т.е. обследование не приводит к установлению причины крапивницы.
Опасны ли крапивница и отек Квинке?
Локальную крапивницу относят к легким аллергическим реакциям, генерализованную крапивницу и отек Квинке — к среднетяжелым и тяжелым. Особенно опасен отек в области лица, шеи, полости рта и гортани, поскольку это может привести к затруднению дыхания и даже смерти от удушья (при отсутствии должного и своевременного лечения).
По данным английского исследователя R. Сhampion, у 20% больных хронической крапивницей заболевание длится до 10 лет., спонтанная ремиссия хронической крапивницы наступает: у 50% больных в течение шести месяцев с момента дебюта заболевания; у 20% больных в течение трех лет с момента дебюта заболевания; у 20% в течение пяти лет с момента дебюта заболевания; у 2% в течение 25 лет с момента дебюта заболевания. Причем у каждого второго больного хронической крапивницей со спонтанной ремиссией в дальнейшем развивается по меньшей мере один рецидив заболевания.
Лечение.
Обучение пациента и устранение причинных и провоцирующих факторов.
Прежде всего, больной должен быть информирован о своем заболевании. Созданы образовательные программы, аллергошколы. Все пациенты должны иметь при себе «паспорт аллергологического больного» с указанием диагноза и рекомендаций.
Все больные крапивницей и отеком Квинке должны избегать приема аспирина и других нестероидных противовоспалительных средств, т.к. они вызывают обострение уже имеющейся крапивницы в 50% случаев. Также следует исключить прием ингибиторов ангиотензинпревращающего фермента (капотен, энап, престариум и др.), т.к. велика вероятность развития отека Квинке. Необходимо избегать неспецифических триггеров, таких как горячая ванна или прием алкоголя.
Следует исключить причинный фактор и возможные триггеры, если их удалось установить. О способах устранения контакта с выявленными аллергенами при бытовой, эпидермальной, пыльцевой, клещевой, пищевой, профессиональной, лекарственной, инсектной, грибковой аллергии см. статьи на сайте. Если удалось установить «виновный» пищевой продукт, то он исключается из диеты. Но нередко при крапивнице имеют место псевдоаллергические реакции на естественные компоненты пищи и пищевые добавки. В таких случаях назначается диета с низким содержанием естественных и искусственных гистаминлибераторов (веществ, способствующих высвобождению гистамина). Если при острой крапивнице устранение причинного фактора приводит к разрешению проявлений через 24-48 часов, то при хронической крапивнице для улучшения состояния требуется 2-3 недели. Подробнее о диетах см. «Реакции на пищу и пищевая аллергия».
Если удалось установить «виновный» пищевой продукт, то он исключается из диеты. Но нередко при крапивнице имеют место псевдоаллергические реакции на естественные компоненты пищи и пищевые добавки. В таких случаях назначается диета с низким содержанием естественных и искусственных гистаминлибераторов (веществ, способствующих высвобождению гистамина). Если при острой крапивнице устранение причинного фактора приводит к разрешению проявлений через 24-48 часов, то при хронической крапивнице для улучшения состояния требуется 2-3 недели. Подробнее о диетах см. «Реакции на пищу и пищевая аллергия».
Следует избегать и таких факторов, как инсоляция при солнечной крапивнице (использование фотозащитных кремов с высоким уровнем защиты), ношения тяжестей при крапивнице, связанной с воздействием физических факторов, купания в холодной воде при холодовой крапивнице и т.д.
Пациентам с наследственным ангионевротическим отеком следует соблюдать особую осторожность при удалении зубов, наркозе с интубацией.
Медикаментозное лечение.
При острой крапивнице и отеке Квинке на первое место выходят мероприятия по быстрому купированию симптомов. Легкие реакции можно лечить только с использование антигистаминных препаратов. Быстрое развитие действия современных антигистаминных препаратов позволяет применять препараты второго и третьего поколения (о них чуть ниже), лишенных седативного эффекта. Нередко положительный эффект оказывают очистительные клизмы и применение энтеросорбентов (активированный уголь, полифепам, альгисорб, энтерос-гель, смекта).
Среднетяжелые и тяжелые реакции требуют применения помимо антигистаминных препаратов адреналина (0,1% раствор по 0,1-0,3 внутримышечно) для быстрого купирования симптомов, преднизолон внутривенно. Среднетяжелые и тяжелые аллергические реакции — показание к госпитализации, а затруднение дыхания, вызванное нарушением проходимости дыхательных путей — прямое показание.
Базисная терапия хронической крапивницы проводится антигистаминными препаратами. Клиническая эффективность их гораздо выше, когда они применяются профилактически, чем в момент интенсивных высыпаний. При этом применение «старых» антигистаминных препаратов ограничено: они вызывают сонливость, сухость во рту, угнетение нервной системы, сравнимое с действием алкоголя. Кроме того, их надо принимать несколько раз в день, а сам препарат менять каждые несколько дней, иначе эффект его исчезнет. Поэтому предпочтение отдается препаратам второго (такие как кестин, кларитин, семпрекс, зиртек и др.) и особенно третьего поколения (телфаст, эриус). При лечении хронической крапивницы часто требуются большие дозы, чем используются при лечении поллиноза. Привыкания, тахифилаксии, сонливости эти препараты не вызывают.
Клиническая эффективность их гораздо выше, когда они применяются профилактически, чем в момент интенсивных высыпаний. При этом применение «старых» антигистаминных препаратов ограничено: они вызывают сонливость, сухость во рту, угнетение нервной системы, сравнимое с действием алкоголя. Кроме того, их надо принимать несколько раз в день, а сам препарат менять каждые несколько дней, иначе эффект его исчезнет. Поэтому предпочтение отдается препаратам второго (такие как кестин, кларитин, семпрекс, зиртек и др.) и особенно третьего поколения (телфаст, эриус). При лечении хронической крапивницы часто требуются большие дозы, чем используются при лечении поллиноза. Привыкания, тахифилаксии, сонливости эти препараты не вызывают.
Противогистаминные препараты с мембраностабилизирующим действием (кетотифен) иногда применяются при псевдоаллергических механизмах развития заболевания.
При тяжелом течении и полной неэффективности антигистаминных применяются системные кортикостероиды короткими курсами (5-7 дней до достижения ремиссии с постепенным снижением дозы). Длительное назначение не рекомендуется из-за риска побочных эффектов, а также из-за возможности обострения при отмене гормонального лечения.
Длительное назначение не рекомендуется из-за риска побочных эффектов, а также из-за возможности обострения при отмене гормонального лечения.
При тяжелом течении аутоиммунной хронической крапивницы требуется специальное лечение (плазмаферез, в/в иммуноглобулин, циклоспорин А), которое должно проводиться в условиях специализированных центров.
Принципиально иначе лечат наследственный ангионевротический отек. В остром периоде вводят свежую или свежезамороженную плазмы (замещение дефицита С1-ингибитора), внутривенно аминокапроновую кислоту. Также можно вводить даназол 800 мг/сут (или станозолол 12 мг/сут). При отеке в области лица и шеи дополнительно вводятся внутривенно фуросемид (лазикс), дексаметазон.
Лечение основного и сопутствующих заболеваний
Санация хронических очагов инфекции, лечение дисбактериоза, эндокринных и других заболеваний. Всех, о которых шла речь выше, в разделах причины и диагностика.
Предостережение
В рекомендации по лечению крапивницы включены методы, эффективность и безопасность которых доказана. В то же время рекламируется немало методов нетрадиционной медицины для лечения крапивницы и различных форм пищевой аллергии. Независимо от активности и степени самоуверенности их приверженцев, эффективность их не доказана или не выдержала проверки объективными методами. Но самое главное, некоторые из этих методов небезопасны для пациента. Если Вы все-таки намерены попробовать лечение нетрадиционным методом, по крайней мере, обсудите с Вашим врачом степень его безопасности.
В то же время рекламируется немало методов нетрадиционной медицины для лечения крапивницы и различных форм пищевой аллергии. Независимо от активности и степени самоуверенности их приверженцев, эффективность их не доказана или не выдержала проверки объективными методами. Но самое главное, некоторые из этих методов небезопасны для пациента. Если Вы все-таки намерены попробовать лечение нетрадиционным методом, по крайней мере, обсудите с Вашим врачом степень его безопасности.
Ознакомиться с перечнем товаров для аллергиков и астматиков Вы можете в нашем каталоге антиаллергенных товаров
При подготовке материала использована литература:1. Лусс Л.В. Хроническая рецидивирующая крапивница, проблемы диагностики и терапии. Роль антигистаминных препаратов в лечении крапивницы. Русский Медицинский Журнал 2003, том 11, №5
2. Л. А. Горячкина, Н. М. Ненашева, Е. Ю. Борзова. Крапивница. Лечащий врач, 2003, №9.
3. Паттерсон Р., Грэммер Л.К., Гринберг П.
 А. Аллергические болезни: диагностика и лечение. Перевод с английского под ред. акад. РАМН Чучалина А.Г., 252-273
А. Аллергические болезни: диагностика и лечение. Перевод с английского под ред. акад. РАМН Чучалина А.Г., 252-273Ангионевротический отек
Практически каждый врач в своей практике встречается с так называемым ангионевротическим отеком, или отеком Квинке. Врачи нашего стационара так же не являются исключением: достаточно часто в стационарное отделение СМП поступают пациенты с указанной нозологией.
Впервые данное заболевания описано в 1586г. Немецкий врач Генрих Квинке подробно описал его в 1882г. В связи с этим в различной медицинской литературе мы часто можем встретить данное заболевание под названием «отек Квинке».
Ангионевротический отёк, или отёк Квинке — реакция на воздействие различных биологических и химических факторов.
Эпидемиология
Всемирная организации по аллергии (The World Allergy Organization) отмечает, что крапивница и ангионевротический отек поражают до 20% населения. По ее оценкам, примерно 10-20% населения могут испытывать по крайней мере 1 эпизод ангионевротического отека в течение жизни.
Около 40-50% пациентов с хронической крапивницей имеют в анамнезе эпизоды ангионевротического отека и около 10% имеют только клинику ангионевротического отека. Около 1% населения страдают хронической крапивницей. Учитывая эти данные, до 0, 5% населения страдают хроническим или рецидивирующим ангионевротическим отеком.
Патофизиология
Ангионевротический отек – это отек глубоких слоев дермы и подкожных тканей вследствие повышения проницаемости сосудов и излияния внутрисосудистой жидкости.
Известными медиаторами повышения проницаемости сосудов являются:
- производные тучных клеток (например, гистамин, лейкотриены, простагландины)
- Брадикинин и медиаторы, производные системы комплемента
Медиаторы, производные тучных клеток имеют тенденцию поражать также и поверхностный слой подкожной ткани. Здесь медиаторы вызывают крапивницу и зуд, которыми обычно сопровождается опосредованный тучными клетками ангионевротический отек. При ангионевротическом отеке, опосредованном брадикидином, крапивница и зуд отсутствуют.
При ангионевротическом отеке, опосредованном брадикидином, крапивница и зуд отсутствуют.
Ангионевротический отек может быть острого и хронического типа (сохраняться более 6 недель). Это заболевание имеет наследственную и приобретенную формы.
Этиология
Более 40% хронического ангионевротического отека является идиопатическим. Иногда причиной является хроническое употребление не вызывающих опасений лекарственных препаратов или иных синтетических продуктов (например, пенициллина в молоке, лекарств безрецептурного отпуска, консервантов, других пищевых добавок). Травма, хирургические процедуры и стресс являются частыми неспецифическими триггерами для приступов ангионевротического отека.
Частыми причинами ангионевротического отека являются:
— Гиперчувствительность (например, продукты питания, лекарства (чаще всего ингибиторов АПФ и НПВС) или укусы насекомых). Ингибиторы АПФ являются в 30% случаев причиной острого ангионевротического отека, наблюдаемого в отделениях скорой помощи. Ингибиторы АПФ непосредственно повышают уровни брадикинина. Крапивницы в данном случае не возникает. Ангионевротический отек может возникнуть вскоре после начала приема препаратов или через годы после начала терапии.
Ингибиторы АПФ непосредственно повышают уровни брадикинина. Крапивницы в данном случае не возникает. Ангионевротический отек может возникнуть вскоре после начала приема препаратов или через годы после начала терапии.
— Физические стимулы (например, холод или вибрации)
— Аутоиммунное заболевание или инфекция
— Наследственные факторы
Демографические данные
Ангионевротический отек встречается во всех возрастных группах. У лиц, предрасположенных к ангионевротическому отеку, имеет место тенденция увеличения частоты приступов после подросткового периода, причем пик заболеваемости приходится на третье десятилетие жизни. Наблюдается постоянное увеличение частоты госпитализаций по поводу ангионевротического отека (3% в год). Уровень госпитализации наиболее высок среди лиц в возрасте 65 лет и старше.
Аллергические реакции на пищу чаще встречаются у детей. Средний возраст ангионевротического отека, вызванного ингибиторами АПФ, составляет 60 лет.
Хронический идиопатический ангионевротический отек чаще встречается у женщин, чем у мужчин. Другие виды ангионевротического отека не демонстрируют сильного полового перевеса.
Никакой специфической расовой предрасположенности к ангионевротическому отеку не существует. Тем не менее, люди негроидной расы более «чувствительны» к ингибиторам АПФ.
Прогноз
Прогноз для пациентов с ангионевротическим отеком зависит от этиологии и определяется следующим образом:
Ангионевротический отек с идентифицируемыми причинами — если триггер (ы) можно определить и избежать, ангионевротический отек можно предотвратить.
Ангионевротический отек без идентифицируемых причин клинически протекает чрезвычайно изменчиво. Течение — от легкого до тяжелого, продолжительность — от нескольких дней до многих лет; ответ на традиционное лечение менее непредсказуем. При хроническом варианте течения заболевания часто необходимо пожизненное медикаментозное лечение.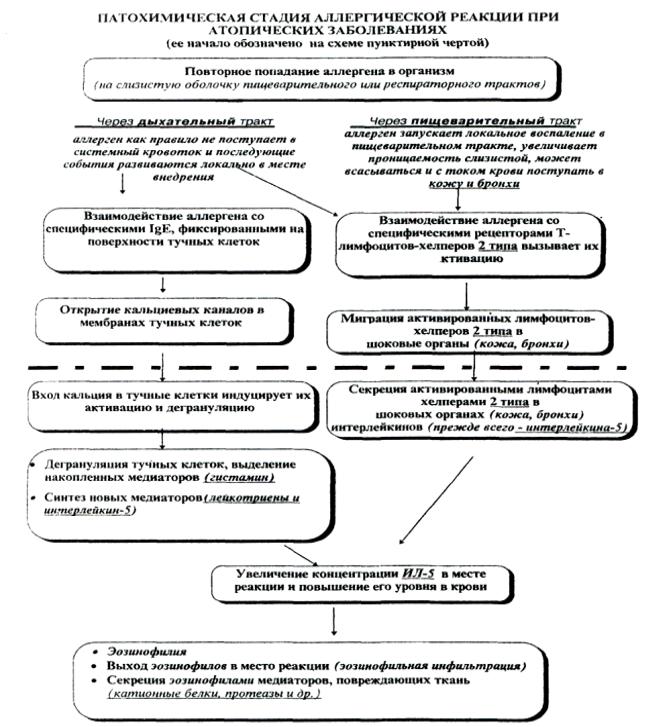
Острый ангионевротический отек
Острый ангионевротический отек является опосредованным тучными клетками в > 90% случаев. Механизмы, опосредованные тучными клетками, обычно сопровождается острой крапивницей (локализованные волдыри и отеки на коже).
Клинические проявления
Ангионевротический отек часто имеет асимметричную форму и слегка болезненен. Особенно подвержены отеку области век, губ, лица, языка, а также тыльная сторона рук и ног, гениталии. Отек верхних дыхательных путей может вызвать респираторный дистресс и стридор, который иногда ошибочно принимают за астму. Может иметь место полная обструкция дыхательных путей. Отек слизистой оболочки кишечника может вызвать тошноту, рвоту, болезненные колики в области живота и/или диарею.
- Может развиться в течение минут или же в течение нескольких часов
- Может сопровождаться проявлениями, свойственными аллергическим реакциям (например, зудом, крапивницей, гиперемией, бронхоспазмом, анафилатическим шоком)
Основа диагностики — клиническая оценка
Пациенты с локализованным отеком без крапивницы опрашиваются, в частности, на предмет использования ингибиторов АПФ. Причина зачастую является очевидной, и диагностические тесты проводятся редко.
Причина зачастую является очевидной, и диагностические тесты проводятся редко.
Общие подходы
Пациенты с умеренной и тяжелой формой ангионевротического отека часто госпитализируются в стационары. Длительное стационарное лечение ангионевротического отека обычно не требуется при своевременном начале терапии.
Клиницисты должны попытаться определить, а пациенты должны избегать таких триггеров, как пищевые аллергены, наркотики, воздействия холода, жары, вибрации, давления, приема НПВС, ингибиторов АПФ. Пациентам с тяжелыми формами отека Квинке в анамнезе следует рекомендовать постоянно носить с собой предварительно заполненный автоинжектор с адреналином и пероральные антигистаминные препараты и, в случае возникновения серьезной реакции, использовать эти средства как можно быстрее, а затем обратиться в отделение неотложной медицинской помощи.
При развитии острого ангионевротического отека на догоспитальном этапе лечения необходимо:
-
- Прекратить дальнейшее поступление предполагаемого аллергена в организм
- Внутривенно или внутримышечно ввести преднизолон 1 мг на кг;
- антигистаминные препараты: димедрол 1%-1мл; тавегил 2%- 2мл, возможно применение препаратов нового поколения (семпрекмс, кларитин и прочие).

- При пищевой аллергии принять слабительное, энтеросорбенты
- при нарастающем отёке гортани с обтурационной дыхательной недостаточностью при неэффективности терапии следует провести интубацию или коникотомию.
Антигистаминные препараты первого поколения недороги и эффективны, но сонливость и антихолинергические эффекты могут вызывать определенные проблемы. Из-за потенциальных седативных эффектов пациенты должны быть предупреждены о вождении автомобиля и эксплуатации тяжелой техники.
ОКАЗАНИЕ СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ НА ГОСПИТАЛЬНОМ ЭТАПЕ В СТАЦИОНАРНОМ ОТДЕЛЕНИИ СКОРОЙ МЕДИЦИНСКОЙ ПОМОЩИ
- Продолжение мероприятий по прекращению поступления аллергена:
- Антигистаминные препараты: димедрол 1%-1мл; тавегил 2%-2 мл
- Глюкокортикоиды: преднизолон из расчета 1 мг на кг или дексаметазон в аналогичной дозировке.
- При развитии отека гортани пациенту необходимо немедленно ввести дополнительно к указанной терапии ГКС и антигистаминными препаратами подкожно 0, 1% раствор адреналина в дозе, соответствующей возрасту (0, 3-0, 5-0, 8 мл).
 При неэффективности терапии следует провести интубацию или коникотомию. Больной с отеком гортани нуждается в срочной госпитализации в отделение реанимации и интенсивной терапии.
При неэффективности терапии следует провести интубацию или коникотомию. Больной с отеком гортани нуждается в срочной госпитализации в отделение реанимации и интенсивной терапии.
При полной регрессии ангионевротического отека на фоне лечения, проведенного на догоспитальном этапе и в СтСМП возможна выписка пациента на амбулаторное лечение.
Для лечения хронических форм ангионевротического отека могут быть использованы антагонисты лейкотриеновых рецепторов (монтелукаст, зафирлукаст), h3-блокаторы (ранитидин, циметидин) трициклические антидепрессанты (doxepin), иммуномодуляторы (ecallantide, icatibant, C1 inhibitor human) , моноклональные антитела (omalizumab)
Учитывая большую распространенность описанной нозологии, с ней может столкнуться врач любой специальности в любое время суток. Отделения стационара, персонал скорой медицинской помощи могут справиться с ситуацией и оказать помощь пациенту с ангионевротическим отеком, возникшем по той или иной причине в полном объеме. Для оказания подобной помощи имеются все необходимое оборудование, а персонал обладает необходимой квалификацией и знаниями для успешного лечения таких пациентов.
Для оказания подобной помощи имеются все необходимое оборудование, а персонал обладает необходимой квалификацией и знаниями для успешного лечения таких пациентов.
Статья добавлена 9 сентября 2019 г.
Какие препараты из класса кортикостероидов используются при лечении ангионевротического отека?
Вакисака М., Шуто М., Абэ Х и др. Компьютерная томография желудочно-кишечных проявлений наследственного ангионевротического отека. Радиат Мед . 2008 26 декабря (10): 618-21. [Медлайн].
Scheirey CD, Scholz FJ, Shortsleeve MJ, Katz DS. Ангионевротический отек тонкой кишки, вызванный ингибиторами ангиотензинпревращающего фермента: клинические данные и результаты визуализации у 20 пациентов. AJR Am J Roentgenol . 2011 Август 197 (2): 393-8. [Медлайн].
Каплан А.П. Крапивница и ангионевротический отек. Адкинсон-младший, штат НФ. Аллергия Миддлтона: принципы и практика . 7-е изд. Мосби; 2009. 1061-81.
Адкинсон-младший, штат НФ. Аллергия Миддлтона: принципы и практика . 7-е изд. Мосби; 2009. 1061-81.
Накамура С., Нагао А., Кишино М., Кониси Х., Ширатори К. Образование и визуализация. Желудочно-кишечный тракт: ангионевротический отек тонкой кишки. Дж Гастроэнтерол Гепатол . 2008 г., 23 июля (7 п.1): 1158. [Медлайн].
Raman SP, Lehnert BE, Pruthi S.Необычный рентгенологический вид лекарственно-индуцированного ангионевротического отека глотки и дифференциальные соображения. AJNR Am J Neuroradiol . 2009 30 января (1): 77-8. [Медлайн].
Донати М. Де медика история мирабили. Мантуя, за о. Osanam . 1586.
Милтон JL. На гигантскую крапивницу. Edinburgh Med J . 1876. 22: 513-26.
Ослер В. Наследственный ангионевротический отек. Am J Med Sci . 1888. 95: 362-7.
Adhikari SP, Schneider JI. Необычная причина болей в животе и гипотонии: ангионевротический отек кишечника. J Emerg Med . 2009 Январь 36 (1): 23-5. [Медлайн].
Каплан А.П. Ангионевротический отек. World Allergy Organ J . 2008 июн.1 (6): 103-13. [Медлайн].
Rye Rasmussen EH, Bindslev-Jensen C, Bygum A.Ангионевротический отек — оценка и лечение. Тидсскр Нор Лаэгефорен . 2012, 12 ноября. 132 (21): 2391-5. [Медлайн].
Маркс Дж., Хокбергер Р., Уоллс Р. Крапивница и ангионевротический отек. Аппарат неотложной помощи Розена . 7-е изд. Мосби; 2009. [Полный текст].
Аппарат неотложной помощи Розена . 7-е изд. Мосби; 2009. [Полный текст].
Mansi M, Zanichelli A, Coerezza A, Suffritti C, Wu MA, Vacchini R, et al. Презентация, диагностика и лечение ангионевротического отека без волдырей: ретроспективный анализ когорты из 1058 пациентов. Дж. Интерн Мед. . 2014 4 сентября [Medline].
[Рекомендации] Чикарди М., Аберер В., Банержи А., Бас М., Бернштейн Дж. А., Борк К. и др. Классификация, диагностика и подход к лечению ангионевротического отека: консенсусный отчет Международной рабочей группы по наследственному ангионевротическому отеку. Аллергия . 2014 май. 69 (5): 602-16. [Медлайн].
Oschatz C, Maas C, Lecher B, Jansen T., Björkqvist J, Tradler T. и др. Тучные клетки увеличивают проницаемость сосудов за счет инициируемого гепарином образования брадикинина in vivo. Иммунитет . 2011 25 февраля. 34 (2): 258-68. [Медлайн].
Иммунитет . 2011 25 февраля. 34 (2): 258-68. [Медлайн].
Asero R, Bavbek S, Blanca M, Blanca-Lopez N, Cortellini G, Nizankowska-Mogilnicka E, et al. Клиническое ведение пациентов с крапивницей / ангионевротическим отеком в анамнезе, вызванными несколькими НПВП: обзор экспертной группы. Int Arch Allergy Immunol . 2013. 160 (2): 126-33. [Медлайн].
Fonacier LS, Dreskin SC, Leung DY. Аллергические кожные заболевания. J Allergy Clin Immunol .2010 февраль 125 (2 приложение 2): S138-49. [Медлайн].
Bas M, Adams V, Suvorava T, Niehues T, Hoffmann TK, Kojda G. Неаллергический ангионевротический отек: роль брадикинина. Аллергия . 2007 августа 62 (8): 842-56. [Медлайн].
Куньо М., Марцано А.В., Асеро Р., Тедески А. Активация свертывания крови при хронической крапивнице: патофизиологические и клинические последствия. Стажер Emerg Med . 2010 апр. 5 (2): 97-101. [Медлайн].
Активация свертывания крови при хронической крапивнице: патофизиологические и клинические последствия. Стажер Emerg Med . 2010 апр. 5 (2): 97-101. [Медлайн].
Zuraw BL.Клиническая практика. Наследственный ангионевротический отек. N Engl J Med . 2008 сентябрь 4. 359 (10): 1027-36. [Медлайн].
Чемпион Р.Х., Робертс С.О., Карпентер Р.Г., Роджер Дж. Крапивница и ангионевротический отек. Обзор 554 пациентов. Br J Dermatol . 1969, август 81 (8): 588-97. [Медлайн].
Галли С.Дж., Цай М. IgE и тучные клетки при аллергических заболеваниях. Нат Мед . 2012 4 мая. 18 (5): 693-704. [Медлайн]. [Полный текст].
Frigas E, Nzeako UC.Ангионевротический отек. Патогенез, дифференциальная диагностика и лечение. Clin Rev Allergy Immunol . 2002 Октябрь, 23 (2): 217-31. [Медлайн].
2002 Октябрь, 23 (2): 217-31. [Медлайн].
Banerji A, Sheffer AL. Спектр хронического ангионевротического отека. Allergy Asthma Proc . 2009 Янв-Фев. 30 (1): 11-6. [Медлайн].
Cugno M, Zanichelli A, Foieni F, Caccia S, Cicardi M. Дефицит C1-ингибитора и ангионевротический отек: молекулярные механизмы и клинический прогресс. Trends Mol Med .2009 15 февраля (2): 69-78. [Медлайн].
Каплан А.П., Гривз М. Патогенез хронической крапивницы. Clin Exp Allergy . 2009 июн. 39 (6): 777-87. [Медлайн].
Zingale LC, Castelli R, Zanichelli A, Cicardi M. Приобретенный дефицит ингибитора первого компонента комплемента: презентация, диагностика, курс и традиционное лечение. Immunol Allergy Clin North Am . 2006 26 ноября (4): 669-90. [Медлайн].
[Медлайн].
Byrd JB, Adam A, Brown NJ.Ангионевротический отек, связанный с ингибиторами ангиотензинпревращающего фермента. Immunol Allergy Clin North Am . 2006 26 ноября (4): 725-37. [Медлайн].
Борк К., Барнштедт С.Е., Кох П., Траупе Х. Наследственный ангионевротический отек с нормальной активностью С1-ингибитора у женщин. Ланцет . 2000 15 июля. 356 (9225): 213-7. [Медлайн].
Bowen T, Cicardi M, Bork K, Zuraw B, Frank M, Ritchie B. и др. Наследственный ангиодема: современный обзор, VII: Канадский Венгерский международный консенсусный алгоритм 2007 г. для диагностики, терапии и лечения наследственного ангионевротического отека. Ann Allergy Asthma Immunol . 2008, январь 100 (1 приложение 2): S30-40. [Медлайн].
Девальд Г. , Борк К. Миссенс-мутации в гене фактора свертывания крови XII (фактор Хагемана) при наследственном ангионевротическом отеке с нормальным ингибитором C1. Biochem Biophys Res Commun . 2006 г. 19 мая. 343 (4): 1286-9. [Медлайн].
, Борк К. Миссенс-мутации в гене фактора свертывания крови XII (фактор Хагемана) при наследственном ангионевротическом отеке с нормальным ингибитором C1. Biochem Biophys Res Commun . 2006 г. 19 мая. 343 (4): 1286-9. [Медлайн].
Bork K, Gül D, Dewald G. Наследственный ангио-отек с нормальным ингибитором C1 в семье с пораженными женщинами и мужчинами. Br J Dermatol .2006 Март 154 (3): 542-5. [Медлайн].
Крейг Т.Дж., Леви Р.Дж., Вассерман Р.Л. и др. Эффективность концентрата ингибитора C1-эстеразы человека по сравнению с плацебо при острых наследственных приступах ангионевротического отека. J Allergy Clin Immunol . 2009 Октябрь 124 (4): 801-8. [Медлайн].
Босси Ф., Фишетти Ф., Реголи Д. и др. Новый патогенетический механизм и терапевтические подходы к ангионевротическому отеку, связанному с дефицитом ингибитора C1. J Allergy Clin Immunol .2009 декабрь 124 (6): 1303-10.e4. [Медлайн]. [Полный текст].
J Allergy Clin Immunol .2009 декабрь 124 (6): 1303-10.e4. [Медлайн]. [Полный текст].
Банерджи А., Веллер П.Ф., Шейх Дж. Цитокин-ассоциированные синдромы ангионевротического отека, включая эпизодический ангионевротический отек с эозинофилией (синдром Глейха). Immunol Allergy Clin North Am . 2006 26 ноября (4): 769-81. [Медлайн].
Феррели С., Пинна А.Л., Ацори Л., Асте Н. Эозинофильный целлюлит (синдром Уэллса): описание нового случая. J Eur Acad Dermatol Venereol . 1999 июл.13 (1): 41-5. [Медлайн].
Браун А.Ф., Маккиннон Д., Чу К. Анафилаксия в отделении неотложной помощи: обзор 142 пациентов за один год. J Allergy Clin Immunol . 2001 ноябрь 108 (5): 861-6. [Медлайн].
Ян М.С., Ли Ш., Ким Т.В. и др. Эпидемиологические и клинические особенности анафилаксии в Корее. Ann Allergy Asthma Immunol . 2008 Январь 100 (1): 31-6. [Медлайн].
Ann Allergy Asthma Immunol . 2008 Январь 100 (1): 31-6. [Медлайн].
Kalmár L, Hegedüs T, Farkas H, Nagy M, Tordai A.HAEdb: новая интерактивная база данных локус-специфических мутаций гена ингибитора C1. Хум Мутат . 2005 25 января (1): 1-5. [Медлайн].
Banerji A, Clark S, Blanda M, LoVecchio F, Snyder B, Camargo CA Jr. Многоцентровое исследование пациентов с ангионевротическим отеком, вызванным ингибитором ангиотензинпревращающего фермента, которые обращаются в отделение неотложной помощи. Ann Allergy Asthma Immunol . 2008 апр. 100 (4): 327-32. [Медлайн].
Фригас Е, Парк М.Идиопатический рецидивирующий ангионевротический отек. Immunol Allergy Clin North Am . 2006 26 ноября (4): 739-51. [Медлайн].
Hentges F, Hilger C, Kohnen M, Gilson G. Ангионевротический отек и эстроген-зависимый ангионевротический отек с активацией контактной системы. J Allergy Clin Immunol . 2009 Январь 123 (1): 262-4. [Медлайн].
Ангионевротический отек и эстроген-зависимый ангионевротический отек с активацией контактной системы. J Allergy Clin Immunol . 2009 Январь 123 (1): 262-4. [Медлайн].
Цишон С., Мартин Л., Хеннис Х.С. и др. Повышенная активность фактора свертывания XII (фактор Хагемана) вызывает наследственный ангионевротический отек III типа. Am J Hum Genet . 2006 декабрь 79 (6): 1098-104. [Медлайн]. [Полный текст].
Gleich GJ, Leiferman KM. Гиперэозинофильные синдромы: современные концепции и методы лечения. Br J Haematol . 2009 Май. 145 (3): 271-85. [Медлайн].
Морган М, Хан Д.А. Терапевтические альтернативы хронической крапивнице: научно обоснованный обзор, часть 2. Ann Allergy Asthma Immunol . 2008 июн. 100 (6): 517-26; викторина 526-8, 544. [Medline].
Sánchez-Borges M, Asero R, Ansotegui IJ, Baiardini I, Bernstein JA, Canonica GW, et al. Диагностика и лечение крапивницы и ангионевротического отека: мировая перспектива. World Allergy Organ J . 2012 г. 5 (11): 125-47.[Медлайн].
Веб-сайт совместной рабочей группы по параметрам практики. Доступно на http://www.allergyparameters.org/. Доступ: 5 июня 2013 г.
Совместная рабочая группа по параметрам практики. Параметры практики ангионевротического отека: обновление 2013 г. J Allergy Clin Immunol . [в печати] Июнь 2013 г.
Ланг Д.М., Аберер В., Бернштейн Дж. А., Чнг Х. Х., Грумах А. С., Хайд М. и др. Международный консенсус по наследственному и приобретенному ангионевротическому отеку. Ann Allergy Asthma Immunol . 2012 декабрь 109 (6): 395-402. [Медлайн].
Пауэлл Р.Дж., Пиявка СК, Тилль С., Хубер ПА, Нассер С.М., Кларк А.Т. Руководство BSACI по лечению хронической крапивницы и ангионевротического отека. Clin Exp Allergy .2015 Март 45 (3): 547-65. [Медлайн].
Craig T, Pürsün EA, Bork K, Bowen T, Boysen H, Farkas H, et al. Руководство WAO по лечению наследственного ангионевротического отека. World Allergy Organ J . 2012 декабрь 5 (12): 182-199. [Медлайн].
World Allergy Organ J . 2012 декабрь 5 (12): 182-199. [Медлайн].
Zuberbier T, Asero R, Bindslev-Jensen C, Walter Canonica G, Church MK, Giménez-Arnau A, et al. EAACI / GA (2) Руководство LEN / EDF / WAO: определение, классификация и диагностика крапивницы. Аллергия .2009 Октябрь 64 (10): 1417-26. [Медлайн].
Феррер М., Састре Дж, Хауреги I, Давила I, Монторо Дж, дель Кувильо А. и др. Эффект повышения дозы антигистаминных препаратов при хронической крапивнице. J Исследование Allergol Clin Immunol . 2011. 21 Дополнение 3: 34–9. [Медлайн].
Handa S, Dogra S, Kumar B. Сравнительная эффективность цетиризина и фексофенадина при лечении хронической идиопатической крапивницы. J Dermatolog Treat . 2004 15 января (1): 55-7.[Медлайн].
Карран депутат, Скотт Л.Дж., Перри К.М. Цетиризин: обзор его использования при аллергических расстройствах. Наркотики . 2004. 64 (5): 523-61. [Медлайн].
Хиндмарч I, Джонсон С., Медоуз Р., Киркпатрик Т., Шамси З.Острые и субхронические эффекты левоцетиризина, цетиризина, лоратадина, прометазина и плацебо на когнитивные функции, психомоторные функции, а также волдыри и вспышки. Curr Med Res Opin . 2001. 17 (4): 241-55. [Медлайн].
Асеро Р., Тедески А., Лорини М. Антагонисты рецепторов лейкотриена при хронической крапивнице. Аллергия . 2001 Май. 56 (5): 456-7. [Медлайн].
2001 Май. 56 (5): 456-7. [Медлайн].
Маурер М., Розен К., Хсие Х. Дж., Сайни С., Граттан С., Хименес-Арнау А. и др.Омализумаб для лечения хронической идиопатической или спонтанной крапивницы. N Engl J Med . 2013 7 марта. 368 (10): 924-35. [Медлайн].
Spector SL, Тан РА. Достижения в области аллергических кожных заболеваний: омализумаб является многообещающим средством лечения крапивницы и ангионевротического отека. J Allergy Clin Immunol . 2009 Январь 123 (1): 273-4. [Медлайн].
Song CH, Stern S, Giruparajah M, Berlin N, Sussman GL. Долгосрочная эффективность омализумаба в фиксированных дозах у пациентов с тяжелой хронической спонтанной крапивницей. Ann Allergy Asthma Immunol . 2013 Февраль 110 (2): 113-7. [Медлайн].
Zuraw BL et al. Нанофильтрованный концентрат ингибитора С1 для лечения наследственного ангионевротического отека. N Engl J Med . Август 2010. 363: 513-22.
Нанофильтрованный концентрат ингибитора С1 для лечения наследственного ангионевротического отека. N Engl J Med . Август 2010. 363: 513-22.
Riedl MA, Hurewitz DS, Levy R, Busse PJ, Fitts D, Kalfus I. Нанофильтрованный ингибитор С1-эстеразы (человек) для лечения острых приступов наследственного ангионевротического отека: открытое испытание. Ann Allergy Asthma Immunol .2012 Январь 108 (1): 49-53. [Медлайн].
Cicardi M et al. Экаллантид для лечения острых приступов наследственного ангионевротического отека. N Engl J Med . Август 2010. 363: 523-31.
Cicardi M, et al. Икатибант, новый антагонист рецепторов брадикинина, при наследственном ангионевротическом отеке. N Engl J Med . 5 августа 2010 г. 363 (6): 532-41. [Медлайн].
[Рекомендации] Чикарди М., Борк К., Кабальеро Т., Крейг Т., Ли Х. Х., Лонгхерст Х и др. Доказательные рекомендации по терапевтическому лечению ангионевротического отека вследствие наследственной недостаточности ингибитора C1: консенсусный отчет Международной рабочей группы. Аллергия . 2012 Февраль 67 (2): 147-57. [Медлайн].
[Рекомендации] Кабальеро Т., Фаркаш Х., Булье Л., Боуэн Т., Гомпель А., Фагерберг С. и др.Международный консенсус и практические рекомендации по гинекологическому и акушерскому ведению пациенток с наследственным ангионевротическим отеком, вызванным дефицитом ингибитора C1. J Allergy Clin Immunol . 2012 Февраль 129 (2): 308-20. [Медлайн].
J Allergy Clin Immunol . 2012 Февраль 129 (2): 308-20. [Медлайн].
Саймонс Ф.Е., Суссман Г.Л., Саймонс К.Дж. Влияние h3-антагониста циметидина на фармакокинетику и фармакодинамику h2-антагонистов гидроксизина и цетиризина у пациентов с хронической крапивницей. J Allergy Clin Immunol .1995 Март 95 (3): 685-93. [Медлайн].
Пауль Э., Bödeker RH. Лечение хронической крапивницы терфенадином и ранитидином. Рандомизированное двойное слепое исследование с участием 45 пациентов. евро J Clin Pharmacol . 1986. 31 (3): 277-80. [Медлайн].
Шарп Г.Р., Шустер С. При дерматографической крапивнице антагонисты рецептора h3 имеют небольшой, но терапевтически не относящийся к делу дополнительный эффект по сравнению с одними антагонистами h2. Br J Dermatol .1993 ноябрь 129 (5): 575-9. [Медлайн].
[Медлайн].
Fedorowicz Z, van Zuuren EJ, Hu N. Антагонисты h3-рецепторов гистамина при крапивнице. Кокрановская база данных Syst Rev . 2012 14 марта 3: CD008596. [Медлайн].
Троян ТД, Хан Д.А. Ингибиторы кальциневрина при хронической крапивнице. Curr Opin Allergy Clin Immunol . 2012 12 августа (4): 412-20. [Медлайн].
Ридл М., Тахджиан Р., Шранц Дж., Медсестра С., Бернштейн Дж.Стабильный эффект лечения ланаделумабом у пациентов с наследственным ангионевротическим отеком (НАО) независимо от исходной частоты приступов в исследовании HELP фазы 3. Представлено на ежегодном собрании Совместного конгресса AAAAI / WAO 2018 г., 2-5 марта 2018 г., Орландо, Флорида. Дж Aller Clin Immunol . 2018 фев. 141 (2; доп.): AB47: [Полный текст].
Декадрон, Дексаметазон Интенсол (дексаметазон) дозировка, показания, взаимодействия, побочные эффекты и многое другое
Противопоказания
Системная грибковая инфекция
Подтвержденная гиперчувствительность
Церебральная малярия
Пациентам, получающим иммуносупрессивные дозы кортикостероидов, противопоказано введение живых или живых аттенуированных вакцин
С осторожностью при циррозе печени, при диверультазе, миастазе, с осторожностью язвенная болезнь, язвенный колит, почечная недостаточность, беременность
Средние и большие дозы кортикостероидов могут вызвать повышение артериального давления, задержку натрия и воды и повышенное выведение калия; эти эффекты менее вероятны для синтетических производных, за исключением случаев, когда они используются в больших дозах; может потребоваться диетическое ограничение соли и добавление калия; все кортикостероиды увеличивают выведение кальция.
В литературе предполагается очевидная связь между применением кортикостероидов и разрывом свободной стенки левого желудочка после недавнего инфаркта миокарда; терапию кортикостероидами следует применять с большой осторожностью у этих пациентов.
Кортикостероиды могут вызывать обратимое подавление гипоталамо-гипофизарной надпочечниковой оси (HPA) с потенциалом глюкокортикостероидной недостаточности после отмены лечения; недостаточность коры надпочечников может возникнуть в результате слишком быстрой отмены; может быть сведено к минимуму постепенным уменьшением дозировки; относительная недостаточность может сохраняться в течение месяцев после прекращения терапии; поэтому в любой стрессовой ситуации, возникающей в этот период, возобновите гормональную терапию; если пациент уже получает стероиды, дозу можно увеличить.
Метаболический клиренс кортикостероидов снижается у пациентов с гипотиреозом и увеличивается у пациентов с гипертиреозом; изменения в статусе щитовидной железы пациента могут потребовать корректировки дозировки
Может обострить системные грибковые инфекции; не для использования при таких инфекциях, за исключением случаев, когда это необходимо для контроля опасных для жизни реакций на лекарства
Может активироваться латентное заболевание или может быть обострение интеркуррентных инфекций, вызванных патогенами, в том числе вызываемыми Amoeba, Candida, Cryptococcus, Mycobacterium, Nocardia , Пневмоцисты, токсоплазма; исключить латентный амебиаз или активный амебиаз перед началом терапии кортикостероидами у любого пациента, который провел время в тропиках, или у любого пациента с необъяснимой диареей
Используйте с большой осторожностью у пациентов с известным или подозреваемым заражением Strongyloides (острицы); иммуносупрессия, вызванная кортикостероидами, может привести к гиперинфекции и распространению Strongyloides с широко распространенной миграцией личинок, часто сопровождающейся тяжелым энтероколитом и потенциально фатальной грамотрицательной септицемией; не для использования при церебральной малярии
Необходимо тщательное наблюдение, если кортикостероиды показаны пациентам с латентным туберкулезом или туберкулиновой реактивностью; может произойти реактивация болезни; во время длительной терапии кортикостероидами эти пациенты должны получать химиопрофилактику.
Использование пероральных кортикостероидов не рекомендуется при лечении неврита зрительного нерва и может привести к увеличению риска новых эпизодов; кортикостероиды не должны использоваться при активном офтальмологическом простом герпесе.
Используйте минимальную возможную дозу для контроля состояния при лечении; Решение о соотношении риск / польза должно приниматься в каждом индивидуальном случае относительно дозы и продолжительности лечения, а также относительно того, следует ли использовать ежедневную или прерывистую терапию.
Может привести к подавлению роста костей у педиатрических пациентов и развитию остеопороза в любом возрасте; Особое внимание следует уделять пациентам с повышенным риском остеопороза (например,g., женщины в постменопаузе) перед началом терапии кортикостероидами
При приеме кортикостероидов могут появиться психические расстройства, от эйфории, бессонницы, перепадов настроения, изменений личности и тяжелой депрессии до явных психотических проявлений; существующая эмоциональная нестабильность или психотические наклонности могут также усугубляться кортикостероидами
Минимальная активность минералокортикоидов
Тромбоэмболические расстройства
Сообщалось о миопатии
Отсроченное заживление ран
Отмена терапии с постепенным снижением дозы на 904 Может иметь системные эффекты
. исследовать суставную жидкость, при необходимости исключить гнойный процесс; избегать инъекции в инфицированный участок; частые внутрисуставные инъекции могут привести к повреждению суставной ткани.
исследовать суставную жидкость, при необходимости исключить гнойный процесс; избегать инъекции в инфицированный участок; частые внутрисуставные инъекции могут привести к повреждению суставной ткани.При контакте с ветряной оспой может быть показана профилактика иммуноглобулином против ветряной оспы (VZIG); при контакте с корью может быть показана профилактика иммуноглобулином (IG); если развивается ветряная оспа, следует рассмотреть возможность лечения противовирусными препаратами
Скрытый туберкулез может быть реактивирован (следует наблюдать за пациентами с положительным туберкулиновым тестом)
Некоторые предположения (не полностью обоснованные) незначительного увеличения риска развития волчьей пасти при применении кортикостероидов во время беременности
Продолжительное использование кортикостероидов может привести к повышению внутриглазного давления, глаукоме или катаракте с возможным повреждением зрительных нервов, а также может способствовать развитию вторичных глазных инфекций, вызванных бактериями, грибами или вирусами; рассмотреть возможность направления к офтальмологу пациентов, у которых развиваются глазные симптомы или которые используют продукты, содержащие кортикостероиды более 6 недель.
Продолжительная терапия связана с развитием саркомы Капоши
Может повлиять на скорость роста у детей; регулярный мониторинг
Пациенту могут потребоваться более высокие дозы при стрессе
Пациентам, получающим кортикостероиды в качестве заместительной терапии в физиологических дозах (например, при болезни Аддисона), могут потребоваться более высокие дозы
Эпидуральная инъекция
- Серьезные неврологические события, сообщалось о некоторых случаях, приводящих к смерти при эпидуральной инъекции
- Сообщалось о конкретных событиях, включая, помимо прочего, инфаркт спинного мозга, параплегию, квадриплегию, корковую слепоту и инсульт
- Сообщалось об этих серьезных неврологических событиях при применении и без рентгеноскопии
- Безопасность и эффективность эпидурального введения кортикостероидов не были установлены, и кортикостероиды не одобрены для этого использования
Обзор лекарственного взаимодействия
Сильные ингибиторы CYP3A4
- Совместное применение сильных 4 и умеренных CYP3A гибиторы увеличивают экспозицию дексаметазона, что может увеличить риск побочных реакций
- Избегайте одновременного приема сильных ингибиторов CYP3A4 или рассмотрите альтернативы, которые не являются сильными ингибиторами CYP3A4
- Если одновременного приема нельзя избежать, внимательно следите за нежелательными лекарственными реакциями
Сильный Индукторы CYP3A4
- Совместное введение сильных индукторов CYP3A4 может снизить воздействие дексаметазона, что может привести к потере эффективности
- Избегайте одновременного введения сильных индукторов CYP3A4 или рассмотрите возможность применения альтернативных лекарств, которые не являются индукторами CYP3A4
- Если нельзя избежать одновременного введения увеличивающих индукторов
- Доза дексаметазона
Холестирамин
- Холестирамин может увеличивать клиренс кортикостероидов и потенциально снижать экспозицию кортикостероидов
- Избегайте совместного приема и рассмотрите альтернативные препараты 9000 7
Антихолинэстеразы
- Одновременное применение антихолинэстеразных препаратов и кортикостероидов может вызвать сильную слабость у пациентов с миастенией гравис
- Если возможно, антихолинэстеразные препараты следует отменить не менее чем за 24 часа до начала терапии кортикостероидами7000
- 97 905
- Эфедрин может снизить экспозицию дексаметазона и может привести к потере эффективности
- Рассмотрите возможность увеличения дозы дексаметазона при использовании с эфедрином
Эстрогены
- Эстрогены могут снизить печеночный метаболизм некоторых кортикостероидов, что может увеличить метаболизм некоторых кортикостероидов в печени.
 риск побочных реакций
риск побочных реакций
- Эстрогены могут снизить печеночный метаболизм некоторых кортикостероидов, что может увеличить метаболизм некоторых кортикостероидов в печени.
Субстраты CYP3A4
- Совместное введение дексаметазона с субстратами может снизить концентрацию этих препаратов, что приведет к потере их эффективности. е препараты
Пероральные антикоагулянты
- Совместное применение антикоагулянтов с кортикостероидами может снизить ответ на антикоагулянты; часто контролируйте показатели свертывания крови для поддержания желаемого антикоагулянтного эффекта
Амфотерицин B для инъекций и средства, истощающие калий
- У пациентов, получающих кортикостероиды, может наблюдаться задержка натрия с последующим отеком и потерей калия; внимательно следить за уровнем калия
Противодиабетические препараты
- Кортикостероиды могут повышать концентрацию глюкозы в крови; при необходимости рассмотреть возможность корректировки дозы противодиабетических средств
Изониазид
- Концентрация изониазида в сыворотке может быть снижена с помощью кортикостероидов
Циклоспорин
- Повышение активности спорина как циклортикостероидов, так и двух кортикостероидов при одновременном применении
- Сообщалось о конвульсиях при таком одновременном применении
Гликозиды наперстянки
- Пациенты, принимающие гликозиды наперстянки, могут иметь повышенный риск развития аритмий из-за гипокалиемии
Нестероидные препараты
- Одновременное использование аспирина (или других НПВП) и кортикостероидов увеличивает риск желудочно-кишечных побочных эффектов; клиренс салицилатов может быть увеличен при одновременном применении кортикостероидов; монитор токсичности
Фенитоин
- В постмаркетинговом опыте были сообщения как об увеличении, так и о снижении уровней фенитоина при одновременном введении дексаметазона, что приводило к изменениям в контроле над приступами
Вакцины на основе кортикостероидов терапия может проявлять сниженный ответ на токсоиды и живые или инактивированные вакцины из-за ингибирования ответа антител
- Кортикостероиды также могут усиливать репликацию некоторых организмов, содержащихся в живых аттенуированных вакцинах
- Если возможно, отложите плановое введение вакцин или токсоидов до тех пор, пока терапия не будет завершена.
 прекращено
прекращено
Сопутствующие терапии, которые могут увеличить риск тромбоэмболии
- Эритропоэтические агенты или другие агенты, которые могут увеличивать риск тромбоэмболии, такие как терапии, содержащие эстроген, одновременно назначены с дексаметазоном возможно повышение риска тромбоэмболии; Монитор риска тромбоэмболии
Талидомид
- Сообщалось о токсическом эпидермальном некролизе при одновременном применении талидомида
- Тщательно контролировать токсичность
Кожные тесты
- 9
Ангионевротический отек — энто.com
Красные флаги
НЕОБХОДИМЫЕ ТРИАДЫ БЕДСТВИТЕЛЬНЫХ ДВИГАТЕЛЕЙ
Быстрое начало афагии или тяжелая дисфагия, часто сопровождающиеся сильной болью в горле
Быстрое начало голоса, хриплый голос, хриплый, хриплый голос
Системно очень плохое самочувствие: гипертермия, тахикардия, тахипноэ
Может быть сопутствующий тризм или кривошея. Остерегайтесь любого пациента, у которого после госпитализации появляются эти признаки: ситуация быстро ухудшается.При травме шеи к любому из вышеперечисленных следует отнестись очень серьезно. Стридор — это поздний признак нарушения дыхательных путей.
Остерегайтесь любого пациента, у которого после госпитализации появляются эти признаки: ситуация быстро ухудшается.При травме шеи к любому из вышеперечисленных следует отнестись очень серьезно. Стридор — это поздний признак нарушения дыхательных путей.
Почему это важно?
Ангионевротический отек — это набухание глубоких кожных, подкожных или подслизистых тканей из-за утечки из сосудов. Обычно он поражает губы, язык, глаза и лицо, но также может поражать другие части тела.
Пациенты с ангионевротическим отеком подвергаются высокому риску обструкции дыхательных путей, поэтому это может потребовать неотложной медицинской помощи.
Некоторые пациенты подвержены риску повторного ангионевротического отека и должны быть обследованы (см. Ниже).
Когда привлекать регистратора ЛОР
Регистраторам ЛОР и анестезиологам следует срочно сообщить, если вы считаете, что дыхательные пути пациента находятся в опасности.
В чрезвычайной ситуации, поскольку большинство регистраторов ЛОР находятся вне рабочего места, целесообразно вызвать экстренную помощь анестезиологу, ODP и бригаде скорой помощи, которые находятся на месте.
Кому принимать
Все пациенты с ангионевротическим отеком должны быть госпитализированы на 24 часа наблюдения. Однако остается спорным, чьей опеке они попадают. Большинство медицинских бригад не хотели бы принимать этих пациентов под свою опеку, поэтому обычно это остается на усмотрение ITU и группы ЛОР.
Мы предлагаем, чтобы любой пациент, имеющий стабильные дыхательные пути с минимальным отеком дыхательных путей, мог наблюдаться под наблюдением ЛОР-бригады в специализированном ЛОР-отделении с надлежащим образом обученными медсестрами и доступной поддержкой в отделениях неотложной помощи.Если, однако, нет специализированного ЛОР-отделения, отделение интенсивной терапии может быть более подходящей средой.
Оценка и распознавание
Пациент должен быть осмотрен в реанимационном отделении с соответствующим мониторингом
Используйте методический подход ABC к пациенту в соответствии с протоколом ALS
Составьте краткий анамнез (включая прошлый медицинский , лекарство и семья) и тщательно осмотрите шею, ротовую полость и верхнюю часть пищеварительного тракта; гибкая насендоскопия неоценима, если вы компетентный эндоскопист.
Помните, обращайтесь за помощью заранее, если есть признаки надвигающейся обструкции дыхательных путей!
Немедленное и ночное лечение
Статическая доза дексаметазона 6.От 6 до 8 мг внутривенно, 4 мг хлорфенамина внутривенно, Heliox (или кислород с высокой скоростью потока, если Heliox недоступен)
Взрослые и дети> 12 лет: 0,5 мл 1: 1000 адреналина внутримышечно (= 500 мкг), если имеется угроза обструкции дыхательных путей (см. алгоритм управления анафилаксией Совета Resus)
В противном случае адреналин 1: 1000 можно вводить в форме небулайзера, обычно разбавленного 4 мл 0,9% физиологического раствора до конечной концентрации 1: 5000
Назначьте PRN адреналина в распыленном виде в случае у пациента проблемы с дыханием в палате
После лечения, описанного выше, дексаметазон 6.Следует назначить от 6 до 8 мг TDS вместе с хлорфенамином. 4 мг QDS
Дозу дексаметазона следует уменьшить, если высокая доза длится более двух или трех дней
Этиология, факторы риска и патофизиология
Идиопатический (40%)
Повышенная чувствительность к внешним раздражителям например, пища, лекарства, укусы насекомых, пыльца, перхоть животных; пациенты с известными атопическими состояниями (астма, экзема, сенная лихорадка, крапивница) подвержены более высокому риску этого заболевания
Наследственные — обычно имеется сильный семейный анамнез.Это связано с мутациями гена ингибирования C1 (C1-INH) и не связано с гиперчувствительностью
Аутоиммунные заболевания — например, волчанка
Злокачественные новообразования — лимфома, лейкемия
Лекарства и НПВП. ингибиторы являются частыми виновниками; пациенты могли принимать эти препараты в течение многих лет
Физические факторы — например, холод, тепло, давление, вибрация и ультрафиолетовое излучение
Дальнейшее лечение
Эти пациенты должны быть обследованы на предмет первопричины.Соответствующие исследования включают:
Комплемент
Триптаза тучных клеток
Уровни ингибитора C1-эстеразы (при наследственной недостаточности ингибитора C1-эстеразы)
ANA (при
RHH)Кожный укол или сыворотка RAST
FBC, U&E, CRP, LFT, скрининг коагуляции
Пациентам с риском повторных эпизодов следует проконсультировать о приеме Эпипена и обратиться за лечением / советом к врачу. специалист по аллергии.
Последняя проверка страницы: 15 декабря 2019 г.
Лечение ангионевротического отека, вызванного ACEi
Введение0
Ангионевротический отек, вызванный ингибиторами АПФ (ACEI-AAG), составляет около трети случаев ангионевротического отека, поступающих в отделение неотложной помощи. Ингибиторы АПФ становятся все более популярными, и в новом руководстве JNC 8 их классифицируется как лекарство первой линии от гипертонии.Таким образом, ACEI-AAG может представлять растущую проблему. К сожалению, это часто лечится неправильно, с помощью режима лечения, направленного против аллергического ангионевротического отека (т. Е. Кортикостероидов и антигистаминных препаратов).0
Физиология ACEI-AAG0
0
ACEI-AAG возникает из-за чрезмерного накопления брадикинина. Причина, по которой только у небольшой части пациентов, получавших ингибиторы АПФ, развиваются ACEI-AAG, может быть связана с генетическими вариациями метаболизма брадикинина.Во время лечения ингибиторами АПФ критическими становятся различные альтернативные ферментативные пути метаболизма брадикинина (например, аминопептидаза Р плазмы). Лица с более низкой активностью этих альтернативных путей клиренса могут подвергаться повышенному риску накопления брадикинина и ACEI-AAG (Campo 2013).0
Коротко о диагностике0
У любого пациента с ангионевротическим отеком, принимающего ингибитор АПФ, должен быть высокий индекс подозрения на АПФ-ААГ.Хотя ACEI-AAG обычно возникает вскоре после начала приема ACEi, это может произойти спустя годы. Заболеваемость среди женщин выше, а среди афроамериканцев — в пять раз (Byrd, 2008).0
Следующие клинические признаки могут помочь дифференцировать ACEI-AAG от гистамин-опосредованного аллергического ангионевротического отека (однако следует отметить, что ACEI-AAG имеет много общих клинических признаков с другими формами ангионевротического отека, индуцированного брадикинином, такими как дефицит ингибитора C1-эстеразы).
0
0
- Отсутствие аллергического триггера (напротив, ACEI-AAG может возникнуть после небольшой травмы)
- Начинается с очаговой припухлости (напр.г. изолированный отек языка или губ, часто асимметричный)
- Развивается с течением времени (более медленное прогрессирование, чем ангионевротический отек, опосредованный гистамином)
- Отсутствие крапивницы или зуда
- Отсутствие реакции на антигистаминные препараты, стероиды, адреналин
0
Стероиды, антигистаминные препараты и адреналин неэффективны для ACEI-AAG.0
ACEI-AAG возникает из-за нарушения метаболизма брадикинина. Стандартные методы лечения аллерген-индуцированного ангионевротического отека (адреналин, стероиды и антигистаминные препараты) на это не влияют.Нет убедительных доказательств того, что эти методы лечения эффективны, как указано в нескольких согласованных руководящих принципах (Cicardi 2014, Zuraw 2013, Lang 2012):0
Как и при лечении острого ангионевротического отека у пациентов с дефицитом С1-ингибитора, введение антигистаминных препаратов, кортикостероидов или адреналина не связано с пользой и не рекомендуется.
— Международный консенсус по наследственным и приобретенным ангионевротическим отекам, Lang 2012.
0
0
Лечение, модифицирующее заболевание: свежезамороженная плазма (FFP), икатибант (FIRAZYR), концентрат C1-ингибитора0
0
СЗП содержит несколько ферментов, которые расщепляют брадикинин, устраняя основное заболевание ACEI-AAG.Это никогда не изучалось в проспективных РКИ. Тем не менее, существует несколько публикаций, описывающих случаи или серии случаев у пациентов с быстрым улучшением после ~ 2-4 единиц СЗП, часто после неоднократного отказа от стероидов, адреналина и антигистаминных препаратов (Karim 2002, Warrier 2004, Stewart 2012, Bolton 2012, Hassen 2013, Шибер 2014). Аналогичным образом было обнаружено, что FFP эффективен при других формах опосредованного брадикинином ангионевротического отека, таких как дефицит C1-эстеразы.0
Икатибант (FIRAZYR) — очень маленький пептид, который блокирует рецепторы брадикинина.До сих пор Икатибант поддерживался описаниями случаев и одним неконтролируемым исследованием. Икатибант имеет некоторые потенциальные преимущества перед СЗП, поскольку он сформулирован в меньшем объеме и не несет риска передачи вируса. Однако это чрезвычайно дорого (23000 долларов за 30 мг, по данным Epocrates; местные цены могут отличаться).0
0
Экаллантид (дорогой рекомбинантный белок, который ингибирует калликреин; рисунок выше) был исследован для лечения ACEI-AAG. Bernstein 2014 был прекращен досрочно из-за бесполезности, в то время как Lewis 2015 показал 10% -ное увеличение возможности раньше выписывать пациентов из отделения неотложной помощи.В целом, клинические результаты применения экаллантида не впечатляют.0
Очищенный концентрат C1-ингибитора был эффективен в описаниях клинических случаев (Nielsen 2006). Этот агент, по-видимому, более популярен в Европе и включен во французское руководство по лечению ACEI-AAG (Nosbaum 2013). В английской литературе существует только один случай, описывающий использование концентрата С1-ингибитора. В настоящее время доказательства, подтверждающие СЗП, кажутся более надежными, но в настоящее время продолжается исследование III фазы концентрата С1-ингибитора, поэтому это может измениться (NCT01843530).
0
Недавние Bas et al. исследование сравнивает Икатибант и Стероид / Антигистамин0
Недавно Bas et al. опубликовали проспективное рандомизированное контролируемое исследование в Медицинском журнале Новой Англии, в котором сравнивали икатибант с антигистаминным препаратом и 500 мг преднизолона для лечения ACEI-AAG. Эти авторы ни разу не упомянули СЗП, но вместо этого заявили, что стероид плюс антигистаминные препараты были «стандартной терапией» для ACEI-AAG. Как и следовало ожидать, Икатибант оказался более эффективным, чем стероид плюс антигистамин, со значительно более быстрым разрешением ангионевротического отека.0
Как обсуждалось выше, стероид плюс антигистаминный препарат не является «стандартной терапией» для ACEI-AAG, но фактически неэффективен. Представление о том, что стероиды и антигистаминные препараты показаны для приема ACEI-AAG, лучше всего рассматривать как миф. В Genius General Hospital мы ранее успешно лечили ACEI-AAG с помощью FFP. В настоящее время не может быть универсальной «стандартной терапии» для ACEI-AAG. Использование СЗП является спорным, но это более рациональная и научно обоснованная терапия, чем стероид плюс антигистамин.
0
Это испытание эффективно сравнивает Икатибант со стероидом / антигистаминным препаратом и плацебо. К сожалению, из-за невозможности сравнить Икатибант и СЗП это исследование не очень полезно для большинства врачей. Икатибант чрезвычайно дорог и не широко доступен. Исследование, оценивающее полезность СЗП, было бы гораздо более полезным для большинства врачей во всем мире, особенно в менее обеспеченных регионах.
0
Программа отраслевых исследований0
Возможные способы лечения ACEI-AAG включают чрезвычайно дорогие пептиды, такие как Икатибант и Экаллантид.Промышленность требует значительного финансирования и давления с целью проведения испытаний этих препаратов и продвижения их использования. К сожалению, нет никаких стимулов проводить испытания FFP. Это привело к однобокому исследовательскому подходу к ACEI-AAG: шесть испытаний, перечисленных на ClinicalTrials.gov, посвященных исследованию дизайнерских пептидов, по сравнению с нулевым исследованием FFP.
0
На сегодняшний день все исследования, спонсируемые отраслью, избегают использования FFP в качестве компаратора. На данный момент Bas 2015 продемонстрировал превосходство Икатибанта по сравнению с неэффективной терапией (стероид / антигистамин), при этом одному пациенту в контрольной группе потребовалась трахеостомия.Этика воспроизведения этого исследования вызывает сомнения, учитывая значительный риск причинения вреда пациентам, не получающим Икатибант. Тем не менее, два исследования, сравнивающих Икатибант с плацебо, перечислены как продолжающиеся (NCT01343823 и NCT011). В идеале будущие испытания должны быть направлены на сравнение Икатибанта и СЗП, а не плацебо или стероидов / антигистаминных препаратов.0
Выводы0
0
- Ангионевротический отек, вызванный ингибиторами АПФ (ACEI-AAG), может быть опасным для жизни и, вероятно, станет более распространенным с расширением использования ингибиторов АПФ.
- ACEI-AAG возникает из-за чрезмерного брадикинина. Это не поддается лечению аллергического ангионевротического отека (например, эпинефрином, стероидами, антигистаминными препаратами).
- До недавнего времени сообщения о клинических случаях предполагали, что свежезамороженная плазма (СЗП) или Икатибант могут быть эффективными для ACEI-AAG. СЗП содержит ферменты, которые метаболизируют брадикинин, тогда как Икатибант блокирует рецепторы брадикинина (рисунок выше).
- Bas et al. провели проспективное рандомизированное контролируемое исследование, в котором сравнивали Икатибант и стероид / антигистамин.Как и ожидалось, Икатибант оказался лучше.
- Икатибант чрезвычайно дорогой и не очень широко доступен. В качестве альтернативы, FFP доступен повсеместно за небольшую часть стоимости. Дополнительная информация необходима для определения относительной эффективности этих методов лечения.
- Если Икатибант недоступен, рассмотрите возможность раннего введения 2–4 единиц СЗП.
Изображение предоставлено: https://en.wikipedia.org/wiki/Compact_car#/media/File:CVC2012aaa.jpg
Джош — создатель PulmCrit.орг. Он доцент кафедры легочной медицины и реанимации в Университете Вермонта.
Последние сообщения Джоша Фаркаса (посмотреть все)Алгоритм лечения острого ангионевротического отека в экстренных случаях …
Контекст 1
… причины отека: следует дифференцировать ряд других причин, включая следующие (52): • • Гидростатический отек • • Онкотический отек • • Синдром Глайха (эпизодический ангионевротический отек, связанный с эозинофилией) • • Синдром Ашера (эпизодический отек век и губ, связанный с эутиреоидным зобом) • • Синдром Мелкерссона – Розенталя (периодический, но часто стойкий гранулематозный отек губ или щеки, трещины или трещины. складчатый язык и паралич Белла) • • Дерматит • • Целлюлит • • Венозные обструктивные заболевания (синдром верхней полой вены, тромбоз глубоких вен) • • Филяриоз При всех формах ангионевротического отека расположение дыхательных путей является первоочередной задачей при остром приступе.Все случаи отека гортани считаются неотложной медицинской помощью, и при наличии признаков нарушения дыхательных путей необходимо провести интубацию (3,68). В случае ангионевротического отека с вовлечением языка оральная интубация затруднена и часто невозможна, поэтому предпочтительным методом является назотрахеальная интубация через оптоволокно (68). Следует предупредить, что физические манипуляции с дыхательными путями во время обследования у пациентов с НАО могут потенциально увеличить количество имеющегося отека и привести к дальнейшему нарушению проходимости дыхательных путей.Способом измерения степени тяжести и риска нарушения проходимости дыхательных путей является система стадирования Ishoo, которая может прогнозировать риск обструкции дыхательных путей в зависимости от анатомического места проявления ангионевротического отека, позволяя проводить соответствующую сортировку по ED (Таблица III) (58). Дополнительный кислород следует давать всем пациентам с ангионевротическим отеком дыхательных путей, особенно если у пациента гипоксия. Алгоритм лечения острого ангионевротического отека представлен на рисунке …
Контекст 2
…. обычно они появляются после внутривенного введения адреналина с раствором, подходящим для внутримышечной инъекции (1: 1000 вместо 1: 100 000) (75,76). Этот тип ангионевротического отека не поддается лечению антигистаминными препаратами, кортикостероидами или адреналином (23). Показания к лечению острых эпизодов зависят от тяжести и локализации эпизодов ангионевротического отека. Следует лечить все эпизоды отека голосовой щели, затрагивающие шейно-лицевую или глоточно-гортанную область, а также эпизоды брюшной полости.Периферические эпизоды следует лечить с учетом их влияния на качество жизни пациента. 2.1.1. Наследственный ангионевротический отек (НАО). Консенсусные подходы к лечению HAE рекомендуют лечить приступы HAE как можно раньше (51,77). Пациенты с НАО вряд ли ответят на антигистаминные препараты или кортикостероиды. При остром приступе важно не откладывать начало лечения, особенно если место приступа опасно для жизни. (rhC1INH). Заместительная терапия C1-INH восстанавливает недостающий C1-INH (5,77).Рекомендуемая дозировка имеющихся в настоящее время препаратов составляет (2): • • Berinert® (CSL Behring, Марбург, Германия). (pdh- C1INH): 20 Ед / кг массы тела в / в. • • Cinryze ® (Viropharma, Брюссель, Бельгия). (pdhC1INH): 1000 UI внутривенно (только для детей 12 лет и взрослых) • • Ruconest® (Pharming NV, Leiden, Netherlads). (rhC1INH: Conestat alfa): 50 Ед / кг массы тела до 4200 Ед (взрослые). При необходимости дозы можно повторить, обычно через 1 час. Возможные побочные эффекты: переносятся хорошо. Основное беспокойство вызывает возможный риск передачи инфекций с учетом того, что они происходят из плазмы, хотя на сегодняшний день сообщений о передаче вирусов не поступало.Соображения: поскольку рекомбинантный препарат (Conestat alfa) производится с помощью технологии рекомбинантной ДНК в молоке трансгенных кроликов, он может вызывать аллергическую реакцию у пациентов с аллергией на кроликов. Таким образом, перед применением рекомендуется определение специфических IgE к кроличьему эпителию. Антагонист рецепторов брадикинина (икатибанта ацетат). Это синтетический декапептид, высокоспецифичный антагонист второго поколения рецептора брадикинина B2 (B2R), который ингибирует вазодилатацию, продуцируемую брадикинином.Его эффективность была показана в клинических испытаниях и в серии пациентов (78,79). Было продемонстрировано, что ранняя блокада, особенно в течение первого часа после начала атаки, значительно сокращает продолжительность атаки и время ее разрешения (78). Дозировка: Firazyr ® (Shire Orphan Therapies GmbH, Берлин, Германия) (икатибант ацетат) 30 мг (предварительно заполненные шприцы 30 мг / 3 мл). Его следует вводить подкожно. Если адекватного ответа не происходит, повторная инъекция показана через 6 часов.Не рекомендуется введение более трех доз в течение 24 часов или более восьми доз в течение 1 месяца. Его не следует применять пациентам с активной ишемической болезнью сердца или тем, кто перенес ишемический инсульт в предшествующие 2 недели (80). Нет информации о его применении у пациентов моложе 18 лет, беременных или кормящих женщин (77). Возможные побочные эффекты: о серьезных побочных реакциях не сообщалось. Единственный значительный побочный эффект — это реакции в месте инъекции, такие как эритема, отек, зуд и боль (78,79).Ингибитор плазменного калликреина (экаллантид). Экаллантид — это ингибитор калликреина плазмы, который эффективен против приступов HAE (81). Это одобрено только FDA. Его нет в Европе (77). Рекомендуемая доза составляет: Kalbitor ® (Dyax Crop. Кембридж, Массачусетс, США) 30 мг (три ампулы по 10 мг / мл), вводимые подкожно в область живота. Возможные побочные эффекты: Сообщалось о реакциях гиперчувствительности (82), включая эпизод анафилаксии (83). По этой причине рекомендуется следить за пациентом в течение нескольких часов после введения экалантида.Антифибринолитические средства. Эти препараты могут быть эффективны при приступе ангионевротического отека, но они рекомендуются только тогда, когда ранее описанные методы лечения недоступны. Нет данных, основанных на контролируемых клинических исследованиях. Используются высокие внутривенные или пероральные дозы транексамовой кислоты (Амчафибрин ®, Роттафарм, Барселона, Испания) (52,77). Это доказало свою эффективность только в продромальных фазах приступа (84). Рекомендуемая дозировка транексамовой кислоты: Амчафибрин ®: 15 мг / кг / 4 часа i.v. Если ни один из этих препаратов недоступен, альтернативой может быть свежезамороженная плазма (85). 2.1.2. Приобретенный ангионевротический отек. Главное — контролировать основное заболевание. Лечение острых приступов такое же, как и для HAE-C1INH, хотя необходимые дозы pdhC1INH могут быть выше из-за присутствия аутоантител против C1INH. Имеется небольшой опыт применения ацетата икатибанта, хотя этот агент можно использовать в случае устойчивости к pdhC1INH (86). Этот тип ангионевротического отека не реагирует на антигистаминные препараты, кортикостероиды или адреналин.2.2.1. По наследству. Основная терапевтическая мера — это профилактика без эстрогенов (51,87). Единого мнения о лечении нет, но сообщалось об отдельных случаях или небольших сериях, в которых транексамовая кислота (1-2 г / 6 часов), pdhC1INH и икатибант ацетат использовались не по назначению с хорошими результатами (87). ингибиторы. Основная терапевтическая мера — избегать антигипертензивных препаратов группы ACEi (88). БРА не следует систематически избегать у пациентов с ангионевротическим отеком, вызванным ИАПФ, хотя их применение следует контролировать (51).Механизм, лежащий в основе ангионевротического отека, вызванного ИАПФ (избыток брадикинина), аналогичен механизму, лежащему в основе HAE. По этой причине агенты, доказавшие свою эффективность при HAE, в том числе антагонист рецепторов брадикинина икатибант, в настоящее время исследуются в клинических исследованиях в качестве лечения острого ангионевротического отека, вызванного ИАПФ. Эффективность икатибанта ацетата была описана в опубликованных сериях, хотя он использовался не по назначению (89, 90). Опубликован один случай успешного лечения транексамовой кислотой (85).В случае ангионевротического отека у пациентов, принимающих ингибиторы DPP-IV, основной терапевтической мерой является отказ от препарата. Тем не менее, поскольку механизм, лежащий в основе DPP-IV-индуцированного ангионевротического отека (избыток брадикинина), аналогичен механизму, лежащему в основе ACEi и HAE, агенты, которые, как было показано, были эффективны в этих условиях, в том числе икатибант антагониста рецептора брадикинина, могут быть полезны в этом тип отека Квинке (44). 2.2.3. Идиопатический ангионевротический отек, опосредованный брадикинином. Группа идиопатического брадикинина не реагирует на профилактику или лечение антигистаминными препаратами (14) и может быть связана с повышением уровня брадикинина (46).По этой причине его нужно лечить так же, как и лежащие в основе ACEi и HAE, как показано на рисунке …
Крапивница и ангионевротический отек | Аллергия, астма и клиническая иммунология
Лечение идиопатического ангионевротического отека аналогично лечению крапивницы. Состояние хорошо поддается профилактическому назначению антигистаминных препаратов. Некоторым людям требуются кортикостероиды. Алкоголь и НПВП могут усугубить это состояние, поэтому рекомендуется избегать.
Лечение HAE и AAE включает как профилактические стратегии для предотвращения приступов ангионевротического отека, так и фармакологические вмешательства для лечения острых приступов (см. Таблицу 4).Учитывая риск смертельной асфиксии с поражением гортани, просвещение пациентов относительно лечения острых приступов является обязательным; Пациенты должны быть проинструктированы немедленно обращаться в отделение неотложной помощи при развитии отека гортани. Поскольку HAE и AAE являются редкими заболеваниями, некоторые сотрудники отделений неотложной помощи не знакомы с лечением этих состояний. Поэтому пациентам рекомендуется иметь при себе карточки бумажника (шаблоны доступны по адресу: http://www.haecanada.com/m.php?p=edownloads), которые кратко объясняют диагноз пациента, описывают указанное лечение острых приступов и предоставляют контактную информацию. информация для лечащего врача [18].У пациентов с AAE также важно лечение основного лимфопролиферативного расстройства.
Таблица 4 Обзор терапевтических вмешательств при HAE и AAE.Профилактическое лечение
Профилактическую терапию следует рассматривать у пациентов, которые переживают более одного серьезного приступа в месяц, или если лечение острых эпизодов недостаточно эффективно или недоступно. Терапевтические варианты включают: избегание триггеров, ослабление андрогенов, транексамовую кислоту и заместительную терапию плазменным ингибитором C1 [18, 24].
Факторы, вызывающие острые приступы AAE и HAE, различаются, но часто включают: легкую травму лица (особенно зубную травму), стресс / тревогу, инфекцию H. pylori , менструацию и прием препаратов, содержащих эстроген (например, заместительная гормональная терапия и контрацептивы) и ингибиторы АПФ. По возможности следует избегать этих триггеров. В некоторых случаях может потребоваться выявление и быстрое лечение инфекций полости рта и зубов, а также скрининг и искоренение инфекции H. pylori [18].
Ослабленные андрогены, такие как даназол и станозолол, повышают уровни ингибиторов C4 и C1 и эффективны как для краткосрочной, так и для долгосрочной профилактики HAE и AAE. Хотя в целом они хорошо переносятся большинством пациентов, побочные эффекты при длительном приеме андрогенов могут включать вирилизацию, нарушения сывороточных трансаминаз, нарушения менструального цикла, рост волос, снижение либидо, увеличение веса, вазомоторные симптомы, нарушения липидного обмена и депрессию. Следовательно, следует использовать самую низкую эффективную дозу (максимальные рекомендуемые длительные дозы составляют 200 мг в день для даназола и 2 мг в день для станозолола), а общий анализ крови пациента, ферменты печени и липидный профиль следует регулярно контролировать (например,г, каждые 6 месяцев) во время терапии. Противопоказания к терапии андрогенами включают: беременность, кормление грудью, рак, гепатит и детский возраст [18].
Антифибринолитический агент, транексамовая кислота, также показал свою эффективность для профилактического лечения HAE и AAE. Данные свидетельствуют о том, что она может быть менее эффективной, чем терапия андрогенами у пациентов с НАО, но более эффективна при НАО [18]. Транексамовая кислота хорошо переносится и обычно предпочтительна для долгосрочной профилактики у беременных женщин, детей и пациентов, которые не переносят андрогены.Наиболее частым побочным эффектом является диспепсия, которую можно уменьшить, принимая препарат во время еды [18].
Регулярные внутривенные инъекции заместительной терапии плазменным ингибитором C1 также эффективны как для краткосрочной, так и для долгосрочной профилактики. Эти инъекции обычно могут вводиться пациентом или опекуном дома. Текущая рекомендуемая доза составляет 20 единиц / кг; пациентам с AAE могут потребоваться более высокие дозы. Поскольку заместительная терапия ингибитором С1 является препаратом крови, важное значение имеют ежегодная гемонадзорность реципиента и отслеживание от вены к вене [18].
Лечение острых приступов
Терапия первой линии для лечения тяжелых острых приступов HAE и AAE включает: заместительную терапию ингибитором C1, экаллантидом и икатибантом [18]. Заместительная терапия ингибитором С1 — наиболее хорошо изученная терапия первой линии; его вводят «по запросу» при первых признаках приступа. Однако некоторые пациенты с AAE со временем могут перестать реагировать на это лечение; У таких пациентов следует рассмотреть возможность применения экалантида и икатибанта [24].
Экаллантид является ингибитором калликреина плазмы (фермент, высвобождающий брадикинин, основной медиатор ангионевротического отека). Недавно он был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) США для лечения приступов острого ангионевротического отека у пациентов с НАО. Обычная рекомендуемая доза составляет 30 мг подкожно (взрослым). Хотя побочные эффекты экаллантида обычно незначительны (например, реакции в месте инъекции, головная боль, тошнота, усталость, диарея), эта терапия была связана с редкими случаями аллергических реакций и анафилаксии.Следовательно, его должен назначать только врач в медицинских учреждениях, оборудованных для лечения анафилаксии и тяжелого ангионевротического отека [18].
Икатибант — блокатор рецепторов брадикинина, одобренный в Европейском Союзе для лечения острых приступов НАО. Обычная рекомендуемая доза для взрослых составляет 30 мг подкожно; педиатрический опыт с этим агентом все еще ожидается. Наиболее частыми побочными эффектами икатибанта являются легкие и преходящие реакции в месте инъекции. К другим, менее частым побочным эффектам относятся: тошнота, расстройство желудочно-кишечного тракта, астения, головокружение и головная боль [18].
Понимание и лечение ангионевротического отека в отделении неотложной помощи | 2016-11-30 | AHC Media
После завершения этого учебного мероприятия участники должны быть в состоянии распознать и продемонстрировать понимание ангионевротического отека, обсудить как дифференциальный диагноз, так и ряд осложнений, связанных с этим состоянием, а также применить современные диагностические и терапевтические методы при оценке. и лечение ангионевротического отека в отделении неотложной помощи (ED).
ВведениеАнгионевротический отек — это отек глубоких кожных, подкожных и подслизистых тканей из-за повышенной проницаемости сосудов.Первое подробное описание отека Квинке было задокументировано в 1876 году доктором Джоном Лоусом Милтоном из Лондона, который первоначально назвал это состояние «гигантской крапивницей». В 1882 году Генрих Квинке дал другое описание ангионевротического отека, которому впоследствии было дано первоначальное название «ангионевротический отек». 1 В 1888 году Уильям Ослер идентифицировал наследственный ангионевротический отек (HAE) как отдельное заболевание после изучения семьи с приступами ангионевротического отека, охватывающего пять поколений, а в 1963 году Дональдсон и Эванс сообщили о причине HAE как снижение уровней ингибитора C1-эстеразы ( тип I). 1-4 Была обнаружена вторая форма HAE с нормальным уровнем ингибитора C1-эстеразы, но с аномальной функцией, что привело к открытию, что обе формы были связаны с мутацией в гене ингибитора C1 ( SERPING1 ) (тип II). Однако была обнаружена новая форма HAE с нормальным SERPING1 . 1
Помимо наследственной недостаточности ингибитора C1, существуют также приобретенные типы. Считается, что они являются вторичными по отношению к аутоантителам, возникающим в результате существующих болезненных процессов, при этом лимфопролиферативные нарушения являются наиболее распространенной этиологией. 1 Дополнительные формы включают ангионевротический отек, индуцированный ингибитором ангиотензин-превращающего фермента (АПФ), и негистаминергический идиопатический ангионевротический отек. Объединяющая тема для этих вариантов вращается вокруг регуляции брадикинина. Другая форма ангионевротического отека является гистаминовым, что проявляется при острых аллергических реакциях и анафилаксии.
Пептид брадикинин и амин гистамин являются мощными вазодилататорами, и их избыточные уровни могут вызвать проницаемость сосудов. Эта сосудистая проницаемость может привести к временному отеку в глубоких слоях дермы и подкожных слоях кожи, а также в подслизистом слое дыхательных путей и желудочно-кишечного тракта.Ангионевротический отек, также известный как ангионевротический отек и отек Квинке, описывает отек, который возникает в этих конкретных слоях ткани, вторичный по отношению к условиям избытка гистамина или брадикинина. 5
Обычно ангионевротический отек без ямок, может быть телесного цвета или эритематозным и часто возникает на участках с дряблой кожей (например, на лице, гениталиях). ( См. Рисунки 1 и 2. ) При припухлости могут присутствовать тепло и боль, но, как правило, это не зуд. 2 Подобный тип реакции наблюдается при крапивнице; однако крапивница — это отек из-за проницаемости сосудов, которая возникает в более поверхностных слоях кожи.Обычно это зуд. Врачам скорой помощи важно знать сходства и различия между крапивницей и ангионевротическим отеком. ( См. Таблицу 1. )
Рисунок 1. Крапивница конечностей
На этой фотографии пациента показаны локализованные эритематозные волдыри, типичные для крапивницы. Воспроизведено с разрешения The Urtikaria Network
© www.urtikaria.net.
Рисунок 2. Ангионевротический отек губ
Эта фотография пациента демонстрирует локализованный отек подслизистой оболочки, наблюдаемый при обострении ангионевротического отека.
Воспроизведено с разрешения The Urtikaria Network © www.urtikaria.net.
Расположение | Только скин | Кожа и слизистые оболочки, особенно веки и губы |
Продолжительность | Переходный (обычно длится | Переходный (обычно длится 24-48 часов) |
Физические знаки | Красные пятна и волдыри | Отек розового или телесного цвета |
Признаки | Обычно ассоциируется с зудом Боль и нежность нечасто | Может вызывать зуд, а может и нет Может сопровождаться болью и нежностью |
Патология | Обширное расширение сосудов, небольшой отек и редкий периваскулярный инфильтрат, состоящий в основном из нейтрофилов, эозинофилов, моноцитов и Т-лимфоцитов в сосочковом слое дермы | Обширный отек, незначительное расширение сосудов и незначительный клеточный инфильтрат или его отсутствие, за исключением аллергического ангионевротического отека, когда эозинофилы могут быть обнаружены в ретикулярном кожном, подкожном / подслизистом слоях |
Наследственный ангионевротический отек. HAE с дефицитом C1-INH является аутосомно-доминантным заболеванием с почти полной пенетрантностью и не имеет склонности к полу или расе. Тип I составляет примерно 85% случаев, а остальные относятся к типу II. Распространенность НАО составляет от 1: 30 000 до 1: 80 000 от общей популяции. 1 Около 20-25% случаев типа I вызваны спонтанной мутацией. 5 Напротив, HAE с нормальным C1-INH (ранее HAE типа III) также является аутосомно-доминантным, но с преобладанием у женщин.( См. Таблицу 2. ) Данные о населении в настоящее время не существуют из-за отсутствия четких диагностических критериев. У мужчин с этим заболеванием есть менее тяжелая версия. 1 Причина HAE с нормальным C1-INH неизвестна, но это может быть связано с ошибками в гене фактора XII. 5,6
Таблица 2. Типы ангионевротического отека
1,2Синдром | Патофизиология | Пострадавшие | Распространенность | C4 Уровень | Антиген C1-INH | C1-INH Функция | C1q Уровень |
Тип I HAE | Мутация в гене SERPING1 , вызывающая дефицит ингибитора C1 | Все | ~ 1: 50 000 | Низкая | Низкая | Низкая | Обычный |
Тип II HAE | Мутация в гене SERPING1 , вызывающая функциональную недостаточность ингибитора C1 | Все | ~ 1: 250 000 | Низкая | Обычный | Низкая | Обычный |
HAE с нормальным C1-INH (ранее называлось HAE типа III) | Неизвестно | Все, но намного больше женщин | Неизвестно | Обычный | Обычный | Обычный | Обычный |
Приобретенный дефицит C1-INH | Чрезмерное потребление ингибитора С1, приводящее к дефициту | Пациенты пожилого возраста | ~ 1: 250 000 | Низкая | Низкая | Низкая | Низкая |
Индуцированный ингибитором АПФ | Ингибирование катаболизма брадикинина | Все, но увеличилось у афроамериканцев | ~ 1: 250 | Обычный | Обычный | Обычный | Обычный |
Аллергический | Сенсибилизация тучных клеток IgE | Все | Неизвестно | Неизвестно | Неизвестно | Неизвестно | Неизвестно |
Идиопатический | Сенсибилизация тучных клеток IgG, связанная с аутоиммунным заболеванием щитовидной железы | Все | Неизвестно | Неизвестно | Неизвестно | Неизвестно | Неизвестно |
Негистаминергические идиопатические | Неизвестно | Неизвестно | Неизвестно | Обычный | Обычный | Обычный | Обычный |
HAE типов I и II вызваны дефицитом C1-INH 1 , вызванным мутациями в гене SERPING1 .C1-INH регулирует многие протеазы. Он участвует в ингибировании классического пути комплемента, кинина, плазмина и систем свертывания крови. 7 C1-INH делает это путем объединения с целевой протеазой с образованием составной протеазы, которая выводится как единое целое. HAE типа I и II являются аутосомно-доминантными заболеваниями, в настоящее время зарегистрировано более 280 различных мутаций гена SERPING1 . Тип II почти исключительно вызван миссенс-мутациями, вызывающими выработку C1-INH, неспособного образовывать сложную протеазу. 1,7
Тип I может быть любым типом мутации, приводящей к недостатку C1-INH, что, в свою очередь, приводит к избытку брадикинина как причине отека, в то время как другой причастной причиной отека является избыток кинина C2. 1,7 Уровни этих двух пептидов повышаются при отсутствии ингибирования. Эти пептиды действуют на посткапиллярную венулу, заставляя эндотелиальные клетки втягиваться, образуя пространство, через которое плазма может просачиваться и в конечном итоге накапливаться в виде отека. 7 Оба этих типа ангионевротического отека, по-видимому, активируют каскад комплемента без использования C1q (первый подкомпонент комплекса C1), о чем свидетельствуют лабораторные исследования, демонстрирующие нормальные уровни C1q и пониженные уровни C4.
Патофизиология HAE с нормальным C1-INH (ранее называвшаяся HAE типа III) изучена недостаточно. Однако примерно у 25% этих пациентов были обнаружены мутации фактора XII. Увеличение брадикинина не было доказано, но сообщения о случаях показали, что лечение, направленное на подавление выработки брадикинина, было наиболее успешным в уменьшении отека. 1
Приобретенный ангионевротический отек. Приобретенный ангионевротический отек (АК) также связан с дефицитом C1-INH; однако этот недостаток не является следствием какой-либо генетической мутации.АА наблюдается у пациентов среднего и старшего возраста с распространенностью от 1: 100 000 до 1: 500 000, хотя статистика населения может быть неточной из-за неправильной диагностики случаев. 1 Были описаны два типа приобретенного дефицита C1-INH, оба вызванные непропорциональным смешиванием и выведением C1-INH по сравнению с продуцированным количеством. Это часто является вторичным по отношению к основному заболеванию, вызывая постоянную активацию пути комплемента (тип I). 1 Наиболее распространенными заболеваниями являются лимфопролиферативные состояния.Однако пациенты с AA также могут продуцировать аутоантитела против C1-INH, которые вызывают его расщепление до неактивной формы без инактивации протеаз, с которыми они связываются (тип II). Поскольку нет прогностической разницы между приобретенным C1-INH с аутоантителами или без них, диагностическое различие между этими двумя типами больше не существует. Это снижение C1-INH неизменно приводит к повышению уровня брадикинина. Следует отметить, что АА отличается от наследственных типов тем, что потребляет как C1q, так и C4 при активации каскада комплемента.
Ингибитор АПФ и лекарственный ангионевротический отек. Ингибиторы АПФ — это обычно назначаемый класс гипотензивных средств. Ангионевротический отек, вызванный ингибиторами АПФ, встречается у 0,2–0,7% пациентов, принимающих эти лекарства, с гораздо более высоким риском для афроамериканцев. Фактически, это заболевание встречается у афроамериканцев в пять раз чаще, чем у белых. 2 Существует также повышенный риск для пациентов, принимающих иммуносупрессивную терапию, которые курили в анамнезе, старше или являются женщинами. 1,8-10 Одно многоцентровое исследование показало, что ангионевротический отек, вызванный ингибиторами АПФ, составляет около одной трети пациентов с ангионевротическим отеком, обращающихся в отделение неотложной помощи, но на их долю приходилось только 0,7 случая на 10 000 посещений отделения неотложной помощи. 11
Ангиотензин-превращающий фермент расщепляет брадикинин и вещество P до неактивных белков. Логично предположить, что препараты ингибиторов АПФ вызывают повышение уровня брадикинина. Уровень предрасположенности пациентов к ангионевротическому отеку может зависеть от наличия других ферментов, расщепляющих брадикинин.Дипептидилпептидаза 4 (DPP-4) является одним из таких ферментов. Пациенты, принимающие как ингибиторы АПФ, так и ингибиторы ДПП-4, класс пероральных гипогликемических препаратов, включая ситаглиптин, используемый для лечения диабета, имеют более высокий риск развития ангионевротического отека. Иммунодепрессанты также могут вызывать снижение DPP-4, что может объяснить повышенный риск ангионевротического отека у этих пациентов. 1,8-10 Однако механизм ангионевротического отека с ингибиторами АПФ не считается иммунологическим, поскольку приступы могут произойти в течение нескольких минут или лет после первого приема этих лекарств. 12 Еще одно лекарство, которое влияет на этот же путь, — это тромболитическая альтеплаза, которая активирует кинин и, как было показано, вызывает оролингвальный ангионевротический отек после использования при лечении пациентов с острым инсультом. 13 Таким образом, следует соблюдать осторожность при совместном применении этих препаратов, поскольку значительно возрастает вероятность отека Квинке.
Аллергический ангионевротический отек. Аллергический ангионевротический отек возникает из-за реакции гиперчувствительности немедленного типа I. Он может проявляться отдельно или с другими признаками и симптомами анафилаксии и является результатом опосредованного IgE высвобождения гистамина и других медиаторов из тучных клеток и базофилов. 5 Роль гистамина в организме в первую очередь иммунологическая, и из четырех известных рецепторов гистамина типы 1 и 2 активны, вызывая расширение сосудов, проницаемость сосудов и накопление жидкости в интерстиции, что в конечном итоге приводит к развитию ангионевротического отека. 4 Аллергический ангионевротический отек считается одной из наиболее часто встречающихся форм; Фактически, исследование 2007 года, проведенное Университетом Махидол в Таиланде, показало, что примерно 45,7% всех включенных в исследование пациентов страдали аллергическим ангионевротическим отеком, из них 41.7% этих случаев вызваны продуктами питания и 39,6% — наркотиками. 14
Идиопатические и другие типы ангионевротического отека. Идиопатический ангионевротический отек может возникнуть в любом возрасте, но чаще всего встречается в возрастной группе от 40 до 50 лет. Женщины страдают чаще, чем мужчины, хотя при отсутствии крапивницы это может быть чаще у мужчин. 2 Конкретная причина хронического идиопатического ангионевротического отека неизвестна, но эпизоды могут повторяться в течение пяти и более лет, а риск возникновения осложнений со стороны дыхательных путей крайне низок. 5
Негистаминергический идиопатический ангионевротический отек используется для описания рецидивирующего ангионевротического отека у пациентов, которые не реагируют на высокие дозы антигистаминных препаратов, не имеют семейной истории ангионевротического отека и имеют повышенный уровень брадикинина. Причина этих повышенных уровней брадикинина в настоящее время не совсем понятна, и этот диагноз ставится только после того, как все другие исследования не смогли объяснить повторяющиеся симптомы у пациентов, перенесших три или более приступов в течение 6–12 месяцев. 1,15 Считается, что другие формы ангионевротического отека, связанные с вибрацией, экстремальными температурами или солнечным излучением (часто сопровождающиеся крапивницей), опосредованы гистамином через дегрануляцию тучных клеток, вторичную по отношению к этим физическим стимулам. В этих случаях антигистаминные препараты могут обеспечить эффективное лечение. 16-18
ОсложненияСуществует множество проявлений ангионевротического отека, в основном из-за сложности и диапазона причин болезненного процесса.Локализация и тяжесть ангионевротического отека зависят от его типа и степени поражения у каждого пациента. Таким образом, осложнения этого заболевания варьируются от просто неприятных, таких как отек конечностей, до опасных для жизни; ангионевротический отек может вызвать значительную заболеваемость и смертность.
Боль в животе относительно часто встречается при НАО. Одно исследование показало, что 153 пациента с НАО сообщили о 33 671 приступе боли в животе за свою жизнь. 19 Другое ретроспективное исследование пациентов с НАО показало, что 195 из 209 пациентов имели рецидивирующие боли в животе, в общей сложности 62 503 приступа брюшной полости. 20 Боль в животе, вторичная по отношению к отеку Квинке, может быть связана с тошнотой, рвотой, диареей, симптомами гипотонии и асцитом. Некоторые сопутствующие симптомы, которые встречаются реже, включают дизурию, геморрагическую диарею, тетанию и инвагинацию; пациенты также могут испытывать шок кровообращения из-за гиповолемии. 19 Абдоминальные симптомы в первую очередь возникают из-за висцерального дискомфорта, вторичного по отношению к отеку стенки кишечника. Таким образом, важно рассматривать ангионевротический отек как потенциальную причину острой боли в животе при ЭД.Знание о том, что у пациента есть личный или семейный анамнез ангионевротического отека или риски для этого заболевания (например, использование ингибитора АПФ), может помочь предотвратить ненужное хирургическое вмешательство. 21
Наиболее опасным и непосредственным осложнением ангионевротического отека является нарушение дыхательных путей. Пациенты, наиболее подверженные риску нарушения проходимости дыхательных путей, включают пациентов с признаками отека лица, губ, гортани, язычка и языка. Отек в этих областях может перерасти в субъективную или объективную одышку, затруднение речи (т.е., горячий картофельный голос), стридор и возможная потеря дыхательных путей. Эти начальные признаки и симптомы нарушения дыхательных путей необходимо своевременно распознавать, чтобы способствовать быстрым и потенциально спасающим жизнь действиям.
Дифференциальная диагностикаСуществует множество болезненных процессов, которые можно принять за отек Квинке. В таблице 3 перечислены некоторые из них, включая как редкие, так и распространенные состояния.
Таблица 3. Дифференциальный диагноз ангионевротического отека: псевдоангионевротический отек
2,27-30Болезнь | Клинические признаки отличия от AE |
Целлюлит лица | Индуцированный, болезненный, часто связанный с лихорадкой, может сохраняться в течение 9000 дней. |
Острый контакт: аллергический или фотодерматит | Связано с воздействием в анамнезе, зудом, везикуляцией, длится более 24-48 ч, гиперчувствительность IV типа |
Болезнь Крона рта и губ | Вызывает гранулематозный отек губ, осложненный лимфедемой У пациентов часто наблюдается утолщение слизистой оболочки щеки булыжником |
Синдром гипокомплементемического уртикарного васкулита (HUVS) | Лейкоцитокластический васкулит, тяжелый ангионевротический отек, отек гортани, связанный с хронической обструктивной болезнью легких, артритом, артралгией, гломерулонефритом и увеитом Наличие антител против C1q |
Дерматомиозит, системная красная волчанка, полимиозит, синдром Шегрена | Обращает внимание на гелиотропный (фиалковый) отек век (только дерматомиозит), малярную сыпь, светочувствительность, язвы во рту и артралгии |
Гидростатический отек | Накопление отека мягких тканей в результате повышенного гидростатического давления в капиллярах, вызванного различными причинами, включая сердечную недостаточность |
Туманная дискоидная волчанка | Красные отечные бляшки на освещенных светом участках лица; настойчивый; может вызвать рубцевание |
Синдром Ашера | Рецидивирующие эпизоды отека век, приводящие к блефарохалазу |
Синдром Мелкерссона-Розенталя | Стойкий гранулематозный отек губ; может быть связан с lingua plicata и / или параличом Белла |
Синдром верхней полой вены | Отек век и губ, связанный с венозным набуханием |
Синдром Глейха: эпизодический ангионевротический отек с эозинофилией | Присутствует при лихорадке, увеличении веса, эозинофилии, повышенном содержании основного основного белка в сыворотке |
Синдром Шницлера: макроглобулинемия, вторичная по отношению к моноклональным IgM | Крапивница и отек без зуда, лихорадка, боль в костях, повышенная скорость оседания эритроцитов |
Синдром Макла-Уэллса | Периодические приступы крапивницы, лихорадки и болей в конечностях, прогрессирующая глухота восприятия нерва, амилоидоз почек, аутосомно-доминантный признак |
Гранулематозный хейлит / хейлит Михера | Идиопатические эпизоды повторяющихся отеков, приводящие к необратимому увеличению губ |
Гипотиреоз | Отечность лица и губ; холодная, сухая кожа; сухие, жесткие, ломкие волосы; претибиальная микседема |
Трихинеллез | Периорбитальный отек, употребление в пищу сырого / недоваренного мяса в анамнезе, миалгии, боли в животе, диарея, рвота |
Филяриальные паразиты | Лимфангит, который выглядит как хроническая отечная припухлость нижних конечностей, локализованные области отека, где в подкожных тканях живут взрослые черви, история посещения Центральной / Западной Африки |
Лимфедема лица | Классически ассоциируется с розацеа или, реже, синдромом Мелкерссона-Розенталя |
Онкотический отек | Накопление отека мягких тканей из-за снижения осмотического давления коллоидов плазмы, вторичного к гипопротеинемии, часто связанного с заболеванием печени или почек |
На догоспитальном этапе лечение отека Квинке должно быть сосредоточено на ABC (дыхательные пути, дыхание, кровообращение).В зависимости от этиологии и локализации у пациентов может развиться гемодинамический коллапс и нарушение проходимости дыхательных путей. Пациентам с гемодинамическими или респираторными изменениями потребуется немедленный кардиологический мониторинг, непрерывная пульсоксиметрия и капнография, если таковые имеются, и они должны получить две внутривенные инъекции большого диаметра, дополнительный кислород и распыленные бета2-агонисты по показаниям (т. Е. Наличие признаков бронхоспазма). Пациенты с известным или возможным аллергическим ангионевротическим отеком, связанным с анафилактическим шоком, должны получить немедленный внутримышечный (IM) адреналин, а также внутривенные (IV) жидкости и добавки с внутривенным или внутримышечным введением антигистаминных препаратов и стероидов.Обеспечение проходимости дыхательных путей на догоспитальном этапе (включая интубацию или другие процедуры прохождения дыхательных путей, как указано и основано на обучении медицинских работников и местных протоколах) следует проводить, если пациент теряет дыхательные пути из-за отека Квинке.
Оценка EDПациенты с ангионевротическим отеком должны быть быстро отсортированы с оценкой жизненно важных функций, а также проходимости дыхательных путей и стабильности гемодинамики. Немедленно обеспокоенных или нестабильных пациентов, включая пациентов с аномальными жизненно важными показателями или отеком головы и / или шеи, следует немедленно помещать в отделение неотложной помощи, особенно в палаты реанимации, как указано.Следует начать неотложный кардиологический мониторинг, непрерывную пульсоксиметрию, маневры дыхательных путей и внутривенный доступ с соответствующей медикаментозной терапией. Пациенты, которые стабильны с нормальными жизненно важными показателями и не имеют признаков или риска нарушения дыхательных путей или кровообращения, не нуждаются в немедленной подстилке ЭД, но должны регулярно проходить повторную оценку, пока они не будут полностью обследованы.
ИсторияИстория ED имеет жизненно важное значение для определения причины и надлежащего ведения каждого проявления ангионевротического отека.Информация, включая время начала, продромальный период, прогрессирование, воздействие и сопутствующие симптомы, будет иметь важное значение для выявления. Врачам неотложной помощи следует узнать о пораженных участках отека, таких как губы или язык, а также о любых изменениях голоса или ощущении одышки или закрытия горла. Другой анамнез включает в себя текущие лекарства, предшествующие эпизоды или семейный анамнез ангионевротического отека, недавние процедуры или травмы, а также общий медицинский анамнез пациента. 3
Медицинский осмотрБолее часто поражаются области тела, включая лицо и конечности, а также желудочно-кишечный тракт (ЖКТ), как обсуждалось ранее, особенно если у пациента в анамнезе имеется наследственный ангионевротический отек.Крапивница и зуд могут сопровождать аллергический ангионевротический отек, но такие признаки и симптомы редко проявляются при других формах. Нарушение проходимости дыхательных путей является наиболее серьезным осложнением ангионевротического отека, и его оценка должна иметь первостепенное значение во время физического осмотра и оценки ЭД. В дополнение к визуальному осмотру на предмет сыпи и отеков, сотрудники службы неотложной помощи могут оценить признаки отека дыхательных путей, выслушивая и выслушивая характерные изменения, такие как охриплость, стридор, хрипы и ненормальные спровоцированные жужжание и звуки голоса. 3
Диагностическая оценкаОсновное внимание при оценке ЭД и лечении отека Квинке уделяется определению наличия и степени поражения дыхательных путей, а также оценке причин, которым может помочь неотложная медицинская помощь, таких как аллергическая и наследственная этиология. При отсутствии лечения любой обструктивный ангионевротический отек верхних дыхательных путей приводит к смертности от 25 до 40%. 3 Аналогичным образом, оценки пожизненной смертности от наследственного ангионевротического отека достигают 30%, при этом обструкция дыхательных путей является основной причиной смерти. 22
Истинную этиологию любого проявления ангионевротического отека часто трудно установить в отделении неотложной помощи, и существует ограниченное количество тестов для экстренной диагностики, которые могут помочь в оценке таких пациентов. Таким образом, клиническая оценка врачом неотложной помощи дыхательных путей и гемодинамической стабильности этих пациентов всегда должна иметь приоритет.
Оценка наличия или отсутствия отека дыхательных путей предпочтительно включает прямую визуализацию с помощью видеоларингоскопии в бодрствующем состоянии или фиброоптической назофарингоскопии, если это возможно.В 2010 году Saxena et al. Продемонстрировали, что о наличии и уровне отека дыхательных путей трудно судить только на основании истории болезни и клинического внешнего вида пациента, и что надгортанный отек часто не коррелирует с отеком языка. 23 При наличии соответствующего оборудования и обучения врачи неотложной помощи могут использовать видео- и оптоволоконную технику для быстрой оценки отека гортани и надгортанника у бодрствующих и находящихся в вертикальном положении пациентов, не требуя дополнительных средств, кроме местного анестетика в виде спрея или геля (также могут вводить лидокаин через небулайзер) для улучшения переносимости пациентом.Однако, если такое оборудование недоступно, и врач считает, что состояние пациента стабильно без риска острой декомпенсации, для оценки отека дыхательных путей можно использовать компьютерную томографию (КТ). Менее чувствительные или надежные методы оценки отека дыхательных путей включают простую рентгенографию, ультрасонографию гортани и непрямую ларингоскопию с использованием зеркала (могут быть полезны, но обычно не доступны в отделениях неотложной помощи). Если пациент очень стабилен и консультация доступна немедленно, опыт консультантов, таких как отоларинголог и анестезиолог, может быть рассмотрен для дальнейшей помощи в оценке отека дыхательных путей и для руководства лечением и диспансеризацией.
КТ и ультрасонография могут быть полезны при оценке отека кишечной стенки и асцита, которые можно увидеть у 93% пациентов с наследственным ангионевротическим отеком. КТ с контрастированием — это метод выбора для диагностики кишечного ангионевротического отека. 24,25 Обычная рентгенография, КТ и УЗИ также могут быть полезны при оценке пациентов с острой гипоксией на наличие отека легких как осложнения НАО. 26
Лабораторная оценка отека Квинке редко дает своевременную информацию в отделении неотложной помощи; однако важно упорядочить уровни C1-INH во время острого приступа у пациентов с подозреваемым, но не диагностированным НАО.Другое тестирование можно сделать во время поступления. Тестирование комплемента на HAE часто начинается с анализа сывороточного C4. Если уровень C4 составляет менее 30% от нормы, впоследствии проверяется уровень и функция C1-INH. Низкий уровень и функция C1-INH указывают на HAE типа I, нормальный уровень C1-INH, но низкая функция указывает на HAE типа II, а нормальный уровень и функция C1-INH в условиях известного семейного анамнеза ангионевротического отека определяет HAE с нормальным C1-INH. Однако скрининговые тесты C4 не продемонстрировали стабильно низкие уровни у пациентов с НАО, что поставило под сомнение надежность этого метода скрининга. 31
Дополнительное тестирование комплемента включает оценку уровней C1q для дифференциации наследственного (нормальный C1q) и приобретенного типа I (снижение C1q) ангионевротического отека. Наличие аутоантител против C1-INH необходимо при диагностике приобретенного ангионевротического отека II типа. Диагностика наследственных и приобретенных случаев ангионевротического отека требует высокого уровня подозрительности со стороны врача, а постановка диагнозов исторически откладывалась. В 1977 году средняя задержка в диагностике НАО составляла 22 года от появления симптомов до постановки диагноза, а более свежие данные за 2013 год показали, что диагностическая задержка составляет около 8 лет.5 лет. 32,33
В настоящее время не существует установленного теста для диагностики ангионевротического отека, вызванного ингибиторами АПФ, который в настоящее время является клиническим диагнозом, несмотря на доказательства предрасположенности. Аллергический ангионевротический отек можно оценить с помощью измерения уровня триптазы в сыворотке крови, чувствительного маркера дегрануляции тучных клеток, который увеличивается во время обострений, а также более специфического тестирования IgE, как указано. 34
ED Управление и общее лечениеПервоначальная оценка ED пациентов с ангионевротическим отеком предоставит жизненно важную информацию о сердечно-легочной стабильности этого пациента.( См. Рисунки 3 и 4. ) Пациентам, у которых наблюдается какой-либо риск или нарушение дыхательных путей или гемодинамики, следует немедленно получить внутривенный доступ, дополнительный O 2 , непрерывную пульсоксиметрию, капнографию (при ее наличии) и кардиомонитор. По мере того, как медработники проводят первичное обследование, необходимо должным образом исследовать дыхательные пути, чтобы обеспечить проходимость, и, в случае нарушения, следует быстро принять решение относительно того, когда и как следует обеспечить безопасность дыхательных путей. После этого момента принятия решения и последующего лечения определение типа ангионевротического отека будет определять лечение.( См. Таблицу 4. ) Если тип ангионевротического отека неизвестен и врач скорой помощи считает, что у пациента может быть анафилактическая реакция, введите адреналин 0,01 мг / кг в / м в концентрации 1 мг / мл (до 0,3 мг у детей и 0,5 мг. мг у взрослых). (Обратите внимание, что по состоянию на май 2016 года адреналин 1: 1000 обозначается как 1 мг / мл). Пероральные (пероральные), внутривенные или внутримышечные антагонисты h2 (например, дифенгидрамин 50 мг) и кортикостероиды перорально, внутривенно или внутримышечно (например, солюмедрол внутривенно от 1-2 мг / кг до 125 мг / доза) будут эффективно лечить аллергический ангионевротический отек. но также может использоваться для лечения людей с ангионевротическим отеком неизвестной этиологии.Может быть добавлен пероральный или внутривенный антагонист h3, такой как фамотидин, если потенциальные гистаминергические симптомы не уменьшаются одними антагонистами h2. 36-38
Рисунок 3. Алгоритм ангионевротического отека дыхательных путей
Рисунок 4. Алгоритм лечения
35,37,49-51Таблица 4. Лечение острых приступов НАО и приобретенного ангионевротического отека
2,36,38,44-47Лекарство | Фирменное наименование | Механизм действия | Доза | Путь введения | Разрешено для самостоятельного управления? | Время облегчить симптомы | Побочные эффекты |
Произведенный из плазмы C1-INH | Беринерт | Замена C1-INH | 20 Ед / кг 500-1000 ЕД при менее тяжелых приступах | IV | Есть | 30 мин (высокая доза) | Анафилаксия, риск инфекций, передающихся через кровь |
Cinryze | Замена C1-INH | 1000 ЕД, 2-я доза через 1 час | IV | Есть | 4 часа | Анафилаксия, риск заражения через кровь. | |
rhC1-INH | Ruconest, Рюцин | Замена C1-INH | 50 Ед / кг или 4200 U | IV | № | 90 мин. | Анафилаксия у кроликов-сенсибилизированных |
Икатибант | Фиразыр | Антагонист рецептора брадикинина В2 | 30 мг каждые 6 часов 90 мг макс / 24 часа | SC | Есть | 2 часа | Преходящая эритема, волдыри / боль в месте инъекции |
Экаллантид | Калбитор | Ингибитор калликреина | 30 мг каждые 1 час 60 мг макс / 24 часа | SC | № | 90 мин. | Анафилаксия, антитела к лекарствам |
FFP | Замена C1-INH | 1-3 U | IV | № | 45 мин. | Обострение ХСН, возможно усиление симптомов |
Пациенты, получающие терапию бета-блокаторами, могут не реагировать эффективно на адреналин внутримышечно, и им могут потребоваться дозы глюкагона для снижения активности их бета-блокаторов и обеспечения полного эффекта любого введенного адреналина (1-5 мг глюкагона внутривенно в течение пяти минут в течение взрослым, также можно давать в виде настоя). 39
Небулизированный рацемический адреналин (0,5-0,75 мл 2,25% раствора, смешанного с 2-3 мл физиологического раствора) был предложен для временного уменьшения отека полости рта и гортани при подготовке к вмешательству на дыхательных путях. 40 Пациентам с гипотензией или гемодинамической нестабильностью следует вводить агрессивные внутривенные жидкости и прессоры.
Пациентам со значительным отеком полости рта и дыхательных путей может потребоваться эндотрахеальная интубация.( См. Рис. 5. ) Надгортанные устройства для спасения, такие как ларингеальные дыхательные пути (LMA) и трубки King Laryngeal Tubes, имеют ограниченное применение и повышенный риск неудач при остром ангионевротическом отеке из-за возможности поражения голосовых связок и надгортанника. Фиброоптическая назотрахеальная интубация в сознании — неизменно предпочтительный метод интубации пациентов с острым ангионевротическим отеком полости рта. 41 Техники интубации в бодрствующем состоянии с использованием седативных средств и местных анестетиков являются предпочтительными, поскольку они позволяют пациентам как можно дольше защищать свои дыхательные пути, пока эндотрахеальная трубка вводится в трахею.Для сравнения, стандартная оротрахеальная интубация с быстрой последовательностью (RSI) с использованием индукционных и паралитических препаратов вызывает расслабление отечного надгортанника и других внутриротовых тканей, которые могут провисать и мешать обзору ларигноскописта. Такое снижение видимости значительно снижает вероятность успешного прохождения эндотрахеальной трубки и может привести к катастрофическому сценарию «не может интубировать, не может вентилировать». У таких пациентов RSI следует применять с осторожностью.
Рис. 5. Интубированный пациент с ангионевротическим отеком полости рта
Фотография воспроизведена с разрешения West Indian Medical Journal .
Попытки оптоволоконной интубации в бодрствующем состоянии могут быть выполнены либо в отделении неотложной помощи, либо в операционной, и, если это возможно, требуют вмешательства анестезиолога и хирургического персонала. Врач должен быть готов к экстренной крикотиротомии. 35,41,42 Тележка с труднопроходимыми дыхательными путями, если таковая имеется, должна находиться у постели больного, чтобы обеспечить различные варианты прохождения дыхательных путей. Видеоларингоскопы и оборудование для волоконно-оптической интубации, если таковые имеются, могут быть полезны. Недавнее исследование Chomansky et al. Показало уменьшение времени до интубации при ангионевротическом отеке дыхательных путей с помощью видеоларингоскопа по сравнению с фиброоптической назотрахеальной интубацией, а также отсутствие статистических различий в попытках первого прохождения, хотя это не было подтверждено в более крупном исследовании. 43
В 1999 году, чтобы помочь поставщикам медицинских услуг в принятии решений по поводу ангионевротического отека дыхательных путей, Ishoo et al. Опубликовали систему стадий, определяющую лечение и устранение ангионевротического отека, основанную на локализации отека дыхательных путей пациента. Пациенты с изменениями только лица и губ считались стадией I, и стадия повышалась по мере приближения отека к гортани, со стадией II для отека мягкого неба, стадией III для отека языка и стадией IV для отека гортани. Стадия III обычно (67%) и стадия IV всегда (100%) требовали госпитализации в ОИТ, а острое вмешательство на дыхательных путях потребовалось у 7% пациентов со стадией III и 24% пациентов со стадией IV. 48 Совсем недавно Чиу и др. Создали алгоритм интубации, основанный на системе оценки степени ангионевротического отека на момент обращения к пациенту. 35 Они использовали три следующих классификации: тип 1, ограниченный лицом и ротовой полостью, за исключением дна рта; тип 2, отек дна ротовой полости и / или ротоглотки; и тип 3, отек ротоглотки, который распространился на надгортанные / голосовые структуры. ( См. Рисунок 3. )
При лечении наследственного ангионевротического отека антигистаминные препараты и кортикостероиды не влияют на патологию заболевания, 2 , но они также вряд ли окажут негативное влияние на пациента.Таким образом, описанный выше эмпирический подход, если он инициирован в ED, не является ни вредным, ни необоснованным. В прошлом свежезамороженная плазма (СЗП) и концентрат С1-ингибитора были основой лечения НАО; однако сейчас доступны более новые методы лечения. СЗП успешно лечит НАО, если в его состав входит C1-INH. Его дозируют от 1 до 3 единиц (ЕД), и он помогает облегчить симптомы в течение 45 минут. 45-47 Тем не менее, у некоторых пациентов после приема СЗП наблюдается рост отеков, поэтому его не рекомендуется применять при опасном для жизни отеке гортани. 3 Beinert представляет собой концентрат C1-ингибитора, который вводится внутривенно в различных дозах, в зависимости от тяжести реакции, и эффективен для облегчения симптомов в течение 30 минут при максимальной дозе. При опасных для жизни приступах, таких как отек гортани или тяжелый отек полости рта, требуется 20 Ед / кг внутривенно. Приступы, не угрожающие жизни, можно лечить с помощью 500 Ед или 1000 ЕД внутривенно. 37 Cinryze — еще один концентрат C1-INH, эффективный для облегчения симптомов в течение четырех часов. Он вводится по 1000 ЕД, при необходимости вторая доза вводится через час.Cinryze был связан с тромботическими событиями, но причинно-следственная связь или частота не были продемонстрированы. 52 Рекомбинантный человеческий C1-INH (rhC1INH) вводится в дозах 50 Ед / кг или 4200 Ед внутривенно и эффективен для облегчения симптомов в течение 90 минут. Экаллантид — это ингибитор калликреина, который вводится подкожно в дозе 30 мг, снимает симптомы в течение 90 минут и может быть повторен один раз. 36,38,44 Икатибант — антагонист рецептора брадикинина B2, который вводится подкожно в дозе 30 мг, снимает симптомы в течение двух часов и может повторяться до двух раз каждые шесть часов в течение 24 часов. 36,38,44 Самым захватывающим аспектом этих новейших методов лечения является их возможность принимать дома, за исключением экалантида и rhC1INH.
Концентраты C1-INH, икатибант и экалантид стоят дорого (от 5000 до 10000 долларов за дозу). 53
В отличие от вышеизложенного, исследования эффективного лечения ангионевротического отека, вызванного ингибиторами АПФ, на сегодняшний день в значительной степени бесплодны. Многочисленные исследования, оценивающие эффективность методов лечения других типов ангионевротического отека, не показали никакой пользы, и в настоящее время лучшим методом лечения ангионевротического отека, вызванного ингибиторами АПФ, по-прежнему является контроль проходимости дыхательных путей и поддерживающая терапия.Медицинские работники неотложной помощи часто назначают этим пациентам лекарства, включая антигистаминные препараты и кортикостероиды, эмпирически. В 2015 году Bas и др. Оценили использование икатибанта по сравнению со стандартной антигистаминной и стероидной терапией при ангионевротическом отеке, вызванном ингибиторами АПФ, и обнаружили, что у пациентов, получавших икатибант, симптомы исчезли на 70% быстрее, чем в контрольной группе (8,0 часов против 27,1 часа, P = 0,002). 54 Однако исследование Shire’s CAMEO, также проведенное в 2015 году, не обнаружило статистически значимой разницы во времени, когда пациенты с ангионевротическим отеком, вызванным ингибитором АПФ, улучшились до соответствия критериям выписки после приема икатибанта по сравнению с плацебо ( P = 0.63), а также отсутствие статистической разницы во времени до облегчения симптомов. 55 Аналогичным образом, исследование Lewis et al., Проведенное в 2014 году, показало, что экаллантид не улучшил ангионевротический отек, вызванный ингибиторами АПФ, по сравнению с плацебо. 56
Наиболее важное сообщение, которое медики экстренной помощи должны извлечь из приведенных выше результатов, заключается в том, что ангионевротический отек, вызванный ингибиторами АПФ, который, как считается, опосредован брадикинином, не должен реагировать на антигистаминные препараты и глюкокортикоиды. Кроме того, текущие данные также не показывают стойкой эффективности при использовании антагонистов рецепторов брадикинина или ингибиторов калликреина.Таким образом, во всех случаях ангионевротического отека, вызванного ингибиторами АПФ, управление проходимостью дыхательных путей и стабилизация должны иметь первостепенное значение, а на медицинские методы лечения пока нельзя полагаться.
РасположениеКак рекомендовано Чиу в алгоритме на Рисунке 3, расположение пациентов с неаллергическим ангионевротическим отеком будет зависеть от того, было ли поражение дыхательных путей и какой уровень неотложной помощи требовался. Интубированные пациенты должны быть помещены в отделение интенсивной терапии для дальнейшего обследования и лечения в соответствии с показаниями.Пациенты с отеком дыхательных путей, не требующие экстренной процедуры на дыхательных путях, могут быть помещены в пол или в реанимацию или даже выписаны домой, в зависимости от места и степени поражения.
Пациенты с аллергическим ангионевротическим отеком подвержены риску двухфазных анафилактических реакций, которые обычно возникают в течение 10 часов после первоначального лечения. Распределение пациентов с анафилаксией должно определяться тяжестью их симптомов и ответом на лечение в отделении неотложной помощи. Согласно обновленным параметрам практики 2015 года Объединенного совета по аллергии, астме и иммунологии, пациенты с не опасными для жизни симптомами могут наблюдаться в течение четырех-восьми часов, если первоначальное лечение является эффективным, и выписываться, если рецидивов нет.Пациенты с рецидивом, требующим второй дозы адреналина, пациенты с анамнезом проглоченного аллергена или пациенты с особенно тяжелыми или опасными проявлениями, такими как свидетельства значительного сердечно-сосудистого и респираторного поражения, требуют либо более длительного наблюдения в отделении неотложной помощи, либо госпитализации для наблюдения. 57
Во всех случаях ангионевротического отека после купирования или разрешения приступов ангионевротического отека следует изучить возможные причины. Пациентам следует прекратить прием лекарств, подозреваемых в провокации (таких как ингибиторы АПФ, новые рецепты антибиотиков и т. Д.).) немедленно, следует избегать подозрений на разжигание аллергенов и получать соответствующие предупреждения и меры предосторожности в отношении этих предполагаемых причин. Всем пациентам с новыми аллергическими реакциями рекомендуется направлять к аллергологу. Ингибиторы АПФ следует заменить антигипертензивными препаратами, не относящимися к классам ингибиторов АПФ, блокаторов рецепторов ангиотензина II или прямых ингибиторов ренина; Пациенты должны быть проинструктированы, чтобы они проконсультировались со своим лечащим врачом для проверки любых изменений в лечении. 58-60
Пациентам, выписываемым после полного разрешения аллергического ангионевротического отека и / или анафилактической реакции, следует назначить автоинъекционный адреналин и лично проинструктировать о его применении; однако этим пациентам не нужно назначать антигистаминные препараты или кортикостероиды при выписке. 57 Хронические случаи аллергического ангионевротического отека можно лечить антагонистами h2-рецепторов, такими как цетиризин, или даже долгосрочными низкими дозами стероидов в рефрактерных случаях. 61
Несколько общепринятых методов лечения, таких как ослабленные андрогены, концентраты C1-INH и рекомбинантный C1-INH, в настоящее время используются для предотвращения приступов HAE. ( См. Таблицу 5. ) Андрогены в низких дозах включают даназол и станозолол, и их дозы составляют 50-300 мг / день и 2-4 мг / день, соответственно. 2,38 Cynryze — единственный концентрат C1-INH, одобренный в настоящее время для профилактического применения в дозе 1000 ЕД каждые 3-4 дня. Также было показано, что rhC1-INH эффективен в профилактике при еженедельной дозе 50 Ед / кг.Транексамовая кислота — еще одно профилактическое средство от НАО, которое назначают по 1 г два раза в день взрослым или 20 мг / кг у детей. Вышеупомянутые методы лечения также эффективны в предотвращении приступов приобретенного ангионевротического отека в сочетании с активным лечением основного заболевания.
Таблица 5. Профилактика НАО и приобретенного ангионевротического отека
Лекарство | Фирменное наименование | Механизм действия | Доза | Путь введения | Побочные эффекты |
Произведенный из плазмы C1-INH | Cinryze | Замена C1-INH | 1000 ЕД каждые 3-4 дня | IV | Анафилаксия, риск инфекций, передающихся через кровь |
rhC1-INH | Ruconest, Рюцин | Замена C1-INH | 50 Ед / кг / неделя | IV | Анафилаксия, риск инфекций, передающихся через кровь |
Андроген | Даназол | Неизвестно | 50-300 мг / сут | PO | Гепатотоксичность, опухоли печени, мужские вторичные половые признаки у женщин |
Станозолол | Неизвестно | 2-4 мг / сут | PO | Гепатотоксичность, опухоли печени, мужские вторичные половые признаки у женщин | |
Транексамовая кислота | Cyklokapron, Lysteda | Связывает сайты связывания плазминогена | Взрослые: 1 г два раза в день Педы: 20 мг / кг / день | PO | Анафилаксия, судороги, тромбоэмболия, отек головного мозга |
При лечении идиопатического ангионевротического отека низкие дозы антагонистов h3 в течение дня вместе с антагонистами h2 на ночь оказались очень эффективными.Для пациентов, которые не реагируют на антигистаминную терапию, можно рассмотреть циклоспорин в дозировках 2,5-4 мг / кг / день в течение максимум трех месяцев, при этом одно испытание продемонстрировало, что у 80% пациентов наблюдается близкое или полное выздоровление. 2,62 Тем, кто не ответил, дали еще один цикл циклоспорина или вместо этого начали метотрексат. Также могут быть назначены ВВИГ, плазмаферез и низкие дозы кортикостероидов.
СводкаАнгионевротический отек — сложное и потенциально смертельное заболевание, имеющее несколько причин, не все из которых хорошо изучены.В то время как для некоторых этиологий существуют медицинские методы лечения, все варианты могут проявляться опасным для жизни отеком дыхательных путей, который необходимо немедленно устранить. Ангионевротический отек — это диагноз, который нельзя пропустить при попадании в отделение неотложной помощи. Подходите к каждому подозрительному случаю с подробным анамнезом, медицинским осмотром и соответствующими клиническими подозрениями. Определите, есть ли у пациента крапивница, ангионевротический отек, анафилаксия или их комбинации. Помните, что ангионевротический отек, в отличие от крапивницы, возникает в подкожном и подслизистом слоях, длится от 24 до 48 часов, проявляется отек розового / телесного цвета, чаще сопровождается болью, чем зудом, и может осложняться болью в животе и нарушение дыхательных путей.Ознакомьтесь с дифференциальной диагностикой ангионевротического отека и используйте подробный анамнез и физический осмотр при оценке псевдоангионевротического отека.
Роль поставщиков услуг на догоспитальном этапе должна быть сосредоточена на оценке и стабилизации ABC при быстрой доставке этих пациентов в ближайшее отделение неотложной помощи. Если у пациентов наблюдаются какие-либо признаки гемодинамических или респираторных изменений, персонал догоспитального и реанимационного отделения должен немедленно получить доступ для внутривенного вливания (предпочтительно два больших диаметра), обеспечить дополнительный кислород и подключить пациента к непрерывной пульсоксиметрии и кардиомонитору.Во время первичного обследования поставщики медицинских услуг должны определить свой уровень комфорта при прохождении дыхательных путей пациента и определить необходимость вмешательства, используя алгоритм, изображенный на рисунке 3. После того, как дыхательные пути будут признаны стабильными или будут защищены, поставщики медицинских услуг могут перейти к первичному и вторичному обследованию. опросы, вмешиваясь, как указано. Знание типа ангионевротического отека поможет ускорить правильное лечение этих пациентов. Поставщики медицинских услуг должны быть осведомлены о наличии и доступности соответствующих фармакологических агентов и должны обеспечить наличие персонала, обученного надлежащему приготовлению и применению этих лекарств.Наконец, медицинские работники могут использовать алгоритм, изображенный на Рисунке 4, для развития комфорта и понимания надлежащего расположения пациентов с ангионевротическим отеком, независимо от того, требуется ли им госпитализация или их можно безопасно выписать домой.
ССЫЛКИ- Наследственный ангионевротический отек и брадикинин-опосредованный ангионевротический отек. В: Адкинсон Н.Ф. младший, Бохнер Б.С., Буркс А.В. и др. Аллергия Миддлтона: принципы и практика . Сондерс; 2014: 588-601.
- Каплан А.П., Гривз М.В.Ангионевротический отек. J Am Acad Dermatol 2005; 53: 373–88. викторина 389-392.
- Токсикология / Инфекции и заболевания шеи и верхних дыхательных путей. В: Tintinalli JE, Stapczynski JS, Jo O. Tintinalli’s Emergency Medicine: A Complete Study Guide , 7-е изд. Нью-Йорк: Макгроу Хилл; 2011: 183-190, 1276, 1591.
- Заболевания иммунитета. В: Kumar V, Abbas AK, Aster JC. Роббинс и Котран Патологическая основа болезни , 9-е изд. Эльзевир; 2015: 64, 245.
- Крапивница, ангионевротический отек и зуд.В: Хабиф Т.П. Клиническая дерматология: Цветное руководство по диагностике и терапии , 6-е изд. Сондерс; 2016: 178-217.
- Борк К., Вульф К., Хардт Дж. И др. Наследственный ангионевротический отек, вызванный миссенс-мутациями в гене фактора XII: клинические особенности, триггерные факторы и терапия. J Allergy Clin Immunol 2009; 124: 129.
- Дополнение. В: Male D, Brostoff J, Roth D, Roitt I. Immunology , 8-е изд. Сондерс; 2013: 71-84.
- Маккензи М., Вуд Л.А.Ангионевротический отек языка, связанный с эверолимусом. Acta Oncol 2010; 49: 107.
- Маэ Э, Морелон Э, Лечатон С. и др. Ангионевротический отек у реципиентов почечного трансплантата, получающих сиролимус. Дерматология 2007; 214: 205.
- Сендур О.Ф., Туран Ю., Беркит И.К., Тастабан Э. Ангио-отек у пациента, получавшего этанерцепт от ревматоидного артрита. Basic Clin Pharmacol Toxicol 2009; 104: 488.
- Банерджи А., Кларк С., Бланда М. и др. Многоцентровое исследование пациентов с ангионевротическим отеком, вызванным ингибитором ангиотензинпревращающего фермента, поступивших в отделение неотложной помощи. Ann Allergy Asthma Immunol 2008; 100: 327.
- Агостони А., Чикарди М., Куньо М. и др. Ангионевротический отек, вызванный ингибиторами ангиотензинпревращающего фермента. Иммунофармакология 1999; 44: 21-25.
- Оттомейер С., Хеннеричи М.Г., Сабо К. Повышение осведомленности об оролингвальном ангионевротическом отеке как осложнении тромболизиса у пациентов с острым инсультом. Цереброваск Дис. 2009; 27: 307.
- Kulthanan K, Jiamton S, Boochangkool K, Jongjarearnprasert K. Ангионевротический отек: клинические и этиологические аспекты. Clin Dev Immunol 2007; 2007: 26438.
- Frigas E, Nzeako UC. Ангионевротический отек. Патогенез, дифференциальная диагностика и лечение. Clin Rev Allergy Immunol 2002; 23: 217-231.
- Bentley B 2nd. Холодовая крапивница и ангионевротический отек: диагностика и лечение. Am J Emerg Med 1993; 11: 43-46.
- Лоулор Ф, Блэк А.К., Бретнах А.С., Гривз М.В. Вибрационный ангионевротический отек: индукция поражения, клинические особенности, лабораторные и ультраструктурные данные и ответ на терапию. Br J Dermatol 1989; 120: 93-99.
- Роуз РФ, Бхушан М., Кинг С.М., Родос ЛЭ. Солнечный ангионевротический отек: необычное заболевание? Фотодерматол Фотоиммунол Photomed 2005; 21: 226-228.
- Bork K, Staubach P, Eckardt AJ, Hardt J. Симптомы, течение и осложнения абдоминальных атак при наследственном ангионевротическом отеке из-за дефицита ингибитора C1. Am J Gastroenterol 2006; 101: 619.
- Борк К., Мэн Дж., Штаубах П., Хардт Дж.Наследственный ангионевротический отек: новые данные о симптомах, пораженных органах и течении болезни. Am J Med 2006; 119: 267.
- Блум А.С., Шранц С. Ингибитор ангиотензинпревращающего фермента, индуцированный ангионевротическим отеком тонкой кишки: имитация хирургической брюшной полости. J Emerg Med 2015; 48: e127.
- Agostoni A, Aygoren-Pursun E, Binkley KE и др. Наследственный и приобретенный ангионевротический отек: проблемы и прогресс: материалы третьего семинара по дефициту ингибитора С1-эстеразы и далее. J Allergy Clin Immunol 2004; 114 (3 приложения): S51-S131.
- Saxena S, Gierl B, Eibling DE. Отек надгортанника может не коррелировать с отеком языка при ангионевротическом отеке, вызванном ингибиторами ангиотензинпревращающего фермента. Ларингоскоп 2010; 120: 62-64.
- Борк К., Мэн Г., Штаубах П., Хардт Дж. Наследственный ангионевротический отек: новые данные о симптомах, пораженных органах и течении. Am J Med 2006; 119: 267-274.
- Scheirey CD, Scholz FJ, Shortsleeve MJ, Katz DS.Ангионевротический отек тонкой кишки, индуцированный ингибиторами ангиотензинпревращающего фермента: клинические и визуальные данные у 20 пациентов. AJR Am J Roentgenol 2011; 197: 393-398.
- да Коста Дж. Т., да Силва Дж. М., Кунья Л. и др. Наследственный ангионевротический отек с респираторным дистресс-синдромом у взрослых. Сундук 1994; 105: 1898-1899.
- Ван Деллен Р.Г., Мэддокс Д.Е., Датта Е.Дж. Маскарады ангионевротического отека и крапивницы. Ann Allergy Asthma Immunol 2002; 88: 10.
- Gleich GJ, Schroeter AL, Marcoux JP, et al. Эпизодический ангионевротический отек, связанный с эозинофилией. N Engl J Med 1984; 310: 1621.
- Хара Л.Дж., Наварро С., Медина Г. и др. Синдром гипокомплементемического уртикарного васкулита. Curr Rheumatol Rep 2009; 11: 410.
- Чарльзуорт EN. Дифференциальный диагноз ангионевротического отека. Allergy Asthma Proc 2002; 23: 337.
- Tarzi MD, Hickey A, Forster T, et al. Оценка тестов, используемых для диагностики и мониторинга дефицита ингибитора С1: нормальный уровень С4 в сыворотке не исключает наследственный ангио-отек. Clin Exp Immunol 2007; 149: 513-516.
- Zuraw BL. Клиническая практика. Наследственный ангионевротический отек. N Engl J Med 2008; 359: 1027-1036.
- Заничелли А., Магерл М., Лонгхерст Н. и др. Наследственный ангионевротический отек с дефицитом ингибитора С1: задержка диагностики в Европе. Allergy, Asthma Clin Immunol 2013; 9: 29.
- Темино В.М., Пиблс Р.С. мл. Спектр и лечение отека Квинке. Am J Med 2008; 121: 282-286.
- Чиу А.Г., Ньюкирк К.А., Дэвидсон Б.Дж. и др. Ангионевротический отек, вызванный ингибитором ангиотензинпревращающего фермента: многоцентровый обзор и алгоритм управления проходимостью дыхательных путей. Энн Отол Ринол Ларингол 2001; 110: 834.
- Чикарди М., Борк К., Кабальеро Т. и др. Основанные на фактах рекомендации по терапевтическому лечению ангионевротического отека вследствие наследственной недостаточности ингибитора C1: консенсусный отчет Международной рабочей группы. Аллергия 2012; 67: 147.
- Американская академия неотложной медицины. Руководство по клинической практике: начальная оценка и ведение пациентов с острой крапивницей или ангионевротическим отеком. Доступно по адресу: http://www.aaem.org/em-resources/position-statements/2006/clinical-practice-guidelines. Проверено 27 ноября 2016 г.
- Борк К. Терапевтический подход к лечению наследственного и приобретенного ангионевротического отека, основанный на доказательствах. Curr Opin Allergy Clin Immunol 2014; 14: 354.
- Sampson HA, Munoz-Furlong A, Campbell RL, et al.Второй симпозиум по определению и лечению анафилаксии: итоговый отчет — второй сетевой симпозиум Национального института аллергии и инфекционных заболеваний / пищевой аллергии и анафилаксии. Ann Emerg Med 2006; 47: 373-380.
- Абдельмалак Б., Дойл Дж. Анестезия для отоларингологической хирургии , 1-е изд. Издательство Кембриджского университета; 2013: 102.
- Надел Э.С., Браун Д.Ф. Ангионевротический отек. J Emerg Med 1998; 16: 477-479.
- Бенцианов Б.Л., Пархискар А., Азер М., Хар-Эль Г.Роль фиброоптической назофарингоскопии в лечении острых дыхательных путей при ангионевротическом отеке. Ларингоскоп 2000; 110: 2016-2019.
- Wood A, Choromanski D, Orlewicz M. Интубация пациентов с ангионевротическим отеком: ретроспективное исследование различных методов за трехлетний период. Int J Crit Illn Inj Sci 2013; 3: 108-112.
- Борк К., Бернштейн Дж., Махниг Т., Крейг Т. Дж. Эффективность различных методов лечения острых приступов гортани наследственного ангионевротического отека, вызванного дефицитом ингибитора C1-эстеразы. J Emerg Med 2016; 50: 567.
- Хассен Г.В., Калантари Х., Паррага М. и др. Свежезамороженная плазма для лечения прогрессирующего и рефрактерного ангионевротического отека, вызванного ингибиторами ангиотензинпревращающего фермента. J Emerg Med 2013; 44: 764.
- Пекдемир М., Эрсель М., Аксай Э. и др. Эффективное лечение наследственного ангионевротического отека свежезамороженной плазмой в отделении неотложной помощи. J Emerg Med 2007; 33: 137.
- Хилл Б.Дж., Томас С.Х., МакКейб К.Свежезамороженная плазма при обострениях наследственного ангионевротического отека. Am J Emerg Med 2004; 22: 633.
- Ishoo E, Shah UK, Grillone GA и др. Прогнозирование риска для дыхательных путей при ангионевротическом отеке: система стадий на основе презентации. Otolaryngol Head Neck Surg 1999; 121: 263-268.
- Боуэн Т., Чикарди М., Фаркас Х. и др. 2010 Международный консенсусный алгоритм диагностики, терапии и лечения наследственного ангионевротического отека. Allergy Asthma Clin Immunol 2010; 6:24.
- Бетчел С., Бадью Дж., Бинкли К. и др. Канадские рекомендации по наследственному ангионевротическому отеку. Allergy Asthma Clin Immunol 2014; 10:50.
- Дикевич MS. Кашель и ангионевротический отек от ингибиторов ангиотензинпревращающего фермента: новое понимание механизмов и управления. Curr Opin Allergy Clin Immunol 2004; 4: 267.
- Ганди П.К., Джентри В.М., Ботторфф МБ. Тромботические события, связанные с продуктами с ингибиторами C1-эстеразы, у пациентов с наследственным ангионевротическим отеком: исследование из базы данных системы отчетности о нежелательных явлениях Управления по санитарному надзору за качеством пищевых продуктов и медикаментов США. Фармакотерапия 2012; 32: 902.
- Cicardi M, Zuraw B. Наследственный ангионевротический отек: лечение острых приступов. В: UpToDate, Post TW (Ed), UpToDate, Waltham, MA. Проверено 22 ноября 2016 г.
- Баш М., Гри Дж., Стелтер К. и др. Рандомизированное исследование икатибанта при ангионевротическом отеке, вызванном ингибиторами АПФ. N Engl J Med 2015; 372: 418-425.
- Sinert, et al. Слепое плацебо-контролируемое исследование безопасности и эффективности икатибанта при ангионевротическом отеке, ингибиторе ангиотензинпревращающего фермента.Исследование CAMEO, проведенное Shire Pharmaceuticals Limited, не опубликовано, прекращено в сентябре 2015 года.
- Льюис Л.М., Граффео С., Крозели П. и др. Экаллантид для неотложного лечения ангионевротического отека, вызванного ингибиторами ангиотензинпревращающего фермента: многоцентровое рандомизированное контролируемое исследование. Ann Emerg Med 2015; 65: 204-213.
- Либерман П., Никлас Р.А., Рэндольф С. и др. Анафилаксия — обновление параметров практики, 2015. Ann Allergy Asthma Immunol 2015; 115: 341-384.
- Toh S, Reichman ME, Houstoun M, et al. Сравнительный риск ангионевротического отека, связанный с применением препаратов, нацеленных на ренин-ангиотензин-альдостероновую систему. Arch Intern Med 2012; 172: 1582-1589.
- Vasekar M, Craig TJ. Ангионевротический отек, вызванный ингибиторами АПФ. Curr Allergy Asthma Rep 2012; 12: 72.
- Берд Дж. Б., Адам А., Браун, штат Нью-Джерси. Ангионевротический отек, связанный с ингибиторами ангиотензинпревращающего фермента. Immunol Allergy Clin North Am 2006; 26: 725.






 При неэффективности терапии следует провести интубацию или коникотомию. Больной с отеком гортани нуждается в срочной госпитализации в отделение реанимации и интенсивной терапии.
При неэффективности терапии следует провести интубацию или коникотомию. Больной с отеком гортани нуждается в срочной госпитализации в отделение реанимации и интенсивной терапии. риск побочных реакций
риск побочных реакций прекращено
прекращено