Радиохирургия в клинике EMC в Москве
Возможность проведения радиохирургии полностью меняет взгляд на лечение пациентов с онкологическими заболеваниями. Эта методика лучевого лечения не имеет практически ограничений в применении. При применении радиохирургии госпитализация в стационар не требуется, так как лечение проходит в амбулаторном режиме. Отличительной особенностью стереотаксических методик лучевой терапии является конформное облучение опухоли при минимальном воздействии на окружающие ткани и высокая точность позиционирования мишени облучения. Это гарантирует минимальный риск лучевых реакций и осложнений при максимальном воздействии на патологическое образование. Эффект этой методики доказан на исследованиях в ведущих клиниках в США, Европе, Израиле.
Для проведения стереотаксической радиохирургии в EMC используются медицинские ускорители последнего поколения EDGE и TrueBeam производства Varian Medical Systems (США).
Специалисты Центра лучевой терапии EMC, прошедшие обучение и стажировки в ведущих клиниках Израиля, Европы и США, обладают значительным опытом проведения лечения по методикам SBRT и SRS.
Что такое стереотаксическая радиохирургия?
Стереотаксическая радиохирургия — это методика, при которой происходит деструкция новообразования (обычно не превышающего 4 см в диаметре) под воздействием большой дозы прецизионного излучения с минимальным воздействием на окружающие здоровые ткани. Данная методика, несмотря на свое название, не предполагает хирургического вмешательства. Радиохирургия является абсолютно безболезненной методикой.
Есть два направления радиохирургии, а именно: стереотаксическая радиохирургия при опухолях головного мозга (SRS) и экстракраниальная стереотаксическая радиотерапия (SBRT).
- Для выполнения радиохирургического лечения требуется проведение трехмерной и /или четырехмерной КТ симуляции для точного определения локализации, конфигурации и размера новообразования и применение устройства для иммобилизации пациента с целью идентичного воспроизведения позиции пациента при радиотерапии.

- Прецизионность (точность) терапии обеспечивается за счет точного воспроизведения укладки больного с помощью фиксирующих устройств и оптического контроля локализации опухоли в течение всего сеанса радиотерапии.
Радиохирургическое лечение применяется:
-
При расположении новообразования в малодоступных для хирургического лечения местах.
-
В случае, когда новообразования расположены близко к жизненно важным органам и структурам.
-
При опухолях, меняющих свое положение в зависимости от дыхания.
-
SBS и SBRT представляют собой альтернативную терапию для больных, которым по каким-либо причинам противопоказано хирургическое лечение.
Когда применяется SRS:
1. Метастазы злокачественных опухолей в головной мозг
2. Все доброкачественные новообразования головного мозга:
-
невриномы слухового нерва и других черепно-мозговых нервов
-
менингиомы любой локализации
-
новообразования шишковидной железы
-
новообразования гипофиза
-
краниофарингиомы
-
хордомы
3.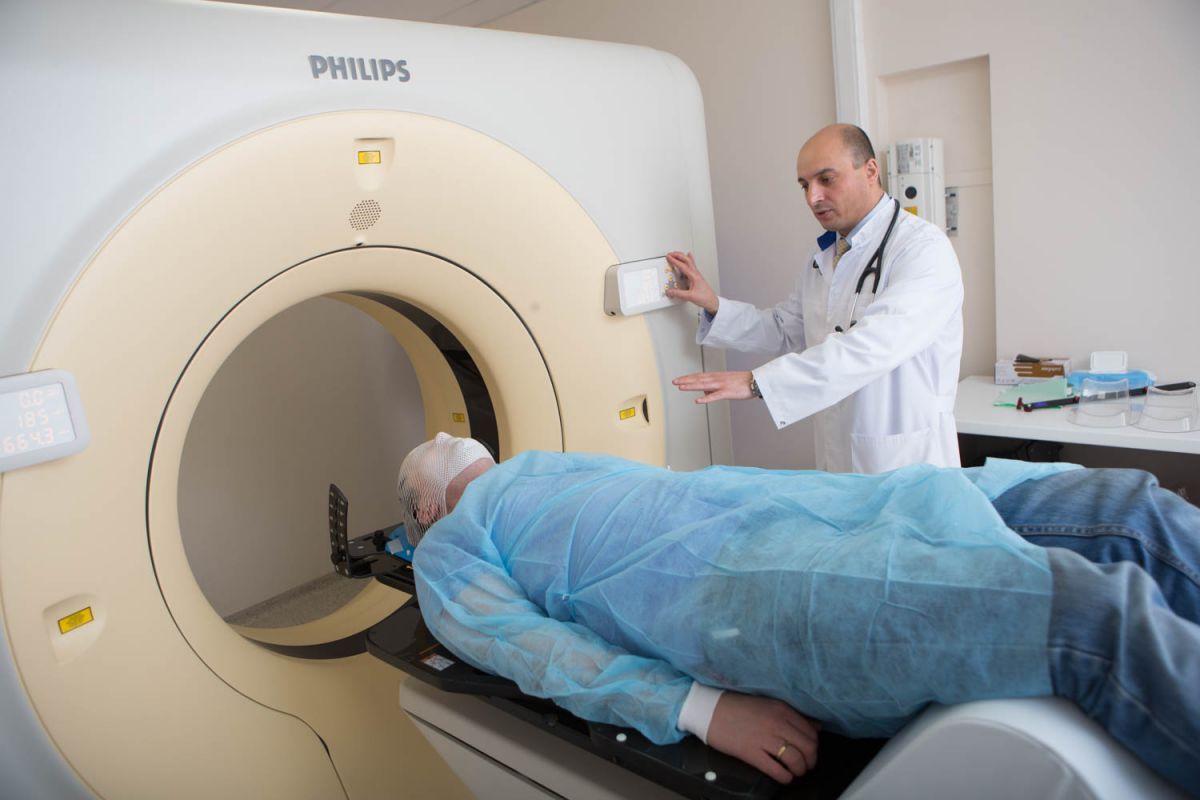 Артерио-венозные мальформации и кавернозные ангиомы
Артерио-венозные мальформации и кавернозные ангиомы
4. Невралгия тройничного нерва
-
Новообразования и метастатические поражения головного и спинного мозга
-
Рецидивы первичных опухолей мозга
Показания для стереотаксической радиотерапии тела (SBRT):
- Метастатические опухоли позвоночника
- Новообразования и метастазы легких
- Первичные и метастатические злокачественные новообразования печени
- Новообразования желчных протоков
- Новообразования поджелудочной железы
- Локализованный рак предстательной железы
- Локализованный рак почки
- Новообразования забрюшинного пространства
- Новообразования женских половых органов
- Новообразования основания черепа
- Новообразования орбиты
- Первичные и рецидивные новообразования носоглотки, полости рта, придаточных пазух носа, гортани
Как проходит радиохирургическое лечение?
Радиохирургия может проводиться за 1-5 лечебных процедур (количество сеансов зависит от размера облучаемого очага).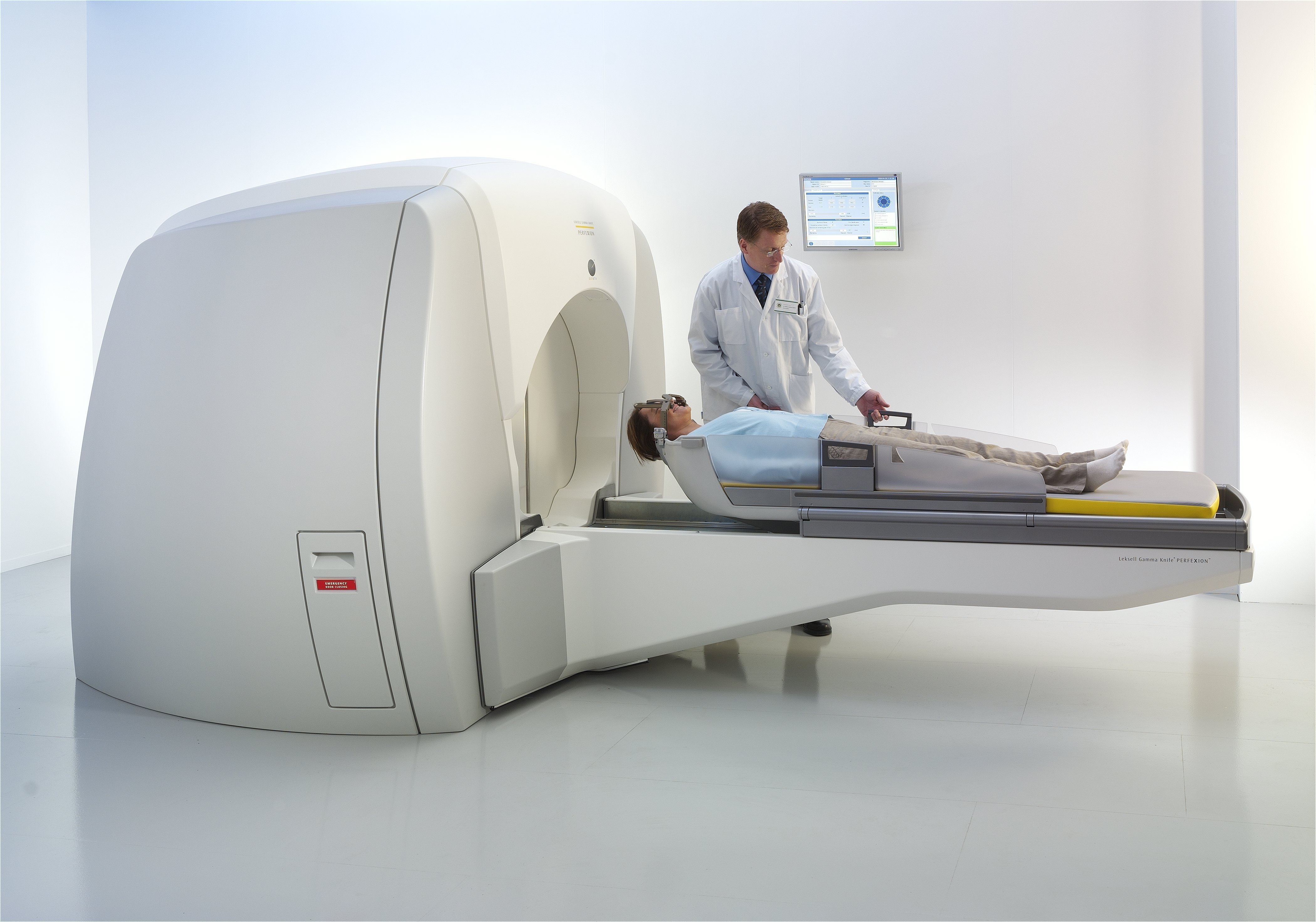
Перед началом лечения выполняется КТ — симуляция. Для проведения радиохирургического лечения требуется правильное положение тела больного на столе, для этой цели применяются фиксирующие устройства. Далее выполняется трехмерная и/или «четырехмерная» компьютерная томография, которая позволяет создать несколько изображений облучаемого объема в движении, например, при дыхании. Это имеет большое значение при наличии новообразований в органах, меняющих свое расположение в соответствии с фазами дыхания (легких, печень и др.).
После КТ симуляции создается план лечения. Радиотерапевт и физик-дозиметрист создают план таким образом, чтобы максимально приблизить конфигурацию пучка лучей к параметрам опухоли. При SRS и SBRT радиотерапия поводится на линейных ускорителях последнего поколения.
Перед проведением терапии больного укладывается на стол с применением изготовленного во время КТ симуляции фиксирующего устройства, после чего выполняется снимок. На основании результатов снимка врач-радиолог меняет положение больного на столе.
Радиохирургия: Кибернож и Гамма-нож
Что такое радиохирургия?
Радиохирургия означает радиотерапевтическую процедуру, при которой небольшая, четко выраженная опухоль облучается с высокой точностью. Размер опухоли-мишени может составлять от 0,5 до 4 см в диаметре. За счет резкого падения энергии применяемых лучей на границе опухоли и здоровой ткани, последняя не повреждается и сохраняется.
Какие методы лечения используются при радиохирургии?
Линейный ускоритель
Для радиохирургии могут быть предложены современные высокопроизводительные линейные ускорители (на основе LINAC). Они ускоряют частицы за счет напряжения и направляют их с помощью магнитного поля по нужной траектории.
Кибернож
Кибернож - это радиохирургический аппарат для лучевой терапии. В отличие от гамма-ножа, применение которого ограничено областью головы, его можно использовать для лечения опухолей по всему телу. Эта технология использует высокую дозу фотонного излучения от линейного ускорителя и выравнивает его с помощью свободно движущейся руки робота точно по направлению к цели.
Эта технология использует высокую дозу фотонного излучения от линейного ускорителя и выравнивает его с помощью свободно движущейся руки робота точно по направлению к цели.
Гамма-нож
Гамма-нож - это радиохирургическое устройство для лучевой терапии. Используется исключительно для облучения внутричерепных структур. Устройство содержит источники кобальта-60, которые расположены в полусферической форме. Из 192 источников лучи направляются на опухоль-мишень, так что там они встречаются и специально выделяют свою энергию. Во время облучения две рентгеновские камеры отслеживают положение пациента и исправляют любые отклонения в запланированных изображениях в режиме реального времени.
Преимущества радиохирургии по сравнению с традиционной лучевой терапией
Радиохирургия позволяет проводить точную терапию тех участков тела, которые труднодоступны для хирургического вмешательства. Кроме того, можно воздействовать на части тела, которые «спрятаны» в глубине, так что, в отличие от обычной лучевой терапии, ткань на пути лучей от кожи к опухоли не повреждается.![]() Сюда относятся опухоли в черепе, так как доступ через черепную кость затруднен. За счет снижения дозы на границе опухоли окружающие ткани сохраняются целыми, так что ожидаемые побочные эффекты уменьшаются, а общее лечение переносится лучше. Это открывает новые возможности лечения для людей более старшего возраста или пациентов с сопутствующими заболеваниями.
Сюда относятся опухоли в черепе, так как доступ через черепную кость затруднен. За счет снижения дозы на границе опухоли окружающие ткани сохраняются целыми, так что ожидаемые побочные эффекты уменьшаются, а общее лечение переносится лучше. Это открывает новые возможности лечения для людей более старшего возраста или пациентов с сопутствующими заболеваниями.
Какие опухоли можно лечить радиохирургией?
Метастазы в головном мозге
Пациенты с первичной опухолью вне головного мозга, у которых есть метастазы в черепе, могут быть подвергнуты радиохирургии. Под сомнение попадают пациенты, у которых есть до четырех метастазов размером до 3 см.
Менингеальные опухоли (менингиомы)
Опухоли, которые расположены внутри черепной кости, труднодоступны и, кроме того, часто находятся вблизи чувствительных структур, таких как сосуды головного мозга. Поэтому эти опухоли особенно подходят для радиохирургии. Менингиомы характеризуются низким профилем риска и незначительным ростом. Они могут быть облучены после полного или частичного хирургического удаления.
Они могут быть облучены после полного или частичного хирургического удаления.
Невринома слухового нерва
Невриномы слухового нерва были первыми опухолями, к которым применялась радиохирургия. Цель состоит в том, чтобы остановить рост опухоли, что удается в 90 % случаев. Таким образом, слух может быть сохранен в большинстве случаев неинвазивно.
Сосудистые мальформации (артериовенозные мальформации, каверномы)
С помощью радиохирургии можно лечить пороки развития сосудов головного мозга ( каверномы , aартериовенозные пороки развития) в его функционально важных областях. Эти пороки развития характеризуются более слабыми стенками сосудов и представляют высокий риск инсульта. Радиохирургия таких мальформаций, которые хирургически недоступны из-за сложного расположения, значительно снижает частоту симптоматического кровотечения.
Функциональная нейрохирургия – лицевая боль
Радиохирургия применяется при лечении лицевых болей на фоне невралгии тройничного нерва . Также радиохирургия помогает пациентам с рассеянным склерозом
Побочные эффекты радиохирургии
Побочные эффекты очень редки и сильно зависят от заболевания, которое лечат, расположения пораженной ткани и требуемой дозы облучения. Поэтому сделать общее заявление об этом заранее невозможно. Индивидуальные риски для определенных побочных эффектов обсуждаются заранее с лечащим врачом.
В случае облучения опухолей в слуховой области это может привести к головокружению, снижению или потере слуха. Как правило, облученные опухоли могут отекать, что приводит к появлению симптомов сдавливания, если опухоль находится в черепе. При более высоких дозах может возникнуть так называемый радионекроз, то есть разрушение тканей из-за внешних воздействий.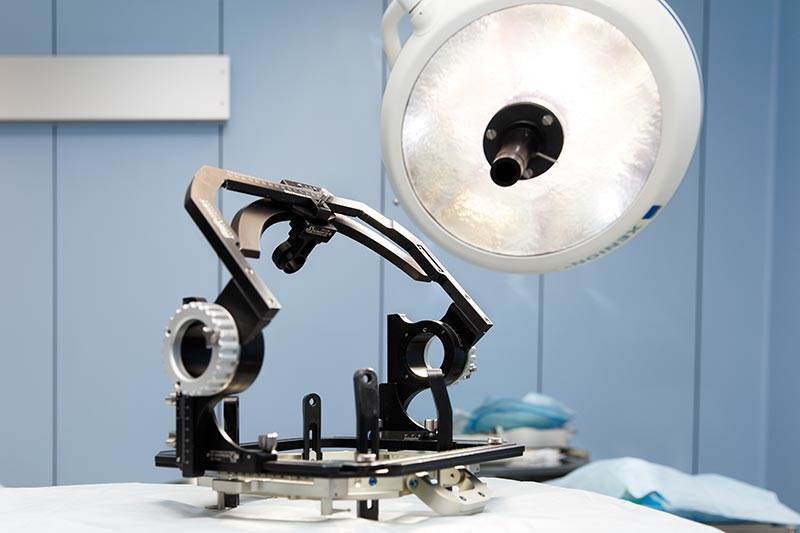
Расходы на радиохирургию и их возмещение медицинскими страховыми компаниями
Как правило, расходы находятся в диапазоне от 7 000 до 10 000 евро. Во многих странах, например, в Нидерландах и Франции радиохирургия является неотъемлемой частью стандартного медицинского обслуживания и оплачивается медицинской страховкой. В Германии затраты на радиохирургическое лечение еще не отражены в общем каталоге фиксированных платежей по обязательному медицинскому страхованию, так что автоматическое выставление счетов по страховому полису невозможно. В принципе, однако, больничные кассы в системе обязательного медицинского страхования могут оплачивать расходы на такое лечение. С одной стороны, есть возможность принятия индивидуальных решений, а с другой стороны – заключение договоров на комплексное обслуживание с поставщиками медицинских услуг.
Какие врачи являются специалистами в области радиохирургии?
Если человеку нужен врач, естественно, что он ищет лучшую медицинскую помощь. Вот почему пациент спрашивает себя о том, где он может найти лучшую клинику? Поскольку на этот вопрос нельзя дать объективный ответ и настоящий врач никогда не будет утверждать, что он лучший, можно полагаться только на его опыт.
Вот почему пациент спрашивает себя о том, где он может найти лучшую клинику? Поскольку на этот вопрос нельзя дать объективный ответ и настоящий врач никогда не будет утверждать, что он лучший, можно полагаться только на его опыт.
Мы поможем вам найти специалиста для лечения вашего заболевания. Все перечисленные врачи и клиники были проверены нами на предмет их высокой квалификации в области стереотаксической радиохирургии. Они ждут ваших вопросов и пожеланий относительно лечения.
Кибернож в Германии и Швейцарии
Центры в Германии
- Мюнхен: Европейский центр кибернетической хирургии Cyberknife, Мюнхен-Гроссхадерн
- Гюстров: Центр радиохирургии Saphir в Северной Германии
- Бохум: Немецкий центр кибернетической хирургии Cyberknife
- Берлин: Центр Шарите Cyberknife
- Гамбург: Центр Cyberknife в Гамбурге
- Кельн: Центр кибернетической хирургии Cyberknife при университетской клинике Кельна
- Эрфурт: Центр Cyberknife, Центральная Германия
Центры в Швейцарии
- Университетская больница Берна
- Центр Gammaknife Цюриха
Гамма-нож в Германии и Швейцарии
Лечение области головы с помощью гамма-ножа в Германии возможно в:
- Крефельд: Центр Gammaknife в Крефельде
- Аахен: Университетская Больница RTWH, г.
 Аахен
Аахен - Франкфурт: Центр Gammaknife во Франкфурте
- Ганновер: Центр Gammaknife в Ганновере
Гамма-нож в Швейцарии:
- Цюрих: клиника Klinik im Park и Hirslanden
- Лозанна: Hirslanden и Clinique Cecil
Источники :
- Тей Д. Ацад, Рохелио Эспаранца: Стереотаксическая радиохирургия при метастазировании в краниовертебральном переходе сохраняет стабильность позвоночника и предлагает облегчение симптомов, J Neurosurg, Spine Volume, 24, февраль 2016 г.
- Пайпер: Внутренняя медицина. 2-е издание. Springer 2012, ISBN 978-3-642-33107-7.
- Хин: Практическая пневмология. 2-е издание. Springer 2011, ISBN 978-3-642-10209-7.
- Ванненмахер и др. (Ред.): Лучевая терапия. 2-е издание. Springer 2013, ISBN 3-540-88304-5.
Стереотаксическая радиохирургия | МедИндия
Стереотаксическая радиохирургия, несмотря на своё название, не является хирургическим методом.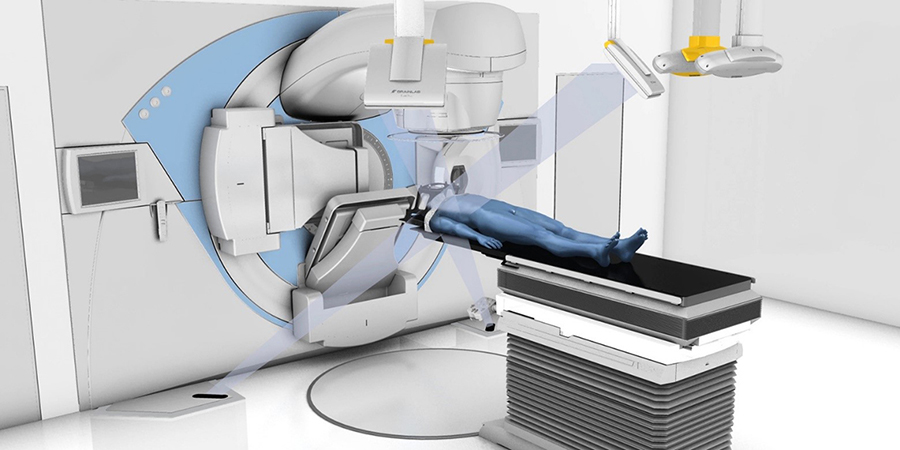 Это неинвазивная процедура, при которой мощные рентгеновские или гамма-лучи направляются потоком на строго определенную часть тела.
Это неинвазивная процедура, при которой мощные рентгеновские или гамма-лучи направляются потоком на строго определенную часть тела.
В лечении заболеваний мозга эта процедура используется уже нескольких лет, но в Индии в последнее время стереотаксической радиохирургии находят применение в лечении заболеваний и других органов, таких как легкие, печень, органы брюшной полости, предстательная железа, голова и шея.
Стереотаксическая радиохирургия эффективно применяется для лечения некоторых видов опухолей головного и спинного мозга и нервов, таких как:
- доброкачественные и злокачественные опухоли головного и спинного мозга
- первичные и метастатические опухоли мозга
- опухоли гипофиза
- опухоли головы и шеи
- невринома слухового нерва
- артериовенозная мальформация
- эпилептические расстройства
- болезнь Паркинсона (для глубокой стимуляции мозга)
- невралгия тройничного нерва
Инвазивная хирургия не применяется в случае, если опухоль или патологическая ткань:
- недоступны (например, при глубинных опухолях головного мозга)
- расположены вблизи важных нервов или жизненно-важных органов, которые могут быть повреждены при выполнении операции методом инвазивной хирургии
И в этих ситуациях, стереотаксическая радиохирургия в Индии является незаменимым вариантом лечения, состоящего из:
- Идентификации опухоли – определение её точной локализации, формы и размеров.
 Для идентификации опухоли используются 3D визуализационные техники, такие как КТ, МРТ и ПЭТ-КТ
Для идентификации опухоли используются 3D визуализационные техники, такие как КТ, МРТ и ПЭТ-КТ - Иммобилизации определенной части тела – специально разработанные приспособления используются для обеспечения неподвижности опухоли, что важно при движении пациента
- Доставки лучевого пучка к месту – сфокусированные и мощные гамма или рентгеновские пучки направляются на место операции под разными углами. Для некоторых заболеваний, одного раза бывает достаточно. В некоторых случаях, когда опухоль превышает 2,5 см, проводятся повторные сессии, которые могут достигать 5-6 раз. Этот метод называется фракционированная стереотаксическая радиохирургия. Доставка лучевого пуска к месту обычно производится с помощью Линейного Ускорителя (LINAC), которые широко представлены во многих госпиталях Индии.
Госпитали в Индии, которые представляем мы, в Дели, Мумбае, Бангалоре, Ченнае и Хайдерабаде имеют Линейные ускорители последнего поколения, такие как Novalis Tx, Кибер-нож и т.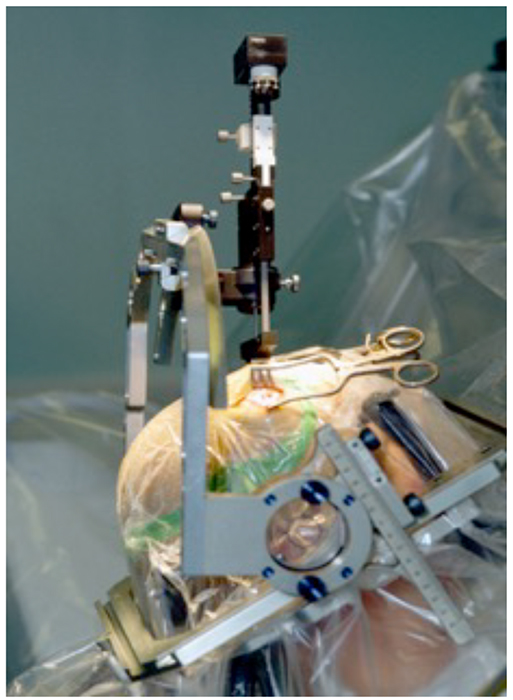 д., что обеспечивает попадание фотонов точно в необходимое место.Доставка лучевого пучка гамма-лучей производится с применением Гамма-ножа, который в Индии считается эффективным в лечении небольших опухолей, в то время, как линейные ускорители могут эффективно применяться и для больших опухолей.
д., что обеспечивает попадание фотонов точно в необходимое место.Доставка лучевого пучка гамма-лучей производится с применением Гамма-ножа, который в Индии считается эффективным в лечении небольших опухолей, в то время, как линейные ускорители могут эффективно применяться и для больших опухолей.
Стереотаксическая хирургия направлена на уничтожение ДНК опухолевых клеток, благодаря чему спустя некоторое время опухоль разрушается. Злокачественные опухоли разрушаются достаточно быстро, в то время как разрушение доброкачественной опухоли может потребовать нескольких лет.
Лечение с использованием стереотаксической радиохирургии проводится командой специалистов состоящей из:
- нейрохирурга – основного врача, отвечающего за лечение пациента
- радиолога, который оценивает результаты КТ, МРТ и ПЭТ-КТ
-
радиационного онколога, который определяет стратегию радиационной нагрузки (место применения, расчет дозы излучения, количество сессий и т.
 д.)
д.) - радиационного физика, который совместно с дозиметристом рассчитывает дозу излучения и специфику его доставки
- радиационного техника, который управляет аппаратом и позиционирует пациента
- Командная работа врачей разных специальностей в индийских госпиталях при лечении пациентов широко известна и является сильной стороной госпиталей Индии в лечении нейрохирургических пациентов.
Госпитализация при проведении стереотаксической радиохирургии не является обязательной. Однако для иностранных пациентов, которые приезжают в Индию для этого лечения, часто бывает удобным находиться в госпитале в течение 2-3 дней, чтобы подготовительная работа, требующая участия пациента, была проведена быстро и комфортно.
После процедуры обычно пациент может вернуться к обычной жизни в течение 1-2 дней.
Радиохирургия — Москва и область
ПРЕИМУЩЕСТВА РАДИОХИРУРГИИ
Преимущества радиохирургии заключаются в следующем:
- Основное преимущество радиохирургии перед обычной (фракционной) лучевой терапией – высокая разовая доза облучения, которая приводит к более эффективному уничтожению злокачественных клеток в опухолевом очаге, как правило, требуется от одного до пяти сеансов лечения;
- Эта методика проводится с помощью специального оборудования и программного обеспечения с высокой степенью точности и с минимальным воздействием на нормальные ткани и качество жизни пациента;
- Несмотря на название “радиохирургия”, данная методика является неинвазивным методом лечения.
 При ее применении не происходит никакого хирургического вмешательства в организм и не требуется наркоз, а сеанс облучения проводится амбулаторно;
При ее применении не происходит никакого хирургического вмешательства в организм и не требуется наркоз, а сеанс облучения проводится амбулаторно; - Благодаря неинвазивности методики, радиохирургия может использоваться как альтернатива хирургическому методу у тех пациентов, которым операция не может быть выполнена из-за сопутствующих заболеваний;
- Радиохирургия применяется не только для лечения начальных стадий первичных опухолей, но и для радикального лечения ограниченного количества метастазов опухолей.
Радиохирургия успешно применяется для лечения первичных злокачественных образований, рецидивов и метастазирования. Благодаря тому, что процедура неинвазивная, СТРХ для многих пациентов становится шансом при наличии противопоказаний к проведению операции. Благодаря неинвазивности методика может применяться у тех пациентов, которым в силу сопутствующих заболеваний противопоказано хирургическое лечение (пациент неоперабелен по медицинским показаниям). У таких пациентов радиохирургия может оказаться единственным возможным методом радикального лечения онкологического заболевания (например, при у пациентов с начальными стадиями рака легкого, которые не могут быть радикально прооперированы из-за сопутствующих заболеваний).
Радиохирургия в «Медскан». Почему мы:
- С первого дня обращения пациента в клинику «Медскан» все решения о тактике лечения принимаются на онкологическом консилиуме. В состав комиссии включаются врачи различных специальностей, как собственные, так и привлеченные узкие специалисты из Израиля и США;
- Наши специалисты для радиохирургии используют передовое оборудование, а именно — линейный ускоритель Varian TrueBeam, оснащенный специальными программными опциями для стереотаксической радиотерапии и радиохирургии;
- Все пациенты «Медскан», столкнувшиеся с онкологией, получают комплексное лечение. Лечащий врач по возможности всегда находится на связи со своим пациентом, доступно объясняет все моменты, связанные с процедурами, и назначает лечение только после тщательного обследования организма пациента.
ЭТАПЫ РАДИОХИРУРГИИ
- Разметка (“топометрия”): изготовление специальных фиксирующих приспособлений (вакуумных матрасов, термопластических масок и др), которые позволяют пациенту сохранять неподвижность во время сеанса облучения в комфортном положении, и последующая компьютерная томография зоны облучения, на основе которой происходит расчет программы лечения.

- Планирование лучевой терапии: во время планирования лечащий врач определяет мишень облучения (опухолевый очаг), окружающие опухоль нормальные органы, и создает задание на планирование, по которому медицинский физик проводит создание дозиметрического плана облучения, а в последующем проверяет соответствие плана облучения критериям качества, заданных врачом.
- Сеанс радиохирургии: так как эта методика проводится с высокой точностью, сеанс радиохирургии длится дольше, чем обычная лучевая терапия (требуется большее количество снимков для контроля положения опухоли во время сеанса) и может занимать от 30-40 минут до 1,5-2 часов.
Для проведения процедуры радиохирургии и стереотаксической радиотерапии в клинике Медскан используется Varian TrueBeam — медицинский линейный ускоритель нового класса, в котором реализованы самые передовые технологии современной дистанционной лучевой терапии: получение изображения опухоли в реальном времени, коррекцию положения пациента, компенсацию движений опухолевого объема, формирование апертуры пучка излучения и подведение дозы.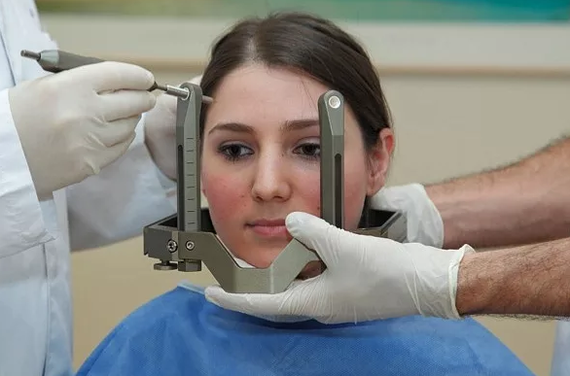 Проверка точности и автоматическая коррекция проводятся непосредственно перед сеансом облучения и во время процедуры.
Проверка точности и автоматическая коррекция проводятся непосредственно перед сеансом облучения и во время процедуры.
По своим характеристикам линейный ускоритель Varian TrueBeam не уступает другим системам, которые используются для проведения стереотаксической радиотерпаии и радиохирургии (например, “Гамма-Нож” и “Кибер-Нож”):
Точность позиционирования мишени облучения в системе TrueBeam находится в пределах 1 мм (аппаратная механическая точность позиционирования в пределах 0,75 мм). Ее обеспечивают новые алгоритмы синхронизации между процессом получения изображения, позиционирования и управления функциями аппарата.
Автоматические системы контроля качества осуществляют проверку позиционирования каждые 10 миллисекунд в течение всего сеанса лечения, непрерывно обеспечивая точность подводимой дозы излучения.
Современный пакет аппаратного и программного обеспечения версии 2.5 системы Varian TrueBeam (Advanced IGRT) позволяет получать снимки на столе линейного ускорителя во время сеанса лечения, контролируя и корректируя по ним отклонение мишени облучения в режиме on-line.
Усовершенствованная модель лечебного стола системы TrueBeam обеспечивает позиционирование пациента с субмиллиметровой точностью, что позволяет корректировать положение облучаемого объема по изображению в режиме реального времени.
Визуальный контроль мишени облучения (IGRT) во время сеанса лечения по технологии RapidArc (VMAT) делает возможным синхронизацию получения изображения с одновременным подведением дозы во время вращения диагностического и лечебного пучков излучения. Быстрая реконструкция рентгеновских снимков в режиме реального времени, по которым врач может определить положение опухоли во время сеанса лучевой терапии, позволяет провести автоматическую коррекцию положения пациента, если опухоль сместилась за время облучения, что обеспечивает высокую точность в подведении запланированной дозы к опухолевому очагу.
Координированная автоматизация технологических процессов еще больше ускоряет лечение, позволяя почти в пять раз сократить затраты времени на получение изображения, позиционирование и подведение дозы.
FAQ
Как назначается стереотаксическая лучевая терапия?
Радиохирургия, как и любой другой вид лечения, проводится по медицинским показаниям, которые определяет врач-радиотерапевт. Благодаря неинвазивности, данная методика широко применяется при лечении как метастатических, так и первичных опухолей, в том числе как альтернатива хирургическому методу лечения.
Решение о проведении радиохирургии тому или иному пациенту принимается специалистами во время медицинского консилиума после изучения всех деталей заболевания!
Если ли противопоказания к радиохирургии?
Как и во всех других методах лечения, существуют ситуации, при которых проведение стереотаксической радиотерапии и радиохирургии противопоказано. Таких ситуаций немного и они могут быть определены только врачом-радиотерапевтом во время консультации с пациентом. Для решения вопроса о показаниях и противопоказаниях всегда требуется консультация со специалистом!
После стереотаксической лучевой терапии остается ли радиация в человеке?
При проведении внешней лучевой терапии тело человека не становится радиоактивным. Поэтому нет необходимости в исключении контакта с людьми после лечения.
Поэтому нет необходимости в исключении контакта с людьми после лечения.
Какие рекомендации необходимо соблюдать пациенту после завершения процедуры радиохирургии?
Как и при других методах онкологического лечения, после завершения лечения требуется выполнение контрольных обследований (КТ, МРТ, ПЭТ/КТ, анализы крови, онкологические маркеры и др) с определенной периодичностью для оценки динамики онкологического заболевания. Все рекомендации по динамическому наблюдению врач-радиотерапевт дает пациенту сразу после последнего сеанса лечения и подробно объясняет, какие обследования и в какие сроки рекомендуется проходить. Также врач-радиотерапевт назначает контрольные осмотры для оценки динамики побочных эффектов и назначает лечение в том, случае, если они развиваются.
Как пройти радиохирургию в клинике “Медскан”?
Радиохирургия проводится в медицинских центрах «Медскан» по доступным ценам.
Для начала необходимо записаться на первичный прием врача-радиотерапевта.
После первичного приема и получения всех необходимых данных обследования случай каждого пациента рассматривается на междисциплинарном консилиуме специалистов клиники “Медскан”, который включает врачей различных специальностей (радиотерапевтов, онкологов, химиотерапевтов, хирургов, рентгенологов и других узких специалистов). Это позволяет максимально правильно и обоснованно подойти к выбору тактики лечения, основываясь на принципах доказательной медицины, как это принято за рубежом. При необходимости случай пациента также рассматривается на международном консилиуме с участием ведущих специалистов-радиотерапевтов и онкологов из США, Израиля и Сингапура.
Лечащий врач-радиотерапевт находится на связи и в любое удобное для пациента время и готов ответить на дополнительные вопросы. Опытный специалист доступно объясняет каждый момент, связанный с процедурами, что исключает вероятность развития осложнений или же позволяет принять меры на начальных этапах развития побочных реакций. Уточняйте цены на стереотаксическую лучевую терапию в Москве по телефону, указанному на сайте.
Уточняйте цены на стереотаксическую лучевую терапию в Москве по телефону, указанному на сайте.
В Центре лучевой терапии провели первую стереотаксическую радиохирургическую операцию
В Центре лучевой терапии, открытом в июле в Свердловском онкодиспансере, провели первую стереотаксическую радиохирургию. Высокоточная методика облучения позволяет прицельно воздействовать на опухоль высокой дозой однократного фотонного излучения, вызывая гибель опухолевых клеток, что повышает шанс на продление жизни тем пациентам, у которых открытые операции противопоказаны из-за труднодоступного расположения опухоли.
«Стереотаксическая радиохирургия приводит к более выраженному повреждению опухоли по сравнению с обычной лучевой терапией, при этом снижается негативное воздействие радиации на окружающие здоровые ткани. Для успешной реализации этой технологии используются данные методов визуализации, таких как КТ (компьютерная томография), МРТ (магнитно-резонансная томография), ПЭТ-КТ (позитронно-эмиссионная томография).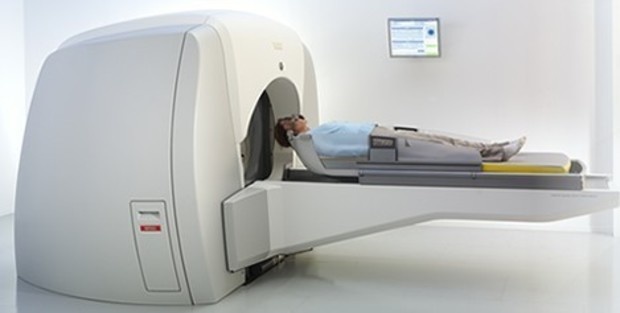 На их основе создается трехмерная модель мишени и окружающих органов, необходимая для проведения дозиметрического планирования облучения», – пояснил руководитель Радиотерапевтической службы Свердловского онкодиспансера Дмитрий Бенцион.
На их основе создается трехмерная модель мишени и окружающих органов, необходимая для проведения дозиметрического планирования облучения», – пояснил руководитель Радиотерапевтической службы Свердловского онкодиспансера Дмитрий Бенцион.
Стереотаксическая радиохирургия применяется для лечения небольших новообразований диаметром до пяти см., это могут быть первичные опухоли практически любых локализаций, а также метастазы.
«Первой пациентке, пролеченной по данной методике, провели стереотаксическую радиохирургию по поводу метастаза рака легкого в головной мозг. Современные системы планирования и реализации лучевой терапии позволяют добиваться оптимального распределения дозы в мишени, что является одним из основных критериев гарантии качества лучевой терапии и соответственно эффективности и безопасности лечения», – пояснила заведующая первым радиотерапевтическим отделением Анастасия Кулакова.
Сеанс длился несколько минут и был абсолютно безболезненный для пациентки. Как правило, для достижения противоопухолевого эффекта достаточно проведения однократного облучения. Результат лечения оценивается через месяц, в случае необходимости процедуру повторяют.
Результат лечения оценивается через месяц, в случае необходимости процедуру повторяют.
Ежегодно в Свердловском онкодиспансере с помощью стереотаксической радиохирургии планируется лечить более 150 пациентов.
Стереотаксическая радиохирургия у больных со злокачественными опухолями верхних дыхательных путей
Заболотный Д.И., Спиженко Ю.П., Лукач Э.В., Сережко Ю.А , Клочков Е.И., Кравченко Д.А.,. ГУ «Институт отоларингологии им. проф. А.И.Коломийченка АМНУ» (дир. акад. Д.И. Заболотный) Центр онкологии и радиохирургии Кибер Клиника Спиженко (дир. акад. Ю.П.Спиженко)
Традиционными методами лечения больных с опухолями головы и шеи являются хирургия, лучевая и лекарственная терапия. Оперативное удаление опухолей занимает ведущее место в комбинированном лечении таких больных, несмотря на то, что часто приводит пациентов к инвалидности. В настоящее время, применение современных технологий, позволяет проводить неинвазивные методы лечения больных с различными опухолями. К таким методам относится радиохирургия с использованием установок Кибер Нож. В настоящий время в мире насчитывается 176 таких установок, из них 115 находятся в центрах и клиниках США (1). Немногим более года, установка Кибер Нож работает в Центре онкологии и радиохирургии Кибер Клиники Спиженко. Уже пролечено около 200 пациентов с доброкачественными и злокачественными опухолями.
К таким методам относится радиохирургия с использованием установок Кибер Нож. В настоящий время в мире насчитывается 176 таких установок, из них 115 находятся в центрах и клиниках США (1). Немногим более года, установка Кибер Нож работает в Центре онкологии и радиохирургии Кибер Клиники Спиженко. Уже пролечено около 200 пациентов с доброкачественными и злокачественными опухолями.
Установка Кибер Нож – на порядок более сложное устройство по сравнению с установкой Гамма Нож, как с технической точки зрения, так и с точки зрения методики облучения. Преимуществом системы Кибер Нож является сочетание роботизированных технологий с системой постоянного контроля по изображению. Считается, что это позволяет с высокой точностью подводить радиационную дозу прямо к опухоли из множества разнообразных направлений. Все излучение высокоэнергетического линейного ускорителя фокусируется в опухоли из 1300 углов подачи. Во время сеанса лечения больных, как утверждают разработчики, практически исключается повреждение окружающих здоровых тканей пациента.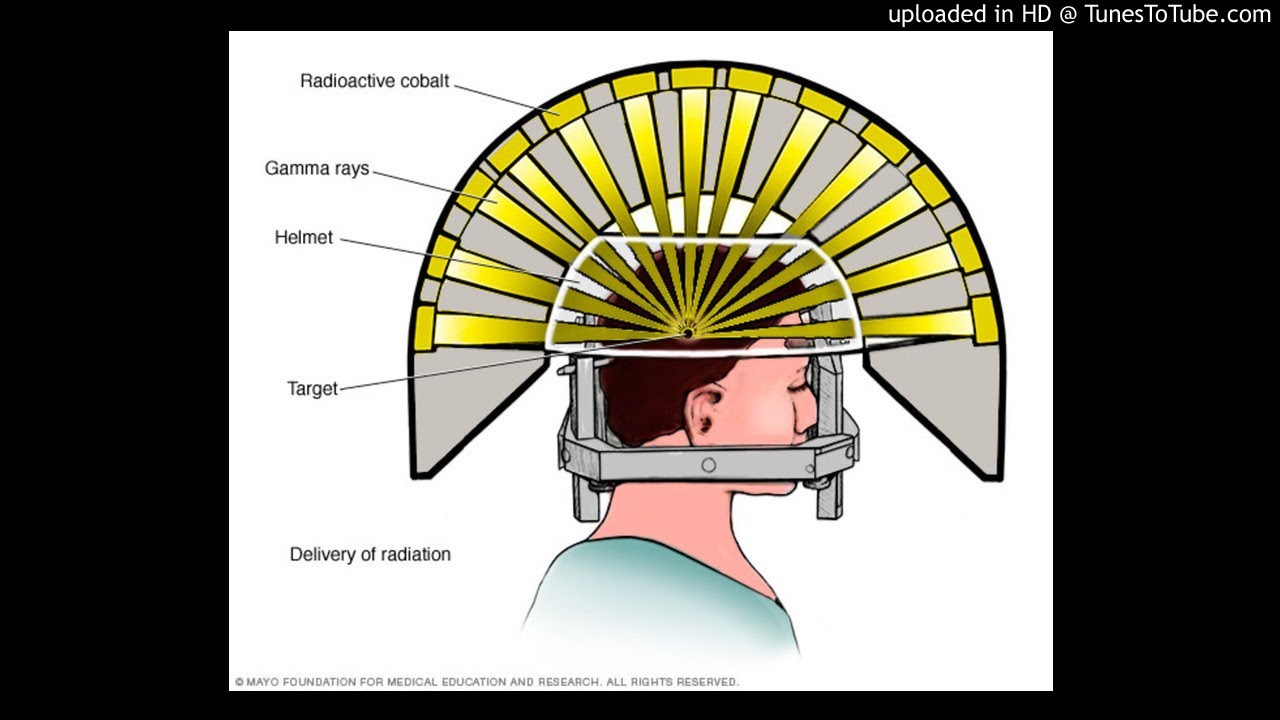 Особенностью системы Кибер Нож является отсутствие необходимости жесткой фиксации пациента во время сеанса стереотаксической радиохирургии так как изначально, система Кибер Нож, разрабатывалась для терапии метастазов печени, рака и метастазов легких, рака простаты (3). Имеется в виду таких функционально подвижных участков тела, в которых опухоль может несколько изменять свое положение во время облучения. Постепенно область применения системы Кибер Нож расширялась, и, уже с 2003 года проводится терапия опухолей любой локализации. За это время, около половины пролеченных пациентов имели опухоль в области «голова и шея». Проводится внедрение разных режимов стереотаксического облучения, как самостоятельного метода лечения, так и в комбинированной терапии «первичных» и рецидивных опухолей данной локализации (2, 4, 5).Использование системы Кибер Нож может быть вариантом терапии при небольших, но сложных для хирургического вмешательства опухолях или для пациентов, которые ищут альтернативы оперативному лечению.
Особенностью системы Кибер Нож является отсутствие необходимости жесткой фиксации пациента во время сеанса стереотаксической радиохирургии так как изначально, система Кибер Нож, разрабатывалась для терапии метастазов печени, рака и метастазов легких, рака простаты (3). Имеется в виду таких функционально подвижных участков тела, в которых опухоль может несколько изменять свое положение во время облучения. Постепенно область применения системы Кибер Нож расширялась, и, уже с 2003 года проводится терапия опухолей любой локализации. За это время, около половины пролеченных пациентов имели опухоль в области «голова и шея». Проводится внедрение разных режимов стереотаксического облучения, как самостоятельного метода лечения, так и в комбинированной терапии «первичных» и рецидивных опухолей данной локализации (2, 4, 5).Использование системы Кибер Нож может быть вариантом терапии при небольших, но сложных для хирургического вмешательства опухолях или для пациентов, которые ищут альтернативы оперативному лечению.
Под нашим наблюдением находилось 13 пациентов со злокачественными опухолями верхних дыхательных путей: в носоглотке – 6, в ротоглотке – 2, в гортани – 2, в гортаноглотке 2, крылонебной ямке -1. Из них с впервые выявленной опухолью было – 4. С рецидивами и остаточными опухолями -9 , отдаленными метастазами (легкие- 1,надпочечник -1, позвоночник-1, кости черепа-1). Из первичных больных с ІІІ стадией было 2 больных, ІV стадией – 1). Диагноз заболевания, у всех больных верифицирован морфологически. Хондросарком – 2, раковые опухоли — 11. Сеансы стереотаксической радиохирургии проводились на установке Кибер Нож CyberKnife G4, установленный в Кибер Клинике Спиженко. При радиохирургическом лечении использовалось однократное подведение дозы более 7 Гр за 2-5 сеансов?. Высокая точность системы КиберНож обеспечивается тщательным предварительным КТ и МРТ исследованием, определяющим точное расположение опухоли. В результате чего, создается трехмерная «карта» для CyberKnife G4. Таким образом, индивидуально для каждого пациента, определяется форма, размер и расположение опухоли, а также ткани и структуру органов, которые должны быть защищены в процессе проведения лечения.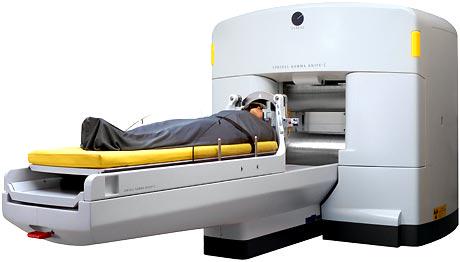 Размер опухолей у пролеченных больных был до 60 мм. Осложнений, связанных с проведением стереотаксической радиохирургии – не наблюдалось. Через месяц после проведенного лечения на установке Кибер Нож отмечался частичный регресс опухоли у пациентов. В последующем, проводились курсы адъювантной полихимиотерапии. Как пример, приводим результат лечения пациентки с рецидивом рака гортани после хирургического лечения. У больной С., 28 лет, в январе 2010 года был диагностирован рак гортани (левой голосовой складки) (рис 1).
Размер опухолей у пролеченных больных был до 60 мм. Осложнений, связанных с проведением стереотаксической радиохирургии – не наблюдалось. Через месяц после проведенного лечения на установке Кибер Нож отмечался частичный регресс опухоли у пациентов. В последующем, проводились курсы адъювантной полихимиотерапии. Как пример, приводим результат лечения пациентки с рецидивом рака гортани после хирургического лечения. У больной С., 28 лет, в январе 2010 года был диагностирован рак гортани (левой голосовой складки) (рис 1).
Рисунок 1. Непрямая ларингоскопия. Опухоль поражает левую голосовую складку.
В феврале больная консультирована в клинике Альфреда Круппа (г. Эссен), где 01.03.10 было произведено эндоскопическое удаление опухоли с применением лазера . Облучение, из-за отказа больной, не проводилось. Пациентка находилась под наблюдением и через месяц, по данным контрольной биопсии – роста опухоли не наблюдалось. Однако, в июне, результаты биопсии показали рецидив рака и поэтому, в клинике Альфреда Круппа ей была произведена повторная эндоскопическая операция с удалением рецидива опухоли в срединном отделе гортани слева. В июле отмечалось продолжение болезни и при повторной биопсии верифицирован плоскоклеточный ороговевающий рак. В Институт отоларингологии больная поступила в тяжелом состоянии при явлениях субстеноза гортани. На МРТ и эндоскопически опухоль левой половины гортани размерами 34х38х65 мм поражала щитовидный хрящ , прорастала в мягкие ткани шеи (рис. 2, 3). В связи с затруднением дыхания была срочно произведена трахеостомия.
В июле отмечалось продолжение болезни и при повторной биопсии верифицирован плоскоклеточный ороговевающий рак. В Институт отоларингологии больная поступила в тяжелом состоянии при явлениях субстеноза гортани. На МРТ и эндоскопически опухоль левой половины гортани размерами 34х38х65 мм поражала щитовидный хрящ , прорастала в мягкие ткани шеи (рис. 2, 3). В связи с затруднением дыхания была срочно произведена трахеостомия.
Рисунок 3. Непряма ларингоскопія. Пухлина закриває просвіт гортані.
Рисунок 2. МРТ шиї, сагіттальна проекція. Визначається утворення в області гортані, яке поширюється в м’які тканини шиї і гортанний відділ глотки.
От предложенного радикального оперативного лечения больная категорически отказалась и как альтернативный вариант, ей было проведено лечение на установке Кибер Нож. За 5 сеансов к опухоли было подведено 37,5 Гр.
После проведеного лечения, амбулаторно, по месту жительства пациентки, проводилась антибактериальная (в течение 7 дней) и симптоматическая терапия. Субъективно пациентка отмечала боль при глотании, которая появилась через неделю после радиохирургического лечения. Интенсивность боли была умеренной, но аналгетиков пациентка не принимала. Кроме этого, пациентка отмечала откашливание некротически измененной ткани. Все перечисленные осложнения продолжались 5 дней. Дыхание осуществлялось естественным путем и через трахеостому. Через две недели произведена деканюляция.
Субъективно пациентка отмечала боль при глотании, которая появилась через неделю после радиохирургического лечения. Интенсивность боли была умеренной, но аналгетиков пациентка не принимала. Кроме этого, пациентка отмечала откашливание некротически измененной ткани. Все перечисленные осложнения продолжались 5 дней. Дыхание осуществлялось естественным путем и через трахеостому. Через две недели произведена деканюляция.
Через месяц после курса лечения на установке Кибер Нож отмечался частичный регресс опухоли (рис. 4). По данным МРТ опухоль имела размеры 16х30х39 мм с центрально расположенным участком некроза (рис 5). Накопление контраста?
Рисунок 5. МРТ шиї, нативне дослідження, горизонтальна проекція.
Рисунок 4. Непряма ларингоскопія. Залишкова пухлина в області лівого серединного відділу гортані.
Определяется гетерогенная опухоль гортани с участком некроза в ее центральном участке.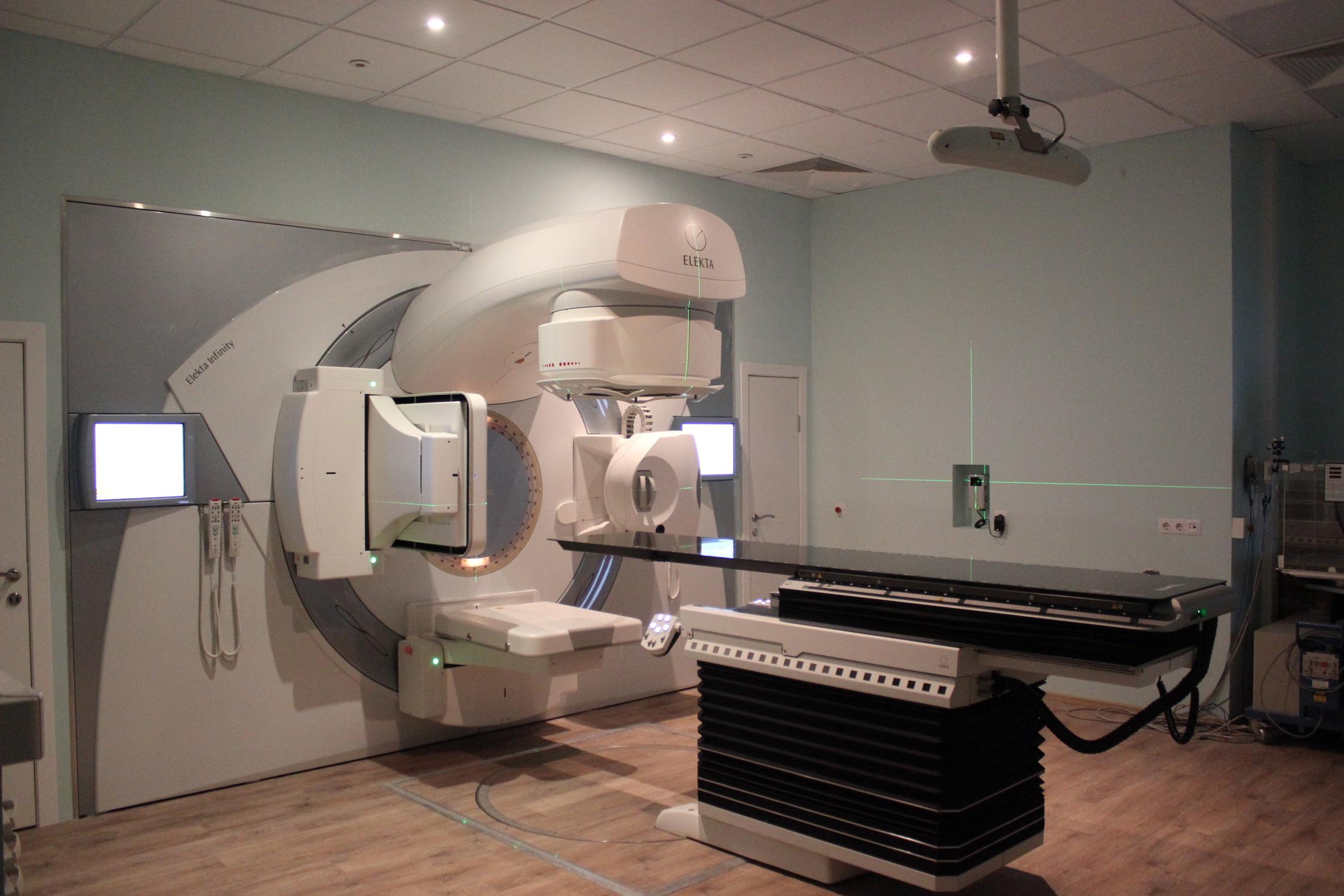 Подвижность обеих половин гортани восстановилось.
Подвижность обеих половин гортани восстановилось.
Дыхание через естественные пути свободное, трахеостомическое отверствие закрылось самостоятельно. Голос хриплый. Произведена бипсия из левой половины гортани. При гистологическом исследовании – рост опухоли не выявлен, патоморфоз ІV. Больная закончила два курса полихимиотерапии в онкологическом диспансере в г. Львове. При контрольном осмотре через два месяца после лечения рецидива опухоли не выявлено эндоскопически и по данным КТ.
Анализируя результаты предварительных данных лечения стереотаксической радиохирургии следует отметить, что большинство из 13 больных страдали запущенными новообразованиями и подвергались предварительному комбинированному лечению что накладывало отпечаток на еффективность. Полный регресс опухоли у трех больных и значительное улучшение качества жизни больных с частичным эффектом позволяет нам рассматривать оптимистически этот метод лечения.
Рис.6 Полный регресс опухоли.
Стереотаксическое облучение на установке Кибер Нож является эффективным и безопасным методом лечения злокачественных опухолей верхних дыхательных путей.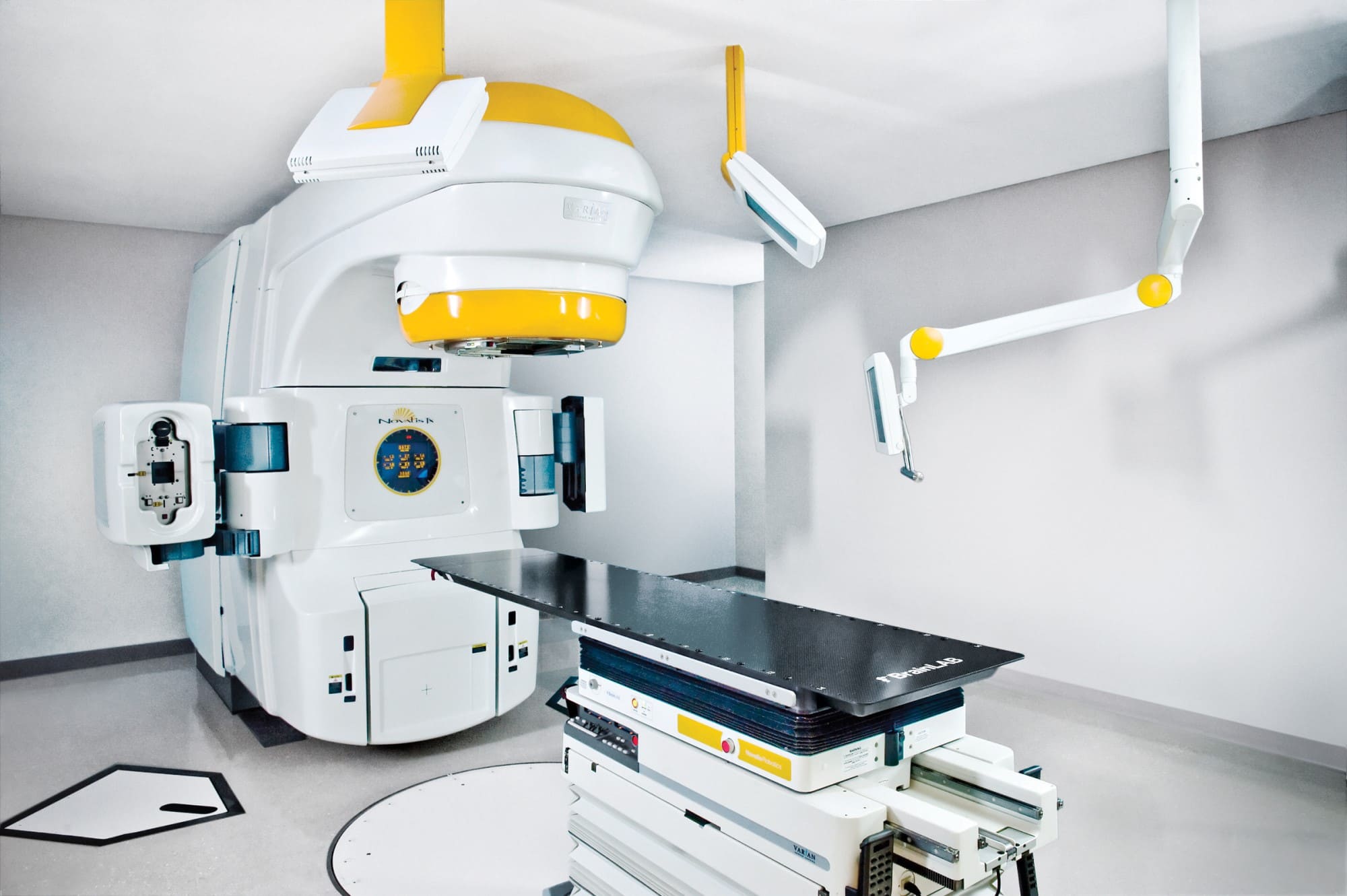 Преимуществом такого лечения является возможность проведения его амбулаторно без анестезиологического, реанимационного и реабилитационного сопровождения.
Преимуществом такого лечения является возможность проведения его амбулаторно без анестезиологического, реанимационного и реабилитационного сопровождения.
Shaw E , Scott C , Souhami L , Dinapoli R , Kline R , Loeffler J , Farnan N // Single dose radiosurgical treatment of recurrent previously irradiated primary brain tumors and brain metastases : final report of RTOG protocol 90-05// Int J Radiat Oncol Biol Phys . May 1;47(2):291-8, 2000). Int J Radiat Oncol Biol Phys . May 1;47(2):291-8, 2000)
- Ильялов С.Р., Голанов А.В., Пронин И.Н.и др.Стереотаксическая радиохирургия внутримозговых метастазов с применением «Гамма-Ножа»: тактика применения и результаты лечения. / Онкохирургия №1/2008
- Голанов А.В., Горлачев Г.Е. Стереотаксическая радиотерапия и радиохирургия в лечении нейрохирургических больных / Онкохирургия 2010, прил.1 . – С.144-145.
- www.MRTInfo.com
- Teguh DN, Levendag PC, Noever I et al. Treatment techniques and site considerations regarding dysphagia-related quality of life in cancer of the oropharynx and nasopharynx.
 / Int. J Radiat. Oncol. Biol. Phys. 2008 Nov 15;72(4):1119-27. Epub 2008 May 28.
/ Int. J Radiat. Oncol. Biol. Phys. 2008 Nov 15;72(4):1119-27. Epub 2008 May 28. - Heron DE, Ferris RL, Karamouzis M et al. Stereotactic body radiotherapy for recurrent squamous cell carcinoma of the head and neck: results of a phase I dose-escalation trial./ Int. J Radiat. Oncol. Biol. Phys. 2009 Dec 1;75(5):1493-500. Epub 2009 May 21.
Центр радиохирургии — Отделение в Киеве
Радиохирургия — метод безоперационного лечения опухолей воздействием ионизирующего излучения, приводящего к биологической гибели опухолевых клеток. КиберНож — наиболее совершенное развитие технологии радиохирургии. Термин “стереотаксическая радиохирургия”, воплощенный в КиберНоже, представляет собой эффективное сочетание мощнейших вычислительных систем, программного обеспечения, медицинской физики и робототехники.
КиберНож в Центре радиохирургии «Клиники Спиженко»
Для пациента это означает, что в каждый кубический миллиметр объема, подлежащего лечению, будет равномерно подана требуемая доза ионизирующего излучения от компактного линейного ускорителя, входящего в состав комплекса КиберНож.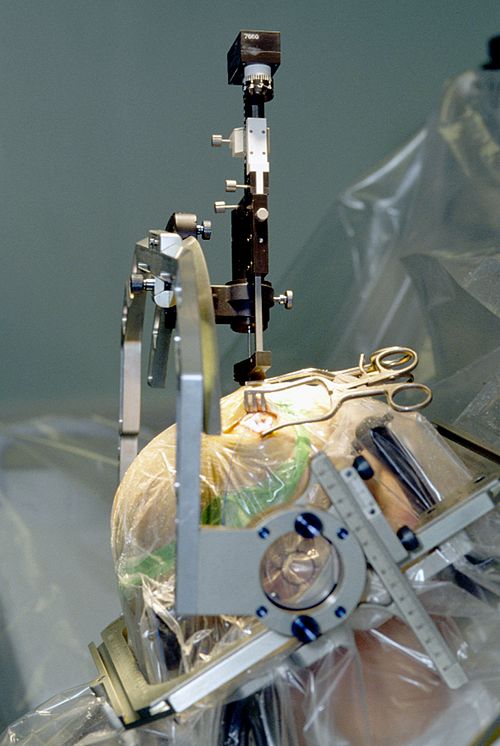
За фразой «Радиохирургия — неинвазивный метод лечения рака» для пациентов скрывается основное отличие радиохирургии от классических методов лечения онкологических заболеваний — операции проводятся без единого разреза и любых других нарушений целостности кожных покровов или костей, позволяя оперировать даже недоступные ранее опухоли.
И это не только опухоль, КиберНож успешно используется в Клинике Спиженко для лечения некоторых неонкологических заболеваний — АВМ, каверномы, невралгии тройничного нерва и др.
В чем особенность лечения рака на КиберНоже?
Радиохирургическая система КиберНож
Радиохирургия практически исключает необходимость послеоперационной реабилитации, что позволяет пациентами сразу после операции возвратиться к своему привычному распорядку дня. Сама процедура (а не операция) в нашем центре радиационной медицины длится менее часа, а курс лечения составляет всего от одного до трех сеансов.
Задача точности подводимой дозы решается путем предварительного создания цифровой пространственной модели расположения участка, подлежащего лечению на КиберНоже, и окружающих его тканей, в которые допускается подача неопасной дозы облучения (так называемая “толерантная доза”, либо тканей, подачу излучения в которые требуется полностью исключить (например, ствол головного мозга, слюнные железы, хрусталик глаза и т.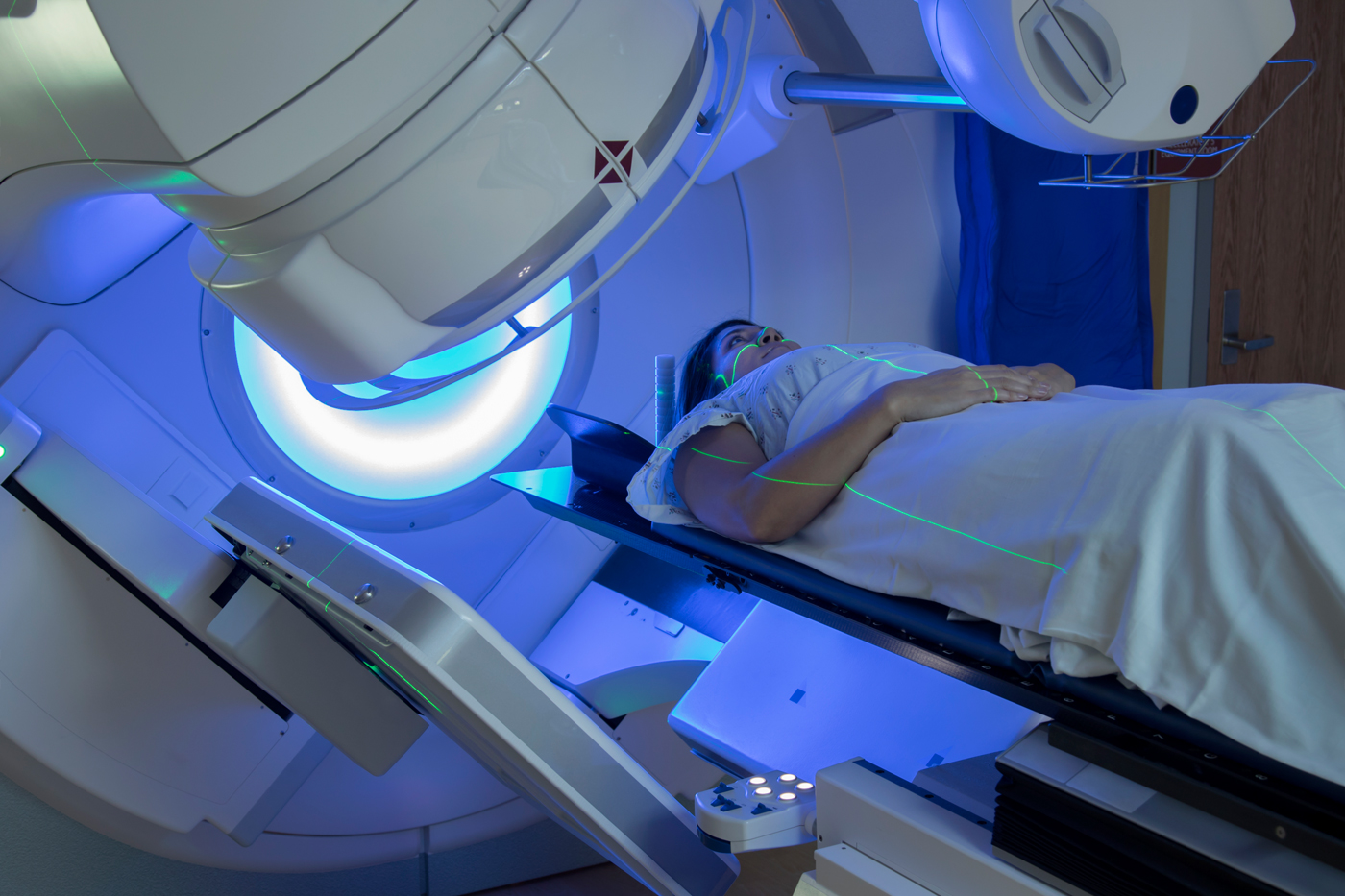 д.).
д.).
Для создания модели используются данные предварительных исследований — снимки КТ (компьютерной томографии), высокоточной МРТ (магнитно-резонансная томография) и т.д. Все исследования в Клинике Спиженко выполняются на собственной территории, в Центре диагностики, оснащенном современным оборудованием.
Точность радиохирургии (КиберНож имеет точность до 0,5 мм) и тщательная предварительная диагностика с определением четкого местоположения опухоли и метастазов, позволяют эффективно удалять опухоли даже в труднодоступных для традиционной хирургии местах.
Радиохирургия исключает получение избыточных доз облучения — полученные при лечении КиберНожом дозы гораздо меньше тех, что применяются в традиционной лучевой терапии, что обусловлено влиянием КиберНожа исключительно на опухолевую ткань и не вредит жизненно важным органам и системам остального организма. Благодаря точному прицеливанию КиберНожа, радиохирургия намного более эффективна по сравнению с классическим лечением, ведь сами опухоли получают значительно большую дозу, то есть облучение попадает только в них.
Квалификация всех специалистов Центра радиохирургии Клиники Спиженко позволяет реализовать максимум потенциала, заложенного производителем в комплекс КиберНож. Радиологи, лучевые терапевты, онкологи, медицинские физики, постоянно находясь в тесном контакте, обеспечивают быстрое и эффективное лечение различных опухолей.
Активное участие в профильном мировом сообществе радиохирургов позволяет не только проводить лечение по методикам, созданным лучшими мировыми специалистами в отрасли радиохирургии, но и вести разработку и внедрение собственных инноваций, получивших поддержку и одобрение зарубежных коллег, которые также берут на вооружение опыт Клиники Спиженко.
Какие опухоли лечит КиберНож?
Среди наиболее востребованных программ — органосохраняющее лечение опухолей почек, в том числе при раке единственной почки, лечение меланомы хориоидеи (меланома глаза) без удаления органа и с сохранением остроты зрения, лечение опухолей и метастазов в печень и другие.
При необходимости, возможности КиберНожа дополняются современной лучевой терапией, химиотерапией, таргетной терапией, хирургической помощью — каждая программа лечения уникальна для конкретного пациента.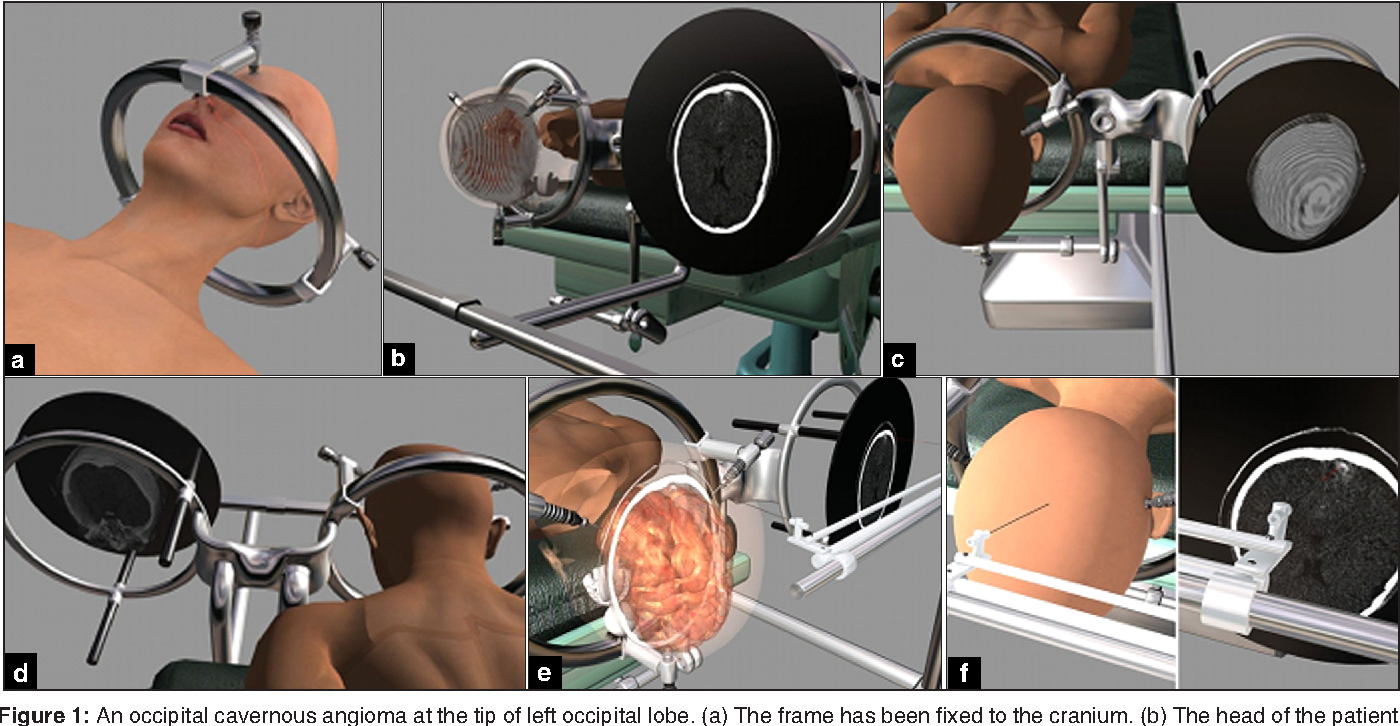 Поэтому в случае необходимости в онкологической помощи обращайтесь в Клинику Спиженко не теряя драгоценного времени.
Поэтому в случае необходимости в онкологической помощи обращайтесь в Клинику Спиженко не теряя драгоценного времени.
Стереотаксическая радиохирургия | Johns Hopkins Medicine
Что такое стереотаксическая радиохирургия?
Стереотаксическая радиохирургия — это очень точная форма терапевтического излучения, которая может использоваться для лечения патологий головного и спинного мозга, включая рак, эпилепсию, невралгию тройничного нерва и артериовенозные мальформации.
Стереотаксическая радиохирургия не предполагает разреза или открытия; он тщательно направляет пучки рентгеновских лучей на патологические ткани через кожу с разных направлений.
Радиохирургия работает так же, как и другие виды терапевтической радиологии: рентгеновские лучи искажают или разрушают ДНК клеток в аномальных областях, поэтому они не могут воспроизводиться и расти. При оптимальном лечении патологическая ткань становится неактивной и постепенно сокращается.
Повреждения позвоночника или других участков можно лечить с помощью механизированной руки, которая перемещается вокруг пациента во время лечения.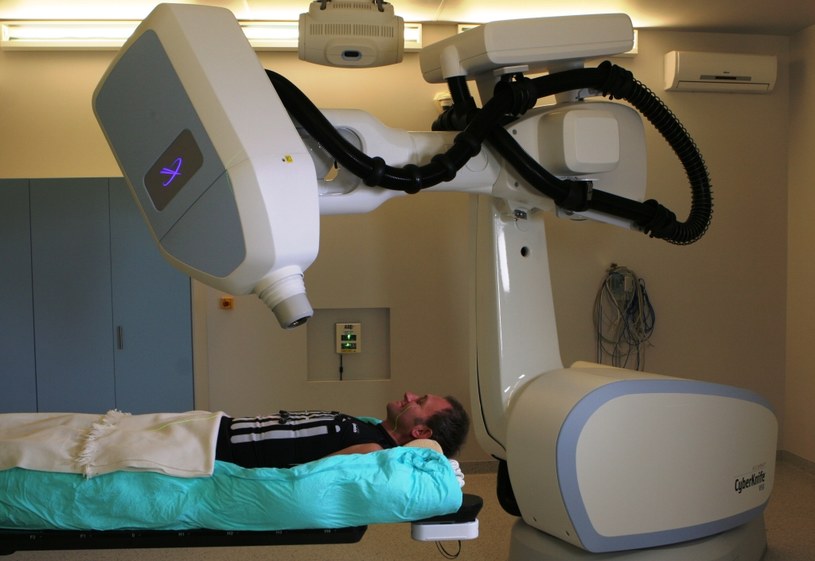
Причины выбора стереотаксической радиохирургии
Хирургическая точность метода особенно полезна при лечении небольших или труднодоступных аномалий головного и спинного мозга.Целенаправленная фокусировка излучения в методах радиохирургии приводит к меньшему повреждению окружающих здоровых тканей и меньшему риску инфицирования, что делает его более безопасным для тех, кто только что перенес операцию.
Возможные побочные эффекты
Стереотаксическая радиохирургия вызывает меньше и более мягкие побочные эффекты, чем обычные радиотерапевтические методы, которые охватывают более широкую область и могут повлиять на здоровые ткани. Следующие побочные эффекты обычно носят временный характер и проходят через несколько недель.
- усталость
- Раздражение кожи в месте обработки
- Выпадение волос на участке лечения
- головная боль
- неврологические симптомы, такие как судороги, онемение / покалывание или слабость
- Желудочно-кишечные симптомы, такие как тошнота, рвота или диарея
Перед процедурой
Стереотаксическая радиохирургия использует командный подход с привлечением специалистов в области радиационной онкологии и нейрохирургии. Эксперт по дозиметрии определяет, как должны быть направлены лучи, а физик рассчитывает количество излучения, которое должен получить пациент, балансируя риск и потенциальную эффективность. Ключевым элементом планирования процедуры является максимальное лечение аномальных тканей при одновременной защите здоровых тканей вокруг аномальной области.
Эксперт по дозиметрии определяет, как должны быть направлены лучи, а физик рассчитывает количество излучения, которое должен получить пациент, балансируя риск и потенциальную эффективность. Ключевым элементом планирования процедуры является максимальное лечение аномальных тканей при одновременной защите здоровых тканей вокруг аномальной области.
Вместе эти эксперты тратят около двух недель на планирование процедуры. В экстренных случаях время на подготовку может быть меньше.
Во время процедуры
Лечение может проходить в амбулаторных условиях.Вы можете рассчитывать провести несколько часов в амбулаторном центре, что включает в себя подготовку к процедуре, лечение и наблюдение после процедуры. Вам нужно будет попросить друга или члена семьи помочь отвезти вас домой. Процедура занимает около 30–60 минут, и вы должны оставаться неподвижными. Нет ни надреза, ни порезов. По прибытии вы встретитесь с командой врачей, включая врачей, медсестер и техников, которые позаботятся о вас. Если вы лечитесь от поражения в мозгу, на голову надевают подголовник, чтобы она оставалась неподвижной.Во время лечения вы будете находиться на жестком столе, например, на столе для МРТ или КТ. Ваша терапевтическая бригада запрограммирует аппарат и доставит вам рентгеновские лучи для лечения, которые включают несколько доз сфокусированного рентгеновского излучения. После процедуры вы будете переведены в зону восстановления, где за вами будут наблюдать, чтобы убедиться, что вы чувствуете себя хорошо. После того, как вы и ваша лечащая бригада почувствуете себя комфортно, вы можете идти домой.
Если вы лечитесь от поражения в мозгу, на голову надевают подголовник, чтобы она оставалась неподвижной.Во время лечения вы будете находиться на жестком столе, например, на столе для МРТ или КТ. Ваша терапевтическая бригада запрограммирует аппарат и доставит вам рентгеновские лучи для лечения, которые включают несколько доз сфокусированного рентгеновского излучения. После процедуры вы будете переведены в зону восстановления, где за вами будут наблюдать, чтобы убедиться, что вы чувствуете себя хорошо. После того, как вы и ваша лечащая бригада почувствуете себя комфортно, вы можете идти домой.
Дома
После лечения вы можете вернуться к своей обычной деятельности.Ваша команда неврологов и нейрохирургов продолжит наблюдение за вами с помощью КТ и МРТ во время последующего наблюдения. Для лечения обычно требуется только один сеанс. Некоторые поражения могут потребовать более одного сеанса лечения, вероятно, за пять сеансов. (Обычная лучевая терапия может потребовать до 10 сеансов.)
Стереотаксическая радиохирургия головного мозга: LINAC
Обзор
Радиохирургия использует высокоэнергетические лучи для уничтожения опухолей и других заболеваний.Лучи радиации направляются в мозг машиной, находящейся вне вашего тела. В радиохирургии используются лучи очень высокой дозы, предназначенные для уничтожения всех клеток в целевой области. Лучи плотно сфокусированы и точны, чтобы не повредить здоровые клетки. Его часто назначают в виде одноразовой терапии в течение одного дня или можно разделить на 2–5 процедур, проводимых в течение недели. Радиохирургия может использоваться как альтернатива традиционной открытой операции на головном мозге, которая требует разреза.
Что такое стереотаксическая радиохирургия?
Радиация повреждает ДНК внутри клеток, делая их неспособными делиться и расти.Польза от радиации проявляется не сразу, а со временем. Агрессивные опухоли, клетки которых быстро делятся, обычно быстро реагируют на радиацию. Со временем аномальные клетки погибают, и опухоль может уменьшиться в размерах. Доброкачественные опухоли, клетки которых медленно делятся, могут проявить эффект от нескольких месяцев до года.
Рисунок 1. Радиохирургия формирует пучки излучения, чтобы они соответствовали точным очертаниям опухоли и сводили к минимуму воздействие на здоровый мозг. Лучи идут под разными углами и пересекаются в опухоли, создавая высокую дозу.Красное кольцо показывает максимальную дозу, а каждое внешнее кольцо представляет все меньшие и меньшие дозы.Высокая точность очень важна, так как смертельная доза применяется только к самой цели, а не к окружающим здоровым тканям или критическим структурам (рис. 1). Для достижения высочайшей точности при планировании и проведении процедуры используется компьютерная технология управления изображениями. Метод наведения на объект с учетом всех трех измерений называется стереотаксисом.
Радиохирургия может быть проведена в виде однодневного сеанса или разделена на 2–5 процедур в течение недели (гипофракционирование).Доставление части общей дозы облучения дает нормальным клеткам время на восстановление между сеансами лечения и может уменьшить побочные эффекты. Врачи могут посоветовать радиохирургию как самостоятельное лечение или в сочетании с хирургией, химиотерапией или иммунотерапией. Облучение может проводиться перед операцией, чтобы уменьшить опухоль или АВМ, или после операции, чтобы остановить рост оставшихся опухолевых клеток.
Основные радиохирургические технологии:
- Гамма-нож использует гамма-лучи кобальта-60
- Системы линейных ускорителей (LINAC) используют рентгеновское излучение высокой энергии; Novalis, TrueBeam или Cyberknife
- В протонной лучевой терапии используются ускоренные протоны
Каждая технология имеет уникальные характеристики, но преследует одни и те же цели:
1.Точно найдите цель (опухоль, поражение)
2. Удерживайте цель неподвижно
3. Точно наведите луч излучения
4. Сформируйте луч излучения на цель
5. Дайте определенную дозу излучения
| В чем разница? | |
| Радиохирургия 1-5 фракций | Несколько раз доставляет радиацию в очень высоких дозах в сильно сфокусированную область.Преимущество заключается в его быстром спаде, что дает меньшую дозу для нормальных клеток. |
| RadioTHERAPY 6-33 фракции | Доставляет радиацию в более низких дозах, в течение нескольких дней и на большие территории. Лечит «край» ткани вокруг опухоли. |
Линейный ускоритель | Одиночный луч вращается вокруг пациента несколько раз, всегда фокусируясь на опухоли.Пациента удерживают либо с помощью подголовника, либо с помощью лицевой маски. |
Гамма-нож | 192 луча точно нацелены на опухоль, причем каждый луч исходит из разных точек. Пациент удерживается на подголовнике. |
Кто кандидат?
Вы можете пройти радиохирургию, если у вас есть:
- Доброкачественная опухоль: невринома слухового нерва, менингиома, аденома гипофиза, краниофарингиома, гемангиобластома, опухоль гломуса
- Метастатическая опухоль: легкое, молочная железа, меланома или другой рак, распространившийся на мозг
- Первичная опухоль головного мозга, например злокачественная глиома
- Артериовенозная мальформация (АВМ)
- Кавернома
- Невралгия тройничного нерва
Кто выполняет процедуру?
Бригада радиохирургии состоит из нейрохирурга, онколога-радиолога, медицинского физика, медсестры-онколога, а иногда и дозиметриста и лучевого терапевта.Нейрохирург и онколог-радиолог несут ответственность за назначение радиохирургии, определение правильной цели и дозы облучения, а также за утверждение плана лечения. Медицинский физик и дозиметрист участвуют в планировании лечения и настройке оборудования. Лучевой терапевт помещает пациента в аппарат и наблюдает за лечением под наблюдением врачей и физика. Медсестра управляет лекарствами и всеми побочными эффектами.
Что происходит до лечения?
Консультация
Ваш первый прием — это консультация нейрохирурга или онколога-радиолога.Ваш врач проведет медицинский осмотр и подтвердит ваш диагноз на основании визуализационных исследований (КТ, МРТ) и отчетов о патологии. Ваш врач обсудит с вами лучший тип лучевой терапии для вашей конкретной опухоли или поражения, объяснит процесс лечения и обсудит потенциальные преимущества и возможные побочные эффекты. Как только вы решите продолжить лечение, вы подпишете формы согласия.
Что происходит дальше, зависит от того, используется ли ваше лечение: маска для лица или оправа для головы.Лицевая маска и визуализация (шаги 1-3) выполняются за 1-2 недели до радиохирургии. Если используется головная рама, все этапы выполняются за один день.
Что происходит во время лечения?
В день обращения приехать в центр и зарегистрироваться у портье. Вы можете привести с собой друга или родственника в компанию. Пожалуйста, попросите кого-нибудь из членов семьи или друга отвезти вас домой после лечения.
В зависимости от размера и местоположения цели будет использоваться маска для лица или оправа для головы, чтобы полностью удерживать голову во время лечения.
Рис. 2. Маска из термопласта адаптируется к контурам вашего лица. Передняя и задняя части сетки прикреплены к U-образному приспособлению, которое прикрепляется к столу для лечения, чтобы удерживать голову в неподвижном состоянии. Шаг 1. Лицевая маска или крепление к оправе
Стереотаксическая лицевая маска изготавливается на заказ, чтобы точно соответствовать вашему лицу. Он будет использоваться во время визуализации и лечения, чтобы ваша голова оставалась неподвижной. Вы будете лежать, положив голову на сетку, натянутую между U-образным прибором.Затем полоски эластичного пластика накладываются на лоб, под нос и подбородок. Вам будет предложено прикусить небольшой кусок пластика передними зубами. Затем термопластичная сетка погружается в водяную баню, что делает ее очень гибкой. Сетка накладывается на лицо и прилегает (рис. 2). Вы сможете легко дышать. Рукавицы от холода помогают сетке остыть и затвердеть. Создание маски занимает около 30 минут.
Может потребоваться стереотаксическая рамка, прикрепленная к голове с помощью небольших булавок.В этом случае вам сделают внутривенную седацию, чтобы минимизировать дискомфорт. Пока вы сидите, рама временно закрепляется на вашей голове с помощью ремней на липучке. Четыре места для булавок очищаются и вводятся под местной анестезией. Вы можете получить легкое успокаивающее средство, чтобы уменьшить дискомфорт. Вы можете почувствовать некоторое давление, когда штифты затянуты. Установка каркаса головы занимает около 30 минут и переносится хорошо.
Рис. 3. Светоотражающие шарики помещаются на лицевую маску перед компьютерной томографией.Маркеры видны на компьютерной томографии и помогают определить точные координаты опухоли или поражения. Шаг 2: получение изображений
Затем вы пройдете сканирование изображений, надев лицевую маску или оправу для головы. Светоотражающие шарики помещаются на лицевую маску и надеваются во время компьютерной томографии (рис. 3). Эти маркеры появляются на снимке и помогают определить точные трехмерные координаты цели в мозгу. Может потребоваться новое сканирование МРТ.
После сканирования вас отвезут в отдельную комнату и дадут легкий перекус, пока врачи планируют назначение лучевой терапии на более поздний срок в тот же день.Ваша семья и друзья могут составить вам компанию. Если к вам прикрепили головной каркас, он останется на месте до завершения лечения.
Рис. 4. Компьютер создает трехмерное изображение вашей анатомии. План лечения определяет количество и угол пучков, размер и форму пучков излучения, а также дозу облучения. Шаг 3. Планирование лечения
Информация о расположении, размере и близости опухоли к критическим структурам собирается с помощью компьютерной томографии или МРТ.Современное компьютерное программное обеспечение использует сканирование для создания трехмерного изображения вашей анатомии и опухоли (рис. 4). Используя программное обеспечение, онколог-радиолог, нейрохирург и физик работают как одна команда, чтобы определить:
- соответствующая цель (и)
- доза облучения
- Количество и угол обработки балок
- размер и форма лучей точно соответствуют опухоли или мишени
Каждый отдельный луч слишком слаб, чтобы повредить здоровый мозг на пути к цели.Но на пересечении всех лучей доза энергии достаточно сильна, чтобы разрушить опухоль.
Шаг 4: расположите пациента
После того, как радиационный аппарат откалиброван и подготовлен для вашего конкретного плана лечения, вы лягте на стол. Маска накладывается на лицо и прикрепляется к столу. Если у вас есть рама для головы, она крепится к лечебному столу.
Юстировочные лазеры и рентгеновские лучи позиционируют вас правильно. Делается стереоскопический рентген и сравнивается с планом лечения.Любые перекосы исправляются перед лечением.
Рис. 5. Лицевая маска прикреплена к терапевтическому столу и удерживает голову пациента в неподвижном состоянии в поле для лечения. Аппарат LINAC вращается вокруг пациента, направляя лучи излучения на опухоль. Шаг 5: доставить излучение
Терапевт выходит из комнаты и управляет аппаратом из диспетчерской. Команда наблюдает за вами через видеомониторы и разговаривает с вами по внутренней связи.Аппарат и лечебный стол время от времени перемещаются, чтобы доставить пучки излучения с одного или нескольких направлений (рис. 5).
Машина большая и издает гудение, когда движется вокруг вашей головы. Его размер и движение могут поначалу пугать. Он может пройти близко к вашему телу, но не коснется вас. Вам не нужно задерживать дыхание — просто дышите нормально. Лечение может занять 30 минут или дольше, в зависимости от количества и сложности целей.
Что происходит после лечения?
После лечения терапевт снимает маску для лица или подголовник и помогает вам встать со стола для лечения.Если запланировано несколько процедур, маска будет храниться в центре для следующего сеанса. Вы будете возвращаться каждый день в назначенное время, чтобы повторять шаги 4 и 5, пока не будут доставлены все фракции полной дозы. Вам могут прописать лекарства на несколько дней или недель после лечения.
Если у вас была рама головы, штифты и рама удаляются. У вас могут быть выделения из участков булавок и легкая головная боль. Затем вы можете собрать свои вещи и отправиться домой. Следуйте этим инструкциям по уходу за участками контактов:
- Если у вас есть дискомфорт или болезненность вокруг участков булавок, может помочь Тайленол.
- Steri-полосы или повязки могут быть наложены на места для булавок. Уберите их на следующий день.
- В первые несколько дней вокруг мест расположения булавок может появиться припухлость. Держите голову приподнятой и приложите к этой области пакет со льдом.
- Обратитесь к врачу, если у вас температура выше 101 градуса, есть дренаж или признаки инфекции в местах расположения булавок.
Какие риски?
Побочные эффекты излучения различаются в зависимости от типа опухоли, дозы, доставленной в опухоль, количества фракций и количества здоровой ткани в целевой области.Некоторые побочные эффекты носят временный характер, а некоторые могут быть постоянными. Спросите своего врача о конкретных побочных эффектах, которые могут возникнуть у вас. Общие побочные эффекты могут включать:
Набухание (отек)
Радиация вызывает гибель опухолевых клеток. Естественная реакция организма на гибель или повреждение клеток — отек. Отек — это избыточная жидкость или припухлость в тканях мозга. Набухание мозга может вызвать головные боли, слабость, судороги, спутанность сознания или затруднение речи. Это также может ухудшить симптомы, которые были до лечения.Если вы начинаете чувствовать дискомфорт из-за головных болей или каких-либо других симптомов, позвоните своему нейрохирургу или онкологу-радиологу. Стероидные препараты (дексаметазон) могут быть назначены для уменьшения отека мозга и уменьшения жидкости в опухоли. Стероиды всегда следует принимать во время еды, чтобы защитить желудок и предотвратить тошноту. Стероиды также могут влиять на нормальные бактерии во рту и вызывать дрожжевую инфекцию, называемую молочницей, которая проявляется в виде беловатых пятен на языке. Не прекращайте прием стероидов резко. Чтобы избежать синдрома отмены, требуется график постепенного снижения дозы.
Лучевой некроз
В некоторых случаях радиохирургия может вызвать некротический (мертвый) центр опухоли. Лучевой некроз может произойти в любое время, но чаще всего он возникает через 6–12 месяцев после радиохирургии. Эта умирающая ткань может стать токсичной для окружающей нормальной ткани, и может возникнуть отек. Лучевой некроз может быть похож на повторный рост опухоли на МРТ. Специализированные тесты, такие как ПЭТ-сканирование или МР-спектроскопия / перфузия, могут помочь отличить некроз от опухоли.Лечение лучевого некроза может включать:
- Лекарства, уменьшающие воспаление, 5-ЛОКСИН (Boswellia serrata).
- Гипербарическая оксигенотерапия (лечение в кислородной камере) может быть назначена для заживления поврежденных тканей головного мозга.
- Лекарство под названием бевацизумаб (Авастин) может быть назначено, если другие методы лечения неэффективны.
- В некоторых случаях для удаления некротической ткани может потребоваться операция.
Какие результаты?
После радиохирургии периодически будут проводиться МРТ-сканирование, чтобы врачи могли искать признаки реакции.Может пройти несколько месяцев, прежде чем станут заметны эффекты от лечения. Некоторые опухоли можно полностью удалить с помощью облучения. Для других опухолей цель — остановить или остановить рост. В некоторых случаях опухоль считается контролируемой, даже если она не сокращается.
Рис. 6. Для медленно растущих опухолей, таких как акустические невриномы, облучение со временем вызывает постепенное уменьшение.В случае доброкачественных опухолей цель состоит в том, чтобы остановить или контролировать рост опухоли. Около 60% пациентов с невриномой слухового нерва или менингиомой показывают уменьшение опухоли после радиохирургии, в то время как около 30% опухолей остаются прежними (рис.6). Менее 10% этих опухолей продолжают расти.
Рис. 7. Для быстрорастущих опухолей, таких как метастатический рак легких, облучение вызывает быстрое сокращение (3 месяца).При метастатических опухолях цель уменьшения размера опухоли или остановки роста опухоли достигается у 80-90% пациентов (рис. 7).
Для злокачественных первичных опухолей результаты различаются в зависимости от размера, местоположения и типа опухоли. Поговорите со своим врачом о своем конкретном прогнозе.
Целью АВМ является утолщение стенок сосудов и образование рубцовой ткани, которая перекрывает кровоснабжение.Для полного закрытия АВМ может потребоваться до 3 лет. Результаты связаны с размером и расходом АВМ. Небольшие АВМ (<3 см) успешны в 90% случаев. Для больших АВМ (> 5 см) может потребоваться несколько сеансов радиохирургии с интервалом от 3 до 6 месяцев.
Источники и ссылки
Если у вас есть вопросы, обращайтесь в Mayfield Brain & Spine по телефону 513-221-1100 или 800-325-7787.
Ссылки
Cancer.gov
Irsa.org
Abta.org
Глоссарий
доброкачественные: незлокачественные.
фракционированный: доза облучения доставляется в течение нескольких сеансов.
злокачественные: злокачественные.
метастатическое: раковая опухоль, которая распространилась из своего первоначального источника.
стереотаксический: точный метод определения местоположения структур внутри тела с использованием трехмерных координат.
цель: зона наведения радиационных лучей; обычно опухоль, порок развития или участок тела.
обновлено: 7.Обзор
(2018)> Рональд Варник, доктор медицины, клиника Мэйфилд, Цинциннати, Огайо
Медицинские информационные материалы, сертифицированные Mayfield, написаны и разработаны клиникой Mayfield Clinic. Эта информация не предназначена для замены медицинских рекомендаций вашего поставщика медицинских услуг.
Стереотаксическая радиохирургия и лучевая терапия — Brigham and Women’s Hospital
Команда стереотаксической лучевой терапии в Brigham and Women’s Hospital предлагает многопрофильный и инновационный стереотаксический подход к лечению доброкачественных и злокачественных опухолей, сосудистых заболеваний, а также других заболеваний нервной системы, таких как болезнь Паркинсона. болезнь.Команда нейрохирургов, онкологов-радиологов, физиков и медперсонала работает вместе, чтобы предоставить каждому пациенту наиболее подходящее, эффективное и безопасное лечение. Большинство пациентов возвращаются домой в конце дня лечения и могут вернуться к своему обычному распорядку дня на следующий день.
Что такое стереотаксическая радиохирургия?
Стереотаксическая радиохирургия (SRS) — это процедура, в которой используется излучение и компьютерное наведение, чтобы направить сфокусированное излучение на определенные цели в головном мозге, что минимизирует повреждение окружающих структур.В стереотаксической радиохирургии используются разные подходы. В Бригаме и женской больнице процедура проводится под местной седацией, пациенты надевают лицевую маску для ориентации. Ни каркас головы, ни хирургический разрез не нужны. Важным преимуществом стереотаксической радиохирургии является ее способность лечить опухоли в местах, труднодоступных с помощью обычных нейрохирургических методов. Эта процедура также полезна при лечении лиц, которые не являются кандидатами на открытую нейрохирургию из-за возраста, состояния здоровья или личных предпочтений.
Что такое стереотаксическая лучевая терапия?
В некоторых случаях (например, при больших опухолях) лучевая терапия делится на несколько дней. В этом случае лечение называется стереотаксической лучевой терапией или СТО.
Болезни, которые мы лечим
Доброкачественные и злокачественные опухоли
Стереотаксическая лучевая терапия наиболее часто используется для лечения доброкачественных и злокачественных опухолей головного мозга, основания черепа, а также головы и шеи и может использоваться отдельно или в сочетании с другими методами лечения, такими как хирургическое вмешательство или химиотерапия.Леченные опухоли могут возникать в другой части тела, такой как грудь или легкие, и распространяться (метастазировать) в мозг, или они могут возникать в головном мозге (включая менингиомы, аденомы гипофиза, акустические невриномы и краниофарингиомы). В некоторых случаях радиохирургия может использоваться для лечения первичных злокачественных опухолей, включая глиому или олигодендроглиому.
Сосудистая нейрохирургия
Стереотаксическая лучевая терапия — важный инструмент для лечения сосудистых поражений, таких как артериовенозные мальформации (АВМ), либо в качестве отдельного лечения, либо в сочетании с дополнительными методами лечения, такими как эмболизация сосудов.
Функциональная нейрохирургия
Это захватывающая и постоянно расширяющаяся область стереотаксической радиохирургии, включающая лечение невралгии тройничного нерва и других болевых синдромов. В настоящее время SRS используется для лечения некоторых форм эпилепсии, в том числе связанных с гамартомами гипоталамуса. Стереотаксическая лучевая терапия также может использоваться для лечения симптомов (в первую очередь тремора), связанных с рядом двигательных расстройств, включая болезнь Паркинсона, дистонию и эссенциальный тремор.Продолжаются исследования в отношении использования стереотаксической радиохирургии для лечения ряда психических расстройств, таких как обсессивно-компульсивное расстройство и мания.
Наша команда
Нейрохирургия
Радиационная онкология
Публикации
- Rajakesari S, Arvold N, Jimenez RB, Christianson LW, Horvath M, Claus EB et al. Фракционная стереотаксическая лучевая терапия метастазов в мозг. J Нейроонкология (в печати)
- Дайер М.А., Келли П.Дж., Чен И-Х, Пиннелл Н., Клаус Э.Б., Ли EQ, Вайс С.Е., Лин Н.Ю., Александр Б.М.Важность статуса экстракраниального заболевания и подтипа опухоли для пациентов, подвергающихся радиохирургии при раке груди с метастазами в мозг
. Int J Radiat Oncol Biol Phys. 2012 15 июля; 83 (4): e479-86 - Клаус ЕБ. Нейрохирургическое лечение метастазов в центральной нервной системе. Нат Рев Клин Онкол 2012; 9, 79–86.
- Kelly PJ, Lin NU, Claus EB, Weiss SE, Александр BM. Спасательная стереотаксическая радиохирургия при метастазах рака молочной железы в мозг: исходы и факторы прогноза. Рак.2012 15 апреля; 118 (8): 2014-20
Чтобы назначить встречу:
Отделение нейрохирургии
Бригам и женская больница
Центр неврологии
Здание трансформационной медицины
60 Фенвуд-роуд, 1-й этаж
Телефон: (617) 732-6600
Факс: (617) 713-3050
Постоянный пациент: Свяжитесь с нами
Стереотаксическая радиохирургия (SRS) — против рака
Стереотаксическая радиохирургия (SRS) включает в себя доставку высокой дозы сфокусированной лучевой терапии на небольшой участок мозга или другие части головы.Обычно это проводится за один, а иногда и за 5 сеансов лечения. Когда используется одно лечение, оно называется SRS, а если используется более одного лечения, оно называется стереотаксической лучевой терапией (SRT).
Несмотря на то, что в названии есть слово «хирургия», он не требует хирургических разрезов и представляет собой неинвазивное лечение пациентов с опухолями или раком головного мозга и области головы.
SRS обычно используется для лечения пациентов с
- вторичный рак, распространившийся на головной мозг (метастазы в головной мозг)
- вторичный рак после резекции
- медленно растущие доброкачественные опухоли (например, невриномы слухового нерва, менингиомы и опухоли гипофиза)
- повторно обработать область, ранее подвергавшуюся лучевой терапии до
- неопухолевые состояния, такие как артериовенозные мальформации (аномальное соединение вен и артерий) и сложные случаи невралгии тройничного нерва.Невралгия тройничного нерва — это лицевая боль, вызванная давлением или повреждением 5 -го черепного нерва, и может возникать как часть некоторых неврологических состояний, таких как рассеянный склероз.
В планировании и проведении SRS задействована большая группа экспертов, в которую входят специалисты-радиологи-онкологи, лучевые терапевты, медицинские физики и медсестры. Обычно пациенты перед лечением обсуждаются на междисциплинарном совещании с участием онкологов-радиологов, хирургов, медицинских онкологов, неврологов и радиологов.Он подходит не всем пациентам, так как перед назначением лечения необходимо тщательно рассмотреть многие факторы. Общее состояние пациента, текущие симптомы и пораженные участки — вот некоторые из многих факторов, которые оцениваются перед лечением.
Поставка стереотаксической радиохирургии
Существуют разные способы предоставления SRS (например, на основе линейного ускорителя, гамма-нож, кибер-нож, томотерапия), но все системы имеют одни и те же основные характеристики. Все системы обеспечивают точную и безопасную лучевую терапию с высокой точностью, чтобы минимизировать дозу облучения здоровых структур, окружающих опухоль или рак.Для этого можно использовать приспособленную подголовник или маску, чтобы свести к минимуму любое движение, гарантируя, что пациенту всегда будет комфортно. Рентгеновские лучи могут быть сделаны, чтобы гарантировать точное положение пациента с измерениями, сделанными до лечения. В зависимости от типа SRS и количества областей, получающих SRS, установка и обработка обычно занимает от 30 минут до 1 часа.
Доставка СГД не болезненна. Обычно он хорошо переносится пациентами. Возможные побочные эффекты лечения варьируются в зависимости от обрабатываемой области.Их обсудит лечащий онколог-радиолог. У некоторых людей после лечения могут появиться побочные эффекты, включая усталость, легкую тошноту или головную боль. Обычно они носят временный и легкий характер. Другие, более редкие побочные эффекты могут возникать через месяцы или годы после лечения, но нечасто. Тщательное планирование и процессы лечения, используемые в SRS, сводят к минимуму эти побочные эффекты.
Ожидаемые результаты лечения варьируются в зависимости от состояния, которое лечат, и поэтому не могут быть легко обобщены.Ваш онколог-радиолог предоставит вам много более подробной информации об этом и всех аспектах процесса SRS, прежде чем будет принято окончательное решение о лечении с помощью этой специальной техники.
Последнее обновление страницы: 23.07.2020
Стереотаксическая радиохирургия — обзор
Роль стереотаксической радиохирургии
Стереотаксическая радиохирургия в форме гамма-ножа или методов линейного ускорителя обеспечивает однократную большую дозу сфокусированного излучения с быстрым спадом в окружающей ткани за счет перекрестного огня со многих направлений, для уничтожения очагов, локализованных стереотаксией.Основным преимуществом этого метода перед традиционной хирургией является то, что он может лечить хирургически недоступные опухоли, особенно там, где во время операции будет нарушен мозг, чтобы достичь поражения. Многие метастазы в мозг, которые раньше можно было лечить только с помощью WBRT, теперь могут быть непосредственно нацелены на SRS. Другие преимущества по сравнению с хирургией заключаются в том, что SRS менее затратна, менее инвазивна (требует только размещения стереотаксического каркаса головы под местной анестезией), требует более короткого пребывания в больнице, потому что дается только одна фракция излучения, и может быть предложена пациентам, которые не могут переносить операцию.На основании ранних ретроспективных отчетов было показано, что SRS эффективен при лечении метастазов в головном мозге, при этом частота местного контроля составляет от 85% до 95%, а среднее время выживания пациента составляет от 7 до 13 месяцев. 63-65 Эти результаты выгодно отличаются от 10–15% случаев местных рецидивов после хирургической резекции. 66 Тем не менее, SRS имеет несколько важных ограничений по сравнению с хирургией. Во-первых, из-за вышеупомянутых ограничений дозирования лечение ограничивается небольшими поражениями, обычно не превышающими 3 см в максимальном диаметре (объем <10–12 см 3 ). 28,29 Во-вторых, с помощью SRS невозможно получить гистологическое подтверждение метастатической природы поражения, что важно, учитывая, что от 5% до 11% пациентов с системным раком имеют неметастатические поражения головного мозга (например, первичный мозг опухоли или абсцессы). 8,12,13 В-третьих, поскольку SRS не оказывает немедленного эффекта в виде экстирпации опухоли, пациентам, возможно, придется оставаться на высоких дозах стероидов в течение более длительных интервалов, а также из-за массовых эффектов опухолей (например, неврологического дефицита и повышения внутричерепного давления) не сразу получают облегчение.
Чтобы определить роль SRS в лечении церебральных метастазов, в последние годы было проведено несколько рандомизированных контролируемых исследований. Чтобы определить преимущества добавления SRS к стандартному WBRT, Kondziolka et al. рандомизировали 27 пациентов с 2–4 церебральными метастазами (≤2,5 см) для получения либо только WBRT, либо WBRT плюс SRS. 67 Они обнаружили, что добавление SRS (16 Гр) к стандартной дозе WBRT 30 Гр значительно увеличило среднее время до отказа местного контроля с 6 до 36 месяцев ( p = 0.0005). Однако среднее время выживания пациентов, получавших WBRT плюс SRS (11 месяцев), не было значительно больше, чем у пациентов, получавших только WBRT (7,5 месяцев, p = 0,22). Примечательно, что мощность этого исследования была сильно ограничена небольшим размером выборки.
В другом проспективном исследовании Andrews et al. ответили на тот же вопрос, сравнивая результаты лечения WBRT с усилением SRS или без него. 68 В этом многоцентровом исследовании, проведенном под эгидой RTOG, 333 пациента с одним или тремя метастазами в мозг (≤4 см в максимальном диаметре) были рандомизированы для получения либо только WBRT, либо WBRT плюс SRS.При первичном анализе всех 333 пациентов не было различий в выживаемости между пациентами, получавшими WBRT плюс SRS, и теми, кто получал только WBRT (6,5 месяцев для WBRT плюс SRS против 5,7 месяцев для только WBRT, p = 0,14) . Однако при анализе данных с точки зрения вторичных исходов пациенты, получавшие комбинированный подход, с большей вероятностью имели стабильный или улучшенный статус работоспособности (43% для WBRT плюс SRS против 27% для одного WBRT, p = 0,03) и снижение использования стероидов при контрольной оценке через 6 месяцев.Наиболее важно то, что в анализе подгруппы, который включал только пациентов с единичными метастазами ( n = 186), было небольшое, но значительное улучшение средней продолжительности жизни в группе WBRT плюс SRS (6,5 месяцев) по сравнению с группой только WBRT. (4,9 месяца, р = 0,04). Это исследование представляет собой первое крупномасштабное рандомизированное исследование SRS в качестве адъюванта WBRT и предоставило важные данные в поддержку положительного влияния SRS при лечении единичных небольших метастазов в головной мозг.
Минимально инвазивная природа SRS привела к важному вопросу о том, должна ли SRS заменить хирургическое вмешательство в качестве основного лечения метастазов в головной мозг, особенно единичных метастазов. На сегодняшний день существует только одно опубликованное рандомизированное исследование 69 , в котором предпринята попытка сравнить эффективность лечения SRS с традиционной хирургией. В частности, Muacevic et al. провели многоцентровое рандомизированное клиническое исследование, в котором пациенты с небольшими (максимальный диаметр <3 см) одиночными метастазами, хорошим статусом работоспособности (оценка KPS ≥ 70) и стабильным системным заболеванием были рандомизированы для получения либо SRS, либо традиционной хирургии плюс WBRT.Изначально это исследование было разработано для набора 240 пациентов, чтобы достичь достаточной статистической мощности для выявления 15% разницы в годичной выживаемости. Однако из-за плохого набора пациентов исследование было прервано, и только 64 пациента были рандомизированы в этом исследовании. Результаты показали, что среднее время выживания составляло 9,5 месяцев в группе хирургии плюс WBRT и 10,3 месяца в группе SRS, разница между которыми не достигла статистической значимости ( p = 0,8). Хотя исследователи пришли к выводу, что результаты подтверждают, что SRS и хирургия являются по существу эквивалентными методами лечения, поскольку исследование было прервано до достижения цели накопления, у него не было возможности продемонстрировать эквивалентность.Из-за этой слабости достоверность статистической оценки сомнительна, а утверждение об эквивалентности, основанное на отрицательных сравнениях, было необоснованным. 70
В отдельных попытках ответить на тот же вопрос группа из онкологического центра доктора медицины Андерсона Техасского университета (MD Anderson) также провела проспективное рандомизированное исследование, сравнивающее SRS с традиционной хирургией, но были представлены только предварительные результаты. в абстрактной форме. 71 В этом клиническом исследовании пациенты старше 16 лет с впервые диагностированными единичными метастазами в головной мозг, получившие оценку KPS> 70, были рандомизированы для прохождения традиционной хирургической операции или SRS.Подобно испытанию Muacevic et al., Это испытание MD Anderson также страдало от плохого начисления. Однако в исследовании MD Anderson подходящим пациентам, отказавшимся от рандомизации, было разрешено выбрать лечение, а затем их наблюдали так же, как и пациентам, которые согласились на рандомизацию. Таким образом, это испытание включало как рандомизированные, так и нерандомизированные группы. Конечными критериями были местный рецидив, отдаленный рецидив и общая выживаемость. Пятьдесят девять пациентов были включены в рандомизированную группу (30 получили хирургическое вмешательство и 29 получили SRS), а 155 пациентов были включены в нерандомизированную группу (89 выбрали операцию и 66 выбрали SRS).В предварительном анализе лечение SRS имело статистически значимый повышенный риск местного рецидива по сравнению с хирургическим вмешательством как в рандомизированной, так и в нерандомизированной группах исследования. На основе многомерного анализа, в котором учитывались рандомизированные и нерандомизированные популяции, с поправкой на смешанные ковариаты (возраст, пол, WBRT, тип первичной опухоли, степень заболевания, объем и расположение опухоли, оценка KPS и класс RPA) и эффекты рандомизации. SRS был связан с почти трехкратным повышением риска местного рецидива по сравнению с хирургическим вмешательством.Что касается общей выживаемости, то меньшее рандомизированное исследование не показало разницы между хирургическим вмешательством и SRS, но было значительное преимущество хирургического вмешательства перед SRS в более крупной нерандомизированной группе. В качестве меры исходной гетерогенности не было различий в частоте отдаленных рецидивов между группами как в рандомизированной, так и в нерандомизированной группах исследования, что позволяет предположить, что пациенты в группе SRS и хирургической группе были одинаковыми в обеих группах исследования. Таким образом, в этом проспективном исследовании, характеризуемом включением рандомизированных и нерандомизированных групп, традиционная хирургия, по-видимому, дает значительное преимущество перед SRS с точки зрения местного рецидива и предполагает, что операция также может обеспечить преимущество с точки зрения общей выживаемости.На основании этих данных исследователи рекомендовали хирургическое вмешательство в качестве лечения выбора при метастазах в головной мозг, которые поддаются любому из этих методов лечения. С другой стороны, SRS может использоваться в качестве основного метода лечения небольших (<1 см) поражений, особенно если они множественные, хирургически недоступны и расположены глубоко в головном мозге. Пациенты с множественными сопутствующими заболеваниями, которые не переносят традиционное хирургическое вмешательство, также являются кандидатами на лечение SRS.
Еще одно соображение при расшифровке роли SRS по сравнению с хирургией в лечении метастазов в головной мозг состоит в том, что частота местного контроля опухоли после SRS резко падает, когда максимальный диаметр опухоли превышает 1: 1.5 см, что было продемонстрировано в двух ретроспективных сериях. 72,73 Следовательно, утверждалось, что верхний предел размера максимального диаметра 3 см может быть слишком высоким для адекватной обработки SRS, 74 , и предполагалось, что нижний порог (например, 2–2,5 см максимального диаметра) может быть более подходящим в качестве верхнего предела для применения SRS. Необходимы более тщательные исследования вопроса о размере опухоли и эффективности радиохирургии.
Стереотаксическая лучевая терапия | Опухоли головного и спинного мозга
Стереотаксическая лучевая терапия — это способ очень точного нацеливания лучевой терапии на опухоль.Этот вид лечения доступен не во всех больницах, потому что он требует специального оборудования и навыков.
Стереотаксическая радиохирургия
Вы могли слышать термин стереотаксическая радиохирургия. Это не операция на головном мозге. Это означает наличие очень высокой дозы стереотаксической лучевой терапии на небольшой площади. Обычно у вас разовое лечение.
Что такое стереотаксическая лучевая терапия?
Стереотаксическая лучевая терапия дает лучевую терапию под разными углами вокруг тела.Лучи встречаются у опухоли. Это означает, что опухоль получает высокую дозу радиации, а ткани вокруг нее — гораздо меньшую дозу. Это снижает риск побочных эффектов.
Обычно вы лечитесь на аппарате с линейным ускорителем (LINAC). Но вы также можете установить его на CyberKnife или GammaKnife.
При стереотаксической лучевой терапии и радиохирургии
Стереотаксическая лучевая терапия и радиохирургия подходят не всем.Вы можете пройти этот вид лечения, если у вас есть:
- вестибулярная шваннома
- менингиома, начавшаяся в основании черепа
- опухоль гипофиза
- рак, распространившийся на мозг из других частей тела (вторичная опухоль головного мозга)
Вероятнее всего, она у вас для небольших опухолей размером менее 3 см в поперечнике.
Вторичные опухоли головного мозга отличаются от первичных опухолей головного мозга. У нас есть отдельная информация о вторичных опухолях головного мозга.
Как часто вы проходите стереотаксическую лучевую терапию и радиохирургию
Полная доза стереотаксической лучевой терапии обычно делится на несколько меньших доз, называемых фракциями. Количество фракций может варьироваться от 3 до 8. У вас есть одна процедура (фракция) в день.
Для радиохирургии обычно используется однократное лечение (фракция).
Перед началом лучевой терапии
Во время лучевой терапии вам нужно держать голову как можно более неподвижной.Это сделано для того, чтобы лечение было максимально точным. Удержание головы неподвижным называется иммобилизацией. Итак, перед тем, как начать лучевую терапию, вам сделают маску для лучевой терапии или подголовник.
Маска для лучевой терапии
У большинства людей маска для лучевой терапии сделана из пластика. Это маска из термопласта. Маска прикрепляется к сканеру или аппарату лучевой терапии, когда вы ее носите. Это означает, что вы не можете двигать головой.
Voiceover : Изготовление сетчатой маски для лучевой терапии занимает несколько минут.
Радиограф : Я просто разогреваю это сейчас, если вы просто будете вести себя вежливо и оставаться на месте и просто хотите закрыть на нас глаза.
Voiceover : рентгенолог смягчает маску, помещая ее в теплую воду на минуту или две. Когда рентгенолог надевает маску на ваше лицо, оно будет теплым и влажным. Затем они прикрепляют его к кровати, на которой вы лежите. Чтобы форма лица высохла, потребуется минута или две. Рентгенологи отметят маску там, где есть светлые линии.
Радиограф : Хорошо, вы просто почувствуете, как мы давим на маску; у тебя все хорошо, ты еще в порядке?
Пациент : Ммм …
Voiceover : Они используют отметки на маске для выравнивания машины каждый раз, когда вы проходите лечение. Маска удерживает вашу голову неподвижно и гарантирует, что ваше лечение направлено на лечение рака. Они пишут ваше имя на маске и хранят ее в отделении лучевой терапии наготове для вашего лечения.
Пациент : Они рассказали мне о процедуре, о том, что маска была подобрана, ну, что она будет сформована по форме моего лица. Умм, что они и сделали, три милые девушки, ммм, успокоили меня, усадили, нагрели маску, прилепили ее к моему лицу, ну, это совсем не неудобно.
Рама головы
Если вы собираетесь лечить на аппарате GammaKnife, то у вас установлена рама головы.
Ваша терапевтическая бригада прикрепляет рамку к вашему черепу с помощью 4 штифтов.Перед тем, как прикрепить каркас, вам делают инъекции местного анестетика, чтобы вы не чувствовали боли. Когда рама установлена, вы можете почувствовать некоторое давление и стеснение, но обычно через несколько минут становится лучше.
Лечебная бригада снимает раму по окончании лечения.
Планирование компьютерной томографии
Перед лечением вам также предстоит плановая компьютерная томография. Это поможет вашим врачам составить карту, куда должна идти радиация.
Кабинет лучевой терапии
Аппараты лучевой терапии очень большие и могут заставить вас нервничать, увидев их впервые.Аппарат вращается вокруг вас для обработки. Но вас это никак не трогает.
Перед первым сеансом лечения рентгенолог объяснит вам, что вы увидите и услышите. В некоторых отделениях процедурные кабинеты имеют док-станции для подключения музыкального плеера. Так что вы можете слушать свою музыку.
После стереотаксической лучевой терапии
Чтобы пройти курс лечения, вы ложитесь на лечебный стол. Поскольку ваше положение очень важно, рентгенологам может потребоваться некоторое время, чтобы подготовить вас.Рентгенологи прикрепляют вашу маску или головную раму к столу для лечения. Затем они покидают комнату до того, как начнется ваше лечение. Это сделано для того, чтобы они не подвергались воздействию радиации.
Рентгенологи смотрят и слушают вас на экране видеонаблюдения в соседней комнате. Сообщите им, если вам нужно переехать или вы хотите, чтобы машина остановилась.
Вам нужно лежать неподвижно. Машина издает жужжащие и пищащие звуки. Вы не можете почувствовать лучевую терапию во время лечения.
Когда лечение закончено, рентгенологи помогут вам выйти из аппарата.Они снимают маску или каркас, и вы можете вернуться домой или в палату.
Даниэль (рентгенолог): Перед началом лечения вашему врачу необходимо будет точно определить, где именно нужно проводить лечение, а также какие части следует избегать при лечении.
Чтобы пройти лучевую терапию, вы должны лежать в той же позе, что и при планировании сканирования.
Чтобы остановить движение и убедиться, что ваше лечение направлено на лечение рака, вы надеваете индивидуальную маску на лицо, которая прикрепляется к кушетке.
Мы выстраиваем машину по отметкам на вашей маске и выходим из комнаты. Мы управляем машиной из отдельной комнаты, чтобы не подвергаться воздействию радиации.
Лечение займет несколько минут, и вы сможете поговорить с нами по внутренней связи. Мы можем видеть и слышать вас, пока вы лечитесь, и проверим, что с вами все в порядке.
Когда начнется лечение, вы ничего не почувствуете. Вы можете слышать, как аппарат движется вокруг вас, воздействуя на вас под разными углами.
Поскольку мы стремимся ежедневно лечить одну и ту же часть тела одним и тем же способом, процесс лечения остается одинаковым каждый день, поэтому вы не должны замечать никаких различий.
Вы будете видеть кого-то из команды, кто будет ухаживать за вами раз в неделю, пока вы лечитесь. Они спросят, как у вас дела, и спросят о побочных эффектах.
Ты не будешь радиоактивным
Этот вид лучевой терапии не сделает тебя радиоактивным. Безопасно находиться рядом с другими людьми, включая беременных женщин и детей.
Поездки на прием к лучевой терапии
Возможно, вам придется каждый день преодолевать большие расстояния для прохождения лучевой терапии, в зависимости от того, где находится ближайший к вам онкологический центр. Это может сильно утомить вас, особенно если у вас есть побочные эффекты от лечения.
Вы можете спросить у терапевтов-рентгенологов удобное для вас время приема. Они будут стараться изо всех сил, но некоторые отделы могут быть очень заняты. Некоторые отделения лучевой терапии открыты с 7:00 до 21:00.
Парковка автомобилей в больницах может быть затруднена.Вы можете спросить у персонала лучевой терапии, могут ли они дать вам разрешение на парковку в больнице для бесплатной парковки или дать совет по поводу парковки со скидкой. Они могут посоветовать, где поблизости есть бесплатные места для парковки.
Персонал лучевой терапии может организовать транспорт, если у вас нет другого пути добраться до больницы. Ваш врач-лучевой терапевт должен согласиться. Это потому, что это только для людей, которые не могут пользоваться общественным транспортом и не имеют доступа к машине.
Некоторые люди могут потребовать возмещения транспортных расходов на лечение.Это зависит от типа приема и от того, претендуете ли вы на определенные льготы. За дополнительной информацией обращайтесь к персоналу лучевой терапии.
В некоторых больницах есть собственные водители, и местные благотворительные организации могут предложить транспорт для больниц. Так что спросите, доступна ли какая-либо помощь в вашем районе.
Побочные эффекты
Стереотаксическая лучевая терапия и радиохирургия имеют меньше побочных эффектов, чем стандартный тип внешней лучевой терапии. Это связано с тем, что обрабатываемая область меньше и поэтому менее здоровые ткани мозга подвергаются облучению.
Вы можете некоторое время чувствовать усталость после лечения. Но есть и другие возможные побочные эффекты.
Стереотаксическая радиохирургия | UF Health, University of Florida Health
Стереотаксическая радиохирургия (SRS) — это форма лучевой терапии, при которой точные высокоэнергетические рентгеновские лучи фокусируются на небольшом участке тела. Хотя это называется радиохирургией, это не хирургическая процедура в традиционном понимании, поскольку здесь нет разреза. В качестве метода лечения лучевой терапией SRS использует трехмерное изображение для определения высоких доз радиации в намеченной области с минимальным воздействием на окружающие здоровые ткани.
UF Health заработал выдающуюся репутацию в этой области с тех пор, как Уильям Фридман, доктор медицины, и Франк Бова, доктор медицины, помогли создать программу радиохирургии Университета Флориды в 1988 году. Вместе они решили приступить к трудному процессу улучшения линейного ускорителя. вариант за счет повышения точности и разработки первой компьютеризированной системы планирования дозы в полевых условиях. Это новаторское открытие побудило команду UF спроектировать и разработать LINAC Scalpel, прецизионный радиохирургический инструмент, который доставляет высокую дозу радиации к внутричерепным целям.Впоследствии UF запатентовала этот подход и передала его по лицензии четырем компаниям. Это привело к появлению сотен версий системы планирования доз по всему миру.
Это было лишь раннее представление о возможной позиции UF в этой области. С момента лечения своего первого пациента в 1988 году UF пролечила еще более 5000 человек. Наше учреждение является автором более 175 публикаций и глав, проведено десятки национальных и международных бесед и приняло сотни посетителей, желающих узнать о радиохирургии.Что наиболее важно, стандарты, разработанные UF для точности, обеспечения качества, наблюдения за пациентами, дозирования и т. Д., Стали стандартами во всем мире. На национальном уровне мы также разработали новое оборудование для радиохирургии / методы лечения, которые используются по всей стране.
Сегодня UF Health предлагает своим пациентам новейшие возможности радиохирургии, обеспечивая передовой подход к лечению и уходу за поражениями головного мозга.
Почему используется процедура?
Кандидатами на SRS являются пациенты с артериовенозными мальформациями, невриномами слухового нерва, менингиомами, опухолями гипофиза, метастатическими опухолями, глиомами и другими поражениями головного мозга.
Это одноразовое амбулаторное радиохирургическое лечение иногда является отличной альтернативой обычным хирургическим процедурам, поскольку оно неинвазивно, высокоэффективно, сопряжено с минимальным риском и не требует длительной госпитализации.
Как выполняется процедура
SRS, как и другие формы излучения, работает, повреждая ДНК клеток-мишеней. Это приводит к тому, что эти клетки теряют способность к воспроизводству, что приводит к их гибели. Для быстрорастущих клеток, таких как рак, эффект резкий и ранний.Для медленно растущих клеток эффект гораздо более постепенный и может приводить или не приводить к их усадке. Основная цель — не допустить роста.
Почему выбирают UF Health?
Наши пациенты, выбравшие радиохирургию, смогут воспользоваться признанным опытом отделения нейрохирургии UF и отделения радиационной онкологии. Наше учреждение было в авангарде этой технологии, известное революционными инновациями, которые теперь стали мировыми стандартами.
.

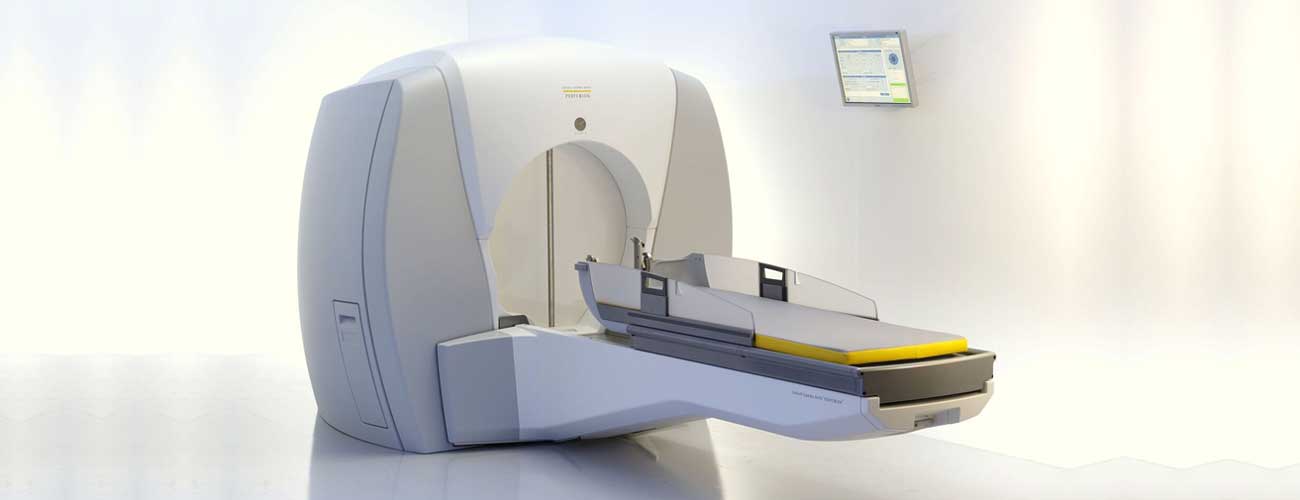
 Аахен
Аахен Для идентификации опухоли используются 3D визуализационные техники, такие как КТ, МРТ и ПЭТ-КТ
Для идентификации опухоли используются 3D визуализационные техники, такие как КТ, МРТ и ПЭТ-КТ д.)
д.) При ее применении не происходит никакого хирургического вмешательства в организм и не требуется наркоз, а сеанс облучения проводится амбулаторно;
При ее применении не происходит никакого хирургического вмешательства в организм и не требуется наркоз, а сеанс облучения проводится амбулаторно;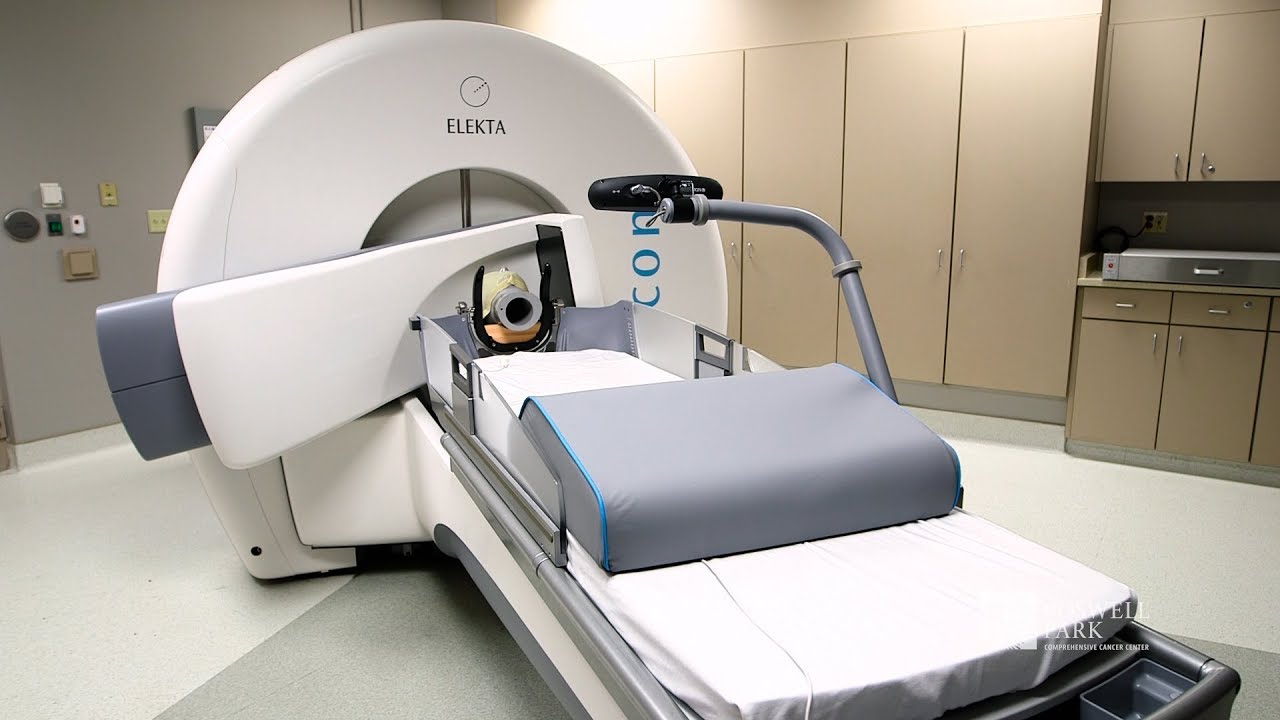
 / Int. J Radiat. Oncol. Biol. Phys. 2008 Nov 15;72(4):1119-27. Epub 2008 May 28.
/ Int. J Radiat. Oncol. Biol. Phys. 2008 Nov 15;72(4):1119-27. Epub 2008 May 28.