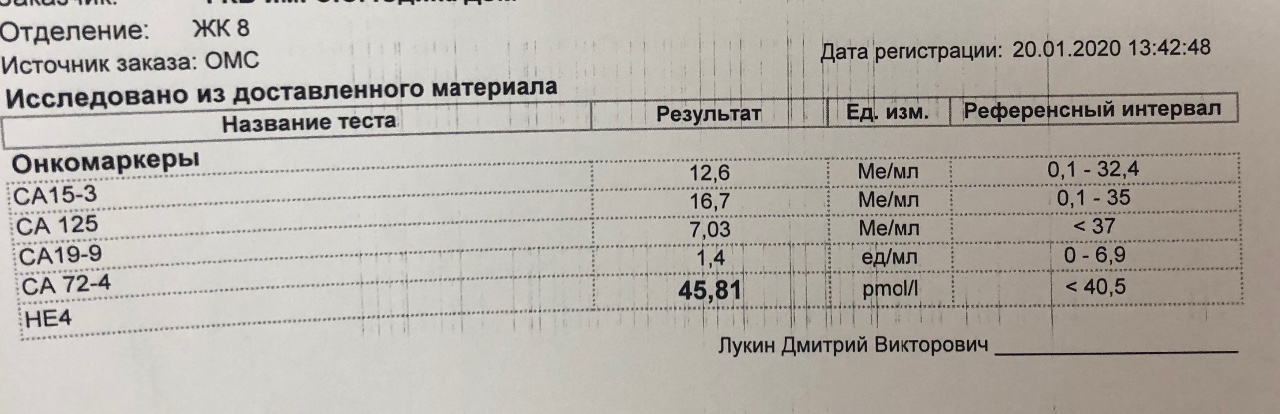
ОНКОМАРКЕРЫ СА 125, НЕ 4 КАК ПРЕДИКТОРНЫЕ ФАКТОРЫ ПРОГНОЗА У БОЛЬНЫХ С ПОГРАНИЧНЫМИ ОПУХОЛЯМИ ЯИЧНИКОВ | Васильев
1. Бохман Я.В. Лекции по онкогинекологии. М., 2007. 167 с.
2. Новикова Е.Г., Батталова Г.Ю. Пограничные опухоли яичников. М., 2007. 151 с.
3. Сергеева Н.С., Маршрутина Н.В. Общие представления о серологических биомаркерах и их месте в онкологии // Практическая онкология. 2011. Т. 12, № 4. С. 147–154.
4. Тюляндин С.А., Моисеенко В.М. Практическая онкология: избранные лекции. СПб., 2004. 784 с.
5. Чернышова А.Л., Чуруксаева О.Н. Роль опухолевого маркера СА-125 в выявлении рецидива рака яичников и определении тактики лечения // Сибирский онкологический журнал.
6. Bast R.C. Jr., Skates S., Lokshin A., Moore R.G. Differential diagnosis of pelvic mass: improved algorithms and novel biomarkers // Int. J. Gynecol. Cancer 2012. Vol. 22. P. 5–8. doi: 10.1097/IGC.0b013e318251c97d.
7. Tropé С.G., Kaern J., Davidson B. Boderline ovarian tumours // Best Pract. Res. Clin. Obstet. Gynaecol. 2012. Vol. 26 (3). P. 325–336. doi: 10.1016/j.bpobgyn.2011.12.006.
8. Kalapotharakos G., Asciutto C., Henic E., Casslen B., Borgfeldt C. High preoperative blood ievels of HE 4 predicts poor prognosis in patients with ovarian cancer // J. Ovarian Res. 2012. Vol. 5 (1). P. 20. doi: 10.1186/1757-2215-5-20.
9. Moore R.G., McMeekin D.S., Brown A. K., DiSilvestro P., Miller M.C., Allard W.Jeffery, Gajewski W., Kurman R., C.Bast Jr. R., Skates S.J. A novel multiple marker bioassay utilizing HE 4 and CA 125 for the prediction of ovarian cancer in patients with a pelvic mass // Gynecol. Oncol. 2009. Vol. 112 (1). P. 40–46. doi: 10.1016/j.ygyno.2008.08.031.
K., DiSilvestro P., Miller M.C., Allard W.Jeffery, Gajewski W., Kurman R., C.Bast Jr. R., Skates S.J. A novel multiple marker bioassay utilizing HE 4 and CA 125 for the prediction of ovarian cancer in patients with a pelvic mass // Gynecol. Oncol. 2009. Vol. 112 (1). P. 40–46. doi: 10.1016/j.ygyno.2008.08.031.Анализы крови на онкомаркеры РЭА, СА 125, СА 15-3, HE-4
Стоимость диагностики
Альфа-фетопротеин (альфа-ФП)
до 9:00 следующего дня
(ПСА общий). Простатспецифический антиген общий
до 9:00 следующего дня
(ПСА общий + ПСА свободный). Онкопрофилактика для мужчин
до 12:00 следующего дня
СА 125. Углеводный антиген. Маркеры опухолевого роста яичников и шейки матки
до 12:00 следующего дня
РЭА. Раково-эмбриональный антиген. Маркер колоректального рака, опухолей молочной железы, желудка, легкого, С-клеточной
до 9:00 следующего дня
SCCA. Антиген плоскоклеточной карциномы
до 3 суток
HE-4. Маркер ранней стадии опухолей яичника
Маркер ранней стадии опухолей яичника
до 12:00 следующего дня
СА 15-3. Маркеры опухолевого роста молочных желез
до 12:00 следующего дня
CA 72-4. Маркер рака яичников
1 сутки
CA 19-9. Маркер карциномы поджелудочной железы
до 12:00 следующего дня
Ген рака молочной железы 2 (BRCA2). Выявление мутации 6174delT (нарушение структуры белка)
до 5 суток
Ген рака молочной железы 1 (BRCA1). Выявление мутации 5382insC (нарушение структуры белка)
до 5 суток
Скрининг миеломной болезни и парапротеинемий (иммунофиксация сыворотки крови с пентавалентной сывороткой)
Онкомаркеры – вещества, образующиеся в организме в ответ на появление злокачественных опухолей. Поэтому обнаружение их в крови позволяет диагностировать рак на той стадии, когда он еще окончательно не развился и может быть вылечен с применением щадящих методик и высокой степенью выживаемости.
Распространенные онкомаркерыК важнейшим онкомаркерам относят:
- РЭА – появление этого антигена в анализе крови в концентрации свыше 10 нг/мл говорит о наличии опухолей кишечника, простаты, молочной железы, печени и костей.
 Повторное обнаружение РЭА в крови после операции по удалению опухоли говорит о метастазировании.
Повторное обнаружение РЭА в крови после операции по удалению опухоли говорит о метастазировании. - СА 125 – углеводный антигенный онкомаркер, концентрация которого в анализе крови свыше 35 Ед/мл, указывает на злокачественные опухоли яичника, матки, легких, поджелудочной железы.
- HE-4 – онкомаркер, появляющийся в анализе крови при опухолях матки и молочных желез. У женщин до наступления менопаузы его концентрация не должна превышать 70 Пмоль/л, а в менопаузе — 140 Пмоль/л.
- СА 15-3 – еще один углеводный антиген, концентрация которого в анализе крови свыше 9,2-38 Ед/л (более 22 ЕД/мл – в при применении специфических методик в ряде лабораторий) указывает на опухоли в тканях молочной железы.
Для определения разных форм раковых опухолей применяются анализы на антигены SCCA, СА 19-9. CA 242, Cyfra-21-1, NSE, β₂-микроглобулин, S-100. Всего онкомаркеров насчитывается около 200 вариантов. Поэтому выгоднее сдавать комплексный анализ сразу на максимальное количество показателей. Цена такого обследования будет ниже, чем отдельное определение каждого маркера. В нашей клинике вы можете пройти онко-генетическое исследование на наличие мутации (дефекта) в генах BRCA1 и BRCA2, обуславливающих развитие наследственного (семейного) рака молочной железы – Breast Cancer Associated genes.
Цена такого обследования будет ниже, чем отдельное определение каждого маркера. В нашей клинике вы можете пройти онко-генетическое исследование на наличие мутации (дефекта) в генах BRCA1 и BRCA2, обуславливающих развитие наследственного (семейного) рака молочной железы – Breast Cancer Associated genes.
Это исследование показано, если вы относитесь к группе риска:
- Если у ваших двух и более близких родственниц (мать, сестра, дочь) был рак молочной железы до 45 лет.
- Если у ваших кровных родственников (мать, сестра, дочь) был рак в обеих молочных железах или рак яичников.
- Если у кого-то из ваших кровных родственников были множественные опухолевые очаги.
При исследовании пациентов в России, было установлено, что у пациенток с семейным раком молочной железы и яичников в 60%-79% случаев была мутация в гене BRCA1.
В статье «Мой медицинский выбор», Анжелина Джоли писала после удаления молочных желез, что ее мать почти десять лет боролась с раком и умерла в 56-летнем возрасте.
«Ведь, по правде говоря, я являюсь носителем «дефектного» гена BRCA1, который резко повышает риск развития рака молочной железы и рака яичников. Я решила упредить события и свести риск к минимуму,»- пишет актриса.
Выявление наличия мутаций в генах BRCA1/BRCA2 важно для формирования программы лечения при онкологии в других органах и тканях. Поскольку при наличии дефектных генов BRCA1/BRCA2 развивается гормон-независимый рак в более молодом возрасте (35-39 лет), склонность к рецидивам после пройденного лечения, развитию рака в противоположной железе, и в целом данный рак имеет худший прогноз благодаря высокой степени злокачественности.
ГЕНЫ ПРОДУЦИРУЮТ БЕЛКИ НАШЕГО ОРГАНИЗМА С РАЗНЫМИ ЗАДАЧАМИ. ЧТО ДЕЛАЮТ БЕЛКИ ЗДОРОВОГО ГЕНА BRCA?- Белки здоровых генов BRCA участвуют в восстановлении разрывов (дефектов) ДНК.
- Белки генов BRCA поддерживают стабильность генома в целом от мутаций
- Белки генов BRCA участвуют в переносе генетической информации, ответственны за деление и выживаемость клеток организма
- Белки генов BRCA подавляют мутагенную активность других «деформированных» генов, вызывающих разнообразные формы рака
- Белки генов BRCA контролируют/сдерживают процесс неконтролируемого клеточного деления в гормон-зависимых тканях.

Переход нормальной клетки в опухолевую происходит через два последовательных мутационных события:
- Повреждение гена в одной цепочке хромосомы (их две, ив обеих есть идентичные гены). НО пока его пара в другой ветке хромосомы здорова – патологические изменения могут не проявляться Поскольку белки гена BRCA отвечают за стабильность генома в целом и восстановление поврежденной ДНК, мутация самого гена BRCA делает уязвимой ДНК. И при наличии других факторов (иммунный статус, наличие хронических заболеваний, образ жизни пациентки), может произойти второе мутационное событие, полностью прекратив сдерживающее действие гена BRCA.
- Повреждение или утеря парного такого же гена во второй цепочке хромосомы, т.е. уже оба гена в обеих цепочках дефектные и не вырабатывают «правильные» белки.
Она дает возможность:
- Как можно более раннего выявления носительства мутации данного гена.

- назначения приема препаратов, способствующих сохранению нормальной копии гена BRCA, повышению уровня белка BRCA до нормального, что способствует стабилизации генома, восстановлению ДНК Т.е. данное лечение препятствует переходу от первого мутационного события ко второму, блокирует начало онкологического процесса.
Если вы в группе риска — проведите онко-генетическое исследование для наиболее раннего выявления мутации гена BRCA.
Поделиться в соц. сетях:
Анализ крови на CA 125 онкомаркер сдать в Москве
Раковый антиген 125 (СА 125) — гликопротеин, в норме обнаруживается в тканях плода, у взрослых — в мезотелии брюшной и плевральной полостей, эндометрии.

Комплексное исследование СА 125 и НЕ 4 более эффективно в диагностике рака яичников (в том числе ранних стадий), также применяется для дифференциальной диагностики доброкачественных и злокачественных заболеваний органов малого таза.
Уровень СА-125 меняется в зависимости от менструального цикла, беременности, что важно учитывать при интерпретации результатов.
Cancer Antigen 125 – это высокомолекулярный протеин. В норме он обнаруживается в клетках брюшины, эндометрия, перикарда, плевры и яичек, но не проникает в кровяное русло. Также этот протеин может производиться опухолями яичников. Значительное превышение его концентрации является маркером рака яичников. Необходимо учитывать, что в некоторых случаях у пациентов с таким диагнозом онкомаркер CA125 находится в пределах нормы. Это связано с тем, что опухоль может не продуцировать раковый антиген. Для таких больных данное исследование не может использоваться в качестве маркера во время терапии.
Если муцин-16 (CA125) присутствует в крови в высокой концентрации, это может указывать на онкологические заболевания не только яичников, а и других тканей и органов (например, толстого кишечника, поджелудочной железы, эндометрия). Биологическим материалом для анализа служит венозная кровь.
Общая информация
Значительное увеличение уровня С служит маркером рака яичников. В большинстве случаев при таком диагнозе исследование показывает превышение нормы в 5 и более раз. В норме этот протеин может попадать в кровь во время менструации (особенно при эндометриозе) и в первом триместре беременности. Анализ обладает невысокой специфичностью. Повышенные показатели могут указывать на онкологические заболевания желудочно-кишечного тракта, эндометрия, а также других внутренних органов и тканей. Также увеличенная концентрация этого вещества нередко наблюдается при воспалениях органов малого таза. У 20% пациенток с раком яичников уровень CA 125 в крови не повышается. Риск развития такого онкологического заболевания повышается при наличии его случаев в семейном анамнезе.
Риск развития такого онкологического заболевания повышается при наличии его случаев в семейном анамнезе.
Интерпретировать результаты анализа на углеводный антиген 125, ставить диагноз, назначать дополнительное обследование и лечение может только врач. Исследование не предназначено для самодиагностики.
Анализ на СА-125. Онкомаркер рака яичников
Референсные значения (вариант нормы):
| Параметр | Референсные значения | Единицы измерения |
|---|---|---|
| CA 125 (Раковый антиген 125, Cancer Antigen 125) | 0 — 35 | Ед/мл |
Дискриминационный уровень*:
* Дискриминационный уровень (ДУ) – верхняя допустимая граница концентраций у здорового человека.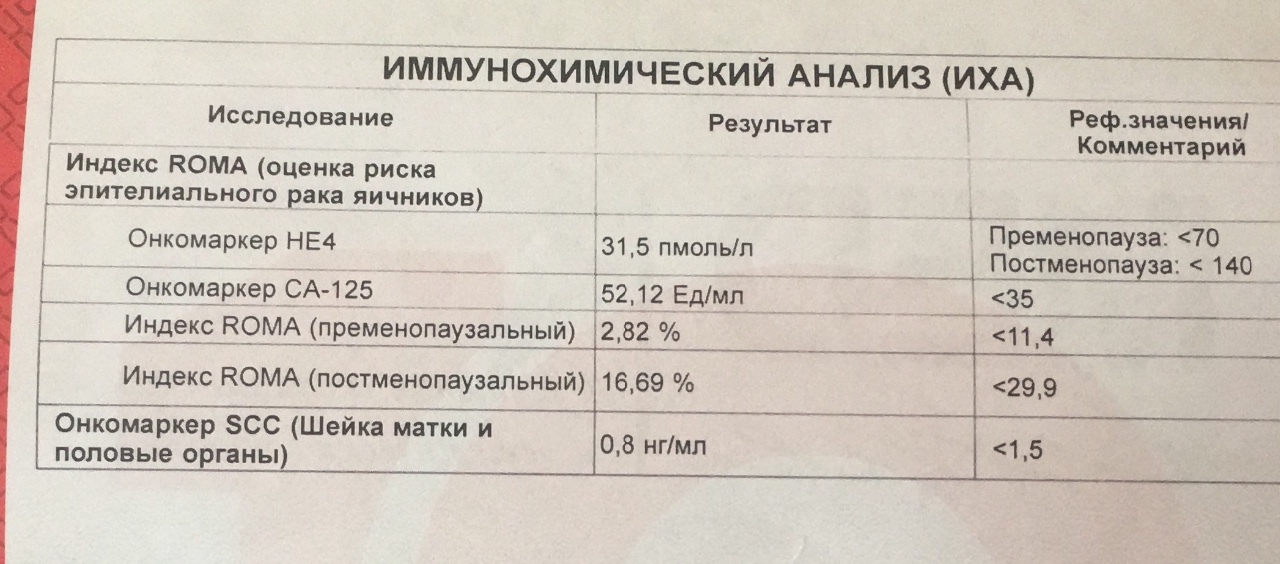
ВНИМАНИЕ! Следует помнить, что незначительное повышение концентрации многих онкомаркёров возможно при различных доброкачественных и воспалительных заболеваниях, физиологических состояниях. Поэтому выявление повышенного содержания того или иного онкомаркёра ещё не является основанием для постановки диагноза злокачественной опухоли, а служит поводом к дальнейшему обследованию.
| Повышение значений |
|---|
|
Обращаем Ваше внимание на то, что интерпретация результатов исследований, установление диагноза, а также назначение лечения, в соответствии с Федеральным законом № 323-ФЗ «Об основах охраны здоровья граждан в Российской Федерации» от 21 ноября 2011 года, должны производиться врачом соответствующей специализации.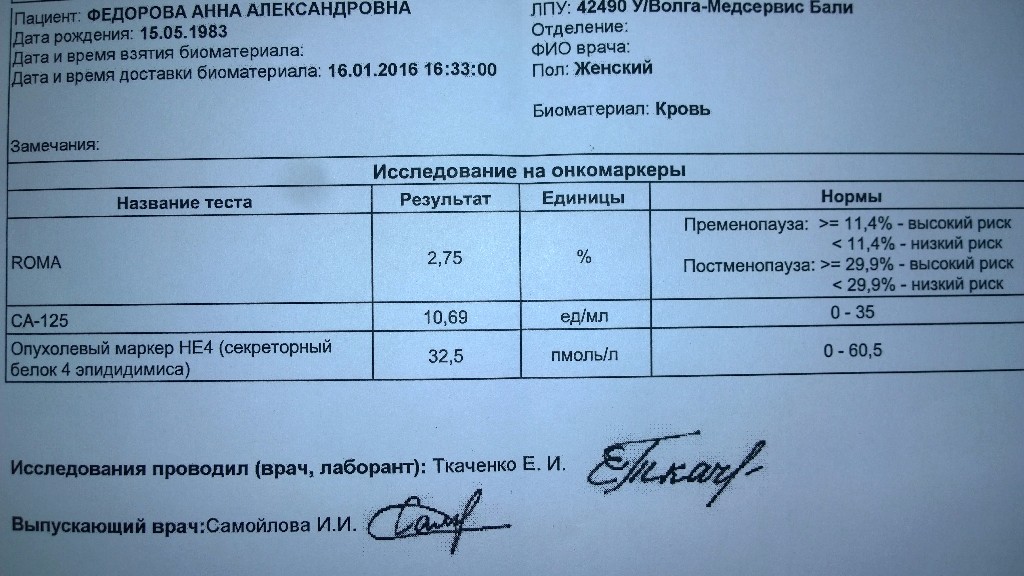
Диагностика рака яичников (СА-125)в Запорожье в МЦ «ШЕКИ»
Рак яичников – серьезное онкологическое заболевание, успех лечения которого во многом зависит от его ранней диагностики. Природа образования опухоли яичников не до конца выяснена, но доказано, что в 10% случаев — она имеет генетическую предрасположенность. Выявить наличие генетической предрасположенности к данному злокачественному заболеванию, можно сдав генетические ПЦР исследования на BRCA1 и BRCA2. Это рекомендуется сделать всем женщинам, у кого есть в роду близкие родственницы, страдающие раком молочной железы или яичников. К еще одному фактору, увеличивающему риск возникновения злокачественного процесса в женских репродуктивных органах, является раннее начало менструаций и поздняя менопауза.
Диагностика рака яичников обязательно предполагает сдачу анализа на онкомаркер СА-125. Быстро и недорого сдать анализ СА-125 в Запорожье можно в МЦ «ШЕКИ».
Что снижает риск заболевания?
Риск заболеть раком яичников снижают следующие факторы:
• Использование женщиной оральных контрацептивов
• Длительный период грудного вскармливания
• Двусторонняя перевязка труб
Симптомы заболевания
На ранней стадии злокачественное заболевание протекает, как правило, бессимптомно и может быть обнаружено только во время профилактического посещения врача-гинеколога. При подозрениях, врач обязательно назначает УЗИ брюшной полости с использование трансвагинального датчика и анализ на маркер СА-125. В комплексе эти два исследования могут ответить на вопрос о наличии у пациентки рака яичников.
На более поздних стадиях, у пациентки могут быть:
• Чувство распирания в животе и желудке
• Частые позывы к мочеиспусканию
• Тяжесть в животе, увеличение объема живота за счет асцита
• Слабость и быстрая утомляемость
• Частые запоры
Онкомаркер СА-125
Референсные значения онкомаркера СА-125 не превышают 35 МЕ/мл. Уровень его повышения говорит о стадии заболевания, его злокачественности. Так, при онкопатологии яичников, он может быть увеличен в пять и более раз. Однако, не стоит забывать и о том, что повышение онкомаркера СА-125 дают и совершенно другие процессы в организме женщины, не связанные с раком, например, менструация, доброкачественные опухоли яичников, в малом тазу, в брюшине и др. При этом, повышение концентрации онкологического маркера не превышает 100МЕ/мл.
Уровень его повышения говорит о стадии заболевания, его злокачественности. Так, при онкопатологии яичников, он может быть увеличен в пять и более раз. Однако, не стоит забывать и о том, что повышение онкомаркера СА-125 дают и совершенно другие процессы в организме женщины, не связанные с раком, например, менструация, доброкачественные опухоли яичников, в малом тазу, в брюшине и др. При этом, повышение концентрации онкологического маркера не превышает 100МЕ/мл.
Важно понимать, что маркер СА-125 при подозрении на диагноз рак яичников, назначается и рассматривается только в комплексе с результатом трансвагинального УЗИ.
Большое значение онкомаркер СА-125 играет при проведении терапии. Снижение или увеличение его концентрации, позволяет врачу четко представлять ответ организма на выбранную тактику лечения. При необходимости, врач может ее изменить и снова назначить тест на СА-125. Важно вести мониторинг исследований, чтобы понимать, как именно организм женщины реагирует на то или иное лечение, на снижение дозировки препаратов, лучевую или химиотерапию. Важно знать, как правильно подготовиться к сдаче анализа!
Важно знать, как правильно подготовиться к сдаче анализа!
Онкомаркеры в Челябинске: сдать анализ крови на онкомаркеры
Ваш возраст Ребенок Взрослый Пенсионер
Ваш пол МужскойЖенский
Клиника ул. 40-летия Победы, д. 33ул. Труда, д. 187 Бпр-т Ленина, д. 17ул. 250-летия Челябинска, д. 73ул. Хариса Юсупова, д. 103 (Парковый)ул. Сони Кривой, д. 32г. Копейск: пр-т Славы, д. 7ул. Барбюса, д. 61Травмпункт, ул.Труда, д. 187 ДПрофосмотры, ул.Труда, д. 183 Бул. Университетская Набережная, д. 28г. Златоуст, пр-т Гагарина 3-й микрорайон, д. 43
Врач Абрамова Наталья НиколаевнаАвдеева Юлия СергеевнаАгеев Юрий ИвановичАкиншина Ирина ВитальевнаАлександрова Татьяна ГеннадьевнаАнашкина Светлана ЮрьевнаАндреева Юлия ЮрьевнаАниськина Наталья НиколаевнаАнтонова Татьяна ВикторовнаАрхипов Дмитрий АнатольевичАсатрян Карен АртуровичАстапенко Ирина АлександровнаАхмедов Назим РамазановичБавыкина Екатерина ЛеонидовнаБастрон Алексей ЮрьевичБахарев Вадим ВладимировичБахарева Ирина НиколаевнаБахтина Татьяна АнатольевнаБелашкина Елена БорисовнаБелоклокова Елена ИвановнаБеляева Ольга ПавловнаБецков Андрей СергеевичБирюкова Юлия АлександровнаБлагих Андрей ВладимировичБлагих Анжелика ВалерьевнаБлинов Александр ЮрьевичБогданчикова Елена ВасильевнаБогдашов Григорий ЮрьевичБоженко Яна ЛеонидовнаБондин Игорь ВладимировичБородина Ксения НиколаевнаБочарников Владислав СергеевичБочкарев Михаил ОлеговичБраилко Ирина ВладимировнаБрискер Кира АлександровнаБрыль Игорь ВладимировичБубнов Василий ВладимировичБубнова Валерия СергеевнаБукреева Елена АлександровнаБулавина Марина СергеевнаБумагина Светлана ГеннадьевнаБуянова Галина ВикторовнаБыбочкин Дмитрий ВладимировичВасильева Марина ИгоревнаВасилькова Ирина ВадимовнаВасильченко Валентина АлександровнаВильданов Булат ФанилевичВильчинская Диана АртуровнаВинокуров Олег ВладимировичВитьшев Александр АлександровичВласова Мария ЕвгеньевнаВласова Евгения ВячеславовнаВойнова Татьяна ГеннадьевнаВолкова Лариса ИвановнаВыборная Надежда ВладимировнаГаврикова Оксана АнатольевнаГадриян Алиса ДмитриевнаГалеев Ильяс НизиповичГаличанин Иван АрхиповичГамза Валерий НиколаевичГерасимова Наталия ВладимировнаГерасимова Дарья ЕвгеньевнаГиберт Константин ВладимировичГильманшина Диана РалифовнаГирлина Светлана ВасильевнаГирфанов Рустам ТимуровичГлотов Евгений Алексеевич Глущенко Елена СергеевнаГнатюк Яков АнатольевичГнусарева Ольга СергеевнаГолубева Венера НафизовнаГорбунова Дарья СергеевнаГорохова Вера ВалерьевнаГорпиняк Галина ВасильевнаГоршкова Лада ЛьвовнаГренадерова Светлана ВладимировнаГригорьева Татьяна СергеевнаГунашян Сюзанна МушеговнаГурьянова Валерия ПавловнаДаниловских Дмитрий АлександровичДанько Николай Александрович Дворянкова Ирина ВладимировнаДеева Екатерина ВикторовнаДемченко Алина ЕвгеньевнаДмитриева Ирина СергеевнаДмитриченко Елена ГеннадьевнаДобрынин Илья НиколаевичДолгушин Илья ИльичДолгушина Валентина ФедоровнаДорохова Ирина АлексеевнаДробинина Ольга АлександровнаДудин Александр ВалерьевичДудкина Наталья АлександровнаЕвдокимова Светлана РудольфовнаЕвсеева Валентина БорисовнаЕгина Ирина АлександровнаЕговцева Арина ИгоревнаЕгоршева Ольга ЮрьевнаЕникеева Юлия ШамильевнаЕремина Алла ОлеговнаЖданова Kсения СергеевнаЖукова Наталья ВладимировнаЗабегаева Наталья ВикторовнаЗавадский Семен ЮрьевичЗайко Мария ФедоровнаЗайцева Алла АлександровнаЗамятина Лариса ВладимировнаЗаряда Анна АндреевнаЗахарова Лариса ВалентиновнаЗеликман Ирина ИгоревнаЗимин Федор НиколаевичЗиновенкова Елена АлексеевнаЗлаказова Анна ЮрьевнаЗубрилин Сергей ЭдуардовичЗуйкова Светлана ЭрнстовнаИванов Андрей ВладимировичИванова Ангелина ВасильевнаИванычева (Сабаева) Татьяна ПавловнаКабанова Елена ВитальевнаКамалетдинова Наталия ЛеонидовнаКарасёва Елена ВасильевнаКарманов Вячеслав АнатольевичКарпенко Олег АнатольевичКашко Татьяна НиколаевнаКирпичникова Светлана ИвановнаКлимовских Татьяна НиколаевнаКобус Алексей ВикторовичКокшарова Ольга ЛеонидовнаКоляда Елена ВалерьевнаКомарова Татьяна МихайловнаКомкова Наталия НиколаевнаКорабельников Артемий ВладимировичКоренев Иван ВикторовичКорнеев Владислав ВладимировичКоролева Марианна БорисовнаКостарев Филипп ИгоревичКотова Ирина ВалерьевнаКочадзе Софио ЕлгуджевнаКочетова Людмила АлексеевнаКрасов Александр НиколаевичКривоногова Галина АнатольевнаКринкер Фаина АлександровнаКрюков Андрей СергеевичКрюковская Ольга ВасильевнаКувайцева Наталья ИгоревнаКудряшова Наталья ВладимировнаКудряшова Юлия ИвановнаКузнецова Ольга ЮрьевнаКузьменко Дмитрий ПетровичКузьмина Елена ЮрьевнаКурбановская Наталия АлександровнаКурченкова Ольга ВалерьевнаЛапицкая Елена ВладимировнаЛапченков Роман ВячеславовичЛарина Татьяна АнатольевнаЛарионова Ольга СергеевнаЛенкова Мария МихайловнаЛесунова Любовь ЮрьевнаЛукин Константин ВладиславовичМазырко Елена ВасильевнаМакодзеба Ольга АлександровнаМаксимовская Алёна ЮрьевнаМалкова Ирина МихайловнаМалыхина Ольга ПавловнаМалышева Светлана СергеевнаМальцева Оксана АлександровнаМальцева Светлана АнатольевнаМамыкин Алексей АлександровичМаркова Татьяна АлександровнаМаркович Анна ВладимировнаМарьина Наталья ВениаминовнаМаслихов Игорь АлександровичМахнанова Марина АлександровнаМаштакова Татьяна ВладимировнаМедведев Антон АлександровичМедведева Анна ВячеславовнаМезенцева Елена АнатольевнаМикуров Александр АлексеевичМиндлина Анна ОлеговнаМиронова Наталья Юрьевна Митькова Ольга ВладимировнаМихалева Ирина ИгоревнаМодебадзе Коба АрчиловичМоисеев Константин ИвановичМоисеева Татьяна НиколаевнаМорозова Юлия ВладимировнаНагорная Анастасия СергеевнаНакарякова Ольга НиколаевнаНасруллаева Галина ТалибовнаНеуймина Татьяна ВалерьевнаНикифоров Евгений ВикторовичНиконова Алёна АлександровнаНисковская Оксана АлександровнаНовокшанова Ольга ВладимировнаНосов Владимир СергеевичНосова Елена ВалерьевнаНужный Виктор ВладимировичОзерова Елена ВикторовнаОлейникова Екатерина ИвановнаОлейникова Виктория ВитальевнаОришич Юлия ПетровнаОрлова Екатерина ГеральдовнаОрлова Анастасия ДмитриевнаОхотникова Елена СергеевнаПавлов Юрий ВасильевичПавлов Александр БорисовичПанченко Владимир ВладимировичПастьян Евгенья АлександровнаПаутова Екатерина ПетровнаПашкина Наталья ВалентиновнаПашнин Павел ЮрьевичПетрова Евгения БорисовнаПетряева Елена СергеевнаПетухов Юрий Дмитриевич Пивоваров Артем ГеоргиевичПименов Иван ВасильевичПименова Ольга НиколаевнаПинелис Людмила Борисовна Пирогова Ирина ЮрьевнаПлаксин Олег ФедоровичПогосян Виген ШаваршовичПогребная Оксана ЕвгеньевнаПодлубная Людмила ВилиновнаПопов Сергей ВладимировичПопова Ольга СергеевнаПоповкина Майя СергеевнаПостовалова Елена ВениаминовнаПрокопьева Ольга БорисовнаПроценко Светлана ГеннадьевнаПрядко Оксана ЮрьевнаПузрин Евгений ВладимировичПустовая Виктория ВикторовнаПястолов Виктор ВладимировичРечкалова Ольга ПетровнаРодина Елена АнатольевнаРодионова Наталья АлексеевнаРудой Даниил Олегович Русина Кристина ИгоревнаРухлов Антон АлександровичРухлова Евгения ИгоревнаСавочкина Альбина ЮрьевнаСаевец Валерия ВладимировнаСамойлова Ольга БорисовнаСанникова Лариса АлександровнаСауткин Анатолий ГеннадьевичСедов Александр ВячеславовичСергеев Дмитрий ИгоревичСеребренникова Дарья АнатольевнаСидорина Ирина ВладимировнаСкакун Артемий ВикторовичСкиба Маргарита МихайловнаСмагина Екатерина СергеевнаСмирнова Ольга АнатольевнаСтаростина Ирина ВладимировнаСтарыгин Алексей АлександровичСтепанова Анастасия ВалентиновнаСтуднева Наталья АлександровнаСтыцин Илья АлександровичСутормин Георгий АнатольевичСысоева Виктория АлександровнаСычугов Глеб ВячеславовичТарелкина Ольга АлександровнаТележинская Ирина МихайловнаТеше Екатерина СергеевнаТимиркаева Анастасия ГригорьевнаТкачев Александр НиколаевичТомилова Светлана БорисовнаТретьякова (Жизнина) Татьяна НиколаевнаТутанина Лариса АлександровнаТюмбарова Юлия АнатольевнаУфимцева Ирина ВладимировнаУфимцева Яна Анатольевна Ушакова Инна ВячеславовнаУшенин Евгений МихайловичУшпик Анатолий ПетровичФалалеев Сергей ИвановичФанина Эльвира РинатовнаХарлова Татьяна ЭдуардовнаХарькова Анна НиколаевнаХрамцов Алексей ВладимировичХудякова Марина ВладимировнаЧалевич Ольга ВячеславовнаЧернова Татьяна ИвановнаЧимитова Елена НиколаевнаШаимова Ирина СергеевнаШаматава Екатерина РомановнаШахова Елена ВикторовнаШевелева Наталья ВладимировнаШевченко Игорь ВладимировичШивцов Дмитрий ВитальевичШилова Татьяна ВасильевнаШмакова Наталья СергеевнаШмыгина Олеся СтаниславовнаШорина (Мещерякова) Анастасия ВикторовнаШтырляева Екатерина АлександровнаШумилова Ирина ВалерьевнаЩеткина Ольга ГеннадьевнаЯкобюк Светлана ВладимировнаЯковлева София ВасильевнаЯпишина Ирина ОлеговнаЯровой Николай Николаевич
СА 125 антиген со скидкой до 50%
Интерпретация результатов исследования «СА 125»
Интерпретация результатов анализов носит информационный характер, не является диагнозом и не заменяет консультации врача. Референсные значения могут отличаться от указанных в зависимости от используемого оборудования, актуальные значения будут указаны на бланке результатов.
Расшифровка выполняется только при возможности проанализировать результаты комплекса анализов и не выполняется при выполнении части анализов. Мы можем отказать в выполнении Расшифровки по своему усмотрению с возвратом оплаты.
Определение уровня CA 125 в сыворотке крови используется для мониторинга течения рака яичников, доклинической диагностики метастазирования и оценки эффективности проводимой терапии рака, диагностики рецидивов рака яичников. Кроме того исследование CA 125 применяется в комплексе диагностики новообразований брюшины, плевры, серозного выпота в полости (перитонит, плеврит), эндометриоза.
Помимо увеличенной продукции CA 125 опухолевой тканью при раке яичников, повышение уровня этого маркера в сыворотке крови может наблюдаться у здоровых лиц (около 1%), у пациентов с незлокачественными патологическими состояниями (около 6%). Иногда увеличение уровня СА 125 в сыворотке крови отмечается у больных с негинекологическими злокачественными новообразованиями (карцинома поджелудочной железы, легких и др.). Поскольку, CA 125 как и другие гликопротеины, разрушается в печени, повышение его уровня можно обнаружить при патологии печени, особенно при циррозе печени. Вследствие невысокой специфичности, тест не рекомендуют применять как скрининговый для обнаружения рака яичников.
Единица измерения: Ед/мл
Референсные значения: < 35,0 Ед/мл
Повышение:
- Онкологические заболевания: рак яичников (в 80% случаев), рак матки, рак эндометрия, рак фаллопиевых труб, рак молочной железы, рак поджелудочной железы, рак прямой кишки, рак желудка, рак легких, рак печени.
- Другие заболевания: эндометриоз, аднекситы, кистозные образования яичников, гинекологическая инфекция, перитонит, плеврит, хронический гепатит, цирроз печени, хронический панкреатит, аутоиммунная патология.
Снижение:
- Диагностического значения не имеет.
Рак яичников: основы практики, история вопроса, патофизиология
Гофф Б.А., Мандель Л.С., Дрешер К.В., Урбан Н., Гоф С., Шурман К.М. и др. Разработка индекса симптомов рака яичников: возможности для более раннего выявления. Рак . 2007 15 января. 109 (2): 221-7. [Медлайн].
Райерсон А.Б., Эхеман С., Бертон Дж., МакКолл Н., Блэкман Д., Субраманиан С. и др. Симптомы, диагнозы и время проведения основных диагностических процедур у пожилых женщин в США с раком яичников. Акушерский гинекол . 2007 май. 109 (5): 1053-61. [Медлайн].
[Рекомендации] Хендерсон Дж. Т., Уэббер Э. М., Савая Г. Ф. Скрининг рака яичников: обновленный отчет о доказательствах и систематический обзор для Целевой группы профилактических служб США. JAMA . 2018 13 февраля. 319 (6): 595-606. [Медлайн]. [Полный текст].
FDA не рекомендует использовать скрининговые тесты для выявления рака яичников: FDA Safety Communication. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США.Доступно по адресу https://wayback.archive-it.org/7993/20171103022558/https://www.fda.gov/Safety/MedWatch/SafetyInformation/SafetyAlertsforHumanMedicalProducts/ucm519540.htm. 7 сентября 2016 г .; Дата обращения: 15 июня 2019 г.
Скрининг рака яичников, маточных труб и первичного рака брюшины (PDQ®) — версия для специалистов в области здравоохранения. Национальный институт рака. Доступно по адресу https://www.cancer.gov/types/ovarian/hp/ovarian-screening-pdq. 20 апреля 2020 г .; Дата обращения: 13 мая 2020 г.
Флейшер А.Рак яичников. Fleischer AC, Javitt MC, Jeffrey RB Jr и др. Клиническая гинекологическая визуализация . Филадельфия, Пенсильвания: Липпинкотт Уильямс и Уилкинс; 1996. 107.
Язбек Дж., Раджу С.К., Бен-Наги Дж., Холланд Т.К., Хиллаби К., Юркович Д. Влияние качества гинекологического УЗИ на ведение пациентов с подозрением на рак яичников: рандомизированное контролируемое исследование. Ланцет Онкол . 2008 г., 9 (2): 124-31. [Медлайн].
Айер В.Р., Ли С.И.МРТ, КТ и ПЭТ / КТ для выявления рака яичников и характеристики поражений придатков. AJR Am J Roentgenol . 2010 Февраль 194 (2): 311-21. [Медлайн].
Рид С.Дж., Маквей Р.М., Тон А.А., Финлейсон С.Дж., Макальпайн Дж. Н., Фунг-Ки-Фунг М. и др. Фаллопиевы трубы как источник тяжелого серозного рака яичников: обзор смены парадигмы. Банка J Obstet Gynaecol . 2014 Февраль 36 (2): 133-40. [Медлайн].
Гарван Х., Банч К.П., Аннунциата К.М.Роль репродуктивных гормонов в эпителиальном канцерогенезе яичников. Endocr Relat Cancer . 2015 22 декабря (6): Р339-63. [Медлайн].
Harmsen MG, Arts-de Jong M, Hoogerbrugge N, Maas AH, Prins JB, Bulten J, et al. Ранняя сальпингэктомия (тубэктомия) с отсроченной овариэктомией для улучшения качества жизни в качестве альтернативы снижающей риск сальпингоовариэктомии у носителей мутации BRCA1 / 2 (исследование TUBA): проспективное нерандомизированное многоцентровое исследование. BMC Рак .2015 19 августа, 15:59. [Медлайн].
Pantoja E, Noy MA, Axtmayer RW, Colon FE, Pelegrina I. Дермоиды яичников и их осложнения. Комплексный исторический обзор. Obstet Gynecol Surv . 1975 30 января (1): 1-20. [Медлайн].
Comerci JT Jr, Licciardi F, Bergh PA, Gregori C, Breen JL. Зрелая кистозная тератома: клинико-патологическая оценка 517 случаев и обзор литературы. Акушерский гинекол . 1994 июл.84 (1): 22-8.[Медлайн].
Hippisley-Cox J, Coupland C. Выявление женщин с подозрением на рак яичников в первичной медико-санитарной помощи: вывод и проверка алгоритма. BMJ . 2011 г. 4 января. 344: d8009. [Медлайн]. [Полный текст].
Комплексный геномный анализ рака яичников. Природа . 2011, 29 июня. 474 (7353): 609-15. [Медлайн].
Koboldt DC, Fulton RS, McLellan MD, Schmidt H, Kalicki-Veizer J, McMichael JF, et al.Комплексные молекулярные портреты опухолей груди человека. Природа . 2012 23 сентября [Medline].
Ramus SJ, Kartsonaki C, Gayther SA, Pharoah PD, Sinilnikova OM, Beesley J, et al. Генетические вариации на 9p22.2 и риск рака яичников для носителей мутаций BRCA1 и BRCA2. Национальный институт рака . 2011, 19 января. 103 (2): 105-116. [Медлайн].
Рафнар Т., Гудбьяртссон Д.Ф., Сулем П. и др. Мутации в BRIP1 связаны с высоким риском рака яичников. Нат Генет . 2011 окт. 2. 43 (11): 1104-7. [Медлайн].
Mørch LS, Løkkegaard E, Andreasen AH, Krüger-Kjaer S, Lidegaard O. Гормональная терапия и рак яичников. JAMA . 2009 15 июля. 302 (3): 298-305. [Медлайн].
Профилактика рака яичников, маточных труб и первичного рака брюшины (PDQ®) — версия для специалистов в области здравоохранения. Национальный институт рака. Доступно по адресу https://www.cancer.gov/types/ovarian/hp/ovarian-prevention-pdq#link/_15.22 апреля 2020 г .; Дата обращения: 13 мая 2020 г.
Aarestrup J, Trabert B, Ulrich LG, Wentzensen N, Sørensen TIA, Baker JL. Детский лишний вес, рост и рост увеличивают риски рака яичников. Биомаркеры эпидемиологии рака Предыдущая . 2019 28 января (1): 183-188. [Медлайн]. [Полный текст].
Краличкова М., Лагана А.С., Гецци Ф., Ветвицка В. Эндометриоз и риск рака яичников: что мы знаем ?. Arch Gynecol Obstet . 2020 Янв.301 (1): 1-10. [Медлайн].
Крамер Д.В., Витонис А.Ф., Терри К.Л., Велч В.Р., Титус Л.Дж. Связь между использованием талька и раком яичников: ретроспективное исследование случай-контроль в двух штатах США. Эпидемиология . 2016 май. 27 (3): 334-46. [Медлайн].
Генкингер Дж. М., Хантер Д. Д., Шпигельман Д., Андерсон К. Э., Арслан А. и др. Молочные продукты и рак яичников: объединенный анализ 12 когортных исследований. Биомаркеры эпидемиологии рака Предыдущая .2006 15 февраля (2): 364-72. [Медлайн].
Лю Дж, Тан В., Санг Л., Дай Х, Вэй Д., Ло И и др. Потребление молока, йогурта и лактозы и риск рака яичников: метаанализ. Nutr Cancer . 2015. 67 (1): 68-72. [Медлайн].
Робертс А.Л., Хуанг Т., Коенен К.С., Ким Й., Кубзанский Л.Д., Творогер С.С. Посттравматическое стрессовое расстройство (ПТСР) связано с повышенным риском рака яичников: проспективное и ретроспективное продольное когортное исследование. Cancer Res . 2019 5 сентября. [Medline]. [Полный текст].
Программа эпиднадзора, эпидемиологии и конечных результатов. Факты статистики рака: рак яичника. Национальный институт рака. Доступно по адресу http://seer.cancer.gov/statfacts/html/ovary.html. Дата обращения: 13 мая 2020 г.
Американское онкологическое общество. Онкологические факты и цифры, 2020. Американское онкологическое общество. Доступно по адресу https://www.cancer.org/content/dam/cancer-org/research/cancer-facts-and-statistics/annual-cancer-facts-and-figures/2020/cancer-facts-and-figures- 2020.pdf. Дата обращения: 13 мая 2020 г.
Статистика рака яичников. Всемирный фонд исследования рака. Доступно на https://www.wcrf.org/dietandcancer/cancer-trends/ovarian-cancer-statistics. Дата обращения: 13 мая 2020 г.
Брей Ф., Ферли Дж., Сурджоматарам И., Сигель Р.Л., Торре Л.А., Джемаль А. Глобальная статистика рака 2018: оценки GLOBOCAN заболеваемости и смертности от 36 раковых заболеваний в 185 странах во всем мире. CA Cancer J Clin . 2018 ноябрь 68 (6): 394-424.[Медлайн]. [Полный текст].
Чан Дж. К., Теох Д., Ху Дж. М., Шин Дж. Й., Осанн К., Капп Д. Имеет ли светлоклеточный рак яичников худший прогноз по сравнению с другими типами эпителиальных клеток? Исследование 1411 светлоклеточных форм рака яичников. Гинеколь Онкол . 2008 июн.109 (3): 370-6. [Медлайн].
Вудворд ER, Sleightholme HV, Considine AM, Williamson S, McHugo JM, Cruger DG. Ежегодное наблюдение со стороны CA125 и трансвагинального УЗИ для выявления рака яичников у женщин как высокого, так и популяционного риска неэффективно. БЖОГ . 2007 декабрь 114 (12): 1500-9. [Медлайн].
Бахру А., Буканович Р. Дж., Григгс Дж. Дж. Влияние диабета на выживаемость у женщин с раком яичников. Гинеколь Онкол . 2011 Апрель 121 (1): 106-11. [Медлайн].
Ян Д., Хан С., Сун Й и др. Связь мутаций BRCA1 и BRCA2 с выживаемостью, чувствительностью к химиотерапии и фенотипом мутатора гена у пациентов с раком яичников. JAMA . 2011 окт 12.306 (14): 1557-65. [Медлайн].
Bolton KL, Chenevix-Trench G, Goh C и др. Связь между мутациями BRCA1 и BRCA2 и выживаемость у женщин с инвазивным эпителиальным раком яичников. JAMA . 2012 25 января. 307 (4): 382-90. [Медлайн].
Гудман А. Использование статинов связано с увеличением выживаемости при раке яичников. Почта ASCO. Доступно по адресу https://www.ascopost.com/news/july-2020/statin-use-linked-to-improvement-in-survival-in-ovarian-cancer/?email=682f66aafa701771e0bff59
b7fb21a2fb0d9a499c2b7fb21a2fb0d9a499c2b7117e4e499c7117e4e499c7117e4 -Шаблон & bc_md5 = 046fca8ed7062b1f9.31 июля 2020 г .; Дата обращения: 8 августа 2020 г.Гофф Б.А., Мандель Л.С., Меланкон С.Х., Мунц Х.Г. Частота симптомов рака яичников у женщин, обращающихся в клиники первичной медико-санитарной помощи. JAMA . 2004 г. 9 июня. 291 (22): 2705-12. [Медлайн]. [Полный текст].
[Рекомендации] Американский колледж акушеров и гинекологов. Бюллетень практики ACOG. Управление придаточными массами. Акушерский гинекол . 2007 июл.110 (1): 201-14. [Медлайн].
Сух-Бургманн Э., Кинни В.Потенциальный вред перевешивает преимущества постоянного мониторинга стабильных придаточных масс. Am J Obstet Gynecol . 2015 Декабрь 213 (6): 816.e1-4. [Медлайн].
Сух-Бургманн Э., Кинни В. Значение ультразвукового мониторинга придаточных масс для раннего выявления рака яичников. Передний Oncol . 2016. 6:25. [Медлайн]. [Полный текст].
Anthoulakis C, Nikoloudis N. МРТ тазовых органов как «золотой стандарт» в последующей оценке поражений придатков, не определяемых ультразвуком: систематический обзор. Гинеколь Онкол . 2014 Март 132 (3): 661-8. [Медлайн].
Коулман Р.Л., Херцог Т.Дж., Чан Д.В., Манро Д.Г., Паппас Т.С., Смит А. и др. Валидация многомерного индексного анализа второго поколения для определения риска злокачественных новообразований придаточных органов. Am J Obstet Gynecol . 2016 9 марта. [Medline].
[Рекомендации] Райт А.А., Болке К., Армстронг Д.К., Букман М.А., Клиби В.А., Коулман Р.Л. и др. Неоадъювантная химиотерапия для недавно диагностированного прогрессирующего рака яичников: Руководство по клинической практике Общества гинекологической онкологии и Американского общества клинической онкологии. Дж. Клин Онкол . 8 августа 2016 г. [Medline]. [Полный текст].
[Рекомендации] Национальная комплексная онкологическая сеть. Руководство NCCN по клинической практике в онкологии, раке яичников, включая рак маточной трубы и первичный рак брюшины. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/ovarian.pdf. Версия 1.2020 — 11 марта 2020 г .; Дата обращения: 13 мая 2020 г.
Танака Й.О., Окада С., Яги Т., Сато Т., Оки А., Цунода Х. и др.МРТ эндометриоидных кист в сочетании с карциномой яичников. AJR Am J Roentgenol . 2010 Февраль 194 (2): 355-61. [Медлайн].
Стани М.П., Максвелл Г.Л., Роуз Г.С. Принятие клинических решений с использованием оценки риска рака яичников. AJR Am J Roentgenol . 2010 Февраль 194 (2): 337-42. [Медлайн].
Байс СС, Партридж Е, Блэк А, Джонсон С.С., Ламерато Л., Айзекс С. и др. Влияние скрининга на смертность от рака яичников: рандомизированное контролируемое исследование скрининга рака простаты, легких, толстой кишки и яичников (PLCO). JAMA . 2011 г. 8 июня. 305 (22): 2295-303. [Медлайн].
Джейкобс И.Дж., Менон Ю., Райан А., Джентри-Махарадж А., Бернелл М. и др. Скрининг рака яичников и смертность в Совместном испытании Великобритании по скринингу рака яичников (UKCTOCS): рандомизированное контролируемое исследование. Ланцет . 2016 г. 5. 387 (10022): 945-56. [Медлайн]. [Полный текст].
Lachance JA, Choudhri AF, Sarti M, et al. Номограмма для оценки вероятности рака яичников. Гинеколь Онкол . 2011 Апрель 121 (1): 2-7. [Медлайн].
van Nagell JR Jr, Miller RW, DeSimone CP, et al. Долгосрочная выживаемость женщин с эпителиальным раком яичников, обнаруженным при ультразвуковом обследовании. Акушерский гинекол . 2011 декабрь 118 (6): 1212-21. [Медлайн].
Хираи М., Хираи Ю., Цучида Т. и др. Стадия IA Рак яичников: сравнение результатов сонографии и гистопатологических типов у пациентов с нормальным и повышенным уровнями антигена 125 рака в сыворотке. J Ультразвук Med . 2011 июл.30 (7): 943-52. [Медлайн].
Байс СС, Куропатка Е, Блэк А и др. Влияние скрининга на смертность от рака яичников: рандомизированное контролируемое исследование скрининга рака простаты, легких, толстой кишки и яичников (PLCO). JAMA . 2011 г. 8 июня. 305 (22): 2295-303. [Медлайн].
№ JH, Jeon YT, Park IA и др. Активация сигнального пути mTOR, связанная с неблагоприятными прогностическими факторами эпителиального рака яичников. Гинеколь Онкол . 2011 Апрель 121 (1): 8-12. [Медлайн].
Tapia V, Gabler F, Munoz M, et al. Рецептор тирозинкиназы А (trkA): потенциальный маркер эпителиального рака яичников. Гинеколь Онкол . 2011 Апрель 121 (1): 13–23. [Медлайн].
Lin HW, Tu YY, Lin SY, et al. Риск рака яичников у женщин с воспалительными заболеваниями органов малого таза: популяционное исследование. Ланцет Онкол . 2011 Сентябрь 12 (9): 900-4. [Медлайн].
Coakley FV. Стадия рака яичников: роль визуализации. Радиол Клин Норт Ам . 2002 май. 40 (3): 609-36. [Медлайн].
Zeppernick F, Meinhold-Heerlein I. Новая система стадирования FIGO для рака яичников, маточной трубы и первичного рака брюшины. Arch Gynecol Obstet . 2014 ноябрь 290 (5): 839-42. [Медлайн].
DiSilvestro P, Colombo N, Scambia G, Kim BG, Oaknin A, Friedlander M, et al.Эффективность поддерживающего олапариба для пациентов с недавно диагностированным распространенным раком яичников с мутацией BRCA: результаты анализа подгрупп из исследования SOLO1. Дж. Клин Онкол . 2020 4 августа. JCO2000799. [Медлайн].
van der Burg ME, van Lent M, Buyse M, et al. Влияние хирургического вмешательства после индукционной химиотерапии на прогноз распространенного эпителиального рака яичников. Совместная группа по гинекологическим онкологическим заболеваниям Европейской организации по исследованию и лечению рака. N Engl J Med . 1995 9 марта. 332 (10): 629-34. [Медлайн].
Роуз П.Г., Неренстон С., Брэди М.Ф., Кларк-Пирсон Д., Олт Г., Рубин СК. Вторичная хирургическая циторедукция при запущенном раке яичников. N Engl J Med . 2004, 9 декабря. 351 (24): 2489-97. [Медлайн].
Tangjitgamol S, Manusirivithaya S, Laopaiboon M, Lumbiganon P. Операция по удалению опухоли на поздних стадиях эпителиального рака яичников. Кокрановская база данных Syst Rev .2009 21 января. CD006014. [Медлайн].
Park JY, Eom JM, Kim DY, Kim JH, Kim YM, Kim YT и др. Вторичная циторедуктивная хирургия в лечении платиночувствительного рецидивирующего эпителиального рака яичников. J Surg Oncol . 15 января 2010 г. [Medline].
Fruscio R, Garbi A, Parma G, Lissoni AA, Garavaglia D, Bonazzi CM и др. Рандомизированное клиническое испытание фазы III по оценке еженедельного приема цисплатина при распространенном эпителиальном раке яичников. Национальный институт рака . 2011 7 января [Medline].
Кацумата Н., Ясуда М., Такахаши Ф., Исониси С., Джобо Т., Аоки Д. и др. Паклитаксел с высокой дозировкой один раз в неделю в комбинации с карбоплатином каждые 3 недели при распространенном раке яичников: открытое рандомизированное контролируемое исследование фазы 3. Ланцет . 17 октября 2009 г. 374 (9698): 1331-8. [Медлайн].
Кацумата Н., Ясуда М., Исониси С. и др., Для Японской группы гинекологической онкологии.Долгосрочные результаты высокодозного паклитаксела и карбоплатина по сравнению с обычным паклитакселом и карбоплатином для лечения распространенного эпителиального рака яичников, маточных труб или первичного рака брюшины (JGOG 3016): рандомизированное контролируемое открытое исследование. Ланцет Онкол . 2013 Сентябрь 14 (10): 1020-6. [Медлайн].
Морган М.А., Силл М.В., Фудзивара К. и др. Исследование фазы I с расширенной когортой для оценки возможности внутрибрюшинного введения карбоплатина и внутривенного паклитаксела при нелеченой карциноме яичников, маточной трубы и первичной перитонеальной карциноме: исследование группы гинекологической онкологии. Гинеколь Онкол . 2011 1 мая. 121 (2): 264-8. [Медлайн]. [Полный текст].
Курц Дж. Э., Каминский М. С., Флоке А. и др. Рак яичников у пожилых пациентов: карбоплатин и пегилированный липосомальный доксорубицин по сравнению с карбоплатином и паклитакселом при позднем рецидиве: суб-исследование CALYPSO Gynecologic Cancer Intergroup (GCIG). Энн Онкол . 2011 22 ноября (11): 2417-23. [Медлайн].
Винтер-Роуч Б.А., Китченер Х.С., Дикинсон ХО. Адъювантная (послеоперационная) химиотерапия при ранней стадии эпителиального рака яичников. Кокрановская база данных Syst Rev . 2009 21 января. CD004706. [Медлайн].
Pignata S, Scambia G, Ferrandina G и др. Карбоплатин плюс паклитаксел в сравнении с карбоплатином плюс пегилированным липосомальным доксорубицином в качестве лечения первой линии для пациентов с раком яичников: рандомизированное исследование фазы III MITO-2. Дж. Клин Онкол . 2011 20 сентября. 29 (27): 3628-35. [Медлайн].
Du Bois A, Floquet A, Kim JW, et al. Рандомизированное двойное слепое исследование фазы III пазопаниба по сравнению с плацебо у женщин, у которых после химиотерапии первой линии не наблюдалось прогрессирования распространенного эпителиального рака яичников, фаллопиевых труб или первичного рака брюшины (AEOC): результаты международного межгруппового исследования (AGO-OVAR16 ).Представлено на 49-м ежегодном собрании Американского общества клинической онкологии; 1 июня 2013 г .; Чикаго, штат Иллинойс. Аннотация LBA5503.
Тевари Д., Ява Дж. Дж., Салани Р., Армстронг Д. К., Маркман М., Херцог Т. и др. Преимущество долгосрочной выживаемости и прогностические факторы, связанные с внутрибрюшинным лечением химиотерапией при распространенном раке яичников: исследование группы гинекологической онкологии. Дж. Клин Онкол . 2015 1 мая. 33 (13): 1460-6. [Медлайн]. [Полный текст].
Армстронг Д.К., Банди Б., Венцель Л., Хуанг, штаб-квартира, Баерген Р., Леле С.Внутрибрюшинное введение цисплатина и паклитаксела при раке яичников. N Engl J Med . 2006, 5 января, 354 (1): 34-43. [Медлайн].
Hess LM, Benham-Hutchins M, Herzog TJ, Hsu CH, Malone DC, Skrepnek GH. Метаанализ эффективности внутрибрюшинного цисплатина для лечения рака яичников на первой линии. Int J Gynecol Cancer . 2007 май-июнь. 17 (3): 561-70. [Медлайн].
Элит Л., Оливер Т.К., Ковенс А, Квон Дж., Фунг М.Ф., Хирте Х.В.Внутрибрюшинная химиотерапия в качестве первой линии лечения женщин с эпителиальным раком яичников III стадии: систематический обзор с метаанализами. Рак . 2007 15 февраля. 109 (4): 692-702. [Медлайн].
Jaaback K, Johnson N, Lawrie TA. Внутрибрюшинная химиотерапия для начального лечения первичного эпителиального рака яичников. Кокрановская база данных Syst Rev . 2011 9 ноября. 11: CD005340. [Медлайн].
Таннер Э.Дж., Блэк Д.Р., Живанович О. и др.Особенности первого рецидива после адъювантной внутрибрюшинной химиотерапии при раке яичников стадии IIIC. Гинеколь Онкол . 2012 Январь 124 (1): 59-62. [Медлайн].
Лечение эпителия яичников, фаллопиевых труб и первичного рака брюшины (PDQ®) — версия для специалистов в области здравоохранения. Национальный институт рака. 5 января 2017 г .; Доступ: 24 февраля 2017 г.
Бристоу RE, Chi DS. Неоадъювантная химиотерапия на основе платины и интервальная хирургическая циторедукция при распространенном раке яичников: метаанализ. Гинеколь Онкол . 2006 декабрь 103 (3): 1070-6. [Медлайн].
Vergote I, Tropé CG, Amant F, Kristensen GB, Ehlen T., Johnson N, et al. Неоадъювантная химиотерапия или первичное хирургическое вмешательство при раке яичников IIIC или IV стадии. N Engl J Med . 2010 сентябрь 2. 363 (10): 943-53. [Медлайн].
Меламед А., Финк Г., Райт А.А., Китинг Н.Л., Гокли А.А., Дель Кармен М.Г. и др. Влияние применения неоадъювантной химиотерапии при распространенном раке яичников на смертность от всех причин: квазиэкспериментальное исследование. BMJ . 3 января 2018 г. 360: j5463. [Медлайн]. [Полный текст].
Маркман М., Лю П. Я., Мун Дж., Монах Б. Дж., Коупленд Л., Вильчинский С. и др. Влияние на выживаемость 12 или 3 месячных циклов паклитаксела (175 мг / м2), вводимых пациентам с распространенным раком яичников, у которых был достигнут полный ответ на первичный прием платина-паклитаксел: последующее наблюдение фазы 3 исследования Юго-Западной онкологической группы и Гинекологической онкологической группы . Гинеколь Онкол . 2009 Август 114 (2): 195-8.[Медлайн]. [Полный текст].
Поддерживающая химиотерапия не приносит пользы ОС при раке яичников. OncLive. Доступно по адресу https://www.onclive.com/view/main maintenance-chemotherapy-yields-no-os-benefit-in-ovarian-cancer. 15 марта 2017 г .; Дата обращения: 15 августа 2020 г.
Coleman RL, et al. Поддерживающая терапия рукапарибом при рецидивной карциноме яичников после ответа на терапию платиной (ARIEL3): рандомизированное двойное слепое плацебо-контролируемое исследование фазы 3. Ланцет . 2017 28 октября. 390 (10106): 1949-1961. [Медлайн]. [Полный текст].
Давенпорт Л. «Выдающаяся» ВБП рака яичников с поддерживающей терапией олапарибом. Медицинские новости Medscape. Доступно на https://www.medscape.com/viewarticle/8. 21 октября 2018 г .; Дата обращения: 1 ноября 2018 г.
Мур К., Коломбо Н., Скамбия Дж., Ким Б.Г., Окнин А., Фридлендер М. и др. Поддерживающая терапия Olaparib у пациентов с недавно диагностированным прогрессирующим раком яичников. N Engl J Med . 2018 21 октября [Medline]. [Полный текст].
FDA одобряет комбинацию бевацизумаба с химиотерапией при раке яичников. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно по адресу https://www.fda.gov/drugs/resources-information-approved-drugs/fda-approves-bevacizumab-combination-chemotherapy-ovarian-cancer?elq=7948f5cecc4942319dba22119368493e&elqCampaignfed8d6128d2d2d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6d6dd6d06d6d6d6dd6d6d06d6d2d6d06d6 13 июня 2018 г .; Дата обращения: 15 июня 2019 г.
Агаджанян С., Бланк С.В., Гофф Б.А., Джадсон П.Л., Тенериелло М.Г., Хусейн А. и др. ОКЕАНЫ: рандомизированное двойное слепое плацебо-контролируемое исследование III фазы химиотерапии с бевацизумабом или без него у пациентов с платиночувствительным рецидивирующим эпителиальным раком яичников, первичным раком брюшины или маточной трубы. Дж. Клин Онкол . 2012 июн 10, 30 (17): 2039-45. [Медлайн].
Агаджанян С., Гофф Б., Найкум Л.Р., Ван Ю.В., Хусейн А., Бланк С.В.Окончательный анализ общей выживаемости и безопасности OCEANS, исследования фазы 3 химиотерапии с бевацизумабом или без него у пациентов с платиночувствительным рецидивирующим раком яичников. Гинеколь Онкол . 2015 Октябрь 139 (1): 10-6. [Медлайн].
Коулман Р.Л., Брэди М.Ф., Херцог Т.Дж., Саббатини П., Армстронг Д.К., Уокер Дж.Л. и др. Химиотерапия бевацизумабом и паклитаксел-карбоплатин и вторичная циторедукция при рецидивирующем, чувствительном к платине раке яичников (исследование NRG Oncology / Gynecologic Oncology Group GOG-0213): многоцентровое открытое рандомизированное исследование фазы 3. Ланцет Онкол . 2017 июн.18 (6): 779-791. [Медлайн]. [Полный текст].
FDA одобряет олапариб плюс бевацизумаб в качестве поддерживающего лечения рака яичников, маточных труб или первичного рака брюшины. Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Доступно по адресу https://www.fda.gov/drugs/drug-approvals-and-databases/fda-approves-olaparib-plus-bevacizumab-main maintenance-treatment-ovarian-fallopian-tube-or-primary. 11 мая 2020 г .; Дата обращения: 5 июня 2020 г.
Ray-Coquard I, Pautier P, Pignata S, et al.Олапариб плюс бевацизумаб в качестве поддерживающей терапии первой линии при раке яичников. N Engl J Med . 2019 декабрь 19. 381 (25): 2416-2428. [Медлайн]. [Полный текст].
Münstedt K, von Georgi R, Franke FE. Корреляция между определяемой MIB1 фракцией роста опухоли и частотой рецидивов опухоли при ранних карциномах яичников. Рак Инвест . 2004. 22 (2): 185-94. [Медлайн].
Дапонте А., Костопулу Э, Коллия П., Папамичали Р., Ванакара П., Хаджихристодулу С. и др.L1 (CAM) (CD171) при серозных новообразованиях яичников. евро J Gynaecol Oncol . 2008. 29 (1): 26-30. [Медлайн].
Parmar MK, Ledermann JA, Colombo N, du Bois A, Delaloye JF, Kristensen GB. Паклитаксел плюс химиотерапия на основе платины по сравнению с традиционной химиотерапией на основе платины у женщин с рецидивом рака яичников: исследование ICON4 / AGO-OVAR-2.2. Ланцет . 2003, 21 июня. 361 (9375): 2099-106. [Медлайн].
Pfisterer J, Plante M, Vergote I, du Bois A, Hirte H, Lacave AJ.Гемцитабин плюс карбоплатин в сравнении с карбоплатином у пациентов с платиночувствительным рецидивирующим раком яичников: межгрупповое исследование AGO-OVAR, NCIC CTG и EORTC GCG. Дж. Клин Онкол . 2006.10.10.24 (29): 4699-707. [Медлайн].
du Bois A, Herrstedt J, Hardy-Bessard AC, Müller HH, Harter P, Kristensen G, et al. Испытание фазы III карбоплатина плюс паклитаксел с гемцитабином или без него в качестве терапии первой линии эпителиального рака яичников. Дж. Клин Онкол . 2010 сен 20. 28 (27): 4162-9. [Медлайн].
Hess LM, Rong N, Monahan PO, Gupta P, Thomaskutty C, Matei D. Продолжение химиотерапии после полного ответа на первичную терапию среди женщин с распространенным раком яичников: метаанализ. Рак . 15 ноября 2010 г. 116 (22): 5251-60. [Медлайн].
Joly F, Ray-Coquard I, Fabbro M и др. Снижение реакций гиперчувствительности при применении липосомального доксорубицина, пегилированного карбоплатином, по сравнению с комбинацией карбоплатин-паклитаксел: анализ из исследования рецидивирующего рака яичников GCIG CALYPSO. Гинеколь Онкол . 2011 августа 122 (2): 226-32. [Медлайн].
Сехули Дж., Стенгель Д., Хартер П., Курцедер С., Белау А., Богенридер Т. и др. Еженедельный график приема топотекана по сравнению с обычным 5-дневным графиком у пациентов с платинорезистентным раком яичников: рандомизированное многоцентровое исследование фазы II, проведенное Группой по изучению рака яичников Северо-Восточного немецкого общества гинекологической онкологии. Дж. Клин Онкол . 2010 29 ноября. [Medline].
Халдар К., Гайтскелл К., Брайант А. и др.Блокаторы рецепторов эпидермального фактора роста для лечения рака яичников. Кокрановская база данных Syst Rev . 2011 г. 5 октября. CD007927. [Медлайн].
Pujade-Lauraine E, Ledermann JA, Selle F, Gebski V, Penson RT, Oza AM и др. Таблетки олапариба в качестве поддерживающей терапии у пациентов с чувствительным к платине рецидивом рака яичников и мутацией BRCA1 / 2 (SOLO2 / ENGOT-Ov21): двойное слепое рандомизированное плацебо-контролируемое исследование фазы 3. Ланцет Онкол .25 июля 2017 г. [Medline].
Ledermann J, Harter P, Gourley C, Friedlander M, Vergote I, Rustin G и др. Поддерживающая терапия олапарибом у пациентов с платиночувствительным рецидивом серозного рака яичников: заранее запланированный ретроспективный анализ результатов по статусу BRCA в рандомизированном исследовании фазы 2. Ланцет Онкол . 2014 июл.15 (8): 852-61. [Медлайн].
Кауфман Б., Шапира-Фроммер Р., Шмутцлер Р.К., Одех М.В., Фридлендер М., Балманья Дж. И др.Монотерапия олапарибом у пациентов с распространенным раком и мутацией BRCA1 / 2 зародышевой линии. Дж. Клин Онкол . 2015 20 января. 33 (3): 244-50. [Медлайн]. [Полный текст].
Кайе С.Б., Любински Дж., Матулонис Ю., Энг Дж. Э., Горли С., Карлан Б. И. и др. Фаза II, открытое, рандомизированное, многоцентровое исследование, сравнивающее эффективность и безопасность олапариба, ингибитора поли (АДФ-рибозы) полимеразы, и пегилированного липосомального доксорубицина у пациентов с мутациями BRCA1 или BRCA2 и рецидивирующим раком яичников. Дж. Клин Онкол . 2012 1 февраля. 30 (4): 372-9. [Медлайн]. [Полный текст].
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США. Пресс-релиз FDA: FDA ускоренно одобряет новый метод лечения рака яичников на поздних стадиях. 2016, 19 декабря. Доступно по адресу http://www.fda.gov/NewsEvents/Newsroom/PressAnnouncements/ucm533873.htm.
Mulcahy N. FDA одобрило применение препарата Рукапариб для лечения рака яичников BRCA. Медицинские новости Medscape . 2016, 19 декабря. Доступно по адресу http: // www.medscape.com/viewarticle/873451.
Рубрака (рукапариб) [вкладыш в упаковке]. Clovis Oncology, Inc. Боулдер, Колорадо. 2016 г., декабрь. Доступно в [Полный текст].
Мирза М.Р., Монк Б.Дж., Херрштедт Дж., Оза А.М., Манер С., Редондо А. и др. Поддерживающая терапия нирапарибом при рецидивирующем раке яичников, чувствительном к платине. N Engl J Med . 2016 декабрь 1. 375 (22): 2154-2164. [Медлайн].
Константинопулос П.А., Вагонер С., Видаль Г.А. и др.Одноуровневое испытание фазы 1 и 2 нирапариба в комбинации с пембролизумабом у пациентов с рецидивирующей платинорезистентной карциномой яичников. JAMA Oncol . 13 июня 2019 г. [Medline]. [Полный текст].
Ахмед Н., Кадиф Э., Раза А., Шорт М., Джубински П. Т., Канноуракис Г. Рак яичников, раковые стволовые клетки и современные стратегии лечения: потенциальная роль магм в современных методах лечения. Ячейки . 2020 14 марта. 9 (3): [Medline]. [Полный текст].
Мур К.Н., Верготе I, Окнин А., Коломбо Н., Банерджи С., Оза А. и др.ВПЕРЕД I: исследование III фазы мирветуксимаба соравтансина в сравнении с химиотерапией при резистентном к платине раке яичников. Future Oncol . 2018 14 (17): 1669-1678. [Медлайн].
van Meurs HS, van Lonkhuijzen LR, Limpens J, van der Velden J, Buist MR. Гормональная терапия при опухолях гранулезных клеток яичников: систематический обзор. Гинеколь Онкол . 2014 июл.134 (1): 196-205. [Медлайн]. [Полный текст].
Бонавентура А., О’Коннелл Р.Л., Мапагу С., Бил П.Дж., МакНалли О.М., Милешкин Л.Р. и др.Paragon (ANZGOG-0903): Фаза 2 исследования анастрозола у женщин с эстрогеном или рецепторами прогестерона, резистентным к платине или рефрактерным рецидивирующим раком яичников. Int J Gynecol Cancer . 2017 июн. 27 (5): 900-906. [Медлайн].
Стоун Р.Л., Ник А.М., Макнейш И.А. и др. Паранеопластический тромбоцитоз при раке яичников. N Engl J Med . 2012 16 февраля. 366 (7): 610-8. [Медлайн].
Рунгруанг Б., Миллер А., Ричард С.Д. и др.Следует ли дополнительно разделить рак яичников на стадии IIIC на внутрибрюшинное или забрюшинное заболевание ?: исследование группы гинекологической онкологии. Гинеколь Онкол . 2012 января 124 (1): 53-8. [Медлайн].
Реббек TR, Lynch HT, Neuhausen SL, Narod SA, Van’t Veer L, Garber JE. Профилактическая овариэктомия у носителей мутаций BRCA1 или BRCA2. N Engl J Med . 2002, 23 мая. 346 (21): 1616-22. [Медлайн].
[Рекомендации] Американский колледж акушеров и гинекологов.Плановая сальпингоофорэктомия, снижающая риск. Национальный информационный центр руководящих принципов. Доступно на http://guideline.gov/content.aspx?id=12190. Доступ: 25 февраля 2017 г.
Финч А.П., Любински Дж., Мёллер П., Зингер К.Ф., Карлан Б., Сентер Л. и др. Влияние овариэктомии на заболеваемость раком и смертность у женщин с мутацией BRCA1 или BRCA2. Дж. Клин Онкол . 2014 24 февраля [Medline]. [Полный текст].
Чжан С., Ройер Р., Ли С. и др.Частота мутаций BRCA1 и BRCA2 среди 1342 невыбранных пациенток с инвазивным раком яичников. Гинеколь Онкол . 2011 1 мая. 121 (2): 353-7. [Медлайн].
Берк В., Дейли М., Гарбер Дж., Боткин Дж., Кан М.Дж., Линч П. и др. Рекомендации по дальнейшему наблюдению за лицами с наследственной предрасположенностью к онкологическим заболеваниям. II. BRCA1 и BRCA2. Консорциум исследований генетики рака. JAMA . 1997 26 марта. 277 (12): 997-1003. [Медлайн].
[Рекомендации] Комитет гинекологов Американского колледжа акушеров и гинекологов.Мнение Комитета № 477: роль акушера-гинеколога в раннем выявлении эпителиального рака яичников. Акушерский гинекол . 2011 Март 117 (3): 742-6. [Медлайн]. [Полный текст].
[Рекомендации] Целевая группа превентивных служб США., Оуэнс Д.К., Дэвидсон К.В., Крист А.Х., Барри М.Дж., Кабана М. и др. Оценка риска, генетическое консультирование и генетическое тестирование на рак, связанный с BRCA: Рекомендация рабочей группы США по профилактическим услугам. JAMA .2019 20 августа. 322 (7): 652-665. [Медлайн]. [Полный текст].
[Рекомендации] Национальная комплексная онкологическая сеть. Генетическая / семейная оценка высокого риска: грудь и яичники. NCCN. Доступно на http://www.nccn.org/professionals/physician_gls/pdf/genetics_screening.pdf. Версия 3.2019 — 18 января 2019 г .; Дата обращения: 15 июня 2019 г.
[Рекомендации] Робсон М.Э., Брэдбери А.Р., Арун Б., Домчек С.М., Форд Дж. М., Хэмпел Х. Л. и др. Заявление о политике Американского общества клинической онкологии: генетическое и геномное тестирование на предрасположенность к раку. Дж. Клин Онкол . 2015 г. 1. 33 (31): 3660-7. [Медлайн]. [Полный текст].
[Рекомендации] Палуч-Шимон С., Кардосо Ф., Сесса С., Бальмана Дж., Кардосо М.Дж., Гилберт Ф. и др. Профилактика и скрининг носителей мутации BRCA и других наследственных синдромов рака груди / яичников: Руководство ESMO по клинической практике по профилактике и скринингу рака. Энн Онкол . 2016, 27 сентября (приложение 5): v103-v110. [Медлайн]. [Полный текст].
[Рекомендации] Американский колледж акушеров и гинекологов, Комитет ACOG по практическим бюллетеням — гинекология, Комитет ACOG по генетике, Общество гинекологов-онкологов.Бюллетень практики ACOG № 103: Наследственный синдром рака груди и яичников. Акушерский гинекол . 2009 Апрель 113 (4): 957-66. [Медлайн].
[Руководство] Общество гинекологической онкологии. Заявление о клинической практике SGO: генетическое тестирование на рак яичников. СГО. Доступно на https://www.sgo.org/clinical-practice/guidelines/genetic-testing-for-ovarian-cancer. Октябрь 2014 г .; Дата обращения: 15 июня 2019 г.
[Руководство] Общество гинекологической онкологии.Заявление SGO о клинической практике: сальпингэктомия для профилактики рака яичников. СГО. Доступно по адресу https://www.sgo.org/clinical-practice/guidelines/sgo-clinical-practice-statement-salpingectomy-for-ovarian-cancer-prevention. Ноябрь 2013; Дата обращения: 15 июня 2019 г.
Прат Дж., Комитет по гинекологической онкологии FIGO. Классификация стадий рака яичника, маточной трубы и брюшины. Int J Gynaecol Obstet . 2014 Январь 124 (1): 1-5. [Медлайн].
Американский объединенный комитет по раку.Рак яичников и первичный рак брюшины. Amin MB, Edge S, Greene F, Byrd DR, Brookland RK и др., Под ред. AJCC Руководство по стадированию рака . 8-е изд. Нью-Йорк, штат Нью-Йорк: Спрингер-Верлаг; 2017.
[Рекомендации] Салани Р., Бэкес Ф.Дж., Фунг М.Ф., Хольшнайдер С.Х., Паркер Л.П., Бристоу Р.Э. и др. Наблюдение после лечения и диагностика рецидивов у женщин с гинекологическими злокачественными новообразованиями: рекомендации Общества гинекологов-онкологов. Am J Obstet Gynecol . 2011 июн.204 (6): 466-78. [Медлайн]. [Полный текст].
Hetland TE, Hellesylt E, Florenes VA и др. Экспрессия ß-тубулина класса III в выпотах серозной карциномы яичников на поздней стадии связана с плохой выживаемостью и первичной химиорезистентностью. Хум Патол . 2011 Июль 42 (7): 1019-26. [Медлайн].
Pujade-Lauraine E, Hilpert F, Weber B, Reuss A, Poveda A, Kristensen G, et al. Бевацизумаб в сочетании с химиотерапией при рецидивирующем раке яичников, резистентном к платине: открытое рандомизированное исследование III фазы AURELIA. Дж. Клин Онкол . 2014 1 мая. 32 (13): 1302-8. [Медлайн].
Ledermann J, Harter P, Gourley C, Friedlander M, Vergote I, Rustin G и др. Поддерживающая терапия олапарибом при рецидиве рака яичников, чувствительного к платине. N Engl J Med . 2012 Апрель 12, 366 (15): 1382-92. [Медлайн].
Анализ крови CA-125 не позволяет диагностировать рак яичников
CA-125 — это биомаркер рака яичников, уровень которого часто повышен в крови людей с раком яичников.Важно понимать, что, хотя анализ крови на CA-125 полезен при диагностике и мониторинге людей с раком яичников, сам по себе тест на CA-125 не является точным диагностическим инструментом. К сожалению, не существует единого надежного диагностического инструмента для обнаружения и диагностики рака яичников. Мы пытаемся изменить это здесь, в Альянсе по изучению рака яичников — и спасти больше жизней — путем инвестирования в исследования по поиску диагностического биомаркера и финансирования инновационных проектов, которые приведут к более эффективной профилактике, лечению и, в конечном итоге, излечению.
Что такое анализ крови CA-125?
CA-125, что означает «раковый антиген 125», представляет собой белок, который может быть обнаружен в больших количествах в крови пациентов с раком яичников. СА-125 вырабатывается на поверхности клеток и попадает в кровоток. Этот белок повышен более чем у 80 процентов женщин с запущенным раком яичников и у 50 процентов женщин с раком на ранней стадии.
Тест CA-125 входит в число анализов крови, которые может назначить врач при подозрении на рак яичников.
Поскольку CA-125 пропускает половину ранних форм рака и может быть повышен при доброкачественных заболеваниях, таких как дивертикулит, эндометриоз, цирроз печени, беременность и миома матки, он не используется сам по себе для диагностики заболевания, а Национальный институт рака и Целевая группа профилактических служб США не рекомендует использовать его для скрининга женщин на рак яичников, которые относятся к группе обычного риска, или среди населения в целом. Исследования новых способов использования CA-125 для более точной идентификации рака яичников продолжаются.
ОднакоCA-125 одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для мониторинга эффективности лечения рака яичников и выявления рецидивов заболевания после лечения.
Как используется тест CA-125?Врачи часто назначают тест на СА-125, если они обеспокоены тем, что у женщины может быть рак яичников. Поскольку уровни CA-125 могут колебаться в зависимости от лечения, тест также используется для отслеживания эффективности лечения или необходимости рассмотрения альтернативного лечения.CA-125 (наряду с компьютерной томографией) также часто используется для отслеживания рецидивов, хотя недавние данные показывают, что это не приносит клинической пользы. Подробнее об этом здесь.
Можно ли использовать CA-125 для скрининга бессимптомных женщин среднего риска на рак яичников?Хотя это иногда используется таким образом, нет никаких доказательств того, что это полезно. Тест CA-125 наиболее точен у женщин в постменопаузе с массой малого таза. Также важно отметить, что примерно в 20 процентах случаев заболевания на поздних стадиях и в 50 процентах случаев на ранних стадиях заболевания СА-125 НЕ повышается, даже если присутствует рак яичников, а СА-125 также может быть повышенным. повышен доброкачественными условиями.По этим причинам Национальный институт рака и Целевая группа профилактических служб США не одобряют его использование для скрининга женщин на рак яичников, которые относятся к группе обычного риска, или среди населения в целом.
Всегда ли высокое значение CA-125 означает рак?Нет, высокое значение CA-125 не всегда означает наличие рака. Вообще говоря, нормальный диапазон CA-125 считается 0-35 единиц / мл, в то время как уровень выше 35 единиц / мл считается высоким уровнем CA-125.Хотя анализ крови на CA-125 может быть полезным инструментом для диагностики рака яичников, нередко уровень CA-125 повышается у женщин в пременопаузе из-за доброкачественных состояний, не связанных с раком яичников, таких как дивертикулит, эндометриоз, цирроз печени, беременность и миома матки, как подробно описывает Medscape. В результате CA-125, как правило, является лишь одним из нескольких инструментов, используемых для диагностики рака яичников у пациенток с массой таза или другими подозрительными клиническими проявлениями.
Существуют ли какие-либо методы раннего выявления или способы выявления рака яичников?На данный момент нет.Никакие исследования не показали, что доступные в настоящее время инструменты или подходы эффективны в предотвращении смерти женщин от рака яичников.
Если нет надежных инструментов скрининга, как диагностируется рак яичников?Когда врач подозревает, что у женщины рак яичников (обычно после теста CA-125, ультразвука и других тестов), для окончательного диагноза рака яичников обычно требуется диагностическая хирургическая процедура, называемая лапаротомией.
Во время этой процедуры необходимо удалить кисты или другие подозрительные участки и провести биопсию.После того, как разрез сделан, хирург оценивает жидкость и клетки в брюшной полости. Если поражение злокачественное, хирург продолжает процесс, называемый хирургической стадией, чтобы установить, насколько далеко распространился рак. В отдельных случаях для подтверждения диагноза используется аспирация асцита, вызванного метастатическим поражением, или лапароскопия.
Почему врачи не делают женщинам тест на СА-125 и трансвагинальное УЗИ каждый год? Разве несовершенный инструмент для проверки не лучше, чем ничего?Исследования показали, что обследование женщин со средним риском рака яичников не улучшило шансы женщин выжить после рака яичников — и фактически подвергло их большему риску из-за осложнений от ненужных операций.
Большое исследование, впервые опубликованное в декабре 2015 года, под названием Совместное испытание Великобритании по скринингу рака яичников (UKCTOCS), показало, что опираясь на использование нескольких значений CA-125, полученных за многие годы, в сочетании с другими факторами и с использованием алгоритма под названием ROCA — более сложный подход, чем полагаться только на значения CA-125 — не смог предотвратить смерть женщин от рака яичников. Дальнейшие результаты исследования, опубликованного в мае 2021 года, подтверждают первоначальные результаты о том, что скрининг на рак яичников среди населения не спасает жизни.Узнайте больше об исследовании на веб-сайте AAFP и ознакомьтесь с отчетом OCRA о самых последних результатах.
В другом исследовании более 78 000 женщин были рандомизированы между группами обычного лечения и скрининга. Протокол скрининга включал ежегодное тестирование CA-125 в течение шести лет и трансвагинальное ультразвуковое исследование в течение четырех лет. Исследование было разработано, чтобы показать влияние скрининга на общую выживаемость при наблюдении за пациентами в течение 13 лет. Исследование показало, что большему количеству женщин был поставлен диагноз в группе скрининга, но больше женщин умерло от рака яичников в группе скрининга.
Кроме того, более 3000 женщин перенесли операции на основании ложноположительных результатов, что привело к более чем 160 женщинам с серьезными осложнениями. Это исследование показало, что скрининг по этому протоколу не снизил смертность от рака яичников.
Что такое тест ROCA?Тест ROCA — это тест, который использует изменение CA-125 с течением времени в сочетании с другими факторами (возраст, статус менопаузы и т. Д.) Для прогнозирования риска развития рака яичников. Тест должен быть заказан врачом, но его можно купить напрямую за 295 долларов.Хотя тест ROCA предлагается женщинам и побуждает их запрашивать его в рамках ежегодного осмотра, нет никаких доказательств того, что этот тест предотвращает смерть женщин от рака яичников. Подробнее читайте здесь.
Безопасен ли тест ROCA?В сентябре 2016 года FDA выпустило Руководство по безопасности при проведении скрининговых тестов на рак яичников и особо упомянуло тест ROCA при обсуждении скрининговых тестов на рак яичников, которые могут быть небезопасными для женщин.
Утвержден ли тест ROCA Test FDA?Тест ROCA не одобрен FDA, поскольку FDA традиционно не регулирует такие тесты тщательно.
002303: Раковый антиген (CA) 125
1. CA 125 на Elecsys 1010/2010 и Modular Analytics E170, [Вставка в пакет]. 2007-08, VII, Индианаполис, Индиана: Диагностика Рош; 2007.
2. Дэвис Х.М., Зуравски В.Р., младший Баст Р.С., Клуг Т.Л. Характеристика антигена CA 125, связанного с эпителиальной карциномой яичников человека. Cancer Res. 1986 Dec; 46 (12, Пет. 1): 6143-6148. 2430690
3. Diamandis EP, Fritsche HA, Lilja H, et al. Онкомаркеры: физиология, патобиология, технология и клиническое применение. 1-е изд. Вашингтон, округ Колумбия: AACC Press; 2002.
4. Kabawat SE, Bast RC, Welch WR, Knapp RC, Colvin RB. Иммунопатологическая характеристика моноклонального антитела, которое распознает общие поверхностные антигены опухолей яичников человека серозного, эндометриоидного и светлоклеточного типов. Am J Clin Pathol. 1983 Jan; 79 (1): 98-104. 6336888
5. Bast RC Jr, Klug TL, St John E, et al. Радиоиммуноанализ с использованием моноклональных антител для мониторинга течения эпителиального рака яичников. N Engl J Med. , 1983, 13 октября; 309 (15): 883-887. 6310399
6. Klug TL, Bast RC Jr, Niloff JM, Knapp RC, Zurawski VR Jr. Иммунорадиометрический анализ моноклональных антител для определения антигенной детерминанты (CA 125), связанной с эпителиальной карциномой яичников человека. Cancer Res. 1984 Mar; 44 (3): 1048-1053. 6198078
7. Хашолцнер У., Баумгартнер Л., Штибер П., Мейер В., Хофманн К., Фатех-Магадам А. Значение онкомаркеров CA 125 II, CA 72-4, CASA и CYFRA 21-1 в карциноме яичников. Anticancer Res. ноябрь-декабрь 1994 г .; 14 (6B): 2743-2746. 7532929
8. Кабават С.Е., Баст Р.С. мл., Бхан А.К., Велч В.Р., Кнапп Р.С., Колвин Р.Б. Распределение в тканях антигена, связанного с целомическим эпителием, распознаваемого моноклональным антителом ОС 125. Int J Gyn Path. 1983; 2 (3): 275-285. 6196309
9. Дауд Э., Бодор Г. Концентрации CA-125 при злокачественных и незлокачественных заболеваниях. Clin Chem. 1991 Nov; 37 (11): 1968-1974. 1934471
10. Кенеманс П., Бон Г.Г., Кесслер А., Верстратен А.А., ван Камп Г.Дж.Многоцентровая техническая и клиническая оценка полностью автоматизированного иммуноферментного анализа на CA 125. Clin Chem. 1992 Aug; 38 (8 Pt 1): 1466-1471. 1643716
11. Hasholzner U, Stieber P, Baumgartner L, et al. Методологическая и клиническая оценка трех автоматизированных анализов CA 125 по сравнению с CA 125 II RIA (Fujirebio). Tumordiagn Ther. 1994; 15: 114-117.
12. Руибаль А., Энкабо Дж., Мартинес-Мираллес Е. и др. Уровни CA 125 серий При доброкачественных патологиях. Бык-Рак. 1984; 71 (2): 145-146. 6203578
13. Zahner J, Schmitz FJ, Schmitz G, et al. CA 125 — онкомаркер ein в лекарственном препарате. Lab Med. 1995; 19: 185-188.
14. Стибер П., Фатех-Могхадам А. Разумное использование онкомаркеров. Марлоффштейн-Ратсберг: Юрген Хартманн Верлаг; 1993. Boehringer Mannheim, Каталог N ° 1536869 (на английском языке), 1320947 (на немецком языке). ISBN 3-926725-07-9 немецкий / английский.
Контуры патологии — CA125
Пятна и маркеры CDCA-125
Тема завершена: 1 ноября 2011 г.
Незначительные изменения: 23 июня 2021 г.
Авторские права: 2003-2021, PathologyOutlines.com, Inc.
Поиск в PubMed: CA-125 [название]
Просмотры страниц в 2020 году: 6,758
Просмотры страниц в 2021 году по настоящее время: 4,067
Цитируйте эту страницу: Pernick N. CA125. Сайт PathologyOutlines.com. https://www.pathologyoutlines.com/topic/stainsca125.html. По состоянию на 4 августа 2021 г.
Определение / общее
- Раковый антиген 125 (CA-125) — это белок, кодируемый геном MUC16, используемый в качестве онкомаркера, поскольку он на 79% чувствителен к раку яичников.
- Не специфичен, поскольку повышен при других опухолях и при воспалительных состояниях
Патофизиология
- Муцин, связанный с высокой молекулярной массой, мембранно-связанный, обнаружен в роговице и конъюнктиве, в респираторном тракте и эпителии женских половых путей
- Как муцин, образует смазывающий барьер против инородных частиц и инфекционных агентов.
Клинические признаки
- Повышенный уровень при карциномах груди, шейки матки (Asian Pac J Cancer Prev 2010; 11: 1745), эндометрия, маточных труб, желудочно-кишечного тракта, легких, яичников; также эндометриоз, беременность, воспалительные заболевания
Интерпретация
- Сильное перепончатое окрашивание, фаллопиевы трубы — хороший контроль
Использование патологами
- (1) При карциноме яичников используйте уровни сыворотки, чтобы отслеживать реакцию на лечение и прогнозировать прогноз (Ann Oncol 2008; 19: 327)
- (2) В Великобритании рекомендуется использовать уровни сыворотки для скрининга женщин с симптомами рака яичников (пресс-релиз Национальной службы здравоохранения).
- (3) Серийные измерения могут быть более специфичными для рака яичников.
- (4) Используется в иммуногистохимии для подтверждения яичникового происхождения опухоли (Am J Surg Pathol 2005; 29: 1482)
- (5) Уровни сыворотки могут иметь значение для оценки сердечной недостаточности (Clin Cardiol 2011; 34: 244, Eur Heart J 2010; 31: 1752)
- Высокий уровень СА-125 в сыворотке крови обусловлен серозными жидкостями и вовлечением серозных клеток в различные заболевания яичников или не яичников (Gynecol Oncol 2002; 85: 108)
- Уровни сыворотки не рекомендуются для общего скрининга рака яичников с низким риском из-за недостаточной чувствительности, особенно для опухолей низкой стадии (чувствительность только 50% для стадии I)
Микроскопические (гистологические) изображения
Положительное окрашивание — нормальное
- Плод: амнион, целомический и мюллеров эпителий (Asia Oceania J Obstet Gynaecol 1990; 16: 379)
- Взрослые: клетки мезотелия и просветная поверхность эпителиальных клеток эндоцервикса, эндометрия, маточной трубы; также в небольших количествах в эпителии апокриновых потовых желез, желчных путях, толстой кишке, молочной железе, поджелудочной железе, желудке
Положительное окрашивание — болезнь
- Карциномы желчевыводящих путей, груди, шейки матки, эндометрия, маточных труб, печени, легкого, яичников (серозные, обычно не муцинозные), поджелудочной железы; опухоли полового канатика яичника
- Альвеолярная рабдомиосаркома матки, десмопластическая мелкоклеточная опухоль брюшины малого таза, эпителиоидная саркома (Arch Pathol Lab Med 2006; 130: 871, Jpn J Clin Oncol 2004; 34: 149), внутрилобарная секвестрация легких (Intern Med 2002; 41: 875), лейомиома брыжейки подвздошной кишки, мезотелиома, аденокарцинома семенного сосуда
- Эндометриоз (Hum Pathol 2008; 39: 954), воспалительные заболевания, лейомиомы брыжейки подвздошной кишки, беременность
Отрицательное окрашивание
- Нормальный яичник, плоскоклеточные клетки
диагностика рака яичников — NHS
Обратитесь к терапевту, если у вас симптомы рака яичников .Они могут сделать некоторые начальные тесты, и вам также могут потребоваться дополнительные тесты в больнице.
На приеме к врачу
Врач общей практики может:
- спросить о ваших симптомах и общем состоянии здоровья
- мягко пощупать животик, чтобы проверить, нет ли опухолей или шишек
- провести внутреннее обследование
- спросить, есть ли в вашей семье в анамнезе рак яичников или груди
- возьмите образец крови — он будет отправлен в лабораторию и проверен на наличие вещества под названием CA125
В некоторых случаях вас могут направить прямо к специалисту больницы (обычно гинекологу) для дальнейших анализов без сдачи анализа крови .
Анализ крови (тест CA125)
Если терапевт считает, что ваши симптомы могут быть вызваны раком яичников, он порекомендует сдать анализ крови на наличие вещества под названием CA125.
CA125 продуцируется некоторыми клетками рака яичников. Высокий уровень CA125 в крови может быть признаком рака яичников.
Но повышенный уровень CA125 не означает, что у вас определенно рак, поскольку он также может быть вызван другими заболеваниями, такими как эндометриоз, миома и даже беременность.
Если тест показывает высокий уровень CA125, вас направят на сканирование для выявления возможных причин.
Иногда уровень CA125 может быть нормальным на ранних стадиях рака яичников. Если у вас был нормальный результат анализа крови, но ваши симптомы не улучшились, вернитесь к терапевту, так как вам может потребоваться повторное обследование.
Lab Tests Online UK содержит дополнительную информацию о тесте CA125.
УЗИ
Лечащий врач назначит вам ультразвуковое исследование, если анализ крови предполагает, что у вас может быть рак яичников.
Это тип сканирования, при котором высокочастотные звуковые волны используются для создания изображения внутренней части вашего тела.
Это можно сделать двумя способами:
- УЗИ брюшной полости — небольшое устройство, называемое ультразвуковым датчиком, перемещается по вашему животу для создания изображения ваших яичников
- трансвагинальное УЗИ — ультразвуковой датчик вводится во влагалище и создайте более четкое изображение ваших яичников
Сканирование может показать изменения в ваших яичниках, которые могут быть вызваны раком или другой проблемой, такой как эндометриоз или скопление жидкости.
Если будут обнаружены какие-либо отклонения от нормы, вас направят к специалисту для проведения дальнейших анализов для подтверждения причины.
Дополнительные испытания
Специалист в больнице может провести следующие тесты для подтверждения или исключения рака яичников:
- КТ — тип сканирования, при котором несколько рентгеновских снимков делаются под разными углами для создания подробного изображения ваших яичников
- рентген грудной клетки, чтобы проверить, распространился ли рак на ваши легкие
- игла биопсия — игла проходит через живот, чтобы взять образец клеток яичников или жидкости вокруг яичников, чтобы ее можно было проверить на рак
- лапароскопия — на животе делается небольшой разрез и вставляется тонкая трубка с камерой на конце, чтобы можно было исследовать яичники; небольшой образец ткани также может быть взят для тестирования.
Если обнаружен рак яичников, эти тесты также могут помочь определить, насколько далеко он уже распространился.
Стадии и степени рака яичников
Если у вас диагностирован рак яичников, ему будет определена «стадия».
Здесь описывается размер рака и степень его распространения. Это может помочь вашим врачам спланировать для вас наилучшее лечение.
Четыре основных стадии рака яичников:
- Стадия 1 — рак поражает только 1 или оба яичника
- Стадия 2 — рак распространился из яичника в таз или матку
- Стадия 3 — рак распространился на слизистую оболочку живота, поверхность кишечника или лимфатические узлы в тазу или животе
- Стадия 4 — рак распространился на другие части тела, такие как печень или легкие
Вашему раку также будет поставлена «оценка».Это способ описания того, насколько быстро рак может расти или распространяться.
Оценки варьируются от 1-го (более медленный рост) до 3-го (более быстрый рост).
Дополнительная информация
Последняя проверка страницы: 10 февраля 2020 г.
Срок следующей проверки: 10 февраля 2023 г.
лабораторных тестов для диагностики и лечения рака
Какие лабораторные тесты используются для диагностики рака?
Врачи могут использовать различные лабораторные тесты при подозрении на рак.При проведении лабораторных тестов на рак образцы крови, мочи, других биологических жидкостей или тканей исследуются на аномальные клетки или опухолевые маркеры, которые могут определить, есть ли у человека заболевание или предраковое состояние. Лабораторные тесты также могут использоваться для скрининга пациентов из группы высокого риска, определения стадии рака, определения вариантов лечения и оценки реакции рака на лечение. Лабораторные тесты также могут использоваться, чтобы определить, есть ли у пациента рецидив рака — болезнь, которая вернулась в исходное место, — или развился новый рак.
Примеры используемых нами лабораторных тестов:
Тест CTC
Cellsearch ™ тесты циркулирующих опухолевых клеток (ЦОК) могут использоваться для мониторинга метастатического рака молочной железы, колоректального рака и рака простаты. Этот диагностический тест помогает захватить, идентифицировать и подсчитать циркулирующие опухолевые клетки в образце крови. ЦКО — это раковые клетки, которые отделяются от солидных опухолей и попадают в кровоток. Этот анализ крови на рак может быть выполнен до начала терапии или во время курса лечения.
Общий анализ крови
Общий анализ крови (CBC) измеряет количество кровяных телец, циркулирующих в кровотоке. В частности, этот анализ крови на рак измеряет в образце крови уровень красных кровяных телец, которые переносят кислород по всему телу; лейкоциты, борющиеся с инфекцией; и тромбоциты, которые способствуют свертыванию крови. Тест также измеряет гемоглобин, белок в красных кровяных тельцах, который переносит кислород, и гематокрит, отношение красных кровяных телец к плазме.
Общий анализ крови может использоваться для обнаружения различных состояний, включая лейкемию, анемию и инфекцию. Кроме того, поскольку некоторые виды лечения рака могут временно снизить показатели крови, онкологи часто используют анализы общего анализа крови на протяжении всего лечения, чтобы внимательно следить за показателями крови пациента.
Проточная цитометрия
Этот тест используется для диагностики и классификации определенных видов рака, таких как лейкемия и лимфома, а также для оценки риска рецидива. Проточная цитометрия также может использоваться как часть процесса трансплантации стволовых клеток.
Проточная цитометрия измеряет свойства клеток в образце костного мозга, лимфатических узлов или крови. Образец сначала обрабатывают специальными антителами и пропускают перед лазерным лучом. Если антитела прикрепляются к клеткам, клетки излучают свет. Присутствие определенных веществ или антигенов на поверхности клеток может помочь определить тип клеток.
Проточная цитометрия также может использоваться для измерения количества ДНК в раковых клетках. В этом случае клетки обрабатываются специальными светочувствительными красителями, вступающими в реакцию с ДНК.Для пациентов с раком груди, простаты или мочевого пузыря аномальное количество ДНК может указывать на рецидив.
Mammaprint + Blueprint
® testАнализ рецидива рака молочной железы с 70 генами Mammaprint ® можно использовать для определения риска рецидива рака у пациента. Оценка высокого риска означает, что вероятность рецидива рака составляет три из 10. Результат с низким уровнем риска дает шанс один из 10. Ни один из результатов не является гарантией того, что злокачественное новообразование вернется или не вернется, но оценка может использоваться для принятия решений о лечении.
Blueprint ® 80-Gene Molecular Subtyping Assay исследует, какие мутации опухоли определяют поведение рака. При использовании с анализом Mammaprint Blueprint может узко определить каждую опухоль в классификацию подтипа, что также может помочь в принятии решений о лечении.
Тест Oncotype DX
®Лабораторный тест Oncotype DX используется для определения пользы от химиотерапии пациентам с раком груди на ранней стадии. Это также помогает оценить вероятность рецидива заболевания.
Этот диагностический тест часто выполняется на небольшом количестве ткани, удаленной во время операции по поводу рака груди, а затем исследуется на молекулярном уровне. Тест Oncotype DX предоставляет конкретную информацию о заболевании, которая может помочь в принятии решения о лечении.
Что такое онкомаркеры?
Онкомаркеры — это вещества в организме, которые вырабатываются в гораздо больших количествах при наличии рака или некоторых доброкачественных заболеваний. Вещества могут быть обнаружены в крови, моче, стуле или опухолевой ткани.Большинство этих веществ являются белками, но иногда в качестве онкомаркеров также используются паттерны экспрессии генов и изменения ДНК.
Поскольку повышенный уровень опухолевого маркера не обязательно указывает на рак, опухолевые маркеры не могут использоваться отдельно для диагностики рака. Обычно измерения маркеров опухолей используются в сочетании с другими тестами, такими как биопсия.
Тесты на онкомаркеры, используемые для диагностики рака, включают:
Тест CA-125
Тест CA-125 измеряет количество ракового антигена 125 (CA-125) в крови человека.CA-125 — это белок, который является биомаркером или онкомаркером. Белок содержится в более высоких концентрациях в раковых клетках, особенно в раковых клетках яичников.
Типы рака, которые могут вызывать уровни CA-125 выше нормы, включают:
Рак, распространившийся на брюшину, слизистую оболочку брюшной полости, также может вызывать уровни СА-125 выше нормы.
Важно отметить, что другие состояния, помимо рака, могут вызывать более высокие уровни CA-125, включая миому матки, эндометриоз.волчанка. болезнь печени и панкреатит
Тест на простатоспецифический антиген
Тест на простат-специфический антиген (ПСА) измеряет уровень ПСА в крови. Предстательная железа вырабатывает ПСА — белок, повышенный уровень которого может быть признаком рака простаты. Высокое значение ПСА также может указывать на доброкачественные состояния, такие как воспаление простаты (простатит) и увеличение простаты (доброкачественная гиперплазия простаты).
Мужчины, у которых есть симптомы, связанные с раком простаты, могут пройти тест на ПСА вместе с пальцевым ректальным исследованием (DRE).По данным Национального института рака, исследования показывают, что у мужчин с раком простаты может быть низкий уровень ПСА, а у мужчин без рака простаты — высокий. Каждый четвертый мужчина с повышенным уровнем ПСА действительно болен раком простаты. Однако повышение уровня ПСА со временем может указывать на рак простаты. Вот почему некоторые мужчины с высоким уровнем ПСА могут находиться под активным наблюдением, которое включает регулярное тестирование на ПСА.
Другие опухолевые маркеры, которые врачи ищут при диагностике и лечении рака, включают:
| Маркер | Ассоциированные раковые образования | Тест | Комментарии |
|---|---|---|---|
| Альфа-фетопротеин (AFP) | Рак печени | Анализ крови | Тесты могут помочь диагностировать и определить стадию рака, определить варианты лечения и измерить реакцию на лечение. |
| Бета-2-микроглобулин (B2M) | Множественная миелома, хронический лимфолейкоз и некоторые лимфомы | Кровь, моча, спинномозговая жидкость | Тесты могут помочь определить реакцию на лечение и прогноз. |
| Бета-хорионический гонадотропин человека (Бета-ХГЧ) | Хориокарцинома и опухоли половых клеток | Моча или кровь | Тесты могут помочь диагностировать и определить стадию рака, определить варианты лечения и измерить реакцию на лечение. |
| CA15-3 / CA27.29 | Рак груди | Кровь | Тесты могут помочь диагностировать рецидив рака и оценить реакцию на лечение. |
| CA19-9 | Рак поджелудочной железы, рак желчного пузыря, рак желчных протоков и рак желудка | Кровь | Тесты могут помочь оценить реакцию на лечение. |
| Кальцитонин | Рак щитовидной железы | Кровь | Тесты могут помочь диагностировать рак и оценить реакцию на лечение. |
| Карциноэмбриональный антиген (СЕА) | Колоректальный рак | Кровь | Тесты могут помочь диагностировать рецидив рака и оценить реакцию на лечение. |
| Хромогранин А (CgA) | Нейроэндокринные опухоли | Кровь | Тесты могут помочь диагностировать рецидив рака и оценить реакцию на лечение. |
| HE4 | Рак яичников | Кровь | Тесты могут помочь определить варианты лечения, отследить рецидивы и измерить реакцию на лечение. |
| Иммуноглобулины | Множественная миелома и неходжкинская лимфома | Кровь и моча | Тесты могут помочь диагностировать заболевание, отслеживать рецидивы и измерять реакцию на лечение. |
| Нейронспецифическая енолаза (NSE) | Рак легкого | Кровь | Тесты могут помочь диагностировать заболевание и оценить реакцию на лечение. |
| Ядерный матричный белок 22 | Рак мочевого пузыря | Моча | Тесты могут помочь оценить реакцию на лечение. |
| Тиреоглобулин | Рак щитовидной железы | Кровь | Тесты могут помочь контролировать реакцию на лечение и диагностировать рецидив. |
Роль CA125 в клинической практике
Антиген CA125 представляет собой высокомолекулярный гликопротеин, который экспрессируется в значительной части эпителиального рака яичников.Он обнаруживается моноклональным антителом OC125, которое было впервые описано Bast et al. в 1981 году. 1 С момента своего открытия CA125 стал хорошо зарекомендовавшим себя в качестве опухолевого маркера эпителиального рака яичников и приобрел важное значение. роль в диагностике, с ее включением в индекс риска злокачественных новообразований. 2 Известно, что чувствительность и специфичность CA125 низкая. Он повышается только примерно в 50% случаев эпителиального рака яичников 1 стадии и у 75–90% пациентов с запущенным заболеванием.Ложноположительные результаты были отмечены при многих заболеваниях, как злокачественных 3– 5 , так и доброкачественных. 6– 8 Этот недостаток специфичности широко исследовался, и теперь было показано, что CA125 является эффективным маркером многих заболеваний, помимо рака яичников. 9– 13 В настоящее время, насколько нам известно, Королевский колледж патологов или Ассоциация клинических биохимиков не разработал руководств, которые помогли бы клиницистам или лабораториям наиболее целесообразно использовать CA125.
«CA125 хорошо зарекомендовал себя как опухолевый маркер эпителиального рака яичников и играет важную роль в диагностике»
Количество запросов на тестирование CA125 увеличивается, но есть предположения, что большая часть этого увеличения является результатом его использования другими специальностями, кроме гинекологии или онкологии, что вызывает опасения, что CA125 используется клиницистами, которые не полностью осведомлены о его ограничения и его роль в развитии рака яичников.Это может привести к пропущенному диагнозу или ненужному обследованию пациентов.
Таким образом, в больнице Квинс, Бертон-апон-Трент, Великобритания, был проведен ретроспективный аудит, чтобы изучить роль CA125 в повседневной клинической практике. Основная цель нашего исследования состояла в том, чтобы определить популяцию пациентов, у которых есть измерение CA125, попытаться определить его вклад в индивидуальное ведение пациентов и улучшить структуру направления к специалистам.
МЕТОДЫ
Наше исследование представляло собой ретроспективный аудит истории болезни с использованием компьютеризированной системы информации о пациентах HISS, проведенный в больнице Квинс, Бертон-апон-Трент, Великобритания.Каждый пациент, у которого в период с апреля 2000 г. по апрель 2002 г. выполнялось измерение CA125, был идентифицирован, и аудиторская группа была выбрана путем взятия первых 799 хронологических номеров больничных отделений. Данные были собраны из отчетов о патологии, радиологии и лабораторных исследований, а также писем о направлениях, клиниках и выписках. Была собрана информация о характеристиках популяции, включая ведущий признак или симптом, индекс CA125 и результаты других опухолевых маркеров (карциноэмбриональный антиген, альфа-фетопротеин (AFP), хорионический гонадотропин человека (ХГЧ), CA19).9 и CA15.3), режим визуализации яичников и окончательный диагноз. Чтобы определить показания для измерения CA125, ведущий признак или симптом пациентки был разделен на «подозрение на рак яичников», «подозрение на злокачественную опухоль», «последующее наблюдение за раком яичников», «скрининг на рак яичников» и пациенты с «подозрением на рак яичников». известное злокачественное новообразование », кроме яичников, у которых не было заподозрено никаких других злокачественных новообразований. Следующей категорией были пациенты, у которых «невозможно было определить показание». Пациенты с массой таза, кистой яичника, асцитом или вздутием живота были включены в группу с подозрением на рак яичников, тогда как неспецифические симптомы, например, боль в животе, анемия, метастатическое заболевание, потеря веса или дерматомиозит, были сгруппированы вместе при подозрении на злокачественное новообразование.Анализы CA125 были выполнены в клинической химической лаборатории больницы, где аномальный результат был принят равным 30 kU / литр или выше. Отдел клинической химии не проводил скрининг запросов, и не существовало больничных руководств, которые помогли бы клиницистам наиболее целесообразно использовать CA125.
Чувствительность определялась как доля пациентов с раком яичников, правильно идентифицированных с помощью CA125, а специфичность — как доля пациентов без рака яичников, правильно идентифицированных с помощью CA125.
РЕЗУЛЬТАТЫ
В исследовании приняли участие 799 пациентов: 751 женщина (94%) и 48 мужчин (6%), из которых 636 (80%) пациентов были старше 50 лет. В этой популяции у 221 (29%) женщин и 22 из 48 пациентов мужского пола результат был ненормальным (рис. 1).
Рисунок 1Распределение аномальных результатов CA125 (n = 243).
Поскольку рак яичников не относился к мужской популяции, эти пациенты были исключены из всех дальнейших анализов.Показания к применению CA125 у пациенток были очевидны в 672 (89%) случаях (рис. 2). Подозрение на рак яичников составило только 259 (34%) из выполненных тестов CA125. Большая часть тестов CA125 — 327 (44%) — была предпринята для исследования пациентов с широким спектром признаков и симптомов (таблица 1).
Таблица 1Клинические показания к измерению CA125 у пациентов женского пола при подозрении на злокачественную опухоль (n = 327)
Рисунок 2Показания для измерения CA125 в женской популяции (n = 751).
Когда концентрация CA125 коррелировала с окончательным диагнозом у пациентов, у которых было измерение CA125 для подозрения на злокачественность / рак яичников, только 39 (20%) аномальных результатов в женской популяции были результатом рака яичников. Чувствительность CA125 к раку яичников у пациенток в этой популяции составляла 88,6%, но со специфичностью только 72,0%. Пациенты без рака яичников имели другое злокачественное новообразование в 48 случаях (26%) — например, молочную железу, кишечник или легкие — или имели доброкачественную патологию яичников (26 случаев; 14%), доброкачественные гинекологические состояния, особенно лейомиому (18 случаев; 9%). , или гепатобилиарное заболевание (12 случаев; 6%) (рис. 3).Когда были проанализированы результаты CA125 более 1000 kU / л, специфичность CA125 увеличилась до 99,1%. Рак яичников был диагностирован в 23 из 28 случаев, но было пять пациентов, у которых концентрация CA125 превышала 1000 kU / литр при отсутствии рака яичников. Было три случая метастазирования из груди, желчного пузыря и неизвестной первичной опухоли, и было два случая цирроза печени. Однако увеличение порогового значения до более чем 1000 kU / л привело к падению чувствительности CA125 к раку яичников до 52.3%.
Рисунок 3Окончательный диагноз у женщин с ненормальным результатом исследования с CA125 (n = 191).
Был проведен обзор радиологических исследований женского населения, обследуемого на предмет подозрения на злокачественные новообразования / рак яичников (рис. 4). Ультрасонография была наиболее часто используемым методом: 310 пациентов (53%) прошли ультразвуковое исследование органов малого таза в качестве единственного исследования и 91 (16%) прошли этот тест в сочетании с компьютерной томографией.Срочная (в течение двух недель) диагностическая лапароскопия была проведена в семи случаях, пяти из которых предшествовало трансвагинальное ультразвуковое исследование. Один пациент был обследован с помощью магнитно-резонансной томографии. Вероятность визуализации яичников увеличивалась с увеличением результата CA125, за исключением пациентов с CA125 между 500,1 и 1000 kU / л. В 134 (23%) случаях визуализация не проводилась; однако 108 (81%) из них имели нормальный результат CA125.
Рисунок 4Визуализация выполнена у обследованных женщин с CA125 (n = 586).КТ, компьютерная томография; МРТ, магнитно-резонансная томография; УЗИ, трансвагинальное УЗИ.
В этом исследовании 44 пациентам был поставлен диагноз «злокачественный рак яичников». В 36 из них показанием для измерения CA125 было то, что они попали в категорию подозрения на рак яичников. Концентрации CA125 у этих пациентов были исследованы и показали широкое распределение результатов: 23 пациента имели более 1000 kU / литр, но пять имели менее 30 kU / литр.
Дополнительные сывороточные опухолевые маркеры, взятые во время получения индекса CA125, показали, что 422 (56%) женского населения имели CA125, взятый изолированно, в отличие от мужского населения, в котором этот показатель составлял 10 случаев (20%). Из 57 пациентов моложе 40 лет только четверым были выполнены ХГЧ и АФП, у одного пациента был только АФП, а у другого только ХГЧ.
Скрининг на рак яичников охватил только 24 пациента. Десять тестов были назначены в отделении первичной медико-санитарной помощи, при этом гинекологи отвечали за семь случаев, а общие хирурги — за четыре.Визуализация яичников с помощью трансвагинального ультразвукового исследования была проведена у 13 из 24 обследованных пациентов.
Окончательный анализ был сосредоточен на отделах, заказывающих измерения CA125. Ревматология, уход за престарелыми, медицина и гематология были сгруппированы как «другие медицинские специальности», а ортопедия и урология — как «другие хирургические специальности». Гинекологи были наиболее частыми пользователями CA125, но на их долю пришлось только 278 (36%) всех тестов, назначенных пациентам-женщинам.Многие другие специальности, в частности, общая хирургия (109 тестов; 15%), первичная медико-санитарная помощь (89 тестов; 12%) и общая медицина (78 тестов; 10%) — отвечали за большую часть оставшейся части (рис. 5).
Рисунок 5отделений, использующих CA125 среди женского населения (n = 751).
Среди мужского населения общая медицина и общая хирургия инициировали большинство запросов на CA125–16 тестов (33%) и 10 тестов (21%), соответственно.
ОБСУЖДЕНИЕ
Наш аудит предоставляет всесторонний обзор модели использования измерения CA125 в районной больнице общего профиля. Это показывает, что CA125 широко используется в качестве диагностического инструмента во всех медицинских областях для целого ряда признаков и симптомов и не ограничивается пациентами с классической картиной рака яичников. Использование CA125 в качестве онкомаркера для мониторинга ответа на лечение и рецидива заболевания у пациентов с известным раком яичников составляет лишь небольшую часть проведенных тестов.
Популяция пациентов, тестируемых на CA125, отражает возрастное распределение рака яичников, поскольку большинство пациентов были женщинами старше 50 лет. Шесть процентов населения составляли мужчины, и было трудно определить причину использования CA125 в этих случаях; однако 38 из этих 48 тестов были заказаны вместе с другими сывороточными онкомаркерами, и возможно, что CA125 был выполнен как часть общего скринингового теста на наличие злокачественного новообразования неизвестного происхождения.Следствием этого аудита является директива, информирующая клиницистов о том, что анализ CA125 используется в качестве маркера патологии яичников и что его использование у мужчин ограничено. Поле, требующее обязательного ответа да / нет на вопрос «пациентка — женщина?» был добавлен в систему ввода приказов компьютерной палаты, чтобы предотвратить несоответствующее тестирование.
«Следствием этого аудита является директива, информирующая врачей о том, что анализ CA125 используется в качестве маркера патологии яичников и что его использование у мужчин ограничено»
Признаки и симптомы рака яичников на ранних стадиях болезни расплывчаты и неспецифичны.Обоснование разделения пациентов на симптомы, наиболее часто связанные с распространенным раком яичников, а именно вздутие живота, асцит, образование в тазовой области или киста яичника 14 , и пациентов с более неспецифическими симптомами состояло в том, чтобы попытаться идентифицировать пациентов, которые были более вероятно, что у вас будет заболевание яичников. Из пациентов в исследуемой популяции, у которых был обнаружен рак яичников, у 36 из 44 было подозрение на категорию рака яичников, и поэтому подробный анамнез и обследование могли бы правильно выбрать их.
Было очевидно, что CA125 в основном использовался для исследования широкого спектра симптомов и часто не использовался в сочетании с визуализацией яичников. Нормальный результат, по-видимому, во многих случаях воспринимался как указание на отсутствие заболевания яичников, потому что у 27% обследованных пациенток СА125 находился в пределах нормы и не было визуализации яичников. Это может быть связано с низким уровнем подозрения на злокачественное новообразование яичников или с тем, что врач не полностью осознавал низкую чувствительность CA125.Тем не менее, Alcazar et al. и Troiano et al показали, что трансвагинальное ультразвуковое исследование имеет большую чувствительность и специфичность, чем CA125 для диагностики рака яичников, 15, 16 , и это подтверждает мнение о том, что CA125 должен быть второстепенным исследованием. для определения характера поражения яичников, выявленного при визуализации. 17 Если ограничить популяцию группой с высоким клиническим подозрением на рак яичников — например, сложное образование в тазовой области или асцит неизвестного происхождения — предположительно повысится как принятая в настоящее время чувствительность, так и специфичность CA125 в диагностике.Несколько пациенток в нашем исследовании были обследованы с использованием CA125 для выявления заболеваний, не связанных с яичниками, таких как эндометриоз, и в некоторых случаях для мониторинга лейкемии.
Количество и комбинация выполненных онкомаркеров не соответствовали шаблону и были результатом индивидуального выбора клинициста. Имеются доказательства того, что комбинация сывороточных онкомаркеров превосходит только СА125 в диагностике рака яичников 18– 20 ; однако в настоящее время нет единого мнения относительно оптимальной комбинации, и некоторые из онкомаркеров, используемых в этих исследованиях, недоступны в большинстве больничных лабораторий клинической химии.Низкий уровень использования АФП и ХГЧ среди населения младше 40 лет свидетельствует о недостаточной осведомленности о опухолях половых клеток яичников, которые чаще встречаются у молодых женщин. 21
Крупные многоцентровые скрининговые исследования рака яичников в настоящее время продолжаются, 22 и ожидаются результаты. У небольшой части нашей популяции (24 пациента) было измерено CA125 для скрининга, проводимого вне клинических испытаний и на индивидуальной клинической основе. Только 13 из этих пациенток прошли визуализацию яичников, часто выполняемую с переменными интервалами, и поэтому не соблюдали общепринятую тактику, включающую ежегодное измерение CA125 и трансвагинальное ультразвуковое сканирование яичников.
Отсутствие специфичности CA125 было подчеркнуто большим количеством ложноположительных результатов — 80% аномальных результатов в женской популяции, проходящей обследование на предмет подозрения на злокачественное новообразование / рак яичников, не были вызваны раком яичников. Как сообщалось ранее, наиболее частыми причинами повышения концентрации CA125 были злокачественные новообразования других локализаций, а также воспалительные или доброкачественные гинекологические заболевания. 23 Специфичность CA125 возрастала с повышением концентрации, хотя все еще было пять ложноположительных результатов с результатами более 1000 kU / литр, что является признанным явлением. 24– 26 Известно, что многочисленные заболевания связаны с ложноположительным результатом; однако многие клиницисты, похоже, не знали об этом, и многие пациенты прошли обследования, которые, возможно, не потребовались, что могло вызвать у пациентов значительное беспокойство и стресс.
Забрать домой сообщенияРезультаты также подтвердили высокий уровень ложноположительных результатов и низкую чувствительность и специфичность CA125 как маркера рака яичников
Чтобы сократить количество несоответствующих тестов, многие лаборатории ввели скрининг запросов на основе клинической информации, сопровождающей образец, что позволяет исключить явно ненужные тесты — например, тесты на пациентах мужского пола.Однако улучшенное образование — лучший способ борьбы с неправильным использованием CA125. Следовательно, сообщение с подробным описанием полезности измерения CA125 было добавлено в компьютерную систему ввода заказов в больнице Королевы. Многопрофильное обучение, включающее как врачей больниц, так и врачей первичной медико-санитарной помощи, может помочь клиницистам принимать информированные решения о том, поможет ли онкомаркер управлять пациентом и исследовать его, и, следовательно, уменьшит потребность отделения клинической химии в управлении службой.Рекомендации по использованию онкомаркеров, выпущенные Ассоциацией клинических биохимиков Ирландии, 27 , могут быть полезным инструментом в этом образовательном процессе.
Результаты этого аудита подтверждают высокий уровень ложноположительных результатов, а также низкую чувствительность и специфичность, связанные с CA125. Существует существенное несоответствующее использование CA125, что привело к результатам, которые бесполезны для клинициста, имеют финансовые последствия и увеличивают беспокойство пациентов и клиническую неопределенность.
ССЫЛКИ
- ↵
Bast RC , Feeney M, Lazarus H, et al. Реактивность моноклонального антитела с карциномой яичников человека. Дж. Клин Инвест, 1981; 68: 1331–7.
- ↵
Tingulstad S , Hagen B, Skjeldestad FE, et al. Оценка индекса риска злокачественных новообразований на основе сывороточного CA125, результатов УЗИ и статуса менопаузы в предоперационной диагностике новообразований в тазу.Br J Obstet Gynaecol 1996; 103: 826–31.
- ↵
Озгуроглу М , Turna H, Demir G, et al. Полезность эпителиального онкомаркера СА125 при неходжкинской лимфоме. Ам Дж. Клин Онкол 1999; 22: 615–18.
Levine CD , Patel UJ, Ghanekar D, et al. Доброкачественные экстраовариальные модели рака яичников. Отличие от визуализационных исследований. Clin Imaging 1997; 21: 350–8.
- ↵
Meden H , Fattahi-Meibodi A. CA125 в доброкачественных гинекологических условиях. Int J Biol Markers 1998; 13: 231–7.
- ↵
Gaspar MJ , Diez H, Rodriguez A, et al. Клиническая ценность CEA и CA125 в отношении рецидивов и метастазов при операбельном немелкоклеточном раке легкого. Anticancer Res 2003; 23: 3427–32.
Krishnan STM , Philipose Z, Rayman G.Гипотиреоз, имитирующий внутрибрюшную злокачественную опухоль. BMJ2002; 325: 946-7.
- ↵
Буама П. . Доброкачественные состояния, связанные с повышенной концентрацией СА125 в сыворотке. J Surg Oncol2000; 75: 264–5.
- ↵
Jhang H , Chuang L, Visintainer P, et al. Уровни CA125 в предоперационной оценке распространенного рака матки. Am J Obstet Gynecol 2003; 188: 1195–7.
Преданик M . Дифференциация трубного аборта от жизнеспособной внематочной беременности с помощью определения сывороточного CA125 и бета-хорионического гонадотропина человека. Fertil Steril 2000; 73: 522–5.
Miralles C , Orea M, Espana P, et al. Раковый антиген 125, связанный с множественными доброкачественными и злокачественными патологиями. Энн Сург Онкол 2003; 10: 150–4.
Yilmaz A , Ece F, Bayramgurler B, et al. Значение CA125 в оценке активности туберкулеза. Респир Мед 2001; 95: 666–9.
- ↵
Petaja J , Pitkanen S, Vettenranta K, et al. Сывороточный онкомаркер CA125 является ранним и чувствительным индикатором веноокклюзионной болезни у детей, перенесших трансплантацию костного мозга. Clin Cancer Res 2000; 6: 531–5.
- ↵
Шен-Гюнтер Дж. , Маннел РС.Асцит как предиктор злокачественного новообразования яичников. Геколь Онкол, 2002; 87: 77–83.
- ↵
Alcazar JL , Errasti T, Zornoza A, et al. Трансвагинальное цветное допплерографическое исследование и CA125 при подозрительных образованиях придатков. Int J Gynaecol Obstet 1999; 66: 255–61.
- ↵
Troiano RN , Quedens-Case C, Taylor KJ. Корреляция результатов трансвагинальной сонографии с уровнями СА125 в сыворотке.AJR Am J Roentgenol1997; 168: 1587–90.
- ↵
Растин Г . Клиническое значение онкомаркеров в лечении рака яичников. Энн Клин Биохим 1996; 33: 284–9.
- ↵
Zhang Z , Barnhill SD, Zhang H, et al. Комбинация нескольких сывороточных маркеров с использованием искусственной нейронной сети для повышения специфичности отличия злокачественных образований от доброкачественных образований таза.Gynecol Oncol 1999; 73: 56–61.
Woolas RP , Conaway MR, Xu F, et al. Комбинации нескольких сывороточных маркеров превосходят индивидуальные тесты для отличия злокачественных образований от доброкачественных образований таза. Gynecol Oncol 1995; 59: 111–16.
- ↵
Schutter EM , Davelaar EM, van Kamp GJ, et al. Дифференциально-диагностический потенциал панели онкомаркеров (антигены C125, CA15-3 и CA72-4) у пациентов с массой малого таза.Am J Obstet Gynecol 2002; 187: 385–92.
- ↵
Kerbrat P , Lhommé C, Fervers B, et al. Стандарты, варианты и рекомендации: рак яичников. Электронный онкологический журнал 2001; 1: 32–42.
- ↵
Menon U , Jacobs IL. Скрининг на рак яичников среди населения в целом. Ультразвуковой акушерский гинекол 2000; 15: 350–3.
- ↵
Шовалл К. , Нильссон Б., Эйнхорн Н.Значение повышения уровня СА125 в сыворотке крови при злокачественных и незлокачественных заболеваниях. Гинекол Онкол, 2002; 85: 175–8.


 Повторное обнаружение РЭА в крови после операции по удалению опухоли говорит о метастазировании.
Повторное обнаружение РЭА в крови после операции по удалению опухоли говорит о метастазировании.