Чесотка
Чесотка человека – это паразитарная инвазия, вызванная Sarcoptes scabiei var hominis. Микроскопический клещ проникает в кожу и откладывает яйца, в конечном итоге вызывая иммунную реакцию у хозяина, которая приводит к сильному зуду и сыпи. Чесотка может усугубляться бактериальными инфекциями, ведущими к развитию кожных язв, которые, в свою очередь, могут приводить к развитию более тяжелых осложнений, таких как сепсис, болезни сердца и хронические заболевания почек. В 2017 г. чесотка и заболевания, вызванные другими эктопаразитами, были причислены к забытым тропическим болезням (ЗТБ) в ответ на просьбы государств-членов и рекомендации Стратегической и технической консультативной группы ВОЗ по ЗТБ.
Масштабы проблемы
Чесотка является одним из наиболее распространенных кожных заболеваний, и в развивающихся странах на нее приходится значительная доля кожных болезней. Предположительно, более 200 миллионов человек в мире заражены чесоткой в любой момент времени, но для более точной оценки этого бремени необходимы дополнительные усилия. По данным из последних публикаций о чесотке, уровни ее распространенности варьируются от 0,2% до 71%.
По данным из последних публикаций о чесотке, уровни ее распространенности варьируются от 0,2% до 71%.
Чесотка является эндемической болезнью во многих тропических районах с ограниченными ресурсами, где средние уровни ее распространенности среди детей составляют предположительно 5-10%. Широко распространены повторные заражения. Тяжелое бремя чесотки и ее осложнений сопряжено с большими расходами для систем здравоохранения. В странах с высоким уровнем дохода происходят отдельные случаи заболевания, однако вспышки чесотки в медицинских учреждениях и уязвимых сообществах приводят к значительным экономическим издержкам для национальных служб здравоохранения.
Чесотка распространена во всем мире, однако особо подвержены заражению чесоткой и развитию вторичных осложнений наиболее уязвимые группы населения – дети раннего возраста и пожилые люди в сообществах с ограниченными ресурсами. Самые высокие показатели заражения наблюдаются в странах с жарким тропическим климатом, особенно в тех сообществах, где люди живут в условиях скученности и нищеты, а доступ к лечению ограничен.
Симптомы
Чесоточные клещи проникают в верхний слой кожи, где взрослые самки откладывают яйца. Через 3-4 дня из яиц появляются личинки, которые за 1-2 недели развиваются во взрослых клещей. Через 4-6 недель у пациента развивается аллергическая реакция на белки и фекалии клещей в чесоточных ходах, что вызывает сильный зуд и сыпь. Большинство людей инфицированы 10-15 клещами.
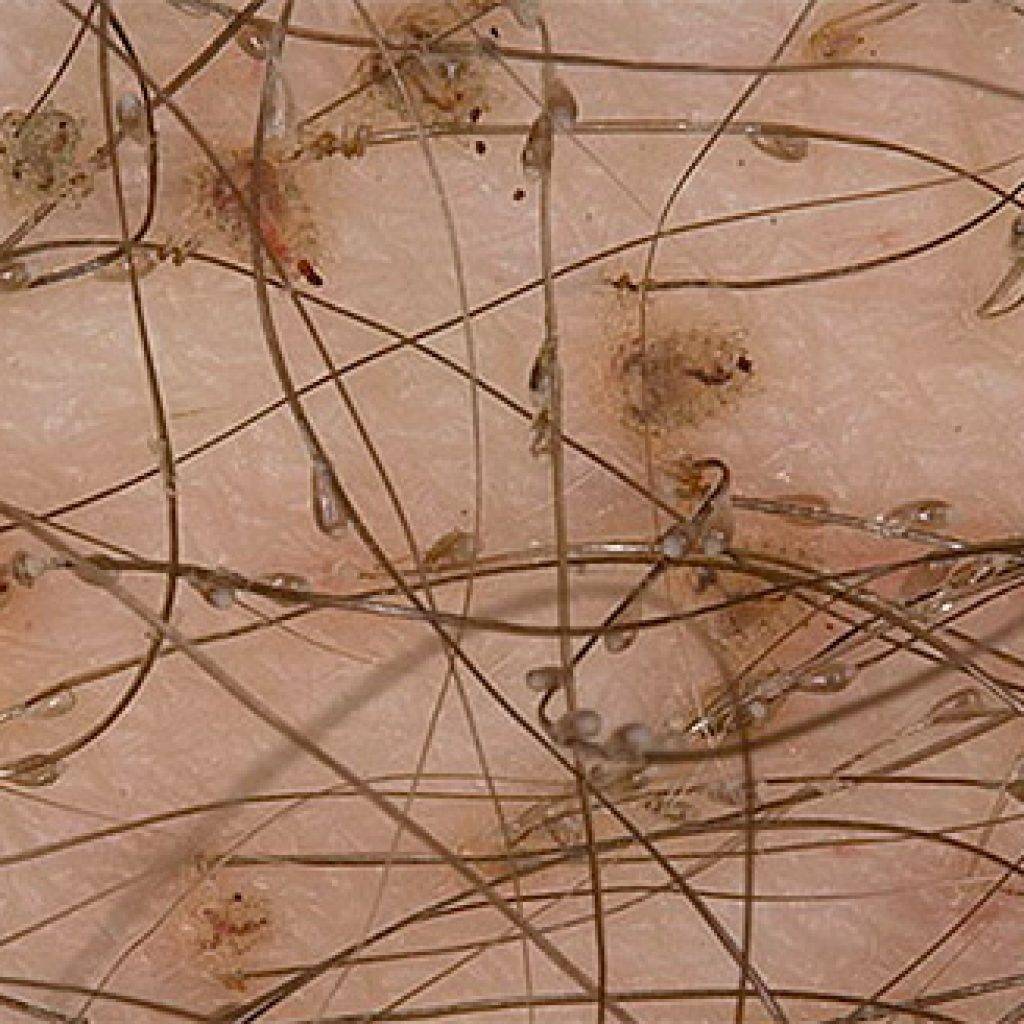
Пациенты, как правило, испытывают сильный зуд, а в межпальцевых промежутках, на запястьях, на верхних и нижних конечностях и в области поясницы появляются клещевые ходы и везикулы. У детей грудного и раннего возраста сыпь может распространяться более широко и охватывать ладони, подошвы ног, щиколотки, а иногда и волосистую часть кожи головы. Воспалительные чесоточные узелки могут обнаруживаться у взрослых мужчин на пенисе и мошонке, а у женщин – в области молочных желез. В связи с тем, что симптомы развиваются через какое-то время после первоначального инфицирования, чесоточные ходы могут выявляться у лиц, имевших тесные контакты с инфицированным человеком, у которых еще не появился зуд.
У людей с корковой чесоткой на коже появляются толстые, отшелушивающиеся корки, которые могут распространяться более широко, в том числе и на лице.
У людей с ослабленным иммунитетом, включая людей с ВИЧ/СПИДом, может развиваться особая форма заболевания, называемая корковой (норвежской) чесоткой. Корковая чесотка представляет собой гиперзаражение, при котором число клещей достигает нескольких тысяч и даже миллионов. Клещи широко распространяются и приводят к образованию корок, но часто не вызывают значительного зуда. При отсутствии лечения для этого заболевания характерна высокая смертность от вторичного сепсиса.
Воздействие клещей на иммунитет, а также прямые последствия расчесывания могут приводить к бактериальному заражению кожи, что приводит к развитию импетиго (кожных язв), особенно в тропических условиях. Импетиго может осложняться более глубокими кожными инфекциями, такими как абсцессы, или тяжелыми инвазивными болезнями, включая сепсис. В тропических условиях кожная инфекция, связанная с чесоткой, является распространенным фактором риска развития заболеваний почек и, возможно, ревматической болезни сердца. Признаки острого поражения почек можно обнаружить у 10% зараженных чесоткой детей в районах с ограниченными ресурсами, и во многих случаях эти симптомы сохраняются в течение многих лет после заражения, что приводит к необратимому повреждению почек.
Признаки острого поражения почек можно обнаружить у 10% зараженных чесоткой детей в районах с ограниченными ресурсами, и во многих случаях эти симптомы сохраняются в течение многих лет после заражения, что приводит к необратимому повреждению почек.
Передача инфекции
Чесотка, как правило, передается от человека к человеку при тесном кожном контакте (например, при совместном проживании) с зараженным человеком. Риск передачи зависит от уровня заражения, причем наиболее высокий риск представляют контакты с лицами, страдающими корковой чесоткой. Вероятность передачи инфекции в результате контакта с зараженными предметами личного обихода (например, с одеждой и постельным бельем) в случае обычной чесотки низкая, а в случае корковой чесотки может быть высокой. С учетом бессимптомного периода заражения передача инфекции может произойти до появления симптомов у первоначально зараженного человека.
Лечение
Первичное лечение зараженных лиц включает использование скабицидов для наружного применения, таких как 5%-ный перметрин, 0,5%-ный малатион на водной основе, 10-25%-ная эмульсия бензилбензоата или 5-10%-ная серная мазь. Пероральный ивермектин также высокоэффективен, и его применение одобрено в ряде стран. Безопасность ивермектина для беременных женщин или детей с массой тела до 15 кг не установлена, поэтому ивермектин не должен применяться в этих группах населения до получения дополнительных данных о безопасности. При эффективном лечении в течение 1-2 недель зуд обычно усиливается, и лиц, проходящих лечение, следует информировать об этом.
Пероральный ивермектин также высокоэффективен, и его применение одобрено в ряде стран. Безопасность ивермектина для беременных женщин или детей с массой тела до 15 кг не установлена, поэтому ивермектин не должен применяться в этих группах населения до получения дополнительных данных о безопасности. При эффективном лечении в течение 1-2 недель зуд обычно усиливается, и лиц, проходящих лечение, следует информировать об этом.
С учетом того, что на ранней стадии нового заражения симптомы могут отсутствовать и поскольку препараты против чесотки не убивают яйца паразита, наилучшие результаты достигаются путем одновременного лечения всех членов семьи и повторного лечения в сроки, соответствующие выбранному лекарственному препарату.
Деятельность ВОЗ
ВОЗ сотрудничает с государствами-членами и партнерами в разработке стратегий борьбы с чесоткой и планов реагирования на вспышки этой болезни. ВОЗ признает, что необходимо более четко определить бремя болезни и риск долговременных осложнений и что стратегии борьбы с чесоткой должны быть увязаны с проводимыми мероприятиями, с тем чтобы содействовать их быстрому и экономически эффективному осуществлению.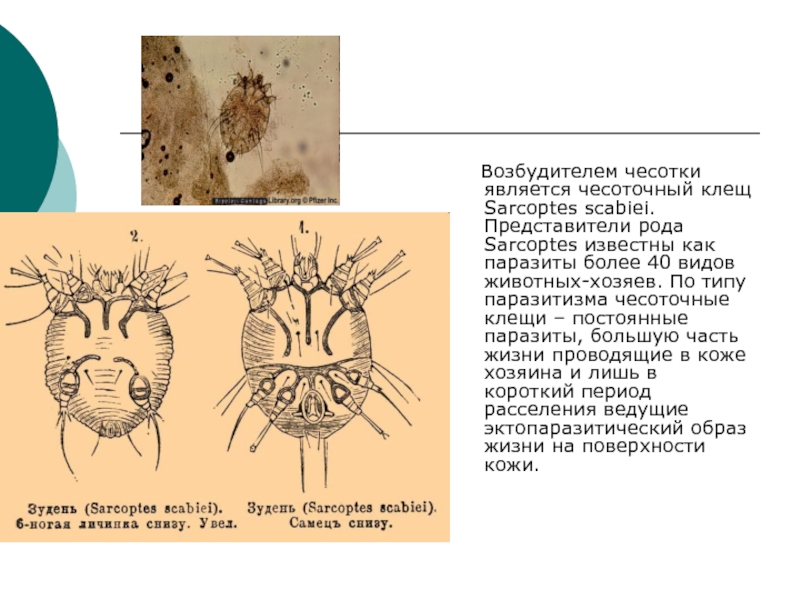 ВОЗ работает над тем, чтобы ивермектин был включен в Примерный перечень основных лекарственных средств ВОЗ при его следующем обновлении. Кроме того, ВОЗ принимает меры для обеспечения того, чтобы качественные и эффективные лекарственные препараты были доступны для нуждающихся в них стран.
ВОЗ работает над тем, чтобы ивермектин был включен в Примерный перечень основных лекарственных средств ВОЗ при его следующем обновлении. Кроме того, ВОЗ принимает меры для обеспечения того, чтобы качественные и эффективные лекарственные препараты были доступны для нуждающихся в них стран.
Чесотка — КВД №2
Чесотка — заразное паразитарное заболевание кожи, вызываемое чесоточным клещом
Sarcoptes scabiei, сопровождающееся зудом, усиливающимся в вечернее и ночное время, и
папулезновезикулезными высыпаниями.
В настоящее время чесотка остается одним из самых распространенных паразитарных
дерматозов и в нашей стране.
Увеличение числа больных чесоткой обычно сопровождает войны, стихийные бедствия,
социальные потрясения, что обусловлено миграцией населения, экономическим спадом,
ухудшением социальнобытовых условий.
Как говорилось выше, возбудителем чесотки является чесоточный клещ — Sarcoptes scabiei.
Этот вид относится к семейству Sarcoptidae, группе Acaridiae, подотряду Sarcoptiphormes,
отряду акариформных клещей Acariphormes. Представители рода Sarcoptes в настоящее
время известны как паразиты более 40 видов животныххозяев, принадлежащих к 17
семействам 7 отрядов млекопитающих.
Морфологический облик чесоточных клещей семейства Sarcoptidae чрезвычайно
своеобразен и обусловлен глубокими приспособлениями к внутрикожному паразитизму.
Cтроение чесоточного зудня, как и большинства клещей, характеризуется строгим
постоянством микроструктур наружного скелета, что связано с их микроскопическими
размерами.
Самка чесоточного клеща внешне напоминает черепаху. Ее размер 0,25–0,35 мм.
Приспособления к внутрикожному паразитизму представлены множественными
щетинками, треугольными выростами кутикулы на спинной поверхности, шипами на всех
лапках, служащими упорами при прогрызании хода, хелицерами грызущего типа,
длинными упругими щетинками на лапках задних пар ног, для выдерживания направления
хода только вперед.
присоски на передних ногах, восковидные щетинки на теле и конечностях, создающие
вокруг клеща обширную механорецепторную сферу и позволяющие ориентироваться на
ощупь без глаз. Скорость движения самки в ходе составляет 0,5–2,5 мм/сут, а на
поверхности кожи 2–3 см/мин. Для чесоточных клещей характерен половой диморфизм.
Основная функция самцов — оплодотворение. Они значительно меньше по размеру —
0,15–0,2 мм, имеют плотные щетинки на теле для защиты от механического воздействия и
присоски также на IV паре ног для прикрепления к самке при спаривании. Соотношение
самок и самцов у чесоточных клещей составляет 2:1.
Жизненный цикл чесоточного клеща отчетливо делится на две части: кратковременную
накожную и длительную внутрикожную. Внутрикожная представлена двумя топически
разобщенными периодами: репродуктивными и метаморфическим. Репродуктивный
осуществляется самкой в прогрызаемом ею чесоточном ходе, где она откладывает яйца.
Вылупляющиеся личинки выходят из ходов на поверхность кожи через отверстия,
проделанные самкой над местом каждой кладки, расселяются на ней и внедряются в
волосяные фолликулы и под чешуйки эпидермиса. Здесь протекает их метаморфоз (линька):
через стадию прото и телеонимфы образуются новые особи (самки и самцы). Самки и
самцы нового поколения выходят на поверхность кожи, где происходит их спаривание.
Дочерние самки мигрируют на кисти, запястья, стопы, внедряются в кожу и сразу начинают
прокладывать ходы и класть яйца. В редких случаях внедрение самок возможно в других
участках кожного покрова (ягодицы, аксиллярные области, живот и др.) за счет
механического прижатия. Клинически это соответствует скабиозной лимфоплазии кожи.
Только самки и личинки являются инвазионными стадиями и участвуют в заражении. При
комнатной температуре и относительной влажности не менее 60% самок сохраняют
подвижность 1–6 суток. Даже при 100% влажности самки в среднем выдерживают до 3
Даже при 100% влажности самки в среднем выдерживают до 3
суток, личинки — до 2 суток.
Для чесоточных клещей характерен строгий суточный ритм активности. Днем самка
находится в состоянии покоя. Вечером и в первую половину ночи она прогрызает одно или
два яйцевых колена под углом к основному направлению хода, в каждом из которых
откладывает по яйцу. Перед откладкой яйца она углубляет дно хода, а в крыше проделывает
выходное отверстие для личинок. Вторую половину ночи самка грызет ход по прямой,
интенсивно питаясь, днем — останавливается и замирает. Суточная программа выполняется
всеми самками синхронно. В результате чесоточный ход на коже больного имеет извитую
форму и состоит из отрезков хода, называемых суточным элементом хода. Задняя часть
хода постепенно отшелушивается, и при клиническом осмотре больного он единовременно
состоит из 4–7 суточных элементов и имеет постоянную длину 5–7 мм. В течение жизни
самка проходит в эпидермисе 3–6 см, выявленный суточный ритм активности имеет
большое практическое значение.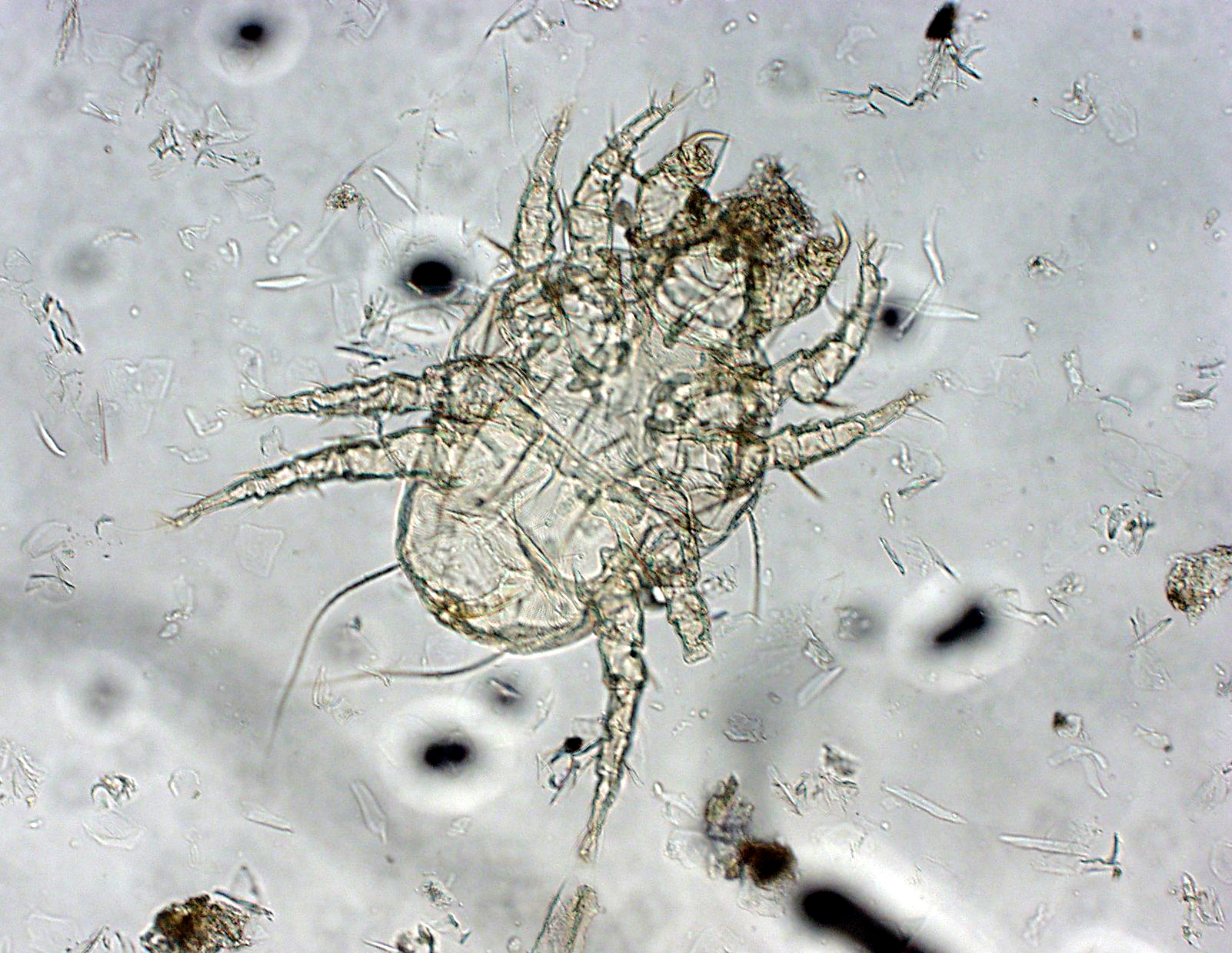 Он объясняет усиление зуда вечером, преобладание
Он объясняет усиление зуда вечером, преобладание
прямого пути заражения при контакте в постели в вечернее и ночное время, эффективность
назначения противочесоточных препаратов на ночь.
Клиническая картина
Клиника чесотки обусловлена особенностями возбудителя и реакцией организма хозяина на
его внедрение.
Инкубационный период при чесотке имеет разную продолжительность и зависит от того,
попала на кожу взрослая самка или личинка. В первом случае он предельно короток, а во
втором составляет 2 недели. Зуд, как основной симптом чесотки, появляется в сроки,
которые колеблются от 14 дней до 6 недель при первичной инфекции и могут быть
предельно коротким, ограничиваясь несколькими днями при реинфекции. Также показано,
что реинфекция в то же время может происходить более трудно у уже
сенсибилизированных лиц, а количество обнаруживаемых чесоточных клещей у таких
пациентов часто оказывается минимальным [7, 9].
Типичная форма чесотки характеризуются наличием кожного зуда, проявляющегося в
наибольшей степени вечером и во время сна. Однако зуд может быть и постоянным. Он
может локализоваться на отдельных участках кожи или распространяться по всему телу, за
исключением кожи лица и волосистой части головы. Чрезвычайно важным признаком
является наличие зуда у членов семьи или коллектива.
При обследовании выявляются специфические высыпания. Основными клиническими
симптомами чесотки являются чесоточные ходы, полиморфные высыпания вне ходов,
характерные места высыпаний, а также симптомы, названные в честь авторов Арди
(наличие пустул и гнойных корочек на логтях и в их окружности), Горчакова (наличие там
же кровянистых корочек), Михаэлиса (наличие кровянистых корочек и импетигинозных
высыпаний в межъягодичной складке с переходом на крестец), Сезари (обнаружение
чесоточных ходов в виде легкого возвышения при пальпации).
Характерными местами локализации высыпаний является преимущественно сгибательная
поверхность суставов (лучезапястных и локтевых), а также переднебоковая поверхностьживота, поясницы, ягодицы, область гениталий, при этом они отсутствуют на верхней
половине спины. Чесоточные ходы и высыпания хорошо выражены в межпальцевых и
подкрыльцовых складках, на околососковых кружках груди женщин, в области пупка.
Высыпания представлены парными папулами и везикулами, чесоточными ходами,
экзематозными псевдовезикулами (жемчужные везикулы) на коже боковых поверхностей
пальцев и ладонях; скабиозными язвами, с корочками на поверхности; а также скабиозными
узелками.
Атипичные формы чесотки, нередко встречающиеся в последние годы, нам кажется
целесообразным классифицировать и представить следующим образом:
чесотка без поражения кожного покрова;
уртикарная чесотка;
чесотка на фоне кортикостероидной терапии;
узелковая (с постскабиозными узелками) чесотка;
экзематизированная чесотка;
чесотка, осложненная пиодермией;
норвежская чесотка;
грудничковая и детская чесотка.
Первые две формы обусловлены преимущественно аллергическими реакциями.
Чесотка без поражения кожного покрова может представлять собой начинающие формы
заболевания у людей, соблюдающих нормы гигиены тела, но чаще проявляется как
аллергическая реакция на антигены клеща в период заболевания или после его лечения. Эта
форма заболевания чаще выявляется при активном осмотре лиц, бывших в контакте с
больным чесоткой.
Уртикарная чесотка представлена мелкими волдырями, обусловленными сенсибилизацией
как к клещам, так и к продуктам их жизнедеятельности. Они возникают чаще на передней
поверхности туловища, бедрах, ягодицах и предплечьях.
Чесотка на фоне местной кортикостероидной терапии, называемая также скрытой чесоткой,
в результате подавления иммунных реакций кожи ведет к потере специфических симптомов
чесотки. Заболевание приобретает папулосквамозный, папуловезикулезный, а иногда даже
гиперкератотический характер высыпаний.
Узелковая чесотка (скабиозная лимфоплазия) характеризуется появлением зудящих узелков
красного, розового или коричневого цвета. На поверхности новых узелков можно
обнаружить чесоточные ходы. Характерная локализация: половой член, мошонка,
подкрыльцовые и межъягодичная складки, околососковые кружки. Узелки обычно
немногочисленны. Иногда они являются единственным диагностическим признаком
чесотки [2, 4].
Экзематизированная чесотка возникает, как правило, у людей с аллергической
предрасположенностью. На местах расчесов могут появляться очаги лихенификации.
всегда может быть заподозрен. Высыпания проявляются на кистях, в подмышечных
впадинах, голенях, кистях. В запущенных случаях высыпания могут приобретать
диссеминированный характер, вплоть до развития эритродермии.
У лиц со сниженной сопротивляемостью организма к экзематизированным поражениям на
местах расчесов может присоединяться вторичная бактериальная инфекция в виде импетиго
или эктим, могут возникать стафилококковые фолликулиты, фурункулы и абсцессы.
Норвежская чесотка (крустозная, корковая) в начальных стадиях представлена как обычная
чесотка или маскируется под атопический дерматит, псориаз, себорейный дерматит.
Характерны ороговение, образование чешуек или толстых корок. При выраженном
иммунодефиците процесс может носить генерализованный характер, при неврологических
заболеваниях — проявляться ограниченной областью нарушения чувствительности.
Грудничковая и детская чесотка характеризуется высыпаниями, напоминающими
крапивницу или детскую почесуху в виде большого количества расчесанных и покрытых
корочкой волдырей с преимущественной локализацией в промежности на мошонке, в
подкрыльцовых складках. Характерные чесоточные ходы можно обнаружить на подошвах.
Диагностика
Диагностика чесотки, помимо клинических данных, основывается на микроскопическом
подтверждении диагноза. Однако эта процедура требует значительного навыка, опытного
микробиолога и при некоторых клинических формах невыполнима. Минимальные
Минимальные
клинические проявления чесотки также затрудняют получение достаточного
биологического материала для исследования. Методика имеет преимущества в
специализированных учреждениях. Существует несколько методик лабораторной
диагностики чесотки: извлечение клеща иглой, метод тонких срезов, соскобы, щелочное
препарирование кожи.
Чесотка — заразное паразитарное заболевание кожи, вызываемое чесоточным клещом Sarcoptes scabiei, сопровождающееся зудом, усиливающимся в вечернее и ночное время, и папулезно-везикулезными высыпаниями.
В настоящее время чесотка остается одним из самых распространенных паразитарных дерматозов и в нашей стране.
Увеличение числа больных чесоткой обычно сопровождает войны, стихийные бедствия, социальные потрясения, что обусловлено миграцией населения, экономическим спадом, ухудшением социально-бытовых условий.
Как говорилось выше, возбудителем чесотки является чесоточный клещ — Sarcoptes scabiei. Этот вид относится к семейству Sarcoptidae, группе Acaridiae, подотряду Sarcoptiphormes, отряду акариформных клещей Acariphormes. Представители рода Sarcoptes в настоящее время известны как паразиты более 40 видов животных-хозяев, принадлежащих к 17 семействам 7 отрядов млекопитающих.
Этот вид относится к семейству Sarcoptidae, группе Acaridiae, подотряду Sarcoptiphormes, отряду акариформных клещей Acariphormes. Представители рода Sarcoptes в настоящее время известны как паразиты более 40 видов животных-хозяев, принадлежащих к 17 семействам 7 отрядов млекопитающих.
Морфологический облик чесоточных клещей семейства Sarcoptidae чрезвычайно своеобразен и обусловлен глубокими приспособлениями к внутрикожному паразитизму. Cтроение чесоточного зудня, как и большинства клещей, характеризуется строгим постоянством микроструктур наружного скелета, что связано с их микроскопическими размерами.
Самка чесоточного клеща внешне напоминает черепаху. Ее размер 0,25–0,35 мм. Приспособления к внутрикожному паразитизму представлены множественными щетинками, треугольными выростами кутикулы на спинной поверхности, шипами на всех лапках, служащими упорами при прогрызании хода, хелицерами грызущего типа, длинными упругими щетинками на лапках задних пар ног, для выдерживания направления хода только вперед. Приспособления для эктопаразитизма — липкие пневматические присоски на передних ногах, восковидные щетинки на теле и конечностях, создающие вокруг клеща обширную механорецепторную сферу и позволяющие ориентироваться на ощупь без глаз. Скорость движения самки в ходе составляет 0,5–2,5 мм/сут, а на поверхности кожи 2–3 см/мин. Для чесоточных клещей характерен половой диморфизм. Основная функция самцов — оплодотворение. Они значительно меньше по размеру — 0,15–0,2 мм, имеют плотные щетинки на теле для защиты от механического воздействия и присоски также на IV паре ног для прикрепления к самке при спаривании. Соотношение самок и самцов у чесоточных клещей составляет 2:1.
Приспособления для эктопаразитизма — липкие пневматические присоски на передних ногах, восковидные щетинки на теле и конечностях, создающие вокруг клеща обширную механорецепторную сферу и позволяющие ориентироваться на ощупь без глаз. Скорость движения самки в ходе составляет 0,5–2,5 мм/сут, а на поверхности кожи 2–3 см/мин. Для чесоточных клещей характерен половой диморфизм. Основная функция самцов — оплодотворение. Они значительно меньше по размеру — 0,15–0,2 мм, имеют плотные щетинки на теле для защиты от механического воздействия и присоски также на IV паре ног для прикрепления к самке при спаривании. Соотношение самок и самцов у чесоточных клещей составляет 2:1.
Жизненный цикл чесоточного клеща отчетливо делится на две части: кратковременную накожную и длительную внутрикожную. Внутрикожная представлена двумя топически разобщенными периодами: репродуктивными и метаморфическим. Репродуктивный осуществляется самкой в прогрызаемом ею чесоточном ходе, где она откладывает яйца. Вылупляющиеся личинки выходят из ходов на поверхность кожи через отверстия, проделанные самкой над местом каждой кладки, расселяются на ней и внедряются в волосяные фолликулы и под чешуйки эпидермиса. Здесь протекает их метаморфоз (линька): через стадию прото- и телеонимфы образуются новые особи (самки и самцы). Самки и самцы нового поколения выходят на поверхность кожи, где происходит их спаривание. Дочерние самки мигрируют на кисти, запястья, стопы, внедряются в кожу и сразу начинают прокладывать ходы и класть яйца. В редких случаях внедрение самок возможно в других участках кожного покрова (ягодицы, аксиллярные области, живот и др.) за счет механического прижатия. Клинически это соответствует скабиозной лимфоплазии кожи. Только самки и личинки являются инвазионными стадиями и участвуют в заражении. При комнатной температуре и относительной влажности не менее 60% самок сохраняют подвижность 1–6 суток. Даже при 100% влажности самки в среднем выдерживают до 3 суток, личинки — до 2 суток.
Здесь протекает их метаморфоз (линька): через стадию прото- и телеонимфы образуются новые особи (самки и самцы). Самки и самцы нового поколения выходят на поверхность кожи, где происходит их спаривание. Дочерние самки мигрируют на кисти, запястья, стопы, внедряются в кожу и сразу начинают прокладывать ходы и класть яйца. В редких случаях внедрение самок возможно в других участках кожного покрова (ягодицы, аксиллярные области, живот и др.) за счет механического прижатия. Клинически это соответствует скабиозной лимфоплазии кожи. Только самки и личинки являются инвазионными стадиями и участвуют в заражении. При комнатной температуре и относительной влажности не менее 60% самок сохраняют подвижность 1–6 суток. Даже при 100% влажности самки в среднем выдерживают до 3 суток, личинки — до 2 суток.
Для чесоточных клещей характерен строгий суточный ритм активности. Днем самка находится в состоянии покоя. Вечером и в первую половину ночи она прогрызает одно или два яйцевых колена под углом к основному направлению хода, в каждом из которых откладывает по яйцу. Перед откладкой яйца она углубляет дно хода, а в крыше проделывает выходное отверстие для личинок. Вторую половину ночи самка грызет ход по прямой, интенсивно питаясь, днем — останавливается и замирает. Суточная программа выполняется всеми самками синхронно. В результате чесоточный ход на коже больного имеет извитую форму и состоит из отрезков хода, называемых суточным элементом хода. Задняя часть хода постепенно отшелушивается, и при клиническом осмотре больного он единовременно состоит из 4–7 суточных элементов и имеет постоянную длину 5–7 мм. В течение жизни самка проходит в эпидермисе 3–6 см, выявленный суточный ритм активности имеет большое практическое значение. Он объясняет усиление зуда вечером, преобладание прямого пути заражения при контакте в постели в вечернее и ночное время, эффективность назначения противочесоточных препаратов на ночь.
Перед откладкой яйца она углубляет дно хода, а в крыше проделывает выходное отверстие для личинок. Вторую половину ночи самка грызет ход по прямой, интенсивно питаясь, днем — останавливается и замирает. Суточная программа выполняется всеми самками синхронно. В результате чесоточный ход на коже больного имеет извитую форму и состоит из отрезков хода, называемых суточным элементом хода. Задняя часть хода постепенно отшелушивается, и при клиническом осмотре больного он единовременно состоит из 4–7 суточных элементов и имеет постоянную длину 5–7 мм. В течение жизни самка проходит в эпидермисе 3–6 см, выявленный суточный ритм активности имеет большое практическое значение. Он объясняет усиление зуда вечером, преобладание прямого пути заражения при контакте в постели в вечернее и ночное время, эффективность назначения противочесоточных препаратов на ночь.
Клиническая картина
Клиника чесотки обусловлена особенностями возбудителя и реакцией организма хозяина на его внедрение.
Инкубационный период при чесотке имеет разную продолжительность и зависит от того, попала на кожу взрослая самка или личинка. В первом случае он предельно короток, а во втором составляет 2 недели. Зуд, как основной симптом чесотки, появляется в сроки, которые колеблются от 14 дней до 6 недель при первичной инфекции и могут быть предельно коротким, ограничиваясь несколькими днями при реинфекции. Также показано, что реинфекция в то же время может происходить более трудно у уже сенсибилизированных лиц, а количество обнаруживаемых чесоточных клещей у таких пациентов часто оказывается минимальным [7, 9].
В первом случае он предельно короток, а во втором составляет 2 недели. Зуд, как основной симптом чесотки, появляется в сроки, которые колеблются от 14 дней до 6 недель при первичной инфекции и могут быть предельно коротким, ограничиваясь несколькими днями при реинфекции. Также показано, что реинфекция в то же время может происходить более трудно у уже сенсибилизированных лиц, а количество обнаруживаемых чесоточных клещей у таких пациентов часто оказывается минимальным [7, 9].
Типичная форма чесотки характеризуются наличием кожного зуда, проявляющегося в наибольшей степени вечером и во время сна. Однако зуд может быть и постоянным. Он может локализоваться на отдельных участках кожи или распространяться по всему телу, за исключением кожи лица и волосистой части головы. Чрезвычайно важным признаком является наличие зуда у членов семьи или коллектива.
При обследовании выявляются специфические высыпания. Основными клиническими симптомами чесотки являются чесоточные ходы, полиморфные высыпания вне ходов, характерные места высыпаний, а также симптомы, названные в честь авторов Арди (наличие пустул и гнойных корочек на логтях и в их окружности), Горчакова (наличие там же кровянистых корочек), Михаэлиса (наличие кровянистых корочек и импетигинозных высыпаний в межъягодичной складке с переходом на крестец), Сезари (обнаружение чесоточных ходов в виде легкого возвышения при пальпации).
Характерными местами локализации высыпаний является преимущественно сгибательная поверхность суставов (лучезапястных и локтевых), а также переднебоковая поверхность живота, поясницы, ягодицы, область гениталий, при этом они отсутствуют на верхней половине спины. Чесоточные ходы и высыпания хорошо выражены в межпальцевых и подкрыльцовых складках, на околососковых кружках груди женщин, в области пупка. Высыпания представлены парными папулами и везикулами, чесоточными ходами, экзематозными псевдовезикулами (жемчужные везикулы) на коже боковых поверхностей пальцев и ладонях; скабиозными язвами, с корочками на поверхности; а также скабиозными узелками.
Атипичные формы чесотки, нередко встречающиеся в последние годы, нам кажется целесообразным классифицировать и представить следующим образом:
· чесотка без поражения кожного покрова;
· уртикарная чесотка;
· чесотка на фоне кортикостероидной терапии;
· узелковая (с постскабиозными узелками) чесотка;
· экзематизированная чесотка;
· чесотка, осложненная пиодермией;
· норвежская чесотка;
· грудничковая и детская чесотка.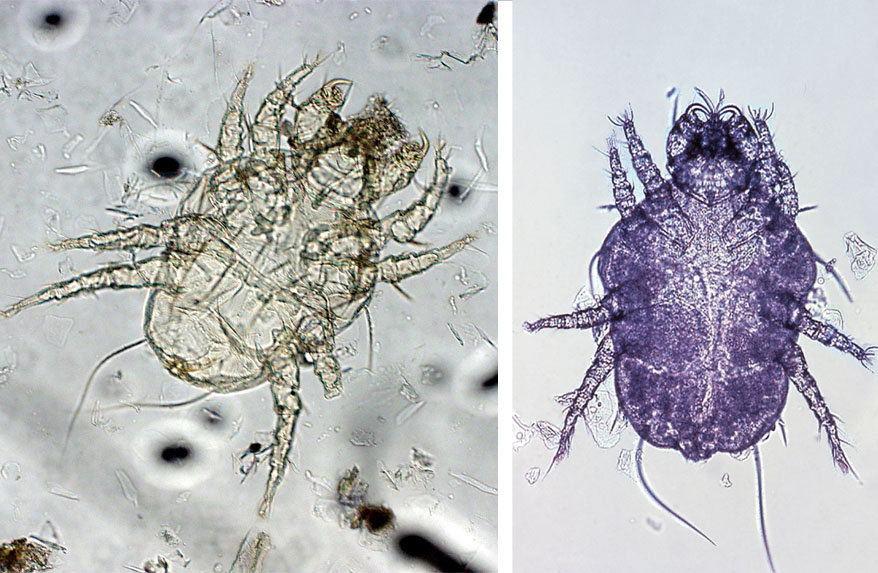
Первые две формы обусловлены преимущественно аллергическими реакциями.
Чесотка без поражения кожного покрова может представлять собой начинающие формы заболевания у людей, соблюдающих нормы гигиены тела, но чаще проявляется как аллергическая реакция на антигены клеща в период заболевания или после его лечения. Эта форма заболевания чаще выявляется при активном осмотре лиц, бывших в контакте с больным чесоткой.
Уртикарная чесотка представлена мелкими волдырями, обусловленными сенсибилизацией как к клещам, так и к продуктам их жизнедеятельности. Они возникают чаще на передней поверхности туловища, бедрах, ягодицах и предплечьях.
Чесотка на фоне местной кортикостероидной терапии, называемая также скрытой чесоткой, в результате подавления иммунных реакций кожи ведет к потере специфических симптомов чесотки. Заболевание приобретает папулосквамозный, папуловезикулезный, а иногда даже гиперкератотический характер высыпаний.
Узелковая чесотка (скабиозная лимфоплазия) характеризуется появлением зудящих узелков красного, розового или коричневого цвета.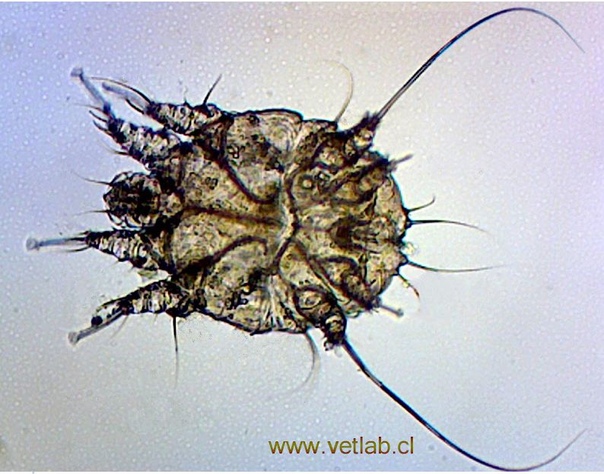 На поверхности новых узелков можно обнаружить чесоточные ходы. Характерная локализация: половой член, мошонка, подкрыльцовые и межъягодичная складки, околососковые кружки. Узелки обычно немногочисленны. Иногда они являются единственным диагностическим признаком чесотки [2, 4].
На поверхности новых узелков можно обнаружить чесоточные ходы. Характерная локализация: половой член, мошонка, подкрыльцовые и межъягодичная складки, околососковые кружки. Узелки обычно немногочисленны. Иногда они являются единственным диагностическим признаком чесотки [2, 4].
Экзематизированная чесотка возникает, как правило, у людей с аллергической предрасположенностью. На местах расчесов могут появляться очаги лихенификации. Однако на первый план обычно выступают экзематозные поражения и диагноз чесотки не всегда может быть заподозрен. Высыпания проявляются на кистях, в подмышечных впадинах, голенях, кистях. В запущенных случаях высыпания могут приобретать диссеминированный характер, вплоть до развития эритродермии.
У лиц со сниженной сопротивляемостью организма к экзематизированным поражениям на местах расчесов может присоединяться вторичная бактериальная инфекция в виде импетиго или эктим, могут возникать стафилококковые фолликулиты, фурункулы и абсцессы.
Норвежская чесотка (крустозная, корковая) в начальных стадиях представлена как обычная чесотка или маскируется под атопический дерматит, псориаз, себорейный дерматит. Характерны ороговение, образование чешуек или толстых корок. При выраженном иммунодефиците процесс может носить генерализованный характер, при неврологических заболеваниях — проявляться ограниченной областью нарушения чувствительности.
Характерны ороговение, образование чешуек или толстых корок. При выраженном иммунодефиците процесс может носить генерализованный характер, при неврологических заболеваниях — проявляться ограниченной областью нарушения чувствительности.
Грудничковая и детская чесотка характеризуется высыпаниями, напоминающими крапивницу или детскую почесуху в виде большого количества расчесанных и покрытых корочкой волдырей с преимущественной локализацией в промежности на мошонке, в подкрыльцовых складках. Характерные чесоточные ходы можно обнаружить на подошвах.
Диагностика чесотки
Диагностика чесотки, помимо клинических данных, основывается на микроскопическом подтверждении диагноза. Однако эта процедура требует значительного навыка, опытного микробиолога и при некоторых клинических формах невыполнима. Минимальные клинические проявления чесотки также затрудняют получение достаточного биологического материала для исследования. Методика имеет преимущества в специализированных учреждениях.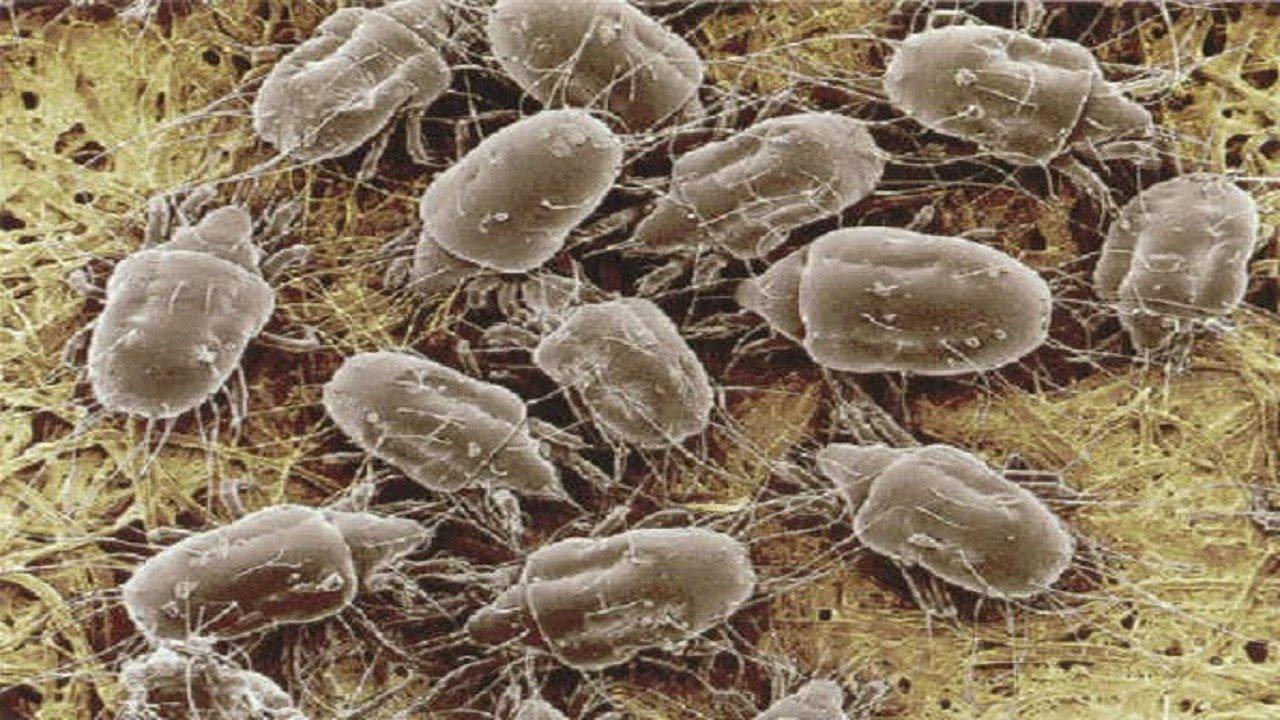 Существует несколько методик лабораторной диагностики чесотки: извлечение клеща иглой, метод тонких срезов, соскобы, щелочное препарирование кожи.
Существует несколько методик лабораторной диагностики чесотки: извлечение клеща иглой, метод тонких срезов, соскобы, щелочное препарирование кожи.
Чесотка. Знать, чтобы не бояться – СПб ГБУЗ Кожно-венерологический диспансер №11
Несмотря на успехи в диагностике и терапии чесотки, проблема заболеваемости этим дерматозом сохраняет актуальность. Согласно официальным статистическим данным, в России заболеваемость чесоткой в последние годы составляет около 100 случаев на 100000 населения. Однако этот показатель фактически значительно больше, так как не все случаи регистрируются, достаточно высокий процент самолечения заболевания.
Причинами высокого уровня заболеваемости чесоткой в настоящее время являются социальные (бедность, несоблюдение надлежащих мер санитарии и гигиены, ранняя половая жизнь, миграция, рост числа путешествий), медицинские (контагиозность инкубационного периода, атипичная форма чесотки) и главным образом, иммунологические (уменьшение иммунных реакций у людей по отношению к чесоточным клещам (Sarcoptes scabiei hominis).
Первые описания чесотки выполнены более 2500 лет назад. Чесотка описана в Ветхом Завете и в трудах Аристотеля. В древней Греции чесотку относили к группе кожных заболеваний объединенных термином «псора». В древнем Риме чесотку называли «скабиес», это название сохранилось до наших дней. В средневековых трактатах выдвигались предположения о паразитарной природе чесотки. Достоверные доказательства роли чесоточных клещей в развитии заболевания появляются только после создания оптического микроскопа. В 1687 г. итальянский врач Джован Козимо Бономо и аптекарь Дьячинто Честони впервые описали связь между чесоточными клещами и типичными кожными симптомами, развивающимися вслед за заражением. Именно они впервые установили, что болезнь может быть вызвана микроскопическим организмом. Полное и достоверное описание этиологии и патогенеза дал в 1844 г. немецкий дерматолог Фердинанд Гебра. Это руководство было в 1876 году переведено на русский язык А. Г. Полотебневым.
Чесотка заболевание, вызываемое клещом (Sarcoptes scabiei), способным паразитировать в коже человека.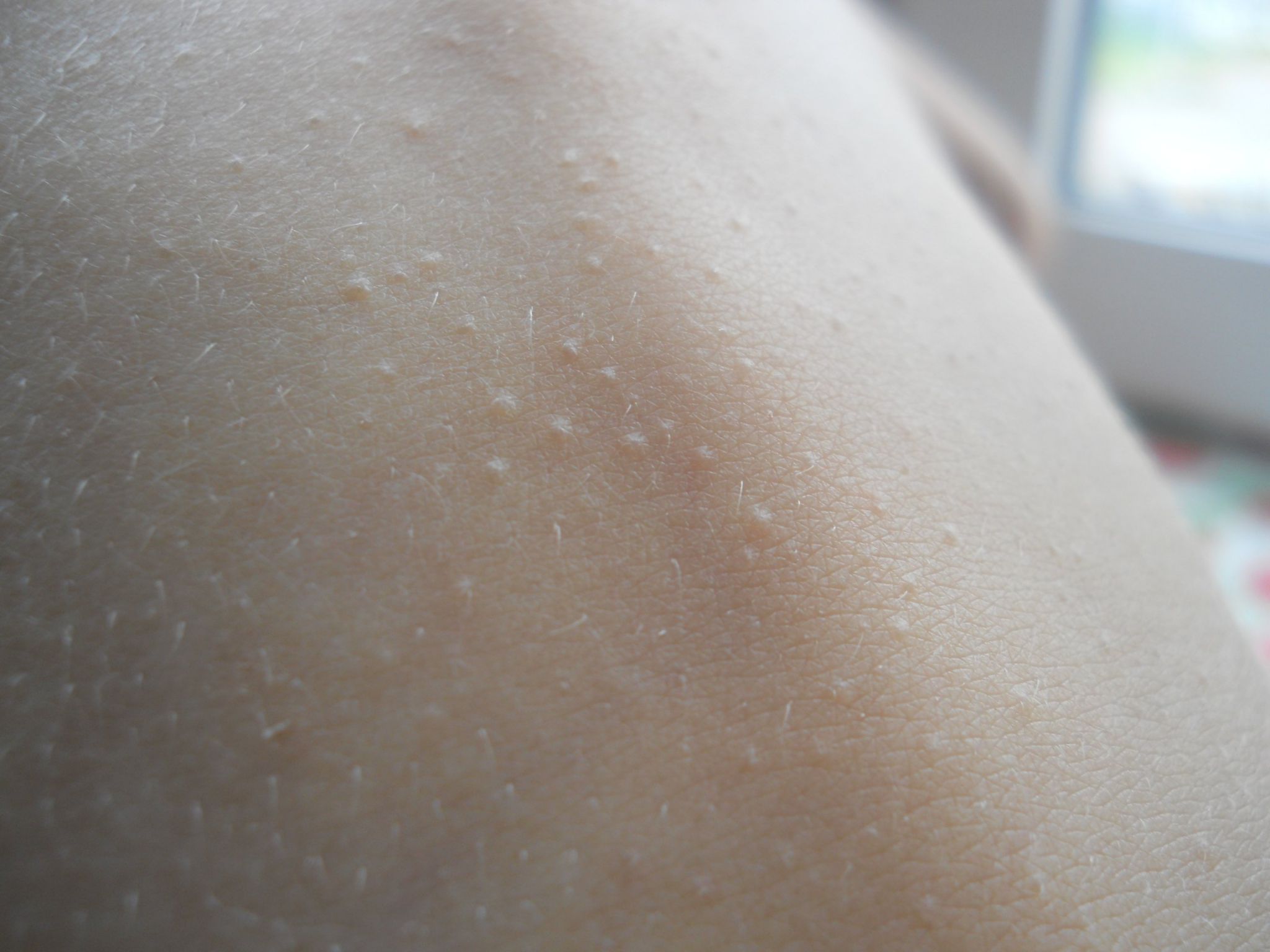 Чесоточный клещ распространен повсеместно, и в мире ежегодно регистрируется не менее 300 млн. больных.
Чесоточный клещ распространен повсеместно, и в мире ежегодно регистрируется не менее 300 млн. больных.
Заражение происходит от больных чесоткой, а также при контакте с одеждой и постельным бельем, на которых находятся клещи.
После оплодотворения самки самец погибает, а самки в коже человека пробуравливают ходы, в которых откладывают до 50 яиц. Развитие клещей от яйца до половозрелых паразитов происходит в течение 4 недель. Взрослые особи живут до 2 месяцев и питаются тканями хозяина, т.е. кожей. При этом поражаются участки нежной кожи. На человеке могут также паразитировать зерновые клещи, а также клещи лошадей, свиней, собак, овец, коз, кошек, птиц. Клещи животных на коже людей длительно не паразитируют.
Клиническая картина
Скрытый период от момента попадания клеща на кожу и до клинических симптомов болезни может быть от 7-10 дней до 4-6 недель. Его продолжительность зависит от массивности первичного заражения.
Ведущим клиническим симптомом чесотки является зуд кожных покровов, особенно по ночам, когда больной согревается. Самка чесоточного клеща проделывает ходы в коже в виде продольных или извилистых серовато-белых линий с двумя черными точками в месте входа и выхода чесоточного клеща. Длина хода 3-10 мм, и поэтому заметно их попарное расположение. На месте входа чесоточного клеща может быть узелок, пузырек или красноватая корочка. При расчесах занесении вторичной инфекции появляются гнойничковые высыпания. Излюбленная локализация поражений кожи при чесотке: живот, боковые поверхности тела, кожа между пальцами рук, боковые поверхности пальцев.
Самка чесоточного клеща проделывает ходы в коже в виде продольных или извилистых серовато-белых линий с двумя черными точками в месте входа и выхода чесоточного клеща. Длина хода 3-10 мм, и поэтому заметно их попарное расположение. На месте входа чесоточного клеща может быть узелок, пузырек или красноватая корочка. При расчесах занесении вторичной инфекции появляются гнойничковые высыпания. Излюбленная локализация поражений кожи при чесотке: живот, боковые поверхности тела, кожа между пальцами рук, боковые поверхности пальцев.
У маленьких детей процесс нередко захватывает ладони, подошвы, волосистую часть головы, лицо и шею, где можно обнаружить чесоточные ходы.
При расчесах ходы вскрываются ногтями и клещи разносятся по всему телу.
Заболевание без лечения может продолжаться в течение нескольких лет. Могут быть и стертые формы болезни, когда слабо выражен зуд и небольшое количество элементов сыпи в нетипичных местах.
Диагностика
Наличие сильного кожного зуда в типичных местах с характерными высыпаниями является основанием для подозрения на чесотку.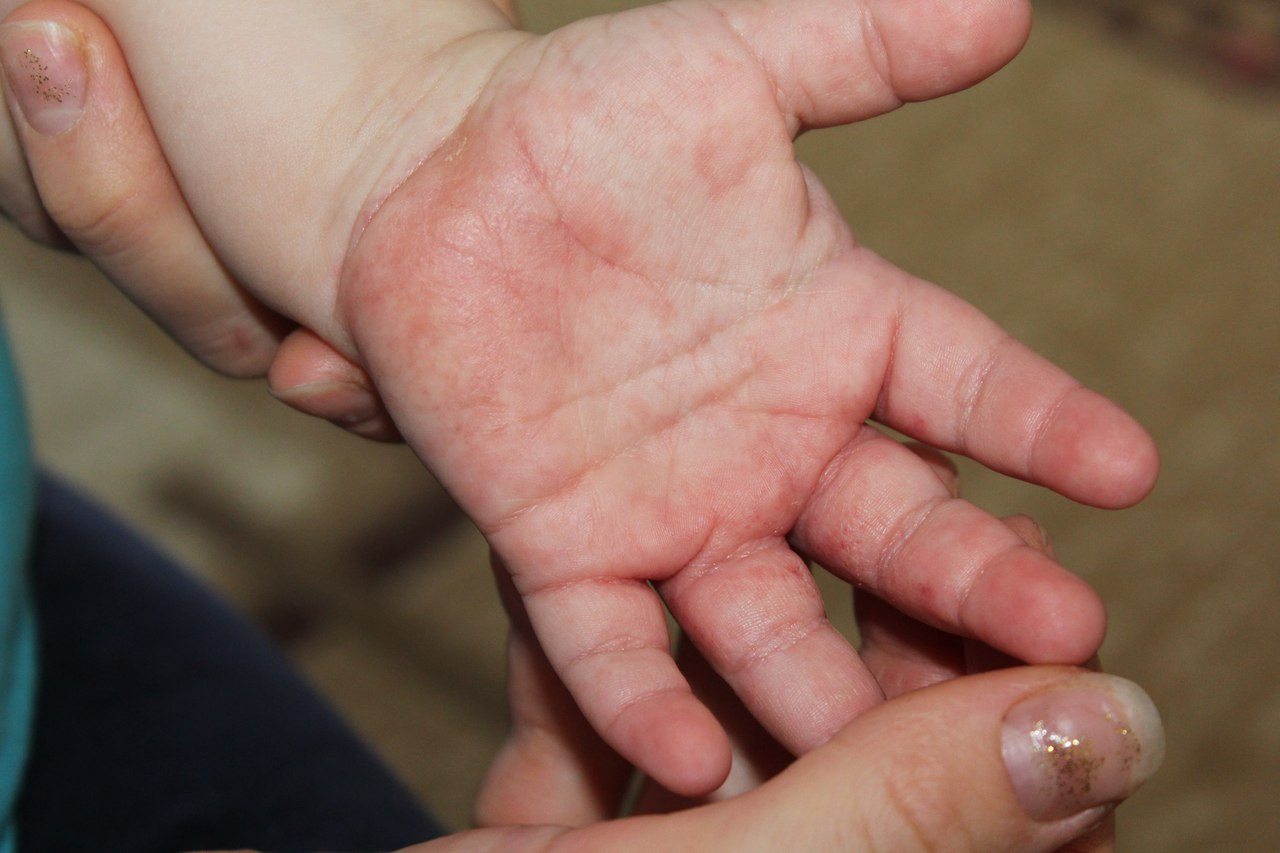 Окончательный диагноз поставит врач-дерматолог после специального обследования. Это необходимо делать в связи с тем, что под маской чесотки могут протекать и другие кожные заболевания: нейродермит, экзема, почесуха, крапивница, аллергические высыпания, токсикодермия и др.
Окончательный диагноз поставит врач-дерматолог после специального обследования. Это необходимо делать в связи с тем, что под маской чесотки могут протекать и другие кожные заболевания: нейродермит, экзема, почесуха, крапивница, аллергические высыпания, токсикодермия и др.
Профилактика
Необходимо выделять личную и общественную профилактику инвазии. Личная предусматривает соблюдение гигиенических правил при общении с животными и больными людьми, а также соблюдение личной гигиены при посещении общественных мест. Больных изолируют и не допускают в детский коллектив до полного излечения от чесотки. Необходимо осматривать на чесотку и других членов семьи.
Общественная профилактика заключается в своевременном выявлении и эффективном лечении больных, противоэпидемических мероприятиях в банях, общежитиях, детских садах, а также санитарно-просветительная работа. Белье больных нужно кипятить, а одежду и постельные принадлежности обрабатываются в дезинфекционных камерах.
Для оказания квалифицированной медицинской помощи пациентам с высыпаниями на коже можно обратиться в СПб ГБУЗ КВД №11в отделения по адресам:
ул. Чайковского, дом 1 (тел. 273-54-61)
ул. Стремянная, дом 4 (тел. 713-12-94)
симптомы, причины, профилактика и лечение
Чесотка (скабиес) входит в число наиболее распространенных паразитарных поражений кожи. Возбудитель патологии – чесоточный клещ-зудень Sarcoptes scabiei. Основными симптомами заболевания становятся высыпания на кожных покровах, хорошо заметные клещевые ходы в верхних слоях дермы и расчесы в местах их локализации. Лечение пациентов проходит под надзором врача-дерматолога.
Этиология заболевания
Причиной развития чесотки становится контакт здорового ребенка или взрослого с носителем чесоточных клещей. Sarcoptes scabiei паразитирует только на человеке. Чесоточные ходы в эпидермисе прокладываются самками, длина тела которых не превышает 100 мкм. Вылупляющиеся личинки выходят на поверхность кожи и самостоятельно внедряются в эпидермис за счет наличия мощного челюстного аппарата. Некоторое время клещи сохраняют жизнеспособность на поверхности бытовых предметов – здоровый человек может стать носителем паразита после использования столовых приборов, посуды, средств личной гигиены. Не меньшую опасность представляют дверные ручки, лестничные перила, телефонные трубки, постельное белье.
Некоторое время клещи сохраняют жизнеспособность на поверхности бытовых предметов – здоровый человек может стать носителем паразита после использования столовых приборов, посуды, средств личной гигиены. Не меньшую опасность представляют дверные ручки, лестничные перила, телефонные трубки, постельное белье.
Внедряется Sarcoptes scabiei под кожу за 20-25 минут. Возбудители заболевания гибнут при температуре выше 50 градусов в течение 10 минут, нагрев окружающей среды до 80 градусов приводит к мгновенному прекращению их жизнедеятельности.
Симптоматика скабиеса
Первые признаки чесотки проявляются у здорового человека через 7-10 дней после контакта с носителем патологии. При внимательном осмотре кожных покровов на 2-3 день можно заметить чесоточные ходы. Симптоматика нарастает при откладывании самками яиц в толще эпидермиса. Пациенты сталкиваются с нестерпимым зудом, который усиливается в вечерние и ночные часы. При укусах Sarcoptes scabiei выделяют химически активные вещества, становящиеся причиной аллергической реакции и локального воспаления кожных покровов. Зуд приводит к появлению расчесов, покрытых кровянистыми струпьями.
Зуд приводит к появлению расчесов, покрытых кровянистыми струпьями.
У вас появились симптомы чесотки?
Точно диагностировать заболевание может только врач. Не откладывайте консультацию — позвоните по телефону +7 (495) 775-73-60Классификация патологии
Выявляемые при осмотре пациентов симптомы чесотки позволяют дерматологам выделять четыре типа заболевания.
| Форма скабиеса | Описание |
|
Чистоплотный |
Рассматривается врачами как стертая форма патологии. Развивается у людей с высокой иммунореактивностью. На кожных покровах не наблюдается аллергической реакции на продукты жизнедеятельности клещей. Аналогичным образом чесотка развивается у людей, уделяющих повышенное внимание личной гигиене (систематическое мытье рук, душ дважды в день). Высыпания на кожных покровах локализованы на животе и грудной клетке. |
|
Типичный |
Высыпания появляются на животе, бедрах, ягодицах, грудной клетке, боковых поверхностях пальцев рук и ног. Мужчины могут столкнуться с поражением кожных покровов полового члена и мошонки. Чесоточные ходы явно выражены, имеют вид белесой или сероватой линии длиной 5-7 мм с папулой или везикулой. Размеры образований не превышают 0,5 мм в диаметре |
|
Узловой |
Высыпания на кожных покровах формируются как аллергическая реакция организма пациента на продукты жизнедеятельности чесоточного зудня. Данная форма патологии развивается на фоне неправильного лечения чесотки или нарушения рекомендаций дерматолога. На коже образуются крупные зудящие узелки красновато-коричневой окраски. Противоскабиозная терапия оказывается неэффективной из-за закупорки ходов в коже плотной коркой в местах формирования везикул |
|
Корковый |
Выявляется у людей с ослабленным иммунитетом, встречается крайне редко. |
Диагностические мероприятия
Диагностика чесотки осуществляется дерматологом, терапевтом или инфекционистом. Основанием для постановки диагноза становятся клинические данные и жалобы пациента. В некоторых случаях назначается соскоб, проводится лабораторное исследование полученного биоматериала. Тест не всегда информативен из-за того, что пациенты посещают душ перед визитом в клинику.
В ходе осмотра врач может нагреть отдельные участки кожи или нанести на них каплю масла. Эти меры повышают двигательную активность чесоточных клещей. Красители позволяют обнаружить чесоточные ходы при отсутствии заметных высыпаний на кожных покровах.
Терапевтический курс
Клинические рекомендации предусматривают обработку всей кожи пациентов эмульсиями или спреями. Исключением становится волосистая часть головы. Антискабиозные препараты обладают малой токсичностью и не причиняют дискомфорта в ходе лечения. Перед первым нанесением средства на основе бензилбензоата пациенту следует посетить душ. Повторная обработка кожных покровов проводится через 48 часов – гибнут клещи, пребывающие в стадии личинок. При полном устранении симптомов новый цикл нанесения препарата не проводится. После завершения лечения пациенту следует использовать антисептик для обработки мебели, предметов домашнего обихода и одежды.
Исключением становится волосистая часть головы. Антискабиозные препараты обладают малой токсичностью и не причиняют дискомфорта в ходе лечения. Перед первым нанесением средства на основе бензилбензоата пациенту следует посетить душ. Повторная обработка кожных покровов проводится через 48 часов – гибнут клещи, пребывающие в стадии личинок. При полном устранении симптомов новый цикл нанесения препарата не проводится. После завершения лечения пациенту следует использовать антисептик для обработки мебели, предметов домашнего обихода и одежды.
Корковая форма чесотки требует иного подхода к лечению. Антискабиозную терапию предваряет этап размягчения и удаления корок посредством мыльно-содовых ванночек или кератолитических мазей. После удаления всех ороговевших слоев пациент может приступать к нанесению раствора бензилбензоата на пораженные участки.
Осложнения и профилактика
Отсутствие лечения чесотки может привести к развитию пиодермии, микробной экземы и дерматита. По этой причине дерматологи рекомендуют пациентам обращаться за медицинской помощью при выявлении первых признаков скабиеса.
По этой причине дерматологи рекомендуют пациентам обращаться за медицинской помощью при выявлении первых признаков скабиеса.
Профилактика чесотки предполагает устранение очагов массового заражения людей (карантины в детских садах и школах). Систематические осмотры детей врачами и соблюдение правил личной гигиены представителями всех возрастных групп существенно снижают риск инфицирования скабиесом.
Статистика
Чесотка распространена среди всех социальных групп москвичей. Сезон наибольшей активности чесоточных клещей длится с апреля по октябрь. На пике заболеваемость достигает 50 случаев на каждые 100 тысяч жителей города. В период убыли эпидемии этот показатель падает до 15-18 случаев. Наибольшему риску подвержены дети и молодежь из-за активного образа жизни и регулярного посещения общественных мест.
Вопросы и ответы
Стоит ли проходить курс лечения родственникам пациента с диагностированной чесоткой?
Вероятность инфицирования лиц, проживающих с носителем скабиеса, очень высока. По этой причине дерматологи часто назначают родственникам пациента курс профилактического лечения с использованием средств на основе бензилбензоата.
По этой причине дерматологи часто назначают родственникам пациента курс профилактического лечения с использованием средств на основе бензилбензоата.
Формируется ли иммунитет к чесотке?
Повторное инфицирование человека скабиесом возможно сразу после завершения текущего курса. Из-за этого врачи настаивают на необходимости антисептической обработки мебели и одежды – у пациентов не формируется иммунитет к чесоточным клещам.
Не нашли ответа на свой вопрос?
Наши специалисты готовы проконсультировать вас по телефону:
симптомы, лечение, причины болезни, первые признаки
Описание
Чесотка – это паразитарное заболевание кожи, которое вызывает Чесоточный клещ (зудень). Чесоточный зудень является облигатным (живущим внутри хозяина) человеческим паразитом. Живёт он в ходах, которые сам прогрызает в поверхностном слое кожи. Оплодотворенная самка попадает на кожу здорового человека, проникает внутрь рогового слоя эпидермиса и откладывает там яйца. Созревшие личинки сами прокладывают себе ходы внутри кожи. Из-за этого появляется специфичный для заболевания симптом – чесоточные ходы. Позже, созревшие формы клеща выходят на поверхность кожи.
Созревшие личинки сами прокладывают себе ходы внутри кожи. Из-за этого появляется специфичный для заболевания симптом – чесоточные ходы. Позже, созревшие формы клеща выходят на поверхность кожи.
Заражение происходит от больного человека. Личинка клеща, покинув клещевой ход, попадает на поверхность кожи. Там она превращается во взрослую форму. В таком виде на поверхности кожи может существовать до одного месяца. С кожи зараженного человека клещ через бытовые контакты клещи распространяются на других людей, может оставаться на одежде, постельном белье, средствах личной гигиены. Покинут тело человека, клещ может оставаться жизнеспособным до трёх суток.
После первого заражения симптомы обычно проявляются не раньше, чем через месяц, что может затруднять поиск очага паразитарной инфекции. Заболеваемость чесоткой характерна для скученных коллективов: детские сады, школы, казармы, больничные палаты. Имеет значение и пора года – в теплое время чесоточный зудень развивается быстрее, чем в холодное. Болезнь распространена во всём мире, но эпидемический характер носит в регионах, для которых характерна бедность, плохое качество или полное отсутствие водоснабжения, низкий уровень санитарных условий.
Болезнь распространена во всём мире, но эпидемический характер носит в регионах, для которых характерна бедность, плохое качество или полное отсутствие водоснабжения, низкий уровень санитарных условий.
Симптомы
Фото: yachist.ru
Выделяют несколько видов чесотки, в зависимости от клинических проявлений. Для нашего региона наиболее характерна классическая форма.
Главный симптом, который больше всего беспокоит пациентов – интенсивный зуд, который усиливается в вечернее и ночное время. Сопровождается зуд эритематозно-папулёзными высыпаниями, которые в первое время появляются в области межпальцевых складок, на сгибательных поверхностях запястий и локтей, в подмышечных впадинах, под молочными железами и ягодицами. При развитии заболевания, папулами могут покрываться любые участки тела, в том числе кожа спины, живота, половых органов. Примечательно, что у взрослых пациентов на коже лица высыпания не наблюдаются. Главным критерием для дифференциальной диагностики будут служить чесоточные ходы – тонкая и извитая линия, длиной от нескольких миллиметров до полутора сантиметров. Кожа возле чесоточных ходов воспалена и шелушится. Типичным расположением чесоточных ходов в начале заболевания будет кожа кистей рук, предплечий, стоп. На одном из концов чесоточного хода под кожей можно заметить маленькое тёмное пятнышко. Так выглядит сам клещ, прокладывающий себе путь внутри кожи. Для классического варианта чесотки характерно не более 10-12 клещей. Из-за открытого доступа внутрь кожи, в чесоточные ходы может попадать и развиваться бактериальная инфекция.
Кожа возле чесоточных ходов воспалена и шелушится. Типичным расположением чесоточных ходов в начале заболевания будет кожа кистей рук, предплечий, стоп. На одном из концов чесоточного хода под кожей можно заметить маленькое тёмное пятнышко. Так выглядит сам клещ, прокладывающий себе путь внутри кожи. Для классического варианта чесотки характерно не более 10-12 клещей. Из-за открытого доступа внутрь кожи, в чесоточные ходы может попадать и развиваться бактериальная инфекция.
Нетипичные проявления классической чесотки могут наблюдаться у людей с темной кожей. В этом случае не наблюдается типичных чесоточных ходов, а образуются гранулематозные узелки, возвышающиеся над окружающей кожей. У маленьких детей типично поражение кожи лица и волосистой части головы, чаще всего в области за ушами, а также стопы и ладонная поверхность кистей. Для пожилых людей характерно отсутствие или очень слабые проявление на любых участках кожи, главным симптомом у них является нестерпимый зуд. Больные, страдающие иммуносупрессией, напротив, могут не испытывать зуд, но у них будет наблюдаться усиленное образование кожных проявлений.
Существуют отдельные формы чесотки, которые требуют обязательного лечения в условиях стационара.
- Крустозная (норвежская) чесотка. Возникает из-за нарушения иммунного ответа организма. В этом случае клещи могут бесконтрольно размножаться внутри кожи, а их число будет насчитывать многие миллионы штук. Эритемы становятся распространёнными, могут полностью покрывать кожу конечностей, туловища и головы.
- Узелковая чесотка. Наиболее типична для детей и младенцев. Представляет собой эритематозные узелки, размерами до 7-8 мм. Чаще всего узелки располагаются в складках кожи – в паху, в области половых органов, ягодиц, в подмышечных впадинах. После излечения, узелки способны сохраняться до полугода.
- Буллезная чесотка. Так же более характерна для детей. При этой форме на месте эритемы образуются буллы – пузырьки, наполненные прозрачной жидкостью. Могут быть разных форм и размеров, но редко превышают 15 миллиметров.
Скрытая чесотка. Так называют вариант, при котором человек заражен клещами, но они никак себя не проявляют. Такая форма возникает у людей, которые длительное время применяют глюкокортикоидные препараты длительное время, в том числе в форме гелей и мазей.
Такая форма возникает у людей, которые длительное время применяют глюкокортикоидные препараты длительное время, в том числе в форме гелей и мазей.
Диагностика
Фото: netrodinkam.ru
Диагностика начинается с типичных жалоб пациента – на сильный зуд, усиливающийся в вечернее и ночное время и наличие кожных проявлений (эритематозно-папулёзных высыпаний и клещевых ходов). Подтверждается диагноз с помощью обнаружения клещей, их яиц и фекалий. Берется соскоб с поверхности высыпаний и из клещевых ходов и исследуется под микроскопом. Нередко не удаётся обнаружить самих клещей, но практически всегда присутствуют продукты их жизнедеятельности. Перед взятием соскоба на папулу или клещевой ход наносят минеральное масло или глицерин, чтобы предотвратить распространение клещей и их яиц во время взятия анализа. После этого скальпелем вскрывается кожа и с открытого места тупым предметом (стеклышко, тупой край скальпеля, шпатель) берётся соскоб. Следует избегать обрабатывать папулы до взятия соскоба, поскольку многие антисептические средства способны растворять фекальные гранулы, что способно затруднить диагностику.
Лечение
Фото: independent.co.uk
Лечение чесотки заключается в назначении препаратов от аллергии, поскольку именно аллергическая реакция на продукты жизнедеятельности вызывает зуд, а также различных местных средств в виде мазей, болтушек, гелей, которые убивают клещей и не дают им размножаться.
При лечении чесотки следует придерживаться определённым правилам.
- Требуется одновременное лечение всех больных из одного эпидемического очага.
- Следует прокипятить постельное бельё, повседневную одежду, полотенца с содой или большим количеством стирального порошка. Сушить на открытом воздухе не менее трёх суток, после чего обязательно прогладить горячим утюгом. Во время болезни следует сменять одежду ежедневно.
- Больным и контактирующим с ними особенно тщательно выполнять требования гигиены: мытьё рук с мылом не менее минуты, пользование отдельным полотенцем, влажная уборка и проветривание помещений.
- При назначении лечения препараты следует втирать в кожу голыми руками, это предотвратит повторное заражение на новых участках кожи.

Яйца клещей способны долгое время оставаться жизнеспособными, если во время расчёсов закрепятся под ногтевыми пластинами, поэтому очень полезным будет постричь ногти.
Лекарства
Фото: netderm.ru
В аптеках предлагают множество лекарственных препаратов, для лечения чесотки и борьбы с чесоточным клещом. Они отличаются ценой за курс лечения и количеством обработок кожи в день, необходимых для надежного избавления от паразита.
- Бензилбензоат. Существует в виде мазей и эмульсий. Препарат изобретен давно, хорошо себя зарекомендовал и широко применяется в лечении чесотки в странах СНГ.
Курс лечения включает две обработки кожи на всём теле, кроме волосистой части головы и лица. Вторую обработку проводят на четвёртый день. Перед втиранием лекарственного средства, тщательно моются под душем, после чего голыми руками обрабатывают всю кожу. Обработку следует проводить в вечернее время. Эффект будет достигнут в случае, если средство препарат оставался на теле не менее 12 часов.
Повторная обработка на 4 день необходима для того, чтобы убить вылупившихся из яиц клещей, поскольку препарат воздействует только на взрослые формы. - Перметин. Продаётся в виде кремов, мазей, спреев, лосьонов. Наиболее популярен в виде 5% крема. Также требуется две обработки. Препарат применяется в том числе для лечения педикулёза.
- Спрегаль. Выпускается в виде аэрозоля. После применения не оставляет следов, практически лишен запаха. Воздействует на яйца клещей, а потому может быть достаточно всего одной обработки, но дерматологи всё же рекомендуют проводить повторную на третий день, для исключения возможности рецидивирования болезни.
Для лечения чесотки существуют и другие методы, но они более трудоёмки и требуют большего количества обработок кожи. К ним относятся:
- Метод Демьяновича. Заключается в последовательном втирании в кожу 60% тиосульфита натрия и 6% соляной кислоты.
- Серная мазь. Требуется ежедневная обработка кожи в течение недели.
 Мазь имеет неприятный запах и маслянистую консистенцию, которая пачкает одежду и полностью не впитывается в кожу.
Мазь имеет неприятный запах и маслянистую консистенцию, которая пачкает одежду и полностью не впитывается в кожу.
Если чесотку сопровождает нестерпимый зуд, для однократного приема могут использовать антигистаминные препараты: Цетиризин, Лоратадин, Супрастин.
Народные средства
Фото: parazitoved.ru
В народе бытует мнение, что керосин является хорошим средством от кожных болезней, в частности при чесотке. Ни в коем случае не следует использовать такое средство, потому что помимо токсических эффектов для всего организма, вызванного всасыванием керосина, может развиться местная аллергическая реакция на коже, что только усугубит состояние.
Для лечения чесотки применяют:
- Хлебный квас. Обильно посолить, подогреть до 60-70 градусов и опускают в него руки. Держать до десяти минут, но только в том случае, если температура ощущается комфортной. В противном случае, от этого средства следует отказаться.
- Лавровый лист измельчают и в равных долях смешивают со сливочным маслом.
 Полученную смесь втирают в пораженные места.
Полученную смесь втирают в пораженные места. - Чистым берёзовым дёгтем смазывают пораженные места на несколько часов, после чего смывают подогретой водой с отрубями.
- Мазь, приготовленная из свиного сала, серы и поваренной соли. Ингредиенты берутся в соотношении 4:2:1 соответственно. Тщательно измельчают, перемешивают до получения однородной массы. Мазь втирают в поражённые участки кожи в течение 5-7 дней.
- Ещё один народный рецепт мази из серы и дёгтя. Берут свиное сало и хозяйственное мыло по столовой ложке, а серу и берёзовый дёготь по чайной. Мыло следует натереть на тёрке. Смешивают до получения однородной мази. После тщательного мытья под горячим душем с мылом и мочалкой, на кожу наносят мазь и не смывают до следующего дня. Процедуру следует повторять три дня подряд.
- Чайную ложку скипидара смешать с двумя столовыми ложками сливочного масла и смазывать поражённые участки кожи.
- Одну часть сока чистотела и четыре части вазелинового масла, смешать и наносить на кожу дважды в день.

- Готовят настойку из травы дымянки лекарственной. Три столовые ложки настаивают в 100 граммах водки в тёмном месте в течение недели. Настойкой следует обрабатывать кожу. Поскольку рецепт требует целую неделю на приготовление, может иметь смысл хранить такой на всякий случай в запасе.
- За пару часов перед применением горячей ванны в пораженные участки кожи втирают лавандовую эссенцию, повторяют такую процедуру по меньшей мере пять дней подряд. Используйте этот способ с осторожностью, возможны аллергические реакции!
- Горячие ванны с отварами крестовника, могильника, вербены. Используется как смесь трав, так и каждая по отдельности. Для одной ванны требуется 30 грамм сухой травы, вскипячённая в литре воды. Перед применением отвар процедить. Применять ванну следует перед сном.
Отвар конского щавеля и компрессы с ним. Отваром смазывать кожу, а свежие листья измельчить в кашицу, приложить к пораженной коже и завернуть в полиэтилен на ночь.
Информация носит справочный характер и не является руководством к действию. Не занимайтесь самолечением. При первых симптомах заболевания обратитесь к врачу.
Не занимайтесь самолечением. При первых симптомах заболевания обратитесь к врачу.Ваши комментарии о симптомах и лечении
Чесотка – причины заражения, первые признаки. Как лечить чесотку на руках и всем теле
Чесотка – первые признаки, средства лечения
Кожное заболевание, вызываемое чесоточным клещом, называется чесоткой. Состояние достаточно неприятное, доставляет массу дискомфорта и является заразным. Знать симптомы заражения чесоточным клещом нужно знать каждому – это поможет сразу начать лечение и предотвратить инфицирование всех окружающих.
Как происходит заражение
Заражение чесоткой через контакт с больным – самый распространенный путь инфицирования. Но это может произойти и при соприкосновении с посудой, полотенцами и любыми предметами, которых касался больной. Грубо говоря, заболеть чесоткой можно даже после поездки в общественном транспорте, если взяться за поручни сразу после инфицированного человека.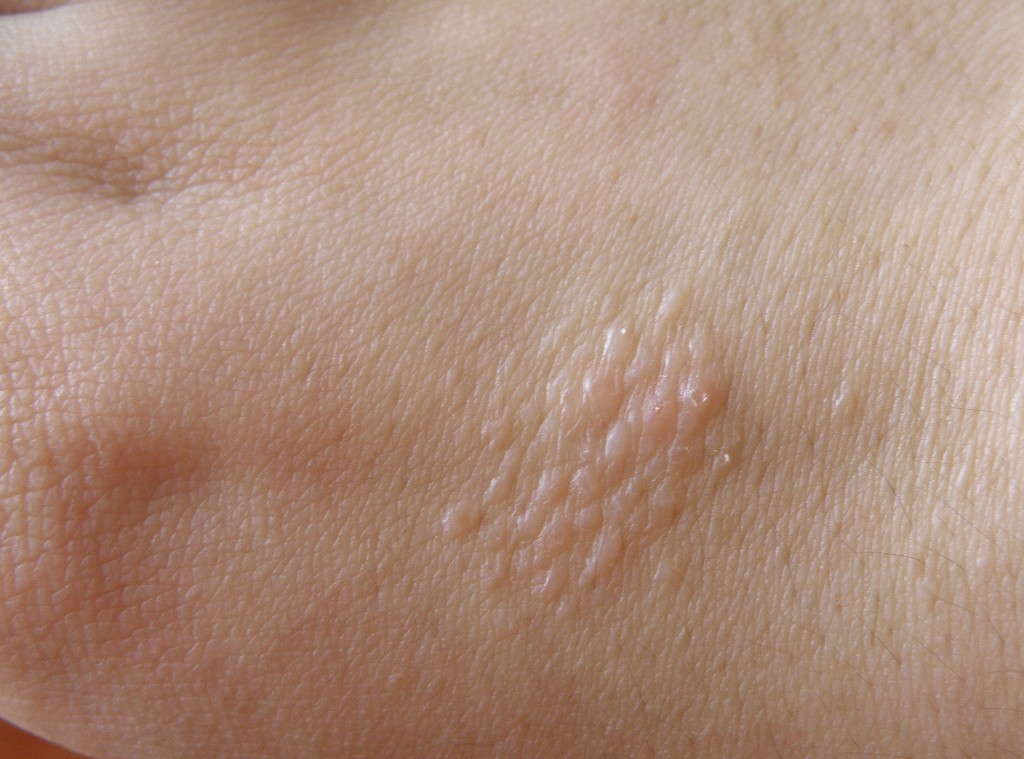
Самка клеща, попавшая на кожу, начинает двигаться по роговому слою и проделывает ходы, где и откладывает яйца-личинки. Через несколько дней из отложенных личинок появляются взрослые особи. Весь процесс от кладки яиц до появления половозрелых особей занимает максимум 14 дней.
Зная движения чесоточного клеща, можно понять, как выглядит чесотка у взрослых – кожа имеет тонкие «ниточки»-ходы, извилистые и слегка прерывистые – это путь, по которому движется самка. В других местах отмечаются маленькие точки-укусы.
Как проявляется чесотка
В медицине принято различать несколько видов рассматриваемого заболевания, которые могут давать разную клиническую картину. Но любая чесотка может проявляться зудом и сыпью – это и есть первые признаки патологии. Характерно, что активную жизнедеятельность чесоточный клещ ведет в ночное время суток, а характерный зуд нарушает сон больного. Результатом становятся не только следы расчесов на коже, но и раздражительность, плохое настроение.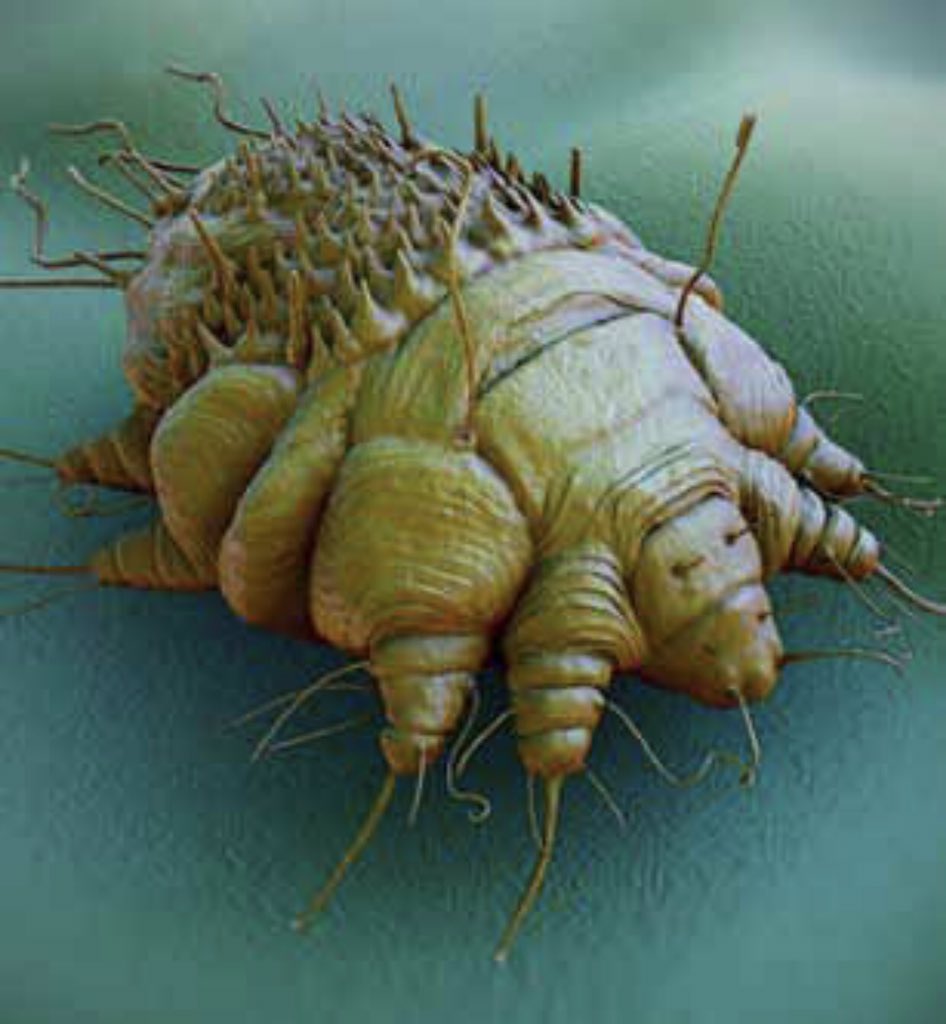
Классически чесотка проявляется на руках (между пальцами и на локтях), на животе, бедрах, реже – на ягодицах и шее.
Существует так называемая ушная чесотка – паразит поселяется в ушных раковинах и человек страдает от сильнейшего зуда, который невозможно унять без применения ушных палочек/спичек и других предметов, представляющих опасность для органов слуха. Начальная стадия ушной чесотки будет сопровождаться легким зудом на руках, но достаточно быстро паразит перемещается в «место постоянной дислокации».
Отдельно стоит упомянуть норвежскую чесотку – инфицирование также происходит через контакт с больным человеком, но интенсивные симптомы появляются только на фоне низкого иммунитета, после параличей, при некоторых генетических заболеваниях. Норвежская чесотка после лечения требует восстановления волос и ногтей.
Диагностические мероприятия
Как только появились первые признаки чесотки на теле, следует обратиться за квалифицированной медицинской помощью. Этой болезнью занимается врач-дерматолог, он же проведет и диагностику.
Этой болезнью занимается врач-дерматолог, он же проведет и диагностику.
Специалисту достаточно посмотреть на участки тела, пораженные чесоточным клещом, и он сможет поставить точный диагноз. При сомнениях эти участки смазываются йодом – после высыхания все ходы будут проявлены коричневой линией.
Как лечить чесотку
Лекарственные препараты и мази от болезни должны соответствовать следующим требованиям:
- уничтожать не только половозрелых особей паразитов, но и их личинки;
- обладать минимальной токсичностью;
- быть простыми в использовании;
- не пачкать одежду и кожу, чтобы больной мог вести привычный образ жизни.
Чаще всего врачи назначают серную мазь, раствор кротамитона или перметрина – эти средства наносятся наружно и способны быстро уничтожить чесоточного клеща и его личинки. Важное значение имеет правильный выбор средства лечения чесотки у детей – оно должно быть абсолютно нетоксичным, гипоаллергенным.
Независимо от того, какой конкретно лекарственный препарат будет выбран для лечения, нужно знать правила его применения:
- Обработка пораженных участков тела должна проводиться в строгом соответствии со схемой, которую даст врач.
- Обрабатывается абсолютно все тело, особое внимание стоит уделить подмышечным впадинам, паховым складкам, подколенным ямкам. Волосистая часть головы обрабатывается только у детей, для взрослых этого делать не нужно.
- Нельзя допускать попадания даже незначительного количества лекарства в глаза. Если же такое произошло, то нужно вызвать бригаду «Скорой помощи» и до прибытия специалистов промыть глаза чистой водой.
- Любое лекарственное средство должно наноситься руками.
Как лечить чесотку у человека:
- Первые сутки – вечером инфицированный моется в душе с мылом, вытирается насухо и обрабатывает все тело выбранным препаратом. Обязательно нужно надеть чистую одежду и сменить постельное белье.

- Вторые-третьи сутки – нельзя принимать душ и менять нательное/постельное белье.
- Четвертые сутки – принять душ с мылом, нанести препарат на кожу, сменить одежду и постельное белье.
- Пятые сутки – больной моется под душем, меняет белье и одежду.
Обратите внимание: многих интересует вопрос «как избавиться от чесотки на руках». Такая локализация заболевания не означает, что можно обрабатывать только пораженные участки – чесоточный клещ может просто уйти в другое место.
После окончания лечения нужно посетить дерматолога для контрольного обследования. Обычно это делают на десятый день после начала терапии, а показателе выздоровления будут отсутствующие чесоточные ходы, зуд и расчесы на коже.
Профилактические мероприятия
Причины и профилактика заболевания чесоткой «ходят» рядом. Ведь заразиться можно только при соприкосновении с уже инфицированным человеком или предметами после его использования, поэтому для профилактики специалисты рекомендуют как можно чаще мыть руки, желательно протирать их жидким антисептиком. Отличным вариантом станет Хлоргекисдин – удобный флакон запросто поместится в сумочку или бардачок автомобиля, а обмывание рук несколько раз в день станет отличной профилактикой чесотки.
Отличным вариантом станет Хлоргекисдин – удобный флакон запросто поместится в сумочку или бардачок автомобиля, а обмывание рук несколько раз в день станет отличной профилактикой чесотки.
Связанные услуги:
Консультация дерматолога
Дерматовенерология
«Чесотка. Симптомы, диагностика, лечение.» – Яндекс.Кью
Что такое чесотка?
Чесотка является очень заразным заболеванием кожи, проявляющимся сыпью с крайне выраженным зудом. Заболевание вызывается специфическим паразитом кожи — чесоточным клещом, который живет на коже и внутри кожи человека. Чесотка передается людям от других людей путем контакта кожа-к-коже. В настоящее время она легко поддается лечению специальными противочесоточными средствами. Обычно достаточно двух применений лосьона с интервалом в одну неделю, для полного выздоровления.
Чесоточные клещи имеют очень маленькие размеры.
Фото 1. Чесоточный клещ (1) под микроскопом, яйца клеща (2).
Под микроскопом легко можно рассмотреть этих паразитов: у них есть тельце кремового цвета, щетинки и шипы на спине, четыре пары ног. Самка клеща имеет более крупные размеры (примерно 0,4 мм х 0,3 мм) по сравнению с самцом (0,2 мм х 0,15 мм).
Фото 2. Чесоточный клещ (1) под микроскопом, яйца клеща (2). Мелкие черные точки около крупных овальных яиц — продукты жизнедеятельности.
Самки клещей бурят в коже человека туннели (на фото 3 указано стрелкой), в которых откладывают яйца.
За жизнь самка откладывает около 40-50 яиц. Из яиц через 3-4 дня вылупляются личинки, которые становятся взрослыми в течение 10-15 дней. Личинки часто гибнут, из каждых 10 личинок половозрелого состояния достигает одна.
Большинство симптомов чесотки обусловлены ответом иммунной системы на самих клещей, их слюну, их яйца, или их фекалии.
Среднее количество половозрелых особей клещей у зараженного человека составляет 12 штук. У детей из неблагополучных районов, с запущенной чесоткой, иногда насчитывается более 100 штук клещей.
Как часто встречается чесотка?
Чесотка является распространенным заболеванием. Например, в Великобритании чесоткой заражается ежемесячно примерно 1 человек на каждую 1000. Чесотка является более распространенной в городских районах, среди женщин и детей (вероятно, вследствие более тесного контакта), в зимнее время (по той же причине — люди больше времени проводят в близком контакте). Общемировая нагрузка чесотки достигает 300 миллионов больных.
Как можно заразиться чесоткой?
Чтобы заразиться, здоровому человеку обычно необходимо иметь тесный контакт кожа-к-коже с больным человеком. Чесоточный клещ не умеет ни летать, ни прыгать.
В большинстве случаев чесотка передается после длительных прикосновений руками к коже инфицированного человека. Именно поэтому первые симптомы чаще всего возникают на руках.
Тесный контакт кожа-к-коже во время секса — второй по распространенности способ заражения чесоткой.
Контакт кожа-к-коже должен быть не мимолетным, и занимать определенное время. Таким образом, вы вряд ли заразитесь чесоткой от инфицированного человека при случайном коротком контакте с ним, например, при рукопожатии или приветственном объятии.
Клещи живут в коже человека, и способны выживать без человека не более 24-36 часов. Поэтому заражение через общее постельное белье, если оно просто лежало 3 дня без обработки. Однако, в связи с потенциальным риском, рекомендуется обработка всех тканевых поверхностей, прикасавшихся к больному, методом горячей стирки.
Иногда вспышки чесотки происходят в местах скученного нахождения людей, таких как детские сады или казармы, где люди находятся в регулярном тесном контакте.
Каковы симптомы и признаки чесотки?
Клещевые ходы (тоннели). Они могут быть замечены на коже в виде мелких, темных или серебристых линий длиной около 2-10 мм (с точкой входа и точкой выхода). Наиболее часто они встречаются на участках кожи между пальцами рук, на внутренней поверхности запястья. Тем не менее, они могут возникнуть на любом участке кожи. Вы можете не заметить ходы, пока не начнется сыпь или не появится выраженный зуд.
Тем не менее, они могут возникнуть на любом участке кожи. Вы можете не заметить ходы, пока не начнется сыпь или не появится выраженный зуд.
Фото 4. Чесоточный ход
- Зуд. Это наиболее тяжелый симптом, начинающийся обычно с какой-то одной области (руки) но быстро распространяющийся на другие места. Зуд, как правило, усиливается в ночные часы и после горячей ванны. Вы можете иметь сильный зуд, даже если заражены всего несколькими клещами.
- Сыпь. Сыпь обычно появляется вскоре после начала зуда. Как правило, это пятнисто-папулезная красная сыпь, которая может появиться на любом участке тела. Сыпь наиболее заметна на внутренней поверхности бедер, на животе и ягодицах, в подмышечной области и вокруг сосков у женщин. Сыпь обычно весьма характерная, и врач легко поставит по ней диагноз. Тем не менее, у некоторых людей сыпь бывает совершенно нетипичной, похожей на совсем другие заболевания кожи, отсюда иногда случаются ошибки в диагностике и терапии чесотки.

Фото 5. Чесоточная сыпь на ягодицах
Фото 6. Сыпь при чесотке в подмышечной впадине
- Расчесы. Расчесы связаны с интенсивным зудом и представляют собой поверхностные повреждения кожи ногтями самого пациента. В некоторых случаях эти повреждения кожи инфицируются болезнетворными бактериями — и возникает вторичная бактериальная инфекция кожи. Такие участки кожи становятся гиперемированными, воспаленными, горячими и болезненными.
Обострение ранее существовавших заболеваний кожи. Чесотка может ухудшить симптомы других заболеваний кожи, особенно болезней, изначально сопровождавшихся зудом, например: атопическая экзема, псориаз и тд. Диагностика чесотки в таких случаях нередко бывает чрезвычайно трудной.
Примечание: зуд и сыпь при чесотке обусловлены аллергической реакцией на чесоточных клещей (или их слюну, фекалии или яйца). Первые симптомы чесотки обычно возникают через 2 — 6 недель от заражения. Зуд и сыпь может развиться на любом участке кожи, а вовсе не только в тех местах, где непосредственно повреждает кожу чесоточный зудень. Помните, что Вы могли быть заразны до появления симптомов, и задолго до того, как Вы узнали, что больны чесоткой.
Зуд и сыпь может развиться на любом участке кожи, а вовсе не только в тех местах, где непосредственно повреждает кожу чесоточный зудень. Помните, что Вы могли быть заразны до появления симптомов, и задолго до того, как Вы узнали, что больны чесоткой.
На фотографии показано несколько типичных чесоточных тоннелей по обе стороны от запястной складки кожи. Этот пациент сфотографирован еще до появления типичной сыпи, возникающей в ответ на укусы клещей.
Сама сыпь, в классическом варианте, выглядит так:
Высыпания, локализованные в типичном месте — межпальцевых промежутках кисти:
А на этой фотографии отлично виден типичный тоннель от чесоточного клеща:
Симптомы при рецидивирующей чесотке
От заражения до появления первых симптомов чесотки обычно проходит 2-6 недель. Однако, если Вы уже болели чесоткой, успешно излечились, но заразились вновь — симптомы могут немного отличаться. В таких случаях сыпь и зуд развиваются гораздо быстрее — в течение одного-двух дней. Это происходит потому, что организм уже сенсибилизирован к аллергенам, выделяемым чесоточным зуднем, и очень бурно на них реагирует.
Это происходит потому, что организм уже сенсибилизирован к аллергенам, выделяемым чесоточным зуднем, и очень бурно на них реагирует.
Как устанавливается диагноз чесотки?
Чесотка является обычно клиническим диагнозом, то есть для ее подтверждения достаточно осмотра врача, без всяких дополнительных тестов и анализов. Врач видит типичную для чесотки сыпь и сразу ставит диагноз и назначает лечение. Но в некоторых сомнительных случаях врач может назначить соскоб с кожи, чтобы найти чесоточного зудня под микроскопом, для подтверждения диагноза. А в случаях, когда зуд и типичная сыпь одновременно развиваются у нескольких людей, проживающих в одном доме — диагноз становится очевидным по осмотру одного из них.
Как это лечится?
Чесотка будет продолжаться бесконечно, если ее не лечить.
Лечение необходимо для:
- Любого человека, заболевшего чесоткой
- Всех членов его семьи
- Всех людей, с которыми он вступал в телесный контакт (массажист, сиделка.
 ..)
..) - Всех сексуальных партнеров.
Лечение проводится всем этим людям, даже если у них нет ни малейших симптомов, так как они могут быть уже заражены и даже заражать других, не имея еще никаких клинических проявлений болезни.
Примечание: все контактные лица должны быть обработаны противочесоточным лосьоном или спреем в тот же день, что и заболевший — для исключения повторного заражения друг от друга.
Какие препараты применяют для лечения?
Чесотка обычно легко излечима. Стандартная терапия чесотки — это кожные препараты, содержащие 5% перметрина (Медифокс, Ниттифор и др). Перметрин — это инсектицид, который убивает чесоточных клещей. Если перметрин не может быть использован (например, из-за аллергии на него), то применяется 0,5% водный раствор малатиона (Пара плюс). Высокоактивным также является сочетание препаратов esdepallethrine + piperonyl butoxide (Спрегаль)
Все эти препараты просты в применении, и обладают высокой эффективностью. Препарат против чесотки наносится на кожу дважды — в первый день терапии, и на седьмой день от первого нанесения. Такая схема гарантированно убивает всех чесоточных клещей на коже человека и внутри нее.
Препарат против чесотки наносится на кожу дважды — в первый день терапии, и на седьмой день от первого нанесения. Такая схема гарантированно убивает всех чесоточных клещей на коже человека и внутри нее.
Обратите внимание, что ежедневные горячие ванны, с мылом или гелем для душа НЕ способны вылечить Вас от чесотки. Использование вышеуказанных инсектицидов — обязательно.
Правила использования препаратов против чесотки
- Прочтите инструкцию к выбранному препарату, уточните для каких участков кожи он разрешен. Некоторые препараты применяются на всех участках тела включая кожу головы и лица, в то время как другие должны быть применены только для кожи ниже шеи.
- Не забудьте обработать труднодоступные места, такие как перианальная область, спина, подошвы ступней, межпальцевые промежутки рук и ног, подногтевые ложа и гениталии.
- Обратите особое внимание на те области, где чаще всего бывают клещевые тоннели: запястья и локти, кожа в складке под женской грудью, подмышечные впадины, а также область вокруг сосков у женщин.

- Взрослому человеку необходимо не менее 30 г крема или 100 мл лосьона для достаточного намазывания на все участки тела. То есть для двукратной обработки одного взрослого человека необходимо приобретать не менее 60 г крема или 200 мл лосьона.
- Наносите крем или лосьон на сухую, не распаренную кожу (не после горячей ванны).
- Крем или лосьон следует оставить на коже столько времени, сколько рекомендовано в его инструкции. Например, средства на основе перметрина следует оставлять на коже 8-12 часов. Средства на основе малатиона не следует смывать 24 часа.
- Дети не должны посещать школу или детский сад, пока не пройдут первый день лечения.
- Если в день лечения вы моете руки, или любую другую часть тела после мытья необходимо повторно нанести крем или лосьон на вымытые участки кожи.
- Матери, кормящие грудью, должны смывать лосьон или крем с сосков перед каждым кормлением младенца, а после кормления — повторно наносить его.
- При лечении ребенка раннего возраста – следует надевать ему варежки на ручки, чтобы предотвратить слизывание ребенком лекарства.

- Одежда, полотенца, и постельное белье, которые соприкасались с заболевшим, должны быть постираны при температуре не ниже 50 С сразу после первого курса лечения. Такая температура убивает чесоточных клещей. Если какую-то вещь нельзя постирать в горячей воде, заверните ее в полиэтиленовые мешки и оставьте без использования не менее 72 часов – клещи погибнут от голода. Допустимо также с целью дезинфекции (дезинсекции) проглаживать ткани горячим утюгом, или помещать в горячую сушилку на 10-30 минут. Однако помните, что обработка высокой температурой предметов мебели, жилых помещений, или домашних животных – нецелесообразна и опасна.
Некоторым пациентам, имеющим симптомы вторичной бактериальной инфекции кожи, могут также понадобиться антибиотики.
Когда лечение неэффективно
Обратитесь к врачу повторно, если зуд сохраняется дольше 2-3 недель после лечения. Иногда первая обработка неэффективна, и ее приходится повторять. Наиболее распространенные причины неэффективности лечения против чесотки:
Наиболее распространенные причины неэффективности лечения против чесотки:
- Крем или лосьон применялся неправильно, с нарушением инструкций препарата.
- Имеется тесный контакт с больным человеком (повторное инфицирование).
Примечание: Помните, что зуд может сохраняться некоторое время после правильного и эффективного лечения, это нормально. Это связано с медленным угасанием аллергической реакции на клещей. Зуд может сохраняться 2-3 недели, а иногда даже до шести недель, и сам по себе он не является надежным признаком неэффективности терапии.
Более того, даже после успешного лечения иногда остаются единичные элементы красно-коричневой узелковой сыпи до 2 см в диаметре. Располагаются такие остаточные элементы чаще всего на половых органах и в подмышечных впадинах. Такая сыпь не говорит о том, что клещи не убиты, или что пациент еще заразен. Это кожная аллергическая реакция на клеща, и она может сохраняться весьма длительное время: от трех месяцев до одного года.
Лечение зуда
Зуд может доставлять значительные неудобства. Он может быть ослаблен или местными препаратами, или с помощью таблеток. Временное облегчение могут дать болтушки с ментолом. Следует избегать применения стероидных кремов, особенно если диагноз чесотки не является несомненным.
Антигистаминные препараты первого поколения также способны ослаблять зуд, и увеличивать сонливость – эти эффекты могут улучшить ваш сон.
Норвежская чесотка
Этот тип чесотки является довольно редким и необычным.
Это наиболее тяжелая форма чесотки, возникающая из-за гиперзаражения чесоточными клещами. При такой форме на человеке обитает несколько тысяч, или даже миллионов клещей, что вызывает чрезмерное шелушение кожи. Чрезмерная десквамация плюс огромное количество клещей – приводят к чрезвычайной заразности такого больного. Обильна сыпь, корки, тяжелые вторичные бактериальные инфекции кожи – делают эту форму болезни очень тяжелой для пациента.
Норвежская чесотка обычно встречается у лиц с резко ослабленным иммунитетом: у пациентов с ВИЧ/СПИДом, пациентов, получающих химиотерапию, у истощенных пациентов пожилого возраста и т.д.
Норвежская чесотка чаще, чем обычная, передается через контакт с полотенцами, постельными принадлежностями и тканью, покрывающей мягкую мебель. Клещи, распространяющиеся от больного норвежской чесоткой, способны выживать вне кожи человека до недели. Даже люди, имеющие минимальный контакт с больным норвежской чесоткой, такие как работники химчисток, способны заражаться, и потому должны получать лечение при устранении вспышки. Вспышка норвежской чесотки в здании, в котором в тесном контакте находится много человек с ослабленным иммунитетом, например в доме престарелых, является чрезвычайно сложной проблемой. В таких ситуациях абсолютно каждый человек, посещавший здание: престарелый пациент, персонал или родственники пациентов, нуждаются в активном лечении.
При контакте с больным норвежской чесоткой, у здорового человека с неповрежденной иммунной системой, развивается обычная чесотка. Чесотку у лиц с ВИЧ-инфекцией бывает очень сложно искоренить, нередки рецидивы даже после нескольких, самых тщательных курсов лечения.
При написании статьи использовались следующие материалы:
CDC — Чесотка — Биология
Возбудитель:
Sarcoptes scabiei var. hominis , чесоточный клещ человека, относится к классу членистоногих Arachnida, подклассу Acari, семейству Sarcoptidae. Клещи проникают в верхний слой кожи, но никогда не ниже рогового слоя. Норы выглядят как крошечные выпуклые змеевидные линии сероватого или телесного цвета и могут достигать сантиметра и более в длину. Другие расы чесоточного клеща могут вызывать заражение у других млекопитающих, таких как домашние кошки, собаки, свиньи и лошади.Следует отметить, что расы клещей, обнаруженные на других животных, могут вызывать самоограниченное заражение людей с временным зудом из-за дерматита; однако они не размножаются на человеческом хозяине.
Жизненный цикл:
Sarcoptes scabiei проходит четыре стадии своего жизненного цикла: яйцо, личинка, нимфа и взрослая особь. Самки откладывают 2-3 яйца в день, зарываясь под кожей. Яйца имеют овальную форму, длину от 0,10 до 0,15 мм и вылупляются через 3-4 дня. После вылупления яиц личинки мигрируют на поверхность кожи и зарываются в неповрежденный роговой слой, образуя почти невидимые короткие норы, называемые мешочками линьки.Личиночная стадия, которая выходит из яиц, имеет всего 3 пары ног и длится от 3 до 4 дней. После линьки личинок у получившихся нимф имеется 4 пары ног. Эта форма перед линькой превращается в личинок немного большего размера. Личинки и нимфы часто можно найти в мешочках линьки или в волосяных фолликулах, они похожи на взрослых особей, только меньшего размера. Взрослые особи — круглые, похожие на мешочки безглазые клещи. Самки имеют длину от 0,30 до 0,45 мм и ширину от 0,25 до 0,35 мм, а самцы чуть больше половины этого размера.Спаривание происходит после того, как активный самец проникает в линьку взрослой самки. Спаривание происходит только один раз, и самка остается фертильной на всю оставшуюся жизнь. Оплодотворенные самки покидают свои линяющие мешочки и блуждают по поверхности кожи, пока не найдут подходящее место для постоянной норы. Находясь на поверхности кожи, клещи держатся за нее с помощью присосок, прикрепленных к двум наиболее передним парам ног. Когда оплодотворенная самка клеща находит подходящее место, она начинает делать свою характерную змеевидную нору, откладывая при этом яйца.После того, как оплодотворенная самка зарывается в кожу, она остается там и продолжает удлинять норку и откладывать яйца до конца своей жизни (1-2 месяца). При самых благоприятных условиях около 10% ее яиц в конечном итоге дают начало взрослым клещам. Самцов можно увидеть редко; они делают в коже временные неглубокие ямки, чтобы питаться, пока не найдут норку самки и не найдут потомство.
Передача происходит в основном при передаче оплодотворенных самок при контакте кожа к коже от человека к человеку.Иногда передача может происходить через фомиты (например, через постельное белье или одежду). Человеческие чесоточные клещи часто обнаруживаются между пальцами рук и на запястьях.
Изображение жизненного цикла и информация любезно предоставлены DPDx.
CDC — Чесотка — Информационный бюллетень
Чесотка — это заболевание кожи, вызываемое клещами. Обычно это приводит к сильному зуду и появлению прыщавой кожной сыпи, которая может поражать различные участки тела. Чесотка заразна и может быстро распространяться в местах, где люди находятся в тесном физическом контакте.
Информационный бюллетень по чесотке — английский
Как я могу заразиться чесоткой?
Чесотка обычно передается при кожном контакте с больным чесоткой.
- Чесотка иногда передается косвенным путем при совместном использовании предметов одежды, полотенец или постельных принадлежностей, которыми пользуется зараженный человек.
- Чесотка легко распространяется в условиях скопления людей, где часто бывает тесный контакт тела и кожи.
Как я могу предотвратить чесотку?
Предотвратите чесотку, избегая контакта кожа к коже с человеком, у которого чесотка, и контакта с такими предметами, как одежда или постельное белье, используемое человеком, зараженным чесоточным клещом.
Косвенное распространение может происходить легче, если у человека есть корка чесотки.
Информационный бюллетень о чесотке — испанский
Каковы симптомы чесотки?
Общие симптомы зуда и прыщавой кожной сыпи могут поражать большую часть тела или ограничиваться общими местами, такими как:
- Между пальцами
- Запястье
- Колено
- Подмышка
- Гениталии
- Ниппель
- Талия
- Ягодицы
- Лопатки
Симптомы поражают голову, лицо, шею, ладони и подошвы у младенцев и очень маленьких детей, но обычно не у взрослых и детей старшего возраста.
Когда человек впервые заражается чесоточным клещом, обычно симптомы появляются через 2-6 недель после заражения. Если человек болел чесоткой раньше, симптомы появляются через 1-4 дня после заражения.
Зараженный человек может передавать чесотку, даже если у него нет симптомов, до тех пор, пока он не будет успешно вылечен и не уничтожены клещи и яйца.
Как лечить чесотку?
Чесотку следует лечить с помощью кремов для местного применения, которые могут убить клещей, которые можно приобрести по рецепту врача.Помимо зараженного человека, лечение рекомендуется также людям, с которыми они контактировали.
Постельное белье, одежда и полотенца, используемые зараженными людьми и людьми, с которыми они находятся в тесном контакте, должны быть обеззаражены. Для дезинфекции вещей,
- Вымойте их в горячей воде и высушите в горячей сушилке или сделайте химчистку.
- Храните вещи, которые нельзя стирать, в герметичном пластиковом пакете не менее 72 часов.
- Тщательно чистые и пылесосные помещения.
Дополнительную информацию о чесотке можно найти на сайте https: // www.cdc.gov/parasites/scabies/
CDC — Чесотка — Лечение
Предлагаемые общие руководящие принципы
Важно помнить, что первый раз, когда человек заболевает чесоткой, у него обычно нет симптомов. Симптомы обычно развиваются через 4-8 недель после заражения; однако они все еще могут распространять чесотку в это время.
Помимо зараженного человека, лечение также рекомендуется для членов семьи и сексуальных контактов, особенно для тех, кто имел длительный прямой контакт кожа к коже с зараженным человеком.Следует обследовать и лечить как половые, так и близкие личные контакты, имевшие прямой продолжительный контакт кожа к коже с инфицированным человеком в течение предыдущего месяца. Все люди должны проходить лечение одновременно, чтобы предотвратить повторное заражение. Чесотка иногда может передаваться половым путем у взрослых, но редко передается половым путем у детей.
Постельное белье, одежда и полотенца, используемые инфицированными людьми или их домашними, сексуальными и близкими контактами (как определено выше) в любое время в течение трех дней до лечения, должны быть обеззаражены путем стирки в горячей воде и сушки в горячей сушилке путем сушки. очистки, либо запечатыванием в полиэтиленовый пакет на срок не менее 72 часов.Чесоточные клещи обычно не выживают более чем на 2–3 дня вдали от кожи человека.
Не рекомендуется использовать инсектицидные спреи и фумиганты.
Лекарства, используемые для лечения чесотки
Продукты, используемые для лечения чесотки, называются чесоточными средствами, потому что они убивают чесоточных клещей; некоторые также убивают яйца клещей. Скабициды, используемые для лечения чесотки у человека, доступны только по рецепту врача. Никакие «внебиржевые» (безрецептурные) продукты не были протестированы и одобрены для лечения чесотки.Всегда внимательно следуйте инструкциям, содержащимся в коробке или напечатанным на этикетке. Всегда обращайтесь к врачу или фармацевту, если не знаете, как использовать конкретное лекарство.
Лосьон или крем против чесотки следует наносить на все участки тела от шеи до ступней и пальцев ног. Кроме того, при лечении младенцев и маленьких детей лосьон или крем от чесотки также следует наносить на всю их голову и шею, потому что чесотка может поразить их лицо, кожу головы и шею, а также остальную часть тела.Младенцам можно использовать только мазь с перметрином или серой. Лосьон или крем следует нанести на чистое тело и оставить на рекомендованное время, прежде чем смыть. После лечения следует носить чистую одежду. Следует обследовать и лечить как половые, так и близкие личные контакты, имевшие прямой продолжительный контакт кожа к коже с инфицированным человеком в течение предыдущего месяца. Все люди должны проходить лечение одновременно, чтобы предотвратить повторное заражение.
Всегда внимательно следуйте инструкциям, содержащимся в коробке или напечатанным на этикетке.Всегда обращайтесь к врачу или фармацевту, если не знаете, как использовать конкретное лекарство.
Поскольку симптомы чесотки возникают из-за реакции гиперчувствительности (аллергии) на клещей и их фекалии (сцибала), зуд может продолжаться в течение нескольких недель после лечения, даже если все клещи и яйца погибнут. Если зуд все еще присутствует более чем через 2–4 недели после лечения или если продолжают появляться новые норки или прыщавые высыпания, может потребоваться повторное лечение.
Зараженные язвы на коже следует лечить соответствующими антибиотиками, прописанными врачом.
Обзор Sarcoptes scabiei: прошлое, настоящее и будущее | Паразиты и переносчики
Происхождение чесоточного клеща Sarcoptes scabiei , паразитирующего на людях и многих семьях млекопитающих, неизвестно. Точно так же неизвестно, как давно началась коэволюция S. scabiei с конкретными млекопитающими-хозяевами и как она развивалась с течением времени. Однако акарологи и маммологи, использующие молекулярные инструменты и геномную информацию, могут со временем прояснить эти вопросы.
Ронкалли [1] и Фридман [2] рассказывают историю чесотки у людей и в ветеринарии с библейских времен до начала 1900-х годов. Самое раннее письменное упоминание о кожном заболевании людей и других млекопитающих, которое могло быть чесоткой, встречается в книге Левит в Библии (1200 г. до н.э.) [1]. Согласно Фридману [2], причинно-следственная связь между чесоточным клещом Acarus scabiei (ныне Sarcoptes scabiei ) и заболеванием человека была обнаружена Бономо и Честони в 1687 году, и «она впервые отметила создание история медицины однозначно известной причины любого из болезней человека ».Сегодня чесотка — это забытое, широко распространенное во всем мире заразное кожное заболевание человека и многих домашних и диких млекопитающих, вызывающее значительную заболеваемость и смертность.
Классификация чесоточных клещей
Sarcoptes scabiei первоначально был отнесен к роду Acarus и назван Acarus scabiei DeGeer, 1778. По мере развития номенклатуры клещей изменилась и классификация S. scabiei . Sarcoptes scabiei теперь помещен в суперсемейство Sarcoptoidea и семейство Sarcoptidae вместе со многими другими эктопаразитарными клещами млекопитающих.Среди акари S. scabiei принадлежат к надотряду Acariformes, отряду Sarcoptiformes, подотряду Oribatida, Infraorder Desmonomata и группе (гипоотряд) Astigmata (вместе с клещами домашней пыли Dermatophagoides farinae , Dermatophagoides farinae , Dermatophagoides farinae , D. maynei ) [3].
Семейство Sarcoptidae включает три подсемейства (Sarcoptinae, Teinocoptinae и Diabolicoptinae), включая 16 родов и 118 видов, которые все являются обитателями кожи млекопитающих [4, 5].Подсемейство Sarcoptinae включает четыре рода Sarcoptes (1 вид), Prosarcoptes (3 вида), Trixacarus (3 вида) и Kutzerocoptes (1 вид). И Sarcoptes , и Trixacarus caviae выглядят очень похоже, и их можно спутать. Trixacarus caviae является паразитом морских свинок и намного меньше, чем Sarcoptes [6]. Trixacarus caviae может вызывать зудящий дерматит у людей, которые держат зараженных морских свинок или имеют дело с ними [7].Помимо различий в размерах, есть несколько других особенностей, которые легко отличают Sarcoptes от T. caviae . Спинные щетинки у самок T. caviae простые, у S. scabiei — конусообразные и шиповидные, а спинные чешуйки у T. caviae более обширны, чем у S. scabiei , и простираются до задняя часть идиосомы [7]. Спинные щетинки sci, l1 и d1 у T. caviae не пластинчатые, как у S.scabiei (рис.1).
Рис. 1Электронные микрофотографии самки Sarcoptes scabiei var. hominis ( a ), S. scabiei var. suis ( b ) и S. scabiei var. canis ( c , d ), демонстрирующий спинные шипы, грубые кутикулярные бороздки и внутренние пластинчатые щетинки лопатки ( sci ), дорсальные щетинки ( d1 ) и спинной щиток (DS). Масштабные линейки : и , 100 мкм; b , 10 мкм; c , 100 мкм; d , 10 мкм
Морфология
Подробные описания S. scabiei со схемами были опубликованы ранее [2, 4,5,6]. Вкратце, S. scabiei имеет овальное черепахоподобное тело (идиосома), которое вентрально плоское и дорсально выпуклое (Рис. 1). Дорсальная идиосома несет толстые боковые ( l ) и дорсальные ( d ) щетинки, кутикулярные шипы и грубые поперечно-гребенчатые кутикулярные бороздки.Дорсальные щетинки sci, l1 и d1 пластинчатые (рис. 1г).
Все ноги у самок и самцов короткие и короткие (рис. 1, 2). Ноги III и IV у обоих полов не выходят за латерально-задний край идиосомы, в то время как ноги I и II выходят за передний край идиосомы с лапкой, на которой находится стебельчатый эмподиум, который заканчивается подушечкой (рис. 2а). . Ноги IV самцов также несут эмподиум на стебле, который заканчивается подушечкой. Все остальные ноги самцов и самок (III и IV ноги самок и III ноги самцов) оканчиваются длинными щетинками.На всех конечных сегментах ног как самцов, так и самок коготки (рис. 2). На конечных сегментах I, II, III и IV ног самок по два шпорцевидных когтя. У самцов по две шпорцевидных когтя на I, II и III ногах и по одной на четвертой.
Рис. 2Сканирующие электронные микрофотографии самки Sarcoptes scabiei var. канис . a Ноги I и II, показывающие лапку с когтями ( c ) и стебельком эмподиум ( e ), который заканчивается подушечкой. b Ноги III и IV с двумя когтями ( c ) и длинной щетинкой ( s ) на предплюсне. c Гнатазома (педипальпы и хелицеры) и нога I. Масштабные линейки : a , 10 мкм; b , 10 мкм; c , 10 мкм
Гнатосома (capitalum) состоит из коротких толстых хелицер и педипальп (рис. 2c). Анальное отверстие у самок является задним / дорсальным, а сосок копулятрисы в форме соска расположен кпереди от анального отверстия (рис.3). Средняя сырая и сухая масса самок составляет 5,62 ± 1,25 мкг и 2,8 ± 0,86 мкг соответственно [8]. Самцы намного мельче: влажный вес 1,49 ± 0,59 мкг и сухой вес 0,39 ± 0,16 мкг [8].
Рис. 3Сканирующая электронная микрофотография (вид сзади) самки Sarcoptes scabiei var. canis в норе в роговом слое, показывая дорсальное терминальное анальное отверстие ( a ) и копулятивный сосочек ( cp ) копулятивной сумки. Шкала : 10 мкм
Животные модели для изучения биологии чесоточного клеща
Отсутствие большого количества S.scabiei var. hominis клещей от человека ограничены обширными исследованиями биологии клещей чесотки человека. Иногда для этой цели можно получить большое количество клещей от пациента с покрытой коркой чесоткой (норвежская чесотка). Таким образом, многие биологические исследования, исследования взаимодействия с хозяином, иммунологические, протеомные и геномные исследования должны опираться на штаммы чесоточных клещей на животных и модели животных-хозяев, таких как кролики или свиньи. Если возможно прямое сравнение, var. canis и var. человекоподобных клещей клещей имеют сходную биологию.
В настоящее время доступны две модели на животных для распространения чесоточного клеща для изучения как клеща, его иммуномодулирующей способности, так и взаимодействий паразит-хозяин, и на них лежит большая часть знаний о чесоточных клещах, полученных за последние 30 лет. Модель чесотки кроликов и собак была разработана много лет назад [9]. Однако неясно, является ли это межвидовой моделью. Вполне может быть модель кролик / кролик. Первоначальным источником чесоточного клеща, использованного для экспериментального заражения кроликов, были бродячие собаки.Но эти собаки могли быть инфицированы от кроликов, на которых собаки охотились в пищу (переход от добычи к хищнику обсуждается в разделе «Переход от одного вида к другому»). Легкость, с которой кролики были заражены клещами, собранными у бродячих собак, предполагает эту возможность, но нет никакого способа узнать происхождение клещей. Другая модель, использованная в более поздних исследованиях, использует клещей свиней (вар. suis ) и свиней-хозяев [10].
Жизненный цикл
Стадии развития S.scabiei состоит из яйца, личинки, протонимфы, тритонимфы и взрослой особи. Этот жизненный цикл типичен для других астигматидных клещей. Существует значительная разница в продолжительности жизненного цикла S. scabiei var. человек . Сообщенная продолжительность жизненного цикла чесоточного клеща от человека составляет от 12 до 17 дней [11], от 17 до 21 дня [12], от 7 до 10 дней [13], от 9 до 15 дней [14] и около 15 дней [2]. ]. В исторической опубликованной литературе предполагается, что самки откладывают 40–50 или более яиц в течение 26–40 дней [2].
Систематическое исследование жизненного цикла S. scabiei var. In vivo. canis с использованием модели кролика сообщил, что продолжительность от яйца до взрослой особи составляет от 10 до 13 дней [15]. Личинки выходили из яиц через 50–53 ч инкубации. Продолжительность личиночной стадии составляла около 3-4 дней, тогда как для протонимфальной и тритонимфальной стадий она составляла около 2-3 дней для каждой стадии жизни. Для var. suis свиней [16].
Причины различий в заявленной продолжительности жизненного цикла S. scabiei неизвестны. Вариации, вероятно, связаны с трудностью наблюдения за их развитием в коже in vivo. Различные методы наблюдения, используемые для получения этой информации, различные условия температуры и относительной влажности во время периодов наблюдения, а также наблюдение за чесоточными клещами от разных хозяев могут быть способствующими факторами.
Ищет хост
Клещи Sarcoptes scabiei ищут источник стимулов, исходящих от хозяина, когда они находятся вне хозяина, но в непосредственной близости от него.Такое поведение может облегчить им поиск хозяина, если они вытеснены из него и загрязняют среду хозяина. Таким образом, прямой контакт с зараженным хозяином может не требоваться для людей и других млекопитающих, чтобы заразиться S. scabiei . В случае чесотки у человека источником инфекции могут быть живые клещи в постельных принадлежностях, мебели, игрушках и одежде. Sarcoptes scabiei var. человек были извлечены из мусорных баков в доме престарелых [17]. Для диких и домашних млекопитающих источником заражения чесоточными клещами могут служить общие или общие места для ночлега, стойла в сараях и загонах.
Эксперименты с вар. canis клещей, показали, что самки клещей, помещенные на металлическую проволоку (диаметром 1 мм, расположенные перпендикулярно хозяину и соприкасающиеся с ним) на разном расстоянии от хозяина, шли по проволоке к хозяину [18]. Более 68% протестированных самок клещей двигались к хозяину при размещении на расстоянии 4,9 см (1,93 дюйма) от него, в то время как 100% перемещались в этом направлении при размещении на расстоянии 4,2 см (1,65 дюйма). Около 20% тестовых клещей мигрировали к хозяину при размещении 11.На расстоянии 2 см (4,41 дюйма). Таким образом, способность воспринимать и реагировать на хозяина уменьшается с увеличением расстояния от источника. В этих экспериментах стимулом хозяина, который вызывал реакцию, мог быть запах тела и тепло, исходящие от хозяина, и / или CO 2 на выдохе.
Дополнительные эксперименты показали, что клещи будут искать источник теплового стимула без присутствия хозяина [18]. Более 83% самок клещей искали источник тепла на расстоянии 5,6 см (2,2 дюйма).Однако самки одинаково (по 50% на каждый) реагировали как на искусственный тепловой стимул, так и на запах от кожи хозяина, когда им давали выбор из двух одновременно и в непосредственной близости (2,5 см = 1 дюйм) к стимулам. На расстоянии 6,5 см (4,41 дюйма) от обоих стимулов 38% клещей выбрали стимулы от живого хозяина, 5% выбрали искусственный тепловой стимул при 32 ° C и 57% не выбрали ни одного, что предполагает, что запах хозяина был сильнее. аттрактант, чем тепло, когда два стимула предлагались вместе. 57%, которые не ответили ни на один из них, возможно, были сбиты с толку двумя стимулами, на которые они ответили, когда каждый из них предлагался отдельно, а теперь предлагался вместе, но с противоположных сторон.В других экспериментах с двумя вариантами выбора чесоточные клещи выбирали воздух, содержащий запах хозяина в отсутствие CO 2 , поэтому CO 2 не требуется для индукции ответа.
Mellanby et al. [19] наблюдали, что S. scabiei var. hominis , помещенный в температурный градиент от 20 ° C до 30 ° C, показал аналогичную термотаксическую реакцию. Sarcoptes scabiei var. hominis , помещенный ниже 24 ° C, переместился в более горячую часть градиента. Клещи не перемещались в районы с температурой ниже 24 ° C.
Эти эксперименты ясно показывают, что чесоточные клещи в окружающей среде рядом с хозяином воспринимают стимулы (запах, температуру тела) от хозяина и будут искать источник.
Фотоответ
Способность обнаруживать свет и его интенсивность могут быть важными факторами наряду с запахом хозяина и теплой температурой тела при обнаружении хозяина клещами Sarcoptes . Фотоответ чесоточного клеща широко не изучался. Sarcoptes scabiei var. hominis , как ранее сообщалось, не реагировал (положительно или отрицательно) на световой раздражитель, хотя данные не были представлены [19].Напротив, S. scabiei var. canis притягивается к люминесцентному потолочному свету в помещении при 63 фк (678 лм / м 2 ) и 100 фк (1076 лм / м 2 ) (Таблица 1). Большинство клещей, появившихся из чешуйчатой корки кожи, мигрировали на свет, а не оставались в темноте на арене наблюдения.
Таблица 1 Распространение Sarcoptes scabiei var. canis на арене выбора света / темноты после выпуска в темнотеВыживание вне хозяина
Контакт с инфицированным хозяином обычно считается основным способом заражения человека чесоткой.Эта идея во многом основана на исследованиях Мелланби [11], который обнаружил, что только 4 человека из 272 протестированных заразились чесоткой после сна в кроватях, используемых сильно инфицированными пациентами. Однако роль фомитов, выживаемость клещей вне организма-хозяина и их инфекционная способность в передаче чесотки никогда широко не исследовались. Способность чесоточных клещей выживать и оставаться заразными вдали от хозяина является ключевым фактором заражения хозяев клещами в окружающей среде.
Штаммы животных S. scabiei являются подходящими моделями для определения выживаемости и сохранения инфекционности клещей в среде хозяина. Исследование Arlian et al. [20] обнаружили, что S. scabiei var. canis самок выживали в течение недели или более при температуре 15 ° C (59 ° F) и относительной влажности (RH) выше 75% (рис. 4). При более высокой температуре 25 ° C (77 ° F) самки выживали 1-2 дня при всех тестируемых RH (рис. 4). Время выживания самцов вне хозяина было намного короче, чем у самок.Эти исследования показали, что обычно более высокие температуры резко сокращают время выживания при каждой влажности. В этом исследовании клещи явно умерли от обезвоживания из-за своей неспособности поддерживать водный баланс (вопрос будет рассмотрен позже). Более высокая относительная влажность и температура ниже 20 ° C позволили увеличить время выживания.
Рис. 4Наблюдаемое время для достижения 100% смертности в тестовых популяциях самок S. scabiei var. canis клещей подвергаются воздействию определенных комбинаций температуры и относительной влажности (RH).Количество клещей в каждой тестовой группе колебалось от 8 до 26. Данные из [20]
С другой стороны, S. scabiei var. hominis самки клещей натощак могут выжить 19 дней при 10 ° C и 97% относительной влажности и 8 дней при 10 ° C и 25% относительной влажности [20]. Sarcoptes scabiei var. hominis , которых держали вдали от хозяина с чередующимися 12-часовыми периодами при 4 ° C или 10 ° C и 95% относительной влажности и комнатных условиях (21 ° C и 45% RH) в течение 4 дней, оставались заразными и все еще могли проникать через кожу кролика [20].
Замораживание может быть средством уничтожения чесоточного клеща в таких предметах, как мягкие и твердые игрушки, маленькие подушки и постельные принадлежности. Замораживание женское вар. canis клещей при -25 ° C и 50% относительной влажности в течение 1,5 ч привели к 100% гибели. После 1 часа замораживания 23% тестовых клещей выжили, но они не начали проникновение, когда их поместили обратно на кожу хозяина [20]. Неизвестно, как долго эти клещи могут выжить при температуре от -15 ° C до -17 ° C, температуре обычной домашней морозильной камеры.
Mellanby et al.[19] определили точку термической смерти S. scabiei var. hominis самок, подвергшихся воздействию различных температур в течение 10 и 30 минут при относительной влажности 0–90%. Летальные температуры составляли 49 ° C (120 ° F) за 10 минут и 47,5 ° C (117,5 ° F) через 30 минут. После извлечения из организма-хозяина они обнаружили, что выживаемость составила 84,7, 30,5, 6,8, 1,7 и 0% в течение 1, 2, 3, 4 и 5 дней воздействия, соответственно, при 21,0–25,5 ° C и относительной влажности 90%. Выживаемость при 24–25 ° C и относительной влажности 30% составила 63,5, 6,8 и 0% через 1, 2 и 3 дня воздействия соответственно.Однако 61, 52, 35, 30 и 26% клещей выжили 5, 6, 7, 9 и 11 дней, соответственно, при относительной влажности 90%, но немногие клещи выжили 14 дней. Напротив, только 4 и 2% клещей выжили 2 и 4 дня соответственно при 30% относительной влажности. Таким образом, высокая относительная влажность и низкая температура также продлевают вар. hominis выживание клещей вне хозяина. Клещи действительно демонстрировали некоторую способность выдерживать отрицательные температуры. Все тестовые клещи выжили 2 дня при 0 ° C, а 28,6% выжили 8 дней.
Инфекционность
Важным аспектом передачи через окружающую среду (фомита) является то, как долго клещи остаются заразными, когда они находятся вне организма-хозяина.Как упоминалось ранее, время выживания вне организма-хозяина напрямую связано с относительной влажностью и температурой окружающей среды. Исследования с использованием кролика-хозяина и S. scabiei var. Штамм canis обнаружил, что большинство клещей, удерживаемых от хозяина в течение 24 часов, инициируют проникновение через кожу очень скоро после того, как их снова поместят на кожу хозяина [20]. Они стали наполовину или полностью погружены во вновь образовавшуюся нору в течение часа. Женский var. Клещи canis начинают проникать примерно через 20 минут, в то время как самцы, нимфы и личинки зарываются менее чем через 5 минут после того, как их помещают на кожу.Восемьдесят процентов самок, которых держали вдали от хозяина в течение 36 часов при относительной влажности 75% и 22 ° C, могли полностью проникнуть через кожу хозяина в среднем за 97 минут. Как отмечалось ранее, самки, которых держали вдали от хозяина в течение 24 часов, проникли через кожу за гораздо меньшее время, в то время как ни один клещ не выжил через 48 часов при относительной влажности 75% и 22 ° C. Для сравнения: живые чесоточные клещи человека (разновидность hominis ), полученные из постельного белья, в котором спали пациенты, сильно инфицированные чесоткой, могли инициировать проникновение через кожу в течение 10 минут после помещения на кролика и полностью проникнуть в течение 31 минуты [20]. .
Таким образом, в домах, школах и домах престарелых не следует требовать тщательной очистки, дезинфекции и стирки для уничтожения клещей чесотки в сухом климате. Если оставить кровать, спальню, постельное белье и одежду изолированными на 48 часов при комнатной температуре, чесоточные клещи погибнут. В сухом климате (<50% относительной влажности) клещи, вероятно, выживают и остаются заразными менее 36 часов.
Проникновение через кожу хозяина
Когда чесоточные клещи заражают хозяина, они сначала должны проникнуть через роговой слой эпидермиса кожи.Наблюдать за этим процессом под микроскопом — утомительная задача. Однако на всех стадиях жизни как S. scabiei var. canis и S. scabiei var. hominis экспериментально наблюдались под микроскопом, когда они проникали через кожу хозяина [20]. Клещи, помещенные на кожу, выделяют прозрачную жидкость (предположительно слюну), которая образует лужу вокруг их тела. Похоже, что роговой слой растворяется (лизируется), и клещ погружается в углубление на коже.Когда он тонет, ноги I и II, кажется, двигаются как черепаха (рытье, ползать / плыть). Действие ног продвигает клеща вперед, так как образуется туннель-нора в роговом слое. Время, чтобы полностью погрузиться в роговой слой, удивительно мало, как описано выше.
Водный баланс
Свежие тела самок и самцов S. scabiei var. canis содержат 57 ± 12% и 69 ± 18% воды по массе соответственно [8]. Получение межклеточной жидкости хозяина, по-видимому, необходимо клещам для получения достаточного количества воды для поддержания своего водного баланса [8].Некоторые виды клещей и клещей обладают способностью поддерживать водный баланс без попадания внутрь воды за счет поглощения воды из ненасыщенного окружающего воздуха, когда относительная влажность превышает критический уровень [21]. Например, родственные клещи домашней пыли, D. farinae и D. pteronyssinus , обладают активным механизмом извлечения воды из ненасыщенного воздуха с относительной влажностью выше примерно 70% для восполнения всей воды, которая теряется при испарении, выделениях и другие процессы в организме (выделение и дефекация) [22, 23].Обезвоженные клещи домашней пыли и клещи набирают воду и, следовательно, массу тела при помещении во влажный воздух с влажностью выше критического уровня. Чесоточные клещи, по-видимому, неспособны активно поглощать достаточное количество воды из ненасыщенного воздуха на поверхности кожи или в норе, чтобы поддерживать водный баланс, а при обезвоживании не могут восстановить потерянную воду из почти насыщенного воздуха (Таблица 2). Чесоточные клещи теряют воду в организме и обезвоживаются, когда их держат вдали от хозяина при относительной влажности 97,5% [8]. Таким образом, в отличие от клещей домашней пыли, чесоточные клещи не могут поглощать водяной пар из ненасыщенного окружающего воздуха, чтобы удовлетворить свои потребности в воде.Самки теряют 30–34% массы воды своего тела при выдерживании в течение 16 часов при 97,5% относительной влажности. Таким образом, они должны глотать / впитывать от хозяина воду, необходимую для поддержания водного баланса.
Таблица 2 Вес самок Sarcoptes scabiei var. canis сразу после удаления с хозяина (в сыром виде) и их вес после удерживания вне хозяина при относительной влажности 97,5% в течение 16 ч для трех групп клещейСкорость метаболизма (потребность в кислороде) чесоточных клещей была определена с использованием декартовской водолазной техники и недостаточна для обеспечения чесоточного клеща значительным количеством метаболической воды [8].
Обеспечение питанием
Чесотные клещи обитают в норах, которые они делают в неживом роговом слое эпидермиса кожи млекопитающих. Когда-то считалось, что эти клещи питаются лизированным роговым слоем. Однако последующие исследования показали, что клещи поглощают межклеточную жидкость (лимфу), которая просачивается в норку вокруг ротового аппарата клеща, когда они зарываются глубоко в роговой слой рядом с живой тканью (клетками) нижнего эпидермиса. Это подтверждают несколько линий доказательств.Как сканирующая электронная микроскопия, так и световая микроскопия показывают, что клещи в роговом слое кожи обитают на границе между прозрачным слоем и зернистым слоем [24,25,26], где межклеточная жидкость находится близко к месту расположения клеща и может проникать в нору. Кажется, что клещи зарываются вниз к дерме, чтобы сохранить это место, поскольку базальный слой клеток разрастается, а верхний слой сухого рогового слоя подталкивается к поверхности кожи. Демонстрация присутствия антител IgG хозяина в пищеводе и средней кишке свежих чесоточных клещей, удаленных от хозяина, является доказательством того, что эти клещи глотают сыворотку хозяина [27].Они, по-видимому, неспособны переваривать IgG и обладают относительно ограниченным набором ферментативной активности, что соответствует сывороточной диете [28].
Чесоточные клещи являются аэробными. Самки и самцы используют 0,00206 мкл O 2 / ч / клеща и 0,00076 мкл O 2 / ч / клеща, соответственно [8]. Экстраполируя это и используя модель-кролика-хозяина с инфицированными 30% площади поверхности тела, было установлено, что энергетические потребности клещей в организме хозяина незначительны, даже несмотря на то, что эти клещи получают все свое питание от хозяина.
Расположение чесоточных клещей на теле хозяина
Инфекции чесоточного клеща человека обычно локализуются в определенных частях тела. Руки, запястья и локти являются наиболее часто инфицированными участками у взрослых пациентов [11]. Однако гениталии, ступни, ягодицы, подмышечные впадины, грудь и талия также являются предпочтительными местами инфицирования [11].
Неизвестно, почему одни участки тела заражаются чаще, чем другие. Инфекции рук и запястий могут быть просто результатом прикосновения к инфицированным людям и работы с материалами, зараженными клещами.Однако характер распределения позволяет предположить, что клещи выбирают предпочтительные участки, и эти участки могут быть предпочтительны отчасти из-за липидного состава и других специфичных для участка факторов кожи на этих участках.
Arlian & Vyszenski-Moher [29] оценили реакцию на всех стадиях жизни S. scabiei var. canis до нескольких концентраций 21 липидного соединения, которые обычно обнаруживаются в эпидермисе кожи человека или на нем. Они обнаружили, что ряд этих липидов привлекает чесоточных клещей, включая 13 жирных кислот, 5 метиловых эфиров жирных кислот, холестерин, сквален и трипальмитин.Молярная концентрация, вызывающая наибольший отклик, варьировалась в зависимости от соединения. Сравнение различных стадий жизни показало, что реакция на стадиях жизни зависит от соединения и молярной концентрации этого конкретного соединения. В некоторых случаях одна стадия жизни реагировала на концентрацию соединения, а другая — нет. В целом, женщины были наиболее отзывчивыми.
Липидное содержание и липидные смеси кожи различаются в разных анатомических областях тела. Следовательно, трудно понять значение реакции чесоточного клеща на различные молярные концентрации этих изолированных липидных соединений.Пристрастие клещей к определенным участкам тела не изучено, но, вероятно, связано с взаимодействием множества факторов на коже и на коже. Исследование ясно продемонстрировало, что чесоточных клещей привлекали многие из липидов кожи, которые были протестированы, и поэтому липиды могут участвовать в привлечении клещей к предпочтительным участкам тела.
Агрегация, пол и феромоны сборки
Было замечено, что чесоточные клещи на всех этапах жизни покидают свои норы и блуждают по коже.Даже при небольшом количестве клещей на хозяине самцы и самки находят друг друга и спариваются. Вероятно, в этих процессах участвуют феромоны, выделяемые клещами. Было показано, что гуанин, другие пуриновые соединения и другие азотистые отходы паукообразных и фенольные соединения являются феромонами сборки-притяжения-прикрепления или половыми феромонами у клещей и клещей [30,31,32,33,34]. Другие акари, такие как S. scabiei , вероятно, продуцируют аналогичные соединения и реагируют на них. В исследовании Arlian & Vyszenski-Moher [35] 10 азотистых метаболитов и 3 фенольных соединения были предложены отдельно для всех стадий жизни S.scabiei var. канис. Гуанин, пурин, аденин, аллантоин, гипоксантин, ксантин, мочевая кислота, хлорид аммония, нитрат аммония и сульфат аммония привлекли значительное количество клещей чесотки. Все этапы жизни также были значительно привлечены тремя тестируемыми фенольными соединениями. К ним относятся 2,6-дихлорфенол, метилсалицилат и 2-нитрофенол. Самки ответили на большинство концентраций различных соединений, а мужчины — на наименьшее.Похоже, что азотистые и фенольные соединения могут действовать как феромоны для чесоточных клещей, как и для других акари.
Взаимодействие паразит-хозяин (иммунная модуляция)
По мере того, как чесоточные клещи проникают в кожу, они выделяют вещества, которые вызывают воспалительные и иммунные реакции хозяина, а также вещества, которые могут подавлять определенные аспекты этих реакций, позволяя клещам обходить защитные механизмы хозяина. Последний помогает клещам изначально выжить в коже хозяина и создать популяцию.На границе раздела клещ-кожа происходит сложное взаимодействие, которое определяет баланс между двумя конкурирующими процессами с течением времени и, следовательно, течение инфекции и возможное проявление клинических симптомов. Поскольку кожные симптомы не проявляются в течение четырех или более недель при первичной инфекции, похоже, что на ранней стадии первичной инфекции врожденные / иммунные события подавляются, но со временем, по мере размножения клещей и создания популяции, происходит переход к проявляются более доминирующие воспалительные и иммунные реакции и симптомы заболевания.Что является причиной сдвига, неизвестно, но неоспоримые доказательства того, что чесоточные клещи, как и многие другие паразиты, могут модулировать различные аспекты врожденных и адаптивных иммунных ответов млекопитающих. Выявленные иммуномодулирующие способности клещей включают противовоспалительную, противоиммунную активность и активность против комплемента.
Из-за того, что клещ находится на границе раздела межклеточной жидкости в эпидермисе, растворимые вещества (включая слюну, ферменты и гормоны линьки, фекалии и азотистые выделения) от клещей, обладающие антигенной и фармакологической активностью, диффундируют в жидкость, омывающую клетки эпидермис и дерма.Эти вещества вызывают ответы клеток в этих тканях, включая кератиноциты, фибробласты, макрофаги, тучные клетки, лимфоциты, клетки Лангерганса и другие дендритные клетки, а также эндотелиальные клетки микрососудов.
Исследования in vitro показывают, что молекулы в экстракте всего тела S. scabiei var. canis стимулировал культивированные нормальные эпидермальные кератиноциты человека для значительного увеличения секреции интерлейкина-6 (IL-6) и фактора роста эндотелия сосудов (VEGF), а также для незначительного увеличения секреции фактора стимуляции колоний гранулоцитов (G-CSF) [36].Никакого влияния на секрецию IL-1α и IL-1β не наблюдалось. Кроме того, экстракт чесоточного клеща вызывал снижение секреции агониста рецептора IL-1 (IL-1ra) и IL-8 этими клетками после того, как они были стимулированы липополисахаридом (LPS). Аналогичным образом, вещества в этом экстракте стимулировали культивированные нормальные дермальные фибробласты человека для увеличения секреции IL-6, IL-8, G-CSF и VEGF. В коже коллективная повышающая регуляция IL-6 и VEGF, сопровождаемая понижающей регуляцией IL-1ra, будет способствовать воспалению (хотя IL-6 может выполнять как провоспалительные, так и противовоспалительные функции).VEGF способствует увеличению проницаемости сосудов, что принесет пользу клещу, предоставив ему больше питательной сыворотки, которую он может проглотить.
Последующее исследование показало, что S. scabiei var. canis экстракт в присутствии провоспалительных цитокинов (IL-1α, IL-1β и фактор некроза опухоли α [TNFα]) вместе с IL-17, которые, вероятно, присутствуют в скабиетических поражениях in vivo , все еще подавлены Уровни ИЛ-8 в супернатантах как эпидермальных кератиноцитов человека, так и дермальных фибробластов через 8 ч, но этот эффект со временем исчез [37].Секреция гранулоцитарно-макрофагального колониестимулирующего фактора (GM-CSF) фибробластами также уменьшалась. Это исследование также показало, что молекулы экстракта чесоточного клеща индуцировали секрецию связанного с ростом онкогена-α (GROα), трансформирующего фактора роста-α (TGFα) и кожного хемокина, привлекающего Т-клетки (CTACK) из кератиноцитов, и подтвердили усиленную секрецию ИЛ-6 и Г-КСФ из фибробластов. Сдвиг уровней IL-8 в супернатантах, вероятно, связан с присутствием в экстракте клещей двух разных молекул: одной, которая стимулирует выработку IL-8, а другой связывается с IL-8 по мере его производства [37].Известно, что клещи продуцируют белок, связывающий IL-8 (Evasin-3), который избирательно связывает и нейтрализует IL-8, подавляя рекрутирование нейтрофилов в место инвазии паразитов [38,39,40].
В живой коже кератиноциты, фибробласты и эндотелиальные клетки микрососудов взаимодействуют друг с другом в коллагеновой матрице и общаются с помощью цитокинов, хемокинов и контакта. Эти взаимодействия могут влиять на реакцию отдельных типов клеток на экстракт чесоточного клеща. Кроме того, живые клещи могут выделять вещества, которые количественно и качественно отличаются от компонентов экстракта всего тела.Таким образом, для моделирования реальной кожи эквиваленты кожи человека (HSE) были заражены S. scabiei var. canis и живыми клещами [41]. Модель HSE состоит из дермы фибробластов в коллагеновой матрице, расположенной ниже эпидермиса, состоящей из слоя многослойных кератиноцитов. Модель HSE допускает взаимодействие фибробластов и кератиноцитов, которое происходит in vivo при стимуляции чесоточными клещами и их продуктами, что невозможно наблюдать в экспериментах по монокультуре клеток.Живые клещи проникают в роговой слой этих эквивалентов кожи точно так же, как они делают это в неповрежденной коже хозяина [41]. Роющие клещи индуцировали секрецию CTACK, стромального лимфопоэтина тимуса (TSLP), IL-1α, IL-1β, IL-1ra, IL-6, IL-8, моноцитарного хемоаттрактантного белка-1 (MCP-1), GM-CSF, и фактор, стимулирующий колонии макрофагов (M-CSF), на поверхность HSE. Основное различие между ответом на экстракт клещей монокультурных кератиноцитов и фибробластов заключалось в том, что HSE продуцировал значительные количества провоспалительных цитокинов IL-1α и IL-1β и их ингибитора IL-1ra в ответ на роющих клещей.Повышенная регуляция IL-1ra может быть важной частью механизма, используемого этими клещами для подавления воспалительной реакции хозяина, позволяя создать популяцию клещей.
Исследования экспрессии генов в HSE также подтвердили и расширили результаты экспериментов по монокультуре in vitro. Чесоточные клещи, зарывающиеся в HSE, индуцировали повышенную экспрессию 189 генов и подавляли экспрессию 152 генов в кератиноцитах и фибробластах в этих HSE [42].Гены ряда цитокинов были активированы, что соответствовало профилям секреции цитокинов, описанным выше [41]. Особо следует отметить усиление концентрации IL-20. Этот цитокин способствует пролиферации кератиноцитов, и его активная регуляция может способствовать развитию чешуйчатой и покрытой коркой кожи, что характерно для хронической чесотки. Кроме того, наиболее активным был ген кератина 1 типа, преобладающего структурного белка в кератиноцитах. Многие другие гены подавлялись, когда клещи зарывались в HSE, включая несколько членов семейства цитохрома p450.Отсылаем читателя к [42], чтобы ознакомиться с полным списком генов, которые дифференциально экспрессировались в ответ на закапывание клещей S. scabiei в модели HSE.
Культивированные эндотелиальные клетки кожных микрососудов человека кожи, стимулированные S. scabiei var. canis Экстракт снижает индуцированную TNFα экспрессию молекул клеточной адгезии Е-селектина и молекулы адгезии сосудистых клеток-1 (VCAM-1), а также уровни IL-8, одновременно повышая экспрессию цитокинового рецептора CXCR-1 [ 43].Последующее исследование подтвердило, что экстракт чесоточного клеща все еще способен снижать TNFα-индуцированную экспрессию VCAM-1 в присутствии некоторых провоспалительных медиаторов (например, гистамина, лейкотриена B4 и цитокинов IL-1), которые могут возникать при чесоточных поражениях in vivo [44]. . Вызванная IL-1α и IL-1β секреция IL-6 также снижалась в присутствии экстракта чесоточного клеща.
Исследования in vitro показывают, что мононуклеарные клетки периферической крови (PBMC, в основном моноциты) от здоровых доноров-людей, стимулированные S.scabiei var. Экстракт canis активирует секрецию IL-1β, IL-6, IL-8 и TNFα [45]. Дендритные клетки, полученные из этих моноцитов, подавляли секрецию IL-6 и IL-8 после того, как они были стимулированы LPS для индукции секреции этих цитокинов [45]. Аналогичным образом Walton et al. [46] обнаружили, что PBMC от пациентов с обычной чесоткой продуцируют более высокие уровни IL-5 и IL-13 и более низкие уровни гамма-интерферона (IFNγ) при стимуляции рекомбинантной цистеиновой протеазой человека Yv5032C08.PBMC от пациентов с обычной чесоткой или чесоткой с коркой также показали сильный пролиферативный ответ при стимуляции этой молекулой.
В другом исследовании смешанные популяции лимфоцитов и моноцитов от здоровых доноров (с предшествующей сенсибилизацией к чесотке и без нее) стимулировали S. scabiei var. canis экстракт [47]. У всех доноров наблюдалась повышенная секреция IL-10 и IFNγ в ответ на стимуляцию экстрактом чесотки. Отсутствие продукции IL-2 или IL-4 предполагает, что регуляторные Т-клетки (Treg) ответственны за создание этого цитокинового профиля.Аналогичным образом, PBMC от людей, не подвергавшихся воздействию чесотки, вырабатывали повышенный уровень IL-10 при стимуляции цистеиновой протеазой Yv5032C08 [46]. Повышенная регуляция продукции IL-10 является значительной, поскольку этот цитокин подавляет воспалительные и иммунные реакции у людей и, таким образом, может способствовать отсроченному проявлению клинических симптомов, характерных для ранних инфекций чесотки.
Проникая в нижний эпидермис кожи, чесоточные клещи поглощают плазму хозяина, которая содержит антитела хозяина [27] и другие компоненты плазмы, включая сериновые протеазы, комплемент и другие ферменты, которые могут повредить слизистую оболочку кишечника клеща, которая имеет решающее значение для переваривание и усвоение питательных веществ.Кишечник клеща секретирует, помимо прочего, каталитически неактивные паралоги сериновых протеаз (SMIPP) [48, 49]. SMIPPs могут ингибировать активность комплемента, связывая C1q, маннозу-связывающий лектин и пропердин в трех путях комплемента, и, таким образом, они защищают слизистую оболочку кишечника клеща от атаки комплемента и повреждения [48,49,50]. Кроме того, ингибиторы сериновых протеаз (серпины), также называемые SMS (от чесоточных серпинов клещей), локализуются в кишечнике и кале клеща [51]. Два рекомбинантных серпина, SMS B3 и SMS B4, могут неэффективно ингибировать сериновые протеазы млекопитающих, но не сериновые или цистеиновые протеазы клещей.Mika et al. [51] показали, что эти серпины клещей могут связываться с несколькими белками плазмы в классической, альтернативной и лектиновой системах комплемента человека, а также, возможно, блокировать или снижать эффективность всех трех систем комплемента. Следовательно, эти клещи развили множество молекул, позволяющих им защищаться от защитных механизмов комплемента хозяина.
Вторичные бактериальные инфекции часто развиваются при чесоточных поражениях и сопровождают чесоточную инфекцию [52,53,54].Ингибиторы комплемента SMIPP и SMS в фекалиях клещей могут способствовать выживанию и росту бактерий на коже хозяина [52, 53]. Клещи откладывают фекальные шарики в норе позади себя, когда кормятся, и удлиняют нору. Таким образом, выделенные фекальные гранулы, содержащие SMIPP и SMS, которые откладываются на коже, могут ингибировать активность комплемента хозяина в коже / плазме, окружающей клещей, а также ингибировать атаку комплемента на бактерии в поражении и, таким образом, способствовать колонизации бактерий, которые часто сопровождает хроническую чесотку.
В совокупности все эти сложные взаимодействия, вероятно, задерживают иммунный и воспалительный ответ на ранней стадии инфекции, пока создается популяция клещей. Эта задержка в конечном итоге преодолевается, когда популяция клещей достигает порогового значения и возникает воспалительная реакция.
Ответ клеток первичной лимфоидной ткани хозяина на молекулы чесотки
Исследования на мышах показывают, что экспрессия мРНК молекулы межклеточной адгезии-1 (ICAM-1), ICAM-2, VCAM-1 и L-селектина и Рецепторы TNF I и II (TNF RI и TNF RII) в ткани селезенки были снижены у мышей, подвергшихся воздействию живых S.scabiei var. canis (первичный ответ) [55]. Напротив, мышей, сначала иммунизированных штаммом S. scabiei var. canis , а затем воздействие живых чесоточных клещей (вторичный ответ) действительно увеличивало экспрессию генов для ICAM-1, ICAM-2, TNF RI и RII. Это говорит о том, что иммунизация соответствующими антигенами чесоточного клеща будет полезна для снижения способности клещей подавлять иммунный ответ и, таким образом, может помочь защитить от чесотки.
Кроме того, экспрессия мРНК B- и T-клетками селезенки мышей, подвергшихся воздействию живых чесоточных клещей, демонстрировала пониженную экспрессию B7–2 / CD86, CD4, CD8 и CD45 [55].Эти мембранные молекулы играют ключевую роль во взаимодействии В-клеток и клеток-помощников Th3, а также между клетками-помощниками Th2 и цитотоксическими Т-клетками в иммунной реакции, и предполагает, что чесоточные клещи производят что-то, что может подавлять иммунную реакцию в лимфоидной ткани.
Профиль Т-хелперов спленоцитов и лимфатических узлов также определялся у мышей [56]. У мышей, подвергшихся воздействию живых чесоточных клещей, увеличивалась продукция IL-4 клетками лимфатических узлов и IFNγ спленоцитами. Напротив, мыши, иммунизированные экстрактом клещей до заражения, смещали ответ клеток лимфатических узлов с ответа Th3 (IL-4) на ответ Th2 (INFγ).
Геномика чесоточных клещей
Развитие молекулярных методов открыло новые направления исследований для понимания биологии чесоточных клещей и взаимодействия между клещами и их хозяевами. Геномы S. scabiei var. канис [57], вар. hominis [58, 59] и var. suis [58, 59] в настоящее время секвенированы, и эти данные доступны для использования в качестве инструментов для выяснения филогенетических взаимоотношений и предпочтений хозяев чесоточных клещей, паразитирующих на различных млекопитающих, идентификации белков, участвующих в модуляции защитных реакций хозяина, и идентификации генов, кодирующих для белков, которые являются антигенными и могут быть кандидатами для включения в вакцину или диагностический анализ крови.
Аннотированный S. scabiei var. canis. Проект генома был получен и доступен в базах данных NCBI и VectorBase [57], в то время как var. hominis и var. suis геномные данные доступны в репозиториях NCBI и GigaScience [58, 59]. В целом геномы трех штаммов очень похожи. Вариант var. canis Геном содержал гены для 10 644 предсказанных белков [57], в то время как var. Геном hominis содержал 13 226 предполагаемых кодирующих последовательностей [58].Для сравнения: оба генома чесоточного клеща имеют меньше генов, чем прогнозировалось для четырех других акари с аннотированными геномами на сегодняшний день. Пылевой клещ Dermatophagoides farinae содержит 16 376 предсказанных белков, в то время как паутинный клещ Tetranychus urticae имеет 18 423 белка, олений клещ Ixodes scapularis — 20 474, а мезостигматидный клещ Metasei, 63620, 6119, Metasei, 636, 640, Occidentalis. ]. S. scabiei var. canis Геном содержит 3351 предсказанный белок, которые не являются ортологами белков, присутствующих в других клещах [57].Это важно, потому что смешивающим фактором при идентификации белков, которые необходимо включить в вакцину или использовать в анализе крови для точного выявления инфекции чесотки, является перекрестная реактивность между многими белками чесоточного клеща и повсеместно распространенными антигенами пылевого клеща.
Используя предсказанный протеом, можно было окончательно идентифицировать> 150 белков, присутствующих в водорастворимых и нерастворимых экстрактах целых тел клещей, с помощью масс-спектрометрии MALDI-TOF / TOF [64]. Многие из этих белков распознаются IgM и / или IgG в сыворотке крови пациентов с обычной чесоткой и могут быть кандидатами для включения в диагностический тест для этого заболевания.Другие не связывают циркулирующие антитела и могут участвовать в модуляции иммунной защиты хозяина для защиты клеща.
Геном также был исследован для идентификации предсказанных белков, которые могут быть связаны с взаимодействиями чесоточного клеща-хозяина и с выбранными важными биологическими процессами [65].
Генетическое разнообразие чесоточных клещей
Одно из первых молекулярно-биологических исследований S. scabiei выявило микросателлиты множественных нуклеотидных последовательностей в частичной геномной библиотеке S.scabiei var . hominis [66]. Среди них повторы динуклеотидного GA (гуанин-аденин) были относительно многочисленными с длиной повтора до 20. Было высказано предположение, что выбранные микросателлитные паттерны могут быть использованы для дифференциации между различными популяциями клещей.
Использование описанного выше метода ДНК-фингерпринта на чесоточных клещах от людей и собак дало некоторые интересные выводы о генетической изменчивости S. scabiei как внутри, так и между видами хозяев [67].Было обнаружено, что образцы микросателлитных нуклеотидных повторов у клещей, собранных у людей в северной Австралии и в Панаме, значительно отличаются от ДНК, выделенной из клещей, собранных у собак (некоторые из тех же мест), что позволяет предположить, что два штамма клещей имеют разные циклы передачи, даже для инфицированные люди и собаки, живущие в одном доме. Таким образом, чесоточные клещи от собак вряд ли являются источником стойких инфекций чесотки у людей, по крайней мере, в северо-западной Австралии.Сравнивая чесоточных клещей от собак в сообществе, они обнаружили, что могут быть значительные генотипические различия, а могут и не быть. Последние данные свидетельствуют о наличии значительных субпопуляций S. scabiei у собак. Когда они сравнили различные человеческие изоляты, обнаружилась также значительная генетическая изменчивость между чесоточными клещами из разных домохозяйств в пределах сообществ в Австралии, но небольшая генетическая дифференциация между чесоточными клещами от людей в одном доме. Последнее открытие указывает на общий источник чесоточного клеща для инфицированных людей, живущих в одном доме.Аналогичным образом, генетические различия существовали между чесоточными клещами от людей в сообществах в Австралии и чесоточными клещами от людей в Панаме. Взятые вместе, эти данные свидетельствуют о наличии субпопуляций чесоточных клещей в пределах одного вида-хозяина, и это повышает вероятность появления нескольких видов чесоточных клещей у людей и других популяций хозяев. Эта концепция была недавно подтверждена исследованиями в Китае, предполагающими, что существует множество различных штаммов (видов) чесоточных клещей, паразитирующих на людях [68].На основе гена субъединицы 1 митохондриальной цитохрома c оксидазы (мтДНК cox 1), Sarcoptes от людей в Австралии, Панаме и двух популяциях в Китае, как сообщается, представляют 4 различных вида Sarcoptes [68] .
Исследования по анализу рибосомной второй внутренней транскрибируемой спейсерной ДНК (рДНК ITS2) и митрохрондриальной 16S ДНК (мтДНК 16S) не обнаружили межвидовых различий между клещами Sarcoptes , собранными от разных видов хозяев [69,70,71,72].Однако другие исследования, в которых анализировали мтДНК 16S и мтДНК cox 1 и рДНК ITS2 чесоточных клещей от разных животных-хозяев, обнаружили, что они обнаруживают различия [73, 74]. Аналогичный анализ Zhao et al. [68] идентифицировали чесоточных клещей от людей и чесоточных клещей от собак в Китае как отдельные популяции Sarcoptes , но люди могли быть инфицированы Sarcoptes от собак [68]. Однако они также пришли к выводу, что на основе гена мтДНК cox 1 длиной 317 п.н. чесоточные клещи буйволов, кроликов, овец, вомбатов, валлаби, свиней, шимпанзе и собак принадлежат к одному и тому же виду и что чесоточные клещи от людей являются отдельный вид от вида животных [68].
Аналогично, Andriantsoanirina et al. [75] путем анализа митрохондриального гена, кодирующего 12S-рРНК клещей от разных хозяев, пришел к выводу, что клещи от вомбатов, собак и людей не отличаются филогенетически и что чесотка у вомбатов в Австралии, вероятно, произошла от людей и / или их животных. Это контрастирует с более ранним исследованием, которое показало, что клещи, собранные у вомбатов, не группируются с клещами, полученными у людей или собак [67].
Другое исследование с использованием cox 1 той же группы [76] также показало, что чесоточные клещи человека не составляют единую гомогенную популяцию.Кроме того, используя полиморфизмы гена cox 1 клещей от людей во Франции, собак и данные из GenBank, они пришли к выводу, что чесоточные клещи от людей были распределены по трем генетически различным и изолированным кладам (A, B и C) и что собака и человек клещи генетически не отличались. Кроме того, Clade C содержал чесоточных клещей от людей и 12 других видов хозяев (собаки, кролики, шимпанзе, свиньи, овцы, водяные буйволы, крупный рогатый скот, вомбат, валлаби, енотовидные собаки, серы и куницы), и этот поток генов происходит между клещами из разных видов. хосты.
Исследование Mofiz et al. [59] сообщили, что последовательности митохондриального генома клещей, собранные у людей, свиней и собак, очень похожи. Затем они идентифицировали однонуклеотидные полиморфизмы (SNP), которые были использованы для обнаружения шести гаплотипов среди var. hominis и var. suis образцов. Данные показали, что клещи от одного пациента-человека выглядели по существу клональными, в то время как клещи, собранные от другого пациента, демонстрировали сильно расходящиеся гаплотипы, в том числе те, которые сгруппировались с гаплотипами, присутствующими у клещей от свиней.
Исследования с использованием микросателлитной ДНК для изучения генетического разнообразия между симпатрическими и несимпатрическими хозяевами и их паразитами чесоточного клеща предоставили некоторую дополнительную интересную косвенную информацию о специфичности хозяина и генетическом разнообразии [74, 77,78,79]. Как правило, микросателлитный анализ предполагает, что существует только один сильно изменчивый вид S. scabiei [74, 77,78,79]. Тем не менее, микросателлитное генотипирование отдельных клещей S. scabiei , собранных в трех европейских странах из 15 популяций диких млекопитающих, принадлежащих к 10 видам хозяев, сгруппированных в 3 группы (производные от таксона-хозяина): полученные от травоядных, полученные от плотоядных и всеядные. [80].Как правило, результаты микросателлитного анализа показывают отсутствие потока генов между этими группами, но поток генов может происходить внутри группы. Однако виды млекопитающих, свободные от чесотки, могут жить в той же географической области, что и паршивые животные, поэтому физиологические, иммунные защиты и другие свойства хозяина предотвращают передачу и колонизацию между различными симпатрическими потенциальными видами хозяев.
Возможно, что генетический состав (наличие и частота аллелей) штамма чесотки может изменяться (дрейфовать) с течением времени.Alasaad et al. [78] с использованием одного мультиплекса из 9 микросателлитных локусов дополнительно исследовали временное генетическое разнообразие в популяциях клещей за 11 лет и обнаружили незначительные изменения в генетическом разнообразии S. scabiei среди симпатрических популяций диких млекопитающих с S. scabiei в популяциях. из пиренейской серны в Астурии (Испания) благородный олень, косуля и рыжая лисица.
Неясно, насколько специфичен для хозяина S. scabiei , собранный от разных млекопитающих-хозяев, и существует ли несколько видов Sarcoptes как внутри, так и между видами хозяев.Исследования кроссбридинга невозможны, а исследования перекрестной инфекционности очень ограничены. Результаты молекулярных исследований дают некоторое интересное понимание этого вопроса, но также не дают однозначных ответов, поскольку в этих исследованиях использовались различные ядерные, рибосомные и митохондриальные гены.
Перекрестный перенос между хозяевами
Клещи от собак, инфицированных чесоткой, могут вызывать постоянные инфекции у домашних кроликов, и эти клещи могут повторно заражать собак [9]. Это говорит о том, что бродячие / выездные домашние собаки и дикие собаки, которые охотятся на диких кроликов с чесоткой, могут заразиться чесоткой от этих хозяев, и, таким образом, чесотка является перекрестной инфекцией между некоторыми видами собак и кроликами-хозяевами.Аналогичным образом было показано, что дикая серна с чесоткой заражает домашних коз, и наоборот, а красные лисицы чесоткой могут заражать домашних собак [81]. Анализ девяти микросателлитных маркеров позволяет предположить, что еноты в Германии могут заразиться чесоткой от зараженных чесоткой красных лисиц [82].
В другом анализе с использованием множества из 9 микросателлитных маркеров Oleaga et al. [83] сравнили генетическое разнообразие чесоточных клещей, собранных у симпатрических иберийских волков, серны, благородного оленя, косули и лисицы.Клещи иберийского волка обладали наибольшим генетическим разнообразием. Это говорит о том, что переход от добычи к хищнику может изменить взаимоотношения таксонов хозяина. Казалось бы логичным, что передача паразита от жертвы к хищнику и коэволюция паразита в этих ассоциациях хищник-жертва важны для передачи S. scabiei между хозяевами и, таким образом, совместного использования общего штамма S. scabiei между хозяевами. жертва и хищник весьма вероятны. Gakuya et al. [84, 85] предложили переход от добычи к хищнику между дикими кошачьими и копытными в Африке.
Диагностика и анализ крови на чесотку
Диагностировать чесотку у людей с покрытой коркой чесотки, а также у домашних и диких животных с запущенной чесоткой (включая собак, лис, койотов, оленей, коз, серну, кроликов и др.) Несложно, потому что на них обитают тысячи клещей, которых легко соскоблить с кожи. Однако ранняя диагностика заражения обычными клещами чесотки очень трудна у людей и других млекопитающих, потому что на ранней стадии заражения поражается очень мало клещей, и в течение многих недель симптомы отсутствуют или проявляются с минимальными симптомами.Сообщается, что количество взрослых клещей, обнаруживаемых у человека с обыкновенной чесоткой, невелико и составляет менее 15 (в среднем 11,2) [86]. Это количество основано на обследовании около 900 взрослых пациентов. Ранние инфекции чесотки у собак и других животных также вызывают мало клещей. Это очень затрудняет постановку диагноза чесотки по ссадине кожи. Кроме того, диагностика чесотки осложняется еще и тем, что клинические проявления чесоточной инфекции сходны с клиническими проявлениями других кожных заболеваний (атопический дерматит, экзема, псориаз, опрелости, укусы насекомых, ядовитый плющ и т. Д.).) и кожные заболевания, вызванные раздражающими веществами (мыло / моющие средства, лосьоны, ароматизаторы, металлы, латекс, резина и другие химические вещества). Предположительный диагноз может быть поставлен на основании клинических симптомов, таких как сильный зуд, сыпь и эритематозные пятна, но окончательный диагноз ставится на основании микроскопического исследования клещей, их яиц и / или фекальных гранул, а также бороздок в эпидермисе, которые удаляются из эпидермиса. кожу соскребом скальпелем. Однако найти и соскоблить чесоточные поражения может быть сложно.Таким образом, существует большой интерес к разработке диагностического анализа крови на чесотку как у людей, так и у животных. Ясно, что инфекции чесоточного клеща вызывают гуморальный ответ хозяина, который приводит к циркуляции антител (которые могут быть, а могут и не быть защитными). Таким образом, анализ крови возможен, но все же требует значительных исследований для достижения почти 100% специфичности и чувствительности. Анализ крови, основанный на обнаружении сывороточных антител к антигенам чесоточного клеща, будет большим преимуществом для ранней диагностики чесотки, когда выявление клещевого материала в соскобе кожи затруднено.
Анализ крови для диагностики инфекции чесотки требует идентификации и выработки соответствующих антигенов чесоточного клеща, а также определения соответствующего изотипа и специфичности антител хозяина. Адекватные количества чесоточных клещей нельзя массово культивировать in vivo или in vitro для получения больших количеств антигена для использования в диагностическом тесте или для разработки вакцины для защиты от инфекции. Из-за нехватки клещевого материала молекулы антигена, необходимые как для диагностического теста, так и для разработки вакцины, вероятно, будут зависеть от идентификации и производства рекомбинантных молекул, которые распознаются циркулирующими антителами, которые хозяин вырабатывает в ответ на активное заражение чесоткой.Некоторые рекомбинантные молекулы были получены и исследованы с этой целью на собаках, свиньях и кроликах. Прогресс наблюдается, но ключевые рекомбинанты еще предстоит идентифицировать. Одной из проблем, которые необходимо преодолеть при разработке этого теста, является высокий уровень перекрестной реактивности между антигенами чесоточных клещей и антигенами родственных повсеместно распространенных клещей домашней пыли. Высокий процент людей во всем мире страдает аллергией на клещей домашней пыли и вырабатывает антитела IgE и IgG к своим аллергенам и антигенам соответственно.Серологический тест, основанный на обнаружении специфических IgE к чесоточным клещам, не годится для выявления инфекций чесоточного клеща, потому что, как и в случае аллергии на клещей домашней пыли, не все пациенты предрасположены к выработке IgE к ним, и, следовательно, у них нет аллергии на их антигены. Пациенты с чесоткой могут иметь или не иметь аллергию на клещей домашней пыли, но большинство пациентов с чесоткой, по-видимому, чувствительны к клещам домашней пыли [87].
Как упоминалось ранее, важен изотип антитела, используемый для обнаружения антигена чесоточного клеща.Хозяева, вероятно, продуцируют антитела IgM к антигену клещей перед переключением на IgG. Таким образом, ранняя диагностика, вероятно, должна основываться на обнаружении IgM или обоих IgM и IgG в крови больных чесоткой. Предварительное исследование поддерживает эту концепцию. Исследование Arlian et al. [87] обнаружили, что 45,1%, 27,5% и 73,6% из 91 пациента с обычной чесоткой имели сывороточные антитела Ig, IgG и IgM к антигенам чесоточного клеща соответственно. Только 2,2% имели IgE, направленный на антигены чесоточного клеща. Однако, как отмечалось ранее, перекрестная реактивность и сенсибилизация к клещам домашней пыли усложняют картину.Из 91 пациента с чесоткой 84,6%, 91,2% и 86,8% имели IgG к D. farinae , D. pteronyssinus и E. maynei соответственно. Аналогичным образом, 75,8%, 83,5% и 84,6% имели IgM, направленный против этих трех видов клещей, соответственно. Но только 2–3% имели IgE, направленный к любому из четырех протестированных видов клещей ( S. scabiei , D. farinae , D. pteronyssinus и E. maynei ). Многие антигены клещей домашней пыли имеют перекрестно-реактивные эпитопы с антигенами чесоточных клещей [88,89,90,91,92].Таким образом, белковые молекулы, используемые для обнаружения антител против чесотки, не должны иметь перекрестной реакции с какими-либо антигенными белками или пептидами клещей домашней пыли. Вероятно, что диагностический анализ крови должен будет содержать смесь белков / пептидов чесоточного клеща [87]. Если действительно существует несколько штаммов S. scabiei , которые инфицируют людей в различных географических регионах мира, как было предложено [68], эта комбинация антигенов и профиль антител в крови может нуждаться в разработке и адаптации к конкретным районам / регионы мира.
В отличие от пациентов с обычной чесоткой, похоже, что большинство пациентов с корковой чесоткой имеют IgE, направленный на антигены чесоточного клеща. Исследование Arlian et al. [93] исследовали профили IgE и IgG у пациентов с обычной и покрытой корками чесоткой. Иммуноблоттинг показал, что 6 из 6 пациентов с корковой чесоткой имели сывороточный IgE, распознающий от 11 до 21 белка / пептида во всем теле S. scabiei var. Экстракт canis , разделенный с помощью SDS-PAGE [93]. Напротив, только 3 из 7 пациентов с обычной чесоткой имели IgE и только 2 из 7 имели IgG, который распознавал белковые полосы, и их связывание было слабее, что указывает на гораздо более низкие титры.Walton et al. [46] также продемонстрировали, что пациенты с корковой чесоткой имели значительно более высокие уровни сывороточного IgE, который распознал 4 рекомбинантных S. scabiei var. hominis белков гомологичны аллергенам пылевых клещей, чем пациенты с обычной формой заболевания.
Серологический иммуноферментный анализ (ELISA) для диагностики чесотки был разработан и оценен для использования в нескольких различных видах хозяев. Эти тесты показали различный успех, и результаты зависели от степени и продолжительности заражения и используемого антигена-мишени.
В первых исследованиях использовались водные антигенные экстракты, полученные из целых тел клещей S. scabiei (Таблица 3). Производство этих экстрактов требовало утомительной работы по сбору клещей от различных хозяев. Лунки в планшетах для ELISA были покрыты антигеном в этих экстрактах. В некоторых случаях антиген клеща соответствовал штамму клеща, ответственному за инфекцию (например, антиген лисьего клеща и инфицированных лисиц, антиген свиного клеща и инфицированных свиней). В других случаях антиген клеща от одного вида хозяев использовали для обнаружения антител в сыворотке от другого вида хозяев, инфицированных чесоткой.Например, антиген лисьего клеща использовали для обнаружения антител в сыворотке инфицированных свиней, а антиген клеща собачьей чесотки использовали для обнаружения антител в сыворотке людей, инфицированных чесоткой. Таким образом, результаты основывались на перекрестной реакции или общих антигенах между чесоточными клещами от разных видов хозяев. Лабораторные исследования с использованием перекрестного иммуноэлектрофореза и иммуноблоттинга прямо продемонстрировали перекрестную реактивность между антигенами чесоточных клещей свиней (var. suis ), собак (var. canis ) и человека (вариант hominis ) и что эти клещи являются источниками перекрестно реагирующих антигенов или эпитопов, что поддерживает подход к использованию антигена, полученного из одного штамма клещей, для обнаружения антител в сыворотке инфицированного хозяина. с другим штаммом [94].
Таблица 3 Характеристики опубликованных ELISA с использованием сырого экстракта клещей в качестве антигена-мишени для обнаружения антител, циркулирующих в сыворотке крови хозяев, страдающих чесоткойHollanders et al.[95] использовали антигены S. scabiei var. vulpes экстракт (гомогенат целого тела клеща из лисьих клещей) в ELISA для обнаружения антител в сыворотке документированных зараженных чесоткой свиней-отъемышей, свиней на откорме и свиноматок. Анализ обнаружил антитела у 80%, 77,8% и 50% отъемышей, откормочных свиней и свиноматок, соответственно, в то время как более 98% контрольных свиней без чесотки не имели обнаруживаемых сывороточных антител к антигенам клещей.
Три коммерческих ИФА (Checkit® Sarcoptest, Sarcoptes-ELISA 2001 PIG и Acar-Test P * ELISA) были использованы для обнаружения антител IgG у свиней, экспериментально зараженных S.scabiei var. suis в разное время по мере прогрессирования инфекции [96]. Это контролируемое исследование показало, что эти системы ELISA могут обнаруживать антитела у большинства инфицированных свиней через 5-6 недель заражения чесоточными клещами. В аналогичном исследовании использовались четыре различных набора ELISA для определения IgG для определения сывороточного IgG к антигену чесоточного клеща у естественно инфицированных свиноматок и свиней, виновных в этом заболевании [97]. В одном тестовом наборе использовался антиген из S. scabiei var. suis (свиньи клещи), тогда как три других набора содержали антиген из S.scabiei var. vulpes (лисий клещ). Серологические положительные результаты варьировались от 30% до 88,6% в зависимости от используемого теста. Однако соскобы кожи были положительными только у 48,6% этих свиней. Таким образом, некоторые диагностические серологические тесты могут значительно улучшить диагностику.
Van der Heijden et al. [98] также разработали ELISA службы здоровья животных (AHS-ELISA) для выявления чесотки у свиней. Детектирующий антигенный материал получали из S. scabiei var. suis клещей собрано от свиноматок с коркой чесотки.AHS-ELISA обнаружил сывороточные антитела через 6 недель у 5% свиней и у 74,2% свиней после 16 недель заражения. Это показывает, что ответы антител развиваются медленно или что титр низкий и ниже предела обнаружения метода во время ранних инфекций чесотки.
Чесотка может быть серьезной угрозой для дикой серны и козерога в южной Европе [99,100,101]. Разработка серологического теста поможет менеджерам по ресурсам отслеживать инфекции у этих животных. Rambozzi et al.[99] разработали ELISA, амплифицированный биотин-авидином (LAB-ELISA), с использованием антигена из S. scabiei var. vulpes от красных лисиц ( Vulpes vulpes ) для выявления антител в сыворотке серны, инфицированной чесоткой, и отличия их от здоровой серны. Используя этот тест, 37 из 40 сывороток, вызванных чесоткой, были положительными по ИФА, а 101 из 104 сывороток, собранных из неинфицированных серн, были отрицательными.
ELISA также использовался для диагностики чесотки у собак. Lower et al. [99] оценили непрямой ИФА (Imovet sarcoptes) у 19 собак с подтвержденными инфекциями чесотки.Захватывающим антигеном в этом тесте был S. scabiei var. vulpes от лисиц и 84,2% собак имели определяемые уровни IgG к антигену лисьего клеща, тогда как 89,2% контрольных собак без чесотки в анамнезе не имели.
ELISA с использованием антигена из S. scabiei var. ovis был использован для обнаружения сывороточных антител у овец, инфицированных var. ovis [102]. Этот ELISA диагностировал 87,6% овец с чесоткой, в то время как только 62,8% были положительными при соскобе кожи.
Bornstein et al. [103] использовали планшеты для ELISA, покрытые водным экстрактом антигенов, полученных из S. scabiei var. vulpes и вторичные антитела против IgG собаки для обнаружения антител в окрашенных кровью жидкостях полостей тела красных лисиц. Наличие антител к антигену чесоточного клеща было обнаружено у 62 из 65 (95%) рыжих лисиц, имевших клинические признаки саркоптоза.
ELISA с использованием моноклональных антител к собаке IgG был использован для обнаружения сывороточного IgG, направленного на антиген из S.scabiei var. vulpes для диагностики у собак, инфицированных S. scabies var. canis клещей [104]. У 10 из 12 (83%) собак подтверждено наличие S. scabiei var. Инфекция canis дала положительный результат ELISA для S. scabiei var. vulpes антигенов.
Haas et al. [105] оценили возможность использования S. scabiei var. vulpes антиген от клещей лисицы в формате ELISA для диагностики чесотки человека.Планшеты для ELISA покрывали антигеном лисьего клеща, а затем реагировали с сывороткой больных чесоткой. Сыворотки 41 человека с подтвержденным диагнозом S. scabiei var. человек подвергали скринингу с помощью ELISA для выявления антител IgG. Сорок восемь процентов больных чесоткой имели сывороточный IgG, который четко распознавал var. vulpes антиген и 17% были погранично положительными. Однако большинство пациентов, у которых не было IgG, распознавшего S. scabiei var. vulpes имел симптомы в течение менее 4 недель, и анализ не тестировал связывание антител IgM.Таким образом, изотип антител IgM, который продуцируется до переключения на продукцию IgG, мог быть лучше для выявления инфекции чесотки, как было предложено Arlian et al. [87].
Более поздние исследования были сосредоточены на использовании рекомбинантных молекул для разработки ELISA для диагностики чесоточного клеща (таблица 4). Иберийский благородный олень ( Cervus elaphus hispanicus ) в европейских странах может быть заражен саркоптозом [106]. Oleaga et al. [106] использовали ELISA для оценки наличия антител, специфичных к чесоточным клещам, в образцах сыворотки, собранных у 327 благородных оленей, без явных саркоптозных поражений.В этом ELISA использовали рекомбинантный антиген чесоточного клеща Ssλ20ΔB3, выделенный из S. scabiei var. Библиотека экспрессии hominis [107]. Он был распознан антителами в сыворотке крови 6 из 8 щитовидных оленей.
Таблица 4 Характеристики опубликованных ELISA с использованием рекомбинантных белков в качестве антигена-мишени для обнаружения антител, циркулирующих в сыворотке скабиетических хозяевВ другом исследовании рекомбинантный Ssλ20ΔB3, полученный из S. scabiei var. hominis показал с помощью ELISA обнаружение антител у 7 серн ( Rupicapra rupicapra ) и 3 оленей с подтвержденной инфекцией чесотки [107]. Из здоровых животных, не подвергавшихся воздействию чесотки, только 1 из 33 серн и 1 из 33 оленей были иммунопозитивными. Хотя размер выборки инфицированных животных был небольшим, исследование показало, что белок чесоточного клеща человека действительно идентифицирует антитела к антигенам чесоточного клеща в крови двух разных видов животных-хозяев.
Дикий европейский кролик ( Oryctolagus cuniculus ) обитает на северо-востоке Средиземноморья в Испании и служит добычей для многих хищников, а также дичью для охотников [108]. Sarcoptes scabiei паразитирует в некоторых популяциях этих кроликов, и есть опасения, что болезнь может значительно повлиять на популяцию кроликов и что она может передаваться другим диким животным. Таким образом, Millan et al. [108] использовали ELISA на основе рекомбинантного человеческого антигена чесоточного клеща Ssλ20ΔB3 для исследования серологической распространенности антител против чесотки у кроликов в отдельных провинциях или на островах Испании. Большинство проанализированных сывороток было получено от кроликов, отстреленных охотниками. Результаты показали, что человеческий антиген клеща можно использовать для выявления чесотки у диких кроликов и что воздействие S.scabiei был широко распространен среди диких кроликов по всей Испании.
He et al. [109] использовали рекомбинантный кальмодулин, клонированный из РНК, экстрагированной из S. scabiei , собранных у кроликов, для разработки ELISA для обнаружения присутствия специфических антител S. scabiei- в сыворотке кроликов, инфицированных S. scabiei или с Psoroptes cunniculi, другим эктопаразитом кроликов. Хотя этот анализ имел чувствительность 88%, его специфичность составила всего 23% из-за перекрестной реактивности высококонсервативного кальмодулина от чесоточных клещей с этим белком из P.Кузнецова .
Mattsson et al. [110] использовали рекомбинантный фрагмент размером 17,5 кДа var. vulpes парамиозин (миниатюрный парамиозин) для обнаружения антител в сыворотках собак и свиней, инфицированных чесоткой, с помощью иммуноблоттинга. Эта молекула распознается антителами иммунизированных кроликов, но не может быть легко обнаружена антителами в сыворотке инфицированных чесоткой собак и свиней.
В совокупности эти исследования демонстрируют достаточную перекрестную реактивность между антигенами чесоточного клеща от разных хозяев, которые являются естественными или рекомбинантными S.scabiei от одного вида хозяев можно использовать для обнаружения сывороточных антител у хозяина, инфицированного другим штаммом чесоточных клещей. Кроме того, эти исследования показывают вариабельность и сложность обнаружения сывороточных антител у естественно инфицированных животных, когда история инфекции неизвестна. Ключевые вопросы, которые влияют на полезность анализа крови на чесотку: (i) сколько времени проходит после начала инфекции, прежде чем антитела могут быть обнаружены в сыворотке, и (ii) какой изотип антител должен обнаруживать этот тест (e.г. IgM, IgG, IgE и т. Д.)? Это факторы, которые еще предстоит определить, но при раннем обнаружении, вероятно, следует искать IgM, поскольку этот изотип вырабатывается на ранней стадии гуморального ответа. Кроме того, должен ли анализ крови быть разработан для обнаружения сывороточных антител, направленных против одного антигена, или он должен будет содержать смесь антигенов для обнаружения сывороточных антител, созданных против нескольких антигенов или определенного профиля антигенов? Например, в исследовании Kuhn [111], может ли смешивание целевых антигенов SsE3 и SsE5 повысить чувствительность до 100% (Таблица 4)? Это важные факторы, которые следует учитывать при разработке анализа крови на чесотку.
Появление молекулярных методов в сочетании с доступностью геномных последовательностей клещей дает возможность для разработки альтернативных методов диагностики. Angelone-Alasaad et al. [112] разработали два основанных на ПЦР метода диагностики чесотки, основанных на амплификации 135 п.н. митохондриальной 16S рДНК. Оба метода были успешно протестированы на чесоточных клещах, собранных у 23 видов хозяев. Использование технологии на основе ПЦР является многообещающим, но по-прежнему требует извлечения клещевого материала в соскобе кожи, что остается сложной задачей.
Вакцинация против заражения чесоточным клещом
Акарициды доступны для лечения чесотки, но развилась значительная резистентность к этим акарицидам, что приводит к неэффективности лечения [113,114,115]. Кроме того, эти химические вещества обладают известным и неизвестным токсическим воздействием на людей и животных. Таким образом, вакцинация для защиты от заражения чесоточными клещами является привлекательной альтернативой доступным в настоящее время химиотерапевтическим средствам.
Вакцинация против S.scabiei — реалистичная цель по нескольким причинам. Чесотные клещи вызывают как врожденный, так и адаптивный иммунный ответ у паразитированного хозяина. Адаптивный ответ включает выработку IgM, IgG и изотипов антител IgE и IgA в некоторых человеческих хозяевах к антигенам, которые клещи высвобождают в эпидермисе, когда зарываются в них. Клещи поглощают сывороточные антитела, когда зарываются в нижний эпидермис и питаются им. Некоторые данные свидетельствуют о том, что сыворотка является составной частью их рациона. Системные акарициды, такие как ивермектин, убивают клещей на коже, предположительно потому, что клещи их проглатывают.Исследование с использованием флуоресцентно меченых антител показало, что антитела хозяина связываются со слизистой оболочкой кишечника живых клещей, удаленных от хозяина [27]. Антитела-хозяева, которые связываются с молекулами клеток кишечника и пищеварительными ферментами, вырабатываемыми этими клетками, которые имеют решающее значение для пищеварения и поглощения питательных веществ, могут блокировать эти процессы и, таким образом, препятствовать выживанию клеща. Точно так же антитело хозяина, направленное на молекулы клеща, которые имеют решающее значение для подавления защитных реакций хозяина, будет препятствовать способности клеща выживать и создавать популяцию в коже хозяина, потому что хозяин теперь может обеспечить успешный защитный ответ.
Другие данные свидетельствуют о том, что вакцинация может вызывать защиту от чесоточных клещей. Было обнаружено, что титры антител-хозяев развиваются быстрее и с большей интенсивностью во время второй инфекции по сравнению с начальной (первичной) инфекцией чесоточными клещами [116]. Животные, выздоровевшие от инфекции чесоточного клеща, демонстрируют снижение уровня клещей при последующей повторной инфекции [11, 116, 117, 118, 119]. Arlian et al. [117] обнаружили, что 8 собак, излеченных от S. scabiei и затем повторно инфицированных, проявили защитный иммунитет.У семи из 8 собак развились кратковременные инфекции, которые полностью исчезли со временем без какого-либо лечения. Наконец, кроликов иммунизировали экстрактом всего тела S. scabiei var. canis продуцировал антител к большему количеству антигенов, чем кролики, инфицированные этим клещом [120].
Опубликованы результаты нескольких испытаний вакцинации. Исследование Tarigan et al. [118] оценили защитный эффект вакцинации коз экстрактом, полученным из целых тел чесоточных клещей, собранных от инфицированных коз, и несколькими фракциями этого экстракта, полученными с помощью анионообменной хроматографии.Они не обнаружили различий в степени тяжести кожных поражений между иммунизированными и неиммунизированными козами в несколько раз после экспериментального заражения, хотя ранее инфицированные животные действительно проявляли защитный иммунитет.
Harumal et al. [121] исследовали защитный эффект иммунизации кроликов рекомбинантными антигенами Ssag1 и Ssag2 (от клещей разновидности hominis ). Иммунизированные кролики продуцировали антитела к обоим антигенам, однако кролики не проявляли защитного иммунитета или снижения численности клещей.Молекулы Ssag 1 и Ssag 2 располагались вокруг внутренних органов и кутикулы чесоточного клеща и в яйцах. По-видимому, эти белковые фрагменты недоступны для антител, или связывание антител с ними не ингибирует жизненно важные функции, необходимые для выживания клещей.
Casias et al. [122] вакцинировали кроликов смесью рекомбинантных антигенов Ssλ20ΔB3 и GST-Ssλ15, полученных из S. scabiei var. человек клещей. Затем этим кроликам вводили S.scabiei var. cuniculi (чесоточные клещи кроликов) и проявляли высокие уровни специфического IgG и повышенные уровни общего IgE, но не были защищены от заражения этими клещами.
Исследования показали, что клещи домашней пыли D. farinae и D. pteronyssinus перекрестно реагируют с антигенами в экстрактах S. scabiei [88, 89]. Это свидетельствует о том, что вакцинация экстрактами клещей домашней пыли может вызывать защиту от S. scabiei .Большое количество чесоточных клещей недоступно для изготовления вакцины для целей иммунизации, но клещей домашней пыли можно культивировать в количествах, равных килограммам. Иммунизация смесью 50/50 экстрактов D. farinae и D. pteronyssinus индуцировала защитный иммунитет к S. scabies var. canis у кроликов, о чем свидетельствует заметное снижение паразитарной нагрузки по сравнению с неиммунизированным контролем [90].
Другие исследования подтверждают принцип защиты от эктопаразитарного клеща.Овец и кроликов вакцинировали родственным клещом парши Psoroptes sp. Частичный иммунитет к инфекции, вызванной P. cuniculi (клещ из парши кролика), развился после четырех иммунизаций экстрактом всего тела [123]. Вакцинированные кролики обеспечивали сопоставимую защиту по сравнению с естественно инфицированными кроликами. Аналогичным образом, вакцинация овец экстрактами всего тела P. ovis (клеща из парши овец), приготовленными в физиологическом растворе или 1% твине, привела к значительной защите от заражения [124].Последующее исследование показало, что конкретная фракция, полученная с помощью анионообменной хроматографии исходного экстракта, дает большую защиту, чем другие фракции, и чем сам исходный экстракт [125]. Однако профиль фракции в SDS-PAGE показал, что она содержит много белков, поэтому молекулы, ответственные за повышенную защиту, не могут быть идентифицированы.
Gu et al. [126] исследовали иммунный ответ, индуцированный у мышей с помощью S. scabiei var. cuniculi ДНК-вакцина, кодирующая парамиозин.ДНК-вакцина вызвала гуморальный и клеточный иммунный ответ, характеризующийся более высокими уровнями IgG, IgG1, IgG2a, IgE и IgM, повышенной секрецией IL-2, IL-4, IL-5 и IFNγ спленоцитами и пролиферацией лимфоцитов в селезенка. Парамиозин является обычным белком у многих беспозвоночных и имеет высокую гомологию между видами. Эти эксперименты создают основу для дальнейшего изучения возможной ДНК-вакцины для защиты от чесотки. Не было определено, вызывает ли это какой-либо защитный иммунитет.
В совокупности все эти данные ясно показывают, что вакцинация — это реальная возможность защитить популяции людей и животных от чесоточных клещей. При рассмотрении испытаний вакцины от чесотки в игру вступают многие факторы, помимо антигена или смеси антигенов. Многие из сообщенных неудачных попыток иммунизации могут быть связаны с адъювантами, графиком иммунизации, дозой антигена и способом доставки. Ключевой антиген или смесь антигенов еще предстоит идентифицировать и получить с помощью рекомбинантной технологии.Кроме того, необходимо будет определить все компоненты протокола иммунизации.
Выводы
Заболевание чесоткой известно на протяжении тысячелетий. Однако отсутствие большого количества чесоточных клещей от гипер-инфицированных хозяев, методов культивирования in vitro или животных моделей in vivo ограничивает типы возможных исследований. Знания о биологии чесоточных клещей, взаимодействиях хозяина и паразита, молекулах, которые производят клещи (антигены, неантигены и иммуномодулирующие), способности модуляции хозяина, врожденных и адаптивных иммунных ответах хозяина, а также протеомике и геномике клещей значительно расширились в течение последние 30 лет.В частности, чесоточные клещи из кроличьей модели позволили систематически определять жизненный цикл и продолжительность жизненных стадий, а также прояснили поведение поиска хозяина и реакцию на стимулы хозяина, реакцию на свет, выживаемость вне хозяина и инфекционность от фомитов. активность проникновения через кожу, водный баланс и снабжение питательными веществами, а также выявленные факторы в коже, которые могут влиять на предпочтительное место клеща на теле хозяина. Клещи от людей, а также модели кроликов и свиней были использованы для определения того, что молекулы клещей модулируют секрецию цитокинов кожными кератиноцитами, эпидермальными фибробластами, лимфоцитами и эндотелиальными клетками микроциркуляторного русла, а также экспрессию молекул клеточной адгезии из последних и блокируют эти три фактора. комплемент пути.Новые молекулярные методы теперь позволяют определять геномные и протеомные характеристики чесоточных клещей и получать рекомбинантные молекулы. Эти более поздние молекулярные инструменты теперь делают реальностью возможность разработки столь необходимого диагностического теста на чесотку и вакцины для защиты от чесотки в уязвимых группах населения. Это просто вопрос времени.
Проблемы диагностики чесотки, глобального заболевания людей и животных
Clin Microbiol Rev. 2007 Апрель; 20 (2): 268–279.
Шелли Ф. Уолтон
Школа медицинских исследований Мензиса, 1 Институт перспективных исследований, Университет Чарльза Дарвина, 2 Клиническая школа Северной территории, Университет Флиндерса и медицинский факультет Королевской больницы Дарвина, Дарвин, Австралия 3
Барт Дж. Карри
Школа медицинских исследований Мензиса, 1 Институт перспективных исследований, Университет Чарльза Дарвина, 2 Клиническая школа Северной территории, Университет Флиндерса и медицинский факультет Королевской больницы Дарвина, Дарвин, Австралия 3
Школа медицинских исследований Мензиса, 1 Институт перспективных исследований, Университет Чарльза Дарвина, 2 Клиническая школа Северной территории, Университет Флиндерса и медицинский факультет Королевской больницы Дарвина, Дарвин, Австралия 3
* Автор, ответственный за переписку.Почтовый адрес: Menzies School of Health Research, P.O. Box 41096, Casuarina NT 0811, Австралия. Телефон: 61 8 828. Факс: 61 8 89275187. Электронная почта: [email protected] © 2007, Американское общество микробиологии Эта статья цитируется в других статьях в PMC.Abstract
Чесотка — всемирное заболевание и серьезная проблема общественного здравоохранения во многих развивающихся странах, связанная в первую очередь с бедностью и перенаселенностью. В отдаленных общинах аборигенов на севере Австралии была описана распространенность до 50% среди детей, несмотря на доступность эффективной химиотерапии.Саркоптоз также является важным ветеринарным заболеванием, вызывающим значительную заболеваемость и смертность диких, домашних и сельскохозяйственных животных. Чесотка вызывается эктопаразитарным клещом Sarcoptes scabiei , который проникает в эпидермис хозяина. Клинические симптомы включают сильно зудящие поражения, которые часто являются предшественниками вторичной бактериальной пиодермии, сепсиса и, у людей, постстрептококкового гломерулонефрита. Хотя диагностированные случаи чесотки могут быть успешно вылечены, для развития сыпи при первичном заражении требуется от 4 до 6 недель, и, таким образом, передача другим людям часто происходит до начала терапии.У людей симптомы заражения чесоткой могут имитировать другие дерматологические кожные заболевания, а точность традиционных тестов для диагностики чесотки составляет менее 50%. Чтобы помочь раннему выявлению заболевания и, следовательно, лечению, необходим простой, дешевый, чувствительный и специфический тест для рутинной диагностики активной чесотки. Недавние разработки, приведшие к экспрессии и очистке рекомбинантных антигенов S. scabiei , позволили идентифицировать ряд молекул с диагностическим потенциалом, и текущие исследования включают изучение и оценку точности этих рекомбинантных белков при идентификации антител у лиц с активной чесоткой и в дифференциации тех, кто был в прошлом.Раннее выявление болезни сделает возможным выборочное лечение пораженных, снизит передачу и потребность в массовом лечении, ограничит возможность эскалации устойчивости к клещам и предоставит еще одно средство борьбы с чесоткой среди популяций в эндемичных районах.
ВВЕДЕНИЕ
Предпосылки
Чесотка — распространенная паразитарная инфекция, вызываемая клещом Sarcoptes scabiei . Заражение происходит, когда «чесоточный» клещ S. scabiei проникает в кожу и поедает эпидермис и сыворотку хозяина.Преобладающие проявления заболевания опосредованы воспалительными и аллергическими реакциями на продукты от клещей, что приводит к сильному зуду. Чесотка — серьезная глобальная проблема здравоохранения для многих коренных народов и общин третьего мира. Он вызывает вспышки в домах престарелых (99) и распознается у лиц, инфицированных вирусом иммунодефицита человека и вирусом Т-клеточного лейкоза человека типа 1 (47, 48, 73, 97). Чесотка передается при контакте кожа к коже, как показали классические исследования Мелланби (79), который показал, что прямой телесный контакт человека с человеком обычно необходим для передачи чесотки.Таким образом, это скорее болезнь перенаселенности и бедности, чем отражение плохой гигиены (57). Было подсчитано, что 300 миллионов человек страдают от заражения чесоткой одновременно (102), хотя это число оспаривается (25). Чесотка — серьезное детское заболевание, но оно встречается у обоих полов, в любом возрасте, во всех этнических группах и на всех социально-экономических уровнях. Важно отметить, что связанная с этим заболеваемость часто недооценивается. В дополнение к дискомфорту, вызываемому сильным зудом, заражения часто становятся вторичными, особенно стрептококками группы A и Staphylococcus aureus. Эпидемический острый постстрептококковый гломерулонефрит (APSGN) часто ассоциируется с эндемической чесоткой в пострадавшем сообществе (29, 96). Несмотря на доступность химиотерапии, повторяющиеся заражения чесоткой и возникающая в результате рецидивирующая пиодермия в настоящее время определены как важные кофакторы крайних уровней почечной и ревматической болезни сердца, наблюдаемых в общинах аборигенов (30, 63, 112). Чесотка также является серьезной проблемой среди крупного рогатого скота и домашних животных: например, примерно 25% свиней в некоторых районах США страдают чесоткой, что приводит к серьезным экономическим потерям (22, 89).Более того, многие миллионы диких животных во всем мире страдают саркоптозом. Несмотря на то, что это всемирное заболевание было признано на протяжении всей истории, в современную эпоху в исследованиях чесотки были длительные перерывы и значительные пробелы. Молекулярные исследования паразита были очень ограниченными из-за в целом низкой нагрузки паразитов и отсутствия системы культивирования in vitro. Первые молекулярные исследования Sarcoptes scabiei var. человек были включены в результате сбора большого количества клещей с кожных покровов больных чесоткой, покрытых коркой в 1997 г. (107).
История
Чесотка известна человечеству с древних времен. Считается, что Аристотель (384–322 гг. До н.э.) первым идентифицировал чесоточных клещей, назвав их «вшами во плоти» и применив термин «акари». ” Впоследствии чесотка упоминалась многими разными авторами, в том числе арабским врачом Абу эль Хасаном Ахмедом эль Табари, около 970 г., Святой Хильдегард (1098–1179 гг.) И мавританским врачом Авензоаром (1091–1162 гг.) (93). В 1687 году Бономо и Честони точно описали причину чесотки в письме (81).Их описание с описанием паразитарной природы, передачи, возможных способов лечения и микроскопических рисунков клеща и яиц S. scabiei считается первым упоминанием паразитарной теории инфекционных заболеваний. Тем не менее, только в 1868 году, два столетия спустя, причина чесотки была установлена после публикации трактата Гебры (19a, 52).
БИОЛОГИЯ
Классификация
S. scabiei является облигатным эктопаразитическим членистоногим, таксономически сгруппированным в класс Arachnida, подкласс Acari, отряд Astigmata и семейство Sarcoptidae (39).Члены Astigmata — относительно медлительные клещи с тонко склеротизированными кожными покровами и без обнаруживаемых дыхалец или трахеальных систем. Было описано более 15 различных разновидностей или штаммов от разных хозяев, хотя морфологически они кажутся похожими (38). Однако эксперименты по перекрестному заражению (10) и исследования молекулярной эпидемиологии (106, 108) указывают на явные физиологические и генетические различия между штаммами-хозяевами.
Life Cycle
Самка клеща зарывается прямо под поверхностью кожи и откладывает два-три яйца в день в роговом слое на срок до 6 недель за раз, в результате чего на поверхности кожи образуются приподнятые папулы.Однако оказалось, что менее 1% отложенных яиц превращаются во взрослых клещей (78). Стадии развития включают яйцо, личинку, протонимфу и тритонимфу (12). Взрослые клещи появляются на поверхности кожи примерно через 2 недели и после спаривания повторно заражают кожу хозяина или другого человека. Сообщается, что самец клеща умирает после спаривания, хотя это оспаривается (1, 54).
Морфология
S. scabiei кремово-белый цвет с коричневыми склеротизированными ножками и ротовым аппаратом (рис.). Взрослая самка составляет примерно 0,3–0,5 мм в длину и 0,3 мм в ширину, а самец немного меньше, примерно 0,25 мм в длину и 0,2 мм в ширину. Личинки имеют шесть ног, а нимфы и взрослые особи — восемь ног, при этом на 1-й и 2-й ногах взрослых клещей мужского и женского пола имеются стебельчатые пульвиллы (присоски), позволяющие им цепляться за субстрат. Кроме того, клещи имеют шпорцевидные когти и шесть или семь пар шиповидных выступов на спинной поверхности. Взрослый самец отличается от самки меньшими размерами, более темным цветом и наличием стебельчатых пульвиллов на ноге 4; нога 4 у взрослой самки оканчивается длинными щетинками.
Самка чесоточного клеща с яйцом, взятым со соскоба кожи.
Инфекция, выживаемость и передача
Передача чесотки опосредуется, прежде всего, тесным, длительным личным контактом с инфицированным человеком и поэтому является обычным явлением среди членов семьи и часто наблюдается в учреждениях. Среди взрослых половой контакт, пожалуй, самый важный способ передачи инфекции. Вероятность заражения зависит от количества клещей на инфицированном человеке и продолжительности контакта.Чесотка нелегко передается через одежду, простыни или другие фомиты (78), но этот способ передачи следует рассматривать в случаях корковой (тяжелой) чесотки из-за чрезмерного количества клещей. Когда клещ отделяется от своего хозяина, он может выжить в течение 24–36 часов при комнатной температуре с нормальной влажностью (21 ° C и относительная влажность от 40 до 80%) и даже дольше при более низких температурах и высокой влажности (9). Однако способность клещей заражать хозяина уменьшается с увеличением времени отсутствия хозяина.Незрячий клещ использует запахи и тепловые раздражители для активных такси хозяина (3, 11).
ЭПИДЕМИОЛОГИЯ
Во многих тропических и субтропических регионах, таких как Африка (85, 100), Египет (53), Центральная и Южная Америка (56, 104), северная и центральная Австралия (109), Карибские острова (96) , Индия (72, 84) и Юго-Восточная Азия (92) чесотка является эндемическим заболеванием. В промышленно развитых странах чесотка наблюдается в основном в отдельных спорадических случаях и в институциональных вспышках (32, 36). Эпидемиологические исследования показывают, что распространенность чесотки не зависит от пола, расы, возраста или социально-экономического статуса.Основными факторами, способствующими заражению чесоткой, по-видимому, являются бедность и перенаселенность (45, 109). Несмотря на это, одни группы более подвержены заболеванию, чем другие. Чесотка чаще всего наблюдается у самых маленьких, за ней следуют дети старшего возраста и молодые люди (1). В ситуациях, когда чесотка носит эндемический характер, это, скорее всего, отражает снижение иммунитета, а также повышенное воздействие (27). К другим возрастным группам, более часто страдающим от заражения чесоткой, относятся матери маленьких детей и пожилые люди в домах престарелых.Последние случаи часто связаны с индексными случаями покрытой коркой чесотки в сочетании с ослабленной иммунной системой и, возможно, сниженной способностью убивать клещей царапинами из-за слабоумия и / или инсультов. Отсутствие сенсибилизации и / или уменьшение расчесывания также считается причиной того, что у пациентов с параличом или сенсорной невропатией могут образовываться локализованные корки в пораженных областях (Б. Дж. Карри и С. Ф. Уолтон, личное наблюдение). Еще предстоит установить, могут ли возникать бессимптомные случаи чесотки и есть ли в анамнезе инфекция S.scabiei вызовет длительный иммунитет.
Цикличность заражения
В ранних отчетах об эпидемиологии чесотки у человека были описаны крупные эпидемии или пандемии чесотки. Основные пики, по-видимому, совпадают с крупными войнами и произошли между 1919 и 1925 годами, 1936 и 1949 годами, а также 1964 и 1979 годами (46). Поскольку чесотка не является заболеванием, подлежащим регистрации, это может не точно отражать ее распространенность, поскольку данные часто основаны на различных методах регистрации и поступают из стран с сильно различающейся социальной и физической средой.Более того, пики заболеваемости не наблюдались одновременно во всех странах (87). Коллективный иммунитет был предложен как причина возможной цикличности заболевания, поскольку было продемонстрировано, что как люди, так и животные с повторным заражением уменьшили паразитарное бремя, а некоторые ранее инфицированные люди могут устранить второе заражение (8, 78). Однако эта теория не учитывает эндемичность чесотки во многих тропических и субтропических сообществах (например, в северной Австралии, Индии и Южной Африке) без каких-либо явных колебаний общей заболеваемости (84, 87, 109).Перенаселенность и постоянное наличие новых когорт восприимчивых детей младшего возраста могут поддерживать цикл инфекции в сообществах, где чесотка является эндемической, тогда как во время войны наиболее вероятной причиной вспышек является скопление взрослых, не имевших отношения к чесотке (27). Следует отметить, что рост чесотки часто идет параллельно с увеличением распространенности других внешних паразитов членистоногих, например, головных или тельцовых вшей. Опять же, это указывает на роль социальной среды в передаче инфекции (34).
Бедность, перенаселенность и плохая гигиена
Связь между распространенностью чесотки и относительными уровнями бедности, скученности и гигиены в сообществе является сложной. Имеющиеся данные свидетельствуют о том, что на чесотку не влияют правила гигиены или наличие воды. Это можно наблюдать во время вспышек заболеваний в учреждениях, где соблюдаются высокие стандарты гигиены (60, 88), и в прибрежных тропических сообществах с большим доступом к воде и тщательной гигиеной (69, 101).Кроме того, известно, что чесотка поражает людей всех социально-экономических уровней, включая зажиточные слои населения, если происходит заражение. Однако бедность и перенаселенность часто сопутствуют друг другу, и считается, что перенаселенность оказывает значительное влияние на распространение чесотки, что отражает фундаментальную роль физического контакта в передаче инфекции от человека к человеку. Бедность также ведет к другим связанным с ней проблемам, таким как плохой статус питания, который, в свою очередь, может влиять на иммунный статус человека и уровни заболеваемости в обществе.Статус питания считается значительным фактором риска вспышки чесотки в индийской деревне (84), а недоедание может предрасполагать людей к покрытой коркой чесотке (97).
Значение для австралийских общин коренных народов
Несмотря на доступность эффективной химиотерапии, чесотка по-прежнему остается серьезной проблемой для многих отдаленных общин аборигенов в Австралии, прежде всего из-за уровня бедности и перенаселенности (30). Carapetis et al. опубликовали данные о 25% распространенности чесотки среди взрослых из этих сообществ (21).Были зарегистрированы более высокие показатели среди школьников — от 30 до 65% (26). Наир и др. связали подобный уровень эндемической чесотки в индийской деревне (84). Чесотка все чаще признается в качестве основной движущей силы стрептококковой пиодермии у детей в этих сообществах, лежащей в основе от 50 до 70% всех кожных инфекций. Стрептококки группы A ответственны за продолжающиеся вспышки APSGN и острой ревматической лихорадки, зарегистрированные в этих сообществах, при этом показатели острой ревматической лихорадки и ревматической болезни сердца являются одними из самых высоких в мире (29).Кроме того, чесотка и кожные инфекции в детстве связаны с чрезвычайно высокими показателями терминальной почечной недостаточности у взрослых коренного населения. У детей с кожными язвами вероятность развития APSGN во время эпидемии в пять раз выше, а у детей с чесоткой риск увеличивается вдвое (65). Наличие APSGN в детстве увеличивает риск заболевания почек у взрослых в шесть раз (112).
КЛИНИЧЕСКИЕ ХАРАКТЕРИСТИКИ
Обычная чесотка
Сообщается, что клиническое проявление первичного заражения чесоткой происходит через 4-6 недель после заражения.Проявляется генерализованный зуд, который, как часто сообщается, усиливается ночью. Зудящие папулы у людей, страдающих чесоткой, классически локализуются в перепонках пальцев, сгибающих сторонах запястий, разгибательных сторонах локтей, околопупочной коже, ягодицах, лодыжках, половом члене у мужчин и периареолярная область у самок. Сообщается, что количество клещей на одного пациента составляет примерно от 10 до 12, и при повторных заражениях это количество существенно сокращается (78).Хотя заражение чесоткой и общее количество клещей у людей обычно самоограничиваются, спонтанное выздоровление от чесотки у людей, как описано, происходит только при последующем повторном заражении (78). В зависимости от степени и тяжести воспалительной реакции клиническая картина чесотки может быть разнообразной, но классическим клиническим признаком для диагностики чесотки является нора. Взрослая самка длиной примерно 0,3 мм делает нору, переваривая и поглощая роговой слой эпидермиса и сыворотки, которые просачиваются в нору из дермы.Норы представляют собой сероватые сероватые линии длиной примерно 5 мм, но часто их невозможно обнаружить, особенно в тропических районах (С. Ф. Уолтон и Б. Дж. Карри, неопубликованные наблюдения; Д. Таплин, личное сообщение). Атипичный вид часто встречается у пациентов с давними инфекциями, у которых может развиться хроническое раздражение и экзематизация кожи. Пациенты, принимающие местные или пероральные стероиды или пациенты с ослабленным иммунитетом из-за других заболеваний, также могут проявлять себя нехарактерно.В некоторых ситуациях сыпь и зуд при чесотке могут сохраняться в течение нескольких недель после лечебного лечения, возможно, из-за мертвых клещей или продуктов клещей, оставшихся в слоях кожи. В некоторых случаях могут развиться узелки (узловая чесотка), которые могут сохраняться в течение нескольких месяцев после успешного лечения. Эти твердые красно-коричневые узелки часто вызывают сильный зуд и обычно обнаруживаются в паховой области, ягодицах и околопупочной области.
Повторное заражение
При повторном заражении сенсибилизация быстро развивается, и связанные с ним поражения и зуд становятся очевидными в течение 24–48 часов.
Дифференциальный диагноз
Клинические признаки и симптомы заражения чесоткой могут имитировать многие другие кожные заболевания. К ним относятся укусы насекомых, таких как мошки, блохи и клопы; инфекции, такие как фолликулит, импетиго, опоясывающий лишай и вирусная экзантема; экзема, контактный дерматит и аллергические реакции, такие как папулезная крапивница; и иммунологически опосредованные заболевания, такие как буллезный пемфигоид и розовый отрубевидный лишай. Поэтому диагностика может быть проблематичной.
Вторичная инфекция
Нелеченная чесотка часто ассоциируется с пиодермией, вызванной вторичной инфекцией стрептококком группы А и S.aureus (19) (рис.). Последствия включают целлюлит, инвазивные бактериальные инфекции и APSGN. Чесотка и кожные инфекции в детстве связаны с чрезвычайно высокими показателями терминальной почечной недостаточности у взрослых коренного населения.
Чесотка кисти при вторичной инфекции.
Покрытая коркой чесотка
Покрытая коркой чесотка была впервые описана среди больных проказой в Норвегии в 1848 году и поэтому исторически известна как норвежская чесотка. Это тяжелое изнурительное заболевание, характеризующееся большим количеством клещей, высоким уровнем иммуноглобулина E (IgE), периферической эозинофилией и развитием гиперкератотических кожных корок, которые могут быть рыхлыми, чешуйчатыми и шелушащимися или толстыми и прилипшими (рис.). Распространение по телу может быть локализованным или обширным и может включать шею, кожу головы, лицо, веки и область под ногтями (рис.). В корках обнаруживается большое количество клещей и яиц, которое в самых тяжелых случаях составляет более миллиона. Следовательно, покрытая коркой чесотка значительно более заразна, чем обычная чесотка. Люди с покрытой коркой чесоткой были признаны «основными переносчиками» (23, 29, 36) и источниками повторного заражения после программ вмешательства (28). Пациенты с покрытой коркой чесоткой также могут оставаться заразными в течение длительных периодов времени из-за трудностей с уничтожением клещей на участках кожи, сильно покрытых коркой.Покрытая коркой чесотка вызывается той же разновидностью клещей, которая вызывает обычную чесотку. Переход от обычной чесотки к чесотке с коркой встречается редко, а предрасположенность к более тяжелой форме заболевания связана с рядом предрасполагающих условий. К ним относятся лепра (рис.), Инфицирование вирусом Т-клеточного лейкоза человека типа 1 и вирусом иммунодефицита человека, а также иммунодепрессия с помощью лекарств. Тем не менее, покрытая коркой чесотка может возникать у лиц с явно иммунной недостаточностью, и некоторая семейная кластеризация предполагает возможность специфического иммунного дефекта у этих людей (97).Кроме того, чесотка с коркой, наблюдаемая у бывших больных лепрой, может возникать спустя долгое время после лечения инфекции и при отсутствии сенсорной нейропатии. Это привело к нашей гипотезе о том, что иммунный дефект, предрасполагающий к клиническому заболеванию лепрой, может также предрасполагать к гиперинфестации после заражения S. scabiei (66). Тем не менее, покрытая коркой чесотка также может иногда возникать локально на парализованной конечности или конечности с сенсорной нейропатией, предположительно отражая отсутствие зуда или невозможность почесать (23).Покрытая коркой чесотка также наблюдалась у пациентов с когнитивным дефицитом и у пациентов в специализированных учреждениях, по-видимому, из-за того, что они не могли должным образом интерпретировать связанный с этим зуд или физически не реагировать на зуд (67). Развитие трещин и вторичные бактериальные инфекции являются обычным явлением и связаны с высокой смертностью от этой формы заболевания (28) (рис.).
Покрытая коркой чесотка стоп.
Корковая чесотка века.
Покрытая коркой чесотка у больного проказой.
Покрытая коркой чесотка с хроническими вторичными язвами и депигментацией.
ЧЕСОТКА ЖИВОТНЫХ
Во всем мире S. scabiei вызывает чесотку у многих домашних животных и домашних животных, а также вызывает эпизоотические заболевания в диких популяциях ряда видов животных (89). Саркоптоз считается основной причиной смертности красных лисиц ( Vulpes vulpes ) (14), койотов (90) и обыкновенных вомбатов ( Vombatus ursinus) ( 74). Ветеринарные проблемы включают трудности в диагностике и контроле, а также экономический эффект чесотки на эффективность преобразования кормов.В производственных стадах интенсивный зуд, связанный с заболеванием, влияет на молочную продуктивность, прибавку в весе и качество кожи и может нанести серьезный экономический ущерб сырьевым отраслям (35, 95).
Клинические признаки чесотки
Клиническими признаками чесотки у животных являются слегка приподнятые красные папулы, наблюдаемые на участках тела с редкой шерстью. Очевиден сильный зуд с последующим расчесыванием, раздражением и воспалением кожи. Если чесотку не лечить, наблюдается выпадение волос, шелушение и образование корки на коже с высохшим экссудатом сыворотки (рис.). Возможна вторичная пиодермия. Передача клещей среди группы животных наиболее вероятна при прямом контакте или через зараженную подстилку.
Корки и алопеция у собаки с тяжелой чесоткой.
Специфичность хозяина
Популяции клещей в основном специфичны для хозяев, с небольшими доказательствами скрещивания между штаммами. Исследования перекрестных инфекций описывают безуспешные экспериментальные попытки передать чесоточного клеща от собак мышам, свиньям, крупному рогатому скоту, козам и овцам (10).Это подтверждается исследованиями молекулярного генотипирования, которые выявляют генетически разные популяции клещей, связанных с собаками и людьми, в аборигенных общинах Австралии, где чесотка является эндемической (106, 108). Сообщалось о единичных случаях чесотки у людей после контакта с чесоткой животных, но эти заражения, как правило, проходят самостоятельно, без каких-либо доказательств того, что долгосрочное размножение происходит у ненормального хозяина (15).
ИММУННЫЙ ОТВЕТ ХОЗЯИНА
Исследования симптомов и признаков чесотки указали на развитие иммунитета хозяина, но до недавнего Проекта по открытию генов чесотки (43) только небольшое количество антигенов, ответственных за иммунные реакции на чесотку, оказывалось секвенированы и охарактеризованы (51, 75).Следовательно, существует нехватка литературы, описывающей гуморальный или клеточный иммунитет против чесотки. Ограниченные прошлые исследования гуморального иммунитета у больных чесоткой показали противоречивые результаты и использовали экстракты цельноклещевой чесотки других хозяев, таких как собаки (82). Исследования иммуноблоттинга демонстрируют, что сыворотки от пациентов с корковой чесоткой показали сильное связывание IgE с 21 S. scabiei var. canis белков (4). Однако личность этих аллергенов была неизвестна.Отмечено, что у пациентов с покрытой коркой чесоткой чрезвычайно высокие уровни общего IgE и IgG в сыворотке крови (97). Клеточно-опосредованные иммунные ответы хозяина были идентифицированы, прежде всего, путем гистопатологического исследования образцов биопсии кожи из скабиетических поражений. Норы клещей окружены инфильтратами воспалительных клеток, состоящими из эозинофилов, лимфоцитов и гистиоцитов (рис.). Кроме того, было обнаружено, что образцы биопсии, содержащие как клещей, так и воспалительные папулы, содержат отложения IgE в стенках сосудов в верхней части дермы (20).Неизвестные компоненты в экстракте S. scabiei var. canis , как было показано, влияет на экспрессию цитокинов в культивируемых кератиноцитах, фибробластах человека, мононуклеарных клетках периферической крови человека и дендритных клетках (5-7). Текущие исследования изучают антитела больных чесоткой и клеточные ответы на специфический рекомбинантный S. scabiei var. hominis антигенов. Результаты выявили у пациентов как с покрытой коркой, так и с обычной чесоткой сильные пролиферативные ответы мононуклеарных клеток периферической крови и ответы антител IgE на множественные S.scabiei является гомологом аллергенов клещей домашней пыли (Walton and Currie, неопубликовано). Инактивированные клещом чесотки паралоги сериновой протеазы были идентифицированы как внутри кишечника клеща, так и снаружи в кале (114). Кроме того, человеческий IgG был идентифицирован в кишечнике клещей, который предположительно должен также содержать каскады сериновых протеаз как путей свертывания крови, так и путей связывания комплемента. Было показано, что комплемент является важным компонентом защиты хозяина от клещей (113).Оба эти пути должны быть заблокированы при одновременном переваривании эпидермального белка во время еды.
Биопсия кожи покрытой коркой чесотки выявляет клещей в эпидермисе с гиперкератозом и воспалительной реакцией.
Реакции гиперчувствительности немедленного типа и замедленного типа на чесоточных клещей
Сильный зуд и папулезная сыпь при первичном заражении сопровождаются поражениями кожи, характеризующимися инфильтратами воспалительных клеток, типичными для опосредованной клетками иммунной реакции замедленной чувствительности.Тем не менее, немедленные реакции на волдыри вызываются внутрикожными инъекциями экстрактов чесоточного клеща как у обычных пациентов, так и у пациентов с корковой чесоткой, но не у здоровых добровольцев (42, 105). Этот ответ со временем ослабевает, и пациенты, которым вводили инъекции через 15-24 месяцев после заражения, не реагировали.
Перекрестная реактивность между инфекциями чесоточного клеща и аллергией на клещей домашней пыли
Исследования показали, что пациенты, чувствительные к клещам домашней пыли, но не болеющие чесоткой в анамнезе, имеют циркулирующие антитела IgE, которые распознают антигены в S.scabiei var. canis экстракт (13). Кроме того, вестерн-блоттинг и радиоаллергосорбентные анализы показали, что у людей с чесоткой наблюдается сильное связывание IgE с экстрактом клещей домашней пыли (40). Конкретные перекрестно-реактивные молекулы остаются неидентифицированными, но могут отражать некоторую перекрестную реактивность IgE, связанного с полисахаридами (71). Клещи чесотки и клещи домашней пыли являются филогенетически родственными членистоногими, и неудивительно, что они или их выделения или выделения имеют гомологичные аллергены.Однако неизвестно, сколько из них будут иметь перекрестную реактивность и каково клиническое значение любой такой перекрестной реактивности. Например, были проведены исследования перекрестной реактивности между аллергенами группы 5 клещей домашней пыли Dermatophagoides pteronyssinus и Blomia tropicalis (Der p 5 и Blo t 5), и, хотя они имеют 43% аминокислотную идентичность, они было обнаружено, что они не обладают перекрестной реактивностью (68).
ЛЕЧЕНИЕ
На рынке имеется ряд средств для лечения чесотки, и выбор в значительной степени зависит от возраста пациента, состояния его здоровья, степени раздражения или экземы, потенциальной токсичности, стоимости и доступности.Например, ранее линдан (гексахлорид гаммабензола) был местным средством, наиболее часто рекомендованным для лечения чесотки в западных странах. Однако из-за потенциальной нейротоксичности он был удален с рынка Австралии и большей части Европы. Пятипроцентный перметрин в настоящее время является наиболее часто назначаемым местным лечением в богатых странах, но его стоимость исключает его использование во многих регионах, где чесотка является эндемической. Местное применение активных веществ является основным средством эффективного лечения, хотя пероральный ивермектин все чаще используется и в настоящее время зарегистрирован для лечения чесотки во Франции (25, 98).В ситуациях, когда чесотка носит эндемический характер, эмпирическое лечение часто более рентабельно, чем попытки лабораторной диагностики. Программы вмешательства в Панаме, Бразилии, на Соломоновых островах и в отдаленных общинах северных австралийских аборигенов привели к резкому снижению распространенности чесотки и кожных язв (58, 103, 116). Эти программы включают либо массовое местное лечение членов сообщества 5% перметрином, либо пероральное введение ивермектина с различными моделями, адаптированными к местным условиям.Успех на уровне отдельных сообществ был разным и не всегда был устойчивым. Часто низкий уровень чесотки сохраняется в сообществах после реализации этих программ на уровне сообществ (115). Кроме того, массовое лечение по месту жительства в эндемичных сообществах создает среду для зарождающейся толерантности к лекарствам или устойчивости, и необходимы новые подходы к борьбе. Опубликованные in vitro исследования эффективности акарицидов показывают, что клещей S. scabiei в северной Австралии становятся все более толерантными к 5% перметрину (111), а недавно была подтверждена клиническая и in vitro устойчивость к ивермектину в случаях чесотки (31).Устойчивость также следует учитывать в регионах, не являющихся эндемичными, когда у пациентов наблюдаются стойкие симптомы в течение нескольких недель после лечебного лечения. Новые многообещающие акарициды включают ряд эфирных масел, в которых терпеноиды, скорее всего, являются основными активными компонентами (110). Обнадеживающие результаты in vitro и в полевых условиях были получены для 5% масла чайного дерева, экстрагированного из дерева Melaleuca alternifolia (110, 111), 20% масла липпии, экстрагированного из Lippia multiflora Moldenke (86), пасты из нима ( Azadirachta indica ADR) и куркумы ( Curcuma longa ) (24), камфорное масло ( Eucalyptus globulus ) (83) и коммерчески доступный репеллент, содержащий масло кокоса и жожоба (55).В регионах, где распространенность чесотки среди детей составляет от 5 до 10%, важно иметь возможность противодействовать эпидемии чесотки с помощью эффективных методов лечения и чувствительного и специфического инструмента, способного определять как клинические, так и субклинические заражения. При лечении корковой чесотки отмечается важность сочетания местной терапии с пероральным приемом ивермектина (77). В тяжелых случаях корковой чесотки может потребоваться до семи доз ивермектина для лечения и искоренения клещей (64, 97).
МЕТОДЫ ДИАГНОСТИКИ
Клинический диагноз
В настоящее время не существует эффективных средств диагностики чесотки у людей или животных. На сегодняшний день диагноз ставится с помощью клинических признаков и микроскопического исследования соскобов кожи, но опыт показал, что чувствительность этих традиционных тестов составляет менее 50%. Обнаружить видимые поражения может быть сложно, так как они часто не видны из-за экземы или импетиго или нетипичны. Обнаружение нор индийскими чернилами пропагандировалось более 20 лет назад (117), но этот тест часто непрактичен и обычно не используется.Предположительный диагноз может быть поставлен на основании типичного анамнеза зуда, зуда, который усиливается ночью, распространения воспалительных папул и контактов с другими случаями чесотки (76).
Микроскопия
Окончательный диагноз основан на выявлении клещей, яиц, фрагментов яичной скорлупы или фекальных гранул клещей в соскобах кожи (например, от скабиетических папул или из-под ногтей) или на обнаружении клеща в конце его нора.Одна или две капли минерального масла наносятся на поражение, которое затем соскабливается или сбривается, и образцы исследуются после очистки в 10% КОН с помощью светового микроскопа при малом увеличении. Этот метод обеспечивает отличную специфичность, но имеет низкую чувствительность при обыкновенной чесотке из-за небольшого количества паразитов. Кроме того, на уровень чувствительности могут влиять несколько факторов, например, клиническая картина (царапины более ценны), количество участков, в которых были взяты образцы, и / или повторных соскобов, а также опыт работы с пробоотборником.Биопсия кожи может подтвердить диагноз чесотки, если можно идентифицировать клеща или его части. Однако в большинстве случаев гистологически проявляется неспецифическая гиперчувствительность замедленного типа с поверхностными и глубокими периваскулярными воспалительными мононуклеарными инфильтратами с многочисленными эозинофилами, папиллярным отеком и эпидермальным спонгиозом (41). На практике выявить клеща сложно, и отрицательный результат, даже от эксперта, не исключает чесотку. Предполагаемая терапия может использоваться в качестве диагноза, но ее ценность сомнительна и осложняется переменной задержкой до исчезновения симптомов после терапии.Положительный ответ на лечение не может исключить спонтанное исчезновение дерматологического заболевания, отличного от чесотки, а отрицательный ответ не исключает чесотку, особенно с устойчивыми клещами (25). В отсутствие подтвержденных клещей диагноз в настоящее время полностью основывается на клинических и эпидемиологических данных. Учитывая обширные дифференциальные диагнозы, специфичность клинического диагноза оставляет желать лучшего, особенно для тех, кто не имеет опыта в отношении чесотки. Кроме того, трудно различить активное заражение, остаточную кожную реакцию и повторное заражение.
Дерматоскопия
Эпилюминесцентная микроскопия и видеодерматоскопия с высоким разрешением — это неинвазивные методы, которые позволяют детально обследовать кожу пациента, от поверхности до поверхностного сосочкового слоя дермы (2, 49, 80). Диагноз ставится на основании наблюдений за рисунком «струя с инверсионным следом» на коже клеща и его норе. Из-за трудностей с получением соскобов кожи у некоторых пациентов, например младенцев, и недостаточной чувствительности классических методов дерматоскопия может быть информативной (49), но исследования, проведенные на больших группах пациентов, отсутствуют (25) и ограничены высокой стоимостью оборудование.
Обнаружение антигенов и ПЦР-диагностика
Ключевым недостатком ПЦР-диагностики чесотки является то, что, как и в случае с микроскопией, она зависит от физического присутствия клеща или его части в образце. Поэтому маловероятно, что он станет жизнеспособным тестом для широкого использования из-за в целом низкой нагрузки клещей и, следовательно, низкой чувствительности. Было предложено, что ПЦР с последующим иммуноферментным анализом обнаружения продукта ПЦР является чувствительным методом диагностики пациентов с атипичной чесоткой (16).Однако описанный метод был трудоемким и длительным.
Внутрикожный кожный тест на чесотку
В настоящее время метод внутрикожного кожного теста невозможно использовать с экстрактом цельного клеща из-за невозможности культивирования достаточных количеств S. scabiei . Кроме того, экстракты целого клеща, полученные на животных моделях, содержат гетерогенную смесь антигенов хозяина и паразита, включая перекрестно-реактивные эпитопы клещей домашней пыли, и различаются по составу, активности и чистоте.Пациенты с чесоткой часто обращаются к врачам с генерализованным зудом неизвестной причины. Очищенные, хорошо изученные рекомбинантные аллергены чесоточного клеща со стандартизованным содержанием белка потенциально могут быть использованы в будущем для кожных тестов на чесотку в клинически трудно диагностируемых случаях и для иммунотерапии.
Обнаружение антител
Исследования подтверждают, что заражение чесоточным клещом вызывает выработку измеримых антител у инфицированных видов хозяев (4, 40).Кроме того, IgG хозяина были продемонстрированы в передней части средней кишки и пищевода свежих клещей (94, 114). В настоящее время разработаны иммуноферментные анализы для обнаружения антител к S. scabiei у свиней и собак, и они коммерчески доступны в Европе (17, 18, 59). Эти анализы основаны на препаратах цельных клещей, полученных из S. scabiei var. suis и чесоточный клещ красной лисы, S. scabiei var. vulpes , поэтому имеют ограничения по доступности и специфичности.Важно отметить, что недавнее исследование перекрестно реагирующих антител IgG к антигену лисьего клеща при чесотке человека показало, что чувствительность составляет всего 48% по сравнению с 80% при чесотке свиней и 84% при чесотке собак (50). Это неудивительно, поскольку исследования с использованием молекулярных маркеров показывают, что организмов S. scabiei от людей и животных генетически различны и что скрещивание или перекрестная инфекция, по-видимому, крайне редки (106, 108).
S. SCABIEI GENE DISCOVERYОсновным ограничением в биомедицинских исследованиях чесотки была сложность получения клещей в достаточном количестве из-за в целом низкой нагрузки паразитов и отсутствия системы культивирования in vitro.Чтобы преодолеть это, в настоящее время сконструированы библиотеки кДНК из S. scabiei var. hominis и S. scabiei var. vulpes (43, 44, 70), и были созданы большие базы данных тегов экспрессируемых последовательностей, содержащие как частичные, так и полные последовательности ДНК генов S. scabiei . Из этих баз данных в настоящее время идентифицированы гомологи чесоточного клеща большинству известных аллергенов клещей домашней пыли, а также многие другие соответствующие молекулы (33, 43, 61, 62, 75, 91).Рекомбинантные антигены обещают постоянное воспроизводимое количество аллергенных белков в очищенной форме, подходящей для использования в анализах in vitro.
Иммунодиагностический анализ с использованием рекомбинантных
аллергенов S. scabieiНедавно было клонировано, экспрессировано и очищено сродство ряда гомологов чесоточного клеща к аллергенам клеща домашней пыли. К ним относятся зрелые формы как активных, так и неактивных гомологов аллергенов группы 1 цистеиновой протеазы (62), зрелые формы активных и неактивных гомологов аллергенов группы 3 сериновой протеазы (61), мю-класс и дельта-класс глутатиона S -трансферазный аллерген группы 8 (33, 91) и гомолог С-концу аллергена аполипопротеиновой группы 14 (51).Иммуногистохимическое окрашивание срезов кожи человека, которые были сильно заражены клещами S. scabiei , показало, что антитела против группы 8 и против группы 14 (генерируемые у мышей и кроликов соответственно) локализованы во внутренних органах чесоточных клещей и кутикула с незначительным окрашиванием в пищеварительной системе (51) (рис.). Более того, аллергены чесоточного клеща группы 1 и группы 3 теперь экспрессируются в Pichia pastoris со значительными доказательствами того, что они находятся в естественной конформации и локализованы в пищеварительной системе клеща (114; D.Кемп и К. Фишер, личное сообщение). В настоящее время проводятся исследования для оценки диагностического потенциала идентифицированных белков путем характеристики конкретных гуморальных и клеточных иммунных ответов человека и животных. Серологические признаки, которые являются диагностически важными, — это интервал между воздействием инфекции и ответом антител, а также природа антител, составляющих ответ.
Серийное рассечение чесоточного клеща человека. Красный цвет показывает связывание поликлональных антител S. scabiei против группы 8, полученных у кроликов, с белком in vivo.(Любезно предоставлено К. Уиллисом, Институт медицинских исследований Квинсленда, Брисбен, Квинсленд, Австралия.)
ВЫВОДЫ
Используя соответствующий рекомбинантный антиген, разработка иммунодиагностического теста S. scabiei стала реальной возможностью. Его разработка позволит избирательно лечить больных людей и животных, снизив потребность в массовом лечении и связанные с этим расходы. Это должно снизить вероятность роста устойчивости к клещам и предоставить еще один способ борьбы с чесоткой в сильно пораженных областях.Существует мало доказательств того, что простое массовое лечение эффективно в долгосрочной перспективе. Молекулярные исследования, направленные на улучшение диагностики и улучшение терапевтических возможностей, внесут значительный вклад в снижение высокой распространенности чесотки, наблюдаемой в настоящее время в общинах с ограниченными ресурсами.
Благодарности
Эта работа была поддержана Австралийским национальным советом по здравоохранению и медицинским исследованиям, грантами 283300 и 320867, а также Фондом детских исследований Channel 7 в Южной Австралии.
СПИСОК ЛИТЕРАТУРЫ
1. Александр, Дж. О. 1984. Членистоногие и кожа человека. Шпрингер-Верлаг, Берлин, Германия.
2. Argenziano, G., G. Fabbrocini и M. Delfino. 1997. Эпилюминесцентная микроскопия. Arch. Дерматол. 133 : 751-753. [PubMed] [Google Scholar] 3. Арлиан, Л. Г., М. Ахмед, Д. Л. Вышенский-Мохер, С. А. Эстес и С. Ахар. 1988. Энергетические отношения Sarcoptes scabiei var. canis (Acari: Sarcoptidae) с лабораторным кроликом.J. Med. Энтомол. 25 : 57-63. [PubMed] [Google Scholar] 4. Арлиан, Л. Г., М. С. Морган, С. А. Эстес, С. Ф. Уолтон, Д. Дж. Кемп и Б. Дж. Карри. 2004. Циркулирующий IgE у пациентов с обыкновенной и покрытой коркой чесоткой. J. Med. Энтомол. 41 : 74-77. [PubMed] [Google Scholar] 5. Арлиан, Л. Г., М. С. Морган и Дж. С. Нил. 2004. Экстракты чесоточных клещей (Sarcoptidae: Sarcoptes scabiei) модулируют экспрессию цитокинов мононуклеарными клетками периферической крови и дендритными клетками.J. Med. Энтомол. 41 : 69-73. [PubMed] [Google Scholar] 6. Арлиан, Л. Г., М. С. Морган и Дж. С. Нил. 2003. Модуляция экспрессии цитокинов в кератиноцитах и фибробластах человека экстрактами чесоточных клещей. Являюсь. J. Trop. Med. Hyg. 69 : 652-656. [PubMed] [Google Scholar] 7. Арлиан, Л. Г., М. С. Морган и К. С. Пол. 2006. Доказательства того, что чесоточные клещи (Acari: Sarcoptidae) влияют на выработку интерлейкина-10 и функцию Т-регуляторных клеток (Tr1) у людей.J. Med. Энтомол. 43 : 283-287. [PubMed] [Google Scholar] 8. Арлиан, Л. Г., М. С. Морган, К. М. Рапп и Д. Л. Вышенски-Мохер. 1996. Развитие защитного иммунитета при чесотке собак. Вет. Паразитол. 62 : 133-142. [PubMed] [Google Scholar] 9. Арлиан, Л. Г., Р. А. Рунян, С. Ачар, С. А. Эстес. 1984. Выживаемость и зараженность Sarcoptes scabiei var. канис и вар. человек . Варенье. Акад. Дерматол.11 : 210-215. [PubMed] [Google Scholar] 10. Арлиан, Л. Г., Р. А. Рунян, С. А. Эстес. 1984. Перекрестная инфекция Sarcoptes scabiei . Варенье. Акад. Дерматол. 10 : 979-986. [PubMed] [Google Scholar] 11. Арлиан, Л. Г., Р. А. Рунян, Л. Б. Сорли и С. А. Эстес. 1984. Поведение Sarcoptes scabiei в поисках хозяина. Варенье. Акад. Дерматол. 11 : 594-598. [PubMed] [Google Scholar] 12. Арлиан, Л. Г., и Д. Л.Вышенский-Мохер. 1988 г. Жизненный цикл Sarcoptes scabiei var canis . J. Parasitol. 74 : 427-430. [PubMed] [Google Scholar] 13. Арлиан Л. Г., Д. Л. Вышенский-Мохер, С. Г. Ахмед и С. А. Эстес. 1991. Перекрестная антигенность чесоточного клеща Sarcoptes scabiei и клеща домашней пыли Dermatophagoides pteronyssinus . J. Investig. Дерматол. 96 : 349-354. [PubMed] [Google Scholar] 14. Бейтс, П. 2003. Саркоптоз ( Sarcoptes scabiei var. vulpes ) у красной лисицы ( Vulpes vulpes ) в северо-западной части графства Суррей. Вет. Рек. 152 : 112-114. [PubMed] [Google Scholar] 15. Бек, А. Л., мл. 1965. Чесотка животных, поражающая человека. Arch. Дерматол. 91 : 54-55. [PubMed] [Google Scholar] 16. Г. Бецольд, М. Ланге, Р. Шинер, Г. Пальмедо, К. А. Сандер, М. Кершер и Р. У. Питер. 2001. Скрытая чесотка: диагностика методом полимеразной цепной реакции.Br. J. Dermatol. 144 : 614-618. [PubMed] [Google Scholar] 17. С. Борнштейн, П. Тибо и Г. Закриссон. 1996. Оценка иммуноферментного анализа (ELISA) для серологической диагностики саркоптоза собак. Вет. Дерматол. 7 : 21-27. [Google Scholar] 18. Bornstein, S., and P. Wallgren. 1997. Серодиагностика саркоптоза свиней. Вет. Рек. 141 : 8-12. [PubMed] [Google Scholar] 19a. Burgess, I. 1994. Sarcoptes scabiei и чесотка.Adv. Паразитол. 33 : 235-292. [PubMed] [Google Scholar] 20. Кабрера Р. и М. В. Даль. 1993. Иммунология чесотки. Семин. Дерматол. 12 : 15-21. [PubMed] [Google Scholar] 21. Карапетис, Дж., К. Коннорс, Д. Ярмирр, В. Краузе и Б. Карри. 1997. Успех программы борьбы с чесоткой в общине австралийских аборигенов. Педиатр. Заразить. Дис. J. 16 : 494-499. [PubMed] [Google Scholar] 22. Каргилл, К. Ф., А. М. Пойнтон, П. Р.Дэвис и Р. Гарсия. 1997. Использование инспекций убоя для оценки зараженности саркоптозом свиней на откорме. Вет. Паразитол. 70 : 191-200. [PubMed] [Google Scholar] 24. Чарльз В. и С. X. Чарльз. 1992. Применение и эффективность Azadirachta indica ADR («Ним») и Curcuma longa («Куркума») при чесотке. Пилотное исследование. Троп. Геогр. Med. 44 : 178-181. [PubMed] [Google Scholar] 26. Connors, C. 1994. Лечение чесотки.К северу. Terr. Commun. Дис. Бык. 2 : 5-6. [Google Scholar]27. Карри Б. и У. Хенгге. 2006. Чесотка, стр. 375-388. В С. Тайринг, О. Лупи и У. Хенгге (ред.), Тропическая дерматология. Эльзевир Черччилл Ливингстон, Лондон, Соединенное Королевство.
28. Карри Б., С. Хаффам, Д. О’Брайен и С. Уолтон. 1997. Ивермектин от чесотки. Lancet 350 : 1551. [PubMed] [Google Scholar] 29. Карри, Б. Дж. И Дж. Карапетис. 2000.Кожные инфекции и инвазии в общинах аборигенов в северной Австралии. Австралас. J. Dermatol. 41 : 139-143. [PubMed] [Google Scholar] 30. Карри, Б. Дж., К. М. Коннорс и В. Л. Краузе. 1994. Программы борьбы с чесоткой в общинах аборигенов. Med. J. Aust. 161 : 636-637. [PubMed] [Google Scholar] 31. Карри, Б. Дж., П. Харумал, М. Маккиннон и С. Ф. Уолтон. 2004. Первое документальное подтверждение устойчивости к ивермектину in vivo и in vitro у Sarcoptes scabiei .Clin. Заразить. Дис. 39 : e8-e12. [PubMed] [Google Scholar] 32. де Бир, Г., М. А. Миллер, Л. Трембле и Дж. Монетт. 2006. Вспышка чесотки в учреждении длительного ухода: роль ошибочного диагноза и затраты, связанные с контролем. Заразить. Control Hosp. Эпидемиол. 27 : 517-518. [PubMed] [Google Scholar] 33. Дугалл А., Д. К. Холт, К. Фишер, Б. Дж. Карри, Д. Дж. Кемп и С. Ф. Уолтон. 2005. Идентификация и характеристика Sarcoptes scabiei и Dermatophagoides pteronyssinus S-трансферазы глутатиона: роль основного потенциального аллергена при корковой чесотке.Являюсь. J. Trop. Med. Hyg. 73 : 977-984. [PubMed] [Google Scholar] 34. Даунс, А. М., И. Харви и К. Т. Кеннеди. 1999. Эпидемиология головных вшей и чесотки в Великобритании. Эпидемиол. Заразить. 122 : 471-477. [Бесплатная статья PMC] [PubMed] [Google Scholar] 35. Эльберс А. Р., П. Г. Рамбагс, Х. М. ван дер Хейден и В. А. Хуннеман. 2000. Производительность и зуд свиней, естественно инфицированных Sarcoptes scabiei var suis в эксперименте по контактной передаче.Вет. В. 22 : 145-149. [PubMed] [Google Scholar] 36. Estes, S. A., and J. Estes. 1993. Терапия чесотки: дома престарелых, больницы, бездомные. Семин. Дерматол. 12 : 26-33. [PubMed] [Google Scholar]37. Ссылка удалена.
38. Файн, А. 1978. Эпидемиологические проблемы чесотки. Int. J. Dermatol. 17 : 20-30. [PubMed] [Google Scholar] 39. Fain, A. 1968. Étude de la variabilit é de Sarcoptes scabiei avec une revision des Sarcoptidae.Acta Zool. Патол. Антверпен. 47 : 1-196. [Google Scholar] 40. Э. Фальк и Р. Болле. 1980. IgE-антитела к клещу домашней пыли у больных чесоткой. Br. J. Dermatol. 102 : 283-288. [PubMed] [Google Scholar] 41. Э. Фальк и Т. Эйде. 1981. Гистологические и клинические данные при чесотке у человека. Int. J. Dermatol. 20 : 600-605. [PubMed] [Google Scholar] 42. Фальк, Э. С. и Р. Болле. 1980. In vitro демонстрация специфической иммунологической гиперчувствительности к чесоточному клещу.Br. J. Dermatol. 103 : 367-373. [PubMed] [Google Scholar] 43. Фишер К., Д. К. Холт, П. Харумал, Б. Дж. Карри, С. Ф. Уолтон и Д. Дж. Кемп. 2003. Получение и характеристика клонов кДНК из Sarcoptes scabiei var. hominis для библиотеки экспрессируемых тегов последовательностей: идентификация гомологов аллергенов клещей домашней пыли. Являюсь. J. Trop. Med. Hyg. 68 : 61-64. [PubMed] [Google Scholar] 44. Фишер К., Д. К. Холт, П. Уилсон, Дж.Дэвис, В. Хьюитт, М. Джонсон, А. МакГрат, Б. Дж. Карри, С. Ф. Уолтон и Д. Дж. Кемп. 2003. Нормализация библиотеки кДНК, клонированной в lZAP, с помощью длинной процедуры ПЦР и реассоциации кДНК. BioTechniques 34 : 250-254. [PubMed] [Google Scholar] 45. Гиббс, С. 1996. Кожные заболевания и социально-экономические условия в сельских районах Африки: Танзания. Int. J. Dermatol. 35 : 633-639. [PubMed] [Google Scholar] 46. Грин, М. С. 1989. Эпидемиология чесотки. Эпидемиол.Ред. 11 : 126-150. [PubMed] [Google Scholar] 47. Д. Гуггисберг, П. А. де Вираг, К. Константин и Р. Г. Паницсон. 1998. Норвежская чесотка у больного с синдромом приобретенного иммунодефицита. Дерматология 197 : 306-308. [PubMed] [Google Scholar] 48. Guldbakke, K. K., and A. Khachemoune. 2006. Корковая чесотка: клинический обзор. J. Drugs Dermatol. 5 : 221-227. [PubMed] [Google Scholar] 49. Н. Хаас и У. Стерри. 2001. Использование ELM для контроля успешности противокабетического лечения.Эпилюминесцентная световая микроскопия. Arch. Дерматол. 137 : 1656-1657. [PubMed] [Google Scholar] 50. Н. Хаас, Б. Вагеманн, Б. Гермес, Б. М. Хенц, К. Хейле и Э. Шайн. 2005. Перекрестно реагирующие антитела IgG против антигенов лисьего клеща при чесотке человека. Arch. Дерматол. Res. 296 : 327-331. [PubMed] [Google Scholar] 51. Харумал П., М. С. Морган, С. Ф. Уолтон, Д. К. Холт, Дж. Роде, Л. Г. Арлиан, Б. Дж. Карри и Д. Дж. Кемп. 2003. Идентификация гомолога аллергена клеща домашней пыли в библиотеке кДНК из Sarcoptes scabiei var. hominis и оценка его вакцинного потенциала на кролике / S. scabiei var. canis модель. Являюсь. J. Trop. Med. Hyg. 68 : 54-60. [PubMed] [Google Scholar] 52. Hebra, F. 1868. О кожных заболеваниях, включая экзантемы, vol. 2, стр. 164–252. Новое общество Сиденхэма, Лондон, Соединенное Королевство. (Перевод К. Х. Фагге и П. Х. Пай-Смита.) [Google Scholar] 53. Хегази, А. А., Н. М. Дарвиш, И. А. Абдель-Хамид и С. М. Хаммад. 1999.Эпидемиология и борьба с чесоткой в египетской деревне. Int. J. Dermatol. 38 : 291-295. [PubMed] [Google Scholar] 54. Heilesen, B. 1946. Исследования Acarus scabiei и чесотки. Acta Dermato-Venereol. 26 (Дополнение) : 1-370. [Google Scholar] 55. Хойкельбах, Дж. И Х. Фельдмайер. 2006. Чесотка. Ланцет 367 : 1767-1774. [PubMed] [Google Scholar] 56. Хойкельбах, Дж., Э. ван Хафф, Б. Рамп, Т. Вилке, Р. К. Моура и Х. Фельдмайер. 2003.Паразитарные кожные заболевания: обращение за медицинской помощью в трущобах на северо-востоке Бразилии. Троп. Med. Int. Здоровье 8 : 368-373. [PubMed] [Google Scholar] 57. Хойкельбах, Дж., С. Ф. Уолтон и Х. Фельдмайер. 2005. Эктопаразитарные инвазии. Curr. Заразить. Дис. Реп.7 : 373-380. [PubMed] [Google Scholar] 58. Хойкельбах, Дж., Т. Вилке, Б. Винтер, Ф. А. Салес де Оливейра, Р. К. Сабоя Моура, Г. Хармс, О. Лизенфельд и Х. Фельдмайер. 2004. Эффективность ивермектина в популяции пациентов, одновременно инфицированных кишечными гельминтами и эктопаразитами.Арзнейм.-Форш. 54 : 416-421. [PubMed] [Google Scholar] 59. Hollanders, W., J. Vercruysse, S. Raes и S. Bornstein. 1997. Оценка иммуноферментного анализа (ELISA) для серологической диагностики саркоптоза у свиней. Вет. Паразитол. 69 : 117-123. [PubMed] [Google Scholar] 60. Холнесс, Л., Дж. Г. ДеКовен и Дж. Р. Нетеркотт. 1992. Чесотка в хронических лечебных учреждениях. Arch. Дерматол. 128 : 1257-1260. [PubMed] [Google Scholar] 61. Холт, Д. К., К. Фишер, Г. Э. Аллен, Д. Уилсон, П. Уилсон, Р. Слейд, Б. Дж. Карри, С. Ф. Уолтон и Д. Дж. Кемп. 2003. Механизмы новой стратегии уклонения от иммунитета у чесоточного клеща Sarcoptes scabiei : мультигенное семейство инактивированных сериновых протеаз. J. Investig. Дерматол. 121 : 1419-1424. [PubMed] [Google Scholar] 62. Холт, Д. К., К. Фишер, С. Дж. Пиццутто, Б. Дж. Карри, С. Ф. Уолтон и Д. Дж. Кемп. 2004. Мультигенное семейство инактивированных цистеиновых протеаз в Sarcoptes scabiei .J. Investig. Дерматол. 123 : 240-241. [PubMed] [Google Scholar] 63. Hoy, W. 1996. Заболевание почек у австралийских аборигенов. Med. J. Aust. 165 : 126-127. [PubMed] [Google Scholar] 64. Huffam, S.E., and B.J. Currie. 1998. Ивермектин для лечения гиперинфестации Sarcoptes scabiei . Int. J. Infect. Дис. 2 : 152-154. [PubMed] [Google Scholar] 65. Кирнс Т., К. Эванс и В. Краузе. 2001 г. Вспышка острого постстрептококкового гломерулонефрита в Северной территории — 2000 г.К северу. Terr. Дис. Контрольный бык. 8 : 6-14. [Google Scholar] 66. Кемп Д., С. Уолтон, П. Харумал и Б. Карри. 2002. Бич чесотки. Биолог 49 : 19-24. [PubMed] [Google Scholar] 67. Колар, К. А. и Р. П. Рапини. 1991. Корковая (норвежская) чесотка. Являюсь. Fam. Врач 44 : 1317-1321. [PubMed] [Google Scholar] 68. Kuo, I.C., N. Cheong, M. Trakultivakorn, B.W. Lee и K.Y. Chua. 2003. Обширное исследование перекрестной реактивности человеческого IgE с Blo t 5 и Der p 5.J. Allergy Clin. Иммунол. 111 : 603-609. [PubMed] [Google Scholar] 69. Лоуренс, Г., Дж. Лифасиа, Дж. Шеридан, С. Хиллс, Дж. Уэйт, К. Уэйт, Дж. Монтгомери, Н. Пандея и Д. Пурди. 2005. Борьба с чесоткой, кожными язвами и гематурией у детей на Соломоновых островах: еще одна роль ивермектина. Бык. W.H.O.83 : 34-42. [Бесплатная статья PMC] [PubMed] [Google Scholar] 70. Ljunggren, E. L., D. Nilsson, and J. G. Mattsson. 2003. Анализ метки экспрессированной последовательности Sarcoptes scabiei .Паразитология 127 : 139-145. [PubMed] [Google Scholar] 71. Malandain, H. 2005. IgE-реактивные углеводные эпитопы — классификация, перекрестная реактивность и клиническое влияние. Аллерг. Иммунол. (Париж) 37 : 122-128. [PubMed] [Google Scholar] 72. Маллик С., Р. Н. Чаудхури, Р. Бисвас и Б. Бисвас. 2004. Исследование показателей заболеваемости детей-рабочих, занятых различными видами деятельности, в районе трущоб Калькутты. J. Indian Med. Доц. 102 : 198-200, 226.[PubMed] [Google Scholar] 73. Марчелл, Н. Л., Дж. Луптон и М. Л. Элгарт. 2002. Болезненные бляшки на подошвах ВИЧ-инфицированного мужчины. Arch. Дерматол. 138 : 973-978. [PubMed] [Google Scholar] 74. Мартин Р. У., К. А. Хандасайд и Л. Ф. Скерратт. 1998. Текущее распространение саркоптоза у вомбатов. Aust. Вет. J. 76 : 411-414. [PubMed] [Google Scholar] 75. Mattsson, J. G., E. L. Ljunggren и K. Bergstrom. 2001. Парамиозин паразитического клеща Sarcoptes scabiei : клонирование кДНК и гетерологичная экспрессия.Паразитология 122 : 555-562. [PubMed] [Google Scholar] 76. Маккарти, Дж. С., Д. Дж. Кемп, С. Ф. Уолтон и Б. Дж. Карри. 2004. Чесотка: больше, чем просто раздражение. Аспирантура. Med. J. 80 : 382-387. [Бесплатная статья PMC] [PubMed] [Google Scholar] 77. Мейнкинг, Т., Д. Таплин, Дж. Хермида, Р. Пардо и Ф. Кердел. 1995. Лечение чесотки ивермектином. N. Engl. J. Med. 333 : 26-30. [PubMed] [Google Scholar] 78. Mellanby, K. 1944.Развитие симптомов паразитарной инфекции и иммунитета при чесотке человека. Паразитология 35 : 197-206. [Google Scholar] 80. Г. Микали, Ф. Лакаррубба и А. Тедески. 2004. Видеодерматоскопия расширяет возможности мониторинга эффективности лечения чесотки и позволяет оптимальное время применения лекарств. J. Eur. Акад. Дерматол. Венереол. 18 : 153-154. [PubMed] [Google Scholar] 81. Монтесу М.А. и Ф. Коттони. 1991. Г. К. Бономо и Д. Честони. Первооткрыватели паразитарного происхождения чесотки.Являюсь. J. Dermatopathol. 13 : 425-427. [PubMed] [Google Scholar] 82. Морган, М. С., Л. Г. Арлиан и С. А. Эстес. 1997. Характеристики кожных проб и радиоаллергосорбентных проб у больных чесоткой. Являюсь. J. Trop. Med. Hyg. 57 : 190-196. [PubMed] [Google Scholar] 83. Морси Т.А., М.А. Рахем, Э.М. эль-Шаркави и М.А. Шатат. 2003. Eucalyptus globulus (камфорное масло) против зоонозной чесотки, Sarcoptes scabiei. J. Egypt. Soc. Паразитол. 33 : 47-53.[PubMed] [Google Scholar] 84. Наир, Б. К. Х., А. Дж. Кандамутан и М. Кандамутан. 1977. Эпидемия чесотки. Indian J. Med. Res. 65 : 513-518. [PubMed] [Google Scholar] 85. Odueko, O.M., O. Onayemi, and G.A. Oyedeji. 2001. Обследование распространенности кожных заболеваний у детей Нигерии. Нигер. J. Med. 10 : 64-67. [PubMed] [Google Scholar] 86. Оладимеджи, Ф. А., О. О. Орафидия, Т. А. Огуннийи и Т. А. Адевунми. 2000. Педикулоцидные и скабицидные свойства эфирного масла Lippia multiflora .J. Ethnopharmacol. 72 : 305-311. [PubMed] [Google Scholar] 88. Parish, L. C., J. A. Witkowski, L.E. Mililikan. 1991. Чесотка в лечебно-профилактическом учреждении. Int. J. Dermatol. 30 : 703-706. [PubMed] [Google Scholar] 89. Пенс, Д. Б. и Э. Иккерманн. 2002 г. Саркоптоз в дикой природе. Rev. Sci. Tech. Выключенный. Int. Эпизоот. 21 : 385-398. [PubMed] [Google Scholar] 90. Пенс, Д. Б., Л. А. Виндберг, Б. К. Пенс и Р. Спроулз. 1983.Эпизоотология и патология саркоптоза у койотов Canis latrans из южного Техаса. J. Parasitol. 69 : 1100-1115. [PubMed] [Google Scholar] 91. Петтерссон, Э. У., Э. Л. Люнггрен, Д. А. Моррисон и Дж. Г. Маттссон. 2005. Функциональный анализ и локализация S-трансферазы глутатиона дельта-класса из Sarcoptes scabiei. Int. J. Parasitol. 35 : 39-48. [PubMed] [Google Scholar] 92. Pruksachatkunakorn, C., A. Wongthanee и V. Kasiwat. 2003.Чесотка в тайских детских домах. Педиатр. Int. 45 : 724-727. [PubMed] [Google Scholar] 93. Ramos-e-Silva, M. 1998. Джован Козимо Бономо (1663-1696): первооткрыватель этиологии чесотки. Int. J. Dermatol. 37 : 625-630. [PubMed] [Google Scholar] 94. Рапп, К. М., М. С. Морган и Л. Г. Арлиан. 2006. Присутствие иммуноглобулина хозяина в кишечнике Sarcoptes scabiei (Acari: Sarcoptidae). J. Med. Энтомол. 43 : 539-542. [PubMed] [Google Scholar] 95. Ребейн С., М. Виссер, Р. Винтер, Б. Троммер, Х. Ф. Маттес, А. Э. Масиэль и С. Е. Марли. 2003. Влияние чесотки крупного рогатого скота на продуктивность и контроль с помощью ивермектина. Вет. Паразитол. 114 : 267-284. [PubMed] [Google Scholar] 96. Рейд, Х. Ф. М., Б. Бирджу, Й. Холдер, Дж. Хоспедалес и Т. Пун-Кинг. 1990 г. Эпидемия чесотки на четырех Карибских островах, 1981-1988 гг. Пер. R. Soc. Троп. Med. Hyg. 84 : 298-300. [PubMed] [Google Scholar] 97. Робертс, Л.J., S.E. Huffam, S.F. Walton и B.J. Currie. 2005. Корковая чесотка: клинические и иммунологические данные у семидесяти восьми пациентов и обзор литературы. J. Infect. 50 : 375-381. [PubMed] [Google Scholar] 98. Санторо, А. Ф., М. А. Резак и Дж. Б. Ли. 2003. Современные тенденции в использовании ивермектина при чесотке. J. Drugs Dermatol. 2 : 397-401. [PubMed] [Google Scholar] 99. Scheinfeld, N. 2004. Контроль чесотки в учреждениях: обзор лекарств, моделей лечения и реализации.Являюсь. J. Clin. Дерматол. 5 : 31-37. [PubMed] [Google Scholar] 100. Schmeller, W., and A. Dzikus. 2001. Кожные заболевания у детей в сельских районах Кении: долгосрочные результаты дерматологического проекта в системе первичной медико-санитарной помощи. Br. J. Dermatol. 144 : 118-124. [PubMed] [Google Scholar] 101. Д. Таплин, К. Арру, Дж. Г. Уокер, В. И. Рот и А. Ривера. 1983. Ликвидация чесотки с помощью единой схемы лечения. Варенье. Акад. Дерматол. 9 : 546-550.[PubMed] [Google Scholar] 102. Д. Таплин, Т. Л. Мейнкинг, Дж. А. Чен и Р. Санчес. 1990. Сравнение крема кротамитона 10% (Eurax) и крема перметрина 5% (Elimite) для лечения чесотки у детей. Педиатр. Дерматол. 7 : 67-73. [PubMed] [Google Scholar] 103. Таплин Д., С. Л. Фарфор, Т. Л. Мейнкинг, Р. Л. Этей, Дж. А. Чен, П. М. Кастильеро и Р. Санчес. 1991. Общественный контроль чесотки: модель, основанная на использовании крема с перметрином. Ланцет 337 : 1016-1018.[PubMed] [Google Scholar] 104. Д. Таплин и А. Ривера. 1983. Сравнительное испытание трех схем лечения для искоренения чесотки. Варенье. Акад. Дерматол. 9 : 550-554. [PubMed] [Google Scholar] 106. Уолтон С., Дж. Лоу Чой, А. Бонсон, А. Валле, Дж. Макбрум, Д. Тэплин, Л. Арлиан, Дж. Мэтьюз, Б. Карри и Д. Кемп. 1999. Генетически отличные Sarcoptes scabiei человеческого и собачьего происхождения в эндемичных по чесотке сообществах на севере Австралии.Являюсь. J. Trop. Med. Hyg. 61 : 542-547. [PubMed] [Google Scholar] 107. Уолтон, С. Ф., Б. Дж. Карри и Д. Дж. Кемп. 1997. Система ДНК-дактилоскопии эктопаразита Sarcoptes scabiei . Мол. Biochem. Паразитол. 85 : 187-196. [PubMed] [Google Scholar] 108. Уолтон, С. Ф., А. Дугалл, С. Пиццутто, Д. К. Холт, Д. Таплин, Л. Г. Арлиан, М. Морган, Б. Дж. Карри и Д. Дж. Кемп. 2004. Генетическая эпидемиология Sarcoptes scabiei (Acari: Sarcoptidae) в северной Австралии.Int. J. Parasitol. 34 : 839-849. [PubMed] [Google Scholar] 109. Уолтон, С. Ф., Д. К. Холт, Б. Дж. Карри и Д. Дж. Кемп. 2004. Чесотка: новое будущее забытой болезни. Adv. Паразитол. 57 : 309-376. [PubMed] [Google Scholar] 110. Уолтон, С. Ф., М. Маккиннон, С. Пиццутто, А. Дугалл, Э. Уильямс и Б. Дж. Карри. 2004. Акарицидная активность масла Melaleuca alternifolia (чайное дерево): чувствительность in vitro Sarcoptes scabiei var. hominis в терпинен-4-ол. Arch. Дерматол. 140 : 563-566. [PubMed] [Google Scholar] 111. Уолтон, С. Ф., М. Р. Майерско и Б. Дж. Карри. 2000. Исследования in vitro по относительной эффективности существующих акарицидов для Sarcoptes scabiei var. человек . Пер. R. Soc. Троп. Med. Hyg. 94 : 92-96. [PubMed] [Google Scholar] 112. Уайт, А., У. Хой и Д. Маккреди. 2001. Постстрептококковый гломерулонефрит в детском возрасте как фактор риска хронического заболевания почек в более позднем возрасте.Med. J. Aust. 174 : 492-496. [PubMed] [Google Scholar] 113. Wikel, S. K. 1979. Приобретенная устойчивость к клещам: выражение устойчивости у морских свинок с дефицитом С4. Являюсь. J. Trop. Med. Hyg. 28 : 586-590. [PubMed] [Google Scholar] 114. Уиллис К., К. Фишер, С. Ф. Уолтон, Б. Дж. Карри и Д. Дж. Кемп. 2006. Паралоги сериновой протеазы, инактивированные чесоточным клещом, присутствуют как внутри кишечника клеща, так и снаружи в кале. Являюсь. J. Trop. Med. Hyg. 75 : 683-687.[PubMed] [Google Scholar] 115. Вонг, Л., Б. Амега, Р. Баркер, К. Коннорс, Д. М., А. Ниннал, М. Кумаи, Л. Колумборт и Б. Карри. 2002. Факторы, поддерживающие устойчивость программы борьбы с чесоткой на уровне сообщества. Австралас. J. Dermatol. 43 : 274-277. [PubMed] [Google Scholar] 116. Вонг, Л. К., Б. Амега, К. Коннорс, Р. Баркер, М. Э. Дулла, А. Ниннал, Л. Колумборт, М. М. Кумаи и Б. Дж. Карри. 2001. Результат интервенционной программы по борьбе с чесоткой в сообществе коренных народов.Med. J. Aust. 175 : 367-370. [PubMed] [Google Scholar] 117. Вудли Д. и Дж. Х. Сорат. 1981. Тест чернил Burrow и чесоточный клещ. Варенье. Акад. Дерматол. 4 : 715-722. [PubMed] [Google Scholar]Чесотка: основы практики, общие сведения, патофизиология
Автор
Меган Барри, MD Врач-резидент, Отделение дерматологии, Медицинский факультет Университета Вирджинии
Раскрытие информации: Ничего не говорится.
Соавтор (ы)
Catharine Lisa Kauffman, MD, FACP Georgetown Dermatology and Georgetown Dermpath
Catharine Lisa Kauffman, MD, FACP является членом следующих медицинских обществ: Американской академии дерматологии, Американской медицинской ассоциации, Королевского медицинского общества, Общества исследователей Дерматология, Женское дерматологическое общество
Сообщение: Ничего не раскрывать.
Барбара Б. Уилсон, доктор медицины Эдвард П. Коули Адъюнкт-профессор кафедры дерматологии, Медицинский факультет Университета Вирджинии
Барбара Б. Уилсон, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, медицинская Общество Вирджинии, Сигма Си, Общество чести научных исследований
Раскрытие информации: нечего раскрывать.
Юджин Розен, MD Врач-резидент, Отделение неотложной медицины, Приемная больница Детройта
Раскрытие: Ничего не говорится.
Адам Дж. Рош, доктор медицины Ассистент-профессор, программный директор, резидентура по неотложной медицине, отделение неотложной медицины, Детройтская приемная больница, медицинский факультет Государственного университета Уэйна
Адам Дж. Рош, доктор медицины, является членом следующих медицинских обществ: Американского Академия неотложной медицины, Американский колледж врачей неотложной помощи, Общество академической неотложной медицины
Раскрытие: нечего раскрывать.
Главный редактор
Дирк М. Элстон, доктор медицины Профессор и заведующий кафедрой дерматологии и дерматологической хирургии Медицинского колледжа Медицинского университета Южной Каролины
Дирк Элстон, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие информации : Нечего раскрывать.
Благодарности
Уильям Д. Биндер, доктор медицины Клинический инструктор по неотложной медицине, Медицинский факультет Университета Брауна; Консультант, инструктор, отделение неотложной медицины, Массачусетская больница общего профиля
Раскрытие информации: нечего раскрывать.
Jennifer R Casatelli, MD Консультант, Отделение педиатрии, Клиника Watson в Лейкленде, Региональный медицинский центр Лейкленда
Раскрытие информации: нечего раскрывать.
Кевин П. Коннелли, DO , доцент кафедры педиатрии, отделение общей педиатрии и неотложной помощи, Медицинский факультет Университета Содружества Вирджинии; Медицинский директор программы посещения домашних животных «Лапы за здоровье» Ричмондской ассоциации охраны здоровья и животных; Педиатрический врач скорой помощи, Emergency Consultants Inc, Медицинский центр Чиппенхэма
Кевин П. Коннелли, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии педиатрии, Американского колледжа педиатров-остеопатов и Американской остеопатической ассоциации
.Раскрытие информации: нечего раскрывать.
Келли М. Кордоро, доктор медицины Доцент кафедры клинической дерматологии и педиатрии, факультет дерматологии Калифорнийского университета, Медицинская школа Сан-Франциско
Келли М. Кордоро, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американская медицинская ассоциация, Ассоциация профессоров дерматологии, Фонд дерматологии, Медицинское общество Вирджинии, Национальный фонд псориаза, Общество детской дерматологии. и Женское дерматологическое общество
Раскрытие информации: нечего раскрывать.
Kenneth E Greer, MD Бывший профессор кафедры дерматологии Медицинской школы Университета Вирджинии; Бывший председатель отделения дерматологии Медицинского центра
Университета ВирджинииРаскрытие информации: нечего раскрывать.
Ульрих Хенгге, MD, MBA Профессор, кафедра дерматологии, Университет Генриха Гейне, Дюссельдорф, Германия
Раскрытие информации: нечего раскрывать.
Дэниел Дж. Хоган, доктор медицины Клинический профессор внутренней медицины (дерматология), Колледж остеопатической медицины Юго-Восточного университета Нова; Исследователь, Hill Top Research, Исследовательский центр Флориды
Дэниел Дж. Хоган, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американской академии дерматологии, Американского общества контактного дерматита и Канадской дерматологической ассоциации
Раскрытие информации: нечего раскрывать.
Камила Джаннигер, доктор медицины Клинический профессор дерматологии, клинический доцент педиатрии, заведующий педиатрической дерматологией, Университет медицины и стоматологии Медицинской школы Нью-Джерси-Нью-Джерси
Камила К. Джаннигер, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие информации: нечего раскрывать.
Пол Крусински, доктор медицины Директор дерматологии, Fletcher Allen Health Care; Профессор кафедры внутренней медицины Медицинского колледжа Вермонтского университета
Пол Крусински, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Американского колледжа врачей и Общества исследовательской дерматологии
Раскрытие информации: нечего раскрывать.
Мудра Кумар, MD, MBBS, MRCP Доцент кафедры педиатрии Медицинского колледжа Университета Южной Флориды
Мудра Кумар, MD, MBBS, MRCP является членом следующих медицинских обществ: Американской академии педиатрии и Американского общества гематологов
Раскрытие информации: нечего раскрывать.
Audra Malerba, MD штатный врач, отделение семейной медицины, Медицинский центр Лонг-Бич, Нью-Йорк
Раскрытие информации: нечего раскрывать.
Эми Л. Маккроски, доктор медицины Врач-резидент, отделение неотложной медицины, Детройтский медицинский центр государственного университета Уэйна, приемная больница Детройта
Эми Л. МакКроски, доктор медицинских наук, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американской ассоциации / фонда студентов-медиков и Общества академической неотложной медицины
Раскрытие информации: нечего раскрывать.
Джузеппе Микали, доктор медицины Заведующий кафедрой дерматологии Медицинской школы Университета Катании, Италия
Джузеппе Микали, доктор медицины, является членом следующих медицинских обществ: Американская академия дерматологии
Раскрытие информации: нечего раскрывать.
Роберт О’Коннор, доктор медицины, магистр здравоохранения Профессор и заведующий кафедрой неотложной медицины, Система здравоохранения Университета Вирджинии
Роберт Э. О’Коннор, доктор медицины, магистр здравоохранения, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американского колледжа врачей, Американской кардиологической ассоциации, Американской медицинской ассоциации, Медицинского общества штата Делавэр, Национальная ассоциация врачей скорой медицинской помощи, Общество академической неотложной медицины и Общество медицины дикой природы
Раскрытие информации: нечего раскрывать.
Адам Дж. Рош, доктор медицины Доцент, отделение неотложной медицины, Детройтская приемная больница, Медицинский факультет Государственного университета Уэйна
Адам Дж. Рош, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи и Общества академической неотложной медицины
Раскрытие информации: нечего раскрывать.
Джозеф А. Саломон III, доктор медицины Адъюнкт-профессор и обслуживающий персонал, Медицинские центры Трумэна, Медицинская школа Университета Миссури в Канзас-Сити; Медицинский директор EMS, Канзас-Сити, Миссури,
Джозеф А. Саломон III, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Национальной ассоциации врачей скорой помощи и Общества академической неотложной медицины
Раскрытие информации: нечего раскрывать.
Роберт А. Шварц, доктор медицины, магистр здравоохранения Профессор и руководитель дерматологии, профессор патологии, педиатрии, медицины, профилактической медицины и общественного здравоохранения, Университет медицины и стоматологии Медицинской школы Нью-Джерси-Нью-Джерси
Роберт А. Шварц, доктор медицины, магистр здравоохранения является членом следующих медицинских обществ: Alpha Omega Alpha, Американская академия дерматологии, Американский колледж врачей и Sigma Xi
.Раскрытие информации: нечего раскрывать.
Joseph Sciammarella, MD, FACP, FACEP, FAAMA Major, MC, USAR Лечащий врач, Департамент неотложной медицины, Медицинский центр Милосердия, Роквилл-центр, Нью-Йорк
Раскрытие информации: нечего раскрывать.
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Medscape Salary Employment
Джетер (Джей) Притчард Тейлор III, MD Специалист по соблюдению нормативных требований, лечащий врач, отделение неотложной медицины, отделение неотложной медицины, Palmetto Health Richland, Школа медицины Университета Южной Каролины; Медицинский директор отделения неотложной медицины, Palmetto Health Baptist
Джетер (Джей) Притчард Тейлор III, доктор медицины, является членом следующих медицинских обществ: Американской академии неотложной медицины, Американского колледжа врачей неотложной помощи, Американской медицинской ассоциации и Общества академической неотложной медицины
Раскрытие информации: нечего раскрывать.
Ричард П. Винсон, доктор медицины Ассистент клинического профессора, кафедра дерматологии, Центр медицинских наук Техасского технологического университета, Медицинская школа Пола Л. Фостера; Консультант, Дерматология Маунтин-Вью, PA
Ричард П. Винсон, доктор медицины, является членом следующих медицинских обществ: Американской академии дерматологии, Ассоциации военных дерматологов, Техасского дерматологического общества и Техасской медицинской ассоциации
.Раскрытие информации: нечего раскрывать.
Мэри Л. Виндл, PharmD Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: нечего раскрывать.
Возможен анализ крови на чесотку
Аннотация
Фон
Чесотка поражает миллионы людей во всем мире, но ее очень трудно диагностировать с помощью обычного кожного соскоба, а предполагаемый диагноз часто ставится на основании таких клинических признаков, как сыпь и сильный зуд.Чувствительный и специфический анализ крови на чесотку позволит врачу быстро поставить правильный диагноз.
Цель
Наша цель состояла в том, чтобы профилировать специфические антитела к клещам, присутствующие в сыворотке крови пациентов с обыкновенной чесоткой.
Методы
Сыворотки 91 пациента были проверены на антитела Ig, IgD, IgE, IgG и IgM к S . scabiei , а также клещам домашней пыли Dermatophagoides farinae , D . pteronyssinus и Euroglyphus maynei .
Результаты
45%, 27% и 2,2% пациентов имели измеримые количества смешанных Ig, IgG и IgE, которые распознавали антигены чесоточного клеща. Однако 73,6% больных чесоткой имели сывороточный IgM, распознающий белки чесотки, и все, кроме двух из них, также имели IgM, распознающий все три вида пылевых клещей. Ни у одного пациента не было сывороточных антител, реагирующих исключительно на антигены чесоточного клеща.
Выводы
Совместная сенсибилизация или перекрестная реактивность между антигенами чесотки и клещей домашней пыли затрудняет проведение анализа крови на чесотку.
Сведения об авторе
Чесотка, вызванная клещом S . чесотка , которая проникает в кожу человека, — это заразное кожное заболевание, от которого страдают миллионы людей во всем мире. Это серьезное бремя для общественного здравоохранения среди экономически неблагополучных слоев населения, и вспышки болезни распространены в домах престарелых, детских садах, школах и на рабочих местах в развитых странах. Это вызывает значительную заболеваемость, а в хронических случаях сопутствующие бактериальные инфекции могут привести к заболеваниям почек и сердца.Чесотку очень сложно диагностировать с помощью обычного кожного соскоба, и предполагаемый диагноз часто ставится на основании таких клинических признаков, как сыпь и зуд, которые могут имитировать другое кожное заболевание. Чувствительный и специфический анализ крови для выявления специфических антител к чесотке позволит врачу быстро поставить правильный диагноз. В нашей рукописи сообщается об изотипических профилях антител сывороток двух групп пациентов с обычной чесоткой (17 из США и 74 из Бразилии) и делается вывод, что такой анализ крови должен основываться на циркулирующих антителах типа IgM, которые также не распознают антигены родственные и вездесущие клещи домашней пыли.Оба эти фактора важны для исследований по разработке анализа крови для диагностики чесотки.
Образец цитирования: Арлиан Л.Г., Фельдмайер Х., Морган М.С. (2015) Возможность проведения анализа крови на чесотку. PLoS Negl Trop Dis 9 (10): e0004188. https://doi.org/10.1371/journal.pntd.0004188
Редактор: Джозеф М. Винетц, Калифорнийский университет, Медицинская школа Сан-Диего, СОЕДИНЕННЫЕ ШТАТЫ
Поступила: 14 июля 2015 г .; Принято к печати: 2 октября 2015 г .; Опубликовано: 22 октября 2015 г.
Авторские права: © 2015 Arlian et al.Это статья в открытом доступе, распространяемая в соответствии с условиями лицензии Creative Commons Attribution License, которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии указания автора и источника
Доступность данных: Предоставляются все соответствующие данные внутри бумаги.
Финансирование: Исследование, описанное в этой публикации, было поддержано Национальным институтом аллергии и инфекционных заболеваний Национального института здравоохранения под номером R01AI017252, присвоенным LGA, и грантом на поездку от Deutscher Akademischer Austauschdienst DAAD, Бонн, Германия, для HF.Авторы несут полную ответственность за содержание, которое не обязательно отражает официальную точку зрения Национальных институтов здравоохранения. Финансирующие организации не играли никакой роли в дизайне исследования, сборе и анализе данных, принятии решения о публикации или подготовке рукописи.
Конкурирующие интересы: Авторы заявили, что никаких конкурирующих интересов не существует.
Введение
Чесотка, вызываемая клещом Sarcoptes scabiei , является паразитарным заболеванием кожи, которое встречается во всем мире [1, 2].Недавно он был добавлен Всемирной организацией здравоохранения в список забытых тропических болезней [3]. Оценки распространенности чесотки варьируются от небольшого процента населения в развитых странах до высокой распространенности в некоторых общинах с ограниченными ресурсами в странах глобального юга, где болезнь может поражать до 50% женщин и детей [4–13] . Кроме того, вспышки заболеваний регистрируются в домах престарелых и детских садах (как среди рабочих, так и среди клиентов), а также в детских садах, общежитиях, школах, среди студентов колледжей и в рабочей среде, где существует много физических контактов между людьми [14–18]. ].
Обычную, в отличие от покрытой коркой, чесотку очень сложно диагностировать. Паразитологические методы довольно нечувствительны, и клинически чесотка может имитировать другие кожные заболевания, такие как экзема, псориаз, атопический дерматит, опрелости, дерматит от ядовитого плюща и кожные реакции на раздражающие вещества, такие как мыло / детергенты, металлы и лосьоны. Предположительный диагноз чесотки требует подтверждения путем выделения клещей, фекальных гранул клещей и яиц из роговичного слоя эпидермиса.Однако на практике у пациентов часто диагностируется чесотка на основании клинических характеристик, таких как сыпь и сильный зуд. Поскольку ни один из симптомов и признаков не является патогномоничным, такой подход часто приводит к ложноположительному диагнозу, что, в свою очередь, подвергает пациента потенциально опасному лечению. Напротив, покрытая коркой чесотка (также известная как «норвежская чесотка») легко распознается по гиперкератозу, который проявляется чешуйчатым и утолщенным (т. Е. Покрытым коркой) роговым корнем и сопутствующим большим количеством клещей по сравнению с низким уровнем клещей и сыпью обычных чесотка.
Чувствительный и специфический анализ крови для выявления циркулирующих антител, специфичных для чесотки, позволит врачу быстро поставить правильный диагноз. Одна из проблем при разработке такого теста заключается в том, что многие антигены чесоточных клещей перекрестно реагируют с антигенами обычных аллергических клещей домашней пыли, Dermatophagoides farinae , D . pteronyssinus и Euroglyphus maynei , которые встречаются во всем мире [19–22]. Мы сообщаем здесь профили изотипов антител сывороток двух групп пациентов с обычной чесоткой (из Бразилии и США), которые распознают антигены чесотки и клещей домашней пыли, и иллюстрируем смешивающую проблему перекрестной реактивности и перекрестной сенсибилизации.
Методы
Заявление об этике
Сыворотка пациентов из США (17 субъектов + положительный отзыв) была собрана в соответствии с Протоколом для субъектов исследования (HSP) № 0205, одобренным Наблюдательным советом государственного университета Райта (IRB). Отрицательные контрольные сыворотки были ранее предоставлены нам без личных идентификаторов в соответствии с протоколом SC # 2714, утвержденным как EXEMPT согласно CFR 46.101 (b) (4) IRB государственного университета Райта.
Сыворотка бразильских пациентов была предоставлена исследователям из штата Райт без личных идентификаторов.Исследование было одобрено как EXEMPT согласно CFR 46.101 (b) (4) и одобрено согласно протоколу SC # 4334 IRB государственного университета Райта. Оригинальное исследование было одобрено Universidade Federal do Céara — Comité de Ética em Pesquisa, протокол 358/08. Текст формы согласия был зачитан вслух в присутствии других членов домохозяйства (как для детей, так и для взрослых), а процедуры сбора и последующие лабораторные методы были объяснены простым языком. Затем все взрослые субъекты и опекуны несовершеннолетних детей подписали прочитанные им формы согласия.
Сыворотка человека
сыворотки было получено после согласия двух групп пациентов с обыкновенной чесоткой на момент постановки первичного диагноза. Сыворотки собирали у пациентов в офисе дерматолога в Цинциннати, штат Огайо, США. Эта группа состояла из 17 субъектов (6 женщин + 11 мужчин, возраст 18–72 лет), у которых была обычная чесотка, подтвержденная выздоровлением живых клещей путем соскабливания кожи во время постановки диагноза, и которые сообщили, что у них были симптомы в течение 0–13 лет. месяцев до постановки диагноза.Сыворотки также были собраны у 74 больных чесоткой (44 женщины + 30 мужчин в возрасте от 5 до 73 лет) в бедном ресурсами сообществе в Форталезе, Северо-Восточная Бразилия. Эти пациенты были идентифицированы путем активного выявления случаев. Клинический диагноз был подтвержден дерматоскопией и соскобом кожи, у 86,3% пациентов были затронуты 3 или более топографических участков. У 42,1% продолжительность заражения была <3 недель.
В качестве положительного эталона использовалась сыворотка, ранее полученная от обычного пациента с чесоткой.Этот 72-летний мужчина, который обратился в кабинет дерматолога в Дейтоне, штат Огайо, сообщил, что у него симптомы чесотки более 4 лет. Ранее было продемонстрировано, что его сыворотка содержит высокие уровни циркулирующих антител к чесотке [23], и тесты на радиоаллергосорбенты (RAST; проведенные Clinical Immunology and Allergy, Liberty, MO) показали общий IgE> 1000 Ед / мл и модифицированные оценки класса 2 RAST ( баллы варьируются от 0 до 6) для специфических IgE к обоим D . farinae и D . pteronyssinus . Пул отрицательных контрольных сывороток готовили путем смешивания равных объемов сыворотки от двух индивидуумов, у которых не было известных случаев чесотки и которые, как ранее было продемонстрировано, имеют низкие уровни циркулирующих антител к экстрактам любого из 9 видов астигматидных клещей [24, 25 ].
Экстракты клещей
Водные экстракты получали из Sarcoptes scabiei var. canis и от клещей домашней пыли Dermatophagoides farinae , D . pteronyssinus и Euroglyphus maynei в соответствии с нашим стандартным протоколом. Вкратце, чесоточных клещей собирали путем аспирации на сетку из нержавеющей стали 38 мкм (Small parts, Inc., Майами Лейкс, Флорида) после того, как они мигрировали из корок. Для удаления материала-хозяина живых клещей промывали последовательным нанесением аликвот по 4 мл PBST (забуференный фосфатом физиологический раствор Дульбекко с 0,05% твина 20), воду, не содержащую эндотоксинов, и 70% этанол через сетку. Клещей убивали путем замораживания при -80 ° C, где они хранились до использования.
Пылевых клещей собирали путем аспирации, когда они мигрировали из культур, убивали замораживанием, лиофилизировали и хранили при -20 ° C до использования. Клещей каждого вида суспендировали в воде, свободной от эндотоксинов (1:10 W: V для пылевых клещей и 1:20 W: V для чесоточных клещей) для экстракции в течение ночи при 4 ° C. На следующий день образцы размалывали 10 движений на льду с использованием гомогенизатора TenBroeck, нерастворимый материал удаляли центрифугированием в течение 10 минут при 14 k x g и супернатанты стерильно фильтровали в стерильные флаконы.Чтобы извлечь как можно больше белка, осадок чесоточного клеща подвергали второй экстракции / гомогенизации / центрифугированию и два супернатанта объединяли. Содержание белка в каждом экстракте определяли по методу Брэдфорда [26], используя бычий сывороточный альбумин (БСА) в качестве стандарта.
Иммуноферментный анализ (ELISA)
Планшеты для микротитрованиядля каждого экстракта клещей покрывали 0,5 мкг белка на лунку в 50 мМ карбонат / бикарбонатном буфере, pH 9,6, и давали им высохнуть.Планшеты готовили двумя партиями (по одной для каждой сыворотки) и хранили в эксикаторе при комнатной температуре до использования. Перед использованием и между всеми этапами планшеты промывали PBST. Планшеты блокировали 1% BSA в PBST и загружали 100 мкл сыворотки, разведенной 1/10 (IgD и IgE) или 1/1000 (Ig, IgG и IgM). Все образцы загружали в дублирующие лунки, и каждый планшет имел параллельный набор положительных и отрицательных контрольных сывороток.
Связывание антител в сыворотке детектировали с использованием биотинилированных антител, специфичных к смешанным IgM человека [IgM + IgG + IgA, H + L], IgD [специфично для δ-цепи], IgE [специфично для Fc-части тяжелой цепи], IgG [специфично для γ-цепи ] или IgM [специфичные для μ-цепи] (все разведены 1/5000), а затем стрептавидин-пероксидаза (1/5000).Все они были приобретены у Southern Biotech (Бирмингем, Алабама). Планшеты проявляли 100 мкл 1 мМ ABTS в 70 мМ цитрат-фосфатном буфере, pH 4,0, с 0,03% перекисью водорода. Развитие останавливали добавлением 50 мкл 0,2% азида натрия, и планшеты немедленно считывали.
Для учета вариабельности от планшета к планшету все данные были нормализованы по завершении исследования. Для каждого класса антител и антигена усредняли оптическую плотность 405 нм всех лунок для положительной контрольной сыворотки.Эти значения затем использовали вместе с контролями для каждого отдельного планшета для расчета нормализованных значений поглощения ELISA для каждой сыворотки / класса антител / антигена.
Результаты
Для этого исследования использованная сыворотка отрицательного контроля представляла собой группу лиц, у которых ранее было определено отсутствие циркулирующих антител, распознающих антигены, присутствующие в экстрактах чесотки, домашней пыли и клещах, хранящихся в продуктах [24, 25]. Положительный титр к любому экстракту клещей определяли как поглощение ELISA, по крайней мере, в 2 раза превышающее поглощение отрицательных контролей для смешанных Ig и IgG или превышающее 0.100 для IgM или 0,050 для IgE. Положительная контрольная сыворотка была получена от одного пациента, который болел чесоткой более 4 лет и у которого ранее было определено высокое содержание антител к чесотке и клещам Dermatophagoides .
АнализELISA сыворотки 91 пациента с чесоткой показал, что 45,1% имели циркулирующие антитела (Ig), которые связывались с антигенами чесотки (Таблица 1). Это включало 6 из 17 пациентов из США (35%) и 35 из 74 пациентов из Бразилии (47%).Из всех 91 пациента 27,5% и 73,6% имели измеряемые уровни сывороточных антител IgG и IgM, соответственно, которые связывались с белками чесотки (таблица 1). Уровни сывороточного IgM к чесотке у бразильских пациентов были выше, чем у американцев, в то время как их уровни Ig и IgG были схожими (рис. 1). Примечательно, что среднее связывание IgM с антигенами чесотки у бразильских пациентов привело к абсорбции ELISA, которая более чем в два раза превышала таковую у пациентов из США. Только у 2 из пациентов с чесоткой (2,2%), оба бразильцев, были циркулирующие антитела IgE, которые связывались с белками чесотки, и оба из них давали очень низкие значения поглощения (0.070 и 0,073). Ни у одного пациента не было измеримых уровней сывороточного IgD, направленного на антигены какого-либо клеща.
Рис. 1. Связывание смешанных сывороточных антител Ig, IgG и IgM с планшетами для ELISA, покрытыми антигенами чесотки или клещей домашней пыли.
Данные представлены как средняя абсорбция ELISA ± стандартная ошибка среднего для сывороток, собранных у пациентов с обычной чесоткой в США (n = 17) и Бразилии (n = 74).
https://doi.org/10.1371/journal.pntd.0004188.g001
Все, кроме двух из 67 пациентов, имевших сывороточные антитела IgM к антигенам чесотки, также имели IgM, распознающие все три вида пылевых клещей, D . farinae , D . pteronyssinus и E . майней . Из 25 больных чесоткой с IgG к чесотке 24 также имели IgG ко всем трем видам пылевых клещей. Ни у одного пациента не было сывороточных антител, реагирующих исключительно на антигены чесоточного клеща.
У бразильских пациентов были значительно более высокие уровни сывороточного IgM, распознающего антигены всех четырех видов клещей, чем у американской когорты (рис. 1). Хотя связывание IgG с белками чесотки было одинаковым для двух групп, связывание IgG с каждым из экстрактов пылевых клещей было выше для бразильской когорты, чем для группы из США.Никаких различий между группами не наблюдалось в отношении связывания Ig с любым из экстрактов клещей.
пациентов из США
Среди 17 пациентов в США 10 имели IgM, 6 — IgG и 6 — Ig, распознающие антигены чесоточного клеща. У пяти пациентов с повышенным уровнем антител IgM к антигенам чесотки не было повышенного уровня IgG или смешанного Ig к чесотке. Напротив, у 3 пациентов были повышенные антитела IgG к чесотке, но не повышенные IgM, а у 3 пациентов не было обнаружено связывания антител с белками чесоточного клеща.Ни у одного пациента из США не было обнаруживаемых уровней IgE к чесоточным клещам.
Хотя не все пациенты в США имели циркулирующие антитела, которые связывались с антигенами чесотки, у всех был повышенный уровень по крайней мере одного класса антител, распознающих антигены клещей домашней пыли D . farinae , D . pteronyssinus и E . майней . Все 6 пациентов с Ig к S . scabiei также имел Ig к D . farinae , D . pteronyssinus и E . майней . Также не было обнаружено связывания IgE ни с одним из экстрактов клещей домашней пыли.
Бразилия пациентов
Среди 74 бразильских пациентов 57 имели IgM и 19 имели IgG, распознающие антигены чесотки, в то время как 35 пациентов имели повышенный уровень смешанного Ig к чесотке. Из 57 пациентов с повышенным уровнем IgM к чесотке у 23 не было повышенного уровня IgG или смешанного Ig к антигенам чесотки. У двух бразильских пациентов обнаруживались уровни IgE к антигенам чесотки.У восьми больных чесоткой не было обнаружено связывания циркулирующих антител с антигенами чесотки.
За исключением одного пациента, у которого не обнаружено связывания антител с D . pteronyssinus , все пациенты из Бразилии имели Ig, IgG и / или IgM, которые связывались с антигенами всех трех видов клещей домашней пыли. Из 57 пациентов, у которых был повышен уровень IgM до чесотки, все, кроме одного, также имели повышенный уровень IgM до D . farinae , D . pteronyssinus и E . майней . Аналогичным образом, из 19 пациентов, у которых был повышен уровень IgG к чесотке, у всех также был повышен уровень IgG ко всем трем пылевым клещам. Из 35 пациентов со смешанным Ig, которые распознали антиген чесоточного клеща, все, кроме двух, также имели Ig, который распознавал антиген всех трех видов пылевых клещей.
Обсуждение
Хотя чесоточные клещи зарываются и обитают в роговом слое эпидермиса, исторические исследования наряду с более поздними исследованиями ясно показывают, что антигены чесоточных клещей вызывают гуморальный ответ у хозяина.Таким образом, теоретически можно разработать анализ крови на чесотку на основе циркулирующих антител, распознающих специфические для чесотки антигены, которые не вступают в перекрестную реакцию с клещами домашней пыли. Мы приводим краткую историю исследований, обобщающую информацию, которая приводит к выводу, что чесотку можно диагностировать с помощью простого анализа крови, но антигены необходимо тщательно выбирать.
В некоторых ранних исследованиях сообщалось о сильно различающихся результатах относительно общих сывороточных уровней IgG, IgA и IgE, а также уровней C3 и C4 комплемента у пациентов с чесоткой по сравнению с контрольными субъектами без чесотки [27–31].Ни в одном из этих исследований напрямую не изучали, были ли измененные уровни изотипа иммуноглобулина в сыворотке результатом заражения чесоткой и были ли они специфичными для антигенов чесоточного клеща. Следовательно, эти исследования не позволяют сделать никаких выводов.
Несколько исследований косвенно связали концентрации антител в сыворотке с заражением чесоткой. Эти исследования, показывающие взаимосвязь между изменениями уровней изотипов антител во время заражения чесоткой по сравнению с исследованиями после успешного лечения, предполагали причинно-следственную связь с заражением чесоткой, хотя наличие специфических антител к антигенам чесотки не определялось [28, 32, 33] .Однако не исключено, что больные чесоткой одновременно инфицированы гельминтами и что наличие гельминтов вызывает иммунологические изменения.
Более поздние исследования с использованием S . scabiei экстракт клещей или рекомбинантные молекулы чесотки, полученные из клещей, собранных у разных видов хозяев, ясно показали, что животные и люди-хозяева вырабатывают антитела к специфическому S . scabiei молекул [21, 23, 34–42]. Два исследования показали, что у людей с корковой чесоткой был повышен общий специфический IgE к чесотке по сравнению с пациентами с обычной чесоткой [35, 43].Walton et al. [43] обнаружили, что у субъектов как с обычной, так и с покрытой коркой чесоткой были повышенные уровни антител, специфичных к нескольким рекомбинантным антигенам чесотки, по сравнению с наивными контрольными субъектами, никогда не подвергавшимися чесотке. Кроме того, иммуноферментный анализ с использованием рекомбинантного белка чесотки rSar s 14.3, который соответствует остаткам 1263–1655 аллергена пылевого клеща Der p 14, показал значительно более высокое связывание IgE с плазмой пациентов с корковой чесоткой, чем у пациентов с обычной чесоткой [44]. Связывание IgE у обычных пациентов с чесоткой также было значительно выше, чем у контрольных, и не наблюдалось перекрестной реактивности с гомологом пылевого клеща.
Получить достаточное количество чесоточного клеща человека для исследовательских целей очень сложно. Однако использование клещей, собранных у собак, свиней и лисиц, в качестве источника материала для исследований по разработке диагностического теста и вакцины от чесотки у человека предлагает многообещающую альтернативу. Непонятно, S . scabiei клещей от таких хозяев являются одними и теми же видами или только тонкими генетическими вариантами, потому что S . scabiei клещей от самых разных видов хозяев морфологически неотличимы.Самое последнее молекулярное исследование показало, что клещей, взятых у людей, можно отличить от клещей, собранных у животных, на основе секвенирования гена мтДНК cox 1 длиной 317 пар оснований, но не при использовании нескольких других молекулярных маркеров [45]. Этот анализ также показал, что все клещи, собранные от различных животных-хозяев, были моноспецифичными, в то время как клещи, выделенные от людей из разных географических мест, сгруппированы в четыре отдельные ветви, представляющие четыре разных вида [45].
Что еще более важно, несколько исследований показали, что существует значительная антигенная перекрестная реактивность между различными штаммами чесоточных клещей от разных хозяев, но существуют также антигены, специфичные для штаммов [23, 46]. Например, S . scabiei var. suis от свиней, вар. canis от собак и вар. человек человека имеют общие перекрестно реагирующие антигены. Точно так же у людей с чесоткой циркулируют антитела, распознающие антигены из S . scabiei var. vulpis от лисиц, вар. канис и вар. suis [23, 46]. Haas et al. [46] обнаружили, что 48% пациентов с чесоткой имели IgG, распознающие антигены лисьих клещей, а пациенты с большей тяжестью и продолжительностью чесотки имели значительно более высокие титры IgG. Кроме того, вестерн-блоттинг показал, что у 72-летнего мужчины с хронической чесоткой был IgG, распознающий более 10 антигенов из S . scabiei var. канис [23].Кроме того, сыворотка от 6 пациентов с покрытой коркой чесоткой содержала IgE к 11–21 и IgG к 1–7 антигенам из S . scabiei var. canis , но пациенты с обычной чесоткой имели сывороточные IgG и IgE, которые распознавали гораздо меньше антигенов [35]. И неочищенный экстракт всего тела S . scabiei var. vulpes , полученное от красных лисиц, содержало антигены, распознаваемые антителами в сыворотке крови свиней, зараженных чесоткой [47], и серны [48]. ELISA с использованием рекомбинантного антигена Ssλ20ΔB3 из S . scabiei var. hominis обнаруживает сывороточные антитела у иберийского благородного оленя, южной серны, свиней и кроликов, инфицированных саркоптозом [49–53]. Аналогичным образом, несколько рекомбинантных белков, полученных из S . scabiei var. suis распознавались антителами в сыворотках людей, инфицированных S . scabiei var. человек [54]. Следовательно, использование клещей, собранных у различных видов хозяев, обеспечивает средства идентификации конкретных молекул и изотипов антител, которые могут быть полезны при разработке диагностического теста на чесотку, и преодолевают проблему ограниченного количества var. человекообразных клещей.
Настоящее исследование с использованием собачьего штамма чесотки для подготовки антигена для использования в ELISA показало, что только 45%, 27% и 2,2% из 91 пациента с обычной чесоткой имели измеримые количества смешанных Ig, IgG и IgE, которые распознавали антигены чесоточного клеща. , соответственно. Ни у одного пациента не было IgD, распознающего антиген чесоточного клеща. Однако 73,6% больных чесоткой имели сывороточный IgM, распознающий S . scabiei антигенов со значительно более высокими уровнями, наблюдаемыми у бразильских пациентов по сравнению с таковыми из США.Это говорит о том, что бразильским пациентам был поставлен диагноз на довольно ранней стадии заражения, поскольку они не переключились на продукцию IgG, которая следует за первоначальным ответом IgM. Напротив, наблюдение, что у большего числа пациентов были IgG к клещам домашней пыли, предполагает более хроническое воздействие этих клещей. На основании этих результатов представляется, что диагностический тест должен основываться на определении сывороточного IgM к антигенам чесотки. Такой тест был бы полезен, потому что IgM — это первый класс продуцируемых антител до того, как произойдет переключение класса на IgG, поэтому он может позволить более раннюю диагностику чесотки.Различия между ответами двух групп пациентов могут отражать различия в штаммах / видах чесоточных клещей, поражающих этих географически удаленных пациентов, как было предложено Zhao et al. исследование [45].
Это исследование снова проливает свет на проблему сенсибилизации или перекрестной реактивности между антигенами клещей домашней пыли, которая затрудняет разработку анализа крови на чесотку. Клещи домашней пыли являются источниками> 25 антигенных белков [55]. Многие антигены клещей домашней пыли перекрестно реагируют с антигенами чесоточных клещей [19–22].Также значительный процент людей чувствителен к вездесущим клещам домашней пыли, D . farinae , D . pteronyssinus и E . майней . Все пациенты с чесоткой в этом исследовании, кроме одного, имели циркулирующие Ig, IgG и / или IgM ко всем трем экстрактам клещей домашней пыли, и ни у одного пациента с чесоткой не было антител исключительно к чесоточным клещам. Таким образом, ключ к диагностическому тесту, обладающему как специфичностью, так и чувствительностью, вероятно, заключается в идентификации ограниченного и определенного набора (используемых в качестве коктейля) белков чесотки (или фрагментов белков), которые не несут эпитопы, перекрестно реагирующие с теми, которые находятся в доме. белки пылевого клеща и связывающие IgM сыворотки больных чесоткой.Для достижения этой цели был проведен подробный и всесторонний протеомный и геномный анализ S . scabiei обязательно.
Благодарности
Авторы благодарят ДиАнн Вышенски-Мохер за техническую помощь в культивировании клещей, использованных в этом исследовании. Мы также с благодарностью отмечаем вклад покойного Стивена А. Эстеса, доктора медицины, который предоставил сыворотку от пациентов с чесоткой в США.
Вклад авторов
Задумал и спроектировал эксперименты: LGA HF MSM.Проведенные эксперименты: МСМ. Проанализированы данные: LGA HF MSM. Предоставленные реагенты / материалы / инструменты анализа: LGA HF MSM. Написал статью: LGA HF MSM.
Ссылки
- 1. Фельдмайер Х., Хойкельбах Дж. Эпидермальные паразитарные кожные заболевания: игнорируемая категория болезней, связанных с бедностью. Bull World Health Organ. 2009 Февраль; 87 (2): 152–9. pmid: 19274368
- 2. Энгельман Д., Кианг К., Чосидоу О., Маккарти Дж., Фуллер С., Ламми П. и др. На пути к глобальной борьбе с чесоткой человека: представление Международного альянса по борьбе с чесоткой.PLoS Negl Trop Dis. 2013 8 августа; 7 (8): e2167. pmid: 23951369
- 3. Всемирная организация здравоохранения, список забытых тропических болезней (NTD) [Интернет]. http://www.who.int/neglected_diseases/diseases/scabies/en/.
- 4. Маунси К.Э., Маккарти Дж.С., Уолтон С.Ф. Почесывая зуд: новые инструменты для более глубокого понимания чесотки. Trends Parasitol. 2013 Янв; 29 (1): 35–42. pmid: 23088958
- 5. Ласса S, Кэмпбелл MJ, Беннетт CE. Эпидемиология распространенности чесотки в США.К. из общей практики. Br J Dermatol. 2011 июн; 164 (6): 1329–34. pmid: 21574970
- 6. Романи Л., Коройвуэта Дж., Стир А.С., Кама М., Калдор Дж. М., Ванд Х и др. Распространенность чесотки и импетиго и факторы риска на Фиджи: национальное исследование. PLoS Negl Trop Dis. 2015 4 марта; 9 (3): e0003452. pmid: 25738499
- 7. Эндрюс Р.М., Кирнс Т., Коннорс С., Паркер С., Карвилл К., Карри Б.Дж. и др. Региональная инициатива по сокращению кожных инфекций среди детей-аборигенов, живущих в отдаленных общинах Северной территории, Австралия.PLoS Negl Trop Dis. 2009 24 ноября; 3 (11): e554. pmid: 19936297
- 8. душ Сантуш М.М., Амарал С., Хармен С.П., Джозеф Н.М., Фернандес Дж.Л., Кунахан М.Л. Распространенность обычных кожных инфекций в четырех округах Тимора-Лешти: перекрестное исследование. BMC Infect Dis. 10 марта 2010 г .; 10: 61,2334-10-61. pmid: 20219136
- 9. Стир А.С., Дженни А.В., Кадо Дж., Батцлофф М.Р., Ла Винсенте С., Вакатакирева Л. и др. Высокое бремя импетиго и чесотки в тропической стране. PLoS Negl Trop Dis.23 июня 2009 г .; 3 (6): e467. pmid: 19547749
- 10. Мухаммад Зайид М., Саидатул Саада Р., Адил А. Р., Рохела М., Джамайя И. Распространенность чесотки и вшей среди детей в доме престарелых в Пулау-Пинанге, Малайзия. Троп Биомед. 2010. 27: 442–6. pmid: 21399584
- 11. МакМениман Э., Холден Л., Кернс Т., Клукас Д. Б., Карапетис Дж. Р., Карри Б. Дж. И др. Кожные заболевания первых двух лет жизни у детей аборигенов Восточного Арнемленда. Australas J Dermatol. 2011 ноябрь; 52 (4): 270–3.pmid: 22070701
- 12. Хойкельбах Дж., Вилке Т., Винтер Б., Фельдмайер Х. Эпидемиология и заболеваемость чесоткой и Pediculosis capitis в бедных ресурсами общинах в Бразилии. Br J Dermatol. Июль 2005 г., 153 (1): 150–6. pmid: 16029341
- 13. Клукас ДБ, Карвилл К.С., Коннорс К., Карри Б.Дж., Карапетис-младший, Эндрюс Р.М. Бремя болезней и посещение поликлиник для детей младшего возраста в отдаленных общинах аборигенов на севере Австралии. Bull World Health Organ.2008 Апрель; 86 (4): 275–81. pmid: 18438516
- 14. Heukelbach J, Feldmeier H. Scabies. Ланцет. 2006 27 мая; 367 (9524): 1767–74. pmid: 16731272
- 15. Росс Б.Г., Райт-Маккарти Дж. К., Деламора, Пенсильвания, Грэм, PL. Передача чесотки в ясли для новорожденных. Инфекционный контроль Hosp Epidemiol. 2011 Май; 32 (5): 516–7. pmid: 21515986
- 16. de Beer G, Miller MA, Tremblay L, Monette J. Вспышка чесотки в учреждении длительного ухода: роль ошибочного диагноза и затраты, связанные с контролем.Инфекционный контроль Hosp Epidemiol. 2006 Май; 27 (5): 517–8. pmid: 16671037
- 17. Bouvresse S, Chosidow O. Чесотка в медицинских учреждениях. Curr Opin Infect Dis. 2010 Апрель; 23 (2): 111–8. pmid: 20075729
- 18. Ларкин М. Чесотка: быстрого облегчения не видно. Ланцетные инфекционные болезни. 2006; 6 (12): 767.
- 19. Фальк Е.С., Дейл С., Болле Р., Ханеберг Б. Антигены, общие для чесотки и клещей домашней пыли. Аллергия. 1981 Май, 36 (4): 233–8. pmid: 7316098
- 20.Арлиан Л.Г., Вышенский-Мохер Д.Л., Гилмор А.М. Перекрестная антигенность между Sarcoptes scabiei и клещом домашней пыли Dermatophagoides farinae (Acari: Sarcoptidae and Pyroglyphidae). J Med Entomol. Июль 1988 г., 25 (4): 240–7. pmid: 3136249
- 21. Арлиан Л.Г., Вышенски-Мохер Д.Л., Ахмед С.Г., Эстес С.А. Перекрестная антигенность чесоточного клеща Sarcoptes scabiei и клеща домашней пыли Dermatophagoides pteronyssinus . J Invest Dermatol.1991 Март; 96 (3): 349–54. pmid: 1705952
- 22. Арлиан Л.Г., Рапп С.М., Морган МС. Устойчивость и иммунный ответ у зараженных чесоткой хозяев, иммунизированных клещами Dermatophagoides . Am J Trop Med Hyg. 1995 июнь; 52 (6): 539–45. pmid: 7611562
- 23. Арлиан Л.Г., Морган М.С., Арендс Дж. Дж. Иммунологическая перекрестная реактивность среди различных штаммов Sarcoptes scabiei . J Parasitol. 1996 Февраль; 82 (1): 66–72. pmid: 8627503
- 24. Кондредди П.К., Старейшина Б.Л., Морган М.С., Вышенский-Мохер Д.Л., Арлиан Л.Г.Важность сенсибилизации к Tyrophagus putrescentiae в США. Ann Allergy Asthma Immunol. 2006 Янв; 96 (1): 124. pmid: 16440545
- 25. Ядав А., старейшина Б.Л., Морган М.С., Вышенский-Мохер Д.Л., Арлиан Л.Г. Распространенность сывороточного IgE к клещам-накопителям в популяции на юго-западе Огайо. Ann Allergy Asthma Immunol. 2006 февраль; 96 (2): 356–62. pmid: 16498860
- 26. Брэдфорд ММ. Быстрый и чувствительный метод количественного определения количества белка в микрограммах, использующий принцип связывания белок-краситель.Анальная биохимия. 7 мая 1976 г., 72: 248–54. pmid: 942051
- 27. Хэнкок Б.В., Уорд А.М. Сывороточный иммуноглобулин при чесотке. J Invest Dermatol. 1974 декабрь, 63 (6): 482–4. pmid: 4214879
- 28. Falk ES. Показатели сывороточного иммуноглобулина у больных чесоткой. Br J Dermatol. 1980 Янв, 102 (1): 57–61. pmid: 6966501
- 29. Senol M, Ozerol IH, Ozerol E, Sasmaz S, Turan F, Soyturk D. Уровни сывороточного иммуноглобулина и комплемента при чесотке. Журнал Медицинского центра Тургут Озал.1997; 4: 37–9.
- 30. Робертс Л.Дж., Хаффам С.Е., Уолтон С.Ф., Карри Б.Дж. Корковая чесотка: клинические и иммунологические данные у семидесяти восьми пациентов и обзор литературы. J Infect. 2005 июн; 50 (5): 375–81. pmid: 153
- 31. Уолтон С.Ф., Берукас Д., Робертс-Томсон П., Карри Б.Дж. Новые взгляды на патогенез заболевания при покрытой коркой (норвежской) чесотке: иммунный ответ кожи при покрытой коркой чесотке. Br J Dermatol. Июнь 2008 г .; 158 (6): 1247–55. pmid: 18422789
- 32.Falk ES. Сывороточный IgE до и после лечения чесотки. Аллергия. 1981 апр; 36 (3): 167–74. pmid: 7235206
- 33. Морси Т.А., Кенави М.З., Зохди Х.А., Абдалла К.Ф., Эль-Факахани А.Ф. Показатели сывороточного иммуноглобулина и комплемента у больных чесоткой. J Egypt Soc Parasitol. 1993, апрель; 23 (1): 221–9. pmid: 8482869
- 34. Арлиан Л.Г., Морган М.С. Сывороточные антитела к Sarcoptes scabiei и клещу домашней пыли до и во время заражения S . scabiei . Vet Parasitol. 2000 4 июля; 90 (4): 315–26. pmid: 10856817
- 35. Арлиан Л.Г., Морган М.С., Эстес С.А., Уолтон С.Ф., Кемп DJ, Карри Б.Дж. Циркулирующий IgE у пациентов с обыкновенной и покрытой корками чесоткой. J Med Entomol. 2004, январь; 41 (1): 74–7. pmid: 14989349
- 36. Морган М.С., Арлиан Л.Г., Эстес С.А. Характеристики кожной пробы и радиоаллергосорбентной пробы у больных чесоткой. Am J Trop Med Hyg. 1997, август; 57 (2): 190–6. pmid: 9288815
- 37. Морган М.С., Арлиан Л.Г.Профили сывороточных антител зараженных или иммунизированных кроликов Sarcoptes scabiei . Folia Parasitol (Прага). 1994. 41 (3): 223–7.
- 38. Арлиан Л.Г., Рунян Р.А., Сорли Л.Б., Вышенский-Мохер Д.Л., Эстес С.А. Характеристика Sarcoptes scabiei var. canis (Acari: Sarcoptidae) антигенов и индуцированные антитела у кроликов. J Med Entomol. 1985 24 мая; 22 (3): 321–3. pmid: 4009629
- 39. Арлиан Л.Г., Морган М.С., Вышенски-Мохер Д.Л., Стеммер Б.Л. Sarcoptes scabiei : ответ циркулирующих антител и индуцированный иммунитет к чесотке. Exp Parasitol. 1994 Февраль; 78 (1): 37–50. pmid: 8299759
- 40. Родригес-Каденас Ф., Карбахал-Гонсалес М.Т., Фрегенеда-Грандес Дж. М., Аллер-Ганседо Дж. М., Рохо-Васкес Ф.А. Клиническая оценка и ответы антител у овец после первичного и вторичного экспериментального заражения чесоточным клещом Sarcoptes scabiei var. овис . Vet Immunol Immunopathol. 2010 15 февраля; 133 (2–4): 109–16.pmid: 19783311
- 41. Bornstein S, Frossling J, Naslund K, Zakrisson G, Morner T. Оценка серологического теста (непрямой ELISA) для диагностики саркоптоза у красных лисиц ( Vulpes vulpes ). Vet Dermatol. 2006 декабрь; 17 (6): 411–6. pmid: 17083572
- 42. Bornstein S, Wallgren P. Серодиагностика саркоптоза у свиней. Vet Rec. 5 июля 1997 г., 141 (1): 8–12. pmid: 16
- 43. Уолтон С.Ф., Пиццутто С., Слендер А., Виберг Л., Холт Д., Хейлз Б.Дж. и др.Повышенный аллергический иммунный ответ на антигенов Sarcoptes scabiei при корковой чесотке по сравнению с обычной чесоткой. Clin Vaccine Immunol. 2010 Сен; 17 (9): 1428–38. pmid: 20631334
- 44. Джаярадж Р., Хейлс Б., Виберг Л., Пиццуто С., Холт Д., Ролланд Дж. М. и др. Диагностический тест на чесотку: специфичность IgE к рекомбинантному аллергену Sarcoptes scabiei . Диагностика Microbiol Infect Dis. 2011 декабрь; 71 (4): 403–7. pmid: 22018936
- 45. Чжао Й, Цао З, Ченг Дж, Ху Л, Ма Дж, Ян Й и др.Идентификация популяции Sarcoptes hominis и Sarcoptes canis в Китае с использованием последовательностей ДНК. Parasitol Res. 2015 Март; 114 (3): 1001–10. pmid: 25547078
- 46. Хаас Н., Вагеманн Б., Гермес Б., Хенц Б.М., Хейле С., Шейн Е. Перекрестно реагирующие антитела IgG против антигенов лисьего клеща при чесотке человека. Arch Dermatol Res. 2005 Янв; 296 (7): 327–31. pmid: 15650895
- 47. Rambozzi L, Menzano A, Molinar Min AR, Rossi L. Иммуноблот-анализ ответа антител IgG на Sarcoptes scabiei у свиней.Vet Immunol Immunopathol. 15 января 2007 г., 115 (1-2): 179–83. pmid: 17126410
- 48. Rambozzi L, Menzano A, Lavin S, Rossi L. Биотин-авидин амплифицированный ELISA для обнаружения антител к Sarcoptes scabiei у серны ( Rupicapra spp .). Vet Res. Ноябрь-декабрь 2004 г.; 35 (6): 701–8. pmid: 15535959
- 49. Casais R, Prieto M, Balseiro A, Solano P, Parra F, Martin Alonso JM. Идентификация и гетерологичная экспрессия кДНК Sarcoptes scabiei , кодирующей структурный антиген с иммунодиагностическим потенциалом.Vet Res. 2007, май-июнь; 38 (3): 435–50. pmid: 17506973
- 50. Олеага А., Касаис Р., Гонсалес-Кирос П., Прието М., Гортасар С. Саркоптоз у благородных оленей из Испании: улучшение эпиднадзора или появление болезни? Vet Parasitol. 14 июня 2008 г.; 154 (1–2): 103–13. pmid: 18430519
- 51. Фалькони С., Олеага А., Лопес-Оливера Дж. Р., Касаис Р., Прието М., Гортасар С. Распространенность антител против отдельных агентов, характерных для кантабрийской серны ( Rubicapra pyrenaica parva ) и домашних коз.Eur J Wildlife Res. 2010; 56: 319–25.
- 52. Миллан Дж., Касаис Р., Делибес-Матеос М., Кальвет С., Руко С., Кастро Ф. и др. Широко распространенное воздействие Sarcoptes scabiei на диких европейских кроликов ( Oryctolagus cuniculus ) в Испании. Vet Parasitol. 2012 10 февраля; 183 (3–4): 323–9. pmid: 21852039
- 53. Касаис Р., Гойена Е., Мартинес-Карраско С., Руис де Ибанес Р., Алонсо де Вега Ф., Рамис Г. и др. Вариабельность результатов ELISA-анализа рекомбинантного антигена Sarcoptes scabiei человеческого происхождения при диагностике чесотки свиней.Vet Parasitol. 2013 г. 18 октября; 197 (1-2): 397-403. pmid: 23683576
- 54. Кун С., Люциус Р., Маттес Х.Ф., Меусель Г., Райх Б., Калинна Б.Х. Характеристика рекомбинантных иммунореактивных антигенов клеща парши Sarcoptes scabiei . Vet Parasitol. 31 мая 2008 г., 153 (3–4): 329–37. pmid: 18359167
- 55. Чан Т.Ф., Джи К.М., Йим А.К., Лю XY, Чжоу Дж.В., Ли Р.К. и др. Проект генома, транскриптома и микробиома Dermatophagoides farinae выявляет широкий спектр аллергенов пылевых клещей.J Allergy Clin Immunol. 2015 февраль; 135 (2): 539–48. pmid: 25445830


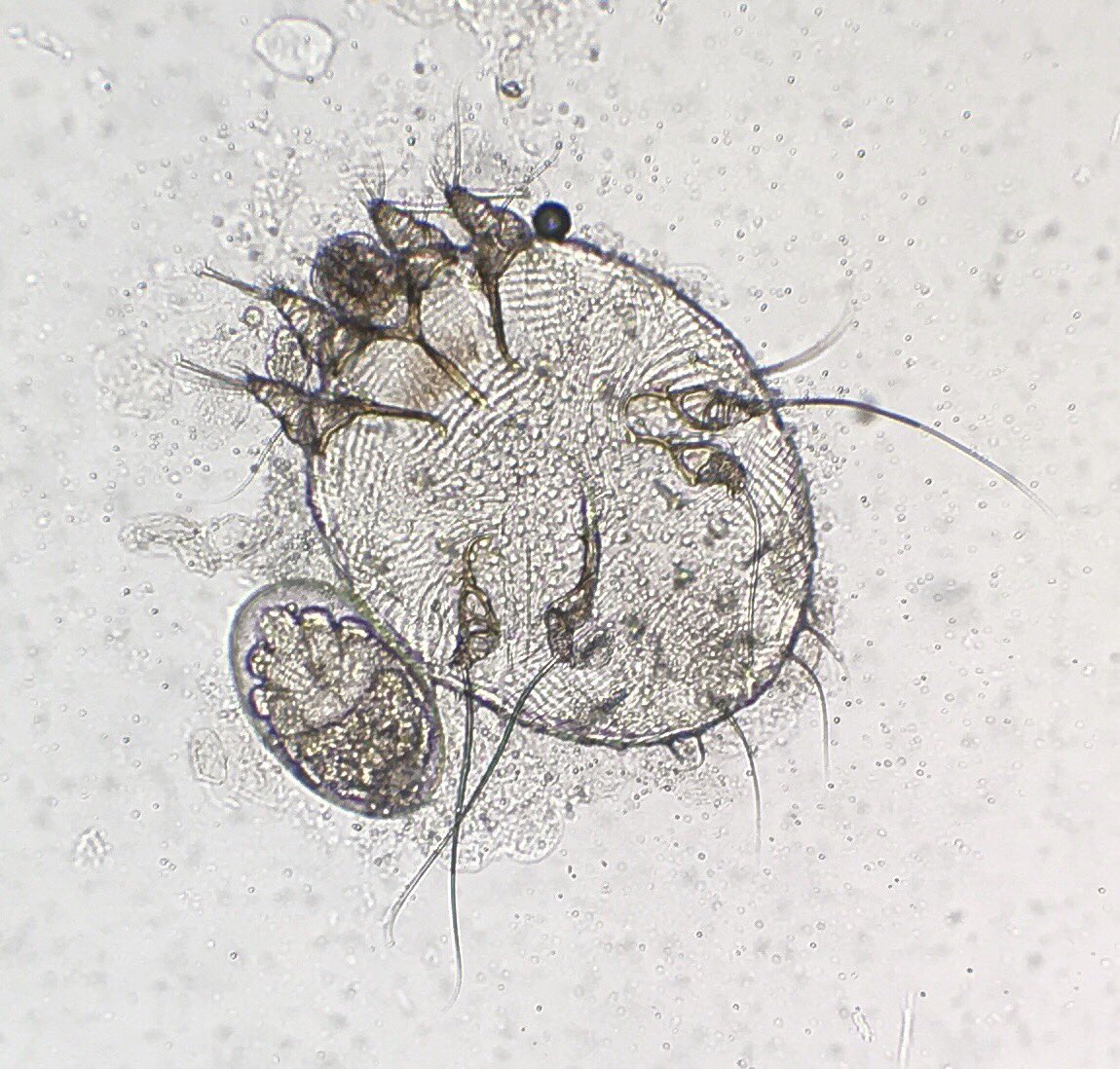 Зуд умеренный, проявляется в ночные часы
Зуд умеренный, проявляется в ночные часы
 Корковая чесотка остается наиболее заразной формой патологии из-за аномально высокой концентрации возбудителей. Развивается на фоне иммунодефицитных состояний организма или продолжительного курса лечения с применением кортикостероидов и цитостатиков
Корковая чесотка остается наиболее заразной формой патологии из-за аномально высокой концентрации возбудителей. Развивается на фоне иммунодефицитных состояний организма или продолжительного курса лечения с применением кортикостероидов и цитостатиков

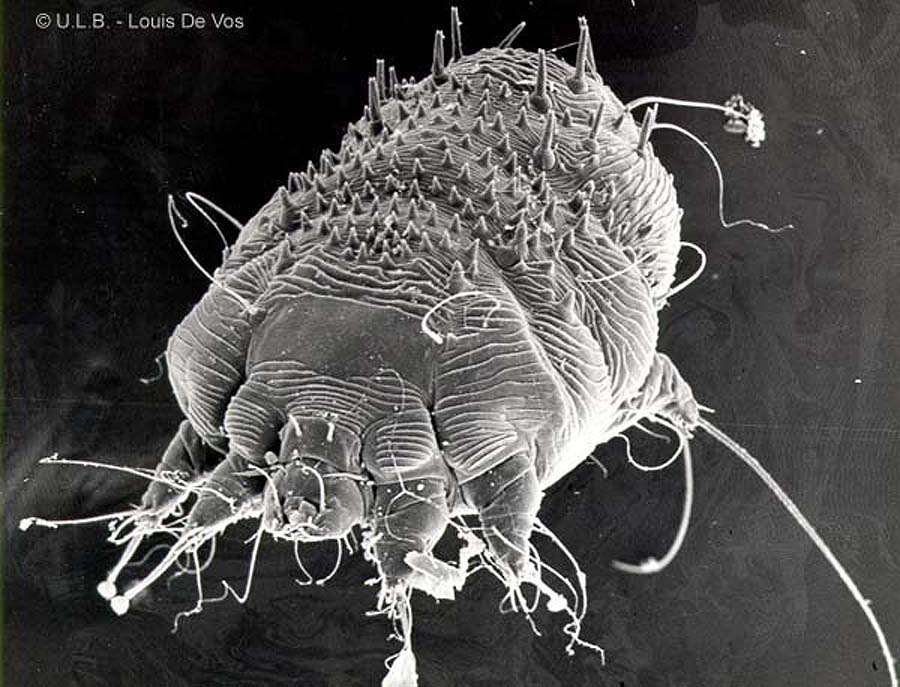
 Мазь имеет неприятный запах и маслянистую консистенцию, которая пачкает одежду и полностью не впитывается в кожу.
Мазь имеет неприятный запах и маслянистую консистенцию, которая пачкает одежду и полностью не впитывается в кожу. Полученную смесь втирают в пораженные места.
Полученную смесь втирают в пораженные места.
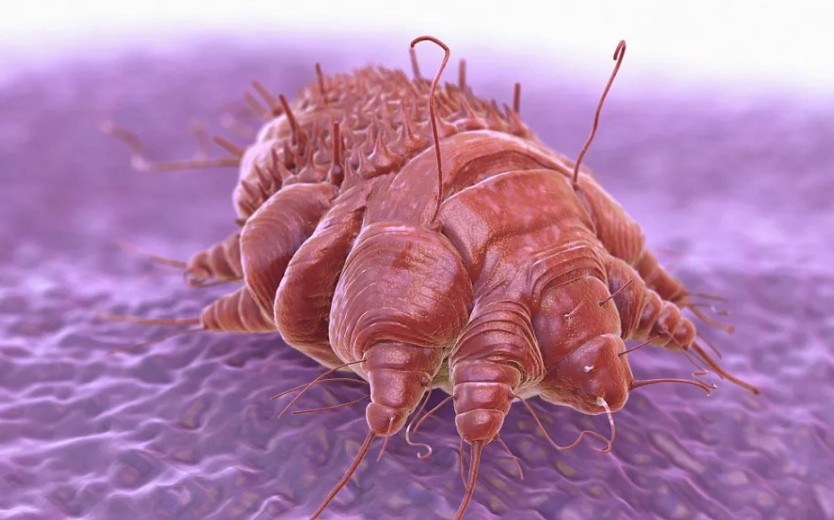

 ..)
..)