Асфиксия у новорожденных детей — Городская поликлиника №20 Управление здравоохранения г. Алматы
Асфиксия новорожденных – звучит, как приговор: страшный, наводящий ужас. Смотришь на только что появившееся на свет дитя и думаешь, какой же этот человечек крохотный и беззащитный. И видишь, как это маленькое тельце борется за свою жизнь, за право существования на этой планете.
Да, асфиксия новорожденных последствия нередко имеет трагические. Однако при правильной и быстрой медицинской помощи, квалифицированном лечении, уходе за новорожденным и пристальном внимании к его здоровью в дальнейшем, возможно полное восстановление организма.
ЧТО ТАКОЕ АСФИКСИЯ И ПРИЧИНЫ ЕЕ ВОЗНИКНОВЕНИЯ
Асфиксия – это нарушение работы дыхательной системы, вследствие которой у ребенка возникает кислородное голодание. Эта патология бывает двух видов: первичная, возникающая при рождении, и вторичная – та, что проявляется в первые минуты-часы жизни младенца.
Причин возникновения патологии – предостаточно. Возникает гипоксия у новорожденных (это другое названия асфиксии) из-за имеющейся в организме матери инфекции. Затруднение дыхания новорожденного происходит по причине закупорки дыхательных путей слизью, и раннего отхождения околоплодных вод, вследствие которых отмечается кислородное голодание. Также асфиксия плода и новорожденного может быть связана с серьезными заболеваниями мамы (диабет, проблемы с сердцем, печенью, респираторные заболевания). Среди причин также отмечается мамин поздний токсикоз (гестоз, преэкламсия), тяжелые и продолжительные роды, отслоение или нарушение целостности плаценты, обвитие пуповиной, переношенная беременность или наоборот раннее излитие околоплодных вод и недоношенная беременность, прием в последние дни беременности некоторых лекарственных препаратов в больших дозировках.
Возникает гипоксия у новорожденных (это другое названия асфиксии) из-за имеющейся в организме матери инфекции. Затруднение дыхания новорожденного происходит по причине закупорки дыхательных путей слизью, и раннего отхождения околоплодных вод, вследствие которых отмечается кислородное голодание. Также асфиксия плода и новорожденного может быть связана с серьезными заболеваниями мамы (диабет, проблемы с сердцем, печенью, респираторные заболевания). Среди причин также отмечается мамин поздний токсикоз (гестоз, преэкламсия), тяжелые и продолжительные роды, отслоение или нарушение целостности плаценты, обвитие пуповиной, переношенная беременность или наоборот раннее излитие околоплодных вод и недоношенная беременность, прием в последние дни беременности некоторых лекарственных препаратов в больших дозировках.
Как видите, причин – предостаточно. Такая патология, как асфиксия плода и новорожденных (что особенно устрашает) – сегодня не редкость. Именно поэтому женщина, находясь в состоянии беременности, должна очень внимательно следить за своим состоянием и в случае малейшего недомогания обращаться к докторам. Самолечение или болезнь, протекающая без вмешательства квалифицированного врача, может привести к серьезному исходу и не всегда приятному разрешению возникшей проблемы.
Самолечение или болезнь, протекающая без вмешательства квалифицированного врача, может привести к серьезному исходу и не всегда приятному разрешению возникшей проблемы.
ЕСЛИ ПОСТАВЛЕН ДИАГНОЗ – АСФИКСИЯ
Неважно, какая причина асфиксии, организм новорожденного тут же реагирует на эту патологию и тотчас перестраивается. Нарушается центральная нервная система, происходит сбой в работе мозга, обменные процессы приостанавливаются. Страдает и сердце, и печень, и почки, и мозг. Сгущение крови приводит к ухудшению работы сердечной мышцы. Подобные сбои в работе внутренних органов могут повлечь за собой отек, кровоизлияния в тканях.
У многих деток, перенесших асфиксию, наблюдается судорожный синдром, повышенная возбудимость, двигательные нарушения, повышенное внутричерепное давление.
УХОД ЗА РЕБЕНКОМ, ПЕРЕНЕСШИМ АСФИКСИЮ
Учитывая тот факт, что у младенца при асфиксии нарушается работа ЦНС, необходимо четко выполнять все назначения врача. Немаловажен для ребенка уход. Полный покой и пристальное внимание. Обычно деток с асфиксией помещают в кувез или палатку, в которую подается кислород.
Полный покой и пристальное внимание. Обычно деток с асфиксией помещают в кувез или палатку, в которую подается кислород.
После выписки из стационара ребенка нужно регулярно показывать невропатологу и педиатру. Дальнейшее лечение, реабилитация зависят только от поставленных диагнозов (если они есть) и симптоматики. При легкой степени асфиксии нарушений в организме ребенка может и не быть. И в таком случае семье нужно просто спокойно жить. У большинства таких деток даже противопоказаний к плановой вакцинации нет.
Помните, что если асфиксия оказала губительное воздействие на ребенка, это будет видно уже в первые дни после рождения.
Асфиксия при родах:Причины патологии,Симптомы асфиксии при родах,Причины патологии
Причины патологии
Асфиксия при родах классифицируется на первичную и вторичную. Первичная асфиксия возникает в процессе родов и в большинстве случаев вызвана острой или хронической внутриутробной гипоксией. Другие причины асфиксии:
- полученная в процессе родов внутричерепная травма;
- пороки развития плода, влияющие на нормальное дыхание;
- иммунологическая несовместимость матери и ребенка;
- пробка в дыхательных путях из-за слизи или околоплодных вод;
- болезни матери;
- патологии пуповины и т.
 д.
д.
Вторичная асфиксия диагностируется спустя несколько часов или дней после родов. Основные причины: поражение центральной нервной системы, порок сердца, нарушение мозгового кровообращения, пневмопатия.
При асфиксии в организме новорожденного изменяются обменные процессы. Могут диагностироваться отеки и кровоизлияния в сердце, головном мозге, почках и других органах, возникающие из-за недостатка кислорода. Сокращается количество сердечных сокращений, нарушается функциональность почек.
Симптомы асфиксии при родах
В первые секунды после завершения родов врач может выявить данное патологическое состояние, оценивая адекватность и частоту дыхания, мышечный тонус, цвет кожи, сердцебиение, рефлексы. Главным симптомом является нарушение дыхательного процесса. В зависимости от степени патологии, отличают легкую, среднюю и тяжелую формы асфиксии, а также клиническую смерть.
При легкой форме вдох ребенок делает в течение первой минуты жизни. Тем не менее, его дыхание ослаблено, а мышечный тонус низкий. При средней форме ребенок также делает вдох в течение первой минуты после появления на свет. Дыхание при этом ослабленное, может быть нерегулярным. Наблюдаются тахикардия, угасающие рефлексы, синюшный оттенок кожи.
При средней форме ребенок также делает вдох в течение первой минуты после появления на свет. Дыхание при этом ослабленное, может быть нерегулярным. Наблюдаются тахикардия, угасающие рефлексы, синюшный оттенок кожи.
При тяжелой форме дыхание нерегулярное либо отсутствующее. Крика нет, только редкое постанывание. Рефлексы отсутствуют, сердцебиение замедленное. Кожа бледная, пуповина не пульсирует. Очень часто следствием тяжелой асфиксии является развитие надпочечниковой недостаточности. При состоянии «клиническая смерть» необходимы срочные реанимационные мероприятия.
Лечение асфиксии
Эффективным способом борьбы с патологией является интенсивная терапия: введение специального зонда в полость рта и носа для очищения дыхательных путей. После извлечения малыша и перерезания пуповины проводится повторная аспирация желудка и носоглотки. После восстановления дыхательной активности действия врачей будут направлены на нормализацию процессов метаболизма, функционирования почек, на ликвидацию отеков и т.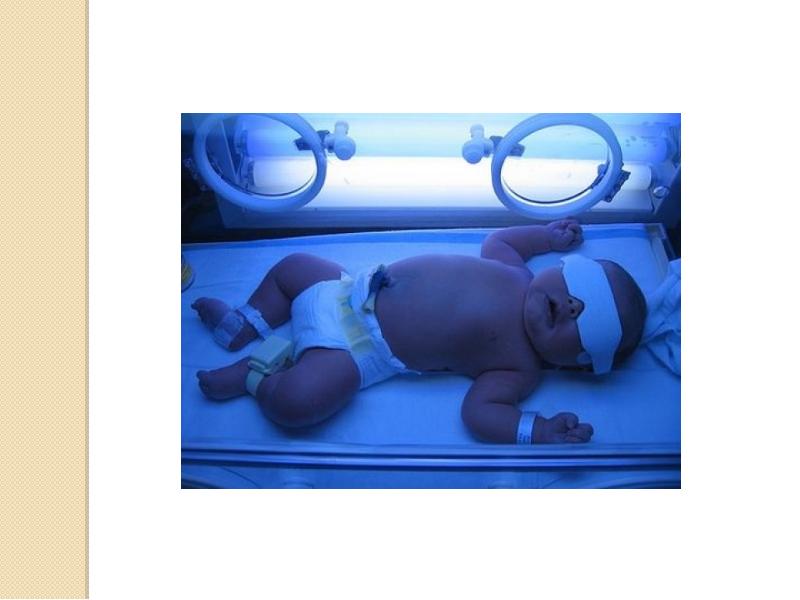 п.
п.
Для принятия комплекса правильных мер при асфиксии, важно, чтобы роды принимал опытный врач-акушер. Большое значение имеет качественная диагностика беременности, позволяющая вовремя обнаружить предрасположенность к асфиксии. Найти лучших медиков по данным направлениям и записаться к ним на прием и консультацию можно на сайте Doc.ua.
Асфиксия новорожденного — причины, симптомы, диагностика и лечение
Асфиксия новорожденного – это патология раннего неонатального периода, обусловленная нарушением дыхания и развитием гипоксии у родившегося ребенка. Асфиксия новорожденного клинически проявляется отсутствием самостоятельного дыхания ребенка в первую минуту после рождения либо наличием отдельных, поверхностных или судорожных нерегулярных дыхательных движений при сохранной сердечной деятельности. Новорожденные с асфиксией нуждаются в проведении реанимационных мероприятий. Прогноз при асфиксии новорожденного зависит от тяжести патологии, своевременности и полноты оказания лечебных мероприятий.
Общие сведения
Из общего количества новорожденных асфиксия диагностируется у 4-6% детей. Тяжесть асфиксии обусловлена степенью нарушения газообмена: накопления углекислоты и недостатка кислорода в тканях и крови новорожденного. По времени развития асфиксия новорожденных бывает первичной (внутриутробной) и вторичной (внеутробной), возникшей в первые сутки после рождения. Асфиксия новорожденных является грозным состоянием и служит одной из частых предпосылок мертворождения или неонатальной смертности.
Асфиксия новорожденного
Причины
Асфиксия новорожденных является синдромом, развивающимся вследствие нарушения течения беременности, заболеваний матери и плода. Первичная асфиксия новорожденного обычно связана с хронической или острой внутриутробной недостаточностью кислорода, обусловленной:
Причинами вторичной асфиксии новорожденного, как правило, служат нарушения мозгового кровообращения ребенка или пневмопатии. Пневмопатии являются перинатальными неинфекционными заболеваниями легких, обусловленными неполным расправлением легочной ткани; проявляются ателектазами, отечно-геморрагическим синдромом, болезнью гиалиновых мембран.
Пневмопатии являются перинатальными неинфекционными заболеваниями легких, обусловленными неполным расправлением легочной ткани; проявляются ателектазами, отечно-геморрагическим синдромом, болезнью гиалиновых мембран.
Факторы риска
Развитию асфиксии новорожденного способствует наличие у беременной:
Патогенез
Независимо от этиологии дыхательных расстройств при асфиксии новорожденного, в его организме развиваются патогенетически одинаковые нарушения метаболизма, микроциркуляции и гемодинамики. Степень тяжести асфиксии новорожденного определяется длительностью и интенсивностью гипоксии. При недостатке кислорода происходит развитие респираторно-метаболического ацидоза, характеризующегося азотемией, гипогликемией, гиперкалиемией (затем гипокалиемией). При дисбалансе электролитов нарастает клеточная гипергидратация.Острая асфиксия новорожденных характеризуется возрастанием объема циркулирующей крови за счет эритроцитов; асфиксия, протекающая на фоне хронической гипоксии – гиповолемией.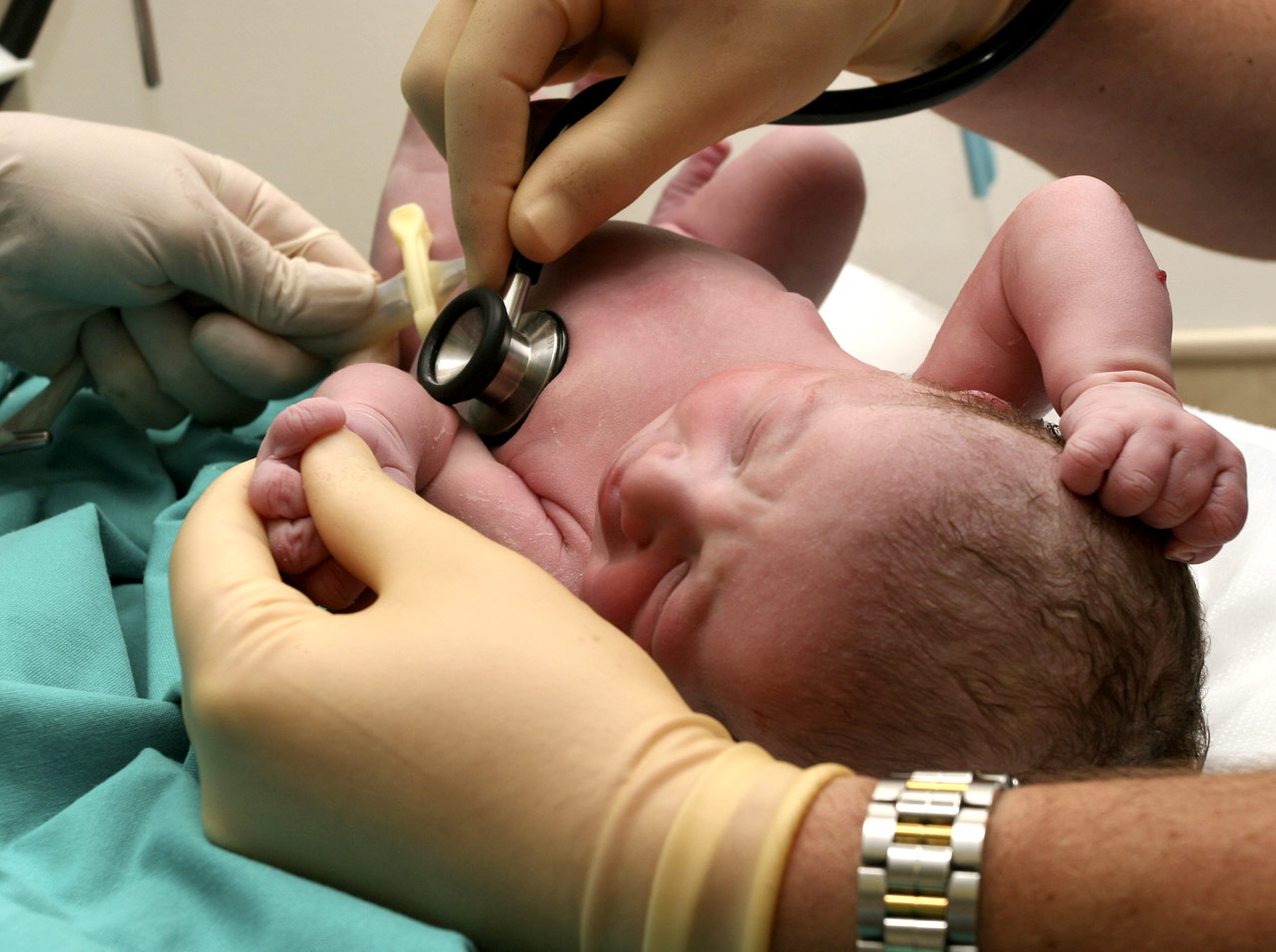 Это приводит к сгущению крови, увеличению ее вязкости, повышению агрегации тромбоцитов и эритроцитов. При таких микроциркуляторных сдвигах у новорожденного страдают головной мозг, почки, сердце, надпочечники, печень, в тканях которых развиваются отек, ишемия, кровоизлияния, гипоксия. В итоге возникают нарушения центральной и периферической гемодинамики, снижается ударный и минутный объем выброса, падает АД.
Это приводит к сгущению крови, увеличению ее вязкости, повышению агрегации тромбоцитов и эритроцитов. При таких микроциркуляторных сдвигах у новорожденного страдают головной мозг, почки, сердце, надпочечники, печень, в тканях которых развиваются отек, ишемия, кровоизлияния, гипоксия. В итоге возникают нарушения центральной и периферической гемодинамики, снижается ударный и минутный объем выброса, падает АД.
Асфиксия новорожденного
Симптомы асфиксии новорожденного
Определяющими критериями асфиксии новорожденного являются дыхательные расстройства, ведущие к нарушению гемодинамики, сердечной деятельности, мышечного тонуса и рефлексов. По тяжести проявлений в акушерстве и гинекологии различают 3 степени асфиксии новорожденных с оценкой в баллах по 10-балльной шкале (методике) Апгар в течение первой минуты после рождения:
- 6-7 баллов – легкая;
- 4-5 баллов – средняя;
- 1-3 балла – тяжелая.
Оценка по шкале Апгар 0 баллов расценивается как клиническая смерть. Критериями оценки тяжести асфиксии новорожденных служат сердцебиение, дыхание, окраска кожи, выраженность тонуса мышц и рефлекторной возбудимости (пяточного рефлекса).
Критериями оценки тяжести асфиксии новорожденных служат сердцебиение, дыхание, окраска кожи, выраженность тонуса мышц и рефлекторной возбудимости (пяточного рефлекса).
При легкой степени асфиксии первый вдох новорожденный делает на первой минуте после рождения, у ребенка выслушивается ослабленное дыхание, выявляется акроцианоз, цианоз носогубной области, сниженный мышечный тонус. Асфиксия новорожденного средней тяжести характеризуется вдохом на первой минуте, ослабленным регулярным или нерегулярным дыханием, слабым криком, брадикардией, сниженным мышечным тонусом и рефлексами, синюшностью кожи лица, стоп и кистей, пульсацией пуповины.
Тяжелой асфиксии новорожденных соответствует нерегулярное дыхание либо апноэ, отсутствие крика, редкое сердцебиение, арефлексия, атония или выраженная гипотония мышц, бледность кожи, отсутствие пульсации пуповины, развитие надпочечниковой недостаточности. В первые сутки жизни у новорожденных с асфиксией может развиваться постгипоксический синдром, проявляющийся поражением ЦНС — нарушением мозгового кровообращения и ликвородинамики.
Диагностика
Асфиксия диагностируется в первую минуту жизни новорожденного с учетом наличия, частоты и адекватности дыхания, показателей сердцебиения, мышечного тонуса, рефлекторной возбудимости, окраски кожи. Кроме внешнего осмотра и оценки тяжести состояния новорожденного по шкале Апгар, диагноз асфиксии подтверждается исследованием кислотно-основного состояния крови.
Методы неврологического обследования и УЗИ головного мозга (ультрасонография) направлены на дифференцирование гипоксического и травматического повреждения ЦНС (обширных субдуральных, субарахноидальных, внутрижелудочковых кровоизлияний и др.). Для новорожденных с гипоксическим поражением ЦНС характерно отсутствие очаговой симптоматики и повышенная нервно-рефлекторная возбудимость (при тяжелой асфиксии — угнетение ЦНС).
Выхаживание новорожденного
Лечение асфиксии новорожденных
Новорожденные с асфиксией нуждаются в экстренном реанимационном пособии, направленном на восстановление дыхательной функции и сердечной деятельности, коррекции расстройств гемодинамики, метаболизма, электролитного обмена.
- Асфиксия легкой и средней тяжести. Производится аспирация содержимого из носоглотки, полости рта и желудка; вспомогательная вентиляция легких масочным способом; введение в пуповинную вену 20% раствора глюкозы и кокарбоксилазы по весу. Если при асфиксии новорожденного средней тяжести спонтанное дыхание после проведенных мероприятий не восстановилось, производится интубация трахеи, аспирация содержимого из дыхательных путей, налаживается аппаратная ИВЛ. Дополнительно внутривенно вводится раствор натрия гидрокарбоната.
- Тяжелая асфиксия.
В дальнейшем новорожденные, перенесшие асфиксию, требуют интенсивного наблюдения и терапии: кислородной поддержки, краниоцеребральной гипотермии, инфузии растворов, витаминов, симптоматического лечения. Новорожденные с легкой асфиксией помещаются в кислородную палатку; со средней и тяжелой – в кувез. Вопрос о кормлении и его методах решается, исходя из состояния новорожденного. После выписки из роддома ребенку, перенесшему асфиксию, требуется наблюдение невролога.
Новорожденные с легкой асфиксией помещаются в кислородную палатку; со средней и тяжелой – в кувез. Вопрос о кормлении и его методах решается, исходя из состояния новорожденного. После выписки из роддома ребенку, перенесшему асфиксию, требуется наблюдение невролога.
Прогноз
Ближайший и отдаленный прогноз определяется тяжестью асфиксии новорожденного, полнотой и своевременностью лечебного пособия. Для оценки прогноза первичной асфиксии производится оценка состояния новорожденного по показателям шкалы Апгар через 5 минут после рождения. При возросшей оценке прогноз для жизни рассматривается как благоприятный. На первом году жизни у детей, родившихся в асфиксии, нередко отмечаются синдромы гипер- и гиповозбудимости, гипертензионно-гидроцефальная или судорожная перинатальная энцефалопатия, диэнцефальные (гипоталамические) нарушения. У части детей возможен летальный исход от последствий асфиксии.
Профилактика
В наше время акушерство и гинекология уделяют большое внимание осуществлению эффективных мер профилактики патологии новорожденных, в том числе и асфиксии новорожденных.
Профилактикой должна заниматься и сама женщина, отказавшись от вредных привычек, соблюдая рациональный режим, выполняя предписания акушера-гинеколога. Профилактика асфиксии новорожденного во время родов требует оказания грамотного акушерского пособия, предупреждения гипоксии плода в родах, освобождения верхних дыхательных путей ребенка сразу после его рождения.
Асфиксия новорожденных. Последствия
Фото: Alex Hockett
Травматичны ли роды, что такое асфиксия новорожденных, и какие она несёт последствия? В родах ребёнок рискует подвергнуться действию разных травмирующих факторов: физического (механического), химического, биологического, психического и их комбинации. Эти травмирующие факторы могут привести к развитию асфиксии. Реанимация ребёнка и его выживание — это не конец, а начало истории его развития.
Эти травмирующие факторы могут привести к развитию асфиксии. Реанимация ребёнка и его выживание — это не конец, а начало истории его развития.
Асфиксия — патологический процесс понижения содержания кислорода в крови и тканях (гипоксия) и повышения содержания в крови и тканях углекислого газа (гиперкапния). Асфиксия новорожденных, асфиксия плода, внутриутробная асфиксия, гипоксия новорожденных, гипоксия плода, гипоксическое повреждение — это асфиксия, произошедшая до рождения (плода) или во время рождения (новорожденного). У плода нет функции внешнего дыхания, у новорожденного — есть, и это условия для уязвимости от действия разных травмирующих факторов.
Объединяет эти понятия один патологический процесс (гипоксия с гиперкапнией), время и условия возникновения: внутриутробная жизнь, роды и первое время после рождения. ВОЗ даёт такое определение асфиксии новорожденных — это неспособность новорожденного начать или поддерживать нормальное самостоятельное дыхание после рождения, вследствие нарушения оксигенации во время схватки и родов (ВОЗ, 2002г).
- Механическая травма в родах
- Сдавление шеи пуповиной (обвитие пуповиной)
- Истинный узел пуповины
- Сдавление тела новорожденного в родовых путях
- Механические повреждения от родовспоможения
- Гематома при разрыве пупочной вены
- Выпадение петель пуповины
- Натяжения пуповины*
+
- Нарушения кровоснабжения матки
- Внутриутробная инфекция
- Нарушения функций дыхания матери
- Токсическое действие лекарств
- Плацентарная недостаточность
- Отслойка плаценты
- Тромбоз доли плаценты
- Морфологические изменения эпителия ворсин
- Диффузионные шунты
+
- Аспирация новорожденным околоплодных вод
- Пороки развития плода, затрудняющие дыхание
- Синдром задержки роста плода
- Диабетическая фетопатия
- Гемолитическая болезнь новорожденных
- Незрелость дыхательного центра и органов дыхания
- Расслаивающая аневризма пупочной артерии
- Другие причины и условия.

(* В экспериментах на животных в 1957 году В.Г. Вартапетова установила наличие рефлексогеннных зон в пуповине и в области пупочного кольца, которые стимулируются при потяге пуповины и вызывают нарушения ритма сердца и депрессию частоты и глубины дыхания).
Асфиксия при обвитии пуповинойДанные о частоте асфиксии новорожденных в результате обвития пуповиной шеи в литературе значительно разнятся, равно как и оценка тяжести последствий обвития шеи плода и новорожденного. Видимо это связано с тем, что сам факт обвития шеи пуповиной ещё не говорит о возникших последствиях нарушения внешнего дыхания, кровообращения головного мозга и других патофизиологических последствий. Важна сила и длительность сдавления.
Ряд авторов говорит о незначительном влиянии обвития пуповиной, другие — наоборот, считают обвитие пуповиной одним из основных факторов асфиксии новорожденного. М.К. Венцковский писал о 10% доле случаев мертворождения по причине асфиксии от обвития шеи пуповиной. М.И. Федоров и соавт. исследовали 20 000 историй родов и установили лишь 148 случаев асфиксии, обусловленных обвитием пуповиной. Возможно, такая низкая частота обусловлена именно источником информации — Истории родов.
М.И. Федоров и соавт. исследовали 20 000 историй родов и установили лишь 148 случаев асфиксии, обусловленных обвитием пуповиной. Возможно, такая низкая частота обусловлена именно источником информации — Истории родов.
По данным В.Б. Файнберг и К.А. Горчаковой дети с обвитием пуповиной шеи рождаются в разной степени асфиксии:
- 10,7% — лёгкая степень асфиксии
- 7,6% — выраженная асфиксия
- 2,4% — асфиксия со смертельным исходом.
Крупные кровоизлияния в мозг новорожденного, или под его оболочки, имеют либо механическое происхождение — черепно-мозговая травма, либо развиваются по механизму геморрагического инсульта. Несмотря на грубость этих кровоизлияний рядом работ (Б.Н. Клосовский, Л.С. Персианинов, Гутнер) показано, что в большой доле случаев кровоизлияния в мозг у новорожденного впоследствии рассасываются без образования рубцовой ткани, что объясняется хорошей пластичностью и способности к регенерации тканей новорожденного ребёнка.
В отличии от выше указанных кровоизлияний мелкие кровоизлияния объясняются проявлением асфиксии. Механизм возникновения этих кровоизлияний — повышение давления в системе кровоснабжения головы ребёнка, резко выраженный венозный застой, который в случае обвития шеи, объясняется сдавлением прежде всего вен шеи, при сохранении, или меньшей степени сдавления артерий, которые имеют более упругие стенки, и большую защиту окружающими тканями, как, например, позвоночные артерии, защищённые позвонками (Л.М. Орлеанский, И.Г. Стадницкий, А.С. Игнатовский, И.В. Давыдовский, Л.С. Персианов и др.).
Асфиксия новорожденных — диапедез
Микроскопические, диапедезные кровоизлияния в мозг также объясняются проявлением асфиксии (гипоксии) плода, которая проходит по механизму гипоксических изменений проницаемости сосудистой стенки. Вместе с мелкими кровоизлияниями при асфиксии происходят выраженные дегенеративные, дистрофические изменения нервной ткани, запускающие вторичные реакции в виде отёка головного мозга и явлений повышения продукции ликвора, направленных на скорейшее вымывание мозговой ткани от токсических продуктов некроза. Позже это приводит к синдрому внутричерепной гипертензии и другим патологическим синдромам.
Позже это приводит к синдрому внутричерепной гипертензии и другим патологическим синдромам.
Есть мнение (P. Brouardel, В.С. Вайль, Ван Лир, Н.Н. Сиротинин, Н.В. Лауэр, Т.С. Федотов, В.А. Неговский и др), что новорожденные менее чувствительны к гипоксии и асфиксии, чем взрослые. Это мнение строится на том, что при наличии асфиксии большая часть детей выживают. С этим мнением можно поспорить, так как нельзя оценивать лишь кратковременные последствия асфиксии, причём категоричные: “умер — выжил”, а стоит оценивать дальнейшее психическое и физическое развитие ребёнка.
Большой вклад в выживание новорожденного в нашей стране внес комплекс организационно-методических мер, принятых в неонатологии в 00х годах, что привело к увеличению количества выживающих детей как в случае гипоксий, так и в случаях недоношенности и незрелости плода. Так, показатель перинатальной смертности — это показатель гибели плодов с 22-й недели беременности и новорожденных в течение первой недели жизни за последние 20 лет, значительно снизился: с 15,3/1000 в 2000 году, до 4,9/1000 в 2019 году.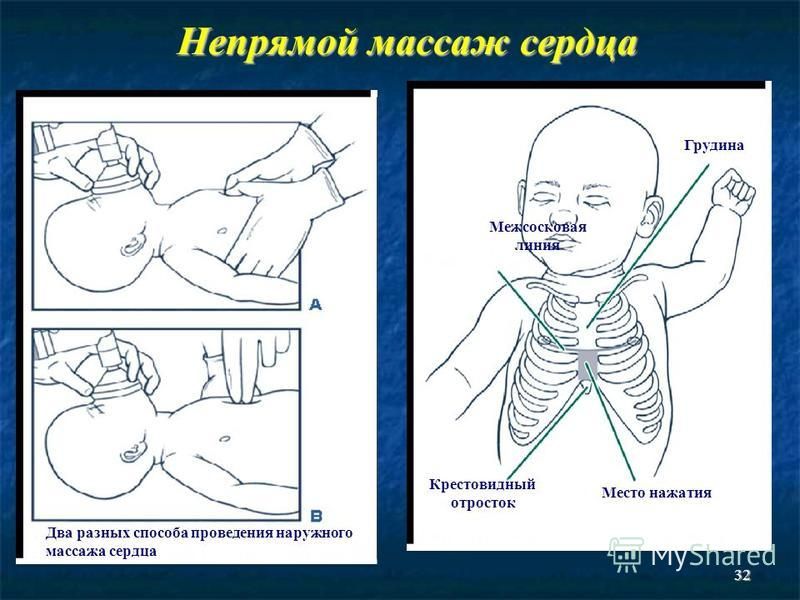 Хотя в дальнейшем эти дети далеко не всегда нормально развиваются и функционируют…
Хотя в дальнейшем эти дети далеко не всегда нормально развиваются и функционируют…
Асфиксия новорожденных — последствия
Многими исследователями (М.Н. Алябьева, П.Я. Барсуков, Ю.И. Барашнев, В.И. Бодяжина, И.О. Гилула, М.Ф. Дещекина, Л.Ю. Долгина, В.И. Евдокимова, Р.О. Клявинь, З.Н. Киселева, Б.Н. Клосовский, Б.В. Лебедев, Е.С. Стальненко, и др) показано, что асфиксия новорожденного влияет на дальнейшее развитие ребёнка.
И.О. Гилула и Е.С. Стальненко (цит. по: М.И. Федоров. Судебно-медицинское и клиническое значение постасфиксических состояний. Татполиграф. Казань, 1967. — 311с). у подавляющего большинства новорожденных, родившихся в асфиксии вследствие обвития шеи пуповиной наблюдали различную патологию нервной системы: запаздывание световых реакций, рефлексов новорожденных: Бабкина, Робинзона, Моро, нарушения сосательного и глотательного рефлексов, рефлексов вегетативной нервной системы, снижение электровозбудимости мышц и нервов, изменения электрической активности коры головного мозга и другие неврологические нарушения.
Разными авторами при наблюдении за детьми, родившимися в асфиксии и гипоксии отмечались: тонические нарушения: мышечная гипотония, впоследствии сменяющаяся гипертонусом, беспокойство, плохое сосание, отставание в физическом и психическом развитии, замедленная реакция на раздражители, тремор, судороги, нарушения дыхания, расстройства питания, задержка развития и другие нарушения речи, косоглазие, нарушения поведения, обучаемости, общего развития.
Р.О. Клявинь исследовала 95 детей с асфиксией в родах и пришла к выводу: между перенесенной во время рождения асфиксией и различными психоневрологическими изменениями в последующем существует несомненная связь. М.В. Дещекина при обследовании 90 детей в возрасте 4-8 лет, имевших в анамнезе асфиксию в родах, не установила у 61 ребёнка каких-то грубых отличий от сверстников, кроме нарушений поведения (гиперактивность, негативизм, эгоцентризм) — у 18 из них и косоглазие — у 13 детей.
У 12 из оставшихся детей была задержка умственного развития и знаки органического поражения ЦНС, у 17 детей отмечались грубые очаговые поражения центральной нервной системы и глубокая умственная отсталость. Б.В. Лебедев и Ю.И. Барашнев на 2 исследованиях (103 и 105 человек) показали, что асфиксия в родах является вредным фактором, влияющим на развитие ребёнка, и может быть причиной умственной отсталости, неврологических нарушений и нарушений поведения и черт характера ребёнка. Степень изменений зависит от продолжительности асфиксии.
Б.В. Лебедев и Ю.И. Барашнев на 2 исследованиях (103 и 105 человек) показали, что асфиксия в родах является вредным фактором, влияющим на развитие ребёнка, и может быть причиной умственной отсталости, неврологических нарушений и нарушений поведения и черт характера ребёнка. Степень изменений зависит от продолжительности асфиксии.
Психоневрологические последствия асфиксии
Представляет интерес исследование Н.Н. Станишевской, которая изучила развитие 54 детей в возрасте от 3 до 12 лет, перенёсших родовую травму. Автор выделила 3 группы детей в соответсвии с нарушениями: 1 группа детей имела двигательное беспокойство, суетливость, грубость, эгоистичность, склонность к фантазированию, невозможность сосредоточится на работе, судорожные припадки и сосудистые кризы. 2 группа — медлительность, вялость, безынициативность, плаксивость, быстрая утомляемость, головные боли и нарушения сна, судорожные припадки и сосудистые кризы. 3 группа отличалась нервозностью, возбуждением, сменяющимся апатией и бездеятельностью, слабостью лицевого и подъязычного нервов, недостаточной оптической конвергенцией, горизонтальным нистагмом, наличием парапарезов и гемипарезов, заиканием и другими нарушениями речи.
Исследованиями 102 детей-школьников, имеющих в анамнезе обвитие шеи пуповиной с асфиксией (М.И. Федоров и соавт.) показана связь родовой асфиксии с последующим снижением памяти, ослаблением внимания, умственной отсталостью, быстрой утомляемостью, неряшливостью, рассеянностью, изменениями характера и поведения: замкнутость, “лень”, неразговорчивость, стремление к одиночеству, или наоборот: нервозность, раздражительность, вспыльчивость, неуравновешенность, эмоциональная лабильность, плаксивость.
У детей с асфиксиями из-за плотного обвития шеи впоследствии (возраст обследуемых 10 — 13 лет) наблюдалась задержка речевого развития и речи, заикание, слабая успеваемость, нарушения сна и поведения: несдержанность, неусидчивость, небрежность. У детей с асфиксией и гипоксией в условиях родов из ягодичного предлежания впоследствии отмечалось запоздалое развитие речи, заикание, косноязычие, спастические параличи, низкая успеваемость, слабая память, замедленное мышление, патологическая пугливость, нервозность. У детей с асфиксией в условиях выпадения петли пуповины и её сдавления отмечалась низкая успеваемость, очень плохая память, плохое внимание, тревожный сон, замкнутый характер, плохой аппетит (М.И. Федоров. Судебно-медицинское и клиническое значение постасфиксических состояний. Татполиграф. Казань, 1967. — 311с.).
У детей с асфиксией в условиях выпадения петли пуповины и её сдавления отмечалась низкая успеваемость, очень плохая память, плохое внимание, тревожный сон, замкнутый характер, плохой аппетит (М.И. Федоров. Судебно-медицинское и клиническое значение постасфиксических состояний. Татполиграф. Казань, 1967. — 311с.).
Показано (Бенарон, Б.В. Лебедев, Ю.И. Барашнев и др.), что несмотря на повреждение нервной ткани при родовой асфиксии нарушение психического и физического развития можно нивелировать и предупредить хорошими условиями жизни, правильным воспитанием ребёнка, комплексным подходом в сопровождении развития ребёнка врачами (невролог, педиатр, остеопат), педагогами, логопедами и другими специалистами.
Решение найдётся!
Врач-остеопат Арсений Гуричев
Асфиксия новорожденных — последствия асфиксии для плода и новорожденного
Асфиксия у новорожденных детей
 Смотришь на только что появившееся на свет дитя и думаешь, какой же этот человечек крохотный и беззащитный. И видишь, как это маленькое тельце борется за свою жизнь, за право существования на этой планете.
Смотришь на только что появившееся на свет дитя и думаешь, какой же этот человечек крохотный и беззащитный. И видишь, как это маленькое тельце борется за свою жизнь, за право существования на этой планете.Да, асфиксия новорожденных последствия нередко имеет трагические. Однако при правильной и быстрой медицинской помощи, квалифицированном лечении, уходе за новорожденным и пристальном внимании к его здоровью в дальнейшем, возможно полное восстановление организма.
Что такое асфиксия и причины ее возникновения
Асфиксия – это нарушение работы дыхательной системы, вследствие которой у ребенка возникает кислородное голодание. Эта патология бывает двух видов: первичная, возникающая при рождении, и вторичная – та, что проявляется в первые минуты-часы жизни младенца.
Причин возникновения патологии – предостаточно. Возникает гипоксия у новорожденных (это другое названия асфиксии) из-за имеющейся в организме матери инфекции. Затруднение дыхания новорожденного происходит по причине закупорки дыхательных путей слизью, и раннего отхождения околоплодных вод, вследствие которых отмечается кислородное голодание. Также асфиксия плода и новорожденного может быть связана с серьезными заболеваниями мамы (диабет, проблемы с сердцем, печенью, респираторные заболевания). Среди причин также отмечается мамин поздний токсикоз (гестоз, преэкламсия), тяжелые и продолжительные роды, отслоение или нарушение целостности плаценты, обвитие пуповиной, переношенная беременность или наоборот раннее излитие околоплодных вод и недоношенная беременность, прием в последние дни беременности некоторых лекарственных препаратов в больших дозировках.
Также асфиксия плода и новорожденного может быть связана с серьезными заболеваниями мамы (диабет, проблемы с сердцем, печенью, респираторные заболевания). Среди причин также отмечается мамин поздний токсикоз (гестоз, преэкламсия), тяжелые и продолжительные роды, отслоение или нарушение целостности плаценты, обвитие пуповиной, переношенная беременность или наоборот раннее излитие околоплодных вод и недоношенная беременность, прием в последние дни беременности некоторых лекарственных препаратов в больших дозировках.
Как видите, причин – предостаточно. Такая патология, как асфиксия плода и новорожденных (что особенно устрашает) – сегодня не редкость. Именно поэтому женщина, находясь в состоянии беременности, должна очень внимательно следить за своим состоянием и в случае малейшего недомогания обращаться к докторам. Самолечение или болезнь, протекающая без вмешательства квалифицированного врача, может привести к серьезному исходу и не всегда приятному разрешению возникшей проблемы.
Если поставлен диагноз – асфиксия
Неважно, какая причина асфиксии, организм новорожденного тут же реагирует на эту патологию и тотчас перестраивается. Нарушается центральная нервная система, происходит сбой в работе мозга, обменные процессы приостанавливаются. Страдает и сердце, и печень, и почки, и мозг. Сгущение крови приводит к ухудшению работы сердечной мышцы. Подобные сбои в работе внутренних органов могут повлечь за собой отек, кровоизлияния в тканях.
Степень асфиксии оценивают по шкале Апгар. В зависимости от того, как сделан первый вдох ребенка, какое дыхание в первую минуту жизни, цвет кожных покровов и какой крик у него (слабый или звонкий громкий) медиками выставляются баллы. Каждый балл соответствует определенной оценке степени тяжести асфиксии.
Благоприятный исход асфиксии во многом зависит от того, насколько правильное было проведено лечение и реабилитация. Также влияет продолжительность кислородного голодания. Такие детки сразу же после рождения требуют реанимации. Реанимационная работа начинается прямо в родильном зале. При помощи специальных отсосов дыхательные пути малыша освобождаются от слизи, перерезается пуповина, ребенок обогревается. Если дыхание не восстанавливается, новорожденного подключают к аппарату искусственного дыхания. Вентиляция легких происходит до тех пор, пока кожа не приобретет естественный розовый цвет, а дыхание не станет ровным (частота сердечных сокращений не менее 100 за минуту). Если в течение 20 минут самостоятельное дыхание не восстанавливается, младенец не сделал ни единого вдоха, реанимация бессмысленна. У здорового ребенка самостоятельное дыхание появляется не позднее 1 минуты со времени родов.
Реанимационная работа начинается прямо в родильном зале. При помощи специальных отсосов дыхательные пути малыша освобождаются от слизи, перерезается пуповина, ребенок обогревается. Если дыхание не восстанавливается, новорожденного подключают к аппарату искусственного дыхания. Вентиляция легких происходит до тех пор, пока кожа не приобретет естественный розовый цвет, а дыхание не станет ровным (частота сердечных сокращений не менее 100 за минуту). Если в течение 20 минут самостоятельное дыхание не восстанавливается, младенец не сделал ни единого вдоха, реанимация бессмысленна. У здорового ребенка самостоятельное дыхание появляется не позднее 1 минуты со времени родов.
У многих деток, перенесших асфиксию, наблюдается судорожный синдром, повышенная возбудимость, двигательные нарушения, повышенное внутричерепное давление.
Уход за ребенком, перенесшим асфиксию
Учитывая тот факт, что у младенца при асфиксии нарушается работа ЦНС, необходимо четко выполнять все назначения врача.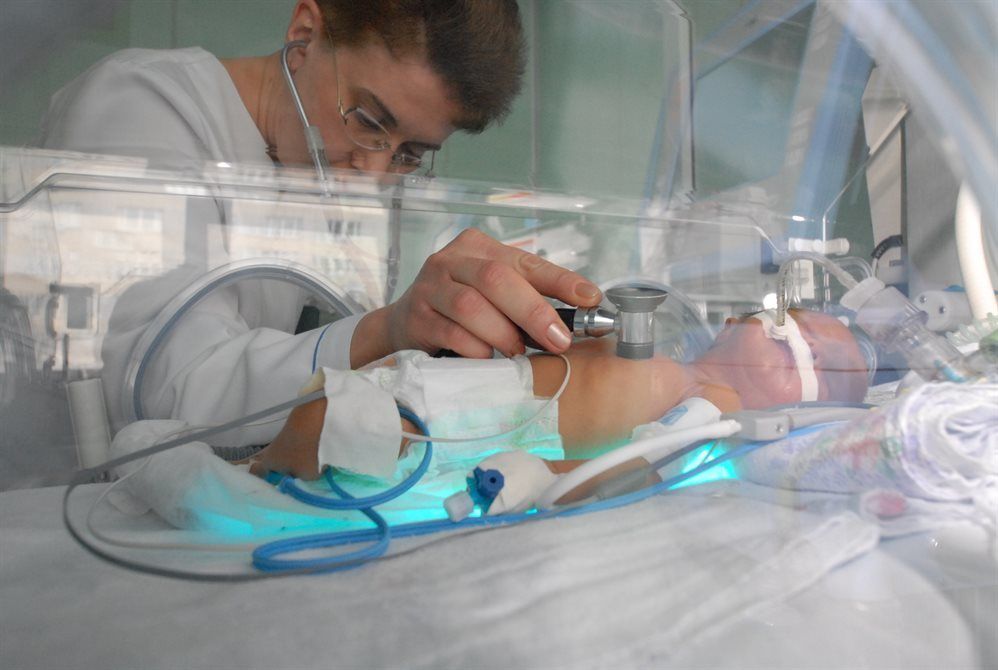 Немаловажен для ребенка уход. Полный покой и пристальное внимание. Обычно деток с асфиксией помещают в кувез или палатку, в которую подается кислород.
Немаловажен для ребенка уход. Полный покой и пристальное внимание. Обычно деток с асфиксией помещают в кувез или палатку, в которую подается кислород.
После выписки из стационара ребенка нужно регулярно показывать невропатологу и педиатру. Дальнейшее лечение, реабилитация зависят только от поставленных диагнозов (если они есть) и симптоматики. При легкой степени асфиксии нарушений в организме ребенка может и не быть. И в таком случае семье нужно просто спокойно жить. У большинства таких деток даже противопоказаний к плановой вакцинации нет.
Помните, что если асфиксия оказала губительное воздействие на ребенка, это будет видно уже в первые дни после рождения.
степени тяжести, причины, терапия, последствия
Асфиксия — опасное патологическое состояние, которое развивается у новорожденных в первые минуты жизни (первичная) или в течение нескольких первых суток (вторичная) после появления на свет. Характеризуется патология нарушением дыхания и развитием дыхательной недостаточности. В медицинской практике принято разделять асфиксию на умеренную и тяжелую.
В медицинской практике принято разделять асфиксию на умеренную и тяжелую.
Причины асфиксии новорожденных при родах
Причины развития патологического состояния находятся в прямой зависимости от вида асфиксии у ребенка. Так, первичная развивается во время родов. Это состояние, как правило, вызвано острой или хронической внутриутробной гипоксией плода. Кроме того, причинами асфиксии новорожденных могут выступать:
- внутричерепная травма у ребенка, которую он получил в процессе родов;
- пороки развития, оказывающие угнетающее воздействие на дыхательную систему и затрудняющие дыхание;
- иммунологическая несовместимость матери и ребенка по группе или резус-фактору крови;
- закупорка дыхательных путей малыша слизью или окоплодными водами;
- наличие у женщины заболеваний сердца и сосудов, сахарного диабета, железодефицитной анемии;
- гестоз (поздний токсикоз) у матери, который сопровождается повышенным АД и сильными отеками конечностей;
- патологическое строение пуповины или плаценты, ее отслоение, неправильное положение головы плода, раннее отхождение околоплодных вод.

Вторичная возникает в течение нескольких часов или даже дней после рождения. Причинами асфиксии у новорожденного в этом случае могут быть:
- нарушения кровообращения в структурах мозга;
- поражение центральной нервной системы ребенка;
- пороки сердца различной степени тяжести;
- пневмопатии: кровоизлияния в легких, закупорка дыхательных путей слизью, дисфункция обменных процессов.
Все эти состояния могут начать развиваться еще во внутриутробном периоде.
Возникновение патологического состояния
При различных степенях асфиксии у новорожденных начинается патологическое изменение обменных процессов в организме. Проявления, выраженность и длительность таких нарушений зависят от степени тяжести асфиксии. Если состояние развивается во время родов, то наблюдается также уменьшение объема крови, ее загустение и вязкость. Возможны отеки в головном мозге, почках и печени, сердце, нередки кровоизлияния, которые появляются из-за недостаточного количества кислорода. Также приводит патология к снижению АД новорожденного, уменьшению сокращений сердца, нарушению мочевыделительной функции.
Также приводит патология к снижению АД новорожденного, уменьшению сокращений сердца, нарушению мочевыделительной функции.
Легкая степень асфиксии: состояние новорожденного
Первичная асфиксия новорожденных возникает в первые минуты жизни. Состояние ребенка оценивается по шкале Апгар. При легкой форме дыхательной недостаточности состояние малыша оценивается в 6-7 баллов. При этом в первые минуты жизни новорожденный самостоятельно делает первый вдох, но затем его дыхание становится прерывистым, слабым. Мышечный тонус обычно снижен, а носогубный треугольник приобретает синюшный оттенок.
Признаки умеренной асфиксии у новорожденных
Симптомами патологии (в умеренном проявлении, то есть средней форме тяжести) являются вялость, безэмоциональный короткий крик, частые срыгивания, спонтанные движения, слабая реакция на раздражающие факторы и осмотр, синюшная окраска кожи, слабое проявление физиологических рефлексов.
Состояние новорожденного в общем оценивается как средней тяжести, оценка по шкале Апгар — 4-5. При этом частота сердечных сокращений в минуту составляет менее 100 (у здоровых детей — 100 и более), наблюдается некоторое сгибание конечностей (у малышей с оценкой 2 отмечают активные движения), прерывистое дыхание, гримаса на лице (здоровые дети кричат, кашляют, чихают), розовая окраска тела и синюшная — конечностей.
При этом частота сердечных сокращений в минуту составляет менее 100 (у здоровых детей — 100 и более), наблюдается некоторое сгибание конечностей (у малышей с оценкой 2 отмечают активные движения), прерывистое дыхание, гримаса на лице (здоровые дети кричат, кашляют, чихают), розовая окраска тела и синюшная — конечностей.
Симптомы тяжелой асфиксии у детей
Тяжелая асфиксия новорожденного проявляется такими признаками:
- тяжелое или очень тяжелое состояние при рождении;
- практически полное отсутствие физиологических рефлексов;
- глухие тона сердца при прослушивании, систолический шум;
- возможен геморрагический шок, при котором глаза ребенка закрыты, самостоятельного дыхания и реакции на боль нет.
В самом худшем случае могут возникать нарушения нормального функционирования многих органов и систем, отсутствие реакции зрачков на свет. Неонатолог при таких симптомах поставит оценку 1-3 балла по шкале Апгар. При этом сердечные сокращения могут отсутствовать, конечности свисают, дыхание и рефлексы отсутствуют, окраска кожи бледная, может быть синюшность.
Клиническая смерть: 0 по шкале Апгар
Самая тяжелая форма асфиксии характеризуется клинической смертью новорожденного. Для спасения жизни ребенка в этом случае врачи немедленно начинают проводить реанимационные мероприятия.
Основные признаки вторичной асфиксии
Вторичная асфиксия новорожденных развивается через несколько часов после родов или в течение первых нескольких суток. Состояние отмечается теми же симптомами. Ребенок становится вялым, дыхание слабеет или пропадает, мышечный тонус снижается, может не реагировать на внешние раздражители. Кожа при этом приобретает синюшный оттенок в области носогубного треугольника.
Ранние и поздние осложнения асфиксии
Ранние осложнения недостаточности дыхания (то есть те, которые наблюдаются в первые сутки жизни) включают в себя:
- легочную гипертензию;
- некрозы мозговых тканей;
- отек мозга;
- внутричерепные кровоизлияния;
- острый почечный некроз;
- тромбоз сосудов почек;
- судорожный синдром;
- патологии кроветворных клеток костного мозга.

Осложнения, которые могут возникать в течение следующих несколько суток при отсутствии адекватного и комплексного лечения асфиксии новорожденных, такие:
- менингит — воспаление оболочек мозга;
- сепсис — общее заражение патогенными бактериями, попавшими в кровь;
- пневмония — воспаление легких;
- гидроцефальный синдром — избыточный синтез спинномозговой жидкости.
Терапия острой асфиксии у ребенка
Этапы реанимации при асфиксии новорожденного были систематизированы в единый алгоритм действий в США. Называется система АВС-шаги. Во-первых, неонатологи должны обеспечить проходимость дыхательных путей новорожденного, во-вторых, следует стимулировать процесс естественного дыхания, в-третьих, необходимо поддержать систему кровообращения.
При появлении ребенка с симптомами асфиксии на свет врачи вводят ему специальный зонд в полость носа и рта. Нередко это действие производится еще при появлении головки ребенка из родовых путей женщины. С помощью зонда из дыхательных путей малыша удаляют остатки слизи и околоплодных вод, которые могут мешать нормальному дыханию.
С помощью зонда из дыхательных путей малыша удаляют остатки слизи и околоплодных вод, которые могут мешать нормальному дыханию.
После извлечения из родовых путей врачи обрезают новорожденному пуповину. После этого его поместят на реанимационный столик, где проведут повторную очистку содержимого носоглотки. В этот раз очистят и желудок. При этом нельзя прикасаться к задней стенке глотки, чтобы не спровоцировать возбуждение нервной системы и брадикардию.
Малыша переносят под инфракрасный нагреватель, его кожу промакивают чистой пеленкой. Чтобы обеспечить максимальную проходимость дыхательных путей, врачи выкладывают новорожденного следующим образом: на спину, под плечи валик, голова умеренно разогнута. Если дыхания вообще нет, то проводят стимуляцию: легко хлопают малыша по пятке, подошве, растирают кожу вдоль позвоночника.
Нельзя при асфиксии давать ребенку в лицо струю кислорода, обливать или брызгать на него водой, сжимать грудную клетку или хлопать по ягодицам.
Описанные выше мероприятия должны проводиться очень быстро, буквально в течение двадцати секунд. После проведения реанимации новорожденного при асфиксии его состояние снова оценивают, обращая внимание на частоту сердечных сокращений, дыхание и оттенок кожных покровов.
После проведения реанимации новорожденного при асфиксии его состояние снова оценивают, обращая внимание на частоту сердечных сокращений, дыхание и оттенок кожных покровов.
Если дыхание отсутствует или недостаточное, то ребенку проводится искусственная вентиляция легких. Помощь при асфиксии новорожденных предполагает введение медикаментов. Среди лекарственных реанимационных средств эффективен раствор адреналина, который быстро вводится внутривенно. Также вводят раствор натрия хлорида в виде капельницы на 5-10 минут. При необходимости на 40-50-й минутах жизни ребенка начинают проведение плановой инфузионной терапии.
Уход за новорожденным после асфиксии
После такого тяжелого состояния, как асфиксия, необходим особенный уход за ребенком. Ему следует обеспечить полный покой. Голова должна находиться в приподнятом состоянии. Нередко врачи — неонатологи и педиатры — назначают таким маленьким пациентам кислородную терапию. Длительность такого лечения различается в каждом отдельном случае и зависит от состояния ребенка. После асфиксии новорожденного помещают в палату с повышенным содержанием кислорода.
После асфиксии новорожденного помещают в палату с повышенным содержанием кислорода.
Обязательно нужно наблюдать за ребенком, который перенес дыхательную недостаточность во время родов. Необходимо систематически измерять температуру тела, контролировать диурез и функционирование кишечника. Нередко малышу необходима повторная очистка дыхательных путей от инородного содержимого.
Первое кормление ребенка с легкой или средней формой дыхательной недостаточности производится через шестнадцать часов после родов. Если состояние малыша было тяжелым, то первое кормление проводят только через сутки и с помощью специального зонда. Время начала естественного грудного вскармливания определяется для каждого случая отдельно.
После выписки из родильного дома малыш должен быть под наблюдением педиатра и невропатолога. Основная цель всех лечебных мероприятий состоит в том, чтобы избежать (или минимизировать, если полностью устранить нет возможности) осложнений со стороны нервной системы.
Прогноз врачей и последствия асфиксии
Прогноз и последствия асфиксии новорожденных зависят от степени тяжести патологии, адекватности действий врачей и своевременности начала терапии. Прогноз прямо зависит от второй оценки его здоровья по шкале Апгар. Вторая оценка ставится неонатологом спустя пять минут после появления малыша на свет. Если вторая оценка будет выше первой, то прогноз, скорее всего, благоприятный.
Какие-либо последствия асфиксии новорожденных в старшем возрасте редко проявляются, если прогноз врачей был благоприятным. Как правило, если ребенок испытал дыхательную недостаточность во время родов, но медикам удалось стабилизировать его состояние и избежать появления осложнений, то в старшем возрасте никаких других последствий опасного состояния не будет.
Основные профилактические мероприятия
Последствия асфиксии новорожденных достаточно серьезные, но их можно постараться избежать. Есть меры профилактики, которые, конечно, не со всеми 100 % вероятности позволят избежать дыхательной недостаточности у плода, но дают результат приблизительно в 40 % случаев.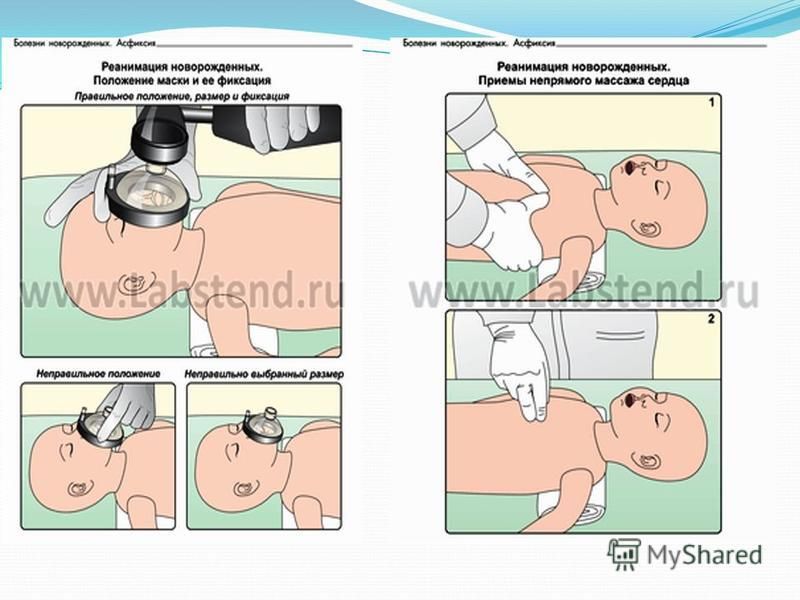 Одной из причин асфиксии, например, может быть внутриутробная гипоксия плода. Чтобы избежать этого, беременной женщине нужно регулярно посещать врача.
Одной из причин асфиксии, например, может быть внутриутробная гипоксия плода. Чтобы избежать этого, беременной женщине нужно регулярно посещать врача.
Также факторами риска, которые впоследствии могут спровоцировать дыхательную недостаточность у плода, являются:
- возраст матери старше 35 лет;
- наличие вредных привычек у беременной;
- сильные стрессы во время беременности;
- нарушения работы эндокринной системы матери;
- изменения гормонального фона женщины;
- инфекционные и другие заболевания, оказывающие негативное воздействие на плод.
Одной из причин асфиксии также является отслойка плаценты или патологии ее развития. В устранении этого фактора важно регулярное наблюдение у специалиста. Врач сможет выявить опасные состояния и вовремя начать терапию, чтобы жизни и здоровью маленького человечка ничего не угрожало.
Вот некоторые общие рекомендации гинекологов беременной женщине, которые позволят снизить риск недостаточности дыхательной системы плода:
- Больше прогуливаться на свежем воздухе.
 Организм женщины насыщается необходимым количеством кислорода, который затем переносится плоду, нуждающемуся в этом элементе.
Организм женщины насыщается необходимым количеством кислорода, который затем переносится плоду, нуждающемуся в этом элементе. - Принимать витамины, назначенные гинекологом. И самой беременной, и малышу, который пока развивается в тесной связи с организмом матери, нужны витамины и полезные вещества.
- Соблюдать режим дня. Ночью будущей маме следует спать не менее девяти часов, днем также рекомендуется выделять пару часов для сна или послеобеденного отдыха (не за экраном компьютера).
- Сохранять душевное спокойствие и положительный настрой. Беременность — это незабываемый период в жизни каждой представительницы прекрасного пола, но связан он также и со стрессами, переживаниями. Для здоровья ребенка и самой женщины необходимо меньше волноваться, научиться спокойно справляться с жизненными коллизиями, больше времени уделять общению с позитивными людьми.
Стоит сказать, что дыхательная недостаточность, то есть асфиксия, является серьезной патологией. Но благодаря современным препаратам и профессиональным действиям медицинского персонала, жизни большинства новорожденных спасают и устраняют возможные последствия патологии.
ЭТО ДОЛЖЕН ЗНАТЬ КАЖДЫЙ РОДИТЕЛЬ: ОСТОРОЖНО АСФИКСИЯ И АСПИРАЦИЯ!
МИНИСТЕРСТВО ЗДРАВООХРАНЕНИЯ РОСТОВСКОЙ ОБЛАСТИ ГБУ РО «МЕДИЦИНСКИЙ ИНФОРМАЦИОННО-АНАЛИТИЧЕСКИЙ ЦЕНТР»
БЕГЕГИТЕ ЖИЗНЬ ДЕТЕЙ! НЕ ОСТАВЛЯЙТЕ ИХ БЕЗ ПРИСМОТРА!
(памятка для родителей)
Внешние причины (не связанные с состоянием здоровья) вызывают смерть детей до года не часто, но составляют до 30-35% от всех причин детской смертности. Особенно высок риск внезапной смерти в кроватке у детей в возрасте 2-4 месяца.
Удушение ребенка происходит зачастую при нахождении ребёнка в одной постели с матерью.
Случайное придавливание ребенка во сне происходит при закрытии отверстий носа и рта мягким предметом. Чаще это в первые месяцы его жизни, когда у него нет силы повернуть в сторону голову, чтобы дышать. В результате перекрытия дыхательных путей и прекращения подачи кислорода повышается уровень углекислого газа и наступает асфиксия – удушение ребенка. Курение родителей также является дополнительным фактором, способствующим вдыханию ребенком отработанного воздуха с высоким содержанием углекислого газа.
Аспирация у детей — попадание в дыхательные пути инородного тела (молоко, молочная смесь, кусочки пищи, содержимое желудка) при вдохе — другая причина смерти детей до года. Это происходит при неправильном положении во время кормления ребенка и обильном срыгивании, когда голова ребенка запрокинута назад, затрудняется процесс глотания, а также, если носовые ходы во время кормления перекрываются молочной железой, ребенок пытается вдохнуть ртом и молоко попадает в дыхательные пути, все это может привести к аспирации.
ПОМНИТЕ! БЕЗОПАСНОСТЬ ДЕТЕЙ – ЗАБОТА ВЗРОСЛЫХ!
Рекомендации для молодых мам: обеспечить малышу безопасную среду и исключить факторы риска!
- удерживать малыша у груди не более 20 минут;
- не закрывать грудью матери носовые ходы во время кормления ребенка;
- кормить ребенка грудью и продолжать естественное вскармливание как можно дольше, особенно в первые 6 месяцев жизни, что укрепляет иммунную систему и снижает риск внезапной смерти ребенка;
- подержать ребенка после кормления «столбиком», прижав вертикально к себе 2-3 минуты, что будет способствовать отхождению воздуха, попавшего при кормлении в желудок;
- укладывать ребенка первых месяцев жизни на бок, чтобы в случае срыгивания желудочное содержимое не попало в дыхательные пути;
- при кормлении из бутылочки следить за тем, чтобы во время кормления горлышко бутылочки и соска постоянно были заполнены смесью и не содержали воздух;
- питательная смесь должна быть теплой, но не холодной или горячей, чтобы не вызвать спазм.
- не следует перекармливать детей;
- не укладывать ребенка на живот для сна пока он сам не начнет активно переворачиваться;
- не допускать укладывания ребенка в постель для сна вместе с собой;
- не укладывать ребенка в кроватку с мягкими одеялами, периной мягкими игрушками; подушка должна быть плоской, не более 3 см толщиной;
- избавиться от никотиновой зависимости: пассивное вдыхание табачного дыма приводит к внезапной смерти ребенка во сне;
- не допускать перегревания или переохлаждения ребенка, что может оказать неблагоприятное влияние на дыхательную и сердечную деятельность;
- не практиковать тугое пеленание, которое может вызвать перегрев малыша и ограничить его двигательную активность;
- обеспечить постоянную оптимальную (23-24 гр.С) температуру в помещении для пребывания ребенка;
- категорически запрещается встряхивание новорожденного при играх, закачивании и т.п., чтобы не повредить тонкие сосуды головного мозга;
- не уклоняться от вакцинации: она защищает младенца от множества серьезных проблем, при отсутствии медицинских противопоказаний ребенок должен быть привит.
При возникновении критических ситуаций, угрожающих жизни ребенка, немедленно обращайтесь за медицинской помощью!
Ведение родильного отделения доношенных и недоношенных младенцев с асфиксией — FullText — Neonatology 2021, Vol. 118, №4
Аннотация
Около 800 000 новорожденных ежегодно умирают от асфиксии при рождении. Реанимация доношенных новорожденных с асфиксией часто происходит неожиданно и является сложной задачей для медицинских работников, поскольку требует опыта и знаний в области реанимации новорожденных. Текущие руководства по реанимации новорожденных часто сосредоточены на реанимации крайне и / или очень недоношенных детей; однако рекомендации для доношенных новорожденных с асфиксией в некоторых аспектах отличаются от рекомендаций для недоношенных детей (т.д., респираторная поддержка, дополнительный кислород и контроль температуры). После обновления рекомендаций по реанимации новорожденных в 2015 году было опубликовано несколько исследований, посвященных изучению различных подходов к реанимации для улучшения исхода у младенцев, страдающих асфиксией. В этом обзоре мы обсуждаем текущие рекомендации и недавние открытия и даем обзор ведения родильного отделения доношенных новорожденных с асфиксией.
© 2021 Автор (ы). Опубликовано С.Karger AG, Базель
Введение
Всем новорожденным требуются базовые вмешательства (например, сушка, стимуляция и поддержание тепла) во время перехода от эмбриональной к неонатальной жизни [1, 2]. Примерно 5% новорожденных (6-7 миллионов во всем мире в год) нуждаются в поддержке дыхания [1, 2], а 0,1% доношенных и 10-15% недоношенных детей (1,5-2,5 миллиона во всем мире) нуждаются в сердечно-легочной реанимации (СЛР) [3-6], определяемый как сжатие грудной клетки, 100% кислород и / или адреналин (адреналин) в родильном зале (DR).Несмотря на получение СЛР, около 800 000 новорожденных ежегодно умирают во всем мире из-за асфиксии при рождении или внутриродовых событий. Существует ряд причин асфиксии при рождении или интранатальных осложнений, включая плохое дородовое наблюдение, а также проблемы со стороны матери, плаценты / пуповины и новорожденных [7-13] (Таблица 1).
Таблица 1.
Причины асфиксии при рождении и перинатальных событий [7-13]
Асфиксия при рождении — это состояние нарушения газообмена и недостаточной перфузии различных органов, что приводит к прогрессирующей гипоксии, гиперкарбии и метаболическому ацидозу [ 9].Асфиксия — основная причина неонатальной смерти и инвалидности. Путем введения воздуха вместо 100% кислорода доношенным или недоношенным новорожденным, нуждающимся в вентиляции с положительным давлением (PPV) десять лет назад, было продемонстрировано 30% снижение смертности [14]. Тем не менее, значительное число смертей можно предотвратить за счет улучшения неонатальной реанимации. Необходимы срочные реанимационные мероприятия для предотвращения повреждения головного мозга путем предотвращения дальнейшей гипоксии и ишемии и обращения вспять респираторного и метаболического ацидоза [13, 15-17].Цель этого обзора — дать обзор ведения ЛР у доношенных и недоношенных новорожденных с асфиксией.
Управление пуповиной
В рекомендациях по реанимации новорожденных указано, что младенцам, которым требуются реанимационные мероприятия, следует немедленно пережать пережатие пуповины [18]. В рекомендациях Европейского совета по реанимации говорится, что там, где отсроченное пережатие пуповины невозможно, следует рассмотреть возможность доения пуповины у младенцев> 28 недель беременности [19]. Однако оптимальная стратегия ведения пуповины, которая улучшает исходы у доношенных новорожденных с асфиксией, остается неизвестной [20].В недавнем систематическом обзоре сравнивались различные стратегии управления пуповиной, включая в общей сложности 9 159 женщин и пар новорожденных у поздних недоношенных (34 +0 –36 +6 недель гестационного возраста) и доношенных (гестационный возраст ≥37 недель) детей. . К сожалению, ни в одном из включенных испытаний не сообщалось о первичном исходе выживаемости без нарушения психического развития от умеренного до тяжелого в раннем детстве. Путем рандомизации здоровых доношенных детей на немедленное пережатие пуповины по сравнению с доением пуповины или отсроченное или немедленное пережатие пуповины, не было обнаружено значительных различий в исходах новорожденных (включая баллы по шкале Апгар, необходимость реанимации или госпитализацию в отделение интенсивной терапии новорожденных) [21 ].Недавно были опубликованы обновленные SpO 2 и процентили ЧСС у доношенных детей с отсроченным пережатием пуповины [22]. Они сообщили о более высоких значениях SpO 2 и ЧСС и более ранней стабилизации по сравнению с доношенными детьми с немедленным пережатием пуповины [22].
Пуповинное доение
Erickson-Owens et al. [23] рандомизировали 24 здоровых доношенных новорожденных для немедленного пережатия пуповины или доения пуповины и сообщили о сопоставимых баллах по шкале Апгар и необходимости реанимации без госпитализации.В то время как исследования показывают, что доение пуповины является альтернативой немедленному пережатию пуповины у энергичных младенцев, данных о неторопливых младенцах нет. Ретроспективный анализ 157 недоношенных и доношенных детей (35-42 недель) с аномальными газами пуповинной крови (артериальный или венозный pH пуповины ≤7,1 или дефицит оснований <−12 ммоль / л) показал меньшее количество новорожденных, нуждающихся в реанимации (38 vs. 56%, p = 0,07) и постоянной респираторной поддержки (19 против 31%, p = 0,16) с доением пуповины по сравнению с немедленным пережатием пуповины [24].Гириш и др. [25] сравнили доение пуповины с немедленным пережатием пуповины у 101 доношенного новорожденного с депрессией при рождении в квазирандомизированном (чередование месяцев) испытании и не сообщили об отсутствии различий в задержке реанимации, усилиях по реанимации и краткосрочных результатах. В настоящее время проводится многоцентровое исследование, посвященное немедленному пережатию пуповины с доением пуповины у нетвердых новорожденных, 35 +0 –41 +6 недель беременности (ClinicalTrials.gov NCT03631940).
Зажатие пуповины по физиологическим причинам
Во время пережатия пуповины по физиологическим причинам младенцы остаются прикрепленными к пуповине до тех пор, пока не произойдет газообмен / аэрация легких, и это может быть альтернативой отсроченному пережатию пуповины и доению пуповины; однако в настоящее время количество доступных данных ограничено.Исследования с использованием ягнят, перенесших асфиксию в ближайшем будущем, показали, что реанимация с неповрежденной пуповиной (i) заметно улучшила сердечно-сосудистую функцию за счет увеличения венозного возврата в правое предсердие и легочного кровотока, (ii) уменьшила рикошетную гипертензию и (iii) уменьшила утечку мозговых сосудов по сравнению с немедленное или отсроченное пережатие пуповины [20, 26, 27]. В недавнем рандомизированном контролируемом исследовании с участием 231 новорожденного без дыхания сравнивали реанимацию с интактной пуповиной или немедленным пережатием пуповины [28].Сатурация периферической артерии кислородом (SpO 2 ) была значительно выше в группе реанимации с интактной пуповиной со средним значением (SD) 90,4 (8,1) по сравнению с 85,4 (2,7)% в группе немедленного пережатия пуповины. Оценка по шкале Апгар также была выше в группе интактной пуповины по сравнению с немедленным пережатием пуповины, в то время как частота сердечных сокращений (ЧСС) была ниже в группе интактной пуповины через 1 и 5 минут по сравнению с немедленным пережатием пуповины [28]. Пока неясно, улучшит ли физиологическое пережатие пуповины или реанимация неповрежденной пуповины исход асфиксированных новорожденных.
Оценка сердечного ритма
Текущие рекомендации по реанимации новорожденных рекомендуют оценивать ЧСС сразу после рождения с помощью пульсоксиметрии или электрокардиографии (ЭКГ) для постоянного наблюдения [18, 29]. Клинические исследования показали, что вариабельность между и внутри наблюдателей при аускультации и пальпации занижает ЧСС примерно на 21 и 14 / мин соответственно [30-32]. Кроме того, ни пальпация, ни аускультация не могут обеспечить непрерывную оценку ЧСС во время реанимации. Следовательно, требуются постоянные, объективные и точные меры.И пульсоксиметрия, и ЭКГ соответствуют этим критериям с очень хорошей точностью [33]. Из-за задержки в получении сигнала пульсоксиметром ЭКГ обеспечивает более точную ЧСС в первые 3 мин после рождения [18]. В 2015 г. руководство по реанимации новорожденных рекомендовало рутинное использование ЭКГ для непрерывного мониторинга ЧСС во время реанимации ДР [34]. Однако Американская кардиологическая ассоциация / Программа реанимации новорожденных (AHA / NRP) рекомендует, чтобы «аускультация прекардиальной области оставалась предпочтительным методом физического обследования для первоначальной оценки частоты сердечных сокращений».Пульсоксиметрия и ЭКГ остаются важными вспомогательными средствами для непрерывной оценки сердечного ритма у младенцев, нуждающихся в реанимации »[2].
Электрическая активность без пульса
Изменение практики после рекомендации ILCOR по применению ЭКГ в первую очередь для определения ЧСС привело к нескольким сообщениям о случаях безимпульсной электрической активности в DR [35, 36]. Беспульсная электрическая активность определяется как наличие электрической активности без какой-либо связанной с ней механической активности [35, 36]. Аналогичные исследования на животных показали электрическую активность без пульса у ~ 50% новорожденных поросят, подвергшихся асфиксии [35, 37-39].Беспульсовая электрическая активность вызывается гипоксией, гипер- / гипокалиемией, гиповолемией, гипотермией, ионами водорода (ацидоз), напряженным пневмотораксом, тампонадой сердца, тромбозом (коронарного и легочного) и токсинами [40]. Эти отчеты вызывают опасения по поводу использования ЭКГ в ДР, и поэтому медицинские работники должны знать о потенциальных подводных камнях с ЭКГ во время реанимации новорожденных [35]. Недавняя серия случаев показала, что если ЧСС отображается на ЭКГ, но ребенок не реагирует, следует подозревать электрическую активность без пульса и начинать компрессионные сжатия грудной клетки [35].Мы предлагаем комбинировать аускультацию, пальпацию, пульсоксиметрию и ЭКГ у новорожденных с асфиксией, что может быть более надежным по сравнению с одной только ЭКГ или пульсоксиметрией [39, 41].
Респираторная поддержка
В первые 1-2 минуты после рождения ∼60 и 17% доношенных детей со спонтанным дыханием имеют ЧСС <100 и <60 / мин, соответственно [42]. Через 3 мин после рождения у 7% этих доношенных детей с самопроизвольным дыханием ЧСС по-прежнему составляет менее 100 / мин [42]. У доношенных детей со спонтанным дыханием потребовалось 1–10 вдохов до первого выдохшего CO 2 (ECO 2 ) и 21–258 с до пика CO 2 , что свидетельствует о полной аэрации легких [43, 44].Точно так же во время PPV уровни ECO 2 тесно связаны с объемами легких в конце раздувания, а ECO 2 впервые обнаруживается, когда аэрация ∼7% дистальных областей легких, а уровни ECO 2 повышаются на ∼30 с. до того, как ЧСС увеличилась> 100 / мин [45, 46].
Хотя эти данные предполагают, что увеличение ЧСС может быть отсрочено, несмотря на адекватную вентиляцию, в учебнике Программы реанимации новорожденных указано, что после начала PPV увеличение ЧСС должно наблюдаться в течение 15 секунд [47].Однако у новорожденных поросят с тяжелой брадикардией, асфиксией, ЧСС увеличивалась только у 50% поросят после 30 с адекватной ППЗ [48]. Saugstad et al. [49] сообщили, что HR у новорожденных с асфиксией составлял в среднем 93 (33) и 113 (30) через 60 и 90 секунд после рождения, соответственно. В другом исследовании Saugstad et al. [14] сообщили, что ЧСС составляла ≤100 / мин примерно у 2/3 и 1/6 новорожденных с депрессией через 1 и 3 минуты после рождения, соответственно. Более того, медленное или нулевое увеличение ЧСС в первые 3 минуты жизни, по-видимому, представляет плохой прогностический признак, давая 9-кратный риск смерти в течение недели [14].
Вентиляция с помощью маски
Текущие рекомендации по реанимации новорожденных рекомендуют вентиляцию с помощью маски с использованием соответствующей лицевой маски, подключенной к ручному вентиляционному устройству [1, 2]. Наиболее часто используемые устройства для обеспечения PPV в DR — это самонадувающийся мешок и реаниматор с тройником [50, 51]. Недавний систематический обзор включал 3 рандомизированных испытания и 1 обсервационное исследование и не сообщил о значительных различиях в выживаемости при выписке, утечке воздуха или краткосрочных и отдаленных исходах [52].Однако вентиляция через маску с реанимационным аппаратом с тройником может привести к меньшему количеству интубаций в DR и более высокому уровню выживаемости до выписки [52].
Во время вентиляции следует использовать начальное пиковое давление на вдохе (PIP) 30 см H 2 O у доношенных новорожденных [18, 19, 53]. Однако оптимальное давление, время надувания и поток газа, необходимые для установления эффективной функциональной остаточной емкости у новорожденных с депрессией, неизвестны. Доусон и др. [50] сообщили, что PIP не является показателем доставки дыхательного объема и что PIP необходимо корректировать во время реанимации, поскольку податливость и сопротивление легких быстро меняются.Однако быстрое увеличение ЧСС выше 100 / мин может быть важным признаком адекватного дыхательного объема, создаваемого выбранным PIP во время реанимации.
2-точечная верхняя фиксация и фиксация обода OK (большой и указательный пальцы образуют С-образную форму) являются наиболее подходящими методами для размещения и удержания лицевой маски и минимизации утечки маски во время PPV [54]. Однако в нескольких исследованиях DR сообщалось, что утечка маски и обструкция дыхательных путей являются обычным явлением во время PPV из мешка и маски, особенно у недоношенных детей [55, 56].Утечка маски и закупорка часто остаются нераспознанными и могут задерживать аэрацию легких, следовательно, эффективный газообмен и повышение ЧСС. В недавнем метаанализе, сравнивающем лицевую маску с назальными канюлями для неинвазивной PPV в DR, было сообщено о незначительном снижении риска компрессионных сжатий грудной клетки (3 исследования, ОР 0,37, 95% ДИ: 0,10–1,33, p = 0,13, I 2 = 28%) и незначительное снижение частоты интубации DR (5 исследований, ОР 0,63, 95% ДИ: 0,39–1,02, p = 0.06, I 2 = 52%) при использовании назальных канюль, предлагая рассмотреть возможность использования назальных канюль в качестве альтернативы лицевой маске PPV [57].
Внутриутробная гипоксия подавляет дыхательные движения плода и вызывает апноэ и закрытие голосовой щели (= обструкцию дыхательных путей) после рождения [58]. У недоношенных кроликов Crawshaw et al. [58] сообщили, что голосовая щель открывается только во время спонтанных дыхательных движений, в то время как она остается закрытой во время апноэ, что может привести к неэффективной PPV [59].Закрытие голосовой щели также может присутствовать у доношенных детей; однако это еще не исследовано.
MR. SOPA
Текущие рекомендации по неонатальной реанимации рекомендуют лицевую маску в сочетании с устройством ручной вентиляции для обеспечения респираторной поддержки после рождения [18, 19]. Плотное уплотнение между маской и лицом и правильное расположение верхних дыхательных путей ребенка важны для эффективной вентиляции маски. Когда младенцы не реагируют на начальные инфляции, программа реанимации новорожденных (NRP, Хьюстон, Техас, США) и группа поддержки жизни новорожденных (NLS, Великобритания) предлагают структурированный подход к эскалации помощи.МИСТЕР. Считается, что SOPA используется в качестве аббревиатуры для M (регулировка маски), R (перемещение дыхательных путей), S (всасывающий рот и нос), O (открытый рот), P (увеличение давления ) и A (альтернативный дыхательный путь) в качестве дыхательного пути ларингеальной маски (LMA) или эндотрахеальной трубки.
Устойчивая инфляция
Действующие европейские рекомендации по неонатальной реанимации рекомендуют 5 последовательных устойчивых инфляций в течение 2–3 секунд для начала PPV [19].Однако нет клинических доказательств того, что эти 5 начальных устойчивых инфляций будут поддерживать аэрацию легких. Исследования на ягнятах, перенесших внутриутробное удушье, показали, что однократное длительное надувание в течение 30 секунд улучшает скорость восстановления кровообращения, кровоток в сонной артерии и доставку кислорода в мозг, а дальнейшая сократимость сердца увеличивается быстрее по сравнению с PPV или 5 последовательными 3-секундными выдержками. инфляции [60, 61]. Однако экстравазация церебрального белка плазмы увеличивалась после однократного устойчивого надувания в течение 30 с, что указывает на большее нарушение гематоэнцефалического барьера, что может усугубить повреждение головного мозга у новорожденных с асфиксией [61].Эти данные предполагают, что одна 30-секундная продолжительная инфляция может улучшить аэрацию легких по сравнению с 5 последовательными 3-х секундными непрерывными инфляциями. В рекомендациях по реанимации новорожденных ILCOR от 2020 года указано, что для доношенных или поздних недоношенных детей, получающих PPV по поводу брадикардии или неэффективного дыхания при рождении, невозможно рекомендовать конкретную продолжительность начального инфляции из-за очень низкой достоверности оценок эффекта [1].
Ротоглоточные дыхательные пути
Ротоглоточные дыхательные пути предназначены для удержания языка от задней стенки глотки, обеспечивая, таким образом, свободный канал / дыхательные пути для вдыхаемых газов.Европейские рекомендации по реанимации новорожденных рекомендуют прохождение ротоглоточных дыхательных путей во время их структурированного подхода для эскалации помощи [19]. Камлин и др. [62] рандомизировали 137 младенцев гестационного возраста <34 недель, чтобы замаскировать PPV отдельно или в сочетании с ротоглоточными дыхательными путями соответствующего размера. В целом, затрудненная инфляция и частичная обструкция чаще наблюдались у младенцев, стабилизированных ротоглоточными дыхательными путями (81 против 64%, p = 0,03 и 70 против 54%, p = 0.04) соответственно [62]. В исследование были включены младенцы <34 недель беременности, что затрудняет перевод на доношенных детей. Однако медицинские работники должны знать, что дыхательные пути ротоглотки могут усилить обструкцию дыхательных путей во время вентиляции с помощью маски.
Ларингеальная маска Дыхательные пути
Текущие рекомендации по реанимации новорожденных рекомендуют LMA в качестве альтернативы интубации трахеи во время реанимации новорожденных на сроке беременности> 34 недель [18, 19]. В недавнем Кокрановском обзоре 794 новорожденных сообщается, что PPV с LMA приводит к меньшей потребности в эндотрахеальной интубации и более короткому времени вентиляции по сравнению с PPV с маской (ОР [95% ДИ]: 0.24 [0,12–0,47], I 2 = 34%, и средняя разница [95% ДИ]: –18,0 с [от –24,35 до –13,44 с], I 2 = 95%), соответственно [63]. Время введения или неправильная установка LMA или эндотрахеальной трубки были одинаковыми [63]. Текущие данные свидетельствуют о том, что LMA может быть адекватной альтернативой во время реанимации доношенного ребенка с тяжелой формой асфиксии. Pejovic et al. [64] сравнили LMA и лицевую маску во время реанимации новорожденных в условиях ограниченных ресурсов и продемонстрировали, что общее время вентиляции и среднее время до самостоятельного дыхания были короче у новорожденных, которые первоначально были реанимированы с помощью LMA.Было высказано предположение, что этот подход может быть очень полезным, особенно в условиях DR с реанимационными бригадами без адекватных навыков интубации трахеи и / или в условиях с низким и средним уровнем ресурсов [65]. Pejovic et al. [66] сообщили, что LMA безопасен в руках акушерок, но не превосходит лицевую маску в отношении ранней неонатальной смерти или умеренной и тяжелой гипоксически-ишемической энцефалопатии (HIE) (скорректированный анализ LMA vs маска для лица: ОР, 95% ДИ: 1,16 [0,90–1,51], p = 0.26) в условиях нехватки ресурсов.
Кислород
Кислород во время респираторной поддержки
Уже десять лет назад исследования показали, что доношенные младенцы, подвергшиеся реанимации с помощью комнатного воздуха, издавали свой первый крик раньше и быстрее достигли устойчивого состояния спонтанного дыхания по сравнению с теми, у кого была 100% кислородная реанимация [ 67, 68]. Vento et al. [69, 70] показали, что использование чистого кислорода для реанимации новорожденных увеличивает окислительный стресс и вызывает большее повреждение органов, включая сердце и почки, у новорожденных с тяжелой асфиксией.Для доношенных и недоношенных новорожденных текущие рекомендации по реанимации новорожденных рекомендуют исходный уровень 21% кислорода во время респираторной поддержки и 100% кислород в начале компрессии грудной клетки [18, 19, 71, 72]. Затем необходимо титровать дополнительный кислород в соответствии с целевыми показателями предуктального насыщения кислородом [18, 19, 72]. Систематический обзор и метаанализ, включающий 5 квазирандомизированных контролируемых испытаний и 1302 новорожденных (средний срок беременности 38 недель и большинство из них умеренно асфиксированы), показали, что исходы: время до первого вдоха> 3, 5-минутный балл по шкале Апгар <7 и выживаемость были лучше для тех, кого реанимировали комнатным воздухом, а не 100% кислородом [73].Кроме того, можно было бы предотвратить 1 смерть на каждые 20 новорожденных, которых реанимировали воздухом, а не 100% кислородом [73]. Следовательно, комнатный воздух вместо реанимации чистым кислородом может предотвратить 200 000 смертей, в дополнение к 300 000 свежих мертворожденных (из примерно 1 миллиона), которых можно спасти с помощью вентиляции комнатным воздухом [74].
Сжатия грудной клетки
Текущие рекомендации по реанимации новорожденных гласят, что если ЧСС остается <60 / мин, несмотря на адекватную вентиляцию, следует начать компрессию грудной клетки [19, 29].Компрессия грудной клетки должна производиться с использованием (i) скоординированного соотношения компрессия: вентиляция 3: 1 (C: V), (ii) нижней трети грудины, (iii) глубины ∼1 / 3 переднезаднего диаметр грудной клетки, (iv) использование техники охвата двумя пальцами, и (v) обеспечение полного расслабления отдачи грудной клетки. Однако эти рекомендации основаны на экстраполяциях математического моделирования, данных на животных, а также исследований у детей и взрослых, так как данных о новорожденных людях недостаточно.
Сжатие грудной клетки: коэффициент вентиляции
Обоснования для использования 3: 1 C: V включают (i) более высокую физиологическую ЧСС 120–160 / мин и (ii) частоту дыхания 40–60 / мин у новорожденных по сравнению со взрослыми .В нескольких исследованиях сравнивали различные соотношения C: V (2: 1, 3: 1, 4: 1, 9: 3 и 15: 2) у новорожденных поросят, подвергшихся асфиксии, и показывали, что время восстановления спонтанного кровообращения (ROSC) было одинаковым, независимо от Соотношение C: V [75-77]. Schmölzer et al. [78] исследовали подход к компрессии грудной клетки с несинхронизированной вентиляцией и сообщили, что дыхательный объем, время до ROSC, выживаемость и восстановление гемодинамики были аналогичны 3: 1 C: V у асфиксированных новорожденных поросят.
Частота сжатия грудной клетки
Математическая модель предполагает, что частота сжатия грудной клетки должна составлять 180 в минуту для доношенных детей [79].Однако это может оказаться невозможным из-за методических ограничений и повышенной утомляемости спасателей при более высокой степени сжатия грудной клетки. Кроме того, в исследованиях на животных сравнивали различные степени сжатия грудной клетки и не сообщали об отсутствии разницы во времени до восстановления спонтанного восстановления сердца или выживаемости [80, 81]. Ни разные скорости сжатия грудной клетки, наложенные на устойчивое инфляция (90 против 120 в минуту), ни разные скорости сжатия грудной клетки при асинхронизированной вентиляции (90, 100 и 120 в минуту) не показали преимущества в отношении времени восстановления спонтанного кровообращения и выживаемости у новорожденных поросят, подвергшихся асфиксии. , хотя маркеры гемодинамического восстановления, церебрального воспалительного процесса и повреждения головного мозга улучшились во время компрессии грудной клетки с асинхронной вентиляцией со скоростью 120 / мин по сравнению с 90 или 100 / мин [80, 81].
Глубина компрессии грудной клетки
Рекомендации относительно глубины компрессии грудной клетки основаны на экстраполяции компьютерной томографии у 54 новорожденных, которая показала, что 1/3 переднезадней глубины приведет к большей фракции выброса по сравнению с 1/4 или 1 / 2 Глубина AP [82]. Основная трудность для реаниматологов — невозможность оценить глубину компрессии грудной клетки при компрессии грудной клетки. Слишком малый передне-задний диаметр может привести к неадекватному сердечному выбросу, а слишком большой передне-задний диаметр может вызвать чрезмерную компрессию, что приведет к переломам ребер, ушибу сердца и травмам грудной клетки.
Техника сжатия грудной клетки
Несколько исследований манекена продемонстрировали, что техника окружения двумя пальцами обеспечивает (i) более высокую долю правильного расположения пальцев / больших пальцев, (ii) большую среднюю (SD) глубину (27,2 [5,7] по сравнению с 22,1 [4,6] мм; p = 0,0008), и (iii) меньшая вариабельность средней (SD) глубины (6,7 [3,2]% против 9,0 [2,8]%; p = 0,002) по сравнению с техникой с двумя пальцами. при компрессии грудной клетки [83, 84]. Было проведено одно исследование на животных, в котором сравнивали технику двумя пальцами и двумя пальцами в 9.4 (SD 0,8) кг новорожденных свиней, у которых были зарегистрированы значительно более высокие систолическое, диастолическое и среднее артериальное давление, а также давление коронарной перфузии [85]. Совсем недавно в исследованиях манекена были описаны более новые методы позиционирования больших пальцев и пальцев во время сжатия грудной клетки; однако срочно необходимы дальнейшие исследования по изучению оптимального положения больших пальцев и пальцев во время сжатия грудной клетки для улучшения краткосрочных и долгосрочных результатов у новорожденных.
Кислород во время сжатия грудной клетки
Текущие рекомендации по реанимации новорожденных рекомендуют увеличивать кислород до 100%, когда начинается сжатие грудной клетки [18]; однако оптимальная / наиболее эффективная концентрация кислорода во время компрессии грудной клетки остается неизвестной / спорной.Хотя данных на людях нет, исследования на животных показали, что 21% O 2 приводит к незначительному изменению времени восстановления спазмов, выживаемости и неврологических исходов по сравнению со 100% O 2 [18]. Недавний метаанализ исследований на животных показал, что объединенный анализ не показал значительных различий в уровне смертности животных, реанимированных воздухом, по сравнению со 100% O 2 (отношение рисков 1,04 [0,35, 3,08], I 2 = 0 %, р = 0,94) [86]. ROSC также был сходным между группами со средней разницей -3.8 (от -29,7 до 22) с, I 2 = 0%, p = 0,77 [86]. Совсем недавно в двух дальнейших исследованиях сравнивали 21% со 100% O 2 с использованием модели неонатального поросенка с асфиксией. Не было обнаружено различий во времени до ROSC, выживаемости, окислительного стресса и маркеров воспаления [87, 88]. Хотя эти исследования показывают, что 21% не отличается от 100% O 2 , о клинических исследованиях не сообщалось и они срочно необходимы.
Сжатие грудной клетки во время продолжительной инфляции
Альтернативный метод компрессии грудной клетки — это компрессия грудной клетки, накладываемая во время продолжительной инфляции (CC + SI), которая (i) сокращает время до ROSC и (ii) улучшает выживаемость, (iii) улучшает гемодинамику (сонная артерия) кровоток и кровоток в легочной артерии) и (iv) приводили к пассивной вентиляции во время сжатия грудной клетки и, таким образом, к увеличению минутной вентиляции по сравнению с соотношением C: V 3: 1 у новорожденных поросят, подвергшихся асфиксии [89].В небольшом пилотном исследовании на людях у недоношенных новорожденных <32 недель время восстановления СК было значительно короче в группе CC + SI по сравнению с группой 3: 1 C: V со средним значением (SD) 31 (9) против 138 (72) с [90]. В настоящее время в исследовании SURV1VE сравнивается, улучшают ли CC + SI с 3: 1 C: V краткосрочные и долгосрочные исходы у недоношенных детей> 28 недель и у доношенных новорожденных (ClinicalTrials.Gov Trial NCT02858583) [91].
Сосудистый доступ
Текущие руководства по реанимации новорожденных рекомендуют как можно скорее установить внутривенный доступ для введения адреналина (адреналина), жидкости или крови, если это необходимо [18, 19, 29].Чаще всего вводят пупочный венозный катетер размером ~ 5 см в пупочную вену [18, 19, 29]. Эта процедура может занять несколько минут, особенно если оборудование не подготовлено или выполнено неопытным врачом [92, 93]. В качестве альтернативы может быть установлен периферический внутривенный доступ или внутрикостной (IO) доступ [1, 19, 94, 95]. Исследования с использованием моделирования показали, что введение интраокулярного катетера происходило быстрее, чем катетера в пупочную вену [96]. Введение иглы в (большеберцовую) кость позволяет быстро вводить лекарство в систему кровеносных сосудов IO даже во время нарушения кровообращения и шока.Исследования на трупах показали, что положение иглы IO (т.е. плечевая и проксимальная большеберцовая кость) возможно как с полуавтоматической дрелью с батарейным питанием, так и с иглами, вводимыми вручную [97, 98]. В недавнем систематическом обзоре были выявлены обсервационные и имитационные исследования, но не рандомизированные испытания [96]. В общей сложности 46 инъекционных игл введено 41 новорожденному (в основном в проксимальный отдел большеберцовой кости) с частотой осложнений 13–31% (например, неправильное расположение игл, смещение игл, экстравазация, местная инфекция, остеомиелит, перелом, синдром компартмента, конечность ишемия, жировая или воздушная эмболия) [96].Совсем недавно Mileder et al. [99] сообщили о 12 дополнительных случаях введения иглы IO с использованием дрели с батарейным питанием у новорожденных с 50% успешностью первой и второй попытки. О долгосрочных осложнениях не сообщалось; тем не менее, незначительные краткосрочные осложнения (например, паравазация и местная инфекция мягких тканей) наблюдались в 33% успешных вставок интраокулярного вмешательства [99]. В рекомендациях ILCOR по неонатальной реанимации 2020 года указано, что если доступ к пупочной вене невозможен, внутривенный выход является разумной альтернативой сосудистому доступу во время реанимации новорожденных.Однако подчеркиваются побочные эффекты, включая переломы большеберцовой кости и экстравазацию жидкости и лекарств, приводящие к компартмент-синдрому и ампутации [1].
Совсем недавно была описана прямая пункция пупочной вены через желе Уортона с использованием канюли 24-го размера в качестве альтернативного метода введения лекарств [100]. Была описана серия из 10 случаев ( n = 4 адреналина во время СЛР и n = 6 премедикаций при интубации), и вся процедура от пункции до введения лекарства заняла 15–20 секунд.Данных недостаточно, и срочно необходимы клинические испытания.
Адреналин (Адреналин)
Текущие рекомендации по реанимации новорожденных рекомендуют вводить адреналин внутривенно в дозе 0,01–0,03 мг / кг в соотношении 1: 10 000 [1]. В качестве альтернативы можно рассмотреть возможность эндотрахеального введения в дозе 0,05–0,1 мг / кг, пока установлен внутривенный доступ [29]. Адреналин действует на α- и β-рецепторы, приводя к (i) увеличению перфузионного давления коронарной артерии за счет периферической вазоконстрикции, (ii) улучшению кровотока к миокарду и (iii) восстановлению истощенных энергетических субстратов, таким образом улучшая сократимость и жизнеспособность миокарда.Однако адреналин также увеличивает потребность миокарда в кислороде и респираторный и метаболический ацидоз, что часто встречается при асфиксии новорожденных [101]. Недавний систематический обзор включал 117 доношенных и недоношенных новорожденных, получавших адреналин в DR, и сообщил об аналогичных исходах в отношении смерти при выписке из больницы (ОР [95% ДИ] 1,03 [0,62–1,71]) или неспособности достичь ROSC, времени до ROSC или пропорции. дополнительный прием адреналина между внутривенным и эндотрахеальным адреналином [102]. Эти данные свидетельствуют о том, что эндотрахеальный и внутривенный адреналин приводят к аналогичной выживаемости и другим результатам.Однако в исследованиях на животных исследователи продолжают предполагать пользу внутривенного введения с использованием рекомендуемых в настоящее время доз. Срочно необходимы клинические испытания на людях.
Нетедные младенцы и околоплодные воды, окрашенные меконием
Околоплодные воды, окрашенные меконием, встречаются почти в 15% родов, 10–20% этих младенцев рождаются нетвердыми [103, 104], а 5–10% этих младенцев разовьется синдром аспирации мекония (MAS) [105, 106]. В 2015 г. рекомендации по реанимации новорожденных изменили свою рекомендацию, сделав упор не на обычную аспирацию у младенцев, не имеющих достаточного количества околоплодных вод, окрашенных меконием [71].В нескольких исследованиях сравнивали результаты до и после изменения рекомендаций и сообщали о меньшем количестве госпитализаций новорожденных в отделения интенсивной терапии, меньшем количестве младенцев, получающих аспирацию из трахеи, и об отсутствии увеличения тяжести MAS или тяжелого респираторного дистресса или других важных неонатальных исходов [107-109]. Примечательно, что Kalra et al. [108] сообщили о подобной распространенности ГИЭ и пневмоторакса, в то время как Edwards et al. [107] сообщили о повышении заболеваемости. Хотя Чируволу и соавт. [103] сообщили, что значительно более высокая доля неторопливых младенцев с околоплодными водами, окрашенными меконием, была госпитализирована с респираторным дистресс-синдромом и респираторной поддержкой.
Недавний метаанализ включал 581 неторопливый младенец с околоплодными водами, окрашенными меконием, и не сообщил об отсутствии различий в неонатальной смертности, частоте MAS и HIE, необходимости в вмешательствах DR, респираторной поддержке или пребывании в больнице между отсасыванием ниже голосовой связки и отсутствием отсасывания. [110, 111]. Эти данные предполагают, что нет четких доказательств преимуществ начальной эндотрахеальной интубации и аспирации трахеи в околоплодных водах, окрашенных меконием; однако, если имеется обструкция дыхательных путей из-за густой вязкости, отсасывание мекония часто является клиническим решением [17].
Управление температурой
Текущие рекомендации по неонатальной реанимации рекомендуют поддерживать температуру тела новорожденных без асфиксии между 36,5 и 37,5 ° C после родов путем госпитализации и стабилизации [19, 29, 72]. У младенцев с ГИЭ терапевтическую гипотермию следует начинать в течение первых 6 часов после рождения [112]. Как активное, так и пассивное охлаждение возможно и безопасно для достижения целевой температуры тела 33–34 ° C у доношенных новорожденных, рожденных от удушья, сроком гестации более 36 недель [113].У новорожденных, страдающих асфиксией, нарушена терморегуляция из-за снижения потребления кислорода и выработки энергии, большой площади поверхности, влажной и тонкой кожи, и они теряют температуру быстрее, чем дети, не страдающие асфиксией. Младенцы с потенциально более высокой степенью повреждения головного мозга быстрее остывают, так как их естественные защитные механизмы подавлены [114, 115]. Более раннее начало охлаждения может предотвратить ухудшение травмы мозговой ткани; поэтому пассивное охлаждение следует начинать после начальной стабилизации или во время транспортировки новорожденного [116].Пассивное охлаждение является хорошей альтернативой как можно раньше, особенно в общественных больницах или отдаленных / сельских районах. В нескольких исследованиях сообщалось, что младенцы, пассивно охлаждаемые во время транспортировки, достигают целевой температуры значительно быстрее по сравнению с младенцами, которые не охлаждались пассивно [117, 118]. Однако пассивное охлаждение во время транспортировки приводило к переохлаждению ~ 1/3 младенцев, особенно у младенцев с в основном тяжелым ГИЭ [118, 119]. Переохлаждения можно избежать, используя серворегулируемое охлаждающее устройство (охлаждающее одеяло и ректальный / пищеводный датчик температуры) во время транспортировки новорожденного.Рандомизированное контролируемое исследование показало, что среднее время достижения целевой температуры с использованием серворегулируемого охлаждающего устройства по сравнению с пассивным и / или активным (лед или гелевые пакеты) охлаждением составляло 44 мин [120]. Таким образом, если серворегулируемое охлаждение будет инициировано вскоре после прибытия транспортной бригады в родильную больницу, многие младенцы достигнут заданной температуры перед отъездом из роддома [120]. Однако нет ни доказательств, ни четких рекомендаций, как обрабатывать температуру тела новорожденных с асфиксией и подозрением на ГИЭ во время реанимации новорожденных.В рекомендациях по реанимации новорожденных ILCOR 2020 г. предлагается, чтобы лечение соответствовало протоколам, используемым в рандомизированных клинических исследованиях [1]. Это включает активное охлаждение с помощью пакетов со льдом [121]; однако следует соблюдать осторожность при использовании этого подхода, поскольку он увеличивает риск переохлаждения.
Реанимация новорожденных в средах с ограниченными ресурсами и средах с избытком ресурсов
Из примерно 2,6 миллиона новорожденных, умирающих ежегодно, 98% происходят в условиях ограниченных ресурсов, а 50–70% неонатальных смертей происходят в первый день после рождения [122].Неонатальная смертность примерно в 50–55 раз выше в странах с низким и средним уровнем доходов по сравнению со странами с высоким уровнем доходов из-за состояния здоровья матери (т. Е. Состояния питания и инфекционного статуса), ограниченных ресурсов и отсутствия квалифицированных акушерок или неспособности обеспечить адекватные условия жизни. базовая реанимация новорожденных при рождении [123, 124].
Асфиксия при рождении определяется по-разному в средах с ограниченными и избыточными ресурсами [125]. Однако в условиях ограниченных ресурсов это обычно определяется как неспособность инициировать или поддерживать самостоятельное дыхание при рождении и в некоторых обстоятельствах включает 1-минутную оценку по шкале Апгар <7; в средах, богатых ресурсами, это биохимическое определение (pH <7.00 и дефицит оснований ≤ −12 ммоль / л), связанный с нарушением газообмена (приводящим к органной недостаточности, включая ГИЭ), из-за прерывания плацентарного кровотока, с прогрессирующей гипоксемией, гиперкапнией и ацидозом при анализе пуповинной артериальной крови после родов новорожденный [125, 126].
Для улучшения результатов новорожденных, рожденных в условиях ограниченных ресурсов, Целевая группа по глобальному внедрению Американской академии педиатрии совместно с другими партнерами разработала тренинг «Помощь младенцам дышать» в 2010 году, метод обучения на основе моделирования, предназначенный для обучения поставщики медицинских услуг в условиях ограниченных ресурсов в области реанимации и ухода за новорожденными [127].Внедрение этого метода обучения и реанимации является простым и недорогим вмешательством, которое снижает количество мертворождений, связанных с родами, и раннюю неонатальную смертность [127]. Этот систематический обзор продемонстрировал умеренные доказательства снижения частоты мертворождения в родах и однодневной неонатальной смертности после внедрения метода обучения и реанимации «Помогаем младенцам дышать» [127]. В таблице 2 представлен обзор различий рекомендаций по реанимации новорожденных в условиях ограниченных и избыточных ресурсов.
Таблица 2.
Неонатальная реанимация доношенных новорожденных с асфиксией в условиях ограниченных ресурсов по сравнению с избыточными ресурсами
Прекращение реанимации
В текущих рекомендациях по реанимации новорожденных [1] указывается, что разумные временные рамки, которые следует рассмотреть, прежде чем прекратить реанимацию, «приблизительны. 20 мин после рождения. Недавно Целевая группа по поддержке жизни новорожденных сообщила, что 40% младенцев с постоянной потребностью в СЛР через 10 минут после рождения выжили, а 11% выжили без умеренных или тяжелых нарушений [128].Однако все включенные исследования имели высокий риск систематической ошибки, учитывая контекстуальные факторы, такие как гестационный возраст, наличие врожденных аномалий или адекватность проведенных реанимационных вмешательств. Эти данные предполагают, что единый временной интервал или продолжительность СЛР после рождения неприменим [128]. Последние рекомендации, предлагающие прекратить реанимацию «примерно через 20 минут после рождения», являются хорошим подходом для пациента, родителей и медицинских работников [1, 41].
Заключение
Лечение ЛР необходимо постоянно оценивать, исследовать и обучать, чтобы улучшить реанимацию новорожденных с асфиксией.Текущие рекомендации по реанимации новорожденных часто ориентированы на недоношенных детей, не рекомендуя различные подходы для доношенных детей, родившихся после асфиксии. Следовательно, необходимо предпринять серьезные усилия для проведения высококачественных исследований в DR для дальнейшего улучшения неонатальной реанимации и улучшения результатов для одной из самых тяжелых групп новорожденных.
Благодарность
Статья сопровождается лекцией «Ведение доношенных детей с асфиксией», которая проводилась в виде вебинара для UENPS (Союза европейских неонатальных и перинатальных обществ) https: // vimeo.com / 423212885 / d
306b.Заявление о конфликте интересов
Авторы не заявляют о конфликте интересов.
Источники финансирования
Авторы не получали финансирования.
Вклад авторов
Концепция и дизайн: M.B., G.L., O.D.S. и G.M.S. Анализ и интерпретация данных: M.B., G.L., O.D.S. и G.M.S. Составление статьи: M.B., G.L., O.D.S. и G.M.S. Критическая доработка статьи на предмет важного интеллектуального содержания: М.Б., Г.Л., О.Д.С. и Г.М.С. Окончательное утверждение статьи: M.B., G.L., O.D.S. и G.M.S.
Список литературы
- Wyckoff MH, Wyllie J, Aziz K, de Almeida MF, Fabres JW, Fawke J, et al. Неонатальная поддержка жизни 2020 Международный консенсус по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи с рекомендациями по лечению.Реанимация. 2020 ноя; 156 (16 приложение 2): A156–87.
- Азиз К., Ли ХК, Эскобедо МБ, Гувер А.В., Камат-Рейн Б.Д., Кападиа В.С. и др. Часть 5: Реанимация новорожденных: Рекомендации Американской кардиологической ассоциации 2020 по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи. Тираж.2020 окт.2020; 142 (16_Suppl l_2): S524–50.
- Barber CA, Wyckoff MH. Использование и эффективность эндотрахеального введения по сравнению с внутривенным адреналином во время сердечно-легочной реанимации новорожденных в родильном зале. Педиатрия. 2006, 1 сентября; 118 (3): 1028–34.
- Харрингтон DJ, Редман CW, Моулден М., Гринвуд CE.Долгосрочный результат у выживших младенцев с нулевым показателем Апгар через 10 минут: систематический обзор литературы и когорты на базе больницы. Am J Obstet Gynecol. 2007 Май, 196 (5): 463–5.
- Шах П.С., Шах П., Тай KFY. Сдавливание грудной клетки и / или адреналин при рождении для недоношенных детей гестационного возраста <32 недель: согласованное когортное исследование исходов новорожденных.J Perinatol. 2009 25 октября; 29 (10): 693–7.
- Сораишам А.С., Лодха А.К., Сингхал Н., Азиз К., Ян Дж., Ли С.К. и др. Неонатальные исходы после обширной сердечно-легочной реанимации в родильном зале для младенцев, родившихся на сроке гестации менее 33 недель. Реанимация. 2014 февраль; 85 (2): 238–43.
- Мартин Р.Дж., Фанаров А.А., Уолш М.С. Неонатально-перинатальная медицина Фанарова и Мартина: болезни плода и младенца. 10-е изд. Филадельфия, Пенсильвания: Elsevier Health Sciences; 2014 г.
- Мир И.Н., Джонсон-Велч С.Ф., Нельсон Д.Б., Браун Л.С., Розенфельд С.Р., Чалак Л.Ф.Патология плаценты связана с тяжестью неонатальной энцефалопатии и неблагоприятными исходами развития после гипотермии. Am J Obstet Gynecol. 2015 декабрь; 213 (6): 849–7.
- Rainaldi MA, Perlman JM. Патофизиология асфиксии при рождении. Clin Perinatol. 2016 сентябрь; 43 (3): 409–22.
- Эррера, Калифорния, Серебро, РМ. Перинатальная асфиксия с акушерской точки зрения: диагностика и вмешательства. Clin Perinatol. 2016; 43 (3): 423–38.
- Рани С., Чавла Д., Хурия А., Джайн С.Факторы риска перинатальной смертности из-за асфиксии среди специалистов по неотложной акушерской помощи в больнице третичного уровня. Indian Pediatr. 2012; 49 (3): 191–4.
- Химмельманн К., Ахлин К., Якобссон Б., Банки С., Торсен П. Факторы риска церебрального паралича у доношенных детей. Acta Obstet Gynecol Scand.2011; 90 (10): 1070–81.
- Маршалл С., Ланг А.М., Перес М., Саугстад ОД. Обработка новорожденных в родильных отделениях. J Perinat Med. 2019 декабря 18; 48 (1): 1–10.
- Саугстад О.Д., Рамджи С., Рутвельт Т., Венто М.Ответ на реанимацию новорожденного: ранние прогностические переменные. Acta Paediatr. 2005. 94 (7): 890–5.
- Всемирная организация здравоохранения. Доклад о состоянии здравоохранения в мире, 1995 г .: устранение пробелов. Женева, Швейцария: Всемирная организация здравоохранения; 1995 г.
- Руководство 2000 г. по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи.Часть 11: реанимация новорожденных. Американская кардиологическая ассоциация в сотрудничестве с Международным комитетом по связи по реанимации. Тираж. 2000; 102 (8 доп.): I-343-57.
- Saugstad OD. Ведение родильного отделения доношенных и недоношенных новорожденных. Неонатология.2015 5 июня; 107 (4): 365–71.
- Перлман Дж. М., Вилли Дж., Каттвинкель Дж., Вайкофф М. Х., Азиз К., Гинзбург Р. и др. Часть 7: неонатальная реанимация: международный консенсус 2015 года в области сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи с рекомендациями по лечению.Реанимация. 2015; 95: e169–1.
- Мадар Дж., Роер С.К., Эйнсворт С., Эрсдал Х., Морли С., Рюдигер М. и др. Рекомендации Европейского совета по реанимации 2021: реанимация новорожденных и поддержка перехода новорожденных при рождении. Реанимация. 2021 апр; 161: 291–326.
- Polglase GR, Blank DA, Barton SK, Miller SL, Stojanovska V, Kluckow M, et al.Пережимание пуповины, основанное на физиологии, стабилизирует сердечный выброс и снижает цереброваскулярное повреждение у ягнят, подвергшихся асфиксии в краткосрочной перспективе. Arch Dis Child Fetal Neonatal Ed. 2018 ноя; 103 (6): F530–8.
- Гомерсалл Дж., Бербер С., Миддлтон П., Макдональд С. Дж., Нирмейер С., Эль-Наггар В. и др. Ведение пуповины при доношенных и поздних преждевременных родах: метаанализ.Педиатрия. 2021 25 марта; 147 (3): e2020015404.
- Padilla-Sánchez C, Baixauli-Alacreu S, Cañada-Martínez AJ, Solaz-García Á, Alemany-Anchel MJ, Vento M. Отсроченное или немедленное пережатие пуповины изменяет насыщение кислородом и структуру сердечного ритма в первые минуты после рождения. J Pediatr.2020 декабрь; 227: 149–56.e1.
- Erickson-Owens DA, Mercer JS, Oh W. Доение пуповины доношенных детей, рожденных путем кесарева сечения: рандомизированное контролируемое испытание. J Perinatol. 2012, 17 августа; 32 (8): 580–4.
- Катерия А., Мерсер Дж., Браун М., Рич В., Бейкер К., Харберт М. и др.Доение пуповины при рождении у доношенных новорожденных с ацидозом: исходы новорожденных. J Perinatol. 2018 12 марта; 38 (3): 240–4.
- Гириш М., Джайн В., Дхокане Р., Гондхали С.Б., Вайдья А., Агай Ж. Доение пуповины для новорожденных с депрессией при рождении: рандомизированное испытание осуществимости.J Perinatol. 2018; 38 (9): 1190–6.
- Bhatt S, Alison BJ, Wallace EM, Crossley KJ, Gill AW, Kluckow M, et al. Отсрочка пережатия пуповины до начала вентиляции улучшает сердечно-сосудистую функцию у недоношенных ягнят при рождении. J Physiol. 2013 Апрель; 591 (8): 2113–26.
- Бхатт С., Полглас Г.Р., Уоллес Э.М., Те Пас А.Б., Хупер С.Б.Вентиляция перед пережатием пуповины улучшает физиологический переход при рождении. Фронт Педиатр. 2014 20 октября; 2: 113.
- Андерссон О., Рана Н., Эвальд Ю., Малквист М., Стриппл Г., Баснет О. и др. Реанимация интактного пуповины в сравнении с ранним пережатием пуповины при лечении новорожденных с депрессией в течение первых 10 минут после рождения (Непкорд III): рандомизированное клиническое испытание.Matern Heal Neonatol Perinatol. 2019; 5 (1): 1–11.
- Wyckoff MH, Aziz K, Escobedo MB, Kapadia VS, Kattwinkel J, Perlman JM, et al. Часть 13: неонатальная реанимация: обновленные рекомендации Американской кардиологической ассоциации 2015 г. по сердечно-легочной реанимации и неотложной сердечно-сосудистой помощи.Тираж. 2015; 132 (18): S543–60.
- О’Доннелл КПФ, Камлин КОФ, Дэвис П.Г., Карлин Дж.Б., Морли С.Дж. Вариабельность 5-минутной оценки по шкале Апгар между наблюдателями. J Pediatr. 2006 Октябрь; 149 (4): 486–9.
- Камлин COF, O’Donnell CPF, Эверест, штат Нью-Джерси, Дэвис П.Г., Морли С.Дж.Точность клинической оценки пульса младенца в родильном зале. Реанимация. 2006 декабрь; 71 (3): 319–21.
- Hawkes G, Hawkes C, Kenosi M, Demeulemeester J, Livingstone V, Ryan C и др. Аускультация, пальпация и постукивание: время для повторной оценки. Acta Paediatr. 2016 Февраль; 105 (2): 178–82.
- Kamlin CO, Dawson JA, O’Donnell CP, Morley CJ, Donath SM, Sekhon J, et al. Точность пульсоксиметрического измерения пульса новорожденных в родильном зале. J Pediatr. Июнь 2008 г .; 152 (6): 756–60.
- Saugstad OD, Soll RF.Оценка частоты сердечных сокращений при рождении: аускультация по-прежнему является золотым стандартом. Неонатология. 2016; 110 (3): 238–40.
- Луонг Д., Чунг П. Я., Баррингтон К. Дж., Дэвис П. Г., Унрау Дж., Дакшинамурти С. и др. Остановка сердца с безимпульсным ритмом электрической активности у новорожденных: серия случаев.Arch Dis Child Fetal Neonatal Ed. 2019; 104 (6): F572–4.
- Силлерс Л., Хэндли С.К., Джеймс Дж. Р., Фолья Э. Импульсная электрическая активность, затрудняющая реанимацию новорожденных. Неонатология. 2019; 115 (2): 95–8.
- Солевог А.Л., Луонг Д., Ли Т.Ф., О’Рейли М., Чунг П.Й., Шмёльцер Г.М.Отсутствие перфузии сердечного ритма у новорожденных поросят, рожденных от удушья. PLoS One. 2019; 14 (4): e0214506–10.
- Луонг Д.Х., Чунг П.-Й, О’Рейли М., Ли Т.Ф., Шмольцер Г.М. Электрокардиография против аускультации для оценки частоты сердечных сокращений во время остановки сердца с электрической активностью без пульса у новорожденных.Фронт Педиатр. 2018 27 ноября; 6: 366–4.
- Patel S, Cheung PY, Solevåg AL, Barrington KJ, Kamlin COF, Davis PG, et al. Беспульсная электрическая активность: неправильно диагностированный объект во время асфиксии у новорожденных? Arch Dis Child Fetal Neonatal Ed. 2019; 104 (2): F215–7.
- Myerburg RJ, Halperin H, Egan DA, Boineau R, Chugh SS, Gillis AM и др.Импульсная электрическая активность: определение, причины, механизмы, управление и приоритеты исследований на следующее десятилетие: отчет семинара Национального института сердца, легких и крови. Тираж. 2013 декабрь; 128 (23): 2532–41.
- Саугстад О.Д., Робертсон Нью-Джерси, Венто М. Критический обзор рекомендаций Международного комитета по связям по реанимации 2020 года по реанимации новорожденного.Acta Paediatr. 2021, 20 апреля; 110 (4): 1107–12.
- Доусон Дж. А., Камлин КОФ, Вонг С., Те Пас А. Б., Венто М., Коул Т. Дж. И др. Изменения ЧСС в первые минуты после рождения. Arch Dis Child Fetal Neonatal Ed. 2010; 95 (3): F177.
- Шмёльцер GM, Хупер С.Б., Вонг К., Камлин КОФ, Дэвис П.Г.Выдыхаемый углекислый газ у здоровых доношенных детей сразу после рождения. J Pediatr. 2015; 166 (4): 844–3.
- Blank DA, Gaertner VD, Kamlin COF, Nyland K, Eckard NO, Dawson JA, et al. Респираторные изменения у доношенных новорожденных сразу после рождения. Реанимация. 2018 сентябрь; 130: 105–10.
- Hooper SB, Fouras A, Siew ML, Wallace MJ, Kitchen MJ, te Pas AB, et al. Уровни выдыхаемого CO2 указывают на степень аэрации легких при рождении. PLoS One. 12 августа 2013 г .; 8 (8): e70895.8
- Nicoll J, Cheung PY, Aziz K, Rajani V, O’Reilly M, Pichler G и др.Выдыхаемый углекислый газ и неонатальные модели дыхания у недоношенных детей после рождения. J Pediatr. 2015; 167 (4): 829–33.e1.
- Американская академия педиатрии и Американская кардиологическая ассоциация. Учебник реанимации новорожденных. 7-е изд. AAP / AHA; 2016 г.
- Эспиноза М.Л., Чунг П.Й., Ли Т.Ф., О’Рейли М., Шмёльцер Г.М.Изменения частоты сердечных сокращений во время вентиляции с положительным давлением после брадикардии, вызванной асфиксией, в модели реанимации новорожденных на свиньях. Arch Dis Child Fetal Neonatal Ed. 2019 Янв; 104 (1): F98–101.
- Saugstad OD, Rootwelt T, Aalen O. Реанимация новорожденных с асфиксией воздухом или кислородом помещения: международное контролируемое исследование: исследование Resair 2.Педиатрия. 1998; 102 (1): e1.
- Доусон Дж. А., Шмёльцер Г. М., Камлин КО, Те Пас А. Б., О’Доннелл С. П., Донат С. М. и др. Оксигенация с Т-образным переходником по сравнению с самонадувающимся мешком для вентиляции крайне недоношенных новорожденных при рождении: рандомизированное контролируемое исследование. J Pediatr. 2011 июнь; 158 (6): 912–8.е1—2.
- Шильд Э., Агилар А., Мусанте Г.А., Вайн Н., Прудент Л., Фабрес Дж. И др. Сравнение аппаратов для вентиляции новорожденных в родильном зале. J Pediatr. 2014 август; 165 (2): 234–9.e3.
- Roehr CC, Davis PG, Weiner GM, Jonathan Wyllie J, Wyckoff MH, Trevisanuto D.Т-образный реанимационный аппарат или самонадувающийся мешок во время реанимации новорожденных: обзор объема работ. Pediatr Res. 2021. 89 (4): 760–6.
- Паз П., Раманатан Р., Эрнандес Р., Бинивале М. Реанимация новорожденных с использованием назальной канюли: опыт с одним центром. Am J Perinatol. 2014. 31 (12): 1031–6.
- Вуд Ф. Э., Морли С. Дж., Доусон Дж. А., Камлин КОФ, Оуэн Л. С., Донат С. и др. Усовершенствованные методы уменьшают утечку лицевой маски во время моделирования реанимации новорожденных: исследование 2. Arch Dis Child Fetal Neonatal Ed. 2008; 93 (3): F230.
- Шмёльцер Г.М., Доусон Дж. А., Камлин КОФ, О’Доннелл КПФ, Морли С.Дж., Дэвис П.Г.Обструкция дыхательных путей и утечка газа при вентиляции недоношенных новорожденных через маску в родильном зале. Arch Dis Child Fetal Neonatal Ed. 2011; 96 (4): F254–7.
- Finer NN, Rich W, Wang C, Leone T. Обструкция дыхательных путей во время вентиляции с помощью маски у младенцев с очень низкой массой тела при рождении во время реанимации новорожденных.Педиатрия. 1 марта 2009 г .; 123 (3): 865–9.
- Mangat A, Bruckner M, Schmölzer GM. Лицевая маска в сравнении с носовым каналом или назофарингеальной трубкой для реанимации новорожденных в родильном зале: систематический обзор и метаанализ. Arch Dis Child Fetal Neonatal Ed. DOI: 10.1136 / archdischild-2020-319460.
- Crawshaw JR, Kitchen MJ, Binder-Heschl C, Thio M, Wallace MJ, Kerr LT и др. Закрытие гортани затрудняет неинвазивную вентиляцию легких при рождении. Arch Dis Child Fetal Neonatal Ed. 2018; 103 (2): F112–9.
- ван Вондерен Дж.Дж., Хупер С.Б., Хаммлер HD, Лоприоре Э., Те Пас АБ.Последствия устойчивой инфляции у недоношенных новорожденных при рождении. J Pediatr. 2014 ноя; 165 (5): 903–8.e1.
- Клингенберг С., Соботка К.С., Онг Т., Эллисон Б.Дж., Шмёльцер Г.М., Мосс Т.Д.М. и др. Эффект продолжительности устойчивой инфляции; реанимация ягнят, перенесших удушье в ближайшее время. Arch Dis Child Fetal Neonatal Ed.2013 Май; 98 (3): F222–7.
- Соботка К.С., Хупер С.Б., Кроссли К.Дж., Онг Т., Шмёльцер Г.М., Бартон С.К. и др. Однократное устойчивое надувание с последующей вентиляцией приводит к быстрому восстановлению сердечно-сосудистой системы, но вызывает утечку сосудов головного мозга у ягнят в краткосрочной перспективе, подвергшихся асфиксии. PLoS One.2016 14 января. 11 (11): e0146574
- Kamlin COF, Schmölzer GM, Dawson JA, McGrory L, O’Shea J, Donath SM и др. Рандомизированное исследование ротоглоточных дыхательных путей для стабилизации состояния недоношенных детей в родильном зале. Реанимация. 2019 ноя; 144 (август): 106–14.
- Куреши М.Дж., Кумар М.Сравнение дыхательных путей с помощью ларингеальной маски и вентиляции с использованием маски с мешком или эндотрахеальной интубации при реанимации новорожденных. Кокрановская база данных Syst Rev.2018; 3 (3): CD003314.
- Pejovic NJ, Trevisanuto D, Lubulwa C, Höök SM, Cavallin F, Byamugisha J, et al. Реанимация новорожденных с использованием дыхательных путей через ларингеальную маску: рандомизированное исследование в Уганде.Arch Dis Child. 2018; 103 (3): 255–60.
- Pejovic NJ, Trevisanuto D, Nankunda J, Tylleskär T. Пилотное исследование манекена показало, что устройство надгортанного дыхательного пути улучшает имитацию вентиляции новорожденных в условиях ограниченных ресурсов. Acta Paediatr. 2016 г. 10 декабря; 105 (12): 1440–3.
- Pejovic NJ, Myrnerts Höök S, Byamugisha J, Alfvén T., Lubulwa C, Cavallin F, et al.Рандомизированное исследование дыхательных путей с ларингеальной маской в реанимации новорожденных. N Engl J Med. 2020; 383 (22): 2138–47.
- Венто М., Асенси М., Састре Дж., Гарсия-Сала Ф., Винья Дж. Шестилетний опыт использования комнатного воздуха для реанимации новорожденных доношенных детей с асфиксией.Biol Neonate. 2001. 79 (3–4): 261–7.
- Saugstad OD, Rootwelt T, Aalen O. Реанимация новорожденных с асфиксией воздухом или кислородом помещения: международное контролируемое исследование: исследование Resair 2. Педиатрия. 1 июля 1998; 102 (1): e1.
- Венто М., Састре Дж., Асенси М.А., Винья Дж.Реанимация с использованием воздуха в помещении вызывает меньшее повреждение сердца и почек, чем 100% кислород. Am J Respir Crit Care Med. 2005 декабрь; 172 (11): 1393–8.
- Vento M, Asensi M, Sastre J, Lloret A, García-Sala F, Viña J. Окислительный стресс у доношенных новорожденных, подвергшихся асфиксии, реанимированных 100% кислородом.J Pediatr. Март 2003 г., 142 (3): 240–6.
- Wyllie J, Bruinenberg J, Roehr CC, Rüdiger M, Trevisanuto D, Urlesberger B. Рекомендации Европейского совета реаниматологов по реанимации 2015 г. Раздел 7. Реанимация и поддержка перехода младенцев при рождении. Реанимация. 2015; 95: 249–63.
- Sweet DG, Carnielli V, Greisen G, Hallman M, Ozek E, Te Pas A и др. Европейское консенсусное руководство по лечению респираторного дистресс-синдрома: обновление 2019 г. Неонатология. 2019; 115 (4): 432–50.
- Дэвис П.Г., Тан А., О’Доннелл С.П., Шульце А.Реанимация новорожденных 100% кислородом или воздухом: систематический обзор и метаанализ. Ланцет. Октябрь 2004 г., 364 (9442): 1329–33.
- Saugstad OD. Реанимация новорожденных: из кислорода в комнатный воздух. Ланцет. 2010 декабрь; 376 (9757): 1970–1.
- Солевог А.Л., Данневиг I, Вайкофф М., Саугстад О.Д., Накстад Б.Расширенная серия компрессий сердца во время СЛР на модели перинатальной асфиксии у свиней. Реанимация. 2010 ноябрь; 81 (11): 1571–6.
- Солеваг А.Л., Данневиг И., Вайкофф М., Саугстад О.Д., Накстад Б. Возврат спонтанного кровообращения с соотношением компрессия: вентиляция 15: 2 по сравнению с 3: 1 у новорожденных свиней с остановкой сердца из-за асфиксии.Arch Dis Child Fetal Neonatal Ed. 1 ноября 2011 г .; 96 (6): F417–21.
- Паскуин М.П., Чунг П.-Й, Патель С., Лу М., Ли Т. Ф., Вагнер М. и др. Сравнение различных соотношений компрессии и вентиляции (2: 1, 3: 1 и 4: 1) во время сердечно-легочной реанимации на модели асфиксии новорожденных у свиней.Неонатология. 2018; 114 (1): 37–45.
- Schmölzer GM, O’Reilly M, LaBossiere J, Lee TF, Cowan S, Nicoll J, et al. 3: 1 Соотношение компрессии к вентиляции по сравнению с непрерывным сжатием грудной клетки с асинхронной вентиляцией в модели реанимации новорожденных на свиньях. Реанимация.2014. 85 (2): 270–5.
- Баббс К.Ф., Мейер А., Надкарни В., СЛР новорожденных. СЛР новорожденных: комната наверху: математическое исследование оптимальной частоты компрессии грудной клетки в зависимости от размера тела. Реанимация. 2009 ноябрь; 80 (11): 1280–4.
- Ли Э.С., Чунг Пи, Ли Т.Ф., Лу М., О’Рейли М., Шмёльцер ГМ.На восстановление спонтанного кровообращения не влияет различная степень сжатия грудной клетки, наложенная на устойчивое инфляция во время сердечно-легочной реанимации у новорожденных поросят. PLoS One. 2016 15 июня; 11 (6): e0157249.
- Патель С., Чунг П.И, Ли Т.Ф., Паскуин М.П., Лу М., О’Рейли М. и др.Асинхронная вентиляция при 120 по сравнению с 90 или 100 сжатиями в минуту улучшает восстановление гемодинамики у новорожденных поросят, подвергшихся асфиксии. Arch Dis Child Fetal Neonatal Ed. 2020 июл; 105 (4): 357–63.
- Мейер А., Надкарни В., Поллок А., Бэббс С., Нишисаки А., Брага М. и др.Оценка глубины сжатия грудной клетки, рекомендованной программой реанимации новорожденных, с использованием компьютерной томографии. Реанимация. 2010. 81 (5): 544–8.
- Шайни С.С., Гупта Н., Кумар П., Бхалла А.К., Каур Х. Сравнение техники сжатия грудной клетки двумя пальцами и техники сжатия двумя большими пальцами рук у новорожденных.J Perinatol. 2012, 17 сентября; 32 (9): 690–4.
- Кристман С., Хемуэй Р.Дж., Вайкофф М.Х., Перлман Дж. М.. Метод двумя пальцами лучше, чем метод двумя пальцами для проведения компрессионных сжатий грудной клетки в модели манекена реанимации новорожденных. Arch Dis Child Fetal Neonatal Ed. 1 марта 2011 г .; 96 (2): F99–101.
- Менегацци Дж. Дж., Обле Т. Э., Никлас К. А., Хосак ГМ, Стойка L, Гуд Дж. С.. Сжатие грудной клетки двумя пальцами по сравнению с двумя пальцами во время CRP в модели остановки сердца у новорожденного свиньи. Ann Emerg Med. 1993 Февраль; 22 (2): 240–3.
- Гарсия-Идальго К., Чунг П.-Й, Солевог А.Л., Венто М., О’Рейли М., Саугстад О. и др.Обзор использования кислорода во время компрессий грудной клетки у новорожденных — метаанализ данных на животных. Фронт Педиатр. 2018 декабрь; 6: 400–7.
- Солевог А.Л., Гарсия-Идальго К., Чунг П.Й., Ли Т.Ф., О’Рейли М., Шмёльцер Г.М. Вентиляция с 18, 21 или 100% кислородом во время сердечно-легочной реанимации задохнувшихся поросят: рандомизированное контролируемое испытание на животных.Неонатология. 2020; 117 (1): 102–10.
- Идальго К.Г., Солеваг А.Л., Ким С.И., Шим Г.Х., Чунг П.Й., Ли Т.Ф. и др. Устойчивое наполнение кислородом 21% по сравнению со 100% во время сердечно-легочной реанимации новорожденных поросят, подвергшихся асфиксии — рандомизированное контролируемое исследование на животных. Реанимация.2020 Октябрь; 155: 39–47.
- Schmölzer GM, O’Reilly M, Labossiere J, Lee TF, Cowan S, Qin S и др. Сердечно-легочная реанимация с компрессиями грудной клетки во время устойчивой инфляции: новый метод реанимации новорожденных, улучшающий восстановление и выживаемость на неонатальной модели свиней.Тираж. 2013. 128 (23): 2495–503.
- Шмёльцер Г.М., О Рейли М., Фрай С., Ван Ос С., Чунг П.-Й. Сжатие грудной клетки во время длительного надувания по сравнению с соотношением компрессия грудной клетки: вентиляция 3: 1 во время сердечно-легочной реанимации новорожденных: рандомизированное исследование осуществимости. Arch Dis Child Fetal Neonatal Ed.2018 сентябрь; 103 (5): F455–60.
- Schmölzer GM, Pichler G, Solevåg AL, Fray C, van Os S, Cheung P-Y. Исследование SURV1VE: устойчивое раздувание и сжатие грудной клетки в сравнении с соотношением компрессии грудной клетки к вентиляции 3: 1 во время сердечно-легочной реанимации новорожденных с асфиксией: протокол исследования для кластерного рандомизированного контролируемого исследования.Испытания. 2019 декабря 19; 20 (1): 139.
- Schwindt EM, Hoffmann F, Deindl P, Waldhoer TJ, Schwindt JC. Продолжительность создания экстренного сосудистого доступа и способы его ускорения: исследование на основе моделирования, проведенное в реальных реанимационных палатах. Pediatr Crit Care Med.2018; 19 (5): 468–76.
- Wagner M, Olischar M, O’Reilly M, Goeral K, Berger A, Cheung PY и др. Обзор способов введения лекарств во время длительной реанимации новорожденных. Pediatr Crit Care Med. 2018; 19 (4): 332–8.
- Байк-Шнедитц Н., Пихлер Г., Швабергер Б., Миледер Л., Авиан А., Урлесбергер Б.Периферический внутривенный доступ недоношенным новорожденным в период постнатальной стабилизации: возможность и безопасность. Фронт Педиатр. 2017 10 августа; 5: 171.
- Маконочи И.К., Бингхэм Р., Эйх К., Лопес-Херсе Дж., Родригес-Нуньес А., Райка Т. и др. Руководство Европейского совета реаниматологов по реанимации 2015: раздел 6.Педиатрическое жизнеобеспечение. Реанимация. 2015 Октябрь; 95: 223–48.
- Scrivens A, Reynolds PR, Emery FE, Roberts CT, Polglase GR, Hooper SB и др. Использование внутрикостных игл у новорожденных: систематический обзор. Неонатология. 2019; 116 (4): 305–14.
- Могале Н., Ван Шур А-Н, Босман М.С.Теоретическая альтернатива внутрикостному вливанию у детей с тяжелой гиповолемией. Afr J Prim Health Care Fam Med. 2015 г. 23 июля; 7 (1).
- Fuchs Z, Scaal M, Haverkamp H, Koerber F, Persigehl T., Eifinger F. Анатомические исследования внутрикостного доступа у мертворожденных — Сравнение различных устройств и методов.Реанимация. 2018 июн; 127: 79–82.
- Миледер Л.П., Урлесбергер Б., Швабергер Б. Использование внутрикостного сосудистого доступа во время реанимации новорожденных в специализированном центре. Фронт Педиатр. 2020; 8 (сентябрь): 571285–5.
- Borrhomée S, Merbouche S, Kern-Duciau N, Boize P.Катетеризация пупочной вены через желе Уортона: возможность быстрого и безопасного лечения в родильном зале? Arch Pediatr. 2019; 26 (6): 381–4.
- O’reilly M, Schmölzer GM. Данные о вазопрессорах во время сердечно-легочной реанимации у новорожденных.Минерва Педиатр. 2019 Февраль; 71 (2): 159–73.
- Исаяма Т., Милденхолл Л., Шмёльцер Г.М., Ким Х.С., Раби И., Зиглер С. и др. Путь, доза и интервал введения адреналина для реанимации новорожденных: систематический обзор. Педиатрия. 2020 9 октября; 146 (4): e20200586.
- Чируволу А., Миклис К.К., Чен Э., Петри Б., Десаи С.Ведение родильного отделения новорожденных с меконием и респираторная поддержка. Педиатрия. 2018; 142 (6): e20181485.
- Фишер Ц., Рыбаковски Ц., Фердинус Ц., Сагот П., Гуйон Дж. Б. Популяционное исследование синдрома аспирации мекония у новорожденных, родившихся на сроке от 37 до 43 недель беременности.Int J Pediatr. 2012; 2012: 321545–7.
- Моисей Д., Холм Б.А., Спитале П., Лю М., Энхорнинг Г. Ингибирование функции легочного сурфактанта меконием. Am J Obstet Gynecol. 1991 Февраль; 164 (2): 477–81.
- Видьясагар Д., Загария А.Исследования повреждения легких, вызванного меконием: экспрессия воспалительных цитокинов и апоптоз. J Perinatol. 5 декабря 2008 г .; 28 (Дополнение 3): S102–7.
- Эдвардс Э.М., Лакшминрусимха С., Эрет ДЭЙ, Хорбар Дж. Д.. Поступления в отделение интенсивной терапии по поводу синдрома аспирации мекония до и после изменения рекомендаций по отсасыванию Национальной программы реанимации.Дети. 2019; 6 (5): 68.
- Kalra VK, Lee HC, Sie L, Ratnasiri AW, Underwood MA, Lakshminrusimha S. Изменение рекомендаций по неонатальной реанимации и тенденции заболеваемости синдромом аспирации мекония в Калифорнии. J Perinatol. 2020; 40 (1): 46–55.
- Ооммен В.И., Рамасвами В.В., Шилд Э., Роер СС.Реанимация неактивных новорожденных, рожденных из околоплодных вод, окрашенных меконием: анализ последствий изменения политики. Arch Dis Child Fetal Neonatal Ed. 2020 22 сентября; фетально-неонатальный-2020-319771.
- Тревизануто Д., Стрэнд М.Л., Каваками М.Д., Фабрес Дж., Шилд Э., Нация К. и др. Отсасывание мекония через трахею при рождении у младенцев, не ведущих активный образ жизни: систематический обзор и метаанализ.Реанимация. 2020; 149 (ноябрь 2019 г.): 117–26.
- Phattraprayoon N, Tangamornsuksan W, Ungtrakul T. Результаты эндотрахеального отсасывания у не энергичных новорожденных, рожденных из околоплодных вод, окрашенных меконием: систематический обзор и метаанализ. Arch Dis Child Fetal Neonatal Ed.2021 Янв; 106 (1): 31–8.
- Джейкобс С.Е., Хант Р., Тарнов-Морди В.О., Индер Т.Э., Дэвис П.Г. Охлаждение новорожденных с гипоксической ишемической энцефалопатией. В: Джейкобс С.Е., редактор. Кокрановская база данных систематических обзоров. Чичестер, Великобритания: John Wiley & Sons, Ltd; 2007 г.
- Daetwyler K, Brotschi B, Berger TM, Wagner BP.Возможность и безопасность пассивного охлаждения в когорте новорожденных с асфиксией. Swiss Med Wkly. 2013; 143 (март): w13767–6.
- Mortola JP. Последствия гипоксического гипометаболизма в онтогенезе млекопитающих. Respir Physiol Neurobiol. 2004, август; 141 (3): 345–56.
- Горелка ED, Cross KW.Ректальная температура у новорожденного после асфиксии родов. Br Med J. 1958, 15 ноября; 2 (5106): 1197–9.
- Джейкобс С.Е., Морли С.Дж., Индер Т.Э., Стюарт М.Дж., Смит К.Р., Макнамара П.Дж. и др. Гипотермия всего тела для доношенных и недоношенных новорожденных с гипоксически-ишемической энцефалопатией: рандомизированное контролируемое исследование.Arch Pediatr Adolesc Med. 1 августа 2011 г .; 165 (8): 692.
- О’Рейли Д., Лабрек М., О’Мелия М., Бачич Дж., Хансен А., Соул Дж. С. Пассивное охлаждение при транспортировке доношенных новорожденных в состоянии асфиксии. J Perinatol. 2013. 33 (6): 435–40.
- Лемир Б., Ли Л., Чау В., Чако А., Барроумен Н., Уайт Н. и др.Начало пассивного охлаждения в специализированном центре является наиболее прогностическим фактором для достижения ранней терапевтической гипотермии у новорожденных, страдающих асфиксией. Педиатр детского здоровья. 2017; 22 (5): 264–8.
- Каррерас Н., Альсина М., Аларкон А., Арка-Диас Г., Агут Т., Гарсия-Аликс А. Эффективность пассивной гипотермии и побочных эффектов при транспортировке новорожденных с асфиксией в зависимости от тяжести гипоксически-ишемической энцефалопатии.J Pediatr. 2018; 94 (3): 251–7.
- Акула В.П., Джо П., Тусу К., Дэвис А.С., Тамарезис Дж. С., Ким С. и др. Рандомизированное клиническое испытание режима терапевтической гипотермии во время транспортировки при неонатальной энцефалопатии. J Pediatr. 2015. 166 (4): 856–2.
- Прашанта Ю.Н., Суман Рао П.Н., Несарги С., Чандракала Б.С., Балла К.С., Шашидхар А.Лечебная гипотермия при умеренной и тяжелой гипоксической ишемической энцефалопатии у новорожденных с использованием недорогих устройств — пакетов со льдом и фазопереходящего материала. Paediatr Int Child Health. 2019 2 октября; 39 (4): 234–9.
- Ван Х., Бхутта З.А., Коутс М.М., Коггешалл М., Дандона Л., Диалло К. и др.Глобальный, региональный, национальный и отдельные субнациональные уровни мертворождений, неонатальной, младенческой и детской смертности, 1980–2015 гг .: систематический анализ для исследования глобального бремени болезней, 2015 г. Lancet. Октябрь 2016 г .; 388 (10053): 1725–74.
- Уолл С.Н., Ли А.С., Нирмейер С., Инглиш М., Кинан В.Дж., Карло В. и др.Реанимация новорожденных в условиях ограниченных ресурсов: что, кто и как преодолевать трудности для расширения масштабов? Int J Gynaecol Obstet. Октябрь 2009 г .; 107 (Дополнение 1): S47–4.
- ЮНИСЕФ, Всемирный банк ВОЗ и ООН. Уровни и тенденции детской смертности в 2020 году. Оценки, разработанные Межведомственной группой ООН для оценки детской смертности.Доступно по адресу: https://www.unicef.org/reports/levels-and-trends-child-mortality-report-2020.
- Моширо Р., Мдоэ П., Перлман Дж. М.. Глобальный взгляд на асфиксию новорожденных и реанимацию. Фронт Педиатр. 2019 26 ноября; 7: 489.
- Гилстрап Л.С., Левено К.Дж., Беррис Дж., Линн Уильямс М., Литтл Б.Б.Диагностика асфиксии при рождении на основании pH плода, шкалы Апгар и церебральной дисфункции новорожденного. Am J Obstet Gynecol. 1989 сентябрь; 161 (3): 825–30.
- Versantvoort JMD, Kleinhout MY, Ockhuijsen HDL, Bloemenkamp K, De Vries WB, Van Den Hoogen A. Помощь младенцам в дыхании и ее влияние на мертворождение во время родов и неонатальную смертность в условиях ограниченных ресурсов: систематический обзор.Arch Dis Child. 2020; 105 (2): 127–33.
- Foglia EE, Weiner G, de Almeida MFB, Wyllie J, Wyckoff MH, Rabi Y, et al. Продолжительность реанимации при рождении, смертность и развитие нервной системы: систематический обзор. Педиатрия. 2020; 146 (3): e20201449.
Автор Контакты
Георг М.Шмёльцер, [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Поступила: 1 марта 2021 г.
Дата принятия: 9 апреля 2021 г.
Опубликована онлайн: 21 мая 2021 г.
Дата выпуска: август 2021 г.
Количество страниц для печати: 13
Количество рисунков: 0
Количество столов: 2
ISSN: 1661-7800 (печатный)
eISSN: 1661-7819 (онлайн)
Для дополнительной информации: https: // www.karger.com/NEO
Лицензия открытого доступа / Дозировка лекарства / Заявление об ограничении ответственности
Эта статья находится под международной лицензией Creative Commons Attribution-NonCommercial 4.0 (CC BY-NC). Для использования и распространения в коммерческих целях требуется письменное разрешение. Дозировка лекарства: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарства, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новый и / или редко применяемый препарат. Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
Лечение асфиксии при родах при родах в сельской местности Гадчироли: влияние двух типов акушерок и реанимационных мероприятий с использованием метода «рот в рот», трубки-маски или мешка-маски
В данном исследовании рассматриваются меры по уходу за новорожденными на дому были завезены в сельский Гадчироли, где более 90% родов происходят на дому.Мероприятия включали обучение грамотной деревенской женщины, VHW, тому, как присутствовать при родах вместе с TBA, и заботиться о новорожденном при рождении, включая реанимацию, если это необходимо. Вмешательства подготовленных VHW снизили смертность, связанную с асфиксией, CF почти на 50% и ASMR на 65% по сравнению с лечением только TBA. Частота легкой асфиксии также снизилась на 60%, но о ее значении нельзя судить, поскольку легкая асфиксия не была связана с риском смерти.Частота тяжелой асфиксии не снизилась. Это было понятно, учитывая тот факт, что исследование не включало каких-либо серьезных акушерских вмешательств и почти полностью упор делался на немедленную диагностику и лечение асфиксии. Это также может быть связано с тем, что некоторые из предотвращенных новых мертворождений могут проявляться как тяжелая асфиксия.
Исследование не предназначалось для сравнения различных методов реанимации. Но сравнение за разные периоды времени показывает, что для такой домашней реанимации мешок и маска были более эффективными и приемлемыми для медицинского работника.Трубка и маска были одинаково эффективны в снижении ASMR, но мешок и маска были более эффективными в снижении CF и свежего SBR, и их было легче использовать для VHW. Реанимационные мероприятия «рот в рот» с применением TBA были наименее эффективными. Для дальнейшего снижения заболеваемости и смертности из-за асфиксии может оказаться полезным улучшение акушерского ухода в указанных родах и предотвращение ненужного использования окситоцитов неквалифицированными врачами во время родов на дому.
На основании этой оценки мы пришли к выводу, что домашние вмешательства, проводимые обученным медперсоналом при рождении, в дополнение к TBA, были эффективными в снижении смертности от асфиксии.Сумка и маска представляются более эффективным оборудованием для реанимации.
У этой оценки есть несколько ограничений. Суммарный эффект асфиксии проявляется в виде МВ, свежих мертворождений и последствий для нервного развития. У нас есть полные данные о смертях (CF и ASMR), данные о свежем SBR только с 1996 г., нет данных о влиянии на развитие нервной системы. Следовательно, оценка в основном возможна только на CF и ASMR.
Это не было контролируемым испытанием лечения асфиксии, и поэтому большинство оценок проводится путем сравнения до и после.Было бы этически невозможно наблюдать асфиксию при рождении, но не вмешиваться в контрольную группу. Возможность наблюдения без вмешательства была доступна только в 1995–1996 годах в зоне вмешательства до того, как VHW были обучены лечению асфиксии при рождении, что предоставило уникальные данные по наблюдению естественной заболеваемости и смертности из-за асфиксии. Следовательно, результаты последующих вмешательств необходимо сравнивать с оценками в 1995–1996 годах. Так же многие другие факторы, такие как созревание навыков по мере увеличения опыта или введение других вмешательств, также могут изменить показатели результатов, прежде чем –После сравнения — менее надежное свидетельство.
Тем не менее, доступно контролируемое сравнение ASMR на основе причины смерти, назначенной путем словесного вскрытия для исходного (1993–1995), периода наблюдения (1995–1996) и периода вмешательства (1996–1999) (Таблица 6). Такое сравнение показывает чистую разницу в ASMR между областями вмешательства и контрольными участками в период с 1993 по 1995 год на 11,7%. Эта разница объясняется более ранним обучением ТАП реанимации «рот в рот» в области вмешательства. Было обнаружено снижение ASMR на 41,8% из-за обучения VHW и использования трубки и маски.Устное вскрытие было остановлено в 1999 году, и поэтому у нас нет результатов с 2000 по 2003 год, когда были введены сумка и маска.
Эффект реанимации «изо рта в рот», оцениваемый ТАП путем сравнения ASMR в интервенции и контрольной зоне в 1993–1995 гг. (Таблица 6), показывающий разницу в 11,7%, следует понимать с двумя квалификациями. Метод вербальной аутопсии никогда не применялся у новорожденных. Оперативные органы в контрольной зоне также прошли обучение по государственной программе.
Полевые исследования асфиксии при рождении в общинах страдают неточностью, поскольку диагностическое определение асфиксии и ее измерение сопряжены с огромными трудностями. 20 Присутствие обученного наблюдателя во время родов на дом, клиническая оценка новорожденного через 1 и 5 минут, точное измерение времени при наличии экстренной ситуации, невозможность последующей контрпроверки правильности записанных данных , отличия асфиксии от других причин нарушения дыхания при рождении, этическая невозможность иметь контрольную группу — все это делает такие полевые исследования очень сложными.Следовательно, относительно неточные измерения, оценки и оценки являются неотъемлемыми ограничениями.
Мы использовали простое клиническое определение, наблюдая за новорожденным через 1 и 5 минут. Это определение было подтверждено в условиях больницы. 7 Мы изменили время первого наблюдения с 1 минуты на 30 секунд, начиная с 1999 года. Это изменение, если оно вообще будет, должно привести к увеличению частоты легкой асфиксии при рождении. Следовательно, снижение заболеваемости асфиксией в годы вмешательства не может быть объяснено изменением определения.Однако более раннее начало реанимации может улучшить результат, такой как% CF при тяжелой асфиксии, наблюдаемой с мешком и маской.
CF и ASMR основаны на смерти — определенном, поддающемся проверке событии. Это исследование показывает большое и значительное снижение этих двух показателей. Снижение смертности может быть вызвано реанимацией при рождении и последующим поддерживающим уходом за такими новорожденными, как дети из группы высокого риска (вставка 1).
Можно ли объяснить наблюдаемый эффект снижения смертности другими изменениями? В течение периода вмешательства произошло небольшое увеличение доли родов в стационаре и кесарева сечения (таблица 2).Это произошло полностью после 1999 г. (годовые данные не представлены) из-за системы стимулирования, введенной правительством в 2000 г. для неизбирательного поощрения институциональных поставок. Но это не объясняет сокращения CF и ASMR (Таблица 4), которые были полностью основаны на домашних родах, наблюдаемых VHW, или сокращении ASMR, наблюдавшемся в период с 1996 по 1999 год (Таблицы 5 и 6). Более того, рост количества родов в больницах очень незначителен. Следовательно, наблюдаемое снижение смертности от асфиксии можно отнести на счет домашних вмешательств.
Есть несколько исследований, с которыми можно сравнить результаты. Мета-анализ оценки обучения ТАП показал, что чистое снижение перинатальной смертности на 8% и на 11% — на ASMR. 21 По нашим оценкам, сокращение ASMR из-за обучения ТАП сопоставимо — 11,7% (Таблица 6). Мы не можем использовать коэффициент перинатальной смертности для оценки эффекта вмешательств против асфиксии, потому что наш пакет вмешательств по уходу за новорожденными на дому включал множество других вмешательств, чтобы повлиять на неонатальную смертность в течение 1-7 дней, что способствует увеличению перинатальной смертности.
В ходе полевых испытаний подготовки трансгендеров в сельской местности на севере Индии эффект повышения квалификации, включая экипировку сумкой и маской, сравнивался с эффектом реанимации «рот в рот». CF был меньше на 20% в группе с сумкой и маской, а ASMR в двух группах составлял 6 на 1000 и 19 на 1000. 22, 23 Наши результаты по ASMR сопоставимы по величине, но по CF мы обнаружили гораздо большее сокращение: на 55%. По нашему опыту, грамотные VHW могут лучше наблюдать и записывать по сравнению с неграмотными TBA, которые не умеют считать или записывать.VHW можно лучше обучить следовать алгоритму (вставка 1). Более того, TBA + VHW помогает лучше управлять матерью и новорожденным в критический момент родов.
Основными ограничивающими факторами внедрения являются стоимость обучения и оборудования, а также редкость использования. Трубка и маска (10 долларов) были дешевле, чем сумка и маска (20 долларов). В среднем TBA в нашем регионе выполняет от 5 до 20 доставок, а VHW обслуживает от 20 до 25 доставок в год. При частоте легкой асфиксии менее 6% (таблица 3) необходимость использования реанимационного оборудования может возникнуть один или два раза в год.Следовательно, коэффициент использования относительно низкий.
В следующей статье, 24 мы подсчитали, что вмешательства на дому в испытании Гадчироли предотвратили 31 неонатальную смерть, связанную с асфиксией, в 39 деревнях в период с 1996 по 2003 год. (Если мешок и маска использовались с начала вмешательства, Вероятно, можно было бы предотвратить больше смертей.) Кроме того, мешок и маска предотвратили шесть новых мертворождений на 1000 рождений (Таблица 5), следовательно, предотвратили бы дополнительно 30 мертворождений в период с 1996 по 2003 год.Предполагая, что одна сумка и маска на деревню (до сих пор не было необходимости в замене оборудования), стоимость сумки и маски оценивалась в 13 долларов на предотвращенную смерть (свежие мертворождения + неонатальные смерти, связанные с асфиксией). Стоимость обучения и вознаграждение VHW, а также результат, такой как предотвращение неврологических последствий, в расчет не принимаются.
Однако более трудным, но важным условием является обеспечение присутствия обученного работника во время доставки на дом.Несмотря на создание штатных оплачиваемых кадров, называемых «вспомогательной медсестрой-акушеркой», одной на 5000 человек населения, почти 15 лет назад во всей стране в рамках национальной программы в Индии сообщалось о присутствии этого работника только в 15% домашних хозяйств. поставки. 25 VHW, будучи жительницей того же села, чаще посещает роды на дому. В исследовании Gadchiroli 84% домашних родов принимали VHW (Таблица 2). Выбор оборудования будет эффективным только в том случае, если работник присутствует при рождении.
Снижение почти на 60% случаев легкой асфиксии является результатом присутствия двух акушерок (TBA + VHW) вместо одной и, как следствие, немедленной сушки, тактильной стимуляции и очистки горла. Это снизило потребность в реанимации с использованием зонда или мешка почти до 6% (частота легкой асфиксии) за последние 5 лет вмешательств. Однако маловероятно, что это окажет какое-либо влияние на смертность, потому что сначала легкая асфиксия не была связана с повышенным риском смерти (Таблица 1).
В сценарии после вмешательства все факторы риска, связанные с тяжелой асфиксией или свежим мертворождением (таблица 7), предположительно были связаны с акушерством. Излишняя практика применения окситоцитов была явно связана с трехкратным риском этих событий. Поскольку длительные роды не показали повышенного риска асфиксии при рождении в этой когорте, они не действовали как фактор, вызывающий ложную связь между применением окситоцитов и асфиксией при рождении. Эта вредная практика требует немедленного внимания.
Факторы риска асфиксии новорожденных в государственных больницах Центральной зоны, Тыграй, Эфиопия 2018 | Примечания к исследованию BMC
Район исследования и период
Исследование проводилось в государственных больницах центральной зоны Тыграй, Эфиопия. Сбор данных для этого исследования проводился с января по февраль 2018 года.
Дизайн исследования
Был использован непревзойденный ретроспективный дизайн исследования случай – контроль, основанный на учреждении.
Исходное население
Исходное население — все матери, родившие своих детей в центральной зоне, Тыграй, Эфиопия.
Исследуемая популяция
Для случаев
Матери с новорожденными с диагнозом асфиксия при рождении.
Для контроля
Матери с новорожденными, которым поставлен диагноз асфиксии без рождения.
Расчет размера выборки
Размер выборки исследования был рассчитан с использованием программного обеспечения EPI Info версии 7.1.1 со следующими параметрами для несравненного исследования случай-контроль: уровень достоверности = 95%; мощность = 80%; отношение шансов = 2,53; соотношение корпуса к контролю = 1: 2; доля контролей с экспозицией 17.7% [16]; доля случаев с воздействием = 35,2%. Предполагая, что уровень неполучения ответов составляет 10%, размер выборки для случаев = 88; размер выборки для контроля = 176, общий размер выборки = 264.
Методика выборки
Метод систематической случайной выборки использовался для отбора субъектов исследования из четырех государственных больниц с каждыми двумя субъектами исследования как для случаев, так и для контроля.
Переменные исследования
Зависимая переменная
Независимые переменные
Дородовые факторы
Внутриродовые факторы
Факторы плода
Операционные определения
Асфиксия при рождении
Когда у новорожденного есть хотя бы один из следующих признаков, отсутствие дыхания, одышка, <30 вдохов в минуту или <7 баллов по шкале APGAR [6].
Низкая масса тела при рождении
При массе новорожденного <2500 г [17].
Недоношенные
При рождении новорожденного <37 гестационного возраста [18].
Инструмент и процедура сбора данных
Данные были собраны с использованием адаптированного структурированного вопросника, администрируемого интервьюером [19], наблюдений и анализа диаграмм. Анкета изначально была подготовлена на английском языке, а затем переведена на язык тигринья. Надежность вопрошающего проверялась с помощью альфы Кронбаха.
Контроль качества данных
Качество данных обеспечивалось с помощью правильно разработанных инструментов сбора данных. Счетчики и контролеры в течение 5 дней прошли обучение процедурам, методам и способам сбора данных. Пятипроцентный предварительный тест был проведен в больнице Шуль, чтобы проверить непротиворечивость опрашивающего. Собранные данные еженедельно просматривались и проверялись на полноту главным исследователем и соисследователями.
План обработки и анализа данных
Данные вводились и очищались с помощью Epi info версии 7.1.1. Данные были проанализированы с использованием статистического программного обеспечения SPSS версии 22.0. Перекрестная таблица была сделана между зависимыми и независимыми переменными. Модель бинарной логистической регрессии использовалась для определения значительной связи между асфиксией при рождении и возможными факторами риска. Переменные, которые показали статистическую значимость во время двумерного анализа при значении p ≤ 0,25, были введены в многомерную логистическую регрессию. Многопараметрическая логистическая регрессия была выполнена с учетом выбранных переменных двумерного анализа логистической регрессии.В конечном итоге данные были представлены и интерпретированы при значении p <0,05, считающемся статистически значимым.
Результаты
Социально-демографические характеристики участников исследования
В этом исследовании в общей сложности 88 новорожденных, перенесших асфиксию при рождении (случаи) с их индексными матерями, и 176 новорожденных, у которых не было асфиксии при рождении (контрольная группа) с их индексными матерями, были Включено 100% ответов. Сорок девять (55,7%) заболевших и 64 (36,4%) контрольной группы проживали в сельской местности.Что касается семейного положения, 75 (85,2%) пациентов и 166 (94,3%) контрольной группы были женаты. 47 (53,4%) случаев и 89 (50,6%) контрольных групп были домашними жёнами, а 30 (34,1%) и 28 (15,9%) контрольных лиц не умели читать и писать (Таблица 1).
Таблица 1 Распределение социально-демографических характеристик случаев и контрольных групп, посещающих государственные больницы Центральной зоны, регион Тыграй, Северная Эфиопия 2018Дородовые факторы участников исследования
Семьдесят шесть (86.В 4%) случаях и 159 (90,3%) контрольных их матерей наблюдались дородовые услуги, а 11 (12,5%) случаев и 6 (3,4%) контрольных их матерей имели преэклампсию. Два (2,3%) случая и 5 (2,8%) контрольных их матерей были с осложнением многоводия, а 6 (6,8%) случаев и 3 (1,7) контрольных их матери имели олигогидрамнион как осложнение. В трех (3,4%) случаях и в 5 (2,8%) контрольной группе их матери были больными анемией, а в 8 (9,1%) и 11 (6,3%) контрольных случаях их матери были инфицированы.В трех (3,4%) случаях их матери имели опыт курения в анамнезе, а в 10 (11,4%) и 34 (19,3%) контрольных группах были аборты в анамнезе. Сорок три (48,9%) случая и 64 (36,4%) контрольных случая были первородными.
Распределение внутриродовых и внутриутробных факторов среди участников
Двадцать три (26,1%) случаев и 36 (20,5%) контрольных их матерей имели опыт длительных родов, а 7 (8,0%) случаев и 8 (4,5%) контрольных их у матери выпадение пуповины было осложнением родов.Шестьдесят три (71,6%) больных и 135 (76,7%) контрольных их матерей родились самопроизвольно, а у 78 (88,6%) и 158 (89,8%) контрольных их матерей было вертикальное предлежание. У 21 (23,9%) случая и 9 (5,1%) контрольных их матерей было окрашено меконий при гинекологическом осмотре. Сорок три (48,9%) случая и 19 (10,5%) контрольной группы имели низкую массу тела при рождении, а 49 (55,7%) случаев и 40 (22,7%) и контрольную группу были преждевременными (Таблица 2).
Таблица 2 Распределение внутриродовых и внутриутробных факторов в случаях и контроле в государственных больницах Центральной зоны, регион Тыграй, Северная Эфиопия 2018Факторы риска асфиксии при рождении
Как показал результат двумерного анализа, 13 переменных действительно показали значительную связь с асфиксией при рождении на уровне значимости 25%.Многовариантная логистическая регрессия была проведена путем одновременного учета 13 переменных. Метод обратного исключения регрессии был использован для оценки смешения.
Образовательный статус матери показал значительную связь с асфиксией при рождении. Шансы не умеют читать и писать были в 6 раз выше по сравнению с теми, кто получил образование выше диплома [AOR = 6; 95% ДИ (1,51, 23,80)].
Рождение ребенка в значительной степени ассоциировалось с асфиксией при рождении. Это исследование показало, что у первородящих в 3 раза выше риск возникновения асфиксии при рождении, чем у повторнородящих [AOR = 3.10; 95% ДИ (1,51, 6,38)].
Дородовое кровотечение в значительной степени ассоциировалось с асфиксией при рождении. Матери, у которых было дородовое кровотечение, имели в 12 раз более высокий риск исхода асфиксии при рождении, чем те, у кого не было дородового кровотечения [AOR = 12; 95% ДИ (2,29, 63,11)].
Состояние окрашивания меконием значимо связано с исходной переменной асфиксией при рождении. У тех, у кого было окрашено меконием, риск рождения асфиксии был в 7,9 раз выше, чем у тех, у кого не было окрашено меконием [AOR = 7.88; 95% ДИ (2,92, 21,29)].
У недоношенных детей риск развития асфиксии при рождении в 2,2 раза выше, чем у доношенных детей [AOR = 2,20; 95% ДИ (1,02, 4,76)]. Точно так же вес новорожденного также имел значительную связь с асфиксией при рождении. Новорожденные с низкой массой тела при рождении были в 6,9 раз выше подвержены риску, чем нормальная масса тела, что является определяющим фактором асфиксии при рождении [AOR = 6,9; 95% ДИ (3,01, 15,81)] (таблица 3).
Таблица 3 Двумерная и многомерная логистическая регрессия между факторами случаев и контроля, посещающих государственные больницы Центральной зоны, регион Тыграй, Северная Эфиопия 2018Обсуждение
Это исследование было направлено на оценку факторов риска асфиксии при рождении, чтобы справиться с бременем болезни и связанных с ней проблем.Он попытался определить детерминанты асфиксии при рождении, включив как можно больше факторов риска.
Это исследование показало, что неграмотные матери часто страдают асфиксией при рождении. Умение читать и писать было в 6 раз выше, чем у тех, кто получил образование выше диплома. Этот результат согласуется с исследованием, проведенным в Непале и Индонезии [18, 20], которое показало, что неграмотность является виновником асфиксии при рождении. Это может быть связано с тем, что материнская неграмотность является очень широким показателем плохих социально-экономических условий, связанных с последующим недоеданием, частыми беременностями, а также влияет на обращение за помощью в дородовой период.
Вес при рождении был значительной ассоциацией с асфиксией при рождении. Вероятность асфиксии при рождении с низкой массой тела была в 6,9 раз выше, чем при нормальной массе тела (≥ 2500 г). Этот результат аналогичен исследованиям, проведенным в Пакистане и Таиланде [19, 21], в которых показано, что низкая масса тела при рождении является фактором риска асфиксии при рождении. Это может быть связано с тем, что низкая масса тела при рождении возникла из-за материнских осложнений, таких как гипертония, сахарный диабет, которые присутствуют до зачатия или до родов.
Недоношенных детей было 2.В 2 раза выше вероятность удушья, чем у доношенных детей. Это исследование согласуется с исследованием, проведенным в Иордании, которое показало, что у недоношенных детей есть риск развития асфиксии при рождении [20, 22]. Это может быть связано с тем, что недоношенные дети более подвержены ишемии из-за неполного формирования гематоэнцефалического барьера. Более того, это может быть связано с тем, что недоношенные дети сталкиваются с множеством заболеваний, включая заболевания органов, незрелость, особенно незрелые легкие, вызывающие дыхательную недостаточность.
Матери, окрашенные меконием, имели значительную связь с асфиксией при рождении.Те, у кого было окрашено меконием, были в 7,9 раз выше риск возникновения асфиксии при рождении, чем у тех, у кого не было окрашено меконием. Это исследование согласуется с другими предыдущими исследованиями [19]. У здоровых, хорошо насыщенных кислородом плодов этот разбавленный меконий легко выводится из легких по нормальному физиологическому механизму, однако в некоторых случаях возникает синдром аспирации мекония.
Паритет имел значительную связь с асфиксией при рождении. У первородящих в 3 раза выше риск возникновения асфиксии при рождении, чем у повторнородящих.Это исследование согласуется с другими исследованиями [23, 24]. Это может быть связано с тем, что первородящие часто игнорируют требования беременности и часто пренебрегают регулярным посещением дородовой помощи. Это может привести к осложнениям, ведущим к перинатальной асфиксии. Однако социально-экономические и культурные факторы также могут способствовать тому же.
Дородовое кровотечение значимо связано с асфиксией при рождении. Матери, у которых было дородовое кровотечение, имели в 12 раз более высокий риск исхода асфиксии при рождении, чем те, у кого не было дородового кровотечения.Это исследование согласуется с ранее опубликованными исследованиями [17]. Это может быть связано с тем, что при дородовом кровотечении снижается кровоток от матери к плаценте, поэтому у плода может возникнуть гипоксемия. Это состояние может привести к перинатальной асфиксии, если переливание крови матери или роды отложены.
Заключение
Асфиксия при рождении — одна из мировых проблем новорожденных. Если заболевание не лечить, возникают разные осложнения и приводят к летальному исходу. Существуют различные факторы, вызывающие асфиксию при рождении.В этом исследовании неграмотность матери, первородящие, низкая масса тела при рождении, преждевременные роды и околоплодные воды, окрашенные меконием, были факторами риска асфиксии при рождении. Большинство этих переменных можно предотвратить с помощью комплексного ухода за беременностью, родами и послеродовым уходом.
Долгосрочные последствия асфиксии при рождении
Ежегодно, по оценкам, около 1000 младенцев в Великобритании будут испытывать черепно-мозговую травму, называемую гипоксически-ишемической энцефалопатией (ГИЭ), после кислородного голодания примерно во время рождения. 1,2 Стандартное лечение, известное как охлаждающая терапия, для многих младенцев спасает жизнь и снижает риск пожизненной инвалидности. Д-р Брижит Фоллмер и ее команда проводят исследование, чтобы лучше понять долгосрочное влияние ГИЭ на жизнь детей, которым изначально была полезна охлаждающая терапия. Ее результаты могут привести к новым способам выявления тех, кому может помочь раннее вмешательство, что позволит улучшить поддержку в школе и в повседневной жизни.
Как сейчас затронуты жизни детей?
Асфиксия при рождении — нехватка кислорода и / или снижение кровоснабжения мозга ребенка во время рождения — может иметь ужасные последствия, включая травму головного мозга, называемую гипоксически-ишемической энцефалопатией (ГИЭ).К сожалению, дети с этим заболеванием могут потерять жизнь или остаться с долгосрочными осложнениями, такими как церебральный паралич.
«К счастью, существует эффективное лечение, которое включает в себя преднамеренное понижение температуры тела новорожденного на срок до трех дней, прежде чем постепенно согревать его», — говорит д-р Фоллмер.
Хотя охлаждающая терапия спасает многих младенцев от смерти и тяжелой инвалидности, мало что известно о долгосрочных последствиях раннего повреждения мозга, HIE, на повседневную жизнь детей.Многие из тех, кто, казалось, избежали наиболее серьезных последствий, имеют проблемы с развитием нервной системы, такие как проблемы с обучением и поведением.
«Нам действительно необходимо лучше понять, как дети, пережившие ГИЭ, продолжают развиваться на протяжении всего своего детства», — говорит д-р Фоллмер.
Чем может помочь это исследование?
«Наша цель — улучшить наши знания о долгосрочном влиянии ГИО на развитие мозга, обучение и поведение ребенка, а также разработать способы выявления тех, кому может быть полезна дополнительная поддержка», — говорит д-р Фоллмер.
Проанализировав информацию, полученную в результате рутинных обследований группы детей, лечившихся от ГИЭ, у которых не развился церебральный паралич, исследователи определили, что эти дети подвергаются повышенному риску поведенческих проблем в возрасте двух лет.
«Сейчас мы планируем следить за примерно 80 детьми, которым в настоящее время от шести до восьми лет, путем проведения оценки обучения и поведения, а также сканирования мозга», — говорит д-р Фоллмер.
Затем команда проанализирует эти данные — вместе со сканированием мозга, сделанным сразу после рождения, — чтобы выявить любые различия в их успеваемости в школе, социальных навыках и качестве жизни по сравнению с аналогичной группой детей, у которых не было ГИЭ.
«В конечном итоге, мы надеемся установить, могут ли сканирование мозга в сочетании с данными рутинных обследований в раннем младенчестве предсказать, как ребенок, прошедший ГИЭ и охлаждающую терапию, будет прогрессировать в своей повседневной жизни, с особым акцентом на навыки и способности, которые важны для школы. готовность и академическая успеваемость — что позволяет раньше идентифицировать тех, кто нуждается в дополнительной поддержке », — говорит д-р Фоллмер.
Список литературы
1. J.J. Куринчук, М. Уайт-Конинг, Н.Бадави. Эпидемиология неонатальной энцефалопатии и гипоксически-ишемической энцефалопатии Early Hum Dev 86, 329-38 (2010).
2. Управление национальной статистики. Статистика естественного движения населения в Великобритании: число рождений, смертей и браков — обновление 2018 г .: https: //www.ons.gov.uk/peoplepopulationandcommunity/populationandmigrati …
| Руководитель проекта | Д-р Бриджит Фоллмер Д-р мед. PhD FRCPCH |
| Команда проекта | Доктор Кэролайн Дж. Эдмондс, доктор психологических наук, доктор наук, доктор Кристин М. Корнфорт, доктор наук, доктор Жак-Дональд Турнье, доктор философии, доктор Анджела Дарекар, доктор философии, профессор MIPEM, Рут М. Пикеринг, бакалавр, магистр наук, доктор философии, CStat |
| Расположение проекта | Клиническая неврология, Саутгемптонский университет |
| Расположение проекта Другое | Школа психологии, Университет Восточного Лондона, Департамент здоровья женщин и детей, Ливерпульский университет, Департамент биомедицинской инженерии, Королевский колледж Лондона, Медицинская физика, Университетская больница Саутгемптона, первичная медико-санитарная помощь и науки о народонаселении, Саутгемптонский университет |
| Срок реализации | 3 года |
| Дата присуждения | 20 ноября 2018 |
| Дата начала проекта | 1 марта 2019 |
| Дата окончания проекта | 31 мая 2022 года |
| Размер гранта | £ 180 783 |
| Код гранта | GN2759 |
Распространенность и сопутствующие факторы перинатальной асфиксии у новорожденных, поступивших в комплексную специализированную больницу Айдер, Северная Эфиопия: перекрестное исследование
Общие сведения .Перинатальная асфиксия определяется как неспособность новорожденного инициировать и поддерживать достаточное дыхание после родов и характеризуется выраженным нарушением газообмена. Это одна из наиболее частых причин неонатальной смертности и заболеваемости. В Тиграе очень мало исследований перинатальной асфиксии, поэтому данное исследование направлено на оценку распространенности и связанных с ней факторов перинатальной асфиксии в комплексной специализированной больнице Айдер ОИТ, Тигрей, Эфиопия. Методы .План перекрестного исследования на базе учреждения был проведен среди новорожденных, поступивших в комплексную специализированную больницу Айдер с 1 января 2016 г. по 30 декабря 2017 г. Медицинские карты 267 новорожденных, поступивших в отделение интенсивной терапии новорожденных, были отобраны методом систематической выборки. , и соответствующая информация была собрана с помощью контрольного списка. Данные были проанализированы с использованием SPSS версии 20. Для определения распространенности асфиксии при рождении были рассчитаны описательные статистические данные, а также социально-демографические и акушерские данные.Для проверки связи между ассоциированными факторами и перинатальной асфиксией использовалась двоичная логистическая регрессия. Первый двумерный анализ был проведен для оценки ассоциации без контроля влияния других независимых переменных. Переменные со значением <0,25 были приспособлены к модели многомерной бинарной логистической регрессии. Наконец, переменные со значением <0,05 были выражены как ассоциированные факторы перинатальной асфиксии. Результатов . Из 267 новорожденных 48 новорожденных страдали перинатальной асфиксией, что составляет 18%.Продолжительные роды (, 95% ДИ: 1,73-15,63), присутствие мекония (, 95% ДИ: 1,34-12,98) и преэклампсия (, 95% ДИ: 2,22-28,37) были важными определяющими факторами асфиксии при рождении. Летальность от перинатальной асфиксии составила 37,5%. Заключение и рекомендации . Распространенность и смертность от асфиксии были высокими. Продолжительные роды, наличие мекония и преэклампсия были определяющими факторами асфиксии при рождении. Раннее выявление и вмешательство матерей из группы высокого риска должны осуществляться поставщиками медицинских услуг, а во время родов следует контролировать состояние матерей с помощью партограммы.
1. Введение
Перинатальная асфиксия определяется как неспособность новорожденного инициировать и поддерживать достаточное дыхание после родов и характеризуется выраженным нарушением газообмена [1].
Перинатальная асфиксия возникает из-за отсутствия кровотока или газообмена у плода на поздних сроках беременности, во время или после рождения новорожденного. Когда плацентарный (до рождения) или легочный (сразу после рождения) газообмен снижен или полностью прекращен, возникает частичный (гипоксия) или полный (аноксия) недостаток кислорода в жизненно важных органах.Это вызывает прогрессирующую гипоксемию и гиперкапнию. Если гипоксемия достаточно серьезна, в тканях и жизненно важных органах (мышцах, печени, сердце и, в конечном итоге, в головном мозге) возникает кислородная недостаточность. Последуют анаэробный гликолиз и лактоацидоз. Гипоксическая ишемическая энцефалопатия новорожденных относится к неврологическим последствиям перинатальной асфиксии [2, 3].
Диагноз перинатальной асфиксии ставится, когда pH артериальной крови пуповины <7, оценка по шкале APGAR (внешний вид, пульс, гримаса, активность и дыхание) составляет 0-3 на пятой минуте, и есть проявления со стороны центральной нервной системы. такие как судороги, летаргия, кома, гипотония или гипертония и дисфункция мультисистемных органов [4].
Заболеваемость перинатальной асфиксией в развитых странах составляет 2 случая на 1000 живорождений, но этот показатель в 10 раз выше в развивающихся странах, где нет адекватного доступа к медицинской помощи матерям и новорожденным. Из этих новорожденных, подвергшихся асфиксии, 15-20% умрут в неонатальном периоде, и около 25% выживших будут иметь постоянный неврологический дефицит [5].
По данным Всемирной организации здравоохранения, перинатальная асфиксия является одной из трех распространенных причин детской смертности в возрасте до пяти лет (11%) после преждевременных родов (17%) и пневмонии (15%) [6].На Африку приходится 11% всего населения мира, но на нее приходится более 25% неонатальной смертности в мире. Неонатальная смертность встречается у каждого четвертого ребенка в Африке [7]. Из-за высокой неонатальной смертности в Африке неонатальная смертность остается высокой во всем мире [8–10]. Новорожденные, рожденные в странах Африки к югу от Сахары, подвержены значительному риску перинатальной асфиксии. Приблизительно 280 000 случаев неонатальной смертности происходят в течение первого дня жизни из-за асфиксии при рождении [7, 8, 11, 12].
В Эфиопии неонатальная смертность составляет 29/1000 живорождений.Многие из этих смертей происходят в первые 48 часов возраста, и тем не менее снижение смертности невелико [13]. В Эфиопии перинатальная асфиксия является одной из ведущих причин неонатальной смертности, составляя 34% [14].
Несмотря на высокую смертность и заболеваемость, связанные с перинатальной асфиксией, распространенность и связанные с ней факторы перинатальной асфиксии недостаточно изучены в Эфиопии, и до сих пор нет сообщений о распространенности и связанных с ними факторах перинатальной асфиксии в исследуемой области.Таким образом, данное исследование направлено на оценку распространенности и сопутствующих факторов перинатальной асфиксии среди новорожденных, поступивших в комплексную специализированную больницу Айдер в Тыграйском районе.
2. Материалы и методы
2.1. Учебное заведение
Айдерская комплексная специализированная больница находится в городе Мекелле района Тыграй, примерно в 778 км от столицы Аддис-Абеба. Он начал свою деятельность как специализированный медицинский центр в 2008 году. Он предоставляет клинические услуги более чем 8 миллионам населения в районах обслуживания Тыграя, Афара и юго-восточной части регионального штата Амхара.Он предоставляет широкий спектр медицинских услуг как стационарным, так и амбулаторным пациентам для всех возрастных групп. Он также служит учебной больницей для студентов нескольких медицинских, стоматологических, медсестринских, акушерских, медицинских, фармацевтических, анестезиологических и медицинских лабораторий как для студентов, так и для аспирантов. Это вторая по величине больница в стране, которая насчитывает более 500 коек в четырех основных отделениях (внутренняя медицина, педиатрия, гинекология и акушерство, хирургия и другие специальности).В отделении педиатрии и детского здоровья работают 18 специалистов (педиатров общего профиля) и 6 узких специалистов. В отделении 43 ординатора и 30-40 медицинских интернов, которые сменяются каждые три месяца.
Отделение интенсивной терапии новорожденных (NICU) обслуживает около 200 новорожденных в месяц с 43 койками и одной палатой для ухода за матерями-кенгуру. В BSC работают 65 медсестер, 1 неонатолог, 1 педиатр общего профиля, 4 ординатора и 8 интернов. Он оснащен 4 лучистыми обогревателями, 6 инкубаторами, 5 аппаратами фототерапии и двумя аппаратами искусственной вентиляции легких.
2.2. Дизайн и период исследования
Был использован институциональный дизайн поперечного исследования и собраны данные для включения новорожденных, обследованных с 1 января 2016 г. по 30 декабря 2017 г.
2.2.1. Исходная популяция
Исходная популяция состояла из всех новорожденных, поступивших в комплексную специализированную больницу Айдер.
2.2.2. Популяция исследования
В исследование были включены все новорожденные, поступившие в комплексную специализированную больницу Айдер, отделение интенсивной терапии интенсивной терапии, в течение периода исследования и соответствующие критериям включения.
2.2.3. Критерии включения
Критерии включения включают всех новорожденных, поступивших в комплексную специализированную больницу Айдер с неделями или.
2.2.4. Критерии исключения
Новорожденные были исключены, если они страдают серьезными врожденными аномалиями или синдромами, например, NTD (дефект нервной трубки), имеют неполную документацию (нет параметров измерения матери или плода), находятся под наблюдением и имеют матери, прошедшие общее обследование. обезболивание.
2.3. Определение размера выборки и метод отбора проб
Размер выборки был определен с использованием формулы единой пропорции. Формула определения размера выборки: где — требуемый размер выборки, — пропорция, — уровень точности или допустимой ошибки. 95% доверительный интервал с уровнем точности 5% и распространенностью перинатальной асфиксии 21,1% использовался в больнице третичного уровня в Нигерии [15]. Общий размер выборки был рассчитан как 256. При уровне непредвиденных обстоятельств 10% окончательная выборка была определена как 282.Наконец, переменные со значением <0,05 были выражены как ассоциированные факторы перинатальной асфиксии. Субъекты исследования были отобраны с помощью метода систематической выборки, а соответствующая информация была собрана с использованием контрольного списка.
2.4. Переменные исследования
Зависимые и независимые переменные представлены в таблице 1.
2.5. Операционные определения
Новорожденными считаются новорожденные младше 28 дней.
Перинатальная асфиксия — это неспособность новорожденного инициировать и поддерживать адекватное дыхание после родов.
Оценка по шкале APGAR — это оценка, используемая в рамках ранней оценки состояния новорожденного.
Перинатальная асфиксия рассматривается, если оценка по шкале APGAR 5 th <7 или новорожденный не плакал или не нуждался в реанимации.
ГИЭ (гипоксическая ишемическая энцефалопатия) — нарушение функции центральной нервной системы в неонатальном периоде, вызванное ишемическим и гипоксическим инсультом.
Продолжительные работы — это общая продолжительность рабочего времени.
Врожденный порок развития — это физический дефект, присутствующий у новорожденного при рождении, который приводит к угнетению центральной нервной системы.
2.6. Процедуры сбора данных
Для сбора информации использовался формат сбора предварительно структурированных данных. Данные были собраны медицинскими интернами. Была получена соответствующая информация, которая включает неонатальную информацию (пол, гестационный возраст, вес при рождении и балл по шкале APGAR), информацию о матери (возраст, число матерей, место жительства, место родов, способ родов и проблемы во время беременности или родов).
2.7. Обработка и анализ данных
Данные были введены в SPSS (Статистический пакет для социальных наук) версии 20 (Армонк, Нью-Йорк: IBM Corp), очищены, закодированы и проверены на нормальность и полноту перед анализом.Описательная статистика использовалась для определения распространенности асфиксии при рождении и социально-демографического, а также акушерского анамнеза. Двумерный и множественный бинарный логистический регрессионный анализ был проведен для выявления связанных факторов PNA. Переменные со значением <0,25 во время двумерного анализа были включены в модель многомерной логистической регрессии. Наконец, переменные со значением <0,05 были выражены как ассоциированные факторы перинатальной асфиксии.
2,8. Этические соображения
Этическое разрешение было получено от Институционального наблюдательного совета (IRB) Колледжа медицинских наук Университета Мекелле.Разрешение было получено из офиса медицинского директора комплексной специализированной больницы Айдер; было получено письмо поддержки от главного клинического директора.
3. Результаты
Всего за период исследования в ОИТН было госпитализировано 3403 новорожденных, с использованием стандартизированной случайной выборки было собрано в общей сложности 282 истории болезни новорожденных, и 267 (94,7%) истории болезни новорожденных содержали полные данные. , а 15 пациентов были исключены из-за неполных данных. Из 267 новорожденных 48 страдали перинатальной асфиксией, что дает нам распространенность 18%.Большинство матерей новорожденных в исследовании (62,2%) были в возрасте от 20 до 35 лет. Более половины матерей (57,6%) были городскими жителями. Из обследованных новорожденных 58,8% () были мужчинами. Большинство новорожденных (82,2%) поступили в первые 72 часа жизни. Средний возраст новорожденных в исследовании при поступлении составлял 2,47 дня с SD (± 3 дня) и 1,25 (± 0,7 дня) для новорожденных с PNA. Большинство матерей новорожденных с ПНА (28, 58,3%) были в возрасте от 20 до 35 лет. Почти все новорожденные (98%) с ПНА были госпитализированы в течение первых 72 часов (таблица 1).
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||


 д.
д.


 Организм женщины насыщается необходимым количеством кислорода, который затем переносится плоду, нуждающемуся в этом элементе.
Организм женщины насыщается необходимым количеством кислорода, который затем переносится плоду, нуждающемуся в этом элементе.