Лечение вируса Эпштейна Барра (ВЭБ) в Санкт-Петербурге. Лечение инфекции герпеса 4 типа у взрослых и детей.
За всю жизнь можно не узнать, что когда-то давно (чаще всего в детстве) обычная респираторная инфекция сделала вас носителем вируса герпеса, название которого всегда напоминает об английских вирусологах, его описавших. Случилось это в 60-х годах прошлого века, и с тех пор выяснилось, что почти 90% населения планеты так или иначе уже проходили лечение вируса Эпштейна-Барра, пусть об этом не подозревали даже врачи. То есть, назначали терапию, традиционную для ОРВИ, вы выздоравливали, а виновник удобно устраивался в клетках вашего организма “спать” до тех пор, когда иммунитет даст слабину.
Сейчас известно, что болезнь Филатова, описанная одним из основателей русской педиатрической школы в конце XIX века и позднее, когда научились детально исследовать кровь, названная инфекционным мононуклеозом, случается из-за ВЭБ. Кроме того, этот вирус обвиняют в содействии возникновения ряда онкологических заболеваний (прежде всего, поражающих клетки крови).
Для диагностики и понимания как лечить вирус Эпштейна-Барра у детей и взрослых, потребуется довольно обширное обследование, в том числе иммунологическое, и тесты, подтверждающие ДНК вируса в крови. Более того, опытные инфекционисты и иммунологи смотрят на происходящие изменения в динамике, то есть, проводят несколько обследований на протяжении некоторого времени.
Симптоматика и лечение вируса Эпштейна-Барра у взрослых и детей
Как уже говорилось, впервые вы можете принять инфекцию за обычную простуду, либо вовсе не обратить внимание на легкое недомогание. Тем более, что чаще всего случается это в детстве, когда растущий организм откликается на любую инфекцию, но при этом неплохо с ней борется.
Однако, ослабленный иммунитет может стать причиной развития инфекционного мононуклеоза и у взрослых, и у малышей.
- Помимо общей слабости, болезнь проявляет себя изначально, как любая респираторная вирусная инфекция — лихорадкой, ощущением ломоты и тяжести в конечностях и, как правило, выраженной болью при глотании;
- Отличительным симптомом считается воспаление лимфатических узлов, которое может протекать очень болезненно, а из-за нарушения оттока лимфы не исключено возникновение лимфостаза, который становится причиной болей в расположенных поблизости суставах. Очевидно, что в данном случае лечение вируса Эпштейна-Барра у взрослых и детей необходимо. Иначе способность этого вируса не убивать клетки, а, напротив, стимулировать их расти и делиться, может привести к увеличению лимфоузлов;
- Нередко болезнь опускается по дыхательным путям, вызывая трахеит или бронхит;
- И еще один отличительный симптом, часто сопровождающий эту болезнь — поражение органов, отвечающих за кроветворение и очистку крови, — селезенки и печени.
 А это значит, что адекватное лечение ВЭБ инфекции у детей способно избавить от развития серьезной патологии в будущем;
А это значит, что адекватное лечение ВЭБ инфекции у детей способно избавить от развития серьезной патологии в будущем; - Заподозрить хроническую форму инфекционного мононуклеоза и вовремя начать лечение герпеса 4 типа, которым является ВЭБ, можно, обратив внимание на частые простуды, а также регулярно возникающие пузырьковые высыпания простого герпеса на губах или лице.
▷ Медицинский центр Eurolab
Общая характеристика
Вирус герпеса IV типа (Эпштейна–Барр) передается несколькими путями:
- воздушно капельным,
- перенатальным,
- половым,
- трансплацентарным.
Он может находится в организме человека на протяжении всей жизни и являться возбудителем таких заболеваний как:
- инфекционный мононуклеоз,
- назофарингеальная карцинома,
- лимфома Беркитта,
- синдром хронической усталости.
В детском возрасте вирус часто носит бессимптомный характер.
Показания для назначения
- обследование при мононуклеозоподобном синдроме, лимфаденопатии, гепатите неясной этиологии, рецидивирующих воспалительных заболеваниях ротовой полости, пневмонии, менингоэнцефалите,
- наличие сложной истории болезни акушерско-гинекологического характера у женщин,
- симптомы врожденной инфекции у новорожденных.

Клиническая значимость
Выявление и количественное определение ДНК вируса Эпштейна-Барр. Оценка вирусной нагрузки для решения вопросов лечения и контроля ее эффективности. Контроль персистенции и выделения вируса.
Методы исследований
Полимеразная цепная реакция в реальном времени
Материал для исследования
Цельная кровь, плазма периферической крови, ликвор, слюна, мазки из ротоглотки, биопсийный и аутопсийный материал, амниотическая жидкость, бронхоальвеолярный лаваж.
Правила подготовки пациента
Кровь
Стандартные условия. Утром натощак, через 8-12 часов после приема пищи. Допускается перерыв 6 часов после приема пищи (жирная пища должна быть исключена).
Соскоб из ротоглотки
Стандартные условия. Натощак или через 2-4 часа после еды. Перед взятием материала необходимо прополоскать рот кипяченой водой.
Слюна
Стандартные условия. В течении 30 минут до забора материала не есть, не пить не курить не чистить зубы. За сутки до анализа исключить: употребление спиртных напитков, попадание губной помады.
В течении 30 минут до забора материала не есть, не пить не курить не чистить зубы. За сутки до анализа исключить: употребление спиртных напитков, попадание губной помады.
Инфекционный мононуклеоз лечение в Минске
Инфекционный мононуклеоз – это широко распространенная вирусная инфекция, наиболее часто встречающаяся в раннем детстве или в позднем подростковом возрасте. Чаще всего возбудителем инфекционного мононуклеоза является вирус Эпштейна – Барр, относящийся к группе вирусов герпеса. Заболевание чаще развивается у молодых людей ранее не встречавшихся с данным вирусом. Очень редко болеют лица старше 40 лет.
Инфекционный мононуклеоз часто называют «болезнью поцелуев». Распространение инфекции происходит через контакт со слюной инфицированного человека: через поцелуи, реже вирус передается при кашле и чихании, совместном использовании посуды с человеком, инфицированным вирусом Эпштейна – Барр.
Инфекционный мононуклеоз может иметь как острое, так и постепенное развитие.
Данные симптомы включают:
- головную боль,
- лихорадку,
- усталость,
- боли в горле,
- появление налета на миндалинах,
- увеличение лимфатических узлов в области шеи, подмышек и паха,
- увеличение селезенки, печени,
- сыпь.
Такие симптомы, как лихорадка и боли в горле, обычно проходят в течение двух недель, усталость, увеличенные лимфатические узлы и селезенка – в течение нескольких недель. В большинстве случаев заболевание имеет благоприятный исход.
Для подтверждения диагноза инфекционного мононуклеоза необходимо сдать кровь на анализы. В диагностике инфекции применяется определение вирус специфических иммуноглобулинов классов М и G с использованием иммуноферментного анализа (ИФА), а также ДНК вируса методом полимеразной цепной реакции (ПЦР). Выявление антител к определенным группам антигенов вируса Эпштейна – Барр позволяет дифференцировать вирусносительство от текущей инфекции.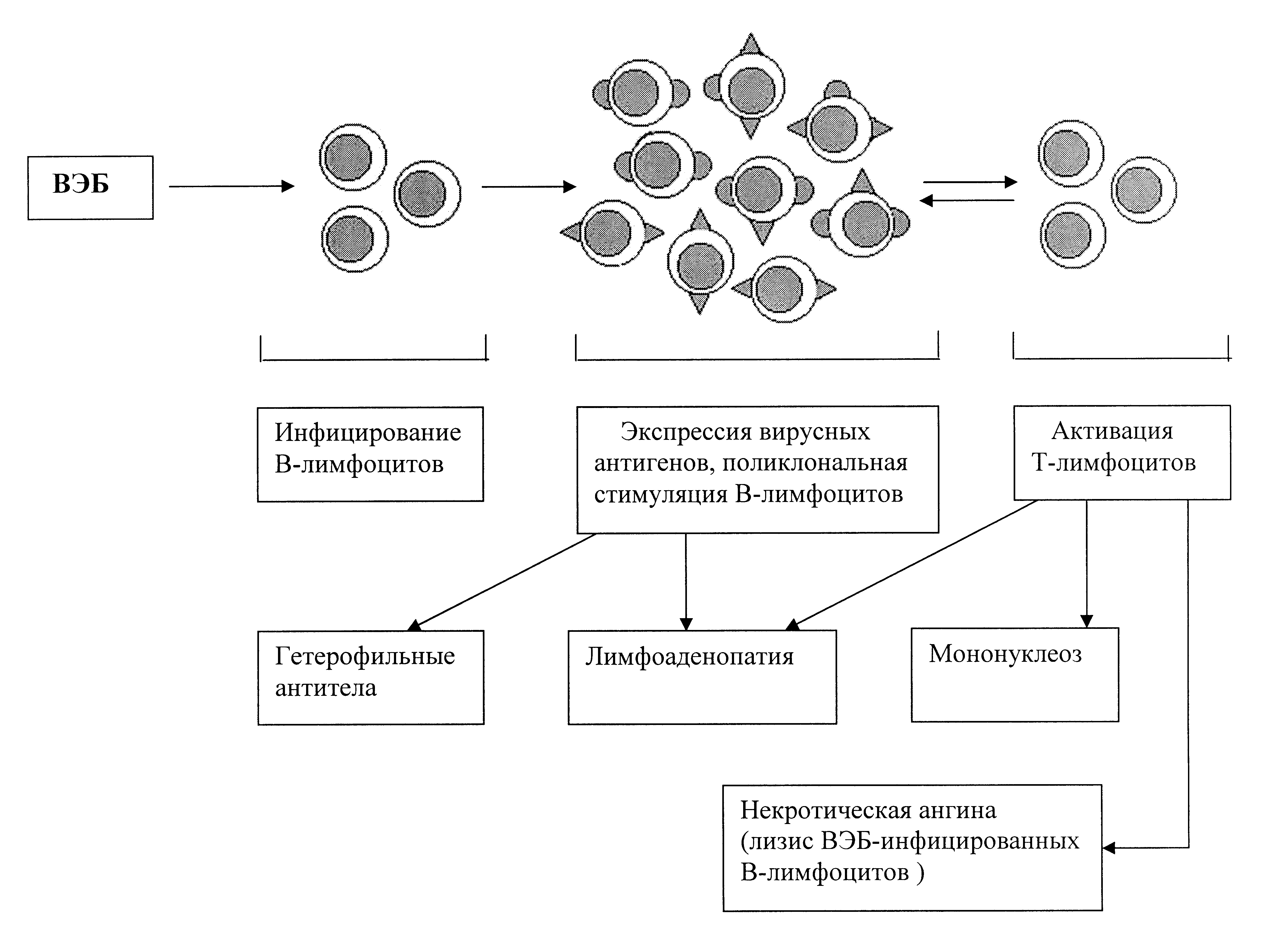
Терапия инфекционного мононуклеоза определяется лечащим врачом на основании:
- степени тяжести состояния;
- возраста;
- общего состояния здоровья, сопутствующих заболеваний;
- индивидуальной переносимости лекарственных препаратов и медицинских процедур.
Все необходимые исследования для диагностики инфекционного мононуклеоза Вы сможете пройти в медицинском центре «Биомедика», также у нас Вы сможете получить квалифицированную консультацию врача-инфекциониста по данному заболеванию.
Инфекционный мононуклеоз:Симптомы,Причины,Лечение | doc.ua
После того, как человек уже переболел инфекционным мононуклеозом, повторное заболевание не случается из-за выработки стойкого иммунитета к вирусу Эпштейн-Барр.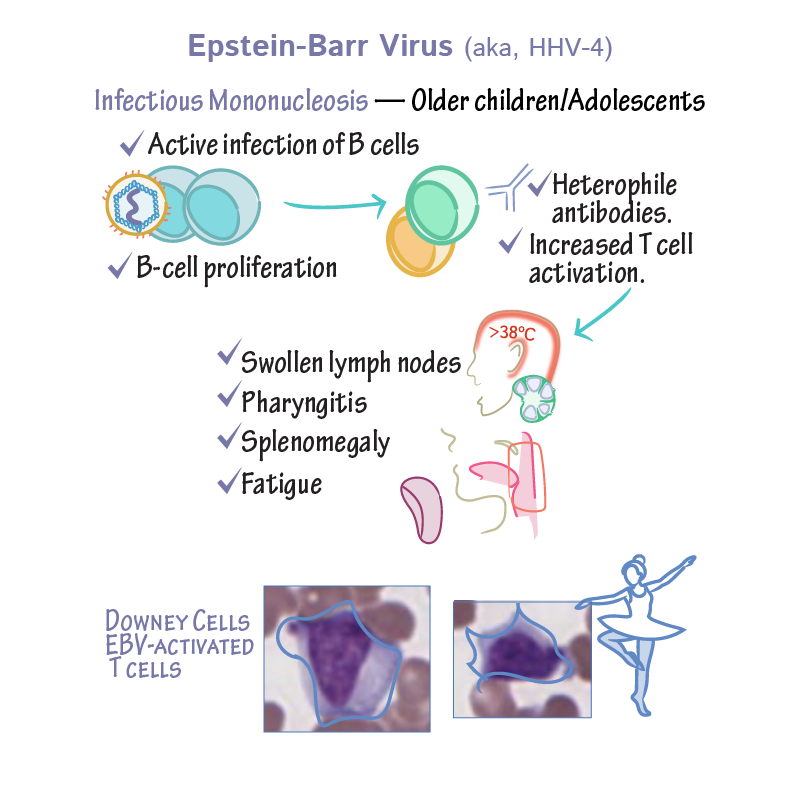
В самом начале инфицирования мононуклеоз проявляет себя как обычное простудное заболевание. У больного наблюдается:
- слабость во всем теле;
- недомогание;
- небольшое повышение температуры;
- легкий насморк.
Когда вирус распространяется по организму, начинают проявляться следующие симптомы инфекционного мононуклеоза:
- сильное повышение температуры и длительная лихорадка;
- увеличение лимфоузлов, которое может длиться до одного месяца;
- тонзиллит (воспаление миндалин), что приводит к затруднению дыхания через нос и глотания;
- боль в горле.
В период выздоровления болевые симптомы пропадают, температура тела нормализируется, печень, селезенка и лимфоузлы становятся нормальных размеров, улучшается общее самочувствие больного. Длительность выздоровления составляет от двух до четырех недель.
Виды
Мононуклеоз бывает типичной и атипичной формы. Типичная форма проходит с ярко выраженными симптомами инфекционного мононуклеоза. Во время атипичной формы заболевания симптомов может не быть или будут нехарактерные проявления:
Типичная форма проходит с ярко выраженными симптомами инфекционного мононуклеоза. Во время атипичной формы заболевания симптомов может не быть или будут нехарактерные проявления:
- в основном поражаются внутренние органы, что приводит к их увеличению;
- незначительная симптоматика, которая быстро проходит;
- бессимптомная форма, при которой человек выступает только носителем инфекции и сам при этом никак не страдает от вируса (определяется только с помощью анализов).
Также классифицируют инфекционный мононуклеоз по степени тяжести (легкая, среднетяжелая и тяжелая формы) и по течению заболевания (острый, осложненный, хронический и затяжной).
Мононуклеоз у детей младше двух лет наблюдается редко. Чаще всего болеют дети от трех лет и взрослые до сорока. При выявлении мононуклеоза в детском саду или школе карантин необязателен. Достаточно ежедневно проводить качественную влажную уборку.
Причины
Основной причиной заболевания мононуклеозом становится инфицированный человек (заболевший или носитель). Так как вирус передается воздушно-капельным и контактно-бытовым путем, обезопасить себя возможно только при знании о болезни другого человека. Большая вероятность заразиться данным заболеванием у людей с ослабленной иммунной системой. Пики распространения мононуклеоза наблюдаются в весенне-осенний период года.
Так как вирус передается воздушно-капельным и контактно-бытовым путем, обезопасить себя возможно только при знании о болезни другого человека. Большая вероятность заразиться данным заболеванием у людей с ослабленной иммунной системой. Пики распространения мононуклеоза наблюдаются в весенне-осенний период года.
Диагностика
Мононуклеоз диагностируют с помощью общего осмотра больного, сопоставления симптомов. Обязательно в таком случае назначается лабораторный анализ крови (проверка на наличие специфических клеток – мононуклеаров). Также проводятся лабораторные тесты на наличие антител ИФА и ДНК возбудителя. Часто назначают консультацию у врача-инфекциониста.
Лечение
При диагнозе инфекционный мононуклеоз лечение проводится в домашних условиях. Госпитализацию предлагают в основном детям и людям с острым течением болезни. Во время высокой температуры и лихорадки больным предписывается постельный режим. В случае сильного увеличения печени и проявления желтушности необходимо соблюдать диету под номером 5, при которой нужно исключить все жареные, копченые, жирные блюда, ограничить специи и потребление соли. Во всех случаях обязательно обильное потребление воды.
Во всех случаях обязательно обильное потребление воды.
Для снятия болевых ощущений в горле необходимо полоскать рот антисептическими препаратами, которые назначит врач. Также врачом выписываются противовирусные, противоаллергические и жаропонижающие препараты. Для поддержания организма назначают прием витаминных комплексов. В случаях осложнений – антибактериальные средства. При тяжелом течении заболевания, а также в случаях угрозы развития осложнений могут быть назначены короткие курсы гормональной терапии.
Осложнения
У ослабленных больных может развиться инфекционный хронический мононуклеоз. При несоблюдении лечения или несвоевременном обращении за квалифицированной медицинской помощью могут возникнуть осложнения в виде разрыва селезенки, пневмонии, угнетения кроветворения, удушья из-за увеличения миндалин в носоглоточной части, ангины, менингита.
Вирус инфекционного мононуклеоза обладает онкогенной активностью. Это значит, что после мононуклеоза возможно развитие более серьезных заболеваний. Поэтому следует периодически проходить лабораторный анализ крови для выявления возможных отклонений и своевременного их устранения. Если вдруг после перенесения болезни в анализе находят атипичные мононуклеары, назначают обязательную консультацию у врача-гематолога.
Поэтому следует периодически проходить лабораторный анализ крови для выявления возможных отклонений и своевременного их устранения. Если вдруг после перенесения болезни в анализе находят атипичные мононуклеары, назначают обязательную консультацию у врача-гематолога.
Профилактика
Для профилактики инфекционного мононуклеоза специальных мероприятий не проводят, так как он передается воздушно-капельным путем и у многих протекает практически бессимптомно.
Для того чтобы уменьшить риск заболевания, необходимо:
- рациональное и сбалансированное питание с исключением жареного, жирного, копченого или минимального употребления такой пищи;
- своевременно лечить хронические инфекции и поддерживать иммунитет;
- избегать прямого контакта с инфицированными людьми.
Что такое вирус Эпштейна-Барр и чем он опасен?
Вирус Эпштейна-Барр (ВЭБ) – это член семейства герпесвирусов. Как показывают исследования, 95% взрослого населения имеет антитела против этого распространенного вируса. Это говорит о том, что в какой-то период жизни абсолютное большинство взрослых обязательно заражаются этой инфекцией.
Это говорит о том, что в какой-то период жизни абсолютное большинство взрослых обязательно заражаются этой инфекцией.
Как правило, вирус остается незамеченным или проявляется в виде слабых симптомов. В некоторых случаях вирусная инфекция Эпштейна-Барра вызывает осложнения и способна провоцировать развитие серьёзных заболеваний, включая некоторые виды рака. Хотя в основном инфекция нацеливается на лейкоциты – клетки крови, участвующие в иммунных реакциях, – она способна нанести урон практически всем органам и системам организма.
Вирус передается при близком контакте от человека к человеку. Сразу после инфицирования признаки вируса Эпштейна-Барра могут не проявляться, хотя иногда появляется ряд симптомов, чаще всего – у детей.
Среди основных признаков инфицирования:
Это самое распространенное заболевание, связанное с ВЭБ. Мононуклеоз характеризуется сильной усталостью, развитием тонзиллита и/или фарингита, увеличением и болезненностью шейных лимфоузлов, а также повышением температуры. Хотя температура и больное горло, как правило, проходят в течение двух недель, усталость ощущается на протяжении нескольких месяцев.
Хотя температура и больное горло, как правило, проходят в течение двух недель, усталость ощущается на протяжении нескольких месяцев.
- Некоторые несерьёзные детские заболевания
Вирус Эпштейна-Барр у детей может вызывать ушные инфекции, диарею и другие нарушения в работе ЖКТ. Также в дополнение к проявляющимся симптомам мононуклеоза добавляются признаки простуды.
- Некоторые неврологические нарушения и патологии крови
В редких случаях первоначальное инфицирование ВЭБ вызывает неврологические нарушения, включая синдром Гийена–Барре и менингоэнцефалит. Среди других редких проявлений инфицирования – патологии крови или системы свертывания крови. Среди них отмечают анемию, болезнь Мошкович, гемолитико-уремический синдром, а также синдром диссеминированного внутрисосудистого свертывания.
Чем опасен вирус Эпштейна-Барр?Осложнения из-за инфекции ВЭБ встречаются редко, но могут угрожать жизни, если не обращать на них внимания. Разрыв селезенки встречается у 1-2 человек на 1000 больных инфекционным мононуклеозом. Второе потенциально смертельное, но поддающееся лечению осложнение – непроходимость дыхательных путей. Непроходимость развивается из-за увеличения лимфатических узлов и отёка воспаленных тканей, которые окружают дыхательные пути.
Разрыв селезенки встречается у 1-2 человек на 1000 больных инфекционным мононуклеозом. Второе потенциально смертельное, но поддающееся лечению осложнение – непроходимость дыхательных путей. Непроходимость развивается из-за увеличения лимфатических узлов и отёка воспаленных тканей, которые окружают дыхательные пути.
Как правило, вирус Эпштейн-Барр живет с инфицированным человеком в течение всей его жизни, хотя и очень редко вызывает серьёзные проблемы. Однако бывают случаи, когда ВЭБ связывают с развитием рака и другими опасными заболеваниями, включая:
- Лимфома Беркитта
Это заболевание имеет 3 разновидности: эндемическую, спорадическую или связанную с иммунодефицитом. Лимфома Беркитта возникает в период раннего инфицирования вирусом Эпштейн-Барр по причине поражения В-лимфоцитов. Спорадическая разновидность болезни поражает лимфоидную ткань кишечника и верхних дыхательных путей. Эндемическая лимфома часто поражает кости лица – особенно челюсть и глазницу у детей.
- Лимфома Ходжкина
Люди, которые перенесли инфекционный мононуклеоз, имеют более высокий риск столкнуться с лимфомой Ходжкина. Но не стоит паниковать. По словам специалистов из Американского онкологического общества, этот риск все равно крайне мал. Очень мало людей, инфицированных вирусом Эпштейна-Барр, сталкиваются с этим опасным заболеванием.
- Т-клеточная лимфома
Крайне редко инфекция становится причиной развития Т-клеточной лимфомы.
- Назофарингеальная карцинома
Многочисленные исследования показали, что этот вид рака связан с ВЭБ, так как генетический материал вируса содержится в раковых клетках больных карциномой. Хотя опять-таки, данный вид рака встречается крайне редко, поэтому паниковать не стоит. У большинства людей, которые сталкиваются с ВЭБ, назофарингеальная карцинома не развивается.
- Гематологические болезни
Иногда ВЭБ провоцирует развитие нарушений, связанных с аномальным ростом и функционированием некоторых компонентов крови. Примерами таких нарушений являются гемофагоцитарный лимфогистиоцитоз и лимфоматоидный гранулематоз.
Примерами таких нарушений являются гемофагоцитарный лимфогистиоцитоз и лимфоматоидный гранулематоз.
Несмотря на разнообразие осложнений и потенциальную угрозу для жизни, большинство людей не сталкивается даже с симптомами вируса Эпштейна-Барра. Часть инфицированных переносят только мононуклеоз, а до развития серьёзных заболеваний дело доходит крайне редко.
Какой врач лечит вирус Эпштейна-Барра?Для того чтобы узнать, заражены ли вы вирусом, необходимо обратиться к терапевту, а в случае с ребенком – к педиатру. Доктор проведет осмотр и назначит анализ крови на антитела к вирусу Эпштейна-Барр.
Если симптомы инфекции не проходят долгое время и стали хроническими, пациента могут направить к инфекционисту или иммунологу. В случае проявления неврологических нарушений человеку необходимо обратиться к неврологу. Увеличенная селезенка просигнализирует о том, что больному необходим прием гематолога. Решение о целесообразности направления к какому-либо из этих специалистов принимает терапевт.
Специальных лекарств для борьбы с ВЭБ не существует. Некоторым пациентам при жалобах на отёки горла или увеличение селезенки назначают кортикостероиды. Если пациент столкнулся с инфекционным мононуклеозом, его лечение ограничивается отдыхом, питьем большого количества жидкости и разнообразным питанием. Подробнее о лечении мононуклеоза читайте в этой статье.
Для проведения диагностики, а также лечения мононуклеоза записывайтесь на прием к терапевту.
Источники:
- The Broad Spectrum of EBV Disease, MedicineNet,
- EPSTEIN-BARR VIRUS, Public Health Agency of Canada,
- Epstein-Barr Virus Infection, eMedicineHealth,
- What Are the Risk Factors for Hodgkin Disease, American Cancer Society.
Страница статьи : Вопросы вирусологии
Straus S.E. The chronic mononucleosis syndrome. J. Infect. Dis. 1988; 157(3): 405-12. Doi: https://doi.org/10.1093/infdis/157.3.405
Hellmann D., Cowan M.J., Ammann A.J., Wara D.W., Chudwin D., Chang R.S. Chronic active Epstein-Barr virus infections in two immunodeficient patients. J. Pediatr. 1983; 103(4): 585-8.
Cohen J.L. Epstein-Barr virus infection. N. Engl. J. Med. 2000; 343(7): 481-92. Doi: https://doi.org/10.1056/NEJM200008173430707
Thorley-Lawson D.A. Epstein-Barr virus: exploiting the immune system. Nat. Rev. Immunol. 2001; 1(1): 75-82. Doi: https://doi.org/10.1038/35095584
Laichalk L.L., Thorley-Lawson D.A. Terminal differentiation into plasma cells initiates the replicative cycle of Epstein-Barr virus in vivo. J. Virol. 2005; 79(2): 1296-307. Doi: https://doi.org/10.1128/JVI.79.2.1296-1307.2005
Kieff E., Rickinson A.B. Epstein-Barr virus and its replication. In: Knipe D.M., Howley P.M, eds. Fields Virology. Philadelphia: Lippincott Williams & Wilkins; 2007.
Laichalk L.L., Hochberg D., Babcock G.J., Freeman R.B., Thorley-Lawson D.A. The dispersal of mucosal memory B cells: evidence from persistent EBV infection. Immunity. 2002; 16(5): 745-54.
Amyes E., Hatton C., Montamat-Sicotte D., Gudgeon N., Rickinson A.B., McMichael A.J., et al. Characterization of the CD4+ T Cell Response to Epstein-Barr Virus during Primary and Persistent Infection. J. Exp. Med. 2003; 198(6): 903-11. Doi: https://doi.org/10.1084/jem.20022058
Marrão G., Habib M., Paiva A., Bicout D., Fallecker C., Franco S., et al. Epstein-Barr virus infection and clinical outcome in breast cancer patients correlate with immune cell TNF-α/IFN-γ response. BMC Cancer. 2014; 14: 665. Doi: https://doi.org/10.1186/1471-2407-14-665
Kimura H., Hoshino Y., Kanegane H., Tsuge I., Okamura T., Kawa K., et al. Clinical and virologic characteristics of chronic active Epstein-Barr virus infection. Blood. 2001; 98(2): 280-6. Doi: https://doi.org/10.1182/blood.v98.2.280
Zhao X., Wu H., Lu H., Li G., Huang Q. Lamp: A database linking antimicrobial peptides. PLoS One. 2013; 8(6): e66557. Doi: https://doi.org/10.1371/journal.pone.0066557
Conlon J.M., Sonnevend A. Antimicrobial peptides in frog skin secretions. Methods Mol. Biol. 2010; 618: 3-14. Doi: https://doi.org/10.1007/978-1-60761-594-1_1
Bahar A.A., Ren D. Antimicrobial peptides. Pharmaceuticals (Basel). 2013; 6(12): 1543-75. Doi: https://doi.org/10.3390/ph6121543.
Altfeld M., Gale M. Innate immunity against HIV-1 infection. Nat. Immunol. 2015; 16(6): 554-62. Doi: https://doi.org/10.1038/ni.3157
Meije Y., Tonjes R.R., Fishman J.A. Retroviral restriction factors and infectious risk in xenotransplantation. Am. J. Transplant. 2010; 10(7): 1511-6. Doi: https://doi.org/10.1111/j.1600-6143.2010.03146.x
Chernysh S., Kim S., Bekker G., Pleskach V.A., Filatova N.A., Anikin V.B., et al. Antiviral and antitumor peptides from insects. Proc. Natl. Acad. Sci. U.S.A. 2002; 99(20): 12628-32. Doi: https://doi.org/10.1073/pnas.192301899
Mabbott N.A., Brown K.L., Manson J., Bruce M.E. T-lymphocyte activation and the cellular form of the prion protein. Immunology. 1997; 92(2): 161-5. Doi: https://doi.org/ 10.1046/j.1365-2567.1997.00331.x
Lee N., Bae S., Kim H., Kong J.M., Kim H.R., Cho B.J., et al. Inhibition of lytic reactivation of Kaposi’s sarcoma-associated herpesvirus by alloferon. Antivir. Ther. 2011; 16(1): 17-26. Doi: https://doi.org/10.3851/IMP1709
Bae S., Oh K., Kim H., Kim Y., Kim H.R., Hwang Y.I., et al. The effect of alloferon on the enhancement of NK cell cytotoxicity against cancer via the up-regulation of perforin/granzyme B secretion. Immunobiology. 2013; 218(8): 1026-33. Doi: https://doi.org/10.1016/j.imbio.2012.12.002
Kim Y., Lee S.K., Bae S., Kim H., Park Y., Chu N.K., et al. The anti-inflammatory effect of alloferon on UVB-induced skin inflammation through the down-regulation of pro-inflammatory cytokines. Immunol. Lett. 2013; 149(1-2): 110-8. Doi: https://doi.org/10.1016/j.imlet.2012.09.005
Kuczer M., Dziubasik K., Midak-Siewirska A., Zahorska R., Łuczak M., Konopińska D. Studies of insect peptides alloferon, Any-GS and their analogues. Synthesis and antiherpes activity. J. Pept. Sci. 2010; 16(4): 186-9. Doi: https://doi.org/10.1002/psc.1219
Kuczer M., Majewska A., Zahorska R. New alloferon analogues: synthesis and antiviral properties. Chem. Biol. Drug Des. 2013; 81(2): 302-9. Doi: https://doi.org/10.1111/cbdd.12020
Kuczer M., Czarniewska E., Majewska A., Różanowska M., Rosiński G., Lisowski M. Novel analogs of alloferon: Synthesis, conformational studies, pro-apoptotic and antiviral activity. Bioorg. Chem. 2016; 66: 12-20. Doi: https://doi.org/10.1016/j.bioorg.2016.03.002
Kragsbjerg P. Chronic active mononucleosis. Scand. J. Infect. Dis. 1997; 29(5): 517-8.
Gustafson E.A., Chillemi A.C., Sage D.R., Fingeroth J.D. The Epstein-Barr virus thymidine kinase does not phosphorylate ganciclovir or acyclovir and demonstrates a narrow substrate specificity compared to the herpes simplex virus type 1 thymidine kinase. Antimicrob. Agents Chemother. 1998; 42(11): 2923-31.
Хахалин Л.Н., Абазова Ф.И. Ацикловир при лечении острых и рецидивирующих герпесвирусных инфекций. Клиническая фармакология и терапия. 1995; 4(4): 78-81
Cohen J.I. Optimal Treatment for Chronic Active Epstein-Barr Virus Disease. Pediatr. Transplant. 2009; 13(4): 393-6. Doi: https://doi.org/10.1111/j.1399-3046.2008.01095.x
De Paor M., O’Brien K., Fahey T., Smith S.M. Antiviral agents for infectious mononucleosis (glandular fever). Cochrane Database Syst Rev. 2016; 12: CD011487. Doi: https://doi.org/10.1002/14651858
Казмирчук В.Е., Мальцев Д.В. Клиника, диагностика и лечение герпесвирусных инфекций человека. Киев: Феникс; 2009
Martinez J.P., Sasse F., Brönstrup M., Diez J., Meyerhans A. Antiviral drug discovery: broad-spectrum drugs from nature. Nat. Prod. Rep. 2015; 32(1): 29-48. Doi: https://doi.org/10.1039/C4NP00085D
Коновалова Н.В., Храменко Н.И., Величко Л.Н., Юрченко Л.А. Роль уровня интерферонов α и γ в крови больных увеитами вирусной этиологии под влиянием лечения препаратом аллокин-альфа. Точка зрения. Восток — Запад. 2018; (4): 26-9. Doi: https://doi.org/10.25276/2410-1257-2018-4-26-29
Серебряков М.Ю., Тищенко М.С., Воронов А.В., Салимов А.Г., Сметанина С.Е., Платонова Т.К. и др. Новые подходы к лечению больных ВЭБ-инфекцией. Сборник научных трудов по препарату Аллокин-альфа. М.; 2016.
Мясников назвал простой способ профилактики вируса Эпштейна-Барр
Вирус Эпштейна-Барр считается одним из самых распространенных. Александр Мясников в эфире канала «Россия 1» сообщил, что носителями является 95% людей. Телеведущий и врач заметил, что правильный образ жизни и физические нагрузки способствуют повышению иммунитета, который «контролирует» вирус. О факторах риска активации вируса Эпштейна-Барр и мерах профилактики Мясников рассказал в программе «О самом главном».
90% людей из всех носителей этого вируса заражаются им еще в детстве, при этом они переболевают бессимптомно. Предотвратить его распространение, как сообщил врач, мы не можем. Однако, по словам Мясникова, вирус Эпштейна-Барр, активируясь, вызывает такие опасные болезни, как лимфома Ходжкина, рак головы и шеи, играет роль в развитии рассеянного склероза, ведет к онкологическим заболеваниям крови. Но пока его контролирует наша иммунная система, бояться нечего.
Правда, все, что снижает человеческий иммунитет, может спровоцировать активацию вируса. К факторам риска относятся стресс, недосыпание, несбалансированный рацион питания, отсутствие лечения при хронических заболеваниях, иммунодефицит и отсутствие физических нагрузок.
«Это лишний раз подчеркивает, что надо вести правильный образ жизни и двигаться», – сообщил телеведущий.
Он добавил, что физические нагрузки дают людям силы сопротивляться болезням. Так, когда к нему в кабинет заходит пациент, Александр Леонидович сразу замечает разницу между активным и бодрым человеком и тем, кто ведет малоподвижный образ жизни и страдает от одышки.
«Если ты активный физически, значит, активен и ментально. Значит, у тебя иммунитет сильный. Потому что в здоровом теле – здоровый иммунитет», – заключил телеведущий. Как считает врач, люди не должны помогать вирусам распространяться, а потому следует прилагать все необходимые усилия для поддержания иммунитета.
«Давайте противопоставлять болезням силу духа и движение и бороться с нашими недостатками. И тогда все у нас будет хорошо», – заверил зрителей Александр Мясников.
Лабораторное тестирование вируса Эпштейна-Барра | CDC
Вирус Эпштейна-Барра (EBV), также известный как вирус герпеса человека 4, представляет собой гамма-вирус герпеса, который встречается только у людей. Лабораторные исследования могут помочь определить, подвержен ли человек заражению ВЭБ, недавно он или перенес инфекцию.
Медицинские работники могут проводить тестирование на антитела к следующим антигенам, связанным с EBV:
На этой микрофотографии изображены лейкозные клетки, содержащие вирус Эпштейна-Барра, с использованием метода окрашивания FA.
- Антиген вирусного капсида (VCA)
- Anti-VCA IgM появляется на ранней стадии инфицирования EBV и обычно исчезает в течение четырех-шести недель.
- Anti-VCA IgG появляется в острой фазе EBV-инфекции, достигает пика через две-четыре недели после начала, слегка снижается, а затем сохраняется на протяжении всей жизни человека.
- Ранний антиген (EA)
Anti-EA IgG появляется в острой фазе болезни и обычно падает до неопределяемого уровня через три-шесть месяцев.У многих людей обнаружение антител к EA является признаком активной инфекции. Однако 20% здоровых людей могут иметь антитела против EA в течение многих лет. - Ядерный антиген EBV (EBNA)
Антитело к EBNA, определенное стандартным иммунофлуоресцентным тестом, не выявляется в острой фазе инфекции EBV, но медленно проявляется через два-четыре месяца после появления симптомов и сохраняется на протяжении всего остального периода. жизнь. Другие иммуноферментные анализы EBNA могут давать ложноположительные результаты. - Тест на одно пятно
Тест на одно пятно не рекомендуется для общего использования.Антитела, обнаруживаемые Monospot, могут быть вызваны другими причинами, кроме инфекционного мононуклеоза. Более того, исследования показали, что Monospot дает как ложноположительные, так и ложноотрицательные результаты. Например, гетерофильные антитела, обнаруживаемые Monospot, часто отсутствуют у детей с инфекционным мононуклеозом. В лучшем случае тест Monospot может указывать на то, что у человека типичный случай инфекционного мононуклеоза, но не подтверждает наличие инфекции EBV.
Интерпретация тестов на антитела к ВЭБ
Тесты на антителак ВЭБ обычно не нужны для диагностики инфекционного мононуклеоза.Однако могут потребоваться специфические тесты на антитела для определения причины заболевания у людей, у которых нет типичного случая инфекционного мононуклеоза или есть другие заболевания, которые могут быть вызваны инфекцией EBV. Симптомы инфекционного мононуклеоза обычно проходят в течение четырех недель. Если человек болеет более шести месяцев и не имеет лабораторно подтвержденного диагноза ВЭБ-инфекции, следует рассмотреть другие причины хронического заболевания или синдрома хронической усталости.
Интерпретация тестов на антитела к ВЭБ требует знакомства с этими тестами и доступа к клинической информации пациента.
Интерпретация тестов на антитела к ВЭБ и диагностика инфекции ВЭБ резюмируется следующим образом:
- Восприимчивость к инфекции
Считается, что люди восприимчивы к ВЭБ-инфекции, если у них нет антител к VCA. - Первичная (новая или недавняя) инфекция
Считается, что люди имеют первичную EBV-инфекцию, если у них есть анти-VCA IgM, но нет антител к EBNA. Другие результаты, которые убедительно указывают на первичную инфекцию, — это высокий или повышающийся уровень анти-VCA IgG и отсутствие антител к EBNA после как минимум четырех недель болезни.Излечение болезни может произойти до того, как появятся диагностические уровни антител. В редких случаях у людей с активной инфекцией ВЭБ может не быть обнаруживаемых антител, специфичных к ВЭБ. - Инфекция в прошлом
Наличие антител как к VCA, так и к EBNA свидетельствует о перенесенной инфекции (от нескольких месяцев до лет назад). Поскольку более 90% взрослых были инфицированы ВЭБ, у большинства взрослых обнаруживаются антитела к ВЭБ от инфекции годами ранее. Высокие или повышенные уровни антител могут присутствовать в течение многих лет и не являются признаком недавней инфекции.
Тестирование парных образцов сыворотки в острой фазе и в фазе выздоровления не помогает различать недавние и перенесенные ВЭБ-инфекции. В большинстве случаев ответ антител происходит быстро во время первичной инфекции EBV. Клинические проявления инфекционного мононуклеоза возникают одновременно с появлением антител IgG и IgM к VCA. Однако структура антител нестабильна до появления симптомов.
Оптимальное лечение хронической активной болезни, вызванной вирусом Эпштейна-Барра
Вирус Эпштейна-Барра (ВЭБ) — это широко распространенный вирус, которым заражено не менее 95% населения.Большинство людей инфицированы в младенчестве и раннем детстве и протекают бессимптомно или имеют неспецифические симптомы (1). Заражение ВЭБ подростков и молодых людей часто приводит к инфекционному мононуклеозу с лихорадкой, лимфаденопатией, ангиной и спленомегалией. Дополнительные признаки и симптомы могут включать усталость, головную боль, гепатомегалию и сыпь. EBV также связан с рядом злокачественных новообразований, включая болезнь Ходжкина, В-клеточные лимфомы и карциному носоглотки. За исключением последнего заболевания, ВЭБ присутствует в В-клетках, где он может приводить к литической инфекции, образованию вирусных частиц или латентной инфекции с различными типами экспрессии вирусных генов.ВЭБ может привести к смертельному исходу у некоторых хозяев. У мужчин с Х-сцепленным лимфопролиферативным заболеванием часто развивается смертельный инфекционный мононуклеоз во время первичной ВЭБ-инфекции. Те, кто выживает после болезни, часто страдают гипогаммаглобулинемией и имеют повышенный риск развития В-клеточных лимфом.
Хроническая активная болезнь EBV (CAEBV) — очень редкое заболевание в Соединенных Штатах и Европе, но чаще встречается в Азии и Южной Америке. В отличие от большинства заболеваний, связанных с EBV, подавляющее большинство случаев CAEBV в Азии и Южной Америке связано с EBV, присутствующим либо в Т-клетках, либо в NK-клетках.Напротив, EBV часто находится в B-клетках у пациентов с CAEBV в Соединенных Штатах. Это заболевание определяется как (а) начинается с острой инфекции EBV, имеет заметно повышенный уровень антител против EBV или имеет заметно повышенный уровень ДНК EBV в крови (<300 копий / мкг ДНК), (b) гистологические доказательства инфильтрации органов с клетками, инфицированными вирусом, и (c) обнаружение белка или нуклеиновой кислоты EBV в ткани (2, 3). Сообщается, что CAEBV является клональным, олигоклональным или поликлональным заболеванием (4).
Большинство пациентов с CAEBV имеют лихорадку, дисфункцию печени и спленомегалию. Около половины пациентов страдают лимфаденопатией, тромбоцитопенией и анемией (3). Другие частые симптомы (встречающиеся у 20–40% пациентов) включают гиперчувствительность к укусам комаров, сыпь, гемофагоцитарный синдром и аневризмы коронарных артерий. Менее распространенными признаками являются кальциноз базальных ганглиев, язвы в ротовой полости, лимфома, интерстициальная пневмония и заболевание центральной нервной системы. Наличие тромбоцитопении, начинающейся в возрасте 8 лет и старше, и инфицирование Т-лимфоцитов EBV было связано с худшим прогнозом (5).Смерть часто наступает из-за печеночной недостаточности, злокачественной лимфомы или оппортунистических инфекций.
При CAEBV было отмечено несколько иммунологических отклонений. Пациенты с заболеванием Т- или NK-клеток часто имеют повышенные уровни про- и противовоспалительных цитокинов, включая интерлейкин (IL) -1β, интерферон (IFN) -γ, IL-10, IL-13, IL-15, фактор некроза опухоли ( TNF) -α и трансформирующий фактор роста (TGF) -β (4, 6). Нарушение активности естественных киллеров (NK), активности лимфокин-активированных киллеров (LAK) и EBV-специфической цитотоксической активности Т-лимфоцитов было зарегистрировано у 11 пациентов с CAEBV по сравнению с контрольной группой (7).EBV-специфические CD8 + Т-клетки часто очень низкие или неопределяемые при CAEBV (8), и сообщалось о нарушении цитотоксических Т-клеточных ответов на EBV-инфицированные NK-клетки (9). В одном сообщении, EBV-специфическая цитотоксическая активность Т-лимфоцитов была нарушена как у детей с CAEBV, так и у их родителей (10).
Этиология хронического активного ВЭБ неизвестна. Ранние исследования предположили, что болезнь может быть вызвана мутантными штаммами EBV, у которых нарушена латентность, и может привести только к литической инфекции (11).Однако последующее исследование показало, что тот же литический штамм присутствовал в контроле (12). Внимание сосредоточено на генетической аномалии клетки-хозяина. В одном большом исследовании 50% пациентов имели хромосомные аномалии (3). CAEBV имеет некоторые общие черты с Х-сцепленным лимфопролиферативным заболеванием, которое возникает из-за мутации в SAP (белок, связанный с SLAM). У многих пациентов с CAEBV развивается гемофагоцитарный синдром; некоторые пациенты с семейным гемофагоцитарным лимфогистиоцитозом имеют мутации в перфорине. Таким образом, внимание было сосредоточено на генах SAP и перфоринов как на возможных причинах CABEV.На сегодняшний день ни один случай CAEBV не был связан с мутациями в SAP (3, 13, неопубликованные данные Cohen et al.), В то время как сообщалось об одном случае, который был вызван мутациями в обоих аллелях гена перфорина (14). В последнем случае был отмечен гемофагоцитарный синдром, и у пациента была незрелая форма перфорина и нарушение активности цитотоксических Т-лимфоцитов (CTL) на основании анализа in vitro. Профили транскрипции клеток пациентов и контрольной группы показали, что 3 гена — гуанилатсвязывающие белки 1 и 5 и белок 6, индуцированный фактором некроза опухоли — были активированы у пациентов с CAEBV (15).
Для лечения CAEBV было испробовано множество средств. В то время как отдельные сообщения предполагают, что противовирусная терапия (например, ацикловир, ганцикловир, видарабин) может быть эффективной в некоторых случаях CAEBV (16, 17, 18), противовирусная терапия обычно неэффективна для этого заболевания. Эти агенты ингибируют вирусную ДНК-полимеразу и, следовательно, ингибируют репликацию EBV в литически инфицированных клетках, которые экспрессируют вирусную полимеразу. EBV-инфицированные NK или Т-клетки пациентов с CAEBV обычно экспрессируют латентные (ядерный антиген EBV [EBNA] -1, латентный мембранный белок [LMP] -1, LMP2A), но не литические (EBV BZLF1, гликопротеин 350) транскрипты вирусных генов ( 4).Репликация латентного ВЭБ в пролиферирующих В-клетках не требует вирусной ДНК-полимеразы, и поэтому противовирусная терапия обычно неэффективна. Иммуноглобулиновая терапия, которая может нейтрализовать бесклеточный вирус, не увенчалась успехом.
Иммунодепрессанты, такие как кортикостероиды и циклоспорин, часто используются для временного уменьшения симптомов у пациентов с CAEBV. Эти агенты оказались успешными для лечения гемофагоцитарного синдрома, который является частым осложнением CAEBV (19).Однако необходимо лечить и основное заболевание, и эти агенты не помогли вылечить пациентов с CAEBV (20). Иммунодепрессанты могут подавлять иммунный ответ на ВЭБ и могут способствовать дальнейшему размножению инфицированных вирусом клеток.
Иммуномодулирующая терапия также была опробована для лечения CAEBV. Сообщалось, что IFN-α (21) и IFN-γ (22) вызывают ремиссии у некоторых пациентов с CAEBV; однако о долгосрочном наблюдении не сообщалось. Сообщалось, что один пациент ответил на ИЛ-2 (23).Однако большинство пациентов не ответили на эти методы лечения (20). Цитотоксическая химиотерапия также использовалась для лечения CAEBV. Были использованы различные агенты, включая циклофосфамид, антрациклины, винкристин, этопозид и преднизон. В большинстве случаев эти агенты в лучшем случае дают временный эффект, но не являются лечебными, и болезнь продолжает прогрессировать с течением времени.
Иммуноклеточная терапия успешно применялась при лечении лимфопролиферативного заболевания EBV, которое возникает после трансплантации солидных органов или гемопоэтических стволовых клеток.Аутологичные клетки LAK, лимфоциты от HLA-идентичных братьев и сестер и аутологичные EBV-специфические CTL успешно использовались для лечения пациентов с посттрансплантационным лимфопролиферативным заболеванием у реципиентов трансплантата твердых органов. Аутологичные ВЭБ-специфические цитотоксические Т-клетки использовались для лечения стойкого активного ВЭБ в одном исследовании (24). Это заболевание определялось как лихорадка, утомляемость, лимфаденопатия, повышенные титры антител против EBV и повышенные уровни ДНК EBV в крови. Однако патология ткани не требовалась для постановки диагноза, болезнь, вероятно, была вызвана EBV в B-клетках, и течение было гораздо менее тяжелым, чем в большинстве случаев CAEBV.Аутологичные ВЭБ-специфические CTL были успешными в 4 из 5 случаев с периодом наблюдения от 6 до 36 месяцев.
Инфузии ВЭБ-специфических цитотоксических Т-лимфоцитов от HLA-идентичного брата мальчику с CAEBV приводили к временному снижению ДНК ВЭБ в плазме и снижению уровней TNF-α в сыворотке; однако пациент умер от инфекции через 4 недели после последней инфузии (25). В другом сообщении (26) пациент с CAEBV получил 13 доз клеток LAK, а затем 4 дозы аутологичных CTL.В то время как у пациента отмечалось временное улучшение со снижением температуры и вирусной нагрузки, панцитопения сохранялась. Второй пациент с NK-клетками CAEBV получил 4 дозы аутологичных CTL; однако вирусная нагрузка и дисфункция печени не улучшились (26). Авторы пришли к выводу, что эффект от этих методов лечения был очень ограниченным.
Соответствующий родственный миелоаблатив (27, 28), подобранный родственный немиелоаблативный (29, 30, 31), подобранный неродственный миелоаблативный (31, 32) и трансплантация стволовых клеток пуповинной крови (33, 34), как сообщалось, были успешными при отчеты о случаях заболевания CAEBV.Важно отметить, что большинство отчетов о трансплантации CAEBV представляют собой отчеты о случаях, описывающих одного или нескольких пациентов, и поэтому часто сообщают об успешных случаях. В наибольшей серии из одного учреждения 8 из 15 пациентов с CAEBV были живы при среднем сроке наблюдения 40 месяцев (31). Семь пациентов умерли в среднем через 3 месяца после трансплантации; 3 пациента умерли от причин, связанных с трансплантацией, 3 — от рецидива болезни и 1 — от энцефаломиелита. Пожилой возраст на момент постановки диагноза, более высокая нагрузка ДНК ВЭБ в плазме на момент постановки диагноза и более длительное время между началом инфекции и постановкой диагноза CAEBV коррелировали с более плохим прогнозом после трансплантации.
В статье в этом выпуске журнала Pediatric Transplantation (35) описаны два пациента с CAEBV. У обоих пациентов была низкая EBV-специфическая активность CTL, но нормальная активность NK-клеток до трансплантации. У одного пациента был EBV в Т-клетках, а у другого — вирус в NK-клетках. Оба пациента были пересажены в течение 6 месяцев после постановки диагноза CAEBV. После трансплантации костного мозга у обоих пациентов был отличный ответ с быстрым восстановлением EBV-специфической активности CTL и резким падением уровня ДНК EBV в крови.Uehara et al. (29) и Yoshiba et al. (30) сообщили о пациентах, перенесших аллогенную немиелоаблативную трансплантацию стволовых клеток по поводу CAEBV; в то время как EBV-специфическая активность CTL не сообщалась до трансплантации, EBV-специфические CTL были обнаружены через 120 дней (30) и один год (29) после трансплантации.
Как трансплантация может вылечить CAEBV? Цитотоксическая химиотерапия может снизить нагрузку на лимфоциты, инфицированные ВЭБ, убить супрессорные (или регуляторные) Т-клетки или освободить место в костном мозге для новых стволовых клеток.Пересаженные стволовые клетки могут убить оставшиеся EBV-инфицированные лимфоциты и обеспечить новую иммунную систему, способную контролировать вирус.
Что ждет пациентов с CAEBV в будущем? Gotoh et al. (31) сообщили, что пациенты с CAEBV могут иметь более высокий уровень осложнений, связанных с трансплантацией, чем другие пациенты из-за полиорганной недостаточности. Таким образом, следует разработать более безопасные альтернативы трансплантации. Более поздние исследования ВЭБ-специфичных CTL нацелены на специфические вирусные белки.Т- или NK-клетки многих пациентов с CAEBV экспрессируют EBNA-1, LMP1 и LMP2; однако клетки могут не экспрессировать белки EBNA-2 (4) или EBNA-3 (36). Белки EBNA-3 представляют собой иммунодоминантные эпитопы, распознаваемые большинством EBV-специфичных CD8 + Т-клеток у здоровых людей (37). Следовательно, CTL, специфичные для EBV LMP1 и LMP2, могут быть более эффективными, чем общие EBV-специфические Т-клетки (которые преимущественно распознают EBNA-3) для пациентов с CAEBV. LMP2-специфические Т-клетки недавно были использованы для лечения пациентов с EBV-положительными лимфомами, которые экспрессируют EBNA-1, LMP1, LMP2, но не EBNA-2 или EBNA-3 (38).Таким образом, лечение, направленное против определенных белков EBV, может обеспечить более безопасную и более специфическую терапию CAEBV в будущем.
Исследованиеможет предложить новый способ борьбы с вирусом Эпштейна-Барра
28 мая 2020 г., 10:00
Санакар Сваминатан, доктор медицины, Динеш Верма, доктор философииГруппа исследователей из Университета здравоохранения штата Юта показала, что вирус Эпштейна-Барра, вызывающий мононуклеоз и связанный с развитием нескольких видов рака, использует новую стратегию выживания.Вирус берет на себя бразды правления клеточным механизмом своего хозяина, чтобы делать копии самого себя и отдавать приоритет производству собственных белков над белками клетки-хозяина. Исследователи говорят, что работа находится на начальной стадии, но однажды они надеются использовать эти знания для разработки нового вида лечения инфекции вирусом Эпштейна-Барра.
Вирус Эпштейна – Барра (EBV) — это вирус герпеса человека, обнаруживаемый у 95% населения. Как и другие герпесвирусы, ВЭБ может передаваться от человека к человеку.Однако вирус обычно остается латентным — то есть он задерживается внутри клеток без активной репликации — в течение всей жизни хозяина и редко вызывает заболевание, выходящее за рамки первоначальной инфекции. Однако в некоторых случаях триггеры окружающей среды, включая стресс или сопутствующие инфекции и подавление иммунитета, создают условия, в которых вирус может процветать, иногда вызывая редкий тип лимфомы или другого рака.
Четыре года назад исследовательская группа U of U Health обнаружила, что спиронолактон, лекарство, обычно используемое для лечения сердечной недостаточности, обладает неожиданной противовирусной активностью против ВЭБ.Они обнаружили, что лекарство нацелено на белок EBV, называемый SM, который, как ранее показала лаборатория Сваминатана и другие исследователи, необходим для репликации EBV.
«Мы были озадачены тем, как спиронолактон, лекарство, которое, как считается, действует на совершенно несвязанный путь, связанный с потоком натрия в почках, может влиять на вирус или на функцию СМ», — говорит старший автор Санкар Сваминатан, доктор медицины, начальник отдела инфекционных болезней в U Health и профессор внутренней медицины.
Теперь они узнали больше о том, как это работает, и опубликовали свои выводы в Proceedings of the National Academy of Sciences.
Несколько лет назад группа французских исследователей обнаружила, что спиронолактон разрушает белок хозяина, называемый XPB, который играет важную роль в клеточной транскрипции — одном из первых шагов в экспрессии генов. Следуя этому примеру, Сваминатан и его коллега Динеш Верма провели серию экспериментов, чтобы изучить потенциальную связь между двумя белками, с которыми взаимодействует препарат, XPB и SM.
Исследователи впервые применили метод молекулярной биологии, чтобы снизить количество XPB в клетках-хозяевах.В результате вирус не смог реактивироваться и начал действовать так, как если бы у него больше не было функционального SM. Затем исследовательская группа показала, что SM переправляет белок XPB непосредственно в вирусную ДНК.
Наконец, исследователи использовали метод, включающий химическое маркирование уридина, одного из четырех строительных блоков алфавита РНК, для изучения репликации вируса. Используя эту технику, они продемонстрировали, что отключение XPB приводит к более низким уровням информационных РНК для 15 специфических вирусных белков, производство которых способствовало SM, в то время как экспрессия других генов EBV не пострадала.
«Мы показали, что SM неожиданно играет роль в активации транскрипции и кооптирует для этого один клеточный белок», — говорит Динеш Верма, доктор философии, доцент кафедры внутренней медицины.
Согласно Сваминатану, эти 15 белков выполняют функции, которые позволяют вирусу размножаться у здоровых людей. «Вирус эволюционировал, чтобы производить эти белки как раз в нужное время, чтобы не дать инфицированным клеткам погибнуть достаточно долго, чтобы сделать несколько копий вируса и, возможно, заразить еще пару клеток, прежде чем иммунная система сработает и позаботится о нем. , — говорит Сваминатан.«Как это часто бывает с вирусами, это решение очень специфично и очень умно».
У пациентов с ослабленной иммунной системой те же самые свойства — поддержание жизни инфицированных клеток и помощь им в обходе иммунной системы — могут привести к неконтролируемой пролиферации, что является общей характеристикой рака.
В настоящее время исследователи пытаются найти новые лекарства, нацеленные на XPB, чтобы предотвратить реактивацию EBV и других герпесвирусов человека у пациентов с трансплантатами, пациентов с ВИЧ и других пациентов с ослабленным иммунитетом.
«Долгосрочная идея заключается в том, что мы сможем разработать лекарства, которые сохранят вирус в полной латентности и что это поможет снизить риск развития рака, связанного с ВЭБ», — говорит Сваминатан.
# #
Динеш Верма, Трентон Мел Черч и Санкар Сваминатан опубликовали статью
«Вирус Эпштейна-Барра кооптирует компонент TFIIH XPB для специфической активации основных вирусных литических промоторов».
Исследование поддержано Национальным институтом рака.
— Автор Крис Палмер
Новости исследований iii
Лекарство от вируса Эпштейна-Барра (ВЭБ) от инфекционного мононуклеоза (моно)
Автор
Картика Шетти, доктор медицины, FACP Директор программы резидентуры по внутренним болезням, Sunrise GME; Медицинский директор учреждения, TEAMHealth, больница Маунтин-Вью
Картика Шетти, доктор медицины, FACP является членом следующих медицинских обществ: Американского колледжа врачей, Ассоциации директоров программ по внутренней медицине, Медицинского совета Индии
Раскрытие информации: не раскрывать .
Соавтор (ы)
Элизабет Бендж, MD Врач-резидент, Отделение внутренней медицины, Консорциум Sunrise Health GME
Элизабет Бендж, доктор медицинских наук, является членом следующих медицинских обществ: Американский колледж врачей, Американская ассоциация женщин-медиков
Раскрытие информации: не раскрывать .
Ванесса Э. Джозеф, доктор медицины, магистр медицины Научный сотрудник по легочным заболеваниям и реанимации, Медицинский факультет Университета Нью-Мексико
Ванесса Э. Джозеф, доктор медицины, магистр медицины, является членом следующих медицинских обществ: Американский колледж грудных врачей, Американский колледж врачей, Американское торакальное общество
Раскрытие информации: нечего раскрывать.
Реза Вагефи, MD Врач-инфекционист, Infectious Disease Partners of Nevada (IDPN), Консорциум Sunrise Health GME
Раскрытие: Ничего не разглашать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу.для: Medscape.
Джон У. Кинг, доктор медицины Профессор медицины, начальник отдела инфекционных заболеваний, директор клиники вирусной терапии гепатита Медицинской школы государственного университета Луизианы в Шривпорте; Консультант по инфекционным заболеваниям, Медицинский центр по делам ветеранов Овертон-Брукс
Джон У. Кинг, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации развития науки, Американского колледжа врачей, Американской федерации медицинских исследований, Американского общества микробиологии. , Ассоциация профессоров узких специальностей, Общество инфекционных болезней Америки, Сигма Си, Общество чести научных исследований
Раскрытие информации: нечего раскрывать.
Главный редактор
Майкл Стюарт Бронз, доктор медицины Дэвид Росс Бойд Профессор и заведующий кафедрой медицины, Стюарт Г. Вольф, заведующий кафедрой внутренней медицины, кафедра медицины, Научный центр здравоохранения Университета Оклахомы; Магистр Американского колледжа врачей; Член Американского общества инфекционных болезней; Член Королевского колледжа врачей, Лондон
Майкл Стюарт Бронз, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей, Американская медицинская ассоциация, Ассоциация профессоров медицины, Общество инфекционных болезней Америки, Государственная медицинская ассоциация Оклахомы, Южное общество клинических исследований
Раскрытие информации: раскрывать нечего.
Дополнительные участники
Burke A Cunha, MD Профессор медицины Медицинской школы государственного университета Нью-Йорка в Стоуни-Брук; Заведующий отделением инфекционных заболеваний, больница Уинтропского университета
Берк А. Кунья, доктор медицины, является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа врачей, Американского общества инфекционных заболеваний
Раскрытие информации: нечего раскрывать.
Чарльз С. Леви, доктор медицины Доцент, кафедра медицины, отделение инфекционных заболеваний, Медицинский факультет Университета Джорджа Вашингтона
Чарльз С. Леви, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей, Общества инфекционных болезней Америки, Медицинское общество округа Колумбия
Раскрытие информации: нечего раскрывать.
Инфекционный мононуклеоз вируса Эпштейна-Барра (ВЭБ) (мононуклеоз): история вопроса, патофизиология, эпидемиология
Автор
Картика Шетти, доктор медицины, FACP Директор программы резидентуры по внутренним болезням, Sunrise GME; Медицинский директор учреждения, TEAMHealth, больница Маунтин-Вью
Картика Шетти, доктор медицины, FACP является членом следующих медицинских обществ: Американского колледжа врачей, Ассоциации директоров программ по внутренней медицине, Медицинского совета Индии
Раскрытие информации: не раскрывать .
Соавтор (ы)
Элизабет Бендж, MD Врач-резидент, Отделение внутренней медицины, Консорциум Sunrise Health GME
Элизабет Бендж, доктор медицинских наук, является членом следующих медицинских обществ: Американский колледж врачей, Американская ассоциация женщин-медиков
Раскрытие информации: не раскрывать .
Ванесса Э. Джозеф, доктор медицины, магистр медицины Научный сотрудник по легочным заболеваниям и реанимации, Медицинский факультет Университета Нью-Мексико
Ванесса Э. Джозеф, доктор медицины, магистр медицины, является членом следующих медицинских обществ: Американский колледж грудных врачей, Американский колледж врачей, Американское торакальное общество
Раскрытие информации: нечего раскрывать.
Реза Вагефи, MD Врач-инфекционист, Infectious Disease Partners of Nevada (IDPN), Консорциум Sunrise Health GME
Раскрытие: Ничего не разглашать.
Специальная редакционная коллегия
Франсиско Талавера, фармацевт, доктор философии Адъюнкт-профессор, Фармацевтический колледж Медицинского центра Университета Небраски; Главный редактор Medscape Drug Reference
Раскрытие информации: Получил зарплату от Medscape за работу.для: Medscape.
Джон У. Кинг, доктор медицины Профессор медицины, начальник отдела инфекционных заболеваний, директор клиники вирусной терапии гепатита Медицинской школы государственного университета Луизианы в Шривпорте; Консультант по инфекционным заболеваниям, Медицинский центр по делам ветеранов Овертон-Брукс
Джон У. Кинг, доктор медицины, является членом следующих медицинских обществ: Американской ассоциации развития науки, Американского колледжа врачей, Американской федерации медицинских исследований, Американского общества микробиологии. , Ассоциация профессоров узких специальностей, Общество инфекционных болезней Америки, Сигма Си, Общество чести научных исследований
Раскрытие информации: нечего раскрывать.
Главный редактор
Майкл Стюарт Бронз, доктор медицины Дэвид Росс Бойд Профессор и заведующий кафедрой медицины, Стюарт Г. Вольф, заведующий кафедрой внутренней медицины, кафедра медицины, Научный центр здравоохранения Университета Оклахомы; Магистр Американского колледжа врачей; Член Американского общества инфекционных болезней; Член Королевского колледжа врачей, Лондон
Майкл Стюарт Бронз, доктор медицины, является членом следующих медицинских обществ: Alpha Omega Alpha, Американский колледж врачей, Американская медицинская ассоциация, Ассоциация профессоров медицины, Общество инфекционных болезней Америки, Государственная медицинская ассоциация Оклахомы, Южное общество клинических исследований
Раскрытие информации: раскрывать нечего.
Дополнительные участники
Burke A Cunha, MD Профессор медицины Медицинской школы государственного университета Нью-Йорка в Стоуни-Брук; Заведующий отделением инфекционных заболеваний, больница Уинтропского университета
Берк А. Кунья, доктор медицины, является членом следующих медицинских обществ: Американского колледжа грудных врачей, Американского колледжа врачей, Американского общества инфекционных заболеваний
Раскрытие информации: нечего раскрывать.
Чарльз С. Леви, доктор медицины Доцент, кафедра медицины, отделение инфекционных заболеваний, Медицинский факультет Университета Джорджа Вашингтона
Чарльз С. Леви, доктор медицины, является членом следующих медицинских обществ: Американского колледжа врачей, Общества инфекционных болезней Америки, Медицинское общество округа Колумбия
Раскрытие информации: нечего раскрывать.
Как я лечу хроническую активную Т-клеточную болезнь Эпштейна-Барра | Кровь
У 25-летней латиноамериканской женщины во время третьей беременности развилась желтуха, жар и озноб.Нарушения ферментов печени сохранялись, у нее была гипоальбуминемия, с коагулопатией и тромбоцитами в диапазоне 90 × 10 9 / л и повышенным билирубином. Ей была сделана биопсия печени, которая показала лёгкий очаговый гепатит без очевидных признаков инфекции. Магнитно-резонансная томография брюшной полости выявила легкую гепатомегалию, селезенка нормальных размеров. Пациент наблюдался амбулаторно, ферменты печени улучшились. Через год она снова забеременела. Опять же, во время беременности у нее повысился уровень трансаминаз.На УЗИ брюшной полости патологий не выявлено, селезенка не увеличена. Ей была сделана еще одна биопсия печени, которая выявила очаговые синусоидальные лимфоциты. У пациентки произошел выкидыш на 20 неделе. За ней продолжали наблюдать в амбулаторных условиях, и она чувствовала себя хорошо до тех пор, пока 3 года спустя у нее не появились периодические озноб и лихорадка до 102 ° F. Пациенту была проведена третья биопсия печени, выявившая смешанный макро- и микровезикулярный стеатоз. РНК EBV была обнаружена в печени. Обзор 3 биопсий печени, взятых за 4-летний период, показал диагноз Т-клеточной инфекции CAEBV.Пациент лечился с помощью CHOP (циклофосфамид, доксорубицин, винкристин и преднизон) и ацикловира. Тем не менее, она прогрессировала с заметно повышенным уровнем ДНК ВЭБ> 200000 копий / мкг ДНК, лихорадкой до 104 ° F, аномальными функциональными тестами печени (LFTs; билирубин 13 мг / дл) и обострением болезни, с подтверждением биопсии костного мозга. гемофагоцитоз. Ее лечили по схеме, включающей бортезомиб и ганцикловир, и у нее был резкий ответ на эту терапию: уровень ДНК EBV упал до <100 копий / мкг ДНК.Клинически у нее не было лихорадки, лимфаденопатии не было, показатели LFT и общий анализ крови были нормальными.
Пациенту поставлен диагноз Т-клеточный CAEBV. Ее болезнь, казалось, нарастала и угасала, первоначально протекая относительно медленно, но с подавлением иммунитета во время беременности. Впоследствии она получила аллогенный трансплантат гемопоэтических клеток (HCT) от неродственного донора EBV + , несоответствующего 8/10 HLA, с использованием схемы пониженной интенсивности (алемтузумаб, вводимый дистально с -14 дня, флударабин 150 мг / м 2 и мелфалан 140 мг / м 2 ), но приживление не удалось, и уровень ДНК ВЭБ резко повысился.Была предпринята попытка второй трансплантации, но пациент умер до приживления кровотечения.
Хотя эта пациентка первоначально поступила с подострым случаем Т-клеточного CAEBV, через 4 года у нее впоследствии появились признаки и симптомы, типичные для острого проявления. Таким образом, этот случай иллюстрирует трудности, с которыми сталкивается клиницист в отношении выбора времени для аллогенной HCT без использования ретроспектоскопа.
Инфекционный мононуклеоз вируса Эпштейна-Барра — Американский семейный врач
1. Bailey RE. Диагностика и лечение инфекционного мононуклеоза. Ам Фам Врач . 1994; 49: 879–88 ….
2. Henke CE, Курляндия LT, Elveback LR. Инфекционный мононуклеоз в Рочестере, штат Миннесота, с 1950 по 1969 год. Am J Epidemiol . 1973; 98: 483–90.
3. Фрай Дж. Инфекционный мононуклеоз: некоторые новые наблюдения 15-летнего исследования. Дж. Фам Практ . 1980; 10: 1087–9.
4. Van Cauwenberge PB, Vander Mijnsbrugge A .. Фарингит: обзор микробиологической этиологии. Pediatr Infect Dis J . 1991; 1010 доп .: S39–42.
5. Конфеты Б, Чалдер Т, Очистить AJ, Уэсли С, Белый ПД, Хотопф М. Выздоровление от инфекционного мононуклеоза: больше, чем симптоматическая терапия? Систематический обзор. Br J Gen Pract .2002; 52: 844–51.
6. Aronson MD, Комаров А.Л., Пройдите TM, Эрвин CT, Филиал WT. Гетерофильные антитела у взрослых с болью в горле: частота и клинические проявления. Энн Интерн Мед. . 1982; 96: 505–8.
7. Andersson JP. Клинические аспекты вирусной инфекции Эпштейна-Барра. Scand J Infect Dis Suppl . 1991; 80: 94–104.
8. Hoagland RJ. Инфекционный мононуклеоз. Prim Care .1975. 2: 295–307.
9. Аксельрод П., Finestone AJ. Инфекционный мононуклеоз у пожилых людей. Ам Фам Врач . 1990; 42: 1599–606.
10. Бригден М.Л., Au S, Томпсон С, Бригден С, Дойл П, Цапарас Ю. Инфекционный мононуклеоз в амбулаторной популяции: диагностическая ценность двух автоматических гематологических анализаторов, а также чувствительность и специфичность критериев Хогланда у гетерофил-положительных пациентов. Арч Патол Лаб Мед . 1999; 123: 875–81.
11. Ho-Yen DO, Мартин К.В. Взаимосвязь атипичного лимфоцитоза и серологических тестов при инфекционном мононуклеозе. J Заразить . 1981; 3: 324–31.
12. Центры по контролю и профилактике заболеваний. Цитомегаловирусная (ЦМВ) инфекция. Доступ онлайн 16 августа 2004 г. по адресу: http://www.cdc.gov/ncidod/diseases/cmv.htm.
13. Реа ТД, Руссо Дж. Э., Катон W, Эшли Р.Л., Баквальд Д.С.Проспективное изучение естественного течения инфекционного мононуклеоза, вызванного вирусом Эпштейна-Барра. J Am Board Fam Pract . 2001; 14: 234–42.
14. Гровер С.А., Баркун А.Н., Сакетт DL. Рациональное клиническое обследование. Есть ли у этого пациента спленомегалия? ЯМА . 1993; 270: 2218–21.
15. Линдерхольм М, Боман Дж, Джуто П, Линде А. Сравнительная оценка девяти наборов для быстрой диагностики инфекционного мононуклеоза и серологии, специфичной для вируса Эпштейна-Барра. Дж. Клин Микробиол . 1994; 32: 259–61.
16. Бруу А.Л., Hjetland R, Холтер Э, Мортенсен Л, Натас О, Петтерсон В., и другие. Оценка 12 коммерческих тестов для обнаружения специфичных к вирусу Эпштейна-Барра и гетерофильных антител. Clin Diagn Lab Immunol . 2000; 7: 451–6.
17. Элгх Ф, Линдерхольм М. Оценка шести имеющихся в продаже наборов с использованием очищенного гетерофильного антигена для быстрой диагностики инфекционного мононуклеоза по сравнению с серологией, специфичной для вируса Эпштейна-Барра. Клин Диагн Вирол . 1996; 7: 17–21.
18. Пол Младший, Баннелл WW. Классика по инфекционным болезням. Присутствие гетерофильных антител при инфекционном мононуклеозе Джона Р. Пола и У. У. Баннелла. Американский журнал медицинских наук, 1932. Rev. Infect Dis . 1982; 4: 1062–8.
19. Дэвидсон И. Серологический диагноз инфекционного мононуклеоза. ЯМА . 1937; 108: 289–95.
20. Грот I, Мимуни Д, Уэрта М, Мимуми М, Коэн Д., Робин Джи, и другие.Клинические и лабораторные проявления инфекционного мононуклеоза с положительным результатом ВЭБ у молодых людей. Эпидемиол. Инфекция . 2003; 131: 683–9.
21. Далримпл В. Инфекционный мононуклеоз. 2. Связь постельного режима и активности с прогнозом. Постградская медицина . 1964; 35: 345–9.
22. Торре Д., Тамбини Р. Ацикловир для лечения инфекционного мононуклеоза: метаанализ. Scand J Infect Dis . 1999; 31: 543–7.
23. Vendelbo Johansen L, Лилдхольдт Т, Бенде М, Тофт А, Браге Педерсен C, Danielsson GP. Инфекционный мононуклеоз, леченный антигистаминными препаратами: сравнение эффективности ранитидина (Зантак) по сравнению с плацебо при лечении инфекционного мононуклеоза. Клин Отоларингол . 1997; 22: 123–5.
24. Болден К.Дж. Кортикостероиды в лечении инфекционного мононуклеоза. Оценка с использованием двойного слепого исследования. J R Coll Gen Pract . 1972; 22: 87–95.
25. Прут С, Далримпл В. Двойное слепое исследование восьмидесяти двух случаев инфекционного мононуклеоза, получавших кортикостероиды. Ассоциация здоровья J Am Coll . 1966; 15: 62–6.
26. Тайнелл Э., Аврелий Э, Бранделл А, Юландер I, Дерево М, Яо QY, и другие. Лечение острого инфекционного мононуклеоза ацикловиром и преднизолоном: многоцентровое двойное слепое плацебо-контролируемое исследование. J Заразить Dis . 1996. 174: 324–31.
27. Рой М., Бейли Б, Амре Д.К., Джиродиас JB, Bussieres JF, Годро П. Дексаметазон для лечения боли в горле у детей с подозрением на инфекционный мононуклеоз: рандомизированное двойное слепое плацебо-контролируемое клиническое исследование. Arch Pediatr Adolesc Med . 2004. 158: 250–4.
28. Вирус Эпштейна-Барра и инфекционный мононуклеоз. Доступ онлайн 16 августа 2004 г., по адресу: http: // www.cdc.gov/ncidod/diseases/ebv.htm.
29. Кретьен Дж. Х., Esswein JG. Насколько часто встречается бактериальная суперинфекция глотки при инфекционном мононуклеозе? Наблюдения за заболеваемостью, распознаванием и лечением антибиотиками. Clin Pediatr [Phila] . 1976; 15: 424–7.
30. Merriam SC, Килинг Р.П. Бета-гемолитический стрептококковый фарингит: нечасто при инфекционном мононуклеозе. Саут Мед Дж. . 1983; 76: 575–6.
31.Доммерби H, Stangerup SE, Станжеруп М, Ханке С. Гепатоспленомегалия при инфекционном мононуклеозе, оцениваемая с помощью ультразвукового сканирования. Дж Ларингол Отол . 1986; 100: 573–9.
32. Берроуз К.Е. Спортсмены возобновляют деятельность после инфекционного мононуклеоза. Арк Фам Мед . 2000; 9: 1122–3.
33. Фарли Д.Р., Zietlow SP, Бэннон депутат, Фарнелл МБ. Самопроизвольный разрыв селезенки из-за инфекционного мононуклеоза. Mayo Clin Proc . 1992; 67: 846–53.
34. Маки Д.Г., Reich RM. Инфекционный мононуклеоз у спортсмена. Диагностика, осложнения и лечение. Am J Sports Med . 1982; 10: 162–73.
35. Eichner ER. Инфекционный мононуклеоз. Физ Спортсмен . 1996; 24: 49–54.
36. Рутков И.М. Разрыв селезенки при инфекционном мононуклеозе: критический обзор. Arch Surg . 1978; 113: 718–20.
37. Sevier TL. Инфекционное заболевание у спортсменов. Мед Клин Норт Ам . 1994; 78: 389–412.
38. Verma N, Арунабх С, Brady TM, Чарытан К. Острый интерстициальный нефрит, вторичный по отношению к инфекционному мононуклеозу. Клин Нефрол . 2002; 58: 151–4.
39. Коннелли К.П., ДеВитт ЛД. Неврологические осложнения инфекционного мононуклеоза. Педиатр Нейрол . 1994; 10: 181–4.
40. Андерсон MD, Кеннеди, Калифорния, Льюис А.В., Кристенсен ГР. Ретробульбарный неврит, осложняющий острую инфекцию, вызванную вирусом Эпштейна-Барра. Клиническая инфекция .


 А это значит, что адекватное лечение ВЭБ инфекции у детей способно избавить от развития серьезной патологии в будущем;
А это значит, что адекватное лечение ВЭБ инфекции у детей способно избавить от развития серьезной патологии в будущем;