Риновирусная инфекция. Этиология. Клиника. Лечения. Профилактика. | EUROLAB
Риновирусная инфекция — острое антропонозное вирусное заболевание с избирательным поражением слизистой оболочки носа.
Краткие исторические сведения
Впервые вирусная этиология так называемого «заразного насморка» установлена И. Фостером (1914), однако возбудитель выделен Ч. Эндрюсом лишь в 1953 г. Позднее Д. Тирелл (1960) выделил целую группу вирусов с аналогичным цитопатическим эффектом, получившую название риновирусов.
Этиология
Возбудители — РНК-геномные вирусы рода Rhinovirus семейства Picomaviridae. В настоящее время известно более 110 серотипов риновирусов, объединённых в группы Н и М. Во внешней среде вирионы нестойки, инактивируются при 50 °С в течение 10 мин, при высушивании на воздухе большая часть теряет инфекционность через несколько минут.
Эпидемиология
Резервуар и источник инфекции — человек (больной или носитель). Больной начинает выделять возбудитель за 1 сут до проявления клинических признаков болезни и на протяжении последующих 5-9 сут. Крупный рогатый скот и лошади заражаются вирусами других серотипов, не представляющими опасности для человека.
Механизм передачи — аэрозольный, возможно заражение контактно-бытовым путём через предметы обихода и руки, контаминированные незадолго до этого выделениями больного из горла и носа.
Естественная восприимчивость людей высокая, не зависит от возраста, хотя заболевание чаще встречают у взрослых.
Основные эпидемиологические признаки. Болезнь распространена повсеместно, в умеренном климате её регистрируют в течение всего года с подъёмом заболеваемости весной и осенью.
Патогенез
Вирусы проникают в организм человека через нос. Их репродукция реализуется в эпителиоцитах слизистой оболочки носа, что сопровождается дегенерацией клеток, развитием местной воспалительной реакции катарального характера с полнокровием и расширением сосудов, умеренной лимфомоноцитарной инфильтрацией, резким набуханием, отёчностью слизистой оболочки и обильной секрецией. У детей воспалительный процесс может захватывать другие отделы дыхательных путей — гортань, трахею, бронхи. Установлено, что риновирусная инфекция может быть причиной развития хронических отоларингологических заболеваний.
В ходе инфекционного процесса образуются вируснейтрализующие антитела, сохраняющиеся в течение нескольких лет. Однако постинфекционный иммунитет строго типоспецифичен, поэтому возможны повторные заболевания при инфицировании возбудителем иного серовара.
Клиническая картина
Инкубационный период не превышает 7 дней, в среднем продолжаясь 1-3 дня. Острое начало заболевания проявляется заложенностью носа, сухостью и саднением в носоглотке, небольшим общим недомоганием. Развивается катаральный ринит с обильным серозным, а затем слизистым отделяемым. Может присоединиться сухой кашель. Выраженный насморк — ведущий и постоянный синдром. Обращает внимание несоответствие выраженного ринита и слабых общетоксических явлений (субфебрильная или нормальная температура тела, удовлетворительное общее состояние).
При осмотре больных отмечают обильную ринорею, гиперемию и небольшой отёк слизистой оболочки ротоглотки, мелкую зернистость мягкого нёба. Иногда наблюдают слезотечение, гиперемию конъюнктив, инъекцию сосудов склер. Длительность клинических проявлений обычно не превышает 1 нед, иногда может затягиваться до 10-14дней.
Дифференциальная диагностика
Риновирусную инфекцию следует отличать от других ОРВИ. Опорные признаки риновируснои инфекции — обильная ринорея при отсутствии или слабой выраженности интоксикации.
Опорные признаки риновируснои инфекции — обильная ринорея при отсутствии или слабой выраженности интоксикации.
Лабораторная диагностика
На практике обычно не применяют, хотя возможны вирусологические и серологические исследования (выделение вируса из смывов из носа, РН и РИФ). Изменения в гемограмме нехарактерны.
Осложнения
Осложнения встречают редко. Обычно они связаны присоединением вторичной, чаще дремлющей, инфекции (синуситы, отиты, бронхиты, пневмонии и др.).
Лечение
Проводят симптоматическую терапию.
Профилактика и меры борьбы
Аналогичны таковым при гриппе. Большое количество антигенных вариантов риновируса затрудняет разработку средств активной профилактики инфекции.
Источник: «Инфекционные болезни и эпидемиология» В. И Покровский, 2007
И Покровский, 2007
Риновирусная инфекция: Безопасная болезнь с угрожающими последствиями
Гомза Я. Ю., К.м.н, доцент кафедры оториноларингологии НМУ им. А. Богомольца
Этиология
Возбудителями являются риновирусы, принадлежащие к семейству пикорнавирусов (Picornaviridae) , включающих в себя энтеровирусы (полиовирусы, вирусы коксаки группы А и В, эховирусы, энтеровирусы, эховирусы и гепатовирусы). Различают примерно 101 серотип. Риновирусы не имеют капсулы, чем обуславливается их неустойчивость к воздействиям внешней среды и быстрая гибель при термической обработке или действии дезинфектантов.
|
Ежегодный вклад риновирусной инфекции в структуру ОРВИ составляет 30–50%, при этом в осенний период этиологическое значение риновирусов возрастает до 80%. В некоторых источниках указывается, что эта вирусная инфекция является относительно безопасной и не требует лечения. |
Эпидемиология
Источником заражения является больной человек. Путь передачи — воздушно-капельный. Однако есть сведения о том, что риновирусы могут распространяться контактным путем через слизистые оболочки носа, рта и коньюктиву. При несоблюдении правил личной гигиены человек может заразить себя сам, касаясь рта носа или глаз грязными руками, на которых могут присутствовать риновирусы с частичками мокроты инфицированного человека.
Риновирусная инфекция наблюдается на протяжении всего года, но ярко выраженные пики заболеваемости приходятся на осень и конец весны. Возможно, это связано со способом передачи – воздушно-капельные инфекции лучше передаются при высокой влажности воздуха. С другой стороны, заболевание связывают со снижением иммунитета в осеннее- зимний период, переохлаждением организма.
Наиболее подвержены инфицированию риновирусами дети дошкольного и младшего школьного возраста. В среднем дети болеют в 2 раза чаще, чем подростки и взрослые.
Патогенез
Входными воротами для риновирусной инфекции чаще всего служат верхние дыхательные пути, реже конъюнктива глаз и ротовая полость. Вирус фиксируется на эпителиальных клетках, а затем проникает в цитоплазму.
Дальнейшая репродукция вируса приводит к дистрофическим изменениям в клетках и воспалительными процессами в слизистой оболочке в местах входных ворот инфекции. При риновирусной инфекции преимущественно поражается слизистый эпителий полости носа.
Возбудитель размножается в клетках эпителия слизистой оболочки полости носа, вызывая местную воспалительную реакцию с резким набуханием, отечностью и обильной секрецией. Вскоре появляется заложенность носа, а уже через несколько часов – обильные серозные выделения. Нередко одновременно с ринореей отмечаются сухой кашель, слезотечение, боль в горле, снижаются обоняние и вкус.
Через поврежденный эпителий вирусы попадают в кровоток. Вирусемия зависит от степени повреждения эпителия, состояния клеточного и гуморального иммунитета.
Осложнения
Риновирусная инфекция опасна своими многочисленными осложнениями, некоторые из которых могут нести угрозу для жизни.
При остром течении заболевания, может развиваться синуит. Инфекция при гнойном синуите, в свою очередь, может распространиться на мозговые оболочки и вызвать менингит, привести к другим внутричерепным осложнениям – развитию субдурального. субарахноидального абсцесса или абсцесса мозга различной локализации.
Так же синуит может стать причиной орбитальных осложнений. При проникновении гноя в орбиту развиваются тяжелые осложнения – от отека век до флегмоны орбиты.
Одним из серьезных осложнений является средний отит, который может привести к развитию тромбоза сигмовидного синуса и отогенного сепсиса.
Риновирусная инфекция может вызывать воспаление небных миндалин, став причиной ангины, которая в свою очередь ведет к развитию гнойных воспалений, локализованных в области шеи, сепсиса. Воспалительные процессы могут опускаться и затрагивать нижние дыхательные пути – трахею, бронхи и легкие.
Вирус может стать причиной воспаления гортани и возникновения ларингита, который может развиться в флегмонозный фарингит, флегмону шеи, медиастинит. Риновирусная инфекция может привести к ларинготрахеобронхиту, проявляющемуся стенозом гортани. Это особенно опасно для новорожденных и детей грудного возраста. У детей возникает лающий кашель. Приступ удушья возникает чаще в ночное время вследствие закрытия просвета гортани, и если вовремя не оказана помощь, может привести к смерти.
Лечить или не лечить?
Лечение риновирусной инфекции просто необходимо. Прежде всего, чтобы не допустить осложнений. При лечении ОРВИ, в том числе вызванных риновирусной инфекцией, необходим домашний режим. Т.к. заболевание как правило происходит в холодное время года, а дополнительное переохлаждение может еще больше ослабить иммунитет и осложнить течение болезни. Во-вторых, в период болезни лучше не вступать в контакт с другими людьми, что бы не стать источником инфицирования.
Т.к. заболевание как правило происходит в холодное время года, а дополнительное переохлаждение может еще больше ослабить иммунитет и осложнить течение болезни. Во-вторых, в период болезни лучше не вступать в контакт с другими людьми, что бы не стать источником инфицирования.
При лечении риновирусной инфекции эффективными остаются простые «дедовские» способы– водочный компрессам на область горла, промыванию носовой полости изотоническим раствором поваренной соли (1 ч.л. на 1 л. воды), питье травяных отваров, есть лук и чеснок. Особенно важно употреблять побольше теплого питья. Так же в первые 3 дня заболевания рекомендуется витамин С, взрослым — в дозе по 0,5 г 2 раза в день.
При тяжелом течении болезни нужно применять медикаментозное лечение. Но все же самое главное – это своевременное принятие профилактических мер для предотвращения болезни: рациональное питание с употреблением достаточного количества белковой пищи – кисломолочных продуктов, мяса, рыбы, овощей и фруктов, соблюдение режима дня, достаточный сон, избегать стрессов и переутомления, заниматься физкультурой, гулять на свежем воздухе.
Влияние карбоцистеина на развитие риновируснойПрепараты карбоцистеина все чаще рекомендуются врачами для лечения ОРВИ, в том числе риновирусной инфекции. Прежде всего, при приеме карбоцистеина ингибурется адгезия вирусов к слизистому эпителию дыхательных путей, в результате чего снижается степень инфицирования. Карбоцистеин объективно снижает титры РВ, количество РНК риновируса в эпителиальных клетках, уменьшает концентрации цитокинов (ИЛ-6 и ИЛ-8) и ICAM-1. Таким образом, карбоцистеин блокирует развитие риновируса, препятствует внедрению вируса в эпителиальные клетки. А за счет снижения выработки цитокинов, карбоцистеин уменьшает воспалительные реакции. В результате действия карбоцистеина, уменьшаются клинические проявления риновируса, выздоровление наступает быстрее, а риск осложнений становится намного ниже. Хорошая комплаентность и минимальные побочные явления при высокой терапевтической эффективности позволяют использовать карбоцистеин для лечения детей с хроническими заболеванями органов дыхания и муковисцидозе, при необходимости назначения мукоактивных препаратов длительными курсами. * * * Проверенным на практике с убедительными результатами клинических исследований и применения в практике является препарат карбоцистеина Флюдитек, который производится французской фармацевтической компанией Laboratorie INNOTECH INTERNATIONAL. Флюдитек – мукоактивное средство с широким спектром показаний, терапевтических эффектов, высокой эффективностью, доказанной безопасностью, обладающее противовирусной активностью. Флюдитек ингибирует развитие риновирусной инфекции что позволяет : уменьшить клинические проявления болезни, снизить частоту осложнений и ускорить выздоровление. Флюдитек – мукоактивное средство первого выбора с выраженной противовирусной активностью. |
Источник: Журнал «Участковый врач», №2, февраль 2012
симптомы и лечение, как лечить риновирусы у детей и взрослых
Среди острых респираторных заболеваний особое место занимает риновирусная инфекция, которая провоцируется вирусом рода Rhinovirus. Заболеванию подвержены как взрослые, так и дети. У ребёнка риновирус обычно сопровождается обильным выделением слизистого экссудата из носа, а также незначительной интоксикацией.
Подобного рода вирусы погибают при воздействии внешних факторов. После высушивания или обработки дезинфекционными средствами риновирус почти мгновенно уничтожается. Не выживает он и в условиях высоких температур. Плохая выживаемость риновирусной инфекции связана с тем, что у вируса отсутствует внешняя оболочка. Тем не менее сырая и холодная погода для этого вируса не опасна. Именно поэтому вспышки заболевания в основном регистрируются в осенне-зимний период. В условиях низких температур вирус начинает интенсивно распространяться, и заболевание принимает эпидемический характер.
В условиях низких температур вирус начинает интенсивно распространяться, и заболевание принимает эпидемический характер.
Риновирусная инфекция у детей
Вероятность заразиться риновирусной инфекцией, именуемой в народе как заразный насморк, довольно велика у детей любой возрастной категории.
В медицине распространено мнение, что дети в течение первого года жизни обладают пассивным иммунитетом. А вот малыши постарше попадают в группу риска, особенно те, кто обладает слабым иммунитетом.
Дети, посещающие территории с большим скоплением людей, например, детский сад, школу или дополнительные секции, чаще остальных подхватывают риновирус. Если в подобных местах появляется заражённый ребёнок, то это автоматически приводит к поголовному заболеванию детей, которые вступили с ним в контакт.
Временной промежуток, спустя который инфицированный ребёнок начинает заражать остальных, колеблется в пределах семи дней. Это период, когда у него наблюдается обильное выделение из полости носа.
Нельзя исключать передачу вируса посредством общих игрушек, однако, это случается редко, так как инфекция относительно нестойка в окружающей среде.
Как показывает практика, дети чаще заражаются воздушно-капельным путём, когда происходит непосредственный контакт.
Инкубационный период риновируса у детей, как правило, длится не больше трёх суток.
Причины заболевания
Человек, болеющий риновирусом, одновременно является переносчиком инфекции. Верхний отдел дыхательных путей и конъюктива — это то, через что вирус проникает в организм.
Основные пути инфицирования:
- Воздушно-капельный. Когда больной человек чихает, высмаркивается или кашляет, то он создаёт риск заражения для других людей. Попавшие в воздушную среду риновирусы вдыхаются здоровыми людьми, что приводит к заболеванию.
- Контактно-бытовой. Риновирусная инфекция попадает в организм человека после контакта с вещами, на поверхности которых находились органические выделения больного.
 В случае если после контакта с такими предметами человек прикоснулся к слизистым оболочкам, то вероятность заражения многократно возрастает.
В случае если после контакта с такими предметами человек прикоснулся к слизистым оболочкам, то вероятность заражения многократно возрастает.
Факторы, увеличивающие риск заражения риновирусной инфекцией:
- Возраст. У людей преклонного возраста и детей по статистике чаще фиксируют риновирусную инфекцию. Нужно сказать, что дети грудного возраста практически не подвержены риновирусу. Это объясняется тем, что, получая материнское молоко, они вместе с ним приобретают антитела к инфекции.
- Табакокурение. Любители сигарет склонны к заражению, поэтому мужчины зачастую замечают у себя симптомы риновирусной инфекции.
- Столпотворение людей. Подхватить вирус можно в любом общественном месте, будь то автобус или магазин.
Не последнюю роль в развитии инфекции играют следующие факторы:
- Контакты с инфицированными людьми
- Снижение защитных функций организма
- Для женщин — период грудного вскармливания
- Обострение имеющихся хронических заболеваний
- Холодное время года
- Длительное пребывание на улице при низких температурах
Симптомы риновируса
Риновирусная инфекция после момента попадания в организм начинает себя проявлять примерно через два-три дня. За это время в слизистой оболочке носа формируется воспалительная реакция. Как только инкубационный срок подходит к концу, появляются катаральные изменения, что означает переход к начальной стадии продромального периода. Больной жалуется на такие симптомы:
За это время в слизистой оболочке носа формируется воспалительная реакция. Как только инкубационный срок подходит к концу, появляются катаральные изменения, что означает переход к начальной стадии продромального периода. Больной жалуется на такие симптомы:
- Постоянная субфебрильная температура
- Слабовыраженная лихорадка
- Ломота в мышцах, суставах и костях
- Отёчность в районе слизистой носа
- Заложенность носа и проблемы с дыханием
- Большой объем выделяемого слизистого содержимого из носа
Спустя какое-то время после заражения вирусом, экссудат, выделяемый из носа, приобретает густую консистенцию. Выраженная интоксикация начинает угасать.
Через несколько часов после инфицирования может появиться першение в горле, чихание и затруднение дыхания носом. Эти процессы протекают на фоне гиперемирования. При этом начинают краснеть и шелушиться ткани крыльев носа. Покраснение распространяется на мелкие сосуды конъюнктивы и склер. Становятся заметны мельчайшие сосуды глазного яблока, появляется слезотечение.
Становятся заметны мельчайшие сосуды глазного яблока, появляется слезотечение.
Диагностика риновирусной инфекции
Для установления диагноза отоларингологу требуется выслушать жалобы больного, собрать эпидемиологический анамнез и визуально осмотреть носоглоточную область.
Постановка точного диагноза становится возможной после проведения современных диагностических тестов:
- Серологическая диагностика. Распознавание вируса с помощью реакции нейтрализации. Лаборант изучает взаимодействие сыворотки больного и соответствующего чужеродного белка или вируса-антигена. Также серодиагностика позволяет определить вид инфекционного агента, выделенного у пациента при реакции между вирусом и иммунной сывороткой.
- Вирусологическое исследование. Микробиологическое исследование органического материала, выделяемого из носа. Забор материал производят в первые три дня болезни.
- Экспресс-диагностика. Специалист в лабораторных условиях проводит полимеразную реакцию, которая позволяет идентифицировать риновирус в отделяемом из верхних дыхательных путей.

Специфической профилактики против риновируса попросту не существует, так как с каждым днём в природе образуются новые серотипы риновирусной инфекции.
Лечение риновирусной инфекции у детей и взрослых
Риновирусная инфекция не представляет серьёзной угрозы для здоровья человека и относительно быстро отступает. Комплекс лечебных мероприятий в первую очередь направлен на облегчение состояния больного и недопущения дальнейшего распространения вируса.
Больному ребёнку необходимо обеспечить покой. Во избежание обезвоживания интоксикации следует следить за питьевым режимом. Обильное питье и противовирусные препараты позволять облегчить болезненное состояние. В комнате должна быть комфортная температура и оптимальный уровень влажности. Эти меры позволять раздражённой носоглотке не затруднять дыхание. Больным взрослым на время болезни нужно отказаться от алкоголя и сигарет, а детей всячески отгородить от табачного дыма.
Справиться с риновирусом используя лишь один определённый препарат невозможно. Только комплексный подход в лечении этого недуга позволит в короткие сроки поднять больного на ноги.
Только комплексный подход в лечении этого недуга позволит в короткие сроки поднять больного на ноги.
Симптомы риновирусной инфекции весьма схожи с пресловутым ОРЗ, поэтому врачи чаще всего назначают противовирусные препараты широкой направленности. Препарат узкого спектра действия целесообразно использовать только после подтверждения диагноза. Практически для любых поражений верхних дыхательных путей, будь то энтеровирус или грипп, используется аналогичная схема лечения.
1. Приём противовирусных средств.
- Арбидол. Действие препарата заключается в торможении проникновения вируса эпителиальные клетки. Приём разрешён детям с двух лет. До семилетнего возраста назначают по 2 таблетки в сутки, детям с семи до двенадцати лет разрешены 4 таблетки в день. Взрослым назначают дозу до 8 таблеток в сутки. Продолжительность курса лечения не более недели.
- Изопринозин. Суточную норму (50 мг/кг) разделяют на несколько приёмов.
 Принимать препарат не меньше пяти — семи дней.
Принимать препарат не меньше пяти — семи дней. - Оксалиновая мазь. Являясь препаратом местного действия, она значительно снижает активность вируса. Вводят мазь интраназально.
- Рибавирин. Разрешён детям старше десяти лет. Дозировка- 15 мг/кг. Лечебный курс составляет семь дней.
2. Использование иммуномодулирующих препаратов, которые не дают вирусам размножаться и стимулируют иммунную реакцию организма.
- Интерферон. Следует принимать по 5 капель каждые 30 минут в течение трёх часов. В дальнейшем дозировку снижают до пяти приёмов в сутки. Курс составляет одну неделю.
- Виферон. Ректальные суппозитории закладывают два раза в сутки.
3. Приём иммуностимуляторов.
- Циклоферон. С пяти лет разрешён приём одной таблетки в сутки, с семи до двенадцати лет по 2 таблетки. Взрослым назначают по 3 таблетки в сутки.
- Анаферон. Разрешается даже самым маленьким детям. В первые сутки принимать по 4 таблетки, а затем снизить дозу до одной. Курс лечения — неделя.
4. Снятие симптомов риновирусной инфекции.
- Для устранения высокой температуры назначают нурофен или парацетамол.
- Препараты от кашля подбираются с учётом его характера и места локализации.
- Для облегчения дыхания носоглотку промывают специальными гипертоническими растворами. Можно использовать хорошо зарекомендовавшие себя Аквамарис или Хьюмер.
- Для снятия отёчности используют капли Пиносол или Ксилен.
Народная медицина в борьбе с риновирусной инфекцией
- Взять в одинаковых пропорциях (одна столовая ложка) перечную мяту, цветки чёрной бузины, соцветия тысячелистника и залить смесь стаканом горячей воды. Настоять в течение 5–10 минут, затем процедить. Принимают настой в теплом виде, перед сном по одному стакану.
- Две столовые ложки душицы заливают кипятком и настаивают в термосе около двух часов. Полученный настой пьют до четырёх раз в сутки по половине стакана до еды.
- Смешивают сок подорожника в объёме 250 мл и 200г мёда. Смесь держат на мелком огне около получаса. Принимают в теплом виде, до еды по столовой ложке.
- Огуречный сок (половина стакана) и чайная ложка мёда. Полученную смесь употребляют по половине стакана два раза в сутки.
- Необходимо варить свёклу до мягкого состояния. Затем мякоть овоща пропускается через мясорубку или же измельчается на тёрке. После этого измельчённый продукт отжимается через марлю. Свекольным соком смазывают полость носа два раза в сутки.
- Сухой измельчённый багульник (одна чайная ложка) заливается половиной стакана подсолнечного масла. Далее смесь выдерживают на водяной бане в течение часа, затем настаивают до охлаждения. Процеженную смесь закапывают в ноздри три раза в сутки.
Меры профилактики
Придерживаясь определённых профилактических мер, можно значительно снизить риск заболевания как у себя, так и у ребёнка:
- В период вспышки респираторных заболеваний следует как можно реже оказываться в местах, где скапливается много людей.
- Следить за гигиеной рук, чаще их мыть и обрабатывать антисептическими растворами.
- Использовать солевые растворы для очищения слизистой оболочки носовых пазух.
- Не забывать проветривать жилое помещение и проводить санитарную уборку дезинфицирующими средствами.
- Чтобы иммунитет всегда был в тонусе необходимо регулярно принимать витаминные комплексы.
- Полезно закаливать ребёнка, но с предельной осторожностью.
- Не допускать переохлаждения организма.
- В случае неизбежности контакта с больным человеком нужно надевать маску-респиратор.
Выполняя эти простые рекомендации, взрослые защищают себя и ребёнка не только от банальной риновирусной инфекции, но и от её осложнений в виде гайморита, тонзиллита и отита.
Риновирусная инфекция, риновирус: возбудитель, симптомы, лечение
Риновирусная инфекция – острый антропоноз, характеризующийся воспалением слизистой оболочки носа. Патология проявляется катаром носоглотки и умеренно выраженным интоксикационным синдромом. О «заразном насморке» впервые заговорили в 1914 году. Возбудитель инфекции был выделен лишь в 1953 году, а риновирусная инфекция получила свое название спустя еще 7 лет.
Этиология и эпидемиология
Возбудитель патологии — мелкий вирус, содержащий одноцепочечную РНК и не имеющий внешней оболочки. Он малоустойчив в окружающей среде и быстро погибает под воздействием неблагоприятных факторов: инактивируется в кислой среде, при нагревании, дезинфекции. При высушивании на воздухе большая часть микробов теряет свои патогенные и вирулентные свойства. Вирусы устойчивы к эфирам и отрицательным температурам.
Механизм передачи возбудителя — аспирационный, реализующийся воздушно-капельным путем. Микробы распространяются во внешней среде и проникают в организм человека вместе с капельками слюны и отделяемым носоглотки. Больной начинает выделять возбудителя за сутки до проявления симптомов патологии и на протяжении последующих десяти дней. Входными воротами инфекции являются носовая и ротовая полость, конъюнктива глаз. Заражение здоровых людей от больных возможно контактным и контактно-бытовым путем через непосредственное прикосновение или предметы обихода. Практически этот путь реализуется крайне редко из-за нестойкости риновируса во внешней среде. Больной остается заразным вплоть до полного прекращения насморка.
Риновирусная инфекция носит характер эпидемии. Пик заболеваемости наблюдается в осенне-весенний период, когда ослабляется иммунитет человека. Риновирусная инфекция прогрессирует в сентябре-октябре и в апреле-мае. Риск заразиться повышается при переохлаждении и при нахождении в местах большой скученности людей. Чаще всего болеют работники небольших коллективов, учащиеся, студенты, военнослужащие.
Восприимчивость к инфекции достаточно высокая. Она зависит от состояния иммунной системы человека, имеющихся факторов риска, длительности контакта с больным. Риновирусной инфекцией болеют лица всех возрастов. Некоторые этнические группы, американцы и эскимосы, более восприимчивы к риновирусам. Это связано с особенностями среды обитания, малообеспеченностью и высокой плотностью населения. Группу риска составляют пожилые люди, дети, ослабленные и истощенные больные. Хороший иммунитет и соблюдение всех профилактических мер позволят предотвратить развитие болезни.
Патогенез и патоморфология
Клетки-мишени для риновирусов — эпителиоциты слизистой носа. После проникновения микробов в организм человека они оседают на слизистой носа и начинают активно размножаться в клетках эпителия. Эпителиоциты постепенно разрушаются, и развивается катаральное воспаление. Слизистая резко отекает и набухает. Возникает гиперсекреция. Заболевание проявляется покраснением и отеком слизистой оболочки и обильным отделяемым из носа. Через носослезный канал носовая полость сообщается с органом зрения, возникает раздражение и инъецирование склеры и конъюнктивы.
Часто воспаление распространяется на соседние отделы дыхательной системы. Возможно проникновение микробов из места первичной локализации в кровеносное русло. Развивается вирусемия, проявляющаяся симптомами общей интоксикации. При ослаблении иммунитета активизируется бактериальная микрофлора, что приводит к появлению тяжелых осложнений болезни — воспаления среднего уха, бронхов, легких.
В крови больных обнаруживаются антитела, которые нейтрализуют вирусы. После перенесенной инфекции развивается непродолжительный типоспецифический иммунитет.
Факторы, предрасполагающие к развитию риновирусной инфекции:
- Курение,
- Мужской пол,
- Прикосновение загрязненными пальцами к носу или глазам,
- Скученность людей,
- Сопутствующая хроническая патология.
Симптоматика
Инкубационный период — время от внедрения вириона в геном клетки до появления клинических признаков. Длится инкубация 1-5 дней. Первичный патологический очаг формируется в полости носа. Воспаление проявляется выраженным катаром и общеинфекционным синдромом.
Признаки интоксикационного синдрома:
- Cубфебрилитет,
- Познабливание,
- Миалгия и артралгия,
- Разбитость,
- Болезненные ощущения в переносице.
В целом состояние больных остается удовлетворительным.
Слизистая оболочка носа отекает, появляются признаки катарального синдрома:
- Массовые водянистые выделения из носа,
- Чихание,
- Першение в горле,
- Сухость и саднение в носоглотке,
- Осиплость голоса,
- Заложенность носа,
- Слезотечение.
По мере присоединения бактериальной инфекции носовое отделяемое становится густым и гнойным. Слизистая оболочка и крылья носа гиперемированы, кожа под носом мацерирована, конъюнктива глаз и склеры инъецированы, веки опухшие. У больных слегка увеличиваются шейные лимфатические узлы, но остаются безболезненными. Длительность клинических проявлений составляет 1-2 недели.
У детей риновирусная инфекция характеризуется более короткой инкубацией: 1-2 суток. У малышей заболевание проявляется лихорадкой, ознобом, сильным и обильным насморком, болью в горле, кашлем. Сильная заложенность носа затрудняет носовое дыхание, нарушает сон и вынуждает ребенка дышать через рот. У больных нарушается обоняние, вкус, восприятие звука. Характерен внешний вид таких детей: у них бледнеет кожа, краснеют глаза, текут слезы, отекает лицо. Ребенок с риновирусной инфекцией становится плаксивым, капризным, раздражительным, беспокойным, вялым. У детей старшего возраста риновирусная инфекция часто протекает по типу трахеобронхита и проявляется кашлем. При этом в легких прослушиваются сухие или влажные хрипы.
У новорожденных заболевание развивается только в том случае, если в организме матери отсутствуют антитела против риновирусов. Заболевание у грудничков проявляется также интоксикацией и катаральными симптомами. Дети беспокойны, плохо спят и отказываются от еды.
Осложнения
Риновирусная инфекция в редких случаях осложняется присоединением вторичной бактериальной флоры и обострением имеющихся в организме хронических заболеваний.
Наиболее распространенными осложнениями риновирусной инфекции являются:
- Синуситы: гайморит, фронтит, этмоидит,
- Отит,
- Ангина,
- Трахеобронхит,
- Хронический ринит,
- Бронхит,
- Пневмония,
- Бронхиальная астма.
Осложнения развиваются, если больные игнорируют инфекцию или занимаются самолечением. Бесконтрольное применение сосудосуживающих капель для носа и прочих лекарственных препаратов может привести к формированию необратимых и печальных последствий.
Диагностика
Диагностика заболевания включает выслушивание жалоб больных, сбор эпидемиологического анамнеза, объективное обследование пациента.
- Специфическая диагностика заключается в проведении вирусологического исследования клинического материала — отделяемого носа, собранного в первые 5 дней болезни. В исследуемых образцах обнаруживают возбудителя инфекции — риновирус.
- Серодиагностика — постановка реакции нейтрализации или иммунофлюоресценции с целью обнаружения в крови антител и антигенов – возбудителей болезни.
- Экспресс-диагностика – полимеразная цепная реакция, позволяющая определить риновирусы в выделениях из дыхательных путей.
Лечение
Лечением и диагностикой риновирусной инфекции занимаются врачи-инфекционисты, пульмонологи и педиатры. Комплексная терапия патологии включает проведение этиотропного, патогенетического и симптоматического лечения.
В помещении, где находится больной, необходимо создать комфортный микроклимат, проводить регулярно влажную уборку, проветривать помещение, менять постельное белье. Больным следует соблюдать правила личной гигиены — тщательно мыть руки, сбалансировано питаться, много пить, при необходимости соблюдать постельный режим. Во время эпидемий респираторных инфекций необходимо минимизировать контакты для предотвращения распространения инфекции и повторного инфицирования. Больным показано теплое питье, горячие ножные ванны, анальгетики при головной боли.
Этиотропное лечение направленно против возбудителя болезни. Больным назначают:
- Противовирусные препараты – «Арбидол», «Изопринозин», «Оксолиновую мазь» для местного использования,
- Иммуномодуляторы — капли в нос «Интерферон», суппозитории ректальные «Виферон»,
- Иммуностимуляторы – «Циклоферон», «Анаферон».
Патогенетическое лечение:
- Противовоспалительные средства – «Ибупрофен», «Нурофен», «Эреспал»,
- Антигистаминные средства – «Супрастин», «Диазолин», «Тавегил»,
- Местные противоотечные препараты – «Тизин», «Ринонорм», «Називин».
Симптоматическое лечение направлено на уменьшение клинических признаков заболевания и облегчение общего состояния больного:
- Жаропонижающие средства – «Парацетамол», «Аспирин»,
- Противокашлевые препараты – «Синекод», «Стоптусин»,
- Противовоспалительные и антимикробные препараты для горла – пастилки, таблетки, спреи, растворы для полосканий – «Стрепсилс», «Септолете», «Фарингосепт»,
- Отхаркивающие препараты – «Лазолван», «Амброксол», «АЦЦ»,
- Средства для промывания носа – « АкваМарис», слабый солевой раствор,
- Антибактериальные спреи для носа – «Изофра», «Полидекса»,
- Витамины группы С.
Средства народной медицины широко применяются для лечения простудных заболеваний.
Прогноз заболевания всегда благоприятный. Все симптомы заболевания проходят полностью в течение недели. Исключением является кашель, который может мучить больных 10-14 дней.
Профилактика
Специфической профилактики риновирусной инфекции не существует. Некоторые лекарства, предназначенные для лечения вирусных заболеваний, применяются и в профилактических целях, но в иной дозировке. К ним относятся «Арбидол», «Кагоцел», «Ингавирин», «Интерферон-α», «Гриппферон», «Циклоферон», «Иммунал».
Общие профилактические мероприятия, позволяющие избежать данного недуга:
- Изоляция больных,
- Проветривание и влажная уборка помещения с использованием дезсредств,
- Кварцевание,
- Кормление больных из отдельной посуды,
- Полноценное питание в опасный период,
- Соблюдение правил личной гигиены,
- Промывание носа солевым раствором после каждого выхода на улицу,
- Прием иммуномодуляторов и витаминов,
- Закаливание организма,
- Использование маски при контакте с больными.
Выполняя эти несложные правила, можно снизить риск заражения риновирусной инфекцией или полностью предотвратить развитие заболевания.
Мнения, советы и обсуждение:
➤ Симптомы и лечение ОРВИ у детей
Опубликовано: 10 ноября 2020
Простудные заболевания, объединенные под аббревиатурой ОРВИ, имеют сходные симптомы и похожую схему лечения как для детей, так и для взрослых. В наше время следует особенно внимательно следить за своим здоровьем, учитывая ситуацию с COVID-19, и уметь вовремя распознать симптомы ОРВИ у ребенка.
В этой статье мы обсудим:
- причины ОРВИ у детей;
- как диагностировать острые респираторные заболевания по первым признакам;
- каким путем передается вирус;
- как лечить простуду у детей разных возрастов;
- какие профилактические меры предпринять;
- в каких случаях стоит обратиться к врачу;
- полезные советы.
ОРВИ – это группа вирусных заболеваний, поражающих слизистые оболочки дыхательных путей и сопровождающихся состоянием интоксикации организма. Часто к имеющейся у ребенка простуде присоединяются бактериальные инфекции и обостряются хронические заболевания. В итоге при несформированном до конца иммунитете дети тяжелее переносят болезнь.
Содержание статьи
Причины ОРВИ у детей
Пик вирусных заболеваний приходится на период с октября по апрель. Переохлаждение организма способствует ослаблению иммунитета и заражению вирусами. И так как их великое множество, то переболев одним и получив от него иммунитет, ребенок может заболеть другим через короткий промежуток времени. Так, ребенок от 3 до 7 лет, посещающий детский сад, может болеть до 8 раз в год.
Дети до года редко страдают от острых респираторных заболеваний, так как в это время формируется иммунитет с помощью грудного вскармливания и благодаря малому количеству контактов. Когда ребенок посещает ясли, детский сад и школу, увеличивается риск подхватить вирусную инфекцию. Поэтому школьники в возрасте от 7 до 16 лет часто страдают от простудных заболеваний.
Дети старше 16 лет уже имеют специфический иммунитет против многих вирусов, поэтому болеют ОРВИ реже и легче переносят его симптомы.
Основные факторы возникновения простуды:
- Переохлаждение организма в осенне-зимне-весенний период.
- Нахождение среди большого скопления людей (детский сад, школа, концерт, магазин, клуб, кинотеатр и т.д.).
- Климат с повышенной влажностью (способствует размножению вирусов).
- Ослабленный или несформированный иммунитет ребенка.
Симптомы ОРВИ
Первые признаки простуды у детей могут быть малозаметны и отличаться от проявлений у взрослого человека. Ситуация усугубляется тем, что малыши не всегда понимают свое состояние и не могут рассказать родителям о своем плохом самочувствии. Если вы заметили, что ребенок стал более спокойным, вялым, сонливым или капризным, что для него не свойственно, то это тревожный знак. Частый плач и плохой сон также свидетельствуют о том, что состояние малыша не в порядке.
Проявления вирусных заболеваний зависят от локализации возбудителя. Например, грипп оседает на трахее и вызывает сухой надрывный кашель. К этому добавляется высокая температура, сильные головные боли и ломота в суставах. Помимо этого может наблюдаться покраснение и выделения из глаз, воспаление гортани.
Если говорить о риновирусной инфекции, то она провоцирует постоянный насморк, чихание и кашель. При этом болезнь легко передается, поэтому часто в детских садах малыши болеют именно подобными заболеваниями.
Есть также респираторно-синцитиальная инфекция, которая локализуется в нижних отделах дыхательных путей. Особо опасна она для грудных детей и тех, у кого в анамнезе присутствует бронхиальная астма или аллергический ринит. Температура тела при этой инфекции может оставаться нормальной или быть слегка повышенной, а вот сухой кашель, переходящий в одышку, является тревожным звоночком.
Основные симптомы, сопровождающие ОРВИ у детей, таковы:
- Апатия, сонливость, вялость.
- Беспокойство, нарушенный режим сна и бодрствования.
- Частый плач, капризы, отсутствие аппетита.
- Покраснение глаз.
- Головные боли.
- Повышение температуры тела.
- Кашель.
- Насморк.
- Боль в горле.
В нижеприведенной таблице мы указали отличительные признаки разных типов вируса для облегчения понимания симптомов ОРВИ у вашего ребенка:
Не стоит впадать в панику, если вы обнаружили признаки ОРВИ у своего ребенка. Как правило, при сформированном иммунитете болезнь проходит за 5-7 дней. В этот период необходимо помочь организму малыша справиться с дискомфортным для него состоянием и избежать осложнений.
Способы передачи вируса
Простуда довольно заразна и легко передается от человека к человеку. Очень часто ребенок в детском саду не успевает выздороветь, как снова заболевает. Дело в том, что существует много групп вирусов и, переболев одним, можно заразиться вирусом другого типа.
Простуда передается в большинстве случаев воздушно-капельным путем при чихании, кашле и даже простом общении. Наиболее заразна она в первые четыре дня. Простудившийся ребенок может передать инфекцию через руки, где она сохраняется минимум два часа. Играя, дети трогают игрушки и взаимодействуют друг с другом, поэтому потрогав глаза, нос или рот руками, ребенок может занести вирус через слизистые оболочки.
Некоторые вирусы могут сохранять жизнеспособность на поверхностях предметов до нескольких дней, так что после контакта с этими предметами дети также могут заболеть.
Лечение ОРВИ у детей
Чтобы избежать появления осложнений после перенесенной простуды, важно своевременно обращаться к врачу, начинать лечение вовремя и не пренебрегать профилактическими мерами.
Как правило, дети переносят ОРВИ дома при соблюдении назначений врача. Для лечения часто используются противовирусные средства. В особо тяжелых случаях или при проявлении хронических патологий ребенка могут госпитализировать.
Суть терапии заключается в комплексном подходе для облегчения состояния малыша и борьбы с проникшим в организм вирусом. Используется как немедикаментозное лечение, так и лекарственные средства. В первом случае необходимо создать благоприятные условия для ребенка и неблагоприятные для вируса:
- Обеспечение покоя и снижение физических нагрузок. Лучше всего в первые несколько дней соблюдать постельный режим, чтобы сэкономить силы ребенка и направить их на борьбу с простудой.
- Соблюдение изоляции. Это поможет как самому ребенку избежать дополнительных инфекций, так и оградит остальных детей от контакта с простудившимся малышом.
- Питьевой режим. Во время болезни происходит усиленное потоотделение, поэтому важно пить как можно больше жидкости, чтобы избавить организм от токсинов.
- Дополнительный прием витаминов. Лучше всего, если это будут натуральные яблоки, цитрусовые, ягоды и другие продукты с высоким содержанием витамина С – естественным иммуномодулятором.
Лекарственная терапия заключается в симптоматическом лечении и приеме противовирусных и иммуномодулирующих средств.
Борьба с симптомами ОРВИ у детей:
- Жаропонижающие препараты. В этой группе важно выбирать лекарства, подходящие для возраста вашего ребенка, так как некоторые из них можно применять только с 6 месяцев или трех лет, а какие-то безопасно использовать с рождения.
- Противокашлевые средства. Детям младше двух лет рекомендуют давать сиропы на основе амброксола и бромгексина, а также на растительных экстрактах. Комбинированные препараты с амброксолом и чабрецом рекомендованы для детей постарше.
- Лекарства от насморка. Для облегчения дыхания используют солевые растворы, приготовленные самостоятельно (разведите 1/2 чайной ложки поваренной или морской соли без добавок в стакане горячей воды до полного растворения) или приобретенные в аптеке, подходящие даже для грудных детей. При необходимости можно использовать сосудосуживающие капли. Маленьким детям до 3 лет с симптомами ОРВИ нельзя применять спреи, так как средство может попасть в слуховой канал и вызвать осложнения.
Помните! Частое использование сосудосуживающих капель может повредить слизистую оболочку носа. Поэтому применять их стоит не чаще 1 – 2 раз в сутки, например, утром и перед сном.
Препараты, направленные на борьбу с вирусами и усиление защитных сил организма:
- Средства на основе интерферона. Детям до года разрешено применять капли и другие средства с природным интерфероном и рекомбинантные препараты. С трех лет можно использовать синтетический интерферон.
- Этиотропные средства. Это лекарства, направленные на устранение причины заболевания. К ним относятся препараты с осельтамивиром в качестве действующего вещества. До года эти средства малоэффективны, так как действуют только на грипп группы А, которым редко болеют груднички. А вот дети старше года могут принимать суспензию из порошка, а с трех лет можно использовать таблетки; с восьми – капсулы.
- Иммуномодуляторы. Одним из наиболее назначаемых препаратов этой группы у детей является «Деринат», который не только активирует защитные функции организма, но и борется с вирусами и укрепляет первый и важнейший барьер организма – слизистую носоглотки. Средство выпускается в форме спрея и капель. Капельная форма особенно удобна для детей до 3 лет. Препарат разрешен к применению с рождения.
Профилактика ОРВИ у детей
Для того чтобы избежать болезни или помочь ребенку как можно легче ее перенести, стоит озаботиться профилактическими мерами.
- На сопротивляемость организма различным простудным заболеваниям влияет уровень закаленности ребенка. С раннего детства родители могут приучать малыша к процедурам закаливания, что укрепляет его иммунитет и здоровье.
- Занятия спортом и правильный режим питания также способствуют получению и выработке необходимых витаминов и минералов, помогающих впоследствии бороться с инфекциями.
- Частое мытье рук предотвращает распространение вирусов. В условиях, где нет возможности использовать воду и мыло, отличной альтернативой служат антисептические гели для дезинфекции рук и поверхностей предметов.
- Изоляция ребенка от уже заболевших детей. А в период пика заболеваемости следует ограничить посещение людных мест: кружков, утренников и других детских мероприятий.
- В холодное время года можно дополнительно принимать препараты, помогающие укреплению собственных защитных сил. Для этой цели хорошо подходит «Деринат».
- Регулярные проветривания помещения, где находится ребенок, влажная уборка, кварцевание и увлажнение воздуха помогают снизить риск заболеть вирусными инфекциями.
- Вакцинация против гриппа является одним из наиболее эффективных методов профилактики, но важно помнить, что прививки защищают только от отдельно взятых штаммов вируса.
Рекомендации и полезные заметки для родителей:
- Не использовать антибиотики при первых симптомах ОРВИ у ребенка. Их применение оправдано только присоединением к вирусу бактериальной инфекции.
- Обильное питье в любом виде помогает выздоровлению. Можно давать малышу любую несладкую жидкость: компот, сок, чай, воду.
- Нельзя укутывать малыша слишком тепло и закрывать все окна, опасаясь сквозняков. Ребенку должно быть комфортно, а помещение необходимо проветривать для поддержания температуры воздуха на уровне 18-22 градусов. В тепле мокрота разбухает и сложно отделяется, что приводит к тяжелым приступам кашля, причиняющим ребенку боль и дискомфорт.
- Прекрасно, если в квартире есть увлажнитель для поддержания влажности воздуха на уровне 50-70%. В противном случае слизистые оболочки в носу ребенка будут пересыхать, что затрудняет борьбу с инфекцией. При хорошей влажности слизь будет выходить наружу через нос, а не спускаться по задней стенке гортани, вызывая кашель. При сухом кашле влажный воздух будет помогать разжижать мокроту и не даст ребенку заходиться удушающими приступами кашля.
- Нельзя сбивать повышенную температуру, если она не превышает 38,5 градусов, так как это показатель того, что организм вырабатывает интерферон и справляется с вирусами с помощью своего иммунитета. Если сразу давать жаропонижающие препараты, то организм привыкнет и в дальнейшем не сможет самостоятельно бороться с простудой. Исключение для этого правила составляют дети грудного возраста и малыши, у которых высокая температура держится более 3 дней. Высокой считается температура свыше 38 градусов.
- Прогулки в любую погоду способствуют улучшению самочувствия. Если ребенок бодр и активен, то можно хотя бы ненадолго выйти прогуляться. Частицы вируса быстро погибают на свежем воздухе. Активность в течение 30 минут на улице помогает разогнать кровь и активизировать иммунитет малыша.
- Если у ребенка диарея и рвота, что свидетельствует о сильной интоксикации, необходимо обеспечить ему обильное питье и давать сорбенты для вывода токсинов и электролиты для поддержания водно-солевого баланса в организме. Обезвоживание особенно опасно в первый год жизни детей.
- Не стоит злоупотреблять сосудосуживающими каплями – использовать их рекомендуется не более 3 дней подряд. Иначе может выработаться зависимость. Симптомами передозировки подобными средствами может быть головная боль, тошнота, рвота, повышение артериального давления.
- Применение противокашлевых препаратов чревато застоем мокроты в бронхах и началом воспалительного процесса в легких. Если ребенок сам в состоянии откашлять появляющийся секрет, то устранять кашель не следует. Для помощи простуженному малышу родители могут использовать народные средства, способные разжижать и выводить мокроту.
- Безопасно и эффективно промывать нос физраствором раз в три часа и полоскать горло хлорофилиптом.
Когда нужно срочно обращаться к врачу
Часто родители легкомысленно относятся к простуде ребенка и предпочитают лечить его самостоятельно. Но стоит помнить о том, что заболевание может грозить серьезными осложнениями:
- Бронхит.
- Пневмония.
- Отек легких.
- Синдром Рея.
- Фебрильные судороги.
- Менингит.
- Бронхиальная астма.
- Муковисцидоз.
Даже при наличии схожих симптомов каждая простуда может отличаться от предыдущей. Важно вовремя определить наличие бактериальной инфекции, чтобы своевременно назначить корректное лечение и исключить развитие сопутствующих патологий.
Определим, когда срочно нужно обращаться к специалисту за помощью:
- Если на четвертые сутки у ребенка не наблюдается улучшения состояния.
- После улучшения состояния оно снова резко ухудшилось.
- Появилась видимая бледность кожи, одышка, повышенная потливость.
- Длительный отказ от приема пищи и жидкости.
- Раздражительность, апатия, постоянный плач.
- Начались гнойные выделения из носа или ушей.
- Появилась боль в различных частях тела.
- Кашель усилился.
- Жаропонижающие средства не дают должного эффекта.
В следующих случаях к врачу нужно обратиться незамедлительно в любом возрасте ребенка:
- Судороги, потеря сознания.
- Рвота в сочетании с высокой температурой.
- Сыпь и отек шеи.
- Затрудненное дыхание.
- Высокая температура дольше трех дней.
- Выраженная желтизна глаз или их покраснение, не связанное с плачем.
- Подозрение на инфекции в ухе (ребенок проявляет беспокойство и постоянно прикасается к ушам, чешет их).
- Заложенность носа в течение длительного времени (дольше 14 дней).
Простуда – это общее название острых респираторных вирусных инфекций, в которые включены разные группы вирусов. Это значит, что ребенок может болеть в год до 8 раз, но возбудителем простуды будут разные вирусы. Сама по себе болезнь очень заразна. Передается по воздуху при дыхании, чихании или кашле, но достаточно легко переносится, если нет отягчающих обстоятельств в виде хронических заболеваний, бактериальных инфекций или ослабленного иммунитета.
Симптомы ОРВИ у детей дают о себе знать спустя пару дней после контакта с заболевшим ребенком. Зачастую болезнь проходит за неделю, оставляя после себя некоторые симптомы: кашель, насморк, боль в горле. При тяжелом течении болезни возможна госпитализация и ряд осложнений. Но в большинстве случаев дети переносят простуду без последствий для здоровья.
Лучшими профилактическими мерами является вакцинация, приём специальных лекарственных препаратов, соблюдение правильного микроклимата дома, поддержание режима сна и бодрствования и качественная еда и обильное питье. Дополнительный прием витаминов и других натуральных микроэлементов способствует укреплению иммунитета ребенка в период простуд и позволяет избежать сложного течения болезни.
Продукция Деринат
Полезные статьи:
Риновирусы : структура, симптомы и лечение
Риновирусы имеют различные механизмы передачи. Чаще всего — прямой контакт или аэрозольный путь. Входными воротами является слизистая оболочка носа и конъюнктива. Основным рецептором взаимодействия в организме человека с риновирусами являются ICAM-1, которые находятся в больших количествах в задней носоглотке. Вопреки распространенному мнению, поцелуи, обычный разговор, кашель не способствуют распространению болезни.
Риновирусы устойчивы к холоду, но погибают из-за нагрева, недостатка влаги и антисептиков. Заразиться вирусом можно при контакте с больным, у которого риновирус присутствует в выделениях из носа. Риновирус распространяется воздушно-капельным путем. Многообразие риновирусов обеспечивает их неуязвимость. Медицинский препарат или вакцина, которые успешно поражают белковую оболочку данного штамма, бессильны в борьбе со штаммами, имеющих такой же белок, но иную структуру. А когда штамм вируса имеет хоть какую-то резистентность к лекарству, природный отбор и мутация приблизит появление штаммов, которые будут абсолютно устойчивы к действию препарата.
Риновирусы атакуют не так много клеток и вреда от них не так уж и много. Тогда откуда такие осложнения? Дело здесь в особенностях механизмов иммунной защиты. Пораженные клетки продуцируют особые молекулы, цитокины, которые служат сигналом для запуска каскада реакций клеточного иммунитета. Именно из-за них у нас такое плохое самочувствие. Цитокины – виновники воспалений в горле и обильного выделения слизи. Почувствовать себя здоровым можно совсем не тогда, когда иммунитет победит риновирус, а только после того как иммунная система станет работать в обычном режиме.
Сегодня у врачей нет средств, которые эффективно борются с риновирусами. Прививки практически бесполезны. Ни один препарат не способен уничтожить вирус. Ошибкой многих является прием антибиотиков, которые эффективны в борьбе с бактериями и абсолютно бессильны в отношении с вирусами. Часто врачи прописывают антибиотики, если даже у них нет уверенности в природе заболевания: это вирусная инфекция или бактериальная. Неосторожное лечение антибиотиками подстегивает к развитию лекарственноустойчивых бактерий.
Мы очень недооцениваем риновирусы. У них много типов и наука лишь начинает постигать их разнообразие. В конце прошлого столетия ученые открыли несколько десятков штаммов, которые отнесли к двум большим родам. В 2006 году в США ученые обнаружили штамм риновируса, которые ни к одному из этих родов не относился. А потом выяснилось, что это – представитель еще одного, третьего рода, который тоже очень распространен. В различных местностях гены штаммов риновируса почти не отличаются. Такой факт служит доказательством очень быстрой распространяемости этого третьего рода, который назвали HRV–C.
Риновирусы имеют генетическое ядро, которое меняется очень незначительно. Зато некоторые гены вирусов меняются очень стремительно. Ученые выяснили, что они необходимы для выживания риновирусов, вступивших в битву с человеческим иммунитетом. После того как организм начал продуцировать антитела, чтобы справиться с одним штаммом вируса, он все еще уязвим для других штаммов, поскольку эти антитела бессильны против их белковой оболочки. Гипотеза подтверждается фактом, что ежегодно человек заражается несколько различными штаммами риновируса.
Несмотря на эти факты, некоторые представители ученого мира с оптимизмом смотрят в будущее и полагают, что разработать лекарство от риновирусов возможно. Поскольку риновирусы обладают одинаковым генетическим ядром, можно предположить, что оно не может мутировать. То есть, риновирусы, мутация которых коснулась ядра, погибают. Когда люди найдут способ влиять на ядро, болезнь можно будет победить.
Но есть ли смысл это делать? Риновирус опасен тем, что он открывает дорогу более опасным возбудителям. Однако сам он относительно безопасен. Через неделю заразившийся человек уже забывает о симптомах, а 40 % тестируемых, у которых анализы обнаружили риновирус, даже не знали об этом – он себя никак не проявлял.
Ученые даже признают благоприятное воздействие риновируса на организм. Собранные данные подтверждают, что дети, перенесшие относительно безопасные вирусные, в том числе, риновирусные, и бактериальные инфекции, в зрелом возрасте меньше подвергаются иммунным расстройствам. Риновирус, можно сказать, тренирует иммунитет, чтобы тот не реагировал слишком активно на незначительные угрозы, а умел сконцентрироваться на действительно серьезных опасностях. Поэтому стоит задуматься и, возможно, изменить взгляд на риновирусы: смотреть на них не как на врагов, а как на мудрых тренеров.
[25], [26], [27], [28], [29], [30], [31]
Риновирусные инфекции — HealthyChildren.org
Автор: Шравани Вундавалли, MD, FAAP
Риновирус ( rhin означает «нос») инфекции вызывают простуду.
Риновирусы могут также вызывать некоторые боли в горле, ушные инфекции и инфекции носовых пазух (отверстия в костях возле носа и глаз). Они также могут вызывать
пневмония и
бронхиолит, но это встречается реже.
Большинство детей болеют от 8 до 10 простудных заболеваний в течение первых 2 лет жизни. Если ребенок проводит время в детских учреждениях, где он или она находится рядом с другими детьми, больными простудой, ребенок может простудиться еще больше. |
Риновирусы легко передаются от одного человека к другому. Когда у ребенка с риновирусной инфекцией появляется насморк, жидкость из его носа попадает в руки, а оттуда — на столы, игрушки и другие места.Ваш ребенок может прикоснуться к рукам или коже другого ребенка или игрушкам, на которых есть вирус, а затем прикоснуться к своим глазам или носу, заразившись. Она также может вдыхать вирусы, которые находятся в воздухе, когда больной ребенок чихает или кашляет.
Несмотря на то, что ваш ребенок может простудиться в любое время года, эти инфекции наиболее распространены осенью и весной.
Что происходит, когда ребенок простужается?
Большинство людей знает признаки и симптомы простуды.Простуда у вашего ребенка может начаться с водянистого насморка, который выглядит как прозрачная жидкость. Позже выделения становятся более густыми и часто имеют коричневатый, серый или зеленоватый цвет. Эти цвета нормально видеть, когда ребенок начинает поправляться от простуды.
Когда ваш ребенок простужен, вы также можете видеть:
- Чихание
- Легкая лихорадка (101–102 ° F или 38,3–38,9 ° C)
- Головные боли
- Боль в горле
- Кашель
- Мышечные боли
- Снижение аппетита
У некоторых детей на миндалинах может появиться гной (беловатая слизь), что может быть признаком инфекции, вызванной бактериями (стрептококками).
Обычно у ребенка с риновирусной инфекцией в течение первых 2–3 дней не проявляется никаких признаков или симптомов. После появления симптомов они обычно длятся от 10 до 14 дней, но иногда ребенку выздоравливает быстрее.
Что я могу сделать, чтобы мой ребенок почувствовал себя лучше?
Если ваш ребенок простудился, убедитесь, что он или она достаточно отдыхает и пьет больше жидкости, если у него или нее температура. Если вашему ребенку неудобно, поговорите с его или ее врачом о том, чтобы давать ацетаминофен, чтобы снизить температуру.Не давай лекарства от простуды и кашля, отпускаемые без рецепта, без предварительной консультации с врачом. Лекарства, отпускаемые без рецепта, не убивают вирус и в большинстве случаев не помогают вашему ребенку чувствовать себя лучше.
Когда мне следует позвонить детскому врачу?
Если вашему ребенку 3 месяца или меньше, и у него появляются симптомы простуды, проконсультируйтесь с врачом. Дети младшего возраста чаще болеют простудными заболеваниями, включая пневмонию или бронхиолит. Детям постарше обычно не нужно обращаться к врачу при простуде.
Позвоните врачу, если у вашего старшего ребенка есть такие симптомы, как:
Как узнать, что мой ребенок простудился?
Вы можете сказать, что у вашего ребенка простуда, по его или ее симптомам. Как правило, лабораторные анализы (например, анализы крови или посев из горла) не нужны, чтобы выяснить, какая инфекция у ребенка с симптомами простуды.
Как я могу вылечить риновирусную инфекцию моего ребенка?
Большинство риновирусных инфекций протекает в легкой форме, и лекарства не требуются.Антибиотики не действуют при простуде и других инфекциях, вызванных вирусами.
Что я могу сделать, чтобы мой ребенок не заразился риновирусной инфекцией?
Держите младенцев младше 3 месяцев подальше от детей или взрослых, больных простудой.
Убедитесь, что ваш ребенок часто моет руки. Это уменьшит шансы, что он или она заразится вирусом.
Дополнительная информация с сайта HealthyChildren.org:
О Dr.Вундавалли:
Шравани Вундавалли, доктор медицины, FAAP, педиатр, практикующий в Университете Висконсина в Мэдисоне. Она закончила бакалавриат в Колумбийском университете в Нью-Йорке и закончила медицинскую школу и стажировку по педиатрии в университетской больнице SUNY Stony Brook University в Нью-Йорке. В Американской академии педиатрии она является членом секции врачей раннего возраста (SOECP).
Информация, содержащаяся на этом веб-сайте, не должна использоваться вместо медицинской помощи и рекомендаций вашего педиатра.Ваш педиатр может порекомендовать лечение по-разному, исходя из индивидуальных фактов и обстоятельств.
Риновирусная инфекция: симптомы и лечение
Инфекционное заболевание, при котором вирусы поражают в основном слизистую оболочку носа, называется риновирусной инфекцией. О симптомах и лечении этого заболевания пойдет речь в статье.
Общие сведения
Заболевание, как правило, сопровождается слабо выраженными признаками общей интоксикации организма.Риновирусы являются частью группы пикорнавирусов, содержащихся в РНК. На сегодняшний день науке известно более 100 серотипов риновирусов. У них нет общего антигена, поэтому каждый из серотипов имеет личный комплемент и вирус-нейтрализующий антиген. Вирусы довольно нестабильны во внешней среде, при сухом воздухе большая часть инфекции теряется через несколько минут, при температуре 50 ° C в течение 10 минут происходит инактивация вируса.
В умеренном климате заражение риновирусом может происходить круглый год.Пик заболеваемости приходится на осенне-весенний период. 20-25% всех острых респираторных заболеваний вызывают риновирусы.
Проникновение в организм
Как было сказано выше, риновирусная инфекция (симптомы и лечение заболевания мы рассмотрим ниже), в основном, проявляется во влажное и холодное время года и чаще всего развивается в небольших группах и закрытых коллективах (семьи, детские сады и др. другие учебные заведения). Риновирусы попадают в организм человека через дыхательные пути.Клинические проявления развиваются в зависимости от места занесения вируса. Если путем проникновения попадает в носоглотку, то у больного развивается ОРЗ. У взрослых воспаляется слизистая носа, у детей наблюдаются воспалительные процессы в гортани и бронхах. Если присоединяется бактериальная флора, развивается пневмония. Возбудитель инфекции размножается, как правило, в клетках эпителия дыхательных путей, что приводит к появлению местной воспалительной реакции, резкому отеку, отечности, обильному выделению.
Риновирусная инфекция: симптомы заболевания
Инкубационный период заболевания 1-6 дней. Признаки болезни легкие. Общее недомогание, тяжесть в голове, мышечная слабость — так проявляется риновирусная инфекция. Симптомы сопровождаются нормальной или субфебрильной температурой. Одновременно возникает катаральный синдром: ощущение зуда в горле, чихание, затруднение носового дыхания, заложенность носа.
Риновирусная инфекция, в первую очередь, проявляется насморком и обильными серозными выделениями, которые в первые дни заболевания носят водянистый характер, в дальнейшем выделения становятся слизистыми.Также наблюдается сухой кашель, гиперемия век, слезотечение. Насморк длится 6-7 дней, но может длиться до 14 дней. Заболевание сопровождается сильным чувством тяжести в носу, эякуляцией, потерей вкуса, слуха, обоняния. Маленьким детям тяжелее переносить болезнь, потому что у них более выражены проявления недуга. Осложнения случаются в очень редких случаях.
Диагностика
Риновирусную инфекцию можно диагностировать несколькими способами, в зависимости от проявлений этого недуга.При ярко выраженном рините врач поставит диагноз на основании опроса и осмотра пациента. Для диагностики заболевания на начальной стадии (до 5 дней) используется вирусологический метод: из полости носа берут промывание и в полученном биологическом материале выявляют возбудителя. Также для определения типа возбудителя и факторов противодействия (антитоксины и антитела) используются серологические методы исследования.
Помимо диагностики могут потребоваться общие анализы (OAK и OAM).Однако считается, что они недостаточно информативны и выявляют только наличие воспалительного процесса или указывают на возможные осложнения со стороны почечно-лоханочной системы.
Риновирусная инфекция: лечение заболевания
Проявления ринита аналогичны таковым при других ОРВИ, поэтому терапия основана на применении препаратов широкого спектра действия. При всех респираторных заболеваниях (грипп, аденовирусная, энтеровирусная или риновирусная инфекция) лечение включает:
Этиотропную терапию, направленную на борьбу с возбудителем заболевания.С этой целью обычно назначают препараты «Арбидол», «Рибавирин», «Изопринозин». Дополнительно назначаются местные средства: Локферон, Бонафтон.
Прием иммуномодуляторов. Рекомендуется отдавать предпочтение интерферонам, так как они подавляют размножение вирусов и поддерживают защитные силы организма. К таким лекарствам относятся суппозитории «Виферон» и капли «Гриппферон».
Использование иммуностимуляторов. Чаще всего назначают таблетки «Циклоферон», альтернативой маленьким пациентам (до 4 лет) является препарат «Анаферон».
Симптоматическое лечение. С этой целью рекомендуется применение жаропонижающих, противовоспалительных, противокашлевых средств. Также желательно промыть нос слабым солевым раствором или использовать каплю «Аквамариса». Помогут вывести такие лекарства, как «Пиносол» и «Ксилен».
Если в течение 3 дней лечения не наблюдается положительной динамики и температура тела стремится к критическим цифрам, лечение риновирусной инфекции у взрослых необходимо дополнить приемом антибиотиков.Детям рекомендуется по возможности избегать сильнодействующих средств. Естественно, что при ухудшении состояния может потребоваться прием антибиотиков, но назначать их должен только врач.
Альтернативная медицина
При этом заболевании не стоит сразу прибегать к лекарствам. Особенно это касается ситуаций, когда во время беременности развивается риновирусная инфекция. В этот период самое главное — не навредить малышу, а бороться с болезнью необходимо.В этом случае на помощь придут рецепты народной медицины.
Отвар шалфея, ромашки, зверобоя, календулы, эвкалипта оказывает противовоспалительное и противомикробное действие. Такой же эффект дает употребление чеснока, лука, малины, ежевики. Эхинацея обладает сильным антибактериальным свойством.
Жаропонижающим действием окажут отвар липы, мачехи, малиновый чай. Избавиться от грудного спазма в бронхах можно с помощью грудного сбора №1, а также отвара ромашки и укропа.Улучшению отведения мокроты способствуют отвары мачехи, айвы, солодки.
Самые действенные народные рецепты
Плоды клюквы или калины измельчить, смешать с медом или сахаром, залить небольшим количеством теплой воды. Принимать лекарство трижды в день по ½ стакана.
Измельчите лук или чеснок, положите в большую емкость и сделайте над ним глубокий вдох в течение 1-2 минут.
Смешать свежий луковый сок и мед, принимать по столовой ложке трижды в день.
Смешайте мед (столовая ложка), топленый жир (30 г), горячее молоко (стакана). Хорошо размешивать и принимать на начальной стадии заболевания 2-3 раза в день.
В стакан молока добавить столовую ложку шалфея, поставить на огонь, довести смесь до кипения и кипятить 10 минут, затем процедить и снова довести до кипения. Слегка остывший отвар выпить перед сном.
Риновирусная инфекция у детей
С рождения до 6 месяцев ребенок имеет пассивный иммунитет.Дети старше полугода предрасположены к развитию респираторных заболеваний. Чаще всего риновирусная инфекция возникает у детей, посещающих детские сады.
В детском возрасте инкубационный период длится в среднем 3 дня. Как правило, на ранней стадии заболевания ребенок чувствует недомогание, озноб, температура тела повышается до 37,5 ºС. Также заболевание проявляется чиханием и заложенностью носа, кашлем.
Лечение риновирусной инфекции у детей имеет свои особенности, так как многие препараты противопоказаны в детском возрасте.Поэтому при появлении симптомов заболевания следует обращаться к специалисту. Врач проведет обследование и назначит соответствующие лечебные процедуры.
Риновирусная инфекция у кошек
Кошки также могут заболеть этим вирусным заболеванием, которое проявляется носовыми и глазными выделениями серозного характера, чиханием, угнетением, потерей аппетита или отказом от корма. Кроме кальцитозного ринотрахеита, это так называемая риновирусная инфекция у кошек (о лечении речь пойдет ниже), сопровождающаяся появлением язв на языке, губах, небе, средней щели ноздрей.Источником инфекции являются больные животные или носители вируса t
Ротавирусная инфекция у детей — что вам нужно знать
Этот материал нельзя использовать в коммерческих целях, в больницах или медицинских учреждениях. Несоблюдение может повлечь судебный иск.
ЧТО НУЖНО ЗНАТЬ:
Что такое ротавирусная инфекция?
Ротавирус — это вирус, вызывающий воспаление тонкой кишки. Инфекция может помешать организму вашего ребенка поглощать воду и питательные вещества из пищи.Это может вызвать сильное обезвоживание. Ротавирус может передаваться через кашель, пищу или воду, а также при контакте с испражнениями инфицированного человека. Ротавирус может оставаться на предметах, таких как одежда или игрушки, в течение многих дней. Инфекция может распространяться при прикосновении к зараженному объекту.
Что увеличивает риск заражения моего ребенка ротавирусной инфекцией?
Ротавирус чаще всего встречается у детей младше 5 лет, особенно в возрасте от 3 месяцев до 2 лет. Ваш ребенок также подвергается риску, если он или она ходит в детский сад или часто путешествует.Слабая иммунная система, например, из-за рака, ВИЧ или трансплантации органов или костного мозга, также может увеличить его или ее риск.
Каковы признаки и симптомы ротавирусной инфекции?
Симптомы обычно появляются через 1–3 дня после заражения. Ротавирусная инфекция может распространяться за 2 дня до появления симптомов и до 10 дней после. Симптомы обычно длятся от 3 до 8 дней и могут включать более одного из следующих признаков:
- Лихорадка
- Тошнота, рвота и боль в животе
- Сильная водянистая диарея, которая обычно начинается через 1-2 дня после лихорадки и рвоты
- Утомляемость и раздражительность
- Головные боли
Как диагностируется ротавирусная инфекция?
Лечащий врач вашего ребенка осмотрит вашего ребенка.Расскажите ему или ей о симптомах вашего ребенка, в том числе о том, когда началась диарея и как часто она возникает. Лечащий врач вашего ребенка проверит вашего ребенка на наличие признаков обезвоживания. Образец испражнения вашего ребенка может быть отправлен в лабораторию для проверки на наличие инфекции.
Как лечится ротавирусная инфекция?
Ротавирусная инфекция может пройти без лечения. Вашему ребенку может потребоваться любое из следующего, если он или она обезвожены или подвержены риску обезвоживания:
- Могут потребоваться дополнительные жидкости .Спросите, сколько жидкости следует пить ребенку каждый день. Хорошо пить воду или фруктовый сок. Вашему ребенку может потребоваться раствор для пероральной регидратации (ПРС). Это напиток, который содержит необходимое количество соли, сахара и минералов в воде. Если вы кормите грудью, продолжайте кормить ребенка грудью.
- Назогастральный зонд (NG) или внутривенное введение может потребоваться, если ваш ребенок не может пить жидкости или обезвоживание тяжелое. Жидкость можно вводить через трубку NG, которая вводится через нос и опускается в желудок.
Что я могу сделать, чтобы предотвратить распространение ротавирусной инфекции?
- Часто мойте руки себе и ребенку. Используйте воду и мыло. Если мыло и вода недоступны, используйте дезинфицирующее средство для рук на гелевой основе. Мойте руки после посещения туалета, смены детских подгузников или чихания. Мойте руки перед приготовлением или едой.
- Узнайте у лечащего врача вашего ребенка о ротавирусной вакцине. Вакцина обычно вводится детям. Ваш ребенок получит дозы в 2 и 4 месяца. Третья доза может потребоваться через 6 месяцев. Окончательную дозу следует ввести не позднее 8-месячного возраста.
- Очистите элементы, которые могут быть заражены. Используйте дезинфицирующие средства на основе хлора для очистки поверхностей, туалетов, игрушек и предметов общего пользования в доме.
- Пусть ваш ребенок останется дома, пока он болеет. Держите ребенка подальше от окружающих до тех пор, пока его или ее лечащий врач предписывает вам это.Не позволяйте ребенку возвращаться в школу или детский сад, пока поставщик не скажет, что это безопасно.
Позвоните на местный номер службы экстренной помощи (911 в США), если:
- Тело вашего ребенка кажется вялым и слабым, или он вообще не реагирует на вас.
- У вашего ребенка проблемы с дыханием или его сердцебиение учащается, чем обычно.
Когда мне следует немедленно обратиться за помощью?
- Мягкое пятно на голове вашего ребенка запало.
- Ваш ребенок не может или не хочет пить.
- У вашего ребенка сухой липкий рот, он плачет без слез или глаза запавшие.
- Ваш ребенок растерянный или более сонный, чем обычно.
- Ваш ребенок не может остановить рвоту.
- Руки и ноги вашего ребенка внезапно похолодели.
Когда мне следует позвонить детскому врачу?
- Ваш ребенок пьет меньше жидкости, чем обычно.
- Ваш ребенок мочится меньше обычного или у вашего ребенка меньше 6 мокрых подгузников за 1 день.
- У вашего ребенка жар, который не проходит или становится хуже.
- У вашего ребенка кровь в кишечнике.
- У вашего ребенка боли в животе, чаще диарея.
- Тело вашего ребенка опухшее и опухшее, а лицо красное.
- У вас есть вопросы или опасения по поводу состояния вашего ребенка или ухода за ним.
Соглашение об уходе
Вы имеете право помогать планировать уход за своим ребенком. Узнайте о состоянии здоровья вашего ребенка и о том, как его можно лечить. Обсудите варианты лечения с поставщиками медицинских услуг вашего ребенка, чтобы решить, какое лечение вы хотите для своего ребенка.Вышеуказанная информация носит исключительно учебный характер. Он не предназначен для использования в качестве медицинского совета по поводу индивидуальных состояний или лечения. Поговорите со своим врачом, медсестрой или фармацевтом перед тем, как следовать любому лечебному режиму, чтобы узнать, безопасно ли оно для вас и эффективно.© Copyright IBM Corporation 2020 Информация предназначена только для использования Конечным пользователем, ее нельзя продавать, распространять или иным образом использовать в коммерческих целях. Все иллюстрации и изображения, включенные в CareNotes®, являются собственностью A.D.A.M., Inc., защищенной авторским правом.или IBM Watson Health
Дополнительная информация
Всегда консультируйтесь со своим поставщиком медицинских услуг, чтобы убедиться, что информация, отображаемая на этой странице, применима к вашим личным обстоятельствам.
Заявление об ограничении ответственности за медицинское обслуживание
Подробнее о ротавирусной инфекции у детей
Сопутствующие препараты
Frontiers | Биология риновирусов, антигенное разнообразие и достижения в разработке вакцины против человеческого риновируса
Введение
Риновирусы человека (HRV) — респираторные вирусы, принадлежащие к семейству Picornaviridae и роду Enterovirus .Впервые ВСР были изолированы в 1950-х годах и остаются основной причиной инфекций верхних дыхательных путей во всем мире (Price, 1956; Jacobs et al., 2013). ВСР остается основным этиологическим агентом простуды и ответственна за значительную заболеваемость, медицинские расходы и пропуски занятий в школе и на рабочем месте (Fendrick et al., 2003; Pappas et al., 2008; Gern, 2010; van der Zalm et al. др., 2011; Jacobs et al., 2013). Годовые экономические затраты, связанные с инфекциями ВСР, вероятно, превысят 60 миллиардов долларов в год (Fendrick et al., 2003). Инфекции ВСР возникают круглый год и во всех частях мира и проявляют сезонность, достигая пика весной и / или осенью (Winther et al., 2006; Miller et al., 2007; Jacobs et al., 2013; Litwin and Bosley. , 2014; Leotte et al., 2017). Помимо возникновения инфекций верхних дыхательных путей, ВСР также связана с развитием и, как было показано, обостряет астму и инфекции нижних дыхательных путей у людей-добровольцев, страдающих астмой (Hicks et al., 2006; Malmstrom et al., 2006; Renwick et al., 2007). ; Джексон и др., 2008, 2014; Сообщение и др., 2008; Герн, 2010; Jacobs et al., 2013; Сарая и др., 2014). Значительное бремя для здоровья, связанное с ВСР, по-прежнему подчеркивает острую необходимость вакцины против ВСР. Тем не менее, ряд проблем помешали разработке эффективной вакцины.
Инфекции и болезни ВСР
Риновирусы являются одними из наиболее распространенных вирусных инфекционных агентов, обнаруживаемых у людей. На ВСР приходится более 50% инфекций верхних дыхательных путей, а частота инфекций среди детей младшего возраста может достигать 8–12 раз в год (Arruda et al., 1995; Тернер, 1997; Паппас и др., 2008). Инфекции ВСР обычно связаны с инкубационным периодом продолжительностью 2 дня, за которым следует симптоматический период продолжительностью 1-2 недели до исчезновения (Pappas et al., 2008). Бессимптомные инфекции носоглотки довольно распространены среди риновирусов, особенно среди детей раннего возраста (van Benten et al., 2003; Iwane et al., 2011). Инфекции верхних дыхательных путей связаны с простудными симптомами, включая ринорею, боль в горле, кашель, чихание, заложенность носа и общее недомогание (Arruda et al., 1997; Jacobs et al., 2013). Помимо простуды, риновирусные инфекции часто связаны с острым средним отитом и риносинуситом, которые также часто совпадают с бактериальной коинфекцией (Pitkaranta et al., 1997; Alper et al., 2007; Jackson et al., 2008; Jacobs et al. др., 2013). Несмотря на оптимальную температуру для репликации ВСР на более прохладных поверхностях (32–33 ° C) верхних дыхательных путей, риновирусы также могут вызывать заболевания нижних дыхательных путей, включая пневмонию, бронхит и бронхиолит, а также обострение астмы (McFadden et al., 1985; Тернер, 1997; Пападопулос и др., 2000; Renwick et al., 2007; Герн, 2010). Известно, что более половины всех случаев обострения астмы связаны с инфекциями ВСР, а ранние инфекции ВСР, приводящие к хрипу, повышают риск развития астмы в более позднем возрасте (Gern and Busse, 1999; Gern et al., 1999; Hayden, 2004; Jackson et al., 2008; Dougherty and Fahy, 2009). Приблизительно у 90% детей, госпитализированных с острыми приступами астмы, обнаруживалась ВСР (Bizzintino et al., 2011). Кроме того, исследование, в котором оценивали пациентов в возрасте от 3 до 18 лет, поступивших с хрипами, выявило почти половину положительных результатов теста на ВСР (Heymann et al., 2004). В совокупности эти исследования демонстрируют, что ВСР, хотя обычно не считается патогеном с высокой смертностью, имеет высокий потенциал для острых респираторных заболеваний и может способствовать развитию или обострению хронических респираторных заболеваний.
Передача ВСР происходит главным образом между людьми при прямом контакте, контакте с фомитами или аэрозолями (Gwaltney and Hendley, 1978; Gwaltney et al., 1978; Дик и др., 1987; Дженнингс и Дик, 1987; Хендли и Гвалтни, 1988). Риновирусы способны оставаться заразными на поверхностях за пределами хозяев в течение нескольких часов, что приводит к высокому потенциалу распространения между инфицированными и неинфицированными людьми (Hendley et al., 1973). Восприимчивость к тяжелым инфекциям и повторным инфекциям связана со многими экологическими и генетическими факторами, включая плохую реакцию на интерферон, существующую аллергию или астму, воздействие загрязнителей воздуха, включая табачный дым, плохое питание и стресс (Gern, 2010; Kang et al., 2012; Jacobs et al., 2013). Частота повторного инфицирования определенными типами ВСР предполагает, что в некоторых случаях инфекции ВСР не может развиться компетентный иммунитет или что ранее существовавший иммунитет не может поддерживаться (Papi et al., 2006).
Структура и биология ВСР
Риновирус человека — это вирус без оболочки с одноцепочечной РНК с положительным смыслом (+ оцРНК) размером примерно 7,2 т.п.н., которая кодирует 11 белков (рис. 1А) (Palmenberg et al., 2009, 2010; Palmenberg and Gern, 2015) . Вирусный капсид ВСР состоит из четырех вирусных белков (VP): VP1, VP2, VP3 и VP4.Остальные вирусные белки отвечают за репликацию вируса и последующую сборку. Антигенная вариабельность между типами ВСР происходит из вариаций открытой поверхности VP1, VP2 и VP3, в то время как встроенный VP4 отвечает за упаковку РНК во время сборки (рис. 1B). По сравнению с остальной частью генома ВСР, белки капсида демонстрируют высокую степень гетерогенности, что приводит к широкому диапазону антигенного разнообразия (Glanville and Johnston, 2015; Lewis-Rogers et al., 2017). Несколько антигенных сайтов были идентифицированы для штаммов HRV посредством изучения связывания нейтрализующих антител.Однако расположение этих сайтов часто не сохраняется (Sherry and Rueckert, 1985; Sherry et al., 1986; Appleyard et al., 1990).
РИСУНОК 1. Геномная организация риновируса человека, структура вириона и виды. (A) Геном 7,21 т.п.н. + оцРНК HRV-16 состоит из одной открытой рамки считывания, кодирующей 11 генных продуктов, которые при трансляции в три различных полипротеина расщепляются протеазами, кодируемыми HRV (2A и 3C). 5′-конец генома кэпирован коротким вирусным прайминговым белком (VPg) для включения во время сборки вириона, а 3′-конец полиаденилируется.Капсидные белки VP1 и VP4 ( * ) обычно используются для филогенетического анализа. RdRP, РНК-зависимая РНК-полимераза; UTR, непереведенный регион. (B) Икосаэдрическая структура вириона ВСР с пентамерной структурой, которая выделяет организацию белков внешнего капсида (VP1, VP2 и VP3). VP1 отвечает за взаимодействие с рецептором, а VP4 располагается под каждой мономерной единицей и отвечает за геномную ассоциацию с VPg. (C) Было идентифицировано три различных вида риновируса человека (HRV-A, HRV-B и HRV-C).Показано приблизительное количество типов в каждой классификации видов и известные рецепторы каждого вида.
VP1 опосредует прикрепление к поверхности клетки за счет взаимодействия с различными рецепторами клеточной поверхности (рис. 1C) (Palmenberg and Gern, 2015; Blaas, 2016). Традиционно было известно, что большинство типов ВСР связываются с рецептором молекулы межклеточной адгезии 1 (ICAM-1), а меньшая часть типов ВСР использовала для связывания рецептор липопротеинов низкой плотности (ЛПНП) (Staunton et al., 1989; Hofer et al. al., 1994; Пальменберг, 2017). Однако с недавней идентификацией конкретного варианта родственного кадгерину члена 3 семейства (CDHR3) в качестве первичного рецептора для разновидностей ВСР C и широты циркулирующих типов ВСР, еще не идентифицированные рецепторы также могут существовать (Бочков и др. ., 2015, 2016; Пальменберг, 2017). ВСР может проникать в клетку несколькими путями, включая макропиноцитоз и клатрин-зависимый и клатриннезависимый эндоцитоз (Blaas, 2016). После проникновения и удаления оболочки вирусный геном транслируется и впоследствии протеолитически процессируется кодируемыми вирусом протеазами 2A и 3C (Fuchs and Blaas, 2010).Во время сборки вириона и геномной упаковки 60 единиц каждого капсидного белка связываются, по 1 единице каждого капсидного белка на каждую грань, чтобы сформировать икосаэдрическую структуру, инкапсулирующую геном РНК вируса (Rossmann et al., 1985; Palmenberg et al., 2010; Liu et al., 2016).
Филогенетическое разнообразие риновирусов
В настоящее время известны три вида риновирусов: HRV-A, HRV-B и HRV-C. Однако секвенирование и серологические методы определили приблизительно 83 типа ВСР-А, 32 типа ВСР-В и 55 типов ВСР-С с потенциально от 150 до 170 серологических различных типов ВСР в обращении (рис. 1С) (Palmenberg et al., 2009; McIntyre et al., 2013). Штаммы риновирусов одного вида имеют более 70% аминокислотной идентичности, и новые типы теперь классифицируются почти исключительно на основе выравнивания последовательностей VP1 или VP4 / VP2 (Palmenberg and Gern, 2015). Изоляты, имеющие более 87% идентичности, могут быть объединены с существующими типами (McIntyre et al., 2013; Palmenberg and Gern, 2015). Основной проблемой при разработке вакцины против ВСР и последующем создании защитного иммунитета является филогенетическая широта существующих серотипов ВСР.Инфекция одним типом ВСР вряд ли обеспечит какой-либо иммунитет к другим типам, что приведет к пожизненным инфекциям от воздействия различных типов ВСР. Однако ограниченная кросс-серотипическая защита была продемонстрирована для некоторых близкородственных типов (Cooney et al., 1973; Glanville and Johnston, 2015). Среди известных типов ВСР, ВСР-А и ВСР-С обычно связаны с более тяжелыми заболеваниями и обострениями астмы, чем ВСР-В (Miller et al., 2009; Piralla et al., 2009; Bochkov et al., 2011; Ли и др., 2012, 2016). Структуры всех трех видов обнаруживают отчетливые различия в поверхностных карманах, которые могут объяснять их фенотипические различия (Palmenberg and Gern, 2015; Liu et al., 2016).
Недавнее открытие и биология HRV-C
HRV-C был недавно идентифицирован в 2006 году и с тех пор признан одним из основных факторов, вызывающих заболевание HRV (Arden et al., 2006; Lamson et al., 2006; Kistler et al., 2007; Renwick et al., 2007; Домингес и др., 2008). Более половины всех инфекций ВСР у детей раннего возраста в настоящее время распознаются как штаммы ВСР-С (Бочков и др., 2011). Кроме того, среди типов ВСР, обнаруживаемых во время эпизодов острой астмы у детей, ВСР-С была наиболее часто обнаруживаемым видом (Bizzintino et al., 2011). После их первоначальной идентификации было идентифицировано около 60 типов, и теперь они классифицированы как отдельные виды ВСР от ВСР-А и ВСР-В (Simmonds et al., 2010; McIntyre et al., 2013; Palmenberg and Gern, 2015). Однако, в отличие от HRV-A и HRV-B, исследование штаммов HRV-C осложнялось невозможностью изначально выращивать эти вирусы в культуре клеток.
Первое сообщение, описывающее успешное восстановление типа ВСР-C (C15) с помощью обратной генетики, было в 2011 году, однако эти вирусы не могли быть впоследствии пассированы (Bochkov et al., 2011). В отличие от своих аналогов, типы HRV-C не используют ICAM-1 или LDLR в качестве первичных рецепторов для прикрепления (Bochkov et al., 2011). Фенотипически ВСР-C может быть более переносимой при более высоких температурах для репликации, что приводит к более выраженным заболеваниям нижних дыхательных путей, чем виды A или B (Ashraf et al., 2013).Более того, вирус нельзя было легко пассировать или культивировать до недавней идентификации CDHR3 в качестве первичного рецептора вируса в 2015 году (Bochkov et al., 2015). Вскоре последовала первая структура капсида типа HRV-C (Liu et al., 2016). В сочетании с ныне культивируемым подходом обратной генетики значительное внимание уделяется изучению биологии ВСР-C. Недавняя работа показала, что HRV-C избирательно нацелен на ресничные эпителиальные клетки дыхательных путей, которые экспрессируют CDHR3 (Griggs et al., 2017). Эти результаты обнадеживают и открывают путь для более тщательного изучения биологии HRV-C и потенциальной разработки противовирусных препаратов и вакцин, специфичных для HRV-C.Из-за его важной роли в развитии заболеваний человека разработка эффективной вакцины против риновируса от простуды должна включать антигенное покрытие репрезентативных штаммов HRV-C.
Проблемы разработки вакцин против ВСР
Разработка вакцины против риновируса остается всеобщей надеждой общественного здравоохранения и научных кругов. Более полувека перспективы разработки вакцины против ВСР оставались мрачными. Для разработки успешной вакцины против ВСР остается множество технических, логистических и фундаментальных биологических проблем.Мыши и хлопковые крысы являются важными моделями для тестирования эффективности вакцин для выработки нейтрализующих антител, однако они не полностью допускают инфекцию и могут лишь напоминать некоторые аспекты патогенеза ВСР у людей (Bartlett et al., 2008; Blanco et al. , 2014а). Недавние достижения в получении мышей, трансгенных по человеческому ICAM-1, сделали их улучшенной моделью для изучения инфекции ВСР (Bartlett et al., 2008). Тем не менее, любой вакцинный препарат, вероятно, придется изучать непосредственно на людях.
В отличие от многих других вирусных патогенов человека, широта сдвига серологически различных типов ВСР представляет собой уникальную и сложную проблему для разработки вакцины. Чтобы разработать вакцину против ВСР, независимо от подхода (например, живая аттенуированная, инактивированная), один или несколько препаратов для вакцинации должны обладать способностью вызывать защитные нейтрализующие антитела к потенциально более чем 150 серологически различным типам, охватывающим три разных вида. Несмотря на успехи в культуре клеток, приводящие к увеличению титров вируса, сложная техническая задача получения достаточного количества и качества антигена для охвата всех типов ВСР остается ключевой технической проблемой.Кроме того, остается недостаточно данных эпидемиологического надзора и эпидемиологических данных, чтобы точно определить, каким конкретным доминантным типам ВСР-А и ВСР-С следует уделить приоритетное внимание при подготовке вакцин для смягчения последствий заболевания. Кроме того, в нескольких исследованиях с использованием как противовирусных препаратов, так и препаратов антигенных пептидов и вирусов сообщалось об индукции мутаций ускользания, часто с помощью одной аминокислоты (Heinz et al., 1989; Appleyard et al., 1990; Speller et al., 1993) . Однако структура большинства типов ВСР еще не решена, и только недавно была определена первая структура ВСР-С (Liu et al., 2016). Несмотря на эти очевидные проблемы, были достигнуты успехи в понимании того, как разработать вакцину против ВСР, и возможности создания прочного защитного иммунитета.
Прошлые и текущие попытки создания вакцины
К 1960-м годам стало очевидно, что существует множество серологически различных штаммов риновируса и что для борьбы с простудой потребуется разработка поливалентного вакцинного препарата (Mitchison, 1965). Ранние попытки разработать вакцину против ВСР в 1960 и 1970-х годах были сосредоточены на следующем: (1) индуцируют ли живые аттенуированные или инактивированные штаммы ВСР антитела и способны ли они обеспечивать защиту; (2) могут ли гетерологичные или дивергентные штаммы вызывать широкую защиту и, наконец, (3) могут ли препараты поливалентной вакцины быть эффективными.Исследование Bynoe et al. (1961) продемонстрировали, что люди способны иметь защитные уровни антисыворотки к конкретному штамму ВСР. Два последующих исследования, опубликованные в 1963 году, продемонстрировали, что один штамм либо живой, не ослабленной ВСР, либо ВСР, инактивированный формалином или теплом, был способен индуцировать антитела после внутримышечной инъекции и что уровни циркулирующих антител обратно коррелировали с ассоциированным заболеванием (Doggett et al. ., 1963; Муфсон и др., 1963). По Митчисону (1965) было очевидно, что вакцинация штаммом HRV способна не только индуцировать защитные антитела, но также может обеспечивать гомологичную защиту того же штамма.Последующие исследования, опубликованные в течение следующих нескольких лет, подтвердили, что вакцины против ВСР могут быть эффективными с устойчивым иммунитетом после гомологичного заражения, но не с гетерологичными штаммами (Perkins et al., 1969a, b; Buscho et al., 1972).
В начале 1970-х годов были опубликованы первые исследования по оценке перекрестной нейтрализации и серологической реактивности между многими типами ВСР, которые открыли дверь для самых ранних попыток создания поливалентных вакцинных препаратов. Куни и др. (1973) продемонстрировали, что кроличьи антисыворотки к 37 типам приводят к ограниченной перекрестной нейтрализации по крайней мере между пятью типами.Эти и более ранние исследования с использованием моновалентных препаратов привели к первой крупной попытке создания поливалентной вакцины против ВСР в Hamory et al. (1975). К этому времени было описано 89 типов ВСР, а несколько других находились на различных стадиях подтверждения. В этом исследовании Hamory et al. (1975) получили два отдельных декавалантных препарата вакцины против ВСР путем объединения 10 уникальных наборов типов, инактивирующих формалин, с начальными титрами 10 1,5 –10 6,0 TCID 50 / мл. К сожалению, эти препараты вакцины привели к низким титрам нейтрализующих антител с обнаруживаемыми ответами хозяина менее чем на 40% вводимых типов.По сравнению с известным в то время количеством типов, разработка эффективной поливалентной вакцины вскоре стала считаться маловероятной или невозможной (Fox, 1976; Couch, 1984).
В течение следующих 30 лет научные успехи в клеточной и молекулярной биологии и продолжающиеся исследования биологии ВСР и типоспецифических различий привели к возобновлению интереса и надежд на разработку вакцины против ВСР. Первая кристаллическая структура капсида HRV (HRV-14) была определена Rossmann et al. (1985). Структуры всех трех видов ВСР вскоре будут определены с помощью более 70 структур, которые сейчас хранятся в банке данных по белкам (PDB) (Palmenberg, 2017).В Palmenberg et al. (2009, 2010), были опубликованы полные геномные последовательности для значительного числа известных штаммов HRV-A и HRV-B, что позволило по-новому взглянуть на эволюцию ВСР, различия между специфическими штаммами и убедительные доказательства рекомбинации антигенных типов.
В свете сложной задачи разработки поливалентного препарата инактивированной вакцины для более чем 100 типов и достижений в понимании структуры ВСР, недавние усилия были сосредоточены на идентификации и использовании консервативных антигенных сайтов с помощью подходов на основе субъединиц и / или Т-клеток.Несколько недавних попыток использования VP1 в качестве иммуногена продемонстрировали, что антитела, реагирующие с перекрестными серотипами, могут быть получены при достаточном воздействии, а рекомбинантный VP1 может быть потенциальным антигеном для индукции ограниченной перекрестной реактивности (Edlmayr et al., 2011; McLean et al., 2012). Кроме того, исследования также показали, что N-конец VP4 способен вызывать антитела перекрестного серотипа (Katpally et al., 2009; Panjwani et al., 2016). Усилия в области гриппа показали, что стимулирование распознавания и иммунитета на основе внутренних эпитопов, экспрессируемых в Т-клетках, может быть эффективным для нацеливания на более консервативные эпитопы и обеспечивать большую активность Th2 и защиту перекрестного серотипа (Lee et al., 2008; Hillaire et al., 2011). Более ранние исследования ВСР продемонстрировали, что популяции Т-клеток распознают как общие, так и типоспецифичные эпитопы (Hastings et al., 1993a, b; Gern et al., 1997). Экспрессия рекомбинантного VP0 в комбинации с Th2-ориентированным адъювантом (комбинация неполных Fruend’s и CpG) была эффективной для стимулирования сильных Th2-специфических перекрестных серотипных ответов антител (Glanville et al., 2013). Эти коллективные исследования демонстрируют, что разработка субъединичной вакцины может быть эффективным подходом к решению проблемы антигенного разнообразия ВСР в препарате вакцины.Кроме того, эти исследования показывают, что перекрестно-реактивные антигены (с использованием специфических адъювантов) могут использоваться для увеличения серологической широты охвата ВСР при ограничении количества необходимых типов антигенов.
Продолжаются исследования препаратов цельного вируса для изучения потенциала вакцин. В Blanco et al. (2014b), было показано, что внутримышечное введение живого HRV-16 индуцирует перекрестный серотип нейтрализующих антител после интраназального введения хлопковых крыс.В прошлом году было показано, что 50-валентный инактивированный вакцинный препарат, состоящий из типов, представляющих разнообразие известных штаммов HRV-A, индуцирует нейтрализующие антитела ко всем, кроме одного типа, испытанному после иммунизации у макак-резусов (Lee et al., 2016). Это исследование Lee et al. (2016) также продемонстрировали использование восстановленного препарата декавалентной вакцины 1975 г. из Hamory et al. (1975) показали, что ловушка этой ранней попытки создания поливалентной вакцины, вероятно, заключалась в сочетании неадекватных уровней антигена и потенциальной потребности в адъюванте.Эти недавние открытия продемонстрировали, что высокая валентность поливалентных вакцинных препаратов, которая, вероятно, была бы необходима для вакцины против ВСР, может быть эффективной для стимулирования длительного иммунитета при условии наличия достаточных уровней антигена.
Заключительные мысли: будущий потенциал вакцины против ВСР
На протяжении большей части прошлого века вакцина против ВСР часто считалась невозможной. Поливалентный вакцинный препарат для любого патогена с валентностью, необходимой для обеспечения защиты циркулирующей ВСР, еще не был продемонстрирован ни в одной коммерческой вакцине.Тем не менее, успехи в нашем понимании типов ВСР, структуры капсида и недавние достижения в идентификации консервативных перекрестно-реактивных антигенных сайтов пролили новый свет на направления, которые следует исследовать при разработке вакцины. Более того, достижения в области обратной генетики ВСР и возможность создания препаратов химерного вируса в совокупности предполагают, что разработка вакцины против ВСР технически не невозможна, но потребует новой изобретательности и постоянного изучения существующих сходств и различий между типами ВСР.
Авторские взносы
Участвовал непосредственно в написании и редактировании, редактировании и окончательном утверждении статьи перед подачей CS, JN и MM.
Заявление о конфликте интересов
MM является соучредителем Meissa Vaccines, Inc. и является главным научным сотрудником компании. MM является автором заявки на патент (PCT / US2016 / 037658), в которой описывается вакцина против риновируса, описанная здесь. Другие авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могут быть истолкованы как потенциальный конфликт интересов.
Благодарности
Эта работа была поддержана финансированием исследовательского гранта факультета (CS) Комитета по присуждению премий Холкомба (HAC), факультета биологических наук Университета Батлера и начального финансирования факультета (CS) Университета Батлера.
Список литературы
Альпер, К. М., Винтер, Б., Мандель, Э. М. и Дойл, В. Дж. (2007). Временные отношения при простудных заболеваниях и среднем отите в парах братьев и сестер. Pediatr. Заразить. Дис. J. 26, 778–781.DOI: 10.1097 / INF.0b013e318124aa31
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Апплеярд, Г., Рассел, С. М., Кларк, Б. Э., Спеллер, С. А., Троубридж, М., и Вадолас, Дж. (1990). Эпитопы нейтрализации риновируса человека типа 2. J. Gen. Virol. 71 (Pt 6), 1275–1282. DOI: 10.1099 / 0022-1317-71-6-1275
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Арден, К. Э., МакЭрлин, П., Ниссен, М. Д., Слоутс, Т. П., и Маккей, И.М. (2006). Частое обнаружение риновирусов, парамиксовирусов, коронавирусов и бокавирусов человека при острых респираторных инфекциях. J. Med. Virol. 78, 1232–1240. DOI: 10.1002 / jmv.20689
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Арруда, Э., Бойл, Т. Р., Винтер, Б., Пивир, Д. К., Гвалтни, Дж. М. младший, и Хайден, Ф. Г. (1995). Локализация репликации риновируса человека в верхних дыхательных путях путем гибридизации in situ. Дж.Заразить. Дис. 171, 1329–1333. DOI: 10.1093 / infdis / 171.5.1329
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Арруда, Э., Питкаранта, А., Витек, Т. Дж. Мл., Дойл, К. А., и Хайден, Ф. Г. (1997). Частота и естественное течение риновирусных инфекций у взрослых осенью. J. Clin. Microbiol. 35, 2864–2868.
Google Scholar
Ашраф, С., Брокман-Шнайдер, Р., Бочков, Ю.А., Пасич, Т.Р., и Герн, Дж. Э. (2013).Биологические характеристики и распространение человеческого риновируса-C в дифференцированных эпителиальных клетках синуса. Вирусология 436, 143–149. DOI: 10.1016 / j.virol.2012.11.002
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бартлетт, Н. В., Уолтон, Р. П., Эдвардс, М. Р., Анищенко, Дж., Карамори, Г., Чжу, Дж. И др. (2008). Мышиные модели заболевания, вызванного риновирусом, и обострения аллергического воспаления дыхательных путей. Нат. Med. 14, 199–204. DOI: 10.1038 / нм 1713
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Биззинтино, Дж., Ли, У. М., Лэйнг, И. А., Ванг, Ф., Папас, Т., Чжан, Г. и др. (2011). Связь между риновирусом С человека и тяжестью острой астмы у детей. Eur. Респир. J. 37, 1037–1042. DOI: 10.1183 / 036.00092410
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бланко, Дж. К., Бухвалова, М. С., Перес, Д. Р., Фогель, С. Н., и Каджон, А.(2014a). Моделирование респираторных вирусных инфекций человека у хлопковой крысы ( Sigmodon hispidus ). J. Antivir. Антиретровир. 6, 40–42. DOI: 10.4172 / jaa.1000093
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бланко, Дж. К., Кор, С., Плетнева, Л. М., Марч, Т. Х., Бухвалова, М. С., Каджон, А. Е. (2014b). Профилактическое лечение антителами и внутримышечная иммунизация снижают инфекционную нагрузку риновируса человека 16 в нижних дыхательных путях зараженных хлопковых крыс. Trials Vaccinol. 3, 52–60. DOI: 10.1016 / j.trivac.2014.02.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бочков, Ю.А., Пальменберг, А.С., Ли, В.М., Рат, Дж. А., Аминева, С. П., Сан, X. и др. (2011). Молекулярное моделирование, культивирование органов и обратная генетика для недавно идентифицированного риновируса человека C. Nat. Med. 17, 627–632. DOI: 10,1038 / нм. 2358
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бочков, Ю.А., Уоттерс, К., Ашраф, С., Григгс, Т. Ф., Деврис, М. К., Джексон, Д. Дж. И др. (2015). Связанный с кадгерином член семьи 3, продукт гена восприимчивости к детской астме, опосредует связывание и репликацию риновируса С. Proc. Natl. Акад. Sci. США 112, 5485–5490. DOI: 10.1073 / pnas.1421178112
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бочков, Ю.А., Уоттерс, К., Баснет, С., Сияпати, С., Хилл, М., Пальменберг, А.С. и др. (2016). Мутации в белках VP1 и 3A улучшают связывание и репликацию риновируса C15 в клетках HeLa-E8. Вирусология 499, 350–360. DOI: 10.1016 / j.virol.2016.09.025
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Бушо Р. Ф., Перкинс Дж. К., Кнопф Х. Л., Капикян А. З. и Чанок Р. М. (1972). Дальнейшая характеристика местного ответа антителами в дыхательных путях, вызванного интраназальной инстилляцией вакцины против инактивированного риновируса 13. J. Immunol. 108, 169–177.
PubMed Аннотация | Google Scholar
Быное, М.Л., Хобсон, Д., Хорнер, Дж., Киппс, А., Шильд, Г. К., и Тиррелл, Д. А. (1961). Прививка добровольцев штаммом вируса, изолированного от простуды. Ланцет 1, 1194–1196. DOI: 10.1016 / S0140-6736 (61) 91941-9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Куни, М. К., Кенни, Г. Э., Там Р. и Фокс, Дж. П. (1973). Перекрестные отношения между 37 риновирусами продемонстрированы нейтрализацией вируса с помощью мощных монотипных кроличьих антисывороток. Заражение.Иммун. 7, 335–340.
PubMed Аннотация | Google Scholar
Дик, Э. К., Дженнингс, Л. К., Минк, К. А., Вартгоу, К. Д., и Инхорн, С. Л. (1987). Аэрозольная передача риновирусных простуд. J. Infect. Дис. 156, 442–448. DOI: 10.1093 / infdis / 156.3.442
CrossRef Полный текст | Google Scholar
Доггетт, Дж. Э., Байно, М. Л., и Тиррелл, Д. А. (1963). Некоторые попытки создать экспериментальную вакцину с риновирусами. Br. Med. Дж. 1, 34–36. DOI: 10.1136 / bmj.1.5322.34
CrossRef Полный текст | Google Scholar
Домингес, С. Р., Бризе, Т., Паласиос, Г., Хуэй, Дж., Виллари, Дж., Капур, В. и др. (2008). Мультиплексная MassTag-PCR на респираторные патогены в педиатрических смывах носоглотки, отрицательная при обычном диагностическом тестировании, показывает высокую распространенность вирусов, принадлежащих к недавно признанной кладе риновирусов. J. Clin. Virol. 43, 219–222. DOI: 10.1016 / j.jcv.2008.06.007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Догерти, Р.Х., Фахи Дж. В. (2009). Острые обострения астмы: эпидемиология, биология и фенотип, предрасположенный к обострениям. Clin. Exp. Аллергия 39, 193–202. DOI: 10.1111 / j.1365-2222.2008.03157.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Эдлмайр, Дж., Несподзиана, К., Попов-Крауп, Т., Кшизанек, В., Фокке-Тейкл, М., Блаас, Д. и др. (2011). Антитела, индуцированные рекомбинантным VP1 из риновируса человека, проявляют перекрестную нейтрализацию. Eur. Респир.J. 37, 44–52. DOI: 10.1183 / 036.00149109
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фендрик А. М., Монто А. С., Найтенгейл Б. и Сарнес М. (2003). Экономическое бремя вирусных респираторных инфекций, не связанных с гриппом, в США. Arch. Междунар. Med. 163, 487–494. DOI: 10.1001 / archinte.163.4.487
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Фокс, Дж. П. (1976). Возможна ли вакцина против риновируса? Am.J. Epidemiol. 103, 345–354. DOI: 10.1093 / oxfordjournals.aje.a112233
CrossRef Полный текст | Google Scholar
Герн, Дж. Э. и Буссе, В. В. (1999). Связь риновирусных инфекций с астмой. Clin. Microbiol. Ред. 12, 9–18.
Google Scholar
Герн, Дж. Э., Дик, Э. К., Келли, Э. А., Вртис, Р., и Кляйн, Б. (1997). Риновирус-специфические Т-клетки распознают как общие, так и ограниченные по серотипу вирусные эпитопы. J. Infect.Дис. 175, 1108–1114. DOI: 10.1086 / 516449
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гланвилл, Н., Маклин, Г. Р., Гай, Б., Лекутюрье, В., Берри, К., Жирр, Ю. и др. (2013). Кросс-серотипический иммунитет, индуцированный иммунизацией консервативным капсидным белком риновируса. PLOS Pathog. 9: e1003669. DOI: 10.1371 / journal.ppat.1003669
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Григгс Т.Ф., Бочков Ю.A., Basnet, S., Pasic, T. R., Brockman-Schneider, R.A., Palmenberg, A.C., et al. (2017). Риновирус C нацелен на мерцательные эпителиальные клетки дыхательных путей. Respir Res 18:84. DOI: 10.1186 / s12931-017-0567-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гвалтни, Дж. М. младший, и Хендли, Дж. О. (1978). Передача риновируса: один — по воздуху, два — вручную. Am. J. Epidemiol. 107, 357–361. DOI: 10.1093 / oxfordjournals.aje.a112555
CrossRef Полный текст | Google Scholar
Гвалтни, Дж.М. мл., Москальский П. Б. и Хендли Дж. О. (1978). Передача риновирусных простуд из рук в руки. Ann. Междунар. Med. 88, 463–467. DOI: 10.7326 / 0003-4819-88-4-463
CrossRef Полный текст | Google Scholar
Хэмори, Б. Х., Хампарян, В. В., Конант, Р. М., и Гвалтни, Дж. М. младший (1975). Ответы человека на две вакцины против декавалентного риновируса. J. Infect. Дис. 132, 623–629. DOI: 10.1093 / infdis / 132.6.623
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гастингс, Г.З., Фрэнсис М. Дж., Роулендс Д. Дж. И Чейн Б. М. (1993a). Процессинг антигена и презентация человеческого риновируса Т-клеткам CD4 облегчается связыванием с клеточными рецепторами вируса. Eur. J. Immunol. 23, 1340–1345. DOI: 10.1002 / eji.1830230623
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Гастингс, Г. З., Фрэнсис, М. Дж., Роулендс, Д. Дж., И Чейн, Б. М. (1993b). Эпитопный анализ ответа Т-клеток на сложный антиген: пролиферативные ответы на капсиды риновируса человека. Eur. J. Immunol. 23, 2300–2305. DOI: 10.1002 / eji.1830230937
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хайнц, Б. А., Рюкерт, Р. Р., Шепард, Д. А., Дутко, Ф. Дж., МакКинли, М. А., Фанчер, М., и др. (1989). Генетический и молекулярный анализ спонтанных мутантов риновируса человека 14, устойчивых к противовирусному соединению. J. Virol. 63, 2476–2485.
PubMed Аннотация | Google Scholar
Хендли, Дж.О., и Гвалтни, Дж. М. младший (1988). Механизмы передачи риновирусных инфекций. Epidemiol. Ред. 10, 243–258. DOI: 10.1093 / oxfordjournals.epirev.a036024
CrossRef Полный текст | Google Scholar
Хендли, Дж. О., Венцель, Р. П., и Гвалтни, Дж. М. младший (1973). Передача риновирусной простуды при самолечении. N. Engl. J. Med. 288, 1361–1364. DOI: 10.1056 / NEJM197306282882601
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хейманн, П.W., Карпер, Х. Т., Мерфи, Д. Д., Платтс-Миллс, Т. А., Патри, Дж., Маклафлин, А. П. и др. (2004). Вирусные инфекции в зависимости от возраста, атопии и сезона госпитализации среди детей, госпитализированных по поводу хрипов. J. Allergy Clin. Иммунол. 114, 239–247. DOI: 10.1016 / j.jaci.2004.04.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хикс, Л. А., Шепард, К. В., Бритц, П. Х., Эрдман, Д. Д., Фишер, М., Фланнери, Б. Л. и др. (2006). Две вспышки тяжелого респираторного заболевания в домах престарелых, связанные с риновирусом. J. Am. Гериатр. Soc. 54, 284–289. DOI: 10.1111 / j.1532-5415.2005.00529.x
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хиллер, М. Л., Остерхаус, А. Д., и Риммельцваан, Г. Ф. (2011). Индукция вирус-специфичных цитотоксических Т-лимфоцитов как основа для разработки широко защищающих противогриппозных вакцин. J. Biomed. Biotechnol. 2011: 939860. DOI: 10.1155 / 2011/939860
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Хофер, Ф., Gruenberger, M., Kowalski, H., Machat, H., Huettinger, M., Kuechler, E., et al. (1994). Члены семейства рецепторов липопротеинов низкой плотности опосредуют проникновение в клетки вируса простуды минорной группы. Proc. Natl. Акад. Sci. США 91, 1839–1842. DOI: 10.1073 / pnas.91.5.1839
CrossRef Полный текст | Google Scholar
Иване, М. К., Прилл, М. М., Лу, X., Миллер, Э. К., Эдвардс, К. М., Холл, К. Б. и др. (2011). Виды человеческого риновируса, связанные с госпитализацией детей раннего возраста в США по поводу острых респираторных заболеваний. J. Infect. Дис. 204, 1702–1710. DOI: 10.1093 / infdis / jir634
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джексон, Д. Дж., Гангнон, Р. Э., Эванс, М. Д., Роберг, К. А., Андерсон, Е. Л., Паппас, Т. Е., и др. (2008). Свистящее риновирусное заболевание в раннем возрасте предсказывает развитие астмы у детей из группы высокого риска. Am. J. Respir. Крит. Care Med. 178, 667–672. DOI: 10.1164 / rccm.200802-309OC
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Джексон, Д.Дж., Макриниоти, Х., Рана, Б. М., Шамджи, Б. В., Трухильо-Торральбо, М. Б., Футит, Дж. И др. (2014). ИЛ-33-зависимое воспаление 2 типа при обострениях астмы, вызванных риновирусом, in vivo. Am. J. Respir. Крит. Care Med. 190, 1373–1382. DOI: 10.1164 / rccm.201406-1039OC
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Дженнингс, Л.С., и Дик, Е.С. (1987). Передача и борьба с риновирусными простудными заболеваниями. Eur. J. Epidemiol. 3, 327–335.DOI: 10.1007 / BF00145641
CrossRef Полный текст | Google Scholar
Кан, М. Дж., Ю, Х. С., Со, Дж. Х., Ким, Х. Ю., Юнг, Ю. Х., Ким, Ю. Дж. И др. (2012). Варианты GSDMB / ORMDL3 вносят вклад в восприимчивость к астме и гиперреактивность бронхов, опосредованную эозинофилами. Hum. Иммунол. 73, 954–959. DOI: 10.1016 / j.humimm.2012.06.009
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Катпалли, У., Фу, Т. М., Фрид, Д. К., Касимиро, Д.Р., Смит Т. Дж. (2009). Антитела к скрытому N-концу риновируса VP4 проявляют кросс-серотипическую нейтрализацию. J. Virol. 83, 7040–7048. DOI: 10.1128 / JVI.00557-09
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Кистлер А., Авила П. К., Рускин С., Ван Д., Уорд Т., Яги С. и др. (2007). Пановирусный скрининг инфекций дыхательных путей у взрослых с астмой и без нее выявляет неожиданное разнообразие коронавирусов человека и риновирусов человека. J. Infect. Дис. 196, 817–825. DOI: 10.1086 / 520816
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ламсон, Д., Ренвик, Н., Капур, В., Лю, З., Паласиос, Г., Джу, Дж. И др. (2006). Обнаружение респираторных патогенов с помощью полимеразной цепной реакции MassTag, включая новый генотип риновируса, которые вызвали гриппоподобное заболевание в штате Нью-Йорк в 2004-2005 гг. J. Infect. Дис. 194, 1398–1402. DOI: 10.1086 / 508551
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, Л.Y., Hado, L.A., Simmons, C., de Jong, M.D., Chau, N.V., Schumacher, R., et al. (2008). Т-клетки памяти, созданные сезонным человеческим гриппом A, перекрестно реагируют с птичьим гриппом A (H5N1) у здоровых людей. J. Clin. Вкладывать деньги. 118, 3478–3490. DOI: 10.1172 / JCI32460
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, С., Нгуен, М. Т., Карриер, М. Г., Дженкинс, Дж. Б., Строберт, Э. А., Каджон, А. Е. и др. (2016). Поливалентная вакцина с инактивированным риновирусом является широко иммуногенной для макак-резусов. Нат. Commun. 7: 12838. DOI: 10.1038 / ncomms12838
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Ли, У. М., Леманске, Р. Ф. младший, Эванс, М. Д., Ванг, Ф., Паппас, Т., Гангнон, Р. и др. (2012). Виды человеческого риновируса и сезон заражения определяют тяжесть заболевания. Am. J. Respir. Крит. Care Med. 186, 886–891. DOI: 10.1164 / rccm.201202-0330OC
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Леотт, Дж., Тромбетта, Х., Фэджион, Х. З., Алмейда, Б. М., Ногейра, М. Б., Видаль, Л. Р. и др. (2017). Воздействие и сезонность риновирусной инфекции человека у госпитализированных пациентов в течение двух лет подряд. J. Pediatr. 93, 294–300. DOI: 10.1016 / j.jped.2016.07.004
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Льюис-Роджерс, Н., Сегер, Дж., И Адлер, Ф. Р. (2017). Разнообразие и эволюция риновирусов человека: как странно переход от большого к второстепенному. Дж.Virol. 91: e01659-16. DOI: 10.1128 / JVI.01659-16
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Литвин, К. М., и Босли, Дж. Г. (2014). Сезонность и распространенность респираторных патогенов, обнаруженных с помощью мультиплексной ПЦР в медицинском центре третичного уровня. Arch. Virol. 159, 65–72. DOI: 10.1007 / s00705-013-1794-4
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Лю Ю., Хилл М. Г., Клозе Т., Чен З., Уоттерс К., Бочков Ю.А. и др. (2016). Атомная структура риновируса С, вида вируса, связанного с тяжелой формой детской астмы. Proc. Natl. Акад. Sci. США 113, 8997–9002. DOI: 10.1073 / pnas.1606595113
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Мальмстрем, К., Питкаранта, А., Карпен, О., Пелконен, А., Мальмберг, Л. П., Турпейнен, М., и др. (2006). Риновирус человека в бронхиальном эпителии младенцев с рецидивирующими респираторными симптомами. J. Allergy Clin.Иммунол. 118, 591–596. DOI: 10.1016 / j.jaci.2006.04.032
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Макфадден, Э. Р. мл., Пичурко, Б. М., Боуман, Х. Ф., Ингенито, Э., Бернс, С., Даулинг, Н., и др. (1985). Тепловое картирование дыхательных путей человека. J. Appl. Physiol. 58, 564–570.
PubMed Аннотация | Google Scholar
Макинтайр, К. Л., Ноулз, Н. Дж., И Симмондс, П. (2013). Предложения по классификации видов риновирусов человека A, B и C на генотипически определенные типы. J. Gen. Virol. 94 (Pt 8), 1791–1806. DOI: 10.1099 / vir.0.053686-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Маклин, Г. Р., Уолтон, Р. П., Шетти, С., Пил, Т. Дж., Пактиавал, Н., Кебадзе, Т. и др. (2012). Риновирусные инфекции и иммунизация индуцируют перекрестно-серотипно-реактивные антитела к VP1. Antiviral Res. 95, 193–201. DOI: 10.1016 / j.antiviral.2012.06.006
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Сообщение, S.Д., Лаза-Станка, В., Маллиа, П., Паркер, Х. Л., Чжу, Дж., Кебадзе, Т. и др. (2008). Вызванное риновирусом заболевание нижних дыхательных путей увеличивается при астме и связано с вирусной нагрузкой и производством цитокинов Th2 / 2 и IL-10. Proc. Natl. Акад. Sci. США 105, 13562–13567. DOI: 10.1073 / pnas.0804181105
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Миллер, Э. К., Хури-Булос, Н., Уильямс, Дж. В., Шехаби, А. А., Фаури, С., Аль-Джунди, И., и др. (2009).Человеческий риновирус C связан с хрипом у госпитализированных детей на Ближнем Востоке. J. Clin. Virol. 46, 85–89. DOI: 10.1016 / j.jcv.2009.06.007
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Миллер, Э. К., Лу, X., Эрдман, Д. Д., Пёлинг, К. А., Чжу, Ю., Гриффин, М. Р. и др. (2007). Госпитализации детей раннего возраста, связанные с риновирусом. J. Infect. Дис. 195, 773–781. DOI: 10.1086 / 511821
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Митчисон, Д.А. (1965). Профилактика простуды с помощью вакцинации против риновируса: доклад научного комитета по вакцинам против простуды. Br. Med. J. 1, 1344–1349. DOI: 10.1136 / bmj.1.5446.1344
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Муфсон, М.А., Людвиг, В.М., Джеймс, Х.Д. мл., Голд, Л.В., Рурк, Дж. А., Холпер, Дж. К. и др. (1963). Влияние нейтрализующих антител на экспериментальную риновирусную инфекцию. JAMA 186, 578–584. DOI: 10.1001 / jama.1963.63710060029013
CrossRef Полный текст | Google Scholar
Пальменберг, А. К., Рат, Дж. А., и Лиггет, С. Б. (2010). Анализ полных последовательностей генома риновируса человека. J. Allergy Clin. Иммунол. 125, 1190–1199; викторина 1200–1191. DOI: 10.1016 / j.jaci.2010.04.010
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пальменберг, А.С., Спиро, Д., Кузьмицкас, Р., Ван, С., Джикенг, А., Рате, Дж. А., и др. (2009).Секвенирование и анализ всех известных геномов риновирусов человека выявили структуру и эволюцию. Science 324, 55–59. DOI: 10.1126 / science.1165557
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Панджвани А., Асфор А. С. и Тутхилл Т. Дж. (2016). Консервативный N-конец капсидного белка VP4 риновируса человека обладает активностью по формированию мембранных пор и является мишенью для нейтрализующих антител. J. Gen. Virol. 97, 3238–3242. DOI: 10.1099 / JGV.0,000629
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пападопулос, Н. Г., Бейтс, П. Дж., Бардин, П. Г., Папи, А., Лейр, С. Х., Френкель, Д. Дж. И др. (2000). Риновирусы поражают нижние дыхательные пути. J. Infect. Дис. 181, 1875–1884. DOI: 10.1086 / 315513
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Папи А., Беллеттато К. М., Браччони Ф., Романьоли М., Касолари П., Карамори Г. и др. (2006). Инфекции и воспаление дыхательных путей при тяжелых обострениях хронической обструктивной болезни легких. Am. J. Respir. Крит. Care Med. 173, 1114–1121. DOI: 10.1164 / rccm.200506-859OC
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Паппас Д. Э., Хендли Дж. О., Хайден Ф. Г. и Винтер Б. (2008). Профиль симптомов простудных заболеваний у детей школьного возраста. Pediatr. Заразить. Дис. J. 27, 8–11. DOI: 10.1097 / INF.0b013e31814847d9
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Перкинс, Дж. К., Такер, Д. Н., Ноуп, Х.Л., Венцель, Р. П., Хорник, Р. Б., Капикян, А. З. и др. (1969a). Доказательства защитного эффекта вакцины от инактивированного риновируса, вводимой через нос. Am. J. Epidemiol. 90, 319–326. DOI: 10.1093 / oxfordjournals.aje.a121076
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Перкинс, Дж. К., Такер, Д. Н., Кнопф, Х. Л., Венцель, Р. П., Капикян, А. З., и Чанок, Р. М. (1969b). Сравнение защитного действия нейтрализующих антител в сыворотке крови и выделениях из носа при экспериментальном заболевании риновирусом 13 типа. Am. J. Epidemiol. 90, 519–526. DOI: 10.1093 / oxfordjournals.aje.a121098
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Пиралла А., Ровида Ф., Кампанини Г., Роньони В., Марчи А., Локателли Ф. и др. (2009). Клиническая серьезность и молекулярное типирование штаммов риновируса С человека во время вспышки падения, затронувшей госпитализированных пациентов. J. Clin. Virol. 45, 311–317. DOI: 10.1016 / j.jcv.2009.04.016
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Питкаранта, А., Арруда, Э., Мальмберг, Х. и Хайден, Ф. Г. (1997). Обнаружение риновируса в чистках носовых пазух пациентов с острым внебольничным синуситом методом обратной транскрипции-ПЦР. J. Clin. Microbiol. 35, 1791–1793.
Google Scholar
Прайс, У. Х. (1956). Выделение нового вируса, ассоциированного с клиническим респираторным заболеванием человека. Proc. Natl. Акад. Sci. США 42, 892–896. DOI: 10.1073 / pnas.42.12.892
CrossRef Полный текст | Google Scholar
Ренвик, Н., Schweiger, B., Kapoor, V., Liu, Z., Villari, J., Bullmann, R., et al. (2007). Недавно идентифицированный генотип риновируса связан с тяжелой инфекцией дыхательных путей у детей в Германии. J. Infect. Дис. 196, 1754–1760. DOI: 10.1086 / 524312
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Россманн, М. Г., Арнольд, Э., Эриксон, Дж. У., Франкенбергер, Э. А., Гриффит, Дж. П., Хехт, Х. Дж. И др. (1985). Структура вируса простуды человека и функциональная связь с другими пикорнавирусами. Природа 317, 145–153. DOI: 10.1038 / 317145a0
CrossRef Полный текст | Google Scholar
Сарая Т., Кураи Д., Исии Х., Ито А., Сасаки Ю., Нива С. и др. (2014). Эпидемиология вирус-индуцированных обострений астмы: особое внимание уделяется роли риновируса человека. Фронт. Microbiol. 5: 226. DOI: 10.3389 / fmicb.2014.00226
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Шерри Б., Моссер А. Г., Колонно Р.Дж. И Рюкерт Р. Р. (1986). Использование моноклональных антител для идентификации четырех нейтрализующих иммуногенов пикорнавируса простуды, риновируса человека 14. J. Virol. 57, 246–257.
PubMed Аннотация | Google Scholar
Шерри Б. и Рюкерт Р. (1985). Доказательства наличия по крайней мере двух доминирующих нейтрализующих антигенов на риновирусе человека 14. J. Virol. 53, 137–143.
PubMed Аннотация | Google Scholar
Симмондс, П., Макинтайр, К., Саволайнен-Копра, К., Таппарел, К., Маккей, И. М., и Хови, Т. (2010). Предложения по классификации человеческого риновируса вида C на генотипически определенные типы. J. Gen. Virol. 91 (Pt 10), 2409–2419. DOI: 10.1099 / vir.0.023994-0
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Спеллер, С. А., Сангар, Д. В., Кларк, Б. Э., и Роулендс, Д. Дж. (1993). Природа и пространственное распределение аминокислотных замен, придающих устойчивость к нейтрализующим моноклональным антителам в человеческом риновирусе типа 2. J. Gen. Virol. 74 (Pt 2), 193–200. DOI: 10.1099 / 0022-1317-74-2-193
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Стонтон Д. Э., Мерлуцци В. Дж., Ротлейн Р., Бартон Р., Марлин С. Д. и Спрингер Т. А. (1989). Молекула клеточной адгезии, ICAM-1, является основным поверхностным рецептором риновирусов. Cell 56, 849–853. DOI: 10.1016 / 0092-8674 (89)
-2CrossRef Полный текст | Google Scholar
Тернер Р. Б. (1997).Эпидемиология, патогенез и лечение простуды. Ann. Allergy Asthma Immunol. 78, 531–539; викторина 539–540. DOI: 10.1016 / S1081-1206 (10) 63213-9
CrossRef Полный текст | Google Scholar
van Benten, I., Koopman, L., Niesters, B., Hop, W., van Middelkoop, B., de Waal, L., et al. (2003). Преобладание риновируса в носу у детей с симптомами и бессимптомно. Pediatr. Allergy Immunol. 14, 363–370. DOI: 10.1034 / j.1399-3038.2003.00064.х
PubMed Аннотация | CrossRef Полный текст | Google Scholar
ван дер Залм, М. М., Уилбринк, Б., ван Эвейк, Б. Э., Овердуин, П., Вольфс, Т. Ф., и ван дер Энт, К. К. (2011). Очень частые инфекции риновирусом человека у здоровых маленьких детей: продольное когортное исследование. J. Clin. Virol. 52, 317–320. DOI: 10.1016 / j.jcv.2011.09.003
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Винтер Б., Хайден Ф. Г. и Хендли Дж.О. (2006). Пикорнавирусные инфекции у детей, диагностированные с помощью ОТ-ПЦР в ходе длительного наблюдения с еженедельным взятием проб: связь с симптоматическим заболеванием и влиянием сезона. J. Med. Virol. 78, 644–650. DOI: 10.1002 / jmv.20588
PubMed Аннотация | CrossRef Полный текст | Google Scholar
Frontiers | Эпидемиология вирусных обострений астмы: особое внимание уделяется роли риновируса человека
Введение
Известно, что более 200 различных типов вирусов, таких как риновирус человека (HRV), метапневмовирус человека (HMPV), респираторно-синцитиальный вирус (RSV) и вирус парагриппа человека (HPIV), вызывают острые респираторные заболевания (ARI; Tsukagoshi et al. al., 2013). Недавно мы сообщили о проблеме «вирус-индуцированного обострения астмы и хронической обструктивной болезни легких» (Kurai et al., 2013a), однако среди этих причинных вирусов ВСР, как теперь признано, оказывает большое влияние на патогенез астмы (Fujitsuka et al. др., 2011). С этой точки зрения мы рассмотрели литературу по эпидемиологии астмы, вызванной ВСР, у взрослых, а также предварительные эпидемиологические данные, полученные в нашем учреждении.
Клиническая вирусология риновируса человека
HRV принадлежит к роду Enterovirus и семейству Picornaviridae (Turner and Couch, 2007).HRV обладает геномом одноцепочечной позитивно-смысловой РНК (оцРНК) размером примерно 7,2 т.п.н. Вирусный капсид состоит из четырех вирусных белков (VP1-4), которые собраны в 60 протомеров, в результате чего образуется небольшая икосаэдрическая структура диаметром примерно 28-30 нм (Turner and Couch, 2007). Генетически ВСР подразделяется на три вида; HRV-A, -B и -C (Simmonds et al., 2010). Кроме того, эти виды ВСР имеют более 150 генотипов (Andries et al., 1990; Arakawa et al., 2012; Kiyota et al., 2013, 2014). Молекулярно-эпидемиологические исследования показывают, что доминирующими видами являются HRV-A и -C, в то время как HRV-B обнаруживается относительно редко (Arakawa et al., 2012; Kiyota et al., 2013). В частности, белки VP1 и VP2 имеют вариации в своих аминокислотных последовательностях, что объясняет большое количество вирусных серотипов (Turner and Couch, 2007). Рецептор хозяина для ВСР в клетках респираторного эпителия представляет собой молекулу внутриклеточной адгезии 1 (ICAM-1, CD54) для 84 основных серотипов ВСР (HRV-A и -B) или рецептор липопротеинов низкой плотности (LDLR) для других второстепенных Серотипы ВСР.Рецептор HRV-C пока не известен. Было высказано предположение, что оптимальной температурой для репликации ВСР является относительно низкая температура (33–35 ° C), что ограничит инфекцию верхних дыхательных путей; однако большие или средние дыхательные пути ниже в дыхательных путях теперь также считаются достаточно прохладными для репликации ВСР, несмотря на более высокую температуру паренхимы легких (37 ° C; McFadden et al., 1985). Следовательно, ВСР потенциально является возбудителем более тяжелых ОРИ, таких как бронхиолит и пневмония (Turner and Couch, 2007; Watanabe et al., 2010; Smuts et al., 2011; Arakawa et al., 2012), и может быть связано с вирусной астмой (Johnston et al., 1995; Linsuwanon et al., 2009; Fujitsuka et al., 2011; Smuts et al., 2011). Следовательно, ВСР может быть вовлечена в различные ОРИ и дополнительные респираторные осложнения (Kiyota et al., 2013). Либерман и др. (2009) сообщили, что при обнаружении любого вируса, включая ВСР, показатели чувствительности мазка из носоглотки (73,3%) выше, чем у мазка из ротоглотки (54,2%), соответственно.
Простуды, вызванные вирусами, и их естественное течение среди населения в целом
Простуда является третьим по частоте первичным диагнозом при визитах к врачу (Hsiao et al., 2010), и это заболевание, как правило, самоограничивается, обычно длится до 10 дней (Fashner et al., 2012). Среди населения в целом инфекция ВСР вызывает простуду с частотой 25–53% (Makela et al., 1998; van Gageldonk-Lafeber et al., 2005). Tyrrell et al. (1993) сообщили, что интраназальная инокуляция серотипов 2, 9 и 14 ВСР, коронавируса типа 229E или RSV у здоровых добровольцев вызывала паттерны развития симптомов, которые существенно не отличались друг от друга.Однако отдельные признаки или симптомы сначала возникали при инфекциях ВСР, затем при коронавирусе и, наконец, при РСВ, проявляясь до 5 дней после инокуляции, что свидетельствует о длительных периодах инкубации РСВ у добровольцев (Tyrrell et al., 1993).
ВСР была выявлена у пациентов с острым средним отитом, обострением хронической обструктивной болезни легких, простудой и инфекциями нижних дыхательных путей у новорожденных, пожилых людей и с ослабленным иммунитетом. Arruda et al. (1997), исследуя частоту и естественную историю инфекций ВСР у взрослых осенью, продемонстрировали, что первым заметным симптомом чаще всего была боль в горле (40%) у пациентов с положительным результатом посева ВСР или ПЦР и заложенность носа у пациентов с отрицательной реакцией на ВСР. (27%), используя образцы для промывания носа.Респираторные симптомы обычно развиваются через 1-2 дня после инокуляции в исследованиях, а неосложненные инфекции ВСР обычно достигают пика через 2-4 дня после инокуляции. Средняя продолжительность простуды, связанной с ВСР, составляет 1 неделю, но до 25% случаев длятся более 2 недель (Gwaltney et al., 1967; Rotbart and Hayden, 2000). Следует отметить, что при заболевании, вызванном ВСР, выделение вируса естественным образом происходит в течение 21 дня, но преимущественно в течение периода 3-4 дней.
Инфекция ВСР среди астматиков: in vivo или in vitro Экспериментальные исследования
HRV-A типа 16 (HRV-16), вирус основной группы, обычно используемый для экспериментальной инфекции человека, и HRV-A типа 1 (HRV-1), который использовался в животных моделях инфекции HRV, тесно связаны.Grunberg et al. (1999) сообщили, что экспериментальная инфекция ВСР-16 через носовые ингаляции приводит к временному снижению ОФВ на 1,0 у пациентов с астмой, и это снижение функции легких коррелирует с усилением симптомов простуды и / или гиперчувствительностью дыхательных путей. Contoli et al. (2006) продемонстрировали, что уровни продукции интерферона III типа (IFN-λ) в ex vivo культурах клеток , полученных из эпителиальных клеток бронхов (BEC) и макрофагов, полученных от пациентов с астмой, были ниже, чем в культурах, полученных от здоровых людей.Кроме того, недостаточная продукция интерферона-λ коррелировала с вирусной нагрузкой ВСР, тяжестью клинических симптомов и ОФВ 1,0 . Сообщение и др. (2008) продемонстрировали, что тяжесть клинического заболевания, вызванного интраназально инокулированной ВСР, у пациентов с астмой коррелировала с вирусной нагрузкой и воспалением нижних дыхательных путей.
С другой стороны, DeMore et al. (2009) сообщили, что не было отмечено различий в клинических симптомах и характере выделения вируса между субъектами со стойкой аллергической астмой и здоровыми субъектами после экспериментального инфицирования ВСР.Эти разные результаты после экспериментальной инфекции ВСР в отдельных исследованиях у пациентов с астмой и здоровых субъектов могут зависеть от тяжести астмы у тех субъектов, которые участвовали в исследованиях. Действительно, в нескольких отчетах не наблюдались ни дефектная индукция ИФН с помощью ВСР, ни повышенная репликация ВСР в первичных БЭК человека, полученных от субъектов с хорошо контролируемой астмой (Lopez-Souza et al., 2009; Bochkov et al., 2010; Sykes et al. ., 2014). Было показано несколько животных моделей риновирусной инфекции, поскольку основная группа ВСР (т.е., HRV-16) не связывает мышиный ICAM-1. Только небольшая группа ВСР (т.е. ВСР-1В) инфицировала мышь. В связи с этим Bartlett et al. (2008) получили трансгенную мышь BALB / c, экспрессирующую химерный рецептор мыши-человека ICAM-1 для инфекции HRV-16. В этом исследовании также была показана модель обострения астмы при интраперитонеальной сенсибилизации овальбумином с гидроксидом алюминия с последующей интраназальной инокуляцией HRV-1B или УФ-инактивированной HRV-1B.
Обострения ВСР и астмы: клинические данные
Хотя данные о вирусных респираторных инфекциях (ВРИ) как ускорителях приступов астмы у взрослых менее ясны, Nicholson et al.(1993) сообщили, что ВРИ так же часто связаны с обострениями у взрослых, как и у детей (Johnston et al., 1996; Fujitsuka et al., 2011). Это исследование показало, что вирусы были обнаружены в 44% клинических эпизодов обострения со снижением максимальной скорости выдоха (PEFR) на 50 мл / мин или более, и наиболее часто выявляемым вирусом была ВСР, за которой следовали коронавирусы и вирусы парагриппа (Nicholson и др., 1993). Таким образом, вирус, чаще всего обнаруживаемый при обострениях астмы, — это ВСР.
Хотя ВСР хорошо известна как наиболее частая причина простуды, последствия инфекции ВСР различаются в зависимости от респираторных заболеваний. В таблице 1 показана частота инфицирования ВСР при различных респираторных заболеваниях взрослых, таких как обострение астмы (Nicholson et al., 1993; Atmar et al., 1998; Tan et al., 2003), простуде (Makela et al., 1998 ; van Gageldonk-Lafeber et al., 2005), обострение ХОБЛ (Seemungal et al., 2001; Rohde et al., 2003; Tan et al., 2003; Beckham et al., 2005; Папи и др., 2006; Hutchinson et al., 2007; Ко и др., 2007; Макманус и др., 2008; Херад и др., 2010; Димопулос и др., 2012; Perotin et al., 2013), внебольничная пневмония (Jennings et al., 2008; Johnstone et al., 2008; Johansson et al., 2010; Lieberman et al., 2010; Fry et al., 2011; Wootton et al., 2008). ., 2011; Luchsinger et al., 2013; Takahashi et al., 2013; Huijskens et al., 2014), обострение идиопатического легочного фиброза (Wootton et al., 2011) и бессимптомная инфекция (Fry et al., 2011).
ТАБЛИЦА 1. Инфекция ВСР и ее частота при острых и хронических респираторных заболеваниях у взрослых.
Риск обострения астмы у взрослых повышается после того, как дети вернутся в школу и примерно 25 декабря (рождественские каникулы в западных странах), и это, вероятно, связано с социальным взаимодействием с детьми в это время. Проспективные мониторинговые исследования с использованием полимеразной цепной реакции с обратной транскрипцией (ОТ-ПЦР) показывают, что до 85% обострений острой астмы у детей и около 60% у взрослых были связаны с наличием инфекций верхних дыхательных путей (ВДП).Corne et al. (2002) обнаружили, что частота выявления ВСР у астматиков (10,1%) и здоровых участников (8,5%) была схожей, но симптомы LRT были значительно более серьезными и продолжительными в группе астматиков, чем в группе здоровых, на основе одного определения. симптомов URT и LRT (таблица 2; Johnston et al., 1995).
ТАБЛИЦА 2. Респираторные симптомы.
Не существует общего антигена для всех штаммов ВСР; поэтому не было разработано надежного метода диагностики инфекции ВСР с использованием антигенов ВСР или антител, специфичных для ВСР.Хотя вирусное культивирование является традиционным методом обнаружения ВСР, методы культивирования неприменимы в клинических условиях для обнаружения ВСР из-за его медленного роста и требований к конкретным условиям культивирования. Кроме того, диагностические возможности методов молекулярной амплификации, таких как амплификация на основе последовательностей нуклеиновых кислот и ОТ-ПЦР, превосходят возможности методов культивирования (Loens et al., 2006).
Патогенез обострений астмы, связанной с ВСР
Было показано, что экспериментальные инфекции ВСР приводят к длительному чрезмерному сужению дыхательных путей у добровольцев, страдающих астмой (Cheung et al., 1995; Grunberg et al., 1999). Следует отметить, что риновирус, в отличие от вирусов гриппа и других вирусов, вызывает минимальную цитотоксичность (Fraenkel et al., 1995), а степень повреждения эпителия не коррелирует с тяжестью симптомов. Инфекция ВСР может вызывать аддитивные или синергические эффекты при обострении астмы за счет притока дополнительных воспалительных клеток в дыхательные пути с уже существовавшим воспалением, что приводит к холинергической гиперреактивности дыхательных путей (Nagarkar et al., 2010) в качестве аллергической реакции.Эффекты инфекции ВСР, такие как усиление сократительной способности клеток гладкой мускулатуры дыхательных путей (ASM) и нарушение релаксации холинергических или β-адренергических агонистов, объясняются исключительно связыванием вируса с его рецептором-хозяином ICAM-1 на поверхности клеток ASM. Этот проастматический эффект был обнаружен даже в ситуации полного ингибирования репликации вируса in vitro , но не в условиях предварительной обработки ASM нейтрализующим антителом, направленным против ICAM-1 (Grunstein et al., 2001). Таким образом, само присоединение ВСР к ICAM-1 может влиять на сократительную способность клеток ASM в отсутствие каких-либо цитопатических эффектов, и Chun et al. (2013) сообщили, что клетки A 549, инфицированные вирусом HRV in vitro , продуцировали более высокое значение IL-8 и RANTES, чем клетки RSV или аденовируса. Кроме того, только комбинация ВСР с Der f1 (антиген клещей домашней пыли) действовала синергетически, индуцируя продукцию ИЛ-8. Эти данные являются причиной того, что ВСР может быть основным возбудителем острого обострения астмы.Мы представляем схему патогенеза обострений астмы, ассоциированных с ВСР (рис. 1), которая требует следующих шагов: (1) прикрепление ВСР к эпителиальным клеткам дыхательных путей, (2) врожденный иммунный ответ, который приводит к повреждению эпителия, (3) инфекция- связанное ремоделирование дыхательных путей.
РИСУНОК 1. HRV прикрепляется к эпителиальным клеткам дыхательных путей через ICAM-1, LDLR и неизвестные рецепторы HRV-C. Эпителиальные клетки бронхов, инфицированные ВСР , секретируют широкий спектр цитокинов (IFN-β, IFN-λ, IL-1, IL-6, GM-CSF) и хемокинов (CXCL10 / IP-10, CCL5 / RANTES, CXCL8 / IL- 8) вместе с NO, VEGF и EGF, FGF, амфирегулином и активином A.Эти цитокины и хемокины привлекают различные воспалительные клетки, такие как DC, с активацией FcεR1, lym, Eo, Neut и Mϕ. VEGF, EGF, FGF, амфирегулин и активин A способствуют высвобождению матричных белков из фибробластов / миофибробластов, которые усиливают продукцию MMP9 эпителиальными клетками дыхательных путей. Эти явления могут привести к ремоделированию дыхательных путей (пунктирная область, т. Е. Утолщение ретикулярной пластинки). Инфекция ВСР вызывает секрецию MUC5AC, что ухудшает мукоцилиарный клиренс.ДК, дендритные клетки; EGF, фактор роста эпидермиса; Эо, эозинофил; FGF, фактор роста фибробластов; GM-CSF, колониестимулирующий фактор гранулоцитарных макрофагов; ICAM-1, молекула межклеточной адгезии 1; LDRL, рецептор липопротеинов низкой плотности; Лимфоцит, лимфоцит; ММП, матриксная металлопротеиназа; Mϕ, макрофаг; Нейтральный, нейтрофильный; NO, синтаза оксида азота; RANTES, регулируется при активации, экспрессируются и секретируются нормальные Т-клетки; VEGF, фактор роста эндотелия сосудов.
Присоединение к эпителиальным клеткам дыхательных путей
Когда ОТ-ПЦР используется для дополнения или замены традиционных методов культивирования, вирусы были обнаружены примерно у половины-трех четвертей взрослых, испытывающих приступ острого свистящего дыхания (Jackson and Johnston, 2010), и у большинства (59%) идентифицированные вирусы были ВСР (Nicholson et al., 1993). Однако доказательств мало, а механизмы плохо изучены. Первоначально HRV-A и -B прикрепляются к эпителиальным клеткам дыхательных путей через ICAM-1 или LDLR (Kennedy et al., 2012). Рецептор или рецепторы для недавно идентифицированной группы HRV-C еще предстоит выяснить. BEC, инфицированные HRV, секретируют широкий спектр цитокинов и хемокинов, таких как IL-1, IL-6, CCL5 / RANTES (регулируется при активации, нормальные Т-клетки экспрессируются и секретируются), CXCL8 / IL-8, GM-CSF и CXCL10. / интерферон-индуцируемый белок 10 (IP-10; Jackson and Johnston, 2010; Proud, 2011), который вызывает нейтрофильное, лимфоцитарное и эозинофильное воспаление вместе с гиперчувствительностью дыхательных путей и ремоделированием дыхательных путей (Wark et al., 2002; Гордый, 2011).
Врожденный иммунный ответ
Удаление вирусных патогенов начинается с секреции интерферона, и предполагается, что недостаточная продукция этих факторов ведет к вирусным обострениям. Существует три типа интерферонов в зависимости от рецепторов, которые они связывают: тип I (IFN-α / β), тип II (IFN-γ) и тип III (IFN-λ). Инфекция ВСР индуцировала эпителиальную экспрессию мРНК IFN как I, так и III типа, и было высказано предположение, что нарушение эпителиальной продукции IFN-β и IFN-λ у пациентов с астмой может способствовать вирусным обострениям астмы (Wark et al., 2005; Contoli et al., 2006). Contoli et al. (2006) показали значительную обратную корреляцию между продукцией ex vivo IFN-λ и тяжестью симптомов, вирусной нагрузкой бронхоальвеолярного лаважа и воспалением дыхательных путей, а также сильную положительную корреляцию со снижением функции легких во время инфекции in vivo . Полногеномные ассоциативные исследования показали, что однонуклеотидные полиморфизмы связаны с различными заболеваниями. Полиморфизм интерферона-λ может влиять на частоту инфицирования ВСР (Russell et al., 2014).
Message et al. (2008) сообщили, что вирусная нагрузка у астматиков связана с усилением воспаления нижних дыхательных путей, и, в свою очередь, усиление воспаления нижних дыхательных путей связано с усилением симптомов, снижением функции легких и увеличением гиперреактивности бронхов. Эти данные предполагают причинную роль инфекции ВСР в патогенезе обострений астмы.
Изучение взаимодействий вирус-аллерген, Durrani et al. (2012) продемонстрировали, что другой механизм, который увеличивает экспрессию и перекрестное связывание высокоаффинного рецептора IgE, FcεRI, на плазматических дендритных клетках, связан со снижением индуцированной ВСР секреции IFN-α и IFN-λ1, и у детей с аллергической астмой наблюдается значительная снижение индуцированной ВСР продукции IFN-α и IFN-λ1 после перекрестного связывания FcεRI.
Тип 2, или индуцибельная синтаза оксида азота (iNOS), является основной изоформой NOS, обнаруженной в эпителиальных клетках, и может генерировать значительные количества оксида азота (NO). Молекулы NO ингибируют репликацию ВСР в эпителиальных клетках дыхательных путей и подавляют продукцию цитокинов, индуцированную ВСР (Proud, 2005). Хотя измерение фракционной концентрации NO в выдыхаемом воздухе (FENO) может использоваться для подтверждения диагноза астмы (Dweik et al., 2011), однако повышение FENO, по-видимому, не всегда коррелирует с вирусной нагрузкой в течение периода ВСР. инфекция (Sanders et al., 2004).
Другие факторы, такие как аллергия, воздействие аллергенов, табачный дым, твердые частицы, озон, стресс и инфекции, такие как синусит, обычно способствуют обострению астмы.
Инфекция ВСР и ремоделирование дыхательных путей
Grainge et al. (2011) сообщили, что повторяющееся бронхоспазм при астме способствует ремоделированию дыхательных путей, и теперь есть четкие доказательства того, что ремоделирование дыхательных путей начинается в раннем детстве и может присутствовать даже до установления клинического диагноза астмы (Pohunek et al., 2005). Растущее количество данных относительно хрипов, вызванных ВСР, или обострения астмы повышает вероятность того, что инфекции ВСР могут способствовать инициированию и последующему прогрессированию ремоделирования дыхательных путей, которое включает множество факторов, таких как повышенное высвобождение эпителием Mucin5AC (MU5AC), активина А, амфирегулина, матрицы металлопротеиназа 9 (MMP9), эпидермальный фактор роста (EGF), фактор роста фибробластов (FGF) и фактор роста эндотелия сосудов (VEGF).
ИнфекцияHRV стимулирует выработку MUC5AC эпителиальными клетками, что приводит к обструкции дыхательных путей при астме (Hewson et al., 2010). Активин A является членом суперсемейства TGF-β, а амфирегулин, член семейства EGF, изменяет процессы репарации (Leigh et al., 2008). И активин А, и амфирегулин связаны с утолщением субэпителиальной базальной мембраны при астме. MMP9, по-видимому, играет важную роль в обострении астмы и ремоделировании дыхательных путей (Sampsonas et al., 2007). Экспрессия VEGF и его рецепторов повышена у пациентов, страдающих астмой, и VEGF является основным проангиогенным активатором в дыхательных путях при астме (Feltis et al., 2006; Simcock et al., 2007).
Влияние вирусной инфекции на обострение астмы: предварительные данные когортного исследования Kyorin
Kuga et al. (2000) сообщили, что 61,5% взрослых пациентов с астмой, страдающих простудой, перенесли приступ астмы, а простуда в значительной степени ассоциировалась с острыми обострениями астмы. Они также заявили, что инфекция ВСР может быть важной, поскольку вирус был обнаружен с помощью ОТ-ПЦР при полоскании горла (Kuga et al., 2000). Обострение астмы, вызванное вирусами, является серьезной проблемой для врача общей практики.Однако среди пациентов с астмой с обострением трудно отличить пациентов, у которых есть ВРИ, и тех, у кого их нет. Более того, эпидемиологические данные об обострениях астмы у взрослых представлены редко. Чтобы исследовать распространенность ВРИ при обострениях астмы у взрослых как у госпитализированных, так и у госпитализированных пациентов, была проведена характеристика клинических и радиологических данных. Проспективное наблюдательное когортное исследование было проведено в больнице Университета Киорин, Токио, Япония, с августа 2012 г. по август 2013 г. (Kurai et al., 2013б). Были включены все пациенты с респираторными симптомами, связанными с обострением астмы, образцы были собраны с помощью мазков из носоглотки или ротоглотки и подвергнуты методу ПЦР для выявления распространенных респираторных вирусов. 44 пациента, которые были включены в исследование, состояли из госпитализированных ( n = 15) или не госпитализированных пациентов ( n = 29; Таблица 3). В этих двух группах биологические данные субъектов были схожими по возрасту, полу, уровню курения и продолжительности заболевания, однако измеренное значение SpO 2 было значительно ниже у госпитализированных пациентов (87 ± 2.3%), чем у не госпитализированных пациентов (96,2 ± 0,7%). Заболеваемость ВРИ была значительно выше в первой группе (46,7%, n = 7), чем во второй группе (6,9%, n = 2; p = 0,002). В последней группе у обоих пациентов был обнаружен только вирус гриппа. Кроме того, все госпитализированные пациенты (100%, n = 15) имели хрипы или тяжелые обострения, согласно заявлению ATS (Американского торакального общества) / ERS (Европейского респираторного общества) (Reddel et al., 2009), тогда как среди не госпитализированных пациентов только девять пациентов (31%) были признаны имеющими тяжелое обострение ( p <0,001), а 10 пациентов (38,4%) имели хрипы ( p <0,001) . Эти данные свидетельствуют о том, что вирусная инфекция, безусловно, была связана с гипоксемией и / или хрипом, которые привели к тяжелому или серьезному приступу астмы, на основании японских руководств (Ohta et al., 2011) или заявления ATS / ERS (Reddel et al. , 2009). Предыдущие исследования с использованием вирусной диагностики на основе ПЦР показали, что вирусные респираторные инфекции выявлялись до 85% обострений астмы у детей и около 50% обострений у взрослых (Nicholson et al., 1993; Johnston et al., 1995), что похоже на наши результаты. Воспалительные или аллергические маркеры в сыворотке крови у госпитализированных и не госпитализированных пациентов не различаются (таблица 3).
ТАБЛИЦА 3. Сравнение клинических характеристик госпитализированных и не госпитализированных пациентов с приступом астмы.
У госпитализированных пациентов идентифицированные вирусы были HRV ( n = 5), HMPV ( n = 1) и RSV ( n = 1). На момент поступления вирус-положительная группа ( n = 7) имела значительно более низкие значения SpO 2 (81.4 ± 3,9%), чем в группе вирус-отрицательных ( n = 8, SpO 2: 91,8 ± 1,3%, p <0,007), а для пациентов, данные которых доступны, частота гиперкапноэ (PaCO 2 45 Торр) было значительно выше в группе с положительным вирусом (66,7%, n = 4), чем в группе с отрицательным вирусом (0%; p = 0,014; Таблица 4). Механизмы гиперкапноэ у инфицированных вирусом людей не выяснены. Однако Cheung et al.(1995) сообщили, что инфекция ВСР вызывает длительное чрезмерное сужение дыхательных путей в ответ на метахолин у пациентов с астмой. Мы предположили, что гладкие мышцы могут играть роль в чрезмерном сужении дыхательных путей у вирус-положительных пациентов с астмой, как описано King et al. (1999).
ТАБЛИЦА 4. Клиническая характеристика госпитализированных пациентов с приступом астмы на основе наличия вирусной инфекции.
Интересно, что частота помутнения матового стекла (GGO) на компьютерной томографии высокого разрешения казалась выше у госпитализированных пациентов с положительным вирусом, чем у пациентов с отрицательным вирусом, но не достигла статистической значимости.Например, на рис. 2А показан неоднородный GGO с утолщением межлобулярных перегородок у 28-летней женщины, поступившей во время приступа астмы, вызванного ВСР-А. На рисунке 2B также показан GGO у 62-летнего мужчины с приступом астмы, вызванным инфекцией HRV-C. Эти GGO у обоих пациентов могли быть обнаружены только при КТВР, но не на рентгенограмме грудной клетки.
РИСУНОК 2. (A) Показывает неоднородный GGO с утолщением межлобулярных перегородок у 28-летней женщины, поступившей во время приступа астмы, вызванного HRV-A. (B) Также показан GGO у 62-летнего мужчины с приступом астмы, вызванным инфекцией HRV-C.
Эти результаты позволили предположить, что ВСР была основной причиной вирусной астмы и, возможно, была вовлечена в особенности паренхимы нижних дыхательных путей или легких, проявляясь как GGO. Вирусная инфекция значительно усугубила респираторный статус (низкий SpO 2 и гиперкапноэ) по сравнению с вирус-отрицательными пациентами с обострением астмы на момент госпитализации. Действительно, в последние годы ВСР была признана частой причиной госпитализации как возбудителя бронхопневмонии, так и в результате обострения хронических легочных состояний даже у пожилых людей старше 65 лет (Pierangeli et al., 2011).
Любопытно, что после начала лечения внутривенным стероидом как вирус-положительная, так и -отрицательная группы не имели значительной разницы в продолжительности дыхательной недостаточности, хрипов, дней пребывания в больнице и даже во времени, необходимом для лечения стероидами.
Лечение
Не существует установленного лечения для профилактики астмы, вызванной ВСР, и мы описываем исследовательские вмешательства следующим образом.
Кортикостероид ингаляционный
Ингаляционный кортикостероид (ИКС) является основным препаратом для регулярной терапии астмы.Лечение ICS улучшило гиперреактивность дыхательных путей у пациентов с астмой, экспериментально испытавших ВСР, однако лечение ICS не уменьшило накопление воспалительных клеток, за исключением эозинофилов в эпителии бронхов (Grunberg et al., 2001). Двухцепочечная РНК (дцРНК), вирусный продукт и лиганд Toll-подобного рецептора-3 (TLR3), усиливает экспрессию воспалительных хемокинов в эпителиальных клетках дыхательных путей. Мацукура и др. (2013) сообщили, что обработка клеток BEAS-2B пропионатом флутиказона значительно и дозозависимо ингибировала индуцированную дцРНК экспрессию белков и мРНК CCL5, CXCL8 и CXCL10.Чтобы подтвердить влияние на оцРНК, например, на ВСР, потребуются дальнейшие исследования.
Антагонист лейкотриеновых рецепторов
Антагонист лейкотриеновых рецепторов назначался пациентам с астмой с ИГС или без него. Лечение монтелукастом не улучшило контроль астмы или оценку симптомов простуды, когда ВСР была экспериментально инокулирована у пациентов с легкой астмой или здоровых субъектов (Kloepfer et al., 2011). Неизвестно, эффективно ли лечение антагонистами лейкотриеновых рецепторов для уменьшения симптомов астмы, связанных с инфекцией ВСР.
Анти-IgE терапия
Zambrano et al. (2003) сообщили, что высокие уровни IgE в сыворотке у детей с легкой астмой с экспериментальной инфекцией ВСР могут быть связаны с усилением симптомов нижних дыхательных путей и повышением воспалительных маркеров, таких как назальный катионный белок эозинофилов и оксид азота с истекшим сроком годности, чем у здоровых субъектов и / или пациенты с астмой с низким уровнем IgE. Распространенность астмы была тесно связана с уровнями IgE в сыворотке, стандартизованными для возраста и пола (Burrows et al., 1989), а гиперреактивность дыхательных путей, по-видимому, тесно связана с аллергическим диатезом, что отражается в уровне общего сывороточного IgE (Sears et al., 1991). Омализумаб, моноклональное антитело против IgE, был показан пациентам с устойчивой аллергической астмой средней и тяжелой степени тяжести, которые лечились высокими дозами ИКС, при недостаточном контроле. Durrani et al. (2012) показали, что рецептор IgE FcεRI обратно связан с секрецией IFN-α и IFN-λ1, когда плазмацитоидные дендритные клетки, полученные от детей с аллергической астмой, были заражены ВСР.Омализумаб подавляет экспрессию FcεRI на дендритных клетках (Prussin et al., 2003), что может уменьшить обострение астмы, связанное с повышенной продукцией IFN, через FcεRI.
Антивирусное лечение
Никакие лекарства не используются в клинической практике при инфекции ВСР, хотя несколько препаратов были опробованы для лечения и профилактики инфекции ВСР. Эти препараты кратко описаны в обзоре (Jacobs et al., 2013). IFNs потенциально обладают защитной ролью при вирусной астме (Cakebread et al., 2011; Gaajetaan et al., 2013). Беккер и др. (2013) показали, что экзогенные IFN-α, IFN-β, IFN-λ1 и IFN-λ2 ингибируют репликацию ВСР в BEC от здоровых доноров.
Макролидная терапия
Макролиды, как известно, обладают противовоспалительным и иммуномодулирующим действием, выходящим за рамки их антибактериальной активности при воспалительных заболеваниях легких (Takizawa et al., 1995; Min and Jang, 2012). Эритромицин подавляет инфекцию ВСР, снижая экспрессию ICAM-1 на поверхности эпителиальных клеток трахеи человека, и модулирует воспаление, подавляя продукцию провоспалительных цитокинов (Suzuki et al., 2002).
Прочие агенты
Yamaya et al. (2014) сообщили, что муколитический препарат амброксола гидрохлорид, антибиотик левофлоксацин (Yamaya et al., 2012b) и бронходилататоры (тиотропий, тулобутерол и прокатерол) при астме или ХОБЛ (Yamaya et al., 2011, 2012a, 2013) может оказывать положительное влияние на инфекцию ВСР, подавляя репликацию ВСР и частично снижая экспрессию ICAM-1 и продукцию кислых эндосом за счет ингибирования активации NF-kappaB (Yamaya, 2012).
Сводка
Мы рассмотрели предыдущие отчеты об обострениях астмы, вызванной ВСР, вместе с нашими результатами институционального проспективного исследования. ВСР является основным патогеном обострений астмы и, безусловно, ассоциируется с более серьезными клиническими состояниями, такими как гипоксемия или гиперкапноэ у госпитализированных пациентов. Дальнейшее накопление доказательств вирусной астмы для мультидисциплинарной оценки было бы полезным для врачей в распознавании состояния или понимании патогенных механизмов.
Заявление о конфликте интересов
Авторы заявляют, что исследование проводилось в отсутствие каких-либо коммерческих или финансовых отношений, которые могли бы быть истолкованы как потенциальный конфликт интересов.
Список литературы
Андрис, К., Девиндт, Б., Сноекс, Дж., Воутерс, Л., Мореелс, Х., Леви, П. Дж. И др. (1990). Две группы риновирусов, выявленные панелью противовирусных соединений, демонстрируют расхождение последовательностей и различную патогенность. Дж.Virol. 64, 1117–1123.
Pubmed Реферат | Pubmed Полный текст
Аракава, М., Окамото-Накагава, Р., Тода, С., Цукагоши, Х., Кобаяси, М., Рио, А. и др. (2012). Молекулярно-эпидемиологическое исследование риновирусов человека видов A, B и C у пациентов с острыми респираторными заболеваниями в Японии. J. Med. Microbiol. 61, 410–419. DOI: 10.1099 / jmm.0.035006-0
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Арруда, Э., Питкаранта, А., Витек, Т. Дж. Мл., Дойл, К. А., Хайден, Ф. Г. (1997). Частота и естественное течение риновирусных инфекций у взрослых осенью. J. Clin. Microbiol. 35, 2864–2868.
Pubmed Реферат | Pubmed Полный текст
Атмар, Р. Л., Гай, Э., Гунтупалли, К. К., Циммерман, Дж. Л., Банди, В. Д., Бакстер, Б. Д. и др. (1998). Вирусные инфекции дыхательных путей у взрослых, страдающих астмой. Arch. Междунар. Med. 158, 2453–2459. DOI: 10.1001 / archinte.158.22.2453
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Бартлетт, Н. В., Уолтон, Р. П., Эдвардс, М. Р., Анищенко, Дж., Карамори, Г., Чжу, Дж. И др. (2008). Мышиные модели заболевания, вызванного риновирусом, и обострения аллергического воспаления дыхательных путей. Нат. Med. 14, 199–204. DOI: 10,1038 / нм1713
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Беккер, Т. М., Дуррани, С. Р., Бочков, Ю. А., Деврис, М. К., Раджаманикам, В., и Джексон, Д. Дж. (2013). Влияние экзогенных интерферонов на репликацию риновирусов и воспалительные реакции дыхательных путей. Ann. Allergy Asthma Immunol. 111, 397–401. DOI: 10.1016 / j.anai.2013.07.029
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Бекхэм, Дж. Д., Кадена, А., Лин, Дж., Пьедра, П. А., Глезен, В. П., Гринберг, С. Б. и др. (2005). Респираторно-вирусные инфекции у пациентов с хронической обструктивной болезнью легких. J. Infect. 50, 322–330.DOI: 10.1016 / j.jinf.2004.07.011
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Бочков, Ю.А., Хансон, К.М., Келес, С., Брокман-Шнайдер, Р.А., Джарджур, Н.Н., Герн, Дж. Э. (2010). Модуляция экспрессии генов в эпителиальных клетках бронхов у пациентов с астмой, индуцированная риновирусом. Mucosal Immunol. 3, 69–80. DOI: 10.1038 / mi.2009.109
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Берроуз, Б., Мартинес, Ф.Д., Халонен, М., Барби, Р. А., и Клайн, М. Г. (1989). Связь астмы с уровнем IgE в сыворотке и реактивностью кожных проб на аллергены. N. Engl. J. Med. 320, 271–277. DOI: 10.1056 / NEJM198
3200502
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Cakebread, J. A., Xu, Y., Grainge, C., Kehagia, V., Howarth, P.H., Holgate, S. T., et al. (2011). Экзогенный IFN-бета обладает противовирусными и противовоспалительными свойствами в первичных эпителиальных клетках бронхов пациентов с астмой, подвергшихся воздействию риновируса. J. Allergy Clin. Иммунол. 127, 1148e9–1154e9. DOI: 10.1016 / j.jaci.2011.01.023
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Cheung, D., Dick, E.C., Timmers, M.C., De Klerk, E.P., Spaan, W.J., и Sterk, P.J. (1995). Вдыхание риновируса вызывает длительное чрезмерное сужение дыхательных путей в ответ на метахолин у астматиков in vivo. Am. J. Respir. Крит. Care Med. 152, 1490–1496. DOI: 10.1164 / ajrccm.152.5.7582282
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Чун, Ю.Х., Парк, Дж. Й., Ли, Х., Ким, Х. С., Вон, С., Джо, Х. Дж. И др. (2013). Эпителиальные клетки, инфицированные риновирусом, производят больше ИЛ-8 и рантезов по сравнению с другими респираторными вирусами. Allergy Asthma Immunol. Res. 5, 216–223. DOI: 10.4168 / aair.2013.5.4.216
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Contoli, M., Message, S. D., Laza-Stanca, V., Edwards, M. R., Wark, P. A., Bartlett, N. W., et al. (2006). Роль дефицитной продукции интерферона-лямбда III типа в обострениях астмы. Нат. Med. 12, 1023–1026. DOI: 10,1038 / нм1462
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Корн, Дж. М., Маршалл, К., Смит, С., Шрайбер, Дж., Сандерсон, Г., Холгейт, С. Т. и др. (2002). Частота, тяжесть и продолжительность риновирусных инфекций у астматиков и неастматиков: продольное когортное исследование. Ланцет 359, 831–834. DOI: 10.1016 / S0140-6736 (02) 07953-9
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
ДеМоре, Дж.П., Вайсхаар, Э. Х., Вртис, Р. Ф., Свенсон, К. А., Эванс, М. Д., Морин, А. и др. (2009). Подобные простуды у субъектов с аллергической астмой и у субъектов без атопии после инокуляции риновирусом-16. J. Allergy Clin. Иммунол. 124, 245–252. DOI: 10.1016 / j.jaci.2009.05.030
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Димопулос, Г., Лерику, М., Циодрас, С., Храниоти, А., Перрос, Э., Анагностопулу, У. и др. (2012). Вирусная эпидемиология обострений хронической обструктивной болезни легких. Pulm. Pharmacol. Ther. 25, 12–18. DOI: 10.1016 / j.pupt.2011.08.004
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Дуррани С. Р., Монтвилль Д. Дж., Пратт А. С., Саху С., Деврис М. К., Раджаманикам В. и др. (2012). Врожденный иммунный ответ на риновирус снижается высокоаффинным рецептором IgE у детей с аллергической астмой. J. Allergy Clin. Иммунол. 130, 489–495. DOI: 10.1016 / j.jaci.2012.05.023
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Двейк, Р.А., Боггс, П. Б., Эрзурум, С. К., Ирвин, К. Г., Ли, М. В., Лундберг, Дж. О. и др. (2011). Официальное руководство по клинической практике ATS: интерпретация уровней оксида азота в выдыхаемом воздухе (FENO) для клинического применения. Am. J. Respir. Крит. Care Med. 184, 602–615. DOI: 10.1164 / rccm.9120-11ST
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Фашнер, Дж., Эриксон, К., Вернер, С. (2012). Лечение насморка у детей и взрослых. Am.Fam. Phys. 86, 153–159.
Фелтис, Б. Н., Вигнараджа, Д., Чжэн, Л., Уорд, К., Рид, Д., Хардинг, Р. и др. (2006). Повышенный фактор роста эндотелия сосудов и рецепторы: связь с ангиогенезом при астме. Am. J. Respir. Крит. Care Med. 173, 1201–1207. DOI: 10.1164 / rccm.200507-1105OC
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Френкель, Д. Дж., Бардин, П. Г., Сандерсон, Г., Лампе, Ф., Джонстон, С. Л., и Холгейт, С.Т. (1995). Воспаление нижних дыхательных путей при риновирусной простуде у здоровых и астматических субъектов. Am. J. Respir. Крит. Care Med. 151, 879–886.
Pubmed Реферат | Pubmed Полный текст
Фрай, А. М., Лу, X., Олсен, С. Дж., Читтаганпитч, М., Саватвонг, П., Чантра, С., и др. (2011). Человеческие риновирусные инфекции в сельских районах Таиланда: эпидемиологические доказательства риновируса как патогена, так и стороннего наблюдателя. PLoS ONE 6: e17780. DOI: 10.1371 / journal.pone.0017780
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Fujitsuka, А., Tsukagoshi, H., Arakawa, M., Goto-Sugai, K., Ryo, A., Okayama, Y., et al. (2011). Молекулярно-эпидемиологическое исследование респираторных вирусов, обнаруженных у японских детей с острым свистящим дыханием. BMC Infect. Дис. 11: 168. DOI: 10.1186 / 1471-2334-11-168
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Gaajetaan, G.R., Geelen, T.H., Vernooy, J.H., Dentener, M.A., Reynaert, N.L., Rohde, G.G., et al. (2013). Интерферон-бета вызывает длительное противовирусное состояние в респираторных эпителиальных клетках человека. J. Infect. 66, 163–169. DOI: 10.1016 / j.jinf.2012.11.008
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Грейндж, К. Л., Лау, Л. К., Уорд, Дж. А., Дулай, В., Лахифф, Г., Уилсон, С. и др. (2011). Влияние бронхоспазма на ремоделирование дыхательных путей при астме. N. Engl. J. Med. 364, 2006–2015. DOI: 10.1056 / NEJMoa1014350
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Грюнберг, К., Шарон, Р. Ф., Сонт, Дж.K., In ‘t Veen, J. C., Van Schadewijk, W. A., De Klerk, E. P., et al. (2001). Воспаление дыхательных путей при астме, вызванное риновирусом: эффект лечения ингаляционными кортикостероидами до и во время экспериментальной инфекции. Am. J. Respir. Крит. Care Med. 164, 1816–1822.
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Грюнберг К., Тиммерс М. К., Де Клерк Э. П., Дик Э. К. и Стерк П. Дж. (1999). Экспериментальная инфекция риновирусом 16 вызывает различную обструкцию дыхательных путей у субъектов с атопической астмой. Am. J. Respir. Крит. Care Med. 160, 1375–1380. DOI: 10.1164 / ajrccm.160.4.9810083
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Грюнштейн, М. М., Хаконарсон, Х., Уилан, Р., Ю, З., Грюнштейн, Дж. С. и Чуанг, С. (2001). Риновирус вызывает проастматические изменения в чувствительности дыхательных путей независимо от вирусной инфекции. J. Allergy Clin. Иммунол. 108, 997–1004. DOI: 10.1067 / mai.2001.120276
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Гвалтни, Дж.М. младший, Хендли Дж. О., Саймон Дж. И Джордан У. С. младший (1967). Риновирусные инфекции у промышленного населения. II. Характеристики болезни и антительный ответ. JAMA 202, 494–500. DOI: 10.1001 / jama.1967.031301
014
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Хьюсон, К. А., Хаас, Дж. Дж., Бартлетт, Н. У., Сообщение, С. Д., Лаза-Станка, В., Кебадзе, Т. и др. (2010). Риновирус индуцирует Muc5ac в модели инфекции человека и in vitro через пути NF-kappaB и EGFR. Eur. Респир. J. 36, 1425–1435. DOI: 10.1183 / 036.00026910
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сяо, К. Дж., Черри, Д. К., Битти, П. К., и Рехтштайнер, Е. А. (2010). Национальное исследование амбулаторной медицинской помощи: итоги 2007 г. Natl. Статистика здоровья. Отчет 1:32.
Хуйскенс, Э. Г., Купманс, М., Палмен, Ф. М., Ван Эркель, А. Дж., Малдер, П. Г. и Россен, Дж. У. (2014). Значение признаков и симптомов для различения бактериальной, вирусной и смешанной этиологии у пациентов с внебольничной пневмонией. J. Med. Microbiol. 63, 441–452. DOI: 10.1099 / jmm.0.067108-0
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Хатчинсон, А.Ф., Гимайр, А.К., Томпсон, М.А., Блэк, Дж. Ф., Бранд, К. А., Лоу, А. Дж. И др. (2007). Согласованное по времени исследование случай-контроль респираторных вирусов и обострений ХОБЛ на уровне сообщества. Респир. Med. 101, 2472–2481. DOI: 10.1016 / j.rmed.2007.07.015
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Дженнингс, Л.К., Андерсон, Т. П., Бейнон, К. А., Чуа, А., Лэйнг, Р. Т., Верно, А. М. и др. (2008). Заболеваемость и характеристики вирусной внебольничной пневмонии у взрослых. Грудь 63, 42–48. DOI: 10.1136 / thx.2006.075077
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Йоханссон, Н., Калин, М., Тивельюнг-Линделл, А., Гиске, К. Г., и Хедлунд, Дж. (2010). Этиология внебольничной пневмонии: повышение микробиологической эффективности с помощью новых методов диагностики. Clin. Заразить. Дис. 50, 202–209. DOI: 10.1086 / 648678
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Джонстон, Дж., Маджумдар, С. Р., Фокс, Дж. Д. и Марри, Т. Дж. (2008). Вирусная инфекция у взрослых, госпитализированных с внебольничной пневмонией: распространенность, возбудители и проявления. Сундук 134, 1141–1148. DOI: 10.1378 / сундук.08-0888
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Джонстон, С. Л., Паттемор, П.К., Сандерсон, Г., Смит, С., Кэмпбелл, М. Дж., Джозефс, Л. К. и др. (1996). Связь между инфекциями верхних дыхательных путей и госпитализацией по поводу астмы: анализ тенденции во времени. Am. J. Respir. Крит. Care Med. 154, 654–660. DOI: 10.1164 / ajrccm.154.3.8810601
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Джонстон, С. Л., Паттемор, П. К., Сандерсон, Г., Смит, С., Лампе, Ф., Джозефс, Л. и др. (1995). Общественное исследование роли вирусных инфекций в обострениях астмы у детей 9-11 лет. BMJ 310, 1225–1229. DOI: 10.1136 / bmj.310.6989.1225
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Кеннеди, Дж. Л., Тернер, Р. Б., Брасиале, Т., Хейманн, П. В., и Бориш, Л. (2012). Патогенез риновирусной инфекции. Curr. Мнение. Virol. 2, 287–293. DOI: 10.1016 / j.coviro.2012.03.008
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Kherad, O., Kaiser, L., Bridevaux, P.O., Sarasin, F., Thomas, Y., Janssens, J. P., et al. (2010). Вирусная инфекция верхних дыхательных путей, биомаркеры и обострения ХОБЛ. Сундук 138, 896–904. DOI: 10.1378 / Chess.09-2225
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Кинг, Г. Г., Паре, П. Д., Сеу, К. Ю. (1999). Механика чрезмерного сужения дыхательных путей при астме: роль гладких мышц. Респир. Physiol. 118, 1–13. DOI: 10.1016 / S0034-5687 (99) 00076-6
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Киёта, Н., Кобаяси, М., Цукагоши, Х., Рио, А., Харада, С., Кусака, Т. и др. (2014). Генетический анализ риновирусов человека видов от A до C, обнаруженных у пациентов с острой респираторной инфекцией в префектуре Кумамото, Япония, 2011–2012 гг. Заражение. Genet. Evol. 21, 90–102. DOI: 10.1016 / j.meegid.2013.10.024
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Киёта, Н., Кусибути, И., Кобаяши, М., Цукагоши, Х., Рио, А., Нишимура, К., и др. (2013). Генетический анализ кодирующей области VP4 / VP2 в человеческом риновирусе вида C у пациентов с острой респираторной инфекцией в Японии. J. Med. Microbiol. 62, 610–617. DOI: 10.1099 / jmm.0.049072-0
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Kloepfer, K. M., Demore, J. P., Vrtis, R. F., Swenson, C. A., Gaworski, K. L., Bork, J. A., et al. (2011). Влияние монтелукаста на пациентов с астмой после экспериментальной инокуляции риновирусом человека 16. Ann. Allergy Asthma Immunol. 106, 252–257. DOI: 10.1016 / j.anai.2010.11.021
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Ко, Ф.W., Ip, M., Chan, P. K., Chan, M. C., To, K. W., Ng, S. S., et al. (2007). Вирусная этиология обострений ХОБЛ в Гонконге. Сундук 132, 900–908. DOI: 10.1378 / сундук.07-0530
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Куга, Х., Хошияма, Ю., Кокубу, Ф., Имаи, Т., Токунага, Х., Мацукура, С., и др. (2000). Корреляция между обострением бронхиальной астмы и пикорнавирусной инфекцией (вирусом носорога человека) при полоскании горла с помощью ОТ-ПЦР. Ареруги 49, 358–364.
Pubmed Реферат | Pubmed Полный текст
Кураи Д., Сарая Т., Исии Х., Вада Х., Цукагоши Х., Такидзава Х. и др. (2013b). Респираторно-вирусная инфекция у взрослых пациентов. Respirology 18, 1–81.
Leigh, R., Oyelusi, W., Wiehler, S., Koetzler, R., Zaheer, R. S., Newton, R., et al. (2008). Риновирусная инфекция человека увеличивает выработку эпителиальными клетками дыхательных путей факторов роста, участвующих в ремоделировании дыхательных путей. J. Allergy Clin. Иммунол. 121, 1238e4–1245e4. DOI: 10.1016 / j.jaci.2008.01.067
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Либерман Д., Либерман Д., Шимони А., Керен-Наус А., Стейнберг Р. и Шемер-Авни Ю. (2009). Идентификация респираторных вирусов у взрослых: выбор образцов из носоглотки и ротоглотки. J. Clin. Microbiol. 47, 3439–3443. DOI: 10.1128 / JCM.00886-09
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Либерман, Д., Шимони, А., Шемер-Авни, Ю., Керен-Наос, А., Штайнберг, Р., и Либерман, Д. (2010). Респираторные вирусы у взрослых с внебольничной пневмонией. Сундук 138, 811–816. DOI: 10.1378 / Chess.09-2717
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Линсуванон, П., Пайунгпорн, С., Самрансамруаджкит, Р., Посуван, Н., Маккоч, Дж., Теанбунлерс, А. и др. (2009). Высокая распространенность инфекции человеческого риновируса С у тайских детей с острым заболеванием нижних дыхательных путей. J. Infect. 59, 115–121. DOI: 10.1016 / j.jinf.2009.05.009
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Loens, K., Goossens, H., De Laat, C., Foolen, H., Oudshoorn, P., Pattyn, S., et al. (2006). Обнаружение риновирусов с помощью культуры ткани и двух независимых методов амплификации, амплификации на основе последовательностей нуклеиновых кислот и ПЦР с обратной транскрипцией, у детей с острыми респираторными инфекциями в зимний период. J. Clin. Microbiol. 44, 166–171. DOI: 10.1128 / JCM.44.1.166-171.2006
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Лопес-Соуза, Н., Фаворето, С., Вонг, Х., Уорд, Т., Яги, С., Шнур, Д. и др. (2009). Восприимчивость к риновирусной инфекции in vitro выше для бронхов, чем для эпителиальных клеток носовых дыхательных путей у людей. J. Allergy Clin. Иммунол. 123, 1384e2–1390e2. DOI: 10.1016 / j.jaci.2009.03.010
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Лучзингер, В., Руис, М., Зунино, Э., Мартинес, М. А., Мачадо, К., Пьедра, П. А. и др. (2013). Внебольничная пневмония в Чили: клиническое значение для обнаружения вирусов и атипичных бактерий. Грудь 68, 1000–1006. DOI: 10.1136 / thoraxjnl-2013-203551
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Макела, М. Дж., Пухакка, Т., Руусканен, О., Лейнонен, М., Сайкку, П., Кимпимаки, М., и др. (1998). Вирусы и бактерии в этиологии простуды. J. Clin. Microbiol. 36, 539–542.
Pubmed Реферат | Pubmed Полный текст
Мацукура С., Курокава М., Хомма Т., Ватанабэ С., Судзуки С., Иеки К. и др. (2013). Фундаментальное исследование вирус-индуцированного обострения астмы: ингибирование воспалительной экспрессии хемокинов флутиказона пропионатом. Внутр. Arch. Allergy Immunol. 161 (Дополнение 2), 84–92. DOI: 10.1159 / 000350455
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Макфадден, Э.Р. мл., Пичурко, Б. М., Боуман, Х. Ф., Ингенито, Э., Бернс, С., Даулинг, Н. и др. (1985). Тепловое картирование дыхательных путей человека. J. Appl. Physiol. 58, 564–570.
Pubmed Реферат | Pubmed Полный текст
Макманус, Т. Е., Марли, А. М., Бакстер, Н., Кристи, С. Н., О’Нил, Х. Дж., Элборн, Дж. С. и др. (2008). Респираторно-вирусная инфекция при обострениях ХОБЛ. Респир. Med. 102, 1575–1580. DOI: 10.1016 / j.rmed.2008.06.006
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сообщение, S.Д., Лаза-Станка, В., Маллиа, П., Паркер, Х. Л., Чжу, Дж., Кебадзе, Т. и др. (2008). Вызванное риновирусом заболевание нижних дыхательных путей увеличивается при астме и связано с вирусной нагрузкой и производством цитокинов Th2 / 2 и IL-10. Proc. Natl. Акад. Sci. США 105, 13562–13567. DOI: 10.1073 / pnas.0804181105
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Нагаркар, Д. Р., Боуман, Э. Р., Шнайдер, Д., Ван, К., Шим, Дж., Чжао, Ю. и др. (2010). Риновирусная инфекция аллерген-сенсибилизированных и инфицированных мышей вызывает высвобождение эотаксина из функционально поляризованных макрофагов. J. Immunol. 185, 2525–2535. DOI: 10.4049 / jimmunol.1000286
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Охта К., Ямагути М., Акияма К., Адачи М., Ичиносе М., Такахаши К. и др. (2011). Японское руководство по астме у взрослых. Аллергол. Int. 60, 115–145. DOI: 10.2332 / аллерголинт.11-RAI-0327
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Папи, А., Беллеттато, К. М., Браччони, Ф., Романьоли, М., Casolari, P., Caramori, G., et al. (2006). Инфекции и воспаление дыхательных путей при тяжелых обострениях хронической обструктивной болезни легких. Am. J. Respir. Крит. Care Med. 173, 1114–1121. DOI: 10.1164 / rccm.200506-859OC
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Perotin, J. M., Dury, S., Renois, F., Deslee, G., Wolak, A., Duval, V., et al. (2013). Выявление множественных вирусных и бактериальных инфекций при обострении хронической обструктивной болезни легких: пилотное проспективное исследование. J. Med. Virol. 85, 866–873. DOI: 10.1002 / jmv.23495
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Пиеранджели А., Скагнолари К., Селваджи К., Верзаро С., Спина М. Т., Брешиани Э. и др. (2011). Риновирус часто обнаруживается у пожилых людей, обращающихся в отделение неотложной помощи. J. Med. Virol. 83, 2043–2047. DOI: 10.1002 / jmv.22205
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Похунек, П., Уорнер, Дж. О., Турзикова, Дж., Кудрманн, Дж., И Рош, В. Р. (2005). Маркеры эозинофильного воспаления и моделирования тканей у детей до клинически диагностированной бронхиальной астмы. Pediatr. Allergy Immunol. 16, 43–51. DOI: 10.1111 / j.1399-3038.2005.00239.x
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Пруссин, К., Гриффит, Д. Т., Бозель, К. М., Лин, Х., Фостер, Б., и Казале, Т. Б. (2003). Лечение омализумабом подавляет экспрессию Fcepsilonri в дендритных клетках. J. Allergy Clin. Иммунол. 112, 1147–1154. DOI: 10.1016 / j.jaci.2003.10.003
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Реддел, Х. К., Тейлор, Д. Р., Бейтман, Э. Д., Буле, Л. П., Буши, Х. А., Бусс, В. В. и др. (2009). Официальное заявление Американского торакального общества / Европейского респираторного общества: борьба с астмой и ее обострения: стандартизация конечных точек для клинических испытаний астмы и клинической практики. Am. J. Respir. Крит. Care Med. 180, 59–99. DOI: 10.1164 / rccm.200801-060ST
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Rohde, G., Wiethege, A., Borg, I., Kauth, M., Bauer, T. T., Gillissen, A., et al. (2003). Респираторные вирусы в обострениях хронической обструктивной болезни легких, требующих госпитализации: исследование случай-контроль. Грудь 58, 37–42. DOI: 10.1136 / торакс.58.1.37
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Рассел К.Д., Гриффитс, С. Дж., И Хаас, Дж. (2014). Генетический полиморфизм лямбда-интерферона и вирусная инфекция: верхушка айсберга? ДНК Cell Biol. 33, 60–63. DOI: 10.1089 / dna.2013.2261
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сампсонас, Ф., Капарианос, А., Ликурас, Д., Каркулиас, К., и Спиропулос, К. (2007). Вариации последовательности ДНК металлопротеиназ: их роль при астме и Copd. Аспирантура. Med. J. 83, 244–250. DOI: 10.1136 / pgmj.2006.052100
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сандерс, С. П., Пруд, Д., Пермут, С., Секерски, Э. С., Ячечко, Р., и Лю, М. К. (2004). Роль назального оксида азота в разрешении экспериментальной риновирусной инфекции. J. Allergy Clin. Иммунол. 113, 697–702. DOI: 10.1016 / j.jaci.2004.01.755
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сирс, М. Р., Берроуз, Б., Фланнери, Э. М., Хербисон, Г.П., Хьюитт, К. Дж., И Холдэуэй, М. Д. (1991). Связь между реактивностью дыхательных путей и сывороточным IgE у детей с астмой и у явно нормальных детей. N. Engl. J. Med. 325, 1067–1071. DOI: 10.1056 / NEJM19
03251504Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Seemungal, T., Harper-Owen, R., Bhowmik, A., Moric, I., Sanderson, G., Message, S., et al. (2001). Респираторные вирусы, симптомы и маркеры воспаления при обострениях и стабильной хронической обструктивной болезни легких. Am. J. Respir. Крит. Care Med. 164, 1618–1623. DOI: 10.1164 / ajrccm.164.9.2105011
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Симкок, Д. Э., Канабар, В., Кларк, Г. В., О’Коннор, Б. Дж., Ли, Т. Х. и Херст, С. Дж. (2007). Проангиогенная активность в жидкости бронхоальвеолярного лаважа пациентов с астмой. Am. J. Respir. Крит. Care Med. 176, 146–153. DOI: 10.1164 / rccm.200701-042OC
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Симмондс, П., Макинтайр, К., Саволайнен-Копра, К., Таппарел, К., Маккей, И. М., и Хови, Т. (2010). Предложения по классификации человеческого риновируса вида C на генотипически определенные типы. J. Gen. Virol. 91, 2409–2419. DOI: 10.1099 / vir.0.023994-0
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Судзуки Т., Ямая М., Секизава К., Хосода М., Ямада Н., Исидзука С. и др. (2002). Эритромицин подавляет риновирусную инфекцию в культивируемых эпителиальных клетках трахеи человека. Am. J. Respir. Крит. Care Med. 165, 1113–1118. DOI: 10.1164 / ajrccm.165.8.2103094
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Сайкс А., Макинтайр Дж., Эдвардс М. Р., Дель Росарио А., Хаас Дж., Гилен В. и др. (2014). Вызванная риновирусом продукция интерферона не является недостаточной при хорошо контролируемой астме. Грудь 69, 240–246. DOI: 10.1136 / thoraxjnl-2012-202909
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Такахаши, К., Suzuki, M., Minh Le, N., Anh, N.H., Huong, L.T., Son, T.V. и др. (2013). Заболеваемость и этиология госпитализированной внебольничной пневмонии среди взрослых вьетнамцев: проспективное наблюдение в Центральном Вьетнаме. BMC Infect. Дис. 13: 296. DOI: 10.1186 / 1471-2334-13-296
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Такидзава, Х., Десаки, М., Отоши, Т., Кикутани, Т., Окадзаки, Х., Сато, М., и др. (1995). Эритромицин подавляет экспрессию интерлейкина 6 эпителиальными клетками бронхов человека: потенциальный механизм его противовоспалительного действия. Biochem. Биофиз. Res. Commun. 210, 781–786. DOI: 10.1006 / bbrc.1995.1727
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Тан, В. К., Сян, X., Цю, Д., Нг, Т. П., Лам, С. Ф., и Хегеле, Р. Г. (2003). Эпидемиология респираторных вирусов у пациентов, госпитализированных с почти смертельной астмой, обострениями астмы или хронической обструктивной болезнью легких. Am. J. Med. 115, 272–277. DOI: 10.1016 / S0002-9343 (03) 00353-X
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Цукагоши, Х., Ишиока, Т., Нода, М., Кодзава, К., и Кимура, Х. (2013). Молекулярная эпидемиология респираторных вирусов при вирус-индуцированной астме. Фронт. Microbiol. 4: 278. DOI: 10.3389 / fmicb.2013.00278
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Тернер, Р. Б., и Коуч, Р. Б. (2007). «Риновирус», в Fields Virology , 5-е изд., Ред. Д. М. Книп, П. М. Хоули, Д. Е. Гриффин, Р. А. Лэмб, М. А. Мартин, Б. Ройзман и С. Е. Штраус (Филадельфия: Липпинкотт Уильямс и Уилкинс), 895–909.
van Gageldonk-Lafeber, A. B., Heijnen, M. L., Bartelds, A. I., Peters, M. F., Van Der Plas, S. M., and Wilbrink, B. (2005). Исследование случай-контроль острой респираторной инфекции у пациентов общей практики в Нидерландах. Clin. Заразить. Дис. 41, 490–497. DOI: 10.1086 / 431982
Pubmed Реферат | Pubmed Полный текст | CrossRef Полный текст
Уорк, П. А., Джонстон, С. Л., Буккьери, Ф., Пауэлл, Р., Пуддикомб, С., Лаза-Станка, В., и др. (2005).Эпителиальные клетки бронхов при астме имеют недостаточный врожденный иммунный ответ на инфекцию риновирусом. J. Exp. Med. 201, 937–947. DOI: 10.1084 / jem.20041901
Риновирусная инфекция: симптомы и лечение
перейти к содержанию- Дом
- Пластическая хирургия
- Альтернативная медицина
- Заболевания и состояния
- Другое
- Здоровое питание
- Стоматология
- Медицина
- Добавки и витамины
- Здоровье женщин
- Велнес
- Зрение
- Психическое здоровье
- Аллергия
- Мужчина 39S Здоровье
- Слух
- Раки
- Сон
- Закрыть меню
- Дом
- Пластическая хирургия
- Альтернативная медицина
- Заболевания и состояния
- Другое
- Здоровое питание
- Стоматология
- Медицина
- Добавки и витамины
- Здоровье женщин
- Велнес
- Зрение
- Психическое здоровье
- Аллергия
- Мужчина 39S Здоровье
- Слух
- Раки
- Сон
- Дом
- Пластическая хирургия
- Альтернативная медицина
- Заболевания и состояния
- Другое
- Здоровое питание
- Стоматология
- Медицина
- Добавки и витамины
- Здоровье женщин
- Велнес
- Зрение
- Психическое здоровье
- Аллергия
- Мужчина 39S Здоровье
- Слух
- Раки
- Сон
- Дом
- Пластическая хирургия
- Альтернативная медицина
- Заболевания и состояния
- Другое
- Здоровое питание
- Стоматология
- Медицина
- Добавки и витамины
- Здоровье женщин
- Велнес
- Зрение
- Психическое здоровье
- Аллергия
- Мужчина 39S Здоровье
- Слух
- Раки
- Сон


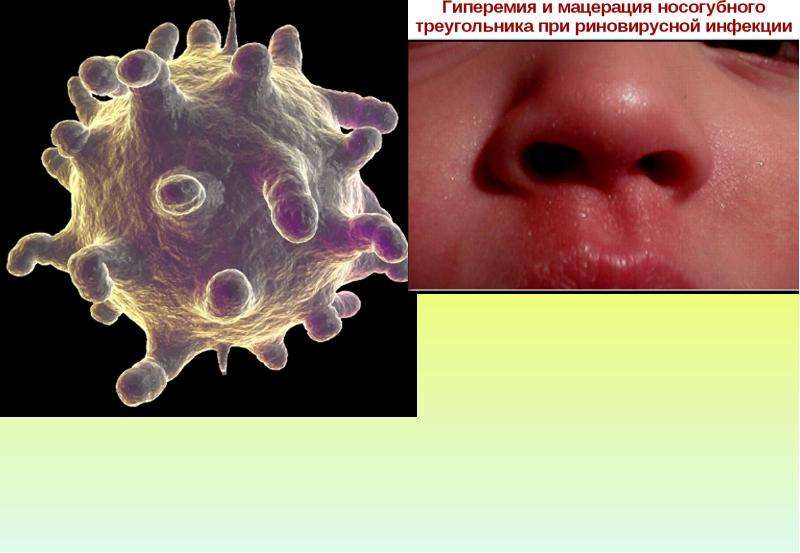 Так ли это?
Так ли это? Карбоцистеин безопасен в отношении бронхообструкции (за счет влияния и на отечный, и на секреторный, и на спастический механизм ее развития), что особенно актуально у детей раннего возраста в связи с высоким риском развития бронхообструктиции при респираторных заболеваниях.
Карбоцистеин безопасен в отношении бронхообструкции (за счет влияния и на отечный, и на секреторный, и на спастический механизм ее развития), что особенно актуально у детей раннего возраста в связи с высоким риском развития бронхообструктиции при респираторных заболеваниях.
 В случае если после контакта с такими предметами человек прикоснулся к слизистым оболочкам, то вероятность заражения многократно возрастает.
В случае если после контакта с такими предметами человек прикоснулся к слизистым оболочкам, то вероятность заражения многократно возрастает.
 Принимать препарат не меньше пяти — семи дней.
Принимать препарат не меньше пяти — семи дней.