Аденовирусная инфекция: лечение, классификация, симптомы
Аденовирусная инфекция — патологический процесс, возникающий на фоне попадания в организм человека аденовируса (Adenoviridae). Заболевание сопровождается поражением органов дыхания, глаз, желудочно-кишечного тракта и лимфатической системы. Инфицированные пациенты страдают от интоксикации, лихорадки, потери голоса, кашля, кишечных расстройств. Постановка диагноза осуществляется на основании клинической картины заболевания и результатов лабораторных исследований. В процессе лечения взрослые и дети получают противовирусные препараты, иммуномодуляторы и средства, снимающие острые симптомы инфекции.
Общие сведения о патологии
Аденовирус относится к группе респираторно-вирусных инфекций. Течение заболевания осложняется конъюнктивитом, ринофарингитом, лимфаденопатией, диспепсическим синдромом. Доля аденовирусных инфекций в общей структуре ОРВИ достигает 20%.
В группу риска входят пациенты в возрасте от полугода до трех лет.
Причины развития патологии
Вирусологи выявили три десятка патогенов, относящихся к семейству Adenoviridae. Возбудители инфекции приспособлены к длительному выживанию в неблагоприятных условиях, хорошо переносят отрицательные температуры и низкую влажность окружающей среды. ДНК патогенов разрушается под воздействием ультрафиолетового излучения и химических соединений на основе хлора.
Инфицированные пациенты распространяют патогены, отделяя носоглоточную слизь. Значительное количество вирусных агентов содержится в каловых массах. Основные пути заражения здоровых людей — воздушно-капельный и фекально-оральный. Посетители бассейнов могут инфицироваться после контакта с водой, в которой плавал носитель патогена.
Пациент, перенесший аденовирусную инфекцию, обладает иммунитетом к определенному типу вируса. Ребенок или взрослый может повторно заболеть, столкнувшись с носителем другого серотипа Adenoviridae. Подобный механизм передачи аденовируса от человека к человеку характерен для внутрибольничных инфекций.
Механизм инфицирования
Первые проявления аденовируса начинают беспокоить пациента после попадания патогенов на слизистые оболочки дыхательных путей и кишечника или конъюнктиву глаза. Вирусы репродуцируются в клетках эпителия, лимфатических узлах и лимфоидных образованиях кишечника. После завершения инкубационного периода пораженные клетки гибнут — вирусы попадают в кровеносную систему человека.
В местах первичного поражения слизистых формируются отёки. Типичная локализация очага воспаления — задняя стенка глотки. Воспалительный процесс протекает на фоне обильного отделения экссудата. При отсутствии лечения пациент может столкнуться с поражением бронхов, почек, печени и селезенки.
Симптоматика патологии
Симптомы попадания аденовируса в организм человека специфичны и зависят от формы, которую приняла инфекция. При поражении дыхательных путей могут развиться фарингиты, тонзиллофарингиты и бронхиты. В случае проникновения инфекции к тканям конъюнктивы пациенты страдают от фарингоконъюнктивной лихорадки и острого конъюнктивита. Попадание вирусов семейства Adenoviridae на слизистые оболочки кишечника провоцирует развитие диарейного синдрома.
Пациенты могут столкнуться с легким, средним и тяжелым течением заболевания. В некоторых случаях патология осложняется присоединением вторичной инфекции. Инкубационный период длится от пяти до семи дней. По его завершении пациент ощущает резкое повышение температуры тела (до 38–39 градусов). Позднее проявляются типичные признаки аденовирусной инфекции:
- снижение аппетита;
- апатия, вялость;
- боль в мышцах и суставах;
- лихорадка;
- обезвоживание.

Перечисленные симптомы аденовируса развиваются у детей и взрослых в течение нескольких часов после повышения температуры. При отсутствии лечения состояние пациентов быстро ухудшается.
Поражение органов дыхания
Распространение инфекции в дыхательных путях провоцирует появление гнойно-слизистого отделяемого из носа. Дыхание человека учащается. При осмотре пациента отоларинголог обнаружит белый налет на миндалинах и выраженный отек слизистой оболочки глотки. Подчелюстные и шейные лимфатические узлы значительно увеличиваются в размерах. Голос ребенка или взрослого обретает характерную осиплость. В некоторых случаях врачи диагностируют у пациентов сухой кашель и одышку.
Поражение конъюнктивы
Репродуцирование вирусов в тканях конъюнктивы приводит к развитию конъюнктивитов различных форм: катаральной, фолликулярной и пленчатой. Патологический процесс начинает развиваться в одном глазу, но постепенно затрагивает и второй. Пациенты жалуются на рези, жжение, ощущение инородного тела. Офтальмологический осмотр позволяет выявить покраснение и отечность кожи век. В некоторых случаях врачи фиксируют образование плотной белесой пленки на конъюнктиве. Запущенная аденовирусная инфекция осложняется кератитом.
Пациенты жалуются на рези, жжение, ощущение инородного тела. Офтальмологический осмотр позволяет выявить покраснение и отечность кожи век. В некоторых случаях врачи фиксируют образование плотной белесой пленки на конъюнктиве. Запущенная аденовирусная инфекция осложняется кератитом.
Поражение желудочно-кишечного тракта
Проникновение Adenoviridae в кишечник человека провоцирует развитие острого болевого синдрома в околопупочной области. Пациент страдает от диареи, систематических приступов тошноты и рвоты. Частично клиническая картина заболевания совпадает с острым аппендицитом.
Возможные осложнения
Тяжелое течение аденовирусной инфекции может привести к развитию менингоэнцефалита. Младенцы страдают от аденовирусной пневмонии и дыхательной недостаточности. Взрослые часто сталкиваются со вторичными инфекциями, на фоне которых развиваются синуситы, отиты и бактериальные пневмонии.
Диагностические мероприятия
Диагностика выполняется терапевтом или отоларингологом — врач проводит осмотр пациента с признаками инфицирования аденовирусом.
Дифференциальная диагностика позволяет исключить из анамнеза человека грипп, инфекционный мононуклеоз, дифтерию глотки, микоплазменную инфекцию. При неясных результатах лабораторных анализов терапевт может направить пациента на офтальмологический осмотр.
Лечение патологии
Медикаментозный курс, назначаемый врачами на фоне подтвержденного диагноза, основан на противовирусных препаратах. Стационарное или амбулаторное лечение лиц, страдающих от аденовируса, предполагает назначение глазных капель, мазей (накладываются на веко), жаропонижающих и противокашлевых средств. При поражении органов дыхания пациенту потребуются регулярные ингаляции и отхаркивающие препараты.
Прогноз и профилактические меры
При неосложненном течении заболевания пациенты добиваются полного выздоровления за пять–семь дней. Осложненная форма аденовирусной инфекции может потребовать госпитализации ребенка или взрослого. В этом случае сроки выздоровления увеличиваются в 1,5–2 раза.
При резком росте инфицирования аденовирусом в детских садах или школах врачи рекомендуют проводить специфическую профилактику. Носителей вируса необходимо направить на амбулаторной или стационарное лечение. Все помещения образовательных учреждений следует обработать антисептическими растворами.
Диагностика и лечение аденовирусной инфекции в Москве
АО «Медицина» (клиника академика Ройтберга) обладает всем необходимым оборудованием для диагностики и лечения аденовирусной инфекции у детей и взрослых. Прием пациентов осуществляется в современном диагностическом комплексе, построенном с учетом последних достижений медицины.
Вопросы и ответы
Какой врач лечит аденовирусную инфекцию?
Лечение детей осуществляется под надзором педиатра. Взрослые могут обратиться к терапевту. При наличии показаний врач направит пациента на консультацию с офтальмологом или отоларингологом.
Существуют ли вакцины, стимулирующие выработку антител к возбудителям аденовирусной инфекции?
Нет, поскольку патогены группы Adenoviridae отличаются значительным разнообразием.
Лечение аденовирусной инфекции | ЛДЦ №1 Липецк
Запись по телефонам
+7 (4742) 37-02-52, +7 (4742) 37-03-52, +7 (4742) 37-04-52
Записаться на приём онлайн
Аденовирусные заболевания вызываются вирусными инфекциями и оказывают патогенное воздействие на слизистые оболочки разных органов: кишечника, дыхательных путей, глаз. Поражают лимфоузлы и провоцируют сильное общее недомогание. Возбудитель болезни можно с легкостью «подхватить», так как в условиях комнатной температуры он способен жить около 2-х недель.
Поражают лимфоузлы и провоцируют сильное общее недомогание. Возбудитель болезни можно с легкостью «подхватить», так как в условиях комнатной температуры он способен жить около 2-х недель.
Аденовирусные заболевания являются весьма распространенными. Примерно до 10% всех болезней вирусной природы относятся именно к указанной категории. Наибольший пик болезней приходится на осень и зиму, так как именно в этот период организм наиболее ослаблен.
Три четверти всех заболевших – это дети, причем, около половины из них имеют возраст до 5-ти лет.
Симптомы
Признаки заболевания дают о себе знать в течение 5-7 дней после заражения:
- ослабление, недомогание;
- повышение температуры – вплоть до 39℃;
- першение и боли в горле;
- озноб;
- вялость, апатия;
- заложенность носа, насморк, сопровождаемый обильным отхождением секрета из носовой полости;
- кашель;
- отечность, покраснение, ощущение жжения конъюнктивы;
- слезотечение, зуд глаз;
- тошнота, рвота;
- увеличение лимфоузлов (подмышечных, шейных, подчелюстных), миндалин.

В зависимости от того, вирус какой подгруппы внедрился в организм, могут возникать и другие симптомы.
Причины аденовирусной инфекции
Заболевания вызываются вирусами, которые могут передаться не только воздушно-капельным путем, но также пищевым и фекально-оральным.
На сегодняшний день открыто 62 вида аденовирусов. Все инфекции такого типа можно разделить на семь групп: А, В, С, D, E, F и G. Общее у них то, что они патогенно влияют на слизистые оболочки. Но, есть и отличия в зависимости от того, как и на какой орган они воздействуют в большей степени:
- кишечная инфекция – вирус подгруппы F;
- явная форма (манифеста) – вирусы В и Е;
- скрытая (латентная) форма – вирусы С, которые могут вызывать воспаление аденоидов, хронический тонзиллит и пр.;
- болезни печени и мочевыводящих путей – вирусы В2;
- конъюнктивит – вирус В и др.
По сути, аденовирусная инфекция – это подвид ОРВИ.
Диагностика аденовирусной инфекции
Чтобы установить диагноз, потребуется изучение анамнеза и жалоб пациента, эпидемиологического окружения. Также проводится осмотр больного. Чтобы определить возбудитель и иметь возможность подобрать наиболее эффективное лечение, применяется ПЦР и иммунофлюоресцентный анализ. Дополнительно потребуется консультация врача-офтальмолога.
Также проводится осмотр больного. Чтобы определить возбудитель и иметь возможность подобрать наиболее эффективное лечение, применяется ПЦР и иммунофлюоресцентный анализ. Дополнительно потребуется консультация врача-офтальмолога.
Лечение аденовирусной инфекции в Липецке
Против аденовирусной инфекции специфических методов лечения нет, поэтому упор делается на симптоматическую терапию. Могут назначаться глазные мази и капли, масляные капли в нос, сосудосуживающие препараты, антибактериальные медикаменты, витамины. Обязательно обильное питье и постельный режим. Если у больного наблюдается особо тяжелое состояние, его лечат в условиях стационара.
В нашем центре вы сможете получить медицинскую помощь в плановом и экстренном порядке. В ЛДЦ№1 работает Кузнецова Лилиана Викторовна – инфекционист, которая на протяжении уже длительного времени ведет врачебную практику. Записаться на прием можно прямо сейчас.
Запишитесь к инфекционисту в Липецке по телефонам +7 (4742) 37-02-52, +7 (4742) 37-03-52, +7 (4742) 37-04-52 или онлайн
симптомы и лечение аденовируса у детей и взрослых
Противовирусные препараты с иммуномодулирующей активностью могут ускорить выздоровление и восстановить ослабленный болезнью иммунитет.

Узнать больше…
Курсовой прием «Амиксина» при лечении и профилактике гриппа и ОРВИ у взрослых состоит всего из 6 таблеток!
Узнать подробнее о схемах приема…
Имеются противопоказания. Необходимо получить консультацию специалиста.
АМИКСИН® способствует подавлению размножения вирусов в инфицированных клетках и восстановлению сниженного иммунитета.
Узнать подробнее про АМИКСИН®…
Имеются противопоказания. Необходимо получить консультацию специалиста.
Противовирусный препарат АМИКСИН® можно принимать как в сочетании с симптоматическими жаропонижающими средствами, так и вместе со средствами народной медицины.
Подробнее о совместимости…
Имеются противопоказания. Необходимо получить консультацию специалиста.
Противовирусные препараты с иммуномодулирующими свойствами обладают способностью активировать выработку собственных интерферонов и стимулировать ослабленный иммунитет на борьбу с инфекцией.

Подробнее…
Противовирусное и иммуностимулирующее средство АМИКСИН® 125 мг отпускается из аптеки без рецепта и может применяться для лечения, а также профилактики гриппа и других ОРВИ по назначению врача.
Узнать больше…
Имеются противопоказания. Необходимо получить консультацию специалиста.
При прочтении диагноза у многих пациентов возникает вопрос: что такое аденовирус и как его лечить? Возбудители аденовирусной инфекции поражают слизистые дыхательных путей, глаз, кишечника, лимфоузлы, вызывая серьезное недомогание. Они легко передаются и в условиях комнатной температуры живут до двух недель, сохраняя угрозу для здоровья[1] . Аденовирусная инфекция характеризуется большой распространенностью: до 10% всех вирусных заболеваний человека приходится именно на эти вирусы. Три четверти заболевших — это дети, а чуть меньше половины из них — малыши до 5 лет[2]. Пик заболеваемости традиционно приходится на осенне-зимний период.
Аденовирус — возбудитель инфекции
На сегодняшний день ученые выявили 62 вида аденовирусов. Также говорят о 49 серотипах, то есть группах вирусов, против которых действует общий антиген[3]. Аденовирусные инфекции по классификации делятся на семь подгрупп, которые обозначаются латинскими буквами А, В, С, D, E, F и G. Общей чертой всех аденовирусов является то, что они воздействуют на слизистые оболочки. В зависимости от конкретного возбудителя, заболевание может протекать:
- в явной форме, так называемой манифестной — возбудителями являются вирусы подгрупп В и Е;
- в скрытой (латентной) форме — вирусы подгруппы С. В этом случае у пациента может начаться хронический тонзиллит, воспаление аденоидов и т.д.[4];
- в форме кишечной инфекции — вирус подгруппы F[5];
- в форме конъюнктивита — вирус подгруппы В[6];
- в форме заболеваний печени и мочевыводящих путей — вирус подгруппы В2[7] и т.д.
Являясь разновидностью ОРВИ, аденовирусная инфекция начинается примерно так же, как грипп. Повышение температуры, озноб, увеличение лимфоузлов, першение в горле, ряд других катаральных явлений (т.е. микровоспалений слизистой верхних дыхательных путей), слезотечение, насморк — перечень симптомов напоминает общее описание ОРВИ[8]. Однако у аденовирусной инфекции есть свои особенности, о которых мы расскажем ниже.
Повышение температуры, озноб, увеличение лимфоузлов, першение в горле, ряд других катаральных явлений (т.е. микровоспалений слизистой верхних дыхательных путей), слезотечение, насморк — перечень симптомов напоминает общее описание ОРВИ[8]. Однако у аденовирусной инфекции есть свои особенности, о которых мы расскажем ниже.
История открытия
Кстати, обнаружены аденовирусы были сравнительно недавно, и начало исследованиям положили работы микробиолога У. Роу в 1953 году. Впервые эти вирусы были выделены из тканей миндалин и аденоидов детей, поэтому они и получили такое название[9]. Исследования продолжили американские специалисты, которые обнаружили аденовирусы в тканях лимфатических узлов, а также выделили их из отделяемого верхних дыхательных путей и глаз. Исследования продолжились, и в 1962 году ученые установили онкогенную активность аденовирусов некоторых серотипов.
Источником аденовирусов являются больные, а кроме того, носители, то есть те люди, у которых уже нет симптомов заболевания, выздоравливающие. Надо отметить, что аденовирусы достаточно «живучи»: они сохраняют способность к заражению до 50 дней, а иногда и дольше[10]. Ученые также отмечают, что носителями аденовирусов, сходных с человеческими, могут быть животные, и сегодня идут активные изыскания в этой области.
Надо отметить, что аденовирусы достаточно «живучи»: они сохраняют способность к заражению до 50 дней, а иногда и дольше[10]. Ученые также отмечают, что носителями аденовирусов, сходных с человеческими, могут быть животные, и сегодня идут активные изыскания в этой области.
Основных механизмов передачи вируса существует два:
- Воздушно-капельный. Вирус выделяется с мокротой и слизью больного при кашле и чихании. Чтобы избежать инфекции, важно соблюдать правила личной гигиены, общаясь с больным, а также проводить регулярную влажную уборку помещения.
- Орально-фекальный. Его еще называют «болезнью немытых рук». Этим путем вирус может передаваться еще на протяжении полутора месяцев после того, как человек отметил у себя первые симптомы ОРВИ. Обычно орально-фекальным способом происходит передача желудочной формы аденовирусной инфекции.
Есть несколько вариантов избавления от аденовируса. Один из них — термическая обработка, т.к. вирус гибнет при температуре выше 50 градусов. Также можно обработать помещение, где был больной, ультрафиолетом или дезинфицирующими средствами, содержащими хлор[11].
Также можно обработать помещение, где был больной, ультрафиолетом или дезинфицирующими средствами, содержащими хлор[11].
Инкубационный период аденовирусной инфекции составляет от 2 до 12 дней, но чаще продолжается 5–7 дней. Надо отметить, что наиболее чувствительны к воздействию аденовирусов дети в возрасте от 6 месяцев до 5 лет. До полугода у детей есть врожденный иммунитет, передающийся от матери. После 5 лет «нарабатываются» собственные защитные механизмы. А вот возрастной промежуток между — наиболее уязвимое время[12].
Важно помнить, что заболевание редко приобретает характер пандемии, но легко распространяется в коллективах, особенно детских. В зимний период школьники и дети, посещающие детский сад, нуждаются в повышенном внимании[13]. Отметим также, что нередко источником инфекции служат общественные бассейны: при нарушении правил дезинфицирования воды посетители бассейнов легко заражаются аденовирусом, вызывающим конъюнктивит[14].
Это важно!
Появление неприятных симптомов аденовируса может следовать не только за контактом с больным человеком. Спровоцировать возникновение заболевания может, например, употребление холодных напитков, мороженого. В этом случае симптомы обычно вызваны аденовирусом, хронически находящимся в лимфоидной ткани. В таком случае необходимо применение противовирусных препаратов. Часто аденовирусную инфекцию может сопровождать бактериальный конъюнктивит. В таком случае в схему лечения включаются антибиотики.
Спровоцировать возникновение заболевания может, например, употребление холодных напитков, мороженого. В этом случае симптомы обычно вызваны аденовирусом, хронически находящимся в лимфоидной ткани. В таком случае необходимо применение противовирусных препаратов. Часто аденовирусную инфекцию может сопровождать бактериальный конъюнктивит. В таком случае в схему лечения включаются антибиотики.
Симптомы и формы аденовирусной инфекции
Основные особенности передачи заболевания мы уже отметили. Перечислим характерные признаки аденовирусной инфекции:
- температура от 37,5°С до 39°С, которая в большинстве случаев быстро снижается;
- вялость, слабость, головная боль;
- першение и боль в горле, особенно при сглатывании, быстрое проявление катаральных поражений с первых дней заболевания;
- заложенность носа и обильные выделения;
- кашель (вначале сухой, а на 3–4 день влажный с отхождением мокроты), отечность миндалин и точечный гнойный налет на них;
- умеренная отечность слизистых;
- слезотечение, отечность век, резь в глазах и иногда — гной;
- ухудшение аппетита;
- нарушения сна, общая слабость, вялость, бледность, повышенная раздражительность;
- боли в районе пупка, иногда бывает рвота и диарея;
- увеличение в размерах шейных лимфатических узлов.

Учитывая, что аденовирусные инфекции относятся к ОРВИ, их проявления многие принимают за грипп. О том, что перед нами именно аденовирус, чаще всего свидетельствует конъюнктивит, который сопровождает заболевание в большинстве случаев. Глаза болят, слезятся, краснеют, появляется ощущение насыпанного песка. Пострадать могут оба глаза или только один — зависит от индивидуального характера протекания заболевания[15].
Второй отличительной особенностью аденовирусной инфекции является то, что период интоксикации продолжается всего 1–2 дня, в то время как неприятные симптомы (тошнота, головная боль, слабость и другие) при гриппе могут сохраняться до 7 суток и более.
Третьим отличием аденовируса от других вирусных инфекций является длительность и характер лихорадки. Температура при аденовирусной инфекции может подниматься в первый день до 38°С, но держится высокой недолго. Если при гриппе лихорадка продолжается несколько дней, а температура достигает 39–40°С, то при аденовирусе изматывающая лихорадка отмечается достаточно редко.
Наиболее типичными проявлениями аденовирусной инфекции являются:
- конъюнктивит — воспаление слизистой оболочки глаз;
- кератоконъюнктивит — сухость слизистой глаза, ощущение рези в глазах;
- ринофарингит — воспаление слизистой носа и глотки;
- ринофарингобронхит — к воспалению слизистых дыхательных путей добавляется воспаление бронхов;
- ринофаринготонзиллит — поражение слизистых дыхательных путей сопровождается воспалением миндалин;
- мезентериальный лимфаденит — воспаление лимфатических узлов живота.
У детей аденовирус имеет свои, более выраженные, проявления. Так как новорожденные имеют остаточный иммунитет к вирусу, у них болезнь протекает при невысокой температуре, редко наблюдается конъюнктивит, не увеличиваются лимфоузлы. У детей первого года жизни нередко развивается пневмония[16]: под действием аденовируса легкие ребенка становятся более восприимчивыми к бактериальным возбудителям этого серьезного заболевания. Пневмония сопровождается хрипами, у ребенка могут начаться судорожные припадки, одышка, рвота. Воспаление легких может начаться и у взрослых: отличие в том, что у детей осложнение развивается резко и внезапно, а у взрослого пациента осложнение наступает примерно на 3–5 день болезни.
Воспаление легких может начаться и у взрослых: отличие в том, что у детей осложнение развивается резко и внезапно, а у взрослого пациента осложнение наступает примерно на 3–5 день болезни.
Также для детей в большей степени, чем для взрослых, характерны кишечные проявления заболевания: стул умеренно учащен, в нем могут быть следы слизи. В некоторых случаях пациенты обращают внимание на сильные боли в животе, которые могут перепутать с приступом аппендицита.
Обратите внимание
При отсутствии должного лечения или при неэффективной терапии могут развиться серьезные осложнения, такие как отит, синусит, ангина, обострение хронических заболеваний, нейротоксикация, ДВС-синдром, стеноз гортани, бронхообструкция. Поэтому особенно важно правильно подобрать меры лечения.
Диагностика
Еще раз подчеркнем, что симптомы аденовируса очень разнообразны и похожи на другие ОРВИ. Их можно спутать с проявлениями гриппа, ротавируса и даже аппендицита. Именно поэтому для выявления вируса необходима комплексная диагностика.
Именно поэтому для выявления вируса необходима комплексная диагностика.
Чтобы выявить инфекцию, применяются следующие методы:
- Общий анализ крови. Необходимо обратить внимание на повышение уровня лейкоцитов — лейкоцитоз. Он может служить признаком начинающейся пневмонии.
- Биохимический анализ крови. Если аденовирусная инфекция протекает без осложнений, заметных нарушений в биохимии крови не отмечается. Если начинается пневмония, то повышается содержание в крови сиаловой кислоты, фибриногена, проба на С-реактивный белок положительная.
- Иммуноферментный анализ — исследование клеток эпителия, которое обнаруживает в них антиген к аденовирусу.
- Реакции иммунофлюоресценции — метод с высокой точностью позволяет выявлять специфические антитела.
- ПЦР-диагностика. Этот метод позволяет выявить ДНК вируса в крови или в мазке из зева.
- Серологические реакции — для диагностики применяются РИФ, ИФА, РИА, ПЦР, метод молекулярной гибридизации, метод иммуноэлектронной микроскопии и другие.

- Исследование мокроты позволяет не только выявить возбудителя аденовирусной инфекции, но и его чувствительность к препаратам.
Лечение аденовирусной инфекции у взрослых и детей
В целом лечение аденовирусной инфекции у взрослых и детей проходит по сходной схеме. Главное направление терапии — снятие неприятных симптомов, улучшение общего состояния пациента, иммунная система которого борется с вирусом. При необходимости можно добавить к лечению антибактериальную терапию, если есть угроза развития осложнений.
Больным обычно рекомендуется соблюдать постельный режим, а также находиться в изолированном помещении, так как аденовирус легко распространяется среди членов семьи. Чтобы уменьшить симптомы интоксикации, необходимо обеспечить обильное питье. Если пациент отказывается от еды, то рекомендуется щадящий режим: больной может чувствовать тошноту, поэтому принудительное питание нежелательно. Госпитализация обычно требуется только в случаях развития осложнений или если состояние пациента (обычно это касается маленьких детей) вызывает серьезные опасения.
Для снятия симптомов (головной боли, кашля, заложенности носа) могут быть рекомендованы безрецептурные препараты, такие как «Коделак» (средство от кашля), «Риностоп» (от насморка), «Максиколд» (борется с температурой) и другие. Для устранения причины заболевания ― вируса ― рекомендуется прием противовирусных препаратов, например, «Амиксина» (противовирусный и иммуномодулирующий препарат). При конъюнктивите или отите препараты назначает врач, так как могут потребоваться в том числе антибиотики.
С наступлением зимы проблема диагностики и лечения аденовирусной инфекции у взрослых и детей встает особенно остро. Важно помнить об особенностях течения заболевания, чтобы отличать его от других разновидностей ОРВИ и применять оптимальное лечение. А также проводить эффективную профилактику, чтобы зима не была связана с болезнями и недомоганием, а проходила активно.
Аденовирус – детская инфекция: типичные симптомы, лечение
Аденовирусная инфекция – это вирусное заболевание, вызываемое аденовирусом, одна из разновидностей ОРВИ. Существует значительное количество видов аденовирусов, они еще не все хорошо изучены, но роль некоторых из них в развитии у человека патологических состояний несомненна. Аденовирусы долго сохраняются вне организма, хорошо выдерживают низкие температуры. Заболеть аденовирусной инфекцией можно в любое время года, небольшой подъём частоты заболевания этой разновидностью ОРВИ наблюдается в осенне-зимний период.
Существует значительное количество видов аденовирусов, они еще не все хорошо изучены, но роль некоторых из них в развитии у человека патологических состояний несомненна. Аденовирусы долго сохраняются вне организма, хорошо выдерживают низкие температуры. Заболеть аденовирусной инфекцией можно в любое время года, небольшой подъём частоты заболевания этой разновидностью ОРВИ наблюдается в осенне-зимний период.
Почему аденовирусными инфекциями чаще всего болеют дети
Первые 6 месяцев жизни дети практически не болеют аденовирусной инфекцией. Это связано с тем, что в этом возрасте дети обладают пассивным иммунитетом, унаследованным ими от матери. Потом врожденный иммунитет утрачивается, и дети начинают болеть.
До 7 лет ребенок успевает переболеть аденовирусной инфекцией несколько раз. Каждый раз организм вырабатывает специфический иммунитет к конкретному виду аденовирусов, но поскольку их несколько, ребенку приходится болеть неоднократно.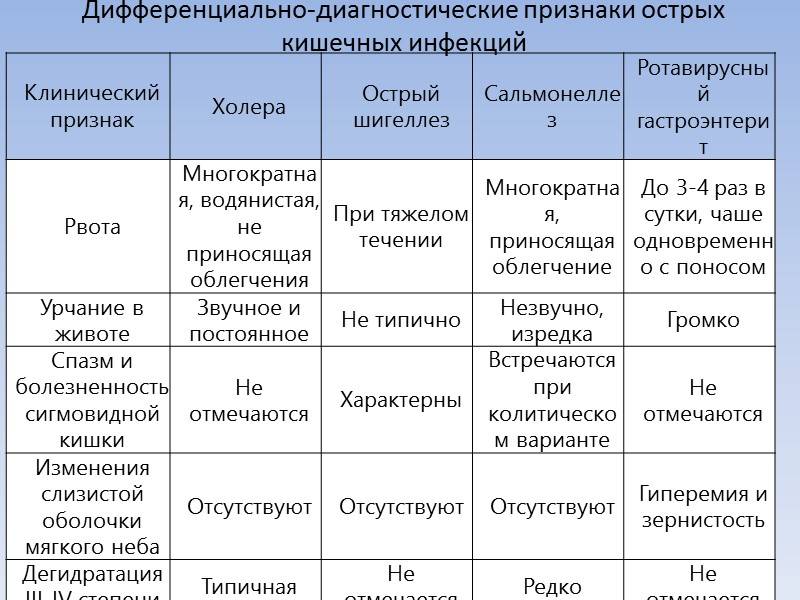 После 7 лет, как правило, приобретенный иммунитет есть уже ко всем видам аденовирусов, и аденовирусная инфекция им уже не страшна.
После 7 лет, как правило, приобретенный иммунитет есть уже ко всем видам аденовирусов, и аденовирусная инфекция им уже не страшна.
Со временем иммунитет утрачивается, поэтому аденовирусной инфекций могут болеть и взрослые люди.
Причины аденовирусной инфекции
Аденовирусы распространяются воздушно-капельным путем, то есть заразиться можно, если кто-то по соседству чихает или кашляет. При этом картина заболевания у носителя инфекции не обязательно должна быть выраженной, заболевание может протекать и в смазанной форме. При этом аденовирус может выделяться в течение двух недель с момента начала болезни.
Другой путь распространения аденовирусной инфекции – фекально-оральный. Этот механизм заражения типичен для детей, которые не могут самостоятельно следить за личной гигиеной и чистотой рук. С фекалиями аденовирусы выделяются в течение полутора месяцев.
Возможен также и бытовой путь, когда аденовирусы переносятся посредством предметов быта.
Воротами, через которые инфекция попадает в организм, является слизистая
верхних дыхательных путей, также возможно проникновение через конъюнктиву —
прозрачную слизистую оболочку глаза. Аденовирус поражает клетки слизистой,
размножается в них, откуда попадает в кровь и разносится по всему
организму.
Симптомы аденовирусной инфекции
Инкубационный период (время от проникновения инфекции до проявления первых симптомов) составляет от одного дня до недели (в некоторых случаях – дольше).
Заболевание, как правило, начинается с появлением признаков интоксикации.
Для аденовирусной инфекции типичен комплекс катаральных явлений (проявления ринофарингита – ринита
и фарингита
одновременно): насморк, заложенность носа, першение в горле. Иногда поражаются нёбные миндалины (наблюдаются симптомы ангины), в таких случаях ставится диагноз ринофаринготонзиллит.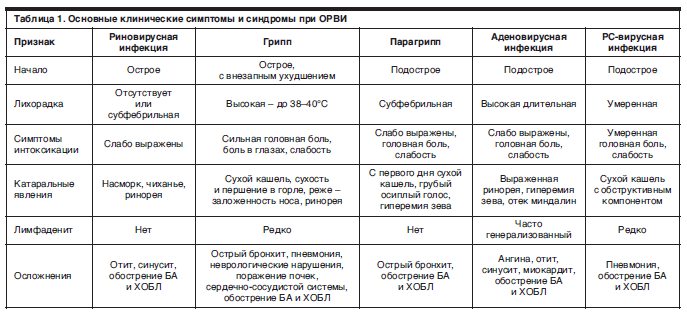
Инфекция может спускаться вниз по дыхательным путям, вызывая бронхит и даже пневмонию. Также возможны осложнения в виде отита (воспаления среднего уха) и гайморита (воспаления слизистой оболочки гайморовой пазухи).
Практически во всех случаях поражения аденовирусом наблюдается воспаление слизистой глаз в той или иной степени. Сочетание симптомов респираторного заболевания и конъюнктивита образуют типичную картину аденовирусной инфекции. При ярком свете симптомы усиливаются.
Существует кишечный вариант протекания заболевания. В этом случае аденовирус поражает слизистую кишечника.
Головная боль
Головная боль – типичный признак интоксикации. Головная боль может наблюдаться при различных инфекционных заболеваниях.
Подробнее о симптоме
Боль в мышцах
Боль в мышцах или суставах — еще один признак интоксикации. Это состояние может описана как ломота во всём теле. Обычно данный симптом предшествует подъему температуры.
Это состояние может описана как ломота во всём теле. Обычно данный симптом предшествует подъему температуры.
Озноб
Больного знобит – это начало повышения температуры
Потеря аппетита
Организм затрачивает много сил на борьбу с инфекцией. Пищеварительные процессы при этом замедляются, аппетит пропадает.
Слабость
Интоксикация организма часто проявляется в виде слабости. Если более ребенок – а в случае с аденовирусной инфекцией обычно так и есть, он становится плаксивым и вялым.
Подробнее о симптоме
Повышение температуры
Подъем температуры начинается несколько позднее появления признаков интоксикации. В большинстве случаев температура остается субфебрильной (до 38°C), но иногда может достигать и 39°C.
Резь в глазах
Воспаление слизистой глаз — типичный симптом аденовирусной инфекции. Обычно оно проявляется как жжение (зуд) в глазах.
Подробнее о симптоме
Слезятся глаза
Боль в животе
Кишечный вариант протекания аденовирусной инфекции обычно проявляется болью в животе.
Расстройство стула
Расстройство стула — еще один симптом кишечного варианта аденовирусной инфекции.
Методы лечения аденовирусной инфекции
Лечение аденовирусной инфекции проводится в домашних условиях, за исключением случаев тяжелого протекания заболевания или развития осложнений. Поскольку аденовирусная инфекция – заразное заболевание, больной должен быть изолирован (особенно важно исключить возможность контакта с детьми).
В большинстве случаев аденовирусная инфекция проходит в течение недели. Насморк может продолжаться до 3-х недель.
Стоит помнить, что осложнения у детей, особенного младшего возраста, могут развиться очень быстро. Поэтому при любом усилении симптомов (ухудшении самочувствия ребенка, возникновении кашля, жалобах на боль в ухе и т.п.) необходимо обратиться к врачу.
Постельный режим
На период повышенной температуры больному необходимо обеспечить постельный режим. Субфебрильную температуру сбивать не рекомендуется.
Симптоматическое лечение
Поскольку заболевание вызвано вирусом, антибиотики не используются (против вирусов они не действуют). Применение антибиотиков уместно только в случае осложнений (если к вирусной инфекции присоединилась бактериальная). Лечение аденовирусной инфекции – симптоматическое. Врач назначит средства, снимающие воспаление верхних дыхательных путей, устраняющие заложенность носа и симптомы конъюнктивита.
Врач назначит средства, снимающие воспаление верхних дыхательных путей, устраняющие заложенность носа и симптомы конъюнктивита.
Прием витаминосодержащих препаратов
В качестве общеукрепляющей терапии назначаются витамины, прежде всего витамин С.
Не занимайтесь самолечением. Обратитесь к нашим специалистам, которые правильно поставят диагноз и назначат лечение.
Оцените, насколько был полезен материал
Спасибо за оценку
Похожие заболевания
Все заболеванияАденовирусная инфекция — причины, симптомы, диагностика и лечение
Аденовирусная инфекция – острый вирусный инфекционный процесс, сопровождающийся поражением дыхательных путей, глаз, лимфоидной ткани, пищеварительного тракта. Признаками аденовирусной инфекции служат умеренная интоксикация, лихорадка, ринорея, осиплость голоса, кашель, гиперемия конъюнктивы, слизистое отделяемое из глаз, нарушение функции кишечника. Кроме клинических проявлений, при постановке диагноза применяются серологические и вирусологические методы исследования. Терапия аденовирусной инфекции проводится противовирусными препаратами (внутрь и местно), иммуномодуляторами и иммуностимуляторами, симптоматическими средствами.
Признаками аденовирусной инфекции служат умеренная интоксикация, лихорадка, ринорея, осиплость голоса, кашель, гиперемия конъюнктивы, слизистое отделяемое из глаз, нарушение функции кишечника. Кроме клинических проявлений, при постановке диагноза применяются серологические и вирусологические методы исследования. Терапия аденовирусной инфекции проводится противовирусными препаратами (внутрь и местно), иммуномодуляторами и иммуностимуляторами, симптоматическими средствами.
Общие сведения
Аденовирусная инфекция – заболевание из группы ОРВИ, вызываемое аденовирусом и характеризующееся развитием ринофарингита, ларинготрахеобронхита, конъюнктивита, лимфаденопатии, диспепсического синдрома. В общей структуре острых респираторных заболеваний аденовирусная инфекция составляет около 20%.
Наибольшую восприимчивость к аденовирусам демонстрируют дети от 6 месяцев до 3-х лет. Считается, что в дошкольном возрасте практически все дети переносят один или несколько эпизодов аденовирусной инфекции. Спорадические случаи аденовирусной инфекции регистрируются круглогодично; в холодное время года заболеваемость носит характер эпидемических вспышек. Пристальное внимание к аденовирусной инфекции приковано со стороны инфекционных болезней, педиатрии, отоларингологии, офтальмологии.
Спорадические случаи аденовирусной инфекции регистрируются круглогодично; в холодное время года заболеваемость носит характер эпидемических вспышек. Пристальное внимание к аденовирусной инфекции приковано со стороны инфекционных болезней, педиатрии, отоларингологии, офтальмологии.
Аденовирусная инфекция
Причины
В настоящее время известно более 30 сероваров вирусов семейства Adenoviridae, вызывающих заболевание человека. Наиболее частой причиной вспышек аденовирусной инфекции у взрослых выступают 3, 4, 7, 14 и 21 серотипы. Серовары типов 1, 2, 5, 6 обычно поражают детей-дошкольников. Возбудителями фарингоконъюнктивальной лихорадки и аденовирусного конъюнктивита в большинстве случаев служат серотипы 3, 4, 7.
Вирионы возбудителя содержат двухцепочечную ДНК, имеют диаметр 70-90 нм и три антигена (группоспецифический А-антиген; определяющий токсические свойства аденовируса В-антиген и типоспецифический С-антиген). Аденовирусы относительно устойчивы во внешней среде: при обычных условиях сохраняются в течение 2-х недель, хорошо переносят низкие температуры и высушивание. Вместе с тем, возбудитель аденовирусной инфекции инактивируется при воздействии ультрафиолетовых лучей и хлорсодержащих дезинфектантов.
Вместе с тем, возбудитель аденовирусной инфекции инактивируется при воздействии ультрафиолетовых лучей и хлорсодержащих дезинфектантов.
Аденовирусы распространяются от больных людей, которые выделяют возбудителя с носоглоточной слизью и фекалиями. Отсюда существует 2 основных пути заражения – в раннем периоде заболевания — воздушно-капельный; в позднем — фекально-оральный – в этом случае заболевание протекает по типу кишечных инфекций. Возможен водный путь заражения, поэтому аденовирусную инфекцию часто называют «болезнью плавательных бассейнов».
Источником аденовирусной инфекции также могут являться вирусоносители, пациенты с бессимптомными и стертыми формами болезни. Иммунитет после перенесенной инфекции типоспецифический, поэтому возможны повторные заболевания, вызванные другим серотипом вируса. Встречается внутрибольничное инфицирование, в т. ч. при проведении парентеральных лечебных процедур.
Патогенез
Аденовирус может проникать в организм через слизистые верхних дыхательных путей, кишечника или конъюнктиву. Репродукция вируса протекает в эпителиальных клетках, регионарных лимфатических узлах и лимфоидных образованиях кишечника, что по времени совпадает с инкубационным периодом аденовирусной инфекции. После гибели пораженных клеток вирусные частицы высвобождаются и проникают в кровь, вызывая вирусемию.
Репродукция вируса протекает в эпителиальных клетках, регионарных лимфатических узлах и лимфоидных образованиях кишечника, что по времени совпадает с инкубационным периодом аденовирусной инфекции. После гибели пораженных клеток вирусные частицы высвобождаются и проникают в кровь, вызывая вирусемию.
Изменения развиваются в оболочке носа, миндалин, задней стенки глотки, конъюнктивы; воспаление сопровождается выраженным экссудативным компонентом, что обусловливает появление серозного отделяемого из полости носа и конъюнктивы. Вирусемия может приводить к вовлечению в патологический процесс бронхов, пищеварительного тракта, почек, печени, селезенки.
Симптомы аденовирусной инфекции
Основными клиническими синдромами, форму которых может принимать данная инфекция, служат катар дыхательных путей (ринофарингит, тонзиллофарингит, ларинготрахеобронхит), фарингоконъюнктивальная лихорадка, острый конъюнктивит и кератоконъюнктивит, диарейный синдром. Течение аденовирусной инфекции может быть легким, среднетяжелым и тяжелым; неосложненным и осложненным.
Течение аденовирусной инфекции может быть легким, среднетяжелым и тяжелым; неосложненным и осложненным.
Инкубационный период при аденовирусной инфекции длится 2-12 дней (чаще 5-7 дней), вслед за чем следует манифестный период с последовательным появлением симптомов. Ранними признаками служат повышение температуры тела до 38-39 °С и умеренно выраженные симптомы интоксикации (вялость, ухудшение аппетита, мышечные и суставные боли).
Поражение дыхательных путей
Катаральные изменения в верхних дыхательных путях возникают одновременно с лихорадкой. Появляются серозные выделения из носа, которые затем становятся слизисто-гнойными; затрудняется носовое дыхание. Отмечается умеренная гиперемия и отечность слизистой оболочки задней стенки глотки, точечный белесоватый налет на миндалинах. При аденовирусной инфекции возникает реакция со стороны подчелюстных и шейных лимфоузлов. В случае развития ларинготрахеобронхита появляется осиплость голоса, сухой лающий кашель, возможна одышка, развитие ларингоспазма.
Поражение конъюнктивы
Поражение конъюнктивы при аденовирусной инфекции может протекать по типу катарального, фолликулярного или пленчатого конъюнктивита. Обычно в патологический процесс глаза вовлекаются поочередно. Беспокоит резь, жжение, слезотечение, ощущение присутствия инородного тела в глазу. При осмотре выявляется умеренное покраснение и отек кожи век, гиперемия и зернистость конъюнктивы, инъецированность склер, иногда – наличие плотной серовато-белой пленки на конъюнктиве. На второй неделе заболевания к конъюнктивиту могут присоединяться признаки кератита.
Кишечная форма
Если аденовирусная инфекция протекает в кишечной форме, возникают приступообразные боли в околопупочной и правой подвздошной области, лихорадка, диарея, рвота, мезентериальный лимфаденит. При выраженном болевом синдроме клиника напоминает острый аппендицит. Лихорадка при аденовирусной инфекции длится 1-2 недели и может носить волнообразный характер. Признаки ринита и конъюнктивита стихают через 7-14 дней, катара верхних дыхательных путей – через 14-21 день.
Осложнения
Диагностика
Распознавание аденовирусной инфекции обычно производится на основании клинических данных: лихорадки, катара дыхательных путей, конъюнктивита, полиаденита, последовательного развития симптомов. Методами экспресс-диагностики аденовирусной инфекции служит реакция иммунофлюоресценции и иммунная электронная микроскопия. Ретроспективное подтверждение этиологического диагноза проводится методами ИФА, РТГА, РСК. Вирусологическая диагностика предполагает выделение аденовируса из носоглоточных смывов, соскоба с конъюнктивы и фекалий больного, однако ввиду сложности и длительности редко используется в клинической практике.
Дифференциальная диагностика
Дифференциальную диагностику различных клинических форм аденовирусной инфекции проводят с гриппом, другими ОРВИ, дифтерией глотки и глаз, инфекционным мононуклеозом, микоплазменной инфекцией, иерсиниозом. С этой целью, а также для назначения местного этиотропного лечения пациенты нуждаются в консультации офтальмолога и отоларинголога.
Лечение аденовирусной инфекции
Общая этиотропная терапия проводится препаратами антивирусного действия (умифеновир, рибавирин, препарат из антител к гамма-интерферону человека). Местная терапия аденовирусной инфекции включает: инстилляции глазных капель (раствора дезоксирибонуклеазы или сульфацила натрия), аппликации ацикловира в виде глазной мази за веко, интраназальное применение оксалиновой мази, эндоназальную и эндофарингеальную инстилляцию интерферона. Проводится симптоматическая и посиндромная терапия: ингаляции, прием жаропонижающих, противокашлевых и отхаркивающих препаратов, витаминов. При аденовирусной инфекции, отягощенной бактериальными осложнениями, назначаются антибиотики.
Прогноз и профилактика
Неосложненные формы аденовирусной инфекции оканчиваются благоприятно. Смертельные исходы могут отмечаться у детей раннего возраста в связи с возникновением тяжелых бактериальных осложнений. Профилактика аналогична предупреждению других ОРВИ. В периоды эпидемических вспышек показана изоляция больных; проведение текущей дезинфекции, проветривания и УФО помещений; назначение интерферона лицам, подвергшимся риску заражения. Специфическая вакцинация против аденовирусной инфекции пока не разработана.
Грипп и простуда — симптомы, различия и способы лечения
29.06.2021 г.
338 702
12 минут
Содержание:
Грипп и его особенности
Что такое простуда
Основные симптомы простуды
Лечение ОРЗ
Респираторные инфекции – целая группа заболеваний, имеющих схожие механизмы передачи возбудителей и симптоматику. Среди них — грипп и другие инфекции, которые принято называть простудой. Как отличить их друг от друга и что делать, чтобы выздороветь быстрее?
Грипп и его особенности
Грипп – это одно из острых респираторных вирусных заболеваний (ОРВИ), которое часто выделяют из общей группы7. Его отличают более тяжелое течение и относительно высокая вероятность развития осложнений. Конечно, любое ОРВИ может протекать тяжело и с осложнениями, но при гриппе это случается чаще1.
Структура гриппа неоднородна. Вирус гриппа А обладает уникальной способностью видоизменяться6. Переболев вызванным им заболеванием, человек остается уязвимым перед другими подтипами вируса и потому может заражаться повторно2. Грипп А часто вызывает эпидемии и пандемии, во время которых инфекция поражает до 20% населения Земли1,3. Самая большая пандемия была в 1918-1919 годах – она унесла около 40 миллионов жизней.
Вирусы гриппа В и С практически не изменяются, они циркулируют вместе с гриппом А, но эпидемий не вызывают2.
Источник инфекции — больной человек. Причем совсем неважно, есть у него симптомы гриппа или нет. Он может болеть стертой формой и при этом быть опасным для окружающих1.
Заражение чаще всего происходит воздушно-капельным путем, однако инфекция может передаваться и через предметы обихода. Возбудители могут долгое время сохранять жизнеспособность в окружающей среде: в воздухе помещения — 2-9 часов, на бумаге, тканях и других рыхлых материалах – до 12 часов, на металлических и пластиковых поверхностях – до 2 суток1.
Наверх к содержанию
Симптомы гриппа у взрослых
Инкубационный период гриппа короткий — от нескольких часов до 1,5 суток2. Болезнь развивается стремительно1.
На первый план при гриппе выступают признаки интоксикации:
Лицо больного во время лихорадки становится одутловатым и красным, губы и видимые слизистые приобретают синеватый оттенок, на белочной оболочке глаз становятся заметны расширенные кровеносные сосуды1,2,7.
К концу первых суток от начала гриппа появляются симптомы ринита: заложенность носа, зуд и щекотание в носу, чихание, жидкие слизистые выделения из носовых ходов. Поражение слизистой оболочки глотки сопровождается першением и болью в горле, покашливанием, типичным для фарингита1,2.
Для гриппа характерно развитие трахеита (воспаления трахеи), проявлениями которого становятся ощущение заложенности за грудиной и кашель, вначале сухой, затем влажный с мокротой1,2.
Вирусы гриппа поражают мелкие кровеносные сосуды. Они становятся ломкими, из-за чего нередко возникают носовые кровотечения, на коже и слизистых появляются мелкие точечные кровоизлияния1,2,7.
Со стороны пищеварительной системы возможны такие симптомы, как тошнота, рвота, частый жидкий стул1.
Поражение нервной системы в легких случаях гриппа у детей и взрослых ограничивается такими симптомами, как головная боль, заторможенность или повышенная возбудимость, в тяжелых случаях возможно развитие менингита и менингоэнцефалита (воспаление головного мозга и его оболочек1,2,7).
Температура при гриппе держится около 4 суток, затем быстро снижается и нормализуется. Одновременно с этим наблюдается обратное развитие других симптомов1,2.
После перенесенного гриппа у 65% взрослых сохраняются признаки послевирусной астении1,7: слабость и плохое настроение, сниженная работоспособность и переносимость нагрузок, проблемы с концентрацией внимания и памятью.
Наверх к содержанию
Осложнения гриппа
Грипп может приводить к заболеваниям дыхательной, сердечно-сосудистой, нервной системы, почек, пищеварительного тракта, органа зрения и других.
Чаще всего возникают респираторные осложнения:
- острый бронхит, или воспаление бронхов — 20–30%;
- круп (затрудненное дыхание, громкий лающий кашель с металлическим оттенком) — до 15%;
- острый средний отит, или воспаление среднего уха: его симптомы обнаруживаются у 35% детей, заболевших гриппом;
- пневмонии, или воспаление легочной ткани1.
Также возможны:
- сердечная недостаточность различной степени тяжести;
- миокардит и перикардит – воспаление мышцы и оболочек сердца;
- вирусный энцефалит (энцефаломиелит), или воспаление оболочки головного мозга;
- нефрит – воспаление почек;
- инфекционно-токсический шок;
- геморрагический шок1.
Грипп может обострять течение хронических заболеваний, поэтому он опасен для больных с патологией сердца, сосудов, дыхательной и нервной системы. Особенно тяжело его переносят новорожденные, беременные женщины и пожилые люди1.
Наверх к содержанию
Нужно ли обращаться к врачу?
При гриппе всегда нужно обращаться к врачу. Только он может оценить клиническую картину, назначить необходимую терапию, вовремя выявить развивающиеся осложнения и при необходимости направить для лечения в стационар.
Наверх к содержанию
Что такое простуда
Простудой в быту чаще называют ОРВИ, отличающиеся от гриппа более легким течением, — по виду возбудителя их насчитывается более 2002,6,7.
В большинстве случаев возбудителями заболевания становятся:
- Риновирусы/энтеровирусы – в 12–45% случаев;
- Вирусы парагриппа — 15–30%;
- Респираторно-синцитиальные вирусы — 10–30%;
- Коронавирусы — 3–13%;
- Аденовирусы — 2–4%.
Как и при гриппе, инфекционный процесс развивается в слизистой оболочке верхних дыхательных путей6, но затем может распространяться в бронхи, бронхиолы и легочную ткань.
Наверх к содержанию
Основные симптомы простуды
Клиническая картина ОРВИ во многом схожа, ее нюансы зависят от возбудителя заболевания2.
Риновирусная инфекция
Риновирусная инфекция «господствует» в осенне-зимний период. Инкубационный период длится 2-3 дня. Температура тела не превышает 37,50 С или остается нормальной. Типичные проявления: обильные жидкие прозрачные пенистые выделения из носовых ходов, зуд и жжение в носу, вызывающие приступы чихания, заложенность носа и снижение обоняния1,4,5. Затекание слизи в носоглотку и глотку может вызывать кашель5.
Течение риновирусной инфекции легкое, общая продолжительность заболевания – 7-14 дней.
Наверх к содержанию
Парагрипп
Сезон парагриппа обычно начинается в конце зимы и продолжается до ранней весны. Заболевание развивается постепенно. Температура редко повышается выше 380 С, симптомы интоксикации тоже выражены слабо3,4
Вирус парагриппа поражает гортань. Простуда сопровождается симптомами ларингита: появлением сухого грубого лающего кашля, осиплостью голоса, болью в области шеи1,2.
Наверх к содержанию
Аденовирусная инфекция
Излюбленные сезоны аденовируса – весна, лето и осень. Интоксикация бывает довольно сильной, температура тела может повышаться до 380 С и выше. Типичный признак простуды, связанной с аденовирусами, – конъюнктивит. Кроме того, вирус поражает лимфоидную ткань глотки и вызывает развитие тонзиллофарингита с типичными для него симптомами: першением и болью в горле, усиливающимися при глотании, и кашлем. Слизистая оболочка глотки становится красной, глоточные миндалины увеличиваются1,4.
Среди других симптомов – увеличение и болезненность лимфатических узлов и печени, иногда диарея4.
Наверх к содержанию
Респираторно-синцитиальная вирусная инфекция
Респираторно-синцитиальная инфекция чаще встречается в холодное время года. Клиническая картина заболевания разворачивается довольно быстро4. Интоксикационный синдром выражен слабо. Температура тела не превышает 37,50 С1 и сохраняется до 2-7 дней2. Вирус поражает крупные и мелкие бронхи, вызывая развитие бронхита и бронхиолита со свойственным им кашлем, хрипами и затрудненным дыханием1,4.
Наверх к содержанию
Другие респираторные заболевания
Острые респираторные заболевания (ОРЗ) могут быть вызваны бактериальной микрофлорой: пневмококками, стрептококками, стафилококками, гемофильной палочкой, микоплазмами, хламидиями и другими микроорганизмами3.
Бактериальные осложнения могут развиваться на фоне ОРВИ. Переохлаждение, физические нагрузки, стрессы и другие факторы, ослабляющие иммунитет, иногда способствуют активизации условно-патогенной микрофлоры и развитию пневмонии3.
О возможном развитии бактериальных осложнений говорят:
- отсутствие улучшений в симптоматике или ухудшение состояния;
- сохраняющаяся более 5 дней высокая температура;
- повторное повышение температуры тела после периода нормальной температуры;
- появление потливости и сильной слабости;
- изменение характера кашля и появление одышки;
- присоединение новых симптомов7.
По статистике, каждый четвертый случай бронхита и каждая пятая пневмония – результат хламидийной или микоплазменной инфекции. У маленьких детей они часто становятся причиной воспаления околоносовых пазух (синусита) и уха (отита)3.
Хламидии могут долгое время находиться в организме, не вызывая при этом каких-либо острых симптомов. Длительно сохраняющийся сухой кашель и увеличение лимфатических узлов могут быть единственными симптомами ОРЗ у взрослого или ребенка. Антибиотики, традиционно используемые для лечения бактериальных пневмоний, оказываются неэффективны и не приносят облегчения, а при рентгенографии обнаруживается двусторонняя пневмония3.
Микоплазма поражает верхние и нижние дыхательные пути. Течение заболевания затяжное, нередко с осложнениями на легкие (плеврит), сердце (миокардит) и оболочки головного мозга (арахноидит)3.
Наверх к содержанию
Когда обращаться к врачу
Несмотря на кажущуюся легкость, не стоит заниматься самолечением и переносить простуду на ногах. Обращаться к врачу все равно нужно, хотя бы для того, чтобы не пропустить заболевания, напоминающие своими симптомами ОРВИ. Их лечение у взрослых и у детей будет в корне отличаться от терапии вирусных инфекций.
Наверх к содержанию
Лечение ОРЗ
Лечение гриппа, других ОРВИ и бактериальных респираторных инфекций имеет общие черты и отличия.
Во всех случаях нужно оставаться дома, по возможности меньше контактировать с другими членами семьи, использовать индивидуальную посуду и столовые принадлежности. Нужно чаще проветривать помещение, регулярно проводить влажную уборку и дезинфекцию предметов быта1.
Во время лихорадочного периода и в течение 3 дней после нормализации температуры необходимо соблюдать постельный режим1. Это особенно важно при лечении ОРВИ у детей, которые при уменьшении симптомов интоксикации сразу возвращаются к обычной физической активности, чего делать нельзя.
Для уменьшения симптомов интоксикации показано обильное питье. Полезны напитки из ягод и фруктов, богатых витамином С: лимона, шиповника, черноплодной рябины, смородины. Диета предусматривает снижение калорийности рациона в первые дни заболевания, частое дробное питание 6-7 раз в сутки и употребление продуктов в жидком и хорошо измельченном виде1.
Наверх к содержанию
Медикаментозная терапия
Медикаментозное лечение ОРЗ включает этиотропную и симптоматическую терапию. Этиотропные препараты действуют на возбудителей заболевания. Так, при симптомах гриппа лечение включает противовирусные средства1. Бактериальные респираторные инфекции лечат антибиотиками с учетом чувствительности к ним возбудителей заболевания3. При ОРВИ используют в основном симптоматическую терапию1.
Симптоматическое лечение ОРЗ предусматривает использование препаратов:
- жаропонижающих, помогающих справиться с лихорадкой1;
- противовоспалительных, уменьшающих проявления воспаления1;
- противокашлевых – для подавления сухого кашля1;
- муколитических и отхаркивающих, облегчающих отхождение мокроты1;
- сосудосуживающих назальных (деконгестантов) – для облегчения носового дыхания5.
Наверх к содержанию
РИНЗА® для симптоматического лечения ОРВИ и гриппа
В лечении ОРЗ широко используются комбинированные препараты, позволяющие бороться с несколькими симптомами заболевания одновременно, такие как РИНЗА®.
Препарат РИНЗА® в таблетках предназначен для детей старше 15 лет и взрослых. В его состав входят парацетамол, фенилэфрин, хлорфенамин и кофеин, помогающие одновременно бороться с лихорадкой и головной болью, заложенностью носа и насморком8.
РИНЗАСИП® с витамином С в форме порошка для приготовления горячих напитков со вкусом лимона, апельсина и черной смородины предназначен для симптоматического лечения взрослых и детей старше 15 лет. За счет включения в состав аскорбиновой кислоты он может способствовать укреплению иммунитета и повышению сопротивляемости инфекции9.
РИНЗАСИП® для детей старше 6 лет выпускается в виде порошка для приготовления напитка с малиновым вкусом. Кроме парацетамола в детской дозировке и витамина С, он содержит сосудосуживающий компонент — фенирамина малеат, действие которого направлено на уменьшение отека слизистой и облегчение заложенности носа10.
Информация в данной статье носит справочный характер и не заменяет профессиональной консультации врача. Для постановки диагноза и назначения лечения обратитесь к квалифицированному специалисту.
Наверх к содержанию
Литература
- Орлова Н. В. Грипп. Диагностика, стратегия выбора противовирусных препаратов // Медицинский совет. — №20. — 2017. — С. 80-86.
- Литвинова С. Н., Ощепкова М. В., Чукаева И. И. Грипп в амбулаторной практике // Лечебное дело. — №1. – 2005. — С. 29-45.
- Орлова Н. В., Суранова Т. Г. Острые респираторные заболевания: особенности течения, медикаментозная терапия // Медицинский совет. — №15. – 2018. — С. 82-88.
- Журавлева М. В., Лазарева Н. Б., Пантелеева Л. Р. ОРВИ: рациональная фармакотерапия с позиции клинической фармакологии // Медицинский совет. — №04. – 2016. – С. 68-72.
- А.А. Зайцев. Грипп и острые респираторные вирусные инфекции: рациональная симптоматическая терапия // Лечебное дело № 3.2016, С. 21-28.
- Л.В. Лусс. Комплексный подход к терапии гриппа и ОРВИ // Медицинский совет №5, 2017, С. 168-173.
- С.С. Якимова. Комплексный подход к лечению гриппа и простудных заболеваний // Медицинский совет, №5, 2013, С. 14-19.
- Инструкция по медицинскому применению РИНЗА® таблетки.
- Инструкция по применению РИНЗАСИП® с витамином С.
- Инструкция по применению РИНЗАСИП® для детей.
Лечение аденовирусной инфекции у детей с применением ингаляций | #06/13
Аденовирусная инфекция (АВ) (МКБ-10: В57) — острое инфекционное заболевание с преимущественным поражением носоглотки, конъюнктивы и лимфоидной ткани. АВ протекает с умеренной интоксикацией, лихорадкой, катаральным синдромом с выраженным экссудативным компонентом [1–3].
Аденовирусы, которые вызывают заболевание у детей, относятся к семейству Adenoviridae, роду Mastadenovirus ДНК-содержащих вирусов средних размеров. В настоящее время выделено около 50 серотипов этого вируса. Наиболее частыми возбудителями аденовирусной инфекции являются 3-й и 7-й серотипы. Аденовирусы обладают тропностью к эпителию дыхательных путей, кишечника и конъюнктивы, а также способностью поражать лимфоидную ткань. Токсичность вирусов этой группы низкая [2].
Источником инфекции является больной или вирусоноситель, пути передачи — воздушно-капельный, водный («болезнь плавательных бассейнов»), а также фекально-оральный. Наиболее восприимчивы к этому вирусу дети от 6 месяцев до 3 лет. АВ регистрируют повсеместно и круглогодично с подъемом заболеваемости в холодное время года. Заболевания наблюдаются в виде спорадических случаев и эпидемических вспышек, для которых характерно медленное развитие и длительное течение. Иммунитет после перенесенного заболевания типоспецифический, продолжительный. Аденовирусы относительно устойчивы в окружающей среде, сохраняются в течение нескольких недель в воде, лекарственных растворах, на предметах обихода, резистентны к эфиру. Разрушаются при температуре +56 °С в течение 30 мин, погибают под воздействием ультрафиолетового облучения и хлорсодержащих препаратов [2, 3].
При заражении вирусы проникают в организм через слизистые оболочки дыхательных путей, а также эпителий тонкой кишки. Благодаря своей лимфотропности, возбудитель внедряется в носоглотку, миндалины, конъюнктиву и вызывает формирование воспалительных очагов. В ходе заболевания увеличиваются все лимфатические узлы, в том числе мезентериальные, возникает гепатоспленомегалия. Инкубационный период длится 4–7 дней. Течение заболевания медленное, волнообразное. Характерен респираторный синдром, конъюнктивит, которые протекают с выраженным экссудативным компонентом. Диарея присоединяется обычно у детей до 2 лет и носит водянистый характер [1].
Патогномоничная форма аденовирусной инфекции — аденофарингоконъюнктивальная лихорадка. Она протекает с подъемом температуры тела до 38–39 °С на протяжении 5–10 дней, фарингитом с зернистостью задней стенки глотки, увеличением и гиперемией миндалин, конъюнктивитом. Нередко развивается тонзиллит, проявляющийся гипертрофией, отечностью и умеренной гиперемией миндалин, а также аденоидит. В ряде случаев на задней стенке глотки, небных миндалинах появляются нежные белесоватые налеты (пленчатый фарингит и тонзиллит) [1, 2].
С первых дней болезни нередко развивается кашель. Характерным для аденовирусной инфекции является синдром полиаденита — увеличение шейных и подчелюстных лимфатических узлов. Наблюдается увеличение печени и селезенки. Возможно развитие мононуклеозоподобного синдрома, для которого характерно сочетание пленчатого тонзиллита, полиаденита и гепатоспленомегалии. Длительность катарального синдрома — 10–15 дней, иногда до 3–4 недель [2, 3].
АВ — одна из распространенных респираторных вирусных инфекций, активно участвующих в формировании у ребенка адекватного противоинфекционного иммунитета, важного для всей последующей жизни.
При нормальном функционировании иммунной системы происходит эффективное взаимодействие интерферона и других лимфокинов, макрофагов, лимфоцитов, специфических антител, приводящее к элиминации возбудителя из макроорганизма и клиническому выздоровлению.
У ребенка раннего возраста направленность иммунной защиты организма изначально носит супрессивный характер. Невысокая активность собственного неспецифического звена иммунитета необходима для профилактики ярких воспалительных реакций, которые могут быстро истощить организм ребенка и привести его к развитию дезадаптации и декомпенсации систем жизнедеятельности. Специфическое звено иммунитета ребенка обусловливает пассивная иммунная защита в виде иммуноглобулинов, транслированных через плаценту, а также попадающих к ребенку вместе с молоком матери при грудном вскармливании.
Формирование надежной и адекватной естественной защиты с преобладанием популяции Тh2-лимфоцитов возможно только при непосредственном контакте ребенка с различными вирусами и «отработке» его иммунной системой паттерна воспалительной реакции, клинически выраженной чаще всего катаральным синдромом с кашлем и лихорадкой. Все проявления острых респираторных инфекций: лихорадка, ринит, кашель, гиперемия сводов зева — носят защитный характер и должны в первую очередь рассматриваться именно в этом контексте, а не представляться досадными помехами, которые надо немедленно купировать. Лихорадка — защитная реакция организма. Только на фоне лихорадки организм дает адекватный иммунный ответ Т-хелперов 1-го типа — продукцию γ-интерферона, интерлейкина-2, фактора некроза опухоли-α, стимулирующих выработку IgG.
Проникновение вируса в организм ребенка запускает каскад иммунных реакций, способствующих стимуляции нейроиммуноэндокринной системы, которая в дальнейшем регулирует процессы дифференцировки и созревания нейроэндокринной оси (рис.).
Защитные реакции кашля и выделения слизи из носовых ходов позволяют качественно осуществить очищение и увлажнение слизистой оболочки дыхательных путей, необходимые для адекватного функционирования мерцательного эпителия. Выделяемая из дыхательных путей мокрота к тому же содержит бесценный материал для выработки специфического иммунитета — фагоциты, которые определили возбудителя и экспрессировали специфические рецепторы для включения в работу высокоспециализированных клеток иммунной системы — лимфоцитов. При заглатывании ребенком мокроты лимфоидная ткань кишечника получает информацию о возбудителе и стимул к выработке регуляторных пептидов.
Покраснение сводов зева сопровождает прилив к слизистой оболочке крови, несущей компоненты гуморального и клеточного иммунитета, и искусственное «тушение» противовоспалительной местной терапией этого проявления неспецифической иммунной реакции мешает первичному этапу иммунной реакции запустить каскад иммунных реакций.
Медикаментозно «притушив» эти проявления, мы никогда не сможем заменить их лекарственными средствами, так как они индивидуальны и адекватны именно этому ребенку с его наследственностью, жизненным опытом и условиями проживания.
К сожалению, отсутствие четкого представления о необходимости некоторого временного периода, в течение которого все неспецифические иммунные процессы должны развернуться и принять участие в формировании гармоничного и полноценного иммунного ответа, в настоящее время приводит к необдуманной агрессивной терапии, целью которой является скорейшее купирование симптомов. По данным С. В. Ключникова (2012), каждому пятому ребенку в возрасте до 1 года назначались антибиотики (в том числе гентамицин, линкомицин). К возрасту 3 года число детей, получавших антибиотики, увеличивается до 28% и достигает 80% к семилетнему возрасту.
Необдуманное применение антибиотиков, недопустимо стремительное купирование естественных проявлений неспецифической иммунной защиты (лихорадка, насморк, кашель, гиперемия и отек сводов зева) ведут к снижению качества защитной биологической пленки на слизистой оболочке дыхательных путей.
В отделении раннего возраста педиатрической клиники МОНИКИ было проведено сравнение результатов микробиологического обследования двух групп детей в возрасте от 4 до 6 лет. Группы были выделены при анкетировании родителей, которым были заданы следующие вопросы:
- Ваш ребенок болеет чаще 6 раз в год?
- Вы сразу даете жаропонижающее средство ребенку при лихорадке до 38,5 °С, не стараясь выдержать ее хотя бы в течение 3–5 часов?
- Вы применяете антибиотики почти при каждом эпизоде острого респираторного заболевания?
- Вы с первых дней даете ребенку местные противовоспалительные препараты?
- Вы не считаете традиционные методы лечения (выпаивание, отвлекающая терапия, щадящий режим в течение 5–7 дней?) действенными в лечении ОРВИ?
Дети, родители которых на все вопросы ответили утвердительно, составили первую группу (20 человек). Дети, родители которых ответили на все вопросы, кроме первого и последнего, отрицательно, вошли во вторую группу (15 человек).
Анализ результатов микробиологического обследования (мазки на флору из зева) выявил, что в первой группе из 20 обследованных у 11 человек (55%), то есть у каждого второго ребенка, в посеве были выделены дрожжевые грибы, а количественный и качественный состав биопленки был представлен малочисленным и довольно однообразным биотопом (6 наименований микробов, количество нормальной флоры не превышает 2 × 103 КОЕ/мл).
Во второй группе количество детей, в мазке которых была выделена грибковая флора, не превысило 11% (2 человека из 15 обследованных), а биотоп был более разнообразным и плотным (8 наименований микробов, количество нормальной флоры 5–6 × 105 КОЕ/мл).
По этой причине агрессивное лечение острых респираторных инфекций и резкое неприятие родителями информации о существовании этапа в жизни ребенка, когда частые острые респираторные вирусные инфекции необходимы для его дальнейшего развития, в настоящее время являются базой для полипрагмазии, а организм ребенка становится полигоном для битвы многочисленных лекарственных средств.
Вместе с тем специфической противовирусной терапии при аденовирусной инфекции нет. Антибактериальная терапия в данном случае не показана. В период лихорадки назначают постельный режим, полноценное питание, обильное питье. Рекомендуется давать обильное горячее питье, чай, кисели, теплые морсы и компоты. Симптоматическое лечение включает применение жаропонижающих средств при лихорадке выше 38,5 °С. Если температура ребенка ниже 37,5 °С, нет необходимости в ее снижении медикаментозными препаратами. При более высокой температуре можно применять физические методы охлаждения. На внутреннюю поверхность рук, бедер, боковую поверхность шеи можно прикладывать смоченные в холодной воде компрессы. При насморке можно промывать нос слабым солевым раствором с помощью шприца или закапывать в нос сосудосуживающие капли. Следует избегать длительного применения капель (не более 5–7 дней), так как они могут вызвать временную дисфункцию слизистой оболочки [3, 4].
Оптимальными средствами для элиминации слизистой оболочки, восстановления ее влажности и создания наилучших условий для функционирования эпителия и слизистых клеток, вырабатывающих иммуноглобулин, лизоцим, лактоферрин и другие ферменты, являются изотонические растворы морской воды (Аква Марис, Физиомер, Долфин и пр.). Содержащиеся в морской воде микроэлементы (селен, йод, цинк) ускоряют регенерацию слизистой оболочки.
При выраженном сухом кашле можно начать лечение с приема грудного сбора в виде горячего отвара. Помогает также щелочное питье в виде горячего молока с небольшим количеством (на кончике ложки) соды. Если ребенок отказывается от молока, можно поить его подогретыми щелочными минеральными водами. Если кашель носит влажный характер с трудно отхаркивающейся мокротой, можно применять отхаркивающие препараты, если кашель длительный, сухой, саднящий — целесообразнее будет применять препараты, подавляющие кашель [4].
В лечении кашля при аденовирусной инфекции важно учитывать, что он может быть как сухим (характерное покашливание при гранулезном фарингите), так и с выраженным отделением мокроты. Поэтому препарат для адекватного сопровождения этого симптома должен быть направлен и на стимуляцию отделения мокроты, и на своевременную поддержку регенерации слизистой оболочки, и при этом должен иметь удовлетворяющие ребенка органолептические характеристики и удобный способ применения. Этим условиям соответствует Амбробене (амброксола гидрохлорид) — муколитический препарат с отхаркивающим действием, который обладает секретомоторным, секретолитическим и отхаркивающим свойствами.
Важным достоинством препарата является продуманное разнообразие лекарственных форм. Это дает преимущества в лечении детей любого возраста, поддерживает оптимальную комплаентность родителей и позволяет достичь адекватности в терапии респираторного синдрома у детей.
Например, можно использовать амброксола гидрохлорид в виде сиропов (детям от 5 до 12 лет — 1 мерная ложка (15 мг) — 2–3 раза в день; детям от 2 до 5 лет — 1/2 мерной ложки (7,5 мл) — 3 раза в день, детям до 2 лет — 1/2 мерной ложки (7,5 мл) после еды 2 раза в день).
Ингаляционная терапия имеет преимущества перед другими формами в том, что она совмещает элиминационные свойства (очищение верхних дыхательных путей от патологического содержимого), увлажнение слизистой оболочки и достаточную глубину проникновения для очищения более нижних отделов органов дыхания и таким образом профилактирует рефлекторный бронхоспазм при избытке мокроты. Лекарственное вещество распыляется и в виде аэрозоля оседает на слизистых оболочках верхних дыхательных путей. При этом возрастает интенсивность всасывания в подслизистом слое верхних дыхательных путей и увеличивается его депонирование.
Раствор для ингаляций применяется в зависимости от возраста детям от 5 до 12 лет — 2 мл (15 мг) — 2–3 раза в день; детям младше 5 лет — 1 мл (7,5 мл) — 3 раза в день.
В терапии аденовирусной инфекции можно использовать также иммунотропные препараты (Кипферон, Виферон, ИРС-19, Деринат), регулирующие неспецифические иммунные реакции (интерфероногенез) и дополняющие реакцию организма наличием специфических антител к представителям флоры, которые могут спровоцировать осложнения в виде пневмонии, бронхитов, синуситов.
Таким образом, обдуманная и максимально индивидуальная поддержка естественных защитных реакций организма ребенка при аденовирусной инфекции позволит сохранить и приумножить защитные силы организма ребенка.
Литература
- Детские инфекции. Справочник практического врача под ред. проф. Л. Н. Мазанковой. М.: МЕДпресс-информ, 2009. 240 с.: ил.
- Острые респираторные заболевания удетей: лечение и профилактика. Научно-практическая программа Союза педиатров России и Международного фонда охраны здоровья матери и ребенка. М., 2002.
- Острые инфекции дыхательных путей. Клинические варианты. Диагностика и лечении едетей с частыми респираторными заболеваниями. Конспект участкового педиатра. О. И. Борисова, Г. В. Римарчук (ред), с соавт. М., 2004.
- Рациональная фармакотерапия заболеваний органов дыхания. А. Г. Чучалин (под ред.) М., 2004.
Л. И. Васечкина1, кандидат медицинских наук
Т. К. Тюрина, кандидат медицинских наук
Е. В. Лукина
М. А. Маяцкая
ГБУЗ МО МОНИКИ им. М. Ф. Владимирского, Москва
1 Контактная информация: [email protected]
Аденовирусные инфекции: причины, симптомы и лечение
Аденовирусы — это группа распространенных вирусов, которые поражают слизистую оболочку глаз, дыхательные пути и легкие, кишечник, мочевыводящие пути и нервную систему. Это частые причины лихорадки, кашля, боли в горле, диареи и розового глаза.
Инфекции у детей случаются чаще, чем у взрослых, но заразиться ими может каждый. К 10 годам у большинства детей будет по крайней мере один тип аденовирусной инфекции.
Инфекции обычно вызывают лишь легкие симптомы и проходят сами по себе через несколько дней.Но они могут быть более серьезными у людей со слабой иммунной системой, особенно у детей.
Как распространяются аденовирусы
Эти вирусы распространены в местах с большими группами детей, таких как детские сады, школы и летние лагеря.
Они очень заразны. Они могут передаваться, когда зараженный кашляет или чихает. Капли, содержащие вирус, взлетают в воздух и приземляются на поверхности.
Ваш ребенок может заразиться вирусом, если он прикоснется к руке того, у кого он есть, или к игрушке или другому предмету, который держит кто-то, а затем коснется своего рта, носа или глаз.Он быстро распространяется среди детей, потому что они с большей вероятностью кладут руки на лицо и в рот.
При смене подгузника можно заразиться. Вы также можете заболеть от еды, приготовленной кем-то, кто неправильно вымыл руки после посещения туалета. Можно заразиться вирусом в воде, например, в небольших озерах или в неухоженном бассейне, но это случается нечасто.
Симптомы
Каждый тип аденовируса может повлиять на вас по-разному:
- Бронхит : кашель, насморк, лихорадка, озноб
- Простуда и другие респираторные инфекции : заложенность и насморк, кашель, боль в горле и т. Д. опухшие железы
- Crou p: Лающий кашель, затрудненное дыхание, высокий звук при дыхании
- Инфекция уха : Боль в ухе, раздражительность, лихорадка
- Розовый глаз (конъюнктивит): Красные глаза, выделения из глаза, слезы, ощущение, будто что-то попало в глаз
- Пневмония : Лихорадка, кашель, затрудненное дыхание
- Желудочные и кишечные инфекции: Диарея, рвота, головная боль, лихорадка, желудочные спазмы
- Отек мозга и спинной мозг (менингит и энцефалит ): головная боль, лихорадка, ригидность шеи, тошнота и рвота (редко)
- Инфекция мочевыводящих путей ons: Жжение и боль при мочеиспускании, частые позывы к мочеиспусканию, кровь в моче
Если вы считаете, что у вашего ребенка может быть один из этих вирусов, проконсультируйтесь с педиатром.Обязательно вызовите врача, если у ребенка младше 3 месяцев наблюдаются симптомы аденовирусной инфекции.
Немедленно обратитесь к врачу, если у вашего ребенка есть какие-либо из этих более серьезных симптомов:
- Проблемы с дыханием
- Отек вокруг глаз
- Лихорадка, которая не проходит через несколько дней
- Признаки обезвоживания, например мало слез или меньше мокрых подгузников
Диагноз
Врач вашего ребенка может назначить медицинский осмотр и, возможно, один или несколько из этих тестов, чтобы определить, не вызвали ли вирус или бактерии инфекцию:
- Анализ крови: A Медсестра возьмет образец крови вашего ребенка из вены на руке.
- Анализ мочи: Ваш ребенок будет писать в чашку, которую дает вам медсестра.
- Мазок для анализа: медсестра возьмет ватный тампон для пробы слизи из носа вашего ребенка.
- Тест стула. Вы собираете образец фекалий вашего ребенка дома и приносите его в кабинет врача.
- Рентген грудной клетки: Ваш ребенок будет лежать неподвижно, в то время как технический специалист использует небольшое количество излучения, чтобы сфотографировать его внутреннюю часть грудной клетки. Это позволит врачу вашего ребенка поближе взглянуть на его сердце и легкие.
Лечение
Антибиотики не помогают при аденовирусных инфекциях, потому что они убивают только бактерии. Часто дети проходят болезнь самостоятельно в течение нескольких дней. Некоторые инфекции, такие как розовый глаз или пневмония, могут длиться неделю и более.
Детям со слабой иммунной системой может потребоваться лечение в больнице, чтобы помочь им выздороветь.
Вы можете сделать несколько вещей, чтобы помочь вашему ребенку почувствовать себя лучше:
- Давайте много жидкости. Дети теряют жидкость от лихорадки, рвоты и диареи. Они могут обезвоживаться. Вода или 100% фруктовый сок — лучший выбор для обезвоживания детей. Вы также можете попробовать детский раствор с электролитами.
- Четкая перегрузка. Помогите ребенку почаще сморкаться. Младенцу закапайте в нос несколько капель солевого раствора или капель. Затем отсосите слизь шприцем с грушей.
- Включите увлажнитель холодного тумана . Влага ослабит заложенность носа и поможет вашему ребенку легче дышать.
- Сбить жар . Спросите своего врача, можно ли дать ребенку ацетаминофен (тайленол) или ибупрофен (мотрин), чтобы облегчить боль и жар. Не давайте детям продукты, содержащие аспирин, так как это может привести к редкому, но серьезному заболеванию, называемому синдромом Рейе.
Профилактика
Чтобы помочь вашему ребенку не заболеть:
- Старайтесь держать ребенка подальше от всех, кого вы знаете, что он болен.
- Мойте ребенку руки — и свои — часто в течение дня, особенно перед едой.Если у вас нет воды и мыла, используйте дезинфицирующее средство для рук на спиртовой основе.
- Очистите поверхности, такие как раковины и столешницы, чтобы избавиться от микробов.
- Не позволяйте им плавать в неухоженных бассейнах.
Держите ребенка дома, когда он болен, чтобы избежать передачи аденовируса другим людям. Скажите им, чтобы они прикрывали нос и рот, когда чихают или кашляют.
Рассмотрение подходов, медицинское обслуживание, консультации
Kopecky-Bromberg SA, Palese P.Рекомбинантные векторы как вакцины против гриппа. Curr Top Microbiol Immunol . 2009. 333: 243-67. [Медлайн].
Харви А.Р., Хеллстрём М., Роджер Дж. Генная терапия и трансплантация ретинофугального пути. Prog Brain Res . 2009. 175: 151-61. [Медлайн].
Лимбах KJ, Ричи TL. Вирусные векторы в разработке вакцины против малярии. Parasite Immunol . 2009 Сентябрь 31 (9): 501-19. [Медлайн].
Vora GJ, Lin B, Gratwick K et al.Сопутствующие инфекции видов аденовируса у ранее вакцинированных пациентов. Emerg Infect Dis . Июнь 2006. 12: 921-30. [Медлайн].
Echavarría M. Аденовирусы у хозяев с ослабленным иммунитетом. Clin Microbiol Ред. . 2008 21 октября (4): 704-15. [Медлайн]. [Полный текст].
Шах К.В. SV40 и рак человека: обзор последних данных. Инт Дж. Рак . 2007 15 января. 120 (2): 215-23. [Медлайн].
Martini F, Corallini A, Balatti V, Sabbioni S, Pancaldi C, Tognon M.Обезьяний вирус 40 у человека. Заражение возбудителя рака . 2007. 2:13. [Медлайн].
Solomon ET, Gari SR, Kloos H, Alemu BM. Влияние мытья рук на заболеваемость диареей у детей в возрасте до 5 лет в сельских районах восточной Эфиопии: кластерное рандомизированное контролируемое исследование. Троп Мед Здоровье . 2021 23 марта 49 (1): 26. [Медлайн]. [Полный текст].
Luby SP, Agboatwalla M, Painter J, Altaf A, Billhimer W., Keswick B. и др. Групповое рандомизированное контролируемое исследование, объединяющее обработку питьевой водой и мытье рук для профилактики диареи. Троп Мед Инт Здоровье . 2006 г., 11 (4): 479-89. [Медлайн]. [Полный текст].
Киллерби М.Э., Розвадовски Ф., Лу Х, Колкрик-Граймс М., МакХью Л., Холдеман А.М. и др. Респираторное заболевание, связанное с новым геномом аденовируса человека типа 7d, Нью-Джерси, 2016-2017 гг. Открытый форум Infect Dis . 2019 11 января. Ofz017. [Медлайн]. [Полный текст].
Kujawski SA, Lu X, Schneider E, Blythe D, Boktor S, Farrehi J, et al. Вспышки респираторного заболевания, связанного с аденовирусом, в пяти университетских городках США. Клиническая инфекция . 2020 23 апреля ciaa465. [Медлайн]. [Полный текст].
Табаин И., Любин-Стернак С., Цепин-Богович Дж, Марковинович Л., Кнезович И., Млинарич-Галинович Г. Аденовирусные респираторные инфекции у госпитализированных детей: клинические данные в отношении видов и серотипов. Pediatr Infect Dis J . 2012 г., 18 апреля [Medline].
Faden H, Wynn RJ, Campagna L, Ryan RM. Вспышка аденовируса 30-го типа в отделении интенсивной терапии новорожденных. Дж. Педиатр . 2005 апр. 146 (4): 523-7. [Медлайн].
Kajon AE, Moseley JM, Metzgar D, Huong HS, Wadleigh A, Ryan MA. Молекулярная эпидемиология инфекций аденовирусом типа 4 у новобранцев в армии США в поствакцинальную эпоху (1997-2003 гг.). J Заразить Dis . 2007 г. 1. 196 (1): 67-75. [Медлайн].
Рассел К.Л., Хоксворт А.В., Райан М.А. и др. Аденовирусное респираторное заболевание, предотвращаемое с помощью вакцин, у новобранцев в армии США, 1999-2004 гг. Вакцина . Апрель 2006. 15: 2835-42. [Медлайн].
Wirsing von König CH, Rott H, Bogaerts H, Schmitt HJ. Серологическое исследование микроорганизмов, возможно, связанных с коклюшным кашлем. Pediatr Infect Dis J . 1998 июл.17 (7): 645-9. [Медлайн].
Versteegh FG, Mooi-Kokenberg EA, Schellekens JF, Roord JJ. Bordetella pertussis и смешанные инфекции. Минерва Педиатр . 2006 апр. 58 (2): 131-7. [Медлайн].
Saiki-Macedo S, Valverde-Ezeta J, Cornejo-Tapia A, Castillo ME, Petrozzi-Helasvuo V, Aguilar-Luis MA, et al. Идентификация вирусных и бактериальных возбудителей коклюшноподобного синдрома у госпитализированных детей до 5 лет. BMC Infect Dis . 2019 21 янв. 19 (1): 75. [Медлайн]. [Полный текст].
Дарт Дж. К., Эль-Амир А. Н., Мэддисон Т., Десаи П., Верма С., Хьюз А. и др. Выявление и лечение нозокомиального аденовирусного кератоконъюнктивита в офтальмологическом отделении. Br J Офтальмол . 2009 январь 93 (1): 18-20. [Медлайн].
Bruno B, Zager RA, Boeckh MJ, et al. Аденовирусный нефрит при трансплантации гемопоэтических стволовых клеток. Трансплантация . 2004 15 апреля. 77 (7): 1049-57. [Медлайн].
Накамура Ю., Охаши К., Накано Н., Немото Т., Фунада Н., Андо М. [Острый некротический тубулоинтерстициальный нефрит, вызванный аденовирусной инфекцией после трансплантации гемопоэтических стволовых клеток: клинические данные, полученные в 4 случаях вскрытия]. Ниппон Дзиндзо Гаккай Ши . 2008. 50 (8): 1036-43. [Медлайн].
Uhnoo I, Wadell G, Svensson L, Johansson ME. Важность кишечных аденовирусов 40 и 41 при остром гастроэнтерите у младенцев и детей раннего возраста. Дж. Клин Микробиол . 1984 Сентябрь 20 (3): 365-72. [Медлайн]. [Полный текст].
Джалал Х., Бибби Д.Ф., Танг Дж. В., Беннетт Дж., Кириаку С., Пеггс К. Впервые сообщили о вспышке диареи из-за аденовирусной инфекции в гематологическом отделении для взрослых. Дж. Клин Микробиол . 2005 июн. 43 (6): 2575-80. [Медлайн].
Munoz FM, Piedra PA, Demmler GJ. Диссеминированное аденовирусное заболевание у детей с ослабленным иммунитетом и иммунокомпетентностью. Клиническая инфекция . 1998, 27 ноября (5): 1194-1200. [Медлайн]. [Полный текст].
Изон МГ. Аденовирусные инфекции у реципиентов трансплантата. Клиническая инфекция . 2006 г. 1. 43 (3): 331-9. [Медлайн].
Hedderwick SA, Greenson JK, McGaughy VR, Clark NM.Аденовирусный холецистит у больного СПИДом. Клиническая инфекция . 1998 26 апреля (4): 997-9. [Медлайн].
Лю М., Уорли С., Арриган С., Аврора П., Баллманн М., Бойер Д. и др. Респираторные вирусные инфекции в течение одного года после трансплантации легких у детей. Transpl Infect Dis . 2009 11 (4): 304-12. [Медлайн].
Echavarria M, Sanchez JL, Kolavic-Gray SA, Polyak CS, Mitchell-Raymundo F, Innis BL, et al. Быстрое обнаружение аденовируса в мазках из горла с помощью ПЦР во время вспышек респираторных заболеваний среди призывников. Дж. Клин Микробиол . 2003 Февраль 41 (2): 810-2. [Медлайн].
Lu X, Trujillo-Lopez E, Lott L, Erdman DD. Панель количественного анализа ПЦР в реальном времени для обнаружения и идентификации типа эпидемических респираторных аденовирусов человека. Дж. Клин Микробиол . 2013 апр. 51 (4): 1089-93. [Медлайн]. [Полный текст].
Lion T, Baumgartinger R, Watzinger F, Matthes-Martin S, Suda M, Preuner S и др. Молекулярный мониторинг аденовируса в периферической крови после аллогенной трансплантации костного мозга позволяет на ранней стадии диагностировать диссеминированное заболевание. Кровь . 1 августа 2003 г. 102 (3): 1114-20. [Медлайн]. [Полный текст].
Марчиори Э., Эскуиссато Д.Л., Гаспаретто Т.Д., Кондера Д.П., Франке Т. «Безумные тротуары» на компьютерных томограммах высокого разрешения у пациентов с легочными осложнениями после трансплантации гемопоэтических стволовых клеток. Корейский J Radiol . 2009 Янв-Фев. 10 (1): 21-4. [Медлайн]. [Полный текст].
Lion T. Аденовирусные инфекции у иммунокомпетентных пациентов и пациентов с ослабленным иммунитетом. Clin Microbiol Ред. . 2014. 27 (3): 441-462. [Медлайн]. [Полный текст].
Matthes-Martin S, Feuchtinger T, Shaw PJ, Engelhard D, Hirsch HH, Cordonnier C, et al. Четвертая Европейская конференция по инфекциям при лейкемии. Европейские рекомендации по диагностике и лечению аденовирусной инфекции при лейкемии и трансплантации стволовых клеток: резюме ECIL-4 (2011). Transpl Infect Dis . 2012 декабря 14 (6): Epub. [Медлайн]. [Полный текст].
Хумар А., Кумар Д., Мацзулли Т., Разонабл Р.Р., Мусса Г., Пайя К.В. и др.Наблюдательное исследование аденовирусной инфекции у взрослых реципиентов трансплантатов твердых органов. Трансплантат Am J . 2005 октября, 5 (10): 2555-9. [Медлайн].
Файюми М.А., Бетенсли А. Успешное лечение тяжелой аденовирусной пневмонии цидофовиром у реципиента трансплантата легкого. Сундук . 2013. 144: 172A-172B.
Feuchtinger T, Lücke J, Hamprecht K, Richard C, Handgretinger R, Schumm M. Обнаружение аденовирус-специфических Т-клеток у детей с аденовирусной инфекцией после трансплантации аллогенных стволовых клеток. Br J Haematol . 2005 февраль 128 (4): 503-9. [Медлайн].
Wy Ip W, Qasim W. Управление аденовирусом у детей после трансплантации аллогенных гемопоэтических стволовых клеток. Adv Hematol . 2013. 2013: 176418. [Медлайн]. [Полный текст].
Creidy R, Moshous D, Touzot F и др. Специфические Т-клетки для лечения цитомегаловируса и / или аденовируса в контексте трансплантации гемопоэтических стволовых клеток. J Allergy Clin Immunol .2016 Сентябрь 138 (3): 920-924.e3. [Медлайн].
Хорлок С., Скулте А., Митра А., Стэнсфилд А., Бхандари С., ИП В. и др. Производство функциональной аденовирусной Т-клеточной терапии, соответствующей требованиям GMP, для лечения посттрансплантационных инфекционных осложнений. Цитотерапия . 2016 Сентябрь 18 (9): 1209-18. [Медлайн].
Barrett AJ, Prockop S, Боллард CM. Вирус-специфические Т-клетки: расширение применимости. Пересадка костного мозга Biol .2018 24 января (1): 13-18. [Медлайн].
Carter BA, Karpen SJ, Quiros-Tejeira RE, et al. Внутривенная терапия цидофовиром для диссеминированного аденовируса у педиатрических реципиентов трансплантата печени. Трансплантация . 2002 15 октября. 74 (7): 1050-2. [Медлайн].
Hayashi M, Lee C, de Magalhaes-Silverman M. Аденовирусные инфекции у пациентов с BMT, успешно пролеченных цидофовиром. Кровь . 2000. 96 (приложение 1): 189a.
Muller WJ, Левин MJ, Shin YK, Robinson C, Quinones R, Malcolm J.Клиническая и in vitro оценка цидофовира для лечения аденовирусной инфекции у детей-реципиентов трансплантатов гемопоэтических стволовых клеток. Клиническая инфекция . 2005 15 декабря. 41 (12): 1812-6. [Медлайн].
Неофитос Д., Охха А., Мукерджи Б., Вагнер Дж., Филико Дж., Фербер А. и др. Лечение аденовирусной болезни у реципиентов трансплантата стволовых клеток цидофовиром. Пересадка костного мозга Biol . 2007 13 января (1): 74-81. [Медлайн].
Юсуф У., Хейл Г.А., Карр Дж., Гу З., Бенаим Э., Вудард П.Цидофовир для лечения аденовирусной инфекции у педиатрических пациентов с трансплантацией гемопоэтических стволовых клеток. Трансплантация . 2006 27 мая. 81 (10): 1398-404. [Медлайн].
Saquib R, Melton LB, Chandrakantan A, Rice KM, Spak CW, Saad RD и др. Диссеминированная аденовирусная инфекция у реципиентов почечного трансплантата: роль цидофовира и внутривенного иммуноглобулина. Transpl Infect Dis . 2009 15 сентября. [Medline].
Софер А, Аргер Н, Вест М.Успешное лечение ОРДС, индуцированного аденовирусом, с помощью цидофовира и ВВИГ. Сундук . 2013. 144: 229A-229B.
Прасад В.К., Папаниколау Г.А., Марон Г.М. и др. Лечение аденовирусной (AdV) инфекции у пациентов с аллогенной трансплантацией гемопоэтических клеток (allo HCT) бринцидофовиром: окончательные 36-недельные результаты AdVise Tria. Биология трансплантации крови и костного мозга . 2017. 23: S57 – S58.
Brundage TM, Vainorius E, Chittick G et al.Бринцидофовир снижает вирусную нагрузку аденовируса, что связано с улучшением смертности у детей, получавших трансплантаты аллогенных гемопоэтических клеток. Биология трансплантации крови и костного мозга . 2018. 24: S372.
Grimley MS, Chemaly RF, Englund JA, Kurtzberg J, Chittick G, Brundage TM и др. Бринцидофовир для бессимптомной аденовирусной виремии у детей и взрослых получателей аллогенных гемопоэтических клеток: рандомизированное плацебо-контролируемое исследование фазы II. Пересадка костного мозга Biol . 2017 23 марта (3): 512-521. [Медлайн].
Chimerix, Inc. Расширенный доступ. Chimerix.com. Доступно по адресу https://www.chimerix.com/patient-resources/expanded-access/#. Дата обращения: 13 апреля 2021 г.
Romanowski EG, Hussein ITM, Cardinale SC, Butler MM, Morin LR, Bowlin TL, et al. Филоцикловир является активным противовирусным агентом против изолятов глазного аденовируса in vitro и в модели глаза кролика Ad5 / NZW. Фармацевтические препараты (Базель) . 2021 26 марта, 14 (4): 294. [Медлайн]. [Полный текст].
Barraza EM, Ludwig SL, Gaydos JC et al. Повторное появление острого респираторного заболевания аденовируса типа 4 у военнослужащих: отчет о вспышке во время перерыва в вакцинации. J Заразить Dis . Июнь 1999. 179: 1531-3. [Медлайн].
Райан М.А., Грей Г.С., Смит Б. и др. Крупная эпидемия респираторных заболеваний, вызванных аденовирусом типов 7 и 3 среди здоровых молодых людей. Клиническая инфекция . 2002 г., 1. 34 (5): 577-82. [Медлайн].
Vora GJ, Lin B, Gratwick K et al. о-инфекции видов аденовируса у ранее вакцинированных пациентов. Emerg Infect Dis . Июнь 2006. 12: 921-30. [Медлайн].
Rutala WA, Peacock JE, Gergen MF, Sobsey MD, Weber DJ. Эффективность госпитальных бактерицидов против аденовируса 8, частой причины эпидемического кератоконъюнктивита в медицинских учреждениях. Противомикробные агенты Chemother .2006 апр. 50 (4): 1419-24. [Медлайн].
Fanourgiakis P, Georgala A, Vekemans M, Triffet A, De Bruyn JM, Duchateau V. Внутрипузырная инстилляция цидофовира при лечении геморрагического цистита, вызванного аденовирусом типа 11, реципиенту трансплантата костного мозга. Клиническая инфекция . 2005 г. 1. 40 (1): 199-201. [Медлайн].
Лечение и профилактика аденовирусной инфекции
Лечение аденовирусной инфекции
Как и большинство других вирусных инфекций, не существует специфических лекарств, которые могут воздействовать на аденовирус.Иммунная система организма борется с инфекцией, и у большинства людей она проходит через 3-5 дней.
Лечение направлено на восстановление симптомов этого состояния и включает: —
- Постельный режим и изоляция для предотвращения распространения инфекции.
- Обильное питье и чистые жидкости. Это предотвращает обезвоживание.
- Безрецептурные средства для снятия лихорадки можно принимать при лихорадке и головной боли. Чаще всего используются парацетамол / ацетаминофен или ибупрофен.У детей младше 12 лет для снятия лихорадки следует использовать аспирин , а не . Использование аспирина при вирусных инфекциях повышает риск повреждения печени и головного мозга, называемого синдромом Рея у детей.
- Увлажнители могут быть назначены для облегчения боли в горле и заложенного носа. Также можно использовать физиологические капли в нос. Пациентам с астмой при затрудненном дыхании назначают лекарства (ингаляторы), расширяющие дыхательные пути.
- Пастилки и капли от кашля можно принимать для облегчения горла и кашля.
- Больным конъюнктивитом рекомендуются глазные капли с антибиотиками и мази.
- Осложнения, такие как пневмония, необходимо лечить в больнице после госпитализации. Необходимы соответствующие антибиотики, кислород, внутривенные жидкости и т. Д.
- Больных менингитом также необходимо госпитализировать и лечить с помощью антибиотиков, кислорода, внутривенных жидкостей и т. Д.
- Пациенты с инфекциями среднего уха или средним отитом могут лечиться в амбулаторных условиях с использованием антибиотиков и поддерживающего лечения боли, лихорадки и других симптомов.
- Цидофовир — это противовирусное средство, которое использовалось для лечения тяжелых аденовирусных инфекций у людей с подавленной или слабой иммунной системой. Цидофовир назначают три раза в неделю в дозе 1 мг / кг / сут. В качестве альтернативы цидофовир можно вводить в дозе 5 мг / кг в неделю. Этот препарат может повредить почки, а также стоит дорого. Он предназначен только для серьезных случаев. Цидофовир следует прекратить, когда аденовирус больше не обнаруживается в крови с помощью ПЦР в двух последовательных образцах.
- Серьезным пациентам, особенно с пониженным иммунитетом, также можно назначать иммуноглобулин в дозе 500 мг / кг еженедельно в течение 3 недель для борьбы с инфекцией.
Профилактика аденовирусной инфекции
Профилактика аденовирусной инфекции основана на здоровых привычках, применимых для предотвращения большинства вирусных инфекций. Эти меры включают: —
- Мытье рук до и после еды или обращения с материалами, используемыми инфицированным человеком. Дезинфицирующие средства для рук на спиртовой основе можно часто использовать, если руки не выглядят грязными.
- Не прикасайтесь к глазам, носу или рту загрязненными руками или пальцами.
- Прикрытие рта и носа салфеткой при кашле или чихании помогает предотвратить распространение вируса.
- Изоляция и избегание работы или учебы при простуде или вирусной инфекции.
- Обеспечение надлежащего хлорирования бассейнов.
- Избегать совместного использования полотенец, посуды и т. Д. С инфицированным человеком. Избегание тесного контакта с человеком, заболевшим аденовирусной инфекцией.
Вакцина против аденовируса
Оральная вакцина против аденовирусов типов 4 и 7 была одобрена U.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США в марте 2011 г. для военнослужащих США. Его можно использовать только в возрасте от 17 до 50 лет.
Вакцина рекомендована Министерством обороны США для военнослужащих для профилактики острых респираторных заболеваний.
Дополнительная литература
случаев аденовирусной инфекции у взрослых, получавших трансплантаты крови и костного мозга | Клинические инфекционные болезни
Аннотация
Аденовирусы становятся все более узнаваемыми патогенами, поражающими реципиентов крови и трансплантата костного мозга (BMT).Был проанализирован опыт 2889 взрослых реципиентов BMT, чтобы изучить частоту, клинический спектр, факторы риска распространения, ответ на терапию и исходы аденовирусных инфекций. Восемь пяти пациентам (3%) был поставлен диагноз путем посева ( n = 85) или посева и гистопатологического исследования ( n = 6). У девяти пациентов была бессимптомная вируса, а у 76 — симптоматические инфекции, в том числе инфекция верхних дыхательных путей ( n = 20), энтерит ( n = 18), геморрагический цистит ( n = 10), пневмония ( n ). = 15) и диссеминированное заболевание ( n = 13).Общая летальность составила 26%. Более высокая смертность наблюдалась среди пациентов с пневмонией (73%) и диссеминированным заболеванием (61%). Факторы риска распространения включали получение аллогенного трансплантата, наличие реакции «трансплантат против хозяина» (GVHD) и получение сопутствующей иммуносупрессивной терапии. Внутривенное введение рибавирина не показало заметного улучшения у 12 пациентов, получавших это лечение. В заключение, аденовирусные инфекции являются важной причиной заболеваемости и смертности взрослых реципиентов BMT, особенно реципиентов аллогенных трансплантатов с GVHD, которые получают иммуносупрессивную терапию.Очевидна необходимость в эффективной нетоксичной противовирусной терапии.
Аденовирусы представляют собой икосаэдрические вирусные частицы без оболочки с линейным двухцепочечным геномом ДНК. Описано более 50 серотипов, которые были разделены на 6 подгрупп (A – F). Аденовирусы вызывают широкий спектр клинических синдромов, включая респираторные заболевания, энтерит, гепатит, геморрагический цистит, нефрит, конъюнктивит и менингоэнцефалит [1]. Чаще всего инфекции возникают в раннем детстве, но они продолжают возникать на протяжении всей жизни.Тесный контакт с людьми в переполненных учреждениях увеличивает риск аденовирусных инфекций. Вспышки такой инфекции описаны в детских садах, больницах, на верфях и в военных частях [1]. В большинстве случаев эти инфекции ограничиваются типоспецифическим иммунным ответом, но латентная инфекция может развиваться в лимфоидной ткани [1].
У лиц с ослабленным иммунитетом, таких как реципиенты трансплантата крови и костного мозга (BMT) и реципиенты трансплантата твердых органов, может развиться тяжелое и часто фатальное локализованное или диссеминированное заболевание [2–19].В течение последнего десятилетия использование более мощных химиотерапевтических и иммунодепрессивных средств, совершенствование методов вирусологической диагностики и лучший контроль цитомегаловирусных (ЦМВ) инфекций были связаны с растущим осознанием роли других вирусов, таких как аденовирус, в развитии инфекции. заболеваемость и смертность реципиентов ТКМ [3–6, 9–15, 17–19]. Чтобы изучить частоту, клинический спектр заболевания, факторы риска распространения, ответ на терапию и исходы аденовирусных инфекций, мы рассмотрели опыт 2889 взрослых, которые прошли BMT в Университете Техаса М.Онкологический центр Д. Андерсона (MDACC), Хьюстон.
Пациенты и методы
Были проанализированы записи вирусологического обследования всех взрослых, которые прошли ТКМ в MDACC с января 1990 г. по декабрь 1998 г. Были изучены медицинские карты всех пациентов, у которых была диагностирована аденовирусная инфекция. Аденовирусные инфекции диагностировали путем выделения аденовируса из культур клеточных линий, которые проявляли характерные цитопатические эффекты, которые затем были подтверждены с помощью непрямого иммунофлуоресцентного анализа антител.Когда были получены образцы тканей, патологические находки были проанализированы на предмет наличия характерных вирусных включений и для подтверждения, сделанного с помощью гибридизации in situ или иммуногистохимии.
В течение периода исследования у реципиентов ТКМ с симптомами были получены образцы для полного культивирования вируса, выполненного по усмотрению лечащего врача. Образцы инокулировали в 5 различных клеточных линиях, 3 из которых (Hep-2, A549 и фибробласты крайней плоти человека) обладали способностью давать аденовирусы.Кроме того, с января 1990 г. по май 1997 г. активное наблюдение за ЦМВ-инфекциями у реципиентов аллогенной ТКМ включало еженедельные мазки лейкоцитарной пленки крови и посевы ЦМВ образцов мочи с 0-го по 100-й день после трансплантации. Эти контрольные образцы мочи инокулировали в клеточные линии фибробластов крайней плоти человека, которые также поддерживали рост аденовируса. После мая 1997 г. образцы мочи для контрольных культур больше не брались.
«Определенное инвазивное заболевание» определялось по совместимой клинической картине, путем выделения аденовируса из вирусных культур и документальным подтверждением тканевой инвазии аденовируса в соответствующем месте в соответствии с наличием характерных внутриядерных вирусных включений, что подтверждалось средства гибридизации in situ или иммуногистохимии.«Вероятное инвазивное заболевание» определялось по совместимой клинической картине и путем выделения аденовируса из вирусных культур образцов, которые были получены из соответствующего сайта. «Распространенное заболевание» определялось наличием инвазивного аденовирусного заболевания в ≥2 системах органов (дыхательных, мочевыводящих и желудочно-кишечных).
Среди реципиентов аллогенных и аутологичных трансплантатов соотношение пациентов со специфическими синдромами сравнивали с использованием критерия χ 2 и точного критерия Фишера.Одномерный анализ переменных, связанных с распространением, был выполнен с использованием критерия χ 2 и точного критерия Фишера. Переменные, включенные в этот анализ, были следующими: тип трансплантата, наличие реакции трансплантат против хозяина (GVHD), использование общего облучения тела для кондиционирования и использование специфической кондиционирующей химиотерапии или иммунодепрессантов (например, циклофосфамид, флударабин, бусульфан, мелфалан, кармустин, тиотепа, цис--платина, таксол, Ara-C, VP-16, циклоспорин A, такролимус, метотрексат, антитимоцитарный глобулин, OKT3 и метилпреднизолон).РТПХ была включена в анализ, когда она была подтверждена анализом биоптатов и была II – IV степени. Иммуносупрессивные препараты, которые использовались для лечения РТПХ, были включены в анализ факторов риска, связанных с диссеминацией, только в том случае, если такое лечение было начато по крайней мере за 1 неделю до получения первого образца, который дал аденовирус. Переменные, которые достигли статистической значимости, согласно одномерному анализу, впоследствии были изучены с помощью многомерного анализа, который проводился с использованием модели пошаговой логистической регрессии.
Результаты
В течение периода исследования 2889 взрослых прошли BMT в MDACC; из этих 2889 у 85 (3%) была диагностирована аденовирусная инфекция. Количество случаев, диагностированных в течение каждого года исследования (1990–1998), составляло 0, 4, 10, 9, 17, 11, 18, 5 и 11 соответственно. Явного сезонного распределения случаев не было. Общее количество случаев, диагностированных в течение каждого месяца (с января по декабрь), составляло 4, 7, 10, 4, 8, 12, 7, 4, 5, 9, 8 и 7 соответственно.Наибольшее количество случаев, диагностированных в течение одного месяца в любой год исследования, составило 4 (как в июле 1992 г., так и в мае 1996 г.).
Демографические и клинические характеристики этих пациентов описаны в таблице 1. Заболеваемость аденовирусной инфекцией была значительно выше среди реципиентов аллогенных BMT, чем среди реципиентов аутологичных BMT (69 [6%] из 1150 пациентов против 16 [0,92%]). ] из 1739 пациентов соответственно; P <0,001). Пятьдесят пять инфекций (65%) были диагностированы в течение первых 100 дней после трансплантации пациенту (среднее время до постановки диагноза - 62 дня; среднее время до постановки диагноза - 155 дней).Аденовирус выделяли из образцов мочи ( n = 32), промывания носоглотки ( n = 28), стула ( n = 28), бронхоальвеолярного лаважа ( n = 15), эндотрахеального аспирата ( n ). = 5), мазок конъюнктивы ( n = 1), костный мозг ( n = 3) и биопсия кожи ( n = 2).
Таблица 1
Характеристики 85 взрослых реципиентов крови и трансплантатов костного мозга, перенесших аденовирусные инфекции.
Таблица 1
Характеристики 85 взрослых реципиентов крови и трансплантатов костного мозга, перенесших аденовирусные инфекции.
Девять пациентов (10%) имели бессимптомную вирусурию, которая была обнаружена в период, когда проводились контрольные посевы мочи на ЦМВ от реципиентов аллогенной BMT. У двоих из этих пациентов была активная РТПХ на момент проведения посева. У семи пациентов был один эпизод, а у 2 пациентов — 2 эпизода.
Среди 76 пациентов с симптоматическими инфекциями у 6 (8%) было определенное инвазивное заболевание, а у 70 (92%) — вероятное инвазивное заболевание.У всех 3 пациентов, которые умерли и подверглись вскрытию, диагноз инвазивной аденовирусной инфекции был подтвержден. Симптоматические инфекции проявлялись в виде заболевания верхних дыхательных путей ( n = 20), энтерита ( n = 18), пневмонии ( n = 15), цистита ( n = 10), диссеминированного заболевания без пневмонии ( n = 8) и диссеминированное заболевание с пневмонией ( n = 5).
Среди пациентов, у которых не было сопутствующих инфекций, средняя продолжительность симптомов составляла 8 дней для пациентов с инфекцией верхних дыхательных путей (URI; диапазон от 3 до 21 дня), 21 день для пациентов с пневмонией (диапазон от 12 до 46 дней). дней), 23 дня для тех, у кого был энтерит (диапазон, 7–44 дня), 26 дней для тех, кто имел геморрагический цистит (диапазон, 10–49 дней), 40 дней для тех, кто имел диссеминированное заболевание без пневмонии (диапазон, 13 –68 дней) и 60 дней для тех, кто имел диссеминированное заболевание с пневмонией (диапазон 27–104 дней).Следует отметить, что только у 2 из 20 пациентов с пневмонией изначально были признаки и симптомы ИВДП.
Частота различных клинических синдромов (за исключением бессимптомной вируса) у 60 реципиентов аллогенной BMT по сравнению с таковой у 16 реципиентов аутологичной BMT была следующей: URI, 28% против 19%; энтерит — 22% против 31%; пневмония — 18% против 25%; геморрагический цистит 10% против 25%; и диссеминированное заболевание — 22% против 0% соответственно. Статистически значимой разницы не наблюдалось, за исключением диссеминированного заболевания ( P =.03).
13 пациентов с диссеминированным заболеванием имели сочетание ≥2 следующих диагнозов: энтерит ( n = 10), геморрагический цистит ( n = 9), URI ( n = 6), пневмония (). n = 5), гепатит ( n = 1) и конъюнктивит ( n = 1). У 3 пациентов вирус был выделен из образцов костного мозга, а у 2 пациентов — из кожных образований (гистологическое исследование выявило неспецифическое воспаление).У шести пациентов с диссеминированным заболеванием были биохимические признаки гепатита; только 1 пациенту была сделана биопсия печени; анализ биоптатов подтвердил диагноз инвазивной аденовирусной инфекции.
Все 13 пациентов с диссеминированным заболеванием были реципиентами аллогенного BMT, а 11 (85%) имели GVHD. Все 13 пациентов получали терапию как минимум двумя иммунодепрессантами, включая циклоспорин А ( n = 9), метилпреднизолон ( n = 12) и такролимус ( n = 7).Среди 56 реципиентов аллогенной BMT с локализованным заболеванием 27 (48%) имели РТПХ и 28 (50%) получали терапию как минимум 2 иммунодепрессантами, включая циклоспорин A ( n = 20), метилпреднизолон ( n = 39) и такролимус ( n = 16). Продолжительность выделения вируса была больше у пациентов с диссеминированной инфекцией, чем у пациентов с локализованным заболеванием (средняя продолжительность, 33 против 9 дней, соответственно). Однако последующие культуры не получали единообразно.
Одномерный анализ показал, что аллогенные трансплантаты ( P = 0,049), GVHD ( P = 0,0023) и использование метилпреднизолона ( P = 0,022), циклоспорина A ( P = 0,005). ) и такролимус ( P = 0,02) были связаны с диссеминацией. Поскольку эти переменные были взаимосвязаны, для реципиентов аллогенных трансплантатов был проведен многомерный анализ. GVHD (OR, 6,23; 95% CI, 1,2–34,2; P = 0,01) и лечение ≥2 иммунодепрессантами (OR, 74.0; 95% ДИ, 44,9–122; P <0,001) были связаны с распространением по модели пошаговой логистической регрессии (соответствие данных Хосмера-Лемешоу, 0,96).
Уровни смертности, связанные с различными клиническими синдромами, приведены в таблице 2. Общий уровень смертности пациентов с симптоматическим заболеванием составил 26% (20 из 76 пациентов). Распространенное заболевание без пневмонии, изолированная пневмония и распространенное заболевание с пневмонией были связаны с самыми высокими показателями смертности: 50% (4 из 8 пациентов), 73% (11 из 15) и 80% (4 из 5), соответственно.Один пациент с подтвержденным биопсией аденовирусным энтеритом умер от тяжелого кишечного кровотечения без какой-либо другой очевидной этиологии. Не удалось определить, способствовал ли аденовирус смерти еще 5 пациентов с энтеритом. Смертных случаев среди пациентов с изолированным URI или геморрагическим циститом не наблюдалось. Коинфекции с потенциально летальными организмами были выявлены у 6 пациентов с пневмонией и у 1 пациента с диссеминированным заболеванием, у которого также была пневмония.
Таблица 2
Смертность, связанная с различными клиническими проявлениями аденовирусных инфекций у взрослых реципиентов крови и трансплантатов костного мозга.
Таблица 2
Смертность, связанная с различными клиническими проявлениями аденовирусных инфекций у взрослых реципиентов крови и трансплантатов костного мозга.
Смертность среди реципиентов аутологичной ТКМ была связана только с изолированной пневмонией, поскольку не было случаев диссеминированного заболевания. Трое из 4 больных аденовирусной пневмонией умерли. Эти 3 пациента включали 2 пациентов с раком молочной железы, один из которых имел сопутствующую ЦМВ-пневмонию, и 1 пациент с рецидивом острого миелогенного лейкоза, который лечился флударабином и имел сопутствующую пневмонию ЦМВ и Pneumocystis carinii .
Лечение 13 пациентов включало внутривенное введение рибавирина ( n = 12) и / или рибавирин в форме аэрозоля ( n = 4). Клиническое улучшение наблюдалось только у 2 пациентов, получавших рибавирин внутривенно (таблица 3). У одного пациента с острым промиелоцитарным лейкозом, который получил аллогенную ТКМ и у которого развилась РТПХ, потребовавшая лечения циклоспорином А и метилпреднизолоном, был диагностирован аденовирусный геморрагический цистит и пневмония. Клиническое улучшение наступило после 9 дней внутривенной терапии рибавирином и завершился 3-недельный курс терапии.У второго пациента, которому была проведена аллогенная ТКМ для лечения хронического лимфолейкоза и профилактики РТПХ циклоспорином А и метилпреднизолоном, были диагностированы аденовирусный энтерит, пневмония и гепатит. Он прошел 2 курса лечения рибавирином внутривенно (продолжительность 2 и 3 недели, соответственно), и у него было клиническое улучшение после 6 и 15 дней терапии, соответственно. Решение о проведении второго курса лечения было вызвано рецидивом его симптомов после отмены первого курса.Эти 2 пациента получали лечение раньше после появления симптомов (среднее время до лечения, 5 дней против 35 дней) и в течение более длительного периода (средняя продолжительность терапии, 28 дней против 9 дней), чем леченные пациенты, которые не лечились. есть улучшение. Однако у 3 из 5 пациентов с диссеминированным заболеванием, которые не получали терапию рибавирином, также наблюдалось улучшение.
Таблица 3
Клинические результаты среди пациентов, получавших и не получавших рибавирин внутривенно.
Таблица 3
Клинические исходы среди пациентов, получавших и не получавших рибавирин внутривенно.
Обсуждение
Роль аденовирусов в заболеваемости и смертности реципиентов BMT получает все большее признание. В настоящем исследовании общая частота аденовирусных инфекций у взрослых реципиентов BMT составила 3%. Вероятно, это недооценка истинного уровня заболеваемости, поскольку диагностические тесты не применялись систематически ко всем реципиентам BMT. Аденовирусные инфекции были обнаружены у значительно более высокой доли взрослых реципиентов аллогенных BMT, чем взрослых реципиентов аутологичных BMT (6% vs.0,92%; P <0,001). В некоторой степени это может отражать более интенсивный мониторинг вирусных инфекций среди реципиентов аллогенной BMT.
Наблюдался широкий спектр клинических проявлений, от бессимптомных инфекций (у 10% пациентов) до локализованного заболевания (у 75%) и диссеминированного заболевания (у 15%). Локализованное заболевание (за исключением бессимптомной вируса) проявляется, прежде всего, в виде респираторных инфекций (у 56% пациентов), желудочно-кишечных инфекций (у 28%) и инфекций мочевыводящих путей (у 16%).Распространенное заболевание проявляется как комбинация этих синдромов плюс гепатит или конъюнктивит. Общая смертность среди пациентов с симптоматическим заболеванием составила 26%, главным образом, из-за пневмонии и диссеминированного заболевания. Относительно низкая частота (8%) подтвержденного инвазивного заболевания, вероятно, была недооценкой, поскольку инвазивные диагностические процедуры часто были противопоказаны. В 5 других исследованиях, в которых участвовали как дети, так и взрослые реципиенты BMT, частота подтвержденного инвазивного заболевания находилась в диапазоне 8–26% [3–6, 18].
Тип трансплантации (аллогенная или аутологичная), наличие РТПХ (II – IV степени) и интенсивность иммуносупрессивного лечения были переменными, которые повлияли на клиническую картину и исход. У реципиентов аутологичного BMT развились те же типы локализованного заболевания, что и у реципиентов аллогенного BMT, но у них не развилось диссеминированное заболевание. Напротив, у 13 (22%) из 60 симптоматических реципиентов аллогенного трансплантата развилось диссеминация. Среди 13 пациентов с диссеминированным заболеванием у 11 (85%) была РТПХ, и все получали агрессивную иммуносупрессивную терапию.Предыдущие исследования также определили РТПХ как фактор риска распространения [3, 4]; однако это первое исследование, показывающее, что интенсивность иммуносупрессивной терапии, выраженная в количестве используемых препаратов, имела независимый вклад в риск распространения.
Широкий спектр клинических проявлений аденовирусных инфекций подчеркивает важность получения образцов для анализа на вирус от реципиентов BMT с совместимыми клиническими синдромами. Хотя обычные вирусные культуры остаются стандартным средством диагностики, для выделения вируса может потребоваться несколько дней.Сообщается, что более новые методы, включая ПЦР-анализ, культивирование из скорлупы и иммунохроматографические методы, обеспечивают более быструю диагностику с разумной чувствительностью и специфичностью [20, 21].
Не существует установленной противовирусной терапии аденовирусных инфекций. Сообщалось об успешном лечении изолированного геморрагического цистита, нефрита, энтерита и пневмонита внутривенным введением рибавирина [22–27]. Однако также сообщалось о неудачах лечения [28–30]. В настоящем исследовании использование рибавириновой терапии не было связано с заметной пользой.Клиническое улучшение наблюдалось у 2 (17%) из 12 пациентов, получавших рибавирин внутривенно, по сравнению с 18 (41%) из 44 пациентов, которые имели аналогичные клинические проявления, но не получали рибавирин. Среди пациентов с диссеминированным заболеванием, у которых тяжесть заболевания была более однородной, клиническое улучшение наблюдалось у 2 из 8 пациентов, получавших рибавирин, и у 3 из 5 пациентов, не получавших рибавирин. У двух пациентов развился гемолиз при внутривенном введении рибавирина; лечение рибавирином было прекращено у 1 пациента.
Цидофовир, противовирусный агент широкого спектра действия, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США для лечения ЦМВ-ретинита у пациентов со СПИДом, как сообщалось, эффективен против аденовирусов in vitro и был связан с благоприятным исходом в двух недавних сообщения о случаях тяжелого аденовирусного заболевания у пациентов с ослабленным иммунитетом [31, 32]. К сожалению, токсичность этого препарата значительна.
Таким образом, аденовирусы могут вызывать широкий спектр проявлений у взрослых реципиентов BMT; эти проявления варьируются от бессимптомного выделения до локально инвазивного и диссеминированного заболевания, которое часто заканчивается летальным исходом.Эти инфекции следует включать в дифференциальную диагностику широкого спектра клинических синдромов, включая ИВЗН, пневмонию, энтерит, гепатит, геморрагический цистит, конъюнктивит и диссеминированное заболевание. Самые высокие показатели смертности наблюдались среди пациентов с пневмонией и диссеминированным заболеванием. Смертельная аденовирусная пневмония произошла как у аутологичных, так и у аллогенных реципиентов BMT; однако диссеминированное заболевание встречалось только у реципиентов аллогенного BMT, особенно у пациентов с GVHD, получавших иммуносупрессивную терапию.Очевидна необходимость в эффективной нетоксичной терапии.
Список литературы
1,,. ,,.Аденовирусы
,Клиническая вирусология
,1997
Нью-Йорк
Черчилль Ливингстон
(стр.525
—47
) 2.Аденовирусы в организме хозяина с ослабленным иммунитетом
,Clin Microbiol Rev
,1992
, vol.5
(стр.262
—74
) 3,,,,.Аденовирусные инфекции у пациентов, перенесших трансплантацию костного мозга
,N Engl J Med
,1985
, vol.312
(стр.529
—33
) 4« и др.Рост заболеваемости аденовирусом при трансплантации костного мозга
,J Infect Dis
,1994
, vol.169
(стр.775
—81
) 5« и др.Аденовирусная инфекция после трансплантации костного мозга детям
,Трансплантация костного мозга
,1999
, т.23
(стр.277
—82
) 6« и др.Эволюционирующие патогены при аллогенной трансплантации костного мозга: увеличение летальных аденовирусных инфекций
,Am J Med
,1995
, vol.99
(стр.326
—8
) 7,,.Распространенная аденовирусная болезнь у детей с ослабленным иммунитетом и иммунокомпетентными
,Clin Infect Dis
,1998
, vol.27
(стр.1194
—200
) 8,,,,.Распространенная аденовирусная инфекция у хозяина с ослабленным иммунитетом
,Am J Med
,1987
, vol.83
(стр.555
—9
) 9« и др.Геморрагический цистит, связанный с аденовирусной инфекцией при трансплантации костного мозга
,Arch Intern Med
,1986
, vol.146
(стр.1400
—1
) 10,,, et al.Геморрагический цистит, связанный с экскрецией аденовируса 11 типа с мочой после аллогенной трансплантации костного мозга
,Трансплантация костного мозга
,1989
, т.4
(стр.533
—5
) 11,,,,.Некротический тубулоинтерстициальный нефрит, связанный с аденовирусной инфекцией
,Hum Pathol
,1991
, vol.22
(стр.1225
—31
) 12,.Геморрагический цистит, вызванный аденовирусной инфекцией после трансплантации костного мозга
,J Urol
,1994
, vol.151
(стр.1013
—4
) 13« и др.Острая почечная недостаточность и дегенеративные поражения канальцев, связанные с образованием аденовирусных иммунных комплексов in situ у пациента с аллогенной трансплантацией костного мозга
,Трансплантация
,1993
, vol.55
(стр.67
—72
) 14« и др.Высокая частота геморрагического цистита, вызванного адено- и полиомавирусами, при аллотрансплантации костного мозга по поводу гематологического злокачественного новообразования после истощения Т-клеток и циклоспорина
,Трансплантация костного мозга
,1998
, vol.22
(стр.889
—93
) 15,,,,.Диффузное изъязвление кишечника после трансплантации костного мозга
,Hum Pathol
,1986
, vol.17
(стр.621
—33
) 16,,,,.Аденовирус в желудочно-кишечном тракте пациентов с ослабленным иммунитетом
,Am J Clin Pathol
,1992
, vol.97
(стр.555
—8
) 17,,,,.История болезни: фульминантный аденовирусный гепатит после аллогенной трансплантации костного мозга
,Трансплантация костного мозга
,1996
, vol.17
(стр.295
—8
) 18,,, et al.Аденовирусные инфекции у реципиентов трансплантата гемопоэтических стволовых клеток
,Clin Infect Dis
,1999
, vol.29
(стр.1494
—501
) 19,,,,.ПЦР-определение аденовируса у реципиента трансплантата костного мозга: геморрагический цистит как проявление диссеминированного заболевания
,J Clin Microbiol
,1999
, vol.37
(стр.686
—9
) 20,,, et al.Иммунохроматографический тест для экспресс-диагностики аденовирусных инфекций дыхательных путей: сравнение с выделением вируса в культуре ткани
,J Clin Microbiol
,1999
, vol.37
(стр.2007
—9
) 21,,,,.Эффективность ПЦР и других методов диагностики для выявления респираторных аденовирусных инфекций
,J Med Virol
,1999
, vol.59
(стр.66
—72
) 22.История болезни: внутривенная терапия рибавирином аденовирусного цистита после аллогенной трансплантации костного мозга
,Трансплантация костного мозга
,1991
, vol.7
(стр.247
—8
) 23,,,,.Тяжелый аденовирусный нефрит после трансплантации костного мозга: успешное лечение рибавирином внутривенно
,Пересадка костного мозга
,1993
, vol.12
(стр.409
—12
) 24,,,.Аденовирус-ассоциированный геморрагический цистит, леченный рибавирином внутривенно
,Дж Урол
,1993
, т.149
(стр.565
—6
) 25,,,,,.Внутривенная терапия рибавирином аденовирусного гастроэнтерита после трансплантации костного мозга
,J Pediatr Gastroenterol Nutr
,1995
, vol.21
(стр.110
—2
) 26,,,,.Аденовирус-ассоциированный геморрагический цистит после трансплантации костного мозга, успешно вылеченный внутривенным рибавирином
,Трансплантация костного мозга
,1995
, vol.15
(стр.651
—2
) 27,,,,,.Аденовирусный пневмонит успешно лечится рибавирином внутривенно
,Haematologica
,1998
, vol.83
(стр.1128
—9
) 28« и др.Неспособность рибавирина устранить аденовирусные инфекции при аллогенной трансплантации костного мозга с истощением Т-лимфоцитов
,Трансплантация костного мозга
,1994
, vol.14
(стр.663
—6
) 29,,,.Фульминантный аденовирусный гепатит после неродственной трансплантации костного мозга: неэффективность внутривенной терапии рибавирином
,Трансплантация костного мозга
,1999
, vol.23
(стр.1209
—11
) 30,,,.Неудача внутривенного введения рибавирина в лечении инвазивной аденовирусной инфекции после аллогенной трансплантации костного мозга: история болезни
,J Infect
,1998
, vol.36
(стр.227
—8
) 31,,,,.Успешное лечение аденовирусной болезни цидофовиром внутривенно у неродственного реципиента трансплантата стволовых клеток
,Clin Infect Dis
,1999
, vol.28
(стр.690
—1
) 32,,,.Аденовирусный холецистит у больного СПИДом
,Clin Infect Dis
,1998
, vol.26
(стр.997
—9
)© 2001 Американское общество инфекционных болезней
Аденовирус (для родителей) — Advocate Aurora Health
Что такое аденовирусы?
Аденовирусы — это группа из
вирусов, которые могут инфицировать мембраны (слизистые оболочки):Что такое аденовирусные инфекции?
Аденовирусы являются частыми причинами лихорадки и таких заболеваний, как:
Аденовирусные (add-eh-noe-VY-rus) инфекции обычно протекают в легкой форме, но могут возникать серьезные инфекции.У младенцев и людей со слабой иммунной системой больше шансов иметь серьезные проблемы. Некоторые типы вируса связаны с более тяжелым заболеванием.
Кто заражается аденовирусными инфекциями?
Аденовирусные инфекции могут поражать детей любого возраста. Но они чаще встречаются у младенцев и маленьких детей. Большинство детей перенесли хотя бы одну аденовирусную инфекцию в возрасте до 10 лет. Существует много различных типов аденовирусов, поэтому люди могут иметь более одной аденовирусной инфекции.
Аденовирусные инфекции могут возникнуть в любое время года.
Каковы признаки и симптомы аденовирусных инфекций?
Симптомы аденовирусных инфекций зависят от типа аденовируса и пораженной части тела. Респираторные симптомы встречаются чаще всего.
Инфекции верхних дыхательных путей могут варьироваться от легких симптомов простуды до симптомов, похожих на грипп. К ним относятся:
Аденовирусы могут также вызывать инфекций нижних дыхательных путей , таких как бронхиолит, круп или пневмония. Аденовирус может вызывать кашель, похожий на коклюш.
Гастроэнтерит — это инфекция желудка и кишечника. Симптомы включают диарею, рвоту, боль в животе и лихорадку.
Инфекции мочевого пузыря: Они могут вызывать частое мочеиспускание, жжение, боль и кровь в моче.
Инфекции глаз:
- Конъюнктивит (конъюнктивит) — легкое воспаление оболочек, покрывающих глаз, и внутренние поверхности век. Симптомы включают покраснение глаз, выделения, слезотечение и ощущение, что что-то попало в глаз.
- Фарингоконъюнктивальная лихорадка вызывает очень красные глаза, боль в горле, лихорадку, насморк и опухшие железы.
- Кератоконъюнктивит — более серьезная инфекция глаза, поражающая как конъюнктиву, так и роговицу (прозрачную переднюю часть глаза). Это вызывает покраснение глаз, светобоязнь (чувствительность к свету), нечеткое зрение, слезотечение и боль.
Инфекции нервной системы:
- Менингит и энцефалит иногда могут возникать из-за аденовирусной инфекции.Симптомы включают жар, головную боль, тошноту и рвоту, ригидность шеи и спутанность сознания.
Аденовирус заразен?
Аденовирус очень заразен. Инфекции распространены в местах с близким контактом, таких как детские сады, школы, больницы и летние лагеря.
Аденовирус может передаваться воздушно-капельным путем при кашле или чихании инфицированного человека. Фекалии (фекалии) могут распространять инфекцию через загрязненную воду, грязные подгузники и плохое мытье рук. Вспышки фарингоконъюнктивальной лихорадки в летних лагерях связаны с загрязненной водой в бассейнах и озерах.
Ребенок также может заразиться вирусом, прикоснувшись к человеку, у которого он есть. Аденовирусы могут выживать на поверхности в течение длительного времени. Таким образом, они могут распространяться на зараженные игрушки, полотенца и другие предметы.
Симптомы обычно появляются от 2 дней до 2 недель после контакта с аденовирусом.
Как диагностируются аденовирусные инфекции?
Симптомы аденовирусной инфекции похожи на симптомы многих других инфекций. Если у человека серьезная инфекция, врачи могут проверить выделения из дыхательных путей или конъюнктивы, образец стула или кровь или мочу для подтверждения диагноза.
Врачи также будут проверять на аденовирус во время подозреваемых вспышек. (Вспышка — это когда у многих людей появляются одни и те же симптомы.)
Как лечат аденовирусные инфекции?
Большинство аденовирусных инфекций проходят сами по себе. Лечение в домашних условиях включает в себя достаточный отдых, употребление достаточного количества жидкости и использование ацетаминофена для лечения лихорадки. Младенцам и детям с рвотой и диареей, которые не могут пить достаточно жидкости, может потребоваться лечение от обезвоживания.
Младенцам (особенно новорожденным и недоношенным), людям со слабой иммунной системой, а также здоровым детям и взрослым с тяжелыми аденовирусными инфекциями могут потребоваться противовирусные препараты и лечение в больнице.Другое лечение, в зависимости от симптомов, может включать внутривенное введение жидкости, кислород и дыхательные процедуры.
Противовирусные препараты для аденовирусов человека
Фармацевтические препараты (Базель). Октябрь 2010 г .; 3 (10): 3343–3354.
Школа биомедицинских наук, Лаборатория геномики человека Краучера, Китайский университет Гонконга, Шатин, штат Нью-Йорк, Гонконг
Поступило 2 сентября 2010 г .; Пересмотрено 23 октября 2010 г .; Принято 25 октября 2010 г.
Авторские права © 2010, авторы; лицензиат MDPI, Базель, Швейцария.Abstract
В разработке нового лекарства от вирусной инфекции много этапов, и такие процессы для аденовируса еще больше усложняются тем фактом, что существует не менее 51 серотипа, образующих шесть отдельных групп (A – F) с разными степень заразности. В этом обзоре делается попытка рассмотреть важность разработки фармацевтических препаратов для лечения аденовируса, а также проанализировать недавние разработки в области открытия лекарственных средств для лечения аденовирусов, включая новые стратегии, такие как подходы к использованию микроРНК.Также будут обсуждены различные стратегии скрининга на наркотики.
Ключевые слова: аденовирус, фармацевтические препараты, микроРНК
Введение
Человеческие аденовирусы считаются инфекционными агентами, вызывающими множество заболеваний, включая инфекции дыхательных путей, заболевания глаз и желудочно-кишечного тракта [1]. Аденовирусы обычно вызывают легкие, самоограничивающиеся респираторные заболевания, в первую очередь у детей, из-за нормальных реакций хозяина, которые включают естественный врожденный иммунный ответ, включающий индукцию цитокинов и активацию эффекторных лейкоцитов [2]; однако сообщалось о потенциально смертельном диссеминированном заболевании у пациентов с сильно ослабленным иммунитетом, особенно у детей-реципиентов трансплантата костного мозга.Лечение таких вирусных инфекций непросто, поскольку большинство вирусных инфекций и антивирусных исследований сталкиваются с такими проблемами, как сильно отличающиеся различия штаммов, вызывающие похожие заболевания. В настоящее время протокол лечения, одобренный Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), не используется для лечения аденовирусной инфекции, а также отсутствуют какие-либо проспективные рандомизированные контролируемые испытания потенциально полезных антиаденовирусных препаратов, хотя некоторые противовирусные препараты использовались у определенных пациентов, например.г. цидофовир используется в качестве противовирусного агента широкого спектра действия [3,4,5,6] или в качестве инфузии донорских лейкоцитов в качестве терапии опасных для жизни аденовирусных инфекций после трансплантации костного мозга с истощением Т-лимфоцитов [7].
Биология и структура аденовируса
Аденовирус — это дцДНК-вирус без оболочки. Существует не менее 51 серотипа аденовируса человека, которые классифицируются на шесть групп (от A до F) на основе их биохимических, иммунологических и морфологических критериев. Аденовирусы имеют размер от 90 до 100 нм, а их структура состоит из икосаэдрического капсида, который состоит из трех основных компонентов: гексона, расположенного на гранях и краях капсида; пентоновое основание, расположенное на 12-ти пятикратных вершинах; тонкие волокна прикреплены к основе пентона.(). Другие второстепенные компоненты: IIIa, VI, VIII и IX также связаны с капсидом. Внутри капсида находится протеаза вириона, которая играет жизненно важную роль в сборке вириона и двухцепочечного генома ДНК, связанного с пятью полипептидами (концевой белок (TP), V, VII, Mu и IVa2).
Структура аденовируса.
Инфекция аденовирусом начинается со связывания волокон со специфическим рецептором на поверхности клетки. Основание пентона взаимодействует с поверхностным белком и интегринами , которые стимулируют проникновение вируса в клетку посредством эндоциктоза.Подкисление эндосомы высвобождает вирион в цитоплазму, а вирион мигрирует в ядро. Внутри ядра частицы аденовируса разбираются, высвобождая вирусную ДНК для репликации вируса.
Цикл репликации аденовируса делится на две стадии: раннюю фазу и позднюю фазу. На ранней стадии экспрессируются регуляторные белки, которые активируют другие вирусные гены, предотвращают преждевременную гибель инфицированных клеток и изменяют экспрессию белков-хозяев для синтеза ДНК.Как только компоненты для репликации ДНК готовы, можно начинать позднюю фазу. Сильный главный поздний промотор (MLP) опосредует транскрипцию поздних вирусных генов, которые кодируют структурные белки вируса и белки для созревания вирусных частиц. Вирус собирается в свой вирион и высвобождается для заражения других клеток посредством лизиса клеток, индуцированного вирусом. обобщил цикл заражения аденовирусом. а подробности репликации аденовируса можно найти в обзоре Рассела [8].
Путь заражения и репликации аденовируса.
Обоснование лечения
Аденовирусная инфекция обычно встречается у иммунокомпетентных людей. В зависимости от инфекционных серотипов инфекция может вызывать различные заболевания, такие как заболевания дыхательных путей, гастроэнтерит, конъюнктивит и геморрагический цистит. Симптомы этих болезней обычно легкие и в большинстве случаев поддаются лечению. Однако в редких случаях могут наблюдаться тяжелые заболевания, такие как гепатит, миокардит и нефрит [9]. Если возникает глазная инфекция, аденовирус может даже вызвать эпидемический кератоконъюнктивит (EKC), что приведет к снижению остроты зрения [10].
У пациентов с ослабленным иммунитетом, таких как реципиенты трансплантатов гемопоэтических стволовых клеток (ТГСК) и пациенты с ВИЧ, аденовирусная инфекция может легко привести к смерти. Установлено, что в ретроспективных исследованиях пациентов, перенесших трансплантацию, реципиенты трансплантата костного мозга имеют высокий риск аденовирусной болезни, особенно при применении алемтузумаба для педиатрических пациентов, получающих трансплантаты стволовых клеток от альтернативных доноров [11,12,13]. Пациенты с болезнью трансплантат против хозяина (РТПХ), истощением трансплантата Т-клетками и получением трансплантата неродственного донора также подвержены высокому риску аденовирусной инфекции [14].Кроме того, риск для педиатрических пациентов в три раза выше, чем для взрослых [15].
Помимо смертельных инфекций, аденовирус может также мешать медикаментозному лечению и генной терапии. Было показано, что инфекции и нормальная флора у нечеловеческих приматов отрицательно влияют на эффективность разработки лекарств [16]. Точно так же можно представить, что у людей аденовирус также может влиять на введение лекарств, а именно на дозировку и протоколы лечения. Для генной терапии, предполагающей использование аденовируса в качестве вектора, ранее существовавшая инфекция может привести к снижению эффективности, а иногда тяжелая реакция иммунной системы может привести к отказу нескольких органов [17].У пациентов с муковисцидозом, получающих генную терапию с использованием аденовируса в качестве векторов, были проведены многочисленные исследования по нейтрализации антител против аденовируса с целью снижения воздействия уже существующего аденовируса [18].
Недавно аденовирус 36 был связан с ожирением у человека. Обследование, проведенное в трех штатах США (Нью-Йорк, Мэдисон, Висконсин и Неаполь, Флорида), показало более высокую распространенность антител к аденовирусу-36 у лиц с ожирением по сравнению с лицами, не страдающими ожирением [19]. Во всей популяции антитела-положительные люди были на 9 единиц ИМТ тяжелее, чем антитела-отрицательные люди [20].Эти данные подтверждаются результатами пар близнецов, не согласующихся с антителами к аденовирусу-36, где положительные по антителам близнецы были немного, но значительно тяжелее и толще, чем их сверстники с отрицательными антителами [20]. Таким образом, возможно, что метаболические синдромы, вызванные ожирением, можно лечить с помощью антиаденовирусной терапии.
Современные противовирусные препараты
Хотя аденовирусы выявлялись в течение многих лет, не существует одобренного FDA препарата для лечения аденовирусной инфекции человека. В настоящее время только два противовирусных препарата, а именно цидофовир и рибавирин, используются в терапии аденовирусов первой линии.
Цидофовир
Цидофовир [( S ) -HPMPC; ( S ) -1- (3-гидрокси-2-фосфонилметоксипропил) цитозин)] представляет собой ациклический нуклеозидфосфонат, который проявляет противовирусную активность против ДНК-вирусов [21]. Он ингибирует репликацию ADV, независимо от серотипа, действуя как монофосфатная форма нуклеотида. При фосфилировании клеточными киназами соединения активируются и становятся аналогами 2’-дезоксирибонуклеозид-5’-трифосфатов (dNTP). Вирусные ДНК-полимеразы связываются с аналогами, что мешает процессу репликации вируса.Это направленное действие цидофовира подтверждается выделением устойчивых к цидофовиру мутантов аденовируса, которые содержат различные последовательности вблизи консервативного сайта связывания нуклеотидов аденовирусных ДНК-полимераз [22].
Рибавирин
Рибавирин — противовирусное средство широкого спектра действия, проявляющее активность в отношении аденовирусных инфекций. Как и цидофовир, рибавирин является аналогом нуклеозидов, но вопрос о том, является ли его мишень действия такой же, как у вирусных ДНК-полимераз, все еще остается спорным. Другие предлагаемые механизмы включают прямое ингибирование аденовирусной инфекции путем иммуномодуляции или истощения пулов внутриклеточного гуанозинтрифосфата и косвенное ингибирование путем вмешательства в кэппирование РНК или индукцию мутации [23].Хотя рибавирин является противовирусным агентом широкого спектра действия, исследование in vitro у пациентов с ТГСК показало, что эффективность рибавирина ограничена только аденовирусной инфекцией вида C. [24].
Эффективность, подтвержденная клиническими исследованиями
Цидофовир
Цидофовир прошел клинические испытания и одобрен в качестве препарата для лечения ЦМВ-ретинита у больных СПИДом. Ряд клинических исследований уже показал эффективность цидофовира для лечения острого аденовирусного кератоконъюнктивита [25,26].В дополнение к глазной аденовирусной инфекции ретроспективные исследования у пациентов с иммунодефицитом также показали эффективность против аденовирусной инфекции [27,28,29]. В сочетании с другими антиаденовирусными препаратами, например При терапии ВВИГ был получен более обнадеживающий результат [30], но индивидуальную эффективность цидофовира оценить сложно. В большинстве исследований эффективность была выше, когда лечение применялось раньше после постановки диагноза аденовирусной инфекции [31]. Хотя цидофовир является эффективным антиаденовирусным препаратом, после приема цидофовира наблюдались серьезные побочные эффекты со стороны ЦНС и токсичность для сетчатки [32].
Рибавирин
Хотя цидофовир показал эффективность против аденовирусной инфекции, при лечении рибавирином у пациентов, инфицированных аденовирусом, наблюдались противоречивые результаты. В некоторых отчетах о случаях рибавирин успешно лечил пациентов с иммунодефицитом с аденовирусной инфекцией [33,34,35]. Однако, когда были проведены более крупномасштабные исследования, значительной эффективности не наблюдалось [36]. Этот противоречивый результат можно объяснить избирательной эффективностью в отношении серотипов аденовирусов. По сравнению с цидофовиром рибавирин обладает меньшей токсичностью и меньшими побочными эффектами у пациентов.
Противовирусные препараты, которые в настоящее время проходят клинические испытания
CMX001
CMX001 (Химерикс, 3-гексадецилокси-1-пропанолцидофовир), представляет собой липидный конъюгат цидофовира, который разрабатывается как противовирусный препарат. Он проявляет противовирусную активность против всех двухцепочечных ДНК-вирусов, включая аденовирусы 3, 5, 7, 8, 31 [37]. Это лекарство вводится перорально и предназначено для прохождения через стенку кишечника и проникновения в клетку-мишень перед расщеплением с высвобождением цидофовира для его действия.Результат фазы I клинического испытания проиллюстрировал пероральную биодоступность CMX001 для людей и продемонстрировал положительный профиль безопасности (идентификатор ClinicalTrials.gov: {«type»: «клиническое испытание», «attrs»: {«text»: «NCT00780182» , «term_id»: «NCT00780182»}} NCT00780182). Другое исследование показало, что CMX001 обладает более высокой противовирусной активностью, чем цидофовир, с меньшей токсичностью для пациентов [38]. В настоящее время препарат изучается в Фазе II, в ходе которой исследуется его эффективность у пациентов с иммунодефицитом и ЦМВ-инфекцией (ClinicalTrials.gov Идентификатор: {«тип»: «клиническое испытание», «attrs»: {«текст»: «NCT00942305», «term_id»: «NCT00942305»}} NCT00942305).
Потенциальные противовирусные препараты
Многие исследования показывают, что различные соединения и молекулы обладают антиаденовирусной активностью, которая может быть преобразована в сильнодействующие препараты против аденовируса.
DHEA и аналог эпиандростерона (EA)
DHEA, EA и два синтетических производных проявляют антиаденовирусную активность, аналогичную цидофовиру. Исследование показало, что эти стероидные соединения ингибируют синтез и репликацию аденовирусного белка с индексами селективности от 42 до 83 [39].
Комплексы переходных металлов
[Co (NH 3 ) 6 ] Cl 3 , комплекс переходных металлов, представляет собой противовирусное соединение широкого спектра действия против вируса Синдбис. Из-за своей высокой плотности положительного заряда металлический комплекс прочно связывается с отрицательно заряженными нуклеотидами и вызывает конденсацию вирусной дцДНК в тороидальную надстройку, нарушая процесс упаковки вирусной ДНК. Исследование Knight et al . показали, что в присутствии [Co (NH 3 ) 6 ] Cl 3 клетки, инфицированные аденовирусом, выживали лучше, а вирусная экспрессия инфицированных клеток снижалась, демонстрируя, что [Co (NH 3 ) 6 ] Cl 3 обладает противовирусной активностью по отношению к аденовирусу [40].
Биспецифические моноклональные антитела
Двусторонняя структура MAb позволяет исследователям помещать терапевтический агент на одну руку, в то время как другая рука целенаправленно нацелена на очаг заболевания. Эта уникальная структура имеет большие перспективы для решения множества терапевтических задач, включая аденовирусную инфекцию. При использовании МАт аденовирусная генная терапия может снизить токсичность за счет снижения применяемой дозы аденовируса [41].
Камптотецин (CPT)
Было показано, что противораковое лекарственное средство камптотецин (CPT) является мощным ингибитором репликации, транскрипции и упаковки аденовирусов, содержащих двухцепочечную ДНК.Он связывается с топоизомеразой II, ферментом клетки-хозяина, необходимым для инициации и завершения вирусных функций, и таким образом предотвращает репликацию вируса [42].
Водорастворимый полимерный комплекс Арбидола
Арбидол — отечественное противовирусное средство, обладающее противовирусным действием широкого спектра действия. Он подавляет слияние липидной оболочки вируса с мембраной эндосом, расположенных внутри клетки. Благодаря свойству нерастворимости в воде арбидол имеет низкую биодоступность и высокую токсичность. Чтобы преодолеть эти ограничения, были синтезированы водорастворимые комплексы между арбидолом и полимерными соединениями.Исследование показало, что этот комплекс обладает широкой противовирусной активностью, включая аденовирус, в то время как токсичность намного ниже, чем у немодифицированного арбидола. Таким образом, комплекс может быть полезен при разработке безопасных антиаденовирусных препаратов [43].
Ставудин
Ставудин представляет собой средство двойного действия против вируса иммунодефицита человека (ВИЧ). Он действует как аналог тимидина и фосфилируется клеточной киназой, превращаясь в ставудинтрифосфат, который прекращает синтез ДНК, встраиваясь в него.Недавние исследования показали, что ставудин избирательно ингибирует человеческий AdV5, что указывает на сильную и селективную антиаденовирусную активность. Было обнаружено, что ведущее соединение ставудина, стэмпидин, является наиболее мощным нетоксичным противовирусным средством, и оно обладало замечательной эффективностью in vitro, и / или in vivo, против чувствительного к лекарствам и устойчивого к лекарствам аденовируса. Предполагается, что стэмпидин имеет клинический потенциал как местное средство двойного действия для профилактики и / или эффективного лечения аденовируса [44].
MicroRNA
Последние достижения в наших основных знаниях о микроРНК были применены при разработке лекарств. Одна из таких стратегий заключается в клонировании сайтов связывания определенных микроРНК для снижения экспрессии вирусных генов. Исследование Cawood et al . показали, что животные, которым вводили десятикратную летальную дозу Ad5 дикого типа (5 × 1010 вирусных частиц / мышь), показали существенную репликацию печеночного генома и обширную патологию печени. Однако, если были добавлены 4 сайта связывания микроРНК, репликация генома уменьшилась в 50 раз и токсичность для печени практически исчезла.МикроРНК должна обеспечить новую стратегию разработки безопасных аттенуированных вакцин, применяемых при широком спектре вирусных заболеваний [45].
Внутривенная иммуноглобулин (ВВИГ) и Т-клеточная иммунотерапия
Внутривенный иммуноглобулин также применялся при аденовирусной пневмонии у детей, хотя терапия контролирует, но не уничтожает аденовирус, если также не проводится иммунотерапия стволовыми клетками [46,47]. Хотя рутинное использование ВВИГ является обычной практикой при таких показаниях, как аллогенная трансплантация костного мозга и первичные иммунодефициты, следует проявлять осторожность во время введения ВВИГ, поскольку побочные эффекты были зарегистрированы у 5-15% пациентов, получающих ВВИГ, и эффекты ВВИГ обычно длятся от 2 до 2 лет. недели и 3 месяца [48].Совсем недавно был описан успешный случай комбинированного применения CDV и IVIG у пациентов с трансплантатом почки с диссеминированной аденовирусной инфекцией [49].
Современные методы скрининга лекарств
Скрининг лекарств важен для открытия противовирусных соединений. Для аденовируса человека существуют различные противовирусные анализы in vitro, и большинство из них основаны на клетках, включая анализ цитопатического эффекта (измерение уменьшения бляшек) и анализ МТТ (измерение изменчивости клеток).Другие анализы, такие как ELISA, также часто используются для обнаружения присутствия аденовирусного белка для исследования цитотоксичности лекарства. Эти антивирусные анализы не стандартизированы и требуют много времени, поэтому для скрининга лекарств все чаще используются другие новые методы.
Новые методы скрининга лекарств
Метод ОТ-ПЦР
Совсем недавно был использован антивирусный анализ на основе ПЦР в реальном времени, и было показано, что это более быстрый и эффективный тест на скрининг лекарств [50]. Следует проявлять некоторую осторожность, поскольку в других анализах с ОТ-ПЦР можно показать, что 23 распространенных респираторных патогена имеют перекрестные реакции в определенных анализах (с периодической перекрестной реакцией на аденовирус при высокой дозировке> 10 (7) TCID50 / мл) [51].Благодаря использованию ПЦР в реальном времени антивирусный анализ становится быстрым, воспроизводимым и может заменить классические и более трудоемкие тесты на инфекционность.
Метод биосенсора с использованием массивов емкостных датчиков
Набор емкостных датчиков может стать новым методом скрининга противовирусных препаратов. Этот массив используется для обнаружения проникновения аденовируса через рецептор-опосредованный эндоцитоз, что также является важным процессом для доставки терапевтического гена / лекарства, нацеленного на определенный тип клеток.Путем скрининга, какие соединения действуют на тип клеток, нацеленных на аденовирус, могут быть открыты новые противовирусные препараты [52].
Метод вычислений
Биоинформатика и вычислительные методы были использованы для открытия новых фармацевтических препаратов. С помощью инструментов и программного обеспечения биоинформатики можно моделировать взаимодействия лекарство-рецептор, прогнозировать биодоступность и биоактивность лекарственного средства и иллюстрировать функциональную структуру лекарственного средства. Вычислительные методы могут быть применены в скрининге противовирусных препаратов, и недавно миметики пептида p16 (INK4a), которые ингибируют циклы вирусных клеток, были идентифицированы посредством виртуального скрининга [53].
Модель на животных
Открытию антиаденовирусных препаратов препятствовало отсутствие разрешающей иммунокомпетентной модели для исследования in vivo . Однако недавние исследования выявили многообещающую модель на животных для анализа антиаденовирусных препаратов [54]. Исследование CMX001 показало, что инфицирование человеческим аденовирусом 5 у сирийских хомяков с ослабленным иммунитетом вызывало тяжелые системные заболевания, аналогичные таковым у пациентов с иммунодефицитом [37]. Эта животная модель допускает репликацию аденовируса и, таким образом, может использоваться для тестирования эффективности антиаденовирусных препаратов.
Выводы
В заключение, существует большая потребность в разработке новых антиаденовирусных агентов, включая предотвращение смертельных заболеваний у пациентов с ослабленным иммунитетом, облегчение испытаний генной терапии с использованием аденовируса в качестве вектора и для будущего развития схемы борьбы с ожирением для тех, чье ожирение может быть связано с аденовирусом 36. Потенциальные антиаденовирусные препараты включают химические вещества, обладающие широким спектром противовирусной активности, а также некоторые новые подходы, такие как стратегии miroRNA.Эти новые лекарства можно было бы разработать дальше с помощью передовых методов скрининга лекарств, таких как биоинформатика и вычислительные методы, биосенсоры, молекулярные зонды для ПЦР, вместе с недавно разработанной моделью на животных.
Выражение признательности
Авторы выражают благодарность Бюро пищевых продуктов и здравоохранения и Исследовательскому фонду по контролю инфекционных заболеваний правительства Гонконга, ЮАР, за финансовую поддержку (RFCID-08070082).
Список литературы
1. Кинчингтон П.Р., Романовски Е.Г., Джерольд Г.Ю. Перспективы противовирусных препаратов аденовируса. J. Antimicrob. Chemother. 2005; 55: 424–429. [PubMed] [Google Scholar] 2. Муруве Д.А. Врожденный иммунный ответ на аденовирусные векторы. Гм. Gene Ther. 2004. 15: 1157–1166. [PubMed] [Google Scholar] 3. Сафрин С., Черрингтон Дж., Джаффе Х.С. Клиническое использование цидофовира. Rev. Med. Virol. 1997. 7: 145–156. [PubMed] [Google Scholar] 4. Хоффман Дж. А., Шах А. Дж., Росс Л. А., Капур Н. Аденовирусные инфекции и проспективное исследование цидофовира при трансплантации педиатрических гемопоэтических стволовых клеток.Биол. Пересадка костного мозга. 2001; 7: 388–394. [PubMed] [Google Scholar] 5. Картер Б.А., Карпен С.Дж., Кирос-Техейра Р.Э., Чанг И.Ф., Кларк Б.С., Деммлер Дж. Дж., Хеслоп Х.Э., Скотт Дж. Д., Сеу П., Госс Дж. А. Внутривенная терапия цидофовиром для диссеминированного аденовируса у педиатрических реципиентов трансплантата печени. Трансплантация. 2002; 74: 1050–1052. [PubMed] [Google Scholar] 6. Ljungman P., Ribaud P., Eyrich M., Matthes-Martin S., Einsele H., Bleakley M., Machaczka M., Bierings M., Bosi A., Gratecos N., Cordonnier C.Цидофовир для лечения аденовирусных инфекций после аллогенной трансплантации гемопоэтических стволовых клеток: исследование Рабочей группы по инфекционным заболеваниям Европейской группы трансплантации крови и костного мозга. Пересадка костного мозга. 2003. 31: 481–486. [PubMed] [Google Scholar] 7. Hromas R., Cornetta K., Srour E., Blanke C., Broun E.R. Инфузия донорских лейкоцитов как терапия угрожающих жизни аденовирусных инфекций после трансплантации костного мозга с истощением Т-клеток. Кровь. 1994; 84: 1689–1690. [PubMed] [Google Scholar] 8.Рассел В. Аденовирусы: обновленная информация о структуре и функциях. Дж. Джин. Virol. 2009; 90: 1–20. [PubMed] [Google Scholar] 9. Wold W.S.M., Horwitz M.S. Аденовирусы. В: Книп Д.М., Хоули П.М., редакторы. Области вирусологии. 7-е. Липпинкотт, Уильямс и Уилкинс; Филадельфия, Пенсильвания, Балтимор, Мэриленд, США: 2007. С. 1723–1740. [Google Scholar] 10. Ренар Г. Аденовирусный кератоконъюнктивит. J. Fr. Офтальмол. 2010. 33: 586–592. [PubMed] [Google Scholar] 11. Фломенберг П., Бэббит Дж., Дробыски В.Р., Эш Р.С., Карриган Д.Р., Седмак Г.В., МакОлифф Т., Камитта Б., Горовиц М.М., Бунин Н. и др. Рост заболеваемости аденовирусом у реципиентов трансплантата костного мозга. J. Infect. Дис. 1994; 169: 775–781. [PubMed] [Google Scholar] 12. Hale G.A., Heslop H.E., Krance R.A., Brenner M.A., Jayawardene D., Srivastava D.K., Patrick C.C. Аденовирусная инфекция после трансплантации костного мозга детям. Пересадка костного мозга. 1999; 23: 277–282. [PubMed] [Google Scholar] 13. Майерс Г.Д., Кранс Р.А., Вайс Х., Куэнле И., Деммлер Г., Heslop H.E., Bollard C.M. Частота аденовирусной инфекции у педиатрических реципиентов аллогенных трансплантатов костного мозга от альтернативных доноров, получающих либо антитимоцитарный глобулин (ATG), либо алемтузумаб (Campath). 2005; 36: 1001–1008. [PubMed] [Google Scholar] 14. Супарно К., Миллиган Д. В., Мосс П. А., Маутнер В. Аденовирусные инфекции у реципиентов трансплантата стволовых клеток: последние достижения в понимании патогенеза, диагностики и лечения. Лейк. Лимфома. 2004. 45: 873–885. [PubMed] [Google Scholar] 15.Ховард Д.С., Филлипс Г.Л., II, Рис Д.Э., Манн Р.К., Хенсли-Дауни Дж., Питтард М., Баркер М., Помрой С. Аденовирусные инфекции у реципиентов трансплантата гемопоэтических стволовых клеток. Clin.Infect.Dis. 1999; 29: 1494–1501. [PubMed] [Google Scholar] 16. Сассвилл В.Г., Дитерс Р.В. Влияние инфекций и нормальной флоры нечеловеческих приматов на разработку лекарств. ИЛАР Дж. 2008; 49: 179–190. [PubMed] [Google Scholar] 18. Пьедра П.А., Поведа Г.А., Рэмси Б., Маккой К., Хиатт П.В. Заболеваемость и распространенность нейтрализующих антител к обычным аденовирусам у детей с муковисцидозом: значение для генной терапии аденовирусными векторами.Педиатрия. 1998; 101: 1013–1019. [PubMed] [Google Scholar] 19. Аткинсон Р.Л.Вирусы как этиология ожирения. Mayo Clin. Proc. 2007; 82: 1192–1198. [PubMed] [Google Scholar] 20. Аткинсон Р.Л., Дхурандхар Н.В., Эллисон Д.Б., Боуэн Р.Л., Израиль Б.А., Альбу Дж.Б., Август А.С. Аденовирус-36 человека связан с увеличением массы тела и парадоксальным снижением липидов в сыворотке крови. Int. J. Obes. (Земля) 2005; 29: 281–286. DOI: 10.1038 / sj.ijo.0802830. [PubMed] [CrossRef] [Google Scholar] 21. Хоффман Дж. А., Шах А.J., Росс Л.А., Капур Н. Аденовирусные инфекции и проспективное испытание цидофовира при трансплантации педиатрических гемопоэтических стволовых клеток. Биол. Пересадка костного мозга. 2001; 7: 388–394. [PubMed] [Google Scholar] 22. Кинчингтон П.Р., Араулло-Круз Т., Вергнес Дж. П., Йейтс К., Гордон Ю.Дж. Изменения последовательности ДНК-полимеразы аденовируса человека 5 типа, связанные с устойчивостью к противовирусному цидофовиру широкого спектра действия. Антивирь. Res. 2002; 56: 73–84. [PubMed] [Google Scholar] 24. Морфин Ф., Дюпюи-Жирод С., Mundweiler S., Falcon D., Carrington D., Sedlacek P., Bierings M., Cetkovsky P., Kroes A.C., van Tol M.J., Thouvenot D. Чувствительность аденовируса к противовирусным препаратам in vitro зависит от вида. Антивирь. 2005. 10: 225–229. [PubMed] [Google Scholar] 25. Hillenkamp J., Reinhard T., Ross RS, Böhringer D., Cartsburg O., Roggendorf M., De Clercq E., Godehardt E., Sundmacher R. Эффекты цидофовира 1% с циклоспорином 1% и без него в качестве препарата местное лечение острого аденовирусного кератоконъюнктивита: контролируемое клиническое пилотное исследование.Офтальмология. 2002; 109: 845–850. [PubMed] [Google Scholar] 26. Hillenkamp J., Reinhard T., Ross RS, Böhringer D., Cartsburg O., Roggendorf M., De Clercq E., Godehardt E., Sundmacher R. Местное лечение острого аденовирусного кератоконъюнктивита с использованием 0,2% цидофовира и 1% циклоспорина: Контролируемое клиническое пилотное исследование. Arch. Офталь. 2001; 119: 1487–1491. [PubMed] [Google Scholar] 27. Фаулер К.Дж., Данлэп Дж., Тройер Д., Стензель П., Эпнер Э., Мазиарц Р.Т. Опасные для жизни аденовирусные инфекции у пациентов с аллогенной трансплантацией стволовых клеток с ослабленным иммунитетом.Adv.Hematol. 2010: 601548. [Бесплатная статья PMC] [PubMed] [Google Scholar] 28. Engelmann G., Heim A., Greil J., Schmitt C.P., Flechtenmacher C., Daum E., Küsters U., Schmidt J., Meyburg J., Schnitzler P. Аденовирусная инфекция и лечение цидофовиром у детей после трансплантации печени. Детская трансплантация. 2009. 13: 421–428. [PubMed] [Google Scholar] 29. Рефаат М., Макнамара Д., Тойтеберг Дж., Кормос Р., Маккарри К., Шулло М., Тойода Ю., Бермудес С. Успешное лечение цидофовиром у взрослого реципиента трансплантата сердца с тяжелой аденовирусной пневмонией.J Пересадка сердца и легких. 2008. 27: 699–700. [PubMed] [Google Scholar] 30. Сакиб Р., Мелтон Л. Б., Чандракантан А., Райс К. М., Спак К. В., Саад Р. Д., Фенвес А. З., Барри Ю. М. Диссеминированная аденовирусная инфекция у реципиентов почечного трансплантата: роль цидофовира и внутривенного иммуноглобулина. Транспл. Заразить. Дис. 2010; 12: 77–83. [PubMed] [Google Scholar] 31. Неофитос Д., Охха А., Мукерджи Б., Вагнер Дж., Филико Дж., Фербер А., Дессейн С., Гроссо Д., Бруннер Дж., Фломенберг Н., Фломенберг П. Лечение аденовирусной болезни стволовыми клетками реципиенты трансплантата цидофовиром.Биологическая трансплантация костного мозга. 2007; 13: 74–81. [PubMed] [Google Scholar] 32. Бхадри В.А., Ли-Хорн Л., Шоу П.Дж. Безопасность и переносимость цидофовира у педиатрических пациентов с высоким риском. Транспл. Заразить. Дис. 2009. 11: 373–379. [PubMed] [Google Scholar] 33. Гэвин П.Дж., Кац Б.З. Внутривенное лечение рибавирином при тяжелой аденовирусной болезни у детей с ослабленным иммунитетом. Педиатрия. 2002; 110: e9. [PubMed] [Google Scholar] 34. Арав-Богер Р., Эчаваррия М., Форман М., Шараш П., Персо Д. Исцеление от аденовирусного гепатита с помощью рибавиринотерапии у педиатрического реципиента трансплантата печени.Педиатр. Заразить. Дис. J. 2000; 19: 1097–1100. [PubMed] [Google Scholar] 35. Кассано В.Ф. Внутривенная терапия рибавирином при аденовирусном цистите после аллогенной трансплантации костного мозга. Пересадка костного мозга. 1991; 7: 247–248. [PubMed] [Google Scholar] 36. Юнгман П. Лечение аденовирусных инфекций у хозяина с ослабленным иммунитетом. Евро. J. Clin. Microbiol. Заразить. Дис. 2004. 23: 583–588. [PubMed] [Google Scholar] 37. Тот К., Спенсер Дж. Ф., Дхар Д., Сагарц Дж. Э., Буллер Р. М., Художник Г. Р., Уолд В. С. Гексадецилоксипропилцидофовир, CMX001, предотвращает вызванную аденовирусом смертность в разрешающей иммуносупрессивной модели животных.Proc. Natl. Акад. Sci. СОЕДИНЕННЫЕ ШТАТЫ АМЕРИКИ. 2008; 105: 7293–7297. [Бесплатная статья PMC] [PubMed] [Google Scholar] 38. Квенел Д.К., Коллинз Д.Дж., Ван В.Б., Бидл Дж.Р., Хостетлер К.Ю., Керн Е.Р. Пероральное лечение коровьей оспы и вирусных инфекций коровьей оспы у мышей эфирными липидными эфирами цидофовира. Антимикробные агенты Chemother. 2004. 48: 404–412. [Бесплатная статья PMC] [PubMed] [Google Scholar] 39. Романутти К., Бруттомессо А.С., Кастилья В., Галаговский Л.Р., Ваксман М.Б. Антиаденовирусная активность производных эпиандростерона и дегидроэпиандростерона.Химиотерапия. 2010. 56: 158–165. [PubMed] [Google Scholar] 40. Найт Д.А., Хики Т.Э., Бонгард Дж.Э., Тхач Д.К., Ингард Р., Чанг Э. Дифференциальное действие аминных комплексов Co (III), Ni (II) и Ru (III) на вирус Синдбис. J. Inorg. Biochem. 2010. 104: 592–598. [PubMed] [Google Scholar] 41. Цао Ю., Лам Л. Конъюгаты биспецифических антител в терапии. Адван. Доставка лекарств Rev.2003; 55: 171–197. [PubMed] [Google Scholar] 42. Pantazis P., Han Z.Y., Chatterjee D., Wyche J. Водонерастворимые аналоги камптотецина как потенциальные противовирусные препараты.J. Biomed. Sci. 1999; 6: 1–7. [PubMed] [Google Scholar] 43. Еропкин М.Ю., Соловский М.В., Смирнова М.Ю., Брязжикова Т.С., Гудкова Т.М., Коновалова Н.И. Синтез и биологическая активность водорастворимых полимерных комплексов арбидола. Pharm. Chem. J. 2009; 43: 563–567. [Google Scholar] 44. Д’Круз О.Дж., Укун Ф.М. Стампидин: селективный окуло-генитальный микробицид. J. Antimicrob. Chemother. 2005; 56: 10–19. [PubMed] [Google Scholar] 45. Кавуд Р., Чен Х.Х., Кэрролл Ф., Базан-Перегрино М., ван Ройен Н., Леонард В.S. Использование тканеспецифической микроРНК для борьбы с патологией аденовируса дикого типа без ослабления его способности убивать раковые клетки. PLoS Pathog. 2009; 5: e1000440. [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Штихм Р.Э., Охс Х.Д., Винкельштейн Дж. Иммунологические нарушения у младенцев и детей. 5-е. Elsesier Health Sciences; Филадельфия, Пенсильвания, США: 2004. стр. 337. [Google Scholar] 47. Ленертс Л., Де Клерк Э., Наесенс Л. Клинические особенности и лечение аденовирусной инфекции. Rev. Med. Virol.2008. 18: 357–374. [PubMed] [Google Scholar] 48. Гарсия Дж. М., Эспаньол Т., Гурбиндо М. Д., Касас К. С. Обновленная информация о лечении первичных иммунодефицитов. Аллергол. Immunopathol. (Мадр) 2007; 35: 184–192. [PubMed] [Google Scholar] 49. Сакиб Р., Мелтон Л. Б., Чандракантан А., Райс К. М., Спак К. В., Саад Р. Д., Фенвес А. З., Барри Ю. М. Диссеминированная аденовирусная инфекция у реципиентов почечного трансплантата: роль цидофовира и внутривенного иммуноглобулина. Транспл. Заразить. Дис. 2010; 12: 77–83. [PubMed] [Google Scholar] 50.Гайнотти Р., Рикарте К., Эбекиан Б., Видела К., Карбаллал Г., Дамонте Э. Б., Эчаваррия М. ПЦР в реальном времени для быстрого определения чувствительности аденовируса к противовирусным препаратам. J. Virol. Методы. 2010. 164: 30–34. [PubMed] [Google Scholar] 51. Beck E.T., Jurgens L.A., Kehl S.C., Bose M.E., Patitucci T., Lague E., Darga P., Wilkinson K., Witt L.M., Fan J., He J., Kumar S., Henrickson K.J. Разработка быстрого автоматизированного мультиплексного анализа ОТ-ПЦР в реальном времени для экспресс-анализа гриппа A, гриппа B и респираторно-синцитиального вируса A / B и его использование во время эпидемии вируса гриппа свиного происхождения h2N1 в 2009 г. в Милуоки, штат Висконсин.J. Mol. Диаг. 2010; 12: 74–81. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Ли Р., Ким П.Х., Чхве Дж.В., О-Джун К., Ким К., Ким Д., Юн С.-О., Ю К.-Х. Мониторинг рецептор-опосредованного эндоцитоза в реальном времени на основе емкости. Биосенс. Биоэлектрон. 2010. 25: 1325–1332. [PubMed] [Google Scholar] 53. Кляйн М.А., Майо К.Х., Кратцке Р.А. p16 (INK4a) Миметики пептидов, идентифицированные с помощью виртуального скрининга. Биоорг. Medicinal Chem. Lett. 2010; 20: 403–405. [PubMed] [Google Scholar] 54. Дьякону И., Серулло В., Эскутенер С., Kanerva A., Bauerschmitz G.J., Hernandez-Alcoceba R., Pesonen S., Hemminki A. Репликацию аденовируса человека у иммунокомпетентных сирийских хомяков можно ослабить с помощью хлорпромазина или цидофовира. J. Gene Med. 2010; 12: 435–445. [PubMed] [Google Scholar]случаев заражения аденовирусом | Симптомы и причины
Каковы симптомы аденовирусной инфекции?
Большинство аденовирусных инфекций протекают в легкой форме с небольшими симптомами. Хотя каждый ребенок может испытывать симптомы по-разному, к наиболее частым относятся:
Респираторные инфекции
Инфекции кишечника
- внезапное начало водянистой диареи
- лихорадка
- Болезненность живота
- вздутие живота
Аденовирус может вызвать некоторые осложнения, хотя и нечасто.В их числе:
Хроническая болезнь легких
- очень редко
- может развиться, если у ребенка развивается пневмония от аденовируса
- этот штамм вируса имеет 10-процентную смертность
> Тяжелые инфекции
Дети с ослабленной иммунной системой в группе риска
Инвагинация
- , когда одна часть кишечника скользит по другой части, как телескоп, вызывая закупорку кишечника
- чаще всего встречается у младенцев
- — неотложная медицинская помощь
- симптомы включают кровавый стул, рвоту, вздутие живота, колени согнуты к груди, громкие крики от боли, слабость и вялость
Хроническая инфекция миндалин и аденоидов
- лимфатическая железа, расположенная в задней части носа и горла
- , когда у вашего ребенка сохраняется аденовирус в течение длительного времени без серьезных симптомов
Что вызывает аденовирусную инфекцию?
Аденовирусы заразны, а это значит, что ваш ребенок может передать их другим детям.





