E21.1 — Вторичный гиперпаратиреоз, не классифицированный в других рубриках
Входит в группу: E21 — Гиперпаратиреоз и другие нарушения паращитовидной [околощитовидной] железы 1
1Найдено препаратов:8
| Земплар® | Капс. 1 мкг: 7, 14, 28 или 56 шт. рег. №: ЛСР-010759/09 от 29.12.09 Дата перерегистрации: 14.12.17 | Фасовка, упаковка и выпускающий контроль качества: AESICA QUEENBOROUGH (Великобритания) или ОРТАТ (Россия) | ||
| Земплар® |  2 мкг: 7, 14, 28 или 56 шт. рег. №: ЛСР-010759/09
от 29.12.09
Дата перерегистрации: 14.12.17 2 мкг: 7, 14, 28 или 56 шт. рег. №: ЛСР-010759/09
от 29.12.09
Дата перерегистрации: 14.12.17 | |||
| Земплар® | Р-р д/в/в введения 5 мкг/1 мл: амп. 1 мл или 2 мл 5 шт. рег. №: ЛСР-004781/09 от 16.06.09 Дата перерегистрации: 11.08.14 | AbbVie (Великобритания) Произведено: HOSPIRA (Италия) | ||
| Парсабив | Р-р д/в/в введения 10 мг/2 мл: фл. | |||
| Парсабив | Р-р д/в/в введения 2.5 мг/0.5 мл: фл. 6 шт. рег. №: ЛП-003993
от 05.12.16 Р-р д/в/в введения 5 мг/мл: фл. 6 шт. рег. №: ЛП-003993 от 05.12.16 | |||
| Рокальтрол® |  0.25 мкг: 30 или 100 шт. рег. №: П N014565/01
от 24.03.09
Дата перерегистрации: 28.02.18 0.25 мкг: 30 или 100 шт. рег. №: П N014565/01
от 24.03.09
Дата перерегистрации: 28.02.18Капс. 0.5 мкг: 30 или 100 шт. рег. №: П N014565/01 от 24.03.09 Дата перерегистрации: 30.07.14 | Выпускающий контроль качества: F.Hoffmann-La Roche (Швейцария) |
Описания препаратов с недействующими рег. уд. или не поставляемые на рынок РФ
уд. или не поставляемые на рынок РФ
| Этальфа® | Капли д/приема внутрь 2 мкг/1 мл: фл. 20 мл с пробкой-капельницей рег. №: П N012029/02 от 28.10.11 | |||
| Этальфа® | Р-р д/в/в введения 2 мкг/1 мл: амп. Р-р д/в/в введения 2 мкг/1 мл: амп. 0.5 мл 10 шт. рег. №: П N012029/03 от 28.10.11 |
Описания активных веществ под международным непатентованным наименованием
Другие подгруппы из нозологической группы: Гиперпаратиреоз и другие нарушения паращитовидной [околощитовидной] железы
Что такое гиперпаратиреоз и чем он опасен?
Гиперпаратиреоз – это нарушение, при котором одна или несколько из паращитовидных желез вырабатывает слишком много паратиреоидного гормона. Эти маленькие железы расположены прямо на щитовидной железе. Паратиреоидный гормон (или паратгормон) помогает поддерживать необходимый баланс кальция в крови и тканях организма, работа которых зависит от этого минерала.
Эти маленькие железы расположены прямо на щитовидной железе. Паратиреоидный гормон (или паратгормон) помогает поддерживать необходимый баланс кальция в крови и тканях организма, работа которых зависит от этого минерала.
Когда проявляются признаки этого нарушения, это свидетельствует о повреждении или дисфункции органов или тканей. Причина этого явления – либо повышенная концентрация кальция в крови и моче, либо его пониженная концентрация в костной массе.
Симптомы гиперпаратиреоза могут быть настолько мягкими и неспецифическими, что человек может и не догадываться о проблеме с паращитовидными железами. Хотя у некоторых признаки заболевания проявляются не так мягко.
В целом симптомы гиперпаратиреоза включают:
- Хрупкие и легко ломающиеся кости (остеопороз),
- Камни в почках,
- Сильную жажду и участившееся мочеиспускание,
- Боль в животе,
- Быстрое утомление или слабость,
- Мышечную слабость,
- Депрессию или забывчивость,
- Боли в костях и суставах,
- Частые жалобы на плохое самочувствие без видимых причин,
- Тошноту, рвоту и потерю аппетита,
- Запоры.

Каковы причины гиперпаратиреоза?
Паращитовидные железы поддерживают нужный баланс кальция и фосфора за счет высвобождения или остановки выработки паращитовидного гормона. Это можно сравнить с работой термостата, который контролирует постоянную температуру воздуха. Если она падает ниже необходимого значения, термостат вырабатывает больше тепла. Если температура слишком высокая, он прекращает вырабатывать тепло. Участие в контроле уровня кальция в крови так же принимает витамин D.
Когда уровень кальция в крови падает ниже нормы, паращитовидные железы вырабатывают паратгормон. Он повышает уровень кальция за счет его выхода из костей, а также увеличивает количество кальция, который абсорбируется в тонкой кишке из пищи.
Когда уровень кальция в крови слишком высокий, паращитовидные железы снижают свою активность. Но иногда одна или несколько желез вырабатывают слишком много паратиреоидного гормона. Это приводит к аномально высокому уровню кальция (гиперкальциемия) и низкому уровню фосфора в крови. В данном случае и развивается гиперпаратиреоз.
В данном случае и развивается гиперпаратиреоз.
Кальций играет критически важную роль для здоровья костей и зубов. Однако этот минерал выполняет и другие функции. Он помогает передавать сигналы между нервными клетками и участвует в сокращении мышц. Фосфор помогает поддерживать эти же функции, работая в союзе с кальцием.
Это заболевание принято разделять на 2 разновидности. Каждую из них мы рассмотрим по отдельности.
Первичный гиперпаратиреоз
При этой разновидности нарушения проблема затрагивает паращитовидные железы. Главные причины:
- Аденома (доброкачественная опухоль) паращитовидных желез – самая распространенная причина первичного гиперпаратиреоза (около 80 % всех случаев),
- Увеличение (гиперплазия) двух или более желез – вторая по распространенности причина,
- Злокачественная опухоль желез (карцинома) – редко, но все же встречается.
Первичный гиперпаратиреоз обычно развивается случайным образом. Хотя некоторые люди наследуют отдельный ген, который вызывает эту болезнь. Риск образования аденомы или карциномы возрастает у людей, которые проходили лучевую терапию в области головы или шеи.
Риск образования аденомы или карциномы возрастает у людей, которые проходили лучевую терапию в области головы или шеи.
Вторичный гиперпаратиреоз
В данном случае виновато нарушение, которое понижает уровень кальция, из-за чего паратиреоидный гормон вырабатывается в повышенных количествах. Таким образом, повышенный паратгормон пытается компенсировать недостаток кальция. В этом могут быть виноваты следующие факторы:
- Проблемы с всасыванием кальция в тонком кишечнике. Организм может недополучать этот минерал из пищи. Зачастую такое происходит из-за нарушений в работе пищеварительной системы, которая по каким-то причинам не всасывает кальций.
- Сильный дефицит витамина D. Этот витамин помогает поддерживать необходимый уровень кальция в крови. Также он способствует его всасыванию в тонкой кишке. Наш организм самостоятельно вырабатывает витамин D, когда кожа подвергается воздействию солнечных лучей. Некоторое количество этого витамина мы получаем с пищей.
 Если у человека дефицит витамина D, уровень кальция в крови может упасть.
Если у человека дефицит витамина D, уровень кальция в крови может упасть. - Хроническая почечная недостаточность – это самая распространенная причина вторичного гиперпаратиреоза. Почки конвертируют витамин D в ту форму, которая используется организмом. Если функция почек нарушена, количество биологически активной формы витамина D может снизиться, что приведет к падению уровня кальция.
Кто входит в группу риска?
В группу риска развития первичного гиперпаратиреоза входят:
- Женщины – после наступления менопаузы,
- Люди с продолжительным и сильным дефицитом кальция или витамина D,
- Лица с редким наследственным нарушением, например, – множественной эндокринной неоплазией 1 типа,
- Люди, которые проходили лучевую терапию в области шеи или головы,
- Лица, принимавшие литий – препарат, который назначают для лечения биполярного расстройства.
Каковы осложнения гиперпаратиреоза?
Обычно осложнения развиваются из-за длительного недостатка кальция в костях и слишком высокого уровня кальция в крови. Самые распространенные осложнения включают:
Самые распространенные осложнения включают:
- Остеопороз. «Выход» кальция из костей приводит к их слабости и увеличивает вероятность переломов.
- Камни в почках. Избыток кальция в крови ведет к повышенной концентрации кальция в моче. Это приводит к образованию в почках маленьких и твердых частиц, которые формируются из кальция и других минералов.
- Кальцификацию роговицы – когда кальций накапливается на поверхности, покрывающей роговицу.
- Панкреатит – высокий уровень кальция из-за гиперпаратиреоза способен привести к воспалению поджелудочной железы.
- Язву желудка. Из-за высокого уровня кальция желудок производит больше соляной кислоты.
- Сердечно-сосудистые заболевания. Хотя точная причинно-следственная связь не установлена, повышенный уровень кальция в крови ассоциируют с сердечно-сосудистыми нарушениями. К ним относят гипертонию и некоторые болезни сердца.
- Неонатальный гипопаратиреоз. Тяжелый и незалеченный гиперпаратиреоз у беременной женщины способен вызвать опасно низкий уровень кальция у новорожденного.

Диагностика гиперпаратиреоза
Первое, что сделает врач – расспросит о симптомах и направит на анализы крови, которые определят:
- Уровень кальция в крови,
- Уровень паратиреоидного гормона.
Иногда врачи назначают дополнительную диагностику гиперпаратиреоза. Это делается для исключения вторичных причин, определения тяжести состояния и выявления осложнений. Для дополнительной диагностики больному могут назначить:
- Анализ мочи,
- Рентген почек,
- Денситометрию (определение минеральной плотности костей).
Каково лечение гиперпаратиреоза?
Врачи не всегда назначают лекарства и направляют на операцию по удалению желез. Иногда больному нужны только регулярные осмотры и контроль. Такой подход используется в следующих ситуациях:
- Если уровень кальция повышен лишь немного,
- Если почки нормально функционируют и у больного нет камней,
- Если минеральная плотность костей в норме или понижена только слегка.

В данном случае больному понадобится проходить регулярные обследования.
Хирургическое лечение
Операция – это самый распространенный и эффективный метод лечения первичного гиперпаратиреоза. Хирург удаляет только увеличенные или аденоматозные железы. Если пострадали все 4 железы, в этом случае хирург удаляет 3 и, возможно, часть четвертой. Так делается для того, чтобы часть паращитовидной железы продолжала выполнять свои функции.
Медикаментозное лечение гиперпаратиреоза
Препараты, которые назначают для лечения этого заболевания, включают:
- Кальцимиметики. Эти лекарства имитируют кальций, который якобы циркулирует в крови. Кальцимиметики в каком-то смысле обманывают паращитовидные железы, из-за чего последние вырабатывают меньше паратгормона.
Управление по надзору за качеством медикаментов (FDA) одобрило использование препарата цинакальцет для лечения гиперпаратиреоза, который был вызван хроническими болезнями почек или раком паращитовидной железы. Некоторые врачи назначают его для лечения первичного гиперпаратиреоза. Цинакальцет принимают пациенты, которым операция либо не помогла, либо не может быть выполнена.
Некоторые врачи назначают его для лечения первичного гиперпаратиреоза. Цинакальцет принимают пациенты, которым операция либо не помогла, либо не может быть выполнена.
- Гормональные лекарства. Если у женщины наступила менопауза и у нее появились признаки остеопороза, прием гормональных препаратов поможет удерживать кальций в костях. Однако стоит понимать, что такое лечение не помогает избавиться от первопричины гиперпаратиреоза. Более того, длительный прием гормональных препаратов способен увеличить риск образования тромбов и рака молочной железы.
- Бисфосфонаты. Эти препараты так же препятствуют выходу кальция из костей и помогают снизить риск развития остеопороза, вызванного гиперпаратиреозом.
Что делать, если пациент решил только наблюдаться?
В данном случае необходимо:
- Контролировать, сколько кальция и витамина D вы получаете из продуктов питания. Ограничения в приеме кальция не рекомендуется.
 Национальный институт медицины дает такие нормы по употреблению кальция: людям в возрасте 19-50 лет – 1000 мг в день; женщинам в возрасте 51 и более лет и мужчинам в возрасте 71 и более лет – 1200 мг. Витамин D рекомендуется употреблять в дозировке 600 МЕ, а людям в возрасте 71 год и старше – 800 МЕ.
Национальный институт медицины дает такие нормы по употреблению кальция: людям в возрасте 19-50 лет – 1000 мг в день; женщинам в возрасте 51 и более лет и мужчинам в возрасте 71 и более лет – 1200 мг. Витамин D рекомендуется употреблять в дозировке 600 МЕ, а людям в возрасте 71 год и старше – 800 МЕ. - Употреблять много жидкости, в основном воды без газа. Моча должна быть практически прозрачной – это поможет снизить риск образования камней в почках.
- Регулярно двигаться и тренироваться. Регулярные тренировки, особенно силовые, помогают поддерживать плотность костей.
- Отказаться от сигарет, если вы курите. Курение способно увеличить потери костной массы.
- Избегать препаратов, которые повышают уровень кальция в крови. К ним относят некоторые мочегонные средства и препарат литий.
Если вы заметили у себя или своих близких симптомы гиперпаратиреоза, лучше как можно скорей обратиться к эндокринологу.
Источники:
- Hyperparathyroidism, Mayo Clinic,
- Hyperparathyroidism,Patient.
 info,
info, - Primary Hyperparathyroidism, The National Institute of Diabetes and Digestive and Kidney Diseases.
запись к врачу — ДокДок СПб
Эндокринологи Санкт-Петербурга — последние отзывы
На модерации, 01 октября 2021
Врач очень понравился, давно таких не встречала. Записана к ней на повторный прием 2 октября, надеюсь доктор поможет мне в моей ситуации. Внимательный, знающий специалист. Анастасия Яковлевна внимательно провела осмотр, все расспросила, что я принимала, на все обратила внимание, назначила необходимые анализы и лечение. У меня было распухшее колено, сейчас делаю уколы и мне помогает. Замечательный, вежливый доктор, знает свое дело, приятная женщина.
Записана к ней на повторный прием 2 октября, надеюсь доктор поможет мне в моей ситуации. Внимательный, знающий специалист. Анастасия Яковлевна внимательно провела осмотр, все расспросила, что я принимала, на все обратила внимание, назначила необходимые анализы и лечение. У меня было распухшее колено, сейчас делаю уколы и мне помогает. Замечательный, вежливый доктор, знает свое дело, приятная женщина.
Галина, 22 сентября 2021
Екатерина Владимировна прекрасный доктор и специалист высокого класса. Великолепный, чудный, чуткий человек. Давно уже хожу к ней. И все мои родственники также обращаются к этому врачу. Думаю, лучше специалиста уже и не найти! Врач очень серьёзно помогла мне снизить вес в своё время. У меня было направление на госпитализацию и от неё мне нужно было разрешение как от лечащего врача. Просто для себя ещё получила необходимую беседу с отличным специалистом.
И все мои родственники также обращаются к этому врачу. Думаю, лучше специалиста уже и не найти! Врач очень серьёзно помогла мне снизить вес в своё время. У меня было направление на госпитализацию и от неё мне нужно было разрешение как от лечащего врача. Просто для себя ещё получила необходимую беседу с отличным специалистом.
Татьяна, 20 сентября 2021
Все подробно объяснили , осталась довольна и нашла своего врача . Рекомендую !
Марианна, 15 сентября 2021
Очень грамотный, профессиональный доктор, уважительный. У меня прием прошел хорошо. Александр Иванович дал много полезных советов, о питании, о приеме препаратов, не только то что связало с сахаром, но и с давлением. В принципе я осень довольна. Думаю сто продолжу у него лечение. Все в порядке.
У меня прием прошел хорошо. Александр Иванович дал много полезных советов, о питании, о приеме препаратов, не только то что связало с сахаром, но и с давлением. В принципе я осень довольна. Думаю сто продолжу у него лечение. Все в порядке.
Галина, 15 сентября 2021
Внимательный, доброжелательный доктор. Лариса Витальевна изучила результаты моих анализов, дала совет по очищению печени и выписала необходимые лекарства. Обратилась бы к данному специалисту повторно, при необходимости. Не очень удобное расположение регистратуры: прямо на лестнице, нет места.
Галина, 10 сентября 2021
Хороший и вежливый доктор. Она осмотрела меня, посмотрела мои анализы, направила на УЗИ, дала рекомендации и записала на повторный прием.
Алена, 29 апреля 2021
Доктор расспросила про мое заболевание, задала вопросы о состоянии моего здоровья, уточнила, какие я принимаю лекарства и сказала, что мне делать. Врач порекомендовала мне препараты, которые стоят кучу денег и продаются у них.
Врач порекомендовала мне препараты, которые стоят кучу денег и продаются у них.
Анна, 26 марта 2021
Внимательный и высокопрофессиональный доктор. Мы обратились к ней с проблемой нарушение сна. Она направила нас на необходимые анализы, полностью расспросила и нашла причину. Врач нам очень помогла!
Татьяна, 15 марта 2021
Отличный врач, большое ей спасибо! Валентина Петровна вежливая и профессиональная. Я так поняла, что опыт работы у этого врача около сорока лет. И мы очень рады, что попали именно к этому специалисту. На приёме доктор полностью измерила и осмотрела ребёнка, сделала УЗИ и выписала лечение. Всё это займёт много времени и пока не могу сказать про эффективность. Также мы уже сдали назначенные анализы и теперь по их результатам будем записываться на повторный приём для консультации.
Я так поняла, что опыт работы у этого врача около сорока лет. И мы очень рады, что попали именно к этому специалисту. На приёме доктор полностью измерила и осмотрела ребёнка, сделала УЗИ и выписала лечение. Всё это займёт много времени и пока не могу сказать про эффективность. Также мы уже сдали назначенные анализы и теперь по их результатам будем записываться на повторный приём для консультации.
Екатерина, 29 сентября 2021
Показать 10 отзывов из 1326Гиперпаратиреоз. Заболевание (пара)щитовидных желез.
Эта тема стала вызывать живой интерес среди врачей разных специальностей. Прежде всего потому, что гиперпаратиреоз может быть в основе таких распространённых патологий, как мочекаменная болезнь, желчнокаменная болезнь, гипертоническая болезнь, язвенная болезнь желудка. Особенно, если эти 4 патологии присутствуют одновременно. Есть еще 5 патология, часто сопровождающая этот квартет – остеопороз, но он может быть не виден, пока не будет поведено исследование костей методом рентгена или рентгеновской денситометрии.
Особенно, если эти 4 патологии присутствуют одновременно. Есть еще 5 патология, часто сопровождающая этот квартет – остеопороз, но он может быть не виден, пока не будет поведено исследование костей методом рентгена или рентгеновской денситометрии.Гиперпаратиреоз (ГПТ) – синдром, обусловленный повышенной/патологической продукцией паратгормона – основного гормона, регулирующего кальций-фосфорный обмен в организме и обмен витамина Д.
ГПТ занимает 3 место по распространённости среди эндокринных заболеваний после сахарного диабета 1 и 2 типа, диффузно-токсического зоба. Чаще встречается у женщин. Сейчас ГПТ стал лучше диагностироваться (во-первых, про него знают, во-вторых, усовершенствовались методики его диагностики).
Ещё раз повторюсь, основные появления ГПТ:
— ЖКБ
— МКБ (особенно коралловидные камни почек)
— язвенная болезнь желудка и 12-перстной кишки
— остеопороз
— гипертоническая болезнь
или сочетание трех из данных патологий, особенно с началом в молодом возрасте, может являться поводом для диагностики ГПТ.
Коралловидные камни почек – самостоятельная причина для диагностики ГТП.
По статистике 27% пациентов с АГ имеют бессимптомное течение гиперпаратиреоза.
Кроме того, рак молочной железы и простаты, могут провоцироваться гиперпаратиреозом.
Другие проявления гиперпаратиреоза встречаются в различной степени выраженности у разных пациентов:
— быстрая мышечная утомляемость, особенно при физической нагрузке (а не судороги)
— боли в мышцах (вплоть до паралича мышц тазового пояса), костях, «утиная походка»
— частое безболезненное мочеиспускание
— жажда
— снижение памяти
— депрессивные расстройства, психозы
— подташнивание (рвота реже встречается)
— зуд кожи
— панкреатит
— камни уретры и т.д.
Различают формы гиперпаратиреоза по клиническому течению (в зависимости от уровня поражения) — костная (3 подтипа – по типу остеопороза, фибозно-кистозная, педжетоидная форма), висцеральная (органная), смешанная.
NB!Сейчас участились случаи сочетания гиперпаратиреоза и диффузно-узлового зоба, поэтому все! больные с узловыми образованиями должны быть обследованы на уровень паратгормона в крови, кальций общий, ионизированный, фосфор.
По причине повышения паратгормона крови выявляют гиперпаратиреоз первичный – самостоятельное заболевание! 1 случай на 2000 человек (причины — аденома/аденомы (доброкачественные опухоли) паращитовидных желез, аденокарциномы (злокачественные) опухоли паращитовидных желез – всего 2% случаев). Паратиром обычно несколько, так как и паращитовидных желез, минимально 4 в организме.
см. фото
К первичному гиперпартиреозу относят такие генетические синдромы как МЭН 1 и МЭН 2А (множественные эндокринные неоплазии). Это сочетание гиперпаратиреоза с опухолями других эндокринных органов – рак щитовидной железы (медуллярный) , опухоль поджелудочной железы, опухоль надпочечников- феохромоцитома и т.д.).
Синдром других заболеваний – вторичный гиперпаратиреоз,
Повышение ПТГ физиологическое на фоне гипокальциемии разных причин: хроническая почечная недостаточность, и самая частая причина повышения паратгормона — дефицит витамина Д (витамина солнца), его длительная хроническая нехватка, особенно в дозах ниже 14 нг\мл, называется «рахитом у взрослых», а правильнее -остеомаляция, и может привести к образованию обратимой гиперплазии паращитовидных желез с повышенной продукцией паратгормона.
Третичный гиперпаратиреоз (чаще вследствие почечной недостаточности уже на гемодиализе!). Это формирование аденомы паращитовидных желез при длительно существующем вторичном гиперпаратиреозе.
Из лабораторных анализов обращает на себя внимание различие в концентрации кальция/фосфора при разных формах ГПТ.
Например, при первичном гиперпаратиреозе – паратгормон в крови повышен, кальций повышен!! (но может быть и нормальная концентрация в крови — нормокальциемический вариант гиперпаратиреоза) 25-ОН витамин Д повышен, фосфор крови снижен, кальций суточной мочи повышен\нормальный (особенно нормокальциурия – подтверждает первичный гиперпаратиреоз) . Кроме того повышено соотношение (более 32) хлор/фосфор – как проявление первичного гиперпаратироеза и его действия на почки.
Вторичный гиперпаратиреоз — паратгормон в крови повышен, кальций снижен!!, фосфор крови повышен, кальций суточной мочи повышен, 25-ОН витамин Д снижен.
При гиперпаратиреозе может наблюдаться дислипидемия, то есть атеросклероз! (повышение ЛПОНП-липопротеидов очень низкой плотности – «плохих жиров», повышен коэффициент атерогенности), что устраняется после оперативного вмешательства.
Итак, диагностика ГПТ включает:
— кровь на кальций ионизированный, общий, фосфор, паратгормон, щелочную фосфатазу, остеокальцин, креатинин, сахар крови, ТТГ, Т4 свободный
— суточная моча на потерю кальция и фосфора
— УЗИ щитовидной железы и паращитовидных желез (есть такая зависимость — при МКБ +гиперпаратиреозе — аденома паращитовидной железы чаще локализуется слева и др.)
— ЭКГ (могут быть изменения — такие как брадикардия, двугорбый ST, укорочение QT и др.)
— лучший метод визуализации паращитовидных железы!сцинтиграфия методом субтракции), проводят в ГБ №31,
см. фото
— рентген костей – наблюдаются явления субпериостальной резорбции, а также для гиперпаратиреоза характерна картина «мыльной пены» за счёт множественных мелких кист, бедренная кость в виде «пастушьего посоха», «колоколообразная» грудная клетка, «рыбьи» позвонки, кальцификация хрящей, истончение кортикального слоя зубных альвеол)
— липидограмма,
— УЗИ ОБП и почек,
— общий белок + белквые фракции+ М – градиент, белок Бенс-Джонса в моче,
— в клиническом анализе крови наблюдается — анемия (угнетение эритропоэза), лейкопения, эозинопения, лимфоцитоз, повышение СОЭ,
— при осмотре окулиста — отложение солей в глазном яблоке «рисовые зёрна» — при выраженном случае видно без щелевой лампы.
— денситомерия – подтверждение остеопороза.
— увеличивается концентрация лимонной кислоты на 70-80%.
Медикаментозные тесты диагностики.
N.B.!Тест с тиазидными диуретиками— до теста определяют потерю кальция с мочой, кальций и паратгормон крови,
затем дают Гипотиазид 50 мг * 2 раза/сут, 3 дня, и см. те же параметры, если – вырастет уровень кальция крови, паратгормон останется неизменным, уменьшится экскреция кальция с мочой, то это Первичный ГПТ.
Тест с гидрокортизоном— по100-200 мг/сут 10 дней ,при гиперпаратиреозе концентрация кальция крови не меняется , при других причинах снижается. (саркоидозе, болезнях крови и др .).
Кроме того, проводится пробное лечение витамином Д: при первичном гиперпаратиреозе, уровень кальция резко повысится, при вторичном гиперпаратиреозе — уровень кальция не меняется.
Лечение: первичного и третичного гиперпаратироеза — только оперативное! Иначе человеку грозит гиперапартиреиодный криз, а это жизнеугрожаемое состояние! особенно при уровне общего кальция более 3 ммоль/л и более 400 мг/выделения кальция в суточной моче).
Показания к оперативному вмешательству:
— эпизоды гиперкальциемических кризов, (даже один!!!)
— уменьшение клиренса креатинина на 30% от возрастной нормы,
— увеличение экскреции кальция с мочой более чем в 2-3 раза, (10 ммоль/сут или 400 мг/24 часа),
— МКБ,
— тяжёлый остеопороз, (Т критерий более !- 2.5 ),
— существенное увеличение серологической концентрации кальция крови. (кальций ионизированный более 3.0 ммоль/л).
Противопоказания к операции – ХПН (хроническая почечная недостаточность).
При более мягких формах и противопоказаниям к операции можно провести лечение ГЗТ (особенно у женщин в менопаузе), ГЗТ снижает немного уровень сыворотчного кальция и лечение бисфосфанатами.
Есть дополнительная альтернатива — это лечение кальций- миметиками (это антагонист кальцийчувствительных рецепторов –снижает концентрацию паратгормона и кальция крови) —МИМПАРА 30 мг, 60 мг, 90 мг, используется совместно с бисфосфонатами.
Мимпара используется только при вторичном и третичной ГПТ!
Данных для использования при первичном гиперпаратиреозе нет.
При первичном гиперпаратиреозе (до операции), под контролем уровня кальция крови;
дополнительная жидкость( 2-2.5-3 л/сут)+лечение бисфосфонатами.
Гиперпаратироез, если он вызван нехваткой витамина Д и кальция, может быть пролечен медикаментозно, и понятно какими препаратами – витамина Д и кальция. Витамин Д используется в больших дозах – 40000 единиц еженедельно первые 8 недель, потом по 20000 в неделю под контролем биохимии крови.
Ниже короткий клинический случай .
Парикальцитол одобрен для лечения вторичного гиперпаратиреоза у детей с 10 лет
Биофармацевтическая компания AbbVie объявила о том, что Министерство здравоохранения Российской Федерации одобрило применение препарата Земплар® (парикальцитол) в капсулах у пациентов в возрасте с 10 лет для профилактики и лечения вторичного гиперпаратиреоза, развивающегося при хронической болезни почек (ХБП) 3 и 4 стадий. Кроме того, Министерством здравоохранения одобрен подбор дозы препарата Земплар® в капсулах у пациентов с ХБП стадий 3 и 4 и вторичным гиперпаратиреозом (ВГПТ) после трансплантации почки: доза подбирается так же, как и у пациентов с ХБП стадий 3 и 4 и вторичным гиперпаратиреозом без трансплантации почки.
У пациентов, перенесших трансплантацию почки, часто развивается ХБП с нарушениями минерального баланса костной ткани (МКН-ХБП). Спустя один год после трансплантации у 25% пациентов отмечается хроническое повышение концентрации гормона паращитовидной железы даже при нормальной функции почек. Это оказывает существенное влияние на качество и сроки выживания реципиентов и почечных трансплантатов. Установлена связь повышенного уровня паратиреоидного гормона (ПТГ) (более 140 пг/мл через 2,5–3 месяца после операции) с развитием сердечно-сосудистых осложнений, потерей трансплантата, увеличением риска общей смертности.
У детей, как и у взрослых пациентов с ХБП, вторичный гиперпаратиреоз, характеризующийся повышенным уровнем паратиреоидного гормона и гиперплазией паращитовидных желез, является ранним и наиболее распространенным осложнением хронической болезни почек. Повышение уровня ПТГ является основным фактором развития болезней костей, наблюдаемых как у взрослых, так и у детей, а также возникновения внескелетной кальцификации, болей в костях и переломов. В отличие от взрослых клинические проявления минерально-костных нарушений у детей с ХБП также включают замедление роста и деформацию опорно-двигательного аппарата.
В отличие от взрослых клинические проявления минерально-костных нарушений у детей с ХБП также включают замедление роста и деформацию опорно-двигательного аппарата.
Многоцентровое клиническое исследование III фазы с участием пациентов в возрасте от 10 до 16 лет с ХБП 3 и 4 стадий показало значимое снижение уровня паратиреоидного гормона в группе детей, принимавших парикальцитол: у 47,1% пациентов наблюдалось два последовательных снижения уровня паратиреоидного гормона не менее чем на 30% по сравнению с исходным, а 29,4% пациентов достигли целевых значений паратиреоидного гормона, установленных международными рекомендациями.
Вторичный гиперпаратиреоз, метаболическая болезнь костей — Черепахи.ру
Другие названия заболевания — Метаболическая болезнь костей (MDB) или Метаболическое поражение костей (МПК), фиброзная остеодистрофия, остеомаляция, вторичный гиперпаратиреоз в результате нарушения рациона, остеопороз и рахит. Это заболевание сложное, но довольно распространенное в террариумистике.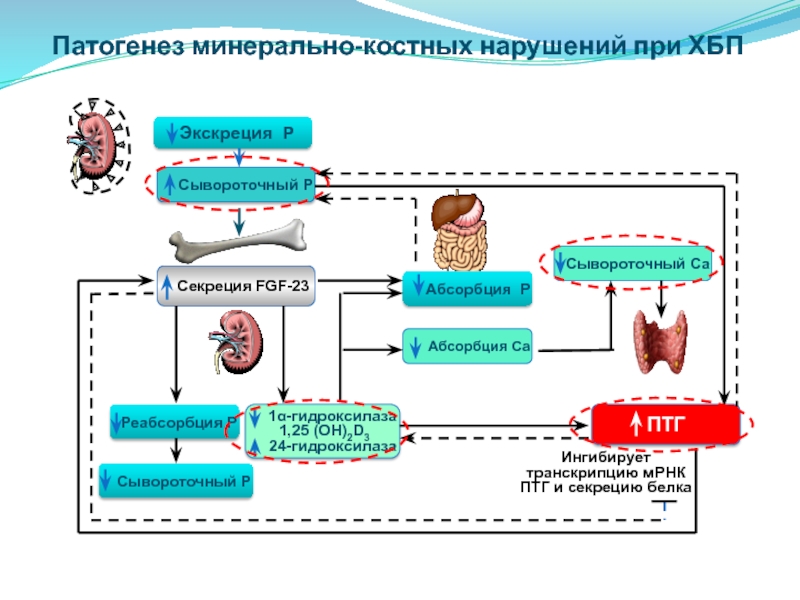 МПК — это общий термин, которым называют различные нарушения целостности и функций костей. Вторичный гиперпаратиреоз вследствие неправильного кормления является самым распространенным МПК, который диагностируют у пресмыкающихся в неволе. Вторичный гиперпаратиреоз — результат нарушений в кормлении и содержании.
МПК — это общий термин, которым называют различные нарушения целостности и функций костей. Вторичный гиперпаратиреоз вследствие неправильного кормления является самым распространенным МПК, который диагностируют у пресмыкающихся в неволе. Вторичный гиперпаратиреоз — результат нарушений в кормлении и содержании.
Причины развития болезни
Возникает в результате несоблюдения условий кормления и содержания. Предрасполагающими факторами является длительный дефицит витамина Д3 и нарушение кальций-фосфорного соотношения (избыток фосфора) или недостаток УФ излучения у дневных животных, возможно также перекорм. Чаще всего встречается у ящериц и водных черепах, хотя может встречаться у всех видов рептилий. В основном болеют молодые рептилии, у которых происходит активный рост костей.
При вторичном гиперпаратиреозе происходит избыточное образование гормона паращитовидной железы в ответ на гипокальциемию, возникшую на фоне неправильного кормления или содержания. Для компенсации дефицита кальций начинает выводиться из костей.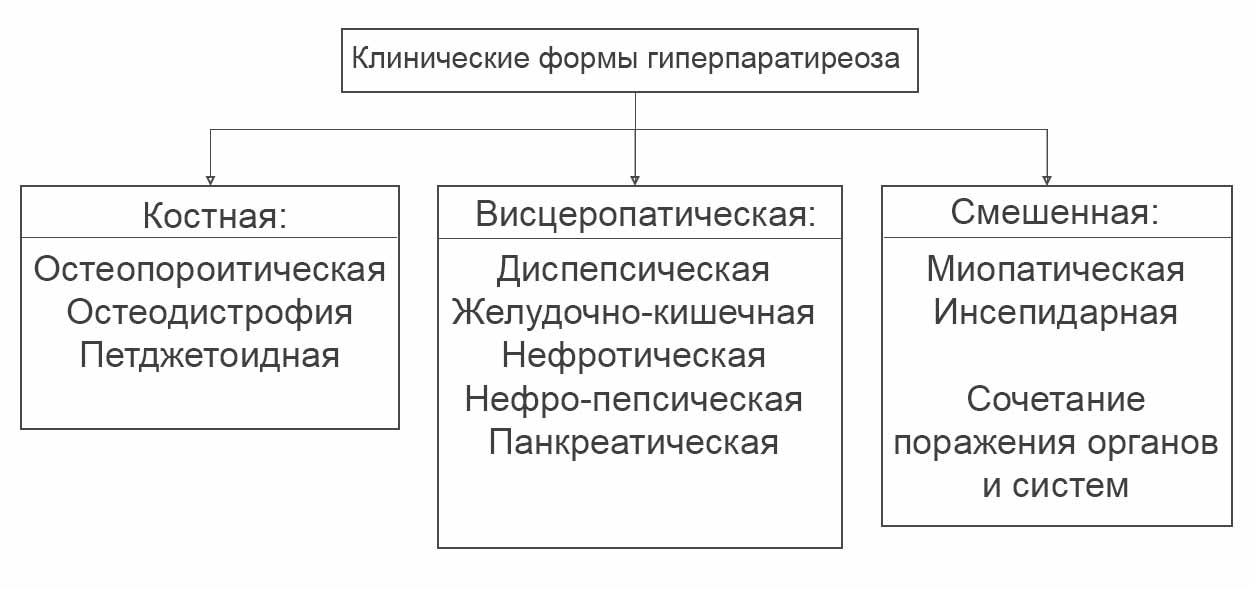 Результирующая остеопения ослабляет целостность костей. У молодых и растущих рептилий это называется рахитом. У старых рептилий — остеомаляцией.
Результирующая остеопения ослабляет целостность костей. У молодых и растущих рептилий это называется рахитом. У старых рептилий — остеомаляцией.
Симптомы болезни
У молодых растущих животных первым симптомом может быть увеличение в размерах суставов на конечностях и самих конечностей. Затем развивается невозможность держать корпус тела параллельно поверхности, наблюдается потеря способности твердо стоять на четырех лапах. Данный симптом может развиваться постепенно, зачастую на начальной стадии MBD ящерица (черепаха) поднимает переднюю половину тела во время ходьбы, волоча при этом хвост и таз по поверхности. По мере прогрессирования болезни животное теряет способность твердо опираться на грудные конечности и, в дальнейшем, отрываться от земли. Челюсти становятся мягкими, нижняя челюсть становится эластичной («синдром резиновой челюсти»), развивается фиброзная остеодистрофия. Ввиду размягчения и деформации челюсти, животному становится трудно питаться, рептилия перестает поедать твердый корм, теряет в весе./16/16.jpg) Рептилия и амфибии, страдающие MBD, зачастую хромают, ввиду довольно сильной болезненности снижается активность, животные слабеют. Так как ослабленные кости очень хрупки, могут возникать спонтанные переломы. Обычно встречаются деформации позвоночника. Развивается слабость тазовых конечностей, со временем приводящая к парализации конечностей. Если это происходит, вероятность выздоровления снижается из-за того, что параллельно с парализацией тазовых конечностей возникают проблемы с самостоятельной дефекацией. У черепах наблюдается размягчение панциря или пластрона с последующей деформацией.
Рептилия и амфибии, страдающие MBD, зачастую хромают, ввиду довольно сильной болезненности снижается активность, животные слабеют. Так как ослабленные кости очень хрупки, могут возникать спонтанные переломы. Обычно встречаются деформации позвоночника. Развивается слабость тазовых конечностей, со временем приводящая к парализации конечностей. Если это происходит, вероятность выздоровления снижается из-за того, что параллельно с парализацией тазовых конечностей возникают проблемы с самостоятельной дефекацией. У черепах наблюдается размягчение панциря или пластрона с последующей деформацией.
Диагностика болезни
Диагноз ставится на основании клинической картины и анамнеза (уточняются условия содержания) подтверждается рентгенологическим исследованием и результатами биохимического анализа крови. На рентгеновском снимке кости организма теряют плотность, становятся истонченными и прозрачными, во многих случаях можно увидеть множество переломов и деформаций.
Лечение болезни
ВНИМАНИЕ: Схемы лечения на сайте могут быть устаревшими! У черепахи может быть несколько заболеваний сразу, и многие заболевания сложно диагностировать без анализов и осмотра ветеринаром, поэтому до начала самостоятельного лечения обратитесь в ветеринарную клинику к проверенному ветеринару-герпетологу, либо к нашему ветеринару-консультанту на форуме.
На начальной незапущенной стадии для лечения MBD достаточно нормализовать условия содержания и сбалансировать рацион рептилии. Запущенные тяжелые случаи требуют интенсивного приема кальция, витаминных препаратов, увеличения интенсивности ультрафиолетового облучения, регулярного контроля состояния ветеринарного врача-герпетолога.
Необходимо обследовать животное на наличие переломов. При длительной анорексии и отсутствии способности самостоятельно потреблять пищу, животному показано стационарное лечение под наблюдением ветеринарного врача-герпетолога, принудительное кормление через зонд. Еженедельный контроль массы тела – одна из обязательных основ терапии MBD. Еженедельный прирост массы – залог скорейшего выздоровления. Если масса не набирается, животному необходимы дополнительные кормления. Без лечения многие пациенты с MBD погибают.
У взрослых и возрастных животных MBD имеет ряд отличий в лечении. Нормализация уровня кальция в крови должна происходить медленно, так как быстрое введение внутривенно может быть очень опасным. Зачастую такие пациенты страдают от обезвоживания, им показана по возможности внутривенная инфузионная терапия для восполнения водно-электролитного баланса. При деформации панциря у черепах по мере роста панцирь может продолжить деформироваться, что со временем приведет к аномальному размещению внутренних органов. В ряде случаев это может привести к летальному исходу.
Зачастую такие пациенты страдают от обезвоживания, им показана по возможности внутривенная инфузионная терапия для восполнения водно-электролитного баланса. При деформации панциря у черепах по мере роста панцирь может продолжить деформироваться, что со временем приведет к аномальному размещению внутренних органов. В ряде случаев это может привести к летальному исходу.
Похожие статьи:
Источники:
Гиперпаратиреоз, лечение и операции | Цены на хирургическое лечение гиперпаратиреоза
Общая информация и виды гиперпаратиреоза
Гиперпаратиреоз – это состояние организма, при котором околощитовидные железы продуцируют слишком большое количество гормона. В результате нарушаются процессы обмена кальция: элемент накапливается в крови и вымывается из костей. Отсутствие лечения способно привести к очень тяжелым состояниям: остеопорозу, артериальной гипертензии, мочекаменной болезни, почечной недостаточности.
Женщины страдают гиперпаратиреозом в 2–3 чаще мужчин и, как правило, он развивается в период менопаузы. Выявить заболевание на ранней стадии очень сложно, поскольку оно протекает практически бессимптомно. Чаще всего патологии паращитовидных желез и, как следствие, гиперпаратиреоз обнаруживают случайно, при обследованиях по другому поводу.
Если у вас диагностировали гиперпаратиреоз, лечение которого требует хирургического вмешательства, не отказывайтесь от операции. Современные технологии, которые применяются в нашем Центре, позволяют устранить патологии быстро, эффективно и с отличным эстетическим результатом.
Виды гиперпаратиреоза
В зависимости от того, почему вырос уровень паратгормона, выделяют несколько форм гиперпаратиреоза.- Первичный гиперпаратиреоз. Основная причина возникновения – образование аденомы на паращитовидной железе – именно поэтому происходит чрезмерная выработка паратгормона.
- Вторичный гиперпаратиреоз.
 Развивается из-за гипокальцемии, вызванной другими заболеваниями: хронической почечной недостаточностью, тяжелыми патологиями печени, а также у больных на гемодиализе. Паращитовидные железы при этом здоровы.
Развивается из-за гипокальцемии, вызванной другими заболеваниями: хронической почечной недостаточностью, тяжелыми патологиями печени, а также у больных на гемодиализе. Паращитовидные железы при этом здоровы. - Третичный гиперпаратиреоз. Редко встречающаяся форма патологии, возникающая как осложнение вторичного гиперпаратиреоза или при гиперплазии паращитовидных желез.
- Псевдогиперпаратиреоз. Состояние, возникающее при злокачественных опухолях (рак молочной железы, почек, легких), которые продуцируют паратгормон.
Симптомы гиперпаратиреоза
Проявления заболевания зависят от его формы. На начальной стадии первичного гиперпаратиреоза большинство пациентов жалуются на общее ухудшение самочувствие, вялость, боли в суставах и костях. Со временем, в результате вымывания кальция из костной ткани, появляются более серьезные проблемы с опорно-двигательным аппаратом: «утиная походка», нарушение тонуса мышц, патологические переломы (при рутинных движениях).
Кроме того, гиперпаратиреоз поражает нервную и сердечно-сосудистую системы, органы желудочно-кишечного тракта, вызывая депрессии, повышение артериального давления, рвоту и тошноту, резкое снижение веса, камни в почках и т.д.
Для вторичного и третичного гиперпаратиреоза в первую очередь характерны повреждения костной ткани, отложения кальция на стенках крупных сосудов, приводящие к стенокардии.
Диагностика гиперпаратиреоза
Поскольку гиперпаратиреоз длительное время протекает без симптомов, при первом подозрении на это заболевание необходимо провести тщательное обследование. В первую очередь необходимо определить уровень кальция, фосфатов и количество паратгормона – для этого пациенты Центра сдают анализы крови и мочи. Если данные лабораторной диагностики подтверждают наличие гиперпаратиреоза, мы проводим ряд инструментальных исследований: УЗИ щитовидной железы, КТ или МРТ области шеи и головы.Оперативное лечение гиперпаратиреоза
Единственный эффективный способ лечения первичной и вторичной формы гиперпаратиреоза – проведение операции.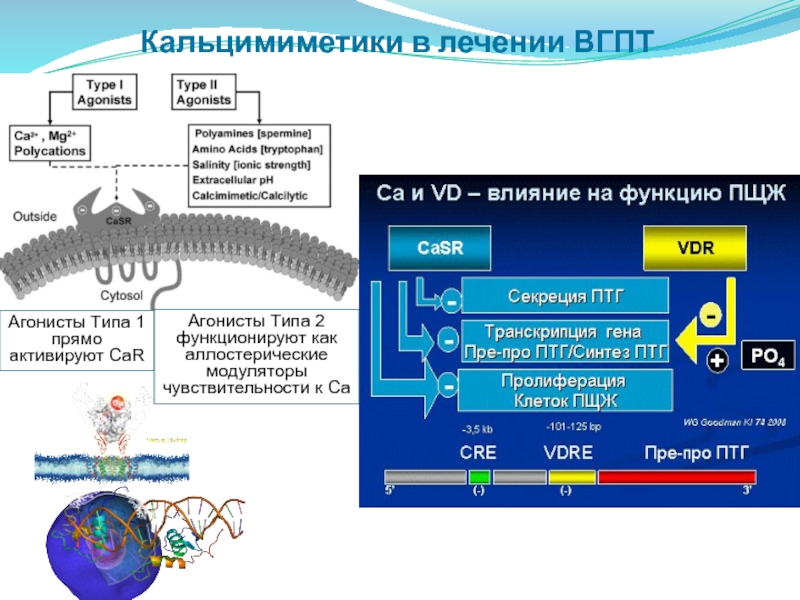 Хирургическое вмешательство направлено на удаление опухоли паращитовидной железы или определенной доли органа при его гиперплазии.
Хирургическое вмешательство направлено на удаление опухоли паращитовидной железы или определенной доли органа при его гиперплазии.Специалисты Центра владеют различными методиками лечения гиперпаратиреоза, выбирая оптимальный вариант в каждом клиническом случае. Так, наши хирурги проводят открытые и эндоскопические операции, отличающиеся высокой эффективностью и отличным косметическим результатом.
Для записи на прием к эндокринному хирургу Центра звоните: +7 (495) 292-59-87.
Вторичный гиперпаратиреоз | Отделение хирургии Колумбийского университета
Вторичный гиперпаратиреоз — это состояние, при котором заболевание за пределами паращитовидных желез приводит к увеличению и гиперактивности всех паращитовидных желез. Наиболее частыми причинами вторичного гиперпаратиреоза являются почечная недостаточность и дефицит витамина D. При почечной недостаточности почки больше не могут производить достаточное количество витамина D или удалять весь фосфор, производимый организмом, что приводит к низкому уровню кальция. Этот низкий уровень кальция стимулирует паращитовидные железы производить больше ПТГ. Со временем эта постоянная стимуляция заставляет паращитовидные железы расти и становиться гиперактивными, и у пациентов может развиться вторичный гиперпаратиреоз. У пациентов с почечной недостаточностью и вторичным гиперпаратиреозом уровень ПТГ может измеряться сотнями и даже тысячами. Иногда у пациентов развивается состояние, называемое кальцифилаксией, при котором отложения кальция образуются в коже и мышцах, вызывая болезненные поражения кожи, которые со временем могут вызвать некроз (т.е. отмирание тканей) и язвы.
Этот низкий уровень кальция стимулирует паращитовидные железы производить больше ПТГ. Со временем эта постоянная стимуляция заставляет паращитовидные железы расти и становиться гиперактивными, и у пациентов может развиться вторичный гиперпаратиреоз. У пациентов с почечной недостаточностью и вторичным гиперпаратиреозом уровень ПТГ может измеряться сотнями и даже тысячами. Иногда у пациентов развивается состояние, называемое кальцифилаксией, при котором отложения кальция образуются в коже и мышцах, вызывая болезненные поражения кожи, которые со временем могут вызвать некроз (т.е. отмирание тканей) и язвы.
Лучшее лечение вторичного гиперпаратиреоза обычно направлено на устранение причины проблемы с паращитовидными железами. Например, пациентов со вторичным гиперпаратиреозом из-за дефицита витамина D лучше всего лечить, повышая уровень витамина D до нормального диапазона. Для пациентов со вторичным гиперпаратиреозом, вызванным почечной недостаточностью, единственным лечением является трансплантация почки. Если основная проблема не может быть решена, лучшим лечением является медикаментозное лечение, а операция проводится только пациентам, у которых оптимальная медикаментозная терапия не работает.Для пациентов с почечной недостаточностью основные методы лечения включают фосфат-связывающие (для связывания лишнего фосфата), добавки витамина D (например, кальцитриол) и кальцимиметики. Кальцимиметики — это препараты, которые «обманом» заставляют клетки паращитовидной железы производить меньше ПТГ. Кальцимиметики, такие как Sensipar, снижают уровень ПТГ в среднем примерно на 50%. Основные побочные эффекты кальцимиметиков включают тошноту и рвоту.
Если основная проблема не может быть решена, лучшим лечением является медикаментозное лечение, а операция проводится только пациентам, у которых оптимальная медикаментозная терапия не работает.Для пациентов с почечной недостаточностью основные методы лечения включают фосфат-связывающие (для связывания лишнего фосфата), добавки витамина D (например, кальцитриол) и кальцимиметики. Кальцимиметики — это препараты, которые «обманом» заставляют клетки паращитовидной железы производить меньше ПТГ. Кальцимиметики, такие как Sensipar, снижают уровень ПТГ в среднем примерно на 50%. Основные побочные эффекты кальцимиметиков включают тошноту и рвоту.
К сожалению, медикаментозная терапия не работает почти у 25% пациентов, и иногда требуется хирургическое вмешательство.Основные причины операции включают: ухудшение плотности костей, сильный зуд (т. Е. Неконтролируемый зуд), кальцифилаксию, уровни ПТГ, которые постоянно превышают 800 пг / мл, и неспособность контролировать уровни кальция и фосфора в крови с помощью диализа. Три основных типа хирургии вторичного гиперпаратиреоза: субтотальная паратиреоидэктомия (то есть удаление 3 и ½ паращитовидных желез), иссечение 4 желез и аутотрансплантация (то есть удаление всех 4 паращитовидных желез и размещение части паращитовидных желез в предплечье) и ПТГ. -управляемая паратиреоидэктомия (т.е. удаление достаточного количества ткани паращитовидной железы для доведения интраоперационного уровня ПТГ до 200–300). Каждый метод имеет свои риски и преимущества, поэтому важно работать со специалистами, чтобы определить, какая операция подходит каждому пациенту. Однако, поскольку ни одна из этих операций не устраняет основную причину вторичного гиперпаратиреоза, пациенты подвергаются высокому риску рецидива (т. Е. Заболевания, которое возвращается).
Три основных типа хирургии вторичного гиперпаратиреоза: субтотальная паратиреоидэктомия (то есть удаление 3 и ½ паращитовидных желез), иссечение 4 желез и аутотрансплантация (то есть удаление всех 4 паращитовидных желез и размещение части паращитовидных желез в предплечье) и ПТГ. -управляемая паратиреоидэктомия (т.е. удаление достаточного количества ткани паращитовидной железы для доведения интраоперационного уровня ПТГ до 200–300). Каждый метод имеет свои риски и преимущества, поэтому важно работать со специалистами, чтобы определить, какая операция подходит каждому пациенту. Однако, поскольку ни одна из этих операций не устраняет основную причину вторичного гиперпаратиреоза, пациенты подвергаются высокому риску рецидива (т. Е. Заболевания, которое возвращается).
Следующие шаги
Если вы столкнулись с проблемой паращитовидной железы, наша команда Колумбийского центра паращитовидных желез всегда готова помочь.Позвоните по телефону (212) 305-0444 или запишитесь на прием онлайн.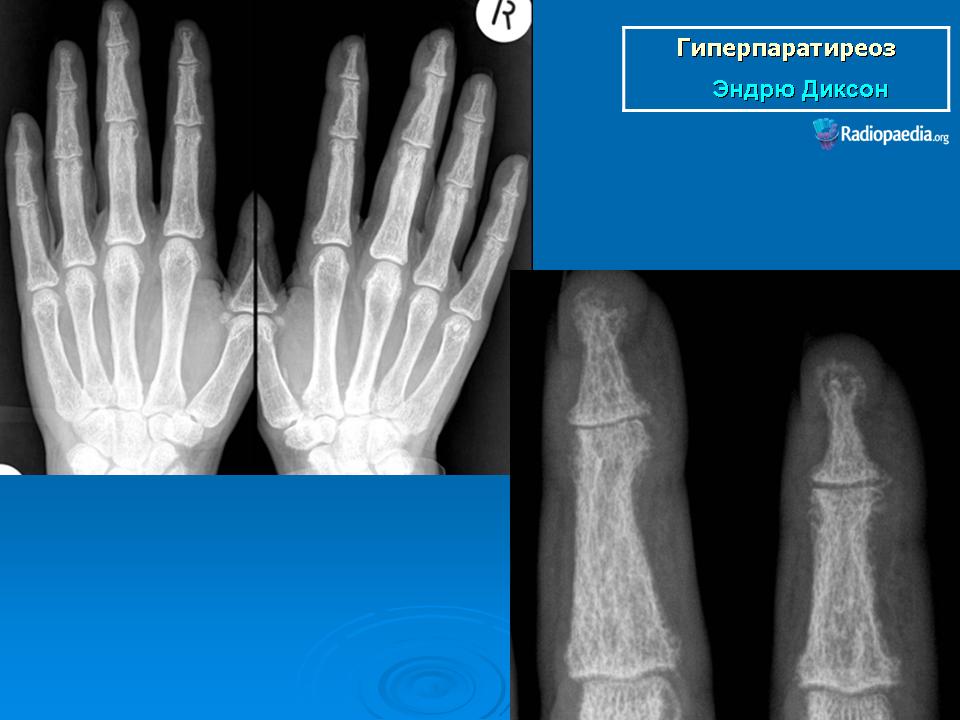
Вторичный гиперпаратиреоз: патогенез, прогрессирование заболевания и варианты лечения
Введение
Вторичный гиперпаратиреоз (ВГПТ) — это адаптивный и во многих случаях в конечном итоге дезадаптивный процесс, который развивается в ответ на снижение функции почек, нарушение экскреции фосфата и неспособность биоактивировать витамин D. Нарушение регуляции гомеостаза кальция и фосфора приводит к снижению почечной экскреции фосфатов, увеличению фосфор сыворотки, повышенные уровни фактора роста фибробластов фосфатонина 23 (FGF-23) и снижение синтеза кальцитриола, активной формы витамина D.Эти изменения приводят к усилению синтеза и секреции паратироидного гормона (ПТГ) и гиперплазии паращитовидных желез, что способствует развитию порочного круга (1). Подробные обзоры потенциальной роли устойчивого повышения уровня ПТГ в качестве уремического токсина были опубликованы, и в 1979 году Массри (2) предложил набор критериев, которым необходимо соответствовать, прежде чем устанавливать роль ПТГ или любого другого предложенного токсина в организме. генез уремической токсичности. Эти критерии включали демонстрацию повышенных уровней в крови, связь между предполагаемым токсином и уремическими проявлениями, улучшение этих проявлений после снижения предполагаемого уровня токсина в крови и демонстрацию токсичности при введении экспериментальным животным.Даже сейчас, примерно 30 лет спустя, остаются значительные сомнения в отношении роли SHPT и его лечения в отношении боли в костях, частоты переломов, мышечной функции, сердечно-сосудистых заболеваний, сексуальной функции, кроветворения, иммунной функции, зуда и кальцифилаксии, и все это может повлиять на продолжительность и качество жизни (3).
генез уремической токсичности. Эти критерии включали демонстрацию повышенных уровней в крови, связь между предполагаемым токсином и уремическими проявлениями, улучшение этих проявлений после снижения предполагаемого уровня токсина в крови и демонстрацию токсичности при введении экспериментальным животным.Даже сейчас, примерно 30 лет спустя, остаются значительные сомнения в отношении роли SHPT и его лечения в отношении боли в костях, частоты переломов, мышечной функции, сердечно-сосудистых заболеваний, сексуальной функции, кроветворения, иммунной функции, зуда и кальцифилаксии, и все это может повлиять на продолжительность и качество жизни (3).
Этот обзор будет посвящен патогенезу SHPT и текущим доступным вариантам лечения. Также будут освещены новые методы лечения, включая кальцимиметики, не содержащие кальция фосфатсвязывающие средства, и достижения в хирургическом вмешательстве.
Патогенез ШПТ
Непрерывная стимуляция паращитовидных желез за счет комбинации повышенной концентрации внеклеточного фосфата, снижения концентрации внеклеточного ионизированного кальция и значительного снижения сывороточного кальцитриола приводит к увеличению синтеза и высвобождения ПТГ.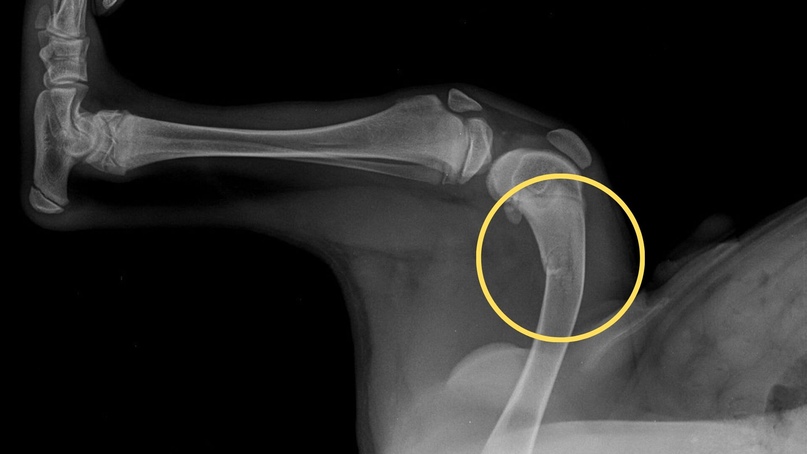 В то же время повышенная экспрессия FGF-23 подавляет остаточную почечную 25 (OH) -1-гидроксилазу, которая усугубляет эффективный дефицит кальцитриола, действуя как дополнительный драйвер SHPT. Даже на ранних стадиях развития гиперпаратиреоза эти изменения усугубляются переменной недостаточной экспрессией рецептора, чувствительного к кальцию (CaSR) и рецептора витамина D (VDR), что делает паращитовидные клетки неспособными должным образом реагировать на окружающий кальций и / или кальцитриол.Возникающее в результате повышение пролиферативной активности паращитовидных желез в конечном итоге приводит к гиперплазии паращитовидных желез (Рисунки 1 и 2) (4–10).
В то же время повышенная экспрессия FGF-23 подавляет остаточную почечную 25 (OH) -1-гидроксилазу, которая усугубляет эффективный дефицит кальцитриола, действуя как дополнительный драйвер SHPT. Даже на ранних стадиях развития гиперпаратиреоза эти изменения усугубляются переменной недостаточной экспрессией рецептора, чувствительного к кальцию (CaSR) и рецептора витамина D (VDR), что делает паращитовидные клетки неспособными должным образом реагировать на окружающий кальций и / или кальцитриол.Возникающее в результате повышение пролиферативной активности паращитовидных желез в конечном итоге приводит к гиперплазии паращитовидных желез (Рисунки 1 и 2) (4–10).
Нормальная функция почек: схематическое изображение взаимодействия различных факторов, регулирующих ПТГ .
Рис. 2. Почечная недостаточность: схематическое изображение взаимодействия различных регулирующих факторов ПТГ . VDR, рецептор витамина D; FGFR, рецептор фактора роста фибробластов; FGF-23, фактор роста фибробластов 23; CaSR, рецептор, чувствительный к кальцию; ПТГ, паратироидный гормон.
Недавнее понимание молекулярных механизмов, лежащих в основе гомеостаза фосфора, показало, что FGF-23 и его рецепторный рецептор фактора роста фибробластов 1 (FGFR1) играют важную роль (11–16). FGF-23 — это гормон, производство которого в остеоцитах и остеобластах стимулируется увеличением фосфатов и кальцитриола. FGF-23 связывается и активирует FGFR1, который функционирует только в том случае, если он коэкспрессируется трансмембранным белком Klotho в виде рецепторного комплекса Klotho-FGF. В проксимальных канальцах FGF-23 снижает реабсорбцию фосфата за счет снижения экспрессии котранспортеров фосфата натрия типа II (NaPi-2a и NaPi-2c).Таким образом, увеличение как сывороточного FGF-23, так и ПТГ у пациентов с хронической болезнью почек (ХБП) снижает реабсорбцию фосфата в проксимальных канальцах и поддерживает нормофосфатемию у большинства пациентов до тех пор, пока СКФ не упадет ниже 20 мл / мин. По мере прогрессирования ХБП эти петли отрицательной обратной связи неизбежно саботируются и в конечном итоге не могут поддерживать гомеостаз фосфатов. FGF-23 также напрямую снижает синтез ПТГ, в то время как косвенно увеличивает синтез за счет снижения продукции почечного кальцитриола.Наблюдалась корреляция между высокими уровнями FGF-23 у диализных пациентов, рефрактерной SHPT и повышенной смертностью (17,18). Это быстро развивающаяся область, и необходимы дальнейшие исследования, чтобы полностью понять роль FGF-23 в SHPT.
Высокий уровень фосфатов усиливает гиперплазию паращитовидных желез. Однако в настоящее время нет доказательств, свидетельствующих о существовании рецептора фосфора на паращитовидной железе. Исследования на мышах с нокаутом VDR предполагают, что пути витамина D играют вторичную роль в развитии гиперплазии паращитовидных желез и что передачи сигналов через CaSR достаточно для предотвращения гиперплазии паращитовидных желез у этих животных (19–22).
Механизмы развития ШПТ
Пациенты на ранних стадиях ХБП обычно не обнаруживают каких-либо изменений в сывороточных уровнях кальция и фосфатов, а их уровни ПТГ могут быть лишь немного выше контрольных значений. В некоторых недавних публикациях сообщается о повышенных уровнях FGF-23 у этих пациентов, что может помочь регулировать уровни фосфата и кальция в сыворотке (23). Стимулы к секреции FGF-23 на ранних стадиях ХЗП до конца не изучены, и в настоящее время это область активных исследований.FGF-23, по-видимому, не является острым постпрандиальным регулятором фосфатурии при ХБП, но несоответствующая постпрандиальная гипокальциемия может представлять ранее не сообщаемый механизм SHPT при ХБП (24). В недавнем исследовании, проведенном на крысах, добавление фосфата непосредственно в тонкий кишечник привело к быстрому увеличению экскреции фосфата. Не было связанных изменений в FGF-23 или других известных фосфатонинах (25), что указывает на то, что факторы, отличные от FGF-23, по-видимому, важны для увеличения постпрандиальной экскреции фосфата.
Исследование влияния FGF-23 на функцию паращитовидных желез в нормальных и гиперпластических паращитовидных железах показало, что FGF-23 снижает секрецию ПТГ (11) и пролиферацию клеток, а также увеличивает экспрессию CaSR и VDR в нормальных железах (16). Напротив, FGF-23 не влиял на гиперпластические железы (12,16). FGF-23 фосфорилировал регулируемую внеклеточными сигналами киназу 1/2 в нормальных паращитовидных железах, но не в гиперпластических. В гиперпластических паращитовидных железах экспрессия FGFR1 и белка Klotho была заметно снижена у людей (13) и экспериментальных животных (16) по сравнению с нормальными паращитовидными железами (13,16), что дает возможное объяснение отсутствия ответа на FGF-23. у уремических животных (12,16).Таким образом, сниженная экспрессия FGFR1 и Klotho препятствует контролю гиперпаратиреоза с помощью FGF-23 при почечной недостаточности (16).
Гиперплазия паращитовидных желез
Длительная стимуляция паращитовидных желез сначала приводит к диффузной поликлональной гиперплазии, а затем к моноклональной узловой гиперплазии, как показано на Рисунке 3 (20,27,28). Исследования на генетически модифицированных мышах показывают, что передача сигнала через CaSR является ключевым фактором пролиферации паратироидных клеток и гиперплазии паращитовидных желез (29).Экспериментальные работы на нормальных крысах и крысиной модели почечной недостаточности продемонстрировали, что пролиферация клеток паращитовидной железы связана со снижением экспрессии CaSR и VDR (7,16,21,26). Возникает вопрос, предшествует ли снижение рецепторов гиперплазии или снижение экспрессии является следствием пролиферации. Некоторые данные предполагают, что гиперплазия клеток паращитовидной железы предшествует подавлению экспрессии CaSR в модели уремических крыс (30), а введение кальцитриола или кальцимиметиков привело к снижению пролиферации клеток паращитовидной железы, связанной с повышением как CaSR, так и VDR (31, 32).Также возможно прямое влияние низких уровней кальция и кальцитриола на экспрессию их рецепторов. Было показано, что возрастающие дозы кальцитриола повышают экспрессию VDR паращитовидных желез у крыс с гиперкальциемией, но не с гипокальциемией (33). Исследования на животных показали, что активация CaSR кальцимиметиками индуцирует экспрессию паращитовидных желез VDR (10). Таким образом, у пациентов, получающих кальцимиметики, VDR активируется, несмотря на то, что уровень кальция может быть низким. Поэтому кажется вероятным, что, если основная роль клеток паращитовидной железы заключается в повышении уровня кальция в сыворотке до нормального уровня, ингибирование кальцитриолом и предотвращение гиперпаратиреоза возможно только при контроле уровня кальция в сыворотке.Canadillas et al. (34) предложила модель внутриклеточного сигнального пути, участвующего в CaSR-зависимой регуляции экспрессии VDR в паратироидных клетках. Внеклеточный кальций стимулирует экспрессию VDR за счет повышения уровня кальция в цитозоле и стимуляции пути киназы 1/2, зависимого от фосфолипазы A2-арахидоновой кислоты, регулируемого внеклеточными сигналами. Активация CaSR заставляет фактор транскрипции Sp1 действовать на промотор VDR.
Рисунок 3.Развитие гиперплазии паращитовидных желез .Этот рисунок перепечатан с разрешения ссылок 20 и 27.
Узловая трансформация при развитом вторичном гиперпаратиреозе сопровождается снижением экспрессии VDR и CaSR и снижением чувствительности к ингибирующему эффекту кальция и кальцитриола на секрецию ПТГ (35). Возникающий в результате тяжелый гиперпаратиреоз может вызвать гиперкальциемию и гиперфосфатемию, вызванную оттоком кальция и фосфора из скелета.
Сосудистая кальцификация
Повышенные уровни кальция и фосфора, связанные с SHPT, были связаны с развитием кальцификации сосудов, что в значительной степени связано с увеличением заболеваемости и смертности.Факторы транскрипции, включая Cbfa-1 / RUNX2 и MSX-2, были идентифицированы в клетках гладких мышц сосудов, прилегающих к участкам кальцификации, у пациентов с ХЗП (36). Костные белки, такие как остеопонтин, костный сиалопротеин, коллаген I типа, остеонектин и щелочная фосфатаза, также локализованы в местах экстраскелетной кальцификации. Многочисленные животные модели кальцификации сосудов, включая гиперфосфатемию, вызванную ХБП, или модели с генетическими модификациями ключевых белков, таких как FGF-23, помогли выяснить сложный патогенез кальцификации сосудов.Важно отметить, что эти модели также использовались для изучения профилактических мер или факторов, снижающих тяжесть состояния (28).
Возраст пациентов и продолжительность диализа связаны с повышенным риском кальцификации сосудов. Однако не у всех пациентов с ХБП, находящихся на диализе, развивается кальцификация сосудов, несмотря на очевидное воздействие одних и тех же факторов риска. Это означает, что естественные защитные факторы, такие как матричный белок Gla, могут играть роль и могут объяснить, почему затронуты только определенные субпопуляции пациентов с ХБП (36–39).Существуют противоречивые данные относительно связи фетуина-A со смертностью как у пациентов с терминальной стадией почечной недостаточности, так и в других условиях (40). Выявление факторов, специфичных для пациентов, у которых не развивается кальцификация сосудов, может указывать на новые методы лечения.
Руководство по эксплуатации SHPT
Отсутствие стандартной классификации и терминологии для заболеваний костей и минералов привело к разработке Руководства по улучшению глобальных результатов почек (KDIGO) для помощи в ведении пациентов с ХБП.Тем не менее, Национальная инициатива по оценке исходов заболеваний почек (NFK / KDOQI) (41) также определила ХБП и ее стадии. В более поздних рекомендациях KDIGO по CKD-MBD (42) использовался более сильный «научно-обоснованный» подход, чем в более ранних рекомендациях KDOQI, с меньшим количеством и, как правило, менее строгими рекомендациями, что отражает ограниченную доступность высококачественных клинических исследований в этой области. В настоящее время ведутся споры о том, как реализовать единую систему классификации.
Текущие варианты лечения
Эффективные терапевтические вмешательства крайне желательны, если мы хотим снизить заболеваемость и смертность, связанные с неконтролируемым SHPT.Однако из-за трудностей, связанных со снижением уровня паратгормона при одновременном контроле уровней кальция и фосфора в сыворотке крови, традиционные методы лечения SHPT имеют несколько ограничений. Следовательно, достижение текущих целей, установленных руководящими принципами NKF / KDOQI или KDIGO для ключевых минеральных параметров, может оказаться сложной задачей. Перерывы в терапии являются обычным явлением и могут способствовать прогрессированию заболевания (43). Широко используемые в настоящее время вмешательства включают модуляцию баланса кальция и фосфора путем приема с пищей и диализа, активных соединений витамина D, таких как кальцитриол и более новые аналоги витамина D, фосфатсвязывающие средства и новейшие кальцимиметики.Бисфосфонаты, ограничивая высокую скорость резорбции кости при тяжелой SHPT, могут играть роль, хотя бы как мост к более окончательному разрешению SHPT. Такое использование бисфосфонатов выходит за рамки разрешенных показаний и из-за их очень медленного удаления из кости сопряжено с риском индукции низкообменной болезни костей, особенно у пациентов, в конечном итоге подвергшихся паратиреоидэктомии. Хирургическое вмешательство в виде паратиреоидэктомии обычно рассматривается только при тяжелой форме SHPT (41).Все эти вмешательства могут улучшить биохимические профили и другие суррогатные маркеры, такие как гистология кости. Однако все они также страдают от недостатка доказательств, связывающих очевидные положительные эффекты этих методов лечения на суррогатные маркеры с улучшением результатов лечения пациентов.
Соединения витамина D
Дефицит эндогенного кальцитриола у пациентов с ХЗП контролируется лечением кальцитриолом или его пролекарством, альфакальцидолом, доксеркальциферолом (витамин D2, эквивалент альфакальцидола), 22-оксакальцитриолом или парикальцитолом.Все эти активные соединения витамина D активируют VDR, хотя и косвенно в случае альфакальцидола и доксеркальциферола. Активные стеролы витамина D увеличивают абсорбцию кальция и фосфора из кишечника и снижают синтез ПТГ. Более высокие (фармакологические) дозы часто приводят к гиперкальциемии и гиперфосфатемии, которые связаны с эктопической кальцификацией (44,45). У многих, хотя и не у всех пациентов, терапевтическое окно для применения активного витамина D является узким.Было показано, что новые аналоги витамина D, такие как доксеркальциферол и парикальцитол, подавляют уровни ПТГ не хуже, чем кальцитриол (46). Проспективное рандомизированное исследование показало, что кальцитриол и парикальцитол в одинаковой степени снижают уровни ПТГ; Предварительно определенные критерии эффективности (снижение уровня ПТГ) и безопасности (гиперкальциемия) не показали разницы, хотя парикальцитол способствует более быстрому снижению ПТГ (47).
Противоречивые данные, однако, показали, что терапия витамином D не влияет на гиперплазию паращитовидных желез на животных моделях (48,49), тогда как пульс-терапия кальцитриолом у пациентов на длительном диализе вызывает умеренную регрессию (50).Ограниченные и смешанные эффекты современных соединений витамина D на гиперплазию паращитовидных желез могут быть результатом ряда факторов, включая снижение экспрессии VDR или изменение каскадов передачи сигнала. Было постулировано, что CaSR более важен, чем VDR при гиперплазии паращитовидных желез после исследований абляции (19). Удаление VDR в паращитовидных железах снижает экспрессию CaSR в паращитовидных железах и лишь умеренно увеличивает базальные уровни ПТГ, предполагая, что VDR действительно влияет на секрецию ПТГ и физиологию паращитовидных желез с помощью различных механизмов, хотя и с ограниченным эффектом в этой модели на мышах (22).
Устойчивость к соединениям активного витамина D также может создавать проблемы, особенно у пациентов с тяжелой формой SHPT, которая прогрессировала до узлового фенотипа (51). Предлагаемые механизмы устойчивости включают снижение экспрессии VDR в клетках паращитовидной железы или неспособность комплекса кальцитриол-VDR взаимодействовать с элементом ответа на витамин D его генов-мишеней (52). Ключевым показателем успеха или неудачи лечения является размер паращитовидной железы. Соединения витамина D обычно хорошо контролируют SHPT у пациентов с умеренно увеличенными железами и хуже — у пациентов с увеличенными железами (53–55).
Некоторые исследования показали, что витамин D имеет двухфазную сердечно-сосудистую кривую «доза-ответ» со склонностью к кальцификации сосудов, возникающей не только из-за избытка витамина D, но и из-за дефицита витамина D (46). Низкое активное воздействие витамина D приводит к увеличению провоспалительных цитокинов, матриксных металлопротеиназ и снижению защитных факторов эндотелиальных клеток, тогда как высокие дозы приводят к гиперкальциемии, медиальной кальцификации, артериальной жесткости и гипертрофии левого желудочка.Однако масса доказательств предполагает, что соответствующее воздействие как природного, так и активного витамина D связано с в целом положительными плейотропными эффектами, из которых наиболее важными могут быть эффекты на сердечно-сосудистую систему. Генетически модифицированные мыши, лишенные фермента VDR (56,57) или 25-гидроксивитамин D 1α-гидроксилазы (CYP27B1) (58), проявляют субоптимальный сердечно-сосудистый фенотип, включая гипертензию, гипертрофию левого желудочка и повышенную регуляцию ренин-ангиотензин-альдостероновой системы. .В случае нокаута CYP27B1 этот фенотип можно исправить физиологической заменой кальцитриолом, но не коррекцией сывороточного кальция и фосфора в отсутствие кальцитриола.
На клиническом уровне крупные исследования, как правило, с историческим дизайном когорт, предполагают преимущество в выживаемости среди диализных пациентов, получавших инъекционные соединения активного витамина D, по сравнению с пациентами, не получавшими такого лечения (59). Хотя Tentori et al. (60) не наблюдали значительного увеличения выживаемости для доксеркальциферола и парикальцитола по сравнению с кальцитриолом в скорректированных моделях, Teng et al. (61) обнаружил значительное преимущество в выживаемости у пациентов, получавших парикальцитол, по сравнению с теми, кто получал кальцитриол. В этих исследованиях обычно участвовали пациенты в Соединенных Штатах, получавшие соединения витамина D внутривенно, но совсем недавно в Южной Америке было проведено такое же крупное историческое когортное исследование, в котором повышенная выживаемость снова наблюдалась у пациентов, получавших активный витамин D, на этот раз с использованием исключительно пероральных препаратов. агентов и демонстрирует очевидный обратный эффект дозозависимости соединений витамина D, при этом наибольший эффект наблюдается при самых низких дозах (62).На сегодняшний день ни в одном крупном ретроспективном исследовании этого типа не было обнаружено увеличения смертности при терапии активацией VDR, и даже с учетом присущих этим исследованиям недостатков, наиболее очевидным из которых является наличие намерения, они создают серьезную проблему для почек. Сообщество для проведения перспективных исследований с надлежащей мощностью и разработкой, способных дать окончательные ответы.
Фосфатные связующие
Было показано, что стойкая гиперфосфатемия снижает эффективность терапии витамином D в некоторых случаях (63), и существует корреляция между уровнями фосфора и смертностью, связанной с SHPT (38).Использование солей кальция для лечения гиперфосфатемии и восстановления нормального уровня фосфора в сыворотке крови увеличивает риск гиперкальциемии, кальцифилаксии и кальцификации сосудов (64). Не содержащие кальция фосфатсвязывающие вещества, такие как севеламер и карбонат лантана, снижают уровень фосфата в сыворотке, но не оказывают связанного воздействия на кальций в сыворотке и не снижают значительно уровни циркулирующего ПТГ (65). Таким образом, фосфатсвязывающие средства имеют ограниченное применение в качестве терапии устоявшейся SHPT, хотя гиперфосфатемия является важным фактором патогенеза ранней SHPT.Это согласуется с незначительным влиянием терапии фосфатным связывающим веществом на развитие и лечение SHPT. Эти наблюдения показывают, что не следует упускать из виду новые методы контроля уровня фосфора, особенно в качестве профилактической меры на ранних стадиях ХБП.
Кальцимиметики
Кальцимиметики, такие как цинакальцет, являются положительными аллостерическими модуляторами CaSR, взаимодействуя с трансдуктивным доменом рецептора, вызывая конформационные изменения, которые усиливают передачу сигнала.Это изменение конформации приводит к повышенной чувствительности к внеклеточному кальцию и, как следствие, к снижению уровней циркулирующего ПТГ (66–68). Исследования показали, что кальцимиметики, вводимые ежедневно в течение 1 недели, повышают экспрессию CaSR и вызывают значительное снижение уровня ПТГ у уремических крыс (7). Было высказано предположение, что наблюдаемая устойчивая долгосрочная эффективность кальцимиметиков в подавлении уровней ПТГ у диализных пациентов может быть связана с их активностью как аллостерических активаторов, а не как агонистов CaSR (69).Следовательно, активность рецепторов может быть более важной, чем уровни экспрессии рецепторов. Кроме того, активация CaSR увеличивает экспрессию VDR (32). Таким образом, добавление витамина D к кальцию может чрезмерно подавлять ПТГ с потенциальными негативными последствиями (70,71).
Обширные доклинические исследования показали, что развитие и прогрессирование гиперплазии паращитовидных желез могут подавляться кальцимиметиками. Цинакальцет подавляет пролиферацию клеток паращитовидной железы в модели нефрэктомии у крыс 5/6, что демонстрируется снижением количества клеток в фазе S, ядерных антиген-положительных клеток пролиферирующих клеток и общего количества клеток паращитовидной железы (72).Кальцимиметики постоянно предотвращают увеличение веса и / или объема паращитовидных желез при введении вскоре после субтотальной нефрэктомии, и этот эффект обратим при отмене лечения. Модели тяжелой SHPT, такие как животные с установленной гиперплазией паращитовидных желез, показали, что кальцимиметики останавливают прогрессирование гиперплазии даже в условиях фосфатной нагрузки (72).
Механизм и динамика кальцимиметического действия на ПТГ отличаются от таковых витамина D.Хотя витамин D снижает транскрипцию гена ПТГ и синтез гормонов в течение нескольких часов или даже дней (73), цинакальцет ингибирует секрецию ПТГ в течение нескольких минут, при этом максимальное снижение происходит в течение 2 часов после приема дозы у пациентов с SHPT. Метаболизм ферментов системы цитохрома Р-450 приводит к циклическому паттерну уровней ПТГ в сыворотке при продолжении приема цинакальцета, что может оказывать анаболическое действие на кости (74). Другие недавние данные указывают на то, что активация CaSR кальцимиметиками снижает стабильность мРНК ПТГ за счет посттрансляционной модификации белка, связывающего мРНК ПТГ, AUF1 (75,76).
Хотя объем паращитовидных желез может уменьшаться у пациентов, получавших цинакальцет, нет никаких доказательств того, что это отражает регресс гиперплазии или усиление апоптоза. Лечение цинакальцетом в сочетании с существующими традиционными методами лечения привело к уменьшению объема изначально меньших желез у пациентов с тяжелой формой SHPT (53–55,77).
Одним из наиболее частых побочных эффектов, наблюдаемых при приеме кальцимиметиков, является гипокальциемия, которая, как полагают, возникает после снижения мобилизации кальция из костей, вызванного снижением уровня ПТГ.У большинства пациентов с этой гипокальциемией легко справиться с помощью корректировки дозы (78) или комбинации с низкими дозами стеролов витамина D у пациентов с умеренной или тяжелой SHPT (79).
Исследование ADVANCE (80), разработанное для оценки эффектов цинакалцета в сочетании с низкими дозами витамина D на кальцификацию сосудов у пациентов с ХБП, находящихся на гемодиализе (81,82), показало, что показатели объема кальция в коронарной артерии были значительно ниже в группе цинакальцет плюс. группа низких доз витамина D, чем группа только стерола витамина D ( P = 0.009), подтверждая гипотезу о том, что цинакальцет может благоприятно влиять на прогрессирование сердечно-сосудистой кальцификации по сравнению с традиционной терапией стеролами витамина D (80). Исследование EVOLVE (http://clinicaltrials.gov/ct2/show/NCT00345839), предназначенное для оценки влияния цинакальцета на смертность и сердечно-сосудистые заболевания, будет доступно в ближайшем будущем и может пролить дополнительный свет на эти проблемы.
Какое будущее у SHPT Management?
Гиперплазия паращитовидных желез часто связана с подавлением апоптоза, и в настоящее время в лечении SHPT актуальной областью является усиление апоптотической активности.Прямая чрескожная инъекция в паращитовидные железы широко используется в Японии. Первоначальные исследования показали хорошие показатели эффективности при использовании этанола, хотя и за счет небольшого числа потенциально серьезных осложнений, отражающих непосредственную близость инъекции этанола к возвратному гортанному нерву и сонным артериям. В более поздних отчетах описывается прямая инъекция активных соединений витамина D, таких как кальцитриол и 22-оксакальцитриол. Эти агенты имеют гораздо более низкую местную токсичность, чем этанол, и не менее эффективны.Японские рекомендации по селективной чрескожной инъекционной терапии этанола (83) хорошо известны. Повторные инъекции активных стеролов витамина D непосредственно в паращитовидную железу показали индукцию апоптоза паратироидных клеток (84), не наблюдаемую при инъекции одного носителя. Неясно, отражают ли эти явления активность лиганда кальцитриола через его ядерный рецептор или высокие токсические локальные концентрации, хотя отсутствие влияния на гистологию железы контрольных инъекций с использованием одного носителя предполагает, что местная токсичность вспомогательных веществ и разбавителей не имеет значения.Эти результаты также демонстрируют поразительную активацию как VDR, так и CaSR в железах, получающих прямую инъекцию кальцитриола / максакальцитола, а также повышенную функциональность CaSR: сигмовидное соотношение между кальцием и ПТГ смещено влево в экспериментальной группе. Количество желез не является ограничивающим фактором, хотя чрезмерно большие (> 2000 мм 3 ) железы оказываются устойчивыми к этому типу вмешательства (85). In vitro культура нормальных желез, вырезанных у собак, показала, что кальцитриол подавляет как пролиферацию, так и апоптоз, но не оказывает общего влияния на размер железы (49).Однако в железах, взятых у пациентов с SHPT, только высокие концентрации кальцитриола были способны ингибировать пролиферацию или апоптоз.
В последнее время у крыс не было обнаружено индукции апоптоза клеток паращитовидной железы после активации CaSR кальцимиметиком R-568 (7). Исследование пациентов с паратиреоидэктомией показало высокое соотношение оксифилов / главных клеток в ткани паращитовидной железы у пациентов, получавших цинакальцет, кальцитриол и фосфатсвязывающие средства, по сравнению с пациентами, получавшими только кальцитриол и фосфатсвязывающие средства (86), что свидетельствует о том, что цинакальцет противодействует SHPT посредством двух синергетических механизмов. : антипролиферативный эффект и проапоптотический эффект на главные клетки (86).Лечение, которое может уменьшить размер увеличенных гиперпластических паращитовидных желез с помощью проапоптотических методов или даже остановить пролиферацию и, таким образом, подавить развитие гиперплазии за счет антипролиферативных эффектов, будет важным лечением SHPT в будущем.
Хирургическое вмешательство
Уменьшение размера паращитовидной железы с помощью фармацевтических средств уменьшит количество пациентов, которым требуется хирургическое вмешательство. Паратиреоидэктомия обычно рассматривается только в том случае, если текущее фармакологическое вмешательство не принесло результатов.Когда консервативная терапия больше не обеспечивает эффективного контроля (стойкие уровни ПТГ в сыворотке крови> 1000 пг / мл, связанные с гиперкальциемией) или резистентна к медикаментозной терапии, и когда объем хотя бы одной гиперпластической железы составляет> 500 мм 3 (41), Подходящим кандидатам проводится паратиреоидэктомия. Это высокоэффективное лечение, которое остается стандартом, по которому следует оценивать новые подходы. Паратиреоидэктомия значительно улучшает SHPT, увеличивая выживаемость и качество жизни пациентов у подходящих кандидатов (87).Однако SHPT может сохраняться или повторяться из-за гиперфункции остатка паращитовидной железы или аутотрансплантированной ткани паращитовидной железы, трансплантированной во избежание гипопаратиреоза. В последние годы хирургия улучшилась благодаря развитию малоинвазивной паратиреоидэктомии, хотя есть некоторые споры по поводу методологий и критериев, используемых в этой процедуре. Более поздние достижения в хирургических процедурах привели к развитию эндоскопической тотальной паратиреоидэктомии с аутотрансплантацией с предоперационной локализацией с помощью ультразвукового исследования паращитовидных желез и высокочувствительного радионуклидного сканирования 99m Tc-sestamibi (88).Эндоскопическая тотальная паратиреоидэктомия с методом аутотрансплантации облегчает предоперационные симптомы, улучшает или нормализует уровень минеральных веществ у большинства пациентов и, как было показано, безопасна для лечения SHPT, обеспечивая короткое пребывание в больнице и низкую частоту рецидивов для пациентов (88). Всем этим вариантам может помочь интраоперационный анализ паратиреоидного гормона, который использовался для руководства хирурга, особенно во время субтотальной паратиреоидэктомии.
Сводка
SHPT — это прогрессирующее заболевание, часто встречающееся у пациентов с ХБП и имеющее серьезные последствия для здоровья пациентов.При плохом контроле SHPT прогрессирует и может привести к заболеванию костей, кальцификации мягких тканей и кальцификации сосудов, что отрицательно влияет на заболеваемость и смертность. Традиционные методы лечения, направленные на снижение уровня витамина D и фосфора, не лишены недостатков. Появление кальцимиметиков и лучшее понимание сильных сторон и ограничений природных и активных соединений витамина D улучшили возможности лечения пациентов с SHPT.
Вторичный гиперпаратиреоз — симптомы, диагностика и лечение
Вторичный гиперпаратиреоз (SHPT) — это повышение уровня паратиреоидного гормона (PTH), вторичное по отношению к гипокальциемии.
ПТГ поддерживает гомеостаз кальция, воздействуя на почечные канальцы, на запасы кальция в скелетной системе и косвенно на желудочно-кишечный тракт за счет активации витамина D и энтерального всасывания.
Болезнь, наиболее часто связанная с SHPT, — это хроническая болезнь почек. Однако наиболее частой причиной SHPT является дефицит витамина D. Недостаточные запасы витамина D часто встречаются у пожилых людей, людей с синдромами мальабсорбции или лиц с ограниченным воздействием солнечного света.
Лечение включает соответствующее лечение основной причины и добавление витамина D. Паратиреоидэктомия требуется нечасто для удаления необратимо увеличенных паращитовидных желез с целью восстановления нормальной физиологии паращитовидных желез.
Без лечения он может привести к серьезным скелетным и сердечно-сосудистым осложнениям, которые способствуют общей заболеваемости и смертности.
Любое заболевание, приводящее к гипокальциемии, приводит к повышению уровня паратироидного гормона и может служить причиной вторичного гиперпаратиреоза (ВГПТ).Наиболее частыми причинами являются хроническая болезнь почек (ХБП), синдромы мальабсорбции и хроническое неадекватное воздействие солнечного света, действующее через изменения витамина D, фосфора и кальция.
SHPT является осложнением ХБП и играет важную роль в патогенезе ХБП-минеральной болезни кости (MBD). ХБП-МБД определяется как системное нарушение минерального и костного метаболизма, вызванное ХБП, проявляющееся одним или комбинацией следующих факторов: нарушения метаболизма кальция, фосфора, ПТГ или витамина D; аномалии обмена костной ткани, минерализации, объема, линейного роста или прочности; кальцификация сосудов или других мягких тканей.[1] Руководство по клинической практике болезни почек: улучшение глобальных результатов (KDIGO). Диагностика, оценка, профилактика и лечение хронической болезни почек — минеральной и костной недостаточности (CKD-MBD). 2009; выборочное обновление 2017 [интернет-издание].
CKD-Mineral and Bone Disorder (CKD-MBD)
Вторичный (почечный) и третичный гиперпаратиреоз
Что такое вторичный гиперпаратиреоз?
При вторичном гиперпаратиреозе что-то в организме заставляет паращитовидные железы производить дополнительный ПТГ.Железы на самом деле делают то, что должны делать. Если проблему в других частях тела можно исправить, паращитовидные железы вернутся к нормальной работе. Вторичный гиперпаратиреоз, вызванный дефицитом витамина D, легко лечится медикаментами и не требует хирургического вмешательства. Вторичный гиперпаратиреоз, вызванный почечной недостаточностью, часто можно контролировать с помощью лекарства под названием цинакальцет. Когда пациенты находятся на диализе в течение многих лет или цинкальцет не может контролировать выработку ПТГ, уровни ПТГ могут быть чрезвычайно высокими, и может потребоваться операция на паращитовидных железах.Все четыре паращитовидные железы вовлечены в этот болезненный процесс.
Помимо симптомов, наблюдаемых при первичном гиперпаратиреозе, могут развиваться другие признаки, симптомы и осложнения вторичного гиперпаратиреоза, в том числе:
- Деформации, переломы и снижение плотности костей
- Отложение кальция в жире
- Сильный кожный зуд
- Открытые незаживающие раны
Тяжелый вторичный гиперпаратиреоз может привести к кальцифилаксии, которая является опасным для жизни состоянием.Кальцифилаксия может привести к ранам мягких тканей, которые не заживут, пока гиперпаратиреоз не будет взят под контроль. Хронические незаживающие раны могут привести к обширной инфекции (сепсису) и смерти.
Что такое третичный гиперпаратиреоз?
У многих пациентов, перенесших трансплантацию почек, функция паращитовидных желез возвращается к норме. У некоторых пациентов паращитовидные железы функционировали ненормально так долго, пока пациенты страдают почечной недостаточностью и находятся на диализе, что функция паращитовидных желез никогда не возвращается к норме.Чрезвычайно важно защитить пересаженную почку от любых негативных эффектов, которые избыток паратиреоидного гормона может оказать на почки (камни в почках, снижение функции, обезвоживание, которое часто сопровождает высокий уровень кальция). Пациенты с третичным гиперпаратиреозом обычно направляются на операцию на паращитовидных железах.
Вторичный гиперпаратиреоз и хроническая болезнь почек
Резюме
Кратко
Вторичный гиперпаратиреоз (SHPT) описывает сложное изменение в кости и минеральный обмен, который происходит в результате хронической почечной недостаточности. болезнь (ХБП).Заболевание костей, хорошо известное осложнение SHPT, представляет собой лишь небольшую проблему в свете данных, которые коррелируют с SHPT с сердечно-сосудистыми заболеваниями и повышенным риском заболеваемости и смертности у пациентов с ХБП. Пациенты с легкой формой ХБП могут протекать бессимптомно и, следовательно, не могут быть идентифицированы до тех пор, пока не начнется патология SHPT. Идентификация пациенты из группы риска и обследование на SHPT обязательно, потому что раннее вмешательство может замедлить или остановить прогрессирование как костной, так и сердечной болезнь.Диетические проблемы, фармакотерапия и приверженность пациента — все это важные соображения при создании успешного плана лечения.
Хроническая болезнь почек (ХБП) — очень распространенная проблема со здоровьем в США и чаще всего является следствием хронических заболеваний, в частности сахарный диабет или гипертония. Поскольку примерно у 40% пациентов с диабетом развивается нефропатия, только диабетики будут составлять 12 миллионов человек с CKD. Пять стадий ХБП используются для стратификации пациентов в зависимости от степени функция почек и действуют как маркеры для прогнозирования развития сопутствующих заболеваний ХБП, например вторичный гиперпаратиреоз (ВГПТ).Исследования показали, что Пациенты с ХБП, которые классифицируются как стадия 3, стадия 4 или стадия 5, находятся в группе риска. для SHPT или, возможно, уже разработали. Раннее выявление и лечение SHPT имеет решающее значение для предотвращения или контроля последствий это осложнение.
Патофизиология SHPT
Паращитовидные железы — это четыре железы размером с горошину, расположенные на щитовидной железе. железа в шее. Хотя их названия похожи, щитовидная железа и паращитовидные железы — это совершенно разные железы, каждая из которых производит разные гормоны со специфическими функциями.Паращитовидные железы выделяют паращитовидные железы. гормон (ПТГ), полипептид, который помогает поддерживать правильный баланс кальций и фосфор в организме. ПТГ участвует в гомеостазе метаболизм костей за счет регулирования уровня кальция в крови, высвобождение кальций из костей, всасывание кальция из кишечника и выведение кальций в моче. Следовательно, уровень кальция и других минералов участвуют в метаболизме костей, такие как фосфор и витамин D, влияют на секреция ПТГ паращитовидной железой.Вся молекула ПТГ состоит из последовательности из 84 аминокислот, называемой интактным гормоном (iPTH). Хотя более мелкие фрагменты этой молекулы могут обладать уникальными действиями в тела, как правило, iPTH измеряется и используется для оценки метаболизма костей и болезнь костей.
Рисунок 1.Патофизиология вторичного гиперпаратиреоза.
SHPT вторичный по отношению к CKD — это перепроизводство PTH, вызванное несколькими изменениями которые происходят в костях и минеральном обмене в результате почечной недостаточности функция (рисунок 1).Первое изменения, которые обычно возникают при снижении функции почек, включают: дефицит активированного витамина D и увеличение выведения фосфора за счет остальные функциональные нефроны. Оба эти изменения стимулируют рост в синтезе и секреции ПТГ.
Витамин D
Термин «витамин D» используется в общем для обозначения многих вещества или формы витамина D. В организме витамин D 3 является активная форма витамина D. Предшественниками гормона витамина D 3 являются полученные из пищевых источников и воздействия ультрафиолета.Эти предшественники затем проходят две важные ферментативные реакции. Образовавшийся кальцитриол или активный витамин D 3 [1,25- (OH) 2 D 3 )] молекула активная форма, которая связывается с рецептором витамина D (VDR). 1 Ниже нормы обстоятельства, витамин D 3 играет жизненно важную роль в регулировании ПТГ синтез и выпуск. Стимулируя VDR паращитовидных желез, он снижает производство ПТГ. Витамин D 3 также косвенно снижает уровень паратгормона. стимуляция VDR в кишечнике, тем самым увеличивая абсорбцию кальция и сыворотки кальций. 2,3 По мере снижения функции почек происходит снижение почечной 1α-гидроксилазы. активность, которая отвечает за окончательную реакцию гидроксилирования в синтез кальцитриола. При обострении ХБП почки становятся менее способными выполнять 1α-гидроксилирование и, следовательно, активный витамин D 3 уровни становятся недостаточными и повышают уровень ПТГ концентрации. 4
Метаболизм фосфора
По мере снижения скорости клубочковой фильтрации (СКФ) до <60 мл / мин / 1,73 m 2 , экскреция фосфора в нефроне нарушается.Несмотря на то что половина нефронов не выводит фосфор, остальные нефроны компенсируют чрезмерное выделение фосфора в сутки для поддержания нормальные концентрации фосфора в сыворотке. Компенсация обычно может продолжаться пока СКФ не снизится до <25–40 мл / мин / 1,73 м 2 . С участием прогрессирующая ХБП, когда оставшиеся нефроны уже не могут в достаточной степени выводят фосфорную нагрузку, обнаруживается гиперфосфатемия.
Кальций, двухвалентный катион, и фосфор, одновалентный анион, имеют высокую связывающее сродство друг к другу.В сыворотке, как концентрация одного или оба иона увеличиваются, существует повышенный риск образования ионной связи, создание нерастворимого комплекса. Этот процесс может привести к появлению экстраскелетных кальцификация и потенциально кальцифилаксия или сердечная болезнь. 5 Кроме того, преципитация может снизить концентрацию кальция в сыворотке крови. дальнейшая стимуляция секреции ПТГ. Фактически, производство и секреция ПТГ могут стимулироваться гипокальциемией, гиперфосфатемией и витамином D дефицит. 6,7 Поскольку ПТГ в основном отвечает за предотвращение гипокальциемии, он стимулирует остеокласты лизируют кость, высвобождая кальций в сыворотку.Под нормальным условий, существует гомеостаз, связанный с активностью остеокластов и остеобластов. синтетическая активность. SHPT вызывает дисбаланс этих действий, что приводит к усиление разрушения костей, которое приводит к почечной остеодистрофия. 8,9
Воздействие и последствия SHPT: Болезнь костей
Почечная остеодистрофия относится к нескольким заболеваниям костей, которые возникают в результате патофизиология костного и минерального обмена при ХБП: фиброзный остит. кистозная болезнь, остеомаляция и адинамическая болезнь костей.Кистозный фиброзный остеит называется болезнью костей с высоким обменом веществ и ассоциируется с повышенным уровнем ПТГ. концентрации, которые стимулируют активность остеокластов, разрушение костей и рассасывание. Остеомаляция («мягкая кость») характеризуется низким оборот костей и аномальная минерализация и исторически связанный с алюминием токсичность. 8,10 Адинамическая болезнь костей относится к малооборотным заболеваниям с нормальным минерализация и может быть результатом низкого уровня ПТГ уровни. 11 В распространенность адинамической болезни костей составляет увеличение 11 и может быть следствием чрезмерного подавления ПТГ из-за употребления витамина D агенты, кальцимиметики и фосфатсвязывающие вещества, по отдельности или в комбинации.
Влияние изменений: внескелетная кальцификация
Помимо минеральных дефектов и болезней костей, изменения в кальции, фосфор, витамин D и ПТГ вызывают другие пагубные последствия для пациенты с ХБП. Внескелетный кальциноз (прежде всего сердечно-сосудистый кальциноз) был зарегистрирован у пациентов с CKD 12 и является напрямую связаны с увеличением сердечно-сосудистой заболеваемости и смертность. 13 Пациенты с ХБП, особенно с терминальной стадией почечной недостаточности (ТПН), имеют повышенный риск сердечно-сосудистых заболеваний и смертности.Фактически, исследования показал, что основной причиной смерти пациентов с ТПН является сердечно-сосудистый болезнь. 14 Исследование пациентов, находящихся на гемодиализе, обнаружили, что даже при стратификации по таким переменным что касается пола, расы и наличия диабета, пациенты на диализе все еще смертность от сердечно-сосудистых заболеваний почти в 30 раз выше, чем общая численность населения. 15
Определенно коморбидные расстройства, такие как диабет, гипертония, гиперлипидемия и анемия играют роль в этих результатах.Однако недавние исследования также определили сердечно-сосудистую кальцификацию как способствующую фактор. Была проведена корреляция между сердечно-сосудистой кальцификацией и такие факторы, как гиперфосфатемия, повышенное содержание фосфора кальция (Ca × P), гиперкальциемия, терапия витамином D и повышенные дозы кальцийсодержащие фосфатсвязывающие и кальциевые добавки.
Баланс кальция, фосфора, витамина D и iPTH сложный и взаимосвязаны. Пациенты должны придерживаться диетических ограничений, диализа. терапии и сложные схемы приема лекарств.Эти факторы создают препятствия достижению и поддержанию контроля над SHPT. Фактически, одно исследование из почти 200 амбулаторные пациенты с хроническим гемодиализом показали, что <10% пациентов могут быть одновременно поддерживается в целевых диапазонах вышеуказанных параметры. 16
Цели лечения SHPT
Конечными целями лечения SHPT являются нормализация минерального обмена, предотвратить заболевание костей и предотвратить экстраскелетные проявления измененных биохимические процессы.Маркеры кальция, фосфора, витамина D и iPTH используются в качестве суррогатных показателей прогрессирования заболевания. Это важно выявить SHPT на ранней стадии. Аномалии могут возникать незаметно, обычно без каких-либо симптомы и могут прогрессировать, вызывая больше осложнений, если не обнаружены на ранней стадии. До недавнего времени считалось, что гиперфосфатемия является самым ранним признаком SHPT и нарушения костного обмена. Однако, когда пациенты достигают 3 стадии ХБП, весьма вероятно, что ни один из биохимических параметров обычно не оценивается будет ненормально.Фактически, уровень iPTH часто повышается перед клиническая гиперфосфатемия происходит. 17–19 По этой причине Национальный фонд почек по результатам заболеваний почек Руководящие принципы Инициативы качества (KQODI) рекомендуют всем пациентам с СКФ <60 мл / мин / 1,73 м 2 пройти оценку сывороточного кальция, уровни фосфора и iPTH (Таблица 1). Кроме того, если концентрация iPTH превышает ХБП специфическая для стадии цель, уровень 25 (OH) D (предшественник активированного витамина D 2,3 ) следует обследовать и лечить.Надеюсь, раньше идентификация и оценка SHPT улучшит метаболизм костей и минералов при ХБП и уменьшить связанные с ней осложнения (например, переломы, боль и сердечно-сосудистая кальцификация).
Таблица 1.Целевые диапазоны и частота мониторинга биохимических Параметры * 20
Ведение SHPT-терапии витамином D на 3-й и 4-й стадиях ХБП
Для пациентов с 3-й или 4-й стадией ХБП, одной из первых аномалий отмеченное при оценке, может быть изолированное увеличение iPTH.Если iPTH превышает целевой диапазон, концентрация 25 (OH) D в сыворотке должна быть измеренным, и если окажется, что он <30 нг / мл, эргокальциферол (витамин D 2 ) следует начать терапию (Таблица 2). Если концентрация 25 (OH) D составляет> 30 нг / мл, а концентрация iPTH превышает целевую диапазона, следует начать прием активированного витамина D (Стол 3). 20 Независимо от того, какой витамин D используется, кальций и фосфор концентрации должны контролироваться и поддерживаться в пределах целевого диапазона, чтобы предотвратить осаждение кальция в мягких тканях и сосудистой сети.
Таблица 2.Дозирование перорального эргокальциферола пациентам с ХБП 3 и 4 20 *
Таблица 3.Начальная доза пероральной терапии стеролами витамина D для лечения повышенного iPTH Концентрации у пациентов с ХБП 3 и 4 33 *
Ограничение количества фосфатов в пище
Гиперфосфатемия обычно становится превалирующей, когда СКФ снижается до < 30 мл / мин / л.73 м 2 .
Ограничение количества фосфатов в пище — одно из первых рекомендованных вмешательств для снижения концентрации фосфата в сыворотке. Продукты с высоким содержанием фосфатов Содержание включает молочные продукты, мясо, бобы, темные газированные напитки, пиво и орехи. Много продукты с высоким содержанием фосфора также являются основными источниками белка, особенно мясо. Как правило, пациентам рекомендуется уменьшить потребление употреблять или избегать продуктов с высоким содержанием фосфора, но не с высоким содержанием белка. Примеры продуктов, которых следует избегать, включают сыр, молоко, мороженое, пиво и темные напитки. газированные напитки.Источники белка не исключаются, потому что плохое питание может привести к гипоальбуминемия, которая была связана с повышенной заболеваемостью и смертность при ХБП. Одного ограничения фосфатов в пище часто недостаточно для поддерживать концентрацию фосфора в сыворотке крови в целевом диапазоне. В этом случае, фосфатсвязывающие средства могут использоваться для предотвращения гиперфосфатемии.
Фосфатсвязывающие агенты
Фосфатсвязывающие агенты снижают концентрацию фосфатов в сыворотке за счет связывания в пищевой фосфат в кишечнике, образуя нерастворимый комплекс, который выводится из организма в кале.Оптимально эти агенты вводить с пищей и обычно принимается три раза в день во время еды. Пациенты, нуждающиеся в энтеральном введении кормления могут потребовать более частого приема. Самый большой вызов Успешное использование фосфатсвязывающих средств — это принятие и соблюдение пациентом режима лечения. Просвещение пациентов является обязательным, потому что эти лекарства необходимо принимать. несколько раз в день и может значительно увеличить прием лекарств пациента груз. В таблице 4 перечислены некоторые из наиболее часто используемые продукты и лекарственные формы.
Таблица 4.Примеры фосфатсвязывающих препаратов и начального дозирования Информация
Фосфатные связующие разных классов можно комбинировать для достижения цели концентрации фосфора и кальция. Фактически, комбинированное использование кальцийсодержащий фосфатный связующий и не содержащий кальций фосфатное связующее может снизить уровень фосфора в сыворотке при сохранении концентрация кальция. Аналогичным образом, использование одного или нескольких не содержащие кальций фосфатсвязывающие вещества (например,g., севеламера гидрохлорид, карбонат лантана и алюминия) может потребоваться пациентам с гиперфосфатемия с сопутствующей гиперкальциемией. Часто пациенты с ХБП требуется терапия для снижения концентрации фосфора в сыворотке крови и iPTH. Фосфат связующие вещества обычно используются одновременно с терапией витамином D или кальцимиметический агент для контроля всех задействованных биохимических параметров (т.е. кальций, фосфор, Ca × P и iPTH).
Терапия витамином D на стадии 5 CKD
Как описано ранее, витамин D необходим для многих физиологических заболеваний. процессы.Терапию эргокальциферолом следует начинать при любой ХБП. стадия, если концентрация 25 (OH) D <30 нг / мл. Для всех пациентов 5 стадии ХБП, а также пациенты 3 и 4 стадий с нормальным или повышенным 25 (OH) D концентрации активированного витамина D следует начинать, когда iPTH уровни превышают цель диапазон. 20
В настоящее время существует три коммерчески доступных препарата витамина D в Соединенные Штаты. Кальцитриол был первым доступным агентом. Он имеет то же самое структура как эндогенный активированный витамин D 3 [1,25 (OH) D 3 ] и, следовательно, те же фармакологические действия.Это стимулирует рецепторы VDR кишечника и паращитовидных желез. Из-за его близости к кишечный VDR, кальцитриол имеет наибольшую склонность к увеличению сывороточного концентрация кальция трех витаминов D агенты. 21,22 Доступны как пероральные, так и инъекционные формы. В целом, кальцитриол является наименее дорогим из имеющихся пероральных или инъекционных продуктов, и агент первой линии. Это особенно полезно, когда уровень кальция в сыворотке меньше средней точки целевого диапазона.
Парикальцитол и доксеркальциферол являются веществами витамина D с меньшим содержанием сродство к кишечным рецепторам и, следовательно, было показано, что они вызывают меньшая частота гиперкальциемия. 23 Некоторые исследования показали, что доксеркальциферол вызывает большую гиперкальциемию, чем парикальцитол. Это открытие спорно; учеба была трудной интерпретировать из-за одновременного приема лекарств, в частности кальцийсодержащий продукты. 24,25 Одно заметное различие между этими двумя агентами заключается в том, что доксеркальциферол является пролекарство витамина D 2 , 1α (OH) D 2 и требует активация печеночной 25-гидроксилазой. Следовательно, доксеркальциферол нельзя используется у пациентов с нарушением функции печени.
При использовании любого витамина D риск повышения уровня кальция в сыворотке крови. концентрации выше при пероральном приеме лекарств, чем при вводится внутривенно. Все препараты витамина D следует титровать до поддерживать iPTH, кальций, фосфор и Ca × P в пределах цели KDOQI диапазоны. Из-за риска гиперкальциемии, недоступности специфического агента или других факторов, может потребоваться переключение продуктов и преобразование дозы. Терапию любыми препаратами витамина D следует начинать только тогда, когда концентрации кальция и фосфора в сыворотке находятся в пределах целевого диапазона.В Дозу витамина D следует уменьшить или временно отменить, если Ca × P составляет> 55 мг 2 / дл 2 , чтобы минимизировать риск экстраскелетный кальциноз. Аналогичным образом следует уменьшить дозу витамина D. или временно прекращено, если концентрация iPTH упадет ниже нижнего предела. предел целевого диапазона, чтобы избежать риска адинамической болезни костей.
Рисунок 2.Пример алгоритма лечения минеральной и костной ткани ХБП расстройства у пациентов с повышенным iPTH и нормальным / низким содержанием кальция концентрации.
Рисунок 3.Пример алгоритма лечения ХБП минералов и костей расстройств у пациентов с повышенными концентрациями iPTH и нормальным / высоким концентрации кальция.
Кальцимиметики
Цинакальцет — первый кальцимиметический агент, доступный в США. Состояния. 26,27 Цинакальцет был одобрен к применению после публикации рекомендаций KDOQI 2003 г. и не фигурирует ни в одном из руководящих принципов или алгоритмов.Он действует путем привязки к и изменение рецептора, чувствительного к кальцию на главной клетке паращитовидная железа. Это изменение вызывает повышенную чувствительность рецептора. к сывороточному кальцию. Цинакальцет эффективен для снижения концентрации iPTH. и поддержание кальция и фосфора концентрации. 28,29 Его можно использовать в сочетании с фосфатсвязывающими веществами и веществами витамина D. В Начальная доза цинакальцета составляет 30 мг внутрь 1 раз в сутки. Доза может быть титруется с шагом 30 мг каждые 2–4 недели, пока iPTH не будет в пределах был достигнут целевой диапазон или максимальная доза 180 мг в день.
Пациенты могут испытывать преходящую тошноту и рвоту. Однако большинство Важным побочным эффектом терапии цинакальцетом является риск гипокальциемии, прямой результат механизма действия cinacalcet. Таким образом, цинакальцет не должен начинать у пациентов, если скорректированная концентрация кальция в сыворотке < 8,4 мг / дл. Кроме того, концентрации кальция и фосфата должны быть полученные в течение 1 недели после начала приема или изменения дозы. Концентрация iPTH следует контролировать между 1 неделей и 1 месяцем от начала или после введения дозы изменение.Поскольку цинакальцет снижает уровень кальция в сыворотке крови, он также может снижать содержание кальция в крови. × P. Как и в случае со всеми препаратами витамина D, доза цинакальцета должна быть снижается или прекращается, если концентрация iPTH падает ниже целевого уровня диапазон для предотвращения адинамической кости болезнь. 30–32
Цинакальцет предлагает новую стратегию лечения, когда используется отдельно, с фосфатом связующие, или в сочетании с фосфат-связующими и терапией витамином D. Рисунки 2 и 3 изображают возможные алгоритмы для использования в фармакотерапии.
Заключение
ШПТ — сложное и непростое состояние. Метаболические параметры, такие как кальций, фосфат, Ca × P, iPTH и витамин D необходимо поддерживать в пределах целевого диапазона для предотвращения заболеваний костей и внескелетной кальцификации, снизить риск сердечных заболеваний и поддерживать гомеостаз других систем организма. Кроме того, все эти параметры необходимо контролировать одновременно, чтобы быть успешным.
Возможно, самая сложная проблема в лечении SHPT — это принятие и соблюдение пациентом режима лечения.Сложные схемы приема лекарств, которые включают: прием лекарств несколько раз в день, высокая дозировка таблеток, сопутствующая патология условия, финансовые ограничения, психосоциальные проблемы и диета ограничения — это все факторы, которые увеличивают частоту несоблюдения и препятствуют успех лечения. Поддержание метаболизма костей и минералов 15 — непростая задача для всех поставщиков медицинских услуг и требует многопрофильного командного подхода. Диетологи могут сыграть решающую роль в лечении SHPT, работая с пациенты для разработки планов питания, которые ограничивают количество фосфора при обеспечении оптимального потребления белка.Они также могут порекомендовать протеин. добавки или другие диетические добавки для оптимального баланса питания. Фармацевтов и социальные работники часто вовлечены в сложный процесс получения лекарства для пациентов с ограниченными ресурсами или льготы на лекарства, отпускаемые по рецепту, которые имеют ограничения для определенных агентов. Некоторые могут работать со страховыми компаниями и врачи для получения предварительного разрешения или доступа к помощи пациента программы через фармацевтическую промышленность или общественные ресурсы. Врачи, медсестры, фармацевты, социальные работники, физиотерапевты и почти все другие специалисты в области здравоохранения могут сыграть свою роль в управлении SHPT.Усиление приверженности к лекарствам, диете и физическим упражнениям и обеспечение положительное подкрепление в разных дисциплинах имеет решающее значение для успешного управление ШПТ.
Сноски
Сара Томаселло, PharmD, BCPS, клинический доцент кафедры аптека и клинический специалист по нефрологии в Школе Эрнеста Марио Аптека в Университете Рутгерса в Пискатауэй, штат Нью-Джерси
- Американская диабетическая ассоциация
Ссылки
- ↵
Haussler MR, Whitfield GK, Haussler CA, Hsieh JC, Thompson PD, Selznick SH, Dominguez CE, Юрутка П.В.: Ядерный рецептор витамина D: биологический и молекулярный выявлены регулирующие свойства.Дж Боун Мин Res13 : 325–349,1998
- ↵
Коричневый AJ: Витамин D. Am J Physiol 277: 157 –175, 1999
- ↵
Holick MF: Витамин D для здоровья и при хронических заболеваниях почек. Сем Диализ 18: 266 –275, 2005
- ↵
Malluche HH, Mawad H, Koszewski NJ: Обновленная информация о витамине D и его новых аналогах: действия и Обоснование лечения хронической почечной недостаточности. Почка Инт 62: 367 –374, 2002
- ↵
Блок GA, порт FK: Метаболизм фосфата кальция и сердечно-сосудистые заболевания у пациентов с хроническое заболевание почек.Семенной диализ16 : 140–147,2003
- ↵
Фридман EA: Последствия и лечение гиперфосфатемии у пациентов с почечной недостаточностью. недостаточность. Почки Инт 65 (Дополнение): S1 – S7,2005
- ↵
Qunibi WY: Последствия гиперфосфатемии у пациентов с терминальной стадией почечной недостаточности (ESRD). Почки Инт 64 (Дополнение): S8 – S12,2004
- ↵
Hernandez JD, Wesseling K, Salusky IB: Роль паратиреоидного гормона и терапия активными стеролы витамина D при почечной остеодистрофии.Сем Диализ 18: 290 –295, 2005
- ↵
Cozzolino M, Бранкаччо Д., Галлиени М., Галасси А., Слатопольский Э., Дуссо А. Патогенез гиперплазия паращитовидных желез при почечной недостаточности. Дж. Нефрол 18 : 5–8,2005
- ↵
Horl WH: клинические последствия вторичного гиперпаратиреоза: акцент на клинические результаты. Пересадка нефрола при диализе19 (Приложение 5): V2 –V8, 2004
- ↵
Coen G: Adynamic болезнь костей: обновление и обзор.Дж. Нефрол 18 : 117–122,2005
- ↵
Goodman WG, Goldin J, Куизон Б.Д., Юн С., Гейлс Б., Сидер Д., Ван И, Чанг Дж., Эмерик А., Гризер Л., Елашов Р.М., Салуский И.Б.: Кальцификация коронарных артерий у молодых людей с терминальная стадия почечной недостаточности, находящихся на диализе. N Engl J Med 342: 1478 –1483, 2000
- ↵
Блок GA, Hulbert-Shearon TE, Levin NW, Port FK: Ассоциация сывороточного фосфора и кальций × фосфатный продукт с риском смерти при хроническом гемодиализе пациенты: национальное исследование.Am J почек 31 : 607–617,1998
- ↵
Система данных по почкам США: USRDS Годовой отчет за 2006 год: Атлас терминальной стадии почечной недостаточности в США Состояния. Бетесада, штат Мэриленд, Национальные институты здравоохранения, Национальный Институт диабета, болезней органов пищеварения и почек, 2006
- ↵
Block GA, Klassen PS, Lazarus JM, Ofsthun N, Lowrie EG, Chertow GM: Минеральный метаболизм, смертность и заболеваемость при поддерживающем гемодиализе. J Am Soc Нефрол 15: 2208 –2218, 2004
- ↵
Tomasello S, Дхупар С., Шерман Р. Фосфатные связующие, рекомендации K / DOQI и соответствие: несчастная реальность.Трансплантация диализа33 : 236–242,2004
- ↵
Cozzolino M, Бранкаччо Д., Галлиени М., Слатопольский Э. Патогенез сосудов кальциноз при хронической болезни почек. Почки Int68 : 429–436,2005
Левин А., Бакрис Г.Л., Молитч М., Смолдерс М., Тиан Дж., Уильямс Л.А., Андресс Д.Л.: Распространенность аномальные уровни витамина D, ПТГ, кальция и фосфора в сыворотке у пациентов с хроническое заболевание почек: результаты исследования для оценки раннего заболевания почек.Почки Инт 71:31 –38, 2007
- ↵
de Francisco ALM: Вторичный гиперпаратиреоз: обзор болезни и способов ее лечения. Clin Ther 26: 1976 –1993, 2004
- ↵
Национальный фонд почек: Bone метаболизм и заболевание при хронической болезни почек. Am J Kidney Дис 43: S1 –S201, 2003
- ↵
Stim JA, Lowe J, Arruda JA, Dunea G: Внутривенное введение кальцитриола один раз в неделю подавляет гиперпаратиреоз у пациентов, находящихся на гемодиализе.ASAIO J41 : M693 – M698,1995
- ↵
Sprague SM, Llach F, Amdahl M, Taccetta C, Batlle D: Парикальцитол по сравнению с кальцитриолом в лечение вторичного гиперпаратиреоза. Почки Int63 : 1483–1490,2003
- ↵
Andress DL: Лечение витамином D при хронической болезни почек. Сем Диализ. 18: 315 –321, 2005
- ↵
Зисман А.Л., Ghantous W, Schinleber P, Roberts L, Sprague SM: Подавление паращитовидных желез гормон: исследование эквивалентности доз парикальцитола и доксеркальциферола.Am J Nephrol 25: 591 –595, 2005
- ↵
Drueke TB: Какой производное витамина D для назначения пациентам с заболеваниями почек. Curr мнение Нефрол Гипертония 14: 343 –349, 2005
- ↵
Quarles LD: Цинакальцет HCl: новое средство лечения вторичного гиперпаратиреоза на стадии 5 хроническое заболевание почек. Почки Int65 (Дополнение): S24 –S28, 2005
- ↵
Joy MS, Кширсагар А.В., Франческини Н.: Кальцимиметики и лечение первичных и вторичных гиперпаратиреоз.Энн Фармакотер38 : 1871–1880,2004
- ↵
Charytan C, Coburn JW, Chonchol M, Herman J, Lien YH, Liu W., Klassen PS, McCary LC, Pichette V: Цинакальцета гидрохлорид является эффективным средством лечения вторичных гиперпаратиреоз у пациентов с ХБП, не получающих диализ. Являюсь Дж. Почки Дис 46:58 –67, 2005
- ↵
Moe SM, Chertow ГМ, Коберн Дж. У., Куорлз Л. Д., Гудман РГ, Блок Г. А., Дрюке Т. Б., Каннингем Дж., Шеррард DJ, Маккари Л.К., Олсон К.А., Тернер С.А., Мартин К.Дж.: достижение NKF-K / DOQI метаболизм костей и цели лечения заболеваний с помощью цинакальцета HCl.Почки Инт 67: 760 –771, 2005
- ↵
Шахапуни I, Mansour J, Harbouche L, Maouad B, Benyahia M, Rahmouni K, Oprisiu R, Bonne JF, Monge M, El Esper N, Presne C, Moriniere P, Choukroun G, Fournier A: Как подходят ли кальцимиметики для лечения паратиреоидного гормона, кальция и фосфатные нарушения у диализных пациентов? Сем Диализ 18: 226 –238, 2005
Moe SM, Cunningham Дж., Боммер Дж., Адлер С., Росанский С.Дж., Урена-Торрес П., Альбизем М.Б., Гуо М.Д., Зани VJ, Goodman WG, Sprague SM: Долгосрочное лечение вторичного гиперпаратиреоз с кальцимиметическим цинакальцетом HCl.Нефрол Пересадка диализа 20: 2186 –2193, 2005
- ↵
Moe SM, Chertow ГМ, Коберн Дж. У., Куорлз Л. Д., Гудман РГ, Блок Г. А., Дрюке Т. Б., Каннингем Дж., Шеррард DJ, Маккари Л.К., Олсон К.А., Тернер С.А., Мартин К.Дж.: достижение NKF-K / DOQI метаболизм костей и цели лечения заболеваний с помощью цинакальцета HCl. Почки Инт 67: 760 –771, 2005
- ↵
Бейли Г.Р., Массри SG, Национальный фонд почек: Руководство по клинической практике для костей метаболизм и болезнь при хронической болезни почек: обзор.Pharmacother 25: 1687 –1707, 2005
Лечение, симптомы, причины и диагностика
Обзор
Четыре паращитовидные железы размером с горошину расположены на внешней стороне щитовидной железы в области шеи.Что такое гиперпаратиреоз?
Гиперпаратиреоз — это состояние, при котором одна или несколько ваших паращитовидных желез становятся сверхактивными и выделяют (секретируют) слишком много паратиреоидного гормона (ПТГ). Это вызывает повышение уровня кальция в крови — состояние, известное как гиперкальциемия.
Что такое паращитовидные железы?
Ваши паращитовидные железы вырабатывают ПТГ, чтобы контролировать уровень кальция и фосфора в организме. У вас есть четыре паращитовидные железы, расположенные на внешних границах тыльной стороны вашей щитовидной железы. Щитовидная железа расположена в передней части шеи.
Что происходит, когда в моем организме циркулирует слишком много гормона паращитовидной железы (ПТГ)?
Если у вас сверхактивная паращитовидная железа, одна или несколько паращитовидных желез вырабатывают слишком много паратироидного гормона (ПТГ).Слишком много ПТГ сигнализирует вашему телу о необходимости сделать больше кальция доступным. Ваше тело отвечает:
- Выделение большего количества кальция в кровь из костей (где хранится большая часть кальция). Потеря кальция из ваших костей ослабляет их и увеличивает риск перелома.
- Ваш пищеварительный тракт усваивает больше кальция из пищи, которую вы едите.
- Почки удерживают кальций и возвращают его в кровь вместо того, чтобы вымывать его с мочой. Избыток кальция в почках может вызвать образование камней в почках.
Кто заболевает гиперпаратиреозом?
Приблизительно у 100 000 человек в США ежегодно развивается гиперпаратиреоз. Пожилые женщины в постменопаузе подвергаются наибольшему риску заболевания.
Симптомы и причины
Как возникает гиперпаратиреоз?
Существует два типа гиперпаратиреоза, первичный и вторичный:
- При первичном гиперпаратиреозе ваши паращитовидные железы вырабатывают слишком много ПТГ, что приводит к повышению уровня кальция в крови.
- При вторичном гиперпаратиреозе гиперактивность паращитовидных желез возникает в ответ на другое состояние, вызывающее потерю кальция. Гиперактивность паращитовидных желез — это попытка вашего тела поддерживать нормальный уровень кальция. Примеры состояний, при которых снижается уровень кальция, включают почечную недостаточность, тяжелый дефицит витамина D и тяжелый дефицит кальция.
Причины первичного гиперпаратиреоза включают:
- Доброкачественное образование, называемое аденомой, формируется на единственной паращитовидной железе.Аденома заставляет железу перерабатывать и вырабатывать больше ПТГ. Это самая частая причина.
- Две или более паращитовидных желез увеличиваются в размерах (состояние, называемое гиперплазией), и производят слишком много гормонов.
- Лучевая терапия в области шеи.
- Унаследованные состояния, например множественная эндокринная неоплазия типа 1. Это редкая причина.
- Рак паращитовидной железы (редко).
Каковы симптомы гиперпаратиреоза?
Если у вас гиперпаратиреоз на ранней стадии, симптомы могут отсутствовать.Если у вас гиперпаратиреоз легкой степени, у вас могут быть следующие симптомы:
- Боль в суставах.
- Мышечная слабость.
- Чувство усталости.
- Депрессия.
- Проблемы с концентрацией внимания.
- Потеря аппетита.
Если ваш гиперпаратиреоз более тяжелый, у вас могут быть следующие симптомы:
- Тошнота и рвота.
- Замешательство, забывчивость.
- Повышенная жажда и потребность в мочеиспускании.
- Запор.
- Боль в костях.
Другие проблемы, связанные с тяжелым гиперпаратиреозом, включают:
Диагностика и тесты
Как диагностируется гиперпаратиреоз?
Поскольку симптомы гиперпаратиреоза могут быть несуществующими, легкими или обычными для многих других заболеваний, диагноз гиперпаратиреоза может быть пропущен. Часто это состояние обнаруживается с помощью анализа крови, который назначают для другого заболевания.
Если у вас первичный гиперпаратиреоз, ваш анализ крови покажет уровень кальция и паратиреоидного гормона выше нормы.Ваш врач может заказать сканирование сестамиби, чтобы проверить наличие каких-либо новообразований на паращитовидных железах или их увеличения.
Могут быть назначены другие тесты для выявления осложнений гиперпаратиреоза. Эти тесты могут включать:
- Анализ крови для проверки уровня витамина D. Низкий уровень витамина D — это обычное явление, если у вас гиперпаратиреоз.
- Тест плотности костной ткани для проверки потери костной массы.
- Ультразвук или другой визуализирующий тест почек для выявления камней в почках.
- 24-часовой тест на сбор мочи для измерения количества кальция и других химических веществ в моче, чтобы помочь определить причину гиперпаратиреоза.
- Анализы крови, чтобы проверить, насколько хорошо работают ваши почки.
Ведение и лечение
Как лечится гиперпаратиреоз?
Если у вас гиперпаратиреоз легкой степени (без симптомов, уровень кальция в крови лишь незначительно повышен), ваш лечащий врач может не сразу приступить к его лечению.Вместо этого ваш врач будет контролировать уровень кальция в крови (каждые шесть месяцев), артериальное давление (каждые шесть месяцев), функцию почек (каждый год) и плотность костей (каждые один-три года).
Если ваш лечащий врач считает, что ваш гиперпаратиреоз не требует немедленного лечения, обязательно:
- Пейте больше воды.
- Сохраняйте активность и делайте больше упражнений, чтобы ваши кости оставались крепкими.
- Не принимайте тиазидные диуретики или литий, потому что эти препараты могут повышать уровень кальция в крови.
- Спросите своего врача, нужно ли вам принимать добавки с витамином D, если у вас низкий уровень витамина D.
Если у вас более серьезные симптомы гиперпаратиреоза, увеличенная паращитовидная железа (или железы) или рост паращитовидной железы, врач может порекомендовать операцию по удалению гиперактивной железы (желез). Операция опытного хирурга может вылечить гиперпаратиреоз примерно в 95% случаев.
Медицинский менеджмент
Цинакальцет (Сенсипар®) был одобрен Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов для лечения вторичного гиперпаратиреоза.Препарат работает, сигнализируя паращитовидным железам о необходимости вырабатывать меньше ПТГ. Хотя цинакалцет предназначен для лечения вторичного гиперпаратиреоза, некоторые медицинские работники назначают его при первичном гиперпаратиреозе.
Другой тип лекарств, который иногда назначают, — это бисфосфонаты. Эти препараты помогают предотвратить потерю кальция из костей, что снижает риск переломов и остеопороза. Примеры бисфосфонатов включают этидронат (Didronel®), алендронат (Fosamax®), золедроновую кислоту (Zometa®) и ибандронат (Boniva®).
Если вы женщина, у вас уже была менопауза и у вас есть признаки остеопороза, ваш врач может назначить заместительную гормональную терапию (ЗГТ). ЗГТ может помочь костям удерживать кальций.
Профилактика
Можно ли предотвратить гиперпаратиреоз?
Нет. Гиперпаратиреоз нельзя предотвратить.
Перспективы / Прогноз
Что мне ожидать, если у меня гиперпаратиреоз?
Хирургия излечит почти все случаи гиперпаратиреоза.Если вам предстоит операция, ваш врач может захотеть проверять уровень кальция и ПТГ через шесть недель после операции, а затем ежегодно. Вы также можете проходить тест на плотность костной ткани каждый год.
Если у вас легкие симптомы и вам не нужна операция прямо сейчас, ваш поставщик медицинских услуг будет внимательно следить за вашим здоровьем и назначать анализы крови для проверки уровня кальция и ПТГ. Он или она также закажет тесты для отслеживания потери костной массы и другие тесты по мере необходимости.
Вторичный гиперпаратиреоз — обзор
Вторичный гиперпаратиреоз
Вторичный гиперпаратиреоз (SHPT) — это заболевание с повышенным уровнем ПТГ, вызванное нарушением одного или нескольких факторов гомеостаза кальция.Когда уровень ионизированного кальция в сыворотке снижается, CaSR отвечает на секрецию ПТГ. Если паращитовидная железа не может компенсировать пониженный уровень ионизированного кальция, у пациентов развивается гипокальциемия и связанные с ней симптомы. Состояниями, которые обычно вызывают SHPT, являются недостаточное потребление кальция или мальабсорбция, дефицит или резистентность витамина D и заболевание почек. Распространенность SHPT неясна из-за множества заболеваний, вызывающих это состояние, но исследование показало, что 60–65% пациентов с хронической болезнью почек (ХБП) стадии 3-4 имеют SHPT (Arevalo-Lorido et al., 2016).
Сообщалось о генетических отклонениях в экспрессии генов, связанных с SHPT. На моделях уремических мышей и у пациентов с SHPT экспрессия CaSR снижается в паращитовидных железах, чтобы усилить секрецию PTH (Canadillas et al., 2005). Кальцитриол, фосфор и кальцимиметики могут влиять на экспрессию CaSR.
Рецептор витамина D (VDR) также играет роль в патогенезе SHPT. Подобно CaSR, экспрессия VDR подавляется у пациентов с SHPT.Подавление передачи сигналов от VDR приводит к усилению экспрессии гена ПТГ. VDR также может быть связан с пролиферацией клеток паращитовидной железы; Ингибирование VDR связано с более низкой экспрессией p21 Cip1 и p27 Kip1 , которые являются ингибиторами клеточного цикла (Tokumoto et al.


 6 шт.
6 шт. 1 мл 10 шт.
1 мл 10 шт.
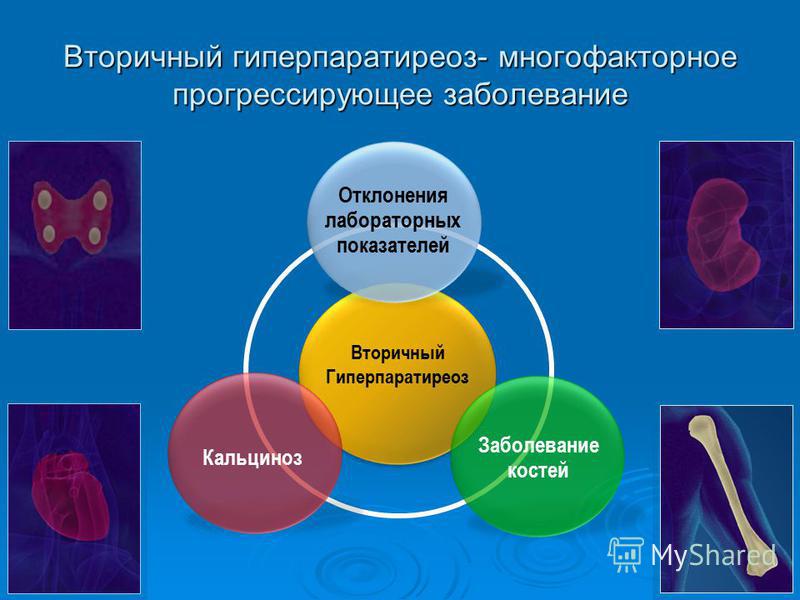 Если у человека дефицит витамина D, уровень кальция в крови может упасть.
Если у человека дефицит витамина D, уровень кальция в крови может упасть.

 Национальный институт медицины дает такие нормы по употреблению кальция: людям в возрасте 19-50 лет – 1000 мг в день; женщинам в возрасте 51 и более лет и мужчинам в возрасте 71 и более лет – 1200 мг. Витамин D рекомендуется употреблять в дозировке 600 МЕ, а людям в возрасте 71 год и старше – 800 МЕ.
Национальный институт медицины дает такие нормы по употреблению кальция: людям в возрасте 19-50 лет – 1000 мг в день; женщинам в возрасте 51 и более лет и мужчинам в возрасте 71 и более лет – 1200 мг. Витамин D рекомендуется употреблять в дозировке 600 МЕ, а людям в возрасте 71 год и старше – 800 МЕ. info,
info, Развивается из-за гипокальцемии, вызванной другими заболеваниями: хронической почечной недостаточностью, тяжелыми патологиями печени, а также у больных на гемодиализе. Паращитовидные железы при этом здоровы.
Развивается из-за гипокальцемии, вызванной другими заболеваниями: хронической почечной недостаточностью, тяжелыми патологиями печени, а также у больных на гемодиализе. Паращитовидные железы при этом здоровы.