Прививка «в комплекте». Вакцинация от кори, краснухи и паротита
Прививка «в комплекте». Вакцинация от кори, краснухи и паротита
Сусанна Харит
Педиатр, руководитель отдела иммунопрофилактики НИИ детских инфекций МЗ РФ, главный внештатный специалист по вакцинопрофилактике детей Комитета здравоохранения Санкт-Петербурга, д.м.н.
Как проявляется инфекция
Корь – острое вирусное заболевание, передающееся воздушно-капельным путем (при разговоре, кашле и чихании). Характеризуется высокой температурой тела (39,0 градусов С и выше), общим тяжелым состоянием, кашлем, насморком, воспалением слизистой оболочки глаз (конъюнктивитом) и сыпью.
Вирус кори легко распространяется на большие расстояния – в соседние комнаты, через коридоры, систему вентиляции. Заражается 95-96% детей, находившихся в контакте с больными. В первые 3-6 дней заболевание выглядит как ОРВИ, но уже в этот период можно увидеть характерные для кори высыпания на слизистой оболочке щек в виде белых точек.

Корь опасна своими осложнениями: такими как отит (воспаление уха; наблюдается у 1 из 20 заболевших), воспаление легких (у 1 из 25 заболевших), поражение крови (тромбоцитопения – сниженное количество тромбоцитов, что опасно кровотечениями; наблюдается у 1 из 3000 заболевших), судороги, развивающиеся на фоне высокой температуры тела (у 1 из 200 заболевших), а также — воспаление головного мозга энцефалит; у 1 из 1000 заболевших).
Кроме того, после кори у переболевшего временно формируется состояние иммунодефицита (снижение защиты от других инфекций), что способствует наслоению тяжелых бактериальных инфекций.
Краснуха — острая вирусная инфекция, передающаяся воздушно-капельным путем. У детей, как правило, протекает легко или в виде заболевания средней тяжести. Заболевают обычно через 11-21 (редко 23 дня) после контакта с больным человеком. Первые 1-5 дней болезни характеризуются подъемом температуры до 38 градусов С, недомоганием, головной болью, увеличением лимфатических узлов, особенно на затылке, за ушами, иногда — коньюнктивитом.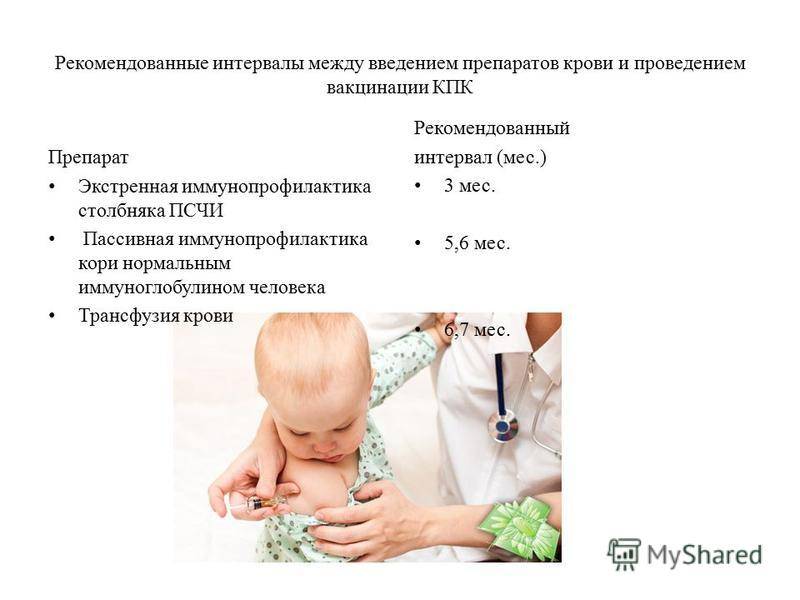
Наиболее опасна краснуха для беременных, т.к. этот вирус способен поражать все ткани плода. Если женщина заболевает краснухой в первую половину беременности, особенно в первые 3 месяца, то в результате может случиться выкидыш, или родится мертвый ребенок. Возможно также появление на свет малыша с синдромом врожденной краснухи (СВС), включающим в себя триаду пороков развития: — врожденный порок сердца, слепоту (катаракту) и глухоту. Кроме того, для СВС характерно поражение мозга, вплоть до умственной отсталости, а также поражение печени, селезенки, тромбоцитов и другие врожденные нарушения. Женщина может переболеть краснухой незаметно: при нормальном самочувствии на 1-2 дня появляется незначительная сыпь, на которую иногда не обращают внимания. |
Не защищено от краснухи 11-30% женщин детородного возраста. Если девушка или молодая женщина не болела краснухой и не привита, то, перед тем, как планировать беременность ей самой нужно подумать о соответствующей прививке Вакцинация защищает практически в 100%, иммунитет после однократной прививки сохраняется в среднем 15-20 лет, потом иммунизацию можно повторить. Необходимо помнить, что после введения краснушной вакцины не рекомендуется беременеть в течение 3-х месяцев. |
Эпидемический паротит («свинка») – острая вирусная инфекция, передающаяся воздушно-капельным путем и поражающая околоушные и подчелюстные слюнные железы. Они распухают, из-за чего лицо округляется (отсюда и название «свинка»). Распространяется этот вирус в окружающем пространстве не так широко, как корь и краснуха. Если заболевший ребенок изолирован в комнате, то не контактирующие с ним непосредственно дети и взрослые не заражаются.
Заболевание начинается с невысокой температуры, недомогания, а через 1-3 дня увеличиваются одна или обе слюнные околоушные железы, больно жевать и глотать.
При осмотре слизистой щек виден воспаленный сосочек выводного протока слюнной железы на стороне поражения. Кроме слюнных желез, примерно в 4% случаев, вирус эпидемического паротита может вызвать воспаление поджелудочной железы (панкреатит), а также оболочек головного мозга (менингит) у 1 из 200-5000 заболевших, очень редко (1 на 10 000 случаев) в процесс вовлекается ткань головного мозга, тогда развивается менингоэнцефалит (воспаление оболочек и вещества головного мозга).
Эпидемический паротит опасен осложнениями. У 20-30 % заболевших мальчиков- подростков и мужчин воспаляются яички (орхит), у девушек и женщин в 5% вирус эпидемического паротита поражает яичники (оофорит). Оба эти процесса могут послужить причиной бесплодия. Возможны смертельные исходы 1:10 000 заболевших.
Все три инфекции (корь, краснуха, эпидемический паротит) вызываются вирусами и не имеют специфической противовирусной терапии. То есть, нет препаратов, которые бы предупреждали тяжелое течение болезни и осложнения. Поэтому основным средством предупреждения этих инфекций является иммунизация.
Средства для защиты
Вакцинацию против кори и эпидемического паротита в рамках национального календаря прививок проводят отечественными вакцинами, а вакцинацию против краснухи – индийским препаратом, который закупает государство. Дети обеспечиваются им бесплатно. Также бесплатно для профилактики кори и паротита используют отечественные монопрепараты и дивакцину, защищающую от двух этих вирусов одновременно.
Прививки против краснухи, кори и паротита проводят согласно календарю прививок, когда ребенку исполняется 1 год и 6 лет. Если ребенок не был привит против краснухи вовремя, вакцинацию ему проводят в подростковом возрасте, в 13 лет.
Таким образом, ребенок при одномоментной иммунизации против кори, паротита и краснухи бесплатными вакцинами получает два укола (дивакцина и краснушная отдельно). В качестве альтернативы (также бесплатно) могут быть использованы импотные ассоциированные вакцины, содержащие все три вируса в одной дозе.
Все упомянутые препараты (и отечественные, и зарубежные) созданы на основе ослабленных (аттенуированных) вирусов, которые, не вызывая заболевания, способны создать стойкий иммунитет против инфекции.
Отечественная коревая вакцина (Л-16) содержит живой ослабленный вирус кори и выпускается как в виде монопрепарата, так и в виде ассоциированной (от лат. associo присоединять) дивакцины — препарата, содержащего ослабленные вирусы кори и паротита. В нашей стране разрешены к применению противокоревые вакцины иностранных фирм – РУВАКС (вакцина против кори), а также ассоциированные тройные вакцины – против кори, краснухи, эпидемического паротита: ММР-II, ПРИОРИКС, АССОЦИИРОВАННАЯ ПАРОТИТНО-КОРЕВАЯ КРАСНУШНАЯ ВАКЦИНА.
В нашей стране разрешены к применению противокоревые вакцины иностранных фирм – РУВАКС (вакцина против кори), а также ассоциированные тройные вакцины – против кори, краснухи, эпидемического паротита: ММР-II, ПРИОРИКС, АССОЦИИРОВАННАЯ ПАРОТИТНО-КОРЕВАЯ КРАСНУШНАЯ ВАКЦИНА.
Для профилактики эпидемического паротита применяют отечественные вакцины: живую, сухую, паротитную аттенуированную (Л-3) или ассоциированную дивакцину (корь-паротит), а также зарубежные ассоциированные тривакцины: MMR-II, ПРИОРИКС, АССОЦИИРОВАННАЯ ПАРОТИТНО-КОРЕВАЯ, КРАСНУШНАЯ ВАКЦИНА.
Российской вакцины против краснухи в настоящее время не выпускают. А для вакцинации против этого вируса в рамках национального календаря прививок (для детей 1 года, 6 лет и подростков 13 лет), помимо уже упомянутых индийского препарата, а также MMRII, ПРИОРИКСА и АССОЦИИРОВАННОЙ ПАРОТИТНО-КОРЕВОЙ КРАСНУШНОЙ ВАКЦИНЫ, зарегистрированы моновакцины РУДИВАКС и ЭРВЕВАКС.
Перечисленные вакцины выпускаются в сухом виде, и перед применением их требуется растворить. Растворитель всегда прилагается в другой ампуле (флаконе). Разведенный препарат хранению не подлежит и должен сразу использоваться, так как под воздействием тепла и света вакцина теряет способность взывать формирование иммунитета.
Метод введения вакцин – подкожный, место введения – подлопаточная область или дельтовидная мышца плеча.
Моновакцины, дивакцину или ассоциированные вакцины против кори, краснухи и паротита можно вводить одномоментно с любыми другими вакцинами, за исключением БЦЖ. Иммуноглобулин[1] и другие препараты крови человека должны вводиться не ранее, чем через 2 недели после прививки, а если по каким-либо причинам ребенку переливались препараты крови, то вакцинацию можно проводить не ранее, чем через 3 месяца после их применения.
Реакция организма
Ни ассоциированные, ни моновакцины не вызывают поствакцинальных реакций[2] у большинства детей.
У 10% привитых возможна местная нормальная (обычная) вакцинальная реакция в первые 1-2 дня в виде красноты, небольшого отека тканей в месте введения препарата. Отек сохраняется в течение 1-2 дней, проходит самостоятельно.
Что касается общих нормальных вакцинальных реакций, то при использовании коревой вакцины они могут появиться у 10-15% детей, начиная с 4-5 по 13-14 дни после прививки. Возможны повышение температуры (с 8 по 11 дни, иногда даже до +39,0 градусов С и выше), насморк, покашливание. После паротитной прививки общие нормальные вакцинальные реакции бывают редко и проявляются в виде повышения температуры тела, покраснения зева, насморка. В редких случаях отмечается кратковременное (в течение 1-3 дней) увеличение околоушных слюнных желез (с одной или двух сторон). Эти симптомы могут возникнуть с 5 до 14 дня после прививки, увеличение околоушных желез может проявиться и на 21 день после иммунизации.
При использовании краснушной вакцины подобные реакции возможны у 4-15% привитых с 4-5-го по 14 день после прививки. Возможно появление насморка, покашливание, повышение температуры тела. Редко встречаются краснухоподобная сыпь, увеличение лимфоузлов.
Возможно появление насморка, покашливание, повышение температуры тела. Редко встречаются краснухоподобная сыпь, увеличение лимфоузлов.
В старшем возрасте или у взрослых после прививки могут возникнуть боли в суставах. При использовании ассоциированных вакцин возможно сочетание всех симптомов в те же сроки, что и при моновакцинации.
Если выше перечисленные или подобные им симптомы начались в первые 4-5 дней после прививки, а также сохраняются или появились после 15 дня, это не имеет отношения к прививке и означает, что ребенок чем-то заболел. Чаще всего, это острая инфекция верхних дыхательных путей. Обязательно нужно вызвать врача, чтобы уточнить характер заболевания и назначить лечение (например, жаропонижающие средства, сосудосуживающие капели в нос, при необходимости — антибактериальные лекарства и т.п.).
Возможные осложнения
Аллергические реакции. Возникают, как правило, на дополнительные вещества, входящие в вакцину.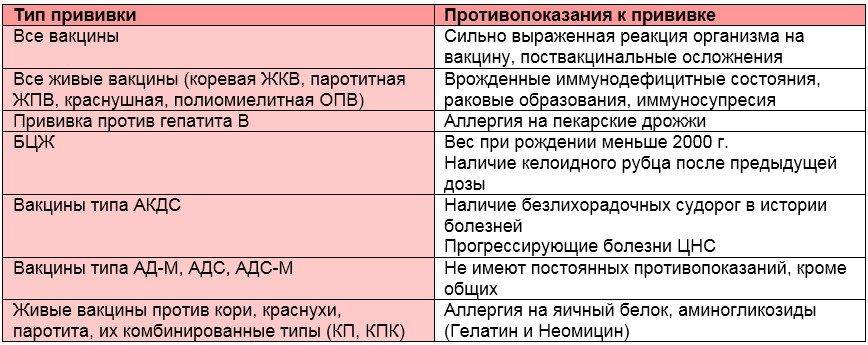 Все противовирусные вакцины содержат небольшое количество антибиотика, а также остаточное количество белка тех сред, на которых выращивали вирус вакцины. Зарубежные вакцины против кори и паротита содержат небольшую долю куриного белка, в отечественных препаратах имеется белок перепелиный. В этом – преимущество российских препаратов, поскольку аллергия на перепелиное яйцо в настоящее время встречается реже, чем на куриное.
Все противовирусные вакцины содержат небольшое количество антибиотика, а также остаточное количество белка тех сред, на которых выращивали вирус вакцины. Зарубежные вакцины против кори и паротита содержат небольшую долю куриного белка, в отечественных препаратах имеется белок перепелиный. В этом – преимущество российских препаратов, поскольку аллергия на перепелиное яйцо в настоящее время встречается реже, чем на куриное.
Местные аллергические реакции возникают в первые 1-2 дня после прививки. В области инъекции появляется отек и краснота более 8 см в диаметре. Для лечения необходимо использовать гормональные мази и иази улучшающие кровообращение (например, троксевазиновую). При очень больших отеках внутрь назначают противоаллергические препараты.
В единичных случаях могут отмечаться общие аллергические реакции в виде сыпи, крапивницы, отека Квинке[3]. При лечении общих аллергических осложнений используют противоаллергические препараты, принимая их внутрь или в виде внутримышечных инъекций.
Прививка от кори, краснухи, паротита: осложнения и противопоказания
Корь — острая вирусная инфекция, которая характеризуется повышением температуры, развитием катаральных явлений и появлением специфической сыпи. Корь очень заразна. Передается от человека к человеку воздушно-капельным путем. Болезнь развивается примерно через 10 дней после контакта.
Проявления болезни начинаются с повышения температуры, насморка, кашля. Развивается конъюнктивит и светобоязнь. Примерно с 4 дня болезни появляется характерная сыпь на слизистых оболочках полости рта и на коже. Сыпь на коже появляется этапами начиная с головы. Затем переходит на туловище, руки и ноги. К 4 дню сыпь начинает темнеть и шелушиться. После сходит в той же последовательности, в которой появлялась. Специфического лечения кори не существует. Осложнения инфекции возникают примерно в четверти случаев заболевания. К ним относятся: бронхиты, синуситы, пневмонии и энцефалиты.
К ним относятся: бронхиты, синуситы, пневмонии и энцефалиты.
Корь очень заразная инфекция при контакте с больным заражаются 9 из 10 непривитых детей. Вирус кори имеет свойство поражать клетки иммунной системы ребенка. Это влечет за собой высокий риск инфекционных осложнений. В дорпрививочную эпоху корь была одной из первых причин детской смертности. Кроме того, корь часто осложняется заболеванием нервной системы. Коревой энцефалит развивается примерно у одного из 300 заболевших детей и не имеет специфического лечения. Из-за высокой «заразности» в мире до сих пор возникают вспышки кори, особенно в коллективах с малым охватом прививками.
Краснуха – вирусная инфекция, для которой характерны неяркие катаральные явления и появление сыпи. Краснуха имеет длительный инкубационный период. От инфицирования до развития болезни проходит 2-4 недели. При этом человек становится заразным уже в середине инкубационного периода и остается заразным после схода краснушной сыпи. Первые симптомы заболевания неспецифические – незначительное повышение температуры, легкий насморк, слабость, увеличение лимфоузлов. Примерно через 2 дня болезни появляется характерная мелкоточечная яркая сыпь. Сначала на голове, затем постепенно спускается на конечности. Через несколько дней сыпь проходит самостоятельно бесследно. Краснуха у детей обычно протекает не тяжело. Редко приводит к осложнениям.
Первые симптомы заболевания неспецифические – незначительное повышение температуры, легкий насморк, слабость, увеличение лимфоузлов. Примерно через 2 дня болезни появляется характерная мелкоточечная яркая сыпь. Сначала на голове, затем постепенно спускается на конечности. Через несколько дней сыпь проходит самостоятельно бесследно. Краснуха у детей обычно протекает не тяжело. Редко приводит к осложнениям.
Краснуха имеет легкое течение у детей. Однако, в связи с тем, что больной длительно заразен, даже не имея клиники, краснуха легко распространяется. Инфицирование краснухой чрезвычайно опасно для беременных женщин, особенно в первом триместре беременности. Примерно в четверти случаев у женщин, перенесших краснуху, рождаются малыши с той или иной тяжелой патологией. Самая частая из них – врожденная катаракта (нарушение зрения, вплоть до слепоты).
Эпидемический паротит (свинка) – острое инфекционное заболевание, характеризующееся поражением желез внутренней секреции (чаще околоушной слюнной железы). Вирус передается воздушно-капельным, реже контактным (с зараженных поверхностей) путем. Болезнь имеет длительный инкубационный период – примерно 16-18 дней. При этом с середины инкубационного периода ребенок может быть заразен. Болезнь начинается с незначительного повышения температуры, общей слабости, сухого кашля. На 2-3 день увеличиваются околоушные слюнные железы. Примерно через неделю, размер желез начинает уменьшаться и больной выздоравливает. В некоторых случаях, выздоровления не происходит, появляются осложнения – поражение поджелудочной, молочной или половых желез, нервной системы, нарушением слуха.Важно отметить, что эпидемический паротит не имеет специфического лечения.
Вирус передается воздушно-капельным, реже контактным (с зараженных поверхностей) путем. Болезнь имеет длительный инкубационный период – примерно 16-18 дней. При этом с середины инкубационного периода ребенок может быть заразен. Болезнь начинается с незначительного повышения температуры, общей слабости, сухого кашля. На 2-3 день увеличиваются околоушные слюнные железы. Примерно через неделю, размер желез начинает уменьшаться и больной выздоравливает. В некоторых случаях, выздоровления не происходит, появляются осложнения – поражение поджелудочной, молочной или половых желез, нервной системы, нарушением слуха.Важно отметить, что эпидемический паротит не имеет специфического лечения.
Онлайн консультация Врача-педиатра Текутьевой Ольги Николаевны
Запись онлайн
В рамках консультации вы сможете озвучить свою проблему, врач уточнит ситуацию, расшифрует анализы, ответит на ваши вопросы и даст необходимые рекомендации.
Эпидемический паротит чаще течет не тяжело и редко дает осложнения. Но эти осложнения сохраняются на всю жизнь. К ним относится бесплодие, глухота или развитие сахарного диабета. Кроме того, у переболевших эпидемическим паротитом, не всегда развивается иммунитет. Может возникнуть повторное заболевание во взрослом возрасте. Риск развития осложнений у взрослых значительно повышается.
Какие бывают прививки от кори, краснухи и эпидемического паротита?
Все прививки от кори, краснухи и эпидемического паротита относятся к живым аттенуированным вакцинам. Это означает, что в препарате содержится живые вирусы, выращенные в искусственных условиях и специальным образом «ослабленные». Так, что они не могут вызвать полноценное заболевание, но при этом формируют стойкий пожизненный иммунитет. Попытки создания инактивированных (не живых) вакцин от этих инфекций были неудачными. Такие вакцины оказывались слишком «слабыми», неспособными вызвать стойкий иммунитет.
Среди вакцин выделяют:
— моновакцины. Отдельно паротитную, коревую и краснушную;
— дивакцины. В нашей стране распространена паротитно-коревая вакцина;
— и тривакцины. К этой группе относится вакцина «ММР» и «Приорикс». Такие вакцины предпочтительны, т.к. вместо двух или трех уколов ребенок получает только одну инъекцию.
Когда делают прививку от кори, краснухи и эпидемического паротита?
Согласно национальному календарю прививок вакцину (или 2 вакцины, отдельно краснушную и паротитно-коревую) вводят в 12 месяцев. Этот возраст выбран потому, что примерно до 11 месяцев у ребенка может сохраняться иммунитет, переданный внутриутробно от матери.
Вторую вакцинацию делают в 6 лет. Повторное введение рекомендовано потому, что первая прививка дает примерно 70 – 80% защиты от инфекции. Повторная вакцинация повышает уровень защиты примерно до 95%.
Отдельно календарем предусмотрена прививка для девушек от 18 до 25 лет. С целью предотвращения развития врожденной краснухи у детей.
С целью предотвращения развития врожденной краснухи у детей.
Прививка от краснухи и беременность.
Доказано, что антитела после прививки от краснухи сохраняется примерно 10 – 20 лет.
- Если женщина, планирующая беременность, уверена, что она была привита не более, чем 10 лет назад, при этом за всю свою жизнь получила не менее 2-х прививок, она может спокойно планировать беременность.
- Второй вариант, если женщина не была привита, график вакцинации был незакончен или она не знает, какие прививки были сделаны и когда. Перед тем, как планировать беременность лучше сделать прививку от краснухи.
- Если женщина была привита двукратно, но после прививки прошло больше 10 лет. В этом случае перед тем как планировать беременность, можно сдать анализ крови на антитела. Если уровень антител будет достаточным, можно планировать беременность. В случае снижения уровня антител или их отсутствия, женщине рекомендуют сделать прививку.

Как быть, если прививки от кори, краснухи и эпидемического паротита не были сделаны вовремя?
Детям, не получившим ни одной прививки, после годовалого возраста также рекомендуют двукратное введение вакцины. Вторая прививка делается минимум через 6 месяцев от первой. Для прививки от краснухи время между первой и второй вакциной можно сократить до 3-х месяцев. Согласно национальному календарю, прививка от кори, краснухи и паротита должна быть сделана всем людям до 35-летнего возраста.
Что входит в состав прививки от кори, краснухи и эпидемического паротита?
Основным компонентом вакцины являются живые, ослабленные и модифицированные вирусы.
Кроме основных компонентов, вакцины содержат консервант (желатин) и стабилизаторы: сахарозу, лактозу, глицин, пролин. Трехкомпонентные вакцины содержат антибиотик неомицин для профилактики развития инфекционных осложнений.
Какие осложнения могут быть после прививки от кори, паротита и коклюша?
Все побочные реакции можно условно разделить на 2 большие группы: неспецифические и специфические.
Неспецифические реакции обычно возникают не позднее третьего дня после прививки. К ним относится:
-повышение температуры до незначительных цифр. Этот симптом встречается нечасто, с ним можно бороться приемом жаропонижающего;
-при высокой температуре, у детей имеющих предрасположенность, могут возникнуть фебрильные судороги. Это доброкачественное состояние, обычно проходящее с возрастом и не требующее специфического лечения. Однако, малыша с приступом таких судорог обязательно должен наблюдать врач. Календарь вакцинации у детей, имеющих такую реакцию на прививку, должен составляться индивидуально;
-общее нарушение самочувствия – слабость сонливость или, наоборот, беспокойство и нарушение сна. Это проходит самостоятельно и коррекции не требуют;
-отечность и покраснение в месте введения. У таких вакцин этот симптом встречается редко, проходит сам и не требует лечения;
-острые аллергические реакции. Очень редкий побочный эффект для этого вида вакцин. Встречается примерно в 1 случае на 3,5 млн прививок. Развивается в первом часу после получения вакцины и требует оказания квалифицированной медицинской помощи. Чтобы успеть помочь малышу, у которого развилась острая аллергическая реакция, маму первые 30-40 мин. после прививки просят находиться в непосредственной близости от лечебного учреждения.
Очень редкий побочный эффект для этого вида вакцин. Встречается примерно в 1 случае на 3,5 млн прививок. Развивается в первом часу после получения вакцины и требует оказания квалифицированной медицинской помощи. Чтобы успеть помочь малышу, у которого развилась острая аллергическая реакция, маму первые 30-40 мин. после прививки просят находиться в непосредственной близости от лечебного учреждения.
Специфические реакции развиваются из-за того, что вакцина содержит живой ослабленный вирус. Такие реакции возникают не сразу, а через 2-3 недели после прививки. К ним относятся:
— общее недомогание, симптомы легкого ОРВИ;
— незначительная сыпь на теле, проходящая самостоятельно через несколько дней;
— легкий отек и болезненность околоушных слюнных желез;
— временное снижение уровня тромбоцитов крови.
Все эти симптомы не требуют лечения.
Когда прививку от кори, краснухи и эпидемического паротита делать нельзя?
- Если в прошлом у ребенка были тяжелые аллергические реакции на аминогликозидный антибиотик.

- Тяжелые иммунодефицитные состояния (ВИЧ-инфекция, онкологические заболевания, заболевания крови). Однако, в период ремиссии и под наблюдением лечащего врача такие дети могут быть привиты.
- Период беременности и грудного вскармливания.
- Выраженная реакция на предыдущее введение препарата (температура выше 40*С, выраженное покраснение и отек).
- Временно прививку откладывают, если у ребенка протекает острая инфекция или обострение хронического заболевания.
Прививка от кори и аллергия на куриные яйца
Все штаммы вирусов, входящие в состав вакцин, произведенных в России, выращиваются на белке перепелиных, а не куриных яиц. Поэтому для отечественных вакцин аллергия на белок куриного яйца не является противопоказанием. Для вакцин импортных («ММР» или «Приорикс») противопоказанием является только тяжелая анафилактическая реакция. Согласно рекомендации ВОЗ при простой пищевой аллергии у ребенка в виде сыпи прививку делать можно.
Прививка от кори и аутизм
В 1998 году британский ученый в научном журнале опубликовал статью о том, что консервант мертиолят ртути, содержащейся в вакцине от кори, вызывает у детей воспаление кишечника и аутизм. Немногим позже другие исследователи опровергли статью и установили, что факты в ней были подтасованы. А сам автор признался, что исследование свое он опубликовал с коммерческой целью. Он хотел поддержать продажи вакцины без мертиолята. Статья была опровергнута, ученый лишен всех регалий и звания врача.
Публикация успела породить такое количество слухов, что и сейчас на приеме я часто слышу предположение о связи прививок с аутизмом. С тех пор проводилось большое количество исследований. Последнее, длительное, с участием 400 тысяч привитых детей завершилось в 2020 году.
Ни одно из проведенных исследований не подтвердило связь прививки с аутизмом. К сожалению, причины развития этого заболевания до сих пор не установлены.
Корь: все, что нужно знать о вакцинации взрослых
- Диана Курышко
- BBC News Украина
Автор фото, YURI DYACHYSHYN Getty
Украина лидирует по количеству больных корью в мире. Только в 2018 году ею заразились 35 тысяч человек, а с начала 2019 года — еще 25 тысяч.
Только в 2018 году ею заразились 35 тысяч человек, а с начала 2019 года — еще 25 тысяч.
Врачи бьют тревогу и призывают делать прививки. Это — единственный способ защититься от болезни, от которой нет лекарств.
Как и где сделать прививку от кори в Украине? Куда делают укол и что можно есть перед вакцинацией? А как насчет секса?
Отвечаем на все популярные вопросы о прививках от кори для взрослых. В этом нам помогают эксперт по вакцинации ЮНИСЕФ Екатерина Булавинова и Минздрав.
Почему корь — это серьезно?
Корь — это вирусное заболевание, которое передается от больного человека воздушно-капельным путем во время чихания, кашля или разговора. Этот вирус может жить в воздухе и на поверхностях еще 2 часа после того, как больной вышел из помещения.
Болезнь может проходить очень тяжело и привести к инвалидности или даже к летальному исходу.
Обычно прививки от кори, а следовательно и иммунитет от этой болезни, делают в детском возрасте — в 12 месяцев и в шесть лет. Но в Украине уровень вакцинации — крайне низкий.
Но в Украине уровень вакцинации — крайне низкий.
Нужно ли взрослым вакцинироваться от кори?
Да, в условиях вспышки кори, который сейчас в Украине, взрослым необходимо вакцинироваться.
Очень многие взрослые не защищены от кори — либо потому что они когда-то получили прививки только одной дозой и, возможно, не выработали иммунитет, либо потому что вакцина неправильно хранилась.
Сейчас вакцина против кори входит в состав комбинированной трехкомпонентной вакцины КПК. Она защищает сразу от трех инфекций — кори, краснухи и паротита.
Как проверить, есть ли у тебя иммунитет против кори? Какие анализы нужно сдавать?
Автор фото, UNIAN
Если есть доступ к вакцине, то никаких анализов сдавать не надо, а надо просто прийти и сделать прививку. Лишним это не будет.
Проверить, есть ли у тебя иммунитет к кори, можно, сдав анализ крови на наличие иммуноглобулинов IgG — это антитела к вирусу кори.
Когда и при каких обстоятельствах делать прививки взрослому против кори нельзя?
• Во время беременности;
• если была серьезная аллергическая реакция (анафилактический шок) на предыдущую дозу этой вакцины, известна аллергическая реакция на один из компонентов вакцины (например, неомицин)
• при остром заболевании с температурой выше 38,5°С;
• также не рекомендуют вводить КПК людям с иммунодефицитом, СПИДом, при лечении препаратами, подавляющими иммунитет, например, при химиотерапии, употреблении больших доз стероидных гормонов;
• следует повременить с прививкой, если пациент получал препараты крови, так как они могут нейтрализовать действие вакцины;
• вакцину вводят детям до шести месяцев.
А вот простуда, «красное горло» и насморк не являются противопоказанием к вакцинации. Вакцину от кори можно вводить в один день с другими вакцинами, например, от дифтерии и столбняка — в разные участки тела.
Чего нельзя делать до и после прививки — алкоголь, секс, есть ли ограничения в еде?
Никаких ограничений нет. Не надо менять обычный образ жизни.
Куда делают укол? Больно ли это?
Это обычный укол. Взрослому человеку советуют делать в плечо левой руки, если он — правша. В месте введения вакцины может появиться местная реакция — боль, покраснение или припухлость, которые обычно проходят быстро.
Вакцина КПК «не любит» прямых солнечных лучей и спирта. Прежде чем делать инъекцию, нужно подождать, пока с поверхности кожи полностью испарится спирт или другие дезинфицирующие средства, поскольку они могут отключить ослабленные вирусы, которые есть в вакцине.
Какая вакцина есть в Украине?
Это бельгийская вакцина «Приорикс» и американская «М-М-Р II». Их для Украины закупает Детский фонд ООН (ЮНИСЕФ).
По состоянию на 7 марта, в Украине было 1,2 млн доз этих вакцин. Они есть во всех государственных медицинских учреждениях, уверяют в Минздраве.
Они есть во всех государственных медицинских учреждениях, уверяют в Минздраве.
Безопасна ли вакцина от кори?
В Минздраве объясняют, что вакцину КПК применяют уже более 50 лет. За это время было сделано более 500 млн прививок в 100 странах мира.
Вакцины, как и любое лекарство, могут вызвать реакции, но серьезные реакции на вакцину — крайне редки, говорят врачи.
Вероятность серьезной аллергической реакции на вакцину КПК — это одна на миллион прививок. Тогда, как из тысячи людей, заразившихся корью, один человек умирает, одна заболеет энцефалитом, а 50 получают тяжелые осложнения, отметили в Минздраве.
Одной из главных причин распространения кори на планете Всемирная организация здравоохранения называет халатность и распространение ложных новостей о вакцинах.
В 90-х годах опасения вызвало дискредитированное исследование британца Эндрю Уэйкфилда, в котором он утверждал, что существует связь между вакциной против кори, паротита и краснухи (MMR) и аутизмом и заболеванием кишечника у детей. Уэйкфилд утверждал, что его выводы основаны на опыте только 12 детей, но ни одно другое исследование не смогло повторить полученные им результаты.
Уэйкфилд утверждал, что его выводы основаны на опыте только 12 детей, но ни одно другое исследование не смогло повторить полученные им результаты.
Впоследствии его удалили из медицинского реестра в Великобритании. Однако слухи о негативных последствиях иммунизации продолжали распространяться, что привело к значительному падению уровня вакцинации по всему миру.
Автор фото, Getty Images
Как проверить, качественная ли вакцина и не нарушались ли условия ее хранения?
Вы можете попросить медсестру показать вам холодильник, где хранятся вакцины, и термометр в нем — температура должна быть от +2 до +8 градусов.
Также можно посмотреть термоиндикаторы на флаконах с вакциной — они выглядят, как квадрат внутри круга.
Если квадрат светлее круга, это значит, что вакцина в порядке, хранилась при нормальной температуре и ее можно использовать.
Могут ли привитые люди заболеть корью?
Если человека привили правильно и качественной вакциной, он не заболеет корью. Но есть люди, которые несмотря на вакцинацию, не могут выработать иммунитет. Процент таких людей очень незначителен.
Но есть люди, которые несмотря на вакцинацию, не могут выработать иммунитет. Процент таких людей очень незначителен.
Заболеть могут те, кому ввели вакцину, которая хранилась при ненадлежащей температуре и утратила свои свойства.
К тому же, справки о прививках часто фальсифицируют.
Как переносят корь взрослые, какие осложнения могут быть?
Спрогнозировать или предотвратить осложнения от кори невозможно. Чаще всего это воспаление легких и энцефалит (воспаление головного мозга). Это тяжелые состояния, которые лечат в реанимации.
Даже если осложнений нет, эта болезнь тяжело переносится. Человек «выпадает из жизни» минимум на месяц.
В начале болезни людям кажется, что у них грипп. Есть температура, кашель, боль в глазах. Через 5-7 дней появляется сыпь, потом могут быть рвота и диарея. Температура весь период высыпаний обычно до 40. Когда сыпь сходит, некоторое время на коже сохраняются пигментные пятна.
Как часто взрослым нужно вакцинироваться?
Нужно получить две дозы вакцины с минимальным интервалом 28 дней. Врачи говорят, что это сформирует иммунитет против кори на долгие годы, вероятно, на всю жизнь.
Пускают ли непривитых людей за границу?
Людей, которые едут работать или учиться за границу надолго, могут попросить сделать дополнительную прививку. Такие прецеденты уже есть.
На сайтах разных стран есть рекомендации для людей, которые въезжают в Украину, сделать дополнительно прививки против кори.
Как и где вакцинироваться взрослому человеку в Украине?
Автор фото, MUNIR UZ ZAMAN Getty
По словам эксперта Минздрава по направлению «Инфекционные болезни» Федора Лапия, прививки от кори для взрослых в Украине — бесплатные. Сейчас в государственных поликлиниках вакцины от кори есть как для взрослых, так и для детей, отметил г-н Лапий.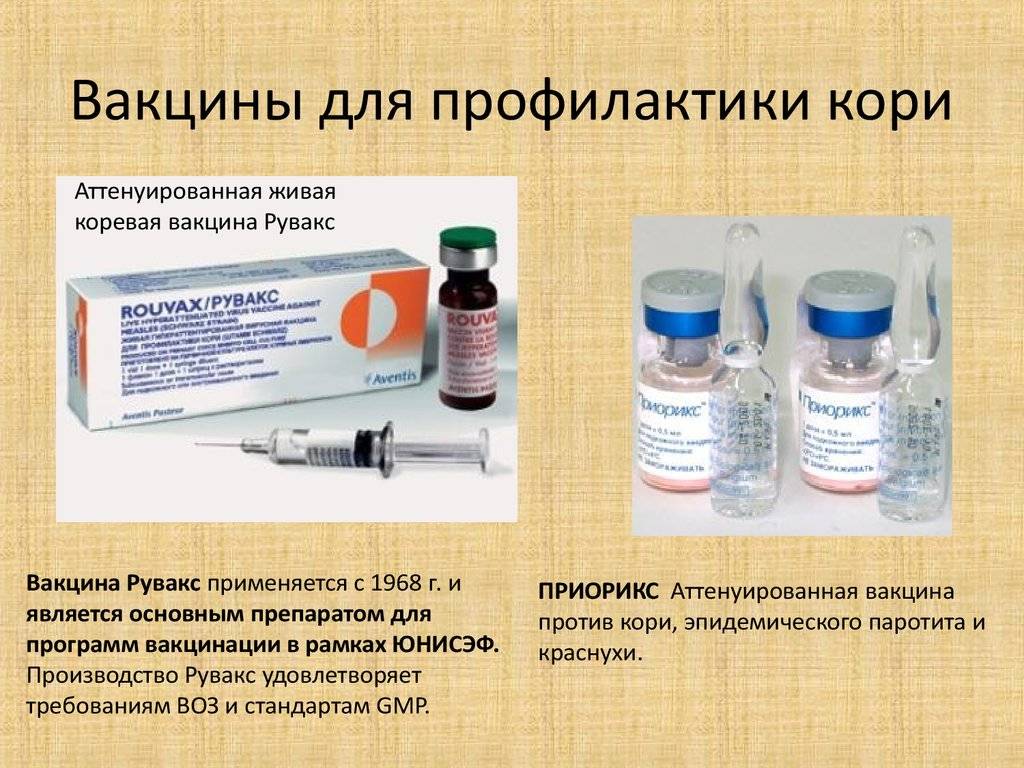
Если в кабинете прививок говорят, что вакцины нет, в Минздраве советуют жаловаться руководителю медучреждения. Если это не поможет, то следует обратиться в департамент/ управление здравоохранения в вашей области. За распределение вакцин в пределах области отвечает местная власть.
Можно ли вакцинироваться после контакта с больным?
В таких случаях также делают вакцинацию. Это соответствует рекомендациям ВОЗ. Таким образом иммунная система начинает «бежать наперегонки» с вирусом, вырабатывая антитела, объясняют в Минздраве.
Чем быстрее сделана вакцинация, тем больше вероятность избежать болезни или хотя бы облегчить ее течение.
Если человек контактировал с больным корью, лучше вакцинироваться в течение первых 72 часов. Позже можно, но эффективность прививки будет не такой высокой.
Что ожидать от индийской вакцины от кори, паротита и краснухи?
В отношении состава и технологии производства принципиальных отличий между индийской и европейскими вакцинами нет. Единственное исключение – отсутствие желатина в вакцине Prioriх(R). В целом, индийская вакцина доступнее для развивающихся стран и является проверенной на миллионах детей качественной альтернативой западных аналогов.
Единственное исключение – отсутствие желатина в вакцине Prioriх(R). В целом, индийская вакцина доступнее для развивающихся стран и является проверенной на миллионах детей качественной альтернативой западных аналогов.
Что делать, если у ребенка аллергия на желатин?
Желатин в составе вакцин является причиной для беспокойства некоторых родителей. Желатин – это вещество, получаемое из коллагена животных, таких как куры, крупный рогатый скот, свиньи и рыба. Коллаген содержится в сухожилиях, связках, костях и хрящах. Желатин используется в вакцинах в качестве стабилизатора для обеспечения длительного хранения. Но нужно отметить, что пищевой желатин и желатин, который используется для производства вакцин – совершенно разные вещи. В фармпроизводстве используется желатин с высокой степенью очистки и, по сути, он расщепляется на очень маленькие молекулы, называемые пептидами. Все формы желатина для использования в лекарствах производятся с соблюдением строгих стандартов безопасности.
Почему так сложно поменять тип стабилизатора или источник желатина?
Для разработки вакцины требуются многие годы лабораторных испытаний, чтобы гарантировать ее безопасность и эффективность. После того, как производитель выбрал стабилизатор для вакцины, любое его изменение может потребовать повторных клинических исследований. Из-за этого разработка новой безопасной и эффективной вакцины с другим стабилизатором может занять несколько лет.
Из повсеместно используемых вакцин против КПК, желатин содержится в вакцине MMR VaxPro® компании Merck, а также в той, что применяется в Казахстане – производства Serum Institute of India.
Если человек предпочитает избежать какого-либо, пусть даже минимального наличия свиного продукта, а также при наличии гиперчувствительности к желатину, можно использовать вакцину Prioriх(R), в которой желатин не используется.
Почему при изготовлении вакцины используются клетки абортированного эмбриона?
Ослабленные штаммы для вакцины КПК были выведены путем выращивания в клетках человека и животных. К примеру, штаммы вируса паротита, используемые в вакцинах, были выращены на куриных эмбрионах. Поэтому им лучше всего подходит культура куриных клеток соединительной ткани (или фибробластов). А штаммы вирусов кори и краснухи из индийской вакцины выращиваются на фибробластах человека. Клетки служат средой для размножения вируса. Ослабленные вирусы выделяются из клеточной культуры и добавляются в вакцину.
К примеру, штаммы вируса паротита, используемые в вакцинах, были выращены на куриных эмбрионах. Поэтому им лучше всего подходит культура куриных клеток соединительной ткани (или фибробластов). А штаммы вирусов кори и краснухи из индийской вакцины выращиваются на фибробластах человека. Клетки служат средой для размножения вируса. Ослабленные вирусы выделяются из клеточной культуры и добавляются в вакцину.
Что такое клеточная культура? Это выращивание клеток определенного типа при максимально комфортных для размножения, стерильных, стандартных условиях. Для поддержания таких условий нам необходимы культуральные среды, которые содержат стерильную (отфильтрованную) смесь питательных веществ (глюкозы, витаминов, аминокислот и т.д.). В составе всех вакцин КПК есть антибиотик сульфат неомицина в остаточных количествах (примерно 25 мкг на дозу). Антибиотик добавляется в клеточную среду, чтобы поддерживать ее стерильность. Следует заметить, что людям с аллергией на неомицин вакцина КПК противопоказана. Однако, такое мизерное количество неомицина вы можете получить, съев две порции телятины или выпив литр молока. Такие малые дозы не оказывают никакого терапевтического действия и тем более не токсичны.
Однако, такое мизерное количество неомицина вы можете получить, съев две порции телятины или выпив литр молока. Такие малые дозы не оказывают никакого терапевтического действия и тем более не токсичны.
Что касается абортированного материала, то дело в том, что для любой клеточной линии нужен донор. Важное преимущество клеток, выделенных из эмбрионов, – их способность делиться. Сделать жизнеспособную клеточную линию из клеток взрослого намного сложнее по двум причинам: они хуже делятся (то есть после определенного количества делений будет достигнут лимит и нужно будет создавать новую линию клеток) и они могут быть с большей вероятностью заражены вирусами, то есть получить стерильную культуру намного сложнее. Ослабленный вирус краснухи – один из компонентов КПК, был выведен на клеточной линии WI-38 (от названия института Wistar). Клетки для этой линии были взяты из фибробластов легких абортированного эмбриона возрастом 12 недель. Из-за непонимания этой темы вокруг абортированного материала возникают всё новые мифы. Нет, производителям не нужны новые аборты для получения материала. Клеточная линия была получена в 1964 году в Швеции, и её используют во всем мире до сих пор. Нет, родителей не заставляли сделать аборт, чтобы получить ценный материал. Этот эмбрион был выбран для получения культуры клеток, так как это был здоровый, нормально развивающийся плод здоровых родителей без каких-либо онкологических или наследственных заболеваний. Создать условия для выращивания ослабленных вирусов довольно сложно. Именно благодаря этой клеточной линии удалось получить оптимальные условия для вируса краснухи.
Нет, производителям не нужны новые аборты для получения материала. Клеточная линия была получена в 1964 году в Швеции, и её используют во всем мире до сих пор. Нет, родителей не заставляли сделать аборт, чтобы получить ценный материал. Этот эмбрион был выбран для получения культуры клеток, так как это был здоровый, нормально развивающийся плод здоровых родителей без каких-либо онкологических или наследственных заболеваний. Создать условия для выращивания ослабленных вирусов довольно сложно. Именно благодаря этой клеточной линии удалось получить оптимальные условия для вируса краснухи.
Не лучше ли ставить моновакцины от каждого из заболеваний (кори, краснухи и паротита)?
Нет, и этому есть несколько причин. Первая и главная – организм ребенка может ответить на 10 000 антигенов (частиц возбудителей болезней, которые помогают выработать антитела в организме – прим. V) одновременно. Обычная простуда – это встреча примерно с десятью антигенами, а ангина – уже 50! Для сравнения, вакцина КПК знакомит нашу иммунную систему с 24 антигенами трех вирусов. Так что ни о какой перегрузке иммунной системы не может быть и речи. Важно отметить, что общее количество антигенов сейчас намного ниже, чем, скажем, 30 лет назад, так как у нас в календаре используется всё больше очищенных вакцин.
Так что ни о какой перегрузке иммунной системы не может быть и речи. Важно отметить, что общее количество антигенов сейчас намного ниже, чем, скажем, 30 лет назад, так как у нас в календаре используется всё больше очищенных вакцин.
Небольшое количество антигенов в КПК позволяет делать её со многими другими вакцинами (АКДС, Пентаксим, Гексаксим – прим. V) в один день без риска осложнения и снижения эффективности.
Вторая причина – это меньшее количество инъекций, а значит и меньший уровень стресса у ребенка и родителей. Третья – снижение числа посещений больницы, а значит и вероятности подхватить какое-либо ОРВИ в очереди к врачу или по дороге к прививочному кабинету.
Может ли вакцина ККП стать причиной или триггером аутизма у ребенка?
Очень сложно переоценить вред, который нанес английский хирург Эндрю Уэйкфилд своей статьей “Гиперплазия подвздошных лимфоузлов, неспецифический язвенный колит и всеобъемлющее нарушение развития у детей” в известном медицинском журнале The Lancet в 1998 году. Вспышки кори по всему миру, растущее количество бесплодных браков и количество врожденных патологий у младенцев можно вполне связать с количеством отказов от прививки КПК. Но мы не будем скатываться до уровня мифов и домыслов, а просто еще раз напомним о статистической выборке.
Вспышки кори по всему миру, растущее количество бесплодных браков и количество врожденных патологий у младенцев можно вполне связать с количеством отказов от прививки КПК. Но мы не будем скатываться до уровня мифов и домыслов, а просто еще раз напомним о статистической выборке.
В исследовании Эндрю Уэйкфилда участвовало 12 детей. Результаты его исследования пытались подтвердить двенадцать независимых групп исследователей в разных странах. Они изучили сотни тысяч детей, привитых и не привитых от кори, краснухи и паротита. Риск аутизма в обеих группах оказался одинаковым.
Зато спустя некоторое время журналист Брайан Дир из лондонской газеты Sunday Times обнаружил, что родители нескольких детей, описанных в статье Уэйкфилда, судились с фармацевтическими компаниями, заявляя, что аутизм у их детей вызван вакциной против кори, краснухи и паротита. Кроме того, Дир узнал, что Ричард Барр, адвокат по делам о причинении вреда здоровью, представлявший в суде этих детей, заплатил Уэйкфилду за статью 440 000 фунтов стерлингов (около 800 000 долларов), в сущности, “отмывая” исковые требования через медицинский журнал. Когда соавторы Уэйкфилда узнали об этих деньгах, 10 из 13 официально отказались от авторства, чтобы не иметь никакого отношения к гипотезе о связи прививки против кори, краснухи и паротита с аутизмом.
Когда соавторы Уэйкфилда узнали об этих деньгах, 10 из 13 официально отказались от авторства, чтобы не иметь никакого отношения к гипотезе о связи прививки против кори, краснухи и паротита с аутизмом.
Вакцинация против кори
Как быть, если произошел контакт с больным корью?
Действия регламентируются Санитарно-эпидемиологические правила СП 3.1.2952-11 «Профилактика кори, краснухи и эпидемического паротита»
5.10. Иммунизации против кори по эпидемическим показаниям подлежат лица, имевшие контакт с больным (при подозрении на заболевание), не болевшие корью ранее, не привитые, не имеющие сведений о прививках против кори, а также лица, привитые против кори однократно – без ограничения возраста.
Иммунизация против кори по эпидемическим показаниям проводится в течение первых 72 часов с момента выявления больного. При расширении границ очага кори (по месту работы, учебы, в пределах района, населенного пункта) сроки иммунизации могут продлеваться до 7 дней с момента выявления первого больного в очаге.
5.12. Детям, не привитым против кори или эпидемического паротита (не достигшим прививочного возраста или не получившим прививки в связи с медицинскими противопоказаниями или отказом от прививок) не позднее 5-го дня с момента контакта с больным вводится иммуноглобулин человека нормальный (далее – иммуноглобулин) в соответствии с инструкцией по его применению.
5.14. Контактные лица из очагов кори, краснухи или эпидемического паротита, не привитые и не болевшие указанными инфекциями ранее, не допускаются к плановой госпитализации в медицинские организации неинфекционного профиля и социальные организации в течение всего периода медицинского наблюдения, указанного в пункте 5.7 настоящих санитарных правил.
Госпитализация таких пациентов в период медицинского наблюдения в медицинские организации неинфекционного профиля осуществляется по жизненным показаниям, при этом в стационаре организуются дополнительные санитарно-противоэпидемические (профилактические) мероприятия в целях предупреждения распространения инфекции.
Что нужно знать родителям о вакцинации ребенка
Что нужно знать родителям о вакцинации ребенка
Для решения вопроса о необходимости вакцинации, определения, какая именно вакцина необходима ребенку, процесса подготовки к прививке и наблюдения после прививки нужно обращаться к врачу.
Необходимо с самого рождения встать на учет в центр семейной медицины, где будет заведена специальная медицинская карта вашего малыша. В эту карту заносятся подробные данные о развитии ребенка, есть ли у него проблемы со здоровьем, а также информация о проведенных прививках. Эти записи могут пригодиться позже, чтобы показать, что ваш ребенок имеет необходимые прививки перед поступлением в детский сад или школу, или на случай переезда или смены врача.
- Показания и противопоказания к прививке
Перед иммунизацией врач (фельдшер) проводит тщательный опрос с целью выявления предшествующих заболеваний, в том числе хронических, наличия реакций или осложнений на предыдущее введение препарата, аллергических реакций на лекарственные препараты, продукты; выявляет индивидуальные особенности организма (недоношенность, родовую травму, судороги), и уточняет, имеются ли контакты с инфекционными больными, а также сроки предшествующих прививок. Помните, что при острых заболеваниях, сопровождающихся повышением температуры (простуда, ангина, бронхит, грипп, пневмония и пр.), прививку, как правило, необходимо будет отложить до выздоровления.
Помните, что при острых заболеваниях, сопровождающихся повышением температуры (простуда, ангина, бронхит, грипп, пневмония и пр.), прививку, как правило, необходимо будет отложить до выздоровления.
- Выраженная аллергическая реакция
Если у ребенка есть аллергические расстройства, то с лечащим врачом нужно заранее обсудить необходимость дополнительных мер.
Помните, что не стоит вводить новые виды пищи за несколько дней до и в первые дни после вакцинации. Если ребенок находится на грудном вскармливании, не включайте в свой рацион новые для себя продукты.
- Анализы и дополнительные разрешения врачей
Лечащий врач может определить, что до прививки могут потребоваться анализы или рекомендации иных специалистов. Например, если педиатру неясен характер изменений нервной системы, он может направить ребенка к неврологу, после чего примет решение о проведении вакцинации и выборе вакцин.
- Советы и рекомендации в день прививки
- Вы имеете право получить у вашего врача информацию о вакцине, необходимости вакцинации, возможных реакциях на вакцинацию и последствиях отказа от вакцинации.
- Врач, в свою очередь, задаст вам вопросы, упомянутые в предыдущем разделе, чтобы определить, имеет ли ваш ребенок какие-либо противопоказания, и нужны ли особые меры предосторожности для проведения вакцинации.
- Не стесняйтесь задавать врачу вопросы. Можно уточнить, например, какой вакциной будет привит ребенок, когда и какие реакции могут возникнуть, и в каких случаях обращаться за медицинской помощью.
- Не следует пугать малыша уколами и врачами. Это может оставить негативный отпечаток на всю жизнь. Если ребёнок уже взрослый, лучше объяснить ему, что будут делать врачи, а главное – для чего. Во время укола можно держать малыша на руках, чтобы исключить неожиданные движения ребенка. Медицинский работник, осуществляющий иммунизацию, не должен сам удерживать ребенка.
 Не следует торопиться покидать центр семейной медицины, обычно врач или медсестра просит родителей посидеть минут 30 неподалеку от кабинета. Это поможет успокоить ребенка и оказать ему помощь в случае возникновения реакций на введение вакцины.
Не следует торопиться покидать центр семейной медицины, обычно врач или медсестра просит родителей посидеть минут 30 неподалеку от кабинета. Это поможет успокоить ребенка и оказать ему помощь в случае возникновения реакций на введение вакцины. - Обсудите с врачом возможность применения и дозировку детского жаропонижающего средства, а также симптомы, при которых обязательно нужно позвонить врачу.
- Погуляйте с ребенком около медицинского учреждения, где была сделана прививка. В случае возникновения аллергических реакций на прививку медицинские работники смогут быстро оказать помощь малышу.
- Дома внимательно следите за самочувствием ребенка. После прививки у ребенка может отмечаться недомогание, беспокойство, повышение температуры. В месте укола может появиться покраснение, уплотнение и болезненность.
- Не накладывайте на место укола компрессы и мази, чтобы снять воспаление. Не занимайтесь самолечением.
- Не купайте ребенка в день прививки, при необходимости можно обтирать теплой водой, не касаясь места укола.

- День после прививки
- Врач может рекомендовать следить за температурой тела малыша в первые дни после прививки. Обсудите с врачом возможность применения и дозировку детского жаропонижающего средства, если это необходимо.
- Если вы беспокоитесь, как выглядит или как ведет себя ребенок после прививки, проконсультируйтесь с врачом.
- Избегайте мест массового скопления людей, не ходите в гости и не приглашайте к себе домой. Ребенок может заразиться от других людей инфекцией, которая может вызвать побочную реакцию после прививки.
- Старайтесь не давать ребенку новый прикорм или новые продукты в течение нескольких дней после прививки. Также не давайте продукты, которые могут вызвать аллергию.
- Если температура ребенка не снижается от приема жаропонижающих препаратов, а наоборот повышается выше 390С и состояние ребенка ухудшается — срочно вызывайте скорую помощь или немедленно доставьте ребенка в больницу.

- В некоторых случаях, когда местные реакции (покраснение, уплотнение и болезненность в месте укола) сильно беспокоят ребенка или сохраняются в течение 3-х дней, необходимо показать ребенка медицинскому работнику и получить рекомендации.
Поствакцинальные реакции
Используемые вакцины в Кыргызстане безопасны, эффективны и соответствуют международным стандартам. Но вакцина, как и любой лекарственный препарат, может вызвать побочные реакции, которые называются побочными проявлениями после иммунизации (ПППИ).
Побочные проявления после иммунизации — любое неблагоприятное изменение в состоянии здоровья, которое возникает после иммунизации и необязательно связано со сделанной прививкой.
В зависимости от причины возникновения ПППИ делятся на 5 типов:
- вакцинальные реакции, связанные со свойствами вакцины
- вакцинальные реакции, связанные дефектом качества вакцины
- вакцинальные реакции, связанные с ошибкой при иммунизации (неправильным обращением, использованием и введением вакцины)
- вакцинальные реакции, связанные с тревожным состоянием при иммунизации (беспокойство и страх укола)
- случайно совпадающие по времени с иммунизацией события
Поствакцинальные реакции относятся к 1-типу ПППИ, являются ответом организма на введение чужеродного антигена и отражают процесс выработки иммунитета. Именно эти реакции обеспечивают защиту детям от тяжелых инфекционных заболеваний и связанных с ними осложнений. Предугадать степень выраженности поствакцинальных реакций невозможно, поскольку это зависит от индивидуальных особенностей организма ребенка.
Именно эти реакции обеспечивают защиту детям от тяжелых инфекционных заболеваний и связанных с ними осложнений. Предугадать степень выраженности поствакцинальных реакций невозможно, поскольку это зависит от индивидуальных особенностей организма ребенка.
В свою очередь поствакцинальные реакции по частоте возникновения и степени тяжести делятся на 2 типа:
- Часто встречающиеся, незначительные реакции на вакцины
- Редко встречающиеся, серьезные реакции на вакцины
Часто встречающиеся, незначительные реакции на вакцины — это индивидуальная реакция организма на отдельные свойства вакцины, которые ожидаемы и указаны в инструкции, приложенной к вакцине. Эти обычные реакции, быстро проходящие и не причиняющие вред здоровью ребенка. Они проявляются в виде менстных и общих реакций.
Местные реакции— это покраснения, болезненности, отеки и уплотнения в месте введения вакцины. Они развиваются в день введения вакцины и держатся не более 2-3 суток и не требуют медицинского вмешательства.
Помните о том, что только врач может порекомендовать лекарства для того, чтобы облегчить болевые ощущения от местной реакции. Использование местных согревающих процедур (медикаментозных, физиолечения) противопоказано.
Если местные реакции, независимо от размеров, сохраняется более 3-х дней, необходимо немедленно обратиться к врачу.
Общиереакции – это изменение общего состояния и поведения ребенка: беспокойство, недомогание, нарушение сна и аппетита, повышение температуры до 380С.
Проконсультируйтесь с врачом после проведения прививки, так как каждая вакцина может вызывать разную реакцию, также организм каждого малыша индивидуален.
Редко встречающиеся или серьезные реакции на вакцины — это чрезмерные реакции организма на конкретный компонент в вакцине, которые не ожидаемы, не желательны и не предсказуемы. Серьезные реакции встречаются очень редко и обычно приводят к смерти или длительной инвалидности.
К редко встречающимся местным побочным проявлениям на введение БЦЖ вакцины являются:
- поверхностная язва — от 3 недель до 6 месяцев после прививки
- келоидный рубец в месте введения вакцины — через 1 год после прививки
- увеличение лимфатических узлов на стороне введения вакцины — спустя 2-6 месяцев после прививки
Сильная местная реакция на введение любой вакцины (гиперемия более 8 см, отек более 5 см в диаметре) является противопоказанием к последующему применению данного препарата.
У детей, имеющих аллергические заболевания, или в результате повышенной чувствительности к компонентам вакцины могут возникнуть аллергические реакции на прививку: крапивница, отек Квинке, анафилактический шок. Они могут возникнуть как при первом введении вакцины, так и при повторной вакцинации.
Прививка от кори, краснухи, паротита, дифтерии, столбняка, коклюша
Каждый здравомыслящий родитель очень трепетно относится к здоровью ребенка, стараясь оградить от опасных инфекций и сформировать крепкий иммунитет – как залог здоровой жизни.
В современном мире вакцинация является основой профилактики целого ряда тяжелейших болезней, опасных своими серьезными осложнениями. Активный иммунитет после проведения прививок сохраняется в течение нескольких лет у вакцинированных против кори, дифтерии, столбняка, полиомиелита, гепатита В или в течение нескольких месяцев у привитых, к примеру, от гриппа, а при своевременной ревакцинации может сохраняться всю жизнь.
Увеличение спектра вакцин позволило значительно расширить возможности профилактики инфекций у детей с хроническими заболеваниями и нарушениями иммунитета, а также обеспечило возможность комбинированного их применения. Кроме того, что постановка комбинированных вакцин создает не менее прочный иммунитет, она еще и уменьшает количество инъекций (а ведь это процедура малоприятна для ребенка) и число посещений медицинских учреждений.
К сожалению, однократная вакцинация не способна подготовить иммунную систему к полноценной, надежной и долговременной защите, поэтому прививки против ряда инфекций приходится проводить 2-х или 3-х кратно. А своевременно проведенная ревакцинация – необходимая процедура для закрепления и поддержания иммунитета – позволит создать крепкую и надежную защиту.
А своевременно проведенная ревакцинация – необходимая процедура для закрепления и поддержания иммунитета – позволит создать крепкую и надежную защиту.
Таким образом, вакцинация очень важное мероприятие – ведь ее целью является создание невосприимчивости к инфекционным заболеваниям.
В нашей стране, полагаясь на опыт многолетних наблюдений, с учетом уровня развития современной медицины и качества вакцин разработан календарь профилактических прививок, который предусматривает вакцинацию от основных опасных инфекций. Кроме того, в альтернативном порядке можно защитить ребенка дополнительно от ряда заболеваний – к примеру, от гриппа, ветряной оспы, гепатита А, клещевого энцефалита, менингококковой инфекции.
Впервые с вопросом о вакцинации новорожденного ребенка мама сталкивается еще в родильном доме – это прививка от гепатита В, которую ставят малышу в первые часы его жизни. Что же это за заболевание и чем оно так опасно?
Гепатит В – инфекционно-вирусное заболевание поражающее преимущественно клетки печени, склонное к затяжному и хроническому течению с формированием таких грозных осложнений как цирроз и рак печени. В редких случаях болезнь может протекать молниеносно, с неблагоприятным исходом.
В редких случаях болезнь может протекать молниеносно, с неблагоприятным исходом.
Для профилактики необходима 3-х кратная вакцинация.
Календарь прививок предполагает также вакцинацию против дифтерии.
Дифтерия – острое инфекционное заболевание, характеризующееся симптомами интоксикации, пленчатой ангиной, воспалением гортани с развитием крупа. Заболевание может протекать в токсической, молниеносной и тяжелой формах с формированием осложнений со стороны сердца, почек, нервной системы.
Профилактику начинают с 3-х месячного возраста, вакцинируя ребенка 3-х кратно с интервалом в 45 дней между прививками, с последующей ревакцинацией в 18 месяцев и дальнейшими возрастными ревакцинациями в 7 лет, 14 лет и у взрослых каждые 10 лет от момента последней ревакцинации.
Обычно вакцинацию от дифтерии совмещают с вакцинацией против коклюша и столбняка. Какую угрозу здоровью несут эти инфекции?
Коклюш – инфекционное заболевание, вызываемое бактериями выделяющими токсины, которые раздражают кашлевой и дыхательный центры. Болезнь характеризуется циклическим затяжным течением и наличием своеобразного судорожного приступообразного кашля. Течение может сопровождаться серьезными осложнениями, такими как: поражение легких, сердца, кровоизлияниями под кожу и слизистые, развитием гипоксии и поражением нервной системы.
Профилактика заключается в 3-х кратной вакцинации с интервалом между прививками в 45 дней, начиная с 3-х месячного возраста ребенка. Ревакцинация однократно в возрасте 18 месяцев.
Столбняк – острое инфекционное заболевание, характеризующееся поражением центральной нервной системы, вызывает развитие судорог и удушья.
Профилактическая схема вакцинации и ревакцинации идентична таковой при дифтерии.
Помимо перечисленных инфекций в календарь профилактических прививок включена вакцинация против полиомиелита.
Полиомиелит – коварен развитием поражений нервной системы (вялые параличи и парезы), длительным и затяжным течением с возможностью инвалидизации.
Вакцину против полиомиелита впервые рекомендуют вводить в 3-х месячном возрасте (совместно с вакцинами против коклюша, дифтерии и столбняка) также 3-х кратно с интервалом в 45 дней между прививками, с ревакцинацией в 18 месяцев, 20 месяцев и 14 лет.
Чем же ребенку грозят такие вирусные заболевания как корь, краснуха и паротит? И почему вакцинацию против них также внесли в прививочный календарь?
Корь – острая вирусная инфекция, часто протекает с лихорадкой, появлением характерной сыпи, симптомами интоксикации, поражением дыхательных путей, полости рта и глаз. Опасна корь развитием осложнений со стороны органов дыхания, нервной системы и присоединением вторичных инфекций на ослабленном фоне.
Краснуха – особенно опасна для беременных формированием пороков развития плода (поражение глаз, глаукома, врожденные пороки сердца, головного мозга).
Паротит – вирусное заболевание, поражающее железистые органы (слюнные железы, поджелудочную железу, яички у мальчиков) и нервную систему (паротитный менингит). Осложнениями паротита могут быть сахарный диабет и мужское бесплодие.
Для того чтобы уберечь малыша от кори, краснухи и паротита достаточно сделать одну прививку в 12 месяцев и выполнить ревакцинацию в 6 лет.
Чтобы сохранить здоровье малыша и создать крепкий иммунитет против опасных инфекций мы предлагаем воспользоваться услугами ДДЦ по вакцинации детей до 18 летнего возраста. В ДДЦ применяются современные, надежные, качественные и хорошо зарекомендовавшие себя вакцины. При вакцинации учитываются индивидуальные особенности здоровья каждого ребенка и переносимость тех или иных прививок. Квалифицированные специалисты помогут создать индивидуальный график вакцинации, с учетом состояния здоровья Вашего ребенка.
Посмотреть цены на прививки ›Вакцины против рака поджелудочной железы
Реферат
Аденокарцинома протока поджелудочной железы (КПК) остается очень смертельным заболеванием; срочно необходимы новые терапевтические методы. Ряд иммунотерапевтических методов, протестированных на доклинических моделях, оказались многообещающими. Клинические испытания ранней фазы продемонстрировали доказательства активации иммунной системы, которая в некоторых случаях коррелирует с клиническим ответом. Более того, недавние данные подчеркивают сложную роль воспаления в ОАП, даже на его самых ранних стадиях.Таким образом, КПК созрел для иммунотерапии; тем не менее, прежде чем добиться успеха, остаются серьезные проблемы. В будущих исследованиях необходимо будет сосредоточить внимание на открытии новых антигенов КПК и идентификации множественных иммуносупрессивных путей в микроокружении опухоли КПК, которые ингибируют эффективный целевой иммунный ответ КПК. Теперь доступны технологии для быстрого продвижения открытий. Быстрое воплощение новых открытий в научно обоснованных клинических испытаниях комбинаций иммунных агентов, вероятно, продолжит сдвигать проканцерогенную среду опухоли в сторону наиболее мощного противоопухолевого ответа.
Ключевые слова: рак поджелудочной железы, иммунотерапия, противораковая вакцина
Введение
Протоковая аденокарцинома поджелудочной железы (КПК) является четвертой ведущей причиной смертей, связанных с раком, в Соединенных Штатах: по оценкам, 43 920 новых случаев и 37 390 смертей в 2012 г. 1 Несмотря на резкое снижение смертности после хирургического вмешательства и открытие новых режимов химиотерапии, за последние 30 лет произошло минимальное улучшение безрецидивной и общей выживаемости.По мере развития области иммунологии рака, более глубокое понимание того, как иммунная система распознает опухолевые клетки и их антигены, превратилось в захватывающие новые методы лечения различных солидных опухолей, включая КПК.
Новые данные подтверждают критическую роль иммунной системы в развитии, прогрессировании и ликвидации опухоли КПК. Кларк и его коллеги разработали доклиническую иммунокомпетентную модель мыши, генетически сконструированную для развития КПК посредством точечной мутации в одном аллеле Kras .Эта мутация Kras инициирует интраэпителиальную неоплазию поджелудочной железы (PanIN), которая в конечном итоге прогрессирует до PDA, и воспроизводит среду стромальных и воспалительных клеток, обнаруженную при развитии PDA человека. 23 Оценка этих мышиных PDA и PanIN показала, что 50% опухоли состоит из лейкоцитов, особенно иммуносупрессивных клеток, включая ассоциированные с опухолью макрофаги (ТАМ), миелоидные супрессорные клетки (MDSC) и регуляторные Т-клетки (Tregs). ), наряду с очень небольшим процентом эффекторных Т-клеток.Таким образом, авторы предполагают участие иммуносупрессивных клеток в раннем онкогенезе КПК и их возможную роль в облегчении прогрессирования заболевания. 3
Другие доклинические исследования недавно продемонстрировали роль хронического воспаления в канцерогенезе КПК. Например, экспрессия конкретных тестовых генов рака, наблюдаемая в образцах хронического панкреатита человека, коррелирует с экспрессией их соответствующими опухолями PDA человека. 4 В качестве другого примера Guerra et al. Обнаружили, что мыши с мутацией Kras нуждались во втором сигнале в форме хронического панкреатита для развития PDA, предполагая, что PDA происходит из комбинации генетического и негенетического (например,ж., хронический панкреатит) события. 5,6 Кроме того, было показано, что инфильтрирующие нейтрофилы вносят вклад в онкогенез КПК и уклонение иммунной системы на доклинических моделях КПК путем активации ангиогенеза на самых ранних стадиях КПК. 7-9 Кроме того, Эспозито и его коллеги показали, что мононуклеарные воспалительные клетки врожденного иммунного ответа привлекаются к КПК и могут влиять на метастатическую способность раковых клеток. 10 Наконец, экспрессия циклооксигненазы-2 (ЦОГ-2) повышается в очагах PDA и PanIN человека и увеличивается с увеличением тяжести PanIN по сравнению с нормальной поджелудочной железой и хроническим панкреатитом. 11,12
Хотя первоначально считалось, что КПК обладает слабой иммуногенностью, недавние данные опровергли это предположение. Во-первых, в костном мозге пациентов с КПК наблюдается высокая частота опухолеспецифических Т-лимфоцитов. 13 Во-вторых, Фукунга и его коллеги проанализировали 80 хирургически резецированных опухолей КПК в поисках Т-клеток CD4 + , Т-клеток CD8 + и дендритных клеток внутри опухоли. Они сообщили, что более высокие уровни CD4 + и CD8 + лимфоцитов, инфильтрирующих опухоль (TIL) в КПК, были связаны с более длительной общей выживаемостью после хирургической резекции.Присутствие TIL CD4 + и CD8 + было независимым благоприятным прогностическим фактором при многомерном анализе. 14 Однако до сих пор не известно, являются ли эти Т-клетки специфичными для КПК.
Эти данные вместе с результатами ранних клинических испытаний иммунотерапии (обсуждаемых ниже) подтверждают гипотезу о том, что КПК способен вызывать противоопухолевый иммунный ответ. Однако это скорее исключение, чем правило, потому что также существует множество механизмов, которые естественным образом подавляют эту реакцию.Важно отметить, что многие из этих механизмов, вероятно, также поддерживают рост и прогрессирование опухоли. Вопрос уже не в том, улучшит ли иммунотерапия результаты КПК, а в том, как улучшить иммунный ответ иммунной системы против КПК и ограничить способность опухоли уклоняться от обнаружения иммунной системой? В этом обзоре будет обсуждаться наше текущее понимание опухолевых антигенов, вакцин, которые способны доставлять эти антигены для индукции PDA-специфического иммунного ответа, и механизмов в микроокружении опухоли, которые подавляют эффективный иммунитет.Кроме того, будут подведены итоги доклинических и клинических исследований, посвященных комбинаторной иммунотерапии, которые обходят механизмы иммунной толерантности для активации наиболее мощного противоопухолевого иммунного ответа.
Опухолевые антигены и иммунная толерантность
Раковые клетки происходят от их нормальных аналогов после генетических изменений, приводящих к их злокачественному фенотипу. Эти генетические изменения приводят к экспрессии ассоциированных с опухолью антигенов (ТАА), которые представляют собой неправильно свернутые измененные белки, экспрессируемые раковыми клетками.TAA представлены молекулами главного комплекса гистосовместимости (MHC) (человеческий лейкоцитарный антиген (HLA) в организме человека) эффекторным Т-клеткам. Эти Т-клетки содержат уникальные Т-клеточные рецепторы, которые распознают специфические антигенные эпитопы, связанные с молекулами MHC. Это взаимодействие известно как «сигнал 1». Одного сигнала 1 недостаточно для соответствующей активации Т-клеток и он приводит к анергии или апоптозу Т-клеток, что позволяет опухоли ускользать от обнаружения иммунной системой. Сопутствующее связывание костимулирующих молекул, таких как B7-1 и CD28, на поверхности антигенпрезентирующих клеток (APC) и Т-клеток, соответственно, приводит к «сигналу 2», критическому компоненту активации Т-клеток ().
A. TAA экспрессируются в виде небольших пептидных фрагментов на молекулах HLA и представляются Т-клеткам для распознавания и активации и упоминаются как Т-клеточный сигнал 1. Однако опухолевые клетки не могут эффективно активировать только Т-клетки, потому что они не экспрессируют костимулирующие молекулы, такие как B7.1 и B7.2, которые обеспечивают сигнал 2. Вакцины предназначены для доставки TAA к антигенпрезентирующим клеткам, которые естественным образом активируют как сигнал 1, так и сигнал 2. Дендритные клетки являются наиболее эффективными антигенпрезентирующими клетками из-за их способность легко обрабатывать опухолевый антиген и представлять их как на поверхностных молекулах MHC I, так и на II, которые затем связываются с рецепторами Т-клеток на Т-клетках CD4 + и CD8 + .DC также усиливают экспрессию B7-1 / B7-2 (сигнал 2) для эффективной активации Т-клеток. Члены иммунорегуляторных рецепторов клеточной поверхности на Т-клетках, таких как CTLA-4, выключают активированные Т-клетки, конкурируя с активирующими рецепторами (сигнал 2) за тот же лиганд, позволяя опухоли уклоняться от иммунного распознавания. Цитокины, продуцируемые Т-клетками, опосредуют как активирующие, так и подавляющие иммунные ответы. B. Примеры различных членов семейства как костимулирующих, так и ингибирующих сигналов на антигенпрезентирующих клетках, которые взаимодействуют с Т-клетками.TCR = рецептор Т-клеток MHC = главный комплекс гистосовместимости
У большинства опухолевых клеток отсутствуют необходимые поверхностные молекулы, то есть B7-1 (CD80) и B7-2 (CD86), для завершения сигнала 2. 15 Профессиональные APC, например дендритные клетки (ДК) являются более эффективными активаторами Т-клеток. Механизмы внутриклеточной обработки, уникальные для DC, позволяют им эффективно обрабатывать опухолевые антигены и представлять их как на поверхностных молекулах MHC I, так и на MHC II, что приводит к активации Т-клеток CD8 + и CD4 + соответственно.Зрелые DC постоянно экспрессируют костимуляторные молекулы в непосредственной близости от комплексов MHC. 16 Примеры членов известных в настоящее время семейств костимуляторов показаны в.
Иммунотерапия рака направлена на использование естественной способности иммунной системы распознавать новые антигены и реагировать на них — в случае рака, TAA. Однако опухолевые клетки используют различные механизмы, чтобы избежать обнаружения иммунной системой. Воспалительные сигналы, например, гамма-интерферон (IFN-γ), трансформирующий фактор роста β (TGF-β) и интерлейкин 10 (IL-10), играют решающую роль как в эрадикации, так и в развитии опухоли (2). 17 Молекулы клеточной поверхности, такие как цитотоксический Т-лимфоцитарный антиген-4 (CTLA-4), PD-1, PD-L1 (B7-h2) и PD-L2 (B7-DC), являются примерами сигнальных путей иммунных контрольных точек, которые подавляют Активация Т-клеток. 18 Другие семейства ингибиторов контрольных точек показаны в.
Опухолевые клетки, стромальные клетки и иммунные клетки в микроокружении опухоли продуцируют факторы, подавляющие ТАА-специфические Т-клеточные ответы. Взаимодействие TGF-β и рецептора TGF-β приводит к ядерной транслокации комплекса SMAD4 / DPC4. 19 Было показано, что комплекс SMAD / DPC4 подавляет рост опухоли и подавляется более чем в 50% современных КПК. 20 TGF-β непосредственно подавляет пролиферацию Т-клеток и подавляет активность Т-клеток CD8 + посредством взаимодействия с внутриклеточным белковым комплексом SMAD4 / DPC4. 19 Более того, TGF-β усиливает экспрессию FoxP3, маркера Tregs CD4 + CD25 + , которые играют неотъемлемую роль в способности опухоли уклоняться от иммунной системы. 19
IL-10, продуцируемый Treg и другими иммунными клетками, способствует иммунной толерантности путем прямого ингибирования дифференцировки и пролиферации APC и Th2-клеток. 21 Анализ клеток рака поджелудочной железы человека после хирургической резекции показал, что производные опухоли TGF-β и IL-10 действуют совместно, способствуя ответу клеток Th3 и ингибируя дифференцировку и пролиферацию клеток Th2. 22 Преобладающие иммунные ответы Th3 связаны с плохой защитой от злокачественных опухолей и снижением выживаемости у пациентов с раком поджелудочной железы по сравнению с ответом Th2. 23,24 Это наиболее вероятно из-за неспособности DC активировать CTL в присутствии IL-10 и способности IL-10 действовать непосредственно на опухолевые клетки и подавлять экспрессию HLA класса I. 21
CTLA-4 экспрессируется на поверхности активированных Т-клеток и конкурирует с CD28 за связывание B7-1. Это взаимодействие выключает активированные Т-клетки, ингибируя внутриклеточный сигнальный каскад B7.1. Взаимодействие CTLA-4 B7.1 ограничивает реакцию активации иммунной системы как на чужеродные, так и на аутоантигены.У мышей с нокаутом CTLA-4 наблюдается тяжелое аутоиммунное заболевание и сокращается продолжительность жизни. 18 Хотя эти иммунологические контрольные точки важны для поддержания самотолерантности, опухолевые клетки используют их, чтобы выключить противоопухолевый иммунный ответ.
B7-h2 (PD-L1) и B7-DC (PD-L2) представляют собой лиганды клеточной поверхности, экспрессируемые многими опухолевыми клетками, DC, активированными T-клетками, B-клетками и макрофагами. Они связываются со своим общим рецептором PD-1 на активированных Т-клетках CD4 + и CD8 + .Взаимодействие PD-L1 или PD-L2 и PD-1 подавляет активированные Т-клетки CD4 + и CD8 + , что приводит к остановке клеточного цикла. 25 Эта опухоль-специфическая иммунологическая контрольная точка — еще один механизм, используемый опухолевыми клетками для уклонения от иммунитета.
Микроокружение опухоли использует различные другие механизмы и факторы, такие как фактор роста эндотелия сосудов (VEGF), интерлейкин (IL-6) и циклооксигеназа 2 (COX-2), чтобы препятствовать дифференцировке и созреванию DC. 16 Более того, в микроокружении опухоли снижается количество активирующих DC цитокинов, таких как фактор, стимулирующий колонии гранулоцитов и макрофагов (GM-CSF) и интерлейкин 4 (IL-4). 16 Стромальные клетки также секретируют цитокины, хемокины и другие факторы, способствующие развитию опухоли, которые препятствуют эффективному уничтожению опухоли. 17 Таким образом, комбинация стромальных клеток, DC, эндотелиальных клеток, макрофагов и опухолевых клеток в микроокружении опухоли секретирует комбинацию цитокинов и клеточных сигналов, которые в конечном итоге определяют, запускается ли проопухолевый или противоопухолевый иммунный ответ.Как обсуждается ниже, иммунотерапия стремится склонить чашу весов в пользу противоопухолевого иммунного ответа.
Идентификация ассоциированного с опухолью антигена и презентация антигена
Идентификация PDA TAA остается критически важной для разработки более эффективной терапии вакцинами и оценки опухолеспецифических Т-клеточных ответов. В течение многих лет вакцины против КПК нацелены на несколько известных белков, которые были либо продуктами онкогенов (мутировавший Kras), либо дифференциально экспрессируемыми гликопротеинами, такими как MUC1 и CEA. 26 Последние разработки в области генетики и протеомики ускорили прогресс в идентификации антигена КПК (). Анализ дифференциальной экспрессии генов позволяет идентифицировать гены с высокой экспрессией в клетках КПК по сравнению с неопухолевыми клетками. В качестве примера, используя серийный анализ экспрессии генов, Аргани и его коллеги определили, что мезотелин сверхэкспрессируется в большинстве (почти 100%) КПК. 27 В ходе последующего исследования использовались иммунизированные лимфоциты пациентов с КПК, получавших вакцину, секретирующую гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF) (GVAX), для скрининга пептидов мезотелина, и было продемонстрировано увеличение поствакцинальных Т-клеток, специфичных для мезотелина, у пациентов. которые продемонстрировали длительную выживаемость без болезней. 28 Мезотелин охватывает многие принципы, необходимые для оптимального опухолевого антигена, поскольку он имеет очень низкий профиль экспрессии в нормальных клетках, высоко экспрессируется в клетках КПК и, возможно, участвует в прогрессировании рака и метастазировании. 17 Антитела против мезотелина использовались в ранней фазе клинических испытаний у пациентов с КПК, мезотелиомой и раком яичников с ограниченной клинической эффективностью. 29 Однако живую аттенуированную рекомбинантную бактериальную вакцину Listeria monocytogenes (LM) , экспрессирующую мезотелин, вводили пациентам с метастатическим ОАП, причем более 37% пациентов жили дольше 15 месяцев. 30 Рандомизированное контролируемое многоцентровое исследование фазы II в настоящее время оценивает комбинацию LM , экспрессирующую мезотелин, в качестве усиления после прайминга с панкреатическим GVAX у взрослых с метастатическим ОАП (обсуждается ниже).
Методы идентификации опухолевых антигеновДифференциальный анализ генов, секвенирование экзома и протеомика — это три различных метода идентификации опухолевых TAA в КПК. Иммуноанализы, проведенные на Т-клетках вакцинированных пациентов с КПК, определяют наличие антиген-специфических цитотоксических Т-клеток CD8 + .Эти антигены затем можно использовать для разработки более эффективных антигенспецифических иммунотерапевтических средств.
В последние годы протеомные подходы, такие как серологический анализ библиотек экспрессии рекомбинантной кДНК, серологический протеомный анализ и технология белковых микроматриц, все использовались в качестве альтернативного подхода для идентификации опухолевых антигенов. Аннексин А2 был недавно идентифицирован как антиген КПК с использованием сыворотки человека для скрининга белков, экспрессируемых КПК GVAX, который служил протеомом.Впоследствии сыворотки до и после лечения были проанализированы у 60 пациентов, получавших GVAX, и продемонстрировали индукцию антител к аннексину A2 после лечения у большинства пациентов с длительной выживаемостью без заболевания. 31 Это предполагает, что ответы антител могут ингибировать опосредованное аннексином А2 прогрессирование опухоли. Доклинические исследования показали, что аннексин А2 играет критическую роль в инвазии и метастазировании рака поджелудочной железы, что делает маловероятным потерю экспрессии аннексина А2 во время прогрессирования рака. 31 Более того, терапия, направленная на аннексин А2, предотвращала метастазы опухоли в двух моделях КПК на мышах, что предполагает критическую роль аннексина А2 в метастатической активности КПК. В настоящее время разрабатываются антитела против аннексина и вакцины для будущих клинических испытаний. 32
Секвенирование экзома — это тип высокопроизводительного анализа дидезокси-секвенирования, который конкретно фокусируется на кодирующей части генома и позволяет идентифицировать большинство типов кодирующих генетических изменений при раке человека. 33 Джонс и его коллеги проанализировали 24 рака поджелудочной железы и обнаружили, что они содержат в среднем 63 генетических изменения. 34 Эти изменения идентифицировали основной набор из 12 клеточных сигнальных путей, включая сигнальные пути Kras, сигнальные пути TGF-β и сигнальные пути hedgehog, которые были изменены в 67–100% опухолей. 34 Все больше и больше опухолей КПК секвенировали с использованием секвенирования экзома. Этот тип высокопроизводительного и эффективного анализа генов дает возможность перейти от генерических вакцин к вакцинам, специфичным для пациента.Теперь можно быстро секвенировать опухоли отдельных пациентов и идентифицировать специфические для пациента мутации, которые могут служить уникальными мишенями для вакцины. Эти новые производные от мутаций TAA, вероятно, будут иметь решающее значение для роста и дифференцировки данной конкретной опухоли, а также для относительно нового изменения в микросреде опухоли, тем самым уменьшая вероятность иммунной толерантности к этим уникальным антигенам. Одно исследование уже показало, что идентификация специфических мутаций с использованием секвенирования экзома может привести к открытию новых и уникальных эпитопов с более высоким сродством к комплексам HLA, тем самым улучшая презентацию антигена. 35 Таким образом, будущая терапия вакциной против рака поджелудочной железы должна быть реально адаптирована к индивидуальному пациенту на основе его собственных характеристик опухоли.
Вакцинотерапия
Самая эффективная вакцинация усиливает презентацию антигена с помощью DC, активируя патоген-специфические эффекторные Т-клетки и Т-клетки памяти. Вакцины против рака были впервые одобрены для профилактики гепатомы и рака шейки матки. Совсем недавно первая вакцина (Provenge, Sipuleucel-T) была одобрена для лечения рака простаты. 36
Антигенспецифические вакцины
Антигенспецифические вакцины нацелены на известные опухолевые антигены, тем самым вызывая опухолеспецифический иммунный ответ. Пептидные или белковые вакцины используют идентифицированные иммунодоминантные опухолевые эпитопы для стимуляции противоопухолевых ответов Т-клеток. В PDA естественной отправной точкой для этих вакцин стали опухолевые маркеры, такие как карциноэмбриональный антиген (CEA) и MUC-1, а также мутировавшие белки, которые играют важную роль в PDA, такие как Ras и теломераза. 37 Преимущества пептидных вакцин включают простоту производства и введения, но они также обладают низкой иммуногенностью и менее способны создавать иммунологическую память. 38 Первой клинически протестированной вакциной КПК была вакцина на основе мутантного пептида Ras, разработанная для стимуляции антимутантного ответа на Ras. Из 5 пациентов с КПК в этом испытании двое прожили более 8 месяцев, и иммунологический анализ показал наличие у обоих этих пациентов Т-клеток CD4 + и CD8 + , специфичных к мутации Ras. 39,40 Однако последующие исследования не показали клинически значимого иммунитета к пептиду, доставленному Kras.
Имеются данные, свидетельствующие о том, что неэффективность лечения этими ранними вакцинами была вызвана неспособностью иммунной системы адекватно реагировать на эти антигены. 41 Это привело к открытию того, что местные цитокины имеют решающее значение для индукции правильного иммунного ответа, и что GM-CSF оказался наиболее эффективным при стимуляции активации как CD4 + , так и CD8 + Т-клеток у мышей. модели опухолей. 41,42 Впоследствии вакцинацию пептидом проводили в сочетании с GM-CSF, вызывая более эффективную активацию дендритных клеток и презентацию антигена. Было проведено второе клиническое испытание мутированной пептидной вакцины ras, в котором 48 гистологически подтвержденных пациентов с PDA получили вакцину мутантного пептида ras, на этот раз в комбинации с внутрикожным GM-CSF. Более 50% пациентов продемонстрировали опухолеспецифический иммунный ответ, связанный с их мутантной вакциной Ras. Более того, эти пациенты продемонстрировали статистически значимое улучшение медианы общей выживаемости по сравнению с их не отвечающими на лечение сверстниками (148 дней vs.61 день, p = 0,0002) (). 43
Таблица 1
Испытания вакцины против рака поджелудочной железы
| Исследование | Популяция пациентов / стадия заболевания | Вакцина | Иммунологический анализ | 9024 9023 9024 Справочная информация о выживаемости Пептидные вакциныGjertsen, 1995 | 5 пациентов с гистологически подтвержденным КПК | Мутантный пептид KRAS | 2/5 с индуцированными вакциной ras-специфическими CD4 + и CD8 + Т-лимфоциты | 2 иммунных ответчика показали более длительный ответ выживаемость | [ 39 ] | |
|---|---|---|---|---|---|---|---|---|---|---|
| Gjertsen, 2001 | 48 пациентов, 10 хирургически удаленных КПК и 38 пациентов с расширенным КПК | Мутантный пептид KRAS с GM-CSF | Специфический ответ на мутантный KRAS у 58% пациентов | 148 дней у респондентов по сравнению с 61 днем у не ответивших | [ 43 ] | |||||
| Bernhardt, 2006 | 48 пациентов с неоперабельным КПК | Теломеразный пептид (GV1001) с GM-CSF | Иммунный ответ измерялся как DTH и пролиферация Т-клеток in vitro у 24 из 38 пациентов (75% промежуточной дозы группа) | 8.6 месяцев в группе со средней дозой | [ 46 ] | |||||
| Gilliam, 2012 | 154 пациента с прогрессирующим ОАП, не желающих или неспособных проходить химиотерапию | Гастрин-пептидная вакцина (G17DT) по сравнению с плацебо | Ответ против G17DT у 78% пациентов в группе G17DT | 151 день (G17DT) по сравнению с 82 днями (плацебо), P = 0,03 | [ 44 ] | |||||
| Рекомбинантные вакцины | Кауфман, 2007 | 10 пациентов с КПК поздней стадии | TRICOM, MUC-1 и CEA в поксвирусе с GM-CSF | Антигенспецифические Т-клеточные ответы у 5 из 8 обследованных пациентов | 15.1 месяц у респондентов против 3,9 месяца у не ответивших (p = 0,002), 6,3 месяца в целом | [ 49 ] | ||||
| Le, 2012 | 28 пациентов с мезотелиомой, раком легких, поджелудочной железы или яичников печень метастазы | Живая аттенуированная вакцина Listeria (ANZ-100) (n = 9) по сравнению с живым аттенуированным мезотелином, экспрессирующим вакцину Listeria (CRS-207) (n = 17) | LLO и мезотелин-специфические Т-клеточные ответы, наблюдаемые в Группа CRS-207 | 37% пациентов в группе CRS-207 живы через 15 месяцев | [ 30 ] | |||||
| Вакцина на основе дендритных клеток | Lepisto, 2008 | 12 пациентов с удаленным раком поджелудочной железы и желчных путей | MUC-1 импульсная аутологичная вакцина постоянного резецированный КПК | GM-CSF-секретирующая цельноклеточная вакцина в сочетании со стандартной химиолучевой терапией | У 3 из 14 пациентов развился ГЗТ к аутологичным опухолевым клеткам | NR (3 из 14 пациентов с пролонгированной безрецидивной выживаемостью) | [ 61 ] | |||
| Laheru, 2008 | 50 пациентов с прогрессирующим ОАП, у которых не удалось по крайней мере 2 режима химиотерапии | Группа A: только цельноклеточная вакцина GM-CSF (n = 20) vs.Группа B: цельноклеточная вакцина GM-CSF и Cy (n = 30) | Усиленные мезотелин-специфические Т-клеточные ответы, связанные в группе B | Группа A: 2,3 месяца Группа B: 4,3 месяца | [ 63 ] | |||||
| Hardacre, 2010 | 62 пациента с резецированным ОАП | Вакцина HyperAcute-Pancreas плюс стандартная химиотерапия на основе гемцитабина / 5-ФУ | NR | NR | [ 66 ] | |||||
| пациентов 2011 60245 L с резецированным КПК | GM-CSF-секретирующая цельноклеточная вакцина в сочетании со стандартной химиолучевой терапией | Индукция CD8 + мезотелин-специфических Т-клеток, коррелирующая с общей выживаемостью | 24.8 месяцев | [ 62 ] | ||||||
| Комбинаторная иммунотерапия | Le, 2012 | 30 пациентов с местнораспространенным, резистентным к лечению или метастатическим ОАП | Ипилимумаб (IPI), цельный IPI плюс GM-CSF клеточная вакцина | IRAE (p = 0,037), мезотелиновые Т-клеточные ответы (p = 0,012) и усиление репертуара Т-клеток (p = 0,026), связанного с OS в обеих группах | Только IPI: 3,3 месяца IPI плюс GM- Вакцина против спинномозговой жидкости: 5.5 месяцев | [ 71 ] |
В другом раннем клиническом исследовании использовалась вакцина на основе гастрина у 154 пациентов с поздней стадией ОАП. Это мультиинституциональное двойное слепое плацебо-контролируемое исследование продемонстрировало почти двукратное увеличение средней общей выживаемости в группе лечения по сравнению с группой плацебо (151 день против 82 дней, соответственно, p = 0,03). 44 Иммунные ответы против гастрина были отмечены у 73,8% пациентов и коррелировали с более длительной общей средней выживаемостью по сравнению с пациентами, не ответившими на лечение, и плацебо (176 vs.63 дня против 83 соответственно, p = 0,003). 44
Теломераза, которая реактивируется более чем в 85% клеток КПК, также использовалась для разработки пептидных вакцин КПК. Клинические испытания фазы I и II с участием пациентов с местнораспространенным и метастатическим PDA также продемонстрировали более длительную выживаемость у иммунных ответчиков по сравнению с пациентами, не отвечающими на лечение, в клинических исследованиях ранней фазы. 45,46 Эти исследования были обнадеживающими, продемонстрировав доказательства иммунной индукции, связанной с преимуществами выживания.Однако очень скромные преимущества в отношении выживаемости, вероятно, были связаны с неоптимальной способностью пептидных вакцин адекватно активировать DC и вызывать наиболее сильный иммунный ответ. 46
Рекомбинантные вакцины содержат бактериальные и вирусные носители антигена, тем самым увеличивая активацию DC и улучшая презентацию антигена. Они стимулируют врожденный иммунный ответ, эффективно рекрутируя и активируя DC. Наиболее распространенными носителями являются Bacille Calmette-Guerin (BCG), Listeria monocytogenes ( LM ), Salmonella и поксвирусы.Клинические испытания с использованием рекомбинантных вакцин CEA и MUC1 показали небольшую эффективность у пациентов с КПК. Однако неудача этого подхода, вероятно, была связана с отсутствием иммуногенности TAA, которые были нацелены, и с продвинутой стадией пациентов с КПК в исследовании. 47-50 Вакцины на основе LM были широко изучены, учитывая внутриклеточный жизненный цикл LM и последующую способность воздействовать на пути MHC класса I и II. 51 Кроме того, LM прост в выращивании, лечении и легко сконструирован для экспрессии антигенов, что делает его идеальным вектором для иммунотерапии опухолей. 51
Генно-инженерные вакцины LM , несущие опухолевые антигены, были изучены на моделях рака груди и толстой кишки у мышей. Вакцинация LM обеспечила регресс опухоли и общее улучшение выживаемости по сравнению с плацебо. 52,53 На доклинической модели метастатического рака толстой кишки было показано, что аттенуированный штамм LM , экспрессирующий иммунодоминантный антиген рака толстой кишки мышей Ah2, увеличивает общую выживаемость. Было отмечено, что LM преимущественно инфицирует печень и способствует перитуморальной провоспалительной среде, ведущей к притоку опухолеспецифических Т-клеток и продукции IFN-γ. 54 Эти результаты послужили толчком к первым исследованиям на людях с использованием антигена, экспрессирующего вакцины на основе LM .
Пациентам с диагнозом метастазы в печень от мезотелиомы, рака яичников, немелкоклеточного рака легких и КПК вводили живой аттенуированный штамм Listeria , экспрессирующий мезотелин, молекулу клеточной поверхности, сверхэкспрессируемую этими опухолями. Вакцина хорошо переносилась с минимальными побочными эффектами. 30 Тридцать семь процентов пациентов выжили более 15 месяцев.Половина из этих пациентов была с метастатическим КПК, и иммунологический анализ выявил листериолизин О и мезотелин-специфические Т-клеточные ответы. 30
Вирусные векторы также были модифицированы для экспрессии ТАА, таких как антиген простатоспецифического антигена (PSA) и антигена вируса папилломы человека (HPV). Также была разработана вакцина против поксвируса PDA, экспрессирующая как MUC-1, так и CEA в сочетании с GM-CSF, под названием PANVAC-V. В исследовании фазы I с участием пациентов с резистентным к позднему лечению ОАП сообщалось о средней общей выживаемости, равной 6.3 месяца. 49 Иммунологический анализ выявил MUC-1 или CEA-специфический Т-клеточный ответ у 62,5% пациентов и был связан со значительным преимуществом выживаемости по сравнению с пациентами, не ответившими на лечение (15,1 месяца по сравнению с 3,9 месяца, соответственно, p = 0,002). 49 Рандомизированное контролируемое клиническое исследование фазы III с участием 255 пациентов с метастатическим раком поджелудочной железы было проведено, в котором PANVAC-V сравнивали со стандартной терапией гемцитабином, и, к сожалению, вакцина не смогла продемонстрировать улучшение общей выживаемости. 50
Как обсуждалось выше, DC играют решающую роль в создании эффективного противоопухолевого иммунного ответа. Вакцины DC пытаются использовать эти характеристики, выделяя DC и загружая их ассоциированными с опухолью антигенами или мРНК опухоли во время культивирования, а затем повторно вводя их пациентам. 55 Терапия вакциной DC в основном изучалась при раке простаты, раке груди, меланоме и почечно-клеточном раке, где она в целом хорошо переносилась, но с невысокой клинической эффективностью. 17 Двенадцать пациентов с хирургически удаленным раком поджелудочной железы и желчных путей лечились вакциной DC, нагруженной MUC-1, в ходе ранней фазы клинических испытаний. Тридцать три процента этих пациентов были живы через четыре года после лечения, хотя иммунологический анализ не выявил повышенных антител против MUC1. 56 В отдельном клиническом исследовании вакцинация DC в сочетании со стандартным гемцитабином у пациентов с неоперабельным КПК, резистентных к стандартному лечению, не продемонстрировала статистически значимого преимущества в выживаемости. 57 Причина этой неудачи может быть связана с отсутствием иммуногенности целевого TAA, с комбинацией с гемцитабином, который может вызывать лимфопению и ослаблять способность иммунной системы реагировать, или с продвинутой стадией пациентов, получавших лечение. .
К сожалению, мы часто не можем определить, какой именно опухолевый антиген приведет к наиболее устойчивому иммунному ответу у каждого конкретного пациента. Идеальный антиген не будет подвержен ранее существовавшей толерантности, будет иметь решающее значение для злокачественного фенотипа опухоли и будет экспрессироваться исключительно опухолью. 17 Учитывая адаптивную способность опухоли и постоянно меняющийся геном, маловероятно, что один-единственный антиген будет соответствовать всем этим критериям.
Цельноклеточные вакцины
Цельноклеточные вакцины исключают необходимость спецификации антигена, поскольку они включают облученные цельные опухолевые клетки. Эти опухолевые клетки трансдуцируются генами GM-CSF и более эффективно запускают иммунную систему за счет усиления презентации антигена DC. Затем несколько опухолевых антигенов могут быть обработаны из облученных опухолевых клеток в присутствии этих активированных DC.
Первое клиническое применение цельноклеточных вакцин, трансдуцированных GM-CSF, было предпринято у пациентов с почечно-клеточной карциномой на поздней стадии. Вакцина хорошо переносилась во всех дозах с минимальными клиническими побочными эффектами. Реакции гиперчувствительности замедленного типа были отмечены у пациентов, получавших аутологичную вакцину GM-CSF, и коррелировали с их клиническим ответом. 58
Аутологичные цельноклеточные вакцины впоследствии были протестированы при меланоме, простате и немелкоклеточном раке легкого.К сожалению, обработка и разработка аутологичных вакцин возможна не для всех видов рака, включая КПК. Альтернативный подход — использование аллогенных цельноклеточных противоопухолевых вакцин. Потенциальный недостаток по сравнению с аутологичными вакцинами заключается в том, что пациентов больше не вакцинируют против их собственных специфических опухолевых антигенов. Однако данные свидетельствуют о том, что презентация антигена DC происходит от хозяина, и поэтому единственная роль вакцинной клетки заключается в презентации антигенов. 41 Кроме того, из опухолевых антигенов, которые мы идентифицировали при меланоме, более 50% являются общими для всех линий опухолевых клеток, что делает аллогенную вакцинацию разумным подходом. 41
Аллогенная вакцина против GM-CSF, называемая GVAX, была протестирована в различных клинических испытаниях на ранней стадии. По большей части он хорошо переносится с минимальными побочными эффектами. 59,60 Первое исследование GVAX поджелудочной железы I фазы было выполнено на 14 пациентах со 2 или 3 стадией хирургического удаления ОАП. Вакцину вводили тремя возрастающими дозами, первая — через 8 недель после хирургической резекции. Затем пациенты получали стандартную адъювантную химиолучевую терапию в течение 6 месяцев с последующими 3 дополнительными ежемесячными вакцинациями.Поствакцинальные реакции гиперчувствительности замедленного типа на аутологичные опухолевые клетки были отмечены у 3 из 14 пациентов, все трое из которых живы более чем через 12 лет после постановки диагноза. 61
Мезотелин считается опухолевым антигеном КПК, поскольку он активируется в большинстве опухолевых клеток поджелудочной железы. Иммунологический анализ фазы I исследования GVAX поджелудочной железы продемонстрировал индукцию Т-клеток CD8 + к множественным HLA-A2, A3 и A24-ограниченным эпитопам мезотелина у трех пациентов, испытывающих ответы на DTH. 28 Ни одна из опухолевых клеток, используемых в GVAX, не экспрессировала HLA-A2, A3 или A24, что дает первое четкое доказательство того, что опухолеспецифические Т-клетки CD8 + могут быть получены с помощью иммунотерапевтического подхода, предназначенного для набора APC. на место вакцинации. 28
Исследование фазы II GVAX было впоследствии проведено у 60 пациентов с хирургически удаленным ОАП. Опять же, пациенты получили свою первую вакцину через 8 недель после хирургической резекции с последующей стандартной химиолучевой терапией.Если к этому моменту пациенты не болели, им делали три дополнительных ежемесячных вакцины. В отличие от исследования фазы I, пациенты в этом исследовании фазы II получали дополнительную и последнюю пятую вакцину через 6 месяцев после четвертой вакцины. Средняя выживаемость без заболевания и общая выживаемость составляли 17,3 месяца (95% ДИ, 14,6–22,8) и 24,8 месяца (95% ДИ, 21,2–31,6) соответственно. 62 Вакцина хорошо переносилась с минимальными побочными эффектами. Более того, иммунологический анализ выявил мезотелин-специфические Т-клетки CD8 + , которые коррелировали с продолжительной выживаемостью без болезни. 62
Во втором клиническом испытании II фазы изучалась комбинация терапии GVAX с иммуномодулирующими дозами циклофосфамида (Cy). Это было также первое исследование, в котором терапия GVAX использовалась для лечения пациентов с метастатическим ОАП. Подходящими пациентами были пациенты с ОАП 4 стадии, которые не прошли терапию гемцитабином. Пятьдесят пациентов были разделены без рандомизации на две группы: 30 пациентов получали только GVAX и 20 пациентов получали внутривенно циклофосфамид за день до терапии GVAX.Средняя выживаемость составила 2,3 месяца в группе только GVAX по сравнению с 4,7 месяца в группе GVAX плюс Cy. 63 Хотя это и не является статистически значимым, присутствие мезотелин-специфических Т-клеток с более высокой авидностью демонстрирует сильную тенденцию к увеличению выживаемости без прогрессирования заболевания. 63 Комбинация Cy и GVAX хорошо переносилась с минимальными побочными эффектами. Авторы пришли к выводу, что вакцинация в сочетании с иммуномодулирующими дозами циклофосфамида является безопасным, выполнимым и приемлемым лечением для пациентов, у которых прогрессирование на схемах химиотерапии первой линии. 63
Наша группа в настоящее время проводит исследование фазы II, чтобы оценить, как долго после первичной вакцинации пациенты с КПК должны продолжать получать бустер-вакцинацию. Подходящие пациенты для этого исследования включают выживших без болезни из вышеупомянутых фаз I и II испытаний GVAX и пациентов, ранее не вакцинированных, которые получили четыре первичных ежемесячных вакцинации. Протокол бустерной вакцинации требует вакцинации каждые 6 месяцев, пока пациент не болеет.
Несмотря на обнадеживающие данные по безопасности и выживаемости, полученные в результате испытаний фазы I и II, толерантность к опухоли продолжает ограничивать вакцинацию.Исследования на животных показывают, что Cy не оказывает стойкого эффекта на истощение Treg, но повторное введение метрономного Cy может привести к стойкому ингибированию Treg. 64 В ходе текущего рандомизированного контролируемого клинического исследования сейчас тестируется GVAX в сочетании с Cy, включая метрономный Cy, у пациентов с резектабельным ОАП в неоадъювантной и адъювантной терапии. Подходящие пациенты рандомизированы в одну из трех групп: только GVAX, GVAX в сочетании с Cy, вводимым за день до каждой вакцинации, или GVAX в сочетании с повторяющимся введением Metronomic Cy.Первичные конечные точки включают оценку инфильтратов иммунных клеток, особенно Treg, эффекторных Т-клеток CD4 + и CD8 + в резецированных опухолях после неоадъювантной вакцинации, а также оценку изменений количества и функции периферических мезотелин-специфические CD8 + Т-клетки. Участники получают первую вакцинацию за две недели до резекции поджелудочной железы (процедура Уиппла) и вторую вакцинацию через 6-10 недель после хирургической резекции с последующей стандартной адъювантной химиолучевой терапией.Если пациенты остаются свободными от болезни через 1-2 месяца после стандартной адъювантной терапии, они получают вакцину один раз каждые 28 дней, всего шесть вакцинаций.
Введение вакцины в условиях неоадъювантной терапии впервые дало понимание способности опухоли уклоняться от иммунной системы и подавлять вакцинацию. Иммуногистохимическое окрашивание резецированных опухолей впервые выявило пери- и внутриопухолевые лимфоидные агрегаты. Более того, PD-1 и B7-h2-положительные иммунные клетки в большом количестве присутствуют в этих агрегатах, что позволяет предположить, что комбинация блокады PD-1 и B7-h2 может дополнительно усилить противоопухолевый эффект терапии GVAX (неопубликованные данные).
В последнее время вакцины HyperAcute, представляющие собой аллогенные цельноклеточные вакцины, состоящие из облученных раковых клеток, которые были генетически модифицированы для добавления остатков α (1,3) -галактозила (αGal) к их клеточной поверхности, были использованы на ранней стадии клинических исследований. испытания с многообещающими результатами. В клетках человека отсутствует ключевой фермент в общем пути эпитопа αGal. Хронический стимул кишечной флоры приводит к высокому уровню циркулирующих антител против αGal. 65 Опосредованное комплементом разрушение опухолевых клеток, меченных αGal, приводит к усилению противоопухолевого иммунного ответа, направленного на опухолевые антигены.Было проведено клиническое испытание фазы II вакцины HyperAcute-Pancreas у пациентов с ранее удаленным ОАП. Hardacre et al. Сообщили о 90% (18/20) общей выживаемости пациентов с периодом наблюдения примерно 1 год. 66 Медиана безрецидивной выживаемости (DFS) не была достигнута, но данные предполагали ожидаемое значительное увеличение медианы DFS по сравнению с историческим контролем. 66 Более того, они не сообщили о значительной токсичности 3 или 4 степени. 66 В настоящее время проводится III фаза клинических испытаний.
Иммуномодулирующие агенты и их комбинации для КПК в стадии разработки.
Иммунотерапия рака поджелудочной железы значительно выиграет от идентификации специфического опухолевого антигена КПК, но опухолевые клетки по-прежнему обладают способностью использовать иммунные контрольные точки, чтобы избежать обнаружения. CTLA-4 и PD-1 хорошо охарактеризованы как индуцирующие апоптоз и анергию Т-клеток при связывании со своими лигандами. Более того, PD-1 и B7-h2 высоко экспрессируются в перитуморальных лимфоидных агрегатах, наблюдаемых при терапии GVAX, что позволяет предположить, что эта иммунологическая контрольная точка используется для уклонения от противоопухолевого иммунного ответа.Терапия монотерапией анти-PD1 и анти-CTLA4 дала многообещающие результаты, но, скорее всего, индивидуальных схем лечения КПК недостаточно. Мезотелин-специфические ответы Т-клеток CD8 + усиливаются, когда GVAX вводят в сочетании с антителами против PD1 по сравнению с одним GVAX на мышиных моделях (неопубликованные данные). Более того, комбинация терапии GVAX и анти-PD1 продемонстрировала преимущество в выживаемости на доклинических моделях метастатического рака поджелудочной железы (неопубликованные данные).
Терапия моноклональными антителами против CTLA-4 привела к стойкой регрессии опухоли на моделях мышиной меланомы и в клинических испытаниях ранней фазы у пациентов с запущенной меланомой. 18,67-69 Несмотря на эти многообещающие результаты, терапия анти-CTLA-4 связана с почти 30% аутоиммунной токсичностью III / IV степени. 69 Эти побочные эффекты включают колит и энцефалит, но также положительно коррелируют с клиническим ответом. 69 В ранней фазе клинического исследования 27 пациентов с местнораспространенным или метастатическим раком поджелудочной железы одно лекарственное средство ипилимумаб, человеческое моноклональное антитело против CTLA-4, не дало ответа, но один субъект действительно испытал значительно отсроченный ответ. 70 Как обсуждалось выше, это было предсказано на доклинических моделях, которые подтверждают, что комбинации иммуномодуляторов с вакциной являются более эффективными, чем иммуномодуляторы с одним агентом, вводимые отдельно.
Комбинация вакцинотерапии и блокады иммунных контрольных точек в настоящее время проходит испытания на ранней стадии клинических испытаний. Ле и его коллеги провели исследование фазы Ib, в котором 30 субъектов с ранее леченным, местнораспространенным или метастатическим ОАП были рандомизированы в одну из двух групп: только ипилимумаб (IPI) или IPI в сочетании с GVAX.Медиана общей выживаемости составила 3,3 месяца при использовании только IPI по сравнению с 5,5 месяца при использовании IPI плюс GVAX (p = 0,12). Общая 12-месячная выживаемость составила 7% против 27% в группе IPI по сравнению с группой IPI плюс GVAX соответственно. 71 Профили побочных эффектов, связанных с иммунитетом, были схожими и были связаны с увеличением общей выживаемости в обеих группах. 71 Несмотря на недостаточную мощность, это исследование предполагает возможную роль комбинаторной иммунотерапии при запущенном PDA.
Противоопухолевый иммунный ответ определяется в микросреде опухоли.Именно здесь сложные взаимодействия между опухолевыми клетками и прилегающей сетью иммунных клеток определяют толерантность к опухоли или ее искоренение. Во многих отчетах документально подтверждено присутствие иммуносупрессивных клеток на ранних этапах развития опухоли, включая Treg, MDSC и TAM. 72 Это привело к обширным усилиям по модификации микросреды опухоли таким образом, чтобы ограничить ее иммуносупрессивные возможности.
Битти и его коллеги использовали агонистические антитела к CD40 в обеих доклинических моделях, чтобы продемонстрировать, что CD40-активированные макрофаги быстро проникают в опухоли, становятся опухолевидными и способствуют истощению стромы опухоли на мышиной модели рака поджелудочной железы. 73 Они также протестировали агонистические антитела к CD40 в комбинации с гемцитабином у пациентов, ранее не получавших химиотерапию и не подвергавшихся хирургическому лечению. Из 21 пациента, получившего антитело, у 4 был частичный ответ, у 4 было прогрессирующее заболевание и у 11 было стабильное заболевание. 73 Два пациента были исключены из анализа из-за нарушения мозгового кровообращения и невозможности получить изображения после лечения. 73 Средняя выживаемость без прогрессирования составила 5,6 месяцев, а медиана общей выживаемости — 7.4 месяца. 73 По сравнению с контрольной группой, получавшей стандартную терапию гемцитабином, терапия анти-CD40 показала многообещающую клиническую эффективность в этом раннем клиническом исследовании.
B7-h2, лиганд для иммунной Т-клетки, экспрессирующей иммунную контрольную точку PD-1, экспрессируется на DC, и его экспрессия активируется некоторыми опухолевыми клетками. 25 PD-1 экспрессируется ассоциированными с опухолью Т-клетками, включая Treg. Взаимодействие PD-1 / B7-h2 снижает продукцию IL-12 DC и ограничивает противоопухолевый иммунный ответ. 25 Моноклональные антитела, направленные на B7-h2 и PD-1 на мышиных моделях, привели к усилению опосредованного цитотоксическими Т-клетками опухолевого специфического иммунитета и в настоящее время исследуются в качестве монотерапевтических препаратов на ранней стадии клинических испытаний. 74 Его профиль побочных эффектов значительно ниже, чем у ипилимумаба. Было обнаружено, что терапия анти-PD-L1 у пациентов с резистентным к лечению немелкоклеточным раком легкого, меланомой и почечно-клеточным раком дает объективный ответ от 6 до 17%. 75 Было отмечено, что терапия Anti-PD1 дает 20-25% объективных ответов в аналогичной популяции пациентов. 76 Оба метода лечения были связаны с аутоиммунной токсичностью III / IV степени у 9–14% пациентов. 75,76
Помимо экспрессии PD-1, Treg обладают множеством механизмов, ограничивающих противоопухолевый иммунный ответ. 77 Было показано, что опухоли вызывают быстрое распространение Treg как в моделях опухолей человека, так и на мышах, что приводит к отсроченному отторжению иммуногенных опухолей. 78-80 Хотя они обычно присутствуют в небольших количествах, присутствие Treg повышено в микросреде опухоли. Они ингибируют CD4 + и CD8 + Т-клетки посредством прямого контакта клетки с клеткой и путем секреции иммунных медиаторов, таких как IL-10 и TGF-β. 17
Хираока и его коллеги проанализировали 198 образцов опухолей КПК вместе с 84 ассоциированными поражениями PanIN, сравнивая популяции опухолевых Т-клеток с неопухолевой тканью поджелудочной железы. Они сообщили о значительно более высоких популяциях Treg в опухолях КПК по сравнению с неопухолевым воспалением (p <0.0001). 81 Более того, более высокая распространенность Treg в образцах опухолей КПК была связана с худшим прогнозом независимо от других факторов выживания (p <0,0001). 81 Анти-Treg-терапия с использованием моноклональных антител, нацеленных на молекулы Treg, такие как глюкокортикоид-индуцированный фактор некроза опухоли и LAG-3, изучается на животных моделях. 82 Иммуномодулирующие дозы циклофосфамида подавляют популяции Treg и усиливают противоопухолевый иммунный ответ у пациентов с КПК при использовании в сочетании с терапией вакцинами. 83
Химиотерапия и иммунотерапия
Недавние сообщения продемонстрировали способность химиотерапии усиливать противоопухолевый иммунный ответ. Например, индуцированный доксорубицином апоптоз опухолевых клеток увеличивает презентацию антигена по сравнению с митомицином. 84 Кроме того, было показано, что доцетаксел и паклитаксел улучшают противоопухолевый иммунитет вакцины GM-CSF за счет своей способности увеличивать присутствие и активацию DC. 85,86 Более того, Plate и его коллеги продемонстрировали, что пациенты с КПК, проходящие терапию гемцитабином, имели снижение Т-клеток памяти и повышенную активацию Т-клеток de novo. 87
Изучение взаимосвязи между иммунотерапией и химиотерапией показывает, что время и доза химиотерапии могут привести к синергетической комбинации. Metronomic Cy является иммуномодулирующим средством, в отличие от Cy в высоких дозах, который истощает лимфоузлы и подавляет иммунитет. 88 Cy повышает противоопухолевый иммунитет за счет уменьшения количества и функции Treg. 89,90 Более того, метрономный Cy способствует трансформации Т-клеток CD4 + в лимфоциты Th2 и Th27, тем самым увеличивая популяцию эффекторных Т-клеток. 91 Доза и время Cy в связи с терапией вакциной для оптимальных иммуномодулирующих эффектов все еще исследуются. Эменс и его коллеги сообщили о клиническом испытании фазы I, в котором изучались диапазоны доз аллогенной Her-2-положительной GM-CSF-секретирующей опухолевой вакцины в сочетании с Cy и доксорубицином у пациентов с метастатическим раком молочной железы. Они пришли к выводу, что иммуномодулирующая активность низкой дозы Cy имеет узкое терапевтическое окно, не превышающее 200 мг / м 2 . 92
Будущее вакцинотерапии
Несмотря на обнадеживающие результаты, результаты клинических испытаний монотерапии иммунотерапией у пациентов с КПК были неутешительными и разочаровывающими.Большинство опухолей желудочно-кишечного тракта обладают иммунной толерантностью и поэтому требуют комбинаторного терапевтического подхода, который включает химиотерапию, лучевую терапию, хирургическое вмешательство и иммунотерапию. По мере того как выявляется все больше и больше опухолевых антигенов, будут разработаны более специфические и сильнодействующие вакцины. Идеальная вакцина будет нацелена на несколько антигенов, которые имеют решающее значение для роста и прогрессирования опухоли. Включение ингибиторов иммунологической блокады контрольных точек позволит повысить активацию Т-клеток и противоопухолевую активность.Модуляторы микроокружения опухоли позволят более эффективно активировать ДК, тем самым улучшая презентацию антигена. Оптимизация терапии вакциной КПК требует дополнительных исследований, чтобы понять, какие агенты наиболее важны для КПК (). Эта информация будет поступать из постоянного внимания к научно обоснованным клиническим испытаниям с доступом к тканям и из генно-инженерных моделей мышей, которые повторяют человеческое заболевание.
Вопросы о болезни Паркинсона и COVID-19
Ответы на ваши вопросы о болезни Паркинсона и коронавирусе 2019 (COVID-19) —
ОбновленоЛюди с болезнью Паркинсона (БП) задают много вопросов о COVID-19 с начала пандемии, и APDA предоставила вам необходимые ответы.
Кроме того, прочтите общую информацию APDA о COVID-19 для сообщества PD. Чтобы получить наиболее точную информацию о вирусе, обратите внимание на надежные веб-сайты, такие как Центры по контролю и профилактике заболеваний (CDC).
Ниже приведены некоторые из вопросов, которые я получил от нашего сообщества PD о COVID-19 через портал веб-сайта Ask A Doctor.
У нас также есть две отличные сессии вопросов и ответов с доктором Джоэлем Перлмуттером из APDA, которые могут быть вам интересны и полезны.Один касается вакцины против COVID-19 и PD, а другой посвящен тому, как решить проблемы, связанные с возвращением из карантина COVID.
В: Существуют ли какие-либо исследования долгосрочных эффектов COVID-19 и людей с БП?
A: В недавнем исследовании изучались симптомы пост-COVID у небольшого числа пациентов с болезнью Паркинсона. Среди симптомов, сохраняющихся после заражения COVID, — ухудшение двигательной функции, повышенная суточная доза леводопы, утомляемость, когнитивные нарушения и нарушения сна.Потребуются дополнительные исследования, чтобы подтвердить и расширить эти выводы.
В: Существуют ли какие-либо исследования воздействия вакцины COVID-19 на людей с БП?
A: В настоящее время нет данных о том, что вакцина COVID-19 оказывает долгосрочное негативное воздействие на кого-либо, в том числе на людей с БП. Некоторые люди с БП сообщают об ухудшении симптомов БП в краткосрочной перспективе после вакцинации, которые затем проходят. Центр по контролю за заболеваниями (CDC) учредил систему мониторинга безопасности вакцины под названием v-safe, которая фиксирует побочные эффекты вакцины.Если у вас есть побочные эффекты от вакцины и у вас есть болезнь Паркинсона, вы можете предупредить CDC, используя эту систему. Это станет бесценным инструментом для ученых, чтобы выявить тенденции в профилях побочных эффектов вакцин.
В: У меня болезнь Паркинсона. Должен ли я получить вакцину от COVID-19?
A: Для получения информации о вакцинах от COVID-19 — о том, как они работают, о безопасности и многом другом — посетите наш обновленный раздел информации о COVID-19. В целом, ваш возраст увеличивает риск осложнений от инфекции COVID-19.В зависимости от того, какие симптомы БП у вас есть, БП также может увеличить риск осложнений от вируса. По этим причинам было бы разумно максимально защитить себя от COVID-19, включая вакцинацию. Как всегда, поговорите со своим врачом о вашей индивидуальной клинической ситуации и узнайте, когда и где вы сможете получить вакцину.
Q: Как вариант Delta влияет на человека с PD?
A: У нас пока нет конкретных данных о том, как вариант Дельта влияет на людей с болезнью Паркинсона.
Вирус COVID-19, как и все вирусы, способен мутировать и создавать собственные варианты. Многие варианты COVID-19 были идентифицированы по всему миру. Однако лишь некоторые из этих вариантов вызывают озабоченность у населения, поскольку они обладают характеристикой, которая делает вирус более легким для передачи или с большей вероятностью может вызвать серьезное заболевание. Вариант Дельта в настоящее время вызывает беспокойство и, как было показано, легче передается от человека к человеку, чем предыдущие варианты COVID.
Вакцины, одобренные в США, действительно обеспечивают защиту от варианта Дельта, но не в той степени, которая наблюдалась в первоначальных испытаниях. Это означает, что полностью вакцинированные люди с большей вероятностью заразятся дельта-вариантом COVID-19, чем другими вариантами. Однако основная цель вакцин — предотвратить тяжелые заболевания, госпитализацию и смерть от COVID-19, и все одобренные вакцины примерно на 90% эффективны в предотвращении этих последствий инфекции.Поэтому вакцинация остается чрезвычайно ценной.
В: Я слышал, что некоторые люди получают третью прививку в качестве усилителя, чтобы защитить себя от варианта Дельта. Следует ли кому-нибудь с PD получить этот бустер?
A: CDC рекомендует ревакцинацию для всех, кто завершил свою первоначальную серию не менее 6 месяцев назад и в возрасте 65 лет и старше, живет в условиях длительного ухода, имеет сопутствующие заболевания или работает в условиях высокого риска.
Болезнь Паркинсона не входит в список основных заболеваний, но многие врачи, занимающиеся двигательными расстройствами, рекомендуют своим пациентам сделать третью вакцину.
В: Я слышал от некоторых моих друзей с БП, что амантадин не следует принимать при вакцинации от COVID-19. Это правда?
A: Хотя может случиться так, что вам не следует принимать вакцину против назального гриппа одновременно с приемом амантадина (потому что это может сделать вакцину менее эффективной), это , а не вакцина COVID. Не должно быть проблем с приемом амантадина во время вакцинации от COVID-19.
Вопрос: В какой группе я должен делать вакцину, с симптомами болезни Паркинсона или без?
A: Поскольку у вас, скорее всего, будут болезненные ощущения в вакцинированной руке в течение 1-2 дней, имеет смысл ввести вакцину в менее функциональную руку.
Q: Следует ли мне придерживаться обычного графика приема лекарств от болезни Паркинсона в день вакцинации от COVID-19?
A: Нет причин менять лекарства от PD в день вакцинации.
В: Какие побочные эффекты можно ожидать от вакцины COVID-19?
A: Несмотря на различные реакции, вакцины от COVID-19 одобрены FDA и считаются безопасными. Некоторые люди могут просто почувствовать легкую боль в руке, и все (как при любой другой инъекции).Некоторые могут иметь более заметную реакцию и чувствовать озноб, ломоту в теле, головную боль и / или усталость в течение 1-2 дней, но обычно они быстро проходят. Также были некоторые анекдотические сообщения (не опубликованные) о временном ухудшении симптомов болезни Паркинсона после вакцинации против COVID-19.
Взвешивая риски заражения COVID-19 у кого-то с БП, а также значительные недостатки всех связанных с пандемией ограничений социальной и физической активности для людей с БП по сравнению с возможностью побочных эффектов от вакцины, я бы предпочел вакцина.Как всегда, обсудите все свои медицинские проблемы со своим неврологом и терапевтом.
В: Я получил вакцину от COVID-19 два дня назад, и у меня усиливается тремор. Как вы думаете, это связано с вакциной?
A: Вакцина, безусловно, способна вызывать краткосрочные побочные эффекты в виде усталости, болей и даже лихорадки. Пока нет обширных данных о том, как это влияет на симптомы болезни Паркинсона, только анекдотические данные. У некоторых людей симптомы БП ухудшаются в краткосрочной перспективе. Это не означает, что ваш PD прогрессировал, и я ожидаю, что вы вернетесь к своему предыдущему исходному уровню в следующие несколько дней.Я бы поговорил с вашим неврологом и о вашем усилении тремора.
В: Может ли вакцина COVID-19 отрицательно повлиять на кого-то с БП и деменцией?
A: Общие побочные эффекты вакцины COVID-19, как правило, включают боль в руке, усталость, головную боль и тому подобное в течение 1-2 дней. Если у кого-то есть деменция, он может действовать или реагировать по-другому, потому что может плохо себя чувствовать. Однако это не означает ухудшение основного неврологического состояния человека. Побочные эффекты должны исчезнуть, и человек должен вернуться к исходному уровню через 1-2 дня.
В: Есть ли причины, по которым человеку с БП не следует делать вакцину от COVID-19?
A: Нет никаких обоснованных научных опасений, позволяющих предположить, что вакцины имеют другой профиль безопасности для людей с БП по сравнению с населением в целом, поэтому то, что мы знаем о вакцинах для всех желающих, будет верным для людей с БП. Наличие БП может привести к более сложной инфекции, если вы заразитесь COVID-19, к тому же люди с БП также имеют тенденцию быть старше, что еще больше увеличивает риск осложненной инфекции COVID-19.Из-за этих проблем вакцинация от COVID-19 для людей с БП — хорошая идея. Обсудите со своим врачом любые опасения по поводу вакцины COVID-19.
В. Могу ли я вернуться к тому, что делал до пандемии, после вакцинации? Появление варианта «Дельта» что-нибудь меняет?
A: CDC постоянно обновляет свои руководящие принципы в ответ на меняющиеся условия общественного здравоохранения.
- Полностью вакцинированные люди могут участвовать во многих мероприятиях, которые они выполняли до пандемии; для некоторых из этих занятий они могут носить маску.
- Чтобы снизить риск заражения вариантом Delta и потенциального распространения его среди других, каждый, включая полностью вакцинированных, должен носить маску в общественных помещениях, если они находятся в зоне значительного или высокого уровня передачи. CDC постоянно обновляет карту округов США, к которым это относится. Вам нужно будет обратиться в местные органы здравоохранения, чтобы определить, относится ли ваш район к региону со значительным или высоким уровнем передачи .
- Полностью вакцинированные люди могут выбрать маскировку независимо от уровня передачи в их районе, особенно если они или кто-либо в их семье имеет ослабленный иммунитет или находится в группе повышенного риска тяжелого заболевания, или если кто-то в их семье не вакцинирован.К людям, подверженным повышенному риску тяжелого заболевания, относятся пожилые люди и люди с определенными заболеваниями, такими как диабет, избыточный вес или ожирение, а также сердечные заболевания.
В: Может ли стресс, связанный с COVID-19, усугубить симптомы Паркинсона?
A: Стресс определенно может усилить симптомы болезни Паркинсона. Раньше я обсуждал взаимосвязь между стрессом, тревогой и БП в целом, и COVID-19, безусловно, создал очень стрессовую среду для всех.Может возникнуть стресс, связанный с заражением вирусом, а также беспокойство и беспокойство по поводу возвращения к деятельности, предшествующей пандемии, теперь, когда жизнь начинает возвращаться к «нормальной». Стресс гораздо острее ощущается пожилыми людьми и людьми с хроническими заболеваниями, членами населения, которые имеют повышенный риск осложнений от инфекции COVID-19. Многие люди с БП испытывают тревогу как немоторную особенность БП, и многие сообщают, что тревога усилилась с начала пандемии.Чтобы свести к минимуму стресс и нормализовать текущую ситуацию, обязательно установите распорядок дня, продолжайте заниматься спортом (дома, если вам так удобнее) и оставайтесь на связи с семьей и друзьями лично, если вы готовы, или онлайн или в сети. телефон. Будьте терпеливы по отношению к себе и другим.
В. У моего мужа БП с умеренными симптомами. Обычно он независим во всех своих действиях, хотя ходит медленно. Однажды его симптомы резко ухудшились, и он не мог ходить.Я отвел его в реанимацию, где у него положительный результат на COVID-19. Его выздоровление было очень медленным, и сейчас он проходит реабилитацию. Это нормально? Он поправится?
A: Как правило, у людей с БП и другими заболеваниями головного мозга часто наблюдается 1) ухудшение симптомов БП перед лицом таких заболеваний, как COVID-19, и 2) более медленное восстановление до исходного уровня после выздоровления. от межтоковой болезни. Похоже, и то, и другое случилось с вашим мужем. Однако при надлежащей реабилитации и некоторой настойчивости есть надежда, что он постепенно вернется к своему исходному состоянию.
В: Что произойдет, если я закашляюсь от COVID-19? Я знаю, что есть определенные лекарства от кашля, которые нельзя принимать людям с болезнью Паркинсона.
A: Вы правы в том, что важно обращать внимание на возможные взаимодействия лекарств. Следует избегать приема лекарств от кашля и простуды, содержащих декстрометорфан, псевдоэфедрин, фенилэфрин и эфедрин, только если вы принимаете ингибитор моноаминоксидазы (ИМАО), такой как разагилин, селегилин или сафинамид. Обязательно проверьте ингредиенты продукта перед покупкой, и если вы не уверены, попросите своего врача или фармацевта уточнить, каких брендов / лекарств следует избегать.Если вы принимаете ИМАО, вам можно принимать любые другие лекарства от простуды без этих ингредиентов. Если вы не принимаете ИМАО, вам подойдет любое лекарство от простуды.
Вот список лекарств, которых следует избегать при БП.
В: Я принимаю амантадин для лечения болезни Паркинсона. Я знаю, что это еще и лекарство от гриппа. Это работает при COVID-19?
A: У нас нет доказательств того, что амантадин действует против COVID-19, поэтому вы должны продолжать предполагать, что он не эффективен против этого коронавируса.
Советы и выводы
- Большинство людей, инфицированных COVID-19, полностью выздоравливают. Однако пожилые люди и люди с сопутствующими медицинскими проблемами, такими как прогрессирующая БП, подвергаются повышенному риску развития серьезных исходов от COVID-19 по сравнению с теми, кто моложе и здоровее.
- Три вакцины против COVID-19 одобрены в США.
- Вакцинация снижает ваши шансы заразиться COVID-19, но те, кто прошел вакцинацию, все еще могут заразиться COVID-19.
- Вакцинация примерно на 90% эффективна в защите от тяжелых заболеваний, госпитализации и смерти даже для нового варианта Delta
- Продолжайте следить за рекомендациями CDC для получения информации о COVID-19.
- Поговорите со своим врачом о любых проблемах, которые у вас возникают в связи с вакцинами от COVID-19 или COVID-19.
У вас есть вопрос или проблема, которые вы бы хотели изучить д-ру Гилберту? Предложить тему
Д-р Ребекка Гилберт
Вице-президент и главный научный сотрудник APDA
Д-р.Гилберт получила степень доктора медицины в Медицинском колледже Вейля Корнельского университета в Нью-Йорке и степень доктора философии в области клеточной биологии и генетики в Высшей школе медицинских наук Вейля. Затем она прошла обучение в неврологической ординатуре, а также в стипендиальной программе по борьбе с двигательными расстройствами в Колумбийском пресвитерианском медицинском центре. До прихода в APDA она была адъюнкт-профессором неврологии в Медицинском центре Лангоне Нью-Йоркского университета. В этой роли она наблюдала за пациентами с двигательными расстройствами, инициировала и руководила Сообществом NYU Movement Disorders Fellowship, участвовала в клинических испытаниях и других исследовательских инициативах по болезни Паркинсона и широко читала лекции об этом заболевании.
Просмотреть все сообщения доктора Ребекки Гилберт
Подробная статья Опубликовано в COVID-19 и PD, Факторы риска болезни ПаркинсонаОТКАЗ ОТ ОТВЕТСТВЕННОСТИ: Любая медицинская информация, распространяемая через этот блог, предназначена исключительно для целей предоставления информации аудитории и является не предназначено как медицинский совет. Наши специалисты в области здравоохранения не могут порекомендовать лечение или поставить диагноз, но могут ответить на общие вопросы. Мы рекомендуем вам задавать любые конкретные вопросы вашим личным поставщикам медицинских услуг.
F.D.A. Группа экспертов дала зеленый свет вакцине Pfizer против Covid
Вакцина Pfizer против Covid-19 в четверг прошла критический рубеж, когда группа экспертов официально рекомендовала Управлению по санитарному надзору за качеством пищевых продуктов и медикаментов разрешить вакцину. Агентство, скорее всего, сделает это в течение нескольких дней, предоставив медицинским работникам и жильцам домов престарелых первоочередное внимание, чтобы начать получать первые прививки в начале следующей недели.
Консультативная группа FDA по вакцинам, состоящая из независимых научных экспертов, врачей-инфекционистов и статистиков, проголосовала 17 голосами против 4, при этом один член воздержался, за экстренное разрешение для людей от 16 лет и старше.За редкими исключениями, F.D.A. следует советам своих консультативных комиссий.
Получив это официальное благословение, страна может наконец начать замедлять распространение вируса сразу после резкого роста числа инфекций и смертей, достигнув рекордного показателя в 3000 смертей в день в среду. F.D.A. Ожидается, что разрешение на использование в экстренных случаях будет выдано в субботу, по словам людей, знакомых с планированием агентства, хотя они предупредили, что в последнюю минуту юридические или бюрократические требования могут перенести объявление на воскресенье или позже.
По словам федеральных чиновников, первоначальная партия из 6,4 миллиона доз покинет склады в течение 24 часов после получения разрешения от FDA. Около половины этих доз будет отправлено по всей стране, а другая половина будет зарезервирована для первоначальных реципиентов, которые получат вторую дозу примерно через три недели.
Прибытие первых вакцин — это начало сложного, рассчитанного на несколько месяцев плана распределения, координируемого федеральными и местными органами здравоохранения, а также крупными больницами и аптечными сетями, который в случае успеха поможет вернуть скорбящую и экономически депрессивную страну обратно в какое-то подобие нормального, может, к лету.
«Ввиду высокой эффективности и хорошего профиля безопасности нашей вакцины и фактического выхода пандемии из-под контроля внедрение вакцины является неотложной необходимостью», — сказала Катрин Янсен, старший вице-президент и руководитель отдела исследований и разработок вакцин в Pfizer, сказал на встрече.
Голосование ограничивает бурный год для Pfizer и ее немецкого партнера BioNTech, которые начали работу над вакциной 11 месяцев назад, побив все рекорды скорости разработки вакцины, которая обычно занимает годы.Это также триумф для FDA, которое сохранило свою репутацию мирового золотого стандарта для обзоров лекарств, несмотря на месяцы политического давления со стороны президента Трампа, который стремился связать свое политическое состояние с успехом вакцины. Вакцина Pfizer уже была введена людям в Бахрейне и Великобритании, где она была разрешена 2 декабря. Канада одобрила ее в среду.
Ожидается, что за разрешением США на вакцину Pfizer вскоре последует вакцина для версии Moderna, которая использует аналогичную технологию и также показала многообещающие результаты в клинических испытаниях.Операция Warp Speed, многомиллиардная программа администрации Трампа по ускорению разработки вакцины, сделала предварительный заказ на 100 миллионов доз вакцины Pfizer в июле и активно поддержала разработку и производство вакцины Moderna.
Более 100 F.D.A. сотрудники работали почти круглосуточно, рассматривая заявку Pfizer, поданную 20 ноября, сжимая месяцы анализа в недели, изучая тысячи страниц данных клинических испытаний и производства.
Ранее на этой неделе профессиональные ученые из F.D.A. опубликовали анализ, показывающий, что вакцина работала в различных демографических группах и что она была в некоторой степени эффективной даже после первой из двух доз.
Во время однодневного заседания в четверг члены комиссии засыпали экспертов компаний и агентств подробными вопросами о безопасности и эффективности вакцины, эффективность которой в клинических испытаниях на поздней стадии составила 95 процентов. Некоторые члены выразили обеспокоенность тем, что не было достаточно данных о 16-17-летних, чтобы знать, поможет ли им вакцина, но комитет решил, что польза для этой группы перевешивает риски.
Некоторые члены спрашивали о вероятности серьезных аллергических реакций, учитывая новости о том, что регуляторы Великобритании на этой неделе рекомендовали людям с анафилактическими аллергическими реакциями на лекарства и продукты в анамнезе не получать вакцину, пока они исследуют два случая аллергических реакций среди здоровья. работники по уходу. Представители Pfizer заявили, что в испытании с участием 44 000 участников не было случаев серьезных аллергических реакций. Люди, у которых в анамнезе были аллергические реакции на вакцины, были исключены из исследования.
Один из членов комиссии, доктор Пол Оффит из Детской больницы Филадельфии, сказал, что он опасается, что заявления британских регулирующих органов, а также замечания Монсефа Слауи, высокопоставленного чиновника по вакцинам США, могут привести к появлению «десятков миллионов» людей. с тяжелой аллергией отказаться от вакцины, хотя доказательства связи с прививками были неясны. Он попросил Pfizer провести отдельное исследование людей с тяжелой аллергией в анамнезе, потому что «эта проблема не исчезнет, пока мы не получим более точные данные.”
The F.D.A. сказал, что попросил Pfizer включить аллергические реакции в свой план отслеживания безопасности и включить предупреждение в свои инструкции по использованию вакцины.
Одним из наиболее спорных вопросов было то, как широкое разрешение на вакцину может повлиять на продолжающееся клиническое испытание. Некоторые эксперты утверждали, что с этической точки зрения добровольцам испытаний, получившим плацебо, следует предложить вакцину, как только это будет разрешено, но другие опасались, что этот шаг может испортить долгосрочные результаты испытания.
Во время публичной части встречи защитники прав потребителей и общественного здравоохранения в значительной степени подтолкнули агентство к разрешению вакцины, отметив безотлагательность пандемии. Один оратор, назвавшийся Кермитом Кубицем, отметил, что у него не было конфликта интересов, о котором можно было бы заявлять, за исключением «большого количества пожилых родственников».
«Им нужна эта вакцина вчера, — сказал он.
Но правозащитники также попросили регулирующие органы быть прозрачными в отношении потенциальных проблем безопасности и внимательно следить за вакциной, как только она станет доступной.Некоторые заявили, что такие меры были необходимы, чтобы успокоить население, которое не решается принимать новую вакцину, особенно чернокожих и коренных американцев, которые исторически подвергались жестокому обращению со стороны медицинского сообщества. «Перед выдачей разрешения затронутые сообщества должны быть уверены в том, что вакцина безопасна и эффективна», — сказала Сара Кристоферсон из Национальной сети здоровья женщин.
Настаивая на голосовании консультативного комитета по любой вакцине, регулирующие органы создали защиту от давления Белого дома с целью одобрить продукт перед президентскими выборами.Когда участники группы встретились в октябре, чтобы обсудить рекомендации FDA по утверждению вакцин против Covid-19, они призвали агентство не торопиться и предупредили, что поспешность процесса может привести к упущению жизненно важных данных по безопасности и дальнейшему подрыву общественного доверия.
Сцена, разыгравшаяся в четверг, в которой внешние эксперты часами вовлекали правительственных чиновников в интенсивную, но зачастую технически сложную дискуссию о науке о вакцинах, не всегда вызывала интерес. Но обстоятельства были определенно драматичными, поскольку экспертов просили тщательно взвесить риски и преимущества вакцины, даже когда Соединенные Штаты достигли мрачной вехи, зарегистрировав более 3000 смертей от коронавируса в среду, и поскольку тысячи людей в Британии уже умерли от коронавируса. уже получил.
The F.D.A. изо всех сил пытается как внутри, так и за пределами страны, быстро продвигать свои обсуждения вакцины и лечения, чтобы обуздать распространение смертельного вируса, но не так быстро, чтобы подорвать доверие общественности. Это была тонкая грань, которую нужно было пройти, и ей не помог поток тревожных обвинений г-на Трампа и его советников в том, что агентство действует слишком медленно.
За несколько дней до того, как Pfizer подал заявку, компания отправила огромный транш производственных данных в F.Д.А. — включая материалы о том, как увеличивалось производство, — заставляя регулирующие органы изо всех сил пытаться оценить это вовремя для возможного разрешения.
В рамках надзора F.D.A. группы также провели проверку производственных мощностей компании и участков клинических испытаний, где они подтвердили, что записи соответствуют счетам, которые Pfizer предоставил федеральным регулирующим органам.
В то же время регулирующие органы оценивали не менее сложную заявку на разрешение в чрезвычайных ситуациях, поданную Moderna, данные которой будут публично изучены во время еще одного F.Д.А. внешнее консультативное совещание на следующей неделе.
Что нужно знать о бустерных прививках от Covid-19
Кто имеет право на бустерные прививки?The F.D.A. разрешила делать бустерные прививки миллионам получателей вакцин Pfizer-BioNTech, Moderna и Johnson & Johnson. К получателям Pfizer и Moderna, имеющим право на ревакцинацию, относятся люди в возрасте 65 лет и старше, а также молодые люди с высоким риском тяжелого заболевания Covid-19 из-за состояния здоровья или места работы. Соответствующие критериям получатели Pfizer и Moderna могут получить ревакцинацию как минимум через шесть месяцев после приема второй дозы.Все получатели Johnson & Johnson будут иметь право на вторую прививку как минимум через два месяца после первой.
Могу ли я поменять вакцину против Covid на бустерную?Да. F.D.A. обновил свои разрешения, чтобы позволить поставщикам медицинских услуг стимулировать людей вакциной, отличной от той, которую они изначально получили, — стратегия, известная как «смешивание и сопоставление». Независимо от того, получали ли вы вакцину Moderna, Johnson & Johnson или Pfizer-BioNTech, вы можете получить ревакцинацию любой другой вакцины. Регулирующие органы не рекомендовали какую-либо одну вакцину вместо другой в качестве бустерной.Они также умалчивают о том, предпочтительно ли придерживаться той же вакцины, когда это возможно.
Какие основные медицинские состояния подходят для ревакцинации?The C.D.C. сказал, что условия, при которых человеку может быть сделана ревакцинация, включают: гипертонию и сердечные заболевания; диабет или ожирение; рак или заболевания крови; ослабленная иммунная система; хронические заболевания легких, почек или печени; слабоумие и определенные нарушения. Беременные женщины, а также нынешние и бывшие курильщики также имеют право на получение помощи.
Какие профессии имеют право на бустеры?The F.D.A. разрешенные вспомогательные средства для рабочих, чья работа подвергает их высокому риску контакта с потенциально заразными людьми. C.D.C. говорит, что в эту группу входят: работники скорой медицинской помощи; работники образования; работники пищевой промышленности и сельского хозяйства; рабочие на производстве; исправительные работники; Работники почтовой службы США; работники общественного транспорта; Работники продуктового магазина.
Могу ли я сделать прививку от гриппа одновременно с вакциной против Covid или ревакцинацией?Да.C.D.C. говорит, что вакцину Covid можно вводить без учета сроков введения других вакцин, и многие аптеки позволяют людям назначать прививку от гриппа одновременно с бустерной дозой.
Регуляторы иногда получали документы от компаний до полуночи и работали в течение праздника Благодарения. Доктор Питер Маркс, главный регулятор вакцин в FDA, пошутил на прошлой неделе на мероприятии, организованном Американской медицинской ассоциацией, что его команда ела бутерброды с индейкой, изучая документы.
«Среди всех глобальных регулирующих органов именно мы на самом деле не просто изучаем таблицы компаний. Мы на самом деле садимся и пачкаемся, и мы смотрим на фактические отчеты о побочных эффектах, неправильные орфографические ошибки, которые иногда допускают врачи, и так далее », — сказал он на мероприятии.
Д-р Стивен М. Хан, Управление по контролю за качеством пищевых продуктов и медикаментов. комиссар, держался на осторожном расстоянии от обзора, по словам людей, знакомых с ним.
Доктор Хан уступил давлению ранее летом, чтобы разрешить старое лекарство от малярии, гидроксихлорохин, для использования у пациентов с Covid, хотя было мало доказательств того, что это работало.Это решение было отменено после того, как агентство обнаружило, что препарат вряд ли будет эффективен у пациентов с Covid и несет в себе риск потенциально опасных побочных эффектов. И доктор Хан столкнулся с резкой критикой со стороны научного сообщества после того, как преувеличил преимущества другого лечения, плазмы выздоравливающих, и эту ошибку он позже исправил.
Г-н Трамп обвинил чиновников агентства в том, что они являются частью «глубинного государства», и намекнул, что вакцина может появиться до «очень особенного дня» — дня выборов.Репутация FDA, похоже, развивалась в том же направлении, что и Центры по контролю и профилактике заболеваний, которые широко критиковались за то, что они не противостояли президенту.
Но старшие регулирующие органы — и в конечном итоге сам доктор Хан — отступили. Высокопоставленные должностные лица агентства опубликовали в USA Today статью, в которой признали, что честность FDA была поставлена под сомнение, и настаивали на том, что они будут «следить за наукой» во время пандемии. Агентство одержало победу в битве с Белым домом за введение более строгих правил для компаний, разрабатывающих вакцины против Covid.
«В такой среде, где было так много давления и беспокойства, процесс действительно обеспечивает важную сдержку и баланс», — сказал д-р Джесси Л. Гудман, который ранее был главным научным сотрудником FDA. Проведение открытого собрания также позволяет общественности «быть уверенным, что более широкое научное и клиническое сообщество удовлетворено этим решением».
Во вторник президент провел саммит, целью которого было продемонстрировать роль администрации в разработке вакцины.«Мы всего в нескольких днях от получения разрешения от F.D.A. и мы сильно их подталкиваем », — сказал Трамп на мероприятии.
Многие медицинские работники по всей стране уже рвутся за вакцину. Доктор Эндрю Баррос, врач интенсивной терапии из Шарлоттсвилля, штат Вирджиния, должен сделать прививку от Pfizer в 14:30. 15 декабря он сказал, что «с нетерпением ждет боли в руке и, надеюсь, станет на шаг ближе к тому, чтобы взять под контроль Covid».
Клинические испытания Pfizer будут продолжены даже после того, как вакцина будет одобрена F.D.A., а также компания и F.D.A. будет продолжать следить за безопасностью.
Pfizer заявила в четверг, что планирует подать заявку на полное одобрение в апреле 2021 года, после того как компания соберет данные о безопасности за шесть месяцев. После этого Pfizer получит право продавать вакцину напрямую больницам и другим поставщикам медицинских услуг.
Карл Циммер и Кэтрин Дж. Ву предоставили репортажи.
Нестабильность вакцины в холодовой цепи: механизмы, анализ и стратегии разработки
https: // doi.org / 10.1016 / j.biologicals.2014.05.007Право на получение и содержаниеРеферат
Нестабильность вакцин часто становится ключевой проблемой во время клинической разработки (от лаборатории до клиники), а также при коммерческом распространении (от фабрики к пациенту). Чтобы получить стабильные, эффективные лекарственные формы вакцины для использования человеком, успешные стратегии составления должны учитывать сочетание взаимосвязанных вопросов, включая стабилизацию антигенов, выбор подходящих адъювантов и разработку аналитических методов, указывающих на стабильность.Этот обзор охватывает ключевые концепции для понимания причин и механизмов нестабильности вакцины, включая (1) сложную и деликатную природу структур антигенов (например, вирусов, белков, углеводов, конъюгатов белок-углевод и т. Д.), (2) использование адъювантов. для дальнейшего усиления иммунных ответов, (3) разработка физико-химических и биологических анализов для оценки целостности и эффективности вакцины и (4) стратегии стабилизации для защиты вакцинных антигенов и адъювантов (и их взаимодействия) во время хранения.Несмотря на эти проблемы, вакцины обычно могут быть достаточно стабилизированы для использования в качестве лекарств за счет комбинации подходов к составлению в сочетании с поддержанием эффективной холодовой цепи (производство, распространение, хранение и введение). Описано несколько иллюстративных тематических исследований, касающихся механизмов нестабильности вакцины, а также подходов к составлению рецептур для стабилизации в холодовой цепи вакцины. К ним относятся живые, аттенуированные (корь, полиомиелит) и инактивированные (грипп, полиомиелит) вирусные вакцины, а также рекомбинантные белковые (гепатит B) вакцины.
Ключевые слова
Холодовая цепь
Вакцина
Стабильность
Состав
Лиофилизация
Адъювант
Рекомендуемые статьи Цитирующие статьи (0)
Copyright © 2014 Авторы. Опубликовано Elsevier Ltd.
Рекомендуемые статьи
Цитирующие статьи
Коронавирус (COVID-19) Обновление: 30 июля 2021 г.
- Для немедленного выпуска:
The U.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США объявило о следующих действиях, предпринимаемых в рамках продолжающихся усилий по борьбе с пандемией COVID-19:
- Сегодня FDA пересмотрело Разрешение на использование в чрезвычайных ситуациях (EUA) для REGEN-COV (казиривимаб и имдевимаб, вводимые вместе), чтобы добавить разрешение на использование REGEN-COV в экстренных случаях в качестве постконтактной профилактики (профилактики) COVID-19 в взрослые и дети (от 12 лет и старше с массой тела не менее 40 килограммов) с высоким риском прогрессирования COVID-19 в тяжелую форму, включая госпитализацию или смерть.REGEN-COV не разрешен для предконтактной профилактики для предотвращения COVID-19 до контакта с вирусом SARS-CoV-2 — только после контакта с вирусом. REGEN-COV следует использовать только в качестве постконтактной профилактики для определенных групп пациентов. Профилактика с помощью REGEN-COV не заменяет вакцинацию против COVID-19. FDA разрешило три вакцины для предотвращения COVID-19 и серьезных клинических исходов, вызванных COVID-19, включая госпитализацию и смерть. FDA призывает вас пройти вакцинацию, если вы имеете на это право.Узнайте больше об усилиях FDA по вакцинации против COVID-19.
- В среду, 28 июля, FDA пересмотрело EUA для барицитиниба (продается под торговой маркой Olumiant), разрешив теперь использовать только барицитиниб для лечения COVID-19 у госпитализированных взрослых и педиатрических пациентов в возрасте двух лет и старше, нуждающихся в дополнительном кислороде. -инвазивная или инвазивная механическая вентиляция легких или экстракорпоральная мембранная оксигенация (ЭКМО). Согласно пересмотренной версии EUA, барицитиниб больше не требуется вводить с ремдесивиром (Veklury).Барицитиниб не одобрен FDA для лечения COVID-19.
- В среду FDA разрешило продлить срок хранения охлажденной вакцины от COVID-19 Janssen (Johnson & Johnson), что позволило хранить продукт при 2-8 градусах Цельсия в течение шести месяцев. Это продление с четырех с половиной месяцев до шести месяцев было предоставлено после тщательного анализа данных, представленных Janssen, и распространяется на все охлажденные флаконы вакцины Janssen COVID-19, которые хранились в соответствии с условиями хранения производителя.Письмо-согласование можно прочитать здесь.
Срок годности вакцин, разрешенных согласно EUA, может быть продлен на основании данных, предоставленных производителями, и в соответствии с разрешением FDA. Поставщики медицинских услуг, применяющие вакцину, должны проверять веб-сайт компании www.vaxcheck.jnj, чтобы узнать самые свежие даты истечения срока годности конкретных партий вакцины Janssen COVID-19.
- В рамках усилий FDA по защите потребителей агентство выпустило письмо с предупреждением оператору сайта www.rxmedkart.com за продажу неутвержденных лекарств от множества заболеваний, включая COVID-19. Лекарства, не соответствующие нормативным требованиям, могут быть зараженными, поддельными, содержать различные количества активных ингредиентов или вообще содержать разные ингредиенты. Потребители могут посетить BeSafeRx, чтобы узнать, как безопасно покупать лекарства в Интернете. Потребители, обеспокоенные COVID-19, должны проконсультироваться со своим врачом.
- На этой неделе FDA добавило три новых часто задаваемых вопроса (FAQ) о вакцинах от COVID-19 и процессе утверждения.Здесь можно найти ответы на часто задаваемые вопросы, а также вопросы:
- Отличается ли разрешение (или утверждение лицензии на биологические препараты) от разрешения на использование в чрезвычайных ситуациях? Изменит ли это доступность вакцин против COVID-19?
- Сколько времени потребуется для утверждения вакцин против COVID-19?
- Насколько важно обеспечить наличие одобренных вакцин по сравнению с другими мерами общественного здравоохранения? У вас есть ресурсы, чтобы сделать это быстро?
- Тестирование обновлений:
- На сегодняшний день, 396 тестов и устройств для сбора образцов одобрены FDA в соответствии с разрешениями на использование в чрезвычайных ситуациях (EUA).К ним относятся 279 молекулярных тестов и устройств для сбора образцов, 86 тестов на антитела и другие тесты иммунного ответа и 31 тест на антигены. Существует 53 разрешения на использование молекул и одно разрешение на антитела, которые можно использовать с образцами, собранными в домашних условиях. Существует один молекулярный тест по рецепту на дому, три теста по рецепту на антиген на дому, пять тестов на антиген без рецепта на дому и два молекулярных теста без рецепта на дому.
- FDA разрешило 12 тестов на антигены и восемь молекулярных тестов для серийных программ скрининга.FDA также санкционировало 593 изменения разрешений EUA.
Связанная информация
###
Заготовка
FDA, агентство в составе Министерства здравоохранения и социальных служб США, защищает здоровье населения, обеспечивая безопасность, эффективность и безопасность лекарственных и ветеринарных препаратов, вакцин и других биологических продуктов для использования людьми, а также медицинских устройств. Агентство также отвечает за безопасность и сохранность продуктов питания, косметики, пищевых добавок, продуктов, излучающих электронное излучение, а также за регулирование табачных изделий.
Текущее содержание с:
Регулируемые продукты
Тема (и) здравоохранения
Наше исследование вакцины против COVID-19 — что дальше?
Компания Pfizer подала запрос в EUA на вакцину против COVID-19. Что дальше?
Pfizer и BioNTech объявили, что они отправили запрос в U.Управление по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) для получения разрешения на использование в чрезвычайных ситуациях (EUA) своего кандидата на вакцину COVID-19. Если это будет разрешено FDA, то экспериментальная вакцина может быть использована в группах высокого риска в США к концу декабря 2020 года. На нашем пути к тому, чтобы сделать потенциальную вакцину общедоступной, мы хотим быть уверены, что общественность будет в курсе последних событий. наш прогресс и следующие шаги в нашем процессе разработки.
Теперь, когда Pfizer и BioNTech подали заявление о вступлении в силу, что будет дальше?
Теперь, когда мы подали заявку на участие в EUA, ученые FDA проанализируют собранные на сегодняшний день данные о нашей вакцине-кандидате от COVID-19.Согласно указаниям FDA, это свидетельство также будет рассмотрено внешней комиссией независимых экспертов, известной как Консультативный комитет по вакцинам и родственным биологическим продуктам (VRBPAC). Будет открыта встреча, на которой Pfizer и BioNTech представят VRBPAC данные о безопасности и эффективности, которые были переданы в FDA, и ответят на вопросы членов комитета. Мы ожидаем, что эта встреча будет намечена на декабрь.
Какие данные Pfizer и BioNTech представят VRBPAC?
Мы представляем все данные, включенные в нашу заявку EUA.Сюда входят данные об эффективности из 170 подтвержденных случаев COVID-19, набранных в нашем исследовании фазы 3, и данные о безопасности, полученные из рандомизированной подгруппы, по крайней мере, из 8000 участников 18 лет и старше. У нас также есть данные о примерно 19 000 участников испытаний, за которыми наблюдали в среднем в течение двух месяцев после введения второй и последней дозы вакцины-кандидата, а также данные о наших производственных процессах.
Какова роль VRBPAC в утверждении EUA?
Как и любой консультативный комитет FDA, VRBPAC предоставит FDA рекомендацию о том, разрешать ли вакцину-кандидат для экстренного использования.FDA принимает во внимание рекомендацию VRBPAC, хотя окончательное решение принимает FDA.
Почему это собрание VRBPAC важно?
Заседание VRBPAC является стандартной частью процесса разработки вакцины. Этот комитет состоит из независимых научных экспертов, которых выбирает FDA для анализа и оценки доказательств того, является ли вакцина или другой биологический продукт безопасным и эффективным для предполагаемого использования. Эта встреча является важной вехой в процессе научной проверки FDA, чтобы гарантировать, что любая исследуемая вакцина COVID-19, которую оно разрешает для использования, была надлежащим образом оценена на предмет безопасности, эффективности и качества.
Что произойдет, если VRBPAC не рекомендует, чтобы FDA разрешило вакцину COVID-19 для экстренного использования? Означает ли это, что FDA его не одобрит?
В конечном итоге FDA принимает решение, одобрять или санкционировать любую медицинскую терапию, включая экспериментальную вакцину против COVID-19. Независимо от результата этой встречи, мы продолжим тесно сотрудничать с FDA в рамках нашего постоянного стремления сделать потенциальную вакцину доступной быстро и безопасно.
18 ноября 2020 г.
Pfizer и BioNTech объявили, что продолжающееся исследование фазы 3 для нашей вакцины-кандидата COVID-19 достигло всех основных конечных точек эффективности.
Анализ данных показывает, что вакцина-кандидат эффективна в предотвращении COVID-19 с общим благоприятным профилем безопасности. На нашем пути к тому, чтобы сделать потенциальную вакцину доступной, мы хотим быть уверены, что общественность будет в курсе нашего прогресса и следующих шагов.
Теперь, когда у Pfizer и BioNTech есть данные об эффективности и безопасности, что будет дальше, когда ваша вакцина-кандидат COVID-19 будет одобрена для использования?
Мы хотим подать заявку в течение нескольких дней в U.S. FDA для разрешения на использование в чрезвычайных ситуациях (EUA). EUA дает FDA право разрешать использование неутвержденных медицинских продуктов во время чрезвычайной ситуации в области общественного здравоохранения, когда нет других адекватных, одобренных или доступных альтернатив. Наше приложение EUA будет включать все данные о нашем кандидате на вакцину COVID-19, собранные на сегодняшний день. Затем эти доказательства будут изучены собственными учеными FDA, а также внешней группой независимых экспертов, известной как Консультативный комитет по вакцинам и родственным биологическим продуктам (VRBPAC).
Прежде чем FDA разрешит использование любой вакцины против COVID-19 для экстренного использования, VRBPAC рассмотрит и обсудит данные на открытом заседании, которое, вероятно, состоится в декабре. Как и любой консультативный комитет FDA, VRBPAC предоставит рекомендации FDA о том, разрешать ли вакцину для экстренного использования, хотя окончательное решение принимает FDA.
По каким критериям кандидат на вакцину COVID-19 может получить EUA?
FDA может выдать EUA после того, как определит, что выполняются следующие требования:
- На основании имеющихся научных данных, включая данные клинических испытаний, разумно полагать, что продукт может быть эффективным для предотвращения и диагностики или лечить такое серьезное или опасное для жизни заболевание или состояние, которое может быть вызвано SARS-CoV-2 (вирус, вызывающий COVID-19)
- Выявленные и потенциальные преимущества продукта при его использовании для диагностики, предотвращения или лечить выявленное серьезное или опасное для жизни заболевание или состояние, перевешивать выявленные и потенциальные риски, связанные с продуктом
- Не существует адекватной, одобренной и доступной альтернативы продукту для диагностики, предотвращения или лечения заболевания или состояния
Если вакцина-кандидат, разрабатываемая Pfizer и BioNTech для предотвращения COVID-19, будет разрешена для экстренного использования, то кто получит ее первым?
Если вакцина-кандидат разрешена для использования в экстренных случаях, правительство и органы здравоохранения сначала предложат вакцину тем, кто, по их мнению, является подходящей и испытывает наибольшую потребность.В США мы ожидаем, что EUA будет специфичным для определенных групп высокого риска, как это определено Центрами по контролю и профилактике заболеваний США (CDC) и основано на данных, которые будут предоставлены в приложении EUA. Мы считаем, что приоритетом будут передовые медицинские работники, основные работники, люди с ослабленным иммунитетом, дома престарелых и сотрудники службы общественной безопасности, но в конечном итоге это решение будет принимать правительства.
Работает ли ваша вакцина-кандидат от COVID-19 для всех, включая разные возрастные группы и этнические группы?
Данные нашего большого исследования фазы 3 с участием почти 44 000 человек показали, что наша кандидатная вакцина на 95% эффективна в предотвращении COVID-19.Эффективность была постоянной по возрастным, расовым и этническим демографическим характеристикам. Наблюдаемая эффективность у взрослых старше 65 лет составила более 94%. Просмотрите наш пресс-релиз для получения дополнительной информации.
Безопасна ли вакцина-кандидат от COVID-19 от Pfizer и BioNTech? Каковы потенциальные риски и побочные эффекты?
На сегодняшний день независимый комитет по мониторингу внешних данных не обнаружил каких-либо серьезных проблем с безопасностью, и данные нашего исследования фазы 3 показали, что наша вакцина-кандидат от COVID-19 хорошо переносится.Просмотрите наш пресс-релиз для получения дополнительной информации.
Могут ли компании Pfizer и BioNTech производить достаточное количество доз вакцины?
Мы увеличили производственные мощности по всему миру, чтобы удовлетворить высокий спрос, связанный с пандемией COVD-19. Основываясь на текущих прогнозах, компании рассчитывают произвести до 50 миллионов доз вакцины в 2020 году и до 1,3 миллиарда доз к концу 2021 года.
Мы уверены в нашем обширном опыте, знаниях и существующей инфраструктуре холодовой цепи для распространения вакцина во всем мире.Вместе с BioNTech мы разработали специально разработанные термические грузоотправители с регулируемой температурой. Их можно использовать в качестве единиц временного хранения на 15 дней, заправив сухим льдом. Каждый грузоотправитель снабжен термодатчиком с функцией GPS, который отслеживает местоположение и температуру каждой партии вакцины по заранее установленным маршрутам с использованием широкой дистрибьюторской сети Pfizer.
Что делать, если вирус SARS-CoV-2 мутирует? Будет ли работать вакцина-кандидат от COVID-19 от Pfizer и BioNTech?
Только через тестирование мы узнаем, работает ли вакцина против мутированной формы вируса SARS-CoV-2.Однако мы думаем, что технология вакцины мРНК может быть легко адаптирована и потенциально модифицирована относительно быстро для устранения новых мутаций вируса. Поскольку эта технология не включает весь или часть фактического патогена, а вместо этого использует генетический код патогена, мы потенциально можем изменить генетический код вакцины-кандидата, чтобы устранить любые изменения в вирусе.
Чтобы узнать больше о SARS-CoV-2, наших научных усилиях и о том, что вы можете сделать сейчас, чтобы оставаться в безопасности и предотвратить распространение, посетите веб-сайт www.pfizer.com/health/coronavirus.
Для получения дополнительной информации о Pfizer, пожалуйста, просмотрите наши документы, поданные в Комиссию по ценным бумагам и биржам США, включая информацию, представленную в разделах «Факторы риска» и «Перспективная информация и факторы, которые могут повлиять на будущие результаты» и пресс-релиз, выпущенный Pfizer и BioNTech 18 ноября 2020 г.
CIR-14-0150 1..12
% PDF-1.4 % 173 0 объект > эндобдж 172 0 объект > поток Издатель расширенной печати Arbortext 9.1.406 / W Unicode2021-11-01T20: 07: 07-07: 002015-03-04T11: 13: 05 + 05: 302021-11-01T20: 07: 07-07: 00application / pdf


 А вирус, циркулируя в крови беременной, попадает через плаценту к плоду. Поэтому при подозрении на инфицирование краснухой беременной женщины необходимо провести специальное исследование (кровь дважды обследуют на содержание противокраснушных антител, и, если их количество существенно увеличивается, что свидетельствует о перенесенной краснухе, на ранних сроках встает вопрос о прерывании беременности, так как велика угроза рождения ребенка с уродствами).
А вирус, циркулируя в крови беременной, попадает через плаценту к плоду. Поэтому при подозрении на инфицирование краснухой беременной женщины необходимо провести специальное исследование (кровь дважды обследуют на содержание противокраснушных антител, и, если их количество существенно увеличивается, что свидетельствует о перенесенной краснухе, на ранних сроках встает вопрос о прерывании беременности, так как велика угроза рождения ребенка с уродствами). Если беременность наступила раньше этого срока или была привита женщина, уже ожидающая ребенка, это не является показанием к прерыванию беременности.
Если беременность наступила раньше этого срока или была привита женщина, уже ожидающая ребенка, это не является показанием к прерыванию беременности.
 Не следует торопиться покидать центр семейной медицины, обычно врач или медсестра просит родителей посидеть минут 30 неподалеку от кабинета. Это поможет успокоить ребенка и оказать ему помощь в случае возникновения реакций на введение вакцины.
Не следует торопиться покидать центр семейной медицины, обычно врач или медсестра просит родителей посидеть минут 30 неподалеку от кабинета. Это поможет успокоить ребенка и оказать ему помощь в случае возникновения реакций на введение вакцины.
