Зачем хранить стволовые клетки
Хранение стволовых клеток
Поскольку пуповинная кровь содержит множество стволовых клеток, они могут быть легко выделены и сохранены (хранение при сверхнизких температурах) в случае, если они понадобятся в будущем. Лечение стволовыми клетками и трансплантации были использованы для широкого спектра заболеваний и, таких как рак (в том числе лимфомы и лейкемии ) и наследственные нарушения обмена веществ. Хранение стволовых клеток имеет большие перспективы на основе текущих результатов исследований стволовых клеток , таких как лечение диабета , болезни Альцгеймера , церебральный паралич, регенерация и восстановление поврежденных органов и тканей. Очень часто возникают проблемы в поиске в государственных банках стволовых клеток подходящий Вам крови, однако, клетки полученные из пуповинной крови Вашего ребенка, идеально подходят для вашего ребенка и Вашей семьи. Кроме того, технологии стволовых клеток развивается быстрыми темпами, можно надеяться, что лечение стволовыми клетками станет неотъемлемой частью поддержания здоровья для будущих поколений.
Статистика показывает, что есть больше шансов на успех в трансплантации стволовых клеток между братьями и сестрами , чем при пересадке неродственных доноров и реципиентов . Существует лишь малая вероятность того что трансплант будет отторгнут организмом хозяина ( РТПХ ), что является основным осложнением при трансплантации стволовых клеток. Стволовые клетки брата или сестры могут также играть важную роль в лечении наследственных генетических заболеваний, таких как серповидно-клеточная анемия, в случаях, когда брат не наследует дефектный ген . В таких случаях , собственные стволовые клетки ребенка не могут быть использованы для трансплантации. Если Вы планируете заводить детей в будущем или же у Вас уже есть дети, мы настоятельно рекомендуем Вам рассмотреть возможность (иногда она может быть только раз в жизни) сохранить стволовые клетки Вашего ребенка для потенциального использования в лечении Вашей семьи, а также для собственных медицинских нужд вашего ребенка.
Хранение пуповинных тканей со стволовыми клетками
Пуповина сама по себе является богатым источником стволовых клеток, называемых мезенхимальные стволовые клетки( МСК ).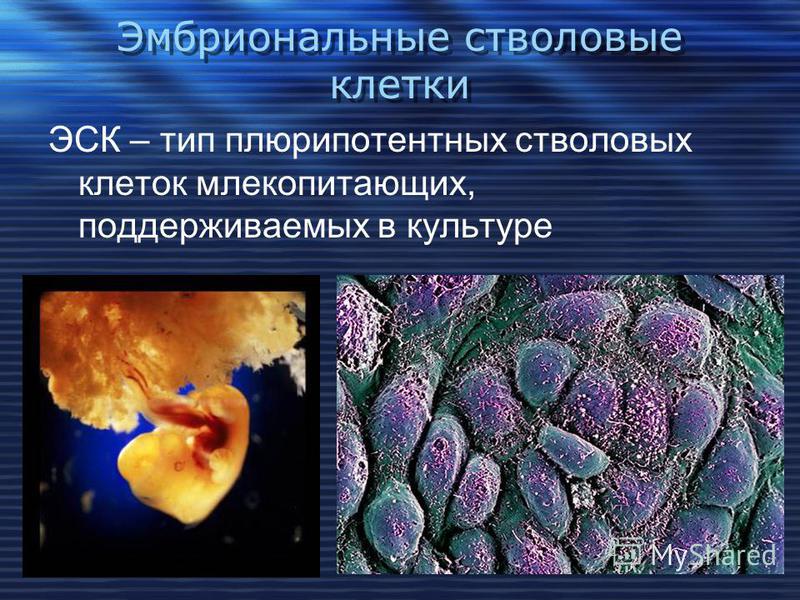 Мезенхимальные стволовые клетки имеют много уникальные функции, в том числе способностью ингибировать воспаление после повреждения ткани секретируют факторы роста, которые помогают в восстановлении тканей и могут использоваться для выращивания различных типов клеток, включая нервные клетки , костные клетки , жировые клетки и хрящи. МСК все чаще используются в регенеративной медицине для широкого круга заболеваний, включая болезни сердца и почек, ALS, заживление ран и аутоиммунных заболеваний.
Мезенхимальные стволовые клетки имеют много уникальные функции, в том числе способностью ингибировать воспаление после повреждения ткани секретируют факторы роста, которые помогают в восстановлении тканей и могут использоваться для выращивания различных типов клеток, включая нервные клетки , костные клетки , жировые клетки и хрящи. МСК все чаще используются в регенеративной медицине для широкого круга заболеваний, включая болезни сердца и почек, ALS, заживление ран и аутоиммунных заболеваний.
Стволовые клетки новорожденных в сравнении со взрослыми
Cryo -Cell рекомендует хранения стволовых клеток пуповинной крови, потому что исследования показали, что в стволовых клетках более взрослых доноров наблюдаются признаки старения , которые снижают их способность функционировать, чем стволовые клетки новорожденных. Некоторые из возрастных изменений, приводят к снижению функции иммунной системы и снижению способности к производству клеток крови
Вся информация, представленная на сайте на русском языке, носит справочный характер и не может быть использована в медицинских или иных целях.
Зачем нужны стволовые клетки? | КриоЦентр
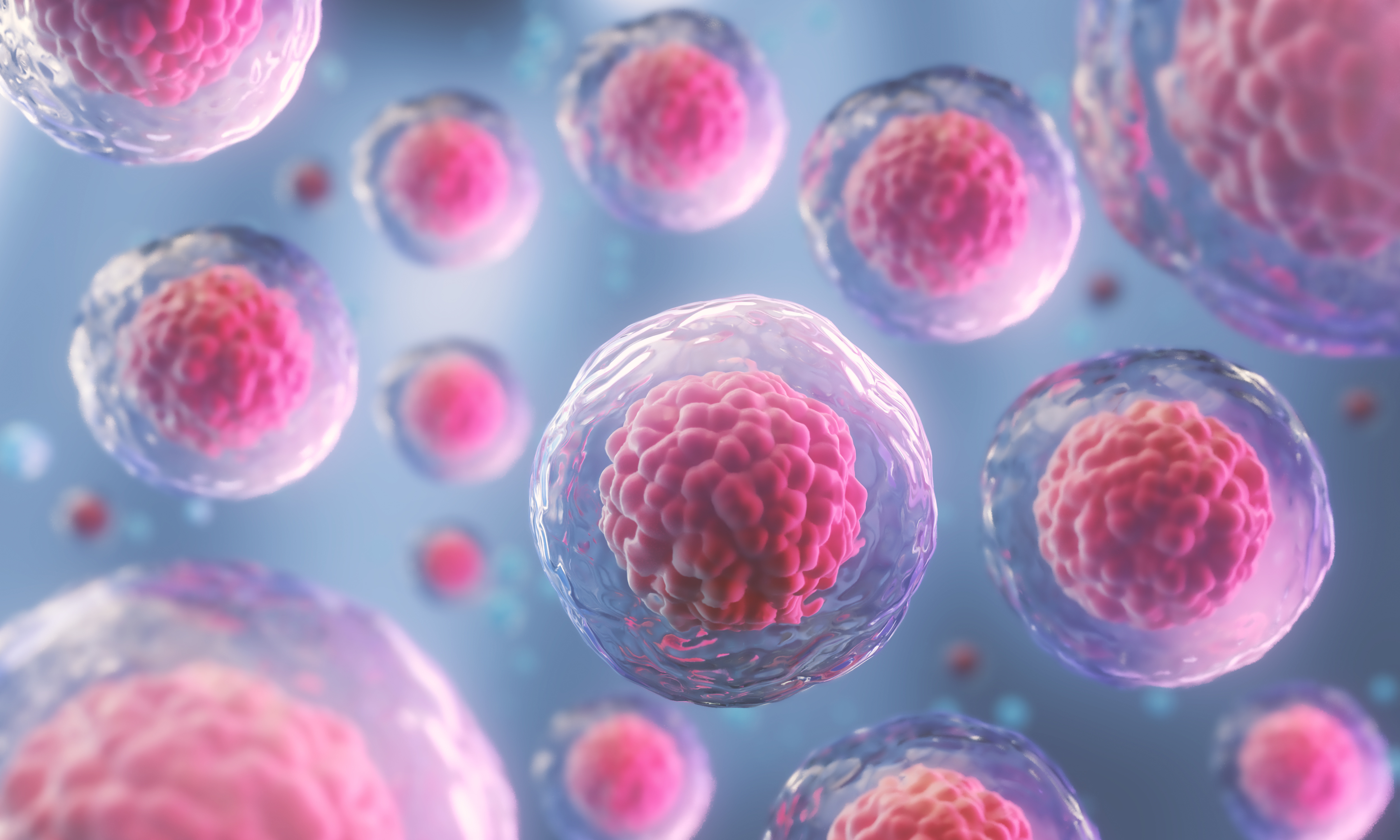
Три-четыре года назад стволовыми клетками всерьез интересовались очень немногие биологи и врачи. Теперь стволовые клетки воспринимают как символ новой медицины двадцать первого столетия. О стволовых клетках говорят римский понтифик и американский президент. О стволовых клетках спорят на страницах газет и трибунах парламентов. Расходы на изучение стволовых клеток исчисляются сотнями миллионов долларов, а потенциальные прибыли от применения стволовых клеток — многими миллиардами. Так что же это такое — стволовые клетки? Их уникальные особенности легче всего понять, если проследить за развитием человеческого эмбриона. Развитие эмбриона начинается с деления оплодотворенной сперматозоидом яйцеклетки. Примерно через четверо суток после первого деления яйцеклетка образует крошечный пузырек — бластоцисту. Внутри бластоциста заполнена клетками, которые называют родоначальными или стволовыми. Это плюрипотентные стволовые клетки.
Что такое стволовые клетки | ivfrigastemcells.lv
Стволовые клетки – это клетки-предшественники всех клеток и тканей нашего организма. Стволовые клетки способны поддерживать свою численность с помощью деления и обладают способностью дифференцироваться (превращаться) в различные типы клеток.
С возрастом количество стволовых клеток в организме человека снижается. Истощение запаса стволовых клеток вследствие старения, тяжелых заболеваний или вредных привычек (курение и употребление алкоголя) лишает организм возможности самовосстановления. Из-за этого может нарушаться функционирование тех или иных органов.
Источники стволовых клеток человека (после рождения):
Стволовые клетки человека условно разделяют на гемопоэтические и мезенхимальные
Гемопоэтические (кроветворные) стволовые клетки (ГСК) образуют разнообразие клеток крови, определяющих иммунитет, борющихся с инфекциями, переносящих кислород и участвующих в процессах свертывания крови. История клинического применения гемопоэтических стволовых клеток началась более 60 лет назад, и сейчас трансплантация гемопоэтических стволовых клеток — метод первого выбора при лечении гематологических, некоторых онкологических и ряда иммунологических и наследственных заболеваний.
История клинического применения гемопоэтических стволовых клеток началась более 60 лет назад, и сейчас трансплантация гемопоэтических стволовых клеток — метод первого выбора при лечении гематологических, некоторых онкологических и ряда иммунологических и наследственных заболеваний.
Гемопоэтические стволовые клетки можно получить из костного мозга, периферической крови (после введения специальных препаратов) и из пуповинной крови. Если в первые десятилетия практически единственным источником служил костный мозг, то с 1988 года — с момента первой (и сразу успешной) трансплантации пуповинной крови профессором E. Gluckman мальчику с анемией Фанкони – пуповинная кровь заняла достойное место в современной трансплантологии.
Часто у пациента просто нет времени ждать вызова донора костного мозга, повторных анализов и подготовки донора к забору костного мозга, кроме того, учитывая жесткие требования по совпадению HLA-генотипа донора и пациента, подобрать образец костного мозга получается не для всех. В таких случаях трансплантация пуповинной крови – не просто альтернатива трансплантации костного мозга, а единственный шанс для пациента.
В таких случаях трансплантация пуповинной крови – не просто альтернатива трансплантации костного мозга, а единственный шанс для пациента.
Но даже в менее «экстремальных» ситуациях, при возможности подбора донора костного мозга, предпочтение может быть отдано именно трансплантации пуповинной крови — за счет сниженных рисков отторжения и возникновения реакции трансплантат против хозяина (РТПХ). Поэтому пуповинная кровь становится все более востребованным источником гемопоэтических стволовых клеток для трансплантации, и на сегодняшний день, по данным World Marrow Donor Association (WMDA), проведено более 30 000 трансплантаций пуповинной крови.
Мезенхимные (стромальные) стволовые клетки (МСК) способны превращаться в клетки костной, хрящевой, соединительной ткани, формировать элементы кровеносных сосудов. Кроме восполнения утраченных элементов этих тканей, мезенхимальные стволовые клетки синтезируют большой набор биологически активных веществ, с помощью которых могут изменять поведение других типов клеток, например, клеток иммунной системы.
Такие биологические функции мезенхимальных стволовых клеток сделали их востребованным источником для регенеративной терапии: к концу 2017 года в международной базе клинических испытаний зарегистрировано более 780 исследований с использованием МСК (https://clinicaltrials.gov). Многообещающие результаты были получены при применении МСК для восстановления тканей при травмах опорно-двигательного аппарата, язвах и ожогах, для профилактики и/или лечения реакции трансплантат против хозяина при онкологических заболеваниях, при терапии иммунопатологических процессов, ишемии нижних конечностей, патологии сердечно-сосудистой системы, дегенеративных процессов в хрящевой ткани и даже в реконструктивной стоматологии. Важно, что по результатам всех клинических исследований применение МСК не приводит к возникновению серьезных побочных эффектов.
В качестве основных источников получения мезенхимальных стволовых клеток выступают костный мозг, жировая ткань и ткани пуповины. В отличие от МСК костного мозга и жировой ткани, мезенхимальные стволовые клетки пуповины – это молодые клетки, не подвергавшиеся действию негативных факторов внешней среды и поэтому обладающие высокой функциональной активностью. Важным преимуществом мезенхимальных стволовых клеток пуповины является также совершенная безболезненность и безопасность сбора ткани для их получения, кроме того, в случае сохранения МСК пуповины эти клетки могут быть в любой момент разморожены и применены значительно быстрее, чем клетки из других источников.
Важным преимуществом мезенхимальных стволовых клеток пуповины является также совершенная безболезненность и безопасность сбора ткани для их получения, кроме того, в случае сохранения МСК пуповины эти клетки могут быть в любой момент разморожены и применены значительно быстрее, чем клетки из других источников.
Существует несколько источников стволовых клеток человека:
- костный мозг;
- жировая ткань;
- периферическая кровь;
- пуповинная кровь (забор стволовых клеток пуповинной крови производится только в момент рождения ребенка)
- ткань пуповины
Банк хранения стволовых клеток пуповинной крови
Заведующая Центром клеточных и репродуктивных технологий
Тел врача: 8 (423) 2-277-883
Часы работы: c 8:00 до 16:00
Структура Отделения клеточных технологий:
|
Лаборатория выделения и культивирования стволовых клеток
|
Банк стволовых клеток
|
|
|
|
Банк стволовых клеток
Персональное банкирование стволовых клеток пуповинной крови
Сегодня вы можете сделать бесценный подарок своему малышу.
Что такое стволовые клетки?
Это прародительницы всех без исключения типов клеток в организме. Они не имеют «специализации», то есть при определённых условиях способны многократно делиться и превращаться в клетки любых органов и тканей. Именно поэтому они являются своего рода экстренной помощью: если где-то в организме возникло нарушение, стволовые клетки направляются туда и способствуют восстановлению повреждённого органа. С возрастом количество стволовых клеток уменьшается и, соответственно, снижаются восстановительные возможности организма.
Для чего нужны стволовые клетки?
Реальность такова, что существует целый ряд тяжёлых заболеваний, в первую очередь лейкозов, при которых единственным спасением для человека является трансплантация кроветворных стволовых клеток костного мозга.
Кроме того, стволовые клетки используются в травматологии и ортопедии — способствуют восстановлению костных и хрящевых тканей, при лечении рубцов, ожогов, коррекции возрастных дефектов кожи. Достаточно успешно стволовые клетки применяются в кардиологии — уже сегодня апробируются методики для лечения инфаркта миокарда, ишемической болезни сердца, хронической сердечной недостаточности.
Уже сегодня перечень болезней, наиболее перспективных в плане применения клеток пуповинной крови исчисляется десятками. Ни у кого не остаётся сомнений в том, что клеточная терапия — основа медицины будущего.
Как получить стволовые клетки пуповинной крови?
Стволовые клетки содержаться в костном мозге, жировой ткани, но оптимальный источник, где их концентрация максимальна, — это кровь, заполняющая плаценту и пуповину новорождённого.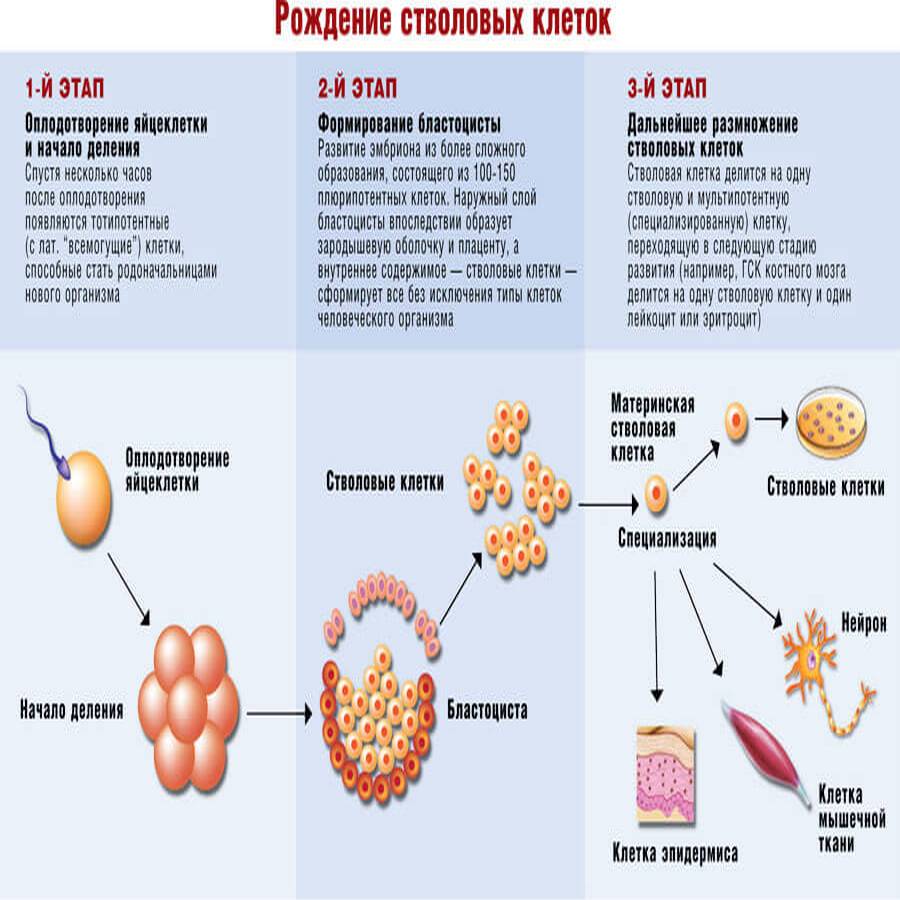 Получить стволовые клетки на пике их потенциала и создать их резерв можно только в момент рождения ребёнка.
Получить стволовые клетки на пике их потенциала и создать их резерв можно только в момент рождения ребёнка.
Процедура забора пуповинной крови абсолютно безопасна для новорождённого и его матери и может осуществляться как при нормальных физиологических родах, так и при кесаревом сечении. После рождения ребёнка врач, принимающий роды, пунктирует иглой пуповинную вену и получает оттуда самотёком от 50 до 250 мл крови. Эта кровь на 3-5% состоит из стволовых клеток.
После забора пуповинная кровь в течении 4-6 часов доставляется в лабораторию, где образец пуповинной крови обрабатывается. Выделение стволовых клеток проводится в сертифицированном «чистом» помещении, соответствующем Российским и международным стандартам, оснащённом подачей стерильного воздуха, и с применением только одноразовых расходных материалов от ведущих мировых производителей.
Используемые в Центре клеточных и репродуктивных технологий уникальные инновационные методики, разрешённые к применению Росздравнадзором, позволяют выделить 95% стволовых клеток из образца пуповинной крови при 98% их жизнеспособности и эффективно подготовить их к криогенному хранению. Все образцы пуповинной крови и выделенных стволовых клеток подлежат серии лабораторных исследований для подтверждения высокого качества и пригодности для последующего клинического использования. Чтобы исключить риск возможного инфицирования бактериальными или вирусными агентами, ни один образец не попадёт в хранилище, не пройдя тщательного бактериологического контроля. Затем стволовые клетки замораживаются и хранятся в жидком азоте при температуре -1960 С сколь угодно долго.
Все образцы пуповинной крови и выделенных стволовых клеток подлежат серии лабораторных исследований для подтверждения высокого качества и пригодности для последующего клинического использования. Чтобы исключить риск возможного инфицирования бактериальными или вирусными агентами, ни один образец не попадёт в хранилище, не пройдя тщательного бактериологического контроля. Затем стволовые клетки замораживаются и хранятся в жидком азоте при температуре -1960 С сколь угодно долго.
Что такое банки стволовых клеток?
Персональные (семейные) банки сохраняют стволовые клетки, являющиеся собственностью конкретного человека. Никто, кроме родителей или самого ребёнка не сможет воспользоваться этим «именным» клеточным вкладом. Сам факт наличия клеток пуповинной крови в криогенном хранилище означает, что в случае необходимости их можно использовать незамедлительно, без потерь времени на поиск (не всегда успешный) совместимого донора. Чем раньше начнётся лечение, тем больше шансов победить заболевание или остановить его прогрессирование.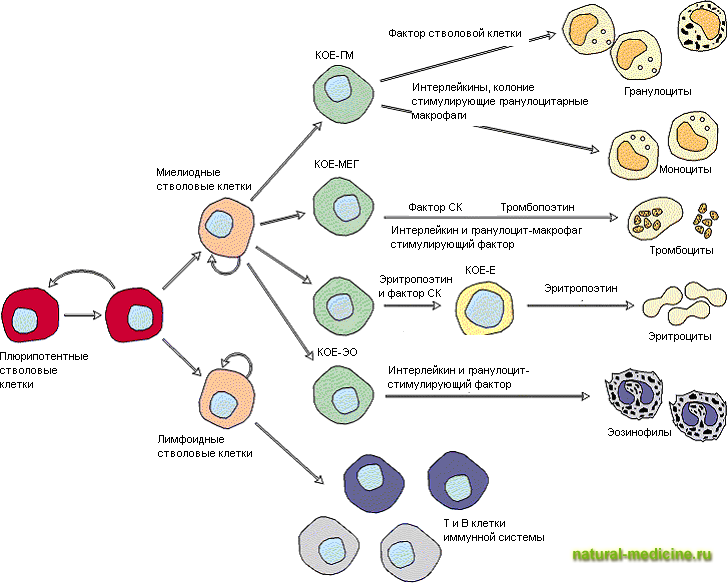 К тому же клетки пуповинной крови обладают меньшей иммуногенностью в случае тарсплантации не полностью идентичному реципиенту, что позволяет успешно их использовать для пересадки близким (кровным) родственникам донора. Но стопроцентно ими может воспользоваться сам ребёнок. А насколько пуповинная кровь подойдёт папе, маме, брату, сестре, дедушке, бабушке, покажет исследование, которое называется HLA-типирование.
К тому же клетки пуповинной крови обладают меньшей иммуногенностью в случае тарсплантации не полностью идентичному реципиенту, что позволяет успешно их использовать для пересадки близким (кровным) родственникам донора. Но стопроцентно ими может воспользоваться сам ребёнок. А насколько пуповинная кровь подойдёт папе, маме, брату, сестре, дедушке, бабушке, покажет исследование, которое называется HLA-типирование.
Некоторые банки, работающие на территории Приморского края, перевозят клетки пуповинной крови на обработку и хранение в Москву. Это очень вредно для образца, так как при длительной транспортировке с каждым часом теряется 10% стволовых клеток и 5% их жизнеспособности. Кроме того, механическая тряска приводит к повреждению мембран клеток пуповинной крови, вызывая их нарушение. Именно поэтому во Владивостоке и был создан свой банк стволовых клеток, чтобы максимально приблизить место обработки и хранения клеток к нашим пациентам. Методики, используемые в Центре клеточных и репродуктивных технологий, отвечают международным требованиям и стандартам, предъявляемым к банкам стволовых клеток крови пуповины.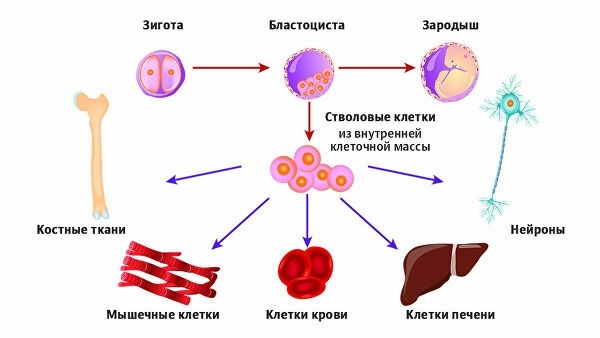
Для криохранения стволовых клеток используется роботизированная система BioArchive («Thermogenesis», США), осуществляющая полностью автоматизированный процесс закладки, хранения и контроля за всеми процессами. Наличие двух программных замораживателей позволяет предохранить образец стволовых клеток от малейщих температурных колебаний, а также контролировать процесс равномерного поэтапного замораживания образца.
Каждый образец стволовых клеток маркируется уникальным буквенным, цифровым и штриховым кодом. Вся информация заносится в автоматизированную базу данных и дублируется. Риск потери или неверной идентификации образца полностью исключён. Для хранения клеток пуповинной крови используют специально разработанные криоконтейнеры. Дополнительные «спутники» позволяют провести необходимые тесты перед клиническим использованием.
При хранении в жидком азоте при температуре -1960 С клетки полностью защищены от внешних воздействий, сохраняют максимальную жизнеспособность и биологическую активность на протяжении проктически неограниченного периода времени. Таким образом «страховка» может сопровождать своего обладателя на протяжении всей жизни. Используемая методика замораживания позволяет получать после размораживания до 85-88% жизнеспособных стволовых клеток.
Таким образом «страховка» может сопровождать своего обладателя на протяжении всей жизни. Используемая методика замораживания позволяет получать после размораживания до 85-88% жизнеспособных стволовых клеток.
Хранилище обеспечено системой бесперебойного электроснабжения и находится под круглосуточной охраной. Электронные датчики контролируют уровень азота 24 часа в сутки 365 дней в году.
Как сдать пуповинную кровь на хранение?
Сегодня родители могут заключить с ГАУЗ «Краевой клинический центр специализированных видов медицинской помощи» договор на индивидуальное хранение стволовых клеток своего ребёнка. Центр клеточных и репродуктивных технологий работает в тесном сотрудничестве со всеми роддомами г. Владивостока. Именной набор для сбора пуповинной крови, содержащий все необходимые материалы в герметичной упаковке будет доставлен непосредственно в родильное отделение. Забор крови проведут специалисты, обученные этой процедуре. В любое время года пуповинная кровь в изотермическом контейнере будет незамедлительно доставлена в специализированную лабораторию центра для выделения стволовых клеток.
Забор крови проведут специалисты, обученные этой процедуре. В любое время года пуповинная кровь в изотермическом контейнере будет незамедлительно доставлена в специализированную лабораторию центра для выделения стволовых клеток.
Вам необходимо только приехать и оформить договор с Центром. Всё остальное сделают его сотрудники. Образец крови может храниться десятилетиями. И если ребёнку потребуется трансплантация стволовых клеток, родителям не придётся тратить драгоценное время и весьма значительную сумму денег и подбирать образец крови в банке доноров (если такой найдётся).
Конечно, взятие, обработка и хранение стволовых клеток стоят денег. Но эти затраты несопоставимы с теми суммами, которые придётся потратить для подбора и покупки донорского образца крови. К тому же получить и сохранить стволовые клетки такими, какими они были при рождении — молодыми, полными сил и энергии, можно только раз в жизни — во время родов, а новые технологии лечения развиваются очень быстро. Возможно, через несколько лет метод трансплантации клеток пуповинной крови будет использоваться очень широко, и Вы пожалеете, что лишили ребёнка уникальной «биологической» страховки и доступности к самым передовым технологиям. И уж однозначно врачи считают, что особенно важно сохранить стволовые клетки ребёнка, если:
И уж однозначно врачи считают, что особенно важно сохранить стволовые клетки ребёнка, если:
· Среди родственников были случаи онкологических заболеваний, сердечно-сосудистых недугов, болезней крови, тяжёлых генетических заболеваний,
· В семье уже есть больные дети, которых можно будет вылечить с использованием стволовых клеток пуповинной крови новорождённого ребёнка,
· Члены семьи являются представителями разных или редких национальностей, что затрудняет подбор совместимого донора
· Вы являетесь многодетными родителями,
· Беременность возникла в результате ЭКО.
Дорогие мамы и папы, бабушки и дедушки, не упустите шанс сделать будущему ребёнку подарок на всю жизнь!
Созданный на базе ГАУЗ «Краевой клинический центр специализированных видов медицинской помощи» Отделения клеточных технологий является единственным в Дальневосточном регионе учреждением подобного профиля, прошедшим сертификацию и получившим лицензию Росздравнадзора на все виды работ и предоставляемых услуг.
Банк хранения стволовых клеток пуповинной крови:
· Соответствие банка всем международным требованиям
· Новейшее оборудование для выделения и хранения стволовых клеток
· Сертифицированные технологии для работы со стволовыми клетками
· Высокоспециализированная лаборатория выделения стволовых клеток
· Определение количества стволовых клеток методом проточной цитофлуориметрии
· Самая эффективная, максимально сберегающая система забора крови
· Надёжное высокотехнологичное криогенное хранилище стволовых клеток
· Автоматизированная система учёта и хранения стволовых клеток
· Культивирование стволовых клеток
· Определение совместимости образцов между ребёнком и родственниками — HLA-типирование
С уважением, коллектив отделения клеточных технологий!
Что такое стволовые клетки и зачем они нужны
Что такое стволовые клетки?
Для начала немного основ.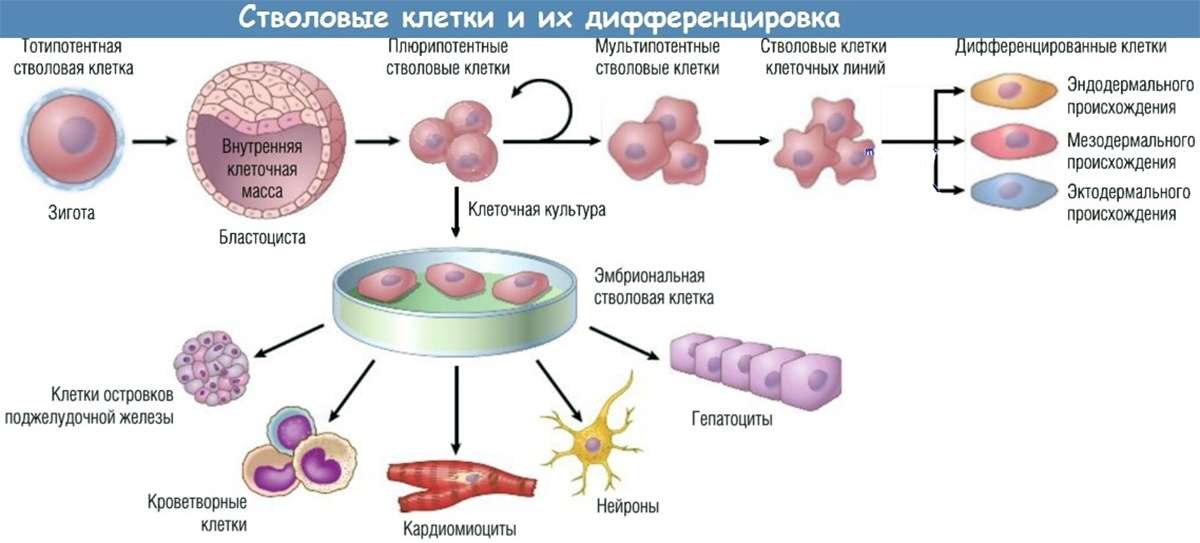 Мозг, мышцы, внутренние органы от сердца до почек, кости, кожа — все элементы нашего тела состоят из клеток. Но они серьёзно отличаются друг от друга. «Мышечная» не сможет заменить собой клетку костной ткани. «Печёночная» не станет мозговой. Клетки, из которых состоят почки, совершенно не похожи на клетки кожи.
Мозг, мышцы, внутренние органы от сердца до почек, кости, кожа — все элементы нашего тела состоят из клеток. Но они серьёзно отличаются друг от друга. «Мышечная» не сможет заменить собой клетку костной ткани. «Печёночная» не станет мозговой. Клетки, из которых состоят почки, совершенно не похожи на клетки кожи.
Объединяет их лишь одно: все они однажды произошли из стволовых (недифференцированных, «неопределённых») клеток.
Стволовые клетки — это то, из чего состоит возникший после зачатия эмбрион на самых ранних стадиях своего развития.
После имплантации в матку эмбрион начинает активно развиваться. В этот период недифференцированные клетки «определяются». Одни из них становятся клетками нервной системы, другие начинают образовывать кости, а третьи — внутренние органы.
По сути, стволовые клетки — это сырьё, из которого только зарождающийся организм полностью выстраивает собственные органы и ткани, превращаясь из крошечной зиготы в ребёнка.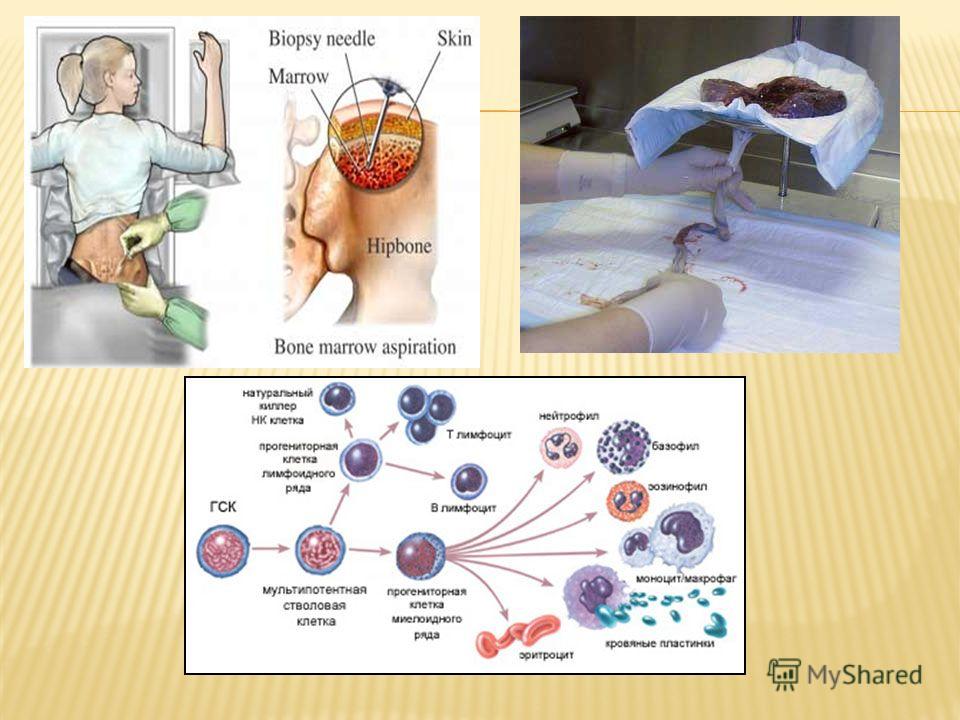
Почему о стволовых клетках так много говорят?
Стволовые клетки можно назвать той самой «волшебной пилюлей» ото всех болезней. И не только.
Из них можно вырастить любой элемент нашего тела. Если вы поломали руку, стволовые клетки помогут отремонтировать кость, сделав её снова юной, крепкой и здоровой — как в молодости, даже если вы уже гораздо старше. Если у вас цирроз печени, из стволовых клеток вырастут свежие гепатоциты, и орган заработает как новенький. То же касается проблем с другими внутренними органами, мышцами, сосудами.
Предполагается , что однажды с помощью стволовых клеток удастся победить болезнь Паркинсона, болезнь Альцгеймера, повреждения спинного мозга, нарушения работы сердца, диабет и артрит.
Недифференцированные клетки дают возможность в любой момент омолодить организм: от сердца, костей, глаз, зубов до кожи и волос.
Научное направление, которое изучает способы применения стволовых клеток, называется регенеративной медициной (она же — терапия стволовыми клетками).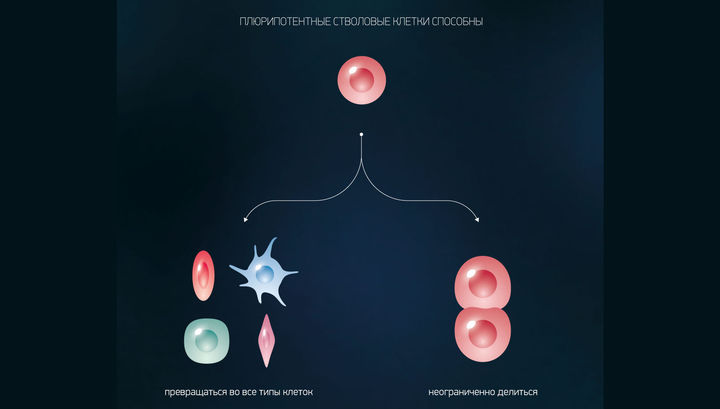
Стволовые клетки есть только у эмбрионов?
Нет. Существует четыре типа стволовых клеток, различающихся происхождением и возможностями.
1. Эмбриональные стволовые клетки
Из них состоят эмбрионы в возрасте примерно 3–5 дней после оплодотворения яйцеклетки. На этом этапе эмбрион называется бластоцистой. В нём содержится около 150 клеток.
Это наиболее универсальные стволовые клетки: потенциально они могут стать основой любого органа и ткани.
2. Взрослые стволовые клетки
Они есть у каждого человека. Правда, в минимальном количестве. Их задача — выращивать новые клетки для восстановления при различных повреждениях. Капелька стволовых клеток есть в сердце, печени, почках. Но больше всего их в костном мозге и жировой ткани.
Минус этого типа — низкая универсальность. Раньше исследователи вообще считали, что взрослые клетки способны превращаться лишь в элементы того органа, в котором находятся. Например, те, что содержатся в костном мозге, могут давать начало только клеткам крови.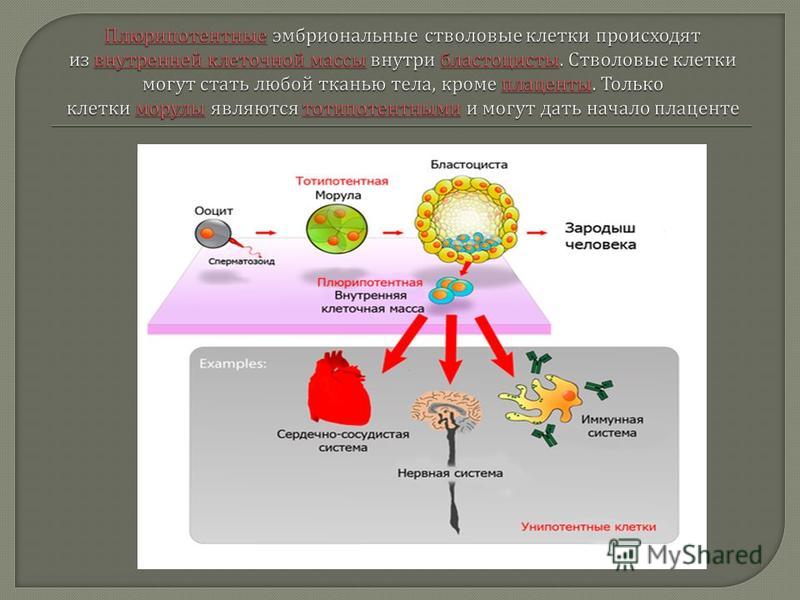 Позже выяснилось, что частицы из костного мозга также могут создавать клетки костей или сердечной мышцы. Но исследования пока ведутся, и у учёных далеко не всегда получается превратить взрослые стволовые клетки в элементы нужного органа.
Позже выяснилось, что частицы из костного мозга также могут создавать клетки костей или сердечной мышцы. Но исследования пока ведутся, и у учёных далеко не всегда получается превратить взрослые стволовые клетки в элементы нужного органа.
3. Индуцированные стволовые клетки (ИСК)
Учёные научились трансформировать обычные клетки в стволовые — с помощью генетического перепрограммирования. Например, клетки, взятые из соединительной ткани, удалось превратить в клетки сердца. Эксперименты над животными с сердечной недостаточностью показали, что ИСК действительно улучшают функции сердца и продлевают жизнь.
Но экспериментировать над людьми исследователи пока не рискуют.
4. Перинатальные стволовые клетки
Так называют недифференцированные клетки, которые были обнаружены в пуповинной крови и амниотической жидкости (околоплодных водах). Их не так много, но они тоже способны превращаться почти в любые специализированные клетки.
Регенеративная медицина уже работает?
Скажем так: активно пытается. Например, некоторые работы показали , что терапия стволовыми клетками действительно помогает при лечении травм и заболеваний опорно-двигательного аппарата — остеоартритов, разрывов сухожилий и связок, дегенерации поясничного диска, незаживающих повреждений костей.
Например, некоторые работы показали , что терапия стволовыми клетками действительно помогает при лечении травм и заболеваний опорно-двигательного аппарата — остеоартритов, разрывов сухожилий и связок, дегенерации поясничного диска, незаживающих повреждений костей.
Другой, ещё более распространённый пример использования регенеративной медицины, — трансплантация стволовых клеток (или пересадка костного мозга). Эту процедуру используют при некоторых видах рака крови: лейкемии, лимфоме, нейробластоме, множественной миеломе. Для пересадки используют взрослые стволовые клетки от донора или полученные из пуповинной крови. Они заменяют собой костный мозг пациента, пострадавший от химиотерапии или болезни.
Но исследования стволовых клеток ещё продолжаются . Поэтому регенеративная медицина пока не стала массовой. И есть вероятность, что и не станет.
Это значит, что секрет вечной молодости и здоровья найден, осталось лишь его доработать?
Терапия стволовыми клетками действительно очень перспективная медицинская отрасль. Однако она связана с целым рядом проблем .
Однако она связана с целым рядом проблем .
- Недифференцированные клетки, попав в организм взрослого человека, вызывают развитие не только здоровых клеток, но и тех, у которых есть патологии. Чем старше пациент, тем выше этот риск.
- Иммунная система человека иногда слишком активно реагирует на донорские стволовые клетки. Организм яростно атакует «вторженцев», и это может привести к непредсказуемым для здоровья последствиям.
- Наиболее универсальными и безопасными считаются эмбриональные стволовые клетки. Но насколько гуманно использовать человеческие эмбрионы (даже те, что были созданы в пробирке специально для медицинских целей), ни исследователи, ни врачи, ни общество в целом пока не определились.
Говорить о повсеместном использовании регенеративной медицины можно будет лишь после того, как наука найдёт ответы на поставленные вопросы. Но до этого ещё далеко.
Читайте также 🩸🩸🩸
Медицинские надежды на стволовые клетки: результаты скромные
https://ria. ru/20190309/1551627354.html
ru/20190309/1551627354.html
Медицинские надежды на стволовые клетки: результаты скромные
Медицинские надежды на стволовые клетки: результаты скромные — РИА Новости, 09.03.2019
Медицинские надежды на стволовые клетки: результаты скромные
Стволовые клетки исследуют уже больше полувека. Ученые создают их из обычных взрослых клеток, моделируют с их помощью различные болезни, выращивают органоиды… РИА Новости, 09.03.2019
2019-03-09T08:00
2019-03-09T08:00
2019-03-09T07:56
наука
клетки
/html/head/meta[@name=’og:title’]/@content
/html/head/meta[@name=’og:description’]/@content
https://cdnn21.img.ria.ru/images/155159/83/1551598383_0:319:3072:2047_1920x0_80_0_0_ea67ef115b9d82f17c8005e922b28fc0.jpg
МОСКВА, 9 мар — РИА Новости, Татьяна Пичугина. Стволовые клетки исследуют уже больше полувека. Ученые создают их из обычных взрослых клеток, моделируют с их помощью различные болезни, выращивают органоиды для трансплантации. Однако терапевтические методы использования стволовых клеток в большинстве случаев не выходят за рамки лабораторий и клинических испытаний.Клеточные яслиВ конце января мир облетела новость: в Японии после успешных клинических испытаний одобрили лечение травм спинного мозга с помощью стволовых клеток. Учитывая, что еще несколько лет назад этот метод отрабатывали исключительно на лабораторных грызунах, прогресс по медицинским меркам стремительный. До сих пор широко практиковали только одну технологию лечения стволовыми клетками — пересадку костного мозга больным лейкемией.Стволовые клетки есть у всех растений и животных, включая человека. Это недозрелые структуры, способные превратиться в любой тип специальных клеток: кровеносные тельца, нейроны, клетки кожи, кости, мышцы, зуба. С их помощью ткани организма постоянно в течение жизни обновляются. Например, клетки слизистой кишечника меняются каждую неделю.Стволовые клетки в теории описывали в начале XX века. Впервые предположение об их существовании высказал биолог из Санкт-Петербурга Александр Максимов.
Однако терапевтические методы использования стволовых клеток в большинстве случаев не выходят за рамки лабораторий и клинических испытаний.Клеточные яслиВ конце января мир облетела новость: в Японии после успешных клинических испытаний одобрили лечение травм спинного мозга с помощью стволовых клеток. Учитывая, что еще несколько лет назад этот метод отрабатывали исключительно на лабораторных грызунах, прогресс по медицинским меркам стремительный. До сих пор широко практиковали только одну технологию лечения стволовыми клетками — пересадку костного мозга больным лейкемией.Стволовые клетки есть у всех растений и животных, включая человека. Это недозрелые структуры, способные превратиться в любой тип специальных клеток: кровеносные тельца, нейроны, клетки кожи, кости, мышцы, зуба. С их помощью ткани организма постоянно в течение жизни обновляются. Например, клетки слизистой кишечника меняются каждую неделю.Стволовые клетки в теории описывали в начале XX века. Впервые предположение об их существовании высказал биолог из Санкт-Петербурга Александр Максимов. Экспериментально это подтвердили в 1960-е годы канадские ученые Эрнест Маккалох и Джеймс Тилл.Они подвергали мышей смертельной дозе рентгеновского излучения, убивая таким образом систему кроветворения, затем пересаживали им разные типы клеток от здоровых особей. Так исследователи увидели, что крови помогают восстановиться клетки костного мозга, причем, чтобы запустить процесс обновления, достаточно всего одной здоровой клетки, но она должна быть незрелой. Сейчас пересадка костного мозга используется для лечения болезней крови по всему миру.Божественная глина для организмаЛюбой многоклеточный организм вырастает из небольшой колонии стволовых клеток. Если ее разделить, к примеру, на две части, то из каждой сформируется полноценный зародыш. Эмбриональные стволовые клетки могут бесконечно делиться в пробирке. Это свойство используют, чтобы создавать клеточные культуры для лабораторных экспериментов и тестирования будущих лекарств. В отличие от стволовых клеток во взрослом организме, служащих для обновления определенного органа, эмбриональные стволовые клетки способны превратиться в любой тип клеток.
Экспериментально это подтвердили в 1960-е годы канадские ученые Эрнест Маккалох и Джеймс Тилл.Они подвергали мышей смертельной дозе рентгеновского излучения, убивая таким образом систему кроветворения, затем пересаживали им разные типы клеток от здоровых особей. Так исследователи увидели, что крови помогают восстановиться клетки костного мозга, причем, чтобы запустить процесс обновления, достаточно всего одной здоровой клетки, но она должна быть незрелой. Сейчас пересадка костного мозга используется для лечения болезней крови по всему миру.Божественная глина для организмаЛюбой многоклеточный организм вырастает из небольшой колонии стволовых клеток. Если ее разделить, к примеру, на две части, то из каждой сформируется полноценный зародыш. Эмбриональные стволовые клетки могут бесконечно делиться в пробирке. Это свойство используют, чтобы создавать клеточные культуры для лабораторных экспериментов и тестирования будущих лекарств. В отличие от стволовых клеток во взрослом организме, служащих для обновления определенного органа, эмбриональные стволовые клетки способны превратиться в любой тип клеток.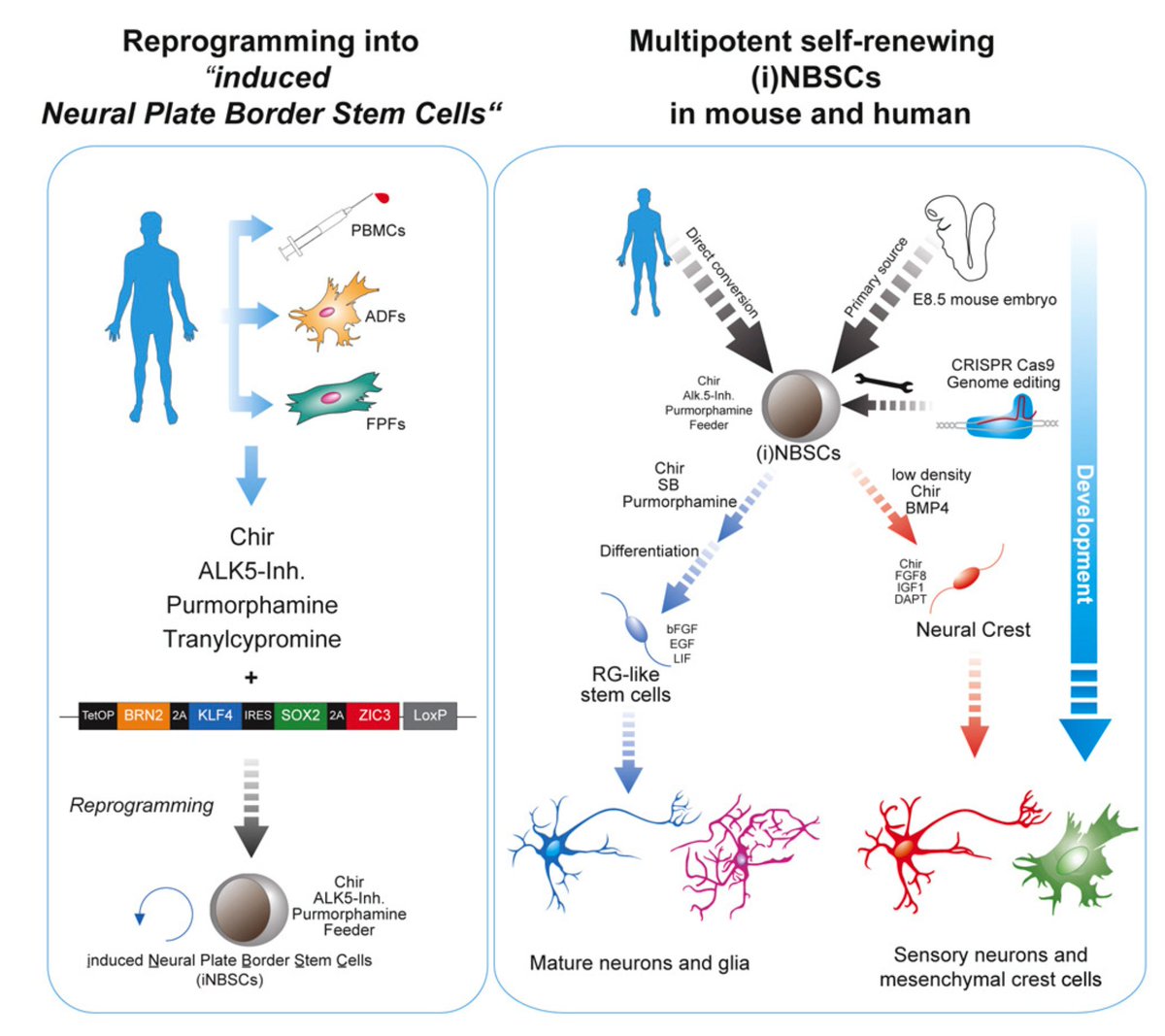 За это их стали называть плюрипотентными, то есть клетками с многочисленными возможностями.Технически можно получить эмбриональные стволовые клетки даже взрослого человека. Для этого нужна донорская яйцеклетка. Из нее удаляют ядро, где хранится ДНК, и помещают туда ядро клетки другого человека. Затем яйцеклетку заставляют делиться и получают эмбрион, развитие которого прекращают на самой ранней стадии. Впервые это продемонстрировал в 2018 году американский генетик Шухрат Миталипов.Пока эти достижения не имеют практического применения, поскольку опыты с эмбриональными клеточными культурами разрешены исключительно в исследовательских целях.Омоложение взрослых клетокСтволовые клетки в сложившемся организме отличаются от эмбриональных тем, что они уже слегка «повзрослели», то есть расположились в каких-либо органах и готовы превращаться в нужный тип ткани. Процесс этот необратим. Если клетка стала, к примеру, эпидермальной клеткой кожи, то обратно стволовой ей не быть. Так считали до 2006 года, пока японский ученый Синъя Яманака не открыл способ генетического перепрограммирования зрелых (соматических) клеток в стволовые.
За это их стали называть плюрипотентными, то есть клетками с многочисленными возможностями.Технически можно получить эмбриональные стволовые клетки даже взрослого человека. Для этого нужна донорская яйцеклетка. Из нее удаляют ядро, где хранится ДНК, и помещают туда ядро клетки другого человека. Затем яйцеклетку заставляют делиться и получают эмбрион, развитие которого прекращают на самой ранней стадии. Впервые это продемонстрировал в 2018 году американский генетик Шухрат Миталипов.Пока эти достижения не имеют практического применения, поскольку опыты с эмбриональными клеточными культурами разрешены исключительно в исследовательских целях.Омоложение взрослых клетокСтволовые клетки в сложившемся организме отличаются от эмбриональных тем, что они уже слегка «повзрослели», то есть расположились в каких-либо органах и готовы превращаться в нужный тип ткани. Процесс этот необратим. Если клетка стала, к примеру, эпидермальной клеткой кожи, то обратно стволовой ей не быть. Так считали до 2006 года, пока японский ученый Синъя Яманака не открыл способ генетического перепрограммирования зрелых (соматических) клеток в стволовые. Из нескольких десятков генов, запускающих развитие эмбриона и впоследствии перестающих работать, он выделил четыре ключевых. Ученый попробовал включить их в зрелых клетках мыши, и это сработало — они приобрели способности незрелых.Белки, вырабатываемые этими четырьмя генами, — Oct4, Sox2, Klf4 и с-Myc — называют теперь «коктейлем Яманаки». В 2012 году за это достижение ученый удостоился Нобелевской премии.Открытие Яманаки буквально развязало руки ученым по всему миру и породило волну исследований с этими новообращенными объектами (их называют индуцированными плюрипотентными стволовыми клетками). Биологами овладела идея пересадки плюрипотентных стволовых клеток в любой поврежденный или состарившийся орган, чтобы его восстановить. Однако реальность оказалась сложнее. Подсаженные стволовые клетки не приживались, погибали, вызывали побочные эффекты либо просто не оказывали никакого действия. Авторы Кокрейновского систематического обзора (эта организация исследует научные доказательства медицинских манипуляций) в 2015 году проанализировали данные о добавлении стволовых к собственным жировым клеткам пациента при трансплантации молочных желез.
Из нескольких десятков генов, запускающих развитие эмбриона и впоследствии перестающих работать, он выделил четыре ключевых. Ученый попробовал включить их в зрелых клетках мыши, и это сработало — они приобрели способности незрелых.Белки, вырабатываемые этими четырьмя генами, — Oct4, Sox2, Klf4 и с-Myc — называют теперь «коктейлем Яманаки». В 2012 году за это достижение ученый удостоился Нобелевской премии.Открытие Яманаки буквально развязало руки ученым по всему миру и породило волну исследований с этими новообращенными объектами (их называют индуцированными плюрипотентными стволовыми клетками). Биологами овладела идея пересадки плюрипотентных стволовых клеток в любой поврежденный или состарившийся орган, чтобы его восстановить. Однако реальность оказалась сложнее. Подсаженные стволовые клетки не приживались, погибали, вызывали побочные эффекты либо просто не оказывали никакого действия. Авторы Кокрейновского систематического обзора (эта организация исследует научные доказательства медицинских манипуляций) в 2015 году проанализировали данные о добавлении стволовых к собственным жировым клеткам пациента при трансплантации молочных желез. Рекламирующие эту процедуру клиники заявляют о том, что приживление в таком случае проходит лучше. Однако аналитики не нашли никаких подтверждений положительного эффекта процедуры — наоборот, указывали на ее возможную опасность.В то же время в систематическом обзоре Кокрейна в 2014 году отмечался положительный эффект в результате лечения травм позвоночника мезенхимальными стволовыми клетками, после которого двигательные функции восстанавливались быстрее. Эти эксперименты в те годы делали исключительно на грызунах и, как показала практика, их результаты применимы для лечения людей. В мире сохраняется колоссальный интерес к стволовым клеткам, потому что они открывают путь к терапии многих заболеваний: нейродегенеративных, сердечно-сосудистых, сахарного диабета, повреждений сетчатки глаза, наследственных. Ученые изучают возможность выращивать из стволовых клеток новые зубы, восстанавливать суставы.
Рекламирующие эту процедуру клиники заявляют о том, что приживление в таком случае проходит лучше. Однако аналитики не нашли никаких подтверждений положительного эффекта процедуры — наоборот, указывали на ее возможную опасность.В то же время в систематическом обзоре Кокрейна в 2014 году отмечался положительный эффект в результате лечения травм позвоночника мезенхимальными стволовыми клетками, после которого двигательные функции восстанавливались быстрее. Эти эксперименты в те годы делали исключительно на грызунах и, как показала практика, их результаты применимы для лечения людей. В мире сохраняется колоссальный интерес к стволовым клеткам, потому что они открывают путь к терапии многих заболеваний: нейродегенеративных, сердечно-сосудистых, сахарного диабета, повреждений сетчатки глаза, наследственных. Ученые изучают возможность выращивать из стволовых клеток новые зубы, восстанавливать суставы.
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og. xn--p1ai/awards/
xn--p1ai/awards/
2019
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
Новости
ru-RU
https://ria.ru/docs/about/copyright.html
https://xn--c1acbl2abdlkab1og.xn--p1ai/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
https://cdnn21.img.ria.ru/images/155159/83/1551598383_540:299:2872:2048_1920x0_80_0_0_de241265c1c09412b6d841daeb559217.jpgРИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
РИА Новости
7 495 645-6601
ФГУП МИА «Россия сегодня»
https://xn--c1acbl2abdlkab1og.xn--p1ai/awards/
клетки
МОСКВА, 9 мар — РИА Новости, Татьяна Пичугина. Стволовые клетки исследуют уже больше полувека. Ученые создают их из обычных взрослых клеток, моделируют с их помощью различные болезни, выращивают органоиды для трансплантации. Однако терапевтические методы использования стволовых клеток в большинстве случаев не выходят за рамки лабораторий и клинических испытаний.
Стволовые клетки исследуют уже больше полувека. Ученые создают их из обычных взрослых клеток, моделируют с их помощью различные болезни, выращивают органоиды для трансплантации. Однако терапевтические методы использования стволовых клеток в большинстве случаев не выходят за рамки лабораторий и клинических испытаний.
Клеточные ясли
В конце января мир облетела новость: в Японии после успешных клинических испытаний одобрили лечение травм спинного мозга с помощью стволовых клеток. Учитывая, что еще несколько лет назад этот метод отрабатывали исключительно на лабораторных грызунах, прогресс по медицинским меркам стремительный. До сих пор широко практиковали только одну технологию лечения стволовыми клетками — пересадку костного мозга больным лейкемией.
Стволовые клетки есть у всех растений и животных, включая человека. Это недозрелые структуры, способные превратиться в любой тип специальных клеток: кровеносные тельца, нейроны, клетки кожи, кости, мышцы, зуба. С их помощью ткани организма постоянно в течение жизни обновляются. Например, клетки слизистой кишечника меняются каждую неделю.
С их помощью ткани организма постоянно в течение жизни обновляются. Например, клетки слизистой кишечника меняются каждую неделю.
Стволовые клетки в теории описывали в начале XX века. Впервые предположение об их существовании высказал биолог из Санкт-Петербурга Александр Максимов. Экспериментально это подтвердили в 1960-е годы канадские ученые Эрнест Маккалох и Джеймс Тилл.
Они подвергали мышей смертельной дозе рентгеновского излучения, убивая таким образом систему кроветворения, затем пересаживали им разные типы клеток от здоровых особей. Так исследователи увидели, что крови помогают восстановиться клетки костного мозга, причем, чтобы запустить процесс обновления, достаточно всего одной здоровой клетки, но она должна быть незрелой. Сейчас пересадка костного мозга используется для лечения болезней крови по всему миру.
Божественная глина для организма
Любой многоклеточный организм вырастает из небольшой колонии стволовых клеток. Если ее разделить, к примеру, на две части, то из каждой сформируется полноценный зародыш.
Эмбриональные стволовые клетки могут бесконечно делиться в пробирке. Это свойство используют, чтобы создавать клеточные культуры для лабораторных экспериментов и тестирования будущих лекарств. В отличие от стволовых клеток во взрослом организме, служащих для обновления определенного органа, эмбриональные стволовые клетки способны превратиться в любой тип клеток. За это их стали называть плюрипотентными, то есть клетками с многочисленными возможностями.
Технически можно получить эмбриональные стволовые клетки даже взрослого человека. Для этого нужна донорская яйцеклетка. Из нее удаляют ядро, где хранится ДНК, и помещают туда ядро клетки другого человека. Затем яйцеклетку заставляют делиться и получают эмбрион, развитие которого прекращают на самой ранней стадии. Впервые это продемонстрировал в 2018 году американский генетик Шухрат Миталипов.
Пока эти достижения не имеют практического применения, поскольку опыты с эмбриональными клеточными культурами разрешены исключительно в исследовательских целях.
Омоложение взрослых клеток
Стволовые клетки в сложившемся организме отличаются от эмбриональных тем, что они уже слегка «повзрослели», то есть расположились в каких-либо органах и готовы превращаться в нужный тип ткани. Процесс этот необратим. Если клетка стала, к примеру, эпидермальной клеткой кожи, то обратно стволовой ей не быть.
Так считали до 2006 года, пока японский ученый Синъя Яманака не открыл способ генетического перепрограммирования зрелых (соматических) клеток в стволовые. Из нескольких десятков генов, запускающих развитие эмбриона и впоследствии перестающих работать, он выделил четыре ключевых. Ученый попробовал включить их в зрелых клетках мыши, и это сработало — они приобрели способности незрелых.
Белки, вырабатываемые этими четырьмя генами, — Oct4, Sox2, Klf4 и с-Myc — называют теперь «коктейлем Яманаки». В 2012 году за это достижение ученый удостоился Нобелевской премии.
Открытие Яманаки буквально развязало руки ученым по всему миру и породило волну исследований с этими новообращенными объектами (их называют индуцированными плюрипотентными стволовыми клетками). Биологами овладела идея пересадки плюрипотентных стволовых клеток в любой поврежденный или состарившийся орган, чтобы его восстановить. Однако реальность оказалась сложнее. Подсаженные стволовые клетки не приживались, погибали, вызывали побочные эффекты либо просто не оказывали никакого действия.
Авторы Кокрейновского систематического обзора (эта организация исследует научные доказательства медицинских манипуляций) в 2015 году проанализировали данные о добавлении стволовых к собственным жировым клеткам пациента при трансплантации молочных желез. Рекламирующие эту процедуру клиники заявляют о том, что приживление в таком случае проходит лучше. Однако аналитики не нашли никаких подтверждений положительного эффекта процедуры — наоборот, указывали на ее возможную опасность.В то же время в систематическом обзоре Кокрейна в 2014 году отмечался положительный эффект в результате лечения травм позвоночника мезенхимальными стволовыми клетками, после которого двигательные функции восстанавливались быстрее. Эти эксперименты в те годы делали исключительно на грызунах и, как показала практика, их результаты применимы для лечения людей.В мире сохраняется колоссальный интерес к стволовым клеткам, потому что они открывают путь к терапии многих заболеваний: нейродегенеративных, сердечно-сосудистых, сахарного диабета, повреждений сетчатки глаза, наследственных. Ученые изучают возможность выращивать из стволовых клеток новые зубы, восстанавливать суставы.
Донорство гемопоэтических стволовых клеток — ФГБУ «НМИЦ гематологии» Минздрава России
Ежегодно в России почти 5 000 человек нуждаются в пересадке костного мозга. Ежегодно делается порядка 1,8 тыс. трансплантаций костного мозга, однако потребность в такой медицинской помощи существенно выше и в настоящее время ограничена недостаточным числом доноров костного мозга. В Национальном регистре доноров костного мозга свыше 44 тыс. потенциальных доноров.
Что такое пересадка костного мозга?
Под пересадкой костного мозга понимается на самом деле трансплантация гемопоэтических стволовых клеток. Гемопоэтические (кроветворные) стволовые клетки образуются в костном мозге человека и являются родоначальниками всех клеток крови: лейкоцитов, эритроцитов и тромбоцитов.
Кто нуждается в пересадке костного мозга?
Для многих пациентов с онкологическими и гематологическими заболеваниями единственным шансом сохранить жизнь является пересадка гемопоэтических стволовых клеток. Это может спасти жизнь тысячам детей и взрослых больных раком, лейкозом, лимфомой или наследственными заболеваниями.
Кто может стать донором гемопоэтических клеток?
Любой здоровый гражданин РФ без хронических заболеваний в возрасте от 18 до 45 лет.
Немаловажным фактором для донорства костного мозга является возраст: чем моложе донор, тем выше концентрация гемопоэтических стволовых клеток в трансплантате и их «качество».
Как происходит типирование костного мозга?
Перед донорством гемопоэтических стволовых клеток нужно пройти типирование (определение HLA-генотипа) костного мозга. И если вы подойдете по типу какому-нибудь пациенту, то Вас пригласят на донорство гемопоэтических стволовых клеток.
Для определения HLA-генотипа (типирования) у вас возьмут 1 пробирку крови. Образец крови (до 10 мл — как при обычном анализе крови) человека, желающего стать донором гемопоэтических стволовых клеток, исследуют в специализированной лаборатории.
Информация о результатах типирования доноров, рекрутированных и HLA-типированных в ФГБУ НМИЦ гематологии Минздрава России, вносится в общероссийскую базу доноров — Национальный регистр доноров костного мозга.
Процедура типирования требует от донора лишь немного времени, не требует затрат и не отличается от обычного анализа крови.
Что происходит после внесения данных в регистр?
При появлении пациента, которому необходимо выполнить трансплантацию костного мозга, его данные HLA-генотипа сравнивают с данными потенциальных доноров, имеющихся в регистре. В результате может быть подобран один или несколько «совместимых» доноров. Потенциальному донору сообщают об этом, и он принимает решение, становиться или нет реальным донором. Для потенциального донора вероятность стать донором реальным составляет не более 1%.
Как происходит процедура донации стволовых клеток?
Если же вы подошли по HLA-генотипу какому-нибудь больному и вам предстоит стать донором костного мозга, то не бойтесь! Получение стволовых клеток из периферической крови — простая, комфортная и безопасная для донора процедура.
У донора берут костный мозг одним из двух способов:
- шприцом из тазовой кости (процедура безболезненна под наркозом),
- с помощью медицинского препарата «выгоняют» клетки костного мозга в кровь и собирают их оттуда через периферическую вену.
Данная процедура напоминает аппаратный тромбоцитаферез (процедура донорства тромбоцитов), но более продолжительная по времени.
Донор отдает лишь малую часть своего костного мозга.
Потеря части стволовых клеток донором не ощущается, и их объем полностью восстанавливается в течение 7—10 дней.
5% стволовых клеток донора достаточно для восстановления кроветворения пациента. Пациенту переливают донорский костный мозг, он приживается и начинает производить кровь. Человек спасен!
Гемопоэтические (кроветворные) стволовые клетки, своевременно трансплантированные больному, способны восстановить его кроветворение и иммунитет, а также спасти ему жизнь.
Как стать потенциальным донором гемопоэтических стволовых клеток?
Если вы хотите стать донором ГСК, обратитесь к ведущему специалисту по работе с донорами: 2-й этаж донорского отделения, стойка «Информации для доноров», Александра или Алена.
Сдать пробирку 10 мл крови на определения HLA-генотипа (типирования) вы можете согласно расписанию.
Если в вашей компании готовы пройти типирование более 30 человек, то мы можем организовать к вам выезд. По дополнительным вопросам звоните с 9:00 до 22:00 по телефону: +7 (905) 568-57-60, Александра.
Мы очень ждем вас!
Что такое стволовые клетки? | Стволовые клетки
Что такое стволовые клетки?
Типы стволовых клеток
Почему стволовые клетки важны?
Могут ли врачи использовать стволовые клетки для лечения пациентов?
Плюсы и минусы использования стволовых клеток
Что такое стволовые клетки?
- Стволовые клетки — это неспециализированные клетки, которые еще не «решили», к какому типу взрослых они будут относиться.
- Они могут самообновляться и производить две новые стволовые клетки
- Они могут дифференцироваться, чтобы образовать несколько типов клеток
- В конечном итоге они усиливаются за счет увеличения количества дифференцированных и зрелых клеток
Есть несколько различных типов стволовых клеток, которые производятся и поддерживаются в нашей системе на протяжении всей жизни. В зависимости от обстоятельств и стадий жизненного цикла эти клетки имеют разные свойства и функции. Есть даже стволовые клетки, созданные в лаборатории, которые могут помочь нам узнать больше о том, как стволовые клетки дифференцируются и функционируют.Прежде чем углубляться в детали, следует помнить несколько ключевых моментов о стволовых клетках:
- Стволовые клетки НЕ новы для науки
- Определение относительно простое (см. Выше)
- Стволовые клетки не все одинаковы. Существуют разные типы стволовых клеток:
- Стволовые клетки взрослых (ASC)
- Эмбриональные стволовые клетки (ESC)
- Индуцированные плюрипотентные стволовые клетки (iPS)
- Стволовые клетки важны для гомеостаза (поддержания), восстановления и регенерации тканей
- Некоторые стволовые клетки (взрослые) клинически полезны СЕЙЧАС
- Другие стволовые клетки (ESC, iPS) МОГУТ когда-нибудь быть клинически полезными — уже полезны в фундаментальных исследованиях
- Все типы стволовых клеток важны в исследованиях
- Использование некоторых типов стволовых клеток связано как с этическими, так и с политическими проблемами.UNMC продолжает тесно сотрудничать с федеральными органами и законодательными органами штатов, а также с Международным обществом исследования стволовых клеток (ISSCR), чтобы продвигать ответственные, прозрачные и единообразные методы, соответствующие как федеральным, так и государственным директивам.
Стволовые клетки — это клетки-основы каждого органа и ткани нашего тела. Высокоспециализированные клетки, из которых состоят эти ткани, первоначально произошли из первоначального пула стволовых клеток, сформированного вскоре после оплодотворения. На протяжении всей нашей жизни мы продолжаем полагаться на стволовые клетки для замены поврежденных тканей и клеток, которые теряются каждый день, например клеток нашей кожи, волос, крови и слизистой оболочки кишечника.
Источник ISSCR
История стволовых клеток
До недавнего времени ученые в основном работали с двумя видами стволовых клеток животных и человека: эмбриональными стволовыми клетками и неэмбриональными «соматическими» или «взрослыми» стволовыми клетками. Ученые открыли способы получения эмбриональных стволовых клеток из ранних эмбрионов мыши почти 30 лет назад, в 1981 году. Подробное изучение биологии стволовых клеток мыши привело к открытию в 1998 году метода получения стволовых клеток из человеческих эмбрионов и их выращивания. клетки в лаборатории.Эти клетки называются эмбриональными стволовыми клетками человека. Эмбрионы, использованные в этих исследованиях, были созданы для репродуктивных целей с помощью процедур экстракорпорального оплодотворения. Когда они больше не были нужны для этой цели, они были переданы для исследования с информированного согласия донора. В 2006 году исследователи совершили еще один прорыв, определив условия, которые позволили бы некоторым специализированным взрослым клеткам генетически «перепрограммироваться», чтобы они приняли состояние, подобное стволовым клеткам. Этот новый тип стволовых клеток теперь известен как индуцированные плюрипотентные стволовые клетки (ИПСК).
Источник NIH
Типы стволовых клеток
Стволовые клетки взрослых (ASC):
ASC — это недифференцированные клетки, обитающие в определенных дифференцированных тканях нашего тела, которые могут обновляться или генерировать новые клетки, которые могут восполнять мертвые или поврежденные ткани. Вы также можете встретить термин «соматические стволовые клетки», используемый для обозначения взрослых стволовых клеток. Термин «соматический» относится к непродуктивным клеткам организма (яйцеклеткам или сперматозоидам).ASC, как правило, мало в нативных тканях, что затрудняет их изучение и извлечение для исследовательских целей.
Обитающие в большинстве тканей человеческого тела, дискретные популяции ASC генерируют клетки для замены тех, которые утрачиваются в результате нормального восстановления, болезни или травмы. ASC обнаруживаются на протяжении всей жизни в таких тканях, как пуповина, плацента, костный мозг, мышцы, мозг, жировая ткань, кожа, кишечник и т. Д. Первые ASC были извлечены и использовались для производства крови в 1948 году.Эта процедура была расширена в 1968 году, когда первые взрослые клетки костного мозга были использованы в клинической терапии болезней крови.
Исследования, доказывающие специфику развития ИСС, противоречивы; некоторые показали, что ASC могут генерировать только типы клеток своей резидентной ткани, тогда как другие показали, что ASC могут быть способны генерировать другие типы тканей, чем те, в которых они находятся. Для подтверждения спора необходимы дополнительные исследования.
Типы взрослых стволовых клеток
- Кроветворные стволовые клетки (стволовые клетки крови)
- Мезенхимальные стволовые клетки
- Нервные стволовые клетки
- Эпителиальные стволовые клетки
- Стволовые клетки кожи
Эмбриональные стволовые клетки (ЭСК):
В течение 3-5 дней после оплодотворения и до имплантации эмбрион (на этой стадии, называемый бластоцистой) содержит внутреннюю клеточную массу, способную генерировать все специализированные ткани, составляющие человеческое тело.ESC происходят из внутренней клеточной массы эмбриона, оплодотворенного in vitro и переданного для исследовательских целей после получения информированного согласия. ESC не являются производными яйцеклеток, оплодотворенных в организме женщины.
Эти плюрипотентные стволовые клетки могут стать практически любым типом клеток и обнаруживаются только на первых стадиях развития. Ученые надеются понять, как эти клетки дифференцируются в процессе развития. По мере того, как мы начинаем понимать эти процессы развития, мы можем применять их к стволовым клеткам, выращенным in vitro, и потенциально восстанавливать клетки, такие как нервы, кожа, кишечник, печень и т. Д., Для трансплантации.
Индуцированные плюрипотентные стволовые клетки (ИПСК)
Индуцированные плюрипотентные стволовые клетки — это стволовые клетки, созданные в лаборатории, золотая среда между взрослыми стволовыми клетками и эмбриональными стволовыми клетками. ИПСК создаются путем введения эмбриональных генов в соматическую клетку (например, клетку кожи), что заставляет ее возвращаться в состояние, подобное «стволовым клеткам». Эти клетки, такие как ESC, считаются плюрипотентными. Этот метод генетического перепрограммирования для создания эмбрионоподобных клеток, открытый в 2007 году, является новым и требует еще многих лет исследований, прежде чем его можно будет использовать в клинической терапии.
NIH
Почему стволовые клетки важны?
Стволовые клетки важны для живых организмов по многим причинам. В 3-5-дневном эмбрионе, называемом бластоцистой, внутренние клетки дают начало всему телу организма, включая все многие специализированные типы клеток и органы, такие как сердце, легкие, кожа, сперма, яйца и другие ткани. В некоторых тканях взрослого организма, таких как костный мозг, мышцы и мозг, отдельные популяции взрослых стволовых клеток создают замену клеткам, которые теряются в результате нормального износа, травм или болезней.
Благодаря своей уникальной регенеративной способности стволовые клетки открывают новые возможности для лечения таких заболеваний, как диабет и болезни сердца. Однако в лаборатории и клинике еще предстоит проделать большую работу, чтобы понять, как использовать эти клетки для клеточной терапии для лечения заболеваний, которые также называют регенеративной или репаративной медициной.
Лабораторные исследования стволовых клеток позволяют ученым узнать об основных свойствах клеток и о том, что отличает их от специализированных типов клеток.Ученые уже используют стволовые клетки в лаборатории для проверки новых лекарств и разработки модельных систем для изучения нормального роста и выявления причин врожденных дефектов.
Исследования стволовых клеток продолжают расширять знания о том, как организм развивается из одной клетки и как здоровые клетки заменяют поврежденные клетки во взрослых организмах. Исследование стволовых клеток — одна из самых увлекательных областей современной биологии, но, как и во многих расширяющихся областях научных исследований, исследования стволовых клеток поднимают научные вопросы так же быстро, как и порождают новые открытия.
Источник NIH
Могут ли врачи использовать стволовые клетки для лечения пациентов?
Некоторые стволовые клетки, такие как взрослые стволовые клетки костного мозга или периферической крови, используются в клинической терапии более 40 лет. Другие методы лечения с использованием стволовых клеток включают замену кожи взрослыми стволовыми клетками, собранными из волосяных фолликулов, выращенных в культуре для получения кожных трансплантатов. Другие клинические испытания нейронального повреждения / заболевания также проводились с использованием нервных стволовых клеток.Эти исследования сопровождались побочными эффектами, поэтому необходимы дальнейшие исследования. Хотя в будущем предстоит провести много исследований, эти исследования дают нам надежду на будущее терапии с помощью исследований стволовых клеток.
Возможные методы лечения стволовыми клетками
Лечение взрослых стволовыми клетками
Трансплантаты костного мозга и стволовых клеток периферической крови используются уже более 40 лет для лечения заболеваний крови, таких как лейкемия и лимфома, среди многих других.Ученые также показали, что стволовые клетки находятся в большинстве тканей тела, и исследования продолжают изучать, как идентифицировать, извлекать и размножать эти клетки для дальнейшего использования в терапии. Ученые надеются найти методы лечения таких заболеваний, как диабет I типа, и восстановление сердечной мышцы после сердечного приступа.
Ученые также показали, что перепрограммирование ASC может привести к их трансдифференцировке (обратному превращению в клетки другого типа, нежели резидентная ткань, которую они пополняли).
Лечение эмбриональными стволовыми клетками (ESC)
У ESC есть потенциал для лечения определенных заболеваний в будущем. Ученые продолжают изучать, как дифференцируются ЭСК, и как только этот метод будет лучше понят, можно надеяться на применение этих знаний, чтобы заставить ЭСК дифференцироваться в выбранную клетку, необходимую для терапии пациента. Заболевания, на которые нацелена терапия ESC, включают диабет, травму спинного мозга, мышечную дистрофию, сердечные заболевания и потерю зрения / слуха.
Терапия индуцированными плюрипотентными стволовыми клетками
Терапия с использованием ИПСК интересна тем, что соматические клетки реципиента могут быть перепрограммированы в состояние, подобное ESC. Затем механизмы дифференциации этих клеток могут быть применены для создания необходимых клеток. Это привлекательно для клиницистов, потому что это позволяет избежать проблемы гистосовместимости и пожизненной иммуносупрессии, которая необходима, если трансплантаты используют донорские стволовые клетки.
iPS-клетки имитируют большинство свойств ESC в том смысле, что они являются плюрипотентными клетками, но в настоящее время не несут этического багажа исследований и использования ESC, поскольку iPS-клетки не могут быть изменены для роста внешнего слоя эмбриональной клетки, необходимого для развития. клетки в человека.
Плюсы и минусы использования различных стволовых клеток
- Можно использовать обильные соматические клетки донора
- Проблем гистосовместимости с трансплантатами донора / реципиента можно избежать
- Очень полезно для разработки лекарств и исследований развития
| Стволовые клетки взрослых | Эмбриональные стволовые клетки | Индуцированные плюрипотентные стволовые клетки | |
| Плюсы |
|
|
|
| Минусы |
|
|
|
| Этические проблемы |
|
|
|
Что это такое и как они работают?
Стволовые клетки: что это такое и как они работают?Что такое стволовые клетки и как они работают?
Есть три типа стволовых клеток.У каждого из них есть потенциал для медицинских исследований и клинического применения, основанный на его уникальных свойствах.
Питер Хоуи, Special To The Chronicle
Стволовые клетки — это строительные блоки человеческого тела. В начале жизни они снова и снова делятся, чтобы из зародыша создать полноценного человека. С возрастом они пополняют клетки нашей крови, костей, кожи и органов. Стволовые клетки могут быть мощным инструментом при лечении травм и болезней.
Эмбриональные стволовые клетки
Первые клетки, которые образуются после того, как сперматозоид оплодотворяет яйцеклетку.
Клетки «с чистого листа»: могут стать клетками любого другого типа в организме.
Можно бесконечно делить и умножать.
Противоречиво в медицине, потому что для получения стволовых клеток необходимо уничтожить эмбрионы.
Стволовые клетки для взрослых
Зрелые стволовые клетки, пополняющие кровь, кожу, кишечник и некоторые другие клетки.
В некоторых случаях может заменить клетки, поврежденные в результате болезни или травмы.
Ограниченная возможность стать другими типами ячеек.
Ограниченная способность делить и умножать.
Индуцированные плюрипотентные стволовые клетки
Взрослые клетки, которые перепрограммированы, чтобы выглядеть и действовать как эмбриональные стволовые клетки.
Может быть получен из кожи, крови и других взрослых клеток.
Из своего эмбрионоподобного состояния может быть далее изменен, чтобы стать любым другим типом клетки.
Хороший потенциал для использования в медицине, но все же новая область исследований.
Эмбриональный
Какие они?
Эмбриональные стволовые клетки — это стартовые клетки человеческого тела. Они недифференцированные, что означает, что они не созрели и не специализировались, и они могут стать клеткой любого другого типа в теле.
У эмбрионов эти клетки размножаются и дифференцируются, превращаясь в органы, кости и мышцы.В лаборатории их можно размножать для создания линий стволовых клеток для изучения или лечения.
Ученые собирают эмбриональные стволовые клетки из трех-пятидневных эмбрионов, пожертвованных людьми, прошедшими экстракорпоральное оплодотворение. Ученые выделили первые эмбриональные стволовые клетки человека в 1998 году.
Чем они отличаются от других стволовых клеток?
Это единственные стволовые клетки, которые естественным образом способны превращаться в клетки любого другого типа и бесконечно размножаться.При определенных обстоятельствах в лаборатории их можно подтолкнуть к превращению в клетки определенного типа.
Почему эти характеристики придают этим клеткам лечебный потенциал?
Из-за их способности дифференцироваться и размножаться, эмбриональные стволовые клетки долгое время считались самыми мощными и, следовательно, имели наибольший потенциал для лечения травм и болезней. Если ученые смогут контролировать, как они дифференцируются и как часто, эмбриональные стволовые клетки можно было бы использовать для замены любой поврежденной части тела — от недостающих инсулино-продуцирующих клеток у людей с диабетом 1 типа до клеток мозга, потерянных при болезни Паркинсона или клеток кожи. рубцы от ожогов.
Каковы ограничения этих методов лечения?
Многие люди имеют этические проблемы, используя человеческие эмбрионы для научных исследований. Кроме того, способность эмбриональных стволовых клеток к бесконечной репликации означает, что у них могут развиваться мутации, которые могут мешать их росту или позволять им продолжать делиться до такой степени, что они могут причинить вред. Найти подходящее медицинское применение для эмбриональных стволовых клеток непросто.
Взрослый
Какие они?
Взрослые стволовые клетки названы так потому, что они более зрелые, чем эмбриональные стволовые клетки, хотя они не обязательно должны происходить от взрослых.Их зрелость означает, что они ограничены в способности различать. Карманы взрослых стволовых клеток находятся во многих наших органах, и они пополняют запасы клеток в органах, в которых они находятся. Типы взрослых стволовых клеток включают:
Кроветворная
Обнаруженные в костном мозге и пуповинной крови, они становятся кровью и иммунными клетками. Это единственные стволовые клетки, одобренные FDA для лечения некоторых видов рака крови.
Мезенхимальный
Эти клетки встречаются по всему телу, в том числе в костном мозге, жировой ткани и органах. Они превращаются в соединительную ткань по всему телу, хотя конкретная клетка, в которую они превращаются, связана с органом, в котором они расположены. Эти стволовые клетки могут уменьшить воспаление.
Плод
Стволовые клетки плодов более зрелые и, следовательно, менее способны к дифференцировке, чем эмбриональные стволовые клетки, но они могут быть более универсальными, чем другие взрослые стволовые клетки.Например, нервные стволовые клетки из ткани мозга плода могут стать несколькими видами нейронов, но нервные стволовые клетки из мозга взрослого человека встречаются редко и имеют очень ограниченную способность к дифференцировке.
Чем они отличаются от других стволовых клеток?
Взрослые стволовые клетки ограничены в своих возможностях. Они могут стать только определенными типами клеток — по этой причине их называют мультипотентными, а не плюрипотентными — и есть предел тому, как часто они могут делиться.
Почему эти характеристики придают этим клеткам лечебный потенциал?
Взрослые стволовые клетки менее мощны, чем эмбриональные, но их проще использовать, поскольку у всех людей есть собственные запасы этих клеток. Они могут быть полезны для уменьшения воспаления.
Каковы ограничения этих методов лечения?
Неясно, насколько полезны эти стволовые клетки, учитывая их ограниченные возможности.Хотя идея подключиться к собственному источнику взрослых стволовых клеток человека и использовать их для лечения привлекательна, эти клетки не могут исправить серьезные повреждения или заменить клетки, утраченные в результате болезни, такие как нейроны или клетки, продуцирующие инсулин.
Индуцированный плюрипотент
Какие они?
Индуцированные плюрипотентные стволовые клетки (IPS) — это взрослые клетки, часто клетки кожи или крови, которые были взяты у человека и перепрограммированы в лаборатории, чтобы стать подобными эмбриональным стволовым клеткам.Затем, как и эмбриональные стволовые клетки, они могут быть преобразованы в клетки любого другого типа. Таким образом, клетка кожи может быть превращена в клетку, подобную эмбриону, а затем превращена в клетку сердца.
Чем они отличаются от других стволовых клеток?
Как эмбриональные стволовые клетки, за исключением того, что они производятся в лаборатории. И поскольку они исходят от человека, они точно соответствуют этому человеку. Ученые все еще изучают, можно ли использовать клетки IPS взаимозаменяемо с эмбриональными стволовыми клетками.
Почему эти характеристики придают этим клеткам лечебный потенциал?
Их можно использовать для замены типов клеток, потерянных в результате болезни или травмы. Кроме того, клетки IPS можно использовать для изучения болезней человека в чашках Петри или на животных. Ученые могут взять клетки кожи у человека с генетической мутацией, преобразовать эти клетки в клетки IPS, а затем изучить эти клетки как живую модель функционирования мутации.
Каковы ограничения этих методов лечения?
Создание ячеек IPS может занять много времени и ресурсов.Но в большинстве случаев IPS-клетки имеют те же ограничения, что и эмбриональные стволовые клетки.
трансплантатов стволовых клеток (для родителей)
Что такое трансплантация стволовых клеток?
Трансплантация стволовых клеток — это когда врачи вводят здоровые стволовые клетки в кровоток, чтобы заменить их стволовые клетки.
Чтобы почувствовать себя лучше после трансплантации стволовых клеток, может потребоваться время, но лечение может быть очень полезным при некоторых заболеваниях.
Что такое стволовые клетки?
Стволовые клетки — это клетки, которые могут развиваться во множество различных типов клеток. Стволовые клетки, используемые для трансплантации, образуют клетки крови. Их стало:
- красных кровяных телец , переносящих кислород
- лейкоциты , борющиеся с инфекцией
- тромбоцитов , способствующих свертыванию крови
Почему делают трансплантацию стволовых клеток?
Пересадка стволовых клеток может помочь людям с:
Откуда берутся стволовые клетки?
Доктора могут получить стволовые клетки от:
- костный мозг (это также называется трансплантатом костного мозга )
- кровоток
- Пуповинная кровь после того, как пуповина больше не прикреплена к новорожденному ребенку
Человек, который предоставляет стволовые клетки, является донором .При некоторых заболеваниях донорами могут быть сами люди. Их стволовые клетки извлекаются, замораживаются и позже пересаживаются. В других случаях стволовые клетки жертвует кто-то другой.
Когда стволовые клетки поступают от другого человека, стволовые клетки должны иметь похожий генетический состав. Обычно брат или сестра ребенка — хорошая пара. Родители или даже посторонние люди иногда могут подойти друг другу.
Что может случиться, если донор не подходит?
Если донорские стволовые клетки не подходят (а иногда и подходят):
- Иммунная система организма может атаковать донорские стволовые клетки.Это называется отклонением .
- Пересаженные клетки могут атаковать клетки организма. Это называется болезнь трансплантат против хозяина .
Как делается трансплантация стволовых клеток?
Перед трансплантацией стволовых клеток врачи устанавливают центральную линию (или центральный венозный катетер). Этот тип внутривенного (внутривенного) введения проходит через кожу и в крупную вену около сердца. Центральная линия может оставаться в организме дольше, чем обычная капельница. Это дает медицинской бригаде возможность давать лекарства и собирать кровь для анализа, не уколовшись иглой.
В больнице делают трансплантацию стволовых клеток. Во-первых, человек, получающий донорские стволовые клетки, получает высокие дозы химиотерапии и / или облучения до:
- убить нездоровые клетки, вызывающие болезнь
- ослабляют их иммунную систему, поэтому она не отторгает донорские стволовые клетки
Затем человек получает донорские стволовые клетки через внутривенную линию (IV).
Что происходит после трансплантации?
После трансплантации стволовых клеток организму нужно время, чтобы вырабатывать новые эритроциты, лейкоциты и тромбоциты.В это время они подвергаются более высокому риску инфекций, кровотечений и других проблем.
Большинство людей остаются в больнице в течение 3-5 недель после трансплантации. Их медицинская бригада:
- Сделайте анализы крови, чтобы увидеть, производят ли пересаженные стволовые клетки новые клетки крови.
- Дайте лекарства, которые помогут предотвратить отторжение и болезнь «трансплантат против хозяина».
- Дать лекарства от инфекций.
- Сделайте переливание эритроцитов, лейкоцитов и тромбоцитов.
- Убедитесь, что органы (например, печень и почки) работают правильно.
- Лечит любые возникающие проблемы, такие как язвы во рту, рвота, диарея, инфекции, кровотечение, отторжение и реакция «трансплантат против хозяина».
- Убедитесь, что пациент получает полноценное питание.
- Убедитесь, что все посетители соблюдают правила профилактики инфекций, которые включают:
- Заболевших посетителей нет.
- Все посетители должны вымыть руки перед входом в комнату.
- Все посетители должны быть в маске, перчатках и халате.
Чем могут помочь родители?
Иммунной системе ребенка требуется около года на восстановление после трансплантации стволовых клеток. А пока дети могут сильно заболеть от инфекций. Даже легкая инфекция, например простуда, может быть серьезной. Чтобы помочь ребенку избежать инфекций:
- Ваш ребенок, члены семьи и посетители должны хорошо мыть руки и часто с антибактериальным мылом и / или дезинфицирующим средством для рук.
- Не подпускайте к ребенку больных людей.
- Ваш ребенок должен купаться каждый день с мягким шампунем и мылом.
Следуйте инструкциям вашей медицинской бригады для:
- когда ваш ребенок может ходить в школу или другие общественные места
- когда ребенку нужно надеть маску
- какие продукты подходят для вашего ребенка
- , если ваш ребенок может находиться рядом с домашними животными
Что еще я должен знать?
Большинство детей, перенесших трансплантацию стволовых клеток, после выписки из больницы со временем чувствуют себя лучше.Ребенку и семье приходится очень много управлять пребыванием в больнице и периодом выздоровления. Найдите поддержку у других членов семьи, у вашей медицинской бригады, консультанта или социального работника. Забота о себе поможет вам позаботиться о своем ребенке.
Чтобы помочь вашему ребенку выздороветь и остаться здоровым:
- Возьмите ребенка на все последующие визиты к врачу.
- Поддержите своего ребенка во время физических изменений, которые могут произойти (например, выпадения волос и усталости от химиотерапии и / или облучения).
- Помогите своему ребенку справиться с одиночеством вдали от друзей и семьи во время выздоровления. Помогите настроить Skype, Google Hangouts или FaceTime, чтобы ваш ребенок мог оставаться на связи.
- Спросите, хочет ли ваш ребенок поговорить с психологом или социальным работником, чтобы помочь справиться с чувствами, которые могут возникнуть во время выздоровления.
- Помогите своему ребенку выработать простой распорядок дня, состоящий из легких упражнений, еды и таких занятий, как игры или чтение.
Когда мне звонить врачу?
Немедленно позвоните своему врачу, если ваш ребенок:
- имеет лихорадку 100.4 ° F (38,0 ° C) или выше при приеме внутрь (во рту)
- насморк, кашель или заложенность носа
- рвота или диарея
- имеет черный стул (какашки)
- имеет легкие синяки или кровотечения
- кровь в мочу
- имеет головную боль, головокружение или помутнение зрения
- кашляет кровью или у него кровотечение из носа, которое не прекращается через несколько минут
Стволовые клетки: прошлое, настоящее и будущее | Исследование стволовых клеток и терапия
Сукоян М.А., Ватолин С.Ю., и др. Эмбриональные стволовые клетки, полученные из морул, внутренней клеточной массы и бластоцист норки: сравнение их плюрипотентности. Embryo Dev. 1993; 36 (2): 148–58
Лариджани Б., Исфахани Э. Н., Амини П., Никбин Б., Алимогаддам К., Амири С., Малекзаде Р., Язди Н. М., Годси М., Довлати И., Сахрайан М. А., Гавамзаде. А. Терапия стволовыми клетками в лечении различных заболеваний. Acta Medica Iranica. 2012: 79–96 https://www.ncbi.nlm.nih.gov/pubmed/22359076.
Салливан С., Стейси Г. Н., Акадзава С. и др. Руководство по качеству индуцированных человеком линий плюрипотентных стволовых клеток клинического уровня. Regenerative Med. 2018; https://doi.org/10.2217/rme-2018-0095.
А, К., Эндрюс П.В. и др. Скрининг этнически разнообразных эмбриональных стволовых клеток человека позволяет выявить минимальный ампликон 20 хромосомы, обеспечивающий преимущество в росте. Nat. Biotechnol. 2011; 29 (12): 1121–44.
Google ученый
Амит М., Ицковиц-Элдор Дж. Атлас плюрипотентных стволовых клеток человека: получение и культивирование. Нью-Йорк: Humana Press; 2012.
Google ученый
Людвиг Т.Э., Бергендаль В., Левенштейн М.Э., Ю. Дж., Пробаско М.Д., Томсон Дж. А.. Корм-независимая культура эмбриональных стволовых клеток человека. Нат методы. 2006; 3: 637–46.
CAS PubMed Google ученый
Канг Мичиган.Переходное метилирование CpG между промоторами и ретроэлементами тканеспецифичных генов во время дифференцировки мезенхимальных клеток человека. J. Cell Biochem. 2007. 102: 224–39.
CAS PubMed Google ученый
Ваес Б., Крейе Д., Пинкстерен Дж. Контроль качества при производстве терапевтического препарата на основе стволовых клеток. BioProcess Int. 2012; 10: 50–5.
Bloushtain-Qimron N. Эпигенетические паттерны эмбриональных и взрослых стволовых клеток.Клеточный цикл. 2009; 8: 809–17.
CAS PubMed Google ученый
Бриндли Д.А. Пиковая сыворотка: последствия поставок сыворотки для производства клеточной терапии. Регенеративная медицина. 2012; 7: 809–17.
Google ученый
Солтер Д., Ноулз ББ. Иммунохирургия бластоцисты мыши. Proc Natl Acad Sci U S. A. 1975; 72: 5099–102.
CAS PubMed PubMed Central Google ученый
Hoepfl G, Gassmann M, Desbaillets I. Дифференциация эмбриональных стволовых клеток в эмбриональные тельца. Методы Mole Biol. 2004; 254: 79–98 https://doi.org/10.1385/1-59259-741-6:079.
Google ученый
Лим В.Ф., Иноуэ-Йоку Т., Тан К.С., Лай М.И., Сугияма Д. Дифференцировка гемопоэтических клеток из эмбриональных и индуцированных плюрипотентных стволовых клеток. Stem Cell Res Ther. 2013; 4 (3): 71. https://doi.org/10.1186/scrt222.
CAS Статья PubMed PubMed Central Google ученый
Mohr JC, de Pablo JJ, Palecek SP. Трехмерная микропланшетная культура эмбриональных стволовых клеток человека. Биоматериалы. 2006. 27 (36): 6032–42. https://doi.org/10.1016/j.biomaterials.2006.07.012.
CAS Статья PubMed Google ученый
Doetschman TC, Eistetter H, Katz M, Schmidt W., Kemler R. Развитие in vitro линий эмбриональных стволовых клеток, полученных из бластоцисты: формирование висцерального желточного мешка, островков крови и миокарда.J Embryol Exp Morphol. 1985; 87: 27–45.
CAS PubMed Google ученый
Куросава HY. Методы индукции образования эмбриоидного тела: система дифференцировки эмбриональных стволовых клеток in vitro. J Biosci Bioeng. 2007; 103: 389–98.
Heins N, Englund MC, Sjoblom C, Dahl U, Tonning A, Bergh C, Lindahl A, Hanson C, Semb H. Получение, характеристика и дифференциация эмбриональных стволовых клеток человека.Стволовые клетки. 2004. 22: 367–76.
Rosowski KA, Mertz AF, Norcross S, Dufresne ER, Horsley V. Края колоний человеческих эмбриональных стволовых клеток демонстрируют различные механические свойства и потенциал дифференцировки. Sci Rep.2015; 5: Номер статьи: 14218.
PubMed Google ученый
Chung Y, Klimanskaya I, Becker S, Li T, Maserati M, Lu SJ, Zdravkovic T., Ilic D, Genbacev O, Fisher S, Krtolica A, Lanza R.Линии эмбриональных стволовых клеток человека, полученные без разрушения эмбриона. Стволовая клетка клетки. 2008; 2: 113–7.
CAS PubMed Google ученый
Чжан X, Стойкович П., Пржиборски С., Кук М., Армстронг Л., Лако М., Стойкович М. Получение человеческих эмбриональных стволовых клеток из развивающихся и задержанных эмбрионов. Стволовые клетки. 2006; 24: 2669–76.
CAS PubMed Google ученый
Бирс Дж., Галбрансон Д. Р., Джордж Н., Синискальчи Л. И., Джонс Дж., Томсон Дж. А., Чен Г. Пассирование и расширение колоний плюрипотентных стволовых клеток человека путем безферментной диссоциации в химически определенных условиях культивирования. Nat Protoc. 2012; 7: 2029–40.
CAS PubMed PubMed Central Google ученый
Эллерстрём К., Хилльнер Дж., Штрел Р. ферментативная диссоциация единичных клеток человеческих эмбриональных стволовых клеток: простой, надежный и стандартизованный метод культивирования.В: Турксен К., редактор. Протоколы эмбриональных стволовых клеток человека. Методы молекулярной биологии: Humana Press; 2009. с. 584.
Heng BC, Liu H, Ge Z, Cao T. Механическая диссоциация колоний человеческих эмбриональных стволовых клеток путем ручного соскоба после обработки коллагеназой гораздо более вредна для жизнеспособности клеток, чем трипсинизация с осторожным пипетированием. Biotechnol Appl Biochem. 2010. 47 (1): 33–7.
Google ученый
Ellerstrom C, Strehl R, Noaksson K, Hyllner J, Semb H. Облегченная экспансия эмбриональных стволовых клеток человека путем ферментативной диссоциации одной клетки. Стволовые клетки. 2007. 25: 1690–6.
PubMed Google ученый
Бримл С.Н., Цзэн Х, Вейлер Д.А., Ло И, Лю И, Лион И.Г., Фрид В.Дж., Робинс А.Дж., Рао М.С., Шульц Т.С. Кариотипическая стабильность, генотипирование, дифференциация, поддержание без кормления и выборка экспрессии генов в трех линиях эмбриональных стволовых клеток человека deri.Stem Cells Dev. 2004. 13: 585–97.
CAS PubMed Google ученый
Watanabe K, Ueno M, Kamiya D, Nishiyama A, Matsumura M, Wataya T, Takahashi JB, Nishikawa S, Nishikawa S, Muguruma K, Sasai Y. Ингибитор ROCK позволяет выжить диссоциированным эмбриональным стволовым клеткам человека . Nat Biotechnol. 2007. 25: 681–6.
CAS PubMed Google ученый
Nie Y, Walsh P, Clarke DL, Rowley JA, Fellner T.Масштабируемое пассирование прикрепленных плюрипотентных стволовых клеток человека. 2014. https://doi.org/10.1371/journal.pone.0088012.
Томсон Дж., Ицковиц-Элдор Дж, Шапиро С.С., Вакниц Массачусетс, Свиергил Дж. Дж., Маршалл В.С., Джонс Дж. М.. Линии эмбриональных стволовых клеток, полученные из бластоцист человека. Наука. 1998. 282: 1145–7.
CAS PubMed Google ученый
Мартин М.Дж., Муотри А., Гейдж Ф., Варки А. Эмбриональные стволовые клетки человека экспрессируют иммуногенную сиаловую кислоту, отличную от человека.Nat. Med. 2005; 11: 228–32.
CAS PubMed Google ученый
Smith AG, Heath JK, Donaldson DD, Wong GG, Moreau J, Stahl M, Rogers D. Ингибирование плюрипотенциальной дифференцировки эмбриональных стволовых клеток очищенными полипептидами. Природа. 1988. 336 (6200): 688–90. https://doi.org/10.1038/336688a0.
CAS Статья PubMed Google ученый
Сюй Ц., Инокума М.С., Денхам Дж., Голдс К., Кунду П., Голд ДжейДи, Карпентер М.К.Рост недифференцированных эмбриональных стволовых клеток человека без кормления. Nature Biotechnol. 2001; 19: 971–4. https://doi.org/10.1038/nbt1001-971.
CAS Статья Google ученый
Weathersbee PS, Pool TB, Ord T. Синтетический заменитель сыворотки (SSS): протеиновая добавка, обогащенная глобулином, для культивирования человеческого эмбриона. J. Assist Reprod Genet. 1995; 12: 354–60.
CAS PubMed Google ученый
Chen G, Gulbranson DR, Hou Z, Bolin JM, Ruotti V, Probasco MD, Smuga-Otto K, Howden SE, Diol NR, Propson NE, Wagner R, Lee GO, Antosiewicz-Bourget J, Teng JM, Thomson JA. Химически определенные условия для получения и культивирования ИПСК человека. Nat. Методы. 2011; 8: 424–9.
CAS PubMed PubMed Central Google ученый
Соммер С.А., Мостославский Г. Экспериментальные подходы к созданию индуцированных плюрипотентных стволовых клеток.Stem Cell Res Ther. 2010; 1:26.
PubMed PubMed Central Google ученый
Такахаши К., Яманака С. Индуцированные плюрипотентные стволовые клетки в медицине и биологии. Разработка. 2013; 140 (12): 2457–61 https://doi.org/10.1242/dev.0.
CAS PubMed Google ученый
Shi D, Lu F, Wei Y, et al. Буйволов ( Bubalus bubalis ) клонировали путем переноса ядра соматических клеток.Биол. Репрод. 2007; 77: 285–91. https://doi.org/10.1095/biolreprod.107.060210.
CAS Статья PubMed Google ученый
Gurdon JB. Способность к развитию ядер, взятых из клеток кишечного эпителия кормящихся головастиков. Разработка. 1962; 10: 622–40 http://dev.biologies.org/content/10/4/622.
CAS Google ученый
Каин К.Рождение клонирования: интервью с Джоном Гардоном. Dis Model Mech. 2009. 2 (1–2): 9–10. https://doi.org/10.1242/dmm.002014.
Артикул PubMed Central Google ученый
Дэвис Р.Л., Вайнтрауб Х., Лассар А.Б. Экспрессия одной трансфицированной кДНК превращает фибробласты в миобласты. Клетка. 1987. 24 (51 (6)): 987–1000.
Google ученый
Quinlan AR, Boland MJ, Leibowitz ML, et al.Секвенирование генома индуцированных мышами плюрипотентных стволовых клеток выявляет стабильность ретроэлементов и редкую реаранжировку ДНК во время репрограммирования. Стволовая клетка клетки. 2011; 9 (4): 366–73.
CAS PubMed PubMed Central Google ученый
Maherali N, Sridharan R, Xie W, Utika LJ, Eminli S, Arnold K, Stadtfeld M, Yachechko R, Tchieu J, Jaenisch R, Plath K, Hochedlinger K. Непосредственно перепрограммированные фибробласты демонстрируют глобальные эпигенетические ремоделирования. широко распространенный вклад тканей.Стволовая клетка клетки. 2007; 1: 55–70.
CAS PubMed Google ученый
Ohi Y, Qin H, Hong C, Blouin L, Polo JM, Guo T, Qi Z, Downey SL, Manos PD, Rossi DJ, Yu J, Hebrok M, Hochedlinger K, Costello JF, Song JS , Ramalho-Santos M. Неполное метилирование ДНК подчеркивает транскрипционную память соматических клеток в IPS-клетках человека. Nat Cell Biol. 2011; 13: 541–9.
CAS PubMed PubMed Central Google ученый
Чжоу К., Браун Дж., Канарек А., Раджагопал Дж., Мелтон Д.А. Перепрограммирование экзокринных клеток поджелудочной железы в бета-клетки in vivo. Природа. 2008; 455: 627–32 https://doi.org/10.1038/nature07314.
CAS PubMed Google ученый
Hilfiker A, Kasper C, Hass R, Haverich A. Мезенхимальные стволовые клетки и клетки-предшественники в инженерии соединительной ткани и регенеративной медицине: есть ли будущее у трансплантации? Langenbecks Arch Surg.2011; 396: 489–97.
PubMed Google ученый
Чжан Венди, Ю., де Алмейда Патрисия, Э. и Ву Джозеф, К. Формирование тератомы: инструмент для мониторинга плюрипотентности в исследованиях стволовых клеток. StemBook, изд. Сообщество исследователей стволовых клеток . 12 июня 2012 г. https://doi.org/10.3824/stembook.1.53.1.
Narsinh KH, Sun N, Sanchez-Freire V, et al. Профили транскрипции отдельных клеток выявляют гетерогенность индуцированных человеком плюрипотентных стволовых клеток.J Clin Invest. 2011; 121 (3): 1217–21.
CAS PubMed PubMed Central Google ученый
Гертов К., Пржиборски С., Лоринг Дж. Ф., Ауэрбах Дж. М., Эпифано О., Отонкоски Т., Дамьянов И., Арлунд Рихтер Л. Выделение тератом, полученных из эмбриональных стволовых клеток человека, для оценки плюрипотентности. Curr Protoc Stem Cell Biol . 2007, Глава 1, Раздел 1B 4. 3: 1B.4.1-1B.4.29.
Кук М.Дж., Стойкович М., Пржиборски С.А.На рост тератом, происходящих из плюрипотентных стволовых клеток человека, влияет место трансплантата. Stem Cells Dev. 2006; 15 (2): 254–9.
CAS PubMed Google ученый
Пржиборски С.А. Дифференциация эмбриональных стволовых клеток человека после трансплантации иммунодефицитным мышам. Стволовые клетки. 2005; 23: 1242–50.
PubMed Google ученый
Tannenbaum SE, Turetsky TT, Singer O, Aizenman E, Kirshberg S, Ilouz N, Gil Y, Berman-Zaken Y, Perlman TS, Geva N, Levy O, Arbell D, Simon A, Ben-Meir А, Шуфаро Ю., Лауфер Н., Рубинов Б.Е.Получение не содержащих ксено и отвечающих требованиям GMP эмбриональных стволовых клеток человека — платформы для будущих клинических применений. PLoS One. 2012; 7: e35325.
CAS PubMed PubMed Central Google ученый
Коэн Д.Е., Мелтон Д. Превращение соломы в золото: определение судьбы клеток для регенеративной медицины. Nat Rev Genet. 2011; 12: 243–52.
CAS PubMed Google ученый
Hwang NS, Varghese S, Elisseeff J. Контролируемая дифференцировка стволовых клеток. Adv Drug Deliv Rev.2007; 60 (2): 199–214. https://doi.org/10.1016/j.addr.2007.08.036.
CAS Статья PubMed PubMed Central Google ученый
Тернер Н., Гроуз Р. Передача сигналов фактора роста фибробластов: от развития до рака. Нат Рев Рак. 2010; 10: 116–29.
CAS PubMed Google ученый
Rao TP, Kuhl M. Обновленный обзор сигнальных путей Wnt: прелюдия к большему. Circ Res. 2010; 106: 1798–806.
CAS PubMed Google ученый
Moustakas A, Heldin CH. Регулирование передачи сигнала TGFbeta. Разработка. 2009; 136: 3699–714.
CAS PubMed Google ученый
Efthymiou AG, Chen G, Rao M, Chen G, Boehm M.Стратегии самообновления и дифференциации клеточных клонов в человеческих эмбриональных стволовых клетках и индуцированных плюрипотентных стволовых клетках. Экспертное мнение Biol Ther. 2014; 14: 1333–44.
PubMed Google ученый
Ян Л., Сунпаа М.Х., Адлер Э.Д., Роепке Т.К., Каттман С.Дж., Кеннеди М., Хенкертс Э., Бонэм К., Эбботт Г.В., Линден Р.М., Филд Л.Дж., Келлер Г.М. Клетки-предшественники сердечно-сосудистой системы человека развиваются из популяции, полученной из эмбриональных стволовых клеток KDR. Природа.2008; 453: 524–8.
CAS PubMed Google ученый
Крон Э., Мартинсон Л.А., Кадоя К., Банг А.Г., Келли О.Г., Элиазер С., Янг Х., Ричардсон М., Смарт Н.Г., Каннингем Дж., Агульник А.Д., Д’амур К.А., Карпентер М.К., Баетге Э. Энтодерма поджелудочной железы, полученная из эмбриональных стволовых клеток человека, генерирует инсулин-секретирующие клетки, чувствительные к глюкозе, in vivo. Nat Biotechnol. 2008. 26 (4): 443–52. https://doi.org/10.1038/nbt1393.
CAS Статья PubMed Google ученый
Валлиер Л., Рейнольдс Д., Педерсен Р.А. Nodal подавляет дифференцировку эмбриональных стволовых клеток человека по нейроэктодермальному пути по умолчанию. Dev Biol. 2004. 275: 403–21.
CAS PubMed Google ученый
Burridge PW, Zambidis ET. Высокоэффективная направленная дифференцировка индуцированных человеком плюрипотентных стволовых клеток в кардиомиоциты. Методы Мол биол. 2013; 997: 149–61.
CAS PubMed Google ученый
Cai J, Zhao Y, Liu Y, Ye F, Song Z, Qin H, Meng S, Chen Y, Zhou R, Song X, Guo Y, Ding M, Deng H. Направленная дифференцировка эмбриональных стволовых клеток человека в функциональные печеночные клетки. клетки. Гепатология. 2007. 45: 1229–39.
CAS PubMed Google ученый
Takasato M, Er PX, Becroft M, Vanslambrouck JM, Stanley EG, Elefanty AG, Little MH. Направление дифференцировки человеческих эмбриональных стволовых клеток к почечной линии порождает самоорганизующиеся почки.Nat Cell Biol. 2014; 16: 118–26.
CAS PubMed Google ученый
Хуанг С.Х., Ислам Миннесота, О’Нил Дж., Ху З., Ян Ю.Г., Чен Ю.В., Мумау М., Грин, доктор медицинских наук, Вунджак Новакович, Г., Бхаттачарья, Дж., Снок, Х.В. Эффективное создание эпителиальных клеток легких и дыхательных путей из плюрипотентных стволовых клеток человека. Nat Biotechnol. 2014; 32: 84–91.
CAS PubMed Google ученый
Кадзик Р.С., Морриси Э.Е. Направление дифференцировки энтодермы легкого в плюрипотентные стволовые клетки. Стволовая клетка клетки. 2012; 10: 355–61.
CAS PubMed PubMed Central Google ученый
Wichterle H, Lieberam I, Porter JA, Jessell TM. Направленная дифференцировка эмбриональных стволовых клеток в двигательные нейроны. Клетка. 2002; 110: 385–97.
CAS PubMed Google ученый
Спенс Дж. Р., Мэйхью С. Н., Рэнкин С. А., Кухар М. Ф., Валланс Дж. Э., Толле К., Хоскинс Е. Е., Калиниченко В. В., Уэллс С. И., Цорн А. М., Шройер Н. Ф., Уэллс Дж. М.. Направленная дифференцировка плюрипотентных стволовых клеток человека в ткань кишечника in vitro. Природа. 2011; 470: 105–9.
PubMed Google ученый
Oldershaw RA, Baxter MA, Lowe ET, Bates N, Grady LM, Soncin F, Brison DR, Hardingham TE, Kimber SJ. Направленная дифференцировка эмбриональных стволовых клеток человека в направлении хондроцитов.Nat Biotechnol. 2010; 28: 1187–94.
CAS PubMed Google ученый
Джун Кай, Энн ДеЛаФорест, Джозеф Фишер, Аманда Урик, Томас Вагнер, Кирк Твароски, Макс Кайо, Масато Нагаока, Стивен А. Дункан. Протокол направленной дифференцировки плюрипотентных стволовых клеток человека в зависимости от судьбы гепатоцитов. 2012. DOI: https://doi.org/10.3824/stembook.1.52.1.
Франк-Каменецкий M, Zhang XM, Bottega S, Guicherit O, Wichterle H, Dudek H, Bumcrot D, Wang FY, Jones S, Shulok J, Rubin LL, Porter JA.Модуляторы низкомолекулярных сигналов hedgehog: идентификация и характеристика сглаженных агонистов и антагонистов. J Biol. 2002; 1: 10.
PubMed PubMed Central Google ученый
Осима К., Шин К., Динстхубер М., Пенг А.В., Риччи А.Дж., Хеллер С. Механочувствительные волосковые клетки из эмбриональных и индуцированных плюрипотентных стволовых клеток. Клетка. 2010; 141: 704–16.
CAS PubMed PubMed Central Google ученый
Осакада Ф., Джин З. Б., Хирами Й., Икеда Х., Данджио Т., Ватанабе К., Сасай Й., Такахаши М. Дифференциация клеток сетчатки in vitro из плюрипотентных стволовых клеток человека с помощью низкомолекулярной индукции. J Cell Sci. 2009; 122: 3169–79.
CAS PubMed Google ученый
Кшитиз П.Дж., Ким П., Хелен В., Энглер А.Дж., Левченко А., Ким Д.Х. Контроль судьбы и функции стволовых клеток с помощью инженерных физических микросред. Интергр Биол (Камб).2012; 4: 1008–18.
CAS PubMed Google ученый
Amps K, Andrews PW, Anyfantis G, Armstrong L, Avery S, Baharvand H, Baker J, Baker D, Munoz MB, Beil S, Benvenisty N, Ben-Yosef D, Biancotti JC, Bosman A, Brena RM, Brison D, Caisander G, Camarasa MV, Chen J, ChiaoE CYM, Choo AB, Collins D, et al. Скрининг этнически разнообразных эмбриональных стволовых клеток человека позволяет выявить минимальный ампликон 20 хромосомы, обеспечивающий преимущество в росте.Nat Biotechnol. 2011; 29: 1132–44.
CAS PubMed Google ученый
Нукая Д., Минами К., Хошикава Р., Йокои Н., Сейно С. Предпочтительная экспрессия генов и эпигенетическая память индуцированных плюрипотентных стволовых клеток, полученных из поджелудочной железы мыши. Гены Клетки. 2015; 20: 367–81.
CAS PubMed Google ученый
Мердок А., Брауд П., Кортни А., Брисон Д., Хант С., Лоуфорд-Дэвис Дж., Мур Н., Стейси Г., Сет С., Рабочая группа по закупкам Национальной клинической больницы Н., Э.S. C. F, National Clinical H, E. S. C. F. Получение клеток для получения линий человеческих эмбриональных стволовых клеток для терапевтического использования: рекомендации по надлежащей практике. Stem Cell Rev.2012; 8: 91–9.
PubMed Google ученый
Hewitson H, Wood V, Kadeva N, Cornwell G, Codognotto S, Stephenson E, Ilic D. Создание линии эмбриональных стволовых клеток человека исследовательского класса KCL035, несущей мутацию в гене HBB. Stem Cell Res.2016; 16: 210–2.
CAS PubMed PubMed Central Google ученый
Дейли Г.К., Хен И., Апперли Дж. Ф., Баркер Р. А., Бенвенисти Н., Бреденоорд А. Л., Брейер К. К., Колфилд Т., Сидарс М. И., Фрей-Васконселлс Дж., Хеслоп Х. Э., Джин И., Ли Р. Т., Маккаб К., Munsie M, Murry CE, Piantadosi S, Rao M, Rooke HM, Sipp D, Studer L, Sugarman J, et al. Установление глобальных стандартов для исследования стволовых клеток и клинического перевода: рекомендации ISSCR 2016 г.Stem Cell Rep. 2016; 6: 787–97.
Google ученый
Такахаши К., Яманака С. Индукция плюрипотентных стволовых клеток из культур эмбриональных и взрослых фибробластов мыши с помощью определенных факторов. Клетка. 2006. 126 (4): 663–76. https://doi.org/10.1016/j.cell.2006.07.024.
CAS Статья PubMed Google ученый
Loh YH, Wu Q, Chew JL, Vega VB, Zhang W, Chen X, Bourque G, George J, Leong B., Liu J и др.Транскрипционная сеть Oct4 и Nanog регулирует плюрипотентность в эмбриональных стволовых клетках мыши. Нат Жене. 2006; 38: 431–40.
CAS PubMed Google ученый
Menasche P, Vanneaux V, Hagege A, Bel A, Cholley B, Cacciapuoti I, Parouchev A, Benhamouda N, Tachdjian G, Tosca L, Trouvin JH, Fabreguettes JR, Bellamy V, GuillemainBo Suberselbielle , Tartour E, Desnos M, Larghero J. Сердечные предшественники, полученные из человеческих эмбриональных стволовых клеток, для лечения тяжелой сердечной недостаточности: отчет о первом клиническом случае.Eur Heart J. 2015; 36: 2011–7.
PubMed Google ученый
Schwartz SD, Regillo CD, Lam BL, Eliott D, Rosenfeld PJ, Gregori NZ, Hubschman JP, Davis JL, Heilwell G, Spirn M, Maguire J, Gay R, Bateman J, Ostrick RM, Morris D , Vincent M, Anglade E, Del Priore LV, Lanza R.Пигментный пигментный эпителий сетчатки, полученный из эмбриональных стволовых клеток человека, у пациентов с возрастной дегенерацией желтого пятна и макулярной дистрофией Штаргардта: наблюдение за двумя открытыми исследованиями фазы 1/2.Ланцет. 2015; 385: 509–16.
PubMed Google ученый
Илич Д., Огилви К. Краткий обзор: эмбриональные стволовые клетки человека — что мы сделали? Что мы делаем? Куда мы идем? Стволовые клетки. 2017; 35: 17–25.
CAS PubMed Google ученый
Rocha V, et al. Клиническое применение гемопоэтических стволовых клеток пуповинной крови. Пересадка костного мозга Biol.2006; 12 (1): 34–4.
Лонго У.Г., Ронга М., Маффулли Н. Sports Med Arthrosc 17: 112–126. Тендинопатия ахиллова сухожилия. Sports Med Arthrosc. 2009. 17: 112–26.
PubMed Google ученый
Темпфер Х., Ленер С., Грюц М., Гевольф Р., Травегер А. Биологическая аугментация для восстановления сухожилий: уроки, которые следует извлечь из исследований развития, болезней и стволовых клеток сухожилий. В: Gimble J, Marolt D, Oreffo R, Redl H, Wolbank S, редакторы.Клеточная инженерия и регенерация. Справочная серия по биомедицинской инженерии. Чам: Спрингер; 2017.
Goldring MB, Goldring SR. Остеоартроз. J. Cell Physiol. 2007; 213: 626–34.
CAS PubMed Google ученый
Widuchowski W, Widuchowski J, Trzaska T. Дефекты суставного хряща: исследование 25 124 артроскопий коленного сустава. Колено. 2007. 14: 177–82.
CAS PubMed Google ученый
Li R, Lin Q-X, Liang X-Z, Liu G-B и др. Терапия стволовыми клетками для лечения остеонекроза головки бедренной кости: от клинических применений до соответствующих фундаментальных исследований. Рес-терапия стволовыми клетками. 2018; 9: 291 https://doi.org/10.1186/s13287-018-1018-7.
Google ученый
Gangji V, De Maertelaer V, Hauzeur JP. Имплантация аутологичных клеток костного мозга при лечении нетравматического остеонекроза головки бедренной кости: пятилетнее наблюдение в проспективном контролируемом исследовании.Кость. 2011; 49 (5): 1005–9.
PubMed Google ученый
Чжао Д., Цуй Д., Ван Б., Тиан Ф, Го Л., Ян Л. и др. Лечение остеонекроза головки бедренной кости на ранней стадии аутологичной имплантацией мезенхимальных стволовых клеток, полученных из костного мозга и культивированных. Кость. 2012; 50 (1): 325–30.
PubMed Google ученый
Сен РК, Трипати СК, Аггарвал С., Марваха Н., Шарма Р.Р., Ханделвал Н.Ранние результаты основной декомпрессии и инстилляции аутологичных мононуклеарных клеток костного мозга при остеонекрозе головки бедренной кости: рандомизированное контрольное исследование. J Arthroplast. 2012. 27 (5): 679–86.
Google ученый
Lapasset L, Milhavet O, Prieur A, Besnard E, Babled A, Aït-Hamou N, Leschik J, Pellestor F, Ramirez JM, De Vos J, Lehmann S, Lemaitre JM. Омоложение стареющих и столетних клеток человека путем перепрограммирования через плюрипотентное состояние.Genes Dev. 2011; 25: 2248–53.
CAS PubMed PubMed Central Google ученый
Сахин Э., Депиньо РА. Связывание функционального снижения теломер, митохондрий и стволовых клеток во время старения. Природа. 2010; 464: 520–8.
Петкович Д.А., Подольский Д.И., Лобанов А.В., Ли С.Г., Миллер Р.А., Гладышев В.Н. Использование профилей метилирования ДНК для оценки воздействия на биологический возраст и долголетие. Cell Metab. 2017; 25: 954–60 https: // doi.org / 10.1016 / j.cmet.2017.03.016.
CAS PubMed PubMed Central Google ученый
Геронтология, Омоложение путем перепрограммирования клеток: новые горизонты. Родольфо Г. Гойя, Марианна Леманн, Присцила Кьявеллини, Мартина Канателли-Маллат, Клаудиа Б. Херену и Оскар А. Браун. Ресурсотерапия стволовыми клетками . 2018, 9: 349. https://doi.org/10.1186/s13287-018-1075-y.
Ocampo A, Reddy P, Martinez-Redondo P, Platero-Luengo A, Hatanaka F, Hishida T, Li M, Lam D, Kurita M, Beyret E, Araoka T., Vazquez-Ferrer E, Donoso D. , Роман JLXJ, Родригес-Эстебан Ч., Нуньес Дж., Нуньес Деликадо Э., Кампистол Дж. М., Гильен I, Гильен П., Изписуа.Устранение возрастных признаков in vivo путем частичного перепрограммирования. Клетка. 2016; 167: 1719–33.
CAS PubMed PubMed Central Google ученый
de Lázaro I, Cossu G, Kostarelos K. Экспрессия транзиторного транскрипционного фактора (OSKM) является ключом к клинической трансляции перепрограммирования клеток in vivo. EMBO Mol Med. 2017; 9: 733–6.
PubMed PubMed Central Google ученый
Сунь С., Ли З.К., Гленсер П., Цай BC, Чжан Х.М., Ян Дж., Ли XR. Акцентирование внимания на возрастной предрасположенности к возрастной макулопатии 2 аллеля высокого риска дегенерации желтого пятна с помощью технологии стволовых клеток. Stem Cell Res Ther. 2017; 8: 135 https://doi.org/10.1186/s13287-017-0584-4.
PubMed PubMed Central Google ученый
Лю Дж. Индуцированные нейральные стволовые клетки, полученные из плюрипотентных стволовых клеток: новая надежда на инсульт? Stem Cell Res Ther.2013; 4: 115 https://doi.org/10.1186/scrt326.
PubMed PubMed Central Google ученый
Шахджалал Х.М., Дайем А.А., Лим К.М., Чон Т.И., Чо С.Г. Генерация β-клеток поджелудочной железы для лечения диабета: достижения и проблемы. Stem Cell ResTher. 2018; 9: 355 https://doi.org/10.1186/s13287-018-1099-3.
Google ученый
Kroon E, Martinson LA, et al.Энтодерма поджелудочной железы, полученная из эмбриональных стволовых клеток человека, генерирует инсулин-секретирующие клетки, чувствительные к глюкозе, in vivo. Nat Biotechnol. 2008; 26; 443–52.
Arora V, Pooja A, Munshi AK. Сохранение стволовых клеток из слущенных временных зубов человека. J Clin Pediatr Dent. 2009. 33 (4): 289–94.
PubMed Google ученый
Mao JJ. Стволовые клетки и будущее стоматологической помощи. New York State Dental J. 2008; 74 (2): 21–4.
Google ученый
Резник, Джей Б. Непрерывное образование: стволовые клетки: новые медицинские и стоматологические методы лечения для профессиональных стоматологов. Журнал Денталтаун . 2008, стр. 42–53.
Артур А., Рычков Г., Ши С., Коблар С.А., Гронтос С. Стволовые клетки пульпы зуба взрослого человека дифференцируются в сторону функционально активных нейронов при соответствующих сигналах окружающей среды. Стволовые клетки. 2008. 26 (7): 1787–95.
CAS PubMed Google ученый
Кордейро М.М., Донг З., Канеко Т., Чжан З., Миядзава М., Ши С., Смит А. Инженерия ткани пульпы зубов со стволовыми клетками из расслоенных. Дж. Эндод. 2008. 34 (8): 962–9.
PubMed Google ученый
Хаяси К., Охта Х., Куримото К., Арамаки С., Сайтоу М. Восстановление пути спецификации зародышевых клеток мыши в культуре с помощью плюрипотентных стволовых клеток.Клетка. 2011. 146 (4): 519–32. https://doi.org/10.1016/j.cell.2011.06.052.
CAS Статья PubMed Google ученый
Садри-Ардекани Х., Атала А. Криоконсервация ткани яичек и трансплантация сперматогониальных стволовых клеток для восстановления фертильности: от скамьи к постели. Stem Cell ResTher. 2014; 5: 68 https://doi.org/10.1186/scrt457.
Google ученый
Zhang Q, Xu M, Yao X, Li T, Wang Q, Lai D. Амниотические эпителиальные клетки человека подавляют апоптоз гранулезных клеток, вызванный химиотерапией, и восстанавливают фертильность. Stem Cell Res Ther. 2015; 6: 152 https://doi.org/10.1186/s13287-015-0148-4.
PubMed PubMed Central Google ученый
Ма Д.К., Бонагиди М.А., Мин Г.Л., Сонг Х. Взрослые нервные стволовые клетки в центральной нервной системе млекопитающих. Cell Res. 2009; 19: 672–82. https: // doi.org / 10.1038 / cr.2009.56.
CAS Статья PubMed PubMed Central Google ученый
Dantuma E, Merchant S, Sugaya K. Стволовые клетки для лечения нейродегенеративных заболеваний. Stem Cell ResTher. 2010; 1:37 https://doi.org/10.1186/scrt37.
Google ученый
Ван Кью, Мацумото Ю., Синдо Т., Мияке К., Синдо А., Каваниси М., Кавай Н., Тамия Т., Нагао С.Трансплантация нервных стволовых клеток в кортекс на мышиной модели болезни Альцгеймера. J Med Invest. 2006; 53: 61–9. https://doi.org/10.2152/jmi.53.61.
Артикул PubMed Google ученый
Moghadam FH, Alaie H, Karbalaie K, Tanhaei S, Nasr Esfahani MH, Baharvand H. Трансплантация примированных или незапраймированных клеток-предшественников нервных клеток, полученных из эмбриональных стволовых клеток мыши, улучшает когнитивные функции у крыс с болезнью Альцгеймера. Дифференциация.2009. 78: 59–68. https://doi.org/10.1016/j.diff.2009.06.005.
CAS Статья PubMed Google ученый
Byrne JA. Разработка методов лечения нейродегенеративных заболеваний на основе нервных стволовых клеток. Stem Cell ResTher. 2014; 5: 72. https://doi.org/10.1186/scrt461.
Google ученый
Awe JP, Lee PC, Ramathal C, Vega-Crespo A, Durruthy-Durruthy J, Cooper A, Karumbayaram S, Lowry WE, Clark AT, Zack JA, Sebastiano V, Kohn DB, Pyle AD, Martin MG, Lipshutz GS, Phelps PE, Pera RA, Byrne JA.Создание и характеристика свободных от трансгенов человеческих плюрипотентных стволовых клеток и преобразование в предполагаемый клинический статус. Stem Cell Res Ther. 2013; 4: 87. https://doi.org/10.1186/scrt246.
CAS Статья PubMed PubMed Central Google ученый
Пэн Дж., Цзэн X. Роль индуцированных плюрипотентных стволовых клеток в регенеративной медицине: нейродегенеративные заболевания. Stem Cell ResTher. 2011; 2:32. https: // doi.org / 10.1186 / scrt73.
CAS Google ученый
Райт Б.Л., Баркер Р.А. Созданные и новые методы лечения болезни Хантингтона. 2007; 7 (6): 579–87 https://www.ncbi.nlm.nih.gov/pubmed/17896994/579-87.
Lin NH, Gronthos S, Bartold PM. Стволовые клетки и регенерация пародонта. Ост Дент Дж. 2008; 53: 108–21.
PubMed Google ученый
Сео Б.М., Миура М., Гронтос С., Бартольд П.М., Батули С., Брахим Дж. И др. Исследование мультипотентных постнатальных стволовых клеток пародонтальной связки человека. Ланцет. 2004; 364: 149–55.
CAS PubMed Google ученый
Ramseier CA, Abramson ZR, Jin Q, Giannobile WV. Генная терапия для регенеративной медицины пародонта. Dent Clin North Am. 2006; 50: 245–63.
PubMed PubMed Central Google ученый
Ши С., Бартольд П.М., Миура М., Сео Б.М., Роби П.Г., Гронтос С. Эффективность мезенхимальных стволовых клеток для регенерации и восстановления зубных структур. OrthodCraniofac Res. 2005; 8: 191–9.
CAS Google ученый
Йохара К., Накашима М., Ито М., Исикава М., Накасима А., Акамине А. Регенерация дентина с помощью терапии стволовыми клетками пульпы зуба с рекомбинантным морфогенетическим белком кости человека. J Dent Res. 2004; 83: 590–5.
CAS PubMed Google ученый
Ху Б., Унда Ф., Бопп-Кучлер С., Хименес Л., Ван XJ, Хайкель Ю. и др. Клетки костного мозга могут давать начало амелобластоподобным клеткам. J Dent Res. 2006; 85: 416–21.
CAS PubMed Google ученый
Liu Y, Liu W, Hu C, Xue Z, Wang G, Ding B, Luo H, Tang L, Kong X, Chen X, Liu N, Ding Y, Jin Y. MiR-17 модулирует остеогенный дифференцировка через связную петлю прямой связи в мезенхимальных стволовых клетках, выделенных из пародонтальных связок пациентов с пародонтитом.Стволовые клетки. 2011. 29 (11): 1804–16. https://doi.org/10.1002/stem.728.
CAS Статья PubMed Google ученый
Raspini G, Wolff J, Helminen M, Raspini G, Raspini M, Sándor GK. Стволовые клетки зубов, полученные с третьих моляров в сочетании с биоактивным стеклом, могут вызывать признаки костеобразования in vitro. J Oral Maxillofac Res. 2018; 9 (1): e2. Опубликовано 31 марта 2018 г. https://doi.org/10.5037/jomr.2018.9102.
Christodoulou I, Goulielmaki M, Devetzi M, Panagiotidis M, Koliakos G, Zoumpourlis V. Мезенхимальные стволовые клетки в доклинической цитотерапии рака: систематический обзор. Stem Cell Res Ther. 2018; 9 (1; 336). https://doi.org/10.1186/s13287-018-1078-8.
Бансал Р., Джайн А. Текущий обзор применения стоматологических стволовых клеток в регенеративной стоматологии. J Nat Sci Biol Med. 2015; 6 (1): 29–34. https://doi.org/10.4103/0976-9668.149074.
Артикул PubMed PubMed Central Google ученый
Эдгар Ледесма-Мартинес, Виктор Мануэль Мендоса-Нуньес, Эдельмиро Сантьяго-Осорио. Мезенхимальные стволовые клетки, полученные из пульпы зуба: обзор. Стволовые клетки Инт . 2016, 4,709,572, стр. doi: https://doi.org/10.1155/2016/4709572].
Grzech-Leśniak K. Использование лазеров в лечении пародонта: новый золотой стандарт? Photomed Laser Surg. 2017; 35 (10): 513–4.
PubMed Google ученый
Миура М., Гронтос С., Чжао М., Лу Б., Фишер Л. В., Роби П. Г., Ши С.SHED: стволовые клетки слущенных временных зубов человека. Proc Natl Acad Sci U S. A. 2003; 100 (10): 5807–12. https://doi.org/10.1073/pnas.0937635100.
CAS Статья PubMed PubMed Central Google ученый
Ясуи Т., Мабучи И., Торими Х., Эбине Т., Ниибе К., Хулихан Д.Д., Морикава С., Онидзава К., Кавана Х., Акадзава С., Судзуки Н., Накагава Т., Окано Х., Мацудзаки Ю. Очищенный человек. стволовые клетки пульпы зуба способствуют остеогенной регенерации.J Dent Res. 2016; 95 (2): 206–14. https://doi.org/10.1177/0022034515610748.
CAS Статья PubMed Google ученый
Ямамото А., Сакаи К., Мацубара К., Кано Ф., Уэда М. Многогранная нейро-регенеративная активность стволовых клеток пульпы зуба человека для функционального восстановления после травмы спинного мозга. Neurosci Res. 2014; 78: 16–20. https://doi.org/10.1016/j.neures.2013.10.010.
Артикул PubMed Google ученый
d’Aquino R, De Rosa A, Lanza V, Tirino V, Laino L, Graziano A, Desiderio V, Laino G, Papaccio G. Восстановление костных дефектов нижней челюсти человека путем трансплантации стволовых клеток пульпы / клеток-предшественников и биокомплексов коллагеновой губки . Eur Cell Mater. 2009; 12, PMID: 19
6: 75–83.Google ученый
Ван Л., Шен Х, Чжэн В., Тан Л., Ян З, Гао Ю., Ян Ц., Ван С., Дуань Ю., Цзинь Ю. Характеристика стволовых клеток из альвеолярной периодонтальной связки.Tissue Eng. Часть A. 2011; 17 (7–8): 1015–26. https://doi.org/10.1089/ten.tea.2010.0140.
CAS Статья PubMed Google ученый
Iwata T, Yamato M, Zhang Z, Mukobata S, Washio K, Ando T, Feijen J, Okano T., Ishikawa I. Валидация клеток, полученных из периодонтальной связки человека, в качестве надежного источника для цитотерапии. J Clin Periodontol. 2010. 37 (12): 1088–99. https://doi.org/10.1111/j.1600-051X.2010.01597.x.
CAS Статья PubMed Google ученый
Chen F-M, Gao L-N, Tian B-M, Zhang X-Y, Zhang Y-J, Dong G-Y, Lu H и др. Лечение внутрикостных дефектов пародонта с использованием аутологичных стволовых клеток периодонтальной связки: рандомизированное клиническое исследование. Stem Cell Res Ther. 2016; 7:33. https://doi.org/10.1186/s13287-016-0288-1.
Артикул PubMed PubMed Central Google ученый
Бакопулу А., Лейхаузен Г., Фольк Дж., Цифтсоглоу А., Гарефис П., Коидис П., Геуртсен В.Сравнительный анализ потенциала остео / одонтогенной дифференцировки in vitro стволовых клеток пульпы человека (DPSC) и стволовых клеток апикального сосочка (SCAP). Arch Oral Biol. 2011. 56 (7): 709–21. https://doi.org/10.1016/j.archoralbio.2010.12.008.
CAS Статья PubMed Google ученый
Han C, Yang Z, Zhou W, Jin F, Song Y, Wang Y, Huo N, Chen L, Qian H, Hou R, Duan Y, Jin Y. Стволовые клетки периапикального фолликула: многообещающий кандидат для регенерации цемента / пародонтальной связки и биокорневой инженерии.Stem Cells Dev. 2010. 19 (9): 1405–15. https://doi.org/10.1089/scd.2009.0277.
CAS Статья PubMed Google ученый
Luan X, Ito Y, Dangaria S, Diekwisch TG. Неоднородность клеток-предшественников зубных фолликулов в развивающемся периодонте мыши. Stem Cells Dev. 2006. 15 (4): 595–608. https://doi.org/10.1089/scd.2006.15.595.
CAS Статья PubMed PubMed Central Google ученый
Ханда К., Сайто М., Цунода А., Ямаути М., Хаттори С., Сато С., Тойода М., Теранака Т., Нараянан А.С. Клетки-предшественники из зубного фолликула способны образовывать цементный матрикс in vivo. Connect Tissue Res. 2002; 43 (2–3): 406–8 PMID: 12489190.
PubMed Google ученый
Гуо В., Чен Л., Гонг К., Дин Б., Дуань Ю., Цзинь Ю. Гетерогенные клетки зубных фолликулов и регенерация сложных тканей пародонта. Тканевая инженерия.Часть A. 2012; 18 (5–6): 459–70 https://doi.org/10.1089/ten.tea.2011.0261.
CAS PubMed PubMed Central Google ученый
Bai, Yudi et al. Формирование ткани, подобной цементу и периодонтальной связке, клеточными листами зубного фолликула, совместно культивированными с эпителиальными клетками оболочки корня Гертвига. Кость. 2011, 48, выпуск 6, стр. 1417–1426, https://doi.org/10.1016/j.bone.2011.02.016.
Кордейро М.М., Донг З., Канеко Т., Чжан З., Миядзава М., Ши С. и др.Инженерия тканей пульпы зубов стволовыми клетками слущенных молочных зубов. 2008, 34, стр. 962–969.
Доби К., Смит Дж., Слоан А.Дж., Смит А.Дж.. Влияние альгината, гидрогелей и TGF-бета 1 на восстановление пульпы зуба человека in vitro. Connect Tissue Res 2. 2002; 43: 387–90.
CAS Google ученый
Friedlander LT, Cullinan MP, Love RM. Стволовые клетки зубов и их потенциальная роль в апексогенезе и апексификации.Инт Эндод Дж. 2009; 42: 955–62.
CAS PubMed Google ученый
Цай Дж, Чжан И, Лю П, Чен С., Ву Х, Сунь И, Ли А., Хуанг К., Ло Р, Ван Л., Лю И, Чжоу Т, Вэй С., Пан Дж, Пей Д. , Генерация зубоподобных структур из свободных от интеграции плюрипотентных стволовых клеток, индуцированных мочой человека. Cell Regen (Лондон). 30 июля 2013 г., 2 (1), стр. 6, DOI: https://doi.org/10.1186/2045-9769-2-6.
Крейг Дж. Тейлор, Элеонора М.Болтон и Дж. Эндрю Брэдли, 12 августа 2011 г. и https://doi.org/10.1098/rstb.2011.0030], 366 (1575): 2312–2322. [doi :. Иммунологические аспекты банка эмбриональных и индуцированных плюрипотентных стволовых клеток. Philos Trans R SocLond B Biol Sci. 2011, 366 (1575), стр. 2312–2322, DOI: https: //doi.org/10.1098/rstb.2011.0030.
T.R. Наяк, Х. Андерсен, В. Макам, К. Хоу, С. Бэ, X.F. Сюй, P.L.R. Ee, J.H. Ан, Б. Хонг, Г. Пасторин, Б. Озилмаз, ACS Nano, 5 (6) (2011), стр. 4. Графен для контролируемой и ускоренной остеогенной дифференцировки мезенхимальных стволовых клеток человека.САУ Нано. 2011. С. 4670–4678.
Ли В.К., Лим К., Ши Х, Тан ЛАЛ, Ван И, Лим Коннектикут, Ло КП. Происхождение усиленного роста и дифференцировки стволовых клеток на графене и оксиде графена. САУ Нано. 2011; 5 (9): 7334–41.
CAS PubMed Google ученый
Kenry LWC, Loh KP, Lim CT. Когда стволовые клетки встречаются с графеном: возможности и проблемы регенеративной медицины. Биоматериалы. 2018; 155: 236–50.
CAS PubMed Google ученый
Юань А., Фарбер Е.Л., Рапопорт А.Л., Техада Д., Денискин Р., Ахмедов Н.Б. и др. Перенос микроРНК микровезикулами эмбриональных стволовых клеток. 2009. 2009, 4 (3), с. https://doi.org/10.1371/journal.pone. 0004722.
Oh, Myeongsik, et al. Экзосомы, полученные из индуцированных человеком плюрипотентных стволовых клеток, улучшают старение фибробластов кожи. Int. J. Mol. Sci. 2018, 19 (6), с. 1715.
Ramirez MI. и другие. Технические проблемы работы с внеклеточными везикулами.Наноразмер. 2018; 10: 881–906.
CAS PubMed Google ученый
Valadi H, et al. Опосредованный экзосомами перенос мРНК и микроРНК — это новый механизм генетического обмена между клетками. Nat. Cell Biol. 2007; 9: 654–9.
CAS PubMed Google ученый
Mateescu B, et al. Препятствия и возможности в функциональном анализе РНК внеклеточных везикул — позиционный документ ISEV.J. Extracell. Везикулы. 2017; 6 (1). https://doi.org/10.1080/20013078.2017.1286095.
Nawaz M, et al. Внеклеточные везикулы: развивающиеся факторы в биологии стволовых клеток. Stem Cells Int. 2016; 2016: 17. Идентификатор статьи 1073140.
Helfrich, Y.R., Sachs, D.L. и Вурхиз, Дж. Дж. Обзор старения кожи и фотостарения. Дерматол. Nurs. 20. С. 177–183, https://www.ncbi.nlm.nih.gov/pubmed/18649702.
Джулия Тиггес, Жан Крутманн, Эллен Фриче, Юдит Хенделер, Хайнер Шааль, Йенс В.Фишер, Фаиза Кальфала, Ханс Рейнке, Гвидо Райфенбергер, Кай Штюлер, Наташиа Вентура, Сабрина Гундерманн, Петра Букамп, Фриц Боэге. Признаки старения фибробластов, механизмы старения и развития, 138, 2014, страницы 26–44. 2014, 138, с. 26–44, ISSN 0047–6374, https://doi.org/10.1016/j.mad.2014.03.004.
Huh MI, Kim MS, Kim HK, et al. Влияние кондиционированной среды, собранной из стволовых клеток, полученных из околоплодных вод человека (hAFSC), на регенерацию кожи и фотостарение.Tissue Eng Regen Med. 2014; 11: 171 https://doi.org/10.1007/s13770-014-0412-1.
Google ученый
Togel F, Hu Z, Weiss K, et al. Вводимые мезенхимальные стволовые клетки защищают от острой ишемической почечной недостаточности посредством механизмов, не зависящих от дифференцировки. Am J Physiol Renal Physiol. 2005; 289: F31.
PubMed Google ученый
Лю Дж, Хан Г, Лю Х и др.Подавление роста клеток холангиокарциномы мезенхимальными стволовыми клетками пуповины человека: возможная роль передачи сигналов Wnt и Akt. PLoS One. 2013; 8: e62844.
CAS PubMed PubMed Central Google ученый
Oh M, et al. Промотирующие эффекты среды, обусловленной плюрипотентными стволовыми клетками человека, на пролиферацию и миграцию дермальных фибробластов. Biotechnol. Bioprocess Eng. 2017; 22: 561–8.
CAS Google ученый
Chen L, Tredget EE, Wu PY, Wu Y. Паракринные факторы мезенхимальных стволовых клеток привлекают макрофаги и клетки эндотелиального происхождения и улучшают заживление ран. PloS One. 2008; 3: e1886.
PubMed PubMed Central Google ученый
Бэ Дж-С, Ли С. Х, Ким Дж. И, Чой Дж. И, Пак Р-З, Пак Дж. Й., Пак Х-С, Сон Й-С, Ли Д. С., Ли Э. Б.. βig-h4 поддерживает адгезию, миграцию и пролиферацию кератиноцитов через интегрин α3β1. Biochem.Биофиз. Res. Commun. 2002; 294: 940–8.
CAS PubMed Google ученый
Zhou BR, Xu Y, Guo SL, Xu Y, Wang Y, Zhu F, Permatasari F, Wu D, Yin ZQ, Luo D. Влияние кондиционированной среды стволовых клеток, полученных из жировой ткани, на заживление ран после абляционной шлифовки фракционным углекислотным лазером. BioMed Res. Int. 2013; 519: 126.
Google ученый
Peng Y, Baulier E, Ke Y, Young A, Ahmedli NB, Schwartz SD, et al. Внеклеточные везикулы эмбриональных стволовых клеток человека и их влияние на иммортализованные клетки Мюллера сетчатки человека. PLoS ONE. 2018, 13 (3), с. https://doi.org/10.1371/journal.pone.019400.
Harris MT, Butler DL, Boivin GP, Florer JB, Schantz EJ, Wenstrup RJ. Мезенхимальные стволовые клетки, используемые для восстановления сухожилий кролика, могут образовывать эктопическую кость и выражать активность щелочной фосфатазы в конструкциях. J Orthop Res.2004; 22: 998–1003.
CAS PubMed Google ученый
Mascetti VL, Pedersen RA. Химеризм человека и мыши подтверждает плюрипотентность стволовых клеток человека. Стволовая клетка клетки. 2016; 18: 67–72.
CAS PubMed PubMed Central Google ученый
Gandia C, Armiñan A, García-Verdugo JM, Lledó E, Ruiz A, Miñana MD, Sanchez-Torrijos J, Payá R, Mirabet V, Carbonell-Uberos F, Llop M, Montero JA, Sepúlveda P .Стволовые клетки пульпы зуба человека улучшают функцию левого желудочка, вызывают ангиогенез и уменьшают размер инфаркта у крыс с острым инфарктом миокарда. Стволовые клетки. 2007. 26 (3): 638–45.
PubMed Google ученый
Perry BC, Zhou D, Wu X, Yang FC, Byers MA, Chu TM, Hockema JJ, Woods EJ, Goebel WS. Сбор, криоконсервация и характеристика мезенхимальных стволовых клеток, полученных из пульпы зуба человека, для банковского и клинического использования.Tissue Eng Часть C Методы. 2008. 14 (2): 149–56.
CAS PubMed PubMed Central Google ученый
Гарсия-Олмо Д., Гарсия-Арранс М., Эррерос Д. и др. Фаза I клинических испытаний лечения свища Крона трансплантацией мезенхимальных стволовых клеток жировой ткани. Dis Colon Rectum. 2005; 48: 1416–23.
PubMed Google ученый
de Mendonça CA, Bueno DF, Martins MT, Kerkis I, Kerkis A, Fanganiello RD, Cerruti H, Alonso N, Passos-Bueno MR.Реконструкция больших черепных дефектов в эксперименте без иммуносупрессии с использованием стволовых клеток пульпы зуба человека. J Craniofac Surg. 2008. 19 (1): 204–10.
Google ученый
Seo BM, Sonoyama W, Yamaza T, Coppe C, Kikuiri T, Akiyama K, Lee JS, Shi S. SHED устраняют критические дефекты свода черепа у мышей. Oral Dis. 2008. 14 (5): 428–34.
CAS PubMed PubMed Central Google ученый
Аббас, Дьяконов И., Шарп П. Происхождение зубных стволовых клеток нервным гребнем. Панъевропейская федерация Международной ассоциации стоматологических исследований (PEF IADR). 2008, Тт. Seq # 96 — Стволовые клетки полости рта.
Керкис И., Амбросио К.Э., Керкис А., Мартинс Д.С., Гайад Т.П., Морини А.С., Виейра Н.М., Марина П. и др. Ранняя трансплантация незрелых стволовых клеток пульпы зуба человека из молочных зубов собакам с мышечной дистрофией золотистого ретривера (GRMD). J Transl Med. 2008; 6: 35.
PubMed PubMed Central Google ученый
Сянжуй Ян, Ли Ли, Ли Сяо, Дунхуэй Чжан. Утилизируйте упаковку стоматологической феи: обзор стволовых клеток пульпы зуба. Стволовые клетки Res Ther . 2018, 9, 1, 1. https://doi.org/10.1186/s13287-018-1094-8.
Wang J, Wang X, Sun Z, Wang X, Yang H, Shi S, Wang S. Стволовые клетки молочных зубов, слущившиеся у человека, могут дифференцироваться в дофаминергические нейроноподобные клетки. Stem Cells Dev. 2010; 19: 1375–83.
CAS PubMed PubMed Central Google ученый
Wang J, et al. Одонтогенная дифференцировка стволовых клеток пульпы зуба человека на нановолоконных каркасах из поли (L-молочной кислоты) in vitro и in vivo. Acta Biomater. 2010. 6 (10): 3856–63.
CAS PubMed Google ученый
Davies OG, Cooper PR, Shelton RM, Smith AJ, Scheven BA. Сравнение минерализации in vitro и дентиногенного потенциала мезенхимальных стволовых клеток, полученных из жировой ткани, костного мозга и пульпы зуба.J Bone Miner Metab. 2015; 33: 371–82.
CAS PubMed Google ученый
Хуанг GT-J, Шаграманова К., Чан SW. Формирование одонтобластоподобных клеток из культивируемых клеток пульпы зуба человека на дентине in vitro. Дж. Эндод. 2006; 32: 1066–73.
PubMed Google ученый
Ши С., Роби П.Г., Гронтос С. Сравнение пульпы зуба человека и стромальных стволовых клеток костного мозга с помощью анализа микроматрицы кДНК.Кость. 2001. 29 (6): 532–9.
CAS PubMed Google ученый
Гронтос С., Манкани М., Брахим Дж., Роби П.Г., Ши С. Постнатальные стволовые клетки пульпы зуба человека (DPSC) in vitro и in vivo. Proc Natl Acad Sci U S. A. 2000; 97: 13625–30.
CAS PubMed PubMed Central Google ученый
Nuti N, Corallo C, Chan BMF, Ferrari M, Gerami-Naini B.Мультипотентная дифференцировка стволовых клеток пульпы зуба человека: обзор литературы. Stem Cell Rev Rep. 2016; 12: 511–23.
CAS Google ученый
Ferro F, et al. Дифференцировка стволовых клеток пульпы зуба открывает новые возможности для понимания динамики Oct4A. PloS One. 2012; 7 (7): e41774.
Conde MCM, Chisini LA, Grazioli G, Francia A, Carvalho RVd, Alcázar JCB, Tarquinio SBC, Demarco FF. Влияет ли криоконсервация на биологические свойства стволовых клеток из тканей зубов? Систематический обзор.Браз Дент Дж. 2016; 1210 (6): 633-40. https://doi.org/10.1590/0103-6440201600980.
Papaccio G, Graziano A, d’Aquino R, Graziano MF, Pirozzi G, Menditti D, De Rosa A, Carinci F, Laino G. Долгосрочная криоконсервация стволовых клеток пульпы зуба (SBP-DPSCs) и их дифференцированные остеобласты: источник клеток для восстановления тканей. J. Cell Physiol. 2006; 208: 319–25.
CAS PubMed Google ученый
Alge DL, Zhou D, Adams LL, et.al. Сопоставление доноров стволовых клеток пульпы зуба и мезенхимальных стволовых клеток костного мозга на модели крыс. J Tissue Eng Regen Med. 2010. 4 (1): 73–81.
Джо И-И, Ли Х-Дж, Кук С.-И, Чонг Х-В, Пак Дж-И, Чунг Дж-Х, Чунг И-Х, Ким И-С, Ян Х-С, Чунг П-Х. Выделение и характеристика постнатальных стволовых клеток из тканей зубов человека. Tissue Eng. 2007; 13: 767–73.
CAS PubMed Google ученый
Gronthos S, Brahim J, Li W, Fisher LW, Cherman N, Boyde A, DenBesten P, Robey PG, Shi S. Свойства стволовых клеток стволовых клеток пульпы зуба человека. J Dent Res. 2002; 81: 531–5.
CAS PubMed Google ученый
Laino G, d’Aquino R, Graziano A, Lanza V, Carinci F, Naro F, Pirozzi G, Papaccio G. Новая популяция стволовых клеток пульпы зуба взрослого человека: полезный источник живых аутологичных волокнистых костная ткань (LAB). J Bone Miner Res.2005; 20: 1394–402.
PubMed Google ученый
Зайнал А., Шахрул Х. и др. Изучение трансформации хондрогенеза in vitro стволовых клеток пульпы зуба мыши. Научный мир J. 2012; 2012: 827149.
Wei X, et al. Экспрессия маркеров минерализации в клетках пульпы зуба. Дж. Эндод. 2007. 33 (6): 703–8.
PubMed Google ученый
Dai J, et al.Влияние совместного культивирования костальных хондроцитов и стволовых клеток пульпы зуба в сочетании с экзогенным белком FGF9 на хондрогенез и оссификацию в сконструированном хряще. Биоматериалы. 2012. 33 (31): 7699–711.
CAS PubMed Google ученый
Vasandan AB, et al. Функциональные отличия мезенхимальных стромальных клеток от пульпы зуба человека и пародонтальной связки. J Cell Mol Med. 2014. 18 (2): 344–54.
CAS PubMed PubMed Central Google ученый
Werle SB, et al. Кариозные молочные зубы являются потенциальным источником стволовых клеток пульпы зуба. Clin Oral Investig. 2015; 20: 75–81.
PubMed Google ученый
Nemeth CL, et al. Усиление хондрогенной дифференцировки стволовых клеток пульпы зуба с использованием гидрогелей PEG-GelMA-HA с нанопокрытием. Tissue Eng A. 2014; 20 (21–22): 2817–29.
CAS Google ученый
Пайно Ф., Риччи Дж., Де Роса А., Д’Акино Р., Лайно Л., Пироцци Дж. И др. Экто-мезенхимальные стволовые клетки пульпы зуба способны дифференцироваться в активные меланоциты. Евро. Cell Mater. 2010. 20: 295–305.
CAS PubMed Google ученый
Ferro F, Spelat R, Baheney CS. Выделение, характеристика и дифференциация стволовых клеток пульпы зуба (DPSC). В: Kioussi C, редактор. Восстановление стволовых клеток и тканей. Методы молекулярной биологии (методы и протоколы): Humana Press.2014; 1210.
Ishkitiev N, Yaegaki K, Imai T., Tanaka T., Nakahara T., Ishikawa H, Mitev V, Haapasalo M. Высокочистая линия печени, дифференцированная из стволовых клеток пульпы зуба в бессывороточной среде. Дж. Эндод. 2012; 38: 475–80.
PubMed Google ученый
Трансплантация стволовых клеток | Общество лейкемии и лимфомы
Что такое стволовые клетки?
Стволовые клетки крови производятся в костном мозге и могут стать любым типом клеток крови, в которых нуждается организм.Стволовые клетки постоянно делятся и созревают в разные типы клеток крови, заменяя старые и изношенные клетки крови в организме. Каждый день они производят миллиарды новых клеток крови. Если стволовые клетки не могут производить достаточно новых клеток крови, может возникнуть множество серьезных проблем со здоровьем. Эти проблемы могут включать инфекции, анемию или кровотечение.
Для жизни необходимы здоровые стволовые клетки. Когда рак или лечение рака разрушают стволовые клетки, трансплантация стволовых клеток (SCT) может быть лучшим вариантом лечения.
Что такое трансплантация стволовых клеток?
Трансплантация стволовых клеток (SCT), иногда называемая трансплантацией костного мозга, — это процедура, при которой пациенту вводятся здоровые стволовые клетки для замены поврежденных стволовых клеток.
Перед ТСК пациент получает высокие дозы химиотерапии, а иногда и лучевую терапию, чтобы подготовить тело к трансплантации. Это называется «кондиционирующим лечением». После того, как стволовые клетки введены в кровоток пациента, они попадают в костный мозг и начинают процесс образования новых здоровых кровяных телец, включая лейкоциты, эритроциты и тромбоциты.Этот процесс называется «приживлением».
Типы трансплантации стволовых клеток
Основные типы SCT:
- Аутологичная трансплантация использует собственные стволовые клетки пациента. Эти клетки удаляются, обрабатываются и возвращаются в его или ее собственное тело после режима кондиционирования.
- В аллогенной трансплантации используются стволовые клетки от донора. Донором может быть член семьи или кто-то, не связанный с пациентом.
Сингенная трансплантация встречается гораздо реже.Сингенная трансплантация встречается редко по той простой причине, что она используется только для однояйцевых близнецов. Кроме того, близнец-донор и близнец-реципиент должны иметь идентичный генетический состав и тип ткани.
Вы кандидат на трансплантацию стволовых клеток?
Трансплантация стволовых клеток использовалась для излечения тысяч людей, больных раком, но это лечение сопряжено с серьезными рисками. Перед трансплантацией стволовых клеток пациенты, рассматривающие это лечение, должны обсудить риски и преимущества со своими врачами.
Не все пациенты подходят для трансплантации стволовых клеток, потому что не все пациенты могут выдерживать режим кондиционирования и побочные эффекты лечения. Некоторые пациенты также могут не соответствовать критериям стандартной трансплантации, если у них есть другие серьезные проблемы со здоровьем. Однако для некоторых из этих пациентов одним из вариантов лечения может быть трансплантация аллогенных стволовых клеток пониженной интенсивности.
Чтобы определить, подходит ли пациент для трансплантации стволовых клеток, медицинская бригада пациента рассмотрит
- Общее состояние здоровья пациента
- Тип и стадия рака или заболевания
- История предшествующего лечения
- Вероятность того, что болезнь отреагирует на трансплантат
- Наличие подходящего донора или возможность использовать собственные стволовые клетки пациента.
Риски трансплантации стволовых клеток уменьшались с каждым десятилетием. Текущие исследования, вероятно, продолжат улучшать процедуру. Однако для некоторых заболеваний и пациентов новые эффективные лекарства и новые виды терапии могут быть лучшими вариантами лечения, чем трансплантация стволовых клеток. Врачи и их пациенты будут учитывать множество факторов при принятии решения о том, является ли трансплантация стволовых клеток лучшим вариантом лечения.
Подготовка к трансплантации
Медицинские обследования. Трансплантация стволовых клеток — это сложная медицинская процедура. Перед трансплантацией пациенты пройдут ряд медицинских анализов, чтобы убедиться, что они достаточно здоровы для процедуры.
Сиделка. Пациентам, готовящимся к трансплантации, важно выбрать лицо, осуществляющее уход. Иногда опекун — это один человек, но часто несколько человек могут помочь в разное время на протяжении всего процесса. Опекун должен постоянно находиться с пациентом после выписки пациента из больницы в случае возникновения неожиданных осложнений и необходимости в помощи.Когда пациент вернется домой, опекун должен будет оказывать медицинскую, эмоциональную и ежедневную поддержку во время выздоровления. Члены медицинской бригады пациента обучат тех, кто за ними ухаживает, необходимым навыкам для ухода за пациентом.
Стоимость трансплантации. Трансплантация стволовых клеток — очень дорогая процедура. Как только пересадка стволовых клеток рассматривается как вариант лечения, пациенты должны обсудить финансовые вопросы со своей лечащей бригадой. В центрах трансплантологии есть сотрудники, которые могут помочь пациентам получить ответы на финансовые вопросы, касающиеся медицинского страхования и финансовой помощи.
Большинство страховых планов покрывают часть затрат на трансплантацию при определенных формах рака или заболеваний. Перед трансплантацией пациенты должны связаться со своими поставщиками медицинской страховки и определить, какие расходы покрывает страховая компания. Если их страховая компания отказывает в покрытии рекомендованного лечения, процедуры или рецептурных лекарств, пациенты могут отменить решение, подав апелляцию в свою страховую компанию. Если претензии неоднократно отклоняются, пациенты могут обратиться в страховое агентство своего штата или к юристу.
За дополнительными ресурсами обращайтесь к информационному специалисту LLS.
Плодородие. Высокие дозы химиотерапии и радиации могут поражать клетки как мужской, так и женской репродуктивной системы. Восстановление после трансплантации стволовых клеток может занять от нескольких месяцев до нескольких лет, а пациенты детородного возраста могут быть физически или психологически не готовы думать о родительстве в течение нескольких лет после трансплантации. Пациенты, которые могут захотеть иметь детей в будущем, должны обсудить варианты сохранения фертильности перед трансплантацией.
Для получения дополнительной информации см. Фертильность.
Введение центрального венозного катетера. В процессе трансплантации пациенту потребуется несколько внутривенных (вводимых непосредственно в вену) инфузий. Помимо инфузии стволовых клеток, пациенты могут также получать другие инфузии, включая жидкости, химиотерапию, антибиотики, другие лекарства и переливание эритроцитов и тромбоцитов. Пациентам также необходимо часто сдавать кровь для тестирования, чтобы следить за своим прогрессом.Эти инъекции, если их вводить индивидуально, были бы болезненными, а вены на руках и руках не могли выдержать так много частых уколов иглой. Поэтому перед трансплантацией пациентам будет вставлен центральный венозный катетер (ЦВК), если он еще не установлен. ЦВК — это трубка, которая вводится через кожу в крупную вену, обычно в верхней части грудной клетки. Размещение обычно проводится под местной анестезией.
Ссылки по теме
Часто задаваемые вопросы о стволовых клетках
Почему доктора и ученые так взволнованы стволовыми клетками?
Стволовые клетки имеют потенциал во многих областях здравоохранения и медицинских исследований.
- Изучение стволовых клеток поможет нам понять, как стволовые клетки превращаются в набор специализированных клеток, из которых состоит человеческое тело. Некоторые из наиболее серьезных заболеваний, такие как рак и врожденные дефекты, могут быть результатом проблем, возникающих в процессе дифференциации. Лучшее понимание нормального развития клеток позволит нам понять и, возможно, исправить ошибки, вызывающие эти заболевания.
- Стволовые клетки станут инструментом для фармакологических разработок.Исследования стволовых клеток должны способствовать развитию популяций клеток с определенным заболеванием. Эти популяции клеток затем можно использовать для первоначального тестирования с кандидатами на лекарства.
- Наконец, возможно, наиболее захватывающим потенциальным применением стволовых клеток является клеточная терапия. Плюрипотентные стволовые клетки предлагают возможность возобновляемого источника замещающих клеток и, возможно, тканей для лечения множества заболеваний, состояний и инвалидностей, включая болезнь Паркинсона, травмы спинного мозга, инсульт, ожоги, болезни сердца, диабет, остеоартрит и ревматоидный артрит.
В чем разница между взрослыми стволовыми клетками и эмбриональными стволовыми клетками?
Взрослые и эмбриональные стволовые клетки различаются типом клеток, которые они могут развить в эмбриональные стволовые клетки, могут стать клетками всех типов организма (они плюрипотентны). Взрослые стволовые клетки находятся в зрелых тканях (костном мозге, коже, головном мозге и т. Д.) И дают начало другим типам клеток из своей ткани или происхождения (они мультипотентны). Например, взрослые стволовые клетки крови дают начало эритроцитам, лейкоцитам и тромбоцитам.
Почему бы не использовать взрослые стволовые клетки вместо эмбриональных стволовых клеток человека в исследованиях?
Считается, что взрослые стволовые клетки присутствуют во всех типах тканей тела. Но на сегодняшний день выделение многих типов взрослых стволовых клеток ограничено. Гемопоэтические (кровяные) стволовые клетки легко доступны через аспирацию костного мозга. Но стволовые клетки для твердых органов, таких как печень или мозг, оказалось труднее идентифицировать и получить. Есть надежда, что чЭСК можно будет использовать для получения всех типов взрослых стволовых клеток в организме, что позволит проводить исследования, которые в настоящее время невозможны.
Откуда берутся эмбриональные стволовые клетки человека?
Эмбриональные стволовые клетки выделяют из эмбрионов человека в возрасте от 3 до 5 дней на стадии бластоцисты. Бластоциста представляет собой полый микроскопический кластер из нескольких сотен недифференцированных клеток.
Что такое линия эмбриональных стволовых клеток человека?
Это культура чЭСК, полученных из одного эмбриона. Поскольку стволовые клетки могут самовоспроизводиться, всего несколько чЭСК могут дать начало целой популяции идентичных чЭСК или линии клеток.
Почему ученые хотят использовать линии стволовых клеток?
После создания клеточная линия может расти в лаборатории неограниченное время, а клетки могут быть заморожены для последующего использования или передачи другим исследователям. Поскольку каждая клеточная линия имеет свой собственный генетический след, исследователи часто заинтересованы в использовании одной и той же клеточной линии для ряда связанных экспериментов.
Были ли эмбриональные стволовые клетки человека уже успешно использованы для лечения каких-либо человеческих заболеваний?
№На данный момент перспективы огромны, но исследования hESC все еще находятся на начальной стадии. Исследования эмбриональных стволовых клеток человека (hESC) начались только в 1998 году, когда группа под руководством доктора Джеймса Томсона из Университета Висконсина разработала методику выделения и выращивания клеток.
В конце января 2009 года калифорнийская компания Geron получила разрешение FDA на начало первого клинического испытания клеток, полученных из эмбриональных стволовых клеток человека.
Напротив, исследования взрослых стволовых клеток, таких как кроветворные стволовые клетки костного мозга (называемые гемопоэтическими стволовыми клетками или HSC), ведутся уже более десятилетий.И это исследование привело к лечению пациентов; например, трансплантация костного мозга (стволовых клеток) проводится уже более 40 лет.
Кроме того, исследования с ограниченным числом пациентов продемонстрировали клинический потенциал взрослых стволовых клеток в лечении других заболеваний человека, включая диабет и распространенный рак почки.
Что такое индуцированные плюрипотентные стволовые клетки?
Индуцированные плюрипотентные стволовые клетки (iPS-клетки) — это клетки, которые начинались как нормальные взрослые клетки (например, клетки кожи) и были сконструированы (« индуцированы ») учеными, чтобы стать плюрипотентными, то есть способными образовывать все типы клеток тело.Этот процесс часто называют «перепрограммированием». Хотя iPS-клетки и эмбриональные стволовые клетки имеют много общих характеристик, они не идентичны. В настоящее время ученые изучают, отличаются ли они клинически значимыми способами.
Исключают ли iPS-клетки необходимость в эмбриональных стволовых клетках?
Технология, используемая для создания iPS-клеток, открывает большие перспективы для создания клеточных линий, специфичных для пациентов и болезней, для исследовательских целей. Эти клетки уже являются полезными инструментами для разработки лекарств, и ученые надеются использовать их в трансплантологии.Однако необходимы дополнительные исследования, прежде чем методы перепрограммирования можно будет использовать для создания стволовых клеток, подходящих для безопасного и эффективного лечения.
Что такое перенос ядра соматической клетки?
Перенос ядра соматической клетки (SCNT) — это метод, при котором ядро соматической клетки (любой клетки тела, кроме сперматозоидов и яйцеклеток) вводится или трансплантируется в яйцеклетку, ядро которой удалено. Продукт SCNT имеет тот же генетический материал, что и донор соматических клеток.
Является ли перенос ядра соматической клетки тем же, что и клонирование?
Да. SCNT — это метод клонирования. Продукт SCNT почти генетически идентичен соматической клетке, используемой в этом процессе. (Следует отметить, что продукт SCNT технически не идентичен на 100% в том смысле, что цитоплазма ооцита включает митохондриальную ДНК.) Хотя SCNT считается клонированием, важно различать терапевтическое и репродуктивное клонирование. В следующем FAQ рассматриваются эти различия.
В чем разница между терапевтическим клонированием и репродуктивным клонированием?
Репродуктивное клонирование включает введение продукта SCNT в матку с целью живорождения. Полученный организм теоретически будет генетической копией донора соматических клеток. Репродуктивное клонирование проводится на животных в течение многих лет и связано с множеством технических и биологических проблем. Только около 1 процента всех яиц, которые получают донорскую ДНК, могут развиться в нормальные выжившие клоны.Терапевтическое клонирование использует SCNT с единственной целью получения клеток для исследований и, возможно, в будущем для терапии. При терапевтическом клонировании продукт SCNT не помещается в матку, и, следовательно, рождение живого ребенка невозможно. Терапевтическое клонирование дает два потенциальных преимущества.
- Первый предназначен для изучения конкретных заболеваний. Если у донора соматических клеток есть генетическое заболевание, такое как мышечная дистрофия, продукт SCNT также будет иметь гены мышечной дистрофии.Клетки, полученные из этого продукта SCNT, затем могут быть использованы для изучения биологии мышечной дистрофии с целью поиска новых способов предотвращения, лечения или даже лечения заболевания.
- Второй — создание «дизайнерских клеток» для трансплантации. Когда клетки, ткани или целые органы пересаживаются от одного человека к другому, иммунная система реципиента воспринимает новый материал как чужеродный и пытается отклонить трансплантат. Чтобы этого избежать, реципиентам трансплантата дают лекарства, которые модулируют иммунную систему реципиента, чтобы избежать отторжения.Возможное решение — терапевтическое клонирование. Если мисс Джонс понадобится трансплантат, соматическая клетка мисс Джонс может быть использована для SCNT. Полученный продукт будет иметь ту же генетику, что и г-жа Джонс. Клетки, полученные и выращенные для трансплантации, будут приняты иммунной системой г-жи Джонс как свои собственные.
Разрешает ли закон штата Массачусетс исследование эмбриональных стволовых клеток человека?
Да. Закон штата Массачусетс, принятый в мае 2005 года, разрешает исследования hESC и позволяет получать hESC из эмбрионов, которые были созданы для репродуктивных целей и больше не нужны для репродукции и переноса ядер соматических клеток.
Каковы рекомендации по NAS?
Национальная академия наук (NAS) выпустила руководящие принципы для исследований hESC в апреле 2005 г. и впоследствии обновила эти руководящие принципы в 2007 и 2008 гг. Текущие руководящие принципы содержат подробные рекомендации в отношении многих аспектов исследования hESC, в том числе:
- Привлечение доноров и информированное согласие
- как следует характеризовать, обрабатывать, передавать и хранить стволовые клетки
- создание местных комитетов по надзору за исследованиями эмбриональных стволовых клеток (ESCRO)
- руководство о том, какие виды исследований следует рассматривать для утверждения, а какие должны быть запрещены в настоящее время
Требуется ли одобрение Институционального наблюдательного совета (IRB) для всех исследований hESC?
№Разрешение IRB требуется для:
- получение чЭСК из существующих эмбрионов или SCNT
- исследования с использованием чЭСК, если исследователю известны доноры гамет и / или соматических клеток. Для использования деидентифицированных существующих чЭСК не требуется одобрения IRB.
Финансирует ли федеральное правительство исследования эмбриональных стволовых клеток?
До недавнего времени федеральное правительство ограничивало финансирование конкретными ЧЭСК, полученными до 9 августа 2001 г.В частности, федеральные фонды были разрешены только на исследования чЭСК, внесенных в реестр Национальных институтов здравоохранения (NIH), и производных продуктов из чЭСК в реестре NIH. 9 марта 2009 года президент Обама подписал указ, открывающий Национальным институтам здравоохранения и другим федеральным агентствам возможность финансировать исследования с использованием всех видов hESC.
Каков источник финансирования исследований стволовых клеток человеческого эмбриона Центром регенеративной медицины?
Исследования эмбриональных стволовых клеток человека в Центре регенеративной медицины были частично поддержаны частными благотворительными пожертвованиями.Эти пожертвования позволили нам поддержать широкий спектр исследовательской деятельности, которая не могла быть поддержана из других источников, таких как финансирование NIH. В будущем мы ожидаем получить поддержку соответствующих мероприятий от NIH и других финансирующих агентств.
Как я могу пожертвовать деньги Центру регенеративной медицины?
Центр регенеративной медицины зависит от благотворительной поддержки. Чтобы узнать, как вы можете помочь ускорить исследования и открытия, нажмите здесь.
В чем особенность Центра регенеративной медицины?
Центр регенеративной медицины посвящен пониманию того, как формируются ткани и как их можно восстановить в условиях травмы. Основная цель центра, расположенного на территории массовой больницы общего профиля, заключается в разработке новых методов лечения для восстановления поврежденных тканей и, таким образом, преодоления изнурительных хронических заболеваний. Успех этих усилий требует сплоченной команды ученых и клиницистов с различными областями знаний, но с общей миссией и преданностью более широкой цели.
Центр регенеративной медицины активно взаимодействует с другими исследователями в Mass General и в более широком сообществе Гарвардского Массачусетского технологического института. Центр помог стимулировать создание Гарвардского института стволовых клеток (HSCI), которым совместно руководят д-р Скадден и д-р Дуглас Мелтон из Гарвардского отделения стволовых клеток и регенеративной биологии и Медицинского института Говарда Хьюза. Являясь важным партнером HSCI, Центр предлагает определенные функции, которые дополняют другие элементы HSCI, включая уникальный опыт клинических исследований стволовых клеток и текущие совместные клинические испытания с использованием трансплантации стволовых клеток.Центр уделяет особое внимание технологиям, которые в конечном итоге будут иметь решающее значение для успеха медицины на основе стволовых клеток, включая биоинженерию, экспертизу биоматериалов, тесные связи с возможностями визуализации in vivo и его GMP-средство для сложных манипуляций с клетками.
Этические проблемы исследования стволовых клеток
Endocr Rev. 2009 May; 30 (3): 204–213.
Программа по медицинской этике, Отделение общей внутренней медицины и Медицинский факультет Калифорнийского университета в Сан-Франциско, Сан-Франциско, Калифорния 94143
Всю корреспонденцию и запросы на перепечатку направляйте по адресу: Dr.Бернард Ло, Программа медицинской этики Калифорнийского университета в Сан-Франциско, 521 Parnassus Avenue, Suite C-126, San Francisco, California 94143. Электронная почта: [email protected].Поступило 10 июля 2008 г .; Принято 10 марта 2009 г.
Эта статья цитировалась в других статьях в PMC.- Дополнительные материалы
[Примечание RPHR]
GUID: F71CC505-D7C5-47E1-80B3-6CCCEC708051
GUID: 3FA9B56E-7CE3-49CF-9AB9-C46497FDE547
Abstract
Исследования стволовых клеток открывают большие перспективы для понимания основных механизмов человеческого развития и дифференциации, а также дают надежду на новые методы лечения таких заболеваний, как диабет, травмы спинного мозга, болезнь Паркинсона и инфаркт миокарда.Однако исследования стволовых клеток человека (ЧСК) также вызывают острые этические и политические споры. Получение линий плюрипотентных стволовых клеток из ооцитов и эмбрионов чревато спорами о зарождении человеческой личности. Перепрограммирование соматических клеток для получения индуцированных плюрипотентных стволовых клеток позволяет избежать этических проблем, характерных для исследований эмбриональных стволовых клеток. Однако в любом исследовании hSC возникают сложные дилеммы в отношении чувствительных последующих исследований, согласия на предоставление материалов для исследования hSC, ранних клинических испытаний методов лечения hSC и надзора за исследованиями hSC.Эти этические и политические вопросы необходимо обсудить наряду с научными проблемами, чтобы гарантировать, что исследования стволовых клеток проводятся этически приемлемым образом. В этой статье представлен критический анализ этих проблем и того, как они решаются в текущих политиках.
I. Введение
II. Мультипотентные стволовые клетки
III. Исследование эмбриональных стволовых клеток
A. Существующие линии эмбриональных стволовых клеток
B.Новые линии эмбриональных стволовых клеток из замороженных эмбрионов
C. Этические проблемы донорства ооцитов для исследований
IV. Перенос ядра соматических клеток (SCNT)
V. Фетальные стволовые клетки
VI. Индуцированные плюрипотентные стволовые клетки (iPS-клетки)
VII. Клинические испытания стволовых клеток
VIII. Институциональный надзор за исследованиями стволовых клеток
I.Введение
ИССЛЕДОВАНИЕ СТВОЛОВЫХ КЛЕТОК открывает большие перспективы для понимания основных механизмов человеческого развития и дифференциации, а также дает надежду на новые методы лечения таких заболеваний, как диабет, травмы спинного мозга, болезнь Паркинсона и инфаркт миокарда (1). Плюрипотентные стволовые клетки сохраняют себя в культуре и могут дифференцироваться во все типы специализированных клеток. Ученые планируют дифференцировать плюрипотентные клетки в специализированные клетки, которые можно будет использовать для трансплантации.
Однако исследования стволовых клеток человека (hSC) также вызывают острые этические и политические споры. Получение линий плюрипотентных стволовых клеток из ооцитов и эмбрионов чревато спорами относительно начала человеческой личности и репродукции человека. Несколько других методов получения стволовых клеток вызывают меньше этических проблем. Перепрограммирование соматических клеток для получения индуцированных плюрипотентных стволовых клеток (iPS-клетки) позволяет избежать этических проблем, характерных для эмбриональных стволовых клеток. Однако при любом исследовании hSC возникают сложные дилеммы, включая согласие на предоставление материалов для исследования hSC, ранние клинические испытания методов лечения hSC и надзор за исследованиями hSC (2).В таблице 1 обобщены этические вопросы, возникающие на разных этапах исследования стволовых клеток.
Таблица 1
Этические проблемы на разных этапах исследования стволовых клеток
| Фаза исследования | Этические вопросы | |
|---|---|---|
| Пожертвование биологических материалов | h Информированное и добровольное согласие на исследования | |
| Уничтожение эмбрионов | ||
| Создание эмбрионов специально для исследовательских целей | ||
| 1.Выплаты донорам ооцитов | ||
| 2. Медицинские риски извлечения ооцитов | ||
| 3. Защита репродуктивных интересов женщин при лечении бесплодия | ||
| Использование линий стволовых клеток, полученных в другом учреждении | Конфликтный закон и этические стандарты | |
| Клинические испытания стволовых клеток | Риски и преимущества экспериментального вмешательства | |
| Информированное согласие |
II.Мультипотентные стволовые клетки
Взрослые стволовые клетки и стволовые клетки пуповинной крови не вызывают особых этических проблем и широко используются в исследованиях и клинической помощи. Однако эти клетки не могут быть размножены in vitro, и окончательно не доказано, что они обладают плюрипотентностью.
A. Стволовые клетки пуповинной крови
Гематопоэтические стволовые клетки из пуповинной крови могут храниться в банках и широко используются для трансплантации аллогенных и аутологичных стволовых клеток при педиатрических гематологических заболеваниях в качестве альтернативы трансплантации костного мозга.
B. Взрослые стволовые клетки крови
Взрослые стволовые клетки встречаются во многих тканях и могут дифференцироваться в специализированные клетки в своей ткани происхождения, а также трансдифференцироваться в специализированные клетки, характерные для других тканей. Например, гемопоэтические стволовые клетки могут дифференцироваться во все три типа клеток крови, а также в нервные стволовые клетки, кардиомиоциты и клетки печени.
Взрослые стволовые клетки можно выделить с помощью плазмафереза. Они уже используются для лечения гематологических злокачественных новообразований и для коррекции побочных эффектов химиотерапии рака.Кроме того, аутологичные стволовые клетки используются в клинических испытаниях у пациентов, перенесших инфаркт миокарда. Их использование в некоторых других условиях не было подтверждено или является экспериментальным, несмотря на некоторые утверждения об обратном (3).
III. Исследование эмбриональных стволовых клеток
Линии плюрипотентных стволовых клеток могут быть получены из внутренней клеточной массы бластоцисты возрастом 5-7 дней. Однако исследование эмбриональных стволовых клеток человека (hESC) является этически и политически спорным, потому что оно связано с разрушением человеческих эмбрионов.В Соединенных Штатах вопрос о том, когда начинается человеческая жизнь, является весьма спорным и тесно связан с дебатами по поводу абортов. То, что эмбрионы могут стать людьми, не оспаривается; при имплантации в матку женщины на соответствующей гормональной фазе эмбрион может имплантироваться, превратиться в плод и стать живорожденным ребенком.
Некоторые люди, однако, считают, что эмбрион — это человек с таким же моральным статусом, что и взрослый или живорожденный ребенок. С точки зрения религиозной веры и моральных убеждений они считают, что «человеческая жизнь начинается с момента зачатия» и, следовательно, эмбрион — это личность.Согласно этой точке зрения, у эмбриона есть интересы и права, которые необходимо уважать. С этой точки зрения взятие бластоцисты и удаление внутренней клеточной массы для получения линии эмбриональных стволовых клеток равносильно убийству (4).
Многие другие люди по-другому смотрят на моральный статус эмбриона, например, что эмбрион становится человеком в моральном смысле на более поздней стадии развития, чем оплодотворение. Однако немногие люди считают, что эмбрион или бластоциста — это просто скопление клеток, которое можно использовать для исследований без ограничений.Многие придерживаются золотой середины, что ранний эмбрион заслуживает особого уважения как потенциальный человек, но что его можно использовать для определенных типов исследований при условии хорошего научного обоснования, тщательного контроля и осознанного согласия женщины или пары на донорство. эмбрион для исследования (5).
Оппозиция исследованиям hESC часто ассоциируется с противодействием аборту и движением «за жизнь». Однако такое противодействие исследованиям стволовых клеток не является монолитным.Ряд лидеров сторонников жизни поддерживают исследования стволовых клеток с использованием замороженных эмбрионов, которые остаются после того, как женщина или пара завершили лечение бесплодия, и которые они решили не передавать другой паре. Такого мнения придерживаются, например, бывшая первая леди Нэнси Рейган и сенатор США Оррин Хэтч.
На своем веб-сайте Сената сенатор Хэтч заявляет: «Поддержка исследований эмбриональных стволовых клеток соответствует ценностям защиты жизни и семьи.
«Я считаю, что человеческая жизнь начинается в утробе матери, а не в чашке Петри или холодильнике….Для меня мораль ситуации диктует, что эти эмбрионы, которые обычно выбрасываются, должны использоваться для улучшения и спасения жизней. Трагедия заключалась бы в том, что эти эмбрионы не использовались для спасения жизней, в то время как альтернатива состоит в том, чтобы их выбросить »(6).
A. Существующие линии эмбриональных стволовых клеток
В 2001 году президент Буш, который придерживается решительных взглядов на жизнь, разрешил федеральным национальным институтам здравоохранения (NIH) финансирование исследований стволовых клеток с использованием линий эмбриональных стволовых клеток, которые уже существовали в то время. , запрещая при этом финансирование NIH для получения или использования дополнительных линий эмбриональных стволовых клеток.Эта политика была ответом на растущее ощущение того, что исследования hESC открывают большие перспективы для понимания и лечения дегенеративных заболеваний, при этом все еще выступая против дальнейшего разрушения человеческих эмбрионов. Многие исследователи рассматривали финансирование NIH как необходимое условие для привлечения ученых к долгосрочному изучению базовой биологии стволовых клеток; без сильной фундаментальной научной платформы терапевтический прорыв был бы менее вероятен.
Президент Буш объяснил эту политику тем, что эмбрионы, из которых были получены эти линии, уже были уничтожены.Если разрешить исследование линий стволовых клеток, то их разрушение может принести пользу. Однако использование только существующих линий эмбриональных стволовых клеток с научной точки зрения проблематично. Первоначально NIH объявил, что более 60 линий hESC будут приемлемы для финансирования NIH. Однако большинство этих линий не подходили для исследования; например, они не были действительно плюрипотентными, были заражены или были недоступны для транспортировки. По состоянию на январь 2009 г. 22 линии hESC имеют право на финансирование NIH.Однако эти линии могут быть небезопасными для трансплантации человеку, и было показано, что давно существующие линии накапливают мутации, в том числе некоторые из них, которые, как известно, предрасполагают к раку. Кроме того, были высказаны опасения по поводу процесса получения согласия на вывод некоторых из этих утвержденных NIH линий (7). Подавляющее большинство научных экспертов, включая директора Национального института здоровья при президенте Буше, считают, что отсутствие доступа к новым линиям эмбриональных стволовых клеток препятствует прогрессу в трансплантации на основе стволовых клеток (8).Например, линии от более широкого круга доноров позволили бы большему количеству пациентов получить трансплантаты стволовых клеток, соответствующие человеческому лейкоцитарному агенту (9).
В настоящее время федеральные фонды не могут быть использованы для получения новых линий эмбриональных стволовых клеток или для работы с линиями чЭСК, не включенными в утвержденный список NIH. Оборудование и лабораторные помещения, финансируемые NIH, не могут использоваться для исследований неутвержденных линий hESC. Как создание новых линий hESC, так и исследования с линиями hESC, не одобренные NIH, могут проводиться при нефедеральном финансировании.Из-за этих ограничений на финансирование NIH ряд штатов учредили программы по финансированию исследований стволовых клеток, включая получение новых линий эмбриональных стволовых клеток. Калифорния, например, выделила 3 миллиарда долларов в течение 10 лет на исследования стволовых клеток.
При президенте Обаме ожидается, что федеральное финансирование будет доступно для проведения исследований с линиями hESC, не включенными в список NIH, и для получения новых линий hESC из замороженных эмбрионов, пожертвованных для исследования после того, как женщина или пара использовали in vitro оплодотворение (ЭКО) определило, что они больше не нужны для репродуктивных целей.Однако федеральное финансирование может быть запрещено для создания эмбрионов специально для исследований или для получения линий стволовых клеток с использованием переноса ядра соматических клеток (SCNT) (10,11).
B. Новые линии эмбриональных стволовых клеток из замороженных эмбрионов
У женщин и супружеских пар, которые проходят лечение от бесплодия, часто остаются замороженные эмбрионы после завершения лечения бесплодия. Решение относительно размещения этих замороженных эмбрионов часто является трудным для них (12). Некоторые предпочитают жертвовать оставшиеся эмбрионы на исследования, а не передавать их другой паре для репродуктивных целей или уничтожать их.При донорстве замороженного эмбриона возникает ряд этических проблем, в том числе информированное согласие женщины или пары, передающей эмбрион, согласие доноров гамет, участвующих в создании эмбриона, и конфиденциальность информации о доноре.
1. Информированное согласие на передачу материалов для исследования стволовых клеток.
Со времен Нюрнбергского кодекса информированное согласие считается основным требованием для исследований с участием людей. Согласие особенно важно при исследованиях с человеческими эмбрионами (13).Представители общественности и потенциальные доноры эмбрионов для исследований придерживаются сильных и разнообразных мнений по этому поводу. Некоторые считают все исследования эмбрионов неприемлемыми; другие поддерживают только некоторые формы исследований. Например, человек может считать исследование бесплодия приемлемым, но возражать против исследования с целью получения линий стволовых клеток или исследований, которые могут привести к патентам или коммерческим продуктам (14). Получение информированного согласия на возможное использование донорского эмбриона в будущем учитывает это разнообразие взглядов.Кроме того, люди обычно придают особое эмоциональное и моральное значение своим репродуктивным материалам по сравнению с другими тканями (15).
2. Отказ от согласия.
В Соединенных Штатах федеральные правила проведения исследований разрешают отказ от информированного согласия на использование в исследованиях деидентифицированных биологических материалов, которые не могут быть связаны с донорами (16). Таким образом, с логистической точки зрения можно было бы проводить исследования эмбрионов и стволовых клеток на деидентифицированных материалах без согласия.Например, во время процедур ЭКО обычно выбрасываются ооциты, которые не могут оплодотворяться, или эмбрионы, которые не могут развиться в достаточной степени для имплантации. Эти материалы могут быть деидентифицированы, а затем использованы исследователями. Кроме того, если у пациентов с бесплодием остались замороженные эмбрионы, оставшиеся после завершения лечения, программа ЭКО обычно связывается с ними, чтобы решить, хотят ли они продолжать хранить эмбрионы (и платить ли они за хранение в морозильной камере), передать их другой бесплодной женщине или пара или отказаться от них.Если пациент решит выбросить эмбрионы, вместо этого можно будет удалить идентификаторы и использовать их для исследований. Еще одна возможность связана с замороженными эмбрионами от пациентов, которые не отвечают на запросы о принятии решения относительно утилизации замороженных эмбрионов. Некоторые практики ЭКО имеют политику отбрасывания таких эмбрионов и информируют пациентов об этой политике, когда они дают согласие на процедуры ЭКО. Опять же, вместо того, чтобы выбрасывать такие замороженные эмбрионы, логично деидентифицировать их и передать исследователям.
Однако этическое обоснование разрешения использования деидентифицированных биологических материалов для исследований без согласия не всегда справедливо для исследований эмбрионов (13). Например, одно из оснований для разрешения использования деидентифицированных материалов состоит в том, что этические риски очень низкие; не может быть нарушения конфиденциальности, что является основной проблемой в исследованиях такого типа. Второе объяснение состоит в том, что люди не возражали бы против использования их материалов таким образом, если бы их спросили.Однако это предположение не обязательно справедливо в контексте исследования эмбрионов. Исследование 2007 года показало, что 49% женщин с замороженными эмбрионами были бы готовы пожертвовать их для исследования (12). Такие доноры могут обидеться или почувствовать себя обиженными, если их замороженные эмбрионы будут использоваться для исследований, на которые они не давали согласия. Деидентификация материалов не решит их проблем.
3. Согласие доноров гамет.
Замороженные эмбрионы могут быть созданы из сперматозоидов или ооцитов от доноров, которые больше не участвуют в вспомогательной репродукции или воспитании детей.Некоторые люди утверждают, что согласие от доноров гамет не требуется для исследования эмбрионов, потому что они уступили свое право на дальнейшее использование своих гамет пациентам, получавшим искусственные репродуктивные технологии (ВРТ). Однако доноры гамет, которые хотят помочь женщинам и супружеским парам иметь детей, могут возражать против использования их генетических материалов для исследований. В одном исследовании 25% женщин, которые пожертвовали ооциты для лечения бесплодия, не хотели, чтобы созданные эмбрионы использовались в исследованиях (17). Этот процент не является неожиданным, потому что репродуктивные материалы имеют особое значение, и многие люди в Соединенных Штатах выступают против исследований эмбрионов.Мало что известно о пожеланиях доноров спермы относительно исследований.
Существуют существенные практические различия между получением согласия на исследование эмбрионов от доноров ооцитов и от доноров спермы. Клиники АРТ могут легко обсудить вопрос о донорстве для исследования с донорами ооцитов во время визитов для стимуляции и извлечения ооцитов. Однако большинство клиник АРТ получают донорскую сперму из банков спермы и, как правило, не имеют прямого контакта с донорами. Кроме того, сперма часто передается анонимно банкам спермы с соблюдением строгих положений о конфиденциальности.
Из уважения к донорам гамет их пожелания относительно получения стволовых клеток должны быть определены и соблюдены (13). Доноры гамет, которые хотят помочь женщинам и супружеским парам иметь детей, могут возражать против использования их генетических материалов для исследований. Конкретное согласие на исследование стволовых клеток от доноров эмбрионов и гамет было рекомендовано Национальной академией наук 2005 г. в Руководстве по исследованиям стволовых клеток человека и было принято Калифорнийским институтом регенеративной медицины (CIRM), государственным агентством, финансирующим исследования стволовых клеток. (18,19).Это требование согласия не обязательно подразумевает, что эмбрионы являются людьми или что гаметы или эмбрионы являются объектами исследования.
4. Конфиденциальность донорской информации.
Необходимо тщательно защищать конфиденциальность в исследованиях эмбрионов и чЭСК, поскольку нарушение конфиденциальности может стать причиной нежелательной огласки или даже преследования доноров со стороны противников исследования чЭСК (20). Хотя идентифицирующая информация о донорах должна быть сохранена в случае аудита Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов в рамках процесса утверждения новых методов лечения, опасения по поводу конфиденциальности могут удерживать некоторых доноров от согласия на повторный контакт.
В последнее время конфиденциальность личной медицинской информации была нарушена в результате преднамеренных нарушений со стороны персонала, взломов компьютерных хакеров, а также в результате потери или кражи портативных компьютеров. Файлы, содержащие данные о лицах, чьи гаметы или эмбрионы использовались для получения линий hESC, должны быть защищены с помощью усиленных мер безопасности (20). Любой компьютер, на котором хранятся такие файлы, должен быть заперт в безопасном помещении и защищен паролем, а доступ должен быть ограничен минимальным числом лиц на основе строгой служебной необходимости.Вход в компьютерное хранилище также должен быть ограничен с помощью ключа-карты или аналогичной системы, которая фиксирует каждую запись. Журналы аудита доступа к информации должны регулярно проверяться на предмет несоответствующего доступа. Файлы с идентификаторами должны быть защищены от копирования и дважды зашифрованы, причем один из ключей должен находиться у высокопоставленного должностного лица учреждения, не участвующего в исследованиях стволовых клеток. Компьютер, на котором хранятся эти данные, не должен быть подключен к Интернету. Чтобы защитить информацию от повестки в суд, следователи должны получить федеральный сертификат конфиденциальности.Также следует учитывать человеческий фактор при нарушении конфиденциальности. Персонал, имеющий доступ к этим идентификаторам, может пройти дополнительную проверку биографических данных, интервью и обучение. Персонал, ответственный за ведение этой конфиденциальной базы данных и контакт с любым донором, не должен входить в состав какой-либо исследовательской группы.
Исследование hESC с использованием свежих ооцитов, пожертвованных для исследований, также поднимает несколько дополнительных этических проблем, которые мы обсудим ниже (21).
C. Этические опасения по поводу донорства ооцитов для исследований
Обеспокоенность по поводу донорства ооцитов специально для исследований особенно серьезна после скандала с Хванем в Южной Корее, в ходе которого были сфабрикованы широко разрекламированные заявления о получении линий SCNT человека.Помимо научного мошенничества, скандал был связан с ненадлежащими выплатами донорам ооцитов, серьезными недостатками в процессе получения информированного согласия, ненадлежащим влиянием на персонал и молодых ученых в качестве доноров и неприемлемо высокой частотой медицинских осложнений при донорстве ооцитов (22,23). , 24). В Калифорнии некоторые законодатели и представители общественности заявили, что клиники по лечению бесплодия преуменьшают риски донорства ооцитов (19). CIRM ввел в действие несколько средств защиты женщин, жертвующих ооциты, в рамках финансируемых государством исследований стволовых клеток.
1. Медицинские риски при извлечении ооцитов.
Медицинские риски при извлечении ооцитов включают синдром гиперстимуляции яичников, кровотечение, инфекцию и осложнения анестезии (25). Эти риски можно минимизировать путем исключения доноров с высоким риском этих осложнений, тщательного мониторинга количества развивающихся фолликулов и корректировки дозы хорионического гонадотропина человека, вводимой для индукции овуляции или отмены цикла (25).
Поскольку синдром тяжелой гиперовуляции может потребовать госпитализации или хирургического вмешательства, женщины, сдающие ооциты для исследований, должны быть защищены от затрат, связанных с осложнениями, связанными с гормональной стимуляцией и извлечением ооцитов (19).В США нет всеобщего медицинского страхования. Честно говоря, женщины, которые подвергаются инвазивной процедуре в интересах науки и не получают оплаты сверх расходов, не должны нести никаких затрат на лечение осложнений. Даже если у женщины есть медицинская страховка, доплаты и отчисления могут быть значительными, и если она позже подаст заявку на индивидуальное страхование здоровья, ее взносы могут оказаться непомерно высокими. Компенсация за травмы, полученные в результате исследований, была рекомендована несколькими У.S. Panel (26), но не был принят из-за трудностей с расчетом долгосрочного актуарного риска и оценкой влияющих факторов, которые могут способствовать или вызывать нежелательные явления.
Требование бесплатной медицинской помощи при краткосрочных осложнениях донорства ооцитов возможно. В Калифорнии исследовательские институты должны обеспечить бесплатное лечение доноров ооцитов в случае прямых и ближайших медицинских осложнений при извлечении ооцитов в рамках исследований, финансируемых государством. Термин «прямой и непосредственный» — это юридическая концепция, определяющая, насколько тесно травма должна быть связана с событием или условием, чтобы возложить ответственность за травму на лицо, выполнившее событие или создавшее состояние.Полисы коммерческого страхования доступны для покрытия краткосрочных осложнений при извлечении ооцитов. CIRM позволяет государственным грантам на стволовые клетки покрывать стоимость такой страховки. Обоснование возложения ответственности за лечение на исследовательские учреждения состоит в том, что они находятся в лучшем положении, чем отдельные исследователи, в плане определения страховых полисов и у них будет стимул рассмотреть вопрос о распространении такого покрытия на другие травмы, полученные в результате исследований.
2. Защита репродуктивных интересов женщин при лечении бесплодия.
Если женщины, проходящие лечение от бесплодия, делятся ооцитами с исследователями — либо своими собственными ооцитами, либо ооцитами от донора ооцитов — их перспектива репродуктивного успеха может быть поставлена под угрозу, поскольку для репродуктивных целей доступно меньшее количество ооцитов (21). В этой ситуации врач, занимающийся извлечением ооцитов и лечением бесплодия, должен уделять приоритетное внимание репродуктивным потребностям пациентки при ЭКО. Ооциты самого высокого качества следует использовать в репродуктивных целях (21).
Как описано в Разделе B.2 , в программах ЭКО некоторые ооциты не могут оплодотворяться, а некоторые эмбрионы не могут развиться в достаточной степени для имплантации. Такие материалы могут быть переданы исследователям. Для защиты репродуктивных интересов доноров необходимо принять ряд мер безопасности (20). Что касается донорства свежих эмбрионов для исследований, решение эмбриолога о том, что эмбрион не подходит для имплантации и, следовательно, его следует выбросить, является предметом суждения. Точно так же определение того, что ооцит не смог оплодотвориться и, следовательно, не может быть использован для воспроизводства, является требованием суждения.Во избежание конфликта интересов эмбриолог не должен знать, согласилась ли женщина на пожертвование на исследование, а также не должен получать финансирование из грантов, связанных с исследованием. Кроме того, лечащие врачи по лечению бесплодия не должны знать, согласны ли их пациенты жертвовать материалы для исследования.
3. Выплата донорам ооцитов.
Во многих юрисдикциях существуют противоречивые правила оплаты донорам ооцитов. Возмещение донорам ооцитов личных расходов не представляет этических проблем, поскольку доноры не получают финансовой выгоды от участия в исследовании.Однако оплата донорам ооцитов сверх разумных личных расходов вызывает споры, и юрисдикции имеют противоречивую политику, которая также может быть внутренне непоследовательной (27,28).
Можно привести веские аргументы как за, так и против выплаты донорам ооцитов, превышающих их расходы (29). С одной стороны, некоторые возражают, что такие выплаты побуждают женщин брать на себя чрезмерный риск, особенно женщин с низким уровнем образования, у которых ограниченные возможности для трудоустройства, как это произошло во время хванского скандала.Однако такие опасения по поводу ненадлежащего влияния могут быть устранены без запрета на оплату. Например, участникам могут быть заданы вопросы, чтобы убедиться, что они понимают ключевые особенности исследования и чувствуют, что у них есть выбор в отношении участия (19). Кроме того, тщательный мониторинг и корректировка доз гормонов могут минимизировать риски, связанные с донорством ооцитов (25). Еще одно возражение состоит в том, что оплата труда женщин, предоставляющих ооциты для исследований, подрывает человеческое достоинство, потому что человеческие биологические материалы и интимные отношения обесцениваются, если эти материалы покупаются и продаются как товары (14,30).
С другой стороны, некоторые утверждают, что несправедливо запрещать выплаты донорам ооцитов для исследований, в то же время позволяя женщинам получать тысячи долларов США для прохождения тех же процедур по предоставлению ооцитов для лечения бесплодия (29). Более того, здоровым добровольцам, мужчинам и женщинам, платят за прохождение других инвазивных исследовательских процедур, таких как биопсия печени, в исследовательских целях. Более того, запреты на оплату донорства ооцитов для исследований критиковались как патерналистские, лишающие женщин права принимать самостоятельные решения (31).С практической точки зрения, без такой оплаты очень сложно привлечь доноров ооцитов для исследования.
4. Информированное согласие на донорство ооцитов.
В Калифорнии CIRM ввел повышенные требования к информированному согласию на донорство ооцитов для исследований (19). Правила CIRM выходят за рамки требований раскрытия информации донорам ооцитов (19). Главный этический вопрос заключается в том, ценят ли доноры ключевую информацию о донорстве ооцитов, а не просто то, была ли им раскрыта эта информация или нет.Как обсуждалось ранее, в других условиях исследования участники исследования часто не понимают информацию в подробных формах согласия (32). Таким образом, CIRM считает, что раскрытие информации, хотя и необходимо, не является достаточным для гарантии информированного согласия. В исследованиях, финансируемых CIRM, донорам ооцитов необходимо задавать вопросы, чтобы убедиться, что они понимают ключевые особенности исследования (19). Оценка понимания возможна, потому что она проводилась в других исследовательских контекстах, таких как испытания средств профилактики ВИЧ в развивающихся странах (33).Согласно показаниям, представленным CIRM, оценка понимания также проводилась в отношении донорства ооцитов для служб клинического бесплодия.
IV. Перенос ядра соматических клеток (SCNT)
Линии плюрипотентных стволовых клеток, ядерная ДНК которых соответствует конкретному человеку, имеют несколько научных преимуществ. Линии стволовых клеток, сопоставленные с людьми с конкретными заболеваниями, могут служить in vitro, моделями заболеваний, выяснять патофизиологию заболеваний и проверять потенциальные новые методы лечения.Линии, предназначенные для конкретных людей, также обещают индивидуальную трансплантацию аутологичных стволовых клеток.
Один из подходов к созданию таких линий — использование SCNT, техники, которая позволила создать овечку Долли. В SCNT перепрограммирование достигается после переноса ядерной ДНК из клетки-донора в ооцит, из которого было удалено ядро. Однако создание линий стволовых клеток человека SCNT на сегодняшний день не только невозможно с научной точки зрения, но и является спорным с этической точки зрения (34,35).
A. Этические проблемы SCNT
1. Возражения против создания эмбрионов специально для исследований.
Некоторые люди, возражающие против SCNT, считают, что создание эмбрионов с намерением использовать их для исследований и их уничтожение в этом процессе нарушает уважение к зарождающейся человеческой жизни. Даже те, кто поддерживает получение линий стволовых клеток из замороженных эмбрионов, которые в противном случае были бы отброшены, иногда отвергают намеренное создание эмбрионов для исследований. В качестве опровержения, однако, некоторые утверждают, что плюрипотентные сущности, созданные посредством SCNT, биологически и этически отличаются от эмбрионов (36).
2. Возражения против воспроизводства человека с использованием SCNT.
Есть несколько веских возражений против использования SCNT для репродукции человека. Во-первых, из-за ошибок при перепрограммировании генетического материала клонированные эмбрионы животных не могут активировать ключевые эмбриональные гены, а новорожденные клоны неправильно экспрессируют сотни генов (37,38). Риск серьезных врожденных дефектов у людей будет недопустимо высоким. Во-вторых, даже если бы SCNT можно было безопасно проводить на людях, некоторые считают, что это нарушает человеческое достоинство и подрывает традиционные, фундаментальные моральные, религиозные и культурные ценности (34).Клонированный ребенок будет иметь только одного генетического родителя и будет генетическим двойником этого родителя. С этой точки зрения, клонирование приведет к тому, что детей будут рассматривать скорее как «продукты продуманного производственного процесса, чем как« подарки », которые их родители готовы принять такими, какие они есть». Более того, клонирование нарушило бы «естественные границы между поколениями» (34). По этим причинам клонирование в репродуктивных целях считается морально неправильным и незаконным в ряде штатов. Более того, некоторые люди утверждают, что, поскольку метод SCNT может быть использован для воспроизведения, его разработка и использование для фундаментальных исследований должны быть запрещены.
3. Использование ооцитов животных для создания линий SCNT с использованием ДНК человека.
Из-за нехватки человеческих ооцитов для исследования SCNT некоторые ученые хотят использовать нечеловеческие ооциты для получения линий с использованием ядерной ДНК человека. Эти так называемые «цитоплазматические гибридные эмбрионы» вызывают ряд этических проблем. Некоторые противники опасаются создания химер — мифических зверей, которые выглядят наполовину людьми и наполовину животными и имеют характеристики как людей, так и животных (39). Оппоненты могут испытывать глубокое моральное беспокойство или отвращение, не выражая своих опасений более конкретно.Некоторые люди считают, что такие гибридные эмбрионы противоречат моральному порядку, воплощенному в мире природы и законах природы. С этой точки зрения, у каждого вида есть определенная моральная цель или цель, которую человечество не должно пытаться изменить. Другие рассматривают такие исследования как неуместное преодоление видовых барьеров, что должно быть неизменной частью естественного замысла. Наконец, некоторые обеспокоены тем, что могут быть попытки имплантировать эти эмбрионы в репродуктивных целях.
В качестве опровержения сторонники такого исследования указывают, что биологические определения видов не являются естественными и неизменными, а являются эмпирическими и прагматическими (40,41,42).Гибриды животных и животных различных видов, такие как мул, существуют и не считаются неприемлемыми с моральной точки зрения. Более того, в медицинских исследованиях человеческие клетки обычно вводятся нечеловеческим животным и включаются в их функционирующие ткани. Действительно, это широко проводится в исследованиях со всеми типами стволовых клеток, чтобы продемонстрировать, что клетки плюрипотентны или дифференцировались в желаемый тип клеток. Кроме того, некоторые проблемы могут быть решены посредством строгого надзора (40), например, запрета репродуктивного использования этих эмбрионов и ограничения развития in vitro до 14 дней или развития примитивной полоски, ограничений, которые широко приняты для других исследований чЭСК. .Наконец, некоторые люди считают отвращение per se неубедительным руководством к этическим суждениям. Люди расходятся во мнениях относительно того, что отвратительно, и их взгляды со временем могут измениться. Переливание крови и трансплантация трупных органов изначально считались отвратительными, но теперь они широко распространены. Более того, после публичного обсуждения и обучения многие люди преодолевают свои первоначальные опасения.
V. Стволовые клетки плода
Плюрипотентные стволовые клетки могут быть получены из ткани плода после аборта.Однако использование тканей плода является спорным с этической точки зрения, потому что оно связано с абортом, против чего многие люди возражают. В соответствии с федеральными правилами исследования с тканями плода разрешены при условии, что передача ткани для исследования рассматривается только после принятия решения о прерывании беременности. Это требование сводит к минимуму возможность того, что на решение женщины о прерывании беременности может повлиять перспектива участия ткани в исследовании. В настоящее время проходит фаза 1 клинических испытаний болезни Баттена, летального дегенеративного заболевания, поражающего детей, с использованием нервных стволовых клеток, полученных из ткани плода (43,44).
VI. Индуцированные плюрипотентные стволовые клетки (iPS-клетки)
Соматические клетки могут быть перепрограммированы с образованием плюрипотентных стволовых клеток (45,46), называемых индуцированными плюрипотентными стволовыми клетками (iPS-клетки). Эти линии iPS-клеток будут иметь ДНК, совпадающую с ДНК доноров соматических клеток, и будут полезны в качестве моделей заболеваний и, возможно, для аллогенной трансплантации.
Ранние клеточные линии iPS были получены путем вставки генов, кодирующих факторы транскрипции, с использованием ретровирусных векторов. Исследователи пытались устранить опасения по поводу безопасности, связанные с внедрением онкогенов и инсерционным мутагенезом.Перепрограммирование было успешно выполнено без известных онкогенов и с использованием аденовирусных векторов, а не ретровирусных векторов. Следующим шагом была недавняя демонстрация того, что человеческие эмбриональные фибробласты могут быть перепрограммированы до плюрипотентного состояния с использованием плазмиды с пептидно-связанной кассетой репрограммирования (47,48). Мало того, что перепрограммирование было выполнено без использования вируса, трансген может быть удален после завершения перепрограммирования. Конечная цель — вызвать плюрипотентность без генетических манипуляций.Из-за нерешенных проблем с iPS-клетками, которые в настоящее время исключают их использование для клеточной терапии, большинство ученых призывают к продолжению исследований с hESC (49).
iPS-клетки избегают жарких споров по поводу этики исследования эмбриональных стволовых клеток, поскольку не используются эмбрионы или ооциты. Кроме того, поскольку биопсия кожи для получения соматических клеток является относительно неинвазивной, риск для доноров вызывает меньше опасений по сравнению с донорством ооцитов. Президентский совет по биоэтике назвал iPS-клетки «этически беспроблемными и приемлемыми для использования на людях» (39).Ни передача материалов для получения iPS-клеток, ни их получение не вызывают особых этических проблем.
A. Последующие исследования
Некоторые потенциальные последующие применения производных iPS-клеток могут быть настолько чувствительными, что ставит под сомнение согласие первоначальных доноров соматических клеток на такое использование (50). iPS-клетки будут широко распространены среди исследователей, которые будут проводить различные исследования с iPS-клетками и их производными, используя общепринятые и общепринятые научные практики, такие как:
Генетические модификации клеток
Инъекция производных клеток в нечеловеческих животных, чтобы продемонстрировать их функции, включая инъекции в мозг нечеловеческих животных.
Крупномасштабное секвенирование генома
Совместное использование клеточных линий с другими исследователями с соответствующими гарантиями конфиденциальности и
Патентование научных открытий и разработка коммерческих тестов и методов лечения без разделения гонорара с донорами (51) .
Эти стандартные методы исследования широко используются в других типах фундаментальных исследований, включая исследования стволовых клеток из других источников. Как правило, доноры биологических материалов явно не информируются об этих исследовательских процедурах, хотя такое раскрытие теперь предлагается для полногеномного секвенирования (52,53).
Такие исследования имеют фундаментальное значение в биологии стволовых клеток, например, для характеристики линий и демонстрации их плюрипотентности. Крупномасштабное секвенирование генома позволит получить представление о патогенезе заболевания и выявить новые цели для лечения. Инъекции человеческих стволовых клеток в мозг нечеловеческих животных потребуются для доклинических испытаний клеточной терапии многих состояний, таких как болезнь Паркинсона, болезнь Альцгеймера и инсульт.
Однако некоторые последующие исследования могут также вызвать этические проблемы.Например, крупномасштабное секвенирование генома может вызвать опасения по поводу конфиденциальности и конфиденциальности. Доноры могут посчитать это нарушением конфиденциальности, если ученые будут знать их будущую предрасположенность ко многим генетическим заболеваниям. Кроме того, возможно повторно идентифицировать донора деидентифицированной крупномасштабной последовательности генома, используя информацию в судебно-медицинских базах данных ДНК или в интернет-компании, предлагающей индивидуальное геномное тестирование (54,55). Другие доноры могут возражать против введения их клеток животным.Например, они могут выступать против всех исследований на животных или иметь религиозные возражения против смешения видов людей и животных. Инъекция человеческих нейральных клеток-предшественников нечеловеческим животным вызвала этические опасения по поводу развития у животных характеристик, которые считаются исключительно человеческими (56,57). Тем не менее другие доноры могут не захотеть патентовать клеточные линии, полученные из их биологических материалов, в качестве шага к разработке новых тестов и методов лечения. Люди вряд ли откажутся от таких возражений, даже если клеточные линии были деидентифицированы или даже если с момента первоначального пожертвования прошло много лет.Таким образом, может возникнуть противоречие между уважением автономии доноров и получением научной пользы от исследований, которое может быть разрешено в процессе получения согласия на первоначальное пожертвование материалов.
Было бы прискорбно, если бы линии iPS-клеток, которые оказались чрезвычайно полезными с научной точки зрения (например, из-за устойчивого роста в культуре ткани), не могли бы использоваться в дополнительных исследованиях, поскольку донор соматических клеток возражал. Один из подходов, позволяющих избежать этого, заключается в предпочтительном использовании соматических клеток от доноров, которые готовы разрешить все такие базовые исследования стволовых клеток и чтобы с ними связывались для будущих чувствительных исследований, которые нельзя ожидать во время получения согласия (50).Донорам также может быть предложено согласие на дополнительные специфические типы чувствительных, но не фундаментальных последующих исследований, таких как аллогенная трансплантация другим людям и репродуктивные исследования, включающие создание тотипотентных сущностей.
Поскольку эти опасения по поводу согласия на чувствительные последующие исследования также применимы к другим типам стволовых клеток, было бы разумно ввести аналогичные стандарты для согласия на пожертвование материалов для получения других типов стволовых клеток.Однако эти опасения особенно важны для iPS-клеток из-за широко распространенного мнения, что эти клетки не вызывают серьезных этических проблем, и потому, что они, вероятно, будут играть все более важную роль в исследованиях стволовых клеток.
VII. Клинические испытания стволовых клеток
Трансплантация клеток, полученных из плюрипотентных стволовых клеток, открывает новые перспективы эффективных методов лечения. Однако такая трансплантация также связана с большой неопределенностью и возможностью серьезных рисков. Было показано, что некоторые методы лечения стволовыми клетками являются эффективными и безопасными, например, трансплантация гемопоэтических стволовых клеток при лейкемии и лечение ожогов и заболеваний роговицы на основе эпителиальных стволовых клеток (58).Однако «в мире есть несколько клиник, которые уже эксплуатируют надежды пациентов, предлагая эффективную терапию стволовыми клетками для тяжелобольных пациентов, как правило, за большие суммы денег, но без надежного научного обоснования, прозрачности, надзора или защиты пациентов» ( 58). Поддерживая медицинские инновации в очень ограниченных обстоятельствах, Международное общество исследований стволовых клеток осудило такое использование недоказанной трансплантации hSC.
Эти клинические испытания должны следовать этическим принципам, которыми руководствуются все клинические исследования, включая соответствующий баланс рисков и преимуществ и информированное, добровольное согласие.Также необходимы дополнительные этические требования для улучшения дизайна испытаний, координации научных и этических обзоров, проверки понимания участниками ключевых особенностей испытания и обеспечения публикации отрицательных результатов (59). Эти меры уместны из-за в высшей степени инновационного характера вмешательства, ограниченного опыта работы с людьми и больших надежд пациентов, у которых нет эффективных методов лечения.
A. Риски и предполагаемые преимущества при клинических испытаниях стволовых клеток
Риски инновационных вмешательств на основе стволовых клеток включают «образование опухоли, иммунологические реакции, неожиданное поведение клеток и неизвестные долгосрочные последствия для здоровья» (58).Доказательства безопасности и доказательства принципа должны быть получены с помощью соответствующих доклинических исследований на соответствующих моделях животных или с помощью исследований аналогичных клеточных вмешательств на людях. Требования к доказательству принципа действия и безопасности должны быть выше, если клетки подвергались интенсивным манипуляциям in vitro или были получены из плюрипотентных стволовых клеток (58).
Однако даже с этими мерами предосторожности из-за высоко инновационного характера вмешательства и ограниченного опыта у людей могут произойти непредвиденные серьезные побочные эффекты.В более ранних клинических испытаниях трансплантации дофаминергических нейронов плода людям с болезнью Паркинсона трансплантированные клетки не улучшали клинические исходы (60,61). Действительно, примерно у 15% пациентов, перенесших трансплантацию с опозданием, развились дискинезии, приводящие к потере трудоспособности, при этом некоторым потребовалась абляционная операция для купирования этих побочных эффектов (60,61). Хотя трансплантированные клетки, локализованные в целевых областях мозга, прижились и функционировали, вырабатывая намеченные нейротрансмиттеры, должным образом регулируемая физиологическая функция не была достигнута.Участники испытаний фазы I могут не до конца осознавать возможность того, что трансплантация чЭСК может ухудшить их состояние.
B. Информированное согласие в ранних клинических испытаниях стволовых клеток
Проблемы с информированным согласием хорошо задокументированы в клинических испытаниях фазы I. Участники клинических испытаний рака обычно ожидают, что они лично выиграют от испытания, хотя основная цель испытаний фазы I — проверить безопасность, а не эффективность (62). Эта тенденция рассматривать клинические исследования как приносящие личную пользу была названа «терапевтическим заблуждением» (32,63).Анализ клинических испытаний онкологических заболеваний показывает, что информация в формах согласия в целом является адекватной. Однако на ранней стадии клинических испытаний переноса генов I описания исследователями непосредственной пользы для участников обычно были расплывчатыми, двусмысленными и неопределенными (64).
Участники фазы I клинических испытаний стволовых клеток могут переоценить свои преимущества и недооценить риски. Научное обоснование трансплантации hSC и доклинические результаты могут показаться убедительными.Кроме того, весьма оптимистичное освещение в прессе может укрепить нереалистичные надежды.
Некоторые меры могут улучшить информированное согласие в ранних клинических испытаниях на основе стволовых клеток (59). Во-первых, исследователи должны реалистично описать риски и предполагаемые преимущества. Исследователи должны показать разницу между долгосрочными надеждами на эффективное лечение и неопределенностью, присущей любому исследованию фазы I. Участники исследований фазы I должны понимать, что это вмешательство никогда ранее не применялось на людях для лечения конкретного состояния, что исследователи не знают, сработает ли оно так, как предполагалось, и что подавляющее большинство участников исследований фазы I не получают прямая выгода.
Во-вторых, исследователи в клинических испытаниях hESC должны обсуждать более широкий спектр информации с потенциальными участниками, чем в других клинических испытаниях. Доктрина информированного согласия требует, чтобы исследователи обсуждали с потенциальными участниками информацию, имеющую отношение к их решению добровольно участвовать в клиническом испытании (65). Как правило, соответствующая информация касается характера изучаемого вмешательства, а также рисков и предполагаемых преимуществ. Однако при трансплантации чЭСК немедицинские проблемы могут быть важными или даже решающими для некоторых участников.Люди, которые считают эмбрион имеющим моральный статус человека, вероятно, будут категорически возражать против пересадки чЭСК. Хотя это вмешательство может принести им пользу с медицинской точки зрения, такие люди могут рассматривать его как соучастие в безнравственном поступке. Таким образом, исследователи в клинических испытаниях трансплантации чЭСК должны проинформировать соответствующих участников о том, что трансплантированный материал произошел от человеческих эмбрионов.
В-третьих, и это наиболее важно, исследователи должны убедиться, что участники реалистично понимают клиническое испытание (59).Ключевым этическим вопросом об информированном согласии является не то, что исследователи раскрывают в формах согласия или обсуждениях, а то, что понимают участники клинических испытаний. В других контекстах некоторые исследователи убедились, что участники понимают ключевые особенности испытания, оценивая свое понимание. В клинических испытаниях на ВИЧ в развивающихся странах, где утверждалось, что участники не понимали этого испытания, многие исследователи сейчас тестируют каждого участника, чтобы убедиться, что он или она понимают основные особенности исследования (33).Такая прямая оценка понимания участниками исследования рекомендуется в более широком смысле в контекстах, в которых вероятны недопонимания (26). Мы настаиваем на проведении таких тестов понимания в фазе I испытаний трансплантации hSC (58,59).
Тщательное внимание к согласию в инновационных клинических испытаниях может предотвратить споры в будущем. В ранних клинических испытаниях трансплантации органов, имплантируемого полностью искусственного сердца и переноса генов возникновение серьезных побочных эффектов привело к утверждениям о том, что участники исследования не совсем понимали природу исследования (66,67,68).Возникшие этические противоречия вызвали негативную огласку и задержки в проведении последующих клинических испытаний.
VIII. Институциональный надзор за исследованиями стволовых клеток
Исследования стволовых клеток человека поднимают некоторые этические вопросы, выходящие за рамки миссии институциональных наблюдательных советов (ЭСО) по защите людей, а также опыта членов ЭСО. Должно быть веское научное обоснование использования человеческих ооцитов и эмбрионов для получения новых линий человеческих стволовых клеток. Однако обычно ЭСО не проводят углубленную научную экспертизу.Некоторые этические вопросы в исследованиях hESC не связаны с защитой людей, например, опасение, что трансплантация человеческих стволовых клеток нечеловеческим животным может привести к характеристикам, которые считаются исключительно человеческими.
A. Комитет по надзору за исследованиями стволовых клеток (SCRO)
Институциональный SCRO с соответствующими научными и этическими знаниями, а также общественные члены должны быть созваны в каждом учреждении для рассмотрения, утверждения и надзора за исследованиями стволовых клеток (18, 69,70).SCRO необходимо будет тесно сотрудничать с IRB и, в случае исследований на животных, с Комитетом по уходу за животными и их использованию. Из-за деликатного характера исследования hSC, SCRO должен включать неаффилированных и непрофессиональных членов, которые могут обеспечить учет интересов общественности.
B. Использование линий стволовых клеток, полученных в другом учреждении
Совместное использование стволовых клеток между учреждениями способствует научному прогрессу и сводит к минимуму количество используемых ооцитов, эмбрионов и соматических клеток.Однако этические проблемы возникают, если исследователи работают с линиями, выведенными в других юрисдикциях, в условиях, которые не были бы разрешены в их учреждении. Исследователи и SCRO должны отличать основные этические стандарты, принятые на основе международного консенсуса — информированное согласие и приемлемый баланс преимуществ и рисков, — от стандартов, которые различаются в зависимости от юрисдикции и культуры. Использование линий, происхождение которых нарушает основные стандарты, подорвало бы этическое проведение исследования, создавая стимулы для других нарушать эти стандарты.
Процесс обзора должен быть сосредоточен на тех типах производных hSC, которые вызывают повышенный уровень этической озабоченности (71). Линии hSC, полученные с использованием свежих ооцитов и эмбрионов, требуют тщательного изучения из-за опасений по поводу медицинских рисков донорства ооцитов, чрезмерного влияния и неудач в достижении репродуктивных целей женщины, проходящей лечение от бесплодия.
Дилеммы возникают, когда доноры исследовательских ооцитов получают платежи, превышающие их расходы, и такие платежи не разрешены в юрисдикции, где будут использоваться клетки hSC.Например, Соединенное Королевство ввело в действие четкую политику, разрешающую такую оплату после публичных консультаций и обсуждений, и предоставило причины для обоснования своего решения (72,73,74,75). Юрисдикции, которые запрещают платежи, должны принять такую тщательно продуманную политику как разумное расхождение во мнениях по сложному вопросу. Опасения по поводу оплаты должно быть меньше, если линии были получены из замороженных эмбрионов, оставшихся после лечения ЭКО, а донорам платили в репродуктивном контексте. Такие платежи, которые производились до того, как фактически рассматривалась возможность пожертвования на исследование, не являются стимулом для исследования чЭСК (71).
Другие дилеммы возникают с линиями hESC, полученными из эмбрионов с использованием доноров гамет. Как обсуждалось ранее, явное согласие на использование репродуктивных материалов в исследованиях стволовых клеток должно быть получено от любых доноров гамет, а также доноров эмбрионов (13,76). Исключение может быть сделано для «дедушек и дедушек» более старых линий, полученных из замороженных эмбрионов, созданных до того, как такое явное согласие стало стандартом лечения, например, до рекомендаций Национальной академии наук 2005 г. (76). Использование таких старых линий целесообразно, поскольку было бы неразумно ожидать от врачей соблюдения стандартов, которые еще не были разработаны (71).Было бы также приемлемо для линий бабушек и дедушек, если бы доноры гамет согласились на неопределенное будущее исследование или передали контроль над замороженными эмбрионами женщине или паре в ЭКО. Тем не менее, вывод должен соответствовать этическим и юридическим стандартам, действовавшим на момент вывода строки.
Таким образом, исследования hSC открывают захватывающие возможности для научных достижений и новых методов лечения, но также поднимают некоторые сложные этические и политические вопросы. Эти вопросы необходимо обсудить наряду с научными проблемами, чтобы гарантировать, что исследования стволовых клеток проводятся этически приемлемым образом.
Footnotes
Эта работа была поддержана Национальным институтом здравоохранения (NIH), грант 1 UL1 RR024131-01, Национальным центром исследовательских ресурсов (NCRR) и Дорожной картой NIH для медицинских исследований, а также Фондом Greenwall. Его содержание является исключительной ответственностью авторов и не обязательно отражает официальную точку зрения NCRR или NIH.
Б.Л. является сопредседателем Рабочей группы по стандартам научной и медицинской отчетности Калифорнийского института регенеративной медицины.
Раскрытие информации Резюме: Авторы не заявляют о конфликте интересов.
Впервые опубликовано в Интернете 14 апреля 2009 г.
Сокращения: ART, Искусственные репродуктивные технологии; hESC, эмбриональные стволовые клетки человека; hSC, человеческие стволовые клетки; iPS-клетки, индуцированные плюрипотентные стволовые клетки; IRB, институциональный наблюдательный совет; ЭКО, in vitro, оплодотворение; SCNT, перенос ядра соматической клетки.
Ссылки
- Комитет по биологическому и биомедицинскому применению исследований стволовых клеток, Комиссия по наукам о жизни, Национальный исследовательский совет, Совет по неврологии и поведенческому здоровью, Институт медицины 2002 Стволовые клетки и будущее регенеративной медицины.Вашингтон, округ Колумбия: National Academies Press [Google Scholar]
- Lo B 2009 Решение этических дилемм в клинических исследованиях. Филадельфия: Липпинкотт Уильямс, Уилкинс [Google Scholar]
- Смит С., Невз В., Тейтельбаум С. 2007 Взрослые и эмбриональные стволовые клетки: методы лечения. Science 316: 1422–1423; ответ автора, 1422–1423 [PubMed] [Google Scholar]
- 2004 Мониторинг исследований стволовых клеток. Вашингтон, округ Колумбия: Президентский совет по биоэтике [Google Scholar]
- 1994 Отчет Группы исследований человеческих эмбрионов.Бетесда, Мэриленд: Национальные институты здравоохранения [Google Scholar]
- 17 июля 2001 г. Заявление сенатора Оррина Г. Хэтча об исследовании стволовых клеток. Доступно по адресу: http://hatch.senate.gov/public/index.cfm? FuseAction = PressReleases.Print & PressRelease_id = fca0c5e3–40c8–4cd3-822e-efff0f2633de & suppresslayouts = true & IsTextOnly = True. По состоянию на 18 декабря 2008 г. [Google Scholar]
- Streiffer R 2008 Информированное согласие и федеральное финансирование исследований стволовых клеток. Hastings Cent Rep 38: 40–47 [PubMed] [Google Scholar]
- Алансо-Залдивар Р., Каплан К. 2007 Ослабление ограничений стволовых клеток.Los Angeles Times, 20 марта 2007 г .; A1 [Google Scholar]
- Dawson L, Bateman-House AS, Mueller Agnew D, Bok H, Brock DW, Chakravarti A, Greene M, King PA, O’Brien SJ, Sachs DH, Schill KE, Siegel A, Solter D, Suter SM, Verfaillie CM, Walters LB, Gearhart JD, Faden RR 2003 Проблемы безопасности в испытаниях вмешательства на основе клеток. Fertil Steril 80: 1077–1085 [PubMed] [Google Scholar]
- 2009 г. Вновь представлен счет стволовых клеток. The New York Times, 27 февраля 2009 г .; A15 [Google Scholar]
- Hulse C 2009 Демократы обсуждают методы прекращения запрета стволовых клеток.The New York Times, 3 января 2009 г .; A11 [Google Scholar]
- Lyerly AD, Faden RR 2007 Эмбриональные стволовые клетки. Готовность сдать замороженные эмбрионы для исследования стволовых клеток. Science 317: 46–47 [PubMed] [Google Scholar]
- Lo B, Chou V, Cedars MI, Gates E, Taylor RN, Wagner RM, Wolf L, Yamamoto KR 2003 Согласие доноров на исследования эмбрионов и стволовых клеток . Science 301: 921 [PubMed] [Google Scholar]
- Radin MJ 1996 Спорные товары.Кембридж, Массачусетс: Издательство Гарвардского университета [Google Scholar]
- 1998 Вспомогательные репродуктивные технологии. Нью-Йорк: Целевая группа штата Нью-Йорк по вопросам жизни и права; 165–169 [Google Scholar]
- 1999 Исследование биологических материалов, хранящихся у человека. Роквилл, Мэриленд: Национальная консультативная комиссия по биоэтике [Google Scholar]
- Kalfoglou AL, Geller G 2000 Последующее исследование с участием доноров ооцитов, изучающее их опыт, знания и отношение к использованию их ооцитов и результатам донорства .Fertil Steril 74: 660–667 [PubMed] [Google Scholar]
- Национальный исследовательский совет и Институт медицины 2005 г. Рекомендации по исследованию эмбриональных стволовых клеток человека. Вашингтон, округ Колумбия: National Academies Press [Google Scholar]
- Lomax GP, Hall ZW, Lo B 2007 Ответственный надзор за исследованиями стволовых клеток человека. Медицинские и этические стандарты Калифорнийского института регенеративной медицины. PLoS Med 4: e114 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Lo B, Zettler P, Cedars MI, Gates E, Kriegstein AR, Oberman M, Reijo Pera R, Wagner RM, Wuerth MT, Wolf LE , Yamamoto KR 2005 Новая эра в этике исследования стволовых клеток человеческого эмбриона.Стволовые клетки 23: 1454–1459 [PubMed] [Google Scholar]
- Levens ED, DeCherney AH 2008 Исследование человеческих ооцитов: этика донорства и защиты доноров. JAMA 300: 2174–2176 [PubMed] [Google Scholar]
- Holden C 2006 Корейский скандал со стволовыми клетками. Шаттен: Комиссия Питта находит «ненадлежащее поведение», но не проступок. Science 311: 928 [PubMed] [Google Scholar]
- Chong S 2006 Нарушение научной дисциплины. Исследования показывают еще больше проблем для исследователей стволовых клеток.Science 311: 754–755 [PubMed] [Google Scholar]
- Chong S, Normile D 2006 Стволовые клетки. Как молодые корейские исследователи помогли разжечь скандал. Science 311: 22–25 [PubMed] [Google Scholar]
- Национальный исследовательский совет и институт медицины 2007 Оценка медицинских рисков донорства человеческих ооцитов для исследования стволовых клеток. Вашингтон, округ Колумбия: National Academies Press [Google Scholar]
- 2001 Этические и политические вопросы в исследованиях с участием людей.Роквилл, Мэриленд: Национальная консультативная комиссия по биоэтике [Google Scholar]
- Spar D 2007 Торговля яйцами — понимание рынка человеческих ооцитов. N Engl J Med 356: 1289–1291 [PubMed] [Google Scholar]
- 2007 г. Пожертвование. Глава 8. Fertil Steril 87: S28 [Google Scholar]
- Hyun I 2006 Справедливая оплата или необоснованное побуждение? Nature 442: 629–630 [PubMed] [Google Scholar]
- Holland S 2001 Спорные товары на обоих концах жизни: покупка и продажа гамет, эмбрионов и тканей тела.Kennedy Inst Ethics J 11: 263–284 [PubMed] [Google Scholar]
- Steinbock B 2004 Плата за донорство яйцеклеток и суррогатное материнство. Mt Sinai J Med 71: 255–265 [PubMed] [Google Scholar]
- Appelbaum PS, Lidz CW 2008 Терапевтическое заблуждение. В: Emanuel EJ, Grady C, Crouch RA, Lie RK, Miller FG, Wendler D, eds. Оксфордский учебник этики клинических исследований. Нью-Йорк: издательство Оксфордского университета; 633–644 [Google Scholar]
- Woodsong C, Karim QA 2005 Модель, разработанная для улучшения информированного согласия: опыт сети испытаний средств профилактики ВИЧ.Am J Public Health 95: 412–419 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- 2002 Клонирование человека и человеческое достоинство: этическое исследование. Вашингтон, округ Колумбия: Президентский совет по биоэтике [Google Scholar]
- 1997 Клонирование человека. Роквилл, Мэриленд: Национальная консультативная комиссия по биоэтике [Google Scholar]
- McHugh PR 2004 Зигота и «клонот» — этическое использование эмбриональных стволовых клеток. N Engl J Med 351: 209–211 [PubMed] [Google Scholar]
- Jaenisch R 2004 Клонирование человека — наука и этика ядерной трансплантации.N Engl J Med 351: 2787–2791 [PubMed] [Google Scholar]
- Национальный исследовательский совет и институт медицины 2002 Научные и медицинские аспекты репродуктивного клонирования человека. Вашингтон, округ Колумбия: National Academies Press [Google Scholar]
- 2005 Белая книга: альтернативные источники плюрипотентных стволовых клеток человека. Вашингтон, округ Колумбия: Президентский совет по биоэтике [Google Scholar]
- Управление оплодотворения человека и эмбриологии 2007 Гибриды и химеры: результаты консультации.Доступно по адресу: http: // www. hfea.gov.uk/en/1581.html. Проверено 22 сентября 2007 г. [Google Scholar]
- Robert JS 2006 Наука и этика создания полулюдейных животных в биологии стволовых клеток. FASEB J 20: 838–845 [PubMed] [Google Scholar]
- Бейлис Ф., Роберт Дж. С. 2007 Химеры, относящиеся к полулюдям: беспокойство по поводу фактов, исследование этики. Am J Bioeth 7: 41–45 [PubMed] [Google Scholar]
- Обзор клинических испытаний: нейрональный цероид липофусциноз (NCL, часто называемый болезнью Баттена).Доступно по адресу: http://www.stemcellsinc.com/clinicaltrials/clinicaltrials.html. По состоянию на 4 марта 2009 г. [Google Scholar]
- 18 декабря 2008 г. StemCells, Inc. получает одобрение FDA на начало клинических испытаний клеток HuCNS-SC при миелиновой болезни. Доступно по адресу: http://www.stemcellsinc.com/news/081218.html. По состоянию на 3 марта 2009 г. [Google Scholar]
- Такахаши К., Танабе К., Охнуки М., Нарита М., Ичисака Т., Томода К., Яманака С. 2007 Индукция плюрипотентных стволовых клеток из фибробластов взрослого человека определенными факторами.Ячейка 131: 861–872 [PubMed] [Google Scholar]
- Park IH, Arora N, Huo H, Maherali N, Ahfeldt T., Shimamura A, Lensch MW, Cowan C, Hochedlinger K, Daley GQ 2008, специфичные для болезни индуцированные плюрипотентные стволовые клетки. Cell 134: 877–886 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Kaji K, Norrby K, Paca A, Mileikovsky M, Mohseni P, Woltjen K 1 марта 2009 г. Безвирусная индукция плюрипотентности и последующее удаление акторов перепрограммирования. Nature 10.1038 / nature07864 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Woltjen K, Michael IP, Mohseni P, Desai R, Mileikovsky M, Hämäläinen R, Cowling R, Wang W, Liu P, Gertsenstein M, Kaji K, Sung HK, Nagy A 1 марта 2009 г. Транспозиция piggyBac перепрограммирует фибробласты в индуцированные плюрипотентные стволовые клетки.Nature 10.1038 / nature07863 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Международное общество исследования стволовых клеток, 2008 г. Поддержите открытое письмо. Поддержите все формы исследований стволовых клеток. Доступно по адресу: http://www.isscr.org/ScienceStatementEndorsers.cfm. По состоянию на 7 января 2009 г. [Google Scholar]
- Aalto-Setala K, Conklin BR, Lo B 24 февраля 2009 г. Получение согласия на будущие исследования индуцированных плюрипотентных клеток: возможности и проблемы. ПЛоС Биол 10.1371 / журнал.pbio.1000042 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Коробкин Р 2007 Стволовые клетки века. Нью-Хейвен, Коннектикут: Издательство Йельского университета [Google Scholar]
- Колфилд Т., Макгуайр А.Л., Чо М., Бьюкенен Дж. А., Берджесс М. М., Данилчик Ю., Диас К. М., Фрайер-Эдвардс К., Грин С. К., Ходош М. А., Юенгст Е. Т., Кей Дж, Кедес Л., Кнопперс Б.М., Лемменс Т., Меслин Э.М., Мерфи Дж., Нуссбаум Р.Л., Отловски М., Пуллман Д., Рэй П.Н., Шугарман Дж., Тиммонс М. 2008 Рекомендации по этике исследований для исследования полного генома: заявление о консенсусе.PLoS Biol 6: e73 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Макгуайр А.Л., Колфилд Т., Чо МК 2008 Этика исследования и проблема секвенирования всего генома. Nat Rev Genet 9: 152–156 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Lowrance WW, Collins FS 2007 Этика. Идентифицируемость в геномных исследованиях. Science 317: 600–602 [PubMed] [Google Scholar]
- Макгуайр А.Л., Гиббс Р.А. 2006 Генетика. Больше не деидентифицирован. Science 312: 370–371 [PubMed] [Google Scholar]
- Greely HT, Cho MK, Hogle LF, Satz DM 2007 Думая о человеческом нейроне мыши.Am J Bioeth 7: 27–40 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Greely HT, Cho MK, Hogle LF, Satz DM 2007 Ответ на открытые комментарии коллег по теме «Размышления о человеческом нейроне мыши. ” Am J Bioeth 7: W4–6 [PubMed] [Google Scholar]
- Hyun I, Lindvall O, Ahrlund-Richter L, Cattaneo E, Cavazzana-Calvo M, Cossu G, De Luca M, Fox IJ, Gerstle C, Гольдштейн Р.А., Хермерен Дж., Хай К.А., Ким Х.о., Ли ХП, Леви-Лахад Э, Ли Л., Ло Б., Маршак Д.Р., Макнаб А., Манси М., Накаучи Х., Рао М., Рук Х.М., Валлес К.С., Шривастава А., Sugarman J, Taylor PL, Veiga A, Wong AL, Zoloth L, Daley GQ 2008 г. В новых рекомендациях ISSCR подчеркиваются основные принципы ответственных исследований трансляционных стволовых клеток.Cell Stem Cell 3: 607–609 [PubMed] [Google Scholar]
- Lo B, Kriegstein A, Grady D 2008 Клинические испытания трансплантации стволовых клеток: руководящие принципы для научного и этического обзора. Clin Trials 5: 517–522 [PubMed] [Google Scholar]
- Olanow CW, Goetz CG, Kordower JH, Stoessl AJ, Sossi V, Brin MF, Shannon KM, Nauert GM, Perl DP, Godbold J, Freeman TB 2003 г. Двойное слепое контролируемое испытание двусторонней трансплантации черного плода при болезни Паркинсона. Ann Neurol 54: 403–414 [PubMed] [Google Scholar]
- Freed CR, Greene PE, Breeze RE, Tsai WY, DuMouchel W, Kao R, Dillon S, Winfield H, Culver S, Trojanowski JQ, Eidelberg D, Fahn S 2001 Трансплантация эмбриональных дофаминовых нейронов при тяжелой болезни Паркинсона.N Engl J Med 344: 710–719 [PubMed] [Google Scholar]
- Joffe S, Cook EF, Cleary PD, Clark JW, Weeks JC 2001 Качество информированного согласия в клинических испытаниях рака: кросс-секционное исследование. Lancet 358: 1772–1777 [PubMed] [Google Scholar]
- Lidz CW, Appelbaum PS, Grisso T., Renaud M 2004 Терапевтическое заблуждение и оценка рисков в клинических испытаниях. Soc Sci Med 58: 1689–1697 [PubMed] [Google Scholar]
- Henderson GE, Davis AM, King NM, Easter MM, Zimmer CR, Rothschild BB, Wilfond BS, Nelson DK, Churchill LR 2004 Неопределенная выгода: исследователи ‘взгляды и сообщения в ранней фазе испытаний генного переноса.Mol Ther 10: 225–231 [PubMed] [Google Scholar]
- Berg JW, Lidz CW, Appelbaum PS 2001 Информированное согласие: теория права и клиническая практика. 2-е изд. Нью-Йорк: Oxford University Press [Google Scholar]
- Fox RC, Swazey JP 1992 Запасные части. Нью-Йорк: Oxford University Press [Google Scholar]
- Couzin J, Kaiser J 2005 Генная терапия. Когда дело Гельсингера заканчивается, генная терапия терпит еще один удар. Science 307: 1028 [PubMed] [Google Scholar]
- Steinbrook R 2008 Дело Гелсингера.В: Emanuel EJ, Grady C, Crouch RA, Lie RK, Miller FG, Wendler D, eds. Оксфордский учебник этики клинических исследований. Нью-Йорк: издательство Оксфордского университета; 110–120 [Google Scholar]
- Zettler P, Wolf LE, Lo B 2007 Установление процедур институционального надзора за исследованиями стволовых клеток. Acad Med 82: 6–10 [PubMed] [Google Scholar]
- Национальный исследовательский совет и институт медицины 2008 Поправки к руководящим принципам национальных академий по исследованиям эмбриональных стволовых клеток человека.Вашингтон, округ Колумбия: National Academy Press [Google Scholar]
- Lo B, Parham L, Broom C, Cedars M, Gates E, Giudice L, Halme DG, Hershon W., Kriegstein A, Kwok PY, Oberman M, Roberts C, Wagner R 2009 Импорт линий плюрипотентных стволовых клеток человека, полученных в другом учреждении: адаптация обзора к этическим соображениям. Cell Stem Cell 4: 115–123 [PubMed] [Google Scholar]
- Управление оплодотворения человека и эмбриологии 2007 Свод правил. 7-е изд. Доступно по адресу: http: // www.hfea.gov.uk/en/371. html. Проверено 16 октября 2008 г. [Google Scholar]
- Human Fertilization and Embryology Authority 2007 Донорство яйцеклеток для исследований: защита доноров. Доступно по адресу: http://www.hfea.gov.uk/en/1417.html. Проверено 18 октября 2008 г. [Google Scholar]
- Human Fertilization and Embryology Authority 2006 Регулирование донорского зачатия: консультации по политике и нормативным мерам, влияющим на донорство спермы, яйцеклеток и эмбрионов в Соединенном Королевстве.

