Бронхиальная астма — причины появления, симптомы заболевания, диагностика и способы лечения
ВАЖНО!
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Бронхиальная астма: причины появления, симптомы, диагностика и способы лечения.Определение
Бронхиальная астма – это хроническое воспалительное заболевание дыхательных путей, которое проявляется приступами одышки, свистящего дыхания, кашля, а в тяжелых случаях – выраженным и даже жизнеугрожающим нарушением функции дыхания. Тактика ведения пациентов и способы лечения бронхиальной астмы достаточно давно исследуются врачами.
В последние годы частота встречаемости бронхиальной астмы неуклонно росла, что привело к успешной разработке новых эффективных препаратов, которые позволяют достичь контроля над клиническими проявлениями заболевания.
Причины появления бронхиальной астмы
Бронхиальная астма в типичном случае является заболеванием аллергической природы и связана с повышенной восприимчивостью организма конкретного человека к какому-либо веществу-аллергену. Именно поэтому бронхиальная астма часто сочетается с аллергическим ринитом, конъюнктивитом, атопическим дерматитом и другими аллергическими заболеваниями. Контакт с аллергеном активирует клетки иммунной системы особым образом. Это приводит к развитию череды характерных для астмы изменений в стенках бронхов: происходит скопление иммунных клеток, развивается воспалительный отек, наблюдается гиперреактивность гладкомышечных компонентов бронхиальной стенки, повышается выработка слизи (мокроты).
Эти четыре механизма приводят к сужению просвета бронхов, что, в свою очередь, затрудняет прохождение воздуха по дыхательным путям, вызывая характерные приступы одышки.
Немаловажную роль в патологических процессах при бронхиальной астме играет функциональное состояние вегетативной нервной системы, наличие хронических заболеваний (особенно дыхательной системы) и вредных привычек. Установлена прямая связь между курением и тяжестью течения заболевания.
Доказано, что вдыхание табачного дыма беременной и младенцем повышает риск развития астмы у ребенка.
Пребывание в среде с повышенным загрязнением воздуха (например, на производстве) провоцирует более тяжелое течение бронхиальной астмы.При постановке диагноза «бронхиальная астма» врачи стараются максимально уточнить характеристики заболевания у конкретного пациента в соответствии с нижеприведенной классификацией. Это позволяет определять тактику ведения пациента, предположительный ответ на терапию и прогноз.
Бронхиальная астма подразделяется на аллергическую, для которой характерны общие механизмы развития и признаки атопических (аллергических) заболеваний, и неаллергическую. Дополнительно астма характеризуется природой аллергена, вызывающего приступ.
Дополнительно астма характеризуется природой аллергена, вызывающего приступ.
В зависимости от частоты развития приступов и возможности их контролировать с помощью проводимой терапии астма бывает интермиттирующей (преходящей) и персистирующей (постоянной). Последняя, в свою очередь, подразделяется по степени тяжести на легкую, среднетяжелую и тяжелую.
Симптомы бронхиальной астмы
Типичным проявлением астмы является синдром бронхиальной обструкции (сужение просвета бронхов). Приступы одышки поначалу развиваются в основном при контакте с причинно-значимым аллергеном.
У больного возникает сухой кашель, затруднение дыхания (преимущественно на выдохе), дыхание может сопровождаться свистящими хрипами.
Во время приступа человек, как правило, испытывает чувство страха и ощущает нехватку воздуха. Состояние немного облегчается, если принять вынужденное положение — сесть, несколько наклонив туловище вперед, с упором вытянутыми руками на колени или край стула. Визуально отмечается бочкообразное вздутие грудной клетки — она словно застывает в положении глубокого вдоха.
Визуально отмечается бочкообразное вздутие грудной клетки — она словно застывает в положении глубокого вдоха.В тяжелых случаях из-за недостаточного обогащения крови кислородом кожа приобретает синеватый оттенок.
По мере прогрессирования заболевания и при отсутствии соответствующего лекарственного контроля приступы астмы начинают развиваться не только в ответ на специфический аллерген, но и при эмоциональной и физической нагрузке, резкой смене температуры окружающего воздуха, в ответ на резкие запахи и т.д.
Диагностика бронхиальной астмы основывается в первую очередь на жалобах пациента, истории болезни и результатах объективного обследования. Для врача крайне важно выяснить, в ответ на что развивается приступ, как долго продолжается, через какое время прекращается, как давно появились первые симптомы заболевания. Для подтверждения диагноза «аллергическая бронхиальная астма» важно выявить наличие у пациента и у его родственников симптомов других аллергических заболеваний.

После постановки предположительного диагноза проводятся специальные инструментальные и лабораторные исследования.
Среди инструментальных методов ведущую роль играют пикфлоуриметрия и спирометрия.
Пациент во время выполнения спирометрии
Данные методы позволяют оценить объем вдыхаемого и выдыхаемого воздуха, скорость выдоха и рассчитать специфические индексы (например, индекс Тиффно), которые характеризуют степень нарушения прохождения воздуха через дыхательные пути. Для этого пациента просят сделать вдох и далее выдохнуть в специальный прибор для измерения вышеперечисленных параметров. Поскольку данные исследования требуют координированных действий врача и пациента, их редко проводят детям младше 5 лет.
Для постановки диагноза нужно сделать пробу с лекарственным препаратом (бронхолитиком), поэтому перед спирометрией пациенту проводят медикаментозную ингаляцию. Данная проба показывает ответ бронхов на препараты и позволяет дифференцировать бронхиальную астму от других заболеваний со схожими симптомами.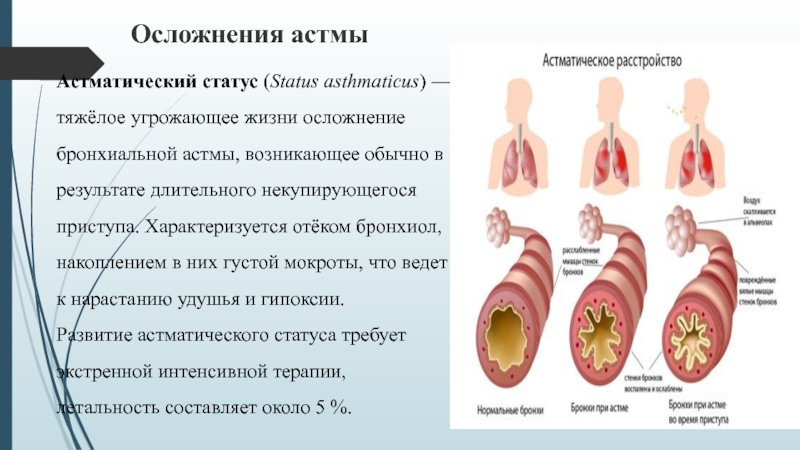
Из лабораторных анализов наиболее диагностически значимым считается серологическое исследование с целью выявления специфических антител (специфические IgE) к возможным причинно-значимым аллергенам.
Бета-2-адренергический рецептор (ADRB2). Выявление мутации G46A (Arg16Gly)
Генетический маркер связан с особенностями работы нейронных рецепторов. Исследуется для выявления предрасположенности к метаболическому синдрому, ожирению, бронхиальной астме, в том числе ночной формы, риска развития артериальной гипертензии у больных сахарным диабетом 2-го типа. Имеет значение в оценке эффективности терапии бронхиальной астмы.
Метод исследования
Полиморфизм длин рестрикционных фрагментов.
Какой биоматериал можно использовать для исследования?
Венозную кровь, буккальный (щечный) эпителий.
Как правильно подготовиться к исследованию?
Специальной подготовки не требуется.
Название гена – ADRB2
OMIM
+109690
Локализация гена на хромосоме – 5q32
Функция гена
Ген ADRB2 кодирует бета-2-адренергический рецептор – ионный белковый канал, встроенный в цитоплазматическую мембрану клетки, имеющий высокую степень сродства к адреналину и обеспечивающий повышение или понижение активности иннервируемой ткани или органа.
Генетический маркер G46A
Участок ДНК в кодирующей белок области гена ADRB2, в которой происходит замена гуанина (G) на аденин (А), называется генетическим маркером G46A. Если в данной позиции находится гуанин (G), такой вариант гена обозначается как G-аллель, а если аденин (А) – A-аллель.
В результате данной замены в аминокислотной последовательности белка ADRB2 в позиции 16 аргинин заменяется на глицин (Arg16Gly).
Возможные генотипы
Встречаемость в популяции
Встречаемость аллеля А в европейской популяции составляет 38 %.
Ассоциация маркера с заболеваниями
- Бронхиальная астма
- Метаболический синдром
Общая информация об исследовании
Передачу сигналов с помощью катехоламиновых медиаторов в организме человека обеспечивают специфические адренергические рецепторы – ионные белковые каналы, встроенные в цитоплазматическую мембрану клетки, воспроизводящие возбуждающие и тормозные влияния симпатико-адреналовой системы на функции и обменные процессы в разных органах.
Различают несколько типов адренергических рецепторов, имеющих различную локализацию в организме и опосредуемые ими эффекты.
На поверхности клеток гладких мышц бронхиол и артерий скелетных мышц, печени и жировой ткани располагаются преимущественно бета-2-рецепторы. При стимуляции бета-2-рецепторов на клетках печени происходит увеличение интенсивности глюконеогенеза и гликогенолиза.
Также активация рецепторов вызывает увеличение интенсивности гликогенолиза в мышцах, увеличение интенсивности секреции инсулина, глюкагона, ренина, уменьшение сократимости гладких мышц бронхов, кровеносных сосудов, мочеполовой системы, желудочно-кишечного тракта.
При взаимодействии с адреналином бета-2-рецепторы бронхиол обеспечивают расслабление гладких мышц бронхиол и снятие обструкции при обострении бронхиальной астмы. Поэтому агонисты (химические вещества, способные связываться с рецептором и приводящие к биологическому эффекту) бета-2-рецепторов часто используются в фармакологии для лечения бронхиальной астмы.
Бета-2-адренергические рецепторы кодируются геном ADRB2. Участок ДНК в кодирующей белок области гена ADRB2, в которой происходит замена гуанина (G) на аденин (А), называется генетическим маркером G46A. Если в данной позиции находится гуанин (G), такой вариант гена обозначается как G-аллель, а если аденин (А) – A-аллель. В результате данной замены в аминокислотной последовательности белка ADRB2 в позиции 16 аргинин заменяется на глицин (Arg16Gly).
В ряде исследований было показано, что генотип А/А ассоциирован с повышенным риском развития более тяжелой формы бронхиальной астмы, а также ее ночной формы, по сравнению с гомозиготами по аллелю G (генотип G/G).
При лечении бронхиальной астмы альбутеролом (бета-агонистом) у гомозигот G/G отмечается снижение скорости выдоха, что может говорить о возможном развитии побочных эффектов при регулярном использовании бета-агонистов и быть причиной выбора для таких пациентов альтернативной терапии.
При исследовании ассоциации полиморфизма G46A и метаболического синдрома было показано, что у мужчин с генотипами G/A и G/G вероятность его развития существенно повышена.
У гомозигот по аллелю G (генотип G/G) риск развития гипертензии на фоне сахарного диабета 2-го типа оказался значительно выше, чему у гомозигот по аллелю А (генотип А/А).
Знание генотипа по маркеру G46A поможет оценить предрасположенность к метаболическому синдрому, бронхиальной астме, в том числе ее ночной формы, риск развития артериальной гипертензии у больных сахарным диабетом 2-го типа, а также оценить эффективность терапии бронхиальной астмы.
Интерпретация результатов
Результаты исследования должны интерпретироваться врачом в комплексе с другими генетическими, анамнестическими, клиническими и лабораторными данными.
Скачать пример результатаВажные замечания
Для данного маркера не существует понятия «норма» и «патология», т.к. исследуется полиморфизм гена.
Литература
- Contopoulos-Ioannidis DG, Manoli EN, Ioannidis JP. Meta-analysis of the association of beta2adrenergic receptor polymorphisms with asthma phenotypes. J Allergy Clin Immunol. 2005 May;115(5):963-72. [PMID: 15867853]
- Israel E et al. The effect of polymorphisms of the beta(2)-adrenergic receptor on the response to regular use of albuterol in asthma. Am J Respir Crit Care Med. 2000 Jul;162(1):75-80. [PMID: 10903223]
- Bengtsson K et al. Beta(2)-adrenergic receptor gene variation and hypertension in subjects with type 2 diabetes. Hypertension. 2001 May;37(5):1303-8. [PMID: 11358945]
- Dallongeville, J., Helbecque, N., Cottel, D., Amouyel, P., Meirhaeghe, A. The gly16-arg16 and gln27-glu27 polymorphisms of beta-2-adrenergic receptor are associated with metabolic syndrome in men. J. Clin. Endocr. Metab. 88: 4862-4866, 2003. [PubMed: 14557466]
Бронхиальная астма, лечение
Бронхиальная астма – это аллергическое рецидивирующее заболевание дыхательных путей, которое сопровождается приступами удушья. Основная причина развития бронхиальной астмы – это сбои в работе иммунной системы.
Основная причина развития бронхиальной астмы – это сбои в работе иммунной системы.
Количество больных постоянно увеличивается из-за аллергизации населения, происходящей на фоне ухудшающейся экологии и бесконтрольного применения антибиотиков.
Симптомы
Симптомы бронхиальной астмы могут существенно различаться у разных людей. Самыми характерными признаками этого заболевания являются:
- незначительная затруднённость дыхания;
- свистящие хрипы, которые слышны даже на расстоянии – они вызываются вибрацией воздуха, который с силой проходит через суженные дыхательные пути;
- кашель – он может быть постоянным, может существенно ухудшаться ночью или после физических усилий;
- одышка (экспираторная, то есть с преимущественным затруднением выдоха), причём дыхание может быть до такой степени ограниченным, что возникает страх невозможности выдохнуть.
Лечение бронхиальной астмы
Успешное лечение бронхиальной астмы подразумевает устранение причин её появления, то есть восстановление нормальной деятельности иммунной системы.
Для уменьшения страданий больного при бронхиальной астме назначают множество разнообразных медикаментов, в том числе и гормональных. Как правило, приём этих медикаментов сопровождается различными побочными эффектами и вызывает привыкание. Но лекарства не убирают причину появления этого заболевания, а симптомы уходят только на время. К сожалению, пока нет препаратов, целенаправленно восстанавливающих функции иммунной системы.
Постепенно заболевание прогрессирует, дозировку лекарств приходится увеличивать, обязательным становится приём гормональных препаратов, а это значит, что применять их уже нужно будет пожизненно. Но самочувствие все равно будет ухудшаться, т.к. причина развития болезни, сбой в иммунной системе — не устраняется медикаментозным лечением.
Для радикальной борьбы с бронхиальной астмой необходимо лечение, направленное на восстановление утраченного иммунитета. Постепенно восстановить работу иммунной системы позволяет компьютерная рефлексотерапия.
Метод компьютерной рефлексотерапии в лечении бронхиальной астмы
Лечение по методу компьютерной рефлексотерапии основано на балансировке нейро-иммуно-эндокринной регуляции всего организма и динамическом восстановлении функции иммунной системы больного.
Лечение осуществляется путем воздействия сверхмалым постоянным током на систему биологически активных точек, связанных в единую сеть с головным мозгом через вегетативную нервную систему человека.
Лечение нормализует деятельность иммунной системы, тем самым убирает основную причину заболевания, даёт выраженный и постоянный клинический эффект без использования гормональной терапии. Постепенно количество приступов удушья и кашля сокращается, они проходят не так интенсивно, а потом и вовсе исчезают. Это комплексный метод лечения бронхиальной астмы без применения гормональных препаратов. Альтернативы такому лечению бронхиальной астмы пока нет.
При лечении астмы методом компьютерной рефлексотерапии происходит следующее:
- приступы кашля и удушья наступают реже и проходят не так интенсивно;
- появляется шанс сократить дозировку медицинских препаратов;
- повышается общее самочувствие, нормализуется сон;
- со временем астматические приступы исчезнут вовсе.

Информация на сайте не предназначена для самодиагностики и самолечения. Если нездоровится, не запускайте болезнь, обратитесь за квалифицированной медицинской помощью.
Обструктивный бронхит. Бронхиальная астма. Часть 1
О причинах нарушения дыхания, отягчающих факторах, фазах заболевания, рассказывает Ирина Викторовна Самойлова, аллерголог, терапевт.
Самойлова Ирина Викторовна, врач аллерголог-иммунолог, врач терапевт. Сегодня хотелось бы поговорить о заболеваниях легких. В перечне заболеваний легких отдельную группу составляют заболевания, сопровождающиеся нарушением бронхиальной проходимости, так называемом бронхообструктивным синдромом, то, что пациент ощущает как нарушение дыхания, затруднение дыхания.
Сегодня хотелось бы поговорить об обструктивном бронхите и бронхиальной астме. Механизм формирования нарушения дыхания состоит из нескольких компонентов. Иногда в процессе формирования затрудненного дыхания присутствует только один компонент. Иногда их бывает несколько в сочетании. Среди этих компонентов: спазм бронхов, отек слизистой бронхов, возникающий вследствие воздействия аллергена или воспалительного процесса. А также обтурация, то есть закупорка полная или частичная бронха мокротой.
Механизм формирования нарушения дыхания состоит из нескольких компонентов. Иногда в процессе формирования затрудненного дыхания присутствует только один компонент. Иногда их бывает несколько в сочетании. Среди этих компонентов: спазм бронхов, отек слизистой бронхов, возникающий вследствие воздействия аллергена или воспалительного процесса. А также обтурация, то есть закупорка полная или частичная бронха мокротой.
В формировании таких заболеваний как обструктивный бронхит, бронхиальная астма есть несколько причин. Для обструктивного бронхита ведущей причиной являются частые простудные заболевания, сопровождающиеся кашлем. Также, как это ни странно, заболевание желудочно-кишечного тракта, сопровождающееся забросом кислого желудочного содержимого в пищевод и формированием спазма бронхом. Фоном в этой ситуации и отягощающим фактором будет являться длительное многолетнее курение.
У бронхиальной астмы причин несколько больше. Это та же инфекционная причина – частые простудные заболевания, сопровождающееся кашлем. Аллергическая причина, реже встречающаяся – дисгармональный вариант. Тот самый вариант, когда в основе спазма бронхов может лежать длительная декомпенсация гормонального фона репродуктивной сферы или щитовидной железы. И так называемой психогенный или нейрогенный вариант, когда психоэмоциональные нагрузки способствуют развитию затрудненного дыхания или даже развернутого приступа удушья.
Аллергическая причина, реже встречающаяся – дисгармональный вариант. Тот самый вариант, когда в основе спазма бронхов может лежать длительная декомпенсация гормонального фона репродуктивной сферы или щитовидной железы. И так называемой психогенный или нейрогенный вариант, когда психоэмоциональные нагрузки способствуют развитию затрудненного дыхания или даже развернутого приступа удушья.
У одного пациента может быть как единственный провокационный момент, так и сочетание нескольких провокационных факторов, которые способствуют возникновению обострения заболевания. Вот почему очень важно обращение к врачу для того, чтобы не только определить полностью весь список причинно-значимых провокационных факторов для пациента, но и всякий раз в период обострения уточнять, какой из этих факторов лежит в основе текущего обострения. Поскольку от этого зависит выбор той схемы ведения пациента, который принесет максимально быстрый удовлетворительный результат от лечения.
Надо помнить, что и хронический обструктивный бронхит и бронхиальная астма – это хронические заболевания, которые в своем течении имеют несколько фаз. Фаза обострения, она понятна пациентам. Это яркие или достаточно значимые проявления заболевания, которые вынуждают пациента обращаться к врачу, вынуждают пациента получать какое-то лечение или изменять схему ранее назначенного лечения. Есть фаза ремиссии. То есть это фаза течения без каких-либо проявлений заболевания. И есть промежуточная фаза – так называемый переходный мостик. Эта фаза очень неудобна для врача и для пациента. Так называемая неполная ремиссия. В таких случаях проявления заболевания есть, но они настолько незначительны, что либо не ощущаются пациентом, либо пациент не придает значения появившимся начальным проявлениям и не стремится как-то к обращению за помощью, не стремится к изменению той схемы лечения, которая была назначена ранее. Если не выполнить своевременно назначение в таких случаях, то фаза неполной ремиссии будет способствовать дальнейшему развитию заболевания. Будет выходить на степень яркого обострения, которое будет требовать еще больших от пациента и врача усилий для его погашения.
Фаза обострения, она понятна пациентам. Это яркие или достаточно значимые проявления заболевания, которые вынуждают пациента обращаться к врачу, вынуждают пациента получать какое-то лечение или изменять схему ранее назначенного лечения. Есть фаза ремиссии. То есть это фаза течения без каких-либо проявлений заболевания. И есть промежуточная фаза – так называемый переходный мостик. Эта фаза очень неудобна для врача и для пациента. Так называемая неполная ремиссия. В таких случаях проявления заболевания есть, но они настолько незначительны, что либо не ощущаются пациентом, либо пациент не придает значения появившимся начальным проявлениям и не стремится как-то к обращению за помощью, не стремится к изменению той схемы лечения, которая была назначена ранее. Если не выполнить своевременно назначение в таких случаях, то фаза неполной ремиссии будет способствовать дальнейшему развитию заболевания. Будет выходить на степень яркого обострения, которое будет требовать еще больших от пациента и врача усилий для его погашения.
При каких обстоятельствах пациент должен насторожиться и принять для себя решение обратиться к врачу с целью диагностики или получения рекомендаций по лечению. В том случае, если диагноз обструктивного бронхита или бронхиальной астмы не был установлен, пациента должно насторожить продолжительный, сверх двух недель кашель после простудного состояния. Ночной или утренний кашель при отсутствии проявлений простудного заболевания. Усиление кашля или появление его в параллель с усилением ощущений изжоги, особенно в ночное время, а также наиболее грозные признаки в виде свистящего затрудненного дыхания.
Для пациентов, у которых диагноз ранее был установлен, моментами, которые должны насторожить, являются изменение характера кашля: его усиление, изменения звука во время кашля, изменение характера мокроты, а также увеличение потребности в ингаляторах скорой помощи, в медикаментах в течение трех, максимум пяти дней, что может свидетельствовать о наличии нестабильности и потребности в применении более действующих схем.
Необычные синдромы астмы и их лечение
Ther Adv Chronic Dis. 2011 июл; 2 (4): 249–264.
Джек А. Кастелик
1 Отделение респираторной медицины, Халл и фонд NHS Восточного Йоркшира, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
1 Отдел респираторной медицины, Hull и East Yorkshire NHS Trust, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
2 Отделение IIR, Школа медицины, Университет Саутгемптона, Больница общего профиля Саутгемптона , Саутгемптон СУ 6YD, Великобритания ку.ca.notos@mbjЭта статья цитируется другими статьями в PMC.Abstract
Астма обычно проявляется симптомами хрипов, одышки и кашля. Однако клиницисты должны знать об атипичных проявлениях этого расстройства, когда кашель является основным или единственным симптомом таких состояний, как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель. Ранняя диагностика и лечение этих состояний с помощью ингаляционных кортикостероидов улучшает симптомы у большинства пациентов.До 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Эти пациенты были охвачены термином «резистентная к лечению астма» (TRA), имеют наибольшую заболеваемость и несут более 50% расходов на здравоохранение. В этом обзоре мы обсуждаем исследования, лечение и патофизиологию различных фенотипов атипичных проявлений астмы, а также новые лицензированные биологические агенты и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности при TRA.
Ранняя диагностика и лечение этих состояний с помощью ингаляционных кортикостероидов улучшает симптомы у большинства пациентов.До 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Эти пациенты были охвачены термином «резистентная к лечению астма» (TRA), имеют наибольшую заболеваемость и несут более 50% расходов на здравоохранение. В этом обзоре мы обсуждаем исследования, лечение и патофизиологию различных фенотипов атипичных проявлений астмы, а также новые лицензированные биологические агенты и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности при TRA.
Ключевые слова: атопический кашель, биопрепараты, кашель, эозинофильный бронхит, моноклональные антитела, тяжелая астма
Введение
От астмы страдают 5,4 миллиона человек в Великобритании [Asthma UK, 2010] и около 300 миллионов человек в мире [Braman , 2006]. Его распространенность составляет 15-20% у детей и 5-10% у взрослых, и считается, что этот показатель будет продолжать расти.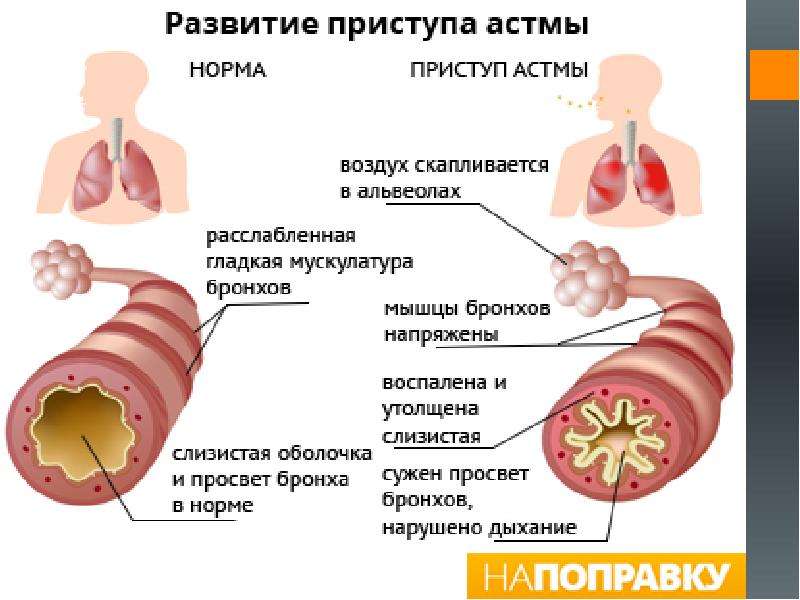 Более 12 миллионов рабочих дней в Великобритании теряются из-за проблем, связанных с астмой [Asthma UK, 2010].Более того, в 2006-2007 финансовом году было зарегистрировано около 80 000 случаев неотложной госпитализации по астме, из которых 41% — дети в возрасте до 14 лет. У большинства пациентов лечение этого состояния на основе международных руководств гарантирует, что астма хорошо контролируется с помощью терапии ингаляционными кортикостероидами (ICS) либо отдельно, либо в сочетании с агонистами β 2 длительного действия (LABA) [BTS / SIGN, 2008 ]. Другие агенты, такие как антилейкотриеновые агенты и теофиллины, также были использованы с хорошим эффектом.Однако до 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Хотя это небольшая часть больных астмой, они имеют наибольшую заболеваемость, рискуют умереть и несут более 50% расходов на здравоохранение, связанных с астмой; следовательно, существует неудовлетворенная потребность в этой группе плохо контролируемых астматиков [Chanez et al.
Более 12 миллионов рабочих дней в Великобритании теряются из-за проблем, связанных с астмой [Asthma UK, 2010].Более того, в 2006-2007 финансовом году было зарегистрировано около 80 000 случаев неотложной госпитализации по астме, из которых 41% — дети в возрасте до 14 лет. У большинства пациентов лечение этого состояния на основе международных руководств гарантирует, что астма хорошо контролируется с помощью терапии ингаляционными кортикостероидами (ICS) либо отдельно, либо в сочетании с агонистами β 2 длительного действия (LABA) [BTS / SIGN, 2008 ]. Другие агенты, такие как антилейкотриеновые агенты и теофиллины, также были использованы с хорошим эффектом.Однако до 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Хотя это небольшая часть больных астмой, они имеют наибольшую заболеваемость, рискуют умереть и несут более 50% расходов на здравоохранение, связанных с астмой; следовательно, существует неудовлетворенная потребность в этой группе плохо контролируемых астматиков [Chanez et al. 2007; Antoncelli et al. 2004; Европейская сеть по изучению механизмов тяжелой астмы, 2003 г.]
2007; Antoncelli et al. 2004; Европейская сеть по изучению механизмов тяжелой астмы, 2003 г.]
Астма — это гетерогенное заболевание, которое на одном конце спектра трудно диагностировать из-за атипичных симптомов, например кашля, а на другом конце — у пациентов с установленным заболеванием. где управление ограничено отсутствием доступных нам текущих терапевтических возможностей.Последнюю часто называют тяжелой астмой. Однако необходимо уточнить, что тяжелую астму можно подразделить на «трудно поддающуюся лечению» и «резистентную к лечению астму» (TRA). Следовательно, важно, чтобы этими двумя объектами управляли должным образом.
Трудно поддающаяся лечению астма может возникнуть по ряду причин [Morjaria and Polosa, 2010; Холгейт, Полоса, 2006]. Тремя основными причинами являются, за исключением состояний, имитирующих тяжелую астму, сопутствующие заболевания, триггеры астмы и, что наиболее важно, несоблюдение режима приема лекарств от астмы.И наоборот, TRA включает пациентов, которые не находятся под адекватным контролем с их лекарствами в соответствии с международными рекомендациями [BTS / SIGN, 2008], то есть на этапах IV и V Глобальной инициативы по астме (GINA) и Британского торакального общества / Шотландской межвузовской сети рекомендаций, где, несмотря на находясь на высоких дозах ICS, LABA и других дополнительных лекарствах и сумев установить контроль над компонентами трудноизлечимой астмы, пациенты сохраняют симптомы. Напротив, большинство пациентов с атипичной астмой, такой как кашлевой вариант астмы, неастматический эозинофильный бронхит или атопический кашель, реагируют на стандартную терапию ИКС и антигистаминными препаратами.Осведомленность о существовании этих состояний и связанная с ними способность диагностировать их являются основными проблемами, связанными с атипичной астмой. Если не лечить атипичную астму, у части пациентов может развиться классическая астма. Например, более трети пациентов с кашлевой астмой может прогрессировать до развития классической астмы [Johnson and Osborn, 1991; Браман и Коррао, 1985]. Напротив, только у очень небольшой части пациентов с атопическим кашлем развивается классическая астма [Fujimura et al. 2003].
Напротив, большинство пациентов с атипичной астмой, такой как кашлевой вариант астмы, неастматический эозинофильный бронхит или атопический кашель, реагируют на стандартную терапию ИКС и антигистаминными препаратами.Осведомленность о существовании этих состояний и связанная с ними способность диагностировать их являются основными проблемами, связанными с атипичной астмой. Если не лечить атипичную астму, у части пациентов может развиться классическая астма. Например, более трети пациентов с кашлевой астмой может прогрессировать до развития классической астмы [Johnson and Osborn, 1991; Браман и Коррао, 1985]. Напротив, только у очень небольшой части пациентов с атопическим кашлем развивается классическая астма [Fujimura et al. 2003].
В этом обзоре мы обсуждаем проблемы, с которыми сталкивается врач при постановке диагноза атипичной астмы. Таким образом, мы описываем исследования и лечение кашлевой астмы, атопического кашля и неастматического эозинофильного бронхита. Кроме того, мы обсуждаем подтверждение и фенотипирование TRA, а также предоставляем обзор новых биологических агентов, которые лицензированы, и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности в TRA. Мы не обсуждаем трудно поддающуюся лечению астму, предполагая, что это учитывалось наряду с соблюдением режима лечения до постановки диагноза TRA.
Мы не обсуждаем трудно поддающуюся лечению астму, предполагая, что это учитывалось наряду с соблюдением режима лечения до постановки диагноза TRA.
Атипичная астма
Текущие рекомендации признают, что диагноз астмы является клиническим [BTS / SIGN, 2008]. Центральным во всех определениях астмы является наличие таких симптомов, как хрип, стеснение в груди, одышка или кашель, а также непостоянная обструкция дыхательных путей. Более поздние описания астмы также включали наличие гиперчувствительности дыхательных путей (AHR) и воспаления дыхательных путей [BTS / SIGN, 2008] .У значительной части пациентов диагноз классической астмы вряд ли вызовет какие-либо трудности. У пациентов с классической астмой наблюдаются хрипы, одышка или кашель. Измерения пикового потока выдоха (ПСВ) различаются по дням и в течение суток (). Бронхопровокационные пробы на гистамин или метахолин положительные. При отклонении от нормы спирометрия обычно выявляет обструкцию дыхательных путей. Однако существуют состояния, такие как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель, которые отличаются от классической астмы по своим фенотипическим характеристикам. Поэтому их диагностика может быть более сложной. Хотя эти состояния могут различаться фенотипически, эозинофильное воспаление дыхательных путей составляет их общий знаменатель. Являются ли эти состояния воплощением «астматического синдрома» или представляют собой независимые сущности per se , остается предметом обсуждения [Mcgarvey et al. 2003]. Фактически, существует множество доказательств того, что у некоторых пациентов с этими состояниями, если они не диагностированы или не пролечены надлежащим образом, на самом деле могут развиваться полные характеристики классической астмы [Irwin et al. 2006; Fujimura et al. 2005a, 2005b, 2005c, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b]. Следовательно, осведомленность и способность ранней диагностики и лечения этих состояний имеют важное клиническое значение.
Поэтому их диагностика может быть более сложной. Хотя эти состояния могут различаться фенотипически, эозинофильное воспаление дыхательных путей составляет их общий знаменатель. Являются ли эти состояния воплощением «астматического синдрома» или представляют собой независимые сущности per se , остается предметом обсуждения [Mcgarvey et al. 2003]. Фактически, существует множество доказательств того, что у некоторых пациентов с этими состояниями, если они не диагностированы или не пролечены надлежащим образом, на самом деле могут развиваться полные характеристики классической астмы [Irwin et al. 2006; Fujimura et al. 2005a, 2005b, 2005c, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b]. Следовательно, осведомленность и способность ранней диагностики и лечения этих состояний имеют важное клиническое значение.
Таблица 1.
Атипичные астматические синдромы.
| Синдром | Вариабельность PEF | Обструкция дыхательных путей | Гиперчувствительность дыхательных путей | Эозинофилия мокроты | Атопия | Стероидный ответ | Результаты биопсии |
|---|---|---|---|---|---|---|---|
| Да | Да 900 | Да | Да | ± | Да | — | |
| Кашлевой вариант астмы | — | Нет | Да | Да | Нет | Да | ↓ толщина субэпителиального слоя по сравнению с классической астмой |
| Эозинофильный бронхит | Нет | Нет | Нет | Да | Нет | Да | ↓ тучные клетки в гладких мышцах дыхательных путей по сравнению с классической астмой |
| Атопический кашель | Нет | Нет | Нет | Да | Да | Да | Эозинофилы в подслизистой оболочке трахеи и бронхов |
Кашлевой вариант астмы
Кашлевый вариант астмы остается частой причиной хронического кашля [Chung and Pavord, 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini el al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981; Poe et al. 1989]. При астме кашель может сопровождаться другими симптомами, такими как хрипы или одышка [Irwin et al. 1990, 1981]. Однако у части пациентов, до 57% случаев в некоторых исследованиях, кашель может быть единственным проявлением этого состояния [Chung et al. 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini et al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1997, 1990, 1981; Poe et al. 1989; Corrao et al. 1979]. В 1979 году Коррао и его коллеги определили «кашлевую астму» как AHR с хроническим кашлем, но без хрипов или обструкции дыхательных путей [Corrao et al.
2005; Brightling et al. 1999a, 1999b; Palombini el al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981; Poe et al. 1989]. При астме кашель может сопровождаться другими симптомами, такими как хрипы или одышка [Irwin et al. 1990, 1981]. Однако у части пациентов, до 57% случаев в некоторых исследованиях, кашель может быть единственным проявлением этого состояния [Chung et al. 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini et al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1997, 1990, 1981; Poe et al. 1989; Corrao et al. 1979]. В 1979 году Коррао и его коллеги определили «кашлевую астму» как AHR с хроническим кашлем, но без хрипов или обструкции дыхательных путей [Corrao et al. 1979]. После этого первоначального описания стало очевидно, что, хотя кашель является преобладающим респираторным симптомом у части пациентов с кашлевой астмой, хрипы также могут присутствовать [Kastelik et al. 2005; Palombini et al. 1999; Brightling et al. 1999a, 1999b; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981, Poe et al. 1989;]. Фактически, у одной трети пациентов, первоначально обследованных Коррао и его коллегами, впоследствии развилось хрипы [Braman and Corrao, 1985; Corrao et al. 1979]. При кашлевой астме оценка пикового потока выдоха (ПСВ) не выявляет дневной или суточной изменчивости, а спирометрические измерения не выявляют обструкции дыхательных путей. Кроме того, об атопии обычно не сообщается. Более того, присутствует AHR к гистамину или метахолину, а также эозинофилия мокроты [Kastelik, 2008; Morice et al.
1979]. После этого первоначального описания стало очевидно, что, хотя кашель является преобладающим респираторным симптомом у части пациентов с кашлевой астмой, хрипы также могут присутствовать [Kastelik et al. 2005; Palombini et al. 1999; Brightling et al. 1999a, 1999b; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981, Poe et al. 1989;]. Фактически, у одной трети пациентов, первоначально обследованных Коррао и его коллегами, впоследствии развилось хрипы [Braman and Corrao, 1985; Corrao et al. 1979]. При кашлевой астме оценка пикового потока выдоха (ПСВ) не выявляет дневной или суточной изменчивости, а спирометрические измерения не выявляют обструкции дыхательных путей. Кроме того, об атопии обычно не сообщается. Более того, присутствует AHR к гистамину или метахолину, а также эозинофилия мокроты [Kastelik, 2008; Morice et al. 2007, 2006; Морис, Кастелик, 2003].
2007, 2006; Морис, Кастелик, 2003].
Неастматический эозинофильный бронхит
Неастматический эозинофильный бронхит был первоначально описан Гибсоном и его коллегами и характеризуется эозинофилией мокроты [Brightling, 2006; Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. При неастматическом эозинофильном бронхите обструкции дыхательных путей нет, поскольку измерения спирометрии в норме. Также отсутствует вариабельность PEF и AHR.Однако индуцированный анализ мокроты выявляет эозинофилию, определяемую как более чем 3% от числа несквамоклеточных эозинофилов [Gibson et al. 2002]. Кроме того, повышается чувствительность кашлевого рефлекса.
Атопический кашель
Fujimura и его коллеги описали пациентов с хроническим непродуктивным кашлем и атопией, резистентным к бронходилататорам, и предложили термин эозинофильный трахеобронхит с гиперчувствительностью дыхательных путей или «атопический кашель» [Fujimura et al. 1992]. «Атопический кашель» характеризуется атопией, определяемой как одно или несколько из следующих: эозинофилия крови или мокроты; повышенные уровни общего или специфического иммуноглобулина (Ig) E; или положительный кожный укол [Fujimura et al. 2000, 1997, 1992]. Кроме того, при атопическом кашле наблюдается хронический непродуктивный кашель, устойчивый к бронходилататорам, отсутствие различной обструкции дыхательных путей и нормальная бронхиальная провокация [Dicpinigaitis, 2006; Fujimura et al. 2000, 1997, 1992]. Это состояние характеризуется повышенной реакцией кашля на вдыхаемый капсаицин, присутствием эозинофилов в мокроте и подслизистой биопсии трахеи и бронхов, но не в бронхоальвеолярном лаваже (БАЛ) [Fujimura et al. 2005, 2003, 2000, 1997, 1992]. Однако эксперты по-прежнему обсуждают, является ли атопический кашель отдельным заболеванием, вызывающим хронический кашель [Fujimura and Ogawa, 2003; Макгарви и Морис, 2003]. Некоторые, действительно, предположили, что пациенты с атопическим кашлем, скорее всего, являются атопическими людьми с кашлевой астмой [Mcgarvey and Morice, 2003].
1992]. «Атопический кашель» характеризуется атопией, определяемой как одно или несколько из следующих: эозинофилия крови или мокроты; повышенные уровни общего или специфического иммуноглобулина (Ig) E; или положительный кожный укол [Fujimura et al. 2000, 1997, 1992]. Кроме того, при атопическом кашле наблюдается хронический непродуктивный кашель, устойчивый к бронходилататорам, отсутствие различной обструкции дыхательных путей и нормальная бронхиальная провокация [Dicpinigaitis, 2006; Fujimura et al. 2000, 1997, 1992]. Это состояние характеризуется повышенной реакцией кашля на вдыхаемый капсаицин, присутствием эозинофилов в мокроте и подслизистой биопсии трахеи и бронхов, но не в бронхоальвеолярном лаваже (БАЛ) [Fujimura et al. 2005, 2003, 2000, 1997, 1992]. Однако эксперты по-прежнему обсуждают, является ли атопический кашель отдельным заболеванием, вызывающим хронический кашель [Fujimura and Ogawa, 2003; Макгарви и Морис, 2003]. Некоторые, действительно, предположили, что пациенты с атопическим кашлем, скорее всего, являются атопическими людьми с кашлевой астмой [Mcgarvey and Morice, 2003]. Однако Fujimura и его коллеги определили атопический кашель с его специфической патофизиологией и отсутствием прогресса в классической астме [Fujimura and Ogawa, 2003].Поэтому для клиницистов важно исследовать и исключить другие распространенные причины хронического кашля, такие как кашлевой вариант астмы, гастроэзофагеальный рефлюкс и ринит, до постановки диагноза атопического кашля.
Однако Fujimura и его коллеги определили атопический кашель с его специфической патофизиологией и отсутствием прогресса в классической астме [Fujimura and Ogawa, 2003].Поэтому для клиницистов важно исследовать и исключить другие распространенные причины хронического кашля, такие как кашлевой вариант астмы, гастроэзофагеальный рефлюкс и ринит, до постановки диагноза атопического кашля.
Патофизиология атипичной астмы
В последние годы наше понимание патофизиологии кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля улучшилось [Brightling et al. 2003, 2002, 2000а, 2000б; Брайтлинг и Паворд, 2000; Niimi et al. 2000, 1998]. Эти три состояния имеют схожие иммунопатологические характеристики с классической астмой в виде воспалительного процесса, вызванного эозинофилами. В то время как эозинофильное воспаление является общей патофизиологической характеристикой классической астмы, кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель различаются из-за различий в расположении воспалительных клеток и толщины субэпителиального слоя, о которых сообщалось в этих состояниях, следовательно, вероятные причины наблюдаемого фенотипического несоответствия [Brightling et al. 2002; Niimi et al. 1998].
2002; Niimi et al. 1998].
Кашлевая астма
Эозинофилы играют важную роль в патофизиологии кашлевой астмы [Niimi et al. 1998]. Таким образом, имеются данные о повышенном количестве эозинофилов в ЖБАЛ и тканях пациентов с кашлевой астмой [Niimi et al. 2000]. Однако Де Диего и его коллеги показали, что не было значительной разницы между кашлевой астмой и классической астмой в уровнях мокроты эозинофильного катионного белка (ECP), интерлейкина (IL) -8, фактора некроза опухоли альфа (TNF-α) и уровни выдыхаемого оксида азота (eNO) [De Diego et al. 2005]. Точно так же Канадзава и его коллеги не смогли найти никакой разницы в уровнях eNO и ECP между пациентами с кашлевой астмой и пациентами с классической астмой [Kanazawa et al. 2005]. Однако уровни фактора роста эндотелия сосудов (VEGF), который может играть роль в проницаемости сосудов из-за воспаления, были значительно выше при классической астме. Niimi и его коллеги сообщили, что утолщение субэпителиального слоя при кашлевой астме не было столь выраженным, как при классической астме [Niimi et al. 1998]. Мацумото и его коллеги наблюдали, что у пациентов с кашлевой астмой наблюдалось утолщение стенки центральных дыхательных путей [Matsumoto et al. 2007]. Хотя уровни eNO были повышены при кашлевой астме, они не отличались от уровней eNO, наблюдаемых при классической астме [Fujimura et al. 2008]. Fujimura и его коллеги наблюдали за 41 пациентом с кашлевой астмой, у семи из которых развилась классическая астма [Fujimura et al. 2005a, 2005b, 2005c].AHR и отсутствие использования ICS были наиболее важными предикторами развития классической астмы. Как и при классической астме, ICS при кашлевой астме снижали AHR [Fujimura et al. 2005a, 2005b, 2005c]. Однако не было изменений порога кашля для ингаляционного капсаицина независимо от использования ICS, что свидетельствует о том, что чувствительность кашлевого рефлекса не участвует в механизмах кашлевой астмы.
1998]. Мацумото и его коллеги наблюдали, что у пациентов с кашлевой астмой наблюдалось утолщение стенки центральных дыхательных путей [Matsumoto et al. 2007]. Хотя уровни eNO были повышены при кашлевой астме, они не отличались от уровней eNO, наблюдаемых при классической астме [Fujimura et al. 2008]. Fujimura и его коллеги наблюдали за 41 пациентом с кашлевой астмой, у семи из которых развилась классическая астма [Fujimura et al. 2005a, 2005b, 2005c].AHR и отсутствие использования ICS были наиболее важными предикторами развития классической астмы. Как и при классической астме, ICS при кашлевой астме снижали AHR [Fujimura et al. 2005a, 2005b, 2005c]. Однако не было изменений порога кашля для ингаляционного капсаицина независимо от использования ICS, что свидетельствует о том, что чувствительность кашлевого рефлекса не участвует в механизмах кашлевой астмы.
Неастматический эозинофильный бронхит
Эозинофилы играют важную роль в патофизиологии неастматического эозинофильного бронхита [Brightling et al. 2003, 2002, 2000a, 2000b, Брайтлинг и Паворд, 2000; Гибсон и др. 1998]. При неастматическом эозинофильном бронхите эозинофилия обнаруживается в мокроте, ЖБАЛ и биоптатах бронхов. Кроме того, в мокроте повышается уровень ECP и цистеинил-лейкотриенов [Brightling et al. 2008, 2000a, 2000b]. Более того, уровни эозинофилии БАЛ, гранулоцитарно-колониестимулирующего фактора и экспрессии гена IL-5 были одинаковыми как при неастматическом эозинофильном бронхите, так и при классической астме [Gibson et al. 1998]. Брайтлинг и его коллеги показали одинаковую степень подслизистой эозинофилии и утолщения базальной мембраны и ретикулярной пластинки как при неастматическом эозинофильном бронхите, так и при классической астме [Brightling et al. 2003, 2002]. Однако количество триптазоположительных тучных клеток в пучках гладких мышц дыхательных путей было ниже при неастматическом эозинофильном бронхите по сравнению с классической астмой. Кроме того, при неастматическом эозинофильном бронхите уровни eNO повышаются, что аналогично ситуации, наблюдаемой при классической астме [Brightling et al.
2003, 2002, 2000a, 2000b, Брайтлинг и Паворд, 2000; Гибсон и др. 1998]. При неастматическом эозинофильном бронхите эозинофилия обнаруживается в мокроте, ЖБАЛ и биоптатах бронхов. Кроме того, в мокроте повышается уровень ECP и цистеинил-лейкотриенов [Brightling et al. 2008, 2000a, 2000b]. Более того, уровни эозинофилии БАЛ, гранулоцитарно-колониестимулирующего фактора и экспрессии гена IL-5 были одинаковыми как при неастматическом эозинофильном бронхите, так и при классической астме [Gibson et al. 1998]. Брайтлинг и его коллеги показали одинаковую степень подслизистой эозинофилии и утолщения базальной мембраны и ретикулярной пластинки как при неастматическом эозинофильном бронхите, так и при классической астме [Brightling et al. 2003, 2002]. Однако количество триптазоположительных тучных клеток в пучках гладких мышц дыхательных путей было ниже при неастматическом эозинофильном бронхите по сравнению с классической астмой. Кроме того, при неастматическом эозинофильном бронхите уровни eNO повышаются, что аналогично ситуации, наблюдаемой при классической астме [Brightling et al. 2003, 2002].
2003, 2002].
Атопический кашель
Атопический кашель характеризуется эозинофильным трахеобронхитом без эозинофилов в ЖБАЛ и гиперчувствительностью кашлевых рецепторов без AHR. При атопическом кашле уровни eNO ниже по сравнению с уровнями, наблюдаемыми при кашлевой астме и классической астме [Fujimura et al. 2008]. В отличие от кашлевой астмы и неастматического эозинофильного бронхита нет данных об изменениях в базальной мембране или распределении воспалительных клеток или процессов у пациентов с атопическим кашлем.Однако, когда Кита и его коллеги изучали эффекты антагониста лейкотриеновых рецепторов монтелейкаста при атопическом кашле и кашлевой астме, авторы заметили, что кашель подавляется только у пациентов с кашлевой астмой [Kita et al. 2010]. Напротив, монтелукаст не влиял на кашель у пациентов с атопическим кашлем, что свидетельствует о различных патофизиологических механизмах этих двух состояний. Другое предположение о различных механизмах, лежащих в основе этих двух состояний, было сделано на основании более низких уровней eNO, наблюдаемых при атопическом кашле по сравнению с уровнями, измеренными при кашлевом варианте астмы [Fujimura et al. 2008].
2008].
Обследование пациентов с атипичной астмой
Диагностика пациентов с атипичной астмой может оказаться сложной задачей для клиницистов. Таким образом, оценка этих пациентов и клиническое подозрение на синдромы атипичной астмы остаются важными проблемами. Клинический анамнез может помочь в диагностике атипичной астмы. Однако клиницисты должны будут исключить другие распространенные причины хронического кашля, включая гастроэзофагеальный рефлюкс, ринит или лекарства, такие как ингибиторы ангиотензинпревращающего фермента (АПФ).Может помочь спирометрия, хотя при синдромах атипичной астмы она будет нормальной, как и рентгенограмма грудной клетки. Бронхопровокационные тесты могут быть положительными при классической астме и кашлевой астме; однако они будут нормальными при неастматическом эозинофильном бронхите и атопическом кашле. Индукция мокроты покажет эозинофилию мокроты при всех атипичных состояниях астмы. Напротив, уровни eNO могут различать неастматический эозинофильный бронхит, кашлевую астму и атопический кашель. Fujimura и коллеги показали, что eNO у пациентов с атопическим кашлем были значительно ниже, чем у пациентов с кашлевой астмой и классической астмой [Fujimura et al. 2008]. Тесты на атопию могут помочь пациентам с атопическим кашлем. При кашлевой астме и при неастматическом эозинофильном бронхите атопия менее вероятно. Следовательно, оценка пациентов с синдромами атипичной астмы должна включать в себя анамнез и обследование, спирометрию, рентгенографию грудной клетки, бронхопровокационные тесты, индукцию мокроты и измерения eNO.Однако диагноз синдромов атипичной астмы может быть подтвержден только в том случае, если наблюдается ответ на специфическую терапию.
Fujimura и коллеги показали, что eNO у пациентов с атопическим кашлем были значительно ниже, чем у пациентов с кашлевой астмой и классической астмой [Fujimura et al. 2008]. Тесты на атопию могут помочь пациентам с атопическим кашлем. При кашлевой астме и при неастматическом эозинофильном бронхите атопия менее вероятно. Следовательно, оценка пациентов с синдромами атипичной астмы должна включать в себя анамнез и обследование, спирометрию, рентгенографию грудной клетки, бронхопровокационные тесты, индукцию мокроты и измерения eNO.Однако диагноз синдромов атипичной астмы может быть подтвержден только в том случае, если наблюдается ответ на специфическую терапию.
Лечение атипичной астмы
Наличие непродуктивного кашля и положительный ответ на ИКС характерны для кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля [Irwin et al. 2006; Kastelik et al. 2005; Fujimura et al. 2005a, 2005b, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b].Есть некоторые свидетельства того, что если не лечить кашлевую астму на ранней стадии, она может прогрессировать до классической астмы, и у пациентов могут развиться симптомы одышки и хрипов [Kastelik, 2008; Fujimura et al. 2003]. Напротив, считалось, что атопический кашель реже прогрессирует до классической астмы, особенно при раннем введении лечения с помощью ИКС [Fujimura et al. 2003]. Точно так же Мацумо и его коллеги обнаружили, что лечение ИКС предотвращает прогрессирование от кашлевой астмы до классической астмы [Matsumoto et al. 2006]. Fujimura и его коллеги изучили влияние ICS на изменения AHR и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой [Fujimura et al. 2005a, 2005b]. Как и при классической астме, AHR снижалась с помощью ICS. Однако не было изменений порога кашля у пациентов с кашлевой астмой, независимо от того, принимали они ИКС или нет. У некоторых пациентов с кашлевой астмой кашель улучшается с помощью антагонистов лейкотриеновых рецепторов, особенно если симптомы резистентны к ингаляционным бронходилататорам или ИКС [Dicpinigaitis et al. 2002]. Например, Дикпинигайтис и его коллеги наблюдали, что в ответ на антагонист лейкотриеновых рецепторов, зафирлукаст, как субъективная оценка кашля, так и чувствительность кашлевого рефлекса к вдыхаемому капсаицину улучшались у пациентов с кашлевой астмой, резистентной к ингаляционным бета-агонистам и ИКС [ Kita et al. 2010; Dicpinigaitis et al. 2002]. В очень тяжелых случаях кашлевой астмы, также называемой «астмой, эквивалентной злокачественному кашлю», могут потребоваться пероральные кортикостероиды [Millar et al. 1998]. В случае неастматического эозинофильного бронхита симптомы обычно улучшаются с помощью ИКС [Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. В частности, есть доказательства того, что ИКС у пациентов с неастматическим эозинофильным бронхитом улучшают эозинофилию мокроты, тяжесть кашля и чувствительность [Brightling et al. 2000a, 2000b]. Атопический кашель успешно лечится антагонистами гистамина (H 1 ) и / или глюкокортикоидами, а иногда и противогрибковыми средствами [Fujimura et al. 2005a, 2005b, 2005c, 2003, 2000, 1992; Огава и др. 2004]. Однако было показано, что антагонисты лейкотриеновых рецепторов не влияют на кашель у пациентов с атопическим кашлем [Kita et al. 2010].
Астма, рефрактерная к лечению
TRA остается неприятной проблемой не только для медицинского персонала, ухаживающего за пациентами, но и для самих пациентов. Ряд клинических определений тяжелой астмы был предложен за последнее десятилетие различными группами, включая функцию легких, обострения и использование кортикостероидов [Wenzel et al. 2009, 2000]. Следовательно, астма и, в частности, TRA все чаще признаются разнообразным заболеванием.
Подтверждение TRA
Чтобы установить, что у пациента есть TRA, необходимо подтвердить в истории болезни, что плохое соблюдение режима (включая технику ингаляции и использование спейсера), сопутствующие заболевания, другие состояния и триггеры были исключены [Morjaria и Полоса, 2010]. Это можно сделать, просмотрев старые записи, анализы крови, рентгенологию и лечение в прошлом.Например, для исключения дисфункции голосовых связок может быть проведена бронхоскопия, а при интерстициальном заболевании легких — анализы крови, а также компьютерная томография с высоким разрешением. Если исследования не проводились ранее, было бы разумно провести их, чтобы исключить другую причину симптомов пациента. Кроме того, полезен подробный анамнез их астмы и ее контроль в настоящее время и ранее, а также медицинский осмотр. Список возможных исследований приведен в.
Таблица 2.
Исследования, помогающие отличить тяжелую астму от других состояний.
| Полный анализ крови (включая количество эозинофилов) |
| Уровни общего IgE (включая исследования RAST) |
| Аутоиммунный скрининг (и иногда ABG) |
| Насыщение кислородом |
| Chest X- ray |
| Тестирование функции легких |
| Оценка обратимости сальбутамола (и / или реакции на кортикостероиды) |
| Бронхиальные провокационные тесты (например,грамм. метахолин, маннит или аденозин) |
| FeNO |
| Кожные уколы |
| Индукция мокроты |
| Компьютерная томография грудной клетки с высоким разрешением |
| Компьютерная томография пазух |
| Бронхоскопия |
| Эхокардиография |
| pH-манометрия |
Фенотипирование TRA
Клинические, физиологические и иммунопатологические области TRA часто сосуществуют, но не связаны между собой, следовательно, это означает, что TRA далека от однородности и могут быть далее разделены на разные фенотипы.Было предложено несколько методов фенотипирования этих пациентов с TRA, но истинное значение фенотипирования TRA может быть твердо установлено после того, как будет проведена подробная характеристика ряда пациентов. Эти вопросы в настоящее время изучаются через установленную сеть U-BIOPRED (Объективные биомаркеры для прогнозирования исходов респираторных заболеваний) [U-BIOPRED, 2008].
До недавнего времени фенотипирование основывалось на клинических или патологических признаках. Клинически пациентов с тяжелой астмой можно разделить на три основные категории: частые обострения, перемежающиеся периодами отсутствия симптомов астмы; фиксированная преграда для воздушного потока; и кортикостероид-зависимые астматики [Polosa and Benfatto, 2009].Патологически с точки зрения бронхиальных дыхательных путей (БАЛ мокроты и биопсия) известны две основные категории: стойкие эозинофильные и неозинофильные подтипы [Wenzel et al. 1999]. Однако в последнее время стало также известно о существовании нейтрофилии как отдельного подтипа с эозинофилией или без нее [Hamilton et al. 2003; Jatakanon et al. 1999]. Более того, новые статистические подходы были применены к клинической информации, полученной от пациентов с астмой, и с использованием методов обработки данных были идентифицированы некоторые фенотипы астмы [Haldar et al. 2008]. Это использует метод, называемый кластерным анализом. Кроме того, с помощью этого метода была сконструирована многомерная картина фенотипов астмы, демонстрирующая клинически значимые различия в результатах, со стратегиями ведения, которые используют меру эозинофильного воспаления для титрования кортикостероидной терапии [Haldar et al. 2008].
Вдобавок к астме причастны инфекции (такие как Chlamydia pneumoniae ) и сенсибилизация к Aspergillus fumigatus . C. pneumoniae — облигатный внутриклеточный паразит, который может вызывать острые и хронические заболевания дыхательных путей, особенно астму, но субклиническая инфекция является обычным явлением [Stephens, 2003; Каннингем и др. 1998; Grayston, 1992]. Ряд групп сообщили, что существует значительная корреляция у людей между тяжестью астмы и инфекцией C. pneumoniae и увеличением антител IgG и IgA к C. pneumoniae (IgG и IgA), но обычно не к другим респираторным патогенам [ Стивенс, 2003; Wark et al. 2002; Ten Brinke et al. 2001; Мартин и др. 2001; Черный et al. 2000; Hammerschlag, 2000; Cook et al. 1998]. Однако неясно, являются ли эти ассоциации преимущественно результатом (1) инфекции, фиксирующей ответы Th3 и способствующей последующему развитию воспаления и астмы, или (2) иммунных ответов, которые приводят к воспалению и астме, также предрасполагающим к атипичной бактериальной инфекции. Следовательно, было предложено, чтобы время заражения зависело от воздействия, возраста первого заражения и / или основного иммунного фенотипа человека, предрасположенного к C.pneumoniae вызывает аллергию и астму, а не природа инфекции per se [Von Hertzen, 2002]. Аналогичным образом, недавно сообщалось, что пациенты с тяжелой астмой, сенсибилизированные к A. fumigatus , которые не соответствуют общепринятым диагностическим критериям аллергического бронхолегочного аспергиллеза, не только имеют радиологические радиологические аномалии на компьютерной томографии высокого разрешения, такие как бронхоэктазы, бронхиальная болезнь. утолщение стенок и расширение бронхов, а также ограничение воздушного потока из-за захвата воздуха [Menzies et al. 2011]. Эти наблюдения предполагают патофизиологические фенотипы TRA.
Следует отметить, что идентифицированные фенотипы не обязательно являются фиксированными и могут изменяться со временем и в зависимости от назначенного лечения [Haldar et al. 2008]. Используя эту фенотипическую информацию (и, возможно, более точные определения различных подтипов в будущем), необходимо определить механизмы, которые имеют решающее значение во взаимодействии между различными фенотипами астмы, и распутать лежащую в основе патобиологию, чтобы не только разработать биомаркеры. болезней, но и для разработки новых методов лечения, адаптированных к потребностям наших пациентов.
Управление TRA
У большинства пациентов астма не контролируется в соответствии с рекомендациями. Это было продемонстрировано в исследовании Gaining Optimal Asthma Control (GOAL): несмотря на оптимизацию, комбинированный ингалятор салметерол / флутиказон позволил только 62% пациентов достичь полного контроля над симптомами астмы [Bateman et al. 2004]. Более того, после курса OCS этот показатель улучшился до 69%. У остальных пациентов по-прежнему наблюдались неконтролируемые симптомы астмы.
Оптимальное лечение должно быть направлено на достижение наилучшего связанного с астмой качества жизни (QoL) и контроль с помощью самых низких доз лекарств, особенно кортикостероидов. При выборе и формулировании используемых терапевтических агентов следует принимать во внимание не только тяжесть и фенотип заболевания, сопутствующие заболевания и предпочтения пациента, терапевтические реакции, но и сообщения о нежелательных явлениях. Следовательно, в дополнение к стандартной терапии ICS и LABA, другие агенты, такие как антилейкотриеновые агенты (для аспирино-чувствительной астмы [Tonelli et al. 2003] и астмы, вызванной физической нагрузкой [Leff et al. 1998]), теофиллины [Vatrella et al. 2005; Робертс и др. 2003], холинолитики [Peters et al. 2011] и внутривенное (IV) введение магния [Beasley and Aldington, 2007; Silverman et al. 2002] подлежит испытанию.
Пероральные кортикостероиды (OCS) использовались при хронических заболеваниях, но были исследования с использованием иммуномодуляторов для ограничения необходимости длительного использования OCS и, таким образом, побочного действия кортикостероидов.Был изучен ряд таких иммуномодулирующих препаратов с некоторой эффективностью и безопасностью, включая метотрексат, циклоспорин А, макролидные антибиотики, азатиоприн, золото и иммуноглобулины для внутривенного введения [Polosa and Morjaria, 2008]. Примечательно, что метотрексат, циклоспорин А и макролидные антибиотики обычно оцениваются как кортикостероидсберегающие препараты.
Совсем недавно биологические агенты были исследованы на предмет использования в качестве средств, сберегающих кортикостероиды. Единственный лицензированный биологический агент — омализумаб.Другие агенты были изучены с ограниченной эффективностью и безопасностью или все еще находятся на предварительных стадиях оценки. Мы обсудим эти агенты дальше (и они кратко описаны в).
Таблица 3.
Резюме обсужденных исследований.
| Агент | Доказательства эффективности | Улучшения параметров |
|---|---|---|
| Анти-IgE: омализумаб (SC / IV) | Milgrom et al. [1999] (DBPC) | Улучшение утреннего PEF, качества жизни при астме; уменьшение обострений астмы и употребление снотворных |
| Busse et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Soler et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Milgrom et al. [2001] (DBPC) | Уменьшение обострений астмы и употребление снотворных | |
| Holgate et al. [2004] (DBPC) | Сокращение использования вспомогательных средств; улучшение оценки симптомов и качества жизни астмы | |
| Humbert et al. [2005] (DBPC) | Уменьшение числа обострений астмы и количества обращений в отделение неотложной помощи; улучшение качества жизни при астме, утреннего PEF, оценки симптомов астмы | |
| Анти-TNF-α: этанерцепт (SC), голимумаб (SC) | Howarth et al. [2005] (открытое исследование) | Улучшение ОФВ 1 , FVC, PEF, AHR и контроль астмы; добровольное прекращение использования небулайзерного облегчения |
| Berry et al. [2006] (CS) | Улучшение FEV 1 , FVC, PEF, AHR и качества жизни астмы | |
| Morjaria et al. [2008] (DBPC) | Улучшение контроля астмы; добровольное прекращение использования небулайзерного облегчения | |
| Wenzel et al. [2009] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам (исследование прекращено досрочно из-за СНЯ) | |
| Анти-ИЛ-5: меполизумаб (IV) | Haldar et al. [2009] (DBPC) | Уменьшение обострений астмы; улучшение качества жизни при астме |
| Nair et al. [2009] (DBPC) | Уменьшение обострений астмы и снижение дозы OCS без обострений; улучшение ОФВ 1 и контроль астмы | |
| Анти-IL-4 рецептор (IL-4Rα): AMG 317 | Corren et al. [2010] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам не было. |
| Анти-CD25: даклизумаб (IV) | Busse et al. [2008] (DBPC) | Улучшение ОФВ 1 , дневных симптомов астмы и использования восстановительных средств; увеличивается во время обострений |
| Anti-SCF / c-kit и рецептор PDGF: маситиниб (PO) | Humbert et al. [2009] (DBPC) | Улучшение контроля астмы |
Омализумаб.
IgE играет ключевую роль в развитии аллергических состояний [Corry and Kheradmand, 1999]. Аллерген-специфический IgE связывается с эффекторными клетками через рецепторы с высоким сродством (FceRI) и низким сродством (FceRII), вызывая их эффекты, такие как индукция дегрануляции тучных клеток и базофилов, вызывая результирующие реакции на ранней и поздней фазах [Gould и Саттон, 2008 г .; Morjaria et al. 2007]. Омализумаб представляет собой рекомбинантное гуманизированное IgE-специфическое моноклональное антитело, которое прерывает взаимодействие между IgE и FceRI на эффекторных клетках [Presta et al. 1994]. Ранние фармакодинамические исследования омализумаба показали, что он снижает воспаление, AHR, аллерген-индуцированные дыхательные пути и кожные пробы [Boulet et al. 1997; Fahy et al. 1997].
Было проведено шесть крупных двойных слепых плацебо-контролируемых (DBPC) исследований III фазы с применением омализумаба подкожно в дозе 0.016 мг / кг / IgE (МЕ / мл) каждые 2 или 4 недели для оценки его безопасности и эффективности при тяжелой атопической астме с симптомами, несмотря на оптимальную терапию [Humbert et al. 2005; Holgate et al. 2004; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. Продолжительность исследований составляла от 25 до 52 недель с участием субъектов с уровнем IgE от 30 до 700 МЕ / мл). В совокупности анализ различных исследований, а также коллективные оценки показали, что добавление омализумаба привело к улучшению субъективных параметров контроля астмы и качества жизни, а также к объективным улучшениям функции легких, а также к сокращению использования вспомогательных средств, использования кортикостероидов, количества обращений в отделение неотложной помощи. и количество обострений астмы [Bousquet et al. 2005, 2004; Chipps et al. 2005; Humbert et al. 2005; Holgate et al. 2004; Finn et al. 2003; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. В период исследования омализумаб был безопасен без значительных побочных эффектов по сравнению с плацебо. Однако в постмаркетинговых отчетах сообщается о незначительном увеличении количества анафилактических и анафилактоидных реакций, злокачественных новообразований и гельминтозов [Cruz et al. 2007; НИЦЦА, 2007; Vignola et al. 2004].
Следует отметить, что пациенты, принимающие омализумаб, проходят 16-недельную оценку эффективности и безопасности, чтобы убедиться, что они получают пользу от терапии анти-IgE. Отчасти это связано со стоимостью препарата. Хотя омализумаб является безопасным и эффективным лекарством, важно помнить, что лишь небольшая часть тяжелых астматиков страдает атопией, и даже из них только две трети получат от него пользу; большинство TRAS не являются атопическими и не подходят для лечения анти-IgE.
Антагонизм фактора некроза опухоли альфа.
TNF-α представляет собой многофункциональный провоспалительный цитокин Th2, который, как предполагается, играет важную роль в инициировании, поддержании и прогрессировании воспаления дыхательных путей при астме [Morjaria et al. 2006]. Сообщается, что уровни TNF-α в дыхательных путях повышаются при тяжелом заболевании. Неспособность кортикостероидов снижать уровень TNF-α и цитокинов, производных Th2, в дыхательных путях астматиков может объяснить, почему кортикостероиды имеют ограниченную эффективность при TRA.Следовательно, было постулировано, что противодействие TNF-α и, следовательно, вмешательство в цитокины, производные Th2, может представлять собой прогресс в лечении TRA.
На основе этой предпосылки два небольших исследования (одно доказательство концепции [Howarth et al. 2005], а другое — перекрестное исследование с плацебо-контролем [Berry et al. 2006]) антагонизма TNF-α с использованием растворимого рецептора этанерцепта. Они сообщили о значительном улучшении качества жизни, связанного с астмой (AQLQ), и контроля астмы, а также спирометрии, PEF и AHR.Однако в более крупном исследовании DBPC с использованием того же растворимого рецептора не сообщалось о таких драматических эффектах, с лишь незначительным улучшением контроля астмы [Morjaria et al. 2008]. Подобно этому исследованию, еще более крупное исследование DBPC с использованием моноклонального антитела к TNF-α, голимумаба, не продемонстрировало улучшения каких-либо измеренных параметров, но на самом деле исследование было прекращено досрочно из-за опасений по поводу безопасности [Wenzel et al. 2009]. Увеличилось не только количество солидных злокачественных новообразований, но и серьезных инфекций, таких как пневмония, сепсис и реактивация туберкулеза.Однако следует отметить, что в двух более крупных исследованиях [Wenzel et al. 2009; Morjaria et al. 2008] упомянули, что у включенных в исследование пациентов было более легкое заболевание по сравнению с пациентами меньших исследований [Berry et al. 2006; Howarth et al. 2005]. Следовательно, даже если можно выделить подгруппы, в которых анти-TNF-α могут быть эффективными, необходимо принять во внимание эти связанные с лечением тяжелые побочные эффекты. В настоящее время нет известных нам исследований, использующих стратегии против TNF-α.
Анти-ИЛ-5: меполизумаб.
Эозинофилия в дыхательных путях и их дегрануляция являются признаком астмы и связаны с цитокинами Th3, а именно с ИЛ-4, ИЛ-5, ИЛ-9, ИЛ-13 и гранулоцитарно-макрофагальным колониестимулирующим фактором [Rothenberg и Хоган, 2006; Simon et al. 2004; Мензис-Гоу и Робинсон, 2002; Сандерсон, 1992]; все они выражены в повышенных количествах при тяжелой астме [Desai and Brightling, 2009]. IL-5 — важный цитокин, специфичный для эозинофилов.На основе этого принципа антагонизация IL-5 с использованием моноклонального антитела, меполизумаба, проводилась у пациентов с легким или умеренным заболеванием без заметных клинических улучшений [Flood-Page et al. 2007, 2003a, 2003b; Buttner et al. 2003; Menzies-Gow et al. 2003; Leckie et al. 2000].
Совсем недавно были проведены два исследования DBPC с участием пациентов, которые имели стойкую эозинофилию, несмотря на терапию кортикостероидами с использованием меполизумаба с хорошей эффективностью и безопасностью [Haldar et al. 2009; Наир и др. 2009]. Они сообщили о значительном сокращении обострений астмы [Haldar et al. 2009; Наир и др. 2009] и снижение дозы ОКС без обострений [Nair et al. 2009], а также значительное улучшение объема форсированного выдоха за одну секунду (FEV 1 ) [Nair et al. 2009], контроль астмы [Nair et al. 2009], AQLQ [Haldar et al. 2009] и резкое снижение эозинофилии мокроты и крови [Haldar et al. 2009; Наир и др. 2009]. В обоих исследованиях не было отмечено серьезных нежелательных явлений. В настоящее время проводятся более крупные исследования для подтверждения результатов этих двух исследований в этой небольшой подгруппе TRA.
Антагонизм рецептора IL-4 альфа (IL-4Rα).
Как упоминалось выше (в разделе об анти-IL-5), IL-4 и IL-13 также являются цитокинами Th3, которые играют роль в патогенезе астмы, и, следовательно, нацеливание на эти цитокины может быть эффективным при тяжелом заболевании [ Webb et al. 2000; Grunig et al. 1998; Wills-Karp et al. 1998]. Следует отметить, что IL-4Ra используется обоими этими цитокинами для проявления своей активности [Rolling et al. 1996]. Имея это в виду, было проведено большое исследование DBPC у умеренных и тяжелых астматиков для оценки безопасности и эффективности полностью гуманизированных моноклональных антител к IL-4Rα, AMG 317 [Corren et al. 2010]. Было отмечено, что не было улучшений ни по одному из параметров, оцениваемых в исследовании.Однако апостериорный анализ показал, что AMG 317 может иметь значение у пациентов с наибольшим количеством симптомов. При использовании AMG 317 не было серьезных проблем с побочными эффектами.
Анти-CD25: даклизумаб.
Т-клетки играют роль в воспалении дыхательных путей при астме, при этом повышенные уровни CD25 Т-клеток и цитокина IL-2 отмечаются при более тяжелых формах заболевания [Kon and Kay, 1999; Park et al. 1994; Робинсон и др. 1993; Azzawi et al. 1992].Используя этот принцип, Буссе и его коллеги провели исследование для оценки безопасности и эффективности гуманизированного моноклонального антитела к альфа-субъединице (CD25) высокоаффинного рецептора IL-2, тем самым препятствуя связыванию IL-2 [Busse et al. . 2008]. В этом исследовании DBPC у умеренно-тяжелых астматиков сообщалось о минимальном значительном улучшении ОФВ 1 , дневных симптомов астмы, увеличения времени до обострения астмы и сокращения использования вспомогательных средств в пользу даклизумаба.Хотя в группе даклизумаба было больше побочных эффектов, они не были значительными. Место даклизумаба в TRA требует дальнейшей оценки в более крупных исследованиях.
Ингибитор тирозинкиназы рецептора фактора стволовых клеток (c-kit) / рецептора тромбоцитарного фактора роста: маситиниб.
Тучные клетки и дендритные клетки являются клетками, участвующими в TRA [Krishnamoorthy et al. 2008; Chanez et al. 2007; Холгейт и Полоса, 2006; Ребер и др. 2006].Они могут быть активированы с помощью рецептора c-kit фактора стволовых клеток (SCF), что приводит к накоплению тучных клеток, AHR и повышению уровня гистамина, эозинофильной инфильтрации, а также продукции IL-4. Более того, фактор роста тромбоцитов (PDGF), фактор роста, участвует в ремоделировании дыхательных путей [Chung et al. 2006; Инграм и Боннер, 2006]. Следовательно, противодействие рецепторам SCF / c-kit и PDGF может быть потенциальной терапевтической мишенью. Имея это в виду, маситиниб, ингибитор тирозинкиназы, который специфически противодействует рецепторам c-kit и PDGF, был использован для оценки его эффективности и безопасности у субъектов с тяжелой персистирующей астмой, несмотря на высокие дозы ICS, а также OCS [Humbert et al. 2009]. В этом исследовании DBPC Humbert и его коллеги рандомизировали 44 пациента для приема маситиниба перорально в трех дозах: 3 ( n = 12), 4,5 ( n = 11) или 6 ( n = 10) мг / кг / день. или плацебо ( n = 11), т.е. 3: 1, в течение 16 недель. Ни первичная конечная точка отлучения от OCS, ни какие-либо параметры функции дыхательных путей не показали существенной разницы между различными дозами маситиниба и / или плацебо. В обеих группах было 14 выбывших, которые были одинаковыми в обеих группах из-за нежелательных явлений или отсутствия терапевтической эффективности.Следует отметить, что единственным показателем значительного улучшения был показатель ACQ в группе маситиниба по сравнению с группой плацебо. Исследователи сообщили о том, что пациенты, принимавшие высокие дозы OCS и получавшие маситиниб ( n = 6), могли быть отлучены от дозы OCS по сравнению с отсутствием в группе плацебо. Также сообщалось, что пациенты, принимавшие маситиниб, имели больше незначительных, а также серьезных побочных эффектов по сравнению с пациентами, принимавшими плацебо. Это исследование фазы IIa показывает, что маситиниб может играть незначительную роль в TRA, если таковая имеется, поскольку были отмечены только субъективные улучшения.
Заключение
Астма остается очень важным условием с точки зрения бремени экономики здравоохранения, заболеваемости, влияния на качество жизни пациентов и вариантов лечения. Ведение пациентов с TRA — огромная проблема для клиницистов. Появление потенциальных новых иммуномодулирующих агентов может предоставить новые терапевтические возможности для TRA в будущем. Напротив, варианты лечения легкой и умеренной астмы хорошо известны. Однако в этой популяции астматиков есть подгруппа пациентов, которые могут проявлять атипичность.Таким образом, осведомленность клиницистов о возможных различных фенотипических подгруппах астмы очень важна. Если эти синдромы атипичной астмы диагностируются на ранней стадии, их лечение относительно просто, и контроль симптомов может быть достигнут у значительной части пациентов.
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Авторы заявляют об отсутствии конфликта интересов при подготовке данной рукописи.
Ссылки
- Antoncelli L., Bucca C., Neri M., De Benedetto F., Saabbatani P.B.F. (2004) Степень тяжести астмы и использование медицинских ресурсов. Eur Respir J 23: 723–729 [PubMed] [Google Scholar]
- Asthma UK (2010) Веб-сайт Asthma UK, http://www.asthma.org.uk (по состоянию на октябрь 2010 г.).
- Аззави М., Джонстон П.В., Маджумдар С., Кей А.Б., Джеффри П.К. (1992) Т-лимфоциты и активированные эозинофилы в слизистой оболочке дыхательных путей при фатальной астме и муковисцидозе. Am Rev Respir Dis 145: 1477–1482 [PubMed] [Google Scholar]
- Бейтман Э.D., Boushey H.A., Bousquet J., Busse W.W., Clark T.J., Pauwels R.A. и др. (2004) Можно ли достичь контроля астмы в соответствии с рекомендациями? Исследование достижения оптимального контроля над астмой. Am J Respir Crit Care Med 170: 836–844 [PubMed] [Google Scholar]
- Бизли Р., Алдингтон С. (2007) Магний в лечении астмы. Curr Opin Allergy Clin Immunol 7: 107–110 [PubMed] [Google Scholar]
- Берри М.А., Харгадон Б., Шелли М., Паркер Д., Шоу Д.Э., Грин Р.Х. и др. (2006) Доказательства роли фактора некроза опухоли альфа при рефрактерной астме.N Engl J Med 354: 697–708 [PubMed] [Google Scholar]
- Black P.N., Scicchitano R., Jenkins C.R., Blasi F., Allegra L., Wlodarczyk J. и др. (2000) Серологические доказательства инфекции Chlamydia pneumoniae связаны с тяжестью астмы. Eur Respir J 15: 254–259 [PubMed] [Google Scholar]
- Boulet L.P., Chapman K.R., Cote J., Kalra S., Bhagat R., Swystun V.A. и др. (1997) Ингибирующее действие анти-IgE-антитела Е25 на индуцированный аллергеном ранний астматический ответ.Am J Respir Crit Care Med 155: 1835–1840 [PubMed] [Google Scholar]
- Bousquet J., Cabrera P., Berkman N., Buhl R., Holgate S., Wenzel S., et al. (2005) Влияние лечения омализумабом, анти-IgE-антителом, на обострения астмы и посещение неотложной медицинской помощи у пациентов с тяжелой персистирующей астмой. Аллергия 60: 302–308 [PubMed] [Google Scholar]
- Bousquet J., Wenzel S., Holgate S., Lumry W., Freeman P., Fox H. (2004) Прогнозирование ответа на омализумаб, антитело против IgE , у пациентов с аллергической астмой.Грудь 125: 1378–1386 [PubMed] [Google Scholar]
- Браман С.С. (2006) Глобальное бремя астмы. Грудь 130: 4S – 12S [PubMed] [Google Scholar]
- Браман С.С., Коррао В.М. (1985) Хронический кашель. Диагностика и лечение. Prim Care 12: 217–225 [PubMed] [Google Scholar]
- Brightling C.E. (2006) Хронический кашель, вызванный неастматическим эозинофильным бронхитом. Руководство по клинической практике, основанное на доказательствах ACCP. Грудь 129: 116–121 с [PubMed] [Google Scholar]
- Брайтлинг К.Э., Брэддинг П., Саймон Ф.А., Холгейт С.Т., Уордлоу А.Дж., Паворд И.Д. (2002) Инфильтрация тучными клетками гладкой мускулатуры дыхательных путей при астме. N Engl J Med 346: 1699–1705 [PubMed] [Google Scholar]
- Brightling C.E., Pavord I.D. (2000) Эозинофильный бронхит — что это такое и почему это важно ?. Clin Exp Allergy 30: 4–6 [PubMed] [Google Scholar]
- Brightling C.E., Symon F.A., Birring S.S., Bradding P., Wardlaw A.J., Pavord I.D. (2003) Сравнение иммунопатологии дыхательных путей эозинофильного бронхита и астмы.Грудная клетка 58: 528–532 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Го К.Л., Уордлоу А.Дж., Паворд И.Д. (1999a) Эозинофильный бронхит — важная причина хронического кашля. Am J Respir Crit Care Med 160: 406–410 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Уордлоу А.Дж., Паворд И.Д. (2000a) Воспаление дыхательных путей, чувствительность дыхательных путей и кашель до и после ингаляции будесонида у пациентов с эозинофильным бронхитом. Eur Respir J 15: 682–686 [PubMed] [Google Scholar]
- Брайтлинг К.E., Ward R., Woltmann G., Bradding P., Sheller J.R., Dworski R. и др. (2000b) Индуцированные концентрации медиатора воспаления в мокроте при эозинофильном бронхите и астме. Am J Respir Crit Care Med 162: 878–882 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Вольтманн Г., Вардлоу А.Дж., Паворд И.Д. (1999b) Развитие необратимой обструкции воздушного потока у пациента с эозинофильным бронхитом без астмы. Eur Respir J 14: 1228–1230 [PubMed] [Google Scholar]
- BTS / SIGN. (2008) BTS / Sign (Британское торакальное общество / Шотландская межвузовская сеть).Британское руководство по лечению астмы: Национальное клиническое руководство. Грудная клетка 63 (Дополнение IV): iv1 – iv121 [PubMed] [Google Scholar]
- Busse W., Corren J., Lanier B.Q., Mcalary M., Fowler-Taylor A., Cioppa G.D., et al. (2001) Омализумаб, рекомбинантное гуманизированное моноклональное антитело против IgE, для лечения тяжелой аллергической астмы. J Allergy Clin Immunol 108: 184–190 [PubMed] [Google Scholar]
- Busse W.W., Israel E., Nelson H.S., Baker J.W., Charous B.L., Young D.Y. и др.(2008) Даклизумаб улучшает контроль астмы у пациентов со средней и тяжелой персистирующей астмой: рандомизированное контролируемое исследование. Am J Respir Crit Care Med 178: 1002–1008 [PubMed] [Google Scholar]
- Buttner C., Lun A., Splettstoesser T., Kunkel G., Renz H. (2003) Лечение моноклональным анти-интерлейкином-5 подавляет эозинофилы, но не Т-клетки функции. Eur Respir J 21: 799–803 [PubMed] [Google Scholar]
- Карни И.К., Гибсон П.Г., Мюрри-Аллен К., Салтос Н., Олсон Л.Г., Хенсли М.J. (1997) Систематическая оценка механизмов хронического кашля. Am J Respir Crit Care Med 156: 211–216 [PubMed] [Google Scholar]
- Chanez P., Wenzel S.E., Anderson G.P., Anto J.M., Bel E.H., Boulet L.P., et al. (2007) Тяжелая форма астмы у взрослых: каковы важные вопросы ?. J Allergy Clin Immunol 119: 1337–1348 [PubMed] [Google Scholar]
- Чиппс Б., Коррен Дж., Финн А., Хеджекок С., Фокс Х., Блог М. (2005) Омализумаб значительно улучшает качество жизни пациентов с тяжелыми формами стойкая астма.J Allergy Clin Immunol 115: S5 – S19 [Google Scholar]
- Chung K.F., Hew M., Score J., Jones A.V., Reiter A., Cross N.C., et al. (2006) Кашель и гиперэозинофилия из-за слитого гена FIP1L1-PDGFRA с тирозинкиназной активностью. Eur Respir J 27: 230–232 [PubMed] [Google Scholar]
- Чунг К.Ф., Паворд И.Д. (2008) Распространенность, патогенез и причины хронического кашля. Ланцет 371: 1364–1374 [PubMed] [Google Scholar]
- Cook P.J., Davies P., Tunnicliffe W., Ayres J.G., Honeybourne D., Wise R. (1998) Chlamydia pneumoniae и астма. Грудная клетка 53: 254–259 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Corrao W.M., Braman S.S., Irwin R.S. (1979) Хронический кашель как единственное проявление бронхиальной астмы. N Engl J Med 300: 633–637 [PubMed] [Google Scholar]
- Corren J., Busse W., Meltzer E.O., Mansfield L., Bensch G., Fahrenholz J. и др. (2010) Рандомизированное контролируемое исследование фазы 2 AMG 317, антагониста IL-4Ralpha, у пациентов с астмой.Am J Respir Crit Care Med 181: 788–796 [PubMed] [Google Scholar]
- Корри Д. Б., Херадманд Ф. (1999) Индукция и регуляция ответа IgE. Природа 402: B18 – B23 [PubMed] [Google Scholar]
- Cruz A.A., Lima F., Sarinho E., Ayre G., Martin C., Fox H., et al. (2007) Безопасность антииммуноглобулиновой терапии омализумабом у пациентов с аллергией, подверженных риску геогельминтной инфекции. Clin Exp Allergy 37: 197–207 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Каннингем А.Ф., Джонстон С.Л., Джулиус С.А., Лампе Ф.С., Уорд М.Е. (1998) Хроническая инфекция Chlamydia pneumoniae и обострения астмы у детей. Eur Respir J 11: 345–349 [PubMed] [Google Scholar]
- Де Диего А., Мартинес Э., Перпина М., Ньето Л., Компте Л., Мачиан В. и др. (2005) Воспаление дыхательных путей и чувствительность к кашлю при кашлевой астме. Аллергия 60: 1407–1411 [PubMed] [Google Scholar]
- Desai D., Brightling C. (2009) Цитокиновая и антицитокиновая терапия при астме: готовы к клинике ?.Клин Эксп Иммунол 158: 10–19 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Dicpinigaitis P.V. (2006) Хронический кашель из-за астмы: клинические рекомендации ACCP, основанные на фактических данных. Грудь 129: 75S – 79S [PubMed] [Google Scholar]
- Dicpinigaitis P.V., Добкин J.B., Reichel J. (2002) Противокашлевое действие антагониста лейкотриеновых рецепторов зафирлукаста у субъектов с кашлевой астмой. J астма 39: 291–297 [PubMed] [Google Scholar]
- Европейская сеть по изучению механизмов тяжелой астмы.(2003) Поперечное европейское многоцентровое исследование клинического фенотипа тяжелой хронической астмы Enfumosa. Eur Respir J 22: 470–477 [PubMed] [Google Scholar]
- Fahy J.V., Fleming H.E., Wong H.H., Liu J.T., Su J.Q., Reimann J., et al. (1997) Влияние моноклонального антитела против IgE на раннюю и позднюю фазу ответа на вдыхание аллергена у пациентов с астмой. Am J Respir Crit Care Med 155: 1828–1834 [PubMed] [Google Scholar]
- Финн А., Гросс Г., Ван Бавель Дж., Ли Т., Виндом Х., Эверхард Ф. и др. (2003) Омализумаб улучшает качество жизни, связанное с астмой, у пациентов с тяжелой аллергической астмой. J Allergy Clin Immunol 111: 278–284 [PubMed] [Google Scholar]
- Флад-Пейдж П., Мензис-Гоу А., Фиппс С., Ин С., Вангу А., Людвиг М.С. и др. (2003a) Лечение анти-IL-5 снижает отложение белков ЕСМ в субэпителиальной базальной мембране бронхов у больных с легкой атопической астмой. J Clin Invest 112: 1029–1036 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Flood-Page P., Свенсон К., Файферман И., Мэтьюз Дж., Уильямс М., Бранник Л. и др. (2007) Исследование по оценке безопасности и эффективности меполизумаба у пациентов с умеренной персистирующей астмой. Am J Respir Crit Care Med 176. Am J Respir Crit Care Med 167: 199–204 [PubMed] [Google Scholar]
- Fujimura M., Або М., Огава Х., Ниси К., Кибе Ю., Хиросе Т. и др. (2005a) Важность атопического кашля, кашлевой астмы и синобронхиального синдрома как причин хронического кашля в районе Хокурику в Японии. Респирология 10: 201–207 [PubMed] [Google Scholar]
- Fujimura M., Hara J., Myou S. (2005b) Изменение бронхиальной реактивности и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой: эффект ингаляционных кортикостероидов. Кашель 1: 5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Nishizawa Y., Nishitsuji M., Nomura S., Abo M., Ogawa H. (2005c) Предикторы типичного начала астмы при кашлевом варианте астмы. J астма 42: 107–111 [PubMed] [Google Scholar]
- Fujimura M., Ogawa H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности. Грудная клетка 58: 737 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Nishizawa Y., Nishi K. (2003) Сравнение атопического кашля с кашлевым вариантом астмы: является ли атопический кашель предшественником астма ?.Грудная клетка 58: 14–18 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Yasui M., Matsuda T. (2000) Эозинофильный трахеобронхит и гиперчувствительность дыхательных путей при хроническом непродуктивном кашле. Clin Exp Allergy 30: 41–47 [PubMed] [Google Scholar]
- Fujimura M., Ohkura N., Abo M., Furusho S., Waseda Y., Ichikawa Y., et al. (2008) Уровни оксида азота в выдыхаемом воздухе у пациентов с атопическим кашлем и кашлевой астмой. Респирология 13: 359–364 [PubMed] [Google Scholar]
- Fujimura M., Сакамото С., Мацуда Т. (1992) Бронходилататорно-резистивный кашель у пациентов с атопией: бронхиальная обратимость и гиперреактивность. Intern Med 31: 447–452 [PubMed] [Google Scholar]
- Fujimura M., Songur N., Kamio Y., Matsuda T. (1997) Обнаружение эозинофилов в мокроте, индуцированной гипертоническим солевым раствором, у пациентов с хроническим непродуктивным кашлем. J астма 34: 119–126 [PubMed] [Google Scholar]
- Гибсон П.Г., Долович Дж., Денбург Дж., Рамсдейл Э. Х., Харгрив Ф. Э. (1989) Хронический кашель: эозинофильный бронхит без астмы.Ланцет 1: 1346–1348 [PubMed] [Google Scholar]
- Гибсон П.Г., Фудзимура М., Ниими А. (2002) Эозинофильный бронхит: клинические проявления и последствия для лечения. Грудная клетка 57: 178–182 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Gibson PG, Zlatic K., Scott J., Sewell W., Woolley K., Saltos N. (1998) Хронический кашель напоминает астму с ИЛ -5 и экспрессия гена колониестимулирующего фактора гранулоцитов-макрофагов в бронхоальвеолярных клетках. J Allergy Clin Immunol 101: 320–326 [PubMed] [Google Scholar]
- Гулд Х.J., Sutton B.J. (2008) IgE при аллергии и астме сегодня. Нат Рев Иммунол 8: 205–217 [PubMed] [Google Scholar]
- Grayston J.T. (1992) Инфекции, вызванные штаммом Chlamydia pneumoniae twar. Clin Infect Dis 15: 757–761 [PubMed] [Google Scholar]
- Grunig G., Warnock M., Wakil A.E., Venkayya R., Brombacher F., Rennick D.M. и др. (1998) Потребность в IL-13 независимо от IL-4 при экспериментальной астме. Наука 282: 2261–2263 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Брайтлинг С.Е., Харгадон Б., Гупта С., Монтейро В., Соуза А. и др. (2009) Меполизумаб и обострения рефрактерной эозинофильной астмы. N Engl J Med 360: 973–984 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Pavord I.D., Shaw D.E., Berry M.A., Thomas M., Brightling C.E., et al. (2008) Кластерный анализ и клинические фенотипы астмы. Am J Respir Crit Care Med 178: 218–224 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hamilton L.M., Torres-Lozano C., Puddicombe S.М., Рихтер А., Кимбер И., Дирман Р. Дж. И др. (2003) Роль рецептора эпидермального фактора роста в поддержании нейтрофильного воспаления при тяжелой астме. Clin Exp Allergy 33: 233–240 [PubMed] [Google Scholar]
- Hammerschlag M.R. (2000) Chlamydia pneumoniae и легкие. Eur Respir J 16: 1001–1007 [PubMed] [Google Scholar]
- Хоффштейн В. (1994) Постоянный кашель у некурящих. Может Респир J 1: 40–47 [Google Scholar]
- Холгейт С.Т., Чучалин А.Г., Хеберт Дж., Лотвалл Дж., Перссон Г. Б., Чунг К. Ф. и др. (2004) Эффективность и безопасность рекомбинантного антитела против иммуноглобулина Е (омализумаб) при тяжелой аллергической астме. Clin Exp Allergy 34: 632–638 [PubMed] [Google Scholar]
- Холгейт С.Т., Полоса Р. (2006) Механизмы, диагностика и лечение тяжелой астмы у взрослых. Ланцет 368: 780–793 [PubMed] [Google Scholar]
- Ховарт П.Х., Бабу К.С., Аршад Х.С., Лау Л.С., Бакли М.Г., Макконнелл В. и др. (2005) Фактор некроза опухоли (TNF {альфа) как новая терапевтическая мишень при симптоматической кортикостероидной астме.Грудная клетка 60: 1012–1018, Epub, 15 сентября 2005 г. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Humbert M., Beasley R., Ayres J., Slavin R., Hebert J., Bousquet J., et al. (2005) Преимущества омализумаба в качестве дополнительной терапии у пациентов с тяжелой персистирующей астмой, которые недостаточно контролируются, несмотря на лучшую доступную терапию (лечение GINA 2002, шаг 4): Innovate. Аллергия 60: 309–316 [PubMed] [Google Scholar]
- Humbert M., De Blay F., Garcia G., Prud’homme A., Leroyer C., Magnan A., и другие. (2009) Маситиниб, ингибитор тирозинкиназы рецептора c-kit / PDGF, улучшает контроль заболевания у тяжелых кортикостероидозависимых астматиков. Аллергия 64: 1194–1201 [PubMed] [Google Scholar]
- Инграм Дж. Л., Боннер Дж. С. (2006) Тирозинкиназы рецепторов EGF и PDGF как терапевтические мишени при хронических заболеваниях легких. Курр Мол Мед 6: 409–421 [PubMed] [Google Scholar]
- Ирвин Р.С., Бауманн М.Х., Болсер Д.К., Буле Л.П., Браман С.С., Брайтлинг С.Э. и др. (2006) Диагностика и лечение кашля. Краткое изложение: клинические рекомендации ACCP, основанные на фактических данных.Грудь 129: 1S – 23S [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Ирвин Р.С., Коррао В.М., Праттер М.Р. (1981) Хронический стойкий кашель у взрослых: спектр и частота причин и успешный результат специфической терапии. Am Rev Respir Dis 123: 413–417 [PubMed] [Google Scholar]
- Ирвин Р.С., Керли Ф.Дж., French C.L. (1990) Хронический кашель. Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Am Rev Respir Dis 141: 640–647 [PubMed] [Google Scholar]
- Ирвин Р.S., French C.T., Smyrnios N.A., Curley F.J. (1997) Интерпретация положительных результатов ингаляционной пробы метахолина и 1 недели использования ингаляционных бронходилататоров при диагностике и лечении кашлевой астмы. Arch Intern Med 157: 1981–1987 [PubMed] [Google Scholar]
- Jatakanon A., Uasuf C., Maziak W., Lim S., Chung K.F., Barnes P.J. (1999) Нейтрофильное воспаление при тяжелой персистирующей астме. Am J Respir Crit Care Med 160: 1532–1539 [PubMed] [Google Scholar]
- Джонсон Д., Осборн Л.М. (1991) Кашлевой вариант астмы: обзор клинической литературы. J астма 28: 85–90 [PubMed] [Google Scholar]
- Kanazawa H., Eguchi Y., Nomura N., Yoshikawa J. (2005) Анализ уровней фактора роста эндотелия сосудов в индуцированных образцах мокроты пациентов с кашлевой астмой. Энн Аллергия Астма Иммунол 95: 266–271 [PubMed] [Google Scholar]
- Kastelik J.A. (2008) Терапия кашлевой астмы. Многопрофильная респираторная медицина 3: 223–227 [Google Scholar]
- Kastelik J.А., Азиз И., Оху Дж. К., Томпсон Р. Х., Редингтон А. Э., Морис А. Х. (2005) Исследование и лечение хронического кашля с использованием вероятностного алгоритма. Eur Respir J 25: 235–243 [PubMed] [Google Scholar]
- Кита Т., Фудзимура М., Огава Х., Накацуми Ю., Номура С., Ишиура Ю. и др. (2010) Противокашлевые эффекты антагониста лейкотриеновых рецепторов монтелукаста у пациентов с кашлевой астмой и атопическим кашлем. Аллергол Инт 59: 185–192 [PubMed] [Google Scholar]
- Кон О.М., Кей А. (1999) Стратегии борьбы с Т-клетками при астме. Воспаление Res 48: 516–523 [PubMed] [Google Scholar]
- Кришнамурти Н., Орисс Т. Б., Паглиа М., Фей М., Ярлагадда М., Ванхасебрук Б. и др. (2008) Активация c-kit в дендритных клетках регулирует дифференцировку Т-хелперных клеток и аллергическую астму. Нат Мед 14: 565–573 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Leckie M.J., Ten Brinke A., Khan J., Diamant Z., O’connor B.J., Walls C.M., et al. (2000) Эффекты моноклональных антител, блокирующих интерлейкин-5, на эозинофилы, гиперчувствительность дыхательных путей и позднюю астматическую реакцию.Ланцет 356: 2144–2148 [PubMed] [Google Scholar]
- Leff J.A., Busse W.W., Pearlman D., Bronsky E.A., Kemp J., Hendeles L., et al. (1998) Монтелукаст, антагонист лейкотриеновых рецепторов, для лечения легкой формы астмы и бронхоспазма, вызванного физической нагрузкой. N Engl J Med 339: 147–152 [PubMed] [Google Scholar]
- Мартин Р.Дж., Крафт М., Чу Х.В., Бернс Э.А., Касселл Г.Х. (2001) Связь между хронической астмой и хронической инфекцией. J Allergy Clin Immunol 107: 595–601 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Табуена Р.П., Такемура М., Уэда Т., Ямагути М. и др. (2007) Утолщение стенки дыхательных путей у пациентов с кашлевой астмой и неастматическим хроническим кашлем. Грудь 131: 1042–1049 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Такемура М., Уэда Т., Табуена Р., Ямагути М. и др. (2006) Прогноз кашлевого варианта астмы: ретроспективный анализ. J астма 43: 131–135 [PubMed] [Google Scholar]
- Mcgarvey L., Morice A.H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности.Грудная клетка 58: 736–737, ответ автора 737-738. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mcgarvey L.P., Heaney L.G., Lawson J.T., Johnston B.T., Scally C.M., Ennis M., et al. (1998) Оценка и исходы пациентов с хроническим непродуктивным кашлем с использованием комплексного диагностического протокола. Грудная клетка 53: 738–743 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Мелло С.Дж., Ирвин Р.С., Керли Ф.Дж. (1996) Прогностические значения характера, времени и осложнений хронического кашля при диагностике его причины.Arch Intern Med 156: 997–1003 [PubMed] [Google Scholar]
- Menzies D., Holmes L., Mccumesky G., Prys-Picard C., Niven R. (2011) Сенсибилизация Aspergillus связана с ограничением воздушного потока и бронхоэктазами при тяжелой астме . Аллергия 66: 679–685 [PubMed] [Google Scholar]
- Мензис-Гоу А., Флад-Пейдж П., Сехми Р., Берман Дж., Хамид К., Робинсон Д.С. и др. (2003) Анти-IL-5 (меполизумаб) терапия вызывает задержку созревания эозинофилов в костном мозге и снижает количество предшественников эозинофилов в слизистой оболочке бронхов у больных атопической астмой.J Allergy Clin Immunol 111: 714–719 [PubMed] [Google Scholar]
- Мензис-Гоу А., Робинсон Д.С. (2002) Эозинофилы, эозинофильные цитокины (интерлейкин-5) и антиэозинофильная терапия при астме. Curr Opin Pulm Med 8: 33–38 [PubMed] [Google Scholar]
- Милгром Х., Бергер В., Наяк А., Гупта Н., Поллард С., Макалари М. и др. (2001) Лечение детской астмы антителом к иммуноглобулину Е (омализумаб). Педиатрия 108: E36. [PubMed] [Google Scholar]
- Милгром Х., Фик Р. Б., младший, Су Дж. К., Рейманн Дж. Д., Буш Р. К., Уотрус М. Л. и др. (1999) Лечение аллергической астмы моноклональными анти-IgE-антителами. Исследовательская группа по Rhumab-E25. N Engl J Med 341: 1966–1973 [PubMed] [Google Scholar]
- Миллар М.М., Макграт К.Г., Паттерсон Р. (1998) Злокачественная астма, эквивалентная кашлю: определение и отчеты о случаях. Энн Аллергия Астма Иммунол 80: 345–351 [PubMed] [Google Scholar]
- Morice A.H., Fontana G.A., Belvisi M.G., Birring S.S., Chung K.F., Dicpinigaitis P.V., et al. (2007) Рекомендации ERS по оценке кашля. Eur Respir J 29: 1256–1276 [PubMed] [Google Scholar]
- Morice A.H., Kastelik J.A. (2003) Кашель. 1: Хронический кашель у взрослых. Грудная клетка 58: 901–907 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Морис А.Х., Макгарви Л., Паворд И. (2006) Рекомендации по лечению кашля у взрослых. Грудная клетка 61 (Приложение 1): i1 – i24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Morjaria J.B., Babu K.S., Holgate S.T., Polosa R.(2006) Фактор некроза опухоли альфа как терапевтическая мишень при астме. Открытие лекарств сегодня: терапевтические стратегии 3: 309–316 [Google Scholar]
- Morjaria J.B., Chauhan A.J., Babu K.S., Polosa R., Davies D.E., Holgate S.T. (2008) Роль слитого белка растворимого рецептора TNF-α (этанерцепта) при резистентной к кортикостероидам астме: двойное слепое рандомизированное плацебо-контролируемое исследование. Грудная клетка 63: 584–591 [PubMed] [Google Scholar]
- Morjaria J.B., Gnanakumaran G., Babu K.S. (2007) Anti-IgE при аллергической астме и рините: обновление.Мнение эксперта Biol Ther 7: 1739–1747 [PubMed] [Google Scholar]
- Morjaria J.B., Polosa R. (2010) Рекомендации по оптимальному ведению тяжелой рефрактерной астмы. J Астма Аллергия 3: 43–56 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Наир П., Пиццичини М.М., Кьярсгаард М., Инман М.Д., Эфтимиадис А., Пиццичини Э. и др. (2009) Меполизумаб для лечения преднизонозависимой астмы с эозинофилией мокроты. N Engl J Med 360: 985–993 [PubMed] [Google Scholar]
- NICE. (2007) Омализумаб при стойкой аллергической астме.NICE Руководство по оценке технологий 133. NICE: Лондон [Google Scholar]
- Niimi A., Amitani R., Suzuki K., Tanaka E., Murayama T., Kuze F. (1998) Эозинофильное воспаление при кашлевом варианте астмы. Eur Respir J 11: 1064–1069 [PubMed] [Google Scholar]
- Ниими А., Мацумото Х., Минакучи М., Китаичи М., Амитани Р. (2000) Ремоделирование дыхательных путей при кашлевой астме. Ланцет 356: 564–565 [PubMed] [Google Scholar]
- Огава Х., Фудзимура М., Тофуку Ю. (2004) Лечение атопического кашля, вызванного антигеном базидиомицетов, низкими дозами итраконазола.Легкое 182: 279–284 [PubMed] [Google Scholar]
- Паломбини Б.С., Вилланова К.А., Араухо Э., Гастал О.Л., Альт Д.К., Штольц Д.П. и др. (1999) Патогенная триада при хроническом кашле: астма, синдром постназального подтекания и гастроэзофагеальная рефлюксная болезнь. Грудь 116: 279–284 [PubMed] [Google Scholar]
- Park C.S., Lee S.M., Chung S.W., Uh S., Kim H.T., Kim Y.H. (1994) Интерлейкин-2 и растворимый рецептор интерлейкина-2 в жидкости бронхоальвеолярного лаважа пациентов с бронхиальной астмой. Грудь 106: 400–406 [PubMed] [Google Scholar]
- Питерс С.П., Кунсельман С.Дж., Ицитович Н., Мур В.С., Паскуаль Р., Амередес Б.Т. и др. (2011) Повышающая терапия тиотропия бромидом для взрослых с неконтролируемой астмой. New Engl J Med 363: 1715–1726 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Poe R.H., Harder R.V., Israel R.H., Kallay M.C. (1989) Хронический непрекращающийся кашель. Опыт диагностики и результатов с использованием протокола анатомической диагностики. Грудь 95: 723–728 [PubMed] [Google Scholar]
- Polosa R., Benfatto G.T. (2009) Ведение пациентов с тяжелой хронической астмой: примите вызов.Eur J Intern Med 20: 114–124 [PubMed] [Google Scholar]
- Polosa R., Morjaria J. (2008) Иммуномодулирующие и биологические методы лечения тяжелой рефрактерной астмы. Респир Мед 102: 1499–1510 [PubMed] [Google Scholar]
- Преста Л., Шилдс Р., О’Коннелл Л., Лар С., Портер Дж., Горман К. и др. (1994) Сайт связывания иммуноглобулина Е человека для его рецептора с высоким сродством. J Biol Chem 269: 26368–26373 [PubMed] [Google Scholar]
- Reber L., Da Silva C.A., Frossard N. (2006) Фактор стволовых клеток и его рецептор c-kit как мишени для воспалительных заболеваний.Eur J Pharmacol 533: 327–340 [PubMed] [Google Scholar]
- Робертс Г., Ньюсом Д., Гомес К., Раффлз А., Саглани С., Бегент Дж. И др. (2003) Внутривенное болюсное введение сальбутамола в сравнении с инфузией эуфиллина у детей с тяжелой астмой: рандомизированное контролируемое исследование. Грудная клетка 58: 306–310 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Робинсон Д.С., Бентли А.М., Хартнелл А., Кей А.Б., Дарем С.Р. (1993) Активированные Т-хелперы памяти в жидкости бронхоальвеолярного лаважа пациентов с атопической астмой: связь с симптомами астмы, функцией легких и реактивностью бронхов.Грудная клетка 48: 26–32 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Rolling C., Treton D., Pellegrini S., Galanaud P., Richard Y. (1996) Рецепторы IL4 и IL13 имеют общую гамма-цепь C и активируют белки Stat6, Stat3 и Stat5 в нормальных В-клетках человека. FEBS Lett 393: 53–56 [PubMed] [Google Scholar]
- Ротенберг М.Э., Хоган С.П. (2006) Эозинофил. Анну Рев Иммунол 24: 147–174 [PubMed] [Google Scholar]
- Sanderson C.J. (1992) Интерлейкин-5, эозинофилы и болезни.Кровь 79: 3101–3109 [PubMed] [Google Scholar]
- Сильверман Р.А., Осборн Х., Рунге Дж., Галлахер Э. Дж., Чан У., Фельдман Дж. И др. (2002) Внутривенное введение сульфата магния в лечении острой тяжелой астмы: многоцентровое рандомизированное контролируемое исследование. Грудь 122: 489–497 [PubMed] [Google Scholar]
- Саймон Д., Браатен Л.Р., Саймон Х.У. (2004) Эозинофилы и атопический дерматит. Аллергия 59: 561–570 [PubMed] [Google Scholar]
- Смирниос Н.А., Ирвин Р.С., Керли Ф.Дж. (1995) Хронический кашель с чрезмерным выделением мокроты в анамнезе.Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Грудь 108: 991–997 [PubMed] [Google Scholar]
- Soler M., Matz J., Townley R., Buhl R., O’brien J., Fox H., et al. (2001) Анти-IgE-антитело омализумаб снижает частоту обострений и потребность в стероидах у аллергических астматиков. Eur Respir J 18: 254–261 [PubMed] [Google Scholar]
- Стивенс Р.С. (2003) Клеточная парадигма патогенеза хламидий. Тенденции Microbiol 11: 44–51 [PubMed] [Google Scholar]
- Тен Бринке А., Ван Диссель Дж. Т., Стерк П. Дж., Звиндерман А. Х., Рабе К. Ф., Бел Э. Х. (2001) Устойчивое ограничение воздушного потока при неатопической астме у взрослых связано с серологическими доказательствами инфекции Chlamydia pneumoniae . J Allergy Clin Immunol 107: 449–454 [PubMed] [Google Scholar]
- Тонелли М., Зингони М., Баччи Э., Денте Ф.Л., Ди Франко А., Джаннини Д. и др. (2003) Кратковременный эффект от добавления антагонистов лейкотриеновых рецепторов к текущей терапии тяжелых астматиков.Пульм Фармакол Тер 16: 237–240 [PubMed] [Google Scholar]
- U-BIOPRED (2008) Объективные биомаркеры для прогнозирования результатов респираторных заболеваний, http://www.fp7-consulting.be/en/ubiopred/
- Vatrella A ., Ponticiello A., Pelaia G., Parrella R., Cazzola M. (2005) Бронходилатирующие эффекты сальметерола, теофиллина и их комбинации у пациентов с умеренной и тяжелой астмой. Пульм Фармакол Тер 18: 89–92 [PubMed] [Google Scholar]
- Виньола А.М., Умберт М., Буске Дж., Буле Л.П., Хеджекок С., Блог М. и др. (2004) Эффективность и переносимость антииммуноглобулиновой терапии омализумабом у пациентов с сопутствующей аллергической астмой и стойким аллергическим ринитом: СОЛАР. Аллергия 59: 709–717 [PubMed] [Google Scholar]
- Фон Герцен Л.С. (2002) Роль персистирующей инфекции в контроле и тяжести астмы: фокус на Chlamydia pneumoniae. Eur Respir J 19: 546–556 [PubMed] [Google Scholar]
- Уорк П.А., Джонстон С.Л., Симпсон Дж. Л., Хенсли М.Дж., Гибсон П.Г. (2002) Chlamydia pneumoniae иммуноглобулин А реактивация и воспаление дыхательных путей при острой астме. Eur Respir J 20: 834–840 [PubMed] [Google Scholar]
- Webb D.C., Mckenzie A.N., Koskinen A.M., Yang M., Mattes J., Foster P.S. (2000) Интегрированные сигналы между IL-13, IL-4 и IL-5 регулируют гиперреактивность дыхательных путей. J Immunol 165: 108–113 [PubMed] [Google Scholar]
- Венцель С., Фахи Дж. В., Ирвин К.Г., Петерс С.П., Спектор С., Сефлер С.Дж. (2000) Материалы семинара ATS по рефрактерной астме: текущее понимание, рекомендации и вопросы без ответа.Am J Respir Crit Care Med 162: 2341–2351 [PubMed] [Google Scholar]
- Венцель С.Э., Барнс П.Дж., Бликер Е.Р., Буске Дж., Бусс В., Дален С.Э. и др. (2009) Рандомизированное двойное слепое плацебо-контролируемое исследование блокады фактора некроза опухоли альфа при тяжелой персистирующей астме. Am J Respir Crit Care Med 179: 549–558 [PubMed] [Google Scholar]
- Венцель С.Э., Шварц Л. (1999) Доказательства того, что тяжелую астму патологически можно разделить на два воспалительных подтипа с различными физиологическими и клиническими характеристиками.Am J Respir Crit Care Med 160: 1001–1008 [PubMed] [Google Scholar]
- Виллс-Карп М., Луимбази Дж., Сюй X., Скофилд Б., Небен Т.Ю., Карп К.Л. и др. (1998) Интерлейкин-13: центральный медиатор аллергической астмы. Наука 282: 2258–2261 [PubMed] [Google Scholar]
Необычные синдромы астмы и их лечение
Ther Adv Chronic Dis. 2011 июл; 2 (4): 249–264.
Джек А. Кастелик
1 Отделение респираторной медицины, Халл и фонд NHS Восточного Йоркшира, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
1 Отдел респираторной медицины, Hull и East Yorkshire NHS Trust, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
2 Отделение IIR, Школа медицины, Университет Саутгемптона, Больница общего профиля Саутгемптона , Саутгемптон СУ 6YD, Великобритания ку.ca.notos@mbjЭта статья цитируется другими статьями в PMC.Abstract
Астма обычно проявляется симптомами хрипов, одышки и кашля. Однако клиницисты должны знать об атипичных проявлениях этого расстройства, когда кашель является основным или единственным симптомом таких состояний, как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель. Ранняя диагностика и лечение этих состояний с помощью ингаляционных кортикостероидов улучшает симптомы у большинства пациентов.До 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Эти пациенты были охвачены термином «резистентная к лечению астма» (TRA), имеют наибольшую заболеваемость и несут более 50% расходов на здравоохранение. В этом обзоре мы обсуждаем исследования, лечение и патофизиологию различных фенотипов атипичных проявлений астмы, а также новые лицензированные биологические агенты и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности при TRA.
Ключевые слова: атопический кашель, биопрепараты, кашель, эозинофильный бронхит, моноклональные антитела, тяжелая астма
Введение
От астмы страдают 5,4 миллиона человек в Великобритании [Asthma UK, 2010] и около 300 миллионов человек в мире [Braman , 2006]. Его распространенность составляет 15-20% у детей и 5-10% у взрослых, и считается, что этот показатель будет продолжать расти. Более 12 миллионов рабочих дней в Великобритании теряются из-за проблем, связанных с астмой [Asthma UK, 2010].Более того, в 2006-2007 финансовом году было зарегистрировано около 80 000 случаев неотложной госпитализации по астме, из которых 41% — дети в возрасте до 14 лет. У большинства пациентов лечение этого состояния на основе международных руководств гарантирует, что астма хорошо контролируется с помощью терапии ингаляционными кортикостероидами (ICS) либо отдельно, либо в сочетании с агонистами β 2 длительного действия (LABA) [BTS / SIGN, 2008 ]. Другие агенты, такие как антилейкотриеновые агенты и теофиллины, также были использованы с хорошим эффектом.Однако до 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Хотя это небольшая часть больных астмой, они имеют наибольшую заболеваемость, рискуют умереть и несут более 50% расходов на здравоохранение, связанных с астмой; следовательно, существует неудовлетворенная потребность в этой группе плохо контролируемых астматиков [Chanez et al. 2007; Antoncelli et al. 2004; Европейская сеть по изучению механизмов тяжелой астмы, 2003 г.]
Астма — это гетерогенное заболевание, которое на одном конце спектра трудно диагностировать из-за атипичных симптомов, например кашля, а на другом конце — у пациентов с установленным заболеванием. где управление ограничено отсутствием доступных нам текущих терапевтических возможностей.Последнюю часто называют тяжелой астмой. Однако необходимо уточнить, что тяжелую астму можно подразделить на «трудно поддающуюся лечению» и «резистентную к лечению астму» (TRA). Следовательно, важно, чтобы этими двумя объектами управляли должным образом.
Трудно поддающаяся лечению астма может возникнуть по ряду причин [Morjaria and Polosa, 2010; Холгейт, Полоса, 2006]. Тремя основными причинами являются, за исключением состояний, имитирующих тяжелую астму, сопутствующие заболевания, триггеры астмы и, что наиболее важно, несоблюдение режима приема лекарств от астмы.И наоборот, TRA включает пациентов, которые не находятся под адекватным контролем с их лекарствами в соответствии с международными рекомендациями [BTS / SIGN, 2008], то есть на этапах IV и V Глобальной инициативы по астме (GINA) и Британского торакального общества / Шотландской межвузовской сети рекомендаций, где, несмотря на находясь на высоких дозах ICS, LABA и других дополнительных лекарствах и сумев установить контроль над компонентами трудноизлечимой астмы, пациенты сохраняют симптомы. Напротив, большинство пациентов с атипичной астмой, такой как кашлевой вариант астмы, неастматический эозинофильный бронхит или атопический кашель, реагируют на стандартную терапию ИКС и антигистаминными препаратами.Осведомленность о существовании этих состояний и связанная с ними способность диагностировать их являются основными проблемами, связанными с атипичной астмой. Если не лечить атипичную астму, у части пациентов может развиться классическая астма. Например, более трети пациентов с кашлевой астмой может прогрессировать до развития классической астмы [Johnson and Osborn, 1991; Браман и Коррао, 1985]. Напротив, только у очень небольшой части пациентов с атопическим кашлем развивается классическая астма [Fujimura et al. 2003].
В этом обзоре мы обсуждаем проблемы, с которыми сталкивается врач при постановке диагноза атипичной астмы. Таким образом, мы описываем исследования и лечение кашлевой астмы, атопического кашля и неастматического эозинофильного бронхита. Кроме того, мы обсуждаем подтверждение и фенотипирование TRA, а также предоставляем обзор новых биологических агентов, которые лицензированы, и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности в TRA.Мы не обсуждаем трудно поддающуюся лечению астму, предполагая, что это учитывалось наряду с соблюдением режима лечения до постановки диагноза TRA.
Атипичная астма
Текущие рекомендации признают, что диагноз астмы является клиническим [BTS / SIGN, 2008]. Центральным во всех определениях астмы является наличие таких симптомов, как хрип, стеснение в груди, одышка или кашель, а также непостоянная обструкция дыхательных путей. Более поздние описания астмы также включали наличие гиперчувствительности дыхательных путей (AHR) и воспаления дыхательных путей [BTS / SIGN, 2008] .У значительной части пациентов диагноз классической астмы вряд ли вызовет какие-либо трудности. У пациентов с классической астмой наблюдаются хрипы, одышка или кашель. Измерения пикового потока выдоха (ПСВ) различаются по дням и в течение суток (). Бронхопровокационные пробы на гистамин или метахолин положительные. При отклонении от нормы спирометрия обычно выявляет обструкцию дыхательных путей. Однако существуют состояния, такие как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель, которые отличаются от классической астмы по своим фенотипическим характеристикам.Поэтому их диагностика может быть более сложной. Хотя эти состояния могут различаться фенотипически, эозинофильное воспаление дыхательных путей составляет их общий знаменатель. Являются ли эти состояния воплощением «астматического синдрома» или представляют собой независимые сущности per se , остается предметом обсуждения [Mcgarvey et al. 2003]. Фактически, существует множество доказательств того, что у некоторых пациентов с этими состояниями, если они не диагностированы или не пролечены надлежащим образом, на самом деле могут развиваться полные характеристики классической астмы [Irwin et al. 2006; Fujimura et al. 2005a, 2005b, 2005c, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b]. Следовательно, осведомленность и способность ранней диагностики и лечения этих состояний имеют важное клиническое значение.
Таблица 1.
Атипичные астматические синдромы.
| Синдром | Вариабельность PEF | Обструкция дыхательных путей | Гиперчувствительность дыхательных путей | Эозинофилия мокроты | Атопия | Стероидный ответ | Результаты биопсии |
|---|---|---|---|---|---|---|---|
| Да | Да 900 | Да | Да | ± | Да | — | |
| Кашлевой вариант астмы | — | Нет | Да | Да | Нет | Да | ↓ толщина субэпителиального слоя по сравнению с классической астмой |
| Эозинофильный бронхит | Нет | Нет | Нет | Да | Нет | Да | ↓ тучные клетки в гладких мышцах дыхательных путей по сравнению с классической астмой |
| Атопический кашель | Нет | Нет | Нет | Да | Да | Да | Эозинофилы в подслизистой оболочке трахеи и бронхов |
Кашлевой вариант астмы
Кашлевый вариант астмы остается частой причиной хронического кашля [Chung and Pavord, 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini el al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981; Poe et al. 1989]. При астме кашель может сопровождаться другими симптомами, такими как хрипы или одышка [Irwin et al. 1990, 1981]. Однако у части пациентов, до 57% случаев в некоторых исследованиях, кашель может быть единственным проявлением этого состояния [Chung et al. 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini et al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1997, 1990, 1981; Poe et al. 1989; Corrao et al. 1979]. В 1979 году Коррао и его коллеги определили «кашлевую астму» как AHR с хроническим кашлем, но без хрипов или обструкции дыхательных путей [Corrao et al. 1979]. После этого первоначального описания стало очевидно, что, хотя кашель является преобладающим респираторным симптомом у части пациентов с кашлевой астмой, хрипы также могут присутствовать [Kastelik et al. 2005; Palombini et al. 1999; Brightling et al. 1999a, 1999b; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981, Poe et al. 1989;]. Фактически, у одной трети пациентов, первоначально обследованных Коррао и его коллегами, впоследствии развилось хрипы [Braman and Corrao, 1985; Corrao et al. 1979]. При кашлевой астме оценка пикового потока выдоха (ПСВ) не выявляет дневной или суточной изменчивости, а спирометрические измерения не выявляют обструкции дыхательных путей. Кроме того, об атопии обычно не сообщается. Более того, присутствует AHR к гистамину или метахолину, а также эозинофилия мокроты [Kastelik, 2008; Morice et al. 2007, 2006; Морис, Кастелик, 2003].
Неастматический эозинофильный бронхит
Неастматический эозинофильный бронхит был первоначально описан Гибсоном и его коллегами и характеризуется эозинофилией мокроты [Brightling, 2006; Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. При неастматическом эозинофильном бронхите обструкции дыхательных путей нет, поскольку измерения спирометрии в норме. Также отсутствует вариабельность PEF и AHR.Однако индуцированный анализ мокроты выявляет эозинофилию, определяемую как более чем 3% от числа несквамоклеточных эозинофилов [Gibson et al. 2002]. Кроме того, повышается чувствительность кашлевого рефлекса.
Атопический кашель
Fujimura и его коллеги описали пациентов с хроническим непродуктивным кашлем и атопией, резистентным к бронходилататорам, и предложили термин эозинофильный трахеобронхит с гиперчувствительностью дыхательных путей или «атопический кашель» [Fujimura et al. 1992]. «Атопический кашель» характеризуется атопией, определяемой как одно или несколько из следующих: эозинофилия крови или мокроты; повышенные уровни общего или специфического иммуноглобулина (Ig) E; или положительный кожный укол [Fujimura et al. 2000, 1997, 1992]. Кроме того, при атопическом кашле наблюдается хронический непродуктивный кашель, устойчивый к бронходилататорам, отсутствие различной обструкции дыхательных путей и нормальная бронхиальная провокация [Dicpinigaitis, 2006; Fujimura et al. 2000, 1997, 1992]. Это состояние характеризуется повышенной реакцией кашля на вдыхаемый капсаицин, присутствием эозинофилов в мокроте и подслизистой биопсии трахеи и бронхов, но не в бронхоальвеолярном лаваже (БАЛ) [Fujimura et al. 2005, 2003, 2000, 1997, 1992]. Однако эксперты по-прежнему обсуждают, является ли атопический кашель отдельным заболеванием, вызывающим хронический кашель [Fujimura and Ogawa, 2003; Макгарви и Морис, 2003]. Некоторые, действительно, предположили, что пациенты с атопическим кашлем, скорее всего, являются атопическими людьми с кашлевой астмой [Mcgarvey and Morice, 2003]. Однако Fujimura и его коллеги определили атопический кашель с его специфической патофизиологией и отсутствием прогресса в классической астме [Fujimura and Ogawa, 2003].Поэтому для клиницистов важно исследовать и исключить другие распространенные причины хронического кашля, такие как кашлевой вариант астмы, гастроэзофагеальный рефлюкс и ринит, до постановки диагноза атопического кашля.
Патофизиология атипичной астмы
В последние годы наше понимание патофизиологии кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля улучшилось [Brightling et al. 2003, 2002, 2000а, 2000б; Брайтлинг и Паворд, 2000; Niimi et al. 2000, 1998]. Эти три состояния имеют схожие иммунопатологические характеристики с классической астмой в виде воспалительного процесса, вызванного эозинофилами. В то время как эозинофильное воспаление является общей патофизиологической характеристикой классической астмы, кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель различаются из-за различий в расположении воспалительных клеток и толщины субэпителиального слоя, о которых сообщалось в этих состояниях, следовательно, вероятные причины наблюдаемого фенотипического несоответствия [Brightling et al. 2002; Niimi et al. 1998].
Кашлевая астма
Эозинофилы играют важную роль в патофизиологии кашлевой астмы [Niimi et al. 1998]. Таким образом, имеются данные о повышенном количестве эозинофилов в ЖБАЛ и тканях пациентов с кашлевой астмой [Niimi et al. 2000]. Однако Де Диего и его коллеги показали, что не было значительной разницы между кашлевой астмой и классической астмой в уровнях мокроты эозинофильного катионного белка (ECP), интерлейкина (IL) -8, фактора некроза опухоли альфа (TNF-α) и уровни выдыхаемого оксида азота (eNO) [De Diego et al. 2005]. Точно так же Канадзава и его коллеги не смогли найти никакой разницы в уровнях eNO и ECP между пациентами с кашлевой астмой и пациентами с классической астмой [Kanazawa et al. 2005]. Однако уровни фактора роста эндотелия сосудов (VEGF), который может играть роль в проницаемости сосудов из-за воспаления, были значительно выше при классической астме. Niimi и его коллеги сообщили, что утолщение субэпителиального слоя при кашлевой астме не было столь выраженным, как при классической астме [Niimi et al. 1998]. Мацумото и его коллеги наблюдали, что у пациентов с кашлевой астмой наблюдалось утолщение стенки центральных дыхательных путей [Matsumoto et al. 2007]. Хотя уровни eNO были повышены при кашлевой астме, они не отличались от уровней eNO, наблюдаемых при классической астме [Fujimura et al. 2008]. Fujimura и его коллеги наблюдали за 41 пациентом с кашлевой астмой, у семи из которых развилась классическая астма [Fujimura et al. 2005a, 2005b, 2005c].AHR и отсутствие использования ICS были наиболее важными предикторами развития классической астмы. Как и при классической астме, ICS при кашлевой астме снижали AHR [Fujimura et al. 2005a, 2005b, 2005c]. Однако не было изменений порога кашля для ингаляционного капсаицина независимо от использования ICS, что свидетельствует о том, что чувствительность кашлевого рефлекса не участвует в механизмах кашлевой астмы.
Неастматический эозинофильный бронхит
Эозинофилы играют важную роль в патофизиологии неастматического эозинофильного бронхита [Brightling et al. 2003, 2002, 2000a, 2000b, Брайтлинг и Паворд, 2000; Гибсон и др. 1998]. При неастматическом эозинофильном бронхите эозинофилия обнаруживается в мокроте, ЖБАЛ и биоптатах бронхов. Кроме того, в мокроте повышается уровень ECP и цистеинил-лейкотриенов [Brightling et al. 2008, 2000a, 2000b]. Более того, уровни эозинофилии БАЛ, гранулоцитарно-колониестимулирующего фактора и экспрессии гена IL-5 были одинаковыми как при неастматическом эозинофильном бронхите, так и при классической астме [Gibson et al. 1998]. Брайтлинг и его коллеги показали одинаковую степень подслизистой эозинофилии и утолщения базальной мембраны и ретикулярной пластинки как при неастматическом эозинофильном бронхите, так и при классической астме [Brightling et al. 2003, 2002]. Однако количество триптазоположительных тучных клеток в пучках гладких мышц дыхательных путей было ниже при неастматическом эозинофильном бронхите по сравнению с классической астмой. Кроме того, при неастматическом эозинофильном бронхите уровни eNO повышаются, что аналогично ситуации, наблюдаемой при классической астме [Brightling et al. 2003, 2002].
Атопический кашель
Атопический кашель характеризуется эозинофильным трахеобронхитом без эозинофилов в ЖБАЛ и гиперчувствительностью кашлевых рецепторов без AHR. При атопическом кашле уровни eNO ниже по сравнению с уровнями, наблюдаемыми при кашлевой астме и классической астме [Fujimura et al. 2008]. В отличие от кашлевой астмы и неастматического эозинофильного бронхита нет данных об изменениях в базальной мембране или распределении воспалительных клеток или процессов у пациентов с атопическим кашлем.Однако, когда Кита и его коллеги изучали эффекты антагониста лейкотриеновых рецепторов монтелейкаста при атопическом кашле и кашлевой астме, авторы заметили, что кашель подавляется только у пациентов с кашлевой астмой [Kita et al. 2010]. Напротив, монтелукаст не влиял на кашель у пациентов с атопическим кашлем, что свидетельствует о различных патофизиологических механизмах этих двух состояний. Другое предположение о различных механизмах, лежащих в основе этих двух состояний, было сделано на основании более низких уровней eNO, наблюдаемых при атопическом кашле по сравнению с уровнями, измеренными при кашлевом варианте астмы [Fujimura et al. 2008].
Обследование пациентов с атипичной астмой
Диагностика пациентов с атипичной астмой может оказаться сложной задачей для клиницистов. Таким образом, оценка этих пациентов и клиническое подозрение на синдромы атипичной астмы остаются важными проблемами. Клинический анамнез может помочь в диагностике атипичной астмы. Однако клиницисты должны будут исключить другие распространенные причины хронического кашля, включая гастроэзофагеальный рефлюкс, ринит или лекарства, такие как ингибиторы ангиотензинпревращающего фермента (АПФ).Может помочь спирометрия, хотя при синдромах атипичной астмы она будет нормальной, как и рентгенограмма грудной клетки. Бронхопровокационные тесты могут быть положительными при классической астме и кашлевой астме; однако они будут нормальными при неастматическом эозинофильном бронхите и атопическом кашле. Индукция мокроты покажет эозинофилию мокроты при всех атипичных состояниях астмы. Напротив, уровни eNO могут различать неастматический эозинофильный бронхит, кашлевую астму и атопический кашель.Fujimura и коллеги показали, что eNO у пациентов с атопическим кашлем были значительно ниже, чем у пациентов с кашлевой астмой и классической астмой [Fujimura et al. 2008]. Тесты на атопию могут помочь пациентам с атопическим кашлем. При кашлевой астме и при неастматическом эозинофильном бронхите атопия менее вероятно. Следовательно, оценка пациентов с синдромами атипичной астмы должна включать в себя анамнез и обследование, спирометрию, рентгенографию грудной клетки, бронхопровокационные тесты, индукцию мокроты и измерения eNO.Однако диагноз синдромов атипичной астмы может быть подтвержден только в том случае, если наблюдается ответ на специфическую терапию.
Лечение атипичной астмы
Наличие непродуктивного кашля и положительный ответ на ИКС характерны для кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля [Irwin et al. 2006; Kastelik et al. 2005; Fujimura et al. 2005a, 2005b, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b].Есть некоторые свидетельства того, что если не лечить кашлевую астму на ранней стадии, она может прогрессировать до классической астмы, и у пациентов могут развиться симптомы одышки и хрипов [Kastelik, 2008; Fujimura et al. 2003]. Напротив, считалось, что атопический кашель реже прогрессирует до классической астмы, особенно при раннем введении лечения с помощью ИКС [Fujimura et al. 2003]. Точно так же Мацумо и его коллеги обнаружили, что лечение ИКС предотвращает прогрессирование от кашлевой астмы до классической астмы [Matsumoto et al. 2006]. Fujimura и его коллеги изучили влияние ICS на изменения AHR и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой [Fujimura et al. 2005a, 2005b]. Как и при классической астме, AHR снижалась с помощью ICS. Однако не было изменений порога кашля у пациентов с кашлевой астмой, независимо от того, принимали они ИКС или нет. У некоторых пациентов с кашлевой астмой кашель улучшается с помощью антагонистов лейкотриеновых рецепторов, особенно если симптомы резистентны к ингаляционным бронходилататорам или ИКС [Dicpinigaitis et al. 2002]. Например, Дикпинигайтис и его коллеги наблюдали, что в ответ на антагонист лейкотриеновых рецепторов, зафирлукаст, как субъективная оценка кашля, так и чувствительность кашлевого рефлекса к вдыхаемому капсаицину улучшались у пациентов с кашлевой астмой, резистентной к ингаляционным бета-агонистам и ИКС [ Kita et al. 2010; Dicpinigaitis et al. 2002]. В очень тяжелых случаях кашлевой астмы, также называемой «астмой, эквивалентной злокачественному кашлю», могут потребоваться пероральные кортикостероиды [Millar et al. 1998]. В случае неастматического эозинофильного бронхита симптомы обычно улучшаются с помощью ИКС [Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. В частности, есть доказательства того, что ИКС у пациентов с неастматическим эозинофильным бронхитом улучшают эозинофилию мокроты, тяжесть кашля и чувствительность [Brightling et al. 2000a, 2000b]. Атопический кашель успешно лечится антагонистами гистамина (H 1 ) и / или глюкокортикоидами, а иногда и противогрибковыми средствами [Fujimura et al. 2005a, 2005b, 2005c, 2003, 2000, 1992; Огава и др. 2004]. Однако было показано, что антагонисты лейкотриеновых рецепторов не влияют на кашель у пациентов с атопическим кашлем [Kita et al. 2010].
Астма, рефрактерная к лечению
TRA остается неприятной проблемой не только для медицинского персонала, ухаживающего за пациентами, но и для самих пациентов. Ряд клинических определений тяжелой астмы был предложен за последнее десятилетие различными группами, включая функцию легких, обострения и использование кортикостероидов [Wenzel et al. 2009, 2000]. Следовательно, астма и, в частности, TRA все чаще признаются разнообразным заболеванием.
Подтверждение TRA
Чтобы установить, что у пациента есть TRA, необходимо подтвердить в истории болезни, что плохое соблюдение режима (включая технику ингаляции и использование спейсера), сопутствующие заболевания, другие состояния и триггеры были исключены [Morjaria и Полоса, 2010]. Это можно сделать, просмотрев старые записи, анализы крови, рентгенологию и лечение в прошлом.Например, для исключения дисфункции голосовых связок может быть проведена бронхоскопия, а при интерстициальном заболевании легких — анализы крови, а также компьютерная томография с высоким разрешением. Если исследования не проводились ранее, было бы разумно провести их, чтобы исключить другую причину симптомов пациента. Кроме того, полезен подробный анамнез их астмы и ее контроль в настоящее время и ранее, а также медицинский осмотр. Список возможных исследований приведен в.
Таблица 2.
Исследования, помогающие отличить тяжелую астму от других состояний.
| Полный анализ крови (включая количество эозинофилов) |
| Уровни общего IgE (включая исследования RAST) |
| Аутоиммунный скрининг (и иногда ABG) |
| Насыщение кислородом |
| Chest X- ray |
| Тестирование функции легких |
| Оценка обратимости сальбутамола (и / или реакции на кортикостероиды) |
| Бронхиальные провокационные тесты (например,грамм. метахолин, маннит или аденозин) |
| FeNO |
| Кожные уколы |
| Индукция мокроты |
| Компьютерная томография грудной клетки с высоким разрешением |
| Компьютерная томография пазух |
| Бронхоскопия |
| Эхокардиография |
| pH-манометрия |
Фенотипирование TRA
Клинические, физиологические и иммунопатологические области TRA часто сосуществуют, но не связаны между собой, следовательно, это означает, что TRA далека от однородности и могут быть далее разделены на разные фенотипы.Было предложено несколько методов фенотипирования этих пациентов с TRA, но истинное значение фенотипирования TRA может быть твердо установлено после того, как будет проведена подробная характеристика ряда пациентов. Эти вопросы в настоящее время изучаются через установленную сеть U-BIOPRED (Объективные биомаркеры для прогнозирования исходов респираторных заболеваний) [U-BIOPRED, 2008].
До недавнего времени фенотипирование основывалось на клинических или патологических признаках. Клинически пациентов с тяжелой астмой можно разделить на три основные категории: частые обострения, перемежающиеся периодами отсутствия симптомов астмы; фиксированная преграда для воздушного потока; и кортикостероид-зависимые астматики [Polosa and Benfatto, 2009].Патологически с точки зрения бронхиальных дыхательных путей (БАЛ мокроты и биопсия) известны две основные категории: стойкие эозинофильные и неозинофильные подтипы [Wenzel et al. 1999]. Однако в последнее время стало также известно о существовании нейтрофилии как отдельного подтипа с эозинофилией или без нее [Hamilton et al. 2003; Jatakanon et al. 1999]. Более того, новые статистические подходы были применены к клинической информации, полученной от пациентов с астмой, и с использованием методов обработки данных были идентифицированы некоторые фенотипы астмы [Haldar et al. 2008]. Это использует метод, называемый кластерным анализом. Кроме того, с помощью этого метода была сконструирована многомерная картина фенотипов астмы, демонстрирующая клинически значимые различия в результатах, со стратегиями ведения, которые используют меру эозинофильного воспаления для титрования кортикостероидной терапии [Haldar et al. 2008].
Вдобавок к астме причастны инфекции (такие как Chlamydia pneumoniae ) и сенсибилизация к Aspergillus fumigatus . C. pneumoniae — облигатный внутриклеточный паразит, который может вызывать острые и хронические заболевания дыхательных путей, особенно астму, но субклиническая инфекция является обычным явлением [Stephens, 2003; Каннингем и др. 1998; Grayston, 1992]. Ряд групп сообщили, что существует значительная корреляция у людей между тяжестью астмы и инфекцией C. pneumoniae и увеличением антител IgG и IgA к C. pneumoniae (IgG и IgA), но обычно не к другим респираторным патогенам [ Стивенс, 2003; Wark et al. 2002; Ten Brinke et al. 2001; Мартин и др. 2001; Черный et al. 2000; Hammerschlag, 2000; Cook et al. 1998]. Однако неясно, являются ли эти ассоциации преимущественно результатом (1) инфекции, фиксирующей ответы Th3 и способствующей последующему развитию воспаления и астмы, или (2) иммунных ответов, которые приводят к воспалению и астме, также предрасполагающим к атипичной бактериальной инфекции. Следовательно, было предложено, чтобы время заражения зависело от воздействия, возраста первого заражения и / или основного иммунного фенотипа человека, предрасположенного к C.pneumoniae вызывает аллергию и астму, а не природа инфекции per se [Von Hertzen, 2002]. Аналогичным образом, недавно сообщалось, что пациенты с тяжелой астмой, сенсибилизированные к A. fumigatus , которые не соответствуют общепринятым диагностическим критериям аллергического бронхолегочного аспергиллеза, не только имеют радиологические радиологические аномалии на компьютерной томографии высокого разрешения, такие как бронхоэктазы, бронхиальная болезнь. утолщение стенок и расширение бронхов, а также ограничение воздушного потока из-за захвата воздуха [Menzies et al. 2011]. Эти наблюдения предполагают патофизиологические фенотипы TRA.
Следует отметить, что идентифицированные фенотипы не обязательно являются фиксированными и могут изменяться со временем и в зависимости от назначенного лечения [Haldar et al. 2008]. Используя эту фенотипическую информацию (и, возможно, более точные определения различных подтипов в будущем), необходимо определить механизмы, которые имеют решающее значение во взаимодействии между различными фенотипами астмы, и распутать лежащую в основе патобиологию, чтобы не только разработать биомаркеры. болезней, но и для разработки новых методов лечения, адаптированных к потребностям наших пациентов.
Управление TRA
У большинства пациентов астма не контролируется в соответствии с рекомендациями. Это было продемонстрировано в исследовании Gaining Optimal Asthma Control (GOAL): несмотря на оптимизацию, комбинированный ингалятор салметерол / флутиказон позволил только 62% пациентов достичь полного контроля над симптомами астмы [Bateman et al. 2004]. Более того, после курса OCS этот показатель улучшился до 69%. У остальных пациентов по-прежнему наблюдались неконтролируемые симптомы астмы.
Оптимальное лечение должно быть направлено на достижение наилучшего связанного с астмой качества жизни (QoL) и контроль с помощью самых низких доз лекарств, особенно кортикостероидов. При выборе и формулировании используемых терапевтических агентов следует принимать во внимание не только тяжесть и фенотип заболевания, сопутствующие заболевания и предпочтения пациента, терапевтические реакции, но и сообщения о нежелательных явлениях. Следовательно, в дополнение к стандартной терапии ICS и LABA, другие агенты, такие как антилейкотриеновые агенты (для аспирино-чувствительной астмы [Tonelli et al. 2003] и астмы, вызванной физической нагрузкой [Leff et al. 1998]), теофиллины [Vatrella et al. 2005; Робертс и др. 2003], холинолитики [Peters et al. 2011] и внутривенное (IV) введение магния [Beasley and Aldington, 2007; Silverman et al. 2002] подлежит испытанию.
Пероральные кортикостероиды (OCS) использовались при хронических заболеваниях, но были исследования с использованием иммуномодуляторов для ограничения необходимости длительного использования OCS и, таким образом, побочного действия кортикостероидов.Был изучен ряд таких иммуномодулирующих препаратов с некоторой эффективностью и безопасностью, включая метотрексат, циклоспорин А, макролидные антибиотики, азатиоприн, золото и иммуноглобулины для внутривенного введения [Polosa and Morjaria, 2008]. Примечательно, что метотрексат, циклоспорин А и макролидные антибиотики обычно оцениваются как кортикостероидсберегающие препараты.
Совсем недавно биологические агенты были исследованы на предмет использования в качестве средств, сберегающих кортикостероиды. Единственный лицензированный биологический агент — омализумаб.Другие агенты были изучены с ограниченной эффективностью и безопасностью или все еще находятся на предварительных стадиях оценки. Мы обсудим эти агенты дальше (и они кратко описаны в).
Таблица 3.
Резюме обсужденных исследований.
| Агент | Доказательства эффективности | Улучшения параметров |
|---|---|---|
| Анти-IgE: омализумаб (SC / IV) | Milgrom et al. [1999] (DBPC) | Улучшение утреннего PEF, качества жизни при астме; уменьшение обострений астмы и употребление снотворных |
| Busse et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Soler et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Milgrom et al. [2001] (DBPC) | Уменьшение обострений астмы и употребление снотворных | |
| Holgate et al. [2004] (DBPC) | Сокращение использования вспомогательных средств; улучшение оценки симптомов и качества жизни астмы | |
| Humbert et al. [2005] (DBPC) | Уменьшение числа обострений астмы и количества обращений в отделение неотложной помощи; улучшение качества жизни при астме, утреннего PEF, оценки симптомов астмы | |
| Анти-TNF-α: этанерцепт (SC), голимумаб (SC) | Howarth et al. [2005] (открытое исследование) | Улучшение ОФВ 1 , FVC, PEF, AHR и контроль астмы; добровольное прекращение использования небулайзерного облегчения |
| Berry et al. [2006] (CS) | Улучшение FEV 1 , FVC, PEF, AHR и качества жизни астмы | |
| Morjaria et al. [2008] (DBPC) | Улучшение контроля астмы; добровольное прекращение использования небулайзерного облегчения | |
| Wenzel et al. [2009] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам (исследование прекращено досрочно из-за СНЯ) | |
| Анти-ИЛ-5: меполизумаб (IV) | Haldar et al. [2009] (DBPC) | Уменьшение обострений астмы; улучшение качества жизни при астме |
| Nair et al. [2009] (DBPC) | Уменьшение обострений астмы и снижение дозы OCS без обострений; улучшение ОФВ 1 и контроль астмы | |
| Анти-IL-4 рецептор (IL-4Rα): AMG 317 | Corren et al. [2010] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам не было. |
| Анти-CD25: даклизумаб (IV) | Busse et al. [2008] (DBPC) | Улучшение ОФВ 1 , дневных симптомов астмы и использования восстановительных средств; увеличивается во время обострений |
| Anti-SCF / c-kit и рецептор PDGF: маситиниб (PO) | Humbert et al. [2009] (DBPC) | Улучшение контроля астмы |
Омализумаб.
IgE играет ключевую роль в развитии аллергических состояний [Corry and Kheradmand, 1999]. Аллерген-специфический IgE связывается с эффекторными клетками через рецепторы с высоким сродством (FceRI) и низким сродством (FceRII), вызывая их эффекты, такие как индукция дегрануляции тучных клеток и базофилов, вызывая результирующие реакции на ранней и поздней фазах [Gould и Саттон, 2008 г .; Morjaria et al. 2007]. Омализумаб представляет собой рекомбинантное гуманизированное IgE-специфическое моноклональное антитело, которое прерывает взаимодействие между IgE и FceRI на эффекторных клетках [Presta et al. 1994]. Ранние фармакодинамические исследования омализумаба показали, что он снижает воспаление, AHR, аллерген-индуцированные дыхательные пути и кожные пробы [Boulet et al. 1997; Fahy et al. 1997].
Было проведено шесть крупных двойных слепых плацебо-контролируемых (DBPC) исследований III фазы с применением омализумаба подкожно в дозе 0.016 мг / кг / IgE (МЕ / мл) каждые 2 или 4 недели для оценки его безопасности и эффективности при тяжелой атопической астме с симптомами, несмотря на оптимальную терапию [Humbert et al. 2005; Holgate et al. 2004; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. Продолжительность исследований составляла от 25 до 52 недель с участием субъектов с уровнем IgE от 30 до 700 МЕ / мл). В совокупности анализ различных исследований, а также коллективные оценки показали, что добавление омализумаба привело к улучшению субъективных параметров контроля астмы и качества жизни, а также к объективным улучшениям функции легких, а также к сокращению использования вспомогательных средств, использования кортикостероидов, количества обращений в отделение неотложной помощи. и количество обострений астмы [Bousquet et al. 2005, 2004; Chipps et al. 2005; Humbert et al. 2005; Holgate et al. 2004; Finn et al. 2003; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. В период исследования омализумаб был безопасен без значительных побочных эффектов по сравнению с плацебо. Однако в постмаркетинговых отчетах сообщается о незначительном увеличении количества анафилактических и анафилактоидных реакций, злокачественных новообразований и гельминтозов [Cruz et al. 2007; НИЦЦА, 2007; Vignola et al. 2004].
Следует отметить, что пациенты, принимающие омализумаб, проходят 16-недельную оценку эффективности и безопасности, чтобы убедиться, что они получают пользу от терапии анти-IgE. Отчасти это связано со стоимостью препарата. Хотя омализумаб является безопасным и эффективным лекарством, важно помнить, что лишь небольшая часть тяжелых астматиков страдает атопией, и даже из них только две трети получат от него пользу; большинство TRAS не являются атопическими и не подходят для лечения анти-IgE.
Антагонизм фактора некроза опухоли альфа.
TNF-α представляет собой многофункциональный провоспалительный цитокин Th2, который, как предполагается, играет важную роль в инициировании, поддержании и прогрессировании воспаления дыхательных путей при астме [Morjaria et al. 2006]. Сообщается, что уровни TNF-α в дыхательных путях повышаются при тяжелом заболевании. Неспособность кортикостероидов снижать уровень TNF-α и цитокинов, производных Th2, в дыхательных путях астматиков может объяснить, почему кортикостероиды имеют ограниченную эффективность при TRA.Следовательно, было постулировано, что противодействие TNF-α и, следовательно, вмешательство в цитокины, производные Th2, может представлять собой прогресс в лечении TRA.
На основе этой предпосылки два небольших исследования (одно доказательство концепции [Howarth et al. 2005], а другое — перекрестное исследование с плацебо-контролем [Berry et al. 2006]) антагонизма TNF-α с использованием растворимого рецептора этанерцепта. Они сообщили о значительном улучшении качества жизни, связанного с астмой (AQLQ), и контроля астмы, а также спирометрии, PEF и AHR.Однако в более крупном исследовании DBPC с использованием того же растворимого рецептора не сообщалось о таких драматических эффектах, с лишь незначительным улучшением контроля астмы [Morjaria et al. 2008]. Подобно этому исследованию, еще более крупное исследование DBPC с использованием моноклонального антитела к TNF-α, голимумаба, не продемонстрировало улучшения каких-либо измеренных параметров, но на самом деле исследование было прекращено досрочно из-за опасений по поводу безопасности [Wenzel et al. 2009]. Увеличилось не только количество солидных злокачественных новообразований, но и серьезных инфекций, таких как пневмония, сепсис и реактивация туберкулеза.Однако следует отметить, что в двух более крупных исследованиях [Wenzel et al. 2009; Morjaria et al. 2008] упомянули, что у включенных в исследование пациентов было более легкое заболевание по сравнению с пациентами меньших исследований [Berry et al. 2006; Howarth et al. 2005]. Следовательно, даже если можно выделить подгруппы, в которых анти-TNF-α могут быть эффективными, необходимо принять во внимание эти связанные с лечением тяжелые побочные эффекты. В настоящее время нет известных нам исследований, использующих стратегии против TNF-α.
Анти-ИЛ-5: меполизумаб.
Эозинофилия в дыхательных путях и их дегрануляция являются признаком астмы и связаны с цитокинами Th3, а именно с ИЛ-4, ИЛ-5, ИЛ-9, ИЛ-13 и гранулоцитарно-макрофагальным колониестимулирующим фактором [Rothenberg и Хоган, 2006; Simon et al. 2004; Мензис-Гоу и Робинсон, 2002; Сандерсон, 1992]; все они выражены в повышенных количествах при тяжелой астме [Desai and Brightling, 2009]. IL-5 — важный цитокин, специфичный для эозинофилов.На основе этого принципа антагонизация IL-5 с использованием моноклонального антитела, меполизумаба, проводилась у пациентов с легким или умеренным заболеванием без заметных клинических улучшений [Flood-Page et al. 2007, 2003a, 2003b; Buttner et al. 2003; Menzies-Gow et al. 2003; Leckie et al. 2000].
Совсем недавно были проведены два исследования DBPC с участием пациентов, которые имели стойкую эозинофилию, несмотря на терапию кортикостероидами с использованием меполизумаба с хорошей эффективностью и безопасностью [Haldar et al. 2009; Наир и др. 2009]. Они сообщили о значительном сокращении обострений астмы [Haldar et al. 2009; Наир и др. 2009] и снижение дозы ОКС без обострений [Nair et al. 2009], а также значительное улучшение объема форсированного выдоха за одну секунду (FEV 1 ) [Nair et al. 2009], контроль астмы [Nair et al. 2009], AQLQ [Haldar et al. 2009] и резкое снижение эозинофилии мокроты и крови [Haldar et al. 2009; Наир и др. 2009]. В обоих исследованиях не было отмечено серьезных нежелательных явлений. В настоящее время проводятся более крупные исследования для подтверждения результатов этих двух исследований в этой небольшой подгруппе TRA.
Антагонизм рецептора IL-4 альфа (IL-4Rα).
Как упоминалось выше (в разделе об анти-IL-5), IL-4 и IL-13 также являются цитокинами Th3, которые играют роль в патогенезе астмы, и, следовательно, нацеливание на эти цитокины может быть эффективным при тяжелом заболевании [ Webb et al. 2000; Grunig et al. 1998; Wills-Karp et al. 1998]. Следует отметить, что IL-4Ra используется обоими этими цитокинами для проявления своей активности [Rolling et al. 1996]. Имея это в виду, было проведено большое исследование DBPC у умеренных и тяжелых астматиков для оценки безопасности и эффективности полностью гуманизированных моноклональных антител к IL-4Rα, AMG 317 [Corren et al. 2010]. Было отмечено, что не было улучшений ни по одному из параметров, оцениваемых в исследовании.Однако апостериорный анализ показал, что AMG 317 может иметь значение у пациентов с наибольшим количеством симптомов. При использовании AMG 317 не было серьезных проблем с побочными эффектами.
Анти-CD25: даклизумаб.
Т-клетки играют роль в воспалении дыхательных путей при астме, при этом повышенные уровни CD25 Т-клеток и цитокина IL-2 отмечаются при более тяжелых формах заболевания [Kon and Kay, 1999; Park et al. 1994; Робинсон и др. 1993; Azzawi et al. 1992].Используя этот принцип, Буссе и его коллеги провели исследование для оценки безопасности и эффективности гуманизированного моноклонального антитела к альфа-субъединице (CD25) высокоаффинного рецептора IL-2, тем самым препятствуя связыванию IL-2 [Busse et al. . 2008]. В этом исследовании DBPC у умеренно-тяжелых астматиков сообщалось о минимальном значительном улучшении ОФВ 1 , дневных симптомов астмы, увеличения времени до обострения астмы и сокращения использования вспомогательных средств в пользу даклизумаба.Хотя в группе даклизумаба было больше побочных эффектов, они не были значительными. Место даклизумаба в TRA требует дальнейшей оценки в более крупных исследованиях.
Ингибитор тирозинкиназы рецептора фактора стволовых клеток (c-kit) / рецептора тромбоцитарного фактора роста: маситиниб.
Тучные клетки и дендритные клетки являются клетками, участвующими в TRA [Krishnamoorthy et al. 2008; Chanez et al. 2007; Холгейт и Полоса, 2006; Ребер и др. 2006].Они могут быть активированы с помощью рецептора c-kit фактора стволовых клеток (SCF), что приводит к накоплению тучных клеток, AHR и повышению уровня гистамина, эозинофильной инфильтрации, а также продукции IL-4. Более того, фактор роста тромбоцитов (PDGF), фактор роста, участвует в ремоделировании дыхательных путей [Chung et al. 2006; Инграм и Боннер, 2006]. Следовательно, противодействие рецепторам SCF / c-kit и PDGF может быть потенциальной терапевтической мишенью. Имея это в виду, маситиниб, ингибитор тирозинкиназы, который специфически противодействует рецепторам c-kit и PDGF, был использован для оценки его эффективности и безопасности у субъектов с тяжелой персистирующей астмой, несмотря на высокие дозы ICS, а также OCS [Humbert et al. 2009]. В этом исследовании DBPC Humbert и его коллеги рандомизировали 44 пациента для приема маситиниба перорально в трех дозах: 3 ( n = 12), 4,5 ( n = 11) или 6 ( n = 10) мг / кг / день. или плацебо ( n = 11), т.е. 3: 1, в течение 16 недель. Ни первичная конечная точка отлучения от OCS, ни какие-либо параметры функции дыхательных путей не показали существенной разницы между различными дозами маситиниба и / или плацебо. В обеих группах было 14 выбывших, которые были одинаковыми в обеих группах из-за нежелательных явлений или отсутствия терапевтической эффективности.Следует отметить, что единственным показателем значительного улучшения был показатель ACQ в группе маситиниба по сравнению с группой плацебо. Исследователи сообщили о том, что пациенты, принимавшие высокие дозы OCS и получавшие маситиниб ( n = 6), могли быть отлучены от дозы OCS по сравнению с отсутствием в группе плацебо. Также сообщалось, что пациенты, принимавшие маситиниб, имели больше незначительных, а также серьезных побочных эффектов по сравнению с пациентами, принимавшими плацебо. Это исследование фазы IIa показывает, что маситиниб может играть незначительную роль в TRA, если таковая имеется, поскольку были отмечены только субъективные улучшения.
Заключение
Астма остается очень важным условием с точки зрения бремени экономики здравоохранения, заболеваемости, влияния на качество жизни пациентов и вариантов лечения. Ведение пациентов с TRA — огромная проблема для клиницистов. Появление потенциальных новых иммуномодулирующих агентов может предоставить новые терапевтические возможности для TRA в будущем. Напротив, варианты лечения легкой и умеренной астмы хорошо известны. Однако в этой популяции астматиков есть подгруппа пациентов, которые могут проявлять атипичность.Таким образом, осведомленность клиницистов о возможных различных фенотипических подгруппах астмы очень важна. Если эти синдромы атипичной астмы диагностируются на ранней стадии, их лечение относительно просто, и контроль симптомов может быть достигнут у значительной части пациентов.
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Авторы заявляют об отсутствии конфликта интересов при подготовке данной рукописи.
Ссылки
- Antoncelli L., Bucca C., Neri M., De Benedetto F., Saabbatani P.B.F. (2004) Степень тяжести астмы и использование медицинских ресурсов. Eur Respir J 23: 723–729 [PubMed] [Google Scholar]
- Asthma UK (2010) Веб-сайт Asthma UK, http://www.asthma.org.uk (по состоянию на октябрь 2010 г.).
- Аззави М., Джонстон П.В., Маджумдар С., Кей А.Б., Джеффри П.К. (1992) Т-лимфоциты и активированные эозинофилы в слизистой оболочке дыхательных путей при фатальной астме и муковисцидозе. Am Rev Respir Dis 145: 1477–1482 [PubMed] [Google Scholar]
- Бейтман Э.D., Boushey H.A., Bousquet J., Busse W.W., Clark T.J., Pauwels R.A. и др. (2004) Можно ли достичь контроля астмы в соответствии с рекомендациями? Исследование достижения оптимального контроля над астмой. Am J Respir Crit Care Med 170: 836–844 [PubMed] [Google Scholar]
- Бизли Р., Алдингтон С. (2007) Магний в лечении астмы. Curr Opin Allergy Clin Immunol 7: 107–110 [PubMed] [Google Scholar]
- Берри М.А., Харгадон Б., Шелли М., Паркер Д., Шоу Д.Э., Грин Р.Х. и др. (2006) Доказательства роли фактора некроза опухоли альфа при рефрактерной астме.N Engl J Med 354: 697–708 [PubMed] [Google Scholar]
- Black P.N., Scicchitano R., Jenkins C.R., Blasi F., Allegra L., Wlodarczyk J. и др. (2000) Серологические доказательства инфекции Chlamydia pneumoniae связаны с тяжестью астмы. Eur Respir J 15: 254–259 [PubMed] [Google Scholar]
- Boulet L.P., Chapman K.R., Cote J., Kalra S., Bhagat R., Swystun V.A. и др. (1997) Ингибирующее действие анти-IgE-антитела Е25 на индуцированный аллергеном ранний астматический ответ.Am J Respir Crit Care Med 155: 1835–1840 [PubMed] [Google Scholar]
- Bousquet J., Cabrera P., Berkman N., Buhl R., Holgate S., Wenzel S., et al. (2005) Влияние лечения омализумабом, анти-IgE-антителом, на обострения астмы и посещение неотложной медицинской помощи у пациентов с тяжелой персистирующей астмой. Аллергия 60: 302–308 [PubMed] [Google Scholar]
- Bousquet J., Wenzel S., Holgate S., Lumry W., Freeman P., Fox H. (2004) Прогнозирование ответа на омализумаб, антитело против IgE , у пациентов с аллергической астмой.Грудь 125: 1378–1386 [PubMed] [Google Scholar]
- Браман С.С. (2006) Глобальное бремя астмы. Грудь 130: 4S – 12S [PubMed] [Google Scholar]
- Браман С.С., Коррао В.М. (1985) Хронический кашель. Диагностика и лечение. Prim Care 12: 217–225 [PubMed] [Google Scholar]
- Brightling C.E. (2006) Хронический кашель, вызванный неастматическим эозинофильным бронхитом. Руководство по клинической практике, основанное на доказательствах ACCP. Грудь 129: 116–121 с [PubMed] [Google Scholar]
- Брайтлинг К.Э., Брэддинг П., Саймон Ф.А., Холгейт С.Т., Уордлоу А.Дж., Паворд И.Д. (2002) Инфильтрация тучными клетками гладкой мускулатуры дыхательных путей при астме. N Engl J Med 346: 1699–1705 [PubMed] [Google Scholar]
- Brightling C.E., Pavord I.D. (2000) Эозинофильный бронхит — что это такое и почему это важно ?. Clin Exp Allergy 30: 4–6 [PubMed] [Google Scholar]
- Brightling C.E., Symon F.A., Birring S.S., Bradding P., Wardlaw A.J., Pavord I.D. (2003) Сравнение иммунопатологии дыхательных путей эозинофильного бронхита и астмы.Грудная клетка 58: 528–532 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Го К.Л., Уордлоу А.Дж., Паворд И.Д. (1999a) Эозинофильный бронхит — важная причина хронического кашля. Am J Respir Crit Care Med 160: 406–410 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Уордлоу А.Дж., Паворд И.Д. (2000a) Воспаление дыхательных путей, чувствительность дыхательных путей и кашель до и после ингаляции будесонида у пациентов с эозинофильным бронхитом. Eur Respir J 15: 682–686 [PubMed] [Google Scholar]
- Брайтлинг К.E., Ward R., Woltmann G., Bradding P., Sheller J.R., Dworski R. и др. (2000b) Индуцированные концентрации медиатора воспаления в мокроте при эозинофильном бронхите и астме. Am J Respir Crit Care Med 162: 878–882 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Вольтманн Г., Вардлоу А.Дж., Паворд И.Д. (1999b) Развитие необратимой обструкции воздушного потока у пациента с эозинофильным бронхитом без астмы. Eur Respir J 14: 1228–1230 [PubMed] [Google Scholar]
- BTS / SIGN. (2008) BTS / Sign (Британское торакальное общество / Шотландская межвузовская сеть).Британское руководство по лечению астмы: Национальное клиническое руководство. Грудная клетка 63 (Дополнение IV): iv1 – iv121 [PubMed] [Google Scholar]
- Busse W., Corren J., Lanier B.Q., Mcalary M., Fowler-Taylor A., Cioppa G.D., et al. (2001) Омализумаб, рекомбинантное гуманизированное моноклональное антитело против IgE, для лечения тяжелой аллергической астмы. J Allergy Clin Immunol 108: 184–190 [PubMed] [Google Scholar]
- Busse W.W., Israel E., Nelson H.S., Baker J.W., Charous B.L., Young D.Y. и др.(2008) Даклизумаб улучшает контроль астмы у пациентов со средней и тяжелой персистирующей астмой: рандомизированное контролируемое исследование. Am J Respir Crit Care Med 178: 1002–1008 [PubMed] [Google Scholar]
- Buttner C., Lun A., Splettstoesser T., Kunkel G., Renz H. (2003) Лечение моноклональным анти-интерлейкином-5 подавляет эозинофилы, но не Т-клетки функции. Eur Respir J 21: 799–803 [PubMed] [Google Scholar]
- Карни И.К., Гибсон П.Г., Мюрри-Аллен К., Салтос Н., Олсон Л.Г., Хенсли М.J. (1997) Систематическая оценка механизмов хронического кашля. Am J Respir Crit Care Med 156: 211–216 [PubMed] [Google Scholar]
- Chanez P., Wenzel S.E., Anderson G.P., Anto J.M., Bel E.H., Boulet L.P., et al. (2007) Тяжелая форма астмы у взрослых: каковы важные вопросы ?. J Allergy Clin Immunol 119: 1337–1348 [PubMed] [Google Scholar]
- Чиппс Б., Коррен Дж., Финн А., Хеджекок С., Фокс Х., Блог М. (2005) Омализумаб значительно улучшает качество жизни пациентов с тяжелыми формами стойкая астма.J Allergy Clin Immunol 115: S5 – S19 [Google Scholar]
- Chung K.F., Hew M., Score J., Jones A.V., Reiter A., Cross N.C., et al. (2006) Кашель и гиперэозинофилия из-за слитого гена FIP1L1-PDGFRA с тирозинкиназной активностью. Eur Respir J 27: 230–232 [PubMed] [Google Scholar]
- Чунг К.Ф., Паворд И.Д. (2008) Распространенность, патогенез и причины хронического кашля. Ланцет 371: 1364–1374 [PubMed] [Google Scholar]
- Cook P.J., Davies P., Tunnicliffe W., Ayres J.G., Honeybourne D., Wise R. (1998) Chlamydia pneumoniae и астма. Грудная клетка 53: 254–259 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Corrao W.M., Braman S.S., Irwin R.S. (1979) Хронический кашель как единственное проявление бронхиальной астмы. N Engl J Med 300: 633–637 [PubMed] [Google Scholar]
- Corren J., Busse W., Meltzer E.O., Mansfield L., Bensch G., Fahrenholz J. и др. (2010) Рандомизированное контролируемое исследование фазы 2 AMG 317, антагониста IL-4Ralpha, у пациентов с астмой.Am J Respir Crit Care Med 181: 788–796 [PubMed] [Google Scholar]
- Корри Д. Б., Херадманд Ф. (1999) Индукция и регуляция ответа IgE. Природа 402: B18 – B23 [PubMed] [Google Scholar]
- Cruz A.A., Lima F., Sarinho E., Ayre G., Martin C., Fox H., et al. (2007) Безопасность антииммуноглобулиновой терапии омализумабом у пациентов с аллергией, подверженных риску геогельминтной инфекции. Clin Exp Allergy 37: 197–207 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Каннингем А.Ф., Джонстон С.Л., Джулиус С.А., Лампе Ф.С., Уорд М.Е. (1998) Хроническая инфекция Chlamydia pneumoniae и обострения астмы у детей. Eur Respir J 11: 345–349 [PubMed] [Google Scholar]
- Де Диего А., Мартинес Э., Перпина М., Ньето Л., Компте Л., Мачиан В. и др. (2005) Воспаление дыхательных путей и чувствительность к кашлю при кашлевой астме. Аллергия 60: 1407–1411 [PubMed] [Google Scholar]
- Desai D., Brightling C. (2009) Цитокиновая и антицитокиновая терапия при астме: готовы к клинике ?.Клин Эксп Иммунол 158: 10–19 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Dicpinigaitis P.V. (2006) Хронический кашель из-за астмы: клинические рекомендации ACCP, основанные на фактических данных. Грудь 129: 75S – 79S [PubMed] [Google Scholar]
- Dicpinigaitis P.V., Добкин J.B., Reichel J. (2002) Противокашлевое действие антагониста лейкотриеновых рецепторов зафирлукаста у субъектов с кашлевой астмой. J астма 39: 291–297 [PubMed] [Google Scholar]
- Европейская сеть по изучению механизмов тяжелой астмы.(2003) Поперечное европейское многоцентровое исследование клинического фенотипа тяжелой хронической астмы Enfumosa. Eur Respir J 22: 470–477 [PubMed] [Google Scholar]
- Fahy J.V., Fleming H.E., Wong H.H., Liu J.T., Su J.Q., Reimann J., et al. (1997) Влияние моноклонального антитела против IgE на раннюю и позднюю фазу ответа на вдыхание аллергена у пациентов с астмой. Am J Respir Crit Care Med 155: 1828–1834 [PubMed] [Google Scholar]
- Финн А., Гросс Г., Ван Бавель Дж., Ли Т., Виндом Х., Эверхард Ф. и др. (2003) Омализумаб улучшает качество жизни, связанное с астмой, у пациентов с тяжелой аллергической астмой. J Allergy Clin Immunol 111: 278–284 [PubMed] [Google Scholar]
- Флад-Пейдж П., Мензис-Гоу А., Фиппс С., Ин С., Вангу А., Людвиг М.С. и др. (2003a) Лечение анти-IL-5 снижает отложение белков ЕСМ в субэпителиальной базальной мембране бронхов у больных с легкой атопической астмой. J Clin Invest 112: 1029–1036 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Flood-Page P., Свенсон К., Файферман И., Мэтьюз Дж., Уильямс М., Бранник Л. и др. (2007) Исследование по оценке безопасности и эффективности меполизумаба у пациентов с умеренной персистирующей астмой. Am J Respir Crit Care Med 176. Am J Respir Crit Care Med 167: 199–204 [PubMed] [Google Scholar]
- Fujimura M., Або М., Огава Х., Ниси К., Кибе Ю., Хиросе Т. и др. (2005a) Важность атопического кашля, кашлевой астмы и синобронхиального синдрома как причин хронического кашля в районе Хокурику в Японии. Респирология 10: 201–207 [PubMed] [Google Scholar]
- Fujimura M., Hara J., Myou S. (2005b) Изменение бронхиальной реактивности и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой: эффект ингаляционных кортикостероидов. Кашель 1: 5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Nishizawa Y., Nishitsuji M., Nomura S., Abo M., Ogawa H. (2005c) Предикторы типичного начала астмы при кашлевом варианте астмы. J астма 42: 107–111 [PubMed] [Google Scholar]
- Fujimura M., Ogawa H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности. Грудная клетка 58: 737 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Nishizawa Y., Nishi K. (2003) Сравнение атопического кашля с кашлевым вариантом астмы: является ли атопический кашель предшественником астма ?.Грудная клетка 58: 14–18 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Yasui M., Matsuda T. (2000) Эозинофильный трахеобронхит и гиперчувствительность дыхательных путей при хроническом непродуктивном кашле. Clin Exp Allergy 30: 41–47 [PubMed] [Google Scholar]
- Fujimura M., Ohkura N., Abo M., Furusho S., Waseda Y., Ichikawa Y., et al. (2008) Уровни оксида азота в выдыхаемом воздухе у пациентов с атопическим кашлем и кашлевой астмой. Респирология 13: 359–364 [PubMed] [Google Scholar]
- Fujimura M., Сакамото С., Мацуда Т. (1992) Бронходилататорно-резистивный кашель у пациентов с атопией: бронхиальная обратимость и гиперреактивность. Intern Med 31: 447–452 [PubMed] [Google Scholar]
- Fujimura M., Songur N., Kamio Y., Matsuda T. (1997) Обнаружение эозинофилов в мокроте, индуцированной гипертоническим солевым раствором, у пациентов с хроническим непродуктивным кашлем. J астма 34: 119–126 [PubMed] [Google Scholar]
- Гибсон П.Г., Долович Дж., Денбург Дж., Рамсдейл Э. Х., Харгрив Ф. Э. (1989) Хронический кашель: эозинофильный бронхит без астмы.Ланцет 1: 1346–1348 [PubMed] [Google Scholar]
- Гибсон П.Г., Фудзимура М., Ниими А. (2002) Эозинофильный бронхит: клинические проявления и последствия для лечения. Грудная клетка 57: 178–182 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Gibson PG, Zlatic K., Scott J., Sewell W., Woolley K., Saltos N. (1998) Хронический кашель напоминает астму с ИЛ -5 и экспрессия гена колониестимулирующего фактора гранулоцитов-макрофагов в бронхоальвеолярных клетках. J Allergy Clin Immunol 101: 320–326 [PubMed] [Google Scholar]
- Гулд Х.J., Sutton B.J. (2008) IgE при аллергии и астме сегодня. Нат Рев Иммунол 8: 205–217 [PubMed] [Google Scholar]
- Grayston J.T. (1992) Инфекции, вызванные штаммом Chlamydia pneumoniae twar. Clin Infect Dis 15: 757–761 [PubMed] [Google Scholar]
- Grunig G., Warnock M., Wakil A.E., Venkayya R., Brombacher F., Rennick D.M. и др. (1998) Потребность в IL-13 независимо от IL-4 при экспериментальной астме. Наука 282: 2261–2263 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Брайтлинг С.Е., Харгадон Б., Гупта С., Монтейро В., Соуза А. и др. (2009) Меполизумаб и обострения рефрактерной эозинофильной астмы. N Engl J Med 360: 973–984 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Pavord I.D., Shaw D.E., Berry M.A., Thomas M., Brightling C.E., et al. (2008) Кластерный анализ и клинические фенотипы астмы. Am J Respir Crit Care Med 178: 218–224 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hamilton L.M., Torres-Lozano C., Puddicombe S.М., Рихтер А., Кимбер И., Дирман Р. Дж. И др. (2003) Роль рецептора эпидермального фактора роста в поддержании нейтрофильного воспаления при тяжелой астме. Clin Exp Allergy 33: 233–240 [PubMed] [Google Scholar]
- Hammerschlag M.R. (2000) Chlamydia pneumoniae и легкие. Eur Respir J 16: 1001–1007 [PubMed] [Google Scholar]
- Хоффштейн В. (1994) Постоянный кашель у некурящих. Может Респир J 1: 40–47 [Google Scholar]
- Холгейт С.Т., Чучалин А.Г., Хеберт Дж., Лотвалл Дж., Перссон Г. Б., Чунг К. Ф. и др. (2004) Эффективность и безопасность рекомбинантного антитела против иммуноглобулина Е (омализумаб) при тяжелой аллергической астме. Clin Exp Allergy 34: 632–638 [PubMed] [Google Scholar]
- Холгейт С.Т., Полоса Р. (2006) Механизмы, диагностика и лечение тяжелой астмы у взрослых. Ланцет 368: 780–793 [PubMed] [Google Scholar]
- Ховарт П.Х., Бабу К.С., Аршад Х.С., Лау Л.С., Бакли М.Г., Макконнелл В. и др. (2005) Фактор некроза опухоли (TNF {альфа) как новая терапевтическая мишень при симптоматической кортикостероидной астме.Грудная клетка 60: 1012–1018, Epub, 15 сентября 2005 г. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Humbert M., Beasley R., Ayres J., Slavin R., Hebert J., Bousquet J., et al. (2005) Преимущества омализумаба в качестве дополнительной терапии у пациентов с тяжелой персистирующей астмой, которые недостаточно контролируются, несмотря на лучшую доступную терапию (лечение GINA 2002, шаг 4): Innovate. Аллергия 60: 309–316 [PubMed] [Google Scholar]
- Humbert M., De Blay F., Garcia G., Prud’homme A., Leroyer C., Magnan A., и другие. (2009) Маситиниб, ингибитор тирозинкиназы рецептора c-kit / PDGF, улучшает контроль заболевания у тяжелых кортикостероидозависимых астматиков. Аллергия 64: 1194–1201 [PubMed] [Google Scholar]
- Инграм Дж. Л., Боннер Дж. С. (2006) Тирозинкиназы рецепторов EGF и PDGF как терапевтические мишени при хронических заболеваниях легких. Курр Мол Мед 6: 409–421 [PubMed] [Google Scholar]
- Ирвин Р.С., Бауманн М.Х., Болсер Д.К., Буле Л.П., Браман С.С., Брайтлинг С.Э. и др. (2006) Диагностика и лечение кашля. Краткое изложение: клинические рекомендации ACCP, основанные на фактических данных.Грудь 129: 1S – 23S [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Ирвин Р.С., Коррао В.М., Праттер М.Р. (1981) Хронический стойкий кашель у взрослых: спектр и частота причин и успешный результат специфической терапии. Am Rev Respir Dis 123: 413–417 [PubMed] [Google Scholar]
- Ирвин Р.С., Керли Ф.Дж., French C.L. (1990) Хронический кашель. Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Am Rev Respir Dis 141: 640–647 [PubMed] [Google Scholar]
- Ирвин Р.S., French C.T., Smyrnios N.A., Curley F.J. (1997) Интерпретация положительных результатов ингаляционной пробы метахолина и 1 недели использования ингаляционных бронходилататоров при диагностике и лечении кашлевой астмы. Arch Intern Med 157: 1981–1987 [PubMed] [Google Scholar]
- Jatakanon A., Uasuf C., Maziak W., Lim S., Chung K.F., Barnes P.J. (1999) Нейтрофильное воспаление при тяжелой персистирующей астме. Am J Respir Crit Care Med 160: 1532–1539 [PubMed] [Google Scholar]
- Джонсон Д., Осборн Л.М. (1991) Кашлевой вариант астмы: обзор клинической литературы. J астма 28: 85–90 [PubMed] [Google Scholar]
- Kanazawa H., Eguchi Y., Nomura N., Yoshikawa J. (2005) Анализ уровней фактора роста эндотелия сосудов в индуцированных образцах мокроты пациентов с кашлевой астмой. Энн Аллергия Астма Иммунол 95: 266–271 [PubMed] [Google Scholar]
- Kastelik J.A. (2008) Терапия кашлевой астмы. Многопрофильная респираторная медицина 3: 223–227 [Google Scholar]
- Kastelik J.А., Азиз И., Оху Дж. К., Томпсон Р. Х., Редингтон А. Э., Морис А. Х. (2005) Исследование и лечение хронического кашля с использованием вероятностного алгоритма. Eur Respir J 25: 235–243 [PubMed] [Google Scholar]
- Кита Т., Фудзимура М., Огава Х., Накацуми Ю., Номура С., Ишиура Ю. и др. (2010) Противокашлевые эффекты антагониста лейкотриеновых рецепторов монтелукаста у пациентов с кашлевой астмой и атопическим кашлем. Аллергол Инт 59: 185–192 [PubMed] [Google Scholar]
- Кон О.М., Кей А. (1999) Стратегии борьбы с Т-клетками при астме. Воспаление Res 48: 516–523 [PubMed] [Google Scholar]
- Кришнамурти Н., Орисс Т. Б., Паглиа М., Фей М., Ярлагадда М., Ванхасебрук Б. и др. (2008) Активация c-kit в дендритных клетках регулирует дифференцировку Т-хелперных клеток и аллергическую астму. Нат Мед 14: 565–573 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Leckie M.J., Ten Brinke A., Khan J., Diamant Z., O’connor B.J., Walls C.M., et al. (2000) Эффекты моноклональных антител, блокирующих интерлейкин-5, на эозинофилы, гиперчувствительность дыхательных путей и позднюю астматическую реакцию.Ланцет 356: 2144–2148 [PubMed] [Google Scholar]
- Leff J.A., Busse W.W., Pearlman D., Bronsky E.A., Kemp J., Hendeles L., et al. (1998) Монтелукаст, антагонист лейкотриеновых рецепторов, для лечения легкой формы астмы и бронхоспазма, вызванного физической нагрузкой. N Engl J Med 339: 147–152 [PubMed] [Google Scholar]
- Мартин Р.Дж., Крафт М., Чу Х.В., Бернс Э.А., Касселл Г.Х. (2001) Связь между хронической астмой и хронической инфекцией. J Allergy Clin Immunol 107: 595–601 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Табуена Р.П., Такемура М., Уэда Т., Ямагути М. и др. (2007) Утолщение стенки дыхательных путей у пациентов с кашлевой астмой и неастматическим хроническим кашлем. Грудь 131: 1042–1049 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Такемура М., Уэда Т., Табуена Р., Ямагути М. и др. (2006) Прогноз кашлевого варианта астмы: ретроспективный анализ. J астма 43: 131–135 [PubMed] [Google Scholar]
- Mcgarvey L., Morice A.H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности.Грудная клетка 58: 736–737, ответ автора 737-738. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mcgarvey L.P., Heaney L.G., Lawson J.T., Johnston B.T., Scally C.M., Ennis M., et al. (1998) Оценка и исходы пациентов с хроническим непродуктивным кашлем с использованием комплексного диагностического протокола. Грудная клетка 53: 738–743 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Мелло С.Дж., Ирвин Р.С., Керли Ф.Дж. (1996) Прогностические значения характера, времени и осложнений хронического кашля при диагностике его причины.Arch Intern Med 156: 997–1003 [PubMed] [Google Scholar]
- Menzies D., Holmes L., Mccumesky G., Prys-Picard C., Niven R. (2011) Сенсибилизация Aspergillus связана с ограничением воздушного потока и бронхоэктазами при тяжелой астме . Аллергия 66: 679–685 [PubMed] [Google Scholar]
- Мензис-Гоу А., Флад-Пейдж П., Сехми Р., Берман Дж., Хамид К., Робинсон Д.С. и др. (2003) Анти-IL-5 (меполизумаб) терапия вызывает задержку созревания эозинофилов в костном мозге и снижает количество предшественников эозинофилов в слизистой оболочке бронхов у больных атопической астмой.J Allergy Clin Immunol 111: 714–719 [PubMed] [Google Scholar]
- Мензис-Гоу А., Робинсон Д.С. (2002) Эозинофилы, эозинофильные цитокины (интерлейкин-5) и антиэозинофильная терапия при астме. Curr Opin Pulm Med 8: 33–38 [PubMed] [Google Scholar]
- Милгром Х., Бергер В., Наяк А., Гупта Н., Поллард С., Макалари М. и др. (2001) Лечение детской астмы антителом к иммуноглобулину Е (омализумаб). Педиатрия 108: E36. [PubMed] [Google Scholar]
- Милгром Х., Фик Р. Б., младший, Су Дж. К., Рейманн Дж. Д., Буш Р. К., Уотрус М. Л. и др. (1999) Лечение аллергической астмы моноклональными анти-IgE-антителами. Исследовательская группа по Rhumab-E25. N Engl J Med 341: 1966–1973 [PubMed] [Google Scholar]
- Миллар М.М., Макграт К.Г., Паттерсон Р. (1998) Злокачественная астма, эквивалентная кашлю: определение и отчеты о случаях. Энн Аллергия Астма Иммунол 80: 345–351 [PubMed] [Google Scholar]
- Morice A.H., Fontana G.A., Belvisi M.G., Birring S.S., Chung K.F., Dicpinigaitis P.V., et al. (2007) Рекомендации ERS по оценке кашля. Eur Respir J 29: 1256–1276 [PubMed] [Google Scholar]
- Morice A.H., Kastelik J.A. (2003) Кашель. 1: Хронический кашель у взрослых. Грудная клетка 58: 901–907 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Морис А.Х., Макгарви Л., Паворд И. (2006) Рекомендации по лечению кашля у взрослых. Грудная клетка 61 (Приложение 1): i1 – i24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Morjaria J.B., Babu K.S., Holgate S.T., Polosa R.(2006) Фактор некроза опухоли альфа как терапевтическая мишень при астме. Открытие лекарств сегодня: терапевтические стратегии 3: 309–316 [Google Scholar]
- Morjaria J.B., Chauhan A.J., Babu K.S., Polosa R., Davies D.E., Holgate S.T. (2008) Роль слитого белка растворимого рецептора TNF-α (этанерцепта) при резистентной к кортикостероидам астме: двойное слепое рандомизированное плацебо-контролируемое исследование. Грудная клетка 63: 584–591 [PubMed] [Google Scholar]
- Morjaria J.B., Gnanakumaran G., Babu K.S. (2007) Anti-IgE при аллергической астме и рините: обновление.Мнение эксперта Biol Ther 7: 1739–1747 [PubMed] [Google Scholar]
- Morjaria J.B., Polosa R. (2010) Рекомендации по оптимальному ведению тяжелой рефрактерной астмы. J Астма Аллергия 3: 43–56 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Наир П., Пиццичини М.М., Кьярсгаард М., Инман М.Д., Эфтимиадис А., Пиццичини Э. и др. (2009) Меполизумаб для лечения преднизонозависимой астмы с эозинофилией мокроты. N Engl J Med 360: 985–993 [PubMed] [Google Scholar]
- NICE. (2007) Омализумаб при стойкой аллергической астме.NICE Руководство по оценке технологий 133. NICE: Лондон [Google Scholar]
- Niimi A., Amitani R., Suzuki K., Tanaka E., Murayama T., Kuze F. (1998) Эозинофильное воспаление при кашлевом варианте астмы. Eur Respir J 11: 1064–1069 [PubMed] [Google Scholar]
- Ниими А., Мацумото Х., Минакучи М., Китаичи М., Амитани Р. (2000) Ремоделирование дыхательных путей при кашлевой астме. Ланцет 356: 564–565 [PubMed] [Google Scholar]
- Огава Х., Фудзимура М., Тофуку Ю. (2004) Лечение атопического кашля, вызванного антигеном базидиомицетов, низкими дозами итраконазола.Легкое 182: 279–284 [PubMed] [Google Scholar]
- Паломбини Б.С., Вилланова К.А., Араухо Э., Гастал О.Л., Альт Д.К., Штольц Д.П. и др. (1999) Патогенная триада при хроническом кашле: астма, синдром постназального подтекания и гастроэзофагеальная рефлюксная болезнь. Грудь 116: 279–284 [PubMed] [Google Scholar]
- Park C.S., Lee S.M., Chung S.W., Uh S., Kim H.T., Kim Y.H. (1994) Интерлейкин-2 и растворимый рецептор интерлейкина-2 в жидкости бронхоальвеолярного лаважа пациентов с бронхиальной астмой. Грудь 106: 400–406 [PubMed] [Google Scholar]
- Питерс С.П., Кунсельман С.Дж., Ицитович Н., Мур В.С., Паскуаль Р., Амередес Б.Т. и др. (2011) Повышающая терапия тиотропия бромидом для взрослых с неконтролируемой астмой. New Engl J Med 363: 1715–1726 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Poe R.H., Harder R.V., Israel R.H., Kallay M.C. (1989) Хронический непрекращающийся кашель. Опыт диагностики и результатов с использованием протокола анатомической диагностики. Грудь 95: 723–728 [PubMed] [Google Scholar]
- Polosa R., Benfatto G.T. (2009) Ведение пациентов с тяжелой хронической астмой: примите вызов.Eur J Intern Med 20: 114–124 [PubMed] [Google Scholar]
- Polosa R., Morjaria J. (2008) Иммуномодулирующие и биологические методы лечения тяжелой рефрактерной астмы. Респир Мед 102: 1499–1510 [PubMed] [Google Scholar]
- Преста Л., Шилдс Р., О’Коннелл Л., Лар С., Портер Дж., Горман К. и др. (1994) Сайт связывания иммуноглобулина Е человека для его рецептора с высоким сродством. J Biol Chem 269: 26368–26373 [PubMed] [Google Scholar]
- Reber L., Da Silva C.A., Frossard N. (2006) Фактор стволовых клеток и его рецептор c-kit как мишени для воспалительных заболеваний.Eur J Pharmacol 533: 327–340 [PubMed] [Google Scholar]
- Робертс Г., Ньюсом Д., Гомес К., Раффлз А., Саглани С., Бегент Дж. И др. (2003) Внутривенное болюсное введение сальбутамола в сравнении с инфузией эуфиллина у детей с тяжелой астмой: рандомизированное контролируемое исследование. Грудная клетка 58: 306–310 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Робинсон Д.С., Бентли А.М., Хартнелл А., Кей А.Б., Дарем С.Р. (1993) Активированные Т-хелперы памяти в жидкости бронхоальвеолярного лаважа пациентов с атопической астмой: связь с симптомами астмы, функцией легких и реактивностью бронхов.Грудная клетка 48: 26–32 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Rolling C., Treton D., Pellegrini S., Galanaud P., Richard Y. (1996) Рецепторы IL4 и IL13 имеют общую гамма-цепь C и активируют белки Stat6, Stat3 и Stat5 в нормальных В-клетках человека. FEBS Lett 393: 53–56 [PubMed] [Google Scholar]
- Ротенберг М.Э., Хоган С.П. (2006) Эозинофил. Анну Рев Иммунол 24: 147–174 [PubMed] [Google Scholar]
- Sanderson C.J. (1992) Интерлейкин-5, эозинофилы и болезни.Кровь 79: 3101–3109 [PubMed] [Google Scholar]
- Сильверман Р.А., Осборн Х., Рунге Дж., Галлахер Э. Дж., Чан У., Фельдман Дж. И др. (2002) Внутривенное введение сульфата магния в лечении острой тяжелой астмы: многоцентровое рандомизированное контролируемое исследование. Грудь 122: 489–497 [PubMed] [Google Scholar]
- Саймон Д., Браатен Л.Р., Саймон Х.У. (2004) Эозинофилы и атопический дерматит. Аллергия 59: 561–570 [PubMed] [Google Scholar]
- Смирниос Н.А., Ирвин Р.С., Керли Ф.Дж. (1995) Хронический кашель с чрезмерным выделением мокроты в анамнезе.Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Грудь 108: 991–997 [PubMed] [Google Scholar]
- Soler M., Matz J., Townley R., Buhl R., O’brien J., Fox H., et al. (2001) Анти-IgE-антитело омализумаб снижает частоту обострений и потребность в стероидах у аллергических астматиков. Eur Respir J 18: 254–261 [PubMed] [Google Scholar]
- Стивенс Р.С. (2003) Клеточная парадигма патогенеза хламидий. Тенденции Microbiol 11: 44–51 [PubMed] [Google Scholar]
- Тен Бринке А., Ван Диссель Дж. Т., Стерк П. Дж., Звиндерман А. Х., Рабе К. Ф., Бел Э. Х. (2001) Устойчивое ограничение воздушного потока при неатопической астме у взрослых связано с серологическими доказательствами инфекции Chlamydia pneumoniae . J Allergy Clin Immunol 107: 449–454 [PubMed] [Google Scholar]
- Тонелли М., Зингони М., Баччи Э., Денте Ф.Л., Ди Франко А., Джаннини Д. и др. (2003) Кратковременный эффект от добавления антагонистов лейкотриеновых рецепторов к текущей терапии тяжелых астматиков.Пульм Фармакол Тер 16: 237–240 [PubMed] [Google Scholar]
- U-BIOPRED (2008) Объективные биомаркеры для прогнозирования результатов респираторных заболеваний, http://www.fp7-consulting.be/en/ubiopred/
- Vatrella A ., Ponticiello A., Pelaia G., Parrella R., Cazzola M. (2005) Бронходилатирующие эффекты сальметерола, теофиллина и их комбинации у пациентов с умеренной и тяжелой астмой. Пульм Фармакол Тер 18: 89–92 [PubMed] [Google Scholar]
- Виньола А.М., Умберт М., Буске Дж., Буле Л.П., Хеджекок С., Блог М. и др. (2004) Эффективность и переносимость антииммуноглобулиновой терапии омализумабом у пациентов с сопутствующей аллергической астмой и стойким аллергическим ринитом: СОЛАР. Аллергия 59: 709–717 [PubMed] [Google Scholar]
- Фон Герцен Л.С. (2002) Роль персистирующей инфекции в контроле и тяжести астмы: фокус на Chlamydia pneumoniae. Eur Respir J 19: 546–556 [PubMed] [Google Scholar]
- Уорк П.А., Джонстон С.Л., Симпсон Дж. Л., Хенсли М.Дж., Гибсон П.Г. (2002) Chlamydia pneumoniae иммуноглобулин А реактивация и воспаление дыхательных путей при острой астме. Eur Respir J 20: 834–840 [PubMed] [Google Scholar]
- Webb D.C., Mckenzie A.N., Koskinen A.M., Yang M., Mattes J., Foster P.S. (2000) Интегрированные сигналы между IL-13, IL-4 и IL-5 регулируют гиперреактивность дыхательных путей. J Immunol 165: 108–113 [PubMed] [Google Scholar]
- Венцель С., Фахи Дж. В., Ирвин К.Г., Петерс С.П., Спектор С., Сефлер С.Дж. (2000) Материалы семинара ATS по рефрактерной астме: текущее понимание, рекомендации и вопросы без ответа.Am J Respir Crit Care Med 162: 2341–2351 [PubMed] [Google Scholar]
- Венцель С.Э., Барнс П.Дж., Бликер Е.Р., Буске Дж., Бусс В., Дален С.Э. и др. (2009) Рандомизированное двойное слепое плацебо-контролируемое исследование блокады фактора некроза опухоли альфа при тяжелой персистирующей астме. Am J Respir Crit Care Med 179: 549–558 [PubMed] [Google Scholar]
- Венцель С.Э., Шварц Л. (1999) Доказательства того, что тяжелую астму патологически можно разделить на два воспалительных подтипа с различными физиологическими и клиническими характеристиками.Am J Respir Crit Care Med 160: 1001–1008 [PubMed] [Google Scholar]
- Виллс-Карп М., Луимбази Дж., Сюй X., Скофилд Б., Небен Т.Ю., Карп К.Л. и др. (1998) Интерлейкин-13: центральный медиатор аллергической астмы. Наука 282: 2258–2261 [PubMed] [Google Scholar]
Необычные синдромы астмы и их лечение
Ther Adv Chronic Dis. 2011 июл; 2 (4): 249–264.
Джек А. Кастелик
1 Отделение респираторной медицины, Халл и фонд NHS Восточного Йоркшира, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
1 Отдел респираторной медицины, Hull и East Yorkshire NHS Trust, Университет Халла, Медицинская школа Халл-Йорка, Больница Касл-Хилл, Касл-роуд, Коттингем, HU16 5JQ, Великобритания
2 Отделение IIR, Школа медицины, Университет Саутгемптона, Больница общего профиля Саутгемптона , Саутгемптон СУ 6YD, Великобритания ку.ca.notos@mbjЭта статья цитируется другими статьями в PMC.Abstract
Астма обычно проявляется симптомами хрипов, одышки и кашля. Однако клиницисты должны знать об атипичных проявлениях этого расстройства, когда кашель является основным или единственным симптомом таких состояний, как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель. Ранняя диагностика и лечение этих состояний с помощью ингаляционных кортикостероидов улучшает симптомы у большинства пациентов.До 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Эти пациенты были охвачены термином «резистентная к лечению астма» (TRA), имеют наибольшую заболеваемость и несут более 50% расходов на здравоохранение. В этом обзоре мы обсуждаем исследования, лечение и патофизиологию различных фенотипов атипичных проявлений астмы, а также новые лицензированные биологические агенты и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности при TRA.
Ключевые слова: атопический кашель, биопрепараты, кашель, эозинофильный бронхит, моноклональные антитела, тяжелая астма
Введение
От астмы страдают 5,4 миллиона человек в Великобритании [Asthma UK, 2010] и около 300 миллионов человек в мире [Braman , 2006]. Его распространенность составляет 15-20% у детей и 5-10% у взрослых, и считается, что этот показатель будет продолжать расти. Более 12 миллионов рабочих дней в Великобритании теряются из-за проблем, связанных с астмой [Asthma UK, 2010].Более того, в 2006-2007 финансовом году было зарегистрировано около 80 000 случаев неотложной госпитализации по астме, из которых 41% — дети в возрасте до 14 лет. У большинства пациентов лечение этого состояния на основе международных руководств гарантирует, что астма хорошо контролируется с помощью терапии ингаляционными кортикостероидами (ICS) либо отдельно, либо в сочетании с агонистами β 2 длительного действия (LABA) [BTS / SIGN, 2008 ]. Другие агенты, такие как антилейкотриеновые агенты и теофиллины, также были использованы с хорошим эффектом.Однако до 10% пациентов с астмой остаются плохо контролируемыми, несмотря на оптимальную стандартную терапию. Хотя это небольшая часть больных астмой, они имеют наибольшую заболеваемость, рискуют умереть и несут более 50% расходов на здравоохранение, связанных с астмой; следовательно, существует неудовлетворенная потребность в этой группе плохо контролируемых астматиков [Chanez et al. 2007; Antoncelli et al. 2004; Европейская сеть по изучению механизмов тяжелой астмы, 2003 г.]
Астма — это гетерогенное заболевание, которое на одном конце спектра трудно диагностировать из-за атипичных симптомов, например кашля, а на другом конце — у пациентов с установленным заболеванием. где управление ограничено отсутствием доступных нам текущих терапевтических возможностей.Последнюю часто называют тяжелой астмой. Однако необходимо уточнить, что тяжелую астму можно подразделить на «трудно поддающуюся лечению» и «резистентную к лечению астму» (TRA). Следовательно, важно, чтобы этими двумя объектами управляли должным образом.
Трудно поддающаяся лечению астма может возникнуть по ряду причин [Morjaria and Polosa, 2010; Холгейт, Полоса, 2006]. Тремя основными причинами являются, за исключением состояний, имитирующих тяжелую астму, сопутствующие заболевания, триггеры астмы и, что наиболее важно, несоблюдение режима приема лекарств от астмы.И наоборот, TRA включает пациентов, которые не находятся под адекватным контролем с их лекарствами в соответствии с международными рекомендациями [BTS / SIGN, 2008], то есть на этапах IV и V Глобальной инициативы по астме (GINA) и Британского торакального общества / Шотландской межвузовской сети рекомендаций, где, несмотря на находясь на высоких дозах ICS, LABA и других дополнительных лекарствах и сумев установить контроль над компонентами трудноизлечимой астмы, пациенты сохраняют симптомы. Напротив, большинство пациентов с атипичной астмой, такой как кашлевой вариант астмы, неастматический эозинофильный бронхит или атопический кашель, реагируют на стандартную терапию ИКС и антигистаминными препаратами.Осведомленность о существовании этих состояний и связанная с ними способность диагностировать их являются основными проблемами, связанными с атипичной астмой. Если не лечить атипичную астму, у части пациентов может развиться классическая астма. Например, более трети пациентов с кашлевой астмой может прогрессировать до развития классической астмы [Johnson and Osborn, 1991; Браман и Коррао, 1985]. Напротив, только у очень небольшой части пациентов с атопическим кашлем развивается классическая астма [Fujimura et al. 2003].
В этом обзоре мы обсуждаем проблемы, с которыми сталкивается врач при постановке диагноза атипичной астмы. Таким образом, мы описываем исследования и лечение кашлевой астмы, атопического кашля и неастматического эозинофильного бронхита. Кроме того, мы обсуждаем подтверждение и фенотипирование TRA, а также предоставляем обзор новых биологических агентов, которые лицензированы, и те, которые были зарегистрированы в клинических испытаниях с точки зрения их эффективности и безопасности в TRA.Мы не обсуждаем трудно поддающуюся лечению астму, предполагая, что это учитывалось наряду с соблюдением режима лечения до постановки диагноза TRA.
Атипичная астма
Текущие рекомендации признают, что диагноз астмы является клиническим [BTS / SIGN, 2008]. Центральным во всех определениях астмы является наличие таких симптомов, как хрип, стеснение в груди, одышка или кашель, а также непостоянная обструкция дыхательных путей. Более поздние описания астмы также включали наличие гиперчувствительности дыхательных путей (AHR) и воспаления дыхательных путей [BTS / SIGN, 2008] .У значительной части пациентов диагноз классической астмы вряд ли вызовет какие-либо трудности. У пациентов с классической астмой наблюдаются хрипы, одышка или кашель. Измерения пикового потока выдоха (ПСВ) различаются по дням и в течение суток (). Бронхопровокационные пробы на гистамин или метахолин положительные. При отклонении от нормы спирометрия обычно выявляет обструкцию дыхательных путей. Однако существуют состояния, такие как кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель, которые отличаются от классической астмы по своим фенотипическим характеристикам.Поэтому их диагностика может быть более сложной. Хотя эти состояния могут различаться фенотипически, эозинофильное воспаление дыхательных путей составляет их общий знаменатель. Являются ли эти состояния воплощением «астматического синдрома» или представляют собой независимые сущности per se , остается предметом обсуждения [Mcgarvey et al. 2003]. Фактически, существует множество доказательств того, что у некоторых пациентов с этими состояниями, если они не диагностированы или не пролечены надлежащим образом, на самом деле могут развиваться полные характеристики классической астмы [Irwin et al. 2006; Fujimura et al. 2005a, 2005b, 2005c, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b]. Следовательно, осведомленность и способность ранней диагностики и лечения этих состояний имеют важное клиническое значение.
Таблица 1.
Атипичные астматические синдромы.
| Синдром | Вариабельность PEF | Обструкция дыхательных путей | Гиперчувствительность дыхательных путей | Эозинофилия мокроты | Атопия | Стероидный ответ | Результаты биопсии |
|---|---|---|---|---|---|---|---|
| Да | Да 900 | Да | Да | ± | Да | — | |
| Кашлевой вариант астмы | — | Нет | Да | Да | Нет | Да | ↓ толщина субэпителиального слоя по сравнению с классической астмой |
| Эозинофильный бронхит | Нет | Нет | Нет | Да | Нет | Да | ↓ тучные клетки в гладких мышцах дыхательных путей по сравнению с классической астмой |
| Атопический кашель | Нет | Нет | Нет | Да | Да | Да | Эозинофилы в подслизистой оболочке трахеи и бронхов |
Кашлевой вариант астмы
Кашлевый вариант астмы остается частой причиной хронического кашля [Chung and Pavord, 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini el al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981; Poe et al. 1989]. При астме кашель может сопровождаться другими симптомами, такими как хрипы или одышка [Irwin et al. 1990, 1981]. Однако у части пациентов, до 57% случаев в некоторых исследованиях, кашель может быть единственным проявлением этого состояния [Chung et al. 2008; Kastelik et al. 2005; Brightling et al. 1999a, 1999b; Palombini et al. 1999; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1997, 1990, 1981; Poe et al. 1989; Corrao et al. 1979]. В 1979 году Коррао и его коллеги определили «кашлевую астму» как AHR с хроническим кашлем, но без хрипов или обструкции дыхательных путей [Corrao et al. 1979]. После этого первоначального описания стало очевидно, что, хотя кашель является преобладающим респираторным симптомом у части пациентов с кашлевой астмой, хрипы также могут присутствовать [Kastelik et al. 2005; Palombini et al. 1999; Brightling et al. 1999a, 1999b; Mcgarvey et al. 1998; Mello et al. 1996; Smyrnios et al. 1995; Хоффштейн, 1994; Ирвин и др. 1990, 1981, Poe et al. 1989;]. Фактически, у одной трети пациентов, первоначально обследованных Коррао и его коллегами, впоследствии развилось хрипы [Braman and Corrao, 1985; Corrao et al. 1979]. При кашлевой астме оценка пикового потока выдоха (ПСВ) не выявляет дневной или суточной изменчивости, а спирометрические измерения не выявляют обструкции дыхательных путей. Кроме того, об атопии обычно не сообщается. Более того, присутствует AHR к гистамину или метахолину, а также эозинофилия мокроты [Kastelik, 2008; Morice et al. 2007, 2006; Морис, Кастелик, 2003].
Неастматический эозинофильный бронхит
Неастматический эозинофильный бронхит был первоначально описан Гибсоном и его коллегами и характеризуется эозинофилией мокроты [Brightling, 2006; Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. При неастматическом эозинофильном бронхите обструкции дыхательных путей нет, поскольку измерения спирометрии в норме. Также отсутствует вариабельность PEF и AHR.Однако индуцированный анализ мокроты выявляет эозинофилию, определяемую как более чем 3% от числа несквамоклеточных эозинофилов [Gibson et al. 2002]. Кроме того, повышается чувствительность кашлевого рефлекса.
Атопический кашель
Fujimura и его коллеги описали пациентов с хроническим непродуктивным кашлем и атопией, резистентным к бронходилататорам, и предложили термин эозинофильный трахеобронхит с гиперчувствительностью дыхательных путей или «атопический кашель» [Fujimura et al. 1992]. «Атопический кашель» характеризуется атопией, определяемой как одно или несколько из следующих: эозинофилия крови или мокроты; повышенные уровни общего или специфического иммуноглобулина (Ig) E; или положительный кожный укол [Fujimura et al. 2000, 1997, 1992]. Кроме того, при атопическом кашле наблюдается хронический непродуктивный кашель, устойчивый к бронходилататорам, отсутствие различной обструкции дыхательных путей и нормальная бронхиальная провокация [Dicpinigaitis, 2006; Fujimura et al. 2000, 1997, 1992]. Это состояние характеризуется повышенной реакцией кашля на вдыхаемый капсаицин, присутствием эозинофилов в мокроте и подслизистой биопсии трахеи и бронхов, но не в бронхоальвеолярном лаваже (БАЛ) [Fujimura et al. 2005, 2003, 2000, 1997, 1992]. Однако эксперты по-прежнему обсуждают, является ли атопический кашель отдельным заболеванием, вызывающим хронический кашель [Fujimura and Ogawa, 2003; Макгарви и Морис, 2003]. Некоторые, действительно, предположили, что пациенты с атопическим кашлем, скорее всего, являются атопическими людьми с кашлевой астмой [Mcgarvey and Morice, 2003]. Однако Fujimura и его коллеги определили атопический кашель с его специфической патофизиологией и отсутствием прогресса в классической астме [Fujimura and Ogawa, 2003].Поэтому для клиницистов важно исследовать и исключить другие распространенные причины хронического кашля, такие как кашлевой вариант астмы, гастроэзофагеальный рефлюкс и ринит, до постановки диагноза атопического кашля.
Патофизиология атипичной астмы
В последние годы наше понимание патофизиологии кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля улучшилось [Brightling et al. 2003, 2002, 2000а, 2000б; Брайтлинг и Паворд, 2000; Niimi et al. 2000, 1998]. Эти три состояния имеют схожие иммунопатологические характеристики с классической астмой в виде воспалительного процесса, вызванного эозинофилами. В то время как эозинофильное воспаление является общей патофизиологической характеристикой классической астмы, кашлевой вариант астмы, неастматический эозинофильный бронхит и атопический кашель различаются из-за различий в расположении воспалительных клеток и толщины субэпителиального слоя, о которых сообщалось в этих состояниях, следовательно, вероятные причины наблюдаемого фенотипического несоответствия [Brightling et al. 2002; Niimi et al. 1998].
Кашлевая астма
Эозинофилы играют важную роль в патофизиологии кашлевой астмы [Niimi et al. 1998]. Таким образом, имеются данные о повышенном количестве эозинофилов в ЖБАЛ и тканях пациентов с кашлевой астмой [Niimi et al. 2000]. Однако Де Диего и его коллеги показали, что не было значительной разницы между кашлевой астмой и классической астмой в уровнях мокроты эозинофильного катионного белка (ECP), интерлейкина (IL) -8, фактора некроза опухоли альфа (TNF-α) и уровни выдыхаемого оксида азота (eNO) [De Diego et al. 2005]. Точно так же Канадзава и его коллеги не смогли найти никакой разницы в уровнях eNO и ECP между пациентами с кашлевой астмой и пациентами с классической астмой [Kanazawa et al. 2005]. Однако уровни фактора роста эндотелия сосудов (VEGF), который может играть роль в проницаемости сосудов из-за воспаления, были значительно выше при классической астме. Niimi и его коллеги сообщили, что утолщение субэпителиального слоя при кашлевой астме не было столь выраженным, как при классической астме [Niimi et al. 1998]. Мацумото и его коллеги наблюдали, что у пациентов с кашлевой астмой наблюдалось утолщение стенки центральных дыхательных путей [Matsumoto et al. 2007]. Хотя уровни eNO были повышены при кашлевой астме, они не отличались от уровней eNO, наблюдаемых при классической астме [Fujimura et al. 2008]. Fujimura и его коллеги наблюдали за 41 пациентом с кашлевой астмой, у семи из которых развилась классическая астма [Fujimura et al. 2005a, 2005b, 2005c].AHR и отсутствие использования ICS были наиболее важными предикторами развития классической астмы. Как и при классической астме, ICS при кашлевой астме снижали AHR [Fujimura et al. 2005a, 2005b, 2005c]. Однако не было изменений порога кашля для ингаляционного капсаицина независимо от использования ICS, что свидетельствует о том, что чувствительность кашлевого рефлекса не участвует в механизмах кашлевой астмы.
Неастматический эозинофильный бронхит
Эозинофилы играют важную роль в патофизиологии неастматического эозинофильного бронхита [Brightling et al. 2003, 2002, 2000a, 2000b, Брайтлинг и Паворд, 2000; Гибсон и др. 1998]. При неастматическом эозинофильном бронхите эозинофилия обнаруживается в мокроте, ЖБАЛ и биоптатах бронхов. Кроме того, в мокроте повышается уровень ECP и цистеинил-лейкотриенов [Brightling et al. 2008, 2000a, 2000b]. Более того, уровни эозинофилии БАЛ, гранулоцитарно-колониестимулирующего фактора и экспрессии гена IL-5 были одинаковыми как при неастматическом эозинофильном бронхите, так и при классической астме [Gibson et al. 1998]. Брайтлинг и его коллеги показали одинаковую степень подслизистой эозинофилии и утолщения базальной мембраны и ретикулярной пластинки как при неастматическом эозинофильном бронхите, так и при классической астме [Brightling et al. 2003, 2002]. Однако количество триптазоположительных тучных клеток в пучках гладких мышц дыхательных путей было ниже при неастматическом эозинофильном бронхите по сравнению с классической астмой. Кроме того, при неастматическом эозинофильном бронхите уровни eNO повышаются, что аналогично ситуации, наблюдаемой при классической астме [Brightling et al. 2003, 2002].
Атопический кашель
Атопический кашель характеризуется эозинофильным трахеобронхитом без эозинофилов в ЖБАЛ и гиперчувствительностью кашлевых рецепторов без AHR. При атопическом кашле уровни eNO ниже по сравнению с уровнями, наблюдаемыми при кашлевой астме и классической астме [Fujimura et al. 2008]. В отличие от кашлевой астмы и неастматического эозинофильного бронхита нет данных об изменениях в базальной мембране или распределении воспалительных клеток или процессов у пациентов с атопическим кашлем.Однако, когда Кита и его коллеги изучали эффекты антагониста лейкотриеновых рецепторов монтелейкаста при атопическом кашле и кашлевой астме, авторы заметили, что кашель подавляется только у пациентов с кашлевой астмой [Kita et al. 2010]. Напротив, монтелукаст не влиял на кашель у пациентов с атопическим кашлем, что свидетельствует о различных патофизиологических механизмах этих двух состояний. Другое предположение о различных механизмах, лежащих в основе этих двух состояний, было сделано на основании более низких уровней eNO, наблюдаемых при атопическом кашле по сравнению с уровнями, измеренными при кашлевом варианте астмы [Fujimura et al. 2008].
Обследование пациентов с атипичной астмой
Диагностика пациентов с атипичной астмой может оказаться сложной задачей для клиницистов. Таким образом, оценка этих пациентов и клиническое подозрение на синдромы атипичной астмы остаются важными проблемами. Клинический анамнез может помочь в диагностике атипичной астмы. Однако клиницисты должны будут исключить другие распространенные причины хронического кашля, включая гастроэзофагеальный рефлюкс, ринит или лекарства, такие как ингибиторы ангиотензинпревращающего фермента (АПФ).Может помочь спирометрия, хотя при синдромах атипичной астмы она будет нормальной, как и рентгенограмма грудной клетки. Бронхопровокационные тесты могут быть положительными при классической астме и кашлевой астме; однако они будут нормальными при неастматическом эозинофильном бронхите и атопическом кашле. Индукция мокроты покажет эозинофилию мокроты при всех атипичных состояниях астмы. Напротив, уровни eNO могут различать неастматический эозинофильный бронхит, кашлевую астму и атопический кашель.Fujimura и коллеги показали, что eNO у пациентов с атопическим кашлем были значительно ниже, чем у пациентов с кашлевой астмой и классической астмой [Fujimura et al. 2008]. Тесты на атопию могут помочь пациентам с атопическим кашлем. При кашлевой астме и при неастматическом эозинофильном бронхите атопия менее вероятно. Следовательно, оценка пациентов с синдромами атипичной астмы должна включать в себя анамнез и обследование, спирометрию, рентгенографию грудной клетки, бронхопровокационные тесты, индукцию мокроты и измерения eNO.Однако диагноз синдромов атипичной астмы может быть подтвержден только в том случае, если наблюдается ответ на специфическую терапию.
Лечение атипичной астмы
Наличие непродуктивного кашля и положительный ответ на ИКС характерны для кашлевой астмы, неастматического эозинофильного бронхита и атопического кашля [Irwin et al. 2006; Kastelik et al. 2005; Fujimura et al. 2005a, 2005b, 2003; Brightling et al. 2003, 2000a, 2000b, 1999a, 1999b].Есть некоторые свидетельства того, что если не лечить кашлевую астму на ранней стадии, она может прогрессировать до классической астмы, и у пациентов могут развиться симптомы одышки и хрипов [Kastelik, 2008; Fujimura et al. 2003]. Напротив, считалось, что атопический кашель реже прогрессирует до классической астмы, особенно при раннем введении лечения с помощью ИКС [Fujimura et al. 2003]. Точно так же Мацумо и его коллеги обнаружили, что лечение ИКС предотвращает прогрессирование от кашлевой астмы до классической астмы [Matsumoto et al. 2006]. Fujimura и его коллеги изучили влияние ICS на изменения AHR и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой [Fujimura et al. 2005a, 2005b]. Как и при классической астме, AHR снижалась с помощью ICS. Однако не было изменений порога кашля у пациентов с кашлевой астмой, независимо от того, принимали они ИКС или нет. У некоторых пациентов с кашлевой астмой кашель улучшается с помощью антагонистов лейкотриеновых рецепторов, особенно если симптомы резистентны к ингаляционным бронходилататорам или ИКС [Dicpinigaitis et al. 2002]. Например, Дикпинигайтис и его коллеги наблюдали, что в ответ на антагонист лейкотриеновых рецепторов, зафирлукаст, как субъективная оценка кашля, так и чувствительность кашлевого рефлекса к вдыхаемому капсаицину улучшались у пациентов с кашлевой астмой, резистентной к ингаляционным бета-агонистам и ИКС [ Kita et al. 2010; Dicpinigaitis et al. 2002]. В очень тяжелых случаях кашлевой астмы, также называемой «астмой, эквивалентной злокачественному кашлю», могут потребоваться пероральные кортикостероиды [Millar et al. 1998]. В случае неастматического эозинофильного бронхита симптомы обычно улучшаются с помощью ИКС [Brightling et al. 1999a, 1999b; Карни и др. 1997; Гибсон и др. 1989]. В частности, есть доказательства того, что ИКС у пациентов с неастматическим эозинофильным бронхитом улучшают эозинофилию мокроты, тяжесть кашля и чувствительность [Brightling et al. 2000a, 2000b]. Атопический кашель успешно лечится антагонистами гистамина (H 1 ) и / или глюкокортикоидами, а иногда и противогрибковыми средствами [Fujimura et al. 2005a, 2005b, 2005c, 2003, 2000, 1992; Огава и др. 2004]. Однако было показано, что антагонисты лейкотриеновых рецепторов не влияют на кашель у пациентов с атопическим кашлем [Kita et al. 2010].
Астма, рефрактерная к лечению
TRA остается неприятной проблемой не только для медицинского персонала, ухаживающего за пациентами, но и для самих пациентов. Ряд клинических определений тяжелой астмы был предложен за последнее десятилетие различными группами, включая функцию легких, обострения и использование кортикостероидов [Wenzel et al. 2009, 2000]. Следовательно, астма и, в частности, TRA все чаще признаются разнообразным заболеванием.
Подтверждение TRA
Чтобы установить, что у пациента есть TRA, необходимо подтвердить в истории болезни, что плохое соблюдение режима (включая технику ингаляции и использование спейсера), сопутствующие заболевания, другие состояния и триггеры были исключены [Morjaria и Полоса, 2010]. Это можно сделать, просмотрев старые записи, анализы крови, рентгенологию и лечение в прошлом.Например, для исключения дисфункции голосовых связок может быть проведена бронхоскопия, а при интерстициальном заболевании легких — анализы крови, а также компьютерная томография с высоким разрешением. Если исследования не проводились ранее, было бы разумно провести их, чтобы исключить другую причину симптомов пациента. Кроме того, полезен подробный анамнез их астмы и ее контроль в настоящее время и ранее, а также медицинский осмотр. Список возможных исследований приведен в.
Таблица 2.
Исследования, помогающие отличить тяжелую астму от других состояний.
| Полный анализ крови (включая количество эозинофилов) |
| Уровни общего IgE (включая исследования RAST) |
| Аутоиммунный скрининг (и иногда ABG) |
| Насыщение кислородом |
| Chest X- ray |
| Тестирование функции легких |
| Оценка обратимости сальбутамола (и / или реакции на кортикостероиды) |
| Бронхиальные провокационные тесты (например,грамм. метахолин, маннит или аденозин) |
| FeNO |
| Кожные уколы |
| Индукция мокроты |
| Компьютерная томография грудной клетки с высоким разрешением |
| Компьютерная томография пазух |
| Бронхоскопия |
| Эхокардиография |
| pH-манометрия |
Фенотипирование TRA
Клинические, физиологические и иммунопатологические области TRA часто сосуществуют, но не связаны между собой, следовательно, это означает, что TRA далека от однородности и могут быть далее разделены на разные фенотипы.Было предложено несколько методов фенотипирования этих пациентов с TRA, но истинное значение фенотипирования TRA может быть твердо установлено после того, как будет проведена подробная характеристика ряда пациентов. Эти вопросы в настоящее время изучаются через установленную сеть U-BIOPRED (Объективные биомаркеры для прогнозирования исходов респираторных заболеваний) [U-BIOPRED, 2008].
До недавнего времени фенотипирование основывалось на клинических или патологических признаках. Клинически пациентов с тяжелой астмой можно разделить на три основные категории: частые обострения, перемежающиеся периодами отсутствия симптомов астмы; фиксированная преграда для воздушного потока; и кортикостероид-зависимые астматики [Polosa and Benfatto, 2009].Патологически с точки зрения бронхиальных дыхательных путей (БАЛ мокроты и биопсия) известны две основные категории: стойкие эозинофильные и неозинофильные подтипы [Wenzel et al. 1999]. Однако в последнее время стало также известно о существовании нейтрофилии как отдельного подтипа с эозинофилией или без нее [Hamilton et al. 2003; Jatakanon et al. 1999]. Более того, новые статистические подходы были применены к клинической информации, полученной от пациентов с астмой, и с использованием методов обработки данных были идентифицированы некоторые фенотипы астмы [Haldar et al. 2008]. Это использует метод, называемый кластерным анализом. Кроме того, с помощью этого метода была сконструирована многомерная картина фенотипов астмы, демонстрирующая клинически значимые различия в результатах, со стратегиями ведения, которые используют меру эозинофильного воспаления для титрования кортикостероидной терапии [Haldar et al. 2008].
Вдобавок к астме причастны инфекции (такие как Chlamydia pneumoniae ) и сенсибилизация к Aspergillus fumigatus . C. pneumoniae — облигатный внутриклеточный паразит, который может вызывать острые и хронические заболевания дыхательных путей, особенно астму, но субклиническая инфекция является обычным явлением [Stephens, 2003; Каннингем и др. 1998; Grayston, 1992]. Ряд групп сообщили, что существует значительная корреляция у людей между тяжестью астмы и инфекцией C. pneumoniae и увеличением антител IgG и IgA к C. pneumoniae (IgG и IgA), но обычно не к другим респираторным патогенам [ Стивенс, 2003; Wark et al. 2002; Ten Brinke et al. 2001; Мартин и др. 2001; Черный et al. 2000; Hammerschlag, 2000; Cook et al. 1998]. Однако неясно, являются ли эти ассоциации преимущественно результатом (1) инфекции, фиксирующей ответы Th3 и способствующей последующему развитию воспаления и астмы, или (2) иммунных ответов, которые приводят к воспалению и астме, также предрасполагающим к атипичной бактериальной инфекции. Следовательно, было предложено, чтобы время заражения зависело от воздействия, возраста первого заражения и / или основного иммунного фенотипа человека, предрасположенного к C.pneumoniae вызывает аллергию и астму, а не природа инфекции per se [Von Hertzen, 2002]. Аналогичным образом, недавно сообщалось, что пациенты с тяжелой астмой, сенсибилизированные к A. fumigatus , которые не соответствуют общепринятым диагностическим критериям аллергического бронхолегочного аспергиллеза, не только имеют радиологические радиологические аномалии на компьютерной томографии высокого разрешения, такие как бронхоэктазы, бронхиальная болезнь. утолщение стенок и расширение бронхов, а также ограничение воздушного потока из-за захвата воздуха [Menzies et al. 2011]. Эти наблюдения предполагают патофизиологические фенотипы TRA.
Следует отметить, что идентифицированные фенотипы не обязательно являются фиксированными и могут изменяться со временем и в зависимости от назначенного лечения [Haldar et al. 2008]. Используя эту фенотипическую информацию (и, возможно, более точные определения различных подтипов в будущем), необходимо определить механизмы, которые имеют решающее значение во взаимодействии между различными фенотипами астмы, и распутать лежащую в основе патобиологию, чтобы не только разработать биомаркеры. болезней, но и для разработки новых методов лечения, адаптированных к потребностям наших пациентов.
Управление TRA
У большинства пациентов астма не контролируется в соответствии с рекомендациями. Это было продемонстрировано в исследовании Gaining Optimal Asthma Control (GOAL): несмотря на оптимизацию, комбинированный ингалятор салметерол / флутиказон позволил только 62% пациентов достичь полного контроля над симптомами астмы [Bateman et al. 2004]. Более того, после курса OCS этот показатель улучшился до 69%. У остальных пациентов по-прежнему наблюдались неконтролируемые симптомы астмы.
Оптимальное лечение должно быть направлено на достижение наилучшего связанного с астмой качества жизни (QoL) и контроль с помощью самых низких доз лекарств, особенно кортикостероидов. При выборе и формулировании используемых терапевтических агентов следует принимать во внимание не только тяжесть и фенотип заболевания, сопутствующие заболевания и предпочтения пациента, терапевтические реакции, но и сообщения о нежелательных явлениях. Следовательно, в дополнение к стандартной терапии ICS и LABA, другие агенты, такие как антилейкотриеновые агенты (для аспирино-чувствительной астмы [Tonelli et al. 2003] и астмы, вызванной физической нагрузкой [Leff et al. 1998]), теофиллины [Vatrella et al. 2005; Робертс и др. 2003], холинолитики [Peters et al. 2011] и внутривенное (IV) введение магния [Beasley and Aldington, 2007; Silverman et al. 2002] подлежит испытанию.
Пероральные кортикостероиды (OCS) использовались при хронических заболеваниях, но были исследования с использованием иммуномодуляторов для ограничения необходимости длительного использования OCS и, таким образом, побочного действия кортикостероидов.Был изучен ряд таких иммуномодулирующих препаратов с некоторой эффективностью и безопасностью, включая метотрексат, циклоспорин А, макролидные антибиотики, азатиоприн, золото и иммуноглобулины для внутривенного введения [Polosa and Morjaria, 2008]. Примечательно, что метотрексат, циклоспорин А и макролидные антибиотики обычно оцениваются как кортикостероидсберегающие препараты.
Совсем недавно биологические агенты были исследованы на предмет использования в качестве средств, сберегающих кортикостероиды. Единственный лицензированный биологический агент — омализумаб.Другие агенты были изучены с ограниченной эффективностью и безопасностью или все еще находятся на предварительных стадиях оценки. Мы обсудим эти агенты дальше (и они кратко описаны в).
Таблица 3.
Резюме обсужденных исследований.
| Агент | Доказательства эффективности | Улучшения параметров |
|---|---|---|
| Анти-IgE: омализумаб (SC / IV) | Milgrom et al. [1999] (DBPC) | Улучшение утреннего PEF, качества жизни при астме; уменьшение обострений астмы и употребление снотворных |
| Busse et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Soler et al. [2001] (DBPC) | Улучшение оценки симптомов, FEV 1 , утренний PEF; уменьшение обострений астмы и употребление снотворных | |
| Milgrom et al. [2001] (DBPC) | Уменьшение обострений астмы и употребление снотворных | |
| Holgate et al. [2004] (DBPC) | Сокращение использования вспомогательных средств; улучшение оценки симптомов и качества жизни астмы | |
| Humbert et al. [2005] (DBPC) | Уменьшение числа обострений астмы и количества обращений в отделение неотложной помощи; улучшение качества жизни при астме, утреннего PEF, оценки симптомов астмы | |
| Анти-TNF-α: этанерцепт (SC), голимумаб (SC) | Howarth et al. [2005] (открытое исследование) | Улучшение ОФВ 1 , FVC, PEF, AHR и контроль астмы; добровольное прекращение использования небулайзерного облегчения |
| Berry et al. [2006] (CS) | Улучшение FEV 1 , FVC, PEF, AHR и качества жизни астмы | |
| Morjaria et al. [2008] (DBPC) | Улучшение контроля астмы; добровольное прекращение использования небулайзерного облегчения | |
| Wenzel et al. [2009] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам (исследование прекращено досрочно из-за СНЯ) | |
| Анти-ИЛ-5: меполизумаб (IV) | Haldar et al. [2009] (DBPC) | Уменьшение обострений астмы; улучшение качества жизни при астме |
| Nair et al. [2009] (DBPC) | Уменьшение обострений астмы и снижение дозы OCS без обострений; улучшение ОФВ 1 и контроль астмы | |
| Анти-IL-4 рецептор (IL-4Rα): AMG 317 | Corren et al. [2010] (DBPC) | Никаких улучшений по каким-либо оцененным параметрам не было. |
| Анти-CD25: даклизумаб (IV) | Busse et al. [2008] (DBPC) | Улучшение ОФВ 1 , дневных симптомов астмы и использования восстановительных средств; увеличивается во время обострений |
| Anti-SCF / c-kit и рецептор PDGF: маситиниб (PO) | Humbert et al. [2009] (DBPC) | Улучшение контроля астмы |
Омализумаб.
IgE играет ключевую роль в развитии аллергических состояний [Corry and Kheradmand, 1999]. Аллерген-специфический IgE связывается с эффекторными клетками через рецепторы с высоким сродством (FceRI) и низким сродством (FceRII), вызывая их эффекты, такие как индукция дегрануляции тучных клеток и базофилов, вызывая результирующие реакции на ранней и поздней фазах [Gould и Саттон, 2008 г .; Morjaria et al. 2007]. Омализумаб представляет собой рекомбинантное гуманизированное IgE-специфическое моноклональное антитело, которое прерывает взаимодействие между IgE и FceRI на эффекторных клетках [Presta et al. 1994]. Ранние фармакодинамические исследования омализумаба показали, что он снижает воспаление, AHR, аллерген-индуцированные дыхательные пути и кожные пробы [Boulet et al. 1997; Fahy et al. 1997].
Было проведено шесть крупных двойных слепых плацебо-контролируемых (DBPC) исследований III фазы с применением омализумаба подкожно в дозе 0.016 мг / кг / IgE (МЕ / мл) каждые 2 или 4 недели для оценки его безопасности и эффективности при тяжелой атопической астме с симптомами, несмотря на оптимальную терапию [Humbert et al. 2005; Holgate et al. 2004; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. Продолжительность исследований составляла от 25 до 52 недель с участием субъектов с уровнем IgE от 30 до 700 МЕ / мл). В совокупности анализ различных исследований, а также коллективные оценки показали, что добавление омализумаба привело к улучшению субъективных параметров контроля астмы и качества жизни, а также к объективным улучшениям функции легких, а также к сокращению использования вспомогательных средств, использования кортикостероидов, количества обращений в отделение неотложной помощи. и количество обострений астмы [Bousquet et al. 2005, 2004; Chipps et al. 2005; Humbert et al. 2005; Holgate et al. 2004; Finn et al. 2003; Busse et al. 2001; Milgrom et al. 2001, 1999; Soler et al. 2001]. В период исследования омализумаб был безопасен без значительных побочных эффектов по сравнению с плацебо. Однако в постмаркетинговых отчетах сообщается о незначительном увеличении количества анафилактических и анафилактоидных реакций, злокачественных новообразований и гельминтозов [Cruz et al. 2007; НИЦЦА, 2007; Vignola et al. 2004].
Следует отметить, что пациенты, принимающие омализумаб, проходят 16-недельную оценку эффективности и безопасности, чтобы убедиться, что они получают пользу от терапии анти-IgE. Отчасти это связано со стоимостью препарата. Хотя омализумаб является безопасным и эффективным лекарством, важно помнить, что лишь небольшая часть тяжелых астматиков страдает атопией, и даже из них только две трети получат от него пользу; большинство TRAS не являются атопическими и не подходят для лечения анти-IgE.
Антагонизм фактора некроза опухоли альфа.
TNF-α представляет собой многофункциональный провоспалительный цитокин Th2, который, как предполагается, играет важную роль в инициировании, поддержании и прогрессировании воспаления дыхательных путей при астме [Morjaria et al. 2006]. Сообщается, что уровни TNF-α в дыхательных путях повышаются при тяжелом заболевании. Неспособность кортикостероидов снижать уровень TNF-α и цитокинов, производных Th2, в дыхательных путях астматиков может объяснить, почему кортикостероиды имеют ограниченную эффективность при TRA.Следовательно, было постулировано, что противодействие TNF-α и, следовательно, вмешательство в цитокины, производные Th2, может представлять собой прогресс в лечении TRA.
На основе этой предпосылки два небольших исследования (одно доказательство концепции [Howarth et al. 2005], а другое — перекрестное исследование с плацебо-контролем [Berry et al. 2006]) антагонизма TNF-α с использованием растворимого рецептора этанерцепта. Они сообщили о значительном улучшении качества жизни, связанного с астмой (AQLQ), и контроля астмы, а также спирометрии, PEF и AHR.Однако в более крупном исследовании DBPC с использованием того же растворимого рецептора не сообщалось о таких драматических эффектах, с лишь незначительным улучшением контроля астмы [Morjaria et al. 2008]. Подобно этому исследованию, еще более крупное исследование DBPC с использованием моноклонального антитела к TNF-α, голимумаба, не продемонстрировало улучшения каких-либо измеренных параметров, но на самом деле исследование было прекращено досрочно из-за опасений по поводу безопасности [Wenzel et al. 2009]. Увеличилось не только количество солидных злокачественных новообразований, но и серьезных инфекций, таких как пневмония, сепсис и реактивация туберкулеза.Однако следует отметить, что в двух более крупных исследованиях [Wenzel et al. 2009; Morjaria et al. 2008] упомянули, что у включенных в исследование пациентов было более легкое заболевание по сравнению с пациентами меньших исследований [Berry et al. 2006; Howarth et al. 2005]. Следовательно, даже если можно выделить подгруппы, в которых анти-TNF-α могут быть эффективными, необходимо принять во внимание эти связанные с лечением тяжелые побочные эффекты. В настоящее время нет известных нам исследований, использующих стратегии против TNF-α.
Анти-ИЛ-5: меполизумаб.
Эозинофилия в дыхательных путях и их дегрануляция являются признаком астмы и связаны с цитокинами Th3, а именно с ИЛ-4, ИЛ-5, ИЛ-9, ИЛ-13 и гранулоцитарно-макрофагальным колониестимулирующим фактором [Rothenberg и Хоган, 2006; Simon et al. 2004; Мензис-Гоу и Робинсон, 2002; Сандерсон, 1992]; все они выражены в повышенных количествах при тяжелой астме [Desai and Brightling, 2009]. IL-5 — важный цитокин, специфичный для эозинофилов.На основе этого принципа антагонизация IL-5 с использованием моноклонального антитела, меполизумаба, проводилась у пациентов с легким или умеренным заболеванием без заметных клинических улучшений [Flood-Page et al. 2007, 2003a, 2003b; Buttner et al. 2003; Menzies-Gow et al. 2003; Leckie et al. 2000].
Совсем недавно были проведены два исследования DBPC с участием пациентов, которые имели стойкую эозинофилию, несмотря на терапию кортикостероидами с использованием меполизумаба с хорошей эффективностью и безопасностью [Haldar et al. 2009; Наир и др. 2009]. Они сообщили о значительном сокращении обострений астмы [Haldar et al. 2009; Наир и др. 2009] и снижение дозы ОКС без обострений [Nair et al. 2009], а также значительное улучшение объема форсированного выдоха за одну секунду (FEV 1 ) [Nair et al. 2009], контроль астмы [Nair et al. 2009], AQLQ [Haldar et al. 2009] и резкое снижение эозинофилии мокроты и крови [Haldar et al. 2009; Наир и др. 2009]. В обоих исследованиях не было отмечено серьезных нежелательных явлений. В настоящее время проводятся более крупные исследования для подтверждения результатов этих двух исследований в этой небольшой подгруппе TRA.
Антагонизм рецептора IL-4 альфа (IL-4Rα).
Как упоминалось выше (в разделе об анти-IL-5), IL-4 и IL-13 также являются цитокинами Th3, которые играют роль в патогенезе астмы, и, следовательно, нацеливание на эти цитокины может быть эффективным при тяжелом заболевании [ Webb et al. 2000; Grunig et al. 1998; Wills-Karp et al. 1998]. Следует отметить, что IL-4Ra используется обоими этими цитокинами для проявления своей активности [Rolling et al. 1996]. Имея это в виду, было проведено большое исследование DBPC у умеренных и тяжелых астматиков для оценки безопасности и эффективности полностью гуманизированных моноклональных антител к IL-4Rα, AMG 317 [Corren et al. 2010]. Было отмечено, что не было улучшений ни по одному из параметров, оцениваемых в исследовании.Однако апостериорный анализ показал, что AMG 317 может иметь значение у пациентов с наибольшим количеством симптомов. При использовании AMG 317 не было серьезных проблем с побочными эффектами.
Анти-CD25: даклизумаб.
Т-клетки играют роль в воспалении дыхательных путей при астме, при этом повышенные уровни CD25 Т-клеток и цитокина IL-2 отмечаются при более тяжелых формах заболевания [Kon and Kay, 1999; Park et al. 1994; Робинсон и др. 1993; Azzawi et al. 1992].Используя этот принцип, Буссе и его коллеги провели исследование для оценки безопасности и эффективности гуманизированного моноклонального антитела к альфа-субъединице (CD25) высокоаффинного рецептора IL-2, тем самым препятствуя связыванию IL-2 [Busse et al. . 2008]. В этом исследовании DBPC у умеренно-тяжелых астматиков сообщалось о минимальном значительном улучшении ОФВ 1 , дневных симптомов астмы, увеличения времени до обострения астмы и сокращения использования вспомогательных средств в пользу даклизумаба.Хотя в группе даклизумаба было больше побочных эффектов, они не были значительными. Место даклизумаба в TRA требует дальнейшей оценки в более крупных исследованиях.
Ингибитор тирозинкиназы рецептора фактора стволовых клеток (c-kit) / рецептора тромбоцитарного фактора роста: маситиниб.
Тучные клетки и дендритные клетки являются клетками, участвующими в TRA [Krishnamoorthy et al. 2008; Chanez et al. 2007; Холгейт и Полоса, 2006; Ребер и др. 2006].Они могут быть активированы с помощью рецептора c-kit фактора стволовых клеток (SCF), что приводит к накоплению тучных клеток, AHR и повышению уровня гистамина, эозинофильной инфильтрации, а также продукции IL-4. Более того, фактор роста тромбоцитов (PDGF), фактор роста, участвует в ремоделировании дыхательных путей [Chung et al. 2006; Инграм и Боннер, 2006]. Следовательно, противодействие рецепторам SCF / c-kit и PDGF может быть потенциальной терапевтической мишенью. Имея это в виду, маситиниб, ингибитор тирозинкиназы, который специфически противодействует рецепторам c-kit и PDGF, был использован для оценки его эффективности и безопасности у субъектов с тяжелой персистирующей астмой, несмотря на высокие дозы ICS, а также OCS [Humbert et al. 2009]. В этом исследовании DBPC Humbert и его коллеги рандомизировали 44 пациента для приема маситиниба перорально в трех дозах: 3 ( n = 12), 4,5 ( n = 11) или 6 ( n = 10) мг / кг / день. или плацебо ( n = 11), т.е. 3: 1, в течение 16 недель. Ни первичная конечная точка отлучения от OCS, ни какие-либо параметры функции дыхательных путей не показали существенной разницы между различными дозами маситиниба и / или плацебо. В обеих группах было 14 выбывших, которые были одинаковыми в обеих группах из-за нежелательных явлений или отсутствия терапевтической эффективности.Следует отметить, что единственным показателем значительного улучшения был показатель ACQ в группе маситиниба по сравнению с группой плацебо. Исследователи сообщили о том, что пациенты, принимавшие высокие дозы OCS и получавшие маситиниб ( n = 6), могли быть отлучены от дозы OCS по сравнению с отсутствием в группе плацебо. Также сообщалось, что пациенты, принимавшие маситиниб, имели больше незначительных, а также серьезных побочных эффектов по сравнению с пациентами, принимавшими плацебо. Это исследование фазы IIa показывает, что маситиниб может играть незначительную роль в TRA, если таковая имеется, поскольку были отмечены только субъективные улучшения.
Заключение
Астма остается очень важным условием с точки зрения бремени экономики здравоохранения, заболеваемости, влияния на качество жизни пациентов и вариантов лечения. Ведение пациентов с TRA — огромная проблема для клиницистов. Появление потенциальных новых иммуномодулирующих агентов может предоставить новые терапевтические возможности для TRA в будущем. Напротив, варианты лечения легкой и умеренной астмы хорошо известны. Однако в этой популяции астматиков есть подгруппа пациентов, которые могут проявлять атипичность.Таким образом, осведомленность клиницистов о возможных различных фенотипических подгруппах астмы очень важна. Если эти синдромы атипичной астмы диагностируются на ранней стадии, их лечение относительно просто, и контроль симптомов может быть достигнут у значительной части пациентов.
Footnotes
Это исследование не получало специального гранта от какого-либо финансирующего агентства в государственном, коммерческом или некоммерческом секторах.
Авторы заявляют об отсутствии конфликта интересов при подготовке данной рукописи.
Ссылки
- Antoncelli L., Bucca C., Neri M., De Benedetto F., Saabbatani P.B.F. (2004) Степень тяжести астмы и использование медицинских ресурсов. Eur Respir J 23: 723–729 [PubMed] [Google Scholar]
- Asthma UK (2010) Веб-сайт Asthma UK, http://www.asthma.org.uk (по состоянию на октябрь 2010 г.).
- Аззави М., Джонстон П.В., Маджумдар С., Кей А.Б., Джеффри П.К. (1992) Т-лимфоциты и активированные эозинофилы в слизистой оболочке дыхательных путей при фатальной астме и муковисцидозе. Am Rev Respir Dis 145: 1477–1482 [PubMed] [Google Scholar]
- Бейтман Э.D., Boushey H.A., Bousquet J., Busse W.W., Clark T.J., Pauwels R.A. и др. (2004) Можно ли достичь контроля астмы в соответствии с рекомендациями? Исследование достижения оптимального контроля над астмой. Am J Respir Crit Care Med 170: 836–844 [PubMed] [Google Scholar]
- Бизли Р., Алдингтон С. (2007) Магний в лечении астмы. Curr Opin Allergy Clin Immunol 7: 107–110 [PubMed] [Google Scholar]
- Берри М.А., Харгадон Б., Шелли М., Паркер Д., Шоу Д.Э., Грин Р.Х. и др. (2006) Доказательства роли фактора некроза опухоли альфа при рефрактерной астме.N Engl J Med 354: 697–708 [PubMed] [Google Scholar]
- Black P.N., Scicchitano R., Jenkins C.R., Blasi F., Allegra L., Wlodarczyk J. и др. (2000) Серологические доказательства инфекции Chlamydia pneumoniae связаны с тяжестью астмы. Eur Respir J 15: 254–259 [PubMed] [Google Scholar]
- Boulet L.P., Chapman K.R., Cote J., Kalra S., Bhagat R., Swystun V.A. и др. (1997) Ингибирующее действие анти-IgE-антитела Е25 на индуцированный аллергеном ранний астматический ответ.Am J Respir Crit Care Med 155: 1835–1840 [PubMed] [Google Scholar]
- Bousquet J., Cabrera P., Berkman N., Buhl R., Holgate S., Wenzel S., et al. (2005) Влияние лечения омализумабом, анти-IgE-антителом, на обострения астмы и посещение неотложной медицинской помощи у пациентов с тяжелой персистирующей астмой. Аллергия 60: 302–308 [PubMed] [Google Scholar]
- Bousquet J., Wenzel S., Holgate S., Lumry W., Freeman P., Fox H. (2004) Прогнозирование ответа на омализумаб, антитело против IgE , у пациентов с аллергической астмой.Грудь 125: 1378–1386 [PubMed] [Google Scholar]
- Браман С.С. (2006) Глобальное бремя астмы. Грудь 130: 4S – 12S [PubMed] [Google Scholar]
- Браман С.С., Коррао В.М. (1985) Хронический кашель. Диагностика и лечение. Prim Care 12: 217–225 [PubMed] [Google Scholar]
- Brightling C.E. (2006) Хронический кашель, вызванный неастматическим эозинофильным бронхитом. Руководство по клинической практике, основанное на доказательствах ACCP. Грудь 129: 116–121 с [PubMed] [Google Scholar]
- Брайтлинг К.Э., Брэддинг П., Саймон Ф.А., Холгейт С.Т., Уордлоу А.Дж., Паворд И.Д. (2002) Инфильтрация тучными клетками гладкой мускулатуры дыхательных путей при астме. N Engl J Med 346: 1699–1705 [PubMed] [Google Scholar]
- Brightling C.E., Pavord I.D. (2000) Эозинофильный бронхит — что это такое и почему это важно ?. Clin Exp Allergy 30: 4–6 [PubMed] [Google Scholar]
- Brightling C.E., Symon F.A., Birring S.S., Bradding P., Wardlaw A.J., Pavord I.D. (2003) Сравнение иммунопатологии дыхательных путей эозинофильного бронхита и астмы.Грудная клетка 58: 528–532 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Го К.Л., Уордлоу А.Дж., Паворд И.Д. (1999a) Эозинофильный бронхит — важная причина хронического кашля. Am J Respir Crit Care Med 160: 406–410 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Уорд Р., Уордлоу А.Дж., Паворд И.Д. (2000a) Воспаление дыхательных путей, чувствительность дыхательных путей и кашель до и после ингаляции будесонида у пациентов с эозинофильным бронхитом. Eur Respir J 15: 682–686 [PubMed] [Google Scholar]
- Брайтлинг К.E., Ward R., Woltmann G., Bradding P., Sheller J.R., Dworski R. и др. (2000b) Индуцированные концентрации медиатора воспаления в мокроте при эозинофильном бронхите и астме. Am J Respir Crit Care Med 162: 878–882 [PubMed] [Google Scholar]
- Брайтлинг К.Э., Вольтманн Г., Вардлоу А.Дж., Паворд И.Д. (1999b) Развитие необратимой обструкции воздушного потока у пациента с эозинофильным бронхитом без астмы. Eur Respir J 14: 1228–1230 [PubMed] [Google Scholar]
- BTS / SIGN. (2008) BTS / Sign (Британское торакальное общество / Шотландская межвузовская сеть).Британское руководство по лечению астмы: Национальное клиническое руководство. Грудная клетка 63 (Дополнение IV): iv1 – iv121 [PubMed] [Google Scholar]
- Busse W., Corren J., Lanier B.Q., Mcalary M., Fowler-Taylor A., Cioppa G.D., et al. (2001) Омализумаб, рекомбинантное гуманизированное моноклональное антитело против IgE, для лечения тяжелой аллергической астмы. J Allergy Clin Immunol 108: 184–190 [PubMed] [Google Scholar]
- Busse W.W., Israel E., Nelson H.S., Baker J.W., Charous B.L., Young D.Y. и др.(2008) Даклизумаб улучшает контроль астмы у пациентов со средней и тяжелой персистирующей астмой: рандомизированное контролируемое исследование. Am J Respir Crit Care Med 178: 1002–1008 [PubMed] [Google Scholar]
- Buttner C., Lun A., Splettstoesser T., Kunkel G., Renz H. (2003) Лечение моноклональным анти-интерлейкином-5 подавляет эозинофилы, но не Т-клетки функции. Eur Respir J 21: 799–803 [PubMed] [Google Scholar]
- Карни И.К., Гибсон П.Г., Мюрри-Аллен К., Салтос Н., Олсон Л.Г., Хенсли М.J. (1997) Систематическая оценка механизмов хронического кашля. Am J Respir Crit Care Med 156: 211–216 [PubMed] [Google Scholar]
- Chanez P., Wenzel S.E., Anderson G.P., Anto J.M., Bel E.H., Boulet L.P., et al. (2007) Тяжелая форма астмы у взрослых: каковы важные вопросы ?. J Allergy Clin Immunol 119: 1337–1348 [PubMed] [Google Scholar]
- Чиппс Б., Коррен Дж., Финн А., Хеджекок С., Фокс Х., Блог М. (2005) Омализумаб значительно улучшает качество жизни пациентов с тяжелыми формами стойкая астма.J Allergy Clin Immunol 115: S5 – S19 [Google Scholar]
- Chung K.F., Hew M., Score J., Jones A.V., Reiter A., Cross N.C., et al. (2006) Кашель и гиперэозинофилия из-за слитого гена FIP1L1-PDGFRA с тирозинкиназной активностью. Eur Respir J 27: 230–232 [PubMed] [Google Scholar]
- Чунг К.Ф., Паворд И.Д. (2008) Распространенность, патогенез и причины хронического кашля. Ланцет 371: 1364–1374 [PubMed] [Google Scholar]
- Cook P.J., Davies P., Tunnicliffe W., Ayres J.G., Honeybourne D., Wise R. (1998) Chlamydia pneumoniae и астма. Грудная клетка 53: 254–259 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Corrao W.M., Braman S.S., Irwin R.S. (1979) Хронический кашель как единственное проявление бронхиальной астмы. N Engl J Med 300: 633–637 [PubMed] [Google Scholar]
- Corren J., Busse W., Meltzer E.O., Mansfield L., Bensch G., Fahrenholz J. и др. (2010) Рандомизированное контролируемое исследование фазы 2 AMG 317, антагониста IL-4Ralpha, у пациентов с астмой.Am J Respir Crit Care Med 181: 788–796 [PubMed] [Google Scholar]
- Корри Д. Б., Херадманд Ф. (1999) Индукция и регуляция ответа IgE. Природа 402: B18 – B23 [PubMed] [Google Scholar]
- Cruz A.A., Lima F., Sarinho E., Ayre G., Martin C., Fox H., et al. (2007) Безопасность антииммуноглобулиновой терапии омализумабом у пациентов с аллергией, подверженных риску геогельминтной инфекции. Clin Exp Allergy 37: 197–207 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Каннингем А.Ф., Джонстон С.Л., Джулиус С.А., Лампе Ф.С., Уорд М.Е. (1998) Хроническая инфекция Chlamydia pneumoniae и обострения астмы у детей. Eur Respir J 11: 345–349 [PubMed] [Google Scholar]
- Де Диего А., Мартинес Э., Перпина М., Ньето Л., Компте Л., Мачиан В. и др. (2005) Воспаление дыхательных путей и чувствительность к кашлю при кашлевой астме. Аллергия 60: 1407–1411 [PubMed] [Google Scholar]
- Desai D., Brightling C. (2009) Цитокиновая и антицитокиновая терапия при астме: готовы к клинике ?.Клин Эксп Иммунол 158: 10–19 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Dicpinigaitis P.V. (2006) Хронический кашель из-за астмы: клинические рекомендации ACCP, основанные на фактических данных. Грудь 129: 75S – 79S [PubMed] [Google Scholar]
- Dicpinigaitis P.V., Добкин J.B., Reichel J. (2002) Противокашлевое действие антагониста лейкотриеновых рецепторов зафирлукаста у субъектов с кашлевой астмой. J астма 39: 291–297 [PubMed] [Google Scholar]
- Европейская сеть по изучению механизмов тяжелой астмы.(2003) Поперечное европейское многоцентровое исследование клинического фенотипа тяжелой хронической астмы Enfumosa. Eur Respir J 22: 470–477 [PubMed] [Google Scholar]
- Fahy J.V., Fleming H.E., Wong H.H., Liu J.T., Su J.Q., Reimann J., et al. (1997) Влияние моноклонального антитела против IgE на раннюю и позднюю фазу ответа на вдыхание аллергена у пациентов с астмой. Am J Respir Crit Care Med 155: 1828–1834 [PubMed] [Google Scholar]
- Финн А., Гросс Г., Ван Бавель Дж., Ли Т., Виндом Х., Эверхард Ф. и др. (2003) Омализумаб улучшает качество жизни, связанное с астмой, у пациентов с тяжелой аллергической астмой. J Allergy Clin Immunol 111: 278–284 [PubMed] [Google Scholar]
- Флад-Пейдж П., Мензис-Гоу А., Фиппс С., Ин С., Вангу А., Людвиг М.С. и др. (2003a) Лечение анти-IL-5 снижает отложение белков ЕСМ в субэпителиальной базальной мембране бронхов у больных с легкой атопической астмой. J Clin Invest 112: 1029–1036 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Flood-Page P., Свенсон К., Файферман И., Мэтьюз Дж., Уильямс М., Бранник Л. и др. (2007) Исследование по оценке безопасности и эффективности меполизумаба у пациентов с умеренной персистирующей астмой. Am J Respir Crit Care Med 176. Am J Respir Crit Care Med 167: 199–204 [PubMed] [Google Scholar]
- Fujimura M., Або М., Огава Х., Ниси К., Кибе Ю., Хиросе Т. и др. (2005a) Важность атопического кашля, кашлевой астмы и синобронхиального синдрома как причин хронического кашля в районе Хокурику в Японии. Респирология 10: 201–207 [PubMed] [Google Scholar]
- Fujimura M., Hara J., Myou S. (2005b) Изменение бронхиальной реактивности и чувствительности кашлевого рефлекса у пациентов с кашлевой астмой: эффект ингаляционных кортикостероидов. Кашель 1: 5. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Nishizawa Y., Nishitsuji M., Nomura S., Abo M., Ogawa H. (2005c) Предикторы типичного начала астмы при кашлевом варианте астмы. J астма 42: 107–111 [PubMed] [Google Scholar]
- Fujimura M., Ogawa H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности. Грудная клетка 58: 737 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Nishizawa Y., Nishi K. (2003) Сравнение атопического кашля с кашлевым вариантом астмы: является ли атопический кашель предшественником астма ?.Грудная клетка 58: 14–18 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Fujimura M., Ogawa H., Yasui M., Matsuda T. (2000) Эозинофильный трахеобронхит и гиперчувствительность дыхательных путей при хроническом непродуктивном кашле. Clin Exp Allergy 30: 41–47 [PubMed] [Google Scholar]
- Fujimura M., Ohkura N., Abo M., Furusho S., Waseda Y., Ichikawa Y., et al. (2008) Уровни оксида азота в выдыхаемом воздухе у пациентов с атопическим кашлем и кашлевой астмой. Респирология 13: 359–364 [PubMed] [Google Scholar]
- Fujimura M., Сакамото С., Мацуда Т. (1992) Бронходилататорно-резистивный кашель у пациентов с атопией: бронхиальная обратимость и гиперреактивность. Intern Med 31: 447–452 [PubMed] [Google Scholar]
- Fujimura M., Songur N., Kamio Y., Matsuda T. (1997) Обнаружение эозинофилов в мокроте, индуцированной гипертоническим солевым раствором, у пациентов с хроническим непродуктивным кашлем. J астма 34: 119–126 [PubMed] [Google Scholar]
- Гибсон П.Г., Долович Дж., Денбург Дж., Рамсдейл Э. Х., Харгрив Ф. Э. (1989) Хронический кашель: эозинофильный бронхит без астмы.Ланцет 1: 1346–1348 [PubMed] [Google Scholar]
- Гибсон П.Г., Фудзимура М., Ниими А. (2002) Эозинофильный бронхит: клинические проявления и последствия для лечения. Грудная клетка 57: 178–182 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Gibson PG, Zlatic K., Scott J., Sewell W., Woolley K., Saltos N. (1998) Хронический кашель напоминает астму с ИЛ -5 и экспрессия гена колониестимулирующего фактора гранулоцитов-макрофагов в бронхоальвеолярных клетках. J Allergy Clin Immunol 101: 320–326 [PubMed] [Google Scholar]
- Гулд Х.J., Sutton B.J. (2008) IgE при аллергии и астме сегодня. Нат Рев Иммунол 8: 205–217 [PubMed] [Google Scholar]
- Grayston J.T. (1992) Инфекции, вызванные штаммом Chlamydia pneumoniae twar. Clin Infect Dis 15: 757–761 [PubMed] [Google Scholar]
- Grunig G., Warnock M., Wakil A.E., Venkayya R., Brombacher F., Rennick D.M. и др. (1998) Потребность в IL-13 независимо от IL-4 при экспериментальной астме. Наука 282: 2261–2263 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Брайтлинг С.Е., Харгадон Б., Гупта С., Монтейро В., Соуза А. и др. (2009) Меполизумаб и обострения рефрактерной эозинофильной астмы. N Engl J Med 360: 973–984 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Haldar P., Pavord I.D., Shaw D.E., Berry M.A., Thomas M., Brightling C.E., et al. (2008) Кластерный анализ и клинические фенотипы астмы. Am J Respir Crit Care Med 178: 218–224 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Hamilton L.M., Torres-Lozano C., Puddicombe S.М., Рихтер А., Кимбер И., Дирман Р. Дж. И др. (2003) Роль рецептора эпидермального фактора роста в поддержании нейтрофильного воспаления при тяжелой астме. Clin Exp Allergy 33: 233–240 [PubMed] [Google Scholar]
- Hammerschlag M.R. (2000) Chlamydia pneumoniae и легкие. Eur Respir J 16: 1001–1007 [PubMed] [Google Scholar]
- Хоффштейн В. (1994) Постоянный кашель у некурящих. Может Респир J 1: 40–47 [Google Scholar]
- Холгейт С.Т., Чучалин А.Г., Хеберт Дж., Лотвалл Дж., Перссон Г. Б., Чунг К. Ф. и др. (2004) Эффективность и безопасность рекомбинантного антитела против иммуноглобулина Е (омализумаб) при тяжелой аллергической астме. Clin Exp Allergy 34: 632–638 [PubMed] [Google Scholar]
- Холгейт С.Т., Полоса Р. (2006) Механизмы, диагностика и лечение тяжелой астмы у взрослых. Ланцет 368: 780–793 [PubMed] [Google Scholar]
- Ховарт П.Х., Бабу К.С., Аршад Х.С., Лау Л.С., Бакли М.Г., Макконнелл В. и др. (2005) Фактор некроза опухоли (TNF {альфа) как новая терапевтическая мишень при симптоматической кортикостероидной астме.Грудная клетка 60: 1012–1018, Epub, 15 сентября 2005 г. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Humbert M., Beasley R., Ayres J., Slavin R., Hebert J., Bousquet J., et al. (2005) Преимущества омализумаба в качестве дополнительной терапии у пациентов с тяжелой персистирующей астмой, которые недостаточно контролируются, несмотря на лучшую доступную терапию (лечение GINA 2002, шаг 4): Innovate. Аллергия 60: 309–316 [PubMed] [Google Scholar]
- Humbert M., De Blay F., Garcia G., Prud’homme A., Leroyer C., Magnan A., и другие. (2009) Маситиниб, ингибитор тирозинкиназы рецептора c-kit / PDGF, улучшает контроль заболевания у тяжелых кортикостероидозависимых астматиков. Аллергия 64: 1194–1201 [PubMed] [Google Scholar]
- Инграм Дж. Л., Боннер Дж. С. (2006) Тирозинкиназы рецепторов EGF и PDGF как терапевтические мишени при хронических заболеваниях легких. Курр Мол Мед 6: 409–421 [PubMed] [Google Scholar]
- Ирвин Р.С., Бауманн М.Х., Болсер Д.К., Буле Л.П., Браман С.С., Брайтлинг С.Э. и др. (2006) Диагностика и лечение кашля. Краткое изложение: клинические рекомендации ACCP, основанные на фактических данных.Грудь 129: 1S – 23S [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Ирвин Р.С., Коррао В.М., Праттер М.Р. (1981) Хронический стойкий кашель у взрослых: спектр и частота причин и успешный результат специфической терапии. Am Rev Respir Dis 123: 413–417 [PubMed] [Google Scholar]
- Ирвин Р.С., Керли Ф.Дж., French C.L. (1990) Хронический кашель. Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Am Rev Respir Dis 141: 640–647 [PubMed] [Google Scholar]
- Ирвин Р.S., French C.T., Smyrnios N.A., Curley F.J. (1997) Интерпретация положительных результатов ингаляционной пробы метахолина и 1 недели использования ингаляционных бронходилататоров при диагностике и лечении кашлевой астмы. Arch Intern Med 157: 1981–1987 [PubMed] [Google Scholar]
- Jatakanon A., Uasuf C., Maziak W., Lim S., Chung K.F., Barnes P.J. (1999) Нейтрофильное воспаление при тяжелой персистирующей астме. Am J Respir Crit Care Med 160: 1532–1539 [PubMed] [Google Scholar]
- Джонсон Д., Осборн Л.М. (1991) Кашлевой вариант астмы: обзор клинической литературы. J астма 28: 85–90 [PubMed] [Google Scholar]
- Kanazawa H., Eguchi Y., Nomura N., Yoshikawa J. (2005) Анализ уровней фактора роста эндотелия сосудов в индуцированных образцах мокроты пациентов с кашлевой астмой. Энн Аллергия Астма Иммунол 95: 266–271 [PubMed] [Google Scholar]
- Kastelik J.A. (2008) Терапия кашлевой астмы. Многопрофильная респираторная медицина 3: 223–227 [Google Scholar]
- Kastelik J.А., Азиз И., Оху Дж. К., Томпсон Р. Х., Редингтон А. Э., Морис А. Х. (2005) Исследование и лечение хронического кашля с использованием вероятностного алгоритма. Eur Respir J 25: 235–243 [PubMed] [Google Scholar]
- Кита Т., Фудзимура М., Огава Х., Накацуми Ю., Номура С., Ишиура Ю. и др. (2010) Противокашлевые эффекты антагониста лейкотриеновых рецепторов монтелукаста у пациентов с кашлевой астмой и атопическим кашлем. Аллергол Инт 59: 185–192 [PubMed] [Google Scholar]
- Кон О.М., Кей А. (1999) Стратегии борьбы с Т-клетками при астме. Воспаление Res 48: 516–523 [PubMed] [Google Scholar]
- Кришнамурти Н., Орисс Т. Б., Паглиа М., Фей М., Ярлагадда М., Ванхасебрук Б. и др. (2008) Активация c-kit в дендритных клетках регулирует дифференцировку Т-хелперных клеток и аллергическую астму. Нат Мед 14: 565–573 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Leckie M.J., Ten Brinke A., Khan J., Diamant Z., O’connor B.J., Walls C.M., et al. (2000) Эффекты моноклональных антител, блокирующих интерлейкин-5, на эозинофилы, гиперчувствительность дыхательных путей и позднюю астматическую реакцию.Ланцет 356: 2144–2148 [PubMed] [Google Scholar]
- Leff J.A., Busse W.W., Pearlman D., Bronsky E.A., Kemp J., Hendeles L., et al. (1998) Монтелукаст, антагонист лейкотриеновых рецепторов, для лечения легкой формы астмы и бронхоспазма, вызванного физической нагрузкой. N Engl J Med 339: 147–152 [PubMed] [Google Scholar]
- Мартин Р.Дж., Крафт М., Чу Х.В., Бернс Э.А., Касселл Г.Х. (2001) Связь между хронической астмой и хронической инфекцией. J Allergy Clin Immunol 107: 595–601 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Табуена Р.П., Такемура М., Уэда Т., Ямагути М. и др. (2007) Утолщение стенки дыхательных путей у пациентов с кашлевой астмой и неастматическим хроническим кашлем. Грудь 131: 1042–1049 [PubMed] [Google Scholar]
- Мацумото Х., Ниими А., Такемура М., Уэда Т., Табуена Р., Ямагути М. и др. (2006) Прогноз кашлевого варианта астмы: ретроспективный анализ. J астма 43: 131–135 [PubMed] [Google Scholar]
- Mcgarvey L., Morice A.H. (2003) Атопический кашель: мало доказательств в поддержку новой клинической сущности.Грудная клетка 58: 736–737, ответ автора 737-738. [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Mcgarvey L.P., Heaney L.G., Lawson J.T., Johnston B.T., Scally C.M., Ennis M., et al. (1998) Оценка и исходы пациентов с хроническим непродуктивным кашлем с использованием комплексного диагностического протокола. Грудная клетка 53: 738–743 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Мелло С.Дж., Ирвин Р.С., Керли Ф.Дж. (1996) Прогностические значения характера, времени и осложнений хронического кашля при диагностике его причины.Arch Intern Med 156: 997–1003 [PubMed] [Google Scholar]
- Menzies D., Holmes L., Mccumesky G., Prys-Picard C., Niven R. (2011) Сенсибилизация Aspergillus связана с ограничением воздушного потока и бронхоэктазами при тяжелой астме . Аллергия 66: 679–685 [PubMed] [Google Scholar]
- Мензис-Гоу А., Флад-Пейдж П., Сехми Р., Берман Дж., Хамид К., Робинсон Д.С. и др. (2003) Анти-IL-5 (меполизумаб) терапия вызывает задержку созревания эозинофилов в костном мозге и снижает количество предшественников эозинофилов в слизистой оболочке бронхов у больных атопической астмой.J Allergy Clin Immunol 111: 714–719 [PubMed] [Google Scholar]
- Мензис-Гоу А., Робинсон Д.С. (2002) Эозинофилы, эозинофильные цитокины (интерлейкин-5) и антиэозинофильная терапия при астме. Curr Opin Pulm Med 8: 33–38 [PubMed] [Google Scholar]
- Милгром Х., Бергер В., Наяк А., Гупта Н., Поллард С., Макалари М. и др. (2001) Лечение детской астмы антителом к иммуноглобулину Е (омализумаб). Педиатрия 108: E36. [PubMed] [Google Scholar]
- Милгром Х., Фик Р. Б., младший, Су Дж. К., Рейманн Дж. Д., Буш Р. К., Уотрус М. Л. и др. (1999) Лечение аллергической астмы моноклональными анти-IgE-антителами. Исследовательская группа по Rhumab-E25. N Engl J Med 341: 1966–1973 [PubMed] [Google Scholar]
- Миллар М.М., Макграт К.Г., Паттерсон Р. (1998) Злокачественная астма, эквивалентная кашлю: определение и отчеты о случаях. Энн Аллергия Астма Иммунол 80: 345–351 [PubMed] [Google Scholar]
- Morice A.H., Fontana G.A., Belvisi M.G., Birring S.S., Chung K.F., Dicpinigaitis P.V., et al. (2007) Рекомендации ERS по оценке кашля. Eur Respir J 29: 1256–1276 [PubMed] [Google Scholar]
- Morice A.H., Kastelik J.A. (2003) Кашель. 1: Хронический кашель у взрослых. Грудная клетка 58: 901–907 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Морис А.Х., Макгарви Л., Паворд И. (2006) Рекомендации по лечению кашля у взрослых. Грудная клетка 61 (Приложение 1): i1 – i24 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Morjaria J.B., Babu K.S., Holgate S.T., Polosa R.(2006) Фактор некроза опухоли альфа как терапевтическая мишень при астме. Открытие лекарств сегодня: терапевтические стратегии 3: 309–316 [Google Scholar]
- Morjaria J.B., Chauhan A.J., Babu K.S., Polosa R., Davies D.E., Holgate S.T. (2008) Роль слитого белка растворимого рецептора TNF-α (этанерцепта) при резистентной к кортикостероидам астме: двойное слепое рандомизированное плацебо-контролируемое исследование. Грудная клетка 63: 584–591 [PubMed] [Google Scholar]
- Morjaria J.B., Gnanakumaran G., Babu K.S. (2007) Anti-IgE при аллергической астме и рините: обновление.Мнение эксперта Biol Ther 7: 1739–1747 [PubMed] [Google Scholar]
- Morjaria J.B., Polosa R. (2010) Рекомендации по оптимальному ведению тяжелой рефрактерной астмы. J Астма Аллергия 3: 43–56 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Наир П., Пиццичини М.М., Кьярсгаард М., Инман М.Д., Эфтимиадис А., Пиццичини Э. и др. (2009) Меполизумаб для лечения преднизонозависимой астмы с эозинофилией мокроты. N Engl J Med 360: 985–993 [PubMed] [Google Scholar]
- NICE. (2007) Омализумаб при стойкой аллергической астме.NICE Руководство по оценке технологий 133. NICE: Лондон [Google Scholar]
- Niimi A., Amitani R., Suzuki K., Tanaka E., Murayama T., Kuze F. (1998) Эозинофильное воспаление при кашлевом варианте астмы. Eur Respir J 11: 1064–1069 [PubMed] [Google Scholar]
- Ниими А., Мацумото Х., Минакучи М., Китаичи М., Амитани Р. (2000) Ремоделирование дыхательных путей при кашлевой астме. Ланцет 356: 564–565 [PubMed] [Google Scholar]
- Огава Х., Фудзимура М., Тофуку Ю. (2004) Лечение атопического кашля, вызванного антигеном базидиомицетов, низкими дозами итраконазола.Легкое 182: 279–284 [PubMed] [Google Scholar]
- Паломбини Б.С., Вилланова К.А., Араухо Э., Гастал О.Л., Альт Д.К., Штольц Д.П. и др. (1999) Патогенная триада при хроническом кашле: астма, синдром постназального подтекания и гастроэзофагеальная рефлюксная болезнь. Грудь 116: 279–284 [PubMed] [Google Scholar]
- Park C.S., Lee S.M., Chung S.W., Uh S., Kim H.T., Kim Y.H. (1994) Интерлейкин-2 и растворимый рецептор интерлейкина-2 в жидкости бронхоальвеолярного лаважа пациентов с бронхиальной астмой. Грудь 106: 400–406 [PubMed] [Google Scholar]
- Питерс С.П., Кунсельман С.Дж., Ицитович Н., Мур В.С., Паскуаль Р., Амередес Б.Т. и др. (2011) Повышающая терапия тиотропия бромидом для взрослых с неконтролируемой астмой. New Engl J Med 363: 1715–1726 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Poe R.H., Harder R.V., Israel R.H., Kallay M.C. (1989) Хронический непрекращающийся кашель. Опыт диагностики и результатов с использованием протокола анатомической диагностики. Грудь 95: 723–728 [PubMed] [Google Scholar]
- Polosa R., Benfatto G.T. (2009) Ведение пациентов с тяжелой хронической астмой: примите вызов.Eur J Intern Med 20: 114–124 [PubMed] [Google Scholar]
- Polosa R., Morjaria J. (2008) Иммуномодулирующие и биологические методы лечения тяжелой рефрактерной астмы. Респир Мед 102: 1499–1510 [PubMed] [Google Scholar]
- Преста Л., Шилдс Р., О’Коннелл Л., Лар С., Портер Дж., Горман К. и др. (1994) Сайт связывания иммуноглобулина Е человека для его рецептора с высоким сродством. J Biol Chem 269: 26368–26373 [PubMed] [Google Scholar]
- Reber L., Da Silva C.A., Frossard N. (2006) Фактор стволовых клеток и его рецептор c-kit как мишени для воспалительных заболеваний.Eur J Pharmacol 533: 327–340 [PubMed] [Google Scholar]
- Робертс Г., Ньюсом Д., Гомес К., Раффлз А., Саглани С., Бегент Дж. И др. (2003) Внутривенное болюсное введение сальбутамола в сравнении с инфузией эуфиллина у детей с тяжелой астмой: рандомизированное контролируемое исследование. Грудная клетка 58: 306–310 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Робинсон Д.С., Бентли А.М., Хартнелл А., Кей А.Б., Дарем С.Р. (1993) Активированные Т-хелперы памяти в жидкости бронхоальвеолярного лаважа пациентов с атопической астмой: связь с симптомами астмы, функцией легких и реактивностью бронхов.Грудная клетка 48: 26–32 [Бесплатная статья PMC] [PubMed] [Google Scholar]
- Rolling C., Treton D., Pellegrini S., Galanaud P., Richard Y. (1996) Рецепторы IL4 и IL13 имеют общую гамма-цепь C и активируют белки Stat6, Stat3 и Stat5 в нормальных В-клетках человека. FEBS Lett 393: 53–56 [PubMed] [Google Scholar]
- Ротенберг М.Э., Хоган С.П. (2006) Эозинофил. Анну Рев Иммунол 24: 147–174 [PubMed] [Google Scholar]
- Sanderson C.J. (1992) Интерлейкин-5, эозинофилы и болезни.Кровь 79: 3101–3109 [PubMed] [Google Scholar]
- Сильверман Р.А., Осборн Х., Рунге Дж., Галлахер Э. Дж., Чан У., Фельдман Дж. И др. (2002) Внутривенное введение сульфата магния в лечении острой тяжелой астмы: многоцентровое рандомизированное контролируемое исследование. Грудь 122: 489–497 [PubMed] [Google Scholar]
- Саймон Д., Браатен Л.Р., Саймон Х.У. (2004) Эозинофилы и атопический дерматит. Аллергия 59: 561–570 [PubMed] [Google Scholar]
- Смирниос Н.А., Ирвин Р.С., Керли Ф.Дж. (1995) Хронический кашель с чрезмерным выделением мокроты в анамнезе.Спектр и частота причин, ключевые компоненты диагностической оценки и исход конкретной терапии. Грудь 108: 991–997 [PubMed] [Google Scholar]
- Soler M., Matz J., Townley R., Buhl R., O’brien J., Fox H., et al. (2001) Анти-IgE-антитело омализумаб снижает частоту обострений и потребность в стероидах у аллергических астматиков. Eur Respir J 18: 254–261 [PubMed] [Google Scholar]
- Стивенс Р.С. (2003) Клеточная парадигма патогенеза хламидий. Тенденции Microbiol 11: 44–51 [PubMed] [Google Scholar]
- Тен Бринке А., Ван Диссель Дж. Т., Стерк П. Дж., Звиндерман А. Х., Рабе К. Ф., Бел Э. Х. (2001) Устойчивое ограничение воздушного потока при неатопической астме у взрослых связано с серологическими доказательствами инфекции Chlamydia pneumoniae . J Allergy Clin Immunol 107: 449–454 [PubMed] [Google Scholar]
- Тонелли М., Зингони М., Баччи Э., Денте Ф.Л., Ди Франко А., Джаннини Д. и др. (2003) Кратковременный эффект от добавления антагонистов лейкотриеновых рецепторов к текущей терапии тяжелых астматиков.Пульм Фармакол Тер 16: 237–240 [PubMed] [Google Scholar]
- U-BIOPRED (2008) Объективные биомаркеры для прогнозирования результатов респираторных заболеваний, http://www.fp7-consulting.be/en/ubiopred/
- Vatrella A ., Ponticiello A., Pelaia G., Parrella R., Cazzola M. (2005) Бронходилатирующие эффекты сальметерола, теофиллина и их комбинации у пациентов с умеренной и тяжелой астмой. Пульм Фармакол Тер 18: 89–92 [PubMed] [Google Scholar]
- Виньола А.М., Умберт М., Буске Дж., Буле Л.П., Хеджекок С., Блог М. и др. (2004) Эффективность и переносимость антииммуноглобулиновой терапии омализумабом у пациентов с сопутствующей аллергической астмой и стойким аллергическим ринитом: СОЛАР. Аллергия 59: 709–717 [PubMed] [Google Scholar]
- Фон Герцен Л.С. (2002) Роль персистирующей инфекции в контроле и тяжести астмы: фокус на Chlamydia pneumoniae. Eur Respir J 19: 546–556 [PubMed] [Google Scholar]
- Уорк П.А., Джонстон С.Л., Симпсон Дж. Л., Хенсли М.Дж., Гибсон П.Г. (2002) Chlamydia pneumoniae иммуноглобулин А реактивация и воспаление дыхательных путей при острой астме. Eur Respir J 20: 834–840 [PubMed] [Google Scholar]
- Webb D.C., Mckenzie A.N., Koskinen A.M., Yang M., Mattes J., Foster P.S. (2000) Интегрированные сигналы между IL-13, IL-4 и IL-5 регулируют гиперреактивность дыхательных путей. J Immunol 165: 108–113 [PubMed] [Google Scholar]
- Венцель С., Фахи Дж. В., Ирвин К.Г., Петерс С.П., Спектор С., Сефлер С.Дж. (2000) Материалы семинара ATS по рефрактерной астме: текущее понимание, рекомендации и вопросы без ответа.Am J Respir Crit Care Med 162: 2341–2351 [PubMed] [Google Scholar]
- Венцель С.Э., Барнс П.Дж., Бликер Е.Р., Буске Дж., Бусс В., Дален С.Э. и др. (2009) Рандомизированное двойное слепое плацебо-контролируемое исследование блокады фактора некроза опухоли альфа при тяжелой персистирующей астме. Am J Respir Crit Care Med 179: 549–558 [PubMed] [Google Scholar]
- Венцель С.Э., Шварц Л. (1999) Доказательства того, что тяжелую астму патологически можно разделить на два воспалительных подтипа с различными физиологическими и клиническими характеристиками.Am J Respir Crit Care Med 160: 1001–1008 [PubMed] [Google Scholar]
- Виллс-Карп М., Луимбази Дж., Сюй X., Скофилд Б., Небен Т.Ю., Карп К.Л. и др. (1998) Интерлейкин-13: центральный медиатор аллергической астмы. Наука 282: 2258–2261 [PubMed] [Google Scholar]
Диагноз астмы, клинический синдром
Врачи сходятся во мнении, что для астмы характерны хроничность и лабильность заболевания. Бывают периоды затрудненного дыхания, шумного дыхания, стеснения в груди и кашля, при которых может выделяться вязкая мокрота.Симптомы часто ухудшаются очень рано утром. Часто сообщается о провоцирующих факторах симптомов: сигаретный дым, парфюмерия, холодный воздух, упражнения, смех, различные «аллергены», инфекции или профессиональные агенты. Периоды ремиссии могут наступить при смене места жительства, климата или отсутствия работы. При клиническом осмотре результаты могут быть вполне нормальными; или может быть легкое тахипноэ, раздражающий кашель и полифонические хрипы при аускультации; или в крайнем случае пациент может быть вялым и холодным, с затрудненным движением грудной клетки, чрезмерно раздутой грудной клеткой и беззвучной аускультацией.Таким образом, астма является клиническим диагнозом, основанным на вышеизложенном, который влечет за собой тщательную клиническую практику исключения ошибочных диагнозов (особенно у маленьких детей вирусный бронхиолит1) и устранения отягчающих факторов. Функциональное тестирование легких в настоящее время является рекомендуемой подтверждающей диагностикой с целью продемонстрировать обструкцию воздушного потока и продемонстрировать ее обратимость; спирометрия, благодаря ее высокой воспроизводимости и четко определенным нормальным диапазонам, является золотым стандартом для обоих.
Американское и британское руководства по лечению астмы предоставляют бесценные практические отчеты о диагностических подходах у взрослых и детей, а также о последовательных терапевтических подходах, которым необходимо следовать в дальнейшем.2, 3
Тем не менее, здесь есть загадка, которая заключается в том, чтобы исключить окончательную бронхиальную патологию в рекомендуемый диагностический процесс. Это примечательно, если учесть, что некоторые случаи ошибочного диагноза могут быть клинически обманчивыми, но особенно если учесть, что астма обычно считается гетерогенным клиническим синдромом (случаи возникают, ведут себя и реагируют на лечение совершенно по-разному4, 5). Более того, патология бронхов теперь готова для проведения различного молекулярного, а также морфологического анализа.Фактически, признание неоднородности астмы (в контексте современной основной диагностической практики) является молчаливым, потому что в клинической практике нет систематического применения в клинической практике окончательной патологической характеристики отдельных случаев астмы.2, 3 Следовательно, врачи формально не знают, как они Пациенты с астмой различаются по частоте и частоте, поэтому дифференцированного подхода к лечению не существует. Все случаи проходят через каскад рекомендуемых терапевтических подходов — некоторые пациенты реагируют безопасно и быстро; некоторые достигают приемлемого клинического статуса в зависимости от лекарств; другие борются, несмотря на то же лечение; и другие, оказавшиеся устойчивыми к лечению.5 Такой подход приводит к частым визитам в клинику и к тому, что многие виды лечения не приносят удовлетворительной пользы для пациента. Неизбежно это очень дорого и разочаровывает значительную часть пациентов с астмой, у которых остаются проблемы после многократных испытаний лечения.
В клинической медицине в целом патологическое исследование ткани пораженного органа признано ключом к надежному диагнозу, что делает фактическое отсутствие патологии бронхов в стандартной клинической практике астмы ( темп усилий, таких как программа исследований тяжелой астмы в США, 6 и серии случаев в других центрах7–9) тем более озадачивают.В обычной практике лечения астмы мы нерегулярно собираем данные о «фенотипе» астмы наших пациентов — а затем часто с помощью косвенных методов (например, подсчета эозинофилов в мокроте) в качестве суррогатов для окончательной бронхиальной патологии. 40 лет назад Браун настаивал на очевидном избытке эозинофилов в мокроте, чтобы характеризовать каждый случай «аллергической астмы», и когда он продемонстрировал эффективность ингаляционных стероидов в сложных случаях11. Неужели мы, сегодняшние врачи-респираторы, не переусердствовали с «комкованием» и не слишком- точность в нашей практической диагностике астмы — почему, когда мы признаем, что астма является гетерогенным клиническим синдромом, мы не рассматриваем регулярно бронхиальную патологию? Наш подход, безусловно, отличается от того, что другие врачи-специалисты используют биопсию для точных морфологических и молекулярных исследований.Нефрологи проводят длительные и систематические биопсии почек для выявления характерных иммунных / воспалительных заболеваний и разработки различных методов лечения таких широких заболеваний, как гломерулонефрит. Гастроэнтерологам требуется колоноскопия с биопсией для диагностики воспалительного заболевания кишечника у детей и взрослых.
Фиброоптическая бронхоскопия — неудобная процедура. Но его можно безопасно и быстро выполнить при астме при наличии надлежащего опыта и протоколов как для диагностических, так и для терапевтических целей.6 Это может потребовать общей анестезии у ребенка, но среди серий случаев бронхиальной патологии видное место занимают случаи детской астмы. 7–9 Бронхоскопическая диагностика является неотъемлемой частью других областей респираторной медицины, включая очень больных пациентов (например, микробная диагностика при пневмониях). у субъектов с ослабленным иммунитетом) .12 Первостепенное значение имеет ряд случаев спорадической бронхиальной патологии при астме, которые уже указывают на ценное открытие разнообразных и непредсказуемых изменений при тяжелой астме, включая неразрешенное эозинофильное воспаление, воспаление разных подтипов, отсутствие воспаления, микробную инфекцию — помимо выявления сомнительных диагнозов, таких как инородное тело или доброкачественная опухоль.7–9, 13 Не пора ли нам пересмотреть роль бронхиальной патологии в практике лечения астмы в целом? Не должны ли мы, по крайней мере, получить биопсию бронхов, когда наши клинические методы оставляют нас под сомнением, а прогресс наших пациентов, согласующихся с лечением, замедляется?
В настоящее время отсутствие у нас систематического подхода к характеристике наших случаев астмы по прямой патологии ограничивает нас довольно неточным представлением о гетерогенности астмы.5 Мы признаем, что многие пациенты с астмой также страдают экземой и ринитом, проявляют аллергию на обычные антигены, и что их астма обычно чувствительна к ингаляционным кортикостероидам.Нам известно, что иммунные механизмы Т-хелпера 2 вызывают бронхит, включая выраженную инфильтрацию / активацию эозинофилов, гипертрофию и гиперсекрецию слизистых желез, а также гиперреактивность гладких мышц (с ремоделированием дыхательных путей) .14 Мы также видим, что многие другие случаи астмы не вписываются в эту «аллергическую» картину — мы рассматриваем их как «разные» и разнородные сами по себе. У меньшинства есть ясная причина (например, профессиональный изоцианат). Но большинство из них имеют неясную природу: астма без атопии, астма с чувствительностью к аспирину, астма более позднего происхождения у женщин с ожирением, астма с поздним началом у курильщиков, астма с воспалением, связанным с нейтрофилами, или астма с небольшим воспалением бронхов; существует клиническое впечатление менее надежного ответа на ингаляционные кортикостероиды.5 У нас еще меньше информации о том, как патология бронхов меняется со временем у любого конкретного пациента с астмой в результате различного воздействия через вдыхание вредных частиц, газов или микробов.
Более того, текущее положение случайных и фрагментарных данных о бронхиальной патологии в популяциях пациентов с астмой и между ними также резко расходится с прогрессом, достигнутым в фундаментальных исследованиях астмы. Недостаток клинической бронхиальной патологии ограничивает возможности достижений фундаментальных исследований по определению и характеристике неоднородности астмы — и, таким образом, замедляет прогресс в направлении эффективных методов лечения астмы в целом.5 Этот дефицит явно противоречит современной трансляционной медицине, которая подчеркивает необходимость объединения фундаментальной и клинической науки. Фундаментальные исследования астмы впечатляюще продвинулись со времени работы доктора Морроу Брауна 11, темпы их развития возрастают с развитием методологий. Мощные полногеномные исследования больших групп пациентов подтверждают гетерогенность астмы и теперь определяют основные локусы, в которых генетические варианты способствуют развитию астмы (подчеркивая полигенные действия в локусах, связанных с эпителиальными и иммунными функциями).15 Более реалистичные модели астмы изучаются в клеточных и молекулярных деталях16, а биопсия бронхов в клинических исследованиях позволила провести протеомный анализ и морфометрический анализ ремоделирования астматического воспаления и хронической обструктивной болезни легких.17, 18 Следовательно, появляются более подробные описания молекулярные элементы, лежащие в основе иммунных / воспалительных явлений и дисфункции эпителия при астме.19 Таким образом, сейчас настоятельно необходимо применить анализ этих элементов в бронхиальной ткани пациентов с астмой в клинической практике, чтобы правильно понять механизмы, характер и клиническую эпидемиологию гетерогенное астматическое расстройство.Существует также нереализованный потенциал применения таких методологий, как эпигенетика, которая может определять паттерны активации и молчания генов, к бронхиальной ткани пациентов с астмой, так что очевидно несопоставимые функции могут быть удовлетворительно поняты как биологические сети.20
Конечно, это действительно так. время соответствовать нашему признанию того, что астма неоднородна, путем принятия бронхиальной патологии с точными морфологическими и молекулярными характеристиками (а не суррогатами) в нашу основную практику лечения астмы.Это немедленно проинформирует наше руководство о больных астмой, которые борются с ней. Это изменит понимание неоднородности астмы на практике как важный шаг на пути к разработке целевых методов лечения.
Подробная информация о протоколе должна быть рассмотрена в другом месте2, 3, но этот автор видит два основных альтернативных клинических момента времени, в которые следует ввести регулярную биопсию бронхов в практику лечения астмы — либо на стыке шага 1 / шага 2, либо на стыке шага 2 / шага. 3 Британских руководящих принципов.3 Второй вариант можно рассматривать как более прагматичное время для проведения биопсии, представляющее собой момент, когда пациенты, соблюдающие режим лечения, по-прежнему обеспокоены астматическими симптомами после тщательного испытания ингаляционных стероидов в умеренных дозах (до 400 или 800 мкг эквивалента беклометазона в день в дети и взрослые соответственно) и до эскалации лечения (шаг 3) по незнанию.
Это утверждение не отрицает, что клинические навыки должны оставаться отправной точкой и краеугольным камнем диагностики астмы или что утвержденные вопросники по симптомам и надежное функциональное тестирование легких должны оставаться важными компонентами процесса диагностики и мониторинга.Утверждение просто состоит в том, что теперь мы можем значительно улучшить нашу диагностику и тем самым заложить основу для будущих достижений в лечении гетерогенной астмы.
Астма: синдром, состоящий из разнородных заболеваний
https://doi.org/10.1016/S1081-1206(10)60826-5Получить права и содержаниеЦель
Пересмотреть концепцию, согласно которой астма включает в себя отдельные гетерогенные воспалительные расстройства, характеризующиеся пациенты, демонстрирующие разные фенотипы с различными генетическими компонентами, экологическими причинами и иммунопатологическими признаками.
Источники данных
Базы данных Ovid MEDLINE и PubMed с 1950 года по настоящее время были подвергнуты поиску соответствующих статей и ссылок, касающихся неоднородности астмы.
Выбор исследования
Для этого обзора были использованы статьи, описывающие различные фенотипы астмы.
Результаты
Астма вряд ли будет отдельным заболеванием, а скорее серией сложных, частично совпадающих отдельных заболеваний или фенотипов, каждый из которых определяется своим уникальным взаимодействием между генетическими факторами и факторами окружающей среды.Эти состояния включают синдромы, характеризующиеся обостренными аллергенами, неаллергическими и аспириновыми факторами, а также синдромы, которые лучше всего различаются по их патологическим проявлениям (эозинофильный, нейтрофильный, малогранулоцитарный), ответ на терапию (резистентность к кортикостероидам) и естественное течение (склонность к ремоделированию). ). Дополнительные фенотипы почти наверняка будут идентифицированы по мере развития генетики и других методов профилирования и будут сопровождаться доступностью четких биомаркеров для их различения.
Выводы
Ответы на лекарства от астмы значительно различаются среди пациентов, вероятно, отражая, по крайней мере частично, различную чувствительность различных фенотипов астмы. Выбор наилучшего курса лечения для отдельных пациентов будет облегчен за счет четкого определения различных фенотипов. Врачам необходимо учитывать это при принятии решений о корректировке лечения для улучшения контроля над астмой.
Рекомендуемые статьиЦитирующие статьи (0)
Полный текстCopyright © 2008 Американский колледж аллергии, астмы и иммунологии.Опубликовано Elsevier Inc. Все права защищены.
Рекомендуемые статьи
Ссылки на статьи
Триада Астма | Michigan Medicine
Астма триады — это клинический синдром, определяемый тремя состояниями, которые существуют вместе:
- Астма
- Чувствительность к аспирину
- Полипы носа
Триада астмы также известна как триада Самтера или респираторное заболевание, связанное с аспирином.
Астма триады обычно начинается у пациентов старше 20 лет, но может возникать и у более молодых людей или даже у детей.В клиниках для взрослых в Мичиганском университете большинство пациентов сообщают о появлении симптомов в возрасте от 20 до 40 лет.
Мы разработали передовые программы лечения пациентов с этим заболеванием, включая послеоперационную десенсибилизацию аспирином — , которая обычно не доступна в большинстве медицинских учреждений. Десенсибилизация аспирином обеспечивает значительное облегчение и гораздо лучшие результаты примерно у 70% пациентов с триадной астмой.
Почему важен правильный диагноз
Пациентам необходимо знать, есть ли у них триадная астма, потому что у них могут быть очень внезапные и очень тяжелые приступы астмы, которые могут быть спровоцированы пищей или лекарствами.Если у вас триадная астма, вы должны знать о своей чувствительности к лекарствам и некоторым продуктам питания и должны принимать меры, чтобы избежать их.
Астму триады бывает сложно диагностировать, потому что не у каждого пациента есть все три состояния одновременно.
Оценка
Мы являемся экспертами в диагностике и лечении триадной астмы. Мы начинаем с сбора хорошей истории болезни, просмотра любых записей, присланных нам вашим врачом, и, возможно, заказа компьютерной томографии (компьютерной томографии), чтобы внимательно осмотреть полость пазухи и определить точную степень заболевания носовых пазух или полипов.
Компьютерная томография занимает около 10-20 минут и обычно дается пациентам довольно легко. Обычно при компьютерной томографии пазух не вводится контрастный краситель или инъекции. Если у вас клаустрофобия или тяжелый артрит шеи, сообщите об этом своему врачу и радиологу.
Лечение
Перед тем, как рекомендовать операцию, мы можем назначить солевые спреи, ежедневные орошения соленой водой, назальные стероидные спреи для носа или короткий курс пероральных стероидов.
Доктор Джеффри Террелл создал короткое видео о триаде астмы и носовых полипов: основной подход отоларинголога, который было бы очень полезно просмотреть перед встречей с одним из наших ринологов.
С учетом операции
Наличие носовых полипов само по себе не обязательно является показанием к хирургическому вмешательству, потому что пациенты с этим заболеванием почти всегда будут иметь носовые полипы в той или иной степени. Решение о проведении операции зависит от ваших симптомов и их влияния на ваш образ жизни. Вот несколько общих рекомендаций:
- Насколько вас беспокоит заложенность носа и ее симптомы (например, храп, потеря сна, постоянное дыхание ртом)?
- Насколько часты и тяжелы ваш синусит? Инфекции носовых пазух у пациентов с триадной астмой часто трудно вылечить, потому что носовые пазухи плохо дренируют и инфицированные полости быстро инфицируются повторно после прекращения приема антибиотиков.
- Проблемы с носовыми пазухами и синусит усугубляют астму? Пациенты, которым требуется значительное количество пероральных стероидных препаратов, могут снизить потребность в лекарствах от астмы после успешной операции.
- Вы испытываете хронические головные боли или другие признаки возможных осложнений из-за полипов и заболеваний носовых пазух? Ваш специалист Мичиганского синусового центра квалифицирован, чтобы оценить эти более необычные причины для операции.
Зачем приезжать в Мичиган для лечения триадной астмы?
- Ежегодно мы лечим более 200 пациентов с этим заболеванием.
- Мы применяем междисциплинарный поэтапный подход, который учитывает вас — как человека в целом.
- Наша программа лечения десенсибилизации аспирином обеспечивает облегчение более чем 70% пациентов, участвующих в лечении.
- Если вам нужны мы для операции, доверьтесь специалистам, которые проводят более 500 операций ежегодно. А когда дело касается хирургии, важен опыт.
Инструмент для выявления симптомов астматического синдрома среди детей раннего возраста в Уганде
Нантанда, Р., Тамвин, Дж. К., Ндизи, Г. и Остергаард, М. С. Астма и пневмония у детей младше пяти лет с острыми респираторными симптомами в больнице Мулаго, Уганда: свидетельства недостаточной диагностики астмы. PLoS ONE 8 , e81562 (2013).
PubMed PubMed Central Google ученый
Ostergaard, M. S., Nantanda, R., Tumwine, J. K. & Aabenhus, R. Детская астма в странах с низким уровнем дохода: невидимый убийца? Прим.Уход Respir. J. 21 , 214–219 (2012).
PubMed PubMed Central Google ученый
Сачдев, Х. П., Махаджан, С. С. и Гарг, А. Улучшение назначения антибиотиков и бронходилататоров у детей с затрудненным дыханием: опыт городской больницы в Индии. Indian Pediatr. 38 , 827–838 (2001).
CAS PubMed Google ученый
Brozek, G. et al. Распространенность детской астмы и факторы риска в трех странах Восточной Европы — Исследование астмы в Беларуси, Украине и Польше (BUPAS): международное исследование распространенности. BMC Pulm. Med. 16 , 11 (2016).
PubMed PubMed Central Google ученый
Сачдев, Х. П., Васанти, Б., Сатьянараяна, Л. и Пури, Р. К. Простые предикторы, позволяющие отличить острую астму от ОРИ у детей: значение для усовершенствования ведения случаев в Программе контроля ОРИ. Indian Pediatr. 31 , 1251–1259 (1994).
CAS PubMed Google ученый
Risk, R. et al. Рациональное назначение лекарств в педиатрии в условиях ограниченных ресурсов. Arch. Дис. Детский 98 , 503–509 (2013).
PubMed Google ученый
Аланис, А. Дж. Устойчивость к антибиотикам: находимся ли мы в постантибиотической эре? Arch.Med. Res. 36 , 697–705 (2005).
PubMed Google ученый
Joloba, M. L., Bajaksouzian, S., Palavecino, E., Whalen, C. & Jacobs, M. R. Высокая распространенность носительства устойчивых к антибиотикам Streptococcus pneumoniae у детей в Кампале, Уганда. Int J. Antimicrob. Агенты 17 , 395–400 (2001).
CAS PubMed Google ученый
Бьяругаба, Д. К. Взгляд на устойчивость к противомикробным препаратам в развивающихся странах и ответственные факторы риска. Int J. Antimicrob. Агенты 24 , 105–110 (2004).
CAS PubMed Google ученый
Йейтс, К., Шай, К., Сотир, М., Мьюзик, С. и Хергет, К. Последствия для здоровья детей с невыявленными астматическими симптомами. Arch. Педиатр. Adolesc. Med. 157 , 540–544 (2003).
PubMed Google ученый
Oostenbrink, R. et al. Качество жизни детей дошкольного возраста с хрипами, связанное со здоровьем. Pediatr. Пульмонол. 41 , 993–1000 (2006).
CAS PubMed Google ученый
Валквист С. и Педерсен С. Фитнес, повседневная активность и состав тела у детей с впервые диагностированной, нелеченой астмой. Аллергия 64 , 1649–1655 (2009).
CAS PubMed Google ученый
Ostergaard, M. S. Детская астма: взгляд родителей — качественное интервью. Fam. Практик. 15 , 153–157 (1998).
CAS PubMed Google ученый
Saglani, S. et al. Раннее обнаружение ремоделирования стенки дыхательных путей и эозинофильного воспаления у детей дошкольного возраста. Am. J. Respir. Крит. Care Med. 176 , 858–864 (2007).
PubMed Google ученый
Мартинес, Ф. Д. На пути к профилактике астмы — действительно ли все, что имеет значение, происходит до того, как мы научимся читать? N. Engl. J. Med. 349 , 1473–1475 (2003).
CAS PubMed Google ученый
Саглани, С. и Буш, А.Астма у дошкольников: следующая проблема. Curr. Opin. Allergy Clin. Иммунол. 9 , 141–145 (2009).
PubMed PubMed Central Google ученый
А, Б. Астма: что нового, а что должно быть старым, а чего нет !! Pediatr. Респир. Крит. Care Med. 1 , 2–10 (2017).
Google ученый
Кейн, Р.С., Ранганатан, С. С. и Маккензи, С. А. Что родители хрипящих детей понимают под «хрипом»? Arch. Дис. Ребенок. 82 , 327–332 (2000).
CAS PubMed PubMed Central Google ученый
Fernandes, R.M. et al. Многозначное значение слова «свистящее дыхание»: анкетный опрос на португальском языке для родителей и медицинских работников. BMC Pediatr. 11 , 112 (2011).
PubMed PubMed Central Google ученый
Michel, G. et al. Понимание родителями хрипов и их влияния на оценки распространенности астмы. евро. Респир. J. 28 , 1124–1130 (2006).
CAS PubMed Google ученый
Shanmugam, S. et al. Родители плохо распознают хрипы у детей: перекрестное исследование. BMC Pediatr. 16 , 80 (2016).
PubMed PubMed Central Google ученый
Jackson, D. J. et al. Заболевания, связанные с риновирусом свистящего дыхания, в раннем возрасте предсказывают развитие астмы у детей из группы высокого риска. Am. J. Respir. Крит. Care Med. 178 , 667–672 (2008).
PubMed PubMed Central Google ученый
Rubner, F. J. et al. Риновирусное свистящее дыхание в раннем возрасте, аллергическая сенсибилизация и риск астмы в подростковом возрасте. J. Allergy Clin. Иммунол. 139 , 501–507 (2017).
PubMed Google ученый
Джартти, Т. и Герн, Дж. Э. Роль вирусных инфекций в развитии и обострении астмы у детей. J. Allergy Clin. Иммунол. 140 , 895–906 (2017).
PubMed PubMed Central Google ученый
Liu, L. et al. Связь между риновирусной болезнью свистящего дыхания и развитием астмы у детей: метаанализ. BMJ Open 7 , e013034 (2017).
PubMed PubMed Central Google ученый
Сингх, А. М., Мур, П. Э., Герн, Дж. Э., Леманске, Р. Ф. младший и Хартерт, Т. В. Бронхиолит к астме: обзор и призыв к исследованиям взаимодействия генов и вирусов в причинно-следственной связи астмы. Am.J. Respir. Крит. Care Med. 175 , 108–119 (2007).
CAS PubMed Google ученый
Бейгельман А. и Бахарьер Л. Б. Роль вирусного бронхиолита в раннем возрасте в возникновении астмы. Curr. Opin. Allergy Clin. Иммунол. 13 , 211–216 (2013).
CAS PubMed PubMed Central Google ученый
Lu, S. et al. Предикторы астмы после тяжелого респираторно-синцитиального вирусного (RSV) бронхиолита в раннем детстве. Pediatr. Пульмонол. 51 , 1382–1392 (2016).
PubMed PubMed Central Google ученый
ЮНИСЕФ / ВОЗ. Комплексное ведение детских болезней (ЮНИСЕФ / ВОЗ, Женева, 2008 г.).
Кейв, А. Дж. И Аткинсон, Л. Л. Астма у детей дошкольного возраста: обзор диагностических проблем. J. Am. Board Fam. Med. 27 , 538–548 (2014).
PubMed Google ученый
Шах Д. и Сачдев Х. П. Оценка алгоритма ВОЗ / ЮНИСЕФ для комплексного ведения детских болезней в возрасте от двух месяцев до пяти лет. Indian Pediatr. 36 , 767–777 (1999).
CAS PubMed Google ученый
Брозек, Г., Зейда, Дж., Фарник, М., Выпич-Слюсарска, А. и Скочински, С. Валидация простого и составного скринингового теста на детскую астму. евро. Респир. J . 48 (2016).
Джеральд, Л. Б. и др. Многоступенчатая процедура скрининга на астму для детей младшего школьного возраста. J. Asthma 39 , 29–36 (2002).
PubMed PubMed Central Google ученый
Сантос, М. К. и Кунья, А. А. Краткая анкета для выявления астмы среди детей и подростков в Рио-де-Жанейро, Бразилия. Allergologia et. иммунопатология 33 , 20–26 (2005).
PubMed Google ученый
Yadav, A. et al. Применение скринингового опросника на астму у детей с серповидноклеточной болезнью. Pediatr. Allergy Immunol. Пульмонол. 28 , 177–182 (2015).
PubMed PubMed Central Google ученый
Gowraiah, V. et al. Можно ли отличить пневмонию от хрипов у детей с тахипноэ в условиях нехватки ресурсов? Проспективное обсервационное исследование в четырех индийских больницах. Arch. Дис. Ребенок. 99 , 899–906 (2014).
PubMed Google ученый
GINA. Карманный справочник по ведению и профилактике астмы у Детей (Публикация NIH No.02-3659), (2005).
Gouws, E. et al. Улучшение использования противомикробных препаратов среди медицинских работников в учреждениях первого уровня: результаты многострановой оценки стратегии комплексного ведения детских болезней. Бык. Всемирный орган здравоохранения. 82 , 509–515 (2004).
PubMed PubMed Central Google ученый
Nantanda, R., Ostergaard, M. S., Ndeezi, G. & Tumwine, J.K. Факторы, связанные с астмой у детей младше пяти лет в больнице Мулаго, Кампала, Уганда: перекрестное исследование. BMC Pediatr. 13 , 141 (2013).
PubMed PubMed Central Google ученый
Министерство здравоохранения. Клинические рекомендации Уганды (Министерство здравоохранения, 2016 г.).
ВОЗ. Карманный справочник по госпитальной помощи детям: руководство по ведению общих заболеваний с ограниченными ресурсами (ВОЗ, Женева, 2005 г.).
O’Callaghan-Gordo, C. et al. Этиология и эпидемиология вирусной пневмонии среди госпитализированных детей в сельских районах Мозамбика: эндемичный по малярии район с высокой распространенностью вируса иммунодефицита человека. Pediatr. Заразить. Дис. J. 30 , 39–44 (2011).
PubMed Google ученый
Mavale-Manuel, S. et al. Факторы риска астмы у детей в Мапуту (Мозамбик). Аллергия 59 , 388–393 (2004).
CAS PubMed Google ученый
Винтер, М. А., Физе, Б. Х., Спаньола, М. и Анбар, Р. Д. Тяжесть астмы, безопасность ребенка и интернализация ребенка: использование техник основы рассказа для оценки значения, которое дети придают семейным событиям и событиям, связанным с конкретными заболеваниями. J. Fam. Psychol. 25 , 857–867 (2011).
PubMed PubMed Central Google ученый
Phankingthongkum, S. et al. Как тайские дети и подростки описывают симптомы астмы? Pediatr. Allergy Immunol. 13 , 119–124 (2002).
PubMed Google ученый
Куанджер П. Х., Лебовиц М. Д., Грегг И., Миллер М. Р. и Педерсен О. Ф. Пиковая скорость выдоха: выводы и рекомендации Рабочей группы Европейского респираторного общества. евро. Респир. J. 24 (доп.), 2С – 8С (1997).
CAS Google ученый
Грин, Р. Дж., Зар, Х. Дж., Джина, П. М., Мадхи, С. А. и Льюис, Х. Южноафриканское руководство по диагностике, лечению и профилактике острого вирусного бронхиолита у детей. S Afr. Med J. 100 , 322–325 (2010).
Google ученый
Martinez, F. D. et al. Астма и хрипы в первые шесть лет жизни.Группа Health Medical Associates. N. Engl. J. Med. 332 , 133–138 (1995).
CAS PubMed Google ученый
Мартинес, Ф. Д. Распознавание астмы на ранней стадии. Аллергия 54 (Дополнение 49), 24–28 (1999).
PubMed Google ученый
Buderer, N. M. Статистическая методология: I. Включение распространенности заболевания в расчет размера выборки для определения чувствительности и специфичности.


