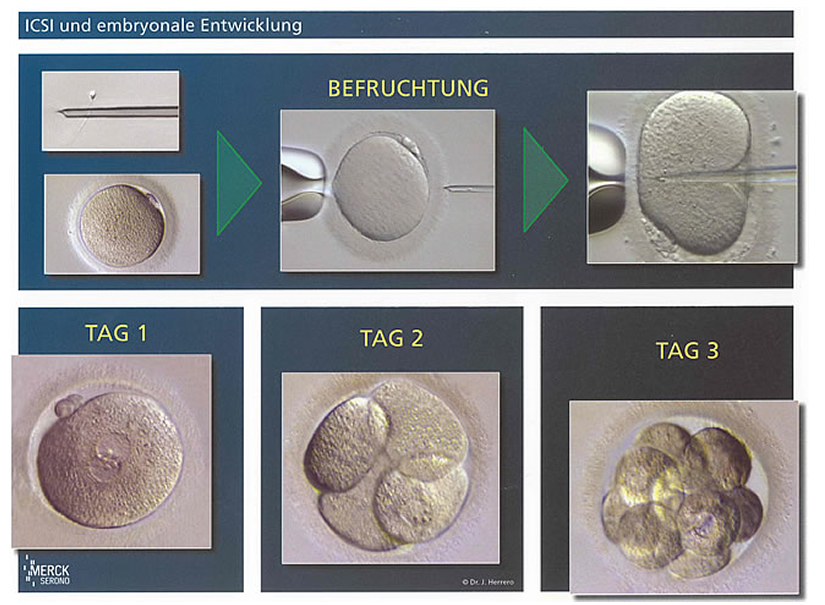
ИКСИ
Процедура ИКСИ (ICSI – intracytoplasmic sperm injection – интрацитоплазматическая инъекция сперматозоида) — это метод искусственного оплодотворения, при котором эмбриолог отбирает сперматозоид и вводит его в яйцеклетку с помощью микроинструментов.
Проведение ЭКО с ИКСИ увеличивает шансы на успешное оплодотворение и наступления беременности при любом диагнозе. На сегодняшний день методика широко применяется в ЭКО при мужском факторе бесплодия или при бесплодии пары, в которой женщина старше 35 лет. Также ИСКИ проводится при получении небольшого числа яйцеклеток (в естественном цикле, при минимальной стимуляции или при синдроме истощенных яичников), при низком качестве полученных яйцеклеток и просто по желанию для повышения выхода ЭКО.
Метод ИКСИ впервые был применен в Центре репродуктивной медицины Брюссельского свободного университета в 1992 году и в течение первых нескольких лет использования развился до современного уровня с максимально возможной эффективностью.
Показания к ИКСИ
Процедура ЭКО с ИКСИ проводится в следующих случаях:
- В сперме содержится недостаточное количество сперматозоидов (олигозооспермия), или они недостаточно активные (астенозооспермия): менее 5 миллионов прогрессивно подвижных сперматозоидов в 1 мл эякулята после обработки.
- В сперме недостаточно сперматозоидов с нормальной морфологией (тератозооспермя).
- Процедура ЭКО без ИКСИ проводилась несколько раз, но все попытки оказались неудачными.
- Сперматозоиды несут АСАТ — антиспермальные антитела (иммунное бесплодие).
- Сперматозоиды или яйцеклетки имеют другие патологии, в том числе недиагностируемые.
- Получено малое количество яйцеклеток (менее 5).
Метод ИКСИ, цена которого увеличивает итоговую стоимость ЭКО не более чем на 15%, значительно увеличивает шансы женщины забеременеть.
Как проводится ЭКО с ИКСИ?
ИКСИ проводится эмбриологом в лаборатории при помощи микроскопа, дающего увеличение в несколько сотен раз. Для операции врач использует микроманипуляторы с закрепленными на них специальными инструментами: микроиглой (для «поимки» и инъекции сперматозоида) и микроприсоской (для удержания яйцеклетки).
Эмбриолог изучает под микроскопом сперматозоиды, отбирает (по одному) наиболее подвижные из них и не имеющие морфологических дефектов, обездвиживает их, перебивая хвостик, после чего засасывает в микроиглу. Далее эмбриолог присасывает яйцеклетку микроприсосокой и аккуратно «впрыскивает» в нее сперматозоид микроиглой. Так осуществляется оплодотворение.
Все эмбрионы, которые получают при помощи ЭКО с ИКСИ, идентичны эмбрионам, полученным при стандартном ЭКО или естественном оплодотворении, а дети, рожденные после такой операции, ничем не отличаются от своих сверстников.
Результаты ЭКО в Европейском медицинском центре
В 2019 году специалисты Клиники репродуктивной и пренатальной медицины провели 575 «свежих» циклов ЭКО и 460 криопереносов.
По результатам 2019 года: частота наступления беременности составила 48%, процент имплантации — 43,5%, что выше, чем в среднем по Москве. Например, по РФ средний показатель наступления беременности 32-34%. Такие цифры достигаются индивидуальным, нешаблонным подходом к каждому пациенту.
ЭКО в EMC начинается с приема врача-репродуктолога. Все репродуктологи EMC — квалифицированные специалисты с опытом работы за рубежом. На приеме врач ознакомится с вашей историей, результатами предыдущих анализов и исследований, проведет УЗИ, а затем составит план дальнейшей диагностики и лечения.
Руководитель Клиники репродуктивной и пренатальной медицины EMC Юлия Вознесенская входит в тройку лучших репродуктологов Москвы. Если вы хотите быть максимально подготовленными к первичной консультации, пожалуйста, подробно заполните анкету пациента, распечатайте ее и принесите на прием.Что такое ИКСИ и как его делают? – статьи о здоровье
Оглавление
Процедура ИКСИ (ICSI – Intra Cytoplasmic Sperm Injection) подразумевает введение (интрацитоплазматическую инъекцию) сперматозоида в цитоплазму яйцеклетки и проводится преимущественно при сниженной концентрации или подвижности сперматозоидов.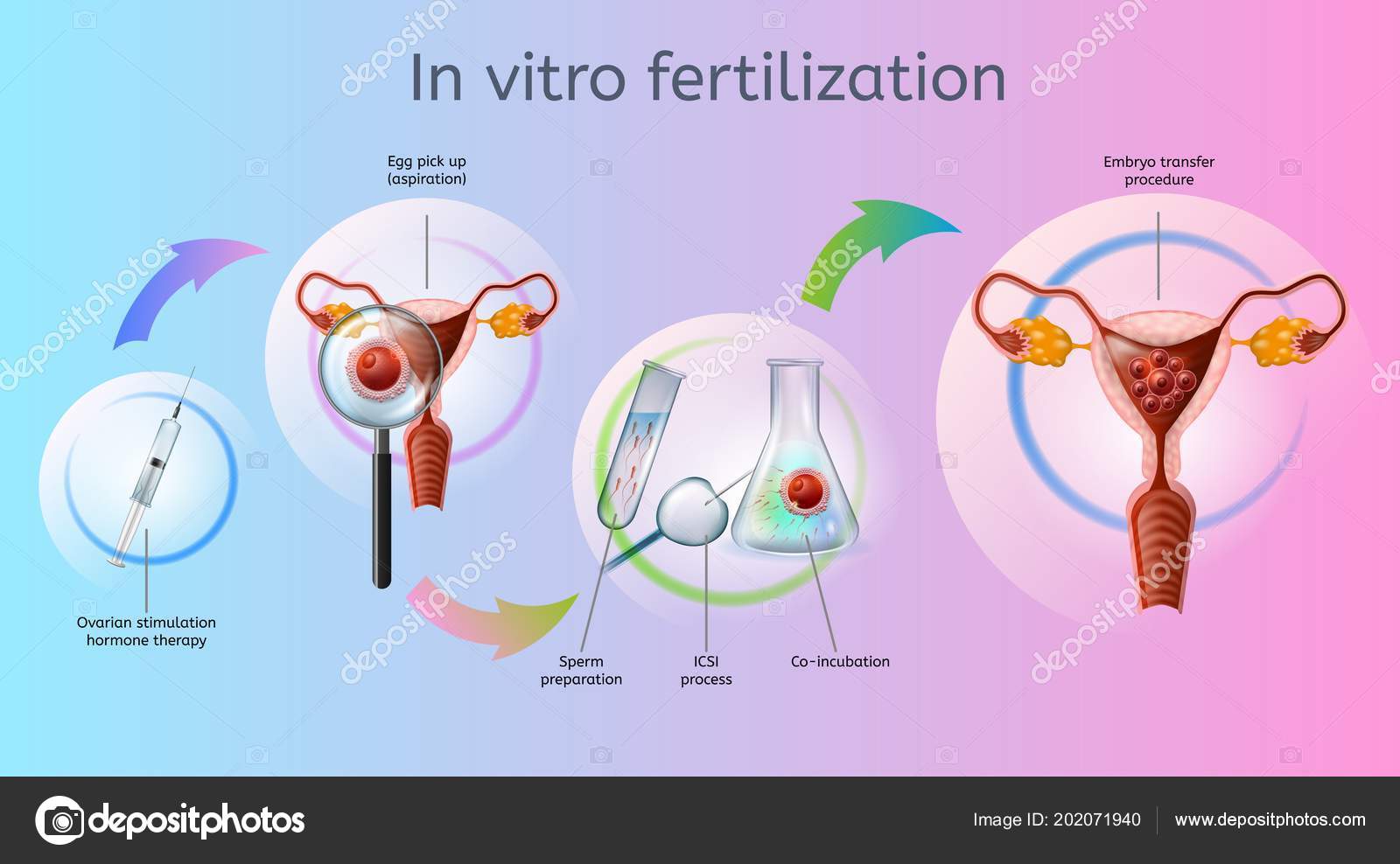 Этот метод лечения бесплодия относится к вспомогательным репродуктивным технологиям и является одним из этапов ЭКО (необязательным). Первая успешная манипуляция была проведена в 1992 году. Уже через год родились дети, зачатые данным способом. В России методика используется с 1996 года. Сегодня она применяется во всем мире и позволяет становиться родителями даже парам с диагнозом «бесплодие».
Этот метод лечения бесплодия относится к вспомогательным репродуктивным технологиям и является одним из этапов ЭКО (необязательным). Первая успешная манипуляция была проведена в 1992 году. Уже через год родились дети, зачатые данным способом. В России методика используется с 1996 года. Сегодня она применяется во всем мире и позволяет становиться родителями даже парам с диагнозом «бесплодие».
Показания к оплодотворению методом ИКСИ
Проведение процедуры рекомендовано в следующих случаях:
- Мужской фактор бесплодия (при значительном снижении концентрации, подвижности и/или морфологии сперматозоидов)
- Использование сперматозоидов, полученных хирургическим путем
- Использование ооцитов после криоконсервации
- Предыдущая неудачная попытка со стандартным эко (если оплодотворилось менее 20% полученных зрелых ооцитов)
- Программы с созреванием ооцитов in vitro
Эффективность метода
Вероятность оплодотворения при проведении ИКСИ может достигать 100%, беременность может наступить даже при тяжелом мужском факторе бесплодия, при котором зачатие естественным путем невозможно.
Как проходит процедура ИКСИ и чем метод отличается от стандартного ЭКО?
Все этапы экстракорпорального оплодотворения с интрацитоплазматической инъекцией идентичны стандартной процедуре до момента оплодотворения. Отличия начинаются именно на этом этапе. Они заключаются в том, что сперматозоид оплодотворяет яйцеклетку не самостоятельно! Специалисты проводят оплодотворение с использованием специального оборудования.
Как происходит процедура ИКСИ?
Проводится она в 4 основных этапа:
- Сбор яйцеклеток во время пункции осуществляется в специальные чашки с культуральной средой. Затем эти чашки помещаются в инкубатор, в котором поддерживаются оптимальные (имитирующие внутреннюю среду организма женщины) стабильные условия. Там яйцеклетки «отдыхают» в течение нескольких часов до момента оплодотворения
- Подготовка сперматозоидов к оплодотворению чаще всего проводится по технологии центрифугирования в градиенте плотности.
 Эякулят наливают поверх суспензии коллоидных частиц определенной плотности и центрифугируют. В результате самые качественные сперматозоиды оказываются на дне пробирки в виде осадка, а семенная плазма, лейкоциты, эпителиальные клетки и неподвижные сперматозоиды задерживаются в верхних слоях раствора
Эякулят наливают поверх суспензии коллоидных частиц определенной плотности и центрифугируют. В результате самые качественные сперматозоиды оказываются на дне пробирки в виде осадка, а семенная плазма, лейкоциты, эпителиальные клетки и неподвижные сперматозоиды задерживаются в верхних слоях раствора - Подготовка яйцеклеток. Ооциты, получаемые во время пункции, окружены большим количеством клеток кумулюса, которые необходимы для их развития внутри фолликулов. Перед проведением ИКСИ кумулюс аккуратно удаляют при помощи фермента гиалуронидазы. Только после этого эмбриолог может оценить зрелость яйцеклетки и провести оплодотворение
- Оплодотворение яйцеклетки производится под микроскопом, с помощью специальных микроинструментов. Эмбриолог «осматривает» сперматозоиды один за другим под очень большим увеличением (в 200-400 раз), оценивает их подвижность и строение головки, шейки и хвоста. Наиболее перспективную по этим характеристикам клетку обездвиживают и засасывают в стеклянную микроиглу, затем этой иглой прокалывают яйцеклетку, удерживая ее при помощи микроприсоски, и выпускают в нее сперматозоид
После этого яйцеклетки возвращаются в инкубатор, и только через 16-20 часов можно понять, эффективна ли была процедура. Если оплодотворение произошло, то за эмбрионами наблюдают в течение 3-6 дней, до момента переноса или криоконсервации.
Если оплодотворение произошло, то за эмбрионами наблюдают в течение 3-6 дней, до момента переноса или криоконсервации.
Последующие этапы программы ЭКО стандартные. В настоящее время чаще всего проводят перенос эмбрионов пятого дня развития. Это обусловлено тем, что именно на данном этапе можно наиболее точно оценить потенциал эмбрионов, выбрать для переноса наиболее перспективный, а значит, повысить вероятность наступления беременности. В ходе переноса эмбрион помещают в мягкий, гибкий катетер, который безболезненно вводится в полость матки. Через 10-14 дней после переноса эмбриона рекомендовано оценить уровень ХГЧ в сыворотке крови с целью определения беременности.
Важно! Уровень рисков при проведении ИКСИ является таким же, как при стандартном ЭКО без данной манипуляции. Процедура не сказывается на состоянии будущего ребенка и не оказывает негативного воздействия на организм матери. При этом даже самые опытные специалисты не могут дать гарантий, что после интрацитоплазматической инъекции наступит беременность и родится здоровый малыш.
Основные риски при экстракорпоральном оплодотворении связаны с особенностями протекания беременности. Может развиться внематочная и многоплодная, возможны рождение мертвого ребенка и самопроизвольный аборт.
Важно! Кроме ИКСИ, существуют и другие вспомогательные технологии. Выбор в пользу подходящей осуществляет исключительно врач. Только он обладает необходимыми знаниями и навыками.
Преимущества проведения процедуры в МЕДСИ
- Персональный врач. Он ведет пару на всем протяжении экстракорпорального оплодотворения и принимает основные решения
- Собственная лаборатория. В ней выполняются все необходимые манипуляции, связанные с ИКСИ и ЭКО в целом. В нашей лаборатории обеспечиваются оптимальные условия успешной работы с биоматериалом (многоступенчатая очистка воздуха, поддержание давления, температуры и влажности в помещениях, постоянный автоматизированный мониторинг условий культивирования)
- Уникальная для России система контроля соответствия образцов биоматериала FertiProof.
 Благодаря ей исключаются любые риски замены биоматериала пациента чужим
Благодаря ей исключаются любые риски замены биоматериала пациента чужим - Соблюдение международных протоколов. Все процедуры проводятся в соответствии с утвержденными нормами и стандартами
- Контроль за состоянием женщины в процессе оплодотворения и после него. Вы можете рассчитывать на постоянную помощь опытных специалистов
Если вы планируете пройти процедуру ИКСИ в нашей клинике, вас интересует ее цена, свяжитесь с нами любым удобным способом. Специалист ответит на возникшие вопросы.
Процедура ИКСИ в Москве 2018 – Как проходит, стоимость, статистика – В чем отличие ИКСИ и ЭКО – Клиника ЦКБ РАН
ИКСИ – это разновидность программы экстракорпорального оплодотворения, при котором в зрелую яйцеклетку искусственным способом вводится морфологически нормальный сперматозоид.Впервые опробованный в 1992 году метод ИКСИ позволил сотням тысяч бесплодных пар стать родителями здоровых малышей.
В чем отличие ЭКО от ИКСИ?
ЭКО Планируя использование вспомогательных репродуктивных технологий, важно понимать, в чем разница обычного ЭКО и ЭКО ИКСИ. В первом случае в лабораторных условиях в пробирке (invitro) соединяются сперматозоиды и ооциты, при этом процесс оплодотворения происходит самостоятельно, когда наиболее активный спермий находит зрелую яйцеклетку. В случае ЭКО ИКСИ вначале эмбриолог выбирает из мужского биоматериала наиболее «эффективный» сперматозоид с использованием электронного микроскопа. Далее сперматозоид вводится непосредственно в цитоплазму ооцита, что повышает шансы на успешное оплодотворение яйцеклетки.
Показания к ИКСИ
Стоимость ИКСИ повышает цену экстракорпорального оплодотворения. Поэтому важно понимать, что интраплазматическая инъекция сперматозоидов не является обязательной при проведении программы ЭКО. Несмотря на повышение вероятности наступления беременности после процедуры, ИКСИ назначается не всем парам, а только при наличии определенных показаний.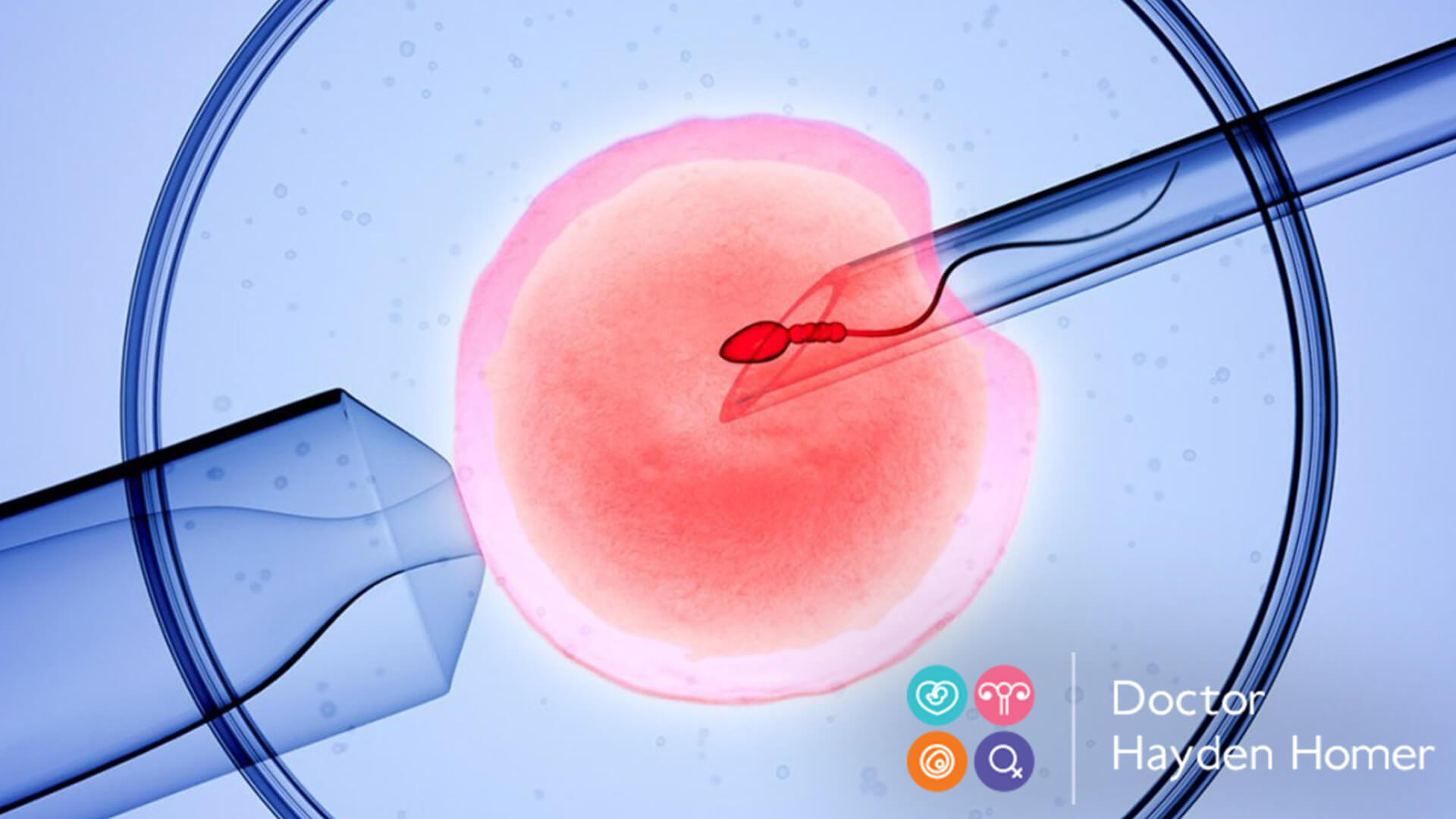
- Если имеет место фактор мужского бесплодия, в частности спермограмма выявила малую подвижность (или отсутствие подвижных) сперматозоидов;
- Если анализ спермы показывает количество в 1 мл жидкости менее 10 000 000 спермиев;
- Если у партнера диагностирована непроходимость семявыводящих каналов;
- Если в анамнезе имеются неудачные попытки ЭКО, связанные с низким процентом оплодотворения, в том числе из-за утолщенной оболочки яйцеклетки.
Подготовка к процедуре
В рамках подготовки к ИКСИ оба партнера проходят предварительную диагностику. Женщине назначается гинекологический осмотр и ультразвуковое обследование. Мужчина сдает спермограмму. Оба партнера обследуются на наличие патологий и венерических заболеваний. Когда результаты анализов получены и проанализированы врачом, выбирается наиболее подходящий метод оплодотворения.
Процедуре ИКСИ предшествуют аналогичные этапы подготовки, что и при классическом протоколе ЭКО в естественном цикле. Пациентке стимулируются яичники, выполняется пункция для забора материала.
Пациентке стимулируются яичники, выполняется пункция для забора материала.
Порядок проведения
ИКСИ выполняется с помощью высокотехнологичного оптического прибора – инвертированного микроскопа.
- Из обработанной спермы выбирается наиболее активный и морфологически нормальный сперматозоид.
- У выбранного спермия аккуратно переламыватся хвостик, чтобы он сохранил свою целостность, но был обездвижен.
- Спермий втягивается в микроиглу.
- Яйцеклетка фиксируется в определенном положении при помощи микропипетки.
- Микропипеткой прокалывается оболочка ооцита и внутрь вводится сперматозоид.
Ооциты со спермиями внутри помещаются в специальный раствор, способствующий правильному созреванию эмбриона.
Результативность ИКСИ
Процедуру ИКСИ можно отнести к категории хорошо отработанных и эффективных, однако для ее проведения необходимо передовое оборудование и высокий профессионализм врача-эмбриолога. Ведь именно на нем лежит ответственность за правильный выбор сперматозоида и его последующее введение внутрь яйцеклетки.
Ведь именно на нем лежит ответственность за правильный выбор сперматозоида и его последующее введение внутрь яйцеклетки.
Где сделать ИКСИ в Москве
Обращайтесь в отделение репродуктивных технологий в клинике ЦКБ РАН в Москве. Звоните и записывайтесь на прием к опытным специалистам. Непосредственно на консультации, вы сможете подробно узнать, сколько стоит процедура, есть ли у вашей пары показания к ИКСИ, а также как сделать интрацитоплазматическую инъекцию по квоте (ЭКО по ОМС бесплатно). Парам, которые столкнулись с проблемой бесплодия, и планируют воспользоваться нашими медицинскими услугами, рекомендуем изучить отзывы на сайте ЦКБ.
Технология ICSI (ИКСИ)
Рекомендуемые статьи
13 июля 2019
С одной стороны, с мужчиной все проще. Его фертильность очень легко оценить по анализу спермы, сдал спермограмму, посмотрели под микроскопом, увидели ситуацию и все стало ясно.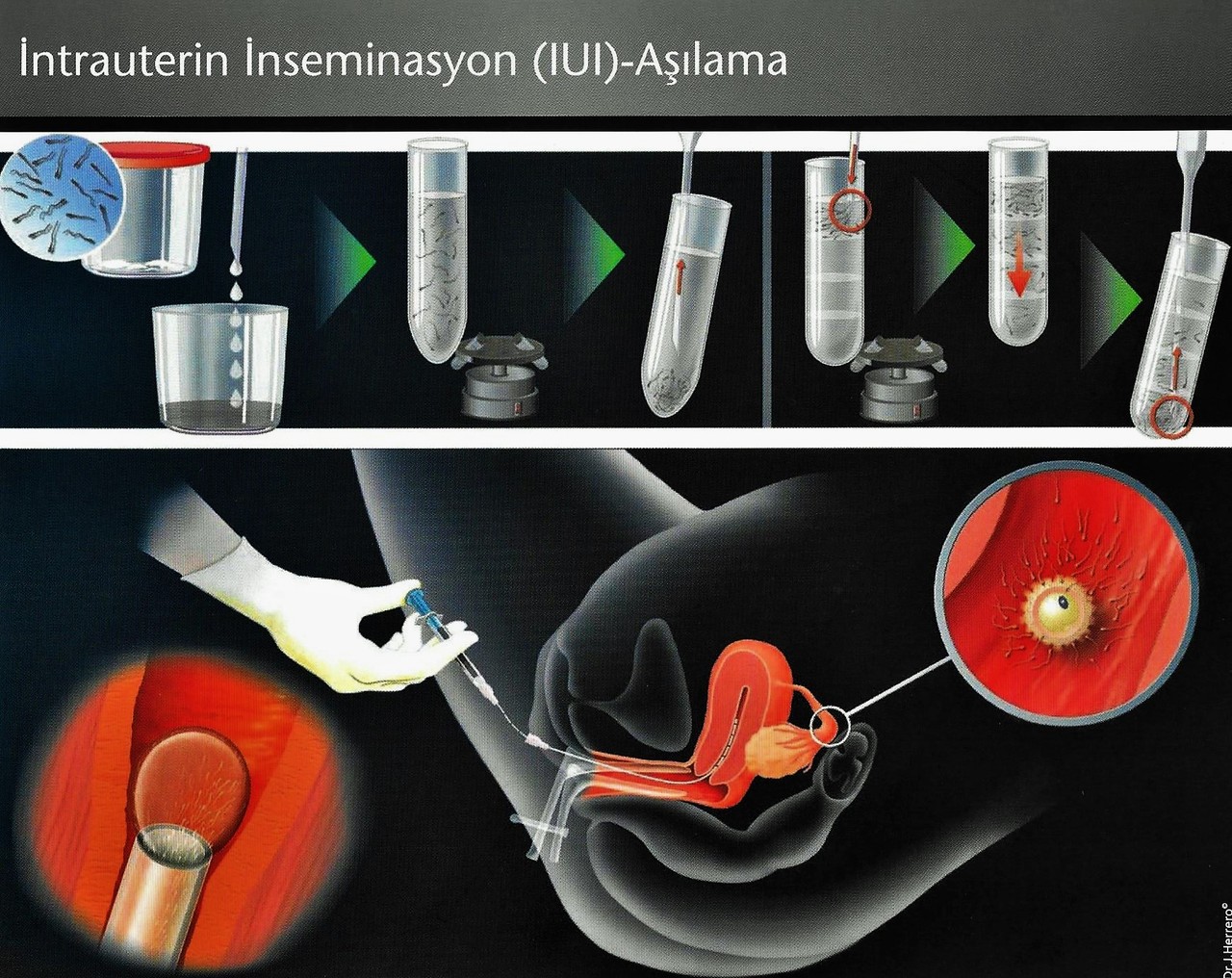 Напомню, сегодняшняя норма — 15 миллионов сперматозоидов в 1 миллилитре с подвижностью А+Б (прямолинейное движение) больше 39% и жизнеспособность 58%, морфологическая норма может быть даже 4%. По сути, красивыми внешне могут быть всего 4 процента сперматозоидов (раньше было 14%). Все это говорит о том, что сперма нормальная.
Напомню, сегодняшняя норма — 15 миллионов сперматозоидов в 1 миллилитре с подвижностью А+Б (прямолинейное движение) больше 39% и жизнеспособность 58%, морфологическая норма может быть даже 4%. По сути, красивыми внешне могут быть всего 4 процента сперматозоидов (раньше было 14%). Все это говорит о том, что сперма нормальная.
13 июля 2019
Итак, из физиологии и биологии мы уже понимаем, что не каждый секс приводит к зачатию. Что же тогда считать бесплодием? Во всем мире принято определение этого состояния, которое сформулировано так: проблему можно рассматривать как бесплодие, если пара 12 месяцев ведет регулярную половую жизнь, но беременность не наступает. Почему именно 12 месяцев?
12 июля 2019
Отдельно можем выделить еще один фактор бесплодия — ВОЗРАСТНОЕ. В европейских странах сложилась опасная демографическая тенденция. Множественные методы контроля рождаемости, контрацептивы, урбанизация плюс наша социальная активность приводят к тому, что замуж сейчас выходят позже, детей думают рожать позже. Сначала образование, карьера, а потом уже дети. И все это заставляет женщину медлить с зачатием ребенка.
В европейских странах сложилась опасная демографическая тенденция. Множественные методы контроля рождаемости, контрацептивы, урбанизация плюс наша социальная активность приводят к тому, что замуж сейчас выходят позже, детей думают рожать позже. Сначала образование, карьера, а потом уже дети. И все это заставляет женщину медлить с зачатием ребенка.
06 августа 2010
Несмотря на значительные достижения в лечении бесплодия за последние 30 лет, эффективность самого лучшего сегодня метода лечения бесплодия — ЭКО остается, относительно ожиданий пациентов, невысокой — 30-40%. Вопрос: почему хорошие эмбрионы не хотят приживаться в матке — все еще остается открытым.
26 июня 2009
Рекомендации по образу жизни и питанию после ЭКО
Процедура ЭКО ИКСИ (ICSI) Киев в клинике лечения бесплодия ИГР
ИКСИ(ICSI) — интрацитоплазматическая инъекция сперматозоида в ооцит в программе экстракорпорального оплодотворения (ЭКО) и переноса эмбрионов в полость матки женщины.
Если говорить более простым языком ИКСИ – это введение с помощью специальных микроманипуляторов одного сперматозоида прямо в цитоплазму яйцеклетки.
Суть новаторской технологии ICSI состоит в следующем: способная к оплодотворению мужская сперма должна содержать не менее 20 миллионов клеток, конечно, не все из них обладают высокой жизнеспособностью и активностью, однако при такой концентрации вероятность зачатия оптимальна. Если концентрация сперматозоидов понижается, можно с успехом использовать метод ЭКО. Однако при выраженных отклонениях от нормы у мужчин он не достаточно эффективен. В этом случае лучше обратиться к специалистам, которые осуществят операцию ICSI. По сути, это инъекция сперматозоидов в яйцеклетку, производимая специальными микрохирургическими инструментами.
Показаниями для применения ICSI являются:
- низкая концентрация сперматозоидов, их слабая активность,
- большое количество в семенной жидкости клеток с патологиями,
- в семенной жидкости слишком много антиспермальных антител,
- нулевая результативность при использовании программы ЭКО.

Уникальность новаторского метода ИКСИ заключается в том, что благодаря определенным манипуляциям зачатие может произойти даже при самых сложных формах мужского бесплодия: например, когда количество клеток в сперме не больше десятка или если эякуляция происходит ретроградно, и сперма попадает в мочевой пузырь. В последнем случае не составляет труда собрать жизнеспособные сперматозоиды в осадке мочи, после чего использовать их для оплодотворения методом ICSI.
Еще одно неоспоримое преимущество данного метода в том, что он позволяет получить родного ребенка даже тогда, когда мужчина страдает асперматизмом. Асперматизм – заболевание, при котором в семенной жидкости вообще не обнаруживаются сперматозоиды. Ранее в подобных случаях приходилось использовать донорскую сперму, что не решало психологической проблемы мужчины, так как генетически ребенок был не от него. При асперматизме метод ИКСИ весьма действенен: сперматозоиды берутся напрямую из яичка с помощью пункции или биопсии.
При использовании технологии ICSI мужская сперма обрабатывается таким образом, чтобы получить из нее хотя бы один подвижный сперматозоид без патологий. После этого врач-оператор вводит полученный сперматозоид в яйцеклетку. ICSI имеет много преимуществ и позволяет стать отцами даже тем мужчинам, которые уже совсем отчаялись получить нужный результат.
Записаться на приёмКак проходит процедура ИКСИ: показания, особенности, подготовка
Что такое ИКСИ
ИКСИ — это введение сперматозоидов под оболочку яйцеклетки методом инъекции. Оно проводится для оплодотворения ооцита и является одной из разновидностей ЭКО. В классическом протоколе сперматозоиды и яйцеклетки соединяются в пробирке, а не в организме женщины. В остальном же условия их слияния можно назвать естественными. В случае использования ИКСИ сперматозоид вводят в яйцеклетку принудительно. Для этого используют тонкую иглу и реактивы. При выборе этого метода зачатие происходит с вероятностью 100 %.
При ИКСИ сперматозоид вводится тонкой иглой
Оплодотворение с использованием технологии ИКСИ назначается в случае мужского бесплодия, которое проявляется в следующих нарушениях в работе половой системы:
- сперматозоиды обладают низкой активностью или вырабатываются в недостаточном количестве;
- в семенной жидкости обнаруживаются антитела;
- есть непроходимость семявыводящих каналов.
Успешность результата применения методики ИКСИ зависит от качества биоматериала, предоставляемого партнерами для оплодотворения. Другие факторы, определяющие положительное завершение искусственного оплодотворения, не отличаются от показаний для проведения классического ЭКО:
- возраст пациентов до 35–40 лет;
- отсутствие тяжелых хронических заболеваний у обоих партнеров;
- хорошая генетическая совместимость.
Женщинам также необходимо пройти тщательное гинекологическое обследование.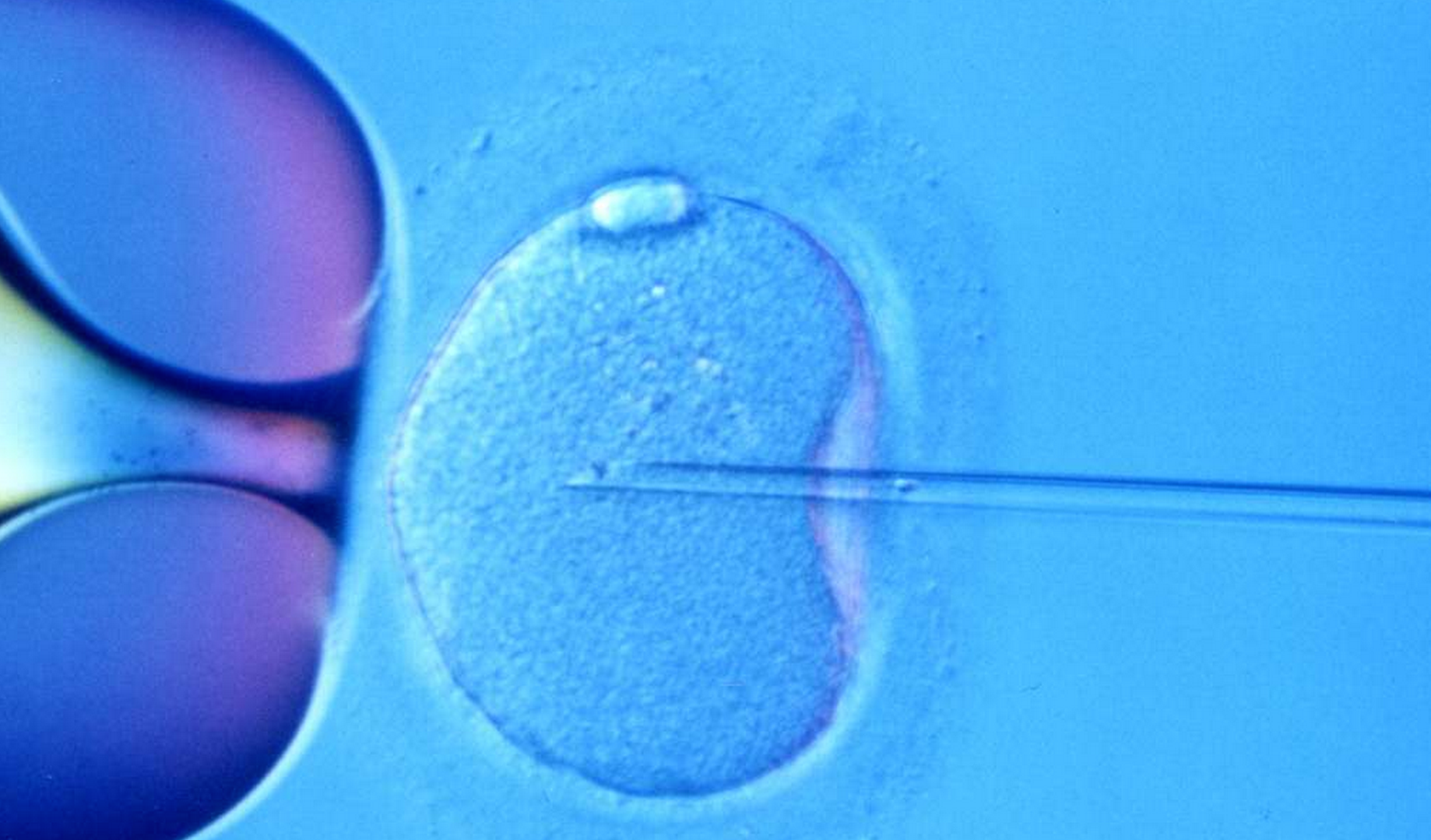 На результат могут повлиять:
На результат могут повлиять:
- аномалии строения матки;
- проблемы с гормональной системой;
- воспаления органов малого таза;
- аборты и другие операции в анамнезе.
В случае наличия этих отклонений у пациентки даже при успешном оплодотворении ооцита методом ИКСИ вынашивание может стать проблематичным, а в некоторых случаях и вовсе невозможным.
Подготовка к ИКСИ
На начальном этапе пара проходит комплексное обследование. В случае обнаружения отклонений, которые можно устранить, необходимо пройти курс лечения и восстановления.
Перед тем как пройти процедуру, пациентам нужно сдать кровь для ряда исследований:
- общеклинический и биохимический анализ;
- определение резус-фактора и группы крови;
- выявление венерических и инфекционных заболеваний;
- проверка свертываемости и уровня гормонов.
Перед проведением ИКСИ необходимо сдать несколько анализов
Помимо этого делается общий анализ мочи. Мужчины дополнительно сдают семенной материал для проведения спермограммы, женщины — мазок для исключения скрытых инфекций.
Мужчины дополнительно сдают семенной материал для проведения спермограммы, женщины — мазок для исключения скрытых инфекций.
Как проходит процедура ИКСИ
Использование в качестве вспомогательной репродуктивной технологии метода ИКСИ включает несколько этапов.
Первый этап
Сначала происходит стимуляция работы яичников. Для этого женщина принимает гормональные препараты, а затем специальные лекарства. Гормоны вводятся в течение 1–2 недель по индивидуальной схеме. Когда с их помощью достигается нужное состояние организма, назначаются средства для гиперстимуляции. Курс их приема также составляет около 2 недель.
Результатом первого этапа является увеличение количества фолликулов. На всем протяжении приема препаратов происходит контроль с помощью УЗИ и анализов крови.
Второй этап
Это этап подготовки к оплодотворению, и он начинается с забора биоматериала партнеров. Ооциты получают из зрелых фолликулов, которые извлекают посредством пункции.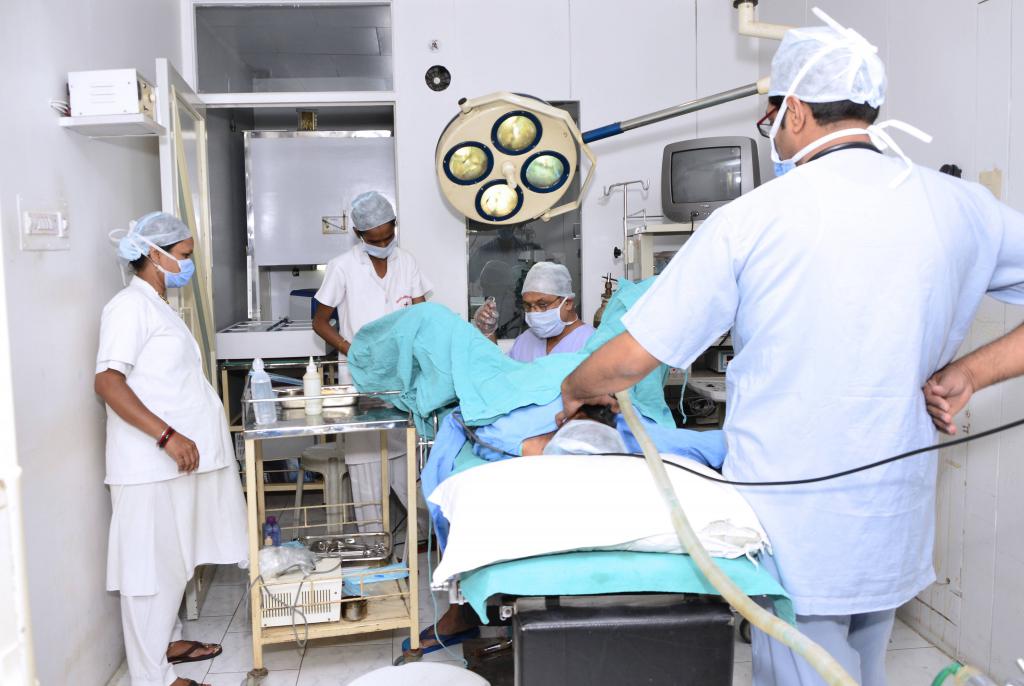 После забора яйцеклеток начинается подготовка эндометрия к вживлению эмбриона, и женщине назначается очередной курс приема гормонов.
После забора яйцеклеток начинается подготовка эндометрия к вживлению эмбриона, и женщине назначается очередной курс приема гормонов.
Параллельно проведению пункции у партнера забирают семенную жидкость. Выбор способа зависит от особенностей нарушений половой системы мужчины. Затем сперматозоиды отделяют и готовят к оплодотворению. Здесь также есть несколько вариантов методик, которые применяются в зависимости от того, насколько жизнеспособны сперматозоиды.
Третий этап
На третьем этапе происходит искусственное оплодотворение. Для этого лаборант берет созревшую яйцеклетку и наиболее подходящий сперматозоид. Отобранный жизнеспособный сперматозоид вводится тонкой инъекционной иглой под оболочку ооцита. Операция проводится вручную. Оплодотворенная яйцеклетка на несколько дней помещается в питательную среду. Когда эмбрион созреет, проводят его трансплантацию в полость матки.
Врач выбирает самые подходящие половые клетки
Четвертый этап
После подготовки, забора биологического материала и оплодотворения яйцеклетки по методике ИКСИ созревший зародыш переносят в матку. Успешным будет считаться исход, если эмбрион приживется и начнет развиваться. Для помощи женскому организму в этом случае назначается прием прогестерона.
Успешным будет считаться исход, если эмбрион приживется и начнет развиваться. Для помощи женскому организму в этом случае назначается прием прогестерона.
Методы ЭКО и ИКСИ отличаются друг от друга только способом оплодотворения яйцеклетки. В первом случае все происходит естественным путем, во втором сперматозоид попадает в ооцит с помощью врача-эмбриолога. В остальном же обе эти процедуры одинаковы, поэтому нельзя однозначно определить, какая из них лучше. Определенно можно лишь сказать, что ИКСИ является более дорогой операцией. Поэтому бесплодным парам сначала проводят классическое ЭКО и лишь после отсутствия результата рекомендуют воспользоваться технологией ИКСИ.
Видео: Что такое ИКСИ?
ИКСИ: показания, успех процедуры и ее стоимость
Стоимость
Цена манипуляции зачастую входит в общую стоимость большинства программ ЭКО.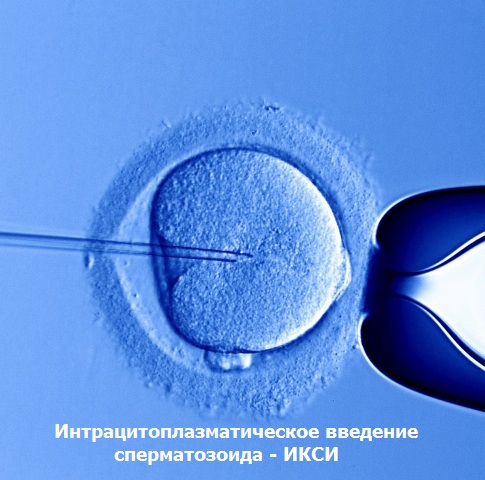
| Программа ЭКО «Классическая» (IVF + ICSI + BC) первая попытка | 38 000 грн. |
| Программа ЭКО «Классическая» (IVF + ICSI + BC) вторая попытка | 36 500 грн. |
| Программа ЭКО «Классическая» (IVF + ICSI + BC) третья попытка | 35 000 грн. |
| Программа ЭКО «Нативная» (в естественном цикле (IVF + ICSI + BC) | 32 000 грн. |
Основные сведения
ИКСИ (интрацитоплазматическая инъекция сперматозоида) — метод искусственного оплодотворения что дополняет процедуру ЭКО. Под процедурой ИКСИ подразумевают инъекцию одного предварительно отобранного сперматозоида в цитоплазму яйцеклетки. Данная методика осуществляется при помощи специального микроскопа и микроинструмента. Это позволяет специалистам зачать новую жизнь.
Записаться на консультациюПоказания для проведения ICSI
Ни для кого ни секрет, что на сегодняшний день около 50% супружеских пар, которые обращаются в клиники ВРТ, сталкиваются с проблемой мужского фактора бесплодия.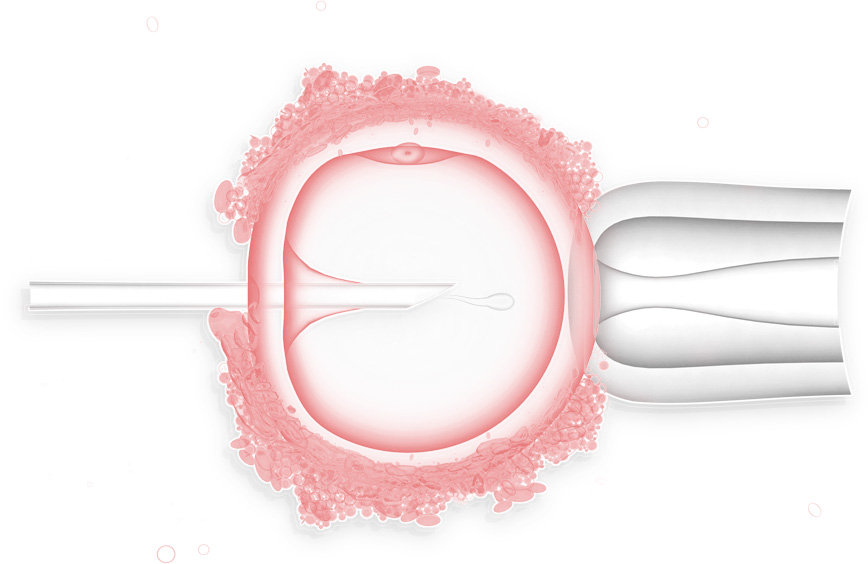
Для проведения ИКСИ существует ряд показаний:
- снижение значений спермограммы (уменьшение концентрации, подвижности и нормальной морфологии мужских половых клеток)
- полное отсутствие сперматозоидов в эякуляте, которые необходимо получить в результате хирургического вмешательства
- если в прошлом у пары было очень мало оплодотворенных яйцеклеток либо оплодотворение вовсе не наступило
- также методика проводится при наличии у мужчины антиспермальных антител
- небольшое число сперматозоидов после криоконсервации
- ICSI также рекомендовано пациентам в возрасте старше 40 лет
В ряде остальных случаев решение о том, прибегать к данному способу или не прибегать, принимается врачом индивидуально.
Записаться на консультациюКак происходит ICSI
Сама по себе процедура не требует никакой подготовки. Однако по рекомендации доктора могут быть назначены препараты для лечения, с помощью которых можно улучшить показатели спермы. Это позволяет специалистам расширить подбор качественных сперматозоидов. Что касается женской части, то здесь важна правильная стимуляция, поддержка и соблюдение всех рекомендаций доктора для получения максимально качественных яйцеклеток.
Это позволяет специалистам расширить подбор качественных сперматозоидов. Что касается женской части, то здесь важна правильная стимуляция, поддержка и соблюдение всех рекомендаций доктора для получения максимально качественных яйцеклеток.
В предварительно подготовленную чашу помещаются ооциты и обработанная сперма. На увеличенном экране специалист отслеживает сперматозоиды и выбирает самый лучший, оцененный по показателям подвижности и морфологии. Этот отобранный сперматозоид обездвиживают и специальным инструментом засасывают в микроиглу. Затем он вводится в яйцеклетку для оплодотворения.
Читать далееСупружеская пара посещает эмбриолога на пятые сутки. Согласовывается количество переносимых эмбрионов и тех, которые уйдут на криоконсервацию. В ходе этой процедуры решается вопрос: сколько эмбрионов нужно перенести. При эндометриозе или эмбрионах низкого качества, неудачных попытках эко в анамнезе, имеет смысл перенести два эмбриона для получения желаемого результата. После согласования всех нюансов под контролем ультразвука эмбрион переносят в полость матки. Женщина около 15 минут находится в клинике и спокойно уходит домой.
Женщина около 15 минут находится в клинике и спокойно уходит домой.
Таким образом проходит процесс ИКСИ и зарождается новая жизнь.
Успех процедуры
При методике ICSI процент зигот в среднем составляет около 70%. Поэтому, когда вы слышите от вашего врача, что целесообразно провести данную процедуру, не стоит переживать и бояться. На состояние здоровья, течение беременности и роды она не оказывает никакого негативного воздействия. Однако ее осуществление должно быть строго по показаниям. Существенным плюсом ИКСИ является то, что методика позволяет ощутить радость деторождения даже тем парам, которым врачи не прогнозировали успешность ЭКО.
Записаться на консультациюКоманда врачей
Стрелко Галина Владимировна
Главный врач клиники Айвимед Киев, врач акушер-гинеколог высшей категории, доктор медицинских наук, репродуктолог
Врачебная практика с 2004 года
Хотите записаться на
прием?
Жмите сюда
Роботизированная хирургия | Шведская больница в Чикаго
Общие хирурги Northshore Medical Group в Шведской больнице обучены использовать роботизированную хирургическую систему da Vinci ™ Xi последнего поколения для широкого спектра операций на передней кишке, общей, толстой и прямой кишке, когда это необходимо.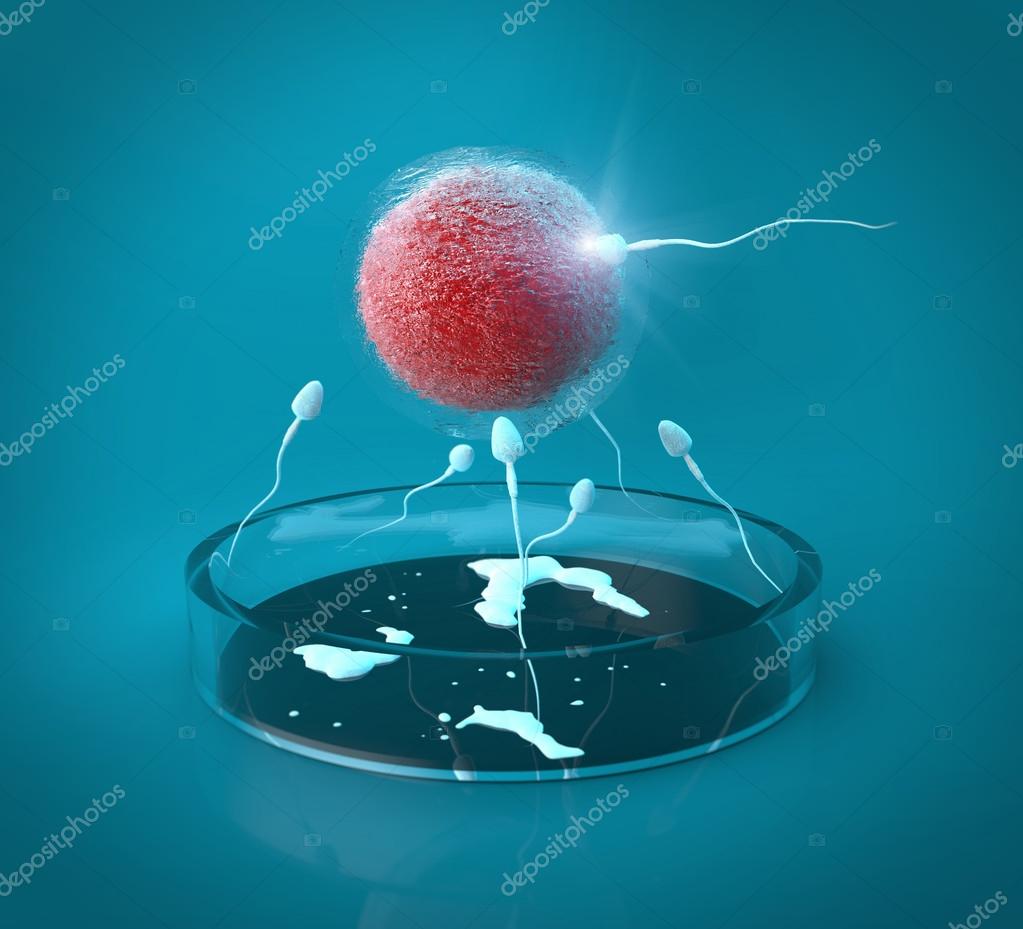
Доказано, что новейшие роботизированные хирургические методы в сочетании с протоколами улучшенного восстановления после операции (ERAS) сокращают пребывание в больнице, приводят к более быстрому заживлению с меньшим количеством перерывов в работе, меньшим количеством послеоперационных осложнений и меньшей послеоперационной болью.
Робот da Vinci Xi преобразует естественные движения руки хирурга в точные движения роботизированных рук, расположенных внутри тела пациента, с помощью небольшой камеры, которая предоставляет хирургу увеличенное трехмерное изображение тела пациента. Роботизированные руки дают хирургу большую ловкость и диапазон движений через несколько небольших разрезов, а не через большой открытый разрез.
Каковы преимущества роботизированной хирургии?
Роботизированная платформа позволяет нашим хирургам выполнять амбулаторные и многие крупные операции, когда это необходимо, через несколько небольших разрезов.
Это приводит к лучшим результатам для пациентов и имеет дополнительное косметическое преимущество, заключающееся в предотвращении нежелательных рубцов.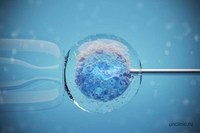
Большинство колоректальных операций в США проводится через большой открытый разрез брюшной полости. В Шведской больнице наши хирурги могут выполнять столь же эффективные и более точные операции на толстой и прямой кишке с использованием роботизированных технологий через несколько разрезов, которые составляют часть размера.
Работают ли роботы?
Многие пациенты обеспокоены тем, что операцию делает робот.Будьте уверены, что робот не думает сам по себе, а, скорее, позволяет хирургу, который постоянно находится под прямым контролем, совершать более точные и сложные движения в небольшом пространстве, которые ранее были невозможны. Хирург также может постоянно визуализировать роботизированные инструменты, находясь на консоли, которая управляет этими инструментами.
Типы роботизированной хирургии
Хирургическая система da Vinci Xi может использоваться при самых разных хирургических вмешательствах, в том числе:Свяжитесь с нами
Чтобы записаться на прием, позвоните по телефону 773-878-6888 .
Ранний клинический опыт использования хирургической системы da Vinci Xi в общей хирургии
Хирургическая система da Vinci Xi (Intuitive Surgical Inc., Саннивейл, Калифорния, США) была выпущена в 2014 году для проведения малоинвазивной хирургии. Новые функции нацелены на облегчение сложных многоквадрантных процедур, но данных пока мало. Были собраны и проанализированы периоперационные данные пациентов, перенесших общую роботизированную операцию с системой da Vinci Xi в течение первых 6 месяцев после установки.Процедуры обходного желудочного анастомоза, выполненные с помощью хирургической системы da Vinci Xi, сравнивали с таким же количеством последних процедур с хирургической системой da Vinci Si. Была проведена 31 операция на передней кишке (28 обходных желудочно-кишечных анастомозов по Ру), 6 колоректальных процедур и 1 ревизионная операция на желчных путях. Среднее время операционной (OR) составляло 221,8 (± 69,0) минут для обходных желудочных анастомозов и 306,5 (± 48,8) для колоректальных процедур со средним временем стыковки 9,4 (± 3,8) минут. Процедура обходного желудочного анастомоза была переведена с гибридного на полностью роботизированный подход.По сравнению с последними 28 процедурами обходного желудочного анастомоза, выполненными с помощью хирургической системы da Vinci Si, время операции было сопоставимым (226,9 против 230,6 мин, p = 0,8094), но время стыковки с хирургической системой da Vinci Xi значительно больше (8,5 против 6,1 мин, p = 0,0415). Все колоректальные процедуры выполнялись с помощью одной роботизированной док-станции. Интраоперационных и двух послеоперационных осложнений не было. Da Vinci Xi может облегчить одиночные установки полностью роботизированного желудочного обходного анастомоза и колоректальные операции.Однако необходимы дальнейшие сопоставимые исследования, чтобы четко определить важность этой последней версии хирургической системы да Винчи.
Процедура обходного желудочного анастомоза была переведена с гибридного на полностью роботизированный подход.По сравнению с последними 28 процедурами обходного желудочного анастомоза, выполненными с помощью хирургической системы da Vinci Si, время операции было сопоставимым (226,9 против 230,6 мин, p = 0,8094), но время стыковки с хирургической системой da Vinci Xi значительно больше (8,5 против 6,1 мин, p = 0,0415). Все колоректальные процедуры выполнялись с помощью одной роботизированной док-станции. Интраоперационных и двух послеоперационных осложнений не было. Da Vinci Xi может облегчить одиночные установки полностью роботизированного желудочного обходного анастомоза и колоректальные операции.Однако необходимы дальнейшие сопоставимые исследования, чтобы четко определить важность этой последней версии хирургической системы да Винчи.
Ключевые слова: Да Винчи; Пищеварительная хирургия; Минимально инвазивная хирургия; Роботизированный; Роботизированная хирургия; Си.
Пациенты, хирурги отмечают сотую процедуру да Винчи Си
Первые 100 пациентов, перенесших роботизированную операцию в больнице Южного округа с помощью хирургической системы da Vinci Xi, были недавно приглашены, чтобы узнать больше об этой передовой технологии от тех, кто знает лучше: их собственных хирургов.
Мероприятие 25 февраля было проведено в ознаменование 100-й успешной операции да Винчи в больнице. В конце программы присутствующим было разрешено управлять устройством da Vinci, чтобы испытать робототехнику на собственном опыте.
«Мне было любопытно, как это работает», — сказал Роберт Нула, которому сделали две процедуры да Винчи в течение 11-недельного периода. «Когда мне сделали операцию, я хотел дождаться снотворного, чтобы поближе познакомиться с системой да Винчи».
Наряду с первыми 100 пациентами, среди других приглашенных гостей были члены правления и администрация больницы.Программа включала выступления и демонстрации хирурга общей практики доктора Джозефа Брэди.
Хирургическая система da Vinci Xi имеет систему трехмерного зрения высокого разрешения, специализированные инструменты и компьютерное программное обеспечение, которое позволяет хирургу работать с улучшенным зрением, точностью, ловкостью и контролем. Для пациентов это означает менее инвазивную процедуру, более быстрое выздоровление и меньшую боль.
Доктор Брэди использует эту технологию для плановой и сложной пластики грыж, хирургии желчного пузыря, толстой и тонкой кишки.
Несмотря на то, что истории пациентов различаются, была одна повторяющаяся тема: каждый хотел сделать операцию с опытным хирургом с использованием новейших технологий. Они оказались в надежных руках, поскольку врачи, использующие да Винчи, провели более 2000 операций с использованием роботизированных технологий.
Пол Джонсон
Пол Джонсон готовился отпраздновать свою 36-ю годовщину свадьбы, когда ему позвонили по телефону и сообщили, что его биопсия подтвердила диагноз рака простаты. После встречи со своими врачами он понял, что хочет, чтобы его операция была проведена с использованием технологии да Винчи.
После встречи со своими врачами он понял, что хочет, чтобы его операция была проведена с использованием технологии да Винчи.
Пол отложил операцию на несколько месяцев, чтобы проводить своих дочерей по проходу на их свадьбах в мае и сентябре 2018 года. Его операция прошла 5 октября 2018 года. Пол очень хвалит свою медицинскую бригаду и других, кто заботился о нем. Больница Южного округа. Он отметил Эмили Коста, медсестру-координатора отделения урологии, за ее знания, сочувствие и доступность, чтобы ответить на любые его вопросы.«Персонал был замечательным, — сказал Пол.
Лучше всего то, что Пол прошел последующее тестирование, и его уровень ПСА сейчас находится на неопределяемом уровне.
Роберт Нула
Роберту Нуле был поставлен диагноз «агрессивная форма рака простаты». В декабре ему была проведена радикальная простатэктомия. Восстанавливаясь после операции, Роберт заметил, что некоторая опухоль и болезненность в одной конкретной области не уменьшаются. После осмотра и анализов было обнаружено, что у него грыжа.
После осмотра и анализов было обнаружено, что у него грыжа.
Его операция была сделана доктором Брэди 21 февраля, и всего четыре дня спустя Роберт был одним из присутствующих на лекции и демонстрации да Винчи. После обеих процедур Роберту не потребовались обезболивающие. Это был его первый опыт работы в больнице Южного округа, и он похвалил персонал и оборудование как выдающиеся.
«У меня было три лучших хирурга в штате, использующих новейшие технологии», — сказал он.
Erik Elsdoerfer
Erik Elsdoerfer также был взволнован, увидев эту технологию в действии, отчасти из-за того, что он работал инженером-электриком.У Эрика была опухоль на животе, которая была диагностирована как грыжа живота, и продолжала расти, пока не потребовалась операция. Его врач порекомендовал ему посетить доктора Брэди, который также использовал робота да Винчи для выполнения своей операции. «Это был отличный опыт», — сказал он.
Брайан Джонс
В 2008 году Брайан Джонс лечился от рака простаты с помощью режима лучевой терапии. В 2018 году ему сделали компьютерную томографию, чтобы еще раз диагностировать то, что, по его мнению, было проблемными камнями в почках.Радиолог увидел то, что, по его мнению, могло быть опухолью на доле его почки.
В 2018 году ему сделали компьютерную томографию, чтобы еще раз диагностировать то, что, по его мнению, было проблемными камнями в почках.Радиолог увидел то, что, по его мнению, могло быть опухолью на доле его почки.
Как и Пол Джонсон, Брайан отложил операцию, чтобы посетить свадьбу (в данном случае его внучка). Его операция прошла 18 октября 2018 года. Он хотел, чтобы операция была проведена с использованием роботизированной технологии да Винчи. «Я не был пациентом в больнице Южного округа, но я знал о ее репутации».
В октябре из доли почки Брайана удалили злокачественную опухоль размером в четверть. После того, как его операция была завершена, Брайан сказал, что его пребывание в больнице было хорошим, и он не чувствовал себя поспешным уезжать.
«Мне нравились все, кого я встречал», — сказал он. «Медсестры были потрясающими. Они были очень внимательны и хорошо проинструктированы во время передачи медсестер между сменами ».
В то время как Брайан составлял истории болезни и сообщал о медицинском обслуживании, «все это не имело значения», — сказал он. «Когда ты пациент, это другая точка зрения. Я был уверен, что все знают, как делать свою работу ».
«Когда ты пациент, это другая точка зрения. Я был уверен, что все знают, как делать свою работу ».
От да Винчи Си до да Винчи Си: реалистичное время при драпировке и стыковке робота
Длительное время работы остается одним из аргументов против роботизированной хирургии.Дополнительное время, необходимое для роботизированной хирургии, можно разделить на дополнительное время, необходимое для подготовки робота, и фактическое время процедуры. Хотя в литературе имеется множество данных о времени консоли, существует пробел в знаниях о точном времени, необходимом на этапе настройки [5,6,7]. Это исследование является первым, в котором точно отслеживается время настройки в опытных операционных группах, работающих с Da Vinci Xi. Это также первая информация о продолжительности адаптации к новому роботизированному устройству.
Представленные данные показывают, что существует относительно короткий период — 18–21 процедура для учреждения с опытным персоналом Da Vinci Si, чтобы адаптироваться к новой системе Xi. Эта переходная фаза приводит к ограниченному количеству дополнительного времени операционной. Обернуть робота можно за 5,0 мин и завершить за время подготовки, необходимое анестезиологу. Это означает, что этап драпировки робота можно рассматривать как задержку, которой можно избежать, и не обязательно влияет на общее время, проведенное в операционной. Однако результаты показывают, что это сильно зависит от эффективности операционной группы. Эффективный способ управления временем был замечен в 55% наблюдаемых процедур в этом исследовании.Было обнаружено различие в частоте, с которой эта наиболее оптимальная форма управления временем использовалась в операционных командах разных специальностей. Этому может способствовать отношение внутри команды.
Эта переходная фаза приводит к ограниченному количеству дополнительного времени операционной. Обернуть робота можно за 5,0 мин и завершить за время подготовки, необходимое анестезиологу. Это означает, что этап драпировки робота можно рассматривать как задержку, которой можно избежать, и не обязательно влияет на общее время, проведенное в операционной. Однако результаты показывают, что это сильно зависит от эффективности операционной группы. Эффективный способ управления временем был замечен в 55% наблюдаемых процедур в этом исследовании.Было обнаружено различие в частоте, с которой эта наиболее оптимальная форма управления временем использовалась в операционных командах разных специальностей. Этому может способствовать отношение внутри команды.
Шаг стыковки робота всегда требует дополнительного времени по сравнению с обычными лапароскопическими процедурами. Этот шаг можно выполнить в среднем за 7 минут. В отличие от многих других исследований, время стыковки не включало размещение порта, так как этот этап также хорошо выполняется при традиционной лапароскопии и не должен рассматриваться как дополнительное время [10, 11].
Иранманеш и др. провели аналогичное исследование с 2006 по 2008 год, точно отслеживая время драпировки и стыковки своего первого опыта работы с хирургической системой Da Vinci. В своей серии из 96 процедур (все общие операции, восемь разных хирургов, неизвестное количество медицинских сестер) они обнаружили, что среднее время драпировки составляет 22 минуты (диапазон 9–50) [5]. Это значительно дольше результатов, полученных в нашем институте. Их среднее время стыковки составляло 10 минут (диапазон 2–70), что ближе к нашим результатам.Обнаруженная разница может быть связана с неопытностью их команды в области роботизированной хирургии в начале исследования и частотой хирургических вмешательств с участием роботов (96 процедур за 30 месяцев по сравнению с 65 процедурами за 6 недель в нашем исследовании). Кроме того, усовершенствования, внесенные в Xi в виде более простой стыковки, размещения портов с лазерным наведением и роботизированных манипуляторов, установленных на стреле, могли сыграть роль в более быстром времени драпировки и стыковки, которое мы обнаружили. Сравнение с другими исследованиями сложно и ненадежно из-за нечетко описанных определений отчетных временных рамок [3, 12,13,14,15,16], различного способа стыковки (трехрычажный или однопортовый) [6, 17, 18] , метод сбора данных и / или дизайн ретроспективного исследования [3, 17,18,19].
Сравнение с другими исследованиями сложно и ненадежно из-за нечетко описанных определений отчетных временных рамок [3, 12,13,14,15,16], различного способа стыковки (трехрычажный или однопортовый) [6, 17, 18] , метод сбора данных и / или дизайн ретроспективного исследования [3, 17,18,19].
Роботизированная хирургия, особенно этап до того, как хирург приступит к работе за консолью, является коллективной работой. Ограничением данного исследования является то, что состав операционных команд по специальностям не был полностью определен. Это было вызвано ежедневной сменой графика работы наших медсестер и более чем одного консультанта по специальности. Однако ротация в основном проводилась в рамках одной из хирургических дисциплин, чтобы свести к минимуму вариабельность. Из-за различного состава хирургических бригад мы не смогли проанализировать кривые обучения для каждой операционной бригады отдельно.Вместо этого была дана институциональная кривая обучения. Это представляет собой реалистичный рабочий процесс в больнице, где различные специалисты используют роботизированное устройство. Таким образом, это увеличивает возможность обобщения наших результатов на другие массовые практики. Кроме того, тот факт, что не было обнаружено никаких статистически значимых различий во времени драпировки и стыковки роботов между тремя специальностями, поддерживает наш метод.
Таким образом, это увеличивает возможность обобщения наших результатов на другие массовые практики. Кроме того, тот факт, что не было обнаружено никаких статистически значимых различий во времени драпировки и стыковки роботов между тремя специальностями, поддерживает наш метод.
В заключение, в роботизированной хирургии можно свести к минимуму время оперирования и стыковки.CUSUM-анализ показал, что при установке нового устройства существует короткая фаза обучения из 21 случая. В специализированных операционных командах нетто дополнительное время, необходимое для подготовки Кси, может быть сокращено до 7 минут, необходимых для стыковки. Следовательно, подготовка Da Vinci Xi должна иметь ограниченное влияние на общее время, проведенное в операционной. С ростом числа операций с использованием роботов, расширяющейся доступностью этой технологии и выходом на рынок новых производителей хирургических роботов, это ценные данные для клиник, внедряющих (нового) робота.
Роботизированная частичная нефрэктомия с помощью аппарата Da Vinci Xi
Назначение. Хирургический опыт выполнения роботизированной частичной нефрэктомии во многом зависит от технологии. Da Vinci Xi (XI) — новейшая роботизированная хирургическая платформа со значительными усовершенствованиями по сравнению со своей предшественницей. Мы описываем нашу оперативную технику и опыт работы с системой XI для роботизированной частичной нефрэктомии (RPN). Материалы и методы. Пациентам с клиническими опухолями почек Т1 была предложена РПН с XI.Мы использовали лазерное наведение, автопозиционирование и новое размещение порта «в линию» для выполнения RPN. Результаты. 15 пациентам выполнено РПН с XI. Интраоперационных осложнений и конверсионных операций не было. Среднее время консоли составило 101,3 минуты (диапазон 44–176 минут). Среднее время ишемии составило 17,5 минут, а расчетная кровопотеря — 120 мл. У 12 из 15 пациентов был почечно-клеточный рак. У двух пациентов была онкоцитома, у одного — доброкачественная кистозная болезнь. У всех пациентов были отрицательные хирургические границы и патологический T1.Было обнаружено два послеоперационных осложнения, в том числе у одного пациента развилась псевдоаневризма и у одного пациента была повторно госпитализирована предполагаемая инфекция мочевыводящих путей. Выводы. РПН с системой XI можно безопасно выполнять. Сочетание нашей хирургической техники с технологическими достижениями XI предлагает пациентам приемлемые патологические и периоперационные результаты.
1. Введение
С нового тысячелетия роботизированная хирургия все чаще используется для различных процедур, включая роботизированную частичную нефрэктомию (RPN).По сравнению с лапароскопической частичной нефрэктомией, РПН технически менее сложна и связана с меньшей вероятностью перехода на радикальную нефрэктомию [1], меньшей кровопотерей [2–4], более коротким временем ишемии [2, 5] и более коротким пребыванием в больнице [2] , 3]. Роботизированная платформа обеспечивает лучшее сочленение запястий и улучшенное зрение в трех измерениях, что позволило сократить время обучения хирургов, применяющих минимально инвазивную хирургию. С 2000 года, когда впервые был использован робот Да Винчи, робот претерпел несколько итераций, каждая с огромным технологическим прогрессом по сравнению с предыдущей версией.Недавно компания Intuitive Surgical представила свою последнюю модернизацию робота Da Vinci Xi (Intuitive Surgical, Саннивейл, Калифорния). В этой статье мы подробно описываем наш первый опыт и уроки, извлеченные из системы Da Vinci Xi для RPN.
2. Материалы и методы
Начиная с мая 2014 г. пациентам, у которых было обнаружено новообразование в почках 1 клинической стадии, было предложено хирургическое вмешательство, наблюдение или абляционная терапия в соответствии с рекомендациями AUA 2009 в отношении новообразований в почках 1 клинической стадии [6 ].Если можно было выполнить частичную нефрэктомию, пациентам предлагалась РПН с хирургической системой Da Vinci Xi. Пациенты с опухолями T2 или очень сложными образованиями почек, у которых частичная нефрэктомия считалась невозможной, не включались в это исследование. Перед операцией пациенты прошли полное предоперационное обследование. Всем пациентам проводилась стандартная лабораторная оценка, включая уровень креатинина сыворотки. Хирург оценил предоперационную компьютерную томографию и МРТ, а также оценил сложность по шкале RENAL Nephrometry [7].Перед операцией всем пациентам было дано письменное информированное согласие. Это исследование было одобрено IRB.
2.1. Общие соображения
Хирургическая платформа Da Vinci Xi (рис. 1) включает множество технологических усовершенствований. В частности, значительные улучшения касаются тележки пациента и процесса стыковки. Тележка пациента оснащена четырьмя роботизированными манипуляторами, установленными на подвижной подвесной штанге, которая обеспечивает поворот на 342 градуса и стыковку из любого квадранта. Лазерное перекрестие на штанге облегчает выравнивание тележки пациента с обозначенным портом камеры.Роботизированные руки тоньше и имеют дополнительные суставы (суставы с зазором от пациента), которые позволяют вращаться от пациента. Эндоскоп был изменен на 8 мм и может быть помещен в любой рабочий порт робота, что позволяет переключаться между портами камеры. После того, как троакары были вставлены, порт камеры сначала стыкуется, и камера фокусируется на целевой анатомии. Затем функция автоматического нацеливания позволяет оставшимся роботизированным манипуляторам автоматически поворачиваться на стреле, чтобы минимизировать столкновения и оптимизировать производительность.
2.2. Методика
2.2.1. Размещение пациента
Катетер Фолея и назогастральный зонд помещаются перед установкой. Затем пациента помещают в модифицированное положение для бокового пролежня под углом 45 градусов с роликом геля, поддерживающим нижнюю часть спины. Передняя часть живота помещается на боковой край кровати, чтобы минимизировать помехи операционному столу. Все точки давления мягкие. Устанавливается подмышечная впадина, и плечо фиксируется над туловищем подушками (см. Рисунок 2).Плотная шелковая лента накладывается на грудь и бедра, чтобы закрепить пациента на операционной кровати. Мягкая обертка используется для фиксации рук на месте.
2.2.2. Размещение порта
Порт-помощник размещается первым с использованием метода открытого Хассона. Мы используем порт Airseal (SurgiQuest Inc., Милфорд, Коннектикут), расположенный по средней линии на три-четыре сантиметра выше пупка. После достижения пневмоперитонеума вводят лапароскоп и осматривают брюшную полость на предмет повреждений или спаек.Четыре порта для роботов линейно расположены под прямым обзором на боковой границе прямой мышцы живота (рис. 3). Эти порты расположены на расстоянии около 6 см друг от друга. Как правило, второй по высоте порт (порт №2) предназначен для камеры и должен находиться ниже уровня ворот почек. Мы также гарантируем, что между портом №1 и портом №2 достаточно места для размещения вспомогательного порта. Для правосторонних процедур мы устанавливаем субксифоидный порт 5 мм для ретракции печени. Порты для левого RPN показаны на рисунке 3.
2.2.3. Стыковка
Когда тележка пациента приводится в движение для стыковки, активируется лазерное наведение для облегчения точного позиционирования. Лазерное перекрестие, проецируемое из потолочной балки, совмещено с обозначенным портом камеры. Затем порт камеры (порт №2) устанавливается на роботизированный манипулятор, и камера вставляется. Мы фокусируем камеру на предполагаемом местоположении ворот почек, а затем активируем функцию автоматического нацеливания. Поскольку почечные ворота не видны при первоначальном размещении порта, мы использовали внешние сигналы (подреберная область) в дополнение к внутренним сигналам (позади нижней части печени с правой стороны или на несколько дюймов каудально от селезенки слева).Автоматическое нацеливание обеспечивает оптимальное вращение стрелы и размещение робота-манипулятора для максимального доступа и минимизации столкновений. После автоматического позиционирования остальные канюли стыковываются, и роботизированные инструменты размещаются. Роботизированные манипуляторы перемещаются близко друг к другу, чтобы минимизировать столкновение (рис. 4). Наконец, суставы с зазором пациента на руках №1 и №4 поворачиваются к пациенту, чтобы максимизировать движение руки.
2.2.4. Роботизированная частичная нефрэктомия
Камера обычно помещается в порт №2.Остальные роботизированные инструменты включают фенестрированные биполярные, монополярные ножницы и ProGrasp в портах 1, 3 и 4 соответственно. Чтобы обнажить фасцию Героты, мы разделяем белую линию Тольдта и втягиваем толстую кишку медиально. Нижняя сторона Героты развивается до тех пор, пока не будет идентифицирован мочеточник. ProGrasp в 4-й руке используется для поднятия мочеточника над поясничной мышцей, обеспечивая свободный путь к воротам почек. Далее обнажаем почечные сосуды. Все основные артериальные ветви идентифицируются и мобилизуются из окружающих структур.Затем мы сосредотачиваемся на идентификации нашей опухоли. Периренальный жир плавно поднимается над капсулой почки, чтобы обеспечить широкое обнажение. Для опухолей, расположенных сзади, мы отделим околопочечный жир вокруг всей почки, чтобы она отражалась на 180 градусов. Как только опухоль идентифицирована, мы вводим ультразвуковой зонд, чтобы определить глубину и границы опухоли. С помощью прижигания оценивают края опухоли. Для борьбы с грудными клетками бульдожьи зажимы Reliance (Scanlan International, Сент-Пол, Миннесота) вводятся лапароскопически и передаются в ProGrasp.Все основные артериальные ветви зажимаются зажимами типа «бульдог» Reliance, что вызывает ишемию почек. 4-я рука используется для удержания почки в оптимальном положении. Ножницы используются для разреза опухоли без прижигания, в то время как фенестрированный биполярный край используется для удаления опухоли. Широкое использование лапароскопической аспирации имеет решающее значение для поддержания отличного зрения и обеспечения доброкачественного внешнего вида краев опухоли. После полного удаления опухоли ее помещают над печенью или селезенкой. Затем берут биопсию глубокого края основания опухоли и любых подозрительных областей, которые сразу же удаляют, как это принято в обычном учреждении.Затем левый и правый роботизированные инструменты заменяются на большие роботизированные иглодержатели. Любые дискретные кровоточащие сосуды или дефекты собирательной системы закрываются швом с зазубринами 2-0. Затем дефект почки закрывают в два слоя методом скользящей реноррафии с помощью швов с зазубринами и зажимов hem-o-lok [8]. После обеспечения гемостаза зажимы снимаются с почечных сосудов. Почечное закрытие и ворот исследуют, опухоль помещается в мешок для эндопротезирования и извлекается.Затем мы помещаем дренаж в боковую почечную ямку. Затем процедуры закрытия выполняются стандартным образом.
3. Результаты
С мая по июль 2014 г. 15 пациентам с новообразованиями почек 1 клинической стадии была выполнена РПН с помощью хирургической системы Da Vinci Xi. РПН удалось успешно выполнить у всех пациентов без перехода на радикальную нефрэктомию или переход на открытую частичную нефрэктомию. В таблице 1 перечислены демографические и предоперационные характеристики пациентов. Средний возраст пациентов составлял 61 год, примерно половину из них составляли женщины.Средний ИМТ пациента составил 30,6. Средняя рСКФ до операции составляла 76,1 мл / мин / 1,73 м 2 . У пяти пациентов была хроническая болезнь почек 3 стадии и выше. Всем пациентам была проведена предоперационная КТ или МРТ. Средний размер опухоли составил 2,74 см. Пациенты имели опухоли различной сложности. Средний балл сложности почечной недостаточности был умеренным. У семи пациентов были поражения низкой сложности, а у трех пациентов — очень сложные поражения.
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Для рабочих параметров (Таблица 2) среднее время консоли составляло 101,3 минуты, а среднее время размещения порта — 17,5 минут. Во время случая было потеряно в среднем 120 мл крови, а средний срок пребывания в больнице составил 2 дня. Время ишемии было постоянно коротким, в среднем 17,5 минут и диапазон 0–40 минут. Одному пациенту сняли зажим.
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
У 12 из 15 пациентов была почечно-клеточная карцинома при окончательной патологии (семь — со светлоклетками, два — с папиллярным типом 1 и три — с хромофобами).У трех пациентов было доброкачественное заболевание, у одного — доброкачественная кистозная болезнь, а у двух — онкоцитома. Все хирургические поля были отрицательными, и у всех пациентов было заболевание pT1. Все биопсии глубокого основания также были отрицательными. Все пациенты были выписаны через POD № 3 и 66% были выписаны через POD № 2. Отмечено два периоперационных осложнения. У одного 30-летнего пациента мужского пола в первый послеоперационный день (POD) уровень гемоглобина упал с 14 до 6 г / дл. Ангиограмма показала псевдоаневризму небольшой артерии у нижнего края дефекта.Это было успешно реализовано. Ему перелили 2 единицы и выписали в ОП №3. Вторым осложнением была повторная госпитализация по поводу возможной ИМП у сорокалетней женщины на POD №4. Культуры и изображения были отрицательными, и ее выписали домой.
4. Обсуждение
Для опытного хирурга-робота RPN может выполняться без проблем на XI с некоторыми заметными отличиями. Размещение портов на XI при этой процедуре значительно отличается от Si. XI разработан для параллельного движения, что означает, что инструменты работают лучше всего, когда они работают в почти параллельной конфигурации.Это делает размещение портов идеальным, когда порты выстроены в линию. В отличие от Si порт 4-го плеча обычно размещается сбоку от других портов. Такое боковое размещение часто вызывает внешнее или внутреннее столкновение. Для RPN размещение порта 4-го плеча по средней линии является преимуществом и обеспечивает большую функциональность с минимальным столкновением. На XI мы можем использовать 4-ю руку для выполнения нескольких задач, включая втягивание кишечника, подъем нижнего полюса почки и удержание почки в нужном положении во время экстирпативной и реконструктивной фаз операции.
Кроме того, порты могут (и должны) располагаться значительно ближе друг к другу по сравнению с Si. Между портами на XI должно быть 6 см по сравнению с 8–10 см для Si. Когда порты расположены близко друг к другу, рычаги могут работать параллельно друг другу. Кроме того, размер камеры на XI составляет 8 мм, что позволяет разместить ее в любом из роботизированных портов. Переключение портов камеры пока что является эксклюзивной особенностью Da Vinci Xi; однако мы не сочли это необходимым для RPN.
Пожалуй, наиболее заметное различие в XI заключается в фазе стыковки.
Тележка пациента XI занимает другое физическое пространство, чем Si. Одним из основных преимуществ является добавление стрелы, которая позволяет роботизированным манипуляторам выдвигаться и вращаться, чтобы облегчить стыковку под разными углами. Это позволяет пациенту более гибко позиционировать себя в операционной. Одним из недостатков стрелы является то, что она создает дополнительную высоту тележки для пациента.В наших операционных это означает более тщательную навигацию по потолочным креплениям. Мы пристыковали робота как с ног (с поворотом стрелы на 90 градусов), так и со стороны пациента (перпендикулярно операционному столу). Боковая стыковка обеспечивает наиболее надежное прицеливание, независимо от роста пациента.
Большая часть оперативной техники для RPN на XI аналогична таковой на Si. Мы отметили несколько изменений с камерой. Видеокамера XI имеет автофокусировку, что позволяет сэкономить время.Однако точность цвета ткани на камере может колебаться, особенно когда на поле есть кровь, иногда с оранжевым оттенком. Кроме того, дым от каутера более навязчивый, чем на Si. Мы использовали бесклапанный порт Airseal с непрерывным отсосом дыма, чтобы устранить это ограничение. Несомненным преимуществом является то, что инструменты для XI на 1,75 дюйма длиннее, что обеспечивает больший радиус действия и способствует мобилизации верхних полюсов почек при РПН.
Наше консольное время и время ишемии были относительно короткими, даже при наличии опухолей средней сложности.Наше среднее время ишемии 17,5 минут и расчетная кровопотеря (EBL) выгодно отличаются от других больших серий роботизированной частичной нефрэктомии с предшествующими моделями Да Винчи [9, 10]. Long et al. описывают среднее время тепловой ишемии 19,2 мин и среднее значение EBL 260 мл у 400 пациентов, получавших лечение с помощью предыдущих моделей роботизированной системы Да Винчи [1]. Более того, недавний метаанализ включал 23 различных исследования с участием 1152 пациентов, получавших РПН, и обнаружил диапазон среднего WIT от 18 до 35,5 минут и диапазон среднего EBL от 93 до 490 мл [6].Хотя сравнительные испытания отсутствуют, наши периоперационные данные показывают, что роботизированная частичная нефрэктомия с помощью Da Vinci Xi, по крайней мере, сопоставима с роботизированной частичной нефрэктомией с предыдущими версиями робота. В текущем исследовании мы сосредоточились на опухолях почек T1; однако в будущем можно рассмотреть более крупные опухоли, которые поддаются частичной нефрэктомии. Пациентам со значительной почечной недостаточностью и сложными образованиями почек была предложена открытая частичная нефрэктомия.
В целом хирурги считают, что XI предлагает значительные улучшения по сравнению с Si для RPN.Стыковка была более точной, а столкновение инструментов было минимальным. В частности, XI добавил полезности 4-му плечу и в целом сделал ход корпуса более плавным. Из-за технологических изменений в роботе размещение портов и процедура стыковки заметно отличаются от типичных процедур с предыдущими версиями робота. Время консервации и время ишемии были ожидаемо короткими. Периоперационные исходы и патологические исходы были аналогичны нашему предыдущему опыту с РПН.
5. Выводы
RPN с системой Da Vinci Xi может выполняться безопасным и воспроизводимым образом.Это последнее обновление обеспечивает несколько преимуществ по сравнению с предыдущей системой, которые могут способствовать более эффективной процедуре, но требуются дальнейшие исследования для полного выяснения результатов производительности в различных условиях.
Конфликт интересов
Джордж Дж. С. Каллингал, Санджая Суэйн, Фади Дарвиче, Санодж Пуннен, Муругесан Манохаран, Марк Л. Гонсалго и Дипен Дж. Парех заявляют, что у них нет личного или институционального конфликта интересов.
Новый хирургический робот Da Vinci Xi оптимизирован для сложных процедур
Способность принимать решения автономно — это не только то, что делает роботов полезными, но и то, что делает роботов роботов .Мы ценим роботов за их способность чувствовать, что происходит вокруг них, принимать решения на основе этой информации, а затем предпринимать полезные действия без нашего участия. В прошлом роботизированный процесс принятия решений следовал четко структурированным правилам — если вы чувствуете это, то делайте то. В структурированной среде, такой как фабрики, это работает достаточно хорошо. Но в хаотических, незнакомых или плохо определенных условиях зависимость от правил делает роботов заведомо плохо справляющимися со всем, что нельзя точно спрогнозировать и спланировать заранее.
RoMan, наряду с многими другими роботами, включая домашних пылесосов, , беспилотные летательные аппараты и автономные автомобили, решает проблемы слабоструктурированной среды с помощью искусственных нейронных сетей — вычислительный подход, который слабо имитирует структуру нейронов в биологическом мозге. Около десяти лет назад искусственные нейронные сети начали применяться к широкому спектру полуструктурированных данных, которые раньше было очень трудно интерпретировать компьютерам, выполняющим программирование на основе правил (обычно называемое символическим мышлением).Вместо того, чтобы распознавать конкретные структуры данных, искусственная нейронная сеть способна распознавать шаблоны данных, идентифицируя новые данные, которые похожи (но не идентичны) на данные, с которыми сеть сталкивалась ранее. Действительно, часть привлекательности искусственных нейронных сетей заключается в том, что они обучаются на примере, позволяя сети принимать аннотированные данные и изучать свою собственную систему распознавания образов. Для нейронных сетей с несколькими уровнями абстракции этот метод называется глубоким обучением.
Несмотря на то, что люди обычно участвуют в процессе обучения, и хотя искусственные нейронные сети были вдохновлены нейронными сетями в человеческом мозгу, способ распознавания образов в системе глубокого обучения принципиально отличается от того, как люди видят мир. Часто почти невозможно понять взаимосвязь между данными, вводимыми в систему, и интерпретацией данных, выводимых системой. И это различие — непрозрачность «черного ящика» глубокого обучения — представляет собой потенциальную проблему для таких роботов, как RoMan, и для лаборатории армейских исследований.
В хаотических, незнакомых или плохо определенных условиях зависимость от правил делает роботов заведомо плохо справляющимися со всем, что нельзя точно спрогнозировать и спланировать заранее.
Эта непрозрачность означает, что роботов, полагающихся на глубокое обучение, нужно использовать осторожно. Система глубокого обучения хороша в распознавании закономерностей, но ей не хватает понимания мира, которое человек обычно использует для принятия решений, поэтому такие системы лучше всего работают, когда их приложения хорошо определены и имеют узкую область применения.«Когда у вас есть хорошо структурированные входы и выходы, и вы можете заключить свою проблему в такие отношения, я думаю, что глубокое обучение очень хорошо работает», — говорит Том Ховард, который руководит лабораторией робототехники и искусственного интеллекта Университета Рочестера и разработал алгоритмы взаимодействия на естественном языке для RoMan и других наземных роботов. «При программировании интеллектуального робота возникает вопрос, в каком практическом масштабе существуют эти строительные блоки для глубокого обучения?» Ховард объясняет, что когда вы применяете глубокое обучение к проблемам более высокого уровня, количество возможных входных данных становится очень большим, и решение проблем такого масштаба может быть сложной задачей.И потенциальные последствия неожиданного или необъяснимого поведения гораздо более значительны, когда это поведение проявляется в 170-килограммовом двуруком военном роботе.
Спустя пару минут Роман не двигался — он все еще сидит, размышляя о ветке дерева, раскинув руки, как богомол. В течение последних 10 лет Альянс Robotics Collaborative Technology Alliance (RCTA) лаборатории армейских исследований работал с робототехниками из Университета Карнеги-Меллона, Университета штата Флорида, General Dynamics Land Systems, JPL, MIT, QinetiQ North America, Университета Центральной Флориды. , Пенсильванский университет и другие ведущие исследовательские институты для разработки автономных роботов для использования в будущих наземных боевых машинах.RoMan — одна из частей этого процесса.
Задача «расчистить путь», над которой медленно обдумывает RoMan, трудна для робота, потому что задача настолько абстрактна. RoMan должен идентифицировать объекты, которые могут блокировать путь, рассуждать о физических свойствах этих объектов, выяснять, как их захватить и какую технику манипуляции лучше всего применить (например, толкать, тянуть или поднимать), а затем Сделай это. Это много шагов и много неизвестного для робота с ограниченным пониманием мира.
В этом ограниченном понимании роботы ARL начинают отличаться от других роботов, которые полагаются на глубокое обучение, — говорит Итан Стамп, главный научный сотрудник программы AI для маневра и мобильности в ARL. «Армия может быть задействована практически в любой точке мира. У нас нет механизма для сбора данных во всех различных областях, в которых мы могли бы работать. Мы можем быть размещены в каком-то неизвестном лесу на другой стороне world, но ожидается, что мы будем работать так же хорошо, как и на собственном заднем дворе », — говорит он.Большинство систем глубокого обучения надежно работают только в тех областях и средах, в которых они прошли обучение. Даже если домен — это что-то вроде «каждой дороги в Сан-Франциско», с роботом все будет в порядке, потому что это уже собранный набор данных. Но, по словам Стампа, это не вариант для военных. Если армейская система глубокого обучения не работает должным образом, они не могут просто решить проблему путем сбора дополнительных данных.
Роботы ARL также должны хорошо понимать, что они делают.«В стандартном операционном порядке для миссии у вас есть цели, ограничения, параграф о намерениях командира — в основном повествование о цели миссии — который предоставляет контекстную информацию, которую люди могут интерпретировать, и дает им структуру, когда им нужно чтобы принимать решения и когда им нужно импровизировать », — объясняет Стамп. Другими словами, РоМану может потребоваться быстро расчистить путь, или ему может потребоваться расчистить путь тихо, в зависимости от более широких целей миссии. Это большая просьба даже для самого продвинутого робота.«Я не могу придумать подход, основанный на глубоком обучении, который мог бы работать с такой информацией», — говорит Стамп.
Пока я смотрю, RoMan сбрасывается для второй попытки удаления ветки. Подход ARL к автономности является модульным, где глубокое обучение сочетается с другими методами, а робот помогает ARL выяснить, какие задачи подходят для каких методов. В настоящее время RoMan тестирует два разных способа идентификации объектов по данным 3D-сенсора: подход UPenn основан на глубоком обучении, а Carnegie Mellon использует метод, называемый восприятием через поиск, который опирается на более традиционную базу данных 3D-моделей.Восприятие посредством поиска работает только в том случае, если вы заранее точно знаете, какие объекты ищете, но обучение проходит намного быстрее, поскольку вам нужна только одна модель для каждого объекта. Он также может быть более точным, когда восприятие объекта затруднено — например, если объект частично скрыт или перевернут. ARL тестирует эти стратегии, чтобы определить, какая из них наиболее универсальна и эффективна, позволяя им работать одновременно и конкурировать друг с другом.
Восприятие — это одна из вещей, в которых глубокое обучение стремится преуспеть.«Сообщество компьютерного зрения добилось сумасшедшего прогресса, используя глубокое обучение для этого», — говорит Мэгги Вигнесс , ученый-компьютерщик из ARL. «Мы добились хороших успехов с некоторыми из этих моделей, которые были обучены в одной среде, обобщенной для новой среды, и мы намерены продолжать использовать глубокое обучение для такого рода задач, потому что это современное состояние».
Модульный подход ARL может сочетать несколько методов таким образом, чтобы максимально использовать их сильные стороны.Например, система восприятия, которая использует зрение на основе глубокого обучения для классификации местности, может работать вместе с автономной системой вождения, основанной на подходе, называемом обучением с обратным подкреплением, где модель может быть быстро создана или уточнена на основе наблюдений людей-солдат. Традиционное обучение с подкреплением оптимизирует решение, основанное на установленных функциях вознаграждения, и часто применяется, когда вы не всегда уверены, как выглядит оптимальное поведение. Это меньше беспокоит армию, которая обычно может предположить, что хорошо обученные люди будут поблизости, чтобы показать роботу, как правильно действовать.«Когда мы запускаем этих роботов, все может измениться очень быстро», — говорит Вигнесс. «Поэтому нам нужна была техника, в которой мы могли бы вмешаться солдата, и с помощью всего лишь нескольких примеров от пользователя в полевых условиях, мы могли бы обновить систему, если нам понадобится новое поведение». По ее словам, метод глубокого обучения потребует «гораздо больше данных и времени».
Глубокое обучение борется не только с проблемами нехватки данных и быстрой адаптацией. Есть также вопросы надежности, объяснимости и безопасности.«Эти вопросы не являются уникальными для военных, — говорит Стамп, — но они особенно важны, когда мы говорим о системах, которые могут включать летальность». Чтобы быть ясным, ARL в настоящее время не работает над летальными автономными системами оружия, но лаборатория помогает заложить основу для автономных систем в армии США в более широком смысле, что означает рассмотрение способов использования таких систем в будущем.
Требования глубокой сети в значительной степени не соответствуют требованиям армейской миссии, и это проблема.
По словам Стампа, безопасность является очевидным приоритетом, и все же нет четкого способа сделать систему глубокого обучения достоверно безопасной. «Глубокое обучение с ограничениями безопасности — это серьезное исследовательское усилие. Трудно добавить эти ограничения в систему, потому что вы не знаете, откуда взялись ограничения, уже существующие в системе. Поэтому, когда меняется миссия или меняется контекст, с этим трудно справиться. Это даже не вопрос данных, это вопрос архитектуры ». Модульная архитектура ARL, будь то модуль восприятия, использующий глубокое обучение, или автономный модуль вождения, использующий обучение с обратным подкреплением, или что-то еще, может формировать части более широкой автономной системы, которая включает в себя те виды безопасности и адаптивности, которые требуются военным.Другие модули в системе могут работать на более высоком уровне, используя другие методы, которые более поддаются проверке или объяснению и которые могут вмешиваться для защиты всей системы от неблагоприятного непредсказуемого поведения. «Если появляется другая информация и меняет то, что нам нужно делать, существует иерархия», — говорит Стамп. «Все происходит рационально».
Николас Рой , который возглавляет группу Robust Robotics Group в Массачусетском технологическом институте и описывает себя как «в некотором роде подстрекатель сброда» из-за своего скептицизма по поводу некоторых заявлений о силе глубокого обучения, соглашается с робототехниками ARL, что Подходы с глубоким обучением часто не могут справиться с проблемами, к которым должна быть готова армия.«Армия всегда входит в новую среду, и противник всегда будет пытаться изменить среду, чтобы тренировочный процесс, через который прошли роботы, просто не соответствовал тому, что они видят», — говорит Рой. «Таким образом, требования глубокой сети в значительной степени не соответствуют требованиям армейской миссии, и это проблема».
Рой, который работал над абстрактными рассуждениями для наземных роботов в рамках RCTA, подчеркивает, что глубокое обучение является полезной технологией в применении к проблемам с четкими функциональными взаимосвязями, но когда вы начинаете смотреть на абстрактные концепции, неясно, подходит ли глубокое обучение. жизнеспособный подход.«Мне очень интересно узнать, как нейронные сети и глубокое обучение могут быть скомпонованы таким образом, чтобы поддерживать рассуждения более высокого уровня», — говорит Рой. «Я думаю, что все сводится к идее объединения нескольких нейронных сетей низкого уровня для выражения концепций более высокого уровня, и я не верю, что мы пока понимаем, как это сделать». Рой приводит пример использования двух отдельных нейронных сетей: одна для обнаружения объектов, которые являются автомобилями, а другая — для обнаружения объектов красного цвета. Объединить эти две сети в одну большую сеть, обнаруживающую красные машины, сложнее, чем если бы вы использовали систему символических рассуждений, основанную на структурированных правилах с логическими отношениями.«Многие люди работают над этим, но я не видел настоящего успеха, который приводил бы к абстрактным рассуждениям подобного рода».
В обозримом будущем ARL следит за тем, чтобы его автономные системы были безопасными и надежными, удерживая людей как для рассуждений на более высоком уровне, так и для случайных советов на низком уровне. Люди могут не всегда быть в курсе событий, но идея состоит в том, что люди и роботы более эффективны, когда работают вместе в команде. По словам Стампа, когда в 2009 году началась последняя фаза программы Robotics Collaborative Technology Alliance, «мы уже много лет прожили в Ираке и Афганистане, где роботы часто использовались в качестве инструментов.Мы пытались выяснить, что мы можем сделать, чтобы превратить роботов от инструментов к тому, чтобы они больше действовали как товарищи по команде в отряде ».
RoMan получает небольшую помощь, когда человек-руководитель указывает на область ветви, где хватание может быть наиболее эффективным. Робот не имеет никаких фундаментальных знаний о том, что на самом деле представляет собой ветвь дерева, и это отсутствие знаний о мире (то, что мы считаем здравым смыслом) является фундаментальной проблемой для автономных систем всех видов. Если человек использует наш обширный опыт в небольшом количестве рекомендаций, это может значительно облегчить работу RoMan.И действительно, на этот раз РоМану удается ухватиться за ветку и с шумом протащить ее через комнату.
Превратить робота в хорошего товарища по команде может быть сложно, потому что бывает сложно найти нужную автономию. Слишком мало, и для управления одним роботом потребуется большая часть или все внимание одного человека, что может быть уместно в особых ситуациях, таких как обезвреживание боеприпасов, но в остальном неэффективно. Слишком большая автономия — и у вас начнутся проблемы с доверием, безопасностью и объяснимостью.
«Я думаю, что уровень, который мы здесь ищем, — это чтобы роботы работали на уровне рабочих собак», — объясняет Стамп. «Они точно понимают, что нам нужно, чтобы они делали в ограниченных обстоятельствах, у них есть небольшая гибкость и творческий подход, если они сталкиваются с новыми обстоятельствами, но мы не ожидаем, что они будут творчески решать проблемы. И если им понадобится помощь , они нападают на нас «.
RoMan вряд ли в ближайшее время обнаружит себя в полевых условиях для выполнения задания, даже в составе команды с людьми.Это во многом исследовательская платформа. Но программное обеспечение, разрабатываемое для RoMan и других роботов в ARL, под названием Adaptive Planner Parameter Learning (APPL) , скорее всего, будет сначала использоваться в автономном вождении, а затем в более сложных роботизированных системах, которые могут включать в себя мобильные манипуляторы, такие как RoMan. APPL сочетает в себе различные методы машинного обучения (включая обучение с обратным подкреплением и глубокое обучение), иерархически организованные под классическими автономными навигационными системами. Это позволяет применять цели и ограничения высокого уровня поверх программирования более низкого уровня.Люди могут использовать дистанционно управляемые демонстрации, корректирующие вмешательства и оценочную обратную связь, чтобы помочь роботам адаптироваться к новым условиям, в то время как роботы могут использовать неконтролируемое обучение с подкреплением для корректировки параметров своего поведения на лету. Результатом является автономная система, которая может пользоваться многими преимуществами машинного обучения, а также обеспечивать безопасность и объяснимость, необходимые армии. С APPL система, основанная на обучении, такая как RoMan, может работать предсказуемым образом даже в условиях неопределенности, прибегая к настройке или демонстрации человеком, если она попадает в среду, слишком отличную от той, в которой она обучалась.
Заманчиво взглянуть на быстрый прогресс коммерческих и промышленных автономных систем (автономные автомобили — лишь один из примеров) и задаться вопросом, почему армия, кажется, несколько отстает от современного уровня техники. Но, как Стамп обнаруживает, что вынужден объяснять армейским генералам, когда дело доходит до автономных систем, «существует множество серьезных проблем, но тяжелые проблемы промышленности отличаются от серьезных проблем армии». Армия не может позволить себе роскошь управлять своими роботами в структурированной среде с большим количеством данных, поэтому ARL приложила так много усилий для APPL и сохранения места для людей.В будущем люди, вероятно, останутся ключевой частью автономной структуры, разрабатываемой ARL. «Это то, что мы пытаемся создать с помощью наших робототехнических систем», — говорит Стамп. «Это наш стикер на бампере:« От инструментов к товарищам по команде ». »
Эта статья появится в выпуске для печати за октябрь 2021 года как «Deep Learning Goes to Boot Camp ».
Статьи с вашего сайта
Статьи по теме в Интернете
Роботизированная системаda Vinci XI предлагает новые хирургические возможности для пациентов — Jagwire
Когда дело доходит до выполнения сложной хирургической операции, даже лучшему хирургу может потребоваться рука помощи, даже если эта рука холодная, металлическая и достаточно сильная, чтобы держать самые маленькие инструменты.По этой причине Управление здравоохранения Университета Огаста вводит da Vinci XI в операционную.
«Использование новой системы XI позволит нам увеличить количество пациентов, которые могут получить свою операцию с помощью роботов», — сказал д-р Рабии Мади, директор отделения роботизированной хирургии и урологической онкологии в отделении здравоохранения Университета Огаста и хирург-онколог-уролог из отделения рака Джорджии. Центр и медицинский колледж Джорджии. «Новый робот был разработан для колоректальных, бариатрических и других общих операций, требующих от хирурга работы в нескольких квадрантах тела.”
Новый робот XI (произносится как X-I), дебютировавший в конце декабря на выставке AU Health, позволит нескольким командам работать вместе над несколькими операциями в одной операционной.
«Представьте себе пациента, у которого опухоль почки и образование в яичнике», — сказала доктор Марта Террис, руководитель отделения урологии Медицинского колледжа Джорджии. «Новый робот позволит мне удалить опухоль почки. Когда я закончу, гинеколог-хирург-онколог сможет взять под контроль робота, чтобы удалить яичник.”
Такой многопрофильный командный подход, который является отличительной чертой ухода за пациентами в Онкологическом центре Джорджии, возможен благодаря штанге, созданной для системы XI. Стрела может поворачиваться почти на 360 градусов. Это позволяет роботу перемещать инструменты вверх из области таза в брюшную полость. Он также может двигаться из стороны в сторону. Все эти движения могут сократить время, необходимое пациенту для пребывания под наркозом, потому что хирургической бригаде не нужно выполнять первую операцию, останавливаться, отстыковывать руки робота, перемещать их во второе положение и затем выполнять вторую процедуру.
«В некоторых случаях настройка второй процедуры может занять около часа», — сказал Террис. «Дизайн новой системы XI позволяет нам быстрее выполнять процедуры для наших пациентов, поэтому они могут быстрее начать выздоровление».
Раньше хирурги, решившие сделать операцию в AU Health, использовали систему SI da Vinci. Хотя система по-прежнему идеально подходит для пациентов, перенесших некоторые операции, наличие новой системы XI сократит время ожидания для пациентов. Наличие двух роботов означает половину времени ожидания для хирургов, которым требуется робот-ассистент для успешной операции.
«Еще одним большим преимуществом является наша способность перемещаться по телу пациента через меньшие разрезы», — сказал Мади. «В системе SI разрез для порта камеры составлял 12 миллиметров. У нового робота XI он составляет всего 8 миллиметров ».
Находясь внутри корпуса, обновления программного обеспечения в новой системе XI помогают инструментам двигаться намного более плавно. Он также включает в себя роботизированный степлер со скобами разного размера.
«Для некоторых бариатрических операций робот SI, возможно, был не лучшим вариантом», — сказал Мади.«Это потому, что он включал скобу только одного размера, что не подходило для этих хирургов».
Умнее стал не только робот. Новая система XI поставляется с «умным» операционным столом. Он знает, как пациент располагается на столе и где внутри его тела происходит операция.
«Вы можете изменить положение пациента, не отстыковывая робота», — сказал Мади. «Инструменты могут даже двигаться вместе со столом».
Конечная цель нового робота всегда сводится к опыту пациента.Каждая новая опция, которая облегчает более короткую и точную операцию, позволяет пациенту быстрее начать выздоровление.


 Эякулят наливают поверх суспензии коллоидных частиц определенной плотности и центрифугируют. В результате самые качественные сперматозоиды оказываются на дне пробирки в виде осадка, а семенная плазма, лейкоциты, эпителиальные клетки и неподвижные сперматозоиды задерживаются в верхних слоях раствора
Эякулят наливают поверх суспензии коллоидных частиц определенной плотности и центрифугируют. В результате самые качественные сперматозоиды оказываются на дне пробирки в виде осадка, а семенная плазма, лейкоциты, эпителиальные клетки и неподвижные сперматозоиды задерживаются в верхних слоях раствора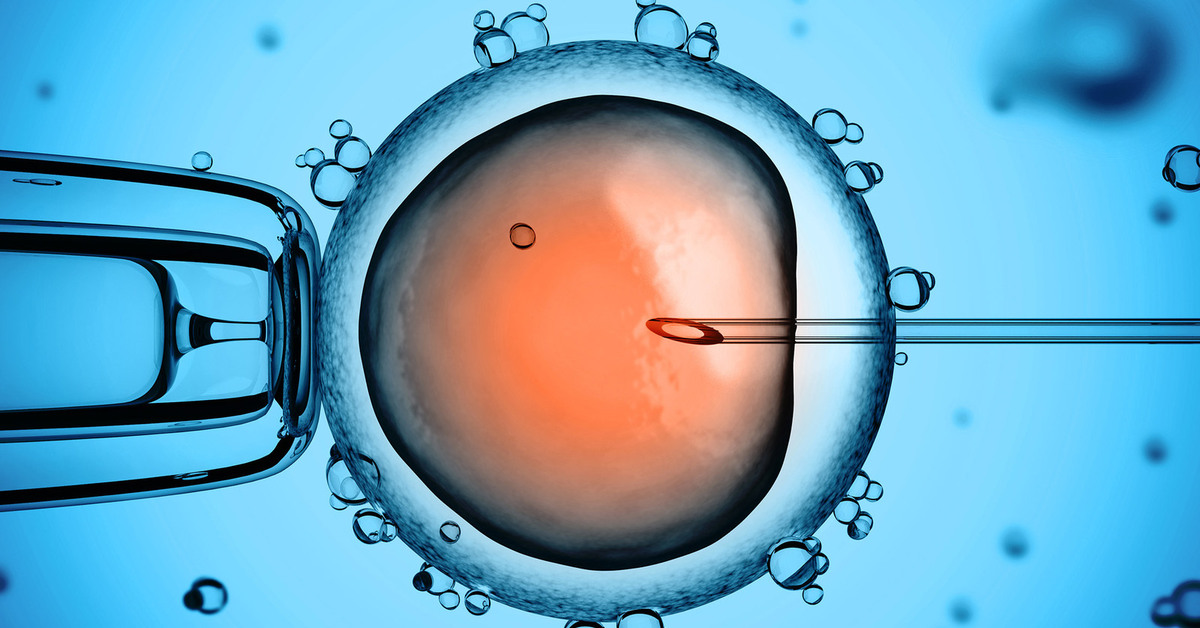 Благодаря ей исключаются любые риски замены биоматериала пациента чужим
Благодаря ей исключаются любые риски замены биоматериала пациента чужим