Гипоксия лечение. Симптомы и лечение у ребенка гипоксии.
Строго говоря, гипоксия — это не диагноз. Так называется состояние, когда организм по тем или иным причинам не получает необходимого для полноценного функционирования количества кислорода. Она может возникать не только у новорожденных, но и у людей взрослого возраста, различны лишь причины, из-за которых возникает кислородное голодание. Следствием гипоксии является нарушение работы жизненно важных органов вплоть до необратимых изменений. Наиболее опасно это состояние для центральной нервной системы. Именно головной мозг получает 20 % всего поступающего в кровь кислорода, поэтому гипоксия может обусловить возникновение неврологических заболеваний.
При возникновении гипоксии симптомы и лечение (если оно вообще требуется) зависят от степени кислородного голодания.
Симптомы гипоксии у детей определяются еще при родах. Сразу после появления ребенка медперсонал оценивает его состояние по шкале Апгар.
Различают три степени гипоксии:
- 8–10 баллов — означает отличное состояние новорожденного;
- 7–6 баллов — гипоксия первой степени, считающаяся легкой формой;
- 5–4 баллов — гипоксия второй степени, классифицируемая как средняя форма;
- 3–0 баллов — третья степень гипоксии, тяжелая форма.
Кислородное голодание легкой степени обычно не сказывается на дальнейшем развитии ребенка, ее симптомы проходят очень быстро. Такая гипоксия лечения не требует.
Гипоксия 2-й степени при должном уходе и лечении редко становится причиной нарушений нормальной работы организма. В первые месяцы лечения возможны нарушения нормального режима сна, тревожность, тремор подбородка.
Тяжелая степень гипоксии может вызвать серьезные последствия в организме ребенка — нередки судороги, задержки в развитии, различные нарушения работы головного мозга.
Если лечение ребенка, перенесшего гипоксию, не начать вовремя, то возможны различные физические и умственные нарушения в развитии. Часто последствиями гипоксии являются гипертонус, задержки психоречевого развития, аутизм, ДЦП, в редких случаях вероятен летальный исход.
Избежать всего этого можно, если еще в раннем возрасте начать лечение последствий гипоксии. Вот почему при выявлении диагноза «гипоксия» у ребенка лечение нужно начинать как можно раньше.
В медицинском центре «Клиника Мельниковой Е.А» проводится полная диагностика раннего выявления нарушений работы головного мозга, после которой высококвалифицированные специалисты дадут все рекомендации для родственников и индивидуально подберут курс лечения.
Головной мозг ребёнка очень чувствителен к гипоксическому повреждению, но в то же время очень пластичен, т. е. от природы наделен восстановительными и компенсаторными функциями.
Поэтому лечение гипоксии и ее последствий по методикам, разработанным главврачом нашей Клиники — врачом-невропатологом высшей категории Мельниковой Е. А. — дает наилучшие положительные результаты при своевременном обращении.
А. — дает наилучшие положительные результаты при своевременном обращении.
Записывайтесь к нам на лечение, либо на консультацию к нашим специалистом!
%PDF-1.6 % 1 0 obj > endobj 4 0 obj /ModDate (D:20160622161537+03’00’) /Subject >> endobj 2 0 obj > stream application/pdf

Внутриутробная гипоксия плода — признаки, острая, хроническая, внутриутробная гипоксия плода последствия
Острая и хроническая гипоксия плода
Внутриутробная гипоксия плода – это патология, при которой еще не рожденному ребенку не хватает кислорода в утробе матери. Давайте поговорим о признаках гипоксии, ее видах, методах диагностики и последствиях.
Типы гипоксии, ее причины и последствия
Нехватка кислорода может быть хронической и острой. Первая встречается чаще и является более благоприятной для матери и ребенка. Признаки гипоксии плода хронической – это различные патологии беременности и заболевания матери, которые могут провоцировать регулярную нехватку кислорода. Это заболевания дыхательной системы (к примеру, бронхиальная астма), курение, фетоплацентарная недостаточность, когда через плаценту к ребенку в кровоток не попадает достаточное количество питания и кислорода, железодефицитная анемия.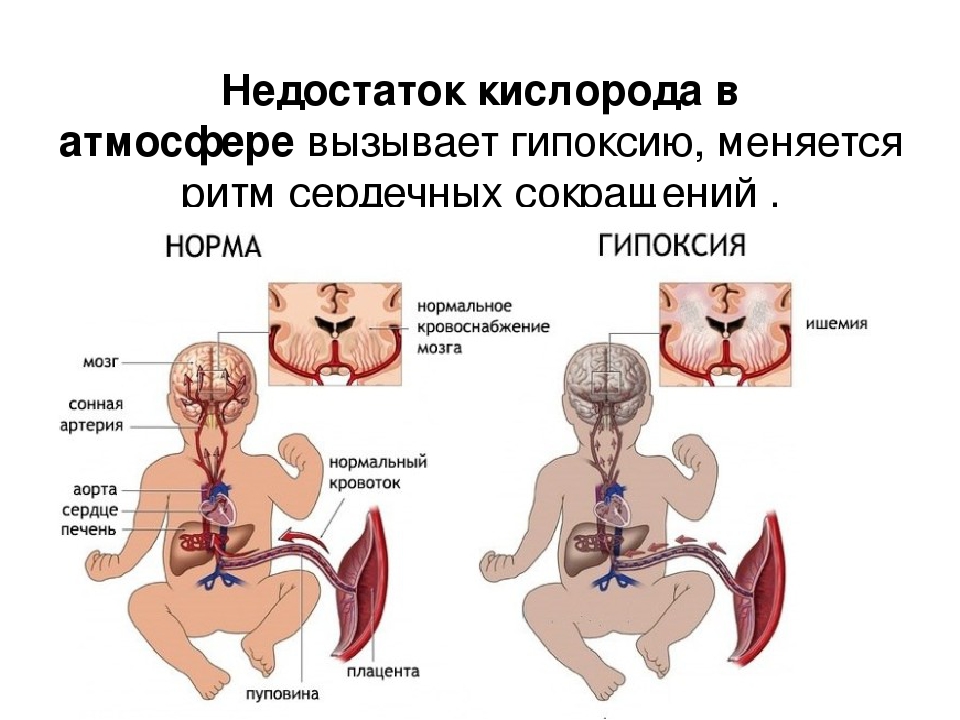
Намного опаснее острая гипоксия плода, когда ребенок может погибнуть за считанные минуты. Такая патология может возникать на любом сроке беременности и в процессе родов. Причиной может стать тугое многократное обвитие пуповиной, узлы на пуповине, разрыв матки, отслойка плаценты и др. Если диагностируется острая нехватка кислорода, женщине проводят экстренную операцию кесарево сечение. В таких случаях каждая минута дорога, так как длительная гипоксия у новорожденных приводит к смерти клеток головного мозга.
Если диагностируется острая нехватка кислорода, женщине проводят экстренную операцию кесарево сечение. В таких случаях каждая минута дорога, так как длительная гипоксия у новорожденных приводит к смерти клеток головного мозга.
Более благоприятный исход, как правило, имеет гипоксия затяжная. Но из-за недостатка кислорода и питательных веществ ребенок может медленно развиваться и даже к моменту родов не быть жизнеспособным в естественных условиях. Таких слабых детей выхаживают в кювезах, с помощью современного медицинского оборудования.
Диагностика кислородного голодания плода
Если с диагностикой острой нехватки кислорода обычно не возникает проблем, то о хронической можно длительное время не подозревать, особенно, если женщина не часто посещает гинеколога и не проходит УЗИ в рекомендованные сроки.
Узнать, достаточно ли ребенку кислорода, в порядке ли кровоток можно 3 способами.
1. Когда врач прослушивает с помощью акушерского стетоскопа сердцебиение ребенка через стенку матки. Врач обращает внимание на частоту сердцебиений. Если она ниже нормы – это признак патологии.
Врач обращает внимание на частоту сердцебиений. Если она ниже нормы – это признак патологии.
2. Более точно проследить сердечный ритм можно с помощью КТГ. Это что-то вроде ЭКГ, но только на нем исследуют сердцебиение плода.
3. С помощью допплерографии. Выполняется также, как обычное УЗИ. Исследуется кровоток в маточных артериях.
Кроме того, сама женщина должна следить за состояние своего ребенка. Это довольно легко сделать с того момента, как начинают ощущаться шевеления. За сутки малыш должен шевелиться не менее 10 раз. Причем увеличение числа шевелений – симптом менее опасный, чем уменьшение. Ребенок может шевелиться более активно, если женщина принимает неудобную позу, может таким образом реагировать на яркий свет и т. д. А меньше дети шевелятся обычно именно из-за недостатка кислорода.
Чтобы вовремя заметить патологию или удостовериться в хорошем самочувствии ребенка, нужно в рекомендованные сроки сдавать все анализы и проходить обследования. Помните, что внутриутробная гипоксия плода последствия может иметь довольно тяжелые. Но ее в большинстве случаев можно предупредить.
Но ее в большинстве случаев можно предупредить.
Развитие детей, перенесших острую и хроническую гипоксию
На правах рукописи —
Пронина Ольга Александровна
РАЗВИТИЕ ДЕТЕЙ, ПЕРЕНЕСШИХ ОСТРУЮ И ХРОНИЧЕСКУЮ ГИПОКСИЮ
14,00.09 — педиатрия
АВТОРЕФЕРАТ
диссертации на соискание ученой степени кандидата медицинских наук
Воронеж — 2009
003469525
Работа выполнена в Государственном образовательном учреждении высшего профессионального образования «Воронежская государственная медицинская академия им. H.H. Бурденко Федерального агентства по здравоохранению и социальному развитию» (ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава)
Научный руководитель: Официальные оппоненты:
Ведущая организация:
доктор медицинских наук, профессор Логвинова Ия Ивановна
доктор медицинских наук, профессор Ситникова Валентина Пантелеевна кандидат медицинских наук Савченко Андрей Пантелеевич
ГОУ ВПО «Волгоградский государственный медицинский университет Федерального агентства по здравоохранению и социальному развитию»
Защита диссертации состоится «2» июня 2009 года в 10°° часов на заседании диссертационного совета Д. 208.009.02 при ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава по адресу: 394036, Россия, г. Воронеж, ул. Студенческая, д. 10.
208.009.02 при ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава по адресу: 394036, Россия, г. Воронеж, ул. Студенческая, д. 10.
С диссертацией можно ознакомиться в библиотеке ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава
Автореферат разослан «30» апреля 2009 года.
Ученый секретарь диссертационного совета
A.B. Будневский
ОБЩАЯ ХАРАКТЕРИСТИКА РАБОТЫ
Актуальность
Перинатальная гипоксия занимает одно из ведущих мест среди перинатальных факторов, оказывающих влияние не только на состояние плода, но и на особенности течения периода новорожденное™, что, в конечном итоге, сказывается на здоровье и дальнейшем развитии ребенка (Баранов A.A., 2001, Балаболкин И.И., 2003). По данным Барашнева Ю.И. (2005) внутриутробная гипоксия и гипоксия в родах в 38,45% случаев является причиной перинатальной смертности, а в 59,04% — причиной мертворождений. Частота перинатальной гипоксии не имеет тенденции к уменьшению. 60-80% всех заболеваний ЦНС детского возраста связано с перинатальной гипоксией (Бадалян Л. О., 2001). Более половины всех случаев расстройств функций ЦНС у детей раннего возраста обусловлено не острой гипоксией в родах, а длительной, хронической гипоксией плода и новорожденного (Paneth N., 1983, Nelsons К.В., 1996, Volpe J.J., 2008). Значимость проблемы состоит в том, что поражения головного мозга гипоксического генеза определяют неврологическое здоровье и инвалидность с детства (Пальчик А.Б,, 2001; Барашнев Ю.И., 2005). Необходим поиск комплекса современных клинических и лабораторных критериев, позволяющих улучшить раннюю диагностику и прогноз повреждений нервной системы у детей. Своевременное выявление постгипоксических нарушений имеет огромное значение для построения адекватной терапии неврологических расстройств и их профилактики (Барашнев Ю.И., 1991, Баранов A.A., 2006).
О., 2001). Более половины всех случаев расстройств функций ЦНС у детей раннего возраста обусловлено не острой гипоксией в родах, а длительной, хронической гипоксией плода и новорожденного (Paneth N., 1983, Nelsons К.В., 1996, Volpe J.J., 2008). Значимость проблемы состоит в том, что поражения головного мозга гипоксического генеза определяют неврологическое здоровье и инвалидность с детства (Пальчик А.Б,, 2001; Барашнев Ю.И., 2005). Необходим поиск комплекса современных клинических и лабораторных критериев, позволяющих улучшить раннюю диагностику и прогноз повреждений нервной системы у детей. Своевременное выявление постгипоксических нарушений имеет огромное значение для построения адекватной терапии неврологических расстройств и их профилактики (Барашнев Ю.И., 1991, Баранов A.A., 2006).
На современном этапе развития медицинской науки установлено, что гипоксия, ишемия, ацидоз индуцируют синтез эндотелина-1 (ЭТ-1) (Isozaki-Fukuda Y., 1991, Антонов А.Г., 2006). ЭТ-1 оказывается причастным к сердечно-сосудистой и почечной патологии, диабету (La М. , 1995, Gray G., 1996, Pernow J., 1997, Rhoten R., 1997, Schiffrin E.L., 2001, D. Behrendt, 2002, Touyz RM, 2003,), а также участвует в патогенезе легочной гипертензии и постгипоксических нарушений сердечно-сосудистой системы у новорожденных (Kumar Р, 1996, Perreault Т, 2003, Зузенкова Л.В., 2008). Роль ЭТ-1 в развитии перинатальных гипоксических поражений ЦНС и их исходов у новорожденных изучена недостаточно.
, 1995, Gray G., 1996, Pernow J., 1997, Rhoten R., 1997, Schiffrin E.L., 2001, D. Behrendt, 2002, Touyz RM, 2003,), а также участвует в патогенезе легочной гипертензии и постгипоксических нарушений сердечно-сосудистой системы у новорожденных (Kumar Р, 1996, Perreault Т, 2003, Зузенкова Л.В., 2008). Роль ЭТ-1 в развитии перинатальных гипоксических поражений ЦНС и их исходов у новорожденных изучена недостаточно.
В связи с изложенным выше, изучение дальнейшего физического, нервно-психического развития, соматической заболеваемости, оптимизация диагностики и прогнозирования неврологической патологии у детей, перенесших острую и хроническую перинатальную гипоксию, а также изучение роли ЭТ-1 в развитии неврологических расстройств у детей являются весьма актуальными.
Цель исследования
Провести мониторинг развития детей, перенесших острую и хроническую перинатальную гипоксию, а также определить роль ЭТ-1 в
развитии неврологических расстройств гипоксического генеза у детей и выявить наиболее значимые факторы, влияющие на их компенсацию.
Задачи исследования
1. Изучить течение раннего неонатального периода у детей, перенесших острую и хроническую гипоксию.
2. Оценить физическое развитие детей до 3-х лет, перенесших острую, хроническую и сочетанную перинатальную гипоксию.
3. Провести анализ соматической заболеваемости у детей до 3-х лет, перенесших внутриутробную и интранатальную гипоксию.
4. Сравнить неврологические нарушения и сроки их компенсации, в зависимости от вида перенесенной гипоксии.
5. Определить факторы, влияющие на наступление неврологической компенсации после 1,5 лет у детей, перенесших перинатальную гипоксию.
6. Изучить роль ЭТ-1 в развитии неврологических расстройств у новорожденных.
Новизна исследования
Установлены особенности течения раннего неонатального периода, физического развития, соматической заболеваемости у детей, перенесших острую, хроническую и сочетанную гипоксию.
Выявлены особенности неврологических нарушений и сроки их компенсации, в зависимости от вида перенесенной гипоксии.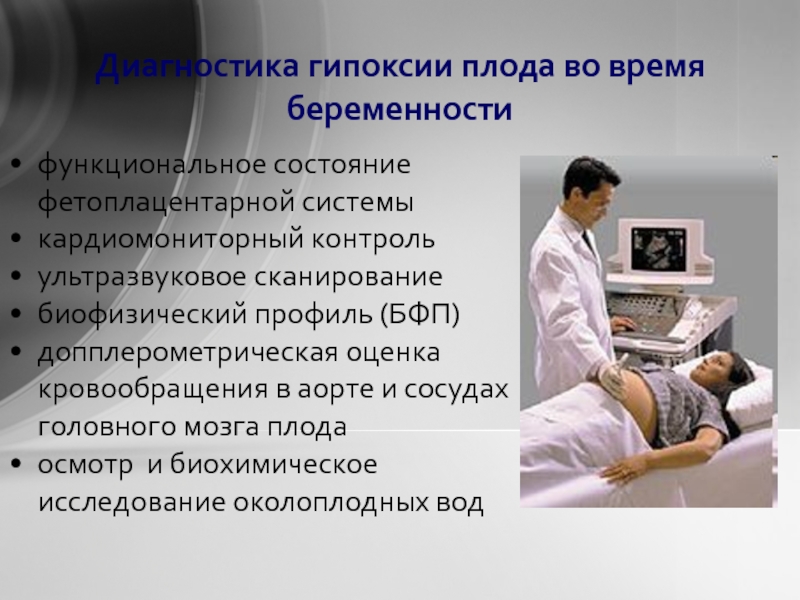
Определен прогностический вклад факторов, влияющих на позднее наступление неврологической компенсации у детей, перенесших перинатальную гипоксию.
Выявлена диагностическая и прогностическая значимость ЭТ-1 в развитии ХВГП и неврологических нарушений у детей, перенесших внутриутробную гипоксию.
Практическая значимость
Определены особенности течения раннего неонатального периода, физического развития, соматической заболеваемости, неврологических нарушений и сроки их компенсации у детей, в зависимости от вида перенесенной гипоксии.
Установлено, что определение концентрации ЭТ-1 в плазме пуповинной крови и в период ранней неонатальной адаптации у детей с высоким риском хронической внутриутробной гипоксии позволяет судить о наличии постгипоксических нарушений. Показатели ЭТ-1 могут служить критерием раннего прогнозирования развития последствий перинатального поражения ЦНС у детей на первом году жизни.
Выявлено, что для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка
группы факторов, включающих антенатальное развитие и интранатальный период, неонатальную заболеваемость и данные нейросонографии, заболеваемость на протяжении первых 3-х лет жизни.
Предложено комплексное обследование и наблюдение детей, перенесших перинатальную гипоксию, включающее в себя определение ЭТ-1 в пуповинной крови, оценку физического развития с обязательным ежемесячным определением окружностей головы и груди на протяжении 11,5 лет, оценку неврологического и соматического статуса, обязательное проведение нейросонографии не однократно, даже при отсутствии патологии при предыдущих исследованиях. Данный комплекс обследования позволяет выявить в более ранние сроки наличие соматических и неврологических расстройств, а также способствует определению «клинически немых» форм поражения головного мозга и своевременной коррекции выявленных нарушений.
Внедрение в практику
Рекомендации, разработанные на основании полученных в ходе диссертационного исследования данных, используются в учебном процессе на кафедре неонатологии ГОУ ВПО ВГМА им. H.H. Бурденко Росздрава.
Основные положения, выносимые иа защиту:
1. Особенности течения раннего неонатального периода, физического развития, соматической заболеваемости, неврологических нарушений и сроки их компенсации у детей, в зависимости от вида перенесенной гипоксии, необходимо учитывать для профилактики развития постгипоксических нарушений у детей сразу после рождения и в раннем возрасте.
2. Определение концентрации ЭТ-1 в плазме пуповинной крови и в период ранней неонатальной адаптации у детей с высоким риском хронической внутриутробной гипоксии позволяет судить о наличии постгипоксических нарушений. Показатели ЭТ-1 в пуповинной крови могут служить критерием раннего прогнозирования развития последствий перинатальных поражений ЦНС у детей на первом году жизни.
3. Для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка группы материнских факторов и факторов, относящихся к состоянию ребенка.
4. Детям, перенесшим перинатальную гипоксию, необходимо комплексное обследование и наблюдение для выявления в более ранние сроки наличия соматических и неврологических расстройств и своевременной их коррекции.
Апробация работы
Основные результаты работы были представлены на III, V, VI Всероссийских университетских научно-практических конференциях молодых ученых и студентов по медицине (Тула, 2004, 2006, 2007), I Всероссийской Бурденковской студенческой научной конференции (Воронеж, 2005), X конгрессе педиатров России (Москва, 2006), Ежегодной междисциплинарной научно-практической конференции стран СНГ (Санкт-Петербург, 2006), ежегодном конгрессе специалистов перинатальной медицины (Москва, 2006), Первом Объединенном научно-практическом форуме детских врачей (Орел, 2008), И научно-практической конференции «Актуальные вопросы организации, оказания первичной, специализированной медицинской помощи в условиях многопрофильного стационара» (Воронеж, 2008).
Публикации
По материалам диссертации опубликовано 10 работ, две из которых в издании, рекомендованном ВАК РФ.
Объем и структура диссертации
Диссертация изложена на 144 страницах машинописного текста, состоит из введения, обзора литературы, главы, посвященной объекту и методам исследования, трех глав собственных исследований, заключения, выводов, практических рекомендаций, указателя литературы. Работа иллюстрирована 10 рисунками и 37 таблицами, содержащимися в тексте. Библиография содержит 286 источников, в том числе 179 отечественных и 107 иностранных авторов.
ОСНОВНОЕ СОДЕРЖАНИЕ РАБОТЫ
Объект и методы исследования
Проведено обследование 157 детей, В данное исследование были включены дети, перенесшие ХВГП и асфиксию новорожденного, со сроком гестации от 37 до 42 недель, рожденные в роддоме «Электроника» и областном родильном доме в 2002-2005 гг. Критериями исключения новорожденных из исследования стали срок гестации менее 37 недель, травматические повреждения и поражения ЦНС при инфекционных заболеваниях перинатального периода, а также врожденные пороки развития.
Перенесенная детьми гипоксия подтверждалась данными повторных (не менее двух) кардиотокографических и ультразвуковых исследований во 2-м и 3-м триместрах беременности, а также антенатальными и интранатальными факторами риска. Асфиксия новорожденного
устанавливалась согласно критериям диагностики — оценка по шкале Апгар и наличие клинических признаков полиорганных нарушений.
Дети были разделены на пять групп. Первая (контрольная) группа состояла из 30 здоровых доношенных новорожденных, матери которых не имели кардиотокографических признаков страдания плода и ультразвуковых признаков ФПН. Вторую группу составили 25 новорожденных с оценкой по шкале Апгар 4-6 баллов, матери которых также не имели кардиотокографических и ультразвуковых признаков хронической гипоксии плода, т.е. перенесших острую умеренную асфиксию в родах. В третью группу вошло 39 детей с признаками хронической внутриутробной гипоксии плода, не достигающими критических значений. В четвертой группе было 27 новорожденных, перенесших умеренную асфиксию в родах, развившуюся на фоне хронической антенатальной гипоксии. Пятую группу составили 36 детей, рожденных в тяжелой асфиксии на фоне хронической внутриутробной гипоксии плода. Основные характеристики детей представлены в таблице 1.
Таблица 1
1 группа (п=30) 2 группа (п=25) 3 группа (п=39) 4 группа (п=27) 5 группа (п=36)
Мальчики/ Девочки (абс(%) 15/15 (50/50) 17/8 (68/32) 14/25 (36/64) 12/15 (44/56) 21/15 (58/42)
Масса тела при рождении, г (М±а) 3509 ±345 3600 ±398 3247 ±339* 3200 ±289* 3394 ±332
Длина тела при рождении, см (М±сг) 53,1 ±1,7 53,8 ±1,9 51,7 ±2,0 52,3 ±2,5 53 ±2,7
Окружность головы, см (М±ст) 34,6 ±1,0 35,2 ±1,1 34,4 ±1,2 34,6 ±1,4 34,1 ±1,7
Окружность груди, см (М±о) 32,5 ±1,6 33,0 ±1,7 31,9 ±1,6 32,1 ±1,7 32,4 ±1,6
Гестационный возраст, нед (М±о) 39,1 ±0,7 39,5 ±1,0 39,1 ±0,9 38,9 ±0,8 39 ±0,9
Оценка по шкале Апгар 1 мин/5 мин (М±о) 7,0/8,0 5,8±0,5/ 7,0±0,5 7,0/ 7,9±0,2 5,9±0,3/ 7,15±0,4 2,0±0,8/ 4,8±1,3
Примечание: * р<0,01 между группами контроля, «с умеренной асфиксией» и группами «с ХВГП», «с ХВГП+ умеренная асфиксия»
Отмечалось отличие по массе тела в группах детей с перенесенной хронической и сочетанной гипоксией с умеренной асфиксией от контрольной группы и группы детей, перенесших острую умеренную асфиксию. Отличие между группами отмечалось также по тяжести состояния при рождении и оценивалось по шкале Апгар.
Обследование новорожденных в родильном доме включало оценку состояния при рождении по шкапе Апгар, морфофункциональной зрелости
и физического развития, неврологического и соматического статуса, общеклиничекие лабораторные исследования.
Последующее наблюдение за детьми осуществлялось до достижения ими трёхлетнего возраста. Пациентам проводился комплекс клинических, лабораторных и инструментальных исследований в динамике. Все дети были консультированы неврологом, офтальмологом, хирургом.
Оценка физического развития детей в возрасте от 1 месяца до 3-х лет проводилась с использованием центильных таблиц И.М. Воронцова и А.Н. Мазурина соответственно возрасту и полу. Уровень психомоторного развития определялся по методике Л.Т. Журбы и Е.М. Мастюковой (1981), а также с использованием методики В.А. Доскина и соавторов (1997). Ультразвуковое исследование головного мозга проводилось аппаратом «Бшепз 80-450» (Германия), секторными датчиками 3,5 и 7,5 МГц.
С целью изучения состояния функций эндотелия у новорожденных, перенесших ХВГП, была определена концентрация ЭТ-1 в плазме крови у детей со сроком гестации 37-42 недели, рожденных в областном роддоме в 2007 году. Нами был обследован 41 ребенок, которые на основании анамнестических, клинических данных, кардиотокографии и допплерометрии перенесли хроническую внутриутробную гипоксию. Эти дети вошли в основную группу. Группу сравнения составили 12 новорожденных, родившихся у матерей с не осложненным течением беременности и родов. В ходе исследования дети основной группы, перенесшие ХВГП, были разделены на 2 подгруппы. В 1А подгруппу вошло 15 детей, которые в раннем неонатальном периоде не имели признаков гипоксически-ишемического поражения ЦНС. 1Б подгруппу составили 26 детей, имеющие в раннем неонатальном периоде признаки церебральной ишемии I и II степени. Общая характеристика обследуемых пациентов представлена в таблице 2.
Таблица 2
Общая характеристика групп детей, обследуемых на эндотелиальную
дисфункцию
Основная группа Группа сравнения (п=12)
1А подгруппа (п=15) 1Б подгруппа (п=26)
Мальчики/ Девочки (абс(%) 4/11 (27/73) 15/11. (58/42) 6/6 (50/50)
Масса тела при рождении, г (М±о) 3706±224 3246±504* 3615±486
Длина тела при рождении, см (М±сг) 54,2±1,5 52,8±2,1 54±2,8
Окружность головы, см (М±а) 35±1,2 33,9±1,3 35,1±1,4
Окружность груди, см (М±о) 33,6±1,4 32,5±1,5 33,6±1,0
Гестационный возраст, нед (М±о) 39,2±0,9 39,2±0,88 38,8±0,22
Примечание: * р<0,05 между 1А подгруппой, группой сравнения и 1Б подгруппой
Оценка по шкале Апгар у всех детей составила 7-8 баллов. Отмечалось отличие по массе тела в подгруппе детей с церебральной ишемией от контрольной группы и подгруппы без поражения ЦНС.
Количественное определение ЭТ-1 в ЭДТА-плазме производили с помощью иммуноферментного анализа (набор Biomedica).
Последующее наблюдение за детьми, у которых был определен ЭТ-1 в крови, осуществлялось на протяжении первого года жизни с оценкой физического и психомоторного развития, изучением соматической и неврологической патологии, проведением ультразвукового исследования головного мозга.
Статистическая обработка
Статистическая обработка полученных результатов проводилась на персональном компьютере с помощью пакета универсальных программ «Excel» и «Statistica v.6» с использованием общепринятых параметрических и непараметрических методов. Обработка вариационных рядов включала подсчет значений средних арифметических величин (М), стандартной ошибки (ш), стандартного отклонения (а). Частота признаков представлена с указанием стандартной ошибки для качественных признаков, стандартного отклонения для количественных признаков. Для сравнения средних величин количественных переменных использовали t-критерий Стьюдента. Качественные показатели сравнивали по критериям Хи-квадрат и Манна-Уитни. Достоверными считались различия между группами при вероятности ошибки менее 5% (р<0,05). Для выявления взаимосвязей между изучаемыми показателями применяли метод корреляционного анализа, включающий как оценку коэффициента корреляции Спирмена (г), так и уровень его значимости (р). Определение факторов риска поздней (после 1,5 лет) неврологической компенсации проводилось с помощью многомерного регрессионного анализа с 95% доверительным интервалом.
Результаты исследований
Был проведен анализ антенатального, интранатального и раннего постнатального периодов каждого ребенка.
Средний возраст матерей в группах «с ХВГП» (3 группа — 26,33±5,90 лет), «с ХВГП + умеренная асфиксия» (4 группа — 28,48±4,95 лет), «с ХВГП + тяжелая асфиксия» (5 группа — 26,56±6,31 лет) достоверно не отличался между группами и от контроля (1 группа — 27,93±6,06 лет). Средний возраст матерей в группе «с умеренной асфиксией» (2 группа) составил 25,08±3,7б лет и достоверно отличался от контрольной группы и от группы «с ХВГП + умеренная асфиксия» (р<0,05). Следует отметить, что в группе «с ХВГП» и обеих группах с сочетанной гипоксией, а также в контрольной группе, женщины старше 35 лет встречались примерно с одинаковой частотой (в 1, 3, 4 группах — по 5 женщин (16,7%, 12,8%, 18,5% соответственно), в 5 группе — 6 (16,7%) женщин). В группе «с умеренной асфиксией» женщины старше 35 лет не встречались.
Анализ соматической заболеваемости показал, что все женщины до наступления настоящей беременности имели ту или иную соматическую патологию. Во всех группах, включая контрольную, женщины имели высокий процент патологии (69,4% до 96,2%). Осложненный соматический анамнез встречался достоверно чаще только в группе «с ХВГП + умеренная асфиксия» (96,2%), чем во всех остальных (р<0,01). Более половины матерей в группах детей с перенесенной острой и/или хронической гипоксией имели осложненный гинекологический анамнез. В группе «с умеренной асфиксией» преобладали воспалительные (56%), а в группе «с ХВГП» невоспалительные (53,8%) болезни женских половых органов. У матерей в группах «с ХВГП + умеренная асфиксия» и «с ХВГП + тяжелая асфиксия» воспалительные и невоспалительные гинекологические заболевания встречались с одинаковой частотой (по 55,6% и 41,6% соответственно). В контрольной группе осложненный гинекологический анамнез имела четвертая часть женщин. Первая беременность регистрировалась почти у половины женщин в группах контроля, «с ХВГП» и «с ХВГП + тяжелая асфиксия». В группе «с ХВГП + умеренная асфиксия» одна треть детей была рождена от первой беременности. Течение беременности в группах детей с хронической и сочетанной гипоксией (3, 4, 5 группы) осложнилось гестозом второй половины у всех женщин. В 3-й, 4-й и 5-й группах у четверти, одной трети и почти у половины матерей, соответственно, гестоз был в виде нефропатии различной степени. Примерно у половины матерей в этих группах регистрировались анемия беременных, ранний токсикоз и угроза прерывания, каждая пятая женщина перенесла ОРВИ во время беременности. Течение беременности в группе «с умеренной асфиксией» осложнилось более чем у половины матерей анемией беременных, ранним токсикозом, водянкой беременных и угрозой прерывания, которая отмечалась однократно и без длительного лечения, каждая пятая перенесла ОРВИ во время беременности. В контрольной группе однократная угроза прерывания беременности регистрировалась в два раза, водянка беременных в пять раз, а токсикоз в семь раз реже, чем в группах с гипоксией (р<0,001).
Наличие внутриутробного страдания плода подтверждалось проведением КТГ и ультразвуковых допплерометрических исследований. Базальный ритм и ПСП в группах с хронической и сочетанной гипоксией был достоверно выше, чем в 1-й и 2-й группах (р<0,001). В группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией выраженное страдание плода отмечалось более чем у половины женщин. В контрольной группе и в группе «с умеренной асфиксией» при кардиотокографическом исследовании патологии не выявлено. Допплерометрическое исследование показало наличие признаков ФПН в группах с хронической и сочетанной гипоксией у всех женщин, тогда как в группе «с умеренной асфиксией» только у 28% беременных (р<0,05). Необходимо отметить, что во 2-й группе встречалась только 1а степень ФПН. В контрольной группе плацентарный кровоток не нарушался.
Самостоятельные роды превалировали в контрольной группе у 66,7% и в группе «с ХВГП» у 53,8% женщин, из них физиологическими были 45% и 23,8% случаев соответственно. В группах «с умеренной асфиксией», «с ХВГП + умеренная асфиксия» и «с ХВГП + тяжелая асфиксия» ни у одной женщины роды не протекали физиологически. Аномалии родовой деятельности в группе «с ХВГП + тяжелая асфиксия» в два раза чаще осложняли течение родов, чем в контрольной группе (р<0,05). Во всех группах с перенесенной гипоксией практически половина родов осложнилась патологией пуповины, что достоверно чаще по сравнению с контролем (р<0,05). Дородовое излитие околоплодных вод в группах «с ХВГП + тяжелая асфиксия» и «с ХВГП» наблюдалось у каждой третьей женщины, что чаще, чем в группах «с умеренной асфиксией» и контроля. Меконий в околоплодных водах встречался примерно у каждой пятой женщины во всех группах с гипоксией.
При анализе течения раннего неонатального периода выявлено, что в контрольной группе наблюдалась низкая заболеваемость. Только у 20% детей встречалась конъюгационная желтуха. В группах с перенесенной гипоксией (2, 3, 4, 5 группы) общая заболеваемость достоверно выше, чем в контрольной группе (р<0,001), и составила от 74,1 до 100%. В 5-й группе наблюдалась самая высокая заболеваемость по сравнению с другими группами (р<0,01). На первом месте во всех группах с перенесенной асфиксией стоят дыхательные и сердечно-сосудистые нарушения, ВЖК также превалировали в этих группах (14-16%). Транзиторное тахипноэ новорожденного достоверно чаще встречалось в 5-й группе, чем в остальных группах с гипоксией (р<0,01). ЗВУР регистрировалась только у детей с хронической гипоксией (3,4, 5 группа) от 14% до 33,3%.
Неврологическая патология в группе «с ХВГП + тяжелая асфиксия» так же, как и соматическая, наблюдалась чаще, чем в других группах. Гипоксическое поражение ЦНС имели все новорожденные этой группы, тогда как во 2-й, 3-й и 4-й группах церебральная ишемия была выявлена у 48%, 38,5%, 59,3% детей соответственно. Ведущим неврологическим синдромом в группах «с умеренной асфиксией», «с ХВГП» и «с ХВГП + умеренная асфиксия» явился гипертензионный синдром (28%, 20,5% и 22,2% соответственно), а в группе «с ХВГП + тяжелая асфиксия» — синдром гипервозбудимости и синдром угнетения (38,9% и 36,1% соответственно). В группе «с ХВГП + тяжелая асфиксия» судорожный синдром встречался у 13,9% детей, а в группе «с умеренной асфиксией» в 4% случаев.
Всем детям были исследованы в капиллярной крови на 1-е и на 5-е сутки концентрация гемоглобина и количество эритроцитов, повышение которых является адаптационным механизмом при кислородной недостаточности. Концентрация гемоглобина и количество эритроцитов на 1-е сутки и количество эритроцитов на 5-е сутки в группе «с ХВГП + тяжелая асфиксия», были достоверно выше, чем в остальных группах. Концентрация гемоглобина на 5-е сутки в группах достоверно не отличалась.
Катамнез детей исследуемых групп
На естественном вскармливании в контрольной группе находилось 76,5% детей, а в группе «с умеренной асфиксией» — 50% детей. Более половины детей в группах с хронической и сочетанной гипоксией вскармливались искусственно (3 группа — 52,3%, 4 группа — 57,1%, 5 группа — 77,8% детей).
При изучении физического развития к вариантам нормы были отнесены характеристики, свойственные 80% популяции и находящиеся в интервале от 10-го до 90-го центиля. К году в группах детей с перенесенной гипоксией от 15% до 50% детей имели дисгармоничное физическое развитие с избытком массы тела. В контрольной группе дисгармоничное физическое развитие с избытком массы тела наблюдалось только у 11,8%. Масса и длина тела ниже 10 центиля на первом году жизни встречалась лишь у детей 4-й (7,1%) и 5-й (5,6%) групп. К трем годам во всех группах отмечалась положительная динамика, кроме группы «с ХВГП», в которой количество детей с гармоничным физическим развитием снизилось до 71,4% (рис. 1).
Длина тела Масса тела
Рис. 1 Физическое развитие детей (длина тела, масса тела)
Окружность груди к году в контрольной группе у всех детей укладывалась в возрастные нормативы. В группе «с ХВГП + умеренная асфиксия» каждый пятый ребенок, а в группе «с ХВГП» более половины детей имели узкую грудную клетку. Показатели окружности головы в контрольной группе в изучаемые возрастные периоды (3 месяца, 1 год) у всех обследуемых укладывались в «коридор» от 10 до 90 центиля. В 4-й группе около половины имели показатели окружности головы ниже 10 центиля. У третьей части детей 5-й группы определялись увеличенные размеры окружности головы. К году в группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией положительной динамики не
наблюдалось, только у половины детей показатели окружности головы находились между 10 и 90 центилем (рис. 2).
Окружность головы Окружность груди
Рис. 2 Физическое развитие детей (окружность головы, окружность груди)
Анализируя соматическую патологию у детей, перенесших острую и хроническую гипоксию, в контрольной группе была выявлена более низкая заболеваемость, чем в группах сравнения (р<0,05). В раннем возрасте 70,5% пациентов перенесли ОРВИ, но только в одном случае вирусная инфекция сопровождалась бронхитом. В группах с перенесенной гипоксией все дети переносили ОРВИ в течение трех лет, из них 25% отнесены к группе часто болеющих. В группе «с ХВГП + тяжелая асфиксия» у половины детей, а в группе «с ХВГП + умеренная асфиксия» в 35,7% случаев ОРВИ осложнялась обструктивным бронхитом. Дисбиоз кишечника, атопический дерматит и анемия явились ведущими среди соматической патологии, наиболее часто выявляющиеся в группе с тяжелой асфиксией. Достаточно часто диагностировались астигматизм, конъюнктивиты и отиты в группах детей с гипоксией.
Анализ неврологической заболеваемости в поздний неонатальный период показал, что процент диагностируемых гипоксических поражений ЦНС в группах с перенесенной гипоксией увеличился до 95,2% — 100%. Всем детям в возрасте 1 и 6 месяцев проводилась нейросонография. В контрольной группе на первом месяце жизни только у 17,6% детей наблюдались признаки перивентрикулярного отека. Ликвородинамические нарушения в группе «с умеренной асфиксией» определялись у 16,7% детей, что достоверно реже, чем в группе «с ХВГП + тяжелая асфиксия» (р<0,01). В группах с хронической гипоксией и сочетанной умеренной и тяжелой асфиксией нарушения ликвородинамики выявлено более чем у половины детей. При повторном нейросонографичсском обследовании в 6 месяцев в группе «с ХВГП» процент ликвородинамических нарушений снизился в 1,5
раза по сравнению с предыдущим исследованием и составил 33,3%, что достоверно ниже, чем в группе «с ХВГП + тяжелая асфиксия» (р<0,05). В группах с острой и сочетанной гипоксией (2, 4 и 5 группы) частота встречаемости признаков нарушения ликвородинамики увеличилась до 64,3%-72,2% (рис. 3).
80 70 60 50 40 30 20 10 О
— 80 — 70 60 — 50 40 30 — 20 -■ 10 О
Признаки Признаки
ликвородинамических ликворалниймических нарушений (1 мес) нарушений (б мес)
-«с умеренной асфиксие й «
■ «ХВГП+умерення и асфиксия»
«ХВГП+тнжвлая асфиксия»
Рис. 3 Результаты нейросонографического обследования в 1 и 6 мес
На первом году жизни среди последствий гипоксических поражений ЦНС ведущее место принадлежит доброкачественной внутричерепной гипертензии, которая была диагностирована более чем у половины детей с перенесенной гипоксией. Сочетанные формы задержки развития, расстройства вегетативной нервной системы и церебрастенический синдром регистрировались только в группах с хронической и сочетанной гипоксией (3, 4, 5 группы). В группе «с умеренной асфиксией» нарушение моторного развития выявлялось достоверно реже, чем в группах «с ХВГП» и «с ХВГП + тяжелая асфиксия» у одной трети и в группе с «ХВГП + умеренная асфиксия» у половины детей (р<0,05). У 50% пациентов 5-й группы имелись клинические признаки гипервозбудимости. Одному ребенку в группе «с ХВГП + тяжелая асфиксия» был поставлен диагноз ДЦП. Следует отметить, что в контрольной группе неврологической патологии выявлено не было.
К 3-м годам нарушения моторного развития имел каждый пятый ребенок в группах с хронической и сочетанной гипоксией. Нарушения развития речи и гиперкинетические расстройства отмечались более чем у половины детей в группе «с ХВГП + тяжелая асфиксия», что достоверно чаще по сравнению с группами «с ХВГП» и с «ХВГП + умеренная асфиксия» (р<0,05). Дети 4-й и 5-й групп в 14,3 и 22,2% соответственно имели нарушения сна. У пятой части детей группы «с ХВГП + умеренная асфиксия» выявлена сообщающаяся гидроцефалия (рис. 4). В контрольной группе патология со стороны нервной системы к 3-м годам также не регистрировалась, а в группе «с умеренной асфиксией» наступила компенсация неврологических нарушений к году у всех обследуемых. Дети, перенесшие ХВГП, достигли компенсации неврологических нарушений к 3-м годам.
Расстройства сна (С 47)
■ Ко1гтрольняя группа О «с умеренной асфиксией» □ «с ХВГП» ЕЗ «с ХВГШ-умерениан асфиксия» И «с ХВГП+тижеляя асфиксия» _
Рис. 4 Структура неврологической заболеваемости к 3-м годам
Факторы, влияющие на компенсацию неврологических нарушений
На первом этапе исследования влияния некоторых факторов на сроки компенсации неврологических нарушений были построены корреляционные матрицы изучаемых факторов (61 фактор). В ходе исследования проведен корреляционный анализ для выявления факторов, имеющих высокую степень взаимосвязи. Статистически значимо с поздним (после 1,5 лет) наступлением компенсации неврологических нарушений связаны: кардиотокографические признаки страдания плода с коэффициентом корреляции г = 0,66 (р<0,0001), степень ФПН г = 0,69 (р<0,0001), степень тяжести гестоза г = 0,63 (р<0,0001), интубация трахеи г = 0,51 (р<0,0001), концентрация гемоглобина в первые сутки г = 0,45 (р<0,001), гипоксически-ишемическое поражение ЦНС в раннем г = 0,51 (р<0,0001) и позднем неонатальном периоде г = 0,65 (р<0,0001), диффузные изменения тканей мозга гипоксически-ишемического характера г = 0,49 (р<0,0001) и признаки ликвородинамических нарушений г = 0,51 (р<0,0001) при проведении нейросонографии. Слабая корреляционная связь обнаружена между поздней неврологической компенсацией и частыми ОРВИ г = 0,39 (р<0,001). Отмечена отрицательная взаимосвязь поздней неврологической компенсации с оценкой по шкале Апгар на первой г = -0,56 (р<0,0001) и пятой минуте г = -0,52 (р<0,0001), массой тела г = -0,33 (р<0,001) и окружностью головы при рождении г = -0,31 (р<0,001).
Мы поставили задачу провести сравнительный анализ зависимостей сочетанного воздействия изучаемых факторов с установлением приоритета каждого из них.
В качестве инструментального метода сравнения был использован многомерный регрессионный анализ. Тактика проведения анализа состояла в выявлении статистически значимых зависимостей каждого из изученных
показателей, установлении наиболее «отзывчивых» во влиянии изученных факторов и параметров.
Изучаемые факторы были разбиты на группы:
1. Группа антенатальных и интранатальных факторов:
а) факторы, отражающие соматическую патологию матери;
б) факторы, отражающие течение настоящей беременности;
в) факторы, отражающие период родов;
2. Группа факторов, относящихся к состоянию новорожденного:
а) параметры, характеризующие состояние ребенка при рождении;
б) параметры, характеризующие течение периода новорожденности;
в) параметры, характеризирующие заболеваемость ребенка в раннем
возрасте.
В ходе исследования взаимосвязи соматической патологии матери и сроков компенсации неврологических нарушений, установлено, что ни одно из заболеваний не оказывало значимого влияния на позднюю (после 1,5 лет) неврологическую компенсацию. Суммарный вклад этой группы факторов составил только 4,46% и явился статистически не значимым (р = 0,9308).
Исследуя влияние течения беременности у матери на сроки неврологической компенсации у детей, установлено, что ни один из изучаемых параметров по отдельности не влиял на позднее наступление неврологической компенсации, но в совокупности факторы, отражающие течение настоящей беременности, дали около 53% вклада с вероятностью статистической значимости 99% (р = 0,0000).
При анализе взаимосвязи периода родов и сроков неврологической компенсации у детей, было выявлено, что из всех осложнений интранатального периода только экстренное кесарево сечение влияет на позднюю компенсацию с вероятностью статистической значимости более 95% (р = 0,0401). Суммарный вклад интранатальных факторов составил 14,72% с вероятностью статистической значимости всего 85%.
Общий вклад параметров, характеризующих состояние ребенка при рождении, в позднее наступление неврологической компенсации у детей составил 34% (р = 0,0006). По отдельности ни один из факторов не влиял на сроки неврологической компенсации.
Изучая влияние течения неонатального периода на позднее наступление компенсации неврологических нарушений, выявлена сильная зависимость между сроками компенсации и степенью тяжести церебральной ишемии (р = 0,0486) и синдромом гипервозбудимости (р = 0,0159). Совокупный вклад всех факторов неонатальной заболеваемости составил 50%.
Концентрация гемоглобина на первые (р = 0,0174) и пятые (р = 0,0078) сутки и количество эритроцитов на пятые сутки (р = 0,0315) влияют на сроки неврологической компенсации со статистической значимостью более 95%. Оценка суммарного воздействия этих параметров свидетельствует, что коэффициент детерминации равен 28% с вероятностью 99% (р = 0,0002).
Анализ влияния нейросонографических изменений головного мозга на сроки неврологической компенсации установил, что диффузные изменения тканей мозга гипоксически-ишемического характера (р = 0,0000), перивентрикулярный отек (р = 0,0202) и признаки ликвородинамических нарушений, сохраняющиеся после полугода жизни (р = 0,0001), влияют на позднее восстановление функций после неврологических нарушений у детей с вероятностью до 99%. В совокупности все нейросонографические изменения голоного мозга статистически значимо (р = 0,0000) влияют на время восстановления функций после неврологических нарушений с коэффициентом детерминации 53%.
Среди патологии детей в раннем возрасте значимо влияющим фактором на сроки неврологической компенсации явилась частота ОРВИ (р = 0,0115). Суммарный вклад заболеваемости детей в раннем возрасте в позднюю компенсацию составил 52%. Статистическая значимость сочетанного воздействия указанных факторов составляет 99% (р = 0,0000).
Исследование показателей эндотелина-1 у новорожденных, перенесших хроническую внутриутробную гипоксию
Концентрация ЭТ-1 была определена в крови у 53 новорожденных (41 ребенок основной группы и ¡2 детей группы сравнения). В ходе исследования дети основной группы, перенесшие ХВГП, были разделены на 2 подгруппы. В 1А подгруппу вошло 15 детей, которые в раннем неонатальном периоде не имели признаков гипоксически-ишемического поражения ЦНС. 1Б подгруппу составили 26 детей с признаками церебральной ишемии I и II степени в раннем неонатальном периоде.
На первом этапе исследования маркера эндотелиальной дисфункции у новорожденных был проведен подробный анализ соматической и гинекологической патологии матери, течение настоящей беременности и родов.
Средний возраст матерей в группах достоверно не отличался и составил в контрольной группе 27,75±3,98 лет, в 1А подгруппе — 28,60±5,96 лет, 1Б подгруппе — 27,12±5,64 лет. Анализ экстрагенитальной патологии матерей показал, что различий в общей заболеваемости в группах не обнаружено. В контрольной группе среди экстрагенитальной патологии расстройства вегетативной нервной системы встречались чаще, чем в группе «с ХВГП с церебральной ишемией» (р<0,05). В подгруппах детей с ХВГП преобладали хронический пиелонефрит и расстройства вегетативной нервной системы.
В гинекологическом анамнезе достоверных различий между группами также не выявлено. Во всех группах преобладали воспалительные болезни женских половых органов.
Течение беременности у матерей в группах детей с хронической гипоксией (1А и 1Б подгруппы) осложнилось гестозом второй половины у всех женщин, угрозой прерывания в 1А подгруппе — у одной трети и в 1Б
подгруппе — у половины женщин. В контрольной группе гестоз и угроза прерывания не регистрировались.
Наличие внутриутробного страдания плода подтверждалось проведением КТГ и ультразвуковых допплерометрических исследований. ПСП, частота встречаемости ФПН и маловодие в группах с хронической гипоксией было достоверно выше, чем в контрольной (р<0,001). В 1Б подгруппе выраженное страдание плода отмечалось более чем у половины женщин, тогда как в 1А только у трети обследуемых. В контрольной группе при кардиотокографическом исследовании патологии не выявлено. Допплерометрическое исследование показало наличие признаков ФПН в грушах с хронической гипоксией у всех женщин. В контрольной группе у половины беременных встречалась только 1а степень ФПН.
Течение интранатального периода в группах не отличалось. Путем самостоятельных родов было рождено более половины детей во всех группах. Аномалии родовой деятельности и патология пуповины осложнили течение родов у одной трети женщин в группах с ХВГП. Дородовое излитие околоплодных вод в группе «с ХВГП с церебральной ишемией» наблюдалось у каждой пятой женщины. В контрольной группе более половины самостоятельных родов протекали физиологически.
Отсутствие достоверных различий в соматической и генитальной патологии у матерей, а также отличий по полу, сроку гестации, оценке по шкале Апгар у детей во всех исследуемых группах позволило нам провести сравнение показателей ЭТ-1 в подгруппах с ХВГП и оценить участие маркера эндотелиальной дисфункции в неонатальной заболеваемости. Для этого концентрация ЭТ-1 была определена у новорожденных в пуповинной крови и на 3-5 сутки (таблица 3).
Таблица 3
Содержание ЭТ-1 в плазме крови новорожденных сразу после рождения
и на 3-5 день жизни
Контрольная группа (п= 12) Основная группа (п=41)
1А(п=15) 1Б (п=26)
ЭТ-1 в плазме пуповинной крови, фмоль/мл 0,81±0,21 2,21±0,66* 1,93±0,87*
ЭТ-1 в плазме на 3-5 сутки, фмоль/мл 1,14±0,42 1,62*0,49″» 1,51*0,49*’
Примечание: * р<0,001 между контрольной группой и группами с ХВГП
*1 р<0,05 между контрольной группой и группами с ХВГП
При анализе полученных данных было выявлено достоверное повышение ЭТ-1 в пуповинной крови как в 1А подгруппе — 2,21±0,17 фмоль/мл, так и в 1Б — 1,93±0,17 фмоль/мл, по сравнению с контрольной группой (р<0,001). Определение уровня ЭТ-1 в крови новорожденных детей в период ранней неонатальной адаптации на 31-5 сутки показало, что произошло его незначительное снижение, но все-таки он оставался
достоверно повышен 1,62±0,16 фмоль/мл в 1А подгруппе и 1,51 ±0,11 фмоль/мл в 1Б, по сравнению с контрольной группой (р<0,05). Вероятно, повышение маркера эндотелиальной дисфункции явилось следствием постгипоксических нарушений у детей в ранний неонатальный период.
Соматическая патология в раннем неонатальном периоде в подгруппе 1Б встречалась чаще, чем в других группах. ЗВУР регистрировалась практически у половины новорожденных в подгруппе 1Б, каждый пятый перенес транзиторное тахипноэ, постгипоксическая кардиолатия и ВУИ были обнаружены по 15,4% случаев. В подгруппе без гипоксического поражения ЦНС были выявлены конъюгационная желтуха у пятой части детей и транзиторное тахипноэ в 13,3% случаев. В контрольной группе превалировали анемия, конъюгационная желтуха и транзиторное тахипноэ у детей рожденных путем кесарева сечения с одинаковой частотой (16,7%).
Критерием включения детей в 1Б подгруппу явилась церебральная ишемия. 1 и II степень тяжести этой патологии встречалась одинаково часто. Синдром гипервозбудимости был определен ведущим и составил 65,4% случаев среди всех неврологических синдромов. Гипертензионный синдром и синдром угнетения регистрировались у пятой части детей, в меньшем проценте (11,5%) встречался синдром вегето-висцеральных дисфункций (рис.5). ________
О Синдром
гипс рвозбуди мости
И Синдром
■ Синдром всгето-висцеральных дисфункций Ш Гипертеизион мый синдром
Рис. 5 Клинические синдромы церебральной ишемии в подгруппе «с ХВГП с церебральной ишемией»
Для выявления участия ЭТ-1 в формировании гипоксического поражения ЦНС было прослежено дальнейшее развитие на первом году жизни у 28 детей.
Показатели физического развития к году у детей в контрольной группе и 1А подгруппе находились между 10 и 90 центилем. В подгруппе «с ХВГП с церебральной ишемией» практически половина детей (41,7%) имели окружность груди ниже 10 центиля, и только у одного ребенка значения роста к году были ниже 10 центиля. Окружность головы на первом году жизни в контрольной группе соответствовала 10-90 центилю у всех обследуемых. Увеличение размеров окружности головы в первом полугодии произошло на 6,9±0,83 см, что соответствовало возрастной норме. Темпы роста окружности головы в первом полугодии у детей основной группы (8,4±1,3 см и 9,2±1,9 см в 1А и 1Б подгруппах соответственно) достоверно выше, чем в контрольной группе (р<0,01).
Всем детям в возрасте 1 месяца проводилась нейросонография. В контрольной группе патологии не было выявлено. В подгруппе «с ХВГП без церебральной ишемии» на первое место выступали перивентрикулярный отек и диффузные изменения тканей мозга гипоксически-ишемического характера по 75% случаев. Эти же изменения в головном мозге у детей подгруппы «с ХВГП с церебральной ишемией» встречались также более чем у половины обследуемых. Более половины детей 1Б подгруппы имели признаки ликвородинамических нарушений, тогда как в 1А признаки нарушения ликвородинамики визуализированы в 37,5% случаев.
При неврологическом обследовании в 1А подгруппе клинические признаки последствий перинатального поражения ЦНС были обнаружены у всех детей, проявляющиеся у 75% нарушением моторного развития, у одной трети — сочетанными формами задержки развития. У половины обследуемых обнаружен гипертензионный синдром. В 1Б подгруппе последствия церебральной ишемии выявлены у 9 пациентов (75%). Среди неврологической патологии в этой подгруппе превалировали сочетанные формы задержки развития (66,7%). Нарушения моторного развития и гипертензионный синдром встречались с одинаковой частотой (по 58,3%)
Рис. 6 Неврологическая патология у детей на первом году жизни
Нужно отметить, что неврологическая патология наблюдалась в группах с ХВГП у детей, Которые имели в раннем неонатальном периоде уровень ЭТ-1 выше, чем максимальное значение у детей в контрольной группе (1,1 фмоль/мл) (рис. 7).
I □ частоте
встречаемости последствий иереребральной ишемии
концентрация ЭТ-1 в пуповинной крови, фмоль/мл
Рис. 7 Частота встречаемости последствий
церебральной ишемии в зависимости от концентрации эндотелина-1
Учитывая, что симптомокомплекс при таких нозологических формах, как нарушение моторного развития и сочетанные формы задержки развития имеет диагностическое значение при исключении других причин, был проведен анализ соматической патологии. Во всех группах на первое место выступали ОРВИ от 62,5% до 83,3%, но в группу часто болеющих не был включен ни один ребенок. У одной трети детей основной группы встречалась анемия, у четверти пациентов — дисбиоз кишечника и атопический дерматит. В контрольной группе процент соматической патологии был ниже, однако, достоверных отличий в заболеваемости детей контрольной и основной групп выявлено не было.
При проведении корреляционного анализа обнаружена прямая взаимосвязь концентрации эндотелина-1 в пуповинной крови с хроническим пиелонефритом у матери с коэффициентом корреляции г = 0,6 (р<0,001), гестозом г = 0,55 (р<0,001), инфекционными заболеваниями матери во время беременности г = 0,65 (р<0,001), концентрацией гемоглобина г = 0,67 (р<0,001) и количеством эритроцитов г = 0,59 (р<0,001) у новорожденных в крови на 1-е сутки. Статистически значимо с концентрацией ЭТ-1 в период ранней неонатальной адаптации связаны многоводие г = 0,58 (р<0,001), кардиотокографические признаками страдания плода г = 0,67 (р<0,001), ВУИ г = 0,58 (р<0,001). Проведенный корреляционный анализ выявил также прямую зависимость между концентрацией эндотелина-1 в пуповинной крови и на 3-5 сутки и диффузными изменениями тканей мозга гипоксически-ишемического характера с коэффициентом корреляции г =
0.67 (р<0,001) и г = 0,56 (р<0,001), сочетанными формами задержки развития г = 0,53 (р<0,001) и г = 0,74 (р<0,0001), нарушением моторного развития г = 0,59 (р<0,001) и г = 0,58 (р<0,001) соответственно. Доброкачественная внутричерепная гипертензия коррелирует только с концентрацией ЭТ-1 на 3-5 сутки г = 0,67 (р<0,001).
На основании изложенного выше, можно сделать вывод, что дети, перенесшие хроническую внутриутробную гипоксию, имеют повышенные показатели ЭТ-1 как в плазме пуповинной крови, так и в плазме крови на 35 сутки. Увеличение уровня ЭТ-1 в крови сохраняется независимо от наличия клинических проявлений, что говорит о сохраняющихся в организме новорожденного постгипоксических нарушениях и о развитии эндотелиальной дисфункции, что впоследствии приводит к неврологическим нарушениям на первом году жизки.
ВЫВОДЫ
1. В раннем неонатальном периоде у трети детей с ХВГП в сочетании и без асфиксии встречалась ЗВУР. У новорожденных, перенесших асфиксию острую или на фоне ХВГП, преобладали дыхательные, сердечно-сосудистые нарушения и ВЖК гипоксического генеза. Наименьший процент
церебральной ишемии приходился на детей, перенесших только хроническую гипоксию.
2. Дисгармоничное физическое развитие с избытком массы тела у детей, перенесших острую и хроническую гипоксию, к году составило от 15% до 50%. Более половины детей с ХВГП в возрасте одного года имели узкую грудную клетку. Только у половины детей с ХВГП в сочетании и без асфиксии окружность головы соответствовала возрастным нормативам. Гармоничное физическое развитие к трем годам реже встречалось у детей, перенесших только ХВГП.
3. При анализе соматической заболеваемости установлено, что от 20% до 30% детей, перенесших острую, хроническую или сочетанную гипоксию, относятся к группе часто болеющих. Анемия, дисбиоз кишечника и атопический дерматит являются преобладающими в структуре заболеваемости.
4. В структуре неврологической заболеваемости на первом году жизни превалировали доброкачественная внутричерепная гипертензия, а к 3-м годам нарушения развития речи и гиперкинетические расстройства. Дети, перенесшие умеренную острую асфиксию, достигли компенсации неврологических нарушений к году, а дети с ХВГП, к 3-м годам. У пятой части детей с тяжелой асфиксией и у одной трети детей с умеренной асфиксией, развившихся на фоне ХВГП, компенсация неврологических нарушений к 3-м годам не наступила. Частота развития ДЦП составила 5,6%.
5. При изучении факторов риска поздней (после 1,5 лет) неврологической компенсации установлено, что наиболее высокая доля вклада принадлежит течению настоящей беременности, патологическим изменениям в головном мозге при нейросонографии и заболеваемости детей в течение 3-х лет (коэффициент детерминации = 53%). Суммарная доля неонатальной заболеваемости составила 50% вклада, а состояние ребенка при рождении -34% вклада.
6. Показатели ЭТ-1 у детей, перенесших хроническую внутриутробную гипоксию, являются повышенными как в пуповинной крови, так и на 3-5 сутки. У детей с ХВГП, имеющих уровень ЭТ-1 в пуповинной крови выше, чем максимальное значение у детей в контрольной группе развиваются неврологические нарушения на первом году жизни. Таким образом, ЭТ-1 можно считать маркером хронической внутриутробной гипоксии, имеющим прогностическое значение в развитии неврологических нарушений.
ПРАКТИЧЕСКИЕ РЕКОМЕНД АЦИИ
1. Для прогнозирования сроков компенсации неврологических расстройств у детей с перинатальной гипоксией (при условии стандартных методов лечения) необходима комплексная оценка группы факторов, включающих антенатальное развитие и интранатальный период, неонатальную заболеваемость и данные нейросонографии, заболеваемость на протяжении первых 3-х лет. Обследование и
наблюдение детей, перенесших перинатальную гипоксию, должно включать в себя оценку физического развития с обязательным ежемесячным определением окружностей головы и груди на протяжении 1-1,5 лет, оценку неврологического и соматического статуса, обязательное проведение нейросонографии всем детям в первом полугодии жизни не менее 2-х раз, даже при отсутствии патологии при предыдущем исследовании. Данный комплекс обследования позволяет выявить в более ранние сроки наличие соматических и неврологических расстройств, а также способствует определению «клинически немых» форм поражения головного мозга, что определяет своевременную коррекцию выявленных нарушений.
2. Рекомендовано внедрить в практическую медицину определение концентрации ЭТ-1 в плазме пуповинной крови у детей с высоким риском хронической внутриутробной гипоксии для выявления наличия постгипоксических нарушений и раннего прогнозирования развития последствий перинатального поражения ЦНС у детей на первом году жизни.
Список работ опубликованных по теме диссертации:
1. Катамнез детей, перенесших тяжелую асфиксию в родах У O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, A.M. Якунинская, Е.В. Минакова // Пути повышения эффективности медицинской помощи детям: материалы X конгресса педиатров России. — М., 2006. — С. 186.
2. Физическое развитие и заболеваемость детей, перенесших тяжелую асфиксию в родах / O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, А.М, Якунинская, Е.В. Минакова // Сборник материалов 5 Всероссийской университетской научно-практической конференции молодых ученых и студентов по медицине. — Тула, 2006. — С. 88 — 89.
3. Оценка физического развития и структуры заболеваемости детей, перенесших тяжелую асфиксию в родах / O.A. Дрожжина, Л.И. Ипполитова, С.Л. Хачатурян, A.M. Якунинская, Е.В. Минакова // Перспективы и пути развития неотложной педиатрии: материалы ежегодной междисциплинарной научно-практической конференции стран СНГ. — Санкт-Петербург, 2006. — С. 69 — 70.
4. Дрожжина O.A. Развитие и структура заболеваемости детей, перенесших тяжелую асфиксию / O.A. Дрожжина // Новые технологии в перинатологии: материалы ежегодного конгресса специалистов перинатальной медицины. — М., 2006. — С. 22.
5. Пронина O.A. Катамнез развития детей, перенесших тяжелую асфиксию интранатально / O.A. Пронина, И.И. Логвинова // Сборник материалов VI Всероссийской университетской научно-практической конференции молодых ученых и студентов по медицине. — Тула, 2007. — С. 204 — 205.
6. Пронина O.A. Исследование показателей эндотелина-1 у новорожденных детей, перенесших хроническую внутриутробную гипоксию / O.A.
Пронина // Системный анализ и управление в биомедицинских системах. — 2008. — Т 7, № 3. — С. 691 — 693.
7. Эндотелии-1 — маркер внутриутробной гипоксии у новорожденных детей / O.A. Пронина, И.И. Логвинова, Л.И. Ипполитова, Л.П. Лободина, Н.П. Стасенкова // Вестник Российского государственного медицинского университета. — 2008. — № 4 (63). — С. 164.
8. Концентрация плазменного эндотелина у новорожденных с перинатальным гипоксическим поражением центральной нервной системы / O.A. Пронина, И.И. Логвинова, М.В. Сулина, Т.Г. Чистотинова, Е.В. Трухачева, Н.В. Заяц // Актуальные вопросы организации, оказания первичной, специализированной медицинской помощи в условиях многопрофильного стационара: материалы II научно-практической конференции, посвященной 130-летию родильного дома ГКБСМП № 10. — Воронеж, 2008. — С. 54 — 57.
9. Пронина O.A. Эндотелиальная дисфункция у новорожденных детей, перенесших хроническую внутриутробную гипоксию / O.A. Пронина, И.И. Логвинова // Современная перинатология: организация, технологии и качество: материалы 3 ежегодного конгресса 6 съезда Российской ассоциации специалистов перинатальной медицины. — 2008. — С. 43.
10. Роль эндотелина-1 в развитии церебральной ишемии у новорожденных / О.А, Пронина, И.И. Логвинова, Л.П. Лободина, Н.П. Стасенкова, Т.Г. Чистотинова // Современные технологии в педиатрии и детской хирургии: материалы VII Российского конгресса. — 2008. — С. 198 — 199.
СПИСОК СОКРАЩЕНИЙ
ВЖК — внутрижелудочковое кровоизлияние ВУИ — внутриутробная инфекция ДЦП — детский церебральный паралич ЗВУР — задержка внутриутробного развития КТГ — кардиотокография
ОРВИ — острая респираторная вирусная инфекция
ПСП — показатель состояния плода
ФПН — фето-плацентарная недостаточность
ХВГП — хроническая внутриутробная гипоксия плода
ЦНС — центральная нервная система
ЭТ — эндотелии
Подписано в печать 15.04.2009 г. Формат 60 х 84/16 . Бумага офсетная. Усл. печ. л. 1,4 Тираж 101 экз. Заказ № 1162
Отпечатано в типографии Воронежский ЦНТИ-филиал ФГУ «Объединение «Росинформресурс» Минпромэнерго России
394730, г. Воронеж, пр. Революции, 30
признаки, причины, терапия и профилактика
Внутриутробная гипоксия плода – опасный процесс, который, к сожалению, встречается весьма часто. Последствия гипоксии могут негативно повлиять на развитие плода и деятельность его внутренних органов. От своевременной диагностики и лечения во многом зависит жизнь и здоровье будущего ребенка.
В ожидании чуда
Период беременности – очень волнительное и радостное время для каждой женщины. Но к радостному предвкушению появления на свет малыша добавляются тревоги за его здоровье. На будущей маме лежит тяжелое бремя ответственности. На протяжении девяти месяцев в ней развивается и растет новая жизнь. Здоровье еще не родившегося малыша напрямую зависит от самочувствия его мамы.
Существует множество рекомендаций о том, как следить за своим здоровьем в период беременности. Это касается питания, образа жизни, эмоциональных нагрузок и многого другого. Несоблюдение этих простых правил может повлечь за собой неблагоприятные последствия и нанести урон здоровью плода.
Одним из таких последствий может стать внутриутробная гипоксия, влекущая за собой нарушения в развитии плода и в некоторых случаях замирание беременности. Чтобы избежать этого, будущей маме необходимо тщательно изучить факторы риска, которые подстерегают ее во время беременности, и попытаться предотвратить их появление.
Что такое гипоксия
«Гипоксия» – древнегреческое слово, которое дословно переводится как «низкий кислород». Данным термином обозначают кислородное голодание, которое испытывает организм или отдельные его органы вследствие воздействия определенных факторов.
При длительном кислородном голодании в организме человека происходят необратимые морфологические процессы. Они изменяют структуру тканей и органов и нарушают их функциональные способности. При кислородном голодании плода замедляется и нарушается процесс формирования внутренних органов, ребенок может родиться с отставанием в развитии жизненно важных систем или погибнуть. Таковы последствия внутриутробной гипоксии. Наиболее сильно гипоксии подвержены сердце, почки, печень и центральная нервная система.
Дефицит кислорода может сопровождать какое-либо заболевание или возникнуть как самостоятельный процесс, влекущий за собой пороки внутренних органов. По этой причине гипоксию нельзя классифицировать как болезнь, она является патологическим процессом, таким же, как воспаление или дистрофия.
Симптомы гипоксии плода
Отмечено, что в первые три месяца беременности кислородное голодание развивается достаточно редко. Чаще всего это может произойти во втором и третьем триместре. Это связано с тем, что с ростом плода возникает и рост его потребности в кислороде, и при некоторых неблагоприятных обстоятельствах организм беременной не справляется с данной задачей.
Дефицит кислорода у малыша сложно выявить без проведения диагностических исследований, особенно на ранних сроках беременности. Но существуют некоторые признаки внутриутробной гипоксии, которые должны стать тревожным сигналом для будущей мамы.
Первое, на что нужно обратить внимание, это активность плода. Нормой считается примерно десять шевелений в сутки. На начальных стадиях гипоксии малыш начинает чувствовать дискомфорт, поэтому чрезмерно активен. При более длительном недостатке кислорода количество шевелений снижается. Кроме того, внутриутробная гипоксия может характеризоваться частым иканием плода.
Если отклонение количества шевелений от нормы и частое икание не связано с физическими нагрузками будущей мамы или пребыванием в неудобном положении, требуется в кратчайшие сроки обратиться к специалисту, который выявит причину такого поведения плода и при необходимости назначит лечение.
Причины возникновения
Причины внутриутробной гипоксии плода могут быть разными. К ним относятся заболевания, которыми страдает беременная женщина, патологии плаценты, занесение инфекции, пороки развития плода.
Из заболеваний матери, ведущих к гипоксии плода, можно выделить следующие:
- анемия;
- нарушения в работе сердечно-сосудистой системы;
- заболевания дыхательных органов;
- сахарный диабет.
Кроме того, на здоровье малыша влияют вредные привычки, которыми страдает будущая мама. Профилактика внутриутробной гипоксии включает в себя полный отказ от курения и алкоголя. К кислородному голоданию плода может привести любое отклонение от общепринятых норм протекания беременности. Такими отклонениями может стать отслойка и преждевременное старение плаценты, перенашивание плода или же повышенный маточный тонус.
Еще одним фактором, влекущим за собой кислородную недостаточность, является несовместимость резус-фактора матери и ребенка. Такая несовместимость может привести к гемолитической болезни плода, которую часто сопровождает гипоксия. Кроме вышеперечисленных факторов, влияние может оказать механическое воздействие на плод – обвитие пуповиной, сдавливание головки во время родов и прочее.
Причины внутриутробной гипоксии могу также стать причинами других, не менее серьезных осложнений. Чтобы избежать неблагоприятного влияния на развитие плода, будущей маме необходимо наблюдаться у квалифицированного специалиста на протяжении всего периода беременности.
Виды гипоксии плода
В зависимости от того, как долго продолжается кислородное голодание, внутриутробная гипоксия имеет две формы: острую и хроническую. Острая гипоксия характеризуется резким снижением поступающего кислорода. Наиболее часто острая форма возникает во время процесса родов или при обильном маточном кровотечении. Хроническая внутриутробная гипоксия формируется на протяжении длительного промежутка времени, постепенно нарушая процессы развития плода.
Степени прогрессирования кислородного голодания
Выделено три степени развития гипоксии плода. Вначале плод, не получив требуемого количества кислорода, пытается компенсировать его нехватку. Первая степень является компенсированием недостатка кислорода. В организме малыша начинают происходить изменения, направленные на увеличение объема поступающего кислорода. Растет уровень гормона, повышающего тонус кровяных сосудов, – кортизола. Повышенный уровень кортизола стимулирует увеличение объема крови, которая циркулирует по сосудам, и рост частоты сердечных сокращений. Меняется состав крови: растет уровень гемоглобина и эритроцитов. Кроме того, отмечается повышенная активность малыша. Он начинает двигаться более интенсивно и совершать дыхательные движения, несмотря на закрытую голосовую щель.
На второй стадии частичного компенсирования защитные функции организма определяют приоритетные органы, которые снабжаются кислородом в первую очередь. Такими органами являются сердце и мозг, соответственно, другие органы (почки, легкие, ЖКТ) получают кровь, бедную кислородом, что ведет к нарушениям в их развитии и работе. Недостаток кислорода также приводит к распаду глюкозы. Это способствует снижению запаса энергии в клетках организма и нарушению обмена веществ.
Хроническая внутриутробная гипоксия плода имеет и третью стадию прогрессирования – декомпенсация. Внешне стадия проявляется как снижение активности плода и уменьшение частоты сердцебиения. Работа защитных механизмов, направленных на обеспечение органов кислородом, дает сбои. Кортизол вырабатывается в недостаточном количестве, соответственно кровоток замедляется, и уменьшается объем циркулирующей крови. Кровь насыщается углекислым газом, свертываемость крови нарушается, что ведет к образованию тромбов и возникновению кровотечений.
Диагностические мероприятия
Определить наличие и степень кислородного голодания помогают методы инструментальной диагностики. Первым таким методом является кардиотокография (КТГ). Этот метод диагностики совершенно безопасен. Аппарат кардиотокографии непрерывно регистрирует частоту сердечных сокращений плода и маточных сокращений. При помощи ультразвукового графика выводится тахограмма. Это график, который отражает количество сокращений сердечной мышцы за отведенный промежуток времени. Тензометрический датчик измеряет колебания давления и маточного тонуса, выводя гистерограмму – график мышечной активности матки. КТГ подсчитывает количество шевелений и позволяет отследить зависимость частоты сердцебиения от активности плода.
Начиная с двадцатой недели беременности, возможно исследование УЗИ с допплерографией. Этот метод направлен на исследование кровотока от матери к плаценте и от плаценты к плоду и позволяет обнаружить нарушения маточно-плацентарного кровообращения. С помощью данного метода диагностики можно также определить качество околоплодных вод.
Кроме вышеуказанных методов, специалист прослушивает сердце плода для оценки его работы с помощью акушерского стетоскопа. Однако этот метод является неточным, поэтому при подозрении на аномалию сердца врач направляет беременную на прохождение КТГ и УЗИ.
Лечение
Лечение внутриутробной гипоксии требует наблюдения беременной в стационаре. Женщине обеспечивается полный покой и назначается терапевтический метод лечения, который направлен не только на обогащение крови кислородом, но и на выявление истинной причины возникновения гипоксии. Как правило, аномалии протекания беременности, такие как внутриутробная гипоксия плода, – последствия или симптомы какого-либо заболевания.
Врач назначает беременной препараты, которые снижают вязкость крови, улучшают кровоток от матери к плаценте и нормализуют обмен веществ между матерью и плодом. Назначение других препаратов и процедур зависит от причины гипоксии, если она выявлена, и направлено на устранение этой причины.
При положительной динамике больную выписывают и дают рекомендации по профилактике гипоксии. К ним относятся прогулки на свежем воздухе, снижение физической активности, отказ от вредных привычек и соблюдение определенных правил в питании. В случае если лечение оказалось безрезультатным, и кислородная недостаточность сохраняется, требуется оперативное извлечение плода. Если срок беременности превышает двадцать восемь недель, врач назначает операцию – кесарево сечение.
Профилактика
Существует ряд простых рекомендаций, соблюдение которых поможет снизить риск кислородной недостаточности малыша. Прежде чем планировать беременность, женщине необходимо заняться лечением хронических болезней, избавиться от вредных привычек. При наступлении беременности важно встать на учет в медицинское учреждение на раннем сроке. На протяжении всего срока беременности необходимо регулярно посещать врача, сдавать анализы и делать УЗИ. Это обеспечит контроль за здоровьем беременной и малыша, а, следовательно, поможет избежать развития возможных патологических состояний плода.
Важным аспектом в профилактике внутриутробной гипоксии является ведение здорового образа жизни. Необходимо много времени проводить на свежем воздухе, спать восемь часов в сутки, сбалансировать рацион питания.
Во время беременности нужно восполнять запас витаминов и питательных веществ, уровень которых снижается в связи дополнительной нагрузкой на организм. Следует поддерживать в норме уровень кальция, магния и других минералов. Особенно важен контроль содержания железа в крови, так как его низкий уровень ведет к анемии – одной из основных причин гипоксии. Принимать витаминные препараты следует согласно назначениям врача.
Последствия
Последствия внутриутробной гипоксии зависят от ее вида. Хроническая гипоксия, начавшаяся на раннем сроке беременности, когда только начинается формирование жизненно важных систем плода, может привести к образованию врожденных пороков. Гипоксия, перенесенная на поздних сроках беременности, способна вызвать задержку развития плода, а также ведет к ишемии и некрозу отдельных органов. У новорожденного малыша часто наблюдается недобор роста и веса, а также тяжелый адаптационный период (перестройка организма в новой среде). В будущем пережитое в утробе матери кислородное голодание способно вызвать такие заболевания, как эпилепсия и детский церебральный паралич.
Острая внутриутробная гипоксия ребенка приводит к ишемии и некрозу тканей. Если острая гипоксия возникла во время родов, возможно несколько вариантов последствий, в зависимости от причины кислородного голодания:
- Дыхательные пути малыша не полностью очищены от околоплодных вод. В данном случае возможно развитие пневмонии, в худшем случае – гибель ребенка от удушья.
- Потеря большого объема крови. У новорожденного развивается геморрагический шок, что нарушает механизмы работы всех систем. При таких обстоятельствах существует угроза жизни не только малышу, но и матери.
После появления на свет малыша, перенесшего гипоксию в утробе матери, ему требуется постоянный контроль квалифицированных специалистов. Последствия кислородного голодания могут проявиться не в первые дни жизни, а значительно позже. Поэтому очень важно отслеживать изменения и аномалии в развитии малыша, чтобы выявить и предупредить развитие неблагоприятных последствий гипоксии.
Гипоксически-ишемическое поражение: Причины развития, диагностика
Гипоксически-ишемическое поражение (ГИП) ЦНС – это комплекс изменений в организме ребенка, возникающий вследствие недостаточного снабжения кислородом органов и тканей. Гипоксия на ранних сроках (6-11 недель) может привести к аномалиям развития структур головного мозга плода, а на поздних стадиях – к задержке внутриутробного развития, поражению ЦНС и снижению адаптационных возможностей малыша после рождения.
Основные причины развития ГИП ЦНС:
— анемия у мамы (снижение количества гемоглобина, при котором снижается доставка кислорода и питательных веществ к тканям организма малыша)
— любые хронические заболевания и пороки: врожденные пороки сердца, легких других органов, заболевания почек, наличие сахарного диабета, которые способствуют нарушению кровообращения
— осложнения беременности и родов (гестоз, угроза преждевременных родов, патология плаценты и пуповины, недонашивание и перенашивание беременности, многоплодная беременность, многоводие и маловодие, различные аномалии родовой деятельности)
— заболевания плода (гемолитическая болезнь новорожденных, внутриутробное инфицирование, кровотечения)
Ощутимые признаки гипоксии плода преимущественно выражаются в изменении его двигательной активности (внезапное усиление, учащение сердцебиения и движений (шевеления) плода при острой или урежение и ослабление их же при хронической гипоксии). При выявлении диагноза внутриутробная гипоксия плода, будущей маме необходимо проведение процедур по выявлению причин с последующим комплексным лечением их источника с возможной госпитализацией в стационар, соблюдением постельного или домашнего режима и режима дня.
Диагностика:
Необходимо проведение ультразвукового исследования плода, применение кардиотокографии (запись сердечной деятельности плода) и доплерометрии (исследование кровотока сосудов матки и пуповины плода) с той частотой, которой назначит лечащий врач. Также применяются аускультация (выслушивание) сердцебиения плода стетоскопом.
Следует отметить, что не каждая беременность протекает на фоне вышеперечисленных заболеваний, осложняя внутриутробную гипоксию плода. Чтобы не допустить возможного появления гипоксии, особое внимание уделяется ее профилактике: длительные прогулки на свежем воздухе, обязательные дозированные физические нагрузки (гимнастика, зарядка, упражнения для беременных и дыхательные упражнения, плавание, йога). Возможно применение гипербарической оксигенации (ГБО) по назначению лечащего врача. Необходимо помнить, что лечение должно быть назначено гинекологом, быть комплексным и учитывать индивидуальный подход к каждой будущей маме.
Ранние симптомы, с которыми следует обратиться к детскому неврологу— вялое сосание груди, поперхивание при кормлении, вытекание молока через носик малыша
— слабый крик ребенка, гнусавый или осиплый голос
— частые срыгивания и недостаточная прибавка в весе
— снижение двигательной активности ребенка, сонливость, вялость или выраженное беспокойство
— дрожание подбородка, верхних и/или нижних конечностей, частые вздрагивания
— трудности при засыпании, частые пробуждения во сне
— запрокидывание головы
— замедление или быстрое увеличение окружности головы
— низкий (дряблые мышцы) или высокий тонус мышц конечностей и туловища
— уменьшение активности движений руки или ноги с какой-либо стороны, ограничение разведения бедер или наличие позы «лягушки» с выраженным разведением бедер, необычная поза ребенка
— косоглазие, кривошея
— рождение ребенка путем кесарева сечения, в тазовом предлежании, с аномалием родовой деятельности или с применением акушерских щипцов, выдавливанием, с обвитием пуповины вокруг шеи
— недоношенность ребенка
— наличие судорог при родах или в послеродовом периоде
Бывают случаи, когда при рождении у малыша имеются минимальные нарушения, но спустя годы, под влиянием тех или иных нагрузок – физических, умственных, эмоциональных – неврологические нарушения проявляются с различной степенью выраженности. Это, так называемые, поздние проявления родового травматизма. Среди них:
— снижение мышечного тонуса (гибкость), которая так часто является дополнительным плюсом при занятиях спортом. Нередко таких детей с радостью принимают в секции спортивной и художественной гимнастики, в хореографические кружки. Но большинство из них не выносят тех физических нагрузок, которые имеют место быть в данных секциях.
— снижение остроты зрения, наличие асимметрии надплечий, углов лопаток, искривления позвоночника, сутулости – признаков возможной родовой травмы шейного отдела позвоночника
-возникновение головных болей, головокружения
При наличии вышеперечисленных жалоб не откладывайте визит к детскому неврологу! Специалист назначит определенные обследования, курс лечения и обязательно поможет Вам!
Внутриутробная гипоксия — обзор
Физиология допплер-велоциметрии
При гипоксии плода или других формах стресса развиваются отклонения формы волны скорости плода. Хотя систолический компонент отражает интенсивность сердечной функции плода, диастолический компонент кривых скорости плода имеет наибольшее значение при оценке состояния плода, поскольку он отражает величину периферического сопротивления, которое нижнее сосудистое русло оказывает сердцу.По мере увеличения периферического сопротивления скорость кровотока уменьшается во время сердечной диастолы. Следовательно, у плода с инфарктом плаценты и связанным с этим увеличением внутриплацентарного сопротивления со временем наблюдается рост систолического отношения к диастолическому. Если сопротивление повышается достаточно высоко, кровоток в диастоле может полностью прекратиться. В крайних случаях может наблюдаться обратный диастолический поток. Многие исследователи сообщали о связи отсутствия конечных диастолических скоростей (AEDV) в пупочной артерии с ЗВУР, аспирацией мекония, внутриутробной гибелью плода и асфиксией при рождении.
При беременности, осложненной ЗВУР, от двух третей до трех четвертей плодов демонстрируют чрезмерно высокий индекс плацентарной резистентности (систолическое / диастолическое соотношение или индекс резистентности) (Trudinger et al, 1991). Плоды с аномальной формой волны скорости кровотока имеют более высокую частоту неонатальной заболеваемости, чем плоды с нормальными результатами исследования.
Гистологически высокое сопротивление плаценты, о чем свидетельствует аномальная форма волны доплеровского кровотока в пуповине, связана с уменьшением количества мелких (диаметром <90 мкм) артерий в третичных ворсинах плаценты (сосуды сопротивления) (Giles et al, 1985) облитерирующие изменения остальных сосудов.
Нарушения скорости кровотока могут возникать в других сосудистых руслах у плода, страдающего гипоксемией. Когда уровень кислорода в пуповинной венозной крови падает, мозговое кровообращение компенсируется увеличением кровотока в сонных артериях. Соответственно, при прогрессирующей гипоксии внутримозговое сосудистое сопротивление обычно падает, а диастолическая скорость увеличивается. Скорость потока в нисходящей аорте, снабжающей большинство внутренних органов плода, может быть нарушена.Уровень внутриутробной гипоксемии в любой момент времени может быть лучше всего выражен как сумма воздействий на пупочное, церебральное и аортальное кровообращение.
Поскольку связь сердца плода с плацентарным, церебральным и висцеральным кровообращением находится в динамическом состоянии потока во время беременности, индексы формы волны скорости плода должны быть скорректированы с учетом гестационного возраста. Нормативные таблицы для индекса пульсации и систолического диастолического отношения были опубликованы Schulman и соавторами (1984).
Нарушения формы волны скорости плода (особенно диастолические изменения) обычно становятся очевидными за 1–3 недели до появления аномалий других клинических параметров, таких как частота сердечных сокращений плода, объем околоплодных вод и АД плода. Во время беременности маточный кровоток заметно увеличивается с минимальным сопротивлением, вторичным по отношению к воздействию эстрогена на маточное кровообращение. На достаточно ранних сроках беременности можно задокументировать кривые скорости плода в маточно-плацентарной циркуляции, а при некоторых материнских заболеваниях, таких как хроническая гипертензия и гипертензия, вызванная беременностью, могут быть задокументированы отклонения в кривых скорости плода в маточно-плацентарной фазе.Фактически, Кэмпбелл и соавторы (1986) отметили аномалии маточно-плацентарного кровообращения примерно с 20 недель беременности, при которых развивались тяжелые ЗВУР или гипертензия, вызванная беременностью.
Влияние внутриутробной реанимации плода кислородом на окислительный стресс в развивающемся мозге крысы
Все экспериментальные процедуры были одобрены Комитетом по уходу и использованию животных в Вашингтонском университете в Сент-Луисе (# 20170010) и соответствуют требованиям исследований на животных: Руководство по отчетности об экспериментах in vivo (ARRIVE).Все предложенные здесь методы были выполнены в соответствии с соответствующими институциональными директивами и правилами.
Животные и лечение
Беременных крыс линии Sprague – Dawley (SD) на время (SAS 400, Charles River Laboratories, Уилмингтон, Массачусетс) получали в эмбриональный день (E) 13 и помещали в стандартные условия содержания до экспериментов. На E20 рандомизированным самкам вводили 100 мкг / кг окситоцина (OXT) (1 мг / мл в стерильном физиологическом растворе, Selleck Chemicals, Хьюстон, Техас) через катетер для хвостовой вены 25G под кратковременной анестезией изофлураном (со сжатым 21% кислородом в качестве газ-носитель), чтобы вызвать 10-минутное тетаническое сокращение матки и острую ишемию-гипоксемию плаценты, как описано нами ранее 11 .В этой парадигме дистресс плода подтверждался повышенным содержанием лактата в головном мозге плода. Мы выбрали эту дозу OXT из-за минимальной трансплацентарной передачи 36 , тем самым исключив возможность прямого воздействия OXT на развивающийся мозг. После лечения самок сразу же случайным образом распределили на две группы во время периода ишемии-реперфузии: комнатный воздух (RA) и 100% кислород (O). В группе RA обработанные самки (n = 8) подвергались воздействию 21% кислорода, вводимого со скоростью 3 л / мин в стандартный контейнер для крыс (Kent Scientific Corporation, Торрингтон, Коннектикут) в течение 6 часов.Аналогичным образом, в группе O плотины (n = 8) подвергались воздействию 100% кислорода с той же скоростью потока в течение 6 часов. Все контейнеры (общий объем 3 л) были предварительно заполнены соответствующими газами со скоростью 5 л / мин в течение не менее 3 минут для достижения необходимой концентрации кислорода. Небольшой выход в контейнере позволял контролировать газы и предотвращал накопление углекислого газа. Все плотины переносили лечение OXT и последующее воздействие различных газов. Через 6 часов после воздействия RA или O плоды были извлечены путем кесарева сечения под кратковременной анестезией изофлураном (в 21% кислороде для группы RA и 100% кислороде для группы O, соответственно, для поддержания концентрации кислорода, специфичной для группы лечения).Щенков быстро определили по полу на основе различий в аногенитальном расстоянии между самцами и самками, и мозг самца и самки извлекали и мгновенно замораживали в жидком азоте для хранения при -80 ° C. Для каждого условия лечения использовали по одному щенку любого пола.
Сбор крови из левого желудочка плода для анализа газов крови
Чтобы оценить, была ли гипероксия матери связана с повышением оксигенации плода, мы провели отдельную серию экспериментов. Вкратце, 6 беременным самкам Sprague Dawley с установленным сроком беременности E20 вводили 100 мкг / кг OXT через катетер для хвостовой вены 25G с последующим случайным назначением либо на обработку комнатным воздухом, либо на обработку 100% кислородом (n = 3 каждая) в течение 6 часов, как описано выше.Впоследствии, по крайней мере, 3 плода были взяты от каждой матери посредством кесарева сечения и немедленно препарированы для доступа к грудной полости. Поскольку пункция левого желудочка была технически сложной из-за высокой частоты сердечных сокращений и чрезвычайно малого времени пребывания крови, мы пересекли левый желудочек, позволили крови скапливаться в грудной полости и немедленно отсосали ее в шприц объемом 1 мл, покрытый гепарином. . Нам удалось собрать примерно 100 мкл на плод, и все 300 мкл от всех трех плодов на каждую мать были тщательно перемешаны в одном шприце перед анализом газов крови с помощью анализатора Stat Profile Prime ® (Nova Biomedical, Waltham, MA) .
Анализы на биомаркеры окислительного стресса
Чтобы оценить, вызывает ли гипероксия матери окислительное повреждение головного мозга плода, мы сначала проверили биомаркеры окислительного стресса. В частности, мы исследовали окислительное повреждение липидов (4-гидроксиноненаль, продукт перекисного окисления липидов), белков (карбонил белка) и ДНК (8-гидрокси-2′-дезоксигуанозин [8-OHdG]) в головном мозге обоих полов. Кроме того, мы проанализировали соотношение глутатиона (GSSG / GSH) как маркер антиоксидантного ответа.Во всех экспериментах использовалось примерно 25–50 мг ткани мозга из коры левого мозга. Концентрацию белка определяли с использованием набора Pierce ™ BCA Protein Assay Kit (ThermoFisher Scientific). Степень окислительного повреждения липидов и белков оценивали с помощью наборов OxiSelect ™ HNE Adduct Competitive ELISA и OxiSelect ™ Protein Carbonyl ELISA (Cell Biolabs), соответственно, в соответствии с инструкциями производителя, но с небольшими изменениями (добавление PEI до конечной концентрации 0 .5% для анализа карбонила белка). Количество 8-OHdG определяли в специально приготовленных лизатах корковой ткани. Вкратце, приблизительно 25 мг корковой ткани гомогенизировали в порошок с жидким азотом с использованием пестика. ДНК экстрагировали с помощью набора DNeasy Blood and Tissue Kit (Qiagen, США) и концентрацию измеряли с помощью спектрофотометра NanoDrop 2000 (Thermo Scientific ™, США). Маркер окислительного повреждения ДНК 8-оксогуанин (8-OHdG) определяли количественно с использованием набора OxiSelect ™ Oxidative DNA Damage ELISA (Cell Biolabs) в соответствии с инструкциями производителя.Поглощение для всех анализов измеряли при 450 нм. Для анализа общего глутатиона (GSSG / GSH) лизаты готовили из примерно 50 мг кортикальной ткани, обработанной 5% метафосфорной кислотой, с последующим количественным определением с помощью набора для анализа общего глутатиона OxiSelect ™ (GSSG / GSH) (Cell Biolabs) в соответствии с инструкциями производителя. . Поглощение сразу измеряли при 405 нм с интервалами 1 мин в течение 10 мин, чтобы определить наклон для окончательных расчетов.
Taqman RT-qPCR для дифференциальной экспрессии генов окислительного стресса
Общая РНК была выделена из коры головного мозга правого плода (прибл.30 мг) с использованием набора RNeasy Mini Kit (Qiagen, Germantown, MD). Геномную ДНК удаляли с помощью QIAshredder (Qiagen, Germantown, MD) и обработки на колонке набором ДНКаз, не содержащих РНКаз (Qiagen, Germantown, MD). 2,5 мкг очищенной РНК (соотношение 260/280 ≥ 2,0) подвергали обратной транскрипции в кДНК с использованием SuperScript ™ IV VILO ™ Master Mix с ферментом ezDNase ™ (ThermoFisher Scientific, Waltham, MA) в конечном объеме 20 мкл при 37 ° C для 30 мин, 50 ° C в течение 10 минут, 85 ° C в течение 5 минут и 4 ° C в течение 30 минут. Впоследствии мы выполнили запланированные сравнения связанных с лечением различий в экспрессии выбранных генов-мишеней, связанных с окислительным стрессом ( Nox1, Nox3, Nos2, Ucp3), антиоксидантной защитой ( Cat, Gpx1, Gpx4, Gsr, Prdx1, Prdx2, Prdx3, Prdx6, Sod1, Sod2, Sod3, Srxn1, Cygb, Ngb, Txnip, Txnrd2 ) и митохондриальная электронная транспортная цепь (ETC) ( Mt-cyb, Mt-nd1, Mt-nd2, Mt-nd4, Mt -nd5, Mt-atp8, Mt-co1, Mt-co3 ).Мы включили митохондриальные гены ETC из-за интегральной роли митохондрий в генерации активных форм кислорода во время окислительного стресса. Настроенный 96-луночный планшет TaqMan Array для FAST (ThermoFisher Scientific, Waltham, MA), содержащий эти 28 предварительно проверенных зондов и 4 эндогенных гена ( 18S рРНК, Actb, Gapdh, Pgk1 ), использовали для кПЦР. Каждые 10 мкл реакционной смеси содержали 5 мкл смеси TaqMan Master Mix (ThermoFisher Scientific, Уолтем, Массачусетс), 3 мкл сверхчистой воды и 2 мкл кДНК. КПЦР выполняли в системе Applied Biosystems 7500 Real-Time PCR System (ThermoFisher Scientific, Уолтем, Массачусетс) при следующих условиях цикла: предварительная инкубация при 50 ° C в течение 2 минут, затем при 95 ° C в течение 10 минут, с последующими 40 циклами амплификации. (95 ° C, 15 с и 60 ° C, 1 мин) и охлаждение (40 ° C, 10 с).Все реакции проводили в трех экземплярах. Из 4 эндогенных референсных генов только Actb и Gapdh стабильно экспрессировались в экспериментальных условиях (алгоритм geNorm; qbase + версия 3.2). Относительную экспрессию мРНК, нормированную к среднему геометрическому Actb и Gapdh , рассчитывали с использованием метода 2 — ΔΔCT с сопоставленными по полу контрольными образцами в качестве эталона.
Вестерн-блоттинг для митохондриального окислительного фосфорилирования
Затем мы выполнили иммуноблоттинг развивающейся коры головного мозга, чтобы количественно оценить влияние материнской кислородной реанимации на систему митохондриального окислительного фосфорилирования (OXPHOS) в развивающемся головном мозге.Вкратце, мы выделили митохондрии примерно из 100 мг коры плода с использованием набора для изоляции митохондрий (ThermoFisher Scientific) с последующим лизисом и гомогенизацией буфером RIPA, содержащим ингибитор протеазы и ингибитор фосфатазы в 1X PBS. Концентрации белка определяли с помощью набора для анализа белка BCA (ThermoFisher Scientific, США). 15 мкг каждого образца обрабатывали восстановленным буфером LDS и нагревали при 50 ° C в течение 5 минут, затем наносили на 10% гель Bolt (ThermoFisher Scientific).Митохондрии сердца крысы использовали в качестве положительного контроля. После разделения в рабочем буфере MES SDS (ThermoFisher Scientific) белки переносили на нитроцеллюлозную мембрану и затем блокировали в течение 2 часов при комнатной температуре в 5% обезжиренном сухом молоке и 1X Tween 20 в трис-буферном солевом растворе (TBS-T). Мембрану инкубировали с первичным мышиным антителом против OXPHOS (OriGene; 1: 3000, разведенным в 5% BSA и 1X TBS-T) в течение ночи при 4 ° C, а затем с конъюгированным с HRP вторичным антителом против мышиного антитела (1: 5000, разведенным в 5%). % обезжиренного сухого молока и 1X TBS-T) в течение 1 ч при комнатной температуре.Для визуализации белков использовали хемилюминесцентный детекторный реагент (ECL Prime, GE Healthcare). После очистки в течение 45 минут с последующим блокированием 5% обезжиренным сухим молоком и 1X TBS-T в течение 30 минут мембрану повторно зондировали кроличьими антителами против VDAC1 (Cell Signaling, США. 1: 5000, разведенными 5% обезжиренными). жирное сухое молоко и 1X TBS-T) в течение 1 часа при комнатной температуре, а затем HRP-конъюгированные вторичные антитела против кролика (1: 5000, разведенные в 5% обезжиренном сухом молоке и 1X TBS-T) в течение 1 часа при комнатной температуре. температура. Впоследствии изображения были обработаны с помощью Image Studio версии 5.2 (LI-COR) для денситометрического количественного определения. Полноразмерные изображения вестерн-блоттинга представлены в качестве дополнительной информации.
Статистический анализ
Выбросы данных были обнаружены и устранены с помощью ROUT (надежная регрессия и анализ выбросов) с Q, установленным на 10%. Нормальность остатков проверялась с помощью комплексного теста Д’Агостино-Пирсона с последующим t-критерием Уэлча для данных по газам в крови и двухфакторным дисперсионным анализом ANOVA и тестом множественных сравнений Сидака для всех остальных данных, в которых пол потомства был переменной.Данные RT-qPCR с ненормальными остатками ( Nox1, Nos2, Prdx3, Sod3, Srxn1, Mt-atp8, Mt-co3 ) были преобразованы по Бокс-Коксу перед статистическим тестированием. Данные представлены как среднее значение ± стандартная ошибка среднего и проанализированы с помощью Prism 8 для Mac OS X (Graphpad Software, Inc, Ла-Холла, Калифорния). Двустороннее значение P ≤ 0,05 считалось статистически значимым.
Презентация на конференции
Этот тезис был представлен на 40-й ежегодной встрече по вопросам беременности, Общество медицины материнского плода, Грейпвайн, Техас, 76501, 3–8 февраля 2020 г.
Сохранение мозга при ограничении внутриутробного развития: рекомендации для неонатолога — FullText — Neonatology 2015, Vol. 108, №4
Абстрактные
Ограничение внутриутробного развития (IUGR) чаще всего вызывается плацентарной недостаточностью, в ответ на которую плод адаптирует свое кровообращение для сохранения поступления кислорода и питательных веществ в мозг («сохранение мозга»). В настоящее время мало что известно о послеродовом течении и последствиях этой антенатальной адаптации мозгового кровообращения.Измененная церебральная гемодинамика может сохраняться после рождения, что предполагает иной подход к церебральному мониторингу и клиническому ведению недоношенных новорожденных с ЗВУР, чем у их соответствующим образом выросших сверстников. По этой теме доступно немного исследований, и небольшое количество доказательств свидетельствует о противоречивости. В этом обзоре обсуждается адаптация церебрального кровообращения у ЗВУР плодов и дается оценка доступной литературы по их постнатальному церебральному кровообращению с потенциальными клиническими последствиями.
© 2015 S. Karger AG, Базель
Введение
Ограничение внутриутробного развития (IUGR) традиционно и чаще всего определяется как масса тела при рождении ниже 10-го процентиля гестационного возраста на соответствующей кривой роста популяции. ЗВУР чаще всего вызывается плацентарной недостаточностью, в ответ на которую плод адаптирует свое кровообращение, чтобы сохранить снабжение мозга кислородом и питательными веществами («бережное отношение к мозгу»).Измененная церебральная гемодинамика может сохраняться после рождения, что подразумевает иной подход к церебральному мониторингу и клиническому ведению недоношенных новорожденных с ЗВУР, чем их сверстники, выращенные надлежащим образом (AGA). В этом обзоре обсуждается адаптация мозгового кровообращения у ЗВУР плодов и дается оценка доступной литературы о послеродовых последствиях этого явления.
Сохранение мозга у поврежденного плода
В ситуации хронической гипоксемии плода или недостаточности питательных веществ плод перераспределяет свой сердечный выброс, чтобы обеспечить максимальное поступление кислорода и питательных веществ в мозг (сохранение мозга).Кровообращение плода представляет собой параллельный контур, в котором большая часть выхода правого желудочка шунтируется через артериальный проток к нисходящей аорте, а левый желудочек в основном снабжает верхнюю часть тела и головной мозг. Сужение сосудов периферических сосудов приводит к увеличению постнагрузки правого желудочка. В случае плацентарной недостаточности повышенное сопротивление сосудов плаценты способствует этому повышенному системному сопротивлению [1]. С другой стороны, расширение сосудов головного мозга вызывает уменьшение постнагрузки левого желудочка.Эти изменения приводят к преимущественному сдвигу сердечного выброса в пользу левого желудочка, что улучшает кровоснабжение головного мозга [2].
Региональное, а не глобальное перераспределение
В настоящее время считается, что сохранение мозга происходит регионально, а не глобально по всему мозгу. Эрнандес-Андраде и др. [3] показали путем измерения фракционного объема движущейся крови (FMBV), что церебральный кровоток (CBF) у IUGR плодов показывает региональные изменения с прогрессированием ухудшения состояния плода.Они увидели первоначальное увеличение лобной FMBV, а затем снижение по мере ухудшения состояния плода. FMBV базальных ганглиев, с другой стороны, демонстрировал устойчивое и значительное увеличение с ухудшением состояния плода. В мозжечке наблюдалась аналогичная тенденция увеличения FMBV, связанная с тяжестью компромисса плода. Увеличение FMBV мозжечка также может означать усиление кровоснабжения ствола мозга, поскольку оба питаются через задний мозговой кровоток. Результаты их исследования позволяют предположить наличие иерархического порядка в мозговом кровоснабжении при хронической гипоксии.На более ранних стадиях защищены высшие когнитивные функции лобных долей; однако в хронических и более угрожающих обстоятельствах акцент, кажется, смещается в сторону выживания, защиты важных структур, таких как базальные ганглии и ствол мозга [3].
Обнаружение сохранения мозга
Изменения CBF, связанные с сохранением мозга, могут быть обнаружены с помощью допплеровской сонографии. Вазодилатация головного мозга и, следовательно, снижение сопротивления сосудов головного мозга приводит к увеличению конечной диастолической скорости кровотока в артериях головного мозга.В результате считается, что расширение сосудов головного мозга и повышение CBF можно обнаружить по снижению индекса пульсации [PI; (пиковая систолическая скорость потока — конечная диастолическая скорость потока) / усредненная по времени скорость потока] или индекс сопротивления [RI; (пиковая систолическая скорость потока — конечная диастолическая скорость потока) / пиковая систолическая скорость потока] церебральных артерий. Средняя мозговая артерия (MCA) используется в качестве золотого стандарта, а MCA-PI ниже 5-го процентиля обычно классифицируется как аномальный [4].Поскольку было показано, что перераспределение кровотока происходит региональным образом [3], сохранение мозга может присутствовать до того, как оно будет обнаружено аномальным MCA-PI [5]. В нескольких исследованиях сообщалось, что изменения CBF в передней мозговой артерии происходят чаще и раньше, чем изменения в MCA [6,7,8]. Это согласуется с теорией иерархического перераспределения CBF: сначала защищают высшие когнитивные функции лобных долей, которые обеспечиваются передней мозговой артерией, а затем более элементарные области мозга, такие как базальные ганглии, которые поставляются MCA.
Ряд авторов предположили, что расчет цереброплацентарного отношения (ЦПР) имеет дополнительную ценность для диагностики сохранения мозга [9,10,11,12,13,14,15,16]. Это соотношение между MCA и UA-PI или -RI может быть уменьшено, в то время как отдельные значения остаются в пределах нормы. Некоторые авторы указали, что СЛР имеет более высокую чувствительность, чем одна только СМА, для прогнозирования перинатального и неонатального исхода [9,11]. Однако многие из этих исследований показали, что плоды с аномальной СЛР родились более преждевременно [9,10,12], что, возможно, исказило их результаты.
Реверс компенсаторного потока
Были сообщения о том, что у плодов с серьезным нарушением ЗВУР наблюдается возврат MCA-PI к нормальным значениям [17,18,19]. Это изменение компенсирующего потока считается предтерминальным признаком. Фактически, в отчете Konje et al. [17], 4 из 8 плодов, у которых была выявлена нормализация СМА, были последующими мертворожденными, а остальные 4 умерли в неонатальном периоде. Не совсем понятно, почему происходит это изменение компенсирующего потока, и причина может быть многофакторной.Было высказано предположение, что хроническая гиперперфузия головного мозга плода приводит к отеку мозга, нарушая CBF [19]. Снижение CBF также может быть результатом сердечной декомпенсации плода [17]. Теоретически это может быть связано со снижением сердечного выброса [17], но более вероятно, что это связано с венозным застоем. В подтверждение этой гипотезы посмертное церебральное исследование плода с ЗВУР, погибшего после нормализации CBF, выявило не только выраженную дилатацию СМА, но и перивентрикулярную радиальную гиперемию [18].Считается, что перивентрикулярный застой имеет венозное происхождение и связан с застоем в вене Галена [20,21]. Сообщалось об усилении кровотока в вене Галена, указывающем на повышенный венозный возврат из-за сохранения мозга, у плодов ЗВУР [22]. В нормальных условиях кровоток в этой вене не показывает пульсации [23], но пульсация описана при беременности, осложненной гипертонией и ЗВУР [22,23]. Считается, что эти пульсации возникают в результате передачи волн давления от венозного кровообращения [23], которые, в свою очередь, являются признаком сердечной недостаточности плода [24].В заключение, сердечная недостаточность плода может нарушить венозный мозговой возврат, что впоследствии может поставить под угрозу сохранение мозга.
Возможные последствия длительного сохранения мозга
Сохранение мозга, по сути, является защитным механизмом при хронической гипоксемии; однако длительное сохранение мозга может привести к изменению структуры и функции сосудистой сети головного мозга.
Ремоделирование сосудов головного мозга
Признаки ремоделирования сосудов системных артерий были обнаружены в исследованиях IUGR как на людях, так и на животных [25,26,27,28,29,30,31,32,33,34].Считается, что этот процесс ремоделирования сосудов вызван системными гемодинамическими изменениями, наблюдаемыми при ЗВУР, которые изменяют напряжение сдвига и натяжение стенки [35]. Поэтому вполне вероятно, что аналогичные изменения сосудистой стенки происходят в сосудах головного мозга, поскольку сохранение мозга оказывает большое влияние на церебральную гемодинамику. Фактически, повышенная частота инсульта была зарегистрирована у взрослых, рожденных с низкой массой тела [36]. Хотя низкая масса тела при рождении связана с другими факторами риска инсульта, такими как артериальная гипертензия [37], связь между низкой массой тела при рождении и инсультом была наиболее выражена для лиц с низкой массой тела при рождении и низкой массой плаценты в зависимости от размера головы [36].Относительно увеличенный размер головы предполагает, что у этих людей была функция сохранения мозга, которая, возможно, сделала их более восприимчивыми к возникновению инсульта [38]. Однако в этой области было проведено очень мало исследований. На животных моделях беременных овец, использующих большую высоту для индукции гипоксии плода, были продемонстрированы изменения в составе сосудистой стенки и сократимости [39]. Было высказано предположение, что такая сосудистая адаптация к хронической гипоксии помогает сохранять энергию, сохраняя при этом базовую сократительную функцию [40].Хотя ремоделирование может помочь сохранить энергию при неблагоприятных внутриутробных обстоятельствах, послеродовые последствия этих адаптаций недостаточно изучены. Фактически, недавнее исследование продемонстрировало нарушение структурной целостности и стабильности микрососудов головного мозга у ягнят с ЗВУР, что увеличивает проницаемость гематоэнцефалического барьера и повышает риск кровоизлияний в мозг [41].
Потеря церебральной вазореактивности
Длительное сохранение мозга и ремоделирование сосудов может привести к снижению функции сосудистой стенки.Пренатальная потеря вазореактивности при ЗВУР была предложена исследованием, в котором человеческие зародыши ЗВУР с сохранением мозга подвергались материнской гипероксигенации. Подгруппа этих плодов не показала ожидаемого повышения церебрального сопротивления в ответ на повышенный уровень кислорода. Обнаружение того, что эти плоды не приспособили свое мозговое кровообращение к новой ситуации, наводит на мысль о нарушении регуляции мозгового кровообращения. Было также обнаружено, что эти «не отвечающие» имеют более высокий риск родов из-за дистресс-синдрома плода, а интервал между допплеровским исследованием и родами был короче по сравнению с «респондентами», что указывает на то, что они были более подвержены риску [42].Нарушение вазореактивности также может быть еще одним объяснением того, почему в конечном итоге может произойти потеря компенсаторной функции сохранения мозга, как описано ранее. Случай, проиллюстрированный Fignon et al. [18] показали, что церебральный RI и CPR перестали показывать нормальные физиологические колебания, указывающие на потерю сосудистой реактивности, до того, как RI и CPR в конечном итоге повысились и компенсация кровотока была обращена на противоположную. Если нарушение вазореактивности сохраняется после рождения, это может нарушить ауторегуляцию головного мозга, что является важным механизмом предотвращения церебральной гипо- и гиперперфузии.
Постнатальное мозговое кровообращение после сохранения мозга
В настоящее время мало что известно о постнатальном мозговом кровообращении у новорожденных с ЗВУР. Небольшой объем данных, имеющихся в литературе, указывает на то, что измененная церебральная гемодинамика, существовавшая до рождения, сохраняется в постнатальном периоде. Подобно пренатальным допплерографическим наблюдениям, более низкие значения PI и RI средней мозговой артерии и передней мозговой артерии были обнаружены до 4 дней после рождения, что указывает на стойкую дилатацию мозговых артерий [43,44,45].В соответствии с этими данными, увеличение CBF, измеренное с помощью ксенона-133, также было зарегистрировано в первый день жизни [46]. Более того, в течение первых 24 часов после рождения сообщалось о более высоком региональном сатурации кислорода в мозге и снижении мозгового извлечения кислорода [47]. Все эти параметры церебральной гемодинамики нормализовались в течение нескольких дней, что указывает на временные различия в мозговом кровообращении [44,46,47].
Несколько доплеровских измерений скорости CBF (включая пиковую систолическую скорость и усредненную по времени максимальную скорость) были использованы для исследования CBF в IUGR, поскольку было показано, что изменения скорости потока MCA хорошо коррелируют с изменениями CBF [48] .Однако сообщалось о противоположных результатах [45,49,50,51]. На скорость кровотока влияют не только объем потока и диаметр сосуда, но и другие факторы, такие как гематокрит и эластические свойства стенки сосуда [52]. Хорошо известно, что новорожденные, которые подвергались хронической гипоксии в утробе матери, могут иметь полицитемию. О повышении гематокрита также сообщалось в некоторых исследованиях, упомянутых ранее [46,47,49]. Более того, изменения в составе стенок сосудов потенциально могут происходить при ЗВУР [39].Эти факторы в сочетании с различными типами измерений скорости кровотока, скорее всего, исказили результаты и привели к расхождениям в отчетах. Важно отметить, что эти факторы, особенно более высокая вязкость крови и повышенная способность переносить кислород, потенциально могут помешать всем исследованиям, посвященным церебральной гемодинамике и оксигенации, что затрудняет интерпретацию и сравнение результатов.
Что защищает мозг?
До сих пор мы называли сохранение мозга защитным механизмом.Важно отметить, что недавние исследования поставили под сомнение эту общепринятую идею. Несколько исследований как в доношенных, так и в недоношенных популяциях продемонстрировали, что субъекты с ЗВРП с сохранением мозга демонстрируют худшие исходы с точки зрения нервного развития и поведения, чем субъекты с ЗВУР без признаков сохранения мозга и контрольная группа [53,54,55,56,57,58]. Хотя не все авторы подтвердили эту связь [59, 60, 61], эти данные предполагают, что сохранение мозга не всегда может защитить от неврологического повреждения [57]. На основании этих исследований даже было высказано предположение, что увеличение CBF отражает прогрессирующие стадии черепно-мозговой травмы; не защитный механизм от него [54,55,57].Как описано ранее, ЗВУР может быть связано с ремоделированием сосудов и снижением вазореактивности [18,39,40,41,42]. Повышенный CBF может частично быть прямым следствием нарушения регуляции кровообращения. Эта теория подтверждается открытием, что CBF остается повышенным после рождения, в то время как новорожденный больше не подвергается воздействию гипоксической среды и больше не нуждается в компенсаторном увеличении CBF [43,44,45,46,47]. Гипотетически продолжение повышенного CBF в постнатальном периоде может вызвать гипероксию в хрупком мозге, что может способствовать неврологическому повреждению [62,63,64].
Большое клиническое значение имеет дальнейшее исследование природы феномена сохранения мозга, поскольку новые взгляды на эту тему могут иметь важные последствия для акушерского ведения беременностей с ЗВРП.
Церебральная ауторегуляция
Ауторегуляция — это способность сосудов головного мозга поддерживать довольно постоянный CBF, несмотря на колебания церебрального перфузионного давления, на которые в основном влияют изменения системного артериального давления [65,66].Когда системное кровяное давление повышается, церебральные артериолы сужаются, чтобы предотвратить гиперперфузию мозга. Снижение артериального давления компенсируется расширением сосудов головного мозга для предотвращения гипоперфузии и ишемии. Считается, что ауторегуляция частично зависит от миогенного рефлекса, при котором гладкомышечные клетки в артериолах сокращаются или расширяются в зависимости от внутрисосудистого давления [65,66]. Другие факторы, влияющие на регуляцию CBF, включают концентрацию кислорода и углекислого газа, метаболические потребности и нейронные влияния [65,66].
Способность к саморегуляции увеличивается с возрастом беременности. Считается, что ауторегуляция нарушена у больных недоношенных новорожденных, и считается, что это способствует ишемическому и геморрагическому повреждению, часто наблюдаемому в этой популяции [65]. Поскольку IUGR-плоды часто рождаются преждевременно, теоретически они подвержены риску нарушения ауторегуляции. Из-за структурных и функциональных изменений сосудов их ауторегуляция может быть еще больше нарушена, и, таким образом, новорожденные с ЗВУР могут быть даже менее подготовлены, чем их сверстники из AGA, для того, чтобы справиться с гипотензивными состояниями.Напротив, Bauer et al. [67,68] обнаружили, что поросята с низкой массой тела при рождении проявляют более адекватную ауторегуляторную реакцию на геморрагическую гипотензию, а также более высокую экстракцию кислорода мозгом во время гиперкапнической гипоксии, чем их сверстники из AGA. Эти результаты предполагают, что хроническая внутриутробная гипоксия может фактически стимулировать созревание защитных механизмов для обеспечения адекватной оксигенации и перфузии мозга. В этом случае субъекты IUGR могут действительно выдерживать периоды гипоперфузии и гипоксии лучше, чем их коллеги из AGA.Однако важно отметить, что эти поросята были получены от неосложненных беременностей. Хотя асимметричный рост этих поросят указывает на то, что имелась щадящая работа мозга и, следовательно, определенная степень внутриутробного кислородного голодания, гемодинамические нарушения и гипоксия могли быть умеренными.
Несмотря на его клиническое значение, литературы по этой теме крайне мало, и на сегодняшний день не проводилось исследований по изучению ауторегуляции мозга у новорожденных с ЗВУР человека.
Гипотензия и персистирующий артериальный проток
Считается, что гипотония и гемодинамически значимый персистирующий артериальный проток (HSPDA) отрицательно влияют на CBF у недоношенных детей AGA [69,70]. Как обсуждалось выше, помимо недоношенности, изменения сосудистой стенки головного мозга могут снижать вазореактивность и, таким образом, ограничивать ауторегуляторную реакцию для защиты мозга IUGR от гипоперфузии в этих обстоятельствах. Более того, ауторегуляторный ответ ограничен максимальным расширением сосудов [65].В случае длительного сохранения мозга из-за хронической гипоксемии максимальная дилатация сосудов, возможно, уже была достигнута, что еще больше ограничило бы защитную реакцию на гипотензию и HSPDA. Кроме того, системное сужение сосудов, связанное с перераспределением кровотока, может все еще иметь место, что ставит под угрозу ответ сосудосуживающего средства на увеличение периферического сопротивления в попытке поднять кровяное давление. Кроме того, сообщалось о сердечной дисфункции у новорожденных с ЗВУР, которая также может ограничивать компенсаторные реакции [32,71].Например, новорожденные с ЗВУР могут иметь диастолическую дисфункцию, ограничивающую наполнение желудочков [32,71]. При таких обстоятельствах тахикардный ответ на гипотензию не будет успешным, поскольку увеличение частоты сердечных сокращений позволит еще меньше времени для уже уменьшенного наполнения желудочков, что еще больше ухудшит сердечный выброс [72].
Напротив, работа с животными Bauer et al. [67,68] предположили, что воздействие хронической (легкой) внутриутробной гипоксии может фактически улучшить ауторегуляцию и мозговую экстракцию кислорода, позволяя мозгу IUGR лучше противостоять эффектам гипотензии и HSPDA . Также можно утверждать, что послеродовая стойкость повышенного CBF может уменьшить влияние системной гипотензии или протокового обкрадывания на мозговое кровообращение. Однако, поскольку послеродовое повышение CBF, по-видимому, является временным явлением, продолжающимся всего несколько дней, а функциональные и структурные аномалии сосудов могут сохраняться, защита от гипоперфузии головного мозга не может быть гарантирована по истечении этого периода. Несмотря на его клиническую важность, у нас мало понимания влияния предполагаемой гипотензии и HSPDA на постнатальную гемодинамику новорожденных с перераспределением IUGR.Большое клиническое значение имеет то, что эти темы будут рассмотрены в будущих исследованиях, поскольку результаты могут иметь значительное влияние на ведение новорожденных, особенно потому, что HSPDA, по-видимому, возникает чаще и в более ранний момент времени у новорожденных с IUGR по сравнению с их сверстниками по AGA [73 ] и диаметр HSPDA также был больше у новорожденных с ЗВР [73]. Неясно, почему частота и размер HSPDA увеличиваются при ЗВУР, но это может быть связано с изменениями сосудистой стенки, которые наблюдались при гистологии артериального протока в этой популяции [74].
Внутричерепное кровоизлияние
Внутричерепное кровоизлияние (ICH) — частое осложнение, связанное с недоношенными. Исследование Alderliesten et al. [75] показали, что у недоношенных новорожденных, у которых развивается тяжелое пери-внутрижелудочковое кровотечение, наблюдаются признаки церебральной гиперперфузии и субоптимальной церебральной ауторегуляции. Таким образом, постнатальное продолжение повышенного CBF [46,47] в сочетании с потенциальной потерей церебральной ауторегуляции [18,65] и повышенной проницаемостью гематоэнцефалического барьера [41] может сделать мозг недоношенных IUGR особенно уязвимым для геморрагических инсультов.Фактически, модель ЗВУР овцы продемонстрировала сильно уменьшенное количество периваскулярных астроцитов и покрытие перицитами микрососудов в нескольких областях мозга, включая зародышевый матрикс [41]. Считается, что эти гистологические изменения приводят к снижению стабильности микрососудов головного мозга и связаны с ICH [41,76]. Более того, новорожденные с ЗВУР имеют более высокое кровяное давление по сравнению с их сверстниками из AGA [32,33,71], что теоретически еще больше увеличивает риск ВЧК.
Два недавних исследования продемонстрировали положительную связь между пренатальными признаками сохранения мозга и ICH [77,78].В своем большом проспективном исследовании 90 субъектов с ЗВУР Cruz-Martinez et al. [77] обнаружили, что у новорожденных с ЗВРП с патологическим пренатальным MCA-PI обнаруживается ICH значительно чаще, чем у их сверстников и контрольных групп, не сохраняющих мозг. В исследовании Ertan et al. [78], хотя данные пренатального допплера были доступны только для подгруппы новорожденных, MCA-RI оказался ниже в их группе ICH. Напротив, другие не смогли продемонстрировать связь между сохранением мозга и ICH. Хотя различия в гестационном возрасте могли искажать результаты нескольких исследований, посвященных этой теме [79, 80, 81], два исследования, в которых учитывался гестационный возраст, не обнаружили корреляции между сохранением мозга и ICH [82,83].Согласно этим исследованиям, сохранение мозга не увеличивает риск геморрагических поражений головного мозга. Одно исследование даже показало снижение риска ВЧК при снижении MCA-PI [84]. Некоторые авторы поэтому предположили, что адаптация к хронической внутриутробной гипоксии могла ускорить созревание ауторегуляторных механизмов, таким образом защищая от ICH [85].
Патология, лежащая в основе ICH, кажется сложной и многофакторной, но было высказано предположение, что ICH возникает после периода церебральной гипоперфузии с последующей реперфузией [86,87].Гипотетически повышенный сердечный выброс и сохранение мозга при ЗВУР могут предотвратить гипоперфузию головного мозга и защитить новорожденного ЗВУР от ICH. Однако, как обсуждалось ранее, «сохранение мозга» не может быть (полностью) защитным механизмом. Гемодинамическая нестабильность и ремоделирование сосудов могут возникать при длительном или тяжелом ЗВУР, что может представлять риск для хрупкого мозга недоношенных ЗВУР. Таким образом, противоречивые результаты исследований, упомянутых ранее, могут быть объяснены не только техническими различиями (различные определения, методы и сроки для выявления сохраняющего мозг и ICH) или сопутствующими факторами (срок беременности, влияние клинического ведения), но также могут зависеть от степени тяжести. ЗВУР и компромисс плода.
В заключение, текущая литература показывает противоречивые результаты и не может исключить негативные последствия сохранения мозга для хрупкой сосудистой сети головного мозга. Дальнейшее изучение этой темы имеет большое клиническое значение.
Церебральная оксигенация для руководства клиническим лечением
Хотя считается, что гипо- и гипертония вредны для головного мозга недоношенных, реальный диапазон артериального давления, обеспечивающий адекватную перфузию мозга, неизвестен [70]. Кроме того, абсолютные значения артериального давления могут не коррелировать с церебральной перфузией [88,89].Интересно, что оксигенация мозга лучше предсказывает исход развития нервной системы, чем наличие гипотензии, определяемой абсолютными значениями артериального давления [90]. Более того, колебания церебральной оксигенации и экстракции кислорода были связаны с возникновением ICH [75,87] . Поэтому было предложено рассматривать измерения церебральной перфузии, а не абсолютные значения артериального давления в качестве основы для ведения новорожденных [88,90]. Показатели церебральной оксигенации, полученные с помощью спектроскопии в ближнем инфракрасном диапазоне, были предложены в качестве полезного инструмента для рутинного клинического мониторинга [90].Поскольку новорожденные с IUGR демонстрируют иную церебральную гемодинамику, чем у сверстников AGA, они образуют отдельную группу в популяции недоношенных NICU. Им потребуется другой подход к интерпретации измерений оксигенации головного мозга и, возможно, потребуются собственные эталонные кривые.
Заключение
Хроническая внутриутробная гипоксия и внутриутробные гемодинамические нарушения вызывают структурные и функциональные изменения мозгового кровообращения. Эти внутриматочные адаптации, по-видимому, сохраняются в постнатальном периоде, и поэтому церебральное кровообращение новорожденных с ЗВУР отличается от их сверстников по AGA, по крайней мере, в первые несколько дней жизни.Однако литературы по этой теме крайне мало, а существующая литература показывает много противоречий. Таким образом, клинические последствия этой измененной церебральной гемодинамики плохо изучены. Таким образом, сложно предсказать, какие плоды подвергаются наибольшему риску неблагоприятных исходов, и в настоящее время у нас мало понимания относительно наиболее подходящих стратегий церебрального мониторинга и лечения для плодов ЗВУР и новорожденных. Международная инициатива, направленная на решение этих проблем, будет иметь большое значение для улучшения лечения, особенно для недоношенных популяций ЗВУР.
Благодарность
Эмили Коэн была предоставлена стипендия SIDS и Kids Australia.
Список литературы
- Spinillo A, Gardella B, Bariselli S, Alfei A, Silini EM, Bello BD: Цереброплацентарный допплер-коэффициент и гистопатологические особенности плаценты при беременности, осложненной задержкой роста плода.Журнал J Perinat Med 2014; 42: 321-328.
- Severi FM, Rizzo G, Bocchi C, D’Antona D, Verzuri MS, Arduini D: задержка внутриутробного развития и сердечная функция плода. Fetal Diag Ther 2000; 15: 8-19.
- Эрнандес-Андраде Э, Фигероа-Дизель Х, Янссон Т., Рангель-Нава Х, Гратакос Э: Изменения региональной перфузии мозгового кровотока плода в связи с ухудшением гемодинамики у плодов с серьезной задержкой роста.Ультразвуковой акушерский гинеколь 2008; 32: 71-76.
- Робсон С., Мартин В., Моррис Р. (ред.): Исследование и ведение плода малого для гестационного возраста, Руководство Green-Top № 312013. 2013. https://www.rcog.org.uk/en / руководящие принципы-исследования-услуги / руководящие принципы / gtg31 /.
- Cruz-Martinez R, Figueras F, Hernandez-Andrade E, Puerto B, Gratacos E: Продольные изменения перфузии головного мозга у плодов с недоношенными размерами для гестационного возраста, измеренные с помощью спектральных допплеровских индексов или фракционного объема движущейся крови.Am J Obstet Gynecol 2010; 203: 42.e1-6.
- Бенавидес-Серральде А, Шайер М., Крус-Мартинес Р., Криспи Ф, Фигерас Ф, Гратакос Э и др.: Изменения в центральном и периферическом кровообращении у плодов с задержкой внутриутробного развития на разных стадиях ухудшения кровотока в пупочной артерии: сердечный и др. параметры мозга.Gynecol Obstet Invest 2011; 71: 274-280.
- Фигероа-Дизель Х, Эрнандес-Андраде Э, Акоста-Рохас Р., Каберо Л., Гратакос Э: Допплеровские изменения в основных артериях головного мозга плода на разных этапах гемодинамической адаптации при серьезном ограничении внутриутробного развития. Ультразвуковой акушерский гинеколь 2007; 30: 297-302.
- Dubiel M, Gunnarsson GO, Gudmundsson S: Перераспределение крови в мозге плода во время хронической гипоксии. Ультразвуковой акушерский гинеколь 2002; 20: 117-121.
- Флад К., Унтершайдер Дж., Дейли С., Гири М. П., Кеннелли М. М., МакОлифф Ф. М. и др.: Роль сохранения мозга в прогнозировании неблагоприятных исходов при ограничении внутриутробного развития: результаты многоцентрового исследования PORTO.Am J Obstet Gynecol 2014; 211: 288.e1-e5.
- Бахадо-Сингх Р.О., Кованчи Э., Джеффрес А., Оз У., Дерен О., Копель Дж. И др.: Допплеровское цереброплацентарное соотношение и перинатальный исход при ограничении внутриутробного развития. Am J Obstet Gynecol 1999; 180: 750-756.
- Odibo AO, Riddick C, Pare E, Stamilio DM, Macones GA: Цереброплацентарный допплер-коэффициент и неблагоприятные перинатальные исходы при ограничении внутриутробного развития: оценка влияния использования эталонных значений, зависящих от гестационного возраста.J Ultrasound Med 2005; 24: 1223-1228.
- Gramellini D, Folli MC, Raboni S, Vadora E, Merialdi A: Церебрально-пупочный допплер-коэффициент как предиктор неблагоприятного перинатального исхода. Obstet Gynecol 1992; 79: 416-420.
- Хабек Д., Салихагик А., Югович Д., Герман Р.: Допплеровское церебро-пупочное соотношение и биофизический профиль плода в оценке перипартальной кардиотокографии у плодов с задержкой роста.Fetal Diagn Ther 2007; 22: 452-456.
- Хабек Д., Ходек Б., Герман Р., Югович Д., Церкез Хабек Дж., Салихагик А. Биофизический профиль плода и церебро-пупочное соотношение в оценке перинатального исхода у плодов с задержкой роста. Fetal Diagn Ther 2003; 18: 12-16.
- Мурата С., Наката М., Сумие М., Сугино Н.: Допплеровское цереброплацентарное соотношение предсказывает неутешительный статус плода у плодов с ограниченным внутриутробным развитием в срок.Журнал J Obstet Gynaecol Res 2011; 37: 1433-1437.
- Cruz-Martinez R, Figueras F, Hernandez-Andrade E, Oros D, Gratacos E: Допплер мозга плода для прогнозирования кесарева сечения для неутешительного состояния плода у доношенных плодов с малым для гестационного возраста плодом. Акушерский гинекол 2011; 117: 618-626.
- Konje JC, Bell SC, Taylor DJ: Аномальная допплеровская велосиметрия и объем кровотока в средней мозговой артерии при очень серьезном ограничении внутриутробного развития: не слишком ли поздно возникновение реверсирования компенсаторного потока? BJOG 2001; 108: 973-979.
- Fignon A, Salihagic A, Akoka S, Moraine C, Lansac J, Laurini R, et al: Двадцатидневный церебральный и пупочный допплеровский мониторинг у плода с задержкой роста и гипоксии. Eur J Obstet Gynecol Reprod Biol 1996; 66: 83-86.
- Вяс С., Николаидес К. Х., Бауэр С., Кэмпбелл С.: Формы волны скорости кровотока в средней мозговой артерии при гипоксемии плода.Br J Obstet Gynaecol 1990; 97: 797-803.
- Лаурини Р.Н.: Патология головного мозга плода и УЗИ; in Червенак Ф.А., Курджак А., Комсток Ч. (ред.): Ультразвук и мозг плода (серия «Прогресс в акушерской и гинекологической сонографии»). Нью-Йорк, Издательство Парфенон, 1995, стр. 27-42.
- Лаурини Р.Н., Арбей Б. Гипоксически-ишемическое повреждение головного мозга у плода человека; in Arbeille P, Maulik D (ред.): Гипоксия плода (серия «Прогресс в акушерской и гинекологической сонографии»). Нью-Йорк, Издательство Парфенон, 1999, стр. 1-14.
- Фигероа-Дизель Х, Эрнандес-Андраде Э, Бенавидес-Серральде А, Криспи Ф, Акоста-Рохас Р., Каберо Л. и др.: Церебральный венозный кровоток у плодов с ограниченным ростом и аномальным кровотоком в пупочной артерии до 32 недель беременности. беременность.Eur J Obstet Gynecol Reprod Biol 2008; 140: 201-205.
- Dubiel M, Breborowicz GH, Laurini R, Gudmundsson S: Скорость кровотока в вене плода Галена и исход беременности с высоким риском. Eur J Obstet Gynecol Reprod Biol 2001; 99: 14-18.
- Башат А.А., Хечер К. Ограничение роста плода из-за болезни плаценты.Семин Перинатол 2004; 28: 67-80.
- Додсон Р.Б., Розанс П.Дж., Петраш С.К., Хантер К.С., Фергюсон В.Л .: Грудная и брюшная аорты становятся жесткими из-за уникальных изменений внеклеточного матрикса у плода овцы с ограничением внутриутробного роста. Am J Physiol Heart Circ Physiol 2014; 306: h529-h537.
- Томпсон Дж. А., Ричардсон Б. С., Ганьон Р., Регно Т. Р.: Хроническая внутриутробная гипоксия препятствует развитию аорты у плода овцы на поздних сроках беременности. J. Physiol 2011; 589: 3319-3332.
- Акира М., Йошиюки С.: Плацентарное кровообращение, рост плода и жесткость брюшной аорты у новорожденных.Журнал Педиатр 2006; 148: 49-53.
- Cosmi E, Visentin S, Fanelli T, Mautone AJ, Zanardo V: Толщина средней интимы аорты у плодов и детей с задержкой внутриутробного развития. Акушер Гинеколь 2009; 114: 1109-1114.
- Cruz-Lemini M, Crispi F, Valenzuela-Alcaraz B, Figueras F, Gomez O, Sitges M, et al: Оценка сердечно-сосудистой системы плода для прогнозирования гипертонии у младенцев и ремоделирования артерий при задержке внутриутробного развития.Am J Obstet Gynecol 2014; 210: 552.e1-e22.
- Коклу Э., Куртоглу С., Акчакус М., Коклу С., Буюккайхан Д., Гумус Х и др.: Увеличение толщины интимы-медиа аорты связано с липидным профилем у новорожденных с ограничением внутриутробного развития. Horm Res 2006; 65: 269-275.
- Koklu E, Ozturk MA, Kurtoglu S, Akcakus M, Yikilmaz A, Gunes T: Толщина интимы-медиа аорты, уровни IGF-I, IGFBP-3 и лептина в сыворотке у новорожденных здоровых матерей с ограниченным внутриутробным развитием.Педиатр Res 2007; 62: 704-709.
- Сегал А., Доктор Т, Менахем С.: Функция сердца и биофизические свойства артерий у маленьких детей гестационного возраста: послеродовые проявления программирования плода. Журнал Педиатр 2013; 163: 1296-1300.
- Сегал А., Доктор Т., Менахем С.: Функция сердца и артериальные показатели у младенцев, рожденных маленькими для гестационного возраста: анализ путем отслеживания спеклов.Acta Paediatr 2014; 103: e49-e54.
- Скилтон М.Р., Эванс Н., Гриффитс К.А., Хармер Дж. А., Целермайер Д.С.: Толщина стенки аорты у новорожденных с ограничением внутриутробного развития. Ланцет 2005; 365: 1484-1486.
- Langille BL: Артериальное ремоделирование: отношение к гемодинамике.Can J. Physiol Pharmacol 1996; 74: 834-841.
- Мартин С.Н., Баркер Д.Д., Осмонд К.: Размер таза матери, рост плода и смерть от инсульта и ишемической болезни сердца у мужчин в Великобритании. Ланцет 1996; 348: 1264-1268.
- Law CM, Shiell AW: Артериальное давление обратно связано с массой тела при рождении? Сила доказательств систематического обзора литературы.J. Hypertens 1996; 14: 935-941.
- Годфри К.М., Баркер DJ: Программирование плода и здоровье взрослых. Общественное здравоохранение Nutr 2001; 4: 611-624.
- Лонго Л.Д., Пирс В.Дж.: Цереброваскулярная акклиматизационная реакция плода на долгосрочную гипоксию на большой высоте: модель пренатального программирования взрослых болезней? Am J Physiol Regul Integr Comp Physiol 2005; 288: R16-R24.
- Пирс В. Гипоксическая регуляция мозгового кровообращения плода. J Appl Physiol 2006; 100: 731-738.
- Кастильо-Мелендес М., Явно Т., Эллисон Б.Дж., Дженкин Г., Уоллес Е.М., Миллер С.Л.: Цереброваскулярная адаптация к хронической гипоксии у ягненка с ограниченным ростом.Int J Dev Neurosci 2015, Epub в преддверии печати.
- Ардуини Д., Риццо Дж., Романини С., Манкузо С. Гемодинамический ответ плода на острую гипероксигенацию матери как предиктор дистресса плода при задержке внутриутробного развития. BMJ 1989; 298: 1561-1562.
- Nishimaki S, Shima Y, Yoda H, Kawakami T., Akamatsu H: Скорость кровотока в мозговых артериях и нисходящей аорте у маленьких для свиданий младенцев.Педиатр Радиол 1993; 23: 575-577.
- van Bel F, van de Bor M, Stijnen T, Ruys JH: Снижение цереброваскулярного сопротивления у маленьких для гестационного возраста младенцев. Eur J Obstet Gynecol Reprod Biol 1986; 23: 137-144.
- Лей Д., Марсал К.: Допплеровская велосиметрия в мозговых сосудах малых для гестационного возраста младенцев.Ранний Hum Dev 1992; 31: 171-180.
- Баензигер О., Джагги Дж.Л., Мюллер А.С., Моралес К.Г., Липп HP, Липп А.Е. и др.: Церебральный кровоток у недоношенных новорожденных, пострадавших от секса, механической вентиляции и внутриутробного развития. Pediatr Neurol 1994; 11: 319-324.
- Исии Х., Таками Т., Фудзиока Т., Мизукаки Н., Кондо А., Сунохара Д. и др.: Сравнение изменений церебральной и системной перфузии у младенцев подходящего и маленького для гестационного возраста возраста в течение первых трех дней после рождения.Brain Dev 2014; 36: 380-387.
- Clark JM, Skolnick BE, Gelfand R, Farber RE, Stierheim M, Stevens WC, et al: Связь церебрального кровотока 133Xe со скоростью артериального кровотока в среднем мозге у мужчин в состоянии покоя. J Cereb Blood Flow Metab 1996; 16: 1255-1262.
- Guajardo CD, Mandelbaum V, Linderkamp O: Сердечный выброс и скорость мозгового кровотока у маленьких детей гестационного возраста в течение первых 5 дней после рождения.Ранний Hum Dev 1994; 37: 187-193.
- Kempley ST, Gamsu HR, Vyas S, Nicolaides K: Влияние задержки внутриутробного развития на постнатальную скорость висцерального и церебрального кровотока. Arch Dis Child 1991; 66: 1115-1118.
- Basu S, Dewangan S, Barman S, Shukla RC, Kumar A: Постнатальные изменения скорости мозгового кровотока у доношенных новорожденных с ограниченным внутриутробным ростом.Paediatr Int Child Health 2014; 34: 189-193.
- Missaridis TX, Shung KK: Влияние гемодинамики, эластичности сосудистой стенки и гематокрита на мощность ультразвукового допплера: исследование in vitro. Ультразвук Med Biol 1999; 25: 549-559.
- Cruz-Martinez R, Figueras F, Oros D, Padilla N, Meler E, Hernandez-Andrade E, et al: Перфузия церебральной крови и нейроповеденческие функции у доношенных плодов с малым для гестационного возраста.Am J Obstet Gynecol 2009; 201: 474.e1-e7.
- Eixarch E, Meler E, Iraola A, Illa M, Crispi F, Hernandez-Andrade E, et al: Исходы нервного развития у 2-летних младенцев, которые были маленькими для гестационного возраста доношенными плодами с перераспределением мозгового кровотока. Ультразвуковой акушерский гинеколь 2008; 32: 894-899.
- Фигерас Ф, Крус-Мартинес Р., Санс-Кортес М., Арранс А., Илла М., Ботет Ф. и др.: Нейроповеденческие исходы у недоношенных детей с задержкой роста с пренатальными продвинутыми признаками сохранения мозга и без них. Ультразвуковой акушерский гинеколь 2011; 38: 288-294.
- Орос Д., Фигерас Ф., Крус-Мартинес Р., Падилья Н., Мелер Е., Эрнандес-Андраде Е. и др.: Допплерография средней и передней мозговых артерий для прогнозирования перинатального исхода и нейроповедения новорожденных у доношенных плодов с нормальной допплерографией пупочной артерии.Ультразвуковой акушерский гинеколь 2010; 35: 456-461.
- Роза С.Дж., Стигерс Э.А., Вербург Б.О., Джаддо В.В., Молл Х.А., Хофман А. и др.: Чего спасает эмбриональный мозг? Перераспределение кровообращения у плода и поведенческие проблемы в общей популяции. Am J Epidemiol 2008; 168: 1145-1152.
- Мюррей Э., Фернандес М., Фазель М., Кеннеди С.Х., Вильяр Дж., Стейн А.: Дифференциальный эффект ограничения внутриутробного развития на развитие нервной системы в детстве: систематический обзор. BJOG 2015; 122: 1062-1072.
- Шерджон С.А., Оостинг Х., Смолдерс-ДеХаас Х., Зондерван Х.А., Кок Дж.Х.: Исход нервного развития в возрасте трех лет после «сохранения мозга» плода.Early Hum Dev 1998; 52: 67-79.
- Scherjon SA, Smolders-DeHaas H, Kok JH, Zondervan HA: Эффект «сохранения мозга»: данные антенатального церебрального допплера в связи с неврологическим исходом у очень недоношенных детей. Ам Дж. Обстет Гинекол 1993; 169: 169-175.
- ван ден Брук AJ, Kok JH, Houtzager BA, Scherjon SA: Поведенческие проблемы в возрасте одиннадцати лет у недоношенных детей с или без сохранения мозга плода: проспективное когортное исследование.Early Hum Dev 2010; 86: 379-384.
- Фельдерхофф-Муэзер У., Биттигау П., Сифрингер М., Ярош Б., Коробович Э., Малер Л. и др.: Кислород вызывает гибель клеток в развивающемся мозге. Нейробиол Дис 2004; 17: 273-282.
- Герстнер Б., ДеСильва TM, Генц К., Армстронг А., Бремер Ф., Неве Р.Л. и др.: Гипероксия вызывает зависимую от созревания гибель клеток в развивающемся белом веществе.J. Neurosci 2008; 28: 1236-1245.
- Йис У, Курул С.Х., Кумрал А., Силакер С., Тугян К., Генч С. и др.: Гипероксическое воздействие приводит к гибели клеток в развивающемся мозге. Brain Dev 2008; 30: 556-562.
- Brew N, Walker D, Wong FY: Регуляция сосудов головного мозга и травмы головного мозга у недоношенных детей.Am J Physiol Regul Integr Comp Physiol 2014; 306: R773-R786.
- Грейзен Дж .: Ауторегуляция церебрального кровотока у новорожденных. Ранний Hum Dev 2005; 81: 423-428.
- Бауэр Р., Вальтер Б., Брандл У.: Ограничение внутриутробного развития улучшает церебральную утилизацию O 2 во время гиперкапнической гипоксии у новорожденных поросят.J. Physiol 2007; 584: 693-704.
- Бауэр Р., Вальтер Б., Волландт Р., Цвинер У.: Ограничение внутриутробного развития улучшает эффекты постепенной геморрагической гипотензии на региональный церебральный кровоток и потребление кислорода мозгом у новорожденных поросят. Педиатр Res 2004; 56: 639-646.
- Lemmers PM, Toet MC, van Bel F: Влияние открытого артериального протока и последующая терапия индометацином на церебральную оксигенацию у недоношенных детей.Педиатрия 2008; 121: 142-147.
- Шорт Б.Л., Ван Мерс К., Эванс-младший; Кардиологическая группа: Краткие выводы кардиологической группы по сердечно-сосудистой нестабильности у недоношенных детей. Педиатрия 2006; 117: S34-S39.
- Фузас С., Караца А.А., Давлурос П.А., Крисис Д., Алексопулос Д., Мантагос С. и др.: Дисфункция сердца новорожденных при ограничении внутриутробного развития.Педиатр Res 2014; 75: 651-657.
- Vitarelli A, Gheorghiade M: Диастолическая сердечная недостаточность: стандартный допплеровский подход и другие варианты. Am J Cardiol 1998; 81: 115G-121G.
- Rakza T, Magnenant E, Klosowski S, Tourneux P, Bachiri A, Storme L: Ранние гемодинамические последствия открытого артериального протока у недоношенных новорожденных с задержкой внутриутробного развития.J Pediatr 2007; 151: 624-628.
- Ибара С., Токунага М., Икеноу Т., Мурата Ю., Хирано Т., Асано Н. и др.: Гистологическое наблюдение артериального протока у недоношенных детей с задержкой внутриутробного развития. J. Perinatol 1994; 14: 411-416.
- Alderliesten T, Lemmers PM, Smarius JJ, van de Vosse RE, Baerts W, van Bel F: Церебральная оксигенация, экстракция и ауторегуляция у очень недоношенных детей, у которых развивается пери-внутрижелудочковое кровоизлияние.Журнал Педиатр 2013; 162: 698-704 e2.
- Ballabh P: Внутрижелудочковое кровоизлияние у недоношенных детей: механизм заболевания. Педиатр Res 2010; 67: 1-8.
- Cruz-Martinez R, Tenorio V, Padilla N, Crispi F, Figueras F, Gratacos E: Риск неонатальных аномалий УЗИ головного мозга при внутриутробном развитии ограниченных плодов, рожденных между 28 и 34 неделями: взаимосвязь с гестационным возрастом при рождении и допплером плода.Ультразвук Obstet Gynecol 2015, Epub опережает печать.
- Эртан А.К., Танриверди Х.А., Мейер М., Шмидт В. Факторы перинатального риска неонатального внутримозгового кровоизлияния у недоношенных детей. Eur J Obstet Gynecol Reprod Biol 2006; 127: 29-34.
- Марсуси В., Бахадори Ф., Исфахани Ф., Гасеми-Рад М.: Роль допплеровских индексов в прогнозировании внутрижелудочкового кровоизлияния и перинатальной смертности при задержке роста плода.Med Ultrason 2012; 14: 125-132.
- Мауну Дж., Экхольм Э., Парккола Р., Пало П., Рикалайнен Х., Лапинлейму Х. и др.: Антенатальные доплеровские измерения и раннее повреждение головного мозга у младенцев с очень низкой массой тела при рождении. Журнал Педиатр 2007; 150: 51-56.e1.
- Scherjon SA, Oosting H, Kok JH, Zondervan HA: Влияние сохранения мозга плода на раннее неонатальное мозговое кровообращение.Arch Dis Child Fetal Neonatal Ed 1994; 71: F11-F15.
- Башат А.А., Гембрух У., Вискарди Р.М., Гортнер Л., Харман ЧР: Антенатальное прогнозирование внутрижелудочкового кровоизлияния при задержке роста плода: какова роль допплера? Ультразвуковой акушерский гинеколь 2002; 19: 334-339.
- Стерн Г., Шилдс Л.Е., Дубинский Т.Дж.: Аномальные церебральные и пупочные измерения плода с допплерометрией у плодов с задержкой внутриутробного развития позволяют прогнозировать тяжесть перинатальной заболеваемости.J Clin Ultrasound 2001; 29: 146-151.
- Мари Г., Абухамад А.З., Келлер М., Верпайройкит Б., Мент Л., Копель Дж.А.: Является ли эффект сохранения мозга плода фактором риска развития внутрижелудочкового кровоизлияния у недоношенного ребенка? Ультразвуковой акушерский гинеколь 1996; 8: 329-332.
- Амато М., Конрад Д., Хуппи П., Донати Ф .: Влияние недоношенности и задержки внутриутробного развития на неонатальное геморрагическое и ишемическое повреждение головного мозга.Eur Neurol 1993; 33: 299-303.
- Noori S, Серия I: Гемодинамические предшественники пери / внутрижелудочкового кровоизлияния у очень недоношенных новорожденных. Semin Fetal Neonatal Med 2015, Epub впереди печати.
- Noori S, McCoy M, Anderson MP, Ramji F, Seri I: Изменения сердечной функции и мозгового кровотока в связи с пери / внутрижелудочковым кровоизлиянием у крайне недоношенных младенцев.Журнал Педиатр 2014; 164: 264-270.e1-e3.
- Bonestroo HJ, Lemmers PM, Baerts W, van Bel F: Влияние антигипотензивной терапии на церебральную оксигенацию недоношенных детей без КПК. Педиатрия 2011; 128: e1502-e1510.
- Kooi EM, van der Laan ME, Verhagen EA, Van Braeckel KN, Bos AF: Увеличение объема не влияет на экстракцию кислорода тканями головного мозга у недоношенных детей с клиническими признаками плохой перфузии.Неонатология 2013; 103: 308-314.
- Alderliesten T, Lemmers PM, van Haastert IC, de Vries LS, Bonestroo HJ, Baerts W. и др.: Гипотония у недоношенных новорожденных: низкое кровяное давление само по себе не влияет на исход нервного развития. Журнал Педиатр 2014; 164: 986-991.
Автор Контакты
Эмили Коэн, доктор медицины
Центр Ричи, Гудзоновский институт медицинских исследований
27-31 Райт-стрит
Клейтон, Виктория 3002 (Австралия)
Электронная почта [email protected]
Подробности статьи / публикации
Предварительный просмотр первой страницы
Получено: 22 марта 2015 г.
Принято: 7 июля 2015 г.
Опубликовано онлайн: 29 августа 2015 г.
Дата выпуска: ноябрь 2015 г.
Количество страниц для печати: 8
Количество рисунков: 0
Количество столов: 0
ISSN: 1661-7800 (печатный)
eISSN: 1661-7819 (онлайн)
Для дополнительной информации: https: // www.karger.com/NEO
Авторские права / Дозировка препарата / Заявление об ограничении ответственности
Авторские права: Все права защищены. Никакая часть данной публикации не может быть переведена на другие языки, воспроизведена или использована в любой форме и любыми средствами, электронными или механическими, включая фотокопирование, запись, микрокопирование или с помощью какой-либо системы хранения и поиска информации, без письменного разрешения издателя. .
Дозировка лекарств: авторы и издатель приложили все усилия, чтобы гарантировать, что выбор и дозировка лекарств, указанные в этом тексте, соответствуют текущим рекомендациям и практике на момент публикации.Тем не менее, ввиду продолжающихся исследований, изменений в правительственных постановлениях и постоянного потока информации, касающейся лекарственной терапии и реакций на них, читателю рекомендуется проверять листок-вкладыш для каждого препарата на предмет любых изменений показаний и дозировки, а также дополнительных предупреждений. и меры предосторожности. Это особенно важно, когда рекомендованным агентом является новое и / или редко применяемое лекарство.
Отказ от ответственности: утверждения, мнения и данные, содержащиеся в этой публикации, принадлежат исключительно отдельным авторам и соавторам, а не издателям и редакторам.Появление в публикации рекламы и / или ссылок на продукты не является гарантией, одобрением или одобрением рекламируемых продуктов или услуг или их эффективности, качества или безопасности. Издатель и редактор (-ы) не несут ответственности за любой ущерб, причиненный людям или имуществу в результате любых идей, методов, инструкций или продуктов, упомянутых в контенте или рекламе.
(PDF) Причины и механизмы внутриутробной гипоксии и ее влияние на сердечно-сосудистую систему плода: обзор
Международный педиатрический журнал 7
с сердечными заболеваниями, Циркуляция, том.105, нет. 18, pp. 2179–
2184, 2002.
[48] S.C.Siu, M.Sermer, J.M.Colmanetal., «Проспективное многоцентровое исследование исходов беременности
у женщин с сердечными заболеваниями
», Circulation, vol. 104, нет. 5, pp. 515–521, 2001.
[49] A. Hameed, IS Karaalp, PP Tummala et al., «Влияние
порока сердца на исход беременности
у матери и плода», Journal of Американский колледж кардиологии, т.
37, вып.3, pp. 893–899, 2001.
[50] П. Пресбитеро, Дж. Сомервилль, С. Стоун, Э. Арута, Д. Шпигельхал —
тер и Ф. Рабайоли, «Беременность при синюшном врожденном сердце.
Болезнь: исход матери и плода // Кровообращение, т. 89,
нет. 6, pp. 2673–2676, 1994.
[51] Дж. С. Селлман и Р. Л. Холман, «Тромбоэмболия во время беременности
: риски, проблемы и рекомендации», Пост-
Медицина, вып. 108, нет. 4. С. 71–84, 2000.
[52] «Технический бюллетень ACOG. Заболевания легких при беременности.
Номер 224 — июнь 1996 г. Американский колледж акушеров
и гинекологов », Международный журнал гинекологии и
акушерства, вып. 54, нет. 2, стр. 187–196, 1996.
[53] Р. Кумар, «Пренатальные факторы и развитие астмы»,
Current Opinion in Pediatrics, vol. 20, нет. 6, pp. 682–687,
2008.
[54] Э. С. Гай, А. Кирумаки, Н. А.Ханания, «Острая астма при беременности
–», Critical Care Clinics, vol. 20, нет. 4, стр. 731–745,
2004.
[55] Л. Д. Инге и Дж. У. Уилсон, «Последние сведения о лечении туберкулеза
», Американский семейный врач, том 78, № 4, стр.
457–470, 2008.
[56] С. М. Роу, С. Миллер, Э. Дж. Соршер, «Кистозный фиброз», Медицинский журнал Новой Англии
, вып. 352, нет. 19, pp. 1992–
2001, 2005.
[57] E.Y. Cheng, C.H.Госс, Э. Ф. МакКоун и др., «Агрессивный пренатальный уход
приводит к успешным исходам плода у женщин с МВ
», Journal of Cystic Fibrosis, vol. 5, вып. 2, pp. 85–91,
2006.
[58] I. degaard, B. Stray-Pedersen, K. Hallberg, OC Haanaes,
OT Storrøsten, и M. Johannesson, «Maternal and
» заболеваемость плода при беременностях в Норвегии и Швеции
женщин с кистозным фиброзом ”, Acta Obstetricia et Gynecologica
Scandinavica, vol.81, нет. 8, pp. 698–705, 2002.
[59] А. Розенберг, «IUGR новорожденный», Семинары по перинатолии. 32, нет. 3, pp. 219–224, 2008.
[60] CH Goss, GD Rubenfeld, K. Otto, и ML Aitken,
«Влияние беременности на выживаемость у женщин с кистозным фиброзом
», Chest, vol. . 124, вып. 4, стр. 1460–1468, 2003.
[61] Д.С. Хардин, Дж. Райс, Р.К. Коэн, К.Дж. Эллис и Дж. А.
Ник, «Метаболические эффекты беременности при кистозном фиброзе»,
Акушерство и гинекология, vol. .106, нет. 2, pp. 367–375, 2005.
[62] S. W. McColgin, L. Glee и B. A. Brian, «Легочное заболевание
приказов, осложняющих беременность», Акушерство и гинекология
Клиники Северной Америки, вып. 19, нет. 4, pp. 697–717, 1992.
[63] Дж. М. Шапиро, «Критическая помощь акушерскому пациенту», Journal
of Intensive Care Medicine, vol. 21, нет. 5, pp. 278–286, 2006.
[64] С. Махаджан, Р. Аалинкил, П. Шах, С. Сингх и Н. Кочупил —
лай, «Нутритивная анемия нарушает регуляцию эндокринного контроля
плодов. рост », British Journal of Nutrition, vol.100, нет. 2, pp.
408–417, 2008.
[65] PN Singla, M. Tyagi, A. Kumar, D. Dash, R. Shankar,
«Рост плода при материнской анемии», Journal of Tropical
Педиатрия, т. 43, нет. 2, pp. 89–92, 1997.
[66] П. Н. Бейкер, С. Дж. Уиллер, Т. А. Сандерс и др., «Проспективное исследование статуса микронутриентов при беременности у подростков
»,
American Journal of Clinical Nutrition, vol. .89, No 4, стр.
1114–1124, 2009.
[67] L.Х. Аллен, «Беременность и дефицит железа: нерешенные проблемы
», Nutrition Reviews, vol. 55, нет. 4, pp. 91–101, 1997.
[68] DJP Barker, AR Bull, C. Osmond, and SJ Simmonds,
«Размер плода и плаценты и риск гипертонии у взрослого
жизни», British Medical Journal , т. 301, нет. 6746, pp. 259–262,
1990.
[69] Т. Т. Лао и В. М. Вонг, «Плацентарное соотношение — его связь
с легкой материнской анемией», Плацента, том.18, No 7, стр.
593–596, 1997.
[70] Л.А. Уильямс, С.Ф. Эванс и Дж. П. Ньюнхэм, «Проспективное когортное исследование
факторов, влияющих на относительный вес плаценты
и новорожденного», British Medical Journal,
об. 314, нет. 7098, pp. 1864–1868, 1997.
[71] SC Davies, E. Cronin, M. Gill, P. Greengross, M. Hickman,
и C. Normand, «Скрининг на серповидно-клеточную анемию и т.
лассемия: систематический обзор с дополнительными исследованиями »,
Health Technology Assessment, vol.4, вып. 3, pp. 1–87, 2000.
[72] А. Г. Мотульски, «Частота серповидных расстройств у чернокожих в США
», Медицинский журнал Новой Англии, вып. 288, нет.
1, стр. 31–33, 1973 г.
[73] «Практический бюллетень ACOG №. 78: гемоглобинопатии при беременности
, Акушерство и гинекология, т. 109, нет. 1, pp.
229–238, 2007.
[74] П.М. Сан, У. Уилберн, Б.Д. Рейнор и Д. Джеймисон, «Серповидноклеточная болезнь
у беременных: двадцать лет опыта в Grady
Memorial. Больница, Атланта, Джорджия », Американский журнал
акушерства и гинекологии, вып.184, нет. 6, pp. 1127–1130,
2001.
[75] M.Koshy, L.Burd, D.Wallace, A.Moawad, J.Baron,
«Профилактические переливания эритроцитов беременным пациенткам с
серповидноклеточная анемия. Рандомизированное совместное исследование », The New
England Journal of Medicine, vol. 319, нет. 22, pp. 1447–1452,
1988.
[76] Х. Казазян-младший, «Синдромы талассемии: молекулярная основа
и пренатальная диагностика в 1990 году», Семинары по гематологии —
ogy, vol.27, нет. 3, pp. 209–228, 1990.
[77] A. Aessopos, F. Karabatsos, D. Farmakis et al., «Беременность у
пациенток с хорошо пролеченной β-талассемией: исход для моли —
. младенцев и новорожденных », Американский журнал акушерства и
гинекологии, вып. 180, нет. 2, часть 1, стр. 360–365, 1999.
[78] CE Jensen, SM Tuck и B. Wonke, «Фертильность при большой βtha-
лассемии: отчет о 16 беременностях, предварительная оценка
и обзор литературы », Британский журнал
акушерства и гинекологии, вып.102, вып. 8, pp. 625–629,
1995.
[79] Х. К. Онг, Дж. К. Уайт и Т. А. Синнатур, «Гемоглобин
Болезнь H и беременность у малазийской женщины», Acta
Haematologica, vol. 58, нет. 4, pp. 229–233, 1977.
[80] JERamsay, F.Stewart, IAGreer, and N..Sattar,
«Дисфункция микрососудов: связь между преэклампсией
и ишемической болезнью сердца у матери». BJOG, т. 110, нет. 11,
pp. 1029–1031, 2003.
[81] B.Дж. Уилсон, М. С. Уотсон, Дж. Дж. Прескотт и др., «Гипертоническая болезнь
беременных и риск гипертонии и инсульта в
последующих годах жизни: результаты когортного исследования», British Medical Journal,
vol. 326, нет. 7394, pp. 845–849, 2003.
[82] Л. Хауккамаа, М. Салминен, Х. Лайвуори, Х. Лейнонен,
В. Хиилесмаа и Р. Каая, «Риск для последующей коронарной
артерии. болезнь после преэклампсии », American Journal of Cardi-
ology, vol.93, нет. 6, pp. 805–808, 2004.
[83] Д. Дж. П. Баркер, «Рост в утробе матери и ишемическая болезнь сердца»,
Nutrition Reviews, vol. 54, нет. 2, pp. S1 – S7, 1996.
Гипоксия: ее краткосрочное и долгосрочное воздействие на развивающийся плод | SFEBES2008 | Общество эндокринологов BES 2008
Помимо традиционных рисков, таких как курение и ожирение, качество нашего пренатального развития играет роль в определении того, страдаем ли мы от болезней. В свою очередь, качество внутриутробной среды во многом определяется доступными питательными веществами и кислородом подрастающего поколения.Таким образом, связь между плохими условиями in utero и повышенным риском заболевания во взрослом возрасте привела к взрыву ряда исследований, изучающих влияние изменений в питании матери и плода на программирование болезни. В отличие от этих международных исследований, вклад гипоксии плода, которая может возникнуть во время преэклампсии или плацентарной недостаточности, в программирование развития сравнительно игнорируется. Кроме того, механизмы, лежащие в основе раннего программирования заболевания при осложненной беременности, остаются неизвестными, что не позволяет выявить потенциальные терапевтические цели для клинического вмешательства.Здесь мы выдвигаем гипотезу о том, что окислительный стресс у плода лежит в основе молекулярной основы, посредством которой пренатальная гипоксия изменяет рост плода и вносит вклад в программирование развития болезни. Наблюдения за беременностью человека на большой высоте и эксперименты на эмбрионах цыплят и крыс показывают, что гипоксия развития, независимая от изменений в питании матери, не только изменяет траекторию роста плода, но также вызывает изменения в сердечно-сосудистой, метаболической и эндокринной системах, которые в норме связанные с болезненными состояниями в более позднем возрасте.Лечение антиоксидантами беременных животных, осложненных снижением доставки кислорода к плоду, предотвращает изменения в росте плода, сердечно-сосудистую, метаболическую и эндокринную перестройку плода, а также повышенный окислительный стресс. В совокупности человеческие и экспериментальные данные подтверждают проверенную гипотезу, а работа предлагает как понимание механизмов, так и возможных терапевтических целей для клинического вмешательства против раннего происхождения заболевания при рискованной беременности.
Гипоксия-ишемия недоношенного плода вызывает гипертонию и двигательный дефицит у новорожденных кроликов: модель церебрального паралича человека?
Введение
Гипоксически-ишемическое повреждение головного мозга приводит к церебральному параличу (ДЦП), умственной отсталости или неспособности к обучению у выживших детей (Robertson and Finer, 1985).В настоящее время широко признано, что большинство случаев терминальной неонатальной энцефалопатии связано с гипоксически-ишемическим поражением головного мозга, которое происходит в утробе матери из различных состояний во время родов (Badawi et al., 1998). Гипоксия-ишемия (H-I) также связана с последующим повреждением головного мозга у непропорционально высокого процента выживших после преждевременных родов (Volpe, 2001). Заболеваемость ХП резко возрастает с уменьшением гестационного возраста при рождении, так что им подвержены 4-12% младенцев с массой тела при рождении <1000 г (Schmidt et al., 2001).
Ввиду большого вклада факторов риска во время родов и недоношенности в последующую неврологическую заболеваемость и смертность, необходимы исследования, направленные на изучение основных механизмов повреждения головного мозга, которое происходит внутриутробно в ЦНС незрелого и недоношенного плода. Отсутствие подходящей модели эмбриона на животных, которая воспроизводит моторный дефицит CP, затрудняет определение этих механизмов. В большинстве предыдущих исследований использовались модели церебральной гипоксии-ишемии у постнатальных животных.Обычно наблюдалась значительная смертность или животные полностью выздоравливали, а нейроповеденческий дефицит было трудно выявить (Wright and Rang, 1990).
Мы разработали модель глобальной гипоксии-ишемии у недоношенного плода кролика, подвергшегося ишемии матки, которая точно отражает острую плацентарную недостаточность у людей (Tan et al., 1999; Derrick et al., 2001). Как стойкая, так и периодическая гипоксия-ишемия плода привели к заметному увеличению продукции активных форм азота и кислорода в мозге плода, а антиоксидантная терапия снизила степень повреждения мозга (Tan et al., 1998; Tan et al., 1999; Tan et al., 2001). In vitro культура нервных клеток, диссоциированных из ишемизированного мозга плода, продемонстрировала увеличение как ранней некротической гибели клеток, так и замедленного апоптоза (Derrick et al., 2001).
В настоящем исследовании была использована новая батарея нейроповеденческих тестов для характеристики двигательной активности новорожденных щенков после устойчивой гипоксии-ишемии у недоношенного плода кролика при 67-70% гестации. Плодам давали возможность родиться спонтанно при доношенной беременности, а затем подвергали нейроповеденческой батарее перед гистологическим анализом повреждения ЦНС.Эта модель предлагает явные преимущества, заключающиеся в том, что, как и у новорожденного человека, у новорожденного кролика незрелая локомоторная функция и полушария головного мозга не полностью миелинизированы. Ишемия матки в матках привела к отчетливому нейроповеденческому фенотипу у новорожденных детенышей, который характеризовался повышением тонуса передних конечностей, что в значительной степени коррелировало с гистологическими доказательствами стойкого повреждения подкорковых моторных путей, вовлекающих базальные ганглии и передний таламус.Эти исследования представляют собой первую модель на животных, в которой предшествующее повреждение во время развития незрелой ЦНС приводит к совокупности гипертонических моторных дефицитов при доношенных родах, которые согласуются с наблюдаемыми при ХП.
Материалы и методы
Хирургия животных . In vivo глобальная гипоксия-ишемия плодов была вызвана ишемией матки у беременных новозеландских белых кроликов (Myrtle’s Rabbits, Thompson Station, Теннесси), как описано ранее (Tan et al., 1998; Деррик и др., 2001). Точный срок беременности обеспечивался наблюдением за спариванием кроликов и ограничением контакта самцов кроликов 5 минутами со стороны продавца. Вкратце, плотин анестезировали внутривенным введением фентанила (75 мкг / кг / час) и дроперидола (3,75 мг / кг / час), а также обеспечивали вентиляцию мешком и маской для поддержания нормального артериального pH (7,35-7,45), Pco 2 (32-45 торр) и Po 2 (70-100 торр). После этого самкам была проведена спинномозговая анестезия введением 0.75% бупивикаина через спинномозговую иглу 25G, введенную в межпозвонковое пространство L4-L5. Доза фентанила и дроперидола была снижена на 60%, чтобы плотина могла самостоятельно дышать через маску. Ишемию матки, которая привела к гипоксии плода, вызывали с помощью артериального катетера для эмболэктомии Fogarty 4 F (Baxter Health Care Corporation, Санта-Ана, Калифорния). Катетер вводили в левую бедренную артерию, продвигали на 10 см в нисходящую аорту выше матки и ниже почечных артерий, и баллон надували 300 мкл физиологического раствора.Артериальное давление правой нижней конечности контролировали с помощью Доплера (Mini Dopplex D500; Huntleigh Technology, Luton, UK), чтобы гарантировать продолжение ишемии. В конце процедуры баллон был спущен и катетер удален. Бедренная артерия ушита швами 7-0, кожа ушита швами 3-0. Мать вернули в клетку. Самкам либо была проведена гистеротомия через 24 часа на 23-й день беременности, либо им разрешили родить в гнездовом ящике в срок (31,5 дня). Все детеныши, найденные мертвыми в период новорожденности, были признаны перинатальными мертворожденными, поскольку их вес был аналогичен весу их живых однопометников.
Протокол гипоксии-ишемии. Недоношенные животные на 21–22 днях беременности [67–70% беременности; эмбриональный день (E) 21-E22] подверглась устойчивой ишемии матки в течение 30, 37, 38 или 40 минут. Это было сделано в попытке смоделировать нарушение плацентарной недостаточности недоношенным детям. Этот протокол у недоношенных кроликов приводит к глобальной гипоксии плода, которая сопровождается немедленной брадикардией плода (от 180 до 80 ударов в минуту) и немедленным падением микрососудистого кровотока к коре головного мозга, как было определено измерениями лазерного допплера (Perimed, Ярфалла, Швеция).Количество самок и детенышей в каждой группе показано в Таблице 1.
Таблица 1.Количество самок и детенышей в каждой группе
Поведенческое тестирование. После естественных родов, в послеродовой день (P) 1, четыре щенка из помета были случайным образом выбраны для поведенческого тестирования. Таким образом, поведенческое тестирование проводилось через 10 дней после гипоксического инсульта на E22 или через 11 дней после инсульта на E21. Если размер помета был меньше четырех живых детенышей, оценивали всех живых детенышей.Этот протокол был выбран, чтобы минимизировать влияние конкретных пометов на общий групповой эффект. Дизайн поведенческой батареи был основан на возможностях новорожденного щенка на P1. Например, в точке P1 детеныши проявляли спонтанное движение и поведенчески реагировали на тактильные и ядовитые раздражители, но не на свет или звук. Детенышей оценивали в их гнездовом ящике. Ректальную температуру регистрировали во время тестирования поведения в подгруппе животных, и не было значительных различий между контрольной группой и группой с 40-минутной ишемией матки (таблица 2).
Таблица 2.Физиологические переменные
Для каждого животного испытание записывалось на видео и оценивалось по шкале от 0 до 3 (0, худший; 3, лучший) двумя слепыми наблюдателями. Описание системы подсчета очков приведено в Таблице 3. Также предоставлены видеозаписи и видеоролики с результатами (доступны на сайте www.jneurosci.org). Передвижение на плоской поверхности оценивали по степени спонтанного движения головы, туловища и конечностей.Тонус оценивался по активному сгибанию и разгибанию передних и задних конечностей и оценивался (0-4) по шкале Ашворта (Damiano et al., 2002). Рефлекс выпрямления оценивали, когда детенышей кладут на спину. Сосание и глотание оценивали путем введения смеси (Similac с железом; Abbott Labs, Abbott Park, IL) в рот щенка с помощью пластиковой пипетки.
Таблица 3.Протокол нейроповеденческой оценки щенков кроликов на P1
Чтобы определить, проявляются ли у недоношенных животных неблагоприятные физиологические последствия, которые могут помешать нейроповеденческому тестированию, в подгруппе случайно выбранных щенков измеряли частоту сердечных сокращений с помощью доплеровского датчика 8 МГц (Mini Dopplex D500; Huntleigh Technology) в точке P1.После этого детенышей умерщвляли и собирали образцы смешанной венозной и артериальной крови. Определение газов артериальной крови проводилось вместе с натрием, калием и ионизированным кальцием на анализаторе серии ABL 700 (Radiometer Medical, Копенгаген, Дания). Уровень глюкозы в сыворотке определяли на приборе SureStepFlexx Meter (Lifescan, Milpitas, CA).
Гистологические исследования. После поведенческого тестирования детенышей P1 анестезировали однократной внутримышечной дозой комбинации кетамина (35-40 мг / кг), ацепромазина (0.75-1,0 мг / кг) и ксилазин (3-5 мг / кг), а затем убивали декапитацией. Мозг пяти контрольных животных и девяти экспериментальных животных фиксировали погружением на 24 часа при 4 ° C в 4% параформальдегид в 0,1 м фосфатном буфере, pH 7,4. Мозг систематически разрезали на коронковые блоки толщиной 2 мм с помощью резака ткани матрикса для получения однородных образцов аналогичных областей в каждом мозге. Альтернативные 2-миллиметровые блоки ткани были заделаны в парафин и нарезаны на срезы 8 мкм или срезы свободно плавающие на 50 мкм с помощью вибрирующего микротома.Области, отобранные для заделки парафина, включали от рострального до каудального среднесептальных ядер переднего мозга, вентрально-заднебокового ядра таламуса и вышележащего образования гиппокампа, лицевого двигательного ядра моста и вышележащего мозжечка, а также шейно-мозгового соединения. Свободно плавающие срезы были вырезаны из 2-миллиметрового блока ткани, который содержал головку хвостатого ядра и передние таламические ядра. Эти срезы окрашивали биотинилированным маркером микроглии-макрофагов Bandeiria griffonia изолектин B4 (1: 100; L2140; Sigma, St.Louis, MO) и визуализировали с помощью X-конъюгированного с родамином красного стрептавидина (1: 400; 016-290-084; Jackson ImmunoResearch, West Grove, PA).
Залитые парафином срезы ткани иммуногистохимически окрашивали в двух экземплярах на макрофаг и активированный маркер микроглии HAM 56. Срезы сначала обрабатывали для извлечения антигена путем погружения в 50 мМ трис-HCl, pH 10, на 25 минут и в паровой бане. нагревают до 100 ° C в рисоварке. Срезы охлаждали на воздухе помещения в течение 20 минут в этом растворе, а затем обрабатывали для иммунопероксидазной гистохимии следующим образом.Срезы обрабатывали 0,3% пероксидазой водорода в течение 5 мин, промывали в 50 мМ Трис-HCl, pH 7,4 и реагировали в течение ночи при 2-4 ° C с первичным антителом HAM 56 IgM (MO632; Dako, Carpinteria, CA), разведенным 1 : 200 в Трис-буфере, содержащем 1% БСА (Sigma). После этого срезы инкубировали с биотинилированным вторичным антителом против μ-цепи IgM мыши (1: 100; BA2020; Vector Laboratories, Burlingame, CA) с использованием набора пероксидазы Vectastain Elite ABC (PK6100; Vector Laboratories) и следуя инструкциям производитель.
Плотность и общую площадь микроглии, меченной HAM 56, определяли маскированно в светлом поле с помощью прямого микроскопа Leica (Nussloch, Германия) DMRX, оснащенного цифровой камерой CCD с охлаждением Orca-ER (C4742-95; Hamamatsu). , Сидзука, Япония), который был сопряжен с программным обеспечением для анализа изображений Open Lab 3.0.4 (пакет морфометрии; Improvision, Бостон, Массачусетс). Для каждой анализируемой области было получено одно оцифрованное изображение с помощью объектива с фазовым контрастом 20x (HC PL Fluotar; числовая температура 0.50, pH 2; Leica), в которых количество клеток, меченных НАМ 56, оказалось максимальным. Все изображения были получены с одинаковыми настройками экспозиции. Анализируемая область была подтверждена морфологией и распределением нейронов, визуализированных с помощью фазово-контрастной микроскопии. Для каждого оцифрованного изображения как количество, так и общая площадь микроглии, меченной HAM 56, были определены с помощью анализа пороговых значений плотности среза, в котором минимальная интенсивность пикселей была установлена на уровне 40 единиц пикселей.
Флуоресценция in situ обнаружение фрагментации ДНК через 24 часа после заражения. Гистеротомия была выполнена четырем маткам через 24 часа после 40-минутной ишемии матки, и плоды были доставлены. Мозг этих плодов E23 фиксировали на 24 часа путем погружения в ледяной 4% параформальдегид в 0,1 м фосфатном буфере перед хранением при 2-4 ° C в PBS. В общей сложности 18 гипоксических мозгов плода сравнивали с шестью контрольными мозгами из двух пометов контрольных животных E23. Свободно плавающие коронковые срезы всего мозга размером 50 мкм были последовательно сделаны в ледяном PBS на вибрирующем микротоме Leica VTS-1000 и проанализированы с интервалами 250 мкм.Срезы тканей были закреплены и высушены на воздухе на предметных стеклах. В предварительных исследованиях срезы тканей подвергали проницаемости в течение 5 минут в смеси 1: 1 этанол: уксусная кислота (-20 ° C) в течение 10 минут в Triton X-100 или в течение 5 минут при комнатной температуре в протеиназе K (20 мкг / мл в PBS). Обработка этанолом: уксусная кислота или Triton X-100 занижали степень опосредованного терминальной дезоксинуклеотидилтрансферазой биотинилированного мечения конца никеля UTP (TUNEL) по сравнению с обработкой протеиназой К, которая использовалась для анализа повреждений.Набор для обнаружения фрагментации ДНК ApopTag-fluorescein in situ (Intergen, Purchase, NY) использовали для визуализации ядер, меченных TUNEL, как сообщалось ранее (Back et al., 2001). Срезы тканей контрастировали Hoechst 33324.
Наше исследование было одобрено Комитетом по обзору животных Северо-западного научно-исследовательского института здравоохранения Эванстона. Все животные получали гуманный уход в соответствии с Принципами лабораторного ухода , сформулированными Национальным обществом медицинских исследований, и Руководством по уходу и использованию лабораторных животных Национального института здравоохранения, подготовленным Национальной академией наук.
Статистический анализ. Животных анализировали в четырех группах: контрольные неишемические животные ( n = 129), гипоксия в течение 30 минут на E22 ( n = 26), гипоксия в течение 37-40 минут на E22 ( n = 102), и гипоксия на 37-40 мин на E21 ( n = 61). Обе последние две группы были обозначены как ≥37 H-I. Порядковые баллы в этих группах были проанализированы с помощью теста Краскела-Уоллиса с post hoc знаковых сравнений Уилкоксона с поправкой α = 0.0224, ввиду множественных сравнений. Рефлекс выпрямления и кратчайшее расстояние между передними конечностями и лапами задних конечностей анализировали с помощью ANOVA со сравнением средних значений с помощью Student Newman Keuls post hoc . Другие переменные, включая вес, частоту сердечных сокращений, газы крови и группы электролитов, сравнивали с тестом с двумя образцами t . Количество и площадь микроглии анализировали с помощью сравнения ранговых знаков Уилкоксона. Связь активированной микроглии (клеток / мм 2 и площадь) с гипертонией (оценка по шкале Ашворта) анализировали с помощью точного критерия Фишера.Весь статистический анализ проводился с использованием SAS для Windows версии 8.2.
Результаты
Мы определили влияние устойчивой гипоксии продолжительностью 30-40 минут на плод 22-й гестации (E22). Как и ожидалось из исследований острой плацентарной недостаточности на людях (Saftlas et al., 1991), у гипоксических животных наблюдались мертворождения. Частота мертворождений увеличивалась с увеличением продолжительности устойчивой гипоксии свыше 30 минут (рис. 1 A ). Средний вес мертворожденных детенышей (контрольная группа) был на 21% ниже, чем живорожденных контрольных детенышей, и аналогичное снижение на 17% наблюдалось для гипоксической группы.Это говорит о том, что время внутриутробной смерти было одинаковым в обеих группах. Затем мы определили ответы выживших новорожденных на батарею нейроповеденческих тестов (таблица 3). Животные, подвергшиеся 30-минутной гипоксии, были неотличимы от контроля (рис. 1, 2, 3, 4). Однако нейроповеденческие изменения наблюдались у животных, подвергшихся длительной гипоксии ≥37 мин. Самым поразительным открытием было наличие явных изменений позы и тонуса у выживших P1 (рис. 1 B ).Эти щенки обычно имели согнутую позу конечностей в состоянии покоя (рис. 1 B , врезка) (дополнительная видеопленка; доступна на www.jneurosci.org). У животных, подвергшихся 40-минутной гипоксии, 37% рождений были мертворожденными, а 83% выживших детенышей были гипертоническими. Наблюдалось значительное увеличение показателя гипертонуса для двух групп животных, подвергшихся длительной гипоксии ≥37 мин на E22 и E21 (рис. 1 C ).
Рисунок 1.A , Частота мертворождений, отмеченная на P1 в контроле и после устойчивой гипоксии в течение 30, 37 или 40 минут на E22. Число на каждой полоске показывает количество щенков в каждой группе. B , Уровни гипертонуса на P1 контроля и после устойчивой гипоксии в течение 30, 37 или 40 минут на E22. Число на каждой полоске показывает количество щенков в каждой группе. На вставке показан щенок, подвергнутый 40 мин на E22, демонстрирующий ненормальную осанку (стрелки). C , Оценка гипертонуса передних и задних конечностей в контроле (C) и после устойчивой гипоксии в течение 30 минут на E22 (h40, E22), 37-40 минут на E22 (H ≥ 37, E22) или на E21 (H ≥ 37, E21).Данные показаны в виде прямоугольников и усов. Черные круги — Среднее; белые круги, 99-й процентиль; группы, достоверно различающиеся по критерию Краскала-Уоллиса. * p <0,0224; Знаковый ранговый тест Вилкоксона по сравнению с контролем.
Фигура 2.Тонус был оценен у подгруппы новорожденных детенышей в состоянии покоя и во время медленного или быстрого растяжения суставов передних конечностей и был основан на исследовании, предложенном Целевой группой по двигательным расстройствам у детей (Sanger et al., 2003). Показана оценка мышечного тонуса при сгибании над пунктирной линией и тонусе при разгибании под пунктирной линией, в состоянии покоя или при медленном (3 секунды) или быстром растяжении сустава. Пунктирная линия на ординате — нулевая точка с увеличением сопротивления дальше от пунктирной линии. На вставках показаны позы животных, для которых показаны данные тона. A , Тонус нормального контрольного щенка на сгибание и разгибание. Врезка показывает типичную позу контрольного животного. B — F , Различные типы нарушений тонуса, наблюдаемые у детенышей после 40 минут устойчивой гипоксии на E22.Стрелки на вставках показывают нарушения осанки.
Рисунок 3.Оценка двигательной активности производилась слепым методом у контрольных детенышей (абсцисса C) и после устойчивой гипоксии в течение 30 минут на E22 (h40 E22), 37-40 минут на E22 (H ≥ 37 E22) или E21 (H ≥ 37 E21). Баллы основывались на оценке качества, интенсивности и продолжительности движений головы ( A ), передних конечностей ( B ) и задних конечностей ( C ) (оценка см. В Таблице 3). D показывает способность щенка двигаться по прямой линии. E показывает количество пересечений перпендикулярной линии за 60 секунд при ходьбе вперед по прямой (см. Таблицу 3). F показывает способность двигаться по кругу. Данные показаны в виде прямоугольников и усов. Черные круги — Среднее; белые круги, 99-й процентиль. Группы существенно различаются по критерию Краскела-Уоллиса. * p <0,0224; Знаковый ранговый тест Вилкоксона по сравнению с контролем.
Рисунок 4.A , Оценка рефлекса выпрямления, оценивающая способность детенышей выпрямляться после того, как их поместили в контрольном положении лежа на спине (абсцисса C) и после устойчивой гипоксии в течение 30 минут на E22 (h40 E22), 37-40 минут на E22 d (H ≥ 37 E22) или при E21 (H ≥ 37 E21). Точно так же B показывает способность сосать и глотать. C показывает способность рефлекторно поворачивать голову в ответ на введение в рот пипетки.Данные показаны в виде прямоугольников и усов. Черные круги — Среднее; белые круги, 99-й процентиль. Группы существенно различаются по критерию Краскела-Уоллиса. * p <0,0224; Знаковый ранговый тест Вилкоксона по сравнению с контролем.
Устойчивая гипоксия при преждевременных родах приводит к гипертоническому двигательному дефициту на уровне P1
В подгруппе детенышей, родившихся после 40 мин гипоксии на ст. E22, мы определили типы нарушений тонуса передних конечностей (рис.2). Тонус оценивался в соответствии с недавними рекомендациями семинара Национального института здравоохранения по двигательным расстройствам у детей (Sanger et al., 2003) и оценивался в покое и во время медленного или быстрого растяжения сустава. В целом, животные в группе с гипоксией демонстрировали повышенный тонус передних конечностей в покое (фиг. 2 C — F ) по сравнению с контрольными животными (фиг. 2 A ). Эта находка обычно сопровождалась фиксированными непроизвольными позами передних конечностей в состоянии покоя (рис.2, врезки, изображения подопытных животных). При медленном или быстром растяжении сустава при сгибании или разгибании, как правило, не наблюдалось зависящего от скорости увеличения сопротивления мышц растяжению. У части животных действительно наблюдалось небольшое повышение тонуса при медленном сгибании конечности (рис. 2 B ). Большинство животных демонстрировали одинаковую степень сопротивления мышцы растяжению с медленной и быстрой скоростью (рис. 2 D — F ) при сгибании, разгибании или обоих. Другая подгруппа показала небольшое снижение тонуса при активном сгибании конечности (рис.2 C, D ).
Устойчивая гипоксия при преждевременных родах приводит к нарушению двигательной активности
Поскольку у большинства выживших после длительной преждевременной гипоксии наблюдались отклонения в тонусе, мы определили, привело ли это повреждение к нарушению двигательной активности. Когда мы сравнили легкую (30 минут) и тяжелую (≥37 минут) гипоксию с контрольной группой, мы обнаружили, что группы гипоксии ≥37 минут были значительно хуже по качеству, интенсивности и продолжительности контроля головы и конечностей.Рисунок 3, A — C , показывает значительно более низкие показатели двигательной активности в группах гипоксии ≥37 минут, которые были определены для контроля головы (рис. 3 A ), передних конечностей (рис. 3 B ). , и задние конечности (рис. 3 C ). Эти нарушения в локомоторном контроле были подтверждены баллами, в которых оценивалась спонтанная двигательная активность вперед (рис. 3 D ), количество прямых пересечений за 60 секунд (рис. 3 E ) и круговое движение (рис. 3 ). F ).Поскольку передние конечности обычно были сильнее задних, щенки с более легким поражением могли двигаться кругами, но не могли двигаться вперед в одном направлении. Наиболее сильно пострадавшие щенки не могли целенаправленно двигать головой или конечностями. Однако у тех щенков, которые могли ходить по прямой линии, кратчайшее расстояние между передними и задними лапами использовалось как мера способности задних конечностей идти в ногу с передними конечностями, и оно не отличалось между контрольной группой. и группы гипоксии (данные не показаны).
Двигательные рефлексы были нарушены в группах гипоксии длительностью ≥37 мин. Рефлекс выпрямления был значительно нарушен в группах с гипоксией (рис. 4 A ). Более низкие баллы для групп с тяжелой гипоксией отражают спектр нарушений. В положении лежа на спине щенки с легкой степенью поражения возвращались в положение лежа на более длительный период времени, тогда как животные с более тяжелым поражением могли только поворачиваться на бок или оставаться на спине. Когда мы подсчитали количество успешных поворотов в положение лежа за 10 попыток, в группе с гипоксией, ≥37 мин на E22, было значительно меньше поворотов (6 ± 1) по сравнению с другими группами (контроль, 9 ± 0; гипоксия, 30 мин. , 10 ± 0; гипоксия, ≥37 мин на ст. 21, 8 ± 1; среднее ± SEM).
Координация сосания и глотания также была значительно нарушена в группах с тяжелой гипоксией (рис. 4 B ). При пероральном кормлении молоком дефицит варьировался от некоторой носовой регургитации у животных с более легкой степенью поражения до неспособности удерживать жидкость во рту у животных с более тяжелым поражением. Мы также наблюдали, что во время кормления введение пластиковой пипетки в боковую часть рта контрольного животного вызывало начальную реакцию, при которой животное отворачивалось от пипетки.Интересно, что этот ответ был наиболее чувствительным дефицитом, который мы наблюдали, и он был значительно нарушен как в 30-минутной, так и в 37-минутной группах гипоксии (рис. 4 C ).
Оценка общего состояния здоровья пациентов группы P1, перенесших преждевременную ишемию матки
Мы провели несколько исследований, чтобы определить влияние предшествующей ишемии матки на общее состояние здоровья животных группы P1. Влияние ишемии матки на внутриутробный рост исследовали путем сравнения веса выживших в группе с наиболее тяжелым поражением, ≥37 мин на ст. E22, с контрольной группой.Разница в весе живых детенышей в группе гипоксии составила 6% по сравнению с контрольной, что было связано с тем фактом, что средний вес детенышей с гипертонией был на 14% меньше, чем у детенышей без гипертонии в группе гипоксии. Затем мы определили, существуют ли физиологические различия между контрольной и экспериментальной группами, которые могут повлиять на производительность во время поведенческого тестирования. Как показано в Таблице 2, не было значительных различий между группами по размеру помета или весу мертворожденных детенышей.У испытуемых животных основная температура тела, частота сердечных сокращений и показатели смешанной венозной крови, такие как pH, Pco 2 , Po 2 , избыток оснований, натрия, калия, ионизированного кальция и глюкозы, не различались между двумя группами. .
Устойчивая гипоксия при преждевременных родах приводит к отсроченному повреждению головного мозга при рождении
Затем мы определили, существует ли модель отсроченного повреждения ЦНС, которая могла бы объяснить двигательный дефицит у животных, которые выжили в течение 10 дней после гипоксического инсульта продолжительностью 40 минут на E22.Мы исследовали четыре различных уровня полушарий головного мозга P1 и ствола головного мозга у пяти контрольных животных и девяти животных с гипоксией (см. Материалы и методы). Первоначальный замаскированный анализ залитых гематоксилином и эозином парафиновых срезов от этих 14 животных показал небольшое различие между контрольной и гипоксической группами, за исключением отдельных популяций активированной микроглии. Визуализация активированной микроглии и фагоцитарных макрофагов с помощью иммуногистохимии с антителом HAM 56 подтвердила присутствие различных скоплений этих клеток в лучевой коронке, хвостатом скорлупе, вентральных ядрах таламуса, образовании гиппокампа (зубчатая извилина, CA1, CA3, парапубикулум и миндалевидная железа). области гиппокампа), полушарий мозжечка и червя.
На фиг. 5 показаны результаты слепого количественного анализа количества клеток, меченных HAM 56, у 14 животных (см. Материалы и методы). По обе стороны от трех областей мозга животных с гипоксией: хвостатая скорлупа (рис. 5 A ), вентральные таламические ядра (рис. 5 C, E, F ) и парасубикулум миндалевидно-гиппокампальной области (данные не показано), было такое же значительное повышение количества клеток, меченных НАМ 56. Мы также количественно оценили общую площадь клеток, меченных HAM 56, потому что мы пришли к выводу, что площадь сомов активированной микроглии может быть больше, чем площадь покоящейся микроглии, и, таким образом, может предоставить дополнительные средства для идентификации областей отсроченного повреждения.Результаты этого анализа продемонстрировали аналогичное значительное увеличение общей площади клеток, меченных НАМ 56, в трех вышеупомянутых областях экспериментальной группы по сравнению с контролем (данные не показаны). Мы не наблюдали скопления активированных микроглиев в субикулюме, ядрах черепных нервов, вентральных мостах, нижних оливковых ядрах или клетках передних рогов шейного отдела спинного мозга.
Рисунок 5.Слепой гистопатологический анализ показывает отсроченное повреждение хвостатой скорлупы и таламуса.Срезы ткани головного мозга, полученные в точке P1 от контроля (C) и выживших после 40-минутной гипоксии на E22 (H), окрашивали на антитело HAM 56. Автоматический подсчет клеток, меченных HAM 56, показан как плотность клеток (клеток / мм 2 ), и его проводили, как описано в разделе «Материалы и методы». Сторона 1 и Сторона 2 относятся к подсчетам, полученным для каждой половины мозга, где сторона была назначена случайным образом. A , Плотность клеток, меченных HAM 56, в хвостатой скорлупе. Данные показаны в виде прямоугольников и усов.Черные круги — Среднее; белые круги, 99-й процентиль. * p <0,05; Знаковый ранговый тест Вилкоксона по сравнению с контролем. B , Связь между количеством активированной микроглии и гипертонией показана для хвостатой скорлупы. Абсцисса — тон с отсечкой 2,5 для определения гипертонуса. Любая точка справа от вертикальной серой линии означает гипертонию. Ордината представляет плотность клеток. Граница 99-го процентиля для контрольной популяции изображена горизонтальной серой линией, и любая точка над этой линией представляет плотность клеток, которая выше, чем 99-й процентиль контролей.Связь 2 × 2, протестированная с помощью точного критерия Фишера, значима ( p <0,05). C , Плотность клеток, меченных HAM 56, в таламусе. Данные показаны в виде прямоугольников и усов. Черные круги — Среднее; белые круги, 99-й процентиль. * p <0,05; Знаковый ранговый тест Вилкоксона по сравнению с контролем. D аналогичен B и показывает связь между количеством активированных микроглии в вентральном таламусе и гипертонией, как описано в тексте.Абсцисса и ордината такие же, как у B . Связь 2 × 2, протестированная с помощью точного критерия Фишера, значима ( p <0,05). E и F показывают репрезентативные изображения из вентральных ядер таламуса животных из контрольной группы и группы гипоксии, соответственно. Стрелками обозначены коллекции клеток, меченных HAM 56. Масштабные линейки, E, F , 100 мкм.
Поскольку этот слепой гистопатологический анализ подтвердил тот факт, что базальные ганглии и таламус получили отложенное повреждение, мы дополнительно оценили степень повреждения этих областей с помощью дополнительного маркера покоящейся и активированной микроглии, изолектина B4.Многочисленные клетки, меченные изолектином B4, были визуализированы в головке хвостатого ядра, скорлупе, внутренней капсуле и в передних ядрах таламуса (данные не показаны). Эти клетки были гораздо более многочисленными и имели реактивный гипертрофический вид у животных из группы с гипоксией, в отличие от контрольных животных, у которых меченые клетки имели вид покоящейся микроглии.
Гипертонус в точке P1 коррелирует с повреждением двигательных путей
Затем мы спросили, связано ли увеличение количества меченных HAM 56 клеток в хвостатой скорлупе и вентральном таламусе в группе гипоксии в точке P1 с двигательными нарушениями, наблюдаемыми в нашей модели.Мы назначили пороги 99-го процентиля количества контрольных клеток и тона ≥2,5 в качестве верхних пределов нормальности и провели 2 × 2 сравнение количества клеток, меченных HAM 56 в областях с тоном. Гипертонус передних конечностей сильно коррелировал с аномальным (> 99-й процентиль количества контрольных клеток) увеличением количества клеток, меченных HAM 56, как в хвостатой скорлупе (рис. 5 B ), так и в таламусе (рис. 5 D ). . Точно так же гипертонус задних конечностей также сильно коррелировал с аномальным количеством клеток, меченных HAM 56 (данные не показаны).Интересно, что не было никакой корреляции между аномальным количеством клеток, меченных HAM 56 в парапубикулуме миндалевидного гиппокампа и гипертонусом ни передних, ни задних конечностей (данные не показаны). Аналогичный анализ с использованием 99-го процентиля общей площади контроля в сравнении с гипертонией также показал аналогичные результаты (данные не показаны).
Гипоксия-ишемия на ст. E22 порождает различные паттерны острого повреждения подкорковых моторных путей
Поскольку в переднем мозге выживших новорожденных были обнаружены признаки повреждения двигательных путей, мы затем определили, получили ли эти области острое повреждение у эмбриональных кроликов E22, подвергшихся 40-минутной гипоксии-ишемии.Чтобы визуализировать масштабы и распределение острой клеточной дегенерации, ядра, меченные TUNEL, были визуализированы у животных, которые выжили в течение 24 часов (см. Материалы и методы). На рисунке 6 схематически показано типичное распределение ядер, меченных TUNEL, на двух уровнях переднего мозга у этих эмбриональных кроликов E23. Вентральная часть переднего мозга всегда была более подвержена травмам, чем задняя часть переднего мозга. Дорсальные корковые структуры обычно имели дискретные очаговые поражения, тогда как повреждение вентральных корковых структур, таких как грушевидная кора, было более диффузным.В основном травма была локализована в основном в корковых и подкорковых структурах серого вещества. В отличие от животных, перенесших гипоксию-ишемию, у контрольных животных были редкие клетки, меченные TUNEL, в областях, показанных на рисунке 6. Этот результат согласуется с очень похожими данными по мозгу плода овцы (Falkowski et al., 2002), которые подтверждают концепция программируемой гибели клеток в этом периоде развития находится на низком уровне.
Рисунок 6.A, B , срезы Ниссля из плода кролика E23 (слева) и соответствующие графики (справа) распределения ядер, меченных TUNEL (красные точки), в коронарных срезах переднего мозга на уровне ядер перегородки ( A ) и на уровне гиппокампа ( B ).Аббревиатуры были получены в основном из классификационной схемы Paxinos et al. (1994). AHA, передняя область гипоталамуса; ATh, передняя ядерная группа таламуса; СА1, СА1 поле гиппокампа; CxP, кортикальная пластинка; CxS, кортикальная субпластина; Ct — хвостатое ядро; ct — хвостатый нейроэпителий; ДГ — зубчатая извилина; ЭК, внешняя капсула; фи, фимбрия свода; GP, globus pallidus; IC, внутренняя капсула; ICx, промежуточная корковая зона; LV, боковой желудочек; Пир, грушевидная кора; Пу, скорлупа; Spt, перегородка; spt, нейроэпителий перегородки; SubV, субвентрикулярная зона; 3V, третий желудочек.
Рисунок 7 A показывает типичное распределение ядер, меченных TUNEL, в кортикальной пластинке. Дегенерирующие ядра были в основном локализованы в мультифокальных корковых поражениях в глубокой корковой мантии и прилегающей корковой субпластине. Небольшие перивентрикулярные поражения локализуются в кортикальном нейроэпителии и субвентрикулярной зоне, но не затрагивают перивентрикулярное белое вещество. В вентральной части переднего мозга, на уровне ядер перегородки (рис.6 A ), повреждение локализуется преимущественно в грушевидной коре, обонятельном бугорке, хвостатом ядре, хвостатом нейроэпителии (рис.7 B ) и брюшной скорлупы (рис.7 C ). В переднем мозге, на уровне гиппокампа (рис. 6 B ), выраженное подкорковое повреждение, локализованное в хвостатом ядре, хвостатом нейроэпителии, скорлупе, бледном шаре (рис. 7 D ) и группе переднего таламического ядра (рис. 7 D ) Рис.7 E ). У некоторых животных также были небольшие дискретные поражения гиппокампа, которые затрагивали слой пирамидных клеток СА1 и СА3 (рис. 7 F ) или зубчатую извилину. Менее выраженное повреждение также редко наблюдалось в передней области гипоталамуса и в вентральном медиальном ядре гипоталамуса (данные не показаны).
Рисунок 7.Флуоресцентные микрофотографии показывают распределение ядер, меченных TUNEL, в основных структурах плода кролика E23, которые были повреждены после гипоксии-ишемии за 24 часа до этого на E22. Мечение TUNEL было незначительным в областях, показанных для контрольных плодов E23 (данные не показаны). A , В кортикальной мантии маркировка TUNEL была сконцентрирована глубоко в кортикальной пластинке (CxP) и прилегающем слое субпластинки (CxS) в дискретных мультифокальных поражениях.Обратите внимание, что промежуточный кортикальный слой (ICx), который дает начало лучистой короне, сохраняется. LV, боковой желудочек. B , Окрашивание TUNEL в вентральном хвостатом нейроэпителии (обозначенном стрелками), расположенном между внутренней капсулой (IC) и боковым желудочком (LV). Повышенное окрашивание TUNEL также наблюдается латеральнее внешней капсулы (внизу слева) в грушевидной коре. C , ТУНЕЛЬНОЕ окрашивание слизистой оболочки (Pu). Обратите внимание, что участки белого вещества внешней капсулы (EC) и внутренней капсулы (IC) в основном сохраняются. D , Окрашивание TUNEL увеличивалось в бледном глобусе; однако прилегающие участки белого вещества внутренней капсулы (IC) не были помечены. E , Обширное окрашивание TUNEL в передней ядерной группе таламуса. eml, внешняя мозговая пластинка; 3V, третий желудочек. F , Рассеянные ядра, меченные TUNEL, визуализировались в гиппокампе в слое пирамидных клеток в полях CA1 и CA3 (стрелки). Д.Г., Зубчатая извилина. Масштабные линейки: A, B, F , 100 мкм; C — E , 50 мкм.
Таким образом, гипоксически-ишемическое повреждение плода E22 не было диффузным, но отдельные области переднего мозга плода были стабильно более уязвимыми. Выраженное повреждение чаще всего наблюдалось в базальных ганглиях и переднем таламусе, в меньшей степени — в коре головного мозга и гиппокампе. Следовательно, чаще всего наблюдалось повреждение подкорковых двигательных путей.
Обсуждение
Это исследование демонстрирует, что in utero гипоксия-ишемия недоношенного плода кролика приводит к двигательным нарушениям у выживших новорожденных.Насколько нам известно, это первая модель антенатального гипоксически-ишемического повреждения развивающегося мозга, которое приводит к моторным фенотипам, совместимым с некоторыми моторными нарушениями, наблюдаемыми у детей с ХП. В частности, гипертония наблюдалась у выживших после гипоксии-ишемии на сроках 67-70% гестации. Это согласуется с данными людей, согласно которым у недоношенных детей с массой тела при рождении <1500 г вероятность развития ХП в ~ 100 раз выше, чем у доношенных детей с массой тела 3000-3500 г (Cummins et al., 1993). В нашей модели нарушения локомоции, рефлекторной двигательной активности и координации сосания и глотания наблюдались после гипоксии-ишемии в утробе матери , аналогично клиническим данным гипоксико-ишемической энцефалопатии у младенцев.
Преимущества новорожденного кролика модели
Перинатальный кролик имеет несколько явных преимуществ по сравнению с другими моделями гипоксически-ишемического повреждения головного мозга на животных. Кролики и люди являются перинатальными разработчиками мозга, в отличие от грызунов (постнатальный) и овец (пренатальный) (van Marthens et al., 1975). Что наиболее важно, новорожденные кролики демонстрируют большой набор спонтанной двигательной активности и рефлекторных реакций, которые воспроизводимо тестируются. Кроме того, новорожденные кролики отличаются большей силой передних конечностей по сравнению с задними.Перинатальная локомоция прогрессирует от способности двигаться по кругу к движению по прямой линии и к способности прыгать, поскольку, предположительно, задние конечности становятся сильнее. Прыжковая способность была значительно снижена в группах с гипоксией, и почти ни одно из животных из группы с гипоксией ≥37 минут не демонстрировало прыжкового поведения (данные не показаны).
Время травмы и факторы, зависящие от созревания
Развитие двигательных систем кроликов происходит быстрее, чем у человека.Например, у кроликов крупный моторный контроль развивается быстрее, чем у людей, и с помощью P3 происходит скоординированное движение задних конечностей с передними. Это может способствовать раннему появлению двигательных нарушений у кроликов, переживших гипоксию-ишемию.
Наши нейропатологические данные согласуются с появляющейся концепцией о том, что восприимчивость развивающегося мозга к травмам зависит от созревания и включает преимущественное повреждение или сохранение определенных популяций клеток.Внутри коры головного мозга мы наблюдали склонность очевидных субпластинчатых нейронов становиться TUNEL-положительными, что согласуется с недавними наблюдениями, что гипоксия-ишемия преимущественно нацеливается на эти нейроны перинатальных крыс (McQuillen et al., 2003). Субпластинчатые нейроны являются критическими для нормального развития коры и участвуют в патогенезе CP, связанного с преждевременным церебральным повреждением человека (Allendoerfer and Shatz, 1994; Volpe, 1996). У людей период высокого риска повреждения белого вещества головного мозга совпадает с периодом развития, когда в белом веществе преобладают предшественники поздних олигодендроцитов (Back et al., 2001). Интересно, что мы не наблюдали предрасположенности к TUNEL-положительным клеткам в белом веществе головного мозга на E23 после гипоксии-ишемии на E22. Одно из объяснений может заключаться в том, что поздние предшественники олигодендроцитов не являются основной популяцией в белом веществе кроликов до E24-E26 (S.A.B. и S.T., неопубликованные наблюдения). С другой стороны, гибель клеток в белом веществе может происходить из-за замедленного апоптоза, как ранее наблюдалось в сером веществе (Northington et al., 2001a).
Гипоксия-ишемия недоношенного плода нацелена на подкорковые моторные пути
После гипоксии-ишемии на E22 плодные кролики получили стойкие острые повреждения базальных ганглиев и переднего таламуса, которые являются основными компонентами подкорковых моторных путей.При рождении поведенческие аномалии у недоношенных выживших также коррелировали с задержкой повышения активированной микроглии в базальных ганглиях и таламусе. Эти области особенно подвержены гипоксически-ишемическому повреждению как у недоношенных, так и у доношенных детей (Schneider et al., 1975; Rutherford et al., 1994; Okumura et al., 1997). Таламус и базальные ганглии особенно подвержены гипоксически-ишемическому повреждению, что наблюдается у постнатальных крыс с перевязкой сонных артерий и гипоксией (Northington et al., 2001b), у доношенных плодных обезьян (Myers, 1975) и у недоношенных и недоношенных плодов овец, подвергшихся глобальной церебральной гипоперфузии (Reddy et al., 1998).
Характер гипертонического двигательного дефицита
Кролики, пережившие гипоксию-ишемию, обычно демонстрировали гипертонус, который проявлялся как при сгибании, так и при разгибании. Наблюдаемый гипертонический дефицит соответствовал выраженной локализации повреждения базальных ганглиев и таламуса (см. Обзор Volpe, 2001).Наше исследование не предназначалось для различения подтипов гипертонии, учитывая отсутствие общепринятых диагностических протоколов у детей (Sanger et al., 2003). В состоянии покоя у большинства животных наблюдался повышенный тонус сгибателей и сгибательные позы, которые клинически напоминали гипертонические контрактуры, связанные со спастичностью. Однако у некоторых животных наблюдалась гипертония без выраженного сопротивления, зависящего от скорости, на сгибание или разгибание конечностей, что является признаком спастической гипертонии.Сопротивление внешнему движению суставов было одинаковым при низкой и высокой скорости у некоторых животных, что является признаком дистонической гипертонии (Sanger et al., 2003). У детей смешанная гипертония чаще встречается, чем чистая спастическая гипертония или чистая дистония (Sanger et al., 2003).
При церебральном параличе у человека гипертония и контрактуры развиваются от месяцев до лет после перинатального инсульта (Back, 1999). Поскольку гипоксические детеныши не могли питаться и выжить после рождения, было невозможно проследить эволюцию двигательных аномалий и невропатологии.Это может быть осуществимо в будущих исследованиях с разработкой долгосрочной поддержки интенсивной терапии, требующей вентиляции (Bernard et al., 2003) и парентерального питания (Loff et al., 1998). У перинатальных грызунов, перенесших гипоксически-ишемическое повреждение головного мозга, нейрональная дегенерация достигает пика в течение первых 24-72 часов в коре, базальных ганглиях и таламусе (Northington et al., 2001a; Han et al., 2002; McQuillen et al., 2003). ).
Гипоксия-ишемия недоношенного плода нарушает сложные двигательные рефлексы
Новорожденные, пережившие гипоксию-ишемию, демонстрировали значительные нарушения координации сосания и глотания.Многие щенки также демонстрировали аномальные реакции на оральную двигательную стимуляцию. Наши невропатологические исследования подтверждают, что оромоторная дисфункция была связана с надъядерным повреждением, поскольку мы не наблюдали ни острого, ни отсроченного повреждения ядер ствола мозга при окрашивании по TUNEL (данные не показаны). Более подробное исследование необходимо для изучения основы такого сложного поведения, которое может быть суммарной реакцией многих рефлексов (Drewett et al., 1982; Keil et al., 1990; Kindermann et al., 1994). Мы также наблюдали дефицит аверсивного поворота головы в ответ на ядовитые обонятельные стимулы, такие как перечная мята или алкоголь (данные не показаны), у P1, переживших гипоксию-ишемию.Необходимы дальнейшие исследования, чтобы выяснить, связано ли нарушение обонятельных реакций с нарушениями моторной интеграции, сенсорной интеграции или того и другого. Интересно, что через 24 часа после гипоксии-ишемии на ст. E22 мы наблюдали обширную острую клеточную дегенерацию в грушевидной коре головного мозга, которая является основной областью, которая интегрирует и передает обонятельную информацию от обонятельной луковицы (Wilson, 2001)
Поведенческие нарушения в других моделях перинатальной гипоксии-ишемии
Предыдущие исследования не создали модели на животных, воспроизводящей двигательные аномалии, характерные для ХП.Перинатальные грызуны, новорожденные поросята, овцы и обезьяны с недоношенным плодом очень восприимчивы к гипоксии-ишемии; однако отчетливый фенотип CP не определен (Raju, 1992; Back, 2001).
Однако отложенные поведенческие аномалии наблюдались во многих моделях (Nyakas et al., 1996). Антенатальная гипоксия у 77% беременных крыс привела к увеличению двигательной активности на P13-P15, дефициту в приобретении пассивного избегания и увеличению латентности бегства при плавании на P28 (Cai et al., 1999). Интересно, что антенатальная гипоксия у крыс не приводит к гистопатологическим отклонениям (Cai et al., 1999).
Постнатальные крысы легко переносят большие гипоксически-ишемические гистопатологические поражения, но не проявляют гипертонуса (Liu et al., 2001). Гипоксия-ишемия в точке P7 у крыс приводит к когнитивным нарушениям в виде кратковременного удержания и задержки бегства при плавании через 6 недель (Liu et al., 2001). Прерывистая гипоксия между 10-30 днями привела к аналогичным нарушениям пространственного обучения при тестировании в водном лабиринте Морриса через 30 дней (Row et al., 2002). Гипоксия-ишемия у двухдневных крыс приводила к двигательному дефициту при тестировании стержней, балок и ступенек через 3 месяца (McQuillen et al., 2003).
Мертворождения и гипоксия-ишемия
При острой плацентарной недостаточности, такой как отслойка плаценты, беременные женщины в 11 раз более склонны к мертворождению (Saftlas et al., 1991). Перинатальная аноксия была основной причиной мертворождений и ранних неонатальных смертей (Gunn and Cable, 1984). Настоящее исследование подтверждает корреляцию между временем инсульта и частотой мертворождений (рис.1 А ). Таким образом, степень нейроповеденческих аномалий, о которых сообщалось в нашем исследовании, на самом деле может быть недооценена, поскольку наиболее пострадавшие животные, вероятно, погибли. В соответствии с этой возможностью, у некоторых из наших мертворожденных были тонические позы, похожие на позы выживших (не контрактуры, потому что конечности можно было пассивно разгибать). Энергичная реанимация неожиданных мертворождений у людей показала, что большинство выживших имеют длительную инвалидность (Casalaz et al., 1998).
Клиническая значимость
Таким образом, мы создали модель антенатальной гипоксии при преждевременной беременности, которая привела к перинатальной смерти и фенотипу у выживших, который напоминает ранние проявления ХП.Эта модель согласуется с формирующейся клинической концепцией, согласно которой антенатальные факторы патогенетически связаны с последующим развитием ХП у многих пациентов. Таким образом, наша модель обеспечивает важную поведенческую конечную точку, которая до сих пор была недоступна для изучения. Необходимы дальнейшие исследования, чтобы определить клеточные и молекулярные механизмы, предшествующие ХП, и оценить, можно ли уменьшить этот дефицит с помощью терапевтических вмешательств.
Плацентарная недостаточность Статья
.Непрерывное образование
Плацентарная недостаточность — это состояние, при котором происходит сбой в ремоделировании сосудов плаценты, что приводит к сбою плаценты, что приводит к ацидозу и гипоксемии плода.Наиболее частыми последствием этого состояния для плода являются задержка внутриутробного развития, недоношенность или, к сожалению, гибель плода. Чтобы снизить риск заболеваемости и смертности плода, особенно при беременностях с высоким риском, необходимо проводить регулярный пренатальный скрининг с помощью ультразвуковой допплерографии, чтобы повысить шансы обнаружения и диагностики. В этом упражнении рассматривается патофизиология, оценка и возможные методы лечения плацентарной недостаточности, а также подчеркивается роль межпрофессиональной группы в ведении пациентов с этим заболеванием.
Целей:
- Рассмотрите факторы риска, связанные с плацентарной недостаточностью.
- Опишите типичные результаты ультразвуковой допплерографии, связанные с плацентарной недостаточностью.
- Определите наиболее частые нежелательные явления, связанные с плацентарной недостаточностью.
Введение
Плацентарная недостаточность связана с различными акушерскими расстройствами, такими как преэклампсия и задержка внутриутробного развития, которые предрасполагают к преждевременным родам, что является основной причиной перинатальной заболеваемости и смертности во всем мире.Плохая функция плаценты чаще всего описывается термином «плацентарная недостаточность» в медицинском сообществе; однако одно исследование выявило проблему отсутствия стандартизированного определения или единого мнения относительно патогномоничных признаков, относящихся к плацентарной недостаточности [1].
Это создает много проблем, когда дело доходит до изучения плацентарной недостаточности в литературе, но общее понимание состоит в том, что плацентарная недостаточность — это процесс, при котором происходит прогрессирующее ухудшение функционирования плаценты, так что перенос кислорода и питательных веществ к плоду через плаценту затруднен. уменьшилась, что привело к декомпенсированной гипоксии и ацидозу.[2] [3] Этот процесс приводит к гипоксемии плода, которая затем стимулирует снижение метаболических требований плода для сохранения уже доступных питательных веществ, что приводит к задержке внутриутробного роста плода. С гистопатологической точки зрения плацентарная недостаточность может быть определена при фиброзе ворсинок хориона, маточно-плацентарном тромбозе, инфаркте плаценты, отложениях фибрина или уменьшении количества и площади поверхности ворсинок капилляров [4].
Следует отметить, что инфаркты плаценты могут быть нормальным явлением, поскольку они наблюдаются примерно в 25% нормальных доношенных беременностей; однако было показано, что учащение инфаркта плаценты связано с плацентарной недостаточностью и, следовательно, с задержкой внутриутробного развития (ЗВУР).И МРТ, и ультразвуковые исследования, направленные на выявление плацентарной недостаточности, продемонстрировали уменьшение площади и объема плаценты, а также увеличение ее толщины в дополнение к плаценте шаровидной формы на МРТ [5].
Этиология
На сегодняшний день основные этиологии, которые могут привести к плацентарной недостаточности, плохо изучены и все еще изучаются. Известны связанные факторы риска для матери, которые включают преэклампсию или другие гипертонические расстройства у матери, употребление сигарет матерью, употребление наркотиков матерью, включая кокаин или героин, потребление алкоголя матерью, первородство, пожилой возраст матери и предшествующие роды новорожденных с ЗВРП.[2] [6]
Исследования, анализирующие формы волны Доплера в различных сосудах плаценты у матерей, которые курили сигареты во время беременности, продемонстрировали снижение формы волны скорости кровотока, что указывает на то, что воздействие никотина может привести к изменению сосудистой сети плаценты. [6]
Любое заболевание матери, которое может привести к нарушению кровообращения плода, подвергает плод риску плацентарной недостаточности. Кроме того, некоторые лекарства, такие как противоопухолевые, противосудорожные или антикоагулянты, могут мешать росту плода.Экстремальные значения индекса массы тела матери, включая недоедание матери, также были связаны с развитием ЗВУР новорожденных [7]. Исследования осложненных беременностей с ЗВУР показали, что имела место неполная трансформация сосудистой сети плаценты на ранних сроках беременности, что может быть обнаружено с помощью ультразвуковых допплеровских исследований. [5] [8]
Эпидемиология
Недоношенность — основная причина перинатальной смерти, за которой следует задержка внутриутробного развития плода, что осложняет примерно от 4% до 6% известных беременностей.Плацентарная недостаточность — потенциальная причина преждевременных родов, преэклампсии, ЗВУР и мертворождений, которые могут возникать в 10-15% беременностей. Для плода с ЗВУР риск самопроизвольных преждевременных родов в три раза выше по сравнению с плодом без задержки роста, а также в пять-шесть раз выше риск развития перинатальной смерти [2]. К сожалению, около 50% новорожденных с ЗВУР выявляются только после родов.
Патофизиология
Хотя основная этиология плацентарной недостаточности неизвестна, существуют предложенные механизмы.Плацентарная недостаточность связана со снижением кровотока через пупок к плоду, что может быть вторичным по отношению к увеличению сопротивления сосудов пуповины и плаценты. Это повышенное сопротивление может быть визуализировано как аномальные формы волны допплеровского кровотока в пупочной артерии и может быть вторичным по отношению к аномалии внедрения ворсинок в плацентарную мембрану, нарушению перфузии между пупком и плацентой или снижению маточно-плацентарного кровотока [2]. Исследования допплерографии пупочной артерии показали, что степень повреждения плаценты напрямую связана со степенью повреждения плода во время беременности.[9]
Основная роль плаценты — служить связующим звеном между кровообращением плода и матери. Для этого необходимо установить прилегание плаценты и ремоделирование маточной артерии, чтобы обеспечить доставку питательных веществ к растущему плоду. Отличительным признаком успешной плацентации является ремоделирование маточных артерий. После оплодотворения образуется бластоциста, которая состоит из внутренней клеточной массы, которая в конечном итоге станет плодом, и внешней оболочки, называемой трофобластом, которая становится эмбриональной частью плаценты.Чтобы способствовать прикреплению плаценты, цитотрофобласт, который является внутренним слоем трофобласта, секретирует матриксные металлопротеиназы, которые разрушают блестящую оболочку, и прилипание облегчается за счет образования закрепляющих ворсинок и экспрессии молекул адгезии. [10] Это вторжение в маточно-плацентарные артерии позволяет преобразоваться в расширенные неэластичные сосуды с низким сопротивлением, которые лишены материнского вазомоторного контроля, что приводит к усилению маточно-плацентарной перфузии, что позволяет удовлетворить потребности плода.[5] Любое нарушение процесса ремоделирования может привести к увеличению сопротивления маточно-плацентарных сосудов, что приведет к гипоперфузии плаценты и ее последующим эффектам, включая активацию коагуляции, дисфункцию эндотелиальных клеток, тромбоз плаценты и отложения фибрина, что связано с разработка ЗВУР. [5] [3] Кроме того, если происходит потеря фокальной адгезии эндоваскулярных трофобластов, может наблюдаться уменьшение площади плацентарной поверхности, связанное с плацентарной недостаточностью.Это уменьшение площади поверхности плаценты, наряду с увеличением ее толщины, создает шаровидный вид плаценты, который, как предполагается, действует как компенсаторный механизм плацентарной недостаточности.
Внутриутробная среда — это среда с низким содержанием кислорода, и поэтому кровообращение плода должно быть гибким, чтобы адаптироваться к любым изменениям, которые происходят с маточно-плацентарной функцией. [9] Эта гипоксическая среда стимулирует ангиогенез, в результате чего между кровообращением матери и межворсинчатым пространством устанавливаются сосудистые связи.Теперь, когда создана сосудистая и питательная сеть поддержки, формируется трофобласт ворсинок, который состоит из микроворсинок матери и базального слоя плода [10]. Для поддержания функции плаценты требуется большое количество энергии, на что указывает тот факт, что в обычном физиологическом состоянии плацента потребляет примерно 70% глюкозы и 40% кислорода, который обычно поступает в матку. Следовательно, для достижения оптимального роста и развития плода доставка питательных веществ в матку должна превышать плацентарную потребность, так что есть остаточные питательные вещества для использования плодами.[10] Следовательно, любое нарушение доставки питательных веществ в матку влияет на доставку питательных веществ к плоду.
На успешную плаценту может отрицательно повлиять латерализация, когда инвазия плаценты благоприятствует одной стороне, а плацента не имплантируется центрально. Если плацента остается асимметричной до срока, ультразвуковая допплерография покажет стойкую выемку на неимплантированной стороне, что приведет к относительной плацентарной недостаточности. Латерализация плаценты также была связана с повышенным риском развития материнской преэклампсии и, следовательно, последующей плацентарной недостаточности.[9] [11]
История и физические данные
Поскольку ограничение внутриутробного развития является одним из основных исходов, связанных с плацентарной недостаточностью, большинство выживших новорожденных рождаются либо преждевременно и известны как новорожденные с крайне низкой массой тела при рождении (ELBW), либо, в зависимости от того, когда произошло нарушение кровоснабжения сосудов, они могут иметь измененные пропорции тела при рождении. [10] Если плацентация неэффективна, последующие эффекты, такие как ЗВУР, клинически очевидны при допплеровских исследованиях примерно на 26 неделе беременности.[9]
Когда есть опасения по поводу ЗВУР, будь то вторичный по отношению к плацентарной недостаточности или другой этиологии, плод получит пользу от частого комбинированного мониторинга с использованием как допплеровского, так и биофизического профилей. Эта комбинация методов скрининга позволяет распознать снижение эффективности, наблюдаемое, когда IUGR связано с проблемами плаценты. Используя допплеровские исследования, неудачную плацентацию можно визуализировать по наличию надреза в маточных артериях, а также по увеличению сопротивления в пупочной артерии с прогрессированием либо до отсутствующего, либо до обратного конечного диастолического объема.Одним из первых признаков, которые можно увидеть на биофизическом профиле, когда есть опасения по поводу компрометации плода, является нереактивное отслеживание сердечного ритма плода. Следующее будет либо плохой, либо потерей движений тела плода, дыхательных движений и тонуса. Эти особенности снижения допплеровского статуса и плохих биофизических профилей типичны при дистрессе плода, что является обычным явлением при плацентарной недостаточности и может указывать на необходимость родов.
Оценка
В настоящее время отсутствуют критерии диагностики плацентарной недостаточности, так как отсутствуют стандартизированные методы диагностики.Частично проблема связана с широким разнообразием терминологии, используемой для описания так называемой «плацентарной недостаточности». [1] Однако по мере совершенствования технологий ультразвуковая допплерография оказалась полезным инструментом для оценки состояния плода. и плацентарное кровообращение как в здоровом, так и в болезненном состоянии. Было обнаружено, что четыре метода допплера являются фундаментальными для получения полезной информации о кровообращении у плода и матери, включая исследования пупочной артерии, исследования маточной артерии, исследования средней мозговой артерии и исследования венозного протока.[9] По мере того, как плод продолжает созревать во время беременности, происходит множество изменений кровообращения, которые можно оценить с помощью ультразвуковой допплерографии.
До наступления беременности маточные артерии демонстрируют низкий диастолический кровоток, высокое сопротивление и эластичную отдачу, отмеченную в виде ранних диастолических насечек. Успешная плацентация включает удаление интимы из сосудистой сети таким образом, чтобы в кровеносных сосудах был сильный диастолический поток, минимальное сопротивление и отсутствие эластичных свойств.Когда плацентация проходит успешно, ультразвуковая допплерография демонстрирует, что ремоделирование происходит быстро, так что к 12 неделе беременности происходит потеря надреза, а сопротивление становится низким к 20 неделе беременности или раньше. Когда происходит неэффективность плацентации, надрез сохраняется, а сопротивление остается высоким, что, как было показано, коррелирует с материнскими гипертензивными осложнениями плода, включая ЗВУР, преэклампсию и гибель плода [9]. Было показано, что использование маточной артерии для допплеровского скрининга для оценки зазубрин и сопротивления, чтобы помочь идентифицировать эти ситуации высокого риска, примерно на 85% чувствительно для выявления тяжелой ЗВУР и преэклампсии.
По мере увеличения сопротивления в плаценте допплеровские исследования пупочной артерии могут продемонстрировать нормальную, пониженную, отсутствующую или обратную конечную диастолическую скорость. [12] [8] Высокое сопротивление плаценты на ранних сроках беременности является нормальным явлением, поэтому можно ожидать, что конечная диастолическая скорость будет отсутствовать при допплеровских исследованиях до 12–14 недель беременности. При успешном прорастании плаценты снижение сопротивления и допплеровские исследования пупочной артерии должны продемонстрировать непрерывный кровоток к 14–18 неделе беременности.[9] Устойчивое сопротивление пупочной артерии на протяжении беременности является показателем повышенного риска плацентарной недостаточности.
В то время как допплеровские исследования пупочной артерии предоставляют важную информацию, относящуюся к возможному поражению плаценты, ценным дополнением является также допплерография средней мозговой артерии (СМА). MCA предоставляет информацию о системных ответных реакциях кровообращения у развивающегося плода, поскольку представляет собой сопротивление в церебральной микроциркуляции.Нормальный допплерография MCA показывает высокое сопротивление на протяжении всей беременности; тем не менее, заболевание плаценты может быть идентифицировано при увеличении диастолического кровотока и снижении индекса пульсации. Следовательно, допплеровские исследования MCA могут предоставить важную дополнительную информацию, когда есть опасения по поводу тяжелой ЗВУР, указывая на то, что может быть компромисс плода и может потребоваться вмешательство.
Другой формой допплерографии, которая дает представление о здоровье плаценты и плода, является венозный допплер, который передает информацию, относящуюся к сердечным данным, когда кровообращение плода испытывает стресс.Венозная волна, которая, как было доказано, обеспечивает наилучшие клинические данные, — это венозный проток. Венозный проток имеет множество преимуществ по сравнению с другими формами венозных волн, в том числе его чувствительность к изменениям оксигенации, он является одним из основных регуляторов венозного возврата при аномальном и нормальном кровообращении плода, он не зависит от сердечной функции, он служит прямой канал для просмотра ретроградных пульсовых волн правого предсердия, и, наконец, поскольку он имеет повышенный цветовой допплеровский сигнал и фокусную скорость уже с 12 недель беременности до 40 недель беременности, его очень легко визуализировать.[9] Если аномальный венозный проток или ретроградная волна предсердий визуализируются с помощью допплера примерно на 12–14 неделе беременности, существует повышенный риск сердечных аномалий плода, а также это может служить в качестве возможного предшественника, указывающего на тяжелую ЗВРП на основе плаценты.
МРТ дает дополнительную информацию для обнаружения и диагностики плацентарной недостаточности. Пустоты потока возникают, когда наблюдается потеря сигнала МРТ в кровеносном сосуде, по которому интенсивно течет кровь.При использовании Т2-взвешенного быстрого сбора данных с усилением релаксации (RARE) плацентарная недостаточность может быть обнаружена, когда наблюдается уменьшение пустот между плацентой и маткой, поскольку это можно рассматривать как отражение снижения маточно-плацентарной перфузии. [5] Дополнительным преимуществом МРТ является то, что она обеспечивает высокий контраст мягких тканей. Поэтому сосудистые патологии плаценты, включая кровоизлияния и инфаркты, могут быть обнаружены с помощью МРТ плаценты, что указывает на высокий риск плацентарной недостаточности и последующего IUGR.
Лечение / менеджмент
В настоящее время не существует известного лечения плацентарной недостаточности, кроме доставки плода, если это возможно. Было показано, что низкие дозы аспирина и использование антиоксидантной терапии, включая витамины C и E, способствуют улучшению плацентации в тех случаях, когда нет уверенности в ее успешности. [9] Исследования показали, что при использовании раннего ультразвукового допплера при подозрении на ЗВУР во время беременности наблюдается снижение перинатальной смертности примерно на 38%.[12] [13]
Женщинам из группы высокого риска, например с хронической гипертензией, коагулопатиями или преэклампсией в анамнезе, может быть полезно пройти ультразвуковое допплеровское обследование на сроке от 12 до 14 недель гестации, потому что, если очевидны двусторонние насечки, затем следует начать терапию низкими дозами аспирина.
Исследования in vitro показали, что гепарин может стимулировать неоангиогенез, а также улучшать перфузию плаценты. Антикоагулянтные свойства гепарина проявляются в его способности мобилизовать фактор ингибирования ткани в кровоток и в том факте, что он также усиливает активность антитромбина.Дополнительные преимущества гепарина при рассмотрении плацентарной недостаточности и ее последующих последствий заключаются в том, что гепарин способствует пролиферации трофобластов, уменьшает воспаление за счет подавления каскада комплемента, снижает апоптоз, а также косвенно действует как фактор роста [3].
Было также показано, что гепарин активирует определенные белки, участвующие в ангиогенезе и развитии плаценты. К ним относятся ангиопоэтин-2, который отвечает за ремоделирование сосудов ворсинок хориона, лептин, который отвечает за регуляцию переноса питательных веществ, а также рецептор-3 фактора роста эндотелия сосудов, тканевый ингибитор матричной металлопротеазы-1, фактор некроза опухоли-альфа. и ангиостатин.Основываясь на его свойствах и предварительных данных, некоторые исследования показали, что гепарин может использоваться в качестве профилактического средства лечения плацентарной болезни.
Дифференциальная диагностика
Существует множество факторов, которые могут способствовать развитию плацентарной недостаточности, и известно, что ЗВУР является основным последующим осложнением; однако иногда бывает трудно дифференцировать новорожденного с малым для гестационного возраста (SGA) новорожденного от новорожденного с IUGR.Одним из основных преимуществ допплерографических исследований, особенно пупочной артерии, является то, что допплерография аномальной пупочной артерии может использоваться для дифференциации патологического ЗВУР и новорожденного с малым для гестационного возраста новорожденным, таким образом определяя, какая беременность потребует тщательного наблюдения. по сравнению с обычным мониторингом. [9] [14]
Когда средний расчетный вес плода ниже 10-го процентиля для определенного гестационного возраста, это плод SGA. И наоборот, плод с ЗВУР не сможет достичь нормального роста, как правило, вследствие плацентарной недостаточности, генетического заболевания или инфекции.[14] Следовательно, новорожденный с SGA будет физически маленьким, но в целом здоровым, по сравнению с новорожденным с ЗВУР, который также может быть физически маленьким, но, вероятно, будет иметь под угрозой его здоровье.
При рассмотрении дифференциальных диагнозов, которые способствуют плацентарной недостаточности, известны сопутствующие заболевания, включая, помимо прочего, преэклампсию, гипертензивные расстройства у матери, поскольку они оба влияют на сопротивление плаценты и маточно-плацентарный кровоток. Другие болезни, которые следует учитывать, включают олигогидрамнион и материнское недоедание или ограничение калорийности.
Прогноз
Если новорожденный пострадал от ЗВУР в результате плацентарной недостаточности и пережил перинатальный период, он подвергается более высокому риску развития когнитивных нарушений в детстве, в том числе церебрального паралича и судорожных припадков, по сравнению с новорожденными без ограничения роста. Пациенты, страдающие плацентарной недостаточностью, часто имеют аномальные формы волны доплеровского кровотока (DFVW) в пупочной артерии, и когда в одном исследовании сравнивали DFVW младенцев, которые испытали плацентарную недостаточность внутриутробно, с младенцами, у которых не было плацентарной недостаточности, они обнаружили, что младенцы, у которых были аномальные У DFVW также был более низкий IQ в 5-летнем возрасте.Есть также свидетельства того, что страдание от ЗВУР в младенчестве предрасполагает к хроническим заболеваниям во взрослом возрасте, включая повышенный риск развития ишемической болезни сердца, гипертонии и диабета. [2]
Чтобы улучшить прогноз для новорожденного, приоритет должен быть сосредоточен на вмешательствах, которые позволяют максимально увеличить гестационный возраст при рождении. Подсчитано, что каждую неделю, когда беременность продлевается для плодов между 24 и 28 неделями беременности, выживаемость без сопутствующих осложнений увеличивается примерно на 10–15%.[3]
Осложнения
Последствия плацентарной недостаточности для развивающегося плода являются сложными и многофакторными; однако основными эффектами, как правило, являются плацентарная дыхательная недостаточность и гипоксемия плода, которые способствуют задержке внутриутробного развития и связанным с этим эффектам, включая недоношенность. [10] [14]
Самым пагубным осложнением, очевидно, является полное отсутствие плацентации и, как следствие, выкидыш.Для развивающегося плода степень аномалий пупочной артерии, наблюдаемых при допплерографии, коррелирует с ацидозом, потребностями в реанимации, прессорной поддержкой, респираторной поддержкой, а также мультисистемной органной недостаточностью, которая обычно возникает при гипоксемии, поскольку это вызывает перераспределение кровотока. у развивающегося плода к важным органам, таким как мозг и сердце, за счет других соответствующих органов, таких как кишечник и почки. [14] Кроме того, когда допплеровские исследования демонстрируют отсутствие или обратный конечный диастолический поток, у новорожденных увеличивается частота внутрижелудочковых кровоизлияний.[9]
С повышением сопротивления плаценты во время беременности плод, уже имеющий ЗВУР, подвергается дополнительному риску гипогликемии, гипоксически-ишемической энцефалопатии, тромбоцитопении, лейкопении и анемии. [8] Кроме того, есть данные, указывающие на то, что младенцы подвержены риску развития когнитивного дефицита в детстве, а затем развития хронических заболеваний во взрослом возрасте.
Сдерживание и обучение пациентов
Во время беременности обязательно проводить регулярный пренатальный скрининг и ультразвуковой мониторинг, чтобы обеспечить наилучший результат для новорожденного.Хотя окончательных профилактических мер плацентарной недостаточности не существует, как только она будет обнаружена с помощью УЗИ, МРТ, ДПП или любой комбинации этих методов, можно начинать такие вмешательства, как терапия гепарином, в надежде продлить срок беременности с надеждой на минимизацию ацидоз и гипоксия и, как следствие, ЗВУР, недоношенность или гибель плода. Необходимо провести дополнительные исследования вмешательств и лечения, которые во время беременности принесут наибольшую пользу развивающемуся плоду.
Жемчуг и другие выпуски
Не существует однозначного лекарства от плацентарной недостаточности, но последствия можно свести к минимуму, если поставить диагноз на ранней стадии, а мать получит адекватную дородовую помощь. Недавний метанализ показал, что гепарин может способствовать росту плода и продлевать беременность, если гепарин назначается при высоком подозрении на плацентарную недостаточность, но не способствует снижению неблагоприятных исходов у новорожденных.
Улучшение результатов команды здравоохранения
На основании допплеровских исследований самые ранние признаки неудачной плацентации, вероятно, не будут обнаружены, по крайней мере, после 12 недель беременности, что коррелирует с проспективным когортным исследованием, которое продемонстрировало скрининговую функцию плаценты у беременных с высоким риском во втором и первом триместре. лучший предиктор неблагоприятных перинатальных исходов. [15]
При обсуждении плацентарной недостаточности будет по крайней мере две команды, если не больше, которые будут участвовать в уходе за пациентами, так как одна команда будет нести ответственность за пренатальный мониторинг матери и плода, а другая команда будет заботиться о них. для новорожденных в послеродовой период.Ведение матери и ребенка с ЗВРП требует наличия междисциплинарной команды, состоящей из акушеров / гинекологов, реаниматологов новорожденных, медсестер акушера и отделения интенсивной терапии, респираторных терапевтов, фармацевтов, пульмонологов, а иногда и других специалистов, включая хирургию, инфекционные заболевания или генетику.
У новорожденных с ЗВРП часто развивается хроническое заболевание легких, вторичное по отношению к их недоношенности, и может потребоваться прием нескольких лекарств, а также домашний кислородный контроль, или у них может развиться несколько инфекций, включая некротический энтероколит или поздний сепсис, все из которых требует координации между вышеупомянутые команды, чтобы обеспечить улучшенные результаты для пациента.

