Опухоли головы и шеи | ГБУЗ Онкологический диспансер №4
Опухоли головы и шеи – онкологические заболевания полости рта, носа, гортани, глотки, слюнных желез и придаточных пазух соединительнотканного, эпителиального и нейрогенного происхождения. Отличаются высокой агрессивностью, активным ростом, множественными метастазами и сложным лечением.
Диагностика и лечение опухолей головы и шеи требует плотного взаимодействия врача-онколога с узкопрофильными специалистами: отоларингологами, дерматологами, стоматологами.
В группу не входят опухоли эндокринной, лимфатической, центральной нервной системы и офтальмологические заболевания.
По степени зрелости выделяется высокодифференцированные опухолевые клетки и незрелые клетки, которые плохо поддаются лечению и ухудшают общий прогноз.
Причины возникновения опухолей головы и шеи
Факторы риска, вызывающие опухоли головы и шеи:
-курение и употребление жевательного и нюхательного табака
-злоупотребление алкоголем
-вирус Эпштейна-Барр, ВПЧ
-длительное воздействие химических веществ: древесная и текстильная пыль, формальдегид, краска, металл
-радиоактивное излучение
-регулярное употребление горячей пищи
-диета с высоким содержанием жиров
-лейкоплакия и эритроплакия – предраковые состояния полости рта
Виды опухолей головы и шеи
Рак полости рта
По распространенности 50% злокачественных опухолей полости рта приходится на рак языка.
Рак дна ротовой полости составляет 20% случаев. По внешнему проявлению опухоль полости рта имеет вид язвы или уплотнения, и может выступать над поверхностью слизистой. Рак полости рта развивается очень быстро, незаметно прорастает в здоровые ткани и дает метастазы в регионарные лимфоузлы.
Первые признаки и симптомы рака полости рта
На начальном этапе у пациентов возникают странные ощущения во рту, появляются небольшие образования, бесцветные пятна, язвочки и уплотнения на слизистой. Часто определить самостоятельно, что это первые признаки злокачественных опухолей полости рта, невозможно. Поэтому стоит регулярно посещать стоматолога и терапевта, чтобы вовремя выявить первые симптомы заболевания.
Обращаться к стоматологу нужно немедленно, если вы обнаружили у себя следующие признаки рака полости рта:
-незаживающие кровоточащие язвы на слизистой оболочке полости рта, десне или губе
-наросты, узелки и уплотнения на внутренней стороне щеки, ощущаемые языком
-онемение части полости рта, потеря чувствительности
-хронические беспричинные боли в полости рта, отдающие в ухо или висок
-повышенное слюноотделение
-трудности при пережевывании и глотании пищи
-отек челюсти
-увеличение лимфатических узлов в области шеи
-изменение голоса
-потеря веса
Формы онкологических заболеваний ротовой полости:
-язвенная форма встречается наиболее часто. Для неё характерно появление в полости рта небольших язвочек, которые долго не заживают и имеют тенденцию разрастаться
Для неё характерно появление в полости рта небольших язвочек, которые долго не заживают и имеют тенденцию разрастаться
-узловатая форма характеризуется образованием в полости уплотнений с четкой формой и белесым окрасом. Новообразование очень быстро разрастается
-папиллярная форма рака представляет собой выросты на слизистой, свисающие в полость рта. У выростов плотная структура, цвет не отличается от покровов слизистой. Хорошо подается лечению, так как новообразования не распространяется на окружающие ткани
Рак языка
Злокачественные опухоли языка занимают всего 2% от общего числа пациентов с онкологическими заболеваниями.
Мужчины подвержены этому заболеванию больше, чем женщины.
Среди факторов риска, способствующих появлению рака языка, отмечаются:
-курение, жевательный табак и никотиновые жвачки
-злоупотребление алкоголем
-химические и термические повреждения слизистой оболочки полости рта
-наследственность
-вирус папилломы человека
-лейкоплакия или длительное механическое повреждение слизистой рта
-воспаление десен
Наиболее часто выявляется рак тела языка, при котором опухоль затрагивает боковые поверхности и срединную его часть – такая локализация встречается в 70% случаев.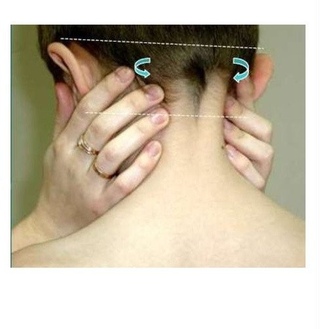
Рак корня языка занимает 20%. Локализация злокачественных опухолей в задней половине ротовой полости обозначается как рак носоглотки и имеет более агрессивное течение.
Рак в нижней части языка диагностируется в 10% случаев.
Симптомы рака языка разнообразны, но чаще всего присутствуют следующие признаки:
-пятна красного или белого цвета
-боль в горле при приеме пищи
-нарушения речи
-увеличение шейных лимфоузлов
-неприятный запах изо рта
-боли в области уха
Диагностировать рак языка можно после визуального осмотра и результатов цитологического и гистологического анализов.
Рак слюнных желез
Рак слюнных желез встречается редко, его доля в структуре опухолей головы и шеи не превышает 7%.
Гистологическая классификация выделяет следующие виды рака:
-плоскоклеточный рак, состоящий из эпителиальных клеток
-цилиндроклеточный, с ходами и просветами, где образовываются сосочковые выросты
-мономорфный, с правильными железистоподобными структурами
-мукоэпидермоидный, клетки которого образуют структуру с полостями, заполненными слизью
-аденокарцинома, железистоподобные и паппилярные клетки без признаков других типов рака
-аденолимфома, опухоль с четко очерченными границами и эластической консистенцией
-недифференцированный рак с неоднородной структурой.
Среди причин, предположительно вызывающих рак слюнных желез, можно выделить:
-длительное курение
-ионизирующее облучение
-вредное производство – тяжелые металлы, цементная пыль, и т.д.
-неправильное питание
-вирусы (мутировавший вирус Эпштейна-Барра)
-гормональный сбой
Ранние стадии рака слюнных желез протекают бессимптомно, появление объемного образования болевых ощущений не вызывает. При прорастании в соседние ткани, рак слюнных желез вызывает парез лицевого нерва, онемение языка, слабость и атрофию мышц языка. Рак слюнных желез дает метастазы в лимфатические узлы, иногда – в легкие и кости.
Рак губы
Рак губы – злокачественная опухоль, которая образуется из плоского эпителия красной каймы губы.
Возникновению заболевания часто предшествуют предраковые состояния – хронические трещины, ограниченный гиперкератоз, и.т.д. Типичное место локализации опухоли – нижняя губа, рак верхней губы встречается значительно реже. Самая распространенная гистологическая форма рака губы – плоскоклеточный рак.
Самая распространенная гистологическая форма рака губы – плоскоклеточный рак.
Факторами, влияющими на возникновение рака, являются:
-курение и злоупотребление алкоголем
-ирусные инфекции
-механические травмы
-химические и термические ожоги
-резкая смена температуры окружающей среды
-нарушение обмена веществ
-желудочные заболевания
-вредная привычка покусывать губы
-дефицит в организме витаминов группы В, С, Е
На ранних стадиях заболевания на губах возникает небольшое образование, внешне похожее на язвочку или трещинку, покрытую чешуйками. Темпы роста опухоли незначительные, однако опасность этой формы рака в том, что метастазы могут распространяться в кости челюсти, образуя новые очаги заболевания.
Симптомы рака губы:
-язвы и уплотнения, покрытые струпом
-шелушение каймы губ
-зуд
-обильное выделение слюны
-неприятные ощущения во время приема пищи
Диагностировать рак губы на ранних стадиях удается благодаря его внешней локализации.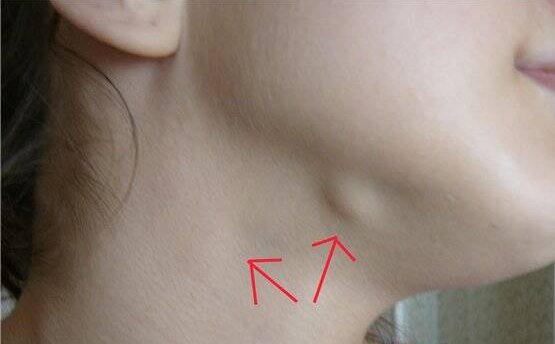 Раннее выявление злокачественной опухоли дает возможность вовремя приступить к лечению и в 70% случаев возможно полное излечение.
Раннее выявление злокачественной опухоли дает возможность вовремя приступить к лечению и в 70% случаев возможно полное излечение.
Рак гортани и глотки
Наиболее часто встречаются два морфологических типа рака гортани: плоскоклеточный рак и аденокарцинома.
Болезнь трудно диагностируется, так как первые признаки рака горла часто напоминают обычные простудные заболевания. Локализация опухолей в труднодоступных местах и отсутствие четко выраженной симптоматики затрудняет диагностику. Злокачественные опухоли обнаруживаются на поздних стадиях, когда у пациента затрудняется носовое дыхание, ухудшается слух, пропадает голос.
Симптомы рака горла:
-кровотечение, заложенность носа
-шум в ушах, потеря слуха на стороне поражения
-шейная лимфаденопатия
-головная боль
-симптомы поражения черепных нервов
-боли в горле, отдающие в ухо
-расстройство глотания (дисфагия)
-боль при прохождении пищи по пищеводу (одинофагия)
-осиплость голоса
-субфебрильная температура
-истощение, слабость.
Для точной диагностики опухолей головы и шеи применяется биопсия. Материал отправляется на исследование в гистологическую лабораторию, и по результатам исследования определяется наличие опухоли.
Диагностика опухолей головы и шеи
Методами диагностики при онкологических заболеваниях головы и шеи являются:
-ультразвуковое исследование шеи и шейных лимфоузлов
-эндоскопические исследования полости носа, носоглотки, гортани
-инцизионная биопсия
-тонкоигольная пункционная биопсия
-рентгенография
-КТ/МРТ
-Сцинтиграфия
-ПЭТ/КТ
УЗИ лимфатических узлов — где сделать УЗИ лимфатических узлов в ЗАО
Увеличение лимфатических узлов – появление небольших уплотнений размером от горошины для голубиного яйца на шее, в подмышечных и паховых областях – зачастую является основным поводом для проведения ультразвукового исследования лимфатической системы.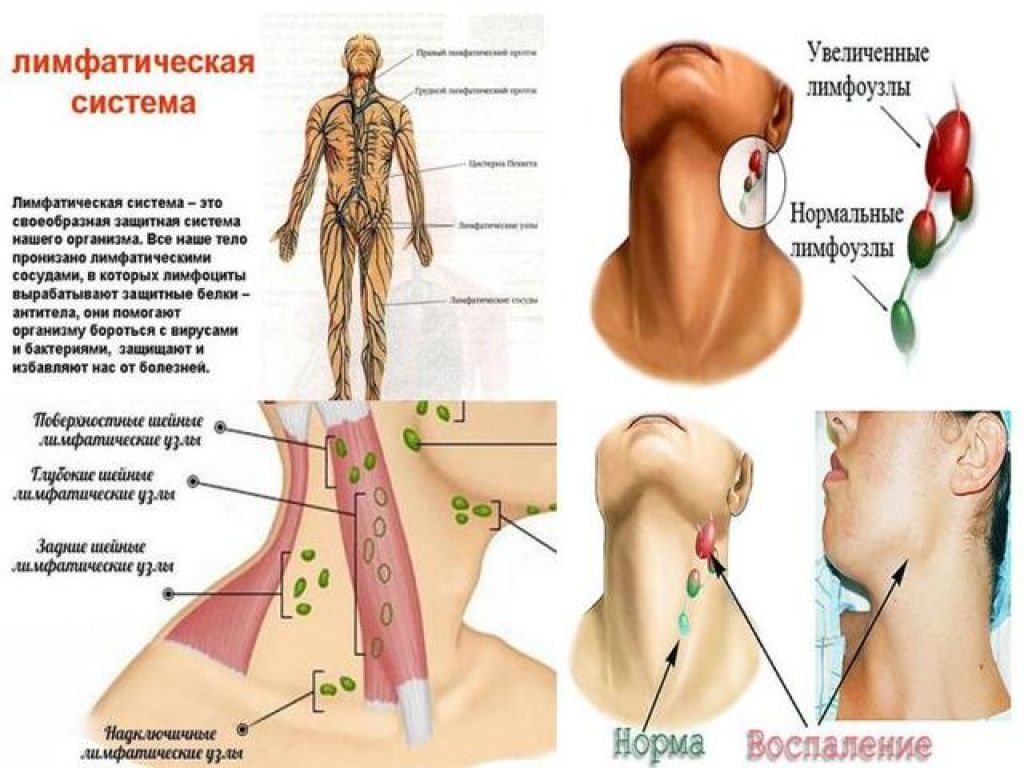 При этом лимфаденопатия может носить как доброкачественный, так и злокачественный характер.
При этом лимфаденопатия может носить как доброкачественный, так и злокачественный характер.
Основная задача, которая стоит при проведении УЗИ – четкое определение, является ли увеличение следствием различных воспалительных заболеваний и неспецифических реакций или же признаком злокачественного процесса. Для этого проводится тщательное исследование лимфоузла, определение его прямого и поперечного размера, капсулы, внутренней структуры и состояния сосудов, осуществляющих его кровоснабжение. Сочетание всех этих параметров позволяет заподозрить опухолевое метастатическое поражение или обычную воспалительную реакцию.
Необходимость исследования лимфоузлов при подозрении на опухолевые процессы обусловлена их физиологическими особенностями. Именно эти структуры первыми поражаются при метастазировании опухолевого процесса. Наличие или отсутствие опухолевого поражения регионарных лимфатических узлов является важным прогностическим признаком, позволяющим определить стадию процесса, возможный прогноз течения заболевания, определить тактику лечения, объем оперативного вмешательства.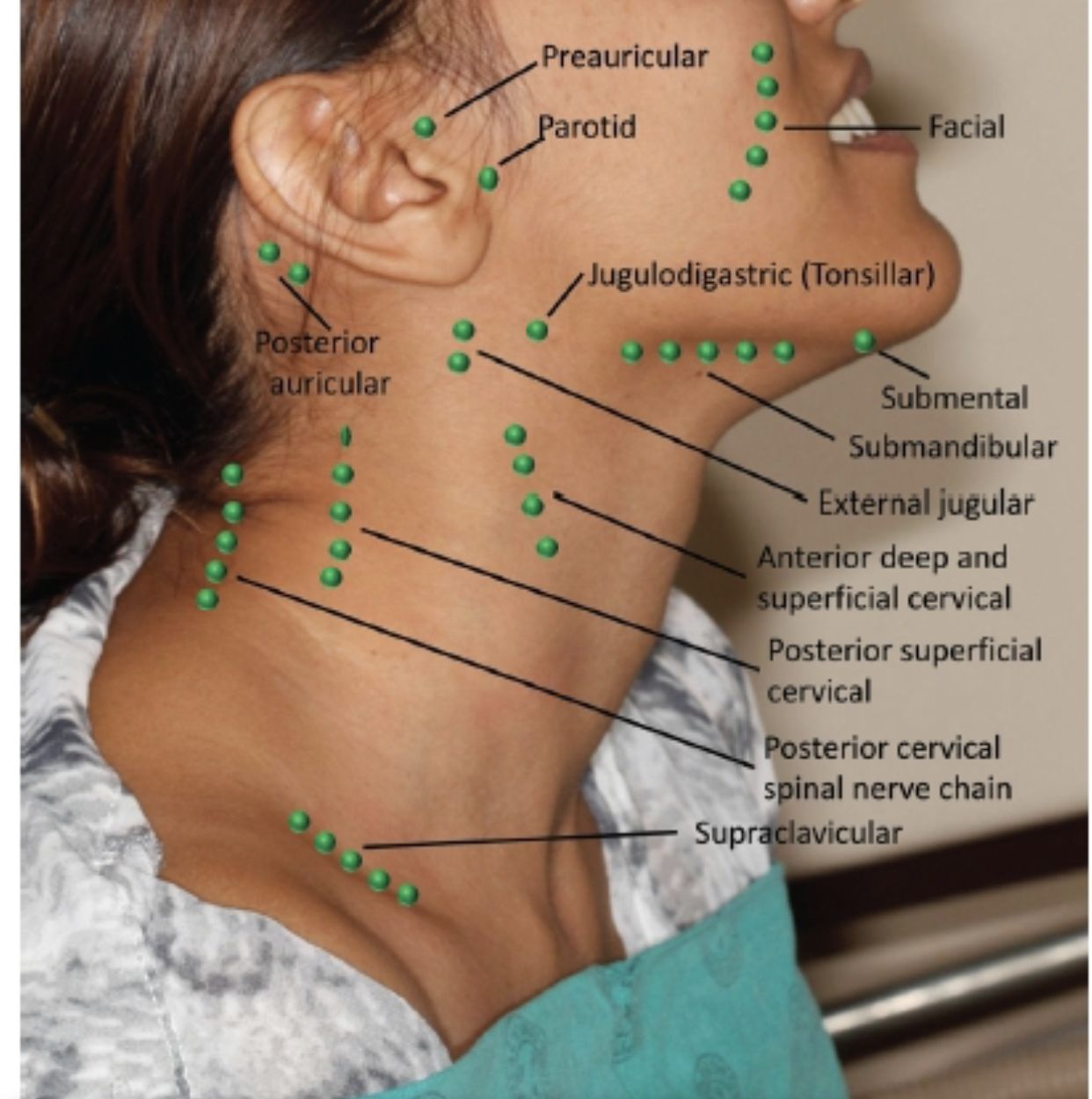
УЗИ лимфатических узлов шеи
Лимфоузлы шеи находятся достаточно близко к поверхности и благодаря этому могут быть тщательно исследованы. При их обследовании определяется местоположение, размер, контур, форма, внутренняя структура и взаимосвязь с окружающими тканями и сосудами. Основными показаниями к проведению ультразвукового исследования являются:
- Увеличение лимфоузлов, которое остается более 2 недель после перенесенного простудного или другого заболевания
- Их увеличение при отсутствии признаков какого-либо инфекционного заболевания горла?, уха, носовых пазух или верхних дыхательных путей.
- Наличие большого, плотного, болезненного, плохо смещающегося узла, спаянного с окружающей тканью
- В случае если один узел значительно увеличен в размерах по сравнению с остальными.
Автор текста: Мусина Ольга Юрьевна
Должность: Врач ультразвуковой диагностики высшей квалификационной категории
Общий стаж: 24 года
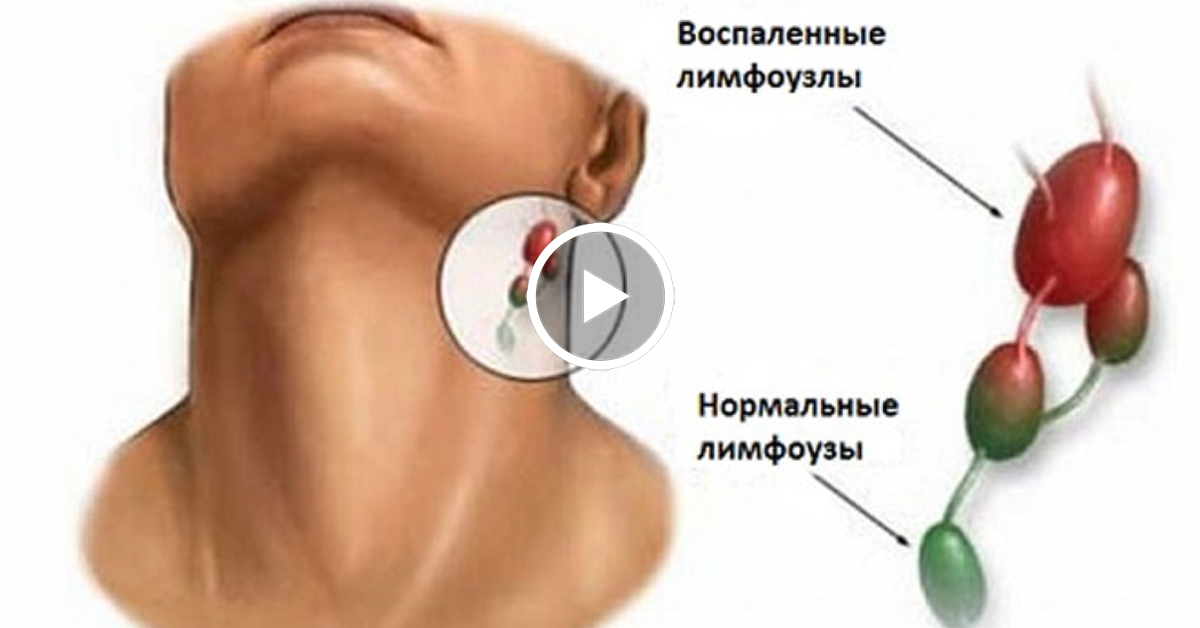
Воспаленные лимфоузлы: как отличить «плохой узел» от «нормального» — Новости здоровья
Врач-инфекционист Елена Луцка рассказала, какие симптомы лимфаденита. Когда увеличенные лимфоузлы представляют угрозу и требуют дальнейшей диагностики, а когда беспокоиться не следует.
Когда увеличенные лимфоузлы представляют угрозу и требуют дальнейшей диагностики, а когда беспокоиться не следует.
Читайте также: Что убивает клетки мозга: ответ ученых
Лимфоузлы — что это?
Лимфоузлы – это образования, расположенные вдоль лимфатических сосудов по всему телу. Служат они своеобразными «фильтрами».
Поэтому абсолютно нормально, когда лимфоузлы шеи и головы периодически увеличиваются, ведь их функция связана с работой ЛОР органов.
Однако, если лимфоузлы увеличены, стоит обратить внимание на такие моменты
Есть ли симптомы инфекции верхних дыхательных путей, ушей, конъюнктивит, кашель, поражения кожи.
Есть ли лихорадка, нарушение общего состояния.
Был ли контакт с животными, особенно котами.
Есть ли проблемы с зубами, были ли недавно стоматологические вмешательства.
Увеличен один лимфоузел, группа или несколько групп.
Характер самого лимфоузла.
При неверном лечении воспаление может распространиться по всему организму
Лимфоузел считается нормальным, если он:
- размером до 2 см
- эластичной консистенции
- не болит
- подвижный, не соединенный с другими тканями
- кожа над ним не изменена
Если лимфоузел болит, кожа над ним горячая, покраснела, нужно обратиться к врачу – может понадобиться хирургическое вмешательство.
Лимфоузлы могут воспаляться и под мышками и в паху
Лимфоузел, который требует дополнительного исследования:
- более 2 сантиметра, непрерывно увеличивается в течение более 2 недель и не имеет тенденции к уменьшению в течение 4-6 недель;
- особенно должны насторожить увеличение надключичных лимфоузлов;
- плотный лимфоузел;
- лимфоузлы подвижные, соединены между собой или с окружающими тканями;
- нет признаков острого воспаления;
- «плохой» лимфоузел, как правило, не болит;
- кожа над ним может покрыться язвами.
В зависимости от ситуации, врач может предложить дополнительные обследования: общий анализ крови, маркеры инфекций, биопсию лимфоузла и другие.
На данный момент нет убедительных доказательств пользы УЗИ, оно не помогает врачу отличить доброкачественный лимфаденит от злокачественного.
Больше новостей, касающихся лечения, медицины, питания, здорового образа жизни и многое другое – читайте в разделе Здоровье.
причины, симптомы и лечение в статье стоматолога-хирурга Козлов П. Ю.
Дата публикации 20 апреля 2021Обновлено 26 апреля 2021
Определение болезни. Причины заболевания
Шейный лимфаденит — это увеличение лимфатических узлов в области шеи, вызванное воспалением.
При остром лимфадените увеличенный лимфоузел становится плотным и болезненным, кожа воспалённой области краснеет, повышается местная температура и появляется слабость. При хроническом лимфадените других симптомов, кроме увеличения лимфоузла, может не быть.
Причины шейного лимфаденита
Лимфатическая система входит в состав иммунной системы, поэтому любая болезнь, при которой активируется клеточный иммунитет, может вызывать воспаление лимфатических узлов [1][2][3].
Лимфаденит может возникать из-за воспаления в зубочелюстной системе и ЛОР-органах. Реже его причиной становятся местные заболевания кожи, например фурункул, карбункул и нагноившаяся эпидермальная киста.
К развитию шейного лимфаденита могут приводить специфические и неспецифические возбудители. В первом случае лимфаденит сопровождает основное заболевание, особенности воспаления лимфоузлов напрямую зависят от возбудителя.
Во втором случае причиной становятся гнойные раны и воспалительные процессы, связанные с тканями зуба и периодонтом, например кариес, осложнённый периодонтитом. Клиническая картина от возбудителя при этом не зависит.
Возбудители специфического лимфаденита:
Возбудители неспецифического лимфаденита:
- бактерии — стафилококки, стрептококки и анаэробные микроорганизмы;
- вирусы — грипп, герпес, аденовирус и т. д.;
- грибы.
Из-за повышенной активности лимфоидной системы у детей заболевание встречается чаще, чем у взрослых [13][14].
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением — это опасно для вашего здоровья!
Симптомы шейного лимфаденита
Когда в организм проникают вирусы и бактерии, лимфатическая система реагирует на них одной из первых.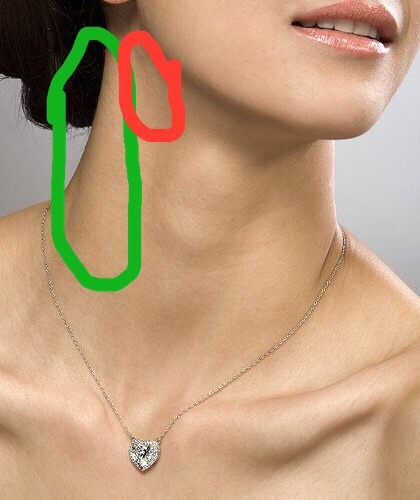 Поэтому шейный лимфаденит может быть первым проявлением основного заболевания. Позже к нему присоединяются другие симптомы, характерные для туберкулёза, сифилиса, чумы, ВИЧ или других инфекций.
Поэтому шейный лимфаденит может быть первым проявлением основного заболевания. Позже к нему присоединяются другие симптомы, характерные для туберкулёза, сифилиса, чумы, ВИЧ или других инфекций.
Симптомы острого лимфаденита
При остром серозном лимфадените:
- пациента беспокоит первичный воспалительный очаг, например зубная боль или боль в горле;
- болезненный и увеличенный лимфатический узел смещается при ощупывании;
- возникает умеренная боль в области лимфатического узла, но дальше она не распространяется;
- может незначительно повыситься температура;
- появляется общая слабость и боль при движении головой [4].
Эти симптомы — повод немедленно обратиться за медицинской помощью.
При остром гнойном лимфадените клинические признаки более выражены. Возбудители воспаления и их токсины распространяются по организму и попадают в системный кровоток, поэтому интоксикация нарастает и симптомы усиливаются.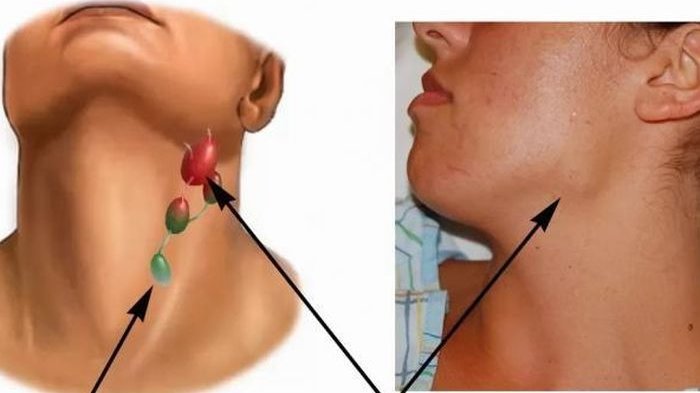
Симптомы острого гнойного лимфаденита:
- лимфоузел увеличивается и спаивается с соседними узлами и окружающими тканями;
- при ощупывании лимфоузла возникает резкая боль;
- повышается местная и общая температура тела;
- появляется озноб, возможна одышка;
- возникает головная боль и слабость;
- развивается покраснение кожи и отёк [5].
На этой стадии лимфатический узел нагнаивается, но близлежащие ткани ещё не поражены. Без своевременной медицинской помощи воспаляются соседние лимфатические узлы и окружающие ткани и возникает осложнение лимфаденита — аденофлегмона.
Симптомы хронического лимфаденита
Хронический лимфаденит часто протекает без симптомов. При обострении основного заболевания, например тонзиллита или ринита, лимфоузел увеличен и причиняет умеренную боль пациенту.
Зачастую при излечении или стабилизации основного заболевания признаки лимфаденита тоже исчезают. Но иногда после нескольких обострений ткани лимфоузла разрастаются.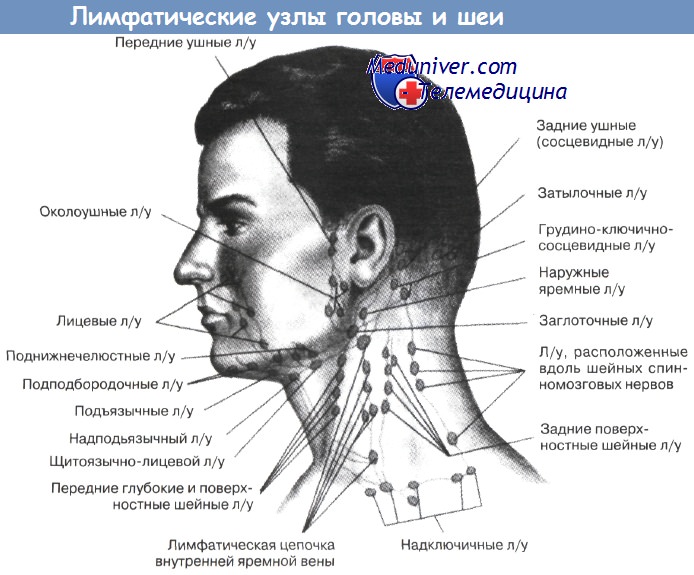 Такой узел не болит, но увеличен. Из-за его поверхностного расположения пациенты часто самостоятельно обнаруживают изменение. Обычно они замечают, что под кожей на шее появился «перекатывающийся шарик». Это свойственно именно хроническому лимфадениту, так как лимфатический узел не сращён с окружающими тканями.
Такой узел не болит, но увеличен. Из-за его поверхностного расположения пациенты часто самостоятельно обнаруживают изменение. Обычно они замечают, что под кожей на шее появился «перекатывающийся шарик». Это свойственно именно хроническому лимфадениту, так как лимфатический узел не сращён с окружающими тканями.
Патогенез шейного лимфаденита
Лимфатическая система — это сеть органов, сосудов и лимфатических узлов, расположенных по всему телу.
Функции лимфатической системы:
- удалять продукты обмена веществ из тканей и транспортировать их к выводящим органам;
- поддерживать постоянство внутренней среды организма;
- вырабатывать лимфоциты — клетки иммунной системы, защищающие организм от вирусов и бактерий [6].
При воспалительных процессах, чаще гнойных, лимфа (бесцветная жидкость с большим количеством лимфоцитов) с бактериями и токсинами из очага поражения поступает в лимфатические узлы — небольшие структуры, которые фильтруют лимфатическую жидкость. Проходя сквозь них, лимфа обогащается лимфоцитами и антителами и очищается от инородных частиц: микробных тел, погибших и опухолевидных клеток, пылевых частиц. Они задерживаются и уничтожаются в лимфоузлах.
Проходя сквозь них, лимфа обогащается лимфоцитами и антителами и очищается от инородных частиц: микробных тел, погибших и опухолевидных клеток, пылевых частиц. Они задерживаются и уничтожаются в лимфоузлах.
Проще говоря, лимфатические узлы выступают барьером, который не даёт инфекции распространяться по организму. Однако при слабом иммунитете и высокой патогенности микробов узел инфицируется и воспаляется. Он увеличивается и становится болезненным, но окружающие ткани в патологический процесс ещё не вовлечены. Затем воспаление нарастает, поражаются близлежащие ткани и симптомы интоксикации становятся более выраженными.
В дальнейшем лимфатический узел нагнаивается. Сперва гной находится внутри него и за пределы капсулы не распространяется. Без лечения пациент чувствует себя всё хуже, гноя в лимфатическом узле становится больше, затем капсула разрывается и гнойное содержимое проникает в окружающие ткани.
Классификация и стадии развития шейного лимфаденита
По типу возбудителяНеспецифические (клиническая картина не зависит от возбудителя):
- бактерии;
- вирусы;
- грибы.

Специфические (лимфаденит сопровождает основное заболевание, его течение напрямую зависит от возбудителя):
По типу течения заболеванияОстрый лимфаденит:
- катаральный;
- серозный;
- гнойный.
Хронический лимфаденит:
- гиперпластический — лимфатический узел увеличивается и становится более плотным; его ткань заменяется на соединительную, появляются участки некроза и кальциноза;
- абсцедирующий (гнойный) [7].
- одонтогенный — при поражении зубов;
- неодонтогенный — при заболевании ЛОР-органов и др.
- Подбородочные лимфатические узлы располагаются непосредственно под мышечным слоем, что затрудняет их выявление. К ним лимфа попадает от тканей нижней губы, подбородка, зубов и кончика языка.

- Поднижнечелюстные лимфатические узлы находятся под челюстью. Они очень чувствительны к воспалительным заболеваниям полости рта и могут воспалиться при периодонтите. В поднижнечелюстные лимфоузлы лимфа оттекает от век, угла глаз, щёк, носа, зубов, верхней и нижней губы.
- Поверхностные шейные лимфатические узлы расположены в верхней трети кивательной мышцы, глубокие шейные лимфоузлы залегают под ней.
- Задние шейные лимфоузлы находятся на задней поверхности шеи по обе стороны от позвоночника.
- Тонзиллярные лимфатические узлы расположены в области углов нижней челюсти с каждой стороны. Они очень уязвимы при заболеваниях гортани и миндалин.
- Заушные лимфатические узлы располагаются позади ушных раковин. В них лимфа поступает от уха, теменной и лобной областей.
Стадии развития заболевания
- Катаральное воспаление. Лимфатический узел увеличивается, становится плотным, болезненным, но окружающие ткани не воспалены.
 Возникает боль в поражённой области, повышается температура, и появляются симптомы интоксикации: головные боли, слабость, ломота в мышцах и суставах.
Возникает боль в поражённой области, повышается температура, и появляются симптомы интоксикации: головные боли, слабость, ломота в мышцах и суставах. - Серозная стадия. Воспаление нарастает и захватывает окружающие ткани. Кожа в проекции поражённого лимфатического узла краснеет, боль усиливается. Температура тела повышается, симптомы интоксикации становятся более выраженными.
- Гнойная стадия. Без лечения лимфатический узел нагнаивается, но гной находится внутри самого узла и за пределы капсулы не выходит. Окружающие ткани отекают и могут срастись с капсулой узла. Появляется жар, озноб, ломота в теле и сильная головная боль. Постепенно в лимфатическом узле становится больше гноя и капсула расплавляется. Гнойное содержимое проникает в окружающие ткани, и происходит их инфицирование.
На начальных стадиях ткани лимфатического узла могут либо полностью восстановиться, либо заболевание переходит в тяжёлую стадию или хроническую форму. Это зависит от характера и агрессивности возбудителя, состояния иммунитета и оказанной медицинской помощи.
Это зависит от характера и агрессивности возбудителя, состояния иммунитета и оказанной медицинской помощи.
При хроническом течении лимфаденита изменяется структура лимфатического узла, лимфоидная ткань разрастается, могут появиться очаги распада и некроза. В таком состоянии узел может находиться много лет, но при этом не беспокоить. Однако при снижении защитных сил организма хроническое воспаление может обостриться и возникнет гнойный процесс.
Осложнения шейного лимфаденита
При своевременном обращении к врачу неспецифический шейный лимфаденит полностью обратим. Если же визит к доктору откладывать, заниматься самолечением или игнорировать проблему, то часто развиваются осложнения.
Одно из них — аденофлегмона, или гнойное воспаление жировой клетчатки, окружающей поражённый лимфоузел. Симптомы аденофлегмоны:
- повышение температуры тела до 39–39,5 °C и более;
- выраженные боли и отёк;
- кожа поражённой области покрасневшая и горячая;
- озноб, слабость и головная боль;
- пальпация области вокруг воспалённого лимфоузла вызывает резкую боль, при этом ощущается плотный воспалительный инфильтрат (скопление крови с лимфой).

Общее состояние пациента тяжёлое, ему требуется неотложная медицинская помощь.
Другое частое осложнение острого лимфаденита — хроническое воспаление лимфатического узла. Заболевание может длительно протекать без симптомов, но такой лимфоузел — это «бомба замедленного действия». При переохлаждении или другом неблагоприятном воздействии защитные силы организма снижаются и вновь может начаться воспалительная реакция с последующим нагноением. Кроме того, существуют гипотезы, что хроническое воспаление приводит к раку [12].
Более редкое осложнение — нагноение лимфатического узла с образованием абсцесса или флегмоны. Флегмона — острое разлитое гнойное воспаление клетчаточных пространств. В отличие от абсцесса она не имеет чётких границ.
При флегмоне и абсцессе потребуется хирургическое вмешательство, после которого на коже могут остаться рубцы. Также при этих осложнениях в организме накапливается большое количество патогенных микроорганизмов, что особенно опасно при снижении иммунитета, например из-за ВИЧ [8].
Активное распространение инфекции в организме может приводить к тяжёлому общему осложнению — сепсису, при котором возбудитель попадает в кровь и может поразить любой орган. При сниженном иммунитете организм не справляется с инфекцией и пациент может погибнуть.
Если организм ослаблен и не может противостоять нагноению лимфатического узла, но ему удаётся не дать инфекции распространиться по организму, то очаг воспаления и здоровых тканей разграничивается. В результате образуется капсула, внутри которой накапливается гной. Со временем гноя становится больше, капсула разрывается и образуется свищевой ход, через который гной выходит наружу. Сформировавшийся свищевой ход после опорожнения абсцесса длительно заживает, и в итоге образуется грубая рубцовая ткань.
При абсцедирующем лимфадените и аденофлегмоне часто развивается тромбофлебит — опасное заболевание, при котором венозная стенка воспаляется, а в просвете сосуда образуется тромб. На фоне тромбофлебита может развиться другое серьёзное заболевание — энцефалит, или воспаление тканей головного мозга.
Диагностика шейного лимфаденита
Диагностические мероприятия при шейном лимфадените можно разделить на клинические, аппаратные и лабораторные.
Клиническое обследование
Сбор жалоб: пациент обычно отмечает боли в области поражённого лимфатического узла, признаки общей интоксикации организма и симптомы основного заболевания.
Изучение анамнеза: врач выясняет интенсивность, характер течения и время появления симптомов. Также он узнаёт о социально-бытовых условиях жизни пациента, иммунном статусе, наличии хронических и вирусных заболеваний.
Клинический осмотр: оценивается симметричность лица и шеи, наличие отёчности и покраснения. Все шейные лимфатические узлы ощупываются с обеих сторон. Если выявлен изменённый лимфоузел, то врач описывает его форму, консистенцию, размер, поверхность, расположение, болезненность, подвижность при попытках смещения и состояние симметричного лимфоузла.
Все лимфатические узлы подразделяются на два вида:
- поверхностные — залегают в подкожно-жировой клетчатке или под ней;
- глубокие — расположены в толще мышц и рядом с внутренними органами.

Шейные лимфоузлы в основном относятся к поверхностным, лишь некоторые из них расположены под мышцами. Поверхностное расположение облегчает диагностику — зачастую воспалённый узел визуально заметен без дополнительных методов.
Аппаратные методы
К ним относятся ультразвуковое исследование (УЗИ), компьютерная томография (КТ) и магнитно-резонансная томография (МРТ).
Ультразвуковая диагностика основана на способности звуковых волн отражаться от разных структур организма.
На УЗИ выявляют:
- расположение, форму, размеры, количество и структуру лимфатических узлов;
- спайки и сращения лимфатического узла с окружающими тканями;
- воспаление в лимфатических сосудах и окружающих тканях.
Метод компьютерной томографии использует рентгеновское излучение. При помощи аппарата КТ делаются послойные снимки, а компьютерная программа собирает их в трёхмерное изображение.
Компьютерная томография позволяет:
- изучить точное расположение, количество, форму и структуру лимфатических узлов;
- выявить очаги некроза или склероза — замещения нормальной ткани соединительной;
- обнаружить сращения лимфатического узла с окружающими тканям;
- выявить воспалительные изменения окружающих тканей;
- обнаружить патологическую жидкость и включения.

При проведении КТ черепа можно выявить причины заболевания, например воспаление в области внутреннего уха, в тканях, окружающих зуб, и в полости верхнечелюстной пазухи.
МРТ схожа с КТ, однако точнее и безопаснее, так как проводится без рентгеновского излучения.
Лабораторные методы- Тесты для выявления возбудителя — основной метод при диагностике специфического лимфаденита.
- Общий анализ крови — особое внимание уделяется показателям СОЭ (скорости оседания эритроцитов), количеству лейкоцитов и их процентному соотношению. Признаки воспаления: СОЭ выше 15 мм/ч и уровень лейкоцитов более 9 x 109.
- Биопсия. При пункционной биопсии материал забирают из поражённого лимфоузла полой иглой. При тонкоигольной аспирационной биопсии применяют тонкую иглу и стерильный шприц. Игла вводится в лимфатический узел, и происходит забор тканей. Чтобы исключить забор тканей вне узла, часто процедуру проводят под контролем УЗИ.

Дифференциальная диагностика
Лимфаденит следует отличать от изменений лимфатических узлов при злокачественных опухолях [9].
Лечение шейного лимфаденита
Устранение первичного очага инфекцииК шейному лимфадениту часто приводит острый или обострившийся периодонтит и осложнения запущенного кариеса, например острый гнойный периостит.
Если зуб можно сохранить, то корневые каналы очищают и пломбируют. Если восстановить зуб невозможно, то его удаляют. При сформировавшемся гнойном очаге больной зуб лечат или удаляют, абсцесс вскрывают. Если шейный лимфаденит развился из-за заболевания ЛОР-органов, также следует устранить очаг острого воспаления.
Медикаментозная терапия- Антибактериальная терапия. Обычно применяются антибиотики широкого спектра, в основном с бактерицидным действием. Компоненты таких препаратов разрушают клеточную стенку бактерии или нарушают процессы её обмена веществ, что приводит к гибели микроба. Если состояние пациента не улучшается, исследуют биологический материал, полученный из лимфатического узла, и выявляют чувствительность микроорганизмов к лекарствам.
- Противовирусные препараты применяются при вирусном происхождении лимфаденита, например при герпесе.
- Противовоспалительные препараты подавляют воспаление на клеточном уровне, уменьшают боль и снижают температуру.
- Антигистаминные препараты уменьшают проницаемость капилляров, что предупреждает развитие отёков и застойных процессов. Также они не дают лейкоцитам проникнуть в очаг поражения и угнетают выработку веществ, способствующих развитию воспаления.
- УВЧ (ультравысокочастотная терапия) направлена на уменьшение отёчности, воспаления и боли.
- Ультразвук применяют, чтобы ускорить разрешение воспалительного процесса.
- УФО (ультрафиолетовое облучение) показан для уменьшения воспаления.
- Лазерная терапия направлена на уменьшение боли, улучшение питания и кровоснабжения поражённого участка.
- Электрофорез — метод, при котором лекарственное вещество проникает в ткани с помощью постоянного электрического тока. При лимфаденитах обычно проводится электрофорез с йодидом калия и протеолитическими ферментами.
- Магнитотерапия направлена на снижение боли, воспаления, отёчности и застойных процессов в тканях.
Физиотерапевтические методы применяют в России для уменьшения сроков медикаментозного лечения, однако научно обоснованных доказательств их эффективности недостаточно.
Хирургическое вмешательствоВскрытие гнойного очага показано при гнойной форме лимфаденита и аденофлегмоне. В зависимости от размеров очага операция проводится под местной или общей анестезией. При хирургическом вмешательстве гнойное содержимое и ткани распавшегося лимфатического узла удаляются.
После хирургической обработки в рану помещают дренаж, который обеспечивает отток гноя и не даёт краям раны срастаться. Затем рану обрабатывают, обновляют её края и ушивают.
Дезинтоксикационная терапияСнижает уровень токсинов в организме путём их разведения, поглощения продуктов распада и усиления диуреза. Для этого пьют больше жидкости, а при тяжёлом состоянии внутривенно вводят «Гемодез» и «Реоглюман».
ДиетаРекомендовано сбалансировано питаться и потреблять достаточно витаминов, макро- и микроэлементов.
Особенности лечения лимфаденита
Лечение шейного лимфаденита напрямую зависит от стадии и формы заболевания.
При остром серозном лимфадените особое внимание уделяется первичному очагу воспаления: воспалительным заболеваниям зубов, полости рта и ЛОР-органов. Если первичный воспалительный процесс остановить на ранних стадиях, то симптомы острого серозного лимфаденита также становятся менее выраженными.
Почти в 98 % случаев при остром лимфадените удаётся выявить первичный очаг поражения [10]. Его устраняют и назначают антибактериальную, противовирусную, противовоспалительную или антигистаминную терапию.
При развитии гнойной формы устраняют первичный очаг, вскрывают гнойник и удаляют ткани распавшегося лимфоузла. Пациент обычно находится в больнице под круглосуточным наблюдением. Проводятся ежедневные перевязки, назначают антибактериальную, противовоспалительную, антигистаминную и дезинтоксикационную терапию.
При хроническом гиперпластическом лимфадените поражённый лимфатический узел удаляют, лечение также проводится в больнице. Фрагменты тканей отправляют в лабораторию, обрабатывают и исследуют под микроскопом. Эта процедура позволяет исключить онкологическое заболевание и предупредить его развитие.
Прогноз. Профилактика
Прогноз благоприятный, если своевременно обратиться к врачу. Раннее лечение поможет предотвратить необратимые изменения лимфатического узла и сохранить его функции.
Для профилактики шейных лимфаденитов нужно раз в полгода посещать стоматолога.
Другие профилактические меры помогут укрепить иммунную систему и не допустить заражения.
Для этого следует:
- есть больше фруктов и овощей;
- высыпаться;
- быть физически активным;
- не курить и не злоупотреблять алкоголем;
- чаще мыть руки и тщательно готовить мясо;
- делать рекомендованные прививки;
- по возможности уменьшить стресс [11].
Увеличен лимфоузел шеи — Вопрос онкологу
Если вы не нашли нужной информации среди ответов на этот вопрос, или же ваша проблема немного отличается от представленной, попробуйте задать дополнительный вопрос врачу на этой же странице, если он будет по теме основного вопроса. Вы также можете задать новый вопрос, и через некоторое время наши врачи на него ответят. Это бесплатно. Также можете поискать нужную информацию в похожих вопросах на этой странице или через страницу поиска по сайту. Мы будем очень благодарны, если Вы порекомендуете нас своим друзьям в социальных сетях.Медпортал 03online.com осуществляет медконсультации в режиме переписки с врачами на сайте. Здесь вы получаете ответы от реальных практикующих специалистов в своей области. В настоящий момент на сайте можно получить консультацию по 71 направлению: специалиста COVID-19, аллерголога, анестезиолога-реаниматолога, венеролога, гастроэнтеролога, гематолога, генетика, гепатолога, гериатра, гинеколога, гинеколога-эндокринолога, гомеопата, дерматолога, детского гастроэнтеролога, детского гинеколога, детского дерматолога, детского инфекциониста, детского кардиолога, детского лора, детского невролога, детского нефролога, детского офтальмолога, детского психолога, детского пульмонолога, детского ревматолога, детского уролога, детского хирурга, детского эндокринолога, дефектолога, диетолога, иммунолога, инфекциониста, кардиолога, клинического психолога, косметолога, логопеда, лора, маммолога, медицинского юриста, нарколога, невропатолога, нейрохирурга, неонатолога, нефролога, нутрициолога, онколога, онкоуролога, ортопеда-травматолога, офтальмолога, паразитолога, педиатра, пластического хирурга, проктолога, психиатра, психолога, пульмонолога, ревматолога, рентгенолога, репродуктолога, сексолога-андролога, стоматолога, трихолога, уролога, фармацевта, физиотерапевта, фитотерапевта, флеболога, фтизиатра, хирурга, эндокринолога.
Мы отвечаем на 97.49% вопросов.
Оставайтесь с нами и будьте здоровы!
Увеличение шейных лимфоузлов — причины, диагностика и лечение
Увеличение шейных лимфоузлов (шейная лимфаденопатия) — это наличие на боковой и задней поверхности шеи образований лимфоидной ткани размером более 5 мм, имеющих эластичную или плотную консистенцию. Симптом наблюдается при вирусных и бактериальных инфекциях ЛОР-органов, воспалительных процессах в ротоглотке, опухолевых образованиях шеи и головы. Для выяснения причины лимфаденопатии назначают УЗИ, пункционную биопсию, лимфографию, лабораторные анализы. Симптоматику купируют с помощью нестероидных противовоспалительных препаратов, анальгетиков, антисептических средств.
Причины увеличения шейных лимфоузлов
Эта группа лимфоузлов дренирует область головы, шеи, верхней части грудной клетки, проксимальных отделов верхних конечностей. Соответственно, увеличенные шейные узлы чаще всего свидетельствуют о наличии заболеваний щитовидной железы, воспалительных процессов в ротоглотке, бактериальных и вирусных инфекций. Симптом патогномоничен для краснухи, развивается при кори, может выявляться при более редких инфекционных патологиях — орнитозе, лихорадке Эбола и Марбург, микоплазменных инфекциях.
Рак щитовидной железы
Неоплазии щитовидки составляют около 1,5% от всех злокачественных новообразований и в большинстве случаев протекают бессимптомно. Наиболее типичным вариантом является папиллярный рак. Достаточно распространены фолликулярные опухоли. При этих объемных образованиях всегда происходит увеличение шейных лимфоузлов, что свидетельствует об усиленной пролиферации злокачественных тиреоцитов, метастазировании опухолевых клеток. Обычно лимфатический узел долгое время остается мягким и подвижным, поскольку процесс не затрагивает капсулу и окружающие ткани.
Пациенты, как правило, обращаются к врачу по поводу случайно обнаруженного узла в щитовидной железе, когда он достигает 1 см и более. По мере роста опухоли присоединяются другие проявления: кашель, охриплость голоса, связанные с компрессией соседних анатомических структур. Большие новообразования способны сдавливать дыхательные пути, вызывая одышку и удушье. При распространении рака за пределы капсулы органа возникает расширение подкожной венозной сети, деформация контуров шеи. У пожилых больных нарастает кахексия.
Шейная лимфаденопатия служит одним из признаков лимфомы щитовидной железы — агрессивной неоплазии, отличающейся интенсивным ростом и вовлечением в патологический процесс соседних органов. Болезнь чаще развивается на фоне аутоиммунного тиреоидита. Опухоль быстро растет, занимая целую долю органа. Пациенты зачастую сами обнаруживают узел деревянистой плотности, который сочетается с увеличением и уплотнением шейных лимфоузлов на стороне поражения. Компрессия окружающих тканей провоцирует дисфагию, парез голосовых связок, смещает пищевод и трахею.
Органические заболевания щитовидной железы
При других поражениях эндокринной железы увеличение лимфоузлов обусловлено повышением кровотока в 10-15 раз, усилением продукции и дифференцировки нормальных лимфоцитов в ответ на стимуляцию чужеродными антигенами. Размеры лимфатических узлов составляют более 1 см, они эластичные, не спаянные с окружающими тканями, иногда бывают чувствительными при пальпации. Симптом характерен для острых воспалительных процессов, однако встречается и при доброкачественных новообразованиях, хроническом аутоиммунном тиреоидите. К шейной лимфаденопатии приводят:
- Острый тиреоидит. Болезнь начинается внезапно с резкой боли в области щитовидной железы, которая иррадиирует в нижнюю челюсть, ухо. Лимфатические узлы увеличиваются с двух сторон, становятся очень болезненными, отмечается покраснение кожи. Гнойный тиреоидит протекает с повышением температуры до фебрильных цифр, выраженными симптомами интоксикации. Возможны жалобы на чувство давления и распирания в шее, усиление симптомов при кашле.
- Узлы и кисты. По данным статистики, различные доброкачественные образования щитовидной железы выявляются у 10% населения, но чаще протекают бессимптомно. Увеличение лимфоузлов в шейной области происходит при воспалении или нагноении кист, гормонально активных неоплазиях. Лимфатические узлы эластичные, практически безболезненные, кожа над ними не изменена. Развернутая клиническая картина поражения щитовидки наблюдается при гиперпродукции гормонов — тиреотоксикозе.
Краснуха и корь
Шейная лимфаденопатия с вовлечением в процесс заднешейных и затылочных узлов является важным симптомом краснухи. Лимфатические узлы умеренно увеличены в размерах, безболезненны, не спаяны с окружающей кожей. Для детей типично появление «картечных» лимфоузлов — множественных мелких образований на шее. Одновременно с лимфаденопатией возникает сыпь — мелкоточечные или папулезные высыпания локализуются на разгибательных поверхностях конечностей, в области туловища и головы. Сыпь исчезает через несколько дней, не оставляя шелушения и пигментации.
Лимфаденит с увеличением шейных лимфоузлов развивается в катаральной стадии кори. Лимфаденопатия сочетается с ринитом, конъюнктивитом, гиперемией зева и одутловатостью лица. У взрослых проявления катарального периода выражены слабее. Патогномоничный признак кори — пятна Бельского-Филатова-Коплика на слизистой щек. Через 4-5 дней начинается вторая волна лихорадки, которая совпадает с появлением пятнисто-папулезной сыпи. В 1-й день высыпания расположены на лице и шее, к концу первых суток распространяются на туловище, на третий день сыпь переходит на конечности.
Другие инфекционные болезни
Шейная лимфаденопатия выявляется при различных инфекциях, протекающих в полости рта, ЛОР-органах. Возможно проявление симптома при системных бактериальных и протозойных поражениях — ангинозно-бубонной форме туляремии, сонной болезни, дифтерии. Увеличение лимфатических узлов связано с первичным проникновением и размножением патогенных микроорганизмов, интенсивной пролиферацией и накоплением специфических клонов лимфоцитов в фолликулярной и паракортикальной зонах. С поражением шейных лимфоидных образований протекают:
- Врожденный листериоз. Инфекционная патология развивается при трансплацентарном или интранатальном инфицировании ребенка и проявляется в первые дни после рождения. Поражение шейных узлов сочетается с фебрильной температурой тела, розеолезной или геморрагической сыпью, гранулемами на слизистой полости рта. Поздняя форма сопровождается мышечным тремором, судорожным синдромом, увеличением печени и селезенки.
- Сифилис. После попадания в организм бледная трепонема размножается в регионарных лимфоузлах, вызывая их увеличение. Шейная лимфаденопатия часто наблюдается при проникновении возбудителя через слизистую оболочку ротовой полости или губ, где и локализуется первичный аффект — твердый шанкр. Спустя месяц шанкр исчезает самостоятельно, затем появляется полиморфная сыпь, что указывает на генерализацию инфекции и развитие вторичного сифилиса.
- Бруцеллез. В продромальном периоде пациенты жалуются на миалгии, артралгии, головные боли. Потом возникает лихорадка, длящаяся от нескольких дней до 3 недель и чередующаяся с проливными потами. На высоте температуры отмечается гиперемия лица, увеличение шейных и подмышечных лимфатических узлов, которые могут быть болезненными при пальпации. При острой форме появляются мелкие фиброзные образования по ходу сухожилий.
- Паховый лимфогранулематоз. Увеличение лимфоузлов шеи и подчелюстной области отмечается во вторичном периоде при локализации первичного аффекта (язвы) в области слизистой рта и глотки. По мере прогрессирования болезни лимфоидные образования превращаются в крупнобугристые опухоли, теряют подвижность. В дальнейшем узлы нагнаиваются, присоединяются лихорадка, интоксикация, формируются свищи.
- Тонзиллит, фарингит. Реакция шейных лимфоузлов выявляется при тонзиллитах, что обусловлено повышенной антигенной стимуляцией лимфоидных образований. Симптом сопровождается болями в горле, покраснением зева и миндалин, лихорадкой. На поверхности гланд можно заметить желтоватые точки или распространенный налет. Увеличение лимфоузлов также обнаруживается при герпетическом фарингите, для которого характерна везикулярная сыпь на слизистой глотки.
Тяжелые случаи тонзиллита могут осложниться заглоточным абсцессом — гнойным воспалением клетчатки глотки. Кроме лимфаденопатии верхних шейных и затылочных лимфатических узлов пациента беспокоят резкие боли в горле, затруднение глотания, при больших размерах гнойника возможны расстройства дыхания. Общее состояние нарушено, температура тела повышается до 39-40° С. Увеличение лимфоузлов, сочетающееся с поражением яремной вены и септицемией, патогномонично для синдрома Лемьера. У детей шейная лимфаденопатия зачастую свидетельствует об аденоидите.
Опухоли головы и шеи
Лимфа от лица и шеи попадает непосредственно в шейные лимфоузлы, поэтому при различных злокачественных образованиях этой зоны они являются типичным местом метастазирования. Лимфатические узлы обычно деревянистой плотности, плотно соединены с кожей и окружающей клетчаткой, малоболезненны. Лимфаденопатия при определенных видах опухолей служит начальным признаком заболевания, когда первичное новообразование еще не вызывает клинической симптоматики. Увеличение лимфоузлов наблюдается при таких злокачественных неоплазиях, как:
- Новообразования челюстей. Опухоль может характеризоваться экзофитным ростом с формированием выступающего узла с изъязвлениями. Возможно протекание по типу длительно незаживающей язвы с гнойно-сукровичным отделяемым. О поражении костей (остеосаркоме) свидетельствуют простреливающие боли, расшатывание и выпадение зубов. Лимфоузлы увеличены с обеих сторон, имеют каменистую плотность, спаяны с кожей, подкожной клетчаткой.
- Рак языка. Хотя при неоплазиях этой локализации чаще отмечается увеличение подчелюстных лимфоузлов, иногда метастазирование происходит и в шейную группу. Неоплазия языка внешне выглядит как диффузное уплотнение органа с формированием язв или локальным выростом ткани. Рано появляется болевой синдром, выражены нарушения приема пищи, прогрессирует исхудание.
- Новообразования ЛОР-органов. Шейная лимфаденопатия — симптом эпителиальных опухолей носоглотки, которые также проявляются носовыми кровотечениями, затруднением дыхания. Симптом определяется при эстезионейробластоме и сочетается с аносмией, заложенностью носа, слизистыми выделениями. Иногда одностороннее увеличение и уплотнение лимфатических узлов указывает на неоплазии уха (базалиомы, эпителиомы, саркомы).
- Опухоли глаз. Увеличенные узлы наблюдаются при запущенной стадии новообразований конъюнктивы, когда злокачественные клетки прорастают в окружающие ткани, распространяются лимфогенным и гематогенным путями. Увеличение лимфоузлов подчелюстной области и шеи встречается при меланоме глаза — агрессивном новообразовании пигментных клеток, которое быстро прогрессирует с развитием отдаленных метастазов.
- Тимома. Увеличение шейных лимфоидных структур выявляется при доброкачественных и злокачественных опухолях вилочковой железы. Инвазивный рост новообразования вызывает компрессионный синдром с интенсивными загрудинными болями, сухим кашлем, затруднением дыхания. При сдавлении периферических нервов возникает синдром Горнера, осиплость голоса, дисфагия. Около 30% случаев болезни сопровождаются миастенией.
Системные поражения лимфоидной ткани
Увеличенные лимфоузлы шеи могут стать первым признаком лимфогранулематоза — злокачественной гиперплазии лимфоидной ткани с образованием специфических гранулем. Для заболевания характерно появление плотных безболезненных узлов, которые располагаются в виде цепочки. При локальной форме поражения происходит увеличение одной группы лимфатических узлов, при генерализованной форме развивается тотальная лимфаденопатия с поражением внутренних органов. Шейные лимфоузлы поражаются при хроническом лимфолейкозе, аутоиммунном лимфопролиферативном синдроме.
Обследование
Увеличение шейных лимфоузлов, которое не сопровождается другими симптомами, является показанием для консультации гематолога. При сочетании лимфаденопатии с признаками поражения органов дыхательной, пищеварительной систем могут потребоваться консультации других специалистов. Диагностика предполагает оценку состояния патологически измененных лимфоузлов и выявление причины состояния. Наиболее ценными являются:
- Ультразвуковое исследование. УЗИ лимфоузла проводится для изучения морфологической структуры пораженной ткани, метод позволяет обнаружить гиперэхогенные и гипоэхогенные зоны. Дополнительно рекомендованы УЗИ щитовидной железы и сонография вилочковой железы для выяснения первопричины лимфаденопатии.
- Анализы крови. Инфекционные и гематологические болезни, при которых возможно увеличение шейных лимфатических узлов, характеризуются изменениями показателей крови. Пациентам назначают стандартный общий анализ, биохимическое исследование, определение уровня острофазовых показателей.
- Биопсия лимфоузла. Забор цитологического материала из пораженного органа с последующим гистологическим исследованием рекомендован для верификации диагноза. Метод преимущественно используется для дифференциальной диагностики злокачественных опухолей лимфоидной ткани и метастазов с другими заболеваниями.
- Лимфография. Радионуклидное исследование лимфатической системы при помощи введения специального радиофармпрепарата назначают для изучения путей лимфооттока и исключения онкопатологии. Метод широко применяется для зоны шеи, поскольку проведение стандартной рентгенографии затруднено.
Дальнейший список исследований формируется с учетом жалоб пациента. Часто требуется обследование верхних отделов дыхательных путей — фарингоскопия, риноскопия, ларингоскопия. Для подтверждения инфекционной этиологии процесса выполняют специфические серологические реакции (РИФ, ИФА, ПЦР). При подозрении на связь поражения шейных лимфатических структур с патологией щитовидной железы проводят анализ крови на трийодтиронин и тироксин, сцинтиграфию с радиоактивным йодом.
Симптоматическая терапия
При инфекционных заболеваниях с поражением зева для снятия локальных симптомов рекомендованы полоскания горла раствором антисептиков, полезны ингаляции и обильное теплое питье. Для купирования болей в области шеи и ЛОР-органов назначаются нестероидные противовоспалительные средства, анальгетики. Этиотропное лечение подбирается только после консультации специалиста. При сочетании шейной лимфаденопатии с фебрильной лихорадкой, пальпируемыми образованиями области головы, шеи, быстрым ухудшением общего состояния необходимо как можно скорее обратиться к врачу.
Лимфоузлы под контролем
Лимфоаденопатия – это не самостоятельное заболевания, а состояние, которое сопровождает активизацию иммунной системы организма. Помните, ещё наши бабушки и про бабушки все рассказывали про желёзки, которые воспалились у кого-то в детстве. Так это и была она самая лимфоаденопатия. Раньше лимфоузлы ошибочно считали железами, что и закрепилось в название ( Aden -это железа).
Лимфоаденопатия может быть визитной карточкой самых разных заболеваний. Именно поэтому врачу часто трудно без обследования объяснить причину её возникновения. Первую оценку состояния лимфоузлов доктор проводит при ощупывании. У здоровых деток они овальные, мягкие и упругие, не больше горошины в диаметре. Обычно прощупывается единичные узелки в двух-трёх местах. К годовалому возрасту две – три группы лимфоузлов можно найти почти у всех здоровых малышей. Обычно лимфотические узлы прощупываются, только если они увеличены. Группы из узелков располагаются в местах слияния крупных сосудов, собирающих особую жидкость – лимфу, она обеспечивает обмен веществ между кровью и тиканьями организма. Основные из них возле ушей, вокруг шеи, в подмышечных ямках и в паху. Отсюда названия групп: затылочные, области сосцевидного отростка, подбородочные, подчелюстные передние и заднешейные, над- и подключичные, подмышечные, грудные, локтевые, паховые и бедренные.
Что от чего? Ищите причину!
Изолированое увеличение в одной области (врачи говорят «увеличение регионарных лимфоузлов), обусловлено изменениям в соответствующей зоне тела, откуда поступает лимфа.
Затылочные: лимфатические узлы обнаруживают при воспалительных процессах волосистой части головы (гнойная сыпь, фурункулы, грибковое поражения и пр).
Лимфоузлы за углом нижней челюсти и по ходу задних мышц шеи: прощупываются при воспалительных процессах в носоглотке или после ангины, при инфекционном мононуклеозе, при хроническом тонзиллите и аденоидных расстояниях, при туберкулёзе миндалин. При дифтерии миндалин происходит симметричное увеличение до больших размеров (вплоть до среднего яблока). Развивается отёк окружающих тканей с утолщением шеи. В случаи тяжелого течения ангины может развиться острое воспаления – лимфаденит и даже его гнойное поражения.
Сочетания ангины, лимфаденита и шелушение ладоней и стоп характерно для стрептококковой инфекции (стрептококковая ангина, скарлатина).
Лимфоузлы в подборочной зоне увеличиваются при абсцессе в участках челюсти, при поражение передних зубов (резцов) стоматите, воспаление нижней губы.
Лимфоузлы под нижней челюстью опухают при воспаление челюсти из-за поражение зубов, стоматита и гингивита (воспаление дёсен).
Лимфоузлы в подмышечных впадинах прощупываются при заболеваниях различной причины в области руки и плеча (гнойное поражение кожи, ветряная оспа). Одностороннее увеличение может развиться после проведения вакцинации или повреждение руки, при «болезни кошачьей царапины.
Локтевые лимфоузлы страдают при инфекциях кисти и предплечья.
Лимфоузлы в паху прощупываются при повреждение кожи ног и стоп. Бывает так, что ранка уже затянулась и все успевают забыть о том, что она была. Но инфекция, попав в лимфу, никуда не исчезает и незаметно «облюбовывает» какой — нибудь ближайший лимфоузел. Если организм справляется сам, то припухлость проходит через некоторое время. Однако порой начинается нагноение, и тогда требуется помощь хирурга. Этот симптом появляется при воспаление суставов, дерматита, при фурункулезе в ягодичной области, после вакцинации БЦЖ при введение в бедро.
Смотрим со всех сторон
При обнаружение одного нескольких увеличенных лимфоузлов надо тщательно осмотреть ребёнка и скользящими движениями пальцев прощупать другие зоны. Ищите узелки через тонкую шелковую ткань, имитируя игру, чтобы не пугать малыша. Обратите внимание на подвижность узелка и их несоединенность между собой и с кожей. Врачи обычно говорят: «спаяны» (или «не спаяны») с окружающими тканями. Подборобные, подключичные, грудные, локтевые, лимфоузлы в норме не прощупываются. Если узлы сильно увеличены, ребёнок сам обратит на это ваше внимание. Появление каких-либо отклонений или болезненности в области лимфоузлов – повод для обращения к врачу.
Ни в коем случае без осмотра доктора нельзя греть увеличенные лимфоузлы!
При чём здесь кошки?
Лимфоузлы увеличиваются и при так называемой «болезни кошачьей царапины» (доброкачественном лимфоретикулёзе). Причем припухают лимфоузлы той области, где находятся ворота инфекции. Спустя некоторое время после неудачной игры с кошкой может начаться ангина, подняться температура. Сами кошки не белеют, они только носят инфекцию на лапах, под когтями. Чтобы избежать заражения, нужно обязательно обработать рану йодом, понаблюдать, пока не заживёт. Если малыш заболел, обратитесь к доктору. Возбудители другой инфекции попадают в организм ребёнка через пищеварительный тракт. У малыша увеличиваются лимфоузлы, держится невысокая температура, иногда опухают, слезятся глаза. Всё это признаки токсоплазмоза, которые лечат в Москве в Центре токсоплазмоза при больнице им. Боткина.
Если узел не уходит…
Если лимфоаденопатия вызвана инфекцией, то после лечения антибиотиками лимфоузлы быстро уменьшаются и восстанавливают свою подвижность при ощипывании. На этом основан диагностический приём, который врачи называют ех juvantbus , что означает диагностика по эффективности лечения. Если при изолированным увеличение какой — либо группы лимфоузлов причины выявить не удаётся, назначают антибиотики курсом на 8-10 дней. Улучшение состояния ребёнка и уменьшение лимфоузлов расценивают как подтверждение бактериальной природы заболевания.
А кроме инфекции?
Поствакцинальная лимфоаденопатия. Изолированное увеличение лимфоузлов в течение 3 месяцев после ведения БЦЖ – норма. Более длительное сохранение симптома может быть косвенным признаком снижения активности иммунной систем.
Вирусные заболевание
Многие заболевание начинаются с увеличения лимфоузла в какой-либо одной зоне, а затем они увеличиваются практически во всех группах. Такая картина наблюдаются при вирусной агрессии – гриппе, крови, краснухе, инфекционном мононуклеозе, вирусной пневмонии, вирусом гепатите, распространённой экземе, врожденном токсоплазме. Могут вызвать лимфоаденопатию и аденовирусные инфекции, именно те, которые скрываются за обширным термином ОРВИ.
Опухолевые процессы и особые нарушения обмена вещества: становятся причиной чуть реже. Лимфоузлы — одна из первых линий обороны против проникновения различных чужеродных агентов.
К увеличению лимфоузлов склоны, как правило, полные, рыхлые дети. Порой припухание узлов у них проходит, не отражаясь на состоянии организма. Причина его не всегда может быть выяснена. Бить тревогу надо, если увеличение держится слишком долго, а узел болезненный и достаточно велик — например, размером с грецкий орех. Нужно обратиться к специалистам, и они выяснят причину появления инфекции. Иногда она может быть самой банальной. Особого внимания требуют одиночные воспалённые узлы, плотные на ощупь. Таких больных, как правило, направляют на приём к онкологу.
Береженого…
Кроме лимфоузлов приподнимать кожу и прощупываться под кожей могут и другие образование.
Например, лимфангиома – мягкая припухлость под кожей без чётких границ. Чаще она бывает на шее, может вызывать затруднения при родах, при глотании и дыхании и нередко требует хирургического лечения.
Даже если, с вашей точки зрения, никаких причин для беспокойства нет, все же лучше перестраховаться и не затягивать визит к доктору. Ведь существует косвенные признаки распространения болезни, которые трудно оценить без специального обследования.
Например, длительная частая икота, нарушения глотания и дыхания в определенных положениях тела могут быть признаками увеличения внутригрудных лимфоузлов. А частые боли в животе сигнализировать об увеличение внутрибрюшных. В ряде случаев диагноз трудно поставить не только по жалобам ребёнка и родителей, данным осмотра, но и по анализам. В таких случаях проводятся УЗИ для определения состояния печени, селезёнки, лимфоузлов брюшной полости, рентгенологические исследования, турберкулиннодиагностика для исключения скрыто протекающего туберкулёза. При подозрение на токсоплазмоз, герпесы, цитомегаловирусы, вирус Эпштейн – Бар берут кровь для проведения специальных серологических исследований. В самых трудных для диагностики случаях делается биопсия лимфатического узла или его пункция с исследованием под микроскопом. Вы способны существенно облегчить постановку правильно диагноза, если точно сообщите врачу, когда впервые заметили увеличение лимфоузлов, каковы были сопутствующие симптомы и обстоятельства (совпадения с поездками, употребление экологических блюд, контакты с заболевшими людьми).
Плотность лимфатических узлов является прогностическим фактором у пациентов с карциномой большой слюнной железы
Oncol Lett. 2015 Dec; 10 (6): 3523–3528.
HIDENORI SUZUKI
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
НОБУХИРО ХАНАЙ
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя 464681, Аичи , Япония
HITOSHI HIRAKAWA
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
ДАЙСУКЕ НИСИКАВА
Отделение хирургии головы и шеи, Больница онкологического центра Аичи, Нагоя, 464 -8681, Япония
ЯСУХИСА ХАСЕГАВА
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
Отделение хирургии головы и шеи, Больница онкологического центра Аити, Нагоя, Аити 464-8681 , Япония
Переписка на номер : д-р Хиденори Судзуки, отделение хирургии головы и шеи, больница онкологического центра Айти, 1-1 Канокоден, Тикуса-ку, Нагоя, Аити 464-8681, Япония, электронная почта: пиджей[email protected]Поступила в редакцию 11 ноября 2014 г .; Принято 18 сентября 2015 г.
Эта статья цитировалась в других статьях в PMC.Abstract
Сообщалось, что плотность лимфатических узлов (LND) является важным показателем выживаемости у пациентов с карциномами полости рта и другими карциномами с положительными лимфатическими узлами. В настоящем исследовании изучали, связана ли LND с общей выживаемостью у субъектов с большой карциномой слюнных желез. В общей сложности 78 пациентам с впервые диагностированной карциномой большой слюнной железы была выполнена резекция первичной опухоли и рассечение шеи без предоперационного лечения.Из этих 78 пациентов 32 с патологически положительными лимфатическими узлами были включены в настоящее исследование. LND рассчитывали как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов. Выживаемость анализировали по методу Каплана-Мейера. Одномерный анализ выживаемости был выполнен с использованием лог-рангового теста, а многомерный анализ выживаемости был выполнен с использованием модели пропорциональных рисков Кокса. Было обнаружено, что LND ≥0,38 достоверно коррелирует с более коротким общим временем выживания в однофакторном анализе (P = 0.017). В многофакторном анализе выживаемости после поправки на анатомическое расположение (околоушная железа / другие) было выявлено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Эти результаты предполагают, что LND функционирует как прогностический фактор в случаях рака большой слюнной железы.
Ключевые слова: плотность лимфатических узлов, карцинома основной слюнной железы, общая выживаемость
Введение
Основные карциномы слюнных желез, которые отличаются от карцином околоушных желез, поднижнечелюстных и подъязычных желез, являются редкими злокачественными опухолями. <5% всех случаев рака головы и шеи (1).Гистологическая классификация основных карцином слюнных желез включает 24 гистологических подтипа с различными злокачественными фенотипами и прогнозами в соответствии с классификацией опухолей Всемирной организации здравоохранения 2005 г. (2). На сегодняшний день в многочисленных исследованиях изучались характеристики и полезные прогностические параметры рака основной слюнной железы с использованием различных подходов, включая клинические, патологические и биологические процедуры (1–4).
Плотность лимфатических узлов (LND), которая рассчитывается как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов, надежно предсказывает выживаемость пациентов с плоскоклеточным раком полости рта (OSCC). карцинома мочевого пузыря и другие карциномы с положительными лимфатическими узлами шеи в недавних исследованиях (5–12).Однако связь между LND и общей выживаемостью у людей с большой карциномой слюнных желез еще не исследована. В настоящем исследовании изучали, коррелирует ли LND с общей выживаемостью в случаях рака большой слюнной железы с положительными лимфатическими узлами.
Пациенты и методы
Данные по населению
В общей сложности 284 пациента с впервые диагностированной большой опухолью слюнной железы в отделении хирургии головы и шеи больницы онкологического центра Аити (Нагоя, Япония) прошли резекцию опухоли в период с января 2004 года по май. 2014; У 93 из этих пациентов при патологическом обследовании была диагностирована первичная карцинома большой слюнной железы.Из этих 93 пациентов 80 были подвергнуты резекции первичной опухоли с рассечением шеи, а у 34 были диагностированы патологические метастазы в лимфатических узлах. Из исследования были исключены один пациент, получавший предоперационную химиотерапию, и один пациент, ранее получавший лучевую терапию по поводу карциномы носоглотки. Таким образом, в исследование были включены 32 пациента с патологически положительными лимфатическими узлами. Этот протокол исследования был одобрен наблюдательным советом больницы онкологического центра Айти, и все пациенты предоставили свое информированное согласие на все виды лечения и обследования.Анатомическое расположение первичной опухоли было следующим: околоушная железа — 21 пациент; подчелюстная железа — 10 пациентов; и подъязычная железа — 1 пациент.
Стадия метастазов в опухолевых узлах (TNM)
При первом посещении были выполнены плановое физикальное обследование и рентгенография грудной клетки. Клиническая стадия определялась по результатам этих обследований, а также по результатам улучшенной компьютерной томографии (КТ) шейки матки или магнитно-резонансной томографии. По возможности выполнялась позитронно-эмиссионная томография с 18F-2-фтордезоксиглюкозой (ПЭТ с 18F-FDG) или ПЭТ с 18F-FDG в сочетании с КТ.Клинические данные о метастазах в лимфатические узлы, обнаруженные на усиленной КТ, включали наличие кольцевидного усиления или диаметр лимфатического узла ≥10 мм. Использовались критерии классификации TNM Международного союза против рака (седьмое издание) (13).
Патологическое обследование
Рассечение шеи, как описано Японской исследовательской группой по расслоению шеи, выполнялось единым блоком (14). После тщательного разделения образцов шеи по шейному отделу было зарегистрировано общее количество лимфатических узлов.Образцы и записи использовались при патологическом исследовании. В соответствии с процедурой, описанной в нашем предыдущем отчете, образцы резецированных опухолей фиксировали формалином и заливали парафином (3). Патологический диагноз (патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологический класс, положительный хирургический край и экстракапсулярное распространение) был поставлен двумя патологами, которые составили все отчеты.
Послеоперационная терапия
После патологического диагноза послеоперационная терапия проводилась у пациентов с положительным хирургическим краем, экстракапсулярным распространением, множественными положительными лимфатическими узлами или карциномой высокой гистологической степени, где это было возможно.По окончании лечения пациенты наблюдались в поликлинике. Были предприняты усилия для выявления лиц с ранним местно-регионарным рецидивом и проведения в таких случаях радикальной терапии. Клинико-патологические параметры пациентов представлены в.
Таблица I.
Клинико-патологические параметры (n = 32).
| Параметр | Значение | ||
|---|---|---|---|
| Возраст, лет | |||
| Среднее ± SD | 61.8 ± 15,1 | ||
| Пол, n | |||
| Мужской | 25 | ||
| Женский | 7 | ||
| Клиническая классификация T, n | |||
| T1 | 0 | ||
| T2 | 8 | ||
| T3 | 7 | ||
| T4 | 17 | ||
| Клиническая классификация N, n | |||
| N0 | 7 | ||
| N1 | 4 | ||
| N2 | 21 | ||
| N3 | 0 | ||
| Клиническая стадия, n | |||
| I | 0 | ||
| II | 2 | ||
| III | 3 | ||
| IV | 27 | ||
| Анатомическое расположение, n | |||
| околоушная железа | 21 | ||
| Поднижнечелюстная | 10 | ||
| Подъязычная | 1 | ||
| Патологическая классификация T, n | |||
| T1 | 1 | T2 | T2 | 0 |
| T3 | 13 | ||
| T4 | 18 | ||
| Патологическая классификация N, n | |||
| N0 | 0 | ||
| N1 | 8 | ||
| N2 | 24 | ||
| N3 | 0 | ||
| Патологическая стадия, n | |||
| I | 0 | ||
| II | 0 | ||
| III | 3 | ||
| IV | 29 | ||
| Гистологическая классификация, n | |||
| Аденокарцинома, если не указано иное | 14 | ||
| Карцинома слюнных протоков | 6 | ||
| Мукоэпидермоидная карцинома | 4 | ||
| Аденоидно-кистозная карцинома | 468 | Карцинома экзлеоморфная аденома | 3 |
| Плоскоклеточный рак | 1 | ||
| Гистологический класс, n | |||
| Высокий | 11 | ||
| Другие | 21 | ||
| Положительный хирургический маржа, n | |||
| Присутствие | 19 | ||
| Отсутствие | 13 | ||
| Экстракапсулярное распространение, n | |||
| Присутствие | 15 | ||
| Отсутствие | 17 | ||
| Положительный хирургический край и / или экстракапсулярное распространение, n | |||
| Наличие | 24 | ||
| Отсутствие | 8 | ||
| Послеоперационная терапия, n | |||
| Химиолучевая терапия | 2 | ||
| Излучение | 21 | ||
| Отсутствие | 9 |
LND
Всего было оценено 1346 лимфатических узлов, из которых 317 (23.6%) оказались патологически положительными. Основываясь на предыдущих исследованиях (5–12), LND рассчитывалась по следующей формуле: LND = количество положительных лимфатических узлов / общее количество иссеченных лимфатических узлов.
Статистический анализ
Статистический анализ проводился с использованием программного пакета JMP (версия 9; SAS Institute, Кэри, Северная Каролина, США). Корреляция между LND и клинико-патологическими параметрами (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) были проанализированы с использованием U-критерия Манна-Уитни.Время выживания определялось как период от операции до целевого события или даты последнего контакта; целевые события включали смертность для расчета общей выживаемости. Применяя метод, описанный в предыдущих исследованиях, метод Каплана-Мейера использовался для оценки кривых выживаемости, а различные пороговые значения LND были протестированы с использованием лог-рангового теста в одномерном анализе общей выживаемости (15, 16). Тридцать два пациента были сгруппированы в две группы на основе LND (LND ≥0,38 и <0,38), как LND 0.38 смогла статистически отличить более короткую группу выживания от более длинной в соответствии с лог-ранговым тестом в одномерном анализе выживаемости. Связь между двумя группами (LND ≥0,38 и <0,38) в отношении клинико-патологических параметров (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) сравнивали с использованием точного критерия Фишера.Модель пропорциональных рисков Кокса использовалась для многомерного анализа выживаемости. Многофакторный анализ проводился с поправкой на анатомическое расположение (околоушная железа / другие). Считалось, что P <0,05 указывает на статистически значимые различия.
Результаты
LND и клинико-патологические параметры
Медиана LND для всех пациентов составила 0,13 (диапазон 0,02–0,88). Распределение LND показано на, а ассоциации между LND и клинико-патологическими параметрами показаны на.LND достоверно коррелировал с патологической классификацией N (P <0,01), патологической стадией (P = 0,04), гистологической классификацией (P = 0,02) и экстракапсулярным распространением (P = 0,01).
Плотность лимфатических узлов и количество пациентов.
Таблица II.
Связь между LND и клинико-патологическими параметрами (n = 32).
| Параметр | n | LND (среднее ± стандартное отклонение) | P-значение a | |
|---|---|---|---|---|
| Возраст, лет | 0.07 | |||
| <65 | 16 | 0,26 ± 0,24 | ||
| ≥65 | 16 | 0,16 ± 0,23 | ||
| Пол | 0,73 | |||
| Мужской | 25 | 0,21 ± 0,22 | ||
| Женский | 7 | 0,21 ± 0,30 | ||
| Клиническая классификация Т | 0.54 | |||
| T1–3 | 15 | 0,24 ± 0,27 | ||
| T4 | 17 | 0,19 ± 0,21 | ||
| Клиническая классификация N | 0,10 | |||
| N0 | 7 | 0,11 ± 0,14 | ||
| N1–2 | 25 | 0,24 ± 0,25 | ||
| Клиническая стадия | 0.06 | |||
| I – III | 5 | 0,06 ± 0,04 | ||
| IV | 27 | 0,24 ± 0,25 | ||
| Анатомическое расположение | 0,21 | |||
| Околоушная железа | 21 | 0,24 ± 0,23 | ||
| Другие | 11 | 0,16 ± 0,25 | ||
| Патологическая классификация T | 0.83 | |||
| T1–3 | 14 | 0,21 ± 0,25 | ||
| T4 | 18 | 0,21 ± 0,23 | ||
| Патологическая классификация N | <0,01 | |||
| N1 | 8 | 0,03 ± 0,01 | ||
| N2 | 24 | 0,27 ± 0,25 | ||
| Патологическая стадия | <0.04 | |||
| III | 3 | 0,03 ± 0,01 | ||
| IV | 29 | 0,23 ± 0,24 | ||
| Гистологическая классификация | <0,03 | |||
| Аденокарцинома , БДУ | 14 | 0,33 ± 0,29 | ||
| Прочие | 18 | 0,12 ± 0,14 | ||
| Гистологический класс | 0.74 | |||
| Высокая | 8 | 0,14 ± 0,11 | ||
| Прочие | 16 | 0,25 ± 0,28 | ||
| Положительный хирургический край | 0,31 | |||
| Наличие | 19 | 0,14 ± 0,11 | ||
| Отсутствие | 13 | 0,25 ± 0,28 | ||
| Экстракапсулярное распространение | <0.02 | |||
| Наличие | 15 | 0,33 ± 0,29 | ||
| Отсутствие | 17 | 0,11 ± 0,10 | ||
| Положительный хирургический край и / или экстракапсулярное распространение | 0,07 | |||
| Присутствие | 8 | 0,08 ± 0,07 | ||
| Отсутствие | 24 | 0,25 ± 0,26 | ||
| Послеоперационная терапия | 0.90 | |||
| Присутствие | 9 | 0,28 ± 0,35 | ||
| Отсутствие | 23 | 0,18 ± 0,18 |
Общий анализ выживаемости
В конце исследования среднее Периоды наблюдения ± стандартное отклонение среди всех пациентов, 16 выживших пациентов (50,0% против всех) и 16 умерших пациентов (50,0%) составили 23,8 ± 19,6, 25,1 ± 19,9 и 22,4 ± 19,8 месяцев, соответственно. Во всей группе пациентов общая 2-, 3- и 5-летняя выживаемость составила 59.2, 43,2 и 25,9% соответственно. Применяя метод, описанный ранее, в нашем и других исследованиях (14, 15), различные пороговые значения LND были протестированы с использованием лог-рангового теста в анализе общей выживаемости. Пороговое значение 0,38 для LND имело самое низкое значение P в этих анализах () и могло использоваться для дифференциации более короткой группы общей выживаемости (LND ≥0,38, n = 8) от более длинной группы общей выживаемости (LND < 0,38, n = 24) на основе лог-рангового теста, как показано на (P = 0017). Никаких значимых ассоциаций с клинико-патологическими параметрами не наблюдалось в двух группах (LND ≥0.38 и <0,38), как показано на. Многофакторный анализ выживаемости был выполнен с поправкой на анатомическое расположение (околоушная железа / другие) для общей выживаемости. Следовательно, было подтверждено, что LND ≥0,38 ассоциируется со значительно более коротким временем выживания. Результаты многомерного анализа выживаемости представлены в.
P-значения согласно логарифмическому критерию общей выживаемости с использованием различных пороговых значений для LND у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами.LND, плотность лимфатических узлов.
Связь между LND и выживаемостью у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами (метод Каплана-Мейера). Было обнаружено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Для статистического анализа использовался лог-ранговый тест. LND, плотность лимфатических узлов.
Таблица III.
Связь между LND (≥0,38 и <0,38) и клинико-патологическими параметрами (n = 32).
| Параметр | LND ≥0.38 (n = 24) | LND <0,38 (n = 8) | Значение P a |
|---|---|---|---|
| Возраст, лет | 0,22 | ||
| <65 | 10 | 6 | |
| ≥65 | 14 | 2 | |
| Пол | 0,65 | ||
| Мужской | 18 | 7 | |
| Женский | 6 | 1 | |
| Клиническая классификация T | 0.42 | ||
| T1–3 | 10 | 5 | |
| T4 | 14 | 3 | |
| Клиническая классификация N | 0,65 | ||
| N0 | 6 | 1 | |
| N1–2 | 18 | 7 | |
| Клиническая стадия | 0,30 | ||
| I – III | 5 | 0 | |
| IV | 19 | 8 | |
| Анатомическое расположение | 0.68 | ||
| околоушная железа | 15 | 6 | |
| Другие | 9 | 2 | |
| Патологическая классификация T | 0,70 | ||
| T1–3 | 10 | 4 | |
| T4 | 14 | 4 | |
| Патологическая классификация N | 0.08 | ||
| N1 | 8 | 0 | |
| N2 | 16 | 8 | |
| Патологическая стадия | 0,55 | ||
| III | 3 | 0 | |
| IV | 21 | 8 | |
| Гистологическая классификация | 0.10 | ||
| Аденокарцинома, БДУ | 8 | 6 | |
| Другое | 16 | 2 | |
| Гистологический класс | 0,21 | ||
| Высокий | 10 | 1 | |
| Другое | 14 | 7 | |
| Положительное хирургическое поле | 0.42 | ||
| Присутствие | 13 | 6 | |
| Отсутствие | 11 | 2 | |
| Экстракапсулярное распространение | 0,11 | ||
| Присутствие | 9 | 6 | |
| Отсутствие | 15 | 2 | |
| Положительный хирургический край и / или экстракапсулярное распространение | 0.08 | ||
| Присутствие | 16 | 8 | |
| Отсутствие | 8 | 0 | |
| Послеоперационная терапия | 0,18 | ||
| Присутствие | 19 | 4 | |
| Отсутствие | 5 | 4 |
Таблица IV.
Многомерный анализ выживаемости a .
| Общая выживаемость | |||
|---|---|---|---|
| Параметр | HR | 95% CI | P-value |
| LND (≥0,38 / <0,38) | 4,02 | 1,21–13,43 | P <0,03 |
| Анатомическое расположение (околоушная / другие) | 2,81 | 0,87–12,53 | P = 0,09 |
Обсуждение
Результаты настоящего исследования продемонстрировали , впервые, что LND ≥0.38 у пациентов с карциномой большой слюнной железы с патологическими метастазами в лимфатические узлы значительно короче общей продолжительности жизни.
LND, определяемая патологическим исследованием, стала прогностическим параметром для различных типов рака, включая рак мочевого пузыря, пищевода и полости рта (5–12). Соотношение LND весит три фактора, которые могут влиять на стадию узлов: опухоль (истинное количество положительных лимфатических узлов), хирургическое (фактическое количество узлов, удаленных во время рассечения шеи) и факторы отбора проб (полнота патологического анализа) факторы (5 ).Недавно мультиинституциональная международная исследовательская группа, состоящая из 11 онкологических центров по всему миру, показала, что LND является важным показателем общей продолжительности жизни среди 4254 пациентов с OSCC (5). Кроме того, в ряде исследований сообщалось, что LND может использоваться для прогнозирования времени выживания пациентов с OSCC, получавших различные процедуры рассечения шеи, такие как одностороннее или двустороннее рассечение шеи (5–10). Настоящие результаты, демонстрирующие связь между LND и общей выживаемостью, согласуются с предыдущими данными (5-10).
Что касается рака головы и шеи, в многочисленных исследованиях сообщается о связи между LND и общей выживаемостью у пациентов с OSCC (5–9). Кроме того, Rudra и др. (10) сообщили, что LND предсказывает общее время выживания у субъектов с поражениями в различных участках головы и шеи, включая ротоглотку, ротовую полость и гортань / гортань; однако в этом исследовании не изучалась взаимосвязь между LND и общей выживаемостью у пациентов с карциномой основной слюнной железы (10).В настоящем исследовании связь между LND и общей выживаемостью оценивалась у субъектов с карциномой основной слюнной железы, демонстрируя, что LND ≥0,38 у пациентов с патологическими метастазами в лимфатические узлы значительно коррелирует с более коротким общим временем выживания.
Преобладающим ограничением текущего исследования было относительно небольшое количество субъектов в выборке. Следовательно, будущий анализ большого числа пациентов даст более статистически точные результаты с большим потенциалом их применения.
В заключение, настоящее исследование впервые продемонстрировало, что LND ≥0,38 у пациентов с карциномой большой слюнной железы с патологическим метастазированием в лимфатические узлы значительно коррелирует с более коротким общим временем выживания. Следовательно, LND является прогностическим фактором у людей с большой карциномой слюнных желез.
Выражение признательности
Настоящее исследование было поддержано Японским обществом содействия научным грантам для научных исследований (грант №247
Ссылки
1. Ettl T, Schwarz-Furlan S, Gosau M, Reichert TE. Карциномы слюнных желез. Oral Maxillofac Surg. 2012; 16: 267–283. DOI: 10.1007 / s10006-012-0350-9. [PubMed] [CrossRef] [Google Scholar] 2. Барнс Л., Эвесон Дж. В., Райхарт П., Сидранский Д., редакторы. Патология и генетика опухолей головы и шеи. Лион: IARC Press; 2005. Классификация опухолей Всемирной организации здравоохранения.[Google Scholar] 3. Окабе М., Миябе С., Нагацука Х., Терада А., Ханаи Н., Йокои М., Симозато К., Эймото Т., Накамура С., Нагаи Н. и др. Транскрипт слияния MECT1-MAML2 определяет благоприятную подгруппу мукоэпидермоидной карциномы. Clin Cancer Res. 2006; 12: 3902–3907. DOI: 10.1158 / 1078-0432.CCR-05-2376. [PubMed] [CrossRef] [Google Scholar] 4. Амит М., Наара С., Шарма К., Рамер Н., Рамер И., Агбетоба А., Глик Дж., Ян Х, Лей Д., Бьорндал К. и др. Избирательная диссекция шеи у пациентов с аденоидно-кистозной карциномой головы и шеи: международное совместное исследование.Энн Сург Онкол. 2015; 22: 1353–1359. DOI: 10.1245 / s10434-014-4106-7. [PubMed] [CrossRef] [Google Scholar] 5. Патель С.Г., Амит М., Йен Т.С., Ляо К.Т., Чатурведи П., Агарвал Дж. П., Ковальски Л. П., Эбрахими А., Кларк Дж. Р., Чернеа С. Р. и др. Плотность лимфатических узлов при раке полости рта: результаты Международного консорциума исследований результатов. Br J Рак. 2013; 109: 2087–2095. DOI: 10.1038 / bjc.2013.570. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ким С.Ю., Нам С.И., Чой С.Х., Чо К.Дж., Ро Дж.Л. Прогностическое значение плотности лимфатических узлов у пациентов с плоскоклеточным раком полости рта с положительными узлами.Энн Сург Онкол. 2011; 18: 2310–2317. DOI: 10.1245 / s10434-011-1614-6. [PubMed] [CrossRef] [Google Scholar] 7. Гил З., Карлсон Д.Л., Бойл Дж.О., Краус Д.Х., Шах Дж.П., Шаха А.Р., Сингх Б., Вонг Р.Дж., Пател С.Г. Плотность лимфатических узлов является важным предиктором исхода у пациентов с раком полости рта. Рак. 2009. 115: 5700–5710. DOI: 10.1002 / cncr.24631. [PubMed] [CrossRef] [Google Scholar] 8. Амар А., Рапопрт А., Куриони О.А., Дедивитис Р.А., Чернеа С.Р., Брандао LG. Плотность метастатических лимфатических узлов как прогностический фактор при плоскоклеточном раке языка и дна рта.Браз Дж Оториноларингол. 2012; 78: 86–90. DOI: 10.1590 / S1808-86Плотность лимфатических узлов является прогностическим фактором у пациентов с карциномой большой слюнной железы
Oncol Lett.2015 Dec; 10 (6): 3523–3528.
HIDENORI SUZUKI
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
НОБУХИРО ХАНАЙ
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя 464681, Аичи , Япония
HITOSHI HIRAKAWA
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
ДАЙСУКЕ НИСИКАВА
Отделение хирургии головы и шеи, Больница онкологического центра Аичи, Нагоя, 464 -8681, Япония
ЯСУХИСА ХАСЕГАВА
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
Отделение хирургии головы и шеи, Больница онкологического центра Аити, Нагоя, Аити 464-8681 , Япония
Переписка на номер : д-р Хиденори Судзуки, отделение хирургии головы и шеи, больница онкологического центра Айти, 1-1 Канокоден, Тикуса-ку, Нагоя, Аити 464-8681, Япония, электронная почта: пиджей[email protected]Поступила в редакцию 11 ноября 2014 г .; Принято 18 сентября 2015 г.
Эта статья цитировалась в других статьях в PMC.Abstract
Сообщалось, что плотность лимфатических узлов (LND) является важным показателем выживаемости у пациентов с карциномами полости рта и другими карциномами с положительными лимфатическими узлами. В настоящем исследовании изучали, связана ли LND с общей выживаемостью у субъектов с большой карциномой слюнных желез. В общей сложности 78 пациентам с впервые диагностированной карциномой большой слюнной железы была выполнена резекция первичной опухоли и рассечение шеи без предоперационного лечения.Из этих 78 пациентов 32 с патологически положительными лимфатическими узлами были включены в настоящее исследование. LND рассчитывали как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов. Выживаемость анализировали по методу Каплана-Мейера. Одномерный анализ выживаемости был выполнен с использованием лог-рангового теста, а многомерный анализ выживаемости был выполнен с использованием модели пропорциональных рисков Кокса. Было обнаружено, что LND ≥0,38 достоверно коррелирует с более коротким общим временем выживания в однофакторном анализе (P = 0.017). В многофакторном анализе выживаемости после поправки на анатомическое расположение (околоушная железа / другие) было выявлено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Эти результаты предполагают, что LND функционирует как прогностический фактор в случаях рака большой слюнной железы.
Ключевые слова: плотность лимфатических узлов, карцинома основной слюнной железы, общая выживаемость
Введение
Основные карциномы слюнных желез, которые отличаются от карцином околоушных желез, поднижнечелюстных и подъязычных желез, являются редкими злокачественными опухолями. <5% всех случаев рака головы и шеи (1).Гистологическая классификация основных карцином слюнных желез включает 24 гистологических подтипа с различными злокачественными фенотипами и прогнозами в соответствии с классификацией опухолей Всемирной организации здравоохранения 2005 г. (2). На сегодняшний день в многочисленных исследованиях изучались характеристики и полезные прогностические параметры рака основной слюнной железы с использованием различных подходов, включая клинические, патологические и биологические процедуры (1–4).
Плотность лимфатических узлов (LND), которая рассчитывается как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов, надежно предсказывает выживаемость пациентов с плоскоклеточным раком полости рта (OSCC). карцинома мочевого пузыря и другие карциномы с положительными лимфатическими узлами шеи в недавних исследованиях (5–12).Однако связь между LND и общей выживаемостью у людей с большой карциномой слюнных желез еще не исследована. В настоящем исследовании изучали, коррелирует ли LND с общей выживаемостью в случаях рака большой слюнной железы с положительными лимфатическими узлами.
Пациенты и методы
Данные по населению
В общей сложности 284 пациента с впервые диагностированной большой опухолью слюнной железы в отделении хирургии головы и шеи больницы онкологического центра Аити (Нагоя, Япония) прошли резекцию опухоли в период с января 2004 года по май. 2014; У 93 из этих пациентов при патологическом обследовании была диагностирована первичная карцинома большой слюнной железы.Из этих 93 пациентов 80 были подвергнуты резекции первичной опухоли с рассечением шеи, а у 34 были диагностированы патологические метастазы в лимфатических узлах. Из исследования были исключены один пациент, получавший предоперационную химиотерапию, и один пациент, ранее получавший лучевую терапию по поводу карциномы носоглотки. Таким образом, в исследование были включены 32 пациента с патологически положительными лимфатическими узлами. Этот протокол исследования был одобрен наблюдательным советом больницы онкологического центра Айти, и все пациенты предоставили свое информированное согласие на все виды лечения и обследования.Анатомическое расположение первичной опухоли было следующим: околоушная железа — 21 пациент; подчелюстная железа — 10 пациентов; и подъязычная железа — 1 пациент.
Стадия метастазов в опухолевых узлах (TNM)
При первом посещении были выполнены плановое физикальное обследование и рентгенография грудной клетки. Клиническая стадия определялась по результатам этих обследований, а также по результатам улучшенной компьютерной томографии (КТ) шейки матки или магнитно-резонансной томографии. По возможности выполнялась позитронно-эмиссионная томография с 18F-2-фтордезоксиглюкозой (ПЭТ с 18F-FDG) или ПЭТ с 18F-FDG в сочетании с КТ.Клинические данные о метастазах в лимфатические узлы, обнаруженные на усиленной КТ, включали наличие кольцевидного усиления или диаметр лимфатического узла ≥10 мм. Использовались критерии классификации TNM Международного союза против рака (седьмое издание) (13).
Патологическое обследование
Рассечение шеи, как описано Японской исследовательской группой по расслоению шеи, выполнялось единым блоком (14). После тщательного разделения образцов шеи по шейному отделу было зарегистрировано общее количество лимфатических узлов.Образцы и записи использовались при патологическом исследовании. В соответствии с процедурой, описанной в нашем предыдущем отчете, образцы резецированных опухолей фиксировали формалином и заливали парафином (3). Патологический диагноз (патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологический класс, положительный хирургический край и экстракапсулярное распространение) был поставлен двумя патологами, которые составили все отчеты.
Послеоперационная терапия
После патологического диагноза послеоперационная терапия проводилась у пациентов с положительным хирургическим краем, экстракапсулярным распространением, множественными положительными лимфатическими узлами или карциномой высокой гистологической степени, где это было возможно.По окончании лечения пациенты наблюдались в поликлинике. Были предприняты усилия для выявления лиц с ранним местно-регионарным рецидивом и проведения в таких случаях радикальной терапии. Клинико-патологические параметры пациентов представлены в.
Таблица I.
Клинико-патологические параметры (n = 32).
| Параметр | Значение | ||
|---|---|---|---|
| Возраст, лет | |||
| Среднее ± SD | 61.8 ± 15,1 | ||
| Пол, n | |||
| Мужской | 25 | ||
| Женский | 7 | ||
| Клиническая классификация T, n | |||
| T1 | 0 | ||
| T2 | 8 | ||
| T3 | 7 | ||
| T4 | 17 | ||
| Клиническая классификация N, n | |||
| N0 | 7 | ||
| N1 | 4 | ||
| N2 | 21 | ||
| N3 | 0 | ||
| Клиническая стадия, n | |||
| I | 0 | ||
| II | 2 | ||
| III | 3 | ||
| IV | 27 | ||
| Анатомическое расположение, n | |||
| околоушная железа | 21 | ||
| Поднижнечелюстная | 10 | ||
| Подъязычная | 1 | ||
| Патологическая классификация T, n | |||
| T1 | 1 | T2 | T2 | 0 |
| T3 | 13 | ||
| T4 | 18 | ||
| Патологическая классификация N, n | |||
| N0 | 0 | ||
| N1 | 8 | ||
| N2 | 24 | ||
| N3 | 0 | ||
| Патологическая стадия, n | |||
| I | 0 | ||
| II | 0 | ||
| III | 3 | ||
| IV | 29 | ||
| Гистологическая классификация, n | |||
| Аденокарцинома, если не указано иное | 14 | ||
| Карцинома слюнных протоков | 6 | ||
| Мукоэпидермоидная карцинома | 4 | ||
| Аденоидно-кистозная карцинома | 468 | Карцинома экзлеоморфная аденома | 3 |
| Плоскоклеточный рак | 1 | ||
| Гистологический класс, n | |||
| Высокий | 11 | ||
| Другие | 21 | ||
| Положительный хирургический маржа, n | |||
| Присутствие | 19 | ||
| Отсутствие | 13 | ||
| Экстракапсулярное распространение, n | |||
| Присутствие | 15 | ||
| Отсутствие | 17 | ||
| Положительный хирургический край и / или экстракапсулярное распространение, n | |||
| Наличие | 24 | ||
| Отсутствие | 8 | ||
| Послеоперационная терапия, n | |||
| Химиолучевая терапия | 2 | ||
| Излучение | 21 | ||
| Отсутствие | 9 |
LND
Всего было оценено 1346 лимфатических узлов, из которых 317 (23.6%) оказались патологически положительными. Основываясь на предыдущих исследованиях (5–12), LND рассчитывалась по следующей формуле: LND = количество положительных лимфатических узлов / общее количество иссеченных лимфатических узлов.
Статистический анализ
Статистический анализ проводился с использованием программного пакета JMP (версия 9; SAS Institute, Кэри, Северная Каролина, США). Корреляция между LND и клинико-патологическими параметрами (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) были проанализированы с использованием U-критерия Манна-Уитни.Время выживания определялось как период от операции до целевого события или даты последнего контакта; целевые события включали смертность для расчета общей выживаемости. Применяя метод, описанный в предыдущих исследованиях, метод Каплана-Мейера использовался для оценки кривых выживаемости, а различные пороговые значения LND были протестированы с использованием лог-рангового теста в одномерном анализе общей выживаемости (15, 16). Тридцать два пациента были сгруппированы в две группы на основе LND (LND ≥0,38 и <0,38), как LND 0.38 смогла статистически отличить более короткую группу выживания от более длинной в соответствии с лог-ранговым тестом в одномерном анализе выживаемости. Связь между двумя группами (LND ≥0,38 и <0,38) в отношении клинико-патологических параметров (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) сравнивали с использованием точного критерия Фишера.Модель пропорциональных рисков Кокса использовалась для многомерного анализа выживаемости. Многофакторный анализ проводился с поправкой на анатомическое расположение (околоушная железа / другие). Считалось, что P <0,05 указывает на статистически значимые различия.
Результаты
LND и клинико-патологические параметры
Медиана LND для всех пациентов составила 0,13 (диапазон 0,02–0,88). Распределение LND показано на, а ассоциации между LND и клинико-патологическими параметрами показаны на.LND достоверно коррелировал с патологической классификацией N (P <0,01), патологической стадией (P = 0,04), гистологической классификацией (P = 0,02) и экстракапсулярным распространением (P = 0,01).
Плотность лимфатических узлов и количество пациентов.
Таблица II.
Связь между LND и клинико-патологическими параметрами (n = 32).
| Параметр | n | LND (среднее ± стандартное отклонение) | P-значение a | |
|---|---|---|---|---|
| Возраст, лет | 0.07 | |||
| <65 | 16 | 0,26 ± 0,24 | ||
| ≥65 | 16 | 0,16 ± 0,23 | ||
| Пол | 0,73 | |||
| Мужской | 25 | 0,21 ± 0,22 | ||
| Женский | 7 | 0,21 ± 0,30 | ||
| Клиническая классификация Т | 0.54 | |||
| T1–3 | 15 | 0,24 ± 0,27 | ||
| T4 | 17 | 0,19 ± 0,21 | ||
| Клиническая классификация N | 0,10 | |||
| N0 | 7 | 0,11 ± 0,14 | ||
| N1–2 | 25 | 0,24 ± 0,25 | ||
| Клиническая стадия | 0.06 | |||
| I – III | 5 | 0,06 ± 0,04 | ||
| IV | 27 | 0,24 ± 0,25 | ||
| Анатомическое расположение | 0,21 | |||
| Околоушная железа | 21 | 0,24 ± 0,23 | ||
| Другие | 11 | 0,16 ± 0,25 | ||
| Патологическая классификация T | 0.83 | |||
| T1–3 | 14 | 0,21 ± 0,25 | ||
| T4 | 18 | 0,21 ± 0,23 | ||
| Патологическая классификация N | <0,01 | |||
| N1 | 8 | 0,03 ± 0,01 | ||
| N2 | 24 | 0,27 ± 0,25 | ||
| Патологическая стадия | <0.04 | |||
| III | 3 | 0,03 ± 0,01 | ||
| IV | 29 | 0,23 ± 0,24 | ||
| Гистологическая классификация | <0,03 | |||
| Аденокарцинома , БДУ | 14 | 0,33 ± 0,29 | ||
| Прочие | 18 | 0,12 ± 0,14 | ||
| Гистологический класс | 0.74 | |||
| Высокая | 8 | 0,14 ± 0,11 | ||
| Прочие | 16 | 0,25 ± 0,28 | ||
| Положительный хирургический край | 0,31 | |||
| Наличие | 19 | 0,14 ± 0,11 | ||
| Отсутствие | 13 | 0,25 ± 0,28 | ||
| Экстракапсулярное распространение | <0.02 | |||
| Наличие | 15 | 0,33 ± 0,29 | ||
| Отсутствие | 17 | 0,11 ± 0,10 | ||
| Положительный хирургический край и / или экстракапсулярное распространение | 0,07 | |||
| Присутствие | 8 | 0,08 ± 0,07 | ||
| Отсутствие | 24 | 0,25 ± 0,26 | ||
| Послеоперационная терапия | 0.90 | |||
| Присутствие | 9 | 0,28 ± 0,35 | ||
| Отсутствие | 23 | 0,18 ± 0,18 |
Общий анализ выживаемости
В конце исследования среднее Периоды наблюдения ± стандартное отклонение среди всех пациентов, 16 выживших пациентов (50,0% против всех) и 16 умерших пациентов (50,0%) составили 23,8 ± 19,6, 25,1 ± 19,9 и 22,4 ± 19,8 месяцев, соответственно. Во всей группе пациентов общая 2-, 3- и 5-летняя выживаемость составила 59.2, 43,2 и 25,9% соответственно. Применяя метод, описанный ранее, в нашем и других исследованиях (14, 15), различные пороговые значения LND были протестированы с использованием лог-рангового теста в анализе общей выживаемости. Пороговое значение 0,38 для LND имело самое низкое значение P в этих анализах () и могло использоваться для дифференциации более короткой группы общей выживаемости (LND ≥0,38, n = 8) от более длинной группы общей выживаемости (LND < 0,38, n = 24) на основе лог-рангового теста, как показано на (P = 0017). Никаких значимых ассоциаций с клинико-патологическими параметрами не наблюдалось в двух группах (LND ≥0.38 и <0,38), как показано на. Многофакторный анализ выживаемости был выполнен с поправкой на анатомическое расположение (околоушная железа / другие) для общей выживаемости. Следовательно, было подтверждено, что LND ≥0,38 ассоциируется со значительно более коротким временем выживания. Результаты многомерного анализа выживаемости представлены в.
P-значения согласно логарифмическому критерию общей выживаемости с использованием различных пороговых значений для LND у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами.LND, плотность лимфатических узлов.
Связь между LND и выживаемостью у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами (метод Каплана-Мейера). Было обнаружено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Для статистического анализа использовался лог-ранговый тест. LND, плотность лимфатических узлов.
Таблица III.
Связь между LND (≥0,38 и <0,38) и клинико-патологическими параметрами (n = 32).
| Параметр | LND ≥0.38 (n = 24) | LND <0,38 (n = 8) | Значение P a |
|---|---|---|---|
| Возраст, лет | 0,22 | ||
| <65 | 10 | 6 | |
| ≥65 | 14 | 2 | |
| Пол | 0,65 | ||
| Мужской | 18 | 7 | |
| Женский | 6 | 1 | |
| Клиническая классификация T | 0.42 | ||
| T1–3 | 10 | 5 | |
| T4 | 14 | 3 | |
| Клиническая классификация N | 0,65 | ||
| N0 | 6 | 1 | |
| N1–2 | 18 | 7 | |
| Клиническая стадия | 0,30 | ||
| I – III | 5 | 0 | |
| IV | 19 | 8 | |
| Анатомическое расположение | 0.68 | ||
| околоушная железа | 15 | 6 | |
| Другие | 9 | 2 | |
| Патологическая классификация T | 0,70 | ||
| T1–3 | 10 | 4 | |
| T4 | 14 | 4 | |
| Патологическая классификация N | 0.08 | ||
| N1 | 8 | 0 | |
| N2 | 16 | 8 | |
| Патологическая стадия | 0,55 | ||
| III | 3 | 0 | |
| IV | 21 | 8 | |
| Гистологическая классификация | 0.10 | ||
| Аденокарцинома, БДУ | 8 | 6 | |
| Другое | 16 | 2 | |
| Гистологический класс | 0,21 | ||
| Высокий | 10 | 1 | |
| Другое | 14 | 7 | |
| Положительное хирургическое поле | 0.42 | ||
| Присутствие | 13 | 6 | |
| Отсутствие | 11 | 2 | |
| Экстракапсулярное распространение | 0,11 | ||
| Присутствие | 9 | 6 | |
| Отсутствие | 15 | 2 | |
| Положительный хирургический край и / или экстракапсулярное распространение | 0.08 | ||
| Присутствие | 16 | 8 | |
| Отсутствие | 8 | 0 | |
| Послеоперационная терапия | 0,18 | ||
| Присутствие | 19 | 4 | |
| Отсутствие | 5 | 4 |
Таблица IV.
Многомерный анализ выживаемости a .
| Общая выживаемость | |||
|---|---|---|---|
| Параметр | HR | 95% CI | P-value |
| LND (≥0,38 / <0,38) | 4,02 | 1,21–13,43 | P <0,03 |
| Анатомическое расположение (околоушная / другие) | 2,81 | 0,87–12,53 | P = 0,09 |
Обсуждение
Результаты настоящего исследования продемонстрировали , впервые, что LND ≥0.38 у пациентов с карциномой большой слюнной железы с патологическими метастазами в лимфатические узлы значительно короче общей продолжительности жизни.
LND, определяемая патологическим исследованием, стала прогностическим параметром для различных типов рака, включая рак мочевого пузыря, пищевода и полости рта (5–12). Соотношение LND весит три фактора, которые могут влиять на стадию узлов: опухоль (истинное количество положительных лимфатических узлов), хирургическое (фактическое количество узлов, удаленных во время рассечения шеи) и факторы отбора проб (полнота патологического анализа) факторы (5 ).Недавно мультиинституциональная международная исследовательская группа, состоящая из 11 онкологических центров по всему миру, показала, что LND является важным показателем общей продолжительности жизни среди 4254 пациентов с OSCC (5). Кроме того, в ряде исследований сообщалось, что LND может использоваться для прогнозирования времени выживания пациентов с OSCC, получавших различные процедуры рассечения шеи, такие как одностороннее или двустороннее рассечение шеи (5–10). Настоящие результаты, демонстрирующие связь между LND и общей выживаемостью, согласуются с предыдущими данными (5-10).
Что касается рака головы и шеи, в многочисленных исследованиях сообщается о связи между LND и общей выживаемостью у пациентов с OSCC (5–9). Кроме того, Rudra и др. (10) сообщили, что LND предсказывает общее время выживания у субъектов с поражениями в различных участках головы и шеи, включая ротоглотку, ротовую полость и гортань / гортань; однако в этом исследовании не изучалась взаимосвязь между LND и общей выживаемостью у пациентов с карциномой основной слюнной железы (10).В настоящем исследовании связь между LND и общей выживаемостью оценивалась у субъектов с карциномой основной слюнной железы, демонстрируя, что LND ≥0,38 у пациентов с патологическими метастазами в лимфатические узлы значительно коррелирует с более коротким общим временем выживания.
Преобладающим ограничением текущего исследования было относительно небольшое количество субъектов в выборке. Следовательно, будущий анализ большого числа пациентов даст более статистически точные результаты с большим потенциалом их применения.
В заключение, настоящее исследование впервые продемонстрировало, что LND ≥0,38 у пациентов с карциномой большой слюнной железы с патологическим метастазированием в лимфатические узлы значительно коррелирует с более коротким общим временем выживания. Следовательно, LND является прогностическим фактором у людей с большой карциномой слюнных желез.
Выражение признательности
Настоящее исследование было поддержано Японским обществом содействия научным грантам для научных исследований (грант №247
Ссылки
1. Ettl T, Schwarz-Furlan S, Gosau M, Reichert TE. Карциномы слюнных желез. Oral Maxillofac Surg. 2012; 16: 267–283. DOI: 10.1007 / s10006-012-0350-9. [PubMed] [CrossRef] [Google Scholar] 2. Барнс Л., Эвесон Дж. В., Райхарт П., Сидранский Д., редакторы. Патология и генетика опухолей головы и шеи. Лион: IARC Press; 2005. Классификация опухолей Всемирной организации здравоохранения.[Google Scholar] 3. Окабе М., Миябе С., Нагацука Х., Терада А., Ханаи Н., Йокои М., Симозато К., Эймото Т., Накамура С., Нагаи Н. и др. Транскрипт слияния MECT1-MAML2 определяет благоприятную подгруппу мукоэпидермоидной карциномы. Clin Cancer Res. 2006; 12: 3902–3907. DOI: 10.1158 / 1078-0432.CCR-05-2376. [PubMed] [CrossRef] [Google Scholar] 4. Амит М., Наара С., Шарма К., Рамер Н., Рамер И., Агбетоба А., Глик Дж., Ян Х, Лей Д., Бьорндал К. и др. Избирательная диссекция шеи у пациентов с аденоидно-кистозной карциномой головы и шеи: международное совместное исследование.Энн Сург Онкол. 2015; 22: 1353–1359. DOI: 10.1245 / s10434-014-4106-7. [PubMed] [CrossRef] [Google Scholar] 5. Патель С.Г., Амит М., Йен Т.С., Ляо К.Т., Чатурведи П., Агарвал Дж. П., Ковальски Л. П., Эбрахими А., Кларк Дж. Р., Чернеа С. Р. и др. Плотность лимфатических узлов при раке полости рта: результаты Международного консорциума исследований результатов. Br J Рак. 2013; 109: 2087–2095. DOI: 10.1038 / bjc.2013.570. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ким С.Ю., Нам С.И., Чой С.Х., Чо К.Дж., Ро Дж.Л. Прогностическое значение плотности лимфатических узлов у пациентов с плоскоклеточным раком полости рта с положительными узлами.Энн Сург Онкол. 2011; 18: 2310–2317. DOI: 10.1245 / s10434-011-1614-6. [PubMed] [CrossRef] [Google Scholar] 7. Гил З., Карлсон Д.Л., Бойл Дж.О., Краус Д.Х., Шах Дж.П., Шаха А.Р., Сингх Б., Вонг Р.Дж., Пател С.Г. Плотность лимфатических узлов является важным предиктором исхода у пациентов с раком полости рта. Рак. 2009. 115: 5700–5710. DOI: 10.1002 / cncr.24631. [PubMed] [CrossRef] [Google Scholar] 8. Амар А., Рапопрт А., Куриони О.А., Дедивитис Р.А., Чернеа С.Р., Брандао LG. Плотность метастатических лимфатических узлов как прогностический фактор при плоскоклеточном раке языка и дна рта.Браз Дж Оториноларингол. 2012; 78: 86–90. DOI: 10.1590 / S1808-86Плотность лимфатических узлов является прогностическим фактором у пациентов с карциномой большой слюнной железы
Oncol Lett.2015 Dec; 10 (6): 3523–3528.
HIDENORI SUZUKI
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
НОБУХИРО ХАНАЙ
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя 464681, Аичи , Япония
HITOSHI HIRAKAWA
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
ДАЙСУКЕ НИСИКАВА
Отделение хирургии головы и шеи, Больница онкологического центра Аичи, Нагоя, 464 -8681, Япония
ЯСУХИСА ХАСЕГАВА
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
Отделение хирургии головы и шеи, Больница онкологического центра Аити, Нагоя, Аити 464-8681 , Япония
Переписка на номер : д-р Хиденори Судзуки, отделение хирургии головы и шеи, больница онкологического центра Айти, 1-1 Канокоден, Тикуса-ку, Нагоя, Аити 464-8681, Япония, электронная почта: пиджей[email protected]Поступила в редакцию 11 ноября 2014 г .; Принято 18 сентября 2015 г.
Эта статья цитировалась в других статьях в PMC.Abstract
Сообщалось, что плотность лимфатических узлов (LND) является важным показателем выживаемости у пациентов с карциномами полости рта и другими карциномами с положительными лимфатическими узлами. В настоящем исследовании изучали, связана ли LND с общей выживаемостью у субъектов с большой карциномой слюнных желез. В общей сложности 78 пациентам с впервые диагностированной карциномой большой слюнной железы была выполнена резекция первичной опухоли и рассечение шеи без предоперационного лечения.Из этих 78 пациентов 32 с патологически положительными лимфатическими узлами были включены в настоящее исследование. LND рассчитывали как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов. Выживаемость анализировали по методу Каплана-Мейера. Одномерный анализ выживаемости был выполнен с использованием лог-рангового теста, а многомерный анализ выживаемости был выполнен с использованием модели пропорциональных рисков Кокса. Было обнаружено, что LND ≥0,38 достоверно коррелирует с более коротким общим временем выживания в однофакторном анализе (P = 0.017). В многофакторном анализе выживаемости после поправки на анатомическое расположение (околоушная железа / другие) было выявлено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Эти результаты предполагают, что LND функционирует как прогностический фактор в случаях рака большой слюнной железы.
Ключевые слова: плотность лимфатических узлов, карцинома основной слюнной железы, общая выживаемость
Введение
Основные карциномы слюнных желез, которые отличаются от карцином околоушных желез, поднижнечелюстных и подъязычных желез, являются редкими злокачественными опухолями. <5% всех случаев рака головы и шеи (1).Гистологическая классификация основных карцином слюнных желез включает 24 гистологических подтипа с различными злокачественными фенотипами и прогнозами в соответствии с классификацией опухолей Всемирной организации здравоохранения 2005 г. (2). На сегодняшний день в многочисленных исследованиях изучались характеристики и полезные прогностические параметры рака основной слюнной железы с использованием различных подходов, включая клинические, патологические и биологические процедуры (1–4).
Плотность лимфатических узлов (LND), которая рассчитывается как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов, надежно предсказывает выживаемость пациентов с плоскоклеточным раком полости рта (OSCC). карцинома мочевого пузыря и другие карциномы с положительными лимфатическими узлами шеи в недавних исследованиях (5–12).Однако связь между LND и общей выживаемостью у людей с большой карциномой слюнных желез еще не исследована. В настоящем исследовании изучали, коррелирует ли LND с общей выживаемостью в случаях рака большой слюнной железы с положительными лимфатическими узлами.
Пациенты и методы
Данные по населению
В общей сложности 284 пациента с впервые диагностированной большой опухолью слюнной железы в отделении хирургии головы и шеи больницы онкологического центра Аити (Нагоя, Япония) прошли резекцию опухоли в период с января 2004 года по май. 2014; У 93 из этих пациентов при патологическом обследовании была диагностирована первичная карцинома большой слюнной железы.Из этих 93 пациентов 80 были подвергнуты резекции первичной опухоли с рассечением шеи, а у 34 были диагностированы патологические метастазы в лимфатических узлах. Из исследования были исключены один пациент, получавший предоперационную химиотерапию, и один пациент, ранее получавший лучевую терапию по поводу карциномы носоглотки. Таким образом, в исследование были включены 32 пациента с патологически положительными лимфатическими узлами. Этот протокол исследования был одобрен наблюдательным советом больницы онкологического центра Айти, и все пациенты предоставили свое информированное согласие на все виды лечения и обследования.Анатомическое расположение первичной опухоли было следующим: околоушная железа — 21 пациент; подчелюстная железа — 10 пациентов; и подъязычная железа — 1 пациент.
Стадия метастазов в опухолевых узлах (TNM)
При первом посещении были выполнены плановое физикальное обследование и рентгенография грудной клетки. Клиническая стадия определялась по результатам этих обследований, а также по результатам улучшенной компьютерной томографии (КТ) шейки матки или магнитно-резонансной томографии. По возможности выполнялась позитронно-эмиссионная томография с 18F-2-фтордезоксиглюкозой (ПЭТ с 18F-FDG) или ПЭТ с 18F-FDG в сочетании с КТ.Клинические данные о метастазах в лимфатические узлы, обнаруженные на усиленной КТ, включали наличие кольцевидного усиления или диаметр лимфатического узла ≥10 мм. Использовались критерии классификации TNM Международного союза против рака (седьмое издание) (13).
Патологическое обследование
Рассечение шеи, как описано Японской исследовательской группой по расслоению шеи, выполнялось единым блоком (14). После тщательного разделения образцов шеи по шейному отделу было зарегистрировано общее количество лимфатических узлов.Образцы и записи использовались при патологическом исследовании. В соответствии с процедурой, описанной в нашем предыдущем отчете, образцы резецированных опухолей фиксировали формалином и заливали парафином (3). Патологический диагноз (патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологический класс, положительный хирургический край и экстракапсулярное распространение) был поставлен двумя патологами, которые составили все отчеты.
Послеоперационная терапия
После патологического диагноза послеоперационная терапия проводилась у пациентов с положительным хирургическим краем, экстракапсулярным распространением, множественными положительными лимфатическими узлами или карциномой высокой гистологической степени, где это было возможно.По окончании лечения пациенты наблюдались в поликлинике. Были предприняты усилия для выявления лиц с ранним местно-регионарным рецидивом и проведения в таких случаях радикальной терапии. Клинико-патологические параметры пациентов представлены в.
Таблица I.
Клинико-патологические параметры (n = 32).
| Параметр | Значение | ||
|---|---|---|---|
| Возраст, лет | |||
| Среднее ± SD | 61.8 ± 15,1 | ||
| Пол, n | |||
| Мужской | 25 | ||
| Женский | 7 | ||
| Клиническая классификация T, n | |||
| T1 | 0 | ||
| T2 | 8 | ||
| T3 | 7 | ||
| T4 | 17 | ||
| Клиническая классификация N, n | |||
| N0 | 7 | ||
| N1 | 4 | ||
| N2 | 21 | ||
| N3 | 0 | ||
| Клиническая стадия, n | |||
| I | 0 | ||
| II | 2 | ||
| III | 3 | ||
| IV | 27 | ||
| Анатомическое расположение, n | |||
| околоушная железа | 21 | ||
| Поднижнечелюстная | 10 | ||
| Подъязычная | 1 | ||
| Патологическая классификация T, n | |||
| T1 | 1 | T2 | T2 | 0 |
| T3 | 13 | ||
| T4 | 18 | ||
| Патологическая классификация N, n | |||
| N0 | 0 | ||
| N1 | 8 | ||
| N2 | 24 | ||
| N3 | 0 | ||
| Патологическая стадия, n | |||
| I | 0 | ||
| II | 0 | ||
| III | 3 | ||
| IV | 29 | ||
| Гистологическая классификация, n | |||
| Аденокарцинома, если не указано иное | 14 | ||
| Карцинома слюнных протоков | 6 | ||
| Мукоэпидермоидная карцинома | 4 | ||
| Аденоидно-кистозная карцинома | 468 | Карцинома экзлеоморфная аденома | 3 |
| Плоскоклеточный рак | 1 | ||
| Гистологический класс, n | |||
| Высокий | 11 | ||
| Другие | 21 | ||
| Положительный хирургический маржа, n | |||
| Присутствие | 19 | ||
| Отсутствие | 13 | ||
| Экстракапсулярное распространение, n | |||
| Присутствие | 15 | ||
| Отсутствие | 17 | ||
| Положительный хирургический край и / или экстракапсулярное распространение, n | |||
| Наличие | 24 | ||
| Отсутствие | 8 | ||
| Послеоперационная терапия, n | |||
| Химиолучевая терапия | 2 | ||
| Излучение | 21 | ||
| Отсутствие | 9 |
LND
Всего было оценено 1346 лимфатических узлов, из которых 317 (23.6%) оказались патологически положительными. Основываясь на предыдущих исследованиях (5–12), LND рассчитывалась по следующей формуле: LND = количество положительных лимфатических узлов / общее количество иссеченных лимфатических узлов.
Статистический анализ
Статистический анализ проводился с использованием программного пакета JMP (версия 9; SAS Institute, Кэри, Северная Каролина, США). Корреляция между LND и клинико-патологическими параметрами (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) были проанализированы с использованием U-критерия Манна-Уитни.Время выживания определялось как период от операции до целевого события или даты последнего контакта; целевые события включали смертность для расчета общей выживаемости. Применяя метод, описанный в предыдущих исследованиях, метод Каплана-Мейера использовался для оценки кривых выживаемости, а различные пороговые значения LND были протестированы с использованием лог-рангового теста в одномерном анализе общей выживаемости (15, 16). Тридцать два пациента были сгруппированы в две группы на основе LND (LND ≥0,38 и <0,38), как LND 0.38 смогла статистически отличить более короткую группу выживания от более длинной в соответствии с лог-ранговым тестом в одномерном анализе выживаемости. Связь между двумя группами (LND ≥0,38 и <0,38) в отношении клинико-патологических параметров (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) сравнивали с использованием точного критерия Фишера.Модель пропорциональных рисков Кокса использовалась для многомерного анализа выживаемости. Многофакторный анализ проводился с поправкой на анатомическое расположение (околоушная железа / другие). Считалось, что P <0,05 указывает на статистически значимые различия.
Результаты
LND и клинико-патологические параметры
Медиана LND для всех пациентов составила 0,13 (диапазон 0,02–0,88). Распределение LND показано на, а ассоциации между LND и клинико-патологическими параметрами показаны на.LND достоверно коррелировал с патологической классификацией N (P <0,01), патологической стадией (P = 0,04), гистологической классификацией (P = 0,02) и экстракапсулярным распространением (P = 0,01).
Плотность лимфатических узлов и количество пациентов.
Таблица II.
Связь между LND и клинико-патологическими параметрами (n = 32).
| Параметр | n | LND (среднее ± стандартное отклонение) | P-значение a | |
|---|---|---|---|---|
| Возраст, лет | 0.07 | |||
| <65 | 16 | 0,26 ± 0,24 | ||
| ≥65 | 16 | 0,16 ± 0,23 | ||
| Пол | 0,73 | |||
| Мужской | 25 | 0,21 ± 0,22 | ||
| Женский | 7 | 0,21 ± 0,30 | ||
| Клиническая классификация Т | 0.54 | |||
| T1–3 | 15 | 0,24 ± 0,27 | ||
| T4 | 17 | 0,19 ± 0,21 | ||
| Клиническая классификация N | 0,10 | |||
| N0 | 7 | 0,11 ± 0,14 | ||
| N1–2 | 25 | 0,24 ± 0,25 | ||
| Клиническая стадия | 0.06 | |||
| I – III | 5 | 0,06 ± 0,04 | ||
| IV | 27 | 0,24 ± 0,25 | ||
| Анатомическое расположение | 0,21 | |||
| Околоушная железа | 21 | 0,24 ± 0,23 | ||
| Другие | 11 | 0,16 ± 0,25 | ||
| Патологическая классификация T | 0.83 | |||
| T1–3 | 14 | 0,21 ± 0,25 | ||
| T4 | 18 | 0,21 ± 0,23 | ||
| Патологическая классификация N | <0,01 | |||
| N1 | 8 | 0,03 ± 0,01 | ||
| N2 | 24 | 0,27 ± 0,25 | ||
| Патологическая стадия | <0.04 | |||
| III | 3 | 0,03 ± 0,01 | ||
| IV | 29 | 0,23 ± 0,24 | ||
| Гистологическая классификация | <0,03 | |||
| Аденокарцинома , БДУ | 14 | 0,33 ± 0,29 | ||
| Прочие | 18 | 0,12 ± 0,14 | ||
| Гистологический класс | 0.74 | |||
| Высокая | 8 | 0,14 ± 0,11 | ||
| Прочие | 16 | 0,25 ± 0,28 | ||
| Положительный хирургический край | 0,31 | |||
| Наличие | 19 | 0,14 ± 0,11 | ||
| Отсутствие | 13 | 0,25 ± 0,28 | ||
| Экстракапсулярное распространение | <0.02 | |||
| Наличие | 15 | 0,33 ± 0,29 | ||
| Отсутствие | 17 | 0,11 ± 0,10 | ||
| Положительный хирургический край и / или экстракапсулярное распространение | 0,07 | |||
| Присутствие | 8 | 0,08 ± 0,07 | ||
| Отсутствие | 24 | 0,25 ± 0,26 | ||
| Послеоперационная терапия | 0.90 | |||
| Присутствие | 9 | 0,28 ± 0,35 | ||
| Отсутствие | 23 | 0,18 ± 0,18 |
Общий анализ выживаемости
В конце исследования среднее Периоды наблюдения ± стандартное отклонение среди всех пациентов, 16 выживших пациентов (50,0% против всех) и 16 умерших пациентов (50,0%) составили 23,8 ± 19,6, 25,1 ± 19,9 и 22,4 ± 19,8 месяцев, соответственно. Во всей группе пациентов общая 2-, 3- и 5-летняя выживаемость составила 59.2, 43,2 и 25,9% соответственно. Применяя метод, описанный ранее, в нашем и других исследованиях (14, 15), различные пороговые значения LND были протестированы с использованием лог-рангового теста в анализе общей выживаемости. Пороговое значение 0,38 для LND имело самое низкое значение P в этих анализах () и могло использоваться для дифференциации более короткой группы общей выживаемости (LND ≥0,38, n = 8) от более длинной группы общей выживаемости (LND < 0,38, n = 24) на основе лог-рангового теста, как показано на (P = 0017). Никаких значимых ассоциаций с клинико-патологическими параметрами не наблюдалось в двух группах (LND ≥0.38 и <0,38), как показано на. Многофакторный анализ выживаемости был выполнен с поправкой на анатомическое расположение (околоушная железа / другие) для общей выживаемости. Следовательно, было подтверждено, что LND ≥0,38 ассоциируется со значительно более коротким временем выживания. Результаты многомерного анализа выживаемости представлены в.
P-значения согласно логарифмическому критерию общей выживаемости с использованием различных пороговых значений для LND у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами.LND, плотность лимфатических узлов.
Связь между LND и выживаемостью у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами (метод Каплана-Мейера). Было обнаружено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Для статистического анализа использовался лог-ранговый тест. LND, плотность лимфатических узлов.
Таблица III.
Связь между LND (≥0,38 и <0,38) и клинико-патологическими параметрами (n = 32).
| Параметр | LND ≥0.38 (n = 24) | LND <0,38 (n = 8) | Значение P a |
|---|---|---|---|
| Возраст, лет | 0,22 | ||
| <65 | 10 | 6 | |
| ≥65 | 14 | 2 | |
| Пол | 0,65 | ||
| Мужской | 18 | 7 | |
| Женский | 6 | 1 | |
| Клиническая классификация T | 0.42 | ||
| T1–3 | 10 | 5 | |
| T4 | 14 | 3 | |
| Клиническая классификация N | 0,65 | ||
| N0 | 6 | 1 | |
| N1–2 | 18 | 7 | |
| Клиническая стадия | 0,30 | ||
| I – III | 5 | 0 | |
| IV | 19 | 8 | |
| Анатомическое расположение | 0.68 | ||
| околоушная железа | 15 | 6 | |
| Другие | 9 | 2 | |
| Патологическая классификация T | 0,70 | ||
| T1–3 | 10 | 4 | |
| T4 | 14 | 4 | |
| Патологическая классификация N | 0.08 | ||
| N1 | 8 | 0 | |
| N2 | 16 | 8 | |
| Патологическая стадия | 0,55 | ||
| III | 3 | 0 | |
| IV | 21 | 8 | |
| Гистологическая классификация | 0.10 | ||
| Аденокарцинома, БДУ | 8 | 6 | |
| Другое | 16 | 2 | |
| Гистологический класс | 0,21 | ||
| Высокий | 10 | 1 | |
| Другое | 14 | 7 | |
| Положительное хирургическое поле | 0.42 | ||
| Присутствие | 13 | 6 | |
| Отсутствие | 11 | 2 | |
| Экстракапсулярное распространение | 0,11 | ||
| Присутствие | 9 | 6 | |
| Отсутствие | 15 | 2 | |
| Положительный хирургический край и / или экстракапсулярное распространение | 0.08 | ||
| Присутствие | 16 | 8 | |
| Отсутствие | 8 | 0 | |
| Послеоперационная терапия | 0,18 | ||
| Присутствие | 19 | 4 | |
| Отсутствие | 5 | 4 |
Таблица IV.
Многомерный анализ выживаемости a .
| Общая выживаемость | |||
|---|---|---|---|
| Параметр | HR | 95% CI | P-value |
| LND (≥0,38 / <0,38) | 4,02 | 1,21–13,43 | P <0,03 |
| Анатомическое расположение (околоушная / другие) | 2,81 | 0,87–12,53 | P = 0,09 |
Обсуждение
Результаты настоящего исследования продемонстрировали , впервые, что LND ≥0.38 у пациентов с карциномой большой слюнной железы с патологическими метастазами в лимфатические узлы значительно короче общей продолжительности жизни.
LND, определяемая патологическим исследованием, стала прогностическим параметром для различных типов рака, включая рак мочевого пузыря, пищевода и полости рта (5–12). Соотношение LND весит три фактора, которые могут влиять на стадию узлов: опухоль (истинное количество положительных лимфатических узлов), хирургическое (фактическое количество узлов, удаленных во время рассечения шеи) и факторы отбора проб (полнота патологического анализа) факторы (5 ).Недавно мультиинституциональная международная исследовательская группа, состоящая из 11 онкологических центров по всему миру, показала, что LND является важным показателем общей продолжительности жизни среди 4254 пациентов с OSCC (5). Кроме того, в ряде исследований сообщалось, что LND может использоваться для прогнозирования времени выживания пациентов с OSCC, получавших различные процедуры рассечения шеи, такие как одностороннее или двустороннее рассечение шеи (5–10). Настоящие результаты, демонстрирующие связь между LND и общей выживаемостью, согласуются с предыдущими данными (5-10).
Что касается рака головы и шеи, в многочисленных исследованиях сообщается о связи между LND и общей выживаемостью у пациентов с OSCC (5–9). Кроме того, Rudra и др. (10) сообщили, что LND предсказывает общее время выживания у субъектов с поражениями в различных участках головы и шеи, включая ротоглотку, ротовую полость и гортань / гортань; однако в этом исследовании не изучалась взаимосвязь между LND и общей выживаемостью у пациентов с карциномой основной слюнной железы (10).В настоящем исследовании связь между LND и общей выживаемостью оценивалась у субъектов с карциномой основной слюнной железы, демонстрируя, что LND ≥0,38 у пациентов с патологическими метастазами в лимфатические узлы значительно коррелирует с более коротким общим временем выживания.
Преобладающим ограничением текущего исследования было относительно небольшое количество субъектов в выборке. Следовательно, будущий анализ большого числа пациентов даст более статистически точные результаты с большим потенциалом их применения.
В заключение, настоящее исследование впервые продемонстрировало, что LND ≥0,38 у пациентов с карциномой большой слюнной железы с патологическим метастазированием в лимфатические узлы значительно коррелирует с более коротким общим временем выживания. Следовательно, LND является прогностическим фактором у людей с большой карциномой слюнных желез.
Выражение признательности
Настоящее исследование было поддержано Японским обществом содействия научным грантам для научных исследований (грант №247
Ссылки
1. Ettl T, Schwarz-Furlan S, Gosau M, Reichert TE. Карциномы слюнных желез. Oral Maxillofac Surg. 2012; 16: 267–283. DOI: 10.1007 / s10006-012-0350-9. [PubMed] [CrossRef] [Google Scholar] 2. Барнс Л., Эвесон Дж. В., Райхарт П., Сидранский Д., редакторы. Патология и генетика опухолей головы и шеи. Лион: IARC Press; 2005. Классификация опухолей Всемирной организации здравоохранения.[Google Scholar] 3. Окабе М., Миябе С., Нагацука Х., Терада А., Ханаи Н., Йокои М., Симозато К., Эймото Т., Накамура С., Нагаи Н. и др. Транскрипт слияния MECT1-MAML2 определяет благоприятную подгруппу мукоэпидермоидной карциномы. Clin Cancer Res. 2006; 12: 3902–3907. DOI: 10.1158 / 1078-0432.CCR-05-2376. [PubMed] [CrossRef] [Google Scholar] 4. Амит М., Наара С., Шарма К., Рамер Н., Рамер И., Агбетоба А., Глик Дж., Ян Х, Лей Д., Бьорндал К. и др. Избирательная диссекция шеи у пациентов с аденоидно-кистозной карциномой головы и шеи: международное совместное исследование.Энн Сург Онкол. 2015; 22: 1353–1359. DOI: 10.1245 / s10434-014-4106-7. [PubMed] [CrossRef] [Google Scholar] 5. Патель С.Г., Амит М., Йен Т.С., Ляо К.Т., Чатурведи П., Агарвал Дж. П., Ковальски Л. П., Эбрахими А., Кларк Дж. Р., Чернеа С. Р. и др. Плотность лимфатических узлов при раке полости рта: результаты Международного консорциума исследований результатов. Br J Рак. 2013; 109: 2087–2095. DOI: 10.1038 / bjc.2013.570. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ким С.Ю., Нам С.И., Чой С.Х., Чо К.Дж., Ро Дж.Л. Прогностическое значение плотности лимфатических узлов у пациентов с плоскоклеточным раком полости рта с положительными узлами.Энн Сург Онкол. 2011; 18: 2310–2317. DOI: 10.1245 / s10434-011-1614-6. [PubMed] [CrossRef] [Google Scholar] 7. Гил З., Карлсон Д.Л., Бойл Дж.О., Краус Д.Х., Шах Дж.П., Шаха А.Р., Сингх Б., Вонг Р.Дж., Пател С.Г. Плотность лимфатических узлов является важным предиктором исхода у пациентов с раком полости рта. Рак. 2009. 115: 5700–5710. DOI: 10.1002 / cncr.24631. [PubMed] [CrossRef] [Google Scholar] 8. Амар А., Рапопрт А., Куриони О.А., Дедивитис Р.А., Чернеа С.Р., Брандао LG. Плотность метастатических лимфатических узлов как прогностический фактор при плоскоклеточном раке языка и дна рта.Браз Дж Оториноларингол. 2012; 78: 86–90. DOI: 10.1590 / S1808-86Плотность лимфатических узлов является прогностическим фактором у пациентов с карциномой большой слюнной железы
Oncol Lett.2015 Dec; 10 (6): 3523–3528.
HIDENORI SUZUKI
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
НОБУХИРО ХАНАЙ
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя 464681, Аичи , Япония
HITOSHI HIRAKAWA
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
ДАЙСУКЕ НИСИКАВА
Отделение хирургии головы и шеи, Больница онкологического центра Аичи, Нагоя, 464 -8681, Япония
ЯСУХИСА ХАСЕГАВА
Отделение хирургии головы и шеи, Больница онкологического центра Айти, Нагоя, Аити 464-8681, Япония
Отделение хирургии головы и шеи, Больница онкологического центра Аити, Нагоя, Аити 464-8681 , Япония
Переписка на номер : д-р Хиденори Судзуки, отделение хирургии головы и шеи, больница онкологического центра Айти, 1-1 Канокоден, Тикуса-ку, Нагоя, Аити 464-8681, Япония, электронная почта: пиджей[email protected]Поступила в редакцию 11 ноября 2014 г .; Принято 18 сентября 2015 г.
Эта статья цитировалась в других статьях в PMC.Abstract
Сообщалось, что плотность лимфатических узлов (LND) является важным показателем выживаемости у пациентов с карциномами полости рта и другими карциномами с положительными лимфатическими узлами. В настоящем исследовании изучали, связана ли LND с общей выживаемостью у субъектов с большой карциномой слюнных желез. В общей сложности 78 пациентам с впервые диагностированной карциномой большой слюнной железы была выполнена резекция первичной опухоли и рассечение шеи без предоперационного лечения.Из этих 78 пациентов 32 с патологически положительными лимфатическими узлами были включены в настоящее исследование. LND рассчитывали как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов. Выживаемость анализировали по методу Каплана-Мейера. Одномерный анализ выживаемости был выполнен с использованием лог-рангового теста, а многомерный анализ выживаемости был выполнен с использованием модели пропорциональных рисков Кокса. Было обнаружено, что LND ≥0,38 достоверно коррелирует с более коротким общим временем выживания в однофакторном анализе (P = 0.017). В многофакторном анализе выживаемости после поправки на анатомическое расположение (околоушная железа / другие) было выявлено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Эти результаты предполагают, что LND функционирует как прогностический фактор в случаях рака большой слюнной железы.
Ключевые слова: плотность лимфатических узлов, карцинома основной слюнной железы, общая выживаемость
Введение
Основные карциномы слюнных желез, которые отличаются от карцином околоушных желез, поднижнечелюстных и подъязычных желез, являются редкими злокачественными опухолями. <5% всех случаев рака головы и шеи (1).Гистологическая классификация основных карцином слюнных желез включает 24 гистологических подтипа с различными злокачественными фенотипами и прогнозами в соответствии с классификацией опухолей Всемирной организации здравоохранения 2005 г. (2). На сегодняшний день в многочисленных исследованиях изучались характеристики и полезные прогностические параметры рака основной слюнной железы с использованием различных подходов, включая клинические, патологические и биологические процедуры (1–4).
Плотность лимфатических узлов (LND), которая рассчитывается как отношение количества положительных лимфатических узлов к общему количеству лимфатических узлов, надежно предсказывает выживаемость пациентов с плоскоклеточным раком полости рта (OSCC). карцинома мочевого пузыря и другие карциномы с положительными лимфатическими узлами шеи в недавних исследованиях (5–12).Однако связь между LND и общей выживаемостью у людей с большой карциномой слюнных желез еще не исследована. В настоящем исследовании изучали, коррелирует ли LND с общей выживаемостью в случаях рака большой слюнной железы с положительными лимфатическими узлами.
Пациенты и методы
Данные по населению
В общей сложности 284 пациента с впервые диагностированной большой опухолью слюнной железы в отделении хирургии головы и шеи больницы онкологического центра Аити (Нагоя, Япония) прошли резекцию опухоли в период с января 2004 года по май. 2014; У 93 из этих пациентов при патологическом обследовании была диагностирована первичная карцинома большой слюнной железы.Из этих 93 пациентов 80 были подвергнуты резекции первичной опухоли с рассечением шеи, а у 34 были диагностированы патологические метастазы в лимфатических узлах. Из исследования были исключены один пациент, получавший предоперационную химиотерапию, и один пациент, ранее получавший лучевую терапию по поводу карциномы носоглотки. Таким образом, в исследование были включены 32 пациента с патологически положительными лимфатическими узлами. Этот протокол исследования был одобрен наблюдательным советом больницы онкологического центра Айти, и все пациенты предоставили свое информированное согласие на все виды лечения и обследования.Анатомическое расположение первичной опухоли было следующим: околоушная железа — 21 пациент; подчелюстная железа — 10 пациентов; и подъязычная железа — 1 пациент.
Стадия метастазов в опухолевых узлах (TNM)
При первом посещении были выполнены плановое физикальное обследование и рентгенография грудной клетки. Клиническая стадия определялась по результатам этих обследований, а также по результатам улучшенной компьютерной томографии (КТ) шейки матки или магнитно-резонансной томографии. По возможности выполнялась позитронно-эмиссионная томография с 18F-2-фтордезоксиглюкозой (ПЭТ с 18F-FDG) или ПЭТ с 18F-FDG в сочетании с КТ.Клинические данные о метастазах в лимфатические узлы, обнаруженные на усиленной КТ, включали наличие кольцевидного усиления или диаметр лимфатического узла ≥10 мм. Использовались критерии классификации TNM Международного союза против рака (седьмое издание) (13).
Патологическое обследование
Рассечение шеи, как описано Японской исследовательской группой по расслоению шеи, выполнялось единым блоком (14). После тщательного разделения образцов шеи по шейному отделу было зарегистрировано общее количество лимфатических узлов.Образцы и записи использовались при патологическом исследовании. В соответствии с процедурой, описанной в нашем предыдущем отчете, образцы резецированных опухолей фиксировали формалином и заливали парафином (3). Патологический диагноз (патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологический класс, положительный хирургический край и экстракапсулярное распространение) был поставлен двумя патологами, которые составили все отчеты.
Послеоперационная терапия
После патологического диагноза послеоперационная терапия проводилась у пациентов с положительным хирургическим краем, экстракапсулярным распространением, множественными положительными лимфатическими узлами или карциномой высокой гистологической степени, где это было возможно.По окончании лечения пациенты наблюдались в поликлинике. Были предприняты усилия для выявления лиц с ранним местно-регионарным рецидивом и проведения в таких случаях радикальной терапии. Клинико-патологические параметры пациентов представлены в.
Таблица I.
Клинико-патологические параметры (n = 32).
| Параметр | Значение | ||
|---|---|---|---|
| Возраст, лет | |||
| Среднее ± SD | 61.8 ± 15,1 | ||
| Пол, n | |||
| Мужской | 25 | ||
| Женский | 7 | ||
| Клиническая классификация T, n | |||
| T1 | 0 | ||
| T2 | 8 | ||
| T3 | 7 | ||
| T4 | 17 | ||
| Клиническая классификация N, n | |||
| N0 | 7 | ||
| N1 | 4 | ||
| N2 | 21 | ||
| N3 | 0 | ||
| Клиническая стадия, n | |||
| I | 0 | ||
| II | 2 | ||
| III | 3 | ||
| IV | 27 | ||
| Анатомическое расположение, n | |||
| околоушная железа | 21 | ||
| Поднижнечелюстная | 10 | ||
| Подъязычная | 1 | ||
| Патологическая классификация T, n | |||
| T1 | 1 | T2 | T2 | 0 |
| T3 | 13 | ||
| T4 | 18 | ||
| Патологическая классификация N, n | |||
| N0 | 0 | ||
| N1 | 8 | ||
| N2 | 24 | ||
| N3 | 0 | ||
| Патологическая стадия, n | |||
| I | 0 | ||
| II | 0 | ||
| III | 3 | ||
| IV | 29 | ||
| Гистологическая классификация, n | |||
| Аденокарцинома, если не указано иное | 14 | ||
| Карцинома слюнных протоков | 6 | ||
| Мукоэпидермоидная карцинома | 4 | ||
| Аденоидно-кистозная карцинома | 468 | Карцинома экзлеоморфная аденома | 3 |
| Плоскоклеточный рак | 1 | ||
| Гистологический класс, n | |||
| Высокий | 11 | ||
| Другие | 21 | ||
| Положительный хирургический маржа, n | |||
| Присутствие | 19 | ||
| Отсутствие | 13 | ||
| Экстракапсулярное распространение, n | |||
| Присутствие | 15 | ||
| Отсутствие | 17 | ||
| Положительный хирургический край и / или экстракапсулярное распространение, n | |||
| Наличие | 24 | ||
| Отсутствие | 8 | ||
| Послеоперационная терапия, n | |||
| Химиолучевая терапия | 2 | ||
| Излучение | 21 | ||
| Отсутствие | 9 |
LND
Всего было оценено 1346 лимфатических узлов, из которых 317 (23.6%) оказались патологически положительными. Основываясь на предыдущих исследованиях (5–12), LND рассчитывалась по следующей формуле: LND = количество положительных лимфатических узлов / общее количество иссеченных лимфатических узлов.
Статистический анализ
Статистический анализ проводился с использованием программного пакета JMP (версия 9; SAS Institute, Кэри, Северная Каролина, США). Корреляция между LND и клинико-патологическими параметрами (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) были проанализированы с использованием U-критерия Манна-Уитни.Время выживания определялось как период от операции до целевого события или даты последнего контакта; целевые события включали смертность для расчета общей выживаемости. Применяя метод, описанный в предыдущих исследованиях, метод Каплана-Мейера использовался для оценки кривых выживаемости, а различные пороговые значения LND были протестированы с использованием лог-рангового теста в одномерном анализе общей выживаемости (15, 16). Тридцать два пациента были сгруппированы в две группы на основе LND (LND ≥0,38 и <0,38), как LND 0.38 смогла статистически отличить более короткую группу выживания от более длинной в соответствии с лог-ранговым тестом в одномерном анализе выживаемости. Связь между двумя группами (LND ≥0,38 и <0,38) в отношении клинико-патологических параметров (возраст, пол, клиническая классификация T и N, клиническая стадия, анатомическое расположение, патологическая классификация T и N, патологическая стадия, гистологическая классификация, гистологическая степень, положительный хирургический край, экстракапсулярное распространение, положительный хирургический край и / или экстракапсулярное распространение и послеоперационная терапия) сравнивали с использованием точного критерия Фишера.Модель пропорциональных рисков Кокса использовалась для многомерного анализа выживаемости. Многофакторный анализ проводился с поправкой на анатомическое расположение (околоушная железа / другие). Считалось, что P <0,05 указывает на статистически значимые различия.
Результаты
LND и клинико-патологические параметры
Медиана LND для всех пациентов составила 0,13 (диапазон 0,02–0,88). Распределение LND показано на, а ассоциации между LND и клинико-патологическими параметрами показаны на.LND достоверно коррелировал с патологической классификацией N (P <0,01), патологической стадией (P = 0,04), гистологической классификацией (P = 0,02) и экстракапсулярным распространением (P = 0,01).
Плотность лимфатических узлов и количество пациентов.
Таблица II.
Связь между LND и клинико-патологическими параметрами (n = 32).
| Параметр | n | LND (среднее ± стандартное отклонение) | P-значение a | |
|---|---|---|---|---|
| Возраст, лет | 0.07 | |||
| <65 | 16 | 0,26 ± 0,24 | ||
| ≥65 | 16 | 0,16 ± 0,23 | ||
| Пол | 0,73 | |||
| Мужской | 25 | 0,21 ± 0,22 | ||
| Женский | 7 | 0,21 ± 0,30 | ||
| Клиническая классификация Т | 0.54 | |||
| T1–3 | 15 | 0,24 ± 0,27 | ||
| T4 | 17 | 0,19 ± 0,21 | ||
| Клиническая классификация N | 0,10 | |||
| N0 | 7 | 0,11 ± 0,14 | ||
| N1–2 | 25 | 0,24 ± 0,25 | ||
| Клиническая стадия | 0.06 | |||
| I – III | 5 | 0,06 ± 0,04 | ||
| IV | 27 | 0,24 ± 0,25 | ||
| Анатомическое расположение | 0,21 | |||
| Околоушная железа | 21 | 0,24 ± 0,23 | ||
| Другие | 11 | 0,16 ± 0,25 | ||
| Патологическая классификация T | 0.83 | |||
| T1–3 | 14 | 0,21 ± 0,25 | ||
| T4 | 18 | 0,21 ± 0,23 | ||
| Патологическая классификация N | <0,01 | |||
| N1 | 8 | 0,03 ± 0,01 | ||
| N2 | 24 | 0,27 ± 0,25 | ||
| Патологическая стадия | <0.04 | |||
| III | 3 | 0,03 ± 0,01 | ||
| IV | 29 | 0,23 ± 0,24 | ||
| Гистологическая классификация | <0,03 | |||
| Аденокарцинома , БДУ | 14 | 0,33 ± 0,29 | ||
| Прочие | 18 | 0,12 ± 0,14 | ||
| Гистологический класс | 0.74 | |||
| Высокая | 8 | 0,14 ± 0,11 | ||
| Прочие | 16 | 0,25 ± 0,28 | ||
| Положительный хирургический край | 0,31 | |||
| Наличие | 19 | 0,14 ± 0,11 | ||
| Отсутствие | 13 | 0,25 ± 0,28 | ||
| Экстракапсулярное распространение | <0.02 | |||
| Наличие | 15 | 0,33 ± 0,29 | ||
| Отсутствие | 17 | 0,11 ± 0,10 | ||
| Положительный хирургический край и / или экстракапсулярное распространение | 0,07 | |||
| Присутствие | 8 | 0,08 ± 0,07 | ||
| Отсутствие | 24 | 0,25 ± 0,26 | ||
| Послеоперационная терапия | 0.90 | |||
| Присутствие | 9 | 0,28 ± 0,35 | ||
| Отсутствие | 23 | 0,18 ± 0,18 |
Общий анализ выживаемости
В конце исследования среднее Периоды наблюдения ± стандартное отклонение среди всех пациентов, 16 выживших пациентов (50,0% против всех) и 16 умерших пациентов (50,0%) составили 23,8 ± 19,6, 25,1 ± 19,9 и 22,4 ± 19,8 месяцев, соответственно. Во всей группе пациентов общая 2-, 3- и 5-летняя выживаемость составила 59.2, 43,2 и 25,9% соответственно. Применяя метод, описанный ранее, в нашем и других исследованиях (14, 15), различные пороговые значения LND были протестированы с использованием лог-рангового теста в анализе общей выживаемости. Пороговое значение 0,38 для LND имело самое низкое значение P в этих анализах () и могло использоваться для дифференциации более короткой группы общей выживаемости (LND ≥0,38, n = 8) от более длинной группы общей выживаемости (LND < 0,38, n = 24) на основе лог-рангового теста, как показано на (P = 0017). Никаких значимых ассоциаций с клинико-патологическими параметрами не наблюдалось в двух группах (LND ≥0.38 и <0,38), как показано на. Многофакторный анализ выживаемости был выполнен с поправкой на анатомическое расположение (околоушная железа / другие) для общей выживаемости. Следовательно, было подтверждено, что LND ≥0,38 ассоциируется со значительно более коротким временем выживания. Результаты многомерного анализа выживаемости представлены в.
P-значения согласно логарифмическому критерию общей выживаемости с использованием различных пороговых значений для LND у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами.LND, плотность лимфатических узлов.
Связь между LND и выживаемостью у 32 пациентов с большой карциномой слюнных желез с положительными лимфатическими узлами (метод Каплана-Мейера). Было обнаружено, что LND ≥0,38 ассоциируется со значительно более коротким общим временем выживания. Для статистического анализа использовался лог-ранговый тест. LND, плотность лимфатических узлов.
Таблица III.
Связь между LND (≥0,38 и <0,38) и клинико-патологическими параметрами (n = 32).
| Параметр | LND ≥0.38 (n = 24) | LND <0,38 (n = 8) | Значение P a |
|---|---|---|---|
| Возраст, лет | 0,22 | ||
| <65 | 10 | 6 | |
| ≥65 | 14 | 2 | |
| Пол | 0,65 | ||
| Мужской | 18 | 7 | |
| Женский | 6 | 1 | |
| Клиническая классификация T | 0.42 | ||
| T1–3 | 10 | 5 | |
| T4 | 14 | 3 | |
| Клиническая классификация N | 0,65 | ||
| N0 | 6 | 1 | |
| N1–2 | 18 | 7 | |
| Клиническая стадия | 0,30 | ||
| I – III | 5 | 0 | |
| IV | 19 | 8 | |
| Анатомическое расположение | 0.68 | ||
| околоушная железа | 15 | 6 | |
| Другие | 9 | 2 | |
| Патологическая классификация T | 0,70 | ||
| T1–3 | 10 | 4 | |
| T4 | 14 | 4 | |
| Патологическая классификация N | 0.08 | ||
| N1 | 8 | 0 | |
| N2 | 16 | 8 | |
| Патологическая стадия | 0,55 | ||
| III | 3 | 0 | |
| IV | 21 | 8 | |
| Гистологическая классификация | 0.10 | ||
| Аденокарцинома, БДУ | 8 | 6 | |
| Другое | 16 | 2 | |
| Гистологический класс | 0,21 | ||
| Высокий | 10 | 1 | |
| Другое | 14 | 7 | |
| Положительное хирургическое поле | 0.42 | ||
| Присутствие | 13 | 6 | |
| Отсутствие | 11 | 2 | |
| Экстракапсулярное распространение | 0,11 | ||
| Присутствие | 9 | 6 | |
| Отсутствие | 15 | 2 | |
| Положительный хирургический край и / или экстракапсулярное распространение | 0.08 | ||
| Присутствие | 16 | 8 | |
| Отсутствие | 8 | 0 | |
| Послеоперационная терапия | 0,18 | ||
| Присутствие | 19 | 4 | |
| Отсутствие | 5 | 4 |
Таблица IV.
Многомерный анализ выживаемости a .
| Общая выживаемость | |||
|---|---|---|---|
| Параметр | HR | 95% CI | P-value |
| LND (≥0,38 / <0,38) | 4,02 | 1,21–13,43 | P <0,03 |
| Анатомическое расположение (околоушная / другие) | 2,81 | 0,87–12,53 | P = 0,09 |
Обсуждение
Результаты настоящего исследования продемонстрировали , впервые, что LND ≥0.38 у пациентов с карциномой большой слюнной железы с патологическими метастазами в лимфатические узлы значительно короче общей продолжительности жизни.
LND, определяемая патологическим исследованием, стала прогностическим параметром для различных типов рака, включая рак мочевого пузыря, пищевода и полости рта (5–12). Соотношение LND весит три фактора, которые могут влиять на стадию узлов: опухоль (истинное количество положительных лимфатических узлов), хирургическое (фактическое количество узлов, удаленных во время рассечения шеи) и факторы отбора проб (полнота патологического анализа) факторы (5 ).Недавно мультиинституциональная международная исследовательская группа, состоящая из 11 онкологических центров по всему миру, показала, что LND является важным показателем общей продолжительности жизни среди 4254 пациентов с OSCC (5). Кроме того, в ряде исследований сообщалось, что LND может использоваться для прогнозирования времени выживания пациентов с OSCC, получавших различные процедуры рассечения шеи, такие как одностороннее или двустороннее рассечение шеи (5–10). Настоящие результаты, демонстрирующие связь между LND и общей выживаемостью, согласуются с предыдущими данными (5-10).
Что касается рака головы и шеи, в многочисленных исследованиях сообщается о связи между LND и общей выживаемостью у пациентов с OSCC (5–9). Кроме того, Rudra и др. (10) сообщили, что LND предсказывает общее время выживания у субъектов с поражениями в различных участках головы и шеи, включая ротоглотку, ротовую полость и гортань / гортань; однако в этом исследовании не изучалась взаимосвязь между LND и общей выживаемостью у пациентов с карциномой основной слюнной железы (10).В настоящем исследовании связь между LND и общей выживаемостью оценивалась у субъектов с карциномой основной слюнной железы, демонстрируя, что LND ≥0,38 у пациентов с патологическими метастазами в лимфатические узлы значительно коррелирует с более коротким общим временем выживания.
Преобладающим ограничением текущего исследования было относительно небольшое количество субъектов в выборке. Следовательно, будущий анализ большого числа пациентов даст более статистически точные результаты с большим потенциалом их применения.
В заключение, настоящее исследование впервые продемонстрировало, что LND ≥0,38 у пациентов с карциномой большой слюнной железы с патологическим метастазированием в лимфатические узлы значительно коррелирует с более коротким общим временем выживания. Следовательно, LND является прогностическим фактором у людей с большой карциномой слюнных желез.
Выражение признательности
Настоящее исследование было поддержано Японским обществом содействия научным грантам для научных исследований (грант №247
Ссылки
1. Ettl T, Schwarz-Furlan S, Gosau M, Reichert TE. Карциномы слюнных желез. Oral Maxillofac Surg. 2012; 16: 267–283. DOI: 10.1007 / s10006-012-0350-9. [PubMed] [CrossRef] [Google Scholar] 2. Барнс Л., Эвесон Дж. В., Райхарт П., Сидранский Д., редакторы. Патология и генетика опухолей головы и шеи. Лион: IARC Press; 2005. Классификация опухолей Всемирной организации здравоохранения.[Google Scholar] 3. Окабе М., Миябе С., Нагацука Х., Терада А., Ханаи Н., Йокои М., Симозато К., Эймото Т., Накамура С., Нагаи Н. и др. Транскрипт слияния MECT1-MAML2 определяет благоприятную подгруппу мукоэпидермоидной карциномы. Clin Cancer Res. 2006; 12: 3902–3907. DOI: 10.1158 / 1078-0432.CCR-05-2376. [PubMed] [CrossRef] [Google Scholar] 4. Амит М., Наара С., Шарма К., Рамер Н., Рамер И., Агбетоба А., Глик Дж., Ян Х, Лей Д., Бьорндал К. и др. Избирательная диссекция шеи у пациентов с аденоидно-кистозной карциномой головы и шеи: международное совместное исследование.Энн Сург Онкол. 2015; 22: 1353–1359. DOI: 10.1245 / s10434-014-4106-7. [PubMed] [CrossRef] [Google Scholar] 5. Патель С.Г., Амит М., Йен Т.С., Ляо К.Т., Чатурведи П., Агарвал Дж. П., Ковальски Л. П., Эбрахими А., Кларк Дж. Р., Чернеа С. Р. и др. Плотность лимфатических узлов при раке полости рта: результаты Международного консорциума исследований результатов. Br J Рак. 2013; 109: 2087–2095. DOI: 10.1038 / bjc.2013.570. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 6. Ким С.Ю., Нам С.И., Чой С.Х., Чо К.Дж., Ро Дж.Л. Прогностическое значение плотности лимфатических узлов у пациентов с плоскоклеточным раком полости рта с положительными узлами.Энн Сург Онкол. 2011; 18: 2310–2317. DOI: 10.1245 / s10434-011-1614-6. [PubMed] [CrossRef] [Google Scholar] 7. Гил З., Карлсон Д.Л., Бойл Дж.О., Краус Д.Х., Шах Дж.П., Шаха А.Р., Сингх Б., Вонг Р.Дж., Пател С.Г. Плотность лимфатических узлов является важным предиктором исхода у пациентов с раком полости рта. Рак. 2009. 115: 5700–5710. DOI: 10.1002 / cncr.24631. [PubMed] [CrossRef] [Google Scholar] 8. Амар А., Рапопрт А., Куриони О.А., Дедивитис Р.А., Чернеа С.Р., Брандао LG. Плотность метастатических лимфатических узлов как прогностический фактор при плоскоклеточном раке языка и дна рта.Браз Дж Оториноларингол. 2012; 78: 86–90. DOI: 10.1590 / S1808-86Nodal staging
Cancer Imaging.2009; 9 (1): 104–111.
Отделение клинической радиологии, Королевская больница Марсден, Даунс-Роуд, Саттон, SM2 5PT, Великобритания
Автор для корреспонденции: д-р Доу-Му Ко, Академический отдел радиологии, Королевская больница Марсден, Даунс-роуд, Саттон, SM2 5PT, Великобритания. Электронная почта: ku.oc.oohay@hsenagsadadnaks Copyright © 2009 Международное общество визуализации рака Эта статья цитируется в других статьях в PMC.Abstract
Метастазы в лимфатические узлы являются плохим прогностическим показателем для многих опухолей, поэтому точное определение стадии важно до начала лечения.Наличие метастазов в лимфатических узлах может значительно изменить ведение пациента, и поэтому точная диагностика наличия и степени поражения лимфоузлов может помочь оптимизировать ведение пациента. В этом обзоре обсуждаются рентгенологические особенности, которые помогают дифференцировать злокачественные и доброкачественные лимфатические узлы. Выделены ключи к успешной интерпретации результатов поперечной компьютерной томографии (КТ) и магнитно-резонансной томографии узловых метастазов. Обсуждается клиническая роль позитронно-эмиссионной томографии-КТ для определения стадии узлов, и рассматриваются новые методы визуализации, которые могут еще больше повысить точность постановки узлов.
Ключевые слова: Лимфатический узел, компьютерная томография, магнитно-резонансная томография
Введение
Узловую болезнь чаще всего определяют с помощью системы стадирования TNM. Это классифицирует опухоли по степени опухоли, вовлечению узлов и наличию или отсутствию метастазов. Узловая стадия имеет прогностическое значение и поэтому влияет на выбор терапии. Узловая стадия некоторых опухолей (например, толстой кишки, желудка, груди и почек) определяется количеством регионарных лимфатических узлов.В других опухолях, таких как легкие, пищевод и простата, узловая стадия определяется участком поражения.
Новые методы визуализации, такие как позитронно-эмиссионная томография (ПЭТ) и ПЭТ-компьютерная томография (КТ), все чаще используются для диагностики поражения узлов.
Визуализация лимфатических узлов в онкологии
Исторически контрастная лимфография использовалась для оценки лимфатических узлов, но ее заменили УЗИ, КТ и магнитно-резонансная томография (МРТ).КТ является основным методом визуализации для начальной оценки узлов и определения стадии опухоли, хотя новые методы, такие как ПЭТ-КТ, используются все чаще. Визуализация с помощью обычных методов используется для различения злокачественных и доброкачественных лимфатических узлов следующим образом.
Ультразвук
Поверхностные лимфатические узлы, особенно в области головы и шеи, подмышечной впадины и паховой области, поддаются ультразвуковой оценке (УЗИ). Нормальный лимфатический узел имеет яйцевидную форму, гипоэхогенный по отношению к соседней мышце и часто содержит эхогенную жировую ткань ворот (а).Хилум представляет собой линейную, эхогенную, незатененную структуру, которая содержит узловые сосуды и кажется непрерывной с жиром вокруг узла. Ключевым преимуществом УЗИ является возможность получения цитологического образца под визуальным контролем (б). К недостаткам ультразвука относятся значительная вариабельность внутри и между операторами, а также его ненадежность для оценки глубоких метастатических лимфатических узлов. Глубоко расположенные лимфатические узлы в теле также трудно визуализировать.
(A) Ультразвук, демонстрирующий нормальный лимфатический узел у 24-летнего мужчины.(B) Ультразвук, демонстрирующий тонкоигольную аспирацию неправильного правого надключичного лимфатического узла у 46-летней женщины с раком груди.
Следующие критерии были применены для различения нормальных и злокачественных узлов при УЗИ.
Размер узла
Лимфатические узлы размером более 1 см в диаметре короткой оси считаются злокачественными. Однако порог размера зависит от анатомического участка и основного типа опухоли; например при раке прямой кишки лимфатические узлы размером более 5 мм считаются патологическими.
Форма узлов
Доброкачественные узлы чаще имеют яйцевидную форму и становятся более округлыми в результате злокачественной инфильтрации. Если отношение диаметра длинной оси к диаметру короткой оси меньше 2, лимфатический узел с большей вероятностью будет злокачественным [ 1 ] .
Узловой вид
Сонографические особенности, которые встречаются при злокачественных новообразованиях, включают потерю эхогенных узловых ворот, нерегулярный узловой контур и внутреннюю узловую неоднородность.
Васкуляризация при ультразвуковой допплерографии
Нормальные и доброкачественные узлы имеют тенденцию проявлять центральную васкуляризацию корней и центральную симметричную васкуляризацию. Злокачественные узлы имеют тенденцию демонстрировать эксцентрическую или отсутствующую внутригрудную васкуляризацию, мультифокальную аберрантную васкуляризацию, периферическую перфузию, очаговые дефекты перфузии или периферическую субкапсулярную васкуляризацию [ 2 , 3 ] . Злокачественные узлы имеют более высокий индекс резистентности (> 1,0) и индекс пульсации (> 1.5) [ 4 , 5 ] . Сонографическая контрастная среда увеличивает восприятие узловых кровеносных сосудов, но это не обязательно улучшает точность обнаружения злокачественных узлов [ 6 , 7 ] .
КТ и МРТ
На КТ-визуализации нормальные лимфатические узлы хорошо видны на КТ. Они имеют яйцевидную форму и имеют плотность мягких тканей. МРТ должна охватывать весь путь локорегионального распространения оцениваемой опухоли, а используемые последовательности зависят от оцениваемой анатомической области.Лимфатические узлы лучше всего демонстрируются на T1-взвешенных изображениях, а нормальные лимфатические узлы обычно равны мышцам на T1-взвешенных изображениях, изоинтенсивны или слегка гиперинтенсивны на T2-взвешенных изображениях. Последовательности с коротким временем инверсии тау (STIR) полезны, поскольку злокачественные узлы могут иметь высокую интенсивность сигнала (). Однако это неспецифично для злокачественных новообразований и поэтому не всегда может использоваться для дифференциации доброкачественных лимфатических узлов от злокачественных. Кроме того, изменение сигнала лимфатического узла во время терапии может быть полезным для оценки ответа на терапию.
Коронарное STIR-изображение, демонстрирующее узел высокой интенсивности сигнала (стрелка) в правой области уровня II у 67-летнего пациента мужского пола с плоскоклеточным раком ротоглотки.
Наиболее широко используемыми критериями КТ и МРТ для определения доброкачественности или злокачественности узла является размер узла. Увеличение узлов может быть результатом реактивной узловой гиперплазии или случайных заболеваний. При оценке поражения узлов необходимо учитывать следующие параметры.
Размер
В настоящее время единственным широко распространенным методом различения нормальных и патологических узлов является их размер.Существуют значительные различия между наблюдателями в оценке лимфатических узлов, и поэтому узлы должны быть измерены с использованием воспроизводимого метода. Диаметр короткой оси лимфатического узла должен быть измерен, поскольку было продемонстрировано, что он постоянен, несмотря на ориентацию, потому что он, вероятно, станет более округлым до того, как удлиняется. Диаметр короткой оси измеряется перпендикулярно самому длинному диаметру лимфатического узла.
В брюшной полости верхний предел диаметра короткой оси нормальных узлов колеблется от 6 до 10 мм [ 8 , 9 ] .Например, верхний предел нормального ретрокрурального узла составляет 6 мм, забрюшинного узла — 10 мм [ 10 ] и 8–10 мм для узлов в тазу [ 10 , 11 , ] .
К сожалению, 10–20% локорегиональных узлов нормального размера будут содержать опухолевые отложения, а 30% увеличенных узлов будут демонстрировать только воспалительную гиперплазию [ 12–14 ] . В некоторых опухолях частота метастазов в узлы нормального размера выше, чем в других.Например, у пациентов с колоректальным раком 90% узловых метастазов возникают в узлах <1 см [ 13 , 15 ] .
Форма и контур
Полезность узловой формы при КТ или МРТ менее определена по сравнению с сообщениями в ультразвуковой литературе. Однако узловой контур на КТ и МРТ может иметь большее различительное значение. Злокачественные узлы демонстрируют неправильные границы из-за экстракапсулярного распространения болезни.Было показано, что это более точно, чем размер узла, при определении вовлечения мезоректальных узлов с использованием МРТ у пациентов с раком прямой кишки [ 16 ] .
Количество узлов
Группа узлов, которые в остальном выглядят нормально на КТ или МРТ, вызывают беспокойство и могут указывать на злокачественные новообразования (например, в корне брыжейки тонкой кишки у пациентов с лимфомой). Однако специфичность этого признака невысока и может привести к ложноположительной интерпретации [ 17 ] .
Морфология узлов
Ряд функций может помочь определить метастатическое поражение на КТ и МРТ:
Плотность жира. Нормальный узел имеет тенденцию иметь однородный вид, а наличие жира часто, но не всегда, указывает на доброкачественность.
Расчеты. Гранулематозная болезнь может вызывать доброкачественные кальцификации средостенных и брыжеечных лимфатических узлов. Это также можно наблюдать на КТ в метастатических узлах, возникающих при раке прямой кишки, молочной железы, мочевого пузыря и яичников.Злокачественные узлы могут иметь кальцификаты после успешного лечения, например, при лимфоме и семиноматозных опухолях зародышевых клеток, но это не является надежным показателем полного ответа опухоли на лечение.
Неоднородный внешний вид. Крупные метастатические узлы часто выглядят неоднородными на КТ с контрастным усилением и МРТ. Узловой центр с более низкой плотностью на КТ может быть результатом некроза, и это особенно часто встречается при первичном плоскоклеточном раке головы и шеи, и даже некротические узлы нормального размера у этих пациентов следует рассматривать как злокачественные.На Т2-взвешенной МРТ центральный некроз демонстрирует высокий сигнал, и это имеет очень высокую положительную прогностическую ценность у пациентов с раком шейки матки [ 18 ] . У пациентов с раком прямой кишки неоднородность узлового сигнала является признаком злокачественных мезоректальных лимфатических узлов на Т2-взвешенной МРТ высокого разрешения [ 16 ] .
КТ с контрастным усилением, демонстрирующая увеличенный гетерогенный правый наружный подвздошный лимфатический узел (стрелка) у 64-летнего пациента с раком эндометрия.
Кистоз низкой плотности. Метастатические узлы, возникающие из несеминоматозной опухоли половых клеток яичек, часто демонстрируют центральную низкую плотность на CT () [ 19 ] . Вероятно, что в эту группу опухолей вовлечен не увеличенный кистозный лимфатический узел. Обычно это высокий сигнал на изображениях, взвешенных по T2. Изменение от твердого до кистозного в лимфатическом узле после химиотерапии у пациентов с несеминоматомозной полноклеточной опухолью представляет собой зрелую дифференцировку тератомы.Узлы с низкой аттенюацией не являются патогномоничными для злокачественной инфильтрации, поскольку они обнаруживаются при туберкулезе и грибковых инфекциях.
КТ с усилением аксиального контрастирования, демонстрирующая большой левый общий подвздошный кистозный лимфатический узел (стрелка) у 34-летнего мужчины с герминогенной опухолью.
Повышение контрастности. Гетерогенное увеличение увеличенного узла, вероятно, представляет собой злокачественную инфильтрацию [ 20 , 21 ] .Метастатические узлы могут демонстрировать картину усиления, аналогичную первичной опухоли [ 22 ] .
Узловые характеристики сигнала на МРТ. Как правило, невозможно различить злокачественные (a, b) и доброкачественные узлы на МРТ только на основании характеристик узлового сигнала, поскольку нормальные узлы возвращают диапазон интенсивностей сигнала на T1- и T2-взвешенных изображениях.
(A) Т1-взвешенное осевое изображение таза, демонстрирующее несколько увеличенных паховых лимфатических узлов (стрелка), которые являются слабым сигналом у 61-летней женщины с раком шейки матки.(B) Насыщенные жиром постконтрастные изображения таза, демонстрирующие несколько увеличенных паховых лимфатических узлов (стрелка), которые имеют высокий сигнал у 61-летней женщины с раком шейки матки.
Возможные ошибки при узловой оценке на CT
Использование многоплоскостного переформатирования снижает вероятность ошибок в интерпретации. И нормальные структуры, и другие патологические процессы могут имитировать узловую болезнь. Распространенные ошибки включают (а) петли тонкой кишки в непосредственной близости от забрюшинного пространства, которые могут имитировать узловую болезнь; (б) нормальные яичники могут имитировать увеличение наружных узлов подвздошной кости; (c) кровеносные сосуды и особенно аберрантные сосуды могут быть ошибочно приняты за лимфатический узел, особенно при КТ без контрастного усиления; нормальные анатомические варианты, такие как левосторонняя нижняя полая вена (НПВ) или дублированная НПВ, могут имитировать узловое заболевание; выступающие цистерны хили могут также имитировать увеличение ретрокруральных узлов [ 23 ] ; (г) узелки брюшины могут имитировать мезентериальные или тазовые лимфатические узлы; (д) послеоперационная гематома и абсцессы могут имитировать лимфоузел; (f) после операции лимфоцели могут имитировать лимфатический узел с низкой аттенюацией.
ПЭТ и ПЭТ-КТ
ПЭТ, выполненный с фтор-2-дезокси-D-глюкозой (ФДГ), оказался ценным в предоставлении важной качественной и количественной метаболической информации, связанной с опухолью, которая имеет решающее значение для диагностики и последующего наблюдения. ПЭТ-КТ — это уникальная комбинация анатомической информации поперечного сечения, предоставленной КТ, и метаболической информации, предоставленной ПЭТ, которые собираются во время одного исследования и объединяются. Поглощение ФДГ используется для различения доброкачественных и злокачественных узлов.ПЭТ-КТ может обнаруживать злокачественные новообразования в неувеличенных узлах, что может привести к изменениям в лечении пациентов. Появляется все больше доказательств использования ПЭТ-КТ для оценки поражения узлов при различных типах опухолей, включая опухоли пищевода, шейки матки, головы и шеи и меланому. Например, при раке пищевода недавнее исследование продемонстрировало, что использование изображений ПЭТ-КТ улучшает стадирование узлов на 30% по сравнению с параллельным чтением изображений ПЭТ и КТ [ 24 ] .
Изображение ПЭТ-КТ, демонстрирующее правый запирательный лимфатический узел (стрелка) у 29-летней женщины с мелкоклеточным раком шейки матки.
Некоторые опухоли являются FDG-отрицательными, и их можно исследовать с помощью других индикаторов, таких как [ 11 C] ацетат. Рак простаты демонстрирует заметное поглощение [ 11 C] ацетата не только при первичном раке простаты, но и в его метастатических участках (включая лимфатические узлы). [ 11 C] Ацетат имеет более высокую чувствительность, чем FDG-PET при оценке пациентов с раком простаты.
Тем не менее, при использовании ПЭТ-КТ для определения стадии узлов существуют некоторые потенциальные подводные камни. К ним относятся: (а) узлы размером менее 1 см могут быть недоступны для ПЭТ-камеры по обнаружению активности индикатора; (б) опухоли с низким метаболизмом ФДГ (например,грамм. бронхоальвеолярно-клеточная карцинома, карцинома предстательной железы, лимфома низкой степени злокачественности) могут привести к ложноотрицательным результатам; (c) воспалительные процессы могут вызывать ложноположительные результаты.
Оптимизация оценки узлов с помощью визуализации
Метастазы часто обнаруживаются в узлах, которые не увеличиваются по общепринятым критериям [ 25 ] . Ключ к успешной интерпретации изображений узловых заболеваний требует глубокого понимания нормальной узловой анатомии, путей распространения, клинических и патологических особенностей заболевания.
Типы распространения опухоли
Понимание пути распространения опухоли позволяет тщательно изучить наиболее вероятные места поражения узлов. Например, карцинома простаты распространяется через лимфатические сосуды в сосудисто-нервных пучках к запирательным, пресакральным, гипогастральным и внешним подвздошным лимфатическим узлам. Далее распространяется на общие подвздошные и парааортальные узлы. Обтюраторные и наружные подвздошные узлы обычно вовлекаются в 50–60% случаев [ 26 ] .Другой пример, когда знание пути распространения помогает в диагностике, — это пациенты с раком яичек. Лимфатическое распространение происходит по лимфатическим каналам, которые сопровождают семенной канатик. Эти лимфатические сосуды стекают в узлы забрюшинного пространства. Как правило, опухоли правого яичка распространяются на забрюшинные узлы справа (прекавальные, паракавальные, аортокавальные и ретрокавальные узлы), а левосторонние опухоли распространяются на левые преаортальные и парааортальные узлы.
Клинические и патологические признаки
Частота узловой болезни увеличивается со стадией первичной опухоли в большинстве опухолей брюшной полости и таза. Степень и другие гистологические характеристики опухолей влияют на вероятность узловых метастазов; например при раннем раке желудка наличие подслизистой и сосудистой инвазии предсказывает вероятность узлового заболевания [ 27 ] . Другие биологические показатели могут помочь предупредить рентгенолога о вероятности узловых метастазов.Например, у пациентов с раком простаты высокий уровень простатоспецифического антигена (ПСА) или высокий балл по шкале Глисона при биопсии имеют более высокую вероятность поражения узлов и экстракапсулярной болезни предстательной железы и узловой болезни.
Подробная информация о предыдущем лечении
Знания о предыдущей терапии жизненно важны, поскольку она изменяет картину лимфоузлов. Например, у пациентов с раком простаты рецидив лимфоузла после лучевой терапии или радикальной простатэктомии обычно происходит за пределами таза [ 28 ] .После операции тотального мезоректального иссечения рака прямой кишки рецидив лимфоузлов может произойти в пределах запирательной цепи вдоль боковой стенки таза или более краниально в забрюшинном пространстве.
Диагностическая точность узловой стадии
Диагностическая точность КТ и МРТ для узловой стадии рака брюшной полости и таза широко варьируется в литературе. Для злокачественных новообразований малого таза точность КТ и МРТ одинакова [ 29–31 ] .Сообщаемая чувствительность составляет от 40 до 87%, а специфичность — от 64 до 100%. В исследовании рака поджелудочной железы чувствительность 14%, специфичность 85% и точность 73% были достигнуты для узловой стадии [ 29–33 ] . Обычные КТ и МРТ ограничены их способностью обнаруживать метастазы в нормальных или минимально увеличенных лимфатических узлах.
У пациентов с лимфомой было обнаружено, что ПЭТ-КТ превосходит визуализацию 67 Ga и равна или превосходит КТ для обнаружения узловой и экстранодальной лимфомы на начальной стадии [ 34 ] .
Оценка узлового ответа на лечение
Согласно недавно пересмотренным критериям RECIST 1.1 [35] , патологические узлы, идентифицированные как целевые поражения, должны соответствовать критерию короткой оси диаметром не менее 15 мм на КТ. Размер нецелевых лимфатических узлов составляет от 10 до 15 мм, а размер лимфатических узлов менее 10 мм считается нормальным.
Лимфатические узлы, идентифицированные как целевые поражения, всегда должны иметь регистрацию фактического измерения по короткой оси, даже если узлы регрессируют до уровня ниже 10 мм.Это означает, что когда лимфатические узлы включены в качестве целевых поражений, сумма поражений может отличаться от нуля, даже если удовлетворяются критерии полного ответа, поскольку нормальный лимфатический узел определяется как имеющий короткую ось <10 мм. Для получения полного ответа каждый узел должен иметь короткую ось <10 мм. Для частичного ответа, стабильного заболевания и прогрессирующего заболевания фактическое измерение узлов по короткой оси включается в сумму целевых поражений.
Достижения в узловой стадии
МР-лимфография
МР-лимфография — это метод визуализации, который помогает различать злокачественные и доброкачественные узлы на основе рисунка и степени усиления контраста независимо от размера или морфологии узлов.МР-лимфография выполняется после введения лимфотрофного МР-контрастного вещества, в котором наиболее широко применяются сверхмалые частицы оксида железа (USPIO).
После введения USPIO частицы проникают в интерстициальные пространства и переносятся лимфатическими сосудами в лимфатические узлы. Внутри лимфатических узлов частицы USPIO фагоцитируются узловыми макрофагами, что приводит к потере сигнала в нормальных узлах на Т2 * -взвешенной визуализации (a, b). Злокачественные узлы имеют высокую интенсивность сигнала на изображениях, взвешенных по Т2 *.
Нормальные боковые узлы (стрелки), полученные с помощью Т2 * -взвешенной МРТ (MEDIC) (A) до и (B) через 24 часа после введения контрастного вещества USPIO 57-летнему мужчине с раком прямой кишки. До введения контрастного вещества кровеносные сосуды и лимфатические узлы имеют относительно высокую интенсивность сигнала. Обратите внимание на потемнение нормальных узлов после контрастирования, что облегчит их обнаружение.
При раке простаты этот метод показал очень обнадеживающие результаты для обнаружения злокачественных узлов размером <10 мм с высокой диагностической чувствительностью и специфичностью по сравнению с традиционными методами визуализации.Основным потенциальным преимуществом метода визуализации является способность обнаруживать частично замещенные не увеличенные злокачественные лимфатические узлы [ 36 ] .
МРТ с усилением USPIO в сочетании с МРТ с диффузионным взвешиванием
Новый подход к визуализации заключается в использовании МРТ с расширением USPIO в сочетании с МРТ с диффузионным взвешиванием (USPIO / DW-MRI). Было обнаружено, что комбинированный подход USPIO / DW-MRI имеет высокую отрицательную прогностическую ценность (86–93%), высокую точность (75–90%) и общую хорошую чувствительность (60–80%) при обнаружении узловых метастазов у пациентов. либо с раком простаты, либо с раком мочевого пузыря, либо с обоими заболеваниями [ 37 ] .Эти результаты были сопоставимы с результатами, полученными при оценке изображений USPIO с DW-MRI и без него. Главное преимущество этого нового подхода в том, что он намного быстрее; 13 минут для комбинированного USPIO / DW-MRI вместо 80 минут.
МРТ с диффузионно-взвешенной визуализацией
Контраст изображения при диффузионно-взвешенной визуализации основан на различиях в подвижности протонов воды между тканями и отражает клеточность ткани и целостность клеточных мембран. Опухолевые ткани, как правило, более клеточные по сравнению с нативными тканями, из которых они происходят, и поэтому они показывают высокий сигнал (ограниченная диффузия) на диффузионно-взвешенной МРТ.Было показано, что диффузионно-взвешенная МРТ улучшает обнаружение лимфатических узлов. Объединенные изображения, созданные путем добавления DW-MRI к обычному T1- или T2-взвешенному изображению, могут улучшить обнаружение небольших узлов по всему телу. Ранние отчеты об использовании диффузно-взвешенной визуализации для выявления злокачественных узлов у пациентов с раком головы и шеи и шейки матки были обнадеживающими.
Заключение
Точная идентификация злокачественных лимфатических узлов является серьезной проблемой в диагностической радиологии.КТ и МРТ ограничены в своей способности обнаруживать метастазы в нормальных или минимально увеличенных лимфатических узлах. Используя комбинацию размера, формы, характеристик и местоположения лимфатических узлов, идентифицированных при визуализации, рентгенолог может лучше определить, является ли лимфатический узел, вероятно, метастатическим. Функциональная визуализация с помощью ПЭТ-КТ повышает чувствительность и специфичность оценки узлов во многих опухолях, но имеет важные ограничения. Новые методы визуализации, такие как USPIO и диффузионно-взвешенная визуализация, по отдельности или в комбинации, могут дополнительно повысить диагностическую точность определения стадии узлов.
Ссылки
1. Steinkamp HJ, Cornehl M, Hosten N, Pegios W., Vogl T., Felix R. Цервикальная лимфаденопатия: отношение диаметра длинной оси к диаметру короткой оси как предиктор злокачественного новообразования. Br J Radiol. 1995; 68: 266–70. DOI: 10.1259 / 0007-1285-68-807-266. PMid: 7735765. [PubMed] [Google Scholar] 2. Na DG, Lim HK, Byun HS, Kim HD, Ko YH, Baek JH. Дифференциальный диагноз шейной лимфаденопатии: полезность цветной допплерографии. AJR Am J Roentgenol. 1997. 168: 1311–6. [PubMed] [Google Scholar] 3. Steinkamp HJ, Mueffelmann M, Böck JC, Thiel T., Kenzel P, Felix R.Дифференциальная диагностика поражений лимфатических узлов: полуколичественный подход с помощью цветного допплеровского ультразвукового исследования. Br J Radiol. 1998. 71: 828–33. [PubMed] [Google Scholar] 4. Чой М.Ю., Ли JW, Чан KJ. Различие между доброкачественными и злокачественными причинами шейной, подмышечной и паховой лимфаденопатии: значение допплеровского спектрального анализа формы волны. AJR Am J Roentgenol. 1995; 165: 981–4. [PubMed] [Google Scholar] 5. Магарелли Н., Гульельми Г., Савастано М. и др. Поверхностная воспалительная и первичная неопластическая лимфаденопатия: диагностическая точность энергетической допплерографии.Eur J Radiol. 2004. 52: 257–63. DOI: 10.1016 / j.ejrad.2003.10.020. PMid: 15544903. [PubMed] [Google Scholar] 8. Дорфман Р.Э., Альперн М.Б., Гросс Б.Х., Сандлер М.А. Лимфатические узлы верхней части живота: критерии нормального размера определяются с помощью КТ. Радиология. 1991; 180: 319–22. [PubMed] [Google Scholar] 9. Магнуссон, А. Размер нормальных забрюшинных лимфатических узлов. Acta Radiol Diagn (Stockh) 1983; 24: 315–8. [PubMed] [Google Scholar] 10. Эйнштейн Д.М., Зингер А.А., Чилкот В.А., Десаи Р.К. Абдоминальная лимфаденопатия: спектр результатов компьютерной томографии.Рентгенография. 1991; 11: 457–72. [PubMed] [Google Scholar] 11. Винникомб С.Дж., Норман А.Р., Николсон В., Муж Дж. Э. Нормальные тазовые лимфатические узлы: оценка с помощью КТ после двуногой лимфангиографии. Радиология. 1995; 194: 349–55. [PubMed] [Google Scholar] 12. Gross BH, Glazer GM, Orringer MB, Spizarny DL, Flint A. Метастатическая бронхогенная карцинома в лимфатические узлы нормального размера: частота и значимость. Радиология. 1988. 166 (1 Pt 1): 71–4. [PubMed] [Google Scholar] 13. Kayser K, Bach S, Bülzebruck H, Vogt-Moykopf I, Probst G.Участок, размер и поражение опухолью резецированных внелегочных лимфатических узлов при раке легкого. J Surg Oncol. 1990; 43: 45–9. DOI: 10.1002 / jso.20112. PMid: 2153261. [PubMed] [Google Scholar] 14. Staples CA, Müller NL, Miller RR, Evans KG, Nelems B. Узлы средостения при бронхогенной карциноме: сравнение КТ и медиастиноскопии. Радиология. 1988. 167: 367–72. [PubMed] [Google Scholar] 15. McLoud TC, Bourgouin PM, Greenberg RW и др. Бронхогенная карцинома: анализ стадирования средостения с помощью КТ путем корреляционного картирования лимфатических узлов и отбора проб.Радиология. 1992; 182: 319–23. [PubMed] [Google Scholar] 16. Браун Дж., Ричардс С.Дж., Борн М.В. и др. Морфологические предикторы состояния лимфатических узлов при раке прямой кишки с использованием МРТ высокого пространственного разрешения с гистопатологическим сравнением. Радиология. 2003. 227: 371–7. DOI: 10.1148 / radiol.2272011747. PMid: 12732695. [PubMed] [Google Scholar] 18. Ян В.Т., Лам В.В., Ю. М.Ю., Чунг Т.Х., Метревели С. Сравнение динамической спиральной компьютерной томографии и динамической МРТ-визуализации при оценке тазовых лимфатических узлов при карциноме шейки матки.AJR Am J Roentgenol. 2000; 175: 759–66. [PubMed] [Google Scholar] 19. Скатаридж Дж. К., Фишман Е. К., Кухайда Ф. П., Тейлор Г. А., Сигельман С. С.. Узловые метастазы низкого ослабления при раке яичка. J Comput Assist Tomogr. 1983; 7: 682–7. [PubMed] [Google Scholar] 20. Barentsz JO, Jager GJ, van Vierzen PB, et al. Определение стадии рака мочевого пузыря после трансуретральной биопсии: ценность быстрой динамической МРТ с контрастированием. Радиология. 1996; 201: 185–93. [PubMed] [Google Scholar] 21. Новорольский С.М., Фишбейн Н.Дж., Каплан М.Дж. и др.Проблемы динамической МРТ-визуализации шейных лимфатических узлов с контрастированием для выявления метастазов. J. Магнитно-резонансная томография. 2003. 17: 455–62. DOI: 10.1002 / jmri.10280. PMid: 12655585. [PubMed] [Google Scholar] 22. Муж Дж. Э., Ко ДМ. Рак мочевого пузыря. В: Муж Дж. Э., Резнек Р. Х., редакторы. Визуализация в онкологии. Лондон: Martin Dunitz Ltd; 2004. С. 343–74. [Google Scholar] 23. Голлуб М.Ю., Кастеллино РА. Хиллы цистерны: потенциальная имитация ретрокруральной лимфаденопатии на компьютерной томографии. Радиология. 1996; 199: 477–80.[PubMed] [Google Scholar] 24. Schreurs LM, Pultrum BB, Koopmans KP и др. Лучшая оценка метастазов в лимфоузлы при помощи слияния ПЭТ / КТ по сравнению с ПЭТ / КТ бок о бок при раке пищевода. Anticancer Res. 2008. 28 (3B): 1867–73. [PubMed] [Google Scholar] 26. Голимбу М., Моралес П., Аль-Аскари С., Браун Дж. Расширенная тазовая лимфаденэктомия при раке простаты. J Urol. 1979; 121: 617–20. [PubMed] [Google Scholar] 27. Сон К.М., Ли Дж. М., Ли Си, Ан Б., Пак С. М., Ким К. М.. Сравнение МРТ и КТ в диагностике рака желудка.AJR Am J Roentgenol. 2000; 174: 1551–7. [PubMed] [Google Scholar] 29. Ким Ш., Чой Б.И., Ли ХП и др. Карцинома шейки матки: сравнение результатов КТ и МРТ. Радиология. 1990; 175: 45–51. [PubMed] [Google Scholar] 30. Ким С.Х., Ким С.К., Чой Б.И., Хан М.С. Карцинома шейки матки: оценка метастазов в тазовые лимфатические узлы с помощью МРТ. Радиология. 1994; 190: 807–11. [PubMed] [Google Scholar] 31. Уильямс А.Д., Кузинс С., Сауттер В.П. и др. Обнаружение метастазов в тазовых лимфатических узлах при гинекологических злокачественных новообразованиях: сравнение КТ, МРТ и позитронно-эмиссионной томографии.AJR Am J Roentgenol. 2001; 177: 343–8. [PubMed] [Google Scholar] 33. Ойен Р. Х., Ван Поппель Х. П., Амей Ф. Э., Ван де Вурде В. А., Баерт А. Л., Баерт Л. В.. Определение стадии локализованной карциномы предстательной железы в лимфатических узлах с помощью тонкоигольной аспирационной биопсии под контролем КТ и КТ: проспективное исследование с участием 285 пациентов. Радиология. 1994; 190: 315–22. [PubMed] [Google Scholar] 34. Костакоглу Л., Леонард Дж. П., Коулман М., Голдсмит С. Дж. Роль изображений FDG-PET в лечении лимфомы. Clin Adv Hematol Oncol. 2004; 2: 115–21. [PubMed] [Google Scholar] 36.Харисингани М.Г., Баренц Дж., Хан П.Ф. и др. Неинвазивное обнаружение клинически скрытых метастазов в лимфатические узлы при раке простаты. N Engl J Med. 2003; 348: 2491–9. DOI: 10.1056 / NEJMoa022749. PMid: 12815134. [PubMed] [Google Scholar] 37. Thoeny HC, Triantafyllou M, Birkhaeuser FD, et al. Комбинированные сверхмалые суперпарамагнитные частицы усиленной оксидом железа и диффузионно-взвешенной магнитно-резонансной томографии надежно обнаруживают метастазы в тазовые лимфатические узлы в узлах нормального размера у пациентов с раком мочевого пузыря и простаты.Eur Urol. 2009; 55: 761–9. DOI: 10.1016 / j.eururo.2008.12.034. PMid: 1Масса шеи у взрослых — Американский семейный врач
1. Бхаттачарья Н. Факторы прогнозирования новообразований и злокачественных новообразований в области шеи. Arch Otolaryngol Head Neck Surg . 1999; 125: 303–7 ….
2. Армстронг В.Б., Giglio MF. Стоит ли беспокоиться об этой шишке на шее? Постградская медицина . 1998. 104: 63–4,67–71,75–6.пассим.
3. Келли Д. Д., Майер К. М.. Врожденные аномалии шеи. В: Твефик Т.Л., дер Калоустян В.М., ред. Врожденные аномалии уха, носа и горла. Нью-Йорк: Oxford University Press, 1997.
4. Гурин К.Г., Джонсон Дж. Т. Частота неожиданных метастазов в боковые кисты шейки матки. Ларингоскоп . 2000; 110 (10 пт 1): 1637–41.
5. Beenken SW, Мэддокс WA, Урист ММ. Обследование пациента с опухолью в шее. Adv Surg . 1995; 28: 371–83.
6. Джонсон И.Дж., Смит I, Акинтунде МО, Робсон А.К., Стаффорд FW. Оценка предоперационных исследований кист щитовидной железы. J R Coll Surg Edinb . 1996; 41: 48–9.
7. Tunkel DE, Domenech EE. Радиоизотопное сканирование щитовидной железы перед иссечением кисты щитовидно-язычного протока. Arch Otolaryngol Head Neck Surg . 1998. 124: 597–9.
8.Рис DH. Хронические воспалительные заболевания слюнных желез. Otolaryngol Clin North Am . 1999; 32: 813–8.
9. Марси С.М. Шейный аденит. Педиатр Инфекция Дис . 1985; 4 (3 доп.): S23–6.
10. Медина М, Гольдфарб Дж. Traquina D, Сили Б., Сабелла К. Аденит шейки матки и глубокая инфекция шеи, вызванные Streptococcus pneumoniae. Pediatr Infect Dis J . 1997; 16: 823–4.
11. McDermott LJ, Глассрот Дж., Mehta JB, Датт АК. Туберкулез. Часть I. Dis Mon . 1997. 43: 113–80.
12. Зюскинд DL, Обработчик SD, Том Л.В., Поцич В.П., Ветмор РФ. Нетуберкулезный микобактериальный цервикальный аденит. Clin Pediatr [Phila] . 1997; 36: 403–9.
13. Бенатор Д.А., Гордин FM. Нетуберкулезные микобактерии у пациентов с инфекцией вируса иммунодефицита человека. Заражение семенами респира . 1996. 11: 285–300.
14. О’Брайен Р.Дж., Гейтер LJ, Снайдер Д.Е. Младший Эпидемиология нетуберкулезных микобактериальных заболеваний в США. Результаты национального опроса. Am Rev Respir Dis . 1987; 135: 1007–14.
15. MacDonell KB, Глассрот Дж. Комплекс Mycobacterium avium и другие нетуберкулезные микобактерии у пациентов с ВИЧ-инфекцией. Заражение семенами респира .1989; 4: 123–32.
16. Карем КЛ, Paddock CD, Regnery RL. Bartonella henselae, B. quintana и B. bacilliformis: исторические патогены новой значимости. Микробы заражают . 2000; 2: 1193–205.
17. McCabe RE, Брукс Р.Г., Дорфман РФ, Remington JS. Клинический спектр в 107 случаях токсоплазматической лимфаденопатии. Ред. Заразить Dis . 1987. 9: 754–74.
18. Энгель Дж., Лидиатт Д.Д., Раскин Дж.Токсоплазмоз, проявляющийся как образование в передней части шеи. Ухо-носовое горло J . 1993; 72: 584–6.
19. Колдвелл DM, Новак З, Рю РК, Brega KE, Biffl WL, Оффнер Пи Джей, и другие. Лечение посттравматических псевдоаневризм внутренних сонных артерий эндоваскулярными стентами. J Травма . 2000; 48: 470–2.
20. Ландау А, Риз DJ, Блюменталь DR, Подбородок NW. Точечное образование на шее, проявляющееся кистой щитовидно-язычного протока. Rheum артрита . 1990; 33: 910–1.
21. Аллен Э.А., Али С.З., Ерозан Ю.С. Опухолевое отложение дигидрата пирофосфата кальция: цитопатологические данные при тонкоигольной аспирации. Диагностика Цитопатол . 1996; 15: 349–51.
22. Hytiroglou P, Брандвейн М.С., Штраухен JA, Миранте JP, Уркен М.Л., Биллер HF. Воспалительная псевдоопухоль парафарингеального пространства: клинический случай и обзор литературы. Голова Шея . 1992; 14: 230–4.
23. Armstrong WB, Эллисон Джи, Пена Ф, Kim JK. Болезнь Кимуры: два клинических случая и обзор литературы. Энн Отол Ринол Ларингол . 1998; 107: 1066–71.
24. Йи А.Ю., деТар М, Беккер Т.С., Рис DH. Гигантская гиперплазия лимфатических узлов головы и шеи (болезнь Кастлмена): отчет о пяти случаях. Отоларингол Хирургия головы и шеи . 1995; 113: 462–6.
25. Шах Великобритания, Белый JA, Gooey JE, Hybels RL. Отоларингологические проявления саркоидоза: картина и диагностика. Ларингоскоп . 1997; 107: 67–75.
26. МакГирт В.Ф. Дифференциальная диагностика новообразований шеи. В: Cummings CW, et al., Eds. Отоларингология — хирургия головы и шеи. 3-е изд. Сент-Луис: Мосби, 1998: 1686–99.
27. Баракат М, Наводнение LM, Осваль В.Х., Ракли RW. Лечение новообразования шеи: признак бессимптомного первичного злокачественного новообразования головы и шеи ?. Ann R Coll Surg Engl . 1987; 69: 181–4.
28. Ванебо HJ, Конесс Р.Дж., Макфарлейн Дж. К., Эйльбер FR, Байерс Р.М., Элиас Э.Г., и другие. Саркома головы и шеи: отчет регистра саркомы головы и шеи. Комитет по исследованиям Общества хирургов головы и шеи. Голова Шея . 1992; 14: 1–7.
29. Moosa M, Mazzaferri EL. Лечение новообразований щитовидной железы. В: Cummings CW, et al., Eds. Отоларингология, хирургия головы и шеи.3-е изд. Сент-Луис: Мосби, 1998: 2480–518.
30. Барнс Л. Патология головы и шеи: общие положения. В: Myers EN, Suen JY, ред. Рак головы и шеи. 3-е изд. Филадельфия: Сондерс, 1996: 17–32.
31. Мартин Х., Morfit HM. В шейной лимфе отмечают метастазирование как первый симптом рака. Surg Gynecol Obstet . 1944; 78: 133–59.
32. Jeghers H, Clark SL Jr, Templeton AC. Лимфаденопатия и лимфатические расстройства.В: Blacklow RS, ed. Признаки и симптомы МакБрайда: прикладная патологическая физиология и клиническая интерпретация. 6-е изд. Филадельфия: Липпинкотт, 1983: 467–533.
33. Шаха А, Уэббер С, Марти Дж. Тонкоигольная аспирация в диагностике шейной лимфаденопатии. Am J Surg . 1986; 152: 420–3.
34. Чао С, Торосян М.Х., Бораас MC, Сигурдсон ER, Хоффман Дж. П., Айзенберг Б.Л., и другие.Местный рецидив рака молочной железы в месте стереотаксической биопсии иглой: отчеты о клинических случаях и обзор литературы. Грудь J . 2001; 7: 124–7.
35. Йошикава Т, Ёсида Дж. Нисимура М, Ёкосэ Т, Нишиваки Y, Нагаи К. Имплантация рака легкого в грудную стенку после чрескожной тонкоигольной аспирационной биопсии. JPN J Clin Oncol . 2000; 30: 450–2.
36. Mighell AJ, Высокий AS.Гистологическая идентификация карциномы по следам иглы 21 калибра после тонкоигольной аспирационной биопсии карциномы головы и шеи. Дж. Клин Патол . 1998; 51: 241–3.
37. Ямагути К.Т., Сильный МС, Шапшай С.М., Сото Э. Посев околоушной карциномы по ходу иглы Вима-Сильвермана. Дж Отоларингол . 1979; 8: 49–52.
38. МакГирт В.Ф. Масса шеи. Мед Клин Норт Ам . 1999; 83: 219–34.
Произошла ошибка при настройке вашего пользовательского файла cookie
Произошла ошибка при настройке вашего пользовательского файла cookieЭтот сайт использует файлы cookie для повышения производительности. Если ваш браузер не принимает файлы cookie, вы не можете просматривать этот сайт.
Настройка вашего браузера для приема файлов cookie
Существует множество причин, по которым cookie не может быть установлен правильно. Ниже приведены наиболее частые причины:
- В вашем браузере отключены файлы cookie.Вам необходимо сбросить настройки своего браузера, чтобы он принимал файлы cookie, или чтобы спросить вас, хотите ли вы принимать файлы cookie.
- Ваш браузер спрашивает вас, хотите ли вы принимать файлы cookie, и вы отказались. Чтобы принять файлы cookie с этого сайта, используйте кнопку «Назад» и примите файлы cookie.
- Ваш браузер не поддерживает файлы cookie. Если вы подозреваете это, попробуйте другой браузер.
- Дата на вашем компьютере в прошлом. Если часы вашего компьютера показывают дату до 1 января 1970 г., браузер автоматически забудет файл cookie.Чтобы исправить это, установите правильное время и дату на своем компьютере.
- Вы установили приложение, которое отслеживает или блокирует установку файлов cookie. Вы должны отключить приложение при входе в систему или проконсультироваться с системным администратором.
Почему этому сайту требуются файлы cookie?
Этот сайт использует файлы cookie для повышения производительности, запоминая, что вы вошли в систему, когда переходите со страницы на страницу.Чтобы предоставить доступ без файлов cookie потребует, чтобы сайт создавал новый сеанс для каждой посещаемой страницы, что замедляет работу системы до неприемлемого уровня.
Что сохраняется в файле cookie?
Этот сайт не хранит ничего, кроме автоматически сгенерированного идентификатора сеанса в cookie; никакая другая информация не фиксируется.
Как правило, в файлах cookie может храниться только информация, которую вы предоставляете, или выбор, который вы делаете при посещении веб-сайта.



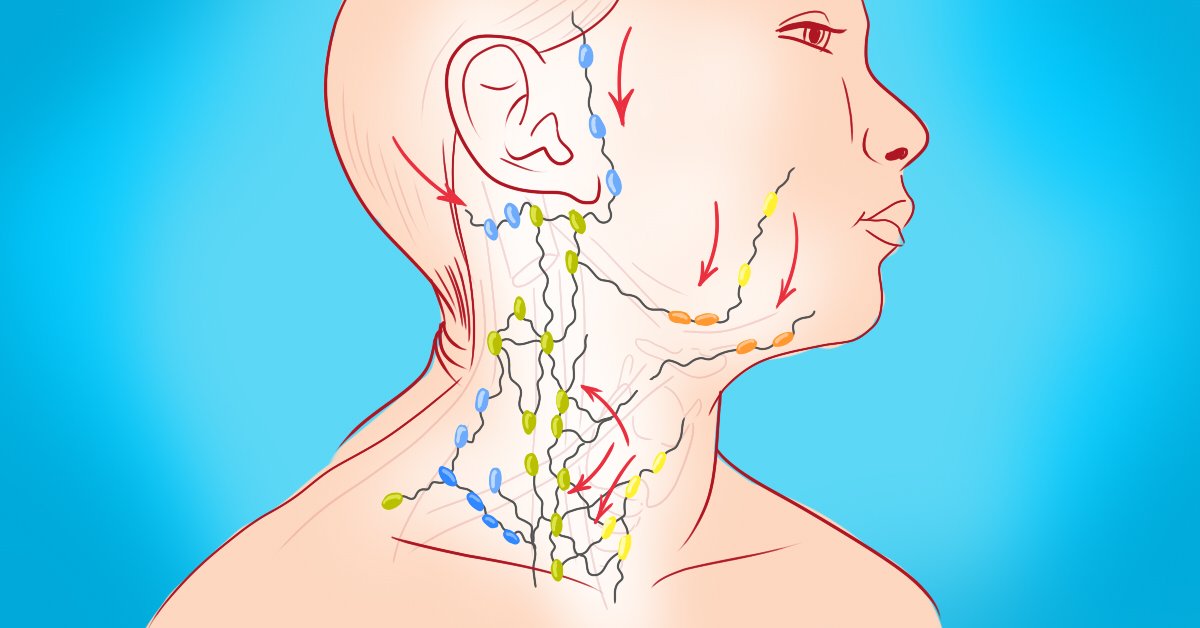
 Возникает боль в поражённой области, повышается температура, и появляются симптомы интоксикации: головные боли, слабость, ломота в мышцах и суставах.
Возникает боль в поражённой области, повышается температура, и появляются симптомы интоксикации: головные боли, слабость, ломота в мышцах и суставах.