| Компрессорные | Мембранный Меш-небулайзер | Ультразвуковой | |
| Стандартные растворы для небулайзерной терапии | C20, C21, С24, С24 Kids, C28, С29, С30, C300, C900 |
Micro A-I-R U22 | NE-U17 |
| М-холинолитики | |||
| Ипратропиум бромид (МНН) | |||
| Атровент (Boehringer Ingelheim), готовый раствор для ингаляций во флаконах по 20 мл | + | + | + |
| Ипратропиум Стери-Неб (Teva, Израиль), готовый раствор ампулах полиэтиленовых по 1 или 2 мл | + | + | + |
| В2-адреномиметики | |||
| Сальбутамол (МНН) | |||
| Вентолин небулы (GlaxoSmithKline, Великобритания), готовый раствор в небулах по 2,5 мл | + | + | + |
| Стери-Неб Саламол (Teva, Израиль), готовый раствор в ампулах по 2,5 мл | + | + | + |
| Фенотерол (МНН) | |||
| Беротек (Boehringer Ingelheim) во флаконах по 20 мл в дозе 1 мг/мл | + | + | + |
| Комбинированные препараты | |||
| Фенотерол + ипратрапиум брамид (МНН) | |||
Беродуал (Boehringer Ingelheim, Австрия). Выпускается во флаконах по 20 мл, 1 мл раствора содержит 250 мкг ипратропиума бромида и 500 мкг фенотерола. Требует разведения в 1-1,5 мл 0,9% раствора хлорида натрия. Выпускается во флаконах по 20 мл, 1 мл раствора содержит 250 мкг ипратропиума бромида и 500 мкг фенотерола. Требует разведения в 1-1,5 мл 0,9% раствора хлорида натрия. |
+ | + | + |
| Сальбутамол + ипратропиум бромид (МНН) | |||
| Ипрамол Стери-Неб (Teva, Израиль), готовый раствор в ампулах полиэтиленовых по 2,5 мл | + | + | + |
| Ингаляционные кортикостероиды | |||
| Будесонид (МНН) | |||
| Пульмикорт (AstraZeneca, Швеция)*, готовая суспензия в пластиковых контейнерах по 2 мл | + | + | — |
| Стабилизаторы мембран тучных клеток | |||
| Кромоглициевая кислота (МНН) Кромогексал (Hexal AG, Германия), готовый раствор в полиэтиленовых флаконах по 2 мл.  Не рекомендуется применять у детей до 2 лет Не рекомендуется применять у детей до 2 лет |
+ | + | + |
| Антибиотики, антисептики | |||
| Колистин натрий (МНН) | |||
| Колистин (ГРЮНЕНТАЛЬ, Германия). Порошок для приготовления раствора для ингаляций во флаконах в комплекте с растворителем (0,9% раствора хлорида натрия). Противопоказан детям до 6 лет. | + | + | — |
| Тиамфеникола глицинат ацетилцистеинат (МНН) | |||
Флуимуцил-антибиотик (Zambon Group, Италия). Комбинированный препарат ацетилцистеина и тиамфеникола антибиотика широкого спектра действия. Выпускается во флаконах в комплекте с растворителем (вода для инъекций). |
+ | + | — |
| Тобрамицин (МНН) | |||
| + | + | — | |
| Муколитики | |||
| Амброксол (МНН) | |||
| Лазолван (Boehringer Ingelheim, Австрия). Раствор для ингаляций во флаконах по 100 мл. Рекомендуемую дозу препарата следует развести стерильным физиологическим раствором (0,9% хлорид натрия) в соотношении1:1 непосредственно перед ингаляцией. | + | + | н/д |
| Ацетилцистеин (МНН) | |||
Флуимуцил (Zambon Group, Италия). Готовый раствор в ампулах из темного стекла по 3 мл Готовый раствор в ампулах из темного стекла по 3 мл |
+ | + | н/д |
| Дорназа альфа (МНН) | |||
| Пульмозим (Roche, США) готовый раствор в ампулах по 2,5 мл. Применять с осторожностью у детей до 5 лет. | + | + | н/д |
| Другие | |||
| Физиологический раствор 0,9% Увлажняют слизистую оболочку на всем ее протяжении от ротоглотки до мелких бронхов, смягчая катаральные явления, и увеличивают жидкую часть бронхиального секрета. |
+ | + | + |
Глава ФМБА рассказала об уникальном препарате от COVID-19
Федеральное медико-биологическое агентство 2 июня сообщило о регистрации нового уникального препарата «Лейтрагин», который предотвращает тяжелые осложнения в результате коронавируса.
— В чем принцип действия «Лейтрагина и почему он эффективен именно при цитокиновом шторме?
«Лейтрагин» — это препарат нового поколения гексапептид, который является аналогом агонистов опиоидных рецепторов. Он имеет целый спектр разных действий. Прежде всего, это снижение синтеза воспалительных цитокинов. Это важно, поскольку в период ранних симптомов ковидной пневмонии есть возможность, применив этот препарат в форме ингаляции, существенно профилактировать как развитие системной воспалительной реакции и, соответственно, развитие цитокинового шторма, так и развитие морфологических изменений в легких. Мы доказали, что препарат очень хорошо переносится и при этом он либо профилактирует, либо смягчает системные воспалительные проявления.
— Когда стоит использовать данное лекарство?
Лучше всего его использовать для пациентов со среднетяжелым COVID-19. В том случае, если на фоне температуры появляется кашель и на компьютерной томограмме есть уже проявление пневмонита ковидного, это показания к тому, чтобы начинать пользоваться этим препаратом.
— Его можно применять только в стационаре или в домашних условиях тоже?
На данном этапе мы зарегистрировали это лекарство для стационара. Это флаконы раствора по 10 миллилитров. Он используется в обычном небулайзере, через системы, позволяющие дышать и проводить ингаляции. Используется от 30 минут до часа, но 30-40 минут достаточно. Через 10 минут есть уже реакция, судя по нашим экспериментальным работам, но второй пик — это реакция через 30 минут с начала момента введения. Максимальный курс приема составляет 10 дней, но обычно, если на ранних стадиях начинать использовать этот препарат, то выраженный положительный эффект отмечается через 5-6 ингаляций.
— Есть ли какие-то побочные действия от «Лейтрагина»?
Мы не отмечали. Более того, мы не видели возможности передозировать этот препарат. Из всех больных, которые прошли, мы не имели ни одного случая утяжеления дыхательной недостаточности, развития острого респираторного дистресс-синдрома и развития цитокинового шторма. Все больные наши хорошо восстанавливались.
Ингаляционная терапия пневмонии. Лечение воспаления легких в Москве
При пневмонии воспалительный процесс развивается в легочной ткани. В бронхах образуется секрет, который нарушает проходимость бронхиального дерева. Нарушаются местные механизмы защиты. Врачи назначают лекарственные препараты, которые вводят в организм разными путями: через рот, внутримышечно, внутривенно. Ингаляции при воспалении лёгких являются элементом физиотерапевтического лечения. Пульмонологи Юсуповской больницы ингаляционным путём вводят антибиотики, бронхолитики, муколитики. Процедуры выполняют с помощью ультразвуковых ингаляторов, небулайзеров.
Процедуры выполняют с помощью ультразвуковых ингаляторов, небулайзеров.
Виды ингаляций
Основная цель ингаляционной терапии – достижение максимального местного терапевтического эффекта в дыхательных путях при незначительных проявлениях системного действия. Ингаляции при пневмонии оказывают следующее действие:
- улучшают дренажную функцию дыхательных путей;
- уменьшают отёк и стимулируют регенерацию;
- снижают активность воспалительного процесса;
- прерывают бронхоспазм;
- воздействуют на местные иммунные реакции респираторного тракта;
- улучшают микроциркуляцию слизистой оболочки дыхательных путей.
При пневмонии можно делать ингаляции, учитывая состояние пациента, показания и противопоказания.
Наиболее распространёнными видами ингаляций являются:
- паровые;
- тепловлажные;
- влажные;
- масляные;
- воздушные;
- ультразвуковые.
Наиболее доступными физиотерапевтическими процедурами являются паровые ингаляции.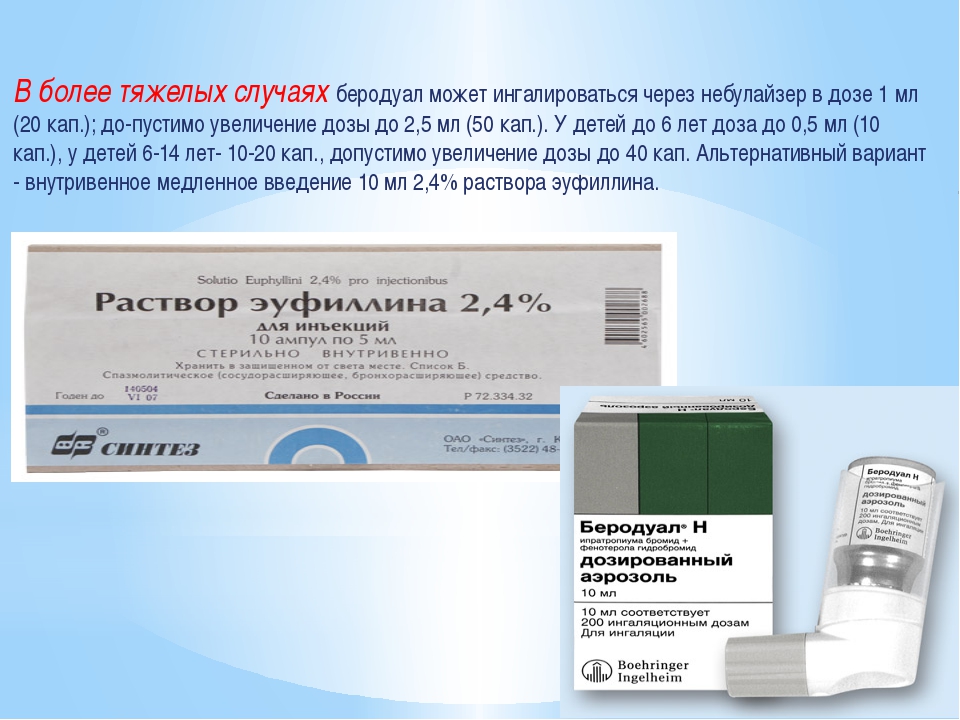 Их проводят с помощью паровых ингаляторов. Процедуры показаны пациентам с острыми и хроническими заболеваниями носовой полости, среднего уха, горла, острыми и хроническими заболеваниями трахеи и бронхов. Их делают при острых респираторных заболеваниях и гриппе, профессиональных заболеваниях органов дыхания. Противопоказаниями к паровым ингаляциям являются тяжёлые формы туберкулёза, пневмония, плеврит, кровохарканье, артериальная гипертензии, ишемическая болезнь сердца, гипертрофия и полипоз слизистых оболочек дыхательных путей.
Их проводят с помощью паровых ингаляторов. Процедуры показаны пациентам с острыми и хроническими заболеваниями носовой полости, среднего уха, горла, острыми и хроническими заболеваниями трахеи и бронхов. Их делают при острых респираторных заболеваниях и гриппе, профессиональных заболеваниях органов дыхания. Противопоказаниями к паровым ингаляциям являются тяжёлые формы туберкулёза, пневмония, плеврит, кровохарканье, артериальная гипертензии, ишемическая болезнь сердца, гипертрофия и полипоз слизистых оболочек дыхательных путей.
При выполнении влажных ингаляций лекарственное вещество с помощью портативного ингалятора распыляется и вводится в дыхательные пути без предварительного подогрева. Их делают с целью предупреждения высыхания слизистой оболочки трахеобронхиального дерева в условиях длительной искусственной вентиляции, для купирования отёка дыхательных путей, предупреждения бронхоспастической реакции, связанной с физической нагрузкой, гигиены дыхательных путей при наличии трахеостомы. Паровые ингаляции применяют в качестве симптоматической терапии заболеваний верхних дыхательных путей.
Паровые ингаляции применяют в качестве симптоматической терапии заболеваний верхних дыхательных путей.
Тепловлажные ингаляции вызывают покраснение слизистой оболочки дыхательных путей, подавляют упорный кашель, разжижают мокроту, ускоряют эвакуацию слизи, улучшают дренирующую функцию бронхов. Процедуры делают пациентам, страдающим подострыми и хроническими заболеваниями носа, горла и среднего уха, острыми и хроническими заболеваниями бронхов и трахеи. Они показаны при абсцессе лёгкого, бронхиальной астме, пневмосклерозе, профессиональных заболеваниях органов дыхания, гриппе и острых респираторных заболеваниях.
Масляные ингаляции основаны на распылении подогретых различных масел, которые обладают трофическим, восстановительным и бронхопротективным действием. Их применяют для лечения и профилактики острого воспаления слизистых дыхательных путей, при набухании и утолщении слизистых оболочек, неприятных ощущениях сухости гортани или в носу. Противопоказаниям являются нарушение дренажной функции бронхов и работа на производствах с большим количеством мелкой пыли.
Воздушные ингаляции проводятся путём распыления находящихся в баллончике лекарственных веществ легко испаряющимся газом или сжатым воздухом. Показаниями являются:
- подострые и хронические заболевания трахеи и бронхов;
- выраженный отёк;
- пневмония в стадии выздоровления;
- бронхиальная астма;
- профессиональные заболевания бронхов и лёгких
- состояния после операции на лёгких, сопровождающиеся гнойными осложнениями.
Во время ультразвуковых ингаляций жидкость разбивается на мелкие частицы при помощи ультразвука или механических колебаний ультравысокой частоты. Ультразвуковые ингаляции являются эффективным средством лечения абсцесса лёгкого, пневмосклероза, пневмонии в фазе выздоровления, профессиональных заболеваний лёгких.
Проведение ингаляций при пневмонии небулайзером
В Юсуповской больнице ингаляции при пневмонии проводят небулайзером. Они помогают остановить воспалительный процесс, улучшают работу бронхов и лёгких, восстанавливают их вентиляционную и дренажную функцию. Суть небулайзера состоит в том, что во время процедуры создаётся аэрозольный пар с частичками лекарственного средства, которое достигает слизистых оболочек бронхов и лёгких. Ингаляции небулайзером способствуют проникновению лекарственных средств в область без воспаления, что позволяет снижать дозу препарата, принимаемого внутрь.
Суть небулайзера состоит в том, что во время процедуры создаётся аэрозольный пар с частичками лекарственного средства, которое достигает слизистых оболочек бронхов и лёгких. Ингаляции небулайзером способствуют проникновению лекарственных средств в область без воспаления, что позволяет снижать дозу препарата, принимаемого внутрь.
Существуют компрессорные и ультразвуковые небулайзеры. Компрессорные небулайзеры преобразуют лекарственные препараты в аэрозольный пар с помощью создания давления в жидкости, а ультразвуковые – ультразвуком. Процедуры не выполняют при наличии следующих противопоказаний:
- индивидуальная непереносимость лекарственных препаратов, используемых для ингаляции;
- высокая температура;
- легочные и носовые кровотечения;
- легочные и сосудов носоглотки;
- артериальная гипертензия;
- инфаркты и инсульты;
- церебральный атеросклероз.
Препараты, применяемые для ингаляций
При вирусной пневмонии с помощью небулайзера распыляют в дыхательные пути следующие противовирусные препараты: человеческий лейкоцитарный интерферон, полудан (индуктор интерферона), аминокапроновая кислота, натрия тиосульфат.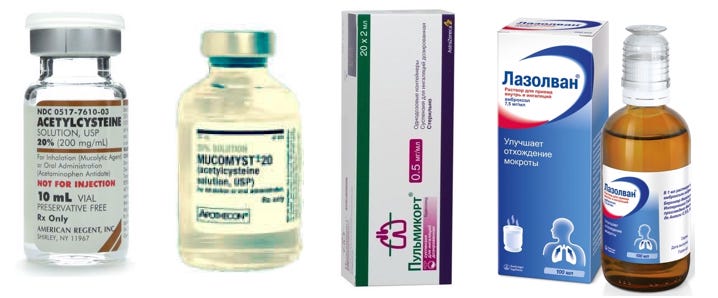 Ингаляционным путём в организм вводят иммуномодуляторы: лейкинферон, деринат. Щелочные растворы (натрия гидрокарбонат), натрия хлорид, аквамарис способствуют разжижжению мокроты.
Ингаляционным путём в организм вводят иммуномодуляторы: лейкинферон, деринат. Щелочные растворы (натрия гидрокарбонат), натрия хлорид, аквамарис способствуют разжижжению мокроты.
Муколитические препараты (АЦЦ, амброксол, флуимуцил, ринофлуимуцил, лазолван) применяют при нарушении бронхиальной проходимости у пациентов с пневмонией. Уменьшают воспалительный процесс препараты для местной антибактериальной терапии. К ним относится изофра (рифамицетин), полидекса, флуимуцил-антибиотик ИТ, амикацин.
Снимают спазм бронхов при пневмонии с помощью β2 агонистов короткого действия: вентолина, беротека. Их вводят с помощью небулайзера. Спазмолитическим эффектом обладают антихолинергические препараты: атровент, беродуал. После ингаляций этих лекарственных средств улучшается бронхиальная проходимость.
Ингаляции способствуют быстрому выздоровлению. Позвоните по телефону Юсуповской больницы, где врачи проводят комплексную терапию пневмоний, используют все пути введения лекарственных препаратов.
«Если пневмония вирусная, антибиотики бесполезны?» Пульмонологи отвечают на вопросы читателей
Пульмонологи отвечают на вопросы читателей
Что делать, если у ребенка частые ларингиты? Как выбрать ингалятор? Пневмонию вызывают вирусы или бактериальная инфекция? Продолжаем отвечать на вопросы читателей.
Наши эксперты:
главный внештатный пульмонолог Минздрава, кандидат медицинских наук, заведующая отделом пульмонологии и хирургических методов лечения болезней органов дыхания РНПЦ пульмонологии и фтизиатрии Елена Давидовская;
главный внештатный детский пульмонолог Минздрава, кандидат медицинских наук, декан педиатрического факультета Белорусского государственного медицинского университета Владимир Бобровничий.
«Какой ингалятор рекомендуют специалисты?»
Владимир Бобровничий: Прежде всего необходимо разобраться с причиной повторяющихся ларингитов. Для этого рекомендуем обратиться за консультацией аллерголога, оториноларинголога и пульмонолога. Выявленная причина позволит разработать тактику профилактики.
— Дочка первый раз обструктивным бронхитом заболела в 4 месяца, за год было 6 эпизодов. Сейчас ей 1,4 года, ставят риск астмы, и мы лечимся у аллерголога. Один раз все равно переболели. Как можно избежать повторной болезни? Какая профилактика? Можно ли сейчас утверждать, что это истинная астма? На каком основании могут поставить диагноз? Куда нам можно обратиться с консультацией?
Владимир Бобровничий: Учитывая описанную Вами ситуацию, необходима консультация пульмонолога.
— Перед покупкой ингалятора изучал интернет, и многие пишут о размере капель в облаке, которое выходит из ингалятора. Пишут, что важно выбирать с размером меньше 5, потому что большие оседают слишком рано и не доходят до бронхов. Так ли это? Потому что в аптеке увидел ингаляторы с значением больше 9 — такой ингалятор вылечит болезнь?
Елена Давидовская, Владимир Бобровничий: Судя по вопросу, речь идет о небулайзерах — ингаляторах, которые превращают лекарственные растворы в аэрозоль. В таком виде лекарственное средство легко вдыхается, попадая в нужные отделы дыхательных путей. Размер формируемых небулайзером частиц имеет принципиальное значение. Частицы диаметром 8−10 микрометров оседают в носоглотке, полости рта и трахее, диаметром от 5 до 8 микрометров — в трахее, от 3 до 5 микрометров — в бронхах, менее 3 микрометров в мелких дыхательных путях. Поэтому выбор небулайзера для аэрозольтерапии определяется локализацией болезни и размерами основной массы генерируемых частиц аэрозоля.
— У сына, после того как стал ходить в садик, начались частые простуды. Врач порекомендовал купить ингалятор. В аптеке широкий выбор от очень больших до совсем крохотных. Что рекомендуют специалисты? Какие новые технологии есть в этой сфере? Можно ли использовать маленькие, ручные?
Елена Давидовская, Владимир Бобровничий: Размер самого небулайзера (ингалятора) не имеет значения. Имеет значение размер частиц, мощность и производительность аппарата. Кроме того, выбор небулайзера определяется задачами самой терапии, состоянием и возрастом пациента. Среди новых технологий можно отметить МЭШ-ингалятроы (мембранные). Они сами по себе небольшого размера, их удобно брать с собой. По техническим характеристикам такие небулайзеры соответствуют всем предъявляемым требованиям.
Если пневмония вирусная, антибиотики бесполезны?
— Правда ли, что, если один раз переболел пневмонией, то потом неизбежны рецидивы? Возможна ли профилактика, чтобы не заболеть воспалением легких повторно?
Елена Давидовская, Владимир Бобровничий: Не правда. Как мы отмечали ранее, пневмония — это острое заболевание, которое в большинстве случаев при благоприятном течении заканчивается полным выздоровлением.
— Мне 38. В последние три года каждую зиму заболеваю воспалением легких. Лечусь в больницах. Чем опасны такие частые и периодичные пневмонии? Приводят ли они к каким-то изменениям в легких?
Елена Давидовская: Неосложненная пневмония не приводит к формированию изменений в легких. Повторяющиеся инфекционные процессы являются поводом для оценки окружающей среды — места, где вы живете и работаете. Помимо этого, вам необходимо пройти дополнительное обследование у пульмонолога.
— При каких симптомах следует обратиться к врачу, чтобы не было осложнений с пневмонией?
Елена Давидовская, Владимир Бобровничий: При наличии любых признаков острого респираторного заболевания необходимо обращаться к врачу.
— Прочитала, что пневмония может быть и грибкового генеза. Если у ребенка (16 лет) в ротовой полости по результатам мазка обнаружена небольшая концентрация candida 10*3, это фактор риска развития пневмонии? Повторный анализ эти грибы не выявил, но обнаружен staphylococuss aureus 10*4. Это количество опасно с точки зрения развития пневмонии? Нужно ли принимать антибиотики для избавления от него и профилактики пневмонии?
Владимир Борбровничий: Риск развития грибковой пневмонии высок у пациентов, получавших (ющих) иммуносупрессивную терапию, ВИЧ-инфицированных, имеющих иммунодефицит. Если у ребенка в мазках обнаружена небольшая концентрация candida — это не является фактором развития пневмонии. Не опасно и количество выявленного staphylococuss aureus. Принимать антистафилококковые антибиотики с целью профилактики пневмонии не нужно.
— В связи с ситуацией с новым китайским коронавирусом пневмонии с удивлением узнала, что, оказывается, пневмония может быть вызвана вирусами, а не только бактериями. Получается, если пневмония вирусная, антибиотики бесполезны? Определяют ли у нас врачи природу пневмонии? Если она вирусная, как ее лечат — без антибиотиков?
Елена Давидовская, Владимир Бобровничий: Действительно, заболевание может быть вирусной природы. В случае вирусной пневмонии антибиотики не эффективны. Однако вирусные инфекции являются своеобразным проводником бактериальной инфекции. Поэтому в клинической практике мы сталкиваемся с пневмониями вирусно-бактериальной природы. Причина пневмонии определяется при проведении лабораторного исследования, как вирусная, так и бактериальная. В случае вирусной природы пневмонии, например, из-за вируса гриппа, существует специфическое противогриппозное лечение препаратами группы ингибиторов нейраминидазы — озельтамивир, занамивир. При присоединении бактериальной инфекции назначается антибактериальная терапия с учетом клинической ситуации.
«Как восстановить легкие после 20 лет курения»
— Моей маме 81 год. Я хотела привить ее от пневмококков, обзвонила частные медцентры — вакцины нет. А ведь мама в группе риска. Где ей можно пройти вакцинацию?
Елена Давидовская: Вашей маме действительно показана вакцинация пневмококковой вакциной. О возможности проведения вакцинации, вам следует уточнить в поликлинике по месту жительства.
— У меня бабушка и мама болели астмой. В 2011 году диагностировали ее и мне. В настоящее время обострение каждый год в начале весны. В другие периоды беспокоит мокрота, которая скапливается периодически. Отдельную тревогу в последние 1,5 года вызывают при откашливании пробки. Горло не болит.
Елена Давидовская, Владимир Бобровничий: В вашем вопросе недостаточно информации. Не понятно, принимаете ли вы что-то из препаратов базисной терапии бронхиальной астмы. Учитывая клиническую симптоматику, рекомендуем обратиться к аллергологу или пульмонологу для обсуждения и коррекции плана лечения.
— Как восстановить легкие после 20-ти лет курения? Обо мне: женщина, 40 лет, сейчас не курю, бронхитом давно не болела, пневмония была в 17 лет, анализы в норме. Хочу избавиться от мокроты. Нужно обратиться к отоларингологу? Какой цвет мокроты в пределах нормы, а при каком нужно бить тревогу?
Елена Давидовская, Владимир Бобровничий: Первый, наиболее важный шаг для восстановления легочного здоровья, вы уже сделали. Откажитесь от вредной привычки раз и навсегда. После отказа от курения начинает восстанавливаться «очистительная» функция бронхов и какое-то время сохраняются кашель и выделение белесоватой или бледно-желтой мокроты. Длительность этого периода индивидуальна. Изменение окраски мокроты на интенсивно-желтый или желто-зеленый с увеличением ее количество может свидетельствовать об обострении бронхита, развившегося за время курения. В таких случаях необходимо обратиться к врачу.
Читать полностью: https://news.tut.by/society/670554.html
Фото: портал «Здоровые люди»
TUT.BY, 29 января 2020
Поделитесь
Как выбрать ингалятор, виды ингаляторов, небулайзеров
Из этой статьи Вы узнаете: как выбрать ингалятор, чем отличается ингалятор от небулайзера, какие существуют виды небулайзеров.
Медицина шагнула далеко вперёд и теперь есть возможность проведения ингаляций дома, без ежедневного посещения физкабинета или доктора. Для этой процедуры существуют специальные лечебно-профилактические приборы, которые называются ингаляторами.
Вас пугает широкий ассортимент предлагаемых ингаляторов? Не знаете, как сделать выбор и на какой модели из них остановиться? Надеемся, что наша статья поможет Вам разобраться в этом вопросе.
Всё гораздо проще, чем может показаться на первый взгляд. Главное, знать и понимать для себя следующие моменты:
- В каких ситуациях и при каком заболевании будет использоваться ингалятор?
- Какие лекарственные средства будут применяться?
- Кого будем лечить с помощью ингаляций?
Начнём с того, что все ингаляторы делятся на два типа: паровые и небулайзеры.
Это самый простой вариант ингаляторов. Работа их основана на испарении лекарственных веществ, частицы водяного пара прогревают носоглотку и верхние дыхательные пути, смягчают слизистые рта и носа. Применяется такой тип ингалятора при ангине, простуде, аллергии, гриппе, ОРЗ. Возможность использования в аппарате минеральных вод, эфирных и ароматических масел, отваров и настоев трав.
Как дополнение паровой ингалятор может применяться в косметических целях (очищающие и увлажняющие маски для лица).
Несмотря на ряд положительных моментов, этот метод (паровых ингаляций) имеет и свои недостатки. Остановимся и на них:
- Нельзя проводить ингаляцию при повышенной температуре тела больного (свыше 37,5С).
- Большинство лекарственных препаратов при нагревании разрушаются и теряют свои полезные свойства, поэтому существенно ограниченный список используемых лекарственных средств.
- Практикуется при заболеваниях только верхних дыхательных путей.
- Из противопоказаний – туберкулёз, воспаление лёгких, заболевания крови и сердечно — сосудистой системы.
Небулайзеры.
Это приборы, способные распылять лекарственное средство, превращать жидкость в аэрозоль. Принцип действия их заключается в дисперсном распылении действующего вещества лекарственного препарата на мелкие частицы (не больше 14 микрон). При проведении ингаляции с помощью небулайзера через специальную маску частицы способны проникать не только в верхние, но и средние, и нижние дыхательные пути. Лекарство легко попадает в организм и быстро усваивается, что способствует скорейшему выздоровлению или облегчению состояния больного.
В небулайзерах разрешён к применению более широкий спектр лекарственных препаратов, соответственно и лечить с помощью таких ингаляций можно значительно больше заболеваний.
Различают три вида небулайзеров:
Ультразвуковые — под воздействием высокочастотных колебаний (ультразвука) жидкое лекарственное средство превращается в аэрозоль и распыляетсяКомпрессорные – аэрозольное облако образуется с помощью поршневого компрессора, формируется мощный поток воздуха с содержанием частиц лекарственного препарата
Меш (электронно-сетчатые) – аэрозоль образуется при просеивании лекарственного раствора через вибрирующую сетку – мембрану с множеством микроскопических отверстий
Расскажем о преимуществах, особенностях и недостатках каждого из видов в сравнительной характеристике в зависимости от различного рода параметров.
Размер получаемых частиц
Компрессорные небулайзеры.
Приборы с одним режимом работы образуют в среднем частицы размеров в 3 микрона (не больше 5мкм), что позволяет им, проходя через верхние дыхательные пути, проникать и оседать в средних и нижних отделах. Чем мельче частица, тем глубже она опускается по дыхательной системе. В ингаляторах с разными режимами работы существует функция выбора размера частиц (переключение режима) для оптимальной ингаляции. Диаметр частиц колеблется в пределах от 0,5 до 14 мкм, что позволяет успешно ингалировать все отделы дыхательных путей. К тому же в комплект таких компрессорных небулайзеров входят специальные насадки и канюли для носа, что даёт возможность без труда лечить насморк, заложенность носа и т.п явления.
Ультразвуковые небулайзеры.
При работе этот вид ингаляторов производит аэрозоль с частицами в среднем от 1,5 до 5,7 мкм. Таким образом, данные приборы позволяют обрабатывать все отделы дыхательных путей, но более эффективно борются с заболеваниями среднего и нижнего отделов, так как частицы достаточно мелкие и проникают глубоко, их практически не остаётся в верхнем отделе. С помощью ультразвуковых аппаратов целесообразно лечить бронхи, лёгкие.
Электронно-сетчатые небулайзеры.
Работают за счёт применения Меш- технологии распыления лекарственных средств. Образуют аэрозольную смесь с мелкодисперсными частицами, размер их тоже не превышает отметку в 5,7 мкм. Примерно 70% из них оседают в нижнем и среднем отделах дыхательных путей и незначительная часть в верхнем. Тем не менее, как и ультразвуковые модели, меш – небулайзеры используются для лечения всех отделов, ведь даже в небольшом количестве, попавший с помощью ингаляции в организм лекарственный препарат, окажет куда больше пользы, чем просто выпитый курс медикаментов.
Режим работы ингалятора, длительность и настройки для оптимального лечения
Модели компрессорных небулайзеров могут быть без переключения режимов работы (управляются одной кнопкой) либо с 3-мя режимами (каждый из которых предназначен для воздействия на определённый отдел дыхательных путей). В режимных ингаляторах переключение происходит при повороте тумблера или смены пистона, помещённого в небулайзерную трубку. Вся эта процедура переключения несложная и займёт несколько секунд.
Режим 1. частицы от 1 до 5 мкм – лечим нижний отдел дыхательных путей
Режим 2. диаметр частиц от 6 до 9 мкм – задействован средний отдел дыхательных путей
Режим 3. диаметр от 10 до 14 мкм – верхние дыхательные пути
Внимательно читайте прилагаемую инструкцию к прибору, потому что у разных моделей ингаляторов может быть запрограммировано разное соответствие режима и размера получаемых частиц на выходе.
В компрессорных небулайзерах (например, модель CN- HT02 Панда, CN- HT03 Ариа, Джино) способ ингаляции, то есть размер получаемых частиц лекарственного препарата, зависит от смены пистона. В комплекте идут три сменных многоразовых пистона:
Пистон А (частицы 8 – 10мкм) – большинство из которых оседает в верхнем отделе дыхательных путей (эффективно можно лечить ринит, синусит, гайморит, ларингит, тонзиллит, фарингит – заболевания носоглотки).
Пистон B (частицы 3 – 5 мкм) – большая часть из них оседает в среднем отделе (в данном случае эффективно лечим трахеит, трахеобронхит, аллергию).
Пистон С (частицы 0,5 – 3 мкм) – большинство как раз и достигает нижнего отдела дыхательных путей (продуктивное воздействие при бронхите, бронхиальной астме, ХОБЛ, бронхопневмонии, воспалении лёгких, туберкулёзе).
Лечебный и профилактический эффект здесь достигается преимущественно за счёт избирательного воздействия определённым медикаментом на ту или иную область дыхательной системы.
Среди компрессорных ингаляторов встречаются аппараты, способные работать в непрерывном режиме, то есть компрессору не требуется время для отдыха, и такие варианты, которые работают по принципу работа/пауза с интервалом 30 мин/ 30 мин.
Ультразвуковые небулайзеры — есть приборы с автоматическим отключением через 10 минут ингаляции и с более продолжительным режимом работы (непрерывное время до 30 минут). Не требуют дополнительной подготовки к работе, управляются с помощью одной кнопки.
Меш-небулайзеры способны работать в течение 20 минут (после чего происходит автоматическое отключение), то есть действуют в рамках работа/пауза , а так же до 4 часов непрерывного ингалирования в зависимости от модели. Если в среднем ингаляция составляет 15 минут, то есть возможность полечить несколько членов семьи за один сеанс. Аппаратам не требуется предварительная подготовка перед ингаляцией, не нужно разводить лекарство.
Уровень шума
Ультразвуковые — Бесшумные
Компрессорные — От минимального уровня от 43-46 дБ до до хорошо уловимого и слышимого в 65 дБ
Меш — небулайзеры — Бесшумные либо с минимальным уровнем до 50 дБ
Ингалируемые лекарства
Самый большой спектр допустимых к использованию лекарственных средств принадлежит компрессорным небулайзерам. В режимных моделях таких ингаляторов возможно использование полного перечня препаратов для небулайзерной терапии, включая гормоны, эфирные и натуральные масла, антибиотики, антисептики, фитосборы, бронходилятаторы, муколитики, щелочные растворы и т.д. В аппаратах, работающих в одном режиме и имеющих выход частиц меньше 5 микрон, не рекомендуется использовать масляные жидкости, так как мелкие частицы аэрозоля проникают глубоко и оседают в нижних отделах дыхательных путей, что может вызвать образование там масляной плёнки и побочного эффекта в виде масляной пневмонии.
С ультразвуковыми небулайзерами допускается использовать ТОЛЬКО лекарства на водной основе, но и здесь существуют ограничения, так как ультразвук может разрушать некоторые активные вещества в лекарственных препаратах, из-за чего теряется мощность и терапевтическая эффективность. Такому воздействию подвержены в частности антибиотики. Но есть и исключения, например, в ультразвуковом ингаляторе Beurer Ih40 возможно использование лекарственных масел.
У меш-небулайзеров (по сравнению с ультразвуковыми) более расширенный список препаратов к использованию Здесь можно применить любые лекарства на водной основе, включая антибиотики, муколитики, гормоны, минеральные воды. Это происходит за счёт того, что низкочастотным колебаниям подвергается сетка – мембрана, а не сам препарат. Следовательно, молекулы лекарственного средства не разрушаются и полностью сохраняется терапевтический эффект.
Применение в детской практике
Все три вида небулайзеров можно эффективно и спокойно применять когда болеют дети. В предназначенный для всей семьи комплект обязательно входят взрослая и детская маски. Ультразвуковые и меш – небулайзеры не испугают ребёнка, так как работают тихо или совсем бесшумно. Образуя достаточно мелкие частички аэрозоля, данные ингаляторы будут способствовать более глубокому проникновению лекарственного вещества. Меш – аппараты можно использовать спящим деткам. Среди компрессорных приборов есть модели, разработанные специально для детей. Они имеют вид игрушки (паровозик, слоник, панда и другие), что конечно же привлечёт внимание малыша и лечение пройдёт в игровой форме. Такие модели небулайзеров как, Omron NE –C24 Kids (имеется специальная маска для грудничков), LD – 207U, LD – 210C, LD – 212C (кроме обычной детской маски снабжёны малой маской для детей) подходят для использования с первых месяцев жизни. Компрессорные ингаляторы производства Babybelle с функцией аспиратора (промывание и очищение полости носа) актуальны для младенцев.
Вес и габариты небулайзера
Меш-небулайзеры являются самыми маленькими, компактными, портативными. Вес от 97 грамм до 300. С лёгкостью умещаются в кармане.
Ультразвуковые приборы тоже небольших размеров, в среднем имеют вес около 1 кг (max 1.5 кг).Компрессорные ингаляторы самые габаритные и объёмные. Вес их достигает 2,7 кг (в среднем от 1,5 до 1,8 кг).
Но и среди их числа имеются исключения. Таковым является небулайзер Omron модель NE- C20-RU. Его вес всего 190 грамм, можно расположить и на ладошке. Детский ингалятор Omron модель NE-C24 Kids с массой в 270 гр.
Вместительность резервуара, экономичность и остаточный объём
Компрессорные. Объём резервуара для лекарственных средств от 6 до 13 мл (в разных моделях может быть разным). Аппараты с большей ёмкостью дают возможность проводить более длительные ингаляции, если таковые назначит врач. Скорость распыления у таких небулайзеров от 0,2 до 0,4 мл/мин. Могут работать с непрерывным выходом аэрозоля, могут активироваться вдохом. Наличие клапана вдоха – выдоха снижает расход лекарственного препарата, он расходуется только на фазе вдоха. Это способствует минимальной потере лекарства. Остаточный объём ингаляционного раствора малый и составляет от 0,5 мл до 1,1 мл максимально (при разных режимах). Компрессорные небулайзеры нельзя наклонять, во время ингаляции они должны находиться на горизонтальной поверхности. Если требуется проведение процедуры лежачему человеку, то осуществить это возможно с помощью длинной соединительной трубки.
Ультразвуковые. Объём их резервуаров от 8 до 12 мл. Для ускорения заполнения имеют пипетку вместимостью 2 мл. Возможны продолжительные, долговременные процедуры. Экономичный вариант небулайзеров. Встроенная система A.D.R. перекрывает подачу лекарства на выдохе. Остаточный объём до 1 мл. С помощью ингалятора B.Well WN-119U , который имеет в комплекте длинный воздуховодный шнур, возможны ингаляции ослабленным и лежачим пациентам. Ультразвуковые приборы работают только в вертикальном положении.
Меш-небулайзеры. Объёмы резервуаров в данном типе до 8 мл. Для этих ингаляторов не требуется разведение лекарства, поэтому работают они уже на малых объёмах от 0,5 мл. Остаточный объём тоже соответственно самый низкий от 0,1 до 0,5 мл. Некоторые модели снабжены датчиком расходования препарата, таким образом, Вы всегда будете знать, когда нужно добавить лекарство. К тому же, их особенностью является то, что меш-приборы можно использовать под наклоном в 45 градусов, камера закрытого типа не допускает проливания, это даёт возможность проведения процедуры лежачим больным или, например, спящим детям.
Потребление энергии
Меш-небулайзеры лёгкие, компактные и имеют возможность работать как от сети, так и от пальчиковых батареек. С их помощью можно проводить ингаляции в любое время и в любом месте, независимо есть там источник питания или его нет. В комплект поставки входят батарейки, а адаптеры к ним приобретаются отдельно.
Компрессорные ингаляторы требуют обязательного подключения к сети (220 – 240В). Есть несколько моделей работающих от источника питания в 12В , их можно подключить в автомобиле, например, от прикуривателя (Omron модели NE-C20 RU , NE-C24 Kids , NE-C24) либо к стабилизированному блоку питания.
Ультразвуковые небулайзеры идут в комплекте с сетевым адаптером и тоже нуждаются в подключении к источнику питания. Для модели B.Well WN-119U разработана аккумуляторная батарея и нагреватель аэрозольного потока, но поставляются они отдельно. С их помощью можно будет проводить ингаляцию в любом удобном Вам месте, даже там где нет электричества.
Среди многообразия ингаляторов и небулайзеров, мы уверены, Вы найдёте свой. Будьте здоровы!
Если у Вас остались вопросы, по видам и эксплуатации ингаляторов и небулайзеров – напишите вопрос в наших сообществах в социальных сетях. Если у Вас вопрос: как выбрать небулайзер в нашем интернет-магазине – закажите обратный звонок или позвоните нам по бесплатному номеру.
Как восстановить легкие после болезни — Российская газета
В Ростове успешно применяется схема восстановительной терапии легких после перенесенных заболеваний дыхательных путей. Теперь на страже здоровья россиян стоят ингаляторы и небулайзеры отечественного производителя «Алмаз».
Слово небулайзер происходит от латинского nebula — туман, облачко. История применения небулайзеров (ингаляторов) насчитывает около 150 лет. И сегодня ингаляторы все шире используются в домашних условиях.
Существует целый ряд лекарственных препаратов, которые воздействуют посредством ингаляторов, но их применение должно проводиться после консультации специалиста.
Грамотная терапия после перенесенных вирусных инфекций, а также при лечении сезонных простудных заболеваний сегодня является одной из наиболее актуальных тем. Так, к примеру, коронавирусная инфекция часто приводит к повреждению легких, а ее осложнением может стать пневмония.
Коронавирус проникает в нижние отделы дыхательных путей, под удар попадают легочные альвеолы, участвующие в акте дыхания и отвечающие за газообмен с легочными капиллярами. Вирус разрушает стенки альвеол, что приводит к нарушению этого процесса, а также накоплению в альвеолах воспалительной жидкости. Воспаление легких, особенно если было поражено более 25 процентов, является основной причиной развития хронической дыхательной недостаточности и других заболеваний, например, пневмофиброза, при котором происходит замещение нормальной легочной ткани соединительной с образованием рубцов.
Для восстановления проходимости дыхательных путей необходимо провести комплексную терапию, включающую дыхательную гимнастику, ингаляцию, вибрационный массаж, физиотерапию. Одним из важнейших элементов восстановительной терапии является ингаляция. Она максимально увлажняет слизистую оболочку и стимулирует иммунную защиту организма, позволяя ему быстрее восстановиться.
Именно поэтому сегодня ингалятор становится в доме столь же необходимой вещью, как и термометр. А непосредственное воздействие лекарства на дыхательные пути сокращает время лечения, а также позволяет уменьшить дозировку таблеток и уколов, что снижает риск нежелательных побочных реакций.
Для эффективной доставки лекарственных препаратов в нижние отделы дыхательных путей необходим ультразвуковой небулайзер, например, «Комфорт» производства компании «Алмаз», поскольку он способен преобразовывать лекарственную смесь в мелкодисперсный аэрозоль с размером частиц менее трех микрометров (мкм), что позволяет им проникать в наиболее глубокие отделы бронхов и легких, достигая альвеол. Следует помнить, что любые ингаляции назначаются только специалистом.
На правах рекламы
Возможны противопоказания, проконсультируйтесь со специалистом
Ошибки при использовании ингалятора, небулайзера, как правильно делать ингаляции
Ингаляция – эффективная процедура при заболеваниях дыхательных путей. Но иногда ингаляции усложняют ситуацию, и причина этому − неправильное применение прибора. Расскажем, какие ошибки при использовании небулайзеров нельзя допускать.Семь ошибок при использовании небулайзера
Выбор лекарственного препарата, длительности и кратности проведения процедур зависит от вида и тяжести заболевания. А диагностика и назначение лечения – это прерогатива врача.- Использование масляных растворов
Для проведения ингаляций можно использовать только специальные лекарства, предназначенные для небулайзерной терапии.
- Использование небулайзера сразу после другого члена семьи
- Несоблюдение времени и кратности выполнения ингаляций
- Отмена процедуры при повышенной температуре тела
Гипертермия является противопоказанием для паровых ингаляций, но небулайзеры работают по другому принципу.
- Проведение ингаляций для лечения заболеваний, при которых небулайзерная терапия неэффективна
- Применение формированного дыхания
Варианты лечения пневмонии
TommL / E + / Getty ImagesЛечение пневмонии зависит от вашего типа и степени тяжести. В большинстве случаев с пневмонией можно справиться с помощью домашних средств, но могут потребоваться другие методы лечения, включая лекарства, отпускаемые без рецепта, антибиотики, противовирусные, противогрибковые и дыхательные препараты. В некоторых случаях может потребоваться госпитализация.
Если вы лечитесь от пневмонии, но чувствуете, что ваши симптомы не улучшаются или они начинают улучшаться, но затем ухудшаются, снова обратитесь к врачу.Это могут быть признаки того, что ваше состояние не поддается лечению или что у вас возникла другая инфекция.
Домашние средства и образ жизни
Большинство случаев пневмонии можно вылечить дома с помощью следующих мер:
- Отдыхайте как можно больше. Если у вас пневмония, вам нужен отдых, чтобы ваше тело могло бороться с инфекцией и выздоравливать. Не пытайтесь делать все, что вы обычно делаете, и отдыхать, когда чувствуете усталость. Чем больше вы сможете отдыхать, тем быстрее вам станет лучше.
- Пейте много жидкости. Вы слышите это часто, независимо от того, какое у вас заболевание, но это действительно важно.Питье большего количества воды поможет разжижить слизь в вашем теле, облегчая ее изгнание при кашле, что является важной частью выздоровления от пневмонии. Пейте бульон, суп, чай или даже горячую воду, чтобы избавиться от озноба и получить дополнительное увлажнение.
- Выпейте чашку кофе или чая с кофеином. Известно, что кофеин является мягким бронходилататором и химически похож на теофиллин, лекарство, которое используется для лечения астмы.Исследования показали, что кофеин может улучшить дыхание, открывая дыхательные пути на срок до четырех часов.
- Принимайте лекарства в соответствии с указаниями. Ваш врач может назначить вам антибиотик, противовирусное или противогрибковое средство в зависимости от того, какой у вас тип пневмонии. Убедитесь, что вы принимаете его в соответствии с инструкциями и выполнили весь рецепт, даже если вы чувствуете себя лучше.
- Запустите увлажнитель. Как и в случае с питьевой водой, увлажнитель будет поддерживать влажность дыхательных путей, особенно когда воздух в доме сухой.
- Полощите горло соленой водой. Полоскание горла несколько раз в день может помочь смыть часть слизи из горла и облегчить боль в горле. Если вы ненавидите соленую воду, полоскание простой водой тоже подойдет.
- Поговорите со своим врачом о лекарствах от кашля. Поскольку вам необходимо кашлять, чтобы избавиться от инфекции, поговорите со своим врачом, прежде чем принимать какие-либо средства от кашля, даже если из-за кашля вам трудно заснуть. Возможно, вы сможете принять небольшую дозу лекарства от кашля, или у вашего врача могут быть другие варианты.
- Бросьте курить и держитесь подальше от дыма. Дым усугубляет симптомы и может продлить время восстановления.
Рецепты
Ваш врач может выписать вам множество рецептов, опять же, в зависимости от типа пневмонии и ваших симптомов.
Антибиотики: Если у вас бактериальная пневмония или аспирационная пневмония, ваш врач пропишет вам антибиотик. Выбор лучшего антибиотика зависит от способности выяснить, каким типом бактерий вы были инфицированы, поэтому могут потребоваться некоторые испытания и ошибка до того, как ваши симптомы начнут улучшаться.
Если у вас легкая пневмония и вы в целом здоровы, врач, вероятно, пропишет вам Зитромакс (азитромицин), Биаксин (кларитромицин) или эритроцин (эритромицин). Вам могут потребоваться более сильные антибиотики, если у вас есть определенные заболевания, такие как сердечные заболевания, хроническая обструктивная болезнь легких (ХОБЛ), диабет или заболевание почек.
Дыхательные процедуры: Ваш врач может также назначить ингалятор или распылитель, чтобы помочь разжижить слизь в легких и улучшить дыхание.Наиболее распространенными лекарствами от этого являются Вентолин, ПроЭир или Провентил (альбутерол).
Противовирусные препараты: Если у вас вирусная пневмония, ваш врач может прописать противовирусное средство, особенно если ваша пневмония была вызвана гриппом или герпесом и заболевание было выявлено на ранней стадии. Могут быть назначены противовирусные препараты, включая тамифлю (осельтамивир), реленза (занамивир), Рапиваб (перамивир), Зовиракс (ацикловир), Цитовен (ганцикловир), Фоскавир (фоскарнет), Вистид (цидофовир), Низорал (кетоконазол) и Виразол (рибавирин).
Противогрибковые препараты: Если у вас грибковая пневмония и ваша иммунная система подавлена, или у вас есть другие серьезные сопутствующие заболевания, ваш врач может назначить вам противогрибковое лечение. Эти лекарства включают амфотерицин B, дифлюкан (флуконазол), онмель или споранокс (итраконазол). ), Вифенд (вориконазол), Ноксафил (позаконазол) или Креземба (изавуконазол).
Терапия, отпускаемая без рецепта
Безрецептурные средства, которые обычно используются для лечения симптомов пневмонии, включают:
- Жаропонижающие / обезболивающие: Тайленол (парацетамол), мотрин или адвил (ибупрофен), алеве (напроксен) или аспирин помогут снизить температуру и уменьшить любую боль, которая может у вас возникнуть.Помните, что никогда не давайте аспирин детям, потому что это увеличивает риск развития синдрома Рея — редкого, но потенциально опасного для жизни заболевания.
- Отхаркивающие средства: Эти лекарства помогают разжижать и выводить слизь из легких. Ваш врач, вероятно, не захочет, чтобы вы принимали средства от кашля, или, по крайней мере, попросит вас принять небольшую дозу, потому что вам нужно чтобы иметь возможность кашлять, чтобы вывести инфекцию.
Госпитализация
Если у вас тяжелые симптомы или у вас есть сопутствующие заболевания, которые повышают вероятность осложнений от пневмонии, вам может потребоваться госпитализация.Вы можете получать внутривенные (IV) лекарства и / или дыхательные процедуры, чтобы улучшить вашу способность легко дышать, уменьшить кашель и раздражение и улучшить оксигенацию. При любом типе пневмонии вам также может потребоваться дополнительный кислород или, в редких случаях, даже вентилятор, чтобы помочь вам дышать.
Причины госпитализации
Госпитализация более вероятна, если к вам относится одна из следующих ситуаций или факторов:
- Вы старше 65
- Вы сбиты с толку или дезориентированы
- У вас другая серьезная проблема со здоровьем, например, диабет, ХОБЛ или болезнь сердца
- Ухудшилась функция почек
- Вы не можете позаботиться о себе дома
- Антибиотик, который вы принимаете, не помогает
- Ты быстро дышишь
- Ваша температура ниже нормы
- У вас медленный или быстрый пульс
У детей госпитализация более вероятна, если верны следующие факторы:
- Ребенку до 2 месяцев
- У него проблемы с дыханием
- Ребенок вялый или более сонный, чем обычно
- Низкий уровень кислорода в крови
- Признаки обезвоживания присутствуют
Дополнительная медицина (CAM)
Поскольку пневмония может быть опасным для жизни заболеванием, вам никогда не следует заменять обычное лечение альтернативной терапией.Однако дополнительная альтернативная медицина (CAM) может дополнять традиционные методы лечения, когда они используются вместе.
Теплые травяные чаи успокаивают боль в горле и согревают, если вас мучает озноб. Мята перечная и эвкалипт особенно полезны, потому что они, кажется, расщепляют слизь и уменьшают воспаление горла.
Пажитник помогает избавиться от заложенности жидкости и очистить горло. Чаепитие из семян пажитника может помочь разрушить слизь и уменьшить постоянный кашель.
Обязательно поговорите со своим врачом, если решите использовать CAM.
В зависимости от типа
Различные типы пневмонии требуют своего собственного лечения.
Бактериальная пневмония: Бактериальная пневмония обычно лечится антибиотиками, респираторными препаратами, лекарствами, отпускаемыми без рецепта, и средствами обеспечения комфорта. Однако, если ваш случай станет тяжелым, вам может потребоваться госпитализация для внутривенного введения антибиотика.
Ваши симптомы должны начать улучшаться через один-три дня после приема антибиотиков, но пройдет не менее недели или дольше, прежде чем вы почувствуете себя полностью лучше, в зависимости от того, насколько вы были здоровы вначале.
Вирусная пневмония: Если у вас диагностирована вирусная пневмония, антибиотики не помогут. Самое главное, вам нужно отдыхать и заботиться о себе. Если вы попытаетесь не отставать от своего обычного распорядка, скорее всего, вам понадобится больше времени на восстановление, поэтому сделайте все возможное, чтобы замедлиться и больше отдыхать.
Ваш лечащий врач может порекомендовать безрецептурные или рецептурные лекарства, которые помогут справиться с вашими симптомами и принесут вам некоторое облегчение от дискомфорта, который они вызывают, но эти меры не вылечат болезнь.Иногда могут быть прописаны противовирусные препараты.
В большинстве случаев вирусная пневмония проходит сама по себе в течение одной-трех недель.
Mycoplasma Pneumonia: Mycoplasma pneumonia обычно не так серьезна, как бактериальная или вирусная пневмония, поэтому курс лечения может немного отличаться. Это часто называют «ходячей пневмонией», что означает, что вы не чувствуете себя настолько больным, что вам нужно оставаться в постели весь день.
Технически микоплазменная пневмония вызывается бактериями и в некоторых случаях лечится антибиотиками, хотя часто она проходит сама по себе без лечения.Хотя вам, возможно, не нужно оставаться в постели при микоплазменной пневмонии, дополнительный отдых, поддержание водного баланса и прием безрецептурных лекарств для облегчения симптомов, которые вы испытываете, должны помочь вам быстрее выздороветь.
Аспирационная пневмония: Аспирационная пневмония лечится путем удаления постороннего предмета, если это возможно, и прекращения аспирации большего количества пищи или жидкости. Это может означать, что вам не разрешают есть, и вам будут вводить калории и жидкости через капельницу или через зонд для кормления.
Антибиотики также являются важной частью лечения, помогая свести к минимуму скопление бактерий в легких и предотвратить обострение инфекции. Этот тип пневмонии сложно лечить и может потребоваться длительный курс лечения антибиотиками.
Часто задаваемые вопросы
Как ваш врач определяет лечение пневмонии?
Ваше лечение зависит от типа пневмонии. Ваш врач может поставить диагноз с помощью медицинского осмотра, лабораторных анализов и визуализации, например рентгеновских лучей.
Как обычно лечат ходячую пневмонию?
Ваш врач может назначить антибиотики, если вероятной причиной являются бактерии. Отдых и питье большого количества жидкости также могут помочь вам быстрее восстановиться. Чтобы облегчить симптомы, ваш врач может порекомендовать лекарства, отпускаемые без рецепта, в том числе антигистимины от заложенности носа и средства для снижения температуры, такие как тайленол (парацетамол) и адвил (ибупрофен).
Ингаляционные препараты для профилактики и лечения пневмонии
Expert Opin Drug Saf.Авторская рукопись; доступно в PMC 2015 7 августа.
Опубликован в окончательной редакции как:
PMCID: PMC4527977
NIHMSID: NIHMS710030
Онкологический центр Андерсона, Хьюстон, Техас, США
† Автор для корреспонденции медицины, Техасский университет, Департамент инфекционных заболеваний, Онкологический центр доктора медицины Андерсона, Инфекционный контроль и здоровье сотрудников, 402, 1515 Holcombe Boulevard, Texas 77030, Хьюстон, США, тел .: +1 713 792 0825; Факс: +1713745 6839; Gro.nosrednadm @ radfasa См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты. Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков.По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями. Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной Pseudomonas aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких. Цитокиновая ингаляционная терапия также изучалась при лечении неопластических и инфекционных заболеваний. Выбор легочных систем доставки лекарств остается критическим, поскольку воздушно-струйный и ультразвуковой небулайзер могут обеспечить субоптимальную концентрацию лекарственного средства при неправильном использовании.В будущем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для снижения патогенной нагрузки в дыхательных путях субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмонии у субъектов с ослабленным иммунитетом с использованием цитокинов. или синтетические аналоги молекулярной структуры, ассоциированные с патогенами, и больше возможностей для использования ингаляционных противомикробных препаратов. Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
Ключевые слова: амикацин, противогрибковый, противовирусный, аспергиллез, рак, колистин, цитокин, ингаляционный тобрамицин, врожденный иммунитет, пневмония, псевдомонады, трансплантация, ванкомицин, вентилятор-ассоциированная пневмония, зигомикоз
1.0002 Введение и людей с ослабленным иммунитетом пневмония остается ведущей причиной преждевременной смерти в мире [1–3]. Восприимчивость легких к инфекции возникает из-за архитектурных требований газообмена и частого вдыхания инфекционных агентов.Для обеспечения вентиляции человек постоянно подвергает 100 м
2 площади поверхности легких воздействию внешней среды. Поскольку каждую минуту вентилируется 5–10 л окружающего воздуха, частицы, капли и болезнетворные микроорганизмы также уносятся. Кроме того, в то время как даже здоровые нормальные добровольцы демонстрируют ночную микроабсорбцию орогастрального содержимого, пациенты с неврологическими, анатомическими или ятрогенными препятствиями для защиты дыхательных путей (например, эндотрахеальные или назогастральные трубки) особенно восприимчивы к аспирации инфицированного материала в обширную поверхность раздела нижних отделов. дыхательные пути.В отличие от кожных поверхностей, обернутых непроницаемой кожей, желудка с его кислым просветом или нижних отделов желудочно-кишечного тракта с толстым слоем прилипшей слизи, обширный интерфейс легких с окружающей средой защищен только минимальной защитой барьера. Легочный барьер ограничен необходимостью беспрепятственной газовой диффузии, поэтому эта нежная ткань тонка капилляров. Тем не менее, несмотря на эту структурную уязвимость, легкие успешно защищаются от большинства инфекционных проблем с помощью различных механизмов [4–9].Большинство вдыхаемых или аспирированных патогенов не достигают периферических дыхательных путей из-за захвата в подвижном слое слизистого геля, выстилающего проксимальные проводящие дыхательные пути, с последующим изгнанием через систему мукоцилиарного эскалатора [4]. Постоянное присутствие антимикробных пептидов и антител в жидкости, выстилающей дыхательные пути, ограничивает рост патогенов, которые успешно проникают в небольшие дыхательные пути. Альвеолярные макрофаги поглощают организмы, которые достигают самых отдаленных воздушных пространств [6,7]. Когда базовые защитные механизмы превышены, эпителий легких реагирует увеличением своих прямых противомикробных свойств (см. Раздел 3) и сигнализирует о привлечении лейкоцитов из кровообращения.
Хотя доступность и большая поверхность легких способствуют их восприимчивости к инфекции, эти особенности также предоставляют уникальную возможность для местной терапии в виде респираторных аэрозолей, как показано ниже. Во-первых, недавно были разработаны стратегии увеличения мукоцилиарного клиренса с использованием аэрозолей гипертонического солевого раствора, которые могут снизить нагрузку патогенов в легких. Во-вторых, недавний прогресс в понимании врожденного иммунитета показал, что резистентность респираторного эпителия к патогенам может быть значительно стимулирована, и применение методов лечения, основанных на этом понимании, может снизить восприимчивость к инфекции у уязвимых групп пациентов.В-третьих, перенаправление отклоненного адаптивного иммунитета на повышение устойчивости к специфическим патогенам за счет аэрозольной доставки цитокинов было подтверждено небольшими исследованиями на людях. В-четвертых, антибиотики могут доставляться респираторным путем, максимизируя концентрацию лекарств в области инфекции, где необходимо уничтожение микробов, и сводя к минимуму системные концентрации лекарств, которые могут приводить к нежелательным побочным эффектам. Теоретическая основа и практический статус каждого из этих методов ингаляционной терапии рассматриваются в следующих разделах.
2. Аэрозольный гипертонический солевой раствор для увеличения мукоцилиарного клиренса легких
Основным стимулом к увеличению выведения слизи из легких стало лечение муковисцидоза (МВ). Традиционно постуральный дренаж, перкуссия и другие физические методы сочетаются с очищением от кашля для мобилизации слизи и мусора из дыхательных путей. Совсем недавно для увеличения мукоцилиарного клиренса были введены эффективные аэрозольные методы лечения. Первичным дефектом при МВ является отсутствие апикального эпителиального хлоридного канала, что приводит к уменьшению объема жидкости на поверхности дыхательных путей [10,11].Это предотвращает эффективное движение ресничек и вызывает обезвоживание слизи, что в совокупности ухудшает мукоцилиарный клиренс и повреждает дыхательные пути. Кроме того, эти изменения приводят к заселению обычно стерильных дыхательных путей бактериями и грибками, вызывая дальнейшее воспаление и повреждение дыхательных путей. По мере углубления понимания этих основных механизмов были введены методы лечения для увеличения объема жидкости на поверхности дыхательных путей (). К ним относятся нуклеотиды, амилорид и гипертонический солевой раствор (HSS), но среди них самые убедительные доказательства поддерживают аэрозольный HSS.
Эпителий дыхательных путей с жидкостью на поверхностиПроводящие дыхательные пути выстланы примерно равным количеством мерцательных и секреторных эпителиальных клеток. Секреторные клетки содержат гранулы, которые включают пептиды и муцины (зеленые), хотя внутриклеточные муцины могут быть обнаружены только в небольших дистальных отделах дыхательных путей с помощью чувствительных иммуногистохимических методов или во время воспалительной метаплазии, когда их продукция увеличивается [15,19]. Жидкость на поверхности дыхательных путей состоит из перицилиарного слоя толщиной 7 мкм (синий) и покрывающего его слоя слизистого геля (зеленый), толщина которого варьируется от <1 мкм в дистальных дыхательных путях до> 50 мкм в проксимальных дыхательных путях человека.Реснички направленно бьют, продвигая слой слизистого геля к головке гортани. Гликопротеины муцина MUC5AC и MUC5B являются основными компонентами слоя слизистого геля и высвобождаются экзоцитарно как из подлежащего поверхностного эпителия (показано), так и из подслизистых желез (не показано). Хотя слой слизистого геля важен для очистки от вдыхаемых патогенов (красный), чрезмерное производство муцина или истощение жидкости на поверхности дыхательных путей может привести к закупорке слизью просвета дыхательных путей, обеспечивая убежище для микробной инфекции.
Ранние исследования 1990-х годов показали, что увеличение концентрации аэрозольных растворов хлорида натрия (физиологического раствора) приводит к увеличению скорости мукоцилиарного клиренса [12–14]. На основании этих результатов, аэрозоли HSS были протестированы при краткосрочном лечении пациентов с CF и показали, что они улучшают функцию легких [12,15]. В 2006 году два крупных исследования с использованием 4 мл 7% физиологического раствора в форме аэрозоля два раза в день продемонстрировали улучшение функции легких и снижение частоты обострений [16,17], и теперь это лечение стало основой лечения МВ.
Есть несколько причин полагать, что лечение аэрозолями HSS принесет пользу не только больным МВ, но и пациентам. Во-первых, скорость мукоцилиарного клиренса увеличивается за счет увеличения гидратации даже у тех, у кого не наблюдается истощения жидкости на поверхности дыхательных путей. Это наблюдалось у пациентов с гиперальдостероном, у которых врожденно снижено всасывание натрия, и у здоровых людей из-за использования аэрозолей HSS [18]. Во-вторых, закупорка мелких дыхательных путей слизью из просвета возникает при заболеваниях легких, помимо МВ, таких как астма, хроническая обструктивная болезнь легких (ХОБЛ) и инфекции дыхательных путей, вызванные вирусными, грибковыми и микобактериальными патогенами [19,20].В-третьих, истощение жидкости на поверхности дыхательных путей происходит при некоторых нарушениях воспаления и инфекции дыхательных путей за счет протеолитической активации апикального эпителиального натриевого канала (ENaC) [21]. Исходя из этого, мы начали использовать аэрозольные 7% HSS у пациентов с закупоркой слизи в дыхательных путях и / или стойкой инфекцией дыхательных путей следующим образом. Для вызванной вирусом гиперсекреции слизи с кашлем у пациентов с астмой, ХОБЛ или посттрансплантационным констриктивным бронхиолитом мы используем HSS вместе с обычным режимом лечения обострения пациента, чтобы облегчить кашель и обеспечить доставку ингаляционных лекарств в дыхательные пути, которые в противном случае были бы забит слизью.У пациентов с аллергическим бронхолегочным аспергиллезом (ABPA) мы используем HSS вместе с некоторыми комбинациями ингаляционных стероидов, системных стероидов, системной противогрибковой и системной анти-IgE-терапией. При атипичной микобактериальной инфекции мы используем HSS либо в качестве монотерапии, либо вместе с ингаляционными и / или пероральными антибиотиками. У пациентов с эндобронхиальным стентом мы используем HSS для предотвращения скопления слизи дистальнее стента, что может привести к ателектазу или пневмонии. Иногда мы лечили пациентов с HSS, у которых были рентгенологические помутнения периферического легочного дерева в почке, для которых нам не удалось идентифицировать патоген.У нас есть неофициальные данные о симптоматических и рентгенологических улучшениях в поддержку всех этих применений, но нам неизвестны данные контролируемых испытаний. Когда используется несколько видов аэрозольной терапии, например, HSS вместе с ингаляционными стероидами, мы сначала применяем HSS, хотя объективных доказательств, подтверждающих эту практику, нет. Были бы полезны исследования, предназначенные для измерения применимости и оптимальных методов аэрозольного HSS при других заболеваниях, кроме МВ.
3. Аэрозольная стимуляция врожденного иммунитета легких
Хотя дыхательные пути и альвеолярный эпителий часто рассматриваются как пассивные барьеры, они дополняют базовую защиту легких, претерпевая значительные местные структурные и функциональные изменения при обнаружении патогенных раздражителей.Например, в ответ на вирусное, грибковое или аллергическое воспаление эпителиальные клетки дыхательных путей быстро приобретают гиперсекреторный фенотип в результате процесса, называемого слизистой метаплазией [22,23]. Предполагается, что адаптивная ценность структурной и молекулярной пластичности респираторного эпителия заключается в усилении защиты от микробных патогенов, и это подтверждается наблюдением улучшенного бактериального клиренса после индукции антимикробных белков, включая дефенсины, кателицидины, лизоцим и генераторы реактивных микроорганизмов. формы кислорода [24–28].В присутствии патогенов дыхательные пути и альвеолярный эпителий также вырабатывают воспалительные цитокины и вовлекают лейкоциты в защиту легких [29]. Подавление адаптивного иммунитета и гематопоэза, которое происходит при гематологических злокачественных новообразованиях и / или цитотоксической химиотерапии, не устраняет врожденный иммунный ответ легких на инфекцию. Скорее, пациенты с глубокой иммуносупрессией вырабатывают замечательные цитокиновые и хемокиновые ответы на легочные инфекции [30].
При врожденном иммунитете лейкоциты и паренхимные клетки идентифицируют присутствие патогенов посредством распознавания патоген-ассоциированных молекулярных паттернов (PAMPs), общих для многих видов патогенов, рецепторами распознавания паттернов, кодируемых зародышевой линией (PRR) [31–35].Распознавание PAMP посредством PRR активирует внутриклеточные сигнальные каскады, приводя к экспрессии продуктов, участвующих в микробной защите, воспалении и модуляции адаптивного иммунитета [36]. До сих пор попытки вызвать врожденный иммунитет легких были направлены на стимуляцию PRR с использованием природных или синтетических лигандов [37]. Наиболее распространенными мишенями были Toll-подобные рецепторы (TLR), хотя NOD-подобные рецепторы использовались в качестве адъювантов вакцины в течение многих лет [37], а другие молекулы, такие как RIG-подобные рецепторы и дектин, считались потенциальными терапевтическими мишенями. [37–42].
Чтобы проверить, можно ли эффективно использовать функциональную пластичность легких для защиты от пневмонии in vivo , наша лаборатория сильно стимулировала врожденный иммунитет перед заражением вдыхаемыми респираторными патогенами. Чтобы добиться этого, мышей подвергали воздействию лизата в виде аэрозоля, изготовленного из нетипируемого Haemophilus influenzae , одновременно стимулируя несколько антимикробных путей [42]. Однократное распыление привело к приобретению высокого уровня устойчивости к заражению вирулентными неконфекционными патогенами в течение 2 часов после лечения ().Мы назвали это явление «стимулированная врожденная резистентность» (StIR), чтобы отразить несколько аспектов защиты. Он считается «стимулированным», поскольку резистентность значительно возрастает после терапевтического применения лизата. Защита отражает действие «врожденных» защит, что демонстрируется несколькими ключевыми характеристиками: i) защита достигается за часы, а не дни или недели, как требуется для адаптивного иммунитета; ii) защита достигается у наивных мышей после лечения, полученного от микроба, не являющегося родственным тому, который использовался в контрольном заражении; iii) эффект сохраняется, несмотря на химическое или генетическое истощение адаптивных лейкоцитов; и iv) защита распространяется на каждый микробный патоген, против которого он был протестирован, что указывает на широкий, неизбирательный ответ.Защита связана с «сопротивлением» следующим образом. Столкнувшись с микробной проблемой, выживание зависит от двух стратегий хозяина: толерантности (способность ограничивать ущерб, причиняемый патогеном) и устойчивости (способности ограничивать бремя патогенов) [43,44]. Мы обнаружили, что обработка лизатом ограничивает количество патогенов, связанных с различными классами организмов. Следовательно, мы определили устойчивость как основное средство защиты лизата.
Выживаемость после заражения Streptococcus pneumoniae (Spn) после лечения аэрозольным лизатом нетипируемого Haemophilus influenze (NTHi)Мышей предварительно обрабатывали в группах по шесть человек аэрозольным лизатом NTHi для стимуляции врожденного иммунитета, затем заражали как одну группу с высокой дозой Spn (6.1 × 10 10 КОЕ / мл). Выживаемость через 7 дней показана как функция интервала между лечением и контрольным заражением (* p = 0,015, ‡ p = 0,002, лечение по сравнению с необработанным) [50].
Сначала мы проверили защитное действие StIR против наиболее распространенной причины бактериальной пневмонии во всем мире, Streptococcus pneumoniae , и обнаружили, что, хотя все нелеченные мыши умерли после ингаляционного заражения, все мыши, обработанные лизатом, выжили. Механистические исследования показали, что защита тесно связана с индукцией антимикробной среды в легких, что демонстрируется быстрым снижением количества патогенов по сравнению с нелеченными мышами [42].Защитный эффект сохранялся, даже если у мышей не было резидентных лейкоцитов в легких (альвеолярных макрофагов и тучных клеток) или у мышей не было рекрутированных нейтрофилов. Последующие исследования также показали, что лимфоциты были незаменимы при StIR, и исследований in vitro показали, что респираторный эпителий был достаточным как для восприятия лечения, так и для воздействия на противомикробный ответ [45].
Стимулированная врожденная резистентность широко распространяется на другие важные бактериальные респираторные патогены.Среди распространенных причин внутрибольничной пневмонии ингаляционное лечение бактериальным лизатом эффективно защищает от Pseudomonas aeruginosa , Klebsiella pneumoniae и лейкоцидин-продуцирующих лейкоцидин Panton-Valentine устойчивых к метициллину Staphylococcus aureus [45]. Дыхательный путь — наиболее вероятный портал входа для агентов биотеррора и единственный способ, с помощью которого такие патогены были успешно доставлены в современную эпоху (например, ингаляционная сибирская язва) [46–49].Мы исследовали, может ли StIR защищать от агентов биотеррора, и обнаружили, что однократное введение аэрозольного лизата значительно увеличивает среднюю выживаемость мышей, зараженных Bacillus anthracis , Yersinia pestis или Francisella tularensis [45]. Для всех исследованных бактериальных патогенов защита от летального исхода была связана со значительным и немедленным сокращением количества патогенов.
Учитывая широту защиты от разнородных видов бактерий и предположение о еще более широком антимикробном действии путем анализа экспрессии гена легких после лечения, также была протестирована защита мышей от грибкового патогена.Поскольку ни мыши, ни люди обычно не восприимчивы к пневмонии Aspergillus при отсутствии иммунодефицита, мышей лечили циклофосфамидом и кортизолом перед контрольным заражением A. fumigatus . Из инфицированных мышей> 70% умерли, если они не прошли предварительную обработку лизатом. Практически все, кто проходил лечение, выжили (93%). Как и в случае с бактериальными патогенами, StIR привел к значительному снижению внутрилегочной грибковой нагрузки [45].
Вирус гриппа является основной причиной смертности от легочных инфекций во всем мире, и эффективный легочный StIR может обеспечить защиту во время пандемий.Мы обнаружили, что в то время как 100% контрольных мышей умерли от геморрагической пневмонии,> 90% выжили после одной предварительной обработки бактериальным лизатом [50]. Мы также обнаружили значительное улучшение показателей выживаемости, если лизат в форме аэрозоля вводили через 1 день после заражения, что указывает на то, что стимуляция врожденного иммунитета может быть полезной для лечения, а также для профилактики пневмонии. Кроме того, мы обнаружили, что добавление рибавирина к лечению лизатом привело к синергетическому улучшению выживаемости (т. Е., лучше, чем аддитивные эффекты одного лечения) при введении после инфекции [50]. Как и в случае со всеми другими исследованными патогенами, защита от гриппа, вызванная лизатом, коррелировала со снижением титров вируса в легких.
В то время как лечение нетипируемым лизатом Haemophilus influenza (NTHi) приводит к быстрой активации врожденного иммунитета слизистой оболочки легких, защитный эффект ослабевает через 4-5 дней [50,51]. Следовательно, для предотвращения пневмонии у групп пациентов, подвергавшихся риску по истечении этого периода, вероятно, потребуется повторное лечение.Мы обнаружили, что повторное дозирование является эффективным и безопасным для мышей. При повторной обработке лизатом мыши показали стойкую устойчивость к заражению S. pneumoniae , P. aeruginosa и гриппом A [45,50]. Мыши, подвергавшиеся обработке лизатом еженедельно в течение 50 недель, не показали явных патологий, таких как преждевременная смерть, потеря веса или изменения поведения [36]. После 8 еженедельных воздействий инфильтрация мононуклеарных клеток окружала дыхательные пути, хотя наблюдалось очень мало альвеолярных воспалительных клеток.После 25 еженедельных воздействий был очевиден легкий фиброз стенки дыхательных путей, который далее прогрессировал после 50 еженедельных воздействий [52]. Увеличенная временная шкала фиброза стенки дыхательных путей и прогрессирующего накопления лимфоцитов предполагает, что фиброз возникает из-за адаптивного иммунного ответа после хронического воздействия бактериального лизата, а не в ответ на саму стимуляцию врожденного иммунитета. Замена макромолекулярных стимуляторов врожденного иммунитета низкомолекулярными аналогами, которые не вызывают адаптивного иммунного ответа, и снижение интенсивности стимуляции, таким образом, позволяет избежать этого долгосрочного осложнения.Действительно, толстая кишка мышей постоянно стимулируется присутствием просветных бактерий, что приводит к конститутивной активации StIR, которая может быть обнаружена как индуцибельно сниженная способность убивать бактерии эпителием толстой кишки после лечения антибиотиками [53], но толстая кишка этого не делает. развивается фиброз.
Данные на мышах показывают, что лечение, индуцирующее врожденную резистентность в легких, должно хорошо переноситься пациентами-людьми. Мы полагаем, что причина того, что мыши могут переносить самые высокие применяемые дозы (в 12 раз превышающие терапевтическую дозу) без явных побочных эффектов [51], заключается в том, что реакция содержится в просвете легких.Несмотря на то, что количество воспалительных цитокинов в жидкости бронхоальвеолярного лаважа увеличивается в несколько тысяч раз по сравнению с исходным уровнем, уровень системных цитокинов почти не увеличивается [50]. Это согласуется с недавней работой Hoogerwerf и его коллег, которые вызвали значительную воспалительную реакцию легких в дыхательных путях у людей, подвергшихся внутрилегочному применению лигандов TLR, липотехоевой кислоты (лиганд TLR2) и липополисахарида (LPS, лиганд TLR4), но не были связаны с любые идентифицируемые клинические признаки или симптомы [54].
Не только наша лаборатория исследует стимуляцию TLR, которая может способствовать увеличению выживаемости хозяина при инфекциях. Несколько групп наблюдали иммуномодулирующие эффекты ЛПС и пытались изменить течение респираторных инфекций, доставляя производные ЛПС [40,41,55] или изменяя структуру ЛПС [39] у патогенов, используемых при экспериментальной пневмонии. У всех была обнаружена некоторая степень защиты за счет применения одного агониста TLR4, как и у нас [51]. Испытания отдельных агонистов TLR также были успешными при инфекционных заболеваниях человека.Например, подкожное введение синтетического агониста TLR9 вызвало системные воспалительные реакции и снизило вирусную нагрузку гепатита C [42], а местный имиквимод (TLR7) оказался многообещающим при лечении кожного лейшманиоза [38]. Однако вполне вероятно, что для достижения полной эффективности и широты действия, продемонстрированных с бактериальным лизатом, потребуются синергетические взаимодействия множественной стимуляции PRR [56-59].
Лизат, используемый для индукции StIR, не обладает антибиотическим действием [45].Скорее, он вызывает собственные защитные продукты хозяина. Индукция выработки антимикробного пептида согласуется как со временем, так и с широтой защиты и демонстрируется с помощью микроматрицы экспрессии генов [45] и протеомного анализа [51]. В будущем, возможно, удастся обойти стадию индукции хозяина и напрямую доставить полезные антимикробные пептиды или миметики малых молекул [43].
В ближайшем будущем стимуляция естественной реакции хозяина на микробные продукты для профилактики и лечения пневмонии может стать основой для разработки новой клинической терапевтической стратегии [44,45].
4. Аэрозольная доставка цитокинов для направленного иммунного отклонения
IFNα-2a, IFNγ-1b и GM-CSF вводились легочным путем пациентам с резистентной легочной инфекцией Mycobacterium tuberculosis и нетуберкулезным микобактериозом (NTM) включая Mycobacterium avium комплексное заболевание легких с переменным успехом. Эти иммунологически разнообразные белки также использовались при неинфекционных легочных заболеваниях, таких как первичный рак легких, метастатический рак в легкие и альвеолярный протеиноз, заболевание, недавно связанное с антителами против нативного GM-CSF [60–62].Ниже приводится краткое описание клинического опыта использования терапии ингаляционными цитокинами при легочной инфекции.
Ингаляционный IFNα переносится в более низких дозах (1-20 MIU) без системных побочных эффектов, тогда как лихорадка, недомогание и головная боль возникали при использовании доз в диапазоне от 60 до 120 MIU и совпадали с обнаруживаемым цитокином в периферическом кровообращении [63, 64]. Бронхоспазм препятствует использованию этого цитокина у пациентов с хроническим бронхитом [65].Спасательная терапия с использованием ингаляционного IFNα для лечения неоперабельного рака легких не обнадеживает [66]. Добавление IFNα 3 MIU 3 раза в неделю к противотуберкулезной терапии было связано с ранним исчезновением лихорадки и быстрым снижением количества кислотоустойчивых бацилл в отхаркиваемой мокроте по сравнению с одной антимикробной терапией [67]. Кроме того, у пациентов с резистентной к лечению туберкулезной инфекцией добавление ингаляционного IFNα показало обнадеживающие результаты, хотя необходимы дальнейшие крупные рандомизированные исследования для подтверждения безопасности, стоимости и эффективности [68].
Низкие дозы ингаляционного IFNγ хорошо переносятся, в том числе пациентами с бронхореактивными состояниями, такими как астма, и после воздействия этого плейотропного провоспалительного цитокина была продемонстрирована измеримая активация альвеолярных макрофагов [69,70]. Имеется значительный клинический опыт использования ингаляционного IFNγ для лечения легочных микобактериальных инфекций. В сочетании с антимикробной терапией терапия IFNγ в виде аэрозоля привела к благоприятным ответам как на лекарственно-чувствительный, так и на лекарственно-устойчивый туберкулез легких, с уничтожением микроорганизмов и улучшением радиографических показателей заболевания [71–73].Однако этого преимущества не наблюдалось у пациентов с тяжелым основным заболеванием легких, у которых был туберкулез легких [74]. Точно так же не было отмечено терапевтического эффекта у пациентов с МВ, получавших высокие дозы (500 или 1000 мкг) ингаляционного IFNγ для снижения риска инфекции, тем не менее, пациенты страдали от серьезной лекарственной токсичности, включая одышку, кровохарканье и госпитализацию [75]. IFNγ также был исследован для профилактики вентилятор-ассоциированной пневмонии (ВАП) у пациентов с тяжелыми травмами [76].Количество ВАП было уменьшено, хотя не наблюдалось улучшения общей смертности у этих пациентов с травмами, которые получали 100 мкг рекомбинантного IFNγ в аэрозольной форме 3 раза в день [76]. Эта неэффективность частично может быть связана с низкой доставкой цитокинов через стандартный распылитель [77]. Рекомбинантный GM-CSF в аэрозольной форме хорошо переносится пациентами с легочными метастазами в дозах 250 мкг дважды в день без серьезных побочных эффектов [78]. О применении аэрозольных GM-CSF для лечения инфекций у людей не сообщалось.Однако эксперименты на животных подтверждают абсорбцию в легких аэрозольного или интратрахеально введенного GM-CSF, и GM-CSF в аэрозольной форме оказался эффективным в искоренении инвазивного легочного аспергиллеза у мышей в модели с ослабленным иммунитетом [79,80].
Другие цитокины, используемые аэрозольным путем, включают IFNβ при лечении рака легких, IL-2 при почечно-клеточной карциноме и другом метастатическом раке легких, растворимый рецептор IL-4 для пациентов с астмой и эритропоэтин для лечения анемии.Ни один из них не использовался для лечения легочной инфекции.
5. Доставка синтетических антибиотиков в аэрозольной форме
В первом подразделе мы обсудим использование аминогликозидов в лечении и профилактике серьезных легочных инфекций у пациентов с высоким риском, а затем кратко ознакомимся с ограниченным клиническим опытом применения других противомикробных препаратов. препараты, которые использовались для спасительной терапии трудноизлечимой пневмонии. Учитывая, что были проведены обширные обзоры ингаляционного пентамидина при ВИЧ-ассоциированной инфекции Pneumocystis jiroveci , эта тема здесь не рассматривается.
5.1 Аэрозольная терапия аминогликозидами
Теоретически аминогликозиды имеют несколько характеристик, которые, по-видимому, способствуют ингаляционному введению. Во-первых, аминогликозиды обладают эффектом уничтожения, зависящим от концентрации, что означает, что высокие уровни, достижимые в дыхательных путях с помощью ингаляционных препаратов, могут привести к повышению клинической эффективности. Более того, аминогликозиды обладают значительной ограничивающей дозу токсичностью для людей, так что дозы, которые можно вводить при системном введении, приводят к относительно низким уровням в паренхиме легких.Наконец, поскольку аминогликозиды использовались относительно редко в течение последних нескольких десятилетий, многие организмы с множественной лекарственной устойчивостью, вызывающие нозокомиальную респираторную инфекцию, остаются восприимчивыми по крайней мере к одному, если не ко многим, обычно используемым аминогликозидам. Действительно, из всех классов антибиотиков данные о доставке антимикробных препаратов путем ингаляции наиболее обширны для аминогликозидов. В этом разделе мы рассмотрим фармакокинетическую, клиническую информацию и информацию о безопасности, касающуюся ингаляционной терапии аминогликозидами.
Разработка аминогликозидов широкого спектра действия, таких как гентамицин, в конце 1960-х — начале 1970-х годов открыла большие перспективы для лечения ранее резистентных респираторных инфекций из-за устойчивых к антимикробным препаратам грамотрицательных палочек, таких как P. aeuroginosa [81] . Однако вскоре исследователи сообщили, что системно вводимый гентамицин часто не лечил легочные инфекции из-за P. aeuroginosa и других грамотрицательных палочек, несмотря на чувствительность in vitro [82].Низкие уровни гентамицина в респираторных секретах заставили исследователей предположить, что беспорядочное проникновение аминогликозидов в очаг инфекции может быть причиной терапевтических неудач, и предположить, что введение гентамицина непосредственно в легкие может улучшить клинический ответ [83,84]. Предварительные исследования 1970-х годов показали, что концентрация гентамицина в мокроте часто была на порядок выше после эндотрахеального введения по сравнению с системным лечением [83,85].
Данные, накопленные в последующие 30 лет, подтвердили предположение этих ранних сообщений о том, что проникновение аминогликозидов в легочную паренхиму является субоптимальным после системного введения [86–93]. Фармакокинетика доставки аминогликозидного лекарственного средства имеет особое значение, поскольку эти агенты обладают зависящим от концентрации эффектом уничтожения, а это означает, что более высокие уровни лекарственного средства связаны с усилением антимикробного действия [94]. Например, оптимальный клинический ответ на терапию аминогликозидами происходит, когда максимальная концентрация препарата (C max ) до минимальной ингибирующей концентрации (МИК) составляет> 8: 1 [95–98].Терапия аминогликозидами при пневмонии обычно рассматривается для относительно устойчивых неферментативных грамотрицательных палочек, таких как P. aeruginosa , Acinetobacter baumanii и Stenotrophomonas maltophila [99]. Хотя они сильно варьируются в зависимости от популяции пациентов и рассматриваемых аминогликозидов, даже для восприимчивых организмов, МПК для этих организмов обычно находятся в диапазоне 1-8 мкг / мл [100]. Таким образом, чтобы максимизировать возможность клинического ответа, необходимы концентрации легочных аминогликозидов ≥ 10-40 мкг / мл.Важно отметить, что ни один из доступных в настоящее время аминогликозидов не достигает таких уровней при системном введении даже в условиях воспалительного процесса, который, как ожидается, приведет к увеличению попадания в легкие из кровотока [85,86,91,92,101] .
В отличие от трудностей достижения удовлетворительных уровней в легких с помощью системного введения аминогликозидов, местная доставка аминогликозидов приводит к концентрациям, которые могут быть эффективными даже против относительно резистентных организмов [85,86,93,102-104].Измерения уровней аминогликозидов в легких после местного введения в значительной степени зависят от механизма, используемого для доставки лекарственного средства, дозы и места отбора пробы. Однако, несмотря на эти различия, исследователи неизменно демонстрируют уровни аминогликозидов> 200 мкг / мл в респираторных образцах после местного применения [85–87,89,101–107]. Данные, касающиеся концентраций аминогликозидов, аналогичны в исследованиях на животных и людях, у больных и здоровых пациентов, а также при использовании инвазивных и неинвазивных методов тестирования [85–87,89,101–107].Таким образом, фармакокинетические данные убедительно свидетельствуют о том, что местное введение аминогликозидов с большей вероятностью приведет к эффективным уровням лекарственного средства по сравнению с системной доставкой.
5.2 Клинические исследования ингаляционных аминогликозидов: муковисцидоз
Контроль над бронхолегочной инфекцией заметно повысил качество и продолжительность жизни пациентов с МВ [108]. Уникальная эндобронхиальная среда пациентов с МВ означает, что легкие таких пациентов колонизируются такими организмами, как S.aureus и H. influenza вскоре после рождения. Однако со временем P. aeuroginosa обычно становится преобладающим легочным патогеном у пациентов с МВ, колонизируя> 80% людей к 18 годам [109]. Взаимодействие «хозяин – патоген» между пациентами с МВ и P. aeuroginosa относительно уникально с точки зрения бактериальных процессов, поскольку однажды установленная эндобронхиальная инфекция, вызванная P. aeuroginosa , редко полностью искореняется [110]. Большая часть терапевтических достижений, достигнутых за последние десятилетия в лечении пациентов с МВ, была достигнута за счет снижения бремени, вызываемого P.aeuroginosa в легких пациентов с МВ, что впоследствии уменьшает воспалительный ответ, ответственный за прогрессирование бронхоэктазов.
В то время как внутривенные антибиотики долгое время были золотым стандартом для лечения инфекции, вызванной P. aeuroginosa у пациентов с МВ, за последние 20 лет серия все более тщательных клинических исследований четко установила роль ингаляционных аминогликозидов в подавлении P. y инфекция aeuroginosa у пациентов с МВ.Первоначально использовался гентамицин, но исследователи перешли к тобрамицину в свете его повышенной активности против Pseudomonas [111–113]. Для удобства в ранних исследованиях использовались небулайзерные флаконы с аминогликозидами, изначально предназначенные для внутривенного введения, которые потенциально могли вызвать раздражение легких из-за присутствия консервантов и антиоксидантов. Важный прогресс произошел, когда Smith et al . разработали препарат тобрамицина без консервантов для распыления, который в дозе 600 мг обеспечивает гораздо более высокую дозу, чем типичный флакон для внутривенного введения на 80 мг [114].Это была доза тобрамицина 600 мг, которая использовалась в критическом исследовании перекрестного дизайна для 71 человека, в котором пациенты получали t.i.d. дозирование. После 1 месяца приема распыленного тобрамицина ключевые параметры легочной функции и плотность мокроты, полученной при использовании P. aeuroginosa , значительно улучшились в группе лечения [107]. Эффективный, но громоздкий характер лечения привел к разработке следующего поколения распыленного тобрамицина, который впоследствии был использован в крупнейшем рандомизированном плацебо-контролируемом исследовании распыленных аминогликозидов.В общей сложности 520 пациентов с CF, которые были колонизированы P. aeuroginosa , были рандомизированы для получения распыленного тобрамицина 300 мг два раза в день. или плацебо, вводимое в 4-недельных блоках включения-выключения в течение 24 недель [115]. Пациенты, получавшие активное лечение, показали улучшение показателей легочной функции, меньшую потребность в госпитализации и значительное снижение плотности P. aeuroginosa в мокроте. Важно отметить, что положительный эффект ингаляционного тобрамицина сохранялся в течение 2 лет после начала лечения [116].Результаты этого исследования привели к одобрению FDA США раствора тобрамицина для ингаляции (TSI) (TOBI ™ , Novartis Corp., Восточный Ганновер, Нью-Джерси), который до сих пор является единственным одобренным антибиотиком для ингаляции дыхательных путей в США. .
Эффективность TOBI в хроническом подавлении P. aeuroginosa у пациентов с МВ привела к исследованиям ингаляционных аминогликозидов при обострениях МВ, но результаты не были столь впечатляющими. Несколько испытаний показали, что добавление ингаляционных аминогликозидов, таких как тобрамицин или амикацин, к системной антипсевдомонадной терапии увеличивает долю пациентов, которые избавляются от P.aeuroginosa из мокроты, но не улучшает клинические исходы, такие как тесты функции легких [117,118]. Недавно завершенное международное исследование в 17 центрах не выявило статистической разницы в клинических исходах при добавлении ингаляционного тобрамицина к системно вводимому ципрофлоксацину у пациентов с МВ, инфицированных P. aeuroginosa, с обострением [119]. Пациенты, получавшие ингаляционный тобрамицин, имели более низкую плотность мокроты P. aeuroginosa , но повышенную частоту свистящего дыхания при ингаляционной терапии, что могло свести на нет пользу от усиленного противомикробного эффекта.Таким образом, в настоящее время ингаляционная терапия не считается частью стандарта помощи пациентам с МВ с обострениями.
5.3 Лечение пациентов с бронхоэктазами без кистозного фиброза ингаляционными аминогликозидами
Хотя МВ является преобладающей причиной бронхоэктазов в развитых странах, существует несколько других заболеваний, которые могут привести к бронхоэктазам [120]. Обнадеживающие результаты лечения бронхоэктазов, связанных с МВ, увеличили давний интерес к лечению пациентов с бронхоэктазами, не связанными с МВ, с помощью ингаляционных аминогликозидов [121].К сожалению, как и в случае острых обострений при МВ, накопленные к настоящему времени данные об эффективности ингаляционных аминогликозидов при бронхоэктазиях, не связанных с МВ, не так сильны, как данные для поддерживающей терапии при МВ. На данный момент четыре опубликованных клинических исследования изучали использование ингаляционных аминогликозидов у пациентов без МВ с бронхоэктазами и хронической инфекцией, вызванной P. aeuroginosa , во всех из которых использовался ингаляционный тобрамицин в дозе 300 мг два раза в день. дозирование [119,122–124]. Подобно основным исследованиям МВ, эти испытания неизменно показывают, что ингаляционный тобрамицин значительно снижает респираторную нагрузку P.aeuroginosa . Однако, в отличие от ситуации с бронхоэктазами, связанными с МВ, снижение уровня P. aeuroginosa у пациентов с бронхоэктазами, не связанными с МВ, не привело к последовательному улучшению объективных клинических показателей, таких как тесты функции легких. Одно исследование обнаружило улучшение «общего состояния здоровья» у пациентов, получавших тобрамицин [123]. Обнаружение того, что у пациентов, получавших тобрамицин, развивался более выраженный бронхоспазм по сравнению с пациентами, получавшими плацебо, значительно ограничило применение аэрозольных антибиотиков при бронхоэктазах без МВ [121].Таким образом, широкое использование ингаляционных аминогликозидов у пациентов с бронхоэктазами без МВ требует разработки препарата, который вызывает меньшее раздражение дыхательных путей при сохранении антипсевдомональной эффективности.
5.4 Профилактика и лечение вентилятор-ассоциированной пневмонии с помощью ингаляционных аминогликозидов
Хотя ИВЛ имеет жизненно важное значение для ведения тяжелобольных пациентов, она часто осложняется развитием респираторных инфекций, вызывающих значительную заболеваемость и смертность [125].Учитывая легкость доступа, обеспечиваемую интубацией трахеи, существует долгая история введения противомикробных препаратов непосредственно в дыхательные пути для лечения и профилактики респираторных инфекций, связанных с аппаратом ИВЛ [83]. Наиболее систематически исследуемой областью в этом отношении было использование местных антибиотиков для предотвращения искусственной вентиляции легких (ВАП) [126]. Хотя самые крупные исследования были проведены с антибиотиками, не являющимися аминогликозидами, и тобрамицин, и гентамицин показали некоторую эффективность в предотвращении ВАП [127, 128].Недавний метаанализ показал, что местное применение антимикробных препаратов значительно снижает частоту ВАП у пациентов с искусственной вентиляцией легких [126]. Эти данные противоречат рекомендациям Центров по контролю и профилактике заболеваний против использования распыленных антибиотиков для предотвращения ВАП из-за опасений по поводу развития устойчивости к противомикробным препаратам и побочных эффектов введения [129].
По сравнению с профилактикой ВАП, существует меньше системных данных об использовании ингаляционных аминогликозидов для терапии ВАП [130].Однако, учитывая рост показателей ВАП из-за множественной лекарственной или даже панрезистентности грамотрицательных патогенов, использование ингаляционных аминогликозидов или других противомикробных препаратов может стать все более распространенным явлением в попытке повысить локальные концентрации лекарств для борьбы с относительно устойчивыми патогенами. Следует отметить, что недавнее ретроспективное исследование онкологических пациентов с грамотрицательной палочкой ВАП показало, что те пациенты, которые получали ингаляционные аминогликозиды, в основном тобрамицин или ингаляционный колистин, имели значительно лучшие клинические результаты по сравнению с пациентами, получавшими терапию системными аминогликозидами или колистином [131].Наконец, Палмер и др. . недавно сообщили о результатах исследования, в котором пациенты с вентилятор-ассоциированным трахеобронхитом (VAT) были рандомизированы для приема ингаляционных противомикробных препаратов, тобрамицина и / или ванкомцина или плацебо [132]. Пациенты, получавшие ингаляционные противомикробные препараты, имели заметное улучшение объективных респираторных показателей и имели значительно меньшую вероятность прогрессирования до ВАП по сравнению с пациентами, получавшими плацебо. В совокупности сочетание повышения лекарственной устойчивости и накопления данных об эффективности ингаляционной терапии указывает на то, что местная терапия аминогликозидами может играть многогранную роль в профилактике и лечении респираторной инфекции у пациентов с механической вентиляцией легких, хотя необходимы многоцентровые проспективные исследования.
5.5 Безопасность ингаляционных аминогликозидов
Двумя основными проблемами, вызывающими обеспокоенность в отношении местной терапии аминогликозидами, являются развитие лекарственной устойчивости и побочные эффекты лекарств или системы доставки лекарств. Учитывая, что местное введение приводит к градиенту концентрации противомикробного препарата от центральных к периферическим дыхательным путям, существует серьезная проблема индукции устойчивости к противомикробным препаратам [121]. Более того, местная терапия часто назначается в течение длительных периодов времени, даже лет, тем самым максимально увеличивая возможность развития лекарственной устойчивости.В то время как отчеты о случаях и серии случаев подтверждают, что резистентные организмы могут возникать во время терапии, тщательное обследование в ходе рандомизированных клинических испытаний не показало, что появление резистентных к лекарствам организмов у пролеченных пациентов является особенно важной проблемой [100, 110, 126]. В свете чрезвычайно высоких уровней аминогликозидов, достижимых с помощью небулайзерной терапии, некоторые страны предложили разработать специфические для ингаляции контрольные точки МИК, при которых очень немногие организмы действительно будут устойчивы к аминогликозидам [133].Приведет ли загрязнение окружающей среды при нозокомиальной небулайзерной терапии к повышению устойчивости к аминогликозидам в медицинских учреждениях, остается теоретическим, но недоказанным вопросом. Выявление бронхоспазма при местной терапии — еще одна важная проблема безопасности, особенно когда распыленные антибиотики используются для облегчения симптомов, например, при бронхоэктазах [121]. Хотя обычно они легко поддаются лечению бронходилататорами, раздражение дыхательных путей распыляемыми аминогликозидами ограничено для многих пациентов, и продолжение исследований по разработке более переносимых методов лечения имеет решающее значение для более широкого использования.
5.6 Другие виды антибактериальной терапии в виде аэрозолей
Клинический опыт аэрозолизации антибактериальных средств, отличных от аминогликозидов, ограничен, но продолжает расти. Заметное увеличение числа грамотрицательных патогенов с множественной лекарственной устойчивостью привело к увеличению использования полимиксинов, противомикробных препаратов, которые были разработаны в 1950-х годах, но их использование быстро сократилось в 1970-х и 1980-х годах из-за опасений по поводу нефротоксичности [134]. Использование колистина (полимиксина E) в последнее время заметно увеличилось, поскольку штаммы P.aeruginosa и A. bauamnnii , устойчивые ко всем другим классам коммерчески доступных антимикробных препаратов, остались чувствительными к колистину [134]. Подобно аминогликозидам, ингаляция является потенциально привлекательным способом введения колистина, учитывая токсичность, наблюдаемую при системном введении. Ретроспективные и нерандомизированные исследования показали обнадеживающие результаты при использовании ингаляционного колистина, хотя исследования противоречат гетерогенности пациентов и назначению дополнительных противомикробных препаратов в сочетании с ингаляционным колистином [130, 131, 134–138].До сих пор сообщалось о минимальной токсичности ингаляционного колистина, хотя систематические данные отсутствуют. Ингаляционный азтреонам представляется безопасной и эффективной альтернативой ингаляционному тобрамицину при муковисцидозе [139]. Наконец, недавнее исследование показало, что ингаляционный ванкомицин эффективен в предотвращении прогрессирования трахеобронхита, связанного с вентилятором, до пневмонии, связанной с вентилятором [132]. Неуклонный рост лекарственной устойчивости среди респираторных патогенов придает дополнительную актуальность продолжению исследований, призванных лучше определить роль ингаляционных противомикробных препаратов при легочных инфекциях.
5.7 Противогрибковая аэрозольная терапия
Несмотря на недавние достижения в области противогрибковой лекарственной терапии, инвазивные грибковые инфекции (ИФИ) остаются серьезной угрозой для больных раком с ослабленным иммунитетом и реципиентов трансплантации органов или гемопоэза [140,141]. Ответ на терапию цитокинами системного усиления иммунитета, такую как рекомбинантный GM-CSF, IFNγ и переливание донорских гранулоцитов, чреват отсутствием исследований по оценке стоимости и полезности и усугубляется неопределенными данными клинической эффективности [142].Инвазивный аспергиллез представляет собой опасную для жизни инфекцию, часто наблюдаемую в течение первых 3 лет после трансплантации сердце-легкие [143], тогда как у реципиентов аллогенной трансплантации стволовых клеток эта инфекция возникает в период нейтропении перед приживлением, во время острой трансплантации вместо трансплантата. болезнь хозяина (GVHD) и в период позднего риска, который включает лечение хронической GVHD [144]. У больных раком пациенты с острым миелогенным лейкозом особенно восприимчивы к ИФИ, и период риска может быть увеличен у пациентов с рефрактерным или рецидивирующим раком [145].Ингаляционный амфотерицин B был исследован для предотвращения ИФИ у восприимчивых пациентов в периоды высокого риска и для терапии спасения у пациентов с трудно поддающимся лечению инвазивным грибковым заболеванием легких.
У реципиентов трансплантата легкие инфекции Aspergillus разновидностей приводят к колонизации, которая часто предшествует инвазивному заболеванию, проявляющемуся как трахеобронхит или инфекции анастомоза, и / или инвазивное заболевание легких; диссеминация грибков у этих пациентов без нейтропении и без рака встречается редко.Большинство этих грибковых инфекций возникает у реципиентов трансплантатов солидных органов без нейтропении в период раннего отторжения трансплантата и иммуносупрессивной терапии отторжения [143]. Интересно отметить, что колонизация видами Aspergillus через 3 месяца после трансплантации чаще встречается у пациентов с человеческим лейкоцитарным антигеном (HLA) A1; однако у этих пациентов, склонных к поздней грибковой колонизации, риск инвазивного грибкового заболевания существенно не увеличивался [143]. Напротив, недавно сообщалось о нескольких грибковых инфекциях у реципиентов трансплантата сердца с рефрактерным отторжением, получавших сиролимус в сочетании с такролимусом, и пациентов с васкулопатией сердечного аллотрансплантата [146].
Ингаляционный амфотерицин B был первым лекарством, используемым для лечения системного микоза, а более ранние эксперименты на животных с использованием аэрозольного амфотерицина B показали благоприятную эффективность при лечении легочного аспергиллеза [147]. Липидные препараты амфотерицина B, такие как липидный комплекс амфотерицина B (ABLC), также эффективно доставлялись аэрозольным путем. Прединфекционная обработка ABLC в дозе 0,4–1,6 мг / кг за 2 дня до инфекции обеспечила увеличение выживаемости на 63–100% в экспериментах на животных [148].Пиковая концентрация амфотерицина B в бронхоальвеолярном лаваже после однократного приема достигается через 30 минут после ингаляции, и он медленно выводится из легких в течение следующих 24 часов [149].
Устройство доставки лекарственного средства остается критически важным для прогнозирования концентрации лекарственного средства, распыляемого в виде аэрозоля. В исследованиях клинической кинетики распределения 10% вдыхаемого ABLC откладывалось в легких при введении через специализированные системы доставки, такие как распылитель AeroEclipse, управляемый сжатым воздухом со скоростью 7-8 л / мин, и это отложение в легких было в два раза выше по сравнению с достигнутыми уровнями. использование стандартных систем доставки аэрозолей для бронхолитической терапии [150].Состав также важен, поскольку в экспериментах на животных концентрация лекарственного средства в аэрозольной форме ABLC в шесть раз выше по сравнению с дезоксихолатом амфотерицина B [148]. Более того, ингаляционный ABLC хорошо переносился при исследовании реципиентов трансплантата легкого, тогда как обычный дезоксихолат амофотерицина B приводил к вдвое большему количеству побочных эффектов, связанных с лечением [151].
Сообщалось о значительном сокращении случаев инвазивного легочного аспергиллеза у пациентов, получавших ингаляционный амфотерицин B во время и после операции по трансплантации сердца и сердце – легкие [152].Аналогичным образом, липидный препарат амфотерицина B (ABLC) также успешно использовался для профилактики трахеобронхита Aspergillus, анастомозов и инвазивных заболеваний легких у реципиентов сердца и легких [143, 153].
Скудность клинических данных по лечению амфотерицином В в аэрозольной форме у пациентов с установленной грибковой инфекцией легких затрудняет рекомендацию этого вмешательства даже в рефрактерных случаях. Вот два примера таких случаев: пациент без иммуносупрессии с поствирусным трахеобронхитом, вызванным Aspergillus, который не ответил на длительную липосомную терапию амфотерицином B, имел благоприятный ответ на длительное лечение ингаляционным дезоксихолатом амфотерицина B плюс GM-CSF и IFNγ-иммунитет. усиление [154].Во-вторых, у пациента с тяжелой иммуносупрессией и инфекцией легкого Rhizomucor, которая в результате эволюции превратилась в Pseudalescheria boydii , инфекция полностью исчезла с помощью ингаляционного ABLC, которая продолжалась в течение 5 месяцев, и при долгосрочном наблюдении рецидива инфекции не наблюдалось [155]. Эти случаи подчеркивают потенциальную роль ингаляционного амфотерицина B в лечении установленного заболевания; однако на основании текущей клинической информации нельзя дать никаких рекомендаций.
5.8 Противовирусная аэрозольная терапия
Вирусные инфекции дыхательных путей обычно протекают в легкой форме и часто поддаются поддерживающей терапии. Однако у пациентов с ослабленным иммунитетом, больных раком или трансплантацией, эти инфекции могут быть связаны с тяжелыми осложнениями, требующими ранней диагностики и своевременной терапии [137]. Обеспокоенность вызывают парамиксовирусы, такие как респираторно-синцитиальный вирус (RSV) и вирус парагриппа (PIV), вирусы гриппа A и B, аденовирус и недавно признанный метапневмовирус человека (hMPV).Рибавирин, аналог пуринового нуклеозида, использовался для лечения хронической инфекции вируса гепатита С пероральным введением, а также для лечения геморрагической лихорадки и диссеминированного hMPV путем внутривенного введения. Рибавирин в аэрозольной форме был одобрен FDA для лечения инфекций RSV у госпитализированных детей. Обычное непрерывное лечение 60 мг рибавирина / мл в течение 18 часов эффективно с внутривенным иммуноглобулином или без него; однако пациенты чувствуют себя сильно изолированными, что может помешать их уходу [138].Периодически вводимый в виде аэрозоля рибавирин в дозе 20 мг / мл в течение 2 ч 3 раза в день также был эффективен у взрослых пациентов с раком и трансплантацией стволовых клеток с инфекцией RSV [140]. У детей с ослабленным иммунитетом и инфекцией RSV периодические высокие дозы (60 мг) рибавирина / мл в течение 2 часов, вводимые 3 раза в день, хорошо переносились, ассоциировались с клиническим ответом, сравнимым со стандартной непрерывной терапией, и ассоциировались со значительно меньшим загрязнением окружающей среды и воздействием на здоровье: медицинским работникам и с большей доступностью для пациентов [141, 142].
Парагрипп ассоциируется с потенциально серьезными осложнениями у реципиентов трансплантата сердце-легкие, с возможной ролью в остром отторжении аллотрансплантата и облитерирующем поствирусном бронхиолите [143]. Ингаляционный рибавирин в этой популяции ассоциировался с клиническим улучшением, хотя клинический опыт ограничен [144]. У реципиентов трансплантата гемопоэтических стволовых клеток парагриппозная вирусная инфекция является серьезной в присутствии других копатогенов и у пациентов с дыхательной недостаточностью, и лечение рибавирином в форме аэрозоля не было связано с уменьшением продолжительности выделения вируса или смертности, связанной с пневмонией [145].
Вирус гриппа А является основной причиной заболеваемости и смертности, и инфекции часто бывают тяжелыми у пациентов с дефектным адаптивным Т-клеточным ответом. Лекарственная устойчивость к ингибиторам нейраминидазы представляет собой серьезную проблему лечения в условиях плохого ответа на обычные вакцины в популяции высокого риска рака и трансплантата [146]. Аэрозольный рибавирин 60 мг / мл для трех дневных доз продолжительностью 15 мин был эффективен против гриппа A и B у мышей [147]. Недавно было показано, что мегадоза рибавирина (100 мг / мл) эффективна у мышей, инфицированных летальным вирусом гриппа A h4N2.Эта мегадозовая терапия в течение всего 4 дней привела к выживаемости> 90% при назначении в течение 24–48 часов после инфицирования [148]. Необходимы дальнейшие клинические исследования для оценки соответствующей дозы и эффективности рибавирина для лечения лекарственно-устойчивой или лекарственно-резистентной вирулентной вирулентной инфекции гриппа.
Метапневмовирус человека возник как распространенный вирусный патоген дыхательных путей, связанный с субклиническим или легким заболеванием. Иногда было показано, что у пациентов с Т-клеточными иммунными дефектами hMPV вызывает диссеминированное смертельное заболевание [149].У пациентов с трансплантацией стволовых клеток или твердых органов эти инфекции, даже при ограниченном течении легочного заболевания, представляют опасность для жизни и повышают риск поствирусной инвазивной грибковой пневмонии [150]. Внутривенный рибавирин считается лучшим доступным лечением этих серьезных диссеминированных или легочных инфекций hMPV, что отражает противовирусный эффект препарата и возможные лекарственные иммуномодулирующие свойства, которые могут еще больше повысить клиренс вируса и помочь в разрешении инфекции, особенно при ослабленном иммунитете. хост [151].
У пациентов с непереносимостью внутривенного рибавирина из-за гемолитической анемии и других серьезных осложнений с некоторым успехом применялось аэрозольное лечение легочного hMPV [152]. Точно так же при лечении пневмотропного аденовируса человека аэрозольный рибавирин предпочтительнее внутривенного из-за высокой концентрации препарата, достигаемой в альвеолах, по сравнению с внутривенной терапией рибавирином, которая может не приводить к цитотоксическим концентрациям в легочной ткани [153]. Однако это может быть не единственным определяющим фактором клинической эффективности терапии рибавирином, поскольку лекарственное усиление активности Т-хелперных Т-клеток Th2 требует дальнейшей оценки в клинических испытаниях [151].
6. Системы распыления
Критическим фактором для всех ингаляционных терапевтических средств являются характеристики системы доставки. Для всех терапий, обсуждаемых здесь, использовались жидкие аэрозоли, чаще всего генерируемые воздушно-струйными небулайзерами, хотя все чаще используются дополнительные технологии [156]. Воздухоструйный и ультразвуковой небулайзеры генерируют аэрозоль под высоким давлением и вибрацией пьезоэлектрического кристалла соответственно. Эти обычно используемые системы доставки обеспечивают адекватное отложение антимикробных препаратов в легких у амбулаторных пациентов, тогда как доставка лекарств ниже у пациентов в критическом состоянии, получающих вспомогательную вентиляцию легких [157,158].В новых электрических генераторах аэрозолей используется вибрирующая сетка или пластина с множеством отверстий, которые увеличивают отложение лекарства в легких в 2–3 раза и значительно повышают выход лекарства по сравнению с аэрозольными небулайзерами. Это следует учитывать для аэрозольной доставки лекарств у пациентов с пневмонией на ИВЛ [159].
Точно так же ингаляционная терапия цитокинами кажется привлекательной для различных трудно поддающихся лечению микобактериальных инфекций, поражающих легкие, хотя доставка этих агентов к месту инфекции представляет собой сложную задачу.В стандартных небулайзерных системах, таких как Respirgard или Misty-neb, только 5–7% общей введенной дозы достигает легочной ткани [74, 160]. Эту трудность можно уменьшить, используя высокоэффективные воздушно-струйные или ультразвуковые небулайзеры или специализированные системы доставки с использованием генераторов электрического аэрозоля нового поколения для достижения терапевтических концентраций иммуномодулирующих цитокинов в месте легочной инфекции. Для получения дополнительной информации отсылаем читателя к недавним обзорным статьям [161].
7. Резюме
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты. Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков. Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
8. Мнение экспертов
По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями низкой остроты.
Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной P. aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких.
В дальнейшем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для уменьшения вызываемых патогенами нарушений дыхательных путей у субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмония у субъектов с ослабленным иммунитетом, использующих цитокины или синтетические аналоги PAMP, и больше возможностей для использования ингаляционных противомикробных препаратов.
Сноски
Заявление о заинтересованности
Это исследование было частично поддержано грантом CA16672 для поддержки онкологических центров от Национальных институтов здравоохранения.
Библиография
1. Доклад о состоянии здравоохранения в мире 2004 г. — Изменяющаяся история. Женева: Всемирная организация здравоохранения; 2004. [Google Scholar] 3. Джоос Л., Тамм М. Нарушение защиты легочного хозяина у хозяина с ослабленным иммунитетом: химиотерапия рака. Proc Am Thorac Soc. 2005. 2 (5): 445–8. [PubMed] [Google Scholar] 4. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 7. Трэвис С.М., Сингх П.К., валлийский MJ.Противомикробные пептиды и белки во врожденной защите поверхности дыхательных путей. Curr Opin Immunol. 2001. 13 (1): 89–95. [PubMed] [Google Scholar] 8. Flanders SACH, Saint S. Нозокомиальная пневмония: состояние науки. Am J Infect Control. 2006; (34): 84–93. [PubMed] [Google Scholar] 9. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Ратьен Ф. Восстановление жидкости на поверхности дыхательных путей при муковисцидозе.N Engl J Med. 2006. 354 (3): 291–3. [PubMed] [Google Scholar] 11. Тарран Р., Дональдсон С., Буше Р. Обоснование применения гипертонической солевой терапии при муковисцидозе легких. Semin Respir Crit Care Med. 2007. 28 (3): 295–302. [PubMed] [Google Scholar] 12. Eng PA, Morton J, Douglass JA и др. Краткосрочная эффективность распыляемого ультразвуком гипертонического раствора при муковисцидозе. Педиатр Пульмонол. 1996. 21 (2): 77–83. [PubMed] [Google Scholar] 13. Робинсон М., Регнис Дж. А., Бейли Д. Л. и др. Влияние гипертонического раствора, амилорида и кашля на мукоцилиарный клиренс у пациентов с муковисцидозом.Am J Respir Crit Care Med. 1996. 153 (5): 1503–1509. [PubMed] [Google Scholar] 14. Суд Н., Беннетт В.Д., Земан К. и др. Повышение концентрации вдыхаемого физиологического раствора с амилоридом или без него: влияние на мукоцилиарный клиренс у нормальных субъектов. Am J Respir Crit Care Med. 2003. 167 (2): 158–63. [PubMed] [Google Scholar] 15. Wark PA, McDonald V. Распыленный гипертонический раствор для лечения муковисцидоза. Кокрановская база данных Syst Rev.2003; (1): CD001506. [PubMed] [Google Scholar] 16. Дональдсон С.Х., Беннетт В.Д., Земан К.Л. и др. Очистка слизи и функция легких при муковисцидозе с применением гипертонического раствора.N Engl J Med. 2006. 354 (3): 241–50. [PubMed] [Google Scholar] 17. Элкинс М.Р., Робинсон М., Роуз Б.Р. и др. Контролируемое испытание длительного применения ингаляционного гипертонического раствора у пациентов с муковисцидозом. N Engl J Med. 2006. 354 (3): 229–40. [PubMed] [Google Scholar] 18. Керем Э., Бистрицер Т., Ханукоглу А. и др. Дисфункция легочного эпителия натриевых каналов и избыток жидкости в дыхательных путях при псевдогипоальдостеронизме. N Engl J Med. 1999. 341 (3): 156–62. [PubMed] [Google Scholar] 19. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Буше RC. Обезвоживание поверхности дыхательных путей при муковисцидозе: патогенез и терапия. Annu Rev Med. 2007. 58: 157–70. [PubMed] [Google Scholar] 22. Эванс С.М., Уильямс О.В., Тувим М.Дж. и др. Муцин продуцируется clara-клетками проксимальных дыхательных путей мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004. 31 (4): 382–94. [PubMed] [Google Scholar] 23. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Акинби Х.Т., Эпод Р., Бхатт Х. и др. Уничтожение бактерий усиливается экспрессией лизоцима в легких трансгенных мышей. J Immunol. 2000. 165 (10): 5760–6. [PubMed] [Google Scholar] 25. Bals R, Weiner DJ, Moscioni AD, et al. Усиление врожденной защиты хозяина за счет экспрессии антимикробного пептида кателицидина. Заражение иммунной. 1999. 67 (11): 6084–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26.Коул А.М., Ляо Х.И., Стучлик О. и др. Катионные полипептиды необходимы для антибактериальной активности жидкости дыхательных путей человека. J Immunol. 2002. 169 (12): 6985–91. [PubMed] [Google Scholar] 27. Коул AM, Thapa DR, Gabayan V и др. Снижение клиренса Pseudomonas aeruginosa из дыхательных путей мышей с дефицитом лизоцима M. J Leukoc Biol. 2005. 78 (5): 1081–5. [PubMed] [Google Scholar] 28. Moser C, Weiner DJ, Lysenko E, et al. бета-дефенсин 1 способствует развитию врожденного иммунитета легких у мышей. Заражение иммунной. 2002. 70 (6): 3068–72.[Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Эванс С.Е., Хан П.Й., Макканн Ф. и др. Бета-глюканы клеточной стенки Pneumocystis стимулируют генерацию хемокинов альвеолярными эпителиальными клетками через механизмы, зависящие от ядерного фактора, каппаB. Am J Respir Cell Mol Biol. 2005. 32 (6): 490–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 30. Агусти С., Рано А., Ровира М. и др. Воспалительный ответ, связанный с легочными осложнениями у пациентов с иммунодефицитом, не связанным с ВИЧ. Грудная клетка. 2004. 59 (12): 1081–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 31.Бартон Г.М., Меджитов Р. Сигнальные пути толл-подобных рецепторов. Наука. 2003. 300 (5625): 1524–15. [PubMed] [Google Scholar] 32. Болдрик Дж. К., Ализаде А. А., Дин М. и др. Стереотипные и специфические программы экспрессии генов в врожденных иммунных реакциях человека на бактерии. Proc Natl Acad Sci USA. 2002. 99 (2): 972–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 33. Капетанович Р., Кавайон Дж. М.. Ранние события врожденного иммунитета при распознавании микробных патогенов. Экспертное мнение Biol Ther. 2007. 7 (6): 907–18. [PubMed] [Google Scholar] 34.Каваи Т., Акира С. Сигнализация TLR. Смерть клетки отличается. 2006. 13 (5): 816–25. [PubMed] [Google Scholar] 35. Копп Э., Меджитов Р. Распознавание микробной инфекции по Toll-подобным рецепторам. Curr Opin Immunol. 2003. 15 (4): 396–401. [PubMed] [Google Scholar] 36. Чжан Г., Гош С. Активация NF-kappaB, опосредованная Toll-подобным рецептором: филогенетически консервативная парадигма врожденного иммунитета. J Clin Invest. 2001; 107 (1): 13–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Улевич Р.Ю. Терапия, направленная на врожденную иммунную систему.Nat Rev Immunol. 2004. 4 (7): 512–20. [PubMed] [Google Scholar] 38. Аревало И., Туллиано Дж., Киспе А. и др. Роль имиквимода и парентерального антимониата меглумина в начальном лечении кожного лейшманиоза. Clin Infect Dis. 2007. 44 (12): 1549–54. [PubMed] [Google Scholar] 39. Канистанон Д., Хаджар А.М., Пеллетье М.Р. и др. Мутант Francisella по углеводной модификации липида А вызывает защитный иммунитет. PLoS Pathog. 2008; 4 (2): e24. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Лембо А., Пеллетье М., Айер Р. и др.Введение синтетического агониста TLR4 защищает мышей от легочной туляремии. J Immunol. 2008. 180 (11): 7574–81. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Лурманн А., Дейтерс Ю., Скокова Дж. И др. Эффекты in vivo синтетического 2-килодальтонного активирующего макрофаги липопептида Mycoplasma fermentans после легочного применения. Заражение иммунной. 2002. 70 (7): 3785–92. [Бесплатная статья PMC] [PubMed] [Google Scholar] 42. МакХатчисон Дж. Г., Бэкон Б. Р., Гордон С. К. и др. Фаза 1B, рандомизированное двойное слепое исследование с увеличением дозы CPG 10101 у пациентов с хроническим вирусом гепатита С.Гепатология. 2007. 46 (5): 1341–9. [PubMed] [Google Scholar] 43. Raberg L, Sim D, Read AF. Распутывание генетической изменчивости для устойчивости и толерантности к инфекционным заболеваниям у животных. Наука. 2007. 318 (5851): 812–4. [PubMed] [Google Scholar] 44. Уильямс Т.Н., Мванги Т.В., Вамбуа С. и др. Отрицательный эпистаз между защитным действием от малярии альфа + -талассемии и серповидно-клеточной характеристикой. Нат Жене. 2005. 37 (11): 1253–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45. Эванс С.Е., Скотт Б.Л., Клемент К.Г. и др.Стимулированная врожденная резистентность эпителия легких защищает мышей от бактерий и грибков. Am J Respir Cell Mol Biol. 2009 27 марта; [Epub перед печатью] [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Деннис Д.Т., Инглсби Т.В., Хендерсон Д.А. и др. Туляремия как биологическое оружие: управление медициной и общественным здравоохранением. ДЖАМА. 2001. 285 (21): 2763–73. [PubMed] [Google Scholar] 47. Хиллеман MR. Обзор: причины и профилактика в биологической войне и биотерроризме. Вакцина. 2002. 20 (25–26): 3055–67. [PubMed] [Google Scholar] 48.Уэйн Конлан Дж., Шен Х., Куоли Р. и др. Аэрозольная, но не внутрикожная иммунизация живым вакцинным штаммом Francisella tularensis защищает мышей от последующего аэрозольного заражения высоковирулентным штаммом патогена типа А посредством механизма, зависимого от Т-лимфоцитов и гамма-интерферона. Вакцина. 2005. 23 (19): 2477–85. [PubMed] [Google Scholar] 50. Тувим М.Дж., Эванс С.Е., Клемент К.Г. и др. Усиленное воспаление легких защищает от пневмонии гриппа А. PLoS ONE. 2009; 4 (1): e4176.[Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Клемент К.Г., Эванс С.Е., Эванс С.М. и др. Стимуляция врожденного иммунитета легких защищает мышей от летальной пневмококковой пневмонии. Am J Respir Crit Care Med. 2008. 177 (12): 1322–30. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Могхаддам С.Дж., Клемент К.Г., Де ла Гарза М.М. и др. Лизат Haemophilus influenzae индуцирует аспекты фенотипа хронической обструктивной болезни легких. Am J Respir Cell Mol Biol. 2008. 38 (6): 629–38. [Бесплатная статья PMC] [PubMed] [Google Scholar] 53.Brandl K, Plitas G, Mihu CN и др. Устойчивые к ванкомицину энтерококки используют вызванный антибиотиками врожденный иммунный дефицит. Природа. 2008. 455 (7214): 804–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Hoogerwerf JJ, de Vos AF, Bresser P, et al. Воспаление легких, вызванное липотейхоевой кислотой или липополисахаридом у человека. Am J Respir Crit Care Med. 2008. 178 (1): 34–41. [PubMed] [Google Scholar] 55. Реппе К., Черниг Т., Лурманн А. и др. Иммуностимуляция липопептидом-2, активирующим макрофаги, увеличивала выживаемость при пневмонии мышей.Am J Respir Cell Mol Biol. 2009. 40 (4): 474–81. [PubMed] [Google Scholar] 56. Багчи А., Херруп Э.А., Уоррен Х.С. и др. MyD88-зависимый и MyD88-независимый пути синергизма, прайминга и толерантности между агонистами TLR. J Immunol. 2007. 178 (2): 1164–71. [PubMed] [Google Scholar] 57. Trinchieri G, Sher A. Сотрудничество сигналов Toll-подобных рецепторов во врожденной иммунной защите. Nat Rev Immunol. 2007. 7 (3): 179–90. [PubMed] [Google Scholar] 58. Меджитов Р. Распознавание микроорганизмов и активация иммунного ответа.Природа. 2007. 449 (7164): 819–26. [PubMed] [Google Scholar] 59. Foster SL, Hargreaves DC, Medzhitov R. Ген-специфический контроль воспаления с помощью TLR-индуцированных модификаций хроматина. Природа. 2007. 447 (7147): 972–8. [PubMed] [Google Scholar] 60. Тазава Р., Хамано Э., Араи Т. и др. Гранулоцитарно-макрофагальный колониестимулирующий фактор и легочный иммунитет при легочном альвеолярном протеинозе. Am J Respir Crit Care Med. 2005. 171 (10): 1142–9. [PubMed] [Google Scholar] 61. Андерсон П.М., Маркович С.Н., Слоан Дж. А. и др. Аэрозольный гранулоцитарный макрофаг-колониестимулирующий фактор: низкая токсичность, легочная биологическая терапия у пациентов с метастазами в легких.Clin Cancer Res. 1999. 5 (9): 2316–23. [PubMed] [Google Scholar] 62. Trapnell BC, Whitsett JA, Nakata K. Легочный альвеолярный протеиноз. N Engl J Med. 2003. 349 (26): 2527–39. [PubMed] [Google Scholar] 63. Киннула В., Маттсон К., Кантелл К. Фармакокинетика и токсичность вдыхаемого человеческого интерферона-альфа у пациентов с раком легких. J Interferon Res. 1989. 9 (4): 419–23. [PubMed] [Google Scholar] 64. Маасилта П., Халме М., Маттсон К. и др. Фармакокинетика ингаляционного рекомбинантного и природного альфа-интерферона. Ланцет.1991; 337 (8737): 371. [PubMed] [Google Scholar] 65. Киннула В., Кантелл К., Маттсон К. Эффект вдыхаемого природного интерферона-альфа на диффузную бронхоальвеолярную карциному. Eur J Cancer. 1990; 26 (6): 740–1. [PubMed] [Google Scholar] 66. Маасилта П., Холсти Л. Р., Халме М. и др. Природный альфа-интерферон в сочетании с гиперфракционированной лучевой терапией при лечении немелкоклеточного рака легкого. Int J Radiat Oncol Biol Phys. 1992. 23 (4): 863–8. [PubMed] [Google Scholar] 67. Giosue S, Casarini M, Alemanno L и др.Эффекты аэрозольного интерферона-альфа у больных туберкулезом легких. Am J Respir Crit Care Med. 1998. 158 (4): 1156–62. [PubMed] [Google Scholar] 68. Giosue S, Casarini M, Ameglio F и др. Аэрозольное лечение интерфероном-альфа у пациентов с туберкулезом легких с множественной лекарственной устойчивостью. Eur Cytokine Netw. 2000. 11 (1): 99–104. [PubMed] [Google Scholar] 69. Мартин Р. Дж., Богуневич М., Хенсон Дж. Э. и др. Воздействие вдыхаемого гамма-интерферона на нормальные дыхательные пути человека. Am Rev Respir Dis. 1993; 148 (6 Pt 1): 1677–82.[PubMed] [Google Scholar] 70. Богуневич М., Мартин Р.Дж., Мартин Д. и др. Эффекты распыленного рекомбинантного гамма-интерферона на астматические дыхательные пути. J Allergy Clin Immunol. 1995. 95 (1 Pt 1): 133–5. [PubMed] [Google Scholar] 71. Кондо Р., Раджу Б., Канова А. и др. Рекомбинантный гамма-интерферон стимулирует передачу сигнала и экспрессию генов в альвеолярных макрофагах in vitro и у больных туберкулезом. Заражение иммунной. 2003. 71 (4): 2058–64. [Бесплатная статья PMC] [PubMed] [Google Scholar] 72. Раджу Б., Хосино Ю., Кувабара К. и др.Аэрозольный гамма-интерферон (IFN-гамма) индуцирует экспрессию генов, кодирующих IFN-гамма-индуцибельный белок 10 килодальтон, но не индуцибельную синтазу оксида азота в легких во время туберкулеза. Заражение иммунной. 2004. 72 (3): 1275–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Кондо R, Rom WN, Schluger NW. Лечение туберкулеза легких с множественной лекарственной устойчивостью с помощью аэрозольного гамма-интерферона. Ланцет. 1997. 349 (9064): 1513–5. [PubMed] [Google Scholar] 74. Condos R, Hull FP, Schluger NW и др.Региональное отложение аэрозольного гамма-интерферона при туберкулезе легких. Грудь. 2004. 125 (6): 2146–55. [PubMed] [Google Scholar] 75. Moss RB, Mayer-Hamblett N, Wagener J, et al. Рандомизированное двойное слепое плацебо-контролируемое исследование с увеличением дозы аэрозольного гамма-1b интерферона у пациентов с кистозным фиброзом легких легкой и средней степени тяжести. Педиатр Пульмонол. 2005. 39 (3): 209–18. [PubMed] [Google Scholar] 76. Накос Г., Маламу-Мици В.Д., Лачана А. и др. Иммунопаралич у больных с тяжелой травмой и действие ингаляционного гамма-интерферона.Crit Care Med. 2002. 30 (7): 1488–94. [PubMed] [Google Scholar] 77. Вирголини I, Куртаран А., Леймер М. и др. Ингаляционная сцинтиграфия с меченным йодом-123 интерфероном гамма-1b: исследование легочного отложения и повышения дозы у здоровых добровольцев. J Nucl Med. 1997. 38 (9): 1475–81. [PubMed] [Google Scholar] 78. Рао Р.Д., Андерсон П.М., Арндт К.А. и др. Терапия аэрозольным гранулоцитарным макрофагальным колониестимулирующим фактором (GM-CSF) при метастатическом раке. Am J Clin Oncol. 2003. 26 (5): 493–8. [PubMed] [Google Scholar] 79.Нивен Р.В., Уиткомб К.Л., Шенер Л. и др. Легочная абсорбция аэрозольного и интратрахеально инстиллированного rhG-CSF и моноПЕГилированного rhG-CSF. Pharm Res. 1995. 12 (9): 1343–9. [PubMed] [Google Scholar] 80. Мачида М., Хаяси М., Авазу С. Абсорбция в легких рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора (rhG-CSF) после интратрахеального введения крысам. Биол Фарм Булл. 1996. 19 (2): 259–62. [PubMed] [Google Scholar] 81. Gatmaitan BG, Carruthers MM, Lerner AM. Гентамицин в лечении первичных грамотрицательных пневмоний.Am J Med Sci. 1970. 260 (2): 90–4. [PubMed] [Google Scholar] 83. Klastersky J, Geuning C, Mouawad E, et al. Эндотрахеальный гентамицин при бронхиальных инфекциях у пациентов с трахеостомией. Грудь. 1972: 61 (2): 117–20. [PubMed] [Google Scholar] 85. Odio W, Van Laer E, Klastersky J. Концентрации гентамицина в бронхиальном секрете после внутримышечного и эндотрахеального введения. J Clin Pharmacol. 1975. 15 (7): 518–24. [PubMed] [Google Scholar] 86. Панидис Д., Маркантонис С.Л., Бутзука Э. и др. Проникновение гентамицина в жидкость выстилки альвеол у пациентов в критическом состоянии с вентилятор-ассоциированной пневмонией.Грудь. 2005. 128 (2): 545–52. [PubMed] [Google Scholar] 87. Каркас А.Дж., Гарсия-Сатуе Д.Л., Сапатер П. и др. Проникновение тобрамицина в эпителиальную выстилочную жидкость пациентов с пневмонией. Clin Pharmacol Ther. 1999. 65 (3): 245–50. [PubMed] [Google Scholar] 88. Valcke YJ, Vogelaers DP, Colardyn FA и др. Проникновение нетилмицина в нижние дыхательные пути после приема один раз в сутки. Грудь. 1992. 101 (4): 1028–32. [PubMed] [Google Scholar] 89. Брауде А.С., Хорнштейн А., Кляйн М. и др. Распределение тобрамицина в легких.Am Rev Respir Dis. 1983; 127 (5): 563–5. [PubMed] [Google Scholar] 90. Kuhn RJ. Фармацевтические соображения при аэрозольной доставке лекарств. Фармакотерапия. 2002; 22 (3 Pt 2): 80S – 5S. [PubMed] [Google Scholar] 91. Goldstein I, Wallet F, Nicolas-Robin A, et al. Отложение в легких и эффективность распыленного амикацина при пневмонии, вызванной Escherichia coli, у вентилируемых поросят. Am J Respir Crit Care Med. 2002. 166 (10): 1375–81. [PubMed] [Google Scholar] 92. Гольдштейн I, Кошелек F, Роберт Дж. И др. Концентрация распыленного амикацина в легочной ткани во время искусственной вентиляции легких у поросят со здоровыми легкими.Am J Respir Crit Care Med. 2002. 165 (2): 171–5. [PubMed] [Google Scholar] 93. Klastersky J, Carpentier-Meunier F, Kahan-Coppens L, et al. Антибиотики при грамотрицательной бронхопневмонии назначаются эндотрахеально. Грудь. 1979; 75 (5): 586–91. [PubMed] [Google Scholar] 94. Флюм П, Клепсер МЭ. Обоснование использования антибиотиков в аэрозольной форме. Фармакотерапия. 2002; 22 (3 Pt 2): 71S – 9S. [PubMed] [Google Scholar] 95. Мур RD, Литман PS, Смит CR. Клинический ответ на терапию аминогликозидами: важность отношения максимальной концентрации к минимальной ингибирующей концентрации.J Infect Dis. 1987. 155 (1): 93–9. [PubMed] [Google Scholar] 96. Мур RD, Смит CR, Литман PS. Связь уровней аминогликозидов в плазме со смертностью у пациентов с грамотрицательной бактериемией. J Infect Dis. 1984. 149 (3): 443–8. [PubMed] [Google Scholar] 97. Schentag JJ. Корреляция фармакокинетических параметров с эффективностью антибиотиков: взаимосвязь между концентрациями в сыворотке, значениями МИК и бактериальной эрадикацией у пациентов с грамотрицательной пневмонией. Scand J Infect Dis Suppl. 1990; 74: 218–34.[PubMed] [Google Scholar] 98. Дезил-Эванс Л.М., Мерфи Дж. Э., Джоб М.Л. Корреляция фармакокинетических показателей с терапевтическим исходом у пациентов, получающих аминогликозиды. Clin Pharm. 1986. 5 (4): 319–24. [PubMed] [Google Scholar] 99. Коллинз Т., Гердинг Д.Н. Аминогликозиды в сравнении с бета-лактамами при грамотрицательной пневмонии. Semin Respir Infect. 1991. 6 (3): 136–46. [PubMed] [Google Scholar] 100. Бернс Дж. Л., Ван Дальфсен Дж. М., Шавар Р. М. и др. Влияние хронического периодического введения ингаляционного тобрамицина на респираторную микробную флору у пациентов с муковисцидозом.J Infect Dis. 1999. 179 (5): 1190–6. [PubMed] [Google Scholar] 101. Valcke Y, Pauwels R, Van der Straeten M. Проникновение аминогликозидов в жидкость выстилки альвеол крыс. Эффект воспаления дыхательных путей. Am Rev Respir Dis. 1990. 142 (5): 1099–103. [PubMed] [Google Scholar] 102. Меерс П., Невилл М., Малинин В. и др. Проникновение биопленки, запускаемое высвобождение и активность ингаляционного липосомального амикацина in vivo при хронических инфекциях легких, вызванных Pseudomonas aeruginosa. J Antimicrob Chemother. 2008. 61 (4): 859–68.[PubMed] [Google Scholar] 103. Дэвис К.К., Као П.Н., Якобс С.С. и др. Аэрозольный амикацин для лечения легочных инфекций Mycobacterium avium: серия наблюдательных случаев. BMC Pulm Med. 2007; 7: 2. [Бесплатная статья PMC] [PubMed] [Google Scholar] 104. Макколл С.Ю., Спруилл В.Дж., Уэйд В.Е. Применение тобрамицина в аэрозольной форме при лечении резистентного псевдомонадного пневмонита. Ther Drug Monit. 1989. 11 (6): 692–5. [PubMed] [Google Scholar] 105. Допфер Р., Брэнд П, Маллингер Б. и др. Ингаляция тобрамицина у больных муковисцидозом: сравнение двух методов.J. Physiol Pharmacol. 2007; 58 (Дополнение 5) (Pt 1): 141–54. [PubMed] [Google Scholar] 106. Ленуар Г., Антипкин Ю.Г., Миано А. и др. Эффективность, безопасность и местная фармакокинетика высококонцентрированного распыленного тобрамицина у пациентов с муковисцидозом, колонизированными синегнойной палочкой. Педиатрические препараты. 2007; 9 (Дополнение 1): 11–20. [PubMed] [Google Scholar] 107. Рэмси Б.В., Доркин Х.Л., Айзенберг Д.Д. и др. Эффективность аэрозольного тобрамицина у пациентов с муковисцидозом. N Engl J Med. 1993. 328 (24): 1740–6. [PubMed] [Google Scholar] 109.Кантон Р., Кобос Н., де Грасиа Дж. И др. Антимикробная терапия легочной патогенной колонизации и инфекции Pseudomonas aeruginosa у пациентов с муковисцидозом. Clin Microbiol Infect. 2005. 11 (9): 690–703. [PubMed] [Google Scholar] 110. Sexauer WP, Fiel SB. Аэрозольные антибиотики при муковисцидозе. Semin Respir Crit Care Med. 2003. 24 (6): 717–26. [PubMed] [Google Scholar] 111. Кун П., Ландау Л.И., Фелан П.Д. Распыленный гентамицин у детей и подростков с муковисцидозом. Aust Paediatr J.1984. 20 (1): 43–5. [PubMed] [Google Scholar] 112. Уолл М.А., Терри А.Б., Айзенберг Дж. И др. Ингаляционные антибиотики при муковисцидозе. Ланцет. 1983; 1 (8337): 1325. [PubMed] [Google Scholar] 113. Стейнкамп Г., Туммлер Б., Гаппа М. и др. Длительная аэрозольная терапия тобрамицином при муковисцидозе. Педиатр Пульмонол. 1989. 6 (2): 91–8. [PubMed] [Google Scholar] 114. Смит А.Л., Рэмси Б.В., Хеджес Д.Л. и др. Безопасность применения аэрозольного тобрамицина в течение 3 месяцев пациентам с муковисцидозом. Педиатр Пульмонол. 1989. 7 (4): 265–71.[PubMed] [Google Scholar] 115. Рэмси Б.В., Пепе М.С., Куан Дж. М. и др. Периодическое введение ингаляционного тобрамицина пациентам с муковисцидозом. Группа по изучению муковисцидоза, вдыхаемого тобрамицином. N Engl J Med. 1999. 340 (1): 23–30. [PubMed] [Google Scholar] 116. Мох РБ. Долгосрочные преимущества ингаляционного тобрамицина у подростков с муковисцидозом. Грудь. 2002. 121 (1): 55–63. [PubMed] [Google Scholar] 117. Стивенс Д., Гэри Н., Айлз А. и др. Эффективность ингаляционного тобрамицина при лечении обострений легких у детей с муковисцидозом.Pediatr Infect Dis. 1983; 2 (3): 209–11. [PubMed] [Google Scholar] 118. Schaad UB, Wedgwood-Krucko J, Suter S и др. Эффективность ингаляционного амикацина в качестве дополнения к внутривенной комбинированной терапии (цефтазидим и амикацин) при муковисцидозе. J Pediatr. 1987. 111 (4): 599–605. [PubMed] [Google Scholar] 119. Билтон Д., Хениг Н., Моррисси Б. и др. Добавление ингаляционного тобрамицина к ципрофлоксацину при обострении инфекции Pseudomonas aeruginosa при бронхоэктазах у взрослых. Грудь. 2006. 130 (5): 1503–10. [PubMed] [Google Scholar] 121.Рубин Б.К. Аэрозольные антибиотики для лечения бронхоэктазов без кистозного фиброза. J Aerosol Med Pulm Drug Deliv. 2008. 21 (1): 71–6. [PubMed] [Google Scholar] 122. Drobnic ME, Sune P, Montoro JB и др. Ингаляция тобрамицина пациентам с не кистозным фиброзом, бронхоэктазами и хронической бронхиальной инфекцией, вызванной синегнойной палочкой. Энн Фармакотер. 2005. 39 (1): 39–44. [PubMed] [Google Scholar] 123. Баркер А.Ф., Коуч Л., Фил С.Б. и др. Раствор тобрамицина для ингаляций снижает плотность мокроты синегнойной палочки при бронхоэктазах.Am J Respir Crit Care Med. 2000. 162 (2 Pt 1): 481–5. [PubMed] [Google Scholar] 124. Шейнберг П., Шор Э. Пилотное исследование безопасности и эффективности раствора тобрамицина для ингаляции у пациентов с тяжелыми бронхоэктазами. Грудь. 2005. 127 (4): 1420–146. [PubMed] [Google Scholar] 125. Додек П., Кинан С., Кук Д. и др. Основанное на фактических данных клиническое руководство по профилактике вентилятор-ассоциированной пневмонии. Ann Intern Med. 2004. 141 (4): 305–13. [PubMed] [Google Scholar] 126. Falagas ME, Siempos II, Bliziotis IA, et al.Введение антибиотиков через дыхательные пути для профилактики пневмонии, приобретенной в ОИТ: метаанализ сравнительных исследований. Crit Care. 2006; 10 (4): R123. [Бесплатная статья PMC] [PubMed] [Google Scholar] 127. Ратгебер Дж., Зильманн С., Панцер С. и др. Профилактика пневмонии путем эндотрахеальной микронебулизации тобрамицина. Анастезиол Интенсивмед Нефалмед Шмерцтер. 1993. 28 (1): 23–9. [PubMed] [Google Scholar] 128. Klastersky J, Huysmans E, Weerts D, et al. Эндотрахеально вводимый гентамицин для профилактики инфекций дыхательных путей у пациентов с трахеостомией: двойное слепое исследование.Грудь. 1974. 65 (6): 650–4. [PubMed] [Google Scholar] 129. Таблан О.К., Андерсон Л.Дж., Бессер Р. и др. Руководство по профилактике пневмонии, связанной с оказанием медицинской помощи, 2003 г .: рекомендации CDC и Консультативного комитета по практике инфекционного контроля в здравоохранении. MMWR Recomm Rep. 2004; 53 (RR-3): 1–36. [PubMed] [Google Scholar] 130. Falagas ME, Agrafiotis M, Athanassa Z и др. Введение антибиотиков через дыхательные пути в качестве монотерапии пневмонии. Эксперт Rev Anti Infect Ther. 2008. 6 (4): 447–52. [PubMed] [Google Scholar] 131.Ghannam DE, Rodriguez GH, Raad II и др. Ингаляционные аминогликозиды у онкологических больных с связанной с вентилятором грамотрицательной бактериальной пневмонией: безопасность и осуществимость в эпоху роста лекарственной устойчивости. Eur J Clin Microbiol Infect Dis. 2009. 28 (3): 253–9. [PubMed] [Google Scholar] 132. Палмер Л. Б., Смолдон Г. К., Чен Дж. Дж. И др. Аэрозольные антибиотики и трахеобронхит, связанный с вентилятором, в отделении интенсивной терапии. Crit Care Med. 2008; 36 (7): 2008–13. [PubMed] [Google Scholar] 133. Морозини М.И., Гарсия-Кастильо М., Лоза Э. и др.Контрольные точки для прогнозирования чувствительности Pseudomonas aeruginosa к вдыхаемому тобрамицину у пациентов с муковисцидозом: использование тест-полосок Etest с высоким диапазоном значений. J Clin Microbiol. 2005. 43 (9): 4480–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 134. Линден П.К., Патерсон Д.Л. Парентеральный и ингаляционный колистин для лечения вентилятор-ассоциированной пневмонии. Clin Infect Dis. 2006; 43 (Дополнение 2): S89 – S4. [PubMed] [Google Scholar] 135. Михалопулос А., Фотакис Д., Вирцили С. и др. Колистин в аэрозольной форме в качестве дополнительного лечения респираторно-ассоциированной пневмонии, вызванной грамотрицательными бактериями с множественной лекарственной устойчивостью: проспективное исследование.Respir Med. 2008. 102 (3): 407–12. [PubMed] [Google Scholar] 136. Kwa AL, Loh C, Low JG и др. Распыленный колистин в лечении пневмонии, вызванной множественной лекарственной устойчивостью Acinetobacter baumannii и Pseudomonas aeruginosa. Clin Infect Dis. 2005. 41 (5): 754–7. [PubMed] [Google Scholar] 137. Берлана Д., Ллоп Дж. М., Форт Е. и др. Использование колистина для лечения грамотрицательных инфекций с множественной лекарственной устойчивостью. Am J Health Syst Pharm. 2005. 62 (1): 39–47. [PubMed] [Google Scholar] 138. Hamer DH. Лечение внутрибольничной пневмонии и трахеобронхита, вызванных синегнойной палочкой с множественной лекарственной устойчивостью, колистином в аэрозольной форме.Am J Respir Crit Care Med. 2000. 162 (1): 328–30. [PubMed] [Google Scholar] 139. Маккой К.С., Квиттнер А.Л., Оерманн С.М. и др. Азтреонам лизин вдыхается при хронической болезни дыхательных путей Pseudomonas aeruginosa при муковисцидозе. Am J Respir Crit Care Med. 2008. 178 (9): 921–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 140. Сафдар А. Стратегии усиления иммунной функции у реципиентов гемопоэтической трансплантации, у которых есть грибковые инфекции. Пересадка костного мозга. 2006. 38 (5): 327–37. [PubMed] [Google Scholar] 141. Сафдар А.Трудности с грибковыми инфекциями у пациентов с острым миелогенным лейкозом: стратегии повышения иммунитета. Онколог. 2007; 12 (Дополнение 2): 2–6. [PubMed] [Google Scholar] 142. Safdar ARG, Lichtiger B, Dickey BF и др. Повышение иммунитета рекомбинантным интерфероном гамма 1b у 20 пациентов с гематологическими злокачественными новообразованиями и системными оппортунистическими инфекциями, получавших переливания донорских гранулоцитов. Рак. 2006. 106 (12): 2664–71. [PubMed] [Google Scholar] 143. Монтойя Дж. Г., Чапарро С. В., Селис Д. и др. Инвазивный аспергиллез на фоне трансплантации сердца.Clin Infect Dis. 2003; 37 (Приложение 3): S281–92. [PubMed] [Google Scholar] 144. Гарсия-Видаль CUA, Кирби К.А., Марр К.А. Эпидемиология инвазивных инфекций плесени у реципиентов аллогенных стволовых клеток: биологические факторы риска инфекции в зависимости от времени после трансплантации. Clin Infect Dis. 2008. 47 (8): 1041–50. [Бесплатная статья PMC] [PubMed] [Google Scholar] 145. Маттиуцци Г.Н., Кантарджиан Х., Фадерл С. и др. Липидный комплекс амфотерицина B как профилактика инвазивных грибковых инфекций у пациентов с острым миелогенным лейкозом и миелодиспластическим синдромом, проходящих индукционную химиотерапию.Рак. 2004. 100 (3): 581–9. [PubMed] [Google Scholar] 146. Сингх Н., Лимай А.П., Форрест Г. и др. Поздний инвазивный аспергиллез у реципиентов трансплантата в современную эпоху. Med Mycol. 2006. 44 (5): 445–9. [PubMed] [Google Scholar] 147. Schmitt HJ, Bernard EM, Hauser M, et al. Аэрозольный амфотерицин B эффективен для профилактики и лечения крысиной модели легочного аспергиллеза. Антимикробные агенты Chemother. 1988. 32 (11): 1676–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 148. Cicogna CE, White MH, Bernard EM и др.Эффективность профилактического аэрозольного липидного комплекса амфотерицина B на модели легочного аспергиллеза на крысах. Антимикробные агенты Chemother. 1997. 41 (2): 259–61. [Бесплатная статья PMC] [PubMed] [Google Scholar] 149. Коидзуми Т., Кубо К., Канеки Т. и др. Фармакокинетическая оценка амфотерицина B в легочной ткани: распределение легочной лимфы после внутривенной инъекции и распределение воздушного пространства после аэрозолизации и ингаляции амфотерицина B. Противомикробные агенты Chemother. 1998. 42 (7): 1597–600. [Бесплатная статья PMC] [PubMed] [Google Scholar] 150.Коркоран Т.Е., Венкатараманан Р., Михельц К.М. и др. Аэрозольное отложение липидного комплекса амфотерицин-B (Abelcet) у реципиентов трансплантата легких. Am J Transplant. 2006. 6 (11): 2765–73. [PubMed] [Google Scholar] 151. Дрю Р.Х., Доддс Эшли Э., Бенджамин Д.К., мл. И др. Сравнительная безопасность липидного комплекса амфотерицина B и дезоксихолата амфотерицина B в качестве противогрибковой профилактики в виде аэрозоля у реципиентов трансплантата легких. Трансплантация. 2004. 77 (2): 232–7. [PubMed] [Google Scholar] 152. Монтойя Дж. Г., Хиральдо Л. Ф., Эфрон Б. и др.Инфекционные осложнения у 620 последовательных пациентов после трансплантации сердца в медицинском центре Стэнфордского университета. Clin Infect Dis. 2001. 33 (5): 629–40. [PubMed] [Google Scholar] 153. Палмер С.М., Дрю Р.Х., Уайтхаус Дж. Д. и др. Безопасность липидного комплекса амфотерицина B в аэрозольной форме у реципиентов трансплантата легких. Трансплантация. 2001. 72 (3): 545–8. [PubMed] [Google Scholar] 154. Ботинки RJ, Патерсон Д.Л., Олворт А.М. и др. Успешное лечение постгриппозного псевдомембранозного некротизирующего аспергиллеза бронхов липосомальным амфотерицином, ингаляционным амфотерицином B, гамма-интерфероном и GM-CSF.Грудная клетка. 1999. 54 (11): 1047–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 155. Сафдар А., О’Брайен С., Кури И.Ф. Эффективность и возможность применения липидной комплексной терапии амфотерицина В в аэрозольной форме при легочном зигомикозе с прорывом каспофунгина. Пересадка костного мозга. 2004. 34 (5): 467–8. [PubMed] [Google Scholar] 156. Дханд Р., Гунтур В.П. Как лучше всего доставлять аэрозольные препараты пациентам, находящимся на ИВЛ. Clin Chest Med. 2008. 29 (2): 277–96. vi. [PubMed] [Google Scholar] 157. Макинтайр Н.Р., Сильвер Р.М., Миллер К.В. и др.Доставка аэрозоля интубированным пациентам на ИВЛ. Crit Care Med. 1985. 13 (2): 81–4. [PubMed] [Google Scholar] 158. Заявление о консенсусе по аэрозолям-1991. Американская ассоциация респираторной помощи. Respir Care. 1991. 36 (9): 916–21. [PubMed] [Google Scholar] 159. Дханд Р., Сохал Х. Система доставки лекарств в легкие для ингаляционной терапии у пациентов с механической вентиляцией легких. Эксперт Rev Med Devices. 2008; 5 (1): 9–18. [PubMed] [Google Scholar] 160. Blanchard JDCD и др. Отложение в легких интерферона гамма-1b после ингаляции через систему AERx vs.Небулайзер Respirgard II ™ . Am J Respir Crit Care Med. 2003; 167: A373. [Аннотация встречи] [Google Scholar] 161. Уоттс А.Б., МакКонвилл Дж. Т., Уильямс РО. Современные методы лечения и технологические достижения в области доставки лекарственных средств в виде водных аэрозолей. Препарат Дев Инд Фарм. 2008. 34 (9): 913–22. [PubMed] [Google Scholar]Ингаляционные терапевтические средства для профилактики и лечения пневмонии
Expert Opin Drug Saf. Авторская рукопись; доступно в PMC 2015 7 августа 2015 г.
Опубликован в окончательной редакции как:
PMCID: PMC4527977
NIHMSID: NIHMS710030
M.Онкологический центр Д. Андерсона, Хьюстон, Техас, США
† Автор для переписки: доцент медицины Техасского университета, Департамент инфекционных заболеваний, Онкологический центр доктора медицины Андерсона, Инфекционный контроль и здоровье сотрудников, 402, 1515 Holcombe Boulevard , Техас 77030, Хьюстон, США, тел .: +1 713 792 0825; Факс: +1713745 6839; gro.nosrednadm@radfasa См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты.Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков. По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями. Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной Pseudomonas aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких.Цитокиновая ингаляционная терапия также изучалась при лечении неопластических и инфекционных заболеваний. Выбор легочных систем доставки лекарств остается критическим, поскольку воздушно-струйный и ультразвуковой небулайзер могут обеспечить субоптимальную концентрацию лекарственного средства при неправильном использовании. В будущем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для снижения патогенной нагрузки в дыхательных путях субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмонии у субъектов с ослабленным иммунитетом с использованием цитокинов. или синтетические аналоги молекулярной структуры, ассоциированные с патогенами, и больше возможностей для использования ингаляционных противомикробных препаратов.Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
Ключевые слова: амикацин, противогрибковый, противовирусный, аспергиллез, рак, колистин, цитокин, ингаляционный тобрамицин, врожденный иммунитет, пневмония, псевдомонады, трансплантация, ванкомицин, вентилятор-ассоциированная пневмония, зигомикоз
1.0002 Введение и людей с ослабленным иммунитетом пневмония остается ведущей причиной преждевременной смерти в мире [1–3]. Восприимчивость легких к инфекции возникает из-за архитектурных требований газообмена и частого вдыхания инфекционных агентов.Для обеспечения вентиляции человек постоянно подвергает 100 м
2 площади поверхности легких воздействию внешней среды. Поскольку каждую минуту вентилируется 5–10 л окружающего воздуха, частицы, капли и болезнетворные микроорганизмы также уносятся. Кроме того, в то время как даже здоровые нормальные добровольцы демонстрируют ночную микроабсорбцию орогастрального содержимого, пациенты с неврологическими, анатомическими или ятрогенными препятствиями для защиты дыхательных путей (например, эндотрахеальные или назогастральные трубки) особенно восприимчивы к аспирации инфицированного материала в обширную поверхность раздела нижних отделов. дыхательные пути.В отличие от кожных поверхностей, обернутых непроницаемой кожей, желудка с его кислым просветом или нижних отделов желудочно-кишечного тракта с толстым слоем прилипшей слизи, обширный интерфейс легких с окружающей средой защищен только минимальной защитой барьера. Легочный барьер ограничен необходимостью беспрепятственной газовой диффузии, поэтому эта нежная ткань тонка капилляров. Тем не менее, несмотря на эту структурную уязвимость, легкие успешно защищаются от большинства инфекционных проблем с помощью различных механизмов [4–9].Большинство вдыхаемых или аспирированных патогенов не достигают периферических дыхательных путей из-за захвата в подвижном слое слизистого геля, выстилающего проксимальные проводящие дыхательные пути, с последующим изгнанием через систему мукоцилиарного эскалатора [4]. Постоянное присутствие антимикробных пептидов и антител в жидкости, выстилающей дыхательные пути, ограничивает рост патогенов, которые успешно проникают в небольшие дыхательные пути. Альвеолярные макрофаги поглощают организмы, которые достигают самых отдаленных воздушных пространств [6,7]. Когда базовые защитные механизмы превышены, эпителий легких реагирует увеличением своих прямых противомикробных свойств (см. Раздел 3) и сигнализирует о привлечении лейкоцитов из кровообращения.
Хотя доступность и большая поверхность легких способствуют их восприимчивости к инфекции, эти особенности также предоставляют уникальную возможность для местной терапии в виде респираторных аэрозолей, как показано ниже. Во-первых, недавно были разработаны стратегии увеличения мукоцилиарного клиренса с использованием аэрозолей гипертонического солевого раствора, которые могут снизить нагрузку патогенов в легких. Во-вторых, недавний прогресс в понимании врожденного иммунитета показал, что резистентность респираторного эпителия к патогенам может быть значительно стимулирована, и применение методов лечения, основанных на этом понимании, может снизить восприимчивость к инфекции у уязвимых групп пациентов.В-третьих, перенаправление отклоненного адаптивного иммунитета на повышение устойчивости к специфическим патогенам за счет аэрозольной доставки цитокинов было подтверждено небольшими исследованиями на людях. В-четвертых, антибиотики могут доставляться респираторным путем, максимизируя концентрацию лекарств в области инфекции, где необходимо уничтожение микробов, и сводя к минимуму системные концентрации лекарств, которые могут приводить к нежелательным побочным эффектам. Теоретическая основа и практический статус каждого из этих методов ингаляционной терапии рассматриваются в следующих разделах.
2. Аэрозольный гипертонический солевой раствор для увеличения мукоцилиарного клиренса легких
Основным стимулом к увеличению выведения слизи из легких стало лечение муковисцидоза (МВ). Традиционно постуральный дренаж, перкуссия и другие физические методы сочетаются с очищением от кашля для мобилизации слизи и мусора из дыхательных путей. Совсем недавно для увеличения мукоцилиарного клиренса были введены эффективные аэрозольные методы лечения. Первичным дефектом при МВ является отсутствие апикального эпителиального хлоридного канала, что приводит к уменьшению объема жидкости на поверхности дыхательных путей [10,11].Это предотвращает эффективное движение ресничек и вызывает обезвоживание слизи, что в совокупности ухудшает мукоцилиарный клиренс и повреждает дыхательные пути. Кроме того, эти изменения приводят к заселению обычно стерильных дыхательных путей бактериями и грибками, вызывая дальнейшее воспаление и повреждение дыхательных путей. По мере углубления понимания этих основных механизмов были введены методы лечения для увеличения объема жидкости на поверхности дыхательных путей (). К ним относятся нуклеотиды, амилорид и гипертонический солевой раствор (HSS), но среди них самые убедительные доказательства поддерживают аэрозольный HSS.
Эпителий дыхательных путей с жидкостью на поверхностиПроводящие дыхательные пути выстланы примерно равным количеством мерцательных и секреторных эпителиальных клеток. Секреторные клетки содержат гранулы, которые включают пептиды и муцины (зеленые), хотя внутриклеточные муцины могут быть обнаружены только в небольших дистальных отделах дыхательных путей с помощью чувствительных иммуногистохимических методов или во время воспалительной метаплазии, когда их продукция увеличивается [15,19]. Жидкость на поверхности дыхательных путей состоит из перицилиарного слоя толщиной 7 мкм (синий) и покрывающего его слоя слизистого геля (зеленый), толщина которого варьируется от <1 мкм в дистальных дыхательных путях до> 50 мкм в проксимальных дыхательных путях человека.Реснички направленно бьют, продвигая слой слизистого геля к головке гортани. Гликопротеины муцина MUC5AC и MUC5B являются основными компонентами слоя слизистого геля и высвобождаются экзоцитарно как из подлежащего поверхностного эпителия (показано), так и из подслизистых желез (не показано). Хотя слой слизистого геля важен для очистки от вдыхаемых патогенов (красный), чрезмерное производство муцина или истощение жидкости на поверхности дыхательных путей может привести к закупорке слизью просвета дыхательных путей, обеспечивая убежище для микробной инфекции.
Ранние исследования 1990-х годов показали, что увеличение концентрации аэрозольных растворов хлорида натрия (физиологического раствора) приводит к увеличению скорости мукоцилиарного клиренса [12–14]. На основании этих результатов, аэрозоли HSS были протестированы при краткосрочном лечении пациентов с CF и показали, что они улучшают функцию легких [12,15]. В 2006 году два крупных исследования с использованием 4 мл 7% физиологического раствора в форме аэрозоля два раза в день продемонстрировали улучшение функции легких и снижение частоты обострений [16,17], и теперь это лечение стало основой лечения МВ.
Есть несколько причин полагать, что лечение аэрозолями HSS принесет пользу не только больным МВ, но и пациентам. Во-первых, скорость мукоцилиарного клиренса увеличивается за счет увеличения гидратации даже у тех, у кого не наблюдается истощения жидкости на поверхности дыхательных путей. Это наблюдалось у пациентов с гиперальдостероном, у которых врожденно снижено всасывание натрия, и у здоровых людей из-за использования аэрозолей HSS [18]. Во-вторых, закупорка мелких дыхательных путей слизью из просвета возникает при заболеваниях легких, помимо МВ, таких как астма, хроническая обструктивная болезнь легких (ХОБЛ) и инфекции дыхательных путей, вызванные вирусными, грибковыми и микобактериальными патогенами [19,20].В-третьих, истощение жидкости на поверхности дыхательных путей происходит при некоторых нарушениях воспаления и инфекции дыхательных путей за счет протеолитической активации апикального эпителиального натриевого канала (ENaC) [21]. Исходя из этого, мы начали использовать аэрозольные 7% HSS у пациентов с закупоркой слизи в дыхательных путях и / или стойкой инфекцией дыхательных путей следующим образом. Для вызванной вирусом гиперсекреции слизи с кашлем у пациентов с астмой, ХОБЛ или посттрансплантационным констриктивным бронхиолитом мы используем HSS вместе с обычным режимом лечения обострения пациента, чтобы облегчить кашель и обеспечить доставку ингаляционных лекарств в дыхательные пути, которые в противном случае были бы забит слизью.У пациентов с аллергическим бронхолегочным аспергиллезом (ABPA) мы используем HSS вместе с некоторыми комбинациями ингаляционных стероидов, системных стероидов, системной противогрибковой и системной анти-IgE-терапией. При атипичной микобактериальной инфекции мы используем HSS либо в качестве монотерапии, либо вместе с ингаляционными и / или пероральными антибиотиками. У пациентов с эндобронхиальным стентом мы используем HSS для предотвращения скопления слизи дистальнее стента, что может привести к ателектазу или пневмонии. Иногда мы лечили пациентов с HSS, у которых были рентгенологические помутнения периферического легочного дерева в почке, для которых нам не удалось идентифицировать патоген.У нас есть неофициальные данные о симптоматических и рентгенологических улучшениях в поддержку всех этих применений, но нам неизвестны данные контролируемых испытаний. Когда используется несколько видов аэрозольной терапии, например, HSS вместе с ингаляционными стероидами, мы сначала применяем HSS, хотя объективных доказательств, подтверждающих эту практику, нет. Были бы полезны исследования, предназначенные для измерения применимости и оптимальных методов аэрозольного HSS при других заболеваниях, кроме МВ.
3. Аэрозольная стимуляция врожденного иммунитета легких
Хотя дыхательные пути и альвеолярный эпителий часто рассматриваются как пассивные барьеры, они дополняют базовую защиту легких, претерпевая значительные местные структурные и функциональные изменения при обнаружении патогенных раздражителей.Например, в ответ на вирусное, грибковое или аллергическое воспаление эпителиальные клетки дыхательных путей быстро приобретают гиперсекреторный фенотип в результате процесса, называемого слизистой метаплазией [22,23]. Предполагается, что адаптивная ценность структурной и молекулярной пластичности респираторного эпителия заключается в усилении защиты от микробных патогенов, и это подтверждается наблюдением улучшенного бактериального клиренса после индукции антимикробных белков, включая дефенсины, кателицидины, лизоцим и генераторы реактивных микроорганизмов. формы кислорода [24–28].В присутствии патогенов дыхательные пути и альвеолярный эпителий также вырабатывают воспалительные цитокины и вовлекают лейкоциты в защиту легких [29]. Подавление адаптивного иммунитета и гематопоэза, которое происходит при гематологических злокачественных новообразованиях и / или цитотоксической химиотерапии, не устраняет врожденный иммунный ответ легких на инфекцию. Скорее, пациенты с глубокой иммуносупрессией вырабатывают замечательные цитокиновые и хемокиновые ответы на легочные инфекции [30].
При врожденном иммунитете лейкоциты и паренхимные клетки идентифицируют присутствие патогенов посредством распознавания патоген-ассоциированных молекулярных паттернов (PAMPs), общих для многих видов патогенов, рецепторами распознавания паттернов, кодируемых зародышевой линией (PRR) [31–35].Распознавание PAMP посредством PRR активирует внутриклеточные сигнальные каскады, приводя к экспрессии продуктов, участвующих в микробной защите, воспалении и модуляции адаптивного иммунитета [36]. До сих пор попытки вызвать врожденный иммунитет легких были направлены на стимуляцию PRR с использованием природных или синтетических лигандов [37]. Наиболее распространенными мишенями были Toll-подобные рецепторы (TLR), хотя NOD-подобные рецепторы использовались в качестве адъювантов вакцины в течение многих лет [37], а другие молекулы, такие как RIG-подобные рецепторы и дектин, считались потенциальными терапевтическими мишенями. [37–42].
Чтобы проверить, можно ли эффективно использовать функциональную пластичность легких для защиты от пневмонии in vivo , наша лаборатория сильно стимулировала врожденный иммунитет перед заражением вдыхаемыми респираторными патогенами. Чтобы добиться этого, мышей подвергали воздействию лизата в виде аэрозоля, изготовленного из нетипируемого Haemophilus influenzae , одновременно стимулируя несколько антимикробных путей [42]. Однократное распыление привело к приобретению высокого уровня устойчивости к заражению вирулентными неконфекционными патогенами в течение 2 часов после лечения ().Мы назвали это явление «стимулированная врожденная резистентность» (StIR), чтобы отразить несколько аспектов защиты. Он считается «стимулированным», поскольку резистентность значительно возрастает после терапевтического применения лизата. Защита отражает действие «врожденных» защит, что демонстрируется несколькими ключевыми характеристиками: i) защита достигается за часы, а не дни или недели, как требуется для адаптивного иммунитета; ii) защита достигается у наивных мышей после лечения, полученного от микроба, не являющегося родственным тому, который использовался в контрольном заражении; iii) эффект сохраняется, несмотря на химическое или генетическое истощение адаптивных лейкоцитов; и iv) защита распространяется на каждый микробный патоген, против которого он был протестирован, что указывает на широкий, неизбирательный ответ.Защита связана с «сопротивлением» следующим образом. Столкнувшись с микробной проблемой, выживание зависит от двух стратегий хозяина: толерантности (способность ограничивать ущерб, причиняемый патогеном) и устойчивости (способности ограничивать бремя патогенов) [43,44]. Мы обнаружили, что обработка лизатом ограничивает количество патогенов, связанных с различными классами организмов. Следовательно, мы определили устойчивость как основное средство защиты лизата.
Выживаемость после заражения Streptococcus pneumoniae (Spn) после лечения аэрозольным лизатом нетипируемого Haemophilus influenze (NTHi)Мышей предварительно обрабатывали в группах по шесть человек аэрозольным лизатом NTHi для стимуляции врожденного иммунитета, затем заражали как одну группу с высокой дозой Spn (6.1 × 10 10 КОЕ / мл). Выживаемость через 7 дней показана как функция интервала между лечением и контрольным заражением (* p = 0,015, ‡ p = 0,002, лечение по сравнению с необработанным) [50].
Сначала мы проверили защитное действие StIR против наиболее распространенной причины бактериальной пневмонии во всем мире, Streptococcus pneumoniae , и обнаружили, что, хотя все нелеченные мыши умерли после ингаляционного заражения, все мыши, обработанные лизатом, выжили. Механистические исследования показали, что защита тесно связана с индукцией антимикробной среды в легких, что демонстрируется быстрым снижением количества патогенов по сравнению с нелеченными мышами [42].Защитный эффект сохранялся, даже если у мышей не было резидентных лейкоцитов в легких (альвеолярных макрофагов и тучных клеток) или у мышей не было рекрутированных нейтрофилов. Последующие исследования также показали, что лимфоциты были незаменимы при StIR, и исследований in vitro показали, что респираторный эпителий был достаточным как для восприятия лечения, так и для воздействия на противомикробный ответ [45].
Стимулированная врожденная резистентность широко распространяется на другие важные бактериальные респираторные патогены.Среди распространенных причин внутрибольничной пневмонии ингаляционное лечение бактериальным лизатом эффективно защищает от Pseudomonas aeruginosa , Klebsiella pneumoniae и лейкоцидин-продуцирующих лейкоцидин Panton-Valentine устойчивых к метициллину Staphylococcus aureus [45]. Дыхательный путь — наиболее вероятный портал входа для агентов биотеррора и единственный способ, с помощью которого такие патогены были успешно доставлены в современную эпоху (например, ингаляционная сибирская язва) [46–49].Мы исследовали, может ли StIR защищать от агентов биотеррора, и обнаружили, что однократное введение аэрозольного лизата значительно увеличивает среднюю выживаемость мышей, зараженных Bacillus anthracis , Yersinia pestis или Francisella tularensis [45]. Для всех исследованных бактериальных патогенов защита от летального исхода была связана со значительным и немедленным сокращением количества патогенов.
Учитывая широту защиты от разнородных видов бактерий и предположение о еще более широком антимикробном действии путем анализа экспрессии гена легких после лечения, также была протестирована защита мышей от грибкового патогена.Поскольку ни мыши, ни люди обычно не восприимчивы к пневмонии Aspergillus при отсутствии иммунодефицита, мышей лечили циклофосфамидом и кортизолом перед контрольным заражением A. fumigatus . Из инфицированных мышей> 70% умерли, если они не прошли предварительную обработку лизатом. Практически все, кто проходил лечение, выжили (93%). Как и в случае с бактериальными патогенами, StIR привел к значительному снижению внутрилегочной грибковой нагрузки [45].
Вирус гриппа является основной причиной смертности от легочных инфекций во всем мире, и эффективный легочный StIR может обеспечить защиту во время пандемий.Мы обнаружили, что в то время как 100% контрольных мышей умерли от геморрагической пневмонии,> 90% выжили после одной предварительной обработки бактериальным лизатом [50]. Мы также обнаружили значительное улучшение показателей выживаемости, если лизат в форме аэрозоля вводили через 1 день после заражения, что указывает на то, что стимуляция врожденного иммунитета может быть полезной для лечения, а также для профилактики пневмонии. Кроме того, мы обнаружили, что добавление рибавирина к лечению лизатом привело к синергетическому улучшению выживаемости (т. Е., лучше, чем аддитивные эффекты одного лечения) при введении после инфекции [50]. Как и в случае со всеми другими исследованными патогенами, защита от гриппа, вызванная лизатом, коррелировала со снижением титров вируса в легких.
В то время как лечение нетипируемым лизатом Haemophilus influenza (NTHi) приводит к быстрой активации врожденного иммунитета слизистой оболочки легких, защитный эффект ослабевает через 4-5 дней [50,51]. Следовательно, для предотвращения пневмонии у групп пациентов, подвергавшихся риску по истечении этого периода, вероятно, потребуется повторное лечение.Мы обнаружили, что повторное дозирование является эффективным и безопасным для мышей. При повторной обработке лизатом мыши показали стойкую устойчивость к заражению S. pneumoniae , P. aeruginosa и гриппом A [45,50]. Мыши, подвергавшиеся обработке лизатом еженедельно в течение 50 недель, не показали явных патологий, таких как преждевременная смерть, потеря веса или изменения поведения [36]. После 8 еженедельных воздействий инфильтрация мононуклеарных клеток окружала дыхательные пути, хотя наблюдалось очень мало альвеолярных воспалительных клеток.После 25 еженедельных воздействий был очевиден легкий фиброз стенки дыхательных путей, который далее прогрессировал после 50 еженедельных воздействий [52]. Увеличенная временная шкала фиброза стенки дыхательных путей и прогрессирующего накопления лимфоцитов предполагает, что фиброз возникает из-за адаптивного иммунного ответа после хронического воздействия бактериального лизата, а не в ответ на саму стимуляцию врожденного иммунитета. Замена макромолекулярных стимуляторов врожденного иммунитета низкомолекулярными аналогами, которые не вызывают адаптивного иммунного ответа, и снижение интенсивности стимуляции, таким образом, позволяет избежать этого долгосрочного осложнения.Действительно, толстая кишка мышей постоянно стимулируется присутствием просветных бактерий, что приводит к конститутивной активации StIR, которая может быть обнаружена как индуцибельно сниженная способность убивать бактерии эпителием толстой кишки после лечения антибиотиками [53], но толстая кишка этого не делает. развивается фиброз.
Данные на мышах показывают, что лечение, индуцирующее врожденную резистентность в легких, должно хорошо переноситься пациентами-людьми. Мы полагаем, что причина того, что мыши могут переносить самые высокие применяемые дозы (в 12 раз превышающие терапевтическую дозу) без явных побочных эффектов [51], заключается в том, что реакция содержится в просвете легких.Несмотря на то, что количество воспалительных цитокинов в жидкости бронхоальвеолярного лаважа увеличивается в несколько тысяч раз по сравнению с исходным уровнем, уровень системных цитокинов почти не увеличивается [50]. Это согласуется с недавней работой Hoogerwerf и его коллег, которые вызвали значительную воспалительную реакцию легких в дыхательных путях у людей, подвергшихся внутрилегочному применению лигандов TLR, липотехоевой кислоты (лиганд TLR2) и липополисахарида (LPS, лиганд TLR4), но не были связаны с любые идентифицируемые клинические признаки или симптомы [54].
Не только наша лаборатория исследует стимуляцию TLR, которая может способствовать увеличению выживаемости хозяина при инфекциях. Несколько групп наблюдали иммуномодулирующие эффекты ЛПС и пытались изменить течение респираторных инфекций, доставляя производные ЛПС [40,41,55] или изменяя структуру ЛПС [39] у патогенов, используемых при экспериментальной пневмонии. У всех была обнаружена некоторая степень защиты за счет применения одного агониста TLR4, как и у нас [51]. Испытания отдельных агонистов TLR также были успешными при инфекционных заболеваниях человека.Например, подкожное введение синтетического агониста TLR9 вызвало системные воспалительные реакции и снизило вирусную нагрузку гепатита C [42], а местный имиквимод (TLR7) оказался многообещающим при лечении кожного лейшманиоза [38]. Однако вполне вероятно, что для достижения полной эффективности и широты действия, продемонстрированных с бактериальным лизатом, потребуются синергетические взаимодействия множественной стимуляции PRR [56-59].
Лизат, используемый для индукции StIR, не обладает антибиотическим действием [45].Скорее, он вызывает собственные защитные продукты хозяина. Индукция выработки антимикробного пептида согласуется как со временем, так и с широтой защиты и демонстрируется с помощью микроматрицы экспрессии генов [45] и протеомного анализа [51]. В будущем, возможно, удастся обойти стадию индукции хозяина и напрямую доставить полезные антимикробные пептиды или миметики малых молекул [43].
В ближайшем будущем стимуляция естественной реакции хозяина на микробные продукты для профилактики и лечения пневмонии может стать основой для разработки новой клинической терапевтической стратегии [44,45].
4. Аэрозольная доставка цитокинов для направленного иммунного отклонения
IFNα-2a, IFNγ-1b и GM-CSF вводились легочным путем пациентам с резистентной легочной инфекцией Mycobacterium tuberculosis и нетуберкулезным микобактериозом (NTM) включая Mycobacterium avium комплексное заболевание легких с переменным успехом. Эти иммунологически разнообразные белки также использовались при неинфекционных легочных заболеваниях, таких как первичный рак легких, метастатический рак в легкие и альвеолярный протеиноз, заболевание, недавно связанное с антителами против нативного GM-CSF [60–62].Ниже приводится краткое описание клинического опыта использования терапии ингаляционными цитокинами при легочной инфекции.
Ингаляционный IFNα переносится в более низких дозах (1-20 MIU) без системных побочных эффектов, тогда как лихорадка, недомогание и головная боль возникали при использовании доз в диапазоне от 60 до 120 MIU и совпадали с обнаруживаемым цитокином в периферическом кровообращении [63, 64]. Бронхоспазм препятствует использованию этого цитокина у пациентов с хроническим бронхитом [65].Спасательная терапия с использованием ингаляционного IFNα для лечения неоперабельного рака легких не обнадеживает [66]. Добавление IFNα 3 MIU 3 раза в неделю к противотуберкулезной терапии было связано с ранним исчезновением лихорадки и быстрым снижением количества кислотоустойчивых бацилл в отхаркиваемой мокроте по сравнению с одной антимикробной терапией [67]. Кроме того, у пациентов с резистентной к лечению туберкулезной инфекцией добавление ингаляционного IFNα показало обнадеживающие результаты, хотя необходимы дальнейшие крупные рандомизированные исследования для подтверждения безопасности, стоимости и эффективности [68].
Низкие дозы ингаляционного IFNγ хорошо переносятся, в том числе пациентами с бронхореактивными состояниями, такими как астма, и после воздействия этого плейотропного провоспалительного цитокина была продемонстрирована измеримая активация альвеолярных макрофагов [69,70]. Имеется значительный клинический опыт использования ингаляционного IFNγ для лечения легочных микобактериальных инфекций. В сочетании с антимикробной терапией терапия IFNγ в виде аэрозоля привела к благоприятным ответам как на лекарственно-чувствительный, так и на лекарственно-устойчивый туберкулез легких, с уничтожением микроорганизмов и улучшением радиографических показателей заболевания [71–73].Однако этого преимущества не наблюдалось у пациентов с тяжелым основным заболеванием легких, у которых был туберкулез легких [74]. Точно так же не было отмечено терапевтического эффекта у пациентов с МВ, получавших высокие дозы (500 или 1000 мкг) ингаляционного IFNγ для снижения риска инфекции, тем не менее, пациенты страдали от серьезной лекарственной токсичности, включая одышку, кровохарканье и госпитализацию [75]. IFNγ также был исследован для профилактики вентилятор-ассоциированной пневмонии (ВАП) у пациентов с тяжелыми травмами [76].Количество ВАП было уменьшено, хотя не наблюдалось улучшения общей смертности у этих пациентов с травмами, которые получали 100 мкг рекомбинантного IFNγ в аэрозольной форме 3 раза в день [76]. Эта неэффективность частично может быть связана с низкой доставкой цитокинов через стандартный распылитель [77]. Рекомбинантный GM-CSF в аэрозольной форме хорошо переносится пациентами с легочными метастазами в дозах 250 мкг дважды в день без серьезных побочных эффектов [78]. О применении аэрозольных GM-CSF для лечения инфекций у людей не сообщалось.Однако эксперименты на животных подтверждают абсорбцию в легких аэрозольного или интратрахеально введенного GM-CSF, и GM-CSF в аэрозольной форме оказался эффективным в искоренении инвазивного легочного аспергиллеза у мышей в модели с ослабленным иммунитетом [79,80].
Другие цитокины, используемые аэрозольным путем, включают IFNβ при лечении рака легких, IL-2 при почечно-клеточной карциноме и другом метастатическом раке легких, растворимый рецептор IL-4 для пациентов с астмой и эритропоэтин для лечения анемии.Ни один из них не использовался для лечения легочной инфекции.
5. Доставка синтетических антибиотиков в аэрозольной форме
В первом подразделе мы обсудим использование аминогликозидов в лечении и профилактике серьезных легочных инфекций у пациентов с высоким риском, а затем кратко ознакомимся с ограниченным клиническим опытом применения других противомикробных препаратов. препараты, которые использовались для спасительной терапии трудноизлечимой пневмонии. Учитывая, что были проведены обширные обзоры ингаляционного пентамидина при ВИЧ-ассоциированной инфекции Pneumocystis jiroveci , эта тема здесь не рассматривается.
5.1 Аэрозольная терапия аминогликозидами
Теоретически аминогликозиды имеют несколько характеристик, которые, по-видимому, способствуют ингаляционному введению. Во-первых, аминогликозиды обладают эффектом уничтожения, зависящим от концентрации, что означает, что высокие уровни, достижимые в дыхательных путях с помощью ингаляционных препаратов, могут привести к повышению клинической эффективности. Более того, аминогликозиды обладают значительной ограничивающей дозу токсичностью для людей, так что дозы, которые можно вводить при системном введении, приводят к относительно низким уровням в паренхиме легких.Наконец, поскольку аминогликозиды использовались относительно редко в течение последних нескольких десятилетий, многие организмы с множественной лекарственной устойчивостью, вызывающие нозокомиальную респираторную инфекцию, остаются восприимчивыми по крайней мере к одному, если не ко многим, обычно используемым аминогликозидам. Действительно, из всех классов антибиотиков данные о доставке антимикробных препаратов путем ингаляции наиболее обширны для аминогликозидов. В этом разделе мы рассмотрим фармакокинетическую, клиническую информацию и информацию о безопасности, касающуюся ингаляционной терапии аминогликозидами.
Разработка аминогликозидов широкого спектра действия, таких как гентамицин, в конце 1960-х — начале 1970-х годов открыла большие перспективы для лечения ранее резистентных респираторных инфекций из-за устойчивых к антимикробным препаратам грамотрицательных палочек, таких как P. aeuroginosa [81] . Однако вскоре исследователи сообщили, что системно вводимый гентамицин часто не лечил легочные инфекции из-за P. aeuroginosa и других грамотрицательных палочек, несмотря на чувствительность in vitro [82].Низкие уровни гентамицина в респираторных секретах заставили исследователей предположить, что беспорядочное проникновение аминогликозидов в очаг инфекции может быть причиной терапевтических неудач, и предположить, что введение гентамицина непосредственно в легкие может улучшить клинический ответ [83,84]. Предварительные исследования 1970-х годов показали, что концентрация гентамицина в мокроте часто была на порядок выше после эндотрахеального введения по сравнению с системным лечением [83,85].
Данные, накопленные в последующие 30 лет, подтвердили предположение этих ранних сообщений о том, что проникновение аминогликозидов в легочную паренхиму является субоптимальным после системного введения [86–93]. Фармакокинетика доставки аминогликозидного лекарственного средства имеет особое значение, поскольку эти агенты обладают зависящим от концентрации эффектом уничтожения, а это означает, что более высокие уровни лекарственного средства связаны с усилением антимикробного действия [94]. Например, оптимальный клинический ответ на терапию аминогликозидами происходит, когда максимальная концентрация препарата (C max ) до минимальной ингибирующей концентрации (МИК) составляет> 8: 1 [95–98].Терапия аминогликозидами при пневмонии обычно рассматривается для относительно устойчивых неферментативных грамотрицательных палочек, таких как P. aeruginosa , Acinetobacter baumanii и Stenotrophomonas maltophila [99]. Хотя они сильно варьируются в зависимости от популяции пациентов и рассматриваемых аминогликозидов, даже для восприимчивых организмов, МПК для этих организмов обычно находятся в диапазоне 1-8 мкг / мл [100]. Таким образом, чтобы максимизировать возможность клинического ответа, необходимы концентрации легочных аминогликозидов ≥ 10-40 мкг / мл.Важно отметить, что ни один из доступных в настоящее время аминогликозидов не достигает таких уровней при системном введении даже в условиях воспалительного процесса, который, как ожидается, приведет к увеличению попадания в легкие из кровотока [85,86,91,92,101] .
В отличие от трудностей достижения удовлетворительных уровней в легких с помощью системного введения аминогликозидов, местная доставка аминогликозидов приводит к концентрациям, которые могут быть эффективными даже против относительно резистентных организмов [85,86,93,102-104].Измерения уровней аминогликозидов в легких после местного введения в значительной степени зависят от механизма, используемого для доставки лекарственного средства, дозы и места отбора пробы. Однако, несмотря на эти различия, исследователи неизменно демонстрируют уровни аминогликозидов> 200 мкг / мл в респираторных образцах после местного применения [85–87,89,101–107]. Данные, касающиеся концентраций аминогликозидов, аналогичны в исследованиях на животных и людях, у больных и здоровых пациентов, а также при использовании инвазивных и неинвазивных методов тестирования [85–87,89,101–107].Таким образом, фармакокинетические данные убедительно свидетельствуют о том, что местное введение аминогликозидов с большей вероятностью приведет к эффективным уровням лекарственного средства по сравнению с системной доставкой.
5.2 Клинические исследования ингаляционных аминогликозидов: муковисцидоз
Контроль над бронхолегочной инфекцией заметно повысил качество и продолжительность жизни пациентов с МВ [108]. Уникальная эндобронхиальная среда пациентов с МВ означает, что легкие таких пациентов колонизируются такими организмами, как S.aureus и H. influenza вскоре после рождения. Однако со временем P. aeuroginosa обычно становится преобладающим легочным патогеном у пациентов с МВ, колонизируя> 80% людей к 18 годам [109]. Взаимодействие «хозяин – патоген» между пациентами с МВ и P. aeuroginosa относительно уникально с точки зрения бактериальных процессов, поскольку однажды установленная эндобронхиальная инфекция, вызванная P. aeuroginosa , редко полностью искореняется [110]. Большая часть терапевтических достижений, достигнутых за последние десятилетия в лечении пациентов с МВ, была достигнута за счет снижения бремени, вызываемого P.aeuroginosa в легких пациентов с МВ, что впоследствии уменьшает воспалительный ответ, ответственный за прогрессирование бронхоэктазов.
В то время как внутривенные антибиотики долгое время были золотым стандартом для лечения инфекции, вызванной P. aeuroginosa у пациентов с МВ, за последние 20 лет серия все более тщательных клинических исследований четко установила роль ингаляционных аминогликозидов в подавлении P. y инфекция aeuroginosa у пациентов с МВ.Первоначально использовался гентамицин, но исследователи перешли к тобрамицину в свете его повышенной активности против Pseudomonas [111–113]. Для удобства в ранних исследованиях использовались небулайзерные флаконы с аминогликозидами, изначально предназначенные для внутривенного введения, которые потенциально могли вызвать раздражение легких из-за присутствия консервантов и антиоксидантов. Важный прогресс произошел, когда Smith et al . разработали препарат тобрамицина без консервантов для распыления, который в дозе 600 мг обеспечивает гораздо более высокую дозу, чем типичный флакон для внутривенного введения на 80 мг [114].Это была доза тобрамицина 600 мг, которая использовалась в критическом исследовании перекрестного дизайна для 71 человека, в котором пациенты получали t.i.d. дозирование. После 1 месяца приема распыленного тобрамицина ключевые параметры легочной функции и плотность мокроты, полученной при использовании P. aeuroginosa , значительно улучшились в группе лечения [107]. Эффективный, но громоздкий характер лечения привел к разработке следующего поколения распыленного тобрамицина, который впоследствии был использован в крупнейшем рандомизированном плацебо-контролируемом исследовании распыленных аминогликозидов.В общей сложности 520 пациентов с CF, которые были колонизированы P. aeuroginosa , были рандомизированы для получения распыленного тобрамицина 300 мг два раза в день. или плацебо, вводимое в 4-недельных блоках включения-выключения в течение 24 недель [115]. Пациенты, получавшие активное лечение, показали улучшение показателей легочной функции, меньшую потребность в госпитализации и значительное снижение плотности P. aeuroginosa в мокроте. Важно отметить, что положительный эффект ингаляционного тобрамицина сохранялся в течение 2 лет после начала лечения [116].Результаты этого исследования привели к одобрению FDA США раствора тобрамицина для ингаляции (TSI) (TOBI ™ , Novartis Corp., Восточный Ганновер, Нью-Джерси), который до сих пор является единственным одобренным антибиотиком для ингаляции дыхательных путей в США. .
Эффективность TOBI в хроническом подавлении P. aeuroginosa у пациентов с МВ привела к исследованиям ингаляционных аминогликозидов при обострениях МВ, но результаты не были столь впечатляющими. Несколько испытаний показали, что добавление ингаляционных аминогликозидов, таких как тобрамицин или амикацин, к системной антипсевдомонадной терапии увеличивает долю пациентов, которые избавляются от P.aeuroginosa из мокроты, но не улучшает клинические исходы, такие как тесты функции легких [117,118]. Недавно завершенное международное исследование в 17 центрах не выявило статистической разницы в клинических исходах при добавлении ингаляционного тобрамицина к системно вводимому ципрофлоксацину у пациентов с МВ, инфицированных P. aeuroginosa, с обострением [119]. Пациенты, получавшие ингаляционный тобрамицин, имели более низкую плотность мокроты P. aeuroginosa , но повышенную частоту свистящего дыхания при ингаляционной терапии, что могло свести на нет пользу от усиленного противомикробного эффекта.Таким образом, в настоящее время ингаляционная терапия не считается частью стандарта помощи пациентам с МВ с обострениями.
5.3 Лечение пациентов с бронхоэктазами без кистозного фиброза ингаляционными аминогликозидами
Хотя МВ является преобладающей причиной бронхоэктазов в развитых странах, существует несколько других заболеваний, которые могут привести к бронхоэктазам [120]. Обнадеживающие результаты лечения бронхоэктазов, связанных с МВ, увеличили давний интерес к лечению пациентов с бронхоэктазами, не связанными с МВ, с помощью ингаляционных аминогликозидов [121].К сожалению, как и в случае острых обострений при МВ, накопленные к настоящему времени данные об эффективности ингаляционных аминогликозидов при бронхоэктазиях, не связанных с МВ, не так сильны, как данные для поддерживающей терапии при МВ. На данный момент четыре опубликованных клинических исследования изучали использование ингаляционных аминогликозидов у пациентов без МВ с бронхоэктазами и хронической инфекцией, вызванной P. aeuroginosa , во всех из которых использовался ингаляционный тобрамицин в дозе 300 мг два раза в день. дозирование [119,122–124]. Подобно основным исследованиям МВ, эти испытания неизменно показывают, что ингаляционный тобрамицин значительно снижает респираторную нагрузку P.aeuroginosa . Однако, в отличие от ситуации с бронхоэктазами, связанными с МВ, снижение уровня P. aeuroginosa у пациентов с бронхоэктазами, не связанными с МВ, не привело к последовательному улучшению объективных клинических показателей, таких как тесты функции легких. Одно исследование обнаружило улучшение «общего состояния здоровья» у пациентов, получавших тобрамицин [123]. Обнаружение того, что у пациентов, получавших тобрамицин, развивался более выраженный бронхоспазм по сравнению с пациентами, получавшими плацебо, значительно ограничило применение аэрозольных антибиотиков при бронхоэктазах без МВ [121].Таким образом, широкое использование ингаляционных аминогликозидов у пациентов с бронхоэктазами без МВ требует разработки препарата, который вызывает меньшее раздражение дыхательных путей при сохранении антипсевдомональной эффективности.
5.4 Профилактика и лечение вентилятор-ассоциированной пневмонии с помощью ингаляционных аминогликозидов
Хотя ИВЛ имеет жизненно важное значение для ведения тяжелобольных пациентов, она часто осложняется развитием респираторных инфекций, вызывающих значительную заболеваемость и смертность [125].Учитывая легкость доступа, обеспечиваемую интубацией трахеи, существует долгая история введения противомикробных препаратов непосредственно в дыхательные пути для лечения и профилактики респираторных инфекций, связанных с аппаратом ИВЛ [83]. Наиболее систематически исследуемой областью в этом отношении было использование местных антибиотиков для предотвращения искусственной вентиляции легких (ВАП) [126]. Хотя самые крупные исследования были проведены с антибиотиками, не являющимися аминогликозидами, и тобрамицин, и гентамицин показали некоторую эффективность в предотвращении ВАП [127, 128].Недавний метаанализ показал, что местное применение антимикробных препаратов значительно снижает частоту ВАП у пациентов с искусственной вентиляцией легких [126]. Эти данные противоречат рекомендациям Центров по контролю и профилактике заболеваний против использования распыленных антибиотиков для предотвращения ВАП из-за опасений по поводу развития устойчивости к противомикробным препаратам и побочных эффектов введения [129].
По сравнению с профилактикой ВАП, существует меньше системных данных об использовании ингаляционных аминогликозидов для терапии ВАП [130].Однако, учитывая рост показателей ВАП из-за множественной лекарственной или даже панрезистентности грамотрицательных патогенов, использование ингаляционных аминогликозидов или других противомикробных препаратов может стать все более распространенным явлением в попытке повысить локальные концентрации лекарств для борьбы с относительно устойчивыми патогенами. Следует отметить, что недавнее ретроспективное исследование онкологических пациентов с грамотрицательной палочкой ВАП показало, что те пациенты, которые получали ингаляционные аминогликозиды, в основном тобрамицин или ингаляционный колистин, имели значительно лучшие клинические результаты по сравнению с пациентами, получавшими терапию системными аминогликозидами или колистином [131].Наконец, Палмер и др. . недавно сообщили о результатах исследования, в котором пациенты с вентилятор-ассоциированным трахеобронхитом (VAT) были рандомизированы для приема ингаляционных противомикробных препаратов, тобрамицина и / или ванкомцина или плацебо [132]. Пациенты, получавшие ингаляционные противомикробные препараты, имели заметное улучшение объективных респираторных показателей и имели значительно меньшую вероятность прогрессирования до ВАП по сравнению с пациентами, получавшими плацебо. В совокупности сочетание повышения лекарственной устойчивости и накопления данных об эффективности ингаляционной терапии указывает на то, что местная терапия аминогликозидами может играть многогранную роль в профилактике и лечении респираторной инфекции у пациентов с механической вентиляцией легких, хотя необходимы многоцентровые проспективные исследования.
5.5 Безопасность ингаляционных аминогликозидов
Двумя основными проблемами, вызывающими обеспокоенность в отношении местной терапии аминогликозидами, являются развитие лекарственной устойчивости и побочные эффекты лекарств или системы доставки лекарств. Учитывая, что местное введение приводит к градиенту концентрации противомикробного препарата от центральных к периферическим дыхательным путям, существует серьезная проблема индукции устойчивости к противомикробным препаратам [121]. Более того, местная терапия часто назначается в течение длительных периодов времени, даже лет, тем самым максимально увеличивая возможность развития лекарственной устойчивости.В то время как отчеты о случаях и серии случаев подтверждают, что резистентные организмы могут возникать во время терапии, тщательное обследование в ходе рандомизированных клинических испытаний не показало, что появление резистентных к лекарствам организмов у пролеченных пациентов является особенно важной проблемой [100, 110, 126]. В свете чрезвычайно высоких уровней аминогликозидов, достижимых с помощью небулайзерной терапии, некоторые страны предложили разработать специфические для ингаляции контрольные точки МИК, при которых очень немногие организмы действительно будут устойчивы к аминогликозидам [133].Приведет ли загрязнение окружающей среды при нозокомиальной небулайзерной терапии к повышению устойчивости к аминогликозидам в медицинских учреждениях, остается теоретическим, но недоказанным вопросом. Выявление бронхоспазма при местной терапии — еще одна важная проблема безопасности, особенно когда распыленные антибиотики используются для облегчения симптомов, например, при бронхоэктазах [121]. Хотя обычно они легко поддаются лечению бронходилататорами, раздражение дыхательных путей распыляемыми аминогликозидами ограничено для многих пациентов, и продолжение исследований по разработке более переносимых методов лечения имеет решающее значение для более широкого использования.
5.6 Другие виды антибактериальной терапии в виде аэрозолей
Клинический опыт аэрозолизации антибактериальных средств, отличных от аминогликозидов, ограничен, но продолжает расти. Заметное увеличение числа грамотрицательных патогенов с множественной лекарственной устойчивостью привело к увеличению использования полимиксинов, противомикробных препаратов, которые были разработаны в 1950-х годах, но их использование быстро сократилось в 1970-х и 1980-х годах из-за опасений по поводу нефротоксичности [134]. Использование колистина (полимиксина E) в последнее время заметно увеличилось, поскольку штаммы P.aeruginosa и A. bauamnnii , устойчивые ко всем другим классам коммерчески доступных антимикробных препаратов, остались чувствительными к колистину [134]. Подобно аминогликозидам, ингаляция является потенциально привлекательным способом введения колистина, учитывая токсичность, наблюдаемую при системном введении. Ретроспективные и нерандомизированные исследования показали обнадеживающие результаты при использовании ингаляционного колистина, хотя исследования противоречат гетерогенности пациентов и назначению дополнительных противомикробных препаратов в сочетании с ингаляционным колистином [130, 131, 134–138].До сих пор сообщалось о минимальной токсичности ингаляционного колистина, хотя систематические данные отсутствуют. Ингаляционный азтреонам представляется безопасной и эффективной альтернативой ингаляционному тобрамицину при муковисцидозе [139]. Наконец, недавнее исследование показало, что ингаляционный ванкомицин эффективен в предотвращении прогрессирования трахеобронхита, связанного с вентилятором, до пневмонии, связанной с вентилятором [132]. Неуклонный рост лекарственной устойчивости среди респираторных патогенов придает дополнительную актуальность продолжению исследований, призванных лучше определить роль ингаляционных противомикробных препаратов при легочных инфекциях.
5.7 Противогрибковая аэрозольная терапия
Несмотря на недавние достижения в области противогрибковой лекарственной терапии, инвазивные грибковые инфекции (ИФИ) остаются серьезной угрозой для больных раком с ослабленным иммунитетом и реципиентов трансплантации органов или гемопоэза [140,141]. Ответ на терапию цитокинами системного усиления иммунитета, такую как рекомбинантный GM-CSF, IFNγ и переливание донорских гранулоцитов, чреват отсутствием исследований по оценке стоимости и полезности и усугубляется неопределенными данными клинической эффективности [142].Инвазивный аспергиллез представляет собой опасную для жизни инфекцию, часто наблюдаемую в течение первых 3 лет после трансплантации сердце-легкие [143], тогда как у реципиентов аллогенной трансплантации стволовых клеток эта инфекция возникает в период нейтропении перед приживлением, во время острой трансплантации вместо трансплантата. болезнь хозяина (GVHD) и в период позднего риска, который включает лечение хронической GVHD [144]. У больных раком пациенты с острым миелогенным лейкозом особенно восприимчивы к ИФИ, и период риска может быть увеличен у пациентов с рефрактерным или рецидивирующим раком [145].Ингаляционный амфотерицин B был исследован для предотвращения ИФИ у восприимчивых пациентов в периоды высокого риска и для терапии спасения у пациентов с трудно поддающимся лечению инвазивным грибковым заболеванием легких.
У реципиентов трансплантата легкие инфекции Aspergillus разновидностей приводят к колонизации, которая часто предшествует инвазивному заболеванию, проявляющемуся как трахеобронхит или инфекции анастомоза, и / или инвазивное заболевание легких; диссеминация грибков у этих пациентов без нейтропении и без рака встречается редко.Большинство этих грибковых инфекций возникает у реципиентов трансплантатов солидных органов без нейтропении в период раннего отторжения трансплантата и иммуносупрессивной терапии отторжения [143]. Интересно отметить, что колонизация видами Aspergillus через 3 месяца после трансплантации чаще встречается у пациентов с человеческим лейкоцитарным антигеном (HLA) A1; однако у этих пациентов, склонных к поздней грибковой колонизации, риск инвазивного грибкового заболевания существенно не увеличивался [143]. Напротив, недавно сообщалось о нескольких грибковых инфекциях у реципиентов трансплантата сердца с рефрактерным отторжением, получавших сиролимус в сочетании с такролимусом, и пациентов с васкулопатией сердечного аллотрансплантата [146].
Ингаляционный амфотерицин B был первым лекарством, используемым для лечения системного микоза, а более ранние эксперименты на животных с использованием аэрозольного амфотерицина B показали благоприятную эффективность при лечении легочного аспергиллеза [147]. Липидные препараты амфотерицина B, такие как липидный комплекс амфотерицина B (ABLC), также эффективно доставлялись аэрозольным путем. Прединфекционная обработка ABLC в дозе 0,4–1,6 мг / кг за 2 дня до инфекции обеспечила увеличение выживаемости на 63–100% в экспериментах на животных [148].Пиковая концентрация амфотерицина B в бронхоальвеолярном лаваже после однократного приема достигается через 30 минут после ингаляции, и он медленно выводится из легких в течение следующих 24 часов [149].
Устройство доставки лекарственного средства остается критически важным для прогнозирования концентрации лекарственного средства, распыляемого в виде аэрозоля. В исследованиях клинической кинетики распределения 10% вдыхаемого ABLC откладывалось в легких при введении через специализированные системы доставки, такие как распылитель AeroEclipse, управляемый сжатым воздухом со скоростью 7-8 л / мин, и это отложение в легких было в два раза выше по сравнению с достигнутыми уровнями. использование стандартных систем доставки аэрозолей для бронхолитической терапии [150].Состав также важен, поскольку в экспериментах на животных концентрация лекарственного средства в аэрозольной форме ABLC в шесть раз выше по сравнению с дезоксихолатом амфотерицина B [148]. Более того, ингаляционный ABLC хорошо переносился при исследовании реципиентов трансплантата легкого, тогда как обычный дезоксихолат амофотерицина B приводил к вдвое большему количеству побочных эффектов, связанных с лечением [151].
Сообщалось о значительном сокращении случаев инвазивного легочного аспергиллеза у пациентов, получавших ингаляционный амфотерицин B во время и после операции по трансплантации сердца и сердце – легкие [152].Аналогичным образом, липидный препарат амфотерицина B (ABLC) также успешно использовался для профилактики трахеобронхита Aspergillus, анастомозов и инвазивных заболеваний легких у реципиентов сердца и легких [143, 153].
Скудность клинических данных по лечению амфотерицином В в аэрозольной форме у пациентов с установленной грибковой инфекцией легких затрудняет рекомендацию этого вмешательства даже в рефрактерных случаях. Вот два примера таких случаев: пациент без иммуносупрессии с поствирусным трахеобронхитом, вызванным Aspergillus, который не ответил на длительную липосомную терапию амфотерицином B, имел благоприятный ответ на длительное лечение ингаляционным дезоксихолатом амфотерицина B плюс GM-CSF и IFNγ-иммунитет. усиление [154].Во-вторых, у пациента с тяжелой иммуносупрессией и инфекцией легкого Rhizomucor, которая в результате эволюции превратилась в Pseudalescheria boydii , инфекция полностью исчезла с помощью ингаляционного ABLC, которая продолжалась в течение 5 месяцев, и при долгосрочном наблюдении рецидива инфекции не наблюдалось [155]. Эти случаи подчеркивают потенциальную роль ингаляционного амфотерицина B в лечении установленного заболевания; однако на основании текущей клинической информации нельзя дать никаких рекомендаций.
5.8 Противовирусная аэрозольная терапия
Вирусные инфекции дыхательных путей обычно протекают в легкой форме и часто поддаются поддерживающей терапии. Однако у пациентов с ослабленным иммунитетом, больных раком или трансплантацией, эти инфекции могут быть связаны с тяжелыми осложнениями, требующими ранней диагностики и своевременной терапии [137]. Обеспокоенность вызывают парамиксовирусы, такие как респираторно-синцитиальный вирус (RSV) и вирус парагриппа (PIV), вирусы гриппа A и B, аденовирус и недавно признанный метапневмовирус человека (hMPV).Рибавирин, аналог пуринового нуклеозида, использовался для лечения хронической инфекции вируса гепатита С пероральным введением, а также для лечения геморрагической лихорадки и диссеминированного hMPV путем внутривенного введения. Рибавирин в аэрозольной форме был одобрен FDA для лечения инфекций RSV у госпитализированных детей. Обычное непрерывное лечение 60 мг рибавирина / мл в течение 18 часов эффективно с внутривенным иммуноглобулином или без него; однако пациенты чувствуют себя сильно изолированными, что может помешать их уходу [138].Периодически вводимый в виде аэрозоля рибавирин в дозе 20 мг / мл в течение 2 ч 3 раза в день также был эффективен у взрослых пациентов с раком и трансплантацией стволовых клеток с инфекцией RSV [140]. У детей с ослабленным иммунитетом и инфекцией RSV периодические высокие дозы (60 мг) рибавирина / мл в течение 2 часов, вводимые 3 раза в день, хорошо переносились, ассоциировались с клиническим ответом, сравнимым со стандартной непрерывной терапией, и ассоциировались со значительно меньшим загрязнением окружающей среды и воздействием на здоровье: медицинским работникам и с большей доступностью для пациентов [141, 142].
Парагрипп ассоциируется с потенциально серьезными осложнениями у реципиентов трансплантата сердце-легкие, с возможной ролью в остром отторжении аллотрансплантата и облитерирующем поствирусном бронхиолите [143]. Ингаляционный рибавирин в этой популяции ассоциировался с клиническим улучшением, хотя клинический опыт ограничен [144]. У реципиентов трансплантата гемопоэтических стволовых клеток парагриппозная вирусная инфекция является серьезной в присутствии других копатогенов и у пациентов с дыхательной недостаточностью, и лечение рибавирином в форме аэрозоля не было связано с уменьшением продолжительности выделения вируса или смертности, связанной с пневмонией [145].
Вирус гриппа А является основной причиной заболеваемости и смертности, и инфекции часто бывают тяжелыми у пациентов с дефектным адаптивным Т-клеточным ответом. Лекарственная устойчивость к ингибиторам нейраминидазы представляет собой серьезную проблему лечения в условиях плохого ответа на обычные вакцины в популяции высокого риска рака и трансплантата [146]. Аэрозольный рибавирин 60 мг / мл для трех дневных доз продолжительностью 15 мин был эффективен против гриппа A и B у мышей [147]. Недавно было показано, что мегадоза рибавирина (100 мг / мл) эффективна у мышей, инфицированных летальным вирусом гриппа A h4N2.Эта мегадозовая терапия в течение всего 4 дней привела к выживаемости> 90% при назначении в течение 24–48 часов после инфицирования [148]. Необходимы дальнейшие клинические исследования для оценки соответствующей дозы и эффективности рибавирина для лечения лекарственно-устойчивой или лекарственно-резистентной вирулентной вирулентной инфекции гриппа.
Метапневмовирус человека возник как распространенный вирусный патоген дыхательных путей, связанный с субклиническим или легким заболеванием. Иногда было показано, что у пациентов с Т-клеточными иммунными дефектами hMPV вызывает диссеминированное смертельное заболевание [149].У пациентов с трансплантацией стволовых клеток или твердых органов эти инфекции, даже при ограниченном течении легочного заболевания, представляют опасность для жизни и повышают риск поствирусной инвазивной грибковой пневмонии [150]. Внутривенный рибавирин считается лучшим доступным лечением этих серьезных диссеминированных или легочных инфекций hMPV, что отражает противовирусный эффект препарата и возможные лекарственные иммуномодулирующие свойства, которые могут еще больше повысить клиренс вируса и помочь в разрешении инфекции, особенно при ослабленном иммунитете. хост [151].
У пациентов с непереносимостью внутривенного рибавирина из-за гемолитической анемии и других серьезных осложнений с некоторым успехом применялось аэрозольное лечение легочного hMPV [152]. Точно так же при лечении пневмотропного аденовируса человека аэрозольный рибавирин предпочтительнее внутривенного из-за высокой концентрации препарата, достигаемой в альвеолах, по сравнению с внутривенной терапией рибавирином, которая может не приводить к цитотоксическим концентрациям в легочной ткани [153]. Однако это может быть не единственным определяющим фактором клинической эффективности терапии рибавирином, поскольку лекарственное усиление активности Т-хелперных Т-клеток Th2 требует дальнейшей оценки в клинических испытаниях [151].
6. Системы распыления
Критическим фактором для всех ингаляционных терапевтических средств являются характеристики системы доставки. Для всех терапий, обсуждаемых здесь, использовались жидкие аэрозоли, чаще всего генерируемые воздушно-струйными небулайзерами, хотя все чаще используются дополнительные технологии [156]. Воздухоструйный и ультразвуковой небулайзеры генерируют аэрозоль под высоким давлением и вибрацией пьезоэлектрического кристалла соответственно. Эти обычно используемые системы доставки обеспечивают адекватное отложение антимикробных препаратов в легких у амбулаторных пациентов, тогда как доставка лекарств ниже у пациентов в критическом состоянии, получающих вспомогательную вентиляцию легких [157,158].В новых электрических генераторах аэрозолей используется вибрирующая сетка или пластина с множеством отверстий, которые увеличивают отложение лекарства в легких в 2–3 раза и значительно повышают выход лекарства по сравнению с аэрозольными небулайзерами. Это следует учитывать для аэрозольной доставки лекарств у пациентов с пневмонией на ИВЛ [159].
Точно так же ингаляционная терапия цитокинами кажется привлекательной для различных трудно поддающихся лечению микобактериальных инфекций, поражающих легкие, хотя доставка этих агентов к месту инфекции представляет собой сложную задачу.В стандартных небулайзерных системах, таких как Respirgard или Misty-neb, только 5–7% общей введенной дозы достигает легочной ткани [74, 160]. Эту трудность можно уменьшить, используя высокоэффективные воздушно-струйные или ультразвуковые небулайзеры или специализированные системы доставки с использованием генераторов электрического аэрозоля нового поколения для достижения терапевтических концентраций иммуномодулирующих цитокинов в месте легочной инфекции. Для получения дополнительной информации отсылаем читателя к недавним обзорным статьям [161].
7. Резюме
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты. Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков. Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
8. Мнение экспертов
По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями низкой остроты.
Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной P. aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких.
В дальнейшем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для уменьшения вызываемых патогенами нарушений дыхательных путей у субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмония у субъектов с ослабленным иммунитетом, использующих цитокины или синтетические аналоги PAMP, и больше возможностей для использования ингаляционных противомикробных препаратов.
Сноски
Заявление о заинтересованности
Это исследование было частично поддержано грантом CA16672 для поддержки онкологических центров от Национальных институтов здравоохранения.
Библиография
1. Доклад о состоянии здравоохранения в мире 2004 г. — Изменяющаяся история. Женева: Всемирная организация здравоохранения; 2004. [Google Scholar] 3. Джоос Л., Тамм М. Нарушение защиты легочного хозяина у хозяина с ослабленным иммунитетом: химиотерапия рака. Proc Am Thorac Soc. 2005. 2 (5): 445–8. [PubMed] [Google Scholar] 4. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 7. Трэвис С.М., Сингх П.К., валлийский MJ.Противомикробные пептиды и белки во врожденной защите поверхности дыхательных путей. Curr Opin Immunol. 2001. 13 (1): 89–95. [PubMed] [Google Scholar] 8. Flanders SACH, Saint S. Нозокомиальная пневмония: состояние науки. Am J Infect Control. 2006; (34): 84–93. [PubMed] [Google Scholar] 9. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Ратьен Ф. Восстановление жидкости на поверхности дыхательных путей при муковисцидозе.N Engl J Med. 2006. 354 (3): 291–3. [PubMed] [Google Scholar] 11. Тарран Р., Дональдсон С., Буше Р. Обоснование применения гипертонической солевой терапии при муковисцидозе легких. Semin Respir Crit Care Med. 2007. 28 (3): 295–302. [PubMed] [Google Scholar] 12. Eng PA, Morton J, Douglass JA и др. Краткосрочная эффективность распыляемого ультразвуком гипертонического раствора при муковисцидозе. Педиатр Пульмонол. 1996. 21 (2): 77–83. [PubMed] [Google Scholar] 13. Робинсон М., Регнис Дж. А., Бейли Д. Л. и др. Влияние гипертонического раствора, амилорида и кашля на мукоцилиарный клиренс у пациентов с муковисцидозом.Am J Respir Crit Care Med. 1996. 153 (5): 1503–1509. [PubMed] [Google Scholar] 14. Суд Н., Беннетт В.Д., Земан К. и др. Повышение концентрации вдыхаемого физиологического раствора с амилоридом или без него: влияние на мукоцилиарный клиренс у нормальных субъектов. Am J Respir Crit Care Med. 2003. 167 (2): 158–63. [PubMed] [Google Scholar] 15. Wark PA, McDonald V. Распыленный гипертонический раствор для лечения муковисцидоза. Кокрановская база данных Syst Rev.2003; (1): CD001506. [PubMed] [Google Scholar] 16. Дональдсон С.Х., Беннетт В.Д., Земан К.Л. и др. Очистка слизи и функция легких при муковисцидозе с применением гипертонического раствора.N Engl J Med. 2006. 354 (3): 241–50. [PubMed] [Google Scholar] 17. Элкинс М.Р., Робинсон М., Роуз Б.Р. и др. Контролируемое испытание длительного применения ингаляционного гипертонического раствора у пациентов с муковисцидозом. N Engl J Med. 2006. 354 (3): 229–40. [PubMed] [Google Scholar] 18. Керем Э., Бистрицер Т., Ханукоглу А. и др. Дисфункция легочного эпителия натриевых каналов и избыток жидкости в дыхательных путях при псевдогипоальдостеронизме. N Engl J Med. 1999. 341 (3): 156–62. [PubMed] [Google Scholar] 19. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Буше RC. Обезвоживание поверхности дыхательных путей при муковисцидозе: патогенез и терапия. Annu Rev Med. 2007. 58: 157–70. [PubMed] [Google Scholar] 22. Эванс С.М., Уильямс О.В., Тувим М.Дж. и др. Муцин продуцируется clara-клетками проксимальных дыхательных путей мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004. 31 (4): 382–94. [PubMed] [Google Scholar] 23. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Акинби Х.Т., Эпод Р., Бхатт Х. и др. Уничтожение бактерий усиливается экспрессией лизоцима в легких трансгенных мышей. J Immunol. 2000. 165 (10): 5760–6. [PubMed] [Google Scholar] 25. Bals R, Weiner DJ, Moscioni AD, et al. Усиление врожденной защиты хозяина за счет экспрессии антимикробного пептида кателицидина. Заражение иммунной. 1999. 67 (11): 6084–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26.Коул А.М., Ляо Х.И., Стучлик О. и др. Катионные полипептиды необходимы для антибактериальной активности жидкости дыхательных путей человека. J Immunol. 2002. 169 (12): 6985–91. [PubMed] [Google Scholar] 27. Коул AM, Thapa DR, Gabayan V и др. Снижение клиренса Pseudomonas aeruginosa из дыхательных путей мышей с дефицитом лизоцима M. J Leukoc Biol. 2005. 78 (5): 1081–5. [PubMed] [Google Scholar] 28. Moser C, Weiner DJ, Lysenko E, et al. бета-дефенсин 1 способствует развитию врожденного иммунитета легких у мышей. Заражение иммунной. 2002. 70 (6): 3068–72.[Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Эванс С.Е., Хан П.Й., Макканн Ф. и др. Бета-глюканы клеточной стенки Pneumocystis стимулируют генерацию хемокинов альвеолярными эпителиальными клетками через механизмы, зависящие от ядерного фактора, каппаB. Am J Respir Cell Mol Biol. 2005. 32 (6): 490–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 30. Агусти С., Рано А., Ровира М. и др. Воспалительный ответ, связанный с легочными осложнениями у пациентов с иммунодефицитом, не связанным с ВИЧ. Грудная клетка. 2004. 59 (12): 1081–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 31.Бартон Г.М., Меджитов Р. Сигнальные пути толл-подобных рецепторов. Наука. 2003. 300 (5625): 1524–15. [PubMed] [Google Scholar] 32. Болдрик Дж. К., Ализаде А. А., Дин М. и др. Стереотипные и специфические программы экспрессии генов в врожденных иммунных реакциях человека на бактерии. Proc Natl Acad Sci USA. 2002. 99 (2): 972–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 33. Капетанович Р., Кавайон Дж. М.. Ранние события врожденного иммунитета при распознавании микробных патогенов. Экспертное мнение Biol Ther. 2007. 7 (6): 907–18. [PubMed] [Google Scholar] 34.Каваи Т., Акира С. Сигнализация TLR. Смерть клетки отличается. 2006. 13 (5): 816–25. [PubMed] [Google Scholar] 35. Копп Э., Меджитов Р. Распознавание микробной инфекции по Toll-подобным рецепторам. Curr Opin Immunol. 2003. 15 (4): 396–401. [PubMed] [Google Scholar] 36. Чжан Г., Гош С. Активация NF-kappaB, опосредованная Toll-подобным рецептором: филогенетически консервативная парадигма врожденного иммунитета. J Clin Invest. 2001; 107 (1): 13–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Улевич Р.Ю. Терапия, направленная на врожденную иммунную систему.Nat Rev Immunol. 2004. 4 (7): 512–20. [PubMed] [Google Scholar] 38. Аревало И., Туллиано Дж., Киспе А. и др. Роль имиквимода и парентерального антимониата меглумина в начальном лечении кожного лейшманиоза. Clin Infect Dis. 2007. 44 (12): 1549–54. [PubMed] [Google Scholar] 39. Канистанон Д., Хаджар А.М., Пеллетье М.Р. и др. Мутант Francisella по углеводной модификации липида А вызывает защитный иммунитет. PLoS Pathog. 2008; 4 (2): e24. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Лембо А., Пеллетье М., Айер Р. и др.Введение синтетического агониста TLR4 защищает мышей от легочной туляремии. J Immunol. 2008. 180 (11): 7574–81. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Лурманн А., Дейтерс Ю., Скокова Дж. И др. Эффекты in vivo синтетического 2-килодальтонного активирующего макрофаги липопептида Mycoplasma fermentans после легочного применения. Заражение иммунной. 2002. 70 (7): 3785–92. [Бесплатная статья PMC] [PubMed] [Google Scholar] 42. МакХатчисон Дж. Г., Бэкон Б. Р., Гордон С. К. и др. Фаза 1B, рандомизированное двойное слепое исследование с увеличением дозы CPG 10101 у пациентов с хроническим вирусом гепатита С.Гепатология. 2007. 46 (5): 1341–9. [PubMed] [Google Scholar] 43. Raberg L, Sim D, Read AF. Распутывание генетической изменчивости для устойчивости и толерантности к инфекционным заболеваниям у животных. Наука. 2007. 318 (5851): 812–4. [PubMed] [Google Scholar] 44. Уильямс Т.Н., Мванги Т.В., Вамбуа С. и др. Отрицательный эпистаз между защитным действием от малярии альфа + -талассемии и серповидно-клеточной характеристикой. Нат Жене. 2005. 37 (11): 1253–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45. Эванс С.Е., Скотт Б.Л., Клемент К.Г. и др.Стимулированная врожденная резистентность эпителия легких защищает мышей от бактерий и грибков. Am J Respir Cell Mol Biol. 2009 27 марта; [Epub перед печатью] [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Деннис Д.Т., Инглсби Т.В., Хендерсон Д.А. и др. Туляремия как биологическое оружие: управление медициной и общественным здравоохранением. ДЖАМА. 2001. 285 (21): 2763–73. [PubMed] [Google Scholar] 47. Хиллеман MR. Обзор: причины и профилактика в биологической войне и биотерроризме. Вакцина. 2002. 20 (25–26): 3055–67. [PubMed] [Google Scholar] 48.Уэйн Конлан Дж., Шен Х., Куоли Р. и др. Аэрозольная, но не внутрикожная иммунизация живым вакцинным штаммом Francisella tularensis защищает мышей от последующего аэрозольного заражения высоковирулентным штаммом патогена типа А посредством механизма, зависимого от Т-лимфоцитов и гамма-интерферона. Вакцина. 2005. 23 (19): 2477–85. [PubMed] [Google Scholar] 50. Тувим М.Дж., Эванс С.Е., Клемент К.Г. и др. Усиленное воспаление легких защищает от пневмонии гриппа А. PLoS ONE. 2009; 4 (1): e4176.[Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Клемент К.Г., Эванс С.Е., Эванс С.М. и др. Стимуляция врожденного иммунитета легких защищает мышей от летальной пневмококковой пневмонии. Am J Respir Crit Care Med. 2008. 177 (12): 1322–30. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Могхаддам С.Дж., Клемент К.Г., Де ла Гарза М.М. и др. Лизат Haemophilus influenzae индуцирует аспекты фенотипа хронической обструктивной болезни легких. Am J Respir Cell Mol Biol. 2008. 38 (6): 629–38. [Бесплатная статья PMC] [PubMed] [Google Scholar] 53.Brandl K, Plitas G, Mihu CN и др. Устойчивые к ванкомицину энтерококки используют вызванный антибиотиками врожденный иммунный дефицит. Природа. 2008. 455 (7214): 804–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Hoogerwerf JJ, de Vos AF, Bresser P, et al. Воспаление легких, вызванное липотейхоевой кислотой или липополисахаридом у человека. Am J Respir Crit Care Med. 2008. 178 (1): 34–41. [PubMed] [Google Scholar] 55. Реппе К., Черниг Т., Лурманн А. и др. Иммуностимуляция липопептидом-2, активирующим макрофаги, увеличивала выживаемость при пневмонии мышей.Am J Respir Cell Mol Biol. 2009. 40 (4): 474–81. [PubMed] [Google Scholar] 56. Багчи А., Херруп Э.А., Уоррен Х.С. и др. MyD88-зависимый и MyD88-независимый пути синергизма, прайминга и толерантности между агонистами TLR. J Immunol. 2007. 178 (2): 1164–71. [PubMed] [Google Scholar] 57. Trinchieri G, Sher A. Сотрудничество сигналов Toll-подобных рецепторов во врожденной иммунной защите. Nat Rev Immunol. 2007. 7 (3): 179–90. [PubMed] [Google Scholar] 58. Меджитов Р. Распознавание микроорганизмов и активация иммунного ответа.Природа. 2007. 449 (7164): 819–26. [PubMed] [Google Scholar] 59. Foster SL, Hargreaves DC, Medzhitov R. Ген-специфический контроль воспаления с помощью TLR-индуцированных модификаций хроматина. Природа. 2007. 447 (7147): 972–8. [PubMed] [Google Scholar] 60. Тазава Р., Хамано Э., Араи Т. и др. Гранулоцитарно-макрофагальный колониестимулирующий фактор и легочный иммунитет при легочном альвеолярном протеинозе. Am J Respir Crit Care Med. 2005. 171 (10): 1142–9. [PubMed] [Google Scholar] 61. Андерсон П.М., Маркович С.Н., Слоан Дж. А. и др. Аэрозольный гранулоцитарный макрофаг-колониестимулирующий фактор: низкая токсичность, легочная биологическая терапия у пациентов с метастазами в легких.Clin Cancer Res. 1999. 5 (9): 2316–23. [PubMed] [Google Scholar] 62. Trapnell BC, Whitsett JA, Nakata K. Легочный альвеолярный протеиноз. N Engl J Med. 2003. 349 (26): 2527–39. [PubMed] [Google Scholar] 63. Киннула В., Маттсон К., Кантелл К. Фармакокинетика и токсичность вдыхаемого человеческого интерферона-альфа у пациентов с раком легких. J Interferon Res. 1989. 9 (4): 419–23. [PubMed] [Google Scholar] 64. Маасилта П., Халме М., Маттсон К. и др. Фармакокинетика ингаляционного рекомбинантного и природного альфа-интерферона. Ланцет.1991; 337 (8737): 371. [PubMed] [Google Scholar] 65. Киннула В., Кантелл К., Маттсон К. Эффект вдыхаемого природного интерферона-альфа на диффузную бронхоальвеолярную карциному. Eur J Cancer. 1990; 26 (6): 740–1. [PubMed] [Google Scholar] 66. Маасилта П., Холсти Л. Р., Халме М. и др. Природный альфа-интерферон в сочетании с гиперфракционированной лучевой терапией при лечении немелкоклеточного рака легкого. Int J Radiat Oncol Biol Phys. 1992. 23 (4): 863–8. [PubMed] [Google Scholar] 67. Giosue S, Casarini M, Alemanno L и др.Эффекты аэрозольного интерферона-альфа у больных туберкулезом легких. Am J Respir Crit Care Med. 1998. 158 (4): 1156–62. [PubMed] [Google Scholar] 68. Giosue S, Casarini M, Ameglio F и др. Аэрозольное лечение интерфероном-альфа у пациентов с туберкулезом легких с множественной лекарственной устойчивостью. Eur Cytokine Netw. 2000. 11 (1): 99–104. [PubMed] [Google Scholar] 69. Мартин Р. Дж., Богуневич М., Хенсон Дж. Э. и др. Воздействие вдыхаемого гамма-интерферона на нормальные дыхательные пути человека. Am Rev Respir Dis. 1993; 148 (6 Pt 1): 1677–82.[PubMed] [Google Scholar] 70. Богуневич М., Мартин Р.Дж., Мартин Д. и др. Эффекты распыленного рекомбинантного гамма-интерферона на астматические дыхательные пути. J Allergy Clin Immunol. 1995. 95 (1 Pt 1): 133–5. [PubMed] [Google Scholar] 71. Кондо Р., Раджу Б., Канова А. и др. Рекомбинантный гамма-интерферон стимулирует передачу сигнала и экспрессию генов в альвеолярных макрофагах in vitro и у больных туберкулезом. Заражение иммунной. 2003. 71 (4): 2058–64. [Бесплатная статья PMC] [PubMed] [Google Scholar] 72. Раджу Б., Хосино Ю., Кувабара К. и др.Аэрозольный гамма-интерферон (IFN-гамма) индуцирует экспрессию генов, кодирующих IFN-гамма-индуцибельный белок 10 килодальтон, но не индуцибельную синтазу оксида азота в легких во время туберкулеза. Заражение иммунной. 2004. 72 (3): 1275–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Кондо R, Rom WN, Schluger NW. Лечение туберкулеза легких с множественной лекарственной устойчивостью с помощью аэрозольного гамма-интерферона. Ланцет. 1997. 349 (9064): 1513–5. [PubMed] [Google Scholar] 74. Condos R, Hull FP, Schluger NW и др.Региональное отложение аэрозольного гамма-интерферона при туберкулезе легких. Грудь. 2004. 125 (6): 2146–55. [PubMed] [Google Scholar] 75. Moss RB, Mayer-Hamblett N, Wagener J, et al. Рандомизированное двойное слепое плацебо-контролируемое исследование с увеличением дозы аэрозольного гамма-1b интерферона у пациентов с кистозным фиброзом легких легкой и средней степени тяжести. Педиатр Пульмонол. 2005. 39 (3): 209–18. [PubMed] [Google Scholar] 76. Накос Г., Маламу-Мици В.Д., Лачана А. и др. Иммунопаралич у больных с тяжелой травмой и действие ингаляционного гамма-интерферона.Crit Care Med. 2002. 30 (7): 1488–94. [PubMed] [Google Scholar] 77. Вирголини I, Куртаран А., Леймер М. и др. Ингаляционная сцинтиграфия с меченным йодом-123 интерфероном гамма-1b: исследование легочного отложения и повышения дозы у здоровых добровольцев. J Nucl Med. 1997. 38 (9): 1475–81. [PubMed] [Google Scholar] 78. Рао Р.Д., Андерсон П.М., Арндт К.А. и др. Терапия аэрозольным гранулоцитарным макрофагальным колониестимулирующим фактором (GM-CSF) при метастатическом раке. Am J Clin Oncol. 2003. 26 (5): 493–8. [PubMed] [Google Scholar] 79.Нивен Р.В., Уиткомб К.Л., Шенер Л. и др. Легочная абсорбция аэрозольного и интратрахеально инстиллированного rhG-CSF и моноПЕГилированного rhG-CSF. Pharm Res. 1995. 12 (9): 1343–9. [PubMed] [Google Scholar] 80. Мачида М., Хаяси М., Авазу С. Абсорбция в легких рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора (rhG-CSF) после интратрахеального введения крысам. Биол Фарм Булл. 1996. 19 (2): 259–62. [PubMed] [Google Scholar] 81. Gatmaitan BG, Carruthers MM, Lerner AM. Гентамицин в лечении первичных грамотрицательных пневмоний.Am J Med Sci. 1970. 260 (2): 90–4. [PubMed] [Google Scholar] 83. Klastersky J, Geuning C, Mouawad E, et al. Эндотрахеальный гентамицин при бронхиальных инфекциях у пациентов с трахеостомией. Грудь. 1972: 61 (2): 117–20. [PubMed] [Google Scholar] 85. Odio W, Van Laer E, Klastersky J. Концентрации гентамицина в бронхиальном секрете после внутримышечного и эндотрахеального введения. J Clin Pharmacol. 1975. 15 (7): 518–24. [PubMed] [Google Scholar] 86. Панидис Д., Маркантонис С.Л., Бутзука Э. и др. Проникновение гентамицина в жидкость выстилки альвеол у пациентов в критическом состоянии с вентилятор-ассоциированной пневмонией.Грудь. 2005. 128 (2): 545–52. [PubMed] [Google Scholar] 87. Каркас А.Дж., Гарсия-Сатуе Д.Л., Сапатер П. и др. Проникновение тобрамицина в эпителиальную выстилочную жидкость пациентов с пневмонией. Clin Pharmacol Ther. 1999. 65 (3): 245–50. [PubMed] [Google Scholar] 88. Valcke YJ, Vogelaers DP, Colardyn FA и др. Проникновение нетилмицина в нижние дыхательные пути после приема один раз в сутки. Грудь. 1992. 101 (4): 1028–32. [PubMed] [Google Scholar] 89. Брауде А.С., Хорнштейн А., Кляйн М. и др. Распределение тобрамицина в легких.Am Rev Respir Dis. 1983; 127 (5): 563–5. [PubMed] [Google Scholar] 90. Kuhn RJ. Фармацевтические соображения при аэрозольной доставке лекарств. Фармакотерапия. 2002; 22 (3 Pt 2): 80S – 5S. [PubMed] [Google Scholar] 91. Goldstein I, Wallet F, Nicolas-Robin A, et al. Отложение в легких и эффективность распыленного амикацина при пневмонии, вызванной Escherichia coli, у вентилируемых поросят. Am J Respir Crit Care Med. 2002. 166 (10): 1375–81. [PubMed] [Google Scholar] 92. Гольдштейн I, Кошелек F, Роберт Дж. И др. Концентрация распыленного амикацина в легочной ткани во время искусственной вентиляции легких у поросят со здоровыми легкими.Am J Respir Crit Care Med. 2002. 165 (2): 171–5. [PubMed] [Google Scholar] 93. Klastersky J, Carpentier-Meunier F, Kahan-Coppens L, et al. Антибиотики при грамотрицательной бронхопневмонии назначаются эндотрахеально. Грудь. 1979; 75 (5): 586–91. [PubMed] [Google Scholar] 94. Флюм П, Клепсер МЭ. Обоснование использования антибиотиков в аэрозольной форме. Фармакотерапия. 2002; 22 (3 Pt 2): 71S – 9S. [PubMed] [Google Scholar] 95. Мур RD, Литман PS, Смит CR. Клинический ответ на терапию аминогликозидами: важность отношения максимальной концентрации к минимальной ингибирующей концентрации.J Infect Dis. 1987. 155 (1): 93–9. [PubMed] [Google Scholar] 96. Мур RD, Смит CR, Литман PS. Связь уровней аминогликозидов в плазме со смертностью у пациентов с грамотрицательной бактериемией. J Infect Dis. 1984. 149 (3): 443–8. [PubMed] [Google Scholar] 97. Schentag JJ. Корреляция фармакокинетических параметров с эффективностью антибиотиков: взаимосвязь между концентрациями в сыворотке, значениями МИК и бактериальной эрадикацией у пациентов с грамотрицательной пневмонией. Scand J Infect Dis Suppl. 1990; 74: 218–34.[PubMed] [Google Scholar] 98. Дезил-Эванс Л.М., Мерфи Дж. Э., Джоб М.Л. Корреляция фармакокинетических показателей с терапевтическим исходом у пациентов, получающих аминогликозиды. Clin Pharm. 1986. 5 (4): 319–24. [PubMed] [Google Scholar] 99. Коллинз Т., Гердинг Д.Н. Аминогликозиды в сравнении с бета-лактамами при грамотрицательной пневмонии. Semin Respir Infect. 1991. 6 (3): 136–46. [PubMed] [Google Scholar] 100. Бернс Дж. Л., Ван Дальфсен Дж. М., Шавар Р. М. и др. Влияние хронического периодического введения ингаляционного тобрамицина на респираторную микробную флору у пациентов с муковисцидозом.J Infect Dis. 1999. 179 (5): 1190–6. [PubMed] [Google Scholar] 101. Valcke Y, Pauwels R, Van der Straeten M. Проникновение аминогликозидов в жидкость выстилки альвеол крыс. Эффект воспаления дыхательных путей. Am Rev Respir Dis. 1990. 142 (5): 1099–103. [PubMed] [Google Scholar] 102. Меерс П., Невилл М., Малинин В. и др. Проникновение биопленки, запускаемое высвобождение и активность ингаляционного липосомального амикацина in vivo при хронических инфекциях легких, вызванных Pseudomonas aeruginosa. J Antimicrob Chemother. 2008. 61 (4): 859–68.[PubMed] [Google Scholar] 103. Дэвис К.К., Као П.Н., Якобс С.С. и др. Аэрозольный амикацин для лечения легочных инфекций Mycobacterium avium: серия наблюдательных случаев. BMC Pulm Med. 2007; 7: 2. [Бесплатная статья PMC] [PubMed] [Google Scholar] 104. Макколл С.Ю., Спруилл В.Дж., Уэйд В.Е. Применение тобрамицина в аэрозольной форме при лечении резистентного псевдомонадного пневмонита. Ther Drug Monit. 1989. 11 (6): 692–5. [PubMed] [Google Scholar] 105. Допфер Р., Брэнд П, Маллингер Б. и др. Ингаляция тобрамицина у больных муковисцидозом: сравнение двух методов.J. Physiol Pharmacol. 2007; 58 (Дополнение 5) (Pt 1): 141–54. [PubMed] [Google Scholar] 106. Ленуар Г., Антипкин Ю.Г., Миано А. и др. Эффективность, безопасность и местная фармакокинетика высококонцентрированного распыленного тобрамицина у пациентов с муковисцидозом, колонизированными синегнойной палочкой. Педиатрические препараты. 2007; 9 (Дополнение 1): 11–20. [PubMed] [Google Scholar] 107. Рэмси Б.В., Доркин Х.Л., Айзенберг Д.Д. и др. Эффективность аэрозольного тобрамицина у пациентов с муковисцидозом. N Engl J Med. 1993. 328 (24): 1740–6. [PubMed] [Google Scholar] 109.Кантон Р., Кобос Н., де Грасиа Дж. И др. Антимикробная терапия легочной патогенной колонизации и инфекции Pseudomonas aeruginosa у пациентов с муковисцидозом. Clin Microbiol Infect. 2005. 11 (9): 690–703. [PubMed] [Google Scholar] 110. Sexauer WP, Fiel SB. Аэрозольные антибиотики при муковисцидозе. Semin Respir Crit Care Med. 2003. 24 (6): 717–26. [PubMed] [Google Scholar] 111. Кун П., Ландау Л.И., Фелан П.Д. Распыленный гентамицин у детей и подростков с муковисцидозом. Aust Paediatr J.1984. 20 (1): 43–5. [PubMed] [Google Scholar] 112. Уолл М.А., Терри А.Б., Айзенберг Дж. И др. Ингаляционные антибиотики при муковисцидозе. Ланцет. 1983; 1 (8337): 1325. [PubMed] [Google Scholar] 113. Стейнкамп Г., Туммлер Б., Гаппа М. и др. Длительная аэрозольная терапия тобрамицином при муковисцидозе. Педиатр Пульмонол. 1989. 6 (2): 91–8. [PubMed] [Google Scholar] 114. Смит А.Л., Рэмси Б.В., Хеджес Д.Л. и др. Безопасность применения аэрозольного тобрамицина в течение 3 месяцев пациентам с муковисцидозом. Педиатр Пульмонол. 1989. 7 (4): 265–71.[PubMed] [Google Scholar] 115. Рэмси Б.В., Пепе М.С., Куан Дж. М. и др. Периодическое введение ингаляционного тобрамицина пациентам с муковисцидозом. Группа по изучению муковисцидоза, вдыхаемого тобрамицином. N Engl J Med. 1999. 340 (1): 23–30. [PubMed] [Google Scholar] 116. Мох РБ. Долгосрочные преимущества ингаляционного тобрамицина у подростков с муковисцидозом. Грудь. 2002. 121 (1): 55–63. [PubMed] [Google Scholar] 117. Стивенс Д., Гэри Н., Айлз А. и др. Эффективность ингаляционного тобрамицина при лечении обострений легких у детей с муковисцидозом.Pediatr Infect Dis. 1983; 2 (3): 209–11. [PubMed] [Google Scholar] 118. Schaad UB, Wedgwood-Krucko J, Suter S и др. Эффективность ингаляционного амикацина в качестве дополнения к внутривенной комбинированной терапии (цефтазидим и амикацин) при муковисцидозе. J Pediatr. 1987. 111 (4): 599–605. [PubMed] [Google Scholar] 119. Билтон Д., Хениг Н., Моррисси Б. и др. Добавление ингаляционного тобрамицина к ципрофлоксацину при обострении инфекции Pseudomonas aeruginosa при бронхоэктазах у взрослых. Грудь. 2006. 130 (5): 1503–10. [PubMed] [Google Scholar] 121.Рубин Б.К. Аэрозольные антибиотики для лечения бронхоэктазов без кистозного фиброза. J Aerosol Med Pulm Drug Deliv. 2008. 21 (1): 71–6. [PubMed] [Google Scholar] 122. Drobnic ME, Sune P, Montoro JB и др. Ингаляция тобрамицина пациентам с не кистозным фиброзом, бронхоэктазами и хронической бронхиальной инфекцией, вызванной синегнойной палочкой. Энн Фармакотер. 2005. 39 (1): 39–44. [PubMed] [Google Scholar] 123. Баркер А.Ф., Коуч Л., Фил С.Б. и др. Раствор тобрамицина для ингаляций снижает плотность мокроты синегнойной палочки при бронхоэктазах.Am J Respir Crit Care Med. 2000. 162 (2 Pt 1): 481–5. [PubMed] [Google Scholar] 124. Шейнберг П., Шор Э. Пилотное исследование безопасности и эффективности раствора тобрамицина для ингаляции у пациентов с тяжелыми бронхоэктазами. Грудь. 2005. 127 (4): 1420–146. [PubMed] [Google Scholar] 125. Додек П., Кинан С., Кук Д. и др. Основанное на фактических данных клиническое руководство по профилактике вентилятор-ассоциированной пневмонии. Ann Intern Med. 2004. 141 (4): 305–13. [PubMed] [Google Scholar] 126. Falagas ME, Siempos II, Bliziotis IA, et al.Введение антибиотиков через дыхательные пути для профилактики пневмонии, приобретенной в ОИТ: метаанализ сравнительных исследований. Crit Care. 2006; 10 (4): R123. [Бесплатная статья PMC] [PubMed] [Google Scholar] 127. Ратгебер Дж., Зильманн С., Панцер С. и др. Профилактика пневмонии путем эндотрахеальной микронебулизации тобрамицина. Анастезиол Интенсивмед Нефалмед Шмерцтер. 1993. 28 (1): 23–9. [PubMed] [Google Scholar] 128. Klastersky J, Huysmans E, Weerts D, et al. Эндотрахеально вводимый гентамицин для профилактики инфекций дыхательных путей у пациентов с трахеостомией: двойное слепое исследование.Грудь. 1974. 65 (6): 650–4. [PubMed] [Google Scholar] 129. Таблан О.К., Андерсон Л.Дж., Бессер Р. и др. Руководство по профилактике пневмонии, связанной с оказанием медицинской помощи, 2003 г .: рекомендации CDC и Консультативного комитета по практике инфекционного контроля в здравоохранении. MMWR Recomm Rep. 2004; 53 (RR-3): 1–36. [PubMed] [Google Scholar] 130. Falagas ME, Agrafiotis M, Athanassa Z и др. Введение антибиотиков через дыхательные пути в качестве монотерапии пневмонии. Эксперт Rev Anti Infect Ther. 2008. 6 (4): 447–52. [PubMed] [Google Scholar] 131.Ghannam DE, Rodriguez GH, Raad II и др. Ингаляционные аминогликозиды у онкологических больных с связанной с вентилятором грамотрицательной бактериальной пневмонией: безопасность и осуществимость в эпоху роста лекарственной устойчивости. Eur J Clin Microbiol Infect Dis. 2009. 28 (3): 253–9. [PubMed] [Google Scholar] 132. Палмер Л. Б., Смолдон Г. К., Чен Дж. Дж. И др. Аэрозольные антибиотики и трахеобронхит, связанный с вентилятором, в отделении интенсивной терапии. Crit Care Med. 2008; 36 (7): 2008–13. [PubMed] [Google Scholar] 133. Морозини М.И., Гарсия-Кастильо М., Лоза Э. и др.Контрольные точки для прогнозирования чувствительности Pseudomonas aeruginosa к вдыхаемому тобрамицину у пациентов с муковисцидозом: использование тест-полосок Etest с высоким диапазоном значений. J Clin Microbiol. 2005. 43 (9): 4480–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 134. Линден П.К., Патерсон Д.Л. Парентеральный и ингаляционный колистин для лечения вентилятор-ассоциированной пневмонии. Clin Infect Dis. 2006; 43 (Дополнение 2): S89 – S4. [PubMed] [Google Scholar] 135. Михалопулос А., Фотакис Д., Вирцили С. и др. Колистин в аэрозольной форме в качестве дополнительного лечения респираторно-ассоциированной пневмонии, вызванной грамотрицательными бактериями с множественной лекарственной устойчивостью: проспективное исследование.Respir Med. 2008. 102 (3): 407–12. [PubMed] [Google Scholar] 136. Kwa AL, Loh C, Low JG и др. Распыленный колистин в лечении пневмонии, вызванной множественной лекарственной устойчивостью Acinetobacter baumannii и Pseudomonas aeruginosa. Clin Infect Dis. 2005. 41 (5): 754–7. [PubMed] [Google Scholar] 137. Берлана Д., Ллоп Дж. М., Форт Е. и др. Использование колистина для лечения грамотрицательных инфекций с множественной лекарственной устойчивостью. Am J Health Syst Pharm. 2005. 62 (1): 39–47. [PubMed] [Google Scholar] 138. Hamer DH. Лечение внутрибольничной пневмонии и трахеобронхита, вызванных синегнойной палочкой с множественной лекарственной устойчивостью, колистином в аэрозольной форме.Am J Respir Crit Care Med. 2000. 162 (1): 328–30. [PubMed] [Google Scholar] 139. Маккой К.С., Квиттнер А.Л., Оерманн С.М. и др. Азтреонам лизин вдыхается при хронической болезни дыхательных путей Pseudomonas aeruginosa при муковисцидозе. Am J Respir Crit Care Med. 2008. 178 (9): 921–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 140. Сафдар А. Стратегии усиления иммунной функции у реципиентов гемопоэтической трансплантации, у которых есть грибковые инфекции. Пересадка костного мозга. 2006. 38 (5): 327–37. [PubMed] [Google Scholar] 141. Сафдар А.Трудности с грибковыми инфекциями у пациентов с острым миелогенным лейкозом: стратегии повышения иммунитета. Онколог. 2007; 12 (Дополнение 2): 2–6. [PubMed] [Google Scholar] 142. Safdar ARG, Lichtiger B, Dickey BF и др. Повышение иммунитета рекомбинантным интерфероном гамма 1b у 20 пациентов с гематологическими злокачественными новообразованиями и системными оппортунистическими инфекциями, получавших переливания донорских гранулоцитов. Рак. 2006. 106 (12): 2664–71. [PubMed] [Google Scholar] 143. Монтойя Дж. Г., Чапарро С. В., Селис Д. и др. Инвазивный аспергиллез на фоне трансплантации сердца.Clin Infect Dis. 2003; 37 (Приложение 3): S281–92. [PubMed] [Google Scholar] 144. Гарсия-Видаль CUA, Кирби К.А., Марр К.А. Эпидемиология инвазивных инфекций плесени у реципиентов аллогенных стволовых клеток: биологические факторы риска инфекции в зависимости от времени после трансплантации. Clin Infect Dis. 2008. 47 (8): 1041–50. [Бесплатная статья PMC] [PubMed] [Google Scholar] 145. Маттиуцци Г.Н., Кантарджиан Х., Фадерл С. и др. Липидный комплекс амфотерицина B как профилактика инвазивных грибковых инфекций у пациентов с острым миелогенным лейкозом и миелодиспластическим синдромом, проходящих индукционную химиотерапию.Рак. 2004. 100 (3): 581–9. [PubMed] [Google Scholar] 146. Сингх Н., Лимай А.П., Форрест Г. и др. Поздний инвазивный аспергиллез у реципиентов трансплантата в современную эпоху. Med Mycol. 2006. 44 (5): 445–9. [PubMed] [Google Scholar] 147. Schmitt HJ, Bernard EM, Hauser M, et al. Аэрозольный амфотерицин B эффективен для профилактики и лечения крысиной модели легочного аспергиллеза. Антимикробные агенты Chemother. 1988. 32 (11): 1676–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 148. Cicogna CE, White MH, Bernard EM и др.Эффективность профилактического аэрозольного липидного комплекса амфотерицина B на модели легочного аспергиллеза на крысах. Антимикробные агенты Chemother. 1997. 41 (2): 259–61. [Бесплатная статья PMC] [PubMed] [Google Scholar] 149. Коидзуми Т., Кубо К., Канеки Т. и др. Фармакокинетическая оценка амфотерицина B в легочной ткани: распределение легочной лимфы после внутривенной инъекции и распределение воздушного пространства после аэрозолизации и ингаляции амфотерицина B. Противомикробные агенты Chemother. 1998. 42 (7): 1597–600. [Бесплатная статья PMC] [PubMed] [Google Scholar] 150.Коркоран Т.Е., Венкатараманан Р., Михельц К.М. и др. Аэрозольное отложение липидного комплекса амфотерицин-B (Abelcet) у реципиентов трансплантата легких. Am J Transplant. 2006. 6 (11): 2765–73. [PubMed] [Google Scholar] 151. Дрю Р.Х., Доддс Эшли Э., Бенджамин Д.К., мл. И др. Сравнительная безопасность липидного комплекса амфотерицина B и дезоксихолата амфотерицина B в качестве противогрибковой профилактики в виде аэрозоля у реципиентов трансплантата легких. Трансплантация. 2004. 77 (2): 232–7. [PubMed] [Google Scholar] 152. Монтойя Дж. Г., Хиральдо Л. Ф., Эфрон Б. и др.Инфекционные осложнения у 620 последовательных пациентов после трансплантации сердца в медицинском центре Стэнфордского университета. Clin Infect Dis. 2001. 33 (5): 629–40. [PubMed] [Google Scholar] 153. Палмер С.М., Дрю Р.Х., Уайтхаус Дж. Д. и др. Безопасность липидного комплекса амфотерицина B в аэрозольной форме у реципиентов трансплантата легких. Трансплантация. 2001. 72 (3): 545–8. [PubMed] [Google Scholar] 154. Ботинки RJ, Патерсон Д.Л., Олворт А.М. и др. Успешное лечение постгриппозного псевдомембранозного некротизирующего аспергиллеза бронхов липосомальным амфотерицином, ингаляционным амфотерицином B, гамма-интерфероном и GM-CSF.Грудная клетка. 1999. 54 (11): 1047–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 155. Сафдар А., О’Брайен С., Кури И.Ф. Эффективность и возможность применения липидной комплексной терапии амфотерицина В в аэрозольной форме при легочном зигомикозе с прорывом каспофунгина. Пересадка костного мозга. 2004. 34 (5): 467–8. [PubMed] [Google Scholar] 156. Дханд Р., Гунтур В.П. Как лучше всего доставлять аэрозольные препараты пациентам, находящимся на ИВЛ. Clin Chest Med. 2008. 29 (2): 277–96. vi. [PubMed] [Google Scholar] 157. Макинтайр Н.Р., Сильвер Р.М., Миллер К.В. и др.Доставка аэрозоля интубированным пациентам на ИВЛ. Crit Care Med. 1985. 13 (2): 81–4. [PubMed] [Google Scholar] 158. Заявление о консенсусе по аэрозолям-1991. Американская ассоциация респираторной помощи. Respir Care. 1991. 36 (9): 916–21. [PubMed] [Google Scholar] 159. Дханд Р., Сохал Х. Система доставки лекарств в легкие для ингаляционной терапии у пациентов с механической вентиляцией легких. Эксперт Rev Med Devices. 2008; 5 (1): 9–18. [PubMed] [Google Scholar] 160. Blanchard JDCD и др. Отложение в легких интерферона гамма-1b после ингаляции через систему AERx vs.Небулайзер Respirgard II ™ . Am J Respir Crit Care Med. 2003; 167: A373. [Аннотация встречи] [Google Scholar] 161. Уоттс А.Б., МакКонвилл Дж. Т., Уильямс РО. Современные методы лечения и технологические достижения в области доставки лекарственных средств в виде водных аэрозолей. Препарат Дев Инд Фарм. 2008. 34 (9): 913–22. [PubMed] [Google Scholar]Ингаляционные терапевтические средства для профилактики и лечения пневмонии
Expert Opin Drug Saf. Авторская рукопись; доступно в PMC 2015 7 августа 2015 г.
Опубликован в окончательной редакции как:
PMCID: PMC4527977
NIHMSID: NIHMS710030
M.Онкологический центр Д. Андерсона, Хьюстон, Техас, США
† Автор для переписки: доцент медицины Техасского университета, Департамент инфекционных заболеваний, Онкологический центр доктора медицины Андерсона, Инфекционный контроль и здоровье сотрудников, 402, 1515 Holcombe Boulevard , Техас 77030, Хьюстон, США, тел .: +1 713 792 0825; Факс: +1713745 6839; gro.nosrednadm@radfasa См. другие статьи в PMC, в которых цитируется опубликованная статья.Abstract
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты.Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков. По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями. Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной Pseudomonas aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких.Цитокиновая ингаляционная терапия также изучалась при лечении неопластических и инфекционных заболеваний. Выбор легочных систем доставки лекарств остается критическим, поскольку воздушно-струйный и ультразвуковой небулайзер могут обеспечить субоптимальную концентрацию лекарственного средства при неправильном использовании. В будущем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для снижения патогенной нагрузки в дыхательных путях субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмонии у субъектов с ослабленным иммунитетом с использованием цитокинов. или синтетические аналоги молекулярной структуры, ассоциированные с патогенами, и больше возможностей для использования ингаляционных противомикробных препаратов.Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
Ключевые слова: амикацин, противогрибковый, противовирусный, аспергиллез, рак, колистин, цитокин, ингаляционный тобрамицин, врожденный иммунитет, пневмония, псевдомонады, трансплантация, ванкомицин, вентилятор-ассоциированная пневмония, зигомикоз
1.0002 Введение и людей с ослабленным иммунитетом пневмония остается ведущей причиной преждевременной смерти в мире [1–3]. Восприимчивость легких к инфекции возникает из-за архитектурных требований газообмена и частого вдыхания инфекционных агентов.Для обеспечения вентиляции человек постоянно подвергает 100 м
2 площади поверхности легких воздействию внешней среды. Поскольку каждую минуту вентилируется 5–10 л окружающего воздуха, частицы, капли и болезнетворные микроорганизмы также уносятся. Кроме того, в то время как даже здоровые нормальные добровольцы демонстрируют ночную микроабсорбцию орогастрального содержимого, пациенты с неврологическими, анатомическими или ятрогенными препятствиями для защиты дыхательных путей (например, эндотрахеальные или назогастральные трубки) особенно восприимчивы к аспирации инфицированного материала в обширную поверхность раздела нижних отделов. дыхательные пути.В отличие от кожных поверхностей, обернутых непроницаемой кожей, желудка с его кислым просветом или нижних отделов желудочно-кишечного тракта с толстым слоем прилипшей слизи, обширный интерфейс легких с окружающей средой защищен только минимальной защитой барьера. Легочный барьер ограничен необходимостью беспрепятственной газовой диффузии, поэтому эта нежная ткань тонка капилляров. Тем не менее, несмотря на эту структурную уязвимость, легкие успешно защищаются от большинства инфекционных проблем с помощью различных механизмов [4–9].Большинство вдыхаемых или аспирированных патогенов не достигают периферических дыхательных путей из-за захвата в подвижном слое слизистого геля, выстилающего проксимальные проводящие дыхательные пути, с последующим изгнанием через систему мукоцилиарного эскалатора [4]. Постоянное присутствие антимикробных пептидов и антител в жидкости, выстилающей дыхательные пути, ограничивает рост патогенов, которые успешно проникают в небольшие дыхательные пути. Альвеолярные макрофаги поглощают организмы, которые достигают самых отдаленных воздушных пространств [6,7]. Когда базовые защитные механизмы превышены, эпителий легких реагирует увеличением своих прямых противомикробных свойств (см. Раздел 3) и сигнализирует о привлечении лейкоцитов из кровообращения.
Хотя доступность и большая поверхность легких способствуют их восприимчивости к инфекции, эти особенности также предоставляют уникальную возможность для местной терапии в виде респираторных аэрозолей, как показано ниже. Во-первых, недавно были разработаны стратегии увеличения мукоцилиарного клиренса с использованием аэрозолей гипертонического солевого раствора, которые могут снизить нагрузку патогенов в легких. Во-вторых, недавний прогресс в понимании врожденного иммунитета показал, что резистентность респираторного эпителия к патогенам может быть значительно стимулирована, и применение методов лечения, основанных на этом понимании, может снизить восприимчивость к инфекции у уязвимых групп пациентов.В-третьих, перенаправление отклоненного адаптивного иммунитета на повышение устойчивости к специфическим патогенам за счет аэрозольной доставки цитокинов было подтверждено небольшими исследованиями на людях. В-четвертых, антибиотики могут доставляться респираторным путем, максимизируя концентрацию лекарств в области инфекции, где необходимо уничтожение микробов, и сводя к минимуму системные концентрации лекарств, которые могут приводить к нежелательным побочным эффектам. Теоретическая основа и практический статус каждого из этих методов ингаляционной терапии рассматриваются в следующих разделах.
2. Аэрозольный гипертонический солевой раствор для увеличения мукоцилиарного клиренса легких
Основным стимулом к увеличению выведения слизи из легких стало лечение муковисцидоза (МВ). Традиционно постуральный дренаж, перкуссия и другие физические методы сочетаются с очищением от кашля для мобилизации слизи и мусора из дыхательных путей. Совсем недавно для увеличения мукоцилиарного клиренса были введены эффективные аэрозольные методы лечения. Первичным дефектом при МВ является отсутствие апикального эпителиального хлоридного канала, что приводит к уменьшению объема жидкости на поверхности дыхательных путей [10,11].Это предотвращает эффективное движение ресничек и вызывает обезвоживание слизи, что в совокупности ухудшает мукоцилиарный клиренс и повреждает дыхательные пути. Кроме того, эти изменения приводят к заселению обычно стерильных дыхательных путей бактериями и грибками, вызывая дальнейшее воспаление и повреждение дыхательных путей. По мере углубления понимания этих основных механизмов были введены методы лечения для увеличения объема жидкости на поверхности дыхательных путей (). К ним относятся нуклеотиды, амилорид и гипертонический солевой раствор (HSS), но среди них самые убедительные доказательства поддерживают аэрозольный HSS.
Эпителий дыхательных путей с жидкостью на поверхностиПроводящие дыхательные пути выстланы примерно равным количеством мерцательных и секреторных эпителиальных клеток. Секреторные клетки содержат гранулы, которые включают пептиды и муцины (зеленые), хотя внутриклеточные муцины могут быть обнаружены только в небольших дистальных отделах дыхательных путей с помощью чувствительных иммуногистохимических методов или во время воспалительной метаплазии, когда их продукция увеличивается [15,19]. Жидкость на поверхности дыхательных путей состоит из перицилиарного слоя толщиной 7 мкм (синий) и покрывающего его слоя слизистого геля (зеленый), толщина которого варьируется от <1 мкм в дистальных дыхательных путях до> 50 мкм в проксимальных дыхательных путях человека.Реснички направленно бьют, продвигая слой слизистого геля к головке гортани. Гликопротеины муцина MUC5AC и MUC5B являются основными компонентами слоя слизистого геля и высвобождаются экзоцитарно как из подлежащего поверхностного эпителия (показано), так и из подслизистых желез (не показано). Хотя слой слизистого геля важен для очистки от вдыхаемых патогенов (красный), чрезмерное производство муцина или истощение жидкости на поверхности дыхательных путей может привести к закупорке слизью просвета дыхательных путей, обеспечивая убежище для микробной инфекции.
Ранние исследования 1990-х годов показали, что увеличение концентрации аэрозольных растворов хлорида натрия (физиологического раствора) приводит к увеличению скорости мукоцилиарного клиренса [12–14]. На основании этих результатов, аэрозоли HSS были протестированы при краткосрочном лечении пациентов с CF и показали, что они улучшают функцию легких [12,15]. В 2006 году два крупных исследования с использованием 4 мл 7% физиологического раствора в форме аэрозоля два раза в день продемонстрировали улучшение функции легких и снижение частоты обострений [16,17], и теперь это лечение стало основой лечения МВ.
Есть несколько причин полагать, что лечение аэрозолями HSS принесет пользу не только больным МВ, но и пациентам. Во-первых, скорость мукоцилиарного клиренса увеличивается за счет увеличения гидратации даже у тех, у кого не наблюдается истощения жидкости на поверхности дыхательных путей. Это наблюдалось у пациентов с гиперальдостероном, у которых врожденно снижено всасывание натрия, и у здоровых людей из-за использования аэрозолей HSS [18]. Во-вторых, закупорка мелких дыхательных путей слизью из просвета возникает при заболеваниях легких, помимо МВ, таких как астма, хроническая обструктивная болезнь легких (ХОБЛ) и инфекции дыхательных путей, вызванные вирусными, грибковыми и микобактериальными патогенами [19,20].В-третьих, истощение жидкости на поверхности дыхательных путей происходит при некоторых нарушениях воспаления и инфекции дыхательных путей за счет протеолитической активации апикального эпителиального натриевого канала (ENaC) [21]. Исходя из этого, мы начали использовать аэрозольные 7% HSS у пациентов с закупоркой слизи в дыхательных путях и / или стойкой инфекцией дыхательных путей следующим образом. Для вызванной вирусом гиперсекреции слизи с кашлем у пациентов с астмой, ХОБЛ или посттрансплантационным констриктивным бронхиолитом мы используем HSS вместе с обычным режимом лечения обострения пациента, чтобы облегчить кашель и обеспечить доставку ингаляционных лекарств в дыхательные пути, которые в противном случае были бы забит слизью.У пациентов с аллергическим бронхолегочным аспергиллезом (ABPA) мы используем HSS вместе с некоторыми комбинациями ингаляционных стероидов, системных стероидов, системной противогрибковой и системной анти-IgE-терапией. При атипичной микобактериальной инфекции мы используем HSS либо в качестве монотерапии, либо вместе с ингаляционными и / или пероральными антибиотиками. У пациентов с эндобронхиальным стентом мы используем HSS для предотвращения скопления слизи дистальнее стента, что может привести к ателектазу или пневмонии. Иногда мы лечили пациентов с HSS, у которых были рентгенологические помутнения периферического легочного дерева в почке, для которых нам не удалось идентифицировать патоген.У нас есть неофициальные данные о симптоматических и рентгенологических улучшениях в поддержку всех этих применений, но нам неизвестны данные контролируемых испытаний. Когда используется несколько видов аэрозольной терапии, например, HSS вместе с ингаляционными стероидами, мы сначала применяем HSS, хотя объективных доказательств, подтверждающих эту практику, нет. Были бы полезны исследования, предназначенные для измерения применимости и оптимальных методов аэрозольного HSS при других заболеваниях, кроме МВ.
3. Аэрозольная стимуляция врожденного иммунитета легких
Хотя дыхательные пути и альвеолярный эпителий часто рассматриваются как пассивные барьеры, они дополняют базовую защиту легких, претерпевая значительные местные структурные и функциональные изменения при обнаружении патогенных раздражителей.Например, в ответ на вирусное, грибковое или аллергическое воспаление эпителиальные клетки дыхательных путей быстро приобретают гиперсекреторный фенотип в результате процесса, называемого слизистой метаплазией [22,23]. Предполагается, что адаптивная ценность структурной и молекулярной пластичности респираторного эпителия заключается в усилении защиты от микробных патогенов, и это подтверждается наблюдением улучшенного бактериального клиренса после индукции антимикробных белков, включая дефенсины, кателицидины, лизоцим и генераторы реактивных микроорганизмов. формы кислорода [24–28].В присутствии патогенов дыхательные пути и альвеолярный эпителий также вырабатывают воспалительные цитокины и вовлекают лейкоциты в защиту легких [29]. Подавление адаптивного иммунитета и гематопоэза, которое происходит при гематологических злокачественных новообразованиях и / или цитотоксической химиотерапии, не устраняет врожденный иммунный ответ легких на инфекцию. Скорее, пациенты с глубокой иммуносупрессией вырабатывают замечательные цитокиновые и хемокиновые ответы на легочные инфекции [30].
При врожденном иммунитете лейкоциты и паренхимные клетки идентифицируют присутствие патогенов посредством распознавания патоген-ассоциированных молекулярных паттернов (PAMPs), общих для многих видов патогенов, рецепторами распознавания паттернов, кодируемых зародышевой линией (PRR) [31–35].Распознавание PAMP посредством PRR активирует внутриклеточные сигнальные каскады, приводя к экспрессии продуктов, участвующих в микробной защите, воспалении и модуляции адаптивного иммунитета [36]. До сих пор попытки вызвать врожденный иммунитет легких были направлены на стимуляцию PRR с использованием природных или синтетических лигандов [37]. Наиболее распространенными мишенями были Toll-подобные рецепторы (TLR), хотя NOD-подобные рецепторы использовались в качестве адъювантов вакцины в течение многих лет [37], а другие молекулы, такие как RIG-подобные рецепторы и дектин, считались потенциальными терапевтическими мишенями. [37–42].
Чтобы проверить, можно ли эффективно использовать функциональную пластичность легких для защиты от пневмонии in vivo , наша лаборатория сильно стимулировала врожденный иммунитет перед заражением вдыхаемыми респираторными патогенами. Чтобы добиться этого, мышей подвергали воздействию лизата в виде аэрозоля, изготовленного из нетипируемого Haemophilus influenzae , одновременно стимулируя несколько антимикробных путей [42]. Однократное распыление привело к приобретению высокого уровня устойчивости к заражению вирулентными неконфекционными патогенами в течение 2 часов после лечения ().Мы назвали это явление «стимулированная врожденная резистентность» (StIR), чтобы отразить несколько аспектов защиты. Он считается «стимулированным», поскольку резистентность значительно возрастает после терапевтического применения лизата. Защита отражает действие «врожденных» защит, что демонстрируется несколькими ключевыми характеристиками: i) защита достигается за часы, а не дни или недели, как требуется для адаптивного иммунитета; ii) защита достигается у наивных мышей после лечения, полученного от микроба, не являющегося родственным тому, который использовался в контрольном заражении; iii) эффект сохраняется, несмотря на химическое или генетическое истощение адаптивных лейкоцитов; и iv) защита распространяется на каждый микробный патоген, против которого он был протестирован, что указывает на широкий, неизбирательный ответ.Защита связана с «сопротивлением» следующим образом. Столкнувшись с микробной проблемой, выживание зависит от двух стратегий хозяина: толерантности (способность ограничивать ущерб, причиняемый патогеном) и устойчивости (способности ограничивать бремя патогенов) [43,44]. Мы обнаружили, что обработка лизатом ограничивает количество патогенов, связанных с различными классами организмов. Следовательно, мы определили устойчивость как основное средство защиты лизата.
Выживаемость после заражения Streptococcus pneumoniae (Spn) после лечения аэрозольным лизатом нетипируемого Haemophilus influenze (NTHi)Мышей предварительно обрабатывали в группах по шесть человек аэрозольным лизатом NTHi для стимуляции врожденного иммунитета, затем заражали как одну группу с высокой дозой Spn (6.1 × 10 10 КОЕ / мл). Выживаемость через 7 дней показана как функция интервала между лечением и контрольным заражением (* p = 0,015, ‡ p = 0,002, лечение по сравнению с необработанным) [50].
Сначала мы проверили защитное действие StIR против наиболее распространенной причины бактериальной пневмонии во всем мире, Streptococcus pneumoniae , и обнаружили, что, хотя все нелеченные мыши умерли после ингаляционного заражения, все мыши, обработанные лизатом, выжили. Механистические исследования показали, что защита тесно связана с индукцией антимикробной среды в легких, что демонстрируется быстрым снижением количества патогенов по сравнению с нелеченными мышами [42].Защитный эффект сохранялся, даже если у мышей не было резидентных лейкоцитов в легких (альвеолярных макрофагов и тучных клеток) или у мышей не было рекрутированных нейтрофилов. Последующие исследования также показали, что лимфоциты были незаменимы при StIR, и исследований in vitro показали, что респираторный эпителий был достаточным как для восприятия лечения, так и для воздействия на противомикробный ответ [45].
Стимулированная врожденная резистентность широко распространяется на другие важные бактериальные респираторные патогены.Среди распространенных причин внутрибольничной пневмонии ингаляционное лечение бактериальным лизатом эффективно защищает от Pseudomonas aeruginosa , Klebsiella pneumoniae и лейкоцидин-продуцирующих лейкоцидин Panton-Valentine устойчивых к метициллину Staphylococcus aureus [45]. Дыхательный путь — наиболее вероятный портал входа для агентов биотеррора и единственный способ, с помощью которого такие патогены были успешно доставлены в современную эпоху (например, ингаляционная сибирская язва) [46–49].Мы исследовали, может ли StIR защищать от агентов биотеррора, и обнаружили, что однократное введение аэрозольного лизата значительно увеличивает среднюю выживаемость мышей, зараженных Bacillus anthracis , Yersinia pestis или Francisella tularensis [45]. Для всех исследованных бактериальных патогенов защита от летального исхода была связана со значительным и немедленным сокращением количества патогенов.
Учитывая широту защиты от разнородных видов бактерий и предположение о еще более широком антимикробном действии путем анализа экспрессии гена легких после лечения, также была протестирована защита мышей от грибкового патогена.Поскольку ни мыши, ни люди обычно не восприимчивы к пневмонии Aspergillus при отсутствии иммунодефицита, мышей лечили циклофосфамидом и кортизолом перед контрольным заражением A. fumigatus . Из инфицированных мышей> 70% умерли, если они не прошли предварительную обработку лизатом. Практически все, кто проходил лечение, выжили (93%). Как и в случае с бактериальными патогенами, StIR привел к значительному снижению внутрилегочной грибковой нагрузки [45].
Вирус гриппа является основной причиной смертности от легочных инфекций во всем мире, и эффективный легочный StIR может обеспечить защиту во время пандемий.Мы обнаружили, что в то время как 100% контрольных мышей умерли от геморрагической пневмонии,> 90% выжили после одной предварительной обработки бактериальным лизатом [50]. Мы также обнаружили значительное улучшение показателей выживаемости, если лизат в форме аэрозоля вводили через 1 день после заражения, что указывает на то, что стимуляция врожденного иммунитета может быть полезной для лечения, а также для профилактики пневмонии. Кроме того, мы обнаружили, что добавление рибавирина к лечению лизатом привело к синергетическому улучшению выживаемости (т. Е., лучше, чем аддитивные эффекты одного лечения) при введении после инфекции [50]. Как и в случае со всеми другими исследованными патогенами, защита от гриппа, вызванная лизатом, коррелировала со снижением титров вируса в легких.
В то время как лечение нетипируемым лизатом Haemophilus influenza (NTHi) приводит к быстрой активации врожденного иммунитета слизистой оболочки легких, защитный эффект ослабевает через 4-5 дней [50,51]. Следовательно, для предотвращения пневмонии у групп пациентов, подвергавшихся риску по истечении этого периода, вероятно, потребуется повторное лечение.Мы обнаружили, что повторное дозирование является эффективным и безопасным для мышей. При повторной обработке лизатом мыши показали стойкую устойчивость к заражению S. pneumoniae , P. aeruginosa и гриппом A [45,50]. Мыши, подвергавшиеся обработке лизатом еженедельно в течение 50 недель, не показали явных патологий, таких как преждевременная смерть, потеря веса или изменения поведения [36]. После 8 еженедельных воздействий инфильтрация мононуклеарных клеток окружала дыхательные пути, хотя наблюдалось очень мало альвеолярных воспалительных клеток.После 25 еженедельных воздействий был очевиден легкий фиброз стенки дыхательных путей, который далее прогрессировал после 50 еженедельных воздействий [52]. Увеличенная временная шкала фиброза стенки дыхательных путей и прогрессирующего накопления лимфоцитов предполагает, что фиброз возникает из-за адаптивного иммунного ответа после хронического воздействия бактериального лизата, а не в ответ на саму стимуляцию врожденного иммунитета. Замена макромолекулярных стимуляторов врожденного иммунитета низкомолекулярными аналогами, которые не вызывают адаптивного иммунного ответа, и снижение интенсивности стимуляции, таким образом, позволяет избежать этого долгосрочного осложнения.Действительно, толстая кишка мышей постоянно стимулируется присутствием просветных бактерий, что приводит к конститутивной активации StIR, которая может быть обнаружена как индуцибельно сниженная способность убивать бактерии эпителием толстой кишки после лечения антибиотиками [53], но толстая кишка этого не делает. развивается фиброз.
Данные на мышах показывают, что лечение, индуцирующее врожденную резистентность в легких, должно хорошо переноситься пациентами-людьми. Мы полагаем, что причина того, что мыши могут переносить самые высокие применяемые дозы (в 12 раз превышающие терапевтическую дозу) без явных побочных эффектов [51], заключается в том, что реакция содержится в просвете легких.Несмотря на то, что количество воспалительных цитокинов в жидкости бронхоальвеолярного лаважа увеличивается в несколько тысяч раз по сравнению с исходным уровнем, уровень системных цитокинов почти не увеличивается [50]. Это согласуется с недавней работой Hoogerwerf и его коллег, которые вызвали значительную воспалительную реакцию легких в дыхательных путях у людей, подвергшихся внутрилегочному применению лигандов TLR, липотехоевой кислоты (лиганд TLR2) и липополисахарида (LPS, лиганд TLR4), но не были связаны с любые идентифицируемые клинические признаки или симптомы [54].
Не только наша лаборатория исследует стимуляцию TLR, которая может способствовать увеличению выживаемости хозяина при инфекциях. Несколько групп наблюдали иммуномодулирующие эффекты ЛПС и пытались изменить течение респираторных инфекций, доставляя производные ЛПС [40,41,55] или изменяя структуру ЛПС [39] у патогенов, используемых при экспериментальной пневмонии. У всех была обнаружена некоторая степень защиты за счет применения одного агониста TLR4, как и у нас [51]. Испытания отдельных агонистов TLR также были успешными при инфекционных заболеваниях человека.Например, подкожное введение синтетического агониста TLR9 вызвало системные воспалительные реакции и снизило вирусную нагрузку гепатита C [42], а местный имиквимод (TLR7) оказался многообещающим при лечении кожного лейшманиоза [38]. Однако вполне вероятно, что для достижения полной эффективности и широты действия, продемонстрированных с бактериальным лизатом, потребуются синергетические взаимодействия множественной стимуляции PRR [56-59].
Лизат, используемый для индукции StIR, не обладает антибиотическим действием [45].Скорее, он вызывает собственные защитные продукты хозяина. Индукция выработки антимикробного пептида согласуется как со временем, так и с широтой защиты и демонстрируется с помощью микроматрицы экспрессии генов [45] и протеомного анализа [51]. В будущем, возможно, удастся обойти стадию индукции хозяина и напрямую доставить полезные антимикробные пептиды или миметики малых молекул [43].
В ближайшем будущем стимуляция естественной реакции хозяина на микробные продукты для профилактики и лечения пневмонии может стать основой для разработки новой клинической терапевтической стратегии [44,45].
4. Аэрозольная доставка цитокинов для направленного иммунного отклонения
IFNα-2a, IFNγ-1b и GM-CSF вводились легочным путем пациентам с резистентной легочной инфекцией Mycobacterium tuberculosis и нетуберкулезным микобактериозом (NTM) включая Mycobacterium avium комплексное заболевание легких с переменным успехом. Эти иммунологически разнообразные белки также использовались при неинфекционных легочных заболеваниях, таких как первичный рак легких, метастатический рак в легкие и альвеолярный протеиноз, заболевание, недавно связанное с антителами против нативного GM-CSF [60–62].Ниже приводится краткое описание клинического опыта использования терапии ингаляционными цитокинами при легочной инфекции.
Ингаляционный IFNα переносится в более низких дозах (1-20 MIU) без системных побочных эффектов, тогда как лихорадка, недомогание и головная боль возникали при использовании доз в диапазоне от 60 до 120 MIU и совпадали с обнаруживаемым цитокином в периферическом кровообращении [63, 64]. Бронхоспазм препятствует использованию этого цитокина у пациентов с хроническим бронхитом [65].Спасательная терапия с использованием ингаляционного IFNα для лечения неоперабельного рака легких не обнадеживает [66]. Добавление IFNα 3 MIU 3 раза в неделю к противотуберкулезной терапии было связано с ранним исчезновением лихорадки и быстрым снижением количества кислотоустойчивых бацилл в отхаркиваемой мокроте по сравнению с одной антимикробной терапией [67]. Кроме того, у пациентов с резистентной к лечению туберкулезной инфекцией добавление ингаляционного IFNα показало обнадеживающие результаты, хотя необходимы дальнейшие крупные рандомизированные исследования для подтверждения безопасности, стоимости и эффективности [68].
Низкие дозы ингаляционного IFNγ хорошо переносятся, в том числе пациентами с бронхореактивными состояниями, такими как астма, и после воздействия этого плейотропного провоспалительного цитокина была продемонстрирована измеримая активация альвеолярных макрофагов [69,70]. Имеется значительный клинический опыт использования ингаляционного IFNγ для лечения легочных микобактериальных инфекций. В сочетании с антимикробной терапией терапия IFNγ в виде аэрозоля привела к благоприятным ответам как на лекарственно-чувствительный, так и на лекарственно-устойчивый туберкулез легких, с уничтожением микроорганизмов и улучшением радиографических показателей заболевания [71–73].Однако этого преимущества не наблюдалось у пациентов с тяжелым основным заболеванием легких, у которых был туберкулез легких [74]. Точно так же не было отмечено терапевтического эффекта у пациентов с МВ, получавших высокие дозы (500 или 1000 мкг) ингаляционного IFNγ для снижения риска инфекции, тем не менее, пациенты страдали от серьезной лекарственной токсичности, включая одышку, кровохарканье и госпитализацию [75]. IFNγ также был исследован для профилактики вентилятор-ассоциированной пневмонии (ВАП) у пациентов с тяжелыми травмами [76].Количество ВАП было уменьшено, хотя не наблюдалось улучшения общей смертности у этих пациентов с травмами, которые получали 100 мкг рекомбинантного IFNγ в аэрозольной форме 3 раза в день [76]. Эта неэффективность частично может быть связана с низкой доставкой цитокинов через стандартный распылитель [77]. Рекомбинантный GM-CSF в аэрозольной форме хорошо переносится пациентами с легочными метастазами в дозах 250 мкг дважды в день без серьезных побочных эффектов [78]. О применении аэрозольных GM-CSF для лечения инфекций у людей не сообщалось.Однако эксперименты на животных подтверждают абсорбцию в легких аэрозольного или интратрахеально введенного GM-CSF, и GM-CSF в аэрозольной форме оказался эффективным в искоренении инвазивного легочного аспергиллеза у мышей в модели с ослабленным иммунитетом [79,80].
Другие цитокины, используемые аэрозольным путем, включают IFNβ при лечении рака легких, IL-2 при почечно-клеточной карциноме и другом метастатическом раке легких, растворимый рецептор IL-4 для пациентов с астмой и эритропоэтин для лечения анемии.Ни один из них не использовался для лечения легочной инфекции.
5. Доставка синтетических антибиотиков в аэрозольной форме
В первом подразделе мы обсудим использование аминогликозидов в лечении и профилактике серьезных легочных инфекций у пациентов с высоким риском, а затем кратко ознакомимся с ограниченным клиническим опытом применения других противомикробных препаратов. препараты, которые использовались для спасительной терапии трудноизлечимой пневмонии. Учитывая, что были проведены обширные обзоры ингаляционного пентамидина при ВИЧ-ассоциированной инфекции Pneumocystis jiroveci , эта тема здесь не рассматривается.
5.1 Аэрозольная терапия аминогликозидами
Теоретически аминогликозиды имеют несколько характеристик, которые, по-видимому, способствуют ингаляционному введению. Во-первых, аминогликозиды обладают эффектом уничтожения, зависящим от концентрации, что означает, что высокие уровни, достижимые в дыхательных путях с помощью ингаляционных препаратов, могут привести к повышению клинической эффективности. Более того, аминогликозиды обладают значительной ограничивающей дозу токсичностью для людей, так что дозы, которые можно вводить при системном введении, приводят к относительно низким уровням в паренхиме легких.Наконец, поскольку аминогликозиды использовались относительно редко в течение последних нескольких десятилетий, многие организмы с множественной лекарственной устойчивостью, вызывающие нозокомиальную респираторную инфекцию, остаются восприимчивыми по крайней мере к одному, если не ко многим, обычно используемым аминогликозидам. Действительно, из всех классов антибиотиков данные о доставке антимикробных препаратов путем ингаляции наиболее обширны для аминогликозидов. В этом разделе мы рассмотрим фармакокинетическую, клиническую информацию и информацию о безопасности, касающуюся ингаляционной терапии аминогликозидами.
Разработка аминогликозидов широкого спектра действия, таких как гентамицин, в конце 1960-х — начале 1970-х годов открыла большие перспективы для лечения ранее резистентных респираторных инфекций из-за устойчивых к антимикробным препаратам грамотрицательных палочек, таких как P. aeuroginosa [81] . Однако вскоре исследователи сообщили, что системно вводимый гентамицин часто не лечил легочные инфекции из-за P. aeuroginosa и других грамотрицательных палочек, несмотря на чувствительность in vitro [82].Низкие уровни гентамицина в респираторных секретах заставили исследователей предположить, что беспорядочное проникновение аминогликозидов в очаг инфекции может быть причиной терапевтических неудач, и предположить, что введение гентамицина непосредственно в легкие может улучшить клинический ответ [83,84]. Предварительные исследования 1970-х годов показали, что концентрация гентамицина в мокроте часто была на порядок выше после эндотрахеального введения по сравнению с системным лечением [83,85].
Данные, накопленные в последующие 30 лет, подтвердили предположение этих ранних сообщений о том, что проникновение аминогликозидов в легочную паренхиму является субоптимальным после системного введения [86–93]. Фармакокинетика доставки аминогликозидного лекарственного средства имеет особое значение, поскольку эти агенты обладают зависящим от концентрации эффектом уничтожения, а это означает, что более высокие уровни лекарственного средства связаны с усилением антимикробного действия [94]. Например, оптимальный клинический ответ на терапию аминогликозидами происходит, когда максимальная концентрация препарата (C max ) до минимальной ингибирующей концентрации (МИК) составляет> 8: 1 [95–98].Терапия аминогликозидами при пневмонии обычно рассматривается для относительно устойчивых неферментативных грамотрицательных палочек, таких как P. aeruginosa , Acinetobacter baumanii и Stenotrophomonas maltophila [99]. Хотя они сильно варьируются в зависимости от популяции пациентов и рассматриваемых аминогликозидов, даже для восприимчивых организмов, МПК для этих организмов обычно находятся в диапазоне 1-8 мкг / мл [100]. Таким образом, чтобы максимизировать возможность клинического ответа, необходимы концентрации легочных аминогликозидов ≥ 10-40 мкг / мл.Важно отметить, что ни один из доступных в настоящее время аминогликозидов не достигает таких уровней при системном введении даже в условиях воспалительного процесса, который, как ожидается, приведет к увеличению попадания в легкие из кровотока [85,86,91,92,101] .
В отличие от трудностей достижения удовлетворительных уровней в легких с помощью системного введения аминогликозидов, местная доставка аминогликозидов приводит к концентрациям, которые могут быть эффективными даже против относительно резистентных организмов [85,86,93,102-104].Измерения уровней аминогликозидов в легких после местного введения в значительной степени зависят от механизма, используемого для доставки лекарственного средства, дозы и места отбора пробы. Однако, несмотря на эти различия, исследователи неизменно демонстрируют уровни аминогликозидов> 200 мкг / мл в респираторных образцах после местного применения [85–87,89,101–107]. Данные, касающиеся концентраций аминогликозидов, аналогичны в исследованиях на животных и людях, у больных и здоровых пациентов, а также при использовании инвазивных и неинвазивных методов тестирования [85–87,89,101–107].Таким образом, фармакокинетические данные убедительно свидетельствуют о том, что местное введение аминогликозидов с большей вероятностью приведет к эффективным уровням лекарственного средства по сравнению с системной доставкой.
5.2 Клинические исследования ингаляционных аминогликозидов: муковисцидоз
Контроль над бронхолегочной инфекцией заметно повысил качество и продолжительность жизни пациентов с МВ [108]. Уникальная эндобронхиальная среда пациентов с МВ означает, что легкие таких пациентов колонизируются такими организмами, как S.aureus и H. influenza вскоре после рождения. Однако со временем P. aeuroginosa обычно становится преобладающим легочным патогеном у пациентов с МВ, колонизируя> 80% людей к 18 годам [109]. Взаимодействие «хозяин – патоген» между пациентами с МВ и P. aeuroginosa относительно уникально с точки зрения бактериальных процессов, поскольку однажды установленная эндобронхиальная инфекция, вызванная P. aeuroginosa , редко полностью искореняется [110]. Большая часть терапевтических достижений, достигнутых за последние десятилетия в лечении пациентов с МВ, была достигнута за счет снижения бремени, вызываемого P.aeuroginosa в легких пациентов с МВ, что впоследствии уменьшает воспалительный ответ, ответственный за прогрессирование бронхоэктазов.
В то время как внутривенные антибиотики долгое время были золотым стандартом для лечения инфекции, вызванной P. aeuroginosa у пациентов с МВ, за последние 20 лет серия все более тщательных клинических исследований четко установила роль ингаляционных аминогликозидов в подавлении P. y инфекция aeuroginosa у пациентов с МВ.Первоначально использовался гентамицин, но исследователи перешли к тобрамицину в свете его повышенной активности против Pseudomonas [111–113]. Для удобства в ранних исследованиях использовались небулайзерные флаконы с аминогликозидами, изначально предназначенные для внутривенного введения, которые потенциально могли вызвать раздражение легких из-за присутствия консервантов и антиоксидантов. Важный прогресс произошел, когда Smith et al . разработали препарат тобрамицина без консервантов для распыления, который в дозе 600 мг обеспечивает гораздо более высокую дозу, чем типичный флакон для внутривенного введения на 80 мг [114].Это была доза тобрамицина 600 мг, которая использовалась в критическом исследовании перекрестного дизайна для 71 человека, в котором пациенты получали t.i.d. дозирование. После 1 месяца приема распыленного тобрамицина ключевые параметры легочной функции и плотность мокроты, полученной при использовании P. aeuroginosa , значительно улучшились в группе лечения [107]. Эффективный, но громоздкий характер лечения привел к разработке следующего поколения распыленного тобрамицина, который впоследствии был использован в крупнейшем рандомизированном плацебо-контролируемом исследовании распыленных аминогликозидов.В общей сложности 520 пациентов с CF, которые были колонизированы P. aeuroginosa , были рандомизированы для получения распыленного тобрамицина 300 мг два раза в день. или плацебо, вводимое в 4-недельных блоках включения-выключения в течение 24 недель [115]. Пациенты, получавшие активное лечение, показали улучшение показателей легочной функции, меньшую потребность в госпитализации и значительное снижение плотности P. aeuroginosa в мокроте. Важно отметить, что положительный эффект ингаляционного тобрамицина сохранялся в течение 2 лет после начала лечения [116].Результаты этого исследования привели к одобрению FDA США раствора тобрамицина для ингаляции (TSI) (TOBI ™ , Novartis Corp., Восточный Ганновер, Нью-Джерси), который до сих пор является единственным одобренным антибиотиком для ингаляции дыхательных путей в США. .
Эффективность TOBI в хроническом подавлении P. aeuroginosa у пациентов с МВ привела к исследованиям ингаляционных аминогликозидов при обострениях МВ, но результаты не были столь впечатляющими. Несколько испытаний показали, что добавление ингаляционных аминогликозидов, таких как тобрамицин или амикацин, к системной антипсевдомонадной терапии увеличивает долю пациентов, которые избавляются от P.aeuroginosa из мокроты, но не улучшает клинические исходы, такие как тесты функции легких [117,118]. Недавно завершенное международное исследование в 17 центрах не выявило статистической разницы в клинических исходах при добавлении ингаляционного тобрамицина к системно вводимому ципрофлоксацину у пациентов с МВ, инфицированных P. aeuroginosa, с обострением [119]. Пациенты, получавшие ингаляционный тобрамицин, имели более низкую плотность мокроты P. aeuroginosa , но повышенную частоту свистящего дыхания при ингаляционной терапии, что могло свести на нет пользу от усиленного противомикробного эффекта.Таким образом, в настоящее время ингаляционная терапия не считается частью стандарта помощи пациентам с МВ с обострениями.
5.3 Лечение пациентов с бронхоэктазами без кистозного фиброза ингаляционными аминогликозидами
Хотя МВ является преобладающей причиной бронхоэктазов в развитых странах, существует несколько других заболеваний, которые могут привести к бронхоэктазам [120]. Обнадеживающие результаты лечения бронхоэктазов, связанных с МВ, увеличили давний интерес к лечению пациентов с бронхоэктазами, не связанными с МВ, с помощью ингаляционных аминогликозидов [121].К сожалению, как и в случае острых обострений при МВ, накопленные к настоящему времени данные об эффективности ингаляционных аминогликозидов при бронхоэктазиях, не связанных с МВ, не так сильны, как данные для поддерживающей терапии при МВ. На данный момент четыре опубликованных клинических исследования изучали использование ингаляционных аминогликозидов у пациентов без МВ с бронхоэктазами и хронической инфекцией, вызванной P. aeuroginosa , во всех из которых использовался ингаляционный тобрамицин в дозе 300 мг два раза в день. дозирование [119,122–124]. Подобно основным исследованиям МВ, эти испытания неизменно показывают, что ингаляционный тобрамицин значительно снижает респираторную нагрузку P.aeuroginosa . Однако, в отличие от ситуации с бронхоэктазами, связанными с МВ, снижение уровня P. aeuroginosa у пациентов с бронхоэктазами, не связанными с МВ, не привело к последовательному улучшению объективных клинических показателей, таких как тесты функции легких. Одно исследование обнаружило улучшение «общего состояния здоровья» у пациентов, получавших тобрамицин [123]. Обнаружение того, что у пациентов, получавших тобрамицин, развивался более выраженный бронхоспазм по сравнению с пациентами, получавшими плацебо, значительно ограничило применение аэрозольных антибиотиков при бронхоэктазах без МВ [121].Таким образом, широкое использование ингаляционных аминогликозидов у пациентов с бронхоэктазами без МВ требует разработки препарата, который вызывает меньшее раздражение дыхательных путей при сохранении антипсевдомональной эффективности.
5.4 Профилактика и лечение вентилятор-ассоциированной пневмонии с помощью ингаляционных аминогликозидов
Хотя ИВЛ имеет жизненно важное значение для ведения тяжелобольных пациентов, она часто осложняется развитием респираторных инфекций, вызывающих значительную заболеваемость и смертность [125].Учитывая легкость доступа, обеспечиваемую интубацией трахеи, существует долгая история введения противомикробных препаратов непосредственно в дыхательные пути для лечения и профилактики респираторных инфекций, связанных с аппаратом ИВЛ [83]. Наиболее систематически исследуемой областью в этом отношении было использование местных антибиотиков для предотвращения искусственной вентиляции легких (ВАП) [126]. Хотя самые крупные исследования были проведены с антибиотиками, не являющимися аминогликозидами, и тобрамицин, и гентамицин показали некоторую эффективность в предотвращении ВАП [127, 128].Недавний метаанализ показал, что местное применение антимикробных препаратов значительно снижает частоту ВАП у пациентов с искусственной вентиляцией легких [126]. Эти данные противоречат рекомендациям Центров по контролю и профилактике заболеваний против использования распыленных антибиотиков для предотвращения ВАП из-за опасений по поводу развития устойчивости к противомикробным препаратам и побочных эффектов введения [129].
По сравнению с профилактикой ВАП, существует меньше системных данных об использовании ингаляционных аминогликозидов для терапии ВАП [130].Однако, учитывая рост показателей ВАП из-за множественной лекарственной или даже панрезистентности грамотрицательных патогенов, использование ингаляционных аминогликозидов или других противомикробных препаратов может стать все более распространенным явлением в попытке повысить локальные концентрации лекарств для борьбы с относительно устойчивыми патогенами. Следует отметить, что недавнее ретроспективное исследование онкологических пациентов с грамотрицательной палочкой ВАП показало, что те пациенты, которые получали ингаляционные аминогликозиды, в основном тобрамицин или ингаляционный колистин, имели значительно лучшие клинические результаты по сравнению с пациентами, получавшими терапию системными аминогликозидами или колистином [131].Наконец, Палмер и др. . недавно сообщили о результатах исследования, в котором пациенты с вентилятор-ассоциированным трахеобронхитом (VAT) были рандомизированы для приема ингаляционных противомикробных препаратов, тобрамицина и / или ванкомцина или плацебо [132]. Пациенты, получавшие ингаляционные противомикробные препараты, имели заметное улучшение объективных респираторных показателей и имели значительно меньшую вероятность прогрессирования до ВАП по сравнению с пациентами, получавшими плацебо. В совокупности сочетание повышения лекарственной устойчивости и накопления данных об эффективности ингаляционной терапии указывает на то, что местная терапия аминогликозидами может играть многогранную роль в профилактике и лечении респираторной инфекции у пациентов с механической вентиляцией легких, хотя необходимы многоцентровые проспективные исследования.
5.5 Безопасность ингаляционных аминогликозидов
Двумя основными проблемами, вызывающими обеспокоенность в отношении местной терапии аминогликозидами, являются развитие лекарственной устойчивости и побочные эффекты лекарств или системы доставки лекарств. Учитывая, что местное введение приводит к градиенту концентрации противомикробного препарата от центральных к периферическим дыхательным путям, существует серьезная проблема индукции устойчивости к противомикробным препаратам [121]. Более того, местная терапия часто назначается в течение длительных периодов времени, даже лет, тем самым максимально увеличивая возможность развития лекарственной устойчивости.В то время как отчеты о случаях и серии случаев подтверждают, что резистентные организмы могут возникать во время терапии, тщательное обследование в ходе рандомизированных клинических испытаний не показало, что появление резистентных к лекарствам организмов у пролеченных пациентов является особенно важной проблемой [100, 110, 126]. В свете чрезвычайно высоких уровней аминогликозидов, достижимых с помощью небулайзерной терапии, некоторые страны предложили разработать специфические для ингаляции контрольные точки МИК, при которых очень немногие организмы действительно будут устойчивы к аминогликозидам [133].Приведет ли загрязнение окружающей среды при нозокомиальной небулайзерной терапии к повышению устойчивости к аминогликозидам в медицинских учреждениях, остается теоретическим, но недоказанным вопросом. Выявление бронхоспазма при местной терапии — еще одна важная проблема безопасности, особенно когда распыленные антибиотики используются для облегчения симптомов, например, при бронхоэктазах [121]. Хотя обычно они легко поддаются лечению бронходилататорами, раздражение дыхательных путей распыляемыми аминогликозидами ограничено для многих пациентов, и продолжение исследований по разработке более переносимых методов лечения имеет решающее значение для более широкого использования.
5.6 Другие виды антибактериальной терапии в виде аэрозолей
Клинический опыт аэрозолизации антибактериальных средств, отличных от аминогликозидов, ограничен, но продолжает расти. Заметное увеличение числа грамотрицательных патогенов с множественной лекарственной устойчивостью привело к увеличению использования полимиксинов, противомикробных препаратов, которые были разработаны в 1950-х годах, но их использование быстро сократилось в 1970-х и 1980-х годах из-за опасений по поводу нефротоксичности [134]. Использование колистина (полимиксина E) в последнее время заметно увеличилось, поскольку штаммы P.aeruginosa и A. bauamnnii , устойчивые ко всем другим классам коммерчески доступных антимикробных препаратов, остались чувствительными к колистину [134]. Подобно аминогликозидам, ингаляция является потенциально привлекательным способом введения колистина, учитывая токсичность, наблюдаемую при системном введении. Ретроспективные и нерандомизированные исследования показали обнадеживающие результаты при использовании ингаляционного колистина, хотя исследования противоречат гетерогенности пациентов и назначению дополнительных противомикробных препаратов в сочетании с ингаляционным колистином [130, 131, 134–138].До сих пор сообщалось о минимальной токсичности ингаляционного колистина, хотя систематические данные отсутствуют. Ингаляционный азтреонам представляется безопасной и эффективной альтернативой ингаляционному тобрамицину при муковисцидозе [139]. Наконец, недавнее исследование показало, что ингаляционный ванкомицин эффективен в предотвращении прогрессирования трахеобронхита, связанного с вентилятором, до пневмонии, связанной с вентилятором [132]. Неуклонный рост лекарственной устойчивости среди респираторных патогенов придает дополнительную актуальность продолжению исследований, призванных лучше определить роль ингаляционных противомикробных препаратов при легочных инфекциях.
5.7 Противогрибковая аэрозольная терапия
Несмотря на недавние достижения в области противогрибковой лекарственной терапии, инвазивные грибковые инфекции (ИФИ) остаются серьезной угрозой для больных раком с ослабленным иммунитетом и реципиентов трансплантации органов или гемопоэза [140,141]. Ответ на терапию цитокинами системного усиления иммунитета, такую как рекомбинантный GM-CSF, IFNγ и переливание донорских гранулоцитов, чреват отсутствием исследований по оценке стоимости и полезности и усугубляется неопределенными данными клинической эффективности [142].Инвазивный аспергиллез представляет собой опасную для жизни инфекцию, часто наблюдаемую в течение первых 3 лет после трансплантации сердце-легкие [143], тогда как у реципиентов аллогенной трансплантации стволовых клеток эта инфекция возникает в период нейтропении перед приживлением, во время острой трансплантации вместо трансплантата. болезнь хозяина (GVHD) и в период позднего риска, который включает лечение хронической GVHD [144]. У больных раком пациенты с острым миелогенным лейкозом особенно восприимчивы к ИФИ, и период риска может быть увеличен у пациентов с рефрактерным или рецидивирующим раком [145].Ингаляционный амфотерицин B был исследован для предотвращения ИФИ у восприимчивых пациентов в периоды высокого риска и для терапии спасения у пациентов с трудно поддающимся лечению инвазивным грибковым заболеванием легких.
У реципиентов трансплантата легкие инфекции Aspergillus разновидностей приводят к колонизации, которая часто предшествует инвазивному заболеванию, проявляющемуся как трахеобронхит или инфекции анастомоза, и / или инвазивное заболевание легких; диссеминация грибков у этих пациентов без нейтропении и без рака встречается редко.Большинство этих грибковых инфекций возникает у реципиентов трансплантатов солидных органов без нейтропении в период раннего отторжения трансплантата и иммуносупрессивной терапии отторжения [143]. Интересно отметить, что колонизация видами Aspergillus через 3 месяца после трансплантации чаще встречается у пациентов с человеческим лейкоцитарным антигеном (HLA) A1; однако у этих пациентов, склонных к поздней грибковой колонизации, риск инвазивного грибкового заболевания существенно не увеличивался [143]. Напротив, недавно сообщалось о нескольких грибковых инфекциях у реципиентов трансплантата сердца с рефрактерным отторжением, получавших сиролимус в сочетании с такролимусом, и пациентов с васкулопатией сердечного аллотрансплантата [146].
Ингаляционный амфотерицин B был первым лекарством, используемым для лечения системного микоза, а более ранние эксперименты на животных с использованием аэрозольного амфотерицина B показали благоприятную эффективность при лечении легочного аспергиллеза [147]. Липидные препараты амфотерицина B, такие как липидный комплекс амфотерицина B (ABLC), также эффективно доставлялись аэрозольным путем. Прединфекционная обработка ABLC в дозе 0,4–1,6 мг / кг за 2 дня до инфекции обеспечила увеличение выживаемости на 63–100% в экспериментах на животных [148].Пиковая концентрация амфотерицина B в бронхоальвеолярном лаваже после однократного приема достигается через 30 минут после ингаляции, и он медленно выводится из легких в течение следующих 24 часов [149].
Устройство доставки лекарственного средства остается критически важным для прогнозирования концентрации лекарственного средства, распыляемого в виде аэрозоля. В исследованиях клинической кинетики распределения 10% вдыхаемого ABLC откладывалось в легких при введении через специализированные системы доставки, такие как распылитель AeroEclipse, управляемый сжатым воздухом со скоростью 7-8 л / мин, и это отложение в легких было в два раза выше по сравнению с достигнутыми уровнями. использование стандартных систем доставки аэрозолей для бронхолитической терапии [150].Состав также важен, поскольку в экспериментах на животных концентрация лекарственного средства в аэрозольной форме ABLC в шесть раз выше по сравнению с дезоксихолатом амфотерицина B [148]. Более того, ингаляционный ABLC хорошо переносился при исследовании реципиентов трансплантата легкого, тогда как обычный дезоксихолат амофотерицина B приводил к вдвое большему количеству побочных эффектов, связанных с лечением [151].
Сообщалось о значительном сокращении случаев инвазивного легочного аспергиллеза у пациентов, получавших ингаляционный амфотерицин B во время и после операции по трансплантации сердца и сердце – легкие [152].Аналогичным образом, липидный препарат амфотерицина B (ABLC) также успешно использовался для профилактики трахеобронхита Aspergillus, анастомозов и инвазивных заболеваний легких у реципиентов сердца и легких [143, 153].
Скудность клинических данных по лечению амфотерицином В в аэрозольной форме у пациентов с установленной грибковой инфекцией легких затрудняет рекомендацию этого вмешательства даже в рефрактерных случаях. Вот два примера таких случаев: пациент без иммуносупрессии с поствирусным трахеобронхитом, вызванным Aspergillus, который не ответил на длительную липосомную терапию амфотерицином B, имел благоприятный ответ на длительное лечение ингаляционным дезоксихолатом амфотерицина B плюс GM-CSF и IFNγ-иммунитет. усиление [154].Во-вторых, у пациента с тяжелой иммуносупрессией и инфекцией легкого Rhizomucor, которая в результате эволюции превратилась в Pseudalescheria boydii , инфекция полностью исчезла с помощью ингаляционного ABLC, которая продолжалась в течение 5 месяцев, и при долгосрочном наблюдении рецидива инфекции не наблюдалось [155]. Эти случаи подчеркивают потенциальную роль ингаляционного амфотерицина B в лечении установленного заболевания; однако на основании текущей клинической информации нельзя дать никаких рекомендаций.
5.8 Противовирусная аэрозольная терапия
Вирусные инфекции дыхательных путей обычно протекают в легкой форме и часто поддаются поддерживающей терапии. Однако у пациентов с ослабленным иммунитетом, больных раком или трансплантацией, эти инфекции могут быть связаны с тяжелыми осложнениями, требующими ранней диагностики и своевременной терапии [137]. Обеспокоенность вызывают парамиксовирусы, такие как респираторно-синцитиальный вирус (RSV) и вирус парагриппа (PIV), вирусы гриппа A и B, аденовирус и недавно признанный метапневмовирус человека (hMPV).Рибавирин, аналог пуринового нуклеозида, использовался для лечения хронической инфекции вируса гепатита С пероральным введением, а также для лечения геморрагической лихорадки и диссеминированного hMPV путем внутривенного введения. Рибавирин в аэрозольной форме был одобрен FDA для лечения инфекций RSV у госпитализированных детей. Обычное непрерывное лечение 60 мг рибавирина / мл в течение 18 часов эффективно с внутривенным иммуноглобулином или без него; однако пациенты чувствуют себя сильно изолированными, что может помешать их уходу [138].Периодически вводимый в виде аэрозоля рибавирин в дозе 20 мг / мл в течение 2 ч 3 раза в день также был эффективен у взрослых пациентов с раком и трансплантацией стволовых клеток с инфекцией RSV [140]. У детей с ослабленным иммунитетом и инфекцией RSV периодические высокие дозы (60 мг) рибавирина / мл в течение 2 часов, вводимые 3 раза в день, хорошо переносились, ассоциировались с клиническим ответом, сравнимым со стандартной непрерывной терапией, и ассоциировались со значительно меньшим загрязнением окружающей среды и воздействием на здоровье: медицинским работникам и с большей доступностью для пациентов [141, 142].
Парагрипп ассоциируется с потенциально серьезными осложнениями у реципиентов трансплантата сердце-легкие, с возможной ролью в остром отторжении аллотрансплантата и облитерирующем поствирусном бронхиолите [143]. Ингаляционный рибавирин в этой популяции ассоциировался с клиническим улучшением, хотя клинический опыт ограничен [144]. У реципиентов трансплантата гемопоэтических стволовых клеток парагриппозная вирусная инфекция является серьезной в присутствии других копатогенов и у пациентов с дыхательной недостаточностью, и лечение рибавирином в форме аэрозоля не было связано с уменьшением продолжительности выделения вируса или смертности, связанной с пневмонией [145].
Вирус гриппа А является основной причиной заболеваемости и смертности, и инфекции часто бывают тяжелыми у пациентов с дефектным адаптивным Т-клеточным ответом. Лекарственная устойчивость к ингибиторам нейраминидазы представляет собой серьезную проблему лечения в условиях плохого ответа на обычные вакцины в популяции высокого риска рака и трансплантата [146]. Аэрозольный рибавирин 60 мг / мл для трех дневных доз продолжительностью 15 мин был эффективен против гриппа A и B у мышей [147]. Недавно было показано, что мегадоза рибавирина (100 мг / мл) эффективна у мышей, инфицированных летальным вирусом гриппа A h4N2.Эта мегадозовая терапия в течение всего 4 дней привела к выживаемости> 90% при назначении в течение 24–48 часов после инфицирования [148]. Необходимы дальнейшие клинические исследования для оценки соответствующей дозы и эффективности рибавирина для лечения лекарственно-устойчивой или лекарственно-резистентной вирулентной вирулентной инфекции гриппа.
Метапневмовирус человека возник как распространенный вирусный патоген дыхательных путей, связанный с субклиническим или легким заболеванием. Иногда было показано, что у пациентов с Т-клеточными иммунными дефектами hMPV вызывает диссеминированное смертельное заболевание [149].У пациентов с трансплантацией стволовых клеток или твердых органов эти инфекции, даже при ограниченном течении легочного заболевания, представляют опасность для жизни и повышают риск поствирусной инвазивной грибковой пневмонии [150]. Внутривенный рибавирин считается лучшим доступным лечением этих серьезных диссеминированных или легочных инфекций hMPV, что отражает противовирусный эффект препарата и возможные лекарственные иммуномодулирующие свойства, которые могут еще больше повысить клиренс вируса и помочь в разрешении инфекции, особенно при ослабленном иммунитете. хост [151].
У пациентов с непереносимостью внутривенного рибавирина из-за гемолитической анемии и других серьезных осложнений с некоторым успехом применялось аэрозольное лечение легочного hMPV [152]. Точно так же при лечении пневмотропного аденовируса человека аэрозольный рибавирин предпочтительнее внутривенного из-за высокой концентрации препарата, достигаемой в альвеолах, по сравнению с внутривенной терапией рибавирином, которая может не приводить к цитотоксическим концентрациям в легочной ткани [153]. Однако это может быть не единственным определяющим фактором клинической эффективности терапии рибавирином, поскольку лекарственное усиление активности Т-хелперных Т-клеток Th2 требует дальнейшей оценки в клинических испытаниях [151].
6. Системы распыления
Критическим фактором для всех ингаляционных терапевтических средств являются характеристики системы доставки. Для всех терапий, обсуждаемых здесь, использовались жидкие аэрозоли, чаще всего генерируемые воздушно-струйными небулайзерами, хотя все чаще используются дополнительные технологии [156]. Воздухоструйный и ультразвуковой небулайзеры генерируют аэрозоль под высоким давлением и вибрацией пьезоэлектрического кристалла соответственно. Эти обычно используемые системы доставки обеспечивают адекватное отложение антимикробных препаратов в легких у амбулаторных пациентов, тогда как доставка лекарств ниже у пациентов в критическом состоянии, получающих вспомогательную вентиляцию легких [157,158].В новых электрических генераторах аэрозолей используется вибрирующая сетка или пластина с множеством отверстий, которые увеличивают отложение лекарства в легких в 2–3 раза и значительно повышают выход лекарства по сравнению с аэрозольными небулайзерами. Это следует учитывать для аэрозольной доставки лекарств у пациентов с пневмонией на ИВЛ [159].
Точно так же ингаляционная терапия цитокинами кажется привлекательной для различных трудно поддающихся лечению микобактериальных инфекций, поражающих легкие, хотя доставка этих агентов к месту инфекции представляет собой сложную задачу.В стандартных небулайзерных системах, таких как Respirgard или Misty-neb, только 5–7% общей введенной дозы достигает легочной ткани [74, 160]. Эту трудность можно уменьшить, используя высокоэффективные воздушно-струйные или ультразвуковые небулайзеры или специализированные системы доставки с использованием генераторов электрического аэрозоля нового поколения для достижения терапевтических концентраций иммуномодулирующих цитокинов в месте легочной инфекции. Для получения дополнительной информации отсылаем читателя к недавним обзорным статьям [161].
7. Резюме
Легкие являются наиболее частым очагом серьезной инфекции из-за их большой площади поверхности, подверженной воздействию внешней среды, и минимальной барьерной защиты. Однако такая архитектура делает легкие доступными для местной терапии. Терапевтические аэрозоли включают аэрозоли, направленные на улучшение мукоцилиарного клиренса патогенов, стимуляцию врожденной устойчивости к микробной инфекции, цитокиновую стимуляцию иммунной функции и доставку антибиотиков. Эти терапевтические средства все еще находятся в зачаточном состоянии, но имеют большие перспективы.
8. Мнение экспертов
По нашему мнению, ингаляционные противомикробные препараты используются недостаточно, особенно у пациентов с трудноизлечимыми легочными инфекциями низкой остроты.
Использование ингаляционной антимикробной терапии стало важной частью лечения инфекции дыхательных путей, вызванной P. aeruginosa при муковисцидозе, и профилактики инвазивной грибковой инфекции у пациентов, перенесших трансплантацию сердца и легких.
В дальнейшем развитии этой области мы рекомендуем сделать акцент на изучении использования аэрозольного гипертонического солевого раствора для уменьшения вызываемых патогенами нарушений дыхательных путей у субъектов, инфицированных микробами с низкой вирулентностью, стимуляции врожденной резистентности для предотвращения пневмония у субъектов с ослабленным иммунитетом, использующих цитокины или синтетические аналоги PAMP, и больше возможностей для использования ингаляционных противомикробных препаратов.
Сноски
Заявление о заинтересованности
Это исследование было частично поддержано грантом CA16672 для поддержки онкологических центров от Национальных институтов здравоохранения.
Библиография
1. Доклад о состоянии здравоохранения в мире 2004 г. — Изменяющаяся история. Женева: Всемирная организация здравоохранения; 2004. [Google Scholar] 3. Джоос Л., Тамм М. Нарушение защиты легочного хозяина у хозяина с ослабленным иммунитетом: химиотерапия рака. Proc Am Thorac Soc. 2005. 2 (5): 445–8. [PubMed] [Google Scholar] 4. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 7. Трэвис С.М., Сингх П.К., валлийский MJ.Противомикробные пептиды и белки во врожденной защите поверхности дыхательных путей. Curr Opin Immunol. 2001. 13 (1): 89–95. [PubMed] [Google Scholar] 8. Flanders SACH, Saint S. Нозокомиальная пневмония: состояние науки. Am J Infect Control. 2006; (34): 84–93. [PubMed] [Google Scholar] 9. Ноулз М.Р., Буше Р.С. Очистка от слизи как основной врожденный защитный механизм дыхательных путей млекопитающих. J Clin Invest. 2002. 109 (5): 571–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 10. Ратьен Ф. Восстановление жидкости на поверхности дыхательных путей при муковисцидозе.N Engl J Med. 2006. 354 (3): 291–3. [PubMed] [Google Scholar] 11. Тарран Р., Дональдсон С., Буше Р. Обоснование применения гипертонической солевой терапии при муковисцидозе легких. Semin Respir Crit Care Med. 2007. 28 (3): 295–302. [PubMed] [Google Scholar] 12. Eng PA, Morton J, Douglass JA и др. Краткосрочная эффективность распыляемого ультразвуком гипертонического раствора при муковисцидозе. Педиатр Пульмонол. 1996. 21 (2): 77–83. [PubMed] [Google Scholar] 13. Робинсон М., Регнис Дж. А., Бейли Д. Л. и др. Влияние гипертонического раствора, амилорида и кашля на мукоцилиарный клиренс у пациентов с муковисцидозом.Am J Respir Crit Care Med. 1996. 153 (5): 1503–1509. [PubMed] [Google Scholar] 14. Суд Н., Беннетт В.Д., Земан К. и др. Повышение концентрации вдыхаемого физиологического раствора с амилоридом или без него: влияние на мукоцилиарный клиренс у нормальных субъектов. Am J Respir Crit Care Med. 2003. 167 (2): 158–63. [PubMed] [Google Scholar] 15. Wark PA, McDonald V. Распыленный гипертонический раствор для лечения муковисцидоза. Кокрановская база данных Syst Rev.2003; (1): CD001506. [PubMed] [Google Scholar] 16. Дональдсон С.Х., Беннетт В.Д., Земан К.Л. и др. Очистка слизи и функция легких при муковисцидозе с применением гипертонического раствора.N Engl J Med. 2006. 354 (3): 241–50. [PubMed] [Google Scholar] 17. Элкинс М.Р., Робинсон М., Роуз Б.Р. и др. Контролируемое испытание длительного применения ингаляционного гипертонического раствора у пациентов с муковисцидозом. N Engl J Med. 2006. 354 (3): 229–40. [PubMed] [Google Scholar] 18. Керем Э., Бистрицер Т., Ханукоглу А. и др. Дисфункция легочного эпителия натриевых каналов и избыток жидкости в дыхательных путях при псевдогипоальдостеронизме. N Engl J Med. 1999. 341 (3): 156–62. [PubMed] [Google Scholar] 19. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 21. Буше RC. Обезвоживание поверхности дыхательных путей при муковисцидозе: патогенез и терапия. Annu Rev Med. 2007. 58: 157–70. [PubMed] [Google Scholar] 22. Эванс С.М., Уильямс О.В., Тувим М.Дж. и др. Муцин продуцируется clara-клетками проксимальных дыхательных путей мышей, зараженных антигеном. Am J Respir Cell Mol Biol. 2004. 31 (4): 382–94. [PubMed] [Google Scholar] 23. Уильямс О.В., Шарафхане А., Ким В. и др.Слизь в дыхательных путях: от производства до секрета. Am J Respir Cell Mol Biol. 2006. 34 (5): 527–36. [Бесплатная статья PMC] [PubMed] [Google Scholar] 24. Акинби Х.Т., Эпод Р., Бхатт Х. и др. Уничтожение бактерий усиливается экспрессией лизоцима в легких трансгенных мышей. J Immunol. 2000. 165 (10): 5760–6. [PubMed] [Google Scholar] 25. Bals R, Weiner DJ, Moscioni AD, et al. Усиление врожденной защиты хозяина за счет экспрессии антимикробного пептида кателицидина. Заражение иммунной. 1999. 67 (11): 6084–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 26.Коул А.М., Ляо Х.И., Стучлик О. и др. Катионные полипептиды необходимы для антибактериальной активности жидкости дыхательных путей человека. J Immunol. 2002. 169 (12): 6985–91. [PubMed] [Google Scholar] 27. Коул AM, Thapa DR, Gabayan V и др. Снижение клиренса Pseudomonas aeruginosa из дыхательных путей мышей с дефицитом лизоцима M. J Leukoc Biol. 2005. 78 (5): 1081–5. [PubMed] [Google Scholar] 28. Moser C, Weiner DJ, Lysenko E, et al. бета-дефенсин 1 способствует развитию врожденного иммунитета легких у мышей. Заражение иммунной. 2002. 70 (6): 3068–72.[Бесплатная статья PMC] [PubMed] [Google Scholar] 29. Эванс С.Е., Хан П.Й., Макканн Ф. и др. Бета-глюканы клеточной стенки Pneumocystis стимулируют генерацию хемокинов альвеолярными эпителиальными клетками через механизмы, зависящие от ядерного фактора, каппаB. Am J Respir Cell Mol Biol. 2005. 32 (6): 490–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 30. Агусти С., Рано А., Ровира М. и др. Воспалительный ответ, связанный с легочными осложнениями у пациентов с иммунодефицитом, не связанным с ВИЧ. Грудная клетка. 2004. 59 (12): 1081–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 31.Бартон Г.М., Меджитов Р. Сигнальные пути толл-подобных рецепторов. Наука. 2003. 300 (5625): 1524–15. [PubMed] [Google Scholar] 32. Болдрик Дж. К., Ализаде А. А., Дин М. и др. Стереотипные и специфические программы экспрессии генов в врожденных иммунных реакциях человека на бактерии. Proc Natl Acad Sci USA. 2002. 99 (2): 972–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 33. Капетанович Р., Кавайон Дж. М.. Ранние события врожденного иммунитета при распознавании микробных патогенов. Экспертное мнение Biol Ther. 2007. 7 (6): 907–18. [PubMed] [Google Scholar] 34.Каваи Т., Акира С. Сигнализация TLR. Смерть клетки отличается. 2006. 13 (5): 816–25. [PubMed] [Google Scholar] 35. Копп Э., Меджитов Р. Распознавание микробной инфекции по Toll-подобным рецепторам. Curr Opin Immunol. 2003. 15 (4): 396–401. [PubMed] [Google Scholar] 36. Чжан Г., Гош С. Активация NF-kappaB, опосредованная Toll-подобным рецептором: филогенетически консервативная парадигма врожденного иммунитета. J Clin Invest. 2001; 107 (1): 13–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 37. Улевич Р.Ю. Терапия, направленная на врожденную иммунную систему.Nat Rev Immunol. 2004. 4 (7): 512–20. [PubMed] [Google Scholar] 38. Аревало И., Туллиано Дж., Киспе А. и др. Роль имиквимода и парентерального антимониата меглумина в начальном лечении кожного лейшманиоза. Clin Infect Dis. 2007. 44 (12): 1549–54. [PubMed] [Google Scholar] 39. Канистанон Д., Хаджар А.М., Пеллетье М.Р. и др. Мутант Francisella по углеводной модификации липида А вызывает защитный иммунитет. PLoS Pathog. 2008; 4 (2): e24. [Бесплатная статья PMC] [PubMed] [Google Scholar] 40. Лембо А., Пеллетье М., Айер Р. и др.Введение синтетического агониста TLR4 защищает мышей от легочной туляремии. J Immunol. 2008. 180 (11): 7574–81. [Бесплатная статья PMC] [PubMed] [Google Scholar] 41. Лурманн А., Дейтерс Ю., Скокова Дж. И др. Эффекты in vivo синтетического 2-килодальтонного активирующего макрофаги липопептида Mycoplasma fermentans после легочного применения. Заражение иммунной. 2002. 70 (7): 3785–92. [Бесплатная статья PMC] [PubMed] [Google Scholar] 42. МакХатчисон Дж. Г., Бэкон Б. Р., Гордон С. К. и др. Фаза 1B, рандомизированное двойное слепое исследование с увеличением дозы CPG 10101 у пациентов с хроническим вирусом гепатита С.Гепатология. 2007. 46 (5): 1341–9. [PubMed] [Google Scholar] 43. Raberg L, Sim D, Read AF. Распутывание генетической изменчивости для устойчивости и толерантности к инфекционным заболеваниям у животных. Наука. 2007. 318 (5851): 812–4. [PubMed] [Google Scholar] 44. Уильямс Т.Н., Мванги Т.В., Вамбуа С. и др. Отрицательный эпистаз между защитным действием от малярии альфа + -талассемии и серповидно-клеточной характеристикой. Нат Жене. 2005. 37 (11): 1253–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 45. Эванс С.Е., Скотт Б.Л., Клемент К.Г. и др.Стимулированная врожденная резистентность эпителия легких защищает мышей от бактерий и грибков. Am J Respir Cell Mol Biol. 2009 27 марта; [Epub перед печатью] [Бесплатная статья PMC] [PubMed] [Google Scholar] 46. Деннис Д.Т., Инглсби Т.В., Хендерсон Д.А. и др. Туляремия как биологическое оружие: управление медициной и общественным здравоохранением. ДЖАМА. 2001. 285 (21): 2763–73. [PubMed] [Google Scholar] 47. Хиллеман MR. Обзор: причины и профилактика в биологической войне и биотерроризме. Вакцина. 2002. 20 (25–26): 3055–67. [PubMed] [Google Scholar] 48.Уэйн Конлан Дж., Шен Х., Куоли Р. и др. Аэрозольная, но не внутрикожная иммунизация живым вакцинным штаммом Francisella tularensis защищает мышей от последующего аэрозольного заражения высоковирулентным штаммом патогена типа А посредством механизма, зависимого от Т-лимфоцитов и гамма-интерферона. Вакцина. 2005. 23 (19): 2477–85. [PubMed] [Google Scholar] 50. Тувим М.Дж., Эванс С.Е., Клемент К.Г. и др. Усиленное воспаление легких защищает от пневмонии гриппа А. PLoS ONE. 2009; 4 (1): e4176.[Бесплатная статья PMC] [PubMed] [Google Scholar] 51. Клемент К.Г., Эванс С.Е., Эванс С.М. и др. Стимуляция врожденного иммунитета легких защищает мышей от летальной пневмококковой пневмонии. Am J Respir Crit Care Med. 2008. 177 (12): 1322–30. [Бесплатная статья PMC] [PubMed] [Google Scholar] 52. Могхаддам С.Дж., Клемент К.Г., Де ла Гарза М.М. и др. Лизат Haemophilus influenzae индуцирует аспекты фенотипа хронической обструктивной болезни легких. Am J Respir Cell Mol Biol. 2008. 38 (6): 629–38. [Бесплатная статья PMC] [PubMed] [Google Scholar] 53.Brandl K, Plitas G, Mihu CN и др. Устойчивые к ванкомицину энтерококки используют вызванный антибиотиками врожденный иммунный дефицит. Природа. 2008. 455 (7214): 804–7. [Бесплатная статья PMC] [PubMed] [Google Scholar] 54. Hoogerwerf JJ, de Vos AF, Bresser P, et al. Воспаление легких, вызванное липотейхоевой кислотой или липополисахаридом у человека. Am J Respir Crit Care Med. 2008. 178 (1): 34–41. [PubMed] [Google Scholar] 55. Реппе К., Черниг Т., Лурманн А. и др. Иммуностимуляция липопептидом-2, активирующим макрофаги, увеличивала выживаемость при пневмонии мышей.Am J Respir Cell Mol Biol. 2009. 40 (4): 474–81. [PubMed] [Google Scholar] 56. Багчи А., Херруп Э.А., Уоррен Х.С. и др. MyD88-зависимый и MyD88-независимый пути синергизма, прайминга и толерантности между агонистами TLR. J Immunol. 2007. 178 (2): 1164–71. [PubMed] [Google Scholar] 57. Trinchieri G, Sher A. Сотрудничество сигналов Toll-подобных рецепторов во врожденной иммунной защите. Nat Rev Immunol. 2007. 7 (3): 179–90. [PubMed] [Google Scholar] 58. Меджитов Р. Распознавание микроорганизмов и активация иммунного ответа.Природа. 2007. 449 (7164): 819–26. [PubMed] [Google Scholar] 59. Foster SL, Hargreaves DC, Medzhitov R. Ген-специфический контроль воспаления с помощью TLR-индуцированных модификаций хроматина. Природа. 2007. 447 (7147): 972–8. [PubMed] [Google Scholar] 60. Тазава Р., Хамано Э., Араи Т. и др. Гранулоцитарно-макрофагальный колониестимулирующий фактор и легочный иммунитет при легочном альвеолярном протеинозе. Am J Respir Crit Care Med. 2005. 171 (10): 1142–9. [PubMed] [Google Scholar] 61. Андерсон П.М., Маркович С.Н., Слоан Дж. А. и др. Аэрозольный гранулоцитарный макрофаг-колониестимулирующий фактор: низкая токсичность, легочная биологическая терапия у пациентов с метастазами в легких.Clin Cancer Res. 1999. 5 (9): 2316–23. [PubMed] [Google Scholar] 62. Trapnell BC, Whitsett JA, Nakata K. Легочный альвеолярный протеиноз. N Engl J Med. 2003. 349 (26): 2527–39. [PubMed] [Google Scholar] 63. Киннула В., Маттсон К., Кантелл К. Фармакокинетика и токсичность вдыхаемого человеческого интерферона-альфа у пациентов с раком легких. J Interferon Res. 1989. 9 (4): 419–23. [PubMed] [Google Scholar] 64. Маасилта П., Халме М., Маттсон К. и др. Фармакокинетика ингаляционного рекомбинантного и природного альфа-интерферона. Ланцет.1991; 337 (8737): 371. [PubMed] [Google Scholar] 65. Киннула В., Кантелл К., Маттсон К. Эффект вдыхаемого природного интерферона-альфа на диффузную бронхоальвеолярную карциному. Eur J Cancer. 1990; 26 (6): 740–1. [PubMed] [Google Scholar] 66. Маасилта П., Холсти Л. Р., Халме М. и др. Природный альфа-интерферон в сочетании с гиперфракционированной лучевой терапией при лечении немелкоклеточного рака легкого. Int J Radiat Oncol Biol Phys. 1992. 23 (4): 863–8. [PubMed] [Google Scholar] 67. Giosue S, Casarini M, Alemanno L и др.Эффекты аэрозольного интерферона-альфа у больных туберкулезом легких. Am J Respir Crit Care Med. 1998. 158 (4): 1156–62. [PubMed] [Google Scholar] 68. Giosue S, Casarini M, Ameglio F и др. Аэрозольное лечение интерфероном-альфа у пациентов с туберкулезом легких с множественной лекарственной устойчивостью. Eur Cytokine Netw. 2000. 11 (1): 99–104. [PubMed] [Google Scholar] 69. Мартин Р. Дж., Богуневич М., Хенсон Дж. Э. и др. Воздействие вдыхаемого гамма-интерферона на нормальные дыхательные пути человека. Am Rev Respir Dis. 1993; 148 (6 Pt 1): 1677–82.[PubMed] [Google Scholar] 70. Богуневич М., Мартин Р.Дж., Мартин Д. и др. Эффекты распыленного рекомбинантного гамма-интерферона на астматические дыхательные пути. J Allergy Clin Immunol. 1995. 95 (1 Pt 1): 133–5. [PubMed] [Google Scholar] 71. Кондо Р., Раджу Б., Канова А. и др. Рекомбинантный гамма-интерферон стимулирует передачу сигнала и экспрессию генов в альвеолярных макрофагах in vitro и у больных туберкулезом. Заражение иммунной. 2003. 71 (4): 2058–64. [Бесплатная статья PMC] [PubMed] [Google Scholar] 72. Раджу Б., Хосино Ю., Кувабара К. и др.Аэрозольный гамма-интерферон (IFN-гамма) индуцирует экспрессию генов, кодирующих IFN-гамма-индуцибельный белок 10 килодальтон, но не индуцибельную синтазу оксида азота в легких во время туберкулеза. Заражение иммунной. 2004. 72 (3): 1275–83. [Бесплатная статья PMC] [PubMed] [Google Scholar] 73. Кондо R, Rom WN, Schluger NW. Лечение туберкулеза легких с множественной лекарственной устойчивостью с помощью аэрозольного гамма-интерферона. Ланцет. 1997. 349 (9064): 1513–5. [PubMed] [Google Scholar] 74. Condos R, Hull FP, Schluger NW и др.Региональное отложение аэрозольного гамма-интерферона при туберкулезе легких. Грудь. 2004. 125 (6): 2146–55. [PubMed] [Google Scholar] 75. Moss RB, Mayer-Hamblett N, Wagener J, et al. Рандомизированное двойное слепое плацебо-контролируемое исследование с увеличением дозы аэрозольного гамма-1b интерферона у пациентов с кистозным фиброзом легких легкой и средней степени тяжести. Педиатр Пульмонол. 2005. 39 (3): 209–18. [PubMed] [Google Scholar] 76. Накос Г., Маламу-Мици В.Д., Лачана А. и др. Иммунопаралич у больных с тяжелой травмой и действие ингаляционного гамма-интерферона.Crit Care Med. 2002. 30 (7): 1488–94. [PubMed] [Google Scholar] 77. Вирголини I, Куртаран А., Леймер М. и др. Ингаляционная сцинтиграфия с меченным йодом-123 интерфероном гамма-1b: исследование легочного отложения и повышения дозы у здоровых добровольцев. J Nucl Med. 1997. 38 (9): 1475–81. [PubMed] [Google Scholar] 78. Рао Р.Д., Андерсон П.М., Арндт К.А. и др. Терапия аэрозольным гранулоцитарным макрофагальным колониестимулирующим фактором (GM-CSF) при метастатическом раке. Am J Clin Oncol. 2003. 26 (5): 493–8. [PubMed] [Google Scholar] 79.Нивен Р.В., Уиткомб К.Л., Шенер Л. и др. Легочная абсорбция аэрозольного и интратрахеально инстиллированного rhG-CSF и моноПЕГилированного rhG-CSF. Pharm Res. 1995. 12 (9): 1343–9. [PubMed] [Google Scholar] 80. Мачида М., Хаяси М., Авазу С. Абсорбция в легких рекомбинантного человеческого гранулоцитарного колониестимулирующего фактора (rhG-CSF) после интратрахеального введения крысам. Биол Фарм Булл. 1996. 19 (2): 259–62. [PubMed] [Google Scholar] 81. Gatmaitan BG, Carruthers MM, Lerner AM. Гентамицин в лечении первичных грамотрицательных пневмоний.Am J Med Sci. 1970. 260 (2): 90–4. [PubMed] [Google Scholar] 83. Klastersky J, Geuning C, Mouawad E, et al. Эндотрахеальный гентамицин при бронхиальных инфекциях у пациентов с трахеостомией. Грудь. 1972: 61 (2): 117–20. [PubMed] [Google Scholar] 85. Odio W, Van Laer E, Klastersky J. Концентрации гентамицина в бронхиальном секрете после внутримышечного и эндотрахеального введения. J Clin Pharmacol. 1975. 15 (7): 518–24. [PubMed] [Google Scholar] 86. Панидис Д., Маркантонис С.Л., Бутзука Э. и др. Проникновение гентамицина в жидкость выстилки альвеол у пациентов в критическом состоянии с вентилятор-ассоциированной пневмонией.Грудь. 2005. 128 (2): 545–52. [PubMed] [Google Scholar] 87. Каркас А.Дж., Гарсия-Сатуе Д.Л., Сапатер П. и др. Проникновение тобрамицина в эпителиальную выстилочную жидкость пациентов с пневмонией. Clin Pharmacol Ther. 1999. 65 (3): 245–50. [PubMed] [Google Scholar] 88. Valcke YJ, Vogelaers DP, Colardyn FA и др. Проникновение нетилмицина в нижние дыхательные пути после приема один раз в сутки. Грудь. 1992. 101 (4): 1028–32. [PubMed] [Google Scholar] 89. Брауде А.С., Хорнштейн А., Кляйн М. и др. Распределение тобрамицина в легких.Am Rev Respir Dis. 1983; 127 (5): 563–5. [PubMed] [Google Scholar] 90. Kuhn RJ. Фармацевтические соображения при аэрозольной доставке лекарств. Фармакотерапия. 2002; 22 (3 Pt 2): 80S – 5S. [PubMed] [Google Scholar] 91. Goldstein I, Wallet F, Nicolas-Robin A, et al. Отложение в легких и эффективность распыленного амикацина при пневмонии, вызванной Escherichia coli, у вентилируемых поросят. Am J Respir Crit Care Med. 2002. 166 (10): 1375–81. [PubMed] [Google Scholar] 92. Гольдштейн I, Кошелек F, Роберт Дж. И др. Концентрация распыленного амикацина в легочной ткани во время искусственной вентиляции легких у поросят со здоровыми легкими.Am J Respir Crit Care Med. 2002. 165 (2): 171–5. [PubMed] [Google Scholar] 93. Klastersky J, Carpentier-Meunier F, Kahan-Coppens L, et al. Антибиотики при грамотрицательной бронхопневмонии назначаются эндотрахеально. Грудь. 1979; 75 (5): 586–91. [PubMed] [Google Scholar] 94. Флюм П, Клепсер МЭ. Обоснование использования антибиотиков в аэрозольной форме. Фармакотерапия. 2002; 22 (3 Pt 2): 71S – 9S. [PubMed] [Google Scholar] 95. Мур RD, Литман PS, Смит CR. Клинический ответ на терапию аминогликозидами: важность отношения максимальной концентрации к минимальной ингибирующей концентрации.J Infect Dis. 1987. 155 (1): 93–9. [PubMed] [Google Scholar] 96. Мур RD, Смит CR, Литман PS. Связь уровней аминогликозидов в плазме со смертностью у пациентов с грамотрицательной бактериемией. J Infect Dis. 1984. 149 (3): 443–8. [PubMed] [Google Scholar] 97. Schentag JJ. Корреляция фармакокинетических параметров с эффективностью антибиотиков: взаимосвязь между концентрациями в сыворотке, значениями МИК и бактериальной эрадикацией у пациентов с грамотрицательной пневмонией. Scand J Infect Dis Suppl. 1990; 74: 218–34.[PubMed] [Google Scholar] 98. Дезил-Эванс Л.М., Мерфи Дж. Э., Джоб М.Л. Корреляция фармакокинетических показателей с терапевтическим исходом у пациентов, получающих аминогликозиды. Clin Pharm. 1986. 5 (4): 319–24. [PubMed] [Google Scholar] 99. Коллинз Т., Гердинг Д.Н. Аминогликозиды в сравнении с бета-лактамами при грамотрицательной пневмонии. Semin Respir Infect. 1991. 6 (3): 136–46. [PubMed] [Google Scholar] 100. Бернс Дж. Л., Ван Дальфсен Дж. М., Шавар Р. М. и др. Влияние хронического периодического введения ингаляционного тобрамицина на респираторную микробную флору у пациентов с муковисцидозом.J Infect Dis. 1999. 179 (5): 1190–6. [PubMed] [Google Scholar] 101. Valcke Y, Pauwels R, Van der Straeten M. Проникновение аминогликозидов в жидкость выстилки альвеол крыс. Эффект воспаления дыхательных путей. Am Rev Respir Dis. 1990. 142 (5): 1099–103. [PubMed] [Google Scholar] 102. Меерс П., Невилл М., Малинин В. и др. Проникновение биопленки, запускаемое высвобождение и активность ингаляционного липосомального амикацина in vivo при хронических инфекциях легких, вызванных Pseudomonas aeruginosa. J Antimicrob Chemother. 2008. 61 (4): 859–68.[PubMed] [Google Scholar] 103. Дэвис К.К., Као П.Н., Якобс С.С. и др. Аэрозольный амикацин для лечения легочных инфекций Mycobacterium avium: серия наблюдательных случаев. BMC Pulm Med. 2007; 7: 2. [Бесплатная статья PMC] [PubMed] [Google Scholar] 104. Макколл С.Ю., Спруилл В.Дж., Уэйд В.Е. Применение тобрамицина в аэрозольной форме при лечении резистентного псевдомонадного пневмонита. Ther Drug Monit. 1989. 11 (6): 692–5. [PubMed] [Google Scholar] 105. Допфер Р., Брэнд П, Маллингер Б. и др. Ингаляция тобрамицина у больных муковисцидозом: сравнение двух методов.J. Physiol Pharmacol. 2007; 58 (Дополнение 5) (Pt 1): 141–54. [PubMed] [Google Scholar] 106. Ленуар Г., Антипкин Ю.Г., Миано А. и др. Эффективность, безопасность и местная фармакокинетика высококонцентрированного распыленного тобрамицина у пациентов с муковисцидозом, колонизированными синегнойной палочкой. Педиатрические препараты. 2007; 9 (Дополнение 1): 11–20. [PubMed] [Google Scholar] 107. Рэмси Б.В., Доркин Х.Л., Айзенберг Д.Д. и др. Эффективность аэрозольного тобрамицина у пациентов с муковисцидозом. N Engl J Med. 1993. 328 (24): 1740–6. [PubMed] [Google Scholar] 109.Кантон Р., Кобос Н., де Грасиа Дж. И др. Антимикробная терапия легочной патогенной колонизации и инфекции Pseudomonas aeruginosa у пациентов с муковисцидозом. Clin Microbiol Infect. 2005. 11 (9): 690–703. [PubMed] [Google Scholar] 110. Sexauer WP, Fiel SB. Аэрозольные антибиотики при муковисцидозе. Semin Respir Crit Care Med. 2003. 24 (6): 717–26. [PubMed] [Google Scholar] 111. Кун П., Ландау Л.И., Фелан П.Д. Распыленный гентамицин у детей и подростков с муковисцидозом. Aust Paediatr J.1984. 20 (1): 43–5. [PubMed] [Google Scholar] 112. Уолл М.А., Терри А.Б., Айзенберг Дж. И др. Ингаляционные антибиотики при муковисцидозе. Ланцет. 1983; 1 (8337): 1325. [PubMed] [Google Scholar] 113. Стейнкамп Г., Туммлер Б., Гаппа М. и др. Длительная аэрозольная терапия тобрамицином при муковисцидозе. Педиатр Пульмонол. 1989. 6 (2): 91–8. [PubMed] [Google Scholar] 114. Смит А.Л., Рэмси Б.В., Хеджес Д.Л. и др. Безопасность применения аэрозольного тобрамицина в течение 3 месяцев пациентам с муковисцидозом. Педиатр Пульмонол. 1989. 7 (4): 265–71.[PubMed] [Google Scholar] 115. Рэмси Б.В., Пепе М.С., Куан Дж. М. и др. Периодическое введение ингаляционного тобрамицина пациентам с муковисцидозом. Группа по изучению муковисцидоза, вдыхаемого тобрамицином. N Engl J Med. 1999. 340 (1): 23–30. [PubMed] [Google Scholar] 116. Мох РБ. Долгосрочные преимущества ингаляционного тобрамицина у подростков с муковисцидозом. Грудь. 2002. 121 (1): 55–63. [PubMed] [Google Scholar] 117. Стивенс Д., Гэри Н., Айлз А. и др. Эффективность ингаляционного тобрамицина при лечении обострений легких у детей с муковисцидозом.Pediatr Infect Dis. 1983; 2 (3): 209–11. [PubMed] [Google Scholar] 118. Schaad UB, Wedgwood-Krucko J, Suter S и др. Эффективность ингаляционного амикацина в качестве дополнения к внутривенной комбинированной терапии (цефтазидим и амикацин) при муковисцидозе. J Pediatr. 1987. 111 (4): 599–605. [PubMed] [Google Scholar] 119. Билтон Д., Хениг Н., Моррисси Б. и др. Добавление ингаляционного тобрамицина к ципрофлоксацину при обострении инфекции Pseudomonas aeruginosa при бронхоэктазах у взрослых. Грудь. 2006. 130 (5): 1503–10. [PubMed] [Google Scholar] 121.Рубин Б.К. Аэрозольные антибиотики для лечения бронхоэктазов без кистозного фиброза. J Aerosol Med Pulm Drug Deliv. 2008. 21 (1): 71–6. [PubMed] [Google Scholar] 122. Drobnic ME, Sune P, Montoro JB и др. Ингаляция тобрамицина пациентам с не кистозным фиброзом, бронхоэктазами и хронической бронхиальной инфекцией, вызванной синегнойной палочкой. Энн Фармакотер. 2005. 39 (1): 39–44. [PubMed] [Google Scholar] 123. Баркер А.Ф., Коуч Л., Фил С.Б. и др. Раствор тобрамицина для ингаляций снижает плотность мокроты синегнойной палочки при бронхоэктазах.Am J Respir Crit Care Med. 2000. 162 (2 Pt 1): 481–5. [PubMed] [Google Scholar] 124. Шейнберг П., Шор Э. Пилотное исследование безопасности и эффективности раствора тобрамицина для ингаляции у пациентов с тяжелыми бронхоэктазами. Грудь. 2005. 127 (4): 1420–146. [PubMed] [Google Scholar] 125. Додек П., Кинан С., Кук Д. и др. Основанное на фактических данных клиническое руководство по профилактике вентилятор-ассоциированной пневмонии. Ann Intern Med. 2004. 141 (4): 305–13. [PubMed] [Google Scholar] 126. Falagas ME, Siempos II, Bliziotis IA, et al.Введение антибиотиков через дыхательные пути для профилактики пневмонии, приобретенной в ОИТ: метаанализ сравнительных исследований. Crit Care. 2006; 10 (4): R123. [Бесплатная статья PMC] [PubMed] [Google Scholar] 127. Ратгебер Дж., Зильманн С., Панцер С. и др. Профилактика пневмонии путем эндотрахеальной микронебулизации тобрамицина. Анастезиол Интенсивмед Нефалмед Шмерцтер. 1993. 28 (1): 23–9. [PubMed] [Google Scholar] 128. Klastersky J, Huysmans E, Weerts D, et al. Эндотрахеально вводимый гентамицин для профилактики инфекций дыхательных путей у пациентов с трахеостомией: двойное слепое исследование.Грудь. 1974. 65 (6): 650–4. [PubMed] [Google Scholar] 129. Таблан О.К., Андерсон Л.Дж., Бессер Р. и др. Руководство по профилактике пневмонии, связанной с оказанием медицинской помощи, 2003 г .: рекомендации CDC и Консультативного комитета по практике инфекционного контроля в здравоохранении. MMWR Recomm Rep. 2004; 53 (RR-3): 1–36. [PubMed] [Google Scholar] 130. Falagas ME, Agrafiotis M, Athanassa Z и др. Введение антибиотиков через дыхательные пути в качестве монотерапии пневмонии. Эксперт Rev Anti Infect Ther. 2008. 6 (4): 447–52. [PubMed] [Google Scholar] 131.Ghannam DE, Rodriguez GH, Raad II и др. Ингаляционные аминогликозиды у онкологических больных с связанной с вентилятором грамотрицательной бактериальной пневмонией: безопасность и осуществимость в эпоху роста лекарственной устойчивости. Eur J Clin Microbiol Infect Dis. 2009. 28 (3): 253–9. [PubMed] [Google Scholar] 132. Палмер Л. Б., Смолдон Г. К., Чен Дж. Дж. И др. Аэрозольные антибиотики и трахеобронхит, связанный с вентилятором, в отделении интенсивной терапии. Crit Care Med. 2008; 36 (7): 2008–13. [PubMed] [Google Scholar] 133. Морозини М.И., Гарсия-Кастильо М., Лоза Э. и др.Контрольные точки для прогнозирования чувствительности Pseudomonas aeruginosa к вдыхаемому тобрамицину у пациентов с муковисцидозом: использование тест-полосок Etest с высоким диапазоном значений. J Clin Microbiol. 2005. 43 (9): 4480–5. [Бесплатная статья PMC] [PubMed] [Google Scholar] 134. Линден П.К., Патерсон Д.Л. Парентеральный и ингаляционный колистин для лечения вентилятор-ассоциированной пневмонии. Clin Infect Dis. 2006; 43 (Дополнение 2): S89 – S4. [PubMed] [Google Scholar] 135. Михалопулос А., Фотакис Д., Вирцили С. и др. Колистин в аэрозольной форме в качестве дополнительного лечения респираторно-ассоциированной пневмонии, вызванной грамотрицательными бактериями с множественной лекарственной устойчивостью: проспективное исследование.Respir Med. 2008. 102 (3): 407–12. [PubMed] [Google Scholar] 136. Kwa AL, Loh C, Low JG и др. Распыленный колистин в лечении пневмонии, вызванной множественной лекарственной устойчивостью Acinetobacter baumannii и Pseudomonas aeruginosa. Clin Infect Dis. 2005. 41 (5): 754–7. [PubMed] [Google Scholar] 137. Берлана Д., Ллоп Дж. М., Форт Е. и др. Использование колистина для лечения грамотрицательных инфекций с множественной лекарственной устойчивостью. Am J Health Syst Pharm. 2005. 62 (1): 39–47. [PubMed] [Google Scholar] 138. Hamer DH. Лечение внутрибольничной пневмонии и трахеобронхита, вызванных синегнойной палочкой с множественной лекарственной устойчивостью, колистином в аэрозольной форме.Am J Respir Crit Care Med. 2000. 162 (1): 328–30. [PubMed] [Google Scholar] 139. Маккой К.С., Квиттнер А.Л., Оерманн С.М. и др. Азтреонам лизин вдыхается при хронической болезни дыхательных путей Pseudomonas aeruginosa при муковисцидозе. Am J Respir Crit Care Med. 2008. 178 (9): 921–8. [Бесплатная статья PMC] [PubMed] [Google Scholar] 140. Сафдар А. Стратегии усиления иммунной функции у реципиентов гемопоэтической трансплантации, у которых есть грибковые инфекции. Пересадка костного мозга. 2006. 38 (5): 327–37. [PubMed] [Google Scholar] 141. Сафдар А.Трудности с грибковыми инфекциями у пациентов с острым миелогенным лейкозом: стратегии повышения иммунитета. Онколог. 2007; 12 (Дополнение 2): 2–6. [PubMed] [Google Scholar] 142. Safdar ARG, Lichtiger B, Dickey BF и др. Повышение иммунитета рекомбинантным интерфероном гамма 1b у 20 пациентов с гематологическими злокачественными новообразованиями и системными оппортунистическими инфекциями, получавших переливания донорских гранулоцитов. Рак. 2006. 106 (12): 2664–71. [PubMed] [Google Scholar] 143. Монтойя Дж. Г., Чапарро С. В., Селис Д. и др. Инвазивный аспергиллез на фоне трансплантации сердца.Clin Infect Dis. 2003; 37 (Приложение 3): S281–92. [PubMed] [Google Scholar] 144. Гарсия-Видаль CUA, Кирби К.А., Марр К.А. Эпидемиология инвазивных инфекций плесени у реципиентов аллогенных стволовых клеток: биологические факторы риска инфекции в зависимости от времени после трансплантации. Clin Infect Dis. 2008. 47 (8): 1041–50. [Бесплатная статья PMC] [PubMed] [Google Scholar] 145. Маттиуцци Г.Н., Кантарджиан Х., Фадерл С. и др. Липидный комплекс амфотерицина B как профилактика инвазивных грибковых инфекций у пациентов с острым миелогенным лейкозом и миелодиспластическим синдромом, проходящих индукционную химиотерапию.Рак. 2004. 100 (3): 581–9. [PubMed] [Google Scholar] 146. Сингх Н., Лимай А.П., Форрест Г. и др. Поздний инвазивный аспергиллез у реципиентов трансплантата в современную эпоху. Med Mycol. 2006. 44 (5): 445–9. [PubMed] [Google Scholar] 147. Schmitt HJ, Bernard EM, Hauser M, et al. Аэрозольный амфотерицин B эффективен для профилактики и лечения крысиной модели легочного аспергиллеза. Антимикробные агенты Chemother. 1988. 32 (11): 1676–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 148. Cicogna CE, White MH, Bernard EM и др.Эффективность профилактического аэрозольного липидного комплекса амфотерицина B на модели легочного аспергиллеза на крысах. Антимикробные агенты Chemother. 1997. 41 (2): 259–61. [Бесплатная статья PMC] [PubMed] [Google Scholar] 149. Коидзуми Т., Кубо К., Канеки Т. и др. Фармакокинетическая оценка амфотерицина B в легочной ткани: распределение легочной лимфы после внутривенной инъекции и распределение воздушного пространства после аэрозолизации и ингаляции амфотерицина B. Противомикробные агенты Chemother. 1998. 42 (7): 1597–600. [Бесплатная статья PMC] [PubMed] [Google Scholar] 150.Коркоран Т.Е., Венкатараманан Р., Михельц К.М. и др. Аэрозольное отложение липидного комплекса амфотерицин-B (Abelcet) у реципиентов трансплантата легких. Am J Transplant. 2006. 6 (11): 2765–73. [PubMed] [Google Scholar] 151. Дрю Р.Х., Доддс Эшли Э., Бенджамин Д.К., мл. И др. Сравнительная безопасность липидного комплекса амфотерицина B и дезоксихолата амфотерицина B в качестве противогрибковой профилактики в виде аэрозоля у реципиентов трансплантата легких. Трансплантация. 2004. 77 (2): 232–7. [PubMed] [Google Scholar] 152. Монтойя Дж. Г., Хиральдо Л. Ф., Эфрон Б. и др.Инфекционные осложнения у 620 последовательных пациентов после трансплантации сердца в медицинском центре Стэнфордского университета. Clin Infect Dis. 2001. 33 (5): 629–40. [PubMed] [Google Scholar] 153. Палмер С.М., Дрю Р.Х., Уайтхаус Дж. Д. и др. Безопасность липидного комплекса амфотерицина B в аэрозольной форме у реципиентов трансплантата легких. Трансплантация. 2001. 72 (3): 545–8. [PubMed] [Google Scholar] 154. Ботинки RJ, Патерсон Д.Л., Олворт А.М. и др. Успешное лечение постгриппозного псевдомембранозного некротизирующего аспергиллеза бронхов липосомальным амфотерицином, ингаляционным амфотерицином B, гамма-интерфероном и GM-CSF.Грудная клетка. 1999. 54 (11): 1047–9. [Бесплатная статья PMC] [PubMed] [Google Scholar] 155. Сафдар А., О’Брайен С., Кури И.Ф. Эффективность и возможность применения липидной комплексной терапии амфотерицина В в аэрозольной форме при легочном зигомикозе с прорывом каспофунгина. Пересадка костного мозга. 2004. 34 (5): 467–8. [PubMed] [Google Scholar] 156. Дханд Р., Гунтур В.П. Как лучше всего доставлять аэрозольные препараты пациентам, находящимся на ИВЛ. Clin Chest Med. 2008. 29 (2): 277–96. vi. [PubMed] [Google Scholar] 157. Макинтайр Н.Р., Сильвер Р.М., Миллер К.В. и др.Доставка аэрозоля интубированным пациентам на ИВЛ. Crit Care Med. 1985. 13 (2): 81–4. [PubMed] [Google Scholar] 158. Заявление о консенсусе по аэрозолям-1991. Американская ассоциация респираторной помощи. Respir Care. 1991. 36 (9): 916–21. [PubMed] [Google Scholar] 159. Дханд Р., Сохал Х. Система доставки лекарств в легкие для ингаляционной терапии у пациентов с механической вентиляцией легких. Эксперт Rev Med Devices. 2008; 5 (1): 9–18. [PubMed] [Google Scholar] 160. Blanchard JDCD и др. Отложение в легких интерферона гамма-1b после ингаляции через систему AERx vs.Небулайзер Respirgard II ™ . Am J Respir Crit Care Med. 2003; 167: A373. [Аннотация встречи] [Google Scholar] 161. Уоттс А.Б., МакКонвилл Дж. Т., Уильямс РО. Современные методы лечения и технологические достижения в области доставки лекарственных средств в виде водных аэрозолей. Препарат Дев Инд Фарм. 2008. 34 (9): 913–22. [PubMed] [Google Scholar]Как небулайзеры помогают при респираторных заболеваниях — Aeroflow Healthcare
Медицинское заключение Келли Рэнделл, MD
Если вы страдаете хроническим или не хроническим заболеванием, небулайзер может быть именно тем устройством, которое вам нужно, чтобы чувствовать себя лучше.Небулайзерная машина похожа на дозирующий ингалятор (MDI) в том, что она распределяет по вашему телу лекарственные препараты, пригодные для дыхания.
Однако, в отличие от ингалятора, который требует, чтобы вы сжали устройство и глубоко вдохнули в нужный момент, небулайзер автоматически превращает ваше лекарство в воздухопроницаемый туман и доставляет его вам через мундштук или маску для лица, устраняя необходимость в точности.
Узнайте больше о том, как небулайзеры можно использовать в качестве более простого решения для лечения различных заболеваний.
Ингалятор для астмы Распылителидоставляют лекарства, спасающие жизнь, когда трудно дышать. Детские небулайзеры также являются хорошим выбором для детей, которые могут не работать с ингалятором самостоятельно. Лекарства от астмы, которые можно использовать с небулайзером для уменьшения симптомов во время приступа астмы, включают ингаляционные кортикостероиды, такие как флутиказон, циклесонид, будесонид, мометазон и беклометазон. Ежедневное использование небулайзера при астме также может предотвратить приступы астмы.
Небулайзер для лечения ХОБЛИспользование небулайзера для лечения ХОБЛ (хронической обструктивной болезни легких) может помочь вам лучше дышать, жить более полноценной жизнью и уменьшить количество обострений. Лечение ХОБЛ может включать ежедневный прием небулайзерных препаратов. Эти лекарства от ХОБЛ могут включать кортикостероиды, холинолитики и бета-агонисты, которые могут быть распределены сразу.
Небулайзер для лечения муковисцидозаДля лечения муковисцидоза требуется ряд ингаляционных лекарств для улучшения функции легких, поэтому использование небулайзера так удобно.Большинство процедур начинается с бронходилататоров, за которыми следует гипертонический раствор, дорназа альфа (пульмозим), антибиотики и стероиды.
Конечно, поскольку люди с муковисцидозом очень восприимчивы к микробам, вам необходимо полностью дезинфицировать небулайзер после каждого использования, кипятя его, ставя в микроволновую печь или пропитывая спиртом или перекисью водорода.
Небулайзер для бронхоэктазовПри использовании небулайзера для лечения бронхоэктазов можно улучшить очистку дыхательных путей и вылечить любые возникающие инфекции.Как правило, вы будете принимать ингаляционные стероиды и бронходилататоры длительного действия два раза в день. Эти лекарства собраны вместе, чтобы сократить время, необходимое для лечения.
Небулайзер для респираторных инфекцийКаждый может заразиться респираторной инфекцией, и использование небулайзера может помочь. Кроме того, небулайзерное лечение может обеспечить более быстрое облегчение для групп риска, таких как дети или пожилые люди.
Распылитель для лечения симптомов пневмонииИспользование небулайзера при пневмонии помогает разжижить слизь в легких, чтобы вы могли лучше дышать.В сочетании с лечением пневмонии альбутерол используется для улучшения дыхания.
Примечание: Небулайзер не лечит пневмонию, он просто поможет вам временно лучше дышать. Симптомы будут возвращаться, пока инфекция не исчезнет.
Небулайзер при бронхитеБронхит — еще одно не хроническое заболевание, которое можно лечить с помощью небулайзера. Альбутерол расслабляет мышцы дыхательных путей, открывая дыхательные пути.
Выберите небулайзер по состоянию здоровья сегодняЕсли у вас респираторное заболевание, обратитесь к врачу. Если вам прописали небулайзер, Aeroflow может помочь поставить его в рамках вашей страховки.
Информация, представленная в блоге Aeroflow Healthcare, не предназначена для замены медицинских консультаций или ухода. Aeroflow Healthcare рекомендует проконсультироваться с врачом, если у вас возникли проблемы со здоровьем или проблемы.
Характеристики идеального небулайзерного антибиотика для лечения пневмонии у интубированного пациента | Анналы интенсивной терапии
Американское торакальное общество / Общество инфекционных болезней Америки (ATS / IDSA). Рекомендации по ведению взрослых с внутрибольничной пневмонией, пневмонией, связанной с аппаратом искусственной вентиляции легких, и пневмонией, связанной с оказанием медицинской помощи. Am J Respir Crit Care Med. 2005; 171: 388–416.
Артикул Google ученый
Каланурия А.А., Зай В., Мирски М. Вентиляционная пневмония в отделении интенсивной терапии. Crit Care. 2014; 18: 208.
Артикул PubMed PubMed Central Google ученый
Melsen WG, Rovers MM, Groenwold RHH, Bergmans DCJJ, Camus C, Bauer TT, Hanisch EW, Klarin B, Koeman M, Krueger WA, Lacherade JC, Lorente L, Memish ZA, Morrow LE, Nardi G, van Nieuwenhoven CA , O’Keefe GE, Джордж Накос Г., Сканнапеко Ф.А., Сегин П., Штаудингер Т., Топели А., Феррер М., Бонтен МДЖМ. Приписываемая смертность от пневмонии, связанной с вентилятором: метаанализ данных отдельных пациентов из рандомизированных профилактических исследований. Lancet Infect Dis. 2013; 13: 665–71.
Артикул PubMed Google ученый
Koenig SM, Truwit JD. Вентиляторно-ассоциированная пневмония: диагностика, лечение и профилактика. Clin Microbiol Rev.2006; 19: 637–57.
Артикул PubMed PubMed Central Google ученый
Луна С., Арудж П., Нидерман М., Гарсон Дж., Виоли Д., Приньони А., Риос Ф., Бакеро С., Гандо С. Уместность и отсрочка начала терапии при пневмонии, связанной с вентилятором. Eur Respir J. 2006; 27: 158–64.
CAS Статья PubMed Google ученый
Chastre J, Wunderink R, Prokocimer P, Lee M, Kaniga K, Friedland I. Эффективность и безопасность внутривенной инфузии дорипенема по сравнению с имипенемом при вентилятор-ассоциированной пневмонии: многоцентровое рандомизированное исследование. Crit Care Med. 2008; 36: 1089–96.
CAS Статья PubMed Google ученый
Дженкинс С., Фишер А., Петерсон Дж., Николсон С., Канига К. Мета-анализ дорипенема по сравнению с препаратами сравнения у пациентов с инфекциями Pseudomonas, участвовавших в четырех клинических испытаниях эффективности и безопасности фазы III.Curr Med Res Opin. 2009. 25: 3029–36.
CAS Статья PubMed Google ученый
Kollef M, Chastre J, Clavel M, Restrepo M, Michiels B, Kaniga K, Cirillo I, Kimko H, Redman R. Рандомизированное испытание 7-дневного дорипенема в сравнении с 10-дневным имипенем-циластатином для ИВЛ. -ассоциированная пневмония. Crit Care. 2012; 16: R218.
Артикул PubMed PubMed Central Google ученый
Awad SS, Rodriguez AH, Chuang YC, Marjanek Z, Pareigis AJ, Reis G, Scheeren TWL, Sánchez AS, Zhou X, Saulay M, Engelhardt M. Рандомизированное двойное слепое сравнение фазы 3 цефтобипрола медокарила и цефтазидима плюс линезолид для лечение госпитальной пневмонии. Clin Infect Dis. 2014; 59: 51–61.
CAS Статья PubMed PubMed Central Google ученый
Флюм П., ВанДевантер Д. Клиническое применение легочной доставки антибиотиков.Adv Drug Deliv Rev.2015; 85: 1–6.
CAS Статья PubMed Google ученый
Bercault N, Boulain T. Уровень смертности, связанной с внутрибольничной пневмонией, связанной с аппаратом искусственной вентиляции легких, в отделении интенсивной терапии для взрослых: проспективное исследование «случай – контроль». Respir Ther. 2001; 29: 2303–9.
CAS Google ученый
Буше Х, Талбот Дж., Брэдли Дж., Эдвардс Дж., Гилберт Д., Райс Л., Шельд М., Спеллберг Б., Бартлетт Дж.Плохие ошибки, никаких лекарств: нет ESKAPE! Новости Общества инфекционных болезней Америки. Clin Infect Dis. 2009; 48: 1–12.
Артикул PubMed Google ученый
Спеллберг Б., Бартлетт Дж., Вундеринк Р., Гилберт Д.Н. Для разработки антибактериальной терапии завтрашнего дня необходимы новые подходы. Am J Respir Crit Care Med. 2015; 191: 135–40.
Артикул PubMed PubMed Central Google ученый
Bassetti M, De Waele JJ, Eggimann P, Garnacho-Montero J, Kahlmeter G, Menichetti F, Nicolau DP, Paiva JA, Tumbarello M, Welte T, Wilcox M, Zahar RJ, Poulakou G. Профилактические и терапевтические стратегии для тяжелобольных пациенты с высокорезистентными бактериями. Intensive Care Med. 2015; 41: 776–95.
CAS Статья PubMed Google ученый
Wise R, Honeybourne D. Фармакокинетика и фармакодинамика фторхинолонов в дыхательных путях.Eur Respir J. 1999; 14: 221–9.
CAS Статья PubMed Google ученый
Ханиборн Д. Проникновение антибиотиков в ткани легких. Грудная клетка. 1994; 49: 104–6.
CAS Статья PubMed PubMed Central Google ученый
Cruciana M, Gatti G, Lazzarini L, Furlan G, Broccali G, Malena M, Franchini C., Concia E. Проникновение ванкомицина в ткань легких человека.J Antimicrob Chemother. 1996; 38: 865–9.
Артикул Google ученый
Имберти Р., Кусато М., Виллани П., Карневале Л., Йотти Г., Лангер М., Регацци М. Фармакокинетика устойчивого состояния и концентрация колистина в БАЛ у пациентов в критическом состоянии после внутривенного введения метансульфоната колистина. Грудь. 2010; 138: 1333–9.
CAS Статья PubMed Google ученый
Avent ML, Rogers BA, Cheng AC, Paterson DL. Текущее использование аминогликозидов: показания, фармакокинетика и мониторинг токсичности. Int Med J. 2011; 41: 441–9.
CAS Статья Google ученый
Арнольд А., Броуз С., Питчер В., Холл Р. Эмпирическая терапия грамотрицательных патогенов при внутрибольничной пневмонии и пневмонии, связанной с оказанием медицинской помощи: начиная с конца. J Intensive Care Med. 2010; 25: 259–70.
Артикул PubMed Google ученый
Смит Б., Йогаратнам Д., Левассер-Франклин К., Форни А., Фонг Дж. Введение в фармакокинетику лекарств у тяжелобольного пациента. Грудь. 2012; 141: 1327–36.
CAS Статья PubMed Google ученый
Blot S, Pea F, Lipman J. Влияние патофизиологии на фармакокинетику у тяжелобольного пациента — концепции, оцененные на примере антимикробных средств. Adv Drug Deliv Rev. 2014; 77: 3–11.
CAS Статья PubMed Google ученый
Винкс А., Дерендорф Х, Мутон Дж. Основы противомикробной фармакокинетики и фармакодинамики. Нью-Йорк / Гейдельберг / Дордрехт / Лондон: Спрингер; 2014. с. 63–72.
Книга Google ученый
Palmer LB. Антибиотики в аэрозольной форме в отделении интенсивной терапии. Клиники Chest Med. 2011; 32: 559–74.
Артикул Google ученый
Лу Кью, Луо Р., Бодин Л., Ян Дж., Зар Н., Обри А., Голмард Дж., Руби Дж.Эффективность распыления высоких доз колистина при респираторно-ассоциированной пневмонии, вызванной множественной лекарственной устойчивостью Pseudomonas aeruginosa и Acinetobacter baumannii . Анестезиология. 2012; 117: 1335–47.
CAS Статья PubMed Google ученый
Le J, Neuhauser M, Brown J, Gentry C, Klepser M, Marr A, Schiller D., Schwiesow J, Tice S, VandenBussche H, Wood C. Консенсусное обобщение антимикробных агентов в аэрозольной форме: применение критериев руководства .Фармакотерапия. 2010. 30: 562–84.
CAS Статья PubMed Google ученый
Wood C. Антибиотики в аэрозольной форме для лечения внутрибольничной пневмонии и пневмонии, связанной с аппаратом искусственной вентиляции легких. Exp Rev Anti-Infect Ther. 2011; 9: 993–1000.
CAS Статья Google ученый
Luyt C-E, Combes A, Nieszkowska A, Trouillet J, Chastre J. Аэрозольные антибиотики для лечения вентилятор-ассоциированной пневмонии.Curr Opin Infect Dis. 2009; 22: 154–8.
Артикул PubMed Google ученый
Абу-Салах Т., Дханд Р. Ингаляционная антибактериальная терапия при трахеобронхите, связанном с вентилятором, и пневмонии, связанной с вентилятором: обновленная информация. Adv Ther. 2011; 29: 728–47.
Артикул Google ученый
Goldstein I, Wallet F, Robert J, Bequemin M, Marquette C, Rouby J.Концентрация распыленного амикацина в легочной ткани во время искусственной вентиляции легких у поросят со здоровыми легкими. Am J Respir Crit Care Med. 2002; 165: 171–5.
Артикул PubMed Google ученый
Голдштейн I, Кошелек F, Николя-Робин A, Феррари F, Маркетт C-H, Руби J-J, Исследовательская группа экспериментального отделения интенсивной терапии. Отложение в легких и эффективность распыленного амикацина при пневмонии Escherichia coli у вентилируемых поросят.Am J Respir Crit Care Med. 2002; 166: 1375–81.
Артикул PubMed Google ученый
Бадиа Дж., Сой Д., Адровер М., Феррер М., Сараса М., Аларкон А., Кодина С., Торрес А. Распределение инстиллированных тобрамицина и имипенема в вентилируемых отделениях интенсивной терапии (ОИТ) по сравнению с небулайзерами. J Antimicrob Chemother. 2004; 54: 508–14.
CAS Статья PubMed Google ученый
Luyt CE, Clavel M, Guntupalli K, Johannigman J, Kennedy J, Wood C, Corkery K, Gribben D, Chastre J. Фармакокинетика и доставка в легкие PDDS-аэрозольного амикацина (NKTR-061) у интубированных и искусственно вентилируемых пациентов с нозокомиальной инфекцией. пневмония. Crit Care. 2009; 13: R200.
Артикул PubMed PubMed Central Google ученый
Cooney G, Lum B, Tomaselli M, Fiel S. Абсолютная биодоступность и характеристики абсорбции аэрозольного тобрамицина у взрослых с муковисцидозом.Clin Pharmacol. 1994; 34: 255–9.
CAS Статья Google ученый
Лу Кью, Ян Дж., Лю З., Гутьеррес К., Эймар Дж., Руби Дж. Дж., Исследовательская группа по распыленным антибиотикам. Распыленный цефтазидим и амикацин при вентилятор-ассоциированной пневмонии, вызванной Pseudomonas aeruginosa . Am J Respir Crit Care Med. 2011; 184: 106–15.
CAS Статья PubMed Google ученый
Дханд Р. Роль противомикробных препаратов в аэрозольной форме в лечении пневмонии, связанной с аппаратом ИВЛ. Respir Care. 2007. 52: 866–84.
PubMed Google ученый
Drlica K, Zhao X. Гипотеза окна выбора мутантов обновлена. Clin Infect Dis. 2007; 44: 681–8.
Артикул PubMed Google ученый
Ramsey BW, Dorkin HL, Eisenberg JD, Gibson RL, Harwood IR, Kravitz RM, Schidlow DV, Wilmott RW, Astley SJ, McBurnie MA, Wentz K, Smith AL.Эффективность аэрозольного тобрамицина у пациентов с муковисцидозом. N Engl J Med. 1993; 328: 1740–6.
CAS Статья PubMed Google ученый
Бернс Дж. Л., Ван Дальфсен Дж. М., Шавар Р. М., Отто К. Л., Гарбер Р. Л., Куан Дж. М., Монтгомери А. Б., Альберс Дж. М., Рэмси Б. В., Смит А. Л.. Влияние хронического периодического введения ингаляционного тобрамицина на респираторную микробную флору у пациентов с муковисцидозом. J Infect Dis. 1999; 179: 1190–6.
CAS Статья PubMed Google ученый
Палмер Л.Б., Смолдон Дж. Снижение бактериальной резистентности с помощью ингаляционных антибиотиков в отделении интенсивной терапии. Am J Respir Crit Care Med. 2014; 189: 1225–33.
Артикул PubMed Google ученый
Niederman M, Chastre J, Corkery K, Fink J, Luyt C-E, Sanchez Garcia M. BAY41-6551 обеспечивает бактерицидные концентрации амикацина в трахеальном аспирате у пациентов с грамотрицательной пневмонией на ИВЛ.Intensive Care Med. 2012; 38: 263–71.
CAS Статья PubMed Google ученый
Chastre J, Luyt C-E. Оптимизация продолжительности антибактериальной терапии респираторной пневмонии. Eur Respir Rev.2007; 16: 40–4.
Артикул Google ученый
Фихман В., Мессика Дж., Хаджаге Д., Турнье В., Годри С., Магдуд Ф., Барно Дж., Бильярд-Помарес Т., Бранжер С., Дрейфус Д., Рикар Дж. Д..Пятилетние тенденции развития вентилятор-ассоциированной пневмонии: корреляция между микробиологическими данными и потреблением противомикробных препаратов. Int J Antimicrob Agents. 2015; 46: 518–25.
CAS Статья PubMed Google ученый
Нидерман М., Частре Дж., Коркери К., Маркантонио А., Финк Дж., Лют С.-Э, Санчес М. и группа по изучению амикацина. NKTR-061 (ингаляционный амикацин) снижает внутривенное использование антибиотиков у интубированных пациентов с механической вентиляцией легких во время лечения грамотрицательной пневмонии.ATS 18–23 мая 2007 г., плакат A326.
Колистин — краткое описание характеристик продукта. https://www.medicines.org.uk/emc/medicine/27647. По состоянию на 25 ноября 2015 г.
Aztreonam: краткое описание характеристик продукта. https://www.medicines.org.uk/emc/medicine/22358. По состоянию на 25 ноября 2015 г.
Тобрамицин, сводка характеристик продукта. https://www.medicines.org.uk/emc/medicine/19020. По состоянию на 25 ноября 2015 г.
Quon B, Goss C, Ramsey B.Ингаляционные антибиотики при инфекциях нижних дыхательных путей. Ann Am Thorac Soc. 2014; 11: 425–34.
CAS Статья PubMed PubMed Central Google ученый
Geller DE. Аэрозольные антибиотики при муковисцидозе. Respir Care. 2009; 54: 658–70.
Артикул PubMed Google ученый
Zampieri F, Nassar A Jr, Gusmao-Flores D, Taniguchi L, Torres A, Ranzani O.Распыляемые антибиотики при вентилятор-ассоциированной пневмонии: систематический обзор и метаанализ. Crit Care. 2015; 19: 150.
Артикул PubMed PubMed Central Google ученый
Rouby J, Bouhemad B, Monsel A, Brisson H, Arbelot C, Lu Q, Группа изучения распыленных антибиотиков. Аэрозольные антибиотики при вентиляции легких: уроки экспериментальных исследований. Анестезиология. 2012; 117: 1364–80.
CAS Статья PubMed Google ученый
Коллеф М., Гамильтон С., Монтгомери А. Антибиотики в аэрозольной форме: добавляют ли они к лечению пневмонии? Curr Opin Infect Dis. 2013; 26: 538–44.
CAS Статья PubMed PubMed Central Google ученый
Дханд Р. Доставка аэрозолей при ИВЛ: от базовых методик к новым устройствам. J Aerosol Med Pulm Drug Deliv. 2008; 21: 45–60.
Артикул PubMed Google ученый
Кадричу Н., Бок С., Коркери К., Чаллонер П. Эффективность in vitro системы вдыхания амикацина, новой интегрированной системы доставки лекарств и устройств. ISICEM, 19–22 марта 2013 г., плакат A384.
Лаубе Б., Янссенс Х., де Йонг Ф., Девадасон С., Дханд Р., Диот П., Эверард М., Хорват I, Навалеси П., Вошаар Т., Кристин Х. Что специалист по легочным заболеваниям должен знать о новой ингаляции терапии. Eur Respir J. 2011; 37: 1308–31.
CAS Статья PubMed Google ученый
Дханд Р. Максимизация доставки аэрозоля во время искусственной вентиляции легких: плыть по течению и действовать медленно. Intensive Care Med. 2003; 29: 1041–2.
Артикул PubMed Google ученый
Миллер Д., Амин М., Палмер Л., Шах А., Смолдон Г. Доставка аэрозолей и современная механическая вентиляция легких: оценка in vitro / in vivo. Am J Respir Crit Care Med. 2003. 168: 1205–9.
Артикул PubMed Google ученый
Рестрепо Р., Уолш Б. Увлажнение во время инвазивной и неинвазивной механической вентиляции: 2012. Respir Care. 2012; 57: 782–8.
Артикул PubMed Google ученый
Lu Q, Girardi C, Zhang M, Bouhemad B, Louchahi K, Petitjean O, Wallet F, Becquemin M, Le Naour G, Marquette C, Rouby J. Колистин в виде распыления и внутривенно при экспериментальной пневмонии, вызванной Синегнойная палочка . Intensive Care Med.2010; 36: 1147–55.
CAS Статья PubMed Google ученый
Манделл Л.А., Вундеринк Р.Г., Анзуэто А., Бартлетт Дж. Г., Кэмпбелл Г.Д., Дин Н.К., Доуэлл С.Ф., Файл Т.М. мл., Мушер Д.М., Нидерман М.С., Торрес А., Уитни К.Г. Общество инфекционных болезней Америки / Американское торакальное общество согласовали руководящие принципы ведения внебольничной пневмонии у взрослых. Clin Infect Dis. 2007; 44: S27–72.
CAS Статья PubMed Google ученый
Masterton RG, Galloway A, French G, Street M, Armstrong E, Brown E, Cleverley J, Dilworth P, Fry C, Gascoigne AD, Knox A, Nathwani D, Spencer R, Wilcox M. Руководство по управлению больницей- приобретенная пневмония в Великобритании: отчет Рабочей группы по внутрибольничной пневмонии Британского общества антимикробной химиотерапии. J Antimicrob Chemother. 2008; 62: 5–34.
CAS Статья PubMed Google ученый
Ehrmann S, Roche-Campo F, Sferrazza Papa G, Isabey D, Brochard L, Apiou-Sbirlea G, исследовательская сеть REVA. Аэрозольная терапия при ИВЛ: международный обзор. Intensive Care Med. 2013; 39: 1048–56.
CAS Статья PubMed Google ученый
PARI eFlow rapid, Технические данные. http://www.pari.de/uk-en/products/lower-airways-1/eflow-rapid-nebuliser-system-1/. По состоянию на 13 ноября 2015 г.
Монтгомери А., Ромберг П., Абуан Т., Уолтерс К., Фламм Р. Амикацин-фосфомицин в соотношении пять к двум: характеристика частоты мутаций в штаммах микробов, вызывающих пневмонию, ассоциированную с вентилятором, и взаимодействия с обычно используемыми антибиотиками. Антимикробные агенты Chemother. 2014. 58: 3707–13.
Google ученый
Монтгомери А., Ромберг П., Абуан Т., Уолтерс К., Фламм Р. Потенцирующие эффекты амикацина и фосфомицина против выбранных невосприимчивых к амикацину грамотрицательных патогенов дыхательных путей.Антимикробные агенты Chemother. 2014; 58: 3714–9.
CAS Статья PubMed PubMed Central Google ученый
Montgomery A, Vallance S, Abuan T., Tservistas M, Davies A. Рандомизированное двойное слепое плацебо-контролируемое исследование фазы 1 повышения дозы аэрозольных амикацина и фосфомицина, доставляемых через PARI Investigational eFlow ® Inline Система небулайзера для пациентов с механической вентиляцией легких. J Aerosol Med Pulm Drug Deliv.2014; 27: 441–8.
CAS Статья PubMed PubMed Central Google ученый
Hallal A, Cohn S, Namias N, Habib F, Baracco G, Manning R, Crookes B., Schulman C. Тобрамицин в аэрозольной форме при лечении вентилятор-ассоциированной пневмонии: пилотное исследование. Хирургическая инфекция (Larchmt). 2007; 8: 73–81.
Артикул Google ученый
Кадричу Н., Коркери К., Данг Т., Чаллонер П.Эффективность ингаляции амикацина: воздействие дополнительного кислорода и ориентация устройства. Crit Care. 2015; 19 (Приложение 1): P120.
Артикул PubMed Central Google ученый
Кадричу Н., Бок С., Коркери К. и Чаллонер П. Влияние увлажнения на доставку дозы амикацина in vitro. Вдыхайте с помощью механической вентиляции. ESICM, 27 сентября — 1 октября 2014 г., Аннотация 0867.
Pritchard JN. Влияние отложения в легких на клинический ответ.J Aerosol Med. 2001; 14 (Дополнение 1): 19–26.
Артикул Google ученый
Aerogen. Aeroneb ® Solo лист данных. http://www.aerogen.com/uploads/datasheets/Aeroneb_Solo_Product_Datasheet_FINAL_A4.pdf. По состоянию на 13 ноября 2015 г.
Aerogen. Часто задаваемые вопросы по Aeroneb ® Solo. http://www.aerogen.com/medical-community/faq/faq-aerogen-solo.html. По состоянию на 13 ноября 2015 г.
Seemann S, Schmitt A, Waldner R, Hug M, Knoch M.Улучшение доставки аэрозольных лекарственных средств при терапии МВ. Европейская конференция по муковисцидозу, 22–26 июня 2005 г., плакат P113.
Альбутерол и ипратропий Устные ингаляции: информация о лекарствах MedlinePlus
Комбинация альбутерола и ипратропия представлена в виде раствора (жидкости) для перорального вдыхания с помощью небулайзера (устройства, которое превращает лекарство в туман, который можно вдыхать) и в виде спрей для вдыхания через рот с помощью ингалятора. Обычно его вдыхают четыре раза в день. Тщательно следуйте инструкциям на этикетке рецепта и попросите своего врача или фармацевта объяснить любую часть, которую вы не понимаете.Используйте альбутерол и ипратропиум точно так, как указано. Не используйте его больше или меньше и не используйте его чаще, чем предписано вашим доктором.
Ваш врач может посоветовать вам использовать дополнительные дозы альбутерола и ипратропия при вдыхании, если вы испытываете такие симптомы, как хрипы, затрудненное дыхание или стеснение в груди. Тщательно следуйте этим указаниям и не используйте дополнительные дозы лекарств, если только ваш врач не скажет вам, что это необходимо. Не используйте более 2 дополнительных доз раствора небулайзера в день.Не используйте спрей для ингаляций более шести раз за 24 часа.
Позвоните своему врачу, если ваши симптомы ухудшатся, если вы чувствуете, что вдыхание альбутерола и ипратропия больше не контролирует ваши симптомы, или если вы обнаружите, что вам нужно чаще использовать дополнительные дозы лекарства.
Если вы используете ингалятор, ваше лекарство будет поставляться в картриджах. Каждый картридж с ингаляционным спреем альбутерола и ипратропия рассчитан на 120 ингаляций. Этого лекарства хватит на один месяц, если вы будете использовать одну ингаляцию четыре раза в день.После того, как вы используете все 120 доз, ингалятор заблокируется и больше не будет выпускать лекарство. На боковой стороне ингалятора есть индикатор дозы, который отслеживает, сколько лекарства осталось в картридже. Время от времени проверяйте индикатор дозы, чтобы узнать, сколько лекарства осталось. Когда указатель на индикаторе дозы переходит в красную область, в картридже содержится достаточно лекарства на 7 дней, и пора пополнить рецепт, чтобы у вас не закончились лекарства.
Будьте осторожны, чтобы не вдыхать альбутерол и ипратропий в глаза.Если вы попали в глаза альбутеролом и ипратропием, у вас может развиться узкоугольная глаукома (серьезное заболевание глаз, которое может вызвать потерю зрения). Если у вас уже есть узкоугольная глаукома, ваше состояние может ухудшиться. У вас могут быть расширенные зрачки (черные круги в центре глаз), боль или покраснение в глазах, нечеткое зрение и изменения зрения, такие как появление ореолов вокруг огней или появление необычных цветов. Если вы попали в глаза альбутерол и ипратропий, позвоните своему врачу. или если у вас появятся эти симптомы.
Ингалятор, который поставляется с альбутеролом и ипратропиумом в виде спрея, предназначен для использования только с картриджем с альбутеролом и ипратропием. Никогда не используйте его для вдыхания каких-либо других лекарств и не используйте другие ингаляторы для вдыхания лекарства в картридже с альбутеролом и ипратропием.
Перед первым применением ингаляции альбутерола и ипратропия прочтите письменные инструкции, прилагаемые к ингалятору или небулайзеру. Попросите вашего врача, фармацевта или респираторного терапевта показать вам, как его использовать.Потренируйтесь пользоваться ингалятором или небулайзером, пока он или она смотрит.
Чтобы подготовить ингалятор к использованию, выполните следующие действия:
- Соберите ингалятор перед его первым использованием. Для начала достаньте ингалятор из коробки и держите оранжевый колпачок закрытым. Нажмите на предохранитель и снимите прозрачное основание ингалятора. Будьте осторожны, чтобы не прикасаться к прокалывающему элементу внутри основания.
- Ингалятор необходимо выбросить через три месяца после того, как вы его собрали.Напишите эту дату на этикетке ингалятора, чтобы не забыть, когда вам нужно выбросить ингалятор.
- Достаньте картридж из коробки и вставьте узкий конец в ингалятор. Вы можете прижать ингалятор к твердой поверхности, чтобы убедиться, что он вставлен правильно. Замените прозрачную пластиковую основу на ингаляторе.
- Держите ингалятор вертикально с закрытым оранжевым колпачком. Поверните прозрачную основу в направлении белых стрелок до щелчка.
- Откиньте оранжевую крышку так, чтобы она полностью открылась.Направьте ингалятор на землю.
- Нажать кнопку сброса дозы. Закройте оранжевую крышку.
- Повторяйте шаги 4–6, пока не увидите, как из ингалятора выходит спрей. Затем повторите эти действия еще три раза.
- Ингалятор заправлен и готов к использованию. Вам не нужно будет повторно заправлять ингалятор, если вы не используете его дольше 3 дней. Если вы не используете ингалятор более 3 дней, вам нужно будет выпустить один спрей на землю, прежде чем вы начнете использовать его снова.Если вы не используете ингалятор более 21 дня, вам нужно будет выполнить шаги 4-7, чтобы снова заправить ингалятор.
Чтобы вдохнуть спрей с помощью ингалятора, выполните следующие действия:
- Держите ингалятор вертикально с закрытым оранжевым колпачком. Поверните прозрачную основу в направлении белых стрелок до щелчка.
- Откройте оранжевую крышку.
- Медленно и полностью выдохните.
- Поместите мундштук в рот и сомкните его губами.Будьте осторожны, не закрывайте губами вентиляционные отверстия.
- Направьте ингалятор в сторону задней стенки горла и вдохните медленно и глубоко.
- На вдохе нажмите кнопку сброса дозы. Продолжайте дышать, пока спрей попадет в ваш рот.
- Задержите дыхание на 10 секунд или столько, сколько вам удобно.
- Выньте ингалятор изо рта и закройте оранжевый колпачок. Держите колпачок закрытым, пока не будете готовы снова использовать ингалятор.
Чтобы вдохнуть раствор с помощью небулайзера, выполните следующие действия:
- Извлеките один флакон с лекарством из пакета из фольги. Положите остальные флаконы обратно в пакет, пока не будете готовы их использовать.
- Открутите верхнюю часть флакона и выжмите всю жидкость в резервуар небулайзера.
- Подсоедините резервуар небулайзера к мундштуку или лицевой маске.
- Подсоедините бачок небулайзера к компрессору.
- Положите мундштук в рот или наденьте лицевую маску.

