Советы — Рост ребенка и гормон роста
Алла Федоровна Козяр, детский эндокринолог высшей категории МЦ «Педиатр»
Вопрос: Моему сыну почти семь лет, а ростом он всего 106 см. Мы считали, что он пошел в родню по линии мужа, и не придавали особого значения. Но недавно нам посоветовали провериться у детского эндокринолога и сдать анализы на гормон роста. Действительно ли нам надо сдавать этот анализ и где можно получить консультацию специалиста?
Ответ: Значительное замедление роста в детском возрасте является наиболее явным признаком пониженной деятельности гипофиза. В будущем такое состояние может привести к карликовости. Карликом считается взрослый, если его рост не превышает 120–130 см. В детском возрасте о низкорослости говорится в том случае, если рост ребенка более чем на 40% отстает от среднего для данного возраста. Кроме того, для таких детей характерна задержка не только роста, но и развития.
Причины низкого роста многообразны. Кроме наследственных, гормональных и алиментарных факторов, на рост оказывают влияние и различные заболевания детей.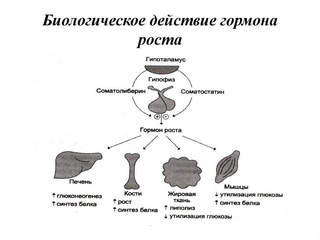 Большая роль принадлежит инфекциям, интоксикациям, травмам и другим патологическим процессам, влияющим на функцию гипоталамо-гипофизарной области в раннем периоде.
Большая роль принадлежит инфекциям, интоксикациям, травмам и другим патологическим процессам, влияющим на функцию гипоталамо-гипофизарной области в раннем периоде.
Как правило, задержка роста выявляется на 4–5 году жизни. Темпы роста снижаются до 1–2 см в год, тогда как здоровый ребенок вырастает на 5–6 см в год. Телосложение имеет нормальные пропорции. Кожа эластичная, тонкая, бледная, склонна к раннему старению. Иногда наблюдается ожирение. Кости растут плохо, сохраняются молочные зубы.
Очень часто вместе с выработкой гормона роста страдает выработка и других гормонов гипофиза, и тогда клиническая картина утяжеляется.
Если Ваш ребенок отстаёт в росте, надо обязательно обследоваться у детского эндокринолога. В настоящее время возможна точная диагностика дефицита гормона роста.
Лечение низкорослости комплексное. Ребенку необходимо обеспечить режим дня, достаточный сон, полноценное питание, — богатое белками и витаминами. Наряду с препаратами, содержащими витамины, — минеральные соли, пищеварительные ферменты, назначается и гормон роста.
Гормон роста был обнаружен в допинг-пробе одного из самых перспективных гребцов РФ Товканя — Спорт
МОСКВА, 24 января. /Корр. ТАСС Альберт Стародубцев/. В допинг-пробе одного из самых перспективных российских гребцов-каноистов Анатолия Товканя была обнаружена запрещенная субстанция — релизинг-пептид гормона роста, которым спортсмен пытался самостоятельно вылечить больное колено. Об этом сообщил ТАСС тренер гребца Андрей Корниевский.
Всероссийская федерация гребли на байдарках и каноэ на основании решения Дисциплинарного антидопингового комитета приняла решение о дисквалификации Анатолия Товканя за нарушение антидопинговых правил на 3 года и 6 месяцев, начиная с 14 сентября 2015 года. В допинг-пробе, взятой у спортсмена 5 сентября во время учебно-тренировочного сбора в Краснодаре, был обнаружен релизинг-пептид гормона роста, входящий в класс S2 Запрещенного списка Всемирного антидопингового агентства за 2015 год.
«Федерация вынесла спортсмену адекватное наказание, — считает Корниевский. — С 2015 года за нарушение антидопинговых правил дают 4 года дисквалификации. В случае с Товканем можно сказать, что ему смягчили наказание на полгода».
— С 2015 года за нарушение антидопинговых правил дают 4 года дисквалификации. В случае с Товканем можно сказать, что ему смягчили наказание на полгода».
Тренер заметил, что сам спортсмен не стал отрицать факт употребления запрещенного вещества. «Он объяснил, что этот препарат ему понадобился для лечения травмированного колена, — продолжил собеседник ТАСС. — Проблемы с коленом действительно подтверждались результатами углубленного медицинского обследования. Но, как сказал Товкань, курс лечения, прописанный врачами Федерального медико- биологического агентства, не помог избавиться от проблемы, поэтому он решил заняться самолечением».
«Я был в шоке от произошедшего, — признался Корниевский. — Для улучшения своих показателей Товканю не требовалось употреблять запрещенные средства, этот спортсмен и так очень одарен функционально, антропометрически, технически. Для дальнейшего раскрытия его таланта нужно было просто продолжать работать, через год-два он бы и так вышел в топ российских спортсменов, да и не только российских. Но, видимо, он хотел достичь результата как можно быстрей. К сожалению, существующая система давит и на спортсменов, и на тренеров. Все требуют результат здесь и сейчас, никто ждать не хочет. От этого у нас в стране так часто допинговые скандалы и происходят».
Но, видимо, он хотел достичь результата как можно быстрей. К сожалению, существующая система давит и на спортсменов, и на тренеров. Все требуют результат здесь и сейчас, никто ждать не хочет. От этого у нас в стране так часто допинговые скандалы и происходят».
21-летний воспитанник дальневосточной школы гребли Товкань является чемпионом России, победителем этапов Кубка мира, призером молодежного первенства мира.
Влияние избытка гормона роста и ИФР-1 на костно- суставную систему при акромегалии
DOI: 10.18508/endo3539
| Авторы: Ю.Е. Потешкин1, В.С. Пронин1, Г.А. Мельниченко2, П.М. Хандаева2, И.А. Соколина1, Ж.Е. Белая2 |
Органицации:
|
Authors: Y.E. Poteshkin1, V.S. Pronin1, I.A. Sokolina1, G.A. Melnichenko2, P.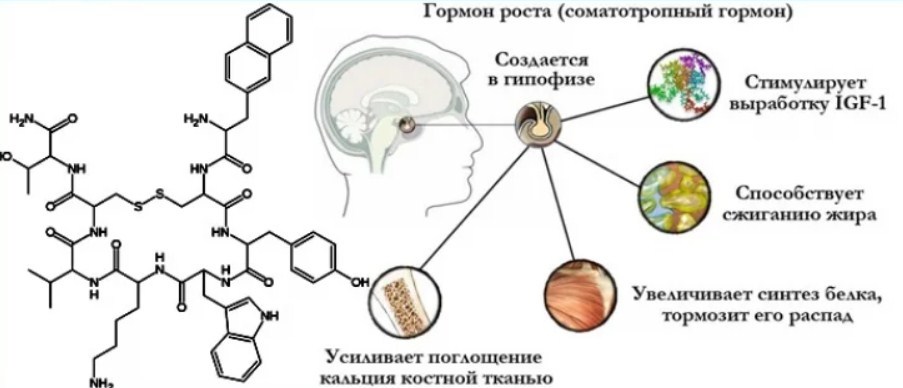 M. Khandaeva2, I.A. Sokolina1, Z.E. Belaya2 M. Khandaeva2, I.A. Sokolina1, Z.E. Belaya2 |
Author affiliation:
|
Abstract: The musculoskeletal system complications are the most common and steadily progressive complication of acromegaly, manifested destruction of bone and ligaments of the spine, deformity of large and small joints, limited physical activity, persistent pain, which ultimately contributes to the development of early disability and reduced quality of life4. Unfortunately there is small number of papers devoted to this topic5–17. It should also be noted that, as a result of delayed diagnosis of acromegaly and complexity of achieving stable disease control (post-operative medication or compensation), this complication usually becomes symptomatic, curation of which requires additional diagnostic and therapeutic efforts. Prevalence of complicated acromegaly forms increases significantly with the number of patients. In particular, due to the high incidence of skeletal disorders, it is important to study the isolated contribution of excess growth hormone activity in the formation of pathological changes of bone tissue in acromegaly and determination of the degree of reversibility any structural abnormality control after reaching the underlying disease. It should also be borne in mind that the development in acromegaly polymorphic structural changes of the axial skeleton and bones are certain features in the interpretation of data, and densitometry studies makes it difficult to dynamically control that requires the allocation of the priority areas that adequately reflect the real state of the bone tissue.
Prevalence of complicated acromegaly forms increases significantly with the number of patients. In particular, due to the high incidence of skeletal disorders, it is important to study the isolated contribution of excess growth hormone activity in the formation of pathological changes of bone tissue in acromegaly and determination of the degree of reversibility any structural abnormality control after reaching the underlying disease. It should also be borne in mind that the development in acromegaly polymorphic structural changes of the axial skeleton and bones are certain features in the interpretation of data, and densitometry studies makes it difficult to dynamically control that requires the allocation of the priority areas that adequately reflect the real state of the bone tissue.
Список сокращений
БАБП-А (PAPP-A)- беременность- ассоциированный белок плазмы А (pregnancy associated plasma protein A)
ГРСБ- гормон роста связывающий белок
ЖМТ- жировая масса тела
ИМТ- индекс массы тела
ИФР-1- инсулиноподобный фактор роста-1
ИФРСБ- ИФР-1 связывающий белок
КТ- компьютерная томография
МАПК- митоген- активируемые протеинкиназы
ММК- минеральная масса костей
МПК- минеральная плотность костей
ППАР (PPAR)- пероксисомный пролифератор- активируемый рецептор (peroxisome proliferator activated receptor)
ПСАТ-5- преобразователь сигнала и активатор транскрипции
ПТГ- паратгормон
рГР- рецептор гормона роста
СКС- стандартизованный коэффициент смертности
ТМТ- тощая масса тела
RANKL- лиганд рецептора ядерного фактора бета
Гормональная регуляция костного метаболизма
ГР и ИФР-1
Развитие и функционирование костной ткани находится под динамическим эндокринным контролем в течение всего онтогенетического периода. В регуляции костного обмена принимают участие гипофизарные, тироидные, надпочечниковые, половые гормоны, а также паратгормон. Ведущую роль в росте организма и формировании костной ткани играет гормон роста (ГР).
В регуляции костного обмена принимают участие гипофизарные, тироидные, надпочечниковые, половые гормоны, а также паратгормон. Ведущую роль в росте организма и формировании костной ткани играет гормон роста (ГР).
Гормон роста (соматотропный гормон (СТГ), соматотропин) представляет собой простой белок, состоящий из 191 аминокислотного остатка. Он продуцируется соматотрофами, локализующимися в передней доле гипофиза. Синтез и секреция ГР находится под постоянным разнонаправленным гипоталамическим контролем путем продукции соматолиберина и соматостатина, секреция которых, в свою очередь, зависит от многих экзогенных и эндогенных факторов, таких как стресс, физическая активность, фазы сна, содержание в крови энергоемких субстратов и ростовых факторов.
Соматолиберин — пептидный гормон, молекула соматолиберина состоит из 37-44 аминокислотных остатков. У человека обнаружены 3 формы соматолиберина, различающиеся длиной полипептидной цепи С-концевого участка. Молекула преобладающей формы соматолиберина состоит из 44 аминокислотных остатков и содержит амидированный С-конец. Молекулы двух других форм имеют укороченную с С-конца полипептидную цепь и состоят из 40 и 37 аминокислотных остатков. Все три формы обладают одинаковой биологической активностью.
Молекулы двух других форм имеют укороченную с С-конца полипептидную цепь и состоят из 40 и 37 аминокислотных остатков. Все три формы обладают одинаковой биологической активностью.
Биосинтез соматолиберина осуществляется в нейросекреторных клетках гипоталамуса. Оттуда через портальную кровеносную систему соматолиберин поступает в гипофиз, где избирательно стимулирует синтез и секрецию ГР 1–3.
Соматостатин синтезируется преимущественно в клетках гипоталамуса. Биологические эффекты соматостатина разнообразны. Соматостатин, синтезирующийся в гипоталамусе, поступает в гипофиз и подавляет секрецию ГР. Кроме того, соматостатин способен угнетать секрецию тиреотропного гормона гипофизом, инсулина и глюкагона в поджелудочной железе, а также секрецию гастрина и секретина в желудочно-кишечном тракте 3–5.
Гормон роста воздействует на все органы и ткани, частично напрямую, частично опосредовано: ГР стимулирует образование инсулиноподобных факторов роста в печени, через которые соматотропный гормон оказывает регулирующее действие на все ткани. Наиболее значимым и изученным из них считается инсулиноподобный фактор роста 1 (ИФР-1), под его влиянием усиливается деление хрящевых клеток, синтез ДНК, РНК, белка, коллагена и сульфирование протеогликанов. ИФР-1 действует на жировую и мышечную ткани, где стимулирует поглощение ими глюкозы и тормозит липолиз в жировой ткани, активирует глюконеогенез в печени.
Наиболее значимым и изученным из них считается инсулиноподобный фактор роста 1 (ИФР-1), под его влиянием усиливается деление хрящевых клеток, синтез ДНК, РНК, белка, коллагена и сульфирование протеогликанов. ИФР-1 действует на жировую и мышечную ткани, где стимулирует поглощение ими глюкозы и тормозит липолиз в жировой ткани, активирует глюконеогенез в печени.
Таким образом, организация соматотропной функции включает несколько уровней: системный вызывает увеличение объема внутренних органов и рост соединительной ткани, ускорение утилизации аминокислот и синтеза белков, стимуляцию пролиферации хрящевой ткани и синтеза антител в лимфоидных клетках. В метаболический уровень входит действие на липидный обмен: в первую фазу (3-6 часов) подавление липолиза и окисления жирных кислот, стимуляцию синтеза липидов печени, во вторую фазу (8-12 часов) мобилизацию липидов из жировых депо, увеличение уровня триглицеридов крови и ускорение бета- окисления жирных кислот. Действие на липидный обмен проявляется стимуляцией секреции глюкагона и серотонина, подавлением окисления глюкозы и стимуляцией глюконеогенеза печени. Воздействие на водно- солевой обмен выражается в повышении уровня неорганических фосфатов в крови, повышение экскреции кальция с мочой, задержкой ионов магния, натрия, калия и хлоридов 5.
Воздействие на водно- солевой обмен выражается в повышении уровня неорганических фосфатов в крови, повышение экскреции кальция с мочой, задержкой ионов магния, натрия, калия и хлоридов 5.
Помимо системных эффектов, гормон роста и ИФР-1 обладают локальным действием, комплексным механизмом регуляции в каждом органе и ткани. В частности, гормон роста и ИФР-1 являются одними из важнейших факторов, влияющих на развитие костной ткани. ГР стимулирует линейный рост эпифизарной пластинки в молодом возрасте, действуя напрямую и через ИФР-1 в хондроцитах 6–8. Зона роста эпифизарной пластинки состоит из 3-х слоев на различной стадии дифференцировки: пограничная зона, пролиферирующая зона и гипертрофированная зона 9. В пограничной зоне прехондроциты медленно делятся, они являются предшественниками пролиферирующих хондроцитов. В пролиферирующей зоне хондроциты делятся с высокой скоростью в одной плоскости, благодаря чему клетки располагаются линейно, увеличивая длину кости. На конце пластины они дифференцируются в гипертрофированные хондроциты и формируют гипертрофированную зону, которую прорастают кровеносные сосуды. При прорастании кровеносными сосудами происходит кальцификация хрящевой ткани и образуется новая костная ткань 9, после чего на протяжении всей жизни она подвергается непрерывному процессу резорбции и синтеза- костному ремоделированию, в котором ГР также принимает участие.
На конце пластины они дифференцируются в гипертрофированные хондроциты и формируют гипертрофированную зону, которую прорастают кровеносные сосуды. При прорастании кровеносными сосудами происходит кальцификация хрящевой ткани и образуется новая костная ткань 9, после чего на протяжении всей жизни она подвергается непрерывному процессу резорбции и синтеза- костному ремоделированию, в котором ГР также принимает участие.
Микроскопически различают два типа костной ткани. Первый – кортикальная или компактная кость, является очень плотной, она пронизана кровеносными сосудами, проходящими через сеть канальцев. В основном, она образует тело длинных костей. Второй тип – трабекулярная или губчатая кость — пористая находится вблизи суставных поверхностей, на конце длинных костей и внутри позвонков. Она имеет сложную трехмерную структуру, состоящую из распорок и пластинок.
В 1892 году, Wolf обнаружил, что ориентация трабекул совпадает с направлением траектории давления. Он предположил, что костная нагрузка, тем или иным образом, ощущается, и кость, соответственно, адаптирует свою структуру к новым условиям 10. Например, при отсутствии физической нагрузки (во время покоя, при космическом полете или долгом пребывании на постельном режиме) – объем костной ткани уменьшается 11–13, тогда как при регулярной физической нагрузке происходит увеличение костной массы 14. Способность кости адаптироваться к механическим нагрузкам реализуется благодаря сопряженному действию остеокластов и остеобластов, способствующих постоянной костной резорбции и новообразованию костной ткани. Frost назвал этот физиологический механизм ремоделированием костной ткани 15. Ремоделирование — это сопряженные во времени процессы локальной резорбции и формирования костной ткани в небольших блоках посредством базисной мультиклеточной единицы, функцией которой является поддержание костной массы.
Например, при отсутствии физической нагрузки (во время покоя, при космическом полете или долгом пребывании на постельном режиме) – объем костной ткани уменьшается 11–13, тогда как при регулярной физической нагрузке происходит увеличение костной массы 14. Способность кости адаптироваться к механическим нагрузкам реализуется благодаря сопряженному действию остеокластов и остеобластов, способствующих постоянной костной резорбции и новообразованию костной ткани. Frost назвал этот физиологический механизм ремоделированием костной ткани 15. Ремоделирование — это сопряженные во времени процессы локальной резорбции и формирования костной ткани в небольших блоках посредством базисной мультиклеточной единицы, функцией которой является поддержание костной массы.
При гомеостатическом равновесии резорбция и синтез сбалансированы, поскольку старая кость непрерывно замещается новой тканью. Это гарантирует сохранение механической целостности кости без серьезных патоморфологических изменений 15.
Под воздействием гормона роста происходит пролиферация и созревание мезенхимальных предшественников до остеобластов и хондроцитов, при этом тормозится их превращение в адипоциты 16. Данному процессу способствует снижение экспрессии фетального антигена-1, который является растворимой формой преадипоцитарного фактора-1 (Pref-1)) 17. Поскольку в хондроцитах и остеобластах экспрессируются рецепторы к ГР, он может воздействовать на эти клетки напрямую 18–20. Сигнал, возникающий при соединении гормона роста с рецептором, передается путем каскадного фосфорилирования белков, в результате которого активируются факторы транскрипции. В остеобластах в качестве таких факторов ГР использует преобразователь сигнала и активатор транскрипции 5 (ПСАТ 5) 21,22, а также митоген- активируемые протеинкиназы (МАПК) 23,24. Факторы МАПК и ПСАТ 5 участвуют в передаче сигнала, способствующего экспрессии различных генов. Эти протеинкиназы увеличивают активность фактора транскрипции-2 (ФТ-2), который является универсальным фактором транскрипции для всех генов, использующих РПК полимеразу 2. В частности ФТ-2 повышает экспрессию костных морфогенетических белков, что приводит к росту и дифференцировке остеобластов и формированию костной ткани 25–27. Таким образом, гормон роста может влиять на функцию остеобластов через различные внутриклеточные сигнальные системы, 20,28,29.
В частности ФТ-2 повышает экспрессию костных морфогенетических белков, что приводит к росту и дифференцировке остеобластов и формированию костной ткани 25–27. Таким образом, гормон роста может влиять на функцию остеобластов через различные внутриклеточные сигнальные системы, 20,28,29.
Известны и другие механизмы супрессивного влияния ГР на функцию остеокластов. Так, ГР стимулирует продукцию и накопление остеопротегерина 30–33, повышение концентрации которого блокирует рецепторы RANK и RANKL, что способствует торможению мобилизации, дифференцировки и активации остеокластов.
При костном ремоделировании образуются различные вещества, по концентрации которых в крови можно судить об интенсивности процессов синтеза и резорбции костей. Так, к маркерам остеобластной активности относятся:
- Остеокальцин (ОС) – небольшой неколлагеновый белок, связывающий гидроксиапатит, он продуцируется остеобластами. Между уровнем ОС в крови и скоростью костеобразования существует высокая корреляция.

- Карбокси (С) и амино (N) – концевые пропептиды проколлагена I типа (СПП I и NПП I; PICP и PINP) – это большие частично глобулярные домены, которые отделяются от синтезированной остеобластами молекулы проколлагена с помощью специфических пептидаз. Образовавшаяся в результате молекула коллагена I типа включается в построение фибрилл костного матрикса, а отщепленные пропептиды из внеклеточной среды поступают в кровоток. Соотношение между числом продуцируемых молекул коллагена и числом образовавшегося и поступающего в кровоток PICP или PINP составляет 1:1, а следовательно, оба пропептида могут быть использованы для количественной оценки вновь синтезируемого остеобластами коллагена I типа и N- и C- концевых прямых участков (N и C-телопептидов) молекул коллагена и связывают их со спиралевидными участками соседних молекул.
Маркеры резорбции (активности остеокластов):
- NTX (NT – N телопептиды, X – сшивка)- большие фрагменты коллагена, которые в результате действия протеолитического фермента остеокластов попадают в кровоток из зоны резорбции кости.
 Уровень NTX в крови или моче, отражает суммарную активность остеокластов, что позволяет его считать одним из лучших маркеров резорбции кости.
Уровень NTX в крови или моче, отражает суммарную активность остеокластов, что позволяет его считать одним из лучших маркеров резорбции кости. - Другой протеолитический фермент образует в зоне резорбции большие фрагменты, состоящие из двух С-телопептидов одной молекулы коллагена I типа, спиралевидного сегмента другой молекулы коллагена и поперечной сшивки между ними. Эти фрагменты: ICTP или CTXMMP попадают в кровоток, их общее название CrossLaps.
- Пиридиновые поперечные связи состоят из пиридинолинов (ПИР) и дезоксипиридинолинов (ДПИР). Из зон резорбции они поступают в кровь, а затем выводятся с мочой. Между такими маркерами резорбции, как NTX, CTXMMP, ПИР, ДПИР и гистоморфометрическими показателями резорбции кости получена хорошая корреляция.
Структурные изменения скелета при акромегалии
Как было описано выше, регуляция костного ремоделирования является многофакторным процессом. Каждый фактор имеет свои клетки- мишени или действует опосредованно. Большинство внекостных факторов влияют на активность остеобластов. Активные остеобласты в процессе синтеза костной ткани вырабатывают вещества, активирующие остеокласты 34. Поэтому при избыточной стимуляции остеобластов, активность остеокластов будет повышаться, и резорбция костной ткани может превосходить остеосинтез. При избытке ГР и ИФР-1 происходит активация остеобластов, а также повышается уровень остеопротегерина, который блокирует активацию остеокластов 35. В результате, это может теоретически приводить как к повышению, так и к снижению минеральной плотности костей. В силу сложности взаимодействий при костном ремоделировании трудно прогнозировать влияние избытка ГР и ИФР-1 на этот процесс.
Активные остеобласты в процессе синтеза костной ткани вырабатывают вещества, активирующие остеокласты 34. Поэтому при избыточной стимуляции остеобластов, активность остеокластов будет повышаться, и резорбция костной ткани может превосходить остеосинтез. При избытке ГР и ИФР-1 происходит активация остеобластов, а также повышается уровень остеопротегерина, который блокирует активацию остеокластов 35. В результате, это может теоретически приводить как к повышению, так и к снижению минеральной плотности костей. В силу сложности взаимодействий при костном ремоделировании трудно прогнозировать влияние избытка ГР и ИФР-1 на этот процесс.
При активной акромегалии по данным исследований Svensson, а позднее Lely, Ueland и Bolanowski был отмечен более высокий костный метаболизм в сравнении с контрольной группой 36–39. Выводы были сделаны по результатам определения маркеров костного ремоделирования, таких как остеокальцин, бета- кросслапс, Д-Пир и N-телопептид коллагена 37,38,40–46. N-телопептид коллагена был повышен у абсолютного большинства пациентов и коррелировал с уровнем гормона роста, уровень остеокальцина был также повышен у 50% пациентов. Во всех вышеперечисленных исследованиях показано, что при акромегалии происходит одновременно повышение маркеров резорбции и синтеза кости, в результате было спрогнозировано снижение МПК губчатых костей за счет преобладания резорбции.
N-телопептид коллагена был повышен у абсолютного большинства пациентов и коррелировал с уровнем гормона роста, уровень остеокальцина был также повышен у 50% пациентов. Во всех вышеперечисленных исследованиях показано, что при акромегалии происходит одновременно повышение маркеров резорбции и синтеза кости, в результате было спрогнозировано снижение МПК губчатых костей за счет преобладания резорбции.
Остеопения и остеопороз сами по себе не имеют симптомов, поэтому для своевременной диагностики необходимо проводить скрининговые исследования. Клиническая манифестация происходит при возникновении осложнения- компрессионного перелома позвонка, которое свойственно пациентам с акромегалией (частота переломов до 6,5 раз чаще, чем в контрольной группе) 47. Снижение плотности позвонков объясняется более высокой чувствительностью трабекулярной костной ткани по сравнению с кортикальной, ее плотность и состав изменяются быстрее всего под воздействием различных факторов, в том числе и ГР и ИФР-1.
Диагностика компрессионных переломов происходит на необратимой стадии: при возникновении болевого синдрома. Кроме того под действием избытка ГР и ИФР-1 происходит разрастание надкостницы, формирование остеофитов, кальцификация связок, что также способствует развитию болевого синдрома, из-за сдавления нервных волокон. Разрастание надкостницы приводит к свойственному для акромегалии укрупнению надбровных дуг, скуловых костей, верхней и нижней челюсти, увеличению размера стоп и кистей, то есть классические симптомы акромегалии – являются проявлением остеоартропатии.
При своевременном выявлении остеопении или остеопороза есть возможность остановить или даже обратить вспять снижение МПК при помощи лекарственных препаратов.
При определении минеральной плотности костей (МПК) у пациентов с акромегалией исследователи в основном акцентируют свое внимание на влиянии таких факторов, как гипогонадизм, пол, возраст и получаемая терапия на МПК 48. Исследование влияния избытка гормона роста на кости 45 в зависимости от гонадного статуса, активности заболевания и пола показало: МПК у больных гипогонадизмом была выше чем у пациентов без гипогонадизма вне зависимости от компенсации заболевания и других исследованных факторов. Это говорит о преобладающем влиянии половых гормонов на МПК, в сравнении с ГР и ИФР-1. Если использовать МПК в качестве группировочного параметра, то в группе с остеопенией большую распространенность и длительность будет иметь гипогонадизм, а также будет выявляться отрицательная корреляция между длительностью гипогонадизма и МПК позвоночника 44. Таким образом, МПК позвоночника всецело зависит от гонадного статуса. В исследовании Bolanowski была выявлена отрицательная корреляция костной плотности в дистальном отделе лучевой кости (у женщин), проксимальным отделом бедренной кости (у мужчин) и гипогонадизмом 38 . Из вышеприведенных данных можно сделать вывод о ведущей роли половых гормонов в поддержании МПК. При сравнении гипо- и эугонадных пациентов роль гормона роста и ИФР-1 остается на втором плане. Для того, чтобы приблизиться к пониманию их роли в костном обмене следует изучить группы пациентов, однородные по гонадному статусу. Кроме заболеваний, вызывающих гипогонадизм, вероятное влияние на МПК может оказывать возрастное снижение половых гормонов.
Это говорит о преобладающем влиянии половых гормонов на МПК, в сравнении с ГР и ИФР-1. Если использовать МПК в качестве группировочного параметра, то в группе с остеопенией большую распространенность и длительность будет иметь гипогонадизм, а также будет выявляться отрицательная корреляция между длительностью гипогонадизма и МПК позвоночника 44. Таким образом, МПК позвоночника всецело зависит от гонадного статуса. В исследовании Bolanowski была выявлена отрицательная корреляция костной плотности в дистальном отделе лучевой кости (у женщин), проксимальным отделом бедренной кости (у мужчин) и гипогонадизмом 38 . Из вышеприведенных данных можно сделать вывод о ведущей роли половых гормонов в поддержании МПК. При сравнении гипо- и эугонадных пациентов роль гормона роста и ИФР-1 остается на втором плане. Для того, чтобы приблизиться к пониманию их роли в костном обмене следует изучить группы пациентов, однородные по гонадному статусу. Кроме заболеваний, вызывающих гипогонадизм, вероятное влияние на МПК может оказывать возрастное снижение половых гормонов. По результатам проспективного исследования МПК мужчин и женщин с 25-44 лет Emaus было выявлено линейное возрастной снижение показателей МПК (по результатам двуэнергетической рентгеновской абсорбциометрии) относительно начальных значений от 25 лет. При этом значимое различие в абсолютных значениях МПК между мужчинами и женщинами было зафиксировано только в возрастном диапазоне 35-39 лет, а стандартное отклонение от среднего значения МПК для данного возраста (Z- критерий) значимо не различалось 49. По результатам исследования Emaus можно сделать вывод об отсутствии различий МПК между мужчинами и женщинами в возрасте от 25 до 44 лет при использовании Z- критерия для интерпретации результатов денситометрии. При оценке МПК мужчин и женщин во всех возрастных группах по результатам исследования Anburajan данных о значимом различии между мужчинами и женщинами получено не было 50. Вышеприведенные исследования свидетельствуют об отсутствии необходимости разделять мужчин и женщин при оценке факторов, влияющих на МПК.
По результатам проспективного исследования МПК мужчин и женщин с 25-44 лет Emaus было выявлено линейное возрастной снижение показателей МПК (по результатам двуэнергетической рентгеновской абсорбциометрии) относительно начальных значений от 25 лет. При этом значимое различие в абсолютных значениях МПК между мужчинами и женщинами было зафиксировано только в возрастном диапазоне 35-39 лет, а стандартное отклонение от среднего значения МПК для данного возраста (Z- критерий) значимо не различалось 49. По результатам исследования Emaus можно сделать вывод об отсутствии различий МПК между мужчинами и женщинами в возрасте от 25 до 44 лет при использовании Z- критерия для интерпретации результатов денситометрии. При оценке МПК мужчин и женщин во всех возрастных группах по результатам исследования Anburajan данных о значимом различии между мужчинами и женщинами получено не было 50. Вышеприведенные исследования свидетельствуют об отсутствии необходимости разделять мужчин и женщин при оценке факторов, влияющих на МПК. Плотность костей очень вариабельный показатель, зависящий от множества факторов, поэтому в среднем в популяции он не различается. Также по результатам исследований было выявлено возрастное снижение МПК у обоих полов с переменной динамикой, однако различие МПК после 50 лет у мужчин и женщин оказалось незначимым 50. Схожие результаты были получены при обследовании 7620 мужчин и женщин всех возрастов в исследовании Berntsen. По результатам оценки МПК предплечья статистически значимого различия между полами ни в одной из возрастных групп получено не было 51. В исследовании Emaus обращается особое внимание на индивидуальность МПК для конкретного человека и высокая зависимость этого показателя от присутствия факторов, способствующих снижению МПК 52. В результате для проведения исследований, связанных с определением МПК можно набирать пациентов любого возраста и пола, эти факторы можно считать незначимыми, а деление на группы лучше осуществлять по предполагаемому фактору, влияющему на МПК.
Плотность костей очень вариабельный показатель, зависящий от множества факторов, поэтому в среднем в популяции он не различается. Также по результатам исследований было выявлено возрастное снижение МПК у обоих полов с переменной динамикой, однако различие МПК после 50 лет у мужчин и женщин оказалось незначимым 50. Схожие результаты были получены при обследовании 7620 мужчин и женщин всех возрастов в исследовании Berntsen. По результатам оценки МПК предплечья статистически значимого различия между полами ни в одной из возрастных групп получено не было 51. В исследовании Emaus обращается особое внимание на индивидуальность МПК для конкретного человека и высокая зависимость этого показателя от присутствия факторов, способствующих снижению МПК 52. В результате для проведения исследований, связанных с определением МПК можно набирать пациентов любого возраста и пола, эти факторы можно считать незначимыми, а деление на группы лучше осуществлять по предполагаемому фактору, влияющему на МПК. Поэтому для оценки влияния гормона роста и ИФР-1 на МПК необходимо исключить пациентов с гипогонадизмом из исследования и разделить оставшихся пациентов на группы по степени активности акромегалии. Пациенты с гипогонадизмом могут быть включены в исследование 36,38 при наличии заместительной терапии, так как все эффекты гипогонадизма на кости при этом гипотетически нивелируются 53.
Поэтому для оценки влияния гормона роста и ИФР-1 на МПК необходимо исключить пациентов с гипогонадизмом из исследования и разделить оставшихся пациентов на группы по степени активности акромегалии. Пациенты с гипогонадизмом могут быть включены в исследование 36,38 при наличии заместительной терапии, так как все эффекты гипогонадизма на кости при этом гипотетически нивелируются 53.
Минеральная плотность костной ткани при акромегалии
Для определения минеральной плотности костей чаще всего используется двуэнергетическая рентгеновская абсорбциометрия- хорошо себя зарекомендовавший метод. Его точность статистически значимо не отличается от компьютерной количественной томографии 54. С ее помощью оценивается преимущественно плотность трабекулярной костной ткани, наиболее чувствительной к метаболическим изменениям костей.
В исследовании Bolanowski получены данные об увеличении плотности трабекулярной ткани под воздействием избытка ГР 55, это подтверждается в исследовании Battista: хронический избыток гормона роста имеет анаболический эффект на губчатую костную массу у пациентов с акромегалией 56. В исследовании Kaji при обследовании пациентов с акромегалией отмечалось повышение МПК позвоночника, проксимального отдела бедренной кости и лучевой кости в сравнении с контролем 57, исходя из этих результатов складывается впечатление, что избыток ГР и ИФР-1 оказывает протективное влияние кости. Это частично было подтверждено Madeira: при проведении множественного линейного регрессионного анализа была выявлена положительная корреляция между ГР и Z-критерием поясничного отдела, а также между тощей массой и МПК проксимального отдела бедра 54. Использование Z- критерия удобно при сравнении плотности костей в любых возрастных группах, однако в клинической практике Z- критерий в старшей возрастной группе не коррелирует с частотой переломов, поэтому предпочтительно использовать различные критерии (T- или Z-) в зависимости от возраста. В исследовании Kotzmann еще раз подтверждается протективное влияние ГР и ИФР-1 на МПК 43. В вышеприведенных исследованиях пациенты не были разделены на группы, при этом гипогонадизм был критерием исключения, рассчитывалась только корреляция анализируемых показателей.
В исследовании Kaji при обследовании пациентов с акромегалией отмечалось повышение МПК позвоночника, проксимального отдела бедренной кости и лучевой кости в сравнении с контролем 57, исходя из этих результатов складывается впечатление, что избыток ГР и ИФР-1 оказывает протективное влияние кости. Это частично было подтверждено Madeira: при проведении множественного линейного регрессионного анализа была выявлена положительная корреляция между ГР и Z-критерием поясничного отдела, а также между тощей массой и МПК проксимального отдела бедра 54. Использование Z- критерия удобно при сравнении плотности костей в любых возрастных группах, однако в клинической практике Z- критерий в старшей возрастной группе не коррелирует с частотой переломов, поэтому предпочтительно использовать различные критерии (T- или Z-) в зависимости от возраста. В исследовании Kotzmann еще раз подтверждается протективное влияние ГР и ИФР-1 на МПК 43. В вышеприведенных исследованиях пациенты не были разделены на группы, при этом гипогонадизм был критерием исключения, рассчитывалась только корреляция анализируемых показателей. Целью исследований было выявить связь активности ГР/ИФР-1 с минеральной плотностью костей. Это единственный тип протокола, позволяющий получить значимые результаты без деления на группы, однако во внимание не принималось специфическое для акромегалии уплотнение окружающих тканей, способное повлиять на результат денситометрии.
Целью исследований было выявить связь активности ГР/ИФР-1 с минеральной плотностью костей. Это единственный тип протокола, позволяющий получить значимые результаты без деления на группы, однако во внимание не принималось специфическое для акромегалии уплотнение окружающих тканей, способное повлиять на результат денситометрии.
В исследовании Savine обследовано менее 30 больных акромегалией и не выявлено корреляции между МПК и содержанием ГР, ИФР-1, тестостероном или эстрадиолом, кроме того концентрация остеокальцина крови не коррелировала ни с одним из вышеперечисленных показателей 52. МПК одинаково у компенсированных, некомпенсированных, эу- и гипогонадных пациентов во всех отделах 58. В этом исследовании используется слишком маленькая выборка пациентов, что не позволило получить статистически значимое число пациентов при делении на группы. Стоит также отдельно отметить, что при делении пациентов на группы по степени компенсации уровни ГР и ИФР-1 должны статистически значимо отличаться, что не было отражено в материалах и методах исследования. Из вышеприведенного примера видно, как дизайн исследования значительным образом влияет на результаты. Один из самых распространенных протоколов исследования МПК и костного обмена при акромегалии включает в себя деление пациентов на группы по активности, проведение им денситометрии, анализ крови на маркеры костного ремоделирования (бета- кросслапс и остеокальцин), но вместе с тем в исследование включались пациенты с различным гонадным статусом 38,40,45,59–61. Основными недостатками таких исследований можно считать включение в исследование пациентов с гипогонадизмом и отсутствие дифференцированного анализа МПК в различных локализациях. В результате оказывается невозможно сделать вывод о влиянии ГР и ИФР-1 на МПК. Количественная компьютерная томография и костная биопсия показали различный ответ трабекулярной и кортикальной кости на избыток ГР/ИФР-1 31. По результатам анализа плотности костей можно сделать вывод о специфическом воздействии ГР/ИФР-1 на метаболизм губчатой и компактной костной ткани.
Из вышеприведенного примера видно, как дизайн исследования значительным образом влияет на результаты. Один из самых распространенных протоколов исследования МПК и костного обмена при акромегалии включает в себя деление пациентов на группы по активности, проведение им денситометрии, анализ крови на маркеры костного ремоделирования (бета- кросслапс и остеокальцин), но вместе с тем в исследование включались пациенты с различным гонадным статусом 38,40,45,59–61. Основными недостатками таких исследований можно считать включение в исследование пациентов с гипогонадизмом и отсутствие дифференцированного анализа МПК в различных локализациях. В результате оказывается невозможно сделать вывод о влиянии ГР и ИФР-1 на МПК. Количественная компьютерная томография и костная биопсия показали различный ответ трабекулярной и кортикальной кости на избыток ГР/ИФР-1 31. По результатам анализа плотности костей можно сделать вывод о специфическом воздействии ГР/ИФР-1 на метаболизм губчатой и компактной костной ткани. Изолированный анализ воздействия избыточной секреции ГР и ИФР-1 на губчатую и трубчатую костную ткань позволяет сделать более точные выводы о их роли в поддержании МПК.
Изолированный анализ воздействия избыточной секреции ГР и ИФР-1 на губчатую и трубчатую костную ткань позволяет сделать более точные выводы о их роли в поддержании МПК.
Клинические проявления снижения МПК у пациентов с акромегалией
При исследовании распространенности переломов позвонков у женщин с акромегалией выявлена положительная корреляция с возрастом и уровнем ИФР-1. Женщины с наличием переломов дольше находятся в постменопаузе, чем женщины без переломов. Частота переломов выше у пациентов с активной акромегалией в сравнении с компенсированной. У женщин с переломами в анамнезе и компенсированной акромегалией в 57,1% был остеопороз, 42,9% была остеопения, у женщин из группы с активной акромегалией в 41,7% был нормальный Т- критерий, у 33,3% была остеопения и у 25,0% был остеопороз 62. По результатам исследования можно сделать вывод о протективном действии избытка ГР и ИФР-1 на МПК позвонков у женщин. По данным Bonadonna с соавторами пациенты с наличием или отсутствием переломов не имеют значимого различия по возрасту или МПК. По данным рентгенографии позвоночные деформации наблюдаются чаще у женщин в менопаузе с активной акромегалией 62, из этого можно сделать вывод о повышенном риске компрессионных переломов позвонков при акромегалии, то есть противоположный предыдущему исследованию. Также в исследовании Bonadonna и соавторов выявлена корреляция наличия деформации позвонков у пациентов с акромегалией с продолжительностью активного заболевания 62. Эти данные подтверждаются Mazziotti с соавторами: согласно многофакторной логической регрессии, единственным фактором риска переломов является продолжительность акромегалии 63. Результаты этого исследования говорят об отрицательном влиянии длительной экспозиции избытка гормона роста на МПК позвонков, что согласуется с описанными выше механизмами действия гормона роста на кости. Наличие корреляции частоты переломов позвонков с продолжительностью акромегалии косвенно свидетельствует об ускорении костного ремоделирования. В то же время при денситометрии у пациентов с активной акромегалией снижение МПК менее выражено, это может быть связано как с уплотнением и оссификацией связочного аппарата позвоночника и маскированием истинной плотности костей, так и с наличием компрессионных переломов позвонков, при которых денситометрия неинформативна.
По данным рентгенографии позвоночные деформации наблюдаются чаще у женщин в менопаузе с активной акромегалией 62, из этого можно сделать вывод о повышенном риске компрессионных переломов позвонков при акромегалии, то есть противоположный предыдущему исследованию. Также в исследовании Bonadonna и соавторов выявлена корреляция наличия деформации позвонков у пациентов с акромегалией с продолжительностью активного заболевания 62. Эти данные подтверждаются Mazziotti с соавторами: согласно многофакторной логической регрессии, единственным фактором риска переломов является продолжительность акромегалии 63. Результаты этого исследования говорят об отрицательном влиянии длительной экспозиции избытка гормона роста на МПК позвонков, что согласуется с описанными выше механизмами действия гормона роста на кости. Наличие корреляции частоты переломов позвонков с продолжительностью акромегалии косвенно свидетельствует об ускорении костного ремоделирования. В то же время при денситометрии у пациентов с активной акромегалией снижение МПК менее выражено, это может быть связано как с уплотнением и оссификацией связочного аппарата позвоночника и маскированием истинной плотности костей, так и с наличием компрессионных переломов позвонков, при которых денситометрия неинформативна.
Эффект лечения акромегалии на МПК
Данные о влиянии лечения акромегалии на костный метаболизм, МПК и частоту переломов весьма ограничены. После проведения трансназальной транссфеноидальной аденомэктомии или назначения аналогов соматостатина происходит снижение концентрации остеокальцина крови. Это свидетельствует о снижении активности остеобластов в результате снижения концентрации ГР в крови. При проведении контрольной денситометрии после достижения компенсации у пациентов с акромегалией использовался метод двуэнергетической абсорбциометрии и оценивалась МПК проксимального отдела бедренной кости и поясничного отдела позвоночника. Снижение активности остеобластов после компенсации акромегалии должно приводить к изменению МПК, так и происходит в проксимальном отделе бедренной кости 64–66. В то же время изменений МПК в поясничном отделе позвоночника после компенсации описано не было. Авторы, как правило, обходят стороной этот факт. Отсутствие изменения МПК позвоночника после снижения концентрации ГР связано с развитием морфологических изменений при активной акромегалии, таких как рост остеофитов, кальцификация межпозвонковых дисков, а также продольных связок позвоночника. Эти изменения маскируют истинную плотность позвонков и не регрессируют после компенсации акромегалии, что говорит о их необратимости. Снижение МПК проксимального отдела бедренной кости после компенсации происходит спустя месяцы, время может значительно различаться в каждом конкретном случае 62.
Помимо снижения активности ГР на костную ткань после компенсации, происходит также изменение концентрации паратгормона, в первую очередь снижение ночного пика секреции. При снижении концентрации ГР происходит снижение чувствительности костной ткани к паратгормону. Эти изменения вызывают снижение остеобластной активности и также способствуют снижению МПК после компенсации 67. При наличии синдрома МЭН 1 с развитием гиперпаратиреоза, уровень паратгормона после компенсации будет оставаться на прежнем уровне, что может способствовать еще большему снижению МПК после компенсации акромегалии. В силу высокого потенциала влияния синдрома МЭН 1 на костный обмен, включение в исследуемую группу лиц с этим синдромом производиться не будет.
Физиологическое и патологическое влияние ГР на тканевой состав тела
Исследование тканевого состава тела за последние годы становится все более актуальным, многие исследователи предполагают, что такие методы как толщина жировой складки, биоэлектрическое сопротивление, подводное взвешивание и двуэнергетическая абсорбциометрия могут быть более точными для определения жировой массы тела и диагностики ожирения при сравнении с индексом массы тела (ИМТ). Эти методы предоставляют более точную персонифицированную информацию о жировой массе человека. Значительным недостатком этих методов является высокая стоимость и необходимость интерпретации специалистом, что значительно сужает сферу их применения. Большая часть приведенных выше методов могут быть непригодны для рутинной клинической практики из-за технической сложности их проведения. Вдобавок, большая часть клинического опыта связана с применением ИМТ, на основании значения которого диагностируется ожирение и рассчитываются кардиоваскулярные риски. Для некоторых вышеприведенных методов определения жировой массы рассчитаны референсные значения, которые, впрочем, не предоставляют информации о персональных рисках для пациента. Вследствие этого, ни один метод, кроме ИМТ, не рекомендован в настоящее время для диагностики ожирения. Из всех методов прямого определения массы жировой ткани можно отдельно выделить рентгеновскую абсорбциометрию. Несомненным преимуществом этого метода является простота в использовании: нужен аппарат для денситометрии с программой расчета массы жировой и тощей массы тела, на столе для обследуемого есть разметка, позволяющая уложить его правильно для интерпретации результатов. Сами результаты представлены как в виде абсолютных, так и в виде относительных значений, которые можно легко интерпретировать. Правильное расположение пациента на столе аппарата позволяет также оценить распределение жировой ткани (подкожно или абдоминально) вплоть до массы жира каждой руки или ноги. Таким образом при проведении одного исследования можно получить довольно много данных. Анализ полученных результатов в перспективе позволит определить ценность каждого параметра и применять их с целью определения индивидуальных рисков для пациента.
Влияние ГР на жировую ткань
ГР модулирует депонирование жировой ткани, а также влияет на адипогенез посредством прямой стимуляции преадипоцитов и адипоцитов через факторы транскрипции, включая сигнальную систему STAT 16,68,69. У пациентов с акромегалией отмечается сниженная жировая масса тела, что связано с прямым липолитическим эффектом ГР 70. Наиболее распространенными методами определения жировой массы тела в настоящее время являются метод биоэлектрического сопротивления и двуэнергетическая рентгеновская абсорбциометрия (ДРА), при использовании этих методов отмечено снижение массы жира у пациентов с акромегалией 57,71, в то же время относительное содержание жира не отличалось от контрольной группы 72. Катаболическое действие избытка ГР на жировую ткань подтверждается потерей жировой массы на фоне прекращения терапии акромегалии 73. Нормализация ГР посредством использовании аналогов соматостатина сопровождается увеличением жировой массы тела через 6 недель после достижения целевых значений ГР 72, такая же тенденция отмечается и после хирургического лечения 74.
Снижение ГР в результате лечения акромегалии приводит к изменению состава тела. Все исследователи отмечают статистически значимый рост жировой ткани после достижения компенсации. Эти изменения были зафиксированы при исследовании состава тела посредством двуэнергетической абсорбциометрии. В то же время вес пациентов достоверно не менялся. Повышение жировой массы тела после компенсации акромегалии связано со снижением катаболического действия ГР на жировую ткань. Повышение жировой массы компенсируется снижением массы воды в межклеточной жидкости, которая при рентгеновской абсорбциометрии включается в тощую массу тела, в результате общий вес не меняется 70.
Влияние ГР на тощую массу тела
Заместительная терапия гормоном роста приводит к увеличению тощей массы тела и снижению жировой, как было показано в исследованиях состава тела у пациентов с приобретенным ГР дефицитом 75,76. Масса жировой ткани пропорционально снижается с повышением концентрации ГР, и эта закономерность прослеживается как у пациентов с ГР дефицитом, получающих заместительную терапию, так и у пациентов с акромегалией. Увеличение массы тощей ткани тела при заместительной терапии ГР может свидетельствовать о восстановлении мышечной массы. Мышечная масса имеет предел увеличения массы под действием ГР, поэтому избыток гормона роста не может привести к ее дальнейшему росту при избытке ГР 77. В то же акромегалия ассоциирована с более высокой тощей массой тела в сравнении с контрольной группой при использовании ДРА 57,72 и биоэлектрического сопротивления 73. Кроме того, терапия акромегалии приводит к снижению тощей массы тела после хирургического лечения 78 и терапии аналогами соматостатина 72, что подтверждено рентгеновской абсорбциометрией. Рост тощей массы тела в условиях избытка ГР может объясняться развитием интерстициального отека за счет усиления реабсорбции и накопления натрия. Наиболее убедительно подтвердить предположение об отеке можно комплексным анализом массы и содержания калия, с помощью этого метода можно определить клеточную массу. Pirlich с соавторами при помощи этого метода определили массу клеток у 18 пациентов с акромегалией и контрольной группы и не нашли различия 79, эти данные подтверждают предположение об интерстициальном отеке при избытке ГР. Масса межклеточной жидкости при использовании ДРА для оценки состава тела входит в тощую массу тела. Доказательством того, что именно избыток ГР приводит к накоплению жидкости могут служить результаты исследования Landin и соавторов 80, по результатам которого у 8 пациентов с акромегалией через 2 недели после хирургического лечения было отмечено снижение тощей массы тела. Быстрое снижение тощей массы тела может происходить только за счет снижения массы жидкости в интерстициальной ткани. Накопление воды является главной теорией, объясняющей увеличение тощей массы тела.
Хотелось бы обратить внимание на отсутствие контрольной группы или группы сравнения в проспективных исследования состава тела у пациентов с акромегалией на фоне лечения. Сравнение с другими группами позволило бы определить, снижается ли тощая масса тела до уровня контрольной группы. Недостаточное снижение тощей массы тела после лечения акромегалии может свидетельствовать о дополнительных факторах, помимо отека, которые приводят к увеличению тощей массы тела при гиперсекреции ГР. Есть вероятность, что имеется гораздо больше факторов, посредством которых изменяется состав тела. Для их выявления необходимо учитывать множество показателей, таких как длительность акромегалии, период ремиссии или компенсации, а также пол и возраст. Если будет выявлена связь между продолжительностью акромегалии, ее активностью или периодом компенсации, это позволит говорить о возможности использования тощей массы тела в качестве дополнительного маркера активности заболевания. Отсутствие полного восстановления тощей массы тела до популяционных значений может говорить о необратимых изменениях в составе тканей, которые потребуют дальнейших целенаправленных исследований.
Список литературы
- Mayo KE, Cerelli GM, Lebo R V, Bruce BD, Rosenfeld MG, Evans RM. Gene encoding human growth hormone-releasing factor precursor: structure, sequence, and chromosomal assignment. Proc Natl Acad Sci U S A. 1985;82(1):63-67.
- Vance ML. Growth-hormone-releasing hormone. Clin Chem. 1990;36(3):415-420. doi:10.1016/j.tem.2011.03.006.
- Пронин ВС, Молитвословова НН, Дедов ИИ. Акромегалия: этиология, патогенез, клиника, диагностика, лечение. (Дедов ИИ, Мельниченко ГА, eds.). ФГУП Издательство “Известия” Управления делами Президента Российской Федерации; 2009. Available at: http://books.google.ru/books/about/???????????.html?id=ph5YSQAACAAJ&pgis=1. Accessed May 6, 2014.
- Ugolev AM. Non-digestive functions of the intestinal hormones (enterines). New data and hypotheses based on experimental duodenectomy (Short review). Acta Hepatogastroenterol (Stuttg). 1975;22(5):320-326.
- Пронин ВС, Потешкин ЮЕ, Гитель ЕП, et al. Современная стратегия диагностики и лечения соматотропином. Москва: “Гэотар- Медиа”; 2013.
- Kaplan SA, Cohen P. The somatomedin hypothesis 2007: 50 years later. J Clin Endocrinol Metab. 2007;92(12):4529-4535. doi:10.1210/jc.2007-0526.
- Green H, Morikawa M, Nixon T. A dual effector theory of growth-hormone action. Differentiation. 1985;29(3):195-198. doi:10.1111/j.1432-0436.1985.tb00316.x.
- Zezulak KM, Green H. The generation of insulin-like growth factor-1—sensitive cells by growth hormone action. Science. 1986;233(4763):551-553.
- Nilsson O, Marino R, De Luca F, Phillip M, Baron J. Endocrine regulation of the growth plate. Horm Res. 2005;64(4):157-165.
- Pearson OM, Lieberman DE. The aging of Wolff’s “law”: ontogeny and responses to mechanical loading in cortical bone. Am J Phys Anthropol. 2004;Suppl 39:63-99. doi:10.1002/ajpa.20155.
- Bauman WA, Spungen AM, Wang J, Pierson RN, Schwartz E. Continuous loss of bone during chronic immobilization: a monozygotic twin study. Osteoporos Int. 1999;10(2):123-127. doi:10.1007/s001980050206.
- Vico L, Collet P, Guignandon A, et al. Effects of long-term microgravity exposure on cancellous and cortical weight-bearing bones of cosmonauts. Lancet. 2000;355(9215):1607-1611. doi:10.1016/S0140-6736(00)02217-0.
- Zerwekh JE, Ruml LA, Gottschalk F, Pak CY. The effects of twelve weeks of bed rest on bone histology, biochemical markers of bone turnover, and calcium homeostasis in eleven normal subjects. J Bone Miner Res. 1998;13(10):1594-1601. doi:10.1359/jbmr.1998.13.10.1594.
- Suominen H. Bone mineral density and long term exercise. An overview of cross-sectional athlete studies. Sports Med. 1993;16(5):316-330.
- Frost HM. A 2003 update of bone physiology and Wolff’s Law for clinicians. Angle Orthod. 2004;74(1):3-15. doi:10.1043/0003-3219(2004)074<0003:AUOBPA>2.0.CO;2.
- Gevers EF, Loveridge N, Robinson ICAF. Bone marrow adipocytes: a neglected target tissue for growth hormone. Endocrinology. 2002;143(10):4065-4073. doi:10.1210/en.2002-220428.
- Abdallah BM, Ding M, Jensen CH, et al. Dlk1/FA1 is a novel endocrine regulator of bone and fat mass and its serum level is modulated by growth hormone. Endocrinology. 2007;148(7):3111-3121. doi:10.1210/en.2007-0171.
- Barnard R, Haynes KM, Werther GA, Waters MJ. The ontogeny of growth hormone receptors in the rabbit tibia. Endocrinology. 1988;122(6):2562-2569.
- Werther GA, Haynes K, Edmonson S, et al. Identification of growth hormone receptors on human growth plate chondrocytes. Acta Paediatr Suppl. 1993;82 Suppl 3:50-3. Available at: http://www.ncbi.nlm.nih.gov/pubmed/8219477. Accessed May 6, 2014.
- Kassem M, Mosekilde L, Eriksen EF. Growth hormone stimulates proliferation of normal human bone marrow stromal osteoblast precursor cells in vitro. Growth Regul. 1994;4(3):131-135.
- Zhu T, Goh EL, Graichen R, Ling L, Lobie PE. Signal transduction via the growth hormone receptor. Cell Signal. 2001;13(9):599-616.
- Sims NA, Clément-Lacroix P, Da Ponte F, et al. Bone homeostasis in growth hormone receptor-null mice is restored by IGF-I but independent of Stat5. J Clin Invest. 2000;106(9):1095-1103.
- Joung YH, Lim EJ, Darvin P, et al. MSM Enhances GH Signaling via the Jak2/STAT5b Pathway in Osteoblast-Like Cells and Osteoblast Differentiation through the Activation of STAT5b in MSCs. PLoS One. 2012;7(10).
- Melmed S, Colao A, Barkan A, et al. Guidelines for acromegaly management: an update. J Clin Endocrinol Metab. 2009;94(5):1509-17. doi:10.1210/jc.2008-2421.
- Nakashima K, Zhou X, Kunkel G, et al. The novel zinc finger-containing transcription factor Osterix is required for osteoblast differentiation and bone formation. Cell. 2002;108(1):17-29.
- Canalis E, Economides AN, Gazzerro E. Bone morphogenetic proteins, their antagonists, and the skeleton. Endocr Rev. 2003;24(2):218-235. doi:10.1210/er.2002-0023.
- Tsuji K, Bandyopadhyay A, Harfe BD, et al. BMP2 activity, although dispensable for bone formation, is required for the initiation of fracture healing. Nat Genet. 2006;38(12):1424-1429. doi:10.1038/ng1916.
- Barnard R, Ng KW, Martin TJ, Waters MJ. Growth hormone (GH) receptors in clonal osteoblast-like cells mediate a mitogenic response to GH. Endocrinology. 1991;128(3):1459-1464.
- Slootweg MC, van Buul-Offers SC, Herrmann-Erlee MP, van der Meer JM, Duursma SA. Growth hormone is mitogenic for fetal mouse osteoblasts but not for undifferentiated bone cells. J Endocrinol. 1988;116(3):R11-R13. doi:10.1677/joe.0.116R011.
- Rubin J, Ackert-Bicknell CL, Zhu L, et al. IGF-I regulates osteoprotegerin (OPG) and receptor activator of nuclear factor-kappaB ligand in vitro and OPG in vivo. J Clin Endocrinol Metab. 2002;87(9):4273-4279. doi:10.1210/jc.2002-020656.
- Ueland T, Bollerslev J, Flyvbjerg A, Hansen TB, Vahl N, Mosekilde L. Effects of 12 months of GH treatment on cortical and trabecular bone content of IGFs and OPG in adults with acquired GH deficiency: a double-blind, randomized, placebo-controlled study.; 2002. doi:10.1210/jc.87.6.2760.
- Ueland T, Odgren PR, Yndestad A, et al. Growth hormone substitution increases gene expression of members of the IGF family in cortical bone from women with adult onset growth hormone deficiency-relationship with bone turn-over. Bone. 2003;33(4):638-645.
- Mrak E, Villa I, Lanzi R, Losa M, Guidobono F, Rubinacci A. Growth hormone stimulates osteoprotegerin expression and secretion in human osteoblast-like cells. J Endocrinol. 2007;192(3):639-645. doi:10.1677/joe.1.07073.
- Giustina A, Mazziotti G, Canalis E. Growth hormone, insulin-like growth factors, and the skeleton. Endocr Rev. 2008;29(5):535-559.
- Killinger Z, Ku??ma M, Steran????kov?? L, Payer J. Osteoarticular changes in acromegaly. Int J Endocrinol. 2012;2012.
- Svensson J. The importance of growth hormone (GH) and GH secretagogues for bone mass and density. Curr Pharm Des. 2002;8(23):2023-2032. doi:10.2174/1381612023393413.
- Ueland T, Fougner SL, Godang K, Schreiner T, Bollerslev J. Serum GH and IGF-I are significant determinants of bone turnover but not bone mineral density in active acromegaly: a prospective study of more than 70 consecutive patients. Eur J Endocrinol. 2006;155(5):709-715. doi:10.1530/eje.1.02285.
- Bolanowski M, Daroszewski J, Medraś M, Zadrozna-Sliwka B. Bone mineral density and turnover in patients with acromegaly in relation to sex, disease activity, and gonadal function. J Bone Miner Metab. 2006;24(1):72-78.
- van der Lely AJ, Tschöp M, Heiman ML, Ghigo E. Biological, physiological, pathophysiological, and pharmacological aspects of ghrelin. Endocr Rev. 2004;25(3):426-457. doi:10.1210/er.2002-0029.
- Halse J, Gordeladze JO. Total and non-dialyzable urinary hydroxyproline in acromegalics and control subjects. Acta Endocrinol (Copenh). 1981;96(4):451-7. Available at: http://www.ncbi.nlm.nih.gov/pubmed/7211103. Accessed May 6, 2014.
- de la Piedra C, Larrañaga J, Castro N, et al. Correlation among plasma osteocalcin, growth hormone, and somatomedin C in acromegaly. Calcif Tissue Int. 1988;43(1):44-45. doi:10.1007/BF02555167.
- Ezzat S, Melmed S, Endres D, Eyre DR, Singer FR. Biochemical assessment of bone formation and resorption in acromegaly. J Clin Endocrinol Metab. 1993;76(6):1452-1457.
- Kotzmann H, Bernecker P, Hübsch P, et al. Bone mineral density and parameters of bone metabolism in patients with acromegaly. J Bone Miner Res. 1993;8(4):459-465. doi:10.1002/jbmr.5650080410.
- Kayath MJ, Vieira JGH. Osteopenia occurs in a minority of patients with acromegaly and is predominant in the spine. Osteoporos Int. 1997;7(3):226-230. doi:10.1007/BF01622293.
- Scillitani A, Chiodini I, Carnevale V, et al. Skeletal involvement in female acromegalic subjects: the effects of growth hormone excess in amenorrheal and menstruating patients. J Bone Miner Res. 1997;12(10):1729-1736. doi:10.1359/jbmr.1997.12.10.1729.
- Skelton DA, Greig CA, Davies JM, Young A. Strength, power and related functional ability of healthy people aged 65-89 years. Age Ageing. 1994;23(5):371-377. doi:10.1093/ageing/23.5.371.
- Wassenaar MJE, Biermasz NR, Hamdy N a T, et al. High prevalence of vertebral fractures despite normal bone mineral density in patients with long-term controlled acromegaly. Eur J Endocrinol. 2011;164(4):475-83. doi:10.1530/EJE-10-1005.
- Bogazzi F, Cosci C, Sardella C, Martino E, Gasperi M. Acromegaly: effects on bone metabolism and mass. J Endocrinol Invest. 2005;28(10 Suppl):33-35.
- Emaus N, Berntsen GKR, Joakimsen RM, Fønnebø V. Longitudinal changes in forearm bone mineral density in women and men aged 25-44 years: the Tromsø study: a population-based study. Am J Epidemiol. 2005;162(7):633-643. doi:10.1093/aje/kwi258.
- Anburajan M, Rethinasabapathi C, Korath MP, et al. Age-related proximal femur bone mineral loss in South Indian women: a dual energy X-ray absorptiometry study. J Assoc Physicians India. 2001;49:442-445.
- Berntsen GK, Fønnebø V, Tollan A, Søgaard AJ, Magnus JH. Forearm bone mineral density by age in 7,620 men and women: the Tromsø study, a population-based study. Am J Epidemiol. 2001;153(5):465-473. doi:10.1093/aje/153.5.465.
- Savine R, Sönksen P. Growth hormone — hormone replacement for the somatopause? Horm Res. 2000;53 Suppl 3:37-41.
- Biermasz NR, Hamdy NAT, Pereira AM, Romijn JA, Roelfsema F. Long-term maintenance of the anabolic effects of GH on the skeleton in successfully treated patients with acromegaly. Eur J Endocrinol. 2005;152(1):53-60. doi:10.1530/eje.1.01820.
- Madeira M, Neto L V, de Lima GAB, et al. Effects of GH-IGF-I excess and gonadal status on bone mineral density and body composition in patients with acromegaly. Osteoporos Int. 2010;21(12):2019-2025. doi:10.1007/s00198-009-1165-x.
- Bolanowski M, Wielgus W, Milewicz A, Marciniak R. Axial bone mineral density in patients with acromegaly. Acad Radiol. 2000;7(8):592-594.
- Battista C, Chiodini I, Muscarella S, et al. Spinal volumetric trabecular bone mass in acromegalic patients: a longitudinal study. Clin Endocrinol (Oxf). 2009;70(3):378-382. doi:10.1016/j.jocd.2008.07.063.
- Kaji H, Sugimoto T, Nakaoka D, Okimura Y, Abe H, Chihara K. Bone metabolism and body composition in Japanese patients with active acromegaly. Clin Endocrinol (Oxf). 2001;55(2):175-181.
- Scillitani A, Battista C, Chiodini I, et al. Bone mineral density in acromegaly: the effect of gender, disease activity and gonadal status. Clin Endocrinol (Oxf). 2003;58(6):725-731.
- Longobardi S, Di Somma C, Di Rella F, et al. Bone mineral density and circulating cytokines in patients with acromegaly. J Endocrinol Invest. 1998;21(10):688-693.
- Lesse GP, Fraser WD, Farquharson R, Hipkin L, Vora JP. Gonadal status is an important determinant of bone density in acromegaly. Clin Endocrinol (Oxf). 1998;48(1):59-65.
- Seeman E, Wahner HW, Offord KP, Kumar R, Johnson WJ, Riggs BL. Differential effects of endocrine dysfunction on the axial and the appendicular skeleton. J Clin Invest. 1982;69(6):1302-1309.
- Bonadonna S, Mazziotti G, Nuzzo M, et al. Increased prevalence of radiological spinal deformities in active acromegaly: a cross-sectional study in postmenopausal women. J Bone Miner Res. 2005;20(10):1837-1844. doi:10.1359/JBMR.050603.
- Mazziotti G, Bianchi A, Bonadonna S, et al. Prevalence of vertebral fractures in men with acromegaly. J Clin Endocrinol Metab. 2008;93(12):4649-4655. doi:10.1210/jc.2008-0791.
- Legovini P, De Menis E, Breda F, et al. Long-term effects of octreotide on markers of bone metabolism in acromegaly: evidence of increased serum parathormone concentrations.; 1997.
- Terzolo M, Piovesan A, Osella G, et al. Serum levels of bone Gla protein (osteocalcin, BGP) and carboxyterminal propeptide of type I procollagen (PICP) in acromegaly: effects of long-term octreotide treatment. Calcif Tissue Int. 1993;52(3):188-191. doi:10.1007/BF00298716.
- Piovesan A, Terzolo M, Reimondo G, et al. Biochemical markers of bone and collagen turnover in acromegaly or Cushing’s syndrome. Horm Metab Res. 1994;26(5):234-237.
- White HD, Ahmad AM, Durham BH, et al. Effect of active acromegaly and its treatment on parathyroid circadian rhythmicity and parathyroid target-organ sensitivity. J Clin Endocrinol Metab. 2006;91(3):913-919. doi:jc.2005-1602.
- Jørgensen JOL, Møller L, Krag M, Billestrup N, Christiansen JS. Effects of growth hormone on glucose and fat metabolism in human subjects. Endocrinol Metab Clin North Am. 2007;36(1):75-87. doi:10.1016/j.ecl.2006.11.005.
- Sanders EJ, Harvey S. Growth hormone as an early embryonic growth and differentiation factor. Anat Embryol (Berl). 2004;209(1):1-9. Available at: <Go to ISI>://WOS:000225224300001.
- Bengtsson BA, Brummer RJ, Edén S, Bosaeus I. Body composition in acromegaly. Clin Endocrinol (Oxf). 1989;30(2):121-130.
- Miyakawa M, Tsushima T, Murakami H, Isozaki O, Demura H, Tanaka T. Effect of growth hormone (GH) on serum concentrations of leptin: study in patients with acromegaly and GH deficiency. J Clin Endocrinol Metab. 1998;83(10):3476-3479. doi:10.1210/jcem.83.10.5161.
- Gibney J, Wolthers T, Burt MG, Leung K-C, Umpleby AM, Ho KKY. Protein metabolism in acromegaly: differential effects of short- and long-term treatment. J Clin Endocrinol Metab. 2007;92(4):1479-1484.
- Rau H, Fischer H, Schmidt K, Lembcke B, Althoff PH. Effect of bromocriptine withdrawal in acromegaly on body composition as assessed by bioelectrical impedance analysis. Acta Endocrinol (Copenh). 1991;125(3):273-279. doi:10.1530/acta.0.1250273.
- Tominaga A, Arita K, Kurisu K, et al. Effects of successful adenomectomy on body composition in acromegaly. Endocr J. 1998;45(3):335-342. doi:10.1507/endocrj.45.335.
- Baum HB, Biller BM, Finkelstein JS, et al. Effects of physiologic growth hormone therapy on bone density and body composition in patients with adult-onset growth hormone deficiency. A randomized, placebo-controlled trial.; 1996.
- Hoffman AR, Kuntze JE, Baptista J, et al. Growth hormone (GH) replacement therapy in adult-onset gh deficiency: effects on body composition in men and women in a double-blind, randomized, placebo-controlled trial. J Clin Endocrinol Metab. 2004;89(5):2048-2056.
- Velloso CP. Regulation of muscle mass by growth hormone and IGF-I. Br J Pharmacol. 2008;154(3):557-568.
- Battezzati A, Benedini S, Fattorini A, et al. Insulin action on protein metabolism in acromegalic patients. Am J Physiol Endocrinol Metab. 2003;284(4):E823-E829.
- Pirlich M, Sch??tz T, Ockenga J, et al. Erratum: “Improved assessment of body cell mass by segmental bioimpedance analysis in malnourished subjects and acromegaly” (Clinical Nutrition (2003) vol. 22 (2) (167-174) 1054/j.clnu.2002.0017). Clin Nutr. 2004;23(2):285-286.
- Landin K, Petruson B, Jakobsson KE, Bengtsson BA. Skeletal muscle sodium and potassium changes after successful surgery in acromegaly: relation to body composition, blood glucose, plasma insulin and blood pressure. Acta Endocrinol (Copenh). 1993;128(5):418-422. doi:10.1530/acta.0.1280418.
Перечень соединений, которые должны рассматриваться как соединения товарной позиции 2937
Перечень соединений, которые должны рассматриваться
как соединения товарной позиции 2937 <*>
———————————
<*> В случае, если лекарственные средства имеют международное несобственное название или международное (модифицированное) несобственное название, опубликованное Всемирной Организацией Здравоохранения, то именно это название приводится первым с пометкой (INN) или (INNM), соответственно.
(А) ПОЛИПЕПТИДНЫЕ ГОРМОНЫ, БЕЛКОВЫЕ И ГЛИКОПРОТЕИНОВЫЕ
ГОРМОНЫ, ИХ ПРОИЗВОДНЫЕ И СТРУКТУРНЫЕ АНАЛОГИ
Сюда включаются, inter alia:
(1) Соматотропин, его производные и структурные аналоги. Соматотропин (гормон роста, GH, STH (соматотропный гормон)). Водорастворимый белок, стимулирующий рост тканей и участвующий в регуляции других фаз белкового обмена. Он секретируется соматотропными клетками передней доли гипофиза. Секреция регулируется высвобождающим фактором (соматолиберином) и ингибитором соматотропина, соматостатином. Гормон роста человека (hGH) представляет собой единственную полипептидную цепочку из 191 аминокислоты, получаемую преимущественно на основе рекомбинантной ДНК. Сюда же включаются производные и аналоги, такие как соматрем (INN) (метионил-hGH), ацетилированный hGH, дезамидо-hGH и сомнопор (INN) и такие антагонисты, как пегвисомант (INN).
(2) Инсулин и его соли. Инсулин представляет собой полипептид, содержащий 51 аминокислотную группу и образующийся в островках Лангерганса поджелудочной железы у многих животных. Человеческий инсулин может быть выделен из поджелудочной железы, модификацией бычьего или свиного инсулина или методами биотехнологии — с применением бактерий или дрожжей для получения рекомбинантного человеческого инсулина. Инсулин обеспечивает захват клетками глюкозы и прочих питательных веществ, а также запасание их в виде гликогена или жира. Чистый инсулин представляет собой белый негигроскопичный порошок аморфной структуры или блестящие кристаллы, растворимые в воде.
В клинике инсулин используют для лечения сахарного диабета. Соли инсулина включают и гидрохлорид инсулина.
(3) Кортикотропин (INN), (ACTH (адренокортикотропный гормон), адренокортикотропин). Полипептид, растворимый в воде. Стимулирует увеличение образования стероидов коры надпочечников. Гирактид (INN) является аналогом кортикотропина.
(4) Лактогенный гормон (LTH, галактин, галактогенный гормон, лютеотропин, маммотропин, пролактин). Полипептид, способный кристаллизоваться. Повышает секрецию молока и влияет на активность желтого тела.
(5) Тиротропин (INN) (тиротропный гормон, TSH (стимулирующий деятельность щитовидной железы)). Гликопротеин, регулирующий действие щитовидной железы на кровь и вывод йода из организма. Он воздействует на рост и секрецию.
(6) Фолликулостимулирующий гормон (FSH). Гликопротеин, растворимый в воде. Активизирует половые функции.
(7) Лютеинизирующий гормон (LH, ICSH (гормон, стимулирующий интерстициальные клетки), лютеиностимулин). Гликопротеин, растворимый в воде. Стимулирует половые функции путем стимуляции секреции стероидов, овуляции и развития интерстициальных клеток.
(8) Хорионический гонадотропин (INN) (hCG (хорионический гонадотропин человека)). Образуется в плаценте; это гликопротеин, извлекаемый из мочи беременных женщин. Белые кристаллы; относительно неустойчивы в водном растворе. Стимулирует созревание фолликулов.
(9) Гонадотропин сыворотки (INN) (гонадотропин сыворотки лошади (eCG)). Гонадостимулирующий гликопротеин, образующийся в плаценте и эндометрии жеребых кобыл. Исходно назывался гонадотропином сыворотки жеребой кобылы.
(10) Окситоцин (INN) (-гипофамин). Растворимый в воде полипептид. Его основное действие — сокращение матки и выделение молока молочными железами. Сюда же включаются и аналоги — карбетоцин (INN), демокситоцин (INN), и т.п.
(11) Вазопрессины: аргипрессин (INN), липрессин (INN), их производные и структурные аналоги. Вазопрессины — это полипептиды, повышающие давление крови и способствующие задержке воды почками. Также сюда включаются аналоги полипептидов, такие как терлипрессин (INN), десмопрессин (INN), и т.п.
(12) Кальцитонин (INN) (TCA (тирокальцитонин)). Гипокальциемический и гипофосфатемический полипептид.
(13) Глюкагон (INN) (HGF (гипергликемическо-гликогенолитический фактор)). Полипептид, способный повышать концентрацию глюкозы в крови.
(14) Тиролиберин (TRF, TRH). Этот полипептид стимулирует секрецию тиротропина.
(15) Гонадорелин (INN) (гонадолиберин, гонадотропина рилизинг-гормон, LRF, GnRH). Этот полипептид усиливает секрецию фолликулостимулирующего и лютеинизирующего гормонов гипофизом. Сюда же включаются полипептиды, аналогичные бусерилину (INN), госерилину (INN), фертирелину (INN), серморелину (INN) и т.п.
(16) Соматостатин (INN) (SS, SRIH, SRIF). Этот полипептид подавляет высвобождение гормона роста и TSH гипофизом и имеет нейротропное действие.
(17) Атриальный натрийуретический гормон (ANH, ANF), полипептидный гормон, выделяемый предсердиями. Когда предсердие растянуто из-за увеличения объема крови, стимулируется секреция ANH. ANH в свою очередь увеличивает экскрецию соли и воды и уменьшает давление крови.
(18) Эндотелин, полипептидный гормон, выделяемый эндотелиальными клетками всех сосудов. Несмотря на то, что эндотелин выделяется в кровоток, он действует локально паракринным образом, сокращая прилегающие гладкие мышцы сосудов и таким образом повышая давление крови.
(19) Ингибин и активин, гормоны, присутствующие в тканях половых желез.
(20) Лептин — полипептидный гормон, продуцируемый жировой тканью и, как считают, действующий на рецепторы мозга в целях регулирования массы тела и отложения жира. Сюда включается также метрелептин (INN) — рекомбинантная метиониловая производная лептина, имеющая подобную ему активность и, как считают, являющаяся аналогом лептина.
(Б) СТЕРОИДНЫЕ ГОРМОНЫ, ИХ ПРОИЗВОДНЫЕ
И СТРУКТУРНЫЕ АНАЛОГИ
(1) Кортикостероидные гормоны, выделяемые корой надпочечников, играют важную роль в процессах обмена веществ в организме. Они также называются гормонами коры надпочечников или кортикоидами и делятся главным образом на следующие две группы в зависимости от их физиологического действия: (i) глюкокортикоиды, регулирующие обмен белков и углеводов и (ii) минералокортикоиды, которые вызывают удерживание натрия и воды в организме и ускорение выведения калия. Свойства минералокортикоидов используются при лечении почечной недостаточности и болезни Аддисона. Сюда же включаются следующие кортикостероидные гормоны, их производные и аналоги:
(а) кортизон (INN). Глюкокортикоид, регулирующий обмен белков и углеводов и обладающий местным противовоспалительным действием;
(б) гидрокортизон (INN) (кортизол). Глюкокортикоид, обладающий действиями, сходными с кортизоном;
(в) преднизон (INN) (дегидрокортизон). Глюкокортикоид. Производное кортизона;
(г) преднизолон (INN) (дегидрогидрокортизон). Глюкокортикоид. Производное гидрокортизона;
(д) альдостерон (INN). Минералокортикоид;
(е) кортодоксон (INN).
Некоторые производные гормонов модифицированы таким образом, что их кортикостероидная активность подавлена, но выражен противовоспалительный эффект, считается, что они обладают гормональным действием. К ним относятся основные производные кортизона (INN), гидрокортизона (INN), преднизона (INN) и преднизолона (INN), которые используются как противовоспалительные и антиревматические средства.
(2) Галогенированные производные кортикостероидных гормонов — это стероиды, в которых атом водорода, главным образом в 6- или 9-положении в гонановом кольце, замещен на атом хлора или фтора (например, дексаметазон (INN), что значительно усиливает глюкокортикоидное и противовоспалительное действие кортикоидов, производными которых они являются. Эти производные часто дополнительно модифицируют и поставляют в виде сложных эфиров, ацетонидов (например, флуоцинолона ацетонид (INN)), и т.п.
(3) Эстрогены и прогестины. Это две главные группы половых гормонов, секретируемые мужскими и женскими репродуктивными органами. Они также могут быть получены путем синтеза. Эти гормоны также называют прогестинами и гестагенами.
Эстрогенами называются женские половые гормоны, вырабатываемые яичниками, мужскими половыми железами, надпочечниками, плацентарными и другими стероидпродуцирующими тканями. Они характеризуются способностью вызывать сильное половое влечение у самок млекопитающих. Эстрогены ответственны за развитие женских половых признаков и используются при лечении менопаузы или при изготовлении противозачаточных средств. Они включают следующие эстрогены, производные и аналоги:
(а) эстрон (INN). Основной эстроген человека;
(б) эстрадиол (INN). Важный природный эстроген;
(в) эстриол (INN). Природный эстроген;
(г) этинилэстрадиол (INN). Важный синтетический эстроген, активный при оральном употреблении и применяемый в качестве основного эстрогенного компонента в составе оральных контрацептивов;
(д) местранол (INN). Простой эфир этинилэстрадиола. Применяется как оральный контрацептив.
Прогестины — класс стероидных гормонов, получивших свое название из-за гестагенных эффектов, имеющих важное значение при возникновении и развитии беременности. Эти женские половые гормоны вырабатываются в матке при возникновении и для сохранения беременности. Из-за того, что прогестагены препятствуют овуляции, они используются как компоненты противозачаточных средств. Они включают:
(а) прогестерон (INN). Главный прогестин человека и промежуточный продукт в биосинтезе эстрогенов, андрогенов и кортикостероидов. Он вырабатывается клетками желтого тела после выхода яйцеклетки и надпочечниками, а также плацентой и мужскими половыми железами;
(б) прегнандиол, встречающийся в природе прогестин с гораздо меньшей физиологической активностью, чем прогестерон.
(4) Прочие стероидные гормоны.
Андрогены — основная группа половых гормонов, которые не были упомянуты выше, вырабатываются главным образом мужскими половыми железами и в меньшей степени яичниками, надпочечниками и плацентой. Андрогены ответственны за развитие мужских половых признаков. Андрогены влияют на обмен веществ, то есть имеют анаболический эффект. Тестостерон (INN) является одним из наиболее важных андрогенов.
Сюда также включаются синтетические стероиды, используемые преимущественно для подавления или устранения действия гормонов, такие как антиэстрогены, антиандрогены и антипрогестины (антиэстагены). Стероидные антипрогестины являются антагонистами прогестина, находящими применение при лечении некоторых заболеваний. Примерами соединений данной группы могут служить онапристон (INN) и аглепристон (INN).
Стероиды, занимающие наиболее важное место в международной торговле, приведены ниже. Соединения перечислены в алфавитном порядке в соответствии с их краткими названиями с указанием их основного гормонального действия. При наличии двух или нескольких названий указывается то, которое принято в международном перечне несобственных названий (International Nonproprietary Names) для фармацевтических препаратов (INN), опубликованном Всемирной Организацией Здравоохранения, или в модифицированном перечне (International Nonproprietary Names Modified) (INNM). Химические названия приведены в соответствии с правилами IUPAC 1957 для номенклатуры стероидов.
Терапия гормоном роста при заболеваниях, сопровождающихся низкорослостью у детей
Авторы: S. Loche, L. Carta, A. Ibba, C. Guzzetti
Статья в формате PDF.
До 1985 года гормон роста (ГР) получали непосредственно из гипофиза животных, поэтому из-за ограниченного количества его использовали только у детей с тяжелым дефицитом ГР. Благодаря технологии рекомбинантной ДНК стало возможным получать неограниченное количество ГР, что позволило не только оптимизировать лечение пациентов с соматотропной недостаточностью, но и оценить эффективность этого препарата при ряде других патологических состояний. В настоящее время применение ГР одобрено для лечения пациентов с синдромом Тернера, хронической почечной недостаточностью, синдромом Прадера-Вилли, синдромом Нунана, дефицитом SHOX, идиопатической низкорослостью, а также детей, рожденных малыми для своего гестационного возраста. В этой статье рассмотрено использование ГР для лечения низкорослости при всех этих состояниях.
Синдром Тернера
Синдром Тернера (СТ) – наиболее распространенная хромосомная аномалия у женщин, встречающаяся с частотой приблизительно 1:2000-2500 живорожденных девочек и являющаяся одной из лидирующих причин низкорослости у женщин. СТ обусловлен отсутствием или структурными аномалиями одной из Х-хромосом. Такие пациентки обычно имеют низкий рост, гипергонадотропный гипогонадизм и легкую скелетную дисплазию. Отставание в росте, как правило, начинается пренатально, и уже в первые годы жизни наблюдается прогрессирующее снижение коэффициента стандартного отклонения роста (SDS).
Патогенез низкорослости у девочек с СТ, вероятно, многофакторный, однако недавние исследования показывают, что одной из ведущих причин является гаплонедостаточность гена SHOX (ген низкорослости, содержащий гомеобокс), расположенного в псевдоаутомосомальной области половых хромосом. Было установлено, что изменения костей кисти и запястья одинаковы у девочек с СТ и у пациентов с гаплонедостаточностью SHOX.
Конечный рост у нелеченных пациенток с СТ примерно на 20 см меньше, чем у женщин без этой патологии.
В ряде исследований была показана эффективность ГР в увеличении темпов роста и улучшении конечного результата при низкорослости у девочек с СТ, что стало одним из первых одобренных показаний для применения ГР помимо соматотропной недостаточности. Первое рандомизированное контролируемое исследование, в котором 61 девочку в возрасте 8-12 лет лечили ГР в дозе 0,3 мг/кг/нед в течение в среднем 5,7 года, показало среднее увеличение роста на 7,2 см (D.K. Stephure, 2005). В более недавнем исследовании с участием 27 девочек терапия ГР в дозе 0,1 мг/кг 3 раза в неделю в течение 7,4 года увеличила конечный рост в среднем на 5 см. Стоит отметить, что в обоих исследованиях лечение было начато в середине или конце детского периода, когда отставание в росте было уже очевидной жалобой. Другие исследования показали, что применение ГР, начатое до достижения возраста 4 лет, может обеспечить достижение нормального роста у большинства пациентов (M.L. Davenport et al., 2007; A. Linglart et al., 2011). Хотя данных о долгосрочной эффективности и безопасности лечения ГР у девочек с СТ, начатого в очень раннем возрасте, пока еще недостаточно.
Рекомендуемая доза ГР у девочек с СТ (0,035-0,050 мг/кг/сут) выше, чем при соматотропной недостаточности.
В целом ГР продемонстрировал хороший профиль безопасности у этой категории пациенток, поскольку до сих пор не было зафиксировано случаев серьезных побочных эффектов, связанных с лечением. Тем не менее рекомендуется рутинный мониторинг уровня инсулиноподобного фактора роста‑1 (ИФР‑1) и показателей углеводного обмена.
Для ускорения роста у девочек с СТ также широко используют анаболические стероиды. Два недавних исследования, проведенных в Европе, показали лучший прирост при добавлении оксандролона к ГР по сравнению с монотерапией ГР. Так, в нидерландском исследовании (L.A. Menke et al., 2010) комбинация ГР (0,045 мг/кг/сут) и оксандролона (0,03 мг/кг/сут) привела к среднему увеличению роста на 2,3 см по сравнению с монотерапией ГР, хотя в группе, получавшей оксандролон, была отмечена небольшая задержка в развитии молочных желез. В британском исследовании (E.J. Gault et al., 2011) добавление оксандролона (0,05 мг/кг/сут) к ГР привело к среднему увеличению роста на 4,5 см по сравнению с группой, получавшей только ГР (0,05 мг/кг/нед при ежедневных инъекциях). Побочные эффекты не были зафиксированы в этом исследовании.
Девочки с СТ почти всегда требуют лечения эстрогенами для коррекции недостаточности яичников. До недавних пор обычной практикой была инициация терапии эстрогенами примерно в середине пубертата во избежание уменьшения конечного роста в связи с эстроген-опосредованным закрытием эпифизарных зон роста. Однако данные относительно влияния задержки полового созревания на рост у девочек с СТ пока еще противоречивы. Так, C.A. Quigley и соавт. (2002) показали, что введение малых доз эстрогенов с 8-летнего возраста не оказывает влияния на конечный рост по сравнению с применением только ГР. Другие исследования продемонстрировали, что лечение ГР и эстрогенами, начатое в пубертатном возрасте (около 12 лет), приводит к нормализации конечного роста (C.A. Quigley et al., 2002; Y.K. van Pareren et al., 2003; O. Mehls et al., 2008). Рандомизированное двойное слепое плацебо-контролируемое исследование, проведенное в Великобритании, показало, что лечение эстрогенами, начатое в 14-летнем возрасте, дало среднее увеличение роста на 3,8 см по сравнению с теми девочками, которых начали лечить с 12 лет (E.J. Gault et al., 2011). В то же время недавние данные указывают на то, что терапия ультранизкими дозами эстрогена, начатая уже в 5-летнем возрасте, оказывает благотворное влияние на рост и другие клинические параметры (J.L. Ross et al., 2011). В двойном слепом плацебо-контролируемом испытании в дополнение к ГР у девочек с СТ применяли эстроген в суточной дозе 25 нг/кг в возрасте от 5 до 8 лет и 50 нг/кг в возрасте от 8 до 12 лет. Затем в пубертате все пациентки получали эстрогензаместительную терапию в более высоких дозах. Третья группа девочек получала только плацебо, а четвертая – только ГР. Средний рост во взрослом возрасте у пациенток, получавших эстроген и ГР, был на 0,37 SD больше, чем при монотерапии ГР.
Хроническая почечная недостаточность
У большинства пациентов с хронической почечной недостаточностью (ХПН) отмечается снижение темпов роста, которые часто не нормализуются при диализе. За замедление роста у этих больных отвечает комбинация нескольких факторов, среди которых наиболее значимыми считаются алиментарная недостаточность, дисфункция оси ГР/ИФР‑1 и терапия кортикостероидами.
Ряд исследований показал, что лечение ГР повышает скорость роста и улучшает конечный результат у детей с ХПН. Так, D. Haffner и соавт. (2000) наблюдали 38 детей с ХПН (средний возраст на момент включения в исследование – 10,4±2,2 года, средний рост – на 3,1±1,2 SD ниже нормы), которые получали ГР (0,33 мг/кг/нед) в среднем в течение 5,3 года, и 50 детей с ХПН, которым не был назначен ГР. Средний конечный рост у детей в группе терапии ГР составил 165 см для мальчиков и 156 см для девочек, при этом он оказался на 1,6±1,2 SD ниже нормы, но в то же время SDS повысился на 1,4 по сравнению с началом исследования (рСиндром Прадера-Вилли
Синдром Прадера-Вилли (СПВ) – редкое генетическое заболевание, которое является результатом отсутствия отцовской копии участка 15-й хромосомы и характеризуется множественными нарушениями, включающими гипотонус, маленькие кисти и стопы, гиперфагию с развитием ожирения, гипогонадизм, низкий рост, общую задержку развития и когнитивные нарушения. Также у этих пациентов часто встречается синдром апноэ во время сна. Распространенность СПВ составляет приблизительно 1:25 000 живорожденных младенцев.
Многие признаки СПВ схожи с симптомами соматотропной недостаточности, в частности замедление роста, снижение мышечного тонуса и изменение конституции тела. Около 80% детей с СПВ имеют дефицит ГР, а также демонстрируют субнормальную реакцию ГР на различные стимулы и снижение спонтанной секреции ГР. У большинства пациентов снижена сывороточная концентрация ИФР‑1.
Контролируемые исследования показали, что у детей с СПВ лечение ГР увеличивает рост, улучшает конституцию тела, повышает мышечную силу и даже оказывает положительное влияние на когнитивные функции (E.P. Siemensma et al., 2012).
Недавно было опубликовано клиническое руководство по терапии ГР у пациентов с СПВ (Growth Hormone Research Society, 2013). Лечение ГР можно начинать с 2 лет (до начала ожирения), хотя некоторые данные предполагают возможность начала терапии в возрасте от 4 до 6 месяцев. Критерии исключения для начала лечения ГР включают: тяжелое ожирение, неконтролируемый диабет, нелеченный тяжелый синдром апноэ во сне, активный рак и психотическое состояние. Сообщалось о нескольких внезапных смертельных исходах у пациентов с СПВ и тяжелым ожирением, получавших ГР.
Лечение ГР у пациентов с СПВ следует начинать с ежедневной дозы 0,5 мг/м2 с последующей корректировкой до рекомендуемой дозы 1,0 мг/м2 (0,035 мг/кг/сут). Уровень ИФР‑1 следует поддерживать в физиологическом диапазоне.
Синдром Нунана
Синдром Нунана (СН) является аутосомно-доминантным заболеванием с примерной частотой 1:1000-2500 живорожденных детей. Клинические признаки включают ранние трудности с кормлением, типичные черты лица, пороки сердца (стеноз клапана легочной артерии или гипертрофическая кардиомиопатия), деформации грудной клетки и позвоночника, умеренную умственную отсталость. У 50-70% пациентов с СН отмечается низкорослость: средний рост взрослых лиц с этой патологией колеблется в диапазоне 145-162,5 см для мужчин и 135-151 см для женщин.
СН обусловлен мутациями в генах, которые кодируют белки сигнального пути RAS-MAPK. Около 30-60% случаев вызваны мутациями гена PTPN11, который кодирует тирозинфосфатазу SHP2. Также описаны мутации в генах KRAS, RAF1, SOS1, NRAS и SHOC2. Однако не все пациенты с СН имеют идентифицируемую мутацию. Низкий рост наиболее часто встречается у пациентов с мутациями в гене PTPN11. Это, вероятно, связано с тем фактом, что SHP2 участвует в передаче сигнала ГР-рецептора. В некоторых исследованиях отмечено ухудшение ответа на лечение ГР, а также более низкую сывороточную концентрацию ИФР‑1 у пациентов с мутацией PTPN11, тогда как другие показали увеличение роста после длительного лечения ГР у детей с СН с мутациями PTPN11 и без них.
Применение ГР у пациентов с СН было недавно одобрено Управлением по контролю за качеством пищевых продуктов и лекарств США (FDA). Исследования показывают, что кратковременная терапия ГР у этой категории больных увеличивает скорость роста. Так, по данным J. Dahlgren (2009) увеличение роста при применении ГР у пациентов с СН составляло 0,6-2,0 SD. A.A. Romano и соавт. (2009) опубликовали результаты ретроспективного исследования с участием 65 пациентов с СН, получавших ГР (средняя доза – 0,047 мг/кг ежедневно) в среднем в течение 5,6 года. Средний прирост по сравнению с прогнозируемым ростом составил 10,9±4,9 см для мужчин и 9,2±4,0 см для женщин.
В представленных исследованиях доза ГР у пациентов с СН варьировала в диапазоне 0,035-0,066 мг/кг/сут, а результат при этом коррелировал с дозой и продолжительностью лечения.
Не сообщалось о побочных эффектах, связанных с лечением. Однако контролируемых исследований по изучению применения ГР у пациентов с СН все еще не хватает.
Недостаточность SHOX
Ген SHOX (short stature homeobox gene) расположен в псевдоаутомосомальной области половых хромосом. Гаплонедостаточность или полная потеря функции SHOX определяют нетипичную пролиферацию и дифференцировку хондроцитов, что вызывает замедленный рост трубчатых костей. Дефицит SHOX отмечен при ряде состояний, включая синдром Лери-Вейля, мезомелическую дисплазию Лангера, СТ, идиопатическую низкорослость.
В двухлетнем рандомизированном исследовании W.F. Blum и соавт. (2007) лечение ГР (0,05 мг/кг/сут) привело к ускорению роста у пациентов с дефицитом SHOX. Более недавнее исследование W.F. Blum и коллег (2013) показало, что 57% пациентов с дефицитом SHOX и 32% больных с СТ, получавших лечение ГР в течение 6-7 лет, достигли роста с отклонением меньше 2SD. Лечение не затрагивало полового созревания в пубертате, а также не сообщалось о других побочных эффектах, связанных с приемом ГР.
Дети, рожденные малыми для гестационного возраста
Дети, родившиеся малыми для гестационного возраста, то есть с дефицитом веса/роста >2 SD, имеют повышенный риск низкорослости во взрослом возрасте. Хотя большинство из них сможет догнать сверстников в первые 2-3 года жизни, около 10% из них все же будут иметь устойчивое отставание в росте.
Был опубликован ряд исследований по лечению ГР у этой категории детей, на основании результатов которых в 2001 году FDA одобрило соответствующее показание для применения ГР (в дозе 0,07 мг/кг/сут у детей, которые родились малыми для гестационного возраста и не смогли наверстать упущенное до 2-летнего возраста). Еще через год такое лечение было одобрено и в Европе (в дозе 0,035 мг/кг/сут с 4 лет).
До настоящего времени опубликовано более 30 исследований по изучению применения ГР у детей, рожденных малыми для гестационного возраста, из которых 4 были контролируемыми. Так, в рандомизированном исследовании Y. van Pareren и соавт. (2003) лечили две группы мальчиков в возрасте до 8 лет ГР в дозе 0,033 или 0,067 мг/кг/сут в течение 7,5-7,9 лет. В результате их рост во взрослом возрасте был на 1,2 и 1,4 SD больше, чем в контрольной группе, соответственно. J.C. Carel и коллеги (2003) лечили 102 пациентов в возрасте в среднем 12,7 лет ГР в дозе 0,067 мг/кг/сут в течение в среднем 2,7 года. Их рост во взрослом возрасте оказался на 1,1 SD больше, чем у лиц из контрольной группы. В исследовании J. Dahlgren и соавт. (2005) 77 пациентов в возрасте в среднем 10,7 года получали ГР в дозе 0,033 мг/кг/сут в течение 5,5-8,8 лет. В итоге средний конечный рост у них был на 0,6 SD больше, чем у нелеченных пациентов. В то же время эти авторы показали, что конечный рост был значительно больше (на 0,4 SD) у пациентов, у которых лечение ГР началось более чем за 2 года до наступления пубертата. M. van Dijk и соавт. (2007) лечили 37 пациентов в возрасте в среднем 8,5 лет ГР в дозе 0,033-0,06 мг/кг/сут в течение в среднем 7,3 года. И снова же, конечный рост у леченных пациентов был на 1,2 SD больше, чем в контрольной группе. A. Maiorana и S. Cianfarani (2009) в своем метаанализе, объединившем 4 контролируемых исследования и 391 пациента, пришли к выводу, что лечение ГР у детей, рожденных малыми для гестационного возраста, приводит к увеличению роста во взрослом возрасте на 0,9 SD по сравнению с контрольной группой без существенных различий между двумя дозами ГР. По данным M.B. Ranke и соавт. (2003), ответ на лечение ГР у данной категории пациентов зависит от дозы, а также от возраста в начале терапии, исходной конституции тела и роста родителей. Показано также, что лечение ГР оказывает положительное влияние на конституцию тела, минеральную плотность костей и мышечную функцию.
До сих пор не было зарегистрировано неблагоприятных эффектов при применении ГР у детей, родившихся малыми для гестационного возраста.
Поскольку есть данные о том, что начало лечения ГР в период пубертата ассоциируется с меньшей эффективностью, A.J. Lem и коллеги (2012) изучили эффективность комбинированной терапии аналогом ГР и аналогом гонадотропин-высвобождающего гормона в рандомизированном исследовании. Они пришли к выводу, что у детей, родившихся малыми для гестационного возраста и имеющих низкий рост в начале пубертата, такое комбинированное лечение может давать преимущества.
Идиопатическая низкорослость
Согласно недавнему консенсусу (Growth Hormone Research Society, Lawson Wilkins Pediatric Endocrine Society и European Society for Paediatric Endocrinology, 2008) идиопатическая низкорослость определяется как состояние, при котором рост индивидуума отстает более чем на 2SD от среднего роста для данного возраста, пола и популяционной группы, без признаков системной, эндокринной, алиментарной и хромосомной патологии. Дети с идиопатической низкорослостью имеют нормальный вес при рождении. В целом этим термином описывают гетерогенную группу детей с отставанием в росте по неизвестным сегодня причинам, включая конституциональную задержку роста и полового созревания, а также семейную форму низкорослости.
В ряде исследований показано, что кратковременный курс лечения ГР (6-12 месяцев) увеличивает скорость роста у подавляющего большинства детей с идиопатической низкорослостью. Ответ на терапию в течение первого года положительно коррелирует с дозой ГР и частотой введения и отрицательно коррелирует со скоростью роста до лечения. На сегодняшний день эффективность ГР у этой категории детей изучена более чем в 20 исследованиях, из которых 3 являются рандомизированными контролируемыми. Так, E.S. McCaughey и соавт. (1998) сообщили о результатах рандомизированного исследования с участием 10 девочек в возрасте 6,2±0,4 года с небольшим ростом, которых лечили ГР в дозе 0,06 мг/кг/сут в течение в среднем 6,2 года. Средний конечный рост у них оказался на 7 см больше, чем в контрольной группе, причем все пациентки в группе лечения достигли своей генетической цели по сравнению с 38% в контрольной группе. E.W. Leshek и соавт. (2004) сообщили, что средний конечный рост у 22 детей с идиопатической низкорослостью (возраст на момент начала лечения – 12,5±1,6 года), получавших ГР в дозе 0,22 мг/кг/нед (разделенную на три инъекции) в течение в среднем 4,4±1,6 года, был на 0,5 SD больше, чем в контрольной группе. В исследовании K. Albertsson-Wikland и др. (2008) средний конечный рост 49 детей с идиопатической низкорослостью (возраст на момент начала лечения – 11,5±1,3 года), получавших ГР в дозе 0,033-0,067 мг/кг/нед, был на 0,6 SD больше, чем в контрольной группе.
Во всех исследованиях наблюдалась большая индивидуальная вариабельность ответа на лечение. Был определен ряд факторов, влияющих на конечный результат: возраст начала лечения (чем моложе, тем лучше), рост в начале лечения (чем выше, тем лучше), ответ в течение первого года, доза ГР и средний рост родителей.
Контролируемые исследования по оценке эффективности ГР у детей с идиопатической низкорослостью были недавно проанализированы в метаанализе (A. Deodati, S. Cianfarani, 2011), показавшем увеличение конечного роста на 0,65 SD (около 4 см) по сравнению с контрольной группой.
В целом лечение ГР при идиопатической низкорослости характеризуется благоприятным профилем безопасности, сходным с таковым у пациентов с дефицитом ГР.
Выводы
Лечение ГР показано не только пациентам с соматотропной недостаточностью, но и при ряде других патологических состояний, проявляющихся низкорослостью (синдром Тернера, хроническая почечная недостаточность, синдром Прадера-Вилли, синдром Нунана, дефицит SHOX, идиопатическая низкорослость, рождение с весом и/или ростом, малыми для гестационного возраста). Имеющиеся данные свидетельствуют о том, что лечение ГР полезно при всех этих состояниях, поскольку оно увеличивает конечный рост, а также оказывает положительное влияние на конституцию тела и метаболизм костной ткани.
Поскольку ответ на терапию ГР демонстрирует значительную межиндивидуальную вариабельность, перед принятием решения в каждом отдельном случае следует тщательно рассмотреть клинические, ауксологические и психосоциальные факторы. В целом ответ на терапию ГР заметно коррелирует с возрастом в начале лечения и дозой препарата.
Почти 30-летний опыт использования рекомбинантных препаратов ГР показал, что такое лечение в целом безопасно и не приводит к развитию серьезных нежелательных явлений.
По материалам Loche S., Carta L., Ibba A., Guzzetti C. Growth hormone treatment in non-growth hormone-deficient children. Annals of Pediatric Endocrinology & Metabolism. 2014; 19(1): 1-7.
Список литературы находится в редакции.
Статья напечатана
при поддержке компании Pfizer
Перевод с англ. Натальи Мищенко
WUKGTR0317008
СТАТТІ ЗА ТЕМОЮ Ендокринологія
15.11.2021 Ендокринологія Нейропротекторні властивості тіоктової кислоти у хворих на діабетДіабет є одним із системних захворювань із великою кількістю ускладнень, які впливають на різні системи організму, в тому числі на серцево-судинну й нервову [1]. Зростання частки в загальній популяції літніх людей призводить до проблем, пов’язаних зі зниженням когнітивних здібностей. Відомо також, що в осіб із діабетом деменція спостерігається у 2-3 рази частіше [2]….
15.11.2021 Ендокринологія Тактика ведення кардіометаболічного пацієнта: на першому місці – контроль інсулінорезистентностіНауково-освітній проєкт «Школа ендокринолога» передбачає не лише класичні лекції, а й консиліуми, під час яких відбувається обговорення окремих клінічних випадків і ситуацій. Так, консиліум № 6 був присвячений обговоренню кардіометаболічного пацієнта, в якому взяли участь старший науковий співробітник ДУ «Національний науковий центр «Інститут кардіології ім. М. Д. Стражеска» НАМН України» (м. Київ), доктор медичних наук Лариса Анатоліївна Міщенко та старший науковий співробітник ДУ «Інститут ендокринології та обміну речовин ім. В. П. Комісаренка НАМН України» (м. Київ), доктор медичних наук Любов Костянтинівна Соколова….
15.11.2021 Ендокринологія Гіперпаратиреоз у практиці лікаря загальної практики: діагностична настороженістьСкладним завданням для лікаря загальної практики є раннє виявлення гіперфункції паращитоподібних залоз (ПЩЗ), частота якої неухильно зростає [1-3]. Поширеність первинного гіперпаратиреозу (ГПТ) досягає 0,3% у загальній популяції, а серед жінок віком >50 років – 1%, але часто ця патологія залишається недіагностованою [4], що зумовлено значним поліморфізмом клінічних ознак унаслідок різноманіття причин і механізмів патогенезу первинного, вторинного чи третинного ГПТ [3, 5]….
15.11.2021 Ендокринологія Фіксована комбінація агоніста рецептора ГПП-1 і базального інсуліну: розбір клінічних випадківНезважаючи на вагомий арсенал цукрознижувальних препаратів (ЦЗП), більшість пацієнтів із цукровим діабетом (ЦД) 2 типу не досягають контролю захворювання. Зі збільшенням тривалості ЦД 2 типу та подальшим його прогресуванням ситуація тільки погіршується, оскільки ефективність дії пероральних ЦЗП починає знижуватися. Виходом із цієї ситуації є своєчасне призначення інсулінотерапії, але таке лікування асоціюється з підвищеним ризиком гіпоглікемії та збільшенням маси тіла. При цьому контроль захворювання в більшості випадків так і залишається незадовільним….
о продуктах с высоким содержанием кальция и других факторах роста
«Будь здоров, расти большой!» — такие слова хотя бы раз говорил своему ребенку, наверное, каждый родитель. Но специалисты утверждают, что такие пожелания, даже самые чистосердечные, на росте ребенка никак не сказываются. А что сказывается?
Конечно, наследственность, роль которой очень важна. Вероятность того, что у невысоких мамы с папой вырастет сын-баскетболист или дочь-модель, невелика (впрочем, бывают и исключения). Но существуют и другие факторы.
Правильное питание и полезные продукты способствующие росту ребенка
Один из таких факторов — правильное питание. В рационе ребенка обязательно должны присутствовать продукты с достаточным содержанием кальция; для нормального роста ребенку 3−4 лет необходимо примерно 800 мг данного вещества в сутки.
Почему кальций так важен? Ответить на этот вопрос нетрудно. Кальций содержится в костной ткани, более того, является преобладающим в ней веществом. Если содержание кальция будет слишком мало, скелет ребенка не сможет формироваться правильно, кости станут хрупкими; о каком уж нормальном росте тут можно говорить.
К счастью, кальций — не такое уж редкое вещество. Оптимальным для ребенка является содержание кальция в молоке (300 мг в одном стакане) и молочных продуктах, йогуртах (около 150 мг в 100 г), твердых сырах (около 600 мг в 100 г). Кальция также много в рыбе и морепродуктах, бобовых, орехах, зеленых овощах, яйцах. Для хорошего усвоения кальция необходим витамин D — тот самый, который вырабатывается в нашем организме под воздействием солнечных лучей. Высокое содержание этого витамина обнаружено в сельди, сардинах, макрели, лососе, тунце, яйцах, печени, молоке и молочных продуктах.
Надежным способом обеспечить ребенка достаточным количеством необходимых веществ являются специальные продукты с высоким содержанием кальция — такие, как лакомства серии «Растишка», которую производит компания Danone. «Растишка» — это обогащенные кальцием и витамином D йогурты, творожки и молочные коктейли, которые производятся из свежего молока и фруктового пюре без добавления консервантов и искусственных красителей. Дети, впрочем, любят «Растишку» не за пользу, а за вкус, и это тоже хорошо: продуктами с высоким содержанием кальция можно заменить вредные кондитерские изделия и сладкие напитки.
Но, как говорится, не кальцием единым. Для роста ребенку также необходимы белки: продукты с высоким содержанием этих веществ — мясо, рыба, творог, сыр, яйца, овощи, крупы, злаки. Очень важен для роста витамин, А — в нем нуждаются клетки хрящевой ткани. Много витамина, А содержит морковь, богаты им также красный перец, зеленый лук, салат, помидоры, тыква. Чтобы витамин, А хорошо усваивался, все эти продукты лучше давать ребенку с растительным маслом или сметаной. Значительную роль играет и образ жизни. Для нормального роста (да и для развития в целом) ребенку нужно много гулять, играть в подвижные игры. Недостаток физических нагрузок и свежего воздуха — это препятствие для нормального роста.
Физиологические и психологические факторы
Нельзя не сказать и о сне, ведь большая часть соматотропина, гормона роста, вырабатывается именно тогда, когда ребенок спит. Поэтому следите за тем, чтобы ребенок соблюдал режим дня и высыпался, даже если ради этого придется пожертвовать любимыми мультфильмами. Врачи отмечают также важность атмосферы в семье: ребенку очень трудно расти большим, если он лишен психологического комфорта, любви и заботы родителей.
Надо сказать, что есть и чисто медицинские факторы, с которыми даже самые внимательные родители не смогут справиться без врача. Рост ребенка зависит от ряда гормонов (гормона передней доли гипофиза, уже упомянутого соматотропина, инсулина, половых гормонов). Если их вырабатывается слишком много или слишком мало, потребуется вмешательство специалистов.
Средний рост трехлетнего ребенка — от 92 см до метра, за год дети вырастают на 4−6 см. Высокими считаются дети, которые к трем годам достигают 1 м 4 см, маленькими — те, чей рост составляет 89−91 см. Если рост ребенка на 20% меньше нормы, это может быть признаком серьезного расстройства, нужно обратиться к эндокринологу.
Доктор Мясников ответил на главные вопросы о гормонах
Все, что происходит в нашем организме, регулируется гормонами. Большинство стероидных гормонов (эстроген, тестостерон, кортизол и другие) происходит из холестерина. И хотя мы часто говорим о вреде повышенного холестерина, при его недостатке организм погибнет быстрее. Проблемам каждой из желез внутренней секреции посвящены целые тома – именно по этой причине пространному рассуждению о гормонах Александр Мясников предпочитает вопросы, которые волнуют зрителей программы «О самом главном».
Врачи часто назначают дорогостоящие анализы на гормоны при жалобах на усталость и недосып. Действительно ли это необходимо и оправдано?
«Когда у меня была частная клиника, я всегда говорил своим врачам: вы можете обмануть человека только один раз, и он больше не придет. Но не только он: ни его родственники, ни друзья. Ты сейчас схватишь три копейки, а потом потеряешь очень много», – поделился доктор. По его словам, в частных клиниках врачи лично заинтересованы назначать как можно больше исследований, поскольку имеют с этого свой процент.
Сам Мясников при подобных жалобах в первую очередь проверил бы функцию щитовидной железы. Впрочем, при серьезных нарушениях, как правило, наблюдаются также другие симптомы: выпадение волос, поражение бровей, склонность к отекам, непереносимость холода.
Стоит ли принимать гормоны, способствующие увеличению мышц, для занятий спортом?
«Если человек – профессиональный спортсмен, он отдает здоровье и получает деньги. Я это осуждаю, но это объяснимо», – отвечает медик. Однако, когда речь о молодом парне, которого сверстники в спортзале агитируют принимать анаболики, это «путь в никуда», считает он. Среди последствий подобных препаратов, которые активно продаются на черном рынке, Мясников называет, прежде всего, импотенцию, о которой в 15 лет никто даже не думает. «Если тебе нужны мышцы, надо приложить усилие», – утверждает доктор и называет употребление стероидов «уродованием себя».
Какие последствия может вызывать гормональная заместительная терапия?
При нормальном уровне гормонов, смысла в заместительной терапии нет, так как она приведет к дисбалансу. Однако в период менопаузы гормональная функция угасает. И если ранее специалисты считали, что долгосрочный прием гормонов может вызывать рак груди, то сейчас эти данные пересмотрены. Гормональную заместительную терапию можно без опасений назначать на пять или даже десять лет, но не более. А вот в качестве профилактики остеопороза или сердечных заболеваний ее не используют, так как принимать препараты приходится десятилетиями.
Стоит ли применять гормон роста для борьбы со старением?
Александр Мясников признался, что в свое время в США был частью сообщества врачей, которые ведут борьбу со старением, основанную на гормональной терапии с применением соматотропина – гормона роста. «Гуру этого метода сказал: чтобы быть молодым и сильным, мужчина старше 40 лет должен колоть себе гормон роста», – вспоминает медик. Однако американские эндокринологи выступили резко против использования гормона роста здоровыми людьми.
«Минусы: это не проверено, это повышает сахар, это вызывает задержку жидкости, боль в суставах, иногда акромегалию, это очень дорого. За – это реально работает: укрепляются кости, увеличивается мышечная масса, уменьшается живот, с потенцией все нормально», – объясняет Александр Леонидович.
В России этот метод не прижился, поскольку пациент, принимающий гормон роста, должен быть абсолютно здоров, а в нашей стране таковых меньшинство. Тем не менее, во всем мире сегодня «антиэйджинг» основан на применении именно соматотропина.
Еще больше интересных новостей – в нашем Instagram и Telegram-канале @smotrim_ru
История терапии гормоном роста
Indian J Endocrinol Metab. 2011 сен; 15 (Дополнение 3): S162 – S165.
Вагиш С. Айяр
Отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия
Отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия
Автор для корреспонденции: Д-р Вагиш С. Айяр, отделение эндокринологии, Медицинский колледж Св. Иоанна, Бангалор, Индия. Электронная почта: moc.liamg@rayyagav Авторские права: © Индийский журнал эндокринологии и метаболизмаЭто статья в открытом доступе, распространяемая в соответствии с условиями Creative Commons Attribution-Noncommercial-Share Alike 3.0 Unported, что разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии правильного цитирования оригинальной работы.
Эта статья цитируется в других статьях в PMC.Abstract
Хотя важность гипофиза для роста была признана в конце 19 века, терапия гормоном роста (GH) стала доступной для детей и подростков с тяжелым дефицитом GH только в конце 1950-х годов. Использование GH для других состояний было ограничено из-за ограниченного количества человеческого гормона, производного от гипофиза.С неограниченной доступностью рекомбинантного человеческого GH (rhGH) сценарий лечения GH сильно изменился. В настоящее время постоянно увеличивается список показаний к лечению гормона роста у детей, подростков и взрослых.
Ключевые слова: Гормон роста, история, гипофиз
ВВЕДЕНИЕ
Борьба за открытие гормона роста (GH) была длительной и тяжелой. В увлекательный обходной путь к открытиям потребовалось множество клиницистов, химиков, физиологов и патологов.Сказка наполнена удивительными прозрениями, а также поразительными ошибками, интуитивной прозорливостью и неудачными трудами, победами и поражениями.
ИСТОРИЯ ГОРМОНА РОСТА
Попытки получить гипофизарный GH для лечения GH-дефицитных детей начались в середине 1940-х годов. Первоначальная работа над субприматами длилась почти десять лет. Эти усилия привели к очистке бычьего GH Ли и Эвансом в Калифорнийском университете в Беркли и Фишманом в Йельском университете. А свиной GH был очищен Рабеном и Вестермейером в Тафтсе.Но ни один из этих препаратов не проявил значительной биохимической или метаболической активности, поскольку действие GH зависит от вида [1].
Гормон роста (GH) впервые был выделен из гипофиза человека в 1956 году Ли и Папкофф в Калифорнии и Рабеном в Массачусетсе, но его биохимическая структура не была выяснена до 1972 года. В 1958 году Рабен сообщил о результатах. первого испытания, демонстрирующего влияние человеческого гормона роста на рост. К 1960 году стало ясно, что дети с дефицитом гормона роста выиграют от гипофизарного гормона роста.В 1960 году было сформировано Национальное агентство по гипофизу (NPA) для достижения целей координации сбора и извлечения гипофиза для поддержки как фундаментальных, так и клинических исследований [1,2]. В период с 1963 по 1985 год NPA контролировало почти все лечение GH в Соединенных Штатах. Состояния. И за этот период около 7700 детей в Соединенных Штатах и 27000 детей во всем мире получали GH, выделенный из гипофиза человека, для лечения тяжелого дефицита гормона роста (GHD). [3,4]
К 1985 году гипофизарный GH использовался почти для всех. 30 лет в США и Канаде в исследовательских или терапевтических целях.В 1985 году Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (US FDA) получило сообщения о четырех молодых людях в Соединенных Штатах с смертельной, медленной вирусной (прионной) болезнью Крейцфельдта-Якоба (CJD), которые лечились GH от NPA в 1960-е годы. Связь была признана при просмотре данных в течение нескольких месяцев FDA и NIH. 19 апреля 1985 г. распространение ГР гипофиза было приостановлено, и использование ГР гипофиза человека быстро прекратилось. И вот захватывающая и важная эпоха в детской эндокринологии внезапно подошла к концу.[5]
Идентификация биохимической структуры GH в 1972 году стала катализатором развития человеческого GH на основе рекомбинантной ДНК, ген которого был впервые клонирован в 1979 году. Компания Genentech (Сан-Франциско, Калифорния) разработала в 1981 году был получен первый рекомбинантный человеческий GH (rhGH) путем биосинтетического процесса. Позже был разработан усовершенствованный процесс выработки rhGH, названный технологией секреции белка. При этом векторная плазмида выделяется из штамма E.coli , а цепь ДНК, которую необходимо клонировать, происходит из соответствующего источника.И плазмида, и необходимая цепь ДНК расщепляются рестрикционными ферментами, соединяются вместе и затем преобразуются в кольцевую структуру. Рекомбинантная плазмида вставляется в E.coli , который затем трансформируется для синтеза желаемого белка. В настоящее время это наиболее распространенный метод, используемый для синтеза rhGH, известного как соматотропин. Прекращение приема человеческого трупного GH привело к быстрому утверждению Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) синтетического метионилового GH компании Genentech, который был представлен в США в 1985 году для лечения тяжелого детского GHD.[6,7]
До открытия rhGH лечение GH применялось только в самых тяжелых случаях GHD и из-за нехватки материалов. С развитием rhGH стал доступен неограниченный коммерческий источник, что позволило получить постоянно растущий список одобренных FDA показаний для использования GH у детей без дефицита GH и дополнительных показаний для взрослых. [8,9]
HISTORY ПОКАЗАНИЯ К ГОРМОННОЙ ТЕРАПИИ У ДЕТЕЙ
Дефицит гормона роста (1985)
GHD может быть результатом нарушения оси GH в гипоталамусе или гипофизе.Эта этиология дисфункции может быть врожденной или приобретенной. Классическое проявление тяжелой формы GHD характеризуется низким ростом, медленным ростом и замедленным созреванием скелета с пониженной секрецией GH в ответ на провокационную стимуляцию. Несмотря на этот обширный список этиологий, причина GHD у большинства детей — идиопатическая. Лечение GH GHD у детей в определенной степени стандартизировано во всем мире. rhGH вводится один раз в день подкожно, обычно вечером, для имитации нормальной физиологии.[3,9]
Хроническая почечная недостаточность (1993)
Дети, страдающие хронической болезнью почек (ХБП), склонны к развитию тяжелой недостаточности роста. Этиология нарушения уремического роста многофакторна. Терапия гормона роста — общепринятая мера для увеличения конечного роста. В различных исследованиях лечение GH при ХБП улучшило конечный рост. У пациентов с ХЗП препубертатного возраста реакция роста положительно связана с продолжительностью терапии гормоном роста и начальной степенью нарушения роста. Это отрицательно было связано с продолжительностью диализа.Дозы, рекомендуемые для детей с ХБП, выше, чем у пациентов с ГСХ. У детей, получавших GH, лечение обычно прекращается после трансплантации, но иногда его возобновляют, если скорость роста остается низкой. Лучшие результаты наблюдаются у детей, которые раньше начинают лечение, которые моложе и у которых наблюдается более легкое ухудшение функции почек. [10,11]
Синдром Тернера (1997)
Синдром Тернера (TS) поражает примерно одного из 1500–2500 живорожденные самки.Один из наиболее распространенных и заметных признаков синдрома — чрезвычайно низкий рост. Женщины, не получающие лечения, примерно на 20–21 см ниже нормальных женщин в своей популяции. rhGH использовался для увеличения роста и окончательного роста у девочек с TS. Хотя органический дефицит GH не является признаком TS, эффективность rhGH в увеличении линейного роста и конечного роста у пациентов с TS хорошо документирована. [12,13]
Синдром Прадера-Вилли (2000)
Синдром Прадера-Вилли ( PWS) — первое заболевание человека, связанное с геномным импринтингом, при котором гены экспрессируются по-разному в зависимости от родителя происхождения.Дети с PWS демонстрируют глубоко ненормальный состав тела с таким же фенотипом, как при классическом GHD. Назначение GH детям с GHD не только восстанавливает линейный рост, но также способствует росту безжировой массы тела, уменьшает жировую массу за счет увеличения окисления жиров и общего расхода энергии тела, увеличивает минеральную плотность костей и снижает факторы риска сердечно-сосудистых заболеваний. Хотя терапия GH в настоящее время одобрена для лечения недостаточности роста, вторичной по отношению к PWS, сами по себе эти другие преимущества могут оправдать испытание терапии GH.[14,15]
Маленький для гестационного возраста (2001)
Маленький для гестационного возраста (SGA) определяется как масса тела при рождении или длина тела, по крайней мере, на 2 SD балла (SDS) ниже среднего гестационного возраста. Независимо от того, рождаются ли эти дети преждевременно или доношенными, большинство младенцев с SGA переживают постнатальный рост, достаточный для нормализации своего роста к 2 годам. Это называется догоняющим ростом. Несколько исследований показали, что большинство детей с SGA получают пользу от терапии GH и достигают нормального взрослого роста.[16,17]
Идиопатический низкий рост (2003)
Идиопатический низкий рост (ISS) определяется как состояние, при котором рост человека более чем на 2 SDS ниже соответствующего среднего роста для данного возраста, пола, и группа населения без признаков системных, эндокринных, пищевых или хромосомных нарушений. В частности, дети с ISS имеют нормальную массу тела при рождении и достаточное количество GH. Показано, что терапия GH увеличивает средний рост взрослого, связанный с терапией GH (средняя продолжительность 4–7 лет) у детей с ISS на 3.5–7,5 см по сравнению с историческим контролем, с прогнозируемым ростом взрослых пациентов до лечения или с контрольными группами, не получавшими лечения, или контрольными группами плацебо. Не было никаких необычных проблем с безопасностью GH у пациентов с ISS. [18,19]
Недостаток гена, содержащего гомеобокс низкого роста (2006)
В 2006 году FDA США одобрило использование rhGH у пациентов с гомеобоксом низкого роста. -содержащий ген (SHOX) дефицит. Гаплонедостаточность гена SHOX связана с низким ростом, деформацией Маделунга и высоким сводчатым небом и считается основной причиной низкого роста у девочек с TS.Ген SHOX является довольно частой причиной низкого роста, и лечение гормона роста эффективно улучшает линейный рост пациентов с различными формами SHOX-D. [19,20]
Синдром Нунан (2007)
Синдром Нунан это клинически неоднородное заболевание, характеризующееся пропорциональным послеродовым низким ростом, дисморфическими чертами лица, деформациями грудной клетки и врожденным пороком сердца. Помимо черт лица и сердечных заболеваний, одним из основных признаков НС является низкий рост.Причина нарушения роста неясна, и были проведены испытания с применением rhGH. Несколько исследований показывают, что краткосрочная терапия гормона роста (1–4 года) способна увеличить скорость роста и улучшить показатель SD по росту (SDS). [19,21]
Дефицит гормона роста у взрослых
Лечение гормона роста у взрослых с дефицитом гормона роста. был одобрен FDA в 1996 году. Впоследствии был оценен большой клинический опыт лечения взрослых с GHD. Хотя в целом лечение кажется безопасным, некоторые области требуют длительного наблюдения, например, риски непереносимости глюкозы, рецидива опухоли гипофиза / гипоталамуса и рака.Преимущества лечения гормоном роста взрослых с дефицитом гормона роста были обнаружены в отношении состава тела, здоровья костей, факторов риска сердечно-сосудистых заболеваний и показателей качества жизни. Однако снижение сердечно-сосудистых событий и смертности еще предстоит продемонстрировать, а затраты на лечение остаются высокими [] [22].
Таблица 1
История терапии гормоном роста
ВЫВОДЫ
GH является важным фактором, способствующим росту. До 1985 года GH получали путем экстракции из трупного гипофиза.В связи с доступностью неограниченного количества рчГР список показаний для детей и взрослых без дефицита ГР постоянно растет. Помимо состояний, упомянутых выше, рчГР также одобрен для лечения истощения, связанного с ВИЧ, и синдрома короткой кишки. В настоящее время имеются сообщения об использовании GH при муковисцидозе, воспалительном заболевании кишечника, ювенильном ревматоидном артрите, остеопорозе и у пациентов, которым требуется хроническое введение глюкокортикоидов. Лечение rhGH действительно увеличивает рост взрослого человека в некоторых случаях и кажется безопасным лечением.Однако недавно Управление США по контролю за продуктами и лекарствами [23] предупредило общественность о результатах французского наблюдательного исследования (SAGhE), описывающего небольшое повышение риска смерти у взрослых, получавших rhGH в детстве, от некоторых типов низкого роста. В настоящее время FDA считает, что преимущества rhGH по-прежнему перевешивают его потенциальные риски. По мере того, как мы узнаем больше о GH, неизбежно, что его использование будет продолжать расширяться.
Примечания
Источник поддержки: Нет
Конфликт интересов: Не объявлен.
СПИСОК ЛИТЕРАТУРЫ
1. Frasier SD. Не очень хорошие старые времена: работа с гормоном роста гипофиза в Северной Америке, 1956–1985 гг. J Pediatr. 1997; 131: S1–4. [PubMed] [Google Scholar] 2. Самнер Дж. Гормон роста человека: текущий статус доступности и полезности. Педиатрия. 1969; 44: 766–7. [Google Scholar] 3. Франклин С.Л., Геффнер МЭ. Гормон роста: расширение доступных продуктов и показаний. Endocrinol Metab Clin North Am. 2009. 38: 587–611. [PubMed] [Google Scholar] 4. Escamilla RF, Hutchings JJ, Deamer WC, Li CH, Forsham PH.Долгосрочные эффекты гормона роста человека (Li) на гипофизарный карлик. J Clin Endocrinol Metab. 1961; 21: 721–6. [PubMed] [Google Scholar] 5. Отчет Комитета по использованию гормона роста Детского эндокринного общества им. Лоусона Уилкинса, май 1985 г. Дегенеративное неврологическое заболевание у пациентов, ранее получавших гормон роста человека. J Pediatr. 1985; 107: 10–2. [PubMed] [Google Scholar] 6. Кронин MJ. Новаторское производство рекомбинантного гормона роста: количество фунтов на милю роста. J Pediatr. 1997; 131: S5–7.[PubMed] [Google Scholar] 7. Флод Х. Гормон роста человека, полученный с помощью технологии рекомбинантной ДНК: Разработка и производство. Acta Paediatr Scand Suppl. 1986; 325: 1–9. [PubMed] [Google Scholar] 8. Такеда А., Купер К., Берд А., Бакстер Л., Фрэмптон Г. К., Господаревская Е. и др. Рекомбинантный гормон роста человека для лечения нарушений роста у детей: систематический обзор и экономическая оценка. Оценка медицинских технологий. 2010; 14: 1. [PubMed] [Google Scholar] 9. Hindmarsh PC, редактор. Эндокринное развитие.2-е изд. Vol. 18. Базель: Karger Publishers; 2010. Текущие показания к терапии гормоном роста; С. 92–108. [PubMed] [Google Scholar] 10. Ниссель Р., Линдберг А., Мельс О., Хаффнер Д. Международная база данных о росте Pfizer (KIGS) Международный совет. Факторы, позволяющие прогнозировать околокональный рост у детей и подростков с хроническим заболеванием почек, принимающих гормон роста. J Clin Endocrinol Metab. 2008; 93: 1359–65. [PubMed] [Google Scholar] 11. Franke D, Zivicnjak M, Ehrich JH. Лечение гормоном роста почечной недостаточности в младенчестве и раннем детстве.Педиатр Нефрол. 2009; 24: 1093–6. [PubMed] [Google Scholar] 12. Бакстер Л., Брайант Дж., Кейв С.Б., Милн Р. Рекомбинантный гормон роста для детей и подростков с синдромом Тернера. Кокрановская база данных Syst Rev.2007: CD003887. [PubMed] [Google Scholar] 13. Болар К., Хоффман А.Р., Манитис Т., Липпе Б. Долгосрочная безопасность рекомбинантного гормона роста человека при синдроме Тернера. J Clin Endocrinol Metab. 2008; 93: 344–51. [PubMed] [Google Scholar] 14. Каррел А.Л., Майерс С.Е., Уитман Б.А., Аллен Д.Б. Преимущества долгосрочной терапии GH при синдроме Прадера-Вилли: 4-летнее исследование.J Clin Endocrinol Metab. 2002; 87: 1581–5. [PubMed] [Google Scholar] 15. Whitman BY, Myers S, Carrel A, Allen D. Поведенческое воздействие лечения гормоном роста детей и подростков с синдромом Прадера-Вилли: 2-летнее контролируемое исследование. Педиатрия. 2002; 109: E35. [PubMed] [Google Scholar] 16. Майорана А., Чианфарани С. Влияние терапии гормоном роста на рост взрослых детей, рожденных маленькими для гестационного возраста. Педиатрия. 2009; 124: e519–31. [PubMed] [Google Scholar] 17. Ли П.А., Чернаусек С.Д., Хоккен-Колега А.С., Чернихов П.Заявление Международной конференции по развитию консенсуса Консультативного совета по малому для гестационного возраста: Ведение маленьких детей, рожденных с малым для гестационного возраста, 24 апреля — 1 октября 2001 г. Педиатрия. 2003; 111: 1253–61. [PubMed] [Google Scholar] 18. Коэн П., Рогол А.Д., Дил С.Л., Сенгер П., Рейтер Е.О., Росс Дж. Л. и др. Участники семинара по консенсусу ISS 2007. Заявление о консенсусе по диагностике и лечению детей с идиопатическим низким ростом: резюме Общества по исследованию гормона роста, Педиатрического эндокринного общества Лоусона Уилкинса и семинара Европейского общества детской эндокринологии.J Clin Endocrinol Metab. 2008; 93: 4210–7. [PubMed] [Google Scholar] 19. Коллетт-Сольберг П.Ф. Обновление гормональной терапии детей. J Clin Endocrinol Metab. 2011; 96: 573–9. [PubMed] [Google Scholar] 20. Блюм В.Ф., Кроу Б.Дж., Куигли К.А., Юнг Х., Цао Д., Росс Дж. Л. и др. SHOX Study Group. Гормон роста эффективен при лечении низкого роста, связанного с дефицитом гомеобокса низкого роста: результаты двухлетнего рандомизированного контролируемого многоцентрового исследования. J Clin Endocrinol Metab.2007. 92: 219–28. [PubMed] [Google Scholar] 21. Феррейра Л.В., Соуза С.А., Арнхольд И.Дж., Мендонка Б.Б., Хорхе А.А. Мутации PTPN11 (Protein Tyrosine Phosphatase, Nonreceptor Type 11) и ответ на терапию гормоном роста у детей с синдромом Нунана. J Clin Endocrinol Metab. 2005; 90: 5156–60. [PubMed] [Google Scholar] 22. Молич М.Э., Клеммонс Д.Р., Малозовски С., Мерриам Г.Р., Шале С.М., Вэнс М.Л. Подкомитет по клиническим рекомендациям эндокринного общества, Stephens PA. Оценка и лечение дефицита гормона роста у взрослых: Руководство по клинической практике эндокринного общества.J Clin Endocrinol Metab. 2006; 91: 1621–34. [PubMed] [Google Scholar] 23. Сообщение о безопасности лекарств, 22 декабря 2010 г. [Последний доступ 1 мая 2011 г.]. Доступна с: http://www.fda.gov.Дефицит гормона роста у взрослых | Сидарс-Синай
Не то, что вы ищете?Обзор
Даже после того, как мы перестанем расти, взрослым по-прежнему нужен гормон роста. Гормон роста — это белок, вырабатываемый гипофизом и попадающий в кровь.
Гормон роста играет роль в здоровых мышцах, в том, как наши тела собирают жир (особенно в области живота), в соотношении липопротеинов высокой и низкой плотности в нашем уровне холестерина и плотности костей. Кроме того, для нормальной работы мозга необходим гормон роста.
У человека, у которого слишком мало гормона роста взрослого, будут следующие симптомы:
- Более высокий уровень жира в организме, особенно в области талии
- Беспокойство и депрессия
- Снижение половой функции и интереса
- Усталость
- Чувство изолированности от других людей
- Повышенная чувствительность к жаре и холоду
- Меньше мышц (безжировая масса тела)
- Меньше силы, выносливости и способности выполнять упражнения без отдыха
- Пониженная плотность костей и тенденция к большему количеству переломов костей по мере взросления
- Изменения в составе холестерина в крови.
У людей с дефицитом гормона роста у взрослых уровни липопротеинов низкой плотности выше нормы по сравнению с их липопротеинами высокой плотности. У них также, как правило, более высокий уровень триглицеридов. (Триглицериды — это еще один тип жира, который циркулирует в крови и способствует закупорке кровеносных сосудов.)
Причины и факторы риска
Недостаток гормона роста обычно вызван повреждением гипофиза или гипоталамуса, части мозга, которая контролирует работу гипофиза.Повреждение может быть связано с опухолью; хирургическому вмешательству или облучению, используемому для лечения опухоли; или к проблемам с кровоснабжением гипофиза.
В некоторых случаях недостаток гормона роста связан с повреждением гипофиза.
Недостаток гормона роста может появиться как в детстве, так и во взрослом возрасте.
Диагностика
Если человек перенес операцию, травму или имел в анамнезе заболевания гипофиза, врач или эндокринолог (специально обученный врач, специализирующийся на здоровье секретирующих гормоны желез) проверит дефицит гормона роста у взрослых.Если есть известное заболевание или проблема с гипофизом, врач, вероятно, назначит магнитно-резонансную томографию (МРТ) до того, как будет проведено какое-либо лечение. Это позволяет врачу более точно контролировать, как лечение влияет на опухоль.
Гормон роста у взрослых быстро всасывается тканями из крови по мере его циркуляции. В результате анализ крови здорового человека покажет низкий уровень гормона роста. Вместо этого эндокринологи проверяют реакцию гипофиза, когда он стимулируется выработкой гормона роста.Эти тесты на стимуляцию гормона роста проводятся в амбулаторных условиях и занимают от двух до трех часов. Перед обследованием вас попросят не есть.
Лечение
После подтверждения дефицита гормона роста у взрослого врач пропишет суточные дозы гормона роста. Гормон вводится в организм пациента; это может сделать либо пациент, либо член его или ее семьи. Каждые четыре-восемь недель пациент будет возвращаться к врачу для наблюдения и анализа крови, чтобы помочь врачу решить, нужно ли больше гормонов или меньше.
Если человек получает слишком много гормона роста, у него или у нее будет боль в мышцах или суставах, отек (задержка жидкости) и боль или онемение в руках из-за синдрома запястного канала. При появлении таких симптомов врач снизит количество вводимого гормона роста.
Если дефицит гормона роста вызван опухолью гипофиза, врач будет ежегодно контролировать опухоль с помощью МРТ. В настоящее время неизвестно, будет ли гормон роста вызывать рост опухолей, которые остаются в гипофизе.
Наконец, будут контролироваться холестерин в крови и плотность костей. При лечении дефицита гормона роста у взрослых обе эти меры должны показать признаки улучшения.
Терапию гормоном роста нельзя назначать людям с активным раком или опухолями. Его также не следует назначать людям, которые серьезно заболели в результате осложнений после операции на открытом сердце или брюшной полости, получили множественные травмы в результате серьезной аварии или имеют проблемы с дыханием. Прием гормона роста не заставит взрослого снова начать расти.
Прием гормона роста может повлиять на то, как организм использует инсулин, поэтому для всех, кто страдает диабетом, важно держать своих врачей в курсе и внимательно следить за уровнем сахара в крови.
© 2000-2021 Компания StayWell, LLC. Все права защищены. Эта информация не предназначена для замены профессиональной медицинской помощи. Всегда следуйте инструкциям лечащего врача.
Не то, что вы ищете?Дефицит гормона роста у детей
Не то, что вы ищете?Что такое дефицит гормона роста у детей?
Дефицит гормона роста (GH) — это когда гипофиз не производит достаточного количества гормона роста.GH необходим для стимуляции роста костей и других тканей. Это состояние может возникнуть в любом возрасте. Дефицит GH не влияет на интеллект ребенка.Что вызывает дефицит гормона роста у ребенка?
ДефицитGH может быть вызван повреждением гипофиза или другой железы, называемой гипоталамусом. Травма может произойти до рождения (врожденная), во время или после рождения (приобретенная).
Гипофиз — это железа размером с горошину, расположенная в основании головного мозга.Это главная эндокринная железа в организме. Гипофиз обычно выделяет до 8 различных гормонов. Эти гормоны контролируют рост, обмен веществ, кровяное давление и другие процессы в организме.
В редких случаях дефицит GH может быть частью генетического синдрома. Во многих случаях причина дефицита GH неизвестна (идиопатическая).
Какие дети подвержены риску дефицита гормона роста?
Ребенок подвергается большему риску дефицита гормона роста, если он или она страдает одним из следующих факторов:
- Травма головного мозга
- Опухоль головного мозга
- Лучевая терапия головы
У некоторых детей с данной проблемой нет факторов риска.
Каковы симптомы дефицита гормона роста у ребенка?
Основным признаком дефицита GH является медленный рост каждый год после трехлетнего возраста ребенка. Это означает, что рост составляет менее 3,5 см (около 1,4 дюйма) в год. У ребенка с дефицитом гормона роста также могут быть:
- Молодое лицо
- Пухлое телосложение
- Нарушение роста волос
- Задержка полового созревания
Важно отметить, что дефицит гормона роста не влияет на интеллект ребенка.
Симптомы дефицита GH могут быть такими же, как и при других состояниях здоровья. Убедитесь, что ваш ребенок посещает своего лечащего врача для постановки диагноза.
Как диагностируется дефицит гормона роста у ребенка?
Чтобы диагностировать дефицит гормона роста, лечащий врач вашего ребенка должен проверить наличие других состояний, например:
- Нормальные вариации роста, например, семейный низкий рост
- Другие заболевания, такие как дефицит гормонов щитовидной железы или заболевание почек
- Генетические условия
Медицинский работник спросит о симптомах и истории здоровья вашего ребенка, а также об истории болезни вашей семьи.Он или она также проведет медицинский осмотр вашего ребенка. Здоровье и рост вашего ребенка можно контролировать в течение нескольких месяцев.
Ваш ребенок также может сдавать анализы, например:
- Анализы крови. Это делается для проверки уровня гормона роста и других связанных с ним гормонов. Иногда анализы крови делают после того, как вашему ребенку дают вещество, которое обычно повышает уровень гормона роста.
- Рентген. В этом тесте используется небольшое количество излучения для получения изображений тканей внутри тела.Может быть сделан рентген левой руки и запястья. Это позволяет оценить костный возраст вашего ребенка. При задержке полового созревания или гормональных проблемах костный возраст часто меньше календарного.
- Компьютерная томография. Этот тест использует серию рентгеновских снимков и компьютер для получения подробных изображений тела. Компьютерная томография может показать кости, мышцы, жир и органы. КТ более детализирована, чем обычные рентгеновские снимки.
- МРТ. В этом тесте используются большие магниты и компьютер для получения подробных изображений тканей тела.
Как лечится дефицит гормона роста у ребенка?
Лечащий врач вашего ребенка будет учитывать его возраст, общее состояние здоровья и другие факторы, рекомендуя лечение. Вашему ребенку может потребоваться посещение детского эндокринолога. Это врач, имеющий дополнительную подготовку по лечению детей с гормональными проблемами. У этого специалиста также будет лучшее оборудование для точного измерения роста вашего ребенка от месяца к месяцу.
Лечение проводится ежедневными инъекциями синтетического гормона роста.Результаты часто видны уже через 3-4 месяца после начала лечения. Лечение длится несколько лет, обычно до позднего полового созревания, когда заканчивается рост. Чем раньше начато лечение, тем больше шансов, что ребенок будет иметь нормальный или почти нормальный рост взрослого человека, который соответствует его или ее семейной модели.
Не все дети хорошо поддаются лечению гормоном роста. Терапия гормоном роста не делает человека выше его или ее родителей.
Какие возможные осложнения дефицита гормона роста у ребенка?
При отсутствии лечения дефицит GH может привести к тому, что ребенок не достигнет своего нормального взрослого роста.Как я могу помочь своему ребенку жить с дефицитом гормона роста?
Дети ниже своих сверстников могут иметь низкую самооценку или депрессию. Об этих проблемах важно поговорить с вашим ребенком и его лечащим врачом. Он или она может порекомендовать вам и вашему ребенку консультации или группы поддержки.
Обсудите с лечащим врачом вашего ребенка потенциальный взрослый рост вашего ребенка. Совместно с лечащими врачами вашего ребенка разработайте постоянный план управления состоянием вашего ребенка.
Когда мне следует позвонить поставщику медицинских услуг для моего ребенка?
Поговорите с лечащим врачом вашего ребенка, если вас беспокоит его рост.Основные сведения о дефиците гормона роста у детей
- Дефицит гормона роста (GH) — это когда гипофиз не производит достаточного количества гормона роста. GH необходим для стимуляции роста костей и других тканей. Дефицит
- GH не влияет на интеллект ребенка.
- Основным признаком дефицита гормона роста является медленный рост каждый год после трехлетнего возраста ребенка. У ребенка с дефицитом гормона роста также может быть моложавое лицо и пухленькое телосложение.
- Лечение проводится ежедневными инъекциями синтетического гормона роста. Результаты часто видны уже через 3-4 месяца после начала лечения. Лечение длится несколько лет, обычно до позднего полового созревания, когда заканчивается рост.
- Чем раньше начато лечение, тем больше шансов, что ребенок будет иметь нормальный или почти нормальный взрослый рост, соответствующий его или ее семейной модели.
- При отсутствии лечения дефицит GH может привести к тому, что ребенок не достигнет своего нормального взрослого роста.
Следующие шаги
Советы, которые помогут вам получить максимальную пользу от посещения лечащего врача вашего ребенка:
- Знайте причину визита и то, что вы хотите.
- Перед визитом запишите вопросы, на которые хотите получить ответы.
- Во время посещения запишите название нового диагноза и любые новые лекарства, методы лечения или тесты.Также запишите все новые инструкции, которые ваш поставщик дает вам для вашего ребенка.
- Узнайте, почему прописано новое лекарство или лечение и как они помогут вашему ребенку. Также знайте, какие бывают побочные эффекты.
- Спросите, можно ли вылечить состояние вашего ребенка другими способами.
- Знайте, почему рекомендуется тест или процедура и что могут означать результаты.
- Знайте, чего ожидать, если ваш ребенок не принимает лекарство, не проходит обследование или процедуру.
- Если вашему ребенку назначен повторный прием, запишите дату, время и цель этого визита.
- Узнайте, как вы можете связаться с лечащим врачом вашего ребенка в нерабочее время. Это важно, если ваш ребенок заболел и у вас есть вопросы или вам нужен совет.
PDB-101: Молекула месяца: гормон роста
Растущие дети и взрослые
По мере роста детей их рост, вес и сила увеличиваются. На этот рост влияет множество факторов, включая генетический состав ребенка, факторы питания и окружающей среды.Специальные посланники, выпускаемые телом, также стимулируют и регулируют рост. Гормон роста — это один из ключевых сигналов роста, высвобождаемый гипофизом, железой размером с горошину, расположенной в основании мозга. Недостаток этого гормона у детей может привести к тому, что они будут ниже среднего роста, а при его избытке они могут вырасти выше, чем большинство. Гормон роста продолжает работать у взрослых, играя важную роль в восстановлении и поддержании различных тканей тела.
Гормоны гипофиза
Гипофиз выделяет несколько гормонов, включая гормон роста, пролактин и плацентарный лактоген.Эти небольшие белковые гормоны похожи по своей последовательности и структуре и играют решающую роль в росте, развитии и производстве молока. Два из них показаны здесь вверху: гормон роста человека (запись PDB 1hgu ) слева и пролактин (запись PDB 1n9d ) справа. Несмотря на их сходство, эти гормоны имеют небольшие различия в общей форме и характеристиках поверхности, что позволяет им связываться с конкретными целями для выполнения своих собственных функций.Содействие росту
Гормон роста перемещается по крови и стимулирует печень к выработке белка, называемого инсулиноподобным фактором роста (IGF-1), который показан внизу здесь с использованием координат в записи PDB 1h02 .IGF-1 помогает клеткам хряща, расположенным на концах длинных костей, размножаться. У детей это приводит к увеличению длины костей и увеличению роста ребенка. Однако в период полового созревания хрящ на концах большинства длинных костей превращается в кость, и последующее действие гормона роста или IGF-1 обычно не может увеличить их длину. IGF-1 также действует на незрелые мышечные клетки, увеличивая мышечную массу. Помимо этих функций, стимулирующих рост, гормон роста участвует в регулировании метаболизма в организме.Он действует на жировые клетки, уменьшая количество накопленных жиров, способствует синтезу белка в клетках и играет роль в регулировании уровня сахара в крови. Таким образом, гормон роста оказывает множество эффектов на общую форму и функции растущего организма.Добавки для гормона роста
Гормон роста был определен в 1920-х годах как фактор, способствующий росту. К середине-концу 1980-х ученые смогли произвести этот гормон белка, состоящего из 191 остатка, в бактериях, используя технологию рекомбинантной ДНК. Благодаря наличию больших количеств этого рекомбинантного гормона стало возможным терапевтическое использование гормона роста.Детей и взрослых с дефицитом гормона роста теперь можно лечить с помощью добавок гормона роста. Кроме того, такие добавки также полезны пациентам, страдающим заболеваниями, которые приводят к истощению и слабости мышц (например, СПИДу). Однако в некоторых случаях эти добавки используются для обращения вспять симптомов старения, увеличения мышечной массы у спортсменов и увеличения роста растущих детей. В пищевой промышленности версии этого рекомбинантного гормонального белка для коров и свиней используются для ускорения роста сельскохозяйственных животных.Хотя были высказаны некоторые опасения относительно возможных последствий употребления мяса и молока этих животных, исследования показывают, что гормон роста этих животных не действует на людей.
Рецептор гормона роста. Гормон показан красным, а участки рецептора, пересекающие мембрану, не входящие в структуру, показаны схематично.
Загрузить высококачественное изображение TIFFГормон роста в действии
Гормон роста (показан здесь красным) выполняет свои многочисленные функции, связываясь с рецепторами гормона роста (показаны здесь синим и зеленым) на своих органах и клетках-мишенях.Эти рецепторы имеют отдельные части снаружи и внутри клетки, соединенные спиральным участком, проходящим через клеточную мембрану. Интересно, что гормон роста должен связываться с двумя молекулами рецептора одновременно, чтобы выполнять свою функцию. Гормон связывается снаружи клетки, сводя вместе два рецептора. Запись PDB 3hhr , показанная здесь, включает внеклеточную часть двух рецепторов, связанных с гормоном роста. Когда два рецептора сводятся вместе, взаимодействие между частями внутри клетки (показано здесь схематически) запускает несколько ферментативных реакций и сигнальных процессов, которые стимулируют рост.Таким образом, образование этого димера рецептора имеет решающее значение для функции гормона роста. Одним из главных сюрпризов этой кристаллической структуры стало открытие того, что две идентичные по структуре молекулы рецепторов связываются с двумя структурно разными сайтами на противоположных сторонах одной молекулы гормона роста. Как и следовало ожидать, сила связывания на этих двух участках также различна: два рецептора гормона роста связываются с гормоном один за другим. Связывание с первым сайтом образует неактивный промежуточный комплекс.Сборка становится функционально активной только тогда, когда вторая молекула рецептора связывается со вторым сайтом связывания на другой стороне гормона. Любой фактор, нарушающий эту сборку, может блокировать функцию гормона. Например, замена одного глицина в положении 120 на аргинин блокирует связывание рецептора на втором сайте. Сравнивая измененный гормон (показанный справа от записи PDB 1hwh ) с нормальным гормоном (показанный слева от записи PDB 1hwg ), вы можете увидеть, что большая боковая цепь аргинина 120 не может быть приспособлена, когда второй рецептор связывается.Этот остаток конфликтует с триптофаном 104 рецептора (показаны зелеными сферами). Таким образом, измененный гормон не может образовывать функциональный комплекс со вторым рецептором и больше не способствует росту — фактически он подавляет рост.Дефицит гормона роста (для родителей)
Что такое гормон роста?
Гормон роста (GH) — это вещество в организме, которое помогает детям расти и развиваться. Его образует гипофиз, небольшая железа между долями мозга.
Что такое дефицит гормона роста?
ДефицитGH возникает, когда организм не вырабатывает достаточно гормона роста, чтобы ребенок мог расти в нормальном темпе.
Двумя видами дефицита GH являются:
- Врожденная недостаточность гормона роста. Это тот вид, с которым рождаются некоторые младенцы. Также у них могут быть проблемы с другими гормонами. Несмотря на то, что они рождаются с этим заболеванием, некоторые дети выглядят так, как будто они растут нормально, пока им не исполнится 6–12 месяцев.
- Приобретенный дефицит GH. Это происходит, когда организм перестает вырабатывать достаточно гормона роста для нормального роста. Это может начаться в любой момент в детстве.
Каковы признаки и симптомы дефицита гормона роста?
Врачи проверяют рост детей во время регулярных осмотров. Со временем врачи могут увидеть, насколько быстро растут дети. Если ребенок растет намного медленнее, чем большинство других детей того же возраста, это называется задержка роста .
Одним из наиболее заметных признаков задержки роста является рост, который намного меньше, чем у большинства других детей того же возраста.Это называется низкорослым . Но у некоторых детей может наблюдаться задержка роста, даже если они невысокого роста.
Другие признаки и симптомы дефицита GH включают:
- задержка полового созревания (выглядят намного моложе, чем другие дети того же возраста)
- зубов, приходящихся на конец
- мышечная слабость
- у мальчиков, маленький половой член при рождении
- с низким содержанием сахара в крови
Что вызывает дефицит гормона роста?
Часто врачи не знают, почему у ребенка дефицит гормона роста.Когда причина обнаружена, она часто связана с проблемами с гипофизом или с мозгом вокруг гипофиза. Опухоли головного мозга, травмы головы и лучевая терапия мозга также могут вызывать дефицит гормона роста.
Как диагностируется недостаточность гормона роста?
Если у вашего ребенка задержка роста или низкий рост даже без каких-либо других признаков или симптомов, ваш врач может направить вас к детскому эндокринологу . Это врач, специализирующийся на детском росте и гормонах.
эндокринолог спросит о росте вашего ребенка и проведет тщательное обследование. Врач назначит несколько тестов для выявления дефицита гормона роста, например:- Анализы крови. Нет простых тестов для измерения уровня GH. GH вырабатывается короткими всплесками, в основном за ночь. В других случаях уровни могут быть неопределяемыми. Это усложняет тестирование, потому что невозможно узнать, когда произойдет всплеск. Поэтому вместо этого врачи изучают уровни двух белков, которые имеют более стабильные уровни и являются маркерами функции GH:
- IGF-I, или инсулиноподобный фактор роста I
- IGFPB-3 или белок-3, связывающий инсулиноподобный фактор роста
Как лечится дефицит гормона роста?
Лечение дефицита гормона роста — это ежедневная инъекция гормона роста.Родители учатся делать эти прививки дома, поэтому им не нужно идти за ними к врачу.
Эндокринолог скажет вам, как часто ваш ребенок должен приходить, когда начинается лечение. При каждом посещении врача:
- проверим рост вашего ребенка
- может заказать анализы крови, чтобы узнать, как организм вашего ребенка реагирует на лекарство
- при необходимости изменить дозу
Побочные эффекты редки при дозах, используемых при дефиците гормона роста.Сообщите врачу, если у вашего ребенка головные боли, изменения зрения или хромота.
Лечение обычно длится до завершения роста, в позднем подростковом возрасте.
Что еще мне нужно знать?
Гормон роста может увеличить скорость роста у ребенка с дефицитом гормона роста. Дети, которые начинают лечение раньше, часто могут наверстать упущенное, чем дети, которые начинают лечение позже.
Когда мы взрослые, наши тела производят гораздо меньшее количество GH. Таким образом, многим детям с дефицитом GH и без других медицинских проблем, которые получают прививки GH, они не понадобятся во взрослом возрасте.
Genentech: понимание гормона роста человека
Общие сведения о гормоне роста (HGH)
Гормон роста человека (hGH или GH) — это белок, вырабатываемый в организме, который важен не только для в детстве, но и во взрослой жизни. Гормон роста вырабатывается гипофизом. железа, которая известна как «главная железа», потому что она секретирует много гормонов, контролирующих действия других желез.Часть мозга, называемая гипоталамусом, посылает сигналы в гипофиз для производства GH, который затем проходит через кровоток, чтобы функционировать в других части тела.
Хотя научные исследования обычно фокусируются на роли GH в процессе роста, его вклад в метаболические процессы взрослых также имеет решающее значение.
Роль GH в росте
Как известно большинству из нас, на рост влияют многие факторы.Правильное питание и общее состояние здоровья влияют на рост, как и гормоны в организме, такие как GH. Однако GH — не единственный гормон, участвующий в процесс роста. Другие гормоны гипофиза, в том числе тиреотропный гормон, адренокортикотропный гормон, лютеинизирующий гормон и фолликулостимулирующий гормон — влияют рост косвенно, действуя через другие железы. Хотя все эти гормоны могут влиять на рост, GH является основным регулятором роста в организме.
Основная задача GH в детстве — стимулировать рост костей и тканей. GH стимулирует эпифизарные пластинки роста в кости, которые отвечают за удлинение кости. GH также запускает высвобождение белка инсулиноподобного фактора роста-I (IGF-I), который стимулирует рост костей, мышц и других тканей в ответ на GH, а также, в свою очередь, регулирует GH выброс из гипофиза.Гормон роста также способствует правильной плотности костей, которая важно как в детстве, так и во взрослом возрасте, когда низкая плотность костной ткани может привести к таким проблемам, как остеопороз.
Этот механизм в сочетании с другими сложными процессами в организме поддерживает рост человек от младенчества до взрослого возраста.
Роль GH в метаболизме
Хотя основная функция GH — способствовать развитию в детстве, GH по-прежнему важен когда-то достигнута зрелость.У взрослых и детей GH помогает регулировать метаболизм — a критический химический процесс, посредством которого организм превращает пищу в энергию, ткани или отходы продукты. GH помогает в транспортировке молекул, сохранении сахаров, построении белков и расщепление жиров. Не только гормон роста, вырабатываемый вашим телом, жизненно важен для поддержания здоровья. состав, он также способствует правильной плотности костей, функции сердечной мышцы и соотношению от «хорошего» до «плохого» холестерина, все из которых важны для снижения риска таких состояний, как высокий холестерин и остеопороз.
Таким образом, как и детям, взрослым также необходимо поддерживать адекватный уровень гормона роста в организме. Без достаточный GH, взрослые имеют повышенный риск развития серьезных проблем со здоровьем, таких как сердечно-сосудистые заболевания и болезни костей в более зрелом возрасте.
Что такое дефицит гормона роста: симптомы, диагностика и лечение
Для многих сегодня начало новой учебы или рабочей недели, но для сообщества редких заболеваний сегодня знаменует начало чего-то большего: Недели осведомленности о росте детей.Редкие заболевания — это больше, чем просто часть нашего бизнеса; это наша страсть, и она определяет решения, которые мы принимаем каждый день ….
В Pfizer Rare Disease мы определяем пребывание «здесь» для сообщества редких заболеваний как обязательство слушать, учиться и помогать изменить жизнь более 350 миллионов человек, страдающих от этого редкого заболевания во всем мире. В течение 30 лет мы сосредоточились на том, чтобы быть …
Pfizer Rare Disease работает над устранением основных причин определенных генетических заболеваний, уделяя особое внимание узкоспециализированным, потенциально одноразовым методам генной терапии.Гены играют важную роль в определении функции каждой клетки в организме, составляя 30 миллионов кодов ДНК. Если даже …
Автор: Get Science Staff: эта статья изначально была опубликована на сайте Get Science. Надежда на горизонт унаследованного нарушения свертывания крови Когда мы получаем порез или травму, более дюжины факторов свертывания крови или специальных белков, циркулирующих в организме, каскадом активируются, чтобы помочь нам остановить кровотечение. & …
Pfizer обращает внимание на женщин, страдающих гемофилией. В ознаменование Всемирного дня гемофилии 17 апреля и повышения осведомленности об этом изнурительном состоянии Всемирная федерация гемофилии решила пролить свет на проблемы, которые оказывают уникальное влияние на женщин в сообществе, связанном с нарушениями свертываемости крови.Много…
Сукирти Багал, доктор медицины, магистр здравоохранения — Эта статья была первоначально опубликована на сайте Get Healthy, Оставайтесь здоровыми. В: Что такое болезнь Гоше? Ответ: Болезнь Гоше — редкое наследственное заболевание. Впервые он был описан доктором Филиппом Гоше в 1882 году и вызван генетическими мутациями (постоянное изменение ДНК гена) и …
Авторы: Дженнифер Шумахер, доктор философии, и Лесли Амасс, доктор философии. Эта статья изначально была опубликована на сайте «Здоровое здоровье». Оставайтесь здоровыми. Вы, вероятно, знаете кого-то с сердечным заболеванием, проблемами желудочно-кишечного тракта или нервными болями.Но есть вероятность, что вы вряд ли знаете кого-нибудь с редким и опасным для жизни заболеванием, которое может вызвать …
Эта статья изначально была опубликована на сайте Get Healthy, Оставайтесь здоровыми. Люди с серповидно-клеточной анемией (ВСС) сейчас живут дольше, чем в предыдущие десятилетия. Врачи лучше понимают болезнь, могут диагностировать ее раньше и могут легче лечить и предотвращать инфекции …
Оттавио В.Витоло, доктор медицинских наук, MMS — Эта статья, первоначально опубликованная на тему «Здоровый образ жизни», «Здоровый образ жизни» Болезнь Хантингтона (БХ) — редкое генетическое заболевание, которое вызывает разрушение нервных клеток в головном мозге. Начало и прогрессирование заболевания варьируется от человека к человеку. Большинство…
Бартоломью Дж. Тортелла, доктор медицины, магистр делового администрирования — Эта статья была первоначально опубликована на сайте Get Healthy, Оставайтесь здоровыми. В: Что такое гемофилия? О: Гемофилия — это заболевание крови, которое в первую очередь поражает мужчин.Люди, страдающие гемофилией, склонны к кровотечению в течение более длительных периодов времени после травмы или операции ….
Эта статья изначально была опубликована на сайте Get Healthy, Оставайтесь здоровыми. Что такое мышечная дистрофия Дюшенна (МДД)? Мышечная дистрофия Дюшенна (МДД) — это мышечная дистрофия, диагностируемая в раннем детстве. По данным Национального исследовательского института генома человека, им страдает примерно 1 из 3500 мужчин …
Рослин Ф.Шнайдер, доктор медицины, магистр медицины — Эта статья изначально была опубликована в статье «Здоровое здоровье». Оставайтесь здоровыми. Что такое саркоидоз? Саркоидоз — это заболевание, характеризующееся воспалением практически любого органа тела и часто поражающим легкие. Воспаление при саркоидозе называется гранулематозным …
Автор: Джилл Сиско. Эта статья была первоначально опубликована в статье «Здоровое здоровье». Акромегалия может быть трудной для диагностики, потому что обычно требуется время, чтобы признаки и симптомы проявились, а затем были распознаны.И у многих людей с этим заболеванием его часто не замечают. Это был …
Эта статья изначально была опубликована на сайте Get Healthy, Оставайтесь здоровыми. Акромегалия — это гормональное заболевание, которое развивается, когда гипофиз вырабатывает слишком много гормона роста (GH).



 Уровень NTX в крови или моче, отражает суммарную активность остеокластов, что позволяет его считать одним из лучших маркеров резорбции кости.
Уровень NTX в крови или моче, отражает суммарную активность остеокластов, что позволяет его считать одним из лучших маркеров резорбции кости.