Об осложнениях гриппа. Почему необходимо обращаться к врачу?
Об осложнениях гриппа. Почему необходимо обращаться к врачу?
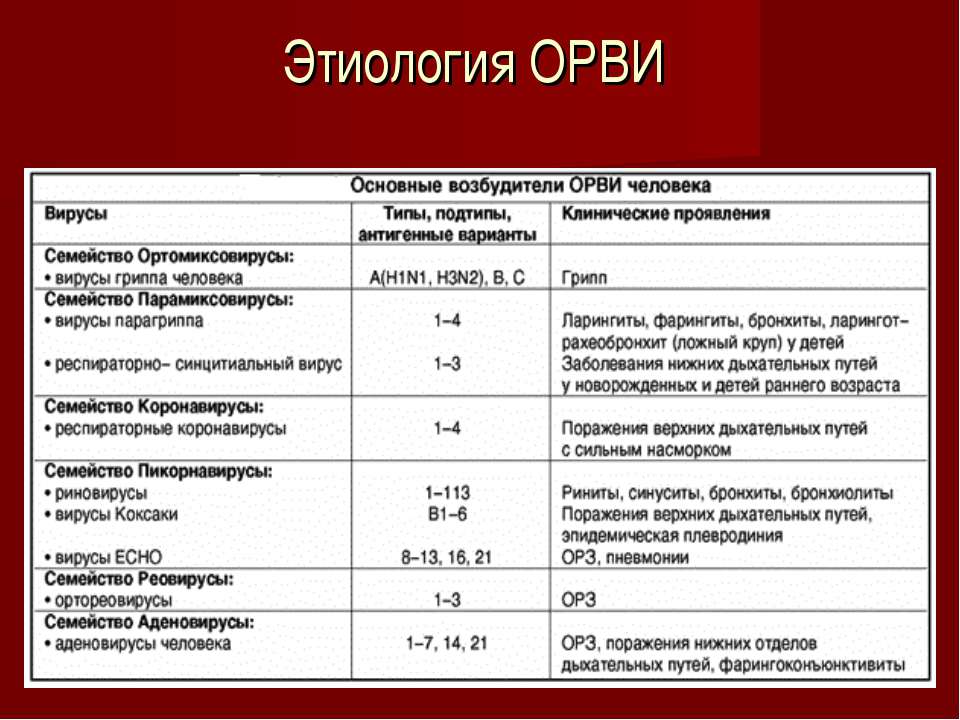
Почему грипп, относясь к группе острых респираторных вирусных инфекций, выделяется как особая инфекция? Почему именно о гриппе говорят врачи, СМИ, популярные сайты сети Интернет?
Ответ прост: грипп – единственная острая респираторная вирусная инфекция (ОРВИ), влекущая за собой серьезные осложнения, которые не только нарушают работу нашего организма, но и опасны для жизни. А осложнения эти возникают очень часто. Чаще всего осложнения гриппа носят отсроченный характер, проявляются спустя некоторое время, когда человек уже забыл о перенесенной инфекции. Начинаются проблемы в функционировании сердечно-сосудистой, нервной и других систем организма.
По данным Всемирной организации здравоохранения (ВОЗ), ежегодно в мире гриппом и ОРВИ заболевает до 500 млн. человек, от осложнений заболевания умирают около 500 тысяч человек.
В Москве на грипп и ОРВИ приходится ежегодно до 90% от всей регистрируемой инфекционной заболеваемости, болеет около 3 млн. человек, из них около 60% — дети.
Общая информация о заболевании.
Грипп – острая вирусная инфекция дыхательных путей, характеризующаяся поражением слизистых оболочек верхних дыхательных путей, лихорадкой, интоксикацией, а также нарушениями деятельности сердечно — сосудистой и нервной систем.
Источником инфекции является больной человек с клинически выраженной или бессимптомной формой гриппа. Важную роль в передаче инфекции играют больные со стертой формой инфекции, переносящие заболевание «на ногах».
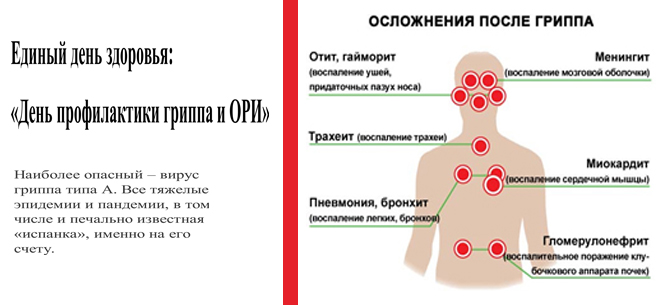
Какие органы чаще всего поражает вирус гриппа?
Наиболее часто встречаются осложнения со стороны дыхательной системы, на втором месте — органы сердечно-сосудистой системы и органы кроветворения, также встречаются осложнения со стороны нервной и моче-половой систем.
Для кого особенно опасны осложнения гриппа?
В группе риска по неблагоприятному исходу заболевания находятся дети до года и взрослые старше 60 лет с сопутствующими заболеваниями органов дыхания, сердечно-сосудистой системы и эндокринной патологией, у которых возможен летальный исход из-за осложнений ранее имевшихся заболеваний.
Осложнения гриппа делятся на 2 группы:
1. Связанные непосредственно с течением гриппа.
Это геморрагический отек легких, менингит, менингоэнцефалит, инфекционно-токсический шок.
2. Возникшие в результате присоединения бактериальной инфекции.
Наиболее опасное и частое осложнение – это пневмония. Пневмония может быть как первичной, которая развилась сразу, так и вторичной – возникшей на фоне присоединения бактериальной инфекции. Бактериальные агенты, наиболее часто вызывающие вторичную пневмонию, – пневмококк и стафилококк. Такие пневмонии развиваются в конце первой – начале второй недели заболевания. Вирусная пневмония может протекать совместно с бактериальной, присоединившейся позднее.
Вирусная пневмония может протекать совместно с бактериальной, присоединившейся позднее.
Еще одним смертельно опасным осложнением гриппа считается острый респираторный дистресс-синдром, заключающийся в нарушении барьерной функции легочной ткани. На фоне данного осложнения возникает серьезнейшая дыхательная недостаточность, нередко несовместимая с жизнью.
Не менее опасными осложнениями являются отит, синусит, гломерулонефрит, гнойный менингит, сепсис.
Токсическое поражение сердечной мышцы, как осложнение гриппа, особенно опасно для пожилых людей.
Поражение центральной нервной системы проявляется менингеальным синдромом, спутанным сознанием, головной болью, рвотой.
О поражении периферической нервной системы свидетельствуют радикулярные и другие невралгические боли.
При развитии отека мозга, геморрагического энцефалита у больного наблюдаются судороги, расстройство сознания. Такие осложнения нередко приводят к смерти вследствие остановки дыхания.
Профилактика гриппа:
Единственным надежным средством профилактики гриппа является вакцинация. Оптимальным временем проведения вакцинации против гриппа является период с сентября по ноябрь.
Оптимальным временем проведения вакцинации против гриппа является период с сентября по ноябрь.
Профилактика осложнений.
Если по каким-либо причинам вакцинацию провести не удалось, — строжайшим образом соблюдайте правила личной гигиены. Во время подъема уровня заболеваемости гриппом постарайтесь не посещать общественные места, не контактируйте с заболевшими.
В случае подозрения у себя вирусной инфекции, в течение ближайших 48 часов обратитесь к врачу.
Не пренебрегайте лечением, которое назначил Вам врач, своевременно принимайте назначенные лекарственные средства.
Обязательным пунктом в профилактике развития осложнений является соблюдение постельного режима во время болезни.
Причиной смерти от вируса гриппа является несвоевременное обращение за медицинской помощью и отказ от лечения.
Проблема бактериальных осложнений при респираторных вирусных инфекциях Текст научной статьи по специальности «Фундаментальная медицина»
MIRJournal
MicrobioLogy Independent Research JournaL
ОБЗОР
Проблема бактериальных осложнений при респираторных вирусных инфекциях
А. Ю. Егоров12*
Ю. Егоров12*
1 Университет природных ресурсов и естественных наук, Вена, Австрия
2 ФГБНУ «Научно-исследовательский институт вакцин и сывороток им. И. И. Мечникова», Москва, Российская Федерация # Для корреспонденции: Андрей Юрьевич Егоров, e-mail: [email protected]
Ключевые слова: вирус, грипп, инфекция, вторичная бактериальная инфекция, вторичная пневмония, интерферон DOI: 10.18527/2500-2236-2018-5-1-1-11
Получен 10 апреля 2018 г. Принят к печати 20 мая 2018 г. Опубликован 22 июня 2018 г.
АННОТАЦИЯ
Разнообразные респираторные вирусы многократно поражают каждого человека в течение жизни и являются фактором риска развития бактериальных осложнений. Наиболее опасным среди возбудителей острых респираторных вирусных заболеваний является вирус гриппа А, способный вызывать катастрофические пандемии, высокая смертность при которых в значительной степени обусловлена вторичной бактериальной пневмонией. В многочисленных исследованиях последних лет показано, что независимо от типа респираторного вируса основным механизмом провоцирования бактериальных инфекций является несбалансированный ответ системы врожденного противовирусного иммунитета — избыточный интерфероновый ответ и неконтролируемое воспаление. Вероятность тяжелых бактериальных осложнений при острых респираторных вирусных инфекциях определяется как вирулентностью самого вируса, так и составом респираторной микробиоты в момент вирусного заражения, а также генетическими особенностями организма и наличием хронических заболеваний, влияющих на регуляцию системы врожденного иммунного ответа. В данном обзоре суммированы современные представления о механизмах развития бактериальных осложнений, следующих за вирусной инфекцией, и возможностях их предотвращения.
В многочисленных исследованиях последних лет показано, что независимо от типа респираторного вируса основным механизмом провоцирования бактериальных инфекций является несбалансированный ответ системы врожденного противовирусного иммунитета — избыточный интерфероновый ответ и неконтролируемое воспаление. Вероятность тяжелых бактериальных осложнений при острых респираторных вирусных инфекциях определяется как вирулентностью самого вируса, так и составом респираторной микробиоты в момент вирусного заражения, а также генетическими особенностями организма и наличием хронических заболеваний, влияющих на регуляцию системы врожденного иммунного ответа. В данном обзоре суммированы современные представления о механизмах развития бактериальных осложнений, следующих за вирусной инфекцией, и возможностях их предотвращения.
The problem of bacterial complications post respiratory viral infections
Andrej Egorov1,2
1 University of Natural Resources and Life Sciences, Vienna, Austria
 com
comKeywords: virus, influenza, infection, secondary bacterial infection, secondary pneumonia, interferon ABSTRACT
Every person in the course of lifetime is repeatedly infected by a variety of respiratory viruses that represent the risk factors for the development of bacterial complications. The most dangerous among the etiological factors of acute respiratory viral diseases is the influenza A virus. This virus is capable to cause catastrophic pandemics with high mortality mainly due to the secondary bacterial pneumonia. As it has been shown in numerous recent studies, the main mechanism of provoking bacterial infections irrespective of the type of respiratory virus is the unbalanced response of the antiviral innate immunity — excessive interferon response and uncontrolled inflammation. The probability of severe bacterial complications in the course of acute respiratory viral infections is determined by both the virulence of the virus itself and by the composition of the respiratory microbiota at the time of the viral infection, as well as by the genetic characteristics of the organism.
По оценкам Всемирной организации здравоохранения (ВОЗ), от острых респираторных вирусных инфекций (ОРВИ) умирает 3,9 млн человек в год [1]. Эти инфекции затрагивают все возрастные группы, но особенно влияют на здоровье детей, а также людей пожилого возраста и имеющих хронические заболевания. Опасность ОРВИ определяется их способностью провоцировать как вирусную пневмонию, так и вторичные бактериальные осложнения, такие как пневмония, отит, менингит, а также хронические легочные заболевания. Так, именно респираторные вирусы вовлечены примерно в 50% случаев внебольничной пневмонии (ВБП) у детей и провоцируют более 90% случаев бронхиолита у младенцев и 85-95% случаев обострения астмы у детей. У взрослых, вне пандемического гриппозного периода, ОРВИ определяют 30-50% случаев ВБП, 80% обострений астмы и 20-60% обострений хронического обструктивного заболевания легких (ХОБЛ). В целом, ОРВИ являются одной из пяти главных причин смертности во всем мире, а во многих развивающихся странах — главной причиной смертности детей в возрасте до 5 лет.
У взрослых, вне пандемического гриппозного периода, ОРВИ определяют 30-50% случаев ВБП, 80% обострений астмы и 20-60% обострений хронического обструктивного заболевания легких (ХОБЛ). В целом, ОРВИ являются одной из пяти главных причин смертности во всем мире, а во многих развивающихся странах — главной причиной смертности детей в возрасте до 5 лет.
В отличие от других респираторных вирусов, вирус гриппа А представляет наибольшую опасность для человека, поскольку циркулирует среди различных видов животных и способен к реассортации геномных фрагментов, что становится причиной смены основных поверхностных антигенов вируса -гемагглютинина (НА) и нейраминидазы (NA) — и носит название антигенного шифта. Именно механизм реассортации лежит в основе появления обновленных антигенных вариантов вируса гриппа А (h2N1, h3N2, h4N2, h2N1pdm09), вызвавших 4 известные пандемии [2, 3].
В межпандемический период вирусы гриппа также претерпевают антигенные изменения, вызываемые постепенным накоплением мутаций в HA и NA (антигенный дрейф), что является причиной сезонных эпидемий.
Даже в начале XXI века, при наличии противогриппозных препаратов и антибиотиков широкого спектра действия, для людей, заболевших сезонным гриппом, существует вероятность развития вирус-индуцированного острого респираторного дистресс-синдрома (ОРДС) в течение первой недели после инфицирования или вторичной бактериальной пневмонии на 6-7 сутки после начала вирусного заболевания. По данным ВОЗ, грипп ежегодно вызывает до 650 000 смертей во всем мире. В США, с населением порядка 300 млн человек, по данным Центров по контролю и профилактике заболеваний (Centers for Disease Control and Prevention, CDC, Атланта, США), смертность от гриппа колеблется в пределах 16 000-56 000 случаев ежегодно. В Российской Федерации, с населением 146 млн человек, статистика смертности от гриппа в открытых официальных источниках отсутствует, однако, по заявлениям представителей надзорных органов, случаи смерти от
гриппа исчисляются несколькими сотнями в год при сезонных вспышках заболеваемости. Различия в данных по смертности от гриппа в разных странах могут определяться методикой учета этиологического фактора как причины смерти. Например, статистика смертности от бактериальных пневмоний может не учитывать роль вирусного этиологического фактора как провокатора вторичной инфекции. Таким образом, лица, умершие от бактериальных пневмоний, могут не учитываться в статистике смертности от гриппа, даже если бактериальное осложнение было спровоцировано первичной гриппозной инфекцией.
Различия в данных по смертности от гриппа в разных странах могут определяться методикой учета этиологического фактора как причины смерти. Например, статистика смертности от бактериальных пневмоний может не учитывать роль вирусного этиологического фактора как провокатора вторичной инфекции. Таким образом, лица, умершие от бактериальных пневмоний, могут не учитываться в статистике смертности от гриппа, даже если бактериальное осложнение было спровоцировано первичной гриппозной инфекцией.
Грипп в отсутствие антибиотиков, антивирусных препаратов и вакцин
Пандемия, вызванная вирусом гриппа A(h2N1) в конце первой мировой войны (1918 г.) и получившая название «испанка», была самой масштабной из когда-либо зарегистрированных: заражению подверглось 50% населения Земли, а погибло около 50 млн человек [4]. Основной группой людей, пострадавших от этой пандемии, были лица в возрасте 20-40 лет, призванные в армию. Следует отметить, что во время «испанки», в начале XX века, этиологический агент заболевания еще не был известен: вирус гриппа открыли только в 1933 году. Микробиологи того времени пытались связать испанский грипп с различными бактериальными агентами и, в частности, с Haemophilus influenzae (H. influenzae) [5]. В настоящее время, благодаря технологии ПЦР, оказалось возможным идентифицировать гены вируса гриппа в патологоанатоми-ческих и гистологических препаратах того времени и реконструировать вирус гриппа 1918 года подтипа h2N1 с помощью методов обратной генетики. Как ни странно, не было выявлено радикальных отличий в генетической структуре вируса гриппа, вызвавшего «испанку», от вируса гриппа того же подтипа, циркулирующего в человеческой популяции в настоящее время [6]. При исследовании патологоанатомических материалов в более чем 90% образцов тканей легкого людей, умерших от гриппа в период пандемии, выявлены признаки бактериальной инфекции [7-9]. Оказалось, что 95% летальных исходов были следствием бактериальной пневмонии, а не первичной вирусной пневмонии.
Следует отметить, что во время «испанки», в начале XX века, этиологический агент заболевания еще не был известен: вирус гриппа открыли только в 1933 году. Микробиологи того времени пытались связать испанский грипп с различными бактериальными агентами и, в частности, с Haemophilus influenzae (H. influenzae) [5]. В настоящее время, благодаря технологии ПЦР, оказалось возможным идентифицировать гены вируса гриппа в патологоанатоми-ческих и гистологических препаратах того времени и реконструировать вирус гриппа 1918 года подтипа h2N1 с помощью методов обратной генетики. Как ни странно, не было выявлено радикальных отличий в генетической структуре вируса гриппа, вызвавшего «испанку», от вируса гриппа того же подтипа, циркулирующего в человеческой популяции в настоящее время [6]. При исследовании патологоанатомических материалов в более чем 90% образцов тканей легкого людей, умерших от гриппа в период пандемии, выявлены признаки бактериальной инфекции [7-9]. Оказалось, что 95% летальных исходов были следствием бактериальной пневмонии, а не первичной вирусной пневмонии.
Пандемический грипп в эпоху антибиотиков при отсутствии вакцинации и противовирусных препаратов
В 1957 г. пандемия азиатского гриппа затронула 40-50% людей во всем мире. Причиной стал штамм вируса гриппа A (h3N2) [12]. Глобальные оценки смертности колеблются между 1,5 и 4 млн человек [13], число погибших в США оценивается в 69 800 [1315]. При анализе постмортальных образцов бактериальная инфекция выявлена в 80% тяжелых случаев и летальных исходов [8, 16, 17]. Следует отметить, что в развитых странах к этому времени уже применялись такие антибиотики, как пенициллин и стрептомицин. Тем не менее, во время этой пандемии в США и многих других странах наблюдалось увеличение числа госпитализаций, связанных с пневмонией, преимущественно вызванной S. pneumoniae, H. influenzae и S. aureus [18]. Аналогичные данные представлены в отчетах из Нидерландов, где из 148 проанализированных летальных исходов, предположительно вызванных азиатским гриппом, 75% были ассоциированы с бактериальной пневмонией, вызванной в 59% случаев S. aureus и в 15% — S. pneumoniae [16]. Возможно, приведенные данные бактериологического обследования могли быть сильно искажены, поскольку многие пациенты уже принимали антибиотики [19].
При анализе постмортальных образцов бактериальная инфекция выявлена в 80% тяжелых случаев и летальных исходов [8, 16, 17]. Следует отметить, что в развитых странах к этому времени уже применялись такие антибиотики, как пенициллин и стрептомицин. Тем не менее, во время этой пандемии в США и многих других странах наблюдалось увеличение числа госпитализаций, связанных с пневмонией, преимущественно вызванной S. pneumoniae, H. influenzae и S. aureus [18]. Аналогичные данные представлены в отчетах из Нидерландов, где из 148 проанализированных летальных исходов, предположительно вызванных азиатским гриппом, 75% были ассоциированы с бактериальной пневмонией, вызванной в 59% случаев S. aureus и в 15% — S. pneumoniae [16]. Возможно, приведенные данные бактериологического обследования могли быть сильно искажены, поскольку многие пациенты уже принимали антибиотики [19].
В течение 1968-1969 гг. от пандемии гонконгского гриппа, вызванной вирусом гриппа A (h4N2), во всем мире погибло около 2 млн человек [20, 21]. В частности, в 1969 году в Великобритании был зарегистрирован 55%-ый рост смертности от респираторных инфекций, большинство из которых ассоциировалось со вторичной бактериальной пневмонией [22]. Стафилококковая пневмония оказалась основной причиной осложненного течения гриппа, вызванного гонконгским штаммом. Например, из 129 обследованных взрослых с диагнозом «пандемический грипп» пневмония была установлена у 16%, из которых 40% случаев (6% всех 129 случаев гриппа) были смертельными. S. aureus или Pseudomonas aeruginosa (P. aeruginosa) присутствовали в 75% постмортальных образцов [23]. Интересно, что при пандемии «испанки» доминирующим патогеном, ассоциированным с пневмонией и летальными исходами, был S. pneumoniae, а при пандемиях 1957 г. и 1968 г. превалирующим этиологическим агентом вторичных бактериальных пневмоний был стафилококк. Возможной причиной этого могло быть широкое применение антибиотиков и, как следствие, развитие антибиотикорезистентности именно у S. aureus.
В частности, в 1969 году в Великобритании был зарегистрирован 55%-ый рост смертности от респираторных инфекций, большинство из которых ассоциировалось со вторичной бактериальной пневмонией [22]. Стафилококковая пневмония оказалась основной причиной осложненного течения гриппа, вызванного гонконгским штаммом. Например, из 129 обследованных взрослых с диагнозом «пандемический грипп» пневмония была установлена у 16%, из которых 40% случаев (6% всех 129 случаев гриппа) были смертельными. S. aureus или Pseudomonas aeruginosa (P. aeruginosa) присутствовали в 75% постмортальных образцов [23]. Интересно, что при пандемии «испанки» доминирующим патогеном, ассоциированным с пневмонией и летальными исходами, был S. pneumoniae, а при пандемиях 1957 г. и 1968 г. превалирующим этиологическим агентом вторичных бактериальных пневмоний был стафилококк. Возможной причиной этого могло быть широкое применение антибиотиков и, как следствие, развитие антибиотикорезистентности именно у S. aureus.
Пандемия гриппа в условиях наличия противогриппозных вакцин, антивирусных препаратов и антибиотиков
В 2009 году вспышка гриппа, вызванная штаммом A(h2N1)pdm09, в течение 4 недель распространилась на 41 страну [20, 24].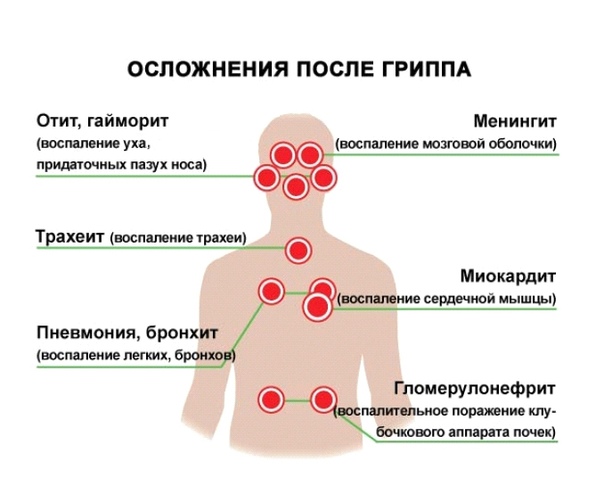 Варианты сезонных гриппозных вакцин, выпущенных в сезон 2009 года, не соответствовали по компоненту h2 антигенным свойствам
Варианты сезонных гриппозных вакцин, выпущенных в сезон 2009 года, не соответствовали по компоненту h2 антигенным свойствам
вновь появившегося пандемического штамма. Считается, что во всем мире эпидемия привела к гибели 284 000 человек [25]. В США во время пандемии гриппа 2009 года частыми причинами смерти также были вторичные бактериальные инфекции, в основном S. pneumoniae и S. pyogenes [26, 27]. Американские исследователи выявили, что 77 летальных исходов в период с мая по август 2009 года были ассоциированы с бактериальными инфекциями почти в 30% случаев, 46% из которых были вызваны S. pneumoniae, 9% -S. aureus и 1% — H. influenzae. Palacios et al. исследовали образцы носоглоточных мазков почти у 200 больных пандемическим гриппом: H. influenzae обнаружена в 52%, S. pneumoniae — в 31% и S. aureus — в 18% образцов [28]. Тяжесть заболевания наиболее часто коррелировала с выделением S. pneumoniae.
В исследовании 838 критически больных детей в США показано, что в течение 72 ч после госпитализации в отделение интенсивной терапии у 33% детей развивалась бактериальная суперинфекция. При этом 48% выделенных патогенов относились к мети-циллинрезистентным штаммам S. aureus (methicillin-resistant S. aureus, MRSA), 5,5% — к S. pneumoniae и 5% -к H. influenzae [29].
При этом 48% выделенных патогенов относились к мети-циллинрезистентным штаммам S. aureus (methicillin-resistant S. aureus, MRSA), 5,5% — к S. pneumoniae и 5% -к H. influenzae [29].
Таким образом, несмотря на широкое внедрение сезонных гриппозных вакцин, противовирусных препаратов и антибиотиков, проблема бактериальных осложнений при гриппе не потеряла актуальности. Более того, развитие резистентности бактериальной флоры к современным антибиотикам может обострить эту проблему при новой пандемии гриппа
[30].
Респираторные вирусные инфекции негриппозной этиологии как триггеры вторичных бактериальных пневмоний
Современное состояние диагностики позволяет проводить анализ бактериальных осложнений при различных респираторных инфекциях негриппозной этиологии. В Таблице 1 суммированы результаты многочисленных исследований, в которых прослежена взаимосвязь возбудителей респираторных вирусных инфекций с определенными бактериальными патогенами, ассоциированными с такими осложнениями, как пневмония, отит, синусит и менингит. Несмотря на отсутствие пандемического потенциала, другие представители респираторных вирусов оказались не менее опасными триггерами вторичных бактериальных осложнений, чем вирусы гриппа. Например, представитель семейства Paramyxoviridae метапневмовирус человека (hMPV) по тяжести осложнений не уступает вирусу гриппа. Осложнения включают как вирусную пневмонию с развитием ОРДС, так и вторичную бактериальную пневмонию
Несмотря на отсутствие пандемического потенциала, другие представители респираторных вирусов оказались не менее опасными триггерами вторичных бактериальных осложнений, чем вирусы гриппа. Например, представитель семейства Paramyxoviridae метапневмовирус человека (hMPV) по тяжести осложнений не уступает вирусу гриппа. Осложнения включают как вирусную пневмонию с развитием ОРДС, так и вторичную бактериальную пневмонию
[31]. Другой представитель этого семейства — респи-раторно-синцитиальный вирус (respiratory syncytial virus, RSV) — оказался более опасным, чем возбудитель гриппа, по параметру смертности пациентов, госпитализированных с диагнозом «пневмония». Оказалось, что смертность от всех причин через 20 суток
после госпитализации среди пациентов с RSV инфекцией (18,4%) выше, чем среди пациентов с гриппом (6,7%) [32]. К сожалению, для профилактики и лечения пневмовирусов отсутствуют вакцины и эффективные противовирусные препараты, как и для большинства респираторных вирусов негриппозной этиологии.
Таблица 1. Респираторные вирусы и ассоциированные с ними бактериальные вторичные инфекции
Вирус Ассоциируемая вторичная инфекция* Ссылка
Вирус гриппа S. pneumoniae, S. aureus, Staphylococcus pyogenes, H. influenzae, Moraxella catarrhalis, Neisseria meningitidis [7], [3340]
КБУ S. pneumoniae [41]
Аденовирус S. pneumoniae, H. influenzae, Moraxella catarrhalis [42]
Риновирус человека S. pneumoniae, S. aureus, H. influenzae, Moraxella catarrhalis [43-45]
Вирус парагриппа Moraxella catarrhalis, S. pneumoniae [46]
ИМРУ S. pneumoniae [47]
* Указаны патогены, которые чаще всего идентифицируют у больных с осложненным течением вирусной инфекции.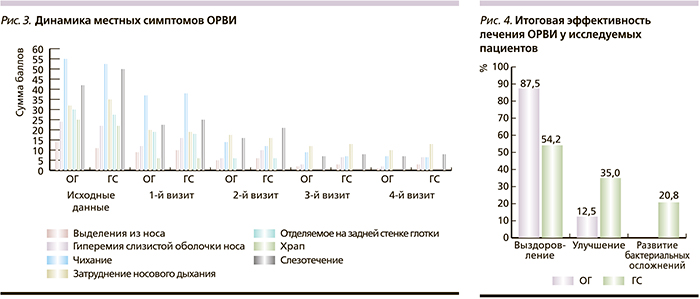
Исследования, проведенные в различных регионах мира, при общности выводов о связи вирусных и бактериальных инфекций могут различаться по выводам о роли различных патогенов в развитии ВБП, поскольку климатические условия и генетические особенности населения могут существенно влиять на распространенность того или иного вирусного и бактериального возбудителя.
В проведенном в США исследовании участвовало 1024 пациента с ВБП и 759 пациентов без выраженных симптомов [48]. Оказалось, что вирусы гриппа, RSV, hMPV, а также, в меньшей степени, вирусы парагриппа и коронавирусы существенно чаще встречались в группе больных пневмонией, независимо от возраста пациентов. В то же время риновирусы были частой причиной ВБП у взрослых, но практически не встречались при пневмонии у детей, тогда как аденовирусы ассоциировались с ВБП только у детей младше 2 лет.
В исследовании, проведенном в Японии, участвовало 2617 пациентов с пневмонией — в основном пожилые люди (старше 65 лет) с хроническими респираторными или другими сопутствующими заболеваниями. Вирусные патогены были обнаружены в 23,1% случаев [49]. Риновирусы были наиболее частой причиной развития пневмонии (9,8%), а вирусы гриппа и RSV встречались в 3,9% случаев каждый. RSV наиболее часто выявляли у лиц с хроническими заболеваниями респираторного тракта, в то время как другие вирусы ассоциировались с пневмонией независимо от наличия респираторных и других хронических заболеваний. В целом, вирусные инфекции не предопределяли повышенный риск смертности у больных пневмонией, однако в случае хронических респираторных заболеваний гриппозная инфекция ассоциировалась с увеличением смертности
Вирусные патогены были обнаружены в 23,1% случаев [49]. Риновирусы были наиболее частой причиной развития пневмонии (9,8%), а вирусы гриппа и RSV встречались в 3,9% случаев каждый. RSV наиболее часто выявляли у лиц с хроническими заболеваниями респираторного тракта, в то время как другие вирусы ассоциировались с пневмонией независимо от наличия респираторных и других хронических заболеваний. В целом, вирусные инфекции не предопределяли повышенный риск смертности у больных пневмонией, однако в случае хронических респираторных заболеваний гриппозная инфекция ассоциировалась с увеличением смертности
пациентов в 3 раза. Таким образом, вклад вирусной инфекции в смертность от пневмонии зависит от типа вирусного агента и наличия сопутствующих заболеваний.
Корейское мета-аналитическое исследование, проведенное на 5298 пациентах различных возрастных групп, показывает, что провокация бактериальной суперинфекции характерна для всех представителей вирусных респираторных инфекций [50], однако вид бактериального возбудителя вторичной инфекции может зависеть как от типа вирусной инфекции, так и от возраста пациента. Например, у взрослых инфекция вирусом гриппа А и В, ринови-русом и hMPV прежде всего вызывала пневмонию, ассоциированную с S. aureus, тогда как инфекции, вызванные коронавирусом, вирусом парагриппа и RSV, осложнялись пневмонией, связанной с грамотрица-тельными бактериями Klebsiella spp. и Acinetobacter spp. У детей наиболее частой причиной возникновения бактериальной пневмонии независимо от типа предшествующего вируса была микоплазменная инфекция (Mycoplasma pneumonia, M. pneumonia). На основании результатов этого исследования можно судить о значимости дифференциальной вирусологической диагностики при вторичной бактериальной пневмонии с точки зрения назначения антибиоти-котерапии. Например, для лечения вторичной пневмонии у младенцев и детей, скорее всего, подойдут антибиотики с активностью против M. pneumoniae (макролиды), взрослым, перенесшим грипп, hMPV или риновирусную инфекцию, — антистафилококковые препараты, а после инфекции коронавирусом и вирусом парагриппа — антибиотики против широкого спектра грамотрицательных бактерий.
Например, у взрослых инфекция вирусом гриппа А и В, ринови-русом и hMPV прежде всего вызывала пневмонию, ассоциированную с S. aureus, тогда как инфекции, вызванные коронавирусом, вирусом парагриппа и RSV, осложнялись пневмонией, связанной с грамотрица-тельными бактериями Klebsiella spp. и Acinetobacter spp. У детей наиболее частой причиной возникновения бактериальной пневмонии независимо от типа предшествующего вируса была микоплазменная инфекция (Mycoplasma pneumonia, M. pneumonia). На основании результатов этого исследования можно судить о значимости дифференциальной вирусологической диагностики при вторичной бактериальной пневмонии с точки зрения назначения антибиоти-котерапии. Например, для лечения вторичной пневмонии у младенцев и детей, скорее всего, подойдут антибиотики с активностью против M. pneumoniae (макролиды), взрослым, перенесшим грипп, hMPV или риновирусную инфекцию, — антистафилококковые препараты, а после инфекции коронавирусом и вирусом парагриппа — антибиотики против широкого спектра грамотрицательных бактерий.
Как отмечено выше, региональные особенности генотипа населения, климата и спектра колонизующей микробной флоры диктуют необходимость проведения подобных наблюдательных исследований в различных странах мира для разработки адекватных медицинских стандартов лечения респираторных инфекций.
Патогенез вторичных бактериальных инфекций при ОРВИ
Человеческий организм является носителем разнообразных бактериальных видов, в совокупности именуемых микробиотой [51]. В норме эти бактерии считаются так называемыми комменсальными штаммами, живущими во взаимовыгодном симбиозе с хозяином и обеспечивающими разнообразные полезные функции, например, защиту организма за счет конкуренции с патогенными штаммами. Обычно небольшие количества патогенных бактерий, включая S. pneumoniae, S. aureus, H. influenzae, S. pyogenes, Moraxella catarrhalis и MRSA, присутствуют в микробиоте верхних отделов респираторного тракта человека без серьезных последствий для организма [52]. Нарушение состава микробиоты в сторону увеличения патогенной флоры может происходить при вирусных респираторных инфекциях за счет
Нарушение состава микробиоты в сторону увеличения патогенной флоры может происходить при вирусных респираторных инфекциях за счет
подавления факторов антибактериальной защиты. В связи с этим вторичные бактериальные инфекции респираторного тракта чаще всего не нуждаются в заражении организма патогенными бактериями извне, а являются результатом спровоцированной вирусом колонизации [53, 54].
В настоящее время известно множество патогенетических факторов, способствующих бактериальной колонизации при вирусной инфекции, которые включают следующие:
1. Нарушение целостности слизистых оболочек под воздействием вирусных и бактериальных ферментов, например NA вируса гриппа [55].
2. Усиление бактериальной адгезии на инфицированные вирусом клетки [54, 56, 57].
3. Нарушение функции цилиарного эпителия при вирусной инфекции, снижающей способность слизистых оболочек респираторного тракта к самоочищению [58, 59].
Нарушение функции цилиарного эпителия при вирусной инфекции, снижающей способность слизистых оболочек респираторного тракта к самоочищению [58, 59].
4. Индукция интерферонов I, II и III типов (IFN) и цитокинов, снижающих эффективность антибактериального иммунитета [60-64].
5. Нарушение антибактериальной активности ней-трофилов и макрофагов за счет уменьшения их количества и фагоцитарной активности в очаге вирусной инфекции [65-67].
Действие большинства перечисленных факторов может зависеть не только от особенностей вирусного возбудителя, но и от колонизующей бактерии. Например, известно, что S. aureus может усиливать вирусную репродукцию, негативно воздействуя на передачу сигнала IFN I типа путем препятствова-ния образованию димера STAT-1-STAT-2 [68]. При RSV-инфекции тяжесть заболевания у детей может определяться превалированием S. pneumoniae и H. influenza в микробиоте перед началом вирусного заболевания [69].
pneumoniae и H. influenza в микробиоте перед началом вирусного заболевания [69].
Тем не менее, в экспериментах на животных и в клинических исследованиях четко показано, что чаще всего триггерами колонизации респираторного тракта патогенной бактериальной флорой служат вирусные инфекции. Первичное заражение мышей сублетальными дозами бактерий с последующим заражением сублетальной дозой вируса гриппа не приводило к вторичной бактериальной пневмонии, в то время как обратная последовательность заражения вызывала пневмонию с летальным исходом [70-72]. Замечено, что как у зараженных вирусами животных, так и при ОРВИ у людей бактериальная суперинфекция чаще всего развивается на 4-7 сутки после вирусной инфекции или клинической манифестации вирусной инфекции соответственно [42, 73]. В этой закономерности, независимо от типа вирусного возбудителя, особую роль играет IFN I типа, фокусирующий систему врожденного иммунитета на борьбу с вирусной инфекцией, но при этом снижающий функцию факторов антибактериальной защиты, таких как фагоцитоз или выработка антибактериальных пептидов.
Роль интерферонового ответа в патогенезе вторичных бактериальных инфекций
Несмотря на различия в структурной и генетической организации вирусов различных семейств, их объединяет общее свойство: все они представляют собой внутриклеточные патогены и индукторы IFN ответа. Система врожденного иммунитета распознает вирусную инфекцию с помощью встроенных в ци-топлазматическую мембрану клеток Toll-подобных или цитоплазматических RIG-1 и MDA5 паттерн-рас-познающих рецепторов (pattern recognition receptors, PRRs), ответственных за обнаружение в очаге инфекции компонентов патогенов, атипичных для нормальных клеток, таких как двуспиральные РНК (dsRNA) или липополисахариды (LPS). Распознавание вирусной инфекции приводит к индукции цито-кинового ответа, и прежде всего IFN I, II и III типов. Система врожденного противовирусного иммунитета подробно описана в обзорах [74, 75]. Защитная функция IFN обусловлена двумя основными факторами: способностью индуцировать синтез множества противовирусных белков в зараженных и окружающих их клетках и иммуномодулирующими функциями, влияющими на миграцию и активацию клеток врожденного иммунитета и определяющими развитие специфического В- и Т-клеточного иммунного ответа [76-78].
В тоже время получено множество экспериментальных и клинических данных, согласно которым IFN ответ при ОРВИ может нести повреждающую функцию. При прогрессирующем развитии инфекции продолжительная и избыточная продукция IFN может приводить к развитию воспаления в связи с гиперпродукцией хе-мокинов, таких как CCL2 и CXCL10, и инфильтрацией альвеол провоспалительными моноцитами/макрофагами и плазмоцитоидными дендритными клетками. При этом попадание в зону воспаления вирусных и бактериальных лигандов Toll-подобных рецепторов, например липополисахарида LPS или dsRNA, может приводить к усиленной выработке этими клетками провоспалительных цитокинов, крайним проявлением которой может явиться так называемый цитокино-вый шторм [79]. При этом интенсивность повреждения легких может зависеть не столько от интенсивности вирусной репродукции, сколько от неконтролируемой выработки провоспалительных цитокинов и чрезмерной инфильтрации тканей легкого клетками врожденного иммунитета [80, 81].
Индуцируемая IFN типа I экспрессия проапопто-тического лиганда TRIAL также приводит к массовому апоптозу эпителиальных клеток, способствующему развитию ОРДС [82].
Существенным фактором риска развития неконтролируемого воспаления является генетическая предрасположенность организма к регуляции IFN ответа. Например, у мышей линии DBA, продуцирующих в ответ на гриппозную инфекцию высокие уровни IFN I типа, летальная инфекция развивается при заражении дозами, безопасными для мышей линии C57BL/6 с умеренной выработкой IFN [83, 84].
У людей с синдромом Дауна выявлена повышенная чувствительность к респираторным инфекциям и высокая вероятность тяжелых осложнений, сопряжённых с генетически обусловленной гиперпродукцией IFN а/у в ответ на вирусную инфекцию [85].
Кроме стимуляции цитокинового шторма, IFN I типа могут быть вовлечены в патогенез вторичной бактериальной инфекции [86, 87]. В частности, развитие IFN ответа при вирусной инфекции приводит к снижению миграции и фагоцитирующей функции нейтрофилов и макрофагов через проапоптотиче-ские механизмы или на уровне эпигенетической регуляции их функций [61, 88, 89].
В частности, развитие IFN ответа при вирусной инфекции приводит к снижению миграции и фагоцитирующей функции нейтрофилов и макрофагов через проапоптотиче-ские механизмы или на уровне эпигенетической регуляции их функций [61, 88, 89].
IFN первого типа также способны подавлять антибактериальную защиту за счет ингибирования продукции Т-клетками IL-17 [63, 90]. Одним из последствий отсутствия IL-17 ответа является снижение выработки антибактериальных пептидов, таких как липокалин 2 и BPIFA1, что также приводит к усилению роста числа бактерий в очаге вирусной инфекции [87].
Существенным доказательством негативного действия избыточной экспрессии IFN является тот факт, что генетически модифицированные мыши, дефицитные по рецепторам IFN типа I (IFNAR), оказались более устойчивы к развитию ОРДС, бактериальной пневмонии или сепсиса по сравнению с мышами, имеющими нормальный IFN сигналинг [61, 62, 84, 91, 92]. Применение индуктора IFN poly (I:C) перед заражением мышей пневмококком приводило к 100-кратному усилению колонизации легких введенными бактериями [64].
Применение индуктора IFN poly (I:C) перед заражением мышей пневмококком приводило к 100-кратному усилению колонизации легких введенными бактериями [64].
Таким образом, возможность развития тяжелых осложнений при ОРВИ может зависеть не только от вирулентности самого вируса или состава респираторной микробиоты в момент вирусного заражения, но и от способности организма регулировать интенсивность реакций системы врожденного иммунитета, одним из основных звеньев которого является IFN ответ.
Роль противовирусной вакцинации и антивирусной терапии в предотвращении вторичных бактериальных осложнений
В настоящее время имеются многочисленные свидетельства того, что противовирусная вакцинация может являться мерой снижения риска бактериальных осложнений при ОРВИ. В случае гриппозной инфекции в опытах на животных было показано, что иммунизация инактивированной гриппозной вакциной, вызывающая антительный ответ к HA и NA, достоверно снижает тяжесть бактериальной суперинфекции у мышей [93]. В другом исследовании было показано, что иммунизация мышей инактивированной или живой гриппозной вакциной может в равной степени снизить летальность при вирусном и последующем бактериальном заражении, не ограничивая, однако, при этом рост S. pyogenes в легких. В этом случае было показано, что противогриппозная вакцинация позволяла, за счет снижения вирусной нагрузки, снижать
В другом исследовании было показано, что иммунизация мышей инактивированной или живой гриппозной вакциной может в равной степени снизить летальность при вирусном и последующем бактериальном заражении, не ограничивая, однако, при этом рост S. pyogenes в легких. В этом случае было показано, что противогриппозная вакцинация позволяла, за счет снижения вирусной нагрузки, снижать
индукцию провоспалительных цитокинов и IFNy в легких при бактериальной суперинфекции [94]. К сожалению, имеется мало сведений о влиянии противогриппозной вакцинации у людей на вторичные бактериальные осложнения, что вызвано сложностью организации таких исследований, требующих параллельной оценки предшествующего противовирусного и противобактериального иммунитета к большому количеству потенциальных патогенов. Тем не менее, в ограниченном исследовании было показано, что гриппозная вакцина снижала частоту заболеваемости, связанной с S. pyogenes, у военных рекрутов в США [95]. Аналогично при вакцинации детей живой холодоадаптированной вакциной наблюдалось снижение частоты развития среднего отита [96].
Аналогично при вакцинации детей живой холодоадаптированной вакциной наблюдалось снижение частоты развития среднего отита [96].
Таким образом, вакцинация против респираторных вирусов может способствовать предотвращению вторичных бактериальных осложнений, по-видимому, за счет различных механизмов неспецифической защиты, обусловленной модуляцией системы врожденного иммунитета. Резонно предположить, что ограничение вирусной репродукции вследствие эффективной вакцинации может приводить к ограничению противовирусного IFN ответа и нивелированию негативного действия IFN на эффекторы антибактериальной защиты. Кроме того, снижение вирусной нагрузки может позитивно сказываться на сохранности респираторного эпителия и уменьшении индукции факторов адгезии для бактериальных клеток [56].
Подобные неспецифические механизмы, связанные с уменьшением вирусной нагрузки, могут лежать и в основе действия противовирусных препаратов, например ингибиторов NA вируса гриппа. Исследования, проведенные на животных моделях, свидетельствуют о том, что ингибиторы нейрами-нидазы способны снизить восприимчивость инфицированных вирусом гриппа животных к вторичной бактериальной пневмонии [97]. Данные о снижении частоты бронхитов и необходимости назначения антибиотиков были получены и в ходе нескольких клинических испытаний эффективности ингибиторов NA (занамивир и оселтамивир) у взрослых и детей [98-101].
Исследования, проведенные на животных моделях, свидетельствуют о том, что ингибиторы нейрами-нидазы способны снизить восприимчивость инфицированных вирусом гриппа животных к вторичной бактериальной пневмонии [97]. Данные о снижении частоты бронхитов и необходимости назначения антибиотиков были получены и в ходе нескольких клинических испытаний эффективности ингибиторов NA (занамивир и оселтамивир) у взрослых и детей [98-101].
ЗАКЛЮЧЕНИЕ
Успехи медицины последних десятилетий, связанные с открытием антибиотиков и разработкой вакцин против вирусов и бактерий, заметно уменьшили вероятность повторения катастрофической пандемии испанского гриппа 1918 г., когда бактериальные суперинфекции оказались основной причиной смертности [102]. Тем не менее, вирусы гриппа и другие респираторные вирусы остаются одной из основных причин бактериальных осложнений и частой этиологической причиной ВБП. Тревожным аспектом является нарастание резистентности бактериальных патогенов к современным антибиотикам вследствие их массового применения.
К сожалению, относительные успехи в разработке гриппозных вакцин и противогриппозных препаратов практически не распространяются на другие респираторные вирусы, которые, как было показано выше, также являются инфекционными агентами, провоцирующими вторичные бактериальные осложнения. Несмотря на прогресс в разработке пневмококковых и других антибактериальных вакцин и множественные усилия в создании вакцин против респираторных вирусов, трудно предположить, что в обозримом будущем будет создана система эффективной сочетанной вакцинации против основных вирусных и бактериальных респираторных патогенов. Невелика и вероятность создания специфических противовирусных препаратов против разных групп респираторных вирусов, существенно влияющих на вирусную нагрузку, особенно при их позднем применении. Такая ситуация диктует необходимость поиска патогенетических препаратов, направленных на предотвращение реакций врожденного иммунитета при вирусных инфекциях, ведущих к ослаблению факторов антибактериальной защиты. Одним из возможных подходов может явиться поиск препаратов, предотвращающих избыточную выработку IFN на пике вирусной инфекции. Демпфирование избыточного IFN сигналинга может явиться терапевтическим подходом к предотвращению как эффектов цитоки-нового шторма, так и развития вторичных бактериальных осложнений в анатомических зонах, примыкающих к респираторному тракту [79, 82, 103-105].
Одним из возможных подходов может явиться поиск препаратов, предотвращающих избыточную выработку IFN на пике вирусной инфекции. Демпфирование избыточного IFN сигналинга может явиться терапевтическим подходом к предотвращению как эффектов цитоки-нового шторма, так и развития вторичных бактериальных осложнений в анатомических зонах, примыкающих к респираторному тракту [79, 82, 103-105].
БЛАГОДАРНОСТИ
Исследования проводились при финансовой поддержке РНФ-FWF: грант № 18-45-05002 по теме «Вирусоподобные частицы для борьбы с постгриппозными бактериальными инфекциями»; получен в рамках конкурса «Проведение фундаментальных научных исследований и поисковых научных исследований международными научными коллективами».
КОНФЛИКТ ИНТЕРЕСОВ
Автор не преследует коммерческих или финансовых интересов.
ЦИТИРОВАНИЕ
А. Егоров. Проблема бактериальных осложнений при респираторных вирусных инфекциях. MIR J, 2018; 5(1), 1-11, doi: 10.18527/2500-2236-2018-5-1-1-11.
АВТОРСКИЕ ПРАВА
© 2018 Егоров. Эта статья публикуется в свободном доступе в соответствии с лицензией Creative Commons AttributionNonCommercial-ShareAlike 4.0 International Public License (CC BY-NC-SA), которая позволяет неограниченное использование, распространение и воспроизведение на любых носителях при условии, что указываются автор и источник публикации, а материал не используется в коммерческих целях.
ЛИТЕРАТУРА
1. Battle against Respiratory Viruses (BRaVe) initiative. World Health Organization. Available: http://www. who.int/influenza/patient_care/clinical/ brave/en/#; http://www.who.int/mediacentre/factsheets/ fs211/en/
who.int/influenza/patient_care/clinical/ brave/en/#; http://www.who.int/mediacentre/factsheets/ fs211/en/
2. Kilbourne ED. Influenza pandemics of the 20th century. Emerg Infect Dis 2006; 12(1), 9-14. doi: 10.3201/eid1201.051254.
3. Cheng VC, To KK, Tse H, Hung IF, Yuen KY. Two years after pandemic influenza A/2009/h2N1: what have we learned? Clin Microbiol Rev 2012; 25(2), 223-63. doi: 10.1128/CMR.05012-11.
4. Oxford JS, Sefton A, Jackson R, Innes W, Daniels RS, Johnson NP. World War I may have allowed the emergence of «Spanish» influenza. Lancet Infect Dis 2002; 2(2), 111-4. PubMed PMID: 11901642.
5. Brem WV, BollingGE, Casper EJ. Pandemic ‘influenza’ and secondary pneumonia at Camp Fremont Calif. J Am Med Assoc 1918; 71, 2138-44. doi: 10.1001/ jama.1918.26020520007010b.
6. Taubenberger JK, Baltimore D, Doherty PC, Markel H, Morens DM, Webster RG, et al. Reconstruction of the 1918 influenza virus: unexpected rewards from the past. MBio 2012; 3(5). doi: 10.1128/mBio.00201-12.
Taubenberger JK, Baltimore D, Doherty PC, Markel H, Morens DM, Webster RG, et al. Reconstruction of the 1918 influenza virus: unexpected rewards from the past. MBio 2012; 3(5). doi: 10.1128/mBio.00201-12.
7. Morris DE, Cleary DW, Clarke SC. Secondary Bacterial Infections Associated with Influenza Pandemics. Front Microbiol 2017; 8, 1041. doi: 10.3389/ fmicb.2017.01041.
8. Morens DM, Taubenberger JK, Fauci AS. Predominant role of bacterial pneumonia as a cause of death in pandemic influenza: implications for pandemic influenza preparedness. J Infect Dis 2008; 198(7), 962-70. doi: 10.1086/591708.
9. Chien YW, Klugman KP, Morens DM. Bacterial pathogens and death during the 1918 influenza pandemic. N Engl J Med 2009; 361(26), 2582-3. doi: 10.1056/NEJMc0908216.
10. Brundage JF, Shanks GD. Deaths from bacterial pneumonia during 1918-19 influenza pandemic. Emerg Infect Dis 2008; 14(8), 1193-9. doi: 10.3201/ eid1408.071313.
Deaths from bacterial pneumonia during 1918-19 influenza pandemic. Emerg Infect Dis 2008; 14(8), 1193-9. doi: 10.3201/ eid1408.071313.
11. Win MK, Chen MI, Barkham T, Lin C, Tan A, Lin R, et al. Influenza disease burden in adults by subtypes following the initial epidemic of pandemic h2N1 in Singapore. Influenza Other Respir Viruses 2011; 5(6), e563-7. doi: 10.1111/j.1750-2659.2011.00282.x.
12. Potter CW. A history of influenza. J Appl Microbiol 2001; 91(4), 572-9. PubMed PMID: 11576290.
13. Viboud C, Simonsen L, Fuentes R, Flores J, Miller MA, Chowell G. Global Mortality Impact of the 1957-1959 Influenza Pandemic. J Infect Dis 2016; 213(5), 73845. doi: 10.1093/infdis/jiv534.
14. Eickhoff TC, Sherman IL, Serfling RE. Observations on excess mortality associated with epidemic influenza. JAMA 1961; 176, 776-82. PubMed PMID: 13726091.
JAMA 1961; 176, 776-82. PubMed PMID: 13726091.
15. Hilleman MR. Realities and enigmas of human viral influenza: pathogenesis, epidemiology and control. Vaccine 2002; 20(25-26), 3068-87. PubMed PMID: 12163258.
16. Hers JF, Masurel N, Mulder J. Bacteriology and histopathology of the respiratory tract and lungs in fatal Asian influenza. Lancet 1958; 2(7057), 1141-3. PubMed PMID: 13612141.
17. Gill JR, Sheng ZM, Ely SF, Guinee DG, Beasley MB, Suh J, et al. Pulmonary pathologic findings of fatal 2009 pandemic influenza A/h2N1 viral infections. Arch Pathol Lab Med 2010; 134(2), 235-43. doi: 10.1043/1543-2165-134.2.235.
18. Petersdorf RG, Fusco JJ, Harter DH, Albrink WS. Pulmonary infections complicating Asian influenza. AMA Arch Intern Med 1959; 103(2), 262-72. PubMed PMID: 13616762.
19. Robertson L, Caley JP, Moore J. Importance of Staphylococcus aureus in pneumonia in the 1957 epidemic of influenza A. Lancet 1958; 2(7040), 2336. PubMed PMID: 13564806.
20. Michaelis M, Doerr HW, Cinatl J, Jr. Novel swine-origin influenza A virus in humans: another pandemic knocking at the door. Med Microbiol Immunol 2009; 198(3), 175-83. doi: 10.1007/s00430-009-0118-5.
21. Klimov A, Simonsen L, Fukuda K, Cox N. Surveillance and impact of influenza in the United States. Vaccine 1999; 17 Suppl 1, S42-6. PubMed PMID: 10471179.
22. Tillett HE, Smith JW, Gooch CD. Excess deaths attributable to influenza in England and Wales: age at death and certified cause. Int J Epidemiol 1983; 12(3), 344-52. PubMed PMID: 6629624.
23. Lindsay MI, Jr. , Herrmann EC, Jr., Morrow GW, Jr., Brown AL, Jr. Hong Kong influenza: clinical, microbiologic, and pathologic features in 127 cases. JAMA 1970; 214(10), 1825-32. PubMed PMID: 5537337.
, Herrmann EC, Jr., Morrow GW, Jr., Brown AL, Jr. Hong Kong influenza: clinical, microbiologic, and pathologic features in 127 cases. JAMA 1970; 214(10), 1825-32. PubMed PMID: 5537337.
24. Wang TT, Palese P. Unraveling the mystery of swine influenza virus. Cell 2009; 137(6), 983-5. doi: 10.1016/j.cell.2009.05.032.
25. Chertow DS, Memoli MJ. Bacterial coinfection in influenza: a grand rounds review. JAMA 2013; 309(3), 275-82. doi: 10.1001/jama.2012.194139.
26. Lee EH, Wu C, Lee EU, Stoute A, Hanson H, Cook HA, et al. Fatalities associated with the 2009 h2N1 influenza A virus in New York city. Clin Infect Dis 2010; 50(11), 1498-504. doi: 10.1086/652446.
27. Lucas S. Predictive clinicopathological features derived from systematic autopsy examination of patients who died with A/h2N1 influenza infection
in the UK 2009-10 pandemic._575.gif) Health Technol Assess 2010; 14(55), 83-114. doi: 10.3310/hta14550-02.
Health Technol Assess 2010; 14(55), 83-114. doi: 10.3310/hta14550-02.
28. Palacios G, Hornig M, Cisterna D, Savji N, Bussetti AV, Kapoor V, et al. Streptococcus pneumoniae coinfection is correlated with the severity of h2N1 pandemic influenza. PLoS One 2009; 4(12), e8540. doi: 10.1371/journal.pone.0008540.
29. Randolph AG, Vaughn F, Sullivan R, Rubinson L, Thompson BT, Yoon G, et al. Critically ill children during the 2009-2010 influenza pandemic in the United States. Pediatrics 2011; 128(6), e1450-8. doi: 10.1542/peds.2011-0774.
30. ZhivichA. Fighting bacterial resistance: approaches, challenges, and opportunities in the search for new antibiotics. Part 1. Antibiotics used in clinical practice: mechanisms of action and the development of bacterial resistance. MIR J 2017; 4(1), 31-51. doi: 10.18527/2500-2236-2017-4-1-31-51.
31. Hasvold J, Sjoding M, Pohl K, Cooke C, Hyzy RC. The role of human metapneumovirus in the critically ill adult patient. J Crit Care 2016; 31(1), 233-7. doi: 10.1016/j.jcrc.2015.09.035.
Hasvold J, Sjoding M, Pohl K, Cooke C, Hyzy RC. The role of human metapneumovirus in the critically ill adult patient. J Crit Care 2016; 31(1), 233-7. doi: 10.1016/j.jcrc.2015.09.035.
32. Kwon YS, Park SH, Kim MA, Kim HJ, Park JS, Lee MY, et al. Risk of mortality associated with respiratory syncytial virus and influenza infection in adults. BMC Infect Dis 2017; 17(1), 785. doi: 10.1186/ s12879-017-2897-4.
33. PrassoJE, DengJC. Postviral Complications: Bacterial Pneumonia. Clin Chest Med 2017; 38(1), 127-38. doi: 10.1016/j.ccm.2016.11.006.
34. Metersky ML, Masterton RG, Lode H, File TM, Jr., Babinchak T. Epidemiology, microbiology, and treatment considerations for bacterial pneumonia complicating influenza. Int J Infect Dis 2012; 16(5), e321-31. doi: 10.1016/j.ijid.2012.01.003.
35. MulcahyME, McLoughlin RM. Staphylococcus aureus and Influenza A Virus: Partners in Coinfection. MBio 2016; 7(6). doi: 10.1128/mBio.02068-16.
MulcahyME, McLoughlin RM. Staphylococcus aureus and Influenza A Virus: Partners in Coinfection. MBio 2016; 7(6). doi: 10.1128/mBio.02068-16.
36. Safaeyan F, Nahaei MR, Seifi SJ, Kafil HS, Sadeghi J. Quantitative detection of Staphylococcus aureus, Streptococcus pneumoniae and Haemophilus influenzae in patients with new influenza A (h2N1)/2009 and influenza A/2010 virus infection. GMS Hyg Infect Control 2015; 10, Doc06. doi: 10.3205/dgkh000249.
37. Jennings LC, Anderson TP, Beynon KA, Chua A, Laing RT, Werno AM, et al. Incidence and characteristics of viral community-acquired pneumonia in adults. Thorax 2008; 63(1), 42-8. doi: 10.1136/thx.2006.075077.
38. Liderot K, Ahl M, Ozenci V. Secondary bacterial infections in patients with seasonal influenza A and pandemic h2N1. Biomed Res Int 2013; 2013, 376219. doi: 10.1155/2013/376219.
39. Chonmaitree T, Jennings K, Golovko G, Khanipov K, Pimenova M, Patel JA, et al. Nasopharyngeal microbiota in infants and changes during viral upper respiratory tract infection and acute otitis media. PLoS One 2017; 12(7), e0180630. doi: 10.1371/ journal.pone.0180630.
40. Jacobs JH, Viboud C, Tchetgen ET, Schwartz J, Steiner C, Simonsen L, et al. The association of meningococcal disease with influenza in the United States, 1989-2009. PLoS One 2014; 9(9), e107486. doi: 10.1371/journal.pone.0107486.
41. Brealey JC, Chappell KJ, Galbraith S, Fantino E, Gaydon J, Tozer S, et al. Streptococcus pneumoniae colonization of the nasopharynx is associated with increased severity during respiratory syncytial virus infection in young children. Respirology 2018; 23(2), 220-7. doi: 10.1111/resp.13179.
42. Hendaus MA, Jomha FA, Alhammadi AH. Virus-induced secondary bacterial infection: a concise review. Ther Clin Risk Manag 2015; 11, 1265-71. doi: 10.2147/TCRM.S87789.
Hendaus MA, Jomha FA, Alhammadi AH. Virus-induced secondary bacterial infection: a concise review. Ther Clin Risk Manag 2015; 11, 1265-71. doi: 10.2147/TCRM.S87789.
43. Louie JK, Roy-Burman A, Guardia-Labar L, Boston EJ, Kiang D, Padilla T, et al. Rhinovirus associated with severe lower respiratory tract infections in children. Pediatr Infect Dis J 2009; 28(4), 337-9. doi: 10.1097/ INF.0b013e31818ffc1b.
44. Mallia P, Footitt J, Sotero R, Jepson A, Contoli M, Trujillo-Torralbo MB, et al. Rhinovirus infection induces degradation of antimicrobial peptides and secondary bacterial infection in chronic obstructive pulmonary disease. Am J Respir Crit Care Med 2012; 186(11), 1117-24. doi: 10.1164/rccm.201205-0806OC.
45. Kloepfer KM, Lee WM, Pappas TE, Kang TJ, Vrtis RF, Evans MD, et al. Detection of pathogenic bacteria during rhinovirus infection is associated with increased respiratory symptoms and asthma exacerbations. J Allergy Clin Immunol 2014; 133(5), 1301-7, 7 e1-3. doi: 10.1016/j.jaci.2014.02.030.
J Allergy Clin Immunol 2014; 133(5), 1301-7, 7 e1-3. doi: 10.1016/j.jaci.2014.02.030.
46. Korppi M, Leinonen M, Makela PH, Launiala K. Bacterial involvement in parainfluenza virus infection in children. Scand J Infect Dis 1990; 22(3), 307-12. PubMed PMID: 2164707.
47. Verkaik NJ, Nguyen DT, de Vogel CP, Moll HA, Verbrugh HA, Jaddoe VW, et al. Streptococcus pneumoniae exposure is associated with human metapneumovirus seroconversion and increased susceptibility to in vitro HMPV infection. Clin Microbiol Infect 2011; 17(12), 1840-4. doi: 10.1111/j.1469-0691.2011.03480.x.
48. Self WH, Williams DJ, Zhu Y, Ampofo K, Pavia AT, Chappell JD, et al. Respiratory Viral Detection in Children and Adults: Comparing Asymptomatic Controls and Patients With Community-Acquired Pneumonia. J Infect Dis 2016; 213(4), 584-91. doi: 10.1093/infdis/jiv323.
49. Katsurada N, Suzuki M, Aoshima M, Yaegashi M, Ishifuji T, AsohN, et al. The impact of virus infections on pneumonia mortality is complex in adults: a prospective multicentre observational study. BMC Infect Dis 2017; 17(1), 755. doi: 10.1186/s12879-017-2858-y.
50. Jung HS, Kang BJ, Ra SW, Seo KW, Jegal Y, Jun JB, et al. Elucidation of Bacterial Pneumonia-Causing Pathogens in Patients with Respiratory Viral
Infection. Tuberc Respir Dis (Seoul) 2017; 80(4), 358-67. doi: 10.4046/trd.2017.0044.
51. Hooper LV, Littman DR, Macpherson AJ. Interactions between the microbiota and the immune system. Science 2012; 336(6086), 1268-73. doi: 10.1126/ science.1223490.
52. Charlson ES, Bittinger K, Haas AR, Fitzgerald AS, Frank I, Yadav A, et al. Topographical continuity of bacterial populations in the healthy human respiratory tract. Am J Respir Crit Care Med 2011; 184(8), 957-63. doi: 10.1164/rccm.201104-06550C.
Topographical continuity of bacterial populations in the healthy human respiratory tract. Am J Respir Crit Care Med 2011; 184(8), 957-63. doi: 10.1164/rccm.201104-06550C.
53. Bogaert D, De Groot R, Hermans PW. Streptococcus pneumoniae colonisation: the key to pneumococcal disease. Lancet Infect Dis 2004; 4(3), 144-54. doi: 10.1016/S1473-3099(04)00938-7.
54. Bosch AA, Biesbroek G, Trzcinski K, Sanders EA, Bogaert D. Viral and bacterial interactions in the upper respiratory tract. PLoS Pathog 2013; 9(1), e1003057. doi: 10.1371/journal.ppat.1003057.
55. Yang X, Steukers L, Forier K, Xiong R, Braeckmans K, Van Reeth K, et al. A beneficiary role for neuraminidase in influenza virus penetration through the respiratory mucus. PLoS One 2014; 9(10), e110026. doi: 10.1371/journal.pone.0110026.
56. Avadhanula V, Rodriguez CA, Devincenzo JP, Wang Y, Webby RJ, Ulett GC, et al. Respiratory viruses augment the adhesion of bacterial pathogens to respiratory epithelium in a viral species- and cell type-dependent manner. J Virol 2006; 80(4), 162936. doi: 10.1128/JVI.80.4.1629-1636.2006.
Avadhanula V, Rodriguez CA, Devincenzo JP, Wang Y, Webby RJ, Ulett GC, et al. Respiratory viruses augment the adhesion of bacterial pathogens to respiratory epithelium in a viral species- and cell type-dependent manner. J Virol 2006; 80(4), 162936. doi: 10.1128/JVI.80.4.1629-1636.2006.
57. Li N, Ren A, Wang X, Fan X, Zhao Y, Gao GF, et al. Influenza viral neuraminidase primes bacterial coinfection through TGF-beta-mediated expression of host cell receptors. Proc Natl Acad Sci U S A 2015; 112(1), 238-43. doi: 10.1073/pnas.1414422112.
58. Carson JL, Collier AM, Hu SS. Acquired ciliary defects in nasal epithelium of children with acute viral upper respiratory infections. N Engl J Med 1985; 312(8), 463-8. doi: 10.1056/NEJM198502213120802.
59. Pittet LA, Hall-Stoodley L, Rutkowski MR, Harmsen AG. Influenza virus infection decreases tracheal mucociliary velocity and clearance of Streptococcus pneumoniae. Am J Respir Cell Mol Biol 2010; 42(4), 450-60. doi: 10.1165/rcmb.2007-04170C.
Am J Respir Cell Mol Biol 2010; 42(4), 450-60. doi: 10.1165/rcmb.2007-04170C.
60. Sun K, Metzger DW. Inhibition of pulmonary antibacterial defense by interferon-gamma during recovery from influenza infection. Nat Med 2008; 14(5), 558-64. doi: 10.1038/nm1765.
61. Shahangian A, Chow EK, Tian X, Kang JR, Ghaffari A, Liu SY, et al. Type I IFNs mediate development of postinfluenza bacterial pneumonia in mice. J Clin Invest 2009; 119(7), 1910-20. doi: 10.1172/JCI35412.
62. Nakamura S, Davis KM, Weiser JN. Synergistic stimulation of type I interferons during influenza virus coinfection promotes Streptococcus pneumoniae colonization in mice. J Clin Invest 2011; 121(9), 3657-65. doi: 10.1172/JCI57762.
63. Kudva A, Scheller EV, Robinson KM, Crowe CR, Choi SM, Slight SR, et al. Influenza A inhibits Th27-mediated host defense against bacterial pneumonia in mice. J Immunol 2011; 186(3), 1666-74. doi: 10.4049/jimmunol.1002194.
J Immunol 2011; 186(3), 1666-74. doi: 10.4049/jimmunol.1002194.
64. Tian X, Xu F, Lung WY, Meyerson C, Ghaffari AA, Cheng G, et al. Poly I:C enhances susceptibility to secondary pulmonary infections by gram-positive bacteria. PLoS One 2012; 7(9), e41879. doi: 10.1371/ journal.pone.0041879.
65. Astry CL, Jakab GJ. Influenza virus-induced immune complexes suppress alveolar macrophage phagocytosis. J Virol 1984; 50(2), 287-92. PubMed PMID: 6708169.
66. Franke-Ullmann G, Pfortner C, Walter P, Steinmuller C, Lohmann-Matthes ML, Kobzik L, et al. Alteration of pulmonary macrophage function by respiratory syncytial virus infection in vitro. J Immunol 1995; 154(1), 268-80. PubMed PMID: 7995946.
67. Jakab GJ. Immune impairment of alveolar macrophage phagocytosis during influenza virus pneumonia. Am Rev Respir Dis 1982; 126(5), 778-82. doi: 10.1164/arrd.1982.126.5.778.
Am Rev Respir Dis 1982; 126(5), 778-82. doi: 10.1164/arrd.1982.126.5.778.
68. Warnking K, Klemm C, Loffler B, Niemann S, van Kruchten A, Peters G, et al. Super-infection with Staphylococcus aureus inhibits influenza virus-induced type I IFN signalling through impaired STAT1-STAT2 dimerization. Cell Microbiol 2015; 17(3), 303-17. doi: 10.1111/cmi.12375.
69. de Steenhuijsen Piters WA, Heinonen S, Hasrat R, Bunsow E, Smith B, Suarez-Arrabal MC, et al. Nasopharyngeal Microbiota, Host Transcriptome, and Disease Severity in Children with Respiratory Syncytial Virus Infection. Am J Respir Crit Care Med 2016; 194(9), 1104-15. doi: 10.1164/rccm.201602-0220OC.
70. Jia L, Xie J, Zhao J, Cao D, Liang Y, Hou X, et al. Mechanisms of Severe Mortality-Associated Bacterial Co-infections Following Influenza Virus Infection. Front Cell Infect Microbiol 2017; 7, 338. doi: 10.3389/fcimb.2017.00338.
doi: 10.3389/fcimb.2017.00338.
71. Jamieson AM, Pasman L, Yu S, Gamradt P, Homer RJ, Decker T, et al. Role of tissue protection in lethal respiratory viral-bacterial coinfection. Science 2013; 340(6137), 1230-4. doi: 10.1126/science.1233632.
72. Lee LN, Dias P, Han D, Yoon S, Shea A, Zakharov V, et al. A mouse model of lethal synergism between influenza virus and Haemophilus influenzae. Am J Pathol 2010; 176(2), 800-11. doi: 10.2353/ ajpath.2010.090596.
73. McCullers JA. The co-pathogenesis of influenza viruses with bacteria in the lung. Nat Rev Microbiol 2014; 12(4), 252-62. doi: 10.1038/nrmicro3231.
74. Tripathi S, Garcia-SastreA. Antiviral innate immunity through the lens of systems biology. Virus Res 2016; 218, 10-7. doi: 10.1016/j.virusres.2015.11.024.
75. Brennan K, Bowie AG. Activation of host pattern recognition receptors by viruses. Curr Opin Microbiol 2010; 13(4), 503-7. doi: 10.1016/j.mib.2010.05.007.
Brennan K, Bowie AG. Activation of host pattern recognition receptors by viruses. Curr Opin Microbiol 2010; 13(4), 503-7. doi: 10.1016/j.mib.2010.05.007.
76. Chen X, Liu S, Goraya MU, Maarouf M, Huang S, Chen JL. Host Immune Response to Influenza A Virus Infection. Front Immunol 2018; 9, 320. doi: 10.3389/fimmu.2018.00320.
77. Shim JM, Kim J, Tenson T, Min JY, Kainov DE. Influenza Virus Infection, Interferon Response, Viral Counter-Response, and Apoptosis. Viruses 2017; 9(8), 223. doi: 10.3390/v9080223.
78. Andreakos E, Salagianni M, Galani IE, Koltsida O. Interferon-lambdas: Front-Line Guardians of Immunity and Homeostasis in the Respiratory Tract. Front Immunol 2017; 8, 1232. doi: 10.3389/ fimmu.2017.01232.
79. Goritzka M, Durant LR, Pereira C, Salek-Ardakani S, Openshaw PJ, Johansson C. Alpha/beta interferon receptor signaling amplifies early proinflammatory cytokine production in the lung during respiratory syncytial virus infection. J Virol 2014; 88(11), 612836. doi: 10.1128/JVI.00333-14.
Alpha/beta interferon receptor signaling amplifies early proinflammatory cytokine production in the lung during respiratory syncytial virus infection. J Virol 2014; 88(11), 612836. doi: 10.1128/JVI.00333-14.
80. Doherty PC, Turner SJ, Webby RG, Thomas PG. Influenza and the challenge for immunology. Nat Immunol 2006; 7(5), 449-55. doi: 10.1038/ni1343.
81. Peiris JS, Yu WC, Leung CW, Cheung CY, Ng WF, Nicholls JM, et al. Re-emergence of fatal human influenza A subtype H5N1 disease. Lancet 2004; 363(9409), 617-9. doi: 10.1016/S0140-6736(04)15595-5.
82. Makris S, Paulsen M, Johansson C. Type I Interferons as Regulators of Lung Inflammation. Front Immunol 2017; 8, 259. doi: 10.3389/fimmu.2017.00259.
83. Srivastava B, Blazejewska P, Hessmann M, Bruder D, Geffers R, Mauel S, et al. Host genetic background strongly influences the response to influenza a virus infections. PLoS One 2009; 4(3), e4857. doi: 10.1371/ journal.pone.0004857.
Host genetic background strongly influences the response to influenza a virus infections. PLoS One 2009; 4(3), e4857. doi: 10.1371/ journal.pone.0004857.
84. Davidson S, Crotta S, McCabe TM, Wack A. Pathogenic potential of interferon alphabeta in acute influenza infection. Nat Commun 2014; 5, 3864. doi: 10.1038/ ncomms4864.
85. Broers CJ, Gemke RJ, WeijermanME, van der Sluijs KF, van Furth AM. Increased pro-inflammatory cytokine production in Down Syndrome children upon stimulation with live influenza A virus. J Clin Immunol 2012; 32(2), 323-9. doi: 10.1007/s10875-011-9625-4.
86. Rynda-Apple A, Robinson KM, Alcorn JF. Influenza and Bacterial Superinfection: Illuminating the Immunologic Mechanisms of Disease. Infect Immun 2015; 83(10), 3764-70. doi: 10.1128/IAI.00298-15.
87. Lee B, Robinson KM, McHugh KJ, Scheller EV, Mandalapu S, Chen C, et al. Influenza-induced type I interferon enhances susceptibility to gram-negative and gram-positive bacterial pneumonia in mice. Am J Physiol Lung Cell Mol Physiol 2015; 309(2), L158-67. doi: 10.1152/ajplung.00338.2014.
Lee B, Robinson KM, McHugh KJ, Scheller EV, Mandalapu S, Chen C, et al. Influenza-induced type I interferon enhances susceptibility to gram-negative and gram-positive bacterial pneumonia in mice. Am J Physiol Lung Cell Mol Physiol 2015; 309(2), L158-67. doi: 10.1152/ajplung.00338.2014.
88. Schliehe C, Flynn EK, Vilagos B, Richson U, Swaminanthan S, Bosnjak B, et al. The methyltransferase Setdb2 mediates virus-induced susceptibility to bacterial superinfection. Nat Immunol 2015; 16(1), 67-74. doi: 10.1038/ni.3046.
89. Kroetz DN, Allen RM, Schaller MA, Cavallaro C, Ito T, Kunkel SL. Type I Interferon Induced Epigenetic Regulation of Macrophages Suppresses Innate and Adaptive Immunity in Acute Respiratory Viral Infection. PLoS Pathog 2015; 11(12), e1005338. doi: 10.1371/journal.ppat.1005338.
90. Cao J, Wang D, Xu F, Gong Y, Wang H, Song Z, et al. Activation of IL-27 signalling promotes development of postinfluenza pneumococcal pneumonia. EMBO Mol Med 2014; 6(1), 120-40. doi: 10.1002/ emmm.201302890.
Activation of IL-27 signalling promotes development of postinfluenza pneumococcal pneumonia. EMBO Mol Med 2014; 6(1), 120-40. doi: 10.1002/ emmm.201302890.
91. Li W, Moltedo B, Moran TM. Type I interferon induction during influenza virus infection increases susceptibility to secondary Streptococcus pneumoniae infection by negative regulation of gammadelta T cells. J Virol 2012; 86(22), 12304-12. doi: 10.1128/JVI.01269-12.
92. Dejager L, Vandevyver S, Ballegeer M, Van Wonterghem E, An LL, Riggs J, et al. Pharmacological inhibition of type I interferon signaling protects mice against lethal sepsis. J Infect Dis 2014; 209(6), 960-70. doi: 10.1093/infdis/jit600.
93. Huber VC, Peltola V, Iverson AR, McCullers JA. Contribution of vaccine-induced immunity toward either the HA or the NA component of influenza viruses limits secondary bacterial complications. J Virol 2010; 84(8), 4105-8. doi: 10.1128/JVI.02621-09.
J Virol 2010; 84(8), 4105-8. doi: 10.1128/JVI.02621-09.
94. Chaussee MS, Sandbulte HR, Schuneman MJ, Depaula FP, Addengast LA, Schlenker EH, et al. Inactivated and live, attenuated influenza vaccines protect mice against influenza: Streptococcus pyogenes super-infections. Vaccine 2011; 29(21), 3773-81. doi: 10.1016/j.vaccine.2011.03.031.
95. Lee SE, Eick A, Bloom MS, Brundage JF. Influenza immunization and subsequent diagnoses of group A streptococcus-illnesses among U.S. Army trainees, 2002-2006. Vaccine 2008; 26(27-28), 3383-6. doi: 10.1016/j.vaccine.2008.04.041.
96. Belshe RB, Gruber WC. Prevention of otitis media in children with live attenuated influenza vaccine given intranasally. Pediatr Infect Dis J 2000; 19(5 Suppl), S66-71. PubMed PMID: 10821474.
97. McCullers JA.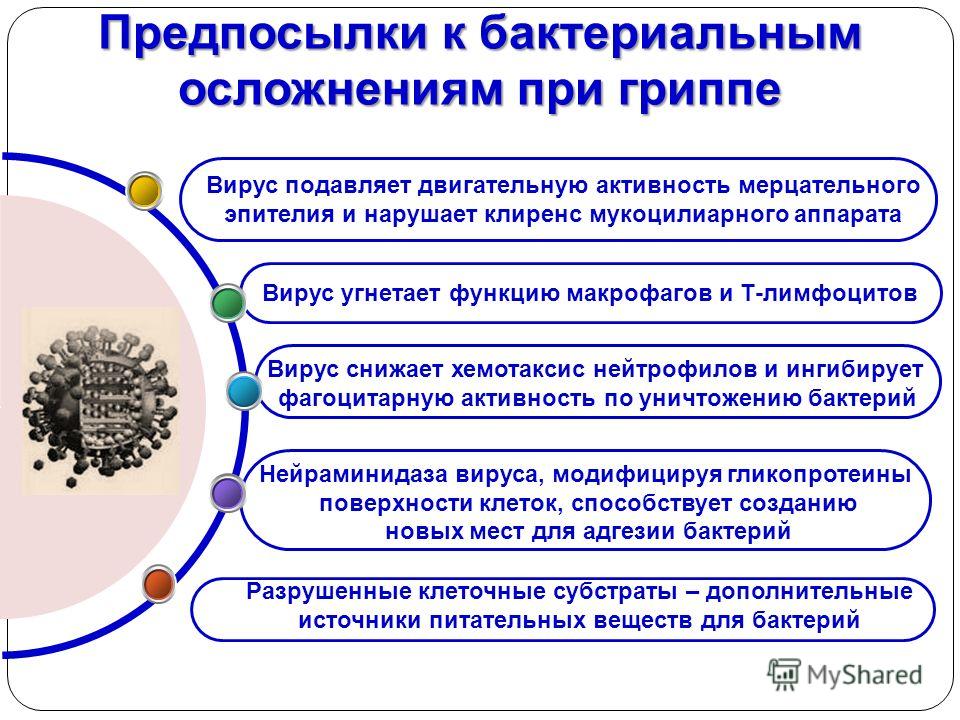 Effect of antiviral treatment on the outcome of secondary bacterial pneumonia after influenza. J Infect Dis 2004; 190(3), 519-26. doi: 10.1086/421525.
Effect of antiviral treatment on the outcome of secondary bacterial pneumonia after influenza. J Infect Dis 2004; 190(3), 519-26. doi: 10.1086/421525.
98. Hayden FG, Osterhaus AD, Treanor JJ, Fleming DM, Aoki FY, Nicholson KG, et al. Efficacy and safety of the neuraminidase inhibitor zanamivir in the treatment of influenzavirus infections. GG167 Influenza Study Group. N Engl J Med 1997; 337(13), 874-80. doi: 10.1056/NEJM199709253371302.
99. Kaiser L, Keene ON, Hammond JM, Elliott M, Hayden FG. Impact of zanamivir on antibiotic use for respiratory events following acute influenza in adolescents and adults. Arch Intern Med 2000; 160(21), 3234-40. PubMed PMID: 11088083.
100. Kaiser L, Wat C, Mills T, Mahoney P, Ward P, HaydenF. Impact of oseltamivir treatment on influenza-related lower respiratory tract complications and hospitalizations. Arch Intern Med 2003; 163(14), 1667-72. doi: 10.1001/archinte.163.14.1667.
Arch Intern Med 2003; 163(14), 1667-72. doi: 10.1001/archinte.163.14.1667.
101. Nicholson KG, Aoki FY, Osterhaus AD, Trottier S, Carewicz O, Mercier CH, et al. Efficacy and safety of oseltamivir in treatment of acute influenza: a randomised controlled trial. Neuraminidase Inhibitor Flu Treatment Investigator Group. Lancet 2000; 355(9218), 1845-50. PubMed PMID: 10866439.
102. Smith AM, Huber VC. The Unexpected Impact of Vaccines on Secondary Bacterial Infections Following Influenza. Viral Immunol 2018; 31(2), 159-73. doi: 10.1089/vim.2017.0138.
103. Zang N, Xie X, Deng Y, Wu S, Wang L, Peng C, et al. Resveratrol-mediated gamma interferon reduction prevents airway inflammation and airway hyperresponsiveness in respiratory syncytial virus-infected immunocompromised mice. J Virol 2011; 85(24), 13061-8. doi: 10.1128/JVI.05869-11.
104. Baumgarth N, Kelso A. In vivo blockade of gamma interferon affects the influenza virus-induced humoral and the local cellular immune response in lung tissue. J Virol 1996; 70(7), 4411-8. PubMed PMID: 8676464.
Baumgarth N, Kelso A. In vivo blockade of gamma interferon affects the influenza virus-induced humoral and the local cellular immune response in lung tissue. J Virol 1996; 70(7), 4411-8. PubMed PMID: 8676464.
105. Wolf S, Johnson S, Perwitasari O, Mahalingam S, Tripp RA. Targeting the pro-inflammatory factor CCL2 (MCP-1) with Bindarit for influenza A (H7N9) treatment. Clin Transl Immunology 2017; 6(3), e135. doi: 10.1038/cti.2017.8.
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ)
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ)
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ) находятся на первом месте по числу ежегодно заболевающих людей
Несмотря на постоянные усилия, направленные на борьбу с возбудителями гриппа, коронавирусной инфекции и других ОРВИ победить их до сих пор не удается.
Ежегодно от осложнений гриппа погибают тысячи человек.
Это связано с тем, что вирусы, прежде всего вирусы гриппа и коронавирусы обладают способностью менять свою структуру и мутировавший вирус, способен поражать человека вновь. Так, переболевший гриппом человек имеет хороший иммунный барьер, но тем не менее новый измененный вирус, способен легко проникать через него, так как иммунитета против этого вида вируса организм пока не выработал.
Для кого наиболее опасна встреча с вирусом?
Особо тяжело переносят инфекцию дети и пожилые люди, для этих возрастных групп очень опасны осложнения, которые могут развиться во время заболевания. Дети болеют более тяжело в связи с тем, что их иммунная система еще не встречалась с данным вирусом, а для пожилых людей, также, как и для людей с хроническими заболеваниями, вирус опасен по причине ослабленной иммунной системы.
Группы риска
• Дети
• Люди старше 60 лет
• Люди с хроническими заболеваниями легких (бронхиальная астма, хроническая обструктивная болезнь легких)
• Люди с хроническими заболеваниями сердечно-сосудистой системы (врожденные пороки сердца, ишемическая болезнь сердца, сердечная недостаточность)
• Беременные женщины
• Медицинские работники
• Работники общественного транспорта, предприятий общественного питания
Каким образом происходит заражение?
Инфекция передается от больного человека здоровому через мельчайшие капельки слюны или слизи, которые выделяются во время чихания, кашля разговора. Возможна и контактная передача.
Возможна и контактная передача.
Симптомы
В зависимости от конкретного вида возбудителя симптомы могут значительно различаться, как по степени выраженности, так и по вариантам сочетания.
• Повышение температуры
• Озноб, общее недомогание, слабость головная боль, боли в мышцах
• Снижение аппетита, возможны тошнота и рвота
• Конъюнктивит (возможно)
• Понос (возможно)
В среднем, болезнь длится около 5 дней. Если температура держится дольше, возможно, возникли осложнения.
Осложнения
• Пневмония
• Энцефалит, менингит
• Осложнения беременности, развитие патологии плода
• Обострение хронических заболеваний
Лечение заболевания проводится под контролем врача, который только после осмотра пациента назначает схему лечения и дает другие рекомендации. Заболевший должен соблюдать постельный режим, полноценно питаться и пить больше жидкости.
Антибиотики
Принимать антибиотики в первые дни заболевания — большая ошибка. Антибиотики не способны справиться с вирусом, кроме того, они неблагоприятно влияют на нормальную микрофлору. Антибиотики назначает только врач, только в случае развития осложнений, вызванных присоединением бактериальной инфекции. Принимать антибактериальные препараты в качестве профилактики развития осложнений- опасно и бесполезно.
Антибиотики не способны справиться с вирусом, кроме того, они неблагоприятно влияют на нормальную микрофлору. Антибиотики назначает только врач, только в случае развития осложнений, вызванных присоединением бактериальной инфекции. Принимать антибактериальные препараты в качестве профилактики развития осложнений- опасно и бесполезно.
Заболевший человек должен оставаться дома и не создавать угрозу заражения окружающих.
Профилактика
Самым эффективным способом профилактики гриппа является ежегодная вакцинация. Состав вакцины против гриппа меняется ежегодно. Прежде всего, вакцинироваться рекомендуется тем, кто входит в группу риска. Оптимальное время для вакцинации октябрь-ноябрь. Вакцинация детей против гриппа возможна, начиная с 6-месячного возраста.
Вакцины против большинства возбудителей острых респираторных вирусных инфекций не разработаны.
Универсальные меры профилактики
• Часто и тщательно мойте руки
• Избегайте контактов с кашляющими людьми
• Придерживайтесь здорового образа жизни (сон, здоровая пища, физическая активность)
• Пейте больше жидкости
• Регулярно проветривайте и увлажняйте воздух в помещении, в котором находитесь
• Реже бывайте в людных местах
• Используйте маску, когда находитесь в транспорте или в людных местах
• Избегайте объятий, поцелуев и рукопожатий при встречах
• Не трогайте лицо, глаза, нос немытыми руками
При первых признаках вирусной инфекции – обратитесь к врачу!
Осложнения простуды и гриппа
Осложнения, развивающиеся после гриппа, зачастую бывают тяжелее самой болезни. Организм, ослабленный инфекцией, не всегда способен справиться со второй волной бактериальной атаки.
Организм, ослабленный инфекцией, не всегда способен справиться со второй волной бактериальной атаки.
Поэтому, чтобы свести к минимуму риск развития осложнений и появления тяжелых, порой хронических заболеваний, очень важно следовать нескольким простым правилам.
Самые важные из них – это соблюдать постельный режим и довести назначенное врачом лечение до конца. Современные противовирусные средства, такие как АРБИДОЛ®, могут весьма хорошо помочь в терапии гриппа на ранних стадиях заболевания.
К сожалению, многие, почувствовав себя лучше, самопроизвольно отменяют назначенные им препараты. Такой подход способен свести на нет все достижения терапии, поскольку каждое лекарство оказывает свое действие только при соблюдении определенной схемы приема.
Наиболее частые осложнения:
Со стороны лор-органов
К самым частым осложнениям, развивающимся после гриппа, можно отнести синусит – воспаление околоносовых пазух. Чаще всего поражается верхнечелюстные (гайморит), также наблюдаются воспаления лобных, клиновидных и решетчатых пазух. Иногда инфекция затрагивает все пазухи сразу (пансинусит). Еще одна распространенная проблема – это ангина (воспаление небных миндалин, вызываемое такими бактериями, как стрептококк и стафилококк). К распространенным осложнениям после гриппа также относятся различные виды отитов.
Чаще всего поражается верхнечелюстные (гайморит), также наблюдаются воспаления лобных, клиновидных и решетчатых пазух. Иногда инфекция затрагивает все пазухи сразу (пансинусит). Еще одна распространенная проблема – это ангина (воспаление небных миндалин, вызываемое такими бактериями, как стрептококк и стафилококк). К распространенным осложнениям после гриппа также относятся различные виды отитов.
Со стороны легких
Повторное повышение температуры, боли в груди, кашель и затруднение дыхания – все это может свидетельствовать о таком осложнении, как пневмония. Воспаление легких – очень серьезный диагноз, требующий немедленного обращения к врачу и госпитализации.
Со стороны сердечно-сосудистой системы
Дополнительная нагрузка на работу сердечно-сосудистой системы при вирусной интоксикации очень велика. А такие бактериальные осложнения гриппа, как миокардит и перикардит, могут проявиться даже у молодых людей. При гриппе смертность среди пациентов, страдающих гипертонией и ишемической болезнью сердца также возрастает, особенно если речь идет о людях пожилого возраста.
А такие бактериальные осложнения гриппа, как миокардит и перикардит, могут проявиться даже у молодых людей. При гриппе смертность среди пациентов, страдающих гипертонией и ишемической болезнью сердца также возрастает, особенно если речь идет о людях пожилого возраста.
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ)
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ)
Грипп, коронавирусная инфекция и другие острые респираторные вирусные инфекции (ОРВИ) находятся на первом месте по числу ежегодно заболевающих людей.
Несмотря на постоянные усилия, направленные на борьбу с возбудителями гриппа, коронавирусной инфекции и других ОРВИ победить их до сих пор не удается.
Ежегодно от осложнений гриппа погибают тысячи человек.
Это связано с тем, что вирусы, прежде всего вирусы гриппа и коронавирусы обладают способностью менять свою структуру и мутировавший вирус, способен поражать человека вновь. Так, переболевший гриппом человек имеет хороший иммунный барьер, но тем не менее новый измененный вирус, способен легко проникать через него, так как иммунитета против этого вида вируса организм пока не выработал.
Так, переболевший гриппом человек имеет хороший иммунный барьер, но тем не менее новый измененный вирус, способен легко проникать через него, так как иммунитета против этого вида вируса организм пока не выработал.
Для кого наиболее опасна встреча с вирусом?
Особо тяжело переносят инфекцию дети и пожилые люди, для этих возрастных групп очень опасны осложнения, которые могут развиться во время заболевания. Дети болеют более тяжело в связи с тем, что их иммунная система еще не встречалась с данным вирусом, а для пожилых людей, также, как и для людей с хроническими заболеваниями, вирус опасен по причине ослабленной иммунной системы.
Группы риска
· Дети
· Люди старше 60 лет
· Люди с хроническими заболеваниями легких (бронхиальная астма, хроническая обструктивная болезнь легких)
· Люди с хроническими заболеваниями сердечно-сосудистой системы (врожденные пороки сердца, ишемическая болезнь сердца, сердечная недостаточность)
· Беременные женщины
· Медицинские работники
· Работники общественного транспорта, предприятий общественного питания
Каким образом происходит заражение?
Инфекция передается от больного человека здоровому через мельчайшие капельки слюны или слизи, которые выделяются во время чихания, кашля, разговора. Возможна и контактная передача.
Возможна и контактная передача.
Симптомы
В зависимости от конкретного вида возбудителя симптомы могут значительно различаться, как по степени выраженности, так и по вариантам сочетания.
· Повышение температуры
· Озноб, общее недомогание, слабость головная боль, боли в мышцах
· Снижение аппетита, возможны тошнота и рвота
· Конъюнктивит (возможно)
· Понос (возможно)
В среднем, болезнь длится около 5 дней. Если температура держится дольше, возможно, возникли осложнения.
Осложнения
· Пневмония
· Энцефалит, менингит
· Осложнения беременности, развитие патологии плода
· Обострение хронических заболеваний
Лечение заболевания проводится под контролем врача, который только после осмотра пациента назначает схему лечения и дает другие рекомендации. Заболевший должен соблюдать постельный режим, полноценно питаться и пить больше жидкости.
Заболевший должен соблюдать постельный режим, полноценно питаться и пить больше жидкости.
Антибиотики
Принимать антибиотики в первые дни заболевания — большая ошибка. Антибиотики не способны справиться с вирусом, кроме того, они неблагоприятно влияют на нормальную микрофлору. Антибиотики назначает только врач, только в случае развития осложнений, вызванных присоединением бактериальной инфекции. Принимать антибактериальные препараты в качестве профилактики развития осложнений- опасно и бесполезно.
Заболевший человек должен оставаться дома и не создавать угрозу заражения окружающих.
Профилактика
Самым эффективным способом профилактики гриппа является ежегодная вакцинация. Состав вакцины против гриппа меняется ежегодно. Прежде всего, вакцинироваться рекомендуется тем, кто входит в группу риска. Оптимальное время для вакцинации октябрь-ноябрь. Вакцинация детей против гриппа возможна, начиная с 6-месячного возраста.
Вакцины против большинства возбудителей острых респираторных вирусных инфекций не разработаны.
Универсальные меры профилактики
· Часто и тщательно мойте руки
· Избегайте контактов с кашляющими людьми
· Придерживайтесь здорового образа жизни (сон, здоровая пища, физическая активность)
· Пейте больше жидкости
· Регулярно проветривайте и увлажняйте воздух в помещении, в котором находитесь
· Реже бывайте в людных местах
· Используйте маску, когда находитесь в транспорте или в людных местах
· Избегайте объятий, поцелуев и рукопожатий при встречах
· Не трогайте лицо, глаза, нос немытыми руками
При первых признаках вирусной инфекции – обратитесь к врачу!
Грипп, коронавирус, другие ОРВИ — поможет маска!
В период активной циркуляции возбудителей гриппа, коронавирусной инфекции, и других возбудителей острых респираторных вирусных инфекций напоминаем о целесообразности использования одноразовой медицинской маски в качестве эффективной меры профилактики заражения и ограничения распространения инфекции.
Эти вирусы передаются от человека к человеку преимущественно воздушно-капельным путём, через микрокапли респираторных выделений, которые образуются, когда инфицированные люди говорят, чихают или кашляют.
С воздухом эти капли могут попасть на поверхность слизистой оболочки верхних дыхательных путей здоровых людей, которые находятся рядом с заражённым человеком.
Заражение может происходить и в результате непосредственного или косвенного контакта здорового человека с респираторными выделениями инфицированного.
Использование одноразовой медицинской маски предотвращает попадание в организм здорового человека капель респираторных выделений, которые могут содержать вирусы, через нос и рот.
· Надевайте маску, когда ухаживаете за членом семьи с симптомами вирусного респираторного заболевания.
· Если вы больны, или у вас симптомы вирусного респираторного заболевания, наденьте маску перед тем, как приближаться к другим людям.
· Если у вас симптомы вирусного респираторного заболевания и вам необходимо обратиться к врачу, заблаговременно наденьте маску, чтобы защитить окружающих в зоне ожидания.
· Носите маску в закрытых помещениях, в местах большого скопления людей.
· Маска должна плотно прилегать к лицу и закрывать рот, нос и подбородок. При наличии вшитого крепления в области носа, его надо плотно прижать к спинке носа.
· Носите маску в закрытых помещениях, в местах большого скопления людей.
· Используйте маску однократно, повторное использование маски недопустимо.
· Меняйте маску каждые 2-3 часа или чаще.
· Если маска увлажнилась, её следует заменить на новую.
· После использования маски, выбросьте её и вымойте руки с мылом.
· Повторно использовать маску нельзя.
· Носить маску на безлюдных открытых пространствах — нецелесообразно.
Одноразовая медицинская маска, при правильном использовании – надёжный и эффективный метод снижения риска заражения и предотвращения распространения гриппа, коронавируса и других возбудителей ОРВИ!
Только в сочетании с тщательной гигиеной рук и карантинными мерами использование маски будет максимально эффективно для предотвращения заражения и распространения инфекции!
Гигиена при гриппе, коронавирусной инфекции и других ОРВИ
Что нужно делать в период активной циркуляции возбудителей гриппа, коронавирусной инфекции и других возбудителей острых респираторных вирусных инфекций (ОРВИ) для того, чтобы предотвратить собственное заражение и обезопасить окружающих, если заболели вы?
Возбудители всех этих заболеваний высоко заразны и передаются преимущественно воздушно-капельным путем.
При чихании и кашле в воздухе вокруг больного человека распространяются микрокапли его слюны, мокроты и респираторных выделений, которые содержат вирусы. Более крупные капли оседают на окружающих предметах, и поверхностях, мелкие -долго находятся в воздухе и переносятся на расстояния до нескольких сот метров, при этом вирусы сохраняют способность к заражению от нескольких часов до нескольких дней. Основные меры гигиенической профилактики направлены на предотвращение контакта здоровых людей с содержащими вирусы частицами выделений больного человека.
Соблюдение следующих гигиенических правил позволит существенно снизить риск заражения или дальнейшего распространения гриппа, коронавирусной инфекции и других ОРВИ.
Как не заразиться
· Мыть руки после посещения любых общественных мест, транспорта, прикосновений к дверным ручкам, деньгам, оргтехнике общественного пользования на рабочем месте, перед едой и приготовлением пищи. Уделите особое внимание тщательному намыливанию (не менее 20 секунд), и последующему полному осушению рук.
Уделите особое внимание тщательному намыливанию (не менее 20 секунд), и последующему полному осушению рук.
· После возвращения с улицы домой — вымыть руки и лицо с мылом, промыть нос изотоническим раствором соли.
· Прикасаться к лицу, глазам-только недавно вымытыми руками. При отсутствии доступа к воде и мылу, для очистки рук использовать дезинфицирующие средства на спиртовой основе. Или воспользоваться одноразовой салфеткой, при необходимости прикосновения к глазам или носу
· Надевать одноразовую медицинскую маску в людных местах и транспорте. Менять маску на новую надо каждые 2-3 часа, повторно использовать маску нельзя.
· Отдавать предпочтение гладким прическам, когда вы находитесь в местах скопления людей, распущенные волосы, часто контактируя с лицом, увеличивают риск инфицирования.
· Избегать близких контактов и пребывания в одном помещении с людьми, имеющими видимые признаки ОРВИ (кашель, чихание, выделения из носа).
· Не прикасаться голыми руками к дверным ручкам, перилам, другим предметам и поверхностям в общественных пространствах.
· Ограничить приветственные рукопожатия, поцелуи и объятия.
· Чаще проветривать помещения.
· Не пользоваться общими полотенцами.
Как не заразить окружающих
· Минимизировать контакты со здоровыми людьми (приветственные рукопожатия, поцелуи).
· Если вы испытываете недомогание, но вынуждены общаться с другими людьми или пользоваться общественным транспортом — использовать одноразовую маску, обязательно меняя ее на новую каждый час.
· При кашле или чихании обязательно прикрывать рот, по возможности — одноразовым платком, если его нет — ладонями или локтевым сгибом.
· Пользоваться только личной или одноразовой посудой.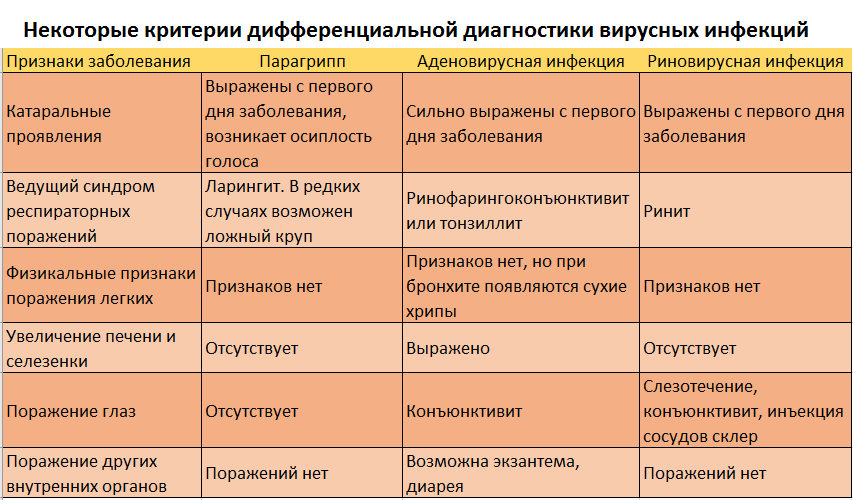
· Изолировать от домочадцев свои предметы личной гигиены: зубную щетку, мочалку, полотенца.
· Проводить влажную уборку дома ежедневно, включая обработку дверных ручек, выключателей, панелей управления оргтехникой.
Памятка: Профилактика гриппа и коронавирусной инфекции
Вирусы гриппа и коронавирусной инфекции вызывают у человека респираторные заболевания разной тяжести. Симптомы заболевания аналогичны симптомам обычного (сезонного) гриппа. Тяжесть заболевания зависит от целого ряда факторов, в том числе от общего состояния организма и возраста.
Предрасположены к заболеванию: пожилые люди, маленькие дети, беременные женщины и люди, страдающие хроническими заболеваниями (астмой, диабетом, сердечно-сосудистыми заболеваниями), и с ослабленным иммунитетом.
ПРАВИЛО 1.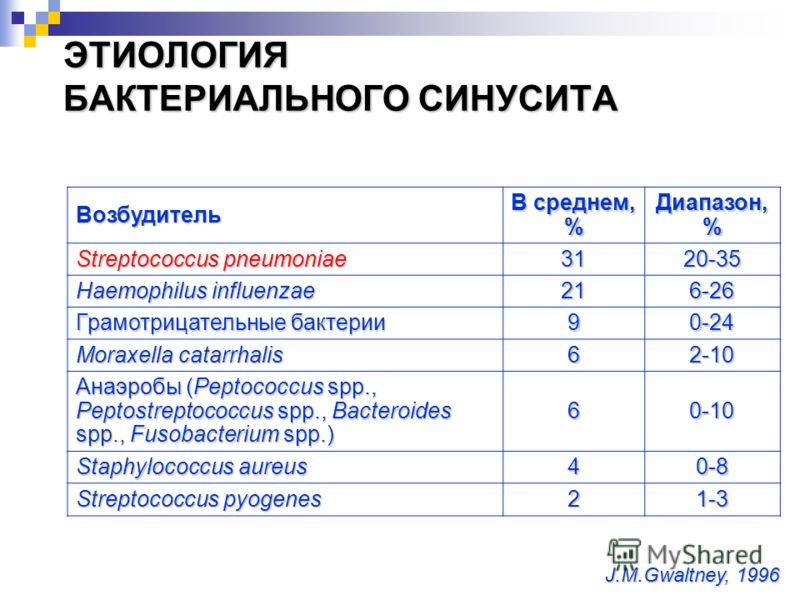 ЧАСТО МОЙТЕ РУКИ С МЫЛОМ
ЧАСТО МОЙТЕ РУКИ С МЫЛОМ
Чистите и дезинфицируйте поверхности, используя бытовые моющие средства.
Гигиена рук — это важная мера профилактики распространения гриппа и коронавирусной инфекции. Мытье с мылом удаляет вирусы. Если нет возможности помыть руки с мылом, пользуйтесь спиртсодержащими или дезинфицирующими салфетками.
Чистка и регулярная дезинфекция поверхностей (столов, дверных ручек, стульев, гаджетов и др.) удаляет вирусы.
ПРАВИЛО 2. СОБЛЮДАЙТЕ РАССТОЯНИЕ И ЭТИКЕТ
Вирусы передаются от больного человека к здоровому воздушно -капельным путем (при чихании, кашле), поэтому необходимо соблюдать расстояние не менее 1 метра от больных.
Избегайте трогать руками глаза, нос или рот. Вирус гриппа и коронавирус распространяются этими путями.
Надевайте маску или используйте другие подручные средства защиты, чтобы уменьшить риск заболевания.
При кашле, чихании следует прикрывать рот и нос одноразовыми салфетками, которые после использования нужно выбрасывать.
Избегая излишние поездки и посещения многолюдных мест, можно уменьшить риск заболевания.
ПРАВИЛО 3. ВЕДИТЕ ЗДОРОВЫЙ ОБРАЗ ЖИЗНИ
Здоровый образ жизни повышает сопротивляемость организма к инфекции. Соблюдайте здоровый режим, включая полноценный сон, потребление пищевых продуктов богатых белками, витаминами и минеральными веществами, физическую активность.
ПРАВИЛО 4. ЗАЩИЩАЙТЕ ОРГАНЫ ДЫХАНИЯ С ПОМОЩЬЮ МЕДИЦИНСКОЙ МАСКИ
Среди прочих средств профилактики особое место занимает ношение масок, благодаря которым ограничивается распространение вируса.
Медицинские маски для защиты органов дыхания используют:
— при посещении мест массового скопления людей, поездках в общественном транспорте в период роста заболеваемости острыми респираторными вирусными инфекциями;
— при уходе за больными острыми респираторными вирусными инфекциями;
— при общении с лицами с признаками острой респираторной вирусной инфекции;
— при рисках инфицирования другими инфекциями, передающимися воздушно-капельным путем.
КАК ПРАВИЛЬНО НОСИТЬ МАСКУ?
Маски могут иметь разную конструкцию. Они могут быть одноразовыми или могут применяться многократно. Есть маски, которые служат 2, 4, 6 часов. Стоимость этих масок различная, из-за различной пропитки. Но нельзя все время носить одну и ту же маску, тем самым вы можете инфицировать дважды сами себя. Какой стороной внутрь носить медицинскую маску — непринципиально.
Чтобы обезопасить себя от заражения, крайне важно правильно ее носить:
— маска должна тщательно закрепляться, плотно закрывать рот и нос, не оставляя зазоров;
— старайтесь не касаться поверхностей маски при ее снятии, если вы ее коснулись, тщательно вымойте руки с мылом или спиртовым средством;
— влажную или отсыревшую маску следует сменить на новую, сухую;
— не используйте вторично одноразовую маску;
— использованную одноразовую маску следует немедленно выбросить в отходы.
При уходе за больным, после окончания контакта с заболевшим, маску следует немедленно снять. После снятия маски необходимо незамедлительно и тщательно вымыть руки.
Маска уместна, если вы находитесь в месте массового скопления людей, в общественном транспорте, а также при уходе за больным, но она нецелесообразна на открытом воздухе.
Во время пребывания на улице полезно дышать свежим воздухом и маску надевать не стоит.
Вместе с тем, медики напоминают, что эта одиночная мера не обеспечивает полной защиты от заболевания. Кроме ношения маски необходимо соблюдать другие профилактические меры.
ПРАВИЛО 5. ЧТО ДЕЛАТЬ В СЛУЧАЕ ЗАБОЛЕВАНИЯ ГРИППОМ, КОРОНАВИРУСНОЙ ИНФЕКЦИЕЙ?
Оставайтесь дома и срочно обращайтесь к врачу.
Следуйте предписаниям врача, соблюдайте постельный режим и пейте как можно больше жидкости.
КАКОВЫ СИМПТОМЫ ГРИППА/КОРОНАВИРУСНОЙ ИНФЕКЦИИ
высокая температура тела, озноб, головная боль, слабость, заложенность носа, кашель, затрудненное дыхание, боли в мышцах, конъюнктивит.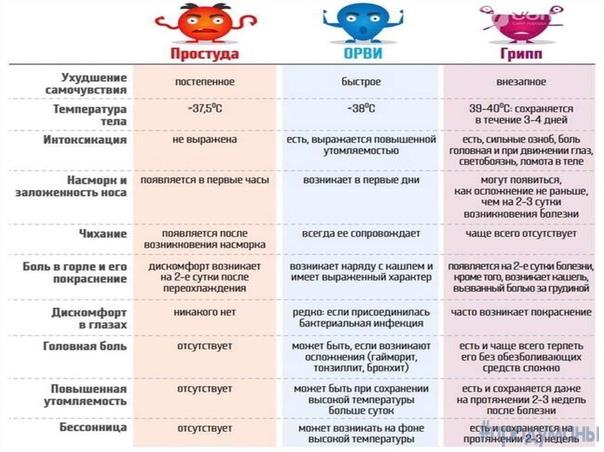
В некоторых случаях могут быть симптомы желудочно-кишечных расстройств: тошнота, рвота, диарея.
КАКОВЫ ОСЛОЖНЕНИЯ
Среди осложнений лидирует вирусная пневмония. Ухудшение состояния при вирусной пневмонии идёт быстрыми темпами, и у многих пациентов уже в течение 24 часов развивается дыхательная недостаточность, требующая немедленной респираторной поддержки с механической вентиляцией лёгких.
Быстро начатое лечение способствует облегчению степени тяжести болезни.
ЧТО ДЕЛАТЬ ЕСЛИ В СЕМЬЕ КТО-ТО ЗАБОЛЕЛ ГРИППОМ/КОРОНАВИРУСНОЙ ИНФЕКЦИЕЙ?
— Вызовите врача.
— Выделите больному отдельную комнату в доме. Если это невозможно, соблюдайте расстояние не менее 1 метра от больного.
— Ограничьте до минимума контакт между больным и близкими, особенно детьми, пожилыми людьми и лицами, страдающими хроническими заболеваниями.
— Часто проветривайте помещение.
— Сохраняйте чистоту, как можно чаще мойте и дезинфицируйте поверхности бытовыми моющими средствами.
— Часто мойте руки с мылом.
— Ухаживая за больным, прикрывайте рот и нос маской или другими защитными средствами (платком, шарфом и др.).
— Ухаживать за больным должен только один член семьи.
Как вирусные поражения дыхательных путей провоцируют бактериальные осложнения
Не секрет, что вирусные заболевания сопровождаются бактериальными осложнениями. Поскольку острыми респираторными вирусными инфекциями и гриппом люди болеют наиболее часто, то бактериальные заболевания становятся неизменными спутниками простуды, изменяя ее течение и влияя на последствия. Почему это происходит? Как вирусам, что поражают дыхательные пути и гриппа удается открыть дверь бактериальным заболеваниям? Рассмотрим в этой статье.
Как вирусы,что поражают дыхательную систему способствуют присоединению бактериальных возбудителейИммунная система организма человека способна справляться с вирусами, которые вызывают воспаление в дыхательной системе. Но вирусы способны вносить коррективы в течение заболевания, с легкостью разрушая защитные барьеры. Подобные изменения иммунного ответа способствуют присоединению бактерий и развитию осложнений.
Но вирусы способны вносить коррективы в течение заболевания, с легкостью разрушая защитные барьеры. Подобные изменения иммунного ответа способствуют присоединению бактерий и развитию осложнений.
Для того, чтобы ослабить защитные механизмы человеческого организма, которые противостоят бактериям, вирусы задействуют несколько способов.
- При вирусных заболеваниях нарушается целостность слизистых оболочек. Это связано с тем, что вирусы проникают и размножаются в клетках эпителия дыхательных путей. Выход вновь образовавшихся вирусов приводит к гибели клеток, целостность эпителия нарушается, что создает условия для проникновения бактерий. Поэтому, чем дальше в дыхательные пути проник вирус, чем выше вероятность того, что бактерии проникнут вслед за ним.
- Наши дыхательные пути выстелены клетками со специальными выростами (ресничками), которые задерживают все вирусы и бактерии, а благодаря их движению, как на эскалаторе вверх, «вывозится» все ненужное.
 При воспалении этот механизм самоочищения (его называют мукоцилиарным клиренсом) имеет важное значение – он предотвращает скопление остатков разрушенных клеток, слизи, содержащей вирусы и бактерии, для которых слизь является питательной средой. Вирусы способствуют разрушению клетки и угнетению движения ресничек. Это приводит к тому, что самоочищающий механизм работает недостаточно эффективно, а бактерии тем временем распространяются в нижние отделы дыхательных путей, околоносовые пазухи, через слуховую трубу в полость среднего уха, и вызывают бактериальные осложнения.
При воспалении этот механизм самоочищения (его называют мукоцилиарным клиренсом) имеет важное значение – он предотвращает скопление остатков разрушенных клеток, слизи, содержащей вирусы и бактерии, для которых слизь является питательной средой. Вирусы способствуют разрушению клетки и угнетению движения ресничек. Это приводит к тому, что самоочищающий механизм работает недостаточно эффективно, а бактерии тем временем распространяются в нижние отделы дыхательных путей, околоносовые пазухи, через слуховую трубу в полость среднего уха, и вызывают бактериальные осложнения. - Во время вирусной инфекции происходит сдвиг в сторону усиления противовирусной и ослабление противобактериальной защиты. А если человек болеет простудой уже не впервые, то подобные нарушения защитных сил отягощаются истощением резервов его организма, что еще больше снижает способность противостоять бактериям.
Вызванные вирусом нарушения защитных барьеров приводят к тому, что спустя некоторое время к вирусам присоединяются бактерии.
Возможны два варианта проникновения бактерий, обуславливающих развитие осложнений: заражение из вне и распространение бактерий, обычно живущих на коже и слизистых оболочках. Чаще всего бактериальные осложнения при острых вирусных поражениях дыхательных путей и гриппе являются следствием активации определенных видов бактерий, которые обитают в организме человека. Не секрет, что человеческий организм «мирно сосуществует» с огромным множеством бактерий, грибков и простейших, которые объединяются в одно общее название микробиота. От такого сотрудничества организм получает много преимуществ.
Читайте еще: Грипп и мы: не играйте в русскую рулетку
Кроме синтеза витаминов и участия в процессах пищеварения, полезные микроорганизмы создают конкурентную среду, которая сдерживает не совсем безобидные (их называют условно-патогенными) бактерии от их болезнетворной активности. В этом им помогают защитные факторы эпителия кожи и слизистых оболочек, а также содержащиеся в слизи лизоцим, лактоферрин и секреторный иммуноглобулин А. При острых поражениях респираторной системы происходит изменение состава микробиоты в сторону увеличения патогенных микроорганизмов, что связано со способностью вирусов влиять на иммунитет и приводить к угнетению защитных факторов слизистых оболочек. В результате механизмы, сдерживающие условно-патогенные бактерии, уже не работают, что создает условия для усиления их агрессивности и способности вызывать заболевания человеческого организма, в котором они живут. Так происходит с бактерией под названием пневмококк, которая у большинства из нас присутствует в носоглотке. При снижении иммунитета пневмококк «спускается» по дыхательным путям в легкие, где вызывает воспаление легких и сегодня считается основной причиной развития этого бактериального осложнения.
При острых поражениях респираторной системы происходит изменение состава микробиоты в сторону увеличения патогенных микроорганизмов, что связано со способностью вирусов влиять на иммунитет и приводить к угнетению защитных факторов слизистых оболочек. В результате механизмы, сдерживающие условно-патогенные бактерии, уже не работают, что создает условия для усиления их агрессивности и способности вызывать заболевания человеческого организма, в котором они живут. Так происходит с бактерией под названием пневмококк, которая у большинства из нас присутствует в носоглотке. При снижении иммунитета пневмококк «спускается» по дыхательным путям в легкие, где вызывает воспаление легких и сегодня считается основной причиной развития этого бактериального осложнения.
В жизни довольно сложно различить, где у заболевшего еще вирусная инфекция, а где – уже наслоившаяся бактериальная. Часто об этом судят по изменениям характера течения самого заболевания: сколько длится заболевание, как изменяются симптомы. Те же кашель, лихорадка, боль в горле могут быть проявлениями как вирусной, так и бактериальной инфекции. Однако их появление или усиление на 4-5 день простудного заболевания с повторным повышением температуры тела будет свидетельствовать о том, что заболевание осложнилось бактериальной инфекцией.
Часто об этом судят по изменениям характера течения самого заболевания: сколько длится заболевание, как изменяются симптомы. Те же кашель, лихорадка, боль в горле могут быть проявлениями как вирусной, так и бактериальной инфекции. Однако их появление или усиление на 4-5 день простудного заболевания с повторным повышением температуры тела будет свидетельствовать о том, что заболевание осложнилось бактериальной инфекцией.
Достаточно сложный вопрос. С одной стороны, чем сильнее иммунитет и лучше работают защитные барьеры, тем меньше шансов не только у бактерий, но и у вирусов. С другой стороны, не всегда стимуляция иммунного ответа при острых респираторных вирусных инфекциях, особенно при затяжном течении заболевания, тем более если оно уже 2 – 3 за сезон, полезна. Ведь попыткой простимулировать иммунный ответ можно добиться прямо противоположного эффекта, а именно – еще больше его истощить, и тогда временное угнетение защитных сил уже гарантировано..jpg) Этот период станет благоприятным для развития множества бактериальных осложнений, затрагивающих не только дыхательную систему, из которых выбраться будет очень непросто.
Этот период станет благоприятным для развития множества бактериальных осложнений, затрагивающих не только дыхательную систему, из которых выбраться будет очень непросто.
Поэтому от использования иммуностимуляторов в чистом виде при вирусных заболеваниях дыхательных путей стоит отказаться. Верным решением в данной ситуации будет применение препаратов с прямым противовирусным действием – Флавовир (обновленный Иммунофлазид). Благодаря тому, что Флавовир уменьшает размножение вирусов в клетках, снижается не только вирусная нагрузка на организм, но и количество пораженных клеток дыхательных путей. Кроме того, Флавовир дополнительно обеспечивает защиту слизистых оболочек верхних дыхательных путей путем нормализации показателей местного иммунитета (лактоферрин, секреторный иммуноглобулин A и лизоцим). При этом, как показано в исследованиях, сироп нормализует образование собственных защитных факторов (интерферонов) и улучшает способность организма человека противостоять вирусной и бактериальной инфекции.
Читайте еще: Заболел – сиди дома, или Почему опасно переносить простуду на ногах
Безусловно, такое двойное влияние на вирус и на организм человека позволяет эффективнее бороться с вирусами поражающие дыхательные пути и вирусами гриппа, а также бактериями, которые могут присоединиться к вирусной инфекции и вызывать различные осложнения.
Читайте еще: Гомеопатия при ОРВИ и гриппе: безопасно не значит эффективно
Грипп, вопросы и ответы
Где чаще всего можно заразиться гриппом?
Потенциально опасными являются места массового скопления людей. Это, прежде всего, общественный транспорт, торговые центры, театры и кинотеатры. Так же опасны небольшие, плохо проветриваемые помещения, если есть необходимость длительно находиться в них. Чаще всего это рабочие кабинеты, учебные классы.
Мой коллега не вышел на работу, заболел гриппом, хотя, накануне не производил впечатления больного человека. Есть ли для меня опасность заболеть тоже?
Да, вероятность очень высока, особенно, если вы не прививались от гриппа. Дело в том, что человек начинает распространять вирус еще за 1-2 дня до появления признаков заболевания (в инкубационном периоде). Если Вы тесно общались с ним в это время — Вы в группе риска.
Дело в том, что человек начинает распространять вирус еще за 1-2 дня до появления признаков заболевания (в инкубационном периоде). Если Вы тесно общались с ним в это время — Вы в группе риска.
Если я в ближайшие дни сделаю прививку от гриппа — будет ли она эффективна?
К сожалению, в настоящее время (середина декабря) вакцинироваться уже поздно, так как для выработки должного количества защитных антител требуется 2-3 недели, и, желательно, в это время не встретиться с больным гриппом. Эпидемиологическая обстановка в России на данный момент такова, что это исключить невозможно. Постарайтесь в следующем году вакцинироваться вовремя ( оптимально — со второй половины сентября до конца ноября).
Сколько чеснока надо есть для гарантированной защиты от гриппа?
Вынуждены Вас огорчить. Чеснок не способен ни предотвратить заражение, ни облегчить течение гриппа. Действительно, эфирное масло чеснока содержит аллицин — вещество, обладающее мягкой антибактериальной активностью, но оно бессильно против вирусов. Так, что в активном употреблении свежего чеснока в пищу, или вдыхании его паров нет никакого смысла.
Так, что в активном употреблении свежего чеснока в пищу, или вдыхании его паров нет никакого смысла.
Утверждают, что постоянное ношение защитной маски исключает вероятность заражения гриппом, если менять ее каждые 2 часа. Могу ли я менять ее реже?
Действительно, такое мнение очень распространено. Но, защитный потенциал маски весьма преувеличен. Даже при использовании маски по всем правилам, с регулярной заменой на новую каждый час-два вероятность заразиться гриппом будет очень высока при близком контакте с заболевшим человеком. Маска защищает только крупных капель слюны, слизи рассеивающихся вокруг чихающего или кашляющего человека, но, вирусы распространяются и просто с током воздуха, беспрепятственно проникая через полотно маски. Вот кому точно следует надевать маску, так это болеющему человеку, при общении со здоровыми людьми, причем надевать ее на краткое время, требующееся для беседы, (15-20) минут, после чего использованную маску утилизировать.
Как часто надо мазать нос оксолиновой мазью, для профилактики гриппа?
Применение оксолиновой мази не защитит вас от заражения гриппом или ОРВИ.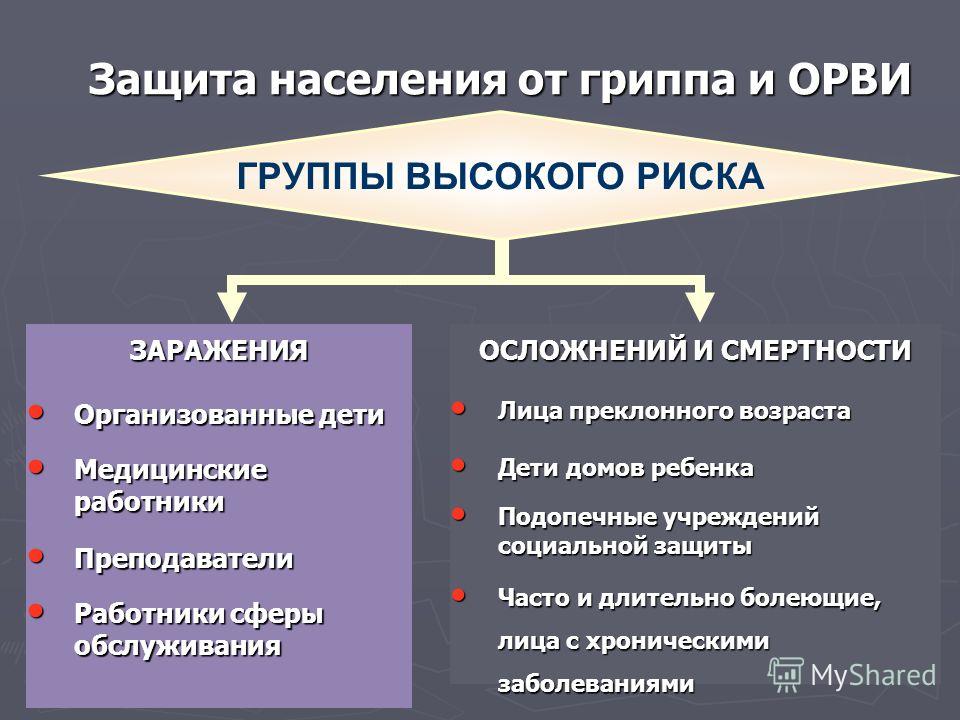 Несмотря на то, что препарат известен уже более 40 лет и активно используется уже несколькими поколениями, следует знать, что противовирусной активностью он не обладает, данный препарат способен только несколько смягчить слизистую оболочку наружных дыхательных путей.
Несмотря на то, что препарат известен уже более 40 лет и активно используется уже несколькими поколениями, следует знать, что противовирусной активностью он не обладает, данный препарат способен только несколько смягчить слизистую оболочку наружных дыхательных путей.
Я заболела, мне поставили диагноз ОРЗ, но я чувствую себя значительно хуже, чем обычно при банальной простуде. Можно ли узнать — не грипп ли это и как?
Диагноз «грипп» можно подтвердить только на основании лабораторного исследования (проведения серологического диагностического теста). В типичных случаях определить грипп или ОРЗ у пациента для врача не представляет затруднений, и диагноз ставится на основании оценки совокупности клинических проявлений заболевания и текущих эпидемиологических данных. Лабораторная диагностика показана только в случаях, когда диагноз вызывает сомнения, при осложненном или нетипичном течении болезни или же в целях эпидемиологического надзора.
В прошлом году я прививалась от гриппа, но все равно болела, и не один раз за зиму. Почему так произошло? Прививка не подействовала?
Почему так произошло? Прививка не подействовала?
Важно понимать – прививаясь, Вы не исключаете вероятность простудного заболевания (вирусов, вызывающих ОРЗ существует более 250 разновидностей!). Вакцина эффективна в отношении только вируса гриппа. Прививка стимулирует выработку антител против определенного вида вируса гриппа, и даже если случится так, что Вы все же заболеете — болезнь будет протекать в легкой форме, а вероятность осложнений будет невелика.
Есть ли смысл при гриппе начинать принимать антибиотики, что бы предотвратить возможные бактериальные осложнения?
Так делать ни в коем случае нельзя! Осложнения, вызванные присоединением бактериальной инфекции после гриппа, даже при его тяжелом течении, развивается далеко не всегда. Необходимость начала антибактериальной терапии определяет только врач! Антибиотики, применяемые без показаний, «про запас», подавляя рост полезной микрофлоры в кишечник, способствуют снижению защитных сил организма, тем самым увеличивая вероятность развития осложнений бактериальной природы.
Почему грипп, относясь к группе острых респираторных вирусных инфекций, выделяется как особая инфекция? Почему именно о гриппе говорят врачи, СМИ, популярные сайты сети Интернет?
Ответ прост: грипп – единственная острая респираторная вирусная инфекция (ОРВИ), влекущая за собой серьезные осложнения, которые не только нарушают работу нашего организма, но и опасны для жизни. А осложнения эти возникают очень часто. Чаще всего осложнения гриппа носят отсроченный характер, проявляются спустя некоторое время, когда человек уже забыл о перенесенной инфекции. Начинаются проблемы в функционировании сердечно-сосудистой, нервной и других систем организма.
По данным Всемирной организации здравоохранения (ВОЗ) ежегодно в мире гриппом и ОРВИ заболевает до 500 млн. человек, от осложнений заболевания умирают около 2 млн. человек.
В Москве на грипп и ОРВИ приходится ежегодно до 90% от всей регистрируемой инфекционной заболеваемости, болеет около 3 млн. человек, из них около 60% — дети.
человек, из них около 60% — дети.
Общая информация о заболевании.
Грипп – острая вирусная инфекция дыхательных путей, характеризующаяся поражением слизистых оболочек верхних дыхательных путей, лихорадкой, интоксикацией, а также нарушением деятельности сердечно — сосудистой и нервной систем.
Источником инфекции является больной человек с клинически выраженной или бессимптомной формой гриппа. Важную роль в передаче инфекции играют больные со стертой формой инфекции, переносящие заболевание «на ногах».
Какие органы чаще всего поражает вирус гриппа?
Наиболее часто встречаются осложнения со стороны дыхательной системы, на втором месте органы сердечно-сосудистой системы и органы кроветворения, также встречаются осложнения со стороны нервной и моче-половой систем.
Для кого особенно опасны осложнения гриппа?
В группе риска по неблагоприятному исходу заболевания находятся дети до года и взрослые, старше 60 лет с сопутствующими заболеваниями органов дыхания, сердечно-сосудистой системы и эндокринной патологией, у которых возможен летальный исход из-за осложнений ранее имевшихся заболеваний.
Осложнения гриппа делятся на 2 группы:
1. Связанные непосредственно с течением гриппа.
Это геморрагический отек легких, менингит, менингоэнцефалит, инфекционно-токсический шок.
2. Возникшие в результате присоединения бактериальной инфекции.
Наиболее опасное и частое осложнение – это пневмония. Пневмония может быть как первичная, которая развилась сразу, а также может быть вторичной – возникшей на фоне присоединения бактериальной инфекции. Бактериальные агенты, наиболее часто вызывающие вторичную пневмонию – пневмококк и стафилококк. Такие пневмонии развиваются в конце первой – начале второй недели заболевания. Вирусная пневмония может протекать совместно с бактериальной, присоединившейся позднее.
Еще одним смертельно опасным осложнением гриппа считается острый респираторный дистресс-синдром, заключающийся в нарушении барьерной функции легочной ткани. На фоне данного осложнения возникает серьезнейшая дыхательная недостаточность, нередко несовместимая с жизнью.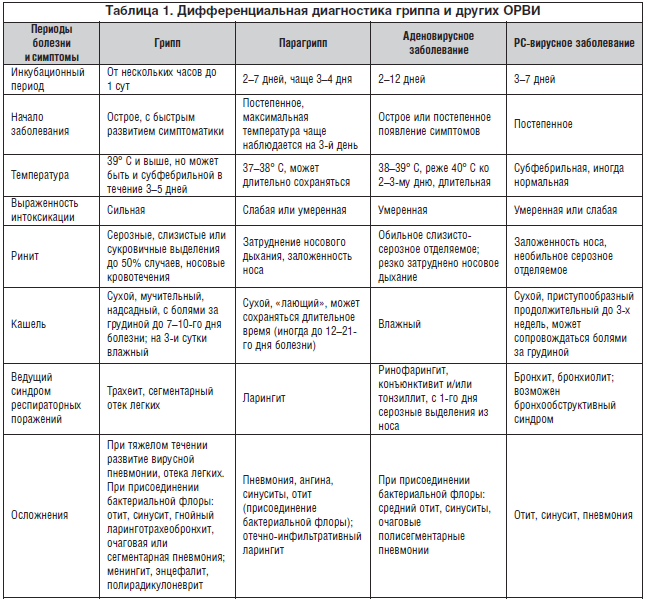
Не менее опасными осложнениями являются отит, синусит, гломерулонефрит, гнойный менингит, сепсис.
Токсическое поражение сердечной мышцы, как осложнение гриппа особенно опасно для пожилых людей.
Поражение центральной нервной системы проявляется менингеальным синдромом, спутанным сознанием, головной болью, рвотой.
О поражении периферической системы свидетельствуют радикулярные и другие невралгические боли.
При развитии отека мозга, геморрагического энцефалита у больного наблюдаются судороги, расстройство сознания. Такие осложнения нередко приводят к смерти вследствие остановки дыхания.
Профилактика гриппа:
Единственным надежным средством профилактики гриппа является вакцинация. Оптимальным временем проведения вакцинации против гриппа является период с сентября по ноябрь.
Профилактика осложнений.
Если по каким-либо причинам вакцинацию провести не удалось — строжайшим образом соблюдайте правила личной гигиены, во время подъема уровня заболеваемости гриппом постарайтесь не посещать общественные места, не контактируйте с заболевшими.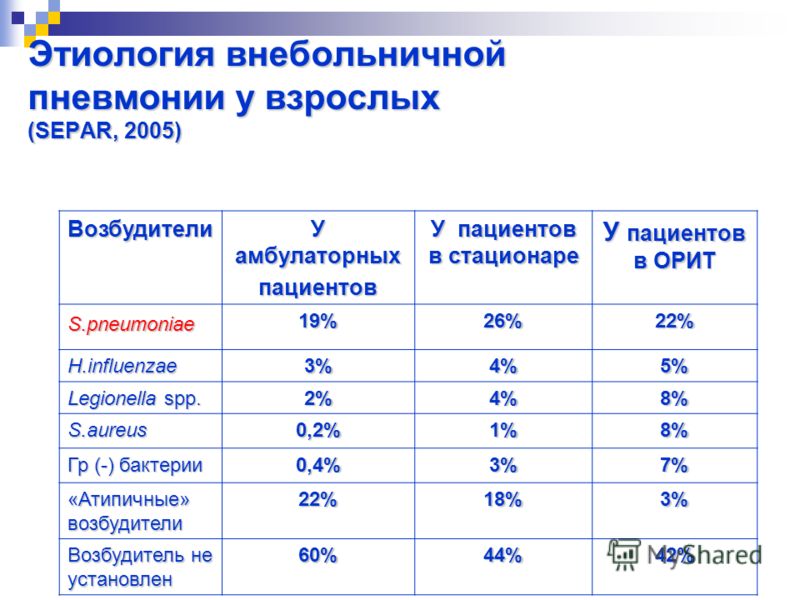
В случае подозрения у себя вирусной инфекции в течение ближайших 48 часов обратитесь к врачу.
Не пренебрегайте лечением, которое назначил Вам врач, своевременно принимайте назначенные лекарственные средства.
Обязательным пунктом в профилактике развития осложнений является соблюдение постельного режима во время болезни.
Причиной смерти от вируса гриппа является несвоевременное обращение за медицинской помощью и отказ от лечения.
|
Профилактика (неспецифическая) |
Гигиена при ОРВИ |
Антибиотики |
ОРВИ |
- < Назад
- Вперёд >
Проблема бактериальных осложнений после респираторных вирусных инфекций
Каждый человек в течение своей жизни неоднократно заражается различными респираторными вирусами, которые представляют собой факторы риска развития бактериальных осложнений. Среди этиологических факторов острых респираторных вирусных заболеваний наиболее опасным является вирус гриппа А. Этот вирус способен вызывать катастрофические пандемии с высокой смертностью, в основном из-за вторичной бактериальной пневмонии.Как показали многочисленные недавние исследования, основным механизмом провоцирования бактериальных инфекций независимо от типа респираторного вируса является несбалансированный ответ противовирусного врожденного иммунитета — чрезмерный ответ интерферона и неконтролируемое воспаление. Вероятность тяжелых бактериальных осложнений в течении ОРВИ определяется как вирулентностью самого вируса, так и составом респираторной микробиоты на момент вирусной инфекции, а также генетическими особенностями организма.На возникновение серьезных бактериальных осложнений также влияют хронические заболевания, которые влияют на регуляцию врожденного иммунного ответа. В этом обзоре обобщены современные представления о механизмах развития поствирусных бактериальных осложнений, а также возможные стратегии профилактики этих осложнений.
Среди этиологических факторов острых респираторных вирусных заболеваний наиболее опасным является вирус гриппа А. Этот вирус способен вызывать катастрофические пандемии с высокой смертностью, в основном из-за вторичной бактериальной пневмонии.Как показали многочисленные недавние исследования, основным механизмом провоцирования бактериальных инфекций независимо от типа респираторного вируса является несбалансированный ответ противовирусного врожденного иммунитета — чрезмерный ответ интерферона и неконтролируемое воспаление. Вероятность тяжелых бактериальных осложнений в течении ОРВИ определяется как вирулентностью самого вируса, так и составом респираторной микробиоты на момент вирусной инфекции, а также генетическими особенностями организма.На возникновение серьезных бактериальных осложнений также влияют хронические заболевания, которые влияют на регуляцию врожденного иммунного ответа. В этом обзоре обобщены современные представления о механизмах развития поствирусных бактериальных осложнений, а также возможные стратегии профилактики этих осложнений.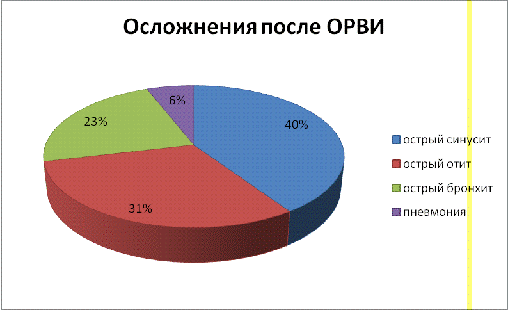
По оценкам Всемирной организации здравоохранения (ВОЗ), от острых респираторных вирусных инфекций (ОРВИ) ежегодно умирает 3,9 миллиона человек [1].Эти инфекции поражают все возрастные группы, но сильнее всего влияют на здоровье детей, пожилых людей и людей с хроническими заболеваниями. Риск ОРВИ определяется их способностью вызывать вирусную пневмонию и вторичные бактериальные инфекции, например бактериальная пневмония, отит, менингит, а также хронические заболевания легких. Таким образом, респираторные вирусы участвуют примерно в половине всех случаев внебольничной пневмонии (ВП) у детей. Кроме того, они вызывают более 90% случаев бронхиолита у младенцев и 85-95% случаев обострения астмы у детей.Вне периода пандемического гриппа ОРВИ являются причиной 30-50% случаев ВП, 80% обострений астмы и 20-60% обострений хронической обструктивной болезни легких (ХОБЛ) у взрослых. В целом эти инфекции являются одной из пяти основных причин смертности среди населения мира, а во многих развивающихся странах они являются ведущими причинами смертности детей в возрасте до пяти лет.
В отличие от других респираторных вирусов, вирус гриппа A представляет наибольшую опасность из-за его циркуляции у разных видов животных и способности реассортировать геномные фрагменты, что приводит к быстрой модификации основных поверхностных антигенов вируса — гемагглютинина (HA) и нейраминидазы ( NA) (антигенный сдвиг).Этот механизм определяет возможность появления новых антигенных вариантов вирусов гриппа A, таких как h2N1, h3N2, h4N2, h2N1pdm09, которые вызвали четыре известные пандемии [2, 3].
В периоды между пандемиями вирусы гриппа также претерпевают антигенные изменения, вызванные постепенным накоплением мутаций в HA и NA (антигенный дрейф), что приводит к возникновению сезонных эпидемий.
Даже сейчас, в 21 веке, когда доступны противогриппозные препараты и антибиотики широкого спектра действия, у людей с сезонным гриппом есть вероятность развития осложнений.Таким образом, как вирус-индуцированный острый респираторный дистресс-синдром (ОРДС), так и вторичная бактериальная пневмония могут развиться в течение первой недели после вирусной инфекции.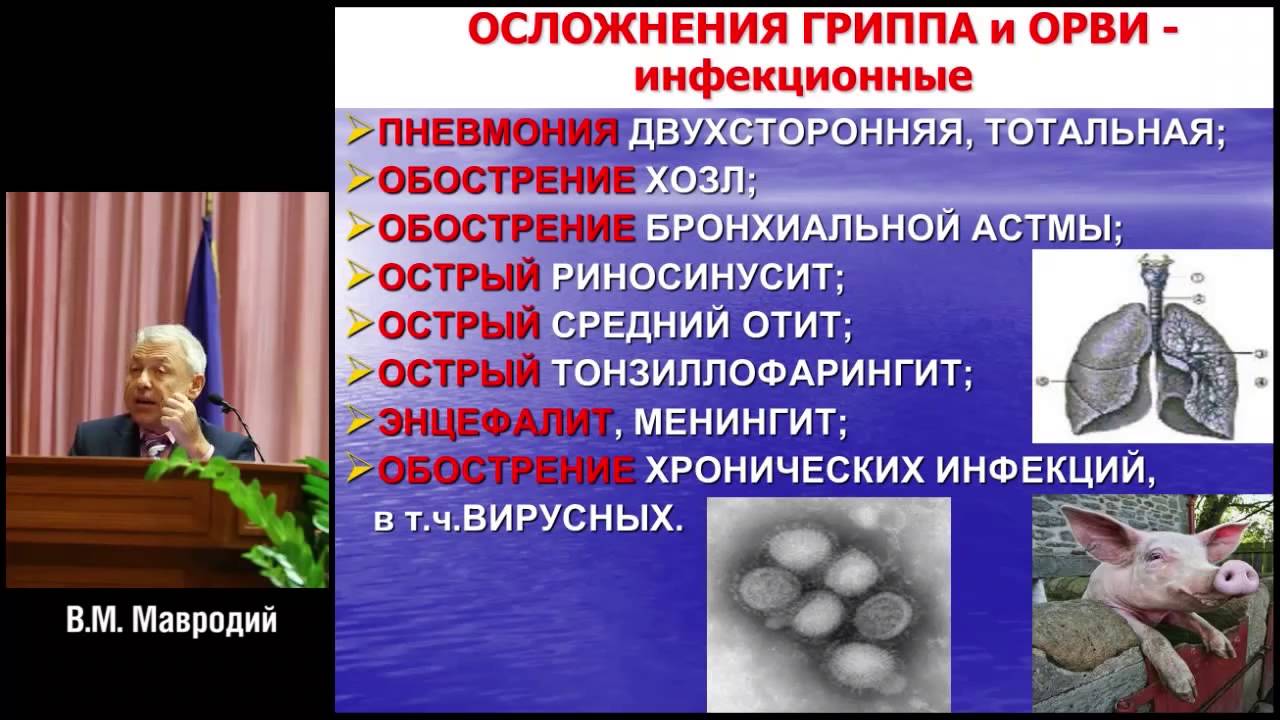 По данным ВОЗ, от гриппа ежегодно умирает до 650 000 человек во всем мире [1]. Согласно данным Центров по контролю и профилактике заболеваний (CDC, Атланта, Джорджия, США), в США с населением около 300 миллионов человек уровень смертности от гриппа колеблется от 16 000 до 56 000 случаев в год. В Российской Федерации с населением около 140 миллионов человек смертность от сезонного гриппа оценивается на уровне нескольких сотен в год, хотя официальных данных в открытом доступе нет.Различие в статистике смертности от гриппа в разных странах можно определить по разнице в методах расчета. Например, статистика смертности от бактериальной пневмонии может не учитывать роль вирусного этиологического фактора как провокатора вторичной инфекции. Таким образом, лица, умершие от бактериальной пневмонии, могут не учитываться при расчете уровня смертности от гриппа, даже если бактериальные осложнения были спровоцированы первичной инфекцией гриппа.
По данным ВОЗ, от гриппа ежегодно умирает до 650 000 человек во всем мире [1]. Согласно данным Центров по контролю и профилактике заболеваний (CDC, Атланта, Джорджия, США), в США с населением около 300 миллионов человек уровень смертности от гриппа колеблется от 16 000 до 56 000 случаев в год. В Российской Федерации с населением около 140 миллионов человек смертность от сезонного гриппа оценивается на уровне нескольких сотен в год, хотя официальных данных в открытом доступе нет.Различие в статистике смертности от гриппа в разных странах можно определить по разнице в методах расчета. Например, статистика смертности от бактериальной пневмонии может не учитывать роль вирусного этиологического фактора как провокатора вторичной инфекции. Таким образом, лица, умершие от бактериальной пневмонии, могут не учитываться при расчете уровня смертности от гриппа, даже если бактериальные осложнения были спровоцированы первичной инфекцией гриппа.
Пандемия вируса гриппа A (h2N1) (испанский грипп) 1918 года была самой смертельной из когда-либо зарегистрированных эпидемий гриппа. В ходе этой пандемии, случившейся во время Первой мировой войны, было инфицировано 50% населения мира, в результате чего погибло около 40-50 миллионов человек [4]. От пандемии больше всего страдали люди в возрасте 20-40 лет, служившие в армии. Поскольку вирус гриппа был открыт в 1933 году, во время пандемии в Испании этиологический агент болезни еще не был идентифицирован.В то время микробиологи пытались связать испанский грипп с различными бактериальными возбудителями, в частности с Haemophilus influenzae (H. influenzae) [5]. Теперь, благодаря доступности метода ПЦР, стало возможным идентифицировать гены вируса гриппа в вскрытых и гистологических образцах того времени и реконструировать испанский вирус h2N1 с помощью обратной генетики. Удивительно, но реконструированный вирус не имел радикальных отличий по генетической структуре от циркулирующих в настоящее время вирусов [6].Последующее исследование вскрытых образцов показало, что более 90% проанализированных образцов легочной ткани умерших во время пандемии гриппа в Испании имели признаки бактериальной инфекции [7-9].
В ходе этой пандемии, случившейся во время Первой мировой войны, было инфицировано 50% населения мира, в результате чего погибло около 40-50 миллионов человек [4]. От пандемии больше всего страдали люди в возрасте 20-40 лет, служившие в армии. Поскольку вирус гриппа был открыт в 1933 году, во время пандемии в Испании этиологический агент болезни еще не был идентифицирован.В то время микробиологи пытались связать испанский грипп с различными бактериальными возбудителями, в частности с Haemophilus influenzae (H. influenzae) [5]. Теперь, благодаря доступности метода ПЦР, стало возможным идентифицировать гены вируса гриппа в вскрытых и гистологических образцах того времени и реконструировать испанский вирус h2N1 с помощью обратной генетики. Удивительно, но реконструированный вирус не имел радикальных отличий по генетической структуре от циркулирующих в настоящее время вирусов [6].Последующее исследование вскрытых образцов показало, что более 90% проанализированных образцов легочной ткани умерших во время пандемии гриппа в Испании имели признаки бактериальной инфекции [7-9]. Выяснилось, что 95% смертей были вызваны не самим вирусом гриппа, а последующей бактериальной пневмонией. В частности, было доказано, что Streptococcus pneumoniae (S. pneumoniae) был основным инфекционным агентом, вызвавшим диагностированную пневмонию [10]. Вскрытие показало наличие S.pneumoniae в легких 44% и в крови 33% больных, умерших от испанского гриппа [10, 11]. Хотя S. pneumoniae было основной причиной смертности, другие инфекционные агенты, такие как Staphylococcus aureus (S. aureus) , H. influenzae и ряд других Streptococcus spp . были также идентифицированы при вскрытии образца легкого [5, 7]. Следовательно, катастрофический исход пандемии гриппа 1918 года мог быть определен нехваткой вакцин и противовирусных препаратов против вируса гриппа, а также отсутствием антибиотиков, которые могли бы подавить вторичные бактериальные осложнения.
Выяснилось, что 95% смертей были вызваны не самим вирусом гриппа, а последующей бактериальной пневмонией. В частности, было доказано, что Streptococcus pneumoniae (S. pneumoniae) был основным инфекционным агентом, вызвавшим диагностированную пневмонию [10]. Вскрытие показало наличие S.pneumoniae в легких 44% и в крови 33% больных, умерших от испанского гриппа [10, 11]. Хотя S. pneumoniae было основной причиной смертности, другие инфекционные агенты, такие как Staphylococcus aureus (S. aureus) , H. influenzae и ряд других Streptococcus spp . были также идентифицированы при вскрытии образца легкого [5, 7]. Следовательно, катастрофический исход пандемии гриппа 1918 года мог быть определен нехваткой вакцин и противовирусных препаратов против вируса гриппа, а также отсутствием антибиотиков, которые могли бы подавить вторичные бактериальные осложнения.
Пандемия гриппа в эпоху антибиотиков при отсутствии вакцинации и противовирусных препаратов
В 1957 году пандемия азиатского гриппа поразила 40-50% людей во всем мире с оценками общей смертности от 1,5 до 4 миллионов человек [13], а число погибших в Соединенных Штатах достигло около 69 800 человек [13-15]. Причиной этой пандемии стал штамм вируса гриппа A (h3N2) [12]. Анализ образцов вскрытия показал наличие бактериальной инфекции в 80% всех тяжелых и летальных случаев [8, 16, 17].Следует отметить, что к этому времени такие антибиотики, как пенициллин и стрептомицин, уже были доступны и использовались в медицинской практике в развитых странах. Однако во время этой пандемии в США и ряде других стран наблюдалось заметное увеличение количества госпитализаций, связанных с пневмонией, вызванной, главным образом, S. pneumoniae , H. influenzae и S. aureus [18 ]. Аналогичные данные были получены в Нидерландах, где из 148 смертей, предположительно вызванных азиатской пандемией гриппа, 75% были связаны с бактериальной пневмонией, спровоцированной в 15% случаев S.pneumoniae и в 59% случаев — S. aureus [16]. Следует отметить, что приведенные данные бактериологического исследования могли быть сильно искажены, поскольку в то время многие пациенты уже получали лечение антибиотиками [19].
Причиной этой пандемии стал штамм вируса гриппа A (h3N2) [12]. Анализ образцов вскрытия показал наличие бактериальной инфекции в 80% всех тяжелых и летальных случаев [8, 16, 17].Следует отметить, что к этому времени такие антибиотики, как пенициллин и стрептомицин, уже были доступны и использовались в медицинской практике в развитых странах. Однако во время этой пандемии в США и ряде других стран наблюдалось заметное увеличение количества госпитализаций, связанных с пневмонией, вызванной, главным образом, S. pneumoniae , H. influenzae и S. aureus [18 ]. Аналогичные данные были получены в Нидерландах, где из 148 смертей, предположительно вызванных азиатской пандемией гриппа, 75% были связаны с бактериальной пневмонией, спровоцированной в 15% случаев S.pneumoniae и в 59% случаев — S. aureus [16]. Следует отметить, что приведенные данные бактериологического исследования могли быть сильно искажены, поскольку в то время многие пациенты уже получали лечение антибиотиками [19].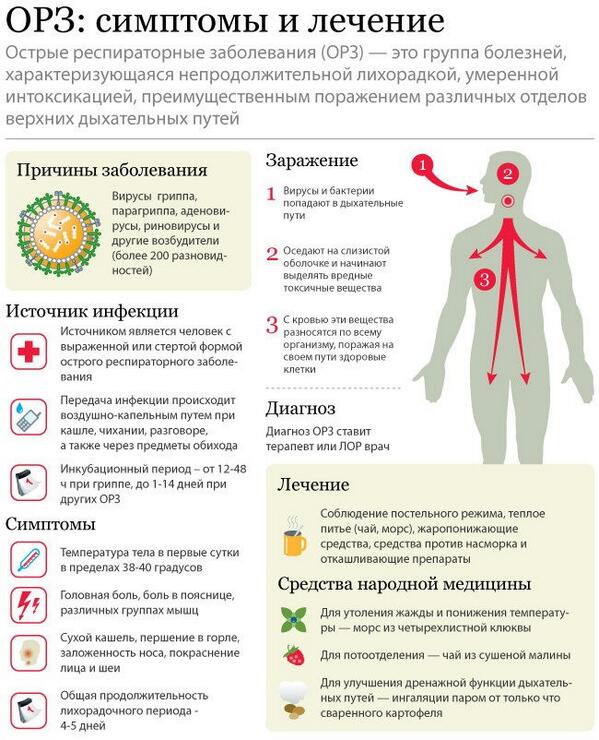
Общее число погибших от пандемии в Гонконге 1968-1969 гг., Вызванной штаммом вируса гриппа A (h4N2), составило около 2 миллионов человек [20, 21]. Увеличение смертности от респираторных инфекций на 55%, большинство случаев сопровождались вторичной бактериальной пневмонией, было зарегистрировано в Великобритании в 1969 г. [22].Стафилококковая пневмония оказалась основным осложнением гонконгского гриппа h4N2. Например, из 129 взрослых с диагнозом пандемический грипп пневмония была обнаружена в 16% случаев, из которых 40% (6% из всех 129 случаев гриппа) закончились летальным исходом. S. aureus или Pseudomonas aeruginosa (P. aeruginosa) были обнаружены в 75% вскрытых образцов умершего [23]. Следует отметить, что в ходе пандемии в Испании большинство летальных случаев вторичной бактериальной пневмонии было вызвано S.pneumonia , но во время пандемий 1957 и 1968 годов преобладающим этиологическим возбудителем вторичной бактериальной пневмонии стал S. aureus . Это можно объяснить повышенной устойчивостью к антибиотикам S. aureus из-за широкого использования антибиотиков населением в то время.
aureus . Это можно объяснить повышенной устойчивостью к антибиотикам S. aureus из-за широкого использования антибиотиков населением в то время.
Пандемия гриппа в присутствии противогриппозных вакцин, противовирусных препаратов и антибиотиков
Вспышка вируса гриппа A (h2N1) pdm09 в 2009 г. распространилась на 41 страну в течение четырех недель и переросла в пандемию [20, 24 ].Компонент h2N1 в вакцинах против сезонного гриппа, произведенных в 2009 г., не соответствовал антигенным свойствам недавно появившемуся пандемическому штамму A (h2N1) pdm09. Считается, что общее число погибших от этой пандемии составило около 284 000 человек во всем мире [25]. Частыми причинами смерти в ходе этой пандемии в США были вторичные бактериальные инфекции, вызванные в основном S. pneumoniae и S. pyogenes [26, 27]. Другие исследования в США показали, что почти в 30% из 77 летальных случаев инфекция гриппа сопровождалась бактериальными инфекциями, 46% из которых были вызваны S. pneumoniae , 9% — S. aureus и 1% — H. influenzae . Palacios et al. исследовал мазки из носоглотки почти 200 пациентов с пандемическим гриппом и обнаружил H. influenzae в 52% образцов, S. pneumoniae в 31% и S. aureus в 18% образцов соответственно [28 ]. Тяжесть заболевания чаще всего была связана с вторичной инфекцией, вызванной S. pneumoniae .
pneumoniae , 9% — S. aureus и 1% — H. influenzae . Palacios et al. исследовал мазки из носоглотки почти 200 пациентов с пандемическим гриппом и обнаружил H. influenzae в 52% образцов, S. pneumoniae в 31% и S. aureus в 18% образцов соответственно [28 ]. Тяжесть заболевания чаще всего была связана с вторичной инфекцией, вызванной S. pneumoniae .
В другом исследовании 838 тяжелобольных детей в США было показано, что через 72 часа после госпитализации в отделение интенсивной терапии бактериальная суперинфекция развилась у 33% пациентов, 48% из которых были вызваны метициллин-резистентными. С.aureus (MRSA), в 5,5% случаев — S. pneumoniae и 5% — H. influenzae [29].
Таким образом, несмотря на повсеместное внедрение сезонных противогриппозных вакцин, противовирусных препаратов и антибиотиков, проблема бактериальных осложнений течения гриппа не перестает быть актуальной. Более того, в связи с развитием устойчивости бактериальной флоры к современным антибиотикам эта проблема может обостриться в случае новой пандемии гриппа [30].
Более того, в связи с развитием устойчивости бактериальной флоры к современным антибиотикам эта проблема может обостриться в случае новой пандемии гриппа [30].
Респираторные вирусные инфекции не гриппозной этиологии как провокаторы вторичной бактериальной пневмонии
Современная диагностика позволяет ученым анализировать бактериальные осложнения при различных респираторных инфекциях, не связанных с гриппом. В таблице 1 обобщены многочисленные исследования, которые показывают связь респираторных вирусных патогенов с некоторыми бактериями, которые могут вызывать пневмонию, средний отит, синусит и менингит в качестве осложнений. Несмотря на то, что другие респираторные вирусы не способны вызывать пандемии, эти вирусы оказались столь же опасными, как и грипп, в провоцировании вторичных бактериальных осложнений.Например, представитель семейства Paramyxoviridae , метапневмовирус человека (hMPV), может вызывать тяжелые осложнения, такие как вирус гриппа, включая как вирусную пневмонию с развитием ОРДС, так и бактериальную пневмонию [31]. Другой представитель этого семейства — респираторно-синцитиальный вирус (РСВ) — оказался даже опаснее гриппа по уровню смертности среди госпитализированных пациентов с диагнозом пневмония. Таким образом, смертность от всех причин через 20 дней после госпитализации была выше у пациентов с RSV-инфекцией (18.4%), чем у больных гриппом (6,7%) [32]. К сожалению, не существует вакцин и эффективных противовирусных препаратов для профилактики и лечения пневмовирусов, а также от большинства респираторных вирусов не гриппозной этиологии.
Другой представитель этого семейства — респираторно-синцитиальный вирус (РСВ) — оказался даже опаснее гриппа по уровню смертности среди госпитализированных пациентов с диагнозом пневмония. Таким образом, смертность от всех причин через 20 дней после госпитализации была выше у пациентов с RSV-инфекцией (18.4%), чем у больных гриппом (6,7%) [32]. К сожалению, не существует вакцин и эффективных противовирусных препаратов для профилактики и лечения пневмовирусов, а также от большинства респираторных вирусов не гриппозной этиологии.
Хотя обсервационные исследования взаимосвязи вирусных и бактериальных инфекций, проведенные в разных регионах мира, приводят к согласованным выводам, они могут различаться в оценке роли, которую различные патогены играют в развитии бактериальной ВП.Это можно объяснить значительным влиянием климатических условий и генетических характеристик населения на распространенность отдельных вирусных и бактериальных патогенов.
В США обследовали 1024 пациента с ВП и сравнили с группой из 759 контрольных пациентов без симптомов [48]. Оказалось, что вирусы гриппа, RSV, hMPV и, в меньшей степени, вирусы парагриппа и коронавирусы значительно чаще выделялись из группы пациентов с диагнозом пневмония, независимо от возраста пациента.В то же время риновирусы были частой причиной ВП у взрослых, но практически не диагностировались у детей с пневмонией. Напротив, аденовирусы были связаны с ВП только у детей младше 2 лет.
Оказалось, что вирусы гриппа, RSV, hMPV и, в меньшей степени, вирусы парагриппа и коронавирусы значительно чаще выделялись из группы пациентов с диагнозом пневмония, независимо от возраста пациента.В то же время риновирусы были частой причиной ВП у взрослых, но практически не диагностировались у детей с пневмонией. Напротив, аденовирусы были связаны с ВП только у детей младше 2 лет.
В исследовании, проведенном в Японии с участием 2617 пожилых (≥65 лет) пациентов с диагнозом хронические респираторные или другие сопутствующие заболевания, вирусные патогены были изолированы в 23,1% случаев [49]. Риновирусы были наиболее частой причиной пневмонии (9.8%), тогда как грипп и RSV были обнаружены в 3,9% случаев. RSV чаще всего диагностировался у лиц с хроническими респираторными заболеваниями, тогда как другие вирусы были связаны с пневмонией, независимо от наличия респираторных и других хронических заболеваний. В целом вирусные инфекции не предопределяли повышенного риска смертности пациентов с пневмонией, но грипп приводил к трехкратному увеличению смертности пациентов с хроническими респираторными заболеваниями.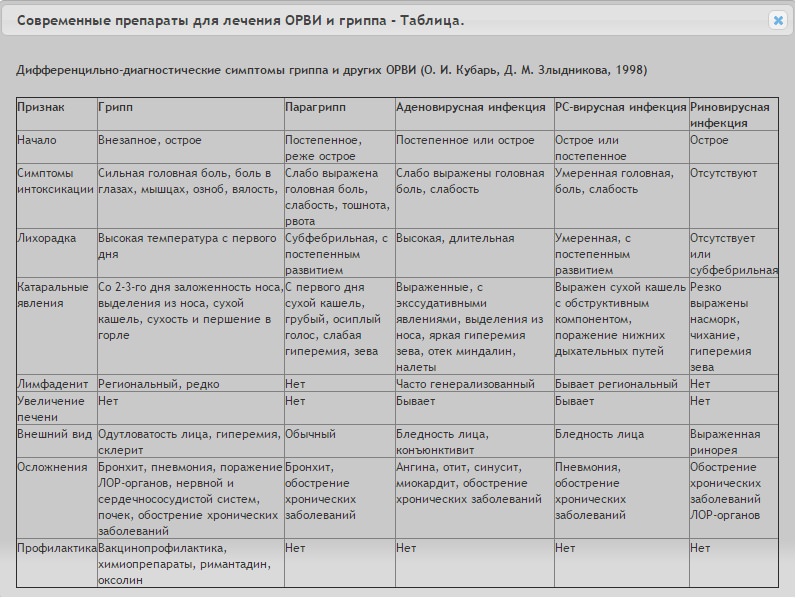 Следовательно, вклад вирусной инфекции в смертность от пневмонии зависит от типа вирусного агента и наличия сопутствующих заболеваний.
Следовательно, вклад вирусной инфекции в смертность от пневмонии зависит от типа вирусного агента и наличия сопутствующих заболеваний.
Южнокорейское метааналитическое исследование, проведенное на 5298 пациентах разных возрастных групп, показало, что провокация бактериальной суперинфекции характерна для всех вирусных респираторных инфекций [50]. Однако тип бактериального патогена, вызывающего вторичную инфекцию, может зависеть как от типа вирусной инфекции, так и от возраста пациента. Например, вирусные инфекции гриппа A и B, риновирус и hMPV вызвали пневмонию у взрослых пациентов, которая была связана с S.aureus , тогда как коронавирус, вирус парагриппа и RSV привели к пневмонии, связанной с грамотрицательными бактериями Klebsiella spp . и Acinetobacter spp. Инфекция микоплазмы ( M. pneumonia ) была наиболее частой причиной бактериальной пневмонии у детей независимо от типа предыдущей вирусной инфекции. Эти исследования подчеркивают важность вирусной диагностики у пациентов с вторичной бактериальной пневмонией с точки зрения выбора правильной антибактериальной терапии.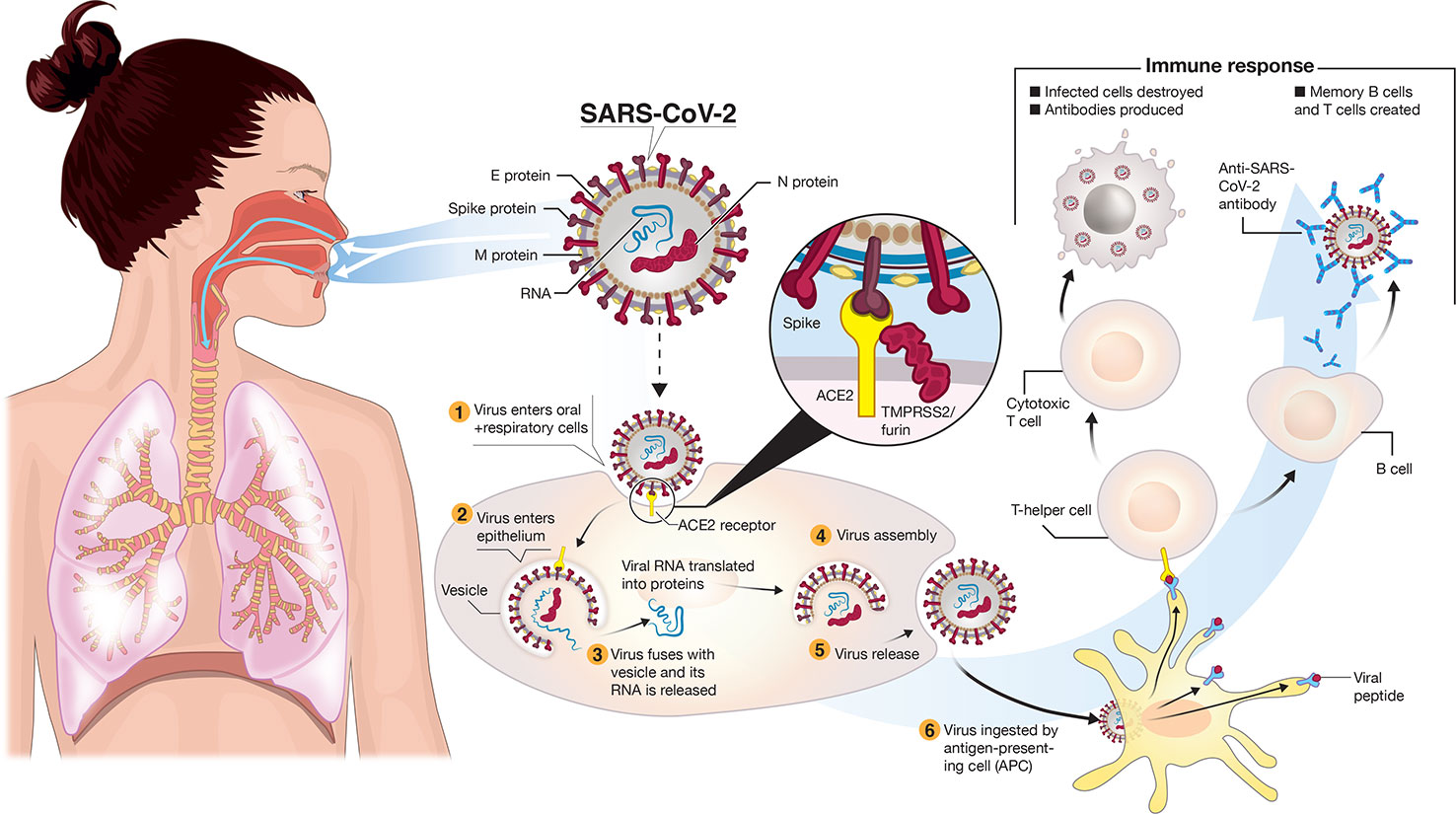 Например, поствирусная пневмония у младенцев и детей должна лечиться антибиотиками, активными против M. pneumoniae (макролиды). Взрослых с гриппом, hMPV или риновирусной инфекцией следует лечить антибиотиками, которые эффективно убивают стафилококковые бактерии, тогда как антибиотики, которые активны против широкого спектра грамотрицательных бактерий, следует назначать в случаях заражения коронавирусом и вирусом парагриппа.
Например, поствирусная пневмония у младенцев и детей должна лечиться антибиотиками, активными против M. pneumoniae (макролиды). Взрослых с гриппом, hMPV или риновирусной инфекцией следует лечить антибиотиками, которые эффективно убивают стафилококковые бактерии, тогда как антибиотики, которые активны против широкого спектра грамотрицательных бактерий, следует назначать в случаях заражения коронавирусом и вирусом парагриппа.
Однако, как отмечалось выше, взаимосвязь между генотипом популяции и климатическими условиями, с одной стороны, и спектром колонизирующей микробной флоры, с другой стороны, требует дальнейшего изучения с целью разработки адекватных медицинских стандартов для лечения респираторные инфекции у пациентов в разных странах.
Человеческое тело является переносчиком различных видов бактерий, которые вместе называются микробиотой [51]. Обычно эти бактерии, которые называются комменсальными штаммами, живут во взаимовыгодном симбиозе с хозяином и обеспечивают множество полезных функций для хозяина, такие как защита организма хозяина посредством конкуренции с патогенными бактериями. Обычно небольшое количество патогенных бактерий, в том числе S. pneumoniae , S. aureus , H.influenzae , S. pyogenes , Moraxella catarrhalis и MRSA присутствуют в микробиоте верхних дыхательных путей человека без серьезных последствий для организма [52]. Сдвиг микробиоты в сторону увеличения количества патогенных штаммов может происходить при вирусных респираторных инфекциях из-за подавления факторов антибактериальной защиты. В результате вторичные бактериальные инфекции дыхательных путей, спровоцированные вирусной инфекцией, чаще всего вызываются резидентными патогенными бактериями, а не внешней инфекцией [53, 54].
Обычно небольшое количество патогенных бактерий, в том числе S. pneumoniae , S. aureus , H.influenzae , S. pyogenes , Moraxella catarrhalis и MRSA присутствуют в микробиоте верхних дыхательных путей человека без серьезных последствий для организма [52]. Сдвиг микробиоты в сторону увеличения количества патогенных штаммов может происходить при вирусных респираторных инфекциях из-за подавления факторов антибактериальной защиты. В результате вторичные бактериальные инфекции дыхательных путей, спровоцированные вирусной инфекцией, чаще всего вызываются резидентными патогенными бактериями, а не внешней инфекцией [53, 54].
На сегодняшний день известно множество факторов, которые способствуют бактериальной колонизации в ходе вирусных инфекций:
Действие большинства из этих факторов зависит не только от природы вирусного патогена, но и от типа колонизирующих бактерий. . Например, известно, что S. aureus может усиливать репродукцию вируса в результате подавления передачи сигнала IFN типа I путем ингибирования димеризации STAT-1 – STAT-2 [68]. При течении RSV-инфекции у детей степень тяжести заболевания можно определить по распространенности S.pneumoniae и H. influenzae в микробиоте до начала вирусного заболевания [69].
При течении RSV-инфекции у детей степень тяжести заболевания можно определить по распространенности S.pneumoniae и H. influenzae в микробиоте до начала вирусного заболевания [69].
Тем не менее, результаты экспериментов на животных и клинических наблюдений показывают, что колонизация дыхательных путей патогенными бактериальными штаммами чаще всего вызывается вирусными инфекциями. Первичное заражение мышей сублетальной дозой бактерий с последующим заражением сублетальной дозой вируса гриппа не приводило к вторичной бактериальной пневмонии, тогда как обратная последовательность инфекций вызывала пневмонию с летальным исходом [70–72].В случае вирусной инфекции бактериальное осложнение чаще всего возникало на 4-й день у животных после вирусной инфекции или на 7-й день у человека после клинического проявления вирусной инфекции [42, 73]. В этом случае, независимо от типа вирусного патогена, ответ IFN типа I играет основную роль, фокусируя действие системы врожденного иммунитета на борьбу с вирусной инфекцией, но в то же время снижая активность факторов антибактериальной защиты, таких как как фагоцитоз или выработка антибактериальных пептидов.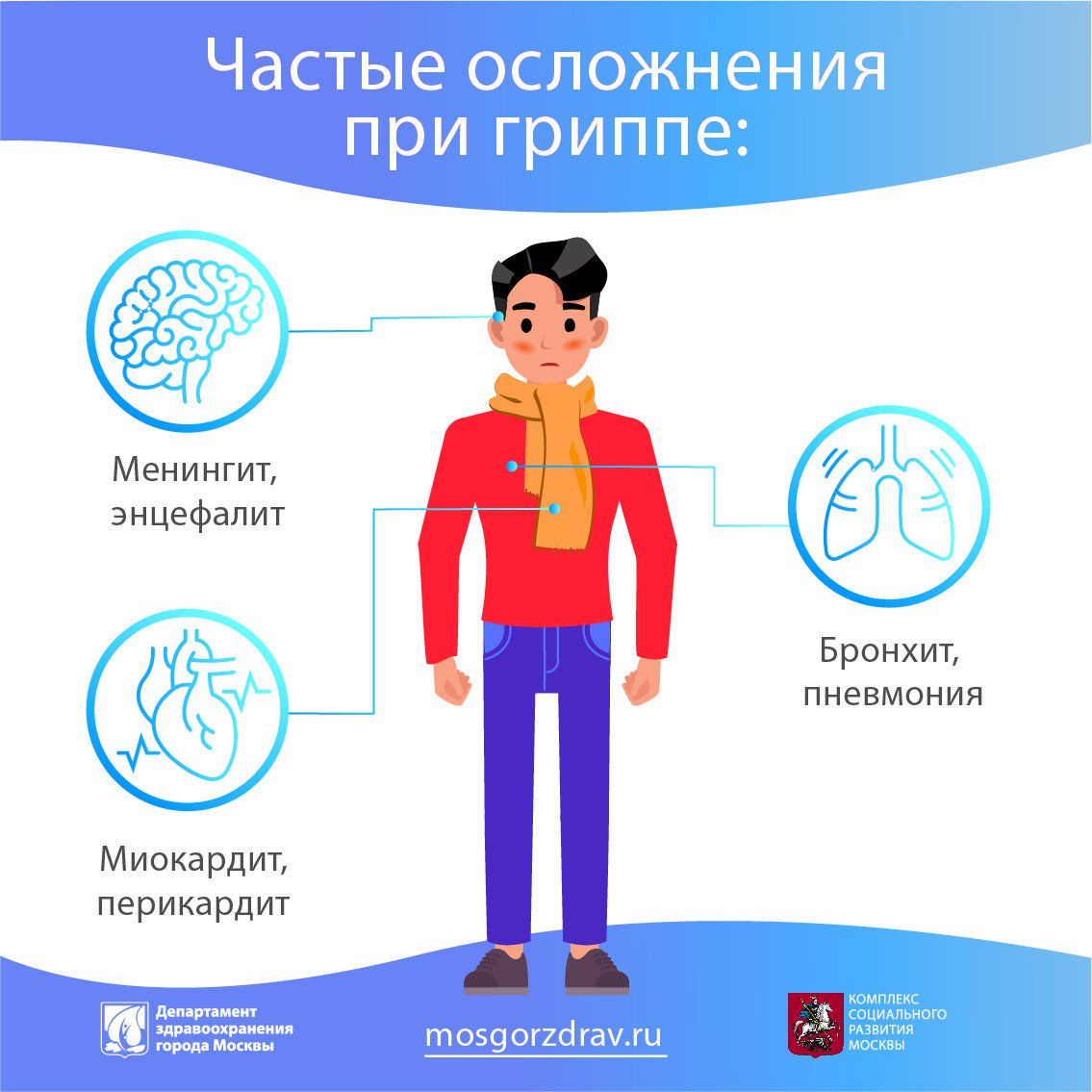
Роль IFN-ответа в патогенезе вторичных бактериальных инфекций
Несмотря на различия в структурной и генетической организации вирусов разных семейств, они имеют общее свойство — все они являются внутриклеточными патогенами, вызывающими IFN-ответ типа I. Система врожденного иммунитета распознает вирусную инфекцию с помощью Toll-подобных рецепторов, расположенных в клеточной мембране или цитоплазматических рецепторов распознавания образов RIG-1 и MDA5 (PRR).Эти рецепторы обнаруживают компоненты патогенов, такие как двухцепочечная РНК (дцРНК) или липосахариды (ЛПС), которые нетипичны для нормальных клеток, но присутствуют в очаге инфекции. Распознавание вирусной инфекции приводит к индукции цитокинового ответа, в первую очередь IFN I, II и III типов. Система врожденного противовирусного иммунитета подробно описана в обзорах [74, 75]. Защитные эффекты IFN обусловлены их способностью индуцировать синтез противовирусных белков в инфицированных и окружающих клетках, а также регулированием активации и миграции клеток врожденного иммунитета, которые определяют развитие специфических B- и T- клеточный иммунный ответ [76–78].
С другой стороны, большая часть недавних экспериментальных данных показывает, что влияние IFN-ответа на течение ОРВИ может быть пагубным. В случае прогрессирующего развития инфекции постоянное и избыточное производство IFN может привести к развитию воспаления из-за гиперпродукции хемокинов, таких как CCL2 и CXCL10, и инфильтрации альвеол провоспалительными моноцитами / макрофагами и плазмацитоидами. дендритные клетки. В этом случае попадание вирусных и бактериальных лигандов Toll-подобных рецепторов, таких как LPS или dsRNA, в зону воспаления может привести к усиленной продукции провоспалительных цитокинов этими клетками с возможностью развития так называемого цитокинового шторма [79]. .Тогда неконтролируемая продукция провоспалительных цитокинов и чрезмерная инфильтрация тканей легких клетками врожденного иммунитета может стать ведущей причиной повреждения легких [80, 81].
Экспрессия проапоптотического лиганда TRIAL, индуцированная IFN типа I, также приводит к массивному апоптозу эпителиальных клеток, которые вносят вклад в развитие ARDS [82].
Важным фактором риска развития неконтролируемого воспаления является генетическая предрасположенность организма к регуляции ответа IFN.Например, мыши DBA, которые продуцируют высокие уровни IFN типа I в ответ на инфекцию гриппа, демонстрируют высокую смертность при инфицировании дозами, безопасными для мышей C57BL / 6 с умеренным продуцированием INF [83, 84]. Люди с синдромом Дауна имеют повышенную чувствительность к респираторным инфекциям и высокую вероятность серьезных осложнений, связанных с генетически обусловленной гиперпродукцией IFN α / γ в ответ на вирусную инфекцию [85].
Помимо стимуляции цитокинового шторма, ИФН I типа могут участвовать в патогенезе вторичной бактериальной инфекции [86, 87].Развитие IFN-ответа в ходе вирусной инфекции приводит к снижению как миграции, так и фагоцитарной функции нейтрофилов и макрофагов за счет проапоптотических механизмов или посредством эпигенетической регуляции их функций [61, 88, 89].
IFN типа I также способны подавлять антибактериальную защиту, подавляя продукцию IL-17 Т-клетками [63, 90]. Отсутствие ответа на ИЛ-17 приводит к снижению продукции антибактериальных пептидов, таких как липокалин 2 и BPIFA1, что, в свою очередь, приводит к увеличению бактериального роста в очаге вирусной инфекции [87].
Отсутствие ответа на ИЛ-17 приводит к снижению продукции антибактериальных пептидов, таких как липокалин 2 и BPIFA1, что, в свою очередь, приводит к увеличению бактериального роста в очаге вирусной инфекции [87].
Тот факт, что генетически модифицированные мыши, дефицитные по рецепторам IFN типа I (IFNAR), были более устойчивы к развитию ARDS, бактериальной пневмонии или сепсиса по сравнению с мышами с нормальной передачей сигналов IFN, доказывает отрицательный эффект сверхэкспрессии IFN [61, 62, 84, 91, 92]. Использование индуктора поли (I: C) IFN до заражения мышей пневмококком привело к 100-кратному увеличению колонизации легких введенными бактериями [64].
Следовательно, развитие тяжелых осложнений после ОРВИ может зависеть не только от вирулентности самого вируса или состава респираторной микробиоты во время вирусной инфекции, но и от способности организма регулировать выраженность реакций врожденного иммунитета, особенно ответа на ИФН.
Роль противовирусной вакцинации и противовирусной терапии в профилактике вторичных бактериальных осложнений
В настоящее время существует множество доказательств того, что противовирусная вакцинация может снизить риск бактериальных осложнений после ОРВИ. Было показано, что иммунизация инактивированной противогриппозной вакциной значительно снижает тяжесть бактериальной суперинфекции у мышей, инфицированных гриппом [93]. В другом исследовании было показано, что иммунизация мышей инактивированной или живой вакциной против гриппа может в равной степени снизить летальность вирусной и последующей бактериальной инфекции, но в то же время она не может ограничить рост S.pyogenes в легких. В этом случае было показано, что вакцинация против гриппа, приводящая к снижению вирусной нагрузки, приводит к снижению провоспалительных цитокинов и индукции IFNγ в легких во время бактериальной суперинфекции [94]. К сожалению, информации о влиянии вакцинации против гриппа на вторичные бактериальные осложнения мало. Это объясняется сложностью подобных исследований, поскольку для этого потребуется параллельная оценка противовирусного и антибактериального иммунитета к большому количеству потенциальных патогенов.Однако в ограниченном исследовании, проведенном в США среди военнослужащих, вакцина против гриппа снизила уровень заболеваемости, вызываемой S.
Было показано, что иммунизация инактивированной противогриппозной вакциной значительно снижает тяжесть бактериальной суперинфекции у мышей, инфицированных гриппом [93]. В другом исследовании было показано, что иммунизация мышей инактивированной или живой вакциной против гриппа может в равной степени снизить летальность вирусной и последующей бактериальной инфекции, но в то же время она не может ограничить рост S.pyogenes в легких. В этом случае было показано, что вакцинация против гриппа, приводящая к снижению вирусной нагрузки, приводит к снижению провоспалительных цитокинов и индукции IFNγ в легких во время бактериальной суперинфекции [94]. К сожалению, информации о влиянии вакцинации против гриппа на вторичные бактериальные осложнения мало. Это объясняется сложностью подобных исследований, поскольку для этого потребуется параллельная оценка противовирусного и антибактериального иммунитета к большому количеству потенциальных патогенов.Однако в ограниченном исследовании, проведенном в США среди военнослужащих, вакцина против гриппа снизила уровень заболеваемости, вызываемой S. pyogenes [95]. Аналогичным образом вакцинация детей живой вакциной, адаптированной к холоду, показала снижение заболеваемости средним отитом [96].
pyogenes [95]. Аналогичным образом вакцинация детей живой вакциной, адаптированной к холоду, показала снижение заболеваемости средним отитом [96].
Таким образом, вакцинация против респираторных вирусов может помочь предотвратить вторичные бактериальные осложнения из-за различных механизмов неспецифической защиты путем модуляции врожденного иммунитета.Разумно предположить, что снижение репродукции вируса из-за эффективной вакцинации может привести к снижению противовирусного ответа IFN и, как следствие, ограничению негативного действия IFN на эффекторы антибактериальной защиты. Кроме того, снижение концентрации вируса может помочь сохранить респираторный эпителий и уменьшить адгезию бактериальных клеток [56].
Действие противовирусных препаратов, таких как ингибиторы NA, на предотвращение вторичных бактериальных инфекций также может быть связано со снижением ответа IFN из-за ингибирования репликации вируса.Исследования на животных моделях показали, что ингибиторы NA могут снижать восприимчивость животных, инфицированных гриппом, к вторичной бактериальной пневмонии [97]. Клинические испытания у взрослых и детей показали, что прием ингибиторов НА (занамивир и осельтамивир) приводит к снижению частоты бронхита и, как следствие, к меньшему количеству назначений антибиотиков [98-101].
Клинические испытания у взрослых и детей показали, что прием ингибиторов НА (занамивир и осельтамивир) приводит к снижению частоты бронхита и, как следствие, к меньшему количеству назначений антибиотиков [98-101].
Открытие антибиотиков и разработка противогриппозных и бактериальных вакцин значительно снизили шансы повторения катастрофических пандемий, таких как испанский грипп 1918 года [102].Однако грипп и другие респираторные вирусы остаются одной из основных причин бактериальных осложнений и ВП. С другой стороны, растущая устойчивость бактериальных патогенов к современным антибиотикам из-за их широкого использования становится все более тревожной.
К сожалению, в настоящее время практически отсутствуют вакцины или противовирусные препараты для профилактики и лечения респираторных вирусов, кроме гриппа. Несмотря на прогресс, достигнутый в разработке пневмококковых и других антибактериальных вакцин и обширные усилия по разработке вакцин против респираторных вирусов, маловероятно, что в обозримом будущем появится эффективная комплексная система вакцинации против распространенных вирусных и бактериальных респираторных патогенов. Создание специфических противовирусных препаратов против различных групп респираторных вирусов, эффективных на поздней стадии инфекции, имеет низкую вероятность успеха. Следовательно, существует острая необходимость в разработке патогенетических препаратов, снижающих реакции врожденного иммунитета, ослабляющие факторы антибактериальной защиты при вирусной инфекции. Одним из возможных подходов может быть поиск лекарств, предотвращающих чрезмерную продукцию IFN на пике вирусной инфекции.Подавление избыточной передачи сигналов IFN может стать важным терапевтическим подходом к предотвращению как эффектов цитокинового шторма, так и развития вторичных бактериальных осложнений в областях, прилегающих к дыхательным путям [79, 82, 103-105].
Создание специфических противовирусных препаратов против различных групп респираторных вирусов, эффективных на поздней стадии инфекции, имеет низкую вероятность успеха. Следовательно, существует острая необходимость в разработке патогенетических препаратов, снижающих реакции врожденного иммунитета, ослабляющие факторы антибактериальной защиты при вирусной инфекции. Одним из возможных подходов может быть поиск лекарств, предотвращающих чрезмерную продукцию IFN на пике вирусной инфекции.Подавление избыточной передачи сигналов IFN может стать важным терапевтическим подходом к предотвращению как эффектов цитокинового шторма, так и развития вторичных бактериальных осложнений в областях, прилегающих к дыхательным путям [79, 82, 103-105].
Эта работа была поддержана грантом RSF-FWF № 18-45-05002 (подход VLP к борьбе с бактериальными инфекциями после гриппа).
Автор не преследует коммерческих или финансовых интересов.
Егоров А. Проблема бактериальных осложнений после респираторных вирусных инфекций. МИР Ж, 2018; 5 (1), 12-21, DOI: 10.18527 / 2500-2236-2018-5-1-12-21.
МИР Ж, 2018; 5 (1), 12-21, DOI: 10.18527 / 2500-2236-2018-5-1-12-21.
© Егоров, 2018. Это статья в открытом доступе, распространяемая в соответствии с условиями Международной общественной лицензии Creative Commons AttributionNonCommercial-ShareAlike 4.0 (CC-BY-NC-SA), которая разрешает неограниченное использование, распространение и воспроизведение на любом носителе при условии, что материал не используется в коммерческих целях при условии ссылки на автора и источник.
1. Инициатива «Битва с респираторными вирусами» (BRaVe).Всемирная организация здоровья. Доступно: http://www.who.int/influenza/patient_care/clinical/brave/en/#; http://www.who.int/mediacentre/factsheets/fs211/en/
2. Kilbourne ED. Пандемии гриппа ХХ века. Emerg Infect Dis 2006; 12 (1), 9-14. DOI: 10.3201 / eid1201.051254.
3. Cheng VC, To KK, Tse H, Hung IF, Yuen KY. Через два года после пандемии гриппа A / 2009 / h2N1: что мы узнали? Clin Microbiol Rev 2012; 25 (2), 223-63.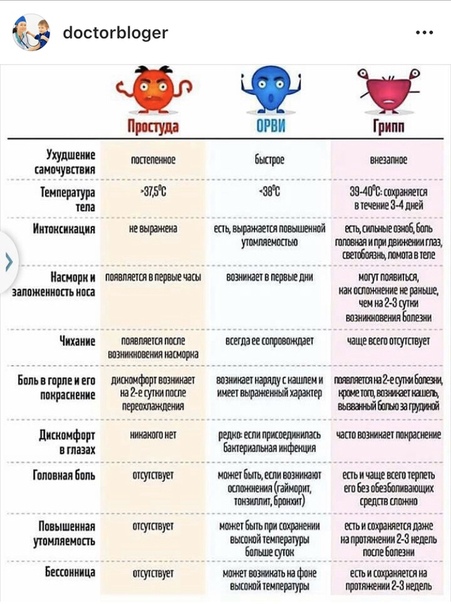 DOI: 10.1128 / CMR.05012-11.
DOI: 10.1128 / CMR.05012-11.
4. Оксфорд Дж. С., Сефтон А., Джексон Р., Иннес В., Дэниэлс Р. С., Джонсон Н. П.. Первая мировая война, возможно, привела к появлению «испанского» гриппа. Lancet Infect Dis 2002; 2 (2), 111-4. PubMed PMID: 11
2.
5. Брем В.В., Боллинг Г.Е., Каспер Э.Дж. Пандемия гриппа и вторичная пневмония в Кэмп-Фремонт, Калифорния. J Am Med Assoc, 1918; 71, 2138-44. DOI: 10.1001 / jama.1918.26020520007010b.
6. Таубенбергер Дж. К., Балтимор Д., Доэрти П. К., Маркель Х., Моренс Д. М., Вебстер Р. Г. и др.Реконструкция вируса гриппа 1918 года: неожиданные награды из прошлого. MBio 2012; 3 (5). DOI: 10.1128 / mBio.00201-12.
7. Моррис Д.Е., Клири Д.В., Кларк СК. Вторичные бактериальные инфекции, связанные с пандемиями гриппа. Front Microbiol 2017; 8, 1041. DOI: 10.3389 / fmicb.2017.01041.
8. Morens DM, Taubenberger JK, Fauci AS. Преобладающая роль бактериальной пневмонии как причины смерти при пандемическом гриппе: последствия для готовности к пандемическому гриппу.J Infect Dis 2008; 198 (7), 962-70. DOI: 10,1086 / 591708.
9. Чиен Ю.В., Клугман К.П., Моренс Д.М. Бактериальные патогены и смерть во время пандемии гриппа 1918 г. N Engl J Med 2009; 361 (26), 2582-3. DOI: 10.1056 / NEJMc0
6.
10. Brundage JF, Shanks GD. Смертность от бактериальной пневмонии во время пандемии гриппа 1918-19 гг. Emerg Infect Dis 2008; 14 (8), 1193-9. DOI: 10.3201 / eid1408.071313.
11. Вин М.К., Чен М.И., Баркхэм Т., Лин Ц., Тан А., Лин Р. и др.Бремя заболевания гриппом среди взрослых по подтипам после начальной эпидемии пандемии h2N1 в Сингапуре. Другие вирусы гриппа Respir 2011; 5 (6), е563-7. DOI: 10.1111 / j.1750-2659.2011.00282.x.
12. Поттер CW. История гриппа. J Appl Microbiol 2001; 91 (4), 572-9. PubMed PMID: 11576290.
13. Вибоуд К., Симонсен Л., Фуэнтес Р., Флорес Дж., Миллер М.А., Човелл Г. Глобальное влияние пандемии гриппа 1957–1959 гг. На смертность. J Infect Dis 2016; 213 (5), 738-45.DOI: 10.1093 / infdis / jiv534.
14. Eickhoff TC, Sherman IL, Serfling RE. Наблюдения за повышенной смертностью, связанной с эпидемическим гриппом. JAMA 1961; 176, 776-82. PubMed PMID: 13726091.
15. Хиллеман MR. Реалии и загадки вирусного гриппа человека: патогенез, эпидемиология и борьба. Вакцина 2002; 20 (25-26), 3068-87. PubMed PMID: 12163258.
16. Херс Дж. Ф., Мазурел Н., Малдер Дж. Бактериология и гистопатология дыхательных путей и легких при фатальном азиатском гриппе.Lancet 1958; 2 (7057), 1141-3. PubMed PMID: 13612141.
17. Гилл Дж. Р., Шенг З. М., Эли С.Ф., Гвине Д.Г., Бисли М.Б., Су Дж. И др. Легочные патологические находки фатальных вирусных инфекций пандемического гриппа A / h2N1 2009 г. Arch Pathol Lab Med 2010; 134 (2), 235-43. DOI: 10.1043 / 1543-2165-134.2.235.
18. Петерсдорф Р.Г., Фуско Дж. Дж., Хартер Д.Х., Олбринк В.С. Легочные инфекции, осложняющие азиатский грипп. AMA Arch Intern Med 1959; 103 (2), 262-72. PubMed PMID: 13616762.
19.Робертсон Л., Кейли Дж. П., Мур Дж. Важность Staphylococcus aureus при пневмонии во время эпидемии гриппа 1957 г. A. Lancet 1958; 2 (7040), 233-6. PubMed PMID: 13564806.
20. Михаэлис М., Дорр Х.В., Цинатл Дж. Мл. Новый вирус гриппа А свиного происхождения у людей: еще одна пандемия, стучащаяся в дверь. Med Microbiol Immunol 2009; 198 (3), 175-83. DOI: 10.1007 / s00430-009-0118-5.
21. Климов А., Симонсен Л., Фукуда К., Кокс Н. Эпиднадзор и влияние гриппа в США.Vaccine 1999; 17 Дополнение 1, S42-6. PubMed PMID: 10471179.
22. Тиллетт Х.Э., Смит Дж. В., Гуч CD. Чрезмерное количество смертей от гриппа в Англии и Уэльсе: возраст на момент смерти и подтвержденная причина. Int J Epidemiol 1983; 12 (3), 344-52. PubMed PMID: 6629624.
23. Линдсей М.И., мл., Херрманн Е.К., мл., Морроу Г.В., мл., Браун А.Л., мл. Гонконгский грипп: клинические, микробиологические и патологические особенности в 127 случаях. JAMA 1970; 214 (10), 1825-32. PubMed PMID: 5537337.
24.Ван Т.Т., Палезе П. Раскрытие тайны вируса свиного гриппа. Cell 2009; 137 (6), 983-5. DOI: 10.1016 / j.cell.2009.05.032.
25. Chertow DS, Memoli MJ. Бактериальная коинфекция при гриппе: общий обзор. JAMA 2013; 309 (3), 275-82. DOI: 10.1001 / jama.2012.194139.
26. Ли Э. Х., Ву С., Ли ЕС, Стаут А., Хэнсон Х., Кук Х. А. и др. Смертельные случаи, связанные с вирусом гриппа A 2009 h2N1 в Нью-Йорке. Clin Infect Dis 2010; 50 (11), 1498-504.DOI: 10,1086 / 652446.
27. Лукас С. Прогностические клинико-патологические особенности, полученные на основе систематического вскрытия трупов пациентов, умерших от инфекции гриппа A / h2N1 в пандемии 2009-10 в Великобритании. Оценка медицинских технологий 2010; 14 (55), 83-114. DOI: 10.3310 / hta14550-02.
28. Паласиос Г., Хорниг М., Цистерна Д., Савджи Н., Буссетти А.В., Капур В. и др. Коинфекция Streptococcus pneumoniae коррелирует с тяжестью пандемического гриппа h2N1. PLoS One 2009; 4 (12), е8540.DOI: 10.1371 / journal.pone.0008540.
29. Рэндольф А.Г., Вон Ф., Салливан Р., Рубинсон Л., Томпсон Б.Т., Юн Г. и др. Дети в критическом состоянии во время пандемии гриппа 2009-2010 гг. В США. Педиатрия 2011; 128 (6), е1450-8. DOI: 10.1542 / peds.2011-0774.
30. Живич А. Борьба с бактериальной устойчивостью: подходы, проблемы и возможности в поиске новых антибиотиков. Часть 1. Антибиотики, применяемые в клинической практике: механизмы действия и развитие резистентности бактерий.МИР Ж 2017; 4 (1), 31-51. DOI: 10.18527 / 2500-2236-2017-4-1-31-51.
31. Хасволд Дж., Сджодинг М., Поль К., Кук С., Хизи Р.С. Роль метапневмовируса человека у взрослого пациента в критическом состоянии. J Crit Care 2016; 31 (1), 233-7. DOI: 10.1016 / j.jcrc.2015.09.035.
32. Квон Ю.С., Пак С.Х., Ким М.А., Ким Х.Дж., Пак Дж.С., Ли М.И. и др. Риск смерти, связанный с респираторно-синцитиальным вирусом и инфекцией гриппа у взрослых. BMC Infect Dis 2017; 17 (1), 785. DOI: 10.1186 / s12879-017-2897-4.
33. Prasso JE, Deng JC. Поствирусные осложнения: бактериальная пневмония. Clin Chest Med 2017; 38 (1), 127-38. DOI: 10.1016 / j.ccm.2016.11.006.
34. Метерский М.Л., Мастертон Р.Г., Лоде Х., Файл TM, мл., Бабинчак Т. Эпидемиология, микробиология и рекомендации по лечению бактериальной пневмонии, осложняющей грипп. Int J Infect Dis 2012; 16 (5), е321-31. DOI: 10.1016 / j.ijid.2012.01.003.
35. Mulcahy ME, McLoughlin RM. Золотистый стафилококк и вирус гриппа А: партнеры в коинфекции.MBio 2016; 7 (6). DOI: 10.1128 / mBio.02068-16.
36. Сафеян Ф., Нахаи М.Р., Сейфи С.Дж., Кафил Х.С., Садеги Дж. Количественное определение Staphylococcus aureus, Streptococcus pneumoniae и Haemophilus influenzae у пациентов с новым вирусом гриппа A (h2N1) / 2009 и гриппом A / 2010. GMS Hyg Infect Control 2015; 10, Doc06. DOI: 10.3205 / dgkh000249.
37. Дженнингс Л.С., Андерсон Т.П., Бейнон К.А., Чуа А., Лэйнг Р.Т., Верно А.М. и др. Заболеваемость и характеристики вирусной внебольничной пневмонии у взрослых.Thorax 2008; 63 (1), 42-8. DOI: 10.1136 / thx.2006.075077.
38. Лидерот К., Ахл М., Озенци В. Вторичные бактериальные инфекции у пациентов с сезонным гриппом A и пандемией h2N1. Biomed Res Int 2013; 2013, 376219. DOI: 10.1155 / 2013/376219.
39. Чонмайтри Т., Дженнингс К., Головко Г., Ханипов К., Пименова М., Патель Дж. А. и др. Микробиота носоглотки у младенцев и изменения во время вирусной инфекции верхних дыхательных путей и острого среднего отита. PLoS One 2017; 12 (7), e0180630.DOI: 10.1371 / journal.pone.0180630.
40. Якобс Дж. Х., Вибоуд К., Тчетген Е. Т., Шварц Дж., Штайнер С., Симонсен Л. и др. Связь менингококковой инфекции с гриппом в США, 1989-2009 гг. PLoS One 2014; 9 (9), e107486. DOI: 10.1371 / journal.pone.0107486.
41. Брили Дж. К., Чаппелл К. Дж., Гэлбрейт С., Фантино Е., Гайдон Дж., Тозер С. и др. Колонизация носоглотки Streptococcus pneumoniae связана с усилением тяжести респираторно-синцитиальной вирусной инфекции у детей раннего возраста.Респирология 2018; 23 (2), 220-7. DOI: 10.1111 / resp.13179.
42. Hendaus MA, Jomha FA, Alhammadi AH. Вторичная бактериальная инфекция, вызванная вирусами: краткий обзор. Ther Clin Risk Manag 2015; 11, 1265-71. DOI: 10.2147 / TCRM.S87789.
43. Луи Дж. К., Рой-Берман А., Гуардия-Лабар Л., Бостон Э. Дж., Кианг Д., Падилла Т. и др. Риновирус, связанный с тяжелыми инфекциями нижних дыхательных путей у детей. Pediatr Infect Dis J 2009; 28 (4), 337-9. DOI: 10.1097 / INF.0b013e31818ffc1b.
44. Маллиа П., Футит Дж., Сотеро Р., Джепсон А., Контоли М., Трухильо-Торральбо МБ и др. Риновирусная инфекция вызывает деградацию антимикробных пептидов и вторичную бактериальную инфекцию при хронической обструктивной болезни легких. Am J Respir Crit Care Med 2012; 186 (11), 1117-24. DOI: 10.1164 / rccm.201205-0806OC.
45. Kloepfer KM, Lee WM, Pappas TE, Kang TJ, Vrtis RF, Evans MD, et al. Обнаружение патогенных бактерий при риновирусной инфекции связано с усилением респираторных симптомов и обострениями астмы.J Allergy Clin Immunol 2014; 133 (5), 1301-7, 7 е1-3. DOI: 10.1016 / j.jaci.2014.02.030.
46. Корппи М., Лейнонен М., Макела PH, Лауниала К. Участие бактерий в вирусной инфекции парагриппа у детей. Scand J Infect Dis 1990; 22 (3), 307-12. PubMed PMID: 2164707.
47. Verkaik NJ, Nguyen DT, de Vogel CP, Moll HA, Verbrugh HA, Jaddoe VW, et al. Воздействие Streptococcus pneumoniae связано с сероконверсией метапневмовируса человека и повышенной восприимчивостью к инфекции HMPV in vitro.Clin Microbiol Infect 2011; 17 (12), 1840-4. DOI: 10.1111 / j.1469-0691.2011.03480.x.
48. Self WH, Williams DJ, Zhu Y, Ampofo K, Pavia AT, Chappell JD, et al. Выявление респираторных вирусов у детей и взрослых: сравнение бессимптомных контролей и пациентов с внебольничной пневмонией. J Infect Dis 2016; 213 (4), 584-91. DOI: 10.1093 / infdis / jiv323.
49. Кацурада Н., Сузуки М., Аошима М., Яэгаши М., Ишифудзи Т., Асо Н. и др. Влияние вирусных инфекций на смертность от пневмонии у взрослых сложное: проспективное многоцентровое обсервационное исследование.BMC Infect Dis 2017; 17 (1), 755. DOI: 10.1186 / s12879-017-2858-у.
50. Юнг Х.С., Кан Б.Дж., Ра С.В., Со К.В., Джегал Й., Джун Дж. Б. и др. Выявление патогенов, вызывающих бактериальную пневмонию, у пациентов с респираторной вирусной инфекцией. Tuberc Respir Dis (Сеул) 2017; 80 (4), 358-67. DOI: 10.4046 / trd.2017.0044.
51. Хупер Л.В., Литтман Д.Р., Макферсон А.Дж. Взаимодействие между микробиотой и иммунной системой. Наука 2012; 336 (6086), 1268-73. DOI: 10.1126 / наука.1223490.
52. Чарлсон Е.С., Биттингер К., Хаас А.Р., Фицджеральд А.С., Франк И., Ядав А. и др. Топографическая преемственность бактериальных популяций в дыхательных путях здорового человека. Am J Respir Crit Care Med 2011; 184 (8), 957-63. DOI: 10.1164 / rccm.201104-0655OC.
53. Богерт Д., Де Гроот Р., Херманс П.В. Колонизация Streptococcus pneumoniae: ключ к пневмококковой инфекции. Lancet Infect Dis 2004; 4 (3), 144-54. DOI: 10.1016 / S1473-3099 (04) 00938-7.
54.Bosch AA, Biesbroek G, Trzcinski K, Sanders EA, Bogaert D. Взаимодействие с вирусами и бактериями в верхних дыхательных путях. PLoS Pathog 2013; 9 (1), e1003057. DOI: 10.1371 / journal.ppat.1003057.
55. Ян Х, Стойкерс Л., Фориер К., Сюн Р., Брекманс К., Ван Рит К. и др. Благоприятная роль нейраминидазы в проникновении вируса гриппа через дыхательную слизь. PLoS One 2014; 9 (10), e110026. DOI: 10.1371 / journal.pone.0110026.
56. Avadhanula V, Rodriguez CA, Devincenzo JP, Wang Y, Webby RJ, Ulett GC, et al.Респираторные вирусы усиливают адгезию бактериальных патогенов к респираторному эпителию в зависимости от вида вируса и типа клеток. J Virol 2006; 80 (4), 1629-36. DOI: 10.1128 / JVI.80.4.1629-1636.2006.
57. Ли Н, Рен А., Ван Х, Фан Х, Чжао И, Гао Г.Ф. и др. Вирусная нейраминидаза гриппа вызывает бактериальную коинфекцию через экспрессию рецепторов клетки-хозяина, опосредованную TGF-бета. Proc Natl Acad Sci U S A 2015; 112 (1), 238-43. DOI: 10.1073 / pnas.1414422112.
58.Карсон Дж. Л., Кольер А. М., Ху СС. Приобретенные дефекты ресничек носового эпителия у детей с острыми вирусными инфекциями верхних дыхательных путей. N Engl J Med 1985; 312 (8), 463-8. DOI: 10.1056 / NEJM198502213120802.
59. Питтет Л.А., Холл-Стодли Л., Рутковски М.Р., Хармсен АГ. Инфекция вируса гриппа снижает мукоцилиарную скорость в трахее и клиренс Streptococcus pneumoniae. Am J Respir Cell Mol Biol 2010; 42 (4), 450-60. DOI: 10.1165 / rcmb.2007-0417OC.
60. Sun K, Metzger DW.Подавление антибактериальной защиты легких интерфероном-гамма во время выздоровления от инфекции гриппа. Nat Med 2008; 14 (5), 558-64. DOI: 10,1038 / нм1765.
61. Shahangian A, Chow EK, Tian X, Kang JR, Ghaffari A, Liu SY, et al. IFNs типа I опосредуют развитие бактериальной пневмонии после гриппа у мышей. J Clin Invest 2009; 119 (7), 1910-20. DOI: 10.1172 / JCI35412.
62. Накамура С., Дэвис К.М., Вайзер Дж. Н.. Синергетическая стимуляция интерферонов типа I во время коинфекции вирусом гриппа способствует колонизации Streptococcus pneumoniae у мышей.J Clin Invest 2011; 121 (9), 3657-65. DOI: 10,1172 / JCI57762.
63. Кудва А., Шеллер Э.В., Робинсон К.М., Кроу С.Р., Чой С.М., Слайт С.Р. и др. Грипп A подавляет Th27-опосредованную защиту хозяина от бактериальной пневмонии у мышей. J Immunol 2011; 186 (3), 1666-74. DOI: 10.4049 / jimmunol.1002194.
64. Тиан X, Сюй Ф., Лунг В.Й., Мейерсон С., Гаффари А.А., Ченг Дж. И др. Поли I: C повышает восприимчивость к вторичным легочным инфекциям, вызываемым грамположительными бактериями. PLoS One 2012; 7 (9), e41879.DOI: 10.1371 / journal.pone.0041879.
65. Astry CL, Jakab GJ. Иммунные комплексы, индуцированные вирусом гриппа, подавляют фагоцитоз альвеолярных макрофагов. J Virol 1984; 50 (2), 287-92. PubMed PMID: 6708169.
66. Franke-Ullmann G, Pfortner C, Walter P, Steinmuller C., Lohmann-Matthes ML, Kobzik L, et al. Изменение функции легочных макрофагов инфекцией респираторно-синцитиального вируса in vitro. J Immunol 1995; 154 (1), 268-80. PubMed PMID: 7995946.
67.Jakab GJ. Иммунное нарушение фагоцитоза альвеолярных макрофагов при пневмонии, вызванной вирусом гриппа. Am Rev Respir Dis 1982; 126 (5), 778-82. DOI: 10.1164 / arrd.1982.126.5.778.
68. Warnking K, Klemm C, Loffler B, Niemann S, van Kruchten A, Peters G, et al. Суперинфекция Staphylococcus aureus подавляет индуцированную вирусом гриппа передачу сигналов IFN типа I за счет нарушения димеризации STAT1-STAT2. Cell Microbiol 2015; 17 (3), 303-17. DOI: 10,1111 / cmi.12375.
69.de Steenhuijsen Piters WA, Heinonen S, Hasrat R, Bunsow E, Smith B, Suarez-Arrabal MC и др. Микробиота носоглотки, транскриптом хозяина и тяжесть заболевания у детей с респираторно-синцитиальной вирусной инфекцией. Am J Respir Crit Care Med 2016; 194 (9), 1104-15. DOI: 10.1164 / rccm.201602-0220OC.
70. Jia L, Xie J, Zhao J, Cao D, Liang Y, Hou X и др. Механизмы сопутствующих бактериальных инфекций, связанных с тяжелой смертностью, после инфицирования вирусом гриппа. Front Cell Infect Microbiol 2017; 7, 338.DOI: 10.3389 / fcimb.2017.00338.
71. Джеймисон А.М., Пашман Л., Ю. С., Гамрад П., Гомер Р. Дж., Деккер Т. и др. Роль защиты тканей при летальной респираторной вирусно-бактериальной коинфекции. Наука 2013; 340 (6137), 1230-4. DOI: 10.1126 / science.1233632.
72. Ли Л.Н., Диас П., Хан Д., Юн С., Ши А., Захаров В. и др. Мышиная модель летального синергизма между вирусом гриппа и Haemophilus influenzae. Am J Pathol 2010; 176 (2), 800-11. DOI: 10.2353 / ajpath.2010.0.
73. McCullers JA. Совместное патогенез вирусов гриппа с бактериями в легких. Nat Rev Microbiol 2014; 12 (4), 252-62. DOI: 10,1038 / nrmicro3231.
74. Трипати С., Гарсиа-Састре А. Противовирусный врожденный иммунитет через призму системной биологии. Virus Res 2016; 218, 10-7. DOI: 10.1016 / j.virusres.2015.11.024.
75. Бреннан К., Боуи АГ. Активация вирусами рецепторов распознавания образов хозяина. Curr Opin Microbiol 2010; 13 (4), 503-7.DOI: 10.1016 / j.mib.2010.05.007.
76. Чен X, Лю С., Горая М.Ю., Мааруф М., Хуанг С., Чен Дж.Л. Иммунный ответ хозяина на инфекцию вирусом гриппа А. Фронт Иммунол 2018; 9, 320. DOI: 10.3389 / fimmu.2018.00320.
77. Шим Дж. М., Ким Дж., Тенсон Т., Мин Дж. Я., Кайнов Д.Е. Инфекция вирусом гриппа, интерфероновый ответ, вирусный контрреагент и апоптоз. Вирусы 2017; 9 (8), 223. DOI: 10.3390 / v23.
78. Андреакос Э., Салагянни М, Галани И.Е., Кольцида О.Интерферон-лямбды: передовые стражи иммунитета и гомеостаза в дыхательных путях. Фронт Иммунол 2017; 8, 1232. DOI: 10.3389 / fimmu.2017.01232.
79. Горицка М., Дюрант Л. Р., Перейра С., Салек-Ардакани С., Опеншоу П. Дж., Йоханссон С. Передача сигналов рецептора альфа / бета интерферона усиливает раннюю продукцию провоспалительных цитокинов в легких во время респираторно-синцитиальной вирусной инфекции. J Virol 2014; 88 (11), 6128-36. DOI: 10.1128 / JVI.00333-14.
80. Доэрти П.С., Тернер С.Дж., Уэбби Р.Г., Томас П.Г.Грипп и вызов иммунологии. Нат Иммунол 2006; 7 (5), 449-55. DOI: 10,1038 / NI1343.
81. Пейрис Дж. С., Ю. В. К., Люнг К. В., Чунг С. Ю., Нг В. Ф., Николлс Дж. М. и др. Повторное появление смертельного человеческого гриппа A подтипа H5N1. Lancet 2004; 363 (9409), 617-9. DOI: 10.1016 / S0140-6736 (04) 15595-5.
82. Макрис С., Полсен М., Йоханссон С. Интерфероны типа I как регуляторы воспаления легких. Фронт Иммунол 2017; 8, 259. DOI: 10.3389 / fimmu.2017.00259.
83.Шривастава Б., Блажеевская П., Хессманн М., Брудер Д., Гефферс Р., Мауэль С. и др. Генетический фон хозяина сильно влияет на реакцию на инфекции вируса гриппа А. PLoS One 2009; 4 (3), е4857. DOI: 10.1371 / journal.pone.0004857.
84. Дэвидсон С., Кротта С., МакКейб TM, Вак А. Патогенный потенциал интерферона алфавита при острой гриппозной инфекции. Nat Commun 2014; 5, 3864. DOI: 10.1038 / ncomms4864.
85. Броерс С.Дж., Гемке Р.Дж., Вейерман М.Э., ван дер Слуис К.Ф., ван Фурт А.М.Повышенная выработка провоспалительных цитокинов у детей с синдромом Дауна при стимуляции живым вирусом гриппа А. J Clin Immunol 2012; 32 (2), 323-9. DOI: 10.1007 / s10875-011-9625-4.
86. Rynda-Apple A, Робинсон KM, Alcorn JF. Грипп и бактериальная суперинфекция: освещение иммунологических механизмов заболевания. Infect Immun 2015; 83 (10), 3764-70. DOI: 10.1128 / IAI.00298-15.
87. Ли Б., Робинсон К.М., МакХью К.Дж., Шеллер Е.В., Мандалапу С., Чен С. и др.Интерферон типа I, индуцированный гриппом, увеличивает восприимчивость к грамотрицательной и грамположительной бактериальной пневмонии у мышей. Am J Physiol Lung Cell Mol Physiol 2015; 309 (2), Л158-67. DOI: 10.1152 / ajplung.00338.2014.
88. Шлихе С., Флинн Е.К., Вилагос Б., Ричсон Ю., Сваминантан С., Босняк Б. и др. Метилтрансфераза Setdb2 опосредует вирус-индуцированную чувствительность к бактериальной суперинфекции. Нат Иммунол 2015; 16 (1), 67-74. DOI: 10.1038 / NI.3046.
89. Кроц Д. Н., Аллен Р. М., Шаллер М. А., Кавалларо К., Ито Т., Кункель С. Л..Эпигенетическая регуляция макрофагов, индуцированная интерфероном I типа, подавляет врожденный и адаптивный иммунитет при острой респираторной вирусной инфекции. PLoS Pathog 2015; 11 (12), e1005338. DOI: 10.1371 / journal.ppat.1005338.
90. Цао Дж., Ван Д., Сюй Ф., Гун Й., Ван Х., Сун З. и др. Активация передачи сигналов IL-27 способствует развитию постгриппозной пневмококковой пневмонии. EMBO Mol Med 2014; 6 (1), 120-40. DOI: 10.1002 / emmm.201302890.
91. Ли В., Мольтедо Б., Моран TM. Индукция интерферона I типа во время инфицирования вирусом гриппа увеличивает восприимчивость к вторичной инфекции Streptococcus pneumoniae за счет отрицательной регуляции гаммадельта-Т-клеток.J Virol 2012; 86 (22), 12304-12. DOI: 10.1128 / JVI.01269-12.
92. Dejager L, Vandevyver S, Ballegeer M, Van Wonterghem E, An LL, Riggs J, et al. Фармакологическое подавление передачи сигналов интерферона типа I защищает мышей от летального сепсиса. J Infect Dis 2014; 209 (6), 960-70. DOI: 10.1093 / infdis / jit600.
93. Хубер В. К., Пелтола В., Айверсон А. Р., МакКуллерс Дж. Вклад вакцинно-индуцированного иммунитета либо в HA, либо в NA компонент вирусов гриппа ограничивает вторичные бактериальные осложнения.J Virol 2010; 84 (8), 4105-8. DOI: 10.1128 / JVI.02621-09.
94. Chaussee MS, Sandbulte HR, Schuneman MJ, Depaula FP, Addengast LA, Schlenker EH, et al. Инактивированные и живые аттенуированные вакцины против гриппа защищают мышей от гриппа: суперинфекций Streptococcus pyogenes. Вакцина 2011; 29 (21), 3773-81. DOI: 10.1016 / j.vaccine.2011.03.031.
95. Ли С.Е., Эйк А., Блум М.С., Брандейдж Дж.Ф. Иммунизация против гриппа и последующая диагностика стрептококковой болезни группы А среди U.С. Стажеры армии, 2002-2006 гг. Вакцина 2008; 26 (27-28), 3383-6. DOI: 10.1016 / j.vaccine.2008.04.041.
96. Белше РБ, Грубер WC. Профилактика среднего отита у детей с помощью живой аттенуированной вакцины против гриппа, вводимой интраназально. Pediatr Infect Dis J 2000; 19 (5 доп.), С66-71. PubMed PMID: 10821474.
97. McCullers JA. Влияние противовирусного лечения на исход вторичной бактериальной пневмонии после гриппа. J Infect Dis 2004; 190 (3), 519-26. DOI: 10,1086 / 421525.
98. Hayden FG, Osterhaus AD, Treanor JJ, Fleming DM, Aoki FY, Nicholson KG, et al. Эффективность и безопасность занамивира, ингибитора нейраминидазы, при лечении гриппозавирусных инфекций. GG167 Исследовательская группа по гриппу. N Engl J Med 1997; 337 (13), 874-80. DOI: 10.1056 / NEJM199709253371302.
99. Кайзер Л., Кин О. Н., Хаммонд Дж. М., Эллиотт М., Хайден Ф. Г.. Влияние занамивира на использование антибиотиков при респираторных осложнениях после острого гриппа у подростков и взрослых.Arch Intern Med 2000; 160 (21), 3234-40. PubMed PMID: 11088083.
100. Кайзер Л., Уот С., Миллс Т., Махони П., Уорд П., Хайден Ф. Влияние лечения осельтамивиром на связанные с гриппом осложнения со стороны нижних дыхательных путей и госпитализации. Arch Intern Med 2003; 163 (14), 1667-72. DOI: 10.1001 / archinte.163.14.1667.
101. Николсон К.Г., Аоки Ф.Й., Остерхаус А.Д., Троттье С., Каревич О., Мерсье С.Х. и др. Эффективность и безопасность осельтамивира при лечении острого гриппа: рандомизированное контролируемое исследование.Группа исследователей лечения гриппа с ингибиторами нейраминидазы. Lancet 2000; 355 (9218), 1845-50. PubMed PMID: 10866439.
102. Смит AM, Huber VC. Неожиданное влияние вакцин на вторичные бактериальные инфекции после гриппа. Вирусный Иммунол 2018; 31 (2), 159-73. DOI: 10.1089 / vim.2017.0138.
103. Zang N, Xie X, Deng Y, Wu S, Wang L, Peng C и др. Опосредованное ресвератролом уменьшение гамма-интерферона предотвращает воспаление дыхательных путей и гиперреактивность дыхательных путей у мышей с иммунодефицитом, инфицированных респираторно-синцитиальным вирусом.J Virol 2011; 85 (24), 13061-8. DOI: 10.1128 / JVI.05869-11.
104. Баумгарт Н., Келсо А. Блокада гамма-интерферона in vivo влияет на гуморальный и местный клеточный иммунный ответ в ткани легких, вызванный вирусом гриппа. J Virol 1996; 70 (7), 4411-8. PubMed PMID: 8676464.
105. Вольф С., Джонсон С., Первитасари О., Махалингам С., Трипп Р.А. Нацеленность на провоспалительный фактор CCL2 (MCP-1) с помощью Биндарита для лечения гриппа A (H7N9). Clin Transl Immunology 2017; 6 (3), е135.DOI: 10.1038 / cti.2017.8.
Лечение гриппа и ОРВИ у детей препаратом Кагоцел ® — Просмотр полного текста
В это неинтервенционное обсервационное исследование вошли 80 пациентов в возрасте от 3 до 11 лет, которые были госпитализированы с симптомами гриппа и ОРВИ в любое время из начало заболевания (до 15 дней) и кому назначен индуктор интерферона Кагоцел в качестве противовирусного препарата.
Диагноз гриппа и ОРВИ подтвержден в соответствии с руководящими принципами Всемирной организации здравоохранения (ВОЗ) по фармакологическому лечению пандемического гриппа A (h2N1) 2009 и других вирусов гриппа.
Все обследования пациентов проводятся в соответствии с местной повседневной клинической практикой и местными и международными стандартами лечения.
После окончания лечения были собраны и проанализированы следующие данные:
- демография
- степень тяжести заболевания
- данных анамнеза (данные о вакцинации против гриппа в текущем сезоне; посещение дошкольных учреждений; предыдущие контакты с больным гриппом / ОРВИ; предыдущая противовирусная терапия по текущему эпизоду заболевания; сопутствующие заболевания)
- температура тела (утро / вечер)
- озноб и лихорадка (совокупная оценка по всем симптомам: 0 — нет симптомов, 1 — легкая, 2 — умеренная, 3 — тяжелая)
- Симптом интоксикации (совокупный балл по всем симптомам: 0 — нет симптомов, 1 — легкая, 2 — умеренная, 3 — тяжелая)
- катаральные симптомы (совокупная оценка по всем симптомам: 0 — нет симптомов, 1 — легкие, 2 — умеренные, 3 — тяжелые)
- сроки: начало болезни, первый визит к врачу, начало лечения, продолжительность заболевания
- определение возбудителя методом ПЦР (при поступлении больных и их выписке через 5-6 дней от начала терапии)
- противовирусная терапия (доза Кагоцела в зависимости от возраста)
- Симптоматическое лечение текущего эпизода гриппа или ОРВИ до и во время госпитализации пациента
- бактериальных обострений (да / нет)
- Лечение бактериальных обострений (название препарата)
- нежелательных явлений
(PDF) КАК ОТЛИЧИТЬ БАКТЕРИАЛЬНУЮ ИНФЕКЦИЮ ОТ ВИРУСНОЙ И ЛЕЧИТЬ
M.Д. Бакрадзе, И.В. Чащина
Научный центр здоровья детей, Москва, Российская Федерация
Как отличить бактериальную инфекцию от вирусной и как ее лечить
Имя автора:
Бакрадзе Майя Джемаловна, кандидат медицинских наук, руководитель отдела диагностики и медицинской реабилитации
отдел ГКЗД РАМН
Адрес: 119991, г. Москва, Ломоносовский проспект, д. 2, тел .: +7 (495) 967-14-21
Статья принята: 04.03.2013. Принята к публикации:
Статья посвящена самой актуальной проблеме детства — лихорадке, причины которой
и, как следствие, правильная тактика ведения пациента трудно определить. Авторы
представляют не только собственный опыт клинической и лабораторной дифференциальной диагностики вирусных
и бактериальных инфекций, но и данные мировой литературы. Перечислены критерии низкого риска бактериальной инфекции
, позволяющие избежать назначения антибактериальных препаратов.Особое внимание
уделяется наиболее важным маркерам воспаления при различных лихорадочных заболеваниях и признакам тяжелой бактериальной инфекции
и лихорадки без явного очага инфекции. Авторы
ирекомендуют использовать экспресс-тесты для подтверждения наличия бактериальной инфекции. Проанализированы показания к назначению антибактериальной терапии
.
Ключевые слова: лихорадка, бактериальная инфекция, вирусная инфекция, дифференциальный диагноз, принципы лечения,
ребенка.
Проблема диагностики инфекционных заболеваний в педиатрии присутствует на протяжении многих
веков. Большинство острых заболеваний у детей сопровождаются лихорадкой, которая помогает заподозрить инфекцию
, хотя этого недостаточно для определения вирусной или бактериальной инфекции.
Родители больше всего боятся лихорадки; это частая и зачастую единственная причина госпитализации
(часто необоснованная). Большинство родителей считают, что важно только понизить температуру
, но врачи не должны следовать этому мнению.
Уровень температуры не всегда коррелирует с тяжестью заболевания. Например, опасные для жизни респираторные вирусные инфекции
часто сопровождаются более высокой температурой, чем угрожающие жизни
пневмонии. Для современного педиатра при лихорадке важна не столько повышение температуры тела
, сколько его причина, потому что при бактериальной инфекции и гриппе можно назначить этиотропную терапию
, а при большинстве вирусных инфекций следует быть
лечиться патогенетическими препаратами или, в большинстве случаев, только симптоматическими препаратами.
Помимо лихорадки, многие инфекции имеют характерные клинические симптомы, которые позволяют достаточно точно определить этиологию
. Среди них основные «детские» экзантематические
инфекции, коклюш, дифтерия, воспалительные заболевания ряда органов (острый средний отит,
лимфаденит, гепатит). Ряд инфекций легко диагностируется с помощью анализов крови и мочи
(например, инфекции мочевыводящих путей) или экспресс-тестов. В настоящее время возможно проведение экспресс-диагностики
стрептококкового тонзиллита, гриппа, адено- и ротавирусных гастроэнтеритов.Нехватка
информации и медленное внедрение экспресс-тестов в широкое использование являются серьезными проблемами.
Дифференциальная диагностика вирусных и бактериальных заболеваний по клиническим данным часто бывает затруднена
из-за схожести клинических проявлений (например, при респираторной патологии
). Также сложно установить диагноз «бактериемия», так как часто отсутствуют какие-либо симптомы
, кроме лихорадки. Это серьезная проблема, поскольку бактериемия часто предшествует развитию таких
тяжелых инвазивных бактериальных инфекций (SBI), как менингококковая, пневмококковая инфекция и гемофильная инфекция типа b
.
Сложность клинической диагностики бактериальных инфекций (не более 5-10% в структуре
острых лихорадок) заставляет врачей прописывать антибиотики «на всякий случай». На практике антибактериальный
ОРВИ — причины, симптомы и лечение
Каждый из нас не раз в жизни сталкивался с диагнозом ОРВИ. Это сокращение расшифровывается как «острая респираторная вирусная инфекция». В народе болезнь называется просто простудой.
ОРВИ объединяет ряд воспалительных заболеваний, для которых характерны следующие симптомы:
- возбудитель — вирус;
- путь заражения воздушно-капельным путем;
- первичное поражение дыхательной системы;
- быстрое развитие и острое течение болезни, которое длится относительно недолго.
Что нужно знать о болезни:
- ОРВИ провоцируют вирусы парагриппа, риновирусы, реовирусы, аденовирусы и многие другие, всего более 200 видов.
- Все они легко передаются воздушно-капельным путем, а также при контакте с кожей. От момента заражения до развития болезни проходит относительно короткое время, около 2 суток.
- При дыхании и чихании пациенты выделяют в воздух болезнетворные микроорганизмы, которые попадают на слизистую оболочку верхних дыхательных путей здоровых людей, оседают там и начинают вырабатывать токсины.Они распространяются по организму и вызывают общую интоксикацию, проявляющуюся в виде головных болей, повышения температуры тела, болей в суставах и мышцах. Также возникают респираторные симптомы: насморк, кашель, боль в горле.
- В остром периоде развития болезни человек чувствует себя подавленным, не может полноценно работать.
Факторы риска
Чаще всего ОРВИ заболевают дети, так как их иммунная система еще только формируется. Заболевание бывает довольно тяжелым, часто возникают осложнения.Взрослые, как правило, реже болеют, иногда у них даже не поднимается температура. Но если ОРВИ диагностировали несколько раз за сезон, нужно бить тревогу. Следует обратиться к врачу и пройти дополнительные обследования.
Многие не относятся серьезно к этому вирусному заболеванию, носят его на ногах, продолжают ходить на работу даже при повышении температуры. Однако не стоит пренебрегать вирусной инфекцией. Сначала больной заражает других. Во-вторых, ОРВИ на ногах чревато серьезными осложнениями, такими как средний отит, синусит, миокардит, пневмония, менингит, то есть на почве вирусной инфекции развивается бактериальная инфекция.Лечение этих заболеваний длительное и дорогое, часто показана госпитализация. Особенно опасно ОРВИ для людей, которые имеют хронические заболевания, ослабленный иммунитет, много работают и плохо питаются.
Осложнения
Сколько дней длится ОРВИ? Обычно острый период вирусного заболевания проходит через 3-4 дня, постепенно исчезают симптомы, исчезает ангина, уменьшается насморк. Но если по истечении 7 дней от начала заболевания симптоматика продолжает оставаться ярко выраженной, возможно появление осложнения.Вирус активно размножается в дыхательных путях, подавляя мерцательный эпителий, который действует как своего рода фильтр легких. Следовательно, в этот период другие вирусы и бактерии могут беспрепятственно проникать в легкие и другие органы. Часто осложнения проходят бессимптомно, но они коварны вдвойне, так как сильно снижают иммунитет.
После ОРВИ врачи могут констатировать развитие многих серьезных заболеваний.
- Самый частый диагноз — бронхит, воспалительный процесс в бронхах.Сопровождается глубоким кашлем, одышкой, повышенной потливостью. При этом не всегда поднимается температура, и кашель, сначала сухой, слезливый, со временем переходит в мокрый. В крайнем случае развивается гнойный бронхит.
- Синусит — это воспаление гайморовых пазух. Подозрение на нее возникает при жалобах больного на ноющую головную боль, стойкую заложенность носа, нарушение носового дыхания, выделения. Температура держится на уровне 37 °. Если не лечить, инфекция может распространиться дальше, что особенно опасно для детей.У взрослых острое состояние может перейти в хроническое.
- Одно из самых опасных осложнений — пневмония, воспаление легочной ткани. Его симптомы (кашель, одышка) похожи на бронхит, но температура держится дольше, наблюдается общая упадок сил. Для подтверждения подозрения на пневмонию назначается рентгенологическое исследование. Лечение длится очень долго, используются сильные антибиотики, показана госпитализация.
- Миокардит — это воспаление сердечной мышцы (миокарда).Часто возникает даже после острой респираторной вирусной инфекции, протекающей в легкой форме. Проявляется общей слабостью, одышкой, нарушениями сердечного ритма. Без надлежащего лечения грозит хроническим заболеванием сердца.
- Когда инфекция из носа переходит в сторону уха, может появиться средний отит, воспаление слизистой оболочки среднего уха и барабанной перепонки. В остром периоде возникают сильные боли, поднимается температура. Без должного лечения ухудшается слух, а при повреждении слухового нерва он может полностью исчезнуть.
- Опасным осложнением ОРВИ является пиелонефрит — воспалительный процесс в почках, характерными признаками которого являются боли в области поясницы. Однако у взрослых заболевание может пройти бессимптомно. Диагноз ставится на основании анализа мочи, показывающего повышенное содержание лейкоцитов.
- Менингит, воспаление слизистой оболочки головного или спинного мозга, может быть смертельным осложнением.
Подготовка к визиту / визиту к врачу
При развитии ОРВИ у детей родители вызывают врача на дом или обращаются в поликлинику.Но большинство взрослых игнорируют простуду. В лучшем случае их лечат дома, в худшем — по советам друзей или по телевизионной рекламе они принимают лекарства и продолжают ходить на работу. В результате по вине самостоятельно назначенных препаратов возникают хронические патологии, осложнения, аллергия, кишечные расстройства.
SARS не так безопасен, как кажется, из-за его воздействия. Врачи настоятельно рекомендуют бороться с ним под наблюдением специалистов и не заниматься самолечением.
Простуда особенно коварна по отношению к пожилым людям и людям с хроническими заболеваниями.SARS вызывается разными вирусами, в каждом случае проявляющими себя по-разному. Только врач способен поставить точный диагноз и выбрать правильную схему лечения. Человек может вызвать терапевта на дом, если он не может прийти на прием из-за следующих симптомов:
- температура 38 ° и выше;
- кумулятивные признаки ОРВИ и гриппа во время эпидемий;
- сильная боль в позвоночнике и суставах;
- повышенное или пониженное артериальное давление, головокружение;
- сильная тошнота и рвота, диарея.
Если температура ниже 38 °, но пациент не может явиться в больницу по причинам, перечисленным выше, он также имеет право вызвать на дом врача с ОРВИ.
Во время осмотра дома или в клинике врач спрашивает пациента о симптомах, длительности температуры, измеряет давление, пальпирует живот и периферические лимфатические узлы, осматривает кожу, слизистые оболочки, постукивает и слушает грудь, сердце и измеряет частоту дыхания.
Диагностика ОРВИ
Врачи диагностируют ОРВИ на основании жалоб пациента и визуального осмотра. Дополнительно назначают анализы мочи и крови. Госпитализация обычно не требуется. Если человек соблюдает рекомендации врача, в домашних условиях инфекция проходит довольно быстро. Поскольку заболеваемость ОРВИ чаще всего носит эпидемический характер, врачи не пытаются выявить конкретный возбудитель.
На этапе диагностики важно не путать ОРВИ с гриппом, так как симптомы очень похожи.
- Обычно ОРВИ развивается постепенно.
- Вначале появляется общая слабость, ощущение слабости, насморк, боль в горле, практически сразу появляется охриплость голоса, может возникнуть головная боль и подняться температура.
- Грипп, в отличие от ОРВИ, всегда начинается очень остро, с сильной головной боли, высокой температуры, болей в глазах, сильных болей в суставах и мышцах.
- Часто человек не может встать с постели из-за слабости и головокружения.
- Только через несколько дней, когда боли проходят и температура снижается, появляется насморк или кашель (катаральные проявления).
В любом случае при наличии вышеперечисленных симптомов самодиагностикой заниматься нельзя. Вам нужно обратиться к врачу.
Как лечить ОРВИ
При ОРВИ рекомендуется постельный режим. Пейте много жидкости. При повышении температуры выше 38,5 ° необходимо принимать жаропонижающие препараты. Остальные лекарства должен назначить врач.
При ОРВИ антибиотики не назначают. Они не действуют против вирусов, а только перегружают печень. Применение таких препаратов целесообразно, если бактериальная инфекция развивается на фоне вирусной инфекции.
- Основная рекомендация врачей при ОРВИ — много пить, чтобы не допустить обезвоживания. Слизистые оболочки выполняют важную функцию — они принимают на себя первый удар, задерживая вирусы. Если слизистая оболочка слишком сухая, она не может выполнять свою работу, и вирусы снова и снова попадают в организм.Слизь в носу, мокрота в бронхах — это тоже защитная реакция организма. Для образования этих веществ также требуется влага, если ее недостаточно, не стоит даже рассчитывать на быстрое восстановление. Влага также теряется при повышении температуры. При простуде рекомендуется выпивать не менее двух литров жидкости в день: теплые травяные чаи, морсы, компоты. Не стоит употреблять алкоголь, кофе и газировку, потому что они имеют обратный эффект — выводят жидкость.
- Важно контролировать влажность в помещении.В квартирах с централизованным отоплением этот показатель иногда опускается до 15–20%, что приводит к пересыханию слизистой оболочки. С этой же целью рекомендуется полоскать нос изотоническим (0,9%) физиологическим раствором, а также полоскать горло, так как соль имеет свойство удерживать влагу.
- Если общее состояние плохое, сильно болят голова и горло, при ОРВИ можно принимать недорогие препараты на основе ибупрофена или парацетамола, которые также обладают свойством понижать температуру.
- Рекомендуется чаще проветривать комнату, ведь вирусы активно размножаются в сухой и теплой среде. Лучше побыть дома несколько дней, чтобы дать организму возможность направить все силы на борьбу с вирусом. Простуда на ногах растянет время болезни, а это грозит осложнениями.
- Беременным женщинам следует особенно внимательно относиться к своему здоровью. При первых симптомах ОРВИ следует обратиться к врачу.Самолечение категорически запрещено. Действительно, некоторые препараты, особенно в первом триместре беременности, опасны для малыша.
Врачи предупреждают об опасности приема даже самых эффективных противовирусных препаратов при ОРВИ без рекомендации терапевта. Это не всегда дает желаемый результат, а побочные эффекты вполне возможны.
Как вылечить ОРВИ домашними средствами
Существует множество народных средств от простуды, многие из них очень эффективны.Однако сегодня они не всегда работают самостоятельно, поскольку вирусы очень быстро мутируют и адаптируются.
Врачи поддерживают совет бабушки пить чай с малиной, молоко с медом и маслом. Очень желательно пить теплые напитки при простуде. Имбирь эффективно борется с вирусами. Чай с имбирем, медом и лимоном — отличное согревающее средство в холодное время года. Он укрепляет иммунную систему, обладает потогонными и противовоспалительными свойствами.
Мифы и опасные заблуждения в лечении ОРВИ
- Сбивать температуру в пределах 37–38 не обязательно.5 °. Это свидетельствует о том, что сработал естественный защитный механизм, заработала иммунная система.
- Рекомендуются ингаляции, но сегодня лучше использовать для этого не горшок с вареным картофелем, а купленные в аптеке безопасные современные ингаляторы.
- Нет смысла использовать банки и горчичники, так как их эффективность доказать еще никому не удалось. Для разогрева (при отсутствии повышенной температуры!) Лучше использовать аптечные мази и сухой жар.
- Не закапывайте в нос неразбавленный сок лука и чеснока, это вызовет ожог носоглотки. Хотя сами эти растения очень полезны, так как содержат фитонциды.
- Считается, что после болезни вырабатывается иммунитет к простуде, однако ОРВИ — это группа респираторных заболеваний, возбудителями которых являются разные вирусы и их штаммы. Заболев однажды, вы вскоре можете снова заболеть, если заражение произошло другим вирусом.К тому же эти агенты очень быстро меняются, поэтому иммунная система не успевает адаптироваться. Однако правильное питание, богатое витаминами и минералами, адекватная физическая активность, прогулки на свежем воздухе и позитивный настрой могут укрепить иммунную систему и противостоять вирусным инфекциям.
Профилактика
- Во время эпидемий врачи рекомендуют детям и людям с ослабленной иммунной системой ограничить посещение общественных мест. В школах для этого вполне разумен карантин.
- Взрослым, которые вынуждены ходить на работу, в магазины за покупками, ездить в общественном транспорте, рекомендуется чаще мыть руки с мылом, пользоваться дезинфицирующим спреем.
- Также не помешает промыть нос изотоническим раствором морской или обычной поваренной соли.
- Заранее подготовьтесь к холодному сезону. Врачи рекомендуют придерживаться принципов здорового питания, есть достаточное количество овощей и фруктов, ограничить употребление алкоголя, не курить и спать не менее 8 часов.
- Закаливание — очень эффективное средство профилактики ОРВИ. Помогает повысить адаптационные свойства организма. У закаленных людей наблюдается более быстрая реакция сосудов на холод, более высокая выработка тепла и диапазон температурной активности. У них улучшается кровообращение, нормализуется обмен веществ.
- Важно поддерживать оптимальную влажность воздуха в доме все время, а не только во время болезни. В городских квартирах в отопительный сезон врачи рекомендуют использовать увлажнители воздуха, чтобы увеличить его минимум до 60%, особенно в детской комнате.
Так как ОРВИ вызывается разными вирусами, универсальной вакцины от простуды пока нет. Но против определенных видов возбудителей ежегодно разрабатываются эффективные препараты. Осенью рекомендуется сделать прививку от гриппа, врачи всегда достаточно точно предсказывают, какой тип вируса будет преобладать в сезон эпидемии. Однако следует учесть: вакцинация не гарантирует, что вы совсем не заболеете, тем не менее, болезнь пройдет намного легче.
Бактериальные и вирусные инфекции: объяснение различий
Бактериальные и вирусные инфекции имеют много общего. Оба типа инфекций вызываются микробами — бактериями и вирусами соответственно — и распространяются такими вещами, как:
- Кашель и чихание.
- Контакт с инфицированными людьми, особенно через поцелуи и секс.
- Контакт с загрязненными поверхностями, продуктами питания и водой.
- Контакт с инфицированными существами, включая домашних животных, домашний скот и насекомых, таких как блохи и клещи.
Микробы также могут вызывать:
- Острые инфекции, которые непродолжительны.
- Хронические инфекции, которые могут длиться недели, месяцы или всю жизнь.
- Скрытые инфекции, которые сначала могут не вызывать симптомов, но могут возобновиться в течение месяцев и лет.
Что наиболее важно, бактериальные и вирусные инфекции могут вызывать легкие, средние и тяжелые заболевания.
На протяжении всей истории миллионы людей умирали от таких болезней, как бубонная чума или Черная смерть, вызываемая бактериями Yersinia pestis, и оспа, вызываемая вирусом натуральной оспы.В последнее время вирусные инфекции стали причиной двух крупных пандемий: эпидемии «испанского гриппа» 1918-1919 годов, унесшей жизни 20-40 миллионов человек, и продолжающейся эпидемии ВИЧ / СПИДа, унесшей жизни примерно 1,5 миллиона человек во всем мире только в 2013 году.
Бактериальные и вирусные инфекции могут вызывать похожие симптомы, такие как кашель и чихание, лихорадка, воспаление, рвота, диарея, усталость и спазмы — все это способы, которыми иммунная система пытается избавить организм от инфекционных организмов.Но бактериальные и вирусные инфекции не похожи друг на друга во многих других важных отношениях, большинство из которых связано со структурными различиями организмов и тем, как они реагируют на лекарства.
Различия между бактериями и вирусами
Хотя бактерии и вирусы слишком малы, чтобы их можно было увидеть без микроскопа, они такие же разные, как жирафы и золотые рыбки.
Бактерии — относительно сложные одноклеточные существа, многие из которых имеют жесткую стенку и тонкую эластичную мембрану, окружающую жидкость внутри клетки.Они могут воспроизводиться самостоятельно. Окаменелые записи показывают, что бактерии существуют около 3,5 миллиардов лет, и бактерии могут выжить в различных средах, включая сильную жару и холод, радиоактивные отходы и человеческое тело.
Большинство бактерий безвредны, а некоторые действительно помогают, переваривая пищу, уничтожая болезнетворные микробы, борясь с раковыми клетками и обеспечивая необходимые питательные вещества. Менее 1% бактерий вызывают заболевания у людей.
Продолжение
Вирусы мельче: самые крупные из них меньше самых маленьких бактерий.Все, что у них есть, — это белковая оболочка и ядро генетического материала, либо РНК, либо ДНК. В отличие от бактерий, вирусы не могут выжить без хозяина. Они могут воспроизводиться, только прикрепляясь к клеткам. В большинстве случаев они перепрограммируют клетки, чтобы производить новые вирусы, пока клетки не лопнут и не погибнут. В других случаях они превращают нормальные клетки в злокачественные или раковые.
Также, в отличие от бактерий, большинство вирусов действительно вызывают болезни, и они довольно специфичны в отношении клеток, которые они атакуют. Например, некоторые вирусы атакуют клетки печени, дыхательной системы или крови.В некоторых случаях вирусы нацелены на бактерии.
Диагностика бактериальных и вирусных инфекций
Вам следует проконсультироваться с врачом, если вы считаете, что у вас бактериальная или вирусная инфекция. Исключение составляет простуда, которая обычно не опасна для жизни.
В некоторых случаях трудно определить, является ли заболевание вирусным или бактериальным, потому что многие заболевания, включая пневмонию, менингит и диарею, могут быть вызваны ими. Но ваш врач может определить причину, выслушав вашу историю болезни и проведя медицинский осмотр.
При необходимости они также могут заказать анализ крови или мочи, чтобы подтвердить диагноз, или «тест на культуру» ткани для выявления бактерий или вирусов. Иногда может потребоваться биопсия пораженной ткани.
Лечение бактериальных и вирусных инфекций
Открытие антибиотиков для лечения бактериальных инфекций считается одним из самых важных достижений в истории медицины. К сожалению, бактерии очень легко приспосабливаются, и чрезмерное использование антибиотиков сделало многие из них устойчивыми к антибиотикам.Это создало серьезные проблемы, особенно в больничных условиях.
Антибиотики не эффективны против вирусов, и многие ведущие организации в настоящее время рекомендуют не использовать антибиотики, если нет явных доказательств бактериальной инфекции.
Продолжение
С начала 20 века разрабатываются вакцины. Вакцины резко сократили количество новых случаев вирусных заболеваний, таких как полиомиелит, корь и ветряная оспа. Кроме того, вакцины могут предотвратить такие инфекции, как грипп, гепатит А, гепатит В, вирус папилломы человека (ВПЧ) и другие.
Но лечение вирусных инфекций оказалось более сложной задачей, прежде всего потому, что вирусы относительно крошечные и воспроизводятся внутри клеток. Для лечения некоторых вирусных заболеваний, таких как инфекции, вызванные вирусом простого герпеса, ВИЧ / СПИД и грипп, стали доступны противовирусные препараты. Но использование противовирусных препаратов было связано с развитием устойчивых к лекарствам микробов.
грипп-2016_ научные треки-рефераты
Том 5, Выпуск 3 (Дополнение)
Вирол Микол 2016
ISSN: 2161-0517 VMID, журнал открытого доступа
Стр.55
Примечания:
Грипп 2016
31 октября — 2 ноября 2016 г.
серия конференций
.com
2
nd
Международная конференция по гриппу
31 октября — 2 ноября 2016 г. Сан-Франциско, США
Влияние использования умифеновира на снижение вторичной бактериальной пневмонии после гриппа
Ирина Ленева
1
, Фалынскова И N
1
, Леонова
Е
I
1
, Селькова Е П
2
и Малеев В В
3
1
Я.НИИ вакцин и сывороток им. И.И. Мечникова, Россия
2
Московский научно-исследовательский институт эпидемиологии и микробиологии им. Габричевского, Россия
3
Центральный научно-исследовательский институт эпидемиологии, Россия
п
невмония часто возникает вторично по отношению к инфекции гриппа и составляет значительную долю заболеваемости и смертности.
связанные со вспышками сезонного и пандемического гриппа. Противовирусный препарат умифеновир (Арбидол) лицензирован в России.
для лечения и профилактики острой респираторной инфекции, включая грипп A и B.В настоящем исследовании мы
исследовали эффективность умифеновира или осельтамивира на мышиной модели вторичного
S. aureus
пневмония после A /
Калифорния / 04/2009 (h2N1) вирусная инфекция. Мы также провели клиническое исследование эффективности умифеновира.
в уменьшении пневмонии, связанной с гриппом. Эксперименты на мышах показали, что пероральное лечение осельтамивиром (20 мг / кг / день) и
умифеновир (40 и 60 мг / кг / день) улучшил выживаемость мышей с 0% до 90%, значительно продлил выживаемость и отменил
потеря веса.Обработка также подавляла титр вируса на ≥2 log и количество жизнеспособных бактерий в легких мышей. Легкие
мыши, получавшие осельтамивир или умифеновир, показали менее серьезные гистопатологические данные по сравнению с контрольной группой. В
Наблюдение за клиническим исследованием случай-контроль было организовано в сезоне 2010/2011 и 2014/2015 гг. и включало 5287 госпитализированных пациентов.
в 88 больниц с острыми респираторными вирусными инфекциями (ОРВИ) из 50 регионов Российской Федерации.Анализ показал
что в группах высокого риска частота бактериальных осложнений (пневмония) была выше, чем в среднем по
исследование населения. Наши обсервационные исследования предполагают пользу раннего лечения умифеновиром (т.е. в течение 48 часов после болезни).
начало) в снижении заболеваемости пневмонией у пациентов из группы высокого риска.
Биография
Ирина Ленева защитила кандидатскую диссертацию в Научно-исследовательском институте вирусных препаратов, Москва, Россия, и докторантуру Центра химии лекарственных средств,
Москва, Россия.Заведующая лабораторией экспериментальной вирусологии Института вакцин и сывороток им. И. Мечникова. Имеет около 50 рецензируемых публикаций.
журналы. Она является ученым советником по вирусологии Российского общества инфекционных болезней. Она является рецензентом нескольких научных журналов в области
вирусология. Ее текущие исследования сосредоточены на патогенезе вирусных респираторных заболеваний, в основном, на разработке вакцин и противовирусных препаратов против биологических агентов.
и новые патогены, клинические испытания противовирусных препаратов и вакцин, мониторинг устойчивости к противовирусным препаратам.Она также заинтересована в разработке новых анализов и исследований на животных.
модели для тестирования новых лекарств против респираторных вирусов.
[электронная почта защищена]Ирина Ленева и др., Virol Mycol 2016, 5: 3 (Дополнение)
http://dx.doi.org/10.4172/2161-0517.C1.014ОРВИ есть. Острая респираторная вирусная инфекция: профилактика, лечение
Содержание
Острая респираторная вирусная инфекция (ОРВИ) — это заболевание, поражающее дыхательную систему человека. Основная причина заболевания — контакт с вирусами.Путь передачи вирусов — воздушно-капельный.
Распространенность ОРВИ
Заболевание ОРВИ распространено повсеместно, особенно в детских садах и школах, рабочих группах. Маленькие дети, пожилые люди и люди с ослабленной иммунной системой имеют повышенный риск заражения.
Источник заражения — инфицированный человек. Высокая восприимчивость людей к вирусам приводит к быстрому распространению болезни, эпидемии ОРВИ — частое явление во всем мире.Несвоевременное лечение болезни может привести к различным осложнениям.
Вспышки респираторных вирусных инфекций происходят круглый год, но эпидемия ОРВИ чаще наблюдается осенью и зимой, особенно при отсутствии качественных профилактических и карантинных мер по выявлению инфекции.
Причины ОРВИ
Причина заболевания — респираторные вирусы, для которых характерен короткий инкубационный период и быстрое распространение. Источник заражения — больной человек.
Вирус SARS боится дезинфицирующих средств, ультрафиолетовых лучей.
Механизм проявки
Попадая в организм через слизистую оболочку верхних дыхательных путей или конъюнктиву глаза, вирусы, проникая в клетки эпителия, начинают размножаться и уничтожать их. В местах внедрения вирусов возникает воспаление.
Через поврежденные сосуды, попадая в кровоток, вирусы распространяются по организму. В этом случае организм выделяет защитные вещества, проявлением которых являются признаки интоксикации.Если иммунитет ослаблен, возможно присоединение бактериальной инфекции.
Симптоматология
Все респираторно-вирусные заболевания имеют похожие симптомы. В начале заболевания у человека появляется насморк, чихание, першение в горле, ноет тело, повышается температура, пропадает аппетит, появляется жидкий стул.
Симптомы ОРВИ у ребенка могут развиваться молниеносно. Быстро нарастает интоксикация, малыш простужается, появляется рвота, выражена гипертермия.Лечение необходимо начинать немедленно, чтобы избежать возможных осложнений.
Признаки отдельных вирусных инфекций
Парагрипп определяется по слизистым выделениям из носа, появлению сухого «лающего» кашля, охриплости голоса. Температура не выше 38 ° С.
Аденовирусная инфекция сопровождается конъюнктивитом. Кроме того, у пациента могут возникнуть ринит, ларингит, трахеит.
При риновирусной инфекции выраженные симптомы интоксикации, повышение температуры не допускается.Заболевание сопровождается обильными слизистыми выделениями из носа.
Респираторно-синцитиальная вирусная инфекция характеризуется невыраженными катаральными симптомами или бронхитом, тяжелой интоксикацией. Температура тела остается нормальной.
В чем разница между гриппом и ОРВИ?
ОРВИ начинается постепенно, развитие гриппа быстрое, человек даже может указать время, когда он почувствовал себя плохо.
При ОРВИ температура тела повышается незначительно, не выше 38.5 С?. Для гриппа характерно резкое повышение температуры до 39-40 ° С. Температуру в этом случае поддерживают от трех до четырех дней.
При ОРВИ симптомы интоксикации практически отсутствуют, человек не дрожит и не потеет, нет сильной головной боли, боли в глазах, светобоязни, головокружения, ломоты в теле, сохраняется трудоспособность.
При гриппе простуда и заложенность носа отсутствуют, это основной симптом ОРВИ.Заболевание сопровождается покраснением горла, при гриппе этот симптом наблюдается не всегда.
При ОРВИ кашель, дискомфорт в груди возникает в самом начале заболевания, он может быть легким или умеренным. Для гриппа характерны болезненный кашель и боль в груди, которые появляются на второй день болезни.
Чихание характерно для простуды, при гриппе такого симптома не наблюдается, но есть покраснение глаз.
После гриппа еще две-три недели человек может чувствовать слабость, головную боль, быстро уставать, после ОРВИ такие симптомы не проходят.
Знание, чем грипп отличается от ОРВИ, поможет человеку оценить свое состояние и вовремя принять необходимые меры, которые помогут быстро избавиться от болезни и избежать осложнений.
Какие симптомы ОРВИ должны насторожить
Срочно обратиться к врачу при повышении температуры до 40С? и многое другое, что не смущает жаропонижающие препараты, при нарушении сознания, сильной головной боли и невозможности сгибать шею, сыпь на теле, затрудненное дыхание, кашель с окрашенной мокротой (особенно с кровью), длительное повышение температуры тела, отеки.
Обращение к врачу необходимо даже в том случае, если признаки ОРВИ не исчезают через 7-10 дней. Особого внимания требуют симптомы ОРВИ у ребенка. При появлении каких-либо подозрительных симптомов следует немедленно обратиться за медицинской помощью.
Диагностика
Диагноз ставит лечащий врач после осмотра носоглотки и изучения симптомов. В некоторых случаях при возникновении осложнений могут потребоваться дополнительные исследования, например, рентген грудной клетки. Это помогает устранить пневмонию.
Осложнения
Частым осложнением ОРВИ является присоединение бактериальной инфекции, провоцирующей развитие воспалительных процессов: бронхита, отита, синусита, пневмонии. Заболевание может осложниться добавлением инфекции мочевыводящих путей, панкреатита, холангита.
Если заболевание протекает с выраженной интоксикацией, результатом может быть развитие судорожного или менингеального синдромов, миокардита. Возможные неврологические проблемы, такие как менингит, неврит, менингоэнцефалит.После перенесения ОРВИ осложнения могут проявиться обострением хронических заболеваний.
У детей частым осложнением является ложный круп.
Чтобы свести к минимуму риск осложнений, лечение нужно начинать вовремя, соблюдая все предписания врача.
Как лечить
Лечение в основном проходит дома. Пациенту необходимо придерживаться полусложного режима, соблюдать молочно-овощную обогащенную диету, употреблять много жидкости для разжижения мокроты, стимулирования потоотделения, снижения уровня токсинов.
Но бешеными современными темпами мало кто следует этому правилу, предпочитая простудиться «на ногах» и облегчить неприятные симптомы симптоматическими средствами. Опасность такого подхода к лечению заключается в том, что часто симптоматические лекарства от простуды содержат фенилэфрин — вещество, повышающее давление и заставляющее сердце работать. Во избежание осложнений простуды нужно выбирать препараты без компонентов подобного рода. Например, «АнтиГриппин» (лучше от «Натура продукт») — это лекарство от простуды без фенилэфрина, которое устраняет неприятные симптомы ОРВИ, не провоцируя повышения давления и не причиняя вреда сердечной мышце.
При лечении используются противовирусные препараты, средства для повышения иммунитета, жаропонижающие, антигистаминные препараты, препараты, способствующие отхождению мокроты, витамины. Местно применяют сосудосуживающие средства, препятствующие размножению вируса на слизистой оболочке носоглотки. Такое лечение важно проводить на начальной стадии заболевания.
Препараты для лечения ОРВИ
В борьбе с возбудителем заболевания эффективны противовирусные препараты: Ремантадин, Амизон, Арбидол, Амиксин.
Применение нестероидных противовоспалительных средств необходимо для снижения температуры тела и уменьшения боли. К таким препаратам относятся «Парацетамол», «Ибупрофен», «Панадол». Необходимо помнить, что температура ниже 38 ° C? не сбивается, потому что при такой температуре организм активирует защитные силы.
Антигистаминные препараты необходимы для уменьшения признаков воспаления: заложенности носа, отека слизистых оболочек. Рекомендован прием «Лоратидин», «Фенистил», «Зиртек».В отличие от препаратов первого поколения они не вызывают сонливости.
Капли в нос нужны для уменьшения отечности, устранения заложенности носа. Стоит помнить, что такие капли нельзя долго использовать, так как это может спровоцировать развитие хронического ринита. Капли используют не более 7 дней, 2-3 раза в день. Для длительного лечения можно использовать препараты на основе эфирных масел.
Средства от боли в горле. Лучше всего в этом случае помогает полоскание горла дезинфицирующими растворами. Для этих целей можно использовать шалфей, ромашку.Полоскать нужно часто, каждые два часа. Эффективно использование дезинфицирующих спреев — «Гексорал», «Биопарокс» и др.
Лекарство от кашля необходимо для разжижения мокроты. В этом помогает употребление «АЦК», «Мукалтина», «Бронхолитина» и др. Важно употреблять много жидкости, что также способствует разжижению мокроты. Средства от кашля нельзя использовать без рецепта врача.
Антибиотики не используются при лечении ОРВИ, необходимо только при присоединении бактериальной инфекции.
Помимо лекарств, эффективно используют физиотерапевтические процедуры, ингаляции, массажные техники, ножные ванны.
Народные средства
Народные средства очень эффективны при лечении ОРВИ. Это может быть дополнением к основному лечению и помогает быстро справиться с болезнью. Можно использовать следующие рецепты.
Неплохо помогает настой плодов калины и цветов липы, которые необходимо измельчить и перемешать. Две столовые ложки сбора нужно залить 500 мл кипятка, настоять час.Полученный настой употребляют перед сном по стакану.
Хорошо побороть болезнь лук и чеснок, которые можно просто съесть. Такое средство полезно как в профилактике, так и в лечении: после еды употребляют несколько зубчиков чеснока и пол чайной ложки сока. Можно разложить в комнате порезанный лук и чеснок и вдохнуть их пары.
Очень эффективное средство из меда и лимонного сока. Для его приготовления мед (100 г) смешивают с соком одного лимона и разбавляют кипяченой водой (800 мл).Полученное средство нужно пить в течение дня.
Профилактика
Какая профилактика ОРВИ у взрослых и детей? Чтобы укрепить защитные силы организма, нужно закаляться, оставаться активным, гулять на свежем воздухе, не пренебрегать отдыхом, избегать стрессов, а также соблюдать гигиену (мыть руки, овощи, регулярно делать влажную уборку).
Профилактика ОРВИ у взрослых предполагает соблюдение правильного режима питания. В меню должны преобладать натуральные продукты. Кисломолочные продукты полезны для поддержания микрофлоры кишечника и укрепления иммунитета.Кроме того, в рационе должна присутствовать клетчатка.
Для профилактики можно принимать противовирусные препараты или делать вакцину. Хотя полностью обезопасить себя с помощью вакцинации невозможно, так как вирусы постоянно мутируют. Вакцинация рекомендована детям, посещающим детские сады и школы, сотрудникам медицинских учреждений.
Во время эпидемий рекомендуется ограничивать посещение общественных мест, для укрепления иммунной системы принимать природные средства или противовирусные препараты в рекомендованной дозировке.
Если профилактические меры не помогли вам избежать заражения, позаботьтесь о своем выздоровлении, а также о людях вокруг вас. Поскольку ОРВИ заразно, не забывайте прикрывать рот и нос при кашле и чихании, проветривать помещение, при необходимости носить марлевую повязку.


 При воспалении этот механизм самоочищения (его называют мукоцилиарным клиренсом) имеет важное значение – он предотвращает скопление остатков разрушенных клеток, слизи, содержащей вирусы и бактерии, для которых слизь является питательной средой. Вирусы способствуют разрушению клетки и угнетению движения ресничек. Это приводит к тому, что самоочищающий механизм работает недостаточно эффективно, а бактерии тем временем распространяются в нижние отделы дыхательных путей, околоносовые пазухи, через слуховую трубу в полость среднего уха, и вызывают бактериальные осложнения.
При воспалении этот механизм самоочищения (его называют мукоцилиарным клиренсом) имеет важное значение – он предотвращает скопление остатков разрушенных клеток, слизи, содержащей вирусы и бактерии, для которых слизь является питательной средой. Вирусы способствуют разрушению клетки и угнетению движения ресничек. Это приводит к тому, что самоочищающий механизм работает недостаточно эффективно, а бактерии тем временем распространяются в нижние отделы дыхательных путей, околоносовые пазухи, через слуховую трубу в полость среднего уха, и вызывают бактериальные осложнения.