🧬 Что нужно знать про тесты на туберкулез
Всероссийское общество фтизиатров утвердило несколько возможных вариантов тестирования, включая не только пробу Манту, но и тестирование с использованием Диаскин-теста и Т-теста. Результаты каждого из этих тестов будут признаваться достаточными для приема ребенка в детский сад, — сообщается на официальном сайте Минздрава.
Медицинский директор, педиатр GMS Clinic Олег Тогоев дал свой комментарий информационному порталу «Здоровые дети».
Манту — не единственный официальный скрининг. Родители могут самостоятельно принимать решения о способе тестирования ребенка.
Что это за тесты и чем они отличаются?
Реакция Манту (туберкулиновая проба) является на сегодняшний день в России основным методом профилактического обследования детей на инфицирование туберкулезом.
- Реакция Манту — это ответ организма на введение туберкулина (несмотря на название, саму туберкулезную палочку препарат не содержит).

- Тест делается один раз в год, начиная с года и до 16 лет.
- Мочить место пробы можно.
Диаскин-тест — это способ диагностики туберкулеза путем введения препарата под кожу ребенка. Он позволяет определить наличие или отсутствие микобактерий туберкулеза в организме ребенка. Диаскин-тест является более чувствительным тестом, поскольку в его состав входят белки, вызывающие иммунную реакцию в организме только на микобактерии, вызывающие туберкулез.
- Тест по сравнению с реакцией Манту позволяет определить не только наличие возбудителя, но и активность микобактерий, вызывающих само заболевание.
- Сегодня этот тест делается в случаях, если проба Манту — положительная.
- Мочить место введения препарата можно.

Т-спот — тест на туберкулез, который проводится путём забора крови ребёнка и ее последующего исследования.
- «T» обозначает T-лимфоциты (клетки крови, на основе ответа которых производится исследование).
- «SPOT» (от англ. — «пятно»). В результате лабораторного опыта образуются пятна, каждое из которых маркирует Т-лимфоцит. Этот способ определения носительства туберкулеза позволяет исключить ложноположительные реакции на носительство микобактерии туберкулеза.
Олег Тогоев, педиатр, медицинский директор GMS Clinic прокомментировал: «Скажу в первую очередь, что дети обязательно должны проходить один из утвержденных скринингов на туберкулез, потому что это заболевание, к несчастью, существует, и оно контагиозно (то есть, заразно — прим. ред.). Моя рекомендация — диаскин-тест, как наиболее оптимальный скрининг на туберкулез. Его основное преимущество в том, что он редко (в 10 случаев из 100) бывает ложноположительным.
 Поэтому старая добрая проба Манту, которой уже почти 100 лет, до сих пор своей актуальности не потеряла, просто нужно правильно и грамотно интерпретировать ее результаты».
Поэтому старая добрая проба Манту, которой уже почти 100 лет, до сих пор своей актуальности не потеряла, просто нужно правильно и грамотно интерпретировать ее результаты».
Источник: healthy-kids.ru
Диаскинтест – что это такое и как его делают?
Туберкулез – болезнь, которая из года в год становится все более и более распространенной среди населения. Заражение наступает воздушно-капельным путем через контакт с больным — кашляющим, чихающим или даже просто что-то говорящим. Не каждое заражение заканчивается болезнью, по оценкам, около 30 % людей являются носителями туберкулезной палочки, которая может годами находится в скрытом состоянии. Однако когда по какой то причине снижается выносливость организма, бактерии активизируются и этот процесс заканчивается то болезнью. Ослабления оборонных сил организма происходит как следствие нерационального питания и неправильного образа жизни: нехватки движения на свежем воздухе, малого количества сна, избытка стимуляторов – например, алкоголя, никотина. Определенные группы лиц, более подвержены заболеванию (старые люди, люди с низкой двигательной активностью).
Определенные группы лиц, более подвержены заболеванию (старые люди, люди с низкой двигательной активностью).
Возбудителем туберкулеза являются бактерии, называемые палочками Коха (микобактерии туберкулеза). Благодаря специальной оболочке, туберкулезные палочки очень стойкие к высыханию и замерзанию. В сухой среде, напр. мокроте, которая засохла, палочки могут жить в течение нескольких месяцев. Солнечные лучи и кипячение в воде убивают их на протяжении нескольких минут. У человека болезнь вызывают не только палочки человеческого туберкулеза, но также палочки скотского туберкулеза. При контакте с больным человеком бактерии туберкулеза добираются до дыхательных (в основном легких), где и развивается болезнь.
Очень важной является ранняя диагностика туберкулеза. Во первых, при обнаружении заболевания на начальных стадиях вероятность быстрого и полного выздоровления намного выше. Во вторых, чем раньше будет выявлен туберкулез у конкретного человека, тем меньшее количество людей он сможет заразить.
Не так давно учеными был разработан новый метод диагностирования туберкулеза – Диаскинтест.
Что такое Диаскинтест?
Диаскинтест – это препарат, который дает возможность подтвердить наличие или отсутствие туберкулезных палочек в организме человека. В его основе лежит белок, состоящий из двух антигенов, которые присутствуют в вирулентных штаммах микобактерий туберкулеза. В результате введения инъекции можно обнаружить возбудителей заболевания, которые находятся в фазе активного размножения. В этом случае тест будет положительным. Если же в организме микобактерии находятся в скрытой фазе – результат будет отрицательным.
Диаскинтест не может спровоцировать заражение туберкулезом, так как в своем составе не содержит возбудителей этого заболевания.
Кроме специфического белка, в состав Диаскинтеста входят фенол, полисорбат 80, вода для инъекций, натрия хлорид, калий фосфорнокислый однозамещенный, натрий фосфорнокислый двузамещенный 2-водный.
Преимуществами Диаскинтеста перед пробой Манту являются его избирательность, высокая чувствительность и возможность отслеживать эффективность лечения по увеличению или снижению активности микобактерий.
Недостатком Диаскинтеста являются частые ложноотрицательные результаты при его проведении, например, когда человек инфицирован другим возбудителем туберкулеза — M.bovis. Также ложноотрицательный результат может наблюдаться при обостренных тяжелых формах туберкулеза на этапе распада.
Как его делают?
Диаскинтест противопоказан людям с кожными и инфекционными заболеваниями, аллергией в обостренной стадии, эпилепсией. При диагностике у детей его проводят не раньше чем через месяц от предыдущей вакцинации.
Проводить тест должен специально обученный медицинский работник.
Дозу инъекции (0,1 мл) вводят внутрикожно туберкулиновым шприцом с тонкой короткой иглой.
Что означают результаты?
После введения препарата в коже наблюдается папула диаметром 8-10 мм.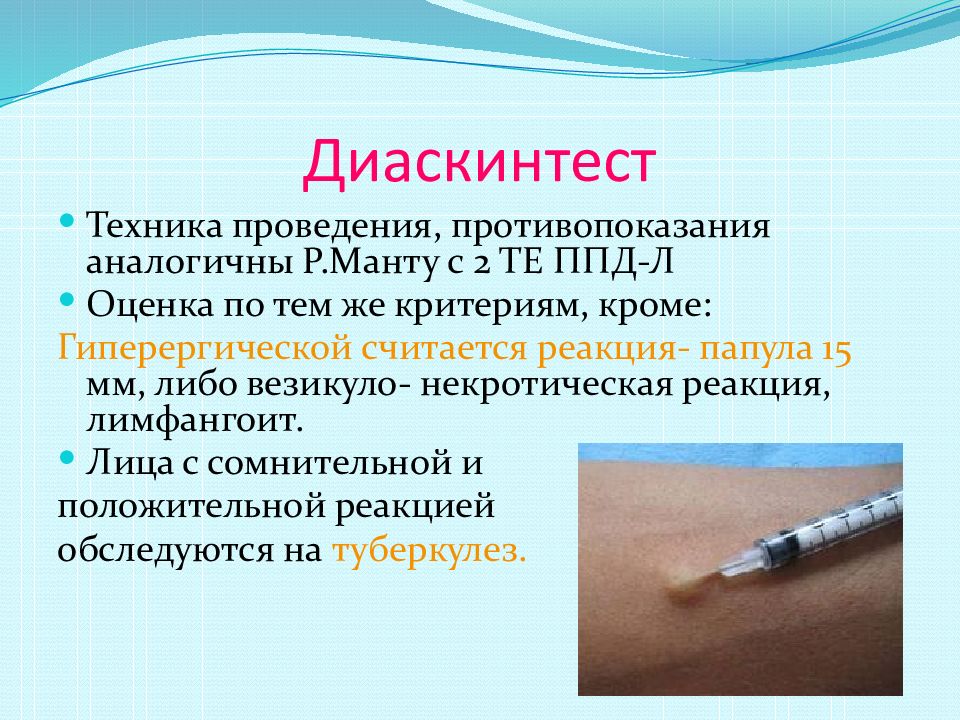
Результаты анализируют спустя 72 часа по размеру инфильтрата и гиперемии.
Папула (инфильтрат) – уплотнение на коже, которое возникает как реакция на пробу в виде бугорка.
Гиперемия – покраснение, размер которого учитывается в результатах, только если папула не появилась
При положительном результате наблюдается инфильтрат (папула) любого размера. При отрицательном результате – инфильтрат и гиперемия отсутствуют (допускается уколочная реакция меньше двух милиметров).
Присутствие гиперемии без инфильтрата (говоря проще, пятно на коже без уплотнения и набухания) ставит под сомнение результаты теста и требует дополнительных исследований.
Диаскинтест не является идеальным препаратом и имеет свои недостатки, однако его роль в раннем диагностировании туберкулеза очень важна и велика.
34
Диагностика туберкулеза: проба Манту или диаскинтест
В СССР диагностика туберкулёза начала проводиться туберкулином с 1965 года.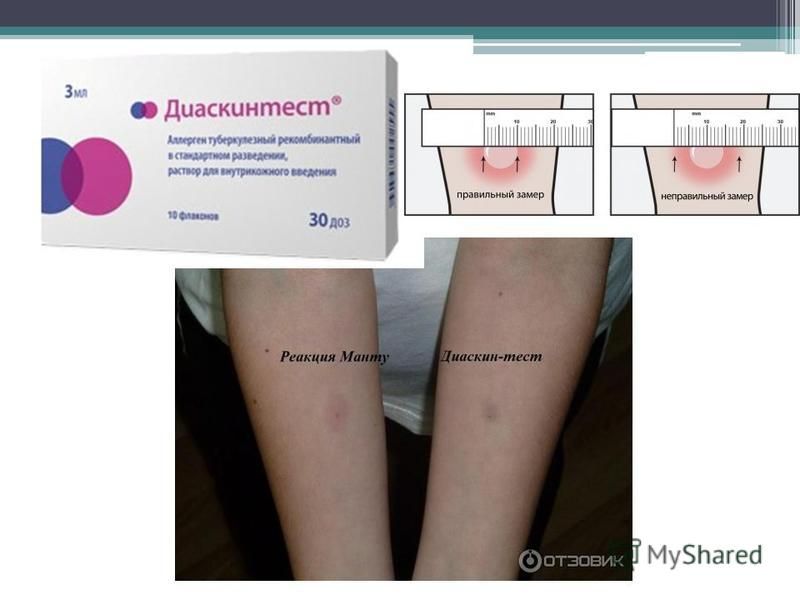 Но, несмотря на такой большой опыт в туберкулинодиагностике, до сих пор продолжаются споры — какой метод лучше выбрать. Рассмотрим 2 основных метода диагностики туберкулёза у детей: проба Манту и диаскинтест.
Но, несмотря на такой большой опыт в туберкулинодиагностике, до сих пор продолжаются споры — какой метод лучше выбрать. Рассмотрим 2 основных метода диагностики туберкулёза у детей: проба Манту и диаскинтест.
Проба Манту
Проба Манту – это внутрикожное введение туберкулина с целью выявления туберкулёза. Несмотря на распространенное мнение – это не прививка, а тест на наличие специфических антител к микобактериям туберкулеза. Это важный метод, потому что позволяет определить туберкулёз на ранних этапах. Проведение его стандартное: 0,1 мл туберкулина вводится в среднюю треть области внутренней поверхности предплечья. Оценка результата осуществляется через 72 часа.
Механизм теста следующий: он вызывает местную аллергическую реакцию замедленного типа. Сопровождается отёком, покраснением, иногда зудом. Если такая реакция возникает, значит, иммунитет к туберкулёзу сформировался, и организм уже умеет распознавать эти бактерии. Если реакции нет, то и иммунитета к микобактериям туберкулёза нет.
Существуют противопоказания для постановки пробы Манту: эпилепсия, ревматизм, опухоли, подтвержденная аллергическая реакция на туберкулин, а так же обострение аллергии, хронических инфекций, карантин в школе и детском саду. Из-за возможных аллергических реакций некоторые родители опасаются делать пробу Манту.
Диаскинтест
Существуют аналогичные методы для диагностики туберкулёза, один из них – диаскинтест.
Это синтетический препарат, что не может не радовать мам, опасающихся введения туберкулина. Так же, как и при постановке пробы Манту, возникает местная аллергическая реакция, но только в случае заболевания туберкулёзом или заражения им, которое может и не перейти в болезнь. Проведение диаскинтеста схоже с проведением пробы Манту, проверка также происходит через 72 часа.
Проводить его можно с 1 года, и одним из плюсов этого метода является отсутствие риска заразиться туберкулёзом. Этот препарат специфичен и не реагирует на другие бактерии, а также исключена реакция по поставленную ранее вакцину БЦЖ. К тому же, диаскинтестом проводят оценку эффективности лечения туберкулёза.
Этот препарат специфичен и не реагирует на другие бактерии, а также исключена реакция по поставленную ранее вакцину БЦЖ. К тому же, диаскинтестом проводят оценку эффективности лечения туберкулёза.
Детям до 8 лет, в анамнезе имеющим аллергические реакции и аллергические дерматиты, рекомендуют проводить диаскинтест. Желательно предварительно проконсультироваться у фтизиатра. В настоящее время детям с 8 лет в целях туберкулинодиагностики уже проводится диаскинтест. Но и для этого теста существуют противопоказания: обострение аллергических дерматитов, эпилепсия, обострение хронических заболеваний и острые инфекционные заболевания, за исключением подозрения на туберкулёз.
В любом случае, в связи со стёртой клинической картиной в начале заболевания туберкулёзом, разнообразием его форм, а также снижением социальной ответственности населения, туберкулинодиагностику необходимо проводить обязательно! А выбор метода нужно доверить грамотному специалисту, учитывая возрастные особенности, аллергоанамнез и состояние пациента на момент осмотра.
Опытные педиатры клиники «Семейный доктор» разъяснят вам различия между методами, подберут оптимальный вариант и проведут быструю и качественную диагностику в комфортных условиях. Чтобы записаться к специалисту клиники «Семейный доктор» на удобное для Вас время, позвоните по телефону единого контакт-центра в Москве +7 (495) 775 75 66, воспользуйтесь сервисом online-записи к врачу или обратитесь в регистратуру клиники.
Информацию для Вас подготовила:
Петрова Оксана Ивановна — врач-педиатр, ведущий специалист клиники, медицинский директор Детского корпуса на Усачева.
Allium test — Викиучебник
Allium test — растительная тест система для анализа мутагенных факторов химической и физической природы на основе растения Allium cepa (сорт Штутгартен). Allium-test — в котором в качестве материала используются корешки проростков репчатого лука Allium cepa, который впервые предложен Шведской Королевской Академией Наук как стандартный тест-объект [2][3].
Субстрат — вода или подготовленный раствор?[править]
Средой для проращивания может служить:
- Вода из под крана:
- Очищенная, и отстоянная
- Пропущенная через фильтр типа «Кувшин»
- Пропущенная через систему тройной фильтрации
- Вода дистиллированная
- Необходимо знать характеристики дистиллятора, поскольку он способен вторично загрязнять чистую воду ионами металлов. Входящих в его конструкцию, например Медью
- Вода искусственная
- Уточнить у славы состав
Рекомендуется использовать искусственную воду и дистиллированную для контроля и дистиллированную воду для эксперимента.
Рассмотрим свойства различной по составу воды:
| Дистиллированная | Солевой состав: отсутствует
pH: сдвинут в сторону (введите значение) и составляет примерно (введите значение)[источник?] Данная вода обладает мутагенным эффектом из-за отсутствия питательных веществ, необходимых для функционирования микроструктур клетки[источник?]. |
| Искусственная | Солевой состав[источник?]: pH: Находится у точки (введите значение)[источник?] Данная вода определяется почти полным отсутствием видимых генетических нарушений. Необходимо проведение теста на CommetAssey для того чтобы убедиться что количество микронарушений так же мало |
Неотсортирвоанные разделы, вы хотите удалить из них мусор?[править]
Биотест Allium test разработан А. Леваном в 1938 году для изучения эффекта влияния W:колхицина, показав в итоге высокую эффективность. В настоящее время Allium-test используется наряду с постоянно увеличивающимся числом объектов (среди растений наиболее часто — горох Pisum sativum и бобы Vicia faba), но продолжает оставаться одним из наилучших тест-объектов для анализа генотоксичности и токсичности различных факторов[2][4].
Данный метод не требует знания кариотипа и идентификации типов повреждений хромосом, является простым, экономичным и достаточно чувствительным для определения «W:мутаген» или «не мутаген» фактор[5].
Allium test рекомендован экспертами ВОЗ как стандарт в цитогенетическом мониторинге окружающей среды, так как результаты, полученные на данном тесте, показывают корреляцию с тестами на других организмах: водорослях, растениях, насекомых, в том числе и млекопитающих и человеке[3][6][7]. Рекомендован в качестве альтернативы in vivo тестам на лабораторных животных по токсикологическому критерию [8]
Преимущества метода Allium cepa[править]
Преимущества растительной тест-системы Allium cepa[править]
Данный метод не требует знания кариотипа и идентификации типов повреждений хромосом, является простым, экономичным и достаточно чувствительным для определения «мутаген» или «не мутаген» фактор[5].
Метод позволяет регистрировать хромосомные мутации типа делеций и транслокаций, следствием которых является наличие мостов и фрагментов в ана- и телофазе. Кроме того метод позволяет выявлять изменение поведения хромосом на веретене деления[5].
Преимущества растительных тест систем на примере лука
Allium cepa[править]Растительные тест-системы в настоящее время получают всё большее распространение при оценке мутагенного загрязнения окружающей среды. Это обусловлено целым рядом преимуществ растений как индикаторов генотоксичности различных факторов, так и сигнальных объектов при генетическом мониторинге за состоянием окружающей среды:
- Растения — неизменный объект для натурных исследований антропогенного влияния на окружающую среду: первыми принимают на себя удар загрязнителей, не мигрируют подобно животным, что позволяет чётко рассчитать время воздействия.
- Растения — эукариотические организмы, поэтому на них, в отличие от микроорганизмов, можно регистрировать все типы генетических повреждений:
- генные,
- хромосомные,
- геномные.
- Методы работы с растительными объектами экономичны, требуют минимального количества оборудования и W:реактивов, выращивание растений менее трудоёмко, чем выращивание животных.

- Можно получать материал нужных стадий.
- Эксперименты можно вести в строго контролируемых условиях — как в острых, так и в хронических опытах (от нескольких часов до нескольких лет).
- Данные по мутагенезу ряда факторов на растительных объектах показывают хорошую корреляцию с результатами тестирования на животных.
- Растения позволяют регистрировать как прямые, так и косвенные мутагены.
- Только растения позволяют выявить такой важный класс мутагенов, как W:химические соединения, приобретающие мутагенность в процессе метаболической активации растительными W:ферментами.
- Некоторые факторы, высокая токсичность которых не позволяет учесть генетические повреждения на животных, могут быть оценены как мутагены только в растительных тест-системах.
- Растения могут выращиваться непосредственно на месте оценки суммарного генетического эффекта загрязнения определяемых участков[9].
- Данные полученные на растительных тест-системах показывают хорошую корреляцию с данными тестов на млекопитающих.
 Более того, высшие растения проявляют себя в экосистеме как стабильный биосенсор и, таким образом позволяют отследить эволюцию генотоксического воздействия (в том случае когда фактор проявляет мутагенный эффект одновременно на растительном и животном тест объектах)[10].
Более того, высшие растения проявляют себя в экосистеме как стабильный биосенсор и, таким образом позволяют отследить эволюцию генотоксического воздействия (в том случае когда фактор проявляет мутагенный эффект одновременно на растительном и животном тест объектах)[10].
Методика проведения тестирования[править]
Подготовка оборудования для тестирования[править]
Химические реактивы[править]
| Ацетоорсеин | 1 г орсеина растворяют в 50 мл горячей уксусной кислоты, доводят до кипения и фильтруют. Используется для окраски корешков |
| Фиксатор Кларка | смесь 96 % этилового спирта и ледяной уксусной кислоты в соотношении 3:1. Используется для фиксации корешков. |
| Спирт 70% | смесь 96 % этилового спирта и дистиллированной воды. Используется для долговременного хранения корешков |
| Уксусная кислота 40% | смесь ледяной уксусной кислоты и дистиллированной воды. Используется для приготовления препаратов Используется для приготовления препаратов |
Подготовка материала для тестирования[править]
Подготовка луковиц[править]
Выберите луковицы для исследования. Выборка должна быть однородной как в контрольном, так и в опытном вариантах опыта. Средняя масса севка — 10-20г, диаметром 1,5-2 см. Выбранные луковицы не должны быть пересушены. Это можно понять сняв лишнюю шелуху, которая так же может мешать и проведению опыта. До начала эксперимента у луковиц не должно быть проклюнувшихся зеленых ростков листьев.
Подготовка фактора мутагенеза и процедура тестирования[править]
Существует два варианта Allium test: оригинальный и модифицированный.
- В оригинальном варианте теста луковицы помещают для проращивания корешков в чистую воду (прим: автор допускает использование водопроводной воды. Следует взять во внимание тот факт, что в Швеции, откуда родом автор водопроводная вода действительно очень чистая. Как вариант можно использовать очищенную питьевую воду низкой минерализации).
 По достижении корешками 1-2 см луковицы переносят в емкости с исследуемым раствором на определенное время (от 2 часов в случае с р-ом колхицина до 3 дней). Оригинальный вариант наиболее удобен при тестировании физических факторов.
По достижении корешками 1-2 см луковицы переносят в емкости с исследуемым раствором на определенное время (от 2 часов в случае с р-ом колхицина до 3 дней). Оригинальный вариант наиболее удобен при тестировании физических факторов. - В модифицированном варианте теста луковицы помещают непосредственно в исследуемый раствор без предварительного проращивания корешков. Данный вариант чаще используется при тестировании химических веществ.
- В оригинальном варианте теста луковицы помещают для проращивания корешков в чистую воду (прим: автор допускает использование водопроводной воды. Следует взять во внимание тот факт, что в Швеции, откуда родом автор водопроводная вода действительно очень чистая. Как вариант можно использовать очищенную питьевую воду низкой минерализации).
Для тестирования подходят факторы различной природы (см. таблицу):
| Физический фактор: |
| В случае с физическим мутагенным фактором луковицы подвергаются воздействию фактора с прочими одинаковыми условиям среды, как в контроле |
| Химический фактор: |
| В случае с химическим мутагенным фактором луковицы проращиваются на растворе или концентрированном растворе химического вещества и воды в заведомо определённой концентрации. 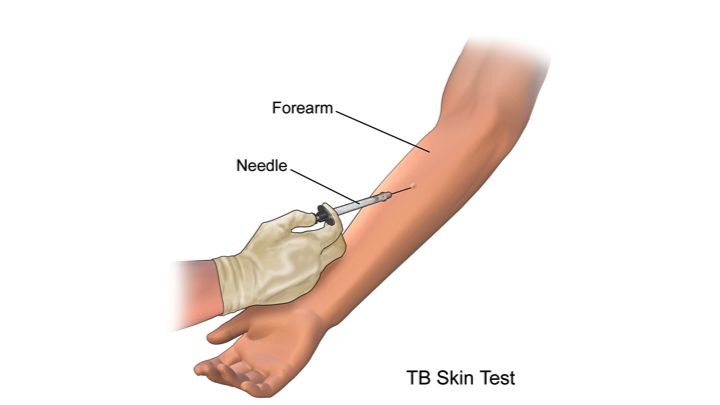 Контроль проращивается на воде без добавления химического мутагенного фактора |
| Биологический фактор: |
| Аналогично предыдущему |
Для чистоты эксперимента допустимо использование дистиллированной воды. При этом луковица будет расти за счёт внутренних питательных резервов. Ограничение тут в том, что дистиллированная вода является мутагеном. Однако и в контроле, и в опыте в этом случае ущерб от дистиллированной воды будем считать равным, как и прочие фоновые условия.
Луковицы проращиваются от 3 до 4 дней. Желательно использовать емкости диаметром 1,5 см и высотой 10 см, чтобы по мере роста корни не упирались в дно ёмкости, в которой они находятся. Иначе это может приводить к некоторым биологическим эффектам — реакция меристемы на препятствие. Для проведения ана-телофазного анализа берут часть корешка длиной около 1 см. Проводят процедуру фиксации (для долговременного хранения). При необходимости корешки отмывают от фиксатора в воде, затем окрашивают ацеторсеином согласно стандартной методике. Для микроскопирования используют кончик корня длиной 1-2 мм — зона активного деления меристематических клеток.
Для проведения ана-телофазного анализа берут часть корешка длиной около 1 см. Проводят процедуру фиксации (для долговременного хранения). При необходимости корешки отмывают от фиксатора в воде, затем окрашивают ацеторсеином согласно стандартной методике. Для микроскопирования используют кончик корня длиной 1-2 мм — зона активного деления меристематических клеток.
Фиксация[править]
Для фиксации корешки помещают в емкости с фиксатором Кларка (см.выше). Емкости герметично закрывают и оставляют для фиксации клеток на 1-2 дня. Затем материал промывают два раза от фиксатора в 70% спирте, и помещают в емкости с 70% спиртом для долговременного хранения. Спирт должен превосходить материал по объему в 4-5 раз.
Окрашивание материала[править]
Окраску корешков производят 2 % ацетоорсеином (см. выше). Корешки отмывают от спирта в воде (удобно в чашках Петри). Материал переносят в небольшие фарфоровые тигли с держателем, которые на 2/3 заполняют красителем. Тигель накрывают предметным стеклом. Нагревают над пламенем спиртов до тайного кипения (запотевание покровного стекла). Тигель с материалом оставляют на некоторое время для прокрашивания хромосом (от 2 часов до 1 суток). После этого можно готовить препараты для микроскопирования.
Нагревают над пламенем спиртов до тайного кипения (запотевание покровного стекла). Тигель с материалом оставляют на некоторое время для прокрашивания хромосом (от 2 часов до 1 суток). После этого можно готовить препараты для микроскопирования.
Методика приготовления препаратов для микроскопического анализа[править]
Готовят временные давленые препараты корневых меристем. Для этого от окрашенного корешка лезвием отрезают кончик меристемы длинной 2-3 мм (кончик отличается по более темной окраске и утолщением), помещают на предметное стекло в каплю 45% уксусной кислоты, накрывают покровным стеклом и с помощью спички аккуратно раздавливают до получения монослоя клеток. Препараты анализируют под микроскопом при увеличении 12,5х1,5х40. На препаратах рассматривают мелкие, округло-квадратной формы клетки с хорошо прокрашенными ядрами и неповрежденными клеточными стенками.
Макроскопические исследования: скринниг-тест[править]
Перед генетическим анализом следует провести первичный скриннинг-тест, который сразу покажет обладает ли фактор выраженной биологической активностью. Основным и наиболее важным изучаемым макропараметром является рост корней. Но помимо него могут еще изучаться другие параметры:
Основным и наиболее важным изучаемым макропараметром является рост корней. Но помимо него могут еще изучаться другие параметры:
- Тургесценция. Твердость кончиков корней связана со степенью токсичности фактора. При высокой токсичности фактора тургесценция падает, что может привести к гибели корней.
- Изменение цвета. В течение эксперимента может меняться цвет корей и причина тому — содержание в воде определенных солей (например сине-зеленый от медного купопроса). Кроме того кончики корней могут стать коричневыми, что связанно с токсическим эффектом фактора, вызывающим клеточную смерть.
В качестве стандартных исследуются следующие параметры:
- Форма корней. Разбухание кончиков корней после 4-5 дней воздействия, свидетельствует об особом типе нарушения с-митозе. Изгиб корней или их кончиков происходит как правило после воздействия растворов определенных солей.
- Длина корней. Это значение средней длины корней (для 1 луковицы).
Методика измерения длины корней[править]
Измерить длину корней можно двумя способами:
- Обычно длина корневой системы измеряется снаружи емкости с помощью рулетки (измерение для каждой луковицы).
 Этот метод позволяет проводить измерения в течение эксперимента.
Этот метод позволяет проводить измерения в течение эксперимента. - Более точным является второй способ. По окончании эксперимента корни срезаются у луковицы под основание, измеряется длина каждого корешка, вычисляется среднее значение (среднее значение для каждой луковицы). Поврежденные корни не учитываются. Затем устанавливается среднее значение длины корней для всей выборки луковиц.
Вычисление параметра корневого прироста[править]
Рассчитывается средняя длина корней для каждой луковицы в опытных и контрольных сериях экспериментов. Затем вычисляется общее среднее значение длины для опытной серии и контрольной. Вычисляется во сколько раз длина корней в опытной серии больше/меньше чем в контрольной и выражается в процентах. Статистическую обработку результатов проводят с использованием дисперсионного анализа.
Изменение длины корней в Allium test-е является показателем токсичности. Это очень чувствительный показатель, который легко регистрируется визуально и не требует никаких специальных реактивов и аппаратуры, хорошо коррелирует с микроскопическими параметрами и потому предложен в качестве краткосрочного скриннинг-теста. Если происходит значительное угнетение роста корней по сравнению с контролем, то отмечают токсический эффект воздействующего фактора. В случае значительного прироста корней, говорят о стимулирующем эффекте.
Если происходит значительное угнетение роста корней по сравнению с контролем, то отмечают токсический эффект воздействующего фактора. В случае значительного прироста корней, говорят о стимулирующем эффекте.
Микроскопические исследования и статистическая обработка[править]
Расчет частоты мутаций[править]
В Allium test для расчета частоты мутаций традиционно применяется метод ана-телофазного анализа частоты хромосомных аберраций. На стадии ана- телофазы регистрируются мутации, связанные с грубым нарушением структуры хромосом, а так же с повреждением митотического веретена (веретена деления) или изменением поведения хромосом на веретене деления[28]:
- отставания хромосом,
- аберрантные митозы:
- трёхполюсные митозы,
- четырёхполюсные митозы,
- несимметричные митозы.
Рекомендации[править]
При оценке мутагенной активности химических веществ достаточно использовать лишь W:ана-телофазный анализ, то есть регистрировать мутации в фазах митоза, так как меристемы в течение всего опыта находятся в контакте с воздействующим фактором. Но при изучении мутагенной активности ЭМИ этого оказалось недостаточно, поскольку воздействию излучения корневые меристемы подвергаются лишь некоторый период времени. В промежутках между облучениями происходит преобразование индуцированных в анафазе и телофазе хромосомных фрагментов — клетки выходят из митоза и переходят в интерфазу, а фрагменты становятся микроядрами. В результате эти мутации остаются неучтенными. В связи с этим была предложена модификация метода Allium test, которая позволяет учитывать всю сумму мутаций. На одном препарате было рекомендовано применять W:ана-телофазный анализ и микроядерный тест. При этом анализируется вся совокупность клеток (делящиеся и не делящиеся), что позволяет избежать ложноотрицательных ответов и дает более достоверные результаты [14].
Но при изучении мутагенной активности ЭМИ этого оказалось недостаточно, поскольку воздействию излучения корневые меристемы подвергаются лишь некоторый период времени. В промежутках между облучениями происходит преобразование индуцированных в анафазе и телофазе хромосомных фрагментов — клетки выходят из митоза и переходят в интерфазу, а фрагменты становятся микроядрами. В результате эти мутации остаются неучтенными. В связи с этим была предложена модификация метода Allium test, которая позволяет учитывать всю сумму мутаций. На одном препарате было рекомендовано применять W:ана-телофазный анализ и микроядерный тест. При этом анализируется вся совокупность клеток (делящиеся и не делящиеся), что позволяет избежать ложноотрицательных ответов и дает более достоверные результаты [14].
Расчет митотического и фазных индексов[править]
Расчёт митотических индексов можно проводить на тех же препаратах, что и W:ана-телофазный анализ. Просматривается от 400 до 600 клеток (больше — лучше). Подсчитывается общее количество делящихся клеток и отдельно клетки на разных стадиях W:митоза.
Подсчитывается общее количество делящихся клеток и отдельно клетки на разных стадиях W:митоза.
| Обозначение фазы / индекса | Характеристика | Расчёт индекса |
|---|---|---|
| митотический (mitotic) индекс (MI, %)
| MitoticI=(P+M+A+T)N∗100%{\displaystyle {\mbox{MitoticI}}={\frac {\mbox{(P+M+A+T)}}{\mbox{N}}}*100\%}
|
| W:профаза (prophase)
| PI=P(P+M+A+T)∗100%{\displaystyle {\mbox{PI}}={\frac {\mbox{P}}{\mbox{(P+M+A+T)}}}*100\%}
|
| W:метафаза (metaphase)
| MetaphaseI=M(P+M+A+T)∗100%{\displaystyle {\mbox{MetaphaseI}}={\frac {\mbox{M}}{\mbox{(P+M+A+T)}}}*100\%}
|
| W:анафаза (anaphase)
| AI=(A)(P+M+A+T)∗100%{\displaystyle {\mbox{AI}}={\frac {\mbox{(A)}}{\mbox{(P+M+A+T)}}}*100\%}
|
| W:телофаза (telophase)
| TI=(T)(P+M+A+T)∗100%{\displaystyle {\mbox{TI}}={\frac {\mbox{(T)}}{\mbox{(P+M+A+T)}}}*100\%}
|
| ана- телофаза
| A-TI=(A+T)(P+M+A+T)∗100%{\displaystyle {\mbox{A-TI}}={\frac {\mbox{(A+T)}}{\mbox{(P+M+A+T)}}}*100\%}
|
Статистическая обработка данных[править]
Проводиться с использованием математических пакетов (Statistica, MS Excel).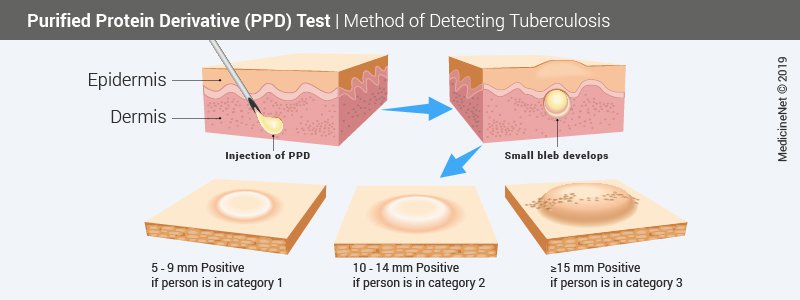 Для статистического анализа данных, полученных методом Allium test (частота хромосомных аберраций и микроядер, фазных индексов и т. д.) была разработана самовычисляющая электронная таблица на основе MS Excel. Она дает возможность эффективно группировать данные на листе, предоставляет выходные данные в удобном для обработки и использования виде, а так же позволяет в будущем наращивать функционал таблицы[29].
Для статистического анализа данных, полученных методом Allium test (частота хромосомных аберраций и микроядер, фазных индексов и т. д.) была разработана самовычисляющая электронная таблица на основе MS Excel. Она дает возможность эффективно группировать данные на листе, предоставляет выходные данные в удобном для обработки и использования виде, а так же позволяет в будущем наращивать функционал таблицы[29].
Источники информации[править]
Примечания[править]
- ↑ Д. С. Песня, А. В. Романовский, И. М. Прохорова, Т. К. Артѐмова, М. И. Ковалѐва, А. Н. Фомичева, Е. С. Кондакова, К. М. Халюто, С. А. Вакорин ИССЛЕДОВАНИЕ МУТАГЕННОГО ЭФФЕКТА МОДУЛИРОВАННОГО УВЧ ИЗЛУЧЕНИЯ СОТОВЫХ ТЕЛЕФОНОВ НА РАСТИТЕЛЬНЫХ И ЖИВОТНЫХ ОРГАНИЗМАХ IN VIVO (рус.). — 2010. — С. 924-929.
- ↑ а б Арефьев В.А., Лисовенко Л.А. Англо-русский толковый словарь генетических терминов. — ВНИРО, 1995. — 407 с.
- ↑ а б Fiskesjо G.
 The Allium Test as a standard in environmental monitoring // Hereditas. — 1985. — Т. 102. — С. 99-112.
The Allium Test as a standard in environmental monitoring // Hereditas. — 1985. — Т. 102. — С. 99-112. - ↑ Sharma C.B. Plant meristems as monitors of genetic toxicity of environmental chemicals // Current science. — 1983. — Т. 52. — № 81. — С. 1000-1002.
- ↑ а б в Прохорова И. М., Фомичёва П. Н., Ковалёва М. И. и др. Особенности пространственной динамики мутагенной активности воды р. Которосль и оз. Неро. // Современные проблемы биологии, экологии, хмимии : Региональный сборник научных трудов. — Ярославль: 2005. — С. 118-119.
- ↑ Constantin M.J., Owens E.T. Introduction and perspectives of plant genetic and cytogenetic assay // Mutat. Res.. — 1982. — С. 1-12.
- ↑ WHO World Health Organization monographs on selected medicinal plants // World Health Organization. — Geneva: 1999. — Т. 1.
- ↑ а б Abu, Ngozi E.
 and Mba, K. C. Mutagenecity testing of phamarceutical effluents on Allium cepa root tip meristems // Toxicology and Environmental Health Sciences. — Academic journals, 2011. — № 3(2). — С. 44-51.
and Mba, K. C. Mutagenecity testing of phamarceutical effluents on Allium cepa root tip meristems // Toxicology and Environmental Health Sciences. — Academic journals, 2011. — № 3(2). — С. 44-51. - ↑ Прохорова И.М. Растительные тест-системы для оценки мутагенов / Сост. И.М. Прохорова. — Ярославль: ЯрГУ, 1988. — 13 с.
- ↑ Paola Poli, Annamaria Buschini, Francesco Maria Restivo, Antonella Ficarelli, Francesca Cassoni1, Iliana Ferrero and Carlo Rossi Comet assay application in environmental monitoring: DNA damage in human leukocytes and plant cells in comparison with bacterial and yeast tests // Mutagenesis. — Oxford University Press: Oxford Journals, 1999. — № 14(6). — С. 547-556.
- ↑ Karl Sax The Behavior of X-Ray Induced Chromosomal Aberrations in Allium Root Tip Cells // Getetics : статья. — Harvard University: 1941. — № 26(4). — С. 418-425.
- ↑ С. А. Мамедли, академик НАН Украины Д. М. Гродзинский Роль типа опыления в проявлении радиационно-индуцированной нестабильности генома у растений // Доповiдi Нацiональної академiї наук України.
 — Национальная Академия Наук Украины, 2007. — № 7. — С. 165-170.
— Национальная Академия Наук Украины, 2007. — № 7. — С. 165-170. - ↑ Романовский А., Песня Д., Прохорова И. Мутагенное действие мобильного телефона // перечень публикаций
- ↑ а б Песня Д.С., Романовский А.В., Прохорова И.М. Разработка методики для оценки влияния УВЧ излучения сотовых телефонов и других приборов с ЭМИ на организмы in vivo // Ярославский Педагогический Вестник. — Ярославль: ЯГПУ им. К.Д. Ушинского, 2010. — Т. 3 (Естественные науки). — № 3. — С. 80-84.
- ↑ Песня Д.С., Романовский А.В., Прохорова И.М., Артёмова Т.К., Ковалева М.И., Фомичева А.Н., Соколов С.А., Кондакова Е.С., Шешина К.А., Вакорин С.А. Исследование биологического эффекта модулированного УВЧ излучения на растительных и животных организмах in vivo // Биомедицинские технологии и радиоэлектроника : статья. — Москва: Радиотехника, 2011. — № 4. — С. 34-45.
- ↑ Mirta Tkalec, Krešimir Malarić, Mirjana Pavlica, Branka Pevalek-Kozlina and Željka Vidaković-Cifrek Effects of radiofrequency electromagneti fields on seed germination and root meristematic cells of Allium cepa L.
 // Mutation Research/Genetic Toxicology and Environmental Mutagenesis. — Elsevier B.V., 2009. — № 642(2). — С. 76-81.
// Mutation Research/Genetic Toxicology and Environmental Mutagenesis. — Elsevier B.V., 2009. — № 642(2). — С. 76-81. - ↑ Olorunfemi D., Iogieseri U. M., Akinboro A. Genotoxicity Screening of Industrial Effluents using Onion bulbs (Allium cepa L.) // Appl. Sci. Environ.. — JASEM, 2011. — С. 211 — 216.
- ↑ de Rainho CR, Kaezer A, Aiub CA, Felzenszwalb I. Ability of Allium cepa L. root tips and Tradescantia pallida var. purpurea in N-nitrosodiethylamine genotoxicity and mutagenicity evaluation // An. Acad.Bras. Cienc.. — 2010. — С. 925 — 932.
- ↑ K. Klancnik, D. Drobne, J. Valant, J. Dolenc Koc Use of a modified Allium test with nanoTiO2 // Ecotoxicology and Environmental Safety. — Elsevier B.V., 2010.
- ↑ K. Babu, M. Deepa, S. G. Shankar & S. Rai Effect of Nano-Silver on Cell Division and Mitotic Chromosomes: A Prefatory Siren // The Internet Journal of Nanotechnology. — ISPUB, 2008.
- ↑ Aganović-Musinović I, Todić M, Becić F, Kusturica J. Genotoxicity evaluation of paracetamol applying Allium test // Medical Arh.. — 2004. — № 58(4). — С. 206-9.
- ↑ Aşkin Celik T., Aslantürk O.S. Evaluation of cytotoxicity and genotoxicity of Inula viscosa leaf extracts with Allium test // J. Biomed. Biotechnol.. — 2010.
- ↑ Magda I. Soliman Genotoxicity testing of neem plant (Azadirachta indica A. Juss) using the Allium cepa chromosome aberration assay // Biological Science. — Asian Network for science information, 2001. — № 1(11). — С. 1021-1027.
- ↑ Barbério A, Barros L, Voltolini JC, Mello ML. Evaluation of the cytotoxic and genotoxic potential of water from the River Paraíba do Sul, in Brazil, with the Allium cepa L. test // Braz. J. Biol.. — 2009. — № 69(3). — С. 837-842.
- ↑ Sandra Radić,, Draženka Stipaničev, Valerija Vujčić, Marija Marijanović Rajčić,Siniša Širac, Branka Pevalek-Kozlina The evaluation of surface and wastewater genotoxicity using the Allium cepa test // Science of the Total Environment. — Elsevier B.V., 2009. — № 408. — С. 1228-1233.
- ↑ D. Lerda, M. Biagi Bistoni, P. Pelliccioni & N. Litterio Allium cepa as a biomonitor of ochratoxin A toxicity and genotoxicity // Plant biology. — 2010. — № 58(4).
- ↑ W.M. Howell, G.E. Keller III, J.D. Kirkpatrick, R.L. Jenkins, R.N. Hunsinger and E.W. McLaughlin Effects of the plant steroidal hormone, 24-epibrassinolide, on the mitotic index and growth of onion (Allium cepa) root tips // Genet. Mol. Res.. — Samford University: GMR, 2007. — № 6(1). — С. 50-58.
- ↑ Песня Д.С., Романовский А.В. Митоз в растительной клетке: норма и патология : Научно-практические пособие. — Москва: JRE – ИРЭ им. В.А.Котельникова РАН, 2010. — С. 929.
- ↑ Романовский А.В., Песня Д.С., Эффективное использование электронных таблиц на примере генотоксикологических исследований проб воды // Биология внутренних вод: Материалы XIV международной школы-конференции молодых ученых. — Борок, ИБВВ им. И.Д. Папанина РАН: Принтхаус, 2010. — С. 120-127.
Ошибка цитирования Тег <ref> с именем «Ivanov71», определённый в <references>, не используется в предшествующем тексте.
Ошибка цитирования Тег <ref> с именем «Tarasov94», определённый в <references>, не используется в предшествующем тексте.
Ошибка цитирования Тег <ref> с именем «INPS», определённый в <references>, не используется в предшествующем тексте.
Ошибка цитирования Тег <ref> с именем «NANO2», определённый в <references>, не используется в предшествующем тексте.
Литература[править]
Fiskesjö, Geirid Биотестирование с помощью лука обыкновенного = Protocol № 8. Allium test. — Швеция: Институт генетики Лундского университета, сентябрь 1989.
Fiskesjö, Geirid Allium screening test = Fiskesjo G., The Allium test as a standard in environmental monitoring, Hereditas., V. 102, 1985, pp. 99‑112. — Швеция: Институт генетики Лундского университета, сентябрь 1989.
Саркома Юинга (краткая информация)
Саркома Юинга — это злокачественная опухоль, которой могут заболеть дети и подростки. В этом тексте Вы получите важную информацию о болезни, о её формах, как часто ею заболевают дети и почему, какие бывают симптомы, как ставят диагноз, как лечат детей и какие у них шансы вылечиться от этой формы рака.
автор: Maria Yiallouros, erstellt am: 2009/02/12, редактор: Dr. Natalie Kharina-Welke, Разрешение к печати: Prof. Dr. med. Uta Dirksen, Prof. Dr. md. U. Creutzig, Переводчик: Dr. Natalie Kharina-Welke, Последнее изменение: 2019/10/29 doi:10.1591/poh.patinfo.ewing.kurz.20101215
Что такое саркома Юинга?
Саркома Юинга – это злокачественная солидная опухоль. Чаще всего она вырастает в костях. Реже она может вырастать в мягких тканях, то есть в соединительных тканях, в жировых, мышечных, или в тканях периферических нервов. Болезнь была названа по имени нью-йоркского исследователя рака Джеймса Юинга (1866-1943), который впервые описал эту опухоль в 1920 году.
Существует целое семейство опухолей саркомы Юинга. В него входят, например, классическая саркома Юинга (в зарубежной литературе принято сокращённое обозначение EWS) и периферические примитивные нейроэктодермальные опухоли (в зарубежной литературе их обозначают PPNET или pPNET; на русском языке можно встретить сокращение ППНЭО, не путать с ПНЭО, опухолями головного мозга). Чаще всего саркомы Юинга растут и дают метастатзы настолько быстро, что без эффективного лечения эта болезнь смертельна.
Как часто у детей встречается саркома Юинга?
Саркомы Юинга встречаются редко. В Германии из 1.000.000 детей в возрасте до 15 лет заболевают 3 ребёнка в год (по статистике всех детей в Германии это около 40 заболевших детей в год). Из 1.000.000 подростков и молодёжи в возрасте от 15 до 25 лет в год заболевает около 2,4 человек.
Больше половины всех заболевших – это дети и подростки в возрасте между 10 и 20 годами. Пик приходится на подростковый возраст — 12 -17 лет. Но саркома Юинга может вырастать и у грудных детей, и у детей младшего возраста, и у школьников, и даже у очень пожилых людей. Мальчики и мужчины по статистике заболевают чаще, чем девочки (соотношение 1,3:1).
Где и как вырастает саркома Юинга?
В принципе в любой кости может появиться саркома Юинга. Чаще всего опухоль вырастает в тазовых костях, далее по частоте появления следуют длинные трубчатые кости бедра и голени, и затем идут рёбра.
Опухоль может разрастаться и внутри кости, в которой они появилась, и в мягких тканях вокруг кости. В редких случаях саркома Юинга вырастает сразу в мягких тканях [мягкие ткани], то есть опухоли нет в кости. В этом случае специалисты говорят о внекостной саркоме Юинга (также используется термин экстраоссальная саркома Юинга).
Саркомы Юинга растут быстро и очень рано дают метастазы. Примерно у четверти заболевших детей во время диагностики уже есть метастазы, которые видны на снимках. Чаще всего они бывают в лёгких, но их также находят и в костях, и в костном мозге [костный мозг]. Кроме этого почти у всех детей есть так называемые микрометастазы. Это такие самые мельчайшие метастазы, которые не способна увидеть никакая визуальная диагностика.
Какие бывают виды опухоли? Что мы знаем о её микроскопических (гистологических) особенностях?
Саркомы Юинга относятся к примитивным [примитивный] злокачественным опухолям. До сих пор точно не известно, какая именно клетка начинает мутировать и в результате начинает вырастать эта опухоль. Современные исследования говорят о том, что клетки саркомы Юинга вырастают из незрелых (или на языке специалистов недифференцированных) клеток ткани, это так называемые мезенхимальные стволовые клетки.
Понять, заболел ли ребёнок саркомой Юинга, или другой злокачественной опухолью, которая тоже состоит из недифференцированных опухолевых клеток (например, это могут быть нейробластома, медуллобластомы, неходжкинские лимфомы, саркомы мягких тканей и ретинобластома), можно только проведя гистологический анализ и специальные молекулярно-генетические [молекулярно-генетический] исследования. Так как все эти виды рака встречаются достаточно редко, то такую диагностику, как правило, способны выполнить только специализированные лаборатории.
В зависимости от микроскопических (гистологических) особенностей опухолевой ткани, а также от того, в каком именно месте выросла опухоль, в семействе сарком Юинга выделяют следующие типы:
- классическая сарокма Юинга (в западной литературе принято сокращение EWS)
- периферическая примитивная нейроэктодермальная опухоль (на русском языке может называться ППНЭО, в зарубежных источниках принято сокращение PPNET или pPNET)
- опухоль Аскина (опухоли грудной стенки)
- внекостная саркома Юинга
Почему дети заболевают саркомой Юинга?
Никто точно не знает, почему дети заболевают саркомой Юинга. Ни какие-то внешние факторы воздействия на организм (например, когда ребёнок ранее получал лучевую терапию [облучение]), ни какие-то наследственные генетические [генетический] факторы (наследственная предрасположенность) не имеют большого значения.
Известно, что у раковых клеток саркомы Юинга есть определённые хромосомные изменения. Эти изменения всегда затрагивают определённый ген на 22-ой хромосоме. Этот ген так и называется ген саркомы Юинга (также можно встретить его друое название EWS-ген). В результате, когда изменения приводят к генной поломке, это приводит к тому, что здоровая клетка становится раковой. Но принципиально все такие генные изменения, которые нашли в ткани опухоли, не передаются по наследству.
Какие бывают симптомы болезни?
Наиболее часто встречающимся симптомом, который появляется из-за саркомы Юинга, являются боли и припухлость в том, месте, где растёт опухоль.
Боли появляются спонтанно. Обычно болеть начинает тогда, когда ребёнок что-то делает с физической нагрузкой. Но часто эти боли ночью полностью не уходят. Чем больше растёт опухоль, то кроме болей у ребёнка становится видна припухлость, либо если припухлость ещё не видна, её уже можно прощупать. Иногда эта зона роста опухоли может быть покрасневшей. А сам участок организма перестаёт нормально работать. Нередко эти симптомы врачи сначала ошибочно воспринимают за болезни роста, воспаление костей или как результат какой-то спортивной травмы.
Но так как саркомы Юинга могут вырастать практически в любой кости и в мягких тканях, то в каждом отдельном случае другие симптомы могут сильно отличаться. Например, если опухоль растёт в области позвоночника или периферических нервов [периферическая нервная система], то у ребёнка в первую очередь могут появиться такие отклонения как потеря двигательной способности (паралич). Если опухоль растёт в тазовых костях, или в районе груди, или же в бедренных костях, то очень долгое время она не даёт каких-то явных симптомов и остаётся незамеченной.
Примерно у трети заболевших детей, у которых появляются такие общие симптомы как повышение температуры, болезненное самочувствие, общая усталость и утомляемость, они начинают худеть, болезнь может находиться уже на поздней стадии. С того момента, когда у ребёнка появились первые симптомы, до того времени, когда ему поставили точный диагноз, может пройти от несколких недель до нескольких месяцев.
Те симптомы у детей и подростков, о которых мы здесь пишем, не обязательно говорят о том, что у ребёнок заболел саркомой Юинга или каким-то другим раком костей. Тем не менее, если у ребёнка или у подростка появляются боли в костях, мы обязательно рекомендуем обратиться к опытному педиатру и выполнить полную диагностику. Чтобы точно быть уверенным в том, что это не онкология.
Как ставят диагноз саркома Юинга?
Если педиатр (или другой специалист) подозревает из истории болезни ребёнка (анамнез) и по результатам наружного осмотра [наружный осмотр] злокачественную опухоль костей, то врач направляет ребёнка в клинику, которая специализируется на лечении рака у детей и подростков (детский онкологический центр/ клиника детской онкологии и гематологии).
Потому что, если подозревают такую опухоль, то полное обследование проводят специалисты разного профиля. Во-первых, они должны подтвердить диагноз, действительно ли у ребёнка злокачественная опухоль костей. Во-вторых, если диагноз подтверждается, они должны сказать, какой конкретный тип опухоли у ребёнка и насколько болезнь успела распространиться по организму. Только ответив на эти вопросы, можно оптимально спланировать тактику лечения и давать прогноз.
Какая необходима визуальная диагностика (диагностика по снимкам)?
Если подозревают рак костей, то чаще всего уже на рентгеновских снимках видны изменения, типичные для болезни. Подозрение на злокачественную опухоль костей чаще всего подтверждают рентгеновские снимки. Дополнительно с помощью таких методов диагностики по снимкам как магнитно-резонансная томография (МРТ) и/или компьютерная томография (КТ) можно точно оценить размер опухоли, где именно она выросла, а также увидеть границы опухоли с соседними структурами (например, с мышцами и сухожилиями, или суставными сумками).
Также на этих снимках можно хорошо рассмотреть близко расположенные метастазы, так называемые „прыгающие“ метастазы ( на языке специалистов „скип“-метастазы). Снимки МРТ (по сравнению со снимками КТ) дают более точную информацию о том, есть ли опухоль внутри костного мозга и в мягких тканях. Поэтому на этапе начальной диагностики врачи предпочитают работать с ними, а также с рентгеновскими снимками костей.
Как исследуют ткань опухоли?
Чтобы окончательно подтвердить диагноз саркомы Юинга, обязательно берут образец опухолевой ткани (биопсия), который исследуют разные специалисты. Биопсию должны выполнять только те специалисты, которые потом будут делать операцию саркомы, или у которых есть опыт оперировать саркомы. Потому что от того, как сделали биопсию, зависит дальнейшая операция. Любая биопсия сначала открывает доступ к самой опухоли. Если этот доступ был запланирован и выполнен неправильно, то это ведёт к дальнейшим проблемам в лечении. В худшем случае к тому, что запланированную дальнейшую операцию придётся выполнять гораздо в большем объёме, чем это было бы нужно изначально.
Как ищут метастазы?
Чтобы найти метастазы, делают рентгеновские снимки и компьютерную томографию лёгких, а также сцинтиграфию [сцинтиграфия] костей. В некоторых случаях также могут помочь снимки ПЭТ (позитронно-эмиссионная томография). Чтобы выяснить, попали раковые клетки в костный мозг, или нет, необходимо также сделать пункцию костного мозга. В зависимости от каждого конкретного случая болезни и от того, как проходит лечение, могут потребоваться дополнительные исследования и анализы.
Исследования и анализы до курса лечения: До начала лечения у детей проверяют, как работает сердце (эхокардиограмма – ЭхоКГ), проверяют слух (аудиометрия), почки и лёгкие, а также делают разные анализы крови. Если во время лечения наступают какие-то изменения, то их обязательно сравнивают с начальными результатами обследования. В зависимости от этого тактика лечения может корректироваться.
Результаты всей диагностики должны показать, какая именно опухоль появилась у ребёнка, где именно она выросла и насколько опухоль уже успела разойтись по организму. По этим результатам составляют максимально возможный индивидуальный план лечения ребёнка (врачи называют его риск-адаптированное лечение.
Как составляют план лечения?
После того, как поставили окончательный диагноз, врачи составляют план лечения. Специалисты, которые ведут ребёнка, составляют индивидуальную программу лечения (т.н. риск-адаптированное лечение), в которой учитываются определённые моменты. Их называют факторами риска (прогностические факторы), и от них зависит прогноз болезни.
Важные прогностические факторы у детей с саркомой Юинга – это конкретный тип опухоли, где именно она выросла и насколько она уже успела разойтись по организму (то есть находится ли саркома только в одном месте, или она уже дала метастазы). Ответы на эти вопросы даёт та диагностика, о которой мы рассказали выше. Также большое значение имеет то, насколько опухоль можно удалить хирургическим путём (то есть полностью, или нет), и как болезнь отвечает на химиотерапию [химиотерапия].
Всё это учитывается, когда врачи составляют план лечения. Его цель – получить максимально эффективные результаты лечения.
Как лечат саркому Юинга?
Лечение детей с саркомой Юинга состоит из операции [операция] и/или лучевой терапии [облучение] (эти виды лечения называются на языке специалистов локальной терапией), а также из курсов химиотерапии [химиотерапия]. Курсы химиотерапии выполняют потому, что в прошлом, когда детей только оперировали и облучали, то врачи убирали таким образом только саму опухоль. Но потом почти у всех детей появлялись метастазы. Поэтому нужен такой вид лечения, который будет действовать на весь организм, а не только на какой-то конкретный участок. Обычно локальную терапию делают между двумя блоками химиотерапии. В общей сложности курс лечения длится приблизительно от 10 до 12 месяцев.
Лечение делится на несколько этапов:
Этап химиотерапии до начала локальной терапии
Лечение начинается с курса интенсивной химиотерапии, который длится несколько недель. Этот курс также называют индукционной химиотерапией. Его цель – уменьшить размер опухоли и количество метастазов, если они видны на снимках, а также убить возможные метастазы, которые не видны. Это помогает сделать операцию более щадящей и более безопасной, и одновременно максимально эффективной. Кроме того химиотерапия способна убивать даже самые маленькие, ещё невидимые микрометастазы, и таким образом блокировать дальнейший рост опухоли.
Чтобы убить по возможности все раковые клетки, используют комбинацию из нескольких препаратов. Эти медикаменты задерживают рост клеток (цитостатики). Они уже доказали свою наибольшую эффективность у детей с саркомой Юинга. В первую очередь это такие препараты, как винкристин, ифосфамид, доксорубицин (= адриамицин) и этопозид.
Дети получают цитостатики в виде инфузии [инфузия] в течении нескольких блоков. Блок длится несколько дней. В это время дети лежат в больнице. В перерывах между курсами/блоками химиотерапии их обычно отпускают домой. Только если у ребёнка появляются тяжёлые побочные эффекты (осложнения), его снова кладут в больницу (стационарное лечение).
Локальная терапия
NЕщё когда не закончились полностью блоки химиотерапии, или самое позднее сразу после химиотерапии начинают локальную терапию. Её предпочтительным видом является операция. Цель операции – по-возможности полностью удалить опухоль. Однако часто полностью удалить опухоль невозможно. Потому что она выросла в таком месте, которое является функционально важной частью тела, то есть без него невозможна нормальная работа организма. Поэтому дополнительно необходимо делать лучевую терапию. В некоторых случаях врачи вместо операции вынуждены идти только на лучевую терапию. Как оба эти виды лечения могут сочетаться друг с другом и в каком объёме они будут проводиться, зависит от каждой индивидуальной ситуации. Поэтому врачи в каждом конкретном случае принимают максимально оптимальное решение для ребёнка.
Специалисты, которые отвечают за лечение ребёнка, проинформируют семью, какая именно операция будет выполняться, как это будет происходить, или расскажут о том, как будет проходить этап облучения. Если опухоль выросла на руках, или на ногах, то сегодня прогресс в лечении конечностей позволяет делать органосберегающие операции. А дополнительное лечение курсами химиотрапии и/или лучевой терапии позволяет отказаться от ампутации.
Сразу после операции патомофолог исследует саму опухоль. Он должен оценить, как опухоль ответила на курсы химиотерапии. Для этого он смотрит, сколько живых раковых клеток ещё осталось в опухоли. Если их меньше 10 %, то врачи говорят о хорошем ответе на лечение. А если их 10% и больше, то специалисты говорят о плохом ответе на лечение. Если во время постановки диагноза у ребёнка уже были метастазы, то их по-возможности также пролечивают локально, как и саму опухоль (на языке специалистов первичная опухоль). То есть их удаляют во время операции и/или облучают.
Этап химиотерапии после локальной терапии
После локальной терапии продолжается химиотерапия. Этот этап называется консолидирующая химиотерапия. Насколько курсы химиотерапии будут интенсивными, зависит от того, как болезнь отвечала на химиотерапию до локального лечения, а также какой был размер начальной опухоли в момент постановки диагноза, и были ли у ребёнка метастазы в тот период времени.
Если был хороший ответ, или начальная опухоль была маленького размера (то есть объём опухоли был меньше 200 мл), то также, как и на первом этапе, ребёнок несколько раз получает блоки химиотерапии из нескольких цитостатиков. Обычно это комбинации из таких препаратов как винкристин, актиномицин D и циклофосфамид, или комбинация из винкристина, актиномицина D и ифосфамида.
Если на этапе индукционной химиотерапии был плохой ответ, или начальная опухоль была большого размера (то есть объём опухоли был больше 200 мл), то по исследовательскому протоколу по саркоме Юинга рекомендуется высокодозная химиотерапия и сразу же за ней трансплантация костного мозга. Исследователи изучают полученные результаты и сравнивают их с теми, когда пациенты получали курсы стандартной химиотерапии. Этот принцип интенсивного лечения также рекомендуется детям, у которых на момент диагноза уже были метастазы.
В некоторых случаях сразу после курсов химиотерапии или после курсов высокодозной химиотерапии детям дополнительно назначают лучевую терапию.
Как лечат рецидивы
Хотя методы лечения саркомы Юинга стали лучше и результаты выше, тем не менее у 30-40% детей обнаруживают рецидив. У детей с рецидивом прогноз хуже. Сегодня для них пока нет стандартной терапии. В зависимости от конкретной ситуации лечить рецидив могут курсами химиотерапии из нескольких препаратов, облучением, хирургическим путём, или же комбинируют эти виды лечения. Иногда врачи рассматривают также возможности высокодозной химиотерапии.
Если по результатам лечения видно, что невозможно полностью вылечить ребёнка, то на первый план выходит сохранение качества жизни. Врачи выполняют, например, обезболивающую терапию и поддерживают определённые функции организма (паллиативная терапия). Исследовательские протоколы работают над тем, как можно повысить шансы на выздоровление этих пациентов. По этим протоколам, например, детям дают новые медикаменты и проверяют их эффективность.
По каким протоколам лечат детей?
В мире во всех крупных лечебных центрах детей и подростков с саркомой Юинга и ППНЭО лечат по стандартизированным протоколам. В Германии такие программы/ протоколы лечения называются исследования оптимизации терапии. По ним лечат всех заболевших детей. Это клинические исследования, они контролируются. Их цель – увеличивать эффективность лечения (медики говорят о долговременной выживаемости). Одновременно они стремятся снижать осложнения от лечения и отдалённые последствия на организм ребёнка.
В Германии детей с болезнями из семейства саркомы Юинга (саркома Юинга, ППНЭО, опухоль Аскина, саркома мягких тканей) лечат по международному протоколу EWING 2008. По этому исследовательскому протоколу работают многочисленные детские клиники и детские онкологические центры по всей Германии, а также клиники других европейских стран, США, Австралии и Новой Зеландии. Центральный исследовательский офис немецкой группы находится в клинике детской и подростковой медицины при университете г. Мюнстер (руководитель: профессор др. мед. Хериберт Юргенс).
Какие шансы вылечиться от саркомы Юинга?
У детей и подростков с саркомой Юинга прогноз болезни зависит от нескольких причин. Главными из них являются: где именно выросла опухоль, какого она размера, насколько болезнь успела распространиться по организму к моменту постановки диагноза и как опухоль ответила на курс химиотерапии [химиотерапия] до операции.
За последние десятилетия результаты лечения саркомы Юинга достигли большого прогресса. Этого удалось достичь благодаря тому, что лечение стало комбинированным, были введены более интенсивные курсы химиотерапии, и всех заболевших детей стали лечить по единым протоколам (исследования оптимизации терапии).
Ещё в 1960-ые годы, когда детей лечили либо только лучевой терапией, либо операцией, выживало менее 10%. Сегодня, когда детей лечат комбинацией разных видов лечения (локальное лечение + химиотерапия), в среднем вылечивают около 65% детей, у которых в диагностике на снимках не было метастазов [метастазы]. О благоприятном прогнозе обычно говорят, если опухоль была полностью удалена хирургическим путём и болезнь хорошо отвечала на курс химиотерапии.
У детей, у которых в момент диагноза уже есть метастазы, прогноз в целом неблагоприятный даже несмотря на то, что они получают более интенсивные курсы химиотерапии (из них 5-летней выживаемости достигает в среднем около 25%). У детей с единичными метастазами в лёгких, которые можно хирургически удалить, шансы вылечиться выше, чем у детей с метастазами в костях или в костном мозге [костный мозг]. Также неблагоприятным является прогноз у тех детей, у которых болезнь возвращается, то есть наступает рецидив. Современные исследовательские протоколы стремятся найти новые подходы в лечении, чтобы улучшить шансы на выздоровление в том числе и этих пациентов.
Необходимое замечание: когда мы называем проценты выздоровевших детей, это значит, что мы даём только точную статистику по этой форме рака у детей. Но никакая статистика не может предсказать, выздоровеет конкретный ребёнок, или нет. Сам термин «выздоровление» надо понимать прежде всего как «отсутствие опухоли». Потому что современные методы лечения могут обеспечивать долговременное отсутствие злокачественной опухоли. Но у них есть нежелательные побочные эффекты и поздние осложнения. Поэтому детям после лечения нужна интенсивная реабилитация. Также им нужна ещё долгое время помощь от специалистов в онкоортопедии.
Список литературы:
- Juergens C, Weston C, Lewis I, Whelan J, Paulussen M, Oberlin O, Michon J, Zoubek A, Jürgens H, Craft A: Safety assessment of intensive induction with vincristine, ifosfamide, doxorubicin, and etoposide (VIDE) in the treatment of Ewing tumors in the EURO-E. W.I. N.G. 99 clinical trial. Pediatric blood & cancer 2006, 47: 22 [PMID: 16572419] JüR2006
- Kaatsch P, Spix C: German Childhood Cancer Registry — Jahresbericht / Annual Report 2015 (1980-2014). Institut für Medizinische Biometrie, Epidemiologie und Informatik (IMBEI), Universitätsmedizin der Johannes Gutenberg-Universität Mainz 2015 [URI: http://www.kinderkrebsregister.de/ dkkr/ ergebnisse/ jahresbericht/ jahresbericht-2015.html] KAA2015a
- Dirksen U, Jürgens H: Ewing-Sarkome des Kindes- und Jugendalters. S1-Leitlinie der Gesellschaft für Pädiatrische Onkologie und Hämatologie (GPOH) AWMF online 2014 [URI: https://www.awmf.org/ uploads/ tx_szleitlinien/ 025-006l_S1_Ewing_Sarkome_Kinder_Jugendliche_2014-06-abgelaufen.pdf] DIR2014
- Haeusler J, Ranft A, Boelling T, Gosheger G, Braun-Munzinger G, Vieth V, Burdach S, van den Berg H, Jürgens H, Dirksen U: The value of local treatment in patients with primary, disseminated, multifocal Ewing sarcoma (PDMES). Cancer 2010, 116: 443 [PMID: 19924786] HAE2010
- Burkhardt B, Reiter A, Landmann E, Lang P, Lassay L, Dickerhoff R, Lakomek M, Henze G, von Stackelberg A: Poor outcome for children and adolescents with progressive disease or relapse of lymphoblastic lymphoma: a report from the berlin-frankfurt-muenster group. Journal of clinical oncology 2009, 27: 3363 [PMID: 19433688] BUR2009
- Wagner LM, McAllister N, Goldsby RE, Rausen AR, McNall-Knapp RY, McCarville MB, Albritton K: Temozolomide and intravenous irinotecan for treatment of advanced Ewing sarcoma. Pediatric blood & cancer 2007, 48: 132 [PMID: 16317751] WAG2007
- Gerth HU, Juergens KU, Dirksen U, Gerss J, Schober O, Franzius C: Significant benefit of multimodal imaging: PET/CT compared with PET alone in staging and follow-up of patients with Ewing tumors. Journal of nuclear medicine : official publication, Society of Nuclear Medicine 2007, 48: 1932 [PMID: 18006618] GER2007
- Germeshausen M, Skokowa J, Ballmaier M, Zeidler C, Welte K: G-CSF receptor mutations in patients with congenital neutropenia. Current opinion in hematology 2008, 15: 332 [PMID: 18536571] GER2007
- Bernstein M, Kovar H, Paulussen M, Randall RL, Schuck A, Teot LA, Jürgens H: Ewing’s sarcoma family of tumors: current management. The oncologist 2006, 11: 503 [PMID: 16720851] BER2006
- Hunold A, Weddeling N, Paulussen M, Ranft A, Liebscher C, Jürgens H: Topotecan and cyclophosphamide in patients with refractory or relapsed Ewing tumors. Pediatric blood & cancer 2006, 47: 795 [PMID: 16411206] HUN2006
- Hawkins DS, Schuetze SM, Butrynski JE, Rajendran JG, Vernon CB, Conrad EU 3rd, Eary JF: [18F]Fluorodeoxyglucose positron emission tomography predicts outcome for Ewing sarcoma family of tumors. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 2005, 23: 8828 [PMID: 16314643] HAW2005
- Dirksen U, Poremba C, Schuck A: Knochentumoren des Kindes-und Jugendalters. Der Onkologe 2005, 10: 1034 DIR2005
- Niemeyer C, Kontny U: Tumoren der Ewing-Sarkom-Familie, in: Gutjahr P (Hrsg.): Krebs bei Kindern und Jugendlichen. Deutscher Ärzte-Verlag Köln 5. Aufl. 2004, 491 [ISBN: 3769104285] NIE2004
- Schuck A, Ahrens S, Paulussen M, Kuhlen M, Konemann S, Rube C, Winkelmann W, Kotz R, Dunst J, Willich N, Jürgens H: Local therapy in localized Ewing tumors: results of 1058 patients treated in the CESS 81, CESS 86, and EICESS 92 trials. Int J Radiat Oncol Biol Phys 2003, 55: 168 [PMID: 12504050] SCh3003g
- Paulussen M, Frohlich B, Jürgens H: Ewing tumour: Incidence, prognosis and treatment options. Paediatr Drugs 2001, 3: 899 [PMID: 11772151] PAU2001c
Кожные пробы на аллергию
Чтобы избежать аллергической реакции, вам нужно знать, на что у вас аллергия. Кожные пробы — один из способов, которым врач может определить причину ваших симптомов.
В этих тестах используются экстракты (концентрированная жидкая форма) распространенных аллергенов, таких как пыльца, плесень, пылевые клещи, шерсть животных и продукты питания. Попав на кожу, они могут вызвать сыпь. Ваша кожа станет раздраженной и может чесаться, как от укуса комара.
По этой реакции врач может сказать, что у вас аллергия на что-то.Когда у вас аллергия, ваша иммунная система вырабатывает антитела и запускает химические вещества, которые срабатывают.
Что происходит во время кожного теста?
Действия различаются в зависимости от типа теста. Есть три основных способа заставить аллергены вступить в реакцию с вашей кожей.
Тест на царапину , также известный как тест на прокол или укол: сначала ваш врач или медсестра осмотрит кожу на вашем предплечье или спине и очистит ее спиртом. Они отметят и отметят участки на вашей коже ручкой.Затем они нанесут каплю потенциального аллергена на каждое из этих пятен. Затем они будут царапать внешний слой вашей кожи, чтобы впустить аллерген. (Это не укол, и вы не будете кровоточить.)
Внутрикожный тест: После того, как они осмотрят вашу кожу и очистят ее, врач или медсестра введут небольшое количество аллергена прямо вам под кожу.
Патч-тест: Ваш врач может нанести аллерген на пластырь, а затем наклеить его вам на руку или спину.
Запланировать часовой прием.Колющая часть царапин и внутрикожных тестов занимает от 5 до 10 минут. Затем вы подождите около 15 минут, чтобы увидеть, как отреагирует ваша кожа.
Патч-тесты требуют больше времени и двух посещений врача. Если у вас отложенная реакция на аллерген, вам придется носить пластырь около 48 часов.
Как подготовиться к тесту
Сообщите своему врачу обо всех лекарствах, которые вы принимаете, включая безрецептурные. Некоторые лекарства могут повлиять на результаты, поэтому ваш врач даст вам список лекарств, которых следует избегать перед тестом.
Если вы не можете прекратить прием лекарства, ваш врач или медсестра могут провести отдельный тест, чтобы выяснить, не повлияет ли это лекарство на результаты.
Поскольку лекарства от аллергии, такие как антигистаминные препараты, отпускаемые без рецепта, останавливают аллергические реакции, вам не следует принимать их за несколько дней до приема. Вы должны позволить своему организму отреагировать на аллергены в тесте.
Это безопасно?
Кожная проба может вызывать легкое раздражение, но большинство людей говорят, что это не больно. Хотя вы контактируете с вещами, на которые может быть аллергия, их очень мало.
Реакции всего тела на кожные аллергические пробы случаются редко, но сразу же сообщите об этом своему врачу, если у вас есть:
После теста
Врач или медсестра очистят спиртом любые экстракты и следы от чернил с вашей кожи. Возможно, вам понадобится мягкий крем с кортизоном, чтобы облегчить зуд.
Если вы пройдете тест на пластырь, вы пойдете домой с повязкой на коже. Не мочите эти участки — ни ванны, ни плавания. Когда вы вернетесь к врачу через пару дней, он еще раз взглянет на вашу кожу.
Ваш врач или аллерголог использует результаты вашего теста, чтобы составить для вас план лечения.
- Если результаты не ясны, ваш врач может захотеть провести дополнительные проверки. Некоторым людям нужны анализы крови или «контрольные тесты», когда вы вдыхаете или принимаете через рот небольшое количество триггера аллергии.
- Как только вы узнаете, на что у вас аллергия, вы можете предпринять шаги, чтобы защитить себя. Например, если проблема связана с пылевыми клещами, вы можете обернуть матрас антиаллергенным чехлом, чтобы они не попали внутрь.
- Ваш врач может порекомендовать лекарство, чтобы контролировать ваши симптомы. Уколы от аллергии также могут помочь, хотя они действуют намного дольше.
Кожный тест Vs. Анализ крови — что лучше?
09 May Кожный тест против анализа крови: какой тест лучше?
Отправлено в 21:05 в кожном тесте автор: mcgallergy18Это пик сезона аллергии, а аллергены повсюду.Это время года, когда вы видите, что ваши симптомы ухудшаются. Они могут даже настолько ухудшиться, что вам понадобится обратиться к врачу.
Специалисты по аллергии используют тесты для определения факторов окружающей среды или продуктов, на которые у пациента аллергия. Обычно аллергологи используют кожные пробы или анализ крови в качестве диагностической процедуры, но это заставляет многих пациентов задуматься, какой тип тестирования лучше. Короткий ответ: у каждого теста есть свои преимущества и ограничения.
Чем похожи анализы крови и кожные пробы?
Тесты крови и кожи позволяют диагностировать аллергены путем обнаружения антител, известных как иммуноглобулин Е (IgE).IgE живут в крови и коже пациента, распознают аллергены и вызывают аллергическую реакцию, что позволяет врачу определить, какие факторы вызывают обострение симптомов у пациента. Анализы крови обнаруживают IgE в крови, а кожные пробы обнаруживают IgE на коже.
Преимущества кожных тестов
Вообще говоря, кожные пробы более чувствительны, чем анализы крови, а это означает, что они с большей вероятностью обнаруживают аллергию, которую может пропустить анализ крови. Кожные пробы также требуют меньше времени ожидания, поскольку результаты обычно выдаются через 15-20 минут, а не через одну-две недели ожидания анализов крови.Кожные пробы также позволяют врачам выбирать более широкий спектр аллергенов. Например, в McGovern Allergy and Asthma Clinic врачи имеют доступ к более чем 150 различным экологическим и пищевым аллергенам, что позволяет им проверять необычные типы аллергии. Анализы крови ограничиваются тем, на какие аллергены тестируют лаборатории — обычно это гораздо меньшее количество, чем кожные пробы. Наконец, кожные пробы намного дешевле, чем анализ крови.
Преимущества анализов крови
Хотя кожные пробы могут показаться подходящим вариантом, они имеют преимущества, которых кожные пробы просто не могут дать.Кожные пробы требуют, чтобы пациенты прекратили прием антигистаминных препаратов за пять-семь дней до обследования. Это связано с тем, что антигистаминные препараты снижают реактивность кожи. Однако на анализы крови лекарства не влияют. Пациенты с тяжелой аллергией, которые не могут прекратить прием лекарств, могут получить пользу от продолжения приема лекарств во время сдачи анализа крови. Кроме того, пациенты с чувствительной кожей (дерматография) или крапивницей могут давать ложноположительные результаты кожной пробы, что снижает ее надежность.
Кроме того, пациенты с экземой или с тяжелыми аллергическими реакциями также являются лучшими кандидатами на анализ крови. Наконец, анализ крови позволяет проводить тестирование компонентов на пищевую аллергию, а это означает, что тест может фактически определить точные белки в пище, на которые у пациента также есть аллергия, и даже может предсказать тяжесть его или ее аллергической реакции.
Что лучше?
На самом деле не существует универсального теста на аллергию. Лучший способ получить максимальную отдачу от теста на аллергию — это проконсультироваться с опытным аллергологом, например, в клинике аллергии и астмы McGovern.Знающий и опытный аллерголог определит, какой тип тестирования лучше всего подходит для каждого отдельного пациента, принимая во внимание его или ее предыдущую историю болезни, а также преимущества и ограничения каждого типа теста. Иногда аллергологи могут даже использовать оба типа тестов, если результаты анализа крови или кожи не являются однозначными.
Свяжитесь с нами
Если вы испытываете симптомы аллергии и ищете облегчения, обратитесь к опытной команде клиники McGovern Allergy and Asthma Clinic прямо сейчас.Посетите https://www.mcgovernallergy.com или позвоните по телефону 713-661-1444, чтобы записаться на прием сегодня.
Кожные тесты на аллергию | Атланта, аллергия и астма,
Информация о кожных пробах на аллергию
Самый надежный и распространенный тест на аллергию — это кожная проба. Это просто, в офисная процедура вводит очень небольшое количество определенного аллергена или аллергены, выбранные аллергологом на основании вашей истории болезни (например, пыльца, пылевого клеща, шерсти животных, плесени и / или пищевых продуктов).Аллерген попадает через вмятина или «укол» на поверхности кожи.
После кожного укола на спине некоторые пациенты могут также получить внутрикожное тестирование, при котором небольшое количество аллергена вводится под кожа руки, чтобы увидеть, вызывает ли она реакцию.
Результаты доступны в течение нескольких минут, позволяя вашему аллергологу разработать план лечения немедленно.
Кожная проба на аллергию — самый точный метод оценки аллергии.Эти тесты безопасны, малоинвазивны и легко интерпретируются. Результаты кожи тестирование оказалось более точным, чем анализ крови при диагностике аллергия.
Прием некоторых лекарств, содержащих антигистаминные препараты, следует прекратить за неделю до кожное тестирование. Щелкните здесь, чтобы просмотреть подробный список лекарств.
Не прекращайте принимать лекарства от астмы или другие обычные лекарства без Проконсультируйтесь с вашим лечащим врачом.
Нажмите здесь, чтобы получить дополнительную информацию о вашем кожном тесте на аллергию. деловое свидание, встреча.
Дети и кожные пробы
Американская академия педиатрии не считает возраст барьером для кожи. тестирование. Подходящий возраст для тестирования зависит от конкретного ребенка и его симптомы. Поговорите со своим аллергологом, чтобы определить надлежащий возраст тестирования на Ваш ребенок. Часто рекомендуется повторно обследовать ребенка по мере его взросления. Много раз могут быть повторно введены определенные продукты, которые когда-то вызывали аллергическую реакцию.
Объяснение кожных тестов на аллергию | Семейная аллергия и астма
Что такое кожная проба на аллергию?
Кожные пробы — самый надежный вид тестирования на аллергию.Поскольку тучные клетки в большом количестве расположены непосредственно под кожей, результаты кожных тестов оказались более точными, чем анализ крови при диагностике аллергии.
Пожалуйста, принесите с собой полный список всех лекарств, а также номер вашей аптеки и адрес. Мы регулярно отправляем рецепты в электронном виде, и для обеспечения точности нам нужна информация о вашей аптеке.
Ваш первый визит займет в общей сложности 2-3 часа. В процессе тестирования мы будем использовать маркер на вашей спине и руках, что может привести к появлению пятен на рубашке.По этой причине мы рекомендуем вам взять с собой более старую рубашку, чтобы надеть ее домой.
Процедура тестирования на аллергию
Кожная проба — это простая серия крошечных царапин на спине. Персонал использует небольшой инструмент, похожий на пластиковую зубочистку, который содержит следовые количества одного аллергена, такого как плесень, пыльца, пылевой клещ и перхоть домашних животных, для проведения теста на аллергию. При положительном результате на коже возникает небольшая реакция, обычно в течение 20 минут. Эта реакция обычно представляет собой небольшую шишку, похожую на укус комара, и может вызвать зуд.Шишка или реакция указывают на то, что у вас аллергия на этот конкретный триггер. После теста на царапину на спине некоторые пациенты также могут пройти внутрикожное тестирование, при котором небольшое количество аллергена вводится под кожу руки, чтобы увидеть, вызывает ли он реакцию.
Вот видео, объясняющее процесс тестирования и иммунотерапии, который мы показываем пациентам после тестирования:
Какие лекарства следует прекратить перед тестированием?
Вам следует прекратить прием некоторых лекарств, содержащих антигистаминные препараты, за три (3) до пяти (5) дней до тестирования.Щелкните здесь, чтобы просмотреть подробный список.
Не прекращайте принимать ингаляционные лекарства от астмы или обычные лекарства, которые лечат высокое кровяное давление, проблемы с сердцем, диабет и т. Д.
Результаты тестов на аллергию:
Наши врачи также изучают историю болезни в дополнение к тесту на аллергию, чтобы определить, какие аллергены вызывают беспокойство, и диагностировать аллергию. Во время первого визита пациенты узнают, на какие аллергены они дали положительный результат. Основываясь на результатах кожного теста на аллергию, наши аллергологи определяют лучшие варианты лечения вашей аллергии и ее симптомов.
В каком возрасте подходит кожная проба на аллергию?
Согласно Американской академии педиатрии, возраст не является препятствием для проведения кожных тестов. Даже младенцы могут получить пользу. По мере развития иммунной системы ребенка необходимо повторно обследовать ребенка для выявления изменений в его / ее иммунном ответе. Часто в рацион можно повторно вводить продукты, которые когда-то вызывали аллергическую реакцию. Помимо аллергии и иммунологии, наши аллергологи проходят обучение либо по педиатрии, либо по внутренним болезням, поэтому мы очень комфортно лечим педиатрических пациентов от аллергии и астмы.
Не страдайте аллергией. Назначьте встречу сегодня с одним из наших сертифицированных аллергологов.
тестов на уколы кожи | Исследования и образование в области пищевой аллергии
Симптомы пищевой аллергии вызваны взаимодействием пищевого аллергена и антитела, известного как IgE (иммуноглобулин E). Чтобы диагностировать пищевую аллергию, ваш аллерголог может использовать кожный укол (SPT), чтобы измерить наличие антител IgE к подозрительной пище. SPT недороги, дают немедленные результаты и могут выполняться в кабинете врача.
Во время этого теста аллерголог помещает каплю раствора, содержащего пищевой аллерген, на ваше предплечье или спину. (При тестировании фруктов или овощей вместо раствора можно использовать свежие продукты.) Используя небольшой пластиковый зонд или иглу, врач осторожно прокалывает или царапает кожу, чтобы небольшое количество раствора проникло чуть ниже поверхности. SPT обычно безболезненен и кровотечения нет. Царапины на поверхности кожи напоминают царапины на ногтях.
В зависимости от вашей истории болезни вы можете пройти тестирование на один или несколько продуктов. Результаты обычно появляются в течение 30 минут. На положительные результаты указывает волдырь — приподнятая белая шишка, окруженная маленьким кружком красной зудящей кожи. В общем, большой волдырь с большей вероятностью указывает на настоящую пищевую аллергию, но размер не всегда является точным предиктором. Если волдырь не появляется, маловероятно, что у вас аллергия на тестируемый продукт.
Точность тестов кожных уколов
SPT редко дают «ложноотрицательные результаты» (ошибочные результаты, указывающие на то, что у вас нет аллергии на какую-либо пищу, хотя это действительно так).Отрицательные результаты почти всегда означают, что у вас нет аллергии на пищу.
Положительные тесты, однако, не всегда точны. Около 50–60 процентов всех SPT дают «ложноположительные» результаты, что означает, что тест дает положительный результат, даже если у вас действительно нет аллергии на тестируемую пищу. Эти результаты возникают по двум причинам:
- Когда вы едите, ваша пищеварительная система постепенно расщепляет пищевые белки на очень мелкие кусочки. В результате аллергенные белки могут быть настолько малы, что антитела IgE не могут их обнаружить, поэтому еда на самом деле безопасна для вас.Но SPT и анализы крови не могут имитировать процесс пищеварения. Поскольку пищевые белки становятся больше, когда они взаимодействуют с вашей кожей или кровью, антителам IgE легче «видеть» аллергены и атаковать их. Вот почему ваши тесты могут показать, что вы более чувствительны к подозрительной пище, чем есть на самом деле.
- Члены пищевой «семьи» часто имеют одинаковые белки. Например, если у вас аллергия на арахис, ваши тесты могут показать положительный ответ на других членов семейства бобовых, таких как стручковая фасоль, даже если употребление стручковой фасоли никогда не было для вас проблемой.Это известно как перекрестная реактивность. Тест положительный, потому что он распознает аналогичный белок в арахисе и стручковой фасоли. Но тест не выявил настоящего виновника — другого белка, который содержится только в арахисе.
Несмотря на высокий уровень ложных срабатываний, в руках опытного аллерголога анализы кожи и крови очень полезны. Например, если ваша история болезни предполагает, что у вас было несколько реакций после употребления соевых продуктов, а кожные прик-тесты показывают положительную реакцию на соевые белки, весьма вероятно, что у вас действительно есть аллергия на сою.При необходимости врач может назначить дополнительные анализы.
Около 50-60 процентов всех SPT дают «ложноположительные» результаты, что означает, что тест дает положительный результат, даже если у вас нет реальной аллергии на тестируемую пищу.
Если вы принимаете антигистаминные препараты, важно помнить, что они могут повлиять на кожные пробы. Если прекращение приема лекарств на короткое время ухудшит ваши симптомы, ваш врач может провести анализ крови.
Другие проверенные методы тестирования:
- Анализ крови
- Устный пищевой вызов
- Элиминационная диета
Кожное тестирование | Центр сино-носовых заболеваний и аллергии UPMC
Есть несколько методов тестирования кожной аллергии.
В Центре сино-назальных заболеваний и аллергии UPMC мы используем кожный укол и внутрикожное разведение на кожную аллергию. Оба теста дают точные показания степени вашей аллергии. Они также позволяют врачу делать уколы от аллергии — если они вам нужны — в максимально безопасной концентрации.
Чего ожидать во время кожного теста на аллергию
Полное кожное тестирование займет около двух часов. Все приемы для тестирования на кожную аллергию включают углубленную консультацию по аллергии на окружающую среду и тщательный обзор нашей программы иммунотерапии.
Во время кожной пробы на аллергию врач введет небольшое количество антигена под верхние слои кожи.
При внутрикожной пробе под кожей образуется небольшая бугорка (4 мм).
Если у вас аллергия, эта шишка увеличится в размере в течение 10 минут. Затем ваш врач измерит размер шишки или рубца.
Как подготовиться к записи на обследование на кожную аллергию
Если вы проходите тест на кожную аллергию в Центре сино-назальных заболеваний и аллергии UPMC, ниже приведены инструкции, которые помогут вам подготовиться к кожным тестам на аллергию:
- Вы должны были записаться на прием к специалисту Университета по уху, носу и горлу в течение последних шести месяцев.
- Наденьте рубашку с короткими рукавами или без рукавов. Воздержитесь от парфюмерии.
- Вы можете поесть перед тестом на кожную аллергию.
- Не выполняйте упражнения до или после теста, так как это может увеличить вероятность реакции.
Лекарства
Некоторые лекарства могут изменить результаты кожных тестов на аллергию.
Чтобы убедиться в точности результатов теста на кожную аллергию и уменьшить синяки или кровотечение во время кожного укола или внутрикожного тестирования:
- Не принимайте аспирин или продукты, содержащие аспирин, в течение за 10 дней до до проверки на кожную аллергию, если только вы не принимаете аспирин по причинам сердечного ритма или для профилактики инсульта.
- Не принимайте ибупрофен или продукты, содержащие ибупрофен (Адвил, Мотрин, Нуприн) в течение за пять дней до теста на кожную аллергию.
- Избегайте обычных безрецептурных и рецептурных лекарств, содержащих антигистаминных препаратов в течение за четыре дня до до вашего теста на кожную аллергию. В таблице ниже представлен список препаратов, содержащих антигистаминные препараты.
Лекарства, содержащие антигистаминные препараты
- Актифед
- Аллегра
- Аллегра-D
- Аллерест
- Алка-Зельцер холод и синус
- Астелин
- Атаракс
- Бенадрил
- Хлорфенирамин
- Хлор-Триметон
- Кларитин
- Кларитин-Д
- Комист
- CoTylenol
- Капли от кашля с жидкими сердцевинами
- Деконамин
- Dimetapp
- Дриксорал
- Драмамин
- Экседрин PM
- Isoclo
- Кронофед А
- Kronofed A, Jr.
- Маракс
- Midol PM
- Motrin PM
- Мотрин синус
- Naldecon
- Нолахист
- Новагистин
- Ноламин
- Найкил
- Optimine
- Фенерган
- Полигистин
- Rondec
- Ру Тусс
- Семпрекс D
- Соминекс
- Тавист I
- Тавист II
- Тельдрин
- Тайленол PM
- Тайленол аллергия / носовые пазухи
- Zyrtec
Вы, , не можете пройти кожную пробу на аллергию или получить прививки от аллергии , если вы принимаете какой-либо из следующих неселективных бета-блокаторов :
Бета-адреноблокаторы, препятствующие тестированию
Неселективные бета-адреноблокаторы
- Betapace (соталол)
- Блокадрен (тимолола малеат)
- Brevibloc (эсмолол HCL)
- Картрол (картолол HCL)
- Corgard (надолол)
- Индерал (пропранолол)
- Леватол (сульфат пенбутолола)
- Normodyne (лабеталол HCL)
- Трандат (лабеталол гидрохлорид)
- Вискен (пиндолол)
- Зебета или Зиак (бисопролола фумарат)
Местно применяемые бета-адреноблокаторы
- Бетаган (левобунолол)
- Бетоптик (бетаксолол)
- Окупресс (картолол)
- Оптипранолол (метипранолол)
- Тимоптик (тимолол)
Комбинированные диуретики с бета-адреноблокаторами
- Корзид (надолол-бендрофлуметиазид)
- Индерид (пропранолол-гидрохлоротиазид)
- Нормозид или трандат (лабеталол-гидрохлоротиазид)
- Тимолид (тимолол-гидрохлоротиазид)
Селективные бета-адреноблокаторы, которые не предотвращают тестирование на аллергию включают:
- Керлон (бетаксолол)
- Лопрессор (метопролол)
- Сектрал (ацебутолол)
- Тенормин (атенолол)
- Теноретик (атенолол и хлорталидон)
Свяжитесь с нами
Позвоните в клинику аллергии UPMC по телефону 412-692-2228 , если у вас возникнут вопросы о тестах на кожную аллергию или ограничениях.
На номер запишитесь на прием или на номер направьте пациента , обратитесь в один из наших центров сино-назальных заболеваний и аллергии.
Назначить встречу
Чтобы записаться на прием или направить пациента, обратитесь в Отделение сино-назальных заболеваний и аллергии.
Узнайте больше об аллергии
Из блога UPMC HealthBeat :
Из нашей библиотеки здоровья :
Кожные пробы на туберкулез (ТБ) (Манту / PPD)
Туберкулез (ТБ)
Туберкулез — это заболевание, вызываемое микробами, которые в основном поражают легкие.В вашем теле могут быть микробы туберкулеза, потому что вы проводили время дома, на работе, в школе или в другом месте с больным туберкулезом. Бактерии туберкулеза передаются при кашле.
Общие симптомы туберкулеза
- Многонедельный кашель
- Усталость
- Лихорадка
- Потеря аппетита
- Ночная потливость
- Похудание
Лечение туберкулеза
Для лечения туберкулеза используются многие лекарства, предназначенные для уничтожения туберкулезных микробов.
Профилактика туберкулеза
- Кожные пробы для людей с высоким риском заражения туберкулезом (медицинский персонал, службы экстренной помощи), или тех, кто путешествовал в страны с высокими показателями туберкулеза, или людей, иммигрирующих из стран высокого риска, и т. Д.
- Обеспечение осмотра и осмотра квалифицированным практикующим врачом людей с симптомами
- Обеспечение того, чтобы люди с диагнозом ТБ получали правильное лечение и соблюдали свой план лечения
Кожное обследование на ТБ (также известное как Манту или PPD)
Кожная проба на туберкулез проводится квалифицированным медицинским работником путем инъекции небольшого количества сыворотки под кожу.Если в организме человека есть туберкулезные микробы, сыворотка вступает в реакцию с этими туберкулезными микробами и вызывает шишку на коже. Сыворотка не может вызвать туберкулез. После того, как тест «посажен», квалифицированный медицинский работник должен «прочитать» его в течение 48-72 часов. Это означает, что для проведения теста на туберкулез необходимо 2 посещения.
У некоторых людей образуется небольшая шишка, но это не обязательно означает, что у человека туберкулез! У некоторых людей на этом участке также может появиться сыпь или зуд. Опять же, это не означает, что тест положительный!
Департамент здравоохранения Вестфорда проводит кожные тесты на туберкулез для жителей города в нашей клинике Millennium.Необходимо записаться на две встречи, и это можно сделать по телефону 978-692-5509. Обычно встречи назначаются по понедельникам или средам, поэтому постарайтесь указать даты, когда вы звоните.
Взимается сбор в размере 15 долларов, оплачиваемый наличными или чеком, выписанным в «Город Уэстфорд».
Основная информация о вашем кожном тесте на туберкулез
- Тестирующий раствор / сыворотка (туберсол) помещается непосредственно под верхний слой вашей кожи.
- Небольшая шишка (похожая на укус комара) появляется при введении сыворотки.Эта шишка может исчезнуть почти сразу или остаться на некоторое время.
- Может быть небольшое кровотечение из пораженного участка, но не используйте повязку. (У некоторых людей от лейкопластыря появляется сыпь, которая может помешать проведению теста.) Вместо этого надавите на сухой кусок марли.
- Иногда в этом месте может появиться зуд, но старайтесь не расчесывать! НЕ используйте на сайте какие-либо кремы (включая Бенадрил или Кортизон), так как они повлияют на результаты вашего теста.
- Вы МОЖЕТЕ приложить к пораженному участку холодный компресс, чтобы уменьшить зуд.
- Вы МОЖЕТЕ купаться и плавать, но ИЗБЕГАЙТЕ нанесения лосьона для загара на место проведения теста.
- У некоторых людей наблюдается покраснение, сыпь, небольшой синяк или небольшая шишка на этом месте. Не волнуйся! Эти реакции распространены и не обязательно означают, что у вас положительный результат теста.
- В редких случаях некоторые люди очень чувствительны к раствору и у них развиваются тяжелые кожные реакции.





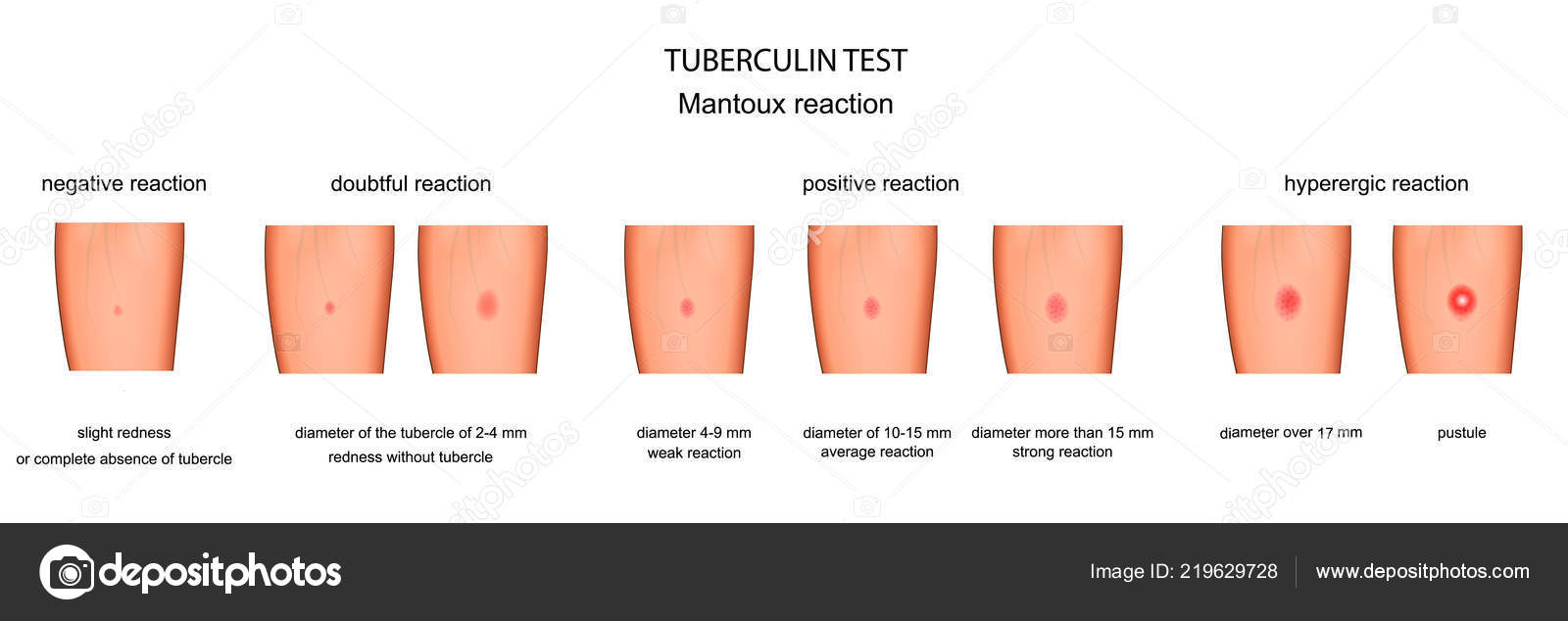
 Более того, высшие растения проявляют себя в экосистеме как стабильный биосенсор и, таким образом позволяют отследить эволюцию генотоксического воздействия (в том случае когда фактор проявляет мутагенный эффект одновременно на растительном и животном тест объектах)[10].
Более того, высшие растения проявляют себя в экосистеме как стабильный биосенсор и, таким образом позволяют отследить эволюцию генотоксического воздействия (в том случае когда фактор проявляет мутагенный эффект одновременно на растительном и животном тест объектах)[10]. По достижении корешками 1-2 см луковицы переносят в емкости с исследуемым раствором на определенное время (от 2 часов в случае с р-ом колхицина до 3 дней). Оригинальный вариант наиболее удобен при тестировании физических факторов.
По достижении корешками 1-2 см луковицы переносят в емкости с исследуемым раствором на определенное время (от 2 часов в случае с р-ом колхицина до 3 дней). Оригинальный вариант наиболее удобен при тестировании физических факторов. Этот метод позволяет проводить измерения в течение эксперимента.
Этот метод позволяет проводить измерения в течение эксперимента. The Allium Test as a standard in environmental monitoring // Hereditas. — 1985. — Т. 102. — С. 99-112.
The Allium Test as a standard in environmental monitoring // Hereditas. — 1985. — Т. 102. — С. 99-112. and Mba, K. C. Mutagenecity testing of phamarceutical effluents on Allium cepa root tip meristems // Toxicology and Environmental Health Sciences. — Academic journals, 2011. — № 3(2). — С. 44-51.
and Mba, K. C. Mutagenecity testing of phamarceutical effluents on Allium cepa root tip meristems // Toxicology and Environmental Health Sciences. — Academic journals, 2011. — № 3(2). — С. 44-51. — Национальная Академия Наук Украины, 2007. — № 7. — С. 165-170.
— Национальная Академия Наук Украины, 2007. — № 7. — С. 165-170. // Mutation Research/Genetic Toxicology and Environmental Mutagenesis. — Elsevier B.V., 2009. — № 642(2). — С. 76-81.
// Mutation Research/Genetic Toxicology and Environmental Mutagenesis. — Elsevier B.V., 2009. — № 642(2). — С. 76-81.