Аденокарцинома лечение, прогноз, признаки и симптомы
Аденокарцинома: классификация, стадии
Что такое
Аденокарцинома — это развивающаяся из клеток секреторного железистого эпителия опухоль злокачественного характера. Локализуется она на разных внутренних органах, на внутренних оболочках полых органов, а также коже человека.
Отличительной особенностью аденокарциномы является возможность выработки секрета.
Такие опухоли могут иметь самые разные размеры и формы, которые имеют прямую зависимость от клеточных и тканевых функций, клеточной и тканевой структуры органа, который был поражен.
Классификация
Аденокарциному принято классифицировать по локации (органу) поражения, по морфологическому признаку, по гистологическому признаку.
По локации поражения (органу)
Аденокарцинома очень часто поражает такие органы, как:
- Легкие,
- Молочные железы,
- Поджелудочную железу,
- Предстательную железу,
- Пищевод,
- Кишечник.

По гистологическому признаку
Аденокарцинома бывает трех типов:
G1 (Высокодифференцированная)
Такой вид аденокарциномы характеризуется злокачественностью малой степени. Морфология такой аденокарциномы: нормальные и не совсем нормальные клетки, способные быстро размножаться.
G2 (Умеренно дифференцированная)
Состав этой аденокарциномы – злокачественные клетки, сильно отличающиеся от здоровых и способные быстро размножаться. Характер этих раковых опухолей более агрессивен.
G3 (Низкодифференцированная)
Клетки этого вида аденокарциномы характеризуются высокой степенью злокачественности. Для них характерная полная утрата признаков нормальных клеток. Они размножаются активно, непредсказуемо и бессистемно.
По морфологическому признаку
По этому признаку аденокарцинома разделяется на следующие подвиды:
Ацинарная
Такая аденокарцинома являет собой опухоль предстательной железы, диагностируется чаще прочих и имеет долгое бессимптомное течение.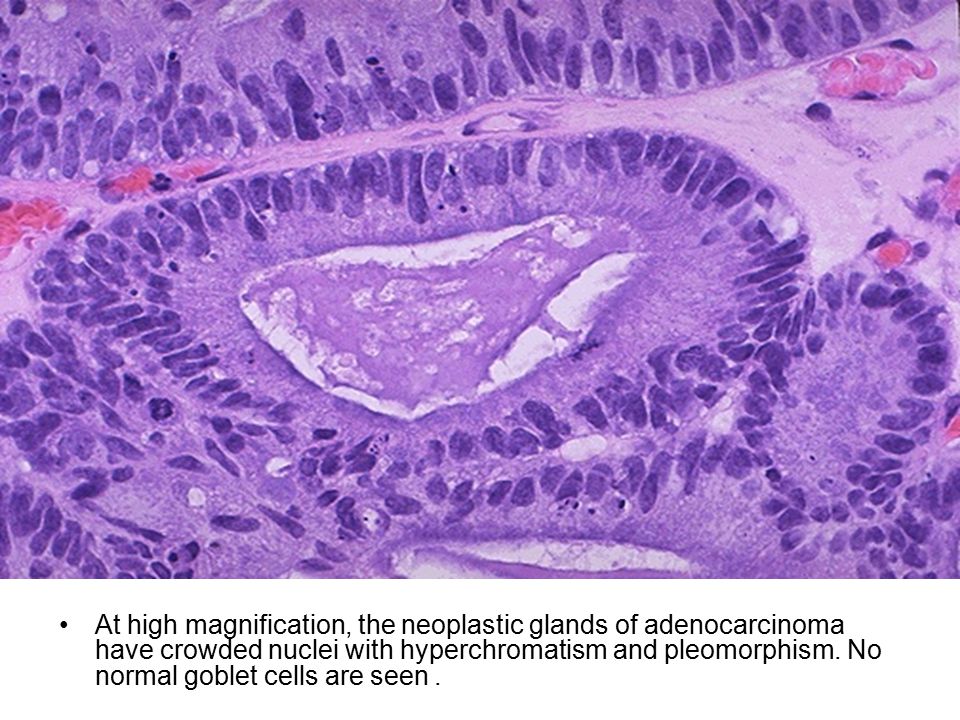 При исследовании хорошо видна дифференцировка тканей: раковые клетки различного размера с ядрами и цитоплазмой.
При исследовании хорошо видна дифференцировка тканей: раковые клетки различного размера с ядрами и цитоплазмой.
Мелкоацинарная
Это вид рака, находящийся в периферической (чаще всего) предстательной железе или переходной зоне простаты. Она состоит из небольших ацинусов с нарушениями структуры в нескольких местах.
Муцинозная
Аденокарцинома с разными видами клеток, характеризующаяся наличием полости с содержанием муцина. Слизь при этом виде опухоли вырабатывается в больших количествах и выходит на поверхность.
Темноклеточная
Рак, внутри клеток которого находятся полиморфные ядра с преобладающим темным цветом. Структура формируется из этих клеток и цитоплазмы. Имеет железистый вид. Обычно такой подвид аденокарциномы протекает быстро, но все зависит от дифференцировки у новообразования.
Серозная
Рак образуется из дифференцированных полиморфных и клеточных структур. Характер такой опухоли довольно агрессивен.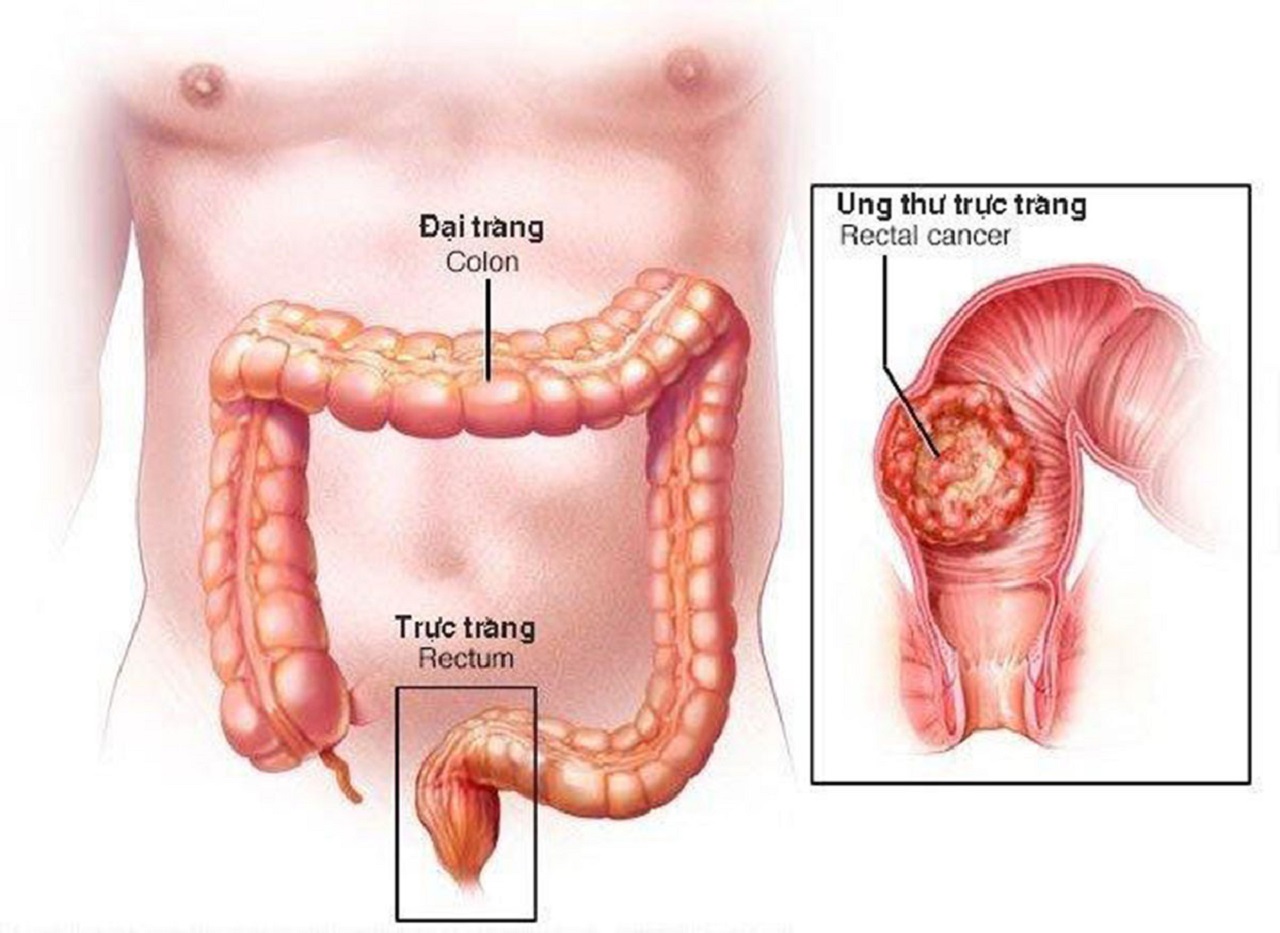
Светлоклеточная
Такая аденокарцинома имеет кистозно-трубчатую структуру, может иметь железистую структуру. Этот рак также развивается стремительно, при нем часто могут возникать метастазы.
Тубулярная
Структура такой аденокарциномы – цилиндры, трубки и кубики (тубулярные структуры). Локализуются они в фиброзной соединительной ткани.
Фолликулярная
Структура такой аденокарциномы представляет коллоидные частицы. Размер опухоли обратно пропорционален процессу протекания поражения: чем больше опухоль, тем протекание медленнее и наоборот. Метастазы при таком подвиде рака распространяются с током крови по различным частям тела.
Сосочковая (папиллярная)
Структура такого подвида рака похожа на сосочки или папилломы. Именно такой вид аденокарциномы имеет хороший прогноз в большинстве случаев, если вовремя произвести лечение.
Инвазивная
Характеризуется проникновением раковых клеток в близко расположенные с ней органы и ткани. Если вдруг такая карцинома попадает в кровь и лимфу, то распространение по частям тела приобретает гематогенный характер.
Если вдруг такая карцинома попадает в кровь и лимфу, то распространение по частям тела приобретает гематогенный характер.
Стадии
Выделяют несколько стадий развития аденокарциномы.
Нулевая стадия
По-другому носит название in situ. Злокачественные клетки присутствуют в организме. При этом они не выходят за пределы слоя эпителия.
Первая стадия
Раковые клетки выходят за пределы эпителия, получая распространение в других слоях, но не идут за границы одного органа.
Вторая стадия
Характеризуется разрастанием ракового образования и наличием метастазов в области лимфатических узлов.
Третья стадия
Аденокарцинома распространяется на органы-соседи, давая метастазы в некоторые группы лимфатических узлов.
Четвертая стадия
Раковая опухоль создает метастазы в лимфатические узлы и органы, находящиеся отдаленно от нее.
Причины аденокарциномы
- Застой, воспаление секреции в органе или полости;
- Неправильное питание;
- Ожирение;
- Отсутствие физической активности;
- Влияние химических веществ;
- Наследственность;
- Болезни, которые были перенесены человеком ранее.

Разберем причины, непосредственно связанные с определенными органами, из-за которых возникает аденокарцинома.
Поджелудочная железа
Аденокарцинома, вероятно, образуется в ней из-за курения или панкреатита.
Желудок
Рак может возникнуть из-за наличия Хелибактера и из-за эпителиальных изменений слизистой органа, а также из-за болезни Менетрие (переразвитие слизистой оболочки желудка), полипов, хронических язв.
Простата
Опухоль возникает из-за наследственности, гормональных изменений, связанных с возрастом, вируса XMRV, из-за хронической интоксикации кадмием, дисбаланса нутриентов.
Симптоматика
На скрытом этапе течения заболевания симптоматика отсутствует.
Первые симптомы появляются из-за разрастания опухоли:
- Боль в той зоне, где локализуется новообразование;
- Наличие сгустков крови;
- Появление запоров;
- Рост лимфатических узлов;
- Потеря в весе;
- Снижение гемоглобина;
- Утомляемость;
- Низкая трудоспособность;
- Плохой сон.

На стадии интенсивного роста раковых клеток и появления метастазов выраженность симптомов усиливается.
Разберем симптоматику при формировании аденокарциномы в различных органах.
Кишечник
- Болезненный живот;
- Неприятные ощущения после приема пищи;
- Плохая проходимость кишечника;
- Жидкий стул, чередующийся с запорами;
- Кровь и слизистые выделения в кале.
Пищевод
- Боль при осуществлении глотания;
- Дисгафия;
- Активное слюнотечение.
Полость носа
- Отек миндалин;
- Не проходящее воспаление миндалин;
- Боли в гортани, глотке, носу;
- Неприятные ощущения при глотании;
- Боль в ушах;
- Нарушение речи;
- Увеличение лимфоузлов.
Печень
- Болезненность в области правого ребра и подреберья;
- Глаза и кожа желтоватого цвета.

Диагностика
Лабораторные исследования
Благодаря ним можно предположить, что у человека есть онкология, если у него изменена лейкоцитарная формула, повышен СОЭ, мало эритроцитов в крови. Анализ на кал может показать наличие следов крови (что, конечно, также является симптомом ряда других заболеваний).
Рентгеноскопия
Это исследование помогает определить размер, форму, расположение опухоли. Процедура осуществляется при помощи использования контрастных веществ. Нередко это – барий.
Эндоскопия
Позиторно-эмиссионная и компьютерная томография
Благодаря этим методам можно определить размеры, форму, расположение аденокарциномы, найти, где находятся метастазы.
Ультразвук
Этот метод считается наиболее информативным для изучения аденокарциномы почек и мочевого пузыря. Ультразвуковое исследование позволяет локализовать очаг заболевания, выявить, насколько сильно поражены стенки органа, оценить, в каком состоянии находятся лимфоузлы.
Лечение
Хирургическое вмешательство
Лечение в основном осуществляется при помощи вмешательства со стороны хирургии.
Для поддержания ослабленного организма специалистами назначается курс физиотерапевтических лекарств.
Томотерапия
Одним из новейших методов лечения аденокарциномы стала томотерапия. Благодаря применению специального сканера 3D, который дает изображение зоны поражения в объеме, можно планировать высокоточное вмешательство. Риск при этой операции будет минимальным.
Химиотерапия
Химиотерапия – метод, благодаря которому возможно излечение от данного вида онкологии. Для применения этой терапии нужно смотреть, на какой стадии находится, как распространяется в организме рак.
Для применения этой терапии нужно смотреть, на какой стадии находится, как распространяется в организме рак.
Если после операции обнаружены лимфоузлы, подвергшиеся поражению, то проводится затем химиотерапия. Длительность курса химиотерапии зависит от самого препарата.
Еще химиотерапия делается при тяжелых случаях, запущенной форме и рецидивах после операции.
Осложнения
Одно из осложнений – распространение метастазов по телу человека с лимфой и кровью. Это может способствовать нарушениям в работе органов и смерти.
Возможно и допущение ошибок со стороны врачей во время хирургического вмешательства и после него.
Прогноз
Для хорошего прогноза нужно диагностировать аденокарциному на начальных стадиях. Если у больного уже есть метастазы, то он будет жить около 4 месяцев, что также будет зависеть от места нахождения очага опухоли.
Если поражен пищевод, то при лечении на первой и второй стадиях заболевания человек живет пять и более лет. При третьей и четвертой степени – смерть в 25% случаях.
При третьей и четвертой степени – смерть в 25% случаях.
Если поражена печень, то больной проживет не более трех лет.
Аденкарцинома – вид ракового заболевания, при котором нужно незамедлительно обратиться к специалисту и провести необходимое лечение в зависимости от вида болезни, локации и степени поражения органа.
Можно ли вылечить рак прямой кишки?
Рак прямой кишки – распространенное онкологическое заболевание. Точных причин роста заболеваемости ученые не называют, но обращают внимание, что…
…в группе риска находится население экономически развитых стран и жители больших городов. Среди основных причин, ведущих к заболеванию, статисты и онкологи выделяют два главных фактора: характер питания и наследственность.
Что вызывает рак прямой кишки
При наличии в семье родственников в разных поколениях с онкологическим заболеванием прямой кишки говорят о наследственной предрасположенности к колоректальному раку.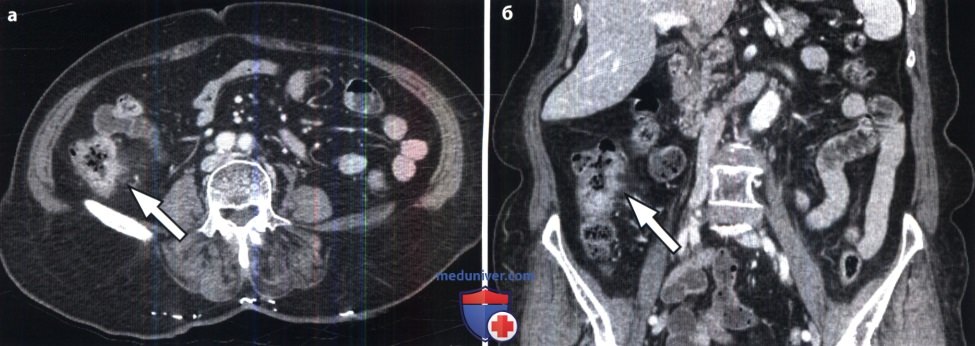 Но неправильное питание и наличие хронических болезней конечных отделов кишечника даже без отягощенной наследственности могут стать причиной появления злокачественной опухоли.
Но неправильное питание и наличие хронических болезней конечных отделов кишечника даже без отягощенной наследственности могут стать причиной появления злокачественной опухоли.
Пищевой рацион, бедный клетчаткой, но с избытком красного мяса, животных жиров, жареного, мучного и сладкого приводит к накоплению в кишечнике жирных кислот, превращающихся в канцерогены. Малоподвижный и сидячий образ жизни в свою очередь способствует застою крови в венах таза и приводит к нарушению функций слизистой оболочки прямой кишки. В толстом кишечнике возникают хронические воспалительные процессы, провоцируя мутации клеток.
Что такое рак прямой кишки?
Рак прямой кишки – это злокачественное новообразование, развивающееся в слизистой оболочке конечной части сегмента толстой кишки, заканчивающейся анусом. Опухоль развивается, расширяет свои границы на слизистой и со временем выходит за ее пределы.
Появляются вторичные патологические очаги (метастазы), которые в первую очередь поражают лимфоузлы и органы малого таза, и постепенно распространяются по всему организму.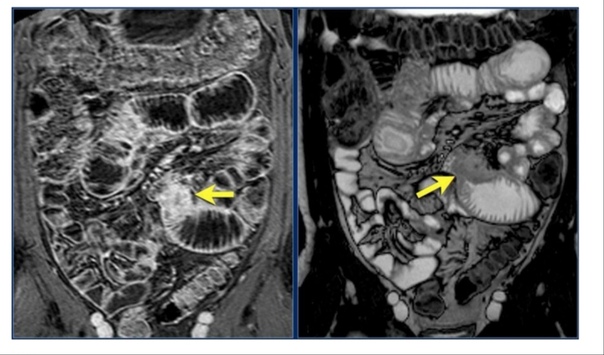 Раковая опухоль в прямой кишке может также развиваться на фоне предраковых заболеваний: полипов, трещин, свищей, проктитов.
Раковая опухоль в прямой кишке может также развиваться на фоне предраковых заболеваний: полипов, трещин, свищей, проктитов.
Даже незначительное, но затянувшееся отклонение от привычного состояния кишечника должно насторожить человека и стать поводом обращения к врачу. Лучше сказать себе: «боюсь, что у меня рак прямой кишки», чем беспечно отмахнуться от проблемы, и услышать этот диагноз на 3-4 стадии заболевания.
Как начинается рак прямой кишки
Первые признаки рака прямой кишки проявляются нарушением стула в виде запоров или диареи, дискомфортом, ощущением тяжести, состоянием слабости. С увеличением размеров опухоли появляются небольшие кровотечения, которые нередко принимаются пациентом за геморроидальные, а появившиеся боли он относит на обострившиеся проблемы с печенью и желчным пузырем.
Постоянный дискомфорт, боли, ложные частые позывы к дефекации вынуждают его посетить вначале гастроэнтеролога или проктолога, и если у доктора возникает подозрение на рак, то пациента перенаправляют к онкологу. К онкологу-колопроктологу больной чаще всего попадает через 3-5 месяцев от начала проявления заболевания.
К онкологу-колопроктологу больной чаще всего попадает через 3-5 месяцев от начала проявления заболевания.
Как определяют рак прямой кишки
Современная онкология имеет высокотехнологичную аппаратуру и позволяет выявить заболевание на любой стадии развития:
- пальцевое исследование позволяет оценить состояние почти половины длины прямой кишки и выявить опухоль у 90% больных с онкологией нижних отделов;
- при выявлении скрытой крови в анализах кала и мочи назначается дальнейшее гистологическое и цитологическое исследование, УЗИ, МРТ, биопсия;
- проводится анализ на онкомаркеры, общий, клинический и биохимический анализы крови.
Онкомаркеры – это белки, которые вырабатываются злокачественными образованиями в процессе их жизнедеятельности. Наибольшая их концентрация в крови, по увеличенному количеству этих своеобразных меток можно выявить участок кишечника с онкологией.
Для этого используют специфические маркеры – СА 242, РЭА и неспецифические – АФП.
Стадии рака прямой кишки
Раковая опухоль прямой кишки развивается медленно, на протяжении нескольких лет, чаще всего бессимптомно на первых порах, и проходит 4 стадии развития:
- 1 степень – опухоль размером до 2 см, близлежащие ткани воспаляются, но метастазов нет.
- 2 степень – размер опухоли до 5 см, метастазы или отсутствуют, или одиночные, появляется болевой синдром.
- 3 степень – опухоль больше 5 см, уже проросла сквозь все слои кишечной стенки и дала множественные метастазы в прилежащие лимфоузлы, слабость, потеря веса.
- 4 степень – метастазы в брюшной полости, печени, легких, позвоночнике, головном мозге, сама опухоль начинает распадаться.
Можно ли обойтись без операции при раке прямой кишки?
Рак прямой кишки может быть излечен только оперативным путем, его также нельзя вылечить народными средствами. Хирургическая операция является основным методом лечения рака толстой и прямой кишки.
Лучевая терапия и химиотерапия используются как дополнение к хирургическому лечению, и имеют второстепенное значение в комплексном лечении. Но, чем раньше диагностирована опухоль, и чем выше она расположена, тем проще операция, лучше результаты и полнее реабилитация.
Но, чем раньше диагностирована опухоль, и чем выше она расположена, тем проще операция, лучше результаты и полнее реабилитация.
Сложные операции с удалением прямой кишки, анального канала и мышц сфинктера требуют формирования у пациента постоянной колостомы на передней брюшной стенке. К ней крепится калоприемник, который надо периодически заменять по утрам или перед сном. За стомой и кожей вокруг отверстия нужно тщательно ухаживать, чтобы не было раздражения.
Сколько живут после операции
Прогноз продолжительности жизни после удаления опухоли на прямой кишке будет зависеть от стадии онкологического поражения, возраста и характера проведенного лечения. Недуг, выявленный на 1-2 этапе поражения, и операция на ранних стадиях, дают хирургу возможность удалить опухоль и первые незначительные метастазы, не затрагивающие жизненно важные органы. В этих случаях 65-85 % молодых пациентов выздоравливают полностью, а остальные имеют от 2 до 5 лет полноценной жизни.
Резко снижается вероятность появления рецидива рака по прошествии 5 лет после операции, поэтому этот период считается критическим.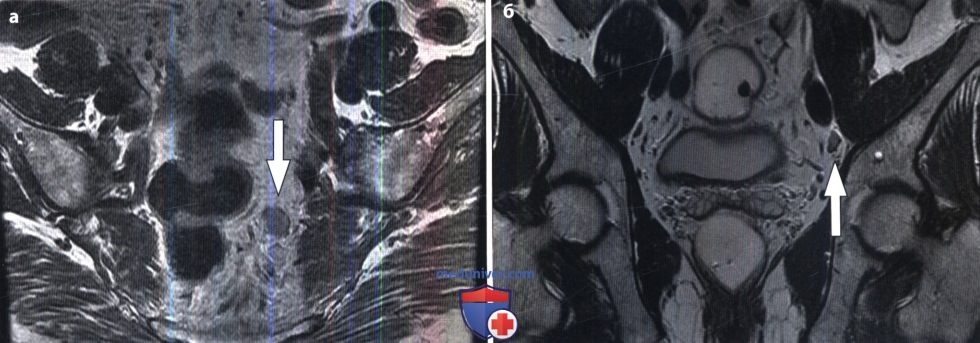 При поражении более 5 лимфатических узлов или при метастазах в соседних органах, в тканях печени и легких шансов продлить больному жизнь очень мало. В этих случаях не доживают до года.
При поражении более 5 лимфатических узлов или при метастазах в соседних органах, в тканях печени и легких шансов продлить больному жизнь очень мало. В этих случаях не доживают до года.
Послеоперационный восстановительный период также занимает важное место в выживаемости пациента. В краткие сроки нужно восстановить организм больного после хирургического вмешательства и химиотерапии с помощью лечебного питания, и не допустить рецидивов заболевания.
Как предотвратить рак прямой кишки
Хорошей профилактикой рака прямой кишки служит правильное питание: употребление продуктов, богатых клетчаткой, овощей и фруктов, каш из злаков, орехов, которые способствуют эффективному очищению кишечника, до 2 литров чистой питьевой воды в день. Кроме этого следует придерживаться следующих правил:
- нужно своевременно лечить предраковые заболевания, которые вызывают воспаление толстой кишки – болезнь Крона.
- не допускать появления запоров, исключить из питания фаст-фуды;
- не контактировать с вредными химическими веществами;
- при отягощенной наследственности необходимо проводить периодические обследования на предмет опухоли в прямой кишке.

После 40 лет рекомендуется проходить скрининг
Во всем мире онкологи отмечают возрастание частоты заболеваний раком прямой кишки, а с возрастом человека риск заболеть увеличивается. С целью своевременной диагностики рака Американское общество рака и Национальный раковый институт США рекомендуют населению всех стран проходить скрининг на рак прямой кишки по следующей методике:
- ежегодно проводить пальцевое исследование прямой кишки лицам старше 40 лет;
- ежегодно выполнять тест на определение скрытой крови в стуле лицам старше 50 лет;
- каждые 3-5 лет проводить фиброколоноскопию лицам старше 50 лет.
В Украине с учетом повышенной радиологической ситуацией фиброколоноскопию нужно проводить каждые 2 года.
Провести диагностику, чтобы заблаговременно выявить заболевание, может каждый житель Украины. Для этого нужно записаться на обследование к проктологу в своем городе.
Запомните! Своевременно диагностированный рак поддается результативному лечению./186450274-56a504703df78cf77285fee3.jpg)
Рейтинг статьи:
4.5 из 5 на основе 4 оценки
Задайте свой вопрос проктологу
«ОН Клиник»
низкодифференцированная, что это такое, сколько проживет человек, умеренно, злокачественная опухоль, прогноз, малодифференцированная, новообразование, выживаемость, лечение, ст
Что такое
Аденокарцинома желудка – раковая патология, которая начинает развиваться из слизистой оболочки эпителия, что устилает внутреннюю поверхность желудка. Когда здоровая клетка меняет свою структуру, то наблюдается ее перерождение в злокачественную. Подобное явление несет угрозу для жизни и здоровья человека.
Чаще всего патология диагностируется в пилорическом и антральном отделе органа, что объясняется частым механическим воздействием в процессе пищеварения некачественно пережеванной пищи.
Риск развития рака возрастает в возрасте после 45 лет, причем в половине случаев выявляется только на 3 и 4 стадиях, поскольку начальные этапы не проявляют себя определенными симптомами.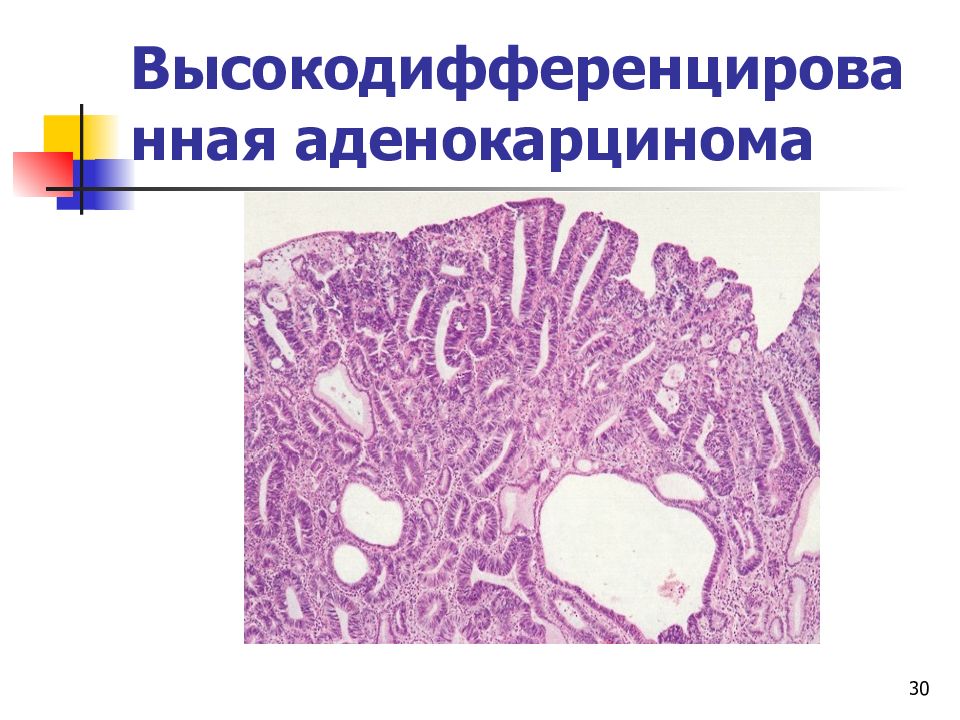 Это объясняется тем, что сам орган достаточно крупный.
Это объясняется тем, что сам орган достаточно крупный.
При диагностировании патологии более чем у 80% пациентов наблюдаются метастазы, часто это становится причиной невозможности проведения операции, поскольку имеются поражения лимфатических узлов, региональных органов и тканей. Чаще от заболевания страдают мужчины.
Профилактика
Профилактика железистого рака желудка заключается в полном исключении этиологических факторов. Существенно снизить риск развития онкологического процесса можно, если применять на практике такие правила:
Существенно снизить риск развития онкологического процесса можно, если применять на практике такие правила:
- исключение или сведение к минимуму потребления солёного, вяленого, копчёного, жирного и острого;исключение алкоголя и спиртного;потребление свежих овощей и фруктов;своевременное лечение всех заболеваний.
Кроме этого, следует не забывать ежегодно проходить медицинское обследование. Особенно, это касается людей, которые находятся в группе риска и возрастной категории 50–65 лет. При первых же симптомах следует обращаться за медицинской помощью, а не заниматься самолечением.
Источник: simptomer.ru
Классификация
В зависимости от гистологии, выделены следующие виды аденокарциномы:
- Полипозная.
- Язвенная.
- Псевдоязвенная.
- Несекреторная.
- Диффузная.
В зависимости от роста бывают следующими:
- Турбулярная – структура состоит из разветвленных либо расширенных образований.
- Папиллярная – имеет сосочковый вид, удлиненную форму в виде пальца.
 Рост наблюдается в полость желудка.
Рост наблюдается в полость желудка. - Перстневидная – поражает непосредственно тело желудка, имеет четкие границы.
- Слизистая – характеризуется постоянной выработкой слизи, которая обнаруживается при проведении гастроскопии.
- Тубулярная – формируется из структур, которые имеют разветвленную либо расширенно-кистозную форму.
По степени дифференцирования подразделяются на 3 типа.
Низкодифференцированная
Данный вид (g3) даже на ранних этапах выпускает метастазы в региональные лимфатические узлы, органы, ткани. Нередко вторичные опухоли распространяются по всему желудочно-кишечному тракту. Прогноз при этом чаще неблагоприятный.
Умеренно дифференцированная
Опухоли подобного вида считаются промежуточным типом. Структура клеток меняется незначительно. Говорить о прогнозе сложно, поскольку он зависит от стадии, на которой началось лечение, от возраста пациента, распространенности патологии.
Высокодифференцированная
Является наиболее благоприятным видом, если говорить о прогнозе, поскольку клетки не полностью утрачивают способность выполнять свои функции, структура меняется незначительно по сравнению со здоровыми элементами. Метастазы отсутствуют, пациенты имеют высокие шансы на выздоровление.
Какие симптомы возникают у человека при таком заболевании?
Диета при онкологическом заболевании подразумевает отказ от большого количества белковой пищи. Предпочтение отдают свежим фруктам и овощам: моркови, капусте, свекле.
Научно доказано, что излечиться от рака также помогают:
- кисломолочные продукты;
- говяжья печень;
- природные добавки, содержащие ферменты поджелудочной железы и тереотропный гормон;
- льняное масло.
Исследования показали, что жиры уменьшают уровень глюкозы в организме, тем самым препятствуя распространению онкологических структур. Этот способ увеличивает выживаемость пациентов с метастазирующим раком до 5-6 лет.
О положительном эффекте от народных средств свидетельствуют люди, которые лечились ядовитыми настойками:
- Отвар болиголова. В оптимальной дозировке растение способствует разрушению раковых структур без вреда для организма. В стеклянную банку помещают 1 соцветие болиголова и заливают 500 мл спирта. Настойку выдерживают не менее 3 недель. Средство принимают ежедневно по 1 капле. Ежедневно количество капель увеличивают до 40 штук.
- Красный мухомор. Положительный опыт больных позволяет онкологам практиковать это растение в терапии раковых новообразований. Фитопрепараты из гриба готовят самостоятельно после одобрения лечащим врачом, так как при превышении дозировок может произойти интоксикация организма, вплоть до летального исхода. Основное действие красного мухомора – приостановка деления аномальных клеток. Для приготовления средства берут шляпки ядовитого гриба, измельчают и заливают спиртом в пропорции 1:1. Лекарство настаивается несколько месяцев в темном месте.
 Лечить рак желудка при помощи мухомора следует по той же схеме, что и болиголовом.
Лечить рак желудка при помощи мухомора следует по той же схеме, что и болиголовом. - Чага. Настойка из гриба рекомендована при невозможности проведения хирургического вмешательства или медикаментозной терапии. Как лечить рак при помощи березового гриба? Гриб измельчают, заливают теплой водой и настаивают 5 часов. Вымоченные кусочки пропускают через мясорубку и заливают теплой водой, подогретой до 50 градусов, в соотношении 1:5. Через 2 дня средство процеживают и принимают по 1 ч. л. несколько раз в день.
Общих причин возникновения такого заболевания, как рак — всегда много и они носят комплексный характер. Сюда относится:
- пониженный иммунитет
- наследственная предрасположенность
- плохая экологическая обстановка
- неправильное питание
- длительные хронические заболевания (гастрит, язва)
- большое количество паразитов, особенно — трихомонад
- курение, алкоголь
- длительная психологическая подавленность, депрессия
- нарушение кислотно-щелочного баланса в организме
Разбирать каждую причину нет необходимости — они общие для любой онкологии. А причины возникновения рака желудка — специфические. Их мы рассмотрим.
А причины возникновения рака желудка — специфические. Их мы рассмотрим.
На этом участке пищеварительной системы происходит процесс переваривания белков животного происхождения под действием соляной кислоты. Немного ниже желудка находится отдел двенадцатиперстной кишки, где сильная щелочная среда переваривает растительную пищу.
А разделены эти два отдела с разным значением pH только мышечной перегородкой. Если этот мышечный клапан не справляется с функцией разделения двух разных участков по перевариванию пищи, щелочь забрасывается в кислую среду желудка. Происходит обыкновенная химическая реакция с образованием соли и газов и в её результате наступает, как следствие, нулевая кислотность.
При этом возникает повышенный метеоризм и отрыжка. Это первые звоночки, на которые необходимо обратить внимание. Если у вас появились симптомы в виде отрыжки и усиленного отхождения газов — рекомендуется пройти обследование у врача-гастроэнтеролога.
В официальной медицине применение фармацевтических препаратов при онкологических заболеваниях приносит большие доходы держателям акций этих компаний.
Любое открытие, которое уменьшит доход фармацевтических компаний, подавляется ими в корне. Фармацевтическим компаниям выгодные больные раком, как источник больших доходов.
Есть много изобретений по излечению рака, патенты которых выкупили фармацевтические компании и мы о них не узнаем никогда. Здоровые люди не нужны — они не приносят доход этим компаниям.
Эта болезнь может развиваться без симптомов. Рак желудка тем коварен, что может долгое время развиваться без симптомов и не вызывать никаких беспокойств достаточно длительное время — в зависимости насколько он агрессивен и в какой части желудка он находится. Потеря веса наблюдается, если опухоль локализована в верхней части желудка, ближе к пищеводу.
Минимальный дискомфорт в виде тяжести в желудке, отрыжки, изжоги должен вызвать необходимость пройти гастроскопию. После 40 лет – это надо делать в профилактических целях и в обязательном порядке раз в год.
К ним можно отнести несколько факторов, являющихся поводом для развития болезни:
- неправильное питание, оснащенное избыточным пребыванием в нем соли, копченых продуктов, жареных блюд, острых приправ, животных масел и других;
- неблагоприятная окружающая среда, вода питьевая;
- заядлые курильщики;
- чрезмерность употребления алкоголя, крепких напитков;
- недостаток в организме аскорбиновой кислоты;
- гастрит, язвы желудка, опухолевые заболевания;
- попадание в стенки желудка бактерий и вирусов, относящихся к канцерогенам;
- особенности анатомического строения;
- возраст заболевших свыше 50 лет.

Недифференцированный рак желудка, который по-другому называют аденогенной опухолью, представляет собой опухоль онкологического характера. Атипичные клетки не являются однородными, они обладают разной структурой и величиной.
При исследовании тканей желудка выясняется, что клетки теряют способность дозревать до конца, поэтому не могут развиваться и функционировать, что неблагоприятно сказывается на состоянии организма. В отличие от нормальных тканей пораженное место имеет наиболее светлый оттенок.
Обычно злокачественное новообразование формируется в верхнем отделе пищеварительного органа. Данная опухоль, у которой наблюдается ярко выраженная способность стремительно расти, проникать в глубокие слои желудка, быстро дает метастазы, поражающие органы, находящиеся рядом.
Недифференцированный аденогенный рак желудка возникает вследствие патогенного изменения клеток данного органа. Такой процесс не происходит просто так. Структура тканей меняется только под воздействием неблагоприятных факторов. К ним относят следующее:
К ним относят следующее:
- Проживание в местности с плохой экологией.
- Неправильное питание, предполагающее потребление вредной пищи, содержащей много канцерогенов, нитратов.
- Вредные привычки.
- Гастрит и язва желудка.
- Хирургическое вмешательство на пищеварительном органе.
- Инфекционные патологии.
- Частый и продолжительный контакт с химическими и токсическими веществами.
- Ослабление иммунитета.
Также не стоит забывать о наследственной предрасположенности. Люди, чьи близкие родственники страдали онкологией, автоматически попадают в группу риска.
Тактика терапии недифференцированного рака желудка проводится после полного обследования пациента. В ходе диагностики назначают лабораторные анализы крови, мочи, кала, ультразвуковое исследование, магнитно-резонансную томографию. Для окончательной постановки диагноза обязательно выполняют биопсию с гистологией пораженных клеток.
При онкологии пищеварительного органа терапия проводится комплексно, методы лечения могут быть разными в зависимости от стадии развития болезни. Если опухоль операбельна, то назначают химиотерапию, лучевую терапию для уменьшения новообразования, подготовки человека к операции. Затем проводят оперативное вмешательство, в процессе которого удаляют пораженные ткани.
Если опухоль операбельна, то назначают химиотерапию, лучевую терапию для уменьшения новообразования, подготовки человека к операции. Затем проводят оперативное вмешательство, в процессе которого удаляют пораженные ткани.
После хирургического лечения также проводят курс химиотерапии. Кроме нее человека необходимо питаться в соответствии с диетой. Все вредные продукты и алкоголь полностью исключаются.
Если же рак невозможно удалить оперативным путем, то назначают химиотерапию для увеличения продолжительности жизни больного, устранения симптомов заболевания.
Прогноз при недифференцированном раке желудка является неблагоприятным при выявлении поздних стадий его развития. При легкой степени онкологии после проведенной комплексной терапии большая часть пациентов выздоравливают. Именно поэтому так важно ежегодно проходить обследование организма, чтобы своевременно обнаруживать болезни и успешно бороться с ними.
Специалисты не готовы назвать точные причину или причину возникновения этого заболевания, Дело в том, что в современном мире есть огромное количество скрытых угроз, которые играют свою роль в возникновении онкологии. Просто невозможно знать их все и избегать, да и часть с них неподтвержденная. Поэтому можно привести только наиболее вероятные причины рака желудка. Среди них:
Просто невозможно знать их все и избегать, да и часть с них неподтвержденная. Поэтому можно привести только наиболее вероятные причины рака желудка. Среди них:
- Чрезмерное употребление алкоголя и сигарет. Такие напитки сами по себе раздражают слизистую желудка, провоцируя паталогические процессы. Курение, а именно влияние его на онкологию, также доказано. Список веществ, содержащихся в сигаретном дыму, не проходит стороной организм человека. На минуточку, в нем содержится половина периодической таблицы Менделеева. Увеличивая количество выкуренных сигарет в сутки, человек приговаривает себя к ряду заболеваниям. Самое страшное то, что люди, находящиеся рядом с курильщиком, не по своей воле становятся участниками «употребления» сигаретного дыма.
- Употребление в пищу продуктов с повышенным содержанием неполезных веществ. Очень обширная тема. К ним относятся, например, фаст-фуд, сложные жиры, искусственные специи и т.д. Особое внимание стоит обратить на генномодифицированные продукты или овощи с повышенным содержанием пестицидов, нитратов, нитритов.
 Проникая в структуру клетки, они вызывают нарушение ее генного материала. В результате клетка не может нормально размножаться, или гибнет вовсе.
Проникая в структуру клетки, они вызывают нарушение ее генного материала. В результате клетка не может нормально размножаться, или гибнет вовсе. - Инфекция в желудочно-кишечном тракте. Многие слышали такое название, как Helicobacter pylori. Это название бактерии, провоцирующей развитие гастрита и язвенной болезни. Согласно бытующему сегодня мнению, эти болезни в ряде случаев стают причинами трансформации их в рак желудка. Эта бактерия способна благополучно существовать в кислотной среде человеческого желудка. Затяжная язва «подготавливает» среду для размножение раковых клеток.
- Продолжительное употребление некоторых медикаментов. К ним можно отнести антибиотики, противовоспалительные средства и т.д. Они являются провокаторами к язве желудка, и как следствие, открывается свободный путь к образованию рака.
- Радиация. Последствия катастрофы на ЧС осущаются до сих пор. Радиационное излучение мутирует клетки и раковые заболевания прогрессируют еще с большей скоростью. Большие дозы радиации само собой приводят к смерти организма.

- Операцию, целью которой является удаление части органа, пораженной опухолью, и окружающих лимфатических узлов, так как в них могут быть метастазы. Называется это субтотальная резекция. В запущенных случаях могут удалить желудок полностью (это называется гастрэктомия). Если есть метастазы в окружающих органах, то операция дополняется их удалением.
- Химиотерапию. Подразумевает введение цитостатических препаратов, угнетающих рост злокачественного новообразования.
- Лучевую терапию (облучение опухоли радиацией, которая уничтожает ее клетки).
Стадии
Стадии заболевания четко определяются при низкодифференцированных опухолях. При 0 стадии симптомы карциномы отсутствуют полностью.
Далее выделяются следующие:
- 1 стадия – в патологический процесс вовлекается лимфатическая система и подслизистая желудка.
- 2 стадия – опухолевый процесс поражает гладкомышечную структуру желудка, лимфоидные клетки.
 Наблюдается распространение к отдельным лимфоузлам.
Наблюдается распространение к отдельным лимфоузлам. - 3 стадия – полное поражение лимфатических узлов, новообразование прорастает через всю желудочную стенку, имеет крупный размер.
- 4 стадия – метастазирование по всему организму, может наблюдаться развитие различных осложнений, которые несут угрозу для жизни.
Каждая стадия развития имеет свою симптоматику, начальные этапы определенными признаками себя не выдают.
Метастазирование аденокарциномы
Метастазирование аденокарциномы осуществляется несколькими способами:
- Лимфогенный — с током лимфы опухолевые клетки сначала попадают в регионарные лимфатические узлы, а оттуда в более отдаленные группы, например, в надключичные.
- Гематогенный способ метастазирования предполагает рассеивание раковых клеток с током крови. Чаще всего образуются метастазы в печени (по воротной вене) и легких. При низкодифференцированных и недифференцированных аденокарциномах возможно поражение костного мозга.

- Если аденокарцинома толстой кишки проросла окружающие органы, возможно имплантационное метастазирование в результате контакта опухоли с воспринимающей поверхностью. В этом случае возможны множественные метастазы по брюшине (канцероматоз).
Причины
Главным этиологическим фактором аденокарциномы желудка считается ухудшение тока крови к органу, это становится причиной нарушения клеточного питания, выработки секретов. Такое патологическое состояние часто провоцируется отравляющим воздействием некоторых веществ.
По теме
- Онкогастроэнтерология
Кал при раке желудка
- Наталья Геннадьевна Буцык
- 6 декабря 2020 г.
Помимо этого, формирование патологии могут вызвать:
- Злоупотребление спиртными и табачными изделиями. У алкоголиков и курильщиков риск развития заболевания существенно выше.
- Неправильное питание – аденокарцинома нередко выявляется у людей, предпочитающих жирную, соленую, копченую пищу.
 При реакции с желудочным соком выделяются вещества, негативно воздействующие на слизистую, тем самым вызывая мутацию клеток.
При реакции с желудочным соком выделяются вещества, негативно воздействующие на слизистую, тем самым вызывая мутацию клеток. - Продолжительные диеты – малое количество поступающей пищи, недостаточный уровень витаминов и микроорганизмов, необходимых для нормальной работы организма.
- Инфицированность Хеликобактер пилори – бактерии способны вызвать инфильтративный гастрит, при котором характерно изменение структуры слизистой. Продолжительное существование инфекции в организме повышает вероятность формирования рака.
- Наследственная предрасположенность – если заболевание выявлялось у близких родственников, то шанс его проявления выше.
Помимо этого, существует ряд заболеваний, которые нередко предшествуют аденокарциноме желудка:
- Хроническая форма гастрита.
- Язвенная болезнь желудка.
- Полипы в желудочно-кишечном тракте, особенно это касается атрального отдела органа.

- Аденома — полиповидное доброкачественное образование, состоящее из трубчатых или ворсинчатых тканей.
- Пережитые хирургические вмешательства на органы пищеварительной системы.
Даже полное отсутствие подобных факторов не дает полной гарантии того, что рак желудка не сформируется.
Излечим ли рак желудка 4 степени
Можно ли вылечить рак желудка 4 стадии при помощи нетрадиционных способов. Ответ на этот вопрос – отрицательный. Успех терапии зависит от множества факторов:
- степени прогрессирования заболевания;
- возраста пациента;
- психологического настроя больного.
При раке желудка лечение народными средствами рассматривается в качестве дополнительно метода терапии, позволяющего укрепить защитные силы организма и снизить симптоматику рака. Надеяться только на этот способ терапии глупо. Настойки и отвары не дадут результата в борьбе с заболеванием без помощи онкологов.
Болезнь может поражать разные органы человека. Также заболевание диагностируется на разных стадиях. То, на какой находится эта болезнь, называется его дифференциацией. Ее принято обозначать буквой G. Если в организме человека присутствуют зараженные клетки, у которых степень видоизменения и отличия от здоровых клеток высокая, то они называются недифференцированными и обозначаются как G3.
Также заболевание диагностируется на разных стадиях. То, на какой находится эта болезнь, называется его дифференциацией. Ее принято обозначать буквой G. Если в организме человека присутствуют зараженные клетки, у которых степень видоизменения и отличия от здоровых клеток высокая, то они называются недифференцированными и обозначаются как G3.
Опухоли, которые относятся к такому виду болезни, имеют то же название, что и ткань, на которой они распространились. Например, аденокарцинома, плоскоклеточный неороговевающий рак и прочие. А недифференцированному раку дается название от формы зараженных клеток. Например, недифференцированный плоскоклеточный рак, перстневидно-клеточный и другие.
Симптомы
На первоначальных этапах патология себя никак не проявляет, в чем и заключается основная опасность рака желудка. Иногда наблюдаются несущественные изменения в работе организма, которые присутствуют при других патологических состояниях и не дают повода пациенту своевременно обратиться к специалисту. К подобным признакам относится постепенное снижение массы тела, общее недомогание, быстрая утомляемость.
К подобным признакам относится постепенное снижение массы тела, общее недомогание, быстрая утомляемость.
По теме
- Онкогастроэнтерология
Первые признаки рецидива рака прямой кишки
- Наталья Геннадьевна Буцык
- 3 декабря 2020 г.
По мере роста новообразования начинают проявляться следующие явления:
- Снижение аппетита.
- Болевой дискомфорт в области живота, зачастую зависят от приема пищи.
- Чувство переедания.
- Частая отрыжка, чувство жжения.
- Застойные процессы в желудке.
- Повышенная работа слюнных желез.
- Невосприятие организма мясных продуктов, другой белковой пиши.
- Малокровие.
- Тошнота, рвота.
- Каловые массы черного цвета – это указывает на внутренние кровоизлияния при распаде новообразования.

Требуется учитывать тот факт, что в некоторых случаях даже на запущенных этапах заболевание может не выражаться яркими симптомами – это напрямую зависит от типа рака, общего состояния больного.
Рак поджелудочной железы
Рак поджелудочной железы — злокачественный неопластический процесс, развивающийся из клеток органа. Это относительно редкое заболевание, на долю которого приходится около 3% от всех онкопатологий. В структуре онкозаболеваемости болезнь занимает 12 место среди мужчин и 10 среди женщин.
Основная проблема врачей, которые сталкиваются с раком поджелудочной железы — поздняя диагностика. Болезнь не имеет специфических маркеров, которые помогли бы обнаружить ее на ранних этапах развития.
Диагностика
Для начала врач собирает анамнез больного: уточняет симптомы, текущие заболевания. Врач-гастроэнтеролог методом пальпации исследует лимфоузлы.
Для уточнения диагноза назначаются инструментальные и лабораторные анализы. Исследование крови дает возможность определить наличие малокровия, которое всегда присуще раковым патологиям.
Проводится гастроскопия, эзофагогастродуоденоскопия, биопсия, что дает возможность более тщательно исследовать опухоль. Здесь устанавливается вид и запущенность процесса, для определения адекватного лечения. Осуществляется рентген с использованием контрастного вещества для выявления границы опухоли.
Компьютерная, магниторезонансная томография применяются для выявления последних стадий рака, при их помощи определяется и наличие метастазов.
Виды и типа рака
По локализации опухоли:
- рак головки, хвоста и тела;
- протока поджелудочной железы;
- островковых зон;
- выходящий за границы указанных зон.
- По степени дифференциации:
- высокодифференцированный;
- умереннодифференцированный;
- низкодифференцированный;
- недифференцированный.
По итогам патоморфологического анализа:
- протоковая аденокарцинома;
- гигантоклеточная опухоль;
- муцинозная цистаденокарцинома;
- серозная цистаденокарцинома;
- папиллярно-муцинозный рак;
- ацинарно-клеточная карцинома;
- панкреатобластома.

Кроме общепринятых классификаций, в ММК Сколково (Москва) пользуются классификацией TNM. Данной классификацией пользуются онкологи всего мира, что позволяет быстро делать выводы о состоянии здоровья конкретного больного и подобрать оптимальное лечение.
Лечение
После постановки диагноза требуется назначение необходимого лечения. При этом врач должен учитывать локализацию опухоли, ее размер, стадию развития, структуру, наличие метастаз, возраст пациента.
Хирургическое вмешательство
Наилучший результат дает проведение оперативного вмешательства, которого существует 2 вида. Осуществление субтотальной резекции подразумевает устранение непосредственно опухоли и пораженных региональных тканей.
При назначении гастрэктомии у пациента удаляется весь орган и близлежащие ткани: часть тонкой кишки, пищевода и окружающие лимфоузлы. Подобная процедура осуществляется в более сложных ситуациях, имеет продолжительный период реабилитации.
Эндолюминальное стенирование
Если проведение хирургии по каким-либо причинам невозможно, то часто терапия осуществляется посредством эндолюминального лазерного лечения.
Для того чтобы больной мог самостоятельно есть, в полость желудка вводится стен. Перед проведением хирургии и после него назначаются химио- и лучевая терапия.
Химиотерапия
Для лечения используются такие препараты, как Фторафур, Блеомицин, Цисплатин. Подобные процедуры дают возможность снизить размер опухоли перед операцией и устранить вторичные опухоли после ее проведения. Данный вид лечения дает возможность снизить риск возникновения рецидива до минимума.
Лучевая терапия
Лучевое лечение назначается перед проведением хирургии, это дает возможность уменьшить новообразование. Также процедура осуществляется после операции, поскольку эффективно разрушает оставшиеся раковые клетки. Помимо этого, использованием лучей можно предупредить внутренние кровотечения, снизить болевой синдром.
Иммунотерапия
Лекарства для химиотерапии неблагоприятно воздействуют не только на аномальные клетки, но и на здоровые ткани, по этой причине необходимо принимать специальные препараты, которые повышают уровень иммунной системы.
Стоимость лечения в клинике Хадасса в Сколково
Узнать точную стоимость можно после консультации. Доктор оценит состояние больного, изучит результаты обследования, составит план лечения и посчитает стоимость. Примерные цены можно узнать, заполнив электронную форму обратной связи или позвонив по указанному на сайте номеру телефона. Наш консультант предоставит нужную информацию.
Некоторым пациентам наши цены кажутся слишком высокими. Действительно, стоимость отдельных процедур может быть выше, чем в других медцентрах Москвы. Однако она окупается хорошими статистическими показателями. Прогноз сколько живут после лечения рака
Однолетняя выживаемость при данном заболевании составляет 26%, пятилетняя — всего 6%. Среди больных, пролеченных на первой стадии, выздоравливают 25%. Низкие показатели выживаемости объясняются поздней диагностикой патологии.
Расшифровывать статистику нужно очень осторожно. Во-первых, составляя прогноз, ученые собирают данные из разных уголков планеты, изучая не менее нескольких тысяч случав патологии. Как поведет себя болезнь в каждом конкретном случае предугадать невозможно. Кроме того, очень сложно сказать, как отреагирует конкретный пациент на лечение. И, наконец, третий момент: последние научные достижения в статистических данных не отображаются. Точный прогноз может дать только лечащий врач.
Как поведет себя болезнь в каждом конкретном случае предугадать невозможно. Кроме того, очень сложно сказать, как отреагирует конкретный пациент на лечение. И, наконец, третий момент: последние научные достижения в статистических данных не отображаются. Точный прогноз может дать только лечащий врач.
Осложнения
Нередко аденокарцинома желудка вызывает ряд опасных для здоровья и жизни осложнений:
- Внутренние кровотечения – новообразование растет, проникает в кровеносные сосуды, повреждая их, что и становится причиной регулярных кровотечений.
- Перфорация желудка – крупная опухоль образует сквозное отверстие в желудочной стенке, что сопровождается попаданием его содержимого в брюшную полость. Это становится причиной формирования перитонита.
- Пилоростеноз – заболевание пищеварительной системы, которое развивается в результате сужения выходного отверстия привратника желудка. Это приводит к ухудшению прохождения еды из желудка в полость кишечника.

- Асцит – скапливание жидкости в брюшной полости, которая образуется благодаря передавливанию новообразования венозных сосудов.
- Малокровие – из-за недостаточного поступления питательных веществ уровень гемоглобина понижается, что и вызывает развитие анемии.
- Проникновение метастазов в другие органы с последующим ухудшением их работы (почки, печень, пищевод, легкие).
При возникновении первых неприятных признаков необходимо обратиться к специалисту, это даст возможность выявить заболевание на ранних стадиях и предотвратит формирование осложнений.
Этиология
Точной картины этиологии на данный момент не существует. Основной причиной развития данного онкологического процесса принято считать длительное воздействие канцерогенных агентов на фоне ухудшения секреции желудка и нарушения кровообращения. Развитию заболевания могут послужить такие этиологические факторы:
- инфекционные заболевания ЖКТ;неправильное питание;злоупотребление спиртными напитками, курение;хроническая язва;длительное воздействие на организм токсических и радиационных веществ;перенесённые ранее заболевания, в лечение которых входили антибиотики, гормональные препараты;операбельное вмешательство в ЖКТ;генетическая предрасположенность.

Риск развития онкологического процесса в разы увеличивается, если человек регулярно и в больших количествах употребляет копчёное, жирное, острое и слишком солёное.
Следует отметить, что железистый рак желудка метастазирует в 90% всех случаев. На ранней стадии данный недуг диагностируют только в 20% случаев.
Выживаемость
Общая пятилетняя выживаемость, по статистике, составляет примерно 20%. Такой прогноз связан с тем, что в основной массе случаев патология обнаруживается на запущенных этапах.
По теме
- Онкогастроэнтерология
Какие боли возникают при раке прямой кишки
- Ольга Владимировна Хазова
- 3 декабря 2020 г.
Более подробно говорить о прогнозах можно исходя из стадии развития ракового заболевания:
- 0 стадия – прогноз благоприятный.
- 1 стадия – примерно 80%.
- 2 стадия — около 40%.
- 3 стадия — 10–20%.
- 4 стадия — ниже 5%.

Если заболевание обнаружено на последних стадиях, то человек может выжить около года, иногда эта цифра может увеличиться до 5 лет. При четком соблюдении всех рекомендаций специалиста и ведения здорового образа жизни наблюдались случаи, когда пациент мог прожить около 10 лет.
Большое значение имеет возрастная категория больного – после 50 лет шансы на выздоровление снижаются примерно на 10%.
Причины развития аденокарциномы толстой кишки
Причины развития аденокарциномы до конца не ясны, но есть некоторые данные, позволяющие определить факторы риска, увеличивающие вероятность развития данной патологии:
- Характер питания — избыточное потребление животных жиров, высокобелковых продуктов и недостаток в рационе клетчатки, а также переедание, злоупотребление алкоголем.
- Наличие полипов толстого кишечника. В большинстве случаев аденокарциномы развиваются из уже имеющихся полипов, причем чем дольше он существует и больше его размер, тем выше риски малигнизации.
 Во многих странах людям старше определённого возраста (50 лет) рекомендуют проходить периодическую колоноскопию с одновременным удалением полипов. На сегодняшний день это наиболее эффективное средство профилактики.
Во многих странах людям старше определённого возраста (50 лет) рекомендуют проходить периодическую колоноскопию с одновременным удалением полипов. На сегодняшний день это наиболее эффективное средство профилактики. - Генетическая предрасположенность. В большинстве случаев аденокарцинома толстой кишки является спорадическим заболеванием, т. е. не связана с наследственными факторами, но есть два случая, где генетика имеет ключевую роль. Это семейный аденоматозный полипоз и наследственный неполипозный рак толстого кишечника (он же синдром Линча).
- Наличие неспецифического язвенного колита и болезни Крона.
- Наличие в анамнезе рака женских половых органов.
- Иммунодефицитные состояния.
Рак ободочной кишки | Онкологический диспансер Санкт-Петербурга
Общая информация
Выделяют наследственный и спорадический (возникший случайным образом) рак ободочной кишки. Развитие наследственного рака генетически связано с некоторыми полипозными или неполипозными синдромами.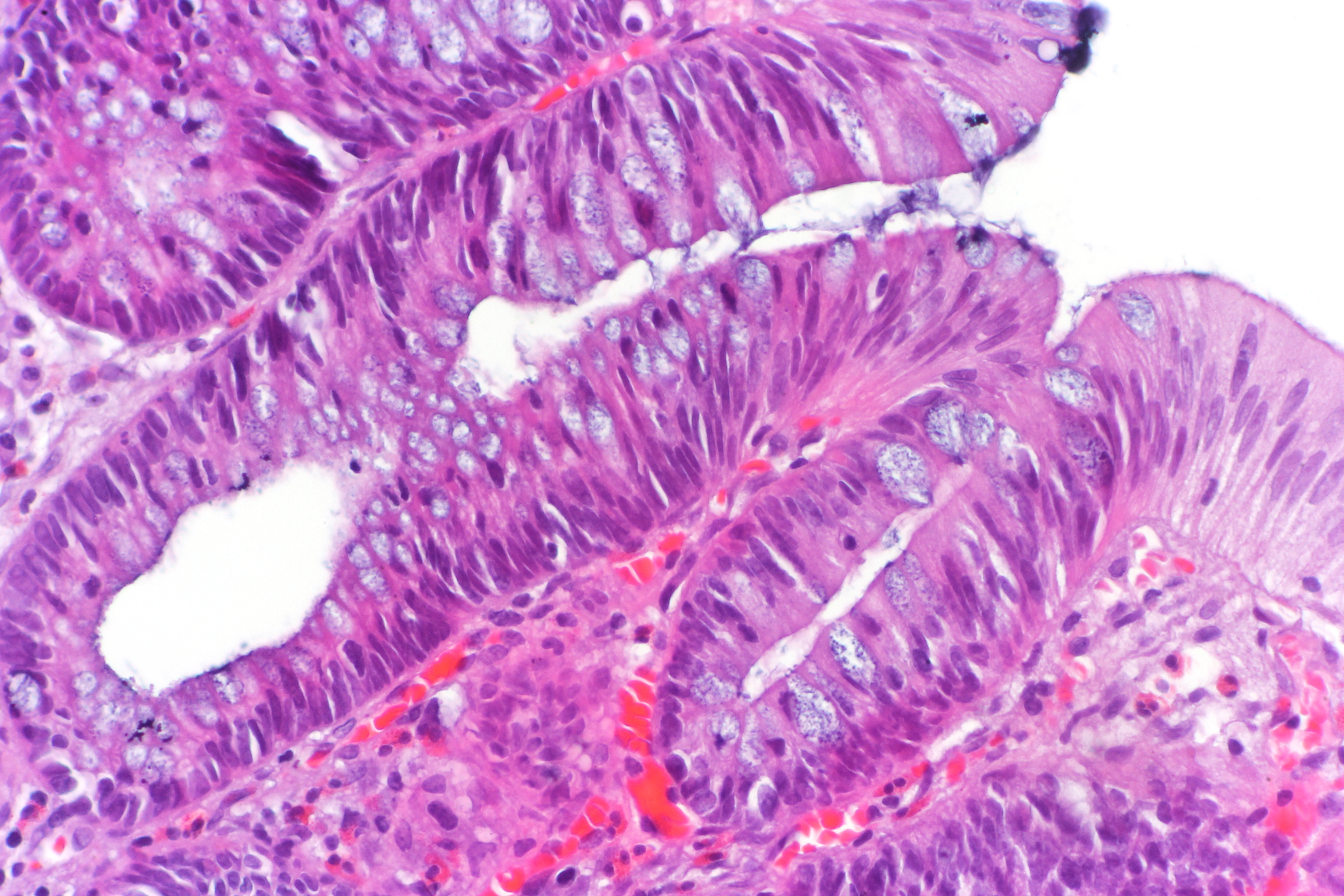 Такие наследственные болезни как семейный диффузный полипоз, синдром Гарднера и синдром Тюрко сопровождаются крайне высоким риском развития рака толстой кишки. Наследственный неполипозный рак ассоциирован с мутациями генов, отвечающих за репарацию ДНК. К 70 годам рак толстой кишки диагностируется примерно у 80% носителей данных мутаций. Кроме того, лица первой степени родства с больными раком толстой кишки имеют высокую степень риска возникновения этого заболевания.
Такие наследственные болезни как семейный диффузный полипоз, синдром Гарднера и синдром Тюрко сопровождаются крайне высоким риском развития рака толстой кишки. Наследственный неполипозный рак ассоциирован с мутациями генов, отвечающих за репарацию ДНК. К 70 годам рак толстой кишки диагностируется примерно у 80% носителей данных мутаций. Кроме того, лица первой степени родства с больными раком толстой кишки имеют высокую степень риска возникновения этого заболевания.
Наиболее важными экзогенными факторами, влияющими на возникновение спорадического рака толстой кишки, являются диета, ожирение и гиподинамия (малоподвижный образ жизни) являются. Частота рака ободочной кишки выше в тех странах, где в рационе основной массы населения преобладает мясо и ограничено потребление растительной клетчатки. Мясная пища вызывает увеличение концентрации жирных кислот, которые в процессе пищеварения превращаются в канцерогенные агенты. Меньшая частота рака толстой кишки отмечается в сельской местности и странах с традиционной растительной диетой (Китай, Индия, страны Средней Азии и Центральной Африки).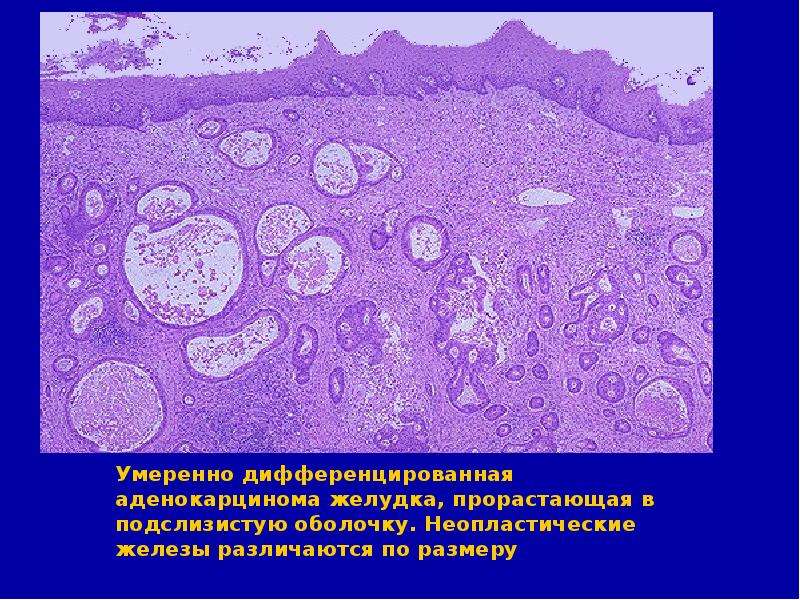 Согласно химической теории происхождения рака толстой кишки злокачественный процесс обусловлен мутагенным действием ряда экзо- и эндогенных химических веществ (канцерогенов) на клетки кишечного эпителия. Наиболее канцерогенными считаются полициклические ароматические углеводороды, ароматические амины и амиды, нитросоединения, а также метаболиты триптофана и тирозина. Канцерогенные вещества (бензпирен) могут образовываться при неправильной термической обработке пищевых продуктов, копчении мяса и рыбы. В результате воздействия канцерогенов на геном клетки происходят точечные мутации, приводящие к трансформации клеточных протоонкогенов в активные онкогены. Последние превращают нормальную клетку в опухолевую.
Согласно химической теории происхождения рака толстой кишки злокачественный процесс обусловлен мутагенным действием ряда экзо- и эндогенных химических веществ (канцерогенов) на клетки кишечного эпителия. Наиболее канцерогенными считаются полициклические ароматические углеводороды, ароматические амины и амиды, нитросоединения, а также метаболиты триптофана и тирозина. Канцерогенные вещества (бензпирен) могут образовываться при неправильной термической обработке пищевых продуктов, копчении мяса и рыбы. В результате воздействия канцерогенов на геном клетки происходят точечные мутации, приводящие к трансформации клеточных протоонкогенов в активные онкогены. Последние превращают нормальную клетку в опухолевую.
Ещё одним доказанным фактором риска возникновения рака толстой кишки являются воспалительные заболевания кишечника (ВЗК). Установлено, что у пациентов с болезнью Крона рак ободочной кишки возникает в 2,5 раза чаще, чем у здоровых людей. Также доказана высокая корреляция между неспецифическим язвенным колитом и колоректальным раком, особенно в случаях распространенного поражения язвенным процессом толстой кишки с анамнезом заболевания более 10 лет. Рак ободочной кишки у таких пациентов диагностируется в 5,2-30% наблюдений.
Полипы толстой кишки также достоверно увеличивают риск возникновения злокачественной опухоли. Индекс малигнизации одиночных полипов составляет 2-4 %, множественных (которые можно сосчитать) – 20 %, ворсинчатых образований – до 40 %. Полипы толстой кишки редко встречаются в молодом возрасте, а у лиц старших возрастных групп наблюдаются часто. По литературным данным, частота выявления полипов при аутопсиях составляет около 30 %.
Рак ободочной кишки развивается в соответствии с основными законами роста и распространения злокачественных опухолей: относительная автономность и нерегулируемость роста опухолевых клеток, снижение их дифференцировки, утрата органо- и гистотипического строения. Вместе с тем, имеются и свои особенности. Так, рост и распространение рака ободочной кишки происходят достоверно медленнее, чем аналогичные процессы, например, при раке желудка и поджелудочной железы. Опухоль толстой кишки длительное время не распространяется за пределы ее стенки.
Стадии рака ободочной кишки
Можно выделить три этапа развития опухолевого процесса:
- I и II стадии – опухоль ограничена самой толстой кишкой (возможно с подрастанием к соседним органам)
- III стадия – появляются метастазы опухоли в регионарные лимфатические узлы
- IV стадия – появляются отдалённые метастазы опухоли (печень, лёгкие, брюшина, отдалённые лимфатические узлы, головной мозг и др.)
I – III стадии можно считать потенциально излечимыми. IV стадия подлежит паллиативному лечению (расценивается как хроническое, неизлечимое заболевание). Следует отметить, что даже при IV стадии возможно длительное продление жизни. В настоящее время имеется определённый процент пациентов, переживающих 10-летний рубеж от момента выявления IV стадии рака ободочной кишки.
Чем ниже дифференцировка опухоли, тем выше ее степень злокачественности (более быстрый рост опухоли и более раннее метастазирование). Метастазирование рака ободочной кишки происходит лимфогенным (наиболее часто), гематогенным и имплантационным путями. Лимфогенное метастазирование идет по ходу питающих кишку сосудов, а также в лимфатические узлы брыжейки. Гематогенные метастазы наиболее часто обнаруживаются в печени, легких, головном мозге. Имплантационные метастазы возникают вследствие прорастания опухолью всех слоев кишечной стенки и распространения опухолевых клеток по брюшине (карциноматоз брюшины).
Клиническая картина рака ободочной кишки
Рак ободочной кишки является полисимптомным заболеванием. Его клинические проявления зависят от локализации опухоли (в правой или левой половине ободочной кишки), характера ее роста, размеров опухоли, стадии злокачественного процесса, наличия осложнений. Ранние формы рака практически всегда протекают бессимптомно и выявляются при колоноскопии по поводу других заболеваний или при диспансерном обследовании.
Большинство пациентов обращаются к врачу по поводу появления крови или слизи в каловых массах, нарушения стула в виде появившихся запоров или, наоборот, поносов, а также изменения формы каловых масс, в связи с кишечным дискомфортом, болевыми ощущениями в животе, ухудшением общего состояния.
При опухолях правой половины толстой кишки,которые более длительное время могут протекать бессимптомно, первыми признаками заболевания часто являются недомогание, слабость, снижение трудоспособности, ухудшение аппетита, похудание, анемия, субфебрильная температура тела (до +37,90С). В некоторых случаях одним из первых симптомов оказывается плотное образование в животе справа, которое обнаружил сам пациент.
Для опухолей левой половины ободочной кишки характерны запоры, которые появились без видимых причин и со временем участились, непостоянная примесь слизи и темной крови в стуле, испражнения в виде овечьего кала, необъяснимый метеоризм и эпизоды внезапных спастических или схваткообразных болей в животе без четкой локализации.
Возможные осложнения рака ободочной кишки:
- кровотечение из опухоли;
- острая обтурационная толстокишечная непроходимость;
- перфорация опухоли;
- параканкрозный абсцесс;
- местное распространение опухоли на соседние органы и ткани с нарушением их функций.
Диагностика рака ободочной кишки
«Diagnosis bona – curatio bona»
«Bene diagnoscitur, bene curatur»
Набор диагностических исследований при раке ободочной кишки имеет свои принципиальные особенности. Недостаточно просто выявить опухоль. Чрезвычайно важным является выполнение комплексного обследования с оценкой гистологического варианта и распространённости опухолевого процесса. От результатов правильно сформулированного диагноза зависит объём лечения и последовательность различных его этапов.
ВАЖНО! Если Вам говорят что-то вроде: «У вас рак! Надо срочно оперировать! Идти к онкологу и обследоваться – бесполезная трата сил и средств!» — ОБРАТИТЕСЬ К СПЕЦИАЛИСТУ-ОНКОЛОГУ!
Оперировать пациента, которому следует начинать лечение с лекарственной или лучевой терапии – неверно! Ошибочный диагноз ведёт к ошибочной лечебной тактике, а это, в свою очередь, ведёт к худшим прогнозам на выздоровление и дальнейшую жизнь!
Примерным минимумом обследований пациента с опухолью ободочной кишки следует считать:
- Комплекс клинических лабораторных исследований: клинический анализ крови, общий анализ мочи, глюкоза, АлТ, АсТ, билирубин общий, белок общий, креатинин, амилаза, С-реактивный белок, ПТВ+МНО, HBsAg, HCV-AT, AT HIV-1,2, антитела к Trep. Pallidum, СА 19-9, РЭА
- Электрокардиография
- Осмотр терапевта с заключением о наличии и выраженности сопутствующей патологии
- КТ грудной клетки и брюшной полости с контрастированием
- Фиброгастроскопия + фиброколоноскопия
- Исследование гистологического материала (биоптатов опухоли)
- Ирригоскопия при наличии стенозирующей опухоли, за которую невозможно зайти эндоскопом
- Женщинам дополнительно: УЗИ малого таза + осмотр гинеколога
По результатам первичного осмотра врача-онколога могут потребоваться дополнительные исследования и консультации (МРТ головного мозга, внутривенная урография, фибробронхоскопия, осмотр невролога, осмотр эндокринолога и т.д.). Их спектр строго индивидуален и зависит от распространённости опухолевого процесса и наличия сопутствующей патологии.
Хирургическое лечение рака ободочной кишки
Хирургия является основным методом лечения рака ободочной кишки при отсутствии отдалённых метастазов. Показания к операции всегда являются абсолютными. Выбор варианта хирургического вмешательства зависит от локализации опухоли, клинической стадии заболевания, наличия или отсутствия осложнений, а также общего состояния больного.
Операция должна выполняться обученными хирургами-онкологами с соблюдением основ онкохирургии – футлярности вмешательства, соблюдения мероприятий абластики и антибластики. Кроме того, для выбора правильной лечебной тактики в дальнейшем, необходимо удалить и исследовать не менее 12 лимфатических узлов.
ВАЖНО! К сожалению, мы регулярно сталкиваемся с негативными последствиями плохо выполненных хирургических вмешательств в неонкологических стационарах города! Тщательно взвешивайте выбор места прохождения планового хирургического лечения.
Лекарственное лечение
Адъювантная (профилактическая) полихимиотерапия (АПХТ) проводится после радикального удаления опухоли при отсутствии видимых опухолевых очагов в организме. Её цель – воздействие на нераспознанные и неопределяемые микрометастазы опухоли, которые теоретически могут иметься у пациента. АПХТ начинается в срок до 60 суток после операции. После 60 суток профилактическая химиотерапия считается неэффективной и необоснованной.
ВАЖНО! Своевременное начало профилактического и других видов лечения – ещё один веский повод проходить лечение в специализированных онкологических учреждениях!
Паллиативная химиотерапия проводится в случае наличия неудалимых очагов опухоли при метастатическом раке ободочной кишки. Её задачами являются увеличение продолжительности и улучшение качества жизни за счет замедления прогрессирования опухолевого процесса.
Наблюдение после окончания лечения
Согласно Приказу Минздрава РФ №915н от 15 ноября 2012 года «Об утверждении Порядка оказания медицинской помощи населению по профилю «онкология»», все пациенты после проведения специального лечения по поводу злокачественных опухолей подлежат пожизненному диспансерному наблюдению районным онкологом (находится в поликлинике по месту жительства). В первый год после окончания лечения пациенты должны осматриваться 1 раз в 3 месяца, второй год – 1 раз в 6 месяцев и начиная с третьего года наблюдения – 1 раз в год. Кроме осмотра пациентам показано выполнение соответствующих лабораторных и инструментальных исследований (зависит от вида и локализации опухолевого процесса).
Чтобы записаться на консультацию и осмотр у врача, обращайтесь к специалисту контактного центра:
Единый колл-центр: +7 (812) 607-03-03
Прогноз рака толстой кишки стадии IV
Когда ваш врач скажет вам, что у вас рак толстой кишки, который распространился на другие части вашего тела, у вас, естественно, возникнет множество вопросов, в том числе, что это будет значить для вашего будущего.
Все разные. Даже если болезнь невозможно вылечить, существуют методы лечения, которые могут помочь вам прожить дольше и уменьшить боль, чтобы качество вашей жизни было как можно лучше.
Вы захотите работать с врачом, который специализируется на лечении рака толстой кишки IV стадии.Вы также можете попросить второе мнение, чтобы быть уверенным в том, что вы понимаете свою ситуацию и возможности.
После лечения
Ваш врач лечит ваш рак толстой кишки с помощью операции, химиотерапии, таргетной терапии, лучевой терапии или комбинации этих методов лечения. Если одно лечение не работает или перестает работать, вы можете попробовать что-нибудь другое.
После того, как вы закончите, вы будете посещать врача каждые несколько месяцев. Одна из причин обратиться к врачу — это контролировать любые побочные эффекты лечения, которые у вас есть.
Ваш врач также проведет анализы, чтобы убедиться, что ваш рак не вернулся. Рак, который возвращается, называется рецидивом. Рак толстой кишки, скорее всего, рецидивирует в течение первых 5 лет после лечения.
Если рак все же возвращается, регулярные посещения врача помогут обнаружить его на ранней стадии, когда его легче всего вылечить. Спросите своего врача, как могут выглядеть симптомы рецидива. Немедленно позвоните, если заметите эти симптомы.
У вас будет лучший результат, если вы останетесь здоровыми во время выздоровления после лечения рака толстой кишки.Следуйте этим советам:
Клинические испытания
Если вы попробовали несколько методов лечения рака толстой кишки, но они не помогли или перестали работать, у вас может быть другой вариант: клинические испытания.
Ученые ищут новые способы лечения рака толстой кишки IV стадии в клинических испытаниях. Эти испытания проверяют новые методы лечения, чтобы убедиться, что они безопасны и работают. Часто они позволяют людям попробовать новое лекарство, доступное далеко не каждому. Ваш врач может сказать вам, подходит ли вам одно из этих испытаний.
Паллиативная помощь
В вашем медицинском обслуживании есть нечто большее, чем лекарства или хирургическое вмешательство, нацеленные на рак. Ваши врачи также должны помочь вам справиться с любой болью, возникающей в результате рака. Ваше социальное, эмоциональное и духовное здоровье также может нуждаться в поддержке, когда вы боретесь с таким серьезным заболеванием.
Паллиативная помощь делает все это. Это не то же самое, что хоспис, и не только для людей, находящихся на грани смерти. Вы по-прежнему будете получать всю остальную медицинскую помощь для борьбы с раком.Паллиативная помощь предоставляется в дополнение к другим видам лечения, а не вместо них.
Национальный институт рака заявляет, что паллиативная помощь «должна начинаться с постановки диагноза» и сосредоточена на качестве вашей жизни. Врачи, медсестры, диетологи, фармацевты и социальные работники — вот некоторые из профессиональных медиков, которые в этом помогают. Они могут стать неоценимым помощником в борьбе с болезнью.
Общая картина
Если один из вопросов, который у вас на уме, касается выживаемости при вашем раке, вы сначала захотите получить некоторую перспективу.Статистика не раскрывает всей картины.
Показатели выживаемости похожи на вид с высоты 30 000 футов: они широкие, но не детализированные. Эти цифры представляют собой приблизительную оценку того, как долго могут жить люди с определенным типом рака и стадией. Относительная 5-летняя выживаемость рака толстой кишки на стадии IV составляет около 14%. Это означает, что около 14% людей с раком толстой кишки IV стадии, вероятно, будут живы через 5 лет после постановки диагноза.
Но ты не номер. Никто, включая вашего врача, не может сказать вам точно, сколько вы проживете.Ваше мировоззрение зависит от многих вещей, в том числе от вашего возраста, состояния здоровья, места распространения рака и вида лечения.
Учтите, что цифры меняются — в лучшую сторону.
Растущее число людей с раком толстой кишки IV стадии живут дольше 2 лет. А для небольшой группы людей с раком, который распространился только на вашу печень или легкие, операция может даже вылечить его.
Также помните, что показатели выживаемости основаны на исследованиях, проведенных несколько лет назад.По мере улучшения лечения эти цифры могут возрасти.
Раньше рак толстой кишки было труднее лечить, если он распространился. Достижения в области лечения улучшили прогноз за счет замедления развития рака.
Большинство выживших после колоректального рака значительную часть оставшейся жизни живут в хорошем состоянии
Борьба с причинами рака. 2012; 23 (9): 1421–1428.
, 1, 2 , 3, 4 , 2, 5 , 6 , 1 и 3, 4Isabelle Soerjomataram
1 Департамент общественного здравоохранения, Erasmus MC, P.O. Box 2040, 3000 CA, Роттердам, Нидерланды
2 Департамент глобального здравоохранения и народонаселения, Гарвардская школа общественного здравоохранения, Бостон, Массачусетс, США
Мелисса С.Ю. Тонг
3 Комплексный онкологический центр Юг, Эйндховен Рак Registry, Эйндховен, Нидерланды
4 Департамент медицинской психологии, Центр исследований психологии соматических заболеваний (CoRPS), Тилбургский университет, Тилбург, Нидерланды
Majid Ezzati
2 Департамент глобального здравоохранения и народонаселения , Гарвардская школа общественного здравоохранения, Бостон, Массачусетс, США
5 Департамент эпидемиологии и биостатистики, Центр окружающей среды и здоровья MRC-HPA, Школа общественного здравоохранения, Имперский колледж, Лондон, Великобритания
Элизабет Б.Lamont
6 Департамент политики здравоохранения, Гарвардская медицинская школа, Бостон, Массачусетс, США
Wilma J. Nusselder
1 Департамент общественного здравоохранения, Erasmus MC, P.O. Box 2040, 3000 CA Роттердам, Нидерланды
Lonneke V. van de Poll-Franse
3 Комплексный онкологический центр Юг, Онкологический реестр Эйндховена, Эйндховен, Нидерланды
4 Департамент медицинской психологии, Центр исследований по психологии соматических заболеваний (CoRPS), Тилбургский университет, Тилбург, Нидерланды
1 Департамент общественного здравоохранения, Erasmus MC, P.O. Box 2040, 3000 CA Роттердам, Нидерланды
2 Департамент глобального здравоохранения и народонаселения, Гарвардская школа общественного здравоохранения, Бостон, Массачусетс, США
3 Южный комплексный онкологический центр, регистр рака Эйндховена, Эйндховен, Нидерланды
4 Департамент медицинской психологии, Центр исследований психологии соматических заболеваний (CoRPS), Тилбургский университет, Тилбург, Нидерланды
5 Департамент эпидемиологии и биостатистики, Центр окружающей среды и здоровья MRC-HPA, Школа общественного здравоохранения, Имперский колледж, Лондон, Великобритания
6 Департамент политики здравоохранения, Гарвардская медицинская школа, Бостон, Массачусетс, США
Автор, ответственный за переписку.Поступило 2 августа 2011 г .; Принято 5 июня 2012 г.
Эта статья распространяется на условиях лицензии Creative Commons Attribution License, которая разрешает любое использование, распространение и воспроизведение на любом носителе при условии указания автора (авторов) и источника.
Эта статья цитируется в других статьях в PMC.Реферат
Цель
Диагностика колоректального рака (CRC) сокращает продолжительность жизни и ухудшает самочувствие пациентов. Мы стремились оценить детерминанты здоровья и функционального статуса, а также оценить долю оставшейся жизни, которую выжившие после КРР проведут с хорошим здоровьем.
Методы
Используя метод Салливана, ожидаемая продолжительность здоровой жизни была рассчитана на основе данных о выживании 14 849 выживших CRC в популяционном регистре рака на юге Нидерландов и информации о качестве жизни среди случайной выборки этих выживших ( n = 1,291 ).
Результаты
В целом, несмотря на небольшую ожидаемую продолжительность жизни (LE в возрасте 50 = 12 лет для мужчин и 13 лет для женщин), большинство выживших после CRC провели большую часть своей оставшейся жизни в хорошем состоянии здоровья (74 и 77% для мужчин. и самки соответственно).Те, кто длительно выжил, могут рассчитывать на нормальную продолжительность жизни (LE в возрасте 50 = 30 лет) и провести большую часть оставшейся жизни в хорошем состоянии здоровья (78%). В отличие от них, у людей с CRC стадии IV осталось жить менее 2 лет, и более половины оставшейся жизни они провели с плохим здоровьем.
Выводы
Большинство пациентов с КРР не ожидают никаких компромиссов в отношении здорового образа жизни, что подчеркивает важность раннего выявления. С другой стороны, высокая доля нездоровых лет среди лиц, переживших КРР на стадии IV, подтверждает важность раннего выявления и паллиативной помощи.
Электронные дополнительные материалы
Онлайн-версия этой статьи (doi: 10.1007 / s10552-012-0010-2) содержит дополнительные материалы, которые доступны авторизованным пользователям.
Ключевые слова: Колоректальный рак, Ожидаемая продолжительность здоровой жизни, Население, Выжившие
Введение
Из-за повышения осведомленности о колоректальном раке (CRC), приводящего к более раннему выявлению и улучшению лечения, выживаемость среди пациентов с CRC увеличивается [ 1].Качество жизни (КЖ) пациентов в первые 3 года после постановки диагноза обычно снижается, хотя со временем с момента постановки диагноза оно может улучшиться [2]. Тем не менее, многие выжившие после CRC продолжают жить с долгосрочными побочными эффектами рака [3], особенно связанными с его лечением. В последнее десятилетие лечение CRC стало более агрессивным. Теперь он включает новые химиотерапевтические агенты и их комбинации, а также новые лучевые и хирургические подходы [4] для пациентов с излечимыми и неизлечимыми заболеваниями на момент постановки диагноза.Хотя эти успехи в лечении были связаны с увеличением выживаемости, они также связаны с увеличением частоты долгосрочных побочных эффектов, таких как усталость, желудочно-кишечные проблемы, недержание мочи и сексуальная дисфункция [4]. Эти побочные эффекты могут быть довольно серьезными и усугубляться тем фактом, что выжившие после КРР, как правило, старше и часто страдают другими сопутствующими хроническими заболеваниями [5]. Помимо физического дискомфорта, CRC также оказывает психологическое воздействие на пациента, то есть страх повторения, беспокойство, депрессия или отрицательный образ тела, которые могут снизить качество жизни [4, 6].
В этом исследовании мы определили факторы, связанные с самооценкой здоровья и физическим функционированием после диагностики CRC, используя популяционные данные. Этот результат был использован для расчета доли ожидаемой продолжительности здоровой жизни и ожидаемой продолжительности жизни без инвалидности для сравнения с долей населения Нидерландов в целом. Оценка доли лет здоровой жизни является новаторским подходом в онкологических исследованиях и может служить инструментом для оценки уровня излечения выживших не только путем оценки выживаемости, но и с учетом имеющейся информации о благополучии и функциональных способностях выживших.В то же время он также выявляет группы с плохим состоянием здоровья, нуждающиеся в дополнительном уходе.
Материалы и методы
Данные
Для анализа мы использовали данные выживших после CRC из популяционного реестра рака Эйндховена (ECR). ECR регистрирует данные обо всех вновь диагностированных случаях рака на юге Нидерландов, в районе с 2,4 миллиона жителей [7]. Зона покрытия реестра на юге Нидерландов постепенно увеличивалась и составила около 0.9 миллионов человек в 1975 году и более 2 миллионов человек с 1988 года. Для всех онкологических больных информация о стадии опухоли на момент постановки диагноза (на основе патологических и клинических метастазов опухолевых узлов (TNM), классифицированных в соответствии с системой UICC [8]), тип первичного данные о лечении (тип хирургии, химиотерапия, гормональная терапия и лучевая терапия) и сопутствующих заболеваниях (собираются с 1993 г.) обычно собираются. Кроме того, регистрируются возраст, пол и социально-экономический класс (на основе почтовых индексов, собираемых с 1983 г.) [9].
Используя голландскую версию SF-36 [10], оценка качества жизни была проведена в 2009 году с помощью почтовых вопросников среди случайной выборки из 1692 выживших после CRC (процент ответов 82%) в пределах ECR [11, 12]. У этих выживших был диагностирован CRC в период с 1998 по 2007 год. Медицинские специалисты отправили своим (бывшим) пациентам письма, чтобы проинформировать их об исследовании вместе с анкетой. Напоминание отправлялось, если анкета не возвращалась в течение 2 месяцев. Утверждение для этого исследования было получено от местного сертифицированного комитета по медицинской этике.
Анализ
Мы выполнили многомерную логистическую регрессию, чтобы оценить связь самооценки здоровья и функциональной инвалидности с историей болезни. Мы скорректировали демографические факторы, такие как пол, возраст (возрастные группы 5 лет и возрастная группа 85 лет и старше) и социально-экономический класс: высокий, средний, низкий и институционализированный (последний был исключен из дальнейшего анализа из-за низких цифр. ). Для клинических факторов мы включили подтип (ободочная и прямая кишка), патологическую стадию (pTNM: I, II, III и IV, 4% неизвестная стадия была исключена), лечение (только хирургическое вмешательство, хирургическое вмешательство с химиотерапией (рак толстой кишки высокого риска, стадия II и все стадии III [13]), а также хирургическое вмешательство с лучевой терапией с химиотерапией или без нее (стадия рака прямой кишки III [13])), сопутствующая патология на момент постановки диагноза (нет и одна или несколько) и время последующего наблюдения (5 лет или меньше и 6 лет и более).
Используя историю выживания в сочетании с оценкой качества жизни, мы рассчитали ожидаемую продолжительность здоровой жизни (HLE) и ожидаемую продолжительность жизни без инвалидности (DFLE). Этот расчет был выполнен только для факторов, которые повлияли на благополучие или функциональные ограничения, проверенные многомерным анализом. Во-первых, ожидаемая продолжительность жизни была рассчитана путем построения таблицы дожития на основе истории выживания выживших после CRC, которые были живы в период с 2005 по 2009 годы. Данные за последние пять календарных лет использовались для обеспечения достаточного количества смертей и получения самых последних оценок для продолжительность жизни.По той же причине мы включили только данные выживших, которым на момент исследования было 50 лет и старше. Наконец, продолжительность жизни была рассчитана на основе данных 14 849 выживших. Что касается состояния здоровья, мы использовали оценку качества жизни выживших старше 50 лет на момент опроса, которые ответили на вопрос об общем состоянии здоровья (93% от общего числа респондентов, n = 1291) и ответивших на вопрос. по ограничению мобильности (88% от общего числа респондентов, n = 1221).Мы разделили 5-уровневые ответы на вопрос SF-36 «Как вы оцениваете свое общее состояние здоровья?» на отлично, очень хорошо и хорошо = хорошо, а удовлетворительно и плохо = плохо. Поскольку один может сообщить о хорошем или здоровом, но имеет функциональную инвалидность, мы также включили в наш анализ показатель ежедневной функциональной способности из SF-36. Распространенность функциональной инвалидности рассчитывалась на основе трехуровневого ответа на вопрос SF-36 «Вы ограничены ходом нескольких сотен метров по состоянию здоровья?» Мы назначили функциональное ограничение тем, кто ответил «да, очень сильно» и «да, немного ограничен».Расчеты были выполнены с использованием метода Салливана, который учитывает перекрестную информацию о повозрастной распространенности общего состояния здоровья [14]. Мы рассчитали общую продолжительность жизни и ожидаемую продолжительность здоровой жизни, используя руководство, рекомендованное Европейским отделом мониторинга ожидаемой продолжительности жизни (EHEMU) [15]. Подробности расчета представлены в Приложении 1 (см. Онлайн-ресурсы). Все расчеты проводились с использованием Stata 11.1 для Windows (StataCorp, Техас, США).
Результаты
В период с 2005 по 2009 год 14 849 человек в возрасте 50 лет и старше были живы с историей диагноза CRC в ECR (53% мужчин, таблица).Большинство выживших были 65 лет и старше (62%) и обычно имели другие хронические заболевания на момент постановки диагноза (63% среди лиц с известным статусом сопутствующих заболеваний). Две трети выживших имели диагноз CRC I или II стадии и получали только хирургическое лечение. Пятилетняя выживаемость по стадиям представлена на рис. Существует заметная разница в выживаемости по стадиям: 57% пациентов со стадией I выживают в течение 10 лет по сравнению с 7% пациентов со стадией IV.
Таблица 1
Характеристики выживших после колоректального рака в 2005–2009 гг.
| Мужчина ( n, %) | Женщина ( n, %) | |
|---|---|---|
| <50 лет | 371 (5) | 312 (4) |
| 50–64 года | 2,753 (35) | 2,143 (31) |
| 65–379 лет | 3,394 (48) | |
| 80+ лет | 800 (10) | 1,177 (17) |
| Возраст в 2005 г. — 2009 a | ||
| 50–64 года | 2329 (30) | 1712 (24) |
| 65–79 лет | 4,127 (53) | 3,423 (49) |
| 80241 80 | 1367 (17) | 1891 (27) |
| Социально-экономическая группа | ||
| Низкий | 1,725 (22) | 1,970 (28) |
| Средний | 3,042 (39) | 2,556 (36) |
| Высокий | 2,531 (32) ) | |
| Учрежден | 257 (3) | 359 (5) |
| Отсутствует | 268 (3) | 257 (4) |
| Место опухоли | ||
| Толстая кишка | 4,731 (60) | 4,875 (69) |
| Прямая кишка | 3,092 (40) | 2,151 (31) |
| Этап | ||
| I | 2,121 (27) | 1,763 (25) |
| II | 2,697 (34) | 2,587 (37) |
| III | 1875 (24) ) | |
| IV | 1,130 (14) | 892 (13) |
| Лечение | ||
| Только хирургия (S) | 4,321 (55) | 4,525 (61) |
| S + химиотерапия | 1,174 (15) | 1027 (14) |
| S + радио- ± ± химиотерапия | 1729 (22) | 1250 (17) |
| Другое | 599 (8) | 635 (8) |
| Коморбидность | ||
| 0 | 2,353 (30) | 2,239 (32) |
| 1 или более | 4,272 (55) | 3,537 (50) |
| Неизвестно | 15243 1,198 (1198) (18)||
| Всего | 7,823 | 7,026 |
Доля выживаемости среди выживших после колоректального рака, живших в период с 2000 по 2009 год
Детерминанты плохого здоровья и физической инвалидности
Плохое здоровье было связано с полом, социально-экономическим статусом, стадией опухоли и сопутствующими заболеваниями при диагностике (таблица).Самым сильным предиктором плохого воспринимаемого здоровья была стадия. Выжившие со стадией IV в шесть раз чаще сообщали о плохом здоровье по сравнению с пациентами со стадией I. Наличие одного или нескольких хронических заболеваний на момент постановки диагноза также было одним из самых сильных предикторов плохого здоровья [Отношение шансов (OR) = 2,5, 95% достоверность интервал (95% ДИ) = 1,8–3,4]. Низкий и средний социально-экономический класс также положительно коррелировал с плохим здоровьем [OR = 2,2 (1,5–3,1) и 1,5 (1,1–2,1), соответственно]. Наконец, выжившие женщины на 50% чаще сообщали о плохом здоровье, чем мужчины.Типы лечения CRC не повлияли на общее состояние здоровья. Если мы не включили стадию в многомерную регрессию, шансы сообщить о плохом общем состоянии здоровья оставались одинаковыми для тех, кто получал лучевую терапию с химиотерапией или без нее, увеличиваясь до 1,1 (95% ДИ: 0,8–1,6, от OR: 0,72) среди тех, кто прошли химиотерапию и до 5,4 (95% ДИ: 1,4–20,1, от OR: 1,2) среди тех, кто получал другую терапию, соответственно (результаты не показаны).
Таблица 2
Воспринимаемое состояние здоровья выживших после колоректального рака в 2009 г.
| Хорошее ( n ,%) | Плохое ( n ,%) | Отношение нечетности a (95% CI ) ) при плохом самочувствии | |
|---|---|---|---|
| Секс | |||
| Мужской | 561 (59) | 169 (51) | 1 |
| Женский | 396 (41) | 165 (49) | 1.49 (1,14–1,95) |
| Возраст при обследовании | |||
| 50–64 года | 289 (30) | 88 (26) | 1 |
| 65–79 лет | 551 (58) | 181 (54) | 0,98 (0,71–1,3 ) |
| 80+ лет | 117 (12) | 65 (19) | 1,48 (0,96–2,27) |
| Социально-экономический статус | |||
| Высокий | 367 (38) | 86 (26) | 1 |
| Средний | 366 (38) | 126 (38) | 1.49 (1.08–2.06) |
| Низкий | 178 (19) | 102 (31) | 2,16 (1,51–3,10) |
| Учрежден | 22 (2) | 9 (3) | 1,23 (0,51–2,96) |
| Неизвестно | 24 (2) | 11 (3) | 1,803 0,8 () |
| Место опухоли | |||
| Толстая кишка | 632 (66) | 224 (67) | 1 |
| Прямая кишка | 325 (34) | 110 (33) | 1.24 (0,81–1,90) |
| Время с момента постановки диагноза | |||
| ≤5 лет | 722 (75) | 263 (79) | 1 |
| 6+ лет | 235 (25) | 71 (21) | 1,05 (0,76–1,45) |
| Стадия диагностики | |||
| I | 270 (28) | 97 (29) | 1 |
| II | 385 (40) | 112 (34) | 0.77 (0,55–1,08) |
| III | 272 (28) | 87 (26) | 1,11 (0,72–1,69) |
| IV | 30 (3) | 38 (11) | 5,76 (2,92–11,38) |
| Коморбидность при постановке диагноза | |||
| 0 | 415 (43) | 86 (26) | 1 |
| 1 или более | 459 (48) | 231 (69) | 2,47 (1.82–3,35) |
| Неизвестно | 83 (9) | 17 (5) | 0,96 (0,53–1,73) |
| Лечение | |||
| Хирургия (S) | 505 (53) | 184 (55) | 1 |
| S + химиотерапия | 200 (21) | 68 (20) | 0,79 (0,49–1,2) |
| S + лучевая терапия ± химиотерапия | 248 (26) | 76 (23) | 0.72 (0,45–1,14) |
| Другое | 4 (0,5) | 6 (2) | 1,22 (0,25–5,84) |
несколько сот метров, таблица). Кроме того, мы заметили, что диагноз CRC III стадии (помимо стадии IV) также положительно связан с функциональной инвалидностью. Хотя это не имеет существенной связи с воспринимаемым здоровьем, более высокий возраст был связан с увеличением функциональных ограничений: выжившие после CRC в возрасте 80+ лет в четыре раза чаще испытывали трудности при ходьбе на несколько сотен метров, чем люди в возрасте 50–64 лет.
Таблица 3
Функциональная инвалидность (ФД) у лиц, переживших колоректальный рак, в 2009 г.
| FD — ( n ,%) | FD + () ,% Отношение нечетных чисел a (95% ДИ) для FD | ||
|---|---|---|---|
| Секс | |||
| Наружный | 488 (59) | 203 (52) | 1 |
| Женский | 342 (41) | 188 (48) | 1.34 (1.03–1.74) |
| Возраст при обследовании | |||
| 50–64 года | 298 (36) | 71 (18) | 1 |
| 65–79 лет | 454 (55) | 235 (60) | 2,03 (1,47–2,81) |
| 80+ лет | 78 (9) | 85 (22) | 3,57 (2,30–5,55) |
| Социально-экономический статус | |||
| Высокий | 339 (41) | 91 (23) | 1 |
| Средний | 320 (39) | 145 (37) | 1.63 (1,19–2,24) |
| Низкий | 137 (17) | 128 (33) | 2,77 (1,94–3,94) |
| Учрежден | 14 (2) | 14 (4) | 2,99 (1,30–6,85) |
| Неизвестно | 20 (2) | 13 (3) | 2,08 (0,96–4,48) |
| Место опухоли | |||
| Толстая кишка | 540 (65) | 275 (70) | 1 |
| Прямая кишка | 290 (35) | 116 (30) | 0.91 (0,59–1,42) |
| Время с момента постановки диагноза | |||
| ≤5 лет | 627 (76) | 309 (79) | 1 |
| 6+ лет | 203 (24) | 82 (21) | 0,98 (0,71–1,35) |
| Стадия диагностики | |||
| I | 247 (30) | 99 (25) | 1 |
| II | 312 (38) | 154 (39) | 1.20 (0,87–1,67) |
| III | 236 (28) | 107 (27) | 1,61 (1,05–2,45) |
| IV | 35 (4) | 31 (8) | 4,14 (2,04 — 8,39) |
| Коморбидность при постановке диагноза | |||
| 0 | 372 (45) | 101 (26) | 1 |
| 1 или более | 389 (47) | 265 (68) | 2.10 (1,57 — 2,81) |
| Неизвестно | 69 (8) | 25 (6) | 1,22 (0,72–2,09) |
| Лечение | |||
| Хирургия (S) | 420 (51) | 227 (58) | 1 |
| S + химиотерапия | 186 (22) | 71 (18) | 1,00 (0,61–1,62) |
| S + лучевая терапия ± химиотерапия | 220 (27) | 87 (22) | 0.64 (0,40–1,00) |
| Прочие | 4 (0,5) | 6 (2) | 1,87 (0,38–9,24) |
Ожидаемая продолжительность здоровой жизни (HLE) и продолжительность жизни без инвалидности (DFLE) )
В среднем 50-летний переживший КРР может прожить еще 12 лет (мужчины) и 13 лет (женщины), при этом большую часть оставшейся жизни они проводят в хорошем состоянии здоровья (77% у мужчин и 74% у женщин). , Стол ). Стадия во многом определяет продолжительность жизни и долю лет жизни, проведенных с хорошим здоровьем.С другой стороны, хотя не было никакой связи между временем наблюдения и состоянием здоровья, у лиц, выживших в долгосрочной перспективе, то есть наблюдаемых в течение 6 и более лет, ожидаемая продолжительность жизни была больше по сравнению с пациентами, перенесшими краткосрочное наблюдение, т.е. в течение 5 лет и менее (ожидаемая продолжительность жизни в 50 лет составила 29,9 против 7,5 лет соответственно). Заметная разница также наблюдалась между группами стадий, например, те, у кого диагностирована стадия I, жили в среднем еще 25–30 лет по сравнению с 2 годами для тех, у кого стадия IV.Кроме того, у переживших КРР стадии IV также была самая короткая часть оставшейся жизни с хорошим здоровьем (47% для мужчин и 40% для женщин). Кроме того, мужчины с колоректальной стадией I – III стадии после постановки диагноза рака провели 76–83% своей жизни без инвалидности по сравнению с только 53% для людей со стадией IV.
Таблица 4
Ожидаемая продолжительность жизни (LE, в годах) Ожидаемая продолжительность здоровой жизни (HLE, в годах) и ожидаемая продолжительность жизни без инвалидности (DFLE) среди выживших после колоректального рака
| Мужчины | Женщины | |||||
|---|---|---|---|---|---|---|
| LE, лет | HLE, лет (%) | DFLE, лет (%) | LE, годы | HLE, лет (%) | DFLE, лет (%) | |
| Возраст a | ||||||
| В возрасте 50 лет | 12.3 | 9,5 (77) | 9,5 (77) | 13,3 | 9,9 (74) | 9,8 (74) |
| В возрасте 65 лет | 9,4 | 7,3 (77) | 6,3 (6,3) | 11,5 | 7,9 (68) | 6,6 (58) |
| В возрасте 80 лет | 5,5 | 3,8 (69) | 3,2 (58) | 7,0 | 4,1 (59) | 37) |
| Социально-экономический статус a, b | ||||||
| Высокая | 12.5 | 10,0 (80) | 10,2 (82) | 14,0 | 11,8 (79) | 11,2 (80) |
| Средний | 13,7 | 10,9 (80) | 10,8 (79) 13,3 | 9,9 (77) | 10,2 (77) | |
| Низкий | 9,3 | 6,0 (65) | 6,3 (68) | 12,1 | 6,5 (56) | 6,8 9023 9023 |
| Время с момента постановки диагноза а, б, в | ||||||
| ≤5 лет | 7.5 | 5,6 (74) | 6,0 (79) | 7,6 | 5,6 (74) | 5,7 (76) |
| 6+ лет | 27,6 | 22,3 (81) | 20,8 (75) | 32,7 | 24,5 (75) | 22,6 (69) |
| Этап b | ||||||
| Стадия I | 25,3 | 19,1 (75) | 19,2 (76) | 29,8 | 21,1 (71) | 21,3 (72) |
| Стадия II | 216,0 (83) | 14,5 (76) | 20,9 | 15,8 (75) | 15,4 (74) | |
| Стадия III | 13,6 | 10,7 (79) | 9023 9023 11,3 (11,3)16,8 | 12,9 (77) | 11,9 (71) | |
| Стадия IV | 2,1 | 1,0 (47) | 1,1 (53) | 2,2 | 0,9 (40) | 1,2 (53) |
| Коморбидность а, б | ||||||
| 0 | 12.8 | 10,4 (81) | 10,6 (83) | 14,8 | 14,8 (84) | 12,2 (82) |
| 1 или более | 11,0 | 7,8 (70) | 7,9 (7,9) | 12,5 | 12,5 (62) | 8,5 (66) |
Из других прогностических факторов возникли две модели. Во-первых, группы, которые прожили большую часть оставшейся жизни с плохим здоровьем. Эта закономерность была показана у женщин из низшего социально-экономического класса, которые могли рассчитывать, что проживут дольше, чем их коллега-мужчина (12 vs.9,9 лет), но 44% оставшейся жизни прожили в плохом состоянии здоровья (по сравнению с мужчинами из низкого социально-экономического класса, 35% — с плохим здоровьем). Другой пример — пожилые выжившие женщины (80+ лет), которые могут рассчитывать на то, что проживут столько же, сколько выжившие мужчины, но проведут 41 и 63% оставшейся жизни с плохим здоровьем и инвалидностью (по сравнению с мужчинами, 31 и 42%, соответственно). . Во-вторых, те, кто прожили долгую жизнь, большая часть которых была здорова, например, выжившие с высоким социально-экономическим статусом и те, кто не имел сопутствующих заболеваний на момент постановки диагноза.В среднем, пережившие КРР мужчины с высоким социально-экономическим статусом могут прожить еще 12,9 лет в возрасте 50 лет и провести 80% из них в здоровой жизни (по сравнению с 9,9 годами и 65% среди выживших с низким социально-экономическим статусом).
Обсуждение
В среднем 50-летний переживший CRC может прожить ¾ оставшейся жизни в хорошем состоянии здоровья и без функциональных ограничений. Диагноз CRC стадии IV является наиболее важным предиктором плохого восприятия здоровья и функциональной инвалидности. Те, у кого была диагностирована продвинутая стадия CRC, имели чрезвычайно низкую продолжительность жизни и показали заметно меньшую долю HLE, поскольку половину своей оставшейся жизни они провели с инвалидностью.Что касается пациентов с КРР I, II или III стадии, они сообщали об аналогичном воспринимаемом состоянии здоровья, хотя пациенты со стадией III с большей вероятностью сообщали о функциональных ограничениях. К другим уязвимым группам относились выжившие с одним или несколькими сопутствующими заболеваниями, женщины, особенно из числа пожилых людей, и лица из низшего социально-экономического класса.
Значение исследования
Сравнение с населением в целом
У лиц, переживших КРР, ожидаемая продолжительность жизни была намного ниже по сравнению с населением Нидерландов в целом (12–13 лет в нашей когорте vs.30–34 года в популяции) [16]. Тем не менее, похоже, что излечение достигается среди тех, кто долгое время выжил, так как ожидаемая продолжительность жизни аналогична продолжительности жизни голландского населения в целом, что подтверждает результаты исследований условной выживаемости [17]. Еще одна хорошая новость заключается в том, что значительная часть оставшихся лет жизни выживших прошли с хорошим здоровьем. Это отражено в исследованиях качества жизни выживших после КРР, которые сообщают о хорошем качестве жизни [2, 6] и аналогичных физических ограничениях, как и у населения в целом [4].По сравнению с голландским населением, выжившие после CRC после постановки диагноза рака провели еще большую часть жизни в хорошем состоянии. В возрасте 50 лет среднестатистические голландские мужчины проводят 66% (против 77% у выживших) оставшейся жизни в хорошем состоянии, а голландские женщины — около 65% (против 74% у выживших) [18]. Одним из объяснений этого открытия может быть отбор на выживание. Те, кто пережил рак, вероятно, являются самыми сильными в популяции, следовательно, их общее состояние здоровья улучшилось. Различие в оценке хорошего или плохого здоровья также может объяснить разницу.Голландская статистика дихотомизировала хорошее и очень хорошее здоровье на здоровое, а те, кто ответили на общий вопрос о состоянии здоровья как среднее, удовлетворительное и плохое, были сгруппированы в нездоровых. В наших анкетах только те, кто ответил удовлетворительно и плохо, были включены в группу нездоровых, потому что у нас не было среднего в качестве варианта ответа. В-третьих, это также может быть связано с отсутствием ответов: 17% выживших не ответили на наши анкеты. Хотя это относительно небольшое число по сравнению с другими исследованиями, основанными на анкетах, тем не менее, не респонденты, вероятно, состояли в основном из лиц с худшим состоянием здоровья [19].Наконец, объяснение этой разницы (более низкая доля HLE среди населения в целом по сравнению с выжившими после рака) может быть положительным отношением, которое выжившие после рака принимают после переживания рака, процесс, который называется «переосмыслением» [20–22].
Уязвимые группы
Группа, которая имела самую короткую продолжительность жизни и провела большую часть оставшейся жизни в плохом состоянии здоровья, была выжившими с CRC IV стадии. Этот вывод согласуется с другими исследованиями, которые показали более низкое качество жизни среди пациентов с запущенным CRC [2].Реальная ситуация, вероятно, хуже, потому что отсутствие ответа было самым высоким среди пациентов со стадией IV, что привело к занижению нашей оценки [19]. Физиологическое бремя более агрессивного и неизлечимого рака и его лечение было предложено как причина плохого качества жизни среди этих пациентов. Наши результаты подчеркивают важность раннего выявления и паллиативной помощи.
Мы не обнаружили связи между различными видами лечения и самооценкой здоровья или функциональной инвалидностью после коррекции наблюдаемых искажающих факторов.В последние несколько лет для пациентов с CRC использовались новые схемы лечения. Поскольку эти методы лечения обычно имеют более выраженные побочные эффекты, мы ожидали некоторого влияния на качество жизни по сравнению с теми, кто получал только хирургическое лечение, особенно среди пожилых людей [5, 23]. Тем не менее, лечение CRC во многом определяется стадией рака на момент проявления болезни, что затрудняет определение их независимого эффекта [13]. В большей когорте внутриэтапная разница в оценке воздействия лечения на качество жизни с поправкой на другие факторы, влияющие на факторы (в т.профиль риска).
Другими группами, которые продемонстрировали более высокую вероятность плохого воспринимаемого здоровья и инвалидности с более низкой долей оставшейся жизни в хорошем состоянии, были выжившие после КРР с сопутствующей патологией на момент постановки диагноза. Пациенты с сопутствующей патологией, вероятно, были курильщиками или бывшими курильщиками, имели избыточный вес и были физически неактивными [24], и это могло быть связано с общим плохим состоянием здоровья. Женщины в возрасте 80 лет и старше, принадлежащие к низшему социально-экономическому классу, также имели низкую долю HLE и DFLE по сравнению с мужчинами из той же группы.Это соответствует результатам других исследований [25]. это выдвинуло гипотезу о связи с наихудшими социальными и психологическими факторами среди пожилых людей и женщин [25]. Таким образом, эти группы могут извлечь выгоду из более здорового образа жизни, лучшего медицинского обслуживания и социальной поддержки.
Соображения относительно интерпретации, ограничений и силы
Ожидаемую продолжительность жизни, указанную в этом исследовании, следует интерпретировать с осторожностью. Его не следует экстраполировать на количество лет, оставшихся жить пациентам с CRC в целом.Выжившие, которые составили когорту в этом исследовании, состояли в основном из пациентов, которым был поставлен диагноз в период исследования: 2005–2009 гг. (49%, тогда как 33 и 21% были диагностированы в 1998–2004 и 1975–1997 годах соответственно). Смертность на раннем этапе после постановки диагноза рака высока [17]. Как видно из нашего анализа, у тех, кого наблюдали только в течение 5 лет, ожидаемая продолжительность жизни была существенно меньше, чем у тех, кто наблюдал более длительное наблюдение. В нашем анализе чувствительности (Приложение 2) мы показали, что включение пациентов с более длительным периодом наблюдения не меняет нашего окончательного вывода.Кроме того, мы также включили пациентов в терминальной стадии, которые способствовали очень высокой смертности и очень малому числу человеко-лет (см. Рис.). Хотя на эти пациенты приходилось только 6% от общего числа человеко-лет в когорте, на них приходилось 27% от общего числа смертей. Эти два упомянутых выше фактора объясняют в целом низкую ожидаемую продолжительность жизни (когда все стадии были объединены в единую оценку продолжительности жизни), о которой сообщается в нашем исследовании.
После ознакомления с нашими выводами следует принять во внимание ряд ограничений.Во-первых, наш результат основывался исключительно на прямых оценках состояния здоровья, измеренных с помощью анкет. Этот подход предполагает, что люди используют одни и те же пороги ответа в отчетности [26]. Однако после постановки диагноза рака у пациентов происходят резкие изменения, которые могут изменить их внутренние ценности, что приведет к изменению реакции на оценку состояния здоровья [27]. Таким образом, группа, у которой ожидалось плохое здоровье или инвалидность, сообщила о таком же или лучшем здоровье, чем группа, которая, как ожидается, будет лучше.Наконец, мы использовали только три пункта из всех областей качества жизни для измерения нашего результата. В Приложении 3 мы оценили влияние включения эмоциональных областей в анализ, что привело к выводу, аналогичному нашему основному анализу. Более ранние исследования показали, что, несмотря на сопоставимое качество жизни, при колоректальном раке наблюдаются стойкие специфические симптомы, такие как усталость, тошнота / рвота, боль, бессонница и потеря аппетита [28]. Меньшие подгруппы пациентов, например, живущие со стомой, также сообщили о более низком качестве жизни [12].Таким образом, ограничения в этих других областях могли быть замаскированы.
Используя данные по населению, мы обеспечили полноту, а также надежность при построении таблицы смертности и ее результатов. В этом исследовании мы включили информацию о выживаемости и качестве жизни пациентов в одну оценку (HLE и DFLE). Оценка прогноза пациентов после постановки диагноза рака в основном основывалась либо на продолжительности жизни, либо на ее качестве. Наличие их обоих в одном измерении облегчит оценку продолжительности жизни после постановки диагноза и будет полезно для информации пациента или рекомендаций при принятии клинического решения.
Выводы
Наши результаты свидетельствуют о высокой доле ожидаемой продолжительности здоровой жизни среди лиц, переживших КРР. Тем более, что для некоторых групп переживших CRC доля HLE превышает таковую в общей популяции, что подчеркивает важность раннего выявления. Люди, пережившие КРР IV стадии, чаще всего сообщают о плохом здоровье и проводят большую часть оставшейся жизни в плохом состоянии, что подчеркивает важность раннего выявления и паллиативной помощи. Выжившие с сопутствующей патологией, пожилые люди, женщины и представители низшего социально-экономического класса также сообщили о высокой распространенности плохого состояния здоровья и инвалидности.Это подчеркивает ценность более здорового образа жизни и совершенствования социальной политики и политики в области здравоохранения.
Дополнительные электронные материалы
Ниже приводится ссылка на дополнительные электронные материалы.
Благодарности
Изабель Сурджоматарам была поддержана Нидерландской организацией научных исследований и стипендией Эразмус. Lonneke van de Poll-Franse был поддержан Голландским онкологическим обществом.
Конфликт интересов
Авторы заявляют об отсутствии конфликта интересов.
Открытый доступ
Эта статья распространяется на условиях лицензии Creative Commons Attribution License, которая разрешает любое использование, распространение и воспроизведение на любом носителе при условии указания автора (авторов) и источника.
Ссылки
1. Гондос А., Брей Ф., Хакулинен Т., Бреннер Х. Тенденции выживаемости от рака в 11 европейских популяциях с 1990 по 2009 год: анализ на основе моделей. Энн Онкол. 2009. 20: 564–573. DOI: 10.1093 / annonc / mdn639. [PubMed] [CrossRef] [Google Scholar] 2.Рэмси С.Д., Андерсен М.Р., Этциони Р. и др. Качество жизни выживших после колоректальной карциномы. Рак. 2000; 88: 1294–1303. DOI: 10.1002 / (SICI) 1097-0142 (20000315) 88: 6 <1294 :: AID-CNCR4> 3.0.CO; 2-M. [PubMed] [CrossRef] [Google Scholar] 3. Gatta G, Ciccolallo L, Faivre J, Bouvier AM, Berrino F, Gerard JP. Поздние исходы лечения колоректального рака: исследование FECS-EUROCARE. J Рак выжил. 2007; 1: 247–254. DOI: 10.1007 / s11764-007-0030-1. [PubMed] [CrossRef] [Google Scholar] 4. Schneider EC, Malin JL, Kahn KL, Ko CY, Adams J, Epstein AM.Выживший после колоректального рака: симптомы, сообщаемые пациентом через 4 года после постановки диагноза. Рак. 2007; 110: 2075–2082. DOI: 10.1002 / cncr.23021. [PubMed] [CrossRef] [Google Scholar] 5. Шахир М.А., Лемменс В.Е., ван де Поль-Франсе Л.В., Воогд А.С., Мартейн Х., Янссен-Хейнен М.Л. Пожилые пациенты с раком прямой кишки имеют более высокий риск связанных с лечением осложнений и более плохой прогноз, чем более молодые пациенты: популяционное исследование. Eur J Cancer. 2006; 42: 3015–3021. DOI: 10.1016 / j.ejca.2005.10.032. [PubMed] [CrossRef] [Google Scholar] 6.Данн Дж., Линч Б., Эйткен Дж., Леггетт Б., Пакенхэм К., Ньюман Б. Качество жизни и колоректальный рак: обзор. Aust N Z J Public Health. 2003. 27: 41–53. DOI: 10.1111 / j.1467-842X.2003.tb00378.x. [PubMed] [CrossRef] [Google Scholar] 7. Янссен-Хейнен М.Л., Лоуман В.Дж., ван де Поль-Франсе Л.В., Коберг Дж.В.В. Результаты 50-летнего онкологического регистра на юге Нидерландов: 1955–2004. Эйндховен: регистр рака Эйндховена; 2005. [Google Scholar] 8. Виттекинд С., Грин Флорида, Хаттер РВП, Климпфингер М., Собин Л.Х.TNM Atlas. 5. Гейдельберг: Спрингер; 2005. [Google Scholar] 9. van Duijn C, Keij I. Индикатор социально-экономического статуса по почтовому индексу. Maandstatistiek van de bevolking. 2002; 50: 32–35. [Google Scholar] 10. Ааронсон Н.К., Мюллер М., Коэн П.Д. и др. Перевод, проверка и нормирование голландской версии Обзора состояния здоровья SF-36 среди населения и населения с хроническими заболеваниями. J Clin Epidemiol. 1998. 51: 1055–1068. DOI: 10.1016 / S0895-4356 (98) 00097-3. [PubMed] [CrossRef] [Google Scholar] 11.Thong MS, Mols F, Lemmens VE, Creemers GJ, Slooter GD, van de Poll-Franse LV. Влияние химиотерапии на состояние здоровья и бремя симптомов у выживших после рака толстой кишки: популяционное исследование. Eur J Cancer. 2011; 47: 1798–1807. DOI: 10.1016 / j.ejca.2011.02.006. [PubMed] [CrossRef] [Google Scholar] 12. Thong MS, Mols F, Lemmens VE, et al. Влияние предоперационной лучевой терапии на общее и конкретное заболевание состояние здоровья выживших после рака прямой кишки: популяционное исследование. Int J Radiat Oncol Biol Phys. 2011; 81: e49 – e58.DOI: 10.1016 / j.ijrobp.2010.12.030. [PubMed] [CrossRef] [Google Scholar] 13. Национальная рабочая группа по раку желудочно-кишечного тракта. Онколайн: руководство по клинической практике рака. Утрехт: VIKC; 2008. [Google Scholar]15. Джаггер С., Кокс Б., Ле Рой С. (2006) EHEMU: расчет ожидаемой продолжительности здоровья по методу Салливана: практическое руководство
17. Янссен-Хейнен М.Л., Гондос А., Брей Ф. и др. . Клиническая значимость условной выживаемости онкологических больных в Европе: возрастные анализы 13 видов рака.J Clin Oncol. 2010. 28: 2520–2528. DOI: 10.1200 / JCO.2009.25.9697. [PubMed] [CrossRef] [Google Scholar] 18. Брюггинк Дж. В., Лоддер Б., Кардал М. Продолжительность здоровой жизни выше. Ден Хааг: Статистическое управление Нидерландов; 2009. [Google Scholar] 19. Мойнпур С.М., Сойерс Триплетт Дж., Макнайт Б. и др. Проблемы, связанные с неслучайным отсутствием данных о качестве жизни в клинических испытаниях запущенной стадии колоректального рака. Психоонкология. 2000. 9: 340–354. DOI: 10.1002 / 1099-1611 (200007/08) 9: 4 <340 :: AID-PON466> 3.0.CO; 2-F.[PubMed] [CrossRef] [Google Scholar] 20. Данн Дж., Линч Б., Ринальдис М. и др. Параметры качества жизни и психосоциальные переменные, наиболее важные для пациентов с колоректальным раком. Психоонкология. 2006; 15: 20–30. DOI: 10.1002 / pon.919. [PubMed] [CrossRef] [Google Scholar] 21. Рамфельт Э., Северинссон Э., Лутцен К. Попытки найти смысл в болезни для достижения эмоциональной согласованности: опыт пациентов с колоректальным раком. Рак Nurs. 2002; 25: 141–149. DOI: 10.1097 / 00002820-200204000-00011. [PubMed] [CrossRef] [Google Scholar] 22.Энтони Т., Джонс С., Антуан Дж., Сивесс-Фрэнкс С., Тернадж Р. Влияние лечения колоректального рака на качество жизни, связанное со здоровьем в долгосрочной перспективе. Энн Сург Онкол. 2001; 8: 44–49. DOI: 10.1007 / s10434-001-0044-2. [PubMed] [CrossRef] [Google Scholar] 23. Marijnen CA, van de Velde CJ, Putter H, et al. Влияние краткосрочной предоперационной лучевой терапии на качество жизни, связанное со здоровьем, и сексуальное функционирование при первичном раке прямой кишки: отчет о многоцентровом рандомизированном исследовании. J Clin Oncol. 2005; 23: 1847–1858.DOI: 10.1200 / JCO.2005.05.256. [PubMed] [CrossRef] [Google Scholar] 24. Трентам-Дитц А., Ремингтон П.Л., Мойнпур К.М., Хэмптон Дж.М., Сапп А.Л., Ньюкомб, Пенсильвания. Качество жизни, связанное со здоровьем у женщин, длительно перенесших колоректальный рак. Онколог. 2003. 8: 342–349. DOI: 10.1634 / теонколог. 8-4-342. [PubMed] [CrossRef] [Google Scholar] 26. Саломон Дж. А., Тандон А., Мюррей С. Дж.. Сопоставимость самооценки здоровья: кросс-секционное многострановое исследование с использованием привязывающих виньеток. BMJ (издание клинических исследований) 2004; 328: 258.DOI: 10.1136 / bmj.37963.6.44. [Бесплатная статья PMC] [PubMed] [CrossRef] [Google Scholar] 27. Oort FJ. Использование моделирования структурных уравнений для обнаружения сдвигов отклика и истинных изменений. Qual Life Res. 2005; 14: 587–598. DOI: 10.1007 / s11136-004-0830-у. [PubMed] [CrossRef] [Google Scholar] 28. Янсен Л., Херрманн А., Стегмайер С., Сингер С., Бреннер Х, Арндт В. Качество жизни, связанное со здоровьем, в течение 10 лет после постановки диагноза колоректального рака: популяционное исследование. J Clin Oncol. 2011; 29: 3263–3269. DOI: 10.1200 / JCO.2010.31.4013. [PubMed] [CrossRef] [Google Scholar]
8 распространенных мифов о раке толстой кишки | Рак
Мы слышим неправильные представления о раке толстой кишки каждый день. Один из них заключается в том, что женщинам не нужно делать колоноскопию.
Это неправда, и у нас есть доказательства из реальной жизни. Одной из наших самых запоминающихся пациенток была женщина в возрасте 30 лет. Она работала в маркетинге и готовилась к марафону, когда заметила кровь в стуле. Она не особо задумывалась об этом, но через месяц она поступила правильно и прошла колоноскопию.
Через несколько дней у нее диагностировали рак толстой кишки 4 стадии. Ее жизнь перевернулась. Используя обычную хирургическую процедуру, мы удалили рак из ее толстой кишки и части ее печени. Прошло уже почти 5 лет, и у нее все отлично.
Как медицинское сообщество, нам предстоит пройти долгий путь в обучении людей и исправлении неправильных представлений о раке толстой кишки. Вот некоторые из самых распространенных мифов, о которых мы слышали:
Миф: если у меня рак толстой кишки, мне понадобится обширное лечение в течение длительного периода времени.
Факт : Получение любого диагноза рака пугает, но у большинства пациентов с диагнозом рака толстой кишки есть решаемая проблема. Многие виды рака толстой кишки можно лечить с помощью относительно распространенной хирургической процедуры, которая выполняется с разрезом не более 3 дюймов.
Миф: В большинстве случаев, когда вам диагностируют рак толстой кишки, он уже распространяется на другие части вашего тела.
Факт : Это просто неправда.Большинство пациентов, у которых диагностирован рак толстой кишки, поддаются лечению и продолжат жить нормальной жизнью. Чем раньше мы определим поражение, тем меньше вероятность, что опухоль распространилась на другие части вашего тела. После того, как рак диагностирован, онкологи проведут несколько простых тестов, чтобы определить, распространилась ли опухоль, и определить следующие шаги лечения.
Миф: если мой рак толстой кишки распространился, я, вероятно, не проживу очень долго. Мой рак никогда не будет вылечен.
Факт : Доступно больше вариантов лечения, чем когда-либо прежде.Рак толстой кишки уникален тем, что у нас есть инструменты для его ранней диагностики. Химиотерапия со временем улучшилась. Сейчас есть больше вариантов лечения, когда рак находится на более поздней стадии. В 1990-е годы общая выживаемость при раке толстой кишки 4 стадии составляла от 6 до 8 месяцев. Сейчас почти 30 месяцев.
Миф: Колоноскопия — единственный способ обнаружить рак толстой кишки.
Факт : Хотя колоноскопия является наиболее точным методом скрининга рака толстой кишки, существуют и другие одобренные методы, позволяющие обнаружить рак или раковые полипы.Рак толстой кишки часто приводит к потере крови, поэтому одна из альтернатив — иммунохимический анализ кала (FIT). Пациент может сделать тест дома, взяв образец стула и отправив его в лабораторию. Получение результатов теста не займет много времени.
Другой одобренный тест — компьютерная томографическая (КТ) колонография, также называемая «виртуальной колоноскопией». Используя эту технологию, врач получает изображение толстой кишки и может идентифицировать опухоли или полипы.
Миф: поскольку я женщина, мне не нужна колоноскопия .
Факт : См. Наш пример выше. Людям старше 50 лет — мужчинам или женщинам — следует проходить колоноскопию каждые 10 лет. Если у вашего близкого родственника был диагностирован рак толстой кишки, вам следует поговорить со своим врачом о проведении колоноскопии в более раннем возрасте.
Миф: мне не нужна колоноскопия, потому что у меня нет никаких симптомов.
Факт : Многим людям ставят диагноз рак толстой кишки, когда они чувствуют себя хорошо. Люди не думают, что у них может быть рак толстой кишки, если они чувствуют себя нормально, но, безусловно, могут.Если вам за 50 и вы откладываете колоноскопию из-за отсутствия симптомов, вы теряете смысл колоноскопии.
Миф: сделать колоноскопию будет ужасным опытом, и она, вероятно, все равно ничего не найдет.
Факт : Наши пациенты обычно очень чувствуют облегчение после колоноскопии. У большинства из них нет рака, и им не нужно беспокоиться о раке толстой кишки в течение следующих 10 лет.
Сама процедура занимает около 30 минут. Из-за седативных препаратов большинство пациентов даже не помнят об этом .Хотя успокоительное означает, что кто-то должен отвезти вас домой, вам, скорее всего, не придется брать на работу больше одного дня.
Часть, которая вызывает больше всего жалоб от пациентов, — это процесс за день до колоноскопии. Пациенту необходимо выпить продукт для очищения толстой кишки, в результате чего происходит несколько дефекаций. После процедуры пациенты могут в течение нескольких дней испытывать повышенное газообразование или вздутие живота.
Миф: мне больше 50, но мой семейный врач не сказал, что мне нужно делать колоноскопию, поэтому она мне не нужна.
Факт : Это одна из наиболее частых причин, по которым люди обращаются к нам, когда они не прошли колоноскопию, но должны были. Они ожидают, что их семейный врач запомнит. Вместо того, чтобы думать об этом так, мы рекомендуем проявить инициативу. Возьмите под контроль свое здоровье и задавайте вопросы.
Рак толстой кишки можно предотвратить, вылечить и победить. Очень важно учиться, особенно если вам больше 50. Если у вас возникнут дополнительные вопросы, запишитесь на прием через Интернет или позвоните в нашу справочную линию по раку по телефону 214-736-9022.
Что это такое, признаки, этапы и лечение
Обзор
Рак прямой кишки: признаки, стадии, причины и лечениеЧто такое рак прямой кишки?
Рак прямой кишки развивается, когда раковые клетки образуются в прямой кишке (последние шесть дюймов толстой кишки). Прямая кишка — это камера, расположенная между толстой кишкой и анусом.
На кого влияет рак прямой кишки?
Рак прямой кишки поражает как мужчин, так и женщин, хотя вероятность развития этого заболевания у мужчин несколько выше.В большинстве случаев люди, у которых диагностировано заболевание, старше 50 лет. Однако у подростков и молодых людей также может развиться рак прямой кишки.
Насколько распространен рак прямой кишки?
Примерно у 5% людей в какой-то момент жизни разовьется рак прямой кишки. Из этих людей около 11% будут моложе 50 лет.
Какая первая стадия рака прямой кишки?
На стадии I рак прямой кишки разросся в глубокие слои стенки прямой кишки, но не распространился на близлежащие области.Люди с раком прямой кишки I стадии могут не испытывать никаких предупреждающих знаков или симптомов. Вот почему так важны рутинные обследования при колоноскопии.
В чем разница между раком прямой кишки и другими видами рака толстой кишки?
Существуют различные виды рака и заболеваний, поражающих прямую кишку. К ним относятся:
- Рак прямой кишки (толстой кишки) : Это широкий термин, описывающий рак толстой, прямой кишки или и того, и другого.Колоректальный рак — третья по распространенности форма рака в США
- Наследственный неполипозный колоректальный рак (HNPCC) : Это заболевание вызывает мутацию в важном гене, который передается по наследству или передается от родителя ребенку. Около 5% людей с колоректальным раком имеют HNPCC.
- Семейный аденоматозный полипоз (FAP) : Это редкое наследственное заболевание вызывает образование множественных предраковых полипов в толстой кишке.У людей с ФАП полипы обычно появляются в подростковом возрасте или в начале 20-летнего возраста. С возрастом полипы становятся более проблематичными, повышая риск колоректального рака.
Симптомы и причины
Каковы признаки рака прямой кишки?
Во многих случаях рак прямой кишки вообще не вызывает симптомов. Однако некоторые люди могут заметить определенные предупреждающие знаки. Симптомы рака прямой кишки могут включать:
Какая основная причина рака прямой кишки?
Точная причина рака прямой кишки неизвестна.Однако есть определенные факторы риска, которые увеличивают вероятность развития болезни, в том числе:
- Возраст: Как и в большинстве других видов рака, риск рака прямой кишки увеличивается с возрастом. Средний возраст постановки диагноза — 63 года как для мужчин, так и для женщин.
- Пол: У мужчин вероятность развития рака прямой кишки несколько выше, чем у женщин.
- Раса: По статистике, у чернокожих людей больше шансов заболеть раком прямой кишки. Причины этого до конца не выяснены.
- Семейный анамнез: Если у члена вашей семьи был диагностирован рак прямой кишки, ваши шансы на его развитие почти вдвое выше.
- Определенные заболевания и состояния: Существует несколько состояний здоровья, которые могут увеличить риск рака прямой кишки, включая воспалительные заболевания кишечника, такие как болезнь Крона и язвенный колит.
- Курение : Недавние исследования показывают, что люди, которые курят, с большей вероятностью умрут от рака прямой кишки, чем люди, которые не курят.
- Употребление обработанного мяса: Люди, которые едят много красного мяса и обработанного мяса, имеют более высокий риск развития рака прямой кишки.
- Ожирение: Люди с ожирением чаще болеют раком прямой кишки, чем люди со здоровым весом.
Эксперты рекомендуют всем людям проходить рутинные колоректальные обследования начиная с 45 лет. Людям с повышенным риском рака прямой кишки следует чаще проходить обследования.Узнайте больше об общих рекомендациях по скринингу на рак, рекомендованных поставщиками медицинских услуг.
Что я должен знать о стадии рака прямой кишки?
Рак прямой кишки подразделяется на пять стадий. Ваш диагноз зависит от размера опухоли рака прямой кишки и от того, распространилась ли она:
- Стадия 0: Раковые клетки были обнаружены на поверхности слизистой оболочки прямой кишки.
- Стадия 1: Опухоль выросла ниже слизистой оболочки и, возможно, в стенку прямой кишки.
- Стадия 2: Опухоль проросла в стенку прямой кишки и может распространиться на ткани вокруг прямой кишки.
- Стадия 3: Опухоль поразила лимфатические узлы рядом с прямой кишкой и некоторые ткани за пределами стенки прямой кишки.
- Стадия 4: Опухоль распространилась на удаленные лимфатические узлы или органы.
Как распространяется рак прямой кишки?
Если у вас метастатический рак прямой кишки 4 стадии, это означает, что рак распространился за пределы прямой кишки на другие части тела.Хотя эти раковые клетки могут путешествовать в любом месте вашего тела, они с большей вероятностью попадут в печень, легкие, мозг или слизистую оболочку брюшной полости.
Диагностика и тесты
Как диагностируется рак прямой кишки?
Большинство случаев рака прямой кишки диагностируется во время плановых обследований. В некоторых случаях ваш врач может заподозрить заболевание на основании ваших симптомов.
Какие тесты будут проводиться для диагностики рака прямой кишки?
Если ваш лечащий врач считает, что у вас может быть рак прямой кишки, он может назначить несколько тестов для подтверждения вашего диагноза.Эти тесты могут включать:
- Колоноскопия : В этом тесте используется длинная трубка с маленькой камерой для обзора внутренней и прямой кишки.
- Биопсия : Ваш лечащий врач берет небольшой образец подозрительной ткани и отправляет его в лабораторию для анализа.
- Сканирование компьютерной томографии (КТ) : В ходе этого визуализирующего теста снимаются рентгеновские лучи вашего тела, а затем их сшиваются вместе для детального обзора ваших костей, органов и тканей.
- Магнитно-резонансная томография (МРТ) : В отличие от рентгеновских лучей, МРТ использует радиоволны и магниты для захвата изображений внутри вашего тела.
- ПЭТ-сканирование (позитронно-эмиссионная томография): Перед проведением ПЭТ-сканирования ваш лечащий врач попросит вас выпить специальный краситель, содержащий радиоактивные индикаторы. (В некоторых случаях краситель можно вводить путем инъекции или вдыхать.) Краситель выделяет участки болезни.
Ведение и лечение
Как лечится рак прямой кишки?
Лечение рака прямой кишки зависит от нескольких факторов, включая расположение, размер и стадию опухоли, а также от вашего общего состояния здоровья и личных предпочтений.Варианты включают:
Хирургия
Операция по удалению раковых клеток — одно из самых распространенных методов лечения рака прямой кишки. В зависимости от ваших потребностей существует несколько различных хирургических вариантов:
- Трансанальная эндоскопическая микрохирургия (TEMS) : Во время этой процедуры ваш хирург удаляет небольшие раковые образования из прямой кишки с помощью специального зонда, вводимого через задний проход. Это лечение рекомендуется, если ваша опухоль небольшого размера, сосредоточена в одной области и маловероятна для распространения.
- Низкая передняя резекция: При более крупном раке прямой кишки может потребоваться полное или частичное удаление прямой кишки. Анус сохраняется, поэтому отходы могут нормально покидать ваше тело.
- Абдоминоперинеальная резекция (APR) : Когда рак находится рядом с анальным отверстием, его невозможно удалить, не повредив мышцы, которые контролируют дефекацию. В этом случае ваш хирург может удалить задний проход, прямую кишку и часть толстой кишки. Затем выполняется колостома, чтобы отходы могли покинуть ваше тело.(Во время процедуры колостомии ваш хирург создает отверстие или стому в вашей брюшной полости. Затем конец толстой кишки прикрепляется к отверстию и зашивается. Когда отходы покидают ваше тело, они собираются в мешок, который соединяется с стома.)
Химиотерапия
Химиотерапия может использоваться перед операцией для уменьшения опухоли или после операции для уничтожения всех оставшихся раковых клеток.
Лучевая терапия
Как и химиотерапия, лучевая терапия может применяться до или после операции.Лучевая терапия использует сильные энергетические лучи, чтобы убить раковые клетки или не дать им расти и делиться. Его можно использовать в сочетании с химиотерапией.
Иммунотерапия
В иммунотерапии используются лекарства, которые укрепляют вашу иммунную систему и учат ваше тело атаковать раковые клетки.
Таргетная лекарственная терапия
Если у вас рак прямой кишки на поздней стадии, ваш онколог может порекомендовать таргетную лекарственную терапию в сочетании с химиотерапией. Эти методы лечения нацелены на определенные аномалии в раковых клетках, вызывая их гибель.
Какие осложнения при лечении рака прямой кишки?
Осложнения могут различаться в зависимости от типа лечения рака прямой кишки. Кроме того, опыт каждого человека может быть разным. То, что у кого-то были определенные осложнения, не означает, что они будут и у вас. Усталость, изменение веса, тошнота / рвота и диарея — наиболее частые побочные эффекты при большинстве методов лечения рака прямой кишки.
Профилактика
Можно ли предотвратить рак прямой кишки?
Хотя полностью предотвратить рак прямой кишки невозможно, есть шаги, которые можно предпринять, чтобы снизить риск.Например:
- Поддерживайте здоровый вес.
- Регулярно занимайтесь спортом.
- Придерживайтесь здоровой, хорошо сбалансированной диеты.
- Избегайте употребления алкоголя.
- Не курите.
Перспективы / Прогноз
Сможете ли вы пережить рак прямой кишки?
Да. При раннем обнаружении и лечении рак прямой кишки можно успешно вылечить.
Какова выживаемость при раке прямой кишки?
Общая пятилетняя выживаемость при раке прямой кишки составляет 63%.Это означает, что вероятность того, что люди с раком прямой кишки выживут через пять лет, примерно на 63% выше, чем у людей, не страдающих раком прямой кишки. Пятилетняя выживаемость при локализованном раке прямой кишки (который не распространился на другие части тела) составляет 91%. Это означает, что у людей с раком прямой кишки на ранней стадии вероятность дожить до жизни через пять лет примерно на 91% выше, чем у людей, не страдающих раком прямой кишки.
Имейте в виду, что показатели выживаемости — это оценки, основанные на людях, у которых в прошлом был рак прямой кишки.Они не могут предсказать, что произойдет или сколько вы проживете. Чтобы узнать больше о выживаемости при раке прямой кишки, поговорите со своим врачом.
Жить с
Когда мне следует обратиться к поставщику медицинских услуг?
Если вы проходите курс лечения рака прямой кишки, немедленно позвоните своему врачу, если у вас разовьется:
Вы знаете свое тело лучше всех, так что доверяйте своей интуиции. Если что-то не так, запишитесь на прием к врачу.Они могут найти способы облегчить ваши симптомы и помочь вам почувствовать себя лучше.
Какие вопросы я должен задать своему врачу?
Если вам диагностировали рак прямой кишки, вам нужно собрать как можно больше информации. Вот несколько вопросов, которые следует задать своему врачу:
- Какая у меня стадия рака прямой кишки?
- Как далеко распространился рак?
- Какие у меня варианты лечения?
- Как лечение повлияет на качество моей жизни?
- Смогу ли я работать во время лечения?
Записка из клиники Кливленда
Диагноз «рак прямой кишки» — непростая задача.Вы можете чувствовать грусть, страх, разочарование или злость. Спросите своего врача о ресурсах, которые помогут вам преодолеть это трудное время. Вы также можете подумать о том, чтобы присоединиться к группе поддержки для людей с раком прямой кишки. Знание — сила. Полное понимание вашего диагноза и вариантов лечения может расширить ваши возможности и помочь вам вернуть контроль над своим здоровьем.
Лечение рака толстой кишки, распространившегося на печень: командный подход
Если у вас или у вашего близкого человека диагностирован рак толстой кишки, существует также вероятность того, что рак распространится (метастазирует) в другие органы, чаще всего в печень.Однако, по словам доктора Ричарда Беркхарта, хирурга и исследователя рака Джонса Хопкинса, успехи в лечении опухолей печени, вызванных раком толстой кишки, резко улучшили показатели выживаемости. Фактически, 40-60 процентов пациентов, получавших лечение по поводу изолированного метастаза рака толстой кишки в печень, все еще живы через пять лет после лечения.
В Johns Hopkins такие исследователи, как доктор Беркхарт, проводят клинические испытания, чтобы найти способы замедлить или предотвратить распространение рака толстой кишки. Эти испытания в сочетании с мультидисциплинарным или групповым подходом с использованием молекулярного тестирования, хирургических методов, химиотерапии и лучевой терапии значительно улучшили ожидаемую продолжительность жизни пациентов за последние 10 лет.
Как многопрофильная бригада лечит рак толстой кишки и печени
Междисциплинарный подход к лечению рака толстой кишки и печени означает, что вы получите оптимизированный план, основанный на вашей индивидуальной истории болезни, типе опухоли и генах. В вашей команде работают несколько видов онкологов, поэтому вы можете извлечь выгоду из их совокупного опыта.
«Центр, в котором вы проходите лечение, должен иметь доступ к нескольким типам врачей, которые регулярно общаются», — говорит д-р.Адриан Мерфи, преподаватель онкологии Медицинского факультета Университета Джона Хопкинса. «Это чрезвычайно важно, потому что один специалист в одиночку не может управлять вашим лечением. Это действительно требует сотрудничества ».
Обычно в мультидисциплинарной онкологической бригаде насчитывается шесть типов специалистов:
Врач-онкологВрач-онколог специализируется на лечении рака с помощью химиотерапии и других методов таргетной терапии. Раньше отчеты о патологии были единственным указанием на диагноз рака толстой кишки.Теперь онкологи-медики могут углубиться в молекулярный состав опухоли. Это молекулярное тестирование помогает при принятии решения о лечении.
Есть два типа молекулярного тестирования. В зависимости от опухоли онколог может использовать следующие тесты:
- Тестирование устойчивости микроспутника
Нестабильность микросателлитов — это нарушение способности исправлять ошибки ДНК в ваших клетках. Знание о стабильности микросателлитов у пациента может помочь предсказать положительный ответ на иммунотерапию.
KRAS — это ген, который часто мутирует при раке толстой кишки. Информация о том, что у пациента есть эта мутация, указывает на отсутствие реакции на определенные лекарства.
После завершения молекулярного тестирования ваши онкологи обсудят лучшее лечение вашего рака, которое часто включает химиотерапию.
ХирургЛучшим методом лечения рака, распространившегося на печень, является хирургическое вмешательство. Печень — единственный орган в организме, который может восстанавливаться, поэтому, пока 20 процентов печени остается после операции, она может вырасти и сохранить функциональность.Если опухоль настолько велика, что требуется удалить более 80 процентов вашей печени, врачи могут рассмотреть возможность использования процедуры, называемой предоперационной эмболизацией, которая блокирует кровоснабжение части печени и опухоли. По сути, это приводит к голоду опухоли и шунтированию крови в здоровую печень, чтобы стимулировать рост печени и обеспечить безопасное выполнение операции.
Если у вас рак печени и толстой кишки, вам может быть назначена операция по удалению обоих видов рака одновременно или поэтапный подход.Ваш хирург обсудит, какой вариант лучше всего подходит для вас.
Радиолог-онкологОнколог-радиолог специализируется на лечении рака с помощью излучения. Если ваша опухоль слишком велика и одно хирургическое вмешательство невозможно, может быть рекомендована операция в сочетании с другими процедурами, такими как лучевая терапия.
Хотя химиотерапию проводит онколог, лучевая терапия также может быть вариантом лечения. Процедура очень похожа на рентген грудной клетки.Онколог-радиолог использует машину для доставки целевых частиц или волн высокой энергии для уничтожения или повреждения раковых клеток в опухоли.
Интервенционный радиологИнтервенционные радиологи выполняют диагностические и терапевтические процедуры под визуальным контролем пациентов с онкологическими и другими заболеваниями. Есть три варианта:
Техника с визуализацией, использующая тепло для разрушения опухоли в печени без ее удаления.
- Наружная лучевая терапия
Процедура, выполняемая вне тела, направленная на опухоль, с сохранением других частей печени.
- Катетер-направленная терапия
Радиолог вводит катетер и вводит химиотерапевтические агенты или облучение в кровеносные сосуды опухоли, чтобы лишить ее крови и провести целенаправленное лечение.
«Цель вашей команды онкологов — работать вместе, чтобы рассмотреть все варианты и методы лечения», — объясняет Мерфи. «Таким образом, они могут использовать самые современные тесты и методы для лечения вашего индивидуального диагноза.”
ПатологоанатомПатологи специализируются на интерпретации тестов тканей, таких как биопсия, для постановки окончательного диагноза. Например, когда они исследуют ткани с помощью биопсии печени, патологи могут помочь установить диагноз, что раковые клетки произошли из толстой кишки. Это важный диагноз, который помогает убедиться, что вы получите правильный вид лечения.
Патологоанатомы также используют свои обширные знания в области биологии рака для проведения комплексного молекулярного тестирования и помощи вашему онкологу в интерпретации результатов.
РадиологРадиологи специализируются на диагностике заболеваний с помощью методов визуализации, таких как компьютерная томография (компьютерная томография) или МРТ (магнитно-резонансная томография). Они особенно важны, когда дело доходит до определения стадии рака толстой кишки и проведения наиболее подходящего визуального исследования для постановки окончательного диагноза.
Радиологи работают с командой, чтобы определить точное местоположение опухоли в печени, чтобы помочь в планировании лечения в отдельных случаях.
Симптомы и лечение рака кишечника — Болезни и состояния
Если рак толстой кишки находится на очень ранней стадии, возможно, удастся удалить лишь небольшой кусок оболочки стенки толстой кишки. Это называется местным иссечением.
Если рак распространяется на мышцы, окружающие толстую кишку, обычно необходимо удалить весь участок толстой кишки. Это называется колэктомией.
Колэктомия может быть выполнена двумя способами:
- открытая колэктомия — хирург делает большой разрез (разрез) на брюшной полости и удаляет часть толстой кишки
- лапароскопическая (замочная скважина) колэктомия — хирург делает несколько небольших разрезов в брюшной полости и использует специальные инструменты, руководствуясь камерой, для удаления части толстой кишки
Во время операции также удаляются близлежащие лимфатические узлы.Обычно после операции по поводу рака кишечника концы кишечника соединяются вместе, но в очень редких случаях это невозможно и требуется стома.
Считается, что как открытая, так и лапароскопическая колэктомия одинаково эффективны при удалении рака и имеют одинаковый риск осложнений.
Однако преимущество лапароскопической колэктомии заключается в более быстром восстановлении и уменьшении послеоперационной боли. Это становится обычным способом выполнения большинства этих операций.
Лапароскопические колэктомии должны быть доступны во всех больницах, где проводятся операции по поводу рака кишечника, хотя не все хирурги проводят этот тип хирургии.Обсудите возможные варианты с вашим хирургом, чтобы узнать, можно ли использовать этот метод.
Операция по поводу рака прямой кишки
Существует ряд различных типов операций, которые могут быть выполнены для лечения рака прямой кишки, в зависимости от того, как далеко распространился рак.
Некоторые из основных используемых методов описаны ниже:
Местная резекция
Если у вас очень маленький рак прямой кишки на ранней стадии, ваш хирург может удалить его с помощью операции, называемой местной резекцией (трансанальной резекцией).
Хирург вводит эндоскоп через задний ход и удаляет опухоль со стенки прямой кишки.
Тотальное иссечение брыжейки
Однако во многих случаях местная резекция невозможна. Вместо этого потребуется удалить большую часть прямой кишки.
Эта область будет включать границу ректальной ткани, свободной от раковых клеток, а также жировую ткань вокруг кишечника (брыжейку). Этот тип операции известен как полное иссечение брыжейки (ТМЭ).
Удаление брыжейки может помочь удалить все раковые клетки, что может снизить риск рецидива рака на более поздней стадии.
В зависимости от того, где находится рак прямой кишки, может быть проведена одна из двух основных операций ТМЭ. Они описаны ниже.
Резекция нижняя передняя
Нижняя передняя резекция — это процедура, используемая для лечения случаев, когда рак находится в верхнем отделе прямой кишки.
Хирург сделает разрез в брюшной полости и удалит верхнюю часть прямой кишки, а также некоторые окружающие ткани, чтобы убедиться, что все лимфатические узлы, содержащие раковые клетки, также удалены.
Затем они прикрепят вашу толстую кишку к нижней части прямой кишки или верхней части анального канала. Иногда они превращают конец толстой кишки во внутренний мешок, заменяющий прямую кишку.
Вам, вероятно, потребуется временная стома, чтобы дать время заживлению соединенной части кишечника.
Абдоминоперинеальная резекция
Абдоминоперинеальная резекция используется для лечения случаев, когда рак находится в самом нижнем отделе прямой кишки.
В этом случае необходимо полностью удалить прямую кишку и окружающие мышцы, чтобы снизить риск повторного роста рака в той же области.
Это включает удаление и закрытие заднего прохода и удаление его мышц сфинктера, поэтому нет другого выхода, кроме как иметь постоянную стому после операции.
Хирурги, специализирующиеся на раке кишечника, всегда делают все возможное, чтобы по возможности не делать людям постоянные стомы.
Операция по удалению стомы
Если часть кишечника удалена, а оставшаяся часть кишечника присоединена, хирург может иногда решить отвести стул от стыка, чтобы дать ему возможность зажить.
Стул временно отводится путем выведения петли кишечника через брюшную стенку и прикрепления ее к коже — это называется стомой.Для сбора стула поверх стомы надевают мешок.
Стома из тонкой кишки (подвздошной кишки) называется илеостомией, а когда стома из толстой кишки (толстой кишки) — колостомией.
Медсестра-специалист, известная как медсестра по уходу за стомой, может посоветовать вам, где лучше всего установить стому перед операцией.
Медсестра примет во внимание такие факторы, как форма вашего тела и образ жизни, хотя это может оказаться невозможным, если операция проводится в экстренных случаях.
В первые несколько дней после операции медсестра по уходу за стомой посоветует, как ухаживать за стомой, и какой тип мешка подходит.
После того, как соединение в кишечнике благополучно зажило, что может занять несколько недель, стому можно закрыть во время дальнейшей операции.
У некоторых людей, по разным причинам, воссоединение кишечника может быть невозможно или может привести к проблемам с контролем функции кишечника, и стома может стать постоянной.
Перед операцией медицинская бригада проинформирует вас о необходимости создания илеостомы или колостомы и о вероятности того, что это будет временным или постоянным.
Существуют группы поддержки пациентов, которые оказывают поддержку пациентам, у которых только что была стома или у которых скоро появится стома. Вы можете получить более подробную информацию у своей медсестры по уходу за стомой или посетить группы в Интернете для получения дополнительной информации.
Сюда входят:
Узнайте больше о том, как справиться со стомой после рака кишечника
Побочные эффекты хирургического вмешательства
Операции при раке кишечника сопряжены с теми же рисками, что и другие серьезные операции, включая кровотечение, инфекцию, образование тромбов или проблемы с сердцем или дыханием.
Все операции сопряжены с рядом рисков, характерных для данной процедуры. Один из рисков заключается в том, что соединенная часть кишечника может не зажить должным образом и протечь в брюшной полости. Обычно это риск только в первые несколько дней после операции.
Другой риск — для людей, перенесших операцию по поводу рака прямой кишки. Нервы, контролирующие мочеиспускание и половую функцию, расположены очень близко к прямой кишке, и иногда операция по удалению рака прямой кишки может повредить эти нервы.
После операции по поводу рака прямой кишки большинству людей необходимо чаще, чем раньше, ходить в туалет, чтобы открыть кишечник, хотя обычно это проходит в течение нескольких месяцев после операции.
Лучевая терапия
Есть два основных способа использования лучевой терапии для лечения рака кишечника. Его можно назначать перед операцией, чтобы уменьшить рак прямой кишки и увеличить шансы на полное удаление, или использовать для контроля симптомов и замедления распространения рака в запущенных случаях (паллиативная лучевая терапия).
Лучевая терапия, проводимая перед операцией по поводу рака прямой кишки, может проводиться двумя способами:
- внешняя лучевая терапия — используется аппарат для излучения волн высокой энергии в прямую кишку для уничтожения раковых клеток
- внутренняя лучевая терапия (брахитерапия) — когда радиоактивная трубка вставляется в задний проход и помещается рядом с опухолью, чтобы уменьшить ее
Внешняя лучевая терапия обычно проводится ежедневно пять дней в неделю с перерывом на выходные.В зависимости от размера опухоли вам может потребоваться от одной до пяти недель лечения. Каждый сеанс лучевой терапии короткий и длится всего 10-15 минут.
Внутреннюю лучевую терапию обычно можно провести за один сеанс, прежде чем через несколько недель будет проведена операция.
Паллиативная лучевая терапия обычно проводится короткими ежедневными сеансами, курсом от 2 до 3 дней, до 10 дней.
Краткосрочные побочные эффекты лучевой терапии могут включать:
- плохое самочувствие
- усталость
- понос
- жжение и раздражение кожи вокруг прямой кишки и таза — похоже на солнечный ожог
- частые позывы к мочеиспусканию
- ощущение жжения при мочеиспускании
Эти побочные эффекты должны пройти после окончания курса лучевой терапии.Сообщите своему лечащему врачу, если побочные эффекты лечения станут особенно неприятными. Часто доступны дополнительные методы лечения, которые помогут вам лучше справиться с побочными эффектами.
Долгосрочные побочные эффекты лучевой терапии могут включать:
Если вы хотите иметь детей, можно сохранить образец вашей спермы или яйцеклеток до начала лечения, чтобы их можно было использовать в лечении бесплодия в будущем.
Химиотерапия
Существует три способа применения химиотерапии для лечения рака кишечника:
- до операции — используется в сочетании с лучевой терапией для уменьшения опухоли
- после операции — для снижения риска рецидива рака
- паллиативная химиотерапия — для замедления распространения рака кишечника на поздних стадиях и для облегчения симптомов
Химиотерапия рака кишечника обычно включает прием комбинации лекарств, убивающих раковые клетки.Их можно вводить в виде таблеток (пероральная химиотерапия), капельного введения в руку (внутривенная химиотерапия) или в виде комбинации того и другого.
Лечение проводится курсами (циклами) продолжительностью от двух до трех недель каждый, в зависимости от стадии или степени вашего рака.
Разовый сеанс внутривенной химиотерапии может длиться от нескольких часов до нескольких дней.
Большинство людей, проходящих пероральную химиотерапию, принимают таблетки в течение двухнедельного курса перед тем, как сделать перерыв в лечении еще на неделю.
Курс химиотерапии может длиться до шести месяцев, в зависимости от того, насколько хорошо вы реагируете на лечение. В некоторых случаях его можно назначать в меньших дозах в течение более длительных периодов времени (поддерживающая химиотерапия).
Побочные эффекты химиотерапии могут включать:
- усталость
- плохое самочувствие
- рвота
- понос
- Язвы во рту
- Выпадение волос при определенных схемах лечения, но это обычно нечасто при лечении рака кишечника
- ощущение онемения, покалывания или жжения в руках, ногах и шее
Эти побочные эффекты должны постепенно исчезнуть после завершения лечения.Если вы испытываете облысение, обычно требуется несколько месяцев, чтобы отрастить волосы.
Химиотерапия также может ослабить вашу иммунную систему, делая вас более уязвимыми для инфекций.
Как можно скорее проинформируйте свою медицинскую бригаду или терапевта, если вы заметили возможные признаки инфекции, включая высокую температуру (лихорадку) или внезапное ощущение плохого самочувствия.
Лекарства, используемые в химиотерапии, могут вызвать временное повреждение мужской спермы и женских яйцеклеток. Это означает, что для беременных женщин или мужчин, ставших отцом ребенка, существует риск для здоровья будущего ребенка.
Поэтому рекомендуется использовать надежный метод контрацепции во время химиотерапевтического лечения и в течение периода после его окончания.
Узнать больше о химиотерапии
Биологические препараты
Биологические препараты, включая цетуксимаб, бевацизумаб и панитумумаб, представляют собой новый тип лекарств, также известный как моноклональные антитела.
Моноклональные антитела — это антитела, которые были генетически сконструированы в лаборатории.Они нацелены на особые белки, обнаруженные на поверхности раковых клеток, известные как рецепторы эпидермального фактора роста (EGFR).
Поскольку EGFR способствуют росту рака, нацеливание на эти белки может помочь уменьшить опухоль и улучшить эффект и результат химиотерапии.
Биологические методы лечения обычно используются в сочетании с химиотерапией, когда рак распространился за пределы кишечника (метастатический рак кишечника).
Эти методы лечения доступны не всем, страдающим раком кишечника.Национальный институт здравоохранения и повышения квалификации (NICE) установил особые критерии, которым необходимо соответствовать, прежде чем они могут быть назначены.
Цетуксимаб доступен только в NHS, когда:
- Операция по удалению рака толстой или прямой кишки была проведена или возможна
- Рак кишечника распространился на печень и не может быть удален хирургическим путем
- человек может пройти операцию по удалению рака печени, если это станет возможным после лечения цетуксимабом
Цетуксимаб, бевацизумаб и панитумумаб доступны в NHS через государственную схему, называемую Фондом противораковых препаратов.Все эти лекарства также доступны в частном порядке, но стоят очень дорого.
Дополнительную информацию обо всем вышеперечисленном можно получить по телефону:
Рак прямой кишки среди молодых людей
, от NCI Staff
Колоректальный рак — основная причина смерти от рака среди людей моложе 50 лет в Соединенных Штатах, при этом количество новых диагнозов в этой возрастной группе все еще растет.
Кредит: Национальный институт рака
Дугу Даллманну было чуть за тридцать, когда он впервые заметил кровь в стуле.
«Но, поскольку это происходило только изредка и не причиняло боли, я не особо задумывался об этом и никогда не обсуждал это со своим врачом», — написал он в личном отчете о своем опыте.
Несколько лет спустя, когда кровотечение стало более частым и интенсивным, он решил проверить его.Ему сказали, что причиной были крошечные разрывы в его кишечнике, которые на самом деле не поддаются лечению.
«Я просто подумал, что это моя судьба жить с кровью в стуле, и вернулся к игнорированию этого», — написал он.
Но потом он почувствовал резкую боль в тазу и понял, что что-то не так. Во время ежегодного медосмотра врачу не потребовалось много времени, чтобы найти опухоль. Когда ему было всего 40 лет, у него диагностировали рак прямой кишки 3 стадии.
К сожалению, опыт Dallmann отражает растущую тенденцию, наблюдаемую по всей стране.С 1990-х годов заболеваемость колоректальным раком (включая рак толстой и прямой кишки) более чем удвоилась среди взрослых моложе 50 лет. Не только это, но и все больше молодых людей умирают от этой болезни.
Этот быстрый рост вызывает особенное недоумение, потому что уровень заболеваемости колоректальным раком резко снизился среди пожилых людей — в основном из-за регулярных колоноскопий и более низкого уровня курения.
«Мы плохо разбираемся в причинах, биологии или способах предотвращения раннего начала болезни», — сказал Фил Дашнер, программный директор отдела биологии рака NCI.«И это важно узнать больше, потому что это может повлиять на [подходы] к лечению и выживаемости при раннем начале рака толстой кишки».
В сентябре более 400 ведущих ученых из академических кругов, промышленности и правительства вместе с защитниками интересов пациентов собрались в Интернете, чтобы обменяться идеями и информацией о колоректальном раке у молодых людей. Целью аналитического центра, организованного NCI и Национальным институтом наук об окружающей среде (NIEHS), было определение приоритетов исследований, направленных на решение важных вопросов, связанных с этим заболеванием.
Хотя участники обсудили несколько различных аспектов раннего колоректального рака, включая профилактику, лечение и выживаемость, выявление факторов риска и причин колоректального рака у молодых людей стало главным приоритетом.
Рост ставок по всему миру
В этом году в Соединенных Штатах почти 18 000 человек в возрасте до 50 лет будет диагностирован колоректальный рак, сказала Ребекка Сигел, магистр здравоохранения Американского онкологического общества. Но болезнь все еще встречается относительно редко и поражает менее 1% молодых людей.
Некоторые группы пострадали от растущей тенденции больше, чем другие. Например, хотя у людей всех рас может развиться колоректальный рак в молодом возрасте, всплеск в основном наблюдается среди коренных жителей Аляски, американских индейцев и белых.
Однако у чернокожих по-прежнему больше шансов заболеть колоректальным раком в молодом возрасте, чем у белых, хотя разрыв сокращается, сказал Натан Эллис, доктор философии из онкологического центра Университета Аризоны.
Соединенные Штаты — не единственная страна, сталкивающаяся с тревожным ростом заболеваемости колоректальным раком с ранним началом, — отметил Джеффри К.Ли, доктор медицины, Kaiser Permanente Northern California. Подобные тенденции также были зарегистрированы в Канаде, Новой Зеландии, Австралии и некоторых частях Европы и Азии. В большинстве этих мест число случаев заболевания среди молодых людей начало расти примерно в 1995 году.
Причины колоректального рака у молодых людей
Эксперты не знают, что вызывает скачок заболеваемости колоректальным раком среди молодых людей. Но им известны некоторые факторы, повышающие риск развития колоректального рака у пожилых людей, включая ожирение, отсутствие физической активности и курение.
«Некоторые из этих [факторов риска] стали более распространенными за последние 45 лет, наряду с ростом числа случаев с ранним началом», — сказал Дашнер, помогавший спланировать работу аналитического центра. «Таким образом, возможно, что одни и те же факторы ответственны за рост раннего начала заболевания», — отметил он.
С другой стороны, может существовать набор уникальных факторов риска колоректального рака у молодых людей, которые исследователи еще не идентифицировали, добавил он.
Хотя определенные генетические состояния, такие как синдром Линча и семейный аденоматозный полипоз, повышают риск развития колоректального рака в молодом возрасте, только от 10% до 20% колоректального рака с ранним началом вызываются наследственными факторами, объяснил Кимми Нг, М.D., онкологического института Дана-Фарбер.
Когда заболеваемость меняется от поколения к поколению, это говорит о том, что виновником является что-то в окружающей среде, а не что-то биологическое, добавил доктор Нг, и многие другие участники встречи согласились с этим.
Диета, кишечные бактерии и воспаление
Большинство дискуссий о возможных причинах раннего начала заболевания сводилось к трем взаимосвязанным факторам: диете, кишечным бактериям и воспалению.
Появляется все больше свидетельств связи нездоровой диеты — в частности, с высоким содержанием обработанного мяса и жира и низким содержанием фруктов и овощей — с ранним началом колоректального рака.
Аналогичным образом, несколько исследований показали, что избыточный вес или ожирение могут повысить вероятность раннего развития колоректального рака. Используя данные из электронных медицинских карт, Натан Бергер, доктор медицины из Центра комплексного лечения рака, обнаружил, что половина молодых людей с колоректальным раком имеют избыточный вес, а 17% страдают ожирением.
Исследователи отметили, что в последние десятилетия нездоровые диеты стали более распространенными. И количество детей и взрослых с избыточным весом или ожирением продолжает расти.
Кроме того, американцы проводят больше времени сидя и меньше — в активности. Исследования показали, что увеличение времени на просмотр телевизора также связано с более высоким риском раннего развития колоректального рака, сказал Инь Цао, доктор медицинских наук, магистр медицины Вашингтонского университета в Сент-Луисе. Но неясно, связано ли это с тем, что менее активный образ жизни может привести к полноте.
Другие ученые сосредоточили свое внимание на бактериях, живущих в кишечнике, также называемых кишечным микробиомом. Определенные типы бактерий считаются соучастниками роста и распространения колоректального рака, а некоторые могут влиять на эффективность определенных методов лечения рака.
В лабораторных исследованиях токсины нескольких типов бактерий, которые обычно встречаются в кишечнике человека, вызывают рак в кишечнике мышей, объяснила Синтия Сирс, доктор медицины, эксперт по инфекционным заболеваниям из Университета Джона Хопкинса.
Изменения в микробиоме кишечника могут влиять на рост заболеваемости колоректальным раком у взрослых в возрасте до 50 лет.
Кредит: Журнал трансляционной медицины.Апрель 2017 г. doi: 10.1186 / s12967-017-1175-y. CC BY 4.0.
Возможно, неудивительно, что на кишечные бактерии влияет пища и химические вещества, которые мы едим, пьем и дышим. Исследования показали, что диета, ожирение, физические упражнения и некоторые лекарства (например, антибиотики) могут изменить количество и типы бактерий в нашем кишечнике.
Нездоровое питание и кишечные бактерии связаны еще одним способом. И то и другое может привести к воспалению — реакции организма на травму, болезнь или раздражение.В одном исследовании на мышах диета с высоким содержанием жиров вызвала воспаление кишечника и ускорила рост опухолей в кишечнике.
Что касается кишечных бактерий, некоторые бактериальные токсины усиливают воспаление, — отметил доктор Сирс. Исследования также показали, что определенные кишечные бактерии могут привлекать иммунные клетки, которые помогают раку расти, а также блокировать иммунные клетки, которые борются с раком. «Воспаление также может генерировать вредные химические вещества, которые могут мутировать ДНК и способствовать развитию рака», — пояснил д-р Нг.
Кроме того, некоторые хронические заболевания, включая синдром раздраженного кишечника, болезнь Крона и диабет, могут вызывать воспаление в кишечнике.Половина молодых людей с колоректальным раком также страдает хроническим заболеванием, которое может вызвать воспаление в кишечнике.
Действие этих факторов может начаться очень рано — в детстве, младенчестве или даже в утробе матери, — отметила Кейтлин Мерфи, доктор философии, магистр медицины из Юго-Западного медицинского центра Техасского университета.
Химические вещества в окружающей среде
Ученые также изучают факторы окружающей среды как потенциальные причины раннего развития колоректального рака. К таким факторам относятся такие вещи, как загрязнение воздуха и воды, химические вещества в почве и продуктах питания, а также использование пестицидов.
Национальная токсикологическая программа, возглавляемая NIEHS, выявила 18 химических веществ, вызывающих рак в кишечнике мышей или крыс, сказал директор NIEHS Рик Войчик, доктор философии, который также возглавляет Национальную токсикологическую программу. Некоторые из этих химикатов могут повредить ДНК, что может привести к вредным мутациям в клетках толстой и прямой кишки.
Другие химические вещества могут иметь более косвенное воздействие, отметила Барбара Кон, доктор философии, магистр медицины Института общественного здравоохранения. Например, смеси определенных химических веществ в окружающей среде (иногда называемых эндокринными разрушителями и ожирением) могут нарушать обмен веществ в организме, что приводит к ожирению, сказала она.Доктор Кон объяснил, что даже несмотря на то, что некоторые из этих химикатов сейчас запрещены, их использование в предыдущие десятилетия могло иметь последствия в более позднем возрасте для людей, родившихся тогда.
Кроме того, некоторые химические вещества в окружающей среде могут оказывать вредное воздействие на сложный набор бактерий в кишечнике, отметил доктор Войчик.
Люди одновременно подвергаются воздействию многих химических веществ, некоторые из которых могут взаимодействовать по-разному, добавил он. Поэтому важно учитывать все воздействия окружающей среды на человека на протяжении его жизни, в том числе воздействие в утробе матери, — сказал доктор.Войчик. По его словам, также важно, как эти химические вещества взаимодействуют с генетическими и эпигенетическими характеристиками человека.
Информационные подходы к профилактике и лечению
Определение причин и факторов риска раннего колоректального рака, вероятно, поможет разработать подходы к профилактике, скринингу и лечению, сказал Дашнер.
Например, медицинские работники могут порекомендовать изменение образа жизни или более частые скрининговые тесты людям, которые из-за воздействия на них подвержены более высокому риску развития колоректального рака в молодом возрасте.
Несколько медицинских организаций снизили рекомендуемый возраст для начала скрининга на колоректальный рак с 50 до 45. Для тех, кто моложе 45 лет, адаптация подходов к скринингу на колоректальный рак для каждого человека на основе их факторов риска (так называемый точный скрининг) может повысить эффективность и стоимость -эффективность скрининга, — сказал д-р Ли.
Изучение причин и факторов риска также поможет ученым раскрыть биологию, лежащую в основе раннего колоректального рака.В частности, это может помочь ученым определить конкретные молекулы, которые вызывают рост колоректального рака у молодых людей. Что, в свою очередь, может породить новые идеи для скрининга и лечения колоректального рака.
Например, некоторые скрининговые тесты проверяют наличие определенных молекул, вырабатываемых колоректальным раком или полипами (новообразованиями, которые могут превратиться в рак). Знание того, какие молекулы являются ключевыми для роста опухолей с ранним началом, может помочь исследователям разработать скрининговые или диагностические тесты, специально предназначенные для молодых людей.Это также может помочь им разработать методы лечения, нацеленные на эти ключевые молекулы (подход, известный как таргетная терапия).
Во-первых, больше осведомленности
Хотя пандемия коронавируса вынудила этот давно запланированный аналитический центр остаться в сети, он все же собрал людей, обладающих опытом во многих различных областях, сказал Дашнер.
«Мы надеемся, что встреча будет стимулировать научное сотрудничество в этих различных областях», чтобы добиться большего прогресса, — добавил он. Чтобы продолжать продвигать исследования в этой области, NCI предоставила возможность финансирования исследований причин рака с ранним началом.
Но пока многие участники встречи согласились с тем, что есть еще более неотложный шаг: распространение информации о ранних предупреждающих признаках рака толстой кишки среди молодых людей.
У Дуга Даллманна диагностировали рак прямой кишки, когда ему было 40 лет.
Кредит: Изображение любезно предоставлено Дугом Даллманном
Как молодые люди, так и врачи должны отказаться от представления о колоректальном раке как о «болезни пожилых людей», подчеркнули несколько участников встречи.Они отметили, что люди должны привыкнуть смотреть на свой стул и замечать изменения.
«Оглядываясь назад, мне жаль, что я не уделял больше внимания симптомам», — отметил Даллманн, молодой человек, который изначально игнорировал свои симптомы и в течение многих лет ему ставили неправильный диагноз. Вот почему он продолжает делиться своей историей. По его словам, это вдохновило нескольких членов семьи и друзей на обследование, и у некоторых были обнаружены полипы.
«Это похоже на небольшую выплату за удивительную излияния поддержки, которую я получил от моих друзей, коллег, семей, моей группы поддержки рака, а также тех в онлайн-сообществе онкологов, с которыми я, вероятно, никогда не встречусь», — сказал он.



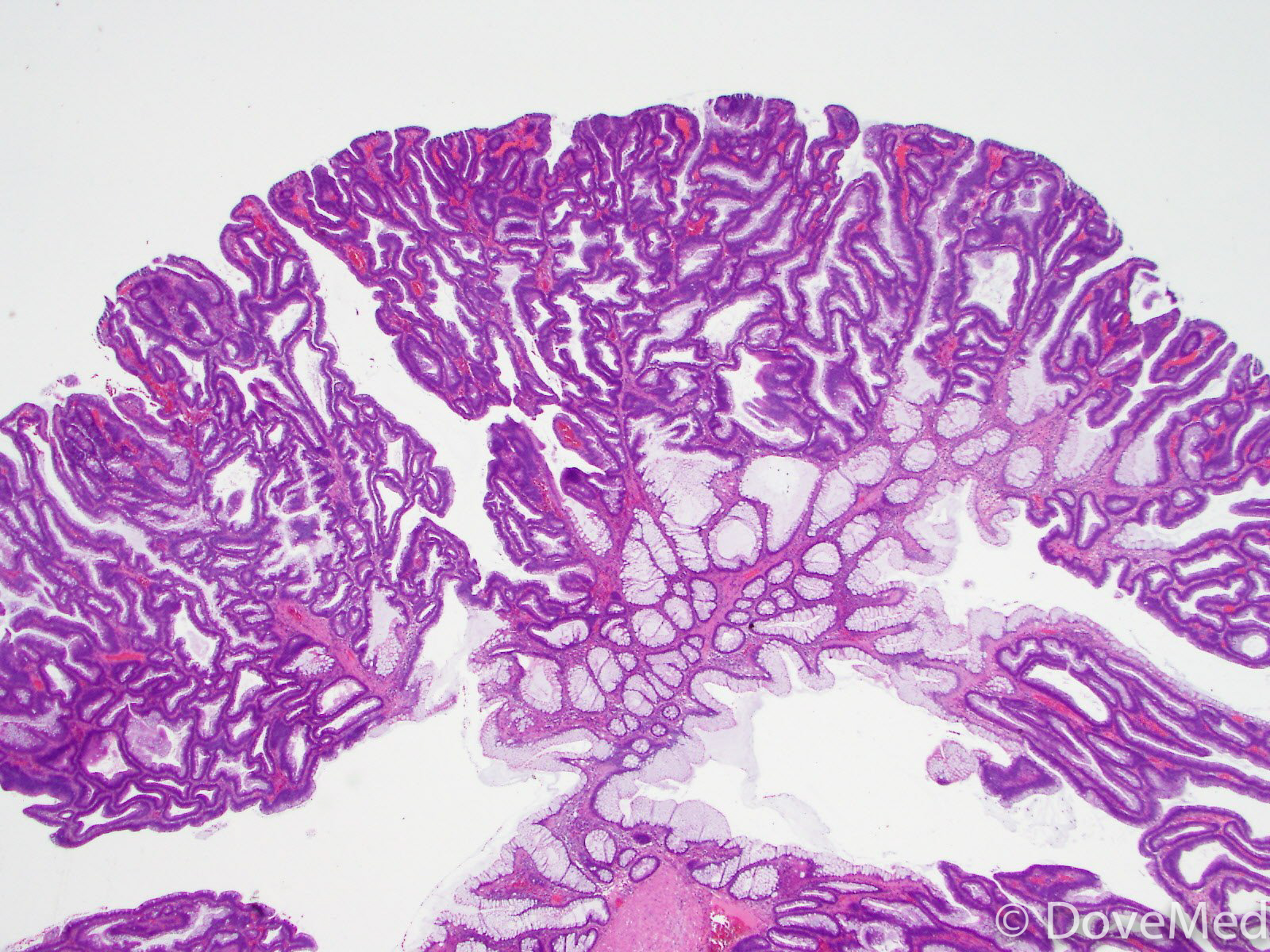



 Рост наблюдается в полость желудка.
Рост наблюдается в полость желудка.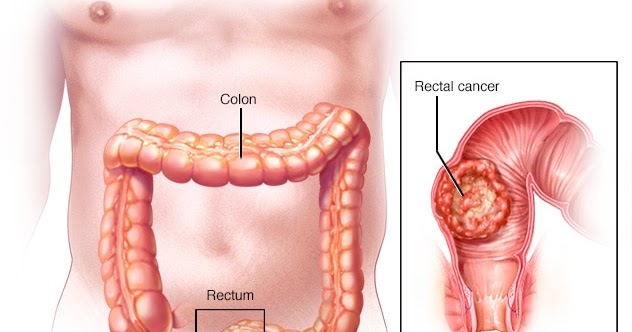 Лечить рак желудка при помощи мухомора следует по той же схеме, что и болиголовом.
Лечить рак желудка при помощи мухомора следует по той же схеме, что и болиголовом.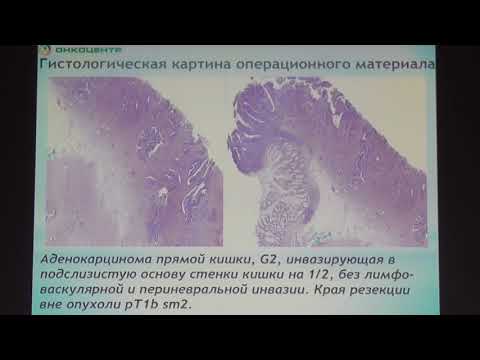
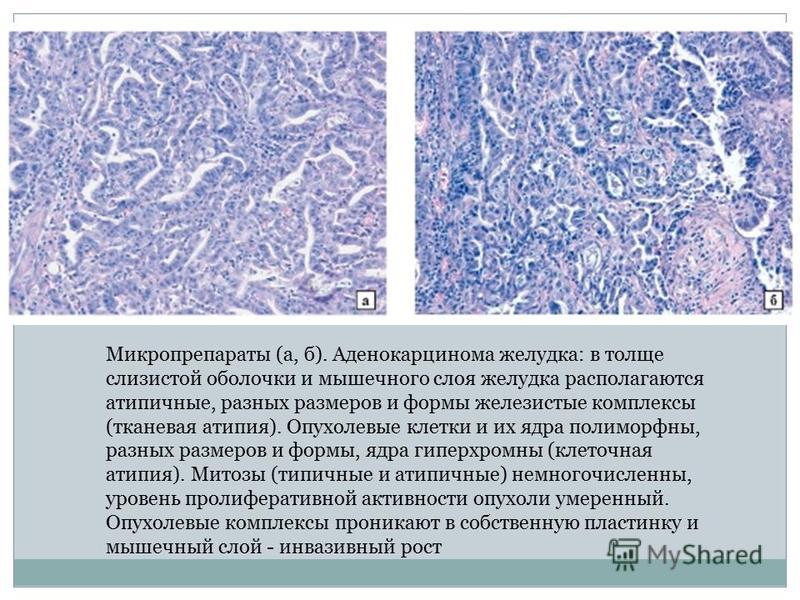
 Проникая в структуру клетки, они вызывают нарушение ее генного материала. В результате клетка не может нормально размножаться, или гибнет вовсе.
Проникая в структуру клетки, они вызывают нарушение ее генного материала. В результате клетка не может нормально размножаться, или гибнет вовсе.
 Наблюдается распространение к отдельным лимфоузлам.
Наблюдается распространение к отдельным лимфоузлам.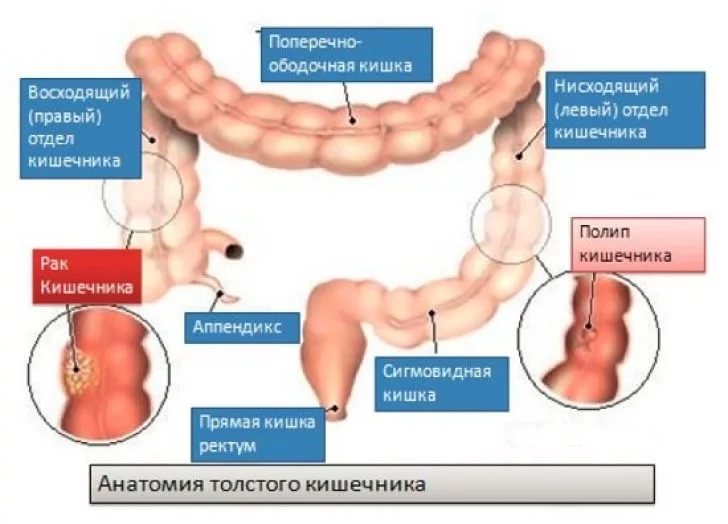
 При реакции с желудочным соком выделяются вещества, негативно воздействующие на слизистую, тем самым вызывая мутацию клеток.
При реакции с желудочным соком выделяются вещества, негативно воздействующие на слизистую, тем самым вызывая мутацию клеток.
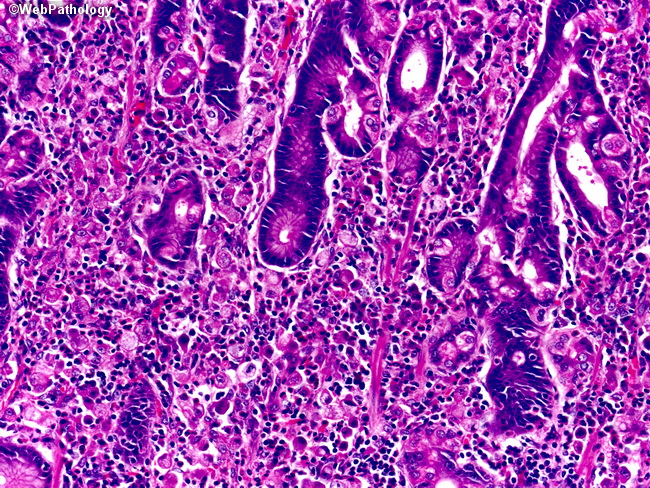

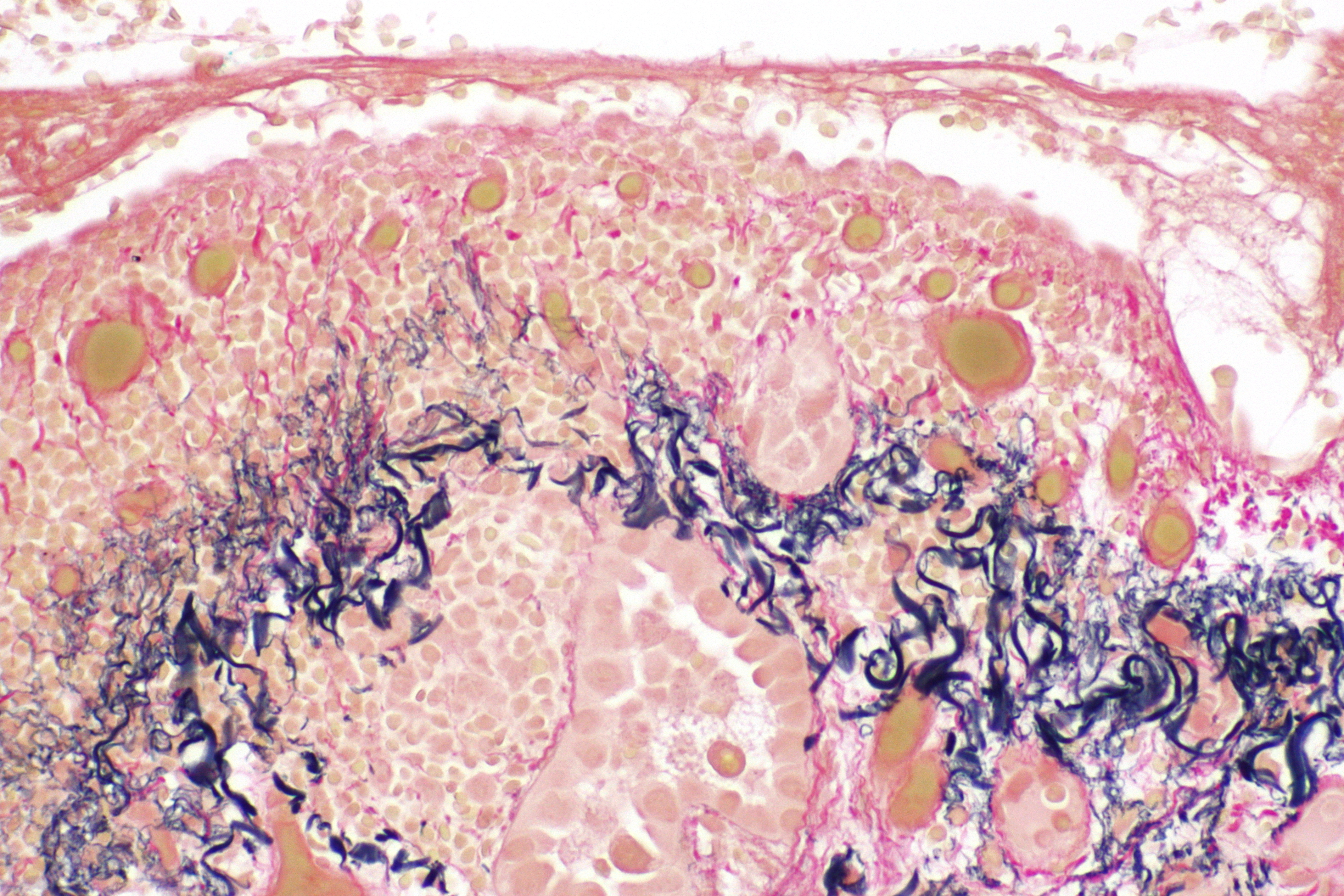
 Во многих странах людям старше определённого возраста (50 лет) рекомендуют проходить периодическую колоноскопию с одновременным удалением полипов. На сегодняшний день это наиболее эффективное средство профилактики.
Во многих странах людям старше определённого возраста (50 лет) рекомендуют проходить периодическую колоноскопию с одновременным удалением полипов. На сегодняшний день это наиболее эффективное средство профилактики.