Посттравматическая энцефалопатия
Посттравматическая энцефалопатия – это состояние, включающее комплекс психических и неврологических расстройств, обусловленных развитием в течение года или более стойких последствий перенесенной черепно-мозговой травмы вследствие рубцовых, атрофических, дистрофических и дегенеративных изменений ткани мозга. Проявления и степень выраженности зависят от локализации и тяжести травмы, возраста больного, эффективности лечения, наличия или отсутствия сосудистых нарушений, хронических интоксикаций, в том числе алкогольной.
В развитии заболевания можно выделить следующие этапы:
- Непосредственное поражение нервной ткани (как правило, лобных и височных долей) в момент травмы.
- Изменение кровоснабжения мозга вследствие отёка головного мозга.
- Нарушение циркуляции спинномозговой жидкости из-за сдавления желудочков.
- При отсутствии регенерации нервных клеток происходит замещение их соединительной тканью с образованием рубцов и спаек.

- Патологический ответ иммунной системы, которая начинает воспринимать собственные нервные клетки как чужеродный агент (аутонейросенсибилизация).
Самый первый сигнал, говорящий о возможных посттравматических изменениях, это нарушения памяти. Другой распространенный симптом – проблемы с вниманием и концентрацией. Помимо этого, встречаются нарушения мышления, которые сказываются в медлительности реакции, неспособности к анализу, логике и другим инструментам когнитивных процессов.
Также возможно появление вегетативных симптомов. Беспричинные приступы рвоты и тошноты, головные боли и головокружения, скачки артериального давления, бледность, холодный пот.
Наиболее частым проявлением энцефалопатии травматического генеза является головная боль. Характерны также головокружение, нарушения сна, слабость, снижение работоспособности, повышенная утомляемость, эмоциональная лабильность (неустойчивое, резко меняющееся настроение), болезненная чувствительность к слабым раздражителям (звукам, свету и т.
Психопатоподобные состояния развиваются постепенно, на фоне постепенного улучшения состояния больного в остром и позднем периоде травмы. Имевшиеся ранее психопатические черты характера усиливаются, «заостряются». Чаще всего наблюдаются немотивированные колебания настроения, склонность к сутяжничеству, взрывчатость с приступами агрессии, злобы и раздражения.
Кроме психоэмоциональных расстройств, при посттравматической энцефалопатии может развиваться ряд синдромов:
Гипертензионно-гидроцефальный синдром (посттравматическая внутричерепная гипертензия). Проявляется головной болью с тошнотой и рвотой, приступообразными вегетативными нарушениями.
Эписиндром (посттравматическая эпилепсия). Возникает вследствие очагового поражения или спаечно-рубцовых изменений в головном мозге. Характерны приступы различных форм — как с утратой сознания, так и без таковой.
Посттравматический паркинсонизм. Развивается в результате длительной гипоксии мозга в период травмы. Отмечается постоянное устойчивое повышение мышечного тонуса по экстрапирамидному типу, акинезия (малоподвижность в силу скованности).
Отмечается постоянное устойчивое повышение мышечного тонуса по экстрапирамидному типу, акинезия (малоподвижность в силу скованности).
Посттравматическая вестибулопатия. Сопровождается головокружениями, рвотой, тошнотой, неуверенностью при стоянии и ходьбе.
В исходе травм средней и тяжелой степени могут формироваться двигательные, речевые дефекты различной выраженности, расстройства чувствительности, тазовые нарушения.
Для подтверждения диагноза необходимо выполнить компьютерную или магниторезонансную томографию, нейропсихологическое тестирование. При этих исследованиях врач получает детальную информацию об очаговых или диффузных изменениях вещества головного мозга. Кроме того, это позволяет исключить другую патологию центральной нервной системы, сопровождающуюся сходной симптоматикой.
В качестве дополнительного метода обследования желательно выполнить электроэнцефалографию, которая помогает выявить патологический очаг эпилептической активности и скорректировать на основе полученных данных лечение.
Лечение посттравматической энцефалопатии должно быть направлено на нейропротекцию (защиту нервных клеток от негативных факторов), нормализацию процессов циркуляции крови, а также восстановление всех когнитивных функций и метаболизм клеток мозга. Также важно симптоматическое лечение, особенно при наличии синдрома гидроцефалии (необходимы специфические средства, снимающие отек мозга), эпилепсии (требуется хороший подбор противоэпилептических препаратов и их доз). Курсы такой комплексной терапии, в зависимости от выраженности проявлений посттравматической энцефалопатии, следует проводить 1-2 раза в год.
Прогноз для жизни, трудоспособности и способности к самообслуживанию, как правило, становится ясен в течение первого года после травмы. Именно в это время важно проводить комплексные реабилитационные мероприятия. Оставшийся неврологический и физический дефицит спустя указанное время достаточно сложно поддается дальнейшей коррекции. Однако даже в случае наличия грубых нарушений их следует пытаться компенсировать в той или иной степени.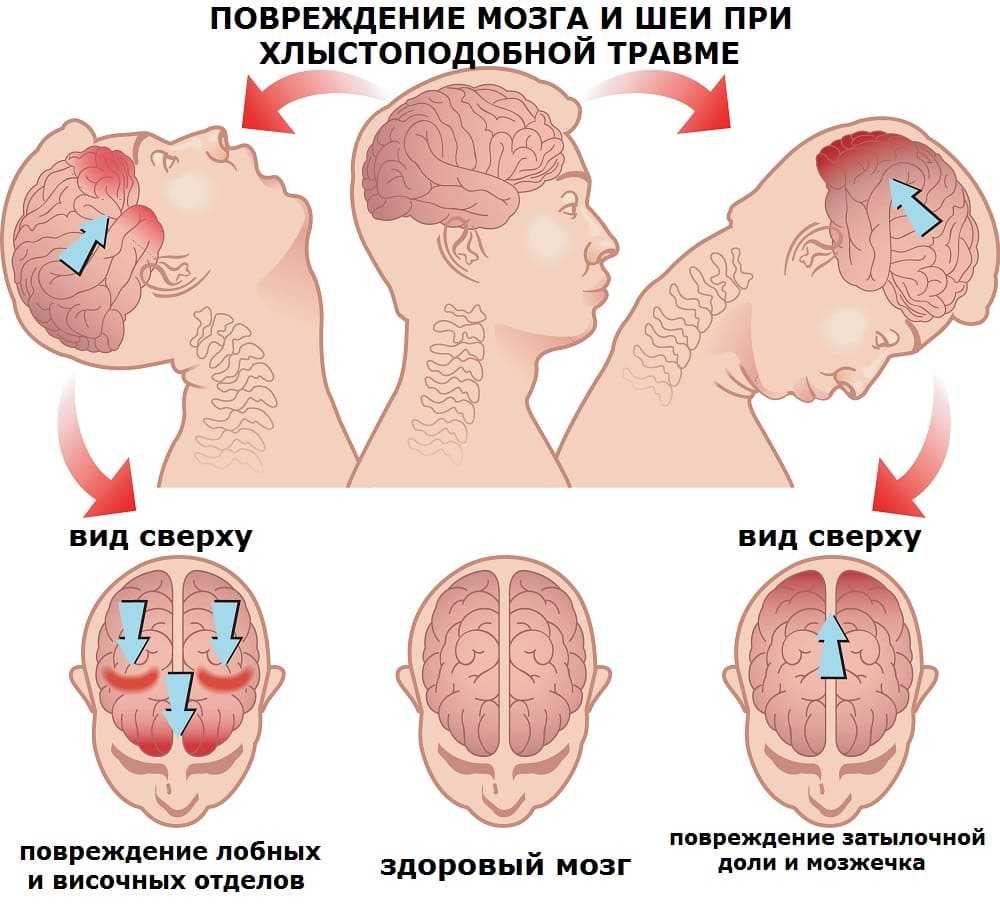
Лечение посттравматической энцефалопатии в Москве на DocDoc.ru
Неврологи Москвы — последние отзывы
Марина Альбертовна провела полный осмотр и расспросила меня. Доктор назначила мне лечение. По времени приём длился минут 40. И этого было вполне достаточно. Очень внимательный, компетентный врач. Знакомым рекомендую.
Артем, 23 сентября 2021
Мне все понравилось в общем то.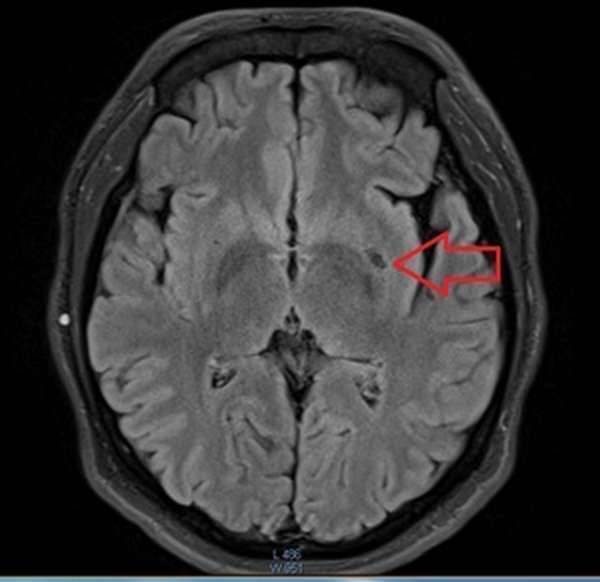 У меня проблема с храпом. Врач еще и невропатолог. На приеме Елена Юрьевна проверила, что с нервами все в порядке, неврологии нет никакой. Исключала все варианты. Задала много вопросов про моей проблеме. Много вариантов лечения предложила, исключая одно, второе, третье и грамотные рекомендации. По итогу направила еще к пульмонологу, эндокринологу, назначила таблетки, для того чтобы некоторые симптомы погасить, пока я буду решать вопрос дальше. Я доволен, спасибо. Доктор подошел очень щепетильно к вопросу, очень хорошо объяснил все. Получил ответ на все вопросы которые возникали.
У меня проблема с храпом. Врач еще и невропатолог. На приеме Елена Юрьевна проверила, что с нервами все в порядке, неврологии нет никакой. Исключала все варианты. Задала много вопросов про моей проблеме. Много вариантов лечения предложила, исключая одно, второе, третье и грамотные рекомендации. По итогу направила еще к пульмонологу, эндокринологу, назначила таблетки, для того чтобы некоторые симптомы погасить, пока я буду решать вопрос дальше. Я доволен, спасибо. Доктор подошел очень щепетильно к вопросу, очень хорошо объяснил все. Получил ответ на все вопросы которые возникали.
Алексей, 13 сентября 2021
Врач хороший, профессионал своего дела.
Роман, 03 сентября 2021
Врач приезжала к нам домой. Нам все понравилось. Елена Александровна очень грамотный, квалифицированный специалист. Дала нам соответствующие назначения. Мы их все выполняем. Доктор уделила нам более чем достаточно времени, очень вдумчиво и не спеша проводила обследование.
Виктория, 29 августа 2021
Врач чудесный и дал очень развёрнутый ответ и выписал препарат, без лишних и навязанных исследований. Клиника сомнительная, один администратор на очень много людей (и на оплату, и на приём), невозможность оплатить картой (только перевод), что дико в наше время уже встречать.
Повторюсь, приём врача отличный, а вот по клинике вопросы.
Клиника сомнительная, один администратор на очень много людей (и на оплату, и на приём), невозможность оплатить картой (только перевод), что дико в наше время уже встречать.
Повторюсь, приём врача отличный, а вот по клинике вопросы.
Петр, 29 августа 2021
Нам всё понравилось. Получили расширенный объём нужной и интересной для нас информации. Доктор проконсультировал и осмотрел. Так же договорились о дальнейшем сотрудничестве. Внимательный специалист.
Иван, 12 августа 2021
/73.jpg) Она опросила меня, осмотрела, поставила предварительный диагноз и выдала рекомендации по обследованиям.
Она опросила меня, осмотрела, поставила предварительный диагноз и выдала рекомендации по обследованиям.Александр, 21 марта 2021
Очень спокойный врач и хороший специалист. Ирина Владимировна опросила меня, внимательно выслушала, пощупала и дала советы. Я обращусь к ней повторно!
Вадим, 04 февраля 2021
Профессиональный доктор. Она дала мне рекомендации. Я всем советую данного врача!
Она дала мне рекомендации. Я всем советую данного врача!
Татьяна, 04 ноября 2020
К доктору обратилась первый раз и не пожалела. Толковый специалист. Наталья Анатольевна смогла при первом же моем визите поставить точный диагноз и рекомендовать нужное лечение. Мне понравилось, что доктор свободно общается, а не прячется за медицинской терминологией. Лечиться я начала, могу сказать, что помогает.
На модерации, 23 сентября 2021
Показать 10 отзывов из 15005Посттравматическая энцефалопатия: симптомы, лечение, мкб 10
Термином посттравматическая энцефалопатия называют такое состояние, при котором имеют место быть стойкие последствия после перенесенной черепено-мозговой травмы в течение года или более. Среди неврологических дефектов при посттравматической энцефалопатии могут встречаться парезы, вестибулярные нарушения, когнитивные нарушения, психические нарушения, эпилептические приступы и иные проявления.
Среди неврологических дефектов при посттравматической энцефалопатии могут встречаться парезы, вестибулярные нарушения, когнитивные нарушения, психические нарушения, эпилептические приступы и иные проявления.
Информация для врачей: по МКБ 10 посттравматическая энцефалопатия кодируется чаще всего под шифром T90.5 (последствия внутричерепной травмы). Также можно использовать шифр G93.8 (другие уточненные заболевания головного мозга). В диагнозе обязательно необходимо указывать травму, её вид (ушиб с указанием степени тяжести, диффузное аксональное повреждение и т.п.), дату (если прошло более 5 лет, о хотя бы год). Также указываются в синдромальной части все проявления. Следует помнить о том, что сотрясение головного мозга не оставляет последствий и посттравматическую энцефалопатию возможно описывать лишь при наличии множественных (и обязательно задокументированных) сотрясений. Наличие посттравматической гидроцефалии и её проявлений как ведущего или единственного синдрома, предполагает возможность кодировки диагноза по МКБ 10 в рубрике G91.
Причины
Причины развития заболевания ясны из названия. Важен факт наличия тяжелой травмы, костных дефектов черепа, сформированных ликворных фистул или иных грубых органических причин формирования последствий травмы. Сотрясение головного мозга, а также частые слова пациентов «я за жизнь ударялся сотню раз» не являются причиной для постановки диагноза посттравматическая энцефалопатия.
Симптомы
Симптомы посттравматической энцефалопатии схожи с таковыми при других органических поражениях головного мозга и могут быть объединены в группы, синдромально. Чаще всего встречаются цефалгический, вестибуло-координаторный синдромы, когнитивное снижение, психические и психологические нарушения. Также достаточно часто при последствиях травм может иметь место эпилептические припадки. В таком случае речь идет о так называемой симптоматической эпилепсии, которую, в случае единственного проявления, лучше называть посттравматической эпилепсией.
Диагностика заболевания требует обязательного подтверждения при помощи нейровизуализационных методов исследования. Очень важно наличие хотя бы 1 снимка МРТ, по которому могут быть видны малейшие изменения вещества головного мозга.
Очень важно наличие хотя бы 1 снимка МРТ, по которому могут быть видны малейшие изменения вещества головного мозга.
Лечение
Лечение посттравматической энцефалопатии должно быть направлено на нейропротекцию (защиту нервных клеток от негативных факторов), нормализацию процессов циркуляции крови, а также восстановление всех когнитивных функций и метаболизм клеток мозга (ноотропная терапия). Также важно симптоматическое лечение, особенно при наличии синдрома гидроцефалии (необходимы специфические средства, снимающие отек мозга, такие как диакарб, глицериновая смесь), эпилепсии (требуется хороший подбор противоэпилептических препаратов и их доз).
Курсы такой комплексной терапии, в зависимости от выраженности проявлений посттравматической энцефалопатии, следует проводить 1-2 раза в год. Чаще всего из нейропротективных средств используются глиатилин (дженерик – церепро), актовегин, мексидол, ноотропная терапия в настоящее время включает группу рацетамов (чаще всего известный препарат пирацетам), а также такие препараты как фенотропил, пантогам (особенно при наличии симптоматической эпилепсии) и другие лекарственные средства. Помимо стандартной медикаментозной терапии при наличии парезов и других двигательных нарушений важны такие методики как ЛФК, массаж.
Помимо стандартной медикаментозной терапии при наличии парезов и других двигательных нарушений важны такие методики как ЛФК, массаж.
Прогноз
Прогноз для жизни, трудоспособности и способности к самообслуживанию, как правило, становится ясен в течение первого года после травмы. Именно в это время важно проводить всевозможные реабилитационные мероприятия. Оставшийся неврологический и физический дефицит достаточно сложно поддается дальнейшей коррекции. Однако даже в случае наличия грубых нарушений не следует терять надежды. Встречаются случаи, когда реабилитация даже через 5-7 лет после перенесенной травмы давала свои результаты.
симптомы, лечение резидуальной энцефалопатии в Ижевске
Резидуальная энцефалопатия – это заболевание головного мозга, вызванное повреждением тканей и гибелью нервных клеток (нейронов). Встречается у людей разного возраста, в том числе и у детей. Болезнь может быть врожденной и приобретенной.Патологические изменения развиваются, если нарушается кровоснабжение в головном мозге и клетки испытывают кислородное голодание. Спровоцировать подобное состояние способны черепно-мозговые травмы, вегетососудистая дистония, атеросклероз, гипертония, инфекции, ишемия, инсульт, сахарный диабет, токсические вещества, радиация, неконтролируемый прием лекарств, употребление наркотиков и психотропных препаратов, операции на головном мозге. Врожденная энцефалопатия может возникать вследствие осложненной беременности, аномалий внутриутробного развития, вредных привычек будущей мамы, родовых травм.
Спровоцировать подобное состояние способны черепно-мозговые травмы, вегетососудистая дистония, атеросклероз, гипертония, инфекции, ишемия, инсульт, сахарный диабет, токсические вещества, радиация, неконтролируемый прием лекарств, употребление наркотиков и психотропных препаратов, операции на головном мозге. Врожденная энцефалопатия может возникать вследствие осложненной беременности, аномалий внутриутробного развития, вредных привычек будущей мамы, родовых травм.
Симптомы резидуальной энцефалопатии
При врожденной форме болезни наблюдаются нервные расстройства. Ребенок становится раздражительным либо апатичным, у него часто изменяется настроение, ухудшается память, возможны судороги.Приобретенная резидуальная энцефалопатия является «бомбой замедленного действия», так как в течение нескольких лет может протекать бессимптомно. На начальной стадии функции погибших клеток берут на себя другие нейроны. Но с возрастом головной мозг теряет компенсаторные свойства.
В результате обнаруживаются следующие симптомы:
- головная боль и головокружение;
- тошнота и рвота;
- бессонница ночью и сонливость днем;
- ослабление остроты зрения и слуха;
- невнятная речь;
- ухудшение умственных способностей;
- нарушение координации;
- заторможенность;
- вялость либо повышенная возбудимость;
- судороги и обмороки;
- парезы (ослабление двигательных функций) и параличи.

Диагностирование болезни
Чтобы поставить правильный диагноз, невролог выслушивает жалобы больного и изучает анамнез заболевания. По показаниям врач направляет пациента на инструментальные и лабораторные обследования (методы диагностики подбирают индивидуально):- рентгенографию шейного отдела;
- эхоэнцефалографию;
- электроэнцефалографию;
- ультразвуковое исследование головного мозга;
- дуплексное сканирование;
- реовазографию;
- компьютерную или магнитно-резонансную томографию;
- анализы крови и мочи.
Лечение резидуальной энцефалопатии
Неврологи клиники Елены Малышевой для каждого больного подбирают индивидуальное лечение, учитывая причины болезни, симптомы и их выраженность, тяжесть состояния.
Обычно резидуальную энцефалопатию лечат консервативными методами, которые могут включать:
- лекарственную терапию – устраняет неприятную симптоматику, восстанавливает деятельность головного мозга, нормализует обмен веществ и мозговое кровообращение;
- физиотерапию – активирует защитные силы организма, мобилизует их на борьбу с болезнью;
- лечебный массаж – стимулирует приток крови к головному мозгу, обеспечивая его питательными веществами и кислородом;
- лечебную физкультуру – активирует циркуляцию крови, восстанавливает двигательную активность, улучшает координацию.
Преимущества лечения в клинике Елены Малышевой
Важное значение для успешного лечения резидуальной энцефалопатии имеет правильная диагностика, что бывает сильно затруднительным. В клинике Елены Малышевой практикуют высококвалифицированные неврологи с многолетним опытом. В своей работе они используют современное оборудование последнего поколения, что обеспечивает правильную постановку диагноза и способствует успешному лечению.
В клинике Елены Малышевой практикуют высококвалифицированные неврологи с многолетним опытом. В своей работе они используют современное оборудование последнего поколения, что обеспечивает правильную постановку диагноза и способствует успешному лечению.Если вы заметили малейшие отклонения в состоянии здоровья, не игнорируйте проблему. Обратитесь к специалистам, что позволит в кратчайшие сроки выявить и вылечить болезнь, предотвратив опасные последствия, приводящие к деградации личности.
Записаться на прием к неврологу можно по телефону (3412) 52-50-50, либо заказав обратный звонок.
Энцефалопатия: симптомы, диагностика и лечение
Энцефалопатия – это органическое поражение головного мозга невоспалительного характера. Может быть врождённой либо приобретённой вследствие перенесенных инфекционных заболеваний, травм, нарушений метаболизма и т.д. Встречается у людей всех возрастов, начиная от новорожденных, но чаще всего регистрируется у пожилом и старческом возрасте. При энцефалопатии происходит дистрофия тканей мозга и, как следствие, нарушение его функционирования.
При энцефалопатии происходит дистрофия тканей мозга и, как следствие, нарушение его функционирования.
Причины развития энцефалопатии
Основной причиной энцефалопатии является хроническое кислородное голодание головного мозга. Развитию этого состояния способствуют:
- патологии беременности и родов (в случае перинатальной энцефалопатии)
- травмы головы и мозга (особенно часто встречается у боксёров «синдром пропущенного удара»)
- сосудистая недостаточность
- атеросклероз
- гипертония, повышенное внутричерепное давление
- почечная или печёночная недостаточность
- метаболические заболевания (диабет)
- алкоголизм или наркотическая зависимость
- приём некоторых медикаментов
- интоксикация химикатами, тяжёлыми металлами
- лучевая болезнь
- последствия перенесенных инфекций (в том числе нейроинфекций)
Виды энцефалопатий и степени тяжести
Заболевание может быть врождённым (развивается с 28-ой недели внутриутробного развития и в течение 1-ой недели жизни). Перинатальная энцефалопатия вызывается генетическим дефектом, болезнями матери во время беременности, аномалией развития головного мозга плода, родовой травмой.
Перинатальная энцефалопатия вызывается генетическим дефектом, болезнями матери во время беременности, аномалией развития головного мозга плода, родовой травмой.
Приобретённая энцефалопатия разделяется на несколько видов, в зависимости от причин развития болезни:
- Энцефалопатия Вернике (Синдром Гайе-Вернике). Возникает вследствие недостатка питания, частой рвоты, авитаминоза, алкоголизма.
- Гипертензивная энцефалопатия – следствие гипертонии (например, подкорковая атеросклеротическая энцефалопатия).
- Посттравматическая (Синдром пропущенного удара).
- Дисциркуляторная энцефалопатия (ДЭП). Характеризуется наличием в головном мозге множественных очагов с нарушение кровообращения в мелких артериях и артериолах.
- Метаболическая энцефалопатия (печёночная, синдром Рея).
- Токсическая энцефалопатия (например, марганцевая).
- Лучевая (пострадиационная) энцефалопатия.
- Прогрессирующая лейкоэнцефалопатия (сосудистая, гипетензивная, мультифокальная).
 Регистрируется при новообразованиях системы кроветворения, ВИЧ.
Регистрируется при новообразованиях системы кроветворения, ВИЧ.
- Энцефалопатия Хасимото возникает вследствие воспаления щитовидной железы и может сопровождаться психозом.
Также поражения головного мозга и последующие нарушения мозговой деятельности имеют три степени тяжести.
І степень – внешние проявления заболевания отсутствуют, при инструментальных исследованиях обнаруживаются небольшие диффузные изменение тканей головного мозга.
ІІ степень – отмечаются нарушения мозговой деятельности, однако они слабо выражены либо преходящие.
ІІІ степень – неврологические расстройства ярко выражены, могут привести к инвалидизации больного.
Симптомы энцефалопатии
Симптомы заболевания могут отличаться, в зависимости от причин его развития, степени и характера поражения, локализации. Признаки энцефалопатии могут проявляться как в вегетативных нарушениях, так и изменениях в эмоциональной либо когнитивной сферах.
- Головокружения, обморочные состояния
- Постоянная «фоновая» головная боль либо острые непродолжительные приступы
- Шум в голове, сложности с концентрацией
- Снижение памяти и мыслительных способностей
- Слабость, быстрая утомляемость
- Сонливость и другие нарушения сна
- Апатия, отсутствие инициативности, мотивации к деятельности, сужение круга интересов
- Депрессия, желание умереть
- Раздражительность, эмоциональная лабильность
- Нарушение координации движений, тремор
- Паркинсонизм, нарушения глотательного рефлекса
- Снижение либидо, расстройство половой функции
- Снижение остроты слуха и зрения
- Вялость речи (медленная, невнятная, тихая, бормочущая)
- Онемение кончиков пальцев, носа, губ
- Судороги
Без соответствующего лечения симптомы будут нарастать, могут появляться расстройства сознания, бред, галлюцинации, вплоть до психозов, изменения личности.
Диагностика и лечение энцефалопатии
Болезнями головного мозга, и энцефалопатией в том числе, занимается врач невролог. Для получения полной картины болезни в первую очередь собираются данные анамнеза: была ли родовая или черепно-мозговая травма, показатели артериального давления, нет ли заболеваний почек/печени/поджелудочной железы, алкоголизм/наркомания и так далее. Далее назначают инструментальные и лабораторные методы диагностики:
Также важно провести диагностику основного заболевания, которое могло вызвать энцефалопатию (например, УЗИ почек, биопсию печени).
Отдельно нужно обратить внимание на диагностику энцефалопатии у детей. Существует практика в первые дни жизни ребёнка проводить эхографию головного мозга для своевременного обнаружения патологии и её лечения.
Лечение энцефалопатии
Тактика лечение всегда зависит от причин, вызвавших энцефалопатию. То есть, в первую очередь, медикаментозное лечение направлено, например, на протекцию печени или лечение нефрита, контроль артериального давления или применения хондропротекторов при заболеваниях суставов шейного отдела позвоночника. Также назначается курс «нейровитаминов».
Также назначается курс «нейровитаминов».
Так как основной причиной энцефалопатии является нарушения кровоснабжения, то второй задачей лечения является восстановление нормального кровотока, укрепление сосудов, «разжижение» крови. В некоторых случаях может потребоваться оперативное вмешательство и процедуры очищения крови.
Однако для достижения результата одного медикаментозного лечения недостаточно, поэтому в комплексе назначают:
- массажи воротниковой зоны
- курс остеопатии
- электрофорез
- магнитотерапия
- иглоукалывание и фармакопунктура
Также больному настоятельно рекомендуется изменить образ жизни: отказаться от алкоголя и наркотиков, сбалансировать питание, «разгружать» сидячий образ жизни.
При соблюдении всех рекомендаций врача и ответственном к ним отношении проявления энцефалопатии можно свести к минимуму и вести обычный образ жизни. Если же заболевание запущено и сопровождается выраженными нарушениями двигательных функций, просто ведя здоровый образ жизни, здоровья не вернуть. В этом случае неврологи клиники Аксимед рекомендуют пройти курс реабилитации в специализированном неврологическом реабилитационном центре, который поможет вернуть свободу движения и повысит качество жизни.
В этом случае неврологи клиники Аксимед рекомендуют пройти курс реабилитации в специализированном неврологическом реабилитационном центре, который поможет вернуть свободу движения и повысит качество жизни.
Лечение дисциркуляторной энцефалопатии в санатории-курорте Шахтер, Ессентуки
Лечение дисциркуляторной энцефалопатии в санатории-курорте Шахтер, Ессентуки Мы заботимся о наших гостях и принимаем меры по борьбе с распространением вируса COVID-19. Мы заботимся о безопасности наших гостей. Подробнее
Гарантия лучшей цены!
Большой крытый бассейн на 25м
Дети до 4х лет проживают бесплатно
Удобное расположение — 100 метров до лечебного парка и бювета с минеральной водой
Бесплатная доставка багажа в номер
Ежедневная анимационная программа
VIP сервис в номерах повышенной комфортности
Уникальные лечебные программы
Для лечения дисцикуляторной энцефалопатии применяют медикаментозную терапию (препараты, снижающие давление, предотвращающие отложение тромбоцитов, улучшающие межнейронные связи, направленные на лечение атеросклероза), а также психотерапию и физиотерапию.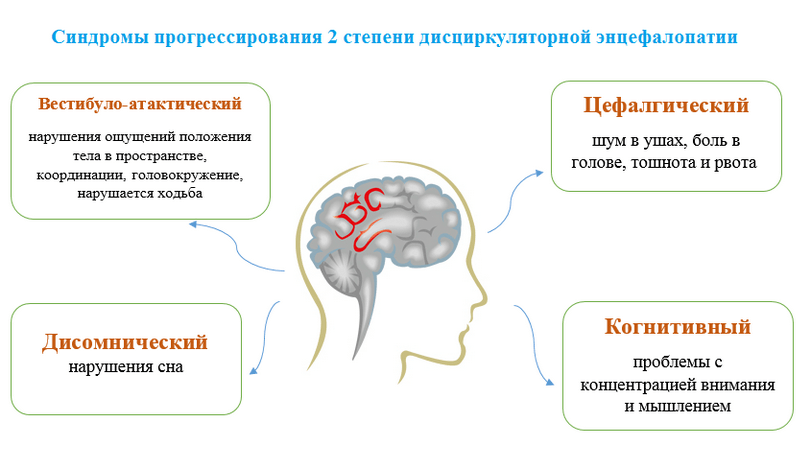 Б/
Б/
Эффективен метод санаторно-курортного лечения. Санаторные программы предлагают специальную низкокалорийную диету, с малым количеством животных жиров, жареных продуктов, яиц (такая диета необходима для успешного лечения), лечебную физкультуру, наблюдений у психотерапевта и физиотерапевтические мероприятия. Лазеротерапия, воздействие гальваническими токами, специальные ванны, УВЧ благоприятно влияют на процесс выздоровления. Также посетителям обычно предлагаются массажи и пешие прогулки на свежем воздухе.
Противопоказания
- ВСД с частыми болевыми присту-пами, сопровождающимися тош- нотой, рвотой
- Дисциркуляторная энцефалопатия 1, 2, 3 степени: атеросклеротическая, гипертензивная, посттравматическая, смешанная
- Противопоказания: ДЭ 3 степени, сопровождающаяся деменцией с нарушением самообслуживания, самостоятельного передвижения и речи.
Результаты лечения
Старания врачей нацелены на замедление болезни.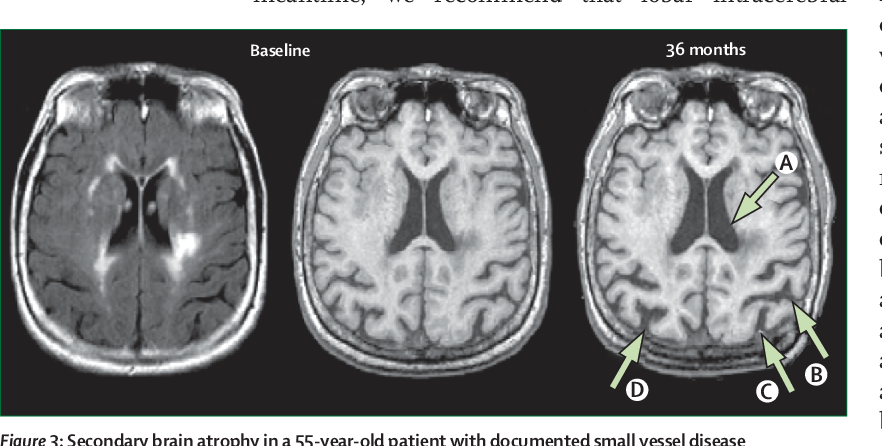 И это удаётся сделать, путём комплексного лечения и постоянного контроля за состоянием больного. В итоге, восстанавливается процесс доставки кислорода к клеткам мозга и состояние пациента улучшается, повышается качество жизни.
И это удаётся сделать, путём комплексного лечения и постоянного контроля за состоянием больного. В итоге, восстанавливается процесс доставки кислорода к клеткам мозга и состояние пациента улучшается, повышается качество жизни.Последствия отсутствия лечения
Осложнения заболевания достаточно серьёзные и могут привести к инвалидизации. Инсульт, закупорка сосудов мозга и его отёки – вот что встречается чаще всего. Дисциркуляторная энцефалопатия — прогрессирующее заболевание головного мозга, связанное с патологией сосудов. В результате этой патологии нарушается кровоток и, как следствие, доставка кислорода к клеткам мозга, происходит кислородное голодание и клетки мозга начинают отмирать. К причинам развития дисцикуляторной энцефалопатии относят атеросклероз, скачкообразное повышение артериального давления, остеохондроз, травмы шейного отдела.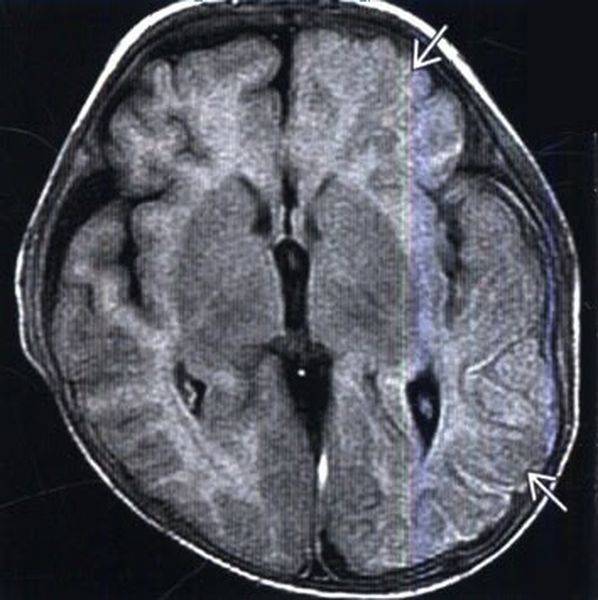
Лечение по данному заболеванию назначают врачи-консультанты санатория «Шахтёр» как сопутствующую патологию к основным заболеваниям, являющимся профильными для санатория – заболевания органов пищеварения и эндокринной системы.
Более подробную консультацию можно получить в отделе продаж курорта: +7 (863) 310-01-43
Санаторно-курортные программы
Травматическая энцефалопатия — причины, симптомы, диагностика и лечение
Травматическая энцефалопатия – это комплексное психоневрологическое расстройство, развивающееся в позднем и отдаленном периоде черепно-мозговой травмы. Возникает на основе дегенеративных, дистрофических, атрофических и рубцовых изменений мозговой ткани. Проявляется слабостью, снижением работоспособности, повышенной утомляемостью, эмоциональной лабильностью, нарушениями сна, головокружениями, гиперчувствительностью к раздражителям. Диагностика включает неврологическое обследование, беседу с психиатром, инструментальные исследования мозга, психологическое тестирование. Лечение – фармакотерапия, психотерапия, общеукрепляющие мероприятия.
Проявляется слабостью, снижением работоспособности, повышенной утомляемостью, эмоциональной лабильностью, нарушениями сна, головокружениями, гиперчувствительностью к раздражителям. Диагностика включает неврологическое обследование, беседу с психиатром, инструментальные исследования мозга, психологическое тестирование. Лечение – фармакотерапия, психотерапия, общеукрепляющие мероприятия.
Общие сведения
Слово энцефалопатия произошло из древнегреческого языка, в переводе означает «болезнь головного мозга». Травматическая энцефалопатия является наиболее частым осложнением ЧМТ. Синонимичные названия – травматическое органическое поражение мозга, посттравматическая энцефалопатия. В Международной классификации болезней 10 пересмотра расстройство чаще относят к рубрике «Последствия внутричерепной травмы» T90.5. Распространенность наиболее велика среди мужчин в возрасте от 20 до 40 лет, особенно среди людей, занимающихся боевыми видами спорта. По разным данным, эпидемиологический показатель у пациентов с ЧМТ достигает 55-80%.
Травматическая энцефалопатия
Причины
Базовым фактором данного осложнения является травматическое поражение головного мозга. Причиной может стать удар, толчок, резкий рывок или встряхивание головой. Вероятность последующего развития энцефалопатии увеличивается при преморбидных сосудистых патологиях, алкоголизме, интоксикациях, тяжелых инфекциях. В группе риска находятся следующие категории пациентов:
- Спортсмены. Боевые и экстремальные виды спорта сопровождаются падениями, ударами, приводящими к травмам. Травматическая энцефалопатия часто диагностируется у боксеров, борцов, хоккеистов, футболистов, велосипедистов, роллеров.
- Служащие силовых структур. Включает представителей профессий, связанных с применением насилия – полицейских, военнослужащих, охранников. Частые ЧМТ формируют хроническую форму энцефалопатии.
- Водители, пассажиры транспортных средств. Травма может быть получена в результате ДТП, крушения. Более подвержены опасности профессиональные водители.
- Пациенты с судорожными приступами. При эпилептических, истерических припадках повышен риск внезапного падения, удара головой о твердые поверхности. Больные неспособны контролировать течение приступа и не всегда успевают занять безопасное положение до его начала.
- Новорожденные. ЧМТ может являться результатом осложнений в родах. Органическое повреждение и его последствия диагностируются в течение первого года жизни.
Патогенез
В основе травматической энцефалопатии лежит поражение тканей мозга диффузного характера – патологические изменения в различных церебральных структурах. Патоморфологически обнаруживаются сосудистые нарушения, обуславливающие гипоксию, дистрофические изменения нейронов и глии, участки рубцовой ткани в оболочках, сращение оболочек между собой и с мозговым веществом, образование кист, гематом, увеличение желудочков мозга. Развитие и клиническое течение энцефалопатии – динамичный многоуровневый процесс, определяющийся характером травмы, тяжестью поражения, индивидуальными способностями организма к восстановлению и противостоянию патологическим воздействиям. В патогенезе чаще доминируют гипоксические и метаболические нарушения в нейронах, изменения ликвородинамики. Вторичное влияние оказывают генетические и преморбидные факторы, общее состояние здоровья, возраст, профессиональные вредности, качество и своевременность лечения острого периода травмы.
Классификация
В зависимости от частоты и выраженности периодов декомпенсации посттравматического процесса выделяют четыре типа течения энцефалопатии: регрессирующий, стабильный, ремиттирующий и прогрессирующий. Данная классификация используется для составления прогноза и оценки эффективности лечения. По характеру клинических проявлений в структуре травматической энцефалопатии различают несколько синдромов:
- Вегето-дистонический. Наиболее распространенный. Вызван поражением центров вегетативной регуляции, нейрогуморальными расстройствами.
- Астенический. Выявляется во всех периодах последствий ЧМТ. Представлен двумя формами: гипостенической и гиперстенической.
- Синдром нарушений ликвородинамики. Наблюдается примерно в трети случаев. Чаще протекает в варианте ликворной гипертензии (увеличение продукции ликвора и нарушение целостности оболочек мозга).
- Церебрально-очаговый. Развивается после тяжелых травм. Может проявляться как корковый, подкорковый, стволовой, проводниковый синдром.
- Психопатологический. Формируется у большинства больных. Характеризуется неврозоподобными, психопатоподобными, делириозными, когнитивными нарушениями.
- Эпилептический. Обнаруживается в 10-15% ЧМТ, является локально обусловленной симптоматической эпилепсией (эпилепсией травматического генеза). Чаще всего приступы возникают в первый год после травмы.
Симптомы травматической энцефалопатии
Клиническая картина, как правило, представлена несколькими синдромами, различными по степени выраженности. При диагностике определяется ведущий синдром. При астеническом варианте наблюдается быстрая утомляемость, истощаемость, эмоциональная лабильность, полиморфные вегетативные симптомы. Больные с трудом выполняют повседневную работу, испытывают сонливость, головные боли. Избегают шумных компаний, длительных нагрузок, поездок. Гиперстенический вариант синдрома характеризуется повышенной раздражительностью, чувствительностью к внешним воздействиям, эмоциональной неустойчивостью. При гипостеническом синдроме преобладает слабость, вялость, апатичность.
Пациенты с выраженным вегетативно-дистоническим синдромом жалуются на преходящие эпизоды повышенного или пониженного артериального давления, учащенного сердцебиения, чувствительность к холоду и жаре. Характерны эндокринные сбои (изменения менструального цикла, импотенция), избыточная потливость, гиперсаливация, сухость кожи и слизистых. При синдроме нарушенной ликвородинамики часто обнаруживается посттравматическая гидроцефалия – избыточное накопление жидкости в ликворных пространствах, сопровождающееся распирающими головными болями, тошнотой, рвотой, головокружениями, нарушениями походки, заторможенностью психических процессов.
При патопсихологическом синдроме развиваются неврозоподобные расстройства – депрессия, ипохондрия, тревожность, страхи, навязчивые мысли и действия. При субпсихотическом варианте формируется гипомания, глубокая депрессия, паранойя (бредовые идеи). Когнитивные нарушения проявляются снижением памяти, трудностями сосредоточения внимания и выполнения интеллектуальных задач. При легком течении заметна утомляемость во время умственных нагрузок, динамические колебания работоспособности. При умеренном – затруднено выполнение сложных заданий, повседневная адаптация сохранена. При тяжелом – пациенты нуждаются в уходе, несамостоятельны.
Для церебрально-очагового синдрома типичны двигательные нарушения (параличи, парезы), изменения чувствительности (анестезия, гипестезия), симптомы поражения лицевого, слухового, глазных нервов, корковые очаговые расстройства. Больные страдают от снижения слуха, косоглазия, диплопии. Возможны нарушения письма, счета, речи, мелкой моторики. Посттравматическая эпилепсия развивается с простыми и сложными парциальными, вторично-генерализованными припадками. Судорожные пароксизмы сопровождаются дисфорией – раздражительностью, гневливостью, агрессивностью.
Осложнения
Характер осложнений травматической энцефалопатии определяется особенностями течения и доминирующим синдромом. Вегето-дистонические нарушения приводят к развитию заболеваний сердечно-сосудистой системы, в частности, раннего церебрального атеросклероза, гипертонической болезни. Астенический, психопатологический, ликвородинамический синдромы снижают качество жизни больных – нарушается работоспособность, пациенты хуже справляются с трудовыми задачами, меняют место работы. Изменения познавательной сферы и психологических процессов могут приобретать стойкий характер. Осложнениями являются расстройства личности и когнитивное расстройство органического генеза.
Диагностика
Обследование пациентов проводится неврологом, при подозрении на психопатологическую симптоматику назначается консультация психиатра. Опираясь на особенности клинической картины, специалисты принимают решение о необходимости инструментальной и психологической диагностики. Комплекс исследований включает следующие процедуры:
- Опрос, осмотр. Врач-невролог собирает анамнез: расспрашивает о давности травмы, ее тяжести, лечении, актуальном самочувствии. Проводит осмотр, выявляя нарушение рефлексов, походки, простых двигательных навыков, чувствительности. Направляет на дальнейшие обследования. По их результатам устанавливает диагноз, определяет доминирующий синдром.
- Клиническая беседа. Психиатр проводит диагностическую консультацию с целью обнаружения психопатологии: поведенческих и эмоционально-волевых нарушений, бредоподобной симптоматики, снижения когнитивных функций. Оценивает способность больного поддерживать контакт, адекватность реакций, сохранность критических способностей.
- Инструментальные методы. Используются нейрофизиологические и нейровизуальные методики: ЭЭГ, РЭГ, УЗДГ сосудов шеи и головного мозга, рентгенография шейного отдела позвоночника, МРТ головного мозга, МРТ сосудов головного мозга. Результаты подтверждают морфологические и функциональные изменения ЦНС.
- Психодиагностические методы. Применяются нейропсихологические и патопсихологические пробы, определяющие сохранность памяти, внимания, мышления, речи, мелкомоторных движений, способности распознавать предметы и звуки. При возможных неврозоподобных, психопатоподобных нарушениях проводятся тесты на тревожность, депрессию, комплексные методики исследования личности.
Лечение травматической энцефалопатии
Основные лечебные мероприятия направлены на нейропротекцию (защиту нейронов), восстановление нормальной циркуляции крови и метаболических процессов в мозге, коррекцию когнитивных и эмоциональных функций. Симптоматическое лечение подбирается индивидуально, при гидроцефалии назначаются препараты, снимающие отек мозга, при эпилепсии – противосудорожные средства. Терапевтическая программа включает следующие методики:
- Фармакотерапия. Ноотропная терапия часто представлена рацетамами. Из нейропротекторных средств используются холиномиметики, антигипоксанты, антиоксиданты.
- Психокоррекция. При снижении когнитивной сферы проводятся коррекционные занятия, включающие упражнения на тренировку внимания, памяти, развитие мышления. Психотерапевтическая помощь необходима при симптомах депрессии, эмоциональной неустойчивости.
- Общеукрепляющие процедуры. Для устранения астенических проявлений, легкой неврологической симптоматики (двигательных нарушений, головокружений) назначается массаж, лечебная физическая культура, лечебные ванны. Показан прием витаминов, аминокислот.
Прогноз и профилактика
Исход лечения травматической энцефалопатии зависит от глубины поражения мозга, характера восстановления. Положительный прогноз наиболее вероятен при своевременном лечении, периодическом повторении курсов, а также при сохранности общего здоровья – ведении здорового образа жизни, отсутствии хронических заболеван ий, вредных привычек. Основной профилактической мерой является качественное комплексное лечение ЧМТ в остром периоде. Рекомендуется избегать повторных травм (приостановить занятия спортом, ведение службы) в период восстановления, отказаться от употребления алкоголя и табака.
Черепно-мозговая травма — Диагностика и лечение
Диагноз
При черепно-мозговой травме возможны неотложные состояния. В случае более тяжелой ЧМТ последствия могут быстро ухудшиться без лечения. Врачам или службам быстрого реагирования необходимо быстро оценить ситуацию.
Шкала комы Глазго
Этот тест из 15 пунктов помогает врачу или другому персоналу скорой медицинской помощи оценить исходную тяжесть черепно-мозговой травмы, проверяя способность человека следовать указаниям и двигать глазами и конечностями.Связность речи также дает важные подсказки.
Способности оцениваются от трех до 15 по шкале комы Глазго. Более высокие баллы означают менее серьезные травмы.
Информация о травме и симптомах
Если вы видели, как кто-то получил травму или прибыл сразу после травмы, вы можете предоставить медицинскому персоналу информацию, которая будет полезна для оценки состояния пострадавшего.
При оценке степени тяжести травмы могут быть полезны ответы на следующие вопросы:
- Как произошла травма?
- Человек потерял сознание?
- Как долго человек находился без сознания?
- Наблюдали ли вы какие-либо другие изменения активности, речи, координации или другие признаки травмы?
- Где был нанесен удар головой или другими частями тела?
- Можете ли вы предоставить какую-либо информацию о силе травмы? Например, что ударило человека по голове, как далеко он упал или его выбросило из машины?
- Тело человека развинчивали или сильно травмировали?
Визуализирующие тесты
- Компьютерная томография (КТ). Этот тест обычно выполняется первым в отделении неотложной помощи при подозрении на черепно-мозговую травму. Скан CT использует серию рентгеновских лучей для создания детального изображения мозга. Сканер CT может быстро визуализировать переломы и выявить признаки кровотечения в головном мозге (кровоизлияние), сгустки крови (гематомы), ушибы мозговой ткани (ушибы) и отек ткани головного мозга.
- Магнитно-резонансная томография (МРТ). MRI использует мощные радиоволны и магниты для создания детального изображения мозга.Этот тест можно использовать после того, как состояние человека стабилизируется или если симптомы не улучшатся вскоре после травмы.
Монитор внутричерепного давления
Набухание ткани в результате черепно-мозговой травмы может увеличить давление внутри черепа и вызвать дополнительное повреждение головного мозга. Врачи могут ввести зонд через череп, чтобы контролировать это давление.
Лечение
Лечение зависит от тяжести травмы.
Легкая травма
Легкие черепно-мозговые травмы обычно не требуют лечения, кроме отдыха и безрецептурных обезболивающих.Тем не менее, за человеком с легкой черепно-мозговой травмой обычно необходимо внимательно следить дома на предмет наличия любых стойких, ухудшающихся или новых симптомов. Он или она также могут посещать врача для последующего наблюдения.
Врач укажет, когда уместно вернуться к работе, учебе или отдыху. Относительный отдых — что означает ограничение физической или мыслительной (когнитивной) активности, которая усугубляет ситуацию — обычно рекомендуется в течение первых нескольких дней или до тех пор, пока ваш врач не посоветует возобновить регулярную деятельность.Не рекомендуется полностью отдыхать от умственной и физической активности. Большинство людей постепенно возвращаются к обычному распорядку дня.
Неотложная неотложная помощь
Неотложная помощь при черепно-мозговой травме средней и тяжелой степени направлена на обеспечение достаточного количества кислорода и кровоснабжения, поддержание артериального давления и предотвращение дальнейших травм головы или шеи.
У людей с тяжелыми травмами могут быть и другие травмы, которые необходимо лечить.Дополнительное лечение в отделении неотложной помощи или отделении интенсивной терапии больницы будет направлено на минимизацию вторичных повреждений из-за воспаления, кровотечения или снижения поступления кислорода в мозг.
Лекарства
Лекарства, ограничивающие вторичное повреждение головного мозга сразу после травмы, могут включать:
Противосудорожные препараты. Люди, перенесшие черепно-мозговую травму средней или тяжелой степени тяжести, подвержены риску судорог в течение первой недели после травмы.
Противосудорожное лекарство может быть дано в течение первой недели, чтобы избежать дополнительного повреждения мозга, которое может быть вызвано припадком. Продолжение противосудорожного лечения используется только в случае возникновения припадков.
- Лекарства, вызывающие кому. Врачи иногда используют лекарства, чтобы ввести людей во временную кому, потому что коматозному мозгу для нормальной работы требуется меньше кислорода. Это особенно полезно, если кровеносные сосуды, сжатые из-за повышенного давления в головном мозге, не могут снабжать клетки мозга нормальным количеством питательных веществ и кислорода.
- Мочегонные средства. Эти препараты уменьшают количество жидкости в тканях и увеличивают диурез. Диуретики, вводимые внутривенно людям с черепно-мозговой травмой, помогают снизить давление внутри мозга.
Хирургия
Может потребоваться экстренная операция, чтобы минимизировать дополнительное повреждение тканей головного мозга. Хирургия может быть использована для решения следующих проблем:
- Удаление свернувшейся крови (гематом). Кровотечение снаружи или внутри мозга может привести к скоплению свернувшейся крови (гематоме), которая оказывает давление на мозг и повреждает ткани мозга.
- Ремонт переломов черепа. Операция может потребоваться для восстановления серьезных переломов черепа или для удаления фрагментов черепа в головном мозге.
- Кровотечение в мозгу. Травмы головы, вызывающие кровотечение в мозг, могут потребовать хирургического вмешательства, чтобы остановить кровотечение.
- Открытие окна в черепе. Хирургическое вмешательство может использоваться для снятия давления внутри черепа путем слива скопившейся спинномозговой жидкости или создания окна в черепе, которое дает больше места для опухших тканей.
Реабилитация
Большинству людей, получивших серьезную черепно-мозговую травму, потребуется реабилитация. Возможно, им потребуется заново освоить базовые навыки, такие как ходьба или разговор. Цель состоит в том, чтобы улучшить свои способности выполнять повседневную деятельность.
Терапия обычно начинается в больнице и продолжается в стационарном реабилитационном отделении, лечебном учреждении по месту жительства или в амбулаторных условиях. Тип и продолжительность реабилитации у всех разная, в зависимости от тяжести черепно-мозговой травмы и того, какая часть головного мозга была повреждена.
В число специалистов по реабилитации могут входить:
- Физиатр, врач, обученный физической медицине и реабилитации, который наблюдает за всем процессом реабилитации, решает проблемы медицинской реабилитации и назначает необходимые лекарства
- Трудотерапевт, , который помогает человеку учиться, переучиваться или совершенствовать навыки для выполнения повседневных дел
- Физиотерапевт, , который помогает с мобильностью и повторным обучением моделей движений, равновесия и ходьбы
- Логопед, , который помогает человеку улучшить коммуникативные навыки и при необходимости использовать вспомогательные коммуникационные устройства
- Нейропсихолог, , который оценивает когнитивные нарушения и работоспособность, помогает человеку управлять поведением или изучать стратегии выживания, а также предоставляет психотерапию, необходимую для эмоционального и психологического благополучия
- Социальный работник или ведущий дела, , который облегчает доступ к сервисным агентствам, помогает в принятии решений и планировании ухода, а также способствует общению между различными профессионалами, поставщиками ухода и членами семьи
- Медсестра-реабилитолог, , которая оказывает постоянную реабилитационную помощь и услуги, а также помогает с планированием выписки из больницы или реабилитационного учреждения
- Медсестра, специалист по черепно-мозговой травме, , которая помогает координировать уход и информирует семью о травмах и процессе восстановления
- Рекреационный терапевт, , который помогает с организацией рабочего времени и проведения досуга
- Консультант по профессиональному обучению, , который оценивает способность вернуться к работе и соответствующие возможности профессионального обучения, а также предоставляет ресурсы для решения общих проблем на рабочем месте
Клинические испытания
Изучите исследования клиники Mayo Clinic, в которых тестируются новые методы лечения, вмешательства и тесты как средства предотвращения, обнаружения, лечения или контроля этого состояния.
Помощь и поддержка
Ряд стратегий может помочь человеку с черепно-мозговой травмой справиться с осложнениями, которые влияют на повседневную деятельность, общение и межличностные отношения. В зависимости от тяжести травмы родственнику или другу может потребоваться помощь в реализации следующих подходов:
- Присоединяйтесь к группе поддержки. Поговорите со своим врачом или реабилитологом о группе поддержки, которая может помочь вам обсудить проблемы, связанные с вашей травмой, узнать новые стратегии выживания и получить эмоциональную поддержку.
- Запишите вещи. Записывайте важные события, имена людей, задачи или другие вещи, которые трудно запомнить.
- Следуйте установленному порядку. Соблюдайте постоянный график, храните вещи в специально отведенных местах, чтобы избежать путаницы, и выбирайте одни и те же маршруты, отправляясь в часто посещаемые места.
- Делайте перерывы. Организуйте на работе или учебе перерывы по мере необходимости.
- Измените рабочие ожидания или задачи. Соответствующие изменения на работе или в школе могут включать в себя чтение инструкций, выделение большего количества времени для выполнения задач или разбиение задач на более мелкие этапы.
- Не отвлекайтесь. Сведите к минимуму отвлекающие факторы, такие как громкий фоновый шум от телевизора или радио.
- Оставайтесь сосредоточенными. Работайте над одной задачей за раз.
4 февраля 2021 г.
Реабилитация после черепно-мозговой травмы
Черепно-мозговая травма (ЧМТ) возникает, когда внезапная травма вызывает повреждение вашего мозга.«Закрытая черепно-мозговая травма» может вызвать повреждение мозга, если что-то сильно ударит вас по голове, но не пробьет череп. «Проникающая травма головы» возникает, когда предмет пробивает череп и попадает в мозг.
Симптомы, которые могут возникнуть после ЧМТ, могут включать:- Головные боли
- Головокружение
- Путаница
- Судороги
- Нарушение координации
- Невнятная речь
- Плохая концентрация
- Проблемы с памятью
- Изменения личности
Если у вас была ЧМТ, реабилитация (или реабилитация) будет важной частью вашего выздоровления. Реабилитация может принимать разные формы в зависимости от ваших потребностей и может включать физическую, профессиональную и логопедическую терапию, а также психиатрическую помощь и социальную поддержку. Все они призваны помочь вам в максимально возможной степени оправиться от последствий травмы.
Почему мне может потребоваться реабилитация после черепно-мозговой травмы?
Реабилитация может помочь:
Повысьте свою способность функционировать дома и в сообществе
Помощь в лечении психических и физических проблем, вызванных ЧМТ
Оказывать социальную и эмоциональную поддержку
Помогает адаптироваться к изменениям, которые происходят во время восстановления
Rehab также может помочь предотвратить осложнения ЧМТ, такие как:
Сгустки крови
Боль
Пролежни, также называемые пролежнями
Проблемы с дыханием и пневмония
Падение артериального давления при движении
Мышечная слабость и мышечный спазм
Проблемы с кишечником и мочевым пузырем
Проблемы репродуктивной и сексуальной функции
Каковы риски реабилитации после черепно-мозговой травмы?
Реабилитация после ЧМТ вряд ли вызовет проблемы.Но всегда существует риск того, что некоторые части лечения, такие как физиотерапия или трудотерапия, могут привести к новым травмам или усугубить существующие симптомы или травмы, если не будут выполнены должным образом.
Вот почему так важно работать в тесном контакте со специалистом по реабилитации, который примет меры для предотвращения проблем. Но они все же могут случиться. Обязательно обсудите любые проблемы со своим врачом перед реабилитацией.
Как подготовиться к реабилитации после черепно-мозговой травмы?
Прежде чем вы сможете начать реабилитацию, вы должны получить помощь и лечение в связи с ранними последствиями ЧМТ.Это может включать:
Неотложная помощь при травмах головы и других травмах
Центр интенсивной терапии
Операция по восстановлению черепно-мозговой травмы
Выздоровление в больнице
Перевод в реабилитационный стационар
Что происходит во время реабилитации после черепно-мозговой травмы?
Потребности и способности каждого человека после ЧМТ различны.У вас будет программа реабилитации, разработанная специально для вас. В вашей программе, вероятно, будут участвовать многие типы поставщиков медицинских услуг. Важно, чтобы у вас был один центральный человек, с которым можно было бы поговорить. Этого человека часто называют координатором вашего дела.
Со временем ваша программа, скорее всего, изменится по мере изменения ваших потребностей и возможностей.
Реабилитация может проходить в различных условиях. Вы, координатор по вашему делу, и ваша семья должны выбрать наиболее подходящую для вас обстановку. Возможные настройки:
Стационар реабилитации
Амбулаторно-реабилитационный стационар
Реабилитация на дому
Комплексная дневная программа
Автономный жилой комплекс
Ваша индивидуальная программа может включать любое или все из этих процедур:
У вас есть много вариантов реабилитационной терапии, и тип реабилитационной терапии, в которой вы нуждаетесь, будет определен вашей медицинской бригадой.Ваша группа по уходу оценит ваши потребности и возможности. Эта оценка может включать:
Контроль кишечника и мочевого пузыря
Способность к речи
Глотание
Сила и координация
Способность понимать язык
Психическое и поведенческое состояние
Потребности в социальной поддержке
Что происходит после реабилитации после черепно-мозговой травмы?
Как долго длится ваша реабилитация и сколько последующего ухода вам понадобится после, зависит от того, насколько серьезным было повреждение вашего мозга и насколько хорошо вы реагируете на терапию.Некоторые люди могут вернуться к тому же уровню способностей, который они имели до ЧМТ. Другим нужен пожизненный уход.
Некоторые долгосрочные последствия ЧМТ могут проявиться спустя годы. Вы можете подвергаться более высокому риску в долгосрочной перспективе таких заболеваний, как болезнь Паркинсона, болезнь Альцгеймера и другие формы деменции.
После реабилитации вам могут дать следующие инструкции:
Симптомы и признаки, по которым вам следует позвонить своему врачу по номеру
Ожидаемые симптомы и признаки
Советы по безопасности и уходу за собой
Консультации по вопросам употребления алкоголя и наркотиков
Ресурсы поддержки сообщества доступны для вас
Вашему основному лечащему врачу должны быть предоставлены все записи и рекомендации вашей терапевтической бригады, чтобы гарантировать, что вы и дальше будете получать надлежащее лечение.
Следующие шаги
Перед тем, как согласиться на тест или процедуру, убедитесь, что вы знаете:
Название теста или процедуры
Причина, по которой вы проходите тест или процедуру
Какие результаты ожидать и что они означают
Риски и преимущества теста или процедуры
Возможные побочные эффекты или осложнения
Когда и где вы должны пройти тест или процедуру
Кто будет проводить тест или процедуру и какова квалификация этого человека
Что бы произошло, если бы вы не прошли тест или процедуру
Любые альтернативные тесты или процедуры, о которых можно подумать
Когда и как вы получите результаты
Кому позвонить после теста или процедуры, если у вас возникнут вопросы или проблемы
Сколько вам придется заплатить за тест или процедуру
Хроническая травматическая энцефалопатия — NHS
Хроническая травматическая энцефалопатия (ХТЭ) — это прогрессирующее заболевание головного мозга, которое, как считается, вызывается повторяющимися ударами по голове и повторяющимися сотрясениями мозга.
Это особенно связано с контактными видами спорта, такими как бокс или американский футбол. Большинство доступных исследований основано на бывших спортсменах.
CTE ранее был известен как синдром «пьяного удара» и пугилистическое слабоумие. Но эти термины больше не используются, потому что теперь известно, что это состояние не ограничивается бывшими боксерами.
До сих пор ведутся споры о том, насколько распространен CTE и как его следует диагностировать.
В настоящее время доступны только поддерживающие методы лечения, и исследования сосредоточены на поиске надежных методов диагностики этого состояния.
Симптомы CTE
Симптомы CTE различаются у разных людей, но имеют тенденцию быть похожими на симптомы других типов дегенеративных состояний мозга, особенно болезни Альцгеймера.
CTE обычно начинается постепенно через несколько лет после получения повторяющихся ударов по голове или повторных сотрясений мозга.
Симптомы влияют на работу мозга и в конечном итоге приводят к слабоумию.
Типичные симптомы CTE включают:
- Кратковременная потеря памяти — например, несколько раз задавать один и тот же вопрос или трудности с запоминанием имен или номеров телефонов
- Изменения настроения, такие как частые перепады настроения, депрессия и усиление беспокойства, разочарования или возбуждения
- усиление замешательства и дезориентации — например, потеря, блуждание или незнание, какое сейчас время суток
- трудности с мышлением — например, затруднение принятия решений
По мере прогрессирования состояния могут появиться следующие симптомы:
- невнятная речь (дизартрия)
- значительные проблемы с памятью
- Паркинсонизм — типичные симптомы болезни Паркинсона, включая тремор, замедленность движений и жесткость мышц
- затруднения при приеме пищи или глотании (дисфагия) — хотя это случается редко
Узнайте больше о симптомах деменции
Причины CTE
Считается, что любая продолжительная деятельность, включающая повторяющиеся удары по голове или повторяющиеся эпизоды сотрясения мозга, увеличивает риск получения CTE.Но CTE и сотрясение мозга — это разные состояния.
У многих людей с сотрясением мозга не развивается CTE, но данные свидетельствуют о том, что повторяющиеся легкие травмы головы повышают риск.
Хотя точные причины до конца не изучены, считается, что определенные группы людей подвергаются наибольшему риску.
Сюда входят:
- спортсменов с повторяющимися легкими черепно-мозговыми травмами в анамнезе, особенно в контактных видах спорта, таких как бокс или боевые искусства, американский футбол, футбол (возможно, связанный с неоднократным подачей мяча головой) и регби
- военнослужащий-ветеран с повторными травмами головы, в том числе взрывными
- человек с историей повторных травм головы, включая членовредительство, жертв повторяющихся нападений или плохо контролируемую эпилепсию, которая приводит к повторным травмам головы
Когда обращаться за медицинской помощью
Если вы беспокоитесь о своей памяти, рекомендуется посетить терапевта.
Если вы беспокоитесь о ком-то другом, вам следует побудить его записаться на прием и, возможно, предложить вам пойти вместе с ним.
Проблемы с памятью вызваны не только слабоумием. Они также могут быть вызваны:
Ваш терапевт может провести несколько простых проверок, чтобы попытаться выяснить, в чем может быть причина, и при необходимости он может направить вас в специализированную клинику памяти для дополнительных анализов.
Прочтите о том, когда обращаться за медицинской помощью по поводу симптомов сотрясения мозга и симптомов легкой травмы головы.
Диагностика CTE
В настоящее время нет тестов для диагностики CTE. Диагноз основывается на истории участия в контактных видах спорта, а также на симптомах и клинических особенностях.
Ваш терапевт расскажет вам о проблемах, с которыми вы сталкиваетесь, и может попросить вас выполнить некоторые простые умственные или физические задачи, например, передвигаться или ходить.
Они могут направить вас в специализированную службу оценки памяти, в которой работают специалисты по диагностике, уходу и консультированию людей с деменцией и их семей.
ПерсоналMemory Clinic может выслушать ваши опасения, оценить ваши навыки и, при необходимости, назначить дополнительные тесты, чтобы исключить другие заболевания.
Сканирование мозга
При КТР изменения в головном мозге не всегда обнаруживаются при обычном сканировании мозга или могут быть похожи на другие состояния.
Это означает, что единственный способ подтвердить CTE — провести вскрытие после смерти человека с этим заболеванием.
Исследования показали, что изменения в мозге, связанные с CTE, отличаются от изменений, наблюдаемых при болезни Альцгеймера.
Но оба состояния связаны с сокращением мозга (атрофией) и наличием нейрофибриллярных клубков, содержащих белок, называемый тау.
Наиболее широко используемыми тестами для исследования нейродегенеративных расстройств являются МРТ и КТ.
Исследования продолжаются, чтобы определить, смогут ли другие методы визуализации мозга помочь в диагностике CTE в будущем.
Подробнее о:
Обработка CTE
Как и многие другие типы деменции, лечение CTE основано на поддерживающей терапии.
Если у вас было диагностировано это заболевание, медицинские работники, такие как ваш терапевт или специалист, и службы социального обеспечения (обычно ваш местный совет, работающий с NHS) обычно будут участвовать в составлении и проведении долгосрочного ухода. план.
Вы также можете обратиться к логопеду или лингвисту или эрготерапевту.
Узнайте больше о планах по уходу за долгосрочными заболеваниями
Руководство NHS по деменции предоставляет подробную информацию для людей с деменцией и их семей, в том числе:
Вам также может быть полезно связаться с местной или национальной группой поддержки больных болезнью Альцгеймера или деменции, такой как Общество Альцгеймера или Dementia UK, для получения дополнительной информации и совета.
Предотвращение CTE
Единственный способ предотвратить CTE — это избегать повторяющихся травм головы. Хотя многие травмы головы сложно предсказать или избежать, есть вещи, которые можно предпринять, чтобы снизить риск.
Например:
- носить рекомендованное защитное снаряжение во время контактных видов спорта
- следуйте рекомендациям врача по возвращению в игру после сотрясения мозга
- убедитесь, что любой контактный вид спорта, в котором вы или ваш ребенок принимаете участие, находится под наблюдением квалифицированного и обученного человека.
- получить медицинскую консультацию, если какие-либо симптомы предыдущей травмы головы вернутся
Узнайте больше о предотвращении сотрясения мозга
Последняя проверка страницы: 17 апреля 2019 г.
Срок следующей проверки: 17 апреля 2022 г.
Хроническая травматическая энцефалопатия (ХТЭ) | Симптомы и лечение
Хроническая травматическая энцефалопатия (ХТЭ) — прогрессирующее и смертельное заболевание головного мозга, связанное с повторными черепно-мозговыми травмами (ЧМТ), включая сотрясения мозга и неоднократные удары по голове.Это также связано с развитием деменции. Исследования показали, что люди, перенесшие ЧМТ в раннем и среднем возрасте, в два-четыре раза больше подвержены риску развития деменции в позднем возрасте. Этот риск, по-видимому, намного выше у людей с несколькими ЧМТ, хотя для подтверждения этого необходимы дополнительные исследования.
Что вызывает CTE?
Наибольшему риску CTE подвержены спортсмены, занимающиеся контактными видами спорта (например, боксеры, футболисты и т. Д.), И ветераны вооруженных сил, вероятно, из-за их повышенных шансов выдержать повторяющиеся удары по голове.
Симптомы
Исследования по диагностике CTE, причинам, симптомам и факторам риска все еще находятся на начальной стадии. Не все ученые согласны с симптомами CTE, но это заболевание связано с:
- Проблемы с памятью и мышлением
- путаница
- изменения личности
- и / или беспорядочное поведение, включая агрессию, депрессию и даже суицидальные мысли.
Диагностика
Диагноз CTE может быть поставлен только после смерти, когда вскрытие может показать, присутствуют ли известные изменения CTE в головном мозге. При подозрении на CTE для исключения других причин можно использовать тщательный сбор анамнеза, тестирование психического статуса, неврологические осмотры, визуализацию мозга и многое другое. Как и болезнь Альцгеймера, CTE включает в себя тау, белок нервных клеток, связанный с деменцией.Однако исследователи обнаружили, что CTE имеет уникальный паттерн аномального накопления тау-белка в тканях вокруг кровеносных сосудов, который отличается от других заболеваний мозга, связанных с тау-белком, включая болезнь Альцгеймера. Поскольку сейчас доступны более совершенные методы визуализации, исследования начинают показывать, что CTE отличается от болезни Альцгеймера. Необходимы дополнительные исследования, чтобы полностью понять изменения мозга, происходящие при CTE, и их связь
слабоумие.
Лечение
Нет лекарства или лечения CTE, но некоторые лекарства могут использоваться для временного лечения когнитивных (память и мышление) и поведенческих симптомов.Проконсультируйтесь с врачом, прежде чем принимать какие-либо лекарства, отпускаемые по рецепту или без рецепта.
Исследования
Несколько организаций, в том числе Национальный институт неврологических расстройств и инсульта, а также научно-исследовательский институт травм головного мозга, инвестируют в исследовательские инициативы, чтобы узнать больше о CTE. Ассоциация Альцгеймера также инвестировала более 2 миллионов долларов в исследовательские гранты, чтобы узнать больше о CTE.
Хроническая травматическая энцефалопатия (ХТЭ)
Обзор
Что такое хроническая травматическая энцефалопатия?
Хроническая травматическая энцефалопатия (ХТЭ) обычно рассматривается как прогрессирующее (постепенно нарастающее) дегенеративное (ухудшающееся) состояние мозга, связанное с повторяющимися ударами по голове в течение длительного периода времени.Это заболевание было обнаружено у спортсменов, занимающихся контактными видами спорта, у военнослужащих, подвергшихся повторяющимся взрывным травмам, и даже у жертв домашнего насилия. Это повреждение мозга вызывает изменения в мышлении, личности, настроении и поведении человека.
Кто подвержен риску хронической травматической энцефалопатии?
Люди, перенесшие повторную травму головы, подвержены риску CTE. В данную группу входят:
- Боксеры и борцы
- Спортсмены, занимающиеся контактными видами спорта, такими как футбол, хоккей и футбол
- Военнослужащие
CTE также был зарегистрирован у людей, страдающих эпилепсией, и у жертв домашнего насилия.
Симптомы и причины
Каковы симптомы хронической травматической энцефалопатии?
Симптомы CTE могут появиться только через много лет после травмы мозга. Некоторые симптомы аналогичны симптомам других дегенеративных состояний мозга, таких как болезнь Альцгеймера и болезнь Паркинсона.
Симптомы CTE могут включать:
- Головные боли
- Потеря памяти
- Импульсивное поведение
- Изменения личности
- Проблемы с ясным мышлением
- Трудности равновесия и передвижения
Изменения личности, связанные с CTE, такие как депрессия и агрессия, могут быть трудными для некоторых людей.Эти чувства иногда приводят к осложнениям, включая несчастные случаи, злоупотребление наркотиками и алкоголем и самоубийство.
Что вызывает хроническую травматическую энцефалопатию?
Повторяющиеся удары головой могут повредить волокна, проходящие через мозг, и повредить сами клетки мозга. Это может быть связано с накоплением белка, известного как тау, который может играть роль в гибели клеток. Утрата этих клеток может нарушить нормальную работу мозга, вызывая неврологические изменения, в том числе потерю памяти, депрессию, агрессивность, а также проблемы с балансом и движением.
Возможно, несколько типов травм головы могут привести к накоплению тау в головном мозге, в том числе:
Неизвестно, сколько травм головы или каких именно видов необходимо для развития CTE.
Диагностика и тесты
Как диагностируется хроническая травматическая энцефалопатия (ХТЭ)?
CTE может быть окончательно диагностирован только при вскрытии после смерти человека. Врач изучит личную историю и проанализирует ткань мозга умерших людей, у которых проявились симптомы этого состояния.Определенный образец белка тау в головном мозге может подтвердить диагноз.
Исследователи работают над разработкой диагностических тестов для официальной идентификации CTE, пока люди еще живы.
Ведение и лечение
Как лечится хроническая травматическая энцефалопатия (ХТЭ)?
Поскольку CTE может быть диагностирован только после смерти человека, лечение может быть сложной задачей. Лечение людей с симптомами CTE включает:
- Поведенческая терапия при перепадах настроения
- Обезболивающая терапия, включая лекарства, массаж и иглоукалывание для снятия дискомфорта
- Упражнения на память для усиления способности вспоминать повседневные события
Люди, которые узнают, как справляться с симптомами CTE, часто имеют лучшее качество жизни, в том числе меньше боли, улучшенную память и меньше перепадов настроения.
Профилактика
Можно ли предотвратить хроническую травматическую энцефалопатию (ХТЭ)?
Вы можете снизить риск CTE, уменьшив количество ударов по голове. Правильный уход за травмой головного мозга, когда она возникает, также может помочь предотвратить заболевание. Для спортсменов это означает выход из игры после травмы головы, отдых и соблюдение правил «вернуться в игру».
Перспективы / Прогноз
Каковы перспективы для людей с хронической травматической энцефалопатией (ХТЭ)?
Многие люди с признаками CTE живут здоровой и полноценной жизнью.Регулярные упражнения и правильное питание могут помочь справиться с симптомами, включая боль и стресс.
Люди могут использовать множество стратегий, чтобы справиться с поведенческими симптомами, связанными с CTE. К ним относятся следующие:
- Установите распорядок дня. Создание ежедневной структуры помогает жизни чувствовать себя более стабильной.
- Делайте заметки. Записывание помогает бороться с проблемами памяти.
- Управляйте чувствами. Такие методы релаксации, как глубокое дыхание, помогают контролировать эмоции.
- Обратитесь за помощью.Делитесь проблемами с друзьями и семьей, чтобы облегчить нагрузку. Иногда в лечении симптомов может быть очень полезно профессиональное консультирование.
Часто задаваемые вопросы о CTE
Что такое CTE?
Хроническая травматическая энцефалопатия (ХТЭ) — прогрессирующее дегенеративное заболевание головного мозга, обнаруживаемое у людей с повторяющимися травмами головного мозга в анамнезе (часто у спортсменов), включая симптоматические сотрясения мозга, а также бессимптомные бессимптомные удары по голове, которые не вызывают симптомов.CTE, как известно, влияет на боксеров с 1920-х годов (когда это первоначально называлось синдромом пьянства от удара или боевым слабоумием).
В последние годы были опубликованы отчеты о невропатологически подтвержденном CTE, обнаруженном у других спортсменов, включая футболистов и хоккеистов (играющих и вышедших на пенсию), а также у ветеранов вооруженных сил, у которых в анамнезе повторялись травмы мозга. CTE не ограничивается действующими профессиональными спортсменами; он также был обнаружен у спортсменов, которые не занимались спортом после школы или колледжа.
Повторяющаяся травма головного мозга вызывает прогрессирующую дегенерацию мозговой ткани, включая накопление аномального белка, называемого тау. Эти изменения в головном мозге могут начаться через месяцы, годы или даже десятилетия после последней травмы мозга или окончания активных занятий спортом. Дегенерация мозга связана с общими симптомами CTE, включая потерю памяти, спутанность сознания, нарушение суждения, проблемы с импульсивным контролем, агрессию, депрессию, суицидальность, паркинсонизм и, в конечном итоге, прогрессирующую деменцию.
На обоих наборах фотографий ниже ткань мозга была иммуноокрашена на белок тау, который имеет темно-коричневый цвет. Иммуноокрашенные тау-белком срезы медиальной височной доли от 3 человек:
Как получить CTE? Могу ли я получить CTE от одного сотрясения мозга / удара в голову?
Мы полагаем, что CTE вызван повторяющейся травмой головного мозга. Эта травма включает в себя как сотрясение мозга, вызывающее симптомы, так и бессимптомные удары по голове.В настоящее время неизвестно количество или тип ударов по голове, необходимых для запуска дегенеративных изменений мозга. Кроме того, вполне вероятно, что другие факторы, такие как генетика, могут играть роль в развитии CTE, поскольку не у всех с историей повторных травм головного мозга развивается это заболевание. Однако эти другие факторы еще не изучены.
Что такое сотрясение мозга?
Сотрясение мозга происходило всякий раз, когда у вас был удар по голове, который вызывал симптомы в течение любого времени.Вам НЕ нужно терять сознание, чтобы получить сотрясение мозга. Эти симптомы включают нечеткость или двоение в глазах, видимость звезд, чувствительность к свету или шуму, головную боль, головокружение или проблемы с равновесием, тошноту, рвоту, проблемы со сном, усталость, спутанность сознания, трудности с запоминанием, трудности с концентрацией внимания или потерю сознания. Сотрясение мозга также происходит, когда человек слышит «звон» или «звонит в колокольчик».
Каковы симптомы CTE?
Симптомы CTE включают потерю памяти, спутанность сознания, нарушение суждения, проблемы с импульсивным контролем, агрессию, депрессию, тревогу, суицидальность, паркинсонизм и, в конечном итоге, прогрессирующую деменцию.Эти симптомы часто проявляются через годы или даже десятилетия после последней травмы головного мозга или прекращения активных занятий спортом.
У меня недавно было сотрясение мозга, и я страдаю рядом симптомов, перечисленных выше. У меня CTE?
Симптомы CTE обычно не проявляются в течение нескольких лет или десятилетий после травмы мозга или после прекращения активных занятий контактными видами спорта. Хотя большинство симптомов сотрясения мозга проходят в течение нескольких недель, симптомы могут длиться месяцами или, в тяжелых случаях, даже годами.Когда это происходит, это называется синдромом после сотрясения мозга. Постконтузионный синдром отличается от КТР, и симптомы постконтузивного синдрома обычно проходят за годы или десятилетия до появления симптомов КТР. Если вы считаете, что страдаете острым сотрясением мозга или постконтузионным синдромом, обратитесь к врачу. Для получения дополнительной информации о сотрясениях мозга посетите Ресурсы Сотрясения мозга Фонда сотрясения мозга. Для получения дополнительной информации о врачах в вашем районе, которые работают с людьми, страдающими травмами головного мозга, воспользуйтесь инструментом поиска Concussion Clinics.Если у меня симптомы CTE, болен ли я самим заболеванием?
Тот факт, что у вас есть некоторые или многие симптомы CTE, не обязательно означает, что у вас есть само заболевание. Есть много возможных причин таких симптомов. Если у вас возникли трудности, вам следует поговорить со своим лечащим врачом или врачом-специалистом.
Как диагностируется ХТР?
В настоящее время CTE может быть диагностирован только после смерти с помощью патологоанатомического анализа.В настоящее время нет известного способа использовать МРТ, КТ или другие методы визуализации мозга для диагностики ХТР. Центр CTE активно проводит исследования, направленные на то, чтобы научиться диагностировать CTE в течение жизни. Узнайте больше о нашем исследовании здесь.Могу ли я пройти обследование в центре BU CTE?
Центр BU CTE — исследовательская группа. На данный момент мы не предлагаем клинические услуги. Если вы хотите пройти клиническое обследование, лучший первый шаг — поговорить с лечащим врачом. Для получения дополнительной информации о врачах в вашем районе, которые работают с людьми, страдающими травмами головного мозга, воспользуйтесь инструментом поиска Concussion Clinics.Вы можете направить меня к врачу?
К сожалению, будучи небольшой исследовательской группой, CTE Center не может вести исчерпывающий список врачей по всей стране, знакомых с черепно-мозговой травмой и связанными с ней вопросами. Для получения дополнительной информации о врачах в вашем районе, которые работают с людьми, страдающими травмами головного мозга, воспользуйтесь инструментом поиска Concussion Clinics.Можно ли вылечить CTE? Что мне делать, если я думаю, что у меня CTE?
К сожалению, в настоящее время нет лекарства от CTE. Тем не менее, Центр CTE в настоящее время проводит текущие клинические исследования, направленные на выяснение того, как развивается и прогрессирует CTE, факторов риска развития заболевания и того, как диагностировать болезнь в течение жизни.Симптомы CTE, такие как депрессия и беспокойство, можно лечить индивидуально. Если вы считаете, что у вас или у вашего близкого может быть CTE, прочтите страницу «Жизнь с CTE» и поговорите со своим врачом. Для получения дополнительной информации о врачах в вашем районе, которые работают с людьми, страдающими травмами головного мозга, воспользуйтесь инструментом поиска Concussion Clinics.В чем разница между CTE и болезнью Альцгеймера (AD)?
Хотя есть некоторые сходства между CTE и болезнью Альцгеймера (AD), существуют значительные различия.Симптомы CTE обычно проявляются раньше (в возрасте 40 лет), чем симптомы AD (в возрасте 60 лет). Первоначальные и наиболее важные симптомы AD включают проблемы с памятью, в то время как первые симптомы CTE обычно включают проблемы с суждением, рассуждением, решением проблем, контролем над импульсами и агрессией. Кроме того, обнаружено, что эти заболевания различаются по посмертным невропатологическим данным.
Чем я могу помочь / как я могу принять участие в исследованиях?
Для получения дополнительной информации о текущих клинических исследованиях CTE Center ознакомьтесь с нашим исследованием LEGEND.Центр CTE также имеет банк головного мозга, который изучает посмертные ткани головного и спинного мозга, чтобы лучше понять последствия повторных травм головного мозга. Действующие и бывшие спортсмены и военнослужащие всех возрастов и уровней могут иметь право пообещать пожертвовать свой мозг (добавлена ссылка к обещанию) и спинной мозг Центру BU CTE после смерти. Донорство мозга похоже на донорство органов, и процедура проводится таким образом, что при желании у донора может быть открытая шкатулка. Персонал центра BU CTE понимает, что это тяжелое время для семьи донора, и прилагает все усилия, чтобы сделать процесс донорства максимально простым для семьи.Для получения дополнительной информации посетите наш Реестр пожертвований мозга.Должен ли я быть спортсменом-любителем или профессионалом высокого уровня, чтобы участвовать в вашем исследовании?
Нет. Центр CTE приглашает спортсменов всех видов спорта и уровней принять участие в нашем исследовании. Хотя некоторые исследования ограничиваются определенными видами спорта и уровнями, другие исследования открыты для всех, кто имеет опыт участия в организованных видах спорта или военной службе.
Могу ли я участвовать в Реестре пожертвований мозга?
Если у вас есть история участия в организованных видах спорта и / или история участия в армии, вы можете иметь право участвовать в реестре донорства мозга.Для получения дополнительной информации, пожалуйста, свяжитесь с координатором реестра донорских мозгов Мэдлин Урецки по телефону 617-358-6027 или по электронной почте [email protected].По вопросам, связанным с регистрационной карточкой донорства мозга, обращайтесь к Келли Дин из Фонда наследия сотрясения мозга по телефону 857-244-0810 или [email protected]
Могу ли я принять участие в исследовании LEGEND?
Если у вас есть история участия в организованных видах спорта, вы можете иметь право участвовать в исследовании LEGEND.Для получения дополнительной информации свяжитесь с координатором исследования LEGEND по электронной почте [email protected].Понимание нейродегенерации после черепно-мозговой травмы: от механизмов до клинических испытаний при деменции
Введение
Травматическая черепно-мозговая травма (ЧМТ) является ведущей причиной смерти и инвалидности во всем мире с различными долгосрочными исходами у выживших. Личные и общественные издержки высоки, их общая стоимость во всем мире оценивается в 400 миллиардов долларов: 0,5% от всего годового мирового производства.1 2 s1 Раньше считалось, что ЧМТ вызывает статический неврологический инсульт. Однако теперь ясно, что это может вызвать прогрессирующую нейродегенерацию и деменцию. Когнитивные нарушения, такие как потеря памяти, проблемы со скоростью обработки информации и исполнительная дисфункция, являются обычными 3, 4 и у некоторых выживших наблюдается когнитивное снижение спустя долгое время после травмы, отчасти из-за развития деменции. 5-7 Долгосрочный риск деменции, по-видимому, повышен. после ЧМТ, ассоциация, которая является наиболее убедительной для болезни Альцгеймера (БА) и болезни Паркинсона (БП), 5 хотя существуют значительные проблемы в интерпретации распространенности посттравматической деменции.Связь между ЧМТ и деменцией имеет важные последствия для общественного здравоохранения. Предполагая, что кумулятивная заболеваемость ЧМТ в течение жизни составляет 10%, а относительный риск деменции увеличивается в 1,5–3 раза после травмы (см. Раздел «Сложности интерпретации эпидемиологических данных»), до 5–15% всех случаев деменции связаны с TBI.8
Клиническая диагностика посттравматической деменции остается сложной задачей. Это усугубляется различными определениями этого термина, при этом некоторые используют «посттравматическое слабоумие» для описания фиксированных посттравматических когнитивных нарушений.9 10 Напротив, мы предпочитаем зарезервировать термин для тех посттравматических когнитивных проблем, которые возникают в результате прогрессирующих нейродегенеративных патологий. Отделить прямые эффекты ЧМТ от эффектов медленно прогрессирующего нейродегенеративного процесса, используя только анамнез и обследование, сложно, а общепринятых клинических критериев для диагностики хронической травматической энцефалопатии (ХТЭ) не существует. Однако использование «нейродегенеративного» подхода к исследованию пациентов с хроническими проблемами после ЧМТ обещает прояснить диагностическую неопределенность и помочь в оценке новых методов лечения.Здесь мы рассматриваем доказательства того, что ЧМТ увеличивает риск развития деменции, кратко описываем механизмы, которые могут объяснить это, и обсуждаем методы оценки нейродегенерации в контексте ЧМТ (вставка 1). Доступен ряд биомаркеров, которые уже применялись при изучении других нейродегенеративных состояний. Подобный подход к ЧМТ может (1) улучшить диагностику отдельных пациентов; (2) помогают определить тип и дозу повреждения, достаточную для того, чтобы вызвать нейродегенерацию; (3) улучшить клинические испытания путем обогащения исследуемых популяций с целью выявления высоких уровней прогрессирующей нейродегенерации; и (4) обеспечить чувствительную меру потери нейронов, которую можно использовать в клинических испытаниях модифицирующих заболевание или нейропротекторных вмешательств.
Вставка 1Ключевые моменты: деменция после черепно-мозговой травмы
Травматическая черепно-мозговая травма (ЧМТ) связана с повышенным риском нейродегенеративного заболевания, включая болезнь Альцгеймера, болезнь Паркинсона и хроническую травматическую энцефалопатию.
Риск деменции от всех причин увеличивается примерно в 1,5 раза, и, по оценкам, около 5% всех случаев деменции во всем мире могут быть связаны с ЧМТ.
Систематическое использование нейровизуализации и измерения биомаркеров нейродегенерации позволит определять эндофенотипы посттравматической деменции.
Прогрессирующая нейродегенерация является обычным явлением после ЧМТ и может быть идентифицирована с помощью МРТ и позитронно-эмиссионной томографии (ПЭТ), а также биомаркеров жидкости, таких как свет нейрофиламентов.
Регулирующие органы все чаще соглашаются с тем, что биомаркеры, такие как частота атрофии головного мозга, являются действительными конечными точками испытаний при предсимптомной болезни Альцгеймера.
Существует терапевтическая возможность вмешаться после ЧМТ до того, как произойдет значительная нейродегенерация, и есть веские причины полагать, что лечение следует первоначально оценивать с учетом биомаркеров, таких как атрофия мозга, а не клинических конечных точек.
Опытные популяции в этой пресимптоматической группе могут быть обогащены на основе биомаркеров аксонального повреждения и нейродегенерации, включая визуализацию тензора диффузии, уровни нейрофиламентов в крови или результаты ПЭТ-сканирования с положительным амилоидом.
Насколько распространено слабоумие после травмы головы?
Деменция всех подтипов
Эпидемиологические данные связывают травму головы с повышенным риском деменции (таблица 1). Недавний метаанализ более двух миллионов человек показал ~ 1.В 6 раз выше риск развития деменции после черепно-мозговой травмы.5 В метаанализе в начале 2015 г., включающем 22 исследования случай-контроль и 8 когортных исследований, сообщалось об относительном риске деменции после ЧМТ в 1,18 раза, но это не достигло статистической значимости (95% ДИ От 0,97 до 1,39). s2 Как ни странно, учитывая большую степень тяжести, те, кто потерял сознание после травмы, не показали повышенного риска деменции в самом последнем метаанализе; это может отражать относительно небольшое количество участников в этой подгруппе.Однако с тех пор в нескольких очень крупных регистровых исследованиях были воспроизведены основные результаты, связывающие травму головы с деменцией. В Финском реестре медицинской помощи было зарегистрировано 0,5 миллиона человеко-лет и показано соотношение доза-реакция между ЧМТ и нейродегенеративным заболеванием: умеренно-тяжелая ЧМТ имела в 1,8 раза больший риск деменции по сравнению с легкой ЧМТ11.
Таблица 1Ключевые исследования, обобщающие взаимосвязь ЧМТ и нейродегенеративного заболевания
Единичная легкая ЧМТ также была связана с повышенным риском деменции, хотя доказательства менее ясны, чем для более тяжелых травм.Систематический обзор 2014 года, посвященный оценке риска деменции после легкой ЧМТ, обнаружил только одно исследование достаточного качества, чтобы оправдать включение, и не сообщил об общем эффекте. s3 Однако с тех пор было опубликовано несколько исследований с другим выводом. Например, недавнее крупное исследование показало удвоение риска деменции после тяжелых травм, а также увеличение в 1,6 раза после легкой ЧМТ6. большие исследования.6 7 Эти результаты были воспроизведены в военном исследовании почти 200 000 ветеранов США с ЧМТ, где ЧМТ различной степени тяжести были связаны с повышенным риском последующего слабоумия, хотя другие исследователи не продемонстрировали такой связи.12 s4
Болезнь Альцгеймера
Относительный риск БА после ЧМТ был оценен в большом метаанализе как увеличенный примерно в 1,5 раза, 5 аналогично более ранним оценкам.13 14 Несколько более высокий риск наблюдался у пациентов, которые потерял сознание после ЧМТ.Однако несколько последующих более мелких исследований не смогли продемонстрировать такую связь. s5 s6 Ограничением многих исследований является отсутствие посмертного подтверждения диагноза БА. Однако исследователи BRAiNS из Кентукки («Биологически устойчивые взрослые в неврологических исследованиях») использовали патологоанатомические данные для 238 пациентов с ЧМТ и сообщили о более высоких показателях невропатологии БА у мужчин, но не у женщин с деменцией после травмы головы. -Риск развития тромбоэмболии у мужчин в обсервационных исследованиях.Дальнейшее исследование подтвержденных аутопсией случаев БА показало более раннее проявление симптомов и диагноз деменции через 3,6 года у пациентов с предшествующей ЧМТ.
Однако данные невропатологии противоречивы. В недавнем исследовании были описаны данные вскрытия около 450 пациентов с историей самооценки ЧМТ, включая потерю сознания. s7 Никакой взаимосвязи между историей TBI и невропатологией AD не наблюдалось, хотя патология TAR ДНК-связывающего белка 43 (TDP-43) чаще наблюдалась в группе с травмой головы.Показатели деменции в группе с ЧМТ были не выше, чем в контрольной популяции. Другое крупное исследование (n = 525) не показало увеличения патологии БА у пациентов, перенесших ЧМТ, хотя патология с тельцами Леви была увеличена.17 Оба исследования основывались на самооценке травмы головы. Это могло привести к получению необычной клинической выборки, поскольку клиническая часть (без невропатологии) исследования Crane et al (n = 7130) также не обнаружила увеличения клинически диагностированной деменции всех типов или БА, но обнаружила повышенный риск PD.
Болезнь Паркинсона
Риск БП повышается после однократной ЧМТ.17 18 Это может иметь место как при легкой, так и при умеренной / тяжелой ЧМТ, поскольку риск БП повышался в недавнем военном исследовании результатов после травм различной степени тяжести (n = 320 000) .19 Повторная ЧМТ легкой степени исторически ассоциировалась с паркинсонизмом в контексте спортивных травм, например, в боксе, что привлекало такие ярлыки, как «Punch Drunk» или «Dementia Pugilistica». Синдром не типичен для идиопатической БП, поскольку экстрапирамидные признаки часто сопровождаются выраженными пирамидными, мозжечковыми и психоневрологическими проблемами.В очень немногих современных исследованиях БП систематически изучалась связь с повторной ЧМТ легкой степени. Одно недавнее исследование, в котором приняли участие около 700 тайских традиционных боксеров, из которых только у 5 развилась болезнь Паркинсона, выявило повышенный риск, но только у тех, кто провел наибольшее количество профессиональных боев (> 100) за карьеру.20
Боковой амиотрофический склероз
Сообщается, что риск бокового амиотрофического склероза (БАС) незначительно повышается после однократной ЧМТ.21 Однако несколько последующих крупных исследований регистров не повторили это открытие. s8 s9 Что касается повторных травм, один метаанализ не показал повышенного риска БАС.21 Несколько небольших исследований сообщили о связи в контексте травм головы, связанных со спортом. Например, повышенные показатели БАС зарегистрированы у бывших футболистов, где риск был пропорционален продолжительности участия. s10–12 Об этой ассоциации у игроков Национальной футбольной лиги постоянно не сообщалось. s13 s14
Лобно-височная деменция
Ни один недавний метаанализ не описывает взаимосвязь между ЧМТ и лобно-височной деменцией (ЛВД).Небольшое количество исследований оценивали этот результат после единичной травмы и сообщают об увеличении ЧСС в диапазоне от ~ 1,5 до 4,5 раз в зависимости от тяжести травмы. Нет убедительных доказательств связи между легкой или повторной легкой ЧМТ и ЛВД. s15–19
Хроническая травматическая энцефалопатия
Несмотря на то, что CTE имеет отличительные нейропатологические особенности, в настоящее время не существует согласованных клинических диагностических критериев. Следовательно, распространенность этого состояния неизвестна. Нейропатологические исследования предполагают гетерогенный клинический фенотип, в значительной степени совпадающий с когнитивными и психиатрическими проблемами, непосредственно вызванными ЧМТ.22 Напротив, многие зарегистрированные случаи CTE на момент смерти протекают бессимптомно. 22 23 s20 Отсутствие отчетливого клинического фенотипа, связанного с невропатологически подтвержденными случаями CTE, делает особенно трудным отделить прямые эффекты TBI от эффектов, вызванных прогрессирующей нейродегенерацией, с помощью перекрестных исследований. Это мотивирует использование подробной продольной оценки пациентов с риском развития CTE с использованием нейродегенеративных подходов, которые мы описываем ниже.24 s21
Сложности интерпретации эпидемиологических данных
Несмотря на то, что появляется все больше доказательств связи между более тяжелой или повторной ЧМТ и деменцией по всем причинам / БА, существуют сложности в интерпретации многих исследований. Центральным вопросом является определение деменции. Неврологи обычно используют термин деменция для обозначения прогрессирующих когнитивных синдромов, предполагая прогрессирующую лежащую в основе нейродегенеративную патологию. Однако во многих диагностических руководствах, включая Международную классификацию болезней (МКБ) ВОЗ и Диагностическое и статистическое руководство по психическим расстройствам Американской психиатрической ассоциации, как прогрессирующие, так и статические когнитивные нарушения описываются как «деменция».9 10 Дальнейшая путаница возникает из-за использования синонима «нейрокогнитивное расстройство» в последних обновлениях. В контексте ЧМТ это означает, что пациент с фиксированным когнитивным дефицитом может быть классифицирован как страдающий посттравматической деменцией. Действительно, МКБ содержит специальный код для «слабоумия из-за травмы головы» (6D85), который относится к когнитивным проблемам из-за ЧМТ, которые «должны возникнуть сразу после травмы…» и не требуют прогрессирования когнитивных нарушений.
Это важный вопрос, так как пациенты часто имеют значительные когнитивные нарушения в результате травм.Существует также широкий спектр траекторий когнитивной функции после ЧМТ, и у большинства пациентов наблюдается спонтанное улучшение в первые месяцы после травмы (рис. 1). Эта неоднородность потенциально затрудняет интерпретацию эпидемиологических исследований ЧМТ. Например, в недавнем исследовании Nordström деменции после ЧМТ в Швеции использовался общий код МКБ (F03.9, «неуточненная деменция»), который включает как статические, так и прогрессирующие когнитивные нарушения. Ранний пик диагностики деменции вскоре после сообщения о ЧМТ (ОР ~ 3.5 ×), с длинным хвостом постоянно повышенного риска (1,25 × 30 лет после ЧМТ). Ранний пик, скорее всего, представляет прямые эффекты ЧМТ без вклада лежащей в основе нейродегенерации (рисунок 1A, зеленая траектория). Напротив, стойкое повышение риска через годы после травмы с большей вероятностью соответствует истинному увеличению риска деменции из-за прогрессирующей основной нейродегенерации (рисунок 1A, желтая траектория) .6 Подобные возможные затруднения возникают при рассмотрении повторных легких ЧМТ, когда каждая травма имеет различное спонтанное выздоровление, а также возможность спровоцировать длительное снижение, связанное с нейродегенерацией (рисунок 1B).По нашему мнению, термин «посттравматическая деменция» следует использовать для обозначения прогрессирующей невропатологии / клинического ухудшения, которое либо подозревается, либо подтверждается, например, при CTE, AD или PD.
Рисунок 1Возможные когнитивные траектории после черепно-мозговой травмы (ЧМТ). (A) Когнитивная функция в отношении одиночной тяжелой ЧМТ (черная стрелка). Заметное раннее ухудшение когнитивных функций, которое может полностью восстановиться (зеленый цвет), частично восстановиться, но впоследствии ухудшиться (прогрессирующая нейродегенерация, желтый цвет) или частично восстановиться, оставляя стойкое непрогрессирующее когнитивное нарушение (черный цвет).Дополнительная деталь траектории A2 (пунктирная рамка), иллюстрирующая, что общая когнитивная функция (желтый цвет) может зависеть от спонтанного восстановления (зеленый цвет) и нейродегенерации (оранжевый цвет). (B) Когнитивная функция в отношении повторяющейся ЧМТ легкой степени или «сотрясения мозга» (маленькие черные стрелки). Возможные траектории включают временное нарушение когнитивных функций, связанное с хорошим восстановлением и отсутствием прогрессирования (зеленый цвет) или позднюю прогрессирующую нейродегенерацию (желтый цвет). ЧМТ может сопровождаться неполным выздоровлением, без позднего прогрессирования (серый цвет) или с поздним прогрессирующим ухудшением (оранжевый цвет).
Еще одним ограничением многих эпидемиологических исследований является нехватка часто доступной клинической информации. Это проблематично, учитывая неоднородность ЧМТ, поскольку это делает невозможным формирование суждений о тяжести или связанных клинических особенностях ЧМТ. Исследования, основанные на самооценке ЧМТ, особенно подвержены путанице в этом отношении, поскольку систематическая ошибка воспоминаний в отношении воздействия травмы является серьезной проблемой.25
Генетические факторы модулируют нейродегенеративные исходы после ЧМТ, и изучение этой взаимосвязи в больших популяциях поможет понять, может ли у человека развиться деменция.Взаимосвязь между мутациями Rep1 и развитием болезни Паркинсона является информативным примером. Расширения в этой области промотора SNCA увеличивают экспрессию альфа-синуклеина и связаны с развитием PD. Два исследования случай – контроль (n> 500) не обнаружили взаимосвязи между ЧМТ и БП. Однако пациенты в этих исследованиях с длинными расширениями Rep1 показали повышенный риск БП (OR 3–5 ×) 26. Аналогичные отношения существуют и для других генетических факторов: статус аполипопротеина E (APOE) связан с неблагоприятными исходами после ЧМТ, 27 s22 и в сочетании с полигенными оценками риска могут предсказать значительную вариабельность нейродегенеративных исходов после ЧМТ. s23
Как ЧМТ вызывает хроническую нейродегенерацию?
Модели на животных и патологоанатомические исследования на людях выявили патологии аномального тау-белка, бета-амилоида и TDP-43 на ранних этапах после травм, которые могут сохраняться в течение месяцев или лет после ЧМТ. s24–26 Доказательства, относящиеся к ранним и поздним невропатологиям, наиболее развиты для амилоидов бета и тау, где животные модели показывают развитие патогенных протеоформ и их последующую эволюцию. Нейротоксичность этих патогенных белков (например, цис, -P-tau), непосредственно влияющая на потерю нейронов, наблюдаемую после повреждения, является потенциальной связью между острыми и хроническими изменениями после ЧМТ.28 Наряду с дегенерацией, подобной Валлерову, это может приводить к нейродегенерации и связанной с ней атрофии головного мозга, которые характерны для хронической фазы единичной тяжелой ЧМТ / ХТЭ.31
Аксональное повреждение является триггером посттравматических нейродегенеративных процессов (рис. 2А). Модели на животных и патологоанатомические исследования ЧМТ на людях показывают постепенную дегенерацию, подобную Валлерову, после травмы, помогая объяснить прогрессирующую атрофию белого вещества, которая характерна для хронической фазы после травмы. s28 s29 Кроме того, TBI может приводить к продукции высокопатогенных видов тау и бета-амилоида в поврежденном аксоне, при этом необходимы дальнейшие механистические исследования для выяснения точного значения повреждения аксонов в возникновении прогрессирующих протеинопатий у человека.29 31 32 s30 Сила сдвига, приложенная к цитоскелету во время травмы, вызывает микроструктурное повреждение и нарушает аксональный транспорт (рис. 2В) .31 В течение нескольких часов после травмы белок-предшественник амилоида и расщепляющие ферменты бета-секретаза 1 и пресенилин 1 накапливаются в варикозных узлах аксонов . Интранейрональный бета-амилоид продуцируется с более поздним накоплением внеклеточных бляшек.33 34 s31 Животные модели травм предполагают, что аналогичные силы сдвига могут приводить к диссоциации тау-белка из микротрубочек, что приводит к гиперфосфорилированию, агрегации и аберрантному процессингу (рис. 2В).31 Это может продуцировать высокопатогенную протеоформу тау ( цис, -P-tau), которая способствует апоптозу, повреждению митохондрий и ненормальной долгосрочной потенциации.32 s32 Остается установить, в какой степени эти механизмы лежат в основе спектра острых и хронических патологий, наблюдаемых у людей с ЧМТ.
Рисунок 2Острые невропатологии и хроническая нейродегенерация (A) Здоровый миелинизированный аксон до черепно-мозговой травмы (ЧМТ). В рамке показаны детали среднего сегмента аксона с центральными микротрубочками, окруженными тау-белком, с присутствующей интактной миелиновой оболочкой.(B) Острое повреждение аксона с демиелинизацией аксона (панели i и ii). Патология тау-белка и демиелинизация аксона: (i) повреждение аксона вызывает нарушение цитоскелета, диссоциацию тау-белка от микротрубочек и его накопление. Тау является аберрантно фосфорилированным и может распространяться по внеклеточным, парацеллюлярным, трансцеллюлярным и глимфатическим механизмам.31 Патология амилоида: (ii) повреждение аксонов вызывает образование луковиц аксонов / варикозного расширения вен. Белок-предшественник амилоида (АРР) накапливается ферментами расщепления бета-сайта ферментом расщепления АРР 1 (BACE-1) и пресенилином 1 (PS-1).В результате образуется бета-амилоид, который может распространяться на окружающие структуры после лизиса поврежденных нейронов. 34 Травматическое повреждение аксонов стимулирует местную воспалительную реакцию, включая активацию микроглии (панели i и ii) .31 (C) Хронические невропатологии. (i) Тау-патология: силы сдвига во время травмы головы локализуются в глубинах кортикальной борозды, вызывая микроструктурные повреждения, нарушение гематоэнцефалического барьера, аксонопатию, астроглиопатию и воспаление. Сулькальная периваскулярная локализация нейрофибриллярных клубков P-tau является патогномоничной для хронической травматической энцефалопатии, видимой на иммуноокрашивании CP13.22 (ii) Амилоидная патология: бета-амилоидные бляшки у женщины среднего возраста, умершей через много десятилетий после ЧМТ, очевидные при иммуногистохимическом окрашивании и окрашивании тиофлавином-S30.
Посттравматические протеинопатии имеют сходство с деменциями, в частности AD.35 Патология тау-белка, наблюдаемая после TBI, имеет биохимический состав, аналогичный AD, но с некоторыми уникальными особенностями. s27 CTE тау-филаменты недавно были охарактеризованы с помощью криоэлектронной микроскопии, выявляя конформации, совершенно отличные от других состояний, таких как AD и болезнь Пика.36 Локализация тау-белка в периваскулярных астроцитах в основании борозд головного мозга является еще одной отличительной особенностью (рис. 2C) .31 Это расположение борозды предсказывается в компьютерных моделях биомеханических сил во время травмы, где напряжение, по-видимому, сосредоточено на анатомические точки перегиба.37 s20
Патологии TDP-43 после травмы более неопределенны: расщепление увеличивается в моделях на животных, генерируя нейротоксические фрагменты и способствуя накоплению убиквитин-положительных включений. s16 s33 Патологический TDP-43, наблюдаемый при CTE, имеет сходство с ALS и FTD, s34 , хотя обнаружение не типично для единичных тяжелых травм у человека, где описана аномальная локализация непатогенного TDP-43, неопределенного значение. s25 Хотя паркинсонические фенотипы описаны после ЧМТ, патологии альфа-синуклеина выявляются редко, что, возможно, указывает на роль других белков, таких как тау (как при прогрессирующем надъядерном параличе) и потери нейронов черной субстанции.31 год
Периваскулярная локализация тау-патологии предполагает, что повреждение нервно-сосудистой единицы может быть важным причинным фактором посттравматической нейродегенерации.22 31 Гематоэнцефалический барьер (ГЭБ) нарушается в первые минуты после травмы, вызывая сложную воспалительную реакцию в часы и дни после ЧМТ.38 s35 — 38 Микроглия и астроциты активируются в ответ на экстравазацию провоспалительных молекул, а инфильтрирующие моноциты вносят вклад в последующий воспалительный ответ (рисунок 2B).31 Микроглия остается активированной в месте повреждения аксонов в течение многих лет после ЧМТ и связана с долгосрочными последствиями диффузного повреждения аксонов.28 Функциональное влияние этих микроглии остается неопределенным, поскольку неясно, когда они проявляют нейровоспалительный или восстановительный фенотип. .28 31 39 40 s38 s39 Пониженный клиренс нейродегенеративных предшественников может также увеличить позднюю нейродегенерацию, потенциально вызванную нарушением нормального функционирования глимфатической системы.Мышиные модели указывают на клиренс неправильно свернутого бета-амилоида и P-tau через глимфатическую систему в процессе, зависящем от водного канала аквапорина-4, расположенного в концевых ногах астроцитов. s40 Ранний реактивный астроглиоз после экспериментальной ЧМТ связан с потерей аквапориновых каналов, снижением оттока спинномозговой жидкости (CSF) и нарушением клиренса белка, что предполагает роль в последующем накоплении нейротоксичных белков. s40
Ключевой задачей является понимание связи между самыми ранними стадиями нейродегенерации, возникающей во время травмы, и широко распространенными патологическими изменениями, наблюдаемыми при вскрытии во многих случаях CTE и других типов деменции.Предполагается, что CTE прогрессирует с течением времени у человека, вовлекая все более крупные части мозга.22 Предложение группы CTE Бостонского университета по стадиям отражает эту гипотезу прогрессирования, но важно отметить, что предлагаемая стадия основана на перекрестном анализе. секционные данные по мере прогрессирования заболевания еще не были охарактеризованы продольно in vivo. Следовательно, важной целью будущих клинических исследований является различение у людей прямых эффектов ЧМТ от действительно прогрессирующего нейродегенеративного процесса, который распространяется с вовлечением нейронов, не обязательно пораженных во время первоначального повреждения.Важным недавним наблюдением является то, что ЧМТ может вызывать прионоподобное распространение самосевной протеинопатии. В моделях ЧМТ на животных P-тау-белок, первоначально присутствующий в месте повреждения, становится обнаруживаемым в контралатеральном полушарии через 6 месяцев после травмы.31 32 34 Кроме того, местная инокуляция здоровых животных гомогенатом ушибленного мозга вызывает прогрессирующую таупатию, что свидетельствует о травме головного мозга. вызывает трансмиссивную самораспространяющуюся тау-патологию.41 s41
Клинические особенности нейродегенерации после ЧМТ
Нам необходимо улучшить наш подход к диагностике посттравматических нейродегенеративных состояний.Это сложная проблема, отчасти потому, что предполагаемые клинические особенности CTE (например, память, поведенческие и психоневрологические проблемы) 24 и других посттравматических деменций пересекаются с прямыми когнитивными и психиатрическими эффектами травмы головного мозга22. коллеги22 24 предлагают стадию CTE на основе прогрессирования невропатологического заболевания и выделяют клинические особенности, характерные для каждой патологической стадии. У людей с патологически подтвержденным CTE сообщалось о различных симптомах, включая головную боль, потерю памяти, трудности с поиском слов и агрессию.Однако они распространены как прямое следствие ЧМТ и часто сохраняются в хронической фазе после травмы. Следовательно, эти проблемы не являются специфической особенностью посттравматической деменции, и примечательно, что до сих пор не установлены согласованные клинические признаки CTE.
Невропатологическое определение CTE со временем может быть уточнено по мере появления новых доказательств. Текущие согласованные критерии NINDS / NIBIB (Национальный институт неврологических расстройств и инсульта США / Национальный институт биомедицинской визуализации и биоинженерии) описываются как « предварительные », что отражает относительно небольшое количество случаев во всем мире, используемых для определения состояния, риски систематической ошибки отбора. и трудности, связанные с одновременным возникновением множества различных протеинопатий у пациентов после ЧМТ.42 s42 Учитывая потенциальную значимость любого индивидуального диагноза CTE, требуется тщательное различие, чтобы отделить патологии CTE от других сущностей, таких как патология AD, первичная возрастная таупатия и возрастная тау-астроглиопатия, что может быть технически сложной задачей. s43 s44 Специфичность текущих критериев консенсуса подвергалась критике, при этом высказывалась озабоченность по поводу сенсационности в сообщениях средств массовой информации об этом состоянии, особенно с учетом наличия патологии у внешне здоровых, бессимптомных людей. s45
На наш взгляд, обычно невозможно отделить прямые эффекты ЧМТ от эффектов, вызванных нейродегенеративными процессами, только на основании клинических признаков. Маловероятно, что клинический фенотип, состоящий из симптомов, неврологических признаков и когнитивного профиля, обладает достаточной специфичностью, чтобы можно было точно диагностировать CTE. Тем не менее, широкий спектр исследований был разработан для других нейродегенеративных состояний, которые могут быть успешно применены для изучения посттравматической нейродегенерации.Они могут выявить отчетливые и информативные «эндофенотипы» основного нейродегенеративного процесса. s46 На наш взгляд, систематическое использование клинических оценок в сочетании с мультимодальными биомаркерами и патологоанатомической проверкой позволит разработать точные диагностические критерии посттравматической деменции, а также облегчить измерение прогрессирования заболевания и прогнозирования. s47
Как исследовать нейродегенерацию после ЧМТ
Атрофия головного мозга и травма аксонов
Атрофия головного мозга является ключевым показателем прогрессирования заболевания при нейродегенеративных состояниях.Потеря нейронов является результатом различных нейродегенеративных процессов и вызывает атрофию, которую можно измерить с помощью серийной МРТ. 43 44 Это чувствительный, хотя и неспецифический способ оценки прогрессирующей нейродегенерации. Он обеспечивает комплексную оценку потери нейронов, наблюдаемой от месяцев до лет после травм, и пространственную информацию о характере этой потери. Стандартным подходом при других нейродегенеративных состояниях является использование повторной объемной Т1 МРТ. Теперь доступно несколько усовершенствованных конвейеров анализа, обеспечивающих точные и чувствительные измерения того, как мозг человека изменяется с течением времени. s48 s49 МРТ уже широко используется при оценке ЧМТ. МРТ чувствительна к ушибам, кровотечениям и особенностям, связанным с диффузным повреждением аксонов, таким как микрокровоизлияния.1 Однако ее применение для исследования посттравматической нейродегенерации на удивление ограничено.
Прогрессирующая атрофия головного мозга очень распространена после ЧМТ и может быть очевидна при сравнении клинических снимков с течением времени.43 Атрофия часто очевидна при стандартной нейровизуализации по увеличению желудочков и прозрачной полой перегородке35, и ее можно количественно оценить с помощью серийной объемной МРТ T1.43 Количественная оценка этих изменений с помощью серийной объемной МРТ показывает поразительно повышенную частоту атрофии, которая продолжается в течение многих лет после умеренно-тяжелой ЧМТ. 43 44 Мы наблюдали ежегодную потерю ~ 1,5% в сером и белом веществе (рисунок 3D, E) . Эти показатели атрофии приближаются к тем, которые наблюдаются при установленном БА, и контрастируют с отсутствием атрофии у здоровых людей того же возраста. s50 Прогрессирующая атрофия наиболее выражена в белом веществе, где часто поражаются обширные тракты. Более высокие показатели наблюдаются при большей тяжести ЧМТ; более низкая шкала комы Глазго (GCS), потеря сознания, длительная кома и длительная посттравматическая амнезия — все это связано с большей атрофией.44 45 s51–54 В нашем исследовании атрофия была значительно выше, чем у различных потенциально мешающих факторов, включая старение. Высокие показатели атрофии наблюдались в бороздах коры по сравнению с извилинами, что, возможно, отражает высокие уровни деформации, которые модели компьютерного повреждения локализуют в бороздах, и, что интересно, соответствует характерному расположению невропатологии CTE в посмертных исследованиях человека.37 42 Степень атрофии головного мозга у человека человек также имеет отношение к когнитивным и функциональным результатам после ЧМТ, 43 44 s55 s56 с высокими показателями атрофии, связанными со снижением производительности памяти.43 год s57 Валидация в клинических испытаниях лечения после травм поможет установить, обязательно ли атрофия является вредной после ЧМТ, или такие изменения являются полезной физиологической реакцией для поддержки восстановления, аналогичной сокращению синапсов при нормальном развитии. Хотя валлеровская дегенерация нейронов наблюдается после травмы и представляет собой организованный ответ на клеточном уровне, s29 нам не известны какие-либо убедительные доказательства, позволяющие предположить «полезную» реорганизацию, вызванную атрофией, на глобальном уровне после травмы.Мы считаем, что прогрессирующая и обширная потеря нейронов после травмы, вероятно, будет пагубной, как и другие нейродегенеративные состояния, такие как AD.
Рисунок 3Количественная оценка нейродегенерации с атрофией головного мозга и нейрофиламентами крови. (A) Уровни света нейрофиламентов плазмы (NFL) нанесены на график для умеренно-тяжелой черепно-мозговой травмы (TBI) в хронической фазе и в контрольной группе. Уровни значительно выше у пациентов с ЧМТ, чем в контрольной группе. 40 (B) Уровни NFL для умеренно-тяжелой ЧМТ в хронической фазе в зависимости от времени, прошедшего с момента травмы (месяцы).40 (C) Среднее значение детерминанты Якоби белого вещества (WM) (среднегодовая частота JD), рассчитанное за 6-месячный интервал сканирования-повторного сканирования у пациентов в хронической фазе после умеренно-тяжелой ЧМТ, нанесенный на график относительно исходного уровня NFL в плазме 40 (D) Пространственные карты средних значений JD в здоровых контрольных группах и группах пациентов с ЧМТ. Заметная прогрессирующая атрофия белого вещества присутствует после ЧМТ средней и тяжелой степени (сине-белые области) с расширением пространств спинномозговой жидкости (красно-желтые области) по сравнению с минимальными изменениями у здоровых людей.43 (E) Прогрессирующая атрофия белого вещества после ЧМТ средней и тяжелой степени. График разброса скоростей JD изменения объема мозга при ЧМТ по сравнению со здоровыми добровольцами того же возраста в белом веществе. Значение JD, равное 0, указывает на отсутствие изменений в объеме мозга в течение периода наблюдения.
Структура мозга также может предоставить информацию о старении.45 Для оценки хронологического возраста здоровых людей можно использовать вариации объема мозга. При болезненных состояниях несоответствие между «возрастом мозга», оцененным с использованием подходов машинного обучения, и хронологическим возрастом пациента может быть информативным.Возраст мозга основан на объемной информации о характере атрофии мозга, полученной с помощью Т1 МРТ. Машинное обучение используется для определения ожидаемого внешнего вида мозга в разном возрасте, с которым затем сравниваются люди. Расхождения из-за повышенной атрофии отражаются в увеличении видимого возраста мозга. Сообщалось о более старом, чем ожидалось, возрасте мозга в таких условиях, как у пациентов с легкими когнитивными нарушениями и БА, и, что важно, когда этот показатель был протестирован в когорте рожденных в Лотиане, люди с более старым мозгом, вероятно, выжили в течение более короткого периода времени.46 Мы показали, что умеренная / тяжелая ЧМТ добавляет около 5 лет к измеренному возрасту мозга по сравнению с хронологическим возрастом, и что эта разница указывает на когнитивные нарушения и увеличивается со временем после травмы.47 Следовательно, мозг выглядит « старше » после значительной травмы головы. , эффект, который усиливается со временем после травмы и коррелирует с посттравматическими когнитивными нарушениями.
Диффузионная МРТ предоставляет дополнительную информацию о локализации и степени диффузного повреждения аксонов.48 Это относится к посттравматической нейродегенерации, поскольку повреждение аксонов связано с образованием протеинопатий бета-амилоида и P-тау.31 49 Визуализация тензора диффузии (DTI) широко используется для исследования повреждения белого вещества, вызванного диффузным повреждением аксонов (DAI). ), хотя есть несколько общепризнанных ограничений этого подхода, таких как трудности с оценкой целостности волокон в областях мозга, где тракты пересекаются друг с другом. s58 Незначительные отклонения в организации белого вещества могут быть обнаружены даже при нормальном внешнем виде при сканировании.Локализация и серьезность этих изменений хорошо коррелируют с когнитивными проблемами после травмы, такими как низкая скорость, исполнительная дисфункция, проблемы с памятью и функциональные исходы.50 Следовательно, DTI можно использовать для определения наличия важного потенциального триггера нейродегенерации, а также предоставляет способ проверить гипотезу о том, что протеинопатии, инициированные ЧМТ, распространяются способом, ограниченным структурой коннектома белого вещества. s59
Жидкие биомаркеры нейродегенерации
Нейровизуализация может быть дополнена биомаркерами нейродегенерации крови, спинномозговой жидкости и микродиализата (рисунок 4).Резкое улучшение чувствительности анализа произошло в результате переноса стандартного ELISA на платформу анализа одиночных молекул (Simoa). Это позволяет проводить сверхчувствительное измерение биомаркеров, таких как нейрофиламентный свет (NFL) и тау, s60 , значительно повышая чувствительность к нейродегенеративным состояниям. NFL — особенно многообещающий биомаркер. Он обнаружен в высоких концентрациях в миелинизированных аксонах, и животные модели нейродегенерации показывают, что NFL является чувствительной мерой начала ряда протеопатических поражений в головном мозге.Изменения уровней NFL можно использовать для отслеживания прогрессирования заболевания и реакции на лечение, 51 а у людей повышенные уровни наблюдаются при различных нейродегенеративных заболеваниях, включая БА и болезнь двигательных нейронов51. s61 — 63 Последовательный отбор образцов НФЛ у лиц с риском БА позволяет прогнозировать частоту атрофии головного мозга, когнитивные нарушения и прогрессирование заболевания52. s62 — 64
Рис. 4Потенциальные траектории продольных биомаркеров после черепно-мозговой травмы (ЧМТ).Предполагаемые траектории биомаркеров после умеренной / тяжелой ЧМТ. Объемы мозга, измеренные с помощью объемной МРТ, могут сначала увеличиваться из-за отека, а затем постепенно уменьшаться и продолжать уменьшаться в результате прогрессирующей нейродегенерации после травмы. Фракционная анизотропия, мера целостности белого вещества, полученная с помощью диффузно-тензорной визуализации (DTI), первоначально увеличивается из-за острого отека, с подострым уменьшением через несколько дней или недель, отражающим повреждение аксонов. Церебральные микрокровоизлияния, маркер диффузного сосудистого поражения, появляются быстро после ЧМТ и не проходят.Наиболее точно они идентифицируются с помощью визуализации, взвешенной по восприимчивости (SWI) 1. s106 Жидкие нейрональные и глиальные маркеры повреждения, такие как убиквитин карбоксиконцевая гидролаза L1, S100B, нейрон-специфическая енолаза, глиальный фибриллярный кислый белок, амилоид и тау, быстро повышаются после ЧМТ. Уровень света нейрофиламентов (NFL) достигает пика позже и может повышаться в хронической фазе, что коррелирует с прогрессирующей атрофией головного мозга. s107 s108 ПЭТ, позитронно-эмиссионная томография.
NFL и тау также использовались для оценки ЧМТ, особенно в острых случаях.54 Уровни в крови и спинномозговой жидкости резко повышаются после травмы головного мозга и зависят от тяжести травмы. s65 53 Концентрации в крови и спинномозговой жидкости резко повышаются даже после легких травм, например, после контактного боя у боксеров или травмы головы в хоккее с шайбой. s66 s67 Уровни NFL, но не тау-белка, остаются повышенными в хронической фазе после ЧМТ у некоторых людей, и уровни коррелируют с показателями диффузного аксонального повреждения и прогрессирующей атрофии головного мозга (рисунок 3E) 40. s68 Это предполагает, что уровни NFL отражают степень травматического повреждения, особенно больших миелинизированных аксонов.В хронической фазе стойкое увеличение NFL в крови может указывать на наличие прогрессирующей посттравматической нейродегенерации. Если это подтвердится в более крупных исследованиях, NFL в плазме может оказаться диагностически полезным для выявления пациентов с риском развития посттравматической деменции различных типов и для стратификации набора пациентов в клинические испытания.
Молекулярная визуализация: активация амилоида, тау и микроглии
МРТ-измерения атрофии головного мозга (рисунок 5A) и уровни NFL обеспечивают чувствительные, но неспецифические измерения посттравматической нейродегенерации.Напротив, методы молекулярной визуализации, такие как позитронно-эмиссионная томография (ПЭТ), позволяют идентифицировать определенные типы протеинопатии (рис. 5D – F). Были разработаны ПЭТ-индикаторы, чувствительные к гиперфосфорилированному тау в нейрофибриллярных клубках и бета-амилоидных агрегатах. Их применение при ЧМТ обещает значительно улучшить исследование посттравматической нейродегенерации и должно облегчить диагностику CTE и других типов посттравматической деменции in vivo.
Рисунок 5Визуализация черепно-мозговой травмы (ЧМТ) и посттравматической нейродегенерации.(A) Прогрессирующая нейродегенерация поддается количественной оценке с помощью повторной МРТ T1, используемой для определения показателей атрофии с течением времени. (B) Визуализация с взвешиванием по восприимчивости (SWI) показывает микрокровотечение с типичным распределением парафальцинов, типичным для диффузных сосудистых повреждений. (C) Диффузионная МРТ позволяет количественно оценить целостность белого вещества после повреждения аксонов и обеспечивает измерение диффузного повреждения аксонов. женщина среднего возраста через несколько лет после ЧМТ средней и тяжелой степени.55 (E) 18 F-AV1451 тау-ПЭТ показывает аномальное связывание после TBI. (F) Стойкая аномальная активация микроглии на ПЭТ-транслокаторе белка-транслокатора 11 C-PBR28 у мужчины среднего возраста через десять лет после умеренно-тяжелой ЧМТ, особенно в регионах белого вещества. 40 DTI, визуализация тензора диффузии.
Амилоидные ПЭТ-индикаторы, такие как 11 C-Питтсбургское соединение-B ( 11 C-PiB), широко используются для выявления патологии фибриллярного бета-амилоида. 11 Связывание C-PiB увеличивается при БА по аналогии с патологией амилоида. s69 s70 В первый год после TBI, 11 C-PiB-связывание также увеличивается в корковом сером веществе и полосатом теле, s71 остается высоким через много лет после травмы у некоторых пациентов (рисунок 5D) .55 Между ними есть сходство. 11 Связывание C-PiB при TBI и AD, хотя связывание обычно намного выше при AD. И AD, и TBI могут приводить к увеличению связывания 11 C-PiB в задней части поясной извилины коры головного мозга. s72 Однако после TBI 11 связывание C-PiB также наблюдается в мозжечке, месте, где повышенный амилоид обычно не наблюдается при AD, что может указывать на особый механизм образования патологии амилоида после TBI.Не все исследователи сообщили об увеличении сигнала ПЭТ амилоида после ЧМТ, что может быть связано с выбором индикатора или тяжестью травмы. s6
Недавняя работа была сосредоточена на разработке индикаторов ПЭТ, специфичных для гиперфосфорилированного тау. Способность идентифицировать тау-патологию in vivo, вероятно, будет ключом к оценке CTE, поэтому эти разработки представляют особый интерес. Некоторые индикаторы кажутся чувствительными и специфичными для тау-патологии в контексте БА. Например, флортауципир ( 18 F-AV1451, 18 F-T807) демонстрирует сильное и специфическое несмещаемое связывание с нейрофибриллярными клубками тау в ткани головного мозга после смерти при БА. s73–75 Флортауципир селективен в отношении тау-белка и незначительно связывается с бета-амилоидом, альфа-синуклеином или TDP-43. s73 Тип связывания относится к клиническому фенотипу, когнитивному профилю и стадиям БА по Брааку и Брааку. s76 s77 Однако при других таупатиях, не связанных с болезнью Альцгеймера, полезность этого лиганда менее очевидна. s75 Некоторые исследования использовали тау-ПЭТ для изучения пациентов с повторяющейся ЧМТ, вызванной спортивными травмами. Недавнее исследование 26 бывших игроков в американский футбол с умеренными когнитивными симптомами показало умеренно повышенное связывание фортауципира по сравнению со здоровыми добровольцами.56 Связывание индикатора связано с годами участия, но не с когнитивными способностями. Техника не могла отличить игроков от контроля на индивидуальном уровне. Однако другие исследования в этой области были небольшими по размеру, часто не имели контроля и обычно не имели невропатологического подтверждения CTE. s78 s79 В одном отчете о случае игрока НФЛ с историей повторяющейся ЧМТ и прогрессирующих психоневрологических симптомов сообщалось об увеличении связывания фортауципира. s78 Во втором исследовании сообщалось об увеличении связывания 18 F-FDDNP (2- (1- [6 — {(2- [18F] фторэтил) (метил) амино} -2-нафтил] этилиден) малононитрила) в Игрок НФЛ с историей повторной ЧМТ легкой степени, у которого позже был диагностирован постмортальный диагноз CTE.В этом случае пространственный паттерн аномальных результатов ПЭТ в некоторой степени коррелировал с пространственным паттерном посмертного P-tau. s80 Текущие исследования фортауципира и других лигандов ПЭТ должны прояснить, будет ли тау-ПЭТ диагностически полезным после ЧМТ (рис. 5E).
ПЭТ-сканирование также позволяет исследовать другие процессы, связанные с нейродегенерацией. Например, активированная микроглия часто сочетается с патологией амилоида и тау. 11 Белок-транслокатор C-PBR28 (TSPO) Лиганды ПЭТ связываются с белком-транслокатором, экспрессируемым в митохондриях активированной микроглии. s81 Они широко использовались при БА, обычно демонстрируя повышенное связывание, которое отслеживает прогрессирование заболевания. s82 В невропатологических исследованиях ЧМТ хроническая активация микроглии связана с признаками стойкого повреждения аксонов (рис. 5F) .28 В соответствии с этими наблюдениями, связывание TSPO с ПЭТ увеличивается через много лет после ЧМТ, преимущественно в подкорковых областях белого вещества и таламуса. .39 40 Высокое связывание наблюдается в областях диффузного повреждения аксонов, которые также демонстрируют прогрессирующую атрофию головного мозга.40 Следовательно, активация микроглии сохраняется в областях аксонального повреждения в течение многих лет после ЧМТ, и в этих местах происходит прогрессирующая нейродегенерация. Ключевой вопрос заключается в том, какую функциональную роль играют эти хронически активированные микроглии. TSPO PET не различает отдельные фенотипы микроглии, поэтому активированная микроглия в этом контексте может быть воспалительной или восстанавливающей. s83 Используя подход экспериментальной медицины, мы объединили фармакологическое вмешательство, нейровизуализацию и биомаркеры жидкости для исследования этой проблемы.Миноциклин использовали для ингибирования хронически активированной микроглии, эффект подтвержден снижением связывания TSPO после лечения. Последовательный мониторинг уровней NFL в крови обеспечивал динамическую оценку нейродегенеративной активности. Увеличение NFL наблюдалось после лечения миноциклином 40, что свидетельствует о том, что ингибирование микроглии увеличивает нейродегенерацию в хронической фазе после ЧМТ. Это говорит о том, что микроглия может выполнять восстановительную функцию на поздних сроках после ЧМТ, что согласуется с работой на нечеловеческих приматах, показывающей трофическую роль хронически активированной микроглии. s37
Повреждение сосудов
Нейродегенеративные аномалии особенно видны в периваскулярной области, что позволяет предположить, что ЧМТ может запускать нейродегенеративный каскад через влияние на проницаемость ГЭБ.22 31 Следовательно, исследование сосудисто-нервных структур может дать представление о триггерах нейродегенерации. . Кровеносные сосуды часто напрямую повреждаются ЧМТ. Крупные внутримозговые кровоизлияния часто встречаются в экстрадуральных, субдуральных и паренхиматозных участках.Это часто является основным направлением первоначального управления. Однако связь большого кровотечения с долгосрочным риском деменции неясна. В других контекстах, таких как интрапаренхиматозное или нетравматическое субарахноидальное кровоизлияние, долгосрочный риск деменции повышается независимо от сосудистых факторов риска: риск деменции значительно выше после геморрагического инсульта по сравнению с ишемическим инсультом. s84 После ЧМТ более тонкое периваскулярное кровотечение также является обычным явлением, и его можно точно оценить с помощью градиентного эхо-сигнала или визуализации, взвешенной по чувствительности. s85 Эти последовательности МРТ в настоящее время обычно используются при оценке ЧМТ, а микрокровоизлияния свидетельствуют о диффузном сосудистом повреждении, которое может не быть очевидным при использовании традиционных методов визуализации (рис. 5В). Диффузное сосудистое повреждение часто связано, но не является синонимом диффузного аксонального повреждения, а расположение и степень микрокровоизлияний могут быть еще одним способом исследования связи между начальной тяжестью травмы и посттравматической нейродегенерацией.
ЧМТ может также вызвать негеморрагическое нарушение сосудисто-нервного аппарата.Проницаемость ГЭБ резко увеличивается после ЧМТ, но продолжительность этого изменения неизвестна. s86 У людей развитие нейровизуализации позволяет идентифицировать тонкое нарушение проницаемости ГЭБ. Например, МРТ с динамическим контрастированием (DCE) с быстрым картированием T1 использовалась для выявления тонких изменений проницаемости BBB при здоровом старении, ранних нейродегенеративных состояниях s87 и игроков в американский футбол в течение сезона игры. s88 Этот подход весьма перспективен.Изменения DCE коррелируют с повреждением BBB на молекулярной визуализации и могут отличить пациентов с TBI от здоровых людей. s89 s90 Недавняя доклиническая работа с легкой закрытой ЧМТ подтверждает DCE как меру негеморрагического разрушения ГЭБ.31 В будущей работе было бы полезно изучить проницаемость ГЭБ в хронической фазе после травмы и прояснить ее связь с атрофией мозга и связанными с ней протеинопатиями.
Посттравматическая нейродегенерация и клинические испытания
Установление четких взаимосвязей между биомаркерами и болезненными состояниями может облегчить разработку новых методов лечения.Например, прогресс в лечении ускорился за счет установления связи между внутриглазным давлением и зрительной функцией при глаукоме; минеральная плотность костей и остеопоротические переломы; и подсчет лимфоцитов CD4 для клинического исхода при ВИЧ-инфекции. Это соображение актуально для ЧМТ, поскольку существует острая необходимость в разработке новых подходов к оценке новых методов лечения. s91 Неоднородность ЧМТ приводит к серьезным проблемам при проведении клинических испытаний. s91 Предыдущие исследования нейрозащиты и модификации болезни в основном дали отрицательные результаты.Однако эти испытания часто были недостаточны для выявления эффектов лечения, которые обычно измерялись с использованием зашумленных клинических конечных точек, таких как шкала результатов Глазго. Следовательно, существует значительный риск того, что мы не смогли должным образом оценить многообещающие новые методы лечения из-за неоптимального дизайна исследования.
Включение биомаркеров нейродегенерации в качестве первичных или вторичных критериев исхода в клинических испытаниях фазы II и III улучшит способность выявлять нейропротекторные и модифицирующие заболевание методы лечения, обеспечивая точные и чувствительные измерения потери нейронов (рис. 6).Жидкие биомаркеры, такие как NFL, являются потенциальным суррогатным маркером нейродегенерации. Например, изменения уровня NFL в крови или спинномозговой жидкости можно использовать в качестве динамической меры лечебных эффектов, которые были подтверждены в исследованиях на животных51 и показывают многообещающие результаты в качестве считывания активной нейродегенерации в нашем экспериментальном медицинском исследовании использования миноциклина40. МРТ-измерения атрофии головного мозга предоставляют второй вариант с сильной достоверностью лица в качестве интегрированного показателя потери нейронов и установленной связи с нейропатологией в других контекстах, таких как AD.57 Атрофия головного мозга установлена при различных нейродегенеративных состояниях, и в клинических испытаниях она все чаще используется в качестве суррогатной конечной точки для прогрессирования заболевания. s91
Рисунок 6Биомаркеры в клинических испытаниях после черепно-мозговой травмы (ЧМТ). Этапы оценки модифицирующего болезнь / нейропротективного лечения после ЧМТ. (i) Набор пациентов с высоким риском нейродегенерации с использованием фонового света нейрофиламентов крови, аномалий визуализации тензора диффузии (DTI) и аномалий позитронно-эмиссионной томографии (ПЭТ).(ii) Фазы 2–3 исследований, основанные на оценке первичного результата измерения изменения частоты атрофии (с использованием повторной Т1 МРТ) с вторичными функциональными / когнитивными результатами / результатами безопасности. (iii) Мета-анализ исследований фазы 2–3 для выяснения взаимосвязи между суррогатным матрицей (частота атрофии T1) и исходами, ориентированными на пациента. (iv) 3–4 фазы поздних стадий испытаний с использованием первичных функциональных или когнитивных результатов. Это может быть составная мера.
Измерения атрофии с помощью МРТ имеют высокую надежность повторных тестов у здоровых субъектов, что позволяет точно определять влияние ЧМТ.Влияние ЧМТ на атрофию головного мозга значительно по сравнению с рядом возможных препятствий. Например, в нашем недавнем исследовании ЧМТ объяснила ~ 20% различий в показателях атрофии по сравнению с ~ 0,5% из-за возраста или пола.43 Следовательно, с помощью этого подхода можно выявить относительно небольшие эффекты лечения на частоту атрофии. s92 s93 Используя наиболее чувствительный метод визуализации атрофии (частота детерминанты Якоби), мы установили, что группы из ~ 200 пациентов в каждой экспериментальной группе были необходимы для выявления уменьшения атрофии, которое, вероятно, будет значимым (вставка 2).43 Размер выборки может быть уменьшен путем обогащения для достижения высоких показателей нейродегенерации с использованием дополнительных биомаркеров, подход, обычно применяемый в исследованиях БА .58 При ЧМТ этот тип обогащения может включать такие критерии включения, как положительный тау-ПЭТ, наличие диффузного повреждения аксонов указывает на наличие диффузного повреждения аксонов. по DTI и высоким уровням NFL в плазме / CSF (рисунок 3). Такой подход облегчит рентабельные и выполнимые клинические испытания фазы II, предоставив надежные доказательства о влиянии нейропротективных или модифицирующих заболевание методов лечения на потерю нейронов после ЧМТ.
Вставка 2Размер выборки в клинических испытаниях средств лечения посттравматической деменции
Оценку новых методов лечения черепно-мозговой травмы (ЧМТ) можно ускорить, приняв биомаркеры нейродегенерации в качестве критериев оценки результатов. Утверждение Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов биомаркеров прогрессирования болезни Альцгеймера (БА) позволит использовать новые методы лечения, направленные на посттравматическую нейродегенерацию, в клинических испытаниях. Атрофия мозга, измеренная с помощью МРТ, является наиболее многообещающим биомаркером в этом отношении.
Использование биомаркеров для визуализации дает важные преимущества с точки зрения дизайна исследования. «Размер эффекта» (ES) любого лечения является ключевым фактором, влияющим на размер выборки (N), а изменчивость основного показателя результатов исследования является основным определяющим фактором ES (см. Уравнения ниже). Использование биомаркера, такого как частота атрофии головного мозга, с высокой надежностью повторного тестирования снижает дисперсию и увеличивает ES, уменьшая необходимый размер выборки. Аналогичным образом, повышение эффективности лечения (разница между средними показателями атрофии в экспериментальной и контрольной группах) также увеличивает ES и уменьшает размер выборки.ES может быть дополнительно увеличен за счет набора пациентов, которые могут ответить на лечение («обогащение населения»). Лица с высоким нейродегенеративным риском могут быть идентифицированы с помощью биомаркеров, таких как свет нейрофиламентов крови, генетический риск, визуализация тензора диффузии, визуализация позитронно-эмиссионной томографии или исходная атрофия (43).
Расчет размера выборки также отражает выбор исследователя в отношении допустимого риска ошибок: чем ниже допустимая частота ошибок, тем больше требуется N.Эти выборы проявляются в критических значениях (z, полученных из стандартного нормального распределения), отображаемых в числителе уравнения размера выборки. Значения z должны вводиться для риска ошибок типа I (α), обычно устанавливаемого на уровне 5%, и для ошибок типа II (1 – β), где степень (β) часто устанавливается на уровне 80%. s104 Величина лечебного эффекта, который считается клинически значимым, включается в знаменатель: в литературе по AD снижение частоты атрофии на 25% считается клинически значимым.Это прагматическая отправная точка в исследованиях ЧМТ. s105 Используя частоту атрофии белого вещества в качестве основного критерия исхода, α = 5% и β = 80%, необходимо 200 участников в каждой группе для выявления атрофии снижения на 25% в хронической фазе ЧМТ (43). любое обогащение исследуемой популяции, которое может еще больше сократить размер выборки.
Существует ряд сложностей, которые необходимо учитывать при использовании МРТ-измерений атрофии головного мозга после ЧМТ.Отек, связанный с травмой, возникший в острой фазе, может ложно повысить частоту атрофии по мере ее исчезновения. Аналогичная проблема обнаруживается при рассеянном склерозе после начала лечения, уменьшающего нейровоспаление («псевдоатрофия»). s94 Исследования, которые точно характеризуют динамику атрофии с помощью повторной МРТ на ранней стадии после ЧМТ, необходимы, чтобы прояснить, как лучше всего точно измерить потерю нейронов и отличить ее от исчезновения отека и любых связанных с лечением эффектов. s95 s96 Методологически более простой подход — измерить атрофию в фазе от подострой до хронической после исчезновения острого отека. Атрофия головного мозга прогрессирует от месяцев до лет после травм, поэтому атрофия может служить интегральной мерой потери нейронов с течением времени. Это может оказаться чувствительной мерой лечебных эффектов, которые применялись в острой фазе до оценки МРТ. Независимо от времени оценки необходимо контролировать очаговые поражения при оценке степени атрофии.Это может быть достигнуто путем определения очаговых поражений и последующего исключения областей очевидных повреждений из расчета частоты атрофии. Это также позволяет исследовать пространственные отношения между атрофией и очаговым повреждением. s97 s98 Другие факторы, не относящиеся к TBI, которые необходимо учитывать, включают состояние гидратации, движение, вариабельность сканера и согласование методик анализа.59 s99 — 101
Другой важный вопрос — понять, как частота атрофии соотносится с клиническими исходами после ЧМТ.Хотя клинические результаты, такие как качество жизни и инвалидность, в конечном итоге являются ключевыми для оценки новых методов лечения, существует сложная взаимосвязь между атрофией мозга и этими клиническими показателями. В целом это верно для нейродегенеративных состояний, но после ЧМТ взаимосвязь, вероятно, будет особенно сложной. Было показано, что пациенты с высокой степенью атрофии имеют худшие функциональные результаты и когнитивные нарушения 43 44 s57 , но требуется дополнительная работа, чтобы правильно охарактеризовать эти отношения.Одна из проблем заключается в том, что спонтанное выздоровление на ранней стадии после ЧМТ вызывает большую часть ранних клинических изменений, поэтому нейродегенерация, вызванная травмой, вряд ли будет иметь четкую связь с этими исходами. Например, когнитивные функции обычно улучшаются в течение первых нескольких месяцев после ЧМТ в результате спонтанного восстановления, поддерживаемого ранним вмешательством нейрореабилитации. s102 В течение этого периода наблюдается высокий уровень атрофии головного мозга, но любое лечебное воздействие на когнитивные функции, вероятно, будет затушевано самопроизвольным выздоровлением (рис. 1A).Следовательно, непосредственное изучение влияния нейропротективных вмешательств на когнитивные функции на ранних этапах после ЧМТ, вероятно, будет затруднено из-за конкурирующих эффектов различных нейродегенеративных процессов и процессов восстановления. Вторая проблема заключается в том, что эффекты ускоренной нейродегенерации могут проявиться через годы, если не десятилетия. Молодой человек с ускоренной нейродегенерацией после ЧМТ, вероятно, будет иметь большой нервный и когнитивный резерв для защиты от воздействия потери нейронов. Следовательно, кумулятивные эффекты прогрессирующей потери нейронов могут не проявиться клинически, пока не пройдет много лет (рис. 1A), и к этому времени связь с предыдущим повреждением может быть не оценена.
Подобные вопросы важны для разработки исследований деменции на ранних стадиях, в которых доклинические эффекты лекарств могут быть модифицирующими течение болезни, но не должны иметь немедленных клинических эффектов (рис. 6). s103 В начале 2018 года Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) выпустило проект руководства по оценке раннего лечения БА.60 В нем признаются проблемы оценки лечения лиц с высоким риском без когнитивных или функциональных нарушений, доклинический период, который они называют «1 стадия» болезни.Примечательно, что FDA признало, что изменения биомаркеров могут быть достаточным основанием для первоначального одобрения с постмаркетинговым надзором:
‘У пациентов на стадии 1 может наблюдаться влияние на характерные патофизиологические изменения БА, о чем свидетельствует влияние на различные биомаркеры. измеряется. Такой эффект, анализируемый как первичная мера эффективности, может, в принципе, служить основанием для ускоренного утверждения (т. Е. Будет обнаружено, что эффекты биомаркеров с достаточной вероятностью предсказывают клиническую пользу, с требованием пост-утверждения для исследование, чтобы подтвердить прогнозируемую клиническую пользу).Как и в случае с использованием нейропсихологических тестов, набор лечебных эффектов, наблюдаемый по множеству индивидуальных биомаркеров, повысит убедительность предполагаемого эффекта »60.
Эти соображения имеют важное значение для дизайна клинических испытаний при ЧМТ. Один из вариантов, учитывая проект руководства FDA по AD, может заключаться в применении показателей атрофии мозга и биомаркеров жидких биомаркеров потери нейронов в качестве первичной конечной точки для первоначальной оценки нейрозащитного лечения с последующим использованием сложных функциональных и когнитивных показателей результатов для постмаркетинговых исследований.Этот подход предполагает признание того, что изменения нейродегенеративных биомаркеров, таких как атрофия головного мозга, обеспечивают законную первоначальную цель лечения, включая клинические оценки после установления эффективности лечения.
Выводы
Существует четко установленная связь между ЧМТ и деменцией, которая все больше понимается на механистическом уровне. Посттравматическая нейродегенерация является обычным явлением, но неясно, как диагностировать отдельные типы посттравматической деменции в клинической практике.Это важно, поскольку значительная ЧМТ усугубляет бремя деменции среди населения. Около 5% всех случаев деменции может быть связано с ЧМТ, если предположить, что относительный риск посттравматической деменции увеличивается в 1,5 раза.8 И наоборот, многие люди обеспокоены долгосрочными последствиями очень незначительных травм головы, которые вряд ли повлияют на них. долгосрочные эффекты, и их следует дифференцировать от более тревожных ситуаций после повторной легкой или однократной умеренно-тяжелой ЧМТ.



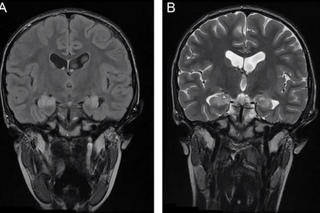

 Регистрируется при новообразованиях системы кроветворения, ВИЧ.
Регистрируется при новообразованиях системы кроветворения, ВИЧ.