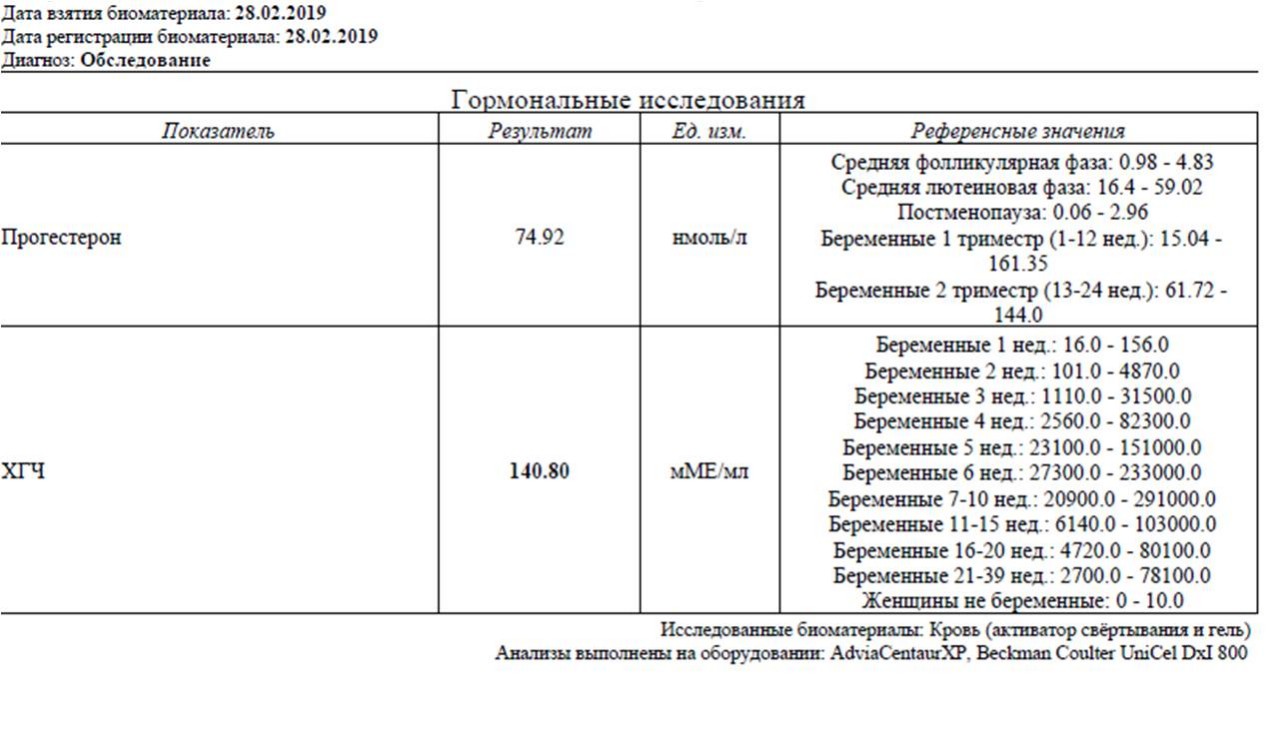
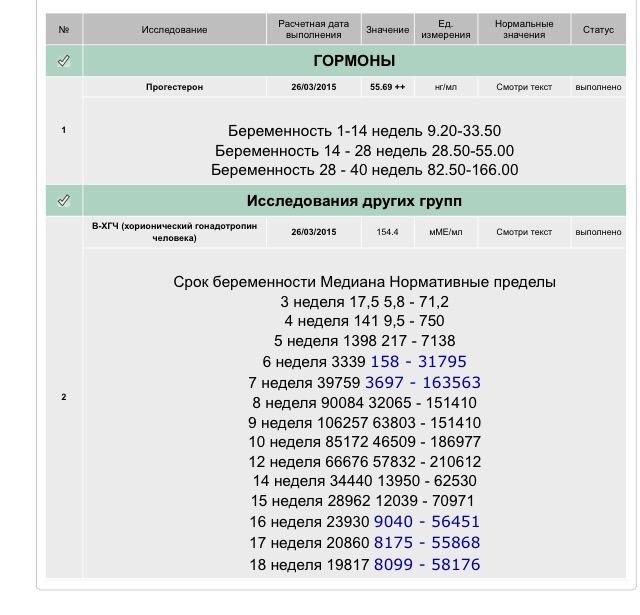
Женское здоровье. Гормоны и беременность.
Течение и сохранение беременности напрямую зависит от гормонального фона. Если при беременности изменяется норма прогестерона, это становится заметно на раннем сроке. Но такое состояние поддается коррекции с учетом правильно проведенного обследования и назначения нужных препаратов.Влияние прогестерона на женский организм начинается со второй половины менструального цикла. Он увеличивает секрецию слизи в фаллопиевых трубах. Она служит питательной средой для продвигающейся оплодотворенной яйцеклетки.
Под влиянием прогестерона протекают следующие процессы:
1. Происходит секреторная трансформация, увеличивается число кровеносных сосудов, которые будут обеспечивать питание бластоцисты после имплантации. Гормон способен тормозить сократительную активность миометрия. Это необходимо для сохранения беременности и предупреждения отторжения зародыша.
2. Перестраивается эпителий канала шейки матки. Он проиводит большое количество слизи, которая не позволяет проникать внутрь патогенным микроорганизмам.
3. В начале беременности происходит усиленное воздействие долек молочной железы и альвеолярных ходов. Грудная железа подготавливается к секреции молока.
Повышенный прогестерон при беременности проявляется:
- Увеличением отложения подкожного жира.
- Задержкой жидкости в организме, что приводит к появлению отеков
- Повышением сальность и кожи и склонностью к образованию угрей
- Ослабление иммунитета для предотвращения отторжения организмом матери плода.
- Нарушение моторики кишечника
- Торможение психических процессов в коре головного мозга – проявляется нестабильность настроения, плаксивость, снижением памяти.
У беременных уровень прогестерона может измениться как в большую, так и в меньшую сторону. Причины снижения концентрации разнообразны. На ранних сроках его недостаточность может говорить о нарушении функции желтого тела и плаценты. Пройти необходимые обследования и получить консультацию опытного специалиста Вы можете в клинике Dixion в удобное для Вас время и день.
 Будьте здоровы!
Будьте здоровы! Анализ крови на прогестерон в Москве. Расшифровка и норма. Сдать анализы в МЦ «Здоровье» ЮАО (Варшавская и Аннино), ЦАО (Краснопресненская и Рижская).
Что показывает анализ крови на прогестерон?
Анализ прогестерона — это один из основных диагностических методов исследования овуляции. Концентрация данного гормона в женском организме изменяется в соответствии с фазами менструального цикла, а перед овуляцией (при отсутствии нарушений) уровень прогестерона возрастает в 10 раз. Если анализ показывает, что повышения прогестерона нет, это прямое указание на то, что есть какие-то отклонения — возможно, опасные.
Недостаточное количество прогестерона при беременности — это потенциальная угроза выкидыша. Исходя из этого, анализ на прогестерон является необходимым мероприятием. В другое время повышение прогестерона указывает на возможность наличия:
- Нарушений менструального цикла
- Кисты желтого тела
- Дисфункциальных маточных кровотечений
- Нарушений развития плаценты
- Нарушения функции надпочечников
- Почечной недостаточности
Нехватка прогестерона может указывать на:
- Нарушенную функцию плаценты либо желтого тела
- Отсутствие овуляции
- Задержку внутриутробного развития плода
- Высокий риск аборта, спровоцированного гормональным дисбалансом
- Хронические воспаления, затрагивающие половые органы
- Маточные кровотечения
Важно учитывать, что повышенный или пониженный прогестерон может быть результатом приёма различных медикаментозных препаратов.
Как делают анализ на прогестерон?
Обычно анализ на прогестерон сдают в период после овуляции — как правило, на 23—24 день (при цикле 29—30 дней). Перед исследованием нужно 8—10 часов ничего не есть и не пить ничего, кроме воды. Анализ сдаётся утром, натощак.
Расшифровка результатов. Нормы прогестерона в крови
Нормы прогестерона (нмоль/л)
Взрослые мужчины:
Взрослые женщины:
- Фолликулярная фаза: от 0,32 до 2,23
- Овуляторная фаза: от 0,48 до 9,41
- Лютеиновая фаза: от 6,99 до 56,63
Беременные женщины:
- 1 триместр: от 8,9 до 468,4
- 2 триместр: от 71,5 до 303,1
- 3 триместр: от 88,7 до 771,5
Где сделать анализ крови на прогестерон?
Обратитесь в медицинский центр «Здоровье». Мы сделаем анализ точно и быстро, подробно объясним его результаты и, при необходимости, предложим необходимое лечение.
Определение уровня прогестерона в крови
Краткое описание:Прогестерон – это стероидный гормон, основной функцией которого является подготовка организма женщины к беременности. Он вырабатывается желтым телом яичников.
Рекомендуется сдавать анализ на 21-23-й день менструального цикла.
Синонимы (rus): Стероидный гормон желтого тела яичников
Синонимы (eng): Progesterone
Единицы измерения: Нг/мл (нанограмм на миллилитр)
Методы: Иммунохемилюминесцентный анализ
Подготовка к исследованию:
• Не принимать пищу в течение 2-3 часов до исследования, можно пить чистую негазированную воду.
• Исключить прием стероидных и тиреоидных гормонов в течение 48 часов до исследования (по согласованию с врачом).
• Исключить физическое и эмоциональное перенапряжение в течение 24 часов до исследования.
• Не курить в течение 3 часов до исследования.
Тип биоматериала: Венозная кровь
Тип пробирки: Вакуумные пробирки с активатором свертывания крови и гелем (Цвет крышки: красная с желтым кольцом)
Цена услуги: 343 руб
Срок выполнения: один рабочий день.
Референсные значения
Для мужчин: 0,2 – 1,4 нг/мл.
Для женщин: Фолликуляр.фаза 0.2-1.5 нг/мл
Фаза овуляции 0.8-3.0 нг/мл
Лютеиновая фаза 1.7-27 нг/мл
Постменопауза 0.1-0.8 нг/мл
Беременность: 1 триместр 11,52-47,19 нг/мл
2 триместр 16,54-49,90 нг/мл
Причины повышенного уровня прогестерона:
киста яичников,
патологическая беременность, а также пузырный занос или хорионкарцинома,
редкие формы опухолей яичников,
врожденная гиперплазия надпочечников.
Причины пониженного уровня прогестерона:
токсикоз на поздних сроках беременности,
пониженная функциональная активность яичников,
отсутствие менструаций,
внематочная беременность,
угроза выкидыша.
Код: A09.05.151
«Дефицит прогестерона. Риски.» — статья о здоровье
Уфилина Алена Владимировна, акушер-гинеколог
Что такое прогестерон?
Прогестерон — это стероидный гормон, продуцируемый у женщин яичниками и в небольшом количестве надпочечниками. Уровень гормона в крови значительно повышается в период овуляции и снижается к моменту менструации.
Прогестерон и сходные с ним синтетические вещества прогестины играют огромную роль в женском организме: стимулируют рост и развитие железистой ткани молочных желез, принимают участие в трансформации эндометрия, готовят женский организм к беременности и ее вынашиванию, влияют на иммунную систему женщины в период беременности, принимают участие в обмене веществ.
Немного о женской анатомии
Для того, чтобы понять действие и значимость этого гормона повторим анатомию и физиологию женских половых органов. К внутренним женским половым органам относится матка, маточные трубы, яичники и шейка матки. Матка имеет грушевидную форму и расположена в проекции малого таза. В верхней части матки по бокам от нее отходят маточные трубы, которые переходят в яичники. Матка с яичниками составляет репродуктивную систему женского организма. В возрасте 8-13 лет в организме девочки начинает происходить ряд изменений, которые впоследствии приводят к первой менструации. Это условно говорит о готовности организма к зачатию, вынашиванию и рождению ребенка.
Фазы менструации
Менструация — это цикличный процесс, зависимый от выработки и действия гормонов и здоровья женского организма в целом. Она состоит из 3 фаз:
- фазы десквамации (или отторжения слизистой полости матки, самой менструации)
- фазы пролиферации (формирование и рост нового слизистого слоя матки)
- фазы секреции (разрастание и дальнейшее изменение слизистой для подготовки к принятию оплодотворенной яйцеклетки при наступлении беременности)
После очередной прошедшей менструации, организм вновь готов к восстановлению. И здесь начинается фаза пролиферации. В яичниках начинают созревать новые фолликулы. Они вырабатывают эстрогены, под действием которых, происходит рост нового слизистого слоя матки.
И здесь начинается фаза пролиферации. В яичниках начинают созревать новые фолликулы. Они вырабатывают эстрогены, под действием которых, происходит рост нового слизистого слоя матки.
В норме один из фолликулов опережает рост других и называется доминантным. Достигая своего максимального размера, примерно к 14 дню цикла, он лопается и из него выходит яйцеклетка, готовая к оплодотворению. Остальные фолликулы, не достигшие финишной прямой, уменьшаются в размерах и отмирают.
В доминантном фолликуле на месте выхода яйцеклетки формируется желтое тело. Это временная эндокринная железа, которая вырабатывает прогестерон. Под его действием слизистая матки продолжает активно разрастаться, трансформируется, становится более «пышной». В ней начинают синтезироваться ряд питательных веществ, ферментов, необходимых для имплантации плодного яйца. Пик секреции прогестерона приходится на 20-21 день цикла.
Если зачатия не происходит и беременность не наступает, желтое тело прекращает свою деятельность и регрессирует.
Если происходит оплодотворение и развивается беременность, желтое тело продолжает выработку прогестерона для создания благоприятных условий имплантации, развития и вынашивания беременности. С 17-18 недель беременности прогестерон вырабатывает плацента. Необходимость в желтом теле отпадает, и оно регрессирует.
Для чего же нужен прогестерон?
Поскольку этот гормон необходим для успешной подготовки организма к предстоящей беременности, вынашиванию и родам — его называют гормон беременности. Он выполняет следующие функции:
- готовит эндометрий, преобразуя его к имплантации плодного яйца,
- снижает тонус миометрия, препятствуя самопроизвольному аборту,
- поддерживает эндометрий в состоянии, необходимом для роста и развития эмбриона,
- снижает иммунореактивность организма, препятствуя отторжению плодного яйца как инородного тела,
- повышает вязкость слизистой пробки в цервикальном канале шейки матки, тем самым создавая защитные ворота, препятствующие проникновению бактерий и инородных веществ в полость матки,
- стимулирует рост матки во время беременности,
- укрепляет мышечный слой шейки матки, не позволяя ей укорачиваться и расслабляться,
- вызывает задержку жидкости в организме,
- готовит молочные железы к лактации-стимулирует пролиферацию и железистую трансформацию альвеол, где секретируется молоко,
- влияет на обмен веществ в организме, увеличивает накопление жира, влияет на углеводный обмен,
- продукты распада Прогестерона мягко воздействуют на нервную систему, вызывая расслабление и сонливость.

Очень часто невозможность зачатия связана с дефицитом прогестерона.
Причины дефицита прогестерона
- хронические воспалительные заболевания женских половых органов,
- эндокринные нарушения (сахарный диабет, заболевания щитовидной железы, повышенная выработка пролактина, повышенная выработка мужских половых гормонов, эндометриоз),
- полипы, миомы матки,
- онкологические заболевания,
- хронический стресс,
- недостаточность желтого тела,
- осложнения аборта,
- дисфункциональные маточные кровотечения,
- чрезмерные физические нагрузки и различные диеты (снижение массы тела),
- обильные менструации,
- прием некоторых лекарственных средств (антибиотики, обезболивающие препараты, контрацептивные средства и т.д)
Как заподозрить у себя дефицит прогестерона?
- отсутствие беременности,
- нарушение менструального цикла, болезненность менструаций, предменструальный синдром,
- частые головные боли,
- изменение эмоционального фона (плаксивость, раздражительность, резкие перепады настроения),
- повышенная утомляемость, вялость,
- бессонница или сонливость,
- выпадение волос,
- нарушение терморегуляции.

Возможна ли беременность при сниженном уровне прогестерона? Возможна. Но такая беременность протекает с угрозой прерывания, тянущими, ноющими болями внизу живота, кровянистыми выделениями из половых путей, замершей беременностью.
При дефиците прогестерона происходит спазм артерий, расплавление соединительных волокон эндометрия, ухудшение трофики тканей. При таком состоянии без гормональной поддержки выносить такую беременность не удастся.
Проверить свой уровень Прогестерона можно сдав анализ крови на 21-23 дни цикла.
Поделиться
Поделиться
← Назад к спискуСдать анализ крови на Прогестерон в лаборатории KDL
Прогестерон 7.2.А5.201 Общие сведения.
Прогестерон – это стероидный гормон, продуцируемый желтым телом яичника. Его основная функция – подготовка организма женщины к беременности и сопровождение развития плода на раннем сроке.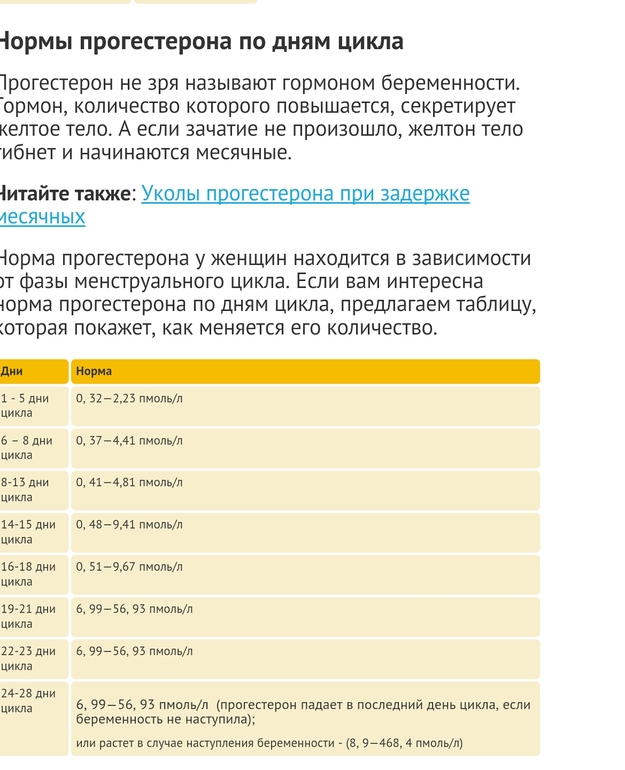 Под его воздействием прогестерона во второй фазе цикла матка становится готовой к имплантации оплодотворенной яйцеклетки. Если же происходит имплантация оплодотворённой яйцеклетки в матку, то желтое тело продолжает продуцировать прогестерон, а яйцеклетка образует трофобласт, который вырабатывает хорионический гонадотропин человека (ХГЧ). Через несколько недель плацента заменяет желтое тело в качестве основного источника гормона, при этом его уровень сохраняется довольно высоким на протяжении всего срока беременности.
Под его воздействием прогестерона во второй фазе цикла матка становится готовой к имплантации оплодотворенной яйцеклетки. Если же происходит имплантация оплодотворённой яйцеклетки в матку, то желтое тело продолжает продуцировать прогестерон, а яйцеклетка образует трофобласт, который вырабатывает хорионический гонадотропин человека (ХГЧ). Через несколько недель плацента заменяет желтое тело в качестве основного источника гормона, при этом его уровень сохраняется довольно высоким на протяжении всего срока беременности.
Прогестерон вырабатывается в небольшом количестве в надпочечниках. У мужчин играет важную роль в процессе сперматогенеза.
В каких случаях обычно назначают исследование?
Анализ на прогестерон – обычный тест при обследовании женщин с бесплодием или с нарушениями менструального цикла. Его также используют при диагностике внематочной или замершей беременности, совместно с измерением ХГЧ.
Что означают результаты теста?
Интерпретация результатов анализа зависит от причины назначения и требует знания фазы менструального цикла или срока беременности пациентки.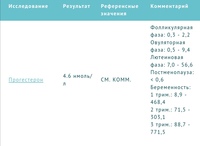
Если уровень прогестерона не повышается и не падает ежемесячно, это говорит об отсутствии овуляции и других нарушениях менструального цикла. Это может быть причиной бесплодия.
Отсутствие повышения концентрации гормона на ранних сроках может указывать на внематочную или замершую беременность, а также быть признаком недостаточной функции желтого тела.
Повышенный уровень прогестерона может наблюдаться при следующих состояниях:
- Нормальная беременность
- Прием гормональных препаратов
- Опухоли яичников
- Врожденная гиперплазия надпочечников
Сроки выполнения теста.
Обычно результат анализа можно получить уже на следующий день.
Как подготовиться к анализу?
Исследование обычно проводится на 19-23 день менструального цикла, если лечащий врач не назначил иначе.
Поддержка лютеиновой фазы при вспомогательной репродукции
Вопрос обзора
Было изучено множество различных способов вмешательства, дозирования и тактик ведения лютеиновой фазы. Мы сравнили семь различных способов и подготовили полный обзор по этой теме.
Мы сравнили семь различных способов и подготовили полный обзор по этой теме.
Актуальность
После овуляции начинается лютеиновая фаза менструального цикла и продолжается до следующей менструации. Остатки овулировавшей яйцеклетки в яичнике известны как ‘corpus luteum’ или желтое тело. Желтое тело вырабатывает гормоны, в том числе прогестерон. Прогестерон стимулирует пролиферацию слизистой оболочки матки для подготовки к имплантации.
Во время осуществления вспомогательной репродукции женский гипофиз десенсибилизируется лекарственными препаратами, что позволяет контролировать стимуляцию яичников. Это способствует образованию более зрелых яйцеклеток, которые могут быть отобраны и оплодотворены вне тела женщины. Гиперстимуляция яичников вызывает дефект лютеиновой фазы, так как желтое тело не способно производить достаточное количество прогестерона.
Поскольку низкий уровень прогестерона может снизить вероятность имплантации, необходимо осуществлять поддержку лютеиновой фазы. Это может включать оральный, вагинальный или внутримышечный прием прогестерона, хорионического гонадотропина человека (ХГЧ) (который стимулирует выработку прогестерона) или агонистов гонадотропин-рилизинг-гормона (ГнРГ). Агонисты ГнРГ стимулируют выработку ГнРГ, гормона, ответственного за фолликулостимулирующий гормон (ФСГ), и лютеинизирующего гормона (ЛГ), который способствует овуляции и развитию желтого тела. Считается, что агонисты ГнРГ восстанавливают уровень ЛГ и естественным образом поддерживают лютеиновую фазу.
Это может включать оральный, вагинальный или внутримышечный прием прогестерона, хорионического гонадотропина человека (ХГЧ) (который стимулирует выработку прогестерона) или агонистов гонадотропин-рилизинг-гормона (ГнРГ). Агонисты ГнРГ стимулируют выработку ГнРГ, гормона, ответственного за фолликулостимулирующий гормон (ФСГ), и лютеинизирующего гормона (ЛГ), который способствует овуляции и развитию желтого тела. Считается, что агонисты ГнРГ восстанавливают уровень ЛГ и естественным образом поддерживают лютеиновую фазу.
Характеристика исследований
Мы нашли 94 рандомизированных контролируемых испытания, в которых сравнивали различные режимы поддержки лютеиновой фазы, в общей сложности, у 26 198 женщин. По нашим наблюдениям, первичным исходом было живорождение или продолжающаяся беременность. Другими исходами были клиническая беременность, синдром гиперстимуляции яичников (СГЯ), выкидыш и многоплодная беременность. Доказательства актуальны на август 2015 года.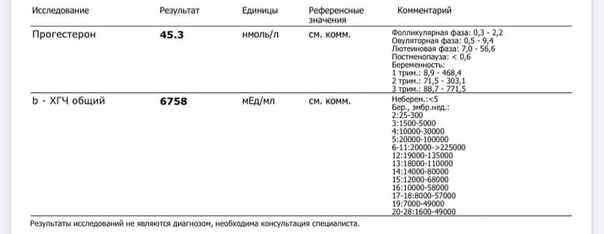
Основные результаты
ХГЧ или прогестерон, полученный во время лютеиновой фазы, может быть связан с более высокой частотой живорождения или продолжающейся беременности, по сравнению с плацебо или отсутствием лечения, но доказательства неоднозначны. Добавление ГнРГ к прогестерону, по всей видимости, улучшает исходы. ХГЧ может увеличить риск СГЯ, по сравнению с плацебо. Более того, ХГЧ, с прогестероном или без, связан с более высокой частотой развития СГЯ, чем прогестерон в одиночку. Ни добавление эстрогена, ни способ введения прогестерона не связаны с улучшением исходов.
Качество доказательств
Доказательства большинства сравнений были низкого или очень низкого качества. Основными ограничениями в доказательствах были неудовлетворительные отчеты о методах исследования и неточности из-за небольших размеров выборки.
Прогестерон | Биомедика
Синонимы: определение концентрации прогестерона, Progesteron, гестаген, P4, pregn-4-ene-3,20-dione.
Связанные тесты: Лютеинизирующий гормон (ЛГ), Фолликулостимулирующий гормон (ФСГ), Хорионический гонадотропин (ХГЧ), тиреотропный гормон (ТТГ), Т4 свободный, адренокортикотропный гормон (АКТГ).
Исследование позволит вашему врачу:Определение концентрации прогестерона в крови проводится при оценке репродуктивной функции.
- Диагностировать нарушение в репродуктивной системе;
- Диагностировать причину бесплодия;
- Выбрать эффективную тактику лечения;
- Контролировать гормональную терапию.
Исследование рекомендуется проводить при:
- нарушении менструального цикла;
- нарушении в репродуктивной системе;
- бесплодии;
- наблюдении за индуцированной овуляцией;
- контроле терапии прогестероном и его аналогами.
Метод:
Иммуноферментный анализ (ИФА).
Чувствительность:
Не менее 0,3 нмоль/л.
Материал для исследования:
Сыворотка крови.
Подготовка к исследованиюИсследование рекомендуется проводить утром натощак; после пробуждения должно пройти 2-3 часа.
Женщины сдают на 22-23 день менструального цикла (или за неделю до предполагаемого начала менструации).
Беременные женщины сдают в любой день.
Особые условия:
Предварительная запись не требуется.
Формат выдачи результата:
Количество прогестерона в 1 л сыворотки крови (нмоль/л).
Норма прогестерона:
Для мужчин: 0,4 – 3,5 нмоль/л;
Для женщин: фолликулярная фаза – не более 5,0 нмоль/л
Лютеиновая фаза – 6 – 70 нмоль/л
Беременные женщины: более 100 нмоль/л
Комментарий:
Повышенный уровень прогестерона может свидетельствовать о:
- беременности;
- нарушении цикла;
- маточных кровотечениях;
- проблемах в работе надпочечников;
- почечной недостаточности;
- нарушениях в работе плаценты;
- многоплодной беременности;
- кистах на яичниках;
- миоме;
- сахарном диабете;
Сниженный уровень прогестерона может свидетельствовать о:
- нарушении цикла;
- отсутствии овуляции;
- воспалительных процессах;
- маточных кровотечениях;
- угрозе выкидыша;
- невынашивании беременности;
- задержке развития плода;
- перенашивании.
Диагноз ставит врач на основании клинических данных и результатах других исследований.
Гормоны во время беременности
Стероидные гормоны, такие как прогестерон, широко изучались в литературе, и в различной литературе возникают разногласия по их использованию на ранних сроках беременности. Целью обзора была роль в предотвращении абортов, повторного невынашивания беременности и преждевременных родов. Была проанализирована роль добавок эстрогена и прогестерона в вспомогательной репродукции. Факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции
Производство стероидных гормонов и требует использования
Прогестерон
Прогестерон в основном вырабатывается желтым телом примерно до 10 недель беременности. 1 Исследование недостаточности яичников и вспомогательной репродукции показало, что сто мг фосфора, вероятно, были супрафизиологической дозой для поддержки беременности через 6-8 недель после зачатия. Фетоплацентарное отделение было пригодным на сроке от 10 до 12 недель беременности. 2 Когда беременность достигает срока, уровень прогестерона колеблется от 100 до 200 нг / мл, а плацента вырабатывает около 250 мг / день. Почти весь прогестерон, продуцируемый плацентой, попадает в плаценту, в отличие от эстрогена.Производство прогестерона не зависит от наличия предшественника, состояния плода, включая самочувствие.
На ранних сроках беременности у матери повышается уровень 17 α-гидроксипрогестерона, что свидетельствует об активности желтого тела. К десятой неделе беременности это соединение вернулось к исходному уровню, что указывает на то, что плацента имеет небольшую активность 17a-гидроксилазы. Однако, начиная примерно с недели 32, 9, 11, 9, 12, происходит второй, более постепенный рост 17a-гидроксипрогестерона из-за использования плацентой предшественников плода.Это важно для понимания профилактики преждевременных родов. Прогестерон также играет важную роль в подавлении материнского иммунологического ответа на антигены плода, тем самым предотвращая материнское отторжение трофобласта. И, конечно же, прогестерон подготавливает и поддерживает эндометрий, что позволяет провести имплантацию раньше. Исследования показали, что желтое тело человека вырабатывает значительное количество эстрадиола, но для успешной имплантации требуется прогестерон, а не эстроген. 3
Эстроген
В плаценте нет всех необходимых ферментов для производства эстрогенов из холестерина или даже прогестерона.В человеческом трофобласте отсутствует 17-гидроксилаза, и поэтому он не может преобразовывать C21-стероиды в C19-стероиды, непосредственные предшественники эстрогена. Чтобы обойти этот дефицит, дегидроизоандростерон сульфат (DHA) из надпочечников плода превращается трофобластами в эстрадиол-17ί. В своем ключевом месте в качестве промежуточной станции между матерью и плодом плацента может использовать прекурсоры от матери или плода, чтобы обойти свой собственный дефицит ферментативной активности. Гормоны действуют как катализаторы химических изменений на клеточном уровне, которые необходимы для роста, развития и получения энергии.У плода отсутствует 3B-гидроксистероиддегидрогеназа, поэтому он не может производить прогестерон, заимствованный из плаценты. Взамен плод дает плаценте то, чего ему не хватает (19 соединений углерода) — предшественника эстрогена.
Белковые гормоны
Белковые гормоны: плацентарный лактоген человека (hPL), хорионический гонадотропин человека (hCG), адренокортикотропный агент (ACTH), вариант гормона роста (hGH-V), белок, связанный с паратиреоидным гормоном (PTH-rP) , Кальцитонин, релаксин, ингибины активины, предсердный натрийуретический пептид, гипоталамические рилизинг-гормоны и ингибирующие гормоны, тиротропин-рилизинг-гормон (TRH), гонадотропин-рилизинг-гормон (GnRH), кортикотропин-рилизинг-гормон (CRH), соматостатин, соматостатин GHRH), альфа-фетопротеин, пролактин, релаксин и другие децидуальные белки.В связи с полнотой вариантов описания гормонов, в этой главе обсуждается клиническая важность ХГЧ для терапии.
Хорионический гонадотропин человека
Наиболее изученным продуктом гормона трофобласта является ХГЧ. Во время беременности этот гликопротеин имеет решающее значение, поскольку он спасает желтое тело от инволюции и поддерживает секрецию прогестерона клетками гранулезы яичника. Его полезность в качестве диагностического маркера беременности связана с тем, что он может быть одним из самых ранних секретируемых продуктов концепта.Во время беременности плацентарная продукция ХГЧ находится на пике между восьмой и десятой неделями беременности и имеет тенденцию к плато на более низком уровне на протяжении оставшейся части беременности.
Единственная определенно известная функция для ХГЧ — это поддержка желтого тела (ХТ), заменяющая ЛГ примерно на восьмой день после овуляции, через 1 день после имплантации, когда b-ХГЧ впервые может быть обнаружен в материнской крови. На стадии 8 клеток ХГЧ был обнаружен в эмбрионе с помощью методов молекулярной биологии.
Имплантация происходит через 5-6 дней после овуляции, а ХГЧ должен появиться к 10 дню овуляции (4 дня после овуляции), чтобы спасти желтое тело.Следовательно, бластоциста должна имплантироваться в узкий промежуток времени. Стимуляция ХГЧ приводит к ежедневной секреции 25 мг P и 0,5 мг E2. Экспрессия гена ХГЧ присутствует как в цитотрофобласте, так и в синцитиотрофобласте, но синтезируется в основном в синцитиотрофобласте. Концентрация циркулирующего ХГЧ у матери составляет примерно 100 МЕ / л во время ожидаемой, но пропущенной менструации. Максимальный уровень около 100 000 МЕ / л в кровотоке матери достигается на 8-10 неделе беременности. Есть два клинических состояния, при которых титры ХГЧ в крови особенно полезны: трофобластическая болезнь и внематочная беременность.Трофобластическая болезнь отличается очень высоким уровнем b-ХГЧ (в 3-100 раз выше, чем при нормальной беременности). Внематочная продукция α- и β-ХГЧ нетрофобластическими опухолями встречается редко, но все же происходит.
Человеческий плацентарный лактоген (hPL) секретируется в основном в материнский кровоток, большинство его функций происходит в местах действия в материнских тканях. Считается, что плацентарный лактоген человека ответственен за заметное повышение концентрации инсулиноподобного фактора роста-1 (IGF-1) в плазме крови матери по мере приближения срока беременности.Плацентарный лактоген человека оказывает метаболическое действие во время беременности через IGF-I. Он связан с инсулинорезистентностью, увеличивает секрецию инсулина, который стимулирует липолиз, увеличивает количество свободных жирных кислот в крови и ингибирует глюконеогенез; по сути, он противодействует действию инсулина, вызывает непереносимость глюкозы, а также липолиз и протеолиз в материнской системе. Таким образом, в клинической практике подчеркивается роль универсального скрининга аномального уровня сахара в крови в начале третьего триместра.
Концентрация кальция у плода регулируется перемещением кальция через плаценту из материнского компартмента. Чтобы поддерживать рост костей плода, материнский отсек подвергается корректировкам, которые обеспечивают чистый перенос достаточного количества кальция к плоду. Изменения материнского компартмента, которые способствуют накоплению кальция, включают увеличение потребления с пищей матери, повышение уровня D3 у матери и повышение уровней паратироидного гормона.
Добавка прогестерона во время беременности: иммунологическая терапия
Есть несколько исследований, чтобы понять поддержание беременности с помощью прогестерона.Было показано, что прогестерон увеличивает количество цитокинов, продуцируемых клетками Th3, которые преобладают над цитокинами, продуцируемыми клетками Th2, что приводит к поддержанию беременности. Клетки Th3 доминируют в децидуальной оболочке на ранних сроках беременности у людей. Цитокины, производные от Th3, ИЛ-4 и ИЛ-6, индуцируют высвобождение ХГЧ из трофобластов, а ХГЧ стимулирует выработку прогестерона желтым телом во время беременности. Было показано, что прогестерон стимулирует секрецию Th3 и снижает секрецию цитокинов Th2.Таким образом, поддержание беременности приписывается цитокину типа Th3. Эта роль в контроле иммунной и эндокринной системы, которая способствует функционированию трофобластов в месте имплантации, кажется интересной. 4 Использование прогестагена при угрозе прерывания беременности является спорным вопросом. 5
Прогестерон при повторном невынашивании беременности
Прогестоген использовался в течение нескольких лет, даже до того, как стали известны иммуномодулирующие свойства прогестерона.С того времени были проведены исследования разного качества, чтобы доказать преимущества приема прогестагенов у больных женщин. Исследование 146 женщин, у которых было легкое или умеренное вагинальное кровотечение в первом триместре беременности, было рандомизировано для приема перорального дидрогестерона (10 мг два раза в день) ( n = 86) или отсутствия лечения ( n = 60). Дидрогестерон был продолжен до 1 недели после остановки кровотечения. Частота невынашивания беременности была значительно ниже в группе дидрогестерона, чем в группе без лечения (17.5% против . 25%; P <0,05). 6 Большинство процитированных клинических испытаний выявили тенденцию к улучшению показателей беременности и увеличению рождаемости в группе лечения прогестагеном, но, к сожалению, многие исследования имели плохой дизайн и методические недостатки. 7 Несколько исследований показали, что поддерживающая терапия на ранних сроках беременности оказывает значительное положительное влияние на исход беременности. Женщин с иным необъяснимым повторным невынашиванием беременности следует проконсультировать относительно возможности успешной беременности без какого-либо лечения, кроме поддерживающей терапии, такой как добавка фолиевой кислоты или витаминов. 7 , 8 Прогестаген вводят в различных формах, но обычно рекомендуется исключительное использование прогестагена без какого-либо (анти-) андрогенного или (анти-) эстрогенного действия. Добавки с прогестагеном доступны в виде вагинальных суппозиториев (0,4 г / день, предпочтительно вечером, потому что естественный прогестерон может вызвать усталость), внутримышечной инъекции (250 мг гидроксипрогестерона в неделю) или перорального приема (например, 10 мг дидрогестерона, стереоизомера природного прогестерона. 9
Добавки прогестерона после вспомогательных репродуктивных технологий
Использование добавок прогестерона в циклах ВРТ более понятно. 10 Продолжительность приема прогестерона после репродуктивной технологии (ВРТ) изучалась в ретроспективном когортном исследовании. Одна группа получала прогестерон в течение первого триместра беременности (протокол первого триместра) до 12 недель, а вторая группа прекращала прием прогестерона после положительного результата теста на бета-ХГЧ через 2 недели после извлечения (лютеиновый протокол).Сходная частота клинических беременностей произошла на сроке 7 недель (81,8% протокол лютеиновой беременности против 85,8% протокола первого триместра) и по частоте живорождений (76,8% протокол лютеиновой беременности против 75,0% протоколу первого триместра). Наблюдалась тенденция к более высокому уровню выкидышей после 7 недель в группе протокола первого триместра (15,5% по сравнению с 4,4%), что указывает на то, что добавление прогестерона в первом триместре может поддерживать раннюю беременность в течение 7 недель за счет отсрочки выкидыша, но не улучшает коэффициенты живорождения.Существуют рандомизированные испытания, поддерживающие рутинное использование лютеиновой поддержки в циклах АРТ с использованием агонистов или антагонистов ГнРГ. Пятьдесят девять исследований были включены в обзор для оценки поддержки лютеиновой фазы с помощью ХГЧ по сравнению с плацебо или отсутствием лечения с точки зрения увеличения частоты продолжающихся беременностей. Поддержка лютеиновой фазы с помощью ХГЧ или прогестерона после вспомогательной репродукции приводит к увеличению частоты наступления беременности. ХГЧ не дает лучших результатов, чем прогестерон, и связан с большим риском СГЯ при использовании с ГнРГ.Оптимальный способ введения прогестерона еще не установлен. 11 Обзор показал значительный эффект в пользу прогестерона для поддержки лютеиновой фазы, в пользу синтетического прогестерона перед микронизированным прогестероном. 12
Профилактика повторных преждевременных родов с помощью 17 альфа-гидроксипрогестерона капроата
Следует ожидать и предотвращать преждевременные роды для снижения перинатальной заболеваемости и смертности. Те женщины, у которых ранее были самопроизвольные преждевременные роды, имеют значительно повышенный риск преждевременных родов при последующих беременностях.Результаты нескольких небольших исследований показали, что 17-альфа-гидроксипрогестерона капроат (17P) может снизить риск преждевременных родов. Было проведено двойное слепое плацебо-контролируемое исследование с участием беременных женщин с задокументированной историей самопроизвольных преждевременных родов. 13 Всего для исследования было выбрано 19 клинических центров, в которые были включены беременные женщины на сроке от 16 до 20 недель гестации, которые были случайным образом распределены центральным центром обработки данных в соотношении 2: 1 для получения либо 250 инъекций еженедельно. мг 17P или еженедельные инъекции инертного масляного плацебо; инъекции продолжали до родов или до 36 недель беременности.Лечение 17P значительно снизило риск родов на сроке менее 37 недель гестации, который составил 36,3% в группе прогестерона против . 54,9 процента в группе плацебо; относительный риск при родах на сроке менее 35 недель беременности составил 20,6% против . 30,7 процента; а роды на сроке менее 32 недель беременности составили 11,4 процента против 19,6 процента. Частота некротического энтероколита, внутрижелудочкового кровоизлияния у младенцев у женщин, получавших 17Р, значительно ниже и потребность в дополнительном кислороде.Таким образом, исследование пришло к выводу, что еженедельные инъекции 17P привели к значительному снижению частоты повторных преждевременных родов среди женщин, которые подвергались особенно высокому риску преждевременных родов, и снизили вероятность нескольких осложнений у их младенцев. В одном двойном слепом рандомизированном плацебо-контролируемом исследовании сообщалось о более низкой частоте преждевременных родов при использовании внутримышечного 17-альфа-гидроксипрогестерона капроата (17P) или интравагинальных микронизированных прогестероновых суппозиториев у женщин с риском преждевременных родов. 14 Период полураспада 17P оценивается примерно в 7,8 дня. Способ введения играет важную роль в профиле безопасности и эффективности препарата. Пероральный прогестерон не применялся для предотвращения преждевременных родов из-за его первого прохождения через печеночный метаболизм, а также отсутствуют данные об эффективности, высоком профиле побочных эффектов и из-за крайней изменчивости концентраций в плазме. Вагинальное введение прогестерона позволяет избежать метаболизма через печень при первом прохождении и связано с быстрым всасыванием, высокой биодоступностью и местным воздействием на эндометрий. 15 Вагинальный путь введения не вызывает местной боли и мало побочных эффектов, это связано с различными концентрациями в крови. 16 Для изучения эффективности прогестерона для поддерживающей токолитической терапии после угрозы преждевременных родов было проведено рандомизированное контролируемое исследование. 17 Исследование проводилось на 70 женщинах с симптомами угрозы преждевременных родов, которые после прекращения активности матки были рандомизированы на терапию прогестероном или отсутствие лечения, и цель этого исследования состояла в том, чтобы определить, можно ли вводить вагинальный прогестерон после подавления активности матки. преждевременные роды связаны с увеличенным латентным периодом и уменьшением повторения преждевременных родов.Группа лечения получала суппозиторий с прогестероном (400 мг) ежедневно до родов, а контрольная группа не получала лечения. В исследовании сделан вывод о том, что использование вагинальных суппозиториев с прогестероном после успешного парентерального токолиза связано с более длительным латентным периодом до родов, но не снижает частоту повторных госпитализаций по поводу преждевременных родов. Добавление дидрогестерона женщинам с угрозой преждевременных родов оказало влияние на цитокиновый профиль, гормональный профиль и фактор блокирования, вызванный прогестероном. 18
Исследование восьмидесяти трех женщин с симптомами угрозы преждевременных родов было рандомизировано в исследуемые группы, получавшие токолитическое лечение в сочетании с интравагинальным микронизированным естественным прогестероном (200 мг в день), или в контрольную группу, получающую только токолиз. Обработка микронизированного природного прогестерона привела к увеличению латентного периода 32,1 ± 17,8 дня по сравнению с 21,2 ± 16,3 дня в контрольной группе и увеличению веса при рождении 2 982,8 ± 697,8 г против 2585,3 ± 746,6 г. 19
Добавки эстрадиола во время лютеиновой фазы in vitro циклов оплодотворения
Было проведено проспективное рандомизированное исследование, чтобы найти оптимальную дозу эстрадиола (E2) для поддержки лютеиновой фазы путем добавления различных доз E2 для поддержки лютеиновой фазы прогестерона (P) у пациентов, подвергающихся лечению длительным оплодотворением (ЭКО) с помощью длинного агониста ГнРГ in vitro . 20 Двести восемьдесят пять женщин, проходящих лечение ЭКО с использованием длительного протокола агонистов ГнРГ, были проспективно рандомизированы на три группы. Группа 1 ( n = 95) получала P и 2 мг E2, группа 2 ( n = 95) получала P и 4 мг E2, а группа 3 ( n = 95) получала P и 6 мг E2 в качестве лютеиновой фазы. служба поддержки. Первичным результатом была частота клинической беременности (PR). Второстепенными интересующими переменными были частота имплантации (IR), частота выкидышей и множественное PR.Клинический PR составил 31,6%, 40% и 32% соответственно в группах 1, 2 и 3, и различия между группами не были статистически значимыми. Однако частота выкидышей была значительно ниже в группе 2 (2,6%), чем в группе 1 (20%), но не была значительно ниже, чем в группе 3 (9,6%). Исследование пришло к выводу, что добавление 2, 4 или 6 мг перорального E2 к P в лютеиновой фазе не создает статистической разницы в показателях частоты наступления беременности. Однако при использовании 2 мг E2 была обнаружена значительно более высокая частота выкидышей.Следовательно, при поддержке лютеиновой фазы 4 мг перорального эстрадиола в дополнение к прогестерону можно рассматривать как снижение частоты выкидышей. По-прежнему необходимы дополнительные исследования для определения группы риска, оптимального гестационного возраста на момент начала, способа введения, дозы прогестерона и долгосрочной безопасности.
Заболевания щитовидной железы
Это имеет большое влияние на фертильность. Глобулин, связывающий половые гормоны (ГСПГ), изменяется при гипертиреозе и гипотиреозе.Он также изменяет уровень пролактина, гонадотропин-рилизинг-гормона и половых стероидов в сыворотке крови. Он также может иметь прямое воздействие на ооциты, поскольку известно, что специфические сайты связывания тироксина обнаруживаются на ооцитах мыши и человека. Также существует связь между дисфункцией щитовидной железы у женщин и заболеваемостью и исходом беременности. У мужчин гипертиреоз вызывает снижение подвижности сперматозоидов. Количество морфологически аномальных сперматозоидов увеличивается при гипотиреозе. Было обнаружено, что при восстановлении эутиреоза оба нарушения улучшаются или нормализуются.У женщин изменения фертильности, вызванные заболеваниями щитовидной железы, более сложны. Гипер- и гипотиреоз являются основными заболеваниями щитовидной железы, которые отрицательно влияют на репродуктивную функцию женщин и вызывают нарушения менструального цикла, в основном гипоменорею и полименорею при гипертиреозе и олигоменорею при гипотиреозе. Все факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции. 21
Контролируемая гиперстимуляция яичников приводит к повышению уровня эстрадиола, что, в свою очередь, может отрицательно влиять на гормоны щитовидной железы и ТТГ. Гиперстимуляция яичников может стать серьезной при наличии аутоиммунного заболевания щитовидной железы в зависимости от ранее существовавших патологий щитовидной железы. Аутоиммунное заболевание щитовидной железы встречается у 5-20% беременных, не прошедших отбор. Изолированная гипотироксинемия описана примерно в 2% беременностей без повышения уровня ТТГ в сыворотке и аутоантител к щитовидной железе.Существует связь между повышенным уровнем самопроизвольных абортов, преждевременных родов и / или низкой массой тела при рождении, дистрессом плода в родах и, возможно, гипертензией, вызванной беременностью, и отслойкой плаценты при явном гипотиреозе. Все антитиреоидные препараты проникают через плаценту и потенциально могут повлиять на функцию щитовидной железы плода. 22
Заболевания щитовидной железы часто встречаются у женщин во время беременности. Если не лечить, как гипотиреоз, так и гипертиреоз связаны с неблагоприятным воздействием на беременность и исходы плода.Важно правильно идентифицировать эти расстройства и лечить их соответствующим образом, чтобы предотвратить осложнения, связанные с беременностью. Показанным лечением является левотироксин при гипотиреозе, а тиоамиды — средство выбора при гипертиреозе; В отдельных случаях может быть показана тиреоидэктомия. 23 , 24 Кокрановский обзор трех РКИ с участием 314 женщин показал в одном испытании с участием 115 женщин, что терапия левотироксином для лечения беременных эутиреоидных женщин антителами к пероксидазе щитовидной железы не снижает преэклампсию, но значительно снижает преждевременные роды на 72 человека. %.В одном испытании с участием 30 женщин с гипотиреозом сравнивали дозы левотироксина, но сообщали только биохимические результаты. В исследовании с участием 169 женщин сравнивали микроэлемент селенометионин (селен) с плацебо, и не было обнаружено значительных различий ни для преэклампсии, ни для преждевременных родов. Ни в одном из трех испытаний не сообщалось о задержке нервного развития у детей. 25
Гормоны во время беременности
Стероидные гормоны, такие как прогестерон, широко изучались в литературе, что вызывает разногласия по поводу их использования на ранних сроках беременности.Целью обзора была роль в предотвращении абортов, повторного невынашивания беременности и преждевременных родов. Была проанализирована роль добавок эстрогена и прогестерона в вспомогательной репродукции. Факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции
Производство стероидных гормонов и требует использования
Прогестерон
Прогестерон в основном вырабатывается желтым телом примерно до 10 недель беременности. 1 Исследование недостаточности яичников и вспомогательной репродукции показало, что сто мг фосфора, вероятно, были супрафизиологической дозой для поддержки беременности через 6-8 недель после зачатия. Фетоплацентарное отделение было пригодным на сроке от 10 до 12 недель беременности. 2 Когда беременность достигает срока, уровень прогестерона колеблется от 100 до 200 нг / мл, а плацента вырабатывает около 250 мг / день. Почти весь прогестерон, продуцируемый плацентой, попадает в плаценту, в отличие от эстрогена.Производство прогестерона не зависит от наличия предшественника, состояния плода, включая самочувствие.
На ранних сроках беременности у матери повышается уровень 17 α-гидроксипрогестерона, что свидетельствует об активности желтого тела. К десятой неделе беременности это соединение вернулось к исходному уровню, что указывает на то, что плацента имеет небольшую активность 17a-гидроксилазы. Однако, начиная примерно с недели 32, 9, 11, 9, 12, происходит второй, более постепенный рост 17a-гидроксипрогестерона из-за использования плацентой предшественников плода.Это важно для понимания профилактики преждевременных родов. Прогестерон также играет важную роль в подавлении материнского иммунологического ответа на антигены плода, тем самым предотвращая материнское отторжение трофобласта. И, конечно же, прогестерон подготавливает и поддерживает эндометрий, что позволяет провести имплантацию раньше. Исследования показали, что желтое тело человека вырабатывает значительное количество эстрадиола, но для успешной имплантации требуется прогестерон, а не эстроген. 3
Эстроген
В плаценте нет всех необходимых ферментов для производства эстрогенов из холестерина или даже прогестерона.В человеческом трофобласте отсутствует 17-гидроксилаза, и поэтому он не может преобразовывать C21-стероиды в C19-стероиды, непосредственные предшественники эстрогена. Чтобы обойти этот дефицит, дегидроизоандростерон сульфат (DHA) из надпочечников плода превращается трофобластами в эстрадиол-17ί. В своем ключевом месте в качестве промежуточной станции между матерью и плодом плацента может использовать прекурсоры от матери или плода, чтобы обойти свой собственный дефицит ферментативной активности. Гормоны действуют как катализаторы химических изменений на клеточном уровне, которые необходимы для роста, развития и получения энергии.У плода отсутствует 3B-гидроксистероиддегидрогеназа, поэтому он не может производить прогестерон, заимствованный из плаценты. Взамен плод дает плаценте то, чего ему не хватает (19 соединений углерода) — предшественника эстрогена.
Белковые гормоны
Белковые гормоны: плацентарный лактоген человека (hPL), хорионический гонадотропин человека (hCG), адренокортикотропный агент (ACTH), вариант гормона роста (hGH-V), белок, связанный с паратиреоидным гормоном (PTH-rP) , Кальцитонин, релаксин, ингибины активины, предсердный натрийуретический пептид, гипоталамические рилизинг-гормоны и ингибирующие гормоны, тиротропин-рилизинг-гормон (TRH), гонадотропин-рилизинг-гормон (GnRH), кортикотропин-рилизинг-гормон (CRH), соматостатин, соматостатин GHRH), альфа-фетопротеин, пролактин, релаксин и другие децидуальные белки.В связи с полнотой вариантов описания гормонов, в этой главе обсуждается клиническая важность ХГЧ для терапии.
Хорионический гонадотропин человека
Наиболее изученным продуктом гормона трофобласта является ХГЧ. Во время беременности этот гликопротеин имеет решающее значение, поскольку он спасает желтое тело от инволюции и поддерживает секрецию прогестерона клетками гранулезы яичника. Его полезность в качестве диагностического маркера беременности связана с тем, что он может быть одним из самых ранних секретируемых продуктов концепта.Во время беременности плацентарная продукция ХГЧ находится на пике между восьмой и десятой неделями беременности и имеет тенденцию к плато на более низком уровне на протяжении оставшейся части беременности.
Единственная определенно известная функция для ХГЧ — это поддержка желтого тела (ХТ), заменяющая ЛГ примерно на восьмой день после овуляции, через 1 день после имплантации, когда b-ХГЧ впервые может быть обнаружен в материнской крови. На стадии 8 клеток ХГЧ был обнаружен в эмбрионе с помощью методов молекулярной биологии.
Имплантация происходит через 5-6 дней после овуляции, а ХГЧ должен появиться к 10 дню овуляции (4 дня после овуляции), чтобы спасти желтое тело.Следовательно, бластоциста должна имплантироваться в узкий промежуток времени. Стимуляция ХГЧ приводит к ежедневной секреции 25 мг P и 0,5 мг E2. Экспрессия гена ХГЧ присутствует как в цитотрофобласте, так и в синцитиотрофобласте, но синтезируется в основном в синцитиотрофобласте. Концентрация циркулирующего ХГЧ у матери составляет примерно 100 МЕ / л во время ожидаемой, но пропущенной менструации. Максимальный уровень около 100 000 МЕ / л в кровотоке матери достигается на 8-10 неделе беременности. Есть два клинических состояния, при которых титры ХГЧ в крови особенно полезны: трофобластическая болезнь и внематочная беременность.Трофобластическая болезнь отличается очень высоким уровнем b-ХГЧ (в 3-100 раз выше, чем при нормальной беременности). Внематочная продукция α- и β-ХГЧ нетрофобластическими опухолями встречается редко, но все же происходит.
Человеческий плацентарный лактоген (hPL) секретируется в основном в материнский кровоток, большинство его функций происходит в местах действия в материнских тканях. Считается, что плацентарный лактоген человека ответственен за заметное повышение концентрации инсулиноподобного фактора роста-1 (IGF-1) в плазме крови матери по мере приближения срока беременности.Плацентарный лактоген человека оказывает метаболическое действие во время беременности через IGF-I. Он связан с инсулинорезистентностью, увеличивает секрецию инсулина, который стимулирует липолиз, увеличивает количество свободных жирных кислот в крови и ингибирует глюконеогенез; по сути, он противодействует действию инсулина, вызывает непереносимость глюкозы, а также липолиз и протеолиз в материнской системе. Таким образом, в клинической практике подчеркивается роль универсального скрининга аномального уровня сахара в крови в начале третьего триместра.
Концентрация кальция у плода регулируется перемещением кальция через плаценту из материнского компартмента. Чтобы поддерживать рост костей плода, материнский отсек подвергается корректировкам, которые обеспечивают чистый перенос достаточного количества кальция к плоду. Изменения материнского компартмента, которые способствуют накоплению кальция, включают увеличение потребления с пищей матери, повышение уровня D3 у матери и повышение уровней паратироидного гормона.
Добавка прогестерона во время беременности: иммунологическая терапия
Есть несколько исследований, чтобы понять поддержание беременности с помощью прогестерона.Было показано, что прогестерон увеличивает количество цитокинов, продуцируемых клетками Th3, которые преобладают над цитокинами, продуцируемыми клетками Th2, что приводит к поддержанию беременности. Клетки Th3 доминируют в децидуальной оболочке на ранних сроках беременности у людей. Цитокины, производные от Th3, ИЛ-4 и ИЛ-6, индуцируют высвобождение ХГЧ из трофобластов, а ХГЧ стимулирует выработку прогестерона желтым телом во время беременности. Было показано, что прогестерон стимулирует секрецию Th3 и снижает секрецию цитокинов Th2.Таким образом, поддержание беременности приписывается цитокину типа Th3. Эта роль в контроле иммунной и эндокринной системы, которая способствует функционированию трофобластов в месте имплантации, кажется интересной. 4 Использование прогестагена при угрозе прерывания беременности является спорным вопросом. 5
Прогестерон при повторном невынашивании беременности
Прогестоген использовался в течение нескольких лет, даже до того, как стали известны иммуномодулирующие свойства прогестерона.С того времени были проведены исследования разного качества, чтобы доказать преимущества приема прогестагенов у больных женщин. Исследование 146 женщин, у которых было легкое или умеренное вагинальное кровотечение в первом триместре беременности, было рандомизировано для приема перорального дидрогестерона (10 мг два раза в день) ( n = 86) или отсутствия лечения ( n = 60). Дидрогестерон был продолжен до 1 недели после остановки кровотечения. Частота невынашивания беременности была значительно ниже в группе дидрогестерона, чем в группе без лечения (17.5% против . 25%; P <0,05). 6 Большинство процитированных клинических испытаний выявили тенденцию к улучшению показателей беременности и увеличению рождаемости в группе лечения прогестагеном, но, к сожалению, многие исследования имели плохой дизайн и методические недостатки. 7 Несколько исследований показали, что поддерживающая терапия на ранних сроках беременности оказывает значительное положительное влияние на исход беременности. Женщин с иным необъяснимым повторным невынашиванием беременности следует проконсультировать относительно возможности успешной беременности без какого-либо лечения, кроме поддерживающей терапии, такой как добавка фолиевой кислоты или витаминов. 7 , 8 Прогестаген вводят в различных формах, но обычно рекомендуется исключительное использование прогестагена без какого-либо (анти-) андрогенного или (анти-) эстрогенного действия. Добавки с прогестагеном доступны в виде вагинальных суппозиториев (0,4 г / день, предпочтительно вечером, потому что естественный прогестерон может вызвать усталость), внутримышечной инъекции (250 мг гидроксипрогестерона в неделю) или перорального приема (например, 10 мг дидрогестерона, стереоизомера природного прогестерона. 9
Добавки прогестерона после вспомогательных репродуктивных технологий
Использование добавок прогестерона в циклах ВРТ более понятно. 10 Продолжительность приема прогестерона после репродуктивной технологии (ВРТ) изучалась в ретроспективном когортном исследовании. Одна группа получала прогестерон в течение первого триместра беременности (протокол первого триместра) до 12 недель, а вторая группа прекращала прием прогестерона после положительного результата теста на бета-ХГЧ через 2 недели после извлечения (лютеиновый протокол).Сходная частота клинических беременностей произошла на сроке 7 недель (81,8% протокол лютеиновой беременности против 85,8% протокола первого триместра) и по частоте живорождений (76,8% протокол лютеиновой беременности против 75,0% протоколу первого триместра). Наблюдалась тенденция к более высокому уровню выкидышей после 7 недель в группе протокола первого триместра (15,5% по сравнению с 4,4%), что указывает на то, что добавление прогестерона в первом триместре может поддерживать раннюю беременность в течение 7 недель за счет отсрочки выкидыша, но не улучшает коэффициенты живорождения.Существуют рандомизированные испытания, поддерживающие рутинное использование лютеиновой поддержки в циклах АРТ с использованием агонистов или антагонистов ГнРГ. Пятьдесят девять исследований были включены в обзор для оценки поддержки лютеиновой фазы с помощью ХГЧ по сравнению с плацебо или отсутствием лечения с точки зрения увеличения частоты продолжающихся беременностей. Поддержка лютеиновой фазы с помощью ХГЧ или прогестерона после вспомогательной репродукции приводит к увеличению частоты наступления беременности. ХГЧ не дает лучших результатов, чем прогестерон, и связан с большим риском СГЯ при использовании с ГнРГ.Оптимальный способ введения прогестерона еще не установлен. 11 Обзор показал значительный эффект в пользу прогестерона для поддержки лютеиновой фазы, в пользу синтетического прогестерона перед микронизированным прогестероном. 12
Профилактика повторных преждевременных родов с помощью 17 альфа-гидроксипрогестерона капроата
Следует ожидать и предотвращать преждевременные роды для снижения перинатальной заболеваемости и смертности. Те женщины, у которых ранее были самопроизвольные преждевременные роды, имеют значительно повышенный риск преждевременных родов при последующих беременностях.Результаты нескольких небольших исследований показали, что 17-альфа-гидроксипрогестерона капроат (17P) может снизить риск преждевременных родов. Было проведено двойное слепое плацебо-контролируемое исследование с участием беременных женщин с задокументированной историей самопроизвольных преждевременных родов. 13 Всего для исследования было выбрано 19 клинических центров, в которые были включены беременные женщины на сроке от 16 до 20 недель гестации, которые были случайным образом распределены центральным центром обработки данных в соотношении 2: 1 для получения либо 250 инъекций еженедельно. мг 17P или еженедельные инъекции инертного масляного плацебо; инъекции продолжали до родов или до 36 недель беременности.Лечение 17P значительно снизило риск родов на сроке менее 37 недель гестации, который составил 36,3% в группе прогестерона против . 54,9 процента в группе плацебо; относительный риск при родах на сроке менее 35 недель беременности составил 20,6% против . 30,7 процента; а роды на сроке менее 32 недель беременности составили 11,4 процента против 19,6 процента. Частота некротического энтероколита, внутрижелудочкового кровоизлияния у младенцев у женщин, получавших 17Р, значительно ниже и потребность в дополнительном кислороде.Таким образом, исследование пришло к выводу, что еженедельные инъекции 17P привели к значительному снижению частоты повторных преждевременных родов среди женщин, которые подвергались особенно высокому риску преждевременных родов, и снизили вероятность нескольких осложнений у их младенцев. В одном двойном слепом рандомизированном плацебо-контролируемом исследовании сообщалось о более низкой частоте преждевременных родов при использовании внутримышечного 17-альфа-гидроксипрогестерона капроата (17P) или интравагинальных микронизированных прогестероновых суппозиториев у женщин с риском преждевременных родов. 14 Период полураспада 17P оценивается примерно в 7,8 дня. Способ введения играет важную роль в профиле безопасности и эффективности препарата. Пероральный прогестерон не применялся для предотвращения преждевременных родов из-за его первого прохождения через печеночный метаболизм, а также отсутствуют данные об эффективности, высоком профиле побочных эффектов и из-за крайней изменчивости концентраций в плазме. Вагинальное введение прогестерона позволяет избежать метаболизма через печень при первом прохождении и связано с быстрым всасыванием, высокой биодоступностью и местным воздействием на эндометрий. 15 Вагинальный путь введения не вызывает местной боли и мало побочных эффектов, это связано с различными концентрациями в крови. 16 Для изучения эффективности прогестерона для поддерживающей токолитической терапии после угрозы преждевременных родов было проведено рандомизированное контролируемое исследование. 17 Исследование проводилось на 70 женщинах с симптомами угрозы преждевременных родов, которые после прекращения активности матки были рандомизированы на терапию прогестероном или отсутствие лечения, и цель этого исследования состояла в том, чтобы определить, можно ли вводить вагинальный прогестерон после подавления активности матки. преждевременные роды связаны с увеличенным латентным периодом и уменьшением повторения преждевременных родов.Группа лечения получала суппозиторий с прогестероном (400 мг) ежедневно до родов, а контрольная группа не получала лечения. В исследовании сделан вывод о том, что использование вагинальных суппозиториев с прогестероном после успешного парентерального токолиза связано с более длительным латентным периодом до родов, но не снижает частоту повторных госпитализаций по поводу преждевременных родов. Добавление дидрогестерона женщинам с угрозой преждевременных родов оказало влияние на цитокиновый профиль, гормональный профиль и фактор блокирования, вызванный прогестероном. 18
Исследование восьмидесяти трех женщин с симптомами угрозы преждевременных родов было рандомизировано в исследуемые группы, получавшие токолитическое лечение в сочетании с интравагинальным микронизированным естественным прогестероном (200 мг в день), или в контрольную группу, получающую только токолиз. Обработка микронизированного природного прогестерона привела к увеличению латентного периода 32,1 ± 17,8 дня по сравнению с 21,2 ± 16,3 дня в контрольной группе и увеличению веса при рождении 2 982,8 ± 697,8 г против 2585,3 ± 746,6 г. 19
Добавки эстрадиола во время лютеиновой фазы in vitro циклов оплодотворения
Было проведено проспективное рандомизированное исследование, чтобы найти оптимальную дозу эстрадиола (E2) для поддержки лютеиновой фазы путем добавления различных доз E2 для поддержки лютеиновой фазы прогестерона (P) у пациентов, подвергающихся лечению длительным оплодотворением (ЭКО) с помощью длинного агониста ГнРГ in vitro . 20 Двести восемьдесят пять женщин, проходящих лечение ЭКО с использованием длительного протокола агонистов ГнРГ, были проспективно рандомизированы на три группы. Группа 1 ( n = 95) получала P и 2 мг E2, группа 2 ( n = 95) получала P и 4 мг E2, а группа 3 ( n = 95) получала P и 6 мг E2 в качестве лютеиновой фазы. служба поддержки. Первичным результатом была частота клинической беременности (PR). Второстепенными интересующими переменными были частота имплантации (IR), частота выкидышей и множественное PR.Клинический PR составил 31,6%, 40% и 32% соответственно в группах 1, 2 и 3, и различия между группами не были статистически значимыми. Однако частота выкидышей была значительно ниже в группе 2 (2,6%), чем в группе 1 (20%), но не была значительно ниже, чем в группе 3 (9,6%). Исследование пришло к выводу, что добавление 2, 4 или 6 мг перорального E2 к P в лютеиновой фазе не создает статистической разницы в показателях частоты наступления беременности. Однако при использовании 2 мг E2 была обнаружена значительно более высокая частота выкидышей.Следовательно, при поддержке лютеиновой фазы 4 мг перорального эстрадиола в дополнение к прогестерону можно рассматривать как снижение частоты выкидышей. По-прежнему необходимы дополнительные исследования для определения группы риска, оптимального гестационного возраста на момент начала, способа введения, дозы прогестерона и долгосрочной безопасности.
Заболевания щитовидной железы
Это имеет большое влияние на фертильность. Глобулин, связывающий половые гормоны (ГСПГ), изменяется при гипертиреозе и гипотиреозе.Он также изменяет уровень пролактина, гонадотропин-рилизинг-гормона и половых стероидов в сыворотке крови. Он также может иметь прямое воздействие на ооциты, поскольку известно, что специфические сайты связывания тироксина обнаруживаются на ооцитах мыши и человека. Также существует связь между дисфункцией щитовидной железы у женщин и заболеваемостью и исходом беременности. У мужчин гипертиреоз вызывает снижение подвижности сперматозоидов. Количество морфологически аномальных сперматозоидов увеличивается при гипотиреозе. Было обнаружено, что при восстановлении эутиреоза оба нарушения улучшаются или нормализуются.У женщин изменения фертильности, вызванные заболеваниями щитовидной железы, более сложны. Гипер- и гипотиреоз являются основными заболеваниями щитовидной железы, которые отрицательно влияют на репродуктивную функцию женщин и вызывают нарушения менструального цикла, в основном гипоменорею и полименорею при гипертиреозе и олигоменорею при гипотиреозе. Все факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции. 21
Контролируемая гиперстимуляция яичников приводит к повышению уровня эстрадиола, что, в свою очередь, может отрицательно влиять на гормоны щитовидной железы и ТТГ. Гиперстимуляция яичников может стать серьезной при наличии аутоиммунного заболевания щитовидной железы в зависимости от ранее существовавших патологий щитовидной железы. Аутоиммунное заболевание щитовидной железы встречается у 5-20% беременных, не прошедших отбор. Изолированная гипотироксинемия описана примерно в 2% беременностей без повышения уровня ТТГ в сыворотке и аутоантител к щитовидной железе.Существует связь между повышенным уровнем самопроизвольных абортов, преждевременных родов и / или низкой массой тела при рождении, дистрессом плода в родах и, возможно, гипертензией, вызванной беременностью, и отслойкой плаценты при явном гипотиреозе. Все антитиреоидные препараты проникают через плаценту и потенциально могут повлиять на функцию щитовидной железы плода. 22
Заболевания щитовидной железы часто встречаются у женщин во время беременности. Если не лечить, как гипотиреоз, так и гипертиреоз связаны с неблагоприятным воздействием на беременность и исходы плода.Важно правильно идентифицировать эти расстройства и лечить их соответствующим образом, чтобы предотвратить осложнения, связанные с беременностью. Показанным лечением является левотироксин при гипотиреозе, а тиоамиды — средство выбора при гипертиреозе; В отдельных случаях может быть показана тиреоидэктомия. 23 , 24 Кокрановский обзор трех РКИ с участием 314 женщин показал в одном испытании с участием 115 женщин, что терапия левотироксином для лечения беременных эутиреоидных женщин антителами к пероксидазе щитовидной железы не снижает преэклампсию, но значительно снижает преждевременные роды на 72 человека. %.В одном испытании с участием 30 женщин с гипотиреозом сравнивали дозы левотироксина, но сообщали только биохимические результаты. В исследовании с участием 169 женщин сравнивали микроэлемент селенометионин (селен) с плацебо, и не было обнаружено значительных различий ни для преэклампсии, ни для преждевременных родов. Ни в одном из трех испытаний не сообщалось о задержке нервного развития у детей. 25
Гормоны во время беременности
Стероидные гормоны, такие как прогестерон, широко изучались в литературе, что вызывает разногласия по поводу их использования на ранних сроках беременности.Целью обзора была роль в предотвращении абортов, повторного невынашивания беременности и преждевременных родов. Была проанализирована роль добавок эстрогена и прогестерона в вспомогательной репродукции. Факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции
Производство стероидных гормонов и требует использования
Прогестерон
Прогестерон в основном вырабатывается желтым телом примерно до 10 недель беременности. 1 Исследование недостаточности яичников и вспомогательной репродукции показало, что сто мг фосфора, вероятно, были супрафизиологической дозой для поддержки беременности через 6-8 недель после зачатия. Фетоплацентарное отделение было пригодным на сроке от 10 до 12 недель беременности. 2 Когда беременность достигает срока, уровень прогестерона колеблется от 100 до 200 нг / мл, а плацента вырабатывает около 250 мг / день. Почти весь прогестерон, продуцируемый плацентой, попадает в плаценту, в отличие от эстрогена.Производство прогестерона не зависит от наличия предшественника, состояния плода, включая самочувствие.
На ранних сроках беременности у матери повышается уровень 17 α-гидроксипрогестерона, что свидетельствует об активности желтого тела. К десятой неделе беременности это соединение вернулось к исходному уровню, что указывает на то, что плацента имеет небольшую активность 17a-гидроксилазы. Однако, начиная примерно с недели 32, 9, 11, 9, 12, происходит второй, более постепенный рост 17a-гидроксипрогестерона из-за использования плацентой предшественников плода.Это важно для понимания профилактики преждевременных родов. Прогестерон также играет важную роль в подавлении материнского иммунологического ответа на антигены плода, тем самым предотвращая материнское отторжение трофобласта. И, конечно же, прогестерон подготавливает и поддерживает эндометрий, что позволяет провести имплантацию раньше. Исследования показали, что желтое тело человека вырабатывает значительное количество эстрадиола, но для успешной имплантации требуется прогестерон, а не эстроген. 3
Эстроген
В плаценте нет всех необходимых ферментов для производства эстрогенов из холестерина или даже прогестерона.В человеческом трофобласте отсутствует 17-гидроксилаза, и поэтому он не может преобразовывать C21-стероиды в C19-стероиды, непосредственные предшественники эстрогена. Чтобы обойти этот дефицит, дегидроизоандростерон сульфат (DHA) из надпочечников плода превращается трофобластами в эстрадиол-17ί. В своем ключевом месте в качестве промежуточной станции между матерью и плодом плацента может использовать прекурсоры от матери или плода, чтобы обойти свой собственный дефицит ферментативной активности. Гормоны действуют как катализаторы химических изменений на клеточном уровне, которые необходимы для роста, развития и получения энергии.У плода отсутствует 3B-гидроксистероиддегидрогеназа, поэтому он не может производить прогестерон, заимствованный из плаценты. Взамен плод дает плаценте то, чего ему не хватает (19 соединений углерода) — предшественника эстрогена.
Белковые гормоны
Белковые гормоны: плацентарный лактоген человека (hPL), хорионический гонадотропин человека (hCG), адренокортикотропный агент (ACTH), вариант гормона роста (hGH-V), белок, связанный с паратиреоидным гормоном (PTH-rP) , Кальцитонин, релаксин, ингибины активины, предсердный натрийуретический пептид, гипоталамические рилизинг-гормоны и ингибирующие гормоны, тиротропин-рилизинг-гормон (TRH), гонадотропин-рилизинг-гормон (GnRH), кортикотропин-рилизинг-гормон (CRH), соматостатин, соматостатин GHRH), альфа-фетопротеин, пролактин, релаксин и другие децидуальные белки.В связи с полнотой вариантов описания гормонов, в этой главе обсуждается клиническая важность ХГЧ для терапии.
Хорионический гонадотропин человека
Наиболее изученным продуктом гормона трофобласта является ХГЧ. Во время беременности этот гликопротеин имеет решающее значение, поскольку он спасает желтое тело от инволюции и поддерживает секрецию прогестерона клетками гранулезы яичника. Его полезность в качестве диагностического маркера беременности связана с тем, что он может быть одним из самых ранних секретируемых продуктов концепта.Во время беременности плацентарная продукция ХГЧ находится на пике между восьмой и десятой неделями беременности и имеет тенденцию к плато на более низком уровне на протяжении оставшейся части беременности.
Единственная определенно известная функция для ХГЧ — это поддержка желтого тела (ХТ), заменяющая ЛГ примерно на восьмой день после овуляции, через 1 день после имплантации, когда b-ХГЧ впервые может быть обнаружен в материнской крови. На стадии 8 клеток ХГЧ был обнаружен в эмбрионе с помощью методов молекулярной биологии.
Имплантация происходит через 5-6 дней после овуляции, а ХГЧ должен появиться к 10 дню овуляции (4 дня после овуляции), чтобы спасти желтое тело.Следовательно, бластоциста должна имплантироваться в узкий промежуток времени. Стимуляция ХГЧ приводит к ежедневной секреции 25 мг P и 0,5 мг E2. Экспрессия гена ХГЧ присутствует как в цитотрофобласте, так и в синцитиотрофобласте, но синтезируется в основном в синцитиотрофобласте. Концентрация циркулирующего ХГЧ у матери составляет примерно 100 МЕ / л во время ожидаемой, но пропущенной менструации. Максимальный уровень около 100 000 МЕ / л в кровотоке матери достигается на 8-10 неделе беременности. Есть два клинических состояния, при которых титры ХГЧ в крови особенно полезны: трофобластическая болезнь и внематочная беременность.Трофобластическая болезнь отличается очень высоким уровнем b-ХГЧ (в 3-100 раз выше, чем при нормальной беременности). Внематочная продукция α- и β-ХГЧ нетрофобластическими опухолями встречается редко, но все же происходит.
Человеческий плацентарный лактоген (hPL) секретируется в основном в материнский кровоток, большинство его функций происходит в местах действия в материнских тканях. Считается, что плацентарный лактоген человека ответственен за заметное повышение концентрации инсулиноподобного фактора роста-1 (IGF-1) в плазме крови матери по мере приближения срока беременности.Плацентарный лактоген человека оказывает метаболическое действие во время беременности через IGF-I. Он связан с инсулинорезистентностью, увеличивает секрецию инсулина, который стимулирует липолиз, увеличивает количество свободных жирных кислот в крови и ингибирует глюконеогенез; по сути, он противодействует действию инсулина, вызывает непереносимость глюкозы, а также липолиз и протеолиз в материнской системе. Таким образом, в клинической практике подчеркивается роль универсального скрининга аномального уровня сахара в крови в начале третьего триместра.
Концентрация кальция у плода регулируется перемещением кальция через плаценту из материнского компартмента. Чтобы поддерживать рост костей плода, материнский отсек подвергается корректировкам, которые обеспечивают чистый перенос достаточного количества кальция к плоду. Изменения материнского компартмента, которые способствуют накоплению кальция, включают увеличение потребления с пищей матери, повышение уровня D3 у матери и повышение уровней паратироидного гормона.
Добавка прогестерона во время беременности: иммунологическая терапия
Есть несколько исследований, чтобы понять поддержание беременности с помощью прогестерона.Было показано, что прогестерон увеличивает количество цитокинов, продуцируемых клетками Th3, которые преобладают над цитокинами, продуцируемыми клетками Th2, что приводит к поддержанию беременности. Клетки Th3 доминируют в децидуальной оболочке на ранних сроках беременности у людей. Цитокины, производные от Th3, ИЛ-4 и ИЛ-6, индуцируют высвобождение ХГЧ из трофобластов, а ХГЧ стимулирует выработку прогестерона желтым телом во время беременности. Было показано, что прогестерон стимулирует секрецию Th3 и снижает секрецию цитокинов Th2.Таким образом, поддержание беременности приписывается цитокину типа Th3. Эта роль в контроле иммунной и эндокринной системы, которая способствует функционированию трофобластов в месте имплантации, кажется интересной. 4 Использование прогестагена при угрозе прерывания беременности является спорным вопросом. 5
Прогестерон при повторном невынашивании беременности
Прогестоген использовался в течение нескольких лет, даже до того, как стали известны иммуномодулирующие свойства прогестерона.С того времени были проведены исследования разного качества, чтобы доказать преимущества приема прогестагенов у больных женщин. Исследование 146 женщин, у которых было легкое или умеренное вагинальное кровотечение в первом триместре беременности, было рандомизировано для приема перорального дидрогестерона (10 мг два раза в день) ( n = 86) или отсутствия лечения ( n = 60). Дидрогестерон был продолжен до 1 недели после остановки кровотечения. Частота невынашивания беременности была значительно ниже в группе дидрогестерона, чем в группе без лечения (17.5% против . 25%; P <0,05). 6 Большинство процитированных клинических испытаний выявили тенденцию к улучшению показателей беременности и увеличению рождаемости в группе лечения прогестагеном, но, к сожалению, многие исследования имели плохой дизайн и методические недостатки. 7 Несколько исследований показали, что поддерживающая терапия на ранних сроках беременности оказывает значительное положительное влияние на исход беременности. Женщин с иным необъяснимым повторным невынашиванием беременности следует проконсультировать относительно возможности успешной беременности без какого-либо лечения, кроме поддерживающей терапии, такой как добавка фолиевой кислоты или витаминов. 7 , 8 Прогестаген вводят в различных формах, но обычно рекомендуется исключительное использование прогестагена без какого-либо (анти-) андрогенного или (анти-) эстрогенного действия. Добавки с прогестагеном доступны в виде вагинальных суппозиториев (0,4 г / день, предпочтительно вечером, потому что естественный прогестерон может вызвать усталость), внутримышечной инъекции (250 мг гидроксипрогестерона в неделю) или перорального приема (например, 10 мг дидрогестерона, стереоизомера природного прогестерона. 9
Добавки прогестерона после вспомогательных репродуктивных технологий
Использование добавок прогестерона в циклах ВРТ более понятно. 10 Продолжительность приема прогестерона после репродуктивной технологии (ВРТ) изучалась в ретроспективном когортном исследовании. Одна группа получала прогестерон в течение первого триместра беременности (протокол первого триместра) до 12 недель, а вторая группа прекращала прием прогестерона после положительного результата теста на бета-ХГЧ через 2 недели после извлечения (лютеиновый протокол).Сходная частота клинических беременностей произошла на сроке 7 недель (81,8% протокол лютеиновой беременности против 85,8% протокола первого триместра) и по частоте живорождений (76,8% протокол лютеиновой беременности против 75,0% протоколу первого триместра). Наблюдалась тенденция к более высокому уровню выкидышей после 7 недель в группе протокола первого триместра (15,5% по сравнению с 4,4%), что указывает на то, что добавление прогестерона в первом триместре может поддерживать раннюю беременность в течение 7 недель за счет отсрочки выкидыша, но не улучшает коэффициенты живорождения.Существуют рандомизированные испытания, поддерживающие рутинное использование лютеиновой поддержки в циклах АРТ с использованием агонистов или антагонистов ГнРГ. Пятьдесят девять исследований были включены в обзор для оценки поддержки лютеиновой фазы с помощью ХГЧ по сравнению с плацебо или отсутствием лечения с точки зрения увеличения частоты продолжающихся беременностей. Поддержка лютеиновой фазы с помощью ХГЧ или прогестерона после вспомогательной репродукции приводит к увеличению частоты наступления беременности. ХГЧ не дает лучших результатов, чем прогестерон, и связан с большим риском СГЯ при использовании с ГнРГ.Оптимальный способ введения прогестерона еще не установлен. 11 Обзор показал значительный эффект в пользу прогестерона для поддержки лютеиновой фазы, в пользу синтетического прогестерона перед микронизированным прогестероном. 12
Профилактика повторных преждевременных родов с помощью 17 альфа-гидроксипрогестерона капроата
Следует ожидать и предотвращать преждевременные роды для снижения перинатальной заболеваемости и смертности. Те женщины, у которых ранее были самопроизвольные преждевременные роды, имеют значительно повышенный риск преждевременных родов при последующих беременностях.Результаты нескольких небольших исследований показали, что 17-альфа-гидроксипрогестерона капроат (17P) может снизить риск преждевременных родов. Было проведено двойное слепое плацебо-контролируемое исследование с участием беременных женщин с задокументированной историей самопроизвольных преждевременных родов. 13 Всего для исследования было выбрано 19 клинических центров, в которые были включены беременные женщины на сроке от 16 до 20 недель гестации, которые были случайным образом распределены центральным центром обработки данных в соотношении 2: 1 для получения либо 250 инъекций еженедельно. мг 17P или еженедельные инъекции инертного масляного плацебо; инъекции продолжали до родов или до 36 недель беременности.Лечение 17P значительно снизило риск родов на сроке менее 37 недель гестации, который составил 36,3% в группе прогестерона против . 54,9 процента в группе плацебо; относительный риск при родах на сроке менее 35 недель беременности составил 20,6% против . 30,7 процента; а роды на сроке менее 32 недель беременности составили 11,4 процента против 19,6 процента. Частота некротического энтероколита, внутрижелудочкового кровоизлияния у младенцев у женщин, получавших 17Р, значительно ниже и потребность в дополнительном кислороде.Таким образом, исследование пришло к выводу, что еженедельные инъекции 17P привели к значительному снижению частоты повторных преждевременных родов среди женщин, которые подвергались особенно высокому риску преждевременных родов, и снизили вероятность нескольких осложнений у их младенцев. В одном двойном слепом рандомизированном плацебо-контролируемом исследовании сообщалось о более низкой частоте преждевременных родов при использовании внутримышечного 17-альфа-гидроксипрогестерона капроата (17P) или интравагинальных микронизированных прогестероновых суппозиториев у женщин с риском преждевременных родов. 14 Период полураспада 17P оценивается примерно в 7,8 дня. Способ введения играет важную роль в профиле безопасности и эффективности препарата. Пероральный прогестерон не применялся для предотвращения преждевременных родов из-за его первого прохождения через печеночный метаболизм, а также отсутствуют данные об эффективности, высоком профиле побочных эффектов и из-за крайней изменчивости концентраций в плазме. Вагинальное введение прогестерона позволяет избежать метаболизма через печень при первом прохождении и связано с быстрым всасыванием, высокой биодоступностью и местным воздействием на эндометрий. 15 Вагинальный путь введения не вызывает местной боли и мало побочных эффектов, это связано с различными концентрациями в крови. 16 Для изучения эффективности прогестерона для поддерживающей токолитической терапии после угрозы преждевременных родов было проведено рандомизированное контролируемое исследование. 17 Исследование проводилось на 70 женщинах с симптомами угрозы преждевременных родов, которые после прекращения активности матки были рандомизированы на терапию прогестероном или отсутствие лечения, и цель этого исследования состояла в том, чтобы определить, можно ли вводить вагинальный прогестерон после подавления активности матки. преждевременные роды связаны с увеличенным латентным периодом и уменьшением повторения преждевременных родов.Группа лечения получала суппозиторий с прогестероном (400 мг) ежедневно до родов, а контрольная группа не получала лечения. В исследовании сделан вывод о том, что использование вагинальных суппозиториев с прогестероном после успешного парентерального токолиза связано с более длительным латентным периодом до родов, но не снижает частоту повторных госпитализаций по поводу преждевременных родов. Добавление дидрогестерона женщинам с угрозой преждевременных родов оказало влияние на цитокиновый профиль, гормональный профиль и фактор блокирования, вызванный прогестероном. 18
Исследование восьмидесяти трех женщин с симптомами угрозы преждевременных родов было рандомизировано в исследуемые группы, получавшие токолитическое лечение в сочетании с интравагинальным микронизированным естественным прогестероном (200 мг в день), или в контрольную группу, получающую только токолиз. Обработка микронизированного природного прогестерона привела к увеличению латентного периода 32,1 ± 17,8 дня по сравнению с 21,2 ± 16,3 дня в контрольной группе и увеличению веса при рождении 2 982,8 ± 697,8 г против 2585,3 ± 746,6 г. 19
Добавки эстрадиола во время лютеиновой фазы in vitro циклов оплодотворения
Было проведено проспективное рандомизированное исследование, чтобы найти оптимальную дозу эстрадиола (E2) для поддержки лютеиновой фазы путем добавления различных доз E2 для поддержки лютеиновой фазы прогестерона (P) у пациентов, подвергающихся лечению длительным оплодотворением (ЭКО) с помощью длинного агониста ГнРГ in vitro . 20 Двести восемьдесят пять женщин, проходящих лечение ЭКО с использованием длительного протокола агонистов ГнРГ, были проспективно рандомизированы на три группы. Группа 1 ( n = 95) получала P и 2 мг E2, группа 2 ( n = 95) получала P и 4 мг E2, а группа 3 ( n = 95) получала P и 6 мг E2 в качестве лютеиновой фазы. служба поддержки. Первичным результатом была частота клинической беременности (PR). Второстепенными интересующими переменными были частота имплантации (IR), частота выкидышей и множественное PR.Клинический PR составил 31,6%, 40% и 32% соответственно в группах 1, 2 и 3, и различия между группами не были статистически значимыми. Однако частота выкидышей была значительно ниже в группе 2 (2,6%), чем в группе 1 (20%), но не была значительно ниже, чем в группе 3 (9,6%). Исследование пришло к выводу, что добавление 2, 4 или 6 мг перорального E2 к P в лютеиновой фазе не создает статистической разницы в показателях частоты наступления беременности. Однако при использовании 2 мг E2 была обнаружена значительно более высокая частота выкидышей.Следовательно, при поддержке лютеиновой фазы 4 мг перорального эстрадиола в дополнение к прогестерону можно рассматривать как снижение частоты выкидышей. По-прежнему необходимы дополнительные исследования для определения группы риска, оптимального гестационного возраста на момент начала, способа введения, дозы прогестерона и долгосрочной безопасности.
Заболевания щитовидной железы
Это имеет большое влияние на фертильность. Глобулин, связывающий половые гормоны (ГСПГ), изменяется при гипертиреозе и гипотиреозе.Он также изменяет уровень пролактина, гонадотропин-рилизинг-гормона и половых стероидов в сыворотке крови. Он также может иметь прямое воздействие на ооциты, поскольку известно, что специфические сайты связывания тироксина обнаруживаются на ооцитах мыши и человека. Также существует связь между дисфункцией щитовидной железы у женщин и заболеваемостью и исходом беременности. У мужчин гипертиреоз вызывает снижение подвижности сперматозоидов. Количество морфологически аномальных сперматозоидов увеличивается при гипотиреозе. Было обнаружено, что при восстановлении эутиреоза оба нарушения улучшаются или нормализуются.У женщин изменения фертильности, вызванные заболеваниями щитовидной железы, более сложны. Гипер- и гипотиреоз являются основными заболеваниями щитовидной железы, которые отрицательно влияют на репродуктивную функцию женщин и вызывают нарушения менструального цикла, в основном гипоменорею и полименорею при гипертиреозе и олигоменорею при гипотиреозе. Все факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции. 21
Контролируемая гиперстимуляция яичников приводит к повышению уровня эстрадиола, что, в свою очередь, может отрицательно влиять на гормоны щитовидной железы и ТТГ. Гиперстимуляция яичников может стать серьезной при наличии аутоиммунного заболевания щитовидной железы в зависимости от ранее существовавших патологий щитовидной железы. Аутоиммунное заболевание щитовидной железы встречается у 5-20% беременных, не прошедших отбор. Изолированная гипотироксинемия описана примерно в 2% беременностей без повышения уровня ТТГ в сыворотке и аутоантител к щитовидной железе.Существует связь между повышенным уровнем самопроизвольных абортов, преждевременных родов и / или низкой массой тела при рождении, дистрессом плода в родах и, возможно, гипертензией, вызванной беременностью, и отслойкой плаценты при явном гипотиреозе. Все антитиреоидные препараты проникают через плаценту и потенциально могут повлиять на функцию щитовидной железы плода. 22
Заболевания щитовидной железы часто встречаются у женщин во время беременности. Если не лечить, как гипотиреоз, так и гипертиреоз связаны с неблагоприятным воздействием на беременность и исходы плода.Важно правильно идентифицировать эти расстройства и лечить их соответствующим образом, чтобы предотвратить осложнения, связанные с беременностью. Показанным лечением является левотироксин при гипотиреозе, а тиоамиды — средство выбора при гипертиреозе; В отдельных случаях может быть показана тиреоидэктомия. 23 , 24 Кокрановский обзор трех РКИ с участием 314 женщин показал в одном испытании с участием 115 женщин, что терапия левотироксином для лечения беременных эутиреоидных женщин антителами к пероксидазе щитовидной железы не снижает преэклампсию, но значительно снижает преждевременные роды на 72 человека. %.В одном испытании с участием 30 женщин с гипотиреозом сравнивали дозы левотироксина, но сообщали только биохимические результаты. В исследовании с участием 169 женщин сравнивали микроэлемент селенометионин (селен) с плацебо, и не было обнаружено значительных различий ни для преэклампсии, ни для преждевременных родов. Ни в одном из трех испытаний не сообщалось о задержке нервного развития у детей. 25
Гормоны во время беременности
Стероидные гормоны, такие как прогестерон, широко изучались в литературе, что вызывает разногласия по поводу их использования на ранних сроках беременности.Целью обзора была роль в предотвращении абортов, повторного невынашивания беременности и преждевременных родов. Была проанализирована роль добавок эстрогена и прогестерона в вспомогательной репродукции. Факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции
Производство стероидных гормонов и требует использования
Прогестерон
Прогестерон в основном вырабатывается желтым телом примерно до 10 недель беременности. 1 Исследование недостаточности яичников и вспомогательной репродукции показало, что сто мг фосфора, вероятно, были супрафизиологической дозой для поддержки беременности через 6-8 недель после зачатия. Фетоплацентарное отделение было пригодным на сроке от 10 до 12 недель беременности. 2 Когда беременность достигает срока, уровень прогестерона колеблется от 100 до 200 нг / мл, а плацента вырабатывает около 250 мг / день. Почти весь прогестерон, продуцируемый плацентой, попадает в плаценту, в отличие от эстрогена.Производство прогестерона не зависит от наличия предшественника, состояния плода, включая самочувствие.
На ранних сроках беременности у матери повышается уровень 17 α-гидроксипрогестерона, что свидетельствует об активности желтого тела. К десятой неделе беременности это соединение вернулось к исходному уровню, что указывает на то, что плацента имеет небольшую активность 17a-гидроксилазы. Однако, начиная примерно с недели 32, 9, 11, 9, 12, происходит второй, более постепенный рост 17a-гидроксипрогестерона из-за использования плацентой предшественников плода.Это важно для понимания профилактики преждевременных родов. Прогестерон также играет важную роль в подавлении материнского иммунологического ответа на антигены плода, тем самым предотвращая материнское отторжение трофобласта. И, конечно же, прогестерон подготавливает и поддерживает эндометрий, что позволяет провести имплантацию раньше. Исследования показали, что желтое тело человека вырабатывает значительное количество эстрадиола, но для успешной имплантации требуется прогестерон, а не эстроген. 3
Эстроген
В плаценте нет всех необходимых ферментов для производства эстрогенов из холестерина или даже прогестерона.В человеческом трофобласте отсутствует 17-гидроксилаза, и поэтому он не может преобразовывать C21-стероиды в C19-стероиды, непосредственные предшественники эстрогена. Чтобы обойти этот дефицит, дегидроизоандростерон сульфат (DHA) из надпочечников плода превращается трофобластами в эстрадиол-17ί. В своем ключевом месте в качестве промежуточной станции между матерью и плодом плацента может использовать прекурсоры от матери или плода, чтобы обойти свой собственный дефицит ферментативной активности. Гормоны действуют как катализаторы химических изменений на клеточном уровне, которые необходимы для роста, развития и получения энергии.У плода отсутствует 3B-гидроксистероиддегидрогеназа, поэтому он не может производить прогестерон, заимствованный из плаценты. Взамен плод дает плаценте то, чего ему не хватает (19 соединений углерода) — предшественника эстрогена.
Белковые гормоны
Белковые гормоны: плацентарный лактоген человека (hPL), хорионический гонадотропин человека (hCG), адренокортикотропный агент (ACTH), вариант гормона роста (hGH-V), белок, связанный с паратиреоидным гормоном (PTH-rP) , Кальцитонин, релаксин, ингибины активины, предсердный натрийуретический пептид, гипоталамические рилизинг-гормоны и ингибирующие гормоны, тиротропин-рилизинг-гормон (TRH), гонадотропин-рилизинг-гормон (GnRH), кортикотропин-рилизинг-гормон (CRH), соматостатин, соматостатин GHRH), альфа-фетопротеин, пролактин, релаксин и другие децидуальные белки.В связи с полнотой вариантов описания гормонов, в этой главе обсуждается клиническая важность ХГЧ для терапии.
Хорионический гонадотропин человека
Наиболее изученным продуктом гормона трофобласта является ХГЧ. Во время беременности этот гликопротеин имеет решающее значение, поскольку он спасает желтое тело от инволюции и поддерживает секрецию прогестерона клетками гранулезы яичника. Его полезность в качестве диагностического маркера беременности связана с тем, что он может быть одним из самых ранних секретируемых продуктов концепта.Во время беременности плацентарная продукция ХГЧ находится на пике между восьмой и десятой неделями беременности и имеет тенденцию к плато на более низком уровне на протяжении оставшейся части беременности.
Единственная определенно известная функция для ХГЧ — это поддержка желтого тела (ХТ), заменяющая ЛГ примерно на восьмой день после овуляции, через 1 день после имплантации, когда b-ХГЧ впервые может быть обнаружен в материнской крови. На стадии 8 клеток ХГЧ был обнаружен в эмбрионе с помощью методов молекулярной биологии.
Имплантация происходит через 5-6 дней после овуляции, а ХГЧ должен появиться к 10 дню овуляции (4 дня после овуляции), чтобы спасти желтое тело.Следовательно, бластоциста должна имплантироваться в узкий промежуток времени. Стимуляция ХГЧ приводит к ежедневной секреции 25 мг P и 0,5 мг E2. Экспрессия гена ХГЧ присутствует как в цитотрофобласте, так и в синцитиотрофобласте, но синтезируется в основном в синцитиотрофобласте. Концентрация циркулирующего ХГЧ у матери составляет примерно 100 МЕ / л во время ожидаемой, но пропущенной менструации. Максимальный уровень около 100 000 МЕ / л в кровотоке матери достигается на 8-10 неделе беременности. Есть два клинических состояния, при которых титры ХГЧ в крови особенно полезны: трофобластическая болезнь и внематочная беременность.Трофобластическая болезнь отличается очень высоким уровнем b-ХГЧ (в 3-100 раз выше, чем при нормальной беременности). Внематочная продукция α- и β-ХГЧ нетрофобластическими опухолями встречается редко, но все же происходит.
Человеческий плацентарный лактоген (hPL) секретируется в основном в материнский кровоток, большинство его функций происходит в местах действия в материнских тканях. Считается, что плацентарный лактоген человека ответственен за заметное повышение концентрации инсулиноподобного фактора роста-1 (IGF-1) в плазме крови матери по мере приближения срока беременности.Плацентарный лактоген человека оказывает метаболическое действие во время беременности через IGF-I. Он связан с инсулинорезистентностью, увеличивает секрецию инсулина, который стимулирует липолиз, увеличивает количество свободных жирных кислот в крови и ингибирует глюконеогенез; по сути, он противодействует действию инсулина, вызывает непереносимость глюкозы, а также липолиз и протеолиз в материнской системе. Таким образом, в клинической практике подчеркивается роль универсального скрининга аномального уровня сахара в крови в начале третьего триместра.
Концентрация кальция у плода регулируется перемещением кальция через плаценту из материнского компартмента. Чтобы поддерживать рост костей плода, материнский отсек подвергается корректировкам, которые обеспечивают чистый перенос достаточного количества кальция к плоду. Изменения материнского компартмента, которые способствуют накоплению кальция, включают увеличение потребления с пищей матери, повышение уровня D3 у матери и повышение уровней паратироидного гормона.
Добавка прогестерона во время беременности: иммунологическая терапия
Есть несколько исследований, чтобы понять поддержание беременности с помощью прогестерона.Было показано, что прогестерон увеличивает количество цитокинов, продуцируемых клетками Th3, которые преобладают над цитокинами, продуцируемыми клетками Th2, что приводит к поддержанию беременности. Клетки Th3 доминируют в децидуальной оболочке на ранних сроках беременности у людей. Цитокины, производные от Th3, ИЛ-4 и ИЛ-6, индуцируют высвобождение ХГЧ из трофобластов, а ХГЧ стимулирует выработку прогестерона желтым телом во время беременности. Было показано, что прогестерон стимулирует секрецию Th3 и снижает секрецию цитокинов Th2.Таким образом, поддержание беременности приписывается цитокину типа Th3. Эта роль в контроле иммунной и эндокринной системы, которая способствует функционированию трофобластов в месте имплантации, кажется интересной. 4 Использование прогестагена при угрозе прерывания беременности является спорным вопросом. 5
Прогестерон при повторном невынашивании беременности
Прогестоген использовался в течение нескольких лет, даже до того, как стали известны иммуномодулирующие свойства прогестерона.С того времени были проведены исследования разного качества, чтобы доказать преимущества приема прогестагенов у больных женщин. Исследование 146 женщин, у которых было легкое или умеренное вагинальное кровотечение в первом триместре беременности, было рандомизировано для приема перорального дидрогестерона (10 мг два раза в день) ( n = 86) или отсутствия лечения ( n = 60). Дидрогестерон был продолжен до 1 недели после остановки кровотечения. Частота невынашивания беременности была значительно ниже в группе дидрогестерона, чем в группе без лечения (17.5% против . 25%; P <0,05). 6 Большинство процитированных клинических испытаний выявили тенденцию к улучшению показателей беременности и увеличению рождаемости в группе лечения прогестагеном, но, к сожалению, многие исследования имели плохой дизайн и методические недостатки. 7 Несколько исследований показали, что поддерживающая терапия на ранних сроках беременности оказывает значительное положительное влияние на исход беременности. Женщин с иным необъяснимым повторным невынашиванием беременности следует проконсультировать относительно возможности успешной беременности без какого-либо лечения, кроме поддерживающей терапии, такой как добавка фолиевой кислоты или витаминов. 7 , 8 Прогестаген вводят в различных формах, но обычно рекомендуется исключительное использование прогестагена без какого-либо (анти-) андрогенного или (анти-) эстрогенного действия. Добавки с прогестагеном доступны в виде вагинальных суппозиториев (0,4 г / день, предпочтительно вечером, потому что естественный прогестерон может вызвать усталость), внутримышечной инъекции (250 мг гидроксипрогестерона в неделю) или перорального приема (например, 10 мг дидрогестерона, стереоизомера природного прогестерона. 9
Добавки прогестерона после вспомогательных репродуктивных технологий
Использование добавок прогестерона в циклах ВРТ более понятно. 10 Продолжительность приема прогестерона после репродуктивной технологии (ВРТ) изучалась в ретроспективном когортном исследовании. Одна группа получала прогестерон в течение первого триместра беременности (протокол первого триместра) до 12 недель, а вторая группа прекращала прием прогестерона после положительного результата теста на бета-ХГЧ через 2 недели после извлечения (лютеиновый протокол).Сходная частота клинических беременностей произошла на сроке 7 недель (81,8% протокол лютеиновой беременности против 85,8% протокола первого триместра) и по частоте живорождений (76,8% протокол лютеиновой беременности против 75,0% протоколу первого триместра). Наблюдалась тенденция к более высокому уровню выкидышей после 7 недель в группе протокола первого триместра (15,5% по сравнению с 4,4%), что указывает на то, что добавление прогестерона в первом триместре может поддерживать раннюю беременность в течение 7 недель за счет отсрочки выкидыша, но не улучшает коэффициенты живорождения.Существуют рандомизированные испытания, поддерживающие рутинное использование лютеиновой поддержки в циклах АРТ с использованием агонистов или антагонистов ГнРГ. Пятьдесят девять исследований были включены в обзор для оценки поддержки лютеиновой фазы с помощью ХГЧ по сравнению с плацебо или отсутствием лечения с точки зрения увеличения частоты продолжающихся беременностей. Поддержка лютеиновой фазы с помощью ХГЧ или прогестерона после вспомогательной репродукции приводит к увеличению частоты наступления беременности. ХГЧ не дает лучших результатов, чем прогестерон, и связан с большим риском СГЯ при использовании с ГнРГ.Оптимальный способ введения прогестерона еще не установлен. 11 Обзор показал значительный эффект в пользу прогестерона для поддержки лютеиновой фазы, в пользу синтетического прогестерона перед микронизированным прогестероном. 12
Профилактика повторных преждевременных родов с помощью 17 альфа-гидроксипрогестерона капроата
Следует ожидать и предотвращать преждевременные роды для снижения перинатальной заболеваемости и смертности. Те женщины, у которых ранее были самопроизвольные преждевременные роды, имеют значительно повышенный риск преждевременных родов при последующих беременностях.Результаты нескольких небольших исследований показали, что 17-альфа-гидроксипрогестерона капроат (17P) может снизить риск преждевременных родов. Было проведено двойное слепое плацебо-контролируемое исследование с участием беременных женщин с задокументированной историей самопроизвольных преждевременных родов. 13 Всего для исследования было выбрано 19 клинических центров, в которые были включены беременные женщины на сроке от 16 до 20 недель гестации, которые были случайным образом распределены центральным центром обработки данных в соотношении 2: 1 для получения либо 250 инъекций еженедельно. мг 17P или еженедельные инъекции инертного масляного плацебо; инъекции продолжали до родов или до 36 недель беременности.Лечение 17P значительно снизило риск родов на сроке менее 37 недель гестации, который составил 36,3% в группе прогестерона против . 54,9 процента в группе плацебо; относительный риск при родах на сроке менее 35 недель беременности составил 20,6% против . 30,7 процента; а роды на сроке менее 32 недель беременности составили 11,4 процента против 19,6 процента. Частота некротического энтероколита, внутрижелудочкового кровоизлияния у младенцев у женщин, получавших 17Р, значительно ниже и потребность в дополнительном кислороде.Таким образом, исследование пришло к выводу, что еженедельные инъекции 17P привели к значительному снижению частоты повторных преждевременных родов среди женщин, которые подвергались особенно высокому риску преждевременных родов, и снизили вероятность нескольких осложнений у их младенцев. В одном двойном слепом рандомизированном плацебо-контролируемом исследовании сообщалось о более низкой частоте преждевременных родов при использовании внутримышечного 17-альфа-гидроксипрогестерона капроата (17P) или интравагинальных микронизированных прогестероновых суппозиториев у женщин с риском преждевременных родов. 14 Период полураспада 17P оценивается примерно в 7,8 дня. Способ введения играет важную роль в профиле безопасности и эффективности препарата. Пероральный прогестерон не применялся для предотвращения преждевременных родов из-за его первого прохождения через печеночный метаболизм, а также отсутствуют данные об эффективности, высоком профиле побочных эффектов и из-за крайней изменчивости концентраций в плазме. Вагинальное введение прогестерона позволяет избежать метаболизма через печень при первом прохождении и связано с быстрым всасыванием, высокой биодоступностью и местным воздействием на эндометрий. 15 Вагинальный путь введения не вызывает местной боли и мало побочных эффектов, это связано с различными концентрациями в крови. 16 Для изучения эффективности прогестерона для поддерживающей токолитической терапии после угрозы преждевременных родов было проведено рандомизированное контролируемое исследование. 17 Исследование проводилось на 70 женщинах с симптомами угрозы преждевременных родов, которые после прекращения активности матки были рандомизированы на терапию прогестероном или отсутствие лечения, и цель этого исследования состояла в том, чтобы определить, можно ли вводить вагинальный прогестерон после подавления активности матки. преждевременные роды связаны с увеличенным латентным периодом и уменьшением повторения преждевременных родов.Группа лечения получала суппозиторий с прогестероном (400 мг) ежедневно до родов, а контрольная группа не получала лечения. В исследовании сделан вывод о том, что использование вагинальных суппозиториев с прогестероном после успешного парентерального токолиза связано с более длительным латентным периодом до родов, но не снижает частоту повторных госпитализаций по поводу преждевременных родов. Добавление дидрогестерона женщинам с угрозой преждевременных родов оказало влияние на цитокиновый профиль, гормональный профиль и фактор блокирования, вызванный прогестероном. 18
Исследование восьмидесяти трех женщин с симптомами угрозы преждевременных родов было рандомизировано в исследуемые группы, получавшие токолитическое лечение в сочетании с интравагинальным микронизированным естественным прогестероном (200 мг в день), или в контрольную группу, получающую только токолиз. Обработка микронизированного природного прогестерона привела к увеличению латентного периода 32,1 ± 17,8 дня по сравнению с 21,2 ± 16,3 дня в контрольной группе и увеличению веса при рождении 2 982,8 ± 697,8 г против 2585,3 ± 746,6 г. 19
Добавки эстрадиола во время лютеиновой фазы in vitro циклов оплодотворения
Было проведено проспективное рандомизированное исследование, чтобы найти оптимальную дозу эстрадиола (E2) для поддержки лютеиновой фазы путем добавления различных доз E2 для поддержки лютеиновой фазы прогестерона (P) у пациентов, подвергающихся лечению длительным оплодотворением (ЭКО) с помощью длинного агониста ГнРГ in vitro . 20 Двести восемьдесят пять женщин, проходящих лечение ЭКО с использованием длительного протокола агонистов ГнРГ, были проспективно рандомизированы на три группы. Группа 1 ( n = 95) получала P и 2 мг E2, группа 2 ( n = 95) получала P и 4 мг E2, а группа 3 ( n = 95) получала P и 6 мг E2 в качестве лютеиновой фазы. служба поддержки. Первичным результатом была частота клинической беременности (PR). Второстепенными интересующими переменными были частота имплантации (IR), частота выкидышей и множественное PR.Клинический PR составил 31,6%, 40% и 32% соответственно в группах 1, 2 и 3, и различия между группами не были статистически значимыми. Однако частота выкидышей была значительно ниже в группе 2 (2,6%), чем в группе 1 (20%), но не была значительно ниже, чем в группе 3 (9,6%). Исследование пришло к выводу, что добавление 2, 4 или 6 мг перорального E2 к P в лютеиновой фазе не создает статистической разницы в показателях частоты наступления беременности. Однако при использовании 2 мг E2 была обнаружена значительно более высокая частота выкидышей.Следовательно, при поддержке лютеиновой фазы 4 мг перорального эстрадиола в дополнение к прогестерону можно рассматривать как снижение частоты выкидышей. По-прежнему необходимы дополнительные исследования для определения группы риска, оптимального гестационного возраста на момент начала, способа введения, дозы прогестерона и долгосрочной безопасности.
Заболевания щитовидной железы
Это имеет большое влияние на фертильность. Глобулин, связывающий половые гормоны (ГСПГ), изменяется при гипертиреозе и гипотиреозе.Он также изменяет уровень пролактина, гонадотропин-рилизинг-гормона и половых стероидов в сыворотке крови. Он также может иметь прямое воздействие на ооциты, поскольку известно, что специфические сайты связывания тироксина обнаруживаются на ооцитах мыши и человека. Также существует связь между дисфункцией щитовидной железы у женщин и заболеваемостью и исходом беременности. У мужчин гипертиреоз вызывает снижение подвижности сперматозоидов. Количество морфологически аномальных сперматозоидов увеличивается при гипотиреозе. Было обнаружено, что при восстановлении эутиреоза оба нарушения улучшаются или нормализуются.У женщин изменения фертильности, вызванные заболеваниями щитовидной железы, более сложны. Гипер- и гипотиреоз являются основными заболеваниями щитовидной железы, которые отрицательно влияют на репродуктивную функцию женщин и вызывают нарушения менструального цикла, в основном гипоменорею и полименорею при гипертиреозе и олигоменорею при гипотиреозе. Все факторы могут быть связаны с изменениями метаболического пути. Адекватные уровни циркулирующих гормонов щитовидной железы имеют первостепенное значение для нормальной репродуктивной функции. 21
Контролируемая гиперстимуляция яичников приводит к повышению уровня эстрадиола, что, в свою очередь, может отрицательно влиять на гормоны щитовидной железы и ТТГ. Гиперстимуляция яичников может стать серьезной при наличии аутоиммунного заболевания щитовидной железы в зависимости от ранее существовавших патологий щитовидной железы. Аутоиммунное заболевание щитовидной железы встречается у 5-20% беременных, не прошедших отбор. Изолированная гипотироксинемия описана примерно в 2% беременностей без повышения уровня ТТГ в сыворотке и аутоантител к щитовидной железе.Существует связь между повышенным уровнем самопроизвольных абортов, преждевременных родов и / или низкой массой тела при рождении, дистрессом плода в родах и, возможно, гипертензией, вызванной беременностью, и отслойкой плаценты при явном гипотиреозе. Все антитиреоидные препараты проникают через плаценту и потенциально могут повлиять на функцию щитовидной железы плода. 22
Заболевания щитовидной железы часто встречаются у женщин во время беременности. Если не лечить, как гипотиреоз, так и гипертиреоз связаны с неблагоприятным воздействием на беременность и исходы плода.Важно правильно идентифицировать эти расстройства и лечить их соответствующим образом, чтобы предотвратить осложнения, связанные с беременностью. Показанным лечением является левотироксин при гипотиреозе, а тиоамиды — средство выбора при гипертиреозе; В отдельных случаях может быть показана тиреоидэктомия. 23 , 24 Кокрановский обзор трех РКИ с участием 314 женщин показал в одном испытании с участием 115 женщин, что терапия левотироксином для лечения беременных эутиреоидных женщин антителами к пероксидазе щитовидной железы не снижает преэклампсию, но значительно снижает преждевременные роды на 72 человека. %.В одном испытании с участием 30 женщин с гипотиреозом сравнивали дозы левотироксина, но сообщали только биохимические результаты. В исследовании с участием 169 женщин сравнивали микроэлемент селенометионин (селен) с плацебо, и не было обнаружено значительных различий ни для преэклампсии, ни для преждевременных родов. Ни в одном из трех испытаний не сообщалось о задержке нервного развития у детей. 25
Симптомы низкого прогестерона и влияние прогестерона на беременность
Что такое прогестерон?
Прогестерон — это гормон, который вырабатывается вашим организмом после овуляции.Подготавливает слизистую оболочку матки к беременности. Уровень прогестерона повышается и понижается при каждом менструальном цикле. Если вы не забеременеете, прогестерон снизится, и у вас начнется менструальный цикл.
Если вы забеременеете, вы продолжите вырабатывать прогестерон, который сохраняет слизистую оболочку матки здоровой и предотвращает сокращение вашего тела по мере роста матки. Прогестерон также помогает вашему телу развивать молочные железы при подготовке к кормлению грудью, и он играет роль в производстве молока после рождения.Ваш уровень прогестерона повысится во время беременности.
Низкий уровень прогестерона также известен как лютеиновая недостаточность. Это потому, что лютеиновая фаза вашего менструального цикла начинается после овуляции, когда увеличивается выработка прогестерона.
Как низкий уровень прогестерона влияет на беременность
Мы не уверены, насколько низкий уровень прогестерона влияет на беременность. Некоторые эксперты говорят, что низкий уровень прогестерона не оказывает никакого влияния, в то время как другие говорят, что без адекватного прогестерона матка не будет подготовлена к беременности, а эмбрион не сможет имплантироваться и процветать в слизистой оболочке матки.
Мы действительно знаем, что у женщин, у которых был выкидыш, как правило, более низкий уровень прогестерона, хотя мы не знаем, вызвал ли выкидыш снижение прогестерона или низкий прогестерон способствовал выкидышу.
Что такое низкий уровень прогестерона?
Уровень прогестерона не будет проверяться вашим опекуном во время беременности. Существует широкий диапазон нормальных значений, и цифры будут колебаться в зависимости от того, когда ваше тело выпустило гормон. Вместо этого прием прогестерона во время беременности будет основываться на факторах риска, таких как ваш анамнез.
Ваш опекун может проверять уровень прогестерона до беременности, например, если у него есть опасения по поводу ваших менструальных циклов или того, происходит ли у вас овуляция.
Нормальные уровни прогестерона:
- До овуляции: менее 1 нанограмма на миллилитр (нг / мл)
- Средний менструальный цикл: от 5 до 20 нг / мл
- Первый триместр беременности: от 11,2 до 90 нг / мл мл
- Второй триместр беременности: от 25,6 до 89,4 нг / мл
- Третий триместр: от 48 до 150 до более 300 нг / мл
Обратите внимание, что разные лаборатории могут использовать разные диапазоны, поэтому обсудите свои результаты со своим опекуном.
Вызывает ли низкий уровень прогестерона бесплодие?
Низкий уровень прогестерона сам по себе не вызывает бесплодия, хотя может быть связан с рядом возможных факторов. Это может привести к неудачной имплантации эмбриона, и, например, у женщин с низким уровнем прогестерона могут возникнуть проблемы с менструальным циклом.
При тестировании во время менструального цикла низкий уровень прогестерона может быть признаком низкой овуляции или бесплодия.
Причины низкого прогестерона
Мы не знаем, что вызывает низкий прогестерон, но низкие уровни могут быть связаны с:
Симптомы низкого прогестерона
Симптомы низкого прогестерона могут включать:
Имейте в виду, что причины, помимо низкого прогестерона, могут вызывают многие из этих симптомов.
Повышает ли низкий прогестерон вероятность выкидыша?
У женщин, переживших выкидыш, как правило, более низкий уровень прогестерона, но мы не знаем, какие причины и какие причины.
Исследования показали, что у женщин, у которых было удалено желтое тело (железа, вырабатывающая прогестерон) до 8 недель беременности, произошел выкидыш.
Помогают ли добавки прогестерона предотвратить выкидыш или преждевременные роды?
Исследователи работают над тем, чтобы определить, могут ли добавки прогестерона помочь предотвратить выкидыш или преждевременные роды.Есть противоречивые выводы. Вот кое-что из того, что мы знаем.
Профилактика выкидыша
Одно исследование с участием более 800 женщин не выявило значительно более высокого уровня живорождений среди женщин с необъяснимыми повторяющимися выкидышами в анамнезе, получавших прогестероновую терапию.
Но другие исследования показали, что добавки с прогестероном могут помочь некоторым женщинам в определенных обстоятельствах, особенно женщинам, у которых были повторяющиеся выкидыши.
Например, одно исследование с участием более 2000 женщин в 14 исследованиях не показало различий в общем риске выкидыша у женщин, получавших прогестерон, и женщин, получавших плацебо или не получавших лечения.Но исследование показало, что лечение прогестероном снижает частоту выкидышей среди женщин, у которых в прошлом было три или более выкидышей подряд.
Другое исследование обнаружило небольшие, но положительные эффекты от лечения женщин, у которых на ранних сроках беременности было вагинальное кровотечение и были выкидыши в прошлом.
Снижение преждевременных родов
Для женщин с укороченной шейкой матки (признаком возможных преждевременных родов) на сроке от 16 до 24 недель беременности вагинальные суппозитории с прогестероном или гель оказались эффективными для предотвращения преждевременных родов.
Было показано, что для женщин, у которых ранее были преждевременные роды до 36 недель, прием прогестерона во время беременности снижает риск преждевременных родов. (Более позднее исследование не подтвердило этот вывод, но это более позднее исследование имело недостаточный размер выборки и не давало окончательных результатов в отношении лечения.)
Обратите внимание, что лечение прогестероном не предотвращает преждевременные роды в случае близнецов или других близнецов.
Несмотря на то, что приговор об эффективности прогестерона еще не вынесен, поскольку они могут помочь и поскольку побочные эффекты минимальны, они по-прежнему регулярно предлагаются некоторым женщинам в надежде на положительный эффект в предотвращении преждевременных родов и выкидышей.
Лечение с низким содержанием прогестерона
Если у вас были повторные выкидыши и у вас низкий уровень прогестерона, или если у вас в анамнезе преждевременные роды или короткая шейка матки, ваш опекун может лечить вас синтетической формой прогестерона. Вам также могут назначить прогестерон, если вы проходите курс лечения ЭКО.
Не принимайте безрецептурные суппозитории с прогестероном и не используйте безрецептурные кремы с прогестероном. Ваш опекун может назначить один из трех вариантов:
- Инъекции прогестерона (17P).Для предотвращения преждевременных родов или для женщин, получающих ЭКО, прогестерон иногда вводят еженедельно.
- Вагинальный гель или свечи с прогестероном. Это еще одна альтернатива для женщин, перенесших ЭКО. Его также назначают женщинам с «короткой шейкой матки» (менее 2,5 сантиметров, которая может открыться раньше). Они поставляются с аппликатором, который выглядит как тампон, и вы применяете его один или два раза в день.
- Пероральные таблетки прогестерона. Их можно назначить, если у вас в прошлом были выкидыши.
Для женщин с короткой шейкой матки или преждевременными родами в анамнезе лечение обычно начинается на 16–20 неделе беременности и заканчивается на 34–36 неделе. Для женщин, принимающих прогестерон из-за повторяющихся выкидышей или из-за того, что они проходят ЭКО, лечение начинается после овуляции или как только пациентка забеременеет и продолжается примерно до 8-10 недель беременности.
Однако лечение прогестероном не оказалось эффективным для женщин, имеющих многоплодную беременность.
В целом лечение прогестероном считается низким риском, но каждое из этих методов лечения имеет возможные побочные эффекты, поэтому обязательно обсудите их со своим опекуном.
Прогестерон и овуляция тесно связаны. Возможно, вам будет интересно узнать больше о симптомах овуляции (как определить, когда у вас овуляция) и использовать тест-полоску на овуляцию.
ПРИМЕЧАНИЕ: Эту статью также провела Эрика Нью, доктор медицины, научный сотрудник по репродуктивной эндокринологии и бесплодию Университета Южной Флориды.
Подробнее:
Базальная температура тела и овуляция
Выявление проблемы с фертильностью
Как быстро забеременеть
Пороговый уровень прогестерона 25 нг / мл для поддержания беременности в первом триместре у женщин с бесплодием в анамнезе или выкидыш
Абстрактные
Введение : Важность выработки прогестерона желтым телом для поддержания беременности в первом триместре была впервые признана в 1970-х годах.С тех пор профилактический прогестерон используется для снижения частоты абортов в первом триместре у женщин с выкидышами в анамнезе. Однако до недавнего времени исследования не смогли установить целевой уровень прогестерона, при котором можно было бы поддерживать беременность в этой популяции.
Цель : Целью исследования было оценить эффективность порогового значения сывороточного прогестерона 25 нг / мл для поддержания беременности в первом триместре у пациенток с бесплодием или выкидышем в анамнезе.
Дизайн исследования : В этот ретроспективный обзор диаграммы мы включили 182 пациентки (329 беременностей) в возрасте от 22 до 45 лет, у которых была хотя бы одна попытка беременности в частной клинике по лечению бесплодия в период с 1996 по 2013 год. Мы исключили пациентов с анатомическими дефектами, внематочными беременностями, молярными беременностями, пораженными яйцеклетками, аномальным уровнем иммунитета или использованием донорских яйцеклеток. Все пациенты прошли полное обследование, включая анатомический скрининг и иммунные медиаторы. Уровни прогестерона регистрировали при первом посещении и через 10 недель.Дополнительный прогестерон вводили в течение первого триместра беременности, если уровни сыворотки упали ниже 25 нг / мл, и продолжали до тех пор, пока не было определено, что плацента взяла на себя выработку прогестерона. Женщины были разделены по возрасту на две группы: возраст бесплодия (22-34 года) и пожилой возраст матери (35-45 лет). Тесты хи-квадрат были выполнены на 329 беременностях для анализа связи между жизнеспособными беременностями в первом триместре и адекватными уровнями прогестерона в сыворотке (≥ 25 нг / мл при начальном и / или 10-недельном посещении) для каждой возрастной группы.
Результаты : Статистически значимая разница в уровне жизнеспособной беременности в первом триместре и адекватных (≥ 25 нг / мл) уровнях прогестерона в сыворотке была обнаружена для обеих возрастных групп первичной фертильности (X 2 = 57,424, N = 221, p <0,0001) и пожилой возрастной группе матери (X 2 = 10,973, N = 108, p = 0,001).
Выводы : Это исследование демонстрирует, что поддержание сывороточного уровня прогестерона 25 нг / мл или выше снижает риск выкидыша в первом триместре у женщин любого репродуктивного возраста.
Ключевые слова
первый триместр, бесплодие, выкидыш, прогестерон, самопроизвольный аборт
Введение
Прогестерон считается «гормоном беременности» из-за его важной роли в подготовке эндометрия к имплантации и поддержании беременности [1]. В течение первого триместра беременности желтое тело в первую очередь отвечает за выработку прогестерона. Желтое тело регрессирует примерно через 9 недель, после чего происходит синтез прогестерона из плаценты [2].Важность выработки прогестерона желтым телом была впервые признана Чапо, который продемонстрировал, что удаление желтого тела до 7-недельного срока беременности всегда приводит к выкидышу. Во время этого исследования он наблюдал постоянное снижение прогестерона, повышение внутриматочного давления и развитие расширения шейки матки перед неизбежным абортом [3]. Основываясь на этих знаниях, он назначил дополнительный прогестерон для предотвращения выкидышей, связанных с отменой прогестерона, вызванной лютеэктомией, что в конечном итоге привело к устойчивой беременности [4].
Выкидыш — частое осложнение беременности на ранних сроках, при этом большинство выкидышей приходится на срок до 8 недель [2,5]. Общий показатель потери беременности на ранних сроках (≥ 12 недель) составляет около 13,5%. Этот показатель увеличивается с возрастом матери после 20 лет, увеличиваясь с 11,5% у женщин 20-24 лет до 18,6% у женщин старше 30 лет [6]. Кроме того, у женщин с бесплодием в анамнезе наблюдалась более высокая частота выкидышей по сравнению с населением в целом [7].
Было высказано предположение, что профилактическое применение прогестерона можно использовать для снижения риска самопроизвольных абортов в первом триместре у женщин с невынашиванием беременности в анамнезе [8]. До недавнего времени исследования не могли установить целевой уровень прогестерона, выше которого беременность, скорее всего, будет продолжаться в этой группе населения. McCord et al. [9] провел ретроспективный анализ 3674 беременностей, чтобы изучить вероятность жизнеспособной внутриутробной беременности для данной концентрации прогестерона в сыворотке.Исследование показало, что вероятность жизнеспособной внутриутробной беременности в зависимости от концентрации прогестерона увеличивалась в виде сигмовидной кривой. Эта кривая выровнялась около 25 нг / мл и коррелировала с вероятностью жизнеспособной внутриутробной беременности 89%, что предполагает 25 нг / мл как важную целевую концентрацию прогестерона для поддержания беременности.
Цель
Мы стремимся оценить эффективность порогового уровня прогестерона 25 нг / мл для поддержания беременности в первом триместре у женщин с выкидышем или бесплодием в анамнезе.
Материалы и методы
Был проведен ретроспективный обзор пациентов из частной клиники по лечению бесплодия в Рокфорде, штат Иллинойс, в период с 1996 по 2013 год. Право на участие имели женщины, у которых была хотя бы одна попытка зачатия в клинике. Мы исключили пациентов с анатомическими дефектами, внематочными беременностями, молярными беременностями, пораженными яйцеклетками, аномальным уровнем иммунитета или использованием донорских яйцеклеток. Все другие эндокринопатии были устранены и исправлены. В исследование были включены 182 женщины в возрасте от 22 до 45 лет, в общей сложности 329 беременных. Эти пациенты были разделены на две группы: первичного фертильного возраста (22-34 года) и пожилого возраста матери (35-45 лет).
Все пациенты прошли полное обследование, включая полный анамнез и физикальное, трансвагинальное ультразвуковое исследование, гистеросальпингограмму и / или соногистерограмму с инфузией физиологического раствора. Уровни прогестерона в сыворотке регистрировали при первом посещении (2-6 недель после зачатия) и 10-недельном посещении и контролировали каждые 2 недели до полного перехода от выработки прогестерона яичниками к плацентарной.Это было определено путем изучения тенденции сывороточного прогестерона в течение первого триместра. После того, как уровни сыворотки повысились до точки, при которой после отмены добавки пациенты все еще оставались на уровне 25 нг / мл или выше, добавление прогестерона было прекращено. Уровни прогестерона проверяли через 2-3 дня после прекращения приема, чтобы убедиться, что уровни были на уровне или выше 25 нг / мл, подтверждая переход к продукции прогестерона плацентой. После выработки прогестерона плацентой уход за пациентом был передан общественным акушерам.За 12 лет беременности требовалась гормональная поддержка на протяжении всей беременности. В течение второго триместра за этими пациентами уход за пациентами по-прежнему осуществляли местные акушеры, но мы продолжали контролировать уровень их гормонов на протяжении всей беременности.
В этом исследовании адекватный уровень прогестерона в сыворотке был определен как ≥ 25 нг / мл при первоначальном и / или 10-недельном посещении. Дополнительный прогестерон вводили пациентам, если уровень прогестерона в сыворотке упал ниже 25 нг / мл во время первого или 10-недельного визита.В случаях, когда пациенты уже получали дополнительный прогестерон, доза прогестерона была увеличена для достижения адекватного уровня прогестерона в сыворотке. Метод добавления прогестерона был определен на основе предпочтений пациента и побочных эффектов и включал: пероральное, вагинальное и внутримышечное введение. Пациентам с плохой абсорбцией или плохой переносимостью прогестерона перорально или вагинально вводили внутримышечно прогестерон в масле.
Первичным результатом была жизнеспособная беременность в первом триместре.Жизнеспособная беременность определялась детальным морфологическим ультразвуковым исследованием плода на сроке 11-13 недель. Мы не вели наблюдение после того, как пациентку передали общественному акушеру, за исключением 12 описанных ранее случаев, которые требовали постоянного наблюдения в течение всего срока беременности. Следует отметить, что все 12 беременностей достигли конца третьего триместра.
Было проведенотестов хи-квадрат для анализа связи между жизнеспособной беременностью и адекватным уровнем прогестерона в сыворотке.Использовался уровень альфа априори 0,05. SPSS Statistics версии 24 использовался для всего статистического анализа.
Результаты
В общей сложности было включено 329 беременностей, из которых 221 — в возрастной группе первичной фертильности (22-34 года) и 108 — в возрастной группе преклонного возраста матери (35-45 лет). У женщин всех возрастов в 287 из 329 беременностей (87%) был достигнут адекватный уровень прогестерона (≥ 25 нг / мл при первоначальном и / или 10-недельном посещении). 188 из 221 (85%) беременностей в возрастной группе с высокой фертильностью и 99 из 108 (92%) в возрастной группе пожилых матерей достигли адекватного уровня прогестерона (Таблица 1).
Адекватный уровень прогестерона с разбивкой по возрастным группам | ||
Недостаточный уровень прогестерона в сыворотке a | Достаточный уровень прогестерона в сыворотке b | |
Все возрасты (22-45 лет) | 42 (13%) | 287 (87%) |
Первичный возраст фертильности (22-34 года) | 33 (15%) | 188 (85%) |
Пожилой возраст матери (35-45 лет) | 9 (8%) | 99 (92%) |
a Менее 25 нг / мл при первоначальном и 10-недельном посещении b Больше или равно 25 нг / мл при первоначальном и / или 10-недельном посещении | ||
Таблица 1. Адекватный уровень прогестерона с разбивкой по возрастным группам.
Показатель жизнеспособной беременности был неизменно выше во всех возрастных группах у тех, у кого был адекватный уровень прогестерона, по сравнению с теми, у кого был недостаточный уровень прогестерона. В общей сложности 208 из 287 (72%) беременностей с адекватным уровнем прогестерона закончились жизнеспособной беременностью, в то время как только 5 из 42 (12%) беременностей с недостаточным уровнем прогестерона закончились жизнеспособной беременностью (n = 329, X 2 58 .883, р <0,0001). В возрастной группе основной фертильности (22-34 года) 151 из 188 (80%) беременностей с адекватным уровнем прогестерона закончилась жизнеспособной беременностью, в то время как только 5 из 33 (15%) беременностей с недостаточным уровнем прогестерона привели к жизнеспособной беременности. (n = 221, X 2 57,424, p <0,0001). В возрастной группе матери преклонного возраста (35-45 лет) 57 из 99 (58%) беременностей с адекватным уровнем прогестерона закончились жизнеспособной беременностью, в то время как 0 из 9 (0%) беременностей с недостаточным уровнем прогестерона закончились жизнеспособной беременностью ( п = 108, Х 2 10.973, p = 0,001) (таблица 2).
Жизнеспособность беременностей в первом триместре с разбивкой по возрастным группам | |||
Жизнеспособная беременность в первом триместре a | Статистическое сравнение d | ||
Недостаточный уровень прогестерона в сыворотке b | Достаточный уровень прогестерона в сыворотке c | ||
Все возрасты (22-45 лет) | 5 (12%) | 208 (72%) | р <0.0001 |
Первичный возраст фертильности (22-34 года) | 5 (15%) | 151 (80%) | р <0,0001 |
Пожилой возраст матери (35-45 лет) | 0 (0%) | 57 (58%) | р = 0.001 |
a Определяется детальным морфологическим ультразвуковым исследованием через 11-13 недель b Менее 25 нг / мл при первом посещении и посещении через 10 недель c Больше или равно 25 нг / мл при первоначальном и / или 10-недельном посещении d X 2 Тест в квадрате для категориальных значений для оценки связи между жизнеспособной беременностью и адекватным уровнем прогестерона в сыворотке | |||
Таблица 2. Жизнеспособность беременностей в первом триместре с разбивкой по возрастным группам.
Обсуждение
Насколько нам известно, это первое исследование, посвященное изучению порогового уровня прогестерона для поддержания беременности. Результаты показывают, что 25 нг / мл — это эффективный пороговый уровень прогестерона в сыворотке крови для поддержания беременности в первом триместре у женщин с выкидышем или бесплодием в анамнезе как у женщин первичного фертильного возраста (22-34 года), так и у женщин пожилого возраста матери (35-35 лет). 45 лет).Данные показывают, что поддержание уровня прогестерона 25 нг / мл в течение первого триместра беременности снижает риск выкидыша в этой популяции.
Это исследование имеет несколько ограничений. Поскольку все пациенты были из одного центра по лечению бесплодия, результаты могут иметь ограниченную применимость к другим группам населения. Будущие многоцентровые исследования с более разнообразным населением и большим размером выборки позволят расширить демографические результаты и сделать возможным дальнейшее расслоение.
Кроме того, у пациентов в этом исследовании различались методы зачатия.Было высказано предположение, что у ранее бесплодных пациенток, зачатых с помощью искусственных репродуктивных технологий (ВРТ), частота самопроизвольных абортов была лишь немного увеличена или схожа по сравнению с беременностями, зачатыми естественным путем [10,11]. Поскольку наша популяция пациентов включает женщин с бесплодием в анамнезе, бесплодные пациенты, зачатые с помощью АРТ, могут не отражать влияние порогового уровня прогестерона 25 нг / мл для этой популяции пациентов.
Метод добавления прогестерона также не контролировался в этом исследовании.Было высказано предположение, что разные способы приема прогестерона по-разному влияют на эндометрий, скорость всасывания и выведения, а также профили распределения. Например, было обнаружено, что пероральный прогестерон неэффективен в отношении секреторной трансформации эндометрия на уровне сывороточного прогестерона, который считается адекватным для этого процесса. Аналогичным образом, вагинальный прогестерон проявлял свое действие на эндометрий при более низких концентрациях в сыворотке крови из-за его выраженного воздействия на матку, так называемый эффект первого прохождения через матку [12].В нашем исследовании предполагалось, что концентрация прогестерона в сыворотке 25 нг / мл или выше, независимо от способа доставки прогестерона, была достаточной для оказания его воздействия на матку во время внутриутробной беременности. Будущие исследования, контролирующие метод приема прогестерона, могут уменьшить несоответствия в изменениях матки, вызванных прогестероном.
Наконец, это исследование не контролировало многоплодную беременность (например, двойню). Исследования подтвердили, что прогестерон является самым сильным предиктором жизнеспособной беременности, и предположили, что для поддержания беременности может потребоваться уровень прогестерона в сыворотке до 58 нг / мл [13,14].В то время как в нашем исследовании было зафиксировано 35 беременностей двойней и тройней в первом триместре с порогом 25 нг / мл, в этих беременностях средний уровень прогестерона превышал 100 нг / мл, что почти вдвое превышает средний показатель жизнеспособных беременностей одноплодной беременностью (65 нг / мл). . Таким образом, часть нежизнеспособных беременностей в нашем исследовании может быть связана с недостаточным уровнем прогестерона у женщин, вынашивающих многоплодную беременность. Дальнейшие исследования помогут определить, нужны ли разные пороги сывороточного прогестерона для одноплодной или многоплодной беременности.
Наши результаты также поддерживают будущие исследования, направленные на установление более высоких пороговых значений сывороточного прогестерона для женщин пожилого возраста матери. В нашем исследовании значительная часть женщин с адекватным уровнем прогестерона в сыворотке в пожилой возрастной группе матери все еще приводила к выкидышу. Кроме того, 0% женщин в пожилой возрастной группе матери с недостаточным уровнем прогестерона имели жизнеспособную беременность. Это говорит о том, что женщинам 35 лет и старше может потребоваться более высокий пороговый уровень прогестерона, чем женщинам моложе 35 лет.Поскольку все больше женщин откладывают беременность до достижения возраста 35 лет, было бы полезно провести дополнительное исследование более высокого порогового уровня для женщин пожилого возраста матери [15].
Насколько нам известно, это первое исследование, в котором установлен эффективный целевой уровень прогестерона для поддержания беременности в первом триместре у женщин с бесплодием или выкидышем в анамнезе. Это исследование демонстрирует необходимость быть более бдительным при мониторинге уровня прогестерона в первом триместре беременности и при необходимости вмешиваться женщинам с бесплодием или выкидышем в анамнезе.
Конфликт интересов
Авторы сообщают об отсутствии конфликта интересов
Финансирование
В данном исследовании не использовались источники финансирования исследований.
Список литературы
- Ragusa A, de Caroli2021 Авторское право OAT. Все права защищены G, et al. (2004) Добавка прогестерона во время беременности: иммунологическая терапия? Волчанка 13: 639-642.[Crossref]
- Габбе С.Г., Нибил Дж. Р., Галан Х. Л. (2012) Акушерство: нормальная и проблемная беременность: нормальная и проблемная беременность. Сент-Луис, США: Сондерс 17: 592-593.
- Csapo A, Pulkkinen M, Kaihola HL (1972) Значение желтого тела человека в поддержании беременности: предварительные исследования. Am J Obstet Gynecol 112: 1061-1067. [Crossref]
- Csapo AI, Pulkkinen MO, Wiest WG (1973) Эффекты лютеэктомии и заместительной терапии прогестероном у пациенток на ранних сроках беременности. Am J Obstet Gynecol 115: 759-765. [Crossref]
- Regan L, Rai R (2000) Эпидемиология и медицинские причины выкидыша. Baillieres Best Practices Clin Obstet Gynaecol 14: 839-854. [Crossref]
- Rossen L, Ahren K, Branum A (2017) Тенденции риска потери беременности среди женщин в США, 1990-2011 гг. Детская и перинатальная эпидемиол.
- Coulam CB (1992) Связь между бесплодием и самопроизвольным абортом. Am J Reprod Immunol 27: 128-129. [Crossref]
- Check JH, Chase JS, Nowroozi K, Wu CH, Adelson HG (1987) Прогестероновая терапия для уменьшения самопроизвольных абортов в первом триместре у предыдущих абортов. Int J Fertil 32: 192-193. [Crossref]
- МакКорд М., Мурам Д., Бастер Дж., Архарт К., Стовалл Т. и др. (1996) Прогестерон в одной сыворотке как скрининг на внематочную беременность: обмен специфичностью и чувствительностью для получения оптимальных результатов теста.Fertil Steril 66: 513-516. [Crossref]
- Wang JX, Norman RJ, Wilcox AJ (2004) Частота самопроизвольных абортов среди беременностей, вызванных вспомогательными репродуктивными технологиями. Репродукция Человека 19: 272-277. [Crossref]
- Schieve LA, Tatham L, Peterson HB, Toner J, Jeng G (2003) Самопроизвольный аборт среди беременных, зачатых с использованием вспомогательных репродуктивных технологий в Соединенных Штатах. Акушерский гинекол 101: 959-967. [Crossref]
- Tavaniotou A, Smitz J, Bourgain C, Devroey P (2000) Сравнение различных способов введения прогестерона в качестве поддержки лютеиновой фазы при лечении бесплодия. Обновление Hum Reprod 6: 139-148. [Crossref]
- Elson J, Salim R, Tailor A, Banerjee S, Zosmer N (2003) Прогнозирование жизнеспособности беременности на ранних сроках при отсутствии эмбриона, определяемого ультразвуком. Ультразвуковой акушерский гинекол 21: 57-61. [ Crossref]
- Гоктолга У, Гунгор С., Джейхан С., Кескин У, Фидан У и др. (2008) Оценка прогностической ценности сывороточного уровня прогестерона для прогноза ранней беременности при спонтанной беременности двойней: проспективное исследование. Eur J Obstet Gynecol Reprod Biol 137: 185-188. [Crossref]
- Мартин Дж., Гамильтон Б., Остерман М., Дрисколл А., Мэтьюз Т. (2017) Рождение: окончательные данные за 2015 год. Natl Vital Stat Rep .
Симптомы, причины и влияние на беременность
Прогестерон — важный гормон, который помогает поддерживать здоровую беременность. Существует много споров о том, как — и может ли — низкий уровень прогестерона повлиять на беременность.Вот что вам нужно знать об этой спорной теме.
Что такое прогестерон?Прогестерон — один из важнейших гормонов, необходимых для поддержания здоровой беременности, и его название говорит само за себя: про беременность. Гормон сначала вырабатывается желтым телом яичника — фолликулом, который опорожнялся, когда яйцеклетка была выпущена во время овуляции. Прогестерон способствует созреванию слизистой оболочки матки, подготавливая матку к потенциальной беременности.
Как только происходит зачатие, гормон беременности хорионический гонадотропин человека (ХГЧ) дает сигнал желтому телу продолжать вырабатывать прогестерон примерно до второго месяца беременности, когда ответственность за секрецию прогестерона берет на себя плацента.Прогестерон сохраняет слизистую оболочку матки здоровой и толстой, обеспечивая правильную среду для развивающегося плода.
Что означает низкий уровень прогестерона?Для нормального протекания беременности необходим нормальный уровень прогестерона, и со временем эти уровни будут увеличиваться. Что считается нормальным с точки зрения уровня прогестерона? Вот диапазон:
- Первый триместр: от 11,2 до 90 нг / мл
- Второй триместр: 25.От 6 до 89,4 нг / мл
- Третий триместр: от 48 до 150 до более 300 нг / мл
Уровень, который значительно ниже нормы (например, ниже 5 нг / мл в первые несколько недель беременности), считается низким. прогестерон, но, к счастью, у большинства женщин уровень прогестерона нормальный, а низкий уровень прогестерона во время беременности встречается довольно редко. На самом деле маловероятно, что вы даже пройдете тест на уровень прогестерона, если ваш практикующий врач не обеспокоен чем-то и не считает, что это важно знать.
Причины низкого прогестеронаНизкий уровень прогестерона на ранних сроках беременности часто является результатом одного из следующих:
- Внематочная беременность
- Выкидыш
- Угроза выкидыша (при вагинальном кровотечении, кровянистых выделениях и / или спазмы в первом триместре)
Симптомы низкого прогестерона могут включать следующее:
Как низкий прогестерон может повлиять на беременность?Вопрос о том, влияет ли низкий прогестерон на беременность, вызывает множество споров.Некоторые эксперты считают, что дефицит прогестерона является реальной проблемой, и такое же количество экспертов говорят, что низкий уровень прогестерона вообще не влияет на беременность.
Те, кто считает, что низкий уровень прогестерона может повлиять на беременность, говорят, что низкий уровень может привести к недостаточно подготовленной матке и что отсутствие толстой оболочки эндометрия в матке может затруднить имплантацию эмбриона или поддержание беременности. сам.
Повышает ли низкий уровень прогестерона вероятность выкидыша?Опять же очень непонятно.Хотя верно, что у женщин, переживших выкидыш, уровень прогестерона обычно ниже, неясно, вызвал ли выкидыш низкий уровень прогестерона или же выкидыш стал причиной низкого уровня прогестерона.
Путаницу усугубляют исследования, в том числе недавнее — и самое крупное на сегодняшний день — рандомизированное исследование, показывающее, что дополнительное назначение прогестерона женщинам с угрозой выкидыша не снижает частоту выкидышей и не увеличивает шансы на продолжение беременности.
Другими словами, наука не поддерживает теорию о том, что низкий уровень прогестерона увеличивает риск выкидыша.
Лечение с низким содержанием прогестеронаЕсли ваш врач по-прежнему считает, что низкий уровень прогестерона может способствовать вашим выкидышам, он может решить попробовать дополнительный прогестерон. Прогестерон можно назначать в следующих формах лечения:
- Инъекции прогестерона
- Вагинальные суппозитории прогестерона
- Таблетки прогестерона для приема внутрь
В случае повторяющихся выкидышей вы должны принять его до зачатия и продолжать принимать его в первые дни беременности. этапы беременности, чтобы помочь сохранить беременность и избежать выкидыша.
Однако имейте в виду, что доказательства не находят положительного эффекта от такого лечения. Единственное исключение: женщины, у которых ранее было не менее трех выкидышей. Исследования показывают, что им может помочь прогестероновая терапия.
Способствует ли низкий прогестерон проблемам фертильности?
Большинство экспертов сходятся во мнении, что низкий уровень прогестерона (или дефицит лютеиновой фазы — когда лютеиновая фаза менструального цикла слишком коротка и, следовательно, уровень прогестерона остается слишком низким) имеет небольшое клиническое значение и не способствует бесплодию.
На самом деле, медицинский консенсус состоит в том, что дефицит лютеиновой фазы не существует сам по себе, а скорее является побочным продуктом других основных гормональных проблем (например, дисфункции щитовидной железы), и что однажды возникает другая гормональная проблема. после лечения нормальная лютеиновая функция (и, следовательно, нормальный уровень прогестерона) восстанавливается.
Может ли низкий прогестерон повлиять на ЭКО?
Цикл ЭКО (при котором гормоны тщательно активируются и деактивируются) отличается от естественного цикла (где яичник вырабатывает прогестерон до тех пор, пока плацента не вступит во владение), потому что некоторые из необходимых лекарств от бесплодия (в частности, агонисты и антагонисты ГнРГ) предотвращают развитие яичников. выработка прогестерона.Это означает, что у женщин, перенесших беременность в результате ЭКО, будет индуцированный низкий прогестерон, и, следовательно, потребуется дополнительный прогестерон, чтобы восполнить дефицит.
В случае беременности с ЭКО прогестерон, принимаемый внутримышечно или через влагалище в виде геля или суппозитория, скорее всего, будет назначен для поддержки развивающейся беременности в течение первых двух-трех месяцев.
Помогают ли добавки прогестерона предотвратить преждевременные роды?
Если вы родили преждевременно во время предыдущей беременности и сейчас вынашиваете только одного ребенка (не многоплодного), еженедельные уколы прогестерона, начиная примерно с 16-20 недели беременности и продолжая до 36 недели, в некоторых исследованиях показали, что снизить риск преждевременных родов.И Американский колледж акушеров и гинекологов (ACOG), и Общество медицины матери и плода говорят, что всем беременным женщинам, которые соответствуют этим критериям, следует предлагать добавки прогестерона, начиная с 16–24 недель беременности.
Если у вас в анамнезе нет преждевременных родов, и ваш врач отмечает, что ваша шейка матки укорочилась ниже 2 см на сроке беременности от 16 до 24 недель (что может увеличить вероятность преждевременных родов), ваш врач может назначить ежедневный гель с прогестероном — он поставляется в виде тампона-аппликатора, который вы помещаете во влагалище, — или вагинальные свечи с прогестероном до 37 недель беременности.
Доказано, что прием прогестерона в таких ситуациях эффективно снижает риск преждевременных родов.
Следует ли использовать безрецептурные свечи с прогестероном или крем с прогестероном при низком уровне прогестерона?
Использование безрецептурных кремов с прогестероном вообще не рекомендуется. Мало того, что такие кремы не регулируются Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA), что означает, что нет установленных стандартов для их состава и уровней концентрации, но также нет исследований, которые показывают какую-либо пользу.
Более того, некоторые типы крема с прогестероном не вызывают значительного повышения уровня прогестерона, поэтому, даже если прогестерон был полезен во время беременности, крем все равно не был бы подходящим источником.
Принимайте прогестероновые свечи только в том случае, если их рекомендовал вам врач.
Есть ли побочные эффекты при приеме крема с прогестероном, прогестероновых суппозиториев или добавок с прогестероном?
Побочных эффектов может не быть — или может быть ряд побочных эффектов.Многое зависит от типа добавки, которую вы принимаете.
Например, суппозитории с прогестероном могут быть грязными и иногда вызывать следующие побочные эффекты:
- Раздражение влагалища
- Зуд
- Жжение
- Дрожжевая инфекция
- Спазмы
- Учащение вагинальных выделений
- Боль
- Отек и синяк в месте инъекции
- Головная боль или мигрень
- Болезненность груди
- Сонливость
- Головокружение
- Задержка жидкости
- Вздутие живота
- Приливы Приливы веса