Тромбоэмболия лёгочной артерии (ТЭЛА) | Статьи клиники Медсервис
Тромбоэмболия лёгочной артерии (ТЭЛА) — закупорка лёгочной артерии или её ветвей тромбами, которые образуются чаще в крупных венах нижних конечностей или таза (эмболия). В зарубежной литературе распространено более широкое понятие лёгочная эмболия, которое также включает в себя редкие воздушные, жировые эмболии, эмболии амниотической жидкостью, инородными телами, опухолевыми клетками.
ТЭЛА — относительно распространённая сердечно-сосудистая патология (примерно 1 случай на тысячу населения в год). В США ТЭЛА наблюдают примерно у 650 000 человек, которая приводит к 350 000 смертям в год. ТЭЛА чаще возникает у пожилых . Данные о связи пола с ТЭЛА разнятся, однако анализ национальной базы данных США выявил, что у мужчин смертность на 20—30% выше, чем у женщин.
Заболеваемость венозной тромбоэмболией среди пожилых выше у мужчин, но у пациентов моложе 55 лет — выше у женщин.
При эмболах небольших размеров симптомы отсутствуют. Крупные эмболы ухудшают перфузию сегментов или даже целых долей лёгкого, что приводит к нарушению газообмена и развитию гипоксии. В ответ на это рефлекторно сужается просвет сосудов малого круга кровообращения, повышается давление в лёгочных артериях.
Увеличивается нагрузка на правый желудочек из-за высокого лёгочного сосудистого сопротивления, вызванного обструкцией и вазоконстрикцией. При тромбоэмболии мелких ветвей лёгочной артерии не сопровождается расстройствами гемодинамики и в 10% случаев развивается инфаркт лёгкого и вторичная инфарктная пневмония.
Диагностика и лечение острой и хронической тромбоэмболии легочной артерии
Авторы: Б.М. Тодуров
Медицина достигла колоссальных успехов в лечении одних заболеваний и достаточно медленно продвигается в решении других. Тромбоэмболия легочной артерии (ТЭЛА) до сих пор остается одной из наиболее серьезных проблем современной медицины и по-прежнему характеризуется очень высокими показателями смертности. О том, как диагностировать и правильно лечить это тяжелое и потенциально фатальное заболевание, участникам Международного конгресса по гемостазиологии, анестезиологии и интенсивной терапии «Black Sea Pearl», проходившего 20-21 мая в г. Одессе, рассказал директор Киевского городского центра сердца, член-корреспондент НАМН Украины, доктор медицинских наук, профессор Борис Михайлович Тодуров.

В начале своего выступления докладчик отметил, что согласно современным представлениям ТЭЛА рассматривается не как отдельная нозология, а как одно из проявлений венозного тромбоэмболизма (ВТЭ), включающего также тромбоз глубоких вен (ТГВ). Обусловлено это тем, что ветви легочной артерии закупориваются не образовавшимся на месте тромбом, а принесенным из венозной системы тромбоэмболом. Так, в 80-90% случаев причиной ТЭЛА становится ТГВ нижних конечностей, реже – ТГВ верхних конечностей либо изолированный тромбоз в системе нижней полой вены. При этом путь миграции тромба достаточно прост: глубокие вены (чаще всего нижних конечностей) → нижняя полая вена → правое предсердие → правый желудочек → легочная артерия и ее ветви.
К факторам риска развития ВТЭ относятся онкологические заболевания, перенесенное хирургическое вмешательство или травма, прием пероральных контрацептивов, длительная иммобилизация, ожирение, сердечная недостаточность, любые воспалительные заболевания органов малого таза, патология свертывающей системы крови и др.
Профессор Б.М. Тодуров подчеркнул, что ТЭЛА является смертельно опасным, зачастую трудно диагностируемым и в то же время широко распространенным патологическим состоянием. Так, по данным B. Lindblad и соавт. (1991), частота развития ТЭЛА составляет приблизительно 70 случаев на 100 тысяч населения в год, а летальность при этой патологии достигает 20-28% (D.E. Lilienfield et al., 1990). В структуре госпитальной летальности на ТЭЛА приходится около 10% (A. Zaccaria et al., 1998). При этом статистика не очень утешительна даже в наиболее экономически развитых странах мира и их ведущих клиниках.
Одной из основных причин высокой летальности при ТЭЛА является ее поздняя диагностика. Приведенные цифры могут шокировать, но прижизненно диагностируется только 20-25% случаев ТЭЛА, причем не менее половины из них – в терминальном состоянии. Такая плачевная ситуация во многом обусловлена частым бессимптомным течением ТГВ. Так, приблизительно 80% случаев ТГВ являются клинически «немыми», поэтому ТЭЛА развивается без каких-либо предвестников. Второй причиной является очень быстрое, иногда молниеносное развитие массивной ТЭЛА, когда пациент очень быстро оказывается в критическом состоянии и ему просто не успевают помочь. И, наконец, третья причина заключается в том, что симптомы ТЭЛА являются не очень специфическими (одышка, тахипноэ, тахикардия), что часто приводит к задержке установления правильного диагноза.
Второй причиной является очень быстрое, иногда молниеносное развитие массивной ТЭЛА, когда пациент очень быстро оказывается в критическом состоянии и ему просто не успевают помочь. И, наконец, третья причина заключается в том, что симптомы ТЭЛА являются не очень специфическими (одышка, тахипноэ, тахикардия), что часто приводит к задержке установления правильного диагноза.
У всех пациентов с такими симптомами, как одышка, тахипноэ и тахикардия, особенно при наличии факторов риска ВТЭ, следует заподозрить наличие ТЭЛА.
Какие же методы диагностики необходимо использовать при подозрении на ТЭЛА? Всегда следует начинать с более простых и доступных методов, которые позволяют определиться с дальнейшей тактикой, – измерение газового состава крови и/или пульсоксиметрия, электрокардиография (ЭКГ), эхокардиография (ЭхоКГ), ультразвуковое исследование вен нижних конечностей. Так, в пользу ТЭЛА будут свидетельствовать снижение насыщения крови кислородом, признаки перегрузки правого желудочка на ЭКГ, недостаточность трехстворчатого клапана и повышенное давление в правом желудочке и легочной артерии по данным ЭхоКГ. Дуплексное сканирование вен нижних конечностей помогает выяснить источник эмболии для дальнейшего решения вопроса об установке кава-фильтра.
Дуплексное сканирование вен нижних конечностей помогает выяснить источник эмболии для дальнейшего решения вопроса об установке кава-фильтра.
Демонстрируя результаты ЭхоКГ у больных ТЭЛА, профессор Б.М. Тодуров обратил внимание на один случай, когда тромбоэмбол был обнаружен в левом предсердии. Он напомнил, что у больного с ТГВ и ТЭЛА в ветвях легочной артерии может быть обнаружен не один тромбоэмбол. Иногда имеет место так называемая парадоксальная эмболизация, когда тромб, образовавшийся в венозной системе, попадает в левое предсердие через овальное окно. Овальное окно остается открытым примерно у 10% людей и обычно прикрыто заслонкой из-за более высокого давления в левом предсердии по сравнению с правым. Но при повышении давления в правых отделах сердца вследствие вызванной ТЭЛА легочной гипертензии овальное окно открывается, что дает возможность еще одному оторвавшемуся тромбу проникнуть в левое предсердие. И тогда эмболизация большого круга кровообращения может привести к развитию, в дополнение к ТЭЛА, еще и инфаркта миокарда, инсульта, инфаркта почки, кишечника и др.
Возвращаясь к диагностическому алгоритму, лектор отметил, что повышение давления в легочной артерии >30 мм рт. ст. по данным ЭхоКГ является показанием для проведения ангиопульмонографии.
Ангиопульмонография – основной и наиболее достоверный на сегодня метод диагностики ТЭЛА. Компьютерную томографию (КТ) с контрастным усилением следует использовать только в тех клиниках, где нет возможностей для проведения ангиопульмонографии, так как при сопоставимой стоимости и лучевой нагрузке диагностическая ценность КТ ниже.
Так, разрешающая способность КТ позволяет выявлять тромбоэмболию только в долевых и сегментарных ветвях легочной артерии, тогда как ангиопульмонография обнаруживает тромбоэмболы диаметром до 1 мм. Бывают ситуации, когда при клинической картине массивной ТЭЛА на КТ ничего не обнаруживается, и причиной этого может быть как раз эмболизация не одной большой ветви, а множества мелких ветвей.
В центре, возглавляемом профессором Б.М. Тодуровым, положительные решения по постановке кава-фильтров принимаются в большинстве случаев массивной ТЭЛА с наличием у пациента ТГВ нижних конечностей. Исключением являются в основном только женщины фертильного возраста, поскольку во время беременности это устройство может вызывать пролежень на матке. В Киевском городском центре сердца было установлено уже более 1000 кава-фильтров и отмечено только 2 случая дислокации, один из которых, правда, закончился летальным исходом. В то же время риск рецидива ТЭЛА у пациентов, которым кава-фильтр не устанавливали, составлял примерно 30% со значительно более высокими показателями летальности (тоже около 30%). Таким образом, по мнению докладчика, соотношение рисков явно свидетельствует в пользу установки кава-фильтра.
Основным методом лечения острой ТЭЛА является тромболитическая терапия.
Согласно инструкциям по применению тромболитики следует использовать в первые трое суток после тромбоза или тромбоэмболии, так как именно в этот промежуток времени они наиболее эффективны. Однако на практике применение современных тромболитиков дает хорошие результаты и в более поздние сроки. Так, в клинике профессора Б.М. Тодурова успешный тромболизис проводился даже через 20-30 дней после манифестации ТЭЛА.
Чаще всего в своей практике профессор отдает предпочтение тромболитику альтеплазе. Во-первых, это синтетический препарат, в то время как другой известный тромболитик – стрептокиназа – имеет биологическое происхождение и поэтому характеризуется высоким риском анафилактической реакции в случае повторного введения. Важно помнить об этом отличии, поскольку у части пациентов возникает необходимость в 2-3-кратном применении тромболитика.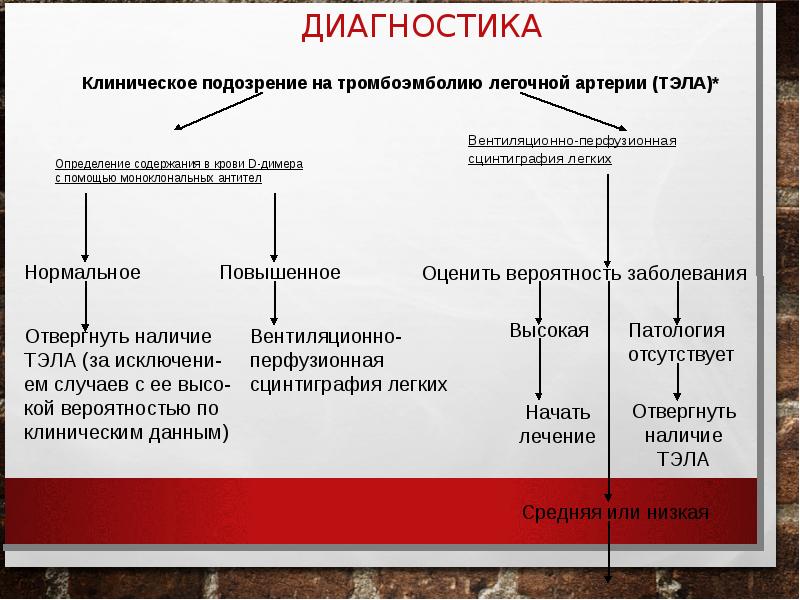 Во-вторых, альтеплаза характеризуется более низким риском геморрагических осложнений из-за более короткого периода полураспада.
Во-вторых, альтеплаза характеризуется более низким риском геморрагических осложнений из-за более короткого периода полураспада.
Основными противопоказаниями к проведению тромболизиса являются: острое кровотечение, значительные нарушения свертывания крови, новообразования с повышенным риском кровотечения, подозрение на расслоение аорты, разрыв аневризмы, неконтролируемая артериальная гипертензия, ранний послеоперационный период, старческий возраст (более 80 лет).
По мнению докладчика, проведение тромболизиса после хирургического вмешательства возможно в том случае, если послеоперационная рана уже не кровоточит и прекратилось выделение кровянистого содержимого по дренажам, что обычно наблюдается на 6-7-е сутки после операции. В этом случае он выполняется с тщательным контролем показателей свертывающей системы крови.
В клинике профессора Б.М. Тодурова отмечено два случая, когда тромболизис был успешно проведен пациентам с массивной ТЭЛА и остановкой сердца одновременно с непрямым массажем сердца. Естественно, что в такой ситуации реанимационные мероприятия следует проводить очень осторожно, стараясь не повредить ребра. С другой стороны, докладчик признал, что реанимировать такого больного без тромболизиса вряд ли удастся.
Естественно, что в такой ситуации реанимационные мероприятия следует проводить очень осторожно, стараясь не повредить ребра. С другой стороны, докладчик признал, что реанимировать такого больного без тромболизиса вряд ли удастся.
После проведения тромболизиса обязательно на 3 дня назначают нефракционированный гепарин (под контролем активированного частичного тромбопластинового времени), а затем для длительной вторичной профилактики – варфарин (под контролем международного нормализованного отношения) или новые пероральные антикоагулянты.
В случае наличия противопоказаний к применению тромболитиков или продолжительности заболевания более 20 дней пациентам с острой ТЭЛА показано хирургическое лечение – тромбоэмболэктомия.
Тромбоэмболэктомия выполняется в условиях остановки сердца и подключения искусственного кровообращения. Свежие тромбы удаляются через открытую легочную артерию механическим путем без каких-либо сложностей.
Особого подхода требуют пациенты с хронической ТЭЛА. Если изначальная эмболизация легочной артерии прошла незамеченной либо под видом инфаркт-пневмонии, тромб организуется и у пациента развивается хроническая легочная гипертензия. Она, в свою очередь, приводит к перегрузке правого желудочка с его дальнейшей гипертрофией и дилатацией фиброзного кольца трехстворчатого клапана, а также с развитием венозного застоя в большом круге кровообращения. Это еще больше усиливает тромбообразование. В итоге новые тромбоэмболы вызывают окклюзию все большего количества ветвей легочной артерии, что замыкает порочный круг. Рано или поздно пациент госпитализируется в связи со значительным ухудшением состояния.
Если изначальная эмболизация легочной артерии прошла незамеченной либо под видом инфаркт-пневмонии, тромб организуется и у пациента развивается хроническая легочная гипертензия. Она, в свою очередь, приводит к перегрузке правого желудочка с его дальнейшей гипертрофией и дилатацией фиброзного кольца трехстворчатого клапана, а также с развитием венозного застоя в большом круге кровообращения. Это еще больше усиливает тромбообразование. В итоге новые тромбоэмболы вызывают окклюзию все большего количества ветвей легочной артерии, что замыкает порочный круг. Рано или поздно пациент госпитализируется в связи со значительным ухудшением состояния.
Лектор отметил, что при острой ТЭЛА давление в легочной артерии в большинстве случаев не превышает 50 мм рт. ст., поскольку неизмененный правый желудочек не способен поддерживать более высокое давление. В свою очередь, при хронической ТЭЛА, когда происходит постепенная адаптация правого желудочка к возрастающей нагрузке (увеличению сопротивления в системе легочной артерии по мере добавления мелких тромбов в ее ветвях), давление, развиваемое правым желудочком, может достигать 120-140 мм рт. ст.
ст.
В связи с тем что старые тромбы уже организованы, тромболизис у пациентов с хронической ТЭЛА не эффективен. В то же время выполнение пациентам с хронической ТЭЛА и выраженной легочной гипертензией только тромбэндартерэктомии из легочной артерии не позволяет устранить венозный застой, поэтому эта операция должна обязательно сопровождаться пластикой трехстворчатого клапана, недостаточность которого в данном случае носит органический характер (дилатация фиброзного кольца).
Пластику трехстворчатого клапана выполняют обычно опорными кольцами, по «клеверной» методике. Без ее проведения венозный застой и повышенное тромбообразование будут сохраняться даже несмотря на применение антикоагулянтов.
Тромбэндартерэктомию при хронической ТЭЛА необходимо выполнять не только при условии гипотермии (иногда до 14 °C) и искусственного кровообращения, но и зачастую с полной остановкой кровообращения или минимальной перфузией в малом кругу. В противном случае даже небольшое повреждение стенки легочной артерии или ее ветвей во время удаления тромба может привести к массивному и неконтролируемому кровотечению, поскольку кровь во время искусственного кровообращения гепаринизирована.
Больным с длительно существующим супрасистемным давлением в легочной артерии на фоне хронической ТЭЛА тромбэктомию выполнять нельзя из-за склерозирования сосудов, в таких случаях показана только трансплантация комплекса «сердце-легкие».
Подготовила Наталья Мищенко
Тромбоэмболия легочной артерии — симптомы, диагностика, лечение, профилактика
Тромбы в большинстве случаев (70%) образуются в венах нижних конечностей и малого таза. Оторвавшийся тромб называют «эмболом». Миграция эмбола по венам в сторону сердца и далее в легочную артерию приводит к закупорке (тромбозу) ствола и ветвей легочной артерии – тромбоэмболии легочной артерии.
В зависимости от размера (диаметра и длины) эмбола различается и клиническая картина тромбоэмболии. Тромбоз мелких ветвей легочной артерии приводит к умеренно выраженной дыхательной недостаточности с последующим развитием инфарктной пневмонии в результате нарушения кровоснабжения тканей легких. В случае тромбоза главных ветвей легочной артерии, помимо инфарктной пневмонии, развиваются более серьезные осложнения – хроническая постэмболическая легочная гипертензия и тяжелая сердечно-легочная недостаточность, приводящие к инвалидизации пациента. Тромбоз крупным эмболом основного ствола легочной артерии в большинстве случаев приводят к гибели пациента.
В случае тромбоза главных ветвей легочной артерии, помимо инфарктной пневмонии, развиваются более серьезные осложнения – хроническая постэмболическая легочная гипертензия и тяжелая сердечно-легочная недостаточность, приводящие к инвалидизации пациента. Тромбоз крупным эмболом основного ствола легочной артерии в большинстве случаев приводят к гибели пациента.
Клиническая картина тромбоэмболии легочной артерии
В зависимости от тяжести поражения легочного русла появляются такие симптомы, как:
- одышка – от легкого затруднения дыхания до полного апноэ;
- снижение давления – от умеренного до очень низкого;
- цианоз – посинение лица, шеи, верхней части грудной клетки;
- боли за грудиной.
Через несколько дней на фоне инфарктной пневмонии появляются кашель, повышение температуры, кровохарканье. Подобные симптомы могут быть причиной и других заболеваний, например инфаркта миокарда. При таких симптомах необходима срочная врачебная помощь.
Подобные симптомы могут быть причиной и других заболеваний, например инфаркта миокарда. При таких симптомах необходима срочная врачебная помощь.
Диагностика
Совокупность вышеописанных симптомов при наличии отека нижних конечностей (тромбоза глубоких вен) чаще всего позволяет предположить тромбоэмболию легочной артерии.
Лечение
Оперативно должны быть приняты следующие меры скорой помощи:
- введение больших доз антикоагулянтов;
- лечебные мероприятия, стабилизирующие сердечно-легочную деятельность.
По прибытии в стационар с диагнозом тромбоэмболия легочной артерии важно уточнить объем поражения, чтобы назначить правильное лечение. Для этого проводится дополнительное исследование – рентген-контрастирование легочной артерии и ее ветвей (ангиопульмонография). При массивной тромбоэмболии легочной артерии применяются следующие методы лечения:
- тромболизис – попытка растворить тромб, находящийся в легочной артерии, путем введения специальных препаратов – тромболитиков;
- удаление тромба специальным катетером или разрушение его на более мелкие части для освобождения основного легочного ствола с целью обеспечения работы сердца и легких.

Для профилактики образования новых тромбов проводят антикоагулянтную терапию. Одновременно проводятся мероприятия по восстановлению и поддержанию работы легких и сердца. Все эти манипуляции осуществляются только в отделении реанимации. В случае угрозы повторной эмболии выполняются оперативные вмешательства – перевязка вены и установка специальных ловушек выше тромба, на пути его возможной миграции в сторону сердца.
Профилактика
- Предупреждение и своевременное лечение заболеваний вен.
- Активный образ жизни.
- Курсовой прием венотоников 2 раза в год.
- Ношение компрессионного трикотажа.
Заметив первые симптомы заболеваний вен – боли, отеки нижних конечностей, уплотнение и покраснение подкожных вен, оперативно обратитесь к врачу-флебологу для проведения УЗИ вен нижних конечностей. Вовремя диагностированное заболевание поможет предотвратить угрозу нарастания тромба в сторону сердца и легочной артерии, сохранив тем самым ваше здоровье.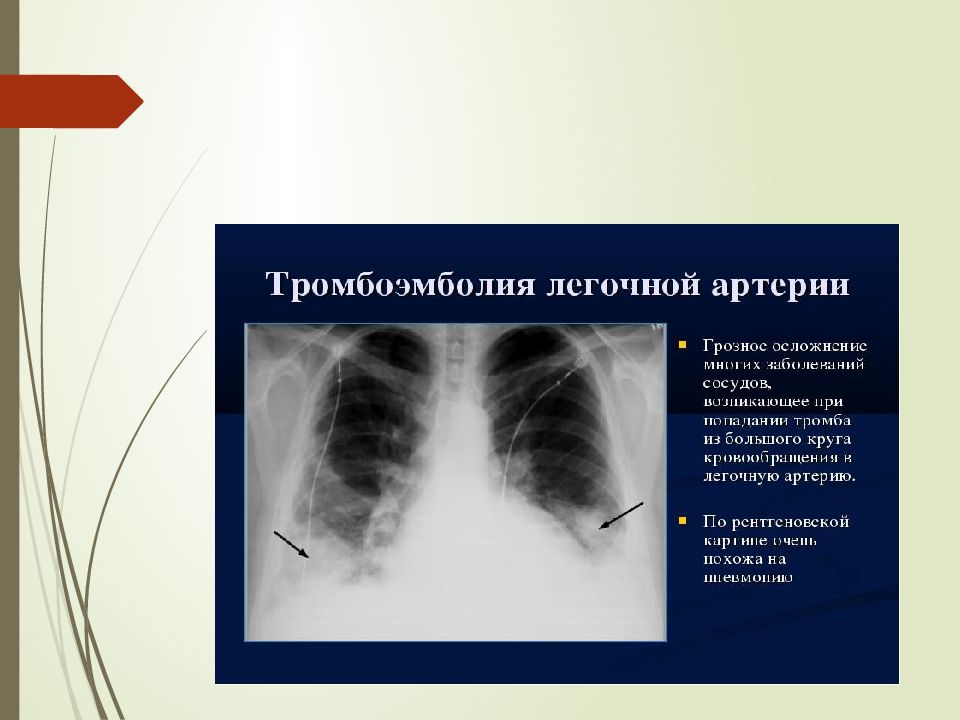
D-димер для исключения тромбоэмболии легочной артерии у пациентов амбулаторных отделений и отделений скорой и неотложной помощи
Вопрос обзора
Оценить возможности теста на D-димер исключать диагноз тромбоэмболии легочной артерии (ТЭЛА) у пациентов, находящихся на лечении в амбулаторном отделении больницы и отделении скорой и неотложной помощи.
Актуальность
Тромбоэмболия легочной артерии (ТЭЛА) – это серьезное состояние с возможным смертельным исходом, которое развивается при закупорке тромбом кровеносных сосудов легких. Когда люди поступают в отделение скорой и неотложной помощи с жалобами на затруднение дыхания, одышку и боль в грудной клетке, возможны несколько объяснений появления этих жалоб, но диагноз необходимо установить быстро. Доступные исследования, позволяющие обнаружить тромбы в легких, могут быть инвазивными, отнимать много времени, нести радиационную нагрузку и могут быть затратными. Быстрые, простые в использовании и недорогие исследования/тесты, позволяющие исключать диагноз, были бы очень ценными.
Одним из таких тестов является тест на D-димер, названный так в связи с тем, что обнаруживает небольшие фрагменты белка в крови, которые называют D-димерами. Когда кто-нибудь поступает в отделение скорой и неотложной помощи стационара c одышкой и болью в грудной клетке, персонал проводит осмотр и расспрашивает пациента об истории его болезни и образе жизни. Это помогает им оценить риск того, что симптомы обусловлены ТЭЛА.
Если, по оценке, риск кровяного сгустка/тромба в легких высок, пациенты немедленно проходят диагностическое сканирование (или же получают лечение в ожидании результатов). Тест на D-димер может быть проведен людям с низким или умеренным (или маловероятным) риском; отрицательный результат на D-димер может исключить диагноз ТЭЛА без необходимости визуализации.
Характеристика исследований
В этом обзоре рассмотрены все доказательства, полученные из исследований, в которых оценивали возможности теста на D-димер исключать ТЭЛА у людей в амбулаторном отделении больницы или отделении скорой и неотложной помощи.
Мы оценили все доступные отчеты исследований, полученные в результате широкого поиска в базах данных медицинской литературы. Два автора обзора независимо оценивали исследования, соответствующие критериям обзора, включая использование дизайна исследования, называемого «поперечное (одномоментное) клиническое исследование»; включение людей с симптомами ТЭЛА, находящихся в амбулаторном отделении больницы и отделении скорой и неотложной помощи; использование шкалы оценки риска и затем теста на D-димер; и сравнение результатов теста на D-димер с результатами лучших из доступных тестов/исследований – вентиляционно-перфузионного сканирования (ВПС), ангиопульмонографии и КТ-ангиопульмонографии.
Основные результаты
Нашим критериям соответствовали 4 исследования, были доступны данные 1585 пациентов. Мы обнаружили доказательства, что отрицательные (отсутствие болезни) результаты теста на D-димер полезны в исключении ТЭЛА и выявлении пациентов без ТЭЛА, однако высокое число ложноположительных результатов теста позволяет предположить, что пациенты с повышенным D-димером могут и не иметь ТЭЛА; следовательно, при положительном результате далее следует провести визуализацию. В одном исследовании ложноположительные результаты чаще встречались у людей старше 65 лет.
Качество доказательств
Поток пациентов, время проведения теста на D-димер и стандартные эталонные тесты вызвали большие методологические опасения; никто из авторов исследований не предоставил диаграмм потока пациентов, и лишь в одном исследовании отчетливо сообщали о времени между назначением изучаемого теста и стандартных эталонных тестов. В оставшихся трех исследованиях о времени между проведением изучаемого теста и завершением стандартных эталонных тестов четко не сообщали, что привело к неясному риску смещения.
Выводы
Ограниченные доказательства из исследований, включенных в этот обзор, позволяют предположить, что количественные тесты на D-димер, применяемые в отделениях неотложной помощи, дают мало ложноотрицательных результатов, но очень много ложноположительных результатов, и имеют высокий уровень чувствительности, согласующийся во всех возрастных группах. Это делает этот тест полезным в качестве теста исключения, однако положительный результат нуждается в подтверждении методами диагностической визуализации.
возможности лучевой диагностики – тема научной статьи по клинической медицине читайте бесплатно текст научно-исследовательской работы в электронной библиотеке КиберЛенинка
Тромбоэмболия легочной артерии: возможности лучевой диагностики
И.Е. Тюрин
Диагностика тромбоэмболии легочной артерии (ТЭЛА) всегда представляла собой трудную задачу. При жизни диагноз ТЭЛА устанавливается менее чем в 70% случаев. Летальность среди пациентов без патогенетической терапии составляет 40% и более, при массивной тромбоэмболии достигает 70%, а при своевременно начатой терапии — 2-8%. Клиническая симптоматика ТЭЛА часто оказывается неспецифичной, что определяет необходимость применения многочисленных лабораторных и инструментальных тестов, среди которых методы лучевой диагностики всегда играли важную роль. В последние годы в этой области произошли существенные изменения, связанные, в первую очередь, с быстрым технологическим прогрессом в рентгеновской компьютерной томографии (КТ).
Клиническая оценка
При ТЭЛА можно выделить два патогенетических механизма, определяющих клиническую симптоматику: “механическая” обструкция сосудистого русла и гуморальные нарушения, возникающие в результате выброса биологически активных веществ. Хотя клинические симптомы ТЭЛА часто неспецифичны, существует ряд “классических” признаков, наличие которых свидетельствует о высокой вероятности этого диагноза. Циркуляторные нарушения могут реализоваться в клиническую картину кардиогенного шока или синкопального состояния, сопровождающихся резким снижением артериального давления, одышкой и болевым синдромом. В случаях посте-
Игорь Евгеньевич Тюрин — профессор, зав. кафедрой лучевой диагностики, лучевой терапии и медицинской физики РМАПО.
пенного развития ТЭЛА наиболее частыми клиническими симптомами становятся немотивированная одышка (80%), плевральные или загрудинные боли (60%), кашель (50%), кровохарканье (25%).
Для оценки вероятности ТЭЛА имеет значение совокупность наиболее типичных клинических симптомов в сочетании с данными инструментальных исследований. Так, в исследовании РЮРЕЭ сочетание высокой клинической вероятности ТЭЛА с высокой вероятностью этого диагноза по данным вентиляционно-перфузионной сцинтиграфии легких (У/О-сканирова-ния) определило положительный предсказательный уровень, равный 96%. Наоборот, нетипичная клиническая картина вместе с низкой вероятностью ТЭЛА при У/О-сканировании обусловила отрицательный предсказательный уровень, равный 97%. К сожалению, более 75% пациентов с ТЭЛА в этом исследовании не могли быть включены ни в одну из названных групп в силу неопределенности клинической и сцинтиграфической картины.
В исследовании Р!8Д-РЕТ было показано, что высокая клиническая вероятность ТЭЛА наряду с типичными изменениями при У/О-сканировании делает диагноз ТЭЛА возможным у большинства больных. Наоборот, низкая клиническая вероятность ТЭЛА при отсутствии характерных изменений на У/О-сканограммах позволяет уверенно исключить этот диагноз. Несоответствие клинических и сцинти-графических данных требует дальнейших инструментальных исследований.
Ультразвуковое исследование
Наиболее частым источником ТЭЛА являются глубокие вены таза и нижних конечностей. Обнаружение венозного
тромбоза (ВТ) этой локализации служит веским аргументом в пользу возможного развития ТЭЛА и начала тромболитической терапии. В настоящее время диагностика тромбоза вен нижних конечностей и таза осуществляется с помощью ультразвукового исследования (УЗИ), которое практически полностью заменило традиционное контрастное рентгеновское исследование периферических вен — флебографию.
УЗИ с использованием высокочастотных датчиков позволяет выявить два основных признака патологии: собственно тромбы в просвете периферических вен и замедление или отсутствие кровотока по венозным сосудам. Чувствительность и специфичность УЗИ у больных с клинической симптоматикой ВТ исключительно высоки — до 97%. При отсутствии клинических проявлений ВТ возможности УЗИ существенно ниже: чувствительность и специфичность колеблются от 35 до 99%. Поэтому отсутствие признаков ВТ при УЗИ вен нижних конечностей не исключает наличия ТЭЛА. Кроме того, в настоящее время не вполне ясно, нужно ли выполнять УЗИ всем больным с предполагаемой ТЭЛА или только пациентам с клиническими симптомами патологии вен нижних конечностей. Известно, что частота ВТ у больных с предполагаемой ТЭЛА составляет около 18%, а у больных с доказанной ТЭЛА — до 35-45%.
Рентгенография легких
Рентгенография органов грудной полости является стандартным и обязательным тестом для больных с предполагаемой ТЭЛА. Среди больных с установленной ТЭЛА патологические изменения выявляются в 86-88%. Эти признаки можно условно разделить на “прямые” и косвенные. В действитель-
Рис. 1. Обзорная рентгенограмма. ТЭЛА: выраженное обеднение легочного рисунка в обоих легких; расширение легочной артерии в корне правого легкого, обрыв ее тени в дистальной части; митральная конфигурация срединной тени.
ности все рентгеновские признаки ТЭЛА являются косвенными, так как при нативном исследовании (без контрастирования легочных сосудов) выявить тромбы в просвете артерий невозможно. Так называемые “прямые” признаки, выявляемые на обзорных рентгенограммах, обусловлены изменениями сосудистого легочного рисунка и крупных артериальных сосудов в корнях легких. Косвенные симптомы в основном отражают рефлекторные изменения органов грудной полости при острой закупорке артериальных сосудов.
Прямыми рентгеновскими признаками ТЭЛА являются локальное обеднение легочного рисунка (симптом Westermark), обрыв крупного артериального сосуда в области корня легкого (симптом Fleischner) и локальное расширение сосуда выше места его ампутации (рис. 1). Эти симпто-
мы выявляются относительно редко — в 10-12% случаев, однако их диагностическое значение исключительно велико, особенно у больных с высокой клинической вероятностью ТЭЛА.
Косвенные признаки включают высокое расположение диафрагмы на стороне поражения, дисковидные ателектазы (коллапсы) в виде горизонтально расположенных линейных теней над диафрагмой, накопление жидкости (часто геморрагической) в плевральной полости. Дополнительными симптомами служат рентгеновские признаки артериальной легочной гипертензии: митральная конфигурация срединной тени на рентгенограмме в прямой проекции при отсутствии увеличения левого предсердия на рентгенограмме в боковой проекции, расширение крупных легочных артерий в об-
ласти корней легких, обеднение сосудистого легочного рисунка на периферии легочных полей (см. рис. 1).
Важным признаком ТЭЛА является инфаркт легкого, который отображается на рентгенограммах и линейных томограммах в виде локального участка уплотнения легочной ткани в суб-плевральных (кортикальных) отделах легкого (рис. 2). Такое уплотнение обычно имеет округлую трапециевидную форму, однородную структуру, среднюю или низкую интенсивность тени, просветы бронхов в нем не прослеживаются. Инфаркт широким основанием прилежит к висцеральной плевре, что устанавливается при многопроекционном исследовании, но особенно отчетливо выявляется при КТ. Размеры инфаркта редко превышают 2-3 см, обычно более крупные участки уплотнения обусловлены проекционным наложением теней нескольких мелких инфарктов. Характерна динамика изменений: интенсивность и размеры тени инфаркта увеличиваются в первые 2-3 дня, затем остаются стабильными в течение нескольких дней, после чего начинается медленное уменьшение их размеров с
Рис. 2. Инфаркт правого легкого. а, б — обзорные рентгенограммы; в — КТ. Уплотнение легочной ткани в кортикальной зоне правого легкого, широким основанием прилежащее к висцеральной плевре. Структура уплотнения однородная, просветы бронхов не видны. На томограмме виден бронхососудистый тяж от корня легкого к зоне инфаркта./О).
Перфузионная сцинтиграфия выполняется при внутривенном вве-
дении макроагрегатов 1 меченного технецием
(99тТс) альбумина с последующей регистрацией изображений в шести стандартных проекциях. Макроагрегаты альбумина, попадая в малый круг кровообращения, вызывают кратковременную эмболию примерно 1/10000 части капиллярного русла, что достаточно для получения изображения легочной перфузии на сцинти-граммах (рис. 3а). Вероятность обнаружения дефектов перфузии при ТЭЛА зависит от их размеров и от длительности окклюзии сосудистого русла. Считается, что сцинти-графия должна быть выполнена в течение первых 24 ч от начала клинических проявлений ТЭЛА.
Вентиляционная сцинтиграфия выполняется при ингаляции смеси воздуха и инертного газа, чаще всего криптона (81тКг), с последующим изображением легочных полей в аналогичных шести стандартных проекциях. Если при перфузионной сцин-тиграфии не выявляют дефектов, ее определяют как нормальную. Если при перфузионной сцинтиграфии выявляется дефект, но вентиляционные сканограммы оказываются нормальными или изменения локализуются в другой зоне, это состояние определяется как вентиляционно-перфузионное несоответствие, имеющее высокую вероятность в отношении ТЭЛА. Если при перфузионной и вентиляционной сцинтиграфии выявляется дефект одинаковой локализации, эти изменения трактуются как низкая вероятность ТЭЛА, но не исключающие ее.
Существуют различные подходы к
оценке результатов вентиляцион-
но-перфузионного сканирования.
Наибольшее распространение получили критерии исследования PIOPED, в соответствии с которыми выделено четыре варианта изменений: высокая, низкая, промежуточная (неопределенная) вероятность ТЭЛА и норма. К сожалению, среди специалистов в области радионуклидной диагностики существуют серьезные различия в понимании перечисленных градаций, особенно касающиеся низкой и неопределенной вероятности. В связи с этим в практике нередко используются более простые классификации. Например, Hull R.D. et al. разделили результаты сцинтиграфии на три группы: норма, высокая вероятность и нерезультативное исследование. При этом норма определяется как отсутствие дефектов перфузии, а высокая вероятность ТЭЛА — как дефекты перфузии, занимающие 25-74% сегмента легкого.
Значение сцинтиграфии в диагностике ТЭЛА до настоящего времени оценивается противоречиво. Известно, что нормальные результаты сканирования позволяют полностью исключить наличие ТЭЛА, вероятность ошибки в этом случае не превышает 0,2%. С другой стороны, при высокой вероятности ТЭЛА по данным сцинти-графии тромбы в легочной артерии обнаруживаются у 88% больных. При этом у большинства пациентов (более 60% во всех исследованиях) с предполагаемой ТЭЛА результаты сцинтиграфии соответствуют промежуточной или низкой вероятности. В клинической практике это не позволяет ни исключить, ни подтвердить ТЭЛА и требует проведения дальнейших диагностических исследований.
Ангиопульмонография
Ангиопульмонография (АПГ) является стандартным методом выявления ТЭЛА и до настоящего времени воспринимается как “золотой стандарт” диагностики (рис. 3б).
Исследование начинается с введения в бедренную вену тонкого катетера, который проводится по венозным сосудам до правого предсердия, далее через трикуспидальный клапан в
Рис. 3. ТЭЛА. Дефект перфузии в верхушечном сегменте нижней доли правого легкого. а — перфузионная сцинтиграфия; б — ангиопульмонография.
формированием рубца, плевральных
> 4*2005
www.atmosphere-ph.ru
правый желудочек и ствол легочной артерии. После пробной инфузии контраста для исключения тромбов в общем стволе катетер устанавливается в правой, а затем в левой легочной артерии. При введении контраста в каждую из артерий выполняется серия рентгенограмм в двух проекциях в условиях дигитальной субтракцион-ной ангиографии. Процедура является относительно безопасной, несмотря на очевидный инвазивный характер. Осложнения АПГ возникают редко (0,3-1,8%), летальные исходы в последние годы не встречаются.
Поскольку АПГ является рефе-ренсным методом в отношении ТЭЛА, трудно говорить о ее информативности. Известно, что чувствительность и специфичность АПГ достигают 96-98%, но снижаются при уменьшении калибра пораженных сосудов, что связано с трудностями интерпретации ангиограмм. Так, в исследовании PIOPED согласованное заключение при тромбоэмболии субсегментарных ветвей легочной артерии было достигнуто только в 66% наблюдений. Однако главная проблема связана с редким клиническим применением АПГ как диагностического теста. В большинстве лечебных учреждений частота выполнения АПГ при подозрении на ТЭЛА не превышает 12-15%, причем этот показатель не меняется на протяжении последних 20 лет.
Спиральная КТ-ангиография
Еще в 1978 г. Sinner W.N. впервые представил данные о возможности выявления тромбов в легочной артерии при пошаговой КТ. Однако длительное время сканирования не позволяло оценить все легочные сосуды, поэтому тромбы в легочных артериях представляли собой случайные находки. Только с появлением в начале 1990-х годов аппаратов для спирального сканирования и с широким внедрением КТ-ангиографии в клиническую практику КТ-диагностика ТЭЛА стала реальной.
Суть спиральной КТ-ангиогра-фии заключается в быстром (в тече-
ние одной задержки дыхания) сканировании грудной полости на фоне введения болюса рентгеноконтрастного вещества в периферическую вену. Контрастированная кровь, заполняя легочные артерии в течение первых 10-15 с введения, обтекает тромботические массы, создавая картину дефектов наполнения в просвете сосудов на КТ (рис. 4). Само исследование можно лишь условно назвать инвазивным, поскольку введение контрастного вещества осуществляется с помощью механического шприца-инъекто-ра через гибкий катетер в периферическую вену (локтевого сгиба или кисти). Осложнения возникают редко (менее 0,1%) и связаны исключительно с тяжелыми реакциями на йодсодержащее контрастное вещество.
Длительное, в течение 14 лет, применение КТ-ангиографии для диагностики ТЭЛА показало высокую чувствительность и специфичность метода, которые достигают в среднем 90-92%. В первые годы применения серьезные трудности возникали при распознавании тромбов в субсегментарных артериях, однако совершенствование аппаратуры практически устранило эту проблему. В современных аппаратах для многослойной КТ исследование может проводиться при толщине томографического слоя 1,0-1,25 мм, а общее время сканирования уменьшено до 12-15 с, что вполне достаточно для выявления большинства тромбов.
Спиральная КТ-ангиография имеет ряд существенных преимуществ перед другими диагностическими технологиями. Прежде всего, это высокая информативность, позволяющая уверенно выявлять тромбы в главных, долевых и сегментарных ветвях легочных артерий. При этом данные КТ обнаруживают прямые признаки ТЭЛА в виде дефектов наполнения или полной обтурации легочных сосудов, в отличие от косвенных данных при рентгенографии и сцинтиграфии. Отсутствие сложных инвазивных процедур, связанных с внутрисосудистыми манипуляциями, позволяет сократить время проведения исследования до
Рис. 4. ТЭЛА. а, б — обзорные рентгенограммы — жидкость в правой плевральной полости; в, г — КТ-ан-гиография — в просветах правой и левой легочных артерий видны множественные дефекты наполнения.
15-20 мин, причем оно может быть выполнено как в амбулаторных, так и в стационарных условиях, вне зависимости от тяжести состояния пациента. Поэтому КТ-ангиография используется существенно чаще, чем АПГ. Наконец, КТ-ангиография позволяет исследовать не только сосуды, но весь объем грудной полости. При этом выявляются все дополнительные признаки ТЭЛА, известные в традиционной рентгеносемиотике, например инфаркты легкого, а также другие патологические состояния, которые могут имитировать ТЭЛА клинически или рентгенологически (см. рис. 4).
Магнитно-резонансная томография
Обычные технологии магнитно-резонансной томографии (МРТ) трудно применять для диагностики ТЭЛА. Это связано с невозможностью получить адекватный сигнал от легочной ткани, в которой расположены большинство долевых и сегментарных сосудов, а также с необходимостью длительной задержки дыхания для исключения динамических артефактов. Современные быстрые технологии МРТ постепенно преодолевают это препятствие. Многочисленные методики магнитнорезонансной ангиографии предложены для оценки легочного кровотока. Показано, что визуализация тромбов в главных и долевых артериях возможна с точностью до 94%, однако такие исследования пока не получили широкого распространения в клинической практике.
Диагностический алгоритм
Выбор диагностической тактики при подозрении на ТЭЛА остается сложной проблемой. Несмотря на большое количество возможных методов и достаточно высокую их информативность, обследование больного с предполагаемой ТЭЛА часто ограничивается обзорной рентгенографией грудной клетки и УЗИ вен нижних конечностей. Более сложные техноло-
гии, такие как радиоизотопное исследование, АПГ или спиральная КТ-ан-гиография, могут быть недоступными, особенно в ургентной ситуации, типичной для острой ТЭЛА.
Тем не менее начиная с 1960-х годов в клинике формировалась стандартная схема обследования пациента при подозрении на ТЭЛА. Помимо анамнеза, клинической картины, обычных лабораторных исследований и электрокардиографии, в нее включались и лучевые методы диагностики. Традиционный подход заключался в выполнении обзорной рентгенографии, которая при необходимости и возможности дополнялась линейной томографией, с последующим проведением перфузионной сцинтиграфии (изолированно или в сочетании с вентиляционной сцинтиграфией). При необходимости обследование заканчивалось АПГ для верификации диагноза. В 1990-х годах эта схема была дополнена УЗИ вен нижних конечностей на начальном этапе обследования. Такой подход имеет ряд серьезных недостатков, которые обусловлены как ограничениями отдельных методов, так и невозможностью их широкого клинического применения у всех пациентов с подозрением на ТЭЛА.
Широкое внедрение в практику спиральной КТ-ангиографии позволило выявлять прямые признаки ТЭЛА с помощью относительно доступного и малоинвазивного теста. В результате всё большее число лечебных учреждений, обладающих этой технологией, постепенно меняют диагностическую тактику у больных с предполагаемой ТЭЛА. Клиническая симптоматика и данные рентгенографии, исключающие другие возможные причины появившихся симптомов (например, пневмоторакс или пневмонию), служат показанием к проведению экстренной спиральной КТ-ангиогра-фии. Результаты этого исследования при должном соблюдении методики позволяют подтвердить или исключить ТЭЛА у большинства больных. При сомнительных результатах КТ-ан-
гиографии может рассматриваться вопрос о прямой ангиопульмоногра-фии. Параллельно с КТ-исследовани-ем может проводиться УЗИ вен нижних конечностей для выявления источника эмболии и эхокардиография для более точной оценки легочной гемодинамики.
Рекомендуемая литература
Афанасьева В.С., Тагер И.Л. Рентгенодиагностика тромбоэмболии легочной артерии. Ташкент, 1976.
Котельников М.В. Тромбоэмболия легочной артерии (современные подходы к диагностике и лечению). М., 2002.
Савельев В.С., Яблоков Е.Г., Кириенко А.И., Тромбоэмболия легочных артерий. М., 1979.
Яковлев В.Б. Тромбоэмболия легочной артерии в многопрофильном клиническом стационаре (распространенность, диагностика, лечение, организация специализированной медицинской помощи): Дис. … докт. мед. наук. М., 1995.
Becker D.M. et al. // Arch. Int. Med. 1989. V. 149. P. 1731.
Blum A.G. et al. // Amer. J. Cardiol. 1994. V. 74. P. 96.
Cogo A. et al. // Br. Med. J. 1998. V. 316. P. 17.
Hull R.D. et al. // Chest. 1985. V. 88. P. 819.
Hull R.D. et al. // Ann. Int. Med. 1991. V. 114. P. 142.
Mayo J.R. et al. // Radiology. 1997. V. 205. P. 447.
Meaney J.F. et al. // N. Engl. J. Med. 1997. V. 336. P. 1422.
Miniati M. et al. // Amer. J. Resp. Crit. Care Med. 1996. V. 154. P. 1387.
PIOPED investigators // JAMA. 1990. V. 263. P. 2753.
Remy-Jardin M. et al. // Radiology. 1996. V. 207. P. 157.
Schiff M.J. et al. // Arch. Int. Med. 1987. V. 147. P. 505.
Sinner W.N. // J. Comput. Assist. Tomogr. 1978. V. 2. P. 395.
Van Beek E.J.R. et al. // Eur. Radiol. 1996. V. 6. P. 415.
Van Erkel A.R., Pattynama P.M.T. // Acad. Radiol. 1998. V. 5. Suppl. 2. P. 321.
Van Rossum A.B. et al. // Eur. Radiol. 1998. V. 8. P. 90.
Wielopolski P.A. et al. // Radiology. 1996. V. 201. P. 202. 4
Рецидивирующая тромбоэмболия легочной артерии. Способы диагностики и лечение
Библиографическое описание:Фролов, И. А. Рецидивирующая тромбоэмболия легочной артерии. Способы диагностики и лечение / И. А. Фролов, А. С. Нагорняк. — Текст : непосредственный // Молодой ученый. — 2016. — № 29.2 (133.2). — С. 25-27. — URL: https://moluch.ru/archive/133/37379/ (дата обращения: 02.06.2021).
Тромбоэмболия лёгочной артерии — закупорка лёгочной артерии или её ветвей тромбами, которые образуются в венах большого круга кровообращения. Тромбоэмболия легочных артерий имеет множество вариантов течения, проявлений, выраженности симптомов и т. д. Поэтому классификация данной патологии осуществляется на основании различных факторов: места закупорки сосуда; величины закупоренного сосуда; объема легочных артерий, кровоснабжение которых прекратилось в результате эмболии; протекания патологического состояния; наиболее выраженных симптомов. Современная классификация тромбоэмболий легочной артерии включает в себя все вышеперечисленные показатели, которые определяют ее степень тяжести, а также принципы и тактику необходимой терапии. Тромбоэмболии легочной артерии классифицируется в зависимости от следующих признаков: локализации тромба на уровне поражаемых артерий; объема пораженных сосудов; в зависимости от стороны поражения. По течению тромбоэмболия легочной артерии может быть острой, хронической и рецидивирующей. Один из важных типов тромбоэмболий — рецидивирующий.
Рецидивирующая тромбоэмболия легочной артерии — это повторяющаяся закупорка мелких легочных артерий. Этой форме заболевания подвержены 10–30 % больных, перенесших тромбоэмболию легочной артерии. Обычно один человек может переносить различное количество эпизодов тромбоэмболии легочной артерии, варьирующее от 1 до 20. Большое количество перенесенных эпизодов тромбоэмболии легочной артерии обычно представлено закупоркой мелких ветвей легочной артерии. Таким образом, рецидивирующая форма течения тромбоэмболии легочной артерии морфологически представляет собой закупорку именно мелких ветвей легочной артерии. Такие многочисленные эпизоды закупорки мелких сосудов легочной артерии приводят к различным последствиям: повышению давления в малом кругу кровообращения и перестройки легочных артерий с формированием «легочного сердца», закупорке крупных ветвей легочной артерии. Развитию рецидивирующей тромбоэмболии легочной артерии способствует наличие хронических заболеваний сердечно-сосудистой и дыхательной систем, а также онкологических патологий и оперативных вмешательств.
Рецидивирующая тромбоэмболия легочной артерии обычно не имеет четких клинических признаков, что обуславливает ее стертое течение. Поэтому данное состояние редко верно диагностируется, поскольку в большинстве случаев невыраженные признаки принимают за симптомы других заболеваний. Диагностика рецидивирующей тромбоэмболии легочной артерии достаточно затруднительна. Чтобы заподозрить именно данное заболевание, следует иметь в виду возможность его развития. Поэтому всегда следует обращать внимание на факторы риска, предрасполагающие к развитию тромбоэмболии легочной артерии. Подробный расспрос пациента представляет собой жизненно важную необходимость, поскольку указание на наличие инфарктов, операций или тромбозов, поможет правильно определить причину образования тромба и область, из которой он был принесен. Помимо данных расспроса больных, необходимо инструментальное обследование пациента — рентгенография легких, на которой будут видны участки инфаркта; ЭКГ; сцинтиография легких; УЗИ вен ног.
Значение рецидивирующей тромбоэмболии легочной артерии можно разобрать на следующем клиническом случае.
Больная З. 51 год, поступила в хирургическое отделение с жалобами на боли, покраснение и инфильтрацию в правой голени, выраженную боль при пальпации в этой зоне, фебрильную температуру, общую слабость. Жалобы появились за 4 дня до поступления в отделение. При осмотре в приемном отделении состояние больной описывается как тяжелое; пульс аритмичный, слабого наполнения и напряжения, 100 ударов в минуту; АД 110/60 мм.рт.ст; по передней поверхности правой голени определяется участок гиперемии и инфильтрации кожи, пальпация в этой зоне болезненна, подвижность сохранена, чувствительность не нарушена. При расспросе кардиологом жаловалась на периодические боли в сердце, иррадиирующие под левую лопатку, в левую руку; повышения АД не отмечала, ощущала «чувство нехватки воздуха при физической нагрузке», наблюдала слабость, головокружение. Данные ЭКГ — фибрилляция предсердия с ЧСЖ 164–188. Был выставлен диагноз: острый восходящий поверхностный тромбофлебит на фоне ИБС; стенокардия напряжения ФК 3; нарушение ритма по типу фибрилляции предсердий, постоянная форма, тахивариант. На 2-ые сутки, в связи с ухудшением состояния, была переведена в отделение АРО, где сразу была заподозрена тромбоэмболия легочной артерии, наблюдались отеки нижних конечностей, ЧДД составляло 26 в минуту, АД 80/50 мм.рт.ст. При обследовании кардиологом было отмечено, что не исключен острый коронарный синдром и тромбоэмболия мелких ветвей легочной артерии. В этот же день проведено обследование вен нижних конечностей, на котором выявлено, что справа глубокие вены голени, подколенная, поверхностная бедренная вены заполнены тромботическими массами. На следующий день при осмотре отмечена отрицательная динамика, нарастание отечности в правой нижней конечности до уровня средней трети бедра, кашель, одышка. Ультразвуковое исследование вен нижних конечностей показало тромбоз глубоких вен правой нижней конечности. В связи с этим, проведена операция — перевязка большой подкожной вены, глубокой бедренной вены, пликация поверхностной бедренной вены. В послеоперационном периоде состояние оставалось стабильно тяжелым, отмечалась умеренная отечность правой нижней конечности. На восьмые сутки проконсультирована ангиохирургом, отметившим, что тромбоза вен нижних левой конечности нет. Через неделю после перевода в АРО отмечено ухудшение состояния, жалобы на резкую слабость, усиление одышки, тошноту. Дыхание жесткое, ослаблено в задне-базальных отделах, там же выслушиваются крепетирующие хрипы. ЧДД 26 в минуту, на кардиомониторе — фибрилляция предсердий тахисистолическая форма, ЧСС 160 в минуту, АД 60/40 мм.рт.ст. Осмотрена кардиологом, который не исключил повторную тромбоэмболию мелких ветвей легочной артерии. Несмотря на проводившуюся терапию, состояние больной ухудшалось — через 5 часов ЧДД составило 36 в минуту, пациентка «металась» в постели, отмечала чувство «нехватки воздуха», сильные боли в правой ноге. Еще через 2 часа состояние резко ухудшилось — появился цианоз губ, одышка до 44 в минуту, АД 50/0 мм.рт.ст., больная была переведена на ИВЛ. Через полчаса наступила клиническая смерть. Далее констатирована биологическая смерть.
На вскрытии выявлено увеличение легочных артерий, наличие тромба в ушке левого предсердия; в просвете крупных и мелких ветвей легочной артерии матовые, темно-красные шероховатые с трудом выделяющиеся тромбы; в S8,S9,S10 сегментах правого легкого множество безвоздушных плотных темно-красных участков с мелкозернистой поверхностью размерам 2х2 см, В S6 сегменте правого легкого под плеврой плотноватый тёмно-красный участок треугольной формы, основанием обращенный к плевре, а верхушкой к корню легкого. Аналогичные участки в S9, S10 сегментах левого легкого. Микроскопическое исследование вен — неравномерная эктазия просвета, склероз стенки, в просвете крупной вены смешанный тромб с явлениями организации. Микроскопическое исследование ткани легких — полнокровие сосудов, в просвете крупных ветвей легочной артерии смешанные тромбы без организации, в просвете мелких ветвей легочной артерии обтурирующие, организованные, реканализированные тромбы, в просвете альвеол — скопления гемосидерофагов.
На основании этих данных поставлен патологоанатомический диагноз: хронический тромбофлебит глубокой бедренной вены правой нижней конечности. Осложнение: рецидивирующая тромбоэмболия легочной артерии.
В данном случае, рецидивирующая тромбоэмболия легочной артерии привела к гипертензии малого круга кровообращения, с прогрессирующей правосердечной недостаточностью или «легочным сердцем» что привело к сердечным жалобам больной, ошибочно расцененных как стенокардия напряжения. Помимо этого, фибрилляция сердца, вызванная сердечной недостаточностью, стала причиной образования тромбов не только в венах правой нижней конечности, но и в полостях сердца. По этой причине, проведённое оперативное вмешательство на венах нижней правой конечности не помогло пациентке.
Литература:
1. Струков А. И. Патологическая анатомия / Струков А. И., Серов В. В. // Патологическая анатомия, тромбоэмболия — М.: Литтерра, 2010.
2. Яковлев В. Б. Тромбоэмболия легочной артерии / Яковлев В. Б., Яковлев М. В. // Тромбоэмболия легочной артерии: патофизиология, диагностика, лечебная тактика — Consiliummedicum, том 7, 2005.
3. Qaseem A., Deep Venous Thrombosis, Pulmonary Embolism / Qaseem A., Snow V., Barry P., Hornbake E. R., Rodnick J. E., Tobolic T., Ireland B., Segal J., Bass E., Weiss K. B., Green L. // Deep Venous Thrombosis, Pulmonary Embolism (Current diagnosis of venous thromboembolism in primary care) — Ann Fam Med. 2007 Jan-Feb;5(1):57–62.
Основные термины (генерируются автоматически): легочная артерия, правая нижняя конечность, тромбоэмболия, ветвь, глубокая бедренная вена, малый круг кровообращения, поверхностная бедренная вена, правая голень, сегмент правого легкого, ухудшение состояния.
ДВУХЛЕТНЕЕ НАБЛЮДЕНИЕ ЗА ПАЦИЕНТКОЙ С РЕЦИДИВИРУЮЩЕЙ ТРОМБОЭМБОЛИЕЙ ЛЕГОЧНОЙ АРТЕРИИ ПОСЛЕ УСПЕШНОГО КОМБИНИРОВАННОГО ЛЕЧЕНИЯ | Баранова
1. Российские клинические рекомендации по диагностике, лечению и профилактике венозных тромбоэмболических осложнений. Флебология 2010;4(1 Вып. 2):2–37. [Russian clinical practice guidelines for diagnostics, management and prevention of venous thromboembolic events. Flebologiya = Phlebology 2010;4(1 Suppl 2):2–37. (In Russ.)]. 1. Laporte S., Mismetti P., Decousus H. et al. Clinical predictor for fatal pulmonary embolism in 15,520 patients with venous thromboembolism: findings from the Registro Informatizado de la Enfermedad TromboEmbolica venosa (RIETE) registry. Circulation 2008; 117(13):1711–6.
2. Dalen J.E. Pulmonary embolism: what have we learned since Virchow? Natural history, pathophysiology, and diagnosis. Chest 2002;122(4):1440–56.
3. Kearon C. Natural history of venous thromboembolism. Circulation 2003;107 (23 Suppl 1):122–30.
4. Dalen J.E., Alpert J.S. Natural history of pulmonary embolism. Prog Cardiovasc Dis 1975;17 (4):259–70.
5. Diebold J., Löhrs U. Venous thrombosis and pulmonary embolism: a study of 5039 autopsies. Pathol Res Pract 1991;187 (2–3):260–6.
6. Pengo V., Lensing A.W., Prins M.H. et al. Incidence of chronic thromboembolic pulmonary hypertension after pulmonary embolism. N Engl J Med 2004; 350(22):2257–64.
7. Becattini C., Agnelli G., Pesavento R. et al. Incidence of chronic thromboembolic pulmonary hypertension after a first episode of pulmonary embolism. Chest 2006;130(1):172–5.
8. Squizzato А., Moja L., Gensini G.F. et al. Is thrombolysis for intermediate-risk pulmonary embolism beneficial? The case of Emeritus Professor Crow. Intern Emerg Med 2009;4(4):339–41.
9. Berghaus T.M., Thilo C., Bluethgen A. et al. Effectiveness of thrombolysis in patients with intermediate-risk pulmonary embolism: influence on length of hospital stay. Adv Ther 2010;27(9):648–54.
10. Konstantinides S.V., Torbicki A., Agnelli G. et al. 2014 ESC guidelines on the diagnosis and management of acute pulmonary embolism. Eur Heart J 2014;35(43):3033–69, 3069a–3069k.
11. Meyer G., Vicaut E., Danays T. et al. Fibrinolysis for patients with intermediate-risk pulmonary embolism. N Engl J Med 2014;370(15):1402–11.
12. Marti C., John G., Konstantinides S. et al. Systemic thrombolytic therapy for acute pulmonary embolism: a systematic review and meta-analysis. Eur Heart J 2015;36(10):605–14.
13. Engelberger R.P., Kucher N. Catheterbased reperfusion treatment of pulmonary embolism. Circulation 2011;124(19):2139–44.
14. Kucher N., Boekstegers P., Muller O.J. et al. Randomized, controlled trial of ultrasound-assisted catheter-directed thrombolysis for acute intermediate-risk pulmonary embolism. Circulation 2014;129(4):479–86.
15. Mizoguchi H., Ogawa A., Munemasa M. et al. Refined balloon pulmonary angioplasty for inoperable patients with chronic thromboembolic pulmonary hypertension. Circ Cardiovasc Interv 2012;5(6):748–55.
16. Inami T., Kataoka M., Shimura N. et al. Pulmonary edema predictive scoring index (PEPSI), a new index to predict risk of reperfusion pulmonary edema and improvement of hemodynamics in percutaneous transluminal pulmonary angioplasty. JACC Cardiovasc Interv 2013;6(7):725–36.
17. Sugimura K., Fukumoto Y., Satoh K. et al. Percutaneous transluminal pulmonary angioplasty markedly improves pulmonary hemodynamics and long-term prognosis in patients with chronic thromboembolic pulmonary hypertension. Circ J 2012;76(2):485–8.
18. Feinstein J.A., Goldhaber S.Z., Lock J.E. et al. Balloon pulmonary angioplasty for treatment of chronic thromboembolic pulmonary hypertension. Circulation 2001;103(1):10–3.
19. Piazza G., Goldhaber S. Chronic thromboembolic pulmonary hypertension. N Engl J Med 2011;364 (4):351–60.
20. Holzer R.J., Gauvreau K., Kreutzer J. et al. Balloon angioplasty and stenting of branch pulmonary arteries: adverse events and procedural characteristics: results of a multi-institutional registry. Circ Cardiovasc Interv 2011;4(3):287–96.
21. Schmitz-Rode T., Verma R., Pfeffer J.G. et al. Temporary pulmonary stent placement as emergency treatment of pulmonary embolism: first experimental evaluation. J Am Coll Cardiol 2006;48(4):812–6.
Симптомы, причины, лечение и тесты
Обзор
Что такое стеноз легочной артерии?
Стеноз легочной артерии — это сужение (стеноз), которое возникает в легочной артерии, большой артерии, которая посылает бедную кислородом кровь в легкие для обогащения кислородом. Сужение может происходить в основной легочной артерии и / или в ветвях левой или правой легочной артерии.Это сужение затрудняет попадание крови в легкие для поглощения кислорода. Без достаточного количества кислорода сердце и тело не могут функционировать должным образом. Чтобы преодолеть сужение, давление в правом желудочке (камера, которая перекачивает кровь в легочные артерии) повышается до уровней, которые могут повредить сердечную мышцу.
Симптомы и причины
Каковы симптомы стеноза легочной артерии?
Если сужение артерии менее 50 процентов, ваш ребенок может не испытывать никаких симптомов.Однако, если сужение артерии превышает 50 процентов, у вашего ребенка могут возникнуть следующие симптомы:
- Одышка
- Усталость
- Тяжелое или учащенное дыхание
- Учащенное сердцебиение
- Отек стоп, лодыжек, лица, век и / или живота
Что вызывает стеноз легочной артерии?
Стеноз легочной артерии — это врожденный порок сердца, то есть дефект, который является врожденным или существует при рождении.Другими словами, дефект — это аномалия, а не болезнь. Стеноз легочной артерии часто сочетается с другими врожденными пороками сердца, такими как:
- Тетралогия Фалло — четырехугольный дефект, состоящий из: 1) дефекта межжелудочковой перегородки, 2) сужения в области легочного клапана или сразу под ним, 3) правого желудочка, который более мускулистый, чем обычно, 4) аорта, расположенная непосредственно над дефектом межжелудочковой перегородки
- Атрезия легочной артерии — отсутствие клапана легочной артерии, препятствующего оттоку крови из правого желудочка в легочную артерию и далее в легкие
- Truncus arteriosus — образование только одной комбинированной артерии вместо нормальных двух выходов из сердца, аорты и легочной артерии
- Стеноз клапана легочной артерии — проблемы с клапаном легочной артерии (например, развитие менее трех створок, створки, которые могут частично срастаться, толстые створки, которые не открываются полностью), затрудняющие работу створок клапана открыть и позволить крови течь из правого желудочка в легкие
- Открытый артериальный проток — открытый проход между легочной артерией и аортой.Обычно этот проход закрывается сам по себе в течение нескольких часов после рождения, но когда этого не происходит, требуется хирургическое вмешательство или амбулаторная катетерная процедура, чтобы закрыть отверстие
Другие причины стеноза легочной артерии могут включать: другие синдромы, поражающие сердце (например, синдром краснухи [группа сердечных и других проблем со здоровьем у младенца, вызванная инфекцией краснухи у матери во время беременности] и синдром Вильямса [группа патологий, поражающих сердце и другие органы]) и хирургические процедуры, используемые для исправления других пороков сердца (например, перевязка легочной артерии — целенаправленное сужение артерии для уменьшения притока крови к легким).
Диагностика и тесты
Как диагностируется стеноз легочной артерии?
Во время обычного осмотра врач вашего ребенка может услышать аномальные сердечные тоны (шум) при прослушивании сердца. Если обнаружены необычные звуки, ваш врач назначит другие тесты, которые могут включать:
- Электрокардиограмма (ЭКГ или ЭКГ) — тест, который регистрирует электрические изменения, происходящие во время сердцебиения; выявляет нарушения сердечного ритма (аритмии) и обнаруживает напряжение сердечной мышцы.
- Рентген грудной клетки — тест для определения размера и формы сердца, легких и легочных артерий.
- Эхокардиограмма — тест, в котором используются звуковые волны для создания движущегося изображения внутренних структур сердца.
- Допплерография — тест, в котором для измерения кровотока используются звуковые волны; обычно в сочетании с эхокардиограммой для оценки внутренней структуры сердца и кровотока через клапаны и сосуды сердца.
- Магнитно-резонансная томография сердца (МРТ) — тест, в котором используется трехмерная визуализация, чтобы выявить, как кровь течет через сердце и сосуды и как оно работает.
- Компьютерная томография — рентгеновская процедура, объединяющая множество рентгеновских изображений с помощью компьютера для создания поперечных сечений сердца. КТ сердца использует передовую технологию КТ с внутривенным (IV) контрастированием (красителем) для визуализации анатомии сердца, коронарного кровообращения и магистральных сосудов.
- Катетеризация сердца — процедура, при которой тонкая трубка (катетер) вводится в вену или артерию и вводится в сердце для определения уровня кислорода, измерения изменений давления и создания рентгеновских снимков сердца и сердца. его внутренние структуры.
- Легочная ангиография — рентгеновский снимок легочных артерий и вен сердца с добавлением красителей.
- Перфузионное сканирование — тест, при котором пациенту вводят небольшое количество радиоактивного материала.Специальная машина показывает, насколько хорошо кровь течет через каждое из двух легких.
При необходимости можно заказать дополнительные тесты.
Ведение и лечение
Как лечится стеноз легочной артерии?
Если у вашего ребенка диагностирован стеноз легочной артерии, ваш педиатр или врач первичной медико-санитарной помощи порекомендуют вам встретиться со специалистом по врожденным порокам сердца (врачом, имеющим подготовку и оборудование, чтобы определить проблему с сердцем у вашего ребенка и заказать необходимые специальные тесты, уход, кардиохирургия и контрольные осмотры).Оптимальный подход к лечению будет зависеть от симптомов вашего ребенка, а также других характеристик стеноза. Легкое или умеренное сужение одной или нескольких ветвей легочной артерии обычно не требует лечения, но в тяжелых случаях требуется определенная терапия. Доступные процедуры включают:
Баллонное расширение
Этот метод лечения заключается в перемещении баллонного катетера расширения в суженную область артерии. Баллон осторожно надувают — сначала под низким, а затем под более высоким давлением — до тех пор, пока суженная область не расширится.Затем баллон сдувается и удаляется. Хотя сужение улучшается у большинства пациентов после баллонной дилатации, со временем артерия может снова сузиться в 15-20% случаев, что потребует дальнейшего баллонирования. В настоящее время разрабатываются различные типы воздушных шаров, которые, вероятно, приведут к лучшим и долгосрочным результатам.
Баллонное расширение и установка стента
Стремясь улучшить результаты баллонной дилатации, был начат поиск более эффективного лечения, который привел к разработке стента из нержавеющей стали, расширяемого баллоном.Установка стента осуществляется путем размещения стента поперек суженного сегмента артерии. Стент устанавливается на катетере для баллонной ангиопластики и покрывается оболочкой при перемещении в нужное положение. Затем оболочку снимают с узла ангиопластики стент-баллон, и баллон надувают до рекомендованного давления, расширяя стент и фиксируя его на месте.
Изображение разрезающего воздушного шара с разрешения Boston Scientific Corporation
The Cutting Balloon ™
Эта процедура аналогична стандартному расширению баллона, но баллон был специально разработан с небольшими лопастями, движущимися вверх и вниз по его длине.Когда баллон надувается, лезвия активируются, и они прорезают суженную область, облегчая расширение сосуда и увеличивая отверстие. Воздушные шары для резки доступны в разных размерах.
Хирургический
Используются различные методы хирургического лечения стеноза легочной артерии, выбор которых зависит от характеристик стеноза и окружающих сосудов и других структур.
Ресурсы
Как найти врача, если у вас врожденный порок сердца у взрослого
Доктора различаются по квалификации из-за разной подготовки и опыта; больницы различаются по количеству доступных услуг.Чем сложнее ваша медицинская проблема, тем значительнее становятся эти различия в качестве и тем большее значение они имеют.
Очевидно, что врач и больница, которые вы выберете для получения комплексной специализированной медицинской помощи, будут иметь прямое влияние на то, насколько хорошо вы себя чувствуете. Чтобы помочь вам сделать этот выбор, ознакомьтесь с результатами нашего Института сердца и сосудов семьи Сиделла и Арнольда Миллер.
T Центр врожденных пороков сердца у взрослых в Семейном институте сердца и сосудов Сиделла и Арнольда Миллер — это специализированный центр, в котором задействована многопрофильная группа специалистов, включая кардиологов, кардиохирургов и медсестер из сердечно-сосудистой медицины и детской кардиологии. , Центр детской и врожденной хирургии сердца, кардиоторакальной хирургии, диагностической радиологии, легочной медицины, аллергии и интенсивной терапии, а также центр трансплантации, которые обеспечивают комплексный подход к диагностике и лечению врожденных пороков сердца у взрослых.
Узнайте больше о специализированных командах врачей, занимающихся лечением врожденных пороков сердца.
Вы также можете воспользоваться консультацией MyConsult о втором мнении через Интернет.
Для молодых пациентов с врожденными пороками сердца:
Узнайте больше о Семейном институте сердца и сосудов Сиделла и Арнольда Миллеров.
Ресурсы и информация для пациентов
Контакт
Если вам нужна дополнительная информация, нажмите здесь, чтобы связаться с нами, поговорите в чате с медсестрой или позвоните медсестре по ресурсам и информации Института сердечно-сосудистых заболеваний семьи Миллер по номеру 216.445.9288 или по бесплатному телефону 866.289.6911. Будем рады вам помочь.
Стать пациентом
Варианты лечения
Руководства по лечению
Диагностические тесты
Врожденный порок сердца диагностируется по шуму при медицинском осмотре и нескольких диагностических тестах:
Анатомия
Веб-чаты
Наши веб-чаты и видеочаты дают пациентам и посетителям еще одну возможность задать вопросы и пообщаться с нашими врачами.
Видео
Интерактивные инструменты
Ссылки на ресурсы
Почему стоит выбрать клинику Кливленда для лечения?
Наши результаты говорят сами за себя.Ознакомьтесь с нашими фактами и цифрами, и если у вас возникнут вопросы, не стесняйтесь их задавать.
Легочная артерия: анатомия, функция и значение
Основная легочная артерия, также называемая легочным стволом, представляет собой сосуд, выходящий из сердца. Он разделяется на левую и правую легочные артерии, по которым кровь с относительно низким содержанием кислорода и высоким содержанием углекислого газа попадает в легкие.
Там он пополняется вдыхаемым кислородом, а избыток углекислого газа «сбрасывается» и выводится из организма при выдохе.
MedicalRF.com/MedicalRF.com/Getty ImagesАнатомия
Легочный ствол, а также левая и правая легочные артерии являются относительно крупными артериями. Каждая из них имеет форму трубок с просветом (отверстием, через которое течет кровь). Левая и правая легочные артерии направляют кровь в левое и правое легкие соответственно.
Структура
Легочный ствол, а также правая и левая легочные артерии имеют форму заглавной буквы «Т», причем ствол образует нижнюю часть, а левая и правая ветви, каждая, образуют одну из двух сторон вверху.
Между правым желудочком сердца и легочным стволом находится клапан. Этот клапан, который состоит из двух створок соединительной ткани, устроен так, чтобы открываться, когда сердце качает кровь, чтобы кровь могла течь из правого желудочка в легочный ствол. Когда сердечная мышца расслабляется, клапаны закрываются, чтобы предотвратить обратный ток крови к сердцу.
Как и все артерии, стенки легочных артерий имеют несколько слоев мышц, которые позволяют им расширяться (расширяться) и сужаться (сужаться).Это сильно отличается от стенок вен, которые тоньше и менее мускулистые.
Большинство артерий в организме несут насыщенную кислородом кровь, но легочные артерии — одно из двух исключений, которые вместо несут дезоксигенированную кровь. (Другая — пупочные артерии, по которым кровь, нуждающаяся в кислороде, поступает от развивающегося ребенка к матери.)
Расположение
Легочный ствол, относительно короткий и широкий, расположен на выходе из правого желудочка.Эта главная артериальная ветвь расположена над сердцем слева от восходящей аорты.
Правая легочная артерия заклинивает в дуге аорты, позади восходящей аорты и впереди нисходящей аорты. Левая легочная артерия проходит рядом с левой стороной аорты.
Эти сосуды пронизывают перикард, соединительную ткань, выстилающую сердце. Поскольку сердце находится с левой стороны грудной клетки, левая легочная артерия находится ближе к легкому, чем правая легочная артерия.
После того, как левая легочная артерия входит в левое легкое, она разделяется на более мелкие ветви. Правая легочная артерия проходит через верхнюю часть грудной клетки и входит в правое легкое. После этого эта артерия разделяется на более мелкие ветви.
Анатомические вариации
Обычно каждая легочная артерия делится на от трех до семи ветвей. Наиболее частыми анатомическими вариациями легочных артерий являются вариации количества артериальных ветвей в легких.А иногда один или несколько отделов могут ответвляться до того, как правая или левая легочная артерия войдет в сердце.
Также встречаются редкие врожденные деформации легочных артерий:
- Атрезия легких : это состояние, при котором легочный клапан не открывается должным образом, что приводит к уменьшению кровотока от сердца к легким. Симптомы, такие как учащенное дыхание и медленный рост в детстве, могут варьироваться в зависимости от степени анатомической аномалии.Этот дефект лечится хирургическим путем.
- Стеноз легочной артерии : Этот врожденный дефект характеризуется узкой легочной артерией. Это может быть связано с различными пороками сердца и вызывать усталость и одышку, а также симптомы любых таких сопутствующих пороков сердца. Хирургическое вмешательство может включать расширение артерии с помощью стента.
- Слинг легочной артерии : это врожденный дефект, при котором левая легочная артерия ответвляется от правой легочной артерии, а не непосредственно от легочного ствола.Дефект связан с сужением трахеи (дыхательного горла) и бронхов (дыхательных путей). Слинг легочной артерии можно лечить хирургическим путем.
Функция
Легочные артерии являются частью малого круга кровообращения, который также включает легочные вены и легочные капилляры. Целью малого круга кровообращения является перенос кислорода и углекислого газа между кровью в организме и воздухом, который вдыхается и выдыхается в легких.
Особая роль легочных артерий — переносить кровь с низким содержанием кислорода и высоким содержанием углекислого газа в легочные капилляры легких, где происходит этот обмен.
Когда кровь обогащается кислородом и очищается от углекислого газа, она возвращается по легочным венам в правый желудочек сердца. Оттуда кровь перекачивается в левый желудочек и, наконец, распространяется через аорту к артериям, которые несут богатую кислородом кровь по всему телу.
Клиническая значимость
Есть два основных состояния, которые влияют на легочные артерии у взрослых — легочная эмболия (ТЭЛА) и легочная артериальная гипертензия.Легочная артериальная гипертензия — редкое заболевание, которое развивается со временем. PE — это сгусток крови в артерии легких, требующий неотложной медицинской помощи.
Легочная эмболия
ПЭ — это состояние, при котором сгусток крови застревает в легочной артерии, блокируя кровоток в легких. Симптомы включают:
- Внезапная одышка
- Боль в груди и спине
- Кашель
- Кровянистая мокрота
- Чрезмерное потоотделение
- Легкомысленность
- Синие губы или ногти
- Потеря сознания
ПЭ может возникнуть, когда сгусток крови образуется в вене (например, в ногах) и проходит через сердце, в конечном итоге застревая в легочной артерии.Факторы риска включают нарушения свертываемости крови, рак и длительную физическую неподвижность.
Тромбоэмболия легочной артерии — это опасная для жизни неотложная медицинская помощь, которую необходимо лечить с помощью антикоагулянтов или интервенционной процедуры.
Легочная артериальная гипертензия
Легочная артериальная гипертензия — это редкий тип легочной гипертензии, характеризующийся сужением, жесткостью и утолщением артерий в легких и вокруг них. Это может вызвать усталость, одышку, кровохарканье (кровохарканье) и отек ног.
Легочная артериальная гипертензия может развиваться без известной причины, а факторы риска включают склеродермию или другие заболевания соединительной ткани, воздействие токсинов и цирроз печени.
Состояние прогрессирует и может привести к тяжелой сердечной недостаточности и инвалидности из-за непереносимости физических нагрузок. Лекарства, отпускаемые по рецепту, могут замедлить прогрессирование легочной артериальной гипертензии.
Слово от Verywell
Легочные артерии переносят кровь из сердца в легкие.Эти сосуды являются частью малого круга кровообращения, и они влияют на другие кровеносные сосуды в этой системе. Врожденные деформации сердца могут быть связаны с изменениями в легочных артериях, и эти проблемы могут потребовать хирургического вмешательства в детстве.
Что такое тромбоэмболия легочной артерии (ТЭЛА)?
Процесс тромбоэмболии легочной артерии (ТЭЛА) был впервые описан Рудольфом Вирховым, известным немецким патологом девятнадцатого века, который назвал перемещающиеся тромбы эмболией.Термины «эмбол» (множественное число: эмболы) и «эмболия» все еще используются для описания сгустка или части сгустка, который образовался в одном месте и переместился в другую часть тела. Когда сгусток заклинивает в одной из легочных артерий или ее ветвях, это называется ПЭ.
Очень большой PE может заблокировать весь ствол легочной артерии (прежде чем он разветвляется на правую и левую легочные артерии) и мгновенно вызвать смерть. Легочная эмболия, которая не настолько велика, может блокировать всю правую или левую легочную артерию, останавливая кровоток во всем легком и, особенно если у человека уже есть заболевание легких или сердца, вызывая смерть.Более мелкие эмболы могут блокировать более мелкие ветви легочной артерии с различными последствиями. Когда кровоснабжение небольшой «конечной артерии» на краю легкого блокируется, кислород к этой части легкого прекращается, и клетки в этой части легкого начинают умирать, что приводит к инфаркту легкого ( то есть отмирание легочной ткани). Когда кровоток блокируется в более крупной ветви легочной артерии, нормальный обмен кислорода на углекислый газ не происходит, и это влияет на все тело.Инфаркт легких обычно возникает из-за более мелких сгустков и маловероятен.
Вероятность смерти от ПЭ во многом зависит от размера ПЭ. Если основная легочная артерия полностью заблокирована, правый желудочек (камера сердца, перекачивающая кровь в легкие) не может получить кровь в легкие; эта «правожелудочковая недостаточность» затем приводит к смерти от ТЭЛА. Возраст и состояние здоровья пострадавшего также являются критическими факторами. Когда у человека уже есть заболевание легких или сердца, ПЭ может иметь более серьезные последствия.В то время как уровень смертности от ПЭ может достигать 25 процентов среди больных, госпитализированных пациентов, уровень смертности среди молодых здоровых людей приближается к 1 проценту.
% PDF-1.4 % 282 0 объект > эндобдж xref 282 210 0000000016 00000 н. 0000005310 00000 п. 0000005469 00000 н. 0000007311 00000 н. 0000007338 00000 н. 0000007491 00000 п. 0000007542 00000 н. 0000007892 00000 н. 0000008153 00000 н. 0000008675 00000 н. 0000009180 00000 н. 0000009422 00000 н. 0000009675 00000 н. 0000009724 00000 н. 0000009775 00000 н. 0000009825 00000 н. 0000009875 00000 н. 0000009926 00000 н. 0000009976 00000 н. 0000010026 00000 п. 0000010076 00000 п. 0000010127 00000 п. 0000010176 00000 п. 0000010225 00000 п. 0000010275 00000 п. 0000010326 00000 п. 0000010376 00000 п. 0000010426 00000 п. 0000010476 00000 п. 0000010526 00000 п. 0000010576 00000 п. 0000010625 00000 п. 0000010674 00000 п. 0000010723 00000 п. 0000010772 00000 п. 0000010821 00000 п. 0000010871 00000 п. 0000010921 00000 п. 0000010971 00000 п. 0000011021 00000 п. 0000011070 00000 п. 0000011119 00000 п. 0000011168 00000 п. 0000011280 00000 п. 0000011330 00000 п. 0000011380 00000 п. 0000011429 00000 п. 0000011480 00000 п. 0000011529 00000 п. 0000011578 00000 п. 0000011627 00000 н. 0000011676 00000 п. 0000011725 00000 п. 0000011774 00000 п. 0000011888 00000 п. 0000023789 00000 п. 0000034351 00000 п. 0000034482 00000 п. 0000034509 00000 п. 0000034649 00000 п. 0000035071 00000 п. 0000035318 00000 п. 0000035700 00000 п. 0000035727 00000 п. 0000036333 00000 п. 0000036644 00000 п. 0000037104 00000 п. 0000047367 00000 п. 0000057854 00000 п. 0000070291 00000 п. 0000070655 00000 п. 0000082237 00000 п. 0000082521 00000 п. 0000094444 00000 п. 0000104845 00000 н. 0000105028 00000 н. 0000105098 00000 н. 0000105345 00000 п. 0000117958 00000 н. 0000120769 00000 н. 0000120855 00000 н. 0000128689 00000 н. 0000128759 00000 н. 0000129263 00000 н. 0000138947 00000 н. 0000139208 00000 н. 0000151171 00000 н. 0000151285 00000 н. 0000151354 00000 н. 0000151416 00000 н. 0000151761 00000 н. 0000151878 00000 н. 0000151996 00000 н. 0000152268 00000 н. 0000152522 00000 н. 0000152639 00000 н. 0000152756 00000 н. 0000153052 00000 н. 0000153130 00000 н. 0000153204 00000 н. 0000153315 00000 н. 0000153592 00000 н. 0000153702 00000 н. 0000153856 00000 н. 0000154011 00000 н. 0000154217 00000 н. 0000154426 00000 н. 0000154496 00000 н. 0000154553 00000 н. 0000154627 00000 н. 0000154713 00000 н. 0000154779 00000 н. 0000154938 00000 н. 0000155145 00000 н. 0000155287 00000 н. 0000155408 00000 н. 0000155465 00000 н. 0000155522 00000 н. 0000155588 00000 н. 0000155863 00000 н. 0000156027 00000 н. 0000156148 00000 н. 0000156210 00000 н. 0000156493 00000 н. 0000156555 00000 н. 0000156629 00000 н. 0000156707 00000 н. 0000156777 00000 н. 0000156834 00000 н. 0000156896 00000 н. 0000158251 00000 н. 0000158552 00000 н. 0000158918 00000 н. 0000160807 00000 н. 0000161083 00000 н. 0000162644 00000 н. 0000162930 00000 н. 0000172054 00000 н. 0000172093 00000 н. 0000186126 00000 н. 0000186165 00000 н. 0000186411 00000 н. 0000186828 00000 н. 0000186949 00000 н. 0000187098 00000 н. 0000187517 00000 н. 0000187614 00000 н. 0000187763 00000 н. 0000188009 00000 н. 0000188449 00000 н. 0000188571 00000 н. 0000188728 00000 н. 0000188844 00000 н. 0000188941 00000 н. 0000189098 00000 н. 0000195336 00000 н. 0000202424 00000 н. 0000202668 00000 н. 0000202917 00000 н. 0000203123 00000 н. 0000203356 00000 н. 0000203542 00000 н. 0000203766 00000 н. 0000203993 00000 н. 0000204262 00000 н. 0000204533 00000 н. 0000205172 00000 н. 0000206277 00000 н. 0000206971 00000 н. 0000207231 00000 н. 0000207492 00000 н. 0000209116 00000 н. 0000210890 00000 н. 0000215447 00000 н. 0000216549 00000 н. 0000216800 00000 н. 0000217049 00000 н. 0000219456 00000 н. 0000219708 00000 н. 0000219967 00000 н. 0000220230 00000 н. 0000222196 00000 н. 0000222527 00000 н. 0000222857 00000 н. 0000223242 00000 н. 0000223625 00000 н. 0000223868 00000 н. 0000224101 00000 п. 0000224347 00000 н. 0000242000 00000 н. 0000242946 00000 н. 0000243207 00000 н. 0000243444 00000 н. 0000244100 00000 н. 0000244552 00000 н. 0000244867 00000 н. 0000245090 00000 н. 0000245315 00000 н. 0000245544 00000 н. 0000246323 00000 н. 0000246988 00000 н. 0000247514 00000 н. 0000247834 00000 н. 0000248061 00000 н. 0000248289 00000 н. 0000248666 00000 н. 0000250292 00000 н. 0000253399 00000 н. 0000005129 00000 н. 0000004496 00000 н. трейлер ] / Назад 344149 / XRefStm 5129 >> startxref 0 %% EOF 491 0 объект > поток h ެ OhAfwc & mJVjiK.6 & FZDTzOA% ‘A4b) * «QDT \ Bl Y) M + 9> x
Легочная гипертензия — NHS
Легочная гипертензия — это высокое кровяное давление в кровеносных сосудах , снабжающих легкие (легочные артерии).
Это серьезное заболевание, которое может повредить правую часть сердца.
Стенки легочных артерий становятся толстыми и жесткими и не могут расширяться, чтобы пропустить кровь.
Из-за пониженного кровотока правой стороне сердца становится труднее перекачивать кровь по артериям.
Если правая сторона вашего сердца должна постоянно работать усерднее, она может постепенно ослабевать. Это может привести к сердечной недостаточности.
Легочная гипертензия — редкое заболевание, которое может поражать людей любого возраста, но чаще встречается у людей с другим заболеванием сердца или легких.
Симптомы легочной гипертензии
Симптомы легочной гипертензии включают:
Симптомы часто ухудшаются во время физических упражнений, что может ограничивать вашу способность принимать участие в физических нагрузках.
Если у вас легочная гипертензия, известная как легочная артериальная гипертензия (ЛАГ), симптомы могут не проявляться до тех пор, пока состояние не станет достаточно серьезным.
Когда обращаться к терапевту
Обратитесь к терапевту, если у вас есть какие-либо симптомы легочной гипертензии. Они могут спросить вас о ваших симптомах и истории болезни, а также могут провести медицинский осмотр.
Правильная диагностика легочной гипертензии иногда требует времени, поскольку ее симптомы аналогичны симптомам многих других заболеваний сердца и легких.
Тесты, которые могут быть у вас, включают тип сканирования сердца, называемый эхокардиограммой, и катетеризацию правых отделов сердца, при которой в легочную артерию вводится тонкая гибкая трубка.
Подробнее о диагностике легочной гипертензии.
Причины легочной гипертензии
Изменения в легочных артериях, которые приводят к легочной гипертензии, могут быть вызваны:
- проблемами с более мелкими ветвями легочных артерий (ЛАГ)
- состояниями, поражающими левую сторону сердца
- Заболевания легких или недостаток кислорода в организме (гипоксия)
- Тромбы, вызывающие сужение или закупорку легочных артерий
Подробнее о причинах легочной гипертензии.
Лечение легочной гипертензии
Легочную гипертензию нельзя вылечить, но лечение может уменьшить симптомы и помочь вам управлять своим состоянием.
Легочная гипертензия обычно со временем ухудшается. При отсутствии лечения это может вызвать сердечную недостаточность, которая может быть фатальной, поэтому важно начать лечение как можно скорее.
Если легочная гипертензия вызвана другим заболеванием, в первую очередь следует лечить основное заболевание.Иногда это может предотвратить необратимое повреждение легочных артерий.
Лечение легочной гипертензии может включать в себя антикоагулянты, снижающие способность крови к сгущению (свертыванию), и диуретики для удаления лишней жидкости в результате сердечной недостаточности.
Вам также могут предложить лекарства для расширения кровеносных сосудов.
Домашнее кислородное лечение также может быть назначено, если уровень кислорода в крови низкий.
Подробнее о лечении легочной гипертензии.
Перспективы
Перспективы легочной гипертензии различаются в зависимости от таких факторов, как:
- , что вызывает ее
- , как быстро диагностируется
- , насколько развиты ваши симптомы
- , есть ли у вас другое основное заболевание
Специалист ответственный за ваше лечение сможет предоставить вам более подробную информацию.
Легочная гипертензия может повлиять на вашу способность выполнять повседневные дела.
Благотворительная ассоциация легочной гипертензии Великобритании предлагает практическую информацию и поддержку людям, страдающим легочной гипертензией, а также их друзьям и семьям.
Последняя проверка страницы: 23 января 2020 г.
Срок следующей проверки: 23 января 2023 г.
Легочная эмболия (PE): основы практики, история вопроса, анатомия
Amesquita M, Cocchi MN, Donnino MW. Легочная эмболия, проявляющаяся как боль в боку: серия клинических случаев. J Emerg Med .2009 26 марта. [Medline].
Carrascosa MF, Batán AM, Novo MF. Делирий и тромбоэмболия легочной артерии у пожилых людей. Mayo Clin Proc . 2009. 84 (1): 91-2. [Медлайн]. [Полный текст].
Tapson VF. Острая тромбоэмболия легочной артерии. N Engl J Med . 2008 6 марта. 358 (10): 1037-52. [Медлайн].
[Рекомендации] Казим А., Сноу В., Барри П., Хорнбейк Э. Р., Родник Дж. Э., Тоболик Т. и др. Текущий диагноз венозной тромбоэмболии в первичной медико-санитарной помощи: руководство по клинической практике Американской академии семейных врачей и Американского колледжа врачей. Энн Фам Мед . 2007 янв-фев. 5 (1): 57-62. [Медлайн]. [Полный текст].
[Рекомендации] Guyatt GH, Akl EA, Crowther M, Gutterman DD, Schuünemann HJ, Группа американских врачей-терапевтов по антитромботической терапии и профилактике тромбозов. Краткое содержание: Антитромботическая терапия и профилактика тромбозов, 9-е изд. Американского колледжа врачей-терапевтов по клинической практике, основанные на фактических данных. Сундук . 2012 фев. 141 (2 доп.): 7С-47С. [Медлайн].
Ozsu S, Oztuna F, Bulbul Y, et al. Роль факторов риска в поздней диагностике тромбоэмболии легочной артерии. Am J Emerg Med . 2011 29 января (1): 26-32. [Медлайн].
Kline JA, Runyon MS. Легочная эмболия и тромбоз глубоких вен. В: Marx JA, Hockenberger RS, Walls RM, eds. Концепции неотложной медицины и клиническая практика Розена . 6-е изд. 1368–1382. Том 2 .:
Бойден EA. Сегментарная анатомия легких: изучение структуры сегментарных бронхов и связанных с ними легочных сосудов .Нью-Йорк, штат Нью-Йорк: Макгроу-Хилл; 1955 г .:. 23-32.
Митчелл Р.Н., Кумар В. Нарушения гемодинамики, тромбозы и шок. В: Kumar V, Cotran RS, Robbins SL, eds. Основная патология . 6-е изд. Филадельфия, Пенсильвания: У. Б. Сондерс; 1997 г .:. 60-80.
Wharton LR, Пирсон JW. ДЖАМА. Малые формы тромбоэмболии легочной артерии после абдоминальных операций .
Малек Дж., Роджерс Р., Куфера Дж., Хиршон Дж. М.. Венозная тромбоэмболия у ВИЧ-инфицированного пациента. Am J Emerg Med . 2011 29 марта (3): 278-82. [Медлайн].
Geerts WH, Code KI, Jay RM, Chen E, Szalai JP. Проспективное исследование венозной тромбоэмболии после обширной травмы. N Engl J Med . 1994 15 декабря. 331 (24): 1601-6. [Медлайн].
van den Heuvel-Eibrink MM, Lankhorst B, Egeler RM, Corel LJ, Kollen WJ. Внезапная смерть из-за тромбоэмболии легочной артерии как симптом опухоли почек. Рак крови у детей .2008 май. 50 (5): 1062-4. [Медлайн].
Arzt M, Luigart R, Schum C, Lüthje L, Stein A, Koper I, et al. Нарушение дыхания во сне при тромбозе глубоких вен и острой тромбоэмболии легочной артерии. Eur Respir J . 2012 Октябрь 40 (4): 919-24. [Медлайн].
Stein PD, Beemath A, Matta F, Weg JG, Yusen RD, Hales CA и др. Клиническая характеристика пациентов с острой тромбоэмболией легочной артерии: данные PIOPED II. Am J Med . 2007 окт.120 (10): 871-9. [Медлайн]. [Полный текст].
Дэвид М., Эндрю М. Венозные тромбоэмболические осложнения у детей. Дж. Педиатр . 1993 Сентябрь 123 (3): 337-46. [Медлайн].
Biss TT, Brandão LR, Kahr WH, Chan AK, Williams S. Клинические особенности и исходы тромбоэмболии легочной артерии у детей. Br J Haematol . 2008 Сентябрь 142 (5): 808-18. [Медлайн].
Nuss R, Hays T, Chudgar U, Manco-Johnson M. Антифосфолипидные антитела и аномалии регуляторных белков свертывания крови у детей с тромбоэмболией легочной артерии. J Педиатр Hematol Oncol . 1997 май-июнь. 19 (3): 202-7. [Медлайн].
Dollery CM. Тромбоэмболия легочной артерии при парентеральном питании. Арч Дис Детский . 1996 Февраль 74 (2): 95-8. [Медлайн]. [Полный текст].
Хорландер К.Т., Маннино Д.М., Липер К.В. Смертность от легочной эмболии в США, 1979–1998 годы: анализ с использованием данных о смертности от нескольких причин. Arch Intern Med . 28 июля 2003 г. 163 (14): 1711-7. [Медлайн].
Burge AJ, Freeman KD, Klapper PJ, Haramati LB.Повышенная диагностика тромбоэмболии легочной артерии без соответствующего снижения смертности в эпоху КТ. Клин Радиол . 2008 апр. 63 (4): 381-6. [Медлайн].
DeMonaco NA, Dang Q, Kapoor WN, Ragni MV. Заболеваемость тромбоэмболией легочной артерии увеличивается с использованием спиральной компьютерной томографии. Am J Med . 2008 июль 121 (7): 611-7. [Медлайн]. [Полный текст].
Сильверштейн, доктор медицины, Хейт Дж. А., Мор Д. Н., Петтерсон Т. М., О’Фаллон В. М., Мелтон Л. Дж. 3-й.Тенденции в частоте тромбоза глубоких вен и тромбоэмболии легочной артерии: 25-летнее популяционное исследование. Arch Intern Med . 1998, 23 марта. 158 (6): 585-93. [Медлайн].
Heit JA. Эпидемиология венозной тромбоэмболии в обществе. Артериосклерный тромб Vasc Biol . 2008 марта, 28 (3): 370-2. [Медлайн]. [Полный текст].
Сандлер Д.А., Мартин Дж.Ф. Тромбоэмболия легочной артерии у пациентов больниц, подтвержденная вскрытием: достаточно ли мы выявляем тромбоз глубоких вен? J R Soc Med . 1989 апр. 82 (4): 203-5. [Медлайн]. [Полный текст].
Коцакис А., Кук Д., Гриффит Л., Антон Н., Массикотт П., МакФарланд К. и др. Клинически важная венозная тромбоэмболия в педиатрической реанимации: канадское исследование. J Crit Care . 2005 Декабрь 20 (4): 373-80. [Медлайн].
Ван Оммен Ч., Питерс М. Острая тромбоэмболия легочной артерии в детстве. Тромб Рес . 2006. 118 (1): 13-25. [Медлайн].
Kabrhel C, Varraso R, Goldhaber SZ, Rimm E, Camargo CA Jr.Низкая физическая активность и идиопатическая тромбоэмболия легочной артерии у женщин: проспективное исследование. BMJ . 2011 г. 4 июля. 343: d3867. [Медлайн].
Schneider D, Lilienfeld DE, Im W. Эпидемиология тромбоэмболии легочной артерии: расовые различия в заболеваемости и летальности в больницах. J Natl Med Assoc . 2006 декабрь 98 (12): 1967-72. [Медлайн]. [Полный текст].
Meyer G, Planquette B, Sanchez O. Отдаленный исход тромбоэмболии легочной артерии. Curr Opin Hematol .2008 15 сентября (5): 499-503. [Медлайн].
Bernstein D, Coupey S, Schonberg SK. Тромбоэмболия легочной артерии у подростков. Ам Дж. Дис Детский . 1986 июл.140 (7): 667-71. [Медлайн].
Эванс Д.А., Уилмотт Р.В. Тромбоэмболия легочной артерии у детей. Педиатр Клиника North Am . 1994 июн. 41 (3): 569-84. [Медлайн].
Rajpurkar M, Warrier I, Chitlur M, Sabo C., Frey MJ, Hollon W. и др. Тромбоэмболия легочной артерии — опыт единой детской больницы. Тромб Рес . 2007. 119 (6): 699-703. [Медлайн].
Куклина Е.В., Мейкл С.Ф., Джеймисон Д.Д., Уайтман М.К., Барфилд В.Д., Хиллис С.Д. и др. Тяжелая акушерская заболеваемость в США: 1998-2005 гг. Акушерский гинеколь . 2009 февраль 113 (2, часть 1): 293-9. [Медлайн]. [Полный текст].
Уорсли Д.Ф., Алави А. Всесторонний анализ результатов исследования PIOPED. Проспективное исследование диагностического исследования легочной эмболии. Дж. Nucl Med .1995 Декабрь 36 (12): 2380-7. [Медлайн].
Cavallazzi R, Nair A, Vasu T, Marik PE. Натрийуретические пептиды при острой тромбоэмболии легочной артерии: систематический обзор. Intensive Care Med . 2008 декабрь 34 (12): 2147-56. [Медлайн].
Alonso-Martínez JL, Urbieta-Echezarreta M, Anniccherico-Sánchez FJ, Abínzano-Guillén ML, Garcia-Sanchotena JL. N-концевой натрийуретический пептид про-B-типа предсказывает бремя тромбоэмболии легочной артерии. Am J Med Sci .2009 Февраль 337 (2): 88-92. [Медлайн].
Ванни С., Вивиани Дж., Байони М., Пепе Дж., Назериан П., Соччи Ф. и др. Прогностическое значение уровней лактата в плазме у пациентов с острой тромбоэмболией легочной артерии: исследование исходов лактата тромбоэмболии. Энн Эмерг Мед . 2013 Март 61 (3): 330-8. [Медлайн].
Goldhaber SZ, Visani L, De Rosa M. Острая тромбоэмболия легочной артерии: клинические результаты в Международном совместном регистре тромбоэмболии легочной артерии (ICOPER). Ланцет . 1999 24 апреля. 353 (9162): 1386-9. [Медлайн].
Дерево KE. Большая легочная эмболия: обзор патофизиологического подхода к золотому часу гемодинамически значимой легочной эмболии. Сундук . 2002, март, 121 (3): 877-905. [Медлайн].
Kucher N, Rossi E, De Rosa M, Goldhaber SZ. Массивная тромбоэмболия легочной артерии. Тираж . 2006 31 января, 113 (4): 577-82. [Медлайн].
[Рекомендации] Konstantinides SV, Torbicki A, Agnelli G, et al.Рекомендации ESC по диагностике и лечению острой тромбоэмболии легочной артерии, 2014 г. Eur Heart J . 2014 14 ноября. 35 (43): 3033-69, 3069a-3069k. [Медлайн].
Ведовати М.К., Бекаттини С., Аньелли Г., Кампхуйзен П.В., Масотти Л., Прущик П. и др. МУЛЬТИДЕТЕКТОРНАЯ КОМПЬЮТЕРНАЯ ТОМОГРАФИЯ ОСТРОЙ ЭМБОЛИИ ЛЕГКИХ: ЭМБОЛИЧЕСКОЕ БРЕМЯ И КЛИНИЧЕСКИЕ ИСХОДЫ. Сундук . 2012 г. 24 мая. [Medline].
Restrepo CS, Artunduaga M, Carrillo JA, Rivera AL, Ojeda P, Martinez-Jimenez S, et al.Силиконовая тромбоэмболия легочной артерии: отчет о 10 случаях и обзор литературы. J Comput Assist Tomogr . 2009 март-апрель. 33 (2): 233-7. [Медлайн].
Вичинский Е.П., Ноймайр Л.Д., Эрлз А.Н., Уильямс Р., Леннетт Е.Т., Дин Д. и др. Причины и исходы острого грудного синдрома при серповидно-клеточной анемии. Национальная группа по изучению острого синдрома грудной клетки. N Engl J Med . 2000, 22 июня. 342 (25): 1855-65. [Медлайн].
Douma RA, Mos IC, Erkens PM, Nizet TA, Durian MF, Hovens MM, et al.Выполнение 4 правил принятия клинических решений при диагностическом ведении острой тромбоэмболии легочной артерии: проспективное когортное исследование. Энн Интерн Мед. . 7 июня 2011 г. 154 (11): 709-18. [Медлайн].
Stein PD, Hull RD, Patel KC, Olson RE, Ghali WA, Brant R и др. D-димер для исключения острого венозного тромбоза и тромбоэмболии легочной артерии: систематический обзор. Энн Интерн Мед. . 2004, 20 апреля. 140 (8): 589-602. [Медлайн].
Кеарон С., Гинзберг Дж. С., Дукетис Дж., Турпи АГ, Бейтс С. М., Ли А. Ю. и др.Оценка D-димера в диагностике легочной эмболии: рандомизированное исследование. Энн Интерн Мед. . 6 июня 2006 г. 144 (11): 812-21. [Медлайн].
Geersing GJ, Erkens PM, Lucassen WA, Büller HR, Cate HT, Hoes AW и др. Безопасное исключение тромбоэмболии легочной артерии с использованием правила Уэллса и качественного тестирования D-димера в первичной медико-санитарной помощи: проспективное когортное исследование. BMJ . 4 октября 2012 г. 345: e6564. [Медлайн]. [Полный текст].
Константинидес С.Клиническая практика. Острая тромбоэмболия легочной артерии. N Engl J Med . 2008 25 декабря. 359 (26): 2804-13. [Медлайн].
Kline JA, Hogg MM, Courtney DM, Miller CD, Jones AE, Smithline HA, et al. D-димер и выдыхаемый CO2 / O2 для выявления сегментарной тромбоэмболии легочной артерии у пациентов с умеренным риском. Am J Respir Crit Care Med . 2010 сен 1. 182 (5): 669-75. [Медлайн]. [Полный текст].
Turedi S, Gunduz A, Mentese A, Topbas M, Karahan SC, Yeniocak S, et al.Значение альбумина, модифицированного ишемией, по сравнению с d-димером в диагностике тромбоэмболии легочной артерии. Respir Res . 30 мая 2008 г. 9:49. [Медлайн]. [Полный текст].
Tick LW, Nijkeuter M, Kramer MH, Hovens MM, Büller HR, Leebeek FW и др. Высокий уровень D-димера увеличивает вероятность тромбоэмболии легочной артерии. Дж. Медицинский работник . 2008 Август 264 (2): 195-200. [Медлайн].
Мейер Т, Биндер Л, Хрушка Н, Люте Н, Бухвальд AB. Повышение сердечного тропонина I при острой тромбоэмболии легочной артерии связано с дисфункцией правого желудочка. Дж. Ам Кол Кардиол . 2000, 1. 36 (5): 1632-6. [Медлайн].
Хименес Д., Уресанди Ф., Отеро Р., Лобо Дж. Л., Монреаль М., Марти Д. и др. Стратификация риска пациентов с острой немассивной тромбоэмболией легочной артерии на основе тропонина: систематический обзор и метаанализ. Сундук . 2009 Октябрь, 136 (4): 974-82. [Медлайн].
Бекаттини С., Ведовати М.К., Аньелли Г. Диагностика и прогноз острой тромбоэмболии легочной артерии: основное внимание уделяется тропонинам сыворотки. Эксперт Рев Мол диагностика . 2008 май. 8 (3): 339-49. [Медлайн].
Kline JA, Zeitouni R, Marchick MR, Hernandez-Nino J, Rose GA. Сравнение 8 биомаркеров для прогнозирования гипокинеза правого желудочка через 6 месяцев после субмассивной тромбоэмболии легочной артерии. Сердце Дж. . 2008 Август 156 (2): 308-14. [Медлайн].
Аксай Э., Янтурали С., Киян С. Может ли повышенный уровень тропонина I предсказать осложненное клиническое течение и внутрибольничную смертность у пациентов с острой тромбоэмболией легочной артерии ?. Am J Emerg Med . 2007 25 февраля (2): 138-43. [Медлайн].
Dellas C, Lankeit M, Reiner C, Schäfer K, Hasenfuß G, Konstantinides S. Независимая от ИМТ обратная зависимость уровней лептина в плазме с исходом у пациентов с острой тромбоэмболией легочной артерии. Инт Дж. Обес (Лондон) . 2012 20 марта. [Medline].
Söhne M, Ten Wolde M, Boomsma F, Reitsma JB, Douketis JD, Büller HR. Натрийуретический пептид мозга при гемодинамически стабильной острой тромбоэмболии легочной артерии. Дж. Тромб Хемост . 2006 марта, 4 (3): 552-6. [Медлайн].
Kucher N, Printzen G, Goldhaber SZ. Прогностическая роль натрийуретического пептида головного мозга при острой тромбоэмболии легочной артерии. Тираж . 2003 27 мая. 107 (20): 2545-7. [Медлайн].
Klok FA, Mos IC, Huisman MV. Уровни натрийуретического пептида головного мозга в прогнозировании неблагоприятного исхода у пациентов с тромбоэмболией легочной артерии: систематический обзор и метаанализ. Am J Respir Crit Care Med .2008 15 августа. 178 (4): 425-30. [Медлайн].
Scherz N, Labarère J, Méan M, Ibrahim SA, Fine MJ, Aujesky D. Прогностическое значение гипонатриемии у пациентов с острой тромбоэмболией легочной артерии. Am J Respir Crit Care Med . 2010, 1. 182 (9): 1178-83. [Медлайн]. [Полный текст].
Готов T. Легочная эмболия с гипердиагностикой при КТ-ангиографии. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/807439. Доступ: 15 июля 2013 г.
Винер Р.С., Шварц Л.М., Волошин С. Когда тест слишком хорош: как КТ-ангиограмма легких обнаруживает легочную эмболию, которую не нужно обнаруживать. BMJ . 2013 г. 2 июля. 347: f3368. [Медлайн].
[Рекомендации] Реми-Жардин М., Пистолези М., Гудман Л. Р., Гефтер В. Б., Готтшалк А., Майо Д. Р. и др. Ведение пациентов с подозрением на острую тромбоэмболию легочной артерии в эпоху КТ-ангиографии: заявление Общества Флейшнера. Радиология .2007 ноябрь 245 (2): 315-29. [Медлайн].
Patel S, Kazerooni EA. Спиральная компьютерная томография для оценки острой тромбоэмболии легочной артерии. AJR Am J Рентгенол . 2005 июл.185 (1): 135-49. [Медлайн].
Stein PD, Woodard PK, Weg JG, Wakefield TW, Tapson VF, Sostman HD и др. Пути диагностики острой тромбоэмболии легочной артерии: рекомендации исследователей PIOPED II. Радиология . 2007 Январь 242 (1): 15-21. [Медлайн].
[Рекомендации] Беттманн М.А., Багински С.Г., Уайт Р.Д., Вудард П.К., Аббара С., Аталай М.К. и др.Критерии соответствия ACR® острая боль в груди — подозрение на тромбоэмболию легочной артерии. Дж. Визуализация грудной клетки . 2012 марта, 27 (2): W28-31. [Медлайн].
Ward MJ, Sodickson A, Diercks DB, Raja AS. Экономическая эффективность компрессионного УЗИ нижних конечностей у пациентов отделения неотложной помощи с высоким риском гемодинамически стабильной тромбоэмболии легочной артерии. Acad Emerg Med . 2011 18 января (1): 22–31. [Медлайн].
Drescher FS, Chandrika S, Weir ID, et al.Эффективность и приемлемость компьютеризированной системы поддержки принятия решений с использованием модифицированных критериев Уэллса для оценки подозреваемой тромбоэмболии легочной артерии. Энн Эмерг Мед . 2011 июн. 57 (6): 613-21. [Медлайн].
Реми-Жардин М., Реми Дж., Дешильдре Ф., Арто Д., Береги Дж. П., Хоссейн-Фуше С. и др. Диагностика тромбоэмболии легочной артерии с помощью спиральной компьютерной томографии: сравнение с ангиографией легких и сцинтиграфией. Радиология . 1996 Сентябрь 200 (3): 699-706. [Медлайн].
Бекаттини С., Аньелли Г., Ведовати М.С. и др. Многодетекторная компьютерная томография при острой тромбоэмболии легочной артерии: диагностика и стратификация риска в одном тесте. Eur Heart J . 2011 июл.32 (13): 1657-63. [Медлайн].
Henzler T, Roeger S, Meyer M, Schoepf UJ, Nance JW Jr, Haghi D, et al. Легочная эмболия: признаки КТ и сердечные биомаркеры для прогнозирования дисфункции правого желудочка. Eur Respir J . 2012 апр.39 (4): 919-26. [Медлайн].
Gottschalk A, Stein PD, Sostman HD, Matta F, Beemath A. Интерпретация результатов V / Q-сканирования легких с очень низкой вероятностью в сочетании с объективной клинической оценкой с низкой вероятностью надежно исключает легочную эмболию: данные PIOPED II. Дж. Nucl Med . 2007 Сентябрь 48 (9): 1411-5. [Медлайн].
Гупта А., Фрейзер К. К., Фергюсон Дж. М., Кумар А. Б., Дэвис С. Дж., Фэллон М. Дж. И др. Острая тромбоэмболия легочной артерии: диагностика с помощью МР-ангиографии. Радиология . 1999 Февраль 210 (2): 353-9. [Медлайн].
Мини JF, Weg JG, Chenevert TL, Stafford-Johnson D, Hamilton BH, Prince MR. Диагностика тромбоэмболии легочной артерии с помощью магнитно-резонансной ангиографии. N Engl J Med . 1997 15 мая. 336 (20): 1422-7. [Медлайн].
Ванни С., Полидори Дж., Вергара Р., Пепе Дж., Назериан П., Морони Ф. и др. Прогностическое значение ЭКГ у пациентов с острой тромбоэмболией легочной артерии и нормальным артериальным давлением. Am J Med . 2009 Март 122 (3): 257-64. [Медлайн].
Боггс В. Прикроватное эхо может облегчить ER-диагностику легочной эмболии. Медицинские новости Medscape. Доступно на http://www.medscape.com/viewarticle/812942. Доступ: 28 октября 2013 г.
Дрезден С., Митчелл П., Рахими Л., Лео М., Рубин-Смит Дж., Биби С. и др. Расширение правого желудочка при прикроватной эхокардиографии, выполняемой врачами скорой помощи при диагностике тромбоэмболии легочной артерии. Энн Эмерг Мед . 2013 23 сентября [Medline].
Штейн П.Д., Матта Ф. Тромболитическая терапия нестабильных пациентов с острой тромбоэмболией легочной артерии: спасает жизни, но используется недостаточно. Am J Med . 2012 май. 125 (5): 465-70. [Медлайн].
Штейн П.Д., Матта Ф, Киз, округ Колумбия, Виллиерд ГЛ. Влияние фильтров полой вены на уровень смертности от легочной эмболии в больницах. Am J Med . 2012 май. 125 (5): 478-84. [Медлайн].
Чаттерджи С., Чакраборти А., Вайнберг И., Кадакия М., Виленски Р.Л., Сардар П. и др.Тромболизис при тромбоэмболии легочной артерии и риск общей смертности, большого кровотечения и внутричерепного кровоизлияния: метаанализ. ДЖАМА . 2014 18 июня. 311 (23): 2414-21. [Медлайн].
Meyer G, Vicaut E, Danays T, Agnelli G, Becattini C, Beyer-Westendorf J, et al. Фибринолиз у пациентов с тромбоэмболией легочной артерии промежуточного риска. N Engl J Med . 2014 10 апреля. 370 (15): 1402-11. [Медлайн].
Эллиотт К.Г. Фибринолиз легочной эмболии — держитесь ближе к Сцилле. N Engl J Med . 2014 10 апреля. 370 (15): 1457-8. [Медлайн].
Barclay L. Фибринолиз при легочной эмболии эффективен, но опасен. Medscape [сериал онлайн]. Доступно на http://www.medscape.com/viewarticle/823427. Доступ: 19 апреля 2014 г.
Ауески Д., Рой П.М., Вершурен Ф. и др. Сравнение амбулаторного и стационарного лечения пациентов с острой тромбоэмболией легочной артерии: международное открытое рандомизированное исследование не меньшей эффективности. Ланцет . 2011 г. 2 июля. 378 (9785): 41-8. [Медлайн].
Büller HR, Prins MH, Lensin AW, Decousus H, Jacobson BF, Minar E, et al. Ривароксабан для перорального применения для лечения симптоматической тромбоэмболии легочной артерии. N Engl J Med . 2012 г., 5. 366 (14): 1287-97. [Медлайн].
Bauersachs R, Berkowitz SD, Brenner B, Buller HR, Decousus H, Gallus AS и др. Пероральный ривароксабан при симптоматической венозной тромбоэмболии. N Engl J Med .23 декабря 2010 г. 363 (26): 2499-510. [Медлайн]. [Полный текст].
Коэн А.Т., Добромирски М. Использование ривароксабана для краткосрочного и длительного лечения венозной тромбоэмболии. Тромб Гемост . 2012 июн 107 (6): 1035-43. [Медлайн].
Romualdi E, Donadini MP, Ageno W. Пероральный ривароксабан после симптоматической венозной тромбоэмболии: исследование продолжения лечения (расширенное исследование EINSTEIN). Эксперт Рев Кардиоваск Тер . 2011 июл.9 (7): 841-4. [Медлайн].
Hughes S. Rivaroxaban Соответствует стандартным антикоагулянтам при лечении ВТЭ. Медицинские новости Medscape. 13 декабря 2012 г. [Полный текст].
Buller HR, от имени следователей EINSTEIN. Пероральный ривароксабан для лечения симптоматической венозной тромбоэмболии: объединенный анализ исследований EINSTEIN DVT и EINSTEIN PE [аннотация 20]. Представлено на: 54-м ежегодном собрании и выставке Американского общества гематологов; 8 декабря 2012 г .; Атланта, Джорджия[Полный текст].
Коэн А.Т., Спиро Т.Э., Бюллер Х.Р., Хаскелл Л., Ху Д., Халл Р. и др. Ривароксабан для тромбопрофилактики у пациентов с острыми заболеваниями. N Engl J Med . 2013 Февраль 7. 368 (6): 513-23. [Медлайн]. [Полный текст].
Spyropoulos AC, Ageno W., Albers GW, Elliott CG, Halperin JL, Hiatt WR, et al. Ривароксабан для тромбопрофилактики после госпитализации по болезни. N Engl J Med . 2018 20 сентября. 379 (12): 1118-1127.[Медлайн]. [Полный текст].
Agnelli G, Buller HR, Cohen A, Curto M, Gallus AS, Johnson M, et al. Апиксабан для перорального применения для лечения острой венозной тромбоэмболии. N Engl J Med . 2013 29 августа. 369 (9): 799-808. [Медлайн]. [Полный текст].
Agnelli G, Buller HR, Cohen A, Curto M, Gallus AS, Johnson M, et al. Апиксабан для расширенного лечения венозной тромбоэмболии. N Engl J Med . 2013 21 февраля. 368 (8): 699-708. [Медлайн].[Полный текст].
Schulman S, Kearon C, Kakkar AK, Mismetti P, Schellong S, Eriksson H, et al. Дабигатран по сравнению с варфарином в лечении острой венозной тромбоэмболии. N Engl J Med . 2009 декабрь 10. 361 (24): 2342-52. [Медлайн]. [Полный текст].
Шульман С., Каккар А.К., Голдхабер С.З., Шеллонг С., Эрикссон Х., Мисметти П. и др. Лечение острой венозной тромбоэмболии дабигатраном или варфарином и объединенный анализ. Тираж .2014 18 февраля. 129 (7): 764-72. [Медлайн].
Büller HR, Décousus H, Grosso MA, Mercuri M, Middeldorp S, Prins MH, et al. Эдоксабан по сравнению с варфарином для лечения симптоматической венозной тромбоэмболии. N Engl J Med . 2013 октябрь 10. 369 (15): 1406-15. [Медлайн]. [Полный текст].
Cohen AT, Harrington RA, Goldhaber SZ, Hull RD, Wiens BL, Gold A, et al. Расширенная тромбопрофилактика бетриксабаном у пациентов с острыми заболеваниями. N Engl J Med .2016 11 августа 375 (6): 534-44. [Медлайн]. [Полный текст].
Гибсон С.М., Чи Дж., Халаби Р., Корджиан С., Даабул И., Джайн П. и др. Бетриксабан с увеличенной продолжительностью действия снижает риск инсульта по сравнению со стандартной дозой эноксапарина среди госпитализированных пациентов с медицинскими заболеваниями: вспомогательное исследование APEX (Профилактика острой соматической венозной тромбоэмболии с помощью бетриксабана с увеличенной продолжительностью действия). Тираж . 2017 14 февраля. 135 (7): 648-655. [Медлайн].
Garcia D, Ageno W, Libby E.Обновленная информация о диагностике и лечении тромбоэмболии легочной артерии. Br J Haematol . 2005 ноябрь 131 (3): 301-12. [Медлайн].
Campbell IA, Bentley DP, Prescott RJ, Routledge PA, Shetty HG, Williamson IJ. Антикоагулянтная терапия в течение трех месяцев по сравнению с шестью месяцами у пациентов с тромбозом глубоких вен или тромбоэмболией легочной артерии или и тем, и другим: рандомизированное исследование. BMJ . 31 марта 2007 г. 334 (7595): 674. [Медлайн]. [Полный текст].
Pinede L, Ninet J, Duhaut P, Chabaud S, Demolombe-Rague S, Durieu I, et al.Сравнение 3 и 6 месяцев терапии пероральными антикоагулянтами после первого эпизода проксимального тромбоза глубоких вен или тромбоэмболии легочной артерии и сравнение 6 и 12 недель терапии после изолированного тромбоза глубоких вен теленка. Тираж . 2001 г. 22 мая. 103 (20): 2453-60. [Медлайн].
Jaff MR, McMurtry MS, Archer SL, Cushman M, Goldenberg N, Goldhaber SZ и др. Управление массивной и субмассивной тромбоэмболией легочной артерии, тромбозом глубоких подвздошных вен и хронической тромбоэмболической легочной гипертензией: научное заявление Американской кардиологической ассоциации. Тираж . 2011 26 апреля. 123 (16): 1788-1830. [Медлайн]. [Полный текст].
Ballew KA, Philbrick JT, Becker DM. Аппараты с фильтром полой вены. Clin Chest Med . 1995 16 июня (2): 295-305. [Медлайн].
Dempfle CE, Elmas E, Link A, et al. Эндогенная плазма активировала уровни протеина С и влияние эноксапарина и дротрекогина альфа (активированного) на маркеры активации коагуляции и фибринолиза при тромбоэмболии легочной артерии. Crit Care . 2011 17 января 15 (1): R23. [Медлайн].
Boutitie F, Pinede L, Schulman S, Agnelli G, Raskob G, Julian J, et al. Влияние предшествующей продолжительности лечения антикоагулянтами и начальных проявлений венозной тромбоэмболии на риск рецидива после прекращения лечения: анализ данных отдельных участников из семи испытаний. BMJ . 2011 24 мая. 342: d3036. [Медлайн]. [Полный текст].
Hippisley-Cox J, Coupland C.Разработка и проверка алгоритма прогнозирования риска (QThrombosis) для оценки будущего риска венозной тромбоэмболии: проспективное когортное исследование. BMJ . 2011 16 августа. 343: d4656. [Медлайн]. [Полный текст].
[Рекомендации] Raja AS, Greenberg JO, Qaseem A., Denberg TD, Fitterman N, Schuur JD, et al. Оценка пациентов с подозрением на острую тромбоэмболию легочной артерии: рекомендации по передовой практике Комитета по клиническим рекомендациям Американского колледжа врачей. Энн Интерн Мед. .2015 3 ноября. 163 (9): 701-11. [Медлайн].
[Рекомендации] Fesmire FM, Brown MD, Espinosa JA, Shih RD, Silvers SM, Wolf SJ, et al. Критические вопросы оценки и ведения взрослых пациентов, поступающих в отделение неотложной помощи с подозрением на тромбоэмболию легочной артерии. Энн Эмерг Мед . 2011 июн. 57 (6): 628-652.e75. [Медлайн].
[Рекомендации] Кеарон С., Акл Э.А., Орнелас Дж., Блайвас А., Хименес Д., Боунамо Х. и др. Антитромботическая терапия при ВТЭ: руководство CHEST и отчет экспертной комиссии. Сундук . 2016 Февраль 149 (2): 315-52. [Медлайн].
[Рекомендации] Джеймс А., Комитет по практическим бюллетеням — акушерство. Бюллетень практики № 123: тромбоэмболия при беременности. Акушерский гинеколь . 2011 Сентябрь 118 (3): 718-29. [Медлайн].
[Рекомендации] Витт Д.М., Ньивлат Р., Кларк Н.П., Анселл Дж., Холбрук А., Сков Дж. И др. Рекомендации Американского общества гематологов по лечению венозной тромбоэмболии 2018 г .: оптимальное лечение антикоагулянтной терапии. Blood Adv . 2018 27 ноября, 2 (22): 3257-3291. [Медлайн].
вариантов лечения CTEPH — Бригам и женская больница
Каждый раз, когда пациент направляется в нашу программу хронической тромбоэмболической легочной гипертензии (CTEPH), врачи, представляющие все компоненты нашей практики — хирургические, интервенционные и медицинские, — собираются вместе, чтобы коллективно оценить состояние пациента. состояние и определить лучший курс лечения. Независимо от лечения, цели одни и те же — полностью удалить закупорки, восстановить кровообращение в легких, впоследствии поддержать это идеальное кровообращение и улучшить качество жизни пациента.Ваша терапия может включать одно или несколько из следующих методов лечения.
Легочная тромбоэндартерэктомия (хирургическое вмешательство)
BWH — один из немногих медицинских центров в США, который предлагает легочную тромбэндартерэктомию (PTE), передовую хирургическую процедуру по удалению закупорки в легких, в качестве лечения CTEPH.
ХТЭЛГ включает хроническое свертывание легочных артерий. Эти сгустки превращаются в массу рубцовой ткани, которая блокирует кровообращение в кровеносных сосудах. Эта блокада, в свою очередь, вызывает резкое повышение артериального давления и создает большую нагрузку на правый желудочек сердца, часть сердца, которая перекачивает кровь в легкие.Цель процедуры PTE — удалить как можно больше этого хронического сгустка, чтобы снизить кровяное давление в легочных артериях и уменьшить нагрузку на правый желудочек.
Чтобы пациент мог быть кандидатом на эту операцию, сгусток должен занимать значительную часть дерева легочной артерии, и сгусток должен быть доступен для хирурга. Хирургу легче получить доступ и удалить закупорки, которые начинаются в направлении центральной (и самой большой) ветви легкого.
Во время процедуры пациента помещают в аппарат искусственного кровообращения, который временно берет на себя функции сердца и легких пациента. Критически важным для успешного выполнения процедуры PTE является способность адекватно визуализировать внутреннюю часть дерева легочной артерии и особенно ее меньшие конечные ветви. Чтобы облегчить эту улучшенную визуализацию, тело пациента охлаждают до очень низкой температуры. Это позволяет безопасно выключать аппарат искусственного кровообращения на период до 15 минут или около того, что создает бескровное рабочее поле.Это помогает хирургу лучше видеть пораженный участок легкого и убедиться, что сгусток полностью удален. Низкие температуры защищают мозг и другие органы от повреждений в те периоды, когда аппарат искусственного кровообращения выключен.
После операции пациент обычно остается в больнице от одной до двух недель, в том числе от двух до четырех дней в отделении интенсивной терапии. Во время выздоровления в больнице пациенту будет помещен фильтр в главную вену нижней части тела, нижнюю полую вену, чтобы предотвратить попадание последующих сгустков крови в легкие.Вскоре после операции пациенты начнут принимать антикоагулянты, чтобы предотвратить дальнейшее образование тромбов и возможное поражение легких.
Интервенционное (катетерное) лечение
Мы также являемся лидером в использовании интервенционных методов для успешного лечения ХТЛГ. Когда закупорки изолированы в дистальных ветвях, сразу за главными ветвями легких, катетерное лечение — в руках опытного кардиолога — может быть столь же эффективным, как и хирургическое вмешательство.
Закупорки в этих областях недоступны для хирурга, но интервенционный кардиолог может добраться до них с помощью катетера (длинного, тонкого, гибкого медицинского инструмента), снабженного баллоном на конце. Как только катетер достигает места закупорки, баллон надувается, чтобы устранить закупорку. Также может быть вставлен стент (короткая расширяемая трубка), чтобы кровеносный сосуд оставался открытым.
Поскольку это не инвазивная процедура, интервенционный кардиолог может выбрать лечение вашего ХТЛГ в течение нескольких сеансов.Это не только помогает улучшить результаты, облегчая физические требования к интервенционисту, но также дает врачу возможность периодически и тщательно оценивать пациентов в ходе их курса лечения.
В дополнение к использованию в качестве основного лечения этот интервенционный подход иногда используется после операции для улучшения результатов у пациентов, у которых все еще есть остаточная дистальная блокада.
Медицинский менеджмент
Когда требуется медицинское лечение, мы используем в основном те же лекарства (антикоагулянты), которые использовались бы при любой форме легочной гипертензии.Наши специалисты по легочной медицине и сосудистой медицине совместно работают над оптимизацией антикоагуляции у пациентов с ХТЛГ, а также исследуют возможности использования новых препаратов.


